CN114893585A - 微流阀和装置 - Google Patents
微流阀和装置 Download PDFInfo
- Publication number
- CN114893585A CN114893585A CN202111648713.5A CN202111648713A CN114893585A CN 114893585 A CN114893585 A CN 114893585A CN 202111648713 A CN202111648713 A CN 202111648713A CN 114893585 A CN114893585 A CN 114893585A
- Authority
- CN
- China
- Prior art keywords
- fluid
- channel
- microfluidic
- capture
- agent
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- F—MECHANICAL ENGINEERING; LIGHTING; HEATING; WEAPONS; BLASTING
- F16—ENGINEERING ELEMENTS AND UNITS; GENERAL MEASURES FOR PRODUCING AND MAINTAINING EFFECTIVE FUNCTIONING OF MACHINES OR INSTALLATIONS; THERMAL INSULATION IN GENERAL
- F16K—VALVES; TAPS; COCKS; ACTUATING-FLOATS; DEVICES FOR VENTING OR AERATING
- F16K99/00—Subject matter not provided for in other groups of this subclass
- F16K99/0001—Microvalves
- F16K99/0003—Constructional types of microvalves; Details of the cutting-off member
- F16K99/0015—Diaphragm or membrane valves
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
- B01L3/5027—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
- B01L3/5027—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip
- B01L3/50273—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip characterised by the means or forces applied to move the fluids
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
- B01L3/5027—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip
- B01L3/502738—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip characterised by integrated valves
-
- F—MECHANICAL ENGINEERING; LIGHTING; HEATING; WEAPONS; BLASTING
- F16—ENGINEERING ELEMENTS AND UNITS; GENERAL MEASURES FOR PRODUCING AND MAINTAINING EFFECTIVE FUNCTIONING OF MACHINES OR INSTALLATIONS; THERMAL INSULATION IN GENERAL
- F16K—VALVES; TAPS; COCKS; ACTUATING-FLOATS; DEVICES FOR VENTING OR AERATING
- F16K7/00—Diaphragm valves or cut-off apparatus, e.g. with a member deformed, but not moved bodily, to close the passage ; Pinch valves
- F16K7/12—Diaphragm valves or cut-off apparatus, e.g. with a member deformed, but not moved bodily, to close the passage ; Pinch valves with flat, dished, or bowl-shaped diaphragm
-
- F—MECHANICAL ENGINEERING; LIGHTING; HEATING; WEAPONS; BLASTING
- F16—ENGINEERING ELEMENTS AND UNITS; GENERAL MEASURES FOR PRODUCING AND MAINTAINING EFFECTIVE FUNCTIONING OF MACHINES OR INSTALLATIONS; THERMAL INSULATION IN GENERAL
- F16K—VALVES; TAPS; COCKS; ACTUATING-FLOATS; DEVICES FOR VENTING OR AERATING
- F16K7/00—Diaphragm valves or cut-off apparatus, e.g. with a member deformed, but not moved bodily, to close the passage ; Pinch valves
- F16K7/12—Diaphragm valves or cut-off apparatus, e.g. with a member deformed, but not moved bodily, to close the passage ; Pinch valves with flat, dished, or bowl-shaped diaphragm
- F16K7/123—Diaphragm valves or cut-off apparatus, e.g. with a member deformed, but not moved bodily, to close the passage ; Pinch valves with flat, dished, or bowl-shaped diaphragm the seat being formed on the bottom of the fluid line
-
- F—MECHANICAL ENGINEERING; LIGHTING; HEATING; WEAPONS; BLASTING
- F16—ENGINEERING ELEMENTS AND UNITS; GENERAL MEASURES FOR PRODUCING AND MAINTAINING EFFECTIVE FUNCTIONING OF MACHINES OR INSTALLATIONS; THERMAL INSULATION IN GENERAL
- F16K—VALVES; TAPS; COCKS; ACTUATING-FLOATS; DEVICES FOR VENTING OR AERATING
- F16K7/00—Diaphragm valves or cut-off apparatus, e.g. with a member deformed, but not moved bodily, to close the passage ; Pinch valves
- F16K7/12—Diaphragm valves or cut-off apparatus, e.g. with a member deformed, but not moved bodily, to close the passage ; Pinch valves with flat, dished, or bowl-shaped diaphragm
- F16K7/126—Diaphragm valves or cut-off apparatus, e.g. with a member deformed, but not moved bodily, to close the passage ; Pinch valves with flat, dished, or bowl-shaped diaphragm the seat being formed on a rib perpendicular to the fluid line
-
- F—MECHANICAL ENGINEERING; LIGHTING; HEATING; WEAPONS; BLASTING
- F16—ENGINEERING ELEMENTS AND UNITS; GENERAL MEASURES FOR PRODUCING AND MAINTAINING EFFECTIVE FUNCTIONING OF MACHINES OR INSTALLATIONS; THERMAL INSULATION IN GENERAL
- F16K—VALVES; TAPS; COCKS; ACTUATING-FLOATS; DEVICES FOR VENTING OR AERATING
- F16K99/00—Subject matter not provided for in other groups of this subclass
- F16K99/0001—Microvalves
- F16K99/0034—Operating means specially adapted for microvalves
- F16K99/0042—Electric operating means therefor
-
- F—MECHANICAL ENGINEERING; LIGHTING; HEATING; WEAPONS; BLASTING
- F16—ENGINEERING ELEMENTS AND UNITS; GENERAL MEASURES FOR PRODUCING AND MAINTAINING EFFECTIVE FUNCTIONING OF MACHINES OR INSTALLATIONS; THERMAL INSULATION IN GENERAL
- F16K—VALVES; TAPS; COCKS; ACTUATING-FLOATS; DEVICES FOR VENTING OR AERATING
- F16K99/00—Subject matter not provided for in other groups of this subclass
- F16K99/0001—Microvalves
- F16K99/0034—Operating means specially adapted for microvalves
- F16K99/0042—Electric operating means therefor
- F16K99/0046—Electric operating means therefor using magnets
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/08—Geometry, shape and general structure
- B01L2300/0809—Geometry, shape and general structure rectangular shaped
- B01L2300/0816—Cards, e.g. flat sample carriers usually with flow in two horizontal directions
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/08—Geometry, shape and general structure
- B01L2300/0887—Laminated structure
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/12—Specific details about materials
- B01L2300/123—Flexible; Elastomeric
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2400/00—Moving or stopping fluids
- B01L2400/04—Moving fluids with specific forces or mechanical means
- B01L2400/0403—Moving fluids with specific forces or mechanical means specific forces
- B01L2400/043—Moving fluids with specific forces or mechanical means specific forces magnetic forces
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2400/00—Moving or stopping fluids
- B01L2400/06—Valves, specific forms thereof
- B01L2400/0633—Valves, specific forms thereof with moving parts
- B01L2400/0655—Valves, specific forms thereof with moving parts pinch valves
Abstract
提供了微流阀组件和微流体感测平台。阀组件对于分离检验流体与软基底(例如PDMS基底)接触具有特别的效用。阀构件包括定位成密封流体通道的可拉伸膜。微流体感测平台特别适合于检测和/或量化流体样本中一种或多种目标剂的存在。该系统包括:微流控芯片,其构造为接收捕获剂和检测剂;控制器,其构造为控制捕获剂和检测剂的流动;以及传感器,其构造为检测目标剂与捕获剂和检测剂的混合物之间的相互作用的结果。
Description
本申请是申请号为201680039266.4(国际申请号为PCT/EP2016/059660)、申请日为2016年4月29日、发明名称为“微流阀和装置”的专利申请的分案申请。
相关申请
本申请要求于2015年4月30日递交的、名称为“微流阀组件(Microfluidic ValveAssembly)”的第62/155,470号美国临时申请的权益,上述申请的内容通过引用整体并入本文。
本申请要求于2015年5月5日递交的、名称为“微流体感测平台(MicrofluidicSensing Platform)”的第62/156,368号美国临时申请的权益,上述申请的内容通过引用整体并入本文。
技术领域
本技术涉及微流体装置和阀,并且更具体地,涉及包括用于选择性地控制微流体装置内的流体的流动的阀的微流体装置。该技术还涉及用于检测和/或量化流体内一种或多种目标剂的存在的微流体系统和方法。
背景技术
包括微尺度和纳米尺度的流体的控制的微流体技术有许多应用。一个领域在于处理少量生物流体,例如血液。具体地,可以在微流控芯片上处理生物流体以确定流体组成并量化流体中某些生物标记的存在。这可以用于许多应用,包括医疗诊断。
微流体在医学应用中的优势之一包括使用较少量的生物流体进行各种检验的能力。例如,对于许多医学检验,可以使用手指穿刺血滴来替代整筒注射器的血液。微流体的其它优点还包括与宏观尺度上的相同检验相比,使用较少的试剂来实行医学诊断检验所需的反应的能力。相对于传统实验室系统,微流体装置(例如微流控芯片和任何相关仪器)的较小尺寸带来显著的优势。具体地,微流体装置可以允许在护理点(point-of-care),例如在诊所或者甚至在患者家中,执行检验。
通常,在微流体工业中广泛使用流体阀,例如叶片型致动器,其允许限制或调节微流体通道中的流体流动。借助流体阀,大多数常规系统能够将样本流体的受控流动提供到微流控芯片上的多个段或通道中。当这样的阀布置不能关闭流体流动时,检验结果可能变得不准确。此外,可以实现复杂的阀元件,但是使用这种阀元件的组件的制造是昂贵的,并且因为这样的微流控布置难以或不可能保持和再使用,所以仅提供一次性使用的检验布置。
此外,在微流体学中,阀组件的质量对于在需要时或如期望的那样确保精确量的流体可以通过微流控芯片中的通道移动、并且不同的流体可以移动到微流控芯片中特定的微流体结构(例如孔、通道等等)是重要的。常规地,微流控芯片上的阀或微流阀由被动阀(例如毛细管阀)和主动阀二者组成,这些阀通过致动力控制。大多数普通类型的主动阀包括:流体通道,其中关注的液体流过该流体通道;以及控制通道,其填充有控制流体,例如流过控制通道的空气或液压流体。控制通道和流体通道可以在它们之间具有可拉伸的材料。当控制通道中的压力增加时,可拉伸材料膨胀并阻碍流体通道内的流动。这些系统的最普遍的例子是Quake阀和门垫式阀(doormat-type valve)系统。Quake阀通常打开,当增大的空气压力通过控制通道施加时,可拉伸材料膨胀以关闭流动通道。
在门垫式阀中,当控制通道的气压足够时,由于可拉伸材料与防止液体通过的柱或其它结构形成紧密接触,所以阀关闭。当空气压力小于流体通道内的液体压力时,通过拉伸可拉伸材料,液体迫使阀打开。因此,这些类型的阀已知为常闭阀,因为它们在可拉伸材料的松弛状态下关闭。Quake阀和门垫式阀仅由单一可拉伸材料构成,例如聚二甲基硅氧烷(PDMS)作为最具拉伸性的固体材料之一。但是,这种材料对于医学诊断应用具有一些缺点。许多这种可拉伸材料在微流体装置的使用中,特别是在诊断中具有显著的限制。例如,根据诸如温度和湿度的环境因素,PDMS显著地膨胀和收缩,因此难以精确地控制其机械加工、模制或以其它方式制造成这种材料的结构的部件特征,例如尺寸。
特征尺寸和其它相关因素的控制对于精确控制流体流动是必不可少的,这对于获得精确的诊断检验结果是必需的。其次,对于许多这样的材料,特别是PDMS,难以稳定地功能化材料的表面。这是因为材料的柔软性质导致聚合物链相对于彼此不断移动,因此表面的组成不断变化。如果没有稳定的功能化,表面对于与PDMS结合的复合介质(例如蛋白质)的组分仍然是开放的,这可能导致通道堵塞以及目标分析物浓度的变化。因此,优选的是避免诸如PDMS的可拉伸膜与复杂分析物接触。因此,长期以来存在但仍未解决对如下微流阀组件的需求:所述微流阀组件可基本上分离检验流体与可拉伸膜或其它相关柔软元件的接触。
目前的标准目标剂量化检验,例如96孔板上的夹心或竞争ELISA,在实验室系统中可用于确定样本中例如蛋白质的目标剂的存在和数量。许多检验,例如对于毒性或某些人类疾病的检验,需要测量检验样本中的多种蛋白标记物,并且这利用这种实验室系统同时进行。然而,情况是:如果可在实验室外进行检验,常常会增加检验的效用,例如,如果疾病诊断检验可以由医生或护士在他们的办公室或甚至在病人的家中进行,即移动或即时医疗形式,能够显著增大检验的效用以及转变疾病治疗和病人护理。
增大效用的移动系统的替代实例是用于可以节省成本的食品检验,或者可用于在实际生产线的食品生产期间测量特定蛋白质(包括毒素)的浓度以及水检验,在水检验中,能够测量河流中或水处理期间的一种或多种分子(诸如蛋白质或盐)的浓度。进一步的考虑是,使用96孔板或其它形式的实验室检验,则每孔需要相对大量的样本。这是重要的考虑,例如还是在医学诊断检验中,样本的数量受到什么容易获得和/或对患者没有不适的限制,并且最佳的是根据微小的手指穿刺样本的血液或类似量的其它外周流体进行的诊断。因此,需要将这样的目标剂(特别是蛋白质)的量化实验室检验转变成小形状因数(smallform factor)集成和自动的形式。这已证明是困难的,特别是例如在需要同时测量多种蛋白质的情况下。目前,采取基于实验室的检验并将其转变为小型化形状因数或移动形式的过程是密集和耗时的过程,这是因为,以实验室为基础的检验转变为移动形式的当前方法具有增加了相当大的研发时间和/或降低蛋白质测量的灵敏度的步骤。这种情况的例子是:当前许多移动形式利用“复用”测量。在实验室检验中,经常是每个孔只能测量样本中的一种蛋白质,因此每个孔只能使用一组捕获抗体和检测抗体。然而,在“复用”形式中,捕获抗体放置在相同的腔室或通道中,同一样本同时在所有捕获抗体上运行,随后检测抗体的混合物自由流动。这种类型的系统的优点是:微流体设计的简单性和所用的样本量少(因为检查单个样本量以确定所有蛋白质的水平)。然而,由于抗体的非特异性和交叉反应性,可能存在严重的问题,并且这给实验室检验的转换过程增加了额外的复杂性和不确定性。对于确定要在相同样本中测定的每种额外蛋白质,由于可能存在与待测量的任何一种或多种抗体和其它蛋白质的非特异性结合和交叉反应性问题,化学的复杂性实质上增加。此外,与实验室检验相比,这种遍布所有捕获抗体的样本流动(随后所有检测抗体处处流动)不是很好地控制,因此其可以降低检测的灵敏度,其中,在所述实验室检验中,样本为特定量且抗体的量精确限定,并且,颜色变化的发展或用于检测的其它方法仅发生在孔中流体的静态体积上,所述体积也由放置在孔中的体积来很好地限定。本公开解决了这些问题中的至少一个。
应该理解,此处对“优选”的引用仅仅是示例性的。
发明内容
本文公开的微流阀组件克服了上述缺点中的一个或多个。特别地,它解决了分离检验流体与柔软基底(例如,PDMS基底)的接触的需要。
根据本公开的第一方案,提供了一种微流阀组件,包括:(i)刚性基底,其具有限定流体通道的至少两个相邻层,其中所述至少两个相邻层包括第一层和第二层;(ii)至少一个阀构件,其包括可拉伸膜,所述可拉伸膜定位成以所述可拉伸膜与所述流体通道基本分离的这种方式来密封所述流体通道,其中所述可拉伸膜固定至所述第一层,并且其中所述至少一个阀构件基于流体通道内存在的压力与从流体通道外侧的区域作用在所述膜上的压力或力之间的差而可操作。
在一些实施例中,阀构件的横截面积不同于流体通道的横截面积。在一些实施例中,可拉伸膜基本平行于每个相邻层。在一些实施例中,流体通道中存在的压力包括流体压力。在一些实施例中,检验流体构造为流过流体通道。在一些实施例中,所述至少一个阀构件的所述可拉伸膜构造成膨胀并接触层中的一个以关闭所述检验流体在所述流体通道中的流动。在一些实施例中,第二层的与所述阀构件相对的区段构造成朝向所述可拉伸膜突出并且接触所述可拉伸膜以在所述流体通道中限定柱构件,其中所述可拉伸膜构造成向流体通道外侧收缩以允许检验流体在流体通道中从柱构件上方流过。在一些实施例中,所述阀构件的所述可拉伸膜构造成稳定地定位在所述柱构件上方以关闭所述检验流体在所述流体通道中的流动。在又一些实施例中,所述柱构件不与所述可拉伸膜接触并且位于所述可拉伸膜下方,其中所述可拉伸膜构造成向所述流体通道外侧收缩以允许检验流体在流体通道中的流动,并且可拉伸膜构造成朝向柱构件的上表面膨胀以关闭检验流体在流体通道中的流动。在某些实施例中,所述第一层包括至少一个通孔,所述至少一个通孔构造成利于所述流体通道与定位在所述第一层上方的所述阀构件之间的连通,以利于所述检验流体基本在流体通道上方流动。在一些实施例中,阀构件的横截面积不同于流体通道的横截面积。在又一些实施例中,阀构件的可拉伸膜嵌入有磁珠,其中阀构件构造成通过磁力致动。在其它实施例中,阀构件构造成通过静电力或电磁力来致动。
根据本公开的第二方案,提供了一种微流阀组件。微流阀组件包括刚性基底,其具有多个层,所述多个层包括第一层、第二层和第三层。所述第一层和所述第二层限定控制通道。所述第二层和第三层限定流体通道。微流阀组件还包括至少一个阀构件,所述阀构件包括可拉伸膜,所述可拉伸膜定位成以所述可拉伸膜与所述流体通道基本分离的这种方式来密封所述流体通道。所述至少一个阀构件基于所述流体通道和控制通道中存在的压力差而可操作。
在一些实施例中,流体通道和控制通道中存在的压力包括流体压力。在一些实施例中,检验流体构造成流过流体通道,并且控制流体构造成流过控制通道。在某些实施例中,所述至少一个阀构件的所述可拉伸膜构造成当流体通道和控制通道之间的压力差为负时膨胀并接触所述第三层以关闭所述检验流体在所述流体通道中的流动。
在一些实施例中,所述第三层的与所述阀构件相对的区段构造成朝向所述可拉伸膜突出并且接触所述可拉伸膜以在所述流体通道中限定柱构件,其中所述可拉伸膜构造成当所述流体通道与所述控制通道之间的压力差为正时朝向所述控制通道收缩以允许所述检验流体在所述流体通道中从所述柱构件上方流过。在某些实施例中,所述阀构件的所述可拉伸膜构造成稳定地定位在所述柱构件上方,以在所述流体通道与控制通道之间的压力差为负时关闭所述检验流体在所述流体通道中的流动。
在一些实施例中,所述柱构件不与所述可拉伸膜接触并且定位在所述可拉伸膜下方,其中所述可拉伸膜构造成当所述流体通道与所述控制通道之间的压力差为正时朝向所述控制通道收缩以允许所述检验流体在所述流体通道中的流动,并且所述可拉伸膜构造成在所述流体通道与控制通道之间的压力差为负时朝向所述柱部件的上表面膨胀以关闭所述检验流体在所述流体通道中的流动。
在一些实施例中,所述第二层包括至少两个通孔,所述至少两个通孔构造成利于所述流体通道与定位在所述第二层上方(例如切入第二层的顶部或制作到第二层的上方的附加流体层中)的所述阀构件之间的连通,以利于所述检验流体基本在所述流体通道的上方流动,其中所述阀构件的横截面积不同于所述流体通道的横截面积。在一些实施例中,阀构件的横截面积不同于流体通道的横截面积。在一些实施例中,阀构件的可拉伸膜嵌入有磁珠,其中阀构件构造为经由磁力致动。在其它实施例中,阀构件构造成经由电磁动力致动。在某些实施例中,阀构件的横截面积不同于流体通道的横截面积。
根据本公开的第三方案,提供了一种用于输送流体的方法。该方法包括以下步骤:(i)提供具有多个层的刚性基底,所述多个层包括第一层、第二层和第三层,其中所述第一层和所述第二层限定控制通道,并且所述第二层和第三层限定流体通道;(ii)引起检验流体流过流体通道;(ii)引起控制流体流过控制通道;以及(iii)操作至少一个阀构件以允许或阻断检验流体流过所述流体通道,其中所述至少一个阀构件包括可拉伸膜,所述可拉伸膜定位成以所述可拉伸膜与所述流体通道基本分离的这种方式来密封所述控制通道,其中所述至少一个阀构件基于所述流体通道中存在的所述检验流体的压力与所述控制通道中的所述控制流体的压力的差而可操作。
合适地,刚性基底由例如聚甲基丙烯酸甲酯(PMMA)、环烯烃共聚物(COC)、环烯烃聚合物(COP)、其它硬聚合物、其它非聚合物材料(例如金属、玻璃、硅等)。合适地,可拉伸膜由PDMS、聚氨酯、聚酯、任何其它柔软或可拉伸或弹性聚合物、可伸展聚合物材料、柔软或可拉伸或弹性非聚合物中的一种或多种制成或由其组合制成。
根据本公开的第四方案,提供了用于检测和/或量化一种或多种目标剂的存在的系统,其包括:
微流控芯片,其包含用于每种目标剂的捕获剂和检测剂;
加载装置,构造为将所述捕获剂和检测剂加载到所述微流控芯片内的期望位置;
控制装置,其构造为控制每种剂在所述微流控芯片内的流动和混合;以及
感测(sensing)器件,其构造成检测和/或量化所述一个或多个目标剂的存在。
在一个实施例中,该系统包括包含控制器件和/或感测器件的装置。在一个实施例中,微流控芯片包括控制器件和/或感测器件。应当理解的是,当微流控芯片包括控制器件和/或感测器件时,该装置可以包括额外的控制和/或感测器件,尤其是,该装置可以额外包括用于激活微流控芯片上的感测器件和读取从感测器件获得的输出的控制器件。
在一个实施例中,控制器件构造为控制捕获剂、检测剂和目标剂以及检测和/或量化过程所需的任何额外试剂的流动和混合。在另一个实施例中,控制器件构造为激活和控制感测器件。
根据本公开的第五方案,提供了检测和/或量化一种或多种目标剂的存在的方法,其包括以下步骤:将用于每种目标剂的捕获剂和检测剂加载到微流控芯片内期望的位置;控制每种剂在所述微流控芯片内的流动和混合;以及通过感测捕获剂和检测剂与所述一种或多种目标剂之间的相互作用来检测和/或量化所述一种或多种目标剂的存在。
捕获剂和检测剂的非限制性实例可以在用于蛋白质测定的标准定义内找到,例如参见由Springer出版的ISBN为978-1-60327-237-7的John R.Crowther,ELISA Guidebook,第2版,分子生物方法(Methods in Molecular Biology),第516卷,其在此通过引用并入本文。
与传统的“复用(multiplex)”系统相对照,本发明的系统使用通道和孔(well)将样本分成子样本。然后控制流入特定腔室或通道并控制子样本与捕获剂和检测剂的混合,使得每个子样本用于测量仅一种目标剂的量或浓度水平,因此仅暴露于一组捕获剂和检测剂。
由于所使用的样本的量必须非常小以提高效用,并且与上述典型的“复用”系统相比,因为本公开潜在地需要更多的通道和/或腔室(用于子样本和每种蛋白质量化的单独的微流体子系统)来量化相同数量的目标剂,因此微流体子系统的体积必须非常小。此外,为了进行高度敏感的目标剂量化,本发明控制样本流体和任何其它流体(例如含有所需的酶、显影剂化学品或纳米颗粒或形成蛋白质检测和量化系统的一部分的任何其它试剂的流体)进入和离开反应区域,其中,在所述反应区域,要测量的目标剂暴露于捕获剂和检测剂,并且进行量化所需的任何进一步的反应和过程在所述反应区域发生。利用不同的方法主动控制流体流动并防止不必要的流出或进入反应区域。这些包括诸如磁珠、金属或其它材料的物理门,其使用静电、电磁或其它控制方法(例如流体流动的直接静电控制或某些类型的阀)来致动以阻断或打开通道。这意味着微流体子系统在设计上也可能是复杂的,以实现控制包括样本流体的各种流体的进入和离开的目的。此外,为了精确测量,应精确控制微流体子系统内保持的流体量。因此,不仅应当很好地确定该控制,也要很好地确定微流体子系统的尺寸。本文的公开内容构想使用已经开发用于微电子、MEMS和其它微系统制造的光刻沉积和其它微米和纳米制造技术。尤其是,这些技术应用于在这种光刻技术充分运用的硬基底(诸如硅作为芯片基底)上的通道的精确制造,或者替代地将光刻应用于硅并且将其用作模具,或者有时直接将这些技术直接应用于软聚合物基底(如果合适的话),或其它这种微米或纳米制造。应该理解,制造工艺和基底材料取决于微流体子系统的设计。这些方法已经开发用于非常精确和复杂的制造,从而实现了芯片设计、受控的尺寸的目标,同时保留了完全实现流体的复杂细分和控制所需的复杂设计。此外,该过程可用于在制造过程期间在传感器(sensor)需要直接暴露于流体时将某些传感器(例如电化学传感器或质量传感器)集成到芯片本身,从而芯片的感测元件和用于控制到感测元件的流体的微流体子系统的制造可以制造为单个工艺的一部分。重要的是,在这种微米和纳米制造中使用的方法本质上是“批量”工艺。也就是说,其利用光刻设计和工艺的方法,一旦设计和优化了子单元,就可以容易地重复相同的子单元。事实上,通常这样的方法在单个基底上同时产生大量的相同的子单元。这只是稍微困难一点,并且产生许多子单元的成本增加非常小。因此,尽管为了用一组捕获剂和检测剂测量一种目标剂或第一目标剂而设计和优化微流体子系统和/或任何芯片上感测系统的制造是复杂的工作,但是,随后,可以使用这种“批量”技术在芯片上的非常小的区域内进行100次或更多次的重复该子系统。子系统则只需要全部连接到初始流体入口和流体出口以完成大比例测量系统。这意味着在现有系统上测量大量目标剂的难度只是稍微困难一些,而且成本仅略高于测量一种蛋白质。因此,与复杂性大大增加以适应样本中大片目标剂的测量-需要量化的蛋白质数量越多,过程越长,适应复用系统的成本也越高,从而可以在捕获剂和检测剂之间没有问题(交叉反应性、取代等)和/或灵敏度低的情况下实现这点-的“复用”系统相比,本文公开的微流控芯片可以快速且容易地生产,以高准确度同时测量和量化许多目标剂,这是因为捕获剂和检测剂不需要从实验室系统中使用的捕获剂和检测剂改变或取代,并且具有大量用于测量非常大量目标剂的微流体子系统的芯片可以容易且标准地生产。
在一个实施例中,本文公开的系统提供了转换如下的标准方法的优点:所述标准方法用于使设计用于测量多种蛋白质的实验室系统改变为自动化工作台或台式和/或手持式移动设计以测量多种蛋白质。这意味着,例如,它适合于在即时医疗诊断面板中测量多种蛋白质生物标志物,因此面板的精确度将与远程实验室检验相同。如果这样的面板是在实验室系统上设计的,则其可以容易地转移到本公开的系统上,同时容易地保持相同的蛋白质测量准确性。将诊断检验转移到当前公开的即时医疗测量系统的过程可以是几周或几天的过程,而不是当前转移到“复用”或当前可用的其它当前诊断系统所需要的多个月。此外,由于测量的目标剂的数量可以容易地增加并且边际成本增加-成本的唯一线性增加是针对试剂,特别是抗体,然而即使抗体的量也可能小于实验室系统,这是因为使用较小量的样本流体,因此使用较小量的试剂。增加在相同芯片上测量的诊断面板的数量变得容易,例如,可以使用单个芯片来测量多种疾病。这将增加实用性并且也潜在地降低用于医学诊断测量的成本,这是因为测量目前公开的系统上的额外目标剂的成本增加很小。在需要量化某些目标剂的食品安全测量和其它诊断方面,能够实现类似的效果。
然而,本文描述的系统的进一步复杂性是将样本蛋白质检测所需的必需试剂(通常但不总是或不仅仅是合适的一组捕获剂和检测剂)加载到芯片上。特别地,尽管以前的系统已经认识到需要将捕获剂加载到芯片上,但是本系统认识到要求将捕获剂和检测剂和/或目标剂量化所需的可能的其它试剂加载到芯片上的可以根据时间主动控制其释放以及彼此的混合的特定位置。因此,除了上述设计有适当通道和腔室的芯片之外,还需要加载设备,以通过如下方式来自动化芯片的制造:将一组或多组捕获剂和检测剂和/或其它必需的试剂加载到至少一个微流控芯片上的可以完全和主动地控制它们的混合和反应的时间和过程的特定位置。事实上,装置通常设计成将所有抗体和其它试剂快速顺序地或平行地加载到至少一个微流控芯片上。此外,加载装置通常还被优化用于将这些试剂高速顺序地或并行地加载到多个芯片上,以使加载机能够大量生产微流控芯片。
优选地,加载装置构造成将一种或多种剂提供到一个或多个孔中。加载装置可以构造用于仅一种类型的剂,例如,加载装置可以构造用于捕获剂,或者加载装置可以构造用于检测剂。本发明的实施例设想了一种系统,该系统包括系统中存在的一种或两种类型的加载装置构造。可以领会的是,加载装置可以构造成将一种或多种试剂提供到除捕获孔和/或检测孔之外的孔或位置,即微流控芯片上的第三类型的孔。在优选实施例中,单个加载装置构造成向捕获孔和检测孔两者提供一种或多种剂。在优选的实施例中,一种或多种试剂选自捕获剂和检测剂及其组合。所述系统和方法进一步包括至少一个加载装置,所述加载装置构造为将每种捕获剂提供到微流控芯片内的这种捕获剂的正确位置,并且将每种检测剂提供到微流控芯片内的这种检测剂的正确位置。
根据第六方案,本公开是一种装置,微流控芯片放置在所述装置中,并且所述装置执行芯片上的感测元件的分析、控制和/或本身包含合适的感测元件。例如,在使用谐振式质量传感器的情况下,所述装置以电子方式激活传感器的谐振并且记录任何这种变化,从而指示绑定事件。在光被传输到样本、试剂或这些的组合的情况下,例如为了记录颜色变化,所述装置使用如下方法产生光并控制光的曝光,使得在特定时间只有微流控芯片的恰当部分暴露:例如使用诸如液晶显示切换或类似的方法,其允许仅对期望像素的光传输的主动控制。在这种情况下,该装置还可以读取输出信号,该输出信号例如可以是电的或者可以是改进的光信号。它可能包含多个感应区域,例如多个光传感器,但是也可以仅包含一个感测区域,这是因为曝光的主动控制意味着在在单个时间段期间,对于曝光信号的改进的输出必须仅到达曝光区域。所述装置产生用于主动控制每个微流控芯片上的流体的电磁场或静电场和/或其它力,并自动控制芯片上的抗体和/或试剂的混合,从而使得这是受控制的,并且除了反应发生在较小的范围内并且一切都通过自动控制完成而不是由实验室技术人员的手动工作完成之外,通常以与实验室检验中的步骤顺序完全相似的方式发生。最后,所述装置具有合适的计算能力、软件、存储器等,以实现必要的控制处理和结果输出数据的记录以及数据的处理和存储,并运行作为非专家用户和设备之间的所需的接口的软件。它还具有必要的光学、有线和/或无线连通性来传输数据和接收命令,并向其它装置以及人类用户执行所有其它必要且有用的通信。
因此,本公开是用于将基于实验室的蛋白质分析检验自动转换成小形状因数(台式、手持式)自动化和一体化蛋白质检测和/或浓度量化检验的完整链,其中基于实验室的蛋白质分析检验只能由经过培训的人员在适当配备的实验室中进行,其中小形状因数(台式、手持式)自动化和一体化蛋白质检测和/或浓度量化检验可以在很多不同的地点由进行最少的培训或不进行培训的人员可能在任何地方进行,从而显著提高许多诊断检验的效用。本公开还使得能够在相同的样本上进行许多更多的检验。
在没有为单独测量每种目标剂而专门设计的具有分离的重复区段的芯片的情况下,样本中存在的目标剂越多,测量目标剂将变得越复杂。该装置控制经过芯片的流体的移动和/或在芯片上需要的每个点的每个目标剂的测量,并且执行所得数据的任何处理和传输。需要特殊的加载机,以便使用者可以简单地将他们的含有每种捕获剂或检测剂的流体放入加载机中,并且这些将被印刷在芯片上精确要求的点上。因此,用户需要做的所有就是准备单独的流体,每种流体含有不同的捕获剂或检测剂,从而他们将立即能够生产准备投放市场的工作台或手持产品。
在前述任一个方案中,将另外的捕获剂、检测剂或其它剂接收到微流控芯片的一个或多个位置或孔中。优选地,这些位置或孔是本文所述的孔或位置,或者可以是存在于微流控芯片上的另外的位置或孔。
另外的目的、优点和新颖的特征将在下面的详细描述中部分地阐述,并且对于本领域技术人员而言,这些在查阅以下详细描述和附图后将变得显而易见,或者可以通过示例实施例的生产或操作。概念的目的和优点可以通过所附权利要求中特别指出的方法、手段和组合来实现和获得。
附图说明
现在将参照附图以举例的方式描述本公开的实施例,在附图中:
图1A示出了根据一个实施例的微流阀组件的正视剖视图。
图1B示出了图1A中所示的微流阀组件的正视剖视图,并进一步显示可拉伸膜的膨胀以关闭检验流体的流动。
图2A示出了根据另一个实施例的微流阀组件的正视剖视图。
图2B示出了图2A中所示的微流阀组件的正视剖视图,并进一步显示可拉伸膜的膨胀以关闭检验流体的流动。
图3A示出了根据另一个实施例的微流阀组件的正视剖视图,并进一步示出了可拉伸膜的收缩以允许检验流体流动。
图3B示出了图3A中所示的微流控阀组件的正视剖视图,并进一步显示了可拉伸膜的正常的平坦取向。
图4A示出了根据又一个实施例的微流阀组件的正视剖视图,并进一步示出了高度减小的柱构件。
图4B示出了图4A中所示的微流阀组件的正视剖视图,并进一步显示可拉伸膜的膨胀以关闭流体通道。
图5示出了微流控阀组件的另一个实施例的俯视透视图的剖视图。
图6示出了包含“N”个量化系统的微流控芯片的示意图,每个量化系统包括用于每种目标剂的捕获剂和检测剂。比例(仅估计)为约2厘米(cm)∶约1毫米(mm)。
图7与图6所示的类似,显示了包含“N”个量化系统的微流控芯片的示意图,但有额外的微流体孔。比例(仅估计)约2厘米∶约1毫米。
图8详细显示了一个可能的量化系统。比例(仅估计)为约4厘米:约100微米(μm)。
图9与图8所示的类似,详细示出了一个可能的量化系统,但有额外的阻断通道和阻断剂(blocking agent)。比例(仅估计)为约4厘米∶约100微米。
图10示出了适于控制芯片内流体的流动和混合并且适于控制感应件的加载装置。比例(仅估计)为约2.5厘米∶约1毫米。
图11示出了有线连接到用于装置操作控制的智能基础设施的加载装置。对于元件600,比例(仅估计)为约1厘米∶约1毫米。对于元件605,比例为约1.5厘米∶约1厘米。
图12示出了配置为将一组或多组捕获和检测剂和/或其它必需的试剂加载到微流控芯片内的期望位置上的加载机。比例(仅估计)为约1厘米∶约1毫米。
具体实施方式
除非另外限定,否则本文使用的所有技术和科学术语具有与本公开所属领域的普通技术人员通常理解的相同的含义。尽管在本公开的实践或检验中可以使用与本文所述相似或等同的任何方法和材料,但是描述了优选的方法和材料。为了本公开的目的,下列术语定义如下。
在此使用冠词“一个(a)”和“一个(an)”以指代文中的语法对象的一个或多于一个(即,至少一个)。举例来说,“一个元件”是指一个元件或多于一个元件。如本文所使用的,除非另有特别说明,否则单数的使用包括复数(反之亦然)。
“约”是指量、水平、值、数目、频率、百分比、尺寸、大小、量、重量或长度相对于基准的量、水平、值、数目、频率、百分比、尺寸、大小、量、重量或长度有15%、14%、13%、12%、11%、10%、9%、8%、7%、6%、5%、4%、3%、2%或1%的变化。
在整个说明书中,除非上下文另有要求,否则词语“包括(comprise)”、“包括(comprises)”和“包括(comprising)”将被理解为暗示包括讲述的步骤或元件或者步骤组或元件组,但不排除任何其它步骤或元件或步骤组或元件组。因此,“包括”等术语的使用表示所列出的元件是必需的或强制性的,但是其它元件是可选的并且可以存在也可以不存在。“由...组成”是指包括并限于在短语“由...组成”之后的任何事物。因此,短语“由...组成”表示列出的元件是必需的或强制的,并且不存在其它元件。“基本上由...组成”是指包括在该短语之后列出的任何元件,并且限于不干扰或有助于对于所列举的元件在本公开中指定的动作或行为的其它元件。因此,短语“基本上由...组成”表示列出的元件是必需的或强制性的,但是其它元件是可选的并且可以存在也可以不存在,这取决于它们是否影响所列元件的动作或行为。
以下详细描述包括对形成详细描述的一部分的附图的参考。附图示出了根据示例实施例的图示。这些在本文中也称为“示例”的示例实施例被足够详细地描述以使得本领域技术人员能够实践本主题。
可以组合实施例,可以使用其它实施例,或者可以在不脱离所要求保护的范围的情况下进行结构的、逻辑的和操作上的改变。因此,以下详细描述不应视为具有限制意义,而其范围由所附权利要求及它们的等同方案限定。
微流阀组件
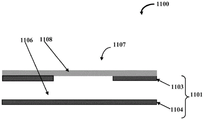
本文描述了一种微流体装置,其包括用于选择性地控制微流体装置内的流体的流动的阀。图1A示例性地示出了根据一个实施例的微流阀组件1100的正视剖视图。微流阀组件1100包括刚性基底1101和至少一个阀构件1107。刚性基底1101包括至少1103和1104两层。这些层1103、1104限定用于输送检验流体的流体通道1106。阀构件1107包括可拉伸膜1108,可拉伸膜1108定位在(并且可选地固定至)层1103上方,从而使得可拉伸膜1108与流体通道1106基本分离。具体地,如图1A所示,层1103可以具有为由可拉伸膜1108覆盖的任何适当形式的通孔(through-hole)或开口,使得在层1103的内表面与可拉伸膜1108的表面之间存在预定距离。
刚性基底1101由例如聚甲基丙烯酸甲酯(PMMA)、环烯烃共聚物(COC)、环烯烃聚合物(COP)、其它硬聚合物、其它非聚合物材料如金属、玻璃、硅等等中的一种或其组合制成。可拉伸膜1108由PDMS、聚氨酯、聚酯、任何其它柔软或可拉伸或弹性聚合物、可伸展聚合物材料、柔软或可拉伸或弹性的非聚合物中的一种或多种制成或由它们的组合制成。
基于朝向可拉伸膜1108施加力,阀构件1107可操作。由于流体通道1106和可拉伸膜1108后面的区域存在流体压力差,因此可以产生力。在其它实施例中,力可以由致动器、马达、压电装置、微机电(MEMS)装置等产生。图1B示例性地示出了微流阀组件1100的正视剖视图,示出了在将外力施加到可拉伸膜1108上时可拉伸膜1108膨胀以关闭流体通道1106。外力在图中用箭头表示。
在替代实施例中,除了与所述阀构件相对的层的区段构造成朝向所述可拉伸膜突出并且接触所述可拉伸膜以在流体通道中限定柱构件之外,结构与图1中所示的相同。当流体通道与膜的外表面之间的压力差为负时,可拉伸膜向控制通道收缩以允许检验流体在流体通道中从柱构件上方流过。如本文所限定的“柱”可以是任何形状或形状的组合,或者由彼此分离的多个结构组成。在这种结构中,PDMS膜通常是平坦的且抵靠位于气动通道或控制通道下方的流体通道中的柱构件。当控制通道中的压力低时,检验流体的压力高于控制流体的压力,因此检验流体的压力推动PDMS膜使PDMS膜变形以打开,从而使得检验流体可以从柱构件上方流过并继续进入出口通道。在实施例中,阀构件的可拉伸膜稳定地定位在柱构件上方,以在当膜的与流体通道相对的侧上的压力大于流体通道中的压力时关闭流体通道中的检验流体的流动。换句话说,在膜的外侧(与面向流体通道侧相对的一侧)施加更多的压力允许PDMS膜定位成平坦取向,从而将PDMS膜压靠柱构件并阻断检验流体的流动。这是一个“常闭”阀结构。
在替代实施例中,除了有柱结构之外,结构与图1A中所示的相同。然而,在该实施例中,柱构件不与可拉伸膜接触并且位于可拉伸膜下方。当流体通道和膜的外表面上的压力(外部,在膜的与面向于朝向流体通道的流体侧的相对侧)之间的压力差为正时,可拉伸膜收缩膨胀远离流体层的底部以允许检验流体在流体通道中流动,并且可拉伸膜构造成当流体通道和膜的外表面之间的压力差为负时朝柱构件的上表面膨胀,以关闭检验流体在流体通道中的流动。
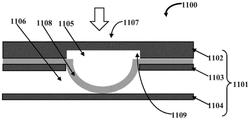
图2A示例性地示出了根据另一个实施例的微流阀组件1100的正视剖视图。如图所示,微流阀组件1100包括刚性基底1101和至少一个阀构件1107。刚性基底1101具有多个层,例如第一层1102,第二层1103和第三层1104。第一层1102和第二层1103限定控制通道1105,第二层1103和第三层1104限定流体通道1106。阀构件1107包括可拉伸膜1108,该可拉伸膜1108定位成以所述可拉伸膜110与所述流体通道基本分离的这种方式来密封控制通道1105,使得可拉伸膜1108与流体通道1106基本分离。刚性基底1101由例如聚甲基丙烯酸甲酯(PMMA)、环烯烃共聚物(COC)、环烯烃聚合物(COP)、其它硬聚合物、其它非聚合物材料如金属、玻璃、硅等等中的一种或其组合制成。可拉伸膜1108由PDMS、聚氨酯、聚酯、聚乙烯(PE)、任何其它柔软或可拉伸聚合物、可伸展聚合物材料中的一种或多种制成或由它们的组合制成。可拉伸膜1108可以是适合可拉伸的非聚合物材料。
阀构件1107基于流体通道1106与控制通道1105之间的压力(例如,流体压力)差可操作。在实施例中,检验流体构造为流过流体通道1106,并且控制流体构造为流过控制通道1105。这里使用的术语“检验流体”是指为实验室检验而提取的任何流体样本,诸如例如血液的生物流体样本,并且可以包括流动固体,例如但不限于如沙状颗粒的流动固体。在优选实施例中,流体样本是生物流体样本,更优选为血液。允许血液样本流过流体通道1106以检验不同通道区域中的特定量的血液。这里使用的术语“控制流体”是指构造为对阀构件1107的可拉伸膜1108施加压力以例如气动地或液压地致动阀构件1107的任何流体或液体,例如空气、气体、油、诸如沙子的流动固体。
图2B示例性地示出了微流阀组件1100的正视剖视图,示出了可拉伸膜1108膨胀以关闭流体通道1106并因此阻断检验流体的流动。在示例中,一个或多个通孔1109被制作在第一层1102和第二层1103中以限定用于阀构件1107的区段或阀点。在实施例中,如图2B中的箭头所示,当流体通道1106和控制通道1105之间的压力差为负时,阀构件1107的可拉伸膜1108膨胀并接触第三层1104,以关闭检验流体在流体通道1106中的流动,所述检验流体为例如用于分析的血液或用于某些化学反应的试剂。这种布置也是有利的,因为阀构件1107可以容易地具有不同的横截面并且因此更易于密封。
换句话说,如图2B的箭头所示,如果控制流体的被施加压力高于检验流体的压力,阀构件1107的可拉伸膜1108膨胀以关闭流体通道1106。在结构中,平坦的PDMS层结合至或简单地保持在顶部PMMA层的顶部的适当位置。气动层或控制通道1105限定在PDMS的顶部上。多个通道切割成第一和第二PMMA层。当气动压力施加到PDMS层时,PDMS层变形以延伸入流体通道1106中以阻断检验流体的流动。这种结构是“常开”阀结构。
根据本公开的各种实施例,作为通过模制或其它技术重塑PDMS以形成微流体结构的流体通道1106和控制通道1105以及其它特征部(例如,微流体特征部、通道、孔等)的替代,PDMS基底被制作在诸如PMMA、COC或COP的硬聚合物基底中。根据本公开的实施例,刚性基底1101具有某些区段,在这些区段处,可拉伸膜1108或PDMS例如经由PMMA的中间层中的通孔(through hole)接近检验流体,其中,PDMS膜位于所述中间层上方。这种设计使得当气动压力施加到PDMS上时,可拉伸膜1108通过所述孔(hole)延伸到下方通道中阻断检验流体在下方通道中的流动。
因此,在本实施例中,组件包括至少一个检验流体通道1106以及一个可拉伸膜1108。可拉伸膜1108可以具有或不具有设计在其中的特征部。组件的设计使得可拉伸膜1108仅在某些点(例如,阀点)处与流体通道1106中的检验流体接触。此外,当气动地或液压地或者通过诸如机械力或电磁力的其它方法增大或减小可拉伸膜1108上的压力时,可拉伸膜1108变形使得该变形关闭或打开流体通道1106。因此,整个组件用作常开或常闭的阀构件1107。压力的变化可以施加在整个组件上,同时在多个“阀点”处使可拉伸膜1108变形,并使得在流体网络中多个位置同时增加或限制检验流体流的流动。
在示例性实施例中,阀构件1107通过柔性膜或可拉伸膜1108的变形来操作,该柔性膜或可拉伸膜1108仅在某些指定点处与流体网络中的检验流体接触,使得对可拉伸膜1108施加的压力引起可拉伸膜1108扭曲到网络中的流体通道1106或其它结构中,从而阻断或限制检验流体在网络中的指定点处的路径。可替代地,可拉伸膜1108扭曲,使得检验流体的路径打开,使流体流动增加。
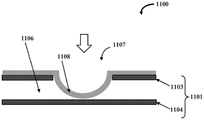
图3A示例性地示出了微流阀组件1100的实施例的正视剖视图,示出了可拉伸膜1108的收缩以允许检验流体的流动,并且图3B示例性地示出了图3A中的微流阀组件1100的另一个正视剖视图,示出了可拉伸膜1108的正常的平坦取向。在实施例中,第三层1104的与阀构件1107相对的区段构造成朝向可拉伸膜1108突出并接触可拉伸膜1108,以在流体通道1106中限定柱构件1110。当流体通道1106与控制通道1105之间的压力差为正时,可拉伸膜1108向控制通道1105收缩以允许检验流体在流体通道1106中流过柱构件1110上方。如本文所限定的“柱”可以是任何形状或形状的组合,或者由彼此分离的多个结构组成。优选地,柱排布是从底表面突出的任何形状的一个或多个结构的组合。
在构造中,PDMS膜通常是平的且抵靠位于气动通道或控制通道1105下方的流体通道1106中的柱构件1110。当控制通道1105中的压力低时,检验流体的压力高于控制流体的压力,因此检验流体的压力推动PDMS膜使PDMS膜变形以打开,从而使检验流体可以流过柱构件1110上方并继续进入出口通道。在实施例中,阀构件1107的可拉伸膜1108稳定地定位在柱构件1110上方,以当流体通道1106与控制通道1105之间的压力差为负时关闭检验流体在流体通道1106中的流动。换句话说,在控制通道1105中施加更多的压力允许PDMS膜定位成平坦取向,使PDMS膜压靠柱构件1110并且阻断检验流体的流动。这是“常闭”阀结构。
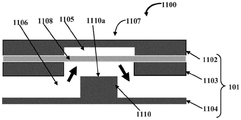
图4A示例性地示出了微流阀组件1100的另一个实施例的正视剖视图,示出了具有降低的高度的柱构件1110,图4B示例性地示出了图4B中的微流阀组件1100的另一个正视剖视图,示出了可拉伸膜1108膨胀以关闭流体通道1106。在实施例中,柱构件110不与可拉伸膜1108接触并且位于可拉伸膜1108下方。当流体通道1106与控制通道1105之间的压力差为正时,可拉伸膜1108向控制通道1105收缩以允许检验流体在流体通道1106中流动,并且可拉伸膜1108构造为当流体通道1106与控制通道1105之间的压力差为负时朝向柱构件1110的上表面1110a膨胀以关闭检验流体在流体通道1106中的流动。
在构造中,该实施例结合了图1A-1B、图2A-2B以及图3A-3B所示的实施例的方案,使得阀构件1107包括不接触可拉伸膜1108的柱构件1110。因此,当控制通道1105中的压力低时,阀构件1107更加灵活地打开,并且检验流体能够流动。当控制通道1105中的压力增加时,阀构件1107关闭。在示例中,当控制通道1105中的压力比如图2A-2B所示的“常闭”阀结构的情况下低时,检验流体可以灵活地流动。然而,由于可拉伸膜1108与柱构件1110的上表面之间的间隔小于流体通道1106的平常深度,所以当对控制通道1105施加压力时更容易抵靠柱构件1110密封可拉伸膜1108,从而比图2A-2B所示的“常开”结构更容易关闭该阀件1107。
在实施例中,除了在阀构件1107之外,在结构的大部分处维持更深的通道深度,使得当检验流体的路径的横截面越大时,检验流体的流动阻力越小并且组件中的背压越小,因此更容易产生或控制组件中的流体流动。在示例中,也可以通过增加流体通道1106的宽度来产生更大的横截面,但是这占据了芯片上的x-y方向上的空间,这意味着由于芯片上可能有非常长的通道的网络,在相同的流体背压下芯片需要大得多。在示例性实施例中,控制通道和流体通道中的每一个具有约50μm至约1mm的宽度和约5μm至200μm的深度(包括端点),但不限于此。在其它示例性实施例中,控制通道和流体通道的尺寸可以是纳米级或微米级,但不限于此。
图5示例性地示出了显示微流阀组件1100的另一个实施例的俯视透视图的剖视图。在该实施例中,第二层1103包括至少两个通孔1111a和1111b,通孔1111a和1111b构造成利于流体通道1106和定位在第二层1103上方的阀构件1107之间的连通,并且进一步利于检验流体基本在流体通道1106上方流过。此外,阀构件1107的横截面积不同于流体通道1106的横截面积。通孔1111a穿过第二层1103,从而允许检验流体通过通孔1111a输送到定位在第二层1103上方的PDMS阀构件1107。当阀构件1107上的外部压力小于检验流体的压力,检验流体流过柱构件1110上方并且通过通孔1111b流回流体通道1106。
在构造中,图5的实施例遵循图1A、图1B、图2A、图2B、图3A、图3B、图4A和图4B的实施例的原理。如在图5中示例性地示出的,在该实施例中,中间的PMMA层具有通孔1111a,检验流体通过通孔1111a从下方的流体通道1106被输送到制作在中间PMMA层的顶侧的阀构件1107,然后,检验流体通过另一个通孔1111b被输送回主流体通道1106。阀构件1107的深度比主流体通道1106浅,并且在该实施例中,在阀构件1107的中间也有柱构件1110。PDMS层直接放置在中间PMMA层的上方和并且抵靠中间PMMA层。从上方向PDMS层施加的增大的压力引起阻断阀构件1107或“阀通道”的向下变形。在实施例中,阀构件1107的可拉伸膜1108嵌入有磁珠,使得阀构件1107构造成经由磁力致动。在其它实施例中,阀构件构造成通过静电力或电磁力来致动。
在实施例中,根据图4A-图4B和图5,阀构件1107的结构设计成使得控制通道1105在阀构件1107处的深度与主流体通道1106中的检验流体的通常深度无关,这是因为当控制通道1105在阀构件1107处的深度大的情况下难以有效地密封这些类型的隔膜阀。然而,如果流体通道1106的深度在整个流体网络中总体很浅,则对于给定的通道宽度,流体通道1106的横截面将较小。这意味着对检验流体的流动的阻抗更大,背压更大,因此需要更多的压力来允许检验流体流过流体网络。因此,需要对流体网络进行有效的密封以使检验流体不泄漏,而这在芯片上的检验流体的流动的较高压力和高速下更难。因此,微流阀组件1100设计成使得控制通道1105在阀构件1107处的深度独立于总体流体通道1106的深度,从而阀构件1107可以更容易地关闭,同时保持流体网络中较低的流体压力。因此,检验流体在阀点处的流动通过具有与流体网络的其余部分相比独立的且具有不同的深度的路径或层。
在另一个实施例中,将PDMS倒入硬质聚合物的空腔中并使其固化。在另一个实施例中,包括多层PMMA层或刚性层和PDMS层或气动层,以实现更复杂的流体路径和控制。在实施例中,微流阀组件1100可应用于微流控芯片和其它结构用于诊断应用和其它应用。此外,阀构件1107实现为宏观和纳米应用。
微流体感测平台
本文所述的技术还涉及用于检测和/或量化一种或多种目标剂的存在的系统和方法。特别地,但不排他地,本公开的实用性的一个实例是用于多蛋白质生物标志物疾病检验,其可以使用从基于手动实验室的蛋白质测定的标准过程转换为可以用于在护理点检验患者的桌式、台式或手持式一体化自动化测定。现在将描述本公开的一些实施例,以便提供对本公开的更详细的理解,并且示出如何将其应用于基于实验室的目标剂量化检验转换为集成的桌式或台式形式。
在一个定义中,集成系统是一个方便的,可能是模块化的包,包括精确操作所需的所有元件。在一个定义中,自动化系统是包含多个操作上相互依赖的部件(其可以通过显著的物理距离分开)的系统,其需要与操作者的最小的相互作用或不相互作用,以便对检验样本进行最佳分析。
图6体现了微流控芯片100的简单和总体的表示。在该实施例中,微流控芯片100具有在毫米范围内的总横向尺寸。这对手持式检验特别有用。在一些其它实施例中,微流控芯片100可以具有不同于毫米范围的横向尺寸,例如在厘米范围内。所示的微流控芯片100可以由多种材料和/或多种材料的组合以多种方式构造。例如,微流控芯片100可以由固体材料构造,包括半导体、陶瓷、金属和聚合物。它可以通过消减方法构造,从一块材料开始,并使用湿式或干式化学或机械方法来去除材料以在材料内形成通道、孔(well)和其它结构。还可以使用添加方法来构造,其中,通过在基底109上使用粘合、蒸发、溅射、化学气相沉积(CVD)或其它类型的沉积,将一个或几个材料的一个或几个层添加到该基底,以形成微流控芯片100结构。可替选地,可以使用如下成形方法来构造:芯片材料弯曲或模制或以其它方式改变形状的方法。物理力或加热/冷却或其它力可用来实现此构造。一些具有随时间和/或当混合/暴露于另一种材料时改变其物理结构的特性的材料也可以用于实现此构造。该方法的一个例子是环氧树脂,其与一些环氧硬化剂混合时会固化。可以使用模具,并且也可以将材料转变成液体状态,然后允许冷却以实现这个模制过程。然后可以以多种方式将模具与微流控芯片100物理分离。一些方式将保持模具和微流控芯片100的形状。一个例子就是“剥离法”。一些其它方式会保持微流控芯片100的形状,但不保持模具的形状。一个例子就是通过将模具浸入化学溶液中来溶解模具。第一种方法通常是优选的,因为它允许多次使用模具来制造许多芯片,从而降低制造成本。也可以使用这些方法和其它方法的组合来构造微流控芯片100。用于构造图6所示的微流控芯片100的常用方法的一些示例包括:(1)在硅或其它半导体(或替代材料)硬质基底上光刻,其中,一些聚合物通过旋转或其它方法被添加到材料上,随后通过特别设计的掩膜暴露于已知强度和波长的光或其它辐射。然后,除去暴露的聚合物(或者可替选地除去未暴露的聚合物),并且然后使用溅射或蒸发或其它添加剂方法将材料沉积到基底上,或者使用蚀刻方法去除没有聚合物的基底材料。随后移除剩余的聚合物,仅留下没有聚合物的额外部分(或移除的材料)。可以使用连续的光刻和加/减步骤来构造微流控芯片100结构。(2)在微流控芯片100基底是聚合物的情况下,将其加热以使聚合物柔软,然后压入由硬质材料构造的模具中并使其冷却,从而使聚合物凝固成所需的芯片设计。然后移除模具。(3)微流控芯片100基底可以由随时间和/或当暴露于不同材料和/或温度变化时改变其物理结构的材料制成。该材料最初可以是流体形式,然后倒入由硬或柔软或柔性材料构成的模具中,并通过将流体暴露于不同的材料和/或温度变化而使其固化。然后移除模具。如果需要,用于构造微流控芯片100的材料可以以流体形式与液体和粉末形式的任何其它材料混合,以改变所得到的芯片材料的物理特性。(4)微流控芯片100的基底可以通过其它机械和光学方法直接成形,例如通过激光-微机械加工,由此将高强度激光引导到由聚合物、金属、玻璃、硅、陶瓷、复合材料或其它材料制成的基底中;能够以极高的分辨率将基底加工成所需的形状。这种或类似的方法也可以加工用于(2)和(3)的合适的模具。
许多上述微流控芯片100的构造方法是分批构造方法,因此可以在微流控芯片100上重复相同或相似的图案,并且所有这样的结构可以通过允许构造一组芯片结构时采用的相同(或几乎相同)的数量的步骤来制造。这允许微流控芯片100制造成包含用于量化多个目标剂的复杂结构,并且这样的微流控芯片100的生产与用于生产含有仅用于量化一种目标剂的一组结构的微流控芯片100的生产具有类似的复杂性。
微流控芯片100的其它实施例可以具有与微流控芯片100不同的芯片形状和部件布局,并且与该特定实施例完全或类似地起作用。在该特定实施例中,微流控芯片100上有磁性点101,以帮助其在放入装置中时正确对准,以便在装置内具有适当的微流控芯片功能。然而,微流控芯片100的其它实施例可以在不影响功能性的情况下替代地包含夹子、槽或其它机械对准方法或静电或电磁对准方法或先前在标准装置中详述的其它形式的对准机构,并且所有这些都是本公开的实施例。
包括各种通道和孔的微流控芯片100的不同结构也可以用各种材料涂覆。在构造微流控芯片100期间,可以通过蒸发或溅射或其它添加方法进行涂覆。可替选地,可以使一种或多种流体通过通道或孔以沉积涂层。涂层可以执行不同的功能,例如它可以是疏水的或带电的,以防止穿过或邻近各种芯片结构的流体中的目标剂、灰尘或其它结构粘附到这些芯片结构的各个表面上。可替选地,微流控芯片100结构的表面可以是亲水的,从而使得一些目标剂附着在其上。不同的芯片结构或结构的一部分可以构造或涂覆以便具有疏水性、亲水性、带电性或具有芯片功能所需的其它特性。
微流控芯片100具有各种通道,所述通道用于传输含有至少一种目标剂和任何试剂的流体以及为了本公开而需要添加的其它流体,以实现其量化至少一种目标剂的功能。包含至少一种目标剂的一种或多种流体可以作为连续的流动来输送,或者可以作为载液内的微液滴输送,或者可以有任何其它的输送流体通过芯片的方法;“微流体”的含意是在芯片上输送流体的结构的尺寸通常小于1mm,但这种指定并非指的是流体输送的任何特定方法。102显示了输入通道。输入通道102可以具有各种形状,并且这个实施例中所示的尺寸在微米范围内,但是在其它实施例中,这些尺寸可以在纳米范围内或者更大或者更小,以与芯片格式和尺寸连续。此外,输入通道102相对于芯片的方向和路径也可以是不影响功能的许多其它形貌。输入通道102是包含至少一个待量化目标剂的至少一种流体的入口点。流体的一个示例可以是正在针对一种或多种目标剂进行检验以确定清洁度的来自储器的水。或者,例如,其可以是针对各种目标剂例如蛋白质生物标志物进行检验的从患者的血液提取的血清。流体可以通过各种方法进入输入通道102,例如,供给输入通道102的孔,其中,流体可以从连接到输入通道102的前部的注射器或“针刺”装置放入输入通道102中,注射器或“针刺”装置穿透病人的皮肤直接抽血。在这种情况下,血液直接进入输入通道或过滤或以其它方式处理,使得提取的全血的血清、血浆或其它成分进入输入通道。注意,不一定要求量化进入输入通道102的流体的量。
103显示输出通道。输出通道103可以具有各种形状,并且如在该实施例中所示的尺寸在微米范围内,但是在其它实施例中,这些可以更大或者更小,以与芯片格式和尺寸连续。
此外,输出通道103相对于芯片的方向和路径也可以是不影响功能的许多其它形貌。输出通道103可以以例如疏水涂层的方式构造或涂覆,以便使流体从输出通道103中洗提出来,可选地,在需要操作时,可以使用诸如静电力或充电或机械力的一些场或力引起流体主动地洗提。在需要时,也可以使用类似方法和输出通道103的物理阻断防止流体从输出通道103中洗提。
104显示捕获孔。微流控芯片100包含至少一个捕获孔104,其可以体现为各种尺寸和形貌。其结构是一个小腔室的结构。除了任何其它涂层之外,该特定结构还包含至少一种捕获剂,其在捕获孔104的构造期间放置在捕获孔104中。可以通过包括滴涂的手工方法将捕获剂放入捕获孔104中。或者,可以使用如下方法将其涂覆到捕获孔104的表面上:将末端浸入流体中或者使流体流到末端上,然后将末端施加到表面上,或者可以使用喷墨印刷方法或类似于喷墨方法的方法将其印刷到表面上,或者将捕获剂喷涂到表面上的其他方法,或者捕获剂可以以本领域中描述的许多其它公知方式施加。其可以以固体形式或以流体或气雾剂形式施用。在后一种情况下,它可能变干燥以在捕获孔104中形成斑点或层。
在该实施例中,捕获孔104仅从一个输入通道102进料。在其它可能的实施例中,捕获孔104可以从两个或更多个输入通道102供给。每个输入通道102是至少一种流体的入口点。在一个实施例中,可以仅通过一个输入通道102将几种流体输入到捕获孔104中。在另一个实施例中,可以通过两个或更多个输入通道102将几种流体输入到捕获孔104中。在另一个实施例中,可以仅通过一个输入通道102将几种流体输入到捕获孔104中。
在该实施例中,捕获孔104仅具有一个输出通道103。在其它可能的实施例中,捕获孔104可以供给两个或更多个输出通道103。每个输出通道103是至少一个过量或废弃流体的出口点。在一个实施例中,可以仅通过一个输出通道103从捕获孔104输出几种流体。在另一个实施例中,可以通过两个或更多个输出通道103从捕获孔104输出几种流体。在另一个实施例中,可以仅通过一个输出通道103从捕获孔104输出几种流体。
在这些实施例中,但不是所有的实施例中,在捕获孔104和检测孔108之间存在连接通道105。在其它实施例中,可能存在零个、一个或多个这些连接通道108。总体而言,只要流体仍然能够流入和流出微流控芯片100并且以正确序列暴露于检测和捕获剂,则可以相对于在此体现的设计来添加或减少芯片的通道。
微流控芯片100包含至少一个检测孔108,检测孔108可以体现为各种尺寸和形貌。它的结构是一个小腔室的结构。
除了任何其它涂层之外,该特定结构还包含至少一种检测剂,其在检测孔108的构造期间放置在检测孔108中。检测剂可以通过手工方法放入孔中,包括滴涂。或者,可以使用如下方法将其涂覆在检测孔108的表面上:将末端浸入流体中或将流体流到末端上,然后将末端施加到表面上,或者可以使用喷墨印刷方法或与喷墨方法类似的方法或者其它方法,其中将检测剂以喷雾形式喷到表面上,或者可以以本领域中描述的许多其它公知方式施用检测剂。它可以以固体形式施用或将流体或气雾剂作为载体施用。在后一种情况下,它可能干燥以在检测孔108中形成斑点或层。
在这个实施例中,检测孔108不从任何输入通道102供给。在其它可能的实施例中,检测孔108可以从一个输入通道102供给。在其它可能的实施例中,检测孔108可以从两个或更多个输入通道102供给。每个输入通道102是至少一种流体的入口点。在一个实施例中,可以仅通过一个输入通道102将几种流体输入到检测孔108中。在另一个实施例中,几种流体可以通过两个或更多个输入通道102输入到检测孔108中。在另一个实施例中,可以仅通过一个输入通道102将几种流体输入到检测孔108中。
在该实施例中,检测孔108具有零个输出通道103。在其它可能的实施例中,检测孔108可以供给一个输出通道。在其它可能的实施例中,检测孔108可以供给两个或更多个输出通道103。每个输出通道103是至少一个过量或废弃流体的出口点。在一个实施例中,可以仅通过一个输出通道从检测孔108输出几种流体。在另一个实施例中,可以通过两个或更多个输出通道103从检测孔108输出几种流体。在另一个实施例中,可以仅通过一个输出通道103从检测孔108输出几种流体。
107显示阻断剂。阻断剂107可以具有各种形状,并且这个实施例中所示的尺寸在微米范围内,但在其它实施例中,这些尺寸可以更大或更小以与通道的形状和尺寸连续。阻断剂107的目的是当它放置在捕获孔104和检测孔108之间时,它抑制流体在这两个孔之间通过。当将阻断剂107从这两个孔之间移出时,流体可以在这两个孔之间通过。在该实施例中,阻断剂107是物理对象。其可以构造成不同的形状,但是在这个实施例中是长方体的形状。阻断剂107也可以由任何材料构成。在这个实施例中,它由诸如镍之类的磁性金属构成。阻断剂107可以涂覆或不涂覆各种涂层或多层涂层,以使其更好地发挥其功能。在该实施例中,阻断剂107涂覆有聚合物,该聚合物防止金属离子渗入流经芯片的任何流体中,并且还减少当阻断剂移动时对通道或孔的摩擦和损坏。聚合物也是疏水的,以抑制任何流体通过阻断剂周围,使得阻断剂更好地发挥其功能。可以使用机械力、磁力、静电力或用于移动对象的在宏观、微观或更小尺度下利用的任何其它力来移动阻断剂107。在该实施例中,利用通过电磁产生的磁力移动阻断剂107。阻断剂107可以被动地或主动地控制。在这个实施例中,电磁以及因此导致的阻断剂107的移动被主动地控制。可替代地,对于该实施例中所示的移动阻断剂107,可以采用阻断流体流动的各种其它方式,例如阀或门。或者,阻断剂107可以是非物理的,例如可以根据需要使用静电力或疏水力或亲水力来防止流体流动或使流体流动。可以采用任何其它公知的阻断流体流动的方法。
在该实施例中,阻断剂107包含在与捕获孔104和检测孔108之间的连接通道105垂直并相交的阻断通道106内。这允许阻断剂107移动到阻断通道106和连接通道105的接合处的位置,以在需要时阻断捕获孔104和检测孔108之间的流体流动,并且在需要使流体流动时移动到阻断通道106内的不同位置,以便不会阻断连接通道105。在一些实施例中,在输入通道102和捕获孔104之间也会存在阻断剂107,或者在捕获孔104和输出通道103之间存在阻断剂107,或者可在微流控芯片100的其它点处或在该实施例中未示出的结构之间存在阻断剂107。阻断剂107可以按相同或不同的原理操作。在所有实施例中,阻断剂107能够控制整个芯片中的流体流动,并且因此能够控制检测剂和捕获剂,因为控制了含有至少一种目标剂的流体暴露于每种捕获剂或每种检测剂。在一些实施例中,阻断剂107还将使得能够控制含有暴露于特定捕获剂或特定检测剂的至少一种目标剂的流体的量,因为阻断剂107将能够在一个特定的受控时期内阻断流体子集进入一个特定的孔或其它芯片结构。类似地,阻断剂107将能够在一受控时期内阻断其它含有其它试剂的流体进入特定的孔或其它芯片结构中。
在替代实施例中,可以将检测剂喷到捕获室中,或者每种试剂可以以固体形式或者携带在液体或其它载体中单独移动或控制以在微流控芯片100周围移动。这些和其它示例中的每一个都是本公开的原理的实施例,其中单独地控制含有至少一种目标剂的流体暴露于每种至少一种捕获剂和每种至少一种检测剂。
在该实施例中,含有至少一种目标剂的流体流入输入通道101并从那里流入捕获孔104。在捕获孔104中,至少一个捕获剂捕获至少一个目标剂。在该实施例中,捕获孔104构造为使得即使任何捕获剂捕获任何目标剂,任何捕获剂仍保持附着在捕获孔104的表面。此外,捕获孔104的不包含捕获剂的任何部分构造成防止目标剂或流经捕获孔104的任何其它材料粘附到捕获孔104的表面。在该第一步骤中,阻断剂阻断连接通道105,防止流体流入检测室。在第二步骤中,用于生物过程的标准洗涤液通过捕获孔104洗涤以洗去含有至少一种目标剂和任何未结合的目标剂的流体。在第三步骤中,阻断剂107从连接通道105移除到阻断通道106的不同区段中。因此,流体流入检测孔108。这引起该孔中的至少一种检测剂与流体混合,并且然后检测剂将穿过捕获孔104中并且与捕获孔104中的结合到至少一种捕获剂的至少一种目标剂反应。在一些实施例中,当在捕获孔104的入口或出口或其它点处也存在其它阻断剂时,可以在所选时间使用这些阻断剂来确保检测剂以特定浓度暴露于捕获孔104的目标剂。在第四步骤中,洗涤液流过以洗掉任何未结合的检测剂。在第五步骤中,确定至少一种捕获的目标剂的存在或者可替代地确定至少一种捕获的目标剂的存在,并且量化所捕获的至少一种目标剂的量(见下文)。
在替代实施例中,在上述第四和第五步骤之间存在中间步骤,从而使含有至少一种试剂的另外的流体流过微流控芯片100,并且该试剂可以结合或以其它方式与捕获剂、目标剂或检测剂或本文所述的本公开的操作涉及的另一种试剂反应。然后进行进一步的洗涤步骤以除去任何未结合的或其它未反应的或不需要的组分。在另一个替代实施例中,可以有使试剂流过微流控芯片100的多个步骤和/或多个洗涤步骤。
在另一个替代实施例中,至少一种其它试剂不是流入微流控芯片100,而是包含在微流控芯片100的另一部分内。在另一个实施例中,其包含在微流控芯片100的另一部分中,并且存在阻断剂107,阻断其与捕获剂、目标剂或检测剂反应,直到阻断剂107被去除。此外在其它实施例中,在微流控芯片100上可以有多个试剂。
在其它实施例中,这些步骤以不同的顺序执行,并且可以根据需要存在附加的或更少的或不同的步骤,其中额外的试剂也存在于微流控芯片100上,或者流动到并穿过微流控芯片100。例如,在另一个实施例中,检测剂可以与含有至少一种目标剂的流体混合。在其它实施例中,试剂可以混合。
在各种其它实施例中,如这些实施例中所阐述的微流控芯片100的各种部件之间的形状、尺寸及其间的连接将是不同的。额外的试剂也可能是需要的并且可能被包含在微流控芯片100上或流到微流控芯片100上或这些的组合中。
在一些实施例中,微流控芯片100还将包含感测结构以形成用于结合的目标剂的量化系统的一部分。这些感测结构优选但不必然位于捕获孔104中或者正好在捕获孔104之下和/或之上。这允许在捕获目标剂时立即量化而不需要进一步处理。这种感测结构的实施例包括(但不限于):
(1).振荡传感器,这是在芯片上的被引起振荡的结构。结构的振荡频率取决于质量,因此振荡频率根据附着到振荡传感器的任何材料的量而变化,并且振荡的这个变化与目标剂的浓度有关。这些传感器的例子包括微型石英晶体微量天平(QCM)和表面声波(SAW)结构;
(2).电化学传感器,由此,与流体中的试剂反应产生与目标剂浓度有关的电信号。典型的电化学传感器包括由绝缘材料薄层隔开的感测电极和反电极组成。这些传感器的例子包括电位式生物传感器;
(3).电子传感器,由此,试剂与传感器的一些部件的相互作用引起传感器的这些部分的电特性的变化,由此,这些特性的变化与目标剂浓度有关。这些传感器的例子包括场效应晶体管(FET),由此,试剂结合到FET的栅极改变了FET的源极和漏极之间的电阻;
(4).霍尔效应传感器,其是响应于磁场而改变其输出电压的转换器。输出电压变化与目标剂浓度有关;
(5).光学传感器,由此,发生与目标剂浓度有关的光吸收或发射。这种光吸收可能是由于例如试剂与酶等其它试剂的化学反应而引起的基底的颜色变化而引起的,其可以通过例如分光光度法测量;或由于试剂的光学特性或由于试剂附着有荧光或发光结构而导致直接吸收或发射特定的波长或多个波长的光。这些传感器的实例包括酶联免疫吸附测定(ELISA)和光致发光传感器;
(6).光学传感器,其利用光学检测的替代方法,由此,光学信号的变化与目标剂的浓度有关。这种光学检测系统的例子包括干涉测量或近场显微镜(倏逝波的变化的测量);和
(7)机械传感器,由此,引起由于试剂附着引起的额外应力而导致的传感器的物理形状的变形。可以通过例如光学干涉测量或材料的电学、机械、磁性或结构特性的变化来检测与目标剂浓度有关的这种变形。这些传感器的例子包括基于悬臂梁的传感器和压电传感器。
为了完整性,含有目标剂的流体的一些例子包括:(1).用于商业或非商业应用的任何溶液或悬浮液,其含有待量化的特定无机化学品,例如用于化学工业;(2).用于商业或非商业应用的含有特定有机化学品的任何溶液或悬浮液;(3).任何生物流体;(4).来自人类或动物的任何流体,但尤其是血液、尿液、粘液、唾液和脑脊髓液;(5).来自其它生物有机体的任何流体,包括植物、真菌、细菌或古细菌;(6).来自任何其它生物实体的任何流体;(7).含有来自食品工业的产品的流体;和(8).来自河流、海洋、雨水、废水植物或其它来源的水。
为了完整性,目标剂的一些例子包括:(1).蛋白质(天然的和合成的),包括抗体、抗原、酶和其它蛋白质;或包含蛋白质的结构;(2).肽(天然的和合成的);(3).氨基酸或包含氨基酸(天然的和合成的)的结构;(4).DNA(天然的和合成的);(5).RNA(天然的和合成的);(6).核酸或包含核酸(天然的和合成的)的结构;(7).糖类(saccharide)或包含糖类(天然的和合成的)的结构;(8).脂类(lipid)或包含脂类(天然的和合成的)的结构;(9).其它生物分子和包括生物分子(天然的和合成的)的结构;(10).全细胞或部分细胞或细胞群(有或没有包含非细胞结构);(11).任何包含细胞的结构;(12).任何其它生物结构;和(13).具有可被捕获剂识别并用于结合和固定目标剂的特定模式的任何非生物化学结构。
为了完整性,捕获剂的一些例子包括:(1).使用无论任何手段产生的抗体,包括单克隆抗体,多克隆抗体或通过纯化学合成产生的抗体;(2).天然存在的、使用生物学方法生产或使用合成化学方法或任何其它天然或合成方法生产的适体;(3).核酸链或结构(天然的和合成的);(4).肽链或结构(天然的和合成的);(5).包括与目标剂上的带电模式互补的电荷模式的分子或其它化学品;(6).包括与目标剂上的模式互补的模式的疏水或亲水区域的模式的分子或其它化学品;(7).包括与目标剂上的这种模式互补的偶极子、四极子或其它更高阶极子的模式的分子或其它化学品;(8).包括与目标剂上的磁性模式互补的磁性区域的模式的分子或其它化学品;(9).可以是天然存在的,也可以是使用任何合成方法或以其它方法制备的无机材料。这种无机结构的例子包括功能化的单壁和多壁的碳纳米管、硅聚合物(例如具有特定电荷模式)和纳米颗粒复合物;和(10).包括上述任何一种作为子结构、部件或元件的结构(包括细胞、组织和其它有机和无机结构)。
为了完整,检测剂的一些例子包括:(1).使用无论任何手段产生的抗体,包括单克隆抗体,多克隆抗体或通过纯化学合成产生的抗体;(2).天然存在的、使用生物学方法生产或使用合成化学方法或任何其它天然或合成方法生产的适体;(3).核酸双链和单链或结构(天然的和合成的);(4).肽链或结构(天然的和合成的);(5).包括与目标剂上的带电模式互补的电荷模式的分子或其它化学品;(6).包括与目标剂上的模式互补的模式的疏水或亲水区域的模式的分子或其它化学品;(7).包括与目标剂上的模式互补的模式的疏水或亲水区域的模式的分子或其它化学品;(8).包括与目标剂上的模式互补的偶极子、四极子或其它更高阶极子的模式的分子或其它化学品;(9).包括与目标剂上的磁性模式互补的磁性区域模式的分子或其它化学品;(10).可以是天然存在的,也可以是使用任何合成方法或其它方法制备的无机材料。这种无机结构的例子包括功能化的单壁和多壁的碳纳米管、硅聚合物(例如具有特定电荷模式)和纳米颗粒复合物;和(11.)包括上述任何一种作为子结构、部件或元件的结构(包括细胞、组织和其它有机和无机结构)。
其它试剂的例子包括通过与检测抗体(或其它试剂)结合而帮助检测目标剂的二抗,其中,检测抗体(或其它试剂)与目标标试剂结合。检测抗体或二抗可能具有结合酶以引起与标准ELISA方法类似的试剂“显影剂”的颜色变化,或者可能具有荧光或电化学发光区域或与所选检测机构有关的其它区域。也可能有多种酶附着于单个检测抗体或二抗。它们结合的方法包括本领域常见的那些方法,如抗生蛋白链菌素-生物素结合。其它试剂可以是与目标剂或检测剂结合的颗粒,包括纳米颗粒。在一个实施例中,使用这样的纳米颗粒使得对每个结合的目标剂的结合至质量传感器的质量增加设定的量,以增强质量传感器(例如上述的振荡传感器或机械传感器系统)的灵敏度。在不同的实施例中,使用磁性纳米颗粒来增加霍尔效应传感器中每单位磁场的输出电压变化。其它试剂可以是与目标剂结合的有机和无机化学品。在一个实施例中,这样的化学品结合到目标剂并促进金属薄膜的氧化,从而使电子传感器中检测到的电信号产生增强的变化。
微流控芯片100由“N”个感测结构及其目标剂量化所需的对应的孔和通道形成;即系统由“N”个量化系统形成。这由图6中的一个或多个量化系统110来指明。“N”可以是1和无穷之间的任何数字;即芯片可以由任何数量的量化系统110构成。例如,芯片可以由一个量化系统110组成。在另一个示例中,芯片可以由十个量化系统110形成。在另一个示例中,传感器可以由一百个量化系统110形成。所有的感测结构和量化系统110优选是相同的。例如,在一个实施例中,所有量化系统110都包括为振荡结构的感测结构。例如,在不同的实施例中,所有量化系统110都包括为一种类型的电化学传感器的传感结构。然而,在一些实施例中,量化系统110可以是不同的。在这样的实施例的示例中,一半量化系统110包括可以是振荡结构的感测结构,另一半量化系统110包括可以是一种类型的光学传感器的感测结构。在这样的实施例的不同示例中,一半的量化系统110包括可以是振荡结构的感测结构,另一半量化系统110包括可以是一种类型的电化学传感器的感测结构。每个量化系统110用于量化一个不同的目标剂。在一些实施例中,可以使用两个或更多个量化系统110来量化用于比较的相同目标剂,然而量化系统110所进行的测量彼此独立;即在芯片内使用若干量化系统来量化相同的目标剂,通过重复性增加对结果的置信度,但不会增加额外的灵敏度,且不需要这样做。
在各种其它实施例中,量化系统110在微流控芯片100内的位置与图6中所示的位置不同。例如,在一个实施例中,多个量化系统110可以在一个线性方向上彼此相邻放置,形成量化系统110的线性阵列。在另一个实施例中,一个或多个量化系统110可以沿着两个线性方向彼此相邻放置,形成二维阵列。例如,在另一个实施例中,量化系统110可以被置于芯片内的随机离散位置。
图7示出了基本类似于图6所示的微流控芯片100的微流控芯片200。微流控芯片200还包括供给输入通道203的输入孔202。输入孔202可以具有各种形状,并且该实施例中所示的尺寸在mm范围内,但是在其它实施例中,这些尺寸可以在cm范围或100μm范围内或者更大或者更小以与芯片格式和尺寸连续。可以将流体从附接至输入通道203的前部的注射器或“针刺(pinprick)”装置放入输入孔中,其中,注射器或“针刺(pinprick)”装置穿透患者的皮肤以直接抽血。在该实施例中,只有一个输入孔202直接供给所有输入通道203,而没有额外的微流体控制。然而,在一些实施例中,可以有多于一个的输入孔202选择性地供给至少一个输入通道203。例如,在一个这样的实施例中,有一个输入孔202供给所有输入通道203。例如,在不同的实施例中,有两个输入孔202供给输入通道203的每一半。在这种实施例的第三个不同的例子中,有两个输入孔202交替地供给所有的输入通道203。图7所示的实施例还包含从输出通道204供给的输出“废物”孔205。输出孔205收集量化过程中产生的过量流体或废液。优选地,只有一个输出孔205包含产生的全部的过量流体和废液。在不太优选的实施例中,微流控芯片200可以包含多于一个输出孔205。在图7所示的实施例中,只有一个直接从所有的输出通道204供给的输出孔205,而没有额外的微流体控制。然而,在本公开的一些实施例中,可以有多于一个输出孔205被从至少一个输出通道204选择性地供给。微流控芯片200可以使用任何组合数量的输入孔202和输出孔205以许多不同的方式设计。
图8示出了根据本公开的实施例的如图6所示的量化系统300的一部分的详细视图。所示出的是输入通道301,其对应于输入通道102;输出通道302,其对应于输出通道103;捕获孔303,其对应于捕获孔104;连接通道304,其对应连接通道105;阻断通道305,其对应于阻断通道106;阻断剂306,其对应于阻断剂107;以及检测孔307,其对应于检测孔108。
图9示出了量化系统400的替代实施例,在量化系统400中,在输入通道408与捕获孔403之间存在阻断剂410,在捕捉孔403与输出通道402之间存在阻断剂412,并且在捕获孔403和检测孔407之间存在阻断剂406。阻断剂406、410和412可以以相同或不同的原理可控地操作。还示出了输入通道408和捕获孔403之间的输入通道401、位于检测孔407和捕获孔403之间的连接通道404以及分别与阻断剂410和412相关联的阻断通道409和411。
图10具体体现了加载装置500,如上所述的微流控芯片100、200插入其中,以确定至少一种目标剂的存在或至少一种目标剂的量化。加载装置500适于控制微流控芯片100、200内的流体的流动和混合,并且适于控制传感器。在该实施例中,加载装置500具有在cm范围内的总横向尺寸。这对手持式检验特别有用。在一些其它实施例中,加载装置500可具有与cm范围不同的横向尺寸,例如在dm范围内。这更适合台式检验。在该实施例中,存在定位机构501,用于确保当微流控芯片100、200被放置在加载装置500上或加载装置500中时插入装置上的正确位置。这种机构可以是纯机械的,或者使用许多不同的标准和公知的操作方法。在该特定实施例中,存在对应于如图6中的101所示的微流控芯片100、200上的磁性点的磁性点,因此吸引微流控芯片上的对应点,确保微流控芯片在装置上正确插入到位。在该特定实施例中,还存在连接电子器件502,其将微流控芯片上的任何电子连接或结构(例如,任何电子操作的感测元件)连接到装置中的控制电子器件。取决于用于检测至少一个目标剂的存在或量化至少一个目标剂的量的感测系统,在该装置中可以存在检测器503。这将包括传感元件和检测操作所需的任何其它结构。例如,在一个实施例中,检测与ELISA系统类似地操作,凭此检测或测量微流控芯片的一些部分中的颜色变化或荧光反应,然后检测器包括照射芯片的光产生元件和可以测量由于微流控芯片中的吸收或发射而引起的光的变化的光传感系统。在该系统的一个实施例中,在光产生元件之间还存在控制机构,其控制微流控芯片100、200的不同区域暴露和不暴露于来自光产生元件的光,并允许微流控芯片的不同区域在不同时间段暴露于、不暴露于或不同程度的暴露于来自光产生元件的光。在一个实施例中,该控制机构是类似于在液晶显示器中使用的液晶面板。在另一个实施例中,存在多个光产生元件。在另一个实施例中,存在多个光产生元件,并且每个光产生元件仅暴露微流控芯片的特定区域。在另一个实施例中,通过单独的光元件对微流控芯片的不同部分进行的这种暴露是通过类似于在LED电视显示器中操作的LED面板完成的。
在图10所示的实施例中,还有嵌入式处理单元/电子器件504。这包括标准的至少一个微控制器或至少一个微处理器、存储器和其它此类标准电子器件,所述标准电子器件已知被用作的目的是处理来自装置上的任何感测部件的数据、装置上的有源部件(如果有的话)的控制以及装置的任何其它功能(如果需要的话)。在这个实施例中有一个处理单元。在替代实施例中,可以有多个处理单元。
装置的该实施例包括壳体505,壳体505是封装电子器件和微流控芯片的标准外壳,并且还可以防止物理颗粒、光或其它不希望的外物污染装置的内部。在该实施例中,还有插入槽506,微流控芯片通过该插入槽506被放置到加载装置500中。装置上可能有其它标准电子器件或连接507以允许其正常或增强操作。
图11示出了替代实施例,在该实施例中,加载装置600没有机载(onboard)处理单元,但是该装置通过有线连接604连接到分离的至少一个智能结构605,所述智能结构605为例如但不限于处理发生的计算机、膝上型计算机、平板装置,移动电话或定制基础设施,并且微流控芯片插入加载装置600中以量化目标剂。有线连接604优选地通过USB/miniUSB/microUSB线缆制成。或者,有线连接604通过RS232、GPIB或不同类型的数据线缆制成。智能结构605优选地通过移动网络连接或通过Wi-Fi连接到互联网。在替代实施例中,加载装置600通过蓝牙或Wi-Fi或替代无线数据连接而无线连接到至少一个智能结构605(发生处理的地方)。在替代实施例中,加载装置600经由因特网或其它网络连接到发生处理的分离的至少一个智能结构。
用于数据采集、处理和装置控制的标准机载和非机载电子器件的任何组合都是本公开的实施例。
图12是加载设备700的实施例。在加载设备上有定位系统,以确保微流控芯片在加载到加载设备700上时被放置在正确的位置。这可以以许多不同的标准方式运行,包括任何公开的已知方式。在该实施例中,使用将吸引如图6中的101所示的微流控芯片上的对应磁性点的磁性点701。在该实施例中,存在插入槽702,微流控芯片放置在插入槽702中。在其它实施例中,微流控芯片可以简单地放置在加载器的顶部,或者插入槽可以具有可选的尺寸或几何形状。在进一步的实施例中,可能存在自动加载设备以从芯片堆或其它芯片集加载芯片。在该实施例中,只有一个插入槽,微流控芯片依次相继地放置在其中。在其它实施例中,可以有多于一个的插入槽702,用于将多个微流控芯片同时加载到不同的槽中。在又一个实施例中,可以有一个插入槽702,多个微流控芯片同时放入其中。在又一个实施例中,可以有多于一个的插入槽702,多个微流控芯片同时放入其中。在该实施例中,各种“墨”被放置在加载设备700中的微型墨孔705中。这里的“墨”是指含有至少一种捕获剂或检测剂的流体。各种“墨”可能包含不同的捕获剂或检测剂。在加载设备700的其它实施例中,可以有其它方法来加载“墨”,例如在一个替代实施例中,其可以首先被加载到随后被放置在加载设备中的墨盒中。在另一个实施例中,所述至少一种捕获剂或至少一种检测剂可以以固体形式放入设备中,并且设备可以在内部将其混合成流体。用于加载“墨”的这些替代方法全部是本公开的各种实施例。在该实施例中,“墨”穿过印刷末端703,印刷末端703接触表面或接近表面,以将墨沉积在特定位置。至少一个末端703的定位在该实施例中被设定,并且微流控芯片被加载在其下方以便使“墨”被放置或“印刷”,使得末端703仅需要在竖直的上下(z)方向移动。在一个替代实施例中,末端703也可以在平面(x-y)方向上水平移动,使得印刷位置可以在运行之间甚至在各个微流控芯片之间改变。在其它实施例中,印刷机构改变,使得墨从末端703喷射到微流控芯片上的正确位置。在其它实施例中,末端的数量与“墨”的数量不同,而是,相同的末端具有多个“墨”流过其中,或者相同的“墨”流过多个末端。在不同的实施例中,末端703可以是完全不同的尺寸或几何形状,包括仅作为孔(well)中的洞(hole)。在其它实施例中,不是墨从孔流入末端703,而是末端703被浸入孔中,使得一些墨附着到其上,然后这种墨被放置在微流控芯片上。在其它实施例中,没有末端703,而是使用诸如操纵静电场或电磁场或亲水或疏水力的一些替代方法来将“墨”从一个或多个孔移动到微流控芯片。还有包含这些替代实施例的各种组合的实施例。加载设备包含用于将至少一种“墨”印刷到微流控芯片上的特定位置的方法的任何系统都是本公开的实施例。也可以有其它的结构形成印刷系统的一部分用于“墨”的移动或传输-在这个实施例中有连接通道707。还有机载电子器件704和其它连接。这包括标准的至少一个微控制器或至少一个微处理器、存储器和其它的这种已知标准电子器件,所述其它的这种已知标准电子器件用于处理来自加载机700上的任何感测部件的处理数据、加载设备上的有源部件的控制以及加载设备的任何其它功能(如果需要的话)。在这个实施例中有一个处理单元。在替代实施例中,存在多个处理单元。在该实施例中,存在到计算机的有线连接706。在替代实施例中,不存在机载处理单元,但系统通过有线连接706而连接到处理发生的分离的至少一个装置或计算机。在替代实施例中,通过蓝牙或Wi-Fi无线连接或替代的无线连接而无线连接到处理发生的分离的至少一个装置或计算机。在另一个实施例中,其通过因特网或其它网络连接到处理发生的分离的至少一个装置或计算机。用于数据采集、处理或加载设备控制的标准机载和非机载电子器件的任意组合是本公开的实施例。
为了说明的目的,现在将描述本公开的两个示例实施例。
在第一示例实施例中,使用由聚合物、玻璃或其它透明材料制成并包含“N”个量化系统的微流控芯片。所有捕获孔用至少一种捕获抗体涂覆。在这个特定的实施例中,存在“N”个捕获孔,每个量化系统一个。在这个特定的实施例中,每个捕获孔被不同的捕获抗体涂覆。所有检测孔用至少一种检测抗体涂覆。在此特定实施例中,存在“N”个检测孔,每个量化系统一个。在这个特定的实施例中,每个检测孔用不同的检测抗体涂覆。
在这个特定的实施例中,在每一对捕获孔和检测孔之间有一个连接通道。在这个特定的实施例中,在每个连接通道处有一个主动控制的(actively controlled)阻断剂。在这个特定的实施例中,所有的阻断剂最初阻断连接通道。在这个特定的实施例中有一个输入孔。在这个特定的实施例中有一个输出孔。在这个特定的实施例中,有一个连接输入孔和捕获孔的输入通道。在这个特定的实施例中,有一个连接捕获孔和输出孔的输出通道。捕获孔和检测孔都使用加载设备涂覆捕获和检测抗体。微流控芯片被引入装置中。在该特定实施例中,装置在捕获孔下方具有像素化的LED灯。在该特定实施例中,装置在捕获孔上方具有光检测器。在该特定实施例中,装置具有嵌入式电子器件以控制LED灯和检测器。
在该特定的实施例中,待分析的流体样本(可能含有目标抗原)被沉积在输入孔中。待分析的流体样本流过输入通道,淹没捕获孔并通过输出通道离开。待分析的样本中的目标抗原(如果存在)特定结合至固定在捕获孔表面的捕获抗体。大量的清洁流体(例如缓冲液)沉积在输入孔中,流过输入通道,淹没捕获孔并通过输出通道离开,清除沉积在捕获孔表面上的松散的剂。现在阻断剂被切换为解除阻断连接通道。已知量的载液沉积在输入孔中。载液流经输入通道,淹没捕获孔,流经连接通道,淹没检测孔。检测抗体通过扩散由流体传送,并结合到固定在捕获孔表面的目标抗原(如果存在)。大量的清洁流体(例如缓冲液)沉积在输入孔中,流过输入通道,淹没捕获孔并通过输出通道离开,清除沉积在捕获孔表面上的松散的剂。将含有酶联二抗的液体沉积到输入孔中,流过输入通道,流过捕获孔并通过输出通道离开。酶联二抗与检测抗体(如果存在)结合。大量的清洁流体(例如缓冲液)沉积在输入孔中,流过输入通道,淹没捕获孔并通过输出通道离开,清除沉积在捕获孔表面上的松散的剂。已知量的显影剂沉积在输入孔中,流过输入通道并淹没捕获孔。颜色变化与存在于待分析的流体样本中的目标抗原的量成比例地产生。LED灯顺序打开/关闭。来自检测器的读数用于检测待分析的流体样本中存在的“N”个不同抗原的浓度。
在第二示例实施例中,使用由硅制成的含有“N”个量化系统的微流控芯片。所有捕获孔用至少一种捕获抗体涂覆。在这个特定的实施例中,存在“N”个捕获孔,每个量化系统一个。在这个特定的实施例中,每个捕获孔由不同的捕获抗体涂覆。在该特定实施例中,捕获孔的底部是已经与硅芯片集成(或内置于其中)的振荡传感器的顶部电极,例如小形状因数石英晶体微量天平。所有检测孔用至少一种检测抗体涂覆。在此特定实施例中,存在“N”个检测孔,每个量化系统一个。在这个特定的实施例中,每个检测孔用不同的检测抗体涂覆。在这个特定的实施例中,每对捕获孔和检测孔之间有一个连接通道。在这个特定的实施例中,在每个连接通道处有一个主动控制的阻断剂。在这个特定的实施例中,所有的阻断剂最初阻断连接通道。在这个特定的实施例中有一个输入孔。在这个特定的实施例中有一个输出孔。在这个特定的实施例中,有一个连接输入孔和捕获孔的输入通道。在这个特定的实施例中,有一个连接捕获孔和输出孔的输出通道。捕获孔和检测孔使用加载设备涂覆捕获和检测抗体。微流控芯片被引入到装置中。在这个特定的实施例中,装置在捕获孔下面具有电连接以驱动振荡传感器。在该特定实施例中,装置具有嵌入式电子器件以测量振荡传感器的频率变化。
在这个特定的实施例中,待分析的流体样本(可能含有目标抗原)被沉积在输入孔中。待分析的流体样本流过输入通道,淹没捕获孔并通过输出通道离开。待分析的样本中的目标抗原(如果存在)特定结合固定在捕获孔表面的捕获抗体。大量的清洁流体,例如缓冲液,被放入输入孔,流经输入通道,淹没捕获孔并通过输出通道离开,清除沉积在捕获孔表面上的松散的剂。现在阻断剂被切换到解除连接通道的阻断。已知量的载液沉积在输入孔中。载液流经输入通道,淹没捕获孔,流经连接通道,淹没检测孔。检测抗体通过扩散通过流体传送,并结合到固定在捕获孔表面的目标抗原(如果存在)。大量的清洁流体,例如缓冲液,被放入输入孔,流经输入通道,淹没捕获孔并通过输出通道离开,清除沉积在捕获孔表面上的松散的剂。包含与二抗结合的金纳米颗粒的流体沉积在输入孔中,流过输入通道,流过捕获孔并通过输出通道离开。金纳米颗粒连接的抗体结合检测抗体(如果存在)。大量的清洁流体(例如缓冲液)沉积在输入孔中,流过输入通道,淹没捕获孔并通过输出通道离开,清除沉积在捕获孔表面上的松散的剂和颗粒。振荡传感器依次激活且嵌入了电子器件的该装置读取频移。来自传感器的读数用于检测待分析的流体样本中存在的“N”种不同抗原的浓度。
因此,已经描述了包括用于选择性地控制微流体装置内的流体的流动的阀和微流体传感平台的微流体装置。尽管已经参照特定的示例实施例描述了实施例,但是显而易见的是,可以对这些示例实施例进行各种修改和改变而不偏离本申请的更广泛的主旨和范围。例如,这种改变可以包括但不限于用于致动阀膜的力的变化,刚性和软质材料的变化以及其它流体层或控制层的变化和/或添加。因此,说明书和附图应被认为是说明性的而不是限制性的。
本公开内容在治疗性或预防性治疗受试者的方法中也特别有用。受试者优选是动物,更优选是哺乳动物,甚至更优选是人。虽然设想本公开也适用于兽医学科。
本文引用的每个专利、专利申请和出版物的公开内容通过引用整体并入本文。
本文任何参考文献的引用不应被解释为承认这种参考文献可作为本申请的“现有技术”。
在整个说明书中,目的是描述本公开的优选实施例,而不将本公开限制为任何一个实施例或特征的特定集合。因此,本领域技术人员将认识到,根据本公开内容,可以在示例的特定实施例中进行各种修改和改变而不脱离本发明的范围。所有这样的修改和改变都旨在被包括在所附权利要求的范围内。
Claims (10)
1.一种微流阀组件,包括:
刚性基底,其具有限定流体通道的至少两个相邻层,其中所述至少两个相邻层包括第一层和第二层;
至少一个阀构件,其与所述第二层相邻地定位;
所述第二层中的至少两个通孔,其构造成利于所述流体通道与所述阀构件之间的连通,以利于检验流体基本与所述流体通道相邻的流动;以及
柱构件,其中,当所述阀构件上的外部压力小于所述检验流体的压力时,所述检验流体流过所述柱构件上方,
其中,所述阀构件制作在所述第二层的顶侧。
2.根据权利要求1所述的微流阀组件,其中,所述检验流体通过所述通孔流回所述流体通道。
3.根据权利要求1所述的微流阀组件,其中,所述阀构件的横截面积不同于所述流体通道的横截面积。
4.根据权利要求1所述的微流阀组件,其中,所述阀构件的深度比所述流体通道浅。
5.根据权利要求1所述的微流阀组件,其中,所述阀构件的可拉伸膜嵌入有导电珠或磁珠,并且其中所述阀构件构造为通过电力或磁力来致动。
6.根据权利要求1所述的微流阀组件,其中,所述阀构件在所述第二层的上方。
7.根据权利要求1所述的微流阀组件,其中,所述检验流体基本在所述流体通道上方流动。
8.根据权利要求1所述的微流阀组件,其中,所述柱构件在所述阀构件的中间。
9.根据权利要求1所述的微流阀组件,其中,控制通道在所述阀构件处的深度独立于所述流体通道的深度,从而所述阀构件更容易关闭,同时保持流体网络中较低的流体压力。
10.一种在根据权利要求1所述的微流阀组件上输送流体的方法,所述方法包括:
使检验流体流过所述刚性基底内的所述流体通道;以及
使所述检验流体流过所述第二层中的所述至少两个通孔,以利于检验流体基本与所述流体通道相邻的流动,其中,当所述阀构件上的外部压力小于所述检验流体的压力时,所述检验流体流过所述柱构件上方。
Applications Claiming Priority (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201562155470P | 2015-04-30 | 2015-04-30 | |
| US62/155,470 | 2015-04-30 | ||
| US201562156368P | 2015-05-04 | 2015-05-04 | |
| US62/156,368 | 2015-05-04 | ||
| PCT/EP2016/059660 WO2016174230A1 (en) | 2015-04-30 | 2016-04-29 | Microfluidic valves and devices |
| CN201680039266.4A CN108136388A (zh) | 2015-04-30 | 2016-04-29 | 微流阀和装置 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201680039266.4A Division CN108136388A (zh) | 2015-04-30 | 2016-04-29 | 微流阀和装置 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN114893585A true CN114893585A (zh) | 2022-08-12 |
Family
ID=55948812
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202111648713.5A Pending CN114893585A (zh) | 2015-04-30 | 2016-04-29 | 微流阀和装置 |
| CN201680039266.4A Pending CN108136388A (zh) | 2015-04-30 | 2016-04-29 | 微流阀和装置 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201680039266.4A Pending CN108136388A (zh) | 2015-04-30 | 2016-04-29 | 微流阀和装置 |
Country Status (7)
| Country | Link |
|---|---|
| US (2) | US20180093269A1 (zh) |
| EP (1) | EP3288681A1 (zh) |
| JP (3) | JP2018522206A (zh) |
| CN (2) | CN114893585A (zh) |
| HK (1) | HK1250681A1 (zh) |
| SG (1) | SG11201708866YA (zh) |
| WO (1) | WO2016174230A1 (zh) |
Families Citing this family (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2020041342A2 (en) * | 2018-08-20 | 2020-02-27 | Vanderbilt University | Cartridge systems, capacitive pumps and multi-throw valves and pump-valve systems and applications of same |
| CN109012769B (zh) * | 2018-07-11 | 2020-01-21 | 西安交通大学 | 一种基于表面声波的微流控液滴生成装置及方法 |
| CN110857743B (zh) * | 2018-08-22 | 2020-10-16 | 厦门大学 | 用于微流控芯片的液流导向阀及微流控芯片 |
| CN109622083A (zh) * | 2019-01-24 | 2019-04-16 | 京东方科技集团股份有限公司 | 一种微流控系统及其制备方法 |
| EP3694227A1 (en) * | 2019-02-07 | 2020-08-12 | Oticon A/s | A hearing device comprising an adjustable vent |
| CN109967144B (zh) * | 2019-03-25 | 2021-02-19 | 宁波美康盛德生物科技有限公司 | 用于检测微流控芯片的干式化学分析仪及微流控芯片 |
| EP3763439A1 (en) * | 2019-07-12 | 2021-01-13 | Curiosity Diagnostics sp. z o.o | Microfluidic chip and valve, production process and uses |
| CN110568202B (zh) * | 2019-09-12 | 2022-05-24 | 重庆科技学院 | 一种自动分样定容免疫荧光定量快速检测微流控芯片 |
| CN110605147B (zh) * | 2019-09-18 | 2021-04-06 | 重庆大学 | 一种基于液晶的温控微阀及其单、多级控制系统 |
| CN110597328B (zh) * | 2019-09-18 | 2021-04-23 | 重庆大学 | 一种基于液晶温控微阀的流量协同控制系统 |
| EP3839467B1 (en) * | 2019-12-19 | 2023-06-14 | Paris Sciences et Lettres | Microfluidic or millifluidic chip comprising a pressure sensing unit using colour-switching hydrogels |
| TW202128281A (zh) * | 2019-12-30 | 2021-08-01 | 美商伊路米納有限公司 | 與流動池一同使用之致動系統及方法 |
| CN113967486A (zh) * | 2020-07-22 | 2022-01-25 | 京东方科技集团股份有限公司 | 离心式微流控芯片 |
| CN112067533B (zh) * | 2020-09-26 | 2024-01-19 | 宁波大学 | 单细胞质谱分析系统及方法 |
| CN114768894B (zh) * | 2021-01-22 | 2023-08-11 | 中国科学院上海微系统与信息技术研究所 | 一种检测芯片及检测方法 |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6899137B2 (en) * | 1999-06-28 | 2005-05-31 | California Institute Of Technology | Microfabricated elastomeric valve and pump systems |
| ES2291363T3 (es) * | 2000-11-02 | 2008-03-01 | Biacore Ab | Valvula integralmente asociada con un conjunto de transporte de liquido microflujo. |
| KR101216828B1 (ko) * | 2002-12-30 | 2013-01-04 | 더 리전트 오브 더 유니버시티 오브 캘리포니아 | 병원균 검출과 분석을 위한 방법과 기구 |
| US20080038714A1 (en) * | 2005-11-02 | 2008-02-14 | Affymetrix, Inc. | Instrument to Pneumatically Control Lab Cards and Method Thereof |
| WO2008036997A1 (en) * | 2006-09-28 | 2008-04-03 | Fluidyx Pty. Limited | A system and method for controlling fluids within a microfluidic device |
| US9579434B2 (en) * | 2010-03-03 | 2017-02-28 | The Secretary Of Atomic Energy, Govt. Of India | Flexible magnetic membrane based actuation system and devices involving the same |
| EP2479466A1 (en) * | 2011-01-21 | 2012-07-25 | Biocartis SA | Micro-Pump or normally-off micro-valve |
| KR20130069304A (ko) * | 2011-12-15 | 2013-06-26 | 삼성전자주식회사 | 미세 유체 소자 및 그 제조방법 |
-
2016
- 2016-04-29 SG SG11201708866YA patent/SG11201708866YA/en unknown
- 2016-04-29 US US15/566,322 patent/US20180093269A1/en not_active Abandoned
- 2016-04-29 CN CN202111648713.5A patent/CN114893585A/zh active Pending
- 2016-04-29 WO PCT/EP2016/059660 patent/WO2016174230A1/en active Application Filing
- 2016-04-29 CN CN201680039266.4A patent/CN108136388A/zh active Pending
- 2016-04-29 JP JP2017556233A patent/JP2018522206A/ja active Pending
- 2016-04-29 EP EP16721128.3A patent/EP3288681A1/en active Pending
-
2018
- 2018-08-02 HK HK18109965.2A patent/HK1250681A1/zh unknown
-
2020
- 2020-10-28 JP JP2020180805A patent/JP7311156B2/ja active Active
- 2020-12-09 US US17/117,027 patent/US20210291180A1/en active Pending
-
2023
- 2023-06-29 JP JP2023107057A patent/JP2023130416A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| JP2018522206A (ja) | 2018-08-09 |
| EP3288681A1 (en) | 2018-03-07 |
| SG11201708866YA (en) | 2017-11-29 |
| US20180093269A1 (en) | 2018-04-05 |
| JP7311156B2 (ja) | 2023-07-19 |
| JP2023130416A (ja) | 2023-09-20 |
| JP2021060118A (ja) | 2021-04-15 |
| HK1250681A1 (zh) | 2019-01-11 |
| CN108136388A (zh) | 2018-06-08 |
| US20210291180A1 (en) | 2021-09-23 |
| WO2016174230A1 (en) | 2016-11-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7311156B2 (ja) | マイクロ流体バルブおよびマイクロ流体デバイス | |
| Culbertson et al. | Micro total analysis systems: fundamental advances and biological applications | |
| Riahi et al. | Automated microfluidic platform of bead-based electrochemical immunosensor integrated with bioreactor for continual monitoring of cell secreted biomarkers | |
| CN107666962B (zh) | 用于样品分析的装置和方法 | |
| Gervais et al. | Microfluidic chips for point‐of‐care immunodiagnostics | |
| Lee et al. | An integrated microfluidic system for fast, automatic detection of C-reactive protein | |
| KR101226957B1 (ko) | 일회용 진단 키트 | |
| US11480567B2 (en) | Enhanced sensitivity and specificity for point-of-care (POC) micro biochip | |
| Akceoglu et al. | A snapshot of microfluidics in point‐of‐care diagnostics: multifaceted integrity with materials and sensors | |
| EP2950096B1 (en) | Sensing device, and sensing system and sensing method using the same | |
| US20100298163A1 (en) | Microfluidic microarray system and method for the multiplexed analysis of biomolecules | |
| Kallempudi et al. | A new microfluidics system with a hand-operated, on-chip actuator for immunosensor applications | |
| He et al. | Composable microfluidic plates (cPlate): A simple and scalable fluid manipulation system for multiplexed enzyme-linked immunosorbent assay (ELISA) | |
| Wiktor et al. | Microreactor array device | |
| Yu et al. | A microfabricated quantum dot-linked immuno-diagnostic assay (μQLIDA) with an electrohydrodynamic mixing element | |
| US9452428B2 (en) | Method of making a microfluidic device | |
| Catarino et al. | Smart devices: Lab-on-a-chip | |
| KR20080007733A (ko) | 면역반응용 마이크로 바이오칩과 이의 제조방법 및 이를이용한 면역반응 여부를 검출하는 방법 | |
| Park et al. | Fabrication and testing of a PDMS multi-stacked hand-operated LOC for use in portable immunosensing systems | |
| Shao et al. | Design, fabrication and test of a pneumatically controlled, renewable, microfluidic bead trapping device for sequential injection analysis applications | |
| US20080160623A1 (en) | Method and device for bioanalyte quantification by on/off kinetics of binding complexes | |
| Khodayaribavil | Capillary-driven Microfluidic Biosensing Platforms for Digital Biomolecule Detection | |
| Jeon et al. | Fabrication of multicomponent protein microarrays with microfluidic devices of poly (dimethylsiloxane) | |
| Kumar et al. | Microfluidics-based devices and their role on point-of-care testing | |
| Isa | Highly sensitive coulometric detection of proteins based on metallization |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |