CN113873998A - 脂质体制剂及其使用和制备方法 - Google Patents
脂质体制剂及其使用和制备方法 Download PDFInfo
- Publication number
- CN113873998A CN113873998A CN202080038191.4A CN202080038191A CN113873998A CN 113873998 A CN113873998 A CN 113873998A CN 202080038191 A CN202080038191 A CN 202080038191A CN 113873998 A CN113873998 A CN 113873998A
- Authority
- CN
- China
- Prior art keywords
- mol
- composition
- phospholipid
- salt
- liposome
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
- A61K9/127—Liposomes
- A61K9/1271—Non-conventional liposomes, e.g. PEGylated liposomes, liposomes coated with polymers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7028—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages
- A61K31/7032—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages attached to a polyol, i.e. compounds having two or more free or esterified hydroxy groups, including the hydroxy group involved in the glycosidic linkage, e.g. monoglucosyldiacylglycerides, lactobionic acid, gangliosides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7004—Monosaccharides having only carbon, hydrogen and oxygen atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/10—Alcohols; Phenols; Salts thereof, e.g. glycerol; Polyethylene glycols [PEG]; Poloxamers; PEG/POE alkyl ethers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/24—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing atoms other than carbon, hydrogen, oxygen, halogen, nitrogen or sulfur, e.g. cyclomethicone or phospholipids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
- A61K9/127—Liposomes
- A61K9/1271—Non-conventional liposomes, e.g. PEGylated liposomes, liposomes coated with polymers
- A61K9/1272—Non-conventional liposomes, e.g. PEGylated liposomes, liposomes coated with polymers with substantial amounts of non-phosphatidyl, i.e. non-acylglycerophosphate, surfactants as bilayer-forming substances, e.g. cationic lipids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Diabetes (AREA)
- Engineering & Computer Science (AREA)
- Molecular Biology (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Dispersion Chemistry (AREA)
- Hematology (AREA)
- Obesity (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Organic Chemistry (AREA)
- Endocrinology (AREA)
- Emergency Medicine (AREA)
- Dermatology (AREA)
- Biophysics (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
本公开提供磷酸化碳水化合物替代疗法(CRT),其包括磷酸化碳水化合物和磷脂的组合物,以及制备这种组合物的方法。这种组合物适用于将磷酸化碳水化合物药物递送至细胞内部、内质网和高尔基体,并且可用于治疗CDG I型和CDG II型疾病以及其他代谢障碍。
Description
相关申请的交叉引用
本申请要求2019年3月29日提交的美国临时专利申请号62/826,874的优先权,该临时专利申请通过引用整体并入本申请。
技术领域
本发明涉及包含包封在脂质体中用于递送至细胞内部的碳水化合物的组合物,将包封的碳水化合物递送至细胞的内部的方法,以及使用这种组合物治疗疾病和障碍(例如先天性糖基化障碍(CDG))的方法。例如,本发明涉及制备用于药物递送至细胞内部、内质网(ER)和高尔基体的碳水化合物和脂质体的方法。
背景技术
糖基化,即碳水化合物(聚糖)与蛋白质和脂质的酶促连接,是一种共翻译和翻译后修饰(PTM),其比任何其他PTM更常见,因为它适用于粗面内质网(ER)中合成的大多数蛋白质。糖基化在膜和分泌蛋白的多种生物过程中起着关键作用。在ER中,糖基化定义了所述蛋白质的结构和折叠,并作为一种质量控制机制,指示将正确折叠的蛋白质输出至高尔基体或靶向错误折叠的蛋白质进行降解。聚糖部分还可以作为细胞表面受体的配体以介导细胞附着或刺激信号转导途径。先天性糖基化障碍,也称为CDG综合症,是一组罕见的遗传性疾病,其中组织蛋白和/或脂质携带有缺陷的糖基化和/或缺乏糖基化。这些疾病与多种酶缺乏有关,经常导致神经系统、肌肉、肠和其他几个器官系统的严重的、有时甚至是致命的损伤。
患有CDG的儿童的常见临床症状包括张力减退、发育迟缓、发育不良、肝功能障碍、凝血病、甲状腺功能减退、内斜视、异常脂肪模式和乳头内陷、低血糖、癫痫发作、小脑发育不全和发育迟缓儿童的类似中风的发作。在较大年龄、在青春期或成年期,表现可能包括运动失调、认知障碍、女性缺乏青春期、男性小睾丸、色素性视网膜炎、脊柱侧凸、关节挛缩和周围神经病变。
CDG可分为两类:CDG I型和CDG II型。CDG I型的特征在于在ER中发生的N-连接的蛋白质糖基化的初始步骤(如长醇焦磷酸连接寡糖(DLO)的生物合成)的缺陷,或将DLO转移至新生多肽的天冬酰胺残基上。CDG II型涉及蛋白结合聚糖的进一步加工(合成或水解)的缺陷。目前,已发现22个CDG I型和14个II型变体。CDG最常见的亚型之一是CDG-Ia(约占所有CDG病例的70%),其特征在于磷酸甘露糖变位酶2(PMM)活性的丧失或降低,导致细胞内N-糖基化的缺乏或不足(Jaeken等,J.of Inherit.Met.Disease.2008,31:669-672)。PMM负责将甘露糖-6-磷酸转化为甘露糖-1-磷酸。
尽管已经探索几种不同的方法来开发用于CDG的疗法,但研究人员仍在继续寻找合适的治疗方法或疗法用于减轻疾病本身。现有的治疗方法包括,例如,营养补充剂、管饲和尝试治疗胃食管反流、持续性呕吐、发育迟缓、眼部异常和甲状腺功能减退的多种治疗。患者还需要针对类似中风发作进行静脉内(IV)水化和物理疗法。具有矫形症状的成年人通常需要轮椅、转移装置和脊柱侧凸手术治疗(Sparks等,Disorders of GlycosylationOverview.2005In:Pagon RA,Adam MP,Bird TD等,editors.GeneReviewsTM.Seattle(WA):University of Washington,Seattle;1993-2013)。
目前,CDG-Ib是一种可进行治疗的(即口服D-甘露糖给药)、已知的CDG。然而,这种疗法在治疗CDG-Ia患者时可能不那么有效,并且目前对其他CDG I型亚型和CDG II型疾病的治疗选择有限。CDG-I障碍缺乏既定疗法的原因之一可能是由于存在过多的异质临床表型,其与PMM酶活性无直接相关性。
PMM活性降低的患者产生的甘露糖-1-磷酸(Man-1-P)减少,并伴有多内脏损伤的症状。为了克服PMM产生不足,为下游酶提供所需的底物(即Man-1-P)非常重要。然而,这种全身供应Man-1-P的输送和维持存在问题,因为当通过口服或静脉给药向外递送时,体液中的细胞外酶降解Man-1-P。向外递送Man-1-P的另一个问题是,其高极性阻止Man-1-P渗透到细胞内部(即胞质溶胶),从而治疗PMM产生缺陷。
可以合成极性Man-1-P的衍生物以使Man-1-P更具细胞渗透性(美国专利公开号2009/0054353)。然而,这种方法也存在问题,因为具有细胞渗透性的Man-1-P衍生物已被证明在临床应用中不稳定或通过Man-1-P衍生物的副产物产生细胞毒性(Eklund等,Glycobiology2005,15:1084-1093;Rutschow等,Bioorg Med Chem 2002,10:4043-4049;和Hardre等,Bioorg Med Chem Lett 2007,17:152-155)。
其他潜在的治疗方法集中于通过抑制磷酸甘露糖异构酶(PMI)来抑制分解代谢甘露糖-6-磷酸(Man-6-P,一种Man-1-P的前体)的酶。所述方法集中于促使反应达到最佳体内平衡,而使用PMI抑制剂可能偏向于Man-6-P的产生。然而,由于其相关的毒性、脱靶副作用和选择性组织渗透性差,这些方法作为临床治疗选择无效。
另一种潜在的解决方案是使用递送载体(例如,脂质颗粒)将Man-1-P包封并递送至所述细胞内部(参见WO 2015/053910)。然而,由于磷酸化碳水化合物通常具有较高的电荷和极性,因此最佳的递送载体必须克服稳定性、磷酸化碳水化合物的负载率和浓度、毒性和递送效率的挑战。
因此,对于需要治疗的个体(包括,例如人类),用于将磷酸化碳水化合物(例如Man-1-P和Man-6-P)递送至所述细胞内部以治疗障碍(如先天性糖基化障碍(CDG))的改进组合物和方法存在未满足需求。
发明内容
本公开通过提供包含由某些脂质体包封的磷酸化碳水化合物的组合物和试剂盒满足上述未满足的需求,所述组合物和试剂盒解决了与渗透细胞或使用脂质颗粒包封磷酸化碳水化合物相关的磷酸化碳水化合物负载效率、细胞毒性和稳定性问题。这种磷酸化碳水化合物可以是内源性碳水化合物,包括,例如甘露糖-1-磷酸。通过利用内吞途径,这些脂质体可以进入细胞内部并将磷酸化碳水化合物递送至细胞的胞质溶胶中。使用某些脂质体以包封磷酸化碳水化合物,同时促进疗法的便利性,允许更高剂量的磷酸化碳水化合物到达生化糖基化途径,以及潜在的给药缓和性。在一些方面,本公开提供用于制备由某些脂质体包封的磷酸化碳水化合物的方法,该磷酸化碳水化合物用于药物递送至细胞内部、内质网和高尔基体。本公开提供用于但不限于治疗CDG I型和CDG II型疾病的磷酸化碳水化合物替代疗法。
本公开还解决了与疾病(例如CDG疾病)有效治疗相关的未满足的需求,以及与这种治疗的递送相关的问题。在一些方面,本公开提供一种将磷酸化碳水化合物(如甘露糖-1-磷酸)递送至细胞的胞质溶胶的方法。不希望受任何理论束缚,据信,这种递送所述磷酸化碳水化合物的方法(例如,作为药物的一部分)将绕过遗传缺陷的胞质溶胶酶(即磷酸甘露糖变位酶(PMM)和磷酸甘露糖异构酶(PMI))的作用,这在CDG I障碍中很普遍。
在一些实施方案中,本公开提供一种组合物,其包含脂质体,所述脂质体包含:
i)1,2-二油酰基-sn-甘油-3-磷酸乙醇胺(DOPE);
ii)一种或多种稳定剂,其选自:
(a)一种或多种具有极性头部基团和脂肪酸尾的磷脂,其中所述极性头部基团选自由甘油、胆碱、磷酸和丝氨酸组成的组,所述脂肪酸尾包括C10-28脂族链,或
(b)酸性胆固醇酯,或(a)和(b)的混合物;和
iii)与至少一种磷脂结合的聚乙二醇(PEG);和
至少一种内源性磷酸化碳水化合物,其中至少一种内源性磷酸化碳水化合物包封在所述脂质体内。
在一些实施方案中,所述与PEG结合的至少一种磷脂是1,2-二硬脂酰-sn-甘油-3-磷酸乙醇胺(DSPE)。在一些实施方案中,所述一种或多种稳定剂包含1,2-二油酰基-sn-甘油-3-磷酸胆碱(DOPC)、1,2-二棕榈酰基-磷脂酰基-甘油(DPPG)、1,2-二硬脂酰基-sn-甘油-3-磷酸(DSPA),或1,2-二油酰基-sn-甘油-3-磷酸-L-丝氨酸(DOPS)。在一些实施方案中,DOPE以至多80mol%的浓度存在。在一些实施方案中,所述脂质体进一步包含胆固醇。
在一些实施方案中,本公开提供一种组合物,其包含脂质体,所述脂质体包含:
i)N-十二酰基-1,2-二-(9Z-十八烯酰基)-sn-甘油-3-磷酸乙醇胺(N-C12-DOPE);和
ii)1,2-二油酰基-sn-甘油-3-磷酸胆碱(DOPC);和
至少一种磷酸化内源性碳水化合物,至少一种内源性碳水化合物包封在所述脂质体内。
在一些实施方案中,所述脂质体进一步包含与至少一种磷脂结合的PEG。在一些实施方案中,所述与PEG结合的至少一种磷脂是1,2-二硬脂酰-sn-甘油-3-磷酸乙醇胺(DSPE)。在一些实施方案中,所述脂质体进一步包含胆固醇。
在一些实施方案中,所述至少一种内源性磷酸化碳水化合物是磷酸化单糖、磷酸化二糖、磷酸化寡糖、磷酸化多糖、磷酸化甘露糖、磷酸化甘露呋喃糖、磷酸化甘露吡喃糖或核苷酸糖,或其任何组合。在一些实施方案中,所述至少一种内源性磷酸化碳水化合物是磷酸化甘露糖。在一些实施方案中,所述磷酸化甘露糖是甘露糖-1-磷酸。在一些实施方案中,所述磷酸化甘露糖是甘露糖-6-磷酸。在一些实施方案中,所述内源性磷酸化碳水化合物以约0.1-75mM的浓度存在。
本公开其他方面还涉及一种药物组合物,其包含任何上述实施方案的组合物,和药学上可接受载体。
本公开其他方面涉及一种试剂盒,其包含用于本文所述的任何方法中的任何上述实施方案的组合物。
本公开其他方面涉及一种通过将任何上述实施方案的组合物给药于个体以将磷酸化碳水化合物递送至有需要的个体的方法。在一些实施方案中,所述组合物经口、局部、经皮、经鼻、静脉内、肌肉内、腹膜内、脑脊髓内、颅内、脊髓内、皮下、关节内、滑膜内或鞘内给药。
本公开其他方面涉及一种通过将任何上述实施方案的组合物给药于个体以将磷酸化碳水化合物递送至有需要个体的细胞内部的方法。在一些实施方案中,所述组合物经口、局部、经皮、经鼻、静脉内、肌肉内、腹膜内、脑脊髓内、颅内、脊髓内、皮下、关节内、滑膜内或鞘内给药。
本公开其他方面涉及一种通过将任何上述实施方案的组合物给药于个体以治疗有需要个体的先天性糖基化障碍(CDG)的方法。在一些实施方案中,先天性糖基化障碍(CDG)选自CDG I型障碍、CDG-Ia障碍、CDG II型障碍、CDG-IIc障碍和CDG-IIf障碍。在一些实施方案中,先天性糖基化障碍(CDG)是CDG-1a障碍。在一些实施方案中,所述组合物经口、局部、经皮、经鼻、静脉内、肌肉内、腹膜内、脑脊髓内、颅内、脊髓内、皮下、关节内、滑膜内或鞘内给药。
附图说明
通过参考以下描述并结合包括在说明书中的附图,可以更好地理解本申请。
图1描述了生理条件下的体外M1P渗漏概况;n=3。
图2A描述了Lipo-M1P在磷酸盐缓冲盐水(PBS)溶液pH 7.4中的聚集概况,其尺寸分布在纳米范围内。图2B描述了PBS pH 7.4中Lipo-M1P的微米级颗粒的浓度。
图3A和3B描述了Lipo-M1P在PMM2-CDG成纤维细胞中的生物活性。Lipo-M1P剂量反应研究见图3A。在剂量反应研究中测试的浓度下,Lipo-M1P的细胞活性见图3B。
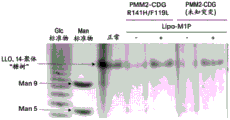
图4描述了在使用Lipo-M1P治疗前后,来自两名患者的正常成纤维细胞和PMM2-CDG成纤维细胞中的LLO的FACE凝胶。
图5描述了未经治疗和使用不同浓度的Lipo-M1P治疗的正常和PMM2-CDG成纤维细胞中的ICAM-1的蛋白质印迹。
图6A描述了Lipo-M1P在肝脏中的分布,以总剂量的百分比表示。图6B描述了肝细胞和NPC对脂质体的吸收。
具体实施方式
本公开基于本发明人的发现,即某些脂质体组合物能够有效地包封磷酸化碳水化合物并将磷酸化碳水化合物递送至细胞内部。本发明提供由这些脂质体包封的磷酸化碳水化合物的组合物,其能够将磷酸化碳水化合物递送至细胞内部,包括,例如细胞质、内质网和高尔基体。在一些实施方案中,所述磷酸化碳水化合物是甘露糖-1-磷酸或甘露糖-6-磷酸。本发明还提供药物组合物和包含这些组合物的试剂盒。本发明还提供通过将这种组合物给药于个体以将磷酸化碳水化合物递送至细胞内部或治疗有需要的个体的先天性糖基化障碍(CDG)的方法。
高负电荷和高极性通常使得磷酸化碳水化合物难以通过所述脂质体的膜。该困难会限制将磷酸化碳水化合物包封到所述脂质体中的方法和时间。
除非另有定义,所有科学和技术术语应理解为具有其所属领域中常用的相同含义。为了本公开的目的,定义以下术语。
本文使用的术语“约”指本技术领域技术人员容易知晓的相应值的通常误差范围。本文提及的“约”值或参数包括(并描述)涉及该值或参数本身的实施方案。例如,“约x”包括并描述“x”本身。在一些实施方案中,术语“约”在与测量相关使用时,或用于修饰值、单位、常数或数值范围时,指+/-2%的变化。
本文提及的“之间”两个值或参数包括(并描述)包含这两个值或参数本身的实施方案。例如,提及“在x和y之间”的描述包括对“x”和“y”本身的描述。此外,还应理解,“在x和y之间”也可表示为“约x至y”或“约x-y”。
如本文所用,摩尔百分比也称为“mol%”。
除非上下文另有明确说明,否则如本文所用的单数形式“一个”、“一种”和“所述”包括复数形式。
组合物
本发明提供组合物,其包含一种脂质体,所述脂质体包含一种或多种脂质颗粒和至少一种磷酸化碳水化合物,其中所述至少一种磷酸化碳水化合物包封在所述脂质体中。
脂质体
在一些实施方案中,所述脂质体是由层状相脂质双层组成的囊泡。可使用本领域已知的任何合适的脂质体。在一些实施方案中,所述脂质体具有层状纳米结构。
本公开的脂质体可通过本领域已知的和本文公开的任何合适的方法制备。制备脂质体的合适方法的示例包括,例如通过机械分散(包括超声处理、薄膜水化、乳液、法式压力池、挤出和干燥囊泡的重建)破坏生物膜;溶剂分散,包括乙醇注射、乙醚注射、双重乳液、反相和气化;和清洁剂去除法。
在某些实施方案中,所述脂质体是可以免疫耐受的隐形脂质体。在一些实施例中,隐形脂质体是能够避免被个体的免疫系统检测的脂质体。因此,隐形脂质体可以是免疫耐受的。例如,个体可能是人。
当活性剂或治疗剂(例如本公开的碳水化合物)包封在脂质体中时,所述脂质体提供完全包封、部分包封或两者的这种活性剂或治疗剂。在一些变型中,至少一部分碳水化合物可以包封在脂质体中并位于脂质体的核心和/或脂质体的内表面(例如膜)内。或者,在其他变型中,整个碳水化合物可包封在脂质体中,并位于脂质体的核心和/或脂质体的内表面(例如膜)内。
本公开的脂质体包含一种或多种脂质。在一些实施方案中,所述脂质包含生物或合成来源的物质,该物质可溶于或部分可溶于有机溶剂,或当存在于水相中时,该物质可分配到疏水环境中。在一些变型中,脂质可分为至少三类:(1)简单脂质,其包括,例如脂肪、油和蜡;(2)复合脂质,其包括,例如磷脂和糖脂;和(3)衍生脂质,其包括,例如类固醇。
在一些变型中,所述脂质可以是中性脂质或两亲性脂质。在一些实施方案中,中性脂质是在选定的pH值下以不带电或中性两性离子形式存在的脂质。在生理pH值下,这种脂质可以包括,例如二酰基磷脂酰胆碱、二酰基磷脂酰乙醇胺、神经酰胺、鞘磷脂、脑磷脂、胆固醇、脑苷脂和二酰基甘油。在一些实施方案中,两亲性脂质是同时包含极性、水溶性基团和非极性、水不溶性基团的脂质。
合适的脂质包括,例如,双层形成脂质、非双层形成脂质、两亲性脂质、天然存在的脂质、磷脂、甘油脂、鞘脂、磷脂酰甘油、磷脂酸、溶血脂质、脂肪酸、鞘磷脂、鞘糖脂、葡萄糖脂、糖脂、硫酯、具有醚连接和酯连接脂肪酸的脂质、可聚合脂质、合成脂质和半合成脂质。合成或半合成脂质可通过天然脂质的脱酰化或再酰化制备。合成和半合成脂质的合适特征包括,例如肉豆蔻酰基、棕榈酰基和硬脂酰基脂肪酸。在一些实施方案中,其中所述脂质包含一种或多种酯连接脂肪酸,所述脂肪酸是肉豆蔻酰基脂肪酸。在某些实施方案中,所述脂质是1,2-二肉豆蔻酰基-甘油(DMG)或其盐。在其他实施方案中,其中所述脂质包含一种或多种酯连接脂肪酸,所述脂肪酸是硬脂酰基脂肪酸。在某些实施方案中,所述脂质是1,2-二硬脂酰基甘油(DSG)或其盐。在一些实施方案中,本公开的脂质体可以包含两种或多种类型的脂质的混合物。这种混合物可以以适合于包封本公开的碳水化合物并将这种碳水化合物递送至细胞内部的任何比例存在。在一些实施方案中,本公开的脂质体可以包含选自磷脂、甘油脂、鞘脂及其任何组合的脂质。如本文所公开的,这种脂质具有可通过例如酯键或醚键连接的极性头部基团和脂肪酸尾。
在一些实施方案中,本公开的脂质体可以包含一种或多种具有极性头部基团的脂质。所述脂质可以包含本领域已知的任何合适的极性头部基团。合适的极性头部基团包括,例如胆碱、乙醇胺、丝氨酸、甘油、肌醇及其任何组合。
在一些实施方案中,本公开的脂质体可以包含一种或多种磷脂。本公开的脂质体可以包含本领域已知的任何合适的磷脂。合适的磷脂包括,例如,磷脂酰胆碱(PC)、磷脂酰乙醇胺(PE)、磷脂酰丝氨酸(PS)、磷脂酰甘油(PG)、磷脂酰肌醇(PI)及其任何组合。在一些实施方案中,本公开的脂质体可以包含磷脂酰胆碱(PC)。在一些实施方案中,本公开的脂质体可以包含磷脂酰乙醇胺(PE)。在某些实施方案中,本公开的脂质体可以包含磷脂酰胆碱(PC)和磷脂酰乙醇胺(PE)。
在一些实施方案中,所述磷脂包含两个疏水性脂肪酸尾。在一些实施方案中,每个脂肪酸尾包含脂族链。在一些实施方案中,所述两个脂肪酸尾是相同的。在一些实施方案中,所述两种脂肪酸尾是不同的。在一些实施方案中,所述脂族链是不饱和的。在一些实施方案中,所述脂族链是饱和的。在一些实施方案中,所述脂族链选自由任选取代的烷基、任选取代的链基和任选取代的炔基组成的组。在一些实施方案中,所述烷基是直链的。在一些实施方案中,每个脂肪酸链是未取代的C4-28烷基。在一些实施方案中,每个脂肪酸链是取代基取代的C4-28烷基,所述取代基选自由酰基、羟基、环烷基、烷氧基、酰氧基、氨基、氨酰基、硝基、卤素、硫醇、硫代烷基、烷基、烯基、炔基和杂环基组成的组。在一些实施方案中,每个脂肪酸链是未取代的C4-28烯基。在一些实施方案中,所述烯基是直链或支链的。在一些实施方案中,每个脂肪酸链具有一个或多个双键。在一些实施方案中,所述双键具有顺式结构。在一些实施方案中,所述双键具有反式结构。在一些实施方案中,每个脂肪酸链是取代基取代的C4-28烯基,所述取代基选自由酰基、羟基、环烷基、烷氧基、酰氧基、氨基、氨酰基、硝基、卤素、硫醇、硫代烷基、烷基、烯基、炔基和杂环基组成的组。在一些实施方案中,每个脂肪酸链选自由任选取代的C10-28烷基、任选取代的C10-28烯基和任选取代的C10-28炔基组成的组。合适的磷脂包括,例如,1,2-二油酰基-sn-甘油-3-磷酸乙醇胺(DOPE)、1,2-二油酰基-sn-甘油-3-磷酸胆碱(DOPC)、1,2-二棕榈酰基-磷脂酰基-甘油(DPPG)、1,2-二油酰基-sn-甘油-3-磷酸甘油(DOPG)、1,2-二硬脂酰基-sn-甘油-3-磷酸(DSPA)、1,2-二油酰基-sn-甘油-3-磷酸-L-丝氨酸(DOPS)、1,2-二硬脂酰-sn-甘油-3-磷酸乙醇胺(DSPE)、N-十二酰基-1,2-二-(9Z-十八烯酰基)-sn-甘油-3-磷酸乙醇胺(N-C12-DOPE)或其盐,或上述的任何组合。
通常应当理解,在本领域中,DPPG通常也称为1,2-二棕榈酰基-sn-甘油-3-磷酸-(1’-rac-甘油);在本领域中,DOPG通常也称为1,2-二油酰基-sn-甘油-3-磷酸-(1’-rac-甘油);并且在本领域中,N-C12-DOPE通常也称为(2R)-5-羟基-2-{[(9Z)-十八-9-烯酰基]氧基}-5,10-二氧代-4,6-二氧杂-9-氮杂-5λ(5)-磷二十一烷-1-基(9Z)-十八-9-烯酸酯。
在一种变型中,所述磷脂是:
在一些实施方案中,所述一种或多种磷脂以至多约10mol%、约15mol%、约20mol%、约25mol%、约30mol%、约35mol%、约40mol%、约45mol%、约50mol%、约55mol%、约60mol%、约65mol%、约70mol%、约75mol%、约80mol%、约85mol%,或约90mol%的量存在。在一些实施方案中,所述一种或多种磷脂以至少5mol%、至少10mol%、至少15mol%、至少20mol%、至少25mol%、至少30mol%、至少35mol%、至少40mol%、至少45mol%、至少50mol%、至少55mol%、至少60mol%、至少65mol%、至少70mol%,或至少75mol%的量存在。
在一些实施方案中,所述脂质体进一步包含在给药于个体时能够最小化脂质颗粒的降解和/或增强所述脂质颗粒的保留,和/或在给药于个体时使所述脂质颗粒免疫耐受的分子。在一些实施方案中,所述分子是隐形分子,例如氧化乙烯、氧化乙烯低聚体、氧化乙烯聚合物、聚乙二醇(PEG),或其任何组合;和/或PEG化的中性脂质。应当理解,在一些变型中,所述PEG化的中性脂质可能在生理条件下带电。
在一些实施方案中,所述PEG化脂质是具有酯连接脂肪酸的脂质。在某些实施方案中,所述PEG化脂质是分子式(X):的脂质,或其盐,其中每个Ry独立地是碳链。在一些实施方案中,每个Ry独立地是不饱和碳链。在其他实施方案中,每个Ry独立地是饱和碳链。在某些实施方案中,每个Ry独立地是C10-28烷基。在一个实施方案中,所述PEG化脂质的脂质是1,2-二肉豆蔻酰基-甘油(DMG)。在一个实施方案中,所述PEG化脂质是PEG(2k)-DMG,也称为DMG-PEG2000。在一个实施方案中,所述PEG化脂质是:或其盐。在另一个实施方案中,所述PEG化脂质的脂质是1,2-二硬脂酰甘油(DSG)。在一个实施方案中,PEG化脂质是PEG(2k)-DSG,也称为DSG-PEG2000。在一个实施方案中,所述PEG化脂质是或其盐。
在其他实施方案中,至少一种磷脂与聚乙二醇(PEG)结合。在一些实施方案中,一种磷脂与PEG结合。所述PEG可以与一种或多种磷脂酰胆碱(PC)、磷脂酰乙醇胺(PE)、磷脂酰丝氨酸(PS)、磷脂酰甘油(PG)、磷脂酰肌醇(PI)及其任何组合结合。在某些实施方案中,本公开的脂质颗粒可以包含与磷脂酰胆碱(PC)结合的PEG。在一些实施方案中,与PEG结合的磷脂是1,2-二油酰基-sn-甘油-3-磷酸乙醇胺(DOPE)、1,2-二油酰基-sn-甘油-3-磷酸胆碱(DOPC)、1,2-二棕榈酰基-磷脂酰基-甘油(DPPG)、1,2-二油酰基-sn-甘油-3-磷酸甘油(DOPG)、1,2-二硬脂酰基-sn-甘油-3-磷酸(DSPA)、1,2-二油酰基-sn-甘油-3-磷酸L-丝氨酸(DOPS),或1,2-二硬脂酰基-sn-甘油-3-磷酸乙醇胺(DSPE),或其盐。在一些实施方案中,与PEG结合的磷脂是1,2-二硬脂酰基-sn-甘油-3-磷酸乙醇胺(DSPE)或其盐。在一些实施方案中,PEG化磷脂是DSPE-PEG。在一些实施方案中,PEG化磷脂是DSPE-PEG2000。在一些实施方案中,所述DSPE-PEG进一步与碳水化合物结合。在某些实施方案中,DSPE-PEG进一步与单糖结合。在一些实施方案中,DSPE-PEG进一步与半乳糖部分结合。在某些实施方案中,DSPE-PEG-半乳糖具有以下结构:
在一些实施方案中,聚乙二醇(PEG)可以以约0.5mol%至约20mol%的浓度存在于本公开的脂质体中。在一些实施方案中,PEG可以以约0.5mol%、约1mol%、约2mol%、约3mol%、约4mol%、约5mol%、约6mol%、约7mol%、约8mol%、约9mol%、约10mol%、约11mol%、约12mol%、约13mol%、约14mol%、约15mol%、约16mol%、约17mol%、约18mol%、约19mol%,或约20mol%的浓度存在于本公开的脂质体中。在一些实施方案中,PEG可以以至少约0.5mol%、至少约1mol%、至少约2mol%、至少约3mol%、至少约4mol%、至少约5mol%、至少约6mol%、至少约7mol%、至少约8mol%、至少约9mol%、至少约10mol%、至少约11mol%、至少约12mol%、至少约13mol%、至少约14mol%、至少约15mol%、至少约16mol%、至少约17mol%、至少约18mol%、至少约19mol%,或至少约20mol%;或0.5mol%至50mol%、0.5mol%至40mol%、0.5mol%至30mol%,或0.5mol%至20mol%的浓度存在于本公开的脂质体中。在某些实施方案中,与聚乙二醇(PEG)结合的磷脂可以以约3mol%的浓度存在于本公开的脂质体中。在某些实施方案中,与聚乙二醇(PEG)结合的磷脂可以以约5mol%的浓度存在于本公开的脂质体中。
在一些实施方案中,聚乙二醇(PEG)可以以约200Da至约40,000Da的分子量存在于本公开的脂质体中。在一些实施方案中,聚乙二醇(PEG)可以以约200Da至约10,000Da的分子量存在于本公开的脂质体中。在一些实施方案中,聚乙二醇(PEG)可以以200Da、约300Da、约400Da、约500Da、约600Da、约700Da、约800Da、约900Da、约1,000Da、约1,500Da、约2,000Da、约2,500Da、约3,000Da、约3,500Da、约4,000Da、约4,500Da、约5,000Da、约5,500Da、约6,000Da、约6,500Da、约7,000Da、约7,500Da、约8,000Da、约8,500Da、约9,000Da、约9,500Da,或约10,000Da;或约200Da至约10,000Da的分子量存在于本公开的脂质体中。
在一些实施方案中,所述脂质体进一步包含一种或多种固醇。在一些实施方案中,所述一种或多种固醇包含一种或多种中性固醇。在其他实施方案中,所述一种或多种固醇包含一种或多种带电固醇。在其他实施方案中,所述一种或多种固醇包括中性固醇和带电固醇的组合。合适的磷脂包括,例如,胆固醇和胆固醇半琥珀酸酯(CHEMS)、双十六烷基磷酸酯和Solulan C24。在一些实施方案中,所述一种或多种带电的固醇包含CHEMS。在其他实施方案中,所述脂质体进一步包含胆固醇,在此也称为“Chol”。在一种变型中,所述脂质体进一步包含:或其盐。
在一些实施方案中,本公开的固醇(如胆固醇或CHEMS)可以以至多约5mol%、约10mol%、约15mol%、约20mol%、约30mol%、约40mol%,或约50mol%;或至少5mol%、至少10mol%、至少15mol%、至少20mol%、至少25mol%、至少30mol%、至少35mol%,或至少40mol%;或5mol%至50mol%的浓度存在于本公开的脂质体中。在某些实施方案中,本公开的固醇(如胆固醇或CHEMS)可以以至多15mol%的浓度存在于本公开的脂质体中。在某些实施方案中,本公开的固醇(如胆固醇或CHEMS)可以以约3mol%、约5mol%、约20mol%或约30mol%的浓度存在于本公开的脂质体中。在一些实施方案中,本公开的固醇(如胆固醇或CHEMS)可以以1:1或2:1的摩尔比存在于本公开的脂质体中。
在一些实施方案中,本公开的脂质体的平均颗粒尺寸范围为直径约0.02微米至约0.5微米。在某些实施方案中,本公开的脂质体的平均颗粒尺寸为直径约0.02微米、约0.03微米、约0.04微米、约0.05微米、约0.06微米、约0.07微米、约0.08微米、约0.09微米、约0.1微米、约0.15微米、约0.2微米、约0.25微米、约0.3微米、约0.35微米、约0.4微米、约0.45微米,或约0.5微米。在一些实施方案中,本公开的脂质体的平均颗粒尺寸为约0.025微米至约0.25微米。在一些实施方案中,本公开的脂质体的平均颗粒尺寸为约0.025微米至约0.05微米、约0.05微米至约0.1微米、约0.1微米至约0.2微米、约0.2微米至约0.3微米、约0.3微米至约0.4微米、约0.4微米至约0.5微米,或约0.04微米至约0.22微米。
在一个方面,所述脂质体包含:
i)至少一种具有乙醇胺头部基团和不饱和脂肪酸尾的磷脂,其中所述不饱和脂肪酸尾包含至少一个C10-28碳链;
ii)一种或多种(a)至(c):
a)至少一种具有极性头部基团和饱和脂肪酸尾的磷脂,
b)至少一种具有极性头部基团和不饱和脂肪酸尾基的磷脂,其中所述极性头部基团包括季铵阳离子、甘油基团或丝氨酸基团,并且
c)至少一种酸性胆固醇酯或胆固醇;和
iii)聚乙二醇(PEG),其中所述PEG与至少一种磷脂结合。
在一些实施方案中,所述脂质体的i)中的不饱和脂肪酸尾选自由任选取代的C10-28烯基和任选取代的C10-28炔基组成的组。在一些实施方案中,每个脂肪酸链是未取代的C10-28烯基。在一些实施方案中,所述烯基是直链或支链的。在一些实施方案中,每个脂肪酸链具有一个或多个双键。在一些实施方案中,每个双键具有顺式结构。在一些实施方案中,每个双键具有反式结构。在一些实施方案中,每个脂肪酸链是取代基取代的C10-28烯基,所述取代基选自由酰基、羟基、环烷基、烷氧基、酰氧基、氨基、氨酰基、硝基、卤素、硫醇、硫代烷基、烷基、烯基、炔基和杂环基组成的组。在一些实施方案中,所述脂质体的i)中至少一种具有乙醇胺头部基团和不饱和脂肪酸尾的磷脂是1,2-二油酰基-sn-甘油-3-磷酸乙醇胺(DOPE)或其盐。在一种变型中,所述脂质体的i)中至少一种具有乙醇胺头部基团和不饱和脂肪酸尾的磷脂是:
在一些实施方案中,i)中的至少一种具有乙醇胺头部基团和不饱和脂肪酸尾的磷脂以至多约15mol%、约20mol%、约25mol%、约30mol%、约35mol%、约40mol%、约45mol%、约50mol%、约55mol%、约60mol%、约65mol%、约70mol%、约75mol%、约80mol%、约85mol%,或约90mol%的量存在。在一些实施方案中,i)中的至少一种具有乙醇胺头部基团和不饱和脂肪酸尾的磷脂以至少约10mol%、至少约20mol%、至少约30mol%、至少约40mol%、至少约50mol%、至少约60mol%、至少约70mol%,或至少约80mol%;或约10mol%至80mol%的量存在。在一些实施方案中,i)中的至少一种具有乙醇胺头部基团和不饱和脂肪酸尾的磷脂以约10-20mol%、约20-30mol%、约30-40mol%、约40-50mol%、约50-60mol%、约60-70mol%、约70-80mol%、约10-30mol%、约30-50mol%、约50-80mol%、约10-50mol%或约40-80mol%的量存在。
在一些实施方案中,所述脂质体的ii)a)中的极性头部基团选自由甘油、胆碱、磷酸和丝氨酸组成的组。在一些实施方案中,所述脂质体的ii)a)中的极性头部基团是胆碱。在一些实施方案中,所述饱和脂肪酸尾是任选取代的烷基。在一些实施方案中,所述饱和脂肪酸尾是未取代的C4-28烷基。在一些实施方案中,所述饱和脂肪酸尾是取代基取代的C4-28烷基,所述取代基选自由酰基、羟基、环烷基、烷氧基、酰氧基、氨基、氨酰基、硝基、卤素、硫醇、硫代烷基、烷基、烯基、炔基和杂环基组成的组。在一些实施方案中,所述脂质体的ii)a)中的至少一种具有极性头部基团和饱和脂肪酸尾的磷脂是1,2-二棕榈酰基-磷脂酰基-甘油(DPPG)、1,2-二硬脂酰基-sn-甘油-3-磷酸(DSPA)、1,2-二硬脂酰基-sn-甘油-3-磷酸乙醇胺(DSPE)或1,2-二硬脂酰基-sn-甘油-3-磷酸胆碱(DSPC)或其盐。在一种变型中,所述脂质体的ii)a)中的至少一种具有极性头部基团和饱和脂肪酸尾的磷脂是:
在一些实施方案中,所述脂质体的ii)b)中的不饱和脂肪酸尾选自由任选取代的烯基和任选取代的炔基组成的组。在一些实施方案中,所述脂质体的ii)b)中的不饱和脂肪酸尾是未取代的C10-28烯基。在一些实施方案中,所述烯基是直链或支链的。在一些实施方案中,所述脂质体的ii)b)中的不饱和脂肪酸尾具有一个或多个双键。在一些实施方案中,每个双键具有顺式结构。在一些实施方案中,每个双键具有反式结构。在一些实施方案中,所述脂质体的ii)b)中的不饱和脂肪酸尾是未取代的C10-28烯基。在一些实施方案中,所述脂质体的ii)b)中的不饱和脂肪酸尾是取代基取代的C10-28烯基,所述取代基选自由酰基、羟基、环烷基、烷氧基、酰氧基、氨基、氨酰基、硝基、卤素、硫醇、硫代烷基、烷基、烯基、炔基和杂环基组成的组。合适的磷脂包括,例如1,2-二油酰基-sn-甘油-3-磷酸胆碱(DOPC)、1,2-二油酰基-sn-甘油-3-磷酸甘油(DOPG)和1,2-二油酰基-sn-甘油-3-磷酸-L-丝氨酸(DOPS)或其盐。在一种变型中,所述磷脂是:
在一些实施方案中,所述脂质体的ii)中的一种或多种a)-c)以至多约5mol%、约10mol%、约15mol%、约20mol%、约25mol%、约30mol%、约35mol%、约40mol%、约45mol%、约50mol%、约55mol%、约60mol%、约65mol%或约70mol%的量存在。在一些实施方案中,所述脂质体的ii)中的一种或多种a)-c)以至少约5mol%、至少约10mol%、至少约15mol%、至少约20mol%、至少约25mol%、至少约30mol%、至少约35mol%、至少约40mol%、至少约45mol%、至少约50mol%、至少约55mol%,或至少约60mol%的量存在。在一些实施方案中,所述脂质体的ii)中的一种或多种a)-c)以约5-10mol%、约10-15mol%、约15-20mol%、约20-25mol%、约25-30mol%、约30-35mol%、约35-40mol%、约40-45mol%、约45-50mol%、约50-55mol%、约55-60mol%、约60-65mol%、约65-70mol%、约5-25mol%、约25-50mol%,或约50-70mol%的量存在。
在一些实施方案中,与PEG结合的至少一种磷脂是磷脂酰胆碱(PC)、磷脂酰乙醇胺(PE)、磷脂酰丝氨酸(PS)、磷脂酰甘油(PG)或磷脂酰肌醇(PI)。在一些实施方案中,这种磷脂是1,2-二油酰基-sn-甘油-3-磷酸乙醇胺(DOPE)、1,2-二油酰基-sn-甘油-3-磷酸胆碱(DOPC)、1,2-二棕榈酰基-磷脂酰基-甘油(DPPG)、1,2-二油酰基-sn-甘油-3-磷酸甘油(DOPG)、1,2-二硬脂酰基-sn-甘油-3-磷酸(DSPA)、1,2-二油酰基-sn-甘油-3-磷酸-L-丝氨酸(DOPS),或1,2-二硬脂酰基-sn-甘油-3-磷酸乙醇胺,或其盐。在一些实施方案中,这种磷脂是1,2-二硬脂酰基-sn-甘油-3-磷酸乙醇胺(DSPE),或其盐。
在一种变型中,与PEG结合的磷脂是:
在一些实施方案中,所结合的PEG以约0.5mol%至约20mol%的浓度存在于所述脂质体中。在一些实施方案中,所结合的PEG以约0.5mol%、约1mol%、约2mol%、约3mol%、约4mol%、约5mol%、约6mol%、约7mol%、约8mol%、约9mol%、约10mol%、约11mol%、约12mol%、约13mol%、约14mol%、约15mol%、约16mol%、约17mol%、约18mol%、约19mol%,或约20mol%;或约0.5至20mol%的浓度存在于所述脂质体中。在某些实施方案中,所结合的PEG以约3mol%的浓度存在于所述脂质体中。在某些实施方案中,所结合的PEG以约5mol%的浓度存在于所述脂质体中。
在一些实施方案中,所述DOPE以约0-80mol%、约10-80mol%、约20-80mol%,或约30-80mol%、约10-70mol%、约20-70mol%、约30-70mol%、约30-60mol%、约40-60mol%、约30-35mol%、约35-40mol%、约40-45mol%、约45-50mol%的量存在于所述脂质体组合物中。在一些变型中,所述DOPE以约0-30mol%、约5-30mol%、约10-30mol%、约15-30mol%、约20-30mol%,或约25-30mol%的量存在。在其他变型中,所述DOPE以约0-5mol%、约0-10mol%、约0-15mol%、约0-20mol%,或约0-25mol%的量存在。
在一些实施方案中,所述脂质体组合物包含N-C12-DOPE。在一些实施方案中,N-C12-DOPE以约0-80mol%、约60-80mol%、约65-80mol%、约70-80mol%,或约75-80mol%的量存在。在其他实施方案中,N-C12-DOPE以约60-65mol%、约65-70mol%、约70-75mol%,或约75-80mol%的量存在。
在一些实施方案中,所述DOPC以约0-75mol%、约10-75mol%、约35-75mol%、约35-70mol%、约35-65mol%、约35-60mol%、约35-55mol%,或约35-50mol%的量存在。在其他实施方案中,所述DOPC以约10-15mol%、约15-20mol%、约20-25mol%、约25-30mol%、约30-35mol%、约35-40mol%、约40-45mol%、约45-50mol%、约50-55mol%、约55-60mol%,或约60-65mol%的量存在。
在一些实施方案中,所述DSPE-PEG以约0-20mol%、约0-10mol%、约0-9mol%、约0-8mol%、约0-7mol%、约0-6mol%、约0-5mol%,或约0-4mol%的量存在。在其他实施方案中,DSPE-PEG以约0.1-10mol%、约0.1-6mol%,或约0.1-4mol%的量存在。
在一些实施方案中,所述脂质体组合物进一步包含固醇。在一些实施方案中,所述固醇是胆固醇。在其他实施方案中,所述固醇是CHEMS。在某些实施方案中,所述固醇以约0-50mol%、约0-45mol%、约0-40mol%、约30-40mol%、约0-25mol%、约0-20mol%、约0-15mol%、约0-10mol%、约0-7mol%、约0-6mol%,或约0-5mol%的量存在。在其他实施方案中,所述固醇以约5-10mol%、约10-15mol%、约15-20mol%、约20-25mol%,或约25-30mol%的量存在。在其他实施方案中,所述固醇以约5-20mol%的量存在。
在一些实施方案中,所述脂质体组合物包含DOPE、DOPC和DSPE-PEG。在某些实施方案中,所述DSPE-PEG是DSPE-PEG350-2000、DSPE-PEG350-5000、DSPE-PEG350-10000或DSPE-PEG350-40000;或DSPE-PEG1000、DSPE-PEG2000、DSPE-PEG5000或DSPE-PEG10000。在其他实施方案中,所述脂质体组合物进一步包含N-C12-DOPE。在其他实施方案中,所述脂质体组合物进一步包含胆固醇。在其他实施方案中,所述脂质体组合物进一步包含CHEMS。
在一些实施方案中,所述脂质体组合物包含N-C12-DOPE、DOPC和DOPE-PEG。在某些实施方案中,所述DSPE-PEG是DSPE-PEG350-2000、DSPE-PEG350-5000、DSPE-PEG350-10000或DSPE-PEG350-40000;或DSPE-PEG1000、DSPE-PEG2000、DSPE-PEG5000或DSPE-PEG10000。在其他实施方案中,所述脂质体组合物进一步包含DOPE。在其他实施方案中,所述脂质体组合物进一步包含胆固醇。
应当理解,本文所述的任何脂质体组合物中列出的每种组分可以以所述量的任何组合存在。
在一个方面,所述脂质体包含:
i)1,2-二油酰基-sn-甘油-3-磷酸乙醇胺(DOPE)或其盐;
ii)一种或多种稳定剂,其选自
(a)一种或多种具有极性头部基团和脂肪酸尾的磷脂,其中所述极性头部基团选自由甘油、胆碱、磷酸和丝氨酸组成的组,所述脂肪酸尾包括C10-28脂族链,或
(b)酸性胆固醇酯,或(a)和(b)的混合物;和
iii)与至少一种磷脂结合的PEG。
在一种变型中,所述脂质体包含:
ii)一种或多种稳定剂,其选自
(a)一种或多种具有极性头部基团和脂肪酸尾的磷脂,其中所述极性头部基团选自由甘油、胆碱、磷酸和丝氨酸组成的组,所述脂肪酸尾包括C10-28脂族链,或
(b)酸性胆固醇酯,或(a)和(b)的混合物;和
iii)与至少一种磷脂结合的PEG。
在一些实施方案中,i)中的DOPE以至多约15mol%、约20mol%、约25mol%、约30mol%、约35mol%、约40mol%、约45mol%、约50mol%、约55mol%、约60mol%、约65mol%、约70mol%、约75mol%、约80mol%、约85mol%,或约90mol%的量存在。在一些实施方案中,i)中的DOPE以至少约10mol%、至少约20mol%、至少约30mol%、至少约40mol%、至少约50mol%、至少约60mol%、至少约70mol%或至少约80mol%的量存在。在一些实施方案中,i)中的DOPE以约10-20mol%、约20-30mol%、约30-40mol%、约40-50mol%、约50-60mol%、约60-70mol%、约70-80mol%、约10-30mol%、约30-50mol%、约50-80mol%、约10-50mol%,或约40-80mol%的量存在。
在一些实施方案中,所述脂质体的ii)a)中的C10-28脂族链是不饱和的。在一些实施方案中,所述脂质体的ii)a)中的C10-28脂族链是饱和的。在一些实施方案中,所述脂质体的ii)a)中的C10-28脂族链选自由任选取代的C10-28烷基、任选取代的C10-28烯基和任选取代的C10-28炔基组成的组。在一些实施方案中,C10-28烷基是直链或支链的。在一些实施方案中,所述脂质体的ii)a)中的C10-28脂族链是未取代的C10-28烷基。在一些实施方案中,所述脂质体的ii)a)中的C10-28脂族链是取代基取代的C10-28烷基,所述取代基选自由酰基、羟基、环烷基、烷氧基、酰氧基、氨基、氨酰基、硝基、卤素、硫醇、硫代烷基、烷基、烯基、炔基和杂环基组成的组。在一些实施方案中,所述脂质体的ii)a)中的C10-28脂族链是未取代的C10-28烯基。在一些实施方案中,所述烯基是直链或支链的。在一些实施方案中,所述脂质体的ii)a)中的C10-28脂族链具有一个或多个双键。在一些实施方案中,每个双键具有顺式结构。在一些实施方案中,每个双键具有反式结构。在一些实施方案中,所述脂质体的ii)a)中的C10-28脂族链是取代基取代的C10-28烯基,所述取代基选自由酰基、羟基、环烷基、烷氧基、酰氧基、氨基、氨酰基、硝基、卤素、硫醇、硫代烷基、烷基、烯基、炔基和杂环基组成的组。合适的磷脂包括,例如1,2-二油酰基-sn-甘油-3-磷酸胆碱(DOPC)、1,2-二棕榈酰基-磷脂酰基-甘油(DPPG)、1,2-二油酰基-sn-甘油-3-磷酸甘油(DOPG)、1,2-二硬脂酰基-sn-甘油-3-磷酸(DSPA)、1,2-二油酰基-sn-甘油-3-磷酸-L-丝氨酸(DOPS),或上述的组合。
在一些实施方案中,所述C10-28脂族链是C10-26脂族链。在其他实施方案中,所述C10-28脂族链是C10-24脂族链。在其他实施方案中,所述C10-28脂族链是C10-22脂族链。在其他实施方案中,所述C10-28脂族链是C10-20脂族链。在其他实施方案中,所述C10-28脂族链是C10-18脂族链。在一些实施方案中,所述C10-28脂族链是C10-16脂族链。在其他实施方案中,所述C10-28脂族链是C10-14脂族链。在其他实施方案中,所述C10-28脂族链是C10-12脂族链。在一些实施方案中,所述C10-28脂族链是C14-18脂族链。
在一些实施方案中,所述脂质体的ii)中的一种或多种稳定剂以至多约5mol%、约10mol%、约15mol%、约20mol%、约25mol%、约30mol%、约35mol%、约40mol%、约45mol%、约50mol%、约55mol%、约60mol%、约65mol%,或约70mol%的量存在。在一些实施方案中,所述脂质体的ii)中的一种或多种稳定剂以至少约5mol%、至少约10mol%、至少约15mol%、至少约20mol%、至少约25mol%、至少约30mol%、至少约35mol%、至少约40mol%、至少约45mol%、至少约50mol%、至少约55mol%,或至少约60mol%的量存在。在一些实施方案中,所述脂质体的ii)中的一种或多种稳定剂以约5-10mol%、约10-15mol%、约15-20mol%、约20-25mol%、约25-30mol%、约30-35mol%、约35-40mol%、约40-45mol%、约45-50mol%、约50-55mol%、约55-60mol%、约60-65mol%、约65-70mol%、约5-25mol%、约25-50mol%,或约50-70mol%的量存在。
在一些实施方案中,与PEG结合的至少一种磷脂选自由磷脂酰胆碱(PC)、磷脂酰乙醇胺(PE)、磷脂酰丝氨酸(PS)、磷脂酰甘油(PG)和磷脂酰肌醇(PI)。在一些实施方案中,这种磷脂是1,2-二油酰基-sn-甘油-3-磷酸乙醇胺(DOPE)、1,2-二油酰基-sn-甘油-3-磷酸胆碱(DOPC)、1,2-二棕榈酰基-磷脂酰基-甘油(DPPG)、1,2-二油酰基-sn-甘油-3-磷酸甘油(DOPG)、1,2-二硬脂酰基-sn-甘油-3-磷酸(DSPA)、1,2-二油酰基-sn-甘油-3-磷酸-L-丝氨酸(DOPS),或1,2-二硬脂酰基-sn-甘油-3-磷酸乙醇胺(DSPE),或其盐。在一些实施方案中,这种磷脂是1,2-二硬脂酰基-sn-甘油-3-磷酸乙醇胺(DSPE),或其盐。
在一种变型中,与PEG结合的磷脂是:
在一些实施方案中,所结合的PEG以约0.5mol%至约20mol%的浓度存在于所述脂质体中。在一些实施方案中,所结合的PEG以约0.5mol%、约1mol%、约2mol%、约3mol%、约4mol%、约5mol%、约6mol%、约7mol%、约8mol%、约9mol%、约10mol%、约11mol%、约12mol%、约13mol%、约14mol%、约15mol%、约16mol%、约17mol%、约18mol%、约19mol%,或约20mol%的浓度存在于所述脂质体中。在某些实施方案中,所结合的PEG以约3mol%的浓度存在于所述脂质体中。在某些实施方案中,所结合的PEG以约5mol%的浓度存在于所述脂质体中。
在一些实施方案中,所述脂质体进一步包含胆固醇。在一些实施方案中,所述胆固醇以至多约10mol%、约15mol%、约20mol%、约25mol%、约30mol%、约35mol%,或约40mol%的量存在。
在另一个方面,所述脂质体包含:
i)式(PL-1)的磷脂:
或其盐,其中,
T1a和T1b的至少之一是不饱和碳链;和
R1是氨基烷基;
ii)式(PL-2)的磷脂的至少之一,式(PL-3)的磷脂的至少之一,或式(CE)的胆固醇酯的至少之一,或上述的任何组合。
或其盐,其中:
T2a和T2b各自是不饱和碳链;和
R2是季铵、甘油取代的烷基或–COOH和–NH2取代的烷基;
或其盐,其中:
T3a和T3b各自是饱和碳链;和
G3是H或至少一个–OH取代的烷基;和
或其盐,其中:
Z1是–COOH取代的烷基;和
iii)聚乙烯醇(PEG),其中所述PEG与至少一种磷脂结合。在又一个方面,所述脂质体包含:
i)式(PL-1)的磷脂:
或其盐,其中,
T1a和T1b的至少之一是不饱和碳链;和
R1是氨基烷基;
ii)式(PL-2)的磷脂的至少之一,式(PL-3)的磷脂的至少之一,
或式(CE)的胆固醇酯的至少之一,或上述的任何组合。
或其盐,其中:
T2a和T2b各自是不饱和碳链;和
R2是季铵、甘油取代的烷基或–COOH和–NH2取代的烷基;
或其盐,其中:
T3a和T3b各自是饱和碳链;和
G3是H或至少一个–OH取代的烷基;和
或其盐,其中:
Z1是–COOH取代的烷基;和
iii)聚乙烯醇(PEG),其中所述PEG与至少一种磷脂结合。
“氨基烷基”是指氨基基团取代的烷基链。因此,在式(PL-1)中,所述烷基链连接至所述磷酸部分的氧原子。在一些实施方案中,式(PL-1)的R1是氨基取代的C1-6烷基。在一些实施方案中,所述氨基取代的C1-6烷基是直链或支链的。在一些实施方案中,式(PL-1)的R1是C1-6烷基-NH2。在一些实施方案中,式(PL-1)的R1是氨基乙基,-CH2CH2NH2。在一些实施方案中,T1a和T1b各自独立地是C10-28烯基或C10-28炔基。在一些实施方案中,所述C10-28烯基是直链或支链的。在一些实施方案中,所述C10-28烯基具有一个或多个双键。在一些实施方案中,每个双键具有顺式结构。在一些实施方案中,每个双键具有反式结构。在一些实施方案中,所述C10-28烯基是取代基取代的,所述取代基选自由酰基、羟基、环烷基、烷氧基、酰氧基、氨基、氨酰基、硝基、卤素、硫醇、硫代烷基、烷基、烯基、炔基和杂环基组成的组。在一些实施方案中,式(PL-1)的磷脂是1,2-二油酰基-sn-甘油-3-磷酸乙醇胺(DOPE)或其盐。在一种变型中,式(PL-1)的磷脂是或其盐。
在一些实施方案中,式(PL-1)的磷脂以至多约15mol%、约20mol%、约25mol%、约30mol%、约35mol%、约40mol%、约45mol%、约50mol%、约55mol%、约60mol%、约65mol%、约70mol%、约75mol%、约80mol%、约85mol%,或约90mol%的量存在。在一些实施方案中,式(PL-1)的磷脂以至少约10mol%、至少约20mol%、至少约30mol%、至少约40mol%、至少约50mol%、至少约60mol%、至少约70mol%,或至少约80mol%的量存在。在一些实施方案中,式(PL-1)的磷脂以约10-20mol%、约20-30mol%、约30-40mol%、约40-50mol%、约50-60mol%、约60-70mol%、约70-80mol%、约10-30mol%、约30-50mol%、约50-80mol%、约10-50mol%,或约40-80mol%的量存在。
在一些实施方案中,式(PL-2)的R2是季铵或甘油取代的烷基。在一些实施方案中,式(PL-2)的R2是季铵或甘油取代的C1-6烷基。在一些实施方案中,所述季铵是在其他实施方案中,季铵包含一个或多个C1-6烷基基团。在一个实施方案中,所述季铵是在一些实施方案中,式(PL-2)的R2是胆碱。在一些实施方案中,式(PL-2)的R2是-COOH和-NH2取代的烷基。在一些实施方案中,式(PL-2)的R2是-COOH和-NH2取代的C1-6烷基。在一些实施方案中,式(PL-2)的R2是丝氨酸。在一些实施方案中,式(PL-2)的R2是L-丝氨酸。在一些实施方案中,T2a和T2b各自独立地是C10-28烯基或C10-28炔基。在一些实施方案中,所述C10-28烯基是直链或支链的。在一些实施方案中,所述C10-28烯基具有一个或多个双键。在一些实施方案中,每个双键具有顺式结构。在一些实施方案中,每个双键具有反式结构。在一些实施方案中,所述C10-28烯基是未取代的。在一些实施方案中,所述C10-28烯基是取代基取代的,所述取代基选自由酰基、羟基、环烷基、烷氧基、酰氧基、氨基、氨酰基、硝基、卤素、硫醇、硫代烷基、烷基、烯基、炔基和杂环基组成的组。在一些实施方案中,式(PL-2)的磷脂是1,2-二油酰基-sn-甘油-3-磷酸胆碱(DOPC)或1,2-二油酰基-sn-甘油-3-磷酸-L-丝氨酸(DOPS)或其盐。
在一些实施方案中,式(PL-3)或式(PL-3A)的G3是H。在一些实施方案中,式(PL-3)或式(PL-3A)的G3是至少一个-OH取代的烷基。在一些实施方案中,式(PL-3)或式(PL-3A)的G3是两个-OH取代的烷基。在一些实施方案中,式(PL-3)或式(PL-3A)的G3是甘油。在式(PL-3)或式(PL-3A)的一些实施方案中,T3a和T3b各自独立地是饱和碳链。在一些实施方案中,所述饱和碳链是任选取代的C10-28烷基。在一些实施方案中,所述C10-28烷基是直链或支链的。在一些实施方案中,所述C10-28烷基是未取代的。在一些实施方案中,T3a和T3b各自独立地是取代基取代的C10-28烷基,所述取代基选自由酰基、羟基、环烷基、烷氧基、酰氧基、氨基、氨酰基、硝基、卤素、硫醇、硫代烷基、烷基、烯基、炔基和杂环基组成的组。在一些实施方案中,式(PL-3)或式(PL-3A)的磷脂是1,2-二棕榈酰基-磷脂酰基-甘油(DPPG)或1,2-二硬脂酰基-sn-甘油-3-磷酸(DSPA)。在式(PL-3A)的一些实施方案中,式(PL-3A)中的T3a和T3b各自独立地是不饱和碳链。在式(PL-3A)的一些实施方案中,式(PL-3A)中的T3a和T3b各自独立地是C10-28烯基或C10-28炔基。在一些实施方案中,所述C10-28烯基是直链或支链的。在一些实施方案中,所述C10-28烯基具有一个或多个双键。在一些实施方案中,每个双键具有顺式结构。在一些实施方案中,每个双键具有反式结构。在一些实施方案中,所述C10-28烯基是未取代的。在一些实施方案中,所述C10-28烯基是取代基取代的,所述取代基选自由酰基、羟基、环烷基、烷氧基、酰氧基、氨基、氨酰基、硝基、卤素、硫醇、硫代烷基、烷基、烯基、炔基和杂环基组成的组。在其他实施方案中,式(PL-3A)的磷脂是1,2-二油酰基-sn-甘油-3-磷酸甘油(DOPG)或其盐。
在一些实施方案中,式(CE)的Z1是-COOH取代的C1-6烷基。在一些实施方案中,式(CE)是胆固醇半琥珀酸酯或其盐。
在一些实施方案中,式(PL-2)的磷脂的至少之一、式(PL-3)的磷脂的至少之一、式(PL-3A)的磷脂的至少之一或式(CE)的胆固醇酯的至少之一或上述的任何组合以至多约5mol%、约10mol%、约15mol%、约20mol%、约25mol%、约30mol%、约35mol%、约40mol%。约45mol%、约50mol%、约55mol%、约60mol%、约65mol%或约70mol%的量存在。在一些实施方案中,式(PL-2)的磷脂的至少之一、式(PL-3)的磷脂的至少之一、式(PL-3A)的磷脂的至少之一或式(CE)的胆固醇酯的至少之一或上述的任何组合以至少约5mol%、至少约10mol%、至少约15mol%、至少约20mol%、至少约25mol%,至少约30mol%、至少约35mol%、至少约40mol%、至少约45mol%、至少约50mol%、至少约55mol%,或至少约60mol%的量存在。在一些实施方案中,式(PL-2)的磷脂的至少之一、式(PL-3)的磷脂的至少之一、式(PL-3A)的磷脂的至少之一或式(CE)的胆固醇酯的至少之一或上述的任何组合以约5-10mol%、约10-15mol%、约15-20mol%、约20-25mol%、约25-30mol%、约30-35mol%、约35-40mol%、约40-45mol%、约45-50mol%、约50-55mol%、约55-60mol%、约60-65mol%、约65-70mol%、约5-25mol%、约25-50mol%,或约50-70mol%的量存在。
在一些实施方案中,与PEG结合的至少一种磷脂选自磷脂酰胆碱(PC)、磷脂酰乙醇胺(PE)、磷脂酰丝氨酸(PS)、磷脂酰甘油(PG)和磷脂酰肌醇(PI)。在一些实施方案中,这种磷脂是1,2-二油酰基-sn-甘油-3-磷酸乙醇胺(DOPE)、1,2-二油酰基-sn-甘油-3-磷酸胆碱(DOPC)、1,2-二棕榈酰基-磷脂酰基-甘油(DPPG)、1,2-二油酰基-sn-甘油-3-磷酸甘油(DOPG)、1,2-二硬脂酰基-sn-甘油-3-磷酸(DSPA)、1,2-二油酰基-sn-甘油-3-磷酸-L-丝氨酸(DOPS)或1,2-二硬脂酰基-sn-甘油-3-磷酸乙醇胺(DSPE),或其盐。在一些实施方案中,这种与PEG结合的磷脂是1,2-二硬脂酰基-sn-甘油-3-磷酸乙醇胺(DSPE),或其盐。
在一种变型中,与PEG结合的磷脂是:
在一些实施方案中,所结合的PEG以约0.5mol%至约20mol%的浓度存在于所述脂质体中。在一些实施方案中,所结合的PEG以约0.5mol%、约1mol%、约2mol%、约3mol%、约4mol%、约5mol%、约6mol%、约7mol%、约8mol%、约9mol%、约10mol%、约11mol%、约12mol%、约13mol%、约14mol%、约15mol%、约16mol%、约17mol%、约18mol%、约19mol%,或20mol%的浓度存在于所述脂质体中。在某些实施方案中,所结合的PEG以约3mol%的浓度存在于所述脂质体中。在某些实施方案中,所结合的PEG以约5mol%的浓度存在于所述脂质体中。
在一些实施方案中,所述脂质体进一步包含胆固醇。在一些实施方案中,所述胆固醇以至多约10mol%、约15mol%、约20mol%、约25mol%、约30mol%、约35mol%或约40mol%的量存在。
在另一个方面,所述脂质体包含:
i)N-十二酰基-1,2-二-(9Z-十八烯酰基)-sn-甘油-3-磷酸乙醇胺,或其盐;和
ii)1,2-二油酰基-sn-甘油-3-磷酸胆碱,或其盐;
在另一个方面,所述脂质体包含:
在一些实施方案中,N-C12-DOPE以至多约40mol%、约45mol%、约50mol%、约55mol%、约60mol%、约65mol%、约70mol%、约75mol%、约80mol%、约85mol%,或约90mol%的量存在。在一些实施方案中,N-C12-DOPE以至少约30mol%、至少约40mol%、至少约50mol%、至少约60mol%、至少约70mol%,或至少约80mol%的量存在。在一些实施方案中,N-C12-DOPE以约30-40mol%、约40-50mol%、约50-60mol%、约60-70mol%、约70-80mol%、约30-50mol%,或约50-80mol%,或约40-80mol%的量存在。
在一些实施方案中,DOPC以至多约5mol%、约10mol%、约15mol%、约20mol%、约25mol%、约30mol%、约35mol%、约40mol%、约45mol%、约50mol%、约55mol%,或约60mol%的量存在。在一些实施方案中,DOPC以至少约5mol%、至少约10mol%、至少约15mol%、至少约20mol%、至少约25mol%、至少约30mol%、至少约35mol%、至少约40mol%、至少约45mol%,或至少约50mol%的量存在。在一些实施方案中,DOPC以约5-10mol%、约10-15mol%、约15-20mol%、约20-25mol%、约25-30mol%、约30-35mol%、约35-40mol%、约40-45mol%、约45-50mol%、约50-55mol%、约55-60mol%、约5-30mol%,或约30-50mol%的量存在。
在一些实施方案中,所述脂质体进一步包含与至少一种磷脂、胆固醇、CHEMS或上述的组合结合的PEG。在一些实施方案中,与PEG结合的至少一种磷脂是磷脂酰胆碱(PC)、磷脂酰乙醇胺(PE)、磷脂酰丝氨酸(PS)、磷脂酰甘油(PG)或磷脂酰肌醇(PI)。在一些实施方案中,这种磷脂是1,2-二油酰基-sn-甘油-3-磷酸乙醇胺(DOPE)、1,2-二油酰基-sn-甘油-3-磷酸胆碱(DOPC)、1,2-二棕榈酰基-磷脂酰基-甘油(DPPG)、1,2-二油酰基-sn-甘油-3-磷酸甘油(DOPG)、1,2-二硬脂酰基-sn-甘油-3-磷酸(DSPA)、1,2-二油酰基-sn-甘油-3-磷酸-L-丝氨酸(DOPS),或1,2-二硬脂酰基-sn-甘油-3-磷酸乙醇胺(DSPE),或其盐。在一些实施方案中,与PEG结合的至少一种磷脂是1,2-二硬脂酰基-sn-甘油-3-磷酸乙醇胺(DSPE),或其盐。
在一些实施方案中,至少一种磷脂、胆固醇、CHEMS或上述的组合以约0.5mol%至约20mol%的浓度存在于所述脂质体中。在一些实施方案中,至少一种磷脂、胆固醇、CHEMS或上述的组合以约0.5mol%、约1mol%、约2mol%、约3mol%、约4mol%、约5mol%、约6mol%、约7mol%、约8mol%、约9mol%、约10mol%、约11mol%、约12mol%、约13mol%、约14mol%、约15mol%、约16mol%、约17mol%、约18mol%、约19mol%,或约20mol%的浓度存在于所述脂质体中。在某些实施方案中,至少一种磷脂、胆固醇、CHEMS或上述的组合以约3mol%的浓度存在于所述脂质体中。在某些实施方案中,至少一种磷脂、胆固醇、CHEMS或上述的组合以约5mol%的浓度存在于所述脂质体中。
在另一个方面,所述脂质体包含式(PL-4)的磷脂:
或其盐,其中:
T1a和T1b中的至少一个是不饱和碳链;并且R4是包含酰胺部分的脂族链。
在一些实施方案中,式(PL-4)的R4是包含酰胺部分的烷基。在一些实施方案中,式(PL-4)的R4是包含酰胺部分的C10-28烷基。在一些实施方案中,式(PL-4)的R4是-C1-12烷基-NH-C(O)-C1-12烷基。在某些实施方案中,式(PL-4)的R4是-CH2CH2-NH-C(O)-C11H23。在一些实施方案中,T4a和T4b各自独立地是C10-28烯基或C10-28炔基。在一些实施方案中,所述C10-28烯基是直链或支链的。在一些实施方案中,所述C10-28烯基具有一个或多个双键。在一些实施方案中,每个双键具有顺式结构。在一些实施方案中,每个双键具有反式结构。在一些实施方案中,所述C10-28烯基是取代基取代的,所述取代基选自由酰基、羟基、环烷基、烷氧基、酰氧基、氨基、氨酰基、硝基、卤素、硫醇、硫代烷基、烷基、烯基、炔基和杂环基组成的组。在一些实施方案中,式(PL-4)的磷脂是N-十二酰基-1,2-二-(9Z-十八烯酰基)-sn-甘油-3-磷酸乙醇胺(N-C12-DOPE)或其盐。在一种变型中,式(PL-4)的磷脂是:
在一些实施方案中,式(PL-4)的磷脂以至多约40mol%、约45mol%、约50mol%、约55mol%、约60mol%、约65mol%、约70mol%、约75mol%、约80mol%、约85mol%或约90mol%的量存在。在一些实施方案中,式(PL-4)的磷脂以至少约30mol%、至少约40mol%、至少约50mol%、至少约60mol%、至少约70mol%或至少约80mol%的量存在。在一些实施方案中,式(PL-4)的磷脂以约30-40mol%、约40-50mol%、约50-60mol%、约60-70mol%、约70-80mol%、约30-50mol%,或约50-80mol%,或约40-80mol%的量存在。
在一些实施方案中,所述脂质体进一步包含1,2-二油酰基-sn-甘油-3-磷酸胆碱(DOPC)、与至少一种磷脂、胆固醇、CHEMS或上述的组合结合的PEG。
在一些方面,本发明提供一种脂质体,其包含至少一种式(A)的磷脂或其盐,其中RX是-SO2,其中-SO2的S原子是任选取代的若丹明取代的,并且每个Ra独立地是碳链。在其他实施方案中,每个Ra独立地是不饱和碳链。在一些实施方案中,每个Ra独立地是饱和碳链。在一些实施方案中,每个Rb是C10-28烷基。在一种变型中,所述脂质体包含RH-DHPE。在一种变型中,所述脂质体包含N-(丽丝胺若丹明B磺酰基)-1,2-双十六酰基-sn-甘油-3-磷酸乙醇胺或其盐。在一种变型中,所述脂质体包含1,2-二油酰基-sn-甘油-3-磷酸乙醇胺-N-(丽丝胺若丹明B磺酰基)或其盐。在一种变型中,所述脂质体包含:或其盐。
在上述方面的一些实施方案中,包含至少一种式(A)的磷脂的脂质体可以与一种或多种脂质和/或本文所述的其他化合物组合。例如,在某些变型中,所述脂质体进一步包含至少一种磷脂酰胆碱或磷脂酰乙醇胺。在其他变型中,所述脂质体进一步包含与至少一种脂质(包含至少一种磷脂)结合的聚乙二醇。在某些变型中,所述脂质体进一步包含胆固醇。在一种变型中,所述脂质体组合物包含:DSPC/DSPE-PEG/RH-DHPE,或DSPC/DSPE-PEG/RH-DHPE/Chol,或DSPC/Chol/DSPE-PEG/DOTAP/RH-DHPE。
在一些方面,所述脂质体包含至少一种式(B)的化合物或其盐,其中:每个Rb独立地是碳链,并且Rc是任选取代的氨基或季铵取代的碳链。在一些实施方案中,每个Rb是饱和碳链。在其他实施方案中,每个Rb是不饱和碳链。在一些实施方案中,每个Rb是C10-28烯基。在某些实施方案中,Rc是-C1-6烷基-N(CH3)2。在其他实施方案中,Rc是取代的-C1-6烷基。在一些实施方案中,至少一种式(B)的化合物是1,2-二油酰基-3-二甲基铵-丙烷(DODAP)或其盐。在一些实施方案中,至少一种式(B)的化合物或其盐。在某些实施方案中,至少一种式(B)的化合物是1,2-二油酰基-3-三甲基铵-丙烷(DOTAP)或其盐。在一些实施方案中,至少一种式(B)化合物是:
在上述方面的一些实施方案中,包含至少一种式(B)的化合物的脂质体可以与一种或多种脂质和本文所述的其他化合物组合。例如,在某些变型中,所述脂质体进一步包含至少一种磷脂酰胆碱或磷脂酰乙醇胺。在其他变型中,所述脂质体进一步包含与至少一种脂质(包含至少一种磷脂)结合的PEG。在某些变型中,所述脂质体进一步包含胆固醇。在一种变型中,所述脂质体组合物包含DSPC/Chol/DSPE-PEG/DOTAP/RH-DHPE。
在一些方面,所述脂质体包含至少一种式(C)的化合物或其盐,其中Rd是任选取代的氨基取代的碳链,并且每个Re独立地是碳链。在一些实施方案中,Rd是取代的氨基取代的C1-6烷基。在某些实施方案中,Rd是-C1-6烷基-N(烷基)2基团。在某些实施方案中,Rd是-C1-6烷基-N(CH3)2基团。在某些实施方案中,Rd是-CH2CH2N(CH3)2。在其他实施方案中,Rd是-CH2CH2CH2N(CH3)2。在一些实施方案中,每个Re是饱和碳链。在其他实施方案中,每个Re是不饱和碳链。在一些实施方案中,每个Re是C10-28烯基。在一些实施方案中,至少一种式(C)的化合物是Dlin-KC2-DMA。在一些实施方案中,至少一种式(C)的化合物是2,2-二亚油基-4-二甲基胺基乙基-[1,3]-二氧戊环或其盐。在某些实施方案中,至少一种式(C)的化合物是或其盐。在其他实施方案中,至少一种式(C)的化合物是Dlin-KC3-DMA。在一些实施方案中,至少一种式(C)的化合物是2,2-二亚油基-4-二甲基氨基丙基-[1,3]-二氧戊环或其盐。在某些变型中,至少一种式(C)的化合物是或其盐。
在上述方面的一些实施方案中,包含至少一种式(C)的化合物的脂质体可以与一种或多种脂质和本文所述的其他化合物组合。例如,在某些变型中,所述脂质体进一步包含至少一种磷脂酰胆碱或磷脂酰乙醇胺。在其他变型中,所述脂质体进一步包含与至少一种脂质(包含至少一种磷脂)结合的PEG。在某些变型中,所述脂质体进一步包含胆固醇。在一种变型中,所述脂质体组合物包含DSPC/DMG-PEG/Dlin-KC2-DMA/Chol。
在一些方面,所述脂质体包含至少一种式(D)的化合物或其盐,其中每个Rf独立地是任选取代的碳链,或者两个与相同N原子结合的Rf结合在一起形成任选取代的环。在一些实施方案中,每个Rf独立地是任选一个或多个-O-C(O)-C10-28烷基取代的C1-6烷基。在其他实施方案中,与相同N原子结合的两个Rf结合在一起形成6元环,其中6元环是C1-6烷基取代的,其中所述C1-6烷基进一步是任选取代的。在一个实施方案中,至少一种式(D)的化合物是ssPalmm,其对应于双{2-{N-甲基-N-(十四酰基丙基)氨基]乙基}二硫化物或其盐。在一个实施方案中,至少一种式(D)的化合物是或其盐。在其他实施方案中,至少一种式(D)的化合物是ssPalme,其对应于双{2-[4-(α-D-生育酚半丁二酸乙基)哌啶基]乙基}二硫化物或其盐。在一个实施方案中,至少一种式(D)的化合物是
在上述方面的一些实施方案中,包含至少一种式(D)的化合物的脂质体可以与一种或多种脂质和本文所述的其他化合物组合。例如,在某些变型中,所述脂质体进一步包含至少一种磷脂酰胆碱或磷脂酰乙醇胺。在其他变型中,所述脂质体进一步包含与至少一种脂质(包含至少一种磷脂)结合的PEG。在某些变型中,所述脂质体进一步包含胆固醇。在一种变型中,所述脂质体组合物包含
ssPalmm/SOPC/PEG(2k)-DSG/Chol;或
ssPalme/SOPC/PEG(2k)-DSG/Chol。
在另一个方面,本发明提供一种包含脂质体的组合物,所述脂质体包含式(PL-2A)的磷脂:
或其盐,其中:
T2a和T2b各自是碳链;和
R2是季铵取代的烷基。
在一些实施方案中,T2a和T2b各自独立地是饱和或不饱和碳链。在某些变型中,季铵是–N+(烷基)3。在上述的一种变型中,所述烷基独立地是C1-6烷基、或C1-4烷基、或甲基、乙基或丙基。在一种变型中,式(PL-2A)的磷脂是1-硬脂酰基-2-油酰基-sn-甘油-3-磷酸胆碱(SOPC)或其盐。在一种变型中,式(PL-2A)的磷脂是或其盐。
在上述方面的一些实施方案中,包含至少一种式(PL-2A)的磷脂的脂质体可以与一种或多种脂质和本文所述的其他化合物组合。例如,在某些变型中,所述脂质体进一步包含至少一种磷脂酰胆碱或磷脂酰乙醇胺。在其他变型中,所述脂质体进一步包含与至少一种脂质(包含至少一种磷脂)结合的PEG。在某些变型中,所述脂质体进一步包含胆固醇。在一种变型中,所述脂质体组合物包含ssPalmm/SOPC/PEG(2k)-DSG/Chol;或
ssPalme/SOPC/PEG(2k)-DSG/Chol。
在一个方面,所述脂质体包含至少一种具有乙醇胺头部基团和不饱和脂肪酸尾的磷脂,其中所述不饱和脂肪酸尾包含至少一个C10-28碳链。在一些实施方案中,所述至少一种具有乙醇胺头部基团和不饱和脂肪酸尾的磷脂是1,2-二硬脂酰基-sn-甘油-3-磷酸胆碱,其中不饱和脂肪酸尾基包含至少一个C10-28碳链。在一些实施方案中,所述脂质体进一步包含至少一种PEG化的磷脂。在一些实施方案中,所述至少一种PEG化的磷脂是1,2-二硬脂酰基-sn-甘油-3-磷酸乙醇胺。在其他实施方案中,所述至少一种PEG化脂质是1,2-二肉豆蔻酰基-甘油(DMG)。在一些实施方案中,所述脂质体进一步包含至少一种式(A)的化合物或其盐,如上定义的。在一些实施方案中,所述至少一种式(A)的化合物是或其盐。在一些实施方案中,所述脂质体进一步包含至少一种固醇。在某些实施方案中,所述至少一种固醇是胆固醇。在某些实施方案中,所述脂质体进一步包含至少一种式(B)的化合物:或其盐,如上定义的。在一些实施方案中,所述至少一种式(B)的化合物是1,2-二油酰基-3-二甲基铵-丙烷(DODAP)或其盐。在某些实施方案中,所述至少一种式(B)的化合物是或其盐。在其他实施方案中,所述脂质体组合物进一步包含至少一种式(C):化合物或其盐,如上定义的。在一些实施方案中,所述至少一种式(C)的化合物是Dlin-KC2-DMA。在其他实施方案中,所述至少一种式(C)的化合物是Dlin-KC3-DMA。在某些实施方案中,所述至少一种式(C)的化合物是或其盐。在其他实施方案中,所述至少一种式(C)的化合物是或其盐。
在一个方面,本发明提供一种脂质体组合物,其包含至少一种式(D)的化合物:或其盐,如上定义的。在一些实施方案中,所述至少一种式(D)的化合物是双{2-{N-甲基-N-(十四酰基丙基)氨基]乙基}二硫化物或其盐。在一个实施方案中,至少一种式(D)的化合物是或其盐。在其他实施方案中,至少一种式(D)的化合物是ssPalme,其对应于双{2-[4-(α-D-生育酚半丁二酸乙基)哌啶基]乙基}二硫化物或其盐。在一个实施方案中,所述至少一种式(D)的化合物是或其盐。在一些实施方案中,所述脂质体进一步包含至少一种具有乙醇胺头部基团和不饱和脂肪酸尾的磷脂,其中所述不饱和脂肪酸尾包含至少一个C10-28的碳链。在一些实施方案中,所述至少一种具有乙醇胺头部基团和不饱和脂肪酸尾的磷脂是1-硬脂酰基-2-油酰基-sn-甘油-3-磷酸胆碱(SOPC),其中所述不饱和脂肪酸尾包含至少一个C10-28碳链。在一些实施方案中,所述脂质体进一步包含至少一种PEG化的磷脂。在一些实施方案中,所述至少一种PEG化的磷脂是1,2-二硬脂酰甘油(DSG)。在一些实施方案中,所述至少一种PEG化的磷脂是PEG(2k)-DSG。在一些实施方案中,所述脂质体进一步包含至少一种固醇。在某些实施方案中,所述至少一种固醇是胆固醇。
在一个方面,本发明提供一种脂质体组合物,其包含一种或多种具有极性头部基团和脂肪酸尾的磷脂,所述所述极性头部基团选自由甘油、胆碱、磷酸和丝氨酸组成的组,所述脂肪酸尾包括C10-28脂族链。在一些实施方案中,所述一种或多种具有选自由甘油、胆碱、磷酸和丝氨酸组成的组中的极性头部基团和包括C10-28脂族链的脂肪酸尾的磷脂是1,2-二硬脂酰基-sn-甘油-3-磷酸(DSPA)。在一些实施方案中,所述脂质体组合物进一步包含至少一种具有乙醇胺头部基团和不饱和脂肪酸尾的磷脂,其中所述不饱和脂肪酸尾包含至少一个C10-28碳链。在一些实施方案中,所述至少一种具有乙醇胺头部基团和不饱和脂肪酸尾的磷脂是1,2-二油酰基-sn-甘油-3-磷酸胆碱(DOPC),其中所述不饱和脂肪酸尾包含至少一个C10-28碳链。在一些实施方案中,所述脂质体进一步包含至少一种PEG化的磷脂。在一些实施方案中,所述至少一种PEG化的磷脂是1,2-二硬脂酰基-sn-甘油-3-磷酸乙醇胺。在一些实施方案中,所述脂质体进一步包含至少一种固醇。在某些实施方案中,所述至少一种固醇是胆固醇。
在一个方面,本发明提供一种脂质体组合物,其包含:
DSPC/DSPE-PEG/RH-DHPE,
DSPC/DSPE-PEG/RH-DHPE/Chol,
DSPC/DODAP/DSPE-PEG/Chol,
DSPC/DMG-PEG/Dlin-KC2-DMA/Chol,
ssPalmm/SOPC/PEG(2k)-DSG/Chol,
ssPalme/SOPC/PEG(2k)-DSG/Chol,
DSPA/DOPC/DSPE-PEG/Chol,
N-C12-DOPE/DOPC,
N-C12-DOPE/DOPC/DSPE-PEG,
N-C12-DOPE/DOPC/DSPE-PEG/Chol,
N-C12-DOPE/DPPE/DOPC/DSPE-PEG,
N-C12-DOPE/DOPE/DOPC/DSPE-PEG,
DOPE/DOPG/DSPE-PEG,
DOPE/DSPA/DSPE-PEG,
DOPE/DC-Chol/DSPE-PEG,
DOPE/DOPC/DSPE-PEG,
DOPE/DPPG/DOPC/DSPE-PEG,
DOPE/DOPC/DSPE-PEG/Chol,
DOPE/DOPS/DSPE-PEG,
DOPE/CHEMS,
DOPE/CHEMS/DSPE-PEG,
DOPE/CHEMS/DSPE-PEG/Chol,
DOPE/CHEMS/DOPC/DSPE-PEG,
或其盐,或上述的任何组合。
在上述的一些变型中,所述PEG可以以约200Da至约40,000Da的分子量存在于所述脂质体中。在一些实施方案中,聚乙二醇(PEG)可以以约200Da至约10,000Da的分子量存在于本公开的脂质体中。在一些实施方案中,聚乙二醇(PEG)可以以约200Da、约300Da、约400Da、约500Da、约600Da、约700Da、约800Da、约900Da、约1,000Da、约1,500Da、约2,000Da、约2,500Da、约3,000Da、约3,500Da、约4,000Da、约4,500Da、约5,000Da、约5,500Da、约6,000Da、约6,500Da、约7,000Da、约7,500Da、约8,000Da、约8,500Da、约9,000Da、约9,500Da,或约10,000Da;或约200Da至约10,000Da的分子量存在于本公开的脂质体中。
在上述的一些变型中,本文所述的脂质(包含磷脂)可以以盐的形式存在于所述脂质体组合物中。例如,在一种变型中,所述磷脂是DOPE或其盐。
碳水化合物
本公开的其他方面涉及包含包封在本公开的脂质体内的碳水化合物的组合物。可使用本领域已知的任何合适的碳水化合物。可使用的合适的碳水化合物包括,例如,单糖、磷酸化单糖、二糖、磷酸化二糖、寡糖、磷酸化寡糖、多糖、磷酸化多糖、核苷酸糖、内源性碳水化合物和磷酸化内源性碳水化合物。在一些实施方案中,所述碳水化合物是内源性碳水化合物。在某些变型中,所述碳水化合物是磷酸化碳水化合物。
在一些实施方案中,本公开的磷酸化碳水化合物是内源性碳水化合物。在一些实施方案中,内源性碳水化合物是作为个体(包括,例如人)中的天然产物发现的碳水化合物。然而,应当理解,内源性碳水化合物可以是(i)个体(包括,例如人)天然产生的,并从该个体的活细胞中提取的;或(ii)合成制备的。在一些实施方案中,所述内源性碳水化合物由个体(包括,例如人)在体内产生。在其他实施方案中,所述内源性碳水化合物由来自个体(包括,例如人)的细胞(例如培养的细胞系)天然产生。因此,这种内源性碳水化合物的来源可包括,例如,合成来源(例如,化学合成)或天然来源(例如,从天然产生内源性碳水化合物的个体或细胞或重组细胞(例如,经基因工程改造以产生内源性碳水化合物的细菌细胞)中提取、分离或纯化)。内源性碳水化合物可以包含,例如,参与蛋白质和脂质糖基化的碳水化合物。
合适的内源性碳水化合物包括,例如,单糖、磷酸化单糖、二糖、磷酸化二糖、寡糖、磷酸化寡糖、多糖、磷酸化多糖、甘露糖、磷酸化甘露糖、甘露呋喃糖、磷酸化甘露呋喃糖、甘露吡喃糖、磷酸化甘露吡喃糖、甘露糖-1-磷酸、甘露糖-6-磷酸、核苷酸糖、尿苷二磷酸、鸟嘌呤二磷酸、胞嘧啶单磷酸、岩藻糖、GDP-岩藻糖、唾液酸、CMP-唾液酸、N-乙酰神经氨酸(Neu5Ac)和CMP-Neu5Ac。在一种变型中,所述碳水化合物是甘露糖-1-磷酸,在本文中也称为“M1P”。
在一些实施方案中,所述碳水化合物是磷酸化内源性碳水化合物。在一些实施方案中,所述磷酸化内源性碳水化合物包括,例如,磷酸化单糖、磷酸化二糖、磷酸化寡糖、磷酸化多糖、磷酸化甘露糖、磷酸化甘露呋喃糖、磷酸化甘露吡喃糖或核苷酸糖,或其任何组合。在一些实施方案中,所述磷酸化内源性碳水化合物是磷酸化单糖。在一些实施方案中,所述磷酸化内源性碳水化合物是甘露糖-1-磷酸。在一些实施方案中,所述磷酸化内源性碳水化合物是甘露糖-6-磷酸。
在上述实施方案的一些变型中,本文所列的任何碳水化合物可以以盐的形式存在于所述脂质体组合物中。例如,在一种变型中,所述磷酸化碳水化合物是甘露糖-1-磷酸或其盐。
包封碳水化合物的脂质体组合物
本文所述的任何脂质体均可用于将碳水化合物包封在脂质体组合物中。本文所述的任何碳水化合物均可包封在脂质体组合物中的脂质体中。
在一个方面,本发明提供一种组合物,其包含:
一种脂质体,其包含:
i)1,2-二油酰基-sn-甘油-3-磷酸乙醇胺(DOPE)或其盐;
ii)一种或多种稳定剂,其选自
(a)一种或多种具有极性头部基团和脂肪酸尾的磷脂,其中所述极性头部基团选自由甘油、胆碱、磷酸和丝氨酸组成的组,所述脂肪酸尾包括C10-28脂族链,或
(b)酸性胆固醇酯,或(a)和(b)的混合物;和
iii)与至少一种磷脂结合的PEG;和
至少一种内源性磷酸化碳水化合物,其中所述至少一种内源性磷酸化碳水化合物包封在所述脂质体中。
在另一个方面,本发明提供一种包含脂质体的组合物,所述脂质体包含:
i)式(PL-1)的磷脂:
或其盐,其中:
T1a和T1b的至少之一是不饱和碳链;和
R1是氨基烷基;
ii)式(PL-2)的磷脂的至少之一,式(PL-3)的磷脂的至少之一,或式(CE)的胆固醇酯的至少之一,或上述的任何组合。
或其盐,其中:
T2a和T2b各自是不饱和碳链;和
R2是季铵、甘油取代的烷基或–COOH和–NH2取代的烷基;
或其盐,其中:
T3a和T3b各自是饱和碳链;和
G3是H或至少一个–OH取代的烷基;和
或其盐,其中:
Z1是–COOH取代的烷基;和
iii)聚乙烯醇(PEG),其中所述PEG与至少一种磷脂结合;
至少一种内源性磷酸化碳水化合物,其中所述至少一种内源性碳水化合物包封在所述脂质体内。
在另一个方面,本发明提供一种包含脂质体的组合物,所述脂质体包含:
i)式(PL-1)的磷脂:
或其盐,其中:
T1a和T1b的至少之一是不饱和碳链;和
R1是氨基烷基;
ii)式(PL-2)的磷脂的至少之一,式(PL-3)的磷脂的至少之一,或式(CE)的胆固醇酯的至少之一,或上述的任何组合。
或其盐,其中:
T2a和T2b各自是不饱和碳链;和
R2是季铵、甘油取代的烷基或–COOH和–NH2取代的烷基;
或其盐,其中:
T3a和T3b各自是碳链;和
G3是H或至少一个–OH取代的烷基;和
或其盐,其中:
Z1是–COOH取代的烷基;和
iii)聚乙烯醇(PEG),其中所述PEG与至少一种磷脂结合;
至少一种磷酸化内源性碳水化合物,其中所述至少一种内源性碳水化合物包封在所述脂质体内。
在另一个方面,本发明提供一种包含脂质体的组合物,所述脂质体包含:
i)N-十二酰基-1,2-二-(9Z-十八烯酰基)-sn-甘油-3-磷酸乙醇胺(N-C12-DOPE)或其盐;
ii)1,2-二油酰基-sn-甘油-3-磷酸胆碱或其盐;和
至少一种磷酸化内源性碳水化合物,其中所述至少一种内源性碳水化合物包封在所述脂质体中。
在另一个方面,本发明提供一种包含脂质体的组合物,所述脂质体包含:
至少一种磷酸化内源性碳水化合物,其中所述至少一种内源性碳水化合物包封在所述脂质体中。
在另一个方面,本发明提供一种包含脂质体的组合物,所述脂质体包含式(PL-4)的磷脂:
或其盐,其中:
T1a和T1b中的至少一个是不饱和碳链;并且R4是包含酰胺部分的脂族链;和
至少一种磷酸化内源性碳水化合物,其中所述至少一种内源性碳水化合物包封在所述脂质体中。
本文所述组合物的至少一种磷酸化内源性碳水化合物以约0.1-75mM、约0.1-0.5mM、约0.1-40mM、约0.1-30mM、约0.1-20mM、约0.1-10mM、约0.5-1.0mM、约1.0-1.5mM、约1.5-2.0mM、约2.0-2.5mM、约2.5-3.0mM、约3.0-3.5mM、约3.5-4.0mM、约4.0-4.5mM、约4.5-5.0mM、约5.0-7.5mM、约7.5-10mM、约10-15mM、约15-20mM、约20-30mM、约30-40mM、约40-50mM、约50-75mM、约0.1-2.5mM、约2.5-5.0mM、约5.0-10mM、约10-25mM、约25-50mM、约50-75mM、约0.1-10mM、约10-30mM或约30-75mM的量存在。
药物组合物
通过将所述组合物与适当的载体(包括,例如,药学上可接受的载体或稀释剂)组合,可以将包含本公开的脂质体和包封在所述脂质体中的本公开的磷酸化碳水化合物的本公开的组合物掺入至多种制剂中用于治疗用途(例如,通过给药)或用于药物制备(例如,用于将本公开的碳水化合物递送至有需要的个体和/或有需要的个体的细胞内部,和/或用于治疗或预防有需要的个体的疾病或障碍,例如先天性糖基化障碍(CDG),并且可以将其配制成例如液体、气溶胶化、半固体或粉末形式的制剂。
在一些实施方案中,载体包含药学上可接受的载体、赋形剂或稳定剂,其在所使用的剂量和浓度下对暴露于其中的细胞或个体无毒性。生理上可接受的载体通常是一种水性的pH缓冲溶液。合适的生理上可接受的载体包括,例如缓冲液,如磷酸盐、柠檬酸盐和其他有机酸);抗氧化剂,其包括抗坏血酸;低分子量(少于约10个残基)多肽;蛋白质,如血清白蛋白、明胶或免疫球蛋白;亲水性聚合物,如聚乙烯吡咯烷酮;氨基酸,如甘氨酸、谷氨酰胺、天冬酰胺、精氨酸或赖氨酸;单糖、二糖和其他碳水化合物,包括葡萄糖、甘露糖或糊精;螯合剂,如EDTA;糖醇,如甘露醇或山梨醇;成盐抗衡离子,如钠;和/或非离子表面活性剂,如TWEENTM、聚乙二醇(PEG)和PLURONICSTM。在某些实施方案中,其中生理上可接受的载体是成盐抗衡离子,如钠,所述钠离子与其他离子(包括,例如氯)一起存在于溶液中。在某些实施方案中,生理上可接受的载体包含盐水溶液。在一些实施方案中,所述盐水溶液以0-200毫米的量存在。在其他实施方案中,所述盐水溶液以0-175毫米的量存在。在其他实施方案中,所述盐溶液以0-150毫米的量存在。
在其他实施方案中,所述药学上可接受载体是甘油、木糖醇、蔗糖、海藻糖、聚山梨醇酯80、丙氨酸、脯氨酸、牛磺酸、甜菜碱、章鱼碱、组氨酸、柠檬酸钙、硫酸铵、尿素或十六烷基甲基铵。
合适的制剂包括,例如溶液、注射剂、吸入剂、微球、气雾剂、凝胶、软膏、乳膏、洗剂、粉末、干燥囊泡粉末、片剂和胶囊。根据所需的制剂,药物组合物可以包含药学上可接受的、无毒的稀释剂载体,该载体通常用于配制用于动物或人给药的药物组合物。选择所述稀释剂以不影响所述组合的生物活性。这种稀释剂包括,例如蒸馏水、缓冲水、生理盐水、磷酸盐缓冲盐水(PBS)、林格氏溶液(Ringer’s solution)、葡萄糖溶液和汉克氏溶液(Hank’ssolution)。本公开的药物组合物或制剂可进一步包含,例如其他载体或无毒、非治疗性、非免疫原性稳定剂,和赋形剂。所述组合物还可以包含接近生理条件的额外物质,例如,pH调节剂和缓冲剂、毒性调节剂、湿润剂和清洁剂。本公开的药物组合物还可以包含任何各种稳定剂,例如抗氧化剂。
对于口服给药,所述活性成分可以以固体剂型(如胶囊、片剂和粉末)或液体剂型(如酏剂、糖浆剂和混悬剂)给药。所述活性成分可以与非活性成分和粉末载体(如葡萄糖、乳糖、蔗糖、甘露醇、淀粉、纤维素或纤维素衍生物、硬脂酸镁、硬脂酸、糖精钠、滑石粉、碳酸镁)一起包封在明胶胶囊。可添加以提供所需的颜色、味道、稳定性、缓冲能力、分散性或其他已知所需特征的额外非活性成分的示例是红色氧化铁、硅胶、十二烷基硫酸钠、二氧化钛和可食用白墨。类似的稀释剂可用于制备压制片剂。片剂和胶囊均可以制成缓释产品,以便在数小时内持续释放药物。压制片剂可以是包有糖衣或膜衣的,以掩盖任何令人不愉快的味道并保护所述片剂免受大气影响,或者是包有肠溶衣的,用于在胃肠道中选择性崩解。用于口服给药的液体剂型可含有色素和调味剂,以增加患者接受度。
适合用于肠胃外给药的制剂包含水性和非水性等渗无菌注射液,其可以包含使所述制剂与预期接受者的血液等渗的抗氧化剂、缓冲剂、抑菌剂和溶质,以及水性和非水性无菌混悬剂,其可以包含悬浮剂、增溶剂、增稠剂、稳定剂和防腐剂。
用于配制所述药物组合物的组分优选具有高纯度,并且基本上不含潜在的有害污染物(例如,至少国家食品(NF)级,通常至少分析级,更典型地至少药物级)。此外,用于体内使用的组合物通常是无菌的。就给定化合物必须在使用前合成而言,所得产品通常基本上不含任何潜在的有毒试剂,尤其是在合成或纯化过程中可能存在的任何内毒素。用于肠胃外给药的组合物也是无菌的、基本等渗的,并在GMP条件下制备。
药物剂量
根据已知方法(例如口服给药、推注或通过在一段时间内连续输注的静脉内给药、经肌内、腹膜内、脑脊髓内、颅内、脊柱内、皮下、关节内、滑膜内、鞘内、口、局部或吸入途径),可使用本公开包含组合物的药物组合物,所述组合物包含本公开的脂质体和由所述脂质体包封的本公开的碳水化合物,例如将本公开的碳水化合物给药于需要治疗的个体,例如人类个体。
本公开的药物组合物的剂量和所需浓度可根据预期的特定用途而变化。适当的剂量或给药途径的确定在普通技术人员能力范围内。动物实验为人类治疗的有效剂量的确定提供可靠的指导。有效剂量的种间按比例调整可按照Mordenti,J.和Chappell,W.“The Useof Interspecies Scaling in Toxicokinetics,”In Toxicokinetics and New DrugDevelopment,Yacobi等,Eds,Pergamon Press,New York 1989,pp.42-46中所述的原理进行。
对于包含本公开的脂质体和由所述脂质体包封的本公开的碳水化合物的本公开的任何组合物的体内给药,正常剂量可在每天10ng/kg至100mg/kg个体的体重之间变化。
包含本公开的脂质体和由所述脂质体包封的本公开的碳水化合物的本公开的组合物的给药可以是连续的或间歇的,取决于例如接受者的生理状况、给药的目的是治疗性的还是预防性的,以及专业人员已知的其他因素。
在本公开的范围内,不同的制剂将对不同的治疗和不同的障碍有效,并且旨在治疗特定器官或组织的给药可能需要以不同于递送至另一个器官或组织的方式进行递送。此外,可以通过一次或多次单独给药或连续注射给药。对于超过数天或更长时间的重复给药,视病症而定,治疗将持续直至疾病症状出现期望的抑制。但是,其他给药方案也可能是有用的。该疗法的进展很容易通过常规技术和分析进行监测。
因此,在一些变型中,本文提供的组合物可以长期或间歇地给药于有需要的个体(包括,例如人)。在某些变型中,长期给药是指以连续而非急性的方式给药,以便长时间维持初始治疗效果(活性)。在某些变型中,间歇给药是指并非不间断地连续进行的治疗,而是实际上是循环的。
制备方法
在某些方面,本文提供制备本文所述的脂质体组合物的方法。在某些实施方案中,所述方法包括:a)溶解脂质于溶剂中以制备混合物;b)干燥所述混合物以形成薄膜;c)用包含磷酸化碳水化合物的水溶液水合所述薄膜;d)加热步骤c)中的溶液以重新悬浮所述薄膜,从而制备悬浮液;和e)至少冻融循环所述混悬剂一次以制备所述脂质体组合物。在一些变型中,所述方法进一步包括:通过超声处理、挤出或微流化或其任何组合来调整所述脂质体组合物的尺寸。
在上述的一些变型中,所述方法进一步包括调节所述脂质体组合物的pH值。在其他变型中,所述方法进一步包括通过透析、固相提取或切向流过滤去除未包封的磷酸化碳水化合物。
在一个实施方案中,将所述脂质体的脂质组分溶解在氯仿中,然后加热所得混合物以完全溶解所述脂质。然后在例如烧瓶或管上干燥所述混合物成薄膜涂层。然后用包含甘露糖-1-磷酸的溶液水合所述薄膜,并且加热、涡旋和超声处理所得的悬液以制备完整的脂质悬液。然后冻融循环脂质体悬液,随后通过例如超声波处理、挤压或微流化进行尺寸测定。在一些变型中,使用透析、固相提取或切向流过滤等技术调整溶液的pH和/或从所述制剂中去除未包封的甘露糖-1-磷酸。
治疗用途
本公开提供包含本公开的脂质体和由所述脂质体包封的本公开的磷酸化碳水化合物的组合物,所述组合物能够将所述碳水化合物递送至细胞内部。这些组合物可用于将本公开的磷酸化碳水化合物递送至需要这种碳水化合物的个体。
在一些实施方案中,所述个体是哺乳动物,例如人;家畜,例如猫或狗个体;农场动物(例如牛、马、山羊、绵羊和猪个体);野生动物(无论是在野生环境中还是在动物园中);研究动物,例如小鼠、大鼠、兔、山羊、绵羊、猪、狗和猫,以及鸟。在一个实施方案中,所述个体是人。
在某些变型中,个体可能处于风险中。例如,在一个变型中,个体是处于风险中的人。处于发展特定疾病、障碍或病症(例如先天性糖基化障碍)风险的个体可能具有或可能不具有可检测的疾病或疾病症状,并且可能或可能没有在本文所述的治疗方法之前已显示可检测的疾病或疾病症状。在某些变型中,“处于风险中”的个体指具有风险因素的个体,此风险因素是本领域已知的与特定疾病、障碍或病症的发展相关的可测量参数。与不具有一种或多种这些风险因素的个体相比,具有一种或多种这些风险因素的个体更有可能发展特定疾病、障碍或病症,例如先天性糖基化障碍。
在一些实施方案中,先天性糖基化障碍(CDG)是导致多种组织蛋白和/或脂质的糖基化缺乏或缺陷的代谢错误的一组遗传障碍。先天性糖基化障碍也称为CDG综合症。在受影响的婴儿中,CDG综合症通常会导致多种不同器官系统(例如神经系统、大脑、肌肉和肠道)出现严重、有时是致命的故障。CDG综合症的表现可能从婴儿时期开始的严重发育迟缓和张力减退,到正常发育的低血糖和蛋白质丢失性肠病。发育迟缓可能是CDG诊断的常见初始迹象。CDG综合症最常见的亚型之一是CDG-Ia(也称为PMM2-CDG),其遗传缺陷导致磷酸甘露糖变位酶2的缺失,其负责将甘露糖-6-磷酸转化为甘露糖-1-磷酸。
CDG综合症可分为I型(CDG-I型)和II型(CDG-II型)。这种分类可能取决于与寡糖转移酶作用相关的代谢途径中生化缺陷的性质和位置。筛查CDG亚型的方法可以包含通过例如等电聚焦或ESI-MS分析转铁蛋白糖基化状态。CDG I型包括,例如Ia(PMM2-CDG)、Ib(MPI-CDG)、Ic(ALG6-CDG)、Id(ALG3-CDG)、Ie(DPM1-CDG)、If(MPDU1-CDG)、Ig(ALG12-CDG)、Ih(ALG8-CDG)、Ii(ALG2-CDG)、Ij(DPAGT1-CDG)、Ik(ALG1-CDG)、1L(ALG9-CDG)、Im(DOLK-CDG)、In(RFT1-CDG)、Io(DPM3-CDG)、Ip(ALG11-CDG)、Iq(SRD5A3-CDG)、Ir(DDOST-CDG)、DPM2-CDG、TUSC3-CDG、MAGT1-CDG、DHDDS-CDG、和I/IIx。CDG II型包括,例如IIa(MGAT2-CDG)、IIb(GCS1-CDG)、IIc(SLC335C1-CDG)、IId(B4GALT1-CDG)、IIe(COG7-CDG)、IIf(SLC35A1-CDG)、IIg(COG1-CDG)、IIh(COG8-CDG)、IIi(COG5-CDG)、IIj(COG4-CDG)、IIL(COG6-CDG)、ATP6V0A2-CDG、MAN1B1-CDG和ST3GAL3-CDG。
可以用包含本公开的脂质体和由所述脂质体包封的本公开的碳水化合物的本公开的组合物治疗的先天性糖基化障碍(CDG)包括,例如Ia(PMM2-CDG)、Ib(MPI-CDG)、Ic(ALG6-CDG)、Id(ALG3-CDG)、Ie(DPM1-CDG)、If(MPDU1-CDG)、Ig(ALG12-CDG)、Ih(ALG8-CDG)、Ii(ALG2-CDG)、Ij(DPAGT1-CDG)、Ik(ALG1-CDG)、1L(ALG9-CDG)、Im(DOLK-CDG)、In(RFT1-CDG)、Io(DPM3-CDG)、Ip(ALG11-CDG)、Iq(SRD5A3-CDG)、Ir(DDOST-CDG)、DPM2-CDG、TUSC3-CDG、MAGT1-CDG、DHDDS-CDG、I/IIx、IIa(MGAT2-CDG)、IIb(GCS1-CDG)、IIc(SLC335C1-CDG)、IId(B4GALT1-CDG)、IIe(COG7-CDG)、IIf(SLC35A1-CDG)、IIg(COG1-CDG)、IIh(COG8-CDG)、IIi(COG5-CDG)、IIj(COG4-CDG)、IIL(COG6-CDG)、ATP6V0A2-CDG、MAN1B1-CDG和ST3GAL3-CDG。
在一些实施方案中,“治疗(treatment)”或“治疗(treating)”包括获得有益的或期望的结果(包括临床结果)的方法。有益的或期望的临床结果可以包括以下一项或多项:a)抑制疾病或病症(例如减少由疾病或病症引起的一种或多种症状,和/或减弱疾病或病症的程度);b)减缓或阻止与疾病或病症相关的一种或多种临床症状的发展(例如稳定所述疾病或病症,预防或延迟所述疾病或病症的恶化或进展,和/或预防或延迟疾病或病症的扩散);和/或c)减轻疾病,即使得临床症状的消退(例如改善疾病状态、提供疾病或病症的部分或全部缓解、增强另一种药物的效果、延缓疾病的进展、提高生活质量和/或延长存活期)。
在一些实施方案中,“预防(prevention)”或“预防(preventing)”包括使得疾病或病症的临床症状不发展的疾病或病症的任何治疗。在一些实施方案中,可将化合物给药于处在风险中或具有疾病或病症家族史的个体(包括人)。
在一些变型中,“有效量”至少是在必要的剂量和时间内有效实现期望的治疗或预防效果的量。有效量可以在一次或多次给药中提供。
在一些变型中,“治疗有效量”至少是实现特定疾病、障碍或病症(例如先天性糖基化障碍)的可测量改善所需的最低浓度。本文的治疗有效量可根据例如个体的疾病状态、年龄、性别和体重以及本公开的脂质组合物在个体中引发所需反应的能力等因素而变化。治疗有效量还指本公开的脂质组合物的任何毒性或有害作用超过治疗有益作用的量。
在一个方面,本发明提供一种将磷酸化碳水化合物递送至有需要的个体的方法。在一些实施方案中,所述方法包括将本文所述的任何组合物给药于个体。
在另一个方面,本发明提供一种将磷酸化碳水化合物递送至有需要的个体的细胞内部的方法。在一些实施方案中,所述方法包括将本文所述的任何组合物给药于个体。在一些实施方案中,至少一部分给药组合物穿过细胞质膜以将碳水化合物递送至所述细胞内部。
在另一个方面,本发明提供一种治疗有需要的个体的先天性糖基化障碍(CDG)的方法。在一些实施方案中,所述方法包括将本文所述的任何组合物给药于个体。在一些实施方案中,所述先天性糖基化障碍(CDG)是CDG-Ia障碍。在一些实施方案中,相比于未将组合物给药于个体的情况下人体内细胞产生的高阶脂质连接的寡糖,所述组合物的给药在人体内诱导细胞产生的高阶脂质连接的寡糖增加0.05倍至至少3倍。
制品和试剂盒
本发明还提供包含本公开的组合物的制品和/或试剂盒,所述组合物包含本公开的脂质体和由所述脂质体包封的本公开的碳水化合物。本公开的制品和/或试剂盒可以包含一个或多个包含本公开的纯化组合物的容器。合适的容器可以包括,例如瓶子、小瓶、注射器和IV溶液袋。所述容器可以由多种材料形成,例如玻璃或塑料。在一些实施方案中,所述制品和/或试剂盒进一步包含根据本公开的任何方法的使用说明。在一些实施方案中,根据本公开的任何方法,这些说明书包括对所述组合物的给药的描述,所述组合物包含本公开的脂质体和由所述脂质体包封的本公开的碳水化合物,以将所述碳水化合物递送至有需要的个体,将所述碳水化合物递送至有需要的个体的细胞内部,或治疗有需要的个体的先天性糖基化障碍(CDG)。在一些实施方案中,所述说明书包括如何检测先天性糖基化障碍(CDG)的描述,例如在个体、在组织样品,或在细胞中。所述制品和/或试剂盒还可以包括基于鉴定个体是否患有疾病和疾病阶段来选择适合治疗的个体的描述。
所述说明书通常包括关于预期治疗的剂量、给药方案和给药途径的信息。所述容器可以是单位剂量、散装包装(例如多剂量包装)或亚单位剂量。本公开的制品和/或试剂盒中提供的说明书通常是在标签或包装说明书(例如,包含在制品和/或试剂盒中的纸张)上的书面说明,但机器可读指令(例如,磁性或光学存储盘上携带的指令)也是可接受的。
标签或包装说明书表明所述组合物用于递送碳水化合物和/或治疗例如先天性糖基化障碍(CDG)。可以提供用于实践本文所述任何方法的说明书。
本公开的制品和/或试剂盒可以处于合适的包装中。合适的包装包括,例如小瓶、瓶子、广口瓶和软包装(例如密封的聚脂薄膜或塑料袋)。还考虑与特定装置(例如吸入器、鼻腔给药装置(例如雾化器)或输液装置(例如微型泵))结合使用的包装。制品和/或试剂盒可具有无菌出入口(例如,容器可以是静脉内溶液袋或具有可由皮下注射针刺穿的塞子的小瓶)。所述容器还可具有无菌出入口(例如,容器可以是静脉内溶液袋或具有可由皮下注射针刺穿的塞子的瓶)。所述组合物中的至少一种活性剂是能够治疗先天性糖基化障碍(CDG)和/或改善其一种或多种症状的碳水化合物。所述容器可进一步包括第二药物活性剂。
制品和/或试剂盒可任选地提供额外的组分,例如缓冲液和解释信息。通常,所述制品和/或试剂盒包括容器和在容器上或与之相关联的标签或包装说明书。
列举的实施方式
以下列举的实施方案代表本公开的一些方面。
1.一种组合物,其包含:
一种脂质体,其包含:
i)1,2-二油酰基-sn-甘油-3-磷酸乙醇胺(DOPE);和
ii)一种或多种稳定剂,其选自由以下组成的组:
(a)一种或多种具有极性头部基团和脂肪酸尾的磷脂,其中所述极性头部基团选自由甘油、胆碱、磷酸和丝氨酸组成的组,所述脂肪酸尾包括C10-28脂族链,和
(b)酸性胆固醇酯,
或(a)和(b)两者;和
iii)与至少一种磷脂结合的PEG;和
至少一种内源性磷酸化碳水化合物,其中所述至少一种内源性磷酸化碳水化合物包封在所述脂质体内。
2.根据实施方案1所述的组合物,其中所述脂质体进一步包含胆固醇。
3.根据实施方案2所述的组合物,其中所述胆固醇以至多25mol%的量存在。
4.根据实施方案1-3任一项所述的组合物,其中所述至少一种内源性磷酸化碳水化合物是磷酸化单糖、磷酸化二糖、磷酸化寡糖、磷酸化多糖、磷酸化甘露糖、磷酸化甘露呋喃糖、磷酸化甘露吡喃糖或核苷酸糖,或其任何组合。
5.根据实施方案1-4任一项所述的组合物,其中所述至少一种内源性磷酸化碳水化合物是磷酸化甘露糖。
6.根据实施方案5所述的组合物,其中所述磷酸化甘露糖是甘露糖-1-磷酸。
7.根据实施方案1-6任一项所述的组合物,其中所述内源性磷酸化碳水化合物以约0.1-75mM的浓度存在。
8.根据实施方案1-7任一项所述的组合物,其中DOPE以至多80mol%的浓度存在。
9.根据实施方案1-8任一项所述的组合物,其中所述一种或多种稳定剂包含1,2-二油酰基-sn-甘油-3-磷酸胆碱(DOPC)。
10.根据实施方案1-8任一项所述的组合物,其中所述一种或多种稳定剂包含1,2-二棕榈酰基-磷脂酰基-甘油(DPPG)。
11.根据实施方案1-8任一项所述的组合物,其中所述一种或多种稳定剂包含1,2-二油酰基-sn-甘油-3-磷酸甘油(DOPG)。
12.根据实施方案1-8任一项所述的组合物,其中所述一种或多种稳定剂包含1,2-二硬脂酰基-sn-甘油-3-磷酸(DSPA)。
13.根据实施方案1-8任一项所述的组合物,其中所述一种或多种稳定剂包含1,2-二油酰基-sn-甘油-3-磷酸-L-丝氨酸(DOPS)。
14.根据实施方案1-13任一项所述的组合物,其中一种或多种稳定剂以至多70mol%的量存在。
15.根据实施方案1-14任一项所述的组合物,其中与PEG结合的至少一种磷脂是1,2-二硬脂酰基-sn-甘油-3-磷酸乙醇胺(DSPE)。
16.根据实施方案15所述的组合物,其中PEG-DSPE以至多5mol%的浓度存在。
17.一种组合物,其包含:
一种脂质体,其包含:
i)N-十二酰基-1,2-二-(9Z-十八烯酰基)-sn-甘油-3-磷酸乙醇胺(N-C12-DOPE);
ii)1,2-二油酰基-sn-甘油-3-磷酸胆碱(DOPC);和
至少一种磷酸化内源性碳水化合物,其中所述至少一种内源性碳水化合物包封在所述脂质体中。
18.根据实施方案17所述的组合物,其中所述至少一种内源性磷酸化碳水化合物是磷酸化单糖、磷酸化二糖、磷酸化寡糖、磷酸化多糖、磷酸化甘露糖、磷酸化甘露呋喃糖、磷酸化甘露吡喃糖或核苷酸糖,或其任何组合。
19.根据实施方案17或实施方案18所述的组合物,其中所述至少一种内源性磷酸化碳水化合物是磷酸化甘露糖。
20.根据实施方案19所述的组合物,其中所述磷酸化甘露糖是甘露糖-1-磷酸。
21.根据实施方案17-20任一项所述的组合物,其中所述内源性磷酸化碳水化合物以约0.1-75mM的浓度存在。
22.根据实施方案17-21任一项所述的组合物,其中N-C12-DOPE以至多80mol%的量存在。
23.根据实施方案17-22任一项所述的组合物,其中DOPC以至多30mol%的量存在。
24.根据实施方案17-23任一项所述的组合物,其中所述脂质体进一步包含与至少一种磷脂结合的PEG。
25.根据实施方案24所述的组合物,其中与PEG结合的至少一种磷脂是1,2-二硬脂酰基-sn-甘油-3-磷酸乙醇胺(DSPE)。
26.根据实施方案25所述的组合物,其中PEG-DSPE以至多5mol%的浓度存在。
27.根据实施方案17-26任一项所述的组合物,其中所述脂质体进一步包含胆固醇。
28.根据实施方案27所述的组合物,其中所述胆固醇以至多25mol%的量存在。
29.一种组合物,其包含:
一种脂质体,其包含:
i)至少一种具有乙醇胺头部基团和不饱和脂肪酸尾的磷脂,其中所述不饱和脂肪酸尾包含至少一个C10-28碳链;
ii)一个或多个(a)至(c):
a)至少一种具有极性头部基团和饱和脂肪酸尾的磷脂,
b)至少一种具有极性头部基团和不饱和脂肪酸尾的磷脂,其中所述极性头部基团包括季铵阳离子、甘油基团或丝氨酸基团,和
c)至少一种酸性胆固醇酯;和
iii)聚乙二醇(PEG),其中所述PEG与至少一种磷脂结合;
和
至少一种磷酸化内源性碳水化合物,其中所述至少一种内源性碳水化合物包封在所述脂质体中。
30.根据实施方案29所述的组合物,其中i)中的至少一种磷脂的不饱和脂肪酸尾包含至少一个双键。
31.根据实施方案29或实施方案30所述的组合物,其中i)中的至少一种磷脂的不饱和脂肪酸尾包含一个双键。
32.根据实施方案29-31任一项所述的组合物,其中所述不饱和脂肪酸尾包含至少一个C16-20碳链。
33.根据实施方案29-32任一项所述的组合物,其中具有乙醇胺头部基团和脂肪酸尾的磷脂是1,2-二油酰基-sn-甘油-3-磷酸乙醇胺(DOPE)。
34.根据实施方案29-33任一项所述的组合物,其中a)中的至少一种磷脂的饱和脂肪酸尾包含至少C16-20碳链。
35.根据实施方案29-34任一项所述的组合物,其中所述至少一种具有极性头部基团和饱和脂肪酸尾的磷脂是1,2-二棕榈酰基-sn-甘油-3-磷酸甘油(DPPG)或1,2-二硬脂酰基-sn-甘油-3-磷酸(DSPA),或两者。
36.根据实施方案29-35任一项所述的组合物,其中b)中的至少一种磷脂的极性头部基团是胆碱。
37.根据实施方案29-36任一项所述的组合物,其中所述至少一种具有含季铵阳离子的极性头部基团和不饱和脂肪酸尾的磷脂是1,2-二油酰基-sn-甘油-3-磷酸胆碱(DOPC)。
38.根据实施方案29-35任一项所述的组合物,其中b)中的至少一种磷脂的极性头部基团是丝氨酸。
39.根据实施方案38所述的组合物,其中所述至少一种具有含丝氨酸基团的极性头部基团和不饱和脂肪酸尾的磷脂是1,2-二油酰基-sn-甘油-3-磷酸-L-丝氨酸(DOPS)。
40.根据实施方案29-35任一项所述的组合物,其中b)中的至少一种磷脂的极性头部基团是甘油。
41.根据实施方案40所述的组合物,其中所述至少一种具有含甘油基团的极性头部基团和不饱和脂肪酸尾的磷脂是1,2-二油酰基-sn-甘油-3-磷酸甘油(DOPG)。
42.根据实施方案29-41任一项所述的组合物,其中所述至少一种酸性胆固醇酯是胆固醇半琥珀酸酯(CHEMS)。
43.根据实施方案29-42任一项所述的组合物,其中与PEG结合的至少一种磷脂是1,2-二硬脂酰基-sn-甘油-3-磷酸乙醇胺(DSPE)。
44.根据实施方案29-43任一项所述的组合物,其中所述至少一种具有乙醇胺头部基团和不饱和脂肪酸尾的磷脂以至多50mol%的浓度存在。
45.根据实施方案29-44任一项所述的组合物,其中一种或多种(a)至(c)以至多70mol%的浓度存在。
46.根据实施方案29-45任一项所述的组合物,其中与至少一种磷脂结合的PEG以至多5mol%的浓度存在。
47.根据实施方案29-45任一项所述的组合物,其中与至少一种磷脂结合的PEG以至多3mol%的浓度存在。
48.根据实施方案29-47任一项所述的组合物,其中所述至少一种内源性磷酸化碳水化合物是磷酸化单糖、磷酸化二糖、磷酸化寡糖、磷酸化多糖、磷酸化甘露糖、磷酸化呋喃糖、磷酸化甘露吡喃糖或核苷酸糖或其任何组合。
49.根据实施方案29-48任一项所述的组合物,其中所述至少一种内源性磷酸化碳水化合物是磷酸化甘露糖。
50.根据实施方案49所述的组合物,其中所述磷酸化甘露糖是甘露糖-1-磷酸。
51.根据实施方案29-50任一项所述的组合物,其中所述内源性磷酸化碳水化合物以约0.1-75mM的浓度存在。
52.根据实施方案29-51任一项所述的组合物,其中所述脂质体进一步包含胆固醇。
53.根据实施方案52所述的组合物,其中所述胆固醇以至多25mol%的量存在。
54.一种组合物,包含:
一种脂质体,包含:
i)式(PL-1)的磷脂:
或其盐,其中:
T1a和T1b中的至少之一是包含C10-28烯基或C10-28炔基的不饱和碳链;和
R1是氨基烷基;
ii)式(PL-2)的磷脂的至少之一、式(PL-3)的磷脂的至少之一,或式(CE)的胆固醇酯的至少之一,或上述的任何组合:
或其盐,其中:
T2a和T2b各自是包含C10-28烯基或C10-28炔基的不饱和碳链;和
R2是季铵、甘油取代的烷基,或-COOH和-NH2取代的烷基;
或其盐,其中:
T3a和T3b各自是饱和碳链;和
G3是H或被至少一个-OH取代的烷基;和
或其盐,其中:
Z1是-COOH取代的烷基;和
iii)聚乙二醇(PEG),其中所述PEG与至少一种磷脂结合;和
至少一种磷酸化内源性碳水化合物,其中所述至少一种内源性碳水化合物包封在所述脂质体中。
55.根据实施方案54所述的组合物,其中T1a、T1b、T2a和T2b各自独立地是包含一个双键的不饱和碳链。
56.根据实施方案55所述的组合物,其中所述不饱和碳链是顺式异构体。
57.根据实施方案54-56任一项所述的组合物,其中每个碳链具有10-28个碳原子。
58.根据实施方案54所述的组合物,其中所述至少一种式(PL-1)的磷脂是DOPE。
59.根据实施方案54或实施方案58所述的组合物,其中所述至少一种式(PL-2)的磷脂是DOPC或DOPS。
60.根据实施方案54、58或59所述的组合物,其中所述至少一种式(PL-3)的磷脂是DPPG、DOPG或DSPA。
61.根据实施方案54-60任一项所述的组合物,其中所述至少一种式(CE)的胆固醇酯是CHEMS。
62.根据实施方案51-61任一项所述的组合物,其中所述脂质体进一步包含胆固醇。
63.根据实施方案62所述的组合物,其中所述胆固醇以至多25mol%的量存在。
64.根据实施方案51-63任一项所述的组合物,其中与PEG结合的至少一种磷脂是1,2-二硬脂酰基-sn-甘油-3-磷酸乙醇胺(DSPE)。
65.根据实施方案64所述的组合物,其中PEG-DSPE以至多5mol%的浓度存在。
66.一种组合物,其包含:
一种包含式(PL-4)的磷脂的脂质体:
或其盐,其中:
T1a和T1b的至少之一是包含C10-28烯基或C10-28炔基的不饱和碳链;和
R4是包含酰胺部分的脂族链;和
至少一种磷酸化内源性碳水化合物,其中所述至少一种内源性碳水化合物包封在所述脂质体中。
67.根据实施方案66所述的组合物,其中PL-4是N-十二酰基-1,2-二-(9Z-十八烯酰基)-sn-甘油-3-磷酸乙醇胺(N-C12-DOPE)。
68.根据实施方案66或实施方案67所述的组合物,其中所述至少一种内源性磷酸化碳水化合物是磷酸化单糖、磷酸化二糖、磷酸化寡糖、磷酸化多糖、磷酸化甘露糖、磷酸化甘露呋喃糖、磷酸化吡喃糖,或核苷酸糖,或其任何组合。
69.根据实施方案66所述的组合物,其中所述至少一种内源性磷酸化碳水化合物是磷酸化甘露糖。
70.根据实施方案69所述的组合物,其中所述磷酸化甘露糖是甘露糖-1-磷酸。
71.根据实施方案66-70任一项所述的组合物,其中所述内源性磷酸化碳水化合物以约0.1-75mM的浓度存在。
72.一种药物组合物,其包含上述任一实施方案的组合物,和药学上可接受载体。
73.一种将碳水化合物递送至有需要的人的方法,其包括将上述任一实施方案的组合物给药于所述人。
74.一种将碳水化合物递送至有需要的个体的细胞内部的方法,其包括将实施方案1至71任一项所述的组合物或实施方案72所述的药物组合物给药于所述个体。其中至少一部分给药组合物穿过细胞质膜以将碳水化合物递送至所述细胞内部。
75.一种治疗有需要的人的先天性糖基化障碍(CDG)的方法,其包括将实施方案1至71任一项所述的组合物或实施方案72所述的药物组合物给药于所述人。
76.根据实施方案75所述的方法,其中所述先天性糖基化障碍(CDG)是CDG-Ia障碍。
77.根据实施方案76所述的方法,其中相比于未将所述组合物给药于人的情况下人体内细胞产生的高阶脂质连接的寡糖,所述组合物的给药在人体内诱导细胞产生的高阶脂质连接的寡糖增加0.05倍至至少3倍。
78.一种试剂盒,其包含:实施方案1至71任一项所述的组合物或实施方案72的药物组合物。
79.根据实施方案78所述的试剂盒,其进一步包含容器和在容器上或与之相关联的标签或包装说明书。
80.一种组合物,其包含:
一种脂质体,其包含:
i)1,2-二油酰基-sn-甘油-3-磷酸乙醇胺或其盐;和
ii)(a)一种或多种具有极性头部基团和脂肪酸尾的磷脂,其中所述极性头部基团包括甘油、胆碱、磷酸和丝氨酸,所述脂肪酸尾包括C10-28脂族链,或
(b)酸性胆固醇酯,
或(a)和(b)两者;和
iii)与至少一种磷脂结合的聚乙二醇(PEG);和
至少一种包封在脂质体中的内源性碳水化合物。
81.根据实施方案80所述的组合物,其中一种或多种具有极性头部基团的磷脂包括:
1,2-二油酰基-sn-甘油-3-磷酸胆碱;
1,2-二棕榈酰基-磷脂酰基-甘油;
1,2-二油酰基-sn-甘油-3-磷酸甘油;
1,2-二硬脂酰基-sn-甘油-3-磷酸;或
1,2-二油酰基-sn-甘油-3-磷酸-L-丝氨酸,
或其盐,或上述的任何组合。
82.根据实施方案81所述的组合物,其中一种或多种具有极性头部基团的磷脂包括1,2-二油酰基-sn-甘油-3-磷酸胆碱或其盐。
83.一种组合物,其包含:
一种脂质体,其包含:
i)N-十二酰基-1,2-二-(9Z-十八烯酰基)-sn-甘油-3-磷酸乙醇胺或其盐;和
ii)1,2-二油酰基-sn-甘油-3-磷酸胆碱或其盐;和
至少一种包封在所述脂质体中的内源性碳水化合物。
84.根据实施方案83所述的组合物,其中所述脂质体进一步包含与至少一种磷脂结合的PEG。
85.一种组合物,其包含:
一种脂质体,其包含:
i)至少一种具有乙醇胺头部基团和至少一种不饱和脂肪酸尾的磷脂,其中每个不饱和脂肪酸尾独立地包含至少一个C10-28碳链;
ii)一种或多种(a)至(c):
a)至少一种具有极性头部基团和至少一个饱和脂肪酸尾的磷脂,
b)至少一种具有极性头部基团和至少一个不饱和脂肪酸尾的磷脂,其中所述极性头部基团包含季铵阳离子、甘油基或丝氨酸基,和
c)至少一种酸性胆固醇酯;和
iii)聚乙二醇(PEG),其中所述PEG与至少一种磷脂结合;和
至少一种包封在所述脂质体中的内源性碳水化合物。
86.根据实施方案85所述的组合物,其中i)中的至少一种磷脂的每个不饱和脂肪酸尾包含至少一个双键。
87.根据实施方案85或86所述的组合物,其中i)中的至少一种磷脂的每个不饱和脂肪酸尾包含一个双键。
88.根据实施方案85-87任一项所述的组合物,其中所述不饱和脂肪酸尾包含至少一个C16-20碳链。
89.根据实施方案85至88任一项所述的组合物,其中所述具有乙醇胺头部基团和至少一个不饱和脂肪酸尾的磷脂是1,2-二油酰基-sn-甘油-3-磷酸乙醇胺或其盐。
90.根据实施方案85-89任一项所述的组合物,其中a)中的至少一种磷脂的饱和脂肪酸尾包含至少C16-20碳链。
91.根据实施方案85-90任一项所述的组合物,其中所述至少一种具有极性头部基团和饱和脂肪酸尾的磷脂是1,2-二棕榈酰基-sn-甘油-3-磷酸甘油或1,2-二硬脂酰基-sn-甘油-3-磷酸,或其盐或上述的组合。
92.根据实施方案85-91任一项所述的组合物,其中b)中的至少一种磷脂的极性头部基团是胆碱。
93.根据实施方案92所述的组合物,其中所述至少一种具有含季铵阳离子的极性头部基团和不饱和脂肪酸尾的磷脂是1,2-二油酰基-sn-甘油-3-磷酸胆碱或其盐。
94.根据实施方案85-91任一项所述的组合物,其中b)中的至少一种磷脂的极性头部基团是丝氨酸。
95.根据实施方案94所述的组合物,其中所述至少一种具有含丝氨酸基团的极性头部基团和不饱和脂肪酸尾的磷脂是1,2-二油酰基-sn-甘油-3-磷酸-L-丝氨酸或其盐。
96.根据实施方案85-91任一项所述的组合物,其中b)中的至少一种磷脂的极性头部基团是甘油。
97.根据实施方案96所述的组合物,其中至少一种具有含甘油基团的极性头部基团和不饱和脂肪酸尾的磷脂是1,2-二油酰基-sn-甘油-3-磷酸甘油或其盐。
98.根据实施方案85-97任一项所述的组合物,其中所述至少一种酸性胆固醇酯是胆固醇半琥珀酸酯。
99.根据实施方案80-82或84-98任一项所述的组合物,其中与PEG结合的至少一种磷脂是1,2-二硬脂基-sn-甘油-3-磷酸乙醇胺或其盐。
100.一种组合物,其包含:
一种脂质体,其包含:
i)式(PL-1)的磷脂:
或其盐,其中:
T1a和T1b的至少之一是包含C10-28烯基或C10-28炔基的不饱和碳链;和
R1是氨基烷基;
ii)式(PL-2)的磷脂的至少之一、式(PL-3A)的磷脂的至少之一,或式(CE)的胆固醇酯的至少之一,或上述的任何组合:
或其盐,其中:
T2a和T2b各自是包含C10-28烯基或C10-28炔基的不饱和碳链;和
R2是季铵、甘油取代的烷基,或-COOH和-NH2取代的烷基;
或其盐,其中:
T3a和T3b各自是碳链;和
G3是H或至少一个-OH取代的烷基;和
或其盐,其中:
Z1是-COOH取代的烷基;和
iii)聚乙二醇(PEG),其中所述PEG与至少一种磷脂结合;
和
至少一种包封在所述脂质体中的内源性碳水化合物。
101.根据实施方案100所述的组合物,其中T1a、T1b、T2a和T2b各自独立地是包含一个双键的不饱和碳链。
102.根据实施方案101所述的组合物,其中所述不饱和碳链是顺式异构体。
103.根据实施方案100-102任一项所述的组合物,其中每个碳链具有10-28个碳原子。
105.根据实施方案100-104任一项所述的组合物,其中至少一种式(PL-2)的磷脂是
106.根据实施方案100-105任一项所述的组合物,其中至少一种式(PL-3A)的磷脂是
109.一种组合物,其包含:
一种包含式(PL-4)的磷脂的脂质体:
或其盐,其中:
T1a和T1b的至少之一是包含C10-28烯基或C10-28炔基的不饱和碳链;和
R4是包含酰胺部分的脂族链;和
至少一种包封在所述脂质体中的内源性碳水化合物。
111.根据实施方案80-110任一项所述的组合物,其中所述至少一种内源性碳水化合物是:
(i)内源性磷酸化碳水化合物;或
(ii)磷酸化单糖、磷酸化二糖、磷酸化寡糖、磷酸化多糖、磷酸化甘露糖、磷酸化甘露呋喃糖、磷酸化甘露吡喃糖或核苷酸糖,或其任何组合。
112.根据实施方案111所述的组合物,其中所述磷酸化甘露糖是甘露糖-1-磷酸。
113.一种药物组合物,其包含上述任一实施方案的组合物和药学上可接受载体。
114.一种将碳水化合物递送至有需要的人的方法,其包括将上述任一实施方案的组合物给药于所述人。
115.一种将碳水化合物递送至有需要的个体的细胞内部的方法,其包括将实施方案1-113任一项所述的组合物递送至所述个体,其中至少一部分给药组合物穿过细胞质膜以将碳水化合物递送至所述细胞内部。
116.一种治疗有需要的人的先天性糖基化障碍(CDG)的方法,其包括将实施方案1-113任一项所述的组合物给药于所述人。
117.根据实施方案116所述的方法,其中所述先天性糖基化障碍(CDG)是CDG-Ia障碍。
118.根据实施方案116或117所述的方法,其中相比于未将所述组合物给药于所述人的情况下人体内细胞产生的高阶脂质连接的寡糖,所述组合物的给药在人体内诱导细胞产生的高阶脂质连接的寡糖增加0.05倍至至少3倍。
119.一种试剂盒,其包含:
实施方案1至113任一项所述的组合物;
容器;
和容器上或与之相关联的标签或包装说明书。
实施例
以下实施例仅是说明性的,并不意味着以任何方式限制本公开的任何方面。
脂质体
用于脂质体制备的材料购自Avanti Polar Lipids、NOF America Corporation、FormuMax Scientific,Inc.、CordenPharma和Lipoid。以下脂质购自Avanti:DOPE、DOPC、DPPG、DOPG、DOPS、N-C12-DOPE、Chol、CHEMS和DSPE-PEG-Gal。以下脂质购自NOF AmericaCorporation:DSPA、DMG-PEG、ssPalmm、ssPalme、SOPC和PEG(2k)-DSG。以下脂质购自FormuMax Scientific,Inc.:RH-DHPE、DODAP和DOTAP。以下脂质购自CordenPharma:Dlink-KC2-DMA。
将脂质原料溶解在三氯甲烷中,加热至完全溶解。然后干燥混合物形成薄膜。然后用包含磷酸化碳水化合物的水溶液水合所述膜。加热溶液并充分混合以重新悬浮所述薄膜。冻融循环所述悬浮液三次。最后,通过超声处理、挤压或微流化调整所述脂质体的尺寸。
细胞系
CDG-Ia人类真皮成纤维细胞和野生型人类真皮成纤维细胞购自CoriellInstitute。
培养基
将RPMI培养基与FBS(10%v/v)、Pen-Strep(1%v/v)和L-谷氨酰胺(1%v/v)混合,以制备完整的RPMI培养基。该培养基用于所述成纤维细胞的扩增。所有这些都购自ThermoFisher Scientific。
实施例1
筛选和选择用于细胞内递送M1P的脂质
为了选择合适的脂质组合用于细胞内递送M1P,评估不同的Lipo-M1P制剂渗透细胞膜的能力,以及促进内体逃逸和将M1P活性成分释放到所述胞质溶胶中的能力。使用基于功能性细胞的测定法测量Lipo-M1P治疗前后的GDP-甘露糖水平,作为各种脂质体组合物的递送和生物活性的测量。使用实验室规模的薄膜水化法制备共34种不同的Lipo-M1P制剂。用不同的Lipo-M1P制剂处理细胞,总脂质浓度至多为5.4mM。使用XTT细胞增殖试验(ThermoFisher Scientific)测定细胞活性,并且33种受试制剂中有28种将细胞活性维持在所需的80%以上。处理后,收获细胞,提取GDP-甘露糖,并通过液相色谱质谱(LC-MS)进行分析。结果总结于表1。
表1.M1P的脂质体制剂及其对GDP-甘露糖合成和细胞活性的影响
*在总脂质浓度为3.2mM时测量的细胞活性
**在总脂质浓度为0.1mM时测量的细胞活性
NP=未进行
实施例2
Lipo-M1P的初始制剂稳定性研究
对脂质体的M1P渗漏进行体外评估,以表征所述脂质双层和包封的M1P的物理状态,从而了解在生理条件下所述脂质体内部的M1P稳定性。在洗涤新鲜制备的Lipo-M1P颗粒以去除游离的未包封的M1P后,将Lipo-M1P重新悬浮在PBS pH 7.4中并在37℃下储存。所述脂质体组合物是DOPE:DOPC:DSPE-PEG2000=48.5:48.5:3(mol%)。在至多24小时的几个时间点,使用10kDa分子量截止膜(MWCO)离心过滤器分离已从所述颗粒中渗漏的M1P,并通过加入新鲜的PBS使所述过滤器中的脂质体达到原始体积。包含渗漏的M1P的过滤液通过二辛可宁酸测定(BCA测定)定量。M1P渗漏量按总Lipo-M1P的百分比计算,并随时间绘制,如图1所示。观察到可忽略的渗漏量,在24小时时间点仅释放2.5%,因此表明Lipo-M1P颗粒在生理缓冲液中表现出良好的稳定性。
图2A和图2B显示在4℃下储存的第2天、第18天和第30天,在含有Lipo-M1P的PBSpH 7.4中所测量的微米级颗粒的纳米颗粒尺寸分布和浓度。第2天所测量的2至5微米范围内的微米级颗粒的数量代表纳米和微米级颗粒总数的10^-7%。在第2天至第30天期间,未观察到颗粒尺寸和分布的显著变化,这表明Lipo-M1P在冷藏期间聚集的趋势非常有限。分别使用NanoSight和FlowCam颗粒成像系统收集纳米级和微米级范围的数据。
为了Lipo-M1P纳米颗粒在10%FBS中的聚集收集进一步的稳定性数据,其首先在37℃下孵育18小时,然后在4℃下储存21天。在第2天和第21天之间,在PBS中未观察到颗粒尺寸分布的变化(数据未显示)。观察到微米级颗粒的浓度存在轻微的增加现象,但这并未改变10^-7%的总体低百分比。
实施例3
PMM2-CDG成纤维细胞中Lipo-M1P生物活性的体外研究
本实施例研究各种Lipo-M1P制剂在患者来源的培养成纤维细胞中的生物活性。使用三种Lipo-M1P制剂:
制剂A:DOPE/DOPC/DSPE-PEG(2000)=58.2:38.8:3;
制剂B:N-C12-DOPE/DOPC/DSPE-PEG(2000)=69.6:27.4:3
制剂C:DSPC/Chol/DSPE-PEG/DOTAP/Rh-DHPE=24:45:5:25:0.5
将患者来源的培养成纤维细胞以0.15-0.72mM浓度范围的制剂A处理18小时。显示未经治疗的患者和正常成纤维细胞的GDP-甘露糖增加的质谱分析见图3A。M1P代谢物的水平通过低剂量的Lipo-M1P(约0.35mM)过夜处理而归一化。正如所预期的,GDP-甘露糖随着Lipo-M1P浓度的增加。在所研究的Lipo-M1P浓度范围内,细胞活性维持在接近100%,见图3B。
为了确定全长成熟LLO水平的降低是否可以用制剂B纠正,将患者成纤维细胞与0.24mM Lipo-M1P(用于LLO研究)和0.06-0.48mM浓度范围的Lipo-M1P(用于ICAM-1)一起孵育。经过18小时处理后,收获细胞,提取LLO,用荧光标记物标记,并通过荧光团辅助碳水化合物电泳(FACE)进行检测。定性结果见图4。Lipo-M1P治疗增加全长LLO的水平,这表明所递送的M1P正在被代谢为GDP-甘露糖并进入LLO生物合成途径。
为了评估治疗对蛋白质生物标记物细胞间粘附分子1(ICAM-1)水平的影响,使用Mem-PERTM Plus膜蛋白提取试剂盒(Thermo Fisher Scientific)提取ICAM-1,并使用抗ICAM-1抗体(R&D)通过蛋白质印迹法可视化。结果见图5。ICAM-1中的浓度依赖性增加提供证据,即制剂C恢复了N-聚糖生物合成途径并纠正患者细胞中的蛋白质低糖基化。
实施例4
CD-1小鼠体内的Lipo-M1P生物分布及药代动力学
在Bayside Biosciences(Santa Clara,CA)进行评估Lipo-M1P在雌性CD-1小鼠体内的药代动力学的研究。十六只CD-1雌性小鼠经尾静脉注射俄勒冈绿色标记的Lipo-M1P,其剂量为250mg/kg脂质和12.5mg/kg M1P。所述脂质体组合物为DOPE:DOPC:DSPE-PEG,DOPE与DOPC的比为1:1(mol%)。将小鼠分为四组,在至多48小时的多个时间点,在每个时间点选择一组进行血浆收集或进行血浆和肝脏收集。使用俄勒冈绿色标记的荧光测量血浆和均质化肝脏中脂质体的浓度。Lipo-M1P的药代动力学概况总结于表2。
表2.Lipo-M1P在小鼠体内的药代动力学概况
n=4;平均值±标准误差
使用Pharsight NLME 7.0软件(Certara)进行总体PK建模。最佳拟合是通过附加2室清除模型获得的。
除了血浆PK之外,评估肝脏中的脂质体PK,如图6A所示。肝脏中的消除半衰期为6.22h。评估Lipo-M1P的肝内分布,并确认Lipo-M1P向肝细胞的递送。四只CD-1雌性小鼠以290mg/kg脂质和15mg/kg M1P的剂量给药俄勒冈绿色标记的Lipo-M1P。注射1小时后处死小鼠,使用肝脏消化培养基(Thermo Fisher Scientific)灌注和消化肝脏。采用Percoll密度梯度离心法从消化的肝脏悬液中分离出肝细胞和非实质细胞(nonparenchymal cell)。使用流式细胞术检测肝细胞和NPC中脂质体的荧光。减去细胞的自发荧光。图6B显示Lipo-M1P优先被肝细胞吸收,而未观察到Lipo-M1P统计显著吸收至NPC。
广泛评估PEG化和所示脂质体的表面上半乳糖部分的存在对Lipo-M1P肝脏吸收的影响(数据未显示)。分子量为2000Da的3%和5%PEG之间的肝脏吸收没有显著差异。将PEG长度减少至350Da并将其百分比增加至7.5%,这导致细胞吸收增加1倍;但是,它显著降低血浆半衰期。半乳糖部分在体外或体内均未显著提高所示脂质体的肝细胞靶向能力。
实施例5
大鼠体内Lipo-M1P的安全性和毒性
在Charles River Laboratories对Sprague Dawley大鼠进行剂量递增和重复剂量研究。动物在研究开始时大约五周龄。通过静脉内(缓慢推注)将Lipo-M1P注射到所述尾静脉中。在剂量递增阶段,将单剂量的Lipo-M1P(DOPE/DOPC/DSPE-PEG/M1P,脂质比:48.5:48.5:3)给药于四组(每组三只雄性)。第1组每kg体重给药100mg脂质,第2组给药250mg/kg,第3组给药500mg/kg,和第4组给药652.8mg/kg。给药最大M1P剂量(第4组)为47.1mg/kgM1P。第4组剂量为10ml/kg的最大可行剂量体积。在进入后续给药组之前,维持24小时的观察期。在任何浓度下均未观察到临床效果。每组三只雌性接受652.8mg/kg脂质的最大剂量。未观察到任何临床效果。在给药后7天从所有动物中抽取血液用于临床化学和血液学分析。在雄性中,观察到红细胞和血小板的小剂量依赖性增加。结果总结于表3。使用类似的方案对大鼠进行Lipo-M1P给药(N-C12-DOPE/DOPC/DSPE-PEG/M1P;脂质比:69.6:27.4:3),其中最大可行剂量为864.2mg/kg(86.42mg/ml脂质的10ml/kg剂量体积),在任何剂量下均未观察到不良临床效果。临床病理学结果总结于表3。
表3剂量递增阶段主要临床病理学发现总结
使用脂质浓度为62mg/ml的Lipo-M1P进行重复剂量研究。一组三只雄性和三只雌性,每组连续七天每天接受620mg/kg脂质(34.3mg/kg M1P)的静脉推注。该剂量代表10ml/kg的最大可行剂量体积。在给药阶段未观察到任何临床效果。在最后一次给药后一天,抽取血液用于临床化学和血液学分析,并进行尸检。未观察到可见病变。临床病理学结果总结于表4和表5。
表4.重复Lipo-M1P剂量阶段的主要临床化学发现总结
表4
表5.重复Lipo-M1P剂量阶段的主要血液学/凝血发现总结
表5
在大鼠体内进行的单次剂量递增研究(最高652.8mg/kg的Lipo-M1P(即47.1mg/kg的M1P))未显示任何临床效果。然后对3只雄性大鼠和3只雌性大鼠进行重复剂量为620mg/kg的Lipo-M1P(即34.3mg/kg的M1P)的每日推注,持续7天。不存在可见临床表现和在尸检下无可见病变。雄性和雌性的血浆胆固醇均存在增加。
Claims (40)
1.一种组合物,其包含:
一种脂质体,其包含:
i)1,2-二油酰基-sn-甘油-3-磷酸乙醇胺或其盐;和
ii)(a)一种或多种具有极性头部基团和脂肪酸尾的磷脂,其中所述极性头部基团包括甘油、胆碱、磷酸和丝氨酸,所述脂肪酸尾包括C10-28脂族链,或
(b)酸性胆固醇酯,
或(a)和(b)两者;和
iii)与至少一种磷脂结合的聚乙二醇(PEG);和
包封在所述脂质体内的至少一种内源性磷酸化碳水化合物。
2.根据权利要求1所述的组合物,其中一种或多种具有极性头部基团的磷脂包括:
1,2-二油酰基-sn-甘油-3-磷酸胆碱;
1,2-二棕榈酰基-磷脂酰基-甘油;
1,2-二油酰基-sn-甘油-3-磷酸甘油;
1,2-二硬脂酰基-sn-甘油-3-磷酸;或
1,2-二油酰基-sn-甘油-3-磷酸-L-丝氨酸,
或其盐,
或上述的任何组合。
3.根据权利要求2所述的组合物,其中一种或多种具有极性头部基团的磷脂包括1,2-二油酰基-sn-甘油-3-磷酸胆碱或其盐。
4.一种组合物,其包含:
一种脂质体,其包含:
i)N-十二酰基-1,2-二-(9Z-十八烯酰基)-sn-甘油-3-磷酸乙醇胺或其盐;和
ii)1,2-二油酰基-sn-甘油-3-磷酸胆碱或其盐;和
包封在所述脂质体内的至少一种内源性磷酸化碳水化合物。
5.根据权利要求4所述的组合物,其中所述脂质体进一步包含与至少一种磷脂结合的PEG。
6.一种组合物,其包含:
一种脂质体,其包含:
i)至少一种具有乙醇胺头部基团和至少一种不饱和脂肪酸尾的磷脂,其中每个不饱和脂肪酸尾独立地包含至少一个C10-28的碳链;
ii)(a)至(c)的一种或多种:
a)至少一种具有极性头部基团和至少一种饱和脂肪酸尾的磷脂,
b)至少一种具有极性头部基团和至少一种不饱和脂肪酸尾的磷脂,其中所述极性头部基团包括季铵阳离子、甘油基团或丝氨酸基团,和
c)至少一种酸性胆固醇酯;和
iii)聚乙二醇(PEG);其中所述PEG与至少一种磷脂结合;和
包封在所述脂质体内的至少一种内源性磷酸化碳水化合物。
7.根据权利要求6所述的组合物,其中i)中的至少一种磷脂的每个不饱和脂肪酸尾包含至少一个双键。
8.根据权利要求6或7所述的组合物,其中i)中的至少一种磷脂的每个不饱和脂肪酸尾包含一个双键。
9.根据权利要求6-8任一项所述的组合物,其中所述不饱和脂肪酸尾包含至少一个C16-20碳链。
10.根据权利要求6-9任一项所述的组合物,其中具有乙醇胺头部基团和至少一种不饱和脂肪酸的磷脂是1,2-二油酰基-sn-甘油-3-磷酸乙醇胺或其盐。
11.根据权利要求6-10任一项所述的组合物,其中a)中的至少一种磷脂的饱和脂肪酸尾包含至少C16-20碳链。
12.根据权利要求6-11任一项所述的组合物,其中至少一种具有极性头部基团和饱和脂肪酸尾的磷脂是1,2-二棕榈酰基-sn-甘油-3-磷酸甘油或1,2-二硬脂酰-sn-甘油-3-磷酸,或其盐,或上述的组合。
13.根据权利要求6-12任一项所述的组合物,其中b)中的至少一种磷脂的极性头部基团是胆碱。
14.根据权利要求6-12任一项所述的组合物,其中所述至少一种具有含季铵阳离子的极性头部基团和不饱和脂肪酸尾的磷脂是1,2-二油酰基-sn-甘油-3-磷酸胆碱或其盐。
15.根据权利要求6-12任一项所述的组合物,其中b)中的至少一种磷脂的极性头部基团是丝氨酸。
16.根据权利要求6-12任一项所述的组合物,其中所述至少一种具有含丝氨酸基团的极性头部基团和不饱和脂肪酸尾的磷脂是1,2-二油酰基-sn-甘油-3-磷酸-L-丝氨酸或其盐。
17.根据权利要求6-12任一项所述的组合物,其中b)中的至少一种磷脂的极性头部基团是甘油。
18.根据权利要求6-12任一项所述的组合物,其中所述至少一种具有含甘油基团的极性头部基团和不饱和脂肪酸尾的磷脂是1,2-二油酰基-sn-甘油-3-磷酸甘油或其盐。
19.根据权利要求6-18任一项所述的组合物,其中所述至少一种酸性胆固醇酯是胆固醇半琥珀酸酯。
20.根据权利要求1-3或5-19任一项所述的组合物,其中所述与PEG结合的至少一种磷脂是1,2-二硬脂酰-sn-甘油-3-磷酸乙醇胺或其盐。
21.一种组合物,其包含:
一种脂质体,其包含:
i)式(PL-1)的磷脂
或其盐,其中:
T1a和T1b的至少之一是不饱和碳链,其包含C10-28烯基或C10-28炔基;和
R1是氨基烷基;
ii)式(PL-2)的磷脂的至少之一,式(PL-3A)的磷脂的至少之一,或式(CE)的胆固醇酯的至少之一,或上述的任何组合:
或其盐,其中:
T2a和T2b各自是不饱和碳链,其包含C10-28烯基或C10-28炔基;和
R2是季铵、甘油取代的烷基或–COOH和–NH2取代的烷基;
或其盐,其中:
T3a和T3b各自是碳链;和
G3是H或至少一个–OH取代的烷基;和
或其盐,其中:
Z1是–COOH取代的烷基;和
iii)聚乙烯醇(PEG),其中所述PEG与至少一种磷脂结合;和包封在所述脂质体内的至少一种内源性磷酸化碳水化合物。
22.根据权利要求21所述的组合物,其中T1a、T1b、T2a、T2b各自独自地是包含一个双键的不饱和碳链其。
23.根据权利要求22所述的组合物,其中所述不饱和碳链是顺式异构体。
24.根据权利要求21-23任一项所述的组合物,其中每个碳链具有10-28个碳原子。
32.根据权利要求1-31任一项所述的组合物,其中所述至少一种内源性磷酸化碳水化合物是磷酸化单糖、磷酸化二糖、磷酸化寡糖、磷酸化多糖、磷酸化甘露糖、磷酸化甘露呋喃糖、磷酸化甘露吡喃糖或核苷酸糖,或其任何组合。
33.根据权利要求32所述的组合物,其中所述磷酸化甘露糖是甘露糖-1-磷酸。
34.一种药物组合物,其包含上述权利要求任一项所述的组合物,和药学上可接受载体。
35.一种用于将碳水化合物递送至有需要的人的方法,其包括将上述权利要求任一项的组合物施用于所述人。
36.一种用于将碳水化合物递送至有需要的个体的细胞内部的方法,其包括将权利要求1-34任一项的组合物施用于所述个体,其中至少一部分给药组合物的穿过所述细胞质膜以将所述碳水化合物递送至所述细胞内部。
37.一种用于治疗有需要的人的先天性糖基化障碍(CDG)的方法,其包括将权利要求1-34任一项的组合物给药于所述人。
38.根据权利要求37所述的方法,其中所述先天性糖基化障碍(CDG)是CDG-Ia障碍。
39.根据权利要求37或38所述的方法,其中相比于未将所述组合物给药于人的情况下人体内细胞产生的高阶脂质连接的寡糖,所述组合物的给药在人体内诱导细胞产生的高阶脂质连接的寡糖增加0.05倍至至少3倍。
40.一种试剂盒,其包括:
权利要求1-34任一项的组合物;
容器;和
在所述容器上或与所述容器相关联的标签或药品说明书。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201962826874P | 2019-03-29 | 2019-03-29 | |
| US62/826,874 | 2019-03-29 | ||
| PCT/US2020/025246 WO2020205530A1 (en) | 2019-03-29 | 2020-03-27 | Liposomal formulations, and methods of using and preparing thereof |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN113873998A true CN113873998A (zh) | 2021-12-31 |
Family
ID=72666933
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202080038191.4A Pending CN113873998A (zh) | 2019-03-29 | 2020-03-27 | 脂质体制剂及其使用和制备方法 |
Country Status (18)
| Country | Link |
|---|---|
| US (1) | US20220184107A1 (zh) |
| EP (1) | EP3946365A4 (zh) |
| JP (1) | JP2022527638A (zh) |
| KR (1) | KR20210143906A (zh) |
| CN (1) | CN113873998A (zh) |
| AR (1) | AR119705A1 (zh) |
| AU (1) | AU2020252005A1 (zh) |
| BR (1) | BR112021019593A2 (zh) |
| CA (1) | CA3134828A1 (zh) |
| CL (1) | CL2021002512A1 (zh) |
| CO (1) | CO2021014274A2 (zh) |
| EA (1) | EA202192663A1 (zh) |
| IL (1) | IL286713A (zh) |
| MX (1) | MX2021011876A (zh) |
| PE (1) | PE20212366A1 (zh) |
| SG (1) | SG11202110623PA (zh) |
| TW (1) | TW202102231A (zh) |
| WO (1) | WO2020205530A1 (zh) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2023205628A1 (en) * | 2022-04-18 | 2023-10-26 | City Of Hope | Lipid nanoparticles, nucleic acids, and methods of use |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1509166A (zh) * | 2001-03-26 | 2004-06-30 | 用于改善治疗物质的细胞内传递的脂质体组合物 | |
| US20110014272A1 (en) * | 2009-05-14 | 2011-01-20 | Sanofi Pasteur | Method for adjuvanting lipopolysaccharide (LPS) of Gram-negative bacteria |
| US20160228364A1 (en) * | 2013-09-16 | 2016-08-11 | Glycomine, Inc. | Pharmaceutical preparation of carbohydrates for therapeutic use |
| US20170165374A1 (en) * | 2015-11-18 | 2017-06-15 | Insmed, Inc. | Compositions and methods for treating bacterial infections |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7491409B1 (en) * | 1999-03-02 | 2009-02-17 | Transave, Inc. | Encapsulation of bioactive complexes in liposomes |
| US7060291B1 (en) * | 1999-11-24 | 2006-06-13 | Transave, Inc. | Modular targeted liposomal delivery system |
| US20090191259A1 (en) * | 2002-01-09 | 2009-07-30 | Transave, Inc. | Efficient liposomal encapsulation |
| EP1478341A4 (en) * | 2002-01-09 | 2009-05-20 | Transave Inc | EFFICIENT ENCAPSULATION OF NUCLEIC ACIDS IN MEDIUM SIZE LIPOSOMES |
-
2020
- 2020-03-27 CA CA3134828A patent/CA3134828A1/en active Pending
- 2020-03-27 BR BR112021019593A patent/BR112021019593A2/pt unknown
- 2020-03-27 EP EP20782039.0A patent/EP3946365A4/en active Pending
- 2020-03-27 AR ARP200100841A patent/AR119705A1/es unknown
- 2020-03-27 JP JP2021560323A patent/JP2022527638A/ja active Pending
- 2020-03-27 MX MX2021011876A patent/MX2021011876A/es unknown
- 2020-03-27 KR KR1020217035257A patent/KR20210143906A/ko unknown
- 2020-03-27 AU AU2020252005A patent/AU2020252005A1/en active Pending
- 2020-03-27 SG SG11202110623PA patent/SG11202110623PA/en unknown
- 2020-03-27 WO PCT/US2020/025246 patent/WO2020205530A1/en active Application Filing
- 2020-03-27 EA EA202192663A patent/EA202192663A1/ru unknown
- 2020-03-27 US US17/593,755 patent/US20220184107A1/en active Pending
- 2020-03-27 TW TW109110461A patent/TW202102231A/zh unknown
- 2020-03-27 CN CN202080038191.4A patent/CN113873998A/zh active Pending
- 2020-03-27 PE PE2021001645A patent/PE20212366A1/es unknown
-
2021
- 2021-09-26 IL IL286713A patent/IL286713A/en unknown
- 2021-09-28 CL CL2021002512A patent/CL2021002512A1/es unknown
- 2021-10-26 CO CONC2021/0014274A patent/CO2021014274A2/es unknown
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1509166A (zh) * | 2001-03-26 | 2004-06-30 | 用于改善治疗物质的细胞内传递的脂质体组合物 | |
| US20110014272A1 (en) * | 2009-05-14 | 2011-01-20 | Sanofi Pasteur | Method for adjuvanting lipopolysaccharide (LPS) of Gram-negative bacteria |
| US20160228364A1 (en) * | 2013-09-16 | 2016-08-11 | Glycomine, Inc. | Pharmaceutical preparation of carbohydrates for therapeutic use |
| US20170165374A1 (en) * | 2015-11-18 | 2017-06-15 | Insmed, Inc. | Compositions and methods for treating bacterial infections |
Also Published As
| Publication number | Publication date |
|---|---|
| CA3134828A1 (en) | 2020-10-08 |
| CL2021002512A1 (es) | 2023-01-06 |
| IL286713A (en) | 2021-10-31 |
| MX2021011876A (es) | 2022-01-04 |
| CO2021014274A2 (es) | 2022-01-17 |
| AR119705A1 (es) | 2022-01-05 |
| EA202192663A1 (ru) | 2022-03-01 |
| EP3946365A4 (en) | 2023-04-19 |
| KR20210143906A (ko) | 2021-11-29 |
| WO2020205530A1 (en) | 2020-10-08 |
| TW202102231A (zh) | 2021-01-16 |
| JP2022527638A (ja) | 2022-06-02 |
| PE20212366A1 (es) | 2021-12-21 |
| EP3946365A1 (en) | 2022-02-09 |
| US20220184107A1 (en) | 2022-06-16 |
| SG11202110623PA (en) | 2021-10-28 |
| BR112021019593A2 (pt) | 2021-12-14 |
| AU2020252005A1 (en) | 2021-11-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11701432B2 (en) | Polyglutamated antifolates and uses thereof | |
| US20240082155A1 (en) | Pharmaceutical preparation of carbohydrates for therapeutic use | |
| US20190307755A1 (en) | Polyglutamated antifolates and uses thereof | |
| US8241663B2 (en) | Liposome preparation | |
| WO2013166498A1 (en) | Lipid-based drug carriers for rapid penetration through mucus linings | |
| KR20140065017A (ko) | 약물 담체 | |
| CN106456546A (zh) | 用于黏膜递送的脂质体组合物 | |
| JP2018508523A (ja) | コクリエート、及び薬理活性物質の組織透過性を高めるためにそれを使用する方法 | |
| CN113873998A (zh) | 脂质体制剂及其使用和制备方法 | |
| US20240123028A1 (en) | Formulated and/or Co-Formulated Liposome Compositions Containing Toll-Like Receptor ("TLR") Agonist Prodrugs Useful In The Treatment of Cancer and Methods Thereof C | |
| JP2005298486A (ja) | リポソームを含む癌治療用医薬組成物 | |
| US20240050575A1 (en) | Formulated and/or co-formulated liposome compositions containg TGFb antagonist prodrugs useful in the treatment of cancer and methods thereof | |
| US20230226031A1 (en) | Formulated and/or Co-Formulated Liposome Compositions Containing Immunogenic Cell Death (ICD) Inducing Prodrugs Useful In The Treatment of Cancer and Methods Thereof | |
| US20210163418A1 (en) | Formulated and/or Co-Formulated Liposome Compositions Containing IDO Antagonist Prodrugs Useful In The Treatment of Cancer and Methods Thereof | |
| US20240108732A1 (en) | Formulated and/or Co-Formulated Lipid Nanocarriers Compositions Containing Toll-Like Receptor ("TLR") Agonist Prodrugs Useful In The Treatment of Cancer and Methods Thereof | |
| US20240082407A1 (en) | Formulated and/or co-formulated liposome compositions containing PD-1 antagonist prodrugs useful in the treatment of cancer and methods thereof | |
| AU2022212571A1 (en) | Oral liposomal compositions | |
| JPH1171266A (ja) | キサンチン誘導体のリポソーム製剤 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |