CN113347976A - 用牛磺罗定水解产物进行的神经母细胞瘤治疗 - Google Patents
用牛磺罗定水解产物进行的神经母细胞瘤治疗 Download PDFInfo
- Publication number
- CN113347976A CN113347976A CN201980071416.3A CN201980071416A CN113347976A CN 113347976 A CN113347976 A CN 113347976A CN 201980071416 A CN201980071416 A CN 201980071416A CN 113347976 A CN113347976 A CN 113347976A
- Authority
- CN
- China
- Prior art keywords
- composition
- oxathiadiazine
- neuroblastoma
- sulfonamide
- administered
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 206010029260 Neuroblastoma Diseases 0.000 title claims abstract description 56
- AJKIRUJIDFJUKJ-UHFFFAOYSA-N taurolidine Chemical compound C1NS(=O)(=O)CCN1CN1CNS(=O)(=O)CC1 AJKIRUJIDFJUKJ-UHFFFAOYSA-N 0.000 title abstract description 42
- 229960004267 taurolidine Drugs 0.000 title abstract description 42
- 239000000413 hydrolysate Substances 0.000 title abstract description 26
- 238000011282 treatment Methods 0.000 title abstract description 9
- 206010028980 Neoplasm Diseases 0.000 claims abstract description 26
- 229940124530 sulfonamide Drugs 0.000 claims abstract description 17
- 241000283690 Bos taurus Species 0.000 claims abstract description 14
- 150000003456 sulfonamides Chemical class 0.000 claims abstract description 14
- 230000000174 oncolytic effect Effects 0.000 claims abstract description 10
- XNWFRZJHXBZDAG-UHFFFAOYSA-N 2-METHOXYETHANOL Chemical compound COCCO XNWFRZJHXBZDAG-UHFFFAOYSA-N 0.000 claims abstract 3
- CKFGINPQOCXMAZ-UHFFFAOYSA-N methanediol Chemical compound OCO CKFGINPQOCXMAZ-UHFFFAOYSA-N 0.000 claims description 42
- 238000000034 method Methods 0.000 claims description 29
- GZJCRTOUHIUTSE-UHFFFAOYSA-N oxathiadiazine Chemical compound O1SN=NC=C1 GZJCRTOUHIUTSE-UHFFFAOYSA-N 0.000 claims description 29
- 239000000203 mixture Substances 0.000 claims description 26
- 239000002105 nanoparticle Substances 0.000 claims description 25
- 230000004044 response Effects 0.000 claims description 18
- 230000003442 weekly effect Effects 0.000 claims description 18
- 238000000576 coating method Methods 0.000 claims description 15
- 239000011248 coating agent Substances 0.000 claims description 14
- 230000007062 hydrolysis Effects 0.000 claims description 10
- 238000006460 hydrolysis reaction Methods 0.000 claims description 10
- 238000001959 radiotherapy Methods 0.000 claims description 9
- -1 tauryl amine Chemical class 0.000 claims description 9
- 239000002202 Polyethylene glycol Substances 0.000 claims description 8
- 239000003795 chemical substances by application Substances 0.000 claims description 8
- 229920001223 polyethylene glycol Polymers 0.000 claims description 8
- 229920000642 polymer Polymers 0.000 claims description 8
- JZFICWYCTCCINF-UHFFFAOYSA-N Thiadiazin Chemical compound S=C1SC(C)NC(C)N1CCN1C(=S)SC(C)NC1C JZFICWYCTCCINF-UHFFFAOYSA-N 0.000 claims description 7
- 230000002028 premature Effects 0.000 claims description 7
- MVQXBXLDXSQURK-UHFFFAOYSA-N 2-aminoethanesulfonamide Chemical compound NCCS(N)(=O)=O MVQXBXLDXSQURK-UHFFFAOYSA-N 0.000 claims description 6
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 claims description 6
- 235000019256 formaldehyde Nutrition 0.000 claims description 6
- 238000003780 insertion Methods 0.000 claims description 5
- 230000037431 insertion Effects 0.000 claims description 5
- 238000012384 transportation and delivery Methods 0.000 claims description 4
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 claims description 3
- 150000002632 lipids Chemical class 0.000 claims description 3
- QMEQBOSUJUOXMX-UHFFFAOYSA-N 2h-oxadiazine Chemical compound N1OC=CC=N1 QMEQBOSUJUOXMX-UHFFFAOYSA-N 0.000 claims 1
- 238000007918 intramuscular administration Methods 0.000 claims 1
- 238000001990 intravenous administration Methods 0.000 claims 1
- 229940079593 drug Drugs 0.000 abstract description 5
- 239000003814 drug Substances 0.000 abstract description 5
- 230000004083 survival effect Effects 0.000 abstract description 5
- 241000124008 Mammalia Species 0.000 abstract description 3
- 201000011510 cancer Diseases 0.000 abstract description 2
- 230000003902 lesion Effects 0.000 abstract description 2
- 238000004113 cell culture Methods 0.000 abstract 2
- 241000283984 Rodentia Species 0.000 abstract 1
- 230000002924 anti-infective effect Effects 0.000 abstract 1
- 238000011808 rodent model Methods 0.000 abstract 1
- 210000004027 cell Anatomy 0.000 description 16
- 238000000338 in vitro Methods 0.000 description 10
- 238000001727 in vivo Methods 0.000 description 9
- 239000004480 active ingredient Substances 0.000 description 8
- 238000002560 therapeutic procedure Methods 0.000 description 7
- 230000015556 catabolic process Effects 0.000 description 6
- 238000006731 degradation reaction Methods 0.000 description 6
- 201000010099 disease Diseases 0.000 description 6
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 6
- SHGAZHPCJJPHSC-NUEINMDLSA-N Isotretinoin Chemical compound OC(=O)C=C(C)/C=C/C=C(C)C=CC1=C(C)CCCC1(C)C SHGAZHPCJJPHSC-NUEINMDLSA-N 0.000 description 5
- 229960005280 isotretinoin Drugs 0.000 description 5
- 238000001356 surgical procedure Methods 0.000 description 5
- 238000011579 SCID mouse model Methods 0.000 description 4
- 230000007246 mechanism Effects 0.000 description 4
- 239000000047 product Substances 0.000 description 4
- 210000001519 tissue Anatomy 0.000 description 4
- 241000699666 Mus <mouse, genus> Species 0.000 description 3
- 241000699670 Mus sp. Species 0.000 description 3
- 238000009175 antibody therapy Methods 0.000 description 3
- 210000002950 fibroblast Anatomy 0.000 description 3
- CMSMOCZEIVJLDB-UHFFFAOYSA-N Cyclophosphamide Chemical compound ClCCN(CCCl)P1(=O)NCCCO1 CMSMOCZEIVJLDB-UHFFFAOYSA-N 0.000 description 2
- 229940123780 DNA topoisomerase I inhibitor Drugs 0.000 description 2
- 229940124087 DNA topoisomerase II inhibitor Drugs 0.000 description 2
- 102000004457 Granulocyte-Macrophage Colony-Stimulating Factor Human genes 0.000 description 2
- 108010017213 Granulocyte-Macrophage Colony-Stimulating Factor Proteins 0.000 description 2
- 108010002350 Interleukin-2 Proteins 0.000 description 2
- 108700026495 N-Myc Proto-Oncogene Proteins 0.000 description 2
- 239000000365 Topoisomerase I Inhibitor Substances 0.000 description 2
- 239000000317 Topoisomerase II Inhibitor Substances 0.000 description 2
- 229940122803 Vinca alkaloid Drugs 0.000 description 2
- 238000007792 addition Methods 0.000 description 2
- 229940100198 alkylating agent Drugs 0.000 description 2
- 239000002168 alkylating agent Substances 0.000 description 2
- 230000000259 anti-tumor effect Effects 0.000 description 2
- 229940045985 antineoplastic platinum compound Drugs 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 229960004562 carboplatin Drugs 0.000 description 2
- YAYRGNWWLMLWJE-UHFFFAOYSA-L carboplatin Chemical compound O=C1O[Pt](N)(N)OC(=O)C11CCC1 YAYRGNWWLMLWJE-UHFFFAOYSA-L 0.000 description 2
- 229960004316 cisplatin Drugs 0.000 description 2
- DQLATGHUWYMOKM-UHFFFAOYSA-L cisplatin Chemical compound N[Pt](N)(Cl)Cl DQLATGHUWYMOKM-UHFFFAOYSA-L 0.000 description 2
- 229960004397 cyclophosphamide Drugs 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- 230000002068 genetic effect Effects 0.000 description 2
- 229960001101 ifosfamide Drugs 0.000 description 2
- HOMGKSMUEGBAAB-UHFFFAOYSA-N ifosfamide Chemical compound ClCCNP1(=O)OCCCN1CCCl HOMGKSMUEGBAAB-UHFFFAOYSA-N 0.000 description 2
- 238000009169 immunotherapy Methods 0.000 description 2
- 230000006698 induction Effects 0.000 description 2
- 208000015181 infectious disease Diseases 0.000 description 2
- 230000002401 inhibitory effect Effects 0.000 description 2
- 238000011368 intensive chemotherapy Methods 0.000 description 2
- 229960004768 irinotecan Drugs 0.000 description 2
- UWKQSNNFCGGAFS-XIFFEERXSA-N irinotecan Chemical compound C1=C2C(CC)=C3CN(C(C4=C([C@@](C(=O)OC4)(O)CC)C=4)=O)C=4C3=NC2=CC=C1OC(=O)N(CC1)CCC1N1CCCCC1 UWKQSNNFCGGAFS-XIFFEERXSA-N 0.000 description 2
- 208000032839 leukemia Diseases 0.000 description 2
- 210000004698 lymphocyte Anatomy 0.000 description 2
- 229960001924 melphalan Drugs 0.000 description 2
- SGDBTWWWUNNDEQ-LBPRGKRZSA-N melphalan Chemical compound OC(=O)[C@@H](N)CC1=CC=C(N(CCCl)CCCl)C=C1 SGDBTWWWUNNDEQ-LBPRGKRZSA-N 0.000 description 2
- 230000001537 neural effect Effects 0.000 description 2
- 150000003058 platinum compounds Chemical class 0.000 description 2
- 238000004393 prognosis Methods 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 238000011476 stem cell transplantation Methods 0.000 description 2
- 210000002820 sympathetic nervous system Anatomy 0.000 description 2
- 229960000303 topotecan Drugs 0.000 description 2
- UCFGDBYHRUNTLO-QHCPKHFHSA-N topotecan Chemical compound C1=C(O)C(CN(C)C)=C2C=C(CN3C4=CC5=C(C3=O)COC(=O)[C@]5(O)CC)C4=NC2=C1 UCFGDBYHRUNTLO-QHCPKHFHSA-N 0.000 description 2
- 230000035899 viability Effects 0.000 description 2
- OGWKCGZFUXNPDA-XQKSVPLYSA-N vincristine Chemical compound C([N@]1C[C@@H](C[C@]2(C(=O)OC)C=3C(=CC4=C([C@]56[C@H]([C@@]([C@H](OC(C)=O)[C@]7(CC)C=CCN([C@H]67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)C[C@@](C1)(O)CC)CC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-XQKSVPLYSA-N 0.000 description 2
- 229960004528 vincristine Drugs 0.000 description 2
- OGWKCGZFUXNPDA-UHFFFAOYSA-N vincristine Natural products C1C(CC)(O)CC(CC2(C(=O)OC)C=3C(=CC4=C(C56C(C(C(OC(C)=O)C7(CC)C=CCN(C67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)CN1CCC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-UHFFFAOYSA-N 0.000 description 2
- RJGYJMFQWGPBGM-UHFFFAOYSA-N 1,2,4-thiadiazinane 1,1-dioxide Chemical compound O=S1(=O)CCNCN1 RJGYJMFQWGPBGM-UHFFFAOYSA-N 0.000 description 1
- VPVXHAANQNHFSF-UHFFFAOYSA-N 1,4-dioxan-2-one Chemical compound O=C1COCCO1 VPVXHAANQNHFSF-UHFFFAOYSA-N 0.000 description 1
- RKDVKSZUMVYZHH-UHFFFAOYSA-N 1,4-dioxane-2,5-dione Chemical compound O=C1COC(=O)CO1 RKDVKSZUMVYZHH-UHFFFAOYSA-N 0.000 description 1
- 108090000312 Calcium Channels Proteins 0.000 description 1
- 102000003922 Calcium Channels Human genes 0.000 description 1
- 108020004414 DNA Proteins 0.000 description 1
- 102000001706 Immunoglobulin Fab Fragments Human genes 0.000 description 1
- 108010054477 Immunoglobulin Fab Fragments Proteins 0.000 description 1
- 102000055056 N-Myc Proto-Oncogene Human genes 0.000 description 1
- 102000004129 N-Type Calcium Channels Human genes 0.000 description 1
- 108090000699 N-Type Calcium Channels Proteins 0.000 description 1
- 206010052399 Neuroendocrine tumour Diseases 0.000 description 1
- 108010009736 Protein Hydrolysates Proteins 0.000 description 1
- 210000001015 abdomen Anatomy 0.000 description 1
- 210000004100 adrenal gland Anatomy 0.000 description 1
- 230000003321 amplification Effects 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 230000000845 anti-microbial effect Effects 0.000 description 1
- 239000004599 antimicrobial Substances 0.000 description 1
- 239000002246 antineoplastic agent Substances 0.000 description 1
- 238000010322 bone marrow transplantation Methods 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 230000003833 cell viability Effects 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 210000003169 central nervous system Anatomy 0.000 description 1
- 208000025997 central nervous system neoplasm Diseases 0.000 description 1
- 238000002512 chemotherapy Methods 0.000 description 1
- 210000000038 chest Anatomy 0.000 description 1
- 230000003750 conditioning effect Effects 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 238000012937 correction Methods 0.000 description 1
- 229940127089 cytotoxic agent Drugs 0.000 description 1
- 238000012217 deletion Methods 0.000 description 1
- 230000037430 deletion Effects 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- 150000002334 glycols Chemical class 0.000 description 1
- 238000011134 hematopoietic stem cell transplantation Methods 0.000 description 1
- 230000003301 hydrolyzing effect Effects 0.000 description 1
- 239000007943 implant Substances 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 230000036210 malignancy Effects 0.000 description 1
- 230000010534 mechanism of action Effects 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 108091070501 miRNA Proteins 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000002625 monoclonal antibody therapy Methods 0.000 description 1
- 210000003739 neck Anatomy 0.000 description 1
- 210000000933 neural crest Anatomy 0.000 description 1
- 208000016065 neuroendocrine neoplasm Diseases 0.000 description 1
- 201000011519 neuroendocrine tumor Diseases 0.000 description 1
- 208000027831 neuroepithelial neoplasm Diseases 0.000 description 1
- 238000003199 nucleic acid amplification method Methods 0.000 description 1
- 210000004197 pelvis Anatomy 0.000 description 1
- 206010034674 peritonitis Diseases 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 230000000306 recurrent effect Effects 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 230000002269 spontaneous effect Effects 0.000 description 1
- 238000011255 standard chemotherapy Methods 0.000 description 1
- 210000000130 stem cell Anatomy 0.000 description 1
- 238000012385 systemic delivery Methods 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 229950007343 taurultam Drugs 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- YFHICDDUDORKJB-UHFFFAOYSA-N trimethylene carbonate Chemical compound O=C1OCCCO1 YFHICDDUDORKJB-UHFFFAOYSA-N 0.000 description 1
- 210000004881 tumor cell Anatomy 0.000 description 1
- PAPBSGBWRJIAAV-UHFFFAOYSA-N ε-Caprolactone Chemical compound O=C1CCCCCO1 PAPBSGBWRJIAAV-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/16—Amides, e.g. hydroxamic acids
- A61K31/18—Sulfonamides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/54—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one sulfur as the ring hetero atoms, e.g. sulthiame
- A61K31/549—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one sulfur as the ring hetero atoms, e.g. sulthiame having two or more nitrogen atoms in the same ring, e.g. hydrochlorothiazide
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/10—Alcohols; Phenols; Salts thereof, e.g. glycerol; Polyethylene glycols [PEG]; Poloxamers; PEG/POE alkyl ethers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/56—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule
- A61K47/59—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes
- A61K47/60—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes the organic macromolecular compound being a polyoxyalkylene oligomer, polymer or dendrimer, e.g. PEG, PPG, PEO or polyglycerol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/51—Nanocapsules; Nanoparticles
- A61K9/5107—Excipients; Inactive ingredients
- A61K9/513—Organic macromolecular compounds; Dendrimers
- A61K9/5146—Organic macromolecular compounds; Dendrimers obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyethylene glycol, polyamines, polyanhydrides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/51—Nanocapsules; Nanoparticles
- A61K9/5107—Excipients; Inactive ingredients
- A61K9/513—Organic macromolecular compounds; Dendrimers
- A61K9/5146—Organic macromolecular compounds; Dendrimers obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyethylene glycol, polyamines, polyanhydrides
- A61K9/5153—Polyesters, e.g. poly(lactide-co-glycolide)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Optics & Photonics (AREA)
- Physics & Mathematics (AREA)
- Biomedical Technology (AREA)
- Nanotechnology (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Dermatology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
神经母细胞瘤为主要影响儿童的肿瘤。除在可手术切除病灶的极少数情况下之外,当前的护理标准是无法治愈的,尽管已对低风险神经母细胞瘤和中风险神经母细胞瘤记录了非常高的存活率。牛磺罗定被开发为抗感染药,但已发现其在细胞培养物中和现在于啮齿动物癌症模型中具有令人惊讶的溶瘤活性。在啮齿动物模型中的功效优于在细胞培养物中的功效。本发明涉及牛磺罗定水解产物(氧氢噻二嗪和/或牛磺酰胺和/或甲二醇和/或其选择的组合)用于在幼年哺乳动物中治疗神经母细胞瘤的用途。
Description
参考待审在先专利申请
该专利申请:
(i) 为CorMedix Inc.和Robert DiLuccio于2017年1月11日提交的关于用于治疗神经母细胞瘤和其他癌症的治疗性纳米颗粒的待审在先美国专利申请序列号15/403,876(代理人案卷号CORMEDIX-14)的部分继续,该专利申请要求由CorMedix Inc.和RobertDiLuccio于2016年1月11日提交的关于用于治疗神经母细胞瘤的纳米颗粒系统的在先美国临时专利申请序列号62/277,243(代理人案卷号CORMEDIX-14 PROV)的权益;和
(ii) 要求由Cormedix Inc.和Bruce Reidenberg等人于2018年8月28日提交的关于用牛磺罗定水解产物进行的神经母细胞瘤治疗的待审在先美国临时专利申请序列号62/723,618(代理人案卷号CORMEDIX-33 PROV)的权益。
上述三(3)个专利申请特此通过参考结合至本文中。
发明领域
本发明总体而言涉及治疗性方法和组合物,并且更具体地讲涉及用于治疗幼年哺乳动物体内神经母细胞瘤的治疗性方法和组合物。
发明背景
神经母细胞瘤(NB)为童年时期最常见的颅外实体癌,也是婴儿期最常见的癌症,在美国发病率为每年约650例,和在英国发病率为每年100例。将近一半的神经母细胞瘤病例发生在小于2岁的儿童中。其为一种神经内分泌肿瘤,由交感神经系统(SNS)的任何神经嵴元件引起。神经母细胞瘤最常源于肾上腺之一,但也可在颈部、胸部、腹部或骨盆的神经组织中形成。注意到,尽管神经母细胞瘤起源于神经组织,但其不是中枢神经系统(CNS)的肿瘤。
神经母细胞瘤为已知表现出从未分化状态到完全良性细胞外观的自发消退的少数几种人类恶性肿瘤之一。
神经母细胞瘤为一种表现出极大异质性的疾病,并且分为3个风险类别:低风险、中风险和高风险。低风险神经母细胞瘤最常见于婴儿,并且在仅观察或手术的情况下就常见良好的预后,而高风险神经母细胞瘤即使用可获得的最密集的多模式疗法也难以成功治疗。
当神经母细胞瘤病灶为局限性的时,其通常是可治愈的。然而,尽管有积极的多模式疗法,例如密集化疗、手术、放射疗法、干细胞移植、分化剂异维A酸(也称为13-顺式-视黄酸),以及经常使用抗GD2免疫疗法和抗GD2单克隆抗体疗法的免疫疗法,但患有晚期疾病的大于18个月的儿童的长期存活仍然较差。
已经鉴定出生物学和遗传学特征,当将其添加至经典的临床分期中时,其已允许将患者分配到风险组中以规划治疗强度。这些标准包括患者的年龄、疾病扩散的程度、显微镜下外观以及包括DNA倍性和N-myc癌基因扩增(N-myc调节微小RNA)在内的遗传特征。这些标准用于将神经母细胞瘤分为低风险、中风险和高风险疾病。最近的一项生物学研究(COGANBL00B1)分析了2,687名神经母细胞瘤患者,并确定了风险分配谱:37%的神经母细胞瘤病例为低风险,18%的神经母细胞瘤病例为中风险,和45%的神经母细胞瘤病例为高风险。注意到,有一些证据表明神经母细胞瘤的高风险和低风险类型为由不同机制引起的,而不仅仅是同一机制的两种不同程度的表达。
用于这些不同风险类别的疗法非常不同。
可以频繁地观察低风险神经母细胞瘤而根本不需要任何治疗,或者可仅用手术治愈低风险神经母细胞瘤。
中风险神经母细胞瘤通常用手术和化学疗法进行治疗。
高风险神经母细胞瘤通常用密集化疗、手术、放射疗法、骨髓/造血干细胞移植、通过13-顺式-视黄酸(异维A酸或异维甲酸)的基于生物制品的疗法和抗体疗法(通常与细胞因子GM-CSF和IL-2细胞因子一起给予)进行治疗。
使用当前的治疗,患有低风险神经母细胞瘤和中风险神经母细胞瘤的患者预后极佳,低风险神经母细胞瘤的治愈率高于90%,和中风险神经母细胞瘤的治愈率为70-90%。相反,在过去的二十年中,用于高风险神经母细胞瘤的疗法仅导致当时治愈约30%。抗体疗法的加入显著提高了高风险神经母细胞瘤的存活率。2009年3月,具有226名高风险神经母细胞瘤患者的儿童肿瘤学组(Children's Oncology Group) (COG)研究的早期分析表明,干细胞移植之后两年,随机接受ch14.18抗体与GM-CSF和IL-2的组中有66%存活且无病,相比之下未接受抗体的组中仅有46%。停止随机,因此所有参加试验的患者均可接受抗体疗法。
已发现组合使用的化学治疗剂对神经母细胞瘤有效。通常用于诱导和用于干细胞移植调理的药物为铂化合物(顺铂、卡铂)、烷化剂(环磷酰胺、异环磷酰胺、美法仑、拓扑异构酶II抑制剂)和长春花生物碱(长春新碱)。一些较新的方案包括诱导中的拓扑异构酶I抑制剂(拓扑替康和伊立替康),发现其对复发性疾病有效。
然而,需要一种对神经母细胞瘤有效的新方法和组合物。
发明概述
根据本发明,所选择的牛磺罗定水解产物用于治疗神经母细胞瘤。所选择的牛磺罗定水解产物可包含来自由以下组成的组中的至少一种:
牛磺酰胺(taurinamide);
氧氢噻二嗪(taurultam);
甲二醇;
以1氧氢噻二嗪: 7牛磺酰胺的比率存在的氧氢噻二嗪和牛磺酰胺;和
以1氧氢噻二嗪: 7牛磺酰胺: 1甲二醇的比率存在的氧氢噻二嗪、牛磺酰胺和甲二醇。
基于个体患者的反应,牛磺酰胺以5 mg/kg-280 mg/kg的剂量范围(最佳范围在5mg/kg-60 mg/kg之间)每天一次至每周一次给予,持续有效的时间段。
基于个体患者的反应,氧氢噻二嗪以5 mg/kg-280 mg/kg的剂量范围(最佳范围在5 mg/kg-60 mg/kg之间)每天一次至每周一次给予,持续有效的时间段。
基于个体患者的反应,甲二醇以2.5 mg/kg-160 mg/kg的剂量范围(最佳范围在2.5 mg/kg-30 mg/kg之间)每天一次至每周一次给予,持续有效的时间段。
基于个体患者的反应,氧氢噻二嗪和牛磺酰胺(以1氧氢噻二嗪: 7牛磺酰胺的比率)以5 mg/kg-280 mg/kg的氧氢噻二嗪剂量范围(最佳范围在5 mg/kg-40 mg/kg之间)与5mg/kg-280 mg/kg的牛磺酰胺(最佳范围为35 mg/kg-40 mg/kg)的组合,每天一次至每周一次给予,持续有效的时间段。
基于个体患者的反应,氧氢噻二嗪、牛磺酰胺和甲二醇(以1氧氢噻二嗪: 7牛磺酰胺: 1甲二醇的比率)以5 mg/kg-280 mg/kg的氧氢噻二嗪剂量范围(最佳范围在5 mg/kg-40 mg/kg之间)与5 mg/kg-280 mg/kg剂量范围(最佳范围为35 mg/kg-40 mg/kg)的牛磺酰胺的组合,进一步地与2.5 mg/kg-160 mg/kg剂量范围(最佳范围为5 mg/kg-40 mg/kg)的甲二醇的组合,每天一次至每周一次给予,持续有效的时间段。
在本发明的一种优选形式中,所选择的水解产物(即活性成分)可以“保护形式”全身性地递送,使得其可到达神经母细胞瘤的部位而不会过早降解。
更特别地,在本发明的一种优选形式中,水解产物可以纳米颗粒的形式递送,其中纳米颗粒包含水解产物的核和外部包衣,所述外部包衣被配置为防止水解产物在纳米颗粒到达肿瘤部位之前过早暴露。外部包衣随着纳米颗粒从插入部位到肿瘤部位行进而分解,以便在肿瘤部位完整地释放水解产物。在本发明的一种优选形式中,包衣包含随着纳米颗粒从插入部位到肿瘤部位行进而分解的可吸收的聚合物或脂质。
在本发明的另一种形式中,水解产物可使用被配置为延迟活性成分的降解的聚合物系统来递送。举例来说但非限制性地,可使用聚乙二醇(PEG)将水解产物“聚乙二醇化”以延迟活性成分的过早降解。
所选择的牛磺罗定水解产物可作为单一药物或与其他溶瘤剂和/或放射疗法组合全身性地给予。
附图简述
通过以下对本发明优选实施方案的详述,将更充分地公开本发明的这些和其他目的和特征,或者使其变得显而易见,所述详述应与附图一起考虑,其中相同的数字表示相同的部分,并且进一步地其中:
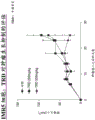
图1为显示在体外(非体内)与健康的淋巴细胞相比较,白血病细胞系似乎对牛磺罗定的作用更敏感的图表;
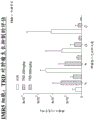
图2为显示在体外(非体内)当与健康的成纤维细胞(图表上的BJ)相比较时,神经母细胞瘤细胞系对由于牛磺罗定引起的生存力下降更敏感的图表;
图3-6为图表或照片,显示对具有来自在CB57 SCID小鼠中皮下植入的神经母细胞瘤细胞系的可测量肿瘤的CB57 SCID小鼠给予牛磺罗定在体内(非体外)在IMR5肿瘤上具有功效,并且在SK-N-AS肿瘤上具有可测量的功效;
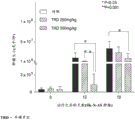
图7和8为图表,显示当给予牛磺罗定以治疗具有也源自神经母细胞瘤的不同细胞系(SK-N-AS)的小鼠时,实现了肿瘤大小的统计学显著减小,但是总生存期与对照没有显著差异;
图9说明牛磺罗定的水解机制;
图10为显示牛磺酰胺的平均药代动力学参数的图表;和
图11为显示氧氢噻二嗪的平均药代动力学参数的图表。
发明详述
牛磺罗定为众所周知的抗微生物剂,具有已发表的作用机制和抗微生物谱。牛磺罗定在循环中不稳定,因此尚未成功开发用于全身性感染。当作为封管溶液(catheter-lock solution)输注时,牛磺罗定已在局部应用中证明对腹膜炎和预防感染有效。
最近已经研究了牛磺罗定的溶瘤活性,并且发现其与标准化学疗法组合或单独使用对培养中的细胞系具有抑制作用。尽管声称可在临床上达到体外抑制浓度,但唯一发表的人类药代动力学研究表明,当5克牛磺罗定通过20分钟输注静脉内给予时,在健康志愿者中没有可测量的牛磺罗定浓度。据信这是由于当在哺乳动物体内全身性给予时牛磺罗定的快速水解引起的。
已经发现,在体外(非体内)与健康的淋巴细胞相比较,白血病细胞系似乎对牛磺罗定的作用更敏感。参见图1。
还已经发现,在体外(非体内)当与健康的成纤维细胞相比较时,神经母细胞瘤细胞系对由于牛磺罗定引起的生存力下降更敏感。参见图2。
此外,对具有来自在CB57 SCID小鼠中皮下植入的神经母细胞瘤细胞系的可测量肿瘤的CB57 SCID小鼠给予牛磺罗定显示出在体内(非体外)在IMR5肿瘤上具有功效,并且在SK-N-AS肿瘤上具有可测量的功效。参见图3-6。
注意到,在测试的两种最高浓度下观察到对神经母细胞瘤细胞系的体外功效,即高于40微摩尔[1摩尔/升x 284 gm/摩尔x 1摩尔/1,000,000微摩尔x 40微摩尔x 1000 mg/克= 11 mg/升= 11 mcg/mL],如图2所示(其中只有SK-N-MC细胞系(一种神经上皮瘤细胞系)的细胞生存力低于50%)。神经母细胞瘤细胞系的IC50值介于80-140微摩尔之间,和正常成纤维细胞的IC50值为200微摩尔(参见图2)。
尽管IRM5的体外IC50相对较高(图2),但在体内用牛磺罗定治疗IMR5细胞植入物观察到的功效(图3-6)支持牛磺罗定的水解产物可具有独立的抗肿瘤活性的结论。换句话说,牛磺罗定在体内对神经母细胞瘤细胞的治疗似乎明显比牛磺罗定在体外对神经母细胞瘤细胞的治疗更加有效。由于已知牛磺罗定在体内代谢为牛磺罗定水解产物,因此这将支持牛磺罗定的水解产物可对神经母细胞瘤细胞具有显著的抗肿瘤活性的结论。事实上,可能牛磺罗定的水解产物比尚未水解的牛磺罗定对神经母细胞瘤细胞具有更高的功效。
当给予牛磺罗定以治疗具有也源自神经母细胞瘤的不同细胞系(SK-N-AS)的小鼠时,实现了肿瘤大小的统计学显著减小,尽管植入肿瘤的小鼠的总生存期与对照没有统计学差异。参见图7和8。
现已发现所选择的牛磺罗定水解产物可用于治疗神经母细胞瘤。牛磺罗定的水解机制如图9所示。可用于治疗神经母细胞瘤的所选择的牛磺罗定水解产物可包括来自由以下组成的组中的至少一种:
牛磺酰胺;
氧氢噻二嗪;
甲二醇;
以1氧氢噻二嗪: 7牛磺酰胺的比率存在的氧氢噻二嗪和牛磺酰胺;和
以1氧氢噻二嗪: 7牛磺酰胺: 1甲二醇的比率存在的氧氢噻二嗪、牛磺酰胺和甲二醇。
基于个体患者的反应,牛磺酰胺以5 mg/kg-280 mg/kg的剂量范围(最佳范围在5mg/kg-60 mg/kg之间)每天一次至每周一次给予,持续有效的时间段。牛磺酰胺的平均药代动力学参数如图10所示。
基于个体患者的反应,氧氢噻二嗪以5 mg/kg-280 mg/kg的剂量范围(最佳范围在5 mg/kg-60 mg/kg之间)每天一次至每周一次给予,持续有效的时间段。氧氢噻二嗪的平均药代动力学参数如图11所示。
基于个体患者的反应,甲二醇以2.5 mg/kg-160 mg/kg的剂量范围(最佳范围在2.5 mg/kg-30 mg/kg之间)每天一次至每周一次给予,持续有效的时间段。
基于个体患者的反应,氧氢噻二嗪和牛磺酰胺(以1氧氢噻二嗪: 7牛磺酰胺的比率)以5 mg/kg-280 mg/kg的氧氢噻二嗪剂量范围(最佳范围在5 mg/kg-40 mg/kg之间)与5mg/kg-280 mg/kg的牛磺酰胺(最佳范围为35 mg/kg-40 mg/kg)的组合,每天一次至每周一次给予,持续有效的时间段。
基于个体患者的反应,氧氢噻二嗪、牛磺酰胺和甲二醇(以1氧氢噻二嗪: 7牛磺酰胺: 1甲二醇的比率)以5 mg/kg-280 mg/kg的氧氢噻二嗪剂量范围(最佳范围在5 mg/kg-40 mg/kg之间)与5 mg/kg-280 mg/kg剂量范围(最佳范围为35 mg/kg-40 mg/kg)的牛磺酰胺的组合,进一步地与2.5 mg/kg-160 mg/kg剂量范围(最佳范围为5 mg/kg-40 mg/kg)的甲二醇的组合,每天一次至每周一次给予,持续有效的时间段。
水解产物的剂量选择如下计算:
AUC 0-inf氧氢噻二嗪/AUC 0-inf牛磺酰胺= 42.9/312.7 = 0.14
由于分子量差异仅为单个甲基,因此无需使用基于重量的AUC进行校正。因此,氧氢噻二嗪和牛磺酰胺组合给予时的目标比率为0.14或1:7。并且氧氢噻二嗪和牛磺酸酰胺和甲二醇组合给予时的目标比率为1:7:1。
有效剂量通过使用以下公式从有效小鼠剂量计算人类等效剂量来计算:
[人类等效剂量=小鼠mg/kg剂量x 1成年人类/12小鼠x 25儿童BSA比率/37成人BSA比率=以mg/kg表示的儿童剂量
(https://www.fda.gov/downloads/drugs/guidances/ucm078932.pdf)。
在本发明的一种优选形式中,所选择的水解产物(活性成分)可以“保护形式”全身性地递送,使得其可到达神经母细胞瘤的部位以避免过早降解。
更特别地,在本发明的一种优选形式中,水解产物可以纳米颗粒的形式递送,其中纳米颗粒包含水解产物的核和外部包衣,所述外部包衣被配置为防止水解产物在纳米颗粒到达肿瘤部位之前过早暴露。外部包衣随着纳米颗粒从插入部位到肿瘤部位行进而分解,以便在肿瘤部位完整地释放水解产物。在本发明的一种优选形式中,包衣包含随着纳米颗粒从插入部位到肿瘤部位行进而分解的可吸收的聚合物或脂质。举例来说但非限制性地,包衣可由衍生自由l-丙交酯、乙交酯、ε-己内酯、对二氧环己酮和三亚甲基碳酸酯构成的聚合物的共聚物和多聚体的组合产生。包衣也可与二醇类比如聚乙二醇(PEG)结合,所述二醇类可为线性或多臂结构。
如果需要的话,纳米颗粒可包含赋形剂(例如缓冲剂,用于提供在纳米颗粒内水解产物增强的水解稳定性)。
另外,如果需要的话,纳米颗粒可进一步包含包衣,其中包衣被配置为使纳米颗粒靶向神经母细胞瘤的部位,从而提高水解产物用于治疗神经母细胞瘤的功效。在本发明的一种优选形式中,包衣包含结合分子,其被配置为使纳米颗粒向特定组织靶向递送。举例来说但非限制性地,用于纳米颗粒的包衣包含针对N型钙通道的单克隆抗体(例如抗N型钙通道面外Fab片段),用于使纳米颗粒结合于神经组织(神经母细胞瘤肿瘤)。
在本发明的另一种形式中,水解产物可使用被配置为延迟活性成分的降解和/或优化活性成分的释放性能的聚合物系统来递送。举例来说但非限制性地,可使用聚乙二醇(PEG)将水解产物“聚乙二醇化”以延迟活性成分的过早降解和/或优化活性成分的释放性能。
所选择的牛磺罗定水解产物可作为单一药物或与其他溶瘤剂和/或放射疗法组合全身性地给予。可与牛磺罗定的水解产物组合以进行全身性递送的溶瘤剂的实例为铂化合物(顺铂、卡铂)、烷化剂(环磷酰胺、异环磷酰胺、美法仑、拓扑异构酶II抑制剂)、长春花生物碱(长春新碱)和拓扑异构酶I抑制剂(拓扑替康和伊立替康)。
修改
尽管已经根据某些示例性优选的实施方案描述了本发明,但是本领域技术人员将易于理解和意识到其不限于此,并且可对上述优选实施方案进行许多增加、删除和修改而仍然处于本发明的范围内。
Claims (27)
1.一种用于治疗神经母细胞瘤的方法,所述方法包括:
将组合物给予患者,其中所述组合物由来自由以下组成的组中的至少一种组成:
牛磺酰胺;
氧氢噻二嗪;
甲二醇;
以1氧氢噻二嗪: 7牛磺酰胺的比率存在的氧氢噻二嗪和牛磺酰胺;和
以1氧氢噻二嗪: 7牛磺酰胺: 1甲二醇的比率存在的氧氢噻二嗪、牛磺酰胺和甲二醇。
2.权利要求1的方法,其中所述组合物由牛磺酰胺组成。
3.权利要求2的方法,其中基于个体患者的反应,剂量范围为5 mg/kg-280 mg/kg每天一次至每周一次持续有效的时间段。
4.权利要求3的方法,其中基于个体患者的反应,所述剂量范围最佳为5 mg/kg-60 mg/kg每天一次至每周一次持续有效的时间段。
5.权利要求2的方法,其中所述组合物连同溶瘤剂和/或放射疗法一起给予。
6.权利要求1的方法,其中所述组合物由氧氢噻二嗪组成。
7.权利要求6的方法,其中基于个体患者的反应,所述剂量范围为5 mg/kg-280 mg/kg每天一次至每周一次持续有效的时间段。
8.权利要求7的方法,其中基于个体患者的反应,所述剂量范围最佳在5 mg/kg-60 mg/kg之间每天一次至每周一次持续有效的时间段。
9.权利要求6的方法,其中所述组合物连同溶瘤剂和/或放射疗法一起给予。
10.权利要求1的方法,其中所述组合物由甲二醇组成。
11.权利要求10的方法,其中基于个体患者的反应,所述剂量范围为2.5 mg/kg-160mg/kg每天一次至每周一次持续有效的时间段。
12.权利要求11的方法,其中基于个体患者的反应,所述剂量范围最佳在2.5 mg/kg-30mg/kg之间每天一次至每周一次持续有效的时间段。
13.权利要求10的方法,其中所述组合物连同溶瘤剂和/或放射疗法一起给予。
14.权利要求1的方法,其中所述组合物由比率为1氧氢噻二嗪: 7牛磺酰胺的氧氢噻二嗪和牛磺酰胺组成。
15.权利要求14的方法,其中基于个体患者的反应,所述氧氢噻二嗪和牛磺酰胺(以1氧氢噻二嗪: 7牛磺酰胺的比率)以最佳范围在5 mg/kg-40 mg/kg之间的5 mg/kg-280 mg/kg的氧氢噻二嗪剂量范围与最佳范围为35 mg/kg-40 mg/kg的5 mg/kg-280 mg/kg的牛磺酰胺的组合,每天一次至每周一次给予持续有效的时间段。
16.权利要求14的方法,其中所述组合物连同溶瘤剂和/或放射疗法一起给予。
17.权利要求1的方法,其中所述组合物由比率为1氧氢噻二嗪: 7牛磺酰胺: 1甲二醇的氧氢噻二嗪、牛磺酰胺和甲二醇组成。
18.权利要求17的方法,其中基于个体患者的反应,所述氧氢噻二嗪、牛磺酰胺和甲二醇(以1氧氢噻二嗪: 7牛磺酰胺: 1甲二醇的比率)以最佳范围在5 mg/kg-40 mg/kg之间的5 mg/kg-280 mg/kg的氧氢噻二嗪剂量范围与最佳范围为35 mg/kg-40 mg/kg的5 mg/kg-280 mg/kg的牛磺酰胺剂量范围的组合,进一步地与最佳范围为5 mg/kg-40 mg/kg的2.5mg/kg-160 mg/kg剂量范围的甲二醇的组合,每天一次至每周一次给予持续有效的时间段。
19.权利要求17的方法,其中所述组合物连同溶瘤剂和/或放射疗法一起给予。
20.权利要求1的方法,其中使用来自由胃肠外递送、肌内递送和静脉内递送组成的组中的一种将所述组合物递送至所述患者。
21.权利要求1的方法,其中所述组合物包含在纳米颗粒中,并且进一步地其中所述纳米颗粒被配置为延迟所述组合物的水解直至所述纳米颗粒到达肿瘤的部位。
22.权利要求21的方法,其中所述纳米颗粒包含所述组合物的核和外部包衣,其中所述外部包衣被配置为防止所述组合物在所述纳米颗粒到达所述肿瘤部位之前暴露。
23.权利要求22的方法,其中所述外部包衣包含随着所述纳米颗粒从插入部位到所述肿瘤部位行进而分解的可吸收的聚合物或脂质。
24.权利要求1的方法,其中使用被配置为延迟所述组合物的水解的聚合物系统递送所述组合物。
25.权利要求24的方法,其中使用聚乙二醇(PEG)“聚乙二醇化”所述组合物以延迟所述组合物的过早水解。
26.权利要求1的方法,其中所述组合物包含来自由牛磺酰胺、氧氢噻二嗪和甲二醇组成的组中的至少两种。
27.权利要求1的方法,其中所述组合物包含来自由牛磺酰胺、氧氢噻二嗪和甲二醇组成的组中的全部3种。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201862723618P | 2018-08-28 | 2018-08-28 | |
| US62/723618 | 2018-08-28 | ||
| PCT/US2019/048592 WO2020047113A1 (en) | 2018-08-28 | 2019-08-28 | Neuroblastoma treatment with taurolidine hydrolysis products |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN113347976A true CN113347976A (zh) | 2021-09-03 |
Family
ID=69645349
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201980071416.3A Pending CN113347976A (zh) | 2018-08-28 | 2019-08-28 | 用牛磺罗定水解产物进行的神经母细胞瘤治疗 |
Country Status (7)
| Country | Link |
|---|---|
| EP (1) | EP3843746A4 (zh) |
| JP (1) | JP2021535163A (zh) |
| KR (1) | KR20210050544A (zh) |
| CN (1) | CN113347976A (zh) |
| AU (1) | AU2019330954A1 (zh) |
| CA (1) | CA3111057A1 (zh) |
| WO (1) | WO2020047113A1 (zh) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN116769723A (zh) * | 2023-08-09 | 2023-09-19 | 山东省成体细胞产业技术研究院有限公司 | 一种gd2嵌合抗原受体修饰的t细胞及其应用 |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5602150A (en) * | 1992-10-02 | 1997-02-11 | Research Foundation For Mental Hygiene, Inc. | Treatment of central nervous system disorders associated with psychotic behavior and dementia with a combination of neuroleptic drugs and taurine, or derivatives thereof, to prevent the development of tardive dyskinesia |
| US6521616B2 (en) * | 1999-12-06 | 2003-02-18 | Rhode Island Hospital, A Lifespan Partner | Methods of treating tumors with taurolidine |
| DE60311958D1 (de) * | 2003-02-03 | 2007-04-05 | Polaschegg Hans Dietrich | Zusammensetzung zur Prävention von Infektionen durch subkutane Prothesen |
| CN103118669A (zh) * | 2010-06-01 | 2013-05-22 | 盖斯特里希医药公司 | 口服药物治疗方法和组合物 |
| CN104244949A (zh) * | 2012-03-30 | 2014-12-24 | 诺华股份有限公司 | 用于治疗神经母细胞瘤、尤文氏肉瘤或横纹肌肉瘤的化合物 |
| US20170196875A1 (en) * | 2016-01-11 | 2017-07-13 | Cormedix Inc. | Therapeutic nanoparticles for the treatment of neuroblastoma and other cancers |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20030027818A1 (en) * | 2001-04-03 | 2003-02-06 | Redmond H. Paul | Treatment of cancers |
| US20050096314A1 (en) * | 2001-04-03 | 2005-05-05 | Ed. Geistlich Soehne Ag Fuer Chemische Industrie | Treatment of cancers with methylol-containing compounds and at least one electrolyte |
| CA2363973C (en) * | 2000-11-28 | 2009-03-10 | Ed. Geistlich Sohne Ag Fur Chemische Industrie | Enhancement of effectiveness of 5-fluorouracil in treatment of tumor metastases and cancer |
| JP2007537200A (ja) * | 2004-05-14 | 2007-12-20 | ハンス−ディートリヒ・ポラシェグ | タウロリジン製剤及び投与:細菌マイクロフィルム形成に対する治療処置及び抗菌保護 |
| EP1976531B1 (en) * | 2006-01-06 | 2011-11-09 | Ed. Geistlich Söhne AG für Chemische Industrie | Irradiated compositions and treatment of cancers with radiation in combination with taurolidine and/or taurultam |
-
2019
- 2019-08-28 CA CA3111057A patent/CA3111057A1/en active Pending
- 2019-08-28 WO PCT/US2019/048592 patent/WO2020047113A1/en unknown
- 2019-08-28 CN CN201980071416.3A patent/CN113347976A/zh active Pending
- 2019-08-28 EP EP19856239.9A patent/EP3843746A4/en active Pending
- 2019-08-28 JP JP2021511544A patent/JP2021535163A/ja active Pending
- 2019-08-28 AU AU2019330954A patent/AU2019330954A1/en active Pending
- 2019-08-28 KR KR1020217008971A patent/KR20210050544A/ko unknown
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5602150A (en) * | 1992-10-02 | 1997-02-11 | Research Foundation For Mental Hygiene, Inc. | Treatment of central nervous system disorders associated with psychotic behavior and dementia with a combination of neuroleptic drugs and taurine, or derivatives thereof, to prevent the development of tardive dyskinesia |
| US6521616B2 (en) * | 1999-12-06 | 2003-02-18 | Rhode Island Hospital, A Lifespan Partner | Methods of treating tumors with taurolidine |
| DE60311958D1 (de) * | 2003-02-03 | 2007-04-05 | Polaschegg Hans Dietrich | Zusammensetzung zur Prävention von Infektionen durch subkutane Prothesen |
| CN103118669A (zh) * | 2010-06-01 | 2013-05-22 | 盖斯特里希医药公司 | 口服药物治疗方法和组合物 |
| CN104244949A (zh) * | 2012-03-30 | 2014-12-24 | 诺华股份有限公司 | 用于治疗神经母细胞瘤、尤文氏肉瘤或横纹肌肉瘤的化合物 |
| US20170196875A1 (en) * | 2016-01-11 | 2017-07-13 | Cormedix Inc. | Therapeutic nanoparticles for the treatment of neuroblastoma and other cancers |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN116769723A (zh) * | 2023-08-09 | 2023-09-19 | 山东省成体细胞产业技术研究院有限公司 | 一种gd2嵌合抗原受体修饰的t细胞及其应用 |
| CN116769723B (zh) * | 2023-08-09 | 2023-11-03 | 山东省成体细胞产业技术研究院有限公司 | 一种gd2嵌合抗原受体修饰的t细胞及其应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3843746A1 (en) | 2021-07-07 |
| WO2020047113A1 (en) | 2020-03-05 |
| CA3111057A1 (en) | 2020-02-05 |
| EP3843746A4 (en) | 2022-10-19 |
| KR20210050544A (ko) | 2021-05-07 |
| AU2019330954A1 (en) | 2021-04-22 |
| JP2021535163A (ja) | 2021-12-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20230390300A1 (en) | Neuroblastoma treatment with taurolidine hydrolysis products | |
| US20170266293A1 (en) | Methods of treating cancers with therapeutic nanoparticles | |
| US20220168426A1 (en) | Bioorthogonal compositions | |
| KR20040058199A (ko) | 폴리 양이온성 폴리머 및 음전하를 띠는 약리학적 활성화합물을 포함하는 제어 방출 약물 전달 조성물 | |
| KR20160024985A (ko) | 암 치료를 위한 도세탁셀 중합체성 나노입자 | |
| Tao et al. | A novel therapeutic system for malignant glioma: nanoformulation, pharmacokinetic, and anticancer properties of cell-nano-drug delivery | |
| JP2021523173A (ja) | 生物応答性ヒドロゲルマトリックス及び使用方法 | |
| US20220323450A1 (en) | Methods and compositions for treating neuroblastoma in a juvenile mammalian body | |
| Li et al. | Nanoengineered therapy aiming at the etiology of rheumatoid arthritis | |
| Naraharisetti et al. | In vivo performance of implantable biodegradable preparations delivering Paclitaxel and Etanidazole for the treatment of glioma | |
| CN113347976A (zh) | 用牛磺罗定水解产物进行的神经母细胞瘤治疗 | |
| Zhang et al. | Co-delivery of sorafenib and metformin from amphiphilic polypeptide-based micelles for colon cancer treatment | |
| CN113164491A (zh) | 用于治疗幼年哺乳动物体内神经母细胞瘤的方法和组合物 | |
| KR20130031557A (ko) | 다기능성 나노입자를 포함하는 류마티스 관절염 치료용 조성물 | |
| US12053478B2 (en) | Taurultam, taurinamide and methylene glycol treatment for MYC—expressing tumors in mammalian bodies | |
| CN113226325A (zh) | 牛磺罗定对哺乳动物体内表达myc的肿瘤的治疗 | |
| CN113905764B (zh) | 用于治疗癌症的前体半胱天冬酶-3活化作用和免疫疗法 | |
| CN112843052B (zh) | 表观遗传因子抑制剂2800z在制备抗肝癌药物增敏剂中的应用 | |
| Fymat | Oncogenomics: a personalized cancer therapy |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |