CN112972712B - 一种用于处理生物墨水的热压灭菌程序及其在人肝类器官3d模型构建中的应用 - Google Patents
一种用于处理生物墨水的热压灭菌程序及其在人肝类器官3d模型构建中的应用 Download PDFInfo
- Publication number
- CN112972712B CN112972712B CN202110285467.5A CN202110285467A CN112972712B CN 112972712 B CN112972712 B CN 112972712B CN 202110285467 A CN202110285467 A CN 202110285467A CN 112972712 B CN112972712 B CN 112972712B
- Authority
- CN
- China
- Prior art keywords
- sterilization
- ink
- culture
- cell
- biological ink
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2/00—Methods or apparatus for disinfecting or sterilising materials or objects other than foodstuffs or contact lenses; Accessories therefor
- A61L2/02—Methods or apparatus for disinfecting or sterilising materials or objects other than foodstuffs or contact lenses; Accessories therefor using physical phenomena
- A61L2/04—Heat
- A61L2/06—Hot gas
- A61L2/07—Steam
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/067—Hepatocytes
- C12N5/0671—Three-dimensional culture, tissue culture or organ culture; Encapsulated cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0693—Tumour cells; Cancer cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2500/00—Specific components of cell culture medium
- C12N2500/30—Organic components
- C12N2500/32—Amino acids
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2513/00—3D culture
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2533/00—Supports or coatings for cell culture, characterised by material
- C12N2533/50—Proteins
- C12N2533/54—Collagen; Gelatin
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2533/00—Supports or coatings for cell culture, characterised by material
- C12N2533/70—Polysaccharides
- C12N2533/74—Alginate
Abstract
本发明公开了一种用于生物墨水灭菌处理的新型热压灭菌程序,包括以下步骤:控制升温速率为5.5℃/min,灭菌条件为121℃,0.1 MPa压力,控制高压蒸汽灭菌的时间为25 min,随后立即以5 L/min的速率排气,10 min内排气结束并降温至100℃以下,立即取出,得到可打印的生物墨水。本发明还公开了一种人肝细胞的3D培养体系及其培养方法。本发明灭菌程序操作简单,不需要大型设备,可以直接应用于不同浓度明胶‑海藻酸钠生物墨水的处理,墨水打印能力良好,细胞生长良好,可维持稳定细胞活力达20天以上。
Description
技术领域
本发明涉及一种生物墨水的灭菌程序及其应用,具体涉及明胶-海藻酸钠生物墨水的灭菌程序及其在人肝细胞的3D培养中的应用。
背景技术
肝脏是一个重要的器官,在蛋白质合成和异物代谢中起着关键作用。世界范围内死于药物性肝损伤(Drug induced liver injury,DILI)的人数正在逐年增加。在药物开发的临床前阶段识别肝毒性化合物是预防DILI的关键。然而,目前使用的动物和二维(2D)体外模型往往不能准确预测临床肝毒性,遗传背景的差异性导致动物实验的预测结果一般不能直接适用于人体,而2D模型与体内生理环境存在巨大的差异。药物筛选亟需构建具有成熟组织器官功能的体外肝脏模型。
近年来,越来越多的研究者专注开发体外肝脏微组织,期望通过模拟体内生理环境摆脱2D培养的局限性。肝细胞三明治培养是一种3D培养的尝试,但缺乏充分的细胞间相互联系。低粘附板是一种商业化的3D细胞培养平台,但随机形成的球样体难以达到均一的大小和形状,在日常的培养以及换液过程中也会导致球体的损失。微流控是一种新兴的培养技术,可以很好地模拟体内的血管网络,但在培养微组织方面难以避免流体剪切力对微组织生长的影响,长期培养的污染问题一直不能很好地解决。更重要的是,有限的局部细胞密度限制了上述方法的实际应用。
3D生物打印技术的发展使得体外组织再生成为可能。与传统组织工程技术相比,3D生物打印具有极高的灵活性和极强的适应性,可根据需要打印出不同的形状且有良好的保真度,细胞装载量提高了几个数量级,极大促进了细胞之间的相互作用。3D生物打印中,生物墨水的灭菌是3D生物打印的一个重要问题。目前,常用的灭菌方法包括放射灭菌(钴-60,γ射线)、紫外照射、环氧乙烷以及过滤除菌。然而,放射灭菌会导致生物墨水中的高分子链断裂,而环氧乙烷灭菌时间较长。上述两种方法都需要特殊仪器和场地,不具有普适性。紫外照射灭菌不能完全除去墨水中的芽孢和孢子,灭菌效果有效。由于墨水的高黏度,过滤除菌难度较大,并且会导致大分子的损失。有文献采用70℃加热-4℃冷却(循环三次)的方式,但明胶因制作工艺,表面覆盖有大量的芽孢和孢子,这种加热-冷却循环灭菌法不能保证灭菌的结果。
高温高压蒸汽灭菌是一种广泛使用且可靠的灭菌方法,然而就生物墨水而言,已有多篇文献明确指出高压蒸汽灭菌不适用于生物墨水灭菌。在详细考察热压灭菌条件对生物墨水性质影响的基础上,本发明采用一种新型的热压灭菌程序作为生物墨水的灭菌手段,有效解决了现有研究的不足。使用明胶和海藻酸钠作为生物墨水的材料,以纯水为溶剂制作生物墨水,结果具有良好的可打印能力。与HepG2细胞悬液混合,使用挤出型3D生物打印机打印,构建人肝类器官模型。操作简单,保真度好,7天有细胞聚集的趋势,14天形成明显的细胞聚集且保持较高的细胞活力。
发明内容
本发明的目的在于解决现有研究的不足,提供一种新型的热压灭菌程序,成功应用于生物墨水的灭菌处理,并利用灭菌处理后的生物墨水构建了人肝脏3D模型。所述处理方法采用常见的高压蒸汽灭菌仪,所述模型由控制程序灭菌后的明胶-海藻酸钠生物墨水构建,操作简单,不需要大型设备,墨水可打印能力良好,细胞生长良好,可维持稳定细胞活力达20天以上。
本发明涉及的生物墨水处理方法相比传统的放射灭菌、环氧乙烷灭菌,能够更快速的完成生物墨水的灭菌步骤,同时不依赖于特殊设备和场地。以此法灭菌的生物墨水,构建了人肝脏3D模型,能够很好地模拟体内的生理条件,支架尺寸灵活多变,可以匹配各种型号的多孔板,满足高通量筛选的需要。这一灭菌方法可以很好地用于明胶-海藻酸钠生物墨水的处理,也为其他配方生物墨水的处理提供了参考。
为了解决目前生物墨水灭菌处理遇到的难题,本发明建立了一种新的生物墨水灭菌方法,不需要特殊仪器,灭菌完全,操作简单方便易行,可以直接应用于不同浓度明胶-海藻酸钠生物墨水的处理,并为其他配方生物墨水的灭菌提供了参考。
为解决上述技术问题,本发明提供了生物墨水的处理方法、性质考察方法及应用。本发明利用灭菌后的明胶-海藻酸钠生物墨水,建立了体外肝脏模型,该模型可模拟体内生理条件下肝脏的生长环境,打印完成后转移至多孔板中培养,无须其他干预条件,细胞在打印的支架内自行增殖聚集,操作简便,可为体外组织再生提供参考。同时也可应用于高通量的药物筛选。
为达到此目的,本发明采用如下技术方案:
一种人肝细胞的3D培养体系,包括装载人肝细胞的生物墨水凝胶支架和人肝细胞3D培养专用培养基。所述3D培养专用培养基为基础培养基(MEM)添加10%(v:v)胎牛血清和1%(v:v)非必需氨基酸。
较佳的,所述非必需氨基酸为890mg/l L-丙氨酸、1320mg/l L-天冬酰胺、1150mg/l L-脯氨酸、1330mg/l L-天(门)冬氨酸、1050mg/l L-丝氨酸、1470mg/l L-谷氨酸和/或750mg/l L-甘氨酸等7种非必须氨基酸的混合溶液。
上述培养成分为实验获取的最佳组成,减少或降低血清或非必需氨基酸的浓度后,3D培养肝细胞的增长速度、成球形态均会受到负面影响,出现大量细胞死亡现象,无法实现长期培养。
较佳的,生物墨水由明胶、海藻酸钠和纯水组成。所述明胶为250g Bloom胶强度的B型明胶,海藻酸钠为分析纯海藻酸钠。明胶具有良好的生物相容性,起到类似细胞外基质的作用,提供细胞黏附生长的位置,本身的可降解性在培养过程中提供了细胞增殖的空间。在钙离子的作用下,海藻酸钠可逆交联形成稳定结构,保持凝胶结构的稳定性。
较佳的,所述生物墨水中明胶浓度为20%(w/v),海藻酸钠浓度为4%(w/v),灭菌时间为25min。
上述浓度为实验获取的最佳组成,降低或改变组分浓度或灭菌时间后,生物墨水的打印能力会受到负面影响,出现流动性过强、打印过程中崩塌等现象,无法实现良好的打印保真度和长期培养。
本发明提供所述处理方法处理后的生物墨水的流动性、挤出特性、流变性和溶胀性能的考察。
本发明还提供所述生物墨水在构建人肝脏细胞3D培养体系及细胞活力检测中的应用。
一种人肝细胞的3D培养方法,包括以下步骤,使用生物墨水装载人肝细胞的3D培养体系培养肝细胞。
优选的,所述生物墨水由明胶和海藻酸钠组成,纯水作为溶剂,开放环境中37℃水浴加热条件下溶解明胶和海藻酸钠,充分搅拌混合后进行高压蒸汽灭菌。
进一步的,所述高压蒸汽灭菌升温速率为5.5℃/min,灭菌条件为121℃,0.1MPa压力,灭菌时间为25min,灭菌完成后立即以5L/min的速率进行排气,10min内排气结束并降温至100℃以下,立即取出生物墨水,室温放置降温,待用。
优选的,所述肝脏细胞为人肝癌细胞HepG2细胞系,由平面扩增或冻存复苏后的HepG2细胞系制备而成。
平面扩增细胞系的处理方法:于平面扩增后的细胞培养皿中用Trypsin消化液消化细胞,低速离心后重悬于新鲜培养基中。
冻存复苏的细胞系处理方法:取出装有人肝细胞的冻存管,立即放入37℃中水浴加热,待冻存液完全融化后立即转移至15ml离心管中,加入10ml新鲜培养基重悬,低速离心后重悬于新鲜培养基中。
进一步的,培养人肝细胞的方法中使用的培养条件为温度37℃,CO2体积浓度为5%。
进一步的,培养人肝细胞的方法中,低速离心后的肝细胞悬液与37℃预热的生物墨水混合,装载1mL至3D生物打印机上,打印多层格栅结构(如4层),打印完成后浸入CaCl2溶液中交联,随后洗净,转移至12孔板中,加入培养液进行培养。混合后肝细胞的密度为1~5×106个细胞/ml;优选为5×106个细胞/ml。初始细胞密度太低不利于细胞生长,细胞密度过高会影响成球效率以及生长,超过1×107个细胞/ml,容易造成局部代谢废物累积,引起细胞死亡。细胞悬液与生物墨水混合体积比为1:1~1:4,优选为1:4。细胞悬液比例过高会影响混合墨水的可打印能力,低于1:4比例,细胞悬液体积过小,浓度过大,容易造成细胞密度的误差,影响实验的重复性。
进一步的,培养人肝细胞的方法中,打印环境温度为26℃,打印速度为3mm/s,打印平台温度为4℃。打印环境温度过高,墨水流动性增强,导致打印过程中的结构坍塌;打印环境温度过低,会造成挤出压力增大,导致大量细胞死亡。打印速度过快会导致可能的打印失真;打印速度过慢会造成线条边缘的不平整,延长打印时间,影响细胞活力。打印平台温度过低会导致细胞活力降低;打印平台温度过高会导致打印过程中凝胶结构不稳定,引起结构坍塌。
进一步的,培养人肝细胞的方法中,CaCl2溶液浓度为3%(w/v,即3gCaCl2溶于100ml水中),交联时间为30s。改变CaCl2溶液浓度,对应的交联时间也需要进行改变。交联时间过短,凝胶稳定性不足,培养过程中可能崩解;交联时间过长会导致细胞损伤,引起大量细胞死亡。
本发明的优点是:
1.本发明提供一种新的生物墨水灭菌处理方法,并用于人肝细胞的3D培养,处理方法简单易行、不依赖于特殊仪器,生物墨水经处理后可在4℃长期保存。
2.本发明得到的基于生物墨水的3D培养体系不需要借助外力,生物墨水装载细胞经打印后,加入培养液培养,细胞在支架内自行生长,减少了悬浮培养体系引入离心力带来的可能的机械损伤。支架装载细胞,大大减少了培养过程中可能的细胞损失,降低换液导致的细胞损失。
3.本发明引入细胞外基质,更好地模拟了体内的生理环境,基质的可降解性降低了支架对细胞增殖的限制。
4.本发明构建的3D培养体系可以匹配各种型号的多孔板,满足高通量筛选的需要。
5.本发明培养的3D模型与2D模型相比,可在体外更好地模拟体内生理环境,细胞增殖空间更大,并维持较长时间、稳定的细胞活力,可以满足长期给药的需求。该模型可用于高通量的药物筛选和疾病研究,为其提供更可靠、真实的数据支持。
附图说明
图1为3D生物打印支架设计模型,
图2为不同灭菌时间空白生物墨水流动性考察,
图3为不同灭菌时间空白生物墨水挤出特性考察,
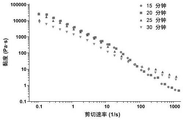
图4为不同灭菌时间的流变性质分析,
图5为灭菌20min、25min、30min与细胞悬液不同比例混合后的流动性考察,
图6为灭菌20min、25min、30min与细胞悬液不同比例混合后的挤出特性考察,A中墨水
︰细胞=1︰1,B中墨水︰细胞=4︰1
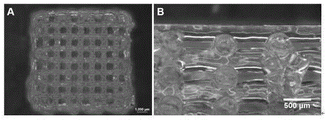
图7为使用灭菌25min墨水打印16层支架的俯视图和横截面图
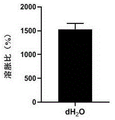
图8为3D凝胶支架的溶胀比,
图9中,1为细胞在支架内生长2天后在Cytation 5细胞成像仪下明场观察图(40×放大倍数,标尺300μm),2为细胞在支架内生长2天、7天、14天后在Cytation 5细胞成像仪下明场观察图(100×放大倍数,标尺100μm),
图10为细胞活力监测。
具体实施方式
下述实施例中所用的实验方法如无特殊说明,均为常规方法。下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。主要试剂:MEM培养基(KeyGEN)、PBS缓冲液(KeyGEN)、非必需氨基酸(Wisent)、胎牛血清(Wisent)、0.25%Trypsin胰酶-EDTA(Gibco)、CCK-8细胞活力检测试剂盒(MCE)、钙黄绿素-碘化丙啶(Calcein-AM/PI)活死细胞染色试剂盒(Yeasen)。
主要材料:明胶,海藻酸钠。
主要仪器:LDZX-50KBS立式压力蒸汽灭菌器(上海申安),细胞培养箱(Thermo)、Cytation5细胞成像仪(Biotek)、超净工作台(苏净安泰),低速台式离心机,Discover HR-2流变仪(TA)。
下面将结合附图对本发明实施例作进一步地详细描述。
实施例1:
选用明胶和海藻酸钠作为生物墨水的组成材料。明胶为B型明胶,来源于动物骨骼。海藻酸钠为分析纯藻酸盐,黏度为350~550mPa·s(1%in H2O,20℃)。另一鱼皮来源的明胶也被用于生物培养,但其形成凝胶的机械性能差,不适用于3D生物打印,所以本发明最终选择了机械性能更佳、使用率更高的动物来源B型明胶作为生物墨水材料进一步研究。
首先在开放环境中配制生物墨水前体溶液,具体方案如下:
步骤1、室温下将明胶加水溶胀,至无明显液体流动,37℃加热溶解后少量多次加入海藻酸钠粉末,充分搅拌溶解。
步骤2、将上述生物墨水前体溶液置于立式高压蒸汽灭菌锅中灭菌,升温速率为5.5℃/min,灭菌条件为121℃,0.1MPa压力,灭菌时间25min,灭菌完成后立即以5L/min的速率进行排气,10min内排气完成并降温至100℃以下,立即取出生物墨水,室温放置降温,待用。
步骤3、超净台内,将1mL上述生物墨水装载于3D生物打印机上,打印环境温度为26℃,打印速度3mm/s,打印平台温度为4℃,开始打印,制作16层格栅结构。打印完成后浸入3%(w/v)CaCl2溶液交联30s。
具体来说,利用上述生物墨水和打印参数制作空白凝胶支架的方法简便可行,打印保真度良好。
如图1所示,为3D生物打印的格栅结构模型示意图。如图7所示,打印出的3D凝胶支架保真度良好,结构完整,不同层之间无明显融合。
实施例2:
与实施例1的区别在于,实施例2为常规灭菌程序,灭菌时间为25min,具体方案如下:
步骤1、室温下将明胶加水溶胀,至无明显液体流动,37℃加热溶解后少量多次加入海藻酸钠粉末,充分搅拌溶解。
步骤2、将上述生物墨水前体溶液置于立式高压蒸汽灭菌锅中灭菌,灭菌时间25min,灭菌完成后按照仪器预制程序自然降温,取出生物墨水,待用。
实施例3:
与实施例1的区别在于,灭菌时间由25min改为30min,灭菌完成后立刻排气,具体方案如下:
步骤1、室温下将明胶加水溶胀,至无明显液体流动,37℃加热溶解后少量多次加入海藻酸钠粉末,充分搅拌溶解。
步骤2、将上述生物墨水前体溶液置于立式高压蒸汽灭菌锅中灭菌,灭菌时间30min,灭菌完成后立刻排气,立即取出生物墨水,室温下放置待用。
实施例4:
与实施例1的区别在于,灭菌时间由25min改为20min,灭菌完成后立刻排气,具体方案如下:
步骤1、室温下将明胶加水溶胀,至无明显液体流动,37℃加热溶解后少量多次加入海藻酸钠粉末,充分搅拌溶解。
步骤2、将上述生物墨水前体溶液置于立式高压蒸汽灭菌锅中灭菌,灭菌时间20min,灭菌完成后立刻排气,立即取出生物墨水,室温下放置待用。
实施例5:
与实施例1的区别在于,灭菌时间由25min改为15min,灭菌完成后立刻排气,具体方案如下:
步骤1、室温下将明胶加水溶胀,至无明显液体流动,37℃加热溶解后少量多次加入海藻酸钠粉末,充分搅拌溶解。
步骤2、将上述生物墨水前体溶液置于立式高压蒸汽灭菌锅中灭菌,灭菌时间15min,灭菌完成后立刻排气,立即取出生物墨水,室温下放置待用。
实施例6:
选用HepG2细胞作为模型细胞。该细胞为人源肝癌细胞系,来源为15岁白人男性的肝癌组织。人原代肝细胞和HepaRG细胞常被用于体外肝脏模型构建,HepaRG细胞是终末分化肝细胞,来源于人肝祖细胞系,保留了许多原代肝细胞的特征。但人原代肝细胞和HepaRG细胞较难获得,培养周期长,所以本发明最终选择了更易获得、文献引用率更高的HepG2细胞系作为模型细胞实现进一步研究。
首先将HepG2细胞与生物墨水混合,装载于3D生物打印机进行打印,制作载细胞3D凝胶支架,具体方案如下:
步骤1、将HepG2细胞于培养皿内进行扩增培养后,收集2.5×107个细胞/ml的HepG2细胞重悬于新鲜培养基中。培养基组成为基础培养基(MEM)添加10%(v:v)胎牛血清和1%(v:v)非必需氨基酸。非必需氨基酸为1320mg/l L-天冬酰胺、1470mg/l L-谷氨酸、1330mg/l L-天(门)冬氨酸、890mg/l L-丙氨酸、1150mg/l L-脯氨酸、1050mg/l L-丝氨酸和750mg/l甘氨酸等7种非必须氨基酸的混合溶液。
步骤2、将200μL上述密度的细胞悬液与800μL生物墨水混合,装载于生物打印机上开始打印制作4层格栅结构,打印参数为,打印环境温度26℃,打印速度3mm/s,打印平台温度4℃。打印完成后浸入3%(w/v)CaCl2溶液中交联30s。轻柔加入1.5ml培养基,放回培养箱培养,条件为37℃,5%(v:v)CO2。
具体来说,利用上述凝胶支架得到的3D细胞培养体系的方法简单可行,且细胞生长状况良好。
效果实验:
1:生物墨水的物理特性
步骤1、吸取1ml不同灭菌程序的生物墨水,置于2ml EP管中,26℃下平放静置10min,观察墨水的流动情况。
如图2所示,常规灭菌程序组(实施例2)呈现明显的流动性,打印过程中易造成结构的塌陷,无法用于3D生物打印。其他灭菌程序组的生物墨水均无明显流动,可进一步考察挤出特性。
步骤2、使用1ml注射器吸取经流动性实验筛选的生物墨水,26℃下观察墨水的挤出行为。
如图3所示,常规灭菌程序组(实施例2,完全灭菌)挤出形态呈液滴状,在低温平台上易扩散,打印过程中结构崩塌,不能形成稳定的凝胶支架,无法用于构建3D培养体系;灭菌15min组(实施例5)挤出形态呈弯曲不均匀线条状,打印过程中层与层之间黏连强度不够,结构不稳定,线条挤出后容易环绕针尖导致打印失败;灭菌20min(实施例4)、25min(实施例1)、30min(实施例3)组挤出形态良好,打印过程中层与层之间黏连良好,线条均匀挤出、分布规则,凝胶支架结构稳定,无塌陷现象。
步骤3、取适量控制灭菌时间的生物墨水至旋转流变仪平台上,25℃条件下测定0.1~1000s-1剪切速率范围内墨水的流变行为。
如图4所示,灭菌后生物墨水仍具备良好的剪切变稀特性。但是,随着灭菌时间的延长,生物墨水的黏度逐渐下降,剪切变稀能力也在逐渐减弱。
2:墨水与细胞悬液的体积比
步骤1、取灭菌20min,25min,30min的生物墨水,与细胞悬液分别以1:1、4:1的比例混合,混合均匀后,比较流动性和挤出特性。
步骤2、吸取1ml混合生物墨水至2ml EP管中,26℃下平放,静置10min,观察墨水的流动情况。
如图5所示,1:1混合的生物墨水均表现出明显的流动性,打印过程中易造成结构的塌陷;而1:4比例混合的墨水,20min与25min无明显流动性,可进一步考察其挤出特性。
步骤3、使用1ml注射器吸取不同灭菌时间的生物墨水,26℃下观察墨水的挤出行为。
如图6所示,与流动性实验相对应的,1:1比例混合后生物墨水挤出呈液滴状,在低温平台上易扩散,打印过程中结构崩塌,不能形成稳定的凝胶支架,无法用于构建3D培养体系。而1:4比例混合的墨水,20min与25min可以线条状挤出,打印过程中层与层之间黏连良好,线条均匀挤出、分布规则,凝胶支架结构稳定,无塌陷现象。
3:3D凝胶支架的溶胀性能
步骤1、取灭菌25min的生物墨水生物打印的16层格栅结构凝胶支架,置于纯水中,37℃溶胀平衡,称重WS,冻干后再次称重Wl,
溶胀比计算公式为:SR(%)=(Ws|W↓l|/W↓l)×100%
如图8所示,灭菌后生物墨水打印的凝胶支架具有良好的溶胀能力,说明该凝胶支架可以具有良好的营养传递能力,利于细胞在支架内的生长。
4:3D凝胶支架中HepG2细胞的增殖能力
步骤1、将HepG2细胞于培养皿内进行扩增培养后,收集2.5×107个细胞/ml的HepG2细胞重悬于新鲜培养基中。培养基组成为基础培养基(MEM)添加10%(v:v)胎牛血清和1%(v:v)非必需氨基酸。非必需氨基酸为1320mg/l L-天冬酰胺、1470mg/l L-谷氨酸、1330mg/l L-天(门)冬氨酸、890mg/l L-丙氨酸、1150mg/l L-脯氨酸、1050mg/l L-丝氨酸和750mg/l甘氨酸等7种非必须氨基酸的混合溶液。
步骤2、将200μL上述密度的细胞悬液与800μL生物墨水混合,装载于生物打印机上开始打印,打印参数为,打印环境温度26℃,打印速度3mm/s,打印平台温度4℃。打印完成后浸入3%(w/v)CaCl2溶液中交联30s。轻柔加入1.5ml培养基,放回培养箱培养,条件为37℃,5%(v:v)CO2。
步骤3、打印后,隔天更换新鲜培养基,6天后每天更换。于第2天、第7天、第14天在细胞成像仪下观察细胞生长,并利用CCK-8试剂盒测定细胞活力,得到细胞增殖曲线图。
如图9-1所示,细胞在支架内生长分布均匀,层与层之间无明显融合。如9-2所示,细胞在支架内生长良好,可在14天内形成明显的细胞聚集。如图10所示,3D凝胶支架内HepG2细胞在接种20天后仍能维持高水平的细胞活力,说明该3D培养体系在体外具有较强的增殖能力,所建立的3D体外模型可满足体外长期给药的需求。
对比例1:与实施例6的区别在于,考察了细胞密度对于3D培养的影响。
步骤1、将HepG2细胞于培养皿内进行扩增培养后,分别收集5×106个细胞/ml、1×107个细胞/ml、1.5×107个细胞/ml、2×107个细胞/ml、3×107个细胞/ml、4×107个细胞/ml的HepG2细胞重悬于新鲜培养基中。培养基组成为基础培养基(MEM)添加10%(v:v)胎牛血清和1%(v:v)非必需氨基酸。
步骤2、将200μL上述密度的细胞悬液分别与800μL生物墨水按照1:4比例混合,最终细胞密度分别为1×106个细胞/ml、2×106个细胞/ml、3×106个细胞/ml、4×106个细胞/ml、6×106个细胞/ml、8×106个细胞/ml,装载于生物打印机上开始打印,打印参数为,打印环境温度26℃,打印速度3mm/s,打印平台温度4℃。打印完成后浸入3%(w/v)CaCl2溶液中交联30s。轻柔加入1.5ml培养基,放回培养箱培养,条件为37℃,5%(v:v)CO2。
步骤3、第2天开始观察细胞生长并使用CCK-8测定细胞活力。
比较后发现,较低或过高的细胞密度均会造成培养过程中大量的细胞死亡,因此选择了密度更为适合的5×106个细胞/ml。
对比例2:与实施例6的区别在于,考察了打印速度对于3D培养的影响。
步骤1、将HepG2细胞于培养皿内进行扩增培养后,收集2.5×107个细胞/ml的HepG2细胞重悬于新鲜培养基中。培养基组成为基础培养基(MEM)添加10%(v:v)胎牛血清和1%(v:v)非必需氨基酸。
步骤2、将200μL上述密度的细胞悬液分别与800μL生物墨水混合,最终细胞密度为5×106个细胞/ml,装载于生物打印机上开始打印,打印参数为,打印环境温度26℃,打印平台温度4℃,分别使用1mm/s、3mm/s、5mm/s的打印速度进行打印。打印完成后浸入3%(w/v)CaCl2溶液中交联30s。轻柔加入1.5ml培养基,放回培养箱培养,条件为37℃,5%(v:v)CO2。
步骤3、第2天开始观察细胞生长并使用CCK-8测定细胞活力。
比较后发现,较快的打印速度会导致挤出压力的提高,在打印过程中造成大量的细胞死亡;较慢的打印速度下,凝胶支架在低温平台上滞留时间过长,影响细胞活力,因此选择了更为合适的3mm/s作为打印速度参数。
因此,结合实施例6和对比例1/2分析可知,本发明优化过的生物打印3D培养体系可以很好地适应人肝细胞模型的形成和生长需求,是体外药物筛选的理想模型,具有良好的市场价值前景。
以上对本发明的具体实施例进行了描述,但需要理解的是,本发明并不局限于上述特定的实施方式,本领域技术人员可以在不脱离本发明构思的前提下,做出各种变形和修改,这些都属于本发明的保护范围。
Claims (6)
1.一种用于生物墨水灭菌处理的热压灭菌程序,其特征在于,包括以下步骤:控制升温速率为5.5℃/min,灭菌条件为121℃,0.1MPa压力,控制高压蒸汽灭菌的时间为25min,随后立即以5L/min的速率排气,10min内排气结束并降温至100℃以下,立即取出,得到可打印的生物墨水;
其中,所述生物墨水配方为20%(w/v)明胶和4%(w/v)海藻酸钠,纯水为溶剂。
2.一种人肝细胞的3D培养体系,其特征在于,包括权利要求1所述灭菌程序灭菌后的人肝细胞生物墨水凝胶支架以及人肝细胞3D培养专用培养基;所述3D培养专用培养基为基础培养基MEM添加10%(v:v)胎牛血清和1%(v:v)非必需氨基酸。
3.如权利要求2所述的人肝细胞的3D培养体系,其中,所述非必需氨基酸为890mg/l L-丙氨酸、1320mg/l L-天冬酰胺、1150mg/l L-脯氨酸、1330mg/l L-天(门)冬氨酸、1050mg/lL-丝氨酸、1470mg/l L-谷氨酸和/或750mg/l L-甘氨酸。
4.一种人肝细胞的3D培养方法,其特征在于,包括以下步骤,使用生物墨水装载人肝细胞的3D培养体系培养肝细胞,所述生物墨水为权利要求1所述灭菌程序灭菌后的生物墨水。
5.如权利要求4所述的培养方法,其中包括以下具体步骤,将200μL低速离心后的肝细胞悬液与800μL37℃预热的生物墨水混合,装载至3D生物打印机上,打印多层格栅结构,打印完成后浸入CaCl2溶液中交联,随后洗净,转移至12孔板中,加入培养液进行培养;混合后肝细胞的密度为1~5×106个细胞/ml;细胞悬液与生物墨水混合体积比为1︰1~1︰4,所述细胞悬液密度为2.5×107个细胞/ml,培养温度为37℃,CO2体积浓度为5%。
6.如权利要求5所述的培养方法,其中,肝脏细胞为人肝癌细胞HepG2细胞系。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202110285467.5A CN112972712B (zh) | 2021-03-17 | 2021-03-17 | 一种用于处理生物墨水的热压灭菌程序及其在人肝类器官3d模型构建中的应用 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202110285467.5A CN112972712B (zh) | 2021-03-17 | 2021-03-17 | 一种用于处理生物墨水的热压灭菌程序及其在人肝类器官3d模型构建中的应用 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN112972712A CN112972712A (zh) | 2021-06-18 |
| CN112972712B true CN112972712B (zh) | 2022-09-30 |
Family
ID=76332662
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202110285467.5A Active CN112972712B (zh) | 2021-03-17 | 2021-03-17 | 一种用于处理生物墨水的热压灭菌程序及其在人肝类器官3d模型构建中的应用 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN112972712B (zh) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN117126914A (zh) * | 2023-10-23 | 2023-11-28 | 深圳市明鉴检测专业技术有限公司 | 一种反应毒副作用的肝类器官模型的药物毒性评价方法 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN108144114A (zh) * | 2018-01-05 | 2018-06-12 | 浙江省医学科学院 | 用于组织工程的3d打印材料及生物可降解支架材料的制备方法 |
| CN110170071A (zh) * | 2019-05-09 | 2019-08-27 | 中国人民解放军总医院 | 促进海藻酸盐基3d打印生物墨水体内外降解和细胞伸展黏附的方法 |
| CN110227184A (zh) * | 2019-07-16 | 2019-09-13 | 南通大学 | 差异性组织工程化神经及应用 |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2019122351A1 (en) * | 2017-12-22 | 2019-06-27 | Cellink Ab | Tissue-specific human bioinks for the physiological 3d-bioprinting of human tissues for in vitro culture and transplantation |
-
2021
- 2021-03-17 CN CN202110285467.5A patent/CN112972712B/zh active Active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN108144114A (zh) * | 2018-01-05 | 2018-06-12 | 浙江省医学科学院 | 用于组织工程的3d打印材料及生物可降解支架材料的制备方法 |
| CN110170071A (zh) * | 2019-05-09 | 2019-08-27 | 中国人民解放军总医院 | 促进海藻酸盐基3d打印生物墨水体内外降解和细胞伸展黏附的方法 |
| CN110227184A (zh) * | 2019-07-16 | 2019-09-13 | 南通大学 | 差异性组织工程化神经及应用 |
Non-Patent Citations (2)
| Title |
|---|
| Effects of Autoclaving, EtOH, and UV Sterilization on the Chemical,Mechanical, Printability, and Biocompatibility Characteristics of Alginate;Parth Chansoria, et al.;《ACS Biomaterials Science & Engineering》;20201231;第6卷;第5191-5201页 * |
| Evaluation of sterilisation methods for bio-ink components: gelatin,gelatin methacryloyl, hyaluronic acid and hyaluronic acid methacryloyl;CathalD O"Connell1, et al.;《Biofabrication》;20190403;第11卷;第1-18页 * |
Also Published As
| Publication number | Publication date |
|---|---|
| CN112972712A (zh) | 2021-06-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Yin et al. | Agarose particle-templated porous bacterial cellulose and its application in cartilage growth in vitro | |
| US6875605B1 (en) | Modular cell culture bioreactor and associated methods | |
| Desai et al. | Three-dimensional in vitro follicle growth: overview of culture models, biomaterials, design parameters and future directions | |
| WO2022237003A1 (zh) | 一种构建复杂异质组织/器官的多级悬浮打印方法 | |
| US20080009064A1 (en) | Temperature-Responsive Microcarrier | |
| CN108587903B (zh) | 一种使用支撑浴的多喷头快速3d打印肿瘤组织模型的方法 | |
| Wu et al. | Recent advances in three-dimensional stem cell culture systems and applications | |
| CN106916781A (zh) | 一种体外三维人体肝组织的构建方法及其应用 | |
| KR102000381B1 (ko) | 폴리이미드 다공질막을 이용하는 세포의 장기 배양, 및 폴리이미드 다공질막을 이용하는 세포의 동결 보존 방법 | |
| CN108410797A (zh) | 在中空纤维生物反应器中扩增干细胞 | |
| US20210062147A1 (en) | Method of manufacturing or differentiating mammalian pluripotent stem cellsor progenitor cells using a hollow fiber bioreactor | |
| Cimetta et al. | Enhancement of viability of muscle precursor cells on 3D scaffold in a perfusion bioreactor | |
| JP2021191305A (ja) | 細胞の培養方法 | |
| JPWO2005014774A1 (ja) | 動物細胞の培養担体と、該培養担体を用いた動物細胞の培養方法および移植方法 | |
| CN112972712B (zh) | 一种用于处理生物墨水的热压灭菌程序及其在人肝类器官3d模型构建中的应用 | |
| CN112522199A (zh) | 一种用于细胞诱导自组织成多细胞球的3d凝胶载体及多细胞球培养方法 | |
| CN113846016B (zh) | 一种高通量多孔阵列芯片、装置、制备方法及应用 | |
| EP2130905A1 (en) | Method for culturing eukaryotic cells | |
| JPH11164685A (ja) | 種々の基質の安定性および/または貯蔵寿命を増加させる方法 | |
| CN114045253A (zh) | 一种基于复合水凝胶的干细胞与胰岛β细胞共培养方法 | |
| BR112020023707A2 (pt) | sistema de cultura celular em biorreator | |
| US9260686B2 (en) | Tubular bioreactor system for use in bone and cartilage tissue engineering | |
| CN116426461A (zh) | 一种体外脂肪肝类器官模型及其制备方法与在药物测试中的应用 | |
| Chen et al. | High-density culture of hepatocytes in a packed-bed bioreactor using a fibrous scaffold from plant | |
| CN102614547B (zh) | 一种快速构建复层细胞的方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant |