CN112789045A - 用于治疗孤独症的组合物和方法 - Google Patents
用于治疗孤独症的组合物和方法 Download PDFInfo
- Publication number
- CN112789045A CN112789045A CN201980048387.9A CN201980048387A CN112789045A CN 112789045 A CN112789045 A CN 112789045A CN 201980048387 A CN201980048387 A CN 201980048387A CN 112789045 A CN112789045 A CN 112789045A
- Authority
- CN
- China
- Prior art keywords
- tyrosine
- autism
- methyl
- study
- week
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 206010003805 Autism Diseases 0.000 title claims abstract description 103
- 208000020706 Autistic disease Diseases 0.000 title claims abstract description 102
- 239000000203 mixture Substances 0.000 title claims abstract description 57
- 238000000034 method Methods 0.000 title claims abstract description 52
- NHTGHBARYWONDQ-UHFFFAOYSA-N (+-)-α-methyl-tyrosine Chemical compound OC(=O)C(N)(C)CC1=CC=C(O)C=C1 NHTGHBARYWONDQ-UHFFFAOYSA-N 0.000 claims abstract description 99
- BTCSSZJGUNDROE-UHFFFAOYSA-N gamma-aminobutyric acid Chemical group NCCCC(O)=O BTCSSZJGUNDROE-UHFFFAOYSA-N 0.000 claims description 24
- OGNSCSPNOLGXSM-UHFFFAOYSA-N (+/-)-DABA Natural products NCCC(N)C(O)=O OGNSCSPNOLGXSM-UHFFFAOYSA-N 0.000 claims description 12
- 241000282414 Homo sapiens Species 0.000 claims description 12
- 229960003692 gamma aminobutyric acid Drugs 0.000 claims description 12
- 239000002775 capsule Substances 0.000 claims description 10
- 210000003169 central nervous system Anatomy 0.000 claims description 10
- 239000003795 chemical substances by application Substances 0.000 claims description 8
- 239000003937 drug carrier Substances 0.000 claims description 8
- 239000000808 adrenergic beta-agonist Substances 0.000 claims description 4
- 239000002552 dosage form Substances 0.000 claims description 4
- 238000013268 sustained release Methods 0.000 claims 1
- 239000012730 sustained-release form Substances 0.000 claims 1
- 238000011282 treatment Methods 0.000 abstract description 75
- 208000024891 symptom Diseases 0.000 abstract description 45
- 230000008859 change Effects 0.000 description 52
- 238000004891 communication Methods 0.000 description 48
- 230000006399 behavior Effects 0.000 description 46
- 239000000902 placebo Substances 0.000 description 46
- 229940068196 placebo Drugs 0.000 description 46
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 45
- 208000029560 autism spectrum disease Diseases 0.000 description 44
- -1 L-AMPT (methylated L-tyrosine Chemical class 0.000 description 36
- 150000001875 compounds Chemical class 0.000 description 34
- 239000003814 drug Substances 0.000 description 34
- 201000010099 disease Diseases 0.000 description 30
- 238000004458 analytical method Methods 0.000 description 28
- 229940122110 Tyrosine hydroxylase inhibitor Drugs 0.000 description 27
- 229940079593 drug Drugs 0.000 description 26
- 230000006872 improvement Effects 0.000 description 25
- 230000000694 effects Effects 0.000 description 21
- 238000005259 measurement Methods 0.000 description 19
- 230000004044 response Effects 0.000 description 18
- 238000012360 testing method Methods 0.000 description 18
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 16
- 230000036470 plasma concentration Effects 0.000 description 16
- 208000035475 disorder Diseases 0.000 description 15
- 150000003839 salts Chemical class 0.000 description 14
- 238000012216 screening Methods 0.000 description 14
- 230000003997 social interaction Effects 0.000 description 14
- NHTGHBARYWONDQ-JTQLQIEISA-N L-α-methyl-Tyrosine Chemical compound OC(=O)[C@](N)(C)CC1=CC=C(O)C=C1 NHTGHBARYWONDQ-JTQLQIEISA-N 0.000 description 13
- 210000004369 blood Anatomy 0.000 description 13
- 239000008280 blood Substances 0.000 description 13
- 230000003989 repetitive behavior Effects 0.000 description 13
- 208000013406 repetitive behavior Diseases 0.000 description 13
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 12
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 12
- 238000003745 diagnosis Methods 0.000 description 12
- 208000019901 Anxiety disease Diseases 0.000 description 11
- 230000036506 anxiety Effects 0.000 description 11
- 238000011156 evaluation Methods 0.000 description 11
- 239000008103 glucose Substances 0.000 description 11
- 206010022998 Irritability Diseases 0.000 description 10
- 230000002411 adverse Effects 0.000 description 10
- 230000008450 motivation Effects 0.000 description 10
- 150000003667 tyrosine derivatives Chemical group 0.000 description 10
- 206010041243 Social avoidant behaviour Diseases 0.000 description 9
- 208000013403 hyperactivity Diseases 0.000 description 9
- 230000003993 interaction Effects 0.000 description 9
- 239000008194 pharmaceutical composition Substances 0.000 description 9
- 208000020016 psychiatric disease Diseases 0.000 description 9
- 208000027765 speech disease Diseases 0.000 description 9
- 230000001225 therapeutic effect Effects 0.000 description 9
- 206010000117 Abnormal behaviour Diseases 0.000 description 8
- 206010024264 Lethargy Diseases 0.000 description 8
- 230000006978 adaptation Effects 0.000 description 8
- 230000008901 benefit Effects 0.000 description 8
- 229910052739 hydrogen Inorganic materials 0.000 description 8
- 239000001257 hydrogen Substances 0.000 description 8
- 230000009467 reduction Effects 0.000 description 8
- 230000003044 adaptive effect Effects 0.000 description 7
- 229940082991 antihypertensives tyrosine hydroxylase inhibitors Drugs 0.000 description 7
- 230000002567 autonomic effect Effects 0.000 description 7
- 230000003542 behavioural effect Effects 0.000 description 7
- 230000006735 deficit Effects 0.000 description 7
- 238000013461 design Methods 0.000 description 7
- 210000002216 heart Anatomy 0.000 description 7
- 125000004435 hydrogen atom Chemical class [H]* 0.000 description 7
- 230000003285 pharmacodynamic effect Effects 0.000 description 7
- 238000011160 research Methods 0.000 description 7
- 238000012552 review Methods 0.000 description 7
- 230000001755 vocal effect Effects 0.000 description 7
- 230000003442 weekly effect Effects 0.000 description 7
- 208000036864 Attention deficit/hyperactivity disease Diseases 0.000 description 6
- WTDRDQBEARUVNC-LURJTMIESA-N L-DOPA Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C(O)=C1 WTDRDQBEARUVNC-LURJTMIESA-N 0.000 description 6
- 208000015802 attention deficit-hyperactivity disease Diseases 0.000 description 6
- 239000002585 base Substances 0.000 description 6
- 238000006243 chemical reaction Methods 0.000 description 6
- 230000034994 death Effects 0.000 description 6
- 231100000517 death Toxicity 0.000 description 6
- 239000003112 inhibitor Substances 0.000 description 6
- 229960004502 levodopa Drugs 0.000 description 6
- 230000004048 modification Effects 0.000 description 6
- 238000012986 modification Methods 0.000 description 6
- 210000002700 urine Anatomy 0.000 description 6
- 206010001497 Agitation Diseases 0.000 description 5
- 208000036640 Asperger disease Diseases 0.000 description 5
- 201000006062 Asperger syndrome Diseases 0.000 description 5
- 102000004190 Enzymes Human genes 0.000 description 5
- 108090000790 Enzymes Proteins 0.000 description 5
- 208000001914 Fragile X syndrome Diseases 0.000 description 5
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 5
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 5
- 108091000117 Tyrosine 3-Monooxygenase Proteins 0.000 description 5
- 102000048218 Tyrosine 3-monooxygenases Human genes 0.000 description 5
- 239000002253 acid Substances 0.000 description 5
- 238000013019 agitation Methods 0.000 description 5
- 150000003943 catecholamines Chemical class 0.000 description 5
- 239000002131 composite material Substances 0.000 description 5
- 230000006870 function Effects 0.000 description 5
- 230000003252 repetitive effect Effects 0.000 description 5
- 229940124597 therapeutic agent Drugs 0.000 description 5
- 238000011269 treatment regimen Methods 0.000 description 5
- 238000002562 urinalysis Methods 0.000 description 5
- UCTWMZQNUQWSLP-VIFPVBQESA-N (R)-adrenaline Chemical compound CNC[C@H](O)C1=CC=C(O)C(O)=C1 UCTWMZQNUQWSLP-VIFPVBQESA-N 0.000 description 4
- 229930182837 (R)-adrenaline Natural products 0.000 description 4
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 4
- 241000725303 Human immunodeficiency virus Species 0.000 description 4
- 241000124008 Mammalia Species 0.000 description 4
- 230000002159 abnormal effect Effects 0.000 description 4
- 238000013459 approach Methods 0.000 description 4
- 230000009286 beneficial effect Effects 0.000 description 4
- FUWUEFKEXZQKKA-UHFFFAOYSA-N beta-thujaplicin Chemical compound CC(C)C=1C=CC=C(O)C(=O)C=1 FUWUEFKEXZQKKA-UHFFFAOYSA-N 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 230000000768 catecholaminergic effect Effects 0.000 description 4
- 230000007547 defect Effects 0.000 description 4
- 230000007812 deficiency Effects 0.000 description 4
- 230000006866 deterioration Effects 0.000 description 4
- 229960005139 epinephrine Drugs 0.000 description 4
- 230000007717 exclusion Effects 0.000 description 4
- 231100000252 nontoxic Toxicity 0.000 description 4
- 230000003000 nontoxic effect Effects 0.000 description 4
- 230000002746 orthostatic effect Effects 0.000 description 4
- 230000002085 persistent effect Effects 0.000 description 4
- 230000000069 prophylactic effect Effects 0.000 description 4
- 235000018102 proteins Nutrition 0.000 description 4
- 102000004169 proteins and genes Human genes 0.000 description 4
- 108090000623 proteins and genes Proteins 0.000 description 4
- 230000002829 reductive effect Effects 0.000 description 4
- 230000001953 sensory effect Effects 0.000 description 4
- 208000011580 syndromic disease Diseases 0.000 description 4
- NHTGHBARYWONDQ-SNVBAGLBSA-N (2r)-2-amino-3-(4-hydroxyphenyl)-2-methylpropanoic acid Chemical compound OC(=O)[C@@](N)(C)CC1=CC=C(O)C=C1 NHTGHBARYWONDQ-SNVBAGLBSA-N 0.000 description 3
- 208000030507 AIDS Diseases 0.000 description 3
- 208000006096 Attention Deficit Disorder with Hyperactivity Diseases 0.000 description 3
- 206010010144 Completed suicide Diseases 0.000 description 3
- LCGLNKUTAGEVQW-UHFFFAOYSA-N Dimethyl ether Chemical compound COC LCGLNKUTAGEVQW-UHFFFAOYSA-N 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- 241000700721 Hepatitis B virus Species 0.000 description 3
- 208000026350 Inborn Genetic disease Diseases 0.000 description 3
- 241001465754 Metazoa Species 0.000 description 3
- 208000028017 Psychotic disease Diseases 0.000 description 3
- 208000006289 Rett Syndrome Diseases 0.000 description 3
- 208000006011 Stroke Diseases 0.000 description 3
- 230000005856 abnormality Effects 0.000 description 3
- 125000000217 alkyl group Chemical group 0.000 description 3
- 150000001412 amines Chemical class 0.000 description 3
- 210000003403 autonomic nervous system Anatomy 0.000 description 3
- 230000036772 blood pressure Effects 0.000 description 3
- 231100000867 compulsive behavior Toxicity 0.000 description 3
- 229940124301 concurrent medication Drugs 0.000 description 3
- 230000007423 decrease Effects 0.000 description 3
- 230000035487 diastolic blood pressure Effects 0.000 description 3
- 230000008451 emotion Effects 0.000 description 3
- 206010015037 epilepsy Diseases 0.000 description 3
- 230000012953 feeding on blood of other organism Effects 0.000 description 3
- 230000014509 gene expression Effects 0.000 description 3
- 208000016361 genetic disease Diseases 0.000 description 3
- 229940093915 gynecological organic acid Drugs 0.000 description 3
- 125000000623 heterocyclic group Chemical group 0.000 description 3
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 3
- 239000003018 immunosuppressive agent Substances 0.000 description 3
- 238000007918 intramuscular administration Methods 0.000 description 3
- 238000001990 intravenous administration Methods 0.000 description 3
- 230000000670 limiting effect Effects 0.000 description 3
- 230000033001 locomotion Effects 0.000 description 3
- 238000007726 management method Methods 0.000 description 3
- 230000007246 mechanism Effects 0.000 description 3
- 238000002483 medication Methods 0.000 description 3
- 150000007522 mineralic acids Chemical class 0.000 description 3
- 238000012544 monitoring process Methods 0.000 description 3
- 150000007524 organic acids Chemical class 0.000 description 3
- 235000005985 organic acids Nutrition 0.000 description 3
- 229920001184 polypeptide Polymers 0.000 description 3
- 102000004196 processed proteins & peptides Human genes 0.000 description 3
- 108090000765 processed proteins & peptides Proteins 0.000 description 3
- 229940001470 psychoactive drug Drugs 0.000 description 3
- 239000004089 psychotropic agent Substances 0.000 description 3
- 238000005070 sampling Methods 0.000 description 3
- 201000000980 schizophrenia Diseases 0.000 description 3
- 238000007920 subcutaneous administration Methods 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 230000002459 sustained effect Effects 0.000 description 3
- 230000035488 systolic blood pressure Effects 0.000 description 3
- 239000003826 tablet Substances 0.000 description 3
- 230000001052 transient effect Effects 0.000 description 3
- 229960004441 tyrosine Drugs 0.000 description 3
- DIWRORZWFLOCLC-HNNXBMFYSA-N (3s)-7-chloro-5-(2-chlorophenyl)-3-hydroxy-1,3-dihydro-1,4-benzodiazepin-2-one Chemical compound N([C@H](C(NC1=CC=C(Cl)C=C11)=O)O)=C1C1=CC=CC=C1Cl DIWRORZWFLOCLC-HNNXBMFYSA-N 0.000 description 2
- 102100036475 Alanine aminotransferase 1 Human genes 0.000 description 2
- 108010082126 Alanine transaminase Proteins 0.000 description 2
- 208000007848 Alcoholism Diseases 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- 108010003415 Aspartate Aminotransferases Proteins 0.000 description 2
- 102000004625 Aspartate Aminotransferases Human genes 0.000 description 2
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- BPYKTIZUTYGOLE-IFADSCNNSA-N Bilirubin Chemical compound N1C(=O)C(C)=C(C=C)\C1=C\C1=C(C)C(CCC(O)=O)=C(CC2=C(C(C)=C(\C=C/3C(=C(C=C)C(=O)N\3)C)N2)CCC(O)=O)N1 BPYKTIZUTYGOLE-IFADSCNNSA-N 0.000 description 2
- 208000024172 Cardiovascular disease Diseases 0.000 description 2
- 206010008190 Cerebrovascular accident Diseases 0.000 description 2
- GJSURZIOUXUGAL-UHFFFAOYSA-N Clonidine Chemical compound ClC1=CC=CC(Cl)=C1NC1=NCCN1 GJSURZIOUXUGAL-UHFFFAOYSA-N 0.000 description 2
- 206010011509 Crystalluria Diseases 0.000 description 2
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- XUMBMVFBXHLACL-UHFFFAOYSA-N Melanin Chemical compound O=C1C(=O)C(C2=CNC3=C(C(C(=O)C4=C32)=O)C)=C2C4=CNC2=C1C XUMBMVFBXHLACL-UHFFFAOYSA-N 0.000 description 2
- 206010028980 Neoplasm Diseases 0.000 description 2
- BHHGXPLMPWCGHP-UHFFFAOYSA-N Phenethylamine Chemical compound NCCC1=CC=CC=C1 BHHGXPLMPWCGHP-UHFFFAOYSA-N 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- 239000002202 Polyethylene glycol Substances 0.000 description 2
- 208000025890 Social Communication disease Diseases 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 206010042458 Suicidal ideation Diseases 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 230000002378 acidificating effect Effects 0.000 description 2
- 150000007513 acids Chemical class 0.000 description 2
- 230000001800 adrenalinergic effect Effects 0.000 description 2
- 230000008484 agonism Effects 0.000 description 2
- NDAUXUAQIAJITI-UHFFFAOYSA-N albuterol Chemical compound CC(C)(C)NCC(O)C1=CC=C(O)C(CO)=C1 NDAUXUAQIAJITI-UHFFFAOYSA-N 0.000 description 2
- 208000025746 alcohol use disease Diseases 0.000 description 2
- 229910052783 alkali metal Inorganic materials 0.000 description 2
- 150000001340 alkali metals Chemical class 0.000 description 2
- 230000004075 alteration Effects 0.000 description 2
- 229940024606 amino acid Drugs 0.000 description 2
- 235000001014 amino acid Nutrition 0.000 description 2
- 150000001413 amino acids Chemical class 0.000 description 2
- 208000006673 asthma Diseases 0.000 description 2
- 230000037424 autonomic function Effects 0.000 description 2
- 239000000090 biomarker Substances 0.000 description 2
- 210000004556 brain Anatomy 0.000 description 2
- 201000011510 cancer Diseases 0.000 description 2
- 125000004432 carbon atom Chemical group C* 0.000 description 2
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 2
- YCIMNLLNPGFGHC-UHFFFAOYSA-N catechol Chemical compound OC1=CC=CC=C1O YCIMNLLNPGFGHC-UHFFFAOYSA-N 0.000 description 2
- 208000026106 cerebrovascular disease Diseases 0.000 description 2
- 230000006949 cholinergic function Effects 0.000 description 2
- 230000001684 chronic effect Effects 0.000 description 2
- 230000000052 comparative effect Effects 0.000 description 2
- DDRJAANPRJIHGJ-UHFFFAOYSA-N creatinine Chemical compound CN1CC(=O)NC1=N DDRJAANPRJIHGJ-UHFFFAOYSA-N 0.000 description 2
- 239000013078 crystal Substances 0.000 description 2
- YPHMISFOHDHNIV-FSZOTQKASA-N cycloheximide Chemical compound C1[C@@H](C)C[C@H](C)C(=O)[C@@H]1[C@H](O)CC1CC(=O)NC(=O)C1 YPHMISFOHDHNIV-FSZOTQKASA-N 0.000 description 2
- 230000001627 detrimental effect Effects 0.000 description 2
- 235000005911 diet Nutrition 0.000 description 2
- VYFYYTLLBUKUHU-UHFFFAOYSA-N dopamine Chemical compound NCCC1=CC=C(O)C(O)=C1 VYFYYTLLBUKUHU-UHFFFAOYSA-N 0.000 description 2
- 230000007613 environmental effect Effects 0.000 description 2
- 230000001747 exhibiting effect Effects 0.000 description 2
- 210000001508 eye Anatomy 0.000 description 2
- 230000008921 facial expression Effects 0.000 description 2
- ASUTZQLVASHGKV-JDFRZJQESA-N galanthamine Chemical compound O1C(=C23)C(OC)=CC=C2CN(C)CC[C@]23[C@@H]1C[C@@H](O)C=C2 ASUTZQLVASHGKV-JDFRZJQESA-N 0.000 description 2
- 230000002068 genetic effect Effects 0.000 description 2
- 230000002008 hemorrhagic effect Effects 0.000 description 2
- 201000001421 hyperglycemia Diseases 0.000 description 2
- 125000004531 indol-5-yl group Chemical group [H]N1C([H])=C([H])C2=C([H])C(*)=C([H])C([H])=C12 0.000 description 2
- 208000015181 infectious disease Diseases 0.000 description 2
- 230000002401 inhibitory effect Effects 0.000 description 2
- 230000005764 inhibitory process Effects 0.000 description 2
- 238000007689 inspection Methods 0.000 description 2
- 230000002452 interceptive effect Effects 0.000 description 2
- 239000007951 isotonicity adjuster Substances 0.000 description 2
- 208000017169 kidney disease Diseases 0.000 description 2
- 208000019423 liver disease Diseases 0.000 description 2
- 230000007774 longterm Effects 0.000 description 2
- 230000001404 mediated effect Effects 0.000 description 2
- 230000002175 menstrual effect Effects 0.000 description 2
- 230000002503 metabolic effect Effects 0.000 description 2
- 210000000056 organ Anatomy 0.000 description 2
- 230000037361 pathway Effects 0.000 description 2
- 230000008447 perception Effects 0.000 description 2
- 210000001428 peripheral nervous system Anatomy 0.000 description 2
- 239000000546 pharmaceutical excipient Substances 0.000 description 2
- 230000000144 pharmacologic effect Effects 0.000 description 2
- 229960002036 phenytoin Drugs 0.000 description 2
- 230000001766 physiological effect Effects 0.000 description 2
- 229920001223 polyethylene glycol Polymers 0.000 description 2
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- 229960002052 salbutamol Drugs 0.000 description 2
- 208000022610 schizoaffective disease Diseases 0.000 description 2
- 230000035945 sensitivity Effects 0.000 description 2
- 210000002966 serum Anatomy 0.000 description 2
- 208000013363 skeletal muscle disease Diseases 0.000 description 2
- 229910052708 sodium Inorganic materials 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 239000000243 solution Substances 0.000 description 2
- 238000001228 spectrum Methods 0.000 description 2
- KZNICNPSHKQLFF-UHFFFAOYSA-N succinimide Chemical compound O=C1CCC(=O)N1 KZNICNPSHKQLFF-UHFFFAOYSA-N 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- 230000005062 synaptic transmission Effects 0.000 description 2
- 230000016978 synaptic transmission, cholinergic Effects 0.000 description 2
- 230000007593 synaptic transmission, glutaminergic Effects 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- 238000002560 therapeutic procedure Methods 0.000 description 2
- 230000000699 topical effect Effects 0.000 description 2
- 231100000331 toxic Toxicity 0.000 description 2
- 230000002588 toxic effect Effects 0.000 description 2
- 230000000472 traumatic effect Effects 0.000 description 2
- 229930007845 β-thujaplicin Natural products 0.000 description 2
- JWZZKOKVBUJMES-UHFFFAOYSA-N (+-)-Isoprenaline Chemical compound CC(C)NCC(O)C1=CC=C(O)C(O)=C1 JWZZKOKVBUJMES-UHFFFAOYSA-N 0.000 description 1
- XWTYSIMOBUGWOL-UHFFFAOYSA-N (+-)-Terbutaline Chemical compound CC(C)(C)NCC(O)C1=CC(O)=CC(O)=C1 XWTYSIMOBUGWOL-UHFFFAOYSA-N 0.000 description 1
- YKJYKKNCCRKFSL-RDBSUJKOSA-N (-)-anisomycin Chemical compound C1=CC(OC)=CC=C1C[C@@H]1[C@H](OC(C)=O)[C@@H](O)CN1 YKJYKKNCCRKFSL-RDBSUJKOSA-N 0.000 description 1
- UIKROCXWUNQSPJ-VIFPVBQESA-N (-)-cotinine Chemical compound C1CC(=O)N(C)[C@@H]1C1=CC=CN=C1 UIKROCXWUNQSPJ-VIFPVBQESA-N 0.000 description 1
- SFLSHLFXELFNJZ-QMMMGPOBSA-N (-)-norepinephrine Chemical compound NC[C@H](O)C1=CC=C(O)C(O)=C1 SFLSHLFXELFNJZ-QMMMGPOBSA-N 0.000 description 1
- VOYCNOJFAJAILW-CAMHOICYSA-N (1r,4s,5s,6s)-4-[[(2s)-2-amino-4-methylsulfanylbutanoyl]amino]-2,2-dioxo-2$l^{6}-thiabicyclo[3.1.0]hexane-4,6-dicarboxylic acid Chemical compound CSCC[C@H](N)C(=O)N[C@@]1(C(O)=O)CS(=O)(=O)[C@H]2[C@H](C(O)=O)[C@@H]12 VOYCNOJFAJAILW-CAMHOICYSA-N 0.000 description 1
- AXDLCFOOGCNDST-SECBINFHSA-N (2r)-3-(4-hydroxyphenyl)-2-(methylazaniumyl)propanoate Chemical compound CN[C@@H](C(O)=O)CC1=CC=C(O)C=C1 AXDLCFOOGCNDST-SECBINFHSA-N 0.000 description 1
- SWZCTMTWRHEBIN-QFIPXVFZSA-N (2s)-2-(9h-fluoren-9-ylmethoxycarbonylamino)-3-(4-hydroxyphenyl)propanoic acid Chemical compound C([C@@H](C(=O)O)NC(=O)OCC1C2=CC=CC=C2C2=CC=CC=C21)C1=CC=C(O)C=C1 SWZCTMTWRHEBIN-QFIPXVFZSA-N 0.000 description 1
- CNBUSIJNWNXLQQ-NSHDSACASA-N (2s)-3-(4-hydroxyphenyl)-2-[(2-methylpropan-2-yl)oxycarbonylamino]propanoic acid Chemical compound CC(C)(C)OC(=O)N[C@H](C(O)=O)CC1=CC=C(O)C=C1 CNBUSIJNWNXLQQ-NSHDSACASA-N 0.000 description 1
- JDKLPDJLXHXHNV-MFVUMRCOSA-N (3s,6s,9r,12s,15s,23s)-15-[[(2s)-2-acetamidohexanoyl]amino]-9-benzyl-6-[3-(diaminomethylideneamino)propyl]-12-(1h-imidazol-5-ylmethyl)-3-(1h-indol-3-ylmethyl)-2,5,8,11,14,17-hexaoxo-1,4,7,10,13,18-hexazacyclotricosane-23-carboxamide Chemical compound C([C@@H]1C(=O)N[C@@H](CCCN=C(N)N)C(=O)N[C@@H](CC=2C3=CC=CC=C3NC=2)C(=O)N[C@@H](CCCCNC(=O)C[C@@H](C(N[C@@H](CC=2NC=NC=2)C(=O)N1)=O)NC(=O)[C@@H](NC(C)=O)CCCC)C(N)=O)C1=CC=CC=C1 JDKLPDJLXHXHNV-MFVUMRCOSA-N 0.000 description 1
- WRIDQFICGBMAFQ-UHFFFAOYSA-N (E)-8-Octadecenoic acid Natural products CCCCCCCCCC=CCCCCCCC(O)=O WRIDQFICGBMAFQ-UHFFFAOYSA-N 0.000 description 1
- RTHCYVBBDHJXIQ-MRXNPFEDSA-N (R)-fluoxetine Chemical compound O([C@H](CCNC)C=1C=CC=CC=1)C1=CC=C(C(F)(F)F)C=C1 RTHCYVBBDHJXIQ-MRXNPFEDSA-N 0.000 description 1
- NDAUXUAQIAJITI-LBPRGKRZSA-N (R)-salbutamol Chemical compound CC(C)(C)NC[C@H](O)C1=CC=C(O)C(CO)=C1 NDAUXUAQIAJITI-LBPRGKRZSA-N 0.000 description 1
- KWTSXDURSIMDCE-QMMMGPOBSA-N (S)-amphetamine Chemical compound C[C@H](N)CC1=CC=CC=C1 KWTSXDURSIMDCE-QMMMGPOBSA-N 0.000 description 1
- 125000003088 (fluoren-9-ylmethoxy)carbonyl group Chemical group 0.000 description 1
- NYPYHUZRZVSYKL-UHFFFAOYSA-N -3,5-Diiodotyrosine Natural products OC(=O)C(N)CC1=CC(I)=C(O)C(I)=C1 NYPYHUZRZVSYKL-UHFFFAOYSA-N 0.000 description 1
- YXAOOTNFFAQIPZ-UHFFFAOYSA-N 1-nitrosonaphthalen-2-ol Chemical compound C1=CC=CC2=C(N=O)C(O)=CC=C21 YXAOOTNFFAQIPZ-UHFFFAOYSA-N 0.000 description 1
- 125000001462 1-pyrrolyl group Chemical group [*]N1C([H])=C([H])C([H])=C1[H] 0.000 description 1
- SVUOLADPCWQTTE-UHFFFAOYSA-N 1h-1,2-benzodiazepine Chemical class N1N=CC=CC2=CC=CC=C12 SVUOLADPCWQTTE-UHFFFAOYSA-N 0.000 description 1
- KMVWNDHKTPHDMT-UHFFFAOYSA-N 2,4,6-tripyridin-2-yl-1,3,5-triazine Chemical compound N1=CC=CC=C1C1=NC(C=2N=CC=CC=2)=NC(C=2N=CC=CC=2)=N1 KMVWNDHKTPHDMT-UHFFFAOYSA-N 0.000 description 1
- CQOZJDNCADWEKH-UHFFFAOYSA-N 2-[3,3-bis(2-hydroxyphenyl)propyl]phenol Chemical group OC1=CC=CC=C1CCC(C=1C(=CC=CC=1)O)C1=CC=CC=C1O CQOZJDNCADWEKH-UHFFFAOYSA-N 0.000 description 1
- 125000005273 2-acetoxybenzoic acid group Chemical group 0.000 description 1
- JZKXXXDKRQWDET-UHFFFAOYSA-N 2-azaniumyl-3-(3-hydroxyphenyl)propanoate Chemical compound OC(=O)C(N)CC1=CC=CC(O)=C1 JZKXXXDKRQWDET-UHFFFAOYSA-N 0.000 description 1
- WRFPVMFCRNYQNR-UHFFFAOYSA-N 2-hydroxyphenylalanine Chemical compound OC(=O)C(N)CC1=CC=CC=C1O WRFPVMFCRNYQNR-UHFFFAOYSA-N 0.000 description 1
- YHGIKDGPTHMIDI-UHFFFAOYSA-N 2-nonoxytetradec-1-ene Chemical group C(CCCCCCCCCCC)C(=C)OCCCCCCCCC YHGIKDGPTHMIDI-UHFFFAOYSA-N 0.000 description 1
- LQJBNNIYVWPHFW-UHFFFAOYSA-N 20:1omega9c fatty acid Natural products CCCCCCCCCCC=CCCCCCCCC(O)=O LQJBNNIYVWPHFW-UHFFFAOYSA-N 0.000 description 1
- KXFYXFVWCIUKDR-UHFFFAOYSA-N 3-(4-tert-butylphenyl)-4-ethyl-1h-1,2,4-triazole-5-thione Chemical compound N1C(=S)N(CC)C(C=2C=CC(=CC=2)C(C)(C)C)=N1 KXFYXFVWCIUKDR-UHFFFAOYSA-N 0.000 description 1
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- ACWBBAGYTKWBCD-ZETCQYMHSA-N 3-chloro-L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C(Cl)=C1 ACWBBAGYTKWBCD-ZETCQYMHSA-N 0.000 description 1
- UQTZMGFTRHFAAM-ZETCQYMHSA-N 3-iodo-L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C(I)=C1 UQTZMGFTRHFAAM-ZETCQYMHSA-N 0.000 description 1
- FBTSQILOGYXGMD-LURJTMIESA-N 3-nitro-L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C([N+]([O-])=O)=C1 FBTSQILOGYXGMD-LURJTMIESA-N 0.000 description 1
- 125000004580 4,5-dihydroimidazol-2-yl group Chemical group N1C(=NCC1)* 0.000 description 1
- 125000002373 5 membered heterocyclic group Chemical group 0.000 description 1
- LSLYOANBFKQKPT-DIFFPNOSSA-N 5-[(1r)-1-hydroxy-2-[[(2r)-1-(4-hydroxyphenyl)propan-2-yl]amino]ethyl]benzene-1,3-diol Chemical compound C([C@@H](C)NC[C@H](O)C=1C=C(O)C=C(O)C=1)C1=CC=C(O)C=C1 LSLYOANBFKQKPT-DIFFPNOSSA-N 0.000 description 1
- SUQZNPQQZDQDPJ-UHFFFAOYSA-N 5-iodoquinolin-8-ol Chemical compound C1=CN=C2C(O)=CC=C(I)C2=C1 SUQZNPQQZDQDPJ-UHFFFAOYSA-N 0.000 description 1
- 125000004070 6 membered heterocyclic group Chemical group 0.000 description 1
- 239000005725 8-Hydroxyquinoline Substances 0.000 description 1
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 1
- QSBYPNXLFMSGKH-UHFFFAOYSA-N 9-Heptadecensaeure Natural products CCCCCCCC=CCCCCCCCC(O)=O QSBYPNXLFMSGKH-UHFFFAOYSA-N 0.000 description 1
- 230000035502 ADME Effects 0.000 description 1
- 241000238876 Acari Species 0.000 description 1
- 208000002874 Acne Vulgaris Diseases 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-M Acrylate Chemical compound [O-]C(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-M 0.000 description 1
- 206010067484 Adverse reaction Diseases 0.000 description 1
- 102000009027 Albumins Human genes 0.000 description 1
- 108010088751 Albumins Proteins 0.000 description 1
- 102000002260 Alkaline Phosphatase Human genes 0.000 description 1
- 108020004774 Alkaline Phosphatase Proteins 0.000 description 1
- 102000034263 Amino acid transporters Human genes 0.000 description 1
- 108050005273 Amino acid transporters Proteins 0.000 description 1
- 229940097396 Aminopeptidase inhibitor Drugs 0.000 description 1
- 239000004382 Amylase Substances 0.000 description 1
- 102000013142 Amylases Human genes 0.000 description 1
- 108010065511 Amylases Proteins 0.000 description 1
- YKJYKKNCCRKFSL-UHFFFAOYSA-N Anisomycin Natural products C1=CC(OC)=CC=C1CC1C(OC(C)=O)C(O)CN1 YKJYKKNCCRKFSL-UHFFFAOYSA-N 0.000 description 1
- 206010002942 Apathy Diseases 0.000 description 1
- KCOULPRVOZDQEL-IFNZWHIZSA-N Aquayamycin Chemical compound C1[C@@H](O)[C@H](O)[C@@H](C)O[C@H]1C1=CC=C(C(=O)C=2[C@]3(C(=O)C[C@](C)(O)C[C@@]3(O)C=CC=2C2=O)O)C2=C1O KCOULPRVOZDQEL-IFNZWHIZSA-N 0.000 description 1
- KCOULPRVOZDQEL-UHFFFAOYSA-N Aquayamycin Natural products C1C(O)C(O)C(C)OC1C1=CC=C(C(=O)C=2C3(C(=O)CC(C)(O)CC3(O)C=CC=2C2=O)O)C2=C1O KCOULPRVOZDQEL-UHFFFAOYSA-N 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- DCXYFEDJOCDNAF-UHFFFAOYSA-N Asparagine Natural products OC(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-N 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-M Bicarbonate Chemical compound OC([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-M 0.000 description 1
- 208000020925 Bipolar disease Diseases 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- 206010048409 Brain malformation Diseases 0.000 description 1
- COVZYZSDYWQREU-UHFFFAOYSA-N Busulfan Chemical compound CS(=O)(=O)OCCCCOS(C)(=O)=O COVZYZSDYWQREU-UHFFFAOYSA-N 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 241000700198 Cavia Species 0.000 description 1
- 108091006146 Channels Proteins 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- 206010010219 Compulsions Diseases 0.000 description 1
- 206010010356 Congenital anomaly Diseases 0.000 description 1
- 206010010904 Convulsion Diseases 0.000 description 1
- UIKROCXWUNQSPJ-UHFFFAOYSA-N Cotinine Natural products C1CC(=O)N(C)C1C1=CC=CN=C1 UIKROCXWUNQSPJ-UHFFFAOYSA-N 0.000 description 1
- 241000938605 Crocodylia Species 0.000 description 1
- 206010011469 Crying Diseases 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- LEVWYRKDKASIDU-QWWZWVQMSA-N D-cystine Chemical compound OC(=O)[C@H](N)CSSC[C@@H](N)C(O)=O LEVWYRKDKASIDU-QWWZWVQMSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- WQZGKKKJIJFFOK-QTVWNMPRSA-N D-mannopyranose Chemical compound OC[C@H]1OC(O)[C@@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-QTVWNMPRSA-N 0.000 description 1
- 206010012335 Dependence Diseases 0.000 description 1
- 239000004375 Dextrin Substances 0.000 description 1
- 229920001353 Dextrin Polymers 0.000 description 1
- 238000008789 Direct Bilirubin Methods 0.000 description 1
- 208000027534 Emotional disease Diseases 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- 241000287828 Gallus gallus Species 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 208000034308 Grand mal convulsion Diseases 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 101000630121 Homo sapiens Probable cysteine-tRNA ligase, mitochondrial Proteins 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical class [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- 108060003951 Immunoglobulin Proteins 0.000 description 1
- 206010022524 Intentional self-injury Diseases 0.000 description 1
- HUYWAWARQUIQLE-UHFFFAOYSA-N Isoetharine Chemical compound CC(C)NC(CC)C(O)C1=CC=C(O)C(O)=C1 HUYWAWARQUIQLE-UHFFFAOYSA-N 0.000 description 1
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 1
- DCXYFEDJOCDNAF-REOHCLBHSA-N L-asparagine Chemical compound OC(=O)[C@@H](N)CC(N)=O DCXYFEDJOCDNAF-REOHCLBHSA-N 0.000 description 1
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 1
- 239000004395 L-leucine Substances 0.000 description 1
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 1
- 102000002704 Leucyl aminopeptidase Human genes 0.000 description 1
- 108010004098 Leucyl aminopeptidase Proteins 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- DUGOZIWVEXMGBE-UHFFFAOYSA-N Methylphenidate Chemical compound C=1C=CC=CC=1C(C(=O)OC)C1CCCCN1 DUGOZIWVEXMGBE-UHFFFAOYSA-N 0.000 description 1
- 208000001089 Multiple system atrophy Diseases 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 1
- 150000001204 N-oxides Chemical class 0.000 description 1
- 208000012902 Nervous system disease Diseases 0.000 description 1
- 102000019315 Nicotinic acetylcholine receptors Human genes 0.000 description 1
- 108050006807 Nicotinic acetylcholine receptors Proteins 0.000 description 1
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 1
- 206010067482 No adverse event Diseases 0.000 description 1
- ZQPPMHVWECSIRJ-UHFFFAOYSA-N Oleic acid Natural products CCCCCCCCC=CCCCCCCCC(O)=O ZQPPMHVWECSIRJ-UHFFFAOYSA-N 0.000 description 1
- 239000005642 Oleic acid Substances 0.000 description 1
- 206010031127 Orthostatic hypotension Diseases 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 241000286209 Phasianidae Species 0.000 description 1
- CXOFVDLJLONNDW-UHFFFAOYSA-N Phenytoin Chemical compound N1C(=O)NC(=O)C1(C=1C=CC=CC=1)C1=CC=CC=C1 CXOFVDLJLONNDW-UHFFFAOYSA-N 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- VQDBNKDJNJQRDG-UHFFFAOYSA-N Pirbuterol Chemical compound CC(C)(C)NCC(O)C1=CC=C(O)C(CO)=N1 VQDBNKDJNJQRDG-UHFFFAOYSA-N 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- 241000288906 Primates Species 0.000 description 1
- 102100026179 Probable cysteine-tRNA ligase, mitochondrial Human genes 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- 208000033712 Self injurious behaviour Diseases 0.000 description 1
- GIIZNNXWQWCKIB-UHFFFAOYSA-N Serevent Chemical compound C1=C(O)C(CO)=CC(C(O)CNCCCCCCOCCCCC=2C=CC=CC=2)=C1 GIIZNNXWQWCKIB-UHFFFAOYSA-N 0.000 description 1
- 102000007562 Serum Albumin Human genes 0.000 description 1
- 108010071390 Serum Albumin Proteins 0.000 description 1
- 208000004301 Sinus Arrhythmia Diseases 0.000 description 1
- 208000032140 Sleepiness Diseases 0.000 description 1
- 206010041349 Somnolence Diseases 0.000 description 1
- 206010042008 Stereotypy Diseases 0.000 description 1
- 206010042464 Suicide attempt Diseases 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- 238000008050 Total Bilirubin Reagent Methods 0.000 description 1
- 206010067584 Type 1 diabetes mellitus Diseases 0.000 description 1
- GXBMIBRIOWHPDT-UHFFFAOYSA-N Vasopressin Natural products N1C(=O)C(CC=2C=C(O)C=CC=2)NC(=O)C(N)CSSCC(C(=O)N2C(CCC2)C(=O)NC(CCCN=C(N)N)C(=O)NCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(CCC(N)=O)NC(=O)C1CC1=CC=CC=C1 GXBMIBRIOWHPDT-UHFFFAOYSA-N 0.000 description 1
- 102000002852 Vasopressins Human genes 0.000 description 1
- 108010004977 Vasopressins Proteins 0.000 description 1
- 241000251539 Vertebrata <Metazoa> Species 0.000 description 1
- 229920002310 Welan gum Polymers 0.000 description 1
- DGEZNRSVGBDHLK-UHFFFAOYSA-N [1,10]phenanthroline Chemical compound C1=CN=C2C3=NC=CC=C3C=CC2=C1 DGEZNRSVGBDHLK-UHFFFAOYSA-N 0.000 description 1
- 210000001015 abdomen Anatomy 0.000 description 1
- 230000001594 aberrant effect Effects 0.000 description 1
- 239000003070 absorption delaying agent Substances 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 125000000738 acetamido group Chemical group [H]C([H])([H])C(=O)N([H])[*] 0.000 description 1
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 1
- OIPILFWXSMYKGL-UHFFFAOYSA-N acetylcholine Chemical compound CC(=O)OCC[N+](C)(C)C OIPILFWXSMYKGL-UHFFFAOYSA-N 0.000 description 1
- 229960004373 acetylcholine Drugs 0.000 description 1
- 206010000496 acne Diseases 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 230000006838 adverse reaction Effects 0.000 description 1
- 230000016571 aggressive behavior Effects 0.000 description 1
- 235000004279 alanine Nutrition 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 150000001336 alkenes Chemical class 0.000 description 1
- 208000026935 allergic disease Diseases 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 125000004202 aminomethyl group Chemical group [H]N([H])C([H])([H])* 0.000 description 1
- 229940025084 amphetamine Drugs 0.000 description 1
- 210000004727 amygdala Anatomy 0.000 description 1
- 235000019418 amylase Nutrition 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 230000000844 anti-bacterial effect Effects 0.000 description 1
- 230000003466 anti-cipated effect Effects 0.000 description 1
- 239000003429 antifungal agent Substances 0.000 description 1
- 229940121375 antifungal agent Drugs 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 235000006708 antioxidants Nutrition 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- KBZOIRJILGZLEJ-LGYYRGKSSA-N argipressin Chemical compound C([C@H]1C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CSSC[C@@H](C(N[C@@H](CC=2C=CC(O)=CC=2)C(=O)N1)=O)N)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCN=C(N)N)C(=O)NCC(N)=O)C1=CC=CC=C1 KBZOIRJILGZLEJ-LGYYRGKSSA-N 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 229960001230 asparagine Drugs 0.000 description 1
- 235000009582 asparagine Nutrition 0.000 description 1
- 230000000386 athletic effect Effects 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- 230000009910 autonomic response Effects 0.000 description 1
- 229940125717 barbiturate Drugs 0.000 description 1
- 150000007514 bases Chemical class 0.000 description 1
- 208000013404 behavioral symptom Diseases 0.000 description 1
- 150000001555 benzenes Chemical group 0.000 description 1
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid group Chemical group C(C1=CC=CC=C1)(=O)O WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 1
- 125000003236 benzoyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C(*)=O 0.000 description 1
- 125000001797 benzyl group Chemical class [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 1
- 229940125388 beta agonist Drugs 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 238000009534 blood test Methods 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 208000029028 brain injury Diseases 0.000 description 1
- 239000012267 brine Substances 0.000 description 1
- 206010006514 bruxism Diseases 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- QXDMQSPYEZFLGF-UHFFFAOYSA-L calcium oxalate Chemical compound [Ca+2].[O-]C(=O)C([O-])=O QXDMQSPYEZFLGF-UHFFFAOYSA-L 0.000 description 1
- 229930003827 cannabinoid Natural products 0.000 description 1
- 239000003557 cannabinoid Substances 0.000 description 1
- FFGPTBGBLSHEPO-UHFFFAOYSA-N carbamazepine Chemical compound C1=CC2=CC=CC=C2N(C(=O)N)C2=CC=CC=C21 FFGPTBGBLSHEPO-UHFFFAOYSA-N 0.000 description 1
- 229960000623 carbamazepine Drugs 0.000 description 1
- 125000004556 carbazol-9-yl group Chemical group C1=CC=CC=2C3=CC=CC=C3N(C12)* 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 235000014633 carbohydrates Nutrition 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 1
- 150000001735 carboxylic acids Chemical class 0.000 description 1
- 230000000747 cardiac effect Effects 0.000 description 1
- 210000004027 cell Anatomy 0.000 description 1
- 210000001638 cerebellum Anatomy 0.000 description 1
- 230000002490 cerebral effect Effects 0.000 description 1
- 208000012056 cerebral malformation Diseases 0.000 description 1
- 239000002738 chelating agent Substances 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 235000013330 chicken meat Nutrition 0.000 description 1
- 208000011654 childhood malignant neoplasm Diseases 0.000 description 1
- 230000008131 children development Effects 0.000 description 1
- 230000001713 cholinergic effect Effects 0.000 description 1
- 150000001860 citric acid derivatives Chemical class 0.000 description 1
- 229960001117 clenbuterol Drugs 0.000 description 1
- STJMRWALKKWQGH-UHFFFAOYSA-N clenbuterol Chemical compound CC(C)(C)NCC(O)C1=CC(Cl)=C(N)C(Cl)=C1 STJMRWALKKWQGH-UHFFFAOYSA-N 0.000 description 1
- 229960002896 clonidine Drugs 0.000 description 1
- 230000015271 coagulation Effects 0.000 description 1
- 238000005345 coagulation Methods 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- ZPUCINDJVBIVPJ-LJISPDSOSA-N cocaine Chemical class O([C@H]1C[C@@H]2CC[C@@H](N2C)[C@H]1C(=O)OC)C(=O)C1=CC=CC=C1 ZPUCINDJVBIVPJ-LJISPDSOSA-N 0.000 description 1
- 230000006999 cognitive decline Effects 0.000 description 1
- 230000008133 cognitive development Effects 0.000 description 1
- 208000010877 cognitive disease Diseases 0.000 description 1
- 230000002860 competitive effect Effects 0.000 description 1
- 229950006073 cotinine Drugs 0.000 description 1
- 229940109239 creatinine Drugs 0.000 description 1
- 229960003067 cystine Drugs 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 230000001934 delay Effects 0.000 description 1
- 229940099398 demser Drugs 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 230000001066 destructive effect Effects 0.000 description 1
- 235000019425 dextrin Nutrition 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- NIJJYAXOARWZEE-UHFFFAOYSA-N di-n-propyl-acetic acid Natural products CCCC(C(O)=O)CCC NIJJYAXOARWZEE-UHFFFAOYSA-N 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- 230000000378 dietary effect Effects 0.000 description 1
- 125000004177 diethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 1
- 150000002016 disaccharides Chemical class 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 239000002612 dispersion medium Substances 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 229950004394 ditiocarb Drugs 0.000 description 1
- 229960003638 dopamine Drugs 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 238000002651 drug therapy Methods 0.000 description 1
- 210000005069 ears Anatomy 0.000 description 1
- 229960001484 edetic acid Drugs 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 230000002996 emotional effect Effects 0.000 description 1
- 230000010482 emotional regulation Effects 0.000 description 1
- 230000006397 emotional response Effects 0.000 description 1
- 238000005538 encapsulation Methods 0.000 description 1
- 230000002124 endocrine Effects 0.000 description 1
- 210000000750 endocrine system Anatomy 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- BQULAXAVRFIAHN-UHFFFAOYSA-N ethyl 2-amino-3-(4-hydroxyphenyl)propanoate;hydron;chloride Chemical compound Cl.CCOC(=O)C(N)CC1=CC=C(O)C=C1 BQULAXAVRFIAHN-UHFFFAOYSA-N 0.000 description 1
- 125000004494 ethyl ester group Chemical group 0.000 description 1
- 230000029142 excretion Effects 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 210000003414 extremity Anatomy 0.000 description 1
- 206010016256 fatigue Diseases 0.000 description 1
- 230000014061 fear response Effects 0.000 description 1
- 229960001022 fenoterol Drugs 0.000 description 1
- 229960002464 fluoxetine Drugs 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 229960002848 formoterol Drugs 0.000 description 1
- BPZSYCZIITTYBL-UHFFFAOYSA-N formoterol Chemical compound C1=CC(OC)=CC=C1CC(C)NCC(O)C1=CC=C(O)C(NC=O)=C1 BPZSYCZIITTYBL-UHFFFAOYSA-N 0.000 description 1
- 229960003980 galantamine Drugs 0.000 description 1
- ASUTZQLVASHGKV-UHFFFAOYSA-N galanthamine hydrochloride Natural products O1C(=C23)C(OC)=CC=C2CN(C)CCC23C1CC(O)C=C2 ASUTZQLVASHGKV-UHFFFAOYSA-N 0.000 description 1
- LNTHITQWFMADLM-UHFFFAOYSA-N gallic acid Chemical class OC(=O)C1=CC(O)=C(O)C(O)=C1 LNTHITQWFMADLM-UHFFFAOYSA-N 0.000 description 1
- 210000001035 gastrointestinal tract Anatomy 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- 230000005484 gravity Effects 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- 210000003128 head Anatomy 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 208000019622 heart disease Diseases 0.000 description 1
- 230000002489 hematologic effect Effects 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 150000004677 hydrates Chemical class 0.000 description 1
- 229920001477 hydrophilic polymer Polymers 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-M hydroxide Chemical compound [OH-] XLYOFNOQVPJJNP-UHFFFAOYSA-M 0.000 description 1
- UWYVPFMHMJIBHE-OWOJBTEDSA-N hydroxymaleic acid group Chemical group O/C(/C(=O)O)=C/C(=O)O UWYVPFMHMJIBHE-OWOJBTEDSA-N 0.000 description 1
- ARZLUCYKIWYSHR-UHFFFAOYSA-N hydroxymethoxymethanol Chemical compound OCOCO ARZLUCYKIWYSHR-UHFFFAOYSA-N 0.000 description 1
- 229940058961 hydroxyquinoline derivative for amoebiasis and other protozoal diseases Drugs 0.000 description 1
- 125000003037 imidazol-2-yl group Chemical group [H]N1C([*])=NC([H])=C1[H] 0.000 description 1
- 102000018358 immunoglobulin Human genes 0.000 description 1
- 229940072221 immunoglobulins Drugs 0.000 description 1
- 229960003444 immunosuppressant agent Drugs 0.000 description 1
- 230000001861 immunosuppressant effect Effects 0.000 description 1
- 229940125721 immunosuppressive agent Drugs 0.000 description 1
- 229940124589 immunosuppressive drug Drugs 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 230000000968 intestinal effect Effects 0.000 description 1
- 238000001361 intraarterial administration Methods 0.000 description 1
- 239000007927 intramuscular injection Substances 0.000 description 1
- 239000007928 intraperitoneal injection Substances 0.000 description 1
- 230000007794 irritation Effects 0.000 description 1
- 229960001268 isoetarine Drugs 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- QXJSBBXBKPUZAA-UHFFFAOYSA-N isooleic acid Natural products CCCCCCCC=CCCCCCCCCC(O)=O QXJSBBXBKPUZAA-UHFFFAOYSA-N 0.000 description 1
- 229940039009 isoproterenol Drugs 0.000 description 1
- AWJUIBRHMBBTKR-UHFFFAOYSA-N isoquinoline Chemical compound C1=NC=CC2=CC=CC=C21 AWJUIBRHMBBTKR-UHFFFAOYSA-N 0.000 description 1
- 238000009592 kidney function test Methods 0.000 description 1
- 230000002045 lasting effect Effects 0.000 description 1
- 229960003136 leucine Drugs 0.000 description 1
- 229950008204 levosalbutamol Drugs 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 1
- 238000001294 liquid chromatography-tandem mass spectrometry Methods 0.000 description 1
- 239000008297 liquid dosage form Substances 0.000 description 1
- 239000006193 liquid solution Substances 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 238000007449 liver function test Methods 0.000 description 1
- 208000004731 long QT syndrome Diseases 0.000 description 1
- 238000011866 long-term treatment Methods 0.000 description 1
- 229960004391 lorazepam Drugs 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- 210000001165 lymph node Anatomy 0.000 description 1
- 208000014432 malignant adrenal gland pheochromocytoma Diseases 0.000 description 1
- 201000006782 malignant pheochromocytoma Diseases 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 231100000682 maximum tolerated dose Toxicity 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 230000003340 mental effect Effects 0.000 description 1
- 230000004630 mental health Effects 0.000 description 1
- 208000030159 metabolic disease Diseases 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- LMOINURANNBYCM-UHFFFAOYSA-N metaproterenol Chemical compound CC(C)NCC(O)C1=CC(O)=CC(O)=C1 LMOINURANNBYCM-UHFFFAOYSA-N 0.000 description 1
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 1
- 229960001344 methylphenidate Drugs 0.000 description 1
- 150000002772 monosaccharides Chemical class 0.000 description 1
- 230000036651 mood Effects 0.000 description 1
- LNOPIUAQISRISI-UHFFFAOYSA-N n'-hydroxy-2-propan-2-ylsulfonylethanimidamide Chemical compound CC(C)S(=O)(=O)CC(N)=NO LNOPIUAQISRISI-UHFFFAOYSA-N 0.000 description 1
- 210000003739 neck Anatomy 0.000 description 1
- IYRGXJIJGHOCFS-UHFFFAOYSA-N neocuproine Chemical compound C1=C(C)N=C2C3=NC(C)=CC=C3C=CC2=C1 IYRGXJIJGHOCFS-UHFFFAOYSA-N 0.000 description 1
- 210000000607 neurosecretory system Anatomy 0.000 description 1
- 230000001561 neurotransmitter reuptake Effects 0.000 description 1
- 239000003901 neurotransmitter uptake inhibitor Substances 0.000 description 1
- 230000003472 neutralizing effect Effects 0.000 description 1
- 239000002547 new drug Substances 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 231100001079 no serious adverse effect Toxicity 0.000 description 1
- 239000002736 nonionic surfactant Substances 0.000 description 1
- 229960002748 norepinephrine Drugs 0.000 description 1
- SFLSHLFXELFNJZ-UHFFFAOYSA-N norepinephrine Natural products NCC(O)C1=CC=C(O)C(O)=C1 SFLSHLFXELFNJZ-UHFFFAOYSA-N 0.000 description 1
- 210000001331 nose Anatomy 0.000 description 1
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 description 1
- 229940005483 opioid analgesics Drugs 0.000 description 1
- 229960002657 orciprenaline Drugs 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- 229960003540 oxyquinoline Drugs 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 210000003800 pharynx Anatomy 0.000 description 1
- KBBSSGXNXGXONI-UHFFFAOYSA-N phenanthro[9,10-b]pyrazine Chemical compound C1=CN=C2C3=CC=CC=C3C3=CC=CC=C3C2=N1 KBBSSGXNXGXONI-UHFFFAOYSA-N 0.000 description 1
- 229940117803 phenethylamine Drugs 0.000 description 1
- WLJVXDMOQOGPHL-UHFFFAOYSA-N phenylacetic acid Chemical compound OC(=O)CC1=CC=CC=C1 WLJVXDMOQOGPHL-UHFFFAOYSA-N 0.000 description 1
- 208000028591 pheochromocytoma Diseases 0.000 description 1
- 235000021317 phosphate Nutrition 0.000 description 1
- 239000002953 phosphate buffered saline Substances 0.000 description 1
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- 230000035790 physiological processes and functions Effects 0.000 description 1
- 239000006187 pill Substances 0.000 description 1
- 229960005414 pirbuterol Drugs 0.000 description 1
- 229920001983 poloxamer Polymers 0.000 description 1
- 229920000136 polysorbate Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 229960002288 procaterol Drugs 0.000 description 1
- FKNXQNWAXFXVNW-BLLLJJGKSA-N procaterol Chemical compound N1C(=O)C=CC2=C1C(O)=CC=C2[C@@H](O)[C@@H](NC(C)C)CC FKNXQNWAXFXVNW-BLLLJJGKSA-N 0.000 description 1
- 229940002612 prodrug Drugs 0.000 description 1
- 239000000651 prodrug Substances 0.000 description 1
- 238000011321 prophylaxis Methods 0.000 description 1
- 230000005180 public health Effects 0.000 description 1
- 150000003242 quaternary ammonium salts Chemical class 0.000 description 1
- MCJGNVYPOGVAJF-UHFFFAOYSA-N quinolin-8-ol Chemical compound C1=CN=C2C(O)=CC=CC2=C1 MCJGNVYPOGVAJF-UHFFFAOYSA-N 0.000 description 1
- 238000009790 rate-determining step (RDS) Methods 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 230000007115 recruitment Effects 0.000 description 1
- 230000001850 reproductive effect Effects 0.000 description 1
- 230000000241 respiratory effect Effects 0.000 description 1
- 230000036387 respiratory rate Effects 0.000 description 1
- 230000004043 responsiveness Effects 0.000 description 1
- RAPZEAPATHNIPO-UHFFFAOYSA-N risperidone Chemical compound FC1=CC=C2C(C3CCN(CC3)CCC=3C(=O)N4CCCCC4=NC=3C)=NOC2=C1 RAPZEAPATHNIPO-UHFFFAOYSA-N 0.000 description 1
- 229960001534 risperidone Drugs 0.000 description 1
- 229960001634 ritodrine Drugs 0.000 description 1
- IOVGROKTTNBUGK-SJCJKPOMSA-N ritodrine Chemical compound N([C@@H](C)[C@H](O)C=1C=CC(O)=CC=1)CCC1=CC=C(O)C=C1 IOVGROKTTNBUGK-SJCJKPOMSA-N 0.000 description 1
- 229960004017 salmeterol Drugs 0.000 description 1
- 239000008299 semisolid dosage form Substances 0.000 description 1
- 210000003491 skin Anatomy 0.000 description 1
- 230000007958 sleep Effects 0.000 description 1
- 208000019116 sleep disease Diseases 0.000 description 1
- 230000037321 sleepiness Effects 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 1
- 239000007909 solid dosage form Substances 0.000 description 1
- 239000012453 solvate Chemical class 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 230000006641 stabilisation Effects 0.000 description 1
- 238000011105 stabilization Methods 0.000 description 1
- 238000007619 statistical method Methods 0.000 description 1
- 230000000707 stereoselective effect Effects 0.000 description 1
- 229960002317 succinimide Drugs 0.000 description 1
- 235000000346 sugar Nutrition 0.000 description 1
- 150000005846 sugar alcohols Polymers 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 229910052717 sulfur Inorganic materials 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 230000035900 sweating Effects 0.000 description 1
- 210000002820 sympathetic nervous system Anatomy 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 230000008685 targeting Effects 0.000 description 1
- 229960000195 terbutaline Drugs 0.000 description 1
- 125000005931 tert-butyloxycarbonyl group Chemical group [H]C([H])([H])C(OC(*)=O)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 238000012956 testing procedure Methods 0.000 description 1
- 238000011287 therapeutic dose Methods 0.000 description 1
- 229940126585 therapeutic drug Drugs 0.000 description 1
- 230000004797 therapeutic response Effects 0.000 description 1
- WJCNZQLZVWNLKY-UHFFFAOYSA-N thiabendazole Chemical compound S1C=NC(C=2NC3=CC=CC=C3N=2)=C1 WJCNZQLZVWNLKY-UHFFFAOYSA-N 0.000 description 1
- 210000001685 thyroid gland Anatomy 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 125000005490 tosylate group Chemical class 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 231100000048 toxicity data Toxicity 0.000 description 1
- 231100000027 toxicology Toxicity 0.000 description 1
- 230000009261 transgenic effect Effects 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- 150000005219 trimethyl ethers Chemical class 0.000 description 1
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 1
- 150000003668 tyrosines Chemical class 0.000 description 1
- 230000002485 urinary effect Effects 0.000 description 1
- MSRILKIQRXUYCT-UHFFFAOYSA-M valproate semisodium Chemical compound [Na+].CCCC(C(O)=O)CCC.CCCC(C([O-])=O)CCC MSRILKIQRXUYCT-UHFFFAOYSA-M 0.000 description 1
- 229960000604 valproic acid Drugs 0.000 description 1
- 229960003726 vasopressin Drugs 0.000 description 1
- 230000000007 visual effect Effects 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/195—Carboxylic acids, e.g. valproic acid having an amino group
- A61K31/197—Carboxylic acids, e.g. valproic acid having an amino group the amino and the carboxyl groups being attached to the same acyclic carbon chain, e.g. gamma-aminobutyric acid [GABA], beta-alanine, epsilon-aminocaproic acid, pantothenic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/195—Carboxylic acids, e.g. valproic acid having an amino group
- A61K31/197—Carboxylic acids, e.g. valproic acid having an amino group the amino and the carboxyl groups being attached to the same acyclic carbon chain, e.g. gamma-aminobutyric acid [GABA], beta-alanine, epsilon-aminocaproic acid, pantothenic acid
- A61K31/198—Alpha-aminoacids, e.g. alanine, edetic acids [EDTA]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
- A61K31/4166—1,3-Diazoles having oxo groups directly attached to the heterocyclic ring, e.g. phenytoin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/55—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
- A61K9/0056—Mouth soluble or dispersible forms; Suckable, eatable, chewable coherent forms; Forms rapidly disintegrating in the mouth; Lozenges; Lollipops; Bite capsules; Baked products; Baits or other oral forms for animals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
Abstract
本发明提供了治疗孤独症的组合物和方法。具体地,本发明涉及通过施用α‑甲基‑DL‑酪氨酸来治疗孤独症的核心症状。
Description
相关申请的交叉引用
本申请要求于2018年7月19日提交的美国专利申请16/040,393的优先权和权益,其整体通过引用并入本文。
技术领域
本发明涉及治疗孤独症(autism)的组合物和方法。具体地,本发明涉及通过施用α-甲基-DL-酪氨酸来治疗孤独症的核心症状。
背景技术
孤独症谱系障碍(ASD)或孤独症在精神疾病诊断与统计手册V(Diagnostic andStatistics Manual of Mental Disorders V,DSM-5)中被定义为“社会沟通和社会交往困难,以及受限的和重复的行为模式、兴趣或活动”。儿童孤独症比儿童癌症、青少年糖尿病和小儿获得性免疫缺陷综合征(AIDS)一起更为普遍,估计患病率在美国(US)为150万,在欧洲为300万儿童,并且在整个世界其他地方为数千万。孤独症在儿童和成人二者中也代表着巨大的经济负担。更令人不安的是,没有明确的原因,儿童孤独症似乎正以每年10-17%的速率增长。最后,目前还没有批准用于治疗孤独症核心症状的药物。孤独症是一种严重的疾病,其代表了巨大的经济负担和未满足的医疗需求的领域。
孤独症最初由Leo Kanner博士于1943年描述,他将5岁的患者描述为:“……当被单独留下时是最快乐的,几乎从未哭着要跟母亲一起出去,似乎没有注意到他父亲的归来,并且对来访的亲戚无动于衷……微笑着游荡,手指做着千篇一律的动作……高兴地旋转任何他在旋转时可以抓住的东西……对他来说,词语具有特定字面、僵化的含义……当处于房间时他完全不理会他人并且立即寻找物体”,如Lai,M.C.,et al.Autism.Lancet,2014.383(9920):p.896-910所引用的。
最初,孤独症被认为是儿童精神分裂症的一种形式。然而,在1980年代中期,发现孤独症是遗传性疾病并且认为具有遗传病因。目前在精神疾病诊断与统计手册第5版(DSM-5)(2013)中将孤独症在诊断上定义为“社会沟通和社会交往困难,以及受限的和重复的行为模式、兴趣或活动”。DSM-5中针对ASD的“社会沟通和社会交往困难”特征的诊断标准包括:(1)社会情绪互惠的缺陷,例如,从异常的社交方式和不能正常来回交谈;到兴趣、情绪或情感的分享降低;到无法发起或回应社会交往;(2)用于社会交往的非言语沟通行为的缺陷,例如,从综合的言语和非言语沟通差;到眼神交流和肢体语言异常或对手势的理解和使用缺陷;到完全缺乏面部表情和非言语沟通;以及(3)发展、维持和理解人际关系的缺陷,例如,从难以调整行为以适应各种社交环境;到难以分享富有想象力的游戏或结交朋友;到对同龄人不感兴趣。
孤独症通常在儿童早期表现,与多种合并症相关,包括癫痫、脆性-X综合征(Fragile-X syndrome)、Retts综合征、注意力缺陷/多动障碍(ADHD)、异常的感觉或运动反应、睡眠障碍、认知功能下降、焦虑和攻击性。
2010年,CDC报告的美国孤独症的比率为68个儿童中的1个,其中男孩的易感性是女孩的5倍。这意味着42个男孩中有1个被诊断患有孤独症。自2014年对孤独症患病率进行评估以来,这一数字提高了约30%,并且是仅12年报告的比率的两倍多,并且这个问题正在迅速增长。在新泽西州(New Jersey),观察到的孤独症比率为46个儿童中的1个,这意味着在新泽西州出生的29个男孩中有1个可能患有孤独症。
养育孤独症儿童的财务费用在2014年估计比养育非孤独症儿童的费用多320万美元,而且这还没有考虑一旦他们的家庭不再能够这么做时维持作为成年人的该群体的社会成本。孤独症的社会成本是广泛而深刻的,而且许多从未探索过。例如,仅在2017年的年中才开发出有关孤独症患者医疗保健利用率的信息,并且发现他们对精神病护理以及对孤独症相关合并症高发率的护理的需求远远超出了普通人群或精神病患者人群的其他亚群。同样,直到2017年9月,孤独症人群的学校停学和开除率显著更高,并且随着孤独症患者数量的增加而提高。
最近,注意力已经集中在孤独症相关的死亡率上。尽管孤独症通常不被认为是致命疾病,但许多研究人员报告了孤独症人群的显著提高的死亡率,死亡的主要原因是自杀。一项基于瑞典国家患者注册中心和死因注册中心(Swedish National Patient Registryand the Cause of Death Registry)的配对病例队列研究注意了1987年至2009年的死亡情况,并且发现孤独症患者的死亡率比普通人群高256%。普通人群死亡时的平均年龄为70.2岁,并且孤独症患者为58.39,自杀与表现较好的患者相关。一项针对1,706名儿童和青少年的综述报告显示,孤独症中的自杀意念或尝试的风险提高18%。在加拿大的一项研究中,有35%的阿斯伯格综合征患者曾尝试自杀。同样,在日本、澳大利亚、英国和比利时也是如此。在法国对PubMed文献的综述中,发现总共21.3%的孤独症患者报告了自杀意念或曾尝试自杀,值得注意的是,“…使用的方法往往是暴力的”。
大量资源被用于研究孤独症的原因。遗传、饮食、发育、药理、环境和行为因素都被认为是该综合征的潜在原因。
已知分子α-甲基-L-酪氨酸(目前以销售)纯化的单一对映体代表抑制酪氨酸羟化酶,酪氨酸羟化酶是归因于酶介导的L-酪氨酸向DOPA(二羟基苯丙氨酸)的转化的儿茶酚胺生物合成中的限速酶。儿茶酚胺合成中的第一步对L-酪氨酸是高度立体定向的。L-AMPT(甲基化的L-酪氨酸)充当了酪氨酸羟化酶的竞争性抑制剂(Prescribing Information,2015;FDA Summary Basis of Approval[SBA]for1979)。最初于1979年被FDA批准,并被指定用于治疗嗜铬细胞瘤的患者,以用于:(1)手术患者的术前准备;(2)手术禁忌患者的管理;以及(3)恶性嗜铬细胞瘤患者的慢性治疗。对于成人和12岁及以上的儿童,建议的初始剂量为每天四次经口250mg。该剂量可以每天提高250mg至500mg,直至4个分开剂量中的最多4.0g/天。尽管是可商购的,但是本领域普通技术人员尚未开发出通过施用α-甲基-DL-酪氨酸的外消旋混合物(即DL-AMPT)来治疗孤独症或其核心症状的方法。
鉴于普遍担心(a)孤独症的患病率急剧上升;(b)该疾病对儿童及其家庭的破坏性影响;以及(c)孤独症对我们社会的社区、教育、医疗和精神卫生系统带来了巨大的社会和经济负担,孤独症代表了突发公共卫生事件。因此,迫切需要用于治疗孤独症,特别是该疾病的核心症状的治疗有效方法。
发明内容
一方面,本发明提供了用于在有此需要的对象中治疗孤独症的方法,所述方法包括向所述对象施用包含治疗有效量的α-甲基-DL-酪氨酸和可药用载体的组合物。在一个示例性的实施方案中,组合物包含约50mg(w/w)至约500mg(w/w)的量的α-甲基-DL-酪氨酸。
另一方面,本发明提供了用于在有此需要的对象中长时期提供一定血浆浓度的治疗药物以用于治疗孤独症的方法,所述方法包括一天三次向所述对象施用约50mg(w/w)至约500mg(w/w)的浓度的所述治疗药物,其中所述治疗药物为α-甲基-DL-酪氨酸,其中所述血浆浓度为约500ng/ml至5000ng/ml,并且其中所述时期为至少1周。
另一方面,本发明提供了用于在有此需要的对象中治疗孤独症相关临床特征的方法,所述方法包括向所述对象施用包含治疗有效量的α-甲基-DL-酪氨酸的组合物,从而在所述对象中治疗所述孤独症相关临床特征。在一个示例性实施方案中,所述临床特征是社会沟通缺陷、社会交往缺陷、社会动机缺陷、嗜睡和社会退缩、不适当言语、多动症、刻板行为、易激惹和激动、限制性行为、重复性行为、仪式行为、同一性行为(samenessbehavior)、强迫行为、自残行为或其组合。
根据以下详细描述实例和附图,本发明的其他特征和优点将变得明显。然而,应当理解,尽管详细描述和具体实例指示了本发明的一些优选实施方案,但是其仅通过举例说明的方式给出,因为通过该详细描述,在本发明的精神和范围内的多种改变和修改对本领域技术人员将变得明显。
附图说明
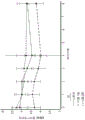
图1描绘了康纳斯父母评定量表数据(Conners Parent Rating Scale Data)结果。
图2说明了患者登记和处置。
图3显示了在研究HT 02-121(实施例6)中的患者中记录的生命体征相对于基线的最大变化实例,并且表明这些变化是短暂的,远未达到直立性标准(orthostaticcriteria)。
图4显示了研究HT 02-121中来自开放标签100mg和200mg TID的按周、总平均值和按患者的随机L1-79血浆浓度(第1天除外*)。*1在第1天,在给药之后1小时评估L-79血浆浓度。
图5显示了研究HT 02-121中来自开放标签100mg TID组的按周(不包括第1天)、总平均值和按患者的随机L1-79血浆浓度。
图6显示了研究HT 02-121中来自开放标签200mg TID组的按周(不包括第1天)、总平均值和按患者的随机L1-79血浆浓度。
图7以图形显示了L1-79与安慰剂相比随时间的CGI-总体严重程度(CGI-S)。
图8以图形显示了L1-79与安慰剂相比随时间的CGI-总体改善(CGI-I)。
图9显示了第4周CGI-S相对于基线的变化(ITT人群,草图)。
图10显示了按患者的从基线至第4周CGI-S的变化(ITT人群,草图)。
图11显示了第4周/LOCF的CGI-S的响应者分析(ITT人群,草图)。
图12显示了第0周至第8周VABS II标准化社会化评分相对基线的变化(ITT人群,草图)。
图13显示了第0周至第8周VABS II标准化沟通评分相对于基线的变化(ITT人群,草图)。
图14显示了第0周至第4周ADOS-2总评分相对于筛选的变化(ITT人群,草图)。
图15显示了第0周至第4周ADOS-2限制性和重复性行为总评分相对于筛选的变化(ITT人群,草图)。
图16显示了第0周至第4周ADOS-2社会影响总评分相对于筛选的变化(ITT人群,草图)。
图17显示了按患者的从筛选至第4周的ADOS-2总评分的变化(ITT人群,草图)。
图18显示了第0周至第8周SRS-2总T评分相对于基线的变化(ITT人群,草图)。
图19显示了第0周至第8周SRS-2 DSM-5社会沟通和交往T评分相对于基线的变化(ITT人群,草图)。
图20显示了第0周至第8周SRS-2社会沟通T评分相对于基线的变化(ITT人群,草图)。
图21显示了第0周至第8周SRS-2社会动机T评分相对于基线的变化(ITT人群,草图)。
图22显示了第0周至第8周SRS-2 DSM-5限制性和重复性行为相对于基线的变化(ITT人群,草图)。
图23显示了按患者的从基线至第4周的SRS-2总T评分的变化(ITT人群,草图)。
图24显示了按患者的从基线至第4周的SRS-2 DSM-5社会沟通和交往T评分的变化(ITT人群,草图)。
图25显示了按患者的从基线至第4周的SRS-2社会沟通T评分的变化(ITT人群,草图)。
图26显示了按患者的从基线至第4周的SRS-2社会动机T评分的变化(ITT人群,草图)。
图27显示了第4周/LOCF的SRS-2总T评分的响应者分析(ITT人群,草图)。
图28显示了第4周/LOCF的SRS-2 DSM-5社会沟通和交往T评分的响应者分析(ITT人群,草图)。
图29显示了第4周/LOCF的SRS-2社会沟通T评分的响应者分析(ITT人群,草图)。
图30显示了第4周/LOCF的SRS-2社会动机T评分的响应者分析(ITT人群,草图)。
图31显示了第0周至第8周ABC-C嗜睡和社会退缩方面相对于基线的变化(ITT人群,草图)。
图32显示了第0周至第8周ABC-C不适当言语方面相对于基线的变化(ITT人群,草图)。
图33显示了第0周至第8周ABC-C多动症和不服从方面相对于基线的变化(ITT人群,草图)。
图34显示了第0周至第8周ABC-C刻板行为方面相对于基线的变化(ITT人群,草图)。
图35显示了第0周至第8周ABC-C易激惹和激动方面相对于基线的变化(ITT人群,草图)。
图36显示了按患者的从基线至第四周ABC-C嗜睡和社会退缩方面的的变化(ITT人群,草图)。
图37显示了按患者的从基线至第四周ABC-C不适当言语方面的变化(ITT人群,草图)。
图38显示了第4周/LOCF的ABC-C嗜睡和社会退缩方面的响应者分析(ITT人群,草图)。
图39显示了第4周/LOCF的ABC-C不适当言语方面的响应者分析(ITT人群,草图)。
图40显示了第0周至第8周RBS-R总评分相对于基线的变化(ITT人群,草图)。
图41显示了第0周至第8周RBS-R限制性行为相对于基线的变化(ITT人群,草图)。与安慰剂相比,通过L1-79 200mg评分的降低记录了RBS-R总评分的平均改善。
图42显示了第0周至第8周RBS-R仪式行为相对于基线的变化(ITT人群,草图)。
图43显示了第0周至第8周RBS-R同一性行为相对于基线的变化(ITT人群,草图)。
图44显示了第0周至第8周RBS-R强迫行为相对于基线的变化(ITT人群,草图)。
图45显示了第0周至第8周RBS-R刻板行为相对于基线的变化(ITT人群,草图)。
图46显示了第0周至第8周RBS-R自残行为相对于基线的变化(ITT人群,草图)。
图47显示了按患者的从基线至第4周RBS-R总评分的变化(ITT人群,草图)。
图48显示了第4周或LOCF的RBS-R总评分的响应者分析(定义为改善或未恶化)。
具体实施方式
通过参考形成本公开内容的一部分的以下详细描述,可以更容易地理解本发明主题。应当理解,本发明不限于本文描述和/或示出的特定产品、方法、条件或参数,并且本文使用的术语仅出于以举例的方式描述特定实施方案的目的,而并非旨在限制要求保护的发明。
除非本文另外定义,否则结合本申请使用的科学和技术术语应具有本领域普通技术人员通常理解的含义。此外,除非上下文另外要求,否则单数术语应包括复数,并且复数术语应包括单数。
如上文和整个公开内容中所采用的,除非另外指出,否则以下术语和缩写应理解为具有以下含义。
在本公开内容中,未用数量词限定的名词包括复数引用,并且除非上下文另有明确说明,否则提及特定数值时至少包括该特定值。因此,例如,提及“化合物”是指本领域技术人员已知的一个或更多个这样的化合物及其等同物,等等。如本文所用,术语“多个”是指多于一个。当表达值的范围时,另一实施方案包括从一个特定值和/或至另一特定值。类似地,当通过使用先行词“约”将值表示为近似值时,应理解特定值形成了另一实施方案。所有范围都是包括性的和可组合的。
如本文所用,术语“组分”、“组合物”、“化合物的组合物”、“化合物”、“药物”、“药理活性剂”、“活性剂”、“治疗剂”、“疗法”、“治疗”或“药物”在本文可互换使用,是指化合物或物质的组合物,当施用于对象(人或动物)时,其通过局部和/或全身作用诱导期望的药理和/或生理作用。
如本文所用,以下术语定义如下:
ABA 应用行为分析
ABC-C 异常行为检查表-社区
ADHD 注意缺陷多动障碍
ADIR 孤独症诊断访谈检查
ADME 吸收、分布、代谢和消除
ADOS-2 孤独症诊断观察方案,第二版
AE 不良事件
AIDS 获得性免疫缺陷综合征
ASD 孤独症谱系障碍
AST 天冬氨酸转氨酶
ALT 丙氨酸转氨酶
AUC 浓度时间曲线下面积
AUC0-8 0至8小时的浓度时间曲线下面积
AUC0-12 0至12小时的浓度时间曲线下面积
AUC0-∞ 0至无穷大的浓度时间曲线下面积
AUC0-tz 0至最后可量化浓度的浓度时间曲线下面积
CFR 美国联邦法规
CGI-I 临床总体印象-总体改善
CGI-S 临床总体印象-疾病严重程度
Cmax 最大浓度
CNS 中枢神经系统
DL-AMPT 外消旋(D和L异构体)α-甲基-对-酪氨酸
DOPA 二羟基苯丙氨酸
DSM-5 精神疾病诊断与统计手册V
EI 早期干预
EOP2 第二阶段结束
FDA 美国食品和药物管理局
FDASIA 美国食品和药物管理局安全与创新法案
FOBs 功能观察组合评价
GMP 良好生产规范
HBV 乙型肝炎病毒
HCVA 出血性脑血管意外
HED 人体等效剂量
HIV 人类免疫缺陷病毒
IEP 个体化教育计划
L-AMPT α-甲基-对-酪氨酸的L异构体
LC-MS/MS 液相色谱质谱
LOCF 末次观测值结转法
LQTS 长QT综合征
MTD 最大耐受剂量
NDA 新药申请
NOAEL 无可见有害作用水平
PD 药效学
PK 药代动力学
PND 产后日
PSP 儿科研究计划
RBS-R 重复性行为评分-修订
SBA 批准的总结基础
SRS-2 社会反应量表,第二版
t1/2 半衰期
TdP 尖端扭转型室速(Torsade’s de Pointes)
TID 每日三次
TK 毒代动力学
TQT 彻底QT(Thorough QT)
ULN 正常上限
USAN 美国采用的名称
VABS II 文兰适应行为量表,第二版
对于孤独症,例如,负面影响或症状可以包括美国精神病学协会的诊断与统计手册第五版(DSM-5,DSM-V)(其内容通过引用并入本文)中针对孤独症谱系障碍所指定的诊断标准的任何对象,例如,社会情绪互惠的缺陷(例如,从异常的社交方式和不能正常来回交谈;到兴趣、情绪或情感的分享降低;到无法发起或回应社会交往);用于社会交往的非言语沟通行为的缺陷(例如,从综合的言语和非言语沟通差;到眼神交流和肢体语言异常或对手势的理解和使用缺陷;到完全缺乏面部表情和非言语沟通);发展、维持和理解人际关系的缺陷(例如,从难以调整行为以适应各种社交环境;到难以分享富有想象力的游戏或结交朋友;到对同龄人不感兴趣);定型或重复性运动、使用物体或言语(例如简单运动定型,排列玩具或翻转物体,模仿言语,特质措辞(idiosyncratic phrase));坚持千篇一律,固执地坚持惯例,或者言语或非言语行为的程式化模式(例如,在具有小的改变时极度痛苦,难以转变,僵化的思维方式,问候程式化,每天需要走相同的路线或吃相同的食物);在强度或注意力上异常的高度限制、固定的兴趣(例如,强烈依恋或沉迷于不寻常物品,过度限制或持久的兴趣);以及对感觉输入的反应过度或反应不足或对环境感觉方面的异常兴趣(例如对疼痛/温度的明显冷漠,对特定声音或纹理的不良反应,过度闻或触摸物体,对灯光或运动的视觉迷恋)。
孤独症谱系的一些患者亚群包括被诊断患有阿斯伯格障碍(即,阿斯伯格综合征)或社会沟通障碍,表现出注意力缺陷多动障碍(ADHD)的症状(例如,注意力不集中、多动和冲动)和/或抽动(运动抽动或发声抽动)的那些患者。参见例如DSM-5。
可以使用本领域已知的方法进行孤独症症状或本公开内容的任何症状的评估。例如,一种评估孤独症症状的方法是基于多种心理测试中相对于基线的变化的临床总体印象(CGI)量表。这些测试可以包括异常行为检查表-社区(ABC-C)、康纳斯父母评定量表和孤独症诊断观察方案(ADOS)。孤独症症状也可以从临床医生个人临床观察,从在定期安排的诊所就诊获得的影像信息以及从对象的照护者随时间提供的信息进行评估。本公开内容的组合物和方法导致康纳斯父母评定量表评估得分的至少一个维度上降低至少1分。
如上文和整个公开内容中所使用的,术语“有效量”是指在必要的剂量和时间段内有效达到在治疗相关障碍、病症或副作用方面所期望的结果的量。应当理解,本发明的组分的有效量将因患者而异,不仅关于所选择的特定化合物、组分或组合物,施用途径,以及组分在个体中引起期望结果的能力,还关于因素如疾病状态或待减轻病症的严重程度,个体的激素水平、年龄、性别、体重,患者的状态以及所治疗的病理状况的严重性,特定患者遵循的并发药物和特殊饮食,以及本领域技术人员将认识到的其他因素,适当的剂量由主治医生决定。可以调整剂量方案以提供改善的治疗响应。有效量也是其中治疗有益作用超过了组分的任何毒性或有害作用的量。
本发明还提供了包含本发明的化合物和一种或更多种可药用载体的药物组合物。“可药用载体”包括在所采用的剂量和浓度下对暴露于其的细胞或哺乳动物无毒的任何赋形剂。药物组合物可以包含一种或另外的治疗剂。
“可药用”是指在合理的医学判断范围内适合与人和动物组织接触而无过度毒性、刺激性、变态反应或其他问题并发症且具有合理的获益/风险比的那些化合物、材料、组合物和/或剂型。
可药用载体的实例包括例如但不限于溶剂、分散介质、缓冲剂、包衣、抗菌和抗真菌剂、润湿剂、防腐剂、buggers、螯合剂、抗氧化剂、等张剂和吸收延迟剂。
可药用载体的实例还包括例如但不限于水;盐水;磷酸盐缓冲盐水;右旋糖;甘油;醇,例如乙醇和异丙醇;磷酸盐、柠檬酸盐和其他有机酸;抗坏血酸;低分子量(少于约10个残基)多肽;蛋白质,例如血清白蛋白、明胶或免疫球蛋白;亲水性聚合物,例如聚乙烯吡咯烷酮;氨基酸,例如甘氨酸、谷氨酰胺、天冬酰胺、精氨酸或赖氨酸;单糖、二糖和其他碳水化合物,包括葡萄糖、甘露糖或糊精;EDTA;成盐的反离子,例如钠;和/或非离子表面活性剂,例如TWEEN、聚乙二醇(PEG)和PLURONICS;等渗剂,例如糖、多元醇(例如甘露醇和山梨糖醇)和氯化钠;以及其组合。
在本发明中,所公开的化合物可以以可药用盐的形式制备。“可药用盐”是指所公开化合物的衍生物,其中母体化合物通过制备其酸式或碱式盐而被修饰。可药用盐的实例包括但不限于碱性残基(例如胺)的无机或有机酸盐;酸性残基(例如羧酸)的碱金属或有机盐;等等。可药用盐包括例如由无毒的无机或有机酸形成的母体化合物的常规无毒盐或季铵盐。例如,这样的常规无毒盐包括衍生自无机酸例如盐酸、氢溴酸、硫酸、氨基磺酸、磷酸、硝酸等的那些;以及由有机酸例如乙酸、丙酸、琥珀酸、乙醇酸、硬脂酸、乳酸、苹果酸、酒石酸、柠檬酸、抗坏血酸、双羟萘酸、马来酸、羟基马来酸、苯乙酸、谷氨酸、苯甲酸、水杨酸、磺胺酸、2-乙酰氧基苯甲酸、富马酸、甲苯磺酸、甲磺酸、乙烷二磺酸、草酸、羟乙磺酸等制备的盐。这些生理上可接受的盐通过本领域已知的方法制备,例如通过将游离胺碱与过量的酸溶解在水性醇中,或将游离羧酸用碱金属碱(例如氢氧化物)或胺中和。
本文所述的化合物可以以替代形式制备。例如,许多含氨基的化合物可以作为酸加成盐使用或制备。通常,这样的盐改善了化合物的分离和处理性能。例如,取决于试剂、反应条件等,本文所述的化合物可以例如作为其盐酸盐或甲苯磺酸盐使用或制备。同构结晶形式、所有手性和外消旋形式、N-氧化物、水合物、溶剂合物和酸盐水合物也被认为在本发明的范围内。
本发明的某些酸性或碱性化合物可以以两性离子存在。化合物的所有形式,包括游离酸、游离碱和两性离子均预期在本发明的范围内。在本领域中公知,包含氨基和羧基二者的化合物通常以其两性离子形式平衡存在。因此,本文描述的包含例如氨基和羧基二者的任何化合物也包括提及其相应的两性离子。
术语“立体异构体”是指具有相同化学组成但是原子或基团在空间中的排列不同的化合物。术语“对映体”是指不可重叠的互为镜像的立体异构体。
术语“施用”是指直接施用本发明的化合物或组合物,或施用将在体内形成等量活性化合物或物质的前药、衍生物或类似物。
本文所用的术语“抑制剂”包括抑制蛋白质、多肽或酶的表达或活性的化合物,并且不一定意味着完全抑制表达和/或活性。相反,抑制包括在足以产生期望效果的程度和一段时间抑制蛋白质、多肽或酶的表达和/或活性。
尽管无意于受到任何特定的操作机制的束缚,但相信根据本发明的酪氨酸羟化酶抑制剂通过减少分泌到血流中的肾上腺素的量而起作用。
酪氨酸羟化酶抑制剂是本领域公知的,并且在例如以下中充分描述:美国专利申请公开US 2015/0290279、US 2015/0216827、US 2015/0111937、US 2015/0111878、US2013/0184214和US 20130183263;美国专利US 8,481,498、US 9,308,188和US 9,326,962;以及PCT专利申请公开WO2015061328,其通过引用整体并入本文。可以使用本领域技术人员已知的任何合适的酪氨酸羟化酶抑制剂。
在某些实施方案中,酪氨酸羟化酶抑制剂是酪氨酸衍生物。酪氨酸衍生物能够以不同的异构体形式存在,包括立体异构体和对映异构体。酪氨酸衍生物可以例如以L形式或D形式二者存在。酪氨酸衍生物也可以例如以外消旋形式存在。
代表性的酪氨酸衍生物包括例如以下一种或更多种:(2R)-2-氨基-3-(2-氯-4羟苯基)丙酸甲酯、D-酪氨酸乙酯盐酸盐、(2R)-2-氨基-3-(2,6-二氯-3,4-二甲氧基苯基)丙酸甲酯H-D-酪氨酸(tBu)-烯丙基酯盐酸盐、(2R)-2-氨基-3-(3-氯-4,5-二甲氧基苯基)丙酸甲酯、(2R)-2-氨基-3-(2-氯-3-羟基-4-甲氧基苯基)丙酸甲酯、(2R)-2-氨基-3-(4-[(2-氯-6-氟苯基)甲氧基]苯基)丙酸甲酯、(2R)-2-氨基-3-(2-氯-3,4-二甲氧基苯基)丙酸甲酯、(2R)-2-氨基-3-(3-氯-5-氟-4-羟苯基)丙酸甲酯、2-(乙酰氨基)-2-(4-[(2-氯-6-氟苄基)氧基]苄基丙二酸二乙酯、(2R)-2-氨基-3-(3-氯-4-甲氧基苯基)丙酸甲酯、(2R)-2-氨基-3-(3-氯-4-羟基-5-甲氧基苯基)丙酸甲酯、(2R)-2-氨基-3-(2,6-二氯-3-羟基-4-甲氧基苯基)丙酸甲酯、(2R)-2-氨基-3-(3-氯-4-羟苯基)丙酸甲酯、H-DL-酪氨酸甲酯盐酸盐、H-3,5-二碘-酪氨酸甲酯盐酸盐、H-D-3,5-二碘-酪氨酸甲酯盐酸盐、H-D-酪氨酸甲酯盐酸盐、D-酪氨酸甲酯盐酸盐、D-酪氨酸-甲酯盐酸盐、甲基D-酪氨酸酯盐酸盐、H-D-酪氨酸甲酯盐酸盐、D-酪氨酸甲酯盐酸盐、H-D-酪氨酸甲酯-盐酸盐、(2R)-2-氨基-3-(4-羟苯基)丙酸、(2R)-2-氨基-3-(4-羟苯基)甲酯盐酸盐、(2R)-2-氨基-3-(4-羟苯基)丙酸甲酯盐酸盐、(2R)-2-氮烷基-3-(4-羟苯基)丙酸甲酯盐酸盐、3-氯-L-酪氨酸、3-硝基-L-酪氨酸、3-硝基-L-酪氨酸乙酯盐酸盐、DL-m-酪氨酸、DL-o-酪氨酸、Boc-酪氨酸(3,5-I2)-OSu、Fmoc-酪氨酸(3-N02)-OH、α-甲基-L-酪氨酸、α-甲基-D-酪氨酸和α-甲基-DL-酪氨酸。在本发明的某些实施方案中,酪氨酸衍生物是如下所示的α-甲基-L-酪氨酸:
在另一些实施方案中,酪氨酸衍生物是α-甲基-D-酪氨酸。在另一些实施方案中,酪氨酸衍生物是如下所示的外消旋形式的α-甲基-DL-酪氨酸:
在一个特定的实施方案中,酪氨酸衍生物是α-甲基-L-酪氨酸或α-甲基-DL-酪氨酸的结构变体。α-甲基-L-酪氨酸或α-甲基-DL-酪氨酸的结构变体在本领域中是公知的,并且在例如美国专利4,160,835中进行了充分描述,该专利通过引用整体并入本文。
在一个实施方案中,本发明的酪氨酸衍生物是具有下式的芳基丙氨酸化合物:
其中R1是氢、甲基或乙基酯基、或1-4个碳原子的烷基;R2是氢、低级烷基、低级烯烃、琥珀酰亚胺、或1-4个碳原子的烷基;R3是以下通式的经取代苯环
其中Y1位于对位,并且是氢、羟基、甲基醚、二甲基醚、三甲基醚、或者未经取代的或卤素取代的苄基;Y2和Y3相同或不同,并且其中Y2和Y3之一或二者位于间位或邻位,并且其中Y2和Y3是氢、羟基、卤素、甲基醚或硝基;并且R4是氢、乙酰基、叔丁氧羰基或芴基甲氧羰基。
在一些实施方案中,Y1和Y2相同或不同,并且选自氢、氰基氨基、羧基、氰基、硫代氨基甲酰基、氨基甲基、胍基、羟基、甲磺酰胺基、硝基、氨基、甲磺酰氧基、羧基甲氧基、甲酰基、甲氧基以及含有碳和一个或更多个氮、硫或氧原子的经取代或未经取代的5或6元杂环,这样的杂环的具体实例是吡咯-1-基、2-羧基吡咯-1-基、咪唑-2-基氨基、吲哚-1-基、咔唑-9-基、4,5-二氢-4-羟基-4-三氟甲基噻唑-3-基、4-三氟甲基噻唑-2-基、咪唑-2-基和4,5-二氢咪唑-2-基,以使得(a)Y1和Y2不能同时为羟基,(b)Y1和Y2不能同时为氢,并且(c)当Y1和Y2之一为氢时,另一个不能为羟基。
在一个实例中,R3是具有下式的经取代或未经取代的苯并杂环:
其中苯并杂环选自:吲哚-5-基、1-(N-苯甲酰基氨基甲酰亚氨基)-吲哚-5-基、1-氨基甲酰亚氨基吲哚-5-基、1H-2-羟吲哚-5-基、吲哚-5-基、2-巯基苯并咪唑-5(6)-基、2-氨基苯并咪唑-5(6)-基、2-甲磺酰胺基-苯并咪唑-5(6)-基、1H-苯并噁唑-2-on-6-基、2-氨基苯并噻唑-6-基、2-氨基-4-巯基苯并噻唑-6-基、2,1,3-苯并噻二唑-5-基、1,3-二氢-2,2-二氧代-2,1,3-苯并噻二唑-5-基、1,3-二氢-1,3-二甲基-2,2-二氧代-2,1,3-苯并噻二唑-5-基、4-甲基-2(1H)-氧代喹啉-6-基、喹喔啉-6-基、2-羟基喹喔啉-6-基、2-羟基喹喔啉-7-基、2,3-二羟基喹喔啉-6-基和2,3-二氢-3(4H)-氧代-1,4-苯并噁嗪-7-基。
在另一个实例中,R3是具有下式的经取代或经未取代的杂环:
其中杂环选自5-羟基-4H-吡喃-4-on-2-基、2-羟基吡啶-4-基、2-氨基吡啶-4-基、2-羧基吡啶-4-基或四唑并[1,5-a]吡啶-7-基。
在一个特定的实施方案中,酪氨酸羟化酶抑制剂是水绫霉素(aquayamycin)。在一个实例中,水绫霉素是下式的化合物。
在另一个特定的实施方案中,酪氨酸羟化酶抑制剂是长根菇素(oudenone)。在一个实例中,长根菇素是下式的化合物。
也可以使用本领域技术人员已知的其他合适的酪氨酸羟化酶抑制剂。其他酪氨酸羟化酶抑制剂的实例包括但不限于例如环己酰亚胺、茴香霉素、3-碘-L-酪氨酸、pyratrione、具有邻苯二酚或三酚环体系的苯基羰基衍生物,例如苯乙胺和没食子酸衍生物、4-异丙基环庚三烯酚酮(4-isopropyltropolone)、2-(4-噻唑基)苯并咪唑、8-羟基喹啉、邻菲罗啉(o-phenantroline)、5-碘-8-羟基喹啉、胆红素、2,9-二甲基-1,10-菲罗啉、α-α′-联吡啶、二苯并[f,h]喹喔啉、2,4,6-三吡啶基-s-三嗪、3-氨基4H-吡咯并异噁唑-5(6H)-羧酸乙酯、α-亚硝基-β-萘酚、二乙基二硫代氨基甲酸钠、乙二胺四乙酸(参见RHochster,Metabolic Inhibitors V4:A Comprehensive Treatise 52Elsevier(2012))。
在一个特定的实施方案中,酪氨酸羟化酶抑制剂是L1:79,其是指外消旋形式的α-甲基-DL-酪氨酸或D,L α-甲基-对酪氨酸(缩写为DL-AMPT)。
α-甲基-DL-酪氨酸抑制酪氨酸羟化酶(TH)的活性,该酶催化儿茶酚胺生物合成的第一个转化,即酪氨酸向二羟基苯丙氨酸(DOPA)的转化,这是儿茶酚胺合成中的限速步骤。α-甲基-DL-酪氨酸是酪氨酸类似物,其竞争性地竞争TH并且在尿中几乎不变地排泄。
在初步测试中,观察到Demser(即,α-甲基-L-酪氨酸)对肠漏的症状具有有益作用,但是这种作用是短暂的。观察到外消旋混合物(即α-甲基-DL-酪氨酸)具有更大的生理作用和半衰期。这可能是由于D氨基酸异构体无法通过体内存在的不同L氨基酸转运系统转运,或者通过允许L异构体持续更长时间的肾排泄完成。
另一方面,本发明提供了包含治疗有效量或剂量的酪氨酸羟化酶抑制剂(例如,α-甲基-DL-酪氨酸)和可药用载体的药物组合物。
如本文所述,用于治疗孤独症的本发明组合物的有效剂量取决于许多不同因素而变化,包括施用方式、靶位点、患者的生理状态、患者是成人还是儿童、施用的其他药物以及治疗是预防性还是治疗性。通常,患者是人,但是也可以治疗非人哺乳动物,包括转基因哺乳动物。可以使用本领域技术人员已知的常规方法来滴定治疗剂量以优化安全性和功效。
本发明的药物组合物可以包含“治疗有效量”。“治疗有效量”是指在必要的剂量和时间段内有效达到期望治疗结果的量。分子的治疗有效量可以根据多种因素而变化,例如个体的疾病状态、年龄、性别和体重以及分子在个体中引起期望响应的能力。治疗有效量也是其中治疗有益作用超过了分子的任何毒性或有害作用的量。
如本文所用,术语“治疗”是指治疗性处理,包括其中目的是阻止或减缓(减轻)与疾病或病症相关的不期望生理变化的预防或预防性措施。有益或期望的临床结果包括但不限于症状的缓解,疾病或病症的程度的减轻,疾病或病症的稳定(即其中疾病或病症没有恶化),疾病或病症的进展的延迟或减慢,疾病或病症的改善或减轻,以及疾病或病症的缓解(无论是部分地还是完全地),无论是可检测的还是不可检测的。需要治疗的那些包括已经患有疾病或病症的那些以及易于患疾病或病症的那些或将要预防疾病或病症的那些。
可以调整剂量方案以提供最佳的期望响应(例如,治疗或预防响应)。
在一个实例中,可以施用单个大剂量(bolus)。在另一个实例中,可以随时间施用数个分开的剂量。在又一个示例中,可以根据治疗情况的紧急程度按比例减少或增加剂量。如本文所用,剂量单位形式是指适合用作治疗哺乳动物对象的单位剂量的物理上离散的单位。每个单位可包含预定量的活性化合物,其经计算以产生期望的治疗效果。在一些实施方案中,本发明的剂量单位形式决定于并且直接取决于活性化合物的独特特征和待实现的特定治疗或预防作用。
本发明的组合物可以施用仅一次,或者其可以多次施用。对于多剂量,可以例如每天三次、每天两次、每天一次、每两天一次、每周两次、每周、每两周一次或每月施用组合物。
要注意的是,剂量值可以随待减轻的病症的类型和严重性而变化。还应理解,对于任何特定的对象,具体的剂量方案应根据个体需要和施用或监督组合物的施用的人的专业判断随时间进行调整,并且本文给出的剂量范围仅是示例性的而不意图限制要求保护的组合物的范围或实践。
向对象的“施用”不限于任何特定的递送系统,并且可以包括但不限于经口(例如,在胶囊、混悬剂或片剂中)、肠胃外(包括皮下、静脉内、髓内、关节内、肌内或腹膜内注射)、表面或经皮。向宿主的施用可以以单剂量或重复施用并且以多种生理上可接受的盐形式中的任一种和/或与作为药物组合物的一部分的可接受药物载体和/或添加剂(如前所述)一起进行。再者,生理上可接受的盐形式和标准药物配制技术是本领域技术人员公知的(参见,例如,Remington′s Pharmaceutical Sciences,Mack Publishing Co.)。
一方面,酪氨酸羟化酶抑制剂的剂量可以为约1mg至约4g。在一个特定的实施方案中,酪氨酸羟化酶抑制剂的剂量可以为约10mg至约1500mg。在本发明的一些合适的实施方案中,组合物包含以下量的酪氨酸羟化酶抑制剂(即α-甲基-DL-酪氨酸):约50mg(w/w)至约1500mg(w/w);约50mg(w/w)至约500mg(w/w);约75mg(w/w)至约350mg(w/w);约90mg(w/w)至约350mg(w/w);约100mg(w/w)至约300mg(w/w);或约100mg(w/w)至约200mg(w/w)。在一个实施方案中,组合物包含约90、100、125、150、175、200、250、300、350、400、500、750、1000或1500mg(w/w/)的量的酪氨酸羟化酶抑制剂(即,α-甲基-DL-酪氨酸)。如本文所用,“组合物”是指包含药学有效量的一种或更多种活性成分(例如,酪氨酸羟化酶抑制剂、另一种痤疮治疗剂或其组合)的任何组合物。
在一些实施方案中,同时或先后施用具有不同剂量的多种组合物。例如,在一个实施方案中,同时施用包含约200mg(w/w)的量的α-甲基-DL-酪氨酸的第一组合物和包含约100mg(w/w)的量的α-甲基-DL-酪氨酸的第二组合物。在另一个实施方案中,先后施用包含约200mg(w/w)的量的α-甲基-DL-酪氨酸的第一组合物和包含约100mg(w/w)的量的α-甲基-DL-酪氨酸的第二组合物。
一方面,将组合物施用至少约1、2、3、4、5、6、7、8、9、10、11或12周。在另一方面,将组合物施用1、2、3、4、5、6、7、8、9、10、11或12周给药期的持续时间。在另一方面,将所述组合物施用1、2、3、4、5、6、7、8、9、10、11或12个月的给药期的持续时间。
另一方面,本发明提供了用于在有此需要的对象中长时期获得一定血浆浓度的治疗性酪氨酸羟化酶抑制剂药物(例如,α-甲基-DL-酪氨酸)以用于治疗孤独症的方法,所述方法包括每日三次向所述对象施用约50mg(w/w)至约500mg(w/w)的浓度的所述治疗药物,其中所述血浆浓度为约500ng/ml至5000ng/ml,并且其中所述时期为至少1周。在一个实施方案中,为了获得期望的血浆浓度,将药物施用至少1天、2天、3天、4天、5天、6天、1周、2周、3周或4周。在一个特定的实施方案中,为了获得期望的血浆浓度,将药物施用约1天至约4周、约2天至约4周、或约1周至约4周的持续时间。在一些实施方案中,为了获得期望的血浆浓度,将药物施用超过6个月的治疗方案持续时间。
施用本发明的组合物可导致血浆浓度为约500ng/ml至5000ng/ml;约800ng/ml至2500ng/ml,或约1400ng/ml至1800ng/ml。
本发明的药物组合物可以以多种方式配制,包括例如固体、半固体和液体剂型,例如胶囊剂、片剂、丸剂、散剂、液体溶液剂(例如可注射和可输注溶液剂)、分散体或混悬剂、脂质体和栓剂。在一些实施方案中,组合物为可注射或可输注溶液剂的形式。组合物为适合于经口、表面、静脉内、动脉内、肌内、皮下、肠胃外、经粘膜或经皮施用的形式。在一个特定的实施方案中,组合物为胶囊剂的形式。在另一个特定的实施方案中,组合物为片剂的形式。
药物组合物的施用可以通过多种途径,包括经口、经鼻、皮下、静脉内、肌内、经皮、阴道、直肠、或其任何组合。经皮施用可以使用例如油酸、1-甲基-2-吡咯烷酮、十二烷基壬氧基乙烯来实现。
一方面,本发明提供了向对象施用治疗有效量的第一酪氨酸羟化酶抑制剂(例如α-甲基-DL-酪氨酸)与治疗有效量的第二酪氨酸羟化酶抑制剂(例如α-甲基-L-酪氨酸)的组合。在另一方面,本发明提供了向对象施用治疗有效量的一种或更多种酪氨酸羟化酶抑制剂(例如α-甲基-DL-酪氨酸和/或α-甲基-L-酪氨酸)与治疗有效量的另一种可用于治疗孤独症的药剂的组合。
在这些方面中的一些中,可以施用γ-氨基丁酸(GABA)与酪氨酸羟化酶抑制剂(例如,α-甲基-DL-酪氨酸)。GABA可以与酪氨酸羟化酶抑制剂同时施用。在另一些方面,GABA可以与酪氨酸羟化酶抑制剂分开施用,例如在一天中的另一时间。在一些方面,在就寝时间施用GABA。通常,GABA的剂量为约5mg至约30mg,例如5、10、15、20、25或约30mg的GABA,15mg的GABA是特别优选的。
在这些方面的另一些中,除了酪氨酸羟化酶抑制剂(例如,α-甲基-DL-酪氨酸)和任选的GABA外,还施用了p4503A4促进剂。优选的p4503A4促进剂包括5,5-二苯基乙内酰脲、丙戊酸和卡马西平。
可以使用本公开内容的方法来治疗孤独症谱系的那些对象,包括被诊断出患有阿斯伯格障碍(阿斯伯格综合征)或社会沟通障碍,还具有ADHD和/或抽动的症状的那些。在这些方面,可以向对象施用有效量的酪氨酸羟化酶抑制剂和有效量的β肾上腺素能激动剂(也称为β激动剂)。酪氨酸羟化酶抑制剂可以是本文所述的任何酪氨酸羟化酶抑制剂,特别优选α-甲基-DL-酪氨酸。β-肾上腺素能激动剂在本领域中是已知的,并且包括例如沙丁胺醇、左沙丁胺醇、非诺特罗、福莫特罗、异丙肾上腺素、间羟异丙肾上腺素(metaproterenol)、沙美特罗、特布他林、克仑特罗、异他林(isoetarine)、吡丁醇(pirbuterol)、丙卡特罗、利托君、肾上腺素及其组合。沙丁胺醇是一种特别优选的β肾上腺素能激动剂。
在这些方面的某些中,酪氨酸羟化酶抑制剂与β肾上腺素能抑制剂同时施用。在另一些方面,β肾上腺素能抑制剂与α-甲基-DL-酪氨酸分开施用,例如在一天中的另一时间。
根据本公开内容,所描述的用于治疗疾病或病症的方法可以与也已知对治疗相同疾病或病症有效的治疗方法组合使用。例如,可以用影响自主神经传递的化合物(例如苯丙胺、哌醋甲酯等)、精神药物(例如利培酮)、神经递质再摄取抑制剂(例如氟西汀)、刺激谷氨酰胺能传递的化合物(例如LY2140023)和/或影响胆碱能神经传递的化合物(例如加兰他敏)治疗孤独症行为和症状。因此,本公开内容还涉及通过施用有效量的酪氨酸羟化酶抑制剂(例如,α-甲基-DL-酪氨酸)和有效量的影响自主神经传递的化合物、精神药物、神经递质再摄取抑制剂、刺激谷氨酰胺能传递的化合物和/或影响胆碱能神经传递的化合物来治疗患者中的孤独症的方法。在一个实施方案中,本发明提供了通过施用治疗有效量的酪氨酸羟化酶抑制剂(例如,α-甲基-DL-酪氨酸)和治疗有效量的中枢神经系统(CNS)药剂来治疗患者中的孤独症的方法。
通过本发明的组合物治疗的疾病或病症包括例如孤独症或其相关疾病或障碍。
自主神经系统牵涉到类似于孤独症中看到的那些的症状。孤独症谱系障碍(ASD)与自主相关结构(包括脑岛和杏仁核)中的异常发现相关。在孤独症中看到了自主相关变化,例如基础心率升高和由于心理社会挑战而导致的降低的心率。孤独症-自主联系以呼吸性窦性心律不齐(RSA)的后果为例,其包括社交困难、语言困难和认知发育延迟。
假设慢性过度激活的自主系统是基于过度焦虑水平的孤独症的相关因素,其导致孤独症、生理性过度觉醒和其他相关因素。焦虑可能是孤独症相关的最大的合并症,并且其可能导致疾病的其他特征,与和自主功能有关的中枢神经系统结构有关。在表型上,孤独症和焦虑都具有刻板的重复性行为和有限的兴趣、逃避行为和言语问题。焦虑与报道的心率升高、出汗和“打架或逃跑”反应的其他后遗症的自主神经症状之间的关系揭示了孤独症中外周神经系统功能的作用。但是,这可继发于中枢自主激活。中枢功能可表现为升高的情绪反应性和夸大的威胁感知或对恐惧反应的减弱的抑制,这与其中自主反应和情绪反应重叠的上述中枢结构有关。
有大量证据表明孤独症与中枢神经系统的胆碱能功能有关,特别是与多种α-亚型烟碱受体(特别是在小脑中)有关。然而,由于通常将自主功能视为胆碱能和儿茶酚胺能系统的平衡,因此感知到的胆碱能功能的升高或降低可能是这些系统具有儿茶酚胺能基调的动态平衡变化的表现。相信通过经由施用α-甲基-DL-酪氨酸的基于乙酰胆碱的操作或多巴胺、去甲肾上腺素或肾上腺素介导的机制的平衡的操作,可在ASD中实现治疗改变。
本发明还涉及通过向有此需要的对象施用α-甲基-DL-酪氨酸来治疗ASD的核心症状。
尽管无意受到任何特定的操作机制的束缚,但是相信根据本发明施用的酪氨酸羟化酶抑制剂(例如,α-甲基-DL-酪氨酸)调节与孤独症有关的儿茶酚胺能途径,更特别地,涉及ASD的核心症状的此类途径,包括CNS和胃肠道中的儿茶酚胺能功能。因此,通过施用酪氨酸羟化酶抑制剂(例如,α-甲基-DL-酪氨酸)来调节儿茶酚胺对内分泌和神经内分泌系统的已知作用,包括但不限于减少分泌到血流中的肾上腺素的量,这可减轻易激惹和激动的强度,以及ASD的其他核心症状。
一方面,本发明提供了用于在有此需要的对象中治疗孤独症谱系障碍(ASD)的核心症状的方法,所述方法包括施用治疗有效量的α-甲基-DL-酪氨酸的外消旋混合物。
另一方面,本发明提供了用于在有此需要的对象中治疗孤独症相关临床特征的方法,所述方法包括向所述对象施用包含治疗有效量的酪氨酸羟化酶抑制剂(例如,α-甲基-DL-酪氨酸)的组合物,从而在所述对象中治疗所述孤独症相关临床特征。
孤独症相关临床特征的实例包括例如但不限于缺乏社会沟通、缺乏社会交往、缺乏社会动机、嗜睡和社会退缩、不适当言语、多动症、刻板行为、易激惹和激动、限制性行为、重复性行为、仪式行为、同一性行为、强迫行为、自残行为或其组合。
在一个实施方案中,基于在一种或更多种心理测试中相对于基线的变化来评估临床特征。心理测验的实例包括但不限于临床总体印象(CGI)评定量表、文兰适应行为量表(VABS)、孤独症诊断观察方案(ADOS)、社会反应量表(SRS)、异常行为检查表-社区(ABC-C)、重复性行为量表(RBS)、康纳斯父母评定量表(CPRS)或其组合。在一个特定的实施方案中,临床特征满足精神疾病诊断与统计手册V(DSM-V)标准中的要求。
术语“对象”、“个体”和“患者”在本文中可互换使用,并且是指向其提供用根据本发明的药物组合物进行的治疗(包括预防性治疗)的动物,例如人。如本文所用,术语“对象”是指人和非人动物。术语“非人动物”和“非人哺乳动物”在本文可互换使用,并且包括所有脊椎动物,例如哺乳动物,例如非人灵长类动物(特别是高等灵长类动物)、绵羊、狗、啮齿动物(例如小鼠或大鼠)、豚鼠、山羊、猪、猫、兔、牛、马,以及非哺乳动物,例如爬行动物、两栖动物、鸡和火鸡。
在一个实施方案中,对象是3岁至21岁、5岁至21岁、或6岁至17岁的人患者。在另一个实施方案中,对象是成人患者。
本说明书中引用的所有专利和参考文献均通过引用整体并入本文。
本文还提供了包含一种或更多种本文所述的分子或组合物的试剂盒。提供以下实施例以补充现有公开内容并提供对本文所述主题的更好理解。这些实施例不应被认为是限制所描述的主题。应当理解,本文描述的实施例和实施方案仅用于举例说明目的,并且根据其进行的各种修改或改变对于本领域技术人员而言将是明显的,并且将被包括在其中,并且可以在不脱离本发明的真实范围的情况下做出。
实施例
实施例1
最初对200名患者进行了筛选。符合研究标准的30名对象同意。九(9)名对象在同意研究之前具有高血糖水平(高血糖)。
高血糖水平(高血糖)被定义为在两种不同情况下的空腹血浆血糖水平为126mg/dl或更高。平均患者年龄为62岁并且中位数患者年龄为60岁。6名患者为女性且3名患者为男性。5名患者为50至60岁且4名患者年龄超过60岁。
研究中的患者施用包含以下的治疗方案:酪氨酸羟化酶抑制剂(即α-甲基-DL酪氨酸)、黑素促进剂(即美拉诺坦II)、p450 3A4促进剂(即5,5-二苯基乙内酰脲)和亮氨酸氨基肽酶抑制剂(即N-[(2S,3R)-3-氨基-2-羟基-4-苯基丁酰基]-L-亮氨酸)。这些化合物在每周五天的每一天施用,持续六周的时期,每周周期之间停药一或两天。每两周监测所有对象的血糖水平。通过每日血糖测试确定血糖水平,随后每两周进行实验室血糖测试。
约两至四周之后,所有九名对象具有正常的血糖水平:定义为在两种不同情况下的空腹血浆血糖水平为125mg/dl或更低。
总体而言,对象对上述治疗良好耐受,没有与治疗相关的不良事件,并且已记录了100%的治疗响应。
实施例2
对患者进行筛选并评估他们满足孤独症谱系障碍的DSM-V标准的程度。这些满足标准中的亚组施用包含以下的治疗方案:酪氨酸羟化酶抑制剂(即α-甲基-DL酪氨酸),剂量为50至100mg,每天3次。另一个亚组施用还包含每日剂量为30mg的p450 3A4促进剂(即5,5-二苯基乙内酰脲)的治疗方案。任选地在就寝时间向两个亚组施用剂量为15mg的γ-氨基丁酸以帮助睡眠并使活动(ticks)和重复行为(如磨齿)安静。根据需要施用血管升压素以辅助脑管理。在每次施用治疗方案之后,再次评估对象满足DSM-5标准的程度的变化。
实施例3
针对AMPT在孤独症治疗中的用途的盲法、随机化、安慰剂对照2期研究
研究设计:盲法、随机化、2组、8周治疗期,随后在接下来的18周内进行另外的停止治疗的随访访视,持续总共26周的研究参与。治疗组由单独的LI-79或安慰剂组成。
样品量:Ll-79 N=30,安慰剂N=10。
研究群体:调查人员认为符合入选标准且表现良好的年龄超过12的孤独症患者。
主要纳入标准:签署知情同意书、正常的临床实验室值、DSM-5符合的孤独症诊断、合格的ADOS评分、足够高的功能以完成方案、至少2周内无精神药物、ABC-C评分>12。
主要排除标准:脆性X综合征、癫痫、使用免费替代药物、任何共病(co-morbidity)、其他精神疾病、超出实验室值范围。
非实验治疗:安慰剂。
剂量和施用:随机化的LI-79或安慰剂将以90mg TID的剂量经口施用。
评价方案:患者将接受8周上述方案,其中1至8周进行每周治疗评价,然后在第10、13和26周进行治疗后随访访视。
安全性测量:定期安排完整的历史记录和体格检查、生命体征、CBC、差异、血小板计数、尿分析、血清酶包括:总蛋白、白蛋白、葡萄糖、BUN、肌酐、直接和总的胆红素、碱性磷酸酶、磷、钙、天冬氨酸转氨酶(“AST”)、丙氨酸转氨酶(“ALT”)、钠、钾、氯化物、碳酸氢盐、T4、TSH和不良事件评估。独立的DMC将监督该试验的进行以确保患者安全。
研究持续时间:最多50周(12周的招募,38的周治疗和随访)。
研究终点:主要终点将是如在临床总体印象(CGI)量表中反映的主治医生的评估,所述评估基于以下变化:在多种心理测试,包括异常行为检查表-群落(ABC-C)、康纳斯父母评价量表和孤独症诊断观察方案(ADOS)中自基线的,以及他们在临床中的个人观察,以及在定期安排的临床访视(根据本方案)时拍摄并由照料者在本研究过程中提供的录像信息。
实施例4
将α-甲基-DL酪氨酸(AMPT)施用于3名患者。该组患者符合孤独症的DSM-5定义并进行治疗。参见表1。
表1
| 患者编号 | 年龄 | 性别 | 剂量 | 不良事件 |
| 01-001 | 3 | 男性 | 90TID | 无 |
| 01-002 | 15 | 男性 | 90TID | 无 |
| 01-003 | 11 | 男性 | 90TID | 无 |
异常行为检核表-群落(ABC-C)、孤独症诊断观察方案(ADOS)、康纳斯父母评价量表和总体临床印象量表用于评估该疾病。在每次访视时都拍摄视频。
这些患者中的两名在该观察前三周的数据在下表中示出。康纳斯父母评价量表数据在图1中示出。这些临床改进显示快速开始并且是持久的。已观察到在数周和数月内的持续改善。除在给药第一天在两名患者中的轻度疲劳之外没有报道不良事件。
表2
表3
表4
实施例5
在患有孤独症的患者中L1-79施用的评价
在两名患者中轶事地使用L1-79,随后在患有孤独症的另外8名患者中进行更结构化的评价。所有患者均施用L1-79的起始剂量,为90mg TID持续至少3个月。在评价期间,使用的剂量高达400mg TID。有关这10名患者的可获得数据的总结在临床效力总结,L1-79治疗孤独症的用途,提交至IND 128673,序列号0005中提供。尽管样品量小且涉及L1-79的开放标签,但结果是令人鼓舞的,其中ABC-C范围持续改善并且ADOS-2平均降低30%以及一名儿童表现出ADOS-2降低60%,这导致他的孤独症诊断的丧失。另外,更长的治疗导致对孤独症的核心症状产生更大量级的治疗益处。此外,当停用研究药物L1-79时,并非所有收益都消退。这些数据表明L1-79具有改善孤独症的核心症状的潜力。
实施例6
在诊断患有孤独症的男性患者中的随机化、双盲安慰剂对照4周研究
该临床研究(在本文中称为“研究HT 02-121”;即实施例6)的目的是确定L1-79是否是用于治疗ASD的良好耐受且临床有用的药剂,以及评估TID给药L1-79四周的PK和药效学(PD)。尽管实施例5的初步研究包括用L1-79进行至少三个月的开放标签治疗,但基于可获得的毒理学数据的限制,本研究仅进行了4周。基于较短的持续时间,与较长的持续时间的初步研究相比,研究HT 02-121中对L1-79的响应预计较小。
该临床研究是随机化双盲、安慰剂对照两队列、4周剂量递增研究,其并入了两个开放标签治疗组,以评估L1-79 100mg和200mg TID在诊断患有孤独症的年龄为12至21岁男性患者中的安全性和效力。第一队列的20名患者由三组患者构成:第一组的五名患者接受了开放标签L1-79 100mg TID并进行PK和EKG评估。该队列中的其余两组由15名患者组成,其在2∶1的基础上随机化以接受L1-79 100mg TID或安慰剂。将来自开放标签L1-79 100mgTID组的PK和安全性数据提交至FDA用于在第二队列纳入之前进行审查和接受。第二队列在程序上与第一队列相同。第二队列的20名患者由相同的三组患者组成,但使用的剂量为200mg TID,而不是100mg TID。主要纳入标准如下:(1)年龄为13至21岁的男性;(2)DSM-5符合的孤独症谱系障碍诊断,其通过孤独症诊断访谈检查(ADIR)和与孤独症诊断一致的ADOS-2评分确认;(3)研究期间必须在不多于一种伴随药物的情况下稳定,并且在心理社交干预方面没有计划的变化。
主要排除标准如下:(1)性活跃男性,(2)有脆性-X综合征、Rett综合征或任何其他共病包括但不限于癌症、遗传病或需要药物治疗的任何疾病或综合征的历史记录,(3)精神分裂症、分裂情感性障碍、酒精使用障碍或注意缺陷多动障碍(ADHD)的DSM-5诊断,(4)患有任何活动性医学问题,包括癫痫和哮喘,(5)不受控制的并发疾病,包括但不限于持续或活动性感染、症状性心血管疾病、肝病、肾病、骨骼肌疾病、人免疫缺陷病毒(HIV)、出血性脑血管意外(HCVA)、乙型肝炎病毒(HBV)或将限制符合研究要求的精神疾病/社交状况,(6)需要长期治疗的任何疾病,(7)需要用免疫抑制剂进行治疗的任何疾病;和/或(8)严重精神疾病的当前或终生诊断。
开放标签患者
分配每个队列中的前五名患者来以开放标签方式接受活性药物。与随机化患者相同对患者进行治疗,以下除外:(1)在基线和给药之后1小时,以及在第1、2、3和4周治疗访视时在给药之后1小时抽取血液样品以确定L1-79的PK,(2)在基线和第1、2、3和4周治疗访视以及第1周和4周给药之后随访访视之前3天内评估EKG,(3)在第1周给药之后访视时进行生命体征、体格检查和ASD评估,(4)在基线和在第1、2、3和4周治疗访视时在给药之后1小时,以及第1周和4周给药之后随访访视时,抽取血液和尿样品用于安全性分析。
随机化患者
与开放标签患者相同对随机化患者进行治疗,以下三个除外:(1)未抽取用于PK的血液样品;(2)未进行ECG;以及(3)这些患者没有1周随访访视,只有4周的随访访视。下表5中提供了该研究的时间和事件方案。
表5时间和事件方案
安全性终点
安全性是研究的主要终点。评估了以下安全性终点:ECG,体格检查,实验室评价(血液学、化学和尿分析),生命体征,包括直立性血压,不良事件(AE)和伴随药物。
效力终点
主要效力终点是由调查人员根据临床总体印象(CGI)评价量表记录的对临床改善的确定。另外的效力终点包括:(1)在文兰适应行为量表,第二版(VABS II)父母/照料者评价表的社会化和交流范围中自基线的变化;(2)在ADOS-2总评分与亚评分中自基线的变化,(3)在社交反应量表,第二版(SRS-2)总评分和分量表中的变化,(4)在ABC-C范围中的变化,(5)在重复行为量表-修订版(RBS-R)总评分和分量表中的变化。鉴于本研究的探索性设计,仅计划描述性统计。
结果
研究群体
图2中总结了患者招募和安排。总共42名患者被随机化并接受至少一剂量的研究药物。一名患者被随机化为开放标签L1-79 200mg TID,但要求父母在临床中接受单剂量的研究药物之后在第0周/基线自愿退出研究。三十九名患者完成了研究。一名用双盲L1-79200mg TID治疗的患者由于AE而退出研究(参见表8)以及一名用安慰剂治疗的患者自愿退出研究。表6中总结了人口统计学特征。
表6人口统计学特征
1一名患者被随机化为开放标签L1-79 200mg TID,并且仅接受单剂量的研究药物。表中不包含来自该患者的数据。
2两名在地点01上连续纳入的在同一天随机化的患者(对象01-008-01-009)在分配与接收药物药盒数量方面存在明显的混淆。由于对两名患者实际接受的治疗存在足够的不确定性,因此通过从效力分析中省略这两名患者,对数据进行了保守分析。来自这两名患者的数据包括在研究群体和安全性分析中(然而,两名对象均未报道AE。)。
安全性
伴随药物和体格检查
大多数患者在研究期间未服用CNS药物。在研究期间使用了以下CNS药物:可乐定(n=2)、(n=1)、(n=3)、劳拉西泮(n=1),(n=1)和(n=1)。在研究期间没有报道临床上显著的体格检查发现。
不良事件
表7中示出了按照主要系统器官类别和优选条目的AE发生率,并且表8中示出了研究期间报道的AE列表。所有AE的强度均为轻度至中度并且是自限性的。
表7按照主要系统器官类别和优选条目的不良事件发生率
表8不良事件的列表
DB=双盲;OL=开放标签
1在4周随访访视时报道的AE
2在治疗前报道的AE
在经历AE的患者中(34.1%,41名患者中的14名),大多数经历了轻度(24.4%,41名患者中的10名)至中度(14.6%,41名患者中的6名)强度的AE。仅多于一名患者报道了三种AE。开放标签100mg组中的两名患者和双盲安慰剂组中的一名患者将故意自我伤害报道为治疗紧急AE。开放标签100mg组中的两名患者将易激惹报道为治疗紧急AE。对于报道故意自我伤害和易激惹的患者之一(02-002),这些症状在退出积极治疗的数天内(即在第4周完成之后)出现。对于另一名患者(02-001),在进行积极药物治疗时症状开始。双盲200mg组中的两名患者在第4周随访访视时,将尿胱氨酸晶体存在报道为未经治疗的紧急AE。
在研究期间没有严重不良事件(SAE)或死亡报道。由于不良事件,总共2名患者退出研究:双盲200mg组中的1名患者经历了癫痫大发作的治疗紧急AE以及双盲安慰剂组中的1名患者经历了故意自我伤害和激动的治疗紧急AE。
生命体征
如研究HT 02-121中所述,在每次访视时采集直立性生命体征。没有观察到满足直立性低血压标准(即收缩压下降20mm Hg,舒张压下降10mm hg或心律增加30次/分钟)的变化。少量对象在第1周或第2周治疗时表现出收缩压和/或舒张压无症状下降以及心率增加,但这些在第4周缓解并且本质上是轻度的(例如,收缩压下降10mm Hg,舒张压下降5mm Hg以及心率增加15至24次/分钟)。图3提供了自所述基线的最大变化的实例,并证明这些变化是短暂的,远远低于直立性标准。
ECGS和实验室评价
在任一名患者中均未注意到自基线EKG的临床显著变化。尿分析未揭示与临床症状相关的发现。值得注意的是,观察到与安慰剂治疗患者的30%相比服用L1-79的一半(50%)患者出现结晶尿。在研究期间出现结晶尿的群体中,约一半(50%)具有浓缩尿(比重>1.025)。大部分结晶尿由草酸钙晶体组成。没有与结晶尿相关的症状。
一名患者在第4周出现无症状的淀粉酶短暂轻度升高(146U/L,正常上限[ULN]为125U/L),其通过4周随访访视解决。
在安全群体中没有注意到AST或ALT或任何其他化学参数的显著升高。
血液学参数评估揭示了在安全群体中没有显著偏差。
药代动力学
在开放标签100mg和200mg TID患者中评估药代动力学。在第1天,在给药之后一小时评估L-79浓度。随后,在第1周、第2周、第3周和第4周评估随机L1-79血浆浓度。在第1天给药之后1小时,100mg和200mg TID的血浆浓度分别为0(<2.5)至736ng/mL和23至1680ng/mL。图4中示出了单个患者和组合的总体平均L1-79随机血浆总浓度的总结。如图5和图6中所示,总体随机L1-79血浆浓度在第1周至第4周内相对稳定。
效力
本研究开始时,缺乏长期的青少年和生殖毒理学数据。申请人进行了持续时间为28天的简短研究,对允许进入该研究中的患者的数目、性别和年龄进行了限制。作为结果,该研究没有被设计或驱动以证明任何效力终点的统计学显著性。因此,如预期的那样,没有一个结果测量达到统计学显著性。预期和观察到的是与孤独症的核心症状改善相一致的在多种装置中的积极趋势。事实上,存在证明在治疗受ASD影响的靶核心社交范围方面类似的改善指标的多种效力测量。另外,仅展示了接受盲法治疗的患者的效力数据。
结果测量
在本研究的队列1和队列2期间,在如何管理问卷方面存在一些差异。在初步研究中,所有表均在存在调查人员的情况下在研究地点完成。在本研究的队列1中,VABS-II、SRS-2、ABC-C和RBS-R由患者/患者家属在治疗访视之前在家中填写,并在治疗访视时归还以加快研究的执行。在治疗访视时未对队列1期间的VABS II、SRS-2、ABC-C和RBS-R进行评估程序,并且作为结果,家属难以正确填写表。为了改善队列2期间问卷的质量和完整性,所有问卷(ADOS-2[由外部认证的ADOS-2测试管理者对两个队列进行管理]和CGI[由两个队列中的调查人员完成]除外)在预先指定的治疗访视时在患者/患者家属的协助下由主要调查人员完成。由于队列2数据更可靠,因此对结果的讨论集中在比较L1-79 200mg与安慰剂,ADOS-2和CGI除外,其中将L1-79 100mg和200mg与安慰剂进行比较。
研究结束之后,发现针对VABS-II的基础锚并不总是恰当地建立。此外,仅对患者完成了两个子范围(交流和社会化),使得不能获得范围或总评分。然而,以下示出了有关VABS II交流和社会化范围的结果。
效力测量的列表总结在以下示出(表9)。对于那些表明有利于L1-79的积极趋势的测量,每种效力测量示出三组数字。这些数字由以下组成:a)线形图,其示出了自筛选/基线至4周(在一些情况下,随后是4周后治疗时间点)的3个治疗组之间的比较变化,b)单个患者响应图,以及c)应答者分析图。对于那些未示出有利于L1-79的积极趋势的效力测量,仅示出了显示自筛选/基线至第4周(在一些情况下,随后是4周后治疗时间点)的3个治疗组之间的比较变化的线形图。
应答者定义:
除通过观察暴露于活性药物的患者的每个效力终点与安慰剂相比的变化量级来分析数据之外,定义“应答者”群体也很重要。通常来说,应答者分析旨在集中于显示出任何益处的患者数目,而不是研究群体的总体变化。通常来说,将应答者定义为其靶症状在效力终点表现出预先指定的改善的患者。该定义与用于在几乎每种障碍(包括孤独症)中判断研究的实验治疗的中期和长期结果的公认标准一致。然而,它并未考虑到在对症状严重程度具有振幅的疾病(如孤独症)的短持续时间的研究中对精确定义的需要。在ASD中,儿童的行为、社交和情感症状调节通常经历轻度至中度的改善或恶化时期,这与多种可确定和尚未确定的因素相关(Boso,2010;Jyonouchi,2011)。因此,在短持续时间研究中,“基线”测量事实上可处于这些振幅之一的顶点、中点或最低点。如果在基线处测量所研究的靶症状时,它们处于顶点或中点,则短持续时间研究可能只通过防止靶症状返回至其振幅最低点来有机会证明初始效力。为了说明这种可能发生在一些研究患者中,应答者定义包括表现出短期稳定性或靶症状改善的患者。因此,对于表现出积极趋势的每个效力终点,如本文所定义的进行应答者分析。
表9中提供了效力测量自筛选/基线变化的列表总结。
表9 L1-79与安慰剂在第4周或LOCF时效力测量自筛选/基线的平均变化的总结比较。
LOCF=末次观测值结转法
临床总体印象(CGI)评价量表
L1-79与安慰剂相比随时间的CGI-总体严重程度(CGI-S)和CGI-总体改善(CGI-I)以图表形式在图7和图8中展示。在第4周或末次观察推进法(LOCF)时自基线的平均CGI-S变化在图9中展示,并且表明与安慰剂组和100mg组中CGIS的相比,200mg组中患者的总体CGIS提高平均0.5分。
患者在CGI-S中自基线至第4周变化的总结在图10中展示。此外,图11中示出了在第4周或LOCF时针对CGIS的应答者分析(定义为改善)。
将针对CGI-S的应答者定义定义为仅改善(而不是改善或没有变化),因为与每周进行的其他测量不同,CGI-S要求临床医生基于所有结果测量以及患者在整个研究中的运动给出患者的临床症状严重程度的总体评估。
在第4周的CGI-S的应答者分析表明了与安慰剂相比,L1-79 100mg和200mg组明显的剂量响应改善趋势。
文兰适应行为量表,第二版(VABS II)
L1-79与安慰剂相比在VABS II标准化社会化评分和VABS II标准化交流评分中自基线随时间的变化以图表形式分别在图12和图13中展示。
孤独症诊断观察方案,第二版(ADOS-2)
L1-79与安慰剂相比在ADOS-2总评分筛选、限制和重复行为总评分和社交影响总评分中随时间的变化以图表形式在图14、图15和图16中展示。尽管通常不用作结果测量,但ADOS-2在短时期内的变化与先前所示的更长持续时间的开放标签初步研究一致。
该作用在多个患者中的一致性通过图17中展示的ADOS-2总评分自筛选至第4周的变化总结表明。
社交响应量表,第二版(SRS-2)
L1-79与安慰剂相比在SRS-2总T评分、SRS-2 DSM-5社交、交流和互动T评分、SRS-2社交交流T评分、SRS-2社交动机T评分和SRS-2 DSM-5限制和重复行为T评分中自基线随时间的变化以图表形式分别在图18、图19、图20、图21和图22中展示。
L1-79 200mg治疗组中的SRS-2总、SRS-2 DSM-5社交交流和互动、SRS-2社交交流和SRS-2社交动机T评分平均提高了近8分或更多(图18、图19、图20和图21)。社交交流和互动量表由DSM-5标准构成,该标准弥补了ASD诊断所需的社交交流和社交互动缺陷。令人相当感兴趣的是发现基线评分为60至83(下降8分或更多)的患者很可能表现出临床严重程度的分类改变,因为症状严重程度的“正常范围内”(低于60T评分)、“轻度范围”(60至65T评分)、“中等范围”(66至75T评分)和“严重范围”(76T评分或更高)的分类是在这些T评分范围内定义的。
每名患者在SRS-2总T评分、SRS-2 DSM-5社交、交流和互动T评分,SRS-2社交交流T评分和SRS-2社交动机T-评分中自基线到第4周的变化的总结分别在图23、图24、图25和图26中展示。
对于SRS-2总、SRS-2 DSM-5社交交流和互动、SRS-2社交交流和SRS-2社交动机T评分,与安慰剂相比,在L1-79 200mg下观察到的应答者的量级和数目二者均更大(图27、图28、图29和图30)。对于SRS-2总T评分,与L1-79 100mg组和安慰剂组二者中的2名相比,L1-79 200mg组中的3名患者具有足够的改善来改变严重程度的分类。对于SRS-2社交动机T评分,与100mg组和安慰剂组中分别为4名和3名患者相比,L1-79 200mg组中的6名患者表现出临床严重程度的分类改变。对于SRS-2 DSM-5社交、交流和互动T评分,与在100mg组和安慰剂组中分别为2名和3名患者相比,200mg组中的4名患者具有严重程度分类的改变。类似地,对于SRS-2社交交流T评分,与安慰剂组和100mg组二者中的3名相比,200mg组中的4名患者表现出分类改善。
在第4周或LOCF时针对SRS-2总T评分、SRS-2 DSM-5社交、交流和互动T评分、SRS-2社交交流T评分和SRS-2社交动机T评分的应答者分析(定义为改善或没有恶化)分别在图27、图28、图29和图30中示出。
图27至30表明,与安慰剂相比,在L1-79 200mg下的应答者百分比(如由改善或没有恶化定义的)更大;参见“应答者定义”(以上部分)。
异常行为检核表-群落(ABC-C)
L1-79与安慰剂相比在ABC-C嗜睡和社交退缩范围、ABC-C不当言语范围,ABC-C多动和不服从范围,ABC-C刻板行为范围以及ABC-C易激惹和激动范围中自基线随时间的变化以图表形式分别在图31、图32、图33、图34和图35中展示。
患者在ABC-C嗜睡和社交退缩范围以及ABC-C不当言语范围中自基线至第4周的变化的总结分别在图36和图37中展示。尽管200mg组与安慰剂组之间的平均变化与基线评分没有区别,但应答者分析的确表明与安慰剂相比,200mg组中患者响应于行为改善或没有恶化的更大的趋势,如分别在图38和图39中所示。
与SRS-2一样,对于那些给予L1-79 200mg的患者,应答者的数目和响应的量级二者均表明了对ABC-C的社交和言语范围区别的趋势。同样值得注意的是,观察到90%至100%的L1-79 200mg患者表现出这些范围的稳定性或改善,已知这些范围在较短时期内强度显著变化。
重复行为量表-修订版(RBS-R)
L1-79与安慰剂相比在RBS-R总评分、RBS-R限制行为、RBS-R仪式行为、RBS-R同一性行为、RBS-R强迫行为、RBS-R刻板行为和RBS-R自我伤害行为中自基线随时间的变化以图表形式在图40、图41、图42、图43、图44、图45和图46中展示。
如通过与安慰剂相比L1-79 200mg评分降低表明的存在RBS-R总评分的平均改善。(图40)。
患者在RBS-R总评分中自基线至第4周的变化的总结在图47中展示。另外,在第4周或LOCF时RBS-R总评分的应答者分析(定义为改善或没有恶化)在图48中示出。
与ABC-C嗜睡和社交退缩以及ABC-C不当言语范围一致,RBS-R总评分示出与安慰剂相比,L1-79 200mg的限制和重复行为的降低量级更大的明显趋势。这通过应答者分析进一步证明,该分析表明与用安慰剂治疗的78%相比,用L1-79 200mg治疗的患者的91%具有改善或稳定的症状。
总体结论
目前用于患有ASD的儿童和成人的可获得治疗仅针对与障碍相关的附带症状(易激惹、激动、冲动、多动),并且具有需要通过血液测试监测代谢参数的副作用。尽管静脉切开术(phlebotomy)对大多数神经型儿童和成人是不愉快的,但对于不能充分传达其恐惧的极度感官敏感性的那些而言,这是相当创伤性的。事实上,这对于这些个体是一个陷阱,因为他们表现出的许多异常行为很可能是由于不能够与他人互动、交流和联系。为他们提供不仅可改善造成这些行为的核心症状的治疗,而且治疗时无需进行侵入式监测的潜力,将大大有利于改善这些儿童的生活质量。
来自研究HT 02-121的结果提供了概念证明,即L1-79显示在治疗ASD的核心症状方面提供益处。ASD主要被定义为社交交流和社交互动中的持续缺陷,以及限制和重复行为模式、兴趣或活动。来自专门用于测量这些核心症状的社交和行为强度二者的多个独立评估的初步证据表明了在多种装置中可重复的一致趋势。尽管研究的规模有限且持续时间短,排除了在所使用的结果测量中显示统计学显著改善的任何期望或能力,但本研究中所利用的多种测量之间的一致性非常令人鼓舞。在少于一个月的治疗中,参与研究的临床医生进行的盲法评估表明,与基线相比,CGI-S改变了近1分。类似地,接受L1-79的患者在同一时期内的ADOS-2评分自基线提高了近1分。
在10位患有孤独症的患者中进行L1-79开放标签施用的先前经验(参见实施例5)清楚地表明,L1-79具有改善孤独症核心症状的潜力。在研究HT 02-121中,多个独立效力测量(包括CGI-S、ADOS-2、SRS-2、ABC-C和RBS-R)证明了在受ASD影响的靶评分社交范围中的持续改善,尽管治疗期短且患者数目小。在28天的治疗期内,L1-79安全且良好耐受。研究结束时,许多父母希望他们的孩子继续接受L1-79治疗。作为结果,在两个临床地点拍摄了圆桌视频,意图是允许这些父母直接与FDA讨论L1-79对患有孤独症的他们的孩子的影响。
实施例7
L1-79用于治疗社交交流功能的核心缺陷和患有孤独症谱系障碍的青少年和成人的随机化、双盲、安慰剂对照的适应试验
完成的研究HT 02-121(实施例6)是L1-79用于孤独症治疗的II期安全性研究。研究HT 02-121是随机双盲、安慰剂对照、两队列、4周剂量递增研究,其并入了2个开放标签治疗组以评估L1-79 100mg和200mg TID在患有孤独症的年龄为13至21岁男性患者中的安全性和效力。来自研究HT 02-121的结果提供了概念证明,即L1-79显示在治疗ASD的核心症状方面提供益处。来自专门用于测量这些核心症状的社交和行为强度二者的多个独立评估的初步证据表明了在多种装置中可重复的一致趋势。尽管研究的规模有限且持续时间短排除了在所使用的结果测量中显示统计学显著改善的任何期望或能力,但本研究中所利用的多种测量之间的一致性非常令人鼓舞。在对来自研究HT02-121的结果进行审查之后,FDA允许L1-79开始进行注册试验,从而获得市场批准,并授予L1-79 IND 128673快速通道名称(Fast Track designation)。
作为结果,发明人正在III期环境中提出一种适应试验方法,该方法将允许方便而又彻底的方法来评价L1-79作为用于治疗社交交流和互动中限定的核心缺陷的治疗。基于来自研究HT 02-121(实施例6)的结果,提出了利用适应设计的两个III期随机化、双盲、并行组、安慰剂对照的临床研究(研究301和研究302),以在研究301的第一部分期间评价最佳纳入标准、样品量和结果测量,基于其孤独症诊断观察方案2(ADOS-2)结果以前瞻性随机化和双盲方式,来量化以200或300mg TID剂量向诊断患有孤独症的对象施用LI-79的安全性和有效性。
L1-79用于治疗孤独症的大多数临床经验是用100至200mg TID剂量。实施例8的研究(在本文中也称为“研究301”)试图基于其孤独症诊断观察方案-2(ADOS-2)结果以前瞻性随机化双盲方式,来量化以200或300mg TID剂量向诊断患有孤独症的对象施用L1-79的安全性和效力。
剂型是包含100mg DL-α-甲基-对-酪氨酸胶囊的胶囊剂(以下称为“L1-79”)。用于III期临床研究(研究301和研究302)的L1-79的预期施用方案是每天3次(TID)经口施用2或3粒胶囊。
研究设计的原理:
ASD是特征为在儿童发展期间缺陷社交互动并存在行为、兴趣或活动限制、重复模式的障碍(Swedo,S.E.,Baird,G.,Cook,E.H.,Happe’,F.G.,Harris,J.C.,Kaufmann,W.E.,…Wright,Harry,H.(Eds.).(2013).Neurodevelopmental Disorders.In AmericanPsychiatric Association.Diagnostic and statistical manual of mental disorders(5th ed.).American Psychiatric Association.)。最近的文献暗示外周和自主神经系统参与患有ASD的儿童和成人(Baker,2017;Fenning,2017)。作为结果,皮肤电(electrodermal)皮肤测试可作为用于更有可能响应于靶向交感神经系统的治疗的患者群体的重要的生物标志物。
主要目标:
本研究的主要目标是评价L1-79与安慰剂相比用于在患有孤独症谱系障碍(ASD)的青少年和成人中治疗社交交流和互动中的核心缺陷的效力、安全性和耐受性。
次要目标:
本研究的次要目标包括以下:
1.在该适应试验的第一部分期间评价最佳纳入标准、样品量和结果测量;
2.评价L1-79与安慰剂相比在降低ASD中的重复和限制行为方面的作用;
3.评价L1-79与安慰剂相比在降低ASD中的异常行为,包括多动、激动和易激惹的作用;以及
4.通过定时间歇性稀疏采样,对L1-79在对象亚组中的药代动力学(PK)和药效学(PD)进行另外的建模。
研究设计:
符合条件的参与者将是年龄为12岁至21岁的青少年和成人,基于临床医生访谈和对ADOS-2的ASD症状的评估,以及临床总体严重程度印象(CGI-S)评价为4或更高(中度或更高),他们符合用于ASD的精神疾病的诊断和统计手册-第5版(DSM-5)标准。
对象将以1∶2∶2的比被随机化为安慰剂、L1-79 200mg或L1-79 300mg每天三次(TID)组。
200和300mg组中的对象将开始服用200mg TID。300mg组中的对象在7天之后将滴定多至300mg TID。
筛选评估将包括ADOS-2,DSM-5和CGI-S对ASD标准的审查。
适应设计将与提出的中期分析一起使用,用于对以下标准做出决策;主要结果的潜在终点,已定义研究群体的修改以及估计的样品量。数据监控委员会和独立统计小组将进行期中分析,并基于预定的标准就研究中提出的改变向主办者提出建议。样品量重新计算将取决于将在中期分析中确定的主要结果和潜在研究群体。样品量重新计算将基于盲法数据。
表30中提供了事件方案。
表30事件方案
表30事件方案
ABC-C=异常行为检核表-群落;ADOS-2=孤独症诊断观察方案-2;ASD=孤独症谱系障碍;CGI-C=临床
总体变化印象;CGI-S=临床总体严重程度印象;DSM-5=精神疾病的诊断和统计手册-第5版;
PSI=父母压力指数;RBS-R=重复行为量表-修订版;SAS=Spence焦虑量表;SSP=Spence焦虑量表;SRS-2=社交
响应量表-2;VABS-3=文兰适应行为量表-第3版;WASI-2=Weschler智力简化量表
1包括对先前/正在进行中的药物的审查
2完整检查,包括对皮肤、头、眼、耳、鼻、喉、颈、甲状腺、肺、心脏、腹部、淋巴结、四肢以及体重的评估
3高度仅在筛选时测量。
4部分检查,以更新在筛选时进行检查的结果
5包括呼吸频率、口腔温度、坐姿和站立直立性血压和脉搏
7仅用于月经初潮后的女性
8对象将仅具有针对访视2、3或4之一进行的随机PK。
9包括血清化学、血液学(包括凝血)和尿分析
10将对ADOS-2进行录像,潜在用作盲审者针对相互社交互动的另外的审查
11仅适应行为复合范围
纳入标准:
1.对象必须是多至21岁的男性或女性青少年或成人
2.对象年龄必须在13至21岁之间
3.月经初潮后的女性(如果合适的话)必须进行节育。
4.基于利用DSM-5标准[例如,孤独症症状量表(ASRS),儿童孤独症量表-2(CARS2)或孤独症诊断访谈-修订版(ADI-R)]的评估工具对ASD进行诊断,并通过ADOS-2(CGI-S评分为4或更高)确认。
5.对象必须在不多于一种伴随药物的情况下稳定,并且在试验期间在心理社交干预中没有计划的变化
6.对象和照料者必须愿意并且能够参加足以获得本文中使用的测试有效评分的测试程序。
7.对象必须具有已经认识他们超过一年、每周至少花费10个小时与他们在一起,并且愿意陪同他们进行每次约会的照料者。
8.对象必须在调查人员看来是足够耐受的,并且能够符合该试验的要求。例如,不耐受抽血或ECG的患者将不是本研究的合格候选者。
9.对象必须能够吞咽胶囊
10.对象及其照料者必须愿意签署知情同意书,或具有由其法定监护人或代理人提供的知情同意书。<18岁的所有对象或不能自我照料的对象必须具有照料者的同意。
排除标准:
1.性活跃的男性和女性
2.不受控制的并发疾病,包括但不限于持续或活动性感染、症状性心血管疾病、肝病、肾病、骨骼肌疾病、HIV、HCVA、HBV或将限制符合研究要求的精神疾病/社交状况。
3.需要用免疫抑制剂进行治疗的任何疾病
4.诊断为脆性-X综合征、Rett综合征或可能是对象孤独症症状的基础的其他神经障碍(例如,先天性或获得性脑损伤、脑畸形、中风、神经遗传障碍或代谢障碍)。
5.DSM-5诊断为精神分裂症、分裂情感性障碍、酒精使用障碍或ADHD、严重精神疾病的当前或终生诊断(例如,双相障碍等);
6.存在任何活动性慢性医学问题,包括但不限于,不受控制的癫痫发作、心脏病、癌症、哮喘、遗传病或需要持续药物治疗的任何疾病或综合征。
7.需要多于一种药物用于治疗孤独症的对象,或尚未断奶至其最低可耐受药物剂量的对象。
8.患有需要用免疫抑制药物进行治疗的任何疾病的对象。
9.存在调查人员认为是临床上有意义的超出范围的肝或肾功能测试或其他无法解释的异常实验室值。
10.不愿意或不能给予知情同意的任何对象或照料者。
研究群体:
计划350名患者。
测试产品、剂量和施用方式:
包封为100和200mg的D-L α-甲基酪氨酸(L1-79)。将测试两个剂量组,为200mgTID(一个200mg剂量与安慰剂组合)和300mg TID(一个200mg胶囊和一个100mg胶囊)。
治疗持续时间:
12周(84天)
效力评估:
未包括在效力测量中的基线评估包括Weschler智力简化量表(WASI-2)和Spence焦虑量表(SAS)。将在基线下进行皮肤电测试,以确定是否更大的自主神经系统变异性与治疗响应相关。(参见研究原理)。主要结果测量将是在第12周时在5要素复合测量上自基线的变化,该复合测量包含来自文兰适应行为量表-第3版(VABS-3)的适应行为复合(ABC)的社会化(SOC)、交流(COM)和日常生活技能(DLS)范围以及社交反应量表-2(SRS-2)的社会化、交流与互动(SCI)和限制兴趣与重复行为(RRB)分量表。主要的次要结果测量将基于在第12周时自基线CGI-S的变化。
另外的次要结果测量将以门控方式(待在中期分析期间确定)评估第12周时自基线评分的变化:
1.异常行为检核表-群落(ABC-C)社交退缩/嗜睡和不当言语范围
2.ABC-C、易激惹、多动和刻板范围
3.重复行为量表-修订版(RBS-R)
4.父母压力指数(PSI)简表
5.感官特征-简表(SSP)
6.Spence焦虑量表(SAS)
7.ADOS-2总评分*(ADOS-2将在筛选和研究结束时进行录像,潜在用于双向互动性的盲性审查。)
安全性评估:
安全性评估包括体格检查、血压和脉搏的直立性测量、标准血液学和临床化学评估、伴随药物使用、尿分析、ECG和自发报道的不良事件。
PK评估:
为了获得对L1-79在患有ASD的患者中的PK和PD的更好地了解,将利用稀疏采样来辅助PK参数建模,并将其与在年轻健康成人中进行的更深入研究中获得的数据进行比较。稀疏采样将限制静脉切开术程序的次数,这在患有ASD的儿童中是重要的考虑因素,他们通常比不患有ASD的同龄人受到抽血程序的创伤多得多。
统计方法:
适应设计将评估研究的三个组分;结果变量,纳入标准的潜在修改以及基于在中期分析时间所做的决定重新计算样品量。纳入标准的修改将基于以下特征的基线严重程度的潜在ASD内表型评估,已知所述以下特征直接影响患有ASD的患者的治疗和干预策略:1)焦虑严重程度基于Spence焦虑量表的评估,基于ABC-C易激惹和多动分量表,通过Weschler智力简化量表和破坏性行为症状严重程度评估IQ。另外,进行皮肤反应性测试来确定自主敏感性将被用作应答者表型的探索性生物标志物(参见研究原理用于这些亚组的正当理由)。主要结果的选择将基于五因素复合测量的条件能力分析,该复合测量包含来自文兰适应行为量表-第3版(VABS-3)的适应行为复合(ABC)的社会化(SOC)、交流(COM)和日常生活技能(DLS)范围以及社交反应量表-2(SRS-2)的社会化、交流与互动(SCI)和限制兴趣与重复行为(RRB)分量表。选择结果和纳入标准之后,将基于盲法数据重新计算样品量。
本领域技术人员将理解,可在不脱离其广泛的发明构思的情况下对上述实施方案进行改变。因此,应理解,本发明不限于所公开的一些具体实施方案,而是旨在包含由所附权利要求书所限定的本发明的精神和范围内的修改。
Claims (19)
1.用于在有此需要的对象中治疗孤独症的方法,所述方法包括向所述对象施用包含治疗有效量的α-甲基-DL-酪氨酸和可药用载体的组合物。
2.权利要求1所述的方法,其中所述组合物包含约50mg(w/w)至约1000mg(w/w)的量的α-甲基-DL-酪氨酸。
3.权利要求1所述的方法,其中所述组合物包含约100mg(w/w/)的量的α-甲基-DL-酪氨酸。
4.权利要求1所述的方法,其中所述组合物包含约200mg(w/w/)的量的α-甲基-DL-酪氨酸。
5.权利要求1所述的方法,其中所述组合物包含约250mg(w/w/)的量的α-甲基-DL-酪氨酸。
6.权利要求1所述的方法,其中所述组合物包含约300mg(w/w/)的量的α-甲基-DL-酪氨酸。
7.权利要求1所述的方法,其中所述组合物以多个分开的剂量施用。
8.权利要求1所述的方法,其中所述组合物以多个分开的剂量施用。
9.权利要求1所述的方法,其中所述组合物以单个持续释放的日剂量施用。
10.权利要求1所述的方法,其中所述组合物以可咀嚼剂型施用于儿科患者。
11.权利要求1所述的方法,其中所述组合物每天施用两次。
12.权利要求1所述的方法,其中所述组合物每天施用三次。
13.权利要求1所述的方法,其还包括向所述对象施用治疗有效量的中枢神经系统(CNS)药剂。
14.权利要求13所述的方法,其中所述药剂是γ-氨基丁酸(GABA)
15.权利要求13所述的方法,其中所述药剂是β-肾上腺素能激动剂。
16.权利要求1所述的方法,其中所述组合物经口施用。
17.权利要求16所述的方法,其中所述组合物为胶囊或片剂的形式。
18.权利要求1所述的方法,其中所述对象是3岁至21岁的人患者。
19.权利要求1所述的方法,其中所述对象是成人患者。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US16/040,393 US10751313B2 (en) | 2013-10-22 | 2018-07-19 | Compositions and methods for treating autism |
| US16/040,393 | 2018-07-19 | ||
| PCT/US2019/040569 WO2020018291A1 (en) | 2018-07-19 | 2019-07-03 | Compositions and methods for treating autism |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN112789045A true CN112789045A (zh) | 2021-05-11 |
Family
ID=69164908
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201980048387.9A Pending CN112789045A (zh) | 2018-07-19 | 2019-07-03 | 用于治疗孤独症的组合物和方法 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20210338619A1 (zh) |
| EP (1) | EP3823626A4 (zh) |
| JP (1) | JP2021530568A (zh) |
| CN (1) | CN112789045A (zh) |
| AU (1) | AU2019306092A1 (zh) |
| WO (1) | WO2020018291A1 (zh) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2024059323A1 (en) * | 2022-09-16 | 2024-03-21 | Halas Francis Peter | Low dose, sustained release formulation for alleviating symptoms caused by increased levels of dopamine and norepinephrine |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20160193169A1 (en) * | 2013-10-22 | 2016-07-07 | Steven Hoffman | Compositions And Methods For Treating Intestinal Hyperpermeability |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9326962B2 (en) * | 2013-10-22 | 2016-05-03 | Steven Hoffman | Compositions and methods for treating intestinal hyperpermeability |
-
2019
- 2019-07-03 JP JP2021526193A patent/JP2021530568A/ja active Pending
- 2019-07-03 US US17/261,397 patent/US20210338619A1/en active Pending
- 2019-07-03 WO PCT/US2019/040569 patent/WO2020018291A1/en active Application Filing
- 2019-07-03 EP EP19838492.7A patent/EP3823626A4/en not_active Withdrawn
- 2019-07-03 AU AU2019306092A patent/AU2019306092A1/en active Pending
- 2019-07-03 CN CN201980048387.9A patent/CN112789045A/zh active Pending
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20160193169A1 (en) * | 2013-10-22 | 2016-07-07 | Steven Hoffman | Compositions And Methods For Treating Intestinal Hyperpermeability |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2021530568A (ja) | 2021-11-11 |
| EP3823626A4 (en) | 2022-03-23 |
| US20210338619A1 (en) | 2021-11-04 |
| AU2019306092A1 (en) | 2021-02-04 |
| EP3823626A1 (en) | 2021-05-26 |
| WO2020018291A1 (en) | 2020-01-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11633372B2 (en) | Compositions and methods for treating autism | |
| US9763903B2 (en) | Compositions and methods for treating intestinal hyperpermeability | |
| WO2022150525A9 (en) | Mdma in the treatment of alcohol use disorder | |
| JP2016516782A (ja) | 心的外傷後ストレス障害を処置するための方法 | |
| JP2014530821A (ja) | ラキニモドおよびフィンゴリモドを組み合わせた多発性硬化症の治療 | |
| TWI428130B (zh) | 治療急性躁狂症之藥學組成物及方法 | |
| US20100178362A1 (en) | Chromium complexes for improvement of memory and cognitive function | |
| TW202142229A (zh) | 治療雷葛氏症候群之病患的方法 | |
| JP6858131B2 (ja) | 自閉症を治療するための組成物及び方法 | |
| JP2022519541A (ja) | 不安関連障害を処置するための組成物および方法 | |
| CN112822997A (zh) | 用于治疗孤独症的组合物和方法 | |
| US10751313B2 (en) | Compositions and methods for treating autism | |
| CN112789045A (zh) | 用于治疗孤独症的组合物和方法 | |
| US20240082225A1 (en) | Methods for the treatment of dyskinesia in cerebral palsy | |
| JP2010500379A (ja) | 線維筋痛症候群に関わる疲労を治療するためのミルナシプラン | |
| US20240122895A1 (en) | Entactogen-assisted therapy for alcohol use disorder and addiction-related conditions and comorbidities | |
| TW202207944A (zh) | 抑鬱症之治療 | |
| DATE | Investigator’s Brochure |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| WD01 | Invention patent application deemed withdrawn after publication |
Application publication date: 20210511 |
|
| WD01 | Invention patent application deemed withdrawn after publication |