CN112469669A - 物质的锰氧化物组合物、以及其合成和其用途 - Google Patents
物质的锰氧化物组合物、以及其合成和其用途 Download PDFInfo
- Publication number
- CN112469669A CN112469669A CN201980043480.0A CN201980043480A CN112469669A CN 112469669 A CN112469669 A CN 112469669A CN 201980043480 A CN201980043480 A CN 201980043480A CN 112469669 A CN112469669 A CN 112469669A
- Authority
- CN
- China
- Prior art keywords
- manganese
- mno
- weak
- matter
- crystalline
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G45/00—Compounds of manganese
- C01G45/02—Oxides; Hydroxides
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
- H01M4/50—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of manganese
- H01M4/502—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of manganese for non-aqueous cells
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2002/00—Crystal-structural characteristics
- C01P2002/20—Two-dimensional structures
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2002/00—Crystal-structural characteristics
- C01P2002/30—Three-dimensional structures
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2002/00—Crystal-structural characteristics
- C01P2002/70—Crystal-structural characteristics defined by measured X-ray, neutron or electron diffraction data
- C01P2002/72—Crystal-structural characteristics defined by measured X-ray, neutron or electron diffraction data by d-values or two theta-values, e.g. as X-ray diagram
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2002/00—Crystal-structural characteristics
- C01P2002/70—Crystal-structural characteristics defined by measured X-ray, neutron or electron diffraction data
- C01P2002/76—Crystal-structural characteristics defined by measured X-ray, neutron or electron diffraction data by a space-group or by other symmetry indications
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2002/00—Crystal-structural characteristics
- C01P2002/70—Crystal-structural characteristics defined by measured X-ray, neutron or electron diffraction data
- C01P2002/77—Crystal-structural characteristics defined by measured X-ray, neutron or electron diffraction data by unit-cell parameters, atom positions or structure diagrams
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/01—Particle morphology depicted by an image
- C01P2004/03—Particle morphology depicted by an image obtained by SEM
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/20—Particle morphology extending in two dimensions, e.g. plate-like
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/60—Particles characterised by their size
- C01P2004/62—Submicrometer sized, i.e. from 0.1-1 micrometer
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/60—Particles characterised by their size
- C01P2004/64—Nanometer sized, i.e. from 1-100 nanometer
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2006/00—Physical properties of inorganic compounds
- C01P2006/40—Electric properties
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M2004/026—Electrodes composed of, or comprising, active material characterised by the polarity
- H01M2004/028—Positive electrodes
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Landscapes
- Chemical & Material Sciences (AREA)
- Inorganic Chemistry (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Inorganic Compounds Of Heavy Metals (AREA)
- Battery Electrode And Active Subsutance (AREA)
Abstract
本发明涉及一种新的合成锰氧化物材料,涉及该新的锰氧化物材料的合成方法以及该新的合成锰氧化物在电化学应用中作为二次电池活性阴极材料的用途。
Description
关于联邦赞助的研究或发展的陈述
不适用。
背景技术
本发明涉及一种新的合成锰氧化物材料ι-MnO2,合成该新的材料ι-MnO2的方法,以及该新的合成锰氧化物ι-MnO2在电化学应用中作为二次电池活性阴极材料的用途。
通式MnO2-X的锰氧化物具有多种应用,包括但不限于颜料/着色剂、生产特殊合金的组分、催化剂、净水剂以及有机合成中的氧化剂。储能应用如锂电池和锂离子电池、超级电容器以及碱性(一次)电池已经越来越多地支配着MnO2-X的市场。
传统的碱性电池通常使用电解二氧化锰(EMD)作为阴极中的活性材料。EMD结构或γ-MnO2通常被描述为在晶格中具有相当大量缺陷的斜方锰矿(R-MnO2)和软锰矿(β-MnO2)隧道MnO2相的共生体(intergrowth)。
在电池放电和EMD还原期间,质子插入到隧道锰氧化物结构中,形成MnOOHX固溶体,其保留着初始锰氧化物的隧道结构。Mn(IV)至Mn(III)的传统1-电子还原的最终产物是δ-MnOOH。理论上,该δ-MnOOH可进一步被还原为Mn(OH)2。然而,实际上导致尖晶石类黑锰矿(Mn3O4)和锌锰矿(ZnMn2O4)形成的溶解-沉淀机理却是更有利的(A.Kozawa,J.F.Yeager,JES,1965,959-963;D.Im,A.Manthiram,B.Coffey,JES 2003,A165159;D.Boden等人,JES1967,415-417;Bode等人,JES 1997,792-801;C.Mandoloni等人,JES,1992,954-59;M.R.Bailey,S.W.Donne,JES,2012,A2010-15)。
隧道式羟基氧化锰(III)和层状氢氧化锰(II)之间的结构差异可能是第二电子转移受阻的原因。在充电或氧化过程中恢复原始的隧道锰氧化物结构也是有问题的。
发明概述
在一方面,本发明的特征在于包含具有通式MnO2-x的材料物质组合物;其中x在0至0.35的范围内;其中所述材料是结晶的;并且其中所述材料具有根据下表的X射线衍射图案:
| 2θ(+/-0.20) | 相对强度 |
| 19.74 | 强 |
| 36.93 | 非常强 |
| 40.16 | 弱 |
| 42.28 | 强 |
| 56.43 | 强 |
| 62.00 | 弱 |
| 66.68 | 中等 |
。
在本发明这个方面的另一实施方案中,该材料的锰原子之间在c-方向上具有约4.487埃的距离。
在另一方面,本发明的特征在于一种制备包含锰和氧的结晶材料的方法,该方法包括在没有水的情况下使固体β-MnOOH与选自以下的组分接触的步骤:臭氧物种、自由基氧物种和上述物种的组合,所述结晶材料在所述接触步骤之后具有根据下表的X射线图案:
| 2θ(+/-0.20) | 相对强度 |
| 19.74 | 强 |
| 36.93 | 非常强 |
| 40.16 | 弱 |
| 42.28 | 强 |
| 56.43 | 强 |
| 62.00 | 弱 |
| 66.68 | 中等 |
。
在该方法的另一实施方案中,该结晶材料的锰原子之间在c-方向上具有约4.487埃的距离。
在本发明这个方面的一个实施方案中,所述材料的锰原子之间在c-方向上具有约4.487埃的距离。
在另一方面,本发明的特征在于一种制备包含锰和氧的结晶材料的方法,该方法包括在没有水的情况下使固体β-MnOOH与选自以下的组分接触的步骤:臭氧物种、自由基氧物种和上述物种的组合,所述结晶材料在所述接触步骤之后为由通式MnO2-x所定义,其中x在0至0.35的范围内;并且其中所述结晶材料具有的空间群。
通过参考以下说明书、权利要求书和附图,本领域技术人员可以进一步了解和理解发明的这些和其它方面、特征、优点以及目的。
附图说明
附图支持本发明的详细描述,并涉及示例性实施方案。所述附图被认为绝不限制本发明的全部范围。
在附图中:
图1所示为斜方锰矿和软锰矿二氧化锰材料的晶格结构;
图2所示为与β-MnOOH和Mn(OH)2结构相比的合成水钠锰矿的结构;
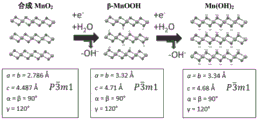
图3所示为根据理想的所需结构以及β-MnOOH和Mn(OH)2结构的合成MnO2结构;
图4所示为与理想结构的预期峰位置相比,根据本发明的非限制性实施方案的新的合成锰氧化物材料ι-MnO2的X射线衍射分析。
图5所示为根据本发明的非限制性实施方案的新的合成锰氧化物材料ι-MnO2的扫描电子显微镜(SEM)图像;
图6所示为用根据本发明的非限制性实施方案的包含新的合成锰氧化物ι-MnO2的二次电池活性阴极材料制造的2032钮扣电池的电压曲线;以及
图7所示为用根据本发明的非限制性实施方案的包含新的合成锰氧化物ι-MnO2的二次电池活性阴极材料制造的2032钮扣电池的MnO2比容量对循环次数的关系图。
发明详述
EMD或γ-锰氧化物是斜方锰矿(1x2通道)和软锰矿(1x1通道)相的共生体。图1所示为斜方锰矿相和软锰矿相的晶格结构。每个的通道由角共享原子形成。当不同的结晶结构在其电化学还原过程中经历质子插入时,其反应不同。斜方锰矿相还原为锰榍石,而软锰矿相则还原为亚锰酸盐。隧道MnOOH进一步还原为Mn(II)应形成羟锰矿,其具有完全不同的层状晶体结构。隧道相的结构重排,无论是锰榍石还是亚锰酸盐都可能施加能垒,这阻止了以有意义的电压放电至Mn(II)。从层状结构羟锰矿重新形成原始隧道材料也是有问题的,这对循环特性会产生负面影响。
溶解Mn(III)物种并随后沉淀出稳定的(非活性)相例如黑锰矿似乎更有利,因此限制隧道MnO2放电至每个Mn为1.33个电子(A.Kozawa,J.F.Yeager,JES,1965,959-963;D.Im,A.Manthiram,B.Coffey,JES 2003,A1651-59;D.Boden等人,JES1967,415-417;Bode等人,JES 1997,792-801;C.Mandoloni等人,JES,1992,954-59;M.R.Bailey,S.W.Donne,JES,2012,A2010-15)。
还已经研究了层状锰氧化物如合成的水钠锰矿用于电池应用。图2显示了合成的水钠锰矿结构与氢氧化锰实质上不同,最显著的是d-间距、对称性、层间物种的存在以及水合。水钠锰矿的还原通常在两个有区别的步骤中进行,其中第二电子的传输电压对于实际应用而言太低(例如小于0.8V)。合成水钠锰矿在Zn/MnO2电池中在放电时不会形成β-MnOOH及随后的Mn(OH)2。合成的水钠锰矿在放电时也倾向于形成更稳定的相,例如隧道结构和尖晶石(Manthiram,J.Electrochem.Soc.149(4)A483,2002;Swinkels,J.Electrochem.Soc.144(9)2949,1997;Yadav/Banerjee Nature Communications 2017,814424)。
在本发明的一个方面,期望与氢氧化锰(II)同构的层状锰(IV)氧化物有助于第二电子转移并促进再充电。所需的层状锰(IV)氧化物的空间群描述为具有空间群(#164国际短符号)的三角晶体系(布拉瓦斯晶格)。图3显示了源自图2的β-MnOOH和氢氧化锰与理想的期望的合成层状锰(IV)氧化物的对比,该层状锰(IV)氧化物与β-MnOOH和氢氧化锰同构。合成层状锰(IV)氧化物以及β-MnOOH和氢氧化锰结构的相似结构允许将锰(III)和锰(II)氧化物氧化至锰(IV)。
传统上,锰氧化物是通过Mn(II)盐的氧化或高锰酸盐的分解而合成的。但是,这些路线仅导致热力学上更稳定的隧道或水钠锰矿结构。氧气使氢氧化锰的自发氧化以及通过可溶性氧化剂氧化β-MnOOH的尝试导致形成方锰矿、方铁锰矿、黑锰矿、水钠锰矿,或结构或氧化态不变。在现有技术中没有合成理想的层状锰(IV)氧化物结构的方法。
实施例1:
根据表1中所描述的方法以多种方式进行β-MnOOH的氧化。表1中还描述了溶解的氧化剂和观察到的结果。
表1
实施例2:
通过用干燥的臭氧/氧气混合物将无水固体β-MnOOH粉末氧化来合成新的合成锰氧化物材料ι-MnO2。对于每克β-MnOOH添加5克10%的臭氧气体。反应在25℃和1大气压的压力下进行。在使2摩尔当量的臭氧通过反应容器后,粉末的颜色从金属棕色变为暗灰色。
臭氧氧化的机制可能涉及直接相互作用或通过自由基氧中间体进行。在后一种情况下,可以使用其他包含或产生自由基氧物种的气体(氧等离子体、.OH、气态过氧化物物种等)代替臭氧。
通过用硫酸亚铁滴定证实了Mn(III)氧化为Mn(IV),并显示4.0的平均氧化态。滴定根据以下所描述的方法进行([Katz,.(J.,Nye,W.F.,&Clarke,R.C.(1956).AvailableOxygen in Manganese Dioxide.Analytical Chemistry,28(4),507-508.https:// doi.org/10.1021/ac50161a028)]。该方法在此通过引用全文结合到本申请中。
该新的经合成的锰氧化物粉末ι-MnO2的粉末X射线衍射(PXRD)分析在Panalytical Empyrean衍射仪上进行,其中Cu K-α辐射在45kV和40mA条件下操作。样品扫描2θ从10-70°,步长为0.141°,扫描速率为每秒0.0090步。
图4所示为该新的合成锰氧化物材料ι-MnO2的X射线衍射(XRD)图案,与由理论XRD垂直线所示的希望的理想层状结构的预期峰位置相比较。
图4中显示的用于该新的合成锰氧化物材料ι-MnO2的XRD图案不匹配以下的XRD图案:α-MnO2(隐钾锰矿),β-MnO2(软锰矿),R-MnO2(斜方锰矿),γ-MnO2(EMD),ε-MnO2(Ahktenskite),δ-MnO2(水钠锰矿/似水锰矿),或λ-MnO2(尖晶石)。
图4中显示的用于该新的合成锰氧化物材料ι-MnO2的XRD图案显示出与理论XRD线的极佳匹配,该理论XRD线针对期望的理想层状结构进行模拟,其等结构于氢氧化锰空间群(#164国际短符号)。以TiS2的cif文件为起点,在VESTA中创建了理想的层状MnO2晶体结构的理论XRD线。使用TiS2是因为TiS2具有2D层状结构,原子的化学计量类似于Mn(OH)2,没有中间层物种,并且与Mn(OH)2占据相同的空间群。首先改变结构参数,使Ti的电子密度变为Mn的电子密度,使S的电子密度变为O的电子密度。其次,改变键距以反映4+氧化态的锰。对于其他MnO2化合物,Mn4+的平均键长为结构完成后,模拟了粉末图案,并在图4中显示。
该新的合成锰氧化物ι-MnO2结构的XRD图案与理想层状MnO2晶体结构的理论垂直XRD线之间的极佳匹配证实,该新的合成ι-MnO2具有与层状β-MnOOH和Mn(OH)2的起始结构相同的空间群和原子连接性。锰阳离子的电荷从3+变为4+导致键距减小,同时保持相同的键结构和对称性。图4显示在37度处发现主要的PXRD 2θ峰,并且在20、42、56和67度处发现了其他峰。空间群(国际短符号)为且编号为164。下表显示了图4的数据,包括相对强度和归一化强度,如下:
| 2θ(+/-0.20) | 相对强度 | 归一化强度 |
| 19.74 | 强 | 49.8 |
| 36.93 | 非常强 | 100.0 |
| 40.16 | 弱 | 5.3 |
| 42.28 | 强 | 50.4 |
| 56.43 | 强 | 53.1 |
| 62.00 | 弱 | 1.4 |
| 66.68 | 中等 | 35.4 |
结构的维度可以由晶体学超级单元内的键连接性来定义。对于3D结构,在所有三个维度中在原子之间都将形成强化学键,如离子键、共价键和金属键等,而任何弱化学键如范德华力和氢键都不会影响超级单元的原子连接性。对于2D结构,在二个维度中在原子之间会形成强化学键,而任何弱化学键都会影响所述超级单元剩余维度的原子连接性。对于1D结构,沿着一个维度在原子之间会形成强化学键,而任何弱化学键都将在超级单元的剩余两个维度中促进原子连接性。3D、2D和1D结构的好例子分别是钻石、石墨烯和聚乙炔。
该新的合成锰氧化物材料ι-MnO2的结构由在两个维度(晶体学晶胞的a轴和b轴)中连接的强Mn-O键组成。第三维度(c轴)仅通过范德华相互作用来保持在一起。在该新的合成锰氧化物材料ι-MnO2的层之间不存在诸如水分子或离子之类的中间层物种。将该新的合成锰材料ι-MnO2的层对齐;它们以与羟锰矿相同的方式对称堆叠。相比之下,水钠锰矿的层彼此错开,这反映在不同的空间群中,并且水钠锰矿通常具有中间层物种,包括但不限于水分子和离子。
图5的扫描电子显微镜(SEM)图像阐明了该新的合成锰氧化物材料ι-MnO2的形态。该新的合成锰氧化物材料ι-MnO2材料具有片状形态。所述片的厚度大约为10-50纳米,长度和宽度在50-600纳米之间。所述片采用六边形图案,边缘之间的角为120°,这被PXRD和理想的晶体结构所证实。
实施例3:
使用Zn粉阳极和用含0.1M硫酸锰的2M的硫酸锌水溶液浸泡的市售的NKK隔片,在标准的2032纽扣电池中评估用新的合成ι-锰氧化物材料ι-MnO2制成的阴极。
使用NMP溶剂和PVDF粘合剂对纽扣电池的阴极和阳极进行浆料浇铸。添加适当量的碳用于电子传导。
图6显示了平滑的电压曲线,图7证实了纽扣电池在150次循环中的稳定的充电和放电,所述纽扣电池包括由根据本发明实施方案的新的合成锰氧化物材料ι-MnO2制成的二次电池活性阴极材料。
尽管在此已经根据某些优选实施方案详细描述了本发明,但是本领域技术人员可以在不脱离本发明的精神的情况下对其进行修改和改变。因此,意图是仅由所附权利要求的范围限制本发明,而不受描述本文所示实施方案的细节和手段的限制。
应当理解,可以在不脱离本发明的概念的情况下对组合物、制品、器件、系统和方法进行变化和改变,并且进一步还应当理解,这些概念意在被接下来的权利要求书所覆盖,除非这些权利要求就其语言来说明确地指出其它。
在不脱离本发明的精神和基本特征的情况下,本发明范围广泛的其他实施方案都是可能的。如这里所讨论的实施方案应被认为仅在所有方面都是说明性的而不是限制性的。是由接下来的权利要求来指示本发明的范围而不是由前述说明书来指示。
Claims (9)
1.物质组合物,其包括:
具有通式MnO2-x的材料;
其中x在0至0.35的范围内;
其中所述材料是结晶的;并且
其中所述材料具有根据下表的X射线衍射图案:
。
3.根据权利要求1所述的物质组合物,其中所述材料的锰原子之间在c-方向上具有约4.487埃的距离。
4.制备包含锰和氧的结晶材料的方法,所述方法包括在没有水的情况下使固体β-MnOOH与选自以下的组分接触的步骤:臭氧物种、自由基氧物种和上述物种的组合,所述结晶材料在所述接触步骤之后具有根据下表的X射线衍射图案:
。
6.根据权利要求4所述的方法,其中所述结晶材料的锰原子之间在c-方向上具有约4.487埃的距离。
8.根据权利要求7所述的物质组合物,其中所述材料的锰原子之间在c-方向上具有约4.487埃的距离。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201862689515P | 2018-06-25 | 2018-06-25 | |
| US62/689,515 | 2018-06-25 | ||
| PCT/US2019/038190 WO2020005700A1 (en) | 2018-06-25 | 2019-06-20 | Manganese oxide composition of matter, and synthesis and use thereof |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN112469669A true CN112469669A (zh) | 2021-03-09 |
Family
ID=68987388
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201980043480.0A Pending CN112469669A (zh) | 2018-06-25 | 2019-06-20 | 物质的锰氧化物组合物、以及其合成和其用途 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US11878916B2 (zh) |
| EP (1) | EP3810552A4 (zh) |
| JP (1) | JP2021529721A (zh) |
| KR (1) | KR102656109B1 (zh) |
| CN (1) | CN112469669A (zh) |
| WO (1) | WO2020005700A1 (zh) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9819053B1 (en) | 2012-04-11 | 2017-11-14 | Ionic Materials, Inc. | Solid electrolyte high energy battery |
| WO2016197098A1 (en) | 2015-06-04 | 2016-12-08 | Ionic Materials, Inc. | Solid state bipolar battery |
| US10559827B2 (en) | 2013-12-03 | 2020-02-11 | Ionic Materials, Inc. | Electrochemical cell having solid ionically conducting polymer material |
| US12074274B2 (en) | 2012-04-11 | 2024-08-27 | Ionic Materials, Inc. | Solid state bipolar battery |
| US11152657B2 (en) | 2012-04-11 | 2021-10-19 | Ionic Materials, Inc. | Alkaline metal-air battery cathode |
| KR102640010B1 (ko) | 2015-06-04 | 2024-02-22 | 아이오닉 머터리얼스, 인코퍼레이션 | 고체 중합체 전해질을 갖는 리튬 금속 배터리 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4405699A (en) * | 1981-06-11 | 1983-09-20 | Varta Batterie Aktiengesellschaft | Manganese dioxide electrode for lithium batteries |
| US20050164085A1 (en) * | 2004-01-22 | 2005-07-28 | Bofinger Todd E. | Cathode material for lithium battery |
| US20110044887A1 (en) * | 2008-03-25 | 2011-02-24 | Nanotecture Ltd. | Mesoporous manganese dioxide |
| CN107709243A (zh) * | 2015-06-22 | 2018-02-16 | 普瑞斯伊诺康私人有限责任公司 | 高纯度水钠锰矿及其制备方法 |
Family Cites Families (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5917693A (en) | 1992-10-26 | 1999-06-29 | Dai-Ichi Kogyo Seiyaku Co., Ltd. | Electrically conductive polymer composition |
| US5378560A (en) | 1993-01-21 | 1995-01-03 | Fuji Photo Film Co., Ltd. | Nonaqueous secondary battery |
| US5989742A (en) | 1996-10-04 | 1999-11-23 | The Research Foundation Of State University Of New York | Blend membranes based on sulfonated poly(phenylene oxide) for enhanced polymer electrochemical cells |
| FR2790330B1 (fr) | 1999-02-25 | 2001-05-04 | Cit Alcatel | Electrode positive de generateur electrochimique rechargeable au lithium a collecteur de courant en aluminium |
| KR100515571B1 (ko) | 2000-02-08 | 2005-09-20 | 주식회사 엘지화학 | 중첩 전기 화학 셀 |
| US6916577B2 (en) | 2002-07-31 | 2005-07-12 | The Gillette Company | Alkaline cell with polymer electrolyte |
| US20110111287A1 (en) | 2008-04-30 | 2011-05-12 | Battelle Memorial Institute | Metal-air battery |
| CN102844908B (zh) | 2010-03-29 | 2016-06-01 | 肖特公开股份有限公司 | 具有低热导率的无机组成部分的电池组电池单元所用的部件 |
| CN103329342A (zh) | 2011-01-19 | 2013-09-25 | 住友化学株式会社 | 铝空气电池 |
| CN102786093A (zh) * | 2011-05-16 | 2012-11-21 | 王强 | 一种超级电容器电极材料MnO2的制备方法 |
| JP6003889B2 (ja) | 2011-05-31 | 2016-10-05 | 日本ゼオン株式会社 | リチウム二次電池正極用複合粒子、リチウム二次電池正極用複合粒子の製造方法、リチウム二次電池用正極の製造方法、リチウム二次電池用正極、及びリチウム二次電池 |
| US9685678B2 (en) | 2013-02-05 | 2017-06-20 | A123 Systems, LLC | Electrode materials with a synthetic solid electrolyte interface |
| WO2014165068A1 (en) | 2013-03-13 | 2014-10-09 | Miles Melvin H | Lithium-air battery for electric vehicles and other applications using molten nitrate electrolytes |
| US20160118685A1 (en) | 2014-10-24 | 2016-04-28 | Battelle Memorial Institute | Methods and compositions for lithium ion batteries |
| KR102640010B1 (ko) | 2015-06-04 | 2024-02-22 | 아이오닉 머터리얼스, 인코퍼레이션 | 고체 중합체 전해질을 갖는 리튬 금속 배터리 |
| KR102002405B1 (ko) | 2016-03-29 | 2019-07-23 | 주식회사 엘지화학 | 전극 슬러리의 제조방법 |
| CN111095438B (zh) | 2017-09-28 | 2021-11-16 | 富士胶片株式会社 | 固体电解质组合物以及含固体电解质的片材、全固态二次电池以及两者的制造方法 |
-
2019
- 2019-06-20 JP JP2020573024A patent/JP2021529721A/ja not_active Ceased
- 2019-06-20 CN CN201980043480.0A patent/CN112469669A/zh active Pending
- 2019-06-20 US US17/251,971 patent/US11878916B2/en active Active
- 2019-06-20 WO PCT/US2019/038190 patent/WO2020005700A1/en unknown
- 2019-06-20 KR KR1020217001135A patent/KR102656109B1/ko active IP Right Grant
- 2019-06-20 EP EP19825537.4A patent/EP3810552A4/en active Pending
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4405699A (en) * | 1981-06-11 | 1983-09-20 | Varta Batterie Aktiengesellschaft | Manganese dioxide electrode for lithium batteries |
| US20050164085A1 (en) * | 2004-01-22 | 2005-07-28 | Bofinger Todd E. | Cathode material for lithium battery |
| US20110044887A1 (en) * | 2008-03-25 | 2011-02-24 | Nanotecture Ltd. | Mesoporous manganese dioxide |
| CN107709243A (zh) * | 2015-06-22 | 2018-02-16 | 普瑞斯伊诺康私人有限责任公司 | 高纯度水钠锰矿及其制备方法 |
| US20180134576A1 (en) * | 2015-06-22 | 2018-05-17 | Prince Erachem Sprl | Highly Pure Birnessite and Method for the Production Thereof |
Non-Patent Citations (6)
| Title |
|---|
| JAMES C. HUNTER ET AL.: "Preparation of a New Crystal Form of Manganese Dioxide: λ-MnO2", 《JOURNAL OF SOLID STATE CHEMIS》 * |
| JOSHUA P. LEFKOWITZ ET AL.: "Influence of pH on the Reductive Transformation of Birnessite by Aqueous Mn(II)", 《ENVIRONMENTAL SCIENCE & TECHNOLOGY》 * |
| MINGXIAO WANG ET AL.: "The effects of Mn loading on the structure and ozone decomposition activity of MnOx supported on activated carbon", 《CHINESE JOURNAL OF CATALYSIS》 * |
| PENG YU ET AL.: "Solution-combustion synthesis of ε-MnO2 for supercapacitors", 《MATERIALS LETTERS》 * |
| S.ARDIZZONE ET AL.: "Mn3O4 and γ-MnOOH powders, preparation, phase composition and XPS characterisation", 《COLLOIDS AND SURFACES A: PHYSICOCHEMICAL AND ENGINEERING ASPECTS》 * |
| XIAODAN SUN ET AL.: "Preparation and characterization of MnOOH and b-MnO2 whiskers", 《INORGANIC CHEMISTRY COMMUNICATIONS》 * |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20210024540A (ko) | 2021-03-05 |
| EP3810552A4 (en) | 2022-03-30 |
| JP2021529721A (ja) | 2021-11-04 |
| US20210253443A1 (en) | 2021-08-19 |
| KR102656109B1 (ko) | 2024-04-09 |
| WO2020005700A1 (en) | 2020-01-02 |
| US11878916B2 (en) | 2024-01-23 |
| EP3810552A1 (en) | 2021-04-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN112469669A (zh) | 物质的锰氧化物组合物、以及其合成和其用途 | |
| Chen et al. | Oxygen vacancies in SnO2 surface coating to enhance the activation of layered Li-Rich Li1. 2Mn0. 54Ni0. 13Co0. 13O2 cathode material for Li-ion batteries | |
| Ryu et al. | Synergistic effects of various morphologies and Al doping of spinel LiMn 2 O 4 nanostructures on the electrochemical performance of lithium-rechargeable batteries | |
| CN103779554B (zh) | 改性高能量密度锂离子电池正极材料及其制备方法 | |
| EP3332437B1 (en) | Sodium layered oxide as cathode material for sodium ion battery | |
| US6720111B2 (en) | Single-phase lithium ferrite based oxide | |
| KR101127554B1 (ko) | 층상형 결정구조의 단일상 리튬-부족형 리튬 다성분계 전이금속 산화물 및 그 제조 방법 | |
| US20150280211A1 (en) | Li-Ni COMPOSITE OXIDE PARTICLES AND NON-AQUEOUS ELECTROLYTE SECONDARY BATTERY | |
| Sharma et al. | Electrical Properties of the Layered Manganese Dioxides M x Mn1− y Co y O 2, M= Na, K | |
| EP3657581A1 (en) | Positive active material for rechargeable lithium battery, method of preparing the same and rechargeable lithium battery including the same | |
| Duncan et al. | Todorokite as a Li Insertion Cathode: Comparison of a Large Tunnel Framework “” Structure with Its Related Layered Structures | |
| JP2002025555A (ja) | マグネシウム二次電池正極活物質用マグネシウム複合酸化物、その製造方法およびそれを用いたマグネシウム二次電池 | |
| Shanmugam et al. | Surface oxygen vacancy engineering and physical protection by in-situ carbon coating process of lithium rich layered oxide | |
| JP6083556B2 (ja) | ナトリウムイオン二次電池用正極活物質 | |
| Wei et al. | One-pot hydrothermal synthesis of peony-like Ag/Ag 0.68 V 2 O 5 hybrid as high-performance anode and cathode materials for rechargeable lithium batteries | |
| Zhang et al. | Electrochemistry of the Layered Manganese Dioxides: A x Mn1− y (Co, Ni, Fe) y O 2 (A= Li, K) Rate Effects | |
| KR101360798B1 (ko) | 층상형 결정구조의 단일상 리튬―부족형 리튬 다성분계 전이금속 산화물 및 그 제조 방법 | |
| Park et al. | Synthesis and electrochemical characterization of M2Mn3O8 (M= Ca, Cu) compounds and derivatives | |
| Mezaal et al. | Promoting the cyclic and rate performance of lithium-rich ternary materials via surface modification and lattice expansion | |
| JP2002226214A (ja) | 新規リチウムマンガン複合酸化物及びその製造方法並びにその用途 | |
| JP2016190782A (ja) | マンガン酸化物およびその製造方法並びにこれを用いるリチウム二次電池 | |
| WO2018181967A1 (ja) | マンガン酸化物、その製造方法、及びリチウム二次電池 | |
| JP2016175825A (ja) | マンガン酸化物およびその製造方法並びにこれを用いるリチウム二次電池 | |
| Ma et al. | Enhancing coulombic efficiency and rate capability of high capacity lithium excess layered oxide cathode material by electrocatalysis of nanogold | |
| JP2002075358A (ja) | リチウムイオン二次電池正極用材料及びその製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| WD01 | Invention patent application deemed withdrawn after publication | ||
| WD01 | Invention patent application deemed withdrawn after publication |
Application publication date: 20210309 |