CN111526870A - 吸入治疗药物的高剂量递送 - Google Patents
吸入治疗药物的高剂量递送 Download PDFInfo
- Publication number
- CN111526870A CN111526870A CN201980007046.7A CN201980007046A CN111526870A CN 111526870 A CN111526870 A CN 111526870A CN 201980007046 A CN201980007046 A CN 201980007046A CN 111526870 A CN111526870 A CN 111526870A
- Authority
- CN
- China
- Prior art keywords
- powder
- particles
- density
- shell
- composition
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 229940126585 therapeutic drug Drugs 0.000 title description 5
- 239000000843 powder Substances 0.000 claims abstract description 202
- 239000002245 particle Substances 0.000 claims abstract description 199
- 239000000203 mixture Substances 0.000 claims abstract description 159
- 238000009472 formulation Methods 0.000 claims abstract description 124
- 238000000034 method Methods 0.000 claims abstract description 87
- 239000003814 drug Substances 0.000 claims abstract description 62
- 239000013543 active substance Substances 0.000 claims abstract description 26
- 239000000443 aerosol Substances 0.000 claims abstract description 24
- 229940112141 dry powder inhaler Drugs 0.000 claims abstract description 18
- 239000000546 pharmaceutical excipient Substances 0.000 claims abstract description 18
- 239000002775 capsule Substances 0.000 claims description 46
- 230000008569 process Effects 0.000 claims description 41
- 210000004072 lung Anatomy 0.000 claims description 31
- 239000007921 spray Substances 0.000 claims description 31
- 239000008186 active pharmaceutical agent Substances 0.000 claims description 30
- 239000003795 chemical substances by application Substances 0.000 claims description 30
- DNDWZFHLZVYOGF-KKUMJFAQSA-N Leu-Leu-Leu Chemical compound CC(C)C[C@H](N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(O)=O DNDWZFHLZVYOGF-KKUMJFAQSA-N 0.000 claims description 27
- 108010049589 leucyl-leucyl-leucine Proteins 0.000 claims description 27
- 239000002671 adjuvant Substances 0.000 claims description 20
- 238000001694 spray drying Methods 0.000 claims description 20
- 239000000463 material Substances 0.000 claims description 17
- 238000011287 therapeutic dose Methods 0.000 claims description 14
- 239000002904 solvent Substances 0.000 claims description 12
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 claims description 11
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 claims description 11
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 10
- 238000012377 drug delivery Methods 0.000 claims description 9
- 238000002360 preparation method Methods 0.000 claims description 9
- 239000000872 buffer Substances 0.000 claims description 8
- 201000010099 disease Diseases 0.000 claims description 8
- 239000002994 raw material Substances 0.000 claims description 8
- 239000003242 anti bacterial agent Substances 0.000 claims description 6
- 208000023504 respiratory system disease Diseases 0.000 claims description 6
- 239000008194 pharmaceutical composition Substances 0.000 claims description 5
- 230000002757 inflammatory effect Effects 0.000 claims description 4
- 230000007246 mechanism Effects 0.000 claims description 4
- 208000035473 Communicable disease Diseases 0.000 claims description 3
- 230000008021 deposition Effects 0.000 claims description 3
- 230000000414 obstructive effect Effects 0.000 claims description 3
- 238000004806 packaging method and process Methods 0.000 claims description 3
- 208000035475 disorder Diseases 0.000 claims description 2
- 208000015181 infectious disease Diseases 0.000 claims description 2
- 239000011859 microparticle Substances 0.000 claims description 2
- 230000003115 biocidal effect Effects 0.000 claims 1
- 239000011521 glass Substances 0.000 claims 1
- 229940079593 drug Drugs 0.000 abstract description 47
- 239000000047 product Substances 0.000 description 65
- 238000001035 drying Methods 0.000 description 40
- 238000011049 filling Methods 0.000 description 23
- 239000007787 solid Substances 0.000 description 18
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 16
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 16
- 238000012856 packing Methods 0.000 description 14
- 150000003839 salts Chemical class 0.000 description 14
- 230000002685 pulmonary effect Effects 0.000 description 13
- 239000008187 granular material Substances 0.000 description 12
- 239000012798 spherical particle Substances 0.000 description 11
- 239000004480 active ingredient Substances 0.000 description 10
- 230000000694 effects Effects 0.000 description 10
- 239000007788 liquid Substances 0.000 description 10
- 238000011068 loading method Methods 0.000 description 10
- 239000000243 solution Substances 0.000 description 10
- 230000007423 decrease Effects 0.000 description 8
- 238000009826 distribution Methods 0.000 description 8
- 238000001704 evaporation Methods 0.000 description 8
- 230000008020 evaporation Effects 0.000 description 8
- 239000007789 gas Substances 0.000 description 8
- NLVFBUXFDBBNBW-PBSUHMDJSA-N tobramycin Chemical compound N[C@@H]1C[C@H](O)[C@@H](CN)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](N)[C@H](O)[C@@H](CO)O2)O)[C@H](N)C[C@@H]1N NLVFBUXFDBBNBW-PBSUHMDJSA-N 0.000 description 8
- -1 cation salts Chemical class 0.000 description 7
- 238000009792 diffusion process Methods 0.000 description 7
- 230000005484 gravity Effects 0.000 description 7
- 239000011164 primary particle Substances 0.000 description 7
- 230000002829 reductive effect Effects 0.000 description 7
- 229960000707 tobramycin Drugs 0.000 description 7
- GSDSWSVVBLHKDQ-JTQLQIEISA-N Levofloxacin Chemical compound C([C@@H](N1C2=C(C(C(C(O)=O)=C1)=O)C=C1F)C)OC2=C1N1CCN(C)CC1 GSDSWSVVBLHKDQ-JTQLQIEISA-N 0.000 description 6
- 230000015572 biosynthetic process Effects 0.000 description 6
- 238000001125 extrusion Methods 0.000 description 6
- 229960003376 levofloxacin Drugs 0.000 description 6
- 238000004519 manufacturing process Methods 0.000 description 6
- 208000006545 Chronic Obstructive Pulmonary Disease Diseases 0.000 description 5
- 229940088710 antibiotic agent Drugs 0.000 description 5
- 208000006673 asthma Diseases 0.000 description 5
- 238000005056 compaction Methods 0.000 description 5
- 239000006185 dispersion Substances 0.000 description 5
- 102000004169 proteins and genes Human genes 0.000 description 5
- 108090000623 proteins and genes Proteins 0.000 description 5
- 230000003746 surface roughness Effects 0.000 description 5
- 230000001225 therapeutic effect Effects 0.000 description 5
- 239000011800 void material Substances 0.000 description 5
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 4
- 238000000889 atomisation Methods 0.000 description 4
- 230000000052 comparative effect Effects 0.000 description 4
- 238000007906 compression Methods 0.000 description 4
- 230000006835 compression Effects 0.000 description 4
- 239000011258 core-shell material Substances 0.000 description 4
- 238000013461 design Methods 0.000 description 4
- 239000013022 formulation composition Substances 0.000 description 4
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 4
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 4
- 238000000338 in vitro Methods 0.000 description 4
- 238000005259 measurement Methods 0.000 description 4
- 230000000704 physical effect Effects 0.000 description 4
- 238000001878 scanning electron micrograph Methods 0.000 description 4
- 238000000935 solvent evaporation Methods 0.000 description 4
- 230000037303 wrinkles Effects 0.000 description 4
- ZEUUPKVZFKBXPW-TWDWGCDDSA-N (2s,3r,4s,5s,6r)-4-amino-2-[(1s,2s,3r,4s,6r)-4,6-diamino-3-[(2r,3r,5s,6r)-3-amino-6-(aminomethyl)-5-hydroxyoxan-2-yl]oxy-2-hydroxycyclohexyl]oxy-6-(hydroxymethyl)oxane-3,5-diol;sulfuric acid Chemical compound OS(O)(=O)=O.N[C@@H]1C[C@H](O)[C@@H](CN)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](N)[C@H](O)[C@@H](CO)O2)O)[C@H](N)C[C@@H]1N ZEUUPKVZFKBXPW-TWDWGCDDSA-N 0.000 description 3
- GIIZNNXWQWCKIB-UHFFFAOYSA-N Serevent Chemical compound C1=C(O)C(CO)=CC(C(O)CNCCCCCCOCCCCC=2C=CC=CC=2)=C1 GIIZNNXWQWCKIB-UHFFFAOYSA-N 0.000 description 3
- 230000002411 adverse Effects 0.000 description 3
- 239000002246 antineoplastic agent Substances 0.000 description 3
- 239000003963 antioxidant agent Substances 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 230000008859 change Effects 0.000 description 3
- 230000000875 corresponding effect Effects 0.000 description 3
- 229940088679 drug related substance Drugs 0.000 description 3
- 238000005429 filling process Methods 0.000 description 3
- 239000010419 fine particle Substances 0.000 description 3
- 238000005243 fluidization Methods 0.000 description 3
- 229910021645 metal ion Inorganic materials 0.000 description 3
- 238000009702 powder compression Methods 0.000 description 3
- 238000012383 pulmonary drug delivery Methods 0.000 description 3
- 239000007858 starting material Substances 0.000 description 3
- 230000009885 systemic effect Effects 0.000 description 3
- 230000008685 targeting Effects 0.000 description 3
- 229960004477 tobramycin sulfate Drugs 0.000 description 3
- 235000012184 tortilla Nutrition 0.000 description 3
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- VOVIALXJUBGFJZ-KWVAZRHASA-N Budesonide Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@@H]2[C@@H]1[C@@H]1C[C@H]3OC(CCC)O[C@@]3(C(=O)CO)[C@@]1(C)C[C@@H]2O VOVIALXJUBGFJZ-KWVAZRHASA-N 0.000 description 2
- LERNTVKEWCAPOY-VOGVJGKGSA-N C[N+]1(C)[C@H]2C[C@H](C[C@@H]1[C@H]1O[C@@H]21)OC(=O)C(O)(c1cccs1)c1cccs1 Chemical compound C[N+]1(C)[C@H]2C[C@H](C[C@@H]1[C@H]1O[C@@H]21)OC(=O)C(O)(c1cccs1)c1cccs1 LERNTVKEWCAPOY-VOGVJGKGSA-N 0.000 description 2
- 239000004471 Glycine Substances 0.000 description 2
- VPNYRYCIDCJBOM-UHFFFAOYSA-M Glycopyrronium bromide Chemical compound [Br-].C1[N+](C)(C)CCC1OC(=O)C(O)(C=1C=CC=CC=1)C1CCCC1 VPNYRYCIDCJBOM-UHFFFAOYSA-M 0.000 description 2
- NTYJJOPFIAHURM-UHFFFAOYSA-N Histamine Chemical compound NCCC1=CN=CN1 NTYJJOPFIAHURM-UHFFFAOYSA-N 0.000 description 2
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 description 2
- 229910019142 PO4 Inorganic materials 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 239000000048 adrenergic agonist Substances 0.000 description 2
- 238000005054 agglomeration Methods 0.000 description 2
- 230000002776 aggregation Effects 0.000 description 2
- BNPSSFBOAGDEEL-UHFFFAOYSA-N albuterol sulfate Chemical compound OS(O)(=O)=O.CC(C)(C)NCC(O)C1=CC=C(O)C(CO)=C1.CC(C)(C)NCC(O)C1=CC=C(O)C(CO)=C1 BNPSSFBOAGDEEL-UHFFFAOYSA-N 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 230000002924 anti-infective effect Effects 0.000 description 2
- 229940121363 anti-inflammatory agent Drugs 0.000 description 2
- 239000002260 anti-inflammatory agent Substances 0.000 description 2
- 239000001961 anticonvulsive agent Substances 0.000 description 2
- 239000002249 anxiolytic agent Substances 0.000 description 2
- 230000000949 anxiolytic effect Effects 0.000 description 2
- 229940005530 anxiolytics Drugs 0.000 description 2
- 229960004436 budesonide Drugs 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 230000001276 controlling effect Effects 0.000 description 2
- 239000006184 cosolvent Substances 0.000 description 2
- 238000000280 densification Methods 0.000 description 2
- 239000010432 diamond Substances 0.000 description 2
- 239000013583 drug formulation Substances 0.000 description 2
- 239000000945 filler Substances 0.000 description 2
- 239000012467 final product Substances 0.000 description 2
- 239000012530 fluid Substances 0.000 description 2
- 229940015042 glycopyrrolate Drugs 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- 239000001307 helium Substances 0.000 description 2
- 229910052734 helium Inorganic materials 0.000 description 2
- SWQJXJOGLNCZEY-UHFFFAOYSA-N helium atom Chemical compound [He] SWQJXJOGLNCZEY-UHFFFAOYSA-N 0.000 description 2
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 2
- 230000003054 hormonal effect Effects 0.000 description 2
- 239000005556 hormone Substances 0.000 description 2
- 229940088597 hormone Drugs 0.000 description 2
- 230000006872 improvement Effects 0.000 description 2
- 229960004078 indacaterol Drugs 0.000 description 2
- QZZUEBNBZAPZLX-QFIPXVFZSA-N indacaterol Chemical compound N1C(=O)C=CC2=C1C(O)=CC=C2[C@@H](O)CNC1CC(C=C(C(=C2)CC)CC)=C2C1 QZZUEBNBZAPZLX-QFIPXVFZSA-N 0.000 description 2
- 239000004615 ingredient Substances 0.000 description 2
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- QLIIKPVHVRXHRI-CXSFZGCWSA-N mometasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(Cl)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CCl)(O)[C@@]1(C)C[C@@H]2O QLIIKPVHVRXHRI-CXSFZGCWSA-N 0.000 description 2
- 229960001664 mometasone Drugs 0.000 description 2
- 230000036961 partial effect Effects 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 2
- 239000010452 phosphate Substances 0.000 description 2
- 108091033319 polynucleotide Proteins 0.000 description 2
- 239000002157 polynucleotide Substances 0.000 description 2
- 102000040430 polynucleotide Human genes 0.000 description 2
- 239000011148 porous material Substances 0.000 description 2
- 102000004196 processed proteins & peptides Human genes 0.000 description 2
- 108090000765 processed proteins & peptides Proteins 0.000 description 2
- 238000012545 processing Methods 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 230000000241 respiratory effect Effects 0.000 description 2
- 238000010079 rubber tapping Methods 0.000 description 2
- 229960005018 salmeterol xinafoate Drugs 0.000 description 2
- 238000005070 sampling Methods 0.000 description 2
- 150000003384 small molecules Chemical class 0.000 description 2
- 238000007711 solidification Methods 0.000 description 2
- 230000008023 solidification Effects 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 239000013589 supplement Substances 0.000 description 2
- 230000001839 systemic circulation Effects 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- 229960000257 tiotropium bromide Drugs 0.000 description 2
- 238000010977 unit operation Methods 0.000 description 2
- 229960005486 vaccine Drugs 0.000 description 2
- 235000012431 wafers Nutrition 0.000 description 2
- RDEIXVOBVLKYNT-VQBXQJRRSA-N (2r,3r,4r,5r)-2-[(1s,2s,3r,4s,6r)-4,6-diamino-3-[(2r,3r,6s)-3-amino-6-(1-aminoethyl)oxan-2-yl]oxy-2-hydroxycyclohexyl]oxy-5-methyl-4-(methylamino)oxane-3,5-diol;(2r,3r,4r,5r)-2-[(1s,2s,3r,4s,6r)-4,6-diamino-3-[(2r,3r,6s)-3-amino-6-(aminomethyl)oxan-2-yl]o Chemical compound OS(O)(=O)=O.O1C[C@@](O)(C)[C@H](NC)[C@@H](O)[C@H]1O[C@@H]1[C@@H](O)[C@H](O[C@@H]2[C@@H](CC[C@@H](CN)O2)N)[C@@H](N)C[C@H]1N.O1C[C@@](O)(C)[C@H](NC)[C@@H](O)[C@H]1O[C@@H]1[C@@H](O)[C@H](O[C@@H]2[C@@H](CC[C@H](O2)C(C)N)N)[C@@H](N)C[C@H]1N.O1[C@H](C(C)NC)CC[C@@H](N)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](NC)[C@@](C)(O)CO2)O)[C@H](N)C[C@@H]1N RDEIXVOBVLKYNT-VQBXQJRRSA-N 0.000 description 1
- OBRNDARFFFHCGE-PERKLWIXSA-N (S,S)-formoterol fumarate Chemical compound OC(=O)\C=C\C(O)=O.C1=CC(OC)=CC=C1C[C@H](C)NC[C@@H](O)C1=CC=C(O)C(NC=O)=C1.C1=CC(OC)=CC=C1C[C@H](C)NC[C@@H](O)C1=CC=C(O)C(NC=O)=C1 OBRNDARFFFHCGE-PERKLWIXSA-N 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 108060003345 Adrenergic Receptor Proteins 0.000 description 1
- 102000017910 Adrenergic receptor Human genes 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- UXVMQQNJUSDDNG-UHFFFAOYSA-L Calcium chloride Chemical compound [Cl-].[Cl-].[Ca+2] UXVMQQNJUSDDNG-UHFFFAOYSA-L 0.000 description 1
- 102000009660 Cholinergic Receptors Human genes 0.000 description 1
- 108010009685 Cholinergic Receptors Proteins 0.000 description 1
- LUKZNWIVRBCLON-GXOBDPJESA-N Ciclesonide Chemical compound C1([C@H]2O[C@@]3([C@H](O2)C[C@@H]2[C@@]3(C[C@H](O)[C@@H]3[C@@]4(C)C=CC(=O)C=C4CC[C@H]32)C)C(=O)COC(=O)C(C)C)CCCCC1 LUKZNWIVRBCLON-GXOBDPJESA-N 0.000 description 1
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 1
- 102000004127 Cytokines Human genes 0.000 description 1
- 108090000695 Cytokines Proteins 0.000 description 1
- CEAZRRDELHUEMR-URQXQFDESA-N Gentamicin Chemical compound O1[C@H](C(C)NC)CC[C@@H](N)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](NC)[C@@](C)(O)CO2)O)[C@H](N)C[C@@H]1N CEAZRRDELHUEMR-URQXQFDESA-N 0.000 description 1
- 229930182566 Gentamicin Natural products 0.000 description 1
- 102000004877 Insulin Human genes 0.000 description 1
- 108090001061 Insulin Proteins 0.000 description 1
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 208000019693 Lung disease Diseases 0.000 description 1
- 229940121948 Muscarinic receptor antagonist Drugs 0.000 description 1
- 241001467460 Myxogastria Species 0.000 description 1
- 208000027771 Obstructive airways disease Diseases 0.000 description 1
- 108091034117 Oligonucleotide Proteins 0.000 description 1
- 108020004459 Small interfering RNA Proteins 0.000 description 1
- 239000000150 Sympathomimetic Substances 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 description 1
- 230000002745 absorbent Effects 0.000 description 1
- 239000002250 absorbent Substances 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 238000012387 aerosolization Methods 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 229940035676 analgesics Drugs 0.000 description 1
- 239000000730 antalgic agent Substances 0.000 description 1
- 230000003288 anthiarrhythmic effect Effects 0.000 description 1
- 230000002280 anti-androgenic effect Effects 0.000 description 1
- 230000002456 anti-arthritic effect Effects 0.000 description 1
- 230000001088 anti-asthma Effects 0.000 description 1
- 230000003474 anti-emetic effect Effects 0.000 description 1
- 230000003556 anti-epileptic effect Effects 0.000 description 1
- 230000003110 anti-inflammatory effect Effects 0.000 description 1
- 230000002141 anti-parasite Effects 0.000 description 1
- 229940035678 anti-parkinson drug Drugs 0.000 description 1
- 239000003416 antiarrhythmic agent Substances 0.000 description 1
- 229940124346 antiarthritic agent Drugs 0.000 description 1
- 239000000924 antiasthmatic agent Substances 0.000 description 1
- 239000003146 anticoagulant agent Substances 0.000 description 1
- 229940127219 anticoagulant drug Drugs 0.000 description 1
- 229940125681 anticonvulsant agent Drugs 0.000 description 1
- 239000003472 antidiabetic agent Substances 0.000 description 1
- 229940125683 antiemetic agent Drugs 0.000 description 1
- 239000002111 antiemetic agent Substances 0.000 description 1
- 229960003965 antiepileptics Drugs 0.000 description 1
- 229940121375 antifungal agent Drugs 0.000 description 1
- 239000002220 antihypertensive agent Substances 0.000 description 1
- 229940030600 antihypertensive agent Drugs 0.000 description 1
- 229960005475 antiinfective agent Drugs 0.000 description 1
- 239000003430 antimalarial agent Substances 0.000 description 1
- 229940033495 antimalarials Drugs 0.000 description 1
- 229940125684 antimigraine agent Drugs 0.000 description 1
- 239000002282 antimigraine agent Substances 0.000 description 1
- 229940034982 antineoplastic agent Drugs 0.000 description 1
- 229940041181 antineoplastic drug Drugs 0.000 description 1
- 229940125687 antiparasitic agent Drugs 0.000 description 1
- 239000003096 antiparasitic agent Substances 0.000 description 1
- 239000000939 antiparkinson agent Substances 0.000 description 1
- 229940127217 antithrombotic drug Drugs 0.000 description 1
- 239000003443 antiviral agent Substances 0.000 description 1
- 229940121357 antivirals Drugs 0.000 description 1
- 239000002830 appetite depressant Substances 0.000 description 1
- 239000003125 aqueous solvent Substances 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 230000017531 blood circulation Effects 0.000 description 1
- 229940124630 bronchodilator Drugs 0.000 description 1
- 239000000168 bronchodilator agent Substances 0.000 description 1
- 239000001110 calcium chloride Substances 0.000 description 1
- 229910001628 calcium chloride Inorganic materials 0.000 description 1
- 239000007963 capsule composition Substances 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 239000002327 cardiovascular agent Substances 0.000 description 1
- 229940125692 cardiovascular agent Drugs 0.000 description 1
- 210000000748 cardiovascular system Anatomy 0.000 description 1
- 210000003169 central nervous system Anatomy 0.000 description 1
- 238000002144 chemical decomposition reaction Methods 0.000 description 1
- 229940044683 chemotherapy drug Drugs 0.000 description 1
- 229960003728 ciclesonide Drugs 0.000 description 1
- 238000004140 cleaning Methods 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 230000002301 combined effect Effects 0.000 description 1
- 229940124558 contraceptive agent Drugs 0.000 description 1
- 239000003433 contraceptive agent Substances 0.000 description 1
- 239000002872 contrast media Substances 0.000 description 1
- 238000013270 controlled release Methods 0.000 description 1
- 230000002596 correlated effect Effects 0.000 description 1
- 239000003246 corticosteroid Substances 0.000 description 1
- 229960001334 corticosteroids Drugs 0.000 description 1
- 238000001739 density measurement Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 239000000032 diagnostic agent Substances 0.000 description 1
- 229940039227 diagnostic agent Drugs 0.000 description 1
- 230000001079 digestive effect Effects 0.000 description 1
- 239000002934 diuretic Substances 0.000 description 1
- 229940030606 diuretics Drugs 0.000 description 1
- 239000003210 dopamine receptor blocking agent Substances 0.000 description 1
- 239000003792 electrolyte Substances 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 230000002124 endocrine Effects 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 230000007717 exclusion Effects 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 239000003925 fat Substances 0.000 description 1
- 230000009969 flowable effect Effects 0.000 description 1
- 229960002714 fluticasone Drugs 0.000 description 1
- MGNNYOODZCAHBA-GQKYHHCASA-N fluticasone Chemical compound C1([C@@H](F)C2)=CC(=O)C=C[C@]1(C)[C@]1(F)[C@@H]2[C@@H]2C[C@@H](C)[C@@](C(=O)SCF)(O)[C@@]2(C)C[C@@H]1O MGNNYOODZCAHBA-GQKYHHCASA-N 0.000 description 1
- WMWTYOKRWGGJOA-CENSZEJFSA-N fluticasone propionate Chemical compound C1([C@@H](F)C2)=CC(=O)C=C[C@]1(C)[C@]1(F)[C@@H]2[C@@H]2C[C@@H](C)[C@@](C(=O)SCF)(OC(=O)CC)[C@@]2(C)C[C@@H]1O WMWTYOKRWGGJOA-CENSZEJFSA-N 0.000 description 1
- 229960000289 fluticasone propionate Drugs 0.000 description 1
- 239000011888 foil Substances 0.000 description 1
- BPZSYCZIITTYBL-UHFFFAOYSA-N formoterol Chemical compound C1=CC(OC)=CC=C1CC(C)NCC(O)C1=CC=C(O)C(NC=O)=C1 BPZSYCZIITTYBL-UHFFFAOYSA-N 0.000 description 1
- 229960002848 formoterol Drugs 0.000 description 1
- 229960000193 formoterol fumarate Drugs 0.000 description 1
- VZCYOOQTPOCHFL-OWOJBTEDSA-L fumarate(2-) Chemical compound [O-]C(=O)\C=C\C([O-])=O VZCYOOQTPOCHFL-OWOJBTEDSA-L 0.000 description 1
- 229960002518 gentamicin Drugs 0.000 description 1
- 238000007496 glass forming Methods 0.000 description 1
- 150000004676 glycans Chemical class 0.000 description 1
- 239000003102 growth factor Substances 0.000 description 1
- 229940127022 high-dose drug Drugs 0.000 description 1
- 229960001340 histamine Drugs 0.000 description 1
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 1
- UFVKGYZPFZQRLF-UHFFFAOYSA-N hydroxypropyl methyl cellulose Chemical compound OC1C(O)C(OC)OC(CO)C1OC1C(O)C(O)C(OC2C(C(O)C(OC3C(C(O)C(O)C(CO)O3)O)C(CO)O2)O)C(CO)O1 UFVKGYZPFZQRLF-UHFFFAOYSA-N 0.000 description 1
- 239000005554 hypnotics and sedatives Substances 0.000 description 1
- 229940005535 hypnotics and sedatives Drugs 0.000 description 1
- 229940126904 hypoglycaemic agent Drugs 0.000 description 1
- 210000000987 immune system Anatomy 0.000 description 1
- IREJFXIHXRZFER-PCBAQXHCSA-N indacaterol maleate Chemical compound OC(=O)\C=C/C(O)=O.N1C(=O)C=CC2=C1C(O)=CC=C2[C@@H](O)CNC1CC(C=C(C(=C2)CC)CC)=C2C1 IREJFXIHXRZFER-PCBAQXHCSA-N 0.000 description 1
- 229960004735 indacaterol maleate Drugs 0.000 description 1
- 238000007373 indentation Methods 0.000 description 1
- 208000027866 inflammatory disease Diseases 0.000 description 1
- 150000002484 inorganic compounds Chemical class 0.000 description 1
- 229940125396 insulin Drugs 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 229940127212 long-acting beta 2 agonist Drugs 0.000 description 1
- 229920002521 macromolecule Polymers 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 229930182817 methionine Natural products 0.000 description 1
- 238000001000 micrograph Methods 0.000 description 1
- 230000004660 morphological change Effects 0.000 description 1
- 239000003149 muscarinic antagonist Substances 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 229940035363 muscle relaxants Drugs 0.000 description 1
- 239000003158 myorelaxant agent Substances 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 239000002773 nucleotide Substances 0.000 description 1
- 125000003729 nucleotide group Chemical group 0.000 description 1
- 235000016709 nutrition Nutrition 0.000 description 1
- 230000000771 oncological effect Effects 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- 210000003300 oropharynx Anatomy 0.000 description 1
- 239000004482 other powder Substances 0.000 description 1
- 239000008188 pellet Substances 0.000 description 1
- 210000000578 peripheral nerve Anatomy 0.000 description 1
- 239000008177 pharmaceutical agent Substances 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 238000005191 phase separation Methods 0.000 description 1
- 230000001766 physiological effect Effects 0.000 description 1
- BXRNXXXXHLBUKK-UHFFFAOYSA-N piperazine-2,5-dione Chemical compound O=C1CNC(=O)CN1 BXRNXXXXHLBUKK-UHFFFAOYSA-N 0.000 description 1
- 229940068196 placebo Drugs 0.000 description 1
- 239000000902 placebo Substances 0.000 description 1
- 229920001184 polypeptide Polymers 0.000 description 1
- 229920001282 polysaccharide Polymers 0.000 description 1
- 239000005017 polysaccharide Substances 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 238000003825 pressing Methods 0.000 description 1
- 230000004845 protein aggregation Effects 0.000 description 1
- 210000004994 reproductive system Anatomy 0.000 description 1
- 229960004017 salmeterol Drugs 0.000 description 1
- 210000002027 skeletal muscle Anatomy 0.000 description 1
- 210000002460 smooth muscle Anatomy 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 239000001509 sodium citrate Substances 0.000 description 1
- NLJMYIDDQXHKNR-UHFFFAOYSA-K sodium citrate Chemical compound O.O.[Na+].[Na+].[Na+].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O NLJMYIDDQXHKNR-UHFFFAOYSA-K 0.000 description 1
- 238000010099 solid forming Methods 0.000 description 1
- 230000001954 sterilising effect Effects 0.000 description 1
- 238000004659 sterilization and disinfection Methods 0.000 description 1
- 150000003431 steroids Chemical class 0.000 description 1
- 239000013526 supercooled liquid Substances 0.000 description 1
- 230000001975 sympathomimetic effect Effects 0.000 description 1
- 229940064707 sympathomimetics Drugs 0.000 description 1
- 239000006068 taste-masking agent Substances 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 229940035289 tobi Drugs 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 239000003204 tranquilizing agent Substances 0.000 description 1
- 230000002936 tranquilizing effect Effects 0.000 description 1
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- ZSDSQXJSNMTJDA-UHFFFAOYSA-N trifluralin Chemical compound CCCN(CCC)C1=C([N+]([O-])=O)C=C(C(F)(F)F)C=C1[N+]([O-])=O ZSDSQXJSNMTJDA-UHFFFAOYSA-N 0.000 description 1
- 230000000007 visual effect Effects 0.000 description 1
- 239000002699 waste material Substances 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1617—Organic compounds, e.g. phospholipids, fats
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/135—Amines having aromatic rings, e.g. ketamine, nortriptyline
- A61K31/137—Arylalkylamines, e.g. amphetamine, epinephrine, salbutamol, ephedrine or methadone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5383—1,4-Oxazines, e.g. morpholine ortho- or peri-condensed with heterocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7028—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages
- A61K31/7034—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages attached to a carbocyclic compound, e.g. phloridzin
- A61K31/7036—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages attached to a carbocyclic compound, e.g. phloridzin having at least one amino group directly attached to the carbocyclic ring, e.g. streptomycin, gentamycin, amikacin, validamycin, fortimicins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39591—Stabilisation, fragmentation
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/16—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing nitrogen, e.g. nitro-, nitroso-, azo-compounds, nitriles, cyanates
- A61K47/18—Amines; Amides; Ureas; Quaternary ammonium compounds; Amino acids; Oligopeptides having up to five amino acids
- A61K47/183—Amino acids, e.g. glycine, EDTA or aspartame
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/007—Pulmonary tract; Aromatherapy
- A61K9/0073—Sprays or powders for inhalation; Aerolised or nebulised preparations generated by other means than thermal energy
- A61K9/0075—Sprays or powders for inhalation; Aerolised or nebulised preparations generated by other means than thermal energy for inhalation via a dry powder inhaler [DPI], e.g. comprising micronized drug mixed with lactose carrier particles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1617—Organic compounds, e.g. phospholipids, fats
- A61K9/1623—Sugars or sugar alcohols, e.g. lactose; Derivatives thereof; Homeopathic globules
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1682—Processes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/5005—Wall or coating material
- A61K9/5015—Organic compounds, e.g. fats, sugars
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M15/00—Inhalators
- A61M15/0001—Details of inhalators; Constructional features thereof
- A61M15/0021—Mouthpieces therefor
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M15/00—Inhalators
- A61M15/0028—Inhalators using prepacked dosages, one for each application, e.g. capsules to be perforated or broken-up
- A61M15/0045—Inhalators using prepacked dosages, one for each application, e.g. capsules to be perforated or broken-up using multiple prepacked dosages on a same carrier, e.g. blisters
- A61M15/0046—Inhalators using prepacked dosages, one for each application, e.g. capsules to be perforated or broken-up using multiple prepacked dosages on a same carrier, e.g. blisters characterized by the type of carrier
- A61M15/0051—Inhalators using prepacked dosages, one for each application, e.g. capsules to be perforated or broken-up using multiple prepacked dosages on a same carrier, e.g. blisters characterized by the type of carrier the dosages being arranged on a tape, e.g. strips
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/24—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against cytokines, lymphokines or interferons
- C07K16/244—Interleukins [IL]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M2202/00—Special media to be introduced, removed or treated
- A61M2202/06—Solids
- A61M2202/064—Powder
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/21—Immunoglobulins specific features characterized by taxonomic origin from primates, e.g. man
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/55—Fab or Fab'
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
Abstract
本发明包括增加药物有效载荷的方法和制剂,特别是涉及基于容器的吸入剂量干粉治疗药物,其中所述方法和制剂的特点是产品密度高,以及每个容器的TLD高,同时保持装置的高效气雾剂性能。本发明实施例包括一种含有可通过干粉吸入器递送的颗粒的喷雾干燥药物粉末,所述组合物包含活性制剂以及成壳辅料,其中所述粉末的特征为产品密度大于50mg/ml。
Description
技术领域
本发明涉及能够在小容量容器(如泡罩或胶囊)中经肺部递送高剂量API的制剂和工艺,以及通过该工艺制成的粉末制剂。本发明的实施例包括致密粉末。该粉末制剂可用于治疗各种疾病和病症,尤其是呼吸系统疾病和病症。
背景技术
用于治疗呼吸系统疾病的活性药物成分(API)通常配制为吸入(或肺部)施用,例如使用便携式吸入器。在特定作用部位(肺)有效提供药物化合物的肺部药物递送方法和组合物,可能有助于最大限度地减少毒副作用、降低给药要求、并降低治疗成本。开发此类肺部药物递送系统,长期以来一直是制药行业的目标。
通常用于将药物局部递送至肺部气道的吸入系统和装置包括干粉吸入器(DPI)、定量吸入器(MDI)、和雾化器。DPI通常完全依赖于患者的主动吸气,将干粉形式的药物引入肺部。这种干粉吸入器通常通过容器(如泡罩或胶囊)分配药物。此类容器的体积必然有限,通常约为0.1mL至1.5mL,例如泡罩为0.06mL至0.2mL,胶囊约为0.1mL至1.4mL。
尽管大多数哮喘和COPD活性药物成分(API)在肺部剂量小于1mg时具有高效力,但当所需的肺总剂量(TLD)为数mg至10mg或更高时,大量的其他API(如抗生素)的效力较低。因此,当通过典型的基于泡罩或基于胶囊的吸入装置给药时,由于泡罩或胶囊容器的体积有限,通常要求多次吸入剂量以实现治疗价值。
尽管可以使用更大的容器,但这将对吸入装置的尺寸产生不利影响,会降低便携性或减少装置内的剂量数,或两者兼而有之。因此,容器尺寸是递送装置(例如吸入器)的重要设计约束,因为容器尺寸对装置设计(人为因素)和最大可能治疗剂量均会产生影响。因此,容器尺寸会对装置形状因素、便携性、和施用剂量产生影响。众所周知,患者接受度、药物依从性、和随后的疗效受到此类人为因素工程的影响。因此,药物有效载荷,即单次吸入可递送的药物量,对患者接受度、依从性、和随后的疗效都很重要。
通常,喷雾干燥的可吸入颗粒设计为低密度,具有多孔(例如PulmoSphereTM)或皱褶(例如PulmoSolTM)表面特性,以尽量减少微粒间作用力。这最大程度提高了工程颗粒的气雾剂分散性,实现了靶向肺递送,同时使颗粒间内聚力降到最低。这种颗粒提高了肺部药物递送效率,然而,由于其密度低和填充特性较差,这些工程颗粒的剂量范围较窄。在上述方法中,必须尽可能降低颗粒密度,以便让工程颗粒保持在最佳空气动力学范围内。
已采用多种方法来增加容器内的粉末灌装质量,包括通过使用具有高真实密度的材料(例如无机盐)配制颗粒,以增加颗粒的真实密度。
在一些现有的技术方法中,工人尝试用金属阳离子盐配制颗粒,以增加喷雾干燥粉末的分散性,从而使得同一单位体积内的剂量更高。然而,这些技术在3号胶囊中未达到超过约40mg的灌装质量,计算的产品密度(如本文所述)也未大于40mg/mL。使用盐的制剂仅适度改善了肺递送效率,并且还存在一个缺点,即金属离子盐可导致在高相对湿度下不稳定的吸湿性制剂。
发明内容
因此,本发明的相应实施例包括增加药物有效载荷的方法和制剂,尤其是基于容器的吸入给药干粉治疗药物。这些方法和制剂的特点是产品密度高。“产品密度”是本发明的一种新度量,它决定了使用容器体积固定的装置可以实现的肺总剂量(TLD)。可通过在固定体积的容器中增加粉末灌装质量(即产品密度),同时保持装置的高效气雾剂性能,以增加每个容器的TLD。
发明人在此将产品密度定义为递送至肺部的药物质量(肺总剂量或TLD)除以容器的总体积,并通过公式1给出:
例如,对于2号胶囊(0.37mL)中载药量为80%且TLD为70%的150mg粉末灌装质量,产品密度为:(150)*(0.8)*(0.7)/(0.37)=227mg/ml。在公式1中,第一个括号内术语(粉末质量/容器体积)与粉末灌装工艺相关,而第二个括号内术语(药物质量/粉末质量)与配制工艺相关,最后一个括号内术语与药物递送相关。因此,“产品密度”包括装入容器中的粉末量、粉末中的载药量、以及肺部的药物递送效率。换言之,产品密度是一个度量,对影响通过给定容器体积可达到的肺部剂量的多个方面或多项特征的共同作用进行定量解释。这些方面或特征包括分散的颗粒密度、装填密度、微粒间作用力、和颗粒的气雾剂特性。
本发明实施例包括一种含有可通过干粉吸入器递送的颗粒的喷雾干燥药物粉末组合物,所述组合物包含活性制剂以及约0.5%至10%(按重量计)的成壳辅料,其中该粉末的特征为产品密度大于50mg/ml。
本发明实施例包括一种喷雾干燥药物组合物,其包括由通过制备原料(包括溶剂、活性制剂、和0.5%-10%的成壳辅料)的工艺制成的颗粒组成的粉末;在佩克莱数为0.5至3的工艺条件下对原料进行喷雾干燥;以及收集所得粉末,其中所述粉末的特征为产品密度大于50mg/mL,可压缩性指数小于20。
本发明实施例包括将包含一种治疗剂量的活性药物制剂的多个颗粒递送至受试者肺部的方法,该方法包括在溶剂中制备活性制剂和成壳辅料的溶液,其中成壳辅料的含量在2%至5%之间;对溶液进行喷雾干燥以获得含有微粒的粉末,其中所述粉末的特征为产品密度至少约为80mg/mL;将喷雾干燥粉末包装在容器中;并提供一种吸入器,具有从容器中提取粉末的装置,其中当通过吸入进行粉末施用时,粉末的肺沉积至少为70%。
本发明实施例包括多剂量粉末吸入装置和药物组合,该药物组合包括一个主体(主体包括一个内腔)和一个可拆卸插入主体内腔的药筒,所述药筒包括一个吸嘴,通过所述吸嘴可将雾化粉末药物递送给使用者,其中,所述药筒中装有一排容器(每个容器适合容纳一剂粉末药物)、一个用于打开每个泡罩的穿孔机构、和一个气雾剂引擎;以及每个容器内包含的粉末药物,其中所述粉末药物包括喷雾干燥药物粉末组合物,包括可从干粉吸入器递送的颗粒,所述组合物包括活性制剂、以及约0.5%-10%(按重量)的成壳辅料,其中粉末的特征为产品密度大于50mg/ml。
本发明实施例提供了产品密度大于60mg/mL(例如大于70mg/mL、大于80mg/mL、大于90mg/mL、和大于100mg/mL)的容器制剂包装。本发明实施例提供了产品密度大于60mg/mL的泡罩—制剂组合。本发明实施例提供了产品密度大于80mg/mL、90mg/mL、或100mg/mL的胶囊—制剂组合。
本发明的实施例包括利用给药腔小、吸入次数最少、或同时具有这两种特点的装置递送高药物有效载荷的方法和制剂。这尤其与通过吸入给药的基于容器的干粉治疗药物相关。
本发明的实施例包括增加药物有效载荷的方法和制剂,而不需要添加盐或其他致密剂或使用盐或其他致密剂进行配制,尤其是与基于容器相关的成分、干粉、肺部给药治疗药物。
本发明的实施例包括设计能够形成紧密填充粉末床的颗粒的方法和制剂。
本发明制剂和工艺的实施例通过使用佩克莱数低的喷雾干燥工艺对颗粒进行工程设计来增加颗粒密度,其中控制了颗粒的表面粗糙度(不规则度),以增加散装粉末的振实密度和挤压密度。
本发明的实施例提供了能够在小体积容器(例如体积为0.37mL或更小的容器)中向肺部递送高剂量API(如肺部总剂量要求为22mg或更高)的组合物和制造工艺。本发明的实施例提供了能够在较小的容器中递送常规大小剂量(例如在0.1mL或更小体积内递送6mg或更大剂量)的组合物和工艺。本发明的实施例提供了能够在常规尺寸的容器中递送较大尺寸的肺总剂量(例如在0.37mL或更小体积中递送50mg或更高剂量)的组合物和工艺。
一方面,本发明的方法和制剂的实施例增加了通过从干粉吸入器递送的API的肺总剂量(TLD)。在其他方面,本发明提供了更高的剂量体积比,这样又可以催生出更小和更符合人体工程学的吸入器,和/或剂量供应量超过一个月,例如两个月、三个月、四个月、五个月、或六个月供应量的多剂量吸入器。这使得供应量为一个月(或更长时间)的多剂量吸入器能够达到高达10mg的肺总剂量,这样有可以以基于泡罩的多剂量干粉吸入器递送许多新类别的药物(包括大多数激素和抗体片段)。
一方面,本发明的方法和制剂的实施例将使得通过小容器(例如0.1mL泡罩)吸入器递送的API的(TLD)从约1mg增加到超过6mg、7mg、8mg、9mg、或10mg。在这些方面,TLD可以是容器灌装质量的50%至60%至70%至80%至90%或更高。这意味着灌装质量能增加12倍至20倍。
一方面,本发明的方法和制剂的实施例将使得通过中型容器(例如0.37mL胶囊)吸入器递送的API的(TLD)从约19mg增加到超过50mg、100mg、150mg、200mg、或250mg。在这些方面,TLD可以是容器灌装质量的50%至60%至70%至80%至90%或更高。这意味着灌装质量能增加2.5倍至13倍以上。
一方面,本发明的方法和制剂的实施例可以将单位剂量或单剂量一次性干粉吸入器中通过单次吸入从容器递送的TLD值增加到超过100mg。
一方面,本发明的方法和制剂的实施例包括能够装入单个容器的整个TLD,和/或通过单次吸入递送的整个TLD。
一方面,本发明的方法和制剂的实施例包括能够装入单个容器,和/或通过单次吸入递送的整个治疗剂量。
一方面,本发明的方法和制剂的实施例包括单个容器内包含的整个TLD。
一方面,本发明的方法和制剂的实施例包括单个容器内包含的整个治疗剂量。
一方面,本方法和制剂的实施例减少了施用治疗剂量所需的处理步骤数量。
因此,在本发明的实施例中,提供了一种用于生产API制剂的工艺,该制剂包括能够装入单个容器内的整个TLD和/或整个治疗剂量。
本发明的实施例提供了一种用于制备吸入用干粉制剂的工艺,其包括喷雾干燥颗粒制剂,所述制剂含有至少一种活性成分,适用于治疗阻塞性或炎症性气道疾病,特别是哮喘和/或COPD。
本发明的实施例提供了一种用于制备吸入用干粉制剂的工艺,其包括喷雾干燥颗粒制剂,所述制剂含有至少一种适用于无创治疗体循环疾病的活性成分。
在本发明的实施例中,粉末不含添加的盐或致密剂。
术语
说明书中使用的术语含义如下:
本文使用的“活性”、“活性成分”、“治疗活性成分”、“活性制剂”、“药物”、或“原料药”是指药物的活性成分,也称为活性药物成分(API)。
本文使用的“无定形”是指一种状态,在该状态下,材料在分子水平上缺乏长程序,并且根据温度,可能表现出固体(玻璃状过冷液体)或液体的物理性质。
“堆密度”定义为不同条件下的“表观”粉末密度。根据ASTM D5004,堆密度为颗粒质量除以其所占的包括颗粒之间空间在内的体积。就本发明而言,我们测量了三种堆密度(即,倾倒堆密度、振实密度、和挤压密度),每种密度均在特定试验条件下测定。
本文使用的“载药量”是指活性成分占制剂总质量的百分比(以质量计)。
本文中使用的“振实密度”或ρ振实按照USP<616>中描述的方法I进行测量。振实密度表示颗粒密度的近似值。可通过将粉末材料置于样品池中,轻拍材料,并向样品池中添加额外材料直至其充满样品池,且在进一步轻拍后不再增加密度来测量振实密度。
“肺总剂量”(TLD)是指沉积在肺部的标称剂量的百分比。TLD的体外度量通常是在4kPa的压降下通过解剖咽喉模型(例如,中等大小的Alberta理想化咽喉)实验确定的。肺总剂量有时在本文中可简称为“剂量”。应将剂量与药物“规格”区分开来,后者为灌装质量乘以载药量。
“真实密度”指颗粒质量除以除开孔和闭孔外的体积。真实密度通常被称为比重瓶密度,因为真实密度通常使用氦气比重瓶测量。
“挤压密度”是通过在0.8巴(24inHg)压力下对散装粉末进行单轴压实测定的堆密度。使用的压力代表将散装粉末挤压成圆饼,然后使用基于滚筒或基于定量器的灌装机将圆饼灌装至容器中所使用的压力。
“生坯密度”是颗粒质量除以其在压缩水平下所占体积,该体积去除了代表颗粒变形程度的游离体积。
“可压缩性指数”(C)是本发明的一个新度量。它提供了一种散装粉末压缩性的度量,并通过公式2给出:
C=100(1-ρT/ρP) 公式2
其中ρT为振实密度,ρP为挤压密度。该指数不同于卡尔指数,后者使用了倾倒堆密度和振实密度。本文所述的可压缩性指数对于在滚筒灌装机上灌装的粉末(使用粉末压缩形成粉末圆饼)而言具有更好的相关性。
本文使用的“递送剂量”或“DD”是指在从粉末容器开始的驱动或分散事件后,从吸入器装置递送干粉的指示。DD定义为吸入器装置递送剂量与标称或定量剂量的比值。DD是通过实验确定的参数,可以使用模拟患者给药的体外装置设置来确定。DD有时也称为喷射剂量(ED)。
本文使用的初级颗粒的“中值空气动力学直径”(MAD),或称Da,根据散装粉末的质量中值直径(通过激光衍射[x50]在足以产生初级颗粒的分散压力[例如4巴]下测定)计算得出,其振实密度为:Da=x50(ρ振实)1/2。
“初级颗粒”是指存在于团聚散装粉末中的单个颗粒。初级粒度分布通过在高压下分散散装粉末和通过激光衍射测量初级粒度分布来确定。绘制粒度随分散压力增加的变化图,直至达到恒定粒度。在该压力下测得的粒度分布代表初级颗粒的粒度分布。
在本说明书和随后的权利要求书中,除非上下文另有要求,否则“包括”一词或其变体(如其第三人称和现在时形式)应理解为暗示所陈述的整数或步骤或一组整数或步骤,但不排除任何其他整数或步骤或一组整数或步骤。
本专利说明书中提到的每项美国专利和国际专利申请的完整披露在所有方面均在本文中通过引用完全并入。
附图说明
本发明的制剂、组合物、和方法可以参考附图来说明。在这些附图中:
图1为液滴干燥的示意图,显示了随时间推移的形态学变化。
图2为三亮氨酸水溶液系统的粒度和密度与佩克莱(Pe)数的关系图。粒度通过标记方块的曲线来显示,曲线从Y轴最下面开始。密度通过标记菱形的曲线报告。
图3是各种密度类型和与之相关的相关配位数(Nc)的图示。就本文而言,配位数代表接触给定颗粒的颗粒数量,并随粉末致密化而增加。
图4是根据实例7(表2-批次761-58-10)制备的不含成壳剂的非工程喷雾干燥细粉末的扫描电子显微照片,显示了导致振实密度较低,不理想的空隙空间(显微照片中的结合区域)。
图5A是可压缩性指数图,而图5B是卡尔指数图。图5显示了包含抗体片段的喷雾干燥粉末的喷射剂量,表示为灌装质量百分比与卡尔指数(5B)和可压缩性指数(5A)构成的函数。将150mg粉末的目标灌装质量灌装至HPMC胶囊中,用于喷射剂量检测。
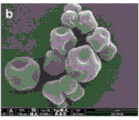
图6A、图6B和图6C是包含抗体片段的喷雾干燥颗粒的扫描电子显微图。图6A显示了按照表2实例7(0%成壳剂)制成的颗粒。图6B显示了由含有抗体片段和亮氨酸的制剂制成的颗粒(未在表2中显示)。因此,图6A显示了在快速干燥条件(低Pe)下喷雾干燥的含0%成壳剂(特征为光滑颗粒形态)的颗粒。图6B显示了含有10%成壳剂(以亮氨酸计)的颗粒,同样进行了喷雾干燥,但在喷雾干燥条件下,导致Pe高于图6A所示颗粒的Pe。可以看出,部分由于成壳剂的存在,图6B中的颗粒表现出凹坑形态。图6C显示了在快速干燥条件(高Pe)下喷雾干燥的含有15%成壳剂(以三亮氨酸计)的颗粒表现出不良(对于高有效载荷应用)皱褶形态。
图7A是包含抗体片段的喷雾干燥粉末的比表面积(SSA)与成壳剂含量(以三亮氨酸计)的关系曲线图,显示SSA随三亮氨酸含量增加而增加。将包含在快速干燥条件(高Pe)下生产的制剂的多个点绘制为菱形,将包含在缓慢干燥条件下(低Pe)的多个点绘制为正方形。图7B是喷射剂量图,表示为灌装质量百分比对比表面积(均用于相同的粉末制剂),显示在考虑高灌装质量(大于100mg)的情况下,在低Pe条件下生产的粉末SSA较低、喷射剂量值较高、喷射剂量变异性较小。两个图中的虚线框分隔了在低Pe下干燥的粉末的实施例,并且其表现出期望的性能。图7A和7B中分析的粉末包括按照实例2制备的抗体片段。
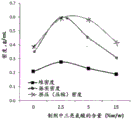
图8是包含抗体片段的喷雾干燥粉末的堆密度和振实密度与三亮氨酸含量的关系曲线图,显示了按照实例2,增加成壳辅料对喷雾干燥制剂的堆密度和振实密度的影响。
图9是标称药物质量(mg)与容器体积(ml)关系的曲线图,其中在70%总肺递送下绘制了四个不同的曲线。曲线A(用虚线表示)表示40mg/mL的产品密度,曲线B(用虚线间隔表示)表示60mg/mL时的产品密度,曲线C(虚线)表示80mg/mL时的产品密度,而曲线D(虚线)表示100mg/mL时的产品密度。图上还绘制了三个产品密度数据点,第一个代表妥布霉素吸入粉雾剂(TIP)市售PilmoSphere制剂的实施例,第二个代表抗体片段(Fab),第三个代表左氧氟沙星制剂。根据本发明的实施例,Fab和左氧氟沙星制剂为喷雾干燥粉末制剂,并按照表5中的实例制备。
具体实施方式
本发明的实施例涉及一种工艺和粉末制剂,该制剂的特征是给定容器体积含有高肺总剂量。在本发明的实施例中,可以在小体积容器(例如泡罩或胶囊)内包含API的高肺总剂量。
在本发明的实施例中,本文制剂的特征是“产品密度”高,它是高剂量递送几个重要方面的一个函数。在公式1中专门定义了产品密度,包含粉末灌装工艺术语、粉末配制过程术语、和粉末递送系统术语。产品密度定义为API的肺总剂量(TLD)(mg)除以含有剂量的容器体积(mL)。因此,这些特性(例如,制剂、粉末生产、灌装、包装、和气雾剂性能)是定义产品密度的重要方面,因此也是本发明的重要方面。仅出于说明目的,下表1显示了标准化胶囊尺寸及其相应的容量(单位:毫升)。
表1
| 大小 | 体积(mL) |
| 000 | 1.37 |
| 00 | 0.95 |
| 0 | 0.68 |
| 1 | 0.50 |
| 2 | 0.37 |
| 3 | 0.30 |
| 4 | 0.21 |
| 5 | 0.13 |
容器可以是泡罩、胶囊、荚状容器、或其他单位体积的容器。在某些实施例中,容器体积可能约为0.37ml或更小(如2号胶囊)。已确定大多数患者可在单次吸入时吸空2号胶囊中的粉末内容物。在某些实施例中,容器体积可能约为0.30mL或更小(如3号胶囊)。在某些实施例中,容器体积可能约为0.50mL或更小(如1号胶囊)。在某些实施例中,容器体积可能约为0.1mL或更小,例如泡罩。
TLD可以通过解剖咽喉模型获得(例如,Alberta理想化咽喉(Alberta IdealizedThroat)和AIT模型)。TLD取决于制剂中的载药量、粉末灌装质量、和使用便携式干粉吸入器给药制剂的气雾剂性能。
本发明制剂的实施例包括大于60mg/ml的产品密度,例如大于70或80或90或100mg/ml的产品密度。当粉末灌装到胶囊中时,产品密度可能更高,例如大于200mg/ml或大于250mg/ml。这比目前达到的最佳产品密度高6倍,例如诺华公司(Novartis)目前以 上市的妥布霉素吸入粉雾剂,产品密度约为48mg/mL。在本发明的实施例中,产品密度在60mg/mL至300mg/m之间,以及它们之间的任何值或值范围。
通过包括吸入治疗制剂的适当颗粒工程的实施例,可获得如此高的产品密度。喷雾干燥是获得工程颗粒的适合技术。图1是液滴和颗粒温度随干燥时间变化的曲线图,以图示显示了液滴随时间发生的形态变。如图1所示,在合理加热期内(即表现出温度升高与潜热的加热期),液滴温度升高至其湿球温度。在恒速干燥期间,液滴表现为纯溶剂;蒸发速率由湿球温度干燥动力学决定。在湿球温度下,随着溶剂通过蒸发迅速损失,液滴收缩。随着蒸发的进行,溶质分子(或乳滴,或悬浮颗粒)根据扩散速率在液滴内排列。当凝固发生时(也称为表皮形成),意味着降速干燥期的开始。在此阶段,可能会发生进一步收缩,根据材料特性,表皮可能会塌陷或断裂。表皮温度随着液体边界向内移动而升高。此时,固化减慢了溶剂向表面输送的蒸发速度,并且干燥受到扩散速率的限制。人们已经认识到,液滴干燥过程中颗粒的形成是控制喷雾干燥颗粒大小、密度、组成分布、和形态的最重要过程。实验数据和理论分析都证明,在干燥过程的恒速期内,溶剂蒸发和溶质扩散速率的相互作用导致形成具有特定特性的颗粒。因此,本文使用佩克莱数来深入了解喷雾干燥期间的颗粒形成机制。
控制具有目标性质的喷雾干燥颗粒的其中一项重要参数是佩克莱数(Pe),是一个与传输现象中的热传质速率相关的无量纲数。佩克莱数定义为热能输送物料速率与浓度梯度输送物料速率的比值。换言之,Pe是喷雾干燥工艺中液体蒸发与溶质扩散的比值。Pe与干燥恒速期间溶剂蒸发和单个液滴溶质积累的界面有关。因此,Pe可通过公式3定义:
其中k是溶剂蒸发速率,D是溶质扩散速率。为澄清说明,本文提到的佩克莱编号连同粉末一起指的是生产工艺的这一方面,而非粉末本身。
图2说明了Pe如何影响粒度和密度。一般而言,在Pe较低的情况下,由于溶剂蒸发速率比溶质扩散速率慢,粒度和密度都会逐渐变化。这使得溶质分子有足够的时间向液滴中心扩散,以便形成固体小颗粒。在这种情况下,颗粒形成接近材料理论密度的致密结构。随着Pe增加,溶质在雾化液滴表面的富集加速,因为介质中的溶质分子没有足够的时间在液滴内扩散和分布。蒸发速率越快,表面越早达到临界过饱和,从而引起早期表皮形成。该条件将增大粒径和降低密度,具有起皱和/或中空颗粒形态。
本发明的实施例包括Pe约为0.5至3(例如0.7至2)的喷雾干燥颗粒(初级粒度为X50=1μm-3μm),其含有少量的成壳辅料,因此存在成壳辅料时颗粒的比表面积与不含成壳剂的相似大小颗粒相当。也就是说,存在如此少量的成壳辅料不会显著改变比表面积(另见图7A)。比表面积取决于颗粒的尺寸和表面形态。这意味着,如果对照颗粒的尺寸较小,比表面积较大,则可掩盖颗粒皱褶度增加的影响。因此,通过与相同尺寸的光滑颗粒进行比较,以比较比表面积。
据认为,成壳辅料会降低控制颗粒装填密度以及气雾剂性能的颗粒间内聚力。内聚力降低可减少了散装粉末中颗粒之间的死腔体积,使得振实密度和挤压密度显著增加,最终又显著增加产品密度。此外,即使粉末被压缩,内聚力降低也会改善粉末流化和扩散。不使用金属离子盐增加材料的真实密度和产生的颗粒密度的情况下就可实现这一目标。
本发明的实施例产生了一种粉末,其包括填充特性优异(振实密度更高)的颗粒。这是通过粒子工程实现专门设计的分数密度并控制颗粒的微粒间作用力来实现的。如果颗皱褶纹过多,微粒间作用力将降至最低,但由于颗粒密度低,灌装质量将显著下降。另一方面,如果颗粒过于光滑且呈球形,由于粉末床中颗粒“桥接”(即颗粒团聚的一种形式)产生的空隙,灌装质量也将会下降。图8显示了在成壳剂(在这种情况下为三亮氨酸)含量上进行粉末填装(振实密度)的实例。由于三亮氨酸会导致表面粗糙,因此x轴可被视为表面粗糙度的间接度量。曲线形状显示在三亮氨酸含量介于无三亮氨酸和15%w/w三亮氨酸极点时达到最大值。因此,在这两个极点之间,存在所需的颗粒形态来优化填充特性。因此,在本发明的实施例中,发现通过引入少量的成壳剂(例如,2.5%-5%w/w的三亮氨酸)可显著改善粉末填装。这会导致表面粗糙,以尽量减少床中颗粒的微粒间作用力。由于制剂中添加的成壳剂的量极少,与表面高度皱褶的颗粒相比,颗粒的分数密度没有显著降低。
研究还发现,通过显著降低颗粒皱褶状态对粉末进行致密化并不是增加灌装质量和肺总剂量的理想方法。如图6A的SEM图像所示,未采用成壳剂(无亮氨酸或三亮氨酸)配制的颗粒具有光滑的球形形状。理论上,光滑的球形颗粒比皱褶颗粒具有更高的分数密度,因此可更有效地填充到固定体积的容器中。然而,光滑球形颗粒的填充不仅与其分数密度相关,而且受颗粒大小的影响很大。大于约100μm的球形颗粒由于其微粒间作用力较弱而装填密度最佳。这类颗粒具有重力稳定性,表明它们可以通过重力进行填充,重力大大超过了内聚力。与大球形颗粒的情况相反,小球形颗粒(小于约100μm)具有重力不稳定性;也就是说,内聚力对颗粒填充的影响比重力更大。图6B显示了皱褶增加的颗粒,如干燥速度缓慢和制剂中10%亮氨酸所指示。图6C显示了干燥速度快和15%三亮氨酸引起的不良皱褶。
图4是通过挤压光滑球形颗粒(X50:1.2μm)创建的粉末床图像。制剂如表2实例7所示。图4所示粉末的振实密度为0.34g/cm3,挤压密度为0.38g/cm3。即使单个颗粒具有光滑的球形形态,使得分数密度较高,但由于形成的较大团聚体在粉末床中产生了较大的空隙,也无法实现紧密填充。如表2所汇总,由于微粒间作用力较强,光滑颗粒的挤压密度和灌装质量低于皱褶颗粒,这也与SEM图像中观察到的颗粒灌装高度一致。除灌装质量低外,由于较强的微粒间作用力,预计制剂A的气雾剂性能较差。
本发明的实施例提供了皱褶度低的颗粒,其具有重力稳定性,颗粒间内聚力较弱。在本发明的实施例中,这些颗粒通常为球形。发明人在本文中发现可压缩性指数(C)与灌装在容器中的粉末的分散性相关。在分散性粉末中,ρ振实和ρ挤压的值接近,C较小(即,低于约15%)。在C大于约20时,分散性降低。可压缩性指数类似于利用堆密度和振实密度的卡尔指数。研究发现,与卡尔指数相比,可压缩性指数与制剂的气雾剂分散性具有更好的相关性。尽管卡尔指数通常用于预测粉末流量,但仅在粉末直径相对较大(几何/空气动力学)时才具有相关性。因此,当考虑工程吸入粉末的特性时,并没有特别意义。与其他形式的粉末药物相比,此类粉末的流动性通常较差。
在本发明的实施例中,存在最佳皱褶度、最佳可压缩性指数、和最佳喷雾干燥条件(后者用佩克莱数表征)。通常,每个结果的数值越高,则密度越低,因为两个颗粒中一个或两个均为低密度,或颗粒因颗粒间内聚力而形成团聚体。数值越低,则密度越高,因为颗皱褶纹越多。
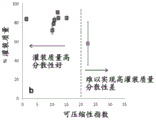
图5A是各种制剂的可压缩性指数(“CI”)与灌装质量百分比关系的曲线图。由此可知,可压缩性指数低于约20的制剂能够实现较高的灌装质量和良好的分散性(ED大于70,例如大于约80)。可压缩性指数高于约20的制剂(如垂直虚线右侧的数据点所示)分散性较差。图5B是喷射剂量(表示为灌装质量的百分比)与卡尔指数关系的曲线图。这两个图表明,可压缩性指数与气雾剂分散性的相关性优于卡尔指数。采用振实密度和挤压密度表示的可压缩性与与生产工艺相关的堆密度(例如,容器的机器灌装)更为一致。
如图5A中CI=20行右侧的点所示,很难将大量传统皱褶(例如Pulmosol)粉末灌装到固定体积的容器中。在采用传统Pulmosol制剂工艺制备的所有制剂中,仅一种制剂:(表2,实例9)达到目标150mg灌装质量。参见表2,实例7至实例12。然而,这种传统Pulmosol制剂的气雾剂性能较低且多变,尤其在治疗相关喷射剂量标准中,因此不适合使用。据信这是因为粉末需要紧密压缩来达到目标灌装质量。与传统制剂相比,本发明的制剂易于达到目标150mg灌装质量,无需大量压缩,并同时维持优越的气雾剂性能,例如,如喷射剂量大于80%至90%所示。参见表2实例1至实例5和图5A(指向CI=20行左侧的点)。
在本发明的实施例中,已经发现可以获得细颗粒的低可压缩性指数,例如,尺寸范围为1μm至5μm的细颗粒。重要的是,可压缩性指数较低的粉末在压缩后粉末流化和分散性改善。考虑到现有技术,这一发现令人惊讶,因为对照工程制剂往往具有较高的可压缩性(例如,大于约20),因为它们表现出一定程度的皱褶和低密度。
制剂/颗粒工程
本发明的实施例包括在小体积容器(如泡罩或胶囊)中制备高剂量API的方法和材料,以及通过该工艺制成的粉末制剂。
本发明的实施例包括一种工艺,通过该工艺,某个API可配制成比传统吸入粉雾剂的产品密度大1.5倍至7倍,例如大2倍至6倍或大3倍至5倍。
本发明的实施例包括一种工艺,通过该工艺,API可以配制成产品密度比传统的低密度工程粉末高50%、或100%、或150%、或200%、或250%、或300%、或350%、或400%、或500%、或600%、或700%。
在本发明的实施例中,该制剂旨在实现至少一项或多项以下目标:(a)通过将辅料和/或高分子量反离子减至最小,最大程度地提高使载药量;(b)将组成颗粒的组分的真实密度增至最大,而不对制剂的化学稳定性和物理稳定性产生不利影响;(c)将颗粒密度增至最大(即,最大限度降低颗粒内的空隙结构或孔隙);(d)最大限度增加粉末的堆密度(即,让颗粒间的游离体积减至最小);以及(e)最大限度增加肺部的气雾剂递送效率。因此,在本发明的实施例中,使用其中一个、两个、三个、四个、或五个特征来最大限度增加本文定义的产品密度。此外,作为灌装工艺的一部分,通过尽量减少容器(如胶囊)中的游离体积,可进一步增加产品密度。
颗粒密度至少可以通过以下两种方式达到最大:(1)用真实密度高的辅料(如金属离子盐)配制,(2)在低Pe条件下制备颗粒。从颗粒工程角度考虑,Pe取决于制剂组成以及工艺条件。对于低Pe(即0.5<Pe<3)条件下产生的颗粒,有足够的时间使溶质扩散到整个蒸发液滴中。此类制剂由几何尺寸较小的固体颗粒组成,颗粒密度更接近组分的真实密度。实验测定颗粒密度可能很困难。通常,会使用振实密度来代替颗粒密度。然而,振实密度也包含颗粒之间游离(间隙)空间的作用,因此颗粒密度被低估。这种间隙空间可能相当大,尤其是在内聚颗粒的团聚中。
相比之下,使用高Pe(即,Pe在约3到10之间)工艺制成的颗粒由低密度核—壳颗粒组成。一般而言,在极低Pe下,颗粒在空间上分布均匀。在极高Pe下,将发生完全相分离,产生“纯”核—壳颗粒。在Pe的中间值,干燥颗粒中存在浓度梯度。对于含有成壳辅料(例如,亮氨酸或三亮氨酸)的制剂,核—壳颗粒可能包括表面富集成壳辅料的皱褶颗粒,以及由原料药和其他在物理和化学上稳定API所需辅料(例如,缓冲液、玻璃形成辅料、抗氧化剂等)组成的内核。
皱褶形态减少了颗粒之间的内聚力,使制剂具有改善的肺部靶向性(即,提高肺递送效率和减少脱靶递送)。相对于含乳糖混合物或球形颗粒的制剂,如此可改善剂量一致性。尽管单独使用低密度核—壳颗粒不足以使产品密度达到最大化,但出现了令人惊讶的发现,即使用少量的成壳辅料在大部分固体、光滑、粒度较细、且Pe较低的颗粒中诱导部分表面皱褶,有益地降低了颗粒间内聚力。这样不仅能够改善气雾剂性能,而且对于实现产品密度最大化也很重要。降低内聚力,在增加喷雾干燥粉末的振实密度方面起着重要作用。经发现这些粉末的可压缩性指数较低,与散装粉末中有限的游离体积一致。对于可压缩性指数高的颗粒(例如,Pe高的低密度、皱褶状颗粒),当使用便携式干粉吸入器递送时,通过粉末压缩增加灌装质量显著降低了粉末有效流化的能力,进而降低了喷射剂量。相比之下,对于可压缩性指数较低的粉末,粉末压缩对喷射剂量的影响较小。
低Pe颗粒通常尺寸较小,只有当存在少量的成壳剂时,才能够实现高效肺递送,以降低颗粒间内聚力,从而改善粉末流化和分散。为了实现有效的肺递送,颗粒的几何尺寸应小于5μm,通常在1μm至3μm之间。给定制剂的Pe取决于待喷雾干燥原料的组成和工艺参数。简而言之,目标是降低成壳剂的浓度,并缓慢干燥颗粒,从而为颗粒内的溶质在整个蒸发液滴中更均匀地扩散留出时间,以便形成表面有轻度皱褶或凹痕的颗粒。
为此,成壳剂的浓度取决于成壳剂的物理性质和原料中的饱和度百分比(即成壳剂浓度与其平衡溶解度的比值)。一般而言,预期成壳剂与其平衡溶解度的比值大于药物和任何其他溶解溶质与其平衡溶解度的比值。这确保了在蒸发过程中成壳剂首先沉淀。也就是说,必须要确保正确的组分(即成壳剂)形成颗粒的外部。
在包含亮氨酸,例如作为成壳剂的单亮氨酸、双亮氨酸、或三亮氨酸的本发明实施例中,固体颗粒中的最佳浓度小于约5%w/w,例如小于4%或3%或2.5%w/w。亮氨酸的实际最低量为0.5%。因此,本发明的实施例可以利用约0.5%至10%之间任何值的三亮氨酸。由于亮氨酸在水中的溶解度较大,因此其最佳上样量预计高于三亮氨酸的观察值,并且无需广泛实验即可测定。在考虑饱和百分比的情况下,可以很容易地测定亮氨酸其他寡聚物的适当重量百分比。实际上,成壳剂的浓度应确保工艺产生的Pe在理想程度下较低(小于约3),并显著增大堆密度(即振实密度和挤压密度)。尽管堆密度显著增加,但颗粒的比表面积(SSA)与不存在成壳辅料时的结果相当,表明颗粒的填充(堆密度和振实密度)得到改善,同时保持其颗粒密度。重要的是,振实密度已显著增加至大于0.5g/ml的值。
可使用其他成壳剂,并且这些成壳剂在浓度低于0.5%和/或浓度高于10%时可达到预期效益。
对于大于100μm的颗粒,重力超过颗粒间内聚力。在这种情况下,球形颗粒的装填密度最有效。对于这样的大颗粒,堆密度随着皱褶度(表面高度振幅小规模变化的一个度量)的增加而降低。然而,随着粒度减小至小于10μm,颗粒间内聚力超过重力,颗粒形态变得更为重要。在这种情况下,光滑的球形颗粒可能配位数较低,并且堆密度降低。再次参考图3,图示说明了各种材料密度,并与配位数(Nc)相关联。配位数代表每个颗粒的接触邻域数,并随粉末致密化而增加。如图4中的圆圈部分所示,粘性光滑球形颗粒在团聚体之间产生较大的空隙空间,因此这些颗粒集合的振实密度较低。然而,需要注意的是,振实密度低并不一定意味着颗粒本身密度低。因此,一定程度的颗粒皱褶,对于“可吸入”大小的颗粒降低颗粒间内聚力和增加配位数非常重要。
本文使用的“皱褶”是工程颗粒表面粗糙度的一个度量。就本发明而言,通过由BET测量获得的比表面积、由氦比重瓶测量获得的真实密度、以及由激光衍射(Sympatec)获得的表面积/体积比计算皱褶度,皱褶度=(SSA·ρtrue)/Sv,Sv=6/D32,其中,D32是基于单位表面积的平均直径。表面粗糙度的增加预期可降低颗粒间内聚力,并改善气雾剂对肺部的靶向性。改善肺靶向性预计可降低患者间变异性以及口咽和体循环中的药物水平。
例如,在本发明的实施例中,颗粒皱褶度可能在约1至3.5之间,例如1至3或1.5至2.5。
本发明的实施例包括皱褶度低的颗粒,其具有重力稳定性,颗粒间内聚力较弱。
可压缩性指数(C)与灌装至容器中粉末的分散性相关。在自由流动粉末中,振实密度(ρ振实)和挤压密度(ρ挤压)值接近,C较小(即小于约15)。在C大于20时,分散性降低。
制剂组成和喷雾干燥工艺参数均影响颗粒形态。在实践中,通过调整制剂组成使微粒间作用力变为最小后,可以通过调整喷雾干燥工艺参数进一步增加装填密度(振实密度)。如表2所汇总,制剂组成相同的颗粒的振实密度随干燥条件而变化;缓慢条件下喷雾干燥的颗粒(样品4)填充优于快速条件下干燥的颗粒(样品8)。该结果表明,在温和条件(低Pe)下干燥的颗粒,由于表面粗糙度低于在快速条件(高Pe)下干燥的颗粒,分数密度更高。比表面积(SSA)结果(表2)与振实密度结果一致。表2还显示,在快速条件下干燥的制剂(样品7至样品12)显示出气雾剂特性较差或粉末填装较差(大多数制剂未达到目标灌装质量,2号胶囊中为150mg)。
工艺
在喷雾干燥工艺中,采用喷嘴将散装原料雾化成液滴槽。液滴粒度分布的控制对于吸入药物递送喷雾干燥颗粒的一致性和有效生产至关重要。通过让溶解固体的质量与干燥颗粒的质量相等,得到以下公式4,可估算最终产品的粒度:
其中d颗粒为颗粒直径;d液滴为液滴直径;Cs为溶液浓度或总固体量;ρ颗粒为颗粒密度;并且ρ溶液为溶液密度。因此,最终产品粒度主要由初始液滴尺寸和溶液浓度控制。
在某些实施例中,使用了双流体雾化器,其利用高速气流(通常为空气)将液体喷射为液滴。雾化通过使用压缩源提供的气流动能来实现,典型压力操作高达100psi。原料的性质对实现低Pe非常重要。固体含量应足够低,以延长恒定干燥期,从而延迟达到过饱和的时间,在过饱和时将形成表皮,以达到低Pe。换言之,工艺中获得的Pe越低,所得粉末越小,密度越高。
为了最大限度增加递送剂量,除了增加产品密度外,在使用干粉吸入器吸入期间,还必须尽可能多地灌装容器中的体积,同时不对粉末流化和分散产生不利影响。可装入容器的药物质量取决于颗粒中存在的游离体积(即其孔隙率)、压缩粉末圆饼中颗粒之间的游离体积、和未被粉末圆饼占据的容器中的游离体积。在挤压密度测量中评估前两个游离体积。
通常用于灌装喷雾干燥粉末的滚筒或基于定量器的灌装机可形成预定形状的近圆柱形粉末丸,例如截锥体。当将圆饼放入容器中时,通常可观察到显著的游离体积。仔细设计圆饼尺寸和形状可灌装更大比例的容器体积,特别是在将多个圆饼灌装到容器中的情况下。或者,可在容器内压缩粉末,随后添加其他圆饼。其他粉末灌装策略可能适用于已知的技术,与本文中的传授内容一致。
喷雾干燥包括四个单元操作:原料制备、将原料雾化以产生微米大小的液滴、在热气中干燥液滴、和用袋式或旋风分离器收集干燥颗粒。本发明的喷雾干燥工艺的实施例包括后三个步骤,但是在一些实施例中,基本上可以同时执行这三个步骤中的两个甚至全部,因此在实践中,该工艺实际上可能会被认为是一个单步单元操作。
在本发明的实施例中,产生干粉颗粒的本发明的工艺包括制备溶液原料以及从原料中除去溶剂(例如通过喷雾干燥),以提供活性干粉颗粒。
在本发明的实施例中,原料包含至少一种溶解在水性液体原料中的活性成分。在某些实施例中,原料包括至少一种溶于水性溶剂或共溶剂系统中的活性制剂。在某些实施例中,原料包括悬浮或分散在溶剂或共溶剂系统中的至少一种活性制剂。
颗粒形成过程复杂,取决于初始液滴尺寸、原料浓度、和蒸发速率等工艺变量之间的耦合相互作用,以及溶解度、表面张力、粘度等制剂理化性质,以及形成颗粒壳的固体机械性能。
在某些实施例中,原料用双流体喷嘴雾化,如美国专利8936813和8524279中所述。在约1.5%w/w以上的固体负荷中,液滴的粒度分布可能显著变宽。
在某些实施例中,可以使用例如美国专利7967221和8616464中披露的平面膜雾化器实现狭窄的液滴尺寸分布,尤其是在较高的固体负载下。在某些实施例中,原料以0.1%-10%w/w(例如1%和5%w/w)之间的固体负荷雾化。
任何喷雾干燥步骤和/或所有喷雾干燥步骤均可使用常规设备进行,该设备用于制备供吸入施用的喷雾干燥颗粒。市售喷雾干燥器包括Büchi Ltd.和Niro Corp.生产的喷雾干燥器。
在某些实施例中,原料喷射到热过滤空气流中,该热过滤空气流蒸发溶剂并将干燥的产品输送到收集器。然后将废空气与溶剂一起排出。可以调整喷雾干燥器的操作条件,如入口和出口温度、进料速率、雾化压力、干燥空气的流速、和喷嘴配置,以便产生所需的粒度、含水量、和所得干燥颗粒的产率。根据本文传授内容,在使用熟练技术工人的前提下选择适当的装置和处理条件,无须过度实验就能完成。
活性制剂
本文中描述的活性制剂可能包括药剂、药物、化合物、物质组成、或其混合物,提供部分药理学(通常是有益的)作用。在本文中,该术语进一步包括在患者中产生局部或全身效应的任何生理或药理学活性物质。本文所述药物制剂中掺入的活性制剂可能是无机或有机化合物,其包括但不限于作用于以下当面的药物:外周神经、肾上腺素能受体、胆碱能受体、骨骼肌、心血管系统、平滑肌、血液循环系统、视物部位、神经效应器结合部位、内分泌和激素系统、免疫系统、生殖系统、骨骼系统、自身样系统、消化和排泄系统、组胺系统、以及中枢神经系统。可从以下药物中选择适当的活性制剂,例如,催眠药和镇静剂、镇定剂、呼吸系统药物、治疗哮喘和COPD的药物、抗惊厥药、肌肉松弛剂、抗帕金森病药(多巴胺拮抗剂)、镇痛药、抗炎药、抗焦虑药(抗焦虑药)、食欲抑制剂、抗偏头痛药、肌肉收缩剂、抗感染药(抗生素、抗病毒药、抗真菌药、疫苗)、抗关节炎药、抗疟药、止吐药、抗癫痫药、支气管扩张剂、细胞因子、生长因子、抗癌药物、抗血栓药、抗高血压药、心血管药物、抗心律失常药、抗氧化剂、抗哮喘药、激素制剂(包括避孕药、拟交感神经药、利尿剂、调脂药、抗雄激素制剂、抗寄生虫药、抗凝剂、肿瘤药、抗肿瘤药、降糖药、营养制剂和补充剂、生长补充剂、抗肠炎剂、疫苗、抗体、诊断剂、和造影剂。当通过吸入施用时,活性制剂可能在局部或全身起作用。在某些实施例中,活性制剂可能是安慰剂。
活性制剂可分为多种结构类别,其包括但不限于小分子、肽、多肽、抗体、抗体片段、蛋白质、多糖、类固醇、能够引起生理效应的蛋白质、核苷酸、寡核苷酸、多核苷酸、脂肪、电解质等。
在本发明的实施例中,活性制剂可能包括或包含用于治疗炎性或阻塞性气道疾病,如哮喘和/或COPD的任何活性药物成分。合适的活性成分包括长效β2激动剂(如沙美特罗、福莫特罗、茚达特罗、及其盐)、毒蕈碱拮抗剂(如噻托溴铵、格隆溴铵、及其盐)和皮质类固醇(包括布地奈德、环索奈德、氟替卡松、莫米松、及其盐)。合适的复方制剂包括(富马酸福莫特罗和布地奈德)、(昔萘酸沙美特罗和丙酸氟替卡松)、(昔萘酸沙美特罗和噻托溴铵)、(马来酸茚达特罗和格隆溴铵)和(茚达特罗和莫米松)。
药物制剂中的活性制剂量将是每单位剂量递送治疗有效量的活性制剂,以达到预期结果所需的剂量。在实践中,该量将因特定制剂、其活性、待治疗疾病的严重程度、患者人群、剂量要求、和预期治疗效果而存在很大差异。该组合物通常含有约1%(按重量计)至约100%(按重量计)的活性制剂,或通常含有约2%至约95%(按重量计)的活性剂量,或更通常含有约5%至85%(按重量计)的活性制剂,并且还将取决于组合物中所含添加剂的相对量。在本发明的实施例中,本发明的组合物对于以0.001mg/天至10g/天,例如从0.01mg/天至1g/天、或从0.1mg/天至500mg/天、或从1mg至1g/天的剂量递送的活性制剂特别有用。在本发明的实施例中,本发明的组合物可用于以每天和/或每剂10纳克-1000纳克的剂量递送的活性制剂。可以理解,在本文所述的制剂中可能会加入一种以上的活性制剂,并且术语“制剂”的使用绝不排除使用两种或多种此类制剂。
缓冲液/可选成分
众所周知,缓冲液用于pH控制,其作为在生理上相容的pH(即,用于改善耐受性)下递送药物以及提供有利于药物化学稳定性的溶液条件的手段。在本发明的制剂和工艺的实施例中,药物的pH环境可以通过将药物和缓冲液在同一颗粒中共同配制来控制。
缓冲液或pH调节剂,如组氨酸或磷酸盐,常用于冻干或喷雾干燥制剂中,以控制蛋白质的溶液和固态化学降解。甘氨酸可用于控制pH值以溶解喷雾干燥原料中的蛋白质(如胰岛素),控制pH值以确保固态时的室温稳定性,并提供接近中性pH值的粉末以帮助确保耐受性。优选的缓冲液包括:组氨酸、甘氨酸、醋酸盐、柠檬酸盐、磷酸盐、和三羟甲基氨基甲烷。
非限制性可选辅料包括盐(如氯化钠、氯化钙、枸橼酸钠)、抗氧化剂(如蛋氨酸)、减少溶液中蛋白质聚集的辅料(如精氨酸)、掩味剂、和旨在改善大分子物质吸收进入体循环的制剂(如富马酸二酮哌嗪)。
实验室规模喷雾干燥器的实例设置如下:进气口温度在80℃-160℃之间,如100℃-140℃之间;约40℃至100℃之间的出气口,例如约50℃至80℃;液体进料速率大约在1g/min至约20g/min之间,例如约3g/min至10g/min;干燥空气流速为约200L/min至约900L/min,如约300L/min至700L/min;雾化空气流速为约5L/min至50L/min之间,如10L/min至30L/min。喷雾干燥原料中的固体含量通常在0.5%w/v(5mg/ml)至10%w/v(100mg/ml)范围内,例如1.0%w/v至5.0%w/v。当然,设置将根据所用设备的规模和类型,以及所用溶剂系统的性质而不同。在任何情况下,使用以上方法和类似方法,均可形成直径适合气雾剂沉积到肺中的颗粒。
在本文的一些实例中,用于生成含有制剂的颗粒的工艺条件如下;固体含量为0.5%至4%;液体进料速率为每分钟2mL至5mL;干燥气体流速为每分钟200L至600L;雾化气流速为每分钟20L至30L;出口温度为40℃至70℃(其中,设定入口温度以生成规定的出口温度)。使用定制的实验室规模干燥器-超级Novartis喷雾干燥器(super Novartis SprayDryer(sNSD))进行喷雾干燥。sNSD的体积容量与市售实验室规模喷雾干燥器(如BucchiB290(Switzerland))的体积容量相似。
按照本发明过程的实施例制成的颗粒可以配制成多种方式递送,例如口服、经皮、皮下、皮内、鼻内、肺部、眼内等。在本发明的实施例中,颗粒制备和设计用于吸入给药。
吸入递送系统
本发明还提供了递送系统,其包括本发明的吸入器和干粉制剂。
在一个实施例中,本发明针对的是一种递送系统,其包括干粉吸入器和吸入用干粉制剂,后者包括含有治疗活性成分的喷雾干燥颗粒,其中体外肺总剂量为标称剂量的50%-100%w/w之间,例如至少为标称剂量的55%、或60%、或65%、或70%、或75%、或80%、或85%。
吸入器
适当的干粉吸入器(DPI)包括单位剂量吸入器,干粉储存在胶囊或泡罩中。使用前,患者将一粒或多粒胶囊或泡罩装入装置中。或者,如果剂量预先包装在铝箔泡罩中,例如在药筒、泡罩条、或转轮中,则考虑使用多剂量干粉吸入器。本发明的制剂适用于各种装置、装置阻力、和装置流速。在本发明的实施例中,本发明的产品和制剂增强了生物利用度。
PCT专利申请出版物WO 2017/125853中描述的诺华多剂量泡罩吸入器(Aspire)通常包括单个泡罩中包含的30份剂量,每个泡罩的体积可确保在泡罩内灌装高达约10mg的常规工程粉末。Aspire多剂量粉末吸入装置通常一个主体(主体包括一个内腔)和一个可拆卸插入主体内腔的药筒,所述药筒包括一个吸嘴,通过所述吸嘴可将雾化粉末药物递送给使用者,其中,所述药筒中装有一排容器(每个容器适合容纳一剂粉末药物)、一个用于打开每个泡罩的穿孔机构、和一个气雾剂引擎。
使用Novartis Pulmosol或Pulmosphere工程粉末,配合Aspire多剂量粉末吸入装置,可达到高达50%的载药量,使得总药物递送量高达150mg。这种递送量超过递送传统药物制剂的传统多剂量吸入器的近10倍。使用本项发明的制剂和方法,在Aspire多剂量粉末吸入装置的产品密度至少为50的情况下,与Pulmosol或Pulmosphere工程粉末相比,递送效率至少高2倍至3倍,因此是相同尺寸吸入装置的药物递送量的2倍至3倍。此外,这意味着比使用传统药物制剂的传统吸入器有20倍至30倍的潜在改善。此外,当然可以让吸入器相应变得更小,也能产生相同的150mg总药物递送量。
可使用各种容器盛装本文提到的粉末,最常见的容器是胶囊和泡罩。泡罩游离空间(空隙空间)相对百分比通常比胶囊更高,因此,使用传统的灌装设备,泡罩通常不能像胶囊一样按比例灌装至高容量。在某些情况下,这只是市售灌装设备的限制。然而,泡罩的实际产品密度可能因此而略低于计算得产品密度,并且可能进一步小于胶囊或其他可完全灌装容器的密度。
如本文所述,已发现可压缩性指数的这一新度量可作为一种有用的预测工具,用于估计容器中高填充致密颗粒的气雾剂化(参见公式2)。在本发明的实施例中,可压缩性指数小于20的粉末气雾剂性能最佳。采用快速干燥条件生产的粉末可压缩性指数较高(大于20),并且这些粉末的ED远低于可压缩性指数较低的粉末。可压缩性指数由振实密度(粉末填装的测量指数)和挤压密度(粉末压缩性的测量指数)推导得出。本发明包括颗粒的粉末实施例,设计意图是即使在对粉末施加较低作用力的情况下也能有效填充,因此,在较高作用力下预计不会出现装填密度的较大差异。因此,在较高作用力(此情况下使用真空)下装填密度增加的制剂表明,颗粒会发生物理性联锁,并且不易从容器中雾化。
治疗中使用
本发明的实施例提供了一种适用于吸入给药的任何疾病或病症的治疗方法。本发明的实施例特别适用于要达到如下理想或有利结果的药物/装置组合中的吸入给药,:使给药装置变小,和/或需要递送高有效载荷的分子变小。因此,本发明的实施例在一系列API效价范围内具有适用性。特别是,本发明的实施例对于需要更高和/或恒定剂量的API,例如抗生素和抗体(或抗体片段)很有用。非限制性的实例包括化疗药物、激素、吸入蛋白、siRNA、和其他多核苷酸,以及辅料含量高的药物制剂(如控释制剂)。本发明的制剂和方法效用的另一个具体实例是用于治疗感染性疾病的粉末吸入施用。
本发明的实施例提供了一种用于治疗呼吸、气道、和肺部疾病,例如阻塞性或炎症性气道疾病(如哮喘和慢性阻塞性肺病)的方法。该方法包括向有需要的受试者施用根据本文实施例制成的有效量的干粉制剂。
本发明的实施例提供了一种治疗全身性疾病(例如,感染性疾病)的方法,所述方法包括向有需要的受试者施用有效量的上述干粉制剂。本发明的组合物和方法的实施例使得可以通过单次吸入2号或或更小容器的内容物达到治疗剂量。
比较例-用于改善剂量的最新技术
比较例1
Novartis 装置是一种单位剂量、基于胶囊的低-中等阻力干粉吸入器(R=0.08cmH2O1/2L-1min)。治疗剂量包括吸入4粒2号羟丙甲纤维素胶囊的内容物,每粒胶囊含有约50mg喷雾干燥PulmoSphereTM粉末(约200mg粉末/治疗剂量)。原料药硫酸妥布霉素含有约85%w/w的粉末组分(即约170mg硫酸妥布霉素/治疗剂量或112mg妥布霉素/治疗剂量)。体外研究显示,约60%的粉末质量被递送至CF患者的肺部(即,约100mg硫酸妥布霉素)。
对于需要从单粒胶囊中吸入粉末的制剂,干粉制剂的施用时间约为1分钟,妥布霉素吸入粉末(4粒胶囊)的施用时间约为5分钟至6分钟。干粉的一个明显优势是,除了简单地擦拭吸嘴,装置不需要清洁和消毒。这将使上述讨论产品的每日治疗负担显著降低为2分钟至12分钟。但是,TOBI Podhaler中需要施用4粒离散胶囊,这增加了与胶囊处理和剂量制备相关的患者错误的可能性。因此,如有可能,在单个容器中灌装和施用整个标称剂量是有利的。
比较例2
Colobreathe含125mg纯微粉化粘菌酯,装于2号胶囊中。使用(PH&T,Milan,Italy)装置,通过3次或3次以上吸入施用。可认为Colbreathe药物装置组合代表了市售装置中的最高药物有效载荷。但是,单粒胶囊中递送的总剂量可提供的TLD较低,从而导致产品密度较低(见表4)。因此,施用治疗剂量至少需要3次吸入。
实验数据-根据本发明实施例的实例
实例1.含有抗体片段的喷雾干燥粉末
使用sNSD喷雾干燥器制备含有抗体片段(CSJ-117)的喷雾干燥粉末制剂。制剂含50%w/w CSJ-117、0-15%w/w三亮氨酸(作为成壳剂)、25%-35%w/w糖类和3%-10%w/w缓冲剂。在快速干燥条件下对一些样品进行喷雾干燥,以生成低密度颗粒。与快速干燥条件一致的喷雾干燥器参数包括固体含量1%至2%,液体进料速率5mL/min至10mL/min;干燥气体流速为每分钟500L至600L;雾化气体流速为每分钟20L至30L,出口温度为60℃至70℃(其中设定入口温度以生成规定的出口温度)。在缓慢干燥条件下对其他样品进行喷雾干燥,以生成更致密的颗粒。与缓慢干燥条件一致的喷雾干燥器参数包括固体含量为1%至3.5%,液体进料速率为2.5mL/min至5mL/min;干燥气体流速为每分钟200L至400L;雾化气体流速为每分钟20L至30L,出口温度为50℃至55℃(其中设定入口温度以生成规定的出口温度)。
不含成壳辅料的抗体片段(CSJ117)喷雾剂干粉的特征为具有光滑颗粒形态和比表面积(SSA)的球形颗粒。SSA是固体的特性,定义为单位质量材料的总表面积。通常,如果颗粒的皱褶或多孔性较差,则表面积更大。本文报告的SSA使用Brunauer-Emmett-Teller(BET)分析方法进行测量。将等份粉末(约500mg)加入1mL体积样品管中,在25℃下脱气960分钟,然后进行分析。氮是分析吸收性物质,在运行MicroActive软件的MicromeriticsTri-Star II表面积和孔隙率分析仪上进行分析。无成壳剂的颗粒的BET SSA为6.35m2/g,振实密度为0.32g/ml(见表2,样品7)。向制剂(样品10)中加入15%w/w的成壳辅料三亮氨酸,得到皱褶状颗粒形态,并将SSA增加至11.8m2/g。得到的振实密度为0.31g/ml,与样品7的振实密度非常相似。据认为,由于颗皱褶纹的增加而导致的颗粒密度的降低被颗粒间内聚力降低导致的颗粒间空隙空间减少所抵消。SSA越高,粉末的振实密度越低,因为颗粒密度降低的影响超过了颗粒填充的改善。令人惊讶的是,加入少量三亮氨酸(2.5%)可导致振实密度急剧增加至约0.60g/ml(图8和表2,样品1和样品2)。这一发现出人意料,因为现有技术喷雾干燥工程颗粒表现出高可压缩性(大于约20),因为它们为皱褶状且密度低。现有的工程颗粒设计成颗粒密度较低。相比之下,本发明旨在增加粉末密度和装填密度,以便将更多的粉末灌装到给定尺寸的容器中。如果颗粒未按照本发明的实施例进行适当设计,则粉末变得非常内聚(重力不稳定),并且不会产生理想的气雾剂填充特性。因此,根据本发明的实施例,粉末产生的颗粒更致密,皱褶更少,但保持良好的气雾剂性质,包括分散性。尽管相对于不含成壳辅料的颗粒,颗粒的SSA未显著增加,但仍发生了这种情况(图7A)。
据信少量的成壳剂降低了颗粒间内聚力,使散装粉末中的颗粒填充更紧密,尽管其Pe较低。与在快速干燥条件下制备的批次相比,在缓慢干燥条件下制备的所有批次均显示出较高的振实密度(表2)。由于三亮氨酸含量的进一步增加会由于颗粒的表面皱褶增加而降低振实密度,因此严格控制向制剂中添加的成壳剂的量。当然,这对于高产品密度制剂的目标并不可取的。
在表2报告的数据中,其他趋势显而易见。三亮氨酸含量低和干燥速率缓慢的颗粒表现出较高的振实密度、较低的压缩性指数、较高的喷射剂量、以及与用于高灌装质量的便携式干粉吸入器更为一致的吸空模式(见图5)。因此,样品1至样品6采用包含缓慢干燥速率(低Pe)的工艺制备,样品7至样品12则采用包含快速干燥速率(高Pe)的工艺制备。低Pe粉末(样品4)的平均ED为86%,相比之下,高Pe粉末(样品8)的平均ED为58%。
表2.包含抗体片段的喷雾干燥粉末的物理特性。样品1至样品6为在缓慢干燥条件(低Pe)下制备的粉末,干燥器出口温度为55℃,干燥空气流速为300L/min。样品7至样品12是使用干燥器出口在快速干燥条件(高Pe)下制备的粉末
温度70℃,干燥空气流速600L/min。
在上表2中,可以看出样品1至样品5具有理想密度,可压缩性指数较低,相应的喷射剂量较高。样品1至样品5含有2.5%至5%的三亮氨酸。样品6含有15%的三亮氨酸,密度不足,可压缩性指数相对较高(大于20)。样品8在快速干燥条件下干燥也具有较高的可压缩性指数。除样品9具有较低的可压缩性指数外,样品9至样品12还含有高水平(10%-15%)的三亮氨酸,并且具有相应的高可压缩性指数。未测量样品6至样品7和样品10至样品12的释放剂量,因为未达到目标150mg灌装质量。
使用Novartis Podhaler干粉吸入器检测表2样品的喷射剂量递送性能。将目标为150mg的各粉末制剂灌装(或尝试灌装)至2号HPMC胶囊中。150mg目标灌装质量为粉末灌装体积的80%,挤压密度为0.5mg/mL。以90L/min的空气流速将其排放到定制的剂量均匀性采样装置(DUSA)中1.3秒,以抽取2L空气,使整个装置的压力降约为2kPa。报告的ED值为3次重复测定的平均值,表示为占灌装质量的百分比。
实例2.含小分子的喷雾干燥粉末
使用实验室规模喷雾干燥器(定制设计超级Novartis喷雾干燥器,sNSD),制备左旋氟沙星和硫酸庆大霉素两种抗生素,和一种β2-肾上腺素能激动剂(硫酸沙丁胺醇)的喷雾干燥制剂。
表3.制剂详细信息,以及由抗生素和β2-肾上腺素能激动剂组成的喷雾干燥粉末的物理特性。在缓慢干燥条件(低Pe)下制备样品,干燥器出口温度为50℃至55℃,干燥空气流速为300L/min。
使用Novartis Podhaler干粉吸入器,检测表3中样品的喷射剂量递送性能。将目标为150mg的各粉末制剂灌装(或尝试灌装)至2号HPMC胶囊中。150mg目标灌装质量为粉末灌装体积的80%,挤压密度为0.5mg/mL。以90L/min的空气流速将其排放到定制的剂量均匀性采样装置(DUSA)中1.3秒,以抽取2L空气,使整个装置的压力降约为2kPa。报告的ED值为3次重复测定的平均值,表示为占灌装质量的百分比。
比较例3.各种高剂量药械组合的计算产品密度
下表4显示了目前上市的几种高剂量制剂(定义为TLD大于10mg)的产品密度数据,以及第三方专有盐制剂技术的数据,该技术利用致密盐增加颗粒密度以实现高剂量递送。目前上市销售的TLD大于10mg的高剂量制剂包括TOBI Podhaler(Novartis)和Colobreathe(Forest)。根据本文方法测定,这些产品的产品密度约为30mg/ml至50mg/ml。根据公开报告的数据,计算使用专有盐制剂技术配制的左氧氟沙星的产品密度。
下表4显示了各种传统和/或现有药物/装置组合的计算产品密度。
表4.
与这些上市产品的产品密度相比,本发明的喷雾干燥制剂产品密度更高,密度在150mg/ml和250mg/ml之间。灌装单个容器(0.095mL)时可达到上述值,无需任何剂量压缩或使用机械方式来增加灌装密度。也就是说,根据本发明的实施例,产品密度的增加完全是通过本发明制剂实现的。
本发明粉末的一个重要方面是TLD高,以标称剂量的百分比表示时,约为60%w/w或更高。很明显,成壳辅料的存在和低Pe制剂的较小几何尺寸,使便携式干粉吸入器(例如Novartis或BreezhalertmDPI)能够实现高递送效率。
下表5显示了根据本发明实施例制备的制剂的计算产品密度。表5中的每种制剂均按照本发明的实例1或实例2制备,并且包括所示的活性成分。
表5
| 活性 | API剂量 | 容器体积 | TLD | TLD | 产品密度 | 实例 |
| mg | mL | mg | %w/w | mg/mL | ||
| 抗体片段 | 75 | 0.37 | 54.9 | 74 | 148.4 | 1 |
| 左氧氟沙星 | 120 | 0.37 | 82.5 | 69 | 223.8 | 2 |
| 庆大霉素 | 45 | 0.37 | 33.4 | 74 | 90.2 | 2 |
| 硫酸沙丁胺醇 | 45 | 0.37 | 33.4 | 74 | 90.2 | 2 |
如表5所示,通过将载药量增加至80%-90%,产品密度可增加至223mg/mL或更高。随机选择并展示了表5中所示的API和载药量百分比,以证明本发明制剂的性能不受API选择或载药量的影响。
除了在一次性或单位剂量装置中的高有效载荷递送外,本发明的粉末在多剂量装置(MD-DPI)中具有显著的优势。此类装置中的一个关键设计约束是可移植性,这取决于装置的总体大小。反之这又会控制可能的剂量数量,并限制单个给药容器的大小(例如,泡罩腔大小)。本发明的粉末的产品密度使得能够在容器体积仅为0.1ml的多剂量干粉吸入器中灌装约10mg的质量和约7mg的TLD。这使得可以将新类别药物引入MD-DPI中。
图9是本发明实施例中四种不同产品密度在70%TLD下的标称药物质量与容器体积的曲线图。在该图上额外绘制了三个常规产品密度点:(i)Novartis的妥布霉素吸入粉雾剂(标记为“TIP”);(ii)含有抗体片段的制剂(标记为“FAB”);和(iii)含有左氧氟沙星的制剂(标记为“Levo”)。平行于X轴的第一条虚线代表小型便携式多剂量泡罩吸入器的假定泡罩容器,体积为0.1mL。两条平行虚线分别代表2号和3号胶囊的体积。基于这些数据,在60%产品密度、80%产品密度和100mg/ml产品密度下,典型药物质量分别约为8mg、11mg和40mg。
或者,可以将这些粉末引入单位剂量或单剂量一次性DPI中。在基于胶囊的吸入器(使用2号胶囊)中,可达到约100mg级别的TLD。对于0号胶囊,可达到约200mg的TLD。这样使得可以通过从单个容器中吸入内容物来有效地递送效力最低的药物(例如抗感染药)。对于2号胶囊,大多数受试者单次吸入即可吸空胶囊内容物,前提是他们能达到至少约1.2L的吸入体积。
已对本发明进行了充分描述,本发明的方法和制剂可在广泛和等同的条件、制剂、和其他参数范围内进行,而不会偏离本发明的范围或其任何实施例,这对于本领域的普通技术人员来说是可理解的。
本文引用的所有专利和出版物均通过援引以其全部内容并入。任何出版物的引用都是为了在申请日之前公开,并且不应解释为承认该出版物是现有技术。
Claims (24)
1.一种含有可通过干粉吸入器递送的颗粒的喷雾干燥药物粉末组合物,所述组合物包含活性制剂以及约0.5%至10%按重量计的成壳辅料,其中所述粉末的特征为产品密度大于50mg/ml。
2.如权利要求1所述的组合物,其中所述容器包含体积容量为0.05mL至0.2mL的泡罩。
3.如权利要求1所述的组合物,其中所述容器包含体积容量为0.21mL至0.5mL的胶囊,并且其中所述粉末特征为产品密度大于80mg/mL。
4.如权利要求1所述的组合物,其中所述成壳辅料包含亮氨酸或三亮氨酸。
5.如权利要求1所述的组合物,其中所述颗粒的特征是皱褶度为1至3。
6.如权利要求1所述的组合物,其中所述产品密度大于100mg/mL。
7.如权利要求1所述的组合物,其中所述粉末在具有以下特征的工艺条件下喷雾干燥:佩克莱数为0.5至3。
8.如权利要求1所述的组合物,其中所述成壳辅料以使得在所述成壳辅料存在下所述颗粒的比表面积与不含成壳剂时的相同大小颗粒的比表面积相当的量存在。
9.如权利要求1所述的组合物,其中所述粉末的特征为可压缩性指数小于20。
10.一种喷雾干燥药物组合物,所述组合物包含粉末,所述粉末包含通过以下工艺制成的颗粒,所述工艺包括:
制备包含溶剂、活性制剂和0.5%-10%的成壳辅料的原料;
在佩克莱数为0.5至3的工艺条件下对所述原料进行喷雾干燥;并且,
收集所得粉末,其中所述粉末的特征为产品密度大于50mg/mL,以及可压缩性指数小于20。
11.如权利要求10所述的组合物,其中所述原料进一步包含一种或多种缓冲液、玻璃成型剂、pH调节剂、和辅料。
12.如权利要求10所述的粉末制剂,其中所述成壳辅料包括亮氨酸或三亮氨酸。
13.如权利要求10所述的粉末,其中所述成壳辅料以使得在所述成壳辅料存在下所述颗粒的比表面积与不含成壳辅料时的相同大小颗粒的比表面积相当的量存在。
14.一种将包含治疗剂量的活性药物制剂的多个颗粒递送至受试者肺部的方法,所述方法包括:
a.制备溶剂中含活性制剂和成壳辅料的溶液,其中所述成壳辅料以2%至5%存在,
b.对所述溶液进行喷雾干燥以获得含有微粒的粉末,其中所述粉末的特征为产品密度至少约为80mg/mL,
c.将喷雾干燥粉末包装在容器中;以及
d.提供吸入器,所述吸入器具有从所述容器中提取所述粉末的装置,其中当通过吸入进行施用时,所述粉末的肺沉积至少为70%。
15.一种治疗疾病或病症的方法,所述方法包括向有需要受试者施用有效量的包含如权利要求1的干粉制剂。
16.如权利要求15所述的方法,其中所述疾病或病症包括阻塞性或炎症性气道疾病。
17.如权利要求15所述的方法,其中所述疾病或病症包括感染性疾病,并且其中治疗剂量以单个2号或更小的容器递送。
18.一种递送系统,所述递送系统包含如权利要求1所述的吸入器和干粉制剂。
19.如权利要求18所述的递送系统,其中所述吸入器包括基于泡罩的多剂量吸入器。
20.如权利要求1所述的组合物,其中所述活性制剂包括抗生素。
21.一种多剂量粉末吸入装置和药物组合,其包括:
包含内腔的主体;和可拆卸插入所述主体的内腔的药筒,所述药筒包括吸嘴,通过所述吸嘴可将雾化粉末药物递送给使用者,其中所述药筒中装有一排容器、每个容器适合容纳一剂粉末药物,用于打开每个泡罩的穿孔机构,和气雾剂引擎;以及
每个容器内包含的粉末药物,其中所述粉末药物包括喷雾干燥药物粉末组合物,所述组合物包括可从干粉吸入器递送的颗粒,所述组合物包括活性制剂以及约0.5%-10%按重量计的成壳辅料,其中所述粉末的特征为产品密度大于50mg/ml。
22.如权利要求21所述的吸入装置和药物组合,其中总药物递送量大于约300mg。
23.如权利要求21所述的吸入装置和药物组合,其中所述容器为体积小于0.95mL的泡罩。
24.如权利要求21所述的吸入装置和药物组合,其中容器为体积小于0.95mL的泡罩,并且从所述泡罩中可递送至少5mg的肺总剂量。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201862622464P | 2018-01-26 | 2018-01-26 | |
| US62/622,464 | 2018-01-26 | ||
| PCT/IB2019/050607 WO2019145897A1 (en) | 2018-01-26 | 2019-01-24 | High dose delivery of inhaled therapeutics |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN111526870A true CN111526870A (zh) | 2020-08-11 |
Family
ID=65635769
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201980007046.7A Pending CN111526870A (zh) | 2018-01-26 | 2019-01-24 | 吸入治疗药物的高剂量递送 |
Country Status (14)
| Country | Link |
|---|---|
| US (1) | US20210069106A1 (zh) |
| EP (1) | EP3743045A1 (zh) |
| JP (1) | JP2021510723A (zh) |
| KR (1) | KR20200115560A (zh) |
| CN (1) | CN111526870A (zh) |
| AR (1) | AR114308A1 (zh) |
| AU (2) | AU2019212586C1 (zh) |
| BR (1) | BR112020014793A2 (zh) |
| CA (1) | CA3089439A1 (zh) |
| CL (1) | CL2020001939A1 (zh) |
| IL (1) | IL276241A (zh) |
| MX (1) | MX2020007745A (zh) |
| RU (1) | RU2020127882A (zh) |
| WO (1) | WO2019145897A1 (zh) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AR120309A1 (es) | 2019-10-28 | 2022-02-09 | Medimmune Ltd | Formulaciones de polvo seco de anticuerpos que se unen a la linfopoyetina del estroma tímico (tslp) y métodos de uso de las mismas |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20170066823A1 (en) * | 2015-09-09 | 2017-03-09 | Matthew John EDWARDS | Thymic stromal lymphopoietin (tslp)-binding molecules and methods of using the molecules |
| CN108348459A (zh) * | 2015-09-09 | 2018-07-31 | 诺华股份有限公司 | 靶向递送喷雾干燥制剂到肺 |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1446104B2 (en) | 2001-11-01 | 2011-08-03 | Novartis AG | Spray drying methods |
| MXPA05007154A (es) | 2002-12-30 | 2005-09-21 | Nektar Therapeutics | Atomizador prepeliculizacion. |
| KR101306384B1 (ko) * | 2004-08-23 | 2013-09-09 | 맨카인드 코포레이션 | 약물 전달용 디케토피페라진염, 디케토모르포린염 또는디케토디옥산염 |
| US8900555B2 (en) * | 2006-07-27 | 2014-12-02 | Nektar Therapeutics | Insulin derivative formulations for pulmonary delivery |
| TR200907236A2 (tr) * | 2009-09-23 | 2011-04-21 | Bi̇lgi̇ç Mahmut | Tiotropyum kuru toz formülasyonunun blister ambalajda taşınması. |
| JOP20120023B1 (ar) * | 2011-02-04 | 2022-03-14 | Novartis Ag | صياغات مساحيق جافة من جسيمات تحتوي على واحد أو اثنين من المواد الفعالة لعلاج امراض ممرات الهواء الانسدادية او الالتهابية |
| CN107596518B (zh) * | 2012-02-29 | 2021-04-23 | 普马特里克斯营业公司 | 可吸入干粉剂 |
| WO2014144364A1 (en) * | 2013-03-15 | 2014-09-18 | Children's Medical Center Corporation | Gas-filled stabilized particles and methods of use |
| RU2727239C2 (ru) * | 2016-01-19 | 2020-07-21 | Новартис Аг | Многодозовый ингалятор |
| SG11201806304PA (en) * | 2016-01-29 | 2018-08-30 | Mannkind Corp | Dry powder inhaler |
-
2019
- 2019-01-24 JP JP2020540345A patent/JP2021510723A/ja active Pending
- 2019-01-24 AU AU2019212586A patent/AU2019212586C1/en active Active
- 2019-01-24 KR KR1020207024324A patent/KR20200115560A/ko not_active Application Discontinuation
- 2019-01-24 EP EP19708669.7A patent/EP3743045A1/en not_active Withdrawn
- 2019-01-24 MX MX2020007745A patent/MX2020007745A/es unknown
- 2019-01-24 CN CN201980007046.7A patent/CN111526870A/zh active Pending
- 2019-01-24 BR BR112020014793-1A patent/BR112020014793A2/pt not_active Application Discontinuation
- 2019-01-24 US US16/963,678 patent/US20210069106A1/en not_active Abandoned
- 2019-01-24 WO PCT/IB2019/050607 patent/WO2019145897A1/en unknown
- 2019-01-24 CA CA3089439A patent/CA3089439A1/en active Pending
- 2019-01-24 RU RU2020127882A patent/RU2020127882A/ru unknown
- 2019-01-24 AR ARP190100160A patent/AR114308A1/es unknown
-
2020
- 2020-07-23 IL IL276241A patent/IL276241A/en unknown
- 2020-07-23 CL CL2020001939A patent/CL2020001939A1/es unknown
-
2022
- 2022-04-05 AU AU2022202278A patent/AU2022202278A1/en active Pending
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20170066823A1 (en) * | 2015-09-09 | 2017-03-09 | Matthew John EDWARDS | Thymic stromal lymphopoietin (tslp)-binding molecules and methods of using the molecules |
| CN108348459A (zh) * | 2015-09-09 | 2018-07-31 | 诺华股份有限公司 | 靶向递送喷雾干燥制剂到肺 |
Also Published As
| Publication number | Publication date |
|---|---|
| RU2020127882A3 (zh) | 2022-02-28 |
| KR20200115560A (ko) | 2020-10-07 |
| AU2019212586A1 (en) | 2020-07-09 |
| BR112020014793A2 (pt) | 2020-12-08 |
| MX2020007745A (es) | 2020-09-25 |
| IL276241A (en) | 2020-09-30 |
| AU2022202278A1 (en) | 2022-04-21 |
| CL2020001939A1 (es) | 2021-01-04 |
| AU2019212586C1 (en) | 2022-04-28 |
| CA3089439A1 (en) | 2019-08-01 |
| WO2019145897A1 (en) | 2019-08-01 |
| AU2019212586B2 (en) | 2022-01-06 |
| US20210069106A1 (en) | 2021-03-11 |
| RU2020127882A (ru) | 2022-02-28 |
| EP3743045A1 (en) | 2020-12-02 |
| AR114308A1 (es) | 2020-08-19 |
| JP2021510723A (ja) | 2021-04-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6721629B2 (ja) | 肺使用のための高服用量のレボドパを含むカプセル | |
| JP4368198B2 (ja) | 肺送達用の改良された粒状組成物 | |
| EP2494962B1 (en) | Pulmonary delivery for levodopa | |
| US8614255B2 (en) | Pulmonary pharmaceutical formulations | |
| JP7236485B2 (ja) | 三流体ノズルを用いた吸入用複合粒子の製造方法 | |
| ITMI20012174A1 (it) | Polvere per somministrazione nasale di farmaci | |
| CN107205936B (zh) | 包含至少一种通过喷雾干燥得到的增加制剂稳定性的干粉的组合物 | |
| US20160317522A1 (en) | Inhalable sustained therapeutic formulations | |
| AU2022202278A1 (en) | High Dose Delivery of Inhaled Therapeutics | |
| Braga et al. | Spray dried composite powders: capsule filling process optimization and aerodynamic performance characterization |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| WD01 | Invention patent application deemed withdrawn after publication |
Application publication date: 20200811 |