CN106857504B - 一种抑制和/或破坏生物膜的方法 - Google Patents
一种抑制和/或破坏生物膜的方法 Download PDFInfo
- Publication number
- CN106857504B CN106857504B CN201710073483.1A CN201710073483A CN106857504B CN 106857504 B CN106857504 B CN 106857504B CN 201710073483 A CN201710073483 A CN 201710073483A CN 106857504 B CN106857504 B CN 106857504B
- Authority
- CN
- China
- Prior art keywords
- biofilm
- staphylococcus aureus
- sample
- bacteria
- forming
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 238000000034 method Methods 0.000 title claims abstract description 48
- 230000002401 inhibitory effect Effects 0.000 title claims abstract description 20
- 239000012528 membrane Substances 0.000 title abstract 5
- 150000001875 compounds Chemical class 0.000 claims abstract description 37
- 241000191967 Staphylococcus aureus Species 0.000 claims description 36
- 239000007788 liquid Substances 0.000 claims description 18
- 238000005286 illumination Methods 0.000 claims description 14
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 5
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 5
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 claims description 3
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 claims description 3
- 229910052794 bromium Inorganic materials 0.000 claims description 3
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 claims description 3
- 241000191940 Staphylococcus Species 0.000 claims 1
- 230000015572 biosynthetic process Effects 0.000 abstract description 13
- 229910052736 halogen Inorganic materials 0.000 abstract description 3
- 150000002367 halogens Chemical class 0.000 abstract description 3
- 241000894006 Bacteria Species 0.000 description 71
- 239000000523 sample Substances 0.000 description 36
- 239000000243 solution Substances 0.000 description 24
- 230000001580 bacterial effect Effects 0.000 description 18
- 239000003642 reactive oxygen metabolite Substances 0.000 description 10
- 239000007787 solid Substances 0.000 description 10
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 9
- 230000032770 biofilm formation Effects 0.000 description 9
- 230000000694 effects Effects 0.000 description 9
- 241000233866 Fungi Species 0.000 description 8
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 8
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 7
- 230000005764 inhibitory process Effects 0.000 description 7
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 6
- 230000003993 interaction Effects 0.000 description 6
- 239000000047 product Substances 0.000 description 6
- 238000010186 staining Methods 0.000 description 6
- 206010059866 Drug resistance Diseases 0.000 description 5
- 102000010834 Extracellular Matrix Proteins Human genes 0.000 description 5
- 108010037362 Extracellular Matrix Proteins Proteins 0.000 description 5
- 239000013078 crystal Substances 0.000 description 5
- 238000012258 culturing Methods 0.000 description 5
- 210000002744 extracellular matrix Anatomy 0.000 description 5
- 238000003384 imaging method Methods 0.000 description 5
- 230000008569 process Effects 0.000 description 5
- 108090000623 proteins and genes Proteins 0.000 description 5
- 102000004169 proteins and genes Human genes 0.000 description 5
- VFNKZQNIXUFLBC-UHFFFAOYSA-N 2',7'-dichlorofluorescein Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC(Cl)=C(O)C=C1OC1=C2C=C(Cl)C(O)=C1 VFNKZQNIXUFLBC-UHFFFAOYSA-N 0.000 description 4
- XDFNWJDGWJVGGN-UHFFFAOYSA-N 2-(2,7-dichloro-3,6-dihydroxy-9h-xanthen-9-yl)benzoic acid Chemical compound OC(=O)C1=CC=CC=C1C1C2=CC(Cl)=C(O)C=C2OC2=CC(O)=C(Cl)C=C21 XDFNWJDGWJVGGN-UHFFFAOYSA-N 0.000 description 4
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 4
- 210000004027 cell Anatomy 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 230000006378 damage Effects 0.000 description 4
- 230000001066 destructive effect Effects 0.000 description 4
- 238000001514 detection method Methods 0.000 description 4
- 238000010586 diagram Methods 0.000 description 4
- 150000004676 glycans Chemical class 0.000 description 4
- 230000002209 hydrophobic effect Effects 0.000 description 4
- 102000039446 nucleic acids Human genes 0.000 description 4
- 108020004707 nucleic acids Proteins 0.000 description 4
- 150000007523 nucleic acids Chemical class 0.000 description 4
- 229920001282 polysaccharide Polymers 0.000 description 4
- 239000005017 polysaccharide Substances 0.000 description 4
- 238000005160 1H NMR spectroscopy Methods 0.000 description 3
- OJMAUBALNSWGDC-UHFFFAOYSA-N 2,7-dibromo-9,9-bis(6-bromohexyl)fluorene Chemical compound C1=C(Br)C=C2C(CCCCCCBr)(CCCCCCBr)C3=CC(Br)=CC=C3C2=C1 OJMAUBALNSWGDC-UHFFFAOYSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 238000002835 absorbance Methods 0.000 description 3
- 125000000217 alkyl group Chemical group 0.000 description 3
- 239000003708 ampul Substances 0.000 description 3
- 210000000170 cell membrane Anatomy 0.000 description 3
- 230000005284 excitation Effects 0.000 description 3
- 238000000799 fluorescence microscopy Methods 0.000 description 3
- 244000005700 microbiome Species 0.000 description 3
- 230000002829 reductive effect Effects 0.000 description 3
- 239000012265 solid product Substances 0.000 description 3
- 239000000758 substrate Substances 0.000 description 3
- 238000005406 washing Methods 0.000 description 3
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- 241000222122 Candida albicans Species 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- 241000192125 Firmicutes Species 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 229940095731 candida albicans Drugs 0.000 description 2
- 238000003235 crystal violet staining Methods 0.000 description 2
- 238000010790 dilution Methods 0.000 description 2
- 239000012895 dilution Substances 0.000 description 2
- 239000012153 distilled water Substances 0.000 description 2
- 239000000975 dye Substances 0.000 description 2
- 150000002632 lipids Chemical class 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 230000003287 optical effect Effects 0.000 description 2
- 239000012074 organic phase Substances 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 230000004083 survival effect Effects 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- JRMUNVKIHCOMHV-UHFFFAOYSA-M tetrabutylammonium bromide Chemical compound [Br-].CCCC[N+](CCCC)(CCCC)CCCC JRMUNVKIHCOMHV-UHFFFAOYSA-M 0.000 description 2
- GETQZCLCWQTVFV-UHFFFAOYSA-N trimethylamine Chemical compound CN(C)C GETQZCLCWQTVFV-UHFFFAOYSA-N 0.000 description 2
- 239000012137 tryptone Substances 0.000 description 2
- 230000003313 weakening effect Effects 0.000 description 2
- CRDAMVZIKSXKFV-FBXUGWQNSA-N (2-cis,6-cis)-farnesol Chemical compound CC(C)=CCC\C(C)=C/CC\C(C)=C/CO CRDAMVZIKSXKFV-FBXUGWQNSA-N 0.000 description 1
- 239000000260 (2E,6E)-3,7,11-trimethyldodeca-2,6,10-trien-1-ol Substances 0.000 description 1
- KZPYGQFFRCFCPP-UHFFFAOYSA-N 1,1'-bis(diphenylphosphino)ferrocene Chemical compound [Fe+2].C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1 KZPYGQFFRCFCPP-UHFFFAOYSA-N 0.000 description 1
- SGRHVVLXEBNBDV-UHFFFAOYSA-N 1,6-dibromohexane Chemical compound BrCCCCCCBr SGRHVVLXEBNBDV-UHFFFAOYSA-N 0.000 description 1
- 238000001644 13C nuclear magnetic resonance spectroscopy Methods 0.000 description 1
- AVXFJPFSWLMKSG-UHFFFAOYSA-N 2,7-dibromo-9h-fluorene Chemical compound BrC1=CC=C2C3=CC=C(Br)C=C3CC2=C1 AVXFJPFSWLMKSG-UHFFFAOYSA-N 0.000 description 1
- 229920001817 Agar Polymers 0.000 description 1
- 241000813307 Candida albicans 3153A Species 0.000 description 1
- 241000675278 Candida albicans SC5314 Species 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- 229920000742 Cotton Polymers 0.000 description 1
- 229920002444 Exopolysaccharide Polymers 0.000 description 1
- 108050001049 Extracellular proteins Proteins 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- SXRSQZLOMIGNAQ-UHFFFAOYSA-N Glutaraldehyde Chemical compound O=CCCCC=O SXRSQZLOMIGNAQ-UHFFFAOYSA-N 0.000 description 1
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 1
- 101150003085 Pdcl gene Proteins 0.000 description 1
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 230000001464 adherent effect Effects 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 239000008272 agar Substances 0.000 description 1
- 230000003321 amplification Effects 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 230000000845 anti-microbial effect Effects 0.000 description 1
- 229940124350 antibacterial drug Drugs 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 230000006907 apoptotic process Effects 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- 235000015278 beef Nutrition 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 230000003115 biocidal effect Effects 0.000 description 1
- 239000012620 biological material Substances 0.000 description 1
- 239000003054 catalyst Substances 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 239000000460 chlorine Substances 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 239000002131 composite material Substances 0.000 description 1
- 238000001218 confocal laser scanning microscopy Methods 0.000 description 1
- 230000001276 controlling effect Effects 0.000 description 1
- 230000002596 correlated effect Effects 0.000 description 1
- 239000006059 cover glass Substances 0.000 description 1
- 239000012043 crude product Substances 0.000 description 1
- 230000000254 damaging effect Effects 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 238000001493 electron microscopy Methods 0.000 description 1
- 230000009881 electrostatic interaction Effects 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 239000000284 extract Substances 0.000 description 1
- 229940043259 farnesol Drugs 0.000 description 1
- 229930002886 farnesol Natural products 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 239000010931 gold Substances 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 238000011081 inoculation Methods 0.000 description 1
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical compound II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 description 1
- 230000001678 irradiating effect Effects 0.000 description 1
- 230000002147 killing effect Effects 0.000 description 1
- 230000035800 maturation Effects 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 239000000203 mixture Substances 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 238000003199 nucleic acid amplification method Methods 0.000 description 1
- 239000002773 nucleotide Substances 0.000 description 1
- 125000003729 nucleotide group Chemical group 0.000 description 1
- 235000015097 nutrients Nutrition 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 229910052763 palladium Inorganic materials 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 239000003208 petroleum Substances 0.000 description 1
- 239000003444 phase transfer catalyst Substances 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- 238000002428 photodynamic therapy Methods 0.000 description 1
- TYJJADVDDVDEDZ-UHFFFAOYSA-M potassium hydrogencarbonate Chemical compound [K+].OC([O-])=O TYJJADVDDVDEDZ-UHFFFAOYSA-M 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 238000010791 quenching Methods 0.000 description 1
- 230000018612 quorum sensing Effects 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 238000010898 silica gel chromatography Methods 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 239000008223 sterile water Substances 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- CRDAMVZIKSXKFV-UHFFFAOYSA-N trans-Farnesol Natural products CC(C)=CCCC(C)=CCCC(C)=CCO CRDAMVZIKSXKFV-UHFFFAOYSA-N 0.000 description 1
- AAAQKTZKLRYKHR-UHFFFAOYSA-N triphenylmethane Chemical group C1=CC=CC=C1C(C=1C=CC=CC=1)C1=CC=CC=C1 AAAQKTZKLRYKHR-UHFFFAOYSA-N 0.000 description 1
- 229910021642 ultra pure water Inorganic materials 0.000 description 1
- 239000012498 ultrapure water Substances 0.000 description 1
- 230000000007 visual effect Effects 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N25/00—Biocides, pest repellants or attractants, or plant growth regulators, characterised by their forms, or by their non-active ingredients or by their methods of application, e.g. seed treatment or sequential application; Substances for reducing the noxious effect of the active ingredients to organisms other than pests
Landscapes
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Health & Medical Sciences (AREA)
- Toxicology (AREA)
- Pest Control & Pesticides (AREA)
- Plant Pathology (AREA)
- Agronomy & Crop Science (AREA)
- Engineering & Computer Science (AREA)
- Dentistry (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Environmental Sciences (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Abstract
Description
技术领域
本发明涉及生物膜领域,具体地,涉及一种抑制和/或破坏生物膜的方法。
背景技术
生物膜是指微生物为了适应环境,粘附于非生物或活性组织表面,分泌大量的多糖、蛋白质和核酸等不均一的胞外基质,将菌体自身包裹在其中而形成的大量菌体聚集膜样物,是菌体在自然界中一种常见的生存状态。生物膜的形成分为以下几个阶段:1、初始粘附,游离的细菌粘附在固体基质表面,并分泌胞外核酸促进粘附。2、微菌落的形成,粘附的细菌经过繁殖扩增形成微菌落,并分泌胞外蛋白促进粘附。3、生物膜成熟,菌体进一步生长并分泌大量的胞外基质,主要成分为胞外多糖,蛋白质,胞外核酸和脂类,形成成熟的生物膜。4、生物膜凋亡,生物膜成熟后,膜内细菌仍然增殖,在微菌落生长后期,生物膜破裂,释放出游离的细菌,可进入下一个生物膜形成周期。相对于游离细菌,生物膜内菌体被胞外基质包裹,形成一层厚厚的生物屏障,阻碍抗菌药物的渗透,增强菌体对不良环境的耐受性。即使抗菌药物渗透到生物膜内部,内部的细菌由于营养物质缺乏、氧气不足等因素生长缓慢或处于休眠期,对抗生素极不敏感,这是导致生物膜无法根除的主要原因。基于耐药性的原因,寻找新的治疗策略以期抑制生物膜的形成同时破坏成熟生物膜是具有挑战性的。
发明内容
为了克服现有技术中生物膜引发的耐药性的缺陷,本发明提供了一种抑制和/或破坏生物膜的方法,采用本发明提供的方法,能够抑制生物膜的形成,还能够破坏成熟的生物膜。
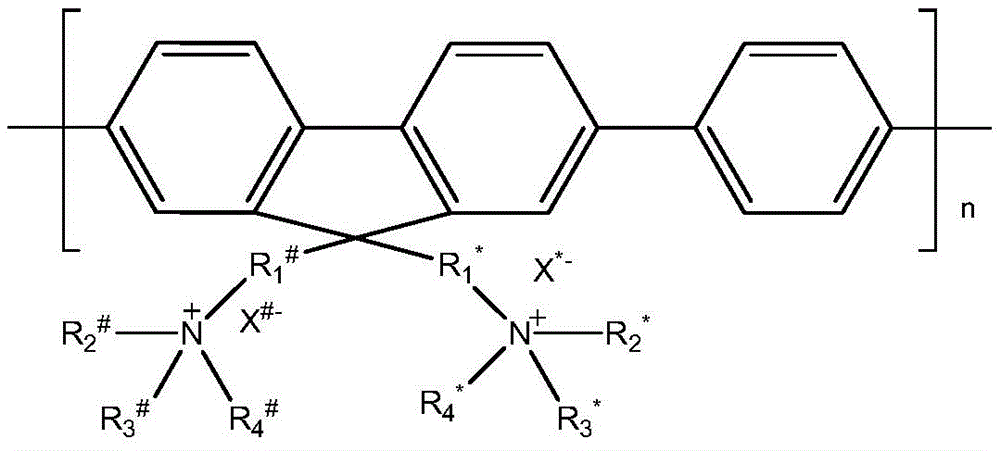
具体的,本发明提供了一种抑制和/或破坏生物膜的方法,该方法包括:将式(I)所示的化合物与样品进行接触,所述样品为含有生物膜的样品和/或能够形成而未形成生物膜的样品;
其中,R1 #、R2 #、R3 #、R4 #、R1 *、R2 *、R3 *和R4 *各自独立地为C1-C12的烷基,X#和X*各自独立地表示卤素;n为8-15的整数;所述式(I)所示的化合物的数均分子量为5000-10000。
本发明的方法能够抑制和破坏生物膜的原因可能为:细菌表面的主要成分为多糖、蛋白质、脂类等,带有负电荷,而式(I)所示化合物带有正电荷,所以细菌通过静电作用和疏水作用与化合物紧密结合。在抑制生物膜形成过程中,将式(I)所示化合物加入到稀释后的细菌溶液中,式(I)所示化合物通过静电作用和疏水作用与细菌结合到一起。当式I所示化合物浓度足够高时,过量的式(I)所示化合物能够包裹细菌,削弱细菌与细菌之间、细菌与基底之间的相互作用,导致生物膜形成能力变弱,达到抑制生物膜形成的效果。在破坏成熟生物膜过程中,将式(I)所示化合物加入到成熟的生物膜中,静电作用和疏水作用使式(I)所示化合物结合到细菌及生物膜表面。这样可以使式(I)所示化合物在光照条件下产生的活性氧与细菌及生物膜足够近,进而有效地破坏生物膜。
本发明提供的抑制生物膜形成及破坏成熟生物膜的方法,克服了现有的破坏生物膜方法容易产生耐药性的难题。在抑制生物膜形成过程中,式(I)所示化合物通过静电和疏水作用将细菌包裹起来,削弱细菌与细菌之间、细菌与基底之间的相互作用,而不是杀死细菌,从源头抑制了耐药性的产生。在破坏成熟生物膜过程中,利用式(I)所示化合物在光照条件下产生的活性氧直接破坏细菌细胞膜,同样避免了耐药性的产生。本发明为建立有效的生物膜去除和预防策略奠定了基础。
本发明的其它特征和优点将在随后的具体实施方式部分予以详细说明。
附图说明
附图是用来提供对本发明的进一步理解,并且构成说明书的一部分,与下面的具体实施方式一起用于解释本发明,但并不构成对本发明的限制。在附图中:
图1是实施例3中的生物膜形成能力曲线图;
图2是实施例4中荧光强度与时间的关系图;
图3是实施例5中的生物膜抑制率曲线图;
图4是实施例6中不同光照时间下死活菌染色荧光比率图;
图5是实施例7中不同光照时间下的电镜成像图。
具体实施方式
以下对本发明的具体实施方式进行详细说明。应当理解的是,此处所描述的具体实施方式仅用于说明和解释本发明,并不用于限制本发明。
在本文中所披露的范围的端点和任何值都不限于该精确的范围或值,这些范围或值应当理解为包含接近这些范围或值的值。对于数值范围来说,各个范围的端点值之间、各个范围的端点值和单独的点值之间,以及单独的点值之间可以彼此组合而得到一个或多个新的数值范围,这些数值范围应被视为在本文中具体公开。
本发明提供了一种抑制和/或破坏生物膜的方法,该方法包括:将式(I)所示的化合物与样品进行接触,所述样品为含有生物膜的样品和/或能够形成而未形成生物膜的样品;
其中,R1 #、R2 #、R3 #、R4 #、R1 *、R2 *、R3 *和R4 *各自独立地为C1-C12的烷基,X#和X*各自独立地表示卤素;n为8-15的整数;所述式(I)所示的化合物的数均分子量为5000-10000。
术语“生物膜”是微生物(特别是细菌)粘附于接触的物体表面,分泌胞外多糖、蛋白质和核苷酸等物质,并将自身包被于其中的大量微生物群聚膜样物。
根据本发明的一种优选的实施方式,在式(I)中,R2 #、R3 #、R4 #、R2 *、R3 *和R4 *相同,均为C1-C5的烷基;R1 #和R1 *相同,为C3-C8的烷基;X#和X*各自独立地选自氯、溴和碘中的至少一种,优选均为溴。
根据本发明的一种具体的实施方式,R2 #、R3 #、R4 #、R2 *、R3 *和R4 *均为甲基,所述R1 #和R1 *均为正己基。
根据本发明的一种具体的实施方式,R2 #、R3 #、R4 #、R2 *、R3 *和R4 *均为乙基,所述R1 #和R1 *均为正己基。
根据本发明的一种具体的实施方式,R2 #、R3 #、R4 #、R2 *、R3 *和R4 *均为甲基,所述R1 #和R1 *均为正戊基。
根据本发明的一种具体的实施方式,R2 #、R3 #、R4 #、R2 *、R3 *和R4 *均为乙基,所述R1 #和R1 *均为正戊基。
根据本发明的一种具体的实施方式,R2 #、R3 #、R4 #、R2 *、R3 *和R4 *均为甲基,所述R1 #和R1 *均为正丁基。
根据本发明的一种具体的实施方式,R2 #、R3 #、R4 #、R2 *、R3 *和R4 *均为乙基,所述R1 #和R1 *均为正丁基。
根据本发明的一种具体的实施方式,R2 #、R3 #、R4 #、R2 *、R3 *和R4 *均为甲基,所述R1 #和R1 *均为正丙基。
根据本发明的一种具体的实施方式,R2 #、R3 #、R4 #、R2 *、R3 *和R4 *均为乙基,所述R1 #和R1 *均为正丙基。
本发明所述抑制和/或破坏生物膜的方法优选为体外和/或非治疗目的的方法。
在本发明中,所述抑制和/或破坏生物膜的方法具体可以分为抑制生物膜的方法和破坏生物膜的方法。所述抑制生物膜的方法指的是抑制生物膜的形成的方法,所述破坏生物膜的方法指的是对于已经形成的成熟的生物膜的破坏方法。
具体的,所述样品为能够形成而未形成生物膜的样品时,所述抑制生物膜的方法可以包括:将式(I)所示的化合物与能够形成而未形成生物膜的样品进行接触。所述能够形成而未形成生物膜的样品指的是具有形成生物膜的能力而还未形成生物膜的样品,例如可以为含有细菌的液体样品和/或含有真菌的液体样品。所述含有细菌的液体样品和/或含有真菌的液体样品中还未形成生物膜。本发明所述的细菌指的是能够形成生物膜的细菌,具体种类没有特别的限定,例如可以为革兰氏阴性菌和/或革兰氏阳性菌,具体可以为金黄色葡萄球菌,进一步优选为金黄色葡萄球菌ATCC 6538、金黄色葡萄球菌ATCC 25923、金黄色葡萄球菌ATCC 29213、金黄色葡萄球菌V 329和金黄色葡萄球菌SA 113(金黄色葡萄球菌V329和金黄色葡萄球菌SA 113的来源可参考Di Poto A,Sbarra M S,Provenza G,etal.The effect of photodynamic treatment combined with antibiotic action orhost defence mechanisms on Staphylococcus aureus biofilms[J].Biomaterials,2009,30(18):3158-3166)中的至少一种。本发明所述的真菌指的是能够形成生物膜的真菌,具体种类也没有特别的限定,例如可以为白色念珠菌,具体可以为白色念珠菌3153A或SC5314(上述两种白色念珠菌的来源可参考Ramage G,Saville S P,Wickes B L,etal.Inhibition of Candida albicans biofilm formation by farnesol,a quorum-sensing molecule[J].Applied and environmental microbiology,2002,68(11):5459-5463)。
优选地,所述能够形成而未形成生物膜的样品为含有细菌的液体样品。所述接触体系中,细菌的数量可以为104-107个/mL。此时进行接触的所述式(I)所示的化合物的用量可以在较大范围内变动,例如,可以为1-100μM(μmol/L),优选为20-50μM。
在本发明中,所述样品为能够形成而未形成生物膜的样品时,所述接触的条件包括:温度可以为37±0.5℃,时间可以10分钟以上,优选为20-30小时。
本发明对上述抑制生物膜的作用强度可以通过结晶紫染色法进行定量检测,并根据式(II)计算生物膜的存活率(VR):
其中,A0为未与式(I)所示的化合物接触的细菌样品在590nm处的吸光值(空白对照),A为与式(I)所示的化合物接触过的细菌样品在590nm处的吸光值。
在本发明中,所述结晶紫染色法可以为本领域的常规选择。所述结晶紫是一种三苯甲烷类染料。电离后,该分子的染色部分带正电荷,可与带负电荷的分子,包括细菌细胞膜表面的分子以及成熟生物膜分泌的胞外基质中的多糖、核酸、蛋白质等结合,使生物膜染色,所以可以用来定量生物膜。
在本发明中,所述样品为含有生物膜的样品时,所述方法还包括:将接触之后的体系进行光照,可以破坏生物膜。此时所述接触的条件没有特别的限定,例如可以包括:温度可以为37±0.5℃;时间可以为10分钟以上,优选10-30分钟。所述光照的条件可以包括:温度可以为15-30℃,时间可以为5-25分钟,光强可以为20-100mW/cm2,光照所使用的光为白光,光照的波长可以为400-800nm。由于白光为复合光,所以波长并不是一个固定数值。
在本发明中,所述含有生物膜的样品可以为含有细菌形成的生物膜的液体样品和/或含有真菌形成的生物膜的液体样品。本发明所述的细菌指的是能够形成生物膜的细菌,具体种类没有特别的限定,例如可以为革兰氏阴性菌和/或革兰氏阳性菌,具体可以为金黄色葡萄球菌,进一步优选为金黄色葡萄球菌ATCC 6538、金黄色葡萄球菌ATCC 25923、金黄色葡萄球菌ATCC 29213、金黄色葡萄球菌V 329和金黄色葡萄球菌SA 113中的至少一种。本发明所述的真菌指的是能够形成生物膜的真菌,具体种类也没有特别的限定,例如可以为白色念珠菌,具体可以为白色念珠菌3153A或SC5314。
将接触的时间控制在上述范围内再配合以光照,特别有利于实现破坏生物膜的目的。对于破坏效果,可以通过培养计数的方式进行定量。例如,对细菌而言,所述破坏生物膜的效果可以通过将光照后的体系中的细菌进行培养计数,根据式(III)计算生物膜的抑制率IR:
其中,C为与式(I)所示的化合物接触的细菌培养后形成的菌落数,C0为未与式(I)所示的化合物接触的细菌培养后形成的菌落数。
根据本发明一种具体的实施方式,所述破坏生物膜的效果检测步骤可以为:将式(I)所示的化合物与含有生物膜的样品(例如菌液)进行接触并光照之后,超声震荡使生物膜分散;将分散后的细菌稀释一定倍数后,取100μL稀释液铺在固体培养基上,37℃培养20h后数平板上的菌落数;然后根据式(III)计算生物膜的抑制率IR。稀释倍数可以根据细菌数目进行确定,使得固体培养基上的菌落数便于统计。
在本发明中,与式(I)所示的化合物接触的含有生物膜的样品的量可以在较大范围内变动,当所述含有生物膜的样品为含有细菌的液体样品时,所述含有生物膜的样品是由包括以下步骤的方法制备得到的:控制细菌的起始数量为104-107个/mL,经过18-30小时的培养形成。温度可以为37±0.5℃。所述接触体系中,式(I)所示的化合物的用量可以在较大范围内变动,例如,可以为1-100μM,优选为20-50μM。
在本发明中,所述式(I)所述的化合物在光照条件下产生活性氧,可以通过活性氧探针进行检测,所述活性氧探针的种类可以为本领域的常规选择,例如具体可以为还原态2,7-二氯荧光素(DCFH)。
本发明还可以通过荧光显微成像实验对式(I)所示的化合物对生物膜的破坏作用进行检测。根据本发明的一种的具体实施方式,可以通过BacLight死活菌染色试剂盒(购自Invitrogen厂家,货号为L13152)进行染色。BacLight死活菌染色试剂盒包含两种染料:PI和SYTO9。检测原理为:SYTO9可以同时对死菌和活菌染色,而PI只能对死菌染色,同时淬灭SYTO9的荧光。最终结果为死菌发红光,活菌发绿光。通过对与式(I)所示的化合物接触和光照之后的生物膜样品进行检测,就可以得出对细菌生物膜的破坏作用的变化情况。例如,未光照组视野中全为绿色,表明细菌全为活菌。随着光照时间的延长,视野中红色增多,则表明式(I)所示的化合物产生的活性氧对生物膜中细菌的破坏作用增强。
另外需要说明的是,对式(I)所示的化合物与能够形成而未形成生物膜的样品进行接触后,也可以再进行光照进一步破坏细菌和/或真菌的细胞膜。光照的条件与和式(I)所示的化合物与含有生物膜的样品接触之后的光照的条件可以相同。
以下将通过实施例对本发明进行详细描述。
在以下实施例中,
金黄色葡萄球菌ATCC 6538购自中国普通微生物菌种保藏管理中心(CGMCC),编号为:CGMCC No.1.2386。
BacLight死活菌染色试剂盒购自Invitrogen厂家,货号为L13152。
2,7-二氯荧光素二乙酯(DCFH-DA)购自Sigma-Aldrich厂家,货号为D6883。
TSB培养基购自美国BD公司,货号为211825。TSBg培养基为TSB培养基中添加0.25质量%的葡萄糖的培养基。
PBS为购自Hyclone厂家的货号为SH30256.01的产品。
结晶紫购自Sigma-Aldrich厂家,货号为C0775。
荧光成像在激光共聚焦扫描显微镜(购自Olympus厂家,型号为FV1000-IX81)仪器上进行。
电镜成像在扫描电子显微镜(购自Hitachi厂家,型号为S-4800)上进行。
其余的化学和生物试剂均为商购获得。
NB液体培养基组成成分按质量体积比(质量体积比指的是质量与体积的比值,单位g/mL,下同)计:1.0%胰蛋白胨(100mL的NB液体培养基中含有1.0g胰蛋白胨),0.3%牛肉浸取物,0.5%氯化钠,98.2%蒸馏水;NB固体培养基配方为:向NB液体培养基中加入1.5重量%的琼脂。
实施例1
本实施例用于说明式(I)所示化合物PFP的合成
PFP的具体结构为:
9,9-二(6′-溴己基)-2,7-二溴芴:1,6-二溴己烷(97.6g,400mmol)加入100ml50%的氢氧化钾溶液中,加入1.28g相转移催化剂四丁基溴化铵(TBAB),反应液温度升至75℃,然后加入2,7-二溴芴(12.96g,40mmol)搅拌15min。反应停止并冷却至室温后,二氯甲烷萃取(100ml×3),合并有机相,并分别用1M盐酸溶液和蒸馏水洗涤,无水硫酸镁干燥,过滤,浓缩。粗产物硅胶柱层析分离纯化,展开剂为二氯甲烷/石油醚(v/v=1/9),得白色固体产物9,9-二(6′-溴己基)-2,7-二溴芴21.4g,产率82%。1H-NMR:(300MHz,CDCl3,ppm)δ:0.58(m,4H),1.08(m,4H),1.21(m,4H),1.66(m,4H),1.91(m,4H),3.29(m,4H),7.43(s,4H),7.53(s,2H);13C-NMR:(100MHz,CDCl3,ppm)δ:23.53,27.80,29.00,32.67,33.92,40.06,55.06,121.30,126.17,130.38,139.09,152.23.EI(m/z):650(100%)[M+]Anal.Calcd forC25H30Br4(650.15):C,46.14,H,4.614.Found:C,45.95,H,4.61.
氮气保护下,将9,9-二(6′-溴己基)-2,7-二溴芴(260mg,0.4mmol)与2′,2′-二甲基-1′,3′-丙二醇-1,4-苯二硼酸酯(120mg,0.4mmol)加入到6.4mL的THF中,溶解后加入1.6mL碳酸钾溶液(2M)与催化量的钯催化剂PdCl2(dppf)(20mg),混合液升温至80℃反应2d。反应液冷却至室温后,将THF减压除去,加入氯仿,洗涤两次,将有机相浓缩,滴加到甲醇中沉淀,离心、干燥后得固体产物(115mg,52%)。
1H NMR(400MHz,CDCl3):δ7.83(m,6H),7.74-7.62(m,4H),3.30(m,4H),2.10(b,4H),1.81(m,4H),1.39-1.13(m,8H),0.79(b,4H)。
PFP:将上一步得到的固体产物(57mg,0.1mmol)溶解在5mL的二氯甲烷溶液中,加入过量的三甲胺的甲醇溶液,室温反应5h。将反应生成的沉淀过滤、洗涤,干燥后得目标产物(60mg,88%)。
1H NMR(400MHz,DMSO-6):δ(ppm)7.91-7.79(m,10H),3.18(b,4H),2.96(b,>15H),2.18-1.91(m,4H),1.47(b,4H),1.09(b,8H),0.67(b,4H)。
实施例2
本实施例用于说明金黄色葡萄球菌的复苏培养
以金黄色葡萄球菌ATCC 6538为模板,在超净工作台中用75体积%酒精脱脂棉对所购装有金黄色葡萄球菌ATCC 6538的安瓿瓶外表面进行消毒后,用火焰加热其顶端,滴400μL无菌水至加热的安瓿瓶顶端使之破裂。吸取300μL适宜的液体培养基(可用无菌水代替),滴入安瓿瓶内,轻轻振荡吹打,使冻干菌体溶解呈悬浮状,吸取全部菌悬液,分别移植于两个NB固体培养基中,37℃培养20小时。用接种环刮取适量菌体画Z型接种到新的NB固体培养基中,37℃继续培养,如此连续传3-4代培养,获得稳定的菌株,放4℃作菌种备用。
实施例3
本实施例用于说明抑制生物膜的方法
(1)生物膜的形成和抑制
挑取固体培养基中适量ATCC 6538菌体于NB液体培养基中,37℃下转速180rpm震荡培养10h。用NB培养基调OD600值为1.0,取少量菌液(10μL)稀释100倍于TSBg培养基中。取90μL稀释后的菌液与10μL不同浓度的PFP混合,置于96孔板中,孔板中PFP的终浓度分别为1μM、5μM、10μM、20μM、50μM和100μM。37℃培养箱中放置24小时。空白对照为加入10μL灭菌水,其余操作与实验组一致。
(2)抑制生物膜效果的检测
取出96孔板,弃去培养基,并用PBS洗三次除去游离的细菌。加入100μL的95体积%乙醇固定15分钟,除去乙醇后,放置至板干。加入100μL的0.1质量体积%结晶紫染色5分钟,除去结晶紫,用灭菌水洗三次。加入110μL的10体积%乙酸溶解结晶紫,检测每孔590nm处吸收值。空白对照记为A0,加入不同浓度PFP的记为A,金黄色葡萄球菌生物膜存活率(VR)根据式(II)计算,并绘制生物膜形成能力曲线,如图1所示。
从图1中可以看出,加入PFP后,金黄色葡萄球菌形成生物膜的能力减弱,且随着PFP浓度的升高,PFP对金黄色葡萄球菌生物膜形成的抑制作用增强。说明PFP能有效抑制金黄色葡萄球菌生物膜的形成。
实施例4
本实施例用于说明PFP光照后产生的活性氧的检测方法
还原态2,7-二氯荧光素(DCFH)的活化:在500μL的2,7-二氯荧光素二乙酯(DCFH-DA)中加入2mL的0.01M的NaOH后室温放置30min,再加入10mL磷酸缓冲液(25mM,pH=7.4),混匀冰上暗处储存待用。
向90μL活化后的DCFH溶液(40μM)加入10μL不同浓度PFP(终浓度分别为5μM、10μM和20μM),用光密度为3mW/cm2白光光源照射样品5min,每隔1min测525nm处的荧光值,激发波长为488nm。空白对照为90μL活化后的DCFH溶液加入10μL灭菌水在光密度为3mW/cm2的白光光源照射5min,每隔1min测525nm处的荧光值,激发波长为488nm,所得525nm处荧光强度与时间的关系见图2。
从图2中可以看出,PFP有很强的产生活性氧的能力,并且随着PFP浓度的升高,产生活性氧的能力变强,可用于光照杀伤周围细菌。
实施例5
本实施例用于说明PFP破坏生物膜的方法
(1)生物膜的形成
挑取固体培养基中适量ATCC 6538菌体于NB液体培养基中,37℃下转速180rpm震荡培养10h。用NB培养基调OD600值为1.0,取少量菌液(10μL)稀释100倍于TSBg培养基中。取100μL稀释后的菌液置于96孔板中,37℃培养箱中放置24小时。
(2)破坏生物膜效果的检测
形成生物膜后,弃去96孔板中培养基,用PBS洗3次除去游离的细菌。加入100μL的PFP溶液(终浓度20μM),放入37℃培养箱中放置15min。空白对照为加入100μL的PBS溶液,其余操作与实验组一致。将96孔板于75mW/cm2光强下光照5-25min,超声震荡使生物膜分散。将分散后的细菌稀释3000倍后,取100μL稀释液铺在NB固体培养基上,37℃培养20h后数平板上的菌落数。空白对照组记为C0,实验组记为C,抑制率(IR)根据式(III)计算,并绘制曲线,如图3所示,
从图3中可以看出,随着光照时间的延长,PFP对生物膜的破坏作用增强。
实施例6
本实施例通过荧光显微成像法证明PFP对生物膜破坏作用
生物膜的形成过程与实施例5的方法相同。
形成生物膜后,弃去96孔板中培养基,用PBS洗3次除去游离的细菌。加入100μL的PFP溶液(终浓度20μM),放入37℃培养箱中放置15min。空白对照为加入100μL的PBS溶液,其余操作与实验组一致。将96孔板于75mW/cm2光强下光照5-25min后,弃去PFP溶液,用PBS洗两次后,用BacLight死活菌染色试剂盒进行染色。最后进行CLSM表征,采集样品的明场和荧光场,对于SYTO9激发波长为488nm,PI为559nm。统计每个视野中绿色荧光和红色荧光的数值,用绿色荧光值除以红色荧光值得到活菌与死菌的比率,结果如图4所示。
从图4中可以看出,加入PFP后,随着光照时间的延长,活菌数逐渐减少,死菌数逐渐增多,表明PFP对生物膜的破坏作用于光照时间呈正相关。
实施例7
本实施例通过电镜说明PFP对生物膜破坏作用
(1)生物膜的形成
挑取固体培养基中适量ATCC 6538菌体于NB液体培养基中,37℃下转速180rpm震荡培养10h。用NB培养基调OD600值为1.0,取少量菌液稀释100倍于TSBg培养基中。取500μL稀释后的菌液于24孔板中(提前放置好Thermanox塑料盖玻片),37℃培养箱中放置24小时。
(2)电镜成像
形成生物膜后,弃去24孔板中培养基,用PBS洗3次除去游离的细菌。加入500μL的PFP溶液(终浓度20μM),放入37℃培养箱中放置15min。空白对照为加入500μL的PBS溶液,其余操作与实验组一致。将24孔板于75mW/cm2光强下光照5-25min后,弃去PFP溶液,用PBS洗两次后,加入含有0.5体积%戊二醛的PBS溶液,4℃固定过夜。样品用超纯水洗涤2次后,依次用体积百分含量分别为20%、40%、50%、70%、90%和100%乙醇梯度脱水,每次5min。待样品自然干燥后,真空冷冻干燥2h,样品喷金处理后可进行表征。结果如图5所示。
从图5中可以看出,没有光照条件下,可以看到细菌成团且被胞外基质紧密包裹。随着光照时间的延长,细菌团块变小,并且能观察到明显的细菌脱落,进一步证明了PFP产生的活性氧对生物膜有破坏作用。
以上详细描述了本发明的优选实施方式,但是,本发明并不限于上述实施方式中的具体细节,在本发明的技术构思范围内,可以对本发明的技术方案进行多种简单变型,这些简单变型均属于本发明的保护范围。
另外需要说明的是,在上述具体实施方式中所描述的各个具体技术特征,在不矛盾的情况下,可以通过任何合适的方式进行组合。为了避免不必要的重复,本发明对各种可能的组合方式不再另行说明。
此外,本发明的各种不同的实施方式之间也可以进行任意组合,只要其不违背本发明的思想,其同样应当视为本发明所公开的内容。
Claims (10)
2.根据权利要求1所述的方法,其中,所述能够形成而未形成生物膜的样品为含有金黄色葡萄球菌的样品时,所述接触的条件包括:温度为37±0.5℃,时间为10分钟以上。
3.根据权利要求2所述的方法,其中,所述能够形成而未形成生物膜的样品为含有金黄色葡萄球菌的样品时,所述接触的条件包括;温度为37±0.5℃,时间为20-30小时。
4.根据权利要求1-3中任意一项所述的方法,其中,所述能够形成而未形成生物膜的样品为含有金黄色葡萄球菌的液体样品,且所述接触体系中,金黄色葡萄球菌的数量为104-107个/mL,式(I)所示的化合物的用量为1-100μM。
5.根据权利要求1-3中任意一项所述的方法,其中,所述金黄色葡萄球菌为金黄色葡萄球菌ATCC 6538、金黄色葡萄球菌ATCC 25923、金黄色葡萄球菌ATCC 29213、金黄色葡萄球菌V 329和金黄色葡萄球菌SA 113中的至少一种。
6.根据权利要求1所述的方法,其中,所述含有生物膜的样品为含有金黄色葡萄球菌形成的生物膜的样品时,所述方法还包括:将接触之后的体系进行光照。
7.根据权利要求6所述的方法,其中,所述接触的条件包括:温度为37±0.5℃,时间为10-30分钟;所述光照的条件包括:温度为15-30℃,时间为5-25分钟,光强为20-100mW/cm2,光照所使用的光为白光,光照的波长为400-800nm。
8.根据权利要求1或6所述的方法,其中,所述含有金黄色葡萄球菌形成的生物膜的样品是由包括以下步骤的方法制备得到的:控制金黄色葡萄球菌的起始数量为104-107个/mL,经过18-30小时的培养形成。
9.根据权利要求1或6所述的方法,其中,所述接触体系中,式(I)所示的化合物的用量为1-100μM。
10.根据权利要求1或6所述的方法,其中,所述金黄色葡萄球菌为金黄色葡萄球菌ATCC6538、金黄色葡萄球菌ATCC 25923、金黄色葡萄球菌ATCC 29213、金黄色葡萄球菌V 329和金黄色葡萄球菌SA 113中的至少一种。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201710073483.1A CN106857504B (zh) | 2017-02-10 | 2017-02-10 | 一种抑制和/或破坏生物膜的方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201710073483.1A CN106857504B (zh) | 2017-02-10 | 2017-02-10 | 一种抑制和/或破坏生物膜的方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN106857504A CN106857504A (zh) | 2017-06-20 |
| CN106857504B true CN106857504B (zh) | 2020-03-10 |
Family
ID=59166959
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201710073483.1A Active CN106857504B (zh) | 2017-02-10 | 2017-02-10 | 一种抑制和/或破坏生物膜的方法 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN106857504B (zh) |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2004001379A2 (en) * | 2002-06-20 | 2003-12-31 | The Regents Of The University Of California | Methods and compositions for detection and analysis of polynucleotides using light harvesting multichromophores |
| WO2004077014A2 (en) * | 2003-02-13 | 2004-09-10 | The Regents Of The University Of California | Methods and compositions for detection and analysis of polynucleotide-binding protein interactions using light harvesting multichromophores |
| CN104788400A (zh) * | 2015-04-22 | 2015-07-22 | 中国科学院化学研究所 | 寡聚芴类化合物及其制备方法 |
-
2017
- 2017-02-10 CN CN201710073483.1A patent/CN106857504B/zh active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2004001379A2 (en) * | 2002-06-20 | 2003-12-31 | The Regents Of The University Of California | Methods and compositions for detection and analysis of polynucleotides using light harvesting multichromophores |
| WO2004077014A2 (en) * | 2003-02-13 | 2004-09-10 | The Regents Of The University Of California | Methods and compositions for detection and analysis of polynucleotide-binding protein interactions using light harvesting multichromophores |
| CN1771335A (zh) * | 2003-02-13 | 2006-05-10 | 加州大学评议会 | 使用集光多生色团检测和分析多核苷酸-结合蛋白相互作用的方法和组合物 |
| CN104788400A (zh) * | 2015-04-22 | 2015-07-22 | 中国科学院化学研究所 | 寡聚芴类化合物及其制备方法 |
Non-Patent Citations (1)
| Title |
|---|
| Cationic Conjugated Polymers-Induced Quorum Sensing of Bacteria;Pengbo Zhang .et.al;《Analytical chemistry》;20160225;第88卷(第6期);2985-2988 * |
Also Published As
| Publication number | Publication date |
|---|---|
| CN106857504A (zh) | 2017-06-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Ye et al. | AIEgens for microorganism‐related visualization and therapy | |
| Sun et al. | Near-infrared triggered antibacterial nanocomposite membrane containing upconversion nanoparticles | |
| CN103881010B (zh) | 一种基于龙脑的高分子抗菌材料 | |
| US20120316305A1 (en) | Antimicrobial compounds and fibers thereof | |
| CN109845761B (zh) | 溶菌酶二维纳米薄膜作为抗菌材料的应用 | |
| Spagnul et al. | Synthesis, characterization and biological evaluation of a new photoactive hydrogel against Gram-positive and Gram-negative bacteria | |
| CN103289963B (zh) | 一株具有环境消毒能力的噬菌体及其用途 | |
| Zhao et al. | Preparations of antibacterial yellow-green-fluorescent carbon dots and carbon dots-lysozyme complex and their applications in bacterial imaging and bacteria/biofilm inhibition/clearance | |
| CN115849347A (zh) | 精氨酸抗菌碳点的制备方法及其应用 | |
| CN108410691A (zh) | 静电纺丝纤维膜的应用及含有该纤维膜的微生物测试片 | |
| CN111943868B (zh) | 一种含二乙胺的吖嗪联肼类化合物及其制备方法与应用 | |
| CN106857504B (zh) | 一种抑制和/或破坏生物膜的方法 | |
| Lu et al. | Layer‐by‐layer structured gelatin nanofiber membranes with photoinduced antibacterial functions | |
| Lv et al. | A fluorescent quaternary phosphonium main-chain-type polymer: an opportunity to fabricate functional materials with excellent antibacterial activity and bacterial imaging capability | |
| CN102706821B (zh) | 一种食源菌生物被膜形成抑制剂的快速鉴定方法 | |
| CN108249420B (zh) | 一种带正电的碳点及其制备方法和应用 | |
| Chen et al. | Mulberry Leaves-Derived Carbon Dots for Photodynamic Treatment of Methicillin-Resistant Staphylococcus aureus-Infected Wounds via Metabolic Perturbation | |
| Du et al. | A novel polythiophene-conjugated polymer photocatalyst under visible light for killing multidrug-resistant bacteria | |
| CN114469893A (zh) | 一种季铵盐化二氧化硅纳米颗粒及制备方法与应用 | |
| CN116986582A (zh) | 一种生物质抗菌碳点及其制备方法 | |
| CN110583697A (zh) | 去除铜绿假单胞菌生物膜用的高效化学生物制剂及其应用 | |
| CN113444201A (zh) | 荧光含糖聚合物及其制备方法 | |
| KR101924496B1 (ko) | 박테리아 진단용 유기 공중합체, 이의 제조방법 및 이를 포함하는 박테리아 진단용 형광센서 | |
| LU504180B1 (en) | Chitosan nano-conjugate for resisting bacterial biofilm, and preparation method and application thereof | |
| CN113440643B (zh) | 一种可吸收外科材料的表面抗菌处理方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant |