CN106794285B - 用于药物释放的医疗装置的可移除覆盖物 - Google Patents
用于药物释放的医疗装置的可移除覆盖物 Download PDFInfo
- Publication number
- CN106794285B CN106794285B CN201580053597.9A CN201580053597A CN106794285B CN 106794285 B CN106794285 B CN 106794285B CN 201580053597 A CN201580053597 A CN 201580053597A CN 106794285 B CN106794285 B CN 106794285B
- Authority
- CN
- China
- Prior art keywords
- sheath
- segment
- balloon
- medical device
- removable delivery
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L29/00—Materials for catheters, medical tubing, cannulae, or endoscopes or for coating catheters
- A61L29/04—Macromolecular materials
- A61L29/041—Macromolecular materials obtained by reactions only involving carbon-to-carbon unsaturated bonds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M25/00—Catheters; Hollow probes
- A61M25/10—Balloon catheters
- A61M25/1018—Balloon inflating or inflation-control devices
- A61M25/10184—Means for controlling or monitoring inflation or deflation
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/95—Instruments specially adapted for placement or removal of stents or stent-grafts
- A61F2/958—Inflatable balloons for placing stents or stent-grafts
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/95—Instruments specially adapted for placement or removal of stents or stent-grafts
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/95—Instruments specially adapted for placement or removal of stents or stent-grafts
- A61F2/954—Instruments specially adapted for placement or removal of stents or stent-grafts for placing stents or stent-grafts in a bifurcation
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/95—Instruments specially adapted for placement or removal of stents or stent-grafts
- A61F2/962—Instruments specially adapted for placement or removal of stents or stent-grafts having an outer sleeve
- A61F2/97—Instruments specially adapted for placement or removal of stents or stent-grafts having an outer sleeve the outer sleeve being splittable
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L29/00—Materials for catheters, medical tubing, cannulae, or endoscopes or for coating catheters
- A61L29/08—Materials for coatings
- A61L29/085—Macromolecular materials
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M25/00—Catheters; Hollow probes
- A61M25/01—Introducing, guiding, advancing, emplacing or holding catheters
- A61M25/06—Body-piercing guide needles or the like
- A61M25/0662—Guide tubes
- A61M25/0668—Guide tubes splittable, tear apart
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/95—Instruments specially adapted for placement or removal of stents or stent-grafts
- A61F2/958—Inflatable balloons for placing stents or stent-grafts
- A61F2002/9583—Means for holding the stent on the balloon, e.g. using protrusions, adhesives or an outer sleeve
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M25/00—Catheters; Hollow probes
- A61M25/01—Introducing, guiding, advancing, emplacing or holding catheters
- A61M25/06—Body-piercing guide needles or the like
- A61M25/0662—Guide tubes
- A61M2025/0681—Systems with catheter and outer tubing, e.g. sheath, sleeve or guide tube
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M25/00—Catheters; Hollow probes
- A61M25/10—Balloon catheters
- A61M2025/1043—Balloon catheters with special features or adapted for special applications
- A61M2025/105—Balloon catheters with special features or adapted for special applications having a balloon suitable for drug delivery, e.g. by using holes for delivery, drug coating or membranes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M25/00—Catheters; Hollow probes
- A61M25/10—Balloon catheters
- A61M2025/1043—Balloon catheters with special features or adapted for special applications
- A61M2025/1081—Balloon catheters with special features or adapted for special applications having sheaths or the like for covering the balloon but not forming a permanent part of the balloon, e.g. retractable, dissolvable or tearable sheaths
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M25/00—Catheters; Hollow probes
- A61M25/10—Balloon catheters
- A61M25/1011—Multiple balloon catheters
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Heart & Thoracic Surgery (AREA)
- Oral & Maxillofacial Surgery (AREA)
- Transplantation (AREA)
- Vascular Medicine (AREA)
- Cardiology (AREA)
- Epidemiology (AREA)
- Anesthesiology (AREA)
- Hematology (AREA)
- Biophysics (AREA)
- Pulmonology (AREA)
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Child & Adolescent Psychology (AREA)
- Materials For Medical Uses (AREA)
- Media Introduction/Drainage Providing Device (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medical Preparation Storing Or Oral Administration Devices (AREA)
- Infusion, Injection, And Reservoir Apparatuses (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Organic Chemistry (AREA)
Abstract
本公开包括可膨胀医疗装置(104)和外护套(120)的组合。所述外护套能够裂开形成多个护套部分(230,232),所述护套部分可被剥离以露出部分或全部可膨胀医疗装置。所述医疗装置以及所述外护套可包括一种或多种用于递送至患者体内治疗区域的治疗剂。
Description
技术领域
本发明一般涉及用于治疗血管系统和类似解剖学上疾病的内用假体,更具体地涉及使用可分开和可移除的递送护套的治疗剂递送系统。
背景技术
治疗剂的全身给药将身体作为整体进行治疗,即使在需要治疗的疾病可能是局部的情况下也是如此。在以下局部疾病的情况中,可能不希望全身给予药物,因为药物试剂可能对非治疗目标的身体部分有不需要的影响,或者因为对身体带病部分的治疗需要通过全身给药可能无法实现的高浓度药物试剂。
因此,经常需要将治疗剂仅给予体内的局部位点。需要这种情况的常见实例包括局部疾病(例如冠心病)和阻塞,损伤或体腔中的其它疾病。进行局部药物递送的几种装置和方法是已知的。在一个实例中,这种装置是药物递送气囊,其使用方法包括以下步骤:用药物和任选的载体基质涂覆与气囊导管附连的气囊,将导管插入血管,将气囊跟踪到期望的位置,以及使气囊膨胀抵靠周围组织以将药物局部地转移至预期的治疗区域。
局部药物递送的潜在缺点之一是药物、载体基质和/或药物/载体基质组合可能过早或不希望地释放。这可能在药物递送装置的治疗区域中跟踪和放置过程中以及当所述装置从体内抽出时的后递送过程中发生。这种不希望的释放可能是由于药物扩散,装置与接近治疗区域的区域接触,或由于血液流动而从递送装置的表面清洗药物导致。当装置包括不希望释放到治疗区域外的组织或血液的类型或剂量的治疗剂时,这是特别关注的。此外,药物可能由于在气囊表面上滑动可伸缩盖而产生的摩擦而从递送装置的外表面过早地释放。
考虑到目前的局部药物递送的潜在缺点,需要允许药物试剂,特别是可溶性试剂的局部控释到哺乳动物体内的特定治疗区域的装置和方法,所述装置和方法能避免微粒化和药物从预期的治疗区域过早或不希望的释放,同时确保产生期望的剂量。
发明概述
根据本发明的可移除递送护套可包括围绕至少部分可膨胀医疗装置的径向可膨胀管状护套,其中通过向启动线施加张力将所述护套分开以形成第一护套段和第二护套段,其中从可膨胀的医疗装置周围除去所述第一护套段,之后从所述可膨胀的医疗装置周围除去所述第二护套段。
根据本发明的治疗方法可包括使可膨胀的医疗装置和围绕至少部分所述可膨胀的医疗装置的径向可膨胀的管状护套进入患者体内的治疗区域,向启动线施加张力将所述护套分开以形成第一护套段和第二护套段,从所述医疗装置除去所述第一护套段中的至少一个。
附图的简要说明
结合附图,通过以下说明书详述,本公开的特征和优势将会更明显,其中:
图1A和1B示出根据本公开的医疗装置递送系统的侧面图和截面图;
图2A和2B示出根据本公开的医疗装置递送系统的透视图;
图3示出根据本公开的医疗装置递送系统的透视图;
图4A和4B示出根据本公开的医疗装置递送系统的透视图;
图5A和5B示出根据本公开的医疗装置递送系统的透视图;
图6A-6D示出根据本公开的医疗装置递送系统在各个展开阶段的透视图;
图7示出用于根据本公开的各个医疗装置递送系统的干及湿模拟操作过程中治疗剂损失的示意图。
所述实施方式的详述
本领域的技术人员应理解,可通过用于发挥所需作用的任何数量的方法和设备来发挥其预期功能。换言之,本文可纳入其它方法和设备以发挥预期的功能。还应注意,本文参考的附图不一定是按比例绘制,而是有可能放大以说明本公开的各个方面,就此而言,附图不应视为限制性的。最后,尽管可以结合各种原理和观点来描述本发明,但是本发明不应受到理论的限制。
在本说明书和权利要求中,术语“内用假体装置”、“内用假体”和“血管装置”等可以表示能在体腔内植入和/或展开的任何医疗装置。在各实施方式中,内用假体可包括支架、支架移植物、移植物、过滤器、封堵器、气囊、导管和能量传送装置,可展开膜片、留置导管等。
此外,在本说明书和权利要求书中,本文所述的递送系统总体上包括由“覆盖件”或“护套”限制的内用假体。在多个实施方式中,所述覆盖件或护套可以包括与内用假体配适的材料片。在本说明书和权利要求书中,术语“延长件”可表示轴样结构,例如导管、导丝、导引护套管等。在多个实施方式中,内用假体可以安装或加载在导管(在本文中也称为内轴)上,以收缩直径状态配适在引导护套管(在本文中也称为外轴)中。
此外,术语“远端”表示距体内引入所述医疗装置的位置更远的相对位置。类似地,术语“远端地”表示远离体内引入所述医疗装置的位置的方向。
术语“近端”表示距体内引入所述医疗装置的位置更近的相对位置。类似地,术语“近端地”表示朝向体内引入所述医疗装置的位置的方向。
虽然不断采用术语近端和远端,但本公开不应当理解为被这些术语限制。相反,本文所述的装置和方法可以根据患者的解剖学改变和/或调节。
在本文中,术语“限制”可以表示(i)限制可膨胀移植物的膨胀(无论是通过自膨胀产生的或装置辅助膨胀产生的)直径,或(ii)覆盖或围绕(但不以其他方式抑制)可膨胀移植物(例如,出于存储或生物相容性原因和/或为了提供对可膨胀移植物和/或血管系统的保护)。
在本文中,术语“脉管”表示体内可以利用这些构建体的任何管腔或管状结构。这包括但不限于动脉血管、血管缺陷如动静脉畸形、动脉瘤等,淋巴系统脉管、食道、肠解剖组织、腔管(sinuous cavity)、子宫等。本发明的实施方式还适用于治疗脉管中的或与脉管有关的恶性疾病(即癌)。
参照图1A,医疗装置递送系统100可包括,例如,安装在延长件102上的医疗装置104。延长件102可包括,例如,近端106和远端108。在多个实施方式中,医疗装置递送系统100可包括近端导丝腔110,近端导丝腔110延伸通过延长件102的长度并在导丝出口112处存在远端108。这种导管和气囊设置通常被称为“覆盖导丝(Over The Wire)”构造。在其他实施方式中,延长件102包括位于近端106和远端108中间的导丝出口112,这通常被称为“快速交换(Rapid Exchange)”构造。
医疗装置递送系统100还可以包括,例如,允许延长件102和医疗装置内腔104(例如气囊104)之间流体连通的近端膨胀出口114。根据医疗器械的应用来选择所述延长件102的长度、内径和外径。例如,延长件102通常具有圆形横截面构造。但也可以使用椭圆和其他横截面构造。例如,医疗装置递送系统100可以与直径为0.038”,0.035”,0.018”或0.014”,0.010”的导丝相容。
在多个实施方式中,医疗装置104包括气囊,例如,药物释放气囊。本发明使用的气囊可以是吹散成型的、可以是非适应性的、适应性的或半适应性的,以及可以是各种形状,例如所谓的“可仿形的(conformable)”“仿形(conforming)”或“转向(steerable)”气囊。气囊104可包括,例如,由包裹膜构建的气囊,纤维缠绕型气囊、长度可变气囊、分段气囊和/或具有可控膨胀概况的气囊。
首先参照图1B,图1A的气囊104可进一步包括结构层122。结构层122可包括可进行膨胀以适应气囊104膨胀的任何材料。这些材料包括但不限于膨胀聚四氟乙烯(ePTFE)、其他含氟聚合物、膨胀聚乙烯、聚氯乙烯、聚氨酯、硅酮、聚乙烯、聚丙烯、聚氨酯、聚乙醇酸、聚酯、聚酰胺(例如尼龙12,尼龙11,尼龙9,尼龙6/9和尼龙6/6)、聚烯烃、聚醚嵌段酰胺、聚酰亚胺、聚碳酸酯、聚苯硫醚、聚亚苯基氧化物(PPO)、聚醚、硅酮、苯乙烯聚合物、其共聚物和它们的混合物。如本文所用,术语“共聚物”用于指代由2种或更多种单体,例如,2、3、4、5等种单体形成的任意聚合物。
这些材料的一些共聚物的示例包括以的商品名购自宾夕法尼亚州费城的埃尔夫阿托化学北美公司(Elf Atochem North America)的聚醚-嵌段-酰胺。另一种合适的共聚物是聚醚酯酰胺。合适的聚酯共聚物包括,例如,聚对苯二甲酸乙二酯和聚对苯二甲酸丁二酯,聚酯醚和聚酯弹性体共聚物,如以的商品名购自特拉华州威名顿市的杜邦公司(DuPont)的那些。
本文也可采用嵌段共聚物弹性体,如具有苯乙烯末端嵌段的那些共聚物,和从丁二烯、异戊二烯、乙烯/丁烯、乙烯/丙烯等形成的中间嵌段。其他苯乙烯类嵌段共聚物包括丙烯腈-苯乙烯和丙烯腈-丁二烯-苯乙烯嵌段共聚物。此外具体的热塑性弹性体嵌段共聚物也可在本文使用,其中所述嵌段共聚物由聚酯或聚酰亚胺硬段和聚醚软段制成。
在多个实施方式中,结构层122的表面或向外构造可以用纹理、折痕、翼、内陷、褶皱、凸出、尖峰、刻痕、凹陷、沟、孔、涂层、颗粒等或它们的组合来修饰。这种凹陷、沟和/或孔可以用来增加其上可以放置涂层的有效表面积。这有助于减少医疗装置和/或气囊104的总长度或轮廓。
在多个实施方式中,结构层122可提供以第一状态被涂覆的均匀的管,所述第一状态将同心地/均匀地膨胀至第二状态。相反,常规的经皮穿刺动脉成形术(PTA)气囊弄成以第二状态涂覆(以其模制的形状),然后压缩至第一状态。结构层122可以在心轴上与医疗装置递送系统100或气囊104分开涂覆,之后组装到气囊104上,具有增加的制造产率、较低的成本和更高的均一性。以下将更详细地描述,所述结构层122上的涂层将被递送护套120覆盖。
气囊104和/或结构层122可以构造为使用一致的“按需”递送将治疗剂递送至脉管位点。例如,气囊104可包括涂层124。在本文中,术语“涂层”表示放置在基材表面上的一种或多种材料。涂层124可以全部放置在气囊104的表面上。涂层124还可以整体或部分设置在结构层122中存在的开口或孔中。
在多个实施方式中,结构层122可用作基材,用于均匀地向气囊104施加涂层124。由于一些气囊材料不利于均匀涂覆,结构层122可以用作支架以实现均匀涂层124。此外,如果结构层122包括弹性体,结构层122有助于下层气囊的再压缩(参见,例如Campbell等的美国专利6,120,477,其通过引用全文纳入本文用于所有目的)。此外,结构层122可以在放置在延长件102上之前用涂层124进行涂覆。采用这种预制的经涂覆的结构层122,任何气囊可以转化为本公开的气囊104。因此,多个实施方式包括将结构层122设置在任意“现成(offthe shelf balloon)气囊”或OEM气囊上,以将OEM气囊转化为本公开的气囊104。
涂层124可以包含赋形剂,例如紫杉醇-赋形剂固体组合物。例如,紫杉醇是一种用于治疗多种癌症并用于预防和治疗再狭窄的市售制剂。已知紫杉醇以多种不同的物理形式存在,包括无定形、玻璃态和晶体形式,其中晶体形式还可分化成多种不同的多晶型物。此外,晶体紫杉醇可以无水或水合形式存在。晶体紫杉醇的可接受熔点是约220℃,取决于加热条件和多晶型物形式(Liggins等,“紫杉醇的固态特征(Solid-state characterizationof paclitaxel)”,J.Pharm.Sci.1997,卷86,第1458–1463页)。已知固体形式中,紫杉醇的特定形式可影响药物的物理性质。具体地,紫杉醇与表面的附着可能受到其物理形式,以及其从表面溶解到周围环境中的速率的影响。因此,采用赋形剂配制固体形式的紫杉醇的效果不容易预测。
涂层124的赋形剂可包括,例如,对氨基苯甲酸、糖精、抗坏血酸、对羟基苯甲酸甲酯、咖啡因、水杨酸钙、三胺五乙酸(pentetic acid)、肌酸酐、乙基脲、对乙酰胺基酚、阿司匹林、可可碱、色氨酸、琥珀酸、戊二酸、己二酸、茶碱、糖精钠、氨基醇、羟基羧酸、羟基羧酸酯、羟基羧酸酐、羟基酮、羟基内酯、羟基酯、磷酸糖类、硫酸糖类、乙基氧化物(ethyloxide)、乙二醇、氨基酸、肽、蛋白、去水山梨糖醇、甘油、多元醇、磷酸酯、硫酸酯、有机酸、有机酸酯、有机酸盐、维生素、氨基醇和有机酸的组合,以及它们的取代的分子。此外,所述赋形剂可包括表面活性剂,所述表面活性剂选自离子型、非离子型、脂族和芳族表面活性剂,包括PEG脂肪酸酯、PEGω-3脂肪酸酯、醚和醇、甘油脂肪酸酯、去水山梨糖醇脂肪酸酯、PEG甘油基脂肪酸酯、PEG去水山梨糖醇脂肪酸酯、糖脂肪酸酯、PEG糖酯和它们的衍生物。
涂层124可进一步包括添加剂,例如,具有一个或多个羟基、氨基、羰基、羧基、酸、酰胺和酯基团的化合物。这种添加剂可以是亲水性的。在多个实施方式中,所述添加剂是表面活性剂和具有一个或多个羟基、氨基、羰基、羧基、酸、酰胺或酯基团的化合物的组合。在另一个实施方式中,所述添加剂是氨基醇和有机酸的组合。所述添加剂还可以包括羟基酮、羟基内酯、羟基酸、羟基酯或羟基酰胺;葡糖酸内酯或核糖酸内酯;葡甲胺盐/乳酸、葡甲胺盐/龙胆酸、葡甲胺盐/乙酸、乳糖酸、聚乙二醇去水山梨糖醇单月桂酸酯(Tween 20/山梨糖醇)、Tween 20/乳糖酸、Tween20/糖或糖衍生物、和N-辛酰基N-甲基葡糖胺;维生素或其衍生物;氨基酸或其衍生物;蛋白或其衍生物;或胚乳。所述添加剂可溶于水性溶剂,并且可溶于有机溶剂。在多个实施方式中,所述添加剂是有机酸或其酸酐。在其他实施方式中,所述添加剂选自去水山梨糖醇油酸酯和去水山梨糖醇脂肪酸酯。
在多个实施方式中,涂层124的添加剂可包括亲水部分和药物亲和部分,其中所述添加剂选自对-异壬基苯氧基聚缩水甘油、PEG月桂酸酯、PEG油酸酯、PEG硬脂酸酯、PEG月桂酸甘油酯、吐温(Tween)20、吐温40、吐温60、PEG油酸甘油酯、PEG硬脂酸甘油酯、月桂酸聚甘油酯、油酸聚甘油酯、肉豆蔻酸聚甘油酯、棕榈酸聚甘油酯、聚甘油基-6月桂酸酯、聚甘油基-6油酸酯、聚甘油基-6肉豆蔻酸酯、聚甘油基-6棕榈酸酯、聚甘油基-10月桂酸酯、聚甘油基-10油酸酯、聚甘油基-10肉豆蔻酸酯、聚甘油基-10棕榈酸酯、PEG去水山梨糖醇单月桂酸酯、PEG去水山梨糖醇单月桂酸酯、PEG去水山梨糖醇单油酸酯、PEG去水山梨糖醇硬脂酸酯、PEG油酰基醚、PEG月桂醚、辛苯聚醇、单人参醇、泰洛沙泊(tyloxapol)、蔗糖单棕榈酯、蔗糖单月桂酸酯、癸酰-N-甲基葡糖酰胺、正-癸基-β-D-吡喃葡糖苷、正-癸基-β-D-麦芽吡喃糖苷、正-十二烷基-β-D-吡喃葡糖苷、正-十二烷基-β-D-麦芽苷、庚酰基-N-甲基葡糖胺、正-庚基-β-D-吡喃葡糖苷、正-庚基-β-D-硫葡糖苷、正-己基-β-D-吡喃葡糖苷、壬酰-N-甲基葡糖胺、正-酰基(n-noyl)-β-D-吡喃葡糖苷、辛酰基-N-甲基葡糖胺、正-辛基-β-D-吡喃葡糖苷、辛基-β-D-硫吡喃葡糖苷;半胱氨酸、酪氨酸、色氨酸、亮氨酸、异亮氨酸、苯丙氨酸、天冬酰胺、天冬氨酸、谷氨酸和甲硫氨酸;醋酸酐、苯酐、抗坏血酸、2-吡咯烷酮-5-羧酸、吡咯烷酮羧酸钠,乙二胺四乙酸二酐,马来酸酐、琥珀酸酐、二甘醇酐、戊二酸酐、二乙酰硫胺、苯磷硫胺、泛酸、乙氧羰硫胺、环硫胺、右泛醇、烟酰胺、烟酸、5-磷酸吡哆醛、烟酰胺抗坏血酸、核黄素、磷酸核黄素、硫胺素、叶酸、二磷酸甲萘氢醌、亚硫酸氢钠甲萘醌、甲萘多昔、维生素B12、维生素K5、维生素K6、维生素K6、和维生素U(S-甲基甲硫氨酸);白蛋白、免疫球蛋白、酪蛋白、血红蛋白、溶菌酶、免疫球蛋白、a-2巨球蛋白、纤连蛋白、玻连蛋白、血纤蛋白原、脂肪酶、苯扎氯铵、苄索氯铵、十二烷基三甲基溴化铵、十二烷基硫酸钠、二烷基二甲基苄基氯化铵和磺基琥珀酸钠的二烷基酯、L-抗坏血酸及其盐、D-葡糖抗坏血酸及其盐、氨丁三醇、三乙醇胺、二乙醇胺、葡甲胺、葡萄糖胺、胺醇、葡庚糖酸,葡萄糖酸、羟基酮、羟基内酯、葡糖酸内酯、葡庚糖酸内酯、葡辛糖酸内酯、古罗糖酸内酯、甘露糖酸内酯、核糖酸内酯、乳糖酸、氨基葡萄糖,谷氨酸、苄醇、苯甲酸、羟基苯甲酸、4-羟基苯甲酸丙酯、赖氨酸醋酸盐、龙胆酸、乳糖酸、乳糖醇、芥子酸、香草酸、香兰素、羟基苯甲酸甲酯、羟基苯甲酸丙酯、山梨醇、木糖醇、环糊精、(2-羟基丙基)-环糊精,对乙酰氨基酚,布洛芬,视黄酸、赖氨酸醋酸盐、龙胆酸、儿茶素,儿茶素没食子酸、替来他明、氯胺酮,丙泊酚,乳酸、乙酸、任何有机酸和有机胺的盐、聚甘油醇、甘油、多甘油、半乳糖醇、双(乙二醇)、三(乙二醇)、四(乙二醇)、五(乙二醇)、聚(乙二醇)低聚物、双(丙二醇)、三(丙二醇)、四(丙二醇)和五(丙二醇)、聚(丙二醇)低聚物和其衍生物和它们的组合。
在多个实施方式中,涂层124的赋形剂是有机添加剂。例如,所述有机添加剂可包括至少一种对-氨基苯甲酸、糖精、抗坏血酸、羟苯甲酸甲酯、咖啡因、水杨酸钙、喷替酸、肌酸酐、乙基脲、乙酰氨基酚、阿司匹林、可可碱、色氨酸、琥珀酸、戊二酸、己二酸、茶碱、和糖精钠。合适地,所述(至少一种)有机添加剂独立选自以下列表:对氨基苯甲酸、对羟基苯甲酸甲酯、咖啡因、水杨酸钙和琥珀酸。在一个实施方式中,有机添加剂是琥珀酸。在另一个实施方式中,有机添加剂是咖啡因。合适地,所述(至少一种)有机添加剂独立选自以下列表:对氨基苯甲酸、对羟基苯甲酸甲酯、咖啡因、水杨酸钙和琥珀酸。在一个实施方式中,有机添加剂是琥珀酸。
在多个实施方式中,涂层124可以通过超高效液相色谱(UPLC)和/或通过质谱进行分子来确定涂料层或涂料组合物中紫杉醇的量。当固体涂层中紫杉醇的重量%已知时,如在二元涂层或组合物(即,紫杉醇+仅一种有机添加剂)的情况中,则有机添加剂的重量%可容易地确定为100-紫杉醇重量%。
在一个实施方式中,涂层124中治疗剂即紫杉醇的重量%为约5重量%至约95重量%,例如,约10重量%至约95重量%、约20重量%至约95重量%、约30重量%至约90重量%、约45重量%至约85重量%、约55重量%至约70重量%、约40重量%至约80重量%、约25重量%至约95重量%、约30重量%至约85重量%、约70重量%至约95重量%、70重量%至约80重量%或约75重量%至约80重量%。
在一个实施方式中,有机添加剂是PABA并且涂层124中紫杉醇的重量%为约30重量%至约90重量%,例如约40重量%至约80重量%。在一个实施方式中,有机添加剂是PABA并且固体组合物或涂层中紫杉醇:PABA的比率(重量%)为约3:7至约9:1,例如约2:3至约4:1。
在一个实施方式中,有机添加剂是羟苯甲酸甲酯并且涂层124中紫杉醇的重量%为约45重量%至约85重量%,例如约55重量%至约70重量%。在一个实施方式中,有机添加剂是羟苯甲酸甲酯并且固体组合物或涂层中紫杉醇:羟苯甲酸甲酯的比率(重量%)为约4:5至约9:1,例如约1:1至约7:3。
在一个实施方式中,有机添加剂是咖啡因并且涂层124中紫杉醇的重量%为约70重量%至约95重量%,例如约75重量%至约90重量%。在一个实施方式中,有机添加剂是咖啡因并且固体组合物或涂层中紫杉醇:咖啡因的比率(重量%)为约7:3至约95:5,例如约3:1至约9:1重量%。
在一个实施方式中,有机添加剂是水杨酸钙并且涂层124中紫杉醇的重量%为约70重量%至约90重量%,例如约75重量%至约80重量%。在一个实施方式中,有机添加剂是水杨酸钙并且固体组合物或涂层中紫杉醇:水杨酸钙的比率(重量%)为约7:3至约9:1,例如约3:1至约4:1。
在一个实施方式中,有机添加剂是琥珀酸并且涂层124中紫杉醇的重量%为约70重量%至约90重量%,例如约75重量%至约85重量%。在一个实施方式中,有机添加剂是琥珀酸并且固体组合物或涂层中紫杉醇:琥珀酸的比率(重量%)为约7:3至约9:1,例如约3:1重量%至约6:1。
在一个实施方式中,有机添加剂选自下组:对氨基苯甲酸(PABA)、糖精、抗坏血酸、对羟基苯甲酸甲酯、咖啡因、水杨酸钙、喷替酸、肌酸酐、乙基脲、对乙酰氨基酚、阿司匹林、可可碱、色氨酸、琥珀酸、戊二酸、己二酸、茶碱、和糖精钠,并且固体组合物或涂层中紫杉醇的重量%是约30重量%至约90重量%,如约50重量%至约90重量%。
在一个实施方式中,有机添加剂选自下组:对氨基苯甲酸、糖精、抗坏血酸、对羟基苯甲酸甲酯、咖啡因、水杨酸钙、喷替酸、肌酸酐、乙基脲、对乙酰氨基酚、阿司匹林、可可碱、色氨酸、琥珀酸、戊二酸、己二酸、茶碱、和糖精钠,并且紫杉醇:有机添加剂的比率(重量%)是约3:7至约9:1,如约1:1至约9:1。
在一个实施方式中,有机添加剂选自下组:对氨基苯甲酸、对羟基苯甲酸甲酯、咖啡因、水杨酸钙和琥珀酸,并且固体组合物或涂层中紫杉醇的重量%为约30重量%至约90重量%,如约50重量%至约90重量%。
在一个实施方式中,有机添加剂选自以下列表:对氨基苯甲酸、对羟基苯甲酸甲酯、咖啡因、水杨酸钙和琥珀酸,并且紫杉醇:有机添加剂的比率(重量%)为约3:7至约9:1,如约1:1至约9:1。
在一个实施方式中,有机添加剂是硬脂酸三(羟甲基)-甲基铵,涂层中紫杉醇的重量%为约80重量%至约99重量%。
在多个实施方式中,涂层124可进一步包括亲水涂层。适用于亲水涂层的组分包括但不限于:离子型表面活性剂,包括苄索氯铵(例如)、苯扎氯铵、西吡氯铵、西他氯铵、月桂基三甲基溴化铵(laurtrimonium bromide)、肉豆蔻基三甲基溴化铵、溴棕三甲铵、西曲溴铵、硬脂氯铵(stearalkonium chloride)、n,n-二甲基烟碱、胆固醇、水杨酸钙、水杨酸甲酯、水杨酸钠、α-生育酚、硫胺、烟酰胺、二甲亚砜、泊洛沙姆(poloxamer)(如101,105,108,122,123,124,181,182,183,184,185,188,212,215,217,231,234,235,237,238,282,284,288,331,333,434,335,338,401,402,403和407)、去水山梨糖醇单月桂酸酯、聚山梨酯20、聚山梨酯40、聚山梨酯60、聚山梨酯80、聚乙烯醇、聚乙二醇(PEG,分子量范围400-50,000,优选700-15,000)、PEG-胺、PEG-改性的生物药物和/或分子、PEG胺(包括叠氮PEG胺和PEG二胺)、(聚氧亚烷基胺)、季铵化合物、1,2-二四癸酰基-sn-甘油-3-磷脂酰胆碱、1,2-二肉豆蔻酰基-sn-甘油-3-磷脂酰-外消旋-(1-甘油)、1,2-二肉豆蔻酰基-sn-甘油-3-磷脂酰胆碱、聚丙二醇、肝素、或肝素衍生物、右旋糖苷、琼脂糖、包括络合物如环状寡糖,例如环糊精及其衍生物,包括羟丙基-β-环糊精(HPβCD)、(CyDex药物有限公司的商品),二甲基-β-环糊精、α-环糊精(αCD)、藻酸盐、聚丙烯酰胺、聚缩水甘油、聚(乙烯醇-共-乙烯)、聚(乙二醇-共-丙二醇)、聚(乙酸乙酯-共-乙烯醇)、聚(四氟乙烯-共-乙烯醇)、聚(丙烯腈-共-丙烯酰胺)、聚(丙烯腈-共-丙烯酸-共-丙烯酰胺)、聚丙烯酸、聚-赖氨酸、聚亚乙基酰亚胺、聚乙烯吡咯烷酮、聚羟乙基甲基丙烯酸酯、环糊精、γ-环糊精、磺基丁基醚-β-环糊精和聚砜、聚多糖及其共聚物、紫胶酸、异内酰胺(ipromide)、脲,单独或组合使用。其他涂层是本领域已知的,参见例如美国专利公开20100233266,通过引用其全文纳入本文用于所有目的,也可以用作本发明的一部分。在其他实施方式中,涂层124是肝素涂层,如美国专利4,810,784和6,559,131中所描述的那些。
涂层124可以进一步包括例如至少一种治疗剂126。在本文中,“治疗剂”可以与术语“药物”互换使用,是诱导生物活性响应的试剂。这种试剂包括但不限于:西洛他唑、热激蛋白、双香豆素、佐他莫司、卡维地洛;抗血栓剂如肝素、肝素类衍生物、尿激酶、右旋苯丙氨酸脯氨酸精氨酸氯甲基酮(dextrophenylalanine proline argininechloromethylketone);消炎剂如地赛米松、泼尼松龙、皮质酮、布地奈德、雌激素、柳氮磺吡啶和美沙拉秦、西罗莫司、和热激蛋白(及相关的类似物);抗肿瘤/抗增殖/抗有丝分裂剂如紫杉烷主域-结合药物,例如紫杉醇及其类似物、大环内酯、淅皮海绵内酯、多西他赛、紫杉醇蛋白质结合的颗粒如(ABRAXANE是阿博利斯生物科学公司(ABRAXISBIOSCIENCE,LLC)的注册商标)、紫杉醇与合适的环糊精(或像环糊精的分子)的复合物、雷帕霉素及其类似物、雷帕霉素及其类似物与合适的环糊精(或像环糊精的分子)的复合物,17β-雌二醇、17β-雌二醇与合适的环糊精的复合物、双香豆素、双香豆素与合适的环糊精的复合物、β-拉帕醌及其类似物、5-氟尿嘧啶、顺铂、长春花碱、克拉屈滨、长春新碱、埃博霉素、内皮他丁、血管他丁、血管肽素、能够阻断平滑肌细胞增殖的单克隆抗体和胸腺嘧啶抑制剂;裂解剂、麻醉剂如利多卡因、布比卡因和罗哌卡因;抗凝血剂如D-Phe-Pro-Arg氯基甲酮、含有RGD的肽化合物、模拟HSP20的AZX100细胞肽(美国顶点治疗公司(CapstoneTherapeutics Corp.,USA))、肝素、水蛭素、抗凝血酶化合物、血小板受体拮抗剂、抗凝血酶抗体、抗血小板受体抗体、阿司匹林、前列腺素抑制剂、血小板抑制剂、和蜱抗血小板肽;血管细胞生长促进因子如生长因子、转录激活子和翻译启动子;血管细胞生长抑制剂如生长因子抑制剂、生长因子受体拮抗剂、转录阻抑物、辅助抑制剂、抑制性抗体、针对生长因子的抗体、由生长因子和细胞毒素组成的功能性分子a)、由抗体和细胞毒素组成的功能性分子b);蛋白质激酶和酪氨酸激酶抑制剂(例如,酪氨酸磷酸化抑制剂、染料木黄酮、喹嗯啉);前列环素类似物;降胆固醇剂;血管生成素;杀菌剂如三氯生、头孢菌素、氨基葡糖苷和呋喃妥因;细胞毒剂、细胞生长抑制剂和细胞增殖影响因子;血管舒张剂;干扰内源血管作用机理的制剂;白细胞募集抑制剂如单克隆抗体;细胞因子;激素;辐射不透性试剂例如碘化造影剂、金或钡;及其组合。合适地,其他涂层包含肝素。
在多个实施方式中,涂层124包括使疏水性治疗剂126的溶解度点升高的至少一种亲水性组分。在本文中,术语“使疏水性治疗剂的溶解度点升高”表示在室温和标准大气压条件下,疏水性治疗剂126在净去离子水中的浓度增加,比治疗剂126的最大溶解度高至少10%。这通常是因为存在使溶解度增加的其他试剂(即,涂层124中的亲水组分)。这仍使得一部分治疗剂126不能溶解于水中。例如,在室温下在净去离子水中紫杉醇的溶解度极限为约0.4μM。添加浓度为60%(w/v,在水中)的羟丙基-β-环糊精使溶液中紫杉醇的溶解浓度升高至约4mM,远高于溶解度增加10%(Sharma等,Journal of Pharmaceutical Sciences84,1223(1995))。
在多个实施方式中,疏水性治疗剂126用一种或多种增溶剂隔离或与一种或多种增溶剂螯合,这样当递送至目标组织位点时,药物从增溶剂中解离并与组织结合。这种增溶剂是本领域已知的(参见例如美国专利20080118544)。
治疗剂126可以以多种结构形式递送至组织,所述结构形式包括但不限于胶束、脂质体、微-团聚体、纳米球、微球、纳米颗粒、微颗粒、微晶、包合配合物、乳液、凝胶、泡沫、乳霜、悬浮液、共晶、小共晶(perieutectic)、溶液或它们的任意组合。在多个实施方式中,治疗剂126以溶解的形式递送至组织。治疗剂126可以以凝胶形式递送至组织。在其他实施方式中,治疗剂126以能从溶液中沉淀为固体形式的溶解形式递送至组织。在其他实施方式中,治疗剂126以溶解形式和固体形式的组合递送至组织。
气囊104可包括置于涂层124和结构层122之间的附着层。所述附着层是涂层124下方的分离的且不同的层,可以改进涂层124与结构层122的粘附,并进一步保持涂层的完整性,特别是在向需要治疗的组织运送的过程中。在一个实施方式中,附着层包含聚合物,其合适地是生物相容的并避免对身体组织的刺激。这类聚合物的示例包括但不限于聚烯烃,聚异丁烯,乙烯-α-烯烃共聚物,丙烯酸聚合物和共聚物,聚乙烯氯,聚乙烯基甲基醚,聚偏二氟乙烯和聚偏二氯乙烯,含氟聚合物,例如,膨胀型聚四氟乙烯(ePTFE)、聚四氟乙烯(PTFE)、氟化乙烯-丙烯(FEP),全氟碳共聚物,例如,四氟乙烯全氟烷基乙烯基醚(TFE/PAVE)共聚物,四氟乙烯(TFE)和全氟甲基乙烯基醚(PMVE)的共聚物,TFE与包括乙酸、醇、胺、酰胺、磺酸功能性基团等的功能性单体的共聚物,如美国专利号8,658,707(戈尔及同仁公司,通过引用纳入本文,及其组合),聚丙烯腈,聚乙烯酮,聚苯乙烯,聚乙酸乙烯酯,乙烯-甲基丙烯酸甲酯共聚物,丙烯腈-苯乙烯共聚物,ABS树脂,尼龙12及其嵌段共聚物,聚己内酯,聚甲醛,聚醚,环氧树脂,聚氨酯,人造丝-三乙酸酯,纤维素,醋酸纤维素,丁酸纤维素,赛璐酚,硝酸纤维素,丙酸纤维素,纤维素醚,羧甲基纤维素,几丁质,聚乳酸,聚乙醇酸,聚乳酸-聚环氧乙烷共聚物,聚乙二醇,聚丙二醇,聚乙烯醇,弹性体聚合物如硅酮(例如,聚硅氧烷和取代的聚硅氧烷),聚氨酯,热塑性弹性体,乙烯乙酸乙烯酯共聚物,聚烯烃弹性体,EPDM橡胶及其混合物。
在另一个实施方式中,包含除紫杉醇之外的治疗剂的其他涂层位于涂层124和结构层122之间。所述涂层是涂层124下方的分开且不同的层,并且可提供除了紫杉醇提供的益处以外的治疗益处,即,允许辅助疗法与紫杉醇-有机添加剂结合。例如,本发明涂层可施加在已经涂覆有固定生物活性肝素涂层的医疗装置上,同时保持两个涂层的活性(即紫杉醇-有机添加剂组合物的抗增殖效应和肝素的抗凝血酶III(ATIII)结核活性,如已知分析方法所测)。因此,具有肝素粘合的下涂层的本发明的涂覆医疗装置在移植后具有使亚急性血栓减少的附加益处。在一个实施方式中,其他涂层包含除紫杉醇以外的治疗剂。或者,包含除紫杉醇以外的治疗剂的所述其他涂层会覆盖涂层124的部分或全部。如上所述,该涂层是覆盖紫杉醇-有机添加剂涂层124的分开且不同的层。
在一个实施方式中,其他涂层含选自下组的治疗剂126:西洛他唑、热激蛋白、双香豆素、佐他莫司、卡维地洛;抗血栓剂如肝素、肝素类衍生物、尿激酶、右旋苯丙氨酸脯氨酸精氨酸氯甲基酮(dextrophenylalanine proline arginine chloromethylketone);消炎剂如地赛米松、泼尼松龙、皮质酮、布地奈德、雌激素、柳氮磺吡啶和美沙拉秦、西罗莫司、和热激蛋白(及相关的类似物);抗肿瘤/抗增殖/抗有丝分裂剂如紫杉烷主域-结合药物,例如紫杉醇及其类似物、大环内酯、淅皮海绵内酯、多西他赛、紫杉醇蛋白质结合的颗粒如(ABRAXANE是阿博利斯生物科学公司(ABRAXIS BIOSCIENCE,LLC)的注册商标)、紫杉醇与合适的环糊精(或像环糊精的分子)的复合物、雷帕霉素及其类似物、雷帕霉素及其类似物与合适的环糊精(或像环糊精的分子)的复合物,17β-雌二醇、17β-雌二醇与合适的环糊精的复合物、双香豆素、双香豆素与合适的环糊精的复合物、β-拉帕醌及其类似物、5-氟尿嘧啶、顺铂、长春花碱、长春新碱、大环内酯,内皮他丁、血管他丁、血管肽素、能够阻断平滑肌细胞增殖的单克隆抗体和胸腺嘧啶抑制剂;裂解剂、麻醉剂如利多卡因、布比卡因和罗哌卡因;抗凝血剂如D-Phe-Pro-Arg氯基甲酮、含有RGD的肽化合物、模拟HSP20的AZX100细胞肽(美国顶点治疗公司(Capstone Therapeutics Corp.,USA))、肝素、水蛭素、抗凝血酶化合物、血小板受体拮抗剂、抗凝血酶抗体、抗血小板受体抗体、阿司匹林、前列腺素抑制剂、血小板抑制剂、和蜱抗血小板肽;血管细胞生长促进因子如生长因子、转录激活子和翻译启动子;血管细胞生长抑制剂如生长因子抑制剂、生长因子抗体拮抗剂、转录阻抑物、辅助抑制剂、抑制性抗体、针对生长因子的抗体、由生长因子和细胞毒素组成的双功能性分子、由抗体和细胞毒素组成的双功能性分子;蛋白质激酶和酪氨酸激酶抑制剂(例如,酪氨酸磷酸化抑制剂、染料木黄酮、喹嗯啉);前列环素类似物;降胆固醇剂;血管生成素;杀菌剂如三氯生、头孢菌素、氨基葡糖苷和呋喃妥因;细胞毒剂、细胞生长抑制剂和细胞增殖影响因子;血管舒张剂;干扰内源血管作用机理的制剂;白细胞募集抑制剂如单克隆抗体;细胞因子;激素;辐射不透性示例例如碘化造影剂、金或钡;及其组合。合适地,其他涂层包含肝素。
在一个实施方式中,所述医疗组织进一步包括覆盖涂层124的保护性顶涂层。顶涂层可进一步使涂层124的紫杉醇-赋形剂在其接触目标组织之前,例如,在装置组装和包装期间,传递到待治疗的部位期间,或者如果该装置是气囊或支架,在挤压涂层与目标组织直接接触之前的膨胀的第一时间期间的损失最小化。在压碎装载期间顶涂层特别有用,例如当可膨胀医疗装置例如气囊、支架、支架-移植物或移植物在收缩至其未膨胀形式之前于其膨胀形式下被涂覆时。涂覆装置的收缩形式通常在使用前长期存放。顶涂层可防止储存期间或展开装置时的膨胀期间涂层124的损失。或者或此外,顶涂层可具有润滑性质亦减小转移时装置上的摩擦力。合适地,顶涂层可降解或溶解并会缓慢释放到体腔中同时保护药物层。若顶涂层包含更多的疏水高分子量添加剂,其溶蚀会更慢。表面活性剂是具有长脂肪链的更疏水结构的示例,例如吐温20和油酸聚甘油酯。高分子量添加剂包括聚环氧乙烷、聚乙二醇和聚乙烯吡咯烷酮。疏水药物本身可作为顶层组分。例如,紫杉醇或雷柏霉素是疏水的。其可用于顶层。另一方面,顶层不能溶蚀太慢或实际上其可能会在靶位置展开期间减缓药物释放。可用作顶层的其他添加剂包括与治疗剂126或涂层124发生强烈相互作用的添加剂,例如对-异壬基苯氧基聚缩水甘油、PEG月桂酸酯、吐温20、吐温40、吐温60、PEG油酸酯、PEG硬脂酸酯、PEG月桂酸甘油酯、PEG油酸甘油酯、PEG硬脂酸甘油酯、月桂酸聚甘油酯、油酸聚甘油酯、肉豆蔻酸聚甘油酯、棕榈酸聚甘油酯、聚甘油基-6月桂酸酯、聚甘油基-6油酸酯、聚甘油基-6肉豆蔻酸酯、聚甘油基-6棕榈酸酯、聚甘油基-10月桂酸酯、聚甘油基-10油酸酯、聚甘油基-10肉豆蔻酸酯、聚甘油基-10棕榈酸酯、PEG单月桂酸去水山梨糖醇酯、PEG单月桂酸去水山梨糖醇酯、PEG单油酸去水山梨糖醇酯、PEG硬脂酸去水山梨糖醇酯、PEG油酰醚、PEG月桂酰醚、辛苯聚醇、单人参醇、泰洛沙泊、蔗糖单棕榈酯、蔗糖单月桂酸酯、癸酰-N-甲基葡糖酰胺、正-癸基-β-D-吡喃葡糖苷、正-癸基-β-D-麦芽吡喃糖苷、正-十二烷基-β-D-吡喃葡糖苷、正-十二烷基-β-D-麦芽苷、庚酰基-N-甲基葡糖胺、正-庚基-β-D-吡喃葡糖苷、正-庚基-β-D-硫葡糖苷、n-己基-β-D-吡喃葡糖苷、壬酰-N-甲基葡糖胺、n-酰基-β-D-吡喃葡糖苷、辛酰基-N-甲基葡糖胺、正-辛基-β-D-吡喃葡糖苷、辛基-β-D-硫吡喃葡糖苷;半胱氨酸、酪氨酸、色氨酸、亮氨酸、异亮氨酸、苯丙氨酸、天冬酰胺、天冬氨酸、谷氨酸和甲硫氨酸;醋酸酐、苯酐、抗坏血酸、2-吡咯烷酮-5-羧酸、吡咯烷酮羧酸钠,乙二胺四乙酸二酐,马来酸酐、琥珀酸酐、二甘醇酐、戊二酸酐、二乙酰硫胺、苯磷硫胺,泛酸;乙氧羰硫胺;环硫胺、右泛醇、烟酰胺、烟酸、5-磷酸吡哆醛、烟酰胺抗坏血酸、核黄素、磷酸核黄素、硫胺素、叶酸、二磷酸甲萘氢醌、亚硫酸氢钠甲萘醌、甲萘多昔、维生素B12、维生素K5、维生素K6、和维生素U;白蛋白、免疫球蛋白、酪蛋白、血红蛋白、溶菌酶、免疫球蛋白、a-2巨球蛋白、纤连蛋白、玻连蛋白、血纤蛋白原、脂肪酶、苯扎氯铵、苄索氯铵、十二烷基三甲基溴化铵、十二烷基硫酸钠、二烷基二甲基苄基氯化铵和磺基琥珀酸钠的二烷基酯、L-抗坏血酸及其盐、D-葡糖抗坏血酸及其盐、氨丁三醇、三乙醇胺、二乙醇胺、葡甲胺、葡萄糖胺、胺醇、葡庚糖酸,葡萄糖酸、羟基酮、羟基内酯、葡糖酸内酯、葡庚糖酸内酯、葡辛糖酸内酯、古罗糖酸内酯、甘露糖酸内酯、核糖酸内酯、乳糖酸、氨基葡萄糖,谷氨酸、苄醇、苯甲酸、羟基苯甲酸、4-羟基苯甲酸丙酯、赖氨酸醋酸盐、龙胆酸、乳糖酸、乳糖、芥子酸、香草酸、香兰素、羟基苯甲酸甲酯、羟基苯甲酸丙酯、山梨醇、木糖醇、环糊精、(2-羟基丙基)-环糊精,对乙酰氨基酚,布洛芬,视黄酸、赖氨酸醋酸盐、龙胆酸、儿茶素,儿茶素没食子酸、替来他明、氯胺酮,丙泊酚,乳酸、乙酸、任何有机酸和有机胺的盐、聚甘油醇、甘油、多甘油、半乳糖醇、双(乙二醇)、三(乙二醇)、四(乙二醇)、五(乙二醇)、、聚(乙二醇)低聚物、双(丙二醇)、三(丙二醇)、四(丙二醇)和五(丙二醇)、聚(丙二醇)低聚物、聚乙二醇和聚丙二醇嵌段共聚物、PTFE、ePTFE和其衍生物或组合。
在多个实施方式中,可以在与气囊104结合的结构组件中形成涂层124。这种构造消除了对结构层122本身的需要,因此完全保留了涂层124提供的重要功能。这种构造还可以改进可制造性,可以与大部分的任意可膨胀部件(如气囊)组合。例如,当医疗装置104包括气囊时,可以由所述涂层的一种或多种材料浇铸或以其他方式形成管状形式,并在放置递送护套120之前设置在气囊104上。在一个实施方式中,这种管状形式可通过将涂层材料溶剂化为粘性状态并通过本领域已知的方法,如凝胶挤出、浇铸、模制或溶液浇铸/成形形成所需的管状形状来制备。接着去除使用的溶剂,以干燥或部分干燥所述管并使其容易放置在气囊104上。
在多个实施方式中,涂层124可以使气囊104非常刚硬。由于其刚性,气囊104难以通过曲折的解剖组织。因此,在一个实施方式中,在将涂层124施用于结构层122和/或气囊104之后,递送护套120在结构层122和/或气囊104上滑动,涂层124由于弯曲和/或翘曲结构层122和/或气囊104而破裂。这可能改进气囊104的适应性同时在治疗之前防止颗粒从递送护套120中逃脱。在其他实施方式中,作为完全涂覆结构层122和/或气囊104的代替,涂层124以“环”形式施加,这样在所述“环”之间,结构层122和/或气囊104是相适应的,这可以允许结构层122和/或气囊104在未涂覆的区域完全或挠曲。在其他实施方式中,除了“环”之外,涂层124可以以挤出的、螺旋向下的连续珠粒形式施用于结构层122和/或气囊104。在其他实施方式中,涂层124可以以离散点或其他形状或离散图案的形式施用于结构层122和/或气囊104。
例如,涂层124可以以不连续的方式施用于结构层122和/或气囊104。例如,涂层124的量或厚度可以随着基材的表面而变化。对于仅在支架的近端和远端需要药物递送的情况,例如,仅向结构层122和/或气囊104的近端和远端部分施用涂层124是希望的,特别是对于治疗或预防支架末端狭窄的情况。类似地,涂层124可随着结构层122和/或气囊104的面积而变化。
如前所述,在多个实施方式中,医疗装置104被可膨胀递送护套120围绕。例如,在医疗装置104追踪并递送至所需治疗位置的过程中,递送护套120可以防止医疗装置104中涂层124和/或治疗剂126大量流出或释放至患者血流中。
例如,递送护套120可以包括非多孔聚合材料或半多孔聚合物材料。例如,除了其他材料之外,递送护套120可以包括PTFE,包括膨胀聚四氟乙烯(ePTFE)、含氟聚合物、膨胀聚乙烯、聚氯乙烯、聚氨酯、硅酮、聚乙烯、聚丙烯、聚氨酯、聚乙醇酸、聚酯、聚酰胺(例如尼龙12,尼龙11,尼龙9,尼龙6/9和尼龙6/6)、聚烯烃、聚醚嵌段酰胺、聚酰亚胺、聚碳酸酯、聚苯硫醚、聚亚苯基氧化物、聚醚、硅酮、苯乙烯聚合物、其共聚物和它们的混合物。如本文所用,术语“共聚物”用于指代由2种或更多种单体,例如,2、3、4、5等种单体形成的任意聚合物。这些材料的一些共聚物的示例包括以的商品名购自宾夕法尼亚州费城的埃尔夫阿托化学北美公司(Elf Atochem North America)的聚醚-嵌段-酰胺。
在多个实施方式中,递送护套120可包括可膨胀聚合物材料,例如,ePTFE的具体形式。此外,递送护套120包括高度取向的聚合物材料。例如,递送护套120可包括具有高度取向节点的聚合物材料。递送护套120可包括卷绕以形成管状结构的这种高度取向膜。在其他实施方式中,递送护套120可包括可膨胀聚合物材料,例如,挤出的ePTFE管。
在多个实施方式中,递送护套120包括通过剥离两个或多个片段将其从气囊104中去除的护套。参照图2A和2B,递送护套120可以包括第一裂开线228a和第二裂开线228b。例如,第一裂开线228a和第二裂开线228b可包括当在特定位置沿具体方向向递送护套施加张力时,递送护套120将沿其裂开的线,这样套筒可以沿第一裂开线228a和第二裂开线228b裂开。在多个实施方式中,递送护套120包括这样的高度取向的膜:当施加张力时,第一裂开线228a和第二裂开线228b表示该膜将沿其“自然”裂开的线。例如,膜中“自然”裂开的线可以沿材料中的节点和纤维的取向方向对齐。在多个实施方式中,递送护套120材料的节点和纤维进行取向,这样裂开线228a和228b与导管102相对平行。虽然对两条裂开线进行了描述,但递送护套120可以包括任意数量的裂开线。
例如,裂开线228a和228b可以包括沿递送护套120的远端和近端之间的纵向方向行进的相对直的线。在其他实施方式中,裂开线228a和228b可以非线性线,如曲线或螺旋线,其总体上沿递送护套120的远端和近端之间的纵向方向行进。虽然对具体形状和构造(例如线性、弯曲、螺旋)进行了描述,裂开线228a和228b可以包括任何形状和构造的线。
例如,递送护套120可进一步包括第一片段230和第二片段232。在多个实施方式中,第一片段230可包括递送护套120在第一裂开线228a和第二裂开线228b之间的部分。在多个实施方式中,第二片段232可包括递送护套120在第一裂开线228a和第二裂开线228b之间且与第一片段230相对的部分。在多个实施方式中,第一片段230和第二片段232具有类似的形状和构造。例如,在第一裂开线228a和第二裂开线228b包括沿递送护套120长度延伸的相对纵向线的实施方式中,第一片段230和第二片段232具有类似或相同的片段。换言之,在多个实施方式中,第一裂开线228a和第二裂开线228b将递送护套120对切为具有近似相等的尺寸和形状的第一片段230和第二片段232。在其他实施方式中,第一片段230和第二片段232具有不同的形状和构造。如上对于第一裂开线228a和第二裂开线228b所述,递送护套120可包括任意数量的片段。
在多个实施方式中,第一片段230包括第一启动线240。例如,可以对第一启动线进行构造,以激发和控制沿第一裂开线228a和/或第二裂开线228b撕裂或裂开。例如,当需要去除递送护套120时,可以拉扯第一启动线240,使第一裂开线228a和/或第二裂开线228b撕裂,进而使得第一片段230与递送护套120分离,并朝向延长件102的近端106剥离。例如,第一启动线240可包括与第一片段230的一端连接的线、纱、带或金属丝。在其他实施方式中,第一启动线240包括第一片段230的锥形部分或延长部分。能剥离第一片段230的第一启动线240的任何构造均落入本公开的范围内。
在多个实施方式中,第一启动线240从延长件102的近端106朝向远端108行进,通过第一出口350将延长件102退出。当朝向延长件102的近端106牵拉第一启动线240时,第一片段230沿第一裂开线228a和第二裂开线228b从气囊104的外表面剥离,暴露出部分气囊104。
与第一启动线240相似,可以朝向延长件102的近端106牵拉第二启动线242,以从气囊104剥离第二片段232。在多个实施方式中,第二启动线242在第一启动线240之后进行活化。这是为了避免外递送护套120全部翻转。当护套或套筒的整个直径从气囊的一端朝向另一端翻转时,发生全部外翻。以这种构造形式,所述套筒或护套保持为完整的单个套筒,不能以套筒或护套片段的形式通过入口350和/或252缩回。
在多个实施方式中,第一启动线240的长度比第二启动线242短。在该实施方式中,第一启动线240和第二启动线242同时启动。由于第二启动线242比第一启动线240长,第二片段232将在第一片段230之后开始剥离。第一启动线240和第二启动线242可具有允许第一片段230和第二片段232彼此独立地剥离的任何构造。
参照图3,第一片段230和/或第二片段232还可以包括,例如,表面334。在多个实施方式中,表面334可包括纹理、凸出、尖峰、刻痕、凹陷、沟、涂层、颗粒等。例如,表面334可以修饰将(或已经)向其中递送治疗剂的组织、控制本发明系统的放置、和引导流体转移。此外,表面334可有助于增加治疗剂转移至更深的组织上,或更深入地和/或进入更深的组织中。此外,表面334的涂层可辅助所述护套材料的微观润湿。在多个实施方式中,表面334包括交联的聚乙烯醇的涂层(参见例如美国专利7,871,659)。在另一实施方式中,表面334的所述涂层包括肝素涂层,如美国专利第4,810,784号、第6,559,131号所述,以上两篇的全部内容通过引用纳入本文用于所有目的。
参照图4A和4B,启动线240和242可以位于递送护套120的内表面(如表面334)和气囊104的外表面之间。在多个实施方式中,向启动线240和242施加张力可以将第一片段230和第二片段232向内翻转,这样该部分在表面334和气囊104的外表面之间行进。这与如图3A和3B所示,第一片段230和第二片段232向外剥离并且不在表面334和气囊104的外侧部分之间行进的实施方式相反。
参照5A和5B,启动线240和242可位于递送护套120内。在多个实施方式中,启动线240和242可位于递送护套120的层内,这样当向启动线240和242施加张力时,第一片段230和第二片段232在递送护套120内被剥离。换言之,递送护套120其本身折叠为第一片段230和第二片段232,通过启动线240和242被剥离。
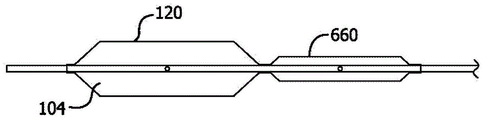
参照图6A-6D,递送护套120可以通过膨胀二级气囊660转换为第一片段230和第二片段232。例如,在气囊104充分膨胀时,二级气囊660开始膨胀。在多个实施方式中,二级气囊660的顺应性与气囊104的顺应性相比更高,这样第二气囊660不会膨胀超过所需的膨胀直径,直至气囊104完全膨胀。二级气囊660可被二级护套662围绕。在多个实施方式中,第一启动线240和第二启动线242与第二护套662附连。在这种实施方式中,当二级气囊660膨胀超过预定的膨胀水平时,二级护套662开始回缩,向第一启动线240和第二启动线242施加张力。该张力导致递送护套120沿裂开线228a和228b裂开,朝二级气囊660翻转。
虽然前述段落结合具体构造进行了描述,能使得第一片段230和第二片段232裂开、剥离并从气囊104去除的任何构造的启动线240和242都落入本公开的范围内。
在另一实施方式中,递送护套120可含有或用辐射不透性标记物标记,或者其整体被构建为辐射不透性。临床医师使用这类辐射不透性指示剂以合适地追踪并放置本发明的可膨胀医疗装置。
在另一实施方式中,可膨胀装置(如支架或支架移植物)可以安装在气囊104上并递送至体内该可膨胀装置膨胀和放置的位点。该应用的优点是治疗剂可以与所述可膨胀装置进行递送的同时递送至治疗区域。这避免了临床医师不得不在支架递送气囊和药物递送气囊之间进行转换。在一个实施方式中,由气囊可膨胀材料,例如不锈钢制作支架。在另一个实施方式中,由自膨胀材料,例如镍钛诺(Nitinol)制作支架。在另一个实施方式中,由生物可降解材料(如生物可降解聚合物)、金属或金属合金制作支架。在另一个实施方式中,支架与移植物附连。在多个实施方式中,所述移植物包括ePTFE。
本公开的医疗装置递送系统适用于广泛应用,包括例如体内的医学治疗应用范围。示例性的应用包括用作转移药物、放置或“修饰”植入的血管移植物、支架、支架移植物、永久或临时假体、或其他类型的医疗植入物的导管气囊,在体内治疗靶组织和治疗任何体腔、空间、或中空器官通道,如血管、泌尿道、肠道、鼻腔、神经护套、椎间区、骨腔、食道、宫腔空间、胰腺和胆管、直肠和之前已经介入的具有可植入血管移植物、支架、假体或其他类型的医疗植入物的身体空间。其他例子包括用于从血管内去除障碍如血栓和栓塞,用作恢复堵塞的体内通道畅通的扩张装置,用作选择性的递送方法(means)以堵塞或填充通道或空间的堵塞装置,以及作为穿腔仪器如导管的居中机械的气囊。在一个实施方式中,本公开的医疗装置递送系统可用于治疗支架再狭窄或处理先前放置的药物洗脱结构已失效的组织位点。在另一个实施方式中,本公开的医疗装置递送系统可用于建立或维持动静脉可及位点,例如,在肾透析期间使用的那些。在一个实施方式中,根据本公开的递送系统可包括用于外周动脉阻塞性疾病患者的经皮穿刺动脉成形术(PTA)的医疗气囊。在另一实施方式中,本发明提供的医疗装置可用于治疗冠状动脉狭窄或阻塞。
在其他实施方式中,根据本公开的递送系统可以以不同于径向圆形的构造施用。例如,这种系统可以与平面装置如伤口辅料、可移植贴片(包括脉管和疝气贴片)、透皮贴片、滤器、多种装置递送组件、封堵器和整形植入物组合使用。在一个实施方式中,这种系统可以结合至可移植导线(例如心脏或神经模拟导线)中,前提是导线与可膨胀部件相容,例如具有可定位可膨胀部件的腔体或袋的特征。
在另一个实施方式中,本公开的递送系统可以与封堵装置(如靠近所述装置放置的气囊)组合。所述封堵装置可以减少远离治疗区域的药物的移动。在一个实施方式中,被该系统隔离的体液可以在去除该系统之前通过吸除从体内抽出。
在多个实施方式中,可以使用医疗装置递送系统100向患者的脉管系统提供治疗。例如,治疗方法可包括将可膨胀医疗装置(如气囊104)和径向可膨胀护套(如递送护套120)推进至患者体内的治疗区域,所述径向可膨胀护套围绕所述可膨胀医疗装置的至少一部分。此外,所述方法可以包括沿着两个裂开线(如裂开线228a和228b)向启动线(如第一启动线240和/或第二启动线242)施加张力以使递送护套裂开,从而形成第一护套片段和第二护套片段(如第一片段230和第二片段232)。在多个实施方式中,所述方法还包括将所述第一护套片段从患者身上去除。如前所述,可以手动、通过二级气囊或以任意其他合适的方式向所述启动线施加张力。
在多个实施方式中,用于治疗患者脉管系统的方法还包括在从患者移除所述第一护套片段之后和移除所述第二护套片段之前对所述可膨胀医疗装置进行取向。在该实施方式中,在所述装置(例如气囊104)放置在患者体内预定的且需要的治疗区域后再移除所述护套片段。
在一个实施方式中,所述气囊104的膨胀直径为约4毫米、约5毫米、约6毫米、约7毫米、约8毫米、约9毫米或约10毫米(直径),长度范围为从约30至约150毫米。在另一个实施方式中,所述导管的长度范围为约90-150cm。在另一个实施方式中,在引入体内血管、体腔或输送管之前气囊104的尺寸为约5,6,7,8,9或10French(Fr)。
在一个实施方式中,可移除的递送护套具有至少一部分被织构化的内层(面向体腔层),从而在护套递送期间与血管壁接触。在其他实施方式中,在气囊上使用多个可移除递送护套,所述多个可移除递送护套中的至少一个包括药物涂层。在一个实施方式中,所述可移除递送护套的内层(面向体腔层)的至少一部分包括药物层。在多个实施方式中,移除多个包括药物涂层的可移动递送护套中的两个将所述护套的内层暴露与血管壁接触,从而得到用于进一步药物治疗的血管壁。在多个实施方式中,可移动递送护套的内层(面向体腔层)包括药物涂层,在可膨胀医疗装置膨胀至所需膨胀直径时,向启动线施加张力,第一护套片段在所述护套的第一层和所述护套的第二层之间翻转,以被放置为与血管壁充分接触,从而得到用于进一步治疗的血管壁。在另一实施方式中,可移动递送护套的内表面包括药物涂层,当可膨胀医疗装置膨胀至所需膨胀直径时,向所述启动线施加张力,所述第一片段在所述嵌的第一层和第二层之间翻转,从而将药物从所述护套的内表面递送至治疗区域。
实施例1
本实施例描述了根据本发明施用于医疗气囊的裂开的可回缩气囊盖的构造。
获得具有如下性质的膨胀聚四氟乙烯(ePTFE)膜:宽度120mm,质量每单位面积约2.43g/m2,厚度约0.0089mm,密度约0.27g/cc,纵向基质拉伸强度约649MPa,横向基质拉伸强度约10.5MPa,异丙醇(IPA)泡点约4.83kPa。
获得长30cm,直径6.4mm的不锈钢心轴。将5层ePTFE膜卷绕在心轴上,ePTFE原纤维总体上平行于心轴的纵向方向取向。得到的ePTFE管长度为120mm。
获得具有如下性质的第二ePTFE膜:宽度25.4mm,质量每单位面积约2.66g/m2,厚度约0.0064mm,密度约0.42g/cc,纵向基质拉伸强度约655MPa,横向基质拉伸强度约16.6MPa,IPA泡点约140.0kPa。
以与心轴的纵轴呈45°角在120mm ePTFE管上螺旋卷绕第二ePTFE膜,每个后续层覆盖之前的层50%,这样完全缠绕120mm管。在缠绕过程中,施加张力,这样第二膜在施用于所述管时,所述第二膜发生颈缩至宽度约15mm。持续卷绕直至四层膜缠绕在所述管上。
在380℃对缠绕的120mm ePTFE管和心轴进行热处理4分钟。冷却至室温之后,移除第二ePTFE膜,在心轴上留下原始的120mm管。在确认所述管的膜层彼此粘附之后,将所述管从心轴上去除。对所述管的末端进行修整以产生清晰的边缘。
得到具有直径5mm×长40mm尼龙气囊的非亲水性、经皮穿刺动脉成形术(PTA)气囊导管(BMT-035 08QL-504A,德国巴伐利亚梅金技术公司(Bavaria Medizin Technologie,GmbH))。供应在导管气囊部分上的包装套筒从气囊近端滑落。将直径为0.089mm的刚性PTFE-涂覆的钢丝心轴导入气囊导管的远端导丝腔。120mm ePTFE管的一端在直径方向纵向裂开,长度10mm,产生两个长10mm的半管状翼。抓紧所述翼,以近端方向(即朝向导管轴心)将所述管牵拉到气囊上。所述翼的近端边缘放置为超过近端气囊密封20mm,这样产生覆盖气囊的盖。
将10mm宽的如前所述的第二类型ePTFE膜对所述盖近端的最后5mm以及靠近所述盖端的5mm裸露的气囊导管轴横向卷绕,从而将所述盖固定到导管轴上。向所述卷绕的膜施加Loctite 7701底漆,然后施加Loctite 4981粘合剂(德国杜塞尔多夫的乐泰公司(Loctite Corporation,Dusseldorf,GmbH))并使其干燥,将所述盖粘附到导管轴上。
所述盖的远端沿长度为10mm的直径纵向裂开,这样产生两个宽度相同的半管状翼。180°牵拉分离所述翼,使气囊肩部远端的裂缝蔓延,产生两个展开的突出部。气囊导管的远端顶端和邻近气囊远端肩部的盖的覆盖部分用Loctite 7701上底漆。将一小滴Loctite 4981粘合剂放置在导管距导管顶端约1mm的一侧,相应的展开突出部压向所述导管15秒,从而将其与导管结合。在导管的另一侧重复该步骤,将另一展开突出部粘附在导管上。
包装套筒远端推进,位于靠近气囊近端,用作回缩护套。展开突出部在所述盖近端翻转并附着在回缩护套上,这样一个突出部的端部邻近使用Loctite 7701底漆和Loctite4981粘合剂的另一个突出部的端部,距离为10mm。这在较远端-附着的展开突出部中产生10mm松弛(slack)。
气囊膨胀至6大气压(约85psi)标称膨胀压(NIP),气囊盖在所述气囊表面保持完整。回缩护套沿所述导管轴远端移动,首先在较近端-附着的展开突出部产生张力。回缩护套的进一步近端移动导致气囊盖的一侧从所述气囊的远端部分剥离。回缩护套的连续近端移动在第二较远端-附着的展开突出部上产生张力,接着使气囊盖的另一侧剥离。包装护套的进一步移动使得两个突出部以交错的方式持续裂开并剥离,直至整个气囊暴露。
实施例2
本实施例描述了施用于医疗气囊的裂开的可回缩气囊盖的构造,其中所述盖材料经过处理以使其具有亲水性,这些都根据本发明进行。
裂开的可回缩气囊盖根据实施例1进行组装,使用以下方法用亲水性涂层进行处理。在放置在气囊上之前,将气囊盖完全浸没在100%IPA浴中30秒,然后转移至包含2%聚乙烯醇的去离子(DI)水浴中,使其停留20分钟。然后在DI水中清洗气囊盖15分钟。清洗完成之后,将气囊盖转移至包含2%戊二醛(mL/mL)和1%氢氯酸(mL/mL)的DI水浴中。气囊盖在该浴中保持15分钟,然后转移至DI水中再清洗15分钟。使气囊盖在环境空气中干燥约2小时,然后如实施例1所述放置在气囊上。
实施例3
在本实施例中,通过将根据本发明覆盖的气囊以及未覆盖的对照气囊模拟操作和展开条件,来评价气囊盖对保护药物涂层的有效性。
取9个直径5mm×长40mm的PTA气囊导管(BMT-035 08QL-504A,德国巴伐利亚梅金技术公司)。所有的气囊用紫杉醇(紫杉醇/S,编号N.:3064055,华盛顿州西雅图的Indena美国公司(Indena USA Inc.))和脲(脲U4884,美国密苏里州圣路易斯的西格玛-奥尔德里奇公司)涂覆。紫杉醇和脲以7:1的干重量比混合,溶解于甲醇(HPLC,≥99.9%,美国密苏里州圣路易斯的西格玛-奥尔德里奇公司),得到具有约3%固体的混合物。各气囊导管放置在0.089mm心轴上,然后将其夹在虎钳中,使导管轴向旋转。然后将气囊膨胀至约30psi,导管以60转每分钟(RPM)绕轴旋转,同时使用沿旋转气囊长度移动的100μl吸液管将100μl紫杉醇/脲溶液分配在气囊表面。根据配制物中固体百分数和分配的体积计算施加的紫杉醇的质量。这在每个气囊上沉积的紫杉醇的质量为约2.004mg。
这些气囊中的三个被如实施例1所述制备的裂开的可回缩气囊盖覆盖。这些气囊中的三个被如实施例2所述制备的裂开的可回缩亲水气囊盖覆盖。气囊中剩下的三个保持不被覆盖,作为对照。
为了模拟使用之前在干燥操作过程中可能导致药物涂层损失的条件,将6个覆盖的气囊和3个未覆盖的气囊分别抵住清洁干燥的15ml离心管壁手动敲打30秒。然后移除气囊,提取离心管内容物,通过超高效液相色谱与UV检测(UPLC-UV)分析总紫杉醇含量。
为了模拟追踪至治疗位点的过程中导致气囊中药物损失的条件,将各气囊再浸没在含DI水的清洁的15ml离心管中30秒。溶液中紫杉醇的量用UPLC-UV测量。
在干和湿模拟操作测试中,证明与未覆盖的对照气囊相比,结合了本发明的裂开的可回缩气囊盖的装置具有改进的在气囊上的药物涂层保持性。在湿和干模拟操作测试中回收的紫杉醇比例(以各气囊上涂覆的原始量的百分数计)以图表形式示于图7和表1。
表1
虽然本文阐述和说明了本发明的具体实施方式,但本发明并不限于这些阐述和说明。显而易见的是,在所附权利要求书的范围内,改变和改进可包括在本发明中,作为本发明的一部分实施。
在前文中详细描述了多种特征和益处,包括装置和/或方法的功能和结构的各种变化和细节。本公开内容仅旨在作为说明性的且不旨在是穷尽性的。本领域的技术人员明白,在本公开内容的主题范围内,根据对所附权利要求书所表达的词语的广泛、通用含义的理解,可以做出许多修改,特别是结构、材料、要素、组分、形状、尺寸以及各部分的安排及组合。在这些各种修改不背离所附权利要求的精神和范围的情况下,其旨在包括于本发明中。
Claims (24)
1.一种可移除的递送护套,其包括:
径向可膨胀的管状护套,所述管状护套围绕可膨胀医疗装置的至少一部分,所述护套包括第一护套片段和第二护套片段,以及限定在所述第一和第二护套片段之间的第一裂开线;以及
启动线,所述启动线包括与所述第一护套片段附连的第一部分和与所述第二护套片段附连的第二部分,在护套未剥离时所述第一部分的长度比所述第二部分的长度短,
其中通过向所述启动线施加张力使所述护套构造成沿所述第一裂开线裂开以形成所述第一护套片段和所述第二护套片段,使得所述各第一和第二护套片段构造成从所述可膨胀医疗装置的周围剥离,以及
将所述第一护套片段构造成从所述可膨胀的医疗装置的第一部分的周围剥离,之后从所述可膨胀的医疗装置的第二部分的周围剥离除去所述第二护套片段。
2.如权利要求1所述的可移除的递送护套,其特征在于,所述可膨胀的医疗装置是气囊。
3.如权利要求2所述的可移除的递送护套,其特征在于,所述气囊包括药物涂层。
4.如权利要求1所述的可移除的递送护套,其特征在于,所述护套是疏水性的。
5.如权利要求1所述的可移除的递送护套,其特征在于,所述护套是亲水性的。
6.如权利要求1所述的可移除的递送护套,其特征在于,所述护套包括挤出的聚合物管。
7.如权利要求1所述的可移除的递送护套,其特征在于,所述护套包括卷绕的聚合物材料。
8.如权利要求1所述的可移除的递送护套,其特征在于,所述护套包括可扩张的且高度取向的聚合物材料。
9.如权利要求8所述的可移除的递送护套,其特征在于,所述聚合物材料包括ePTFE。
10.如权利要求1所述的可移除的递送护套,其特征在于,向所述启动线施加张力时,将所述第一护套片段构造成朝向所述可膨胀医疗装置的近端牵拉。
11.如权利要求1所述的可移除的递送护套,其特征在于,向所述启动线施加张力时,将所述第一护套片段朝向所述可膨胀医疗装置的远端牵拉。
12.如权利要求1所述的可移除的递送护套,其特征在于,所述第一护套片段构造成在所述第二护套片段被拉回之前将所述第一护套片段从所述可膨胀医疗装置移除。
13.如权利要求1所述的可移除的递送护套,其特征在于,所述第一护套片段构造成沿着与所述可膨胀医疗装置的纵轴平行的两条裂开线裂开。
14.如权利要求1所述的可移除的递送护套,其特征在于,所述启动线构造成能够向所述启动线手动施加张力。
15.如权利要求2所述的可移除的递送护套,其特征在于,所述可移除的递送护套还包括第二气囊,所述第二气囊的顺应性比所述气囊的顺应性更高并与所述气囊流体连通,当膨胀所述第二气囊时,向所述启动线施加张力。
16.如权利要求1所述的可移除的递送护套,其特征在于,将所述第一护套片段的远端和所述第二护套片段的远端固定在延长件上。
17.如权利要求16所述的可移除的递送护套,其特征在于,通过构造成当所述可膨胀医疗装置膨胀时启动的机械装置将所述第一护套片段和所述第二护套片段固定在延长件上。
18.如权利要求1所述的可移除的递送护套,其特征在于,所述护套包括第一层和第二层,向所述启动线施加张力时,所述第一护套片段构造成在所述护套的第一层和所述护套的第二层之间翻转。
19.如权利要求1所述的可移除的递送护套,其特征在于,所述启动线包括位于所述可膨胀医疗装置的外表面和所述护套的内表面之间的带材。
20.如权利要求1所述的可移除的递送护套,其特征在于,所述可膨胀的医疗装置是支架。
21.如权利要求17所述的可移除的递送护套,其特征在于,不将所述第二片段从所述可膨胀医疗装置中去除。
22.如权利要求2所述的可移除的递送护套,其特征在于,所述护套的内层的一部分是有织纹的。
23.如权利要求22所述的可移除的递送护套,其特征在于,所述护套的内层的一部分包括药物涂层。
24.如权利要求1所述的可移除的递送护套,其特征在于,所述可移除的递送护套还包括围绕所述可膨胀医疗装置的至少一部分的多个径向可膨胀管式护套。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202110096426.1A CN113143558A (zh) | 2014-10-03 | 2015-10-02 | 用于药物释放的医疗装置的可移除覆盖物 |
Applications Claiming Priority (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201462059408P | 2014-10-03 | 2014-10-03 | |
| US62/059,408 | 2014-10-03 | ||
| US201462075574P | 2014-11-05 | 2014-11-05 | |
| US62/075,574 | 2014-11-05 | ||
| US14/872,439 US10569063B2 (en) | 2014-10-03 | 2015-10-01 | Removable covers for drug eluting medical devices |
| US14/872,439 | 2015-10-01 | ||
| PCT/US2015/053770 WO2016054537A1 (en) | 2014-10-03 | 2015-10-02 | Removable covers for drug eluting medical devices |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202110096426.1A Division CN113143558A (zh) | 2014-10-03 | 2015-10-02 | 用于药物释放的医疗装置的可移除覆盖物 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN106794285A CN106794285A (zh) | 2017-05-31 |
| CN106794285B true CN106794285B (zh) | 2021-02-19 |
Family
ID=54293421
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202110096426.1A Pending CN113143558A (zh) | 2014-10-03 | 2015-10-02 | 用于药物释放的医疗装置的可移除覆盖物 |
| CN201580053597.9A Active CN106794285B (zh) | 2014-10-03 | 2015-10-02 | 用于药物释放的医疗装置的可移除覆盖物 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202110096426.1A Pending CN113143558A (zh) | 2014-10-03 | 2015-10-02 | 用于药物释放的医疗装置的可移除覆盖物 |
Country Status (9)
| Country | Link |
|---|---|
| US (2) | US10569063B2 (zh) |
| EP (2) | EP3733136B1 (zh) |
| JP (4) | JP6767364B2 (zh) |
| KR (1) | KR20170068515A (zh) |
| CN (2) | CN113143558A (zh) |
| AU (2) | AU2015327943B2 (zh) |
| CA (1) | CA2960874C (zh) |
| ES (1) | ES2930181T3 (zh) |
| WO (1) | WO2016054537A1 (zh) |
Families Citing this family (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2928646C (en) | 2013-11-08 | 2020-05-05 | Hollister Incorporated | Oleophilic lubricated catheters |
| EP2995339B1 (de) * | 2014-09-15 | 2020-01-08 | Biotronik AG | Ballonkatheter |
| US10569063B2 (en) | 2014-10-03 | 2020-02-25 | W. L. Gore & Associates, Inc. | Removable covers for drug eluting medical devices |
| US10561766B2 (en) * | 2015-09-15 | 2020-02-18 | W. L. Gore & Associates, Inc. | Drug composition and coating |
| CN108295359B (zh) * | 2016-12-30 | 2021-05-07 | 先健科技(深圳)有限公司 | 载药器械及其制备方法 |
| CN107028680A (zh) * | 2017-06-06 | 2017-08-11 | 贾伟 | 一种腔静脉过滤器 |
| EP3533421A1 (de) * | 2018-03-02 | 2019-09-04 | Biotronik AG | Reibkraftminimierung durch unterbindung von proteinadhäsion |
| GB201820899D0 (en) * | 2018-12-20 | 2019-02-06 | Vascutek Ltd | Stent device delivery tool and associated method of use |
| BR112022010919A2 (pt) * | 2019-12-06 | 2022-09-06 | Tufts College | Coquetel de múltiplos fármacos regenerativos de tecido e aparelho para a entrega deste |
| WO2022140628A1 (en) * | 2020-12-22 | 2022-06-30 | Boston Scientific Scimed Inc. | Constraint delivery - hinge & constraint delivery - corset |
| US20220193392A1 (en) * | 2020-12-23 | 2022-06-23 | Boston Scientific Scimed Inc. | Facilitate Delivery of Devices with High Friction - Braid |
| CN112642045A (zh) * | 2021-01-08 | 2021-04-13 | 北京先瑞达医疗科技有限公司 | 一种药物涂层输送装置及其制备方法 |
| US20240091038A1 (en) * | 2022-09-20 | 2024-03-21 | Madan M. Acharya | Splittable delivery sheath |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5269755A (en) * | 1992-09-11 | 1993-12-14 | Sherwood Medical Company | Catheter with outer membrane medicament delivery system |
| CN103501830A (zh) * | 2011-03-04 | 2014-01-08 | W.L.戈尔及同仁股份有限公司 | 洗脱医疗装置 |
Family Cites Families (54)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4306562A (en) * | 1978-12-01 | 1981-12-22 | Cook, Inc. | Tear apart cannula |
| SE8200751L (sv) | 1982-02-09 | 1983-08-10 | Olle Larm | Forfarande for kovalent koppling for framstellning av konjugat och hervid erhallna produkter |
| US4798876A (en) * | 1985-11-12 | 1989-01-17 | Tyndale Plains-Hunter Ltd. | Hydrophilic polyurethane composition |
| US5304121A (en) * | 1990-12-28 | 1994-04-19 | Boston Scientific Corporation | Drug delivery system making use of a hydrogel polymer coating |
| US5195978A (en) | 1991-12-11 | 1993-03-23 | Baxter International Inc. | Rapid exchange over-the-wire catheter with breakaway feature |
| FR2688401B1 (fr) | 1992-03-12 | 1998-02-27 | Thierry Richard | Endoprothese expansible pour organe tubulaire humain ou animal, et outil de mise en place. |
| US5246452A (en) | 1992-04-13 | 1993-09-21 | Impra, Inc. | Vascular graft with removable sheath |
| US5765682A (en) | 1994-10-13 | 1998-06-16 | Menlo Care, Inc. | Restrictive package for expandable or shape memory medical devices and method of preventing premature change of same |
| US6039755A (en) | 1997-02-05 | 2000-03-21 | Impra, Inc., A Division Of C.R. Bard, Inc. | Radially expandable tubular polytetrafluoroethylene grafts and method of making same |
| US5647857A (en) | 1995-03-16 | 1997-07-15 | Endotex Interventional Systems, Inc. | Protective intraluminal sheath |
| DE69626108T2 (de) | 1995-04-14 | 2003-11-20 | Boston Scient Ltd | Stentanbringungsvorrichtung mit rollmembran |
| US5868704A (en) | 1995-09-18 | 1999-02-09 | W. L. Gore & Associates, Inc. | Balloon catheter device |
| US5868707A (en) | 1996-08-15 | 1999-02-09 | Advanced Cardiovascular Systems, Inc. | Protective sheath for catheter balloons |
| DE69726317T2 (de) * | 1996-09-18 | 2004-09-16 | Micro Therapeutics, Inc., Irvine | Intrakranialer stent |
| US6254628B1 (en) | 1996-12-09 | 2001-07-03 | Micro Therapeutics, Inc. | Intracranial stent |
| US6596020B2 (en) * | 1996-11-04 | 2003-07-22 | Advanced Stent Technologies, Inc. | Method of delivering a stent with a side opening |
| EP0952795B1 (en) | 1996-11-15 | 2007-01-03 | Cook Incorporated | Splittable sleeve, stent deployment device |
| US6152944A (en) | 1997-03-05 | 2000-11-28 | Scimed Life Systems, Inc. | Catheter with removable balloon protector and stent delivery system with removable stent protector |
| FR2772618B1 (fr) | 1997-12-18 | 2000-02-18 | Ifremer | Utilisation de fucane comme regulateur de la reconstruction des tissus conjonctifs |
| US8177743B2 (en) * | 1998-05-18 | 2012-05-15 | Boston Scientific Scimed, Inc. | Localized delivery of drug agents |
| DE19936207A1 (de) | 1999-08-02 | 2001-02-15 | Angiomed Ag | Katheter und Einführbesteck mit Trenneinrichtung |
| US6899727B2 (en) | 2001-01-22 | 2005-05-31 | Gore Enterprise Holdings, Inc. | Deployment system for intraluminal devices |
| US20030004561A1 (en) | 2001-06-28 | 2003-01-02 | Steve Bigus | Peeling sheath for self-expanding stent |
| AU2003223749A1 (en) * | 2002-04-25 | 2003-11-10 | The Board Of Trustees Of The Leland Stanford Junior University | Expandable guide sheath and apparatus and methods using such sheaths |
| US6939327B2 (en) | 2002-05-07 | 2005-09-06 | Cardiac Pacemakers, Inc. | Peel-away sheath |
| US20030225439A1 (en) | 2002-05-31 | 2003-12-04 | Cook Alonzo D. | Implantable product with improved aqueous interface characteristics and method for making and using same |
| GB2392460B (en) | 2002-08-29 | 2006-02-08 | Schlumberger Holdings | Delayed-gelation solution |
| US7753945B2 (en) | 2003-01-17 | 2010-07-13 | Gore Enterprise Holdings, Inc. | Deployment system for an endoluminal device |
| US7198636B2 (en) | 2003-01-17 | 2007-04-03 | Gore Enterprise Holdings, Inc. | Deployment system for an endoluminal device |
| US8308789B2 (en) * | 2004-07-16 | 2012-11-13 | W. L. Gore & Associates, Inc. | Deployment system for intraluminal devices |
| US7347868B2 (en) | 2004-10-26 | 2008-03-25 | Baronova, Inc. | Medical device delivery catheter |
| FR2885794B1 (fr) | 2005-05-19 | 2007-08-17 | Perouse Soc Par Actions Simpli | Necessaire de largage d'un organe de traitement d'une cavite et procede de preparation d'un organe de traitement associe |
| US9375215B2 (en) * | 2006-01-20 | 2016-06-28 | W. L. Gore & Associates, Inc. | Device for rapid repair of body conduits |
| US20080175887A1 (en) | 2006-11-20 | 2008-07-24 | Lixiao Wang | Treatment of Asthma and Chronic Obstructive Pulmonary Disease With Anti-proliferate and Anti-inflammatory Drugs |
| US20080140003A1 (en) | 2006-12-06 | 2008-06-12 | Advanced Cardiovascular Systems, Inc. | Balloon catheter having a regrooming sheath and method for collapsing an expanded medical device |
| WO2008121380A1 (en) * | 2007-03-31 | 2008-10-09 | Cook Incorporated | Medical device delivery system with sheath separation |
| US8690823B2 (en) * | 2007-07-13 | 2014-04-08 | Abbott Cardiovascular Systems Inc. | Drug coated balloon catheter |
| EP2190388B1 (en) | 2007-10-17 | 2014-03-05 | Angiomed GmbH & Co. Medizintechnik KG | Delivery system for a self-expanding device for placement in a bodily lumen |
| US20090112239A1 (en) | 2007-10-31 | 2009-04-30 | Specialized Vascular Technologies, Inc. | Sticky dilatation balloon and methods of using |
| EP2273948A4 (en) | 2008-04-03 | 2014-01-01 | Gardia Medical Ltd | DISCONNECTING CATHETER WITH A STOP SLOT AND METHOD FOR STORING MEDICAL DEVICES IN A BODY LUMEN |
| CA2720466A1 (en) | 2008-05-09 | 2009-11-12 | Juergen Dorn | Method of loading a stent into a sheath |
| US20100228333A1 (en) | 2009-03-04 | 2010-09-09 | William Joseph Drasler | Drug eluting surface covering |
| US20100233266A1 (en) | 2009-03-13 | 2010-09-16 | Cleek Robert L | Articles and methods of treating vascular conditions |
| US8658707B2 (en) | 2009-03-24 | 2014-02-25 | W. L. Gore & Associates, Inc. | Expandable functional TFE copolymer fine powder, the expanded functional products obtained therefrom and reaction of the expanded products |
| US20110009943A1 (en) * | 2009-07-09 | 2011-01-13 | Paul Ram H | Delivery system with medical device release by evertable sleeve |
| CN203400395U (zh) | 2009-12-18 | 2014-01-22 | 拜耳制药股份公司 | 撕开护套和气囊导管 |
| JP2013523286A (ja) * | 2010-04-02 | 2013-06-17 | カペラ, インコーポレイテッド | 身体内腔にステントを搬送するためのシステムと方法 |
| US20120172887A1 (en) | 2011-01-05 | 2012-07-05 | Wilson-Cook Medical, Inc. d/b/a Cook Endoscopy | Proximal Release Expandable Prosthesis Delivery System |
| US9415193B2 (en) | 2011-03-04 | 2016-08-16 | W. L. Gore & Associates, Inc. | Eluting medical devices |
| EP3741314B1 (en) * | 2011-05-23 | 2022-12-21 | Covidien LP | Retrieval systems |
| US8414528B2 (en) | 2011-05-27 | 2013-04-09 | Abbott Cardiovascular Systems Inc. | Polymer scaffold sheaths |
| US10173038B2 (en) | 2012-09-05 | 2019-01-08 | W. L. Gore & Associates, Inc. | Retractable sheath devices, systems, and methods |
| US10123805B2 (en) | 2013-06-26 | 2018-11-13 | W. L. Gore & Associates, Inc. | Space filling devices |
| US10569063B2 (en) | 2014-10-03 | 2020-02-25 | W. L. Gore & Associates, Inc. | Removable covers for drug eluting medical devices |
-
2015
- 2015-10-01 US US14/872,439 patent/US10569063B2/en active Active
- 2015-10-02 CA CA2960874A patent/CA2960874C/en active Active
- 2015-10-02 ES ES20180394T patent/ES2930181T3/es active Active
- 2015-10-02 EP EP20180394.7A patent/EP3733136B1/en active Active
- 2015-10-02 CN CN202110096426.1A patent/CN113143558A/zh active Pending
- 2015-10-02 EP EP15779159.1A patent/EP3200732B1/en active Active
- 2015-10-02 CN CN201580053597.9A patent/CN106794285B/zh active Active
- 2015-10-02 WO PCT/US2015/053770 patent/WO2016054537A1/en active Application Filing
- 2015-10-02 JP JP2017517099A patent/JP6767364B2/ja active Active
- 2015-10-02 KR KR1020177012201A patent/KR20170068515A/ko unknown
- 2015-10-02 AU AU2015327943A patent/AU2015327943B2/en active Active
-
2019
- 2019-01-11 AU AU2019200196A patent/AU2019200196B2/en active Active
- 2019-03-20 JP JP2019053093A patent/JP6849725B2/ja active Active
-
2020
- 2020-02-06 US US16/783,612 patent/US11679240B2/en active Active
- 2020-12-18 JP JP2020210462A patent/JP7326245B2/ja active Active
-
2022
- 2022-08-05 JP JP2022125772A patent/JP2022169605A/ja active Pending
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5269755A (en) * | 1992-09-11 | 1993-12-14 | Sherwood Medical Company | Catheter with outer membrane medicament delivery system |
| CN103501830A (zh) * | 2011-03-04 | 2014-01-08 | W.L.戈尔及同仁股份有限公司 | 洗脱医疗装置 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3200732A1 (en) | 2017-08-09 |
| AU2019200196A1 (en) | 2019-01-31 |
| ES2930181T3 (es) | 2022-12-07 |
| EP3733136A1 (en) | 2020-11-04 |
| JP2022169605A (ja) | 2022-11-09 |
| US11679240B2 (en) | 2023-06-20 |
| JP7326245B2 (ja) | 2023-08-15 |
| US20200188645A1 (en) | 2020-06-18 |
| EP3733136B1 (en) | 2022-08-17 |
| JP2019134930A (ja) | 2019-08-15 |
| WO2016054537A1 (en) | 2016-04-07 |
| JP2021072876A (ja) | 2021-05-13 |
| CA2960874C (en) | 2020-12-01 |
| KR20170068515A (ko) | 2017-06-19 |
| AU2015327943A1 (en) | 2017-05-18 |
| AU2015327943B2 (en) | 2018-10-11 |
| CN106794285A (zh) | 2017-05-31 |
| US10569063B2 (en) | 2020-02-25 |
| JP2017529943A (ja) | 2017-10-12 |
| CN113143558A (zh) | 2021-07-23 |
| AU2019200196B2 (en) | 2020-08-13 |
| EP3200732B1 (en) | 2020-07-01 |
| US20160096006A1 (en) | 2016-04-07 |
| JP6849725B2 (ja) | 2021-03-24 |
| JP6767364B2 (ja) | 2020-10-14 |
| CA2960874A1 (en) | 2016-04-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN106794285B (zh) | 用于药物释放的医疗装置的可移除覆盖物 | |
| US20200324092A1 (en) | Drug coated balloon | |
| EP3178501B1 (en) | Eluting medical devices | |
| US20140066898A1 (en) | Retractable sheath devices, systems, and methods | |
| JP6643488B2 (ja) | 医薬組成物および塗膜 | |
| JP5480272B2 (ja) | 薬剤送達用医療器具 | |
| JP2018068724A (ja) | バルーンカテーテル | |
| US20240024642A1 (en) | Removable covers for drug eluting medical devices |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant |