CN106413543B - 成像装置、成像方法以及医疗成像系统 - Google Patents
成像装置、成像方法以及医疗成像系统 Download PDFInfo
- Publication number
- CN106413543B CN106413543B CN201580026353.1A CN201580026353A CN106413543B CN 106413543 B CN106413543 B CN 106413543B CN 201580026353 A CN201580026353 A CN 201580026353A CN 106413543 B CN106413543 B CN 106413543B
- Authority
- CN
- China
- Prior art keywords
- speckle
- fluid
- optical device
- light
- numerical aperture
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 238000003384 imaging method Methods 0.000 title claims abstract description 102
- 238000002059 diagnostic imaging Methods 0.000 title claims description 14
- 230000003287 optical effect Effects 0.000 claims abstract description 122
- 230000001427 coherent effect Effects 0.000 claims abstract description 32
- 238000000034 method Methods 0.000 claims abstract description 18
- 230000008569 process Effects 0.000 claims abstract description 9
- 239000012530 fluid Substances 0.000 claims description 142
- 210000004369 blood Anatomy 0.000 claims description 12
- 239000008280 blood Substances 0.000 claims description 12
- 238000012545 processing Methods 0.000 claims description 10
- 239000002245 particle Substances 0.000 claims description 5
- 238000004458 analytical method Methods 0.000 description 61
- 230000017531 blood circulation Effects 0.000 description 55
- 238000010586 diagram Methods 0.000 description 24
- 230000014509 gene expression Effects 0.000 description 11
- 230000006870 function Effects 0.000 description 10
- 238000001514 detection method Methods 0.000 description 8
- 230000035945 sensitivity Effects 0.000 description 8
- 238000005286 illumination Methods 0.000 description 7
- 230000004048 modification Effects 0.000 description 7
- 238000012986 modification Methods 0.000 description 7
- 230000000694 effects Effects 0.000 description 6
- 230000004075 alteration Effects 0.000 description 4
- 238000012360 testing method Methods 0.000 description 4
- 230000008859 change Effects 0.000 description 3
- 238000004891 communication Methods 0.000 description 3
- 238000009826 distribution Methods 0.000 description 3
- 239000004973 liquid crystal related substance Substances 0.000 description 3
- 238000005259 measurement Methods 0.000 description 3
- 238000000149 argon plasma sintering Methods 0.000 description 2
- 239000002473 artificial blood Substances 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 210000004204 blood vessel Anatomy 0.000 description 2
- 239000003086 colorant Substances 0.000 description 2
- 230000008878 coupling Effects 0.000 description 2
- 238000010168 coupling process Methods 0.000 description 2
- 238000005859 coupling reaction Methods 0.000 description 2
- 238000013461 design Methods 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 238000002073 fluorescence micrograph Methods 0.000 description 2
- 230000001678 irradiating effect Effects 0.000 description 2
- 238000013507 mapping Methods 0.000 description 2
- 230000010287 polarization Effects 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 230000001360 synchronised effect Effects 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 1
- 239000006096 absorbing agent Substances 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 230000007423 decrease Effects 0.000 description 1
- 230000035622 drinking Effects 0.000 description 1
- 238000001839 endoscopy Methods 0.000 description 1
- 238000005206 flow analysis Methods 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 239000008267 milk Substances 0.000 description 1
- 210000004080 milk Anatomy 0.000 description 1
- 235000013336 milk Nutrition 0.000 description 1
- 239000013307 optical fiber Substances 0.000 description 1
- 230000005693 optoelectronics Effects 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 230000010355 oscillation Effects 0.000 description 1
- 239000010453 quartz Substances 0.000 description 1
- 239000011347 resin Substances 0.000 description 1
- 229920005989 resin Polymers 0.000 description 1
- 239000004065 semiconductor Substances 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N silicon dioxide Inorganic materials O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/02—Detecting, measuring or recording pulse, heart rate, blood pressure or blood flow; Combined pulse/heart-rate/blood pressure determination; Evaluating a cardiovascular condition not otherwise provided for, e.g. using combinations of techniques provided for in this group with electrocardiography or electroauscultation; Heart catheters for measuring blood pressure
- A61B5/026—Measuring blood flow
- A61B5/0261—Measuring blood flow using optical means, e.g. infrared light
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/05—Detecting, measuring or recording for diagnosis by means of electric currents or magnetic fields; Measuring using microwaves or radio waves
- A61B5/053—Measuring electrical impedance or conductance of a portion of the body
- A61B5/0538—Measuring electrical impedance or conductance of a portion of the body invasively, e.g. using a catheter
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B1/00—Instruments for performing medical examinations of the interior of cavities or tubes of the body by visual or photographical inspection, e.g. endoscopes; Illuminating arrangements therefor
- A61B1/00002—Operational features of endoscopes
- A61B1/00043—Operational features of endoscopes provided with output arrangements
- A61B1/00045—Display arrangement
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B1/00—Instruments for performing medical examinations of the interior of cavities or tubes of the body by visual or photographical inspection, e.g. endoscopes; Illuminating arrangements therefor
- A61B1/04—Instruments for performing medical examinations of the interior of cavities or tubes of the body by visual or photographical inspection, e.g. endoscopes; Illuminating arrangements therefor combined with photographic or television appliances
- A61B1/044—Instruments for performing medical examinations of the interior of cavities or tubes of the body by visual or photographical inspection, e.g. endoscopes; Illuminating arrangements therefor combined with photographic or television appliances for absorption imaging
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/0059—Measuring for diagnostic purposes; Identification of persons using light, e.g. diagnosis by transillumination, diascopy, fluorescence
- A61B5/0062—Arrangements for scanning
- A61B5/0066—Optical coherence imaging
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/74—Details of notification to user or communication with user or patient ; user input means
- A61B5/742—Details of notification to user or communication with user or patient ; user input means using visual displays
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Surgery (AREA)
- Heart & Thoracic Surgery (AREA)
- Molecular Biology (AREA)
- Veterinary Medicine (AREA)
- Biophysics (AREA)
- Pathology (AREA)
- Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Public Health (AREA)
- Medical Informatics (AREA)
- Physics & Mathematics (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Radiology & Medical Imaging (AREA)
- Optics & Photonics (AREA)
- Hematology (AREA)
- Cardiology (AREA)
- Physiology (AREA)
- Investigating Or Analysing Materials By Optical Means (AREA)
- Measuring Pulse, Heart Rate, Blood Pressure Or Blood Flow (AREA)
Abstract
一些实施方式涉及成像装置。该成像装置包括:光源,发射相干光以使物体成像。该成像装置还包括光学装置,所述光学装置对来自物体的光进行光学处理。光学装置具有数值孔径。该成像装置还包括成像器,该成像器接收由光学装置光学处理过的光。该成像装置还包括电路,该电路被配置为基于由成像器接收到的光来获取散斑数据并且基于散斑数据控制光学装置的数值孔径。
Description
相关申请的交叉引用
本申请要求于2014年5月30日提交的日本优先权专利申请第JP 2014-112436号的权益以及于2014年12月24日提交的日本优先权专利申请第JP 2014-260054号的权益,通过引用将其全部内容结合于本文中。
技术领域
本技术涉及一种流体分析设备、流体分析方法、程序以及流体分析系统,并且具体地,涉及检测和分析诸如血流的流体的技术。
背景技术
在医疗领域中,例如在医学治疗期间,在某些情况下,必须检测流体(诸如血液等)的流动。在PTL 1中,公开了获取血管区域的相干光(coherent light)图像的成像系统的技术。例如,根据该技术,可以区分器官的内部血管以及覆盖生物体表面的血液。
引用列表
专利文献
PTL 1:日本未经审查专利申请公开第2009-136396号
发明内容
技术问题
然而,存在提高上述的相关技术中的成像系统中的流体(诸如血流)的检测灵敏度的需求。
因此,本发明内容的主要目的是提供一种能够提高流体的流动的检测精确度的流体分析设备,流体分析方法、程序以及流体分析系统。
问题的解决方案
一些实施方式涉及成像装置,该成像装置包括:光源,其发射相关干以将物体成像;
光学装置,对来自物体的光进行光学处理,该光学装置具有数值孔径(numericalaperture);成像器(imager),接收由光学装置光学处理的光;以及电路,被配置为基于由成像器接收到的光获取散斑数据(speckle data);并且基于散斑数据控制光学装置的数值孔径。
一些实施方式涉及成像方法,包括:发射相关干以将物体成像;使用具有数值孔径的光学装置来光学处理来自物体的光;基于由光学装置光学处理的光获取散斑数据;并且基于散斑数据控制光学装置的数值孔径。
一些实施方式涉及医疗成像系统,包括:
成像装置,该成像装置包括:光源,其发射相关干以将物体成像;光学装置,对来自物体的光进行光学处理,该光学装置具有数值孔径;成像器,其接收由光学装置光学处理过的光;以及
电路,被配置为基于由成像器接收到的光获取散斑数据并且基于散斑数据控制光学装置的数值孔径。
发明的有益效果
根据本公开内容,可以提高流体的流动的检测精确度。此外,本文中描述的效果是示例而不旨在限制本公开内容,并且可以是在本公开内容中描述的效果的任何一种。
附图说明
[图1]图1是示意性地示出本公开内容的第一实施方式的流体分析设备1的结构示例的示图。
[图2]图2是示意性地示出第一实施方式的另一种流体分析设备1的结构示例的示图。
[图3]图3是示出使用成像光学系统(image forming optical system)3的光形成的图像的状态的示图。
[图4A]图4A是示出散斑图像的示例的示图。
[图4B]图4B是示出散斑图像的示例的示图。
[图5]图5是示出映射散斑图像的状态的示图。
[图6]图6是示出数值孔径和散斑对比度之间的关系的曲线图。
[图7]图7是表示数值孔径与血流X的散斑对比度与其它非血流X的血流的散斑对比度之间的差的之间的关系的曲线图。
[图8]图8是示意性地示出第一实施方式的变形例的流体分析设备11的结构示例的示图。
[图9A]图9A是示出了使流体循环的工具100的结构的示图。
[图9B]图9B是示出了使流体循环的工具100的结构的示图。
[图9C]图9C是示出了使流体循环的工具100的结构的示图。
[图10A]图10A是示出散斑图像的示例的示图。
[图10B]图10B是示出散斑图像的示例的示图。
[图10C]图10C是示出散斑图像的示例的示图。
[图10D]图10D是示出散斑图像的示例的示图。
[图11]图11是示出针对在图10A到图10D中所示的散斑图像的数值孔径与散斑对比度之间的关系的曲线图。
[图12]图12是示出针对在图10A到图10D中所示的散斑图像的数值孔径与血流X的散斑对比度与其它非血流X的血流的散斑对比度之间的差的之间的关系的曲线图。
[图13]图13示出根据一些实施方式的一种医疗成像系统,具体地是内窥镜系统的示图。
具体实施方式
在下文中,参照附图对本公开内容的实施方式进行详细描述。此外,本公开内容并不限于下述实施方式。此外,该描述如下所示:
1.第一实施方式
(用于基于散斑数据来调节数值孔径的流体分析设备的示例)
2.第二实施方式
(基于散斑数据来调节数值孔径的流体分析系统的示例)
(1.第一实施方式)
<流体分析设备1的结构>
首先,对本公开内容的第一实施方式的流体分析设备1进行说明。图1是示意性地示出本实施方式的流体分析设备1的示图。本实施方式的流体分析设备1包括:相干光照射单元2,其用相干光L照射流体X;成像光学系统3,其使用施加到流体X的光来成像;以及数据获取单元4,其获取流体的散斑数据,并且成像光学系统3基于该散斑数据调整数值孔径。
另外,在本实施方式的流体分析设备1中,没有特别限制流体X,只要它具有光散射材料即可。但是,优选使用血液。在这一点上,流体分析设备1被用作血流分析设备,因此当对动物(诸如人类)进行治疗时,该流体分析设备1能够检测其血流,并分析该血流。在下文中,流体X一般被描述为血流X。
<相干光照射单元2>
包括在实施方式的流体分析设备1的相干光照射单元2使用相干光L照射血流X。相干光照射部2可以被用作使用相干光L进行照射的光源。如下所述,没有特别限制相干光L,只要可以从施加到血流X的光来获得散斑数据,并且,激光束可以被用作相干光L。此外,可以在相干光照射单元2和血流X之间设置光束扩展器21。
<成像光学系统3>
包括在本实施方式的流体分析设备1的成像光学系统3使用施加到血流X的光来形成图像。此外,成像光学系统3基于由如下所述的数据获取单元4所获取的散斑数据来调整数值孔径。优选的是,该散斑数据是散斑对比度的数据,并且在这一点上,成像光学系统3调节数值孔径,使得散斑对比度变成最大。因此,可以提高血流X的流体的检测精确度。此外,如下描述了散斑对比度的细节。
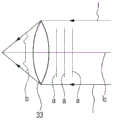
成像光学系统3主要包括:第一透镜31,其作为聚光透镜使施加到血流X的光l聚集;光圈32,其能够改变在平行于傅立叶表面的平面方向上的开口直径;以及第二透镜33,其作为成像透镜聚焦如下所述的成像设备41。成像光学系统3可通过调节光圈32的尺寸来调节数值孔径。
图2是示出流体分析设备1的另一设备结构的概念的示图。如在图2所示,成像光学系统3可具有可选的空间光调制器34,而不是光圈32。在本实施方式的流体分析设备1中,可通过控制空间光调制器34的开口,而不是调整光圈32的尺寸,来使得散斑图像的散斑对比度最大化。
另外,可以通过使用数字微设备(DMD)来操作本实施方式的流体分析设备1。此外,在上述光圈32的位置,可以设置可选的光阀,其可以通过电子或机械方式控制数值孔径。至于使成像光学系统3改变数值孔径的设备,可以使用可选光学调制元件,诸如机械可变光阑、液晶快门、电致变色器件,以及电泳设备。
<数据获取单元4>
包含在本实施方式的流体分析设备1中的数据获取单元4获取用相干光L照射的血流X的散斑数据。具体地,数据获取单元4可以包括作为CCD照相机的成像设备41,并且它可以使用成像设备41来获取血流X的散斑图像,并获取散斑数据。
数据获取单元4能够将与所获取的散斑数据相关的信号发送到如下所述的控制单元5,并通过控制单元5来调整成像光学系统3的数值孔径。并且,在本实施方式的流体分析设备1中,为了以统计的方式处理如下所述的散斑图,并准确地获得相对于数值孔径的散斑对比度的数据,由成像设备41获取到的图像的像素尺寸优选小于散斑颗粒尺寸(specklegrain size)。
<控制单元5>
本实施方式的流体分析设备1可进一步包括控制单元5。在控制单元5中,设置了中央处理单元(CPU)、存储器、输入和输出接口单元、硬盘等。将在下面描述的流体分析方法中说明其细节。然而,控制单元5可以基于由数据获取单元4所获取的散斑数据来生成用于每个数值孔径的散斑数据。具体地,控制单元5可以生成每个数值孔径的散斑对比度的数据。此外,控制单元5可以基于由数据获取单元4所获取的散斑数据,来调整在成像光学系统3中的光圈32的数值孔径。
<流体分析法>
接着,说明了由本实施方式的流体分析设备1执行的血流X的流体分析方法的示例。流体分析方法包括:数据获取步骤,用相干光照射血流X并获取用相干光所照射的流体的散斑数据;以及调整成像光学系统3的数值孔径的步骤,基于散斑数据使用施加到流体的光来成像。
在本实施方式的流体分析设备1中,成像光学系统3的光圈32的数值孔径由控制单元5调整到优选值,因此通过从数据获取单元4所获取的散斑数据可以最明显地观察到血流X的散射流体的移动。具体地,成像光学系统3调整数值孔径,使得散斑对比度变成最大。
<散斑数据>
这里,对用于调整数值孔径的散斑数据进行更具体的描述。图3是示出通过使用成像光学系统3的光来成像的状态的示图。如图3所示,在波面上,靠近施加到血流X的光的光轴I0的光线没有受到干扰,但是随着光线离光轴(在图中,参考a和b)越来越远,该光线在波面上会受到干扰,并且,由于散射波的随机干扰,发生散斑现象。因此,成像设备41可以获取血流X的斑点图案图像(散斑图像)。
在这一点上,成像光学系统3使数值孔径变大,使得入射光的角度和方向以及相位进行变化,并且散射波被补偿。因此,散斑对比度降低。另一方面,当成像光学系统3使数值孔径变小时,散斑对比度变大。此外,如果在成像光学系统3中的波前像差(wave frontaberration)变小,则由于从血流X的粗糙表面的散射而引起主相位差。在这一点上,如果通过从血流X的散射而施加的相位差在1周期(-pi到pi)的范围内时,则通过成像光学系统3产生称为“未显影散斑(undeveloped speckle)”的现象,使得散斑图案进行变化,并且在图像表面的散斑对比度减小。
如果通过使用散斑数据的变化来检测血流X,则它被认为是当散斑对比度很大时,流动测量灵敏度或精确度变高。因此,如果忽略不计空间分辨率,则可以通过减小成像光学系统3的数值孔径(尽可能小到没有显影散斑的范围之内),以高精确度来测量流体。
在这一点上,数值孔径响应于由于血流X(其是测量物体)发生的相位差、成像光学系统3的像差(aberration)、照明系统的数值孔径,以及二维成像设备41的灵敏度而进行变化。成像光学系统3基于由数据获取单元4通过获取散斑图像而获取的散斑数据(散斑对比度的强度、散斑图案等)来改变数值孔径。
如上所述,作为基于来自从控制单元5获取的散斑数据的信号,调整成像光学系统3的数值孔径的设备,可以使用可选的光调制元件,诸如机械可变光阑、液晶快门、电致变色设备以及电泳设备。
接着,参考图4A和图4B,如下描述了上述未显影的散斑和充分显影的散斑。图4A和图4B是示出散斑图像的示例的示图。
<充分显影的散斑>
通常,在图像表面上的可选观察点x的复数振幅A由以下表达式(1)给出(参见Speckle phenomena in optics:theory and applications,第2章,第7-23页,Roberts&Company,Englewood,Colorado,由J.W.Goodman所著)。
[数学式1]
此外,在表达式(1)中,θ表示相位。
以下通过表达式(2)表示了在图像表面由N个分散物体(诸如血流)的点形成的光的复数振幅。
[数学式2]
如果来自散射物体的N个散射点的各光的相位分布分别是相同的,则从中央极限定理通过表达式(3)来表示相对于复数振幅的实部Ar和虚部Ai的概率密度函数。
[数学式3]
另外,在表达式(3)中,σ表示Ar和Ai之间的标准偏差。
在这一点上,通过以下的表达式(4)和(5)来分别表示散斑的强度I和相位θ。因此,通过以下表达式(6)和(7)来分别表示强度概率密度函数PI(I)和相位概率密度函数Pθ(θ)。
[数学式4]
[数学式5]
[数学式6]
[数学式7]
由概率密度函数表示的散斑可以称为充分显影散斑,且在图4A中所示的图样是其的示例。
<未显影散斑>
同时,如果相位是在-pi<=θ<=pi的范围内,并且分布不是均匀的,则通过以下的通用高斯概率密度函数的表达式(8)来表示概率密度函数。
[数学式8]
此外,在表达式(8)中,ρ是Ar和Ai之间的相关系数,ΔAr=Ar-<Ar>,以及ΔAi=Ai-<Ai>。
由概率密度函数表示的散斑被称为未显影散斑,在图4B中所示的图样是示例。
<散斑对比度>
控制单元5可以通过在由数据获取单元4所获取的散斑数据上执行数据处理,将血流X的信息转换成散斑对比度。通过以下的表达式(9)来表示散斑对比度(CS)。此外,光散射流体(诸如血流X)的速度反比于散斑对比度的平方(参见Opt.Commun.37(5)第325页(1981年)等)。
[数学式9]
图5是示意性地示出映射散斑图像的状态的示图。相对于在图4A和图4B中所示的散斑图像,如在图5中所示,每个像素的图像41的整个范围被映射,因此能够生成血流X的图像,并且能够观察到血流X的移动和流动。
例如,如在图5中所示,图像41的区域(其中执行用于计算散斑对比度的统计处理)被设置成正方形区域42,其中,分别在水平方向和垂直方向上布置五个像素。例如,在正方形区域42的中心43的散斑对比度可被计算为正方形区域的散斑对比度。可选范围可以根据散斑图像的分辨率和血流X的流动的测量精确度而被设置为统计处理区域。
图6是表示数值孔径和散斑对比度之间的关系的曲线图。在图6中所示的曲线图中,成像光学系统3可以调整数值孔径,使得散斑对比度变成最大。因此,可以提高血流X的流动的检测精确度。
此外,数据获取单元4获取非所述流体(诸如血流X)的散斑对比度的数据,并且成像光学系统3可以调节数值孔径,使得血流动X的散斑对比度与非血流X的散斑对比度变成最大。图7是示出数值孔径以及散斑对比度之间的关系的曲线图。具体地,图7是示出数值孔径以及血流X的散斑对比度与非血流X的散斑对比度之间的差的曲线图。可以通过调整数值孔径来进一步增大血流X的流动的检测精确度,使得血流X(在图7中的流)的散斑对比度与非血流X(在图7中的幻影)的散斑对比度之间的差变得最大。
在以上内容中,描述了调整数值孔径使得散斑对比度成为最大的方法,但是成像光学系统3可基于散斑图像的粒度或条纹密度来调整数值孔径。参考图4A和图4B,在图4A中所示的散斑图像具有比在图4B中所示的散斑图像的粒度大的粒度。同时,在图4B中所示的散斑图像具有比在图4A中所示的散斑图像的条纹密度大的条纹密度。控制单元5可以响应于它的粒度和条纹密度的值(例如,通过分配多少像素(具有相同的亮度值或者在一定范围内是连续并和彼此相邻的亮度值))来控制数值孔径。以这种方式,成像光学系统3能够调整数值孔径使得散斑图像的粒度变的最大。
如上所述,由于在实施方式的流体分析设备1中,成像光学系统3基于散斑数据来调整数值孔径,因此可能提高血流X的流动的检测精确度。具体地,可使用作为散斑数据的散斑对比度的数据,通过使成像光学系统3调整数值孔径使得散斑对比度变的最大,来准确观察血流X。此外,可通过使成像光学系统3调整数值孔径使得血流X的散斑对比度与非血流X的散斑对比度之间的差变得最大,来准确观察血流X。
(变形例)
图8是示意性地表示本实施方式的变形例的流体分析设备11的结构示例的示图。该实施方式的变形例的流体分析设备11不同于上述的第一实施方式的流体分析设备1,在该实施方式中,流体分析设备11包括非相干光照射单元6,其使用非相干光L'照射血流X。因此,在本文中,主要描述了非相干光照射单元6的结构以及其功能。
如在图8中所示的,当通过非相干光照射单元6使用非相干光L照射血流X来观察亮场图像或者荧光图像时,并且使用成像光学系统3(其与相干光照射单元6相同)时,所需的分辨率和亮度是不同的。因此,成像光学系统3能够调整光圈32,使得孔径的尺寸变的适合用于散斑图像以及亮场图像和荧光图像。由于没有特别限制非相干光照射单元6,因此可以使用具有低相关性的可见光激光器(诸如Xe灯)。
此外,在本变形例的流体分析设备11中,可以在相干光照射单元2和光束扩展器21之间设置旋转斩波器61。此外,可以在光束扩展器21与血流X之间设置偏振光束分离器62。例如,来自Xe灯的平行光可以穿过旋转带通滤波器63,其可以在偶数时间间隔阻止红光、绿光,以及蓝光,并被入射并反射在偏振光束分离器62。旋转斩波器61和旋转带通滤波器63可以是同步的,并且可以用红、率和蓝的自然发射光以及近红外激光照射光束在特定的时间间隔照射血流X的相同位置。
此外,除了上述内容之外,本实施方式的流体分析系统的结构和效果与在第一实施方式中的结构和效果相同。
(2.第二实施方式)
随后,描述了根据本公开内容的第二实施方式的流体分析系统。在第二实施方式的流体分析系统中,与第一实施方式的流体分析设备1和第一实施方式的变型示例的流体分析设备11相比,控制单元5可以被设置在来自流体分析设备1和11的不同设备中。因此,例如,控制单元5可以经由网络,基于流体分析设备1的成像光学系统3的散斑数据来调节数值孔径。
例如,不考虑是有线的或者无线的,该网络包括:公共网络(如因特网)、电话网络、卫星通信网络,以及广播通信路径,或租用线路网络,如广域网(WAN),局域网(LAN)、因特网协议-虚拟专用网络(IP-VPN),以太网(注册商标),以及无线LAN。另外,该网络可以是专门设置在本实施方式的流体分析系统的通信信道网络。
另外,可以在实施方式的流体分析系统中设置服务器、图像显示装置等。在这种情况下,流体分析设备1和11、服务器,以及图像显示装置可直接连接,或者可以经由网络以可通信的方式进行连接。
此外,除了以上所描述的之外,本实施方式的流体分析系统的结构和效果与在第一实施方式中的结构和效果相同。
图13示出根据某些实施方式的医疗成像系统的示图,具体地,内窥镜系统130的示图。如在图13中所示,内窥镜系统130具有光源132。如上所讨论的,光源132可包括相干光照射单元2、非相干光照射单元6,或者相干光照射单元2、非相干光照射单元6两者。光源132发射提供给内窥镜主体134的光来执行内窥镜检查。
内窥镜主体134可以包括从光源132接收光的照明光学系统136。照明光学系统136可包括任何合适的光学组件,诸如一个或多个透镜、一个或多个光学纤维、光束扩展器21、分束器(例如偏振分束器62)、滤波器(旋转带通滤波器63),或者这些组件的任何合适的组合。然而,在本文中所描述的技术不限于被包含在内窥镜主体134内的照明光学系统136,如在一些实施方式中,照明光学系统136的一个或多个组件可以被设备在内窥镜主体134的外部。可以从照明光学系统136发出光,以照亮生物体(诸如人体)的区域,以执行内窥镜检查。
如上所述,内窥镜主体134还可以包括成像光学系统3和数据获取单元4,该数据获取单元可包括成像元件41。
内窥镜系统130可以包括控制单元5,其从数据获取单元4接收数据,并控制成像光学系统3。该控制单元5和/或数据获取单元4可包括处理器,其处理所接收到的图像数据以获取散斑数据(诸如散斑对比度)。在一些实施方式中,控制单元5可控制光源132。
的内窥镜系统130可以包括显示器138,用于显示由数据获取单元4和/或控制单元5生成的图像。显示器138可以是用于将图像显示给用户的任何合适类型的显示器。
在一些实施方式中,医疗成像系统可包括显微镜,其包括通过示例的方式在以上描述的以及在图1中所示的光学装置。
另外,本公开内容可以具有如下所述的结构:
(1)流体分析设备,包括使用相干光对流体进行照射的相干光照射单元;
成像光学系统,其使用施加到流体的光来形成图像;以及
数据获取单元,其获取流体的散斑数据,
其中,成像光学系统基于散斑数据调整数值孔径。
(2)根据(1)的流体分析设备,其中,散斑数据是散斑对比度的数据。
(3)根据项(2)的流体分析设备,其中,成像光学系统调整数值孔径,使得散斑对比度变为最大。
(4)根据(2)或(3)的流体分析设备,其中,数据获取单元获取散斑对比度的数据而不是流体的数据,并且
成像光学系统调整数值孔径,使得流体的散斑对比度与其它流体的散斑对比度之间的差变成最大。
(5)根据(1)至(4)中任一项的流体分析设备,进一步包括使用非相干光对流体进行照射的非相干光照射单元。
(6)根据(1)至(5)中任一项的流体分析设备,其中,流体是血液。
(7)一种流体分析方法,包括以下步骤:
使用相干光对流体进行照射并获取使用相干光所照射的流体的散斑数据;并且
调整耦合光学系统的数值孔径,该耦合光学系统基于散斑数据使用施加到流体的光形成图像。
(8)一种用于使流体分析设备执行以下步骤的程序:
获取用相干光照射的流体的散斑数据的数据获取功能;并且
调整耦合光学系统的数值孔径的功能,该耦合光学系统基于散斑数据使用施加到流体的光形成图像。
(9)一种流体分析系统,包括:
相干光照射单元,使用相干光对流体进行照射;
成像光学系统,使用施加到流体的光来形成图像;以及
数据获取单元,获取流体的散斑数据,
其中,成像光学系统基于散斑数据调整数值孔径。
一些实施方式涉及成像装置,包括:光源,该光源发射相干光以将物体成像;
光学装置,对来自物体的光进行光学处理,光学装置具有数值孔径;成像器,接收由光学装置光学处理的光;以及电路,被配置为基于由成像器接收到的光来获取散斑数据;并且基于散斑数据来控制光学装置的数值孔径。
在一些实施方式中,散斑数据是散斑对比度。
在一些实施方式中,该电路被配置成控制光学装置的数值孔径以增加散斑对比度。
在一些实施方式中,该电路被配置成控制光学装置的数值孔径以使散斑对比度最大化。
在一些实施方式中,物体包括流体。
在一些实施方式中,该电路被配置为基于散斑数据来产生图像数据,图像数据指示流体的位置。
在一些实施方式中,该电路被配置成控制光学装置的数值孔径以增大流体的散斑数据与非流体的散斑数据之间的差。
在一些实施方式中,散斑数据是散斑对比度并且电路被配置为控制光学装置的数值孔径以使流体的散斑对比度与非流体的散斑对比度之间的差最大化。
在一些实施方式中,流体包括血液并且成像装置使血液成像。
在一些实施方式中,电路包括控制器。
在一些实施方式中,成像器具有小于来自物体的光的散斑颗粒尺寸的像素尺寸。
在一些实施方式中,光源是第一光源并且成像装置进一步包括:第二光源,第二光源发射非相干光以使物体成像,其中,成像器使用非相干光使物体成像。
在一些实施方式中,电路被配置为通过改变在光学装置中的开口的尺寸来控制光学装置的数值孔径。
在一些实施方式中,光学装置包括光圈。
在一些实施方式中,光学装置包括空间光学调制器。
一些实施方式涉及一种成像方法,包括:发射相关干以将物体成像;使用具有数值孔径的光学装置来光学处理来自物体的光;基于由光学装置光学处理的光,来获取散斑数据;并且基于散斑数据来控制光学装置的数值孔径。
一些实施方式涉及一种医疗成像系统,包括:
成像装置,该成像装置包括:光源,光源发射相关干以将物体成像;光学装置,其光学处理来自物体的光,光学装置具有数值孔径;成像器,其接收由光学装置光学处理的光;以及
电路,被配置为基于由成像器接收到的光获取散斑数据并且基于散斑数据来控制光学装置的数值孔径。
在一些实施方式中,流体是血液并且成像装置使血液成像。
在一些实施方式中,医疗成像系统包括显微镜或者内窥镜。
在一些实施方式中,医疗成像系统进一步包括显示器,显示器显示由成像装置产生的图像。
示例
参考本公开内容的示例对本公开内容的效果进行详细描述。
示例1
使用在图1中所示的流体分析设备来观察流体。具体地,由Sacher Lasertechnik制造的外部共振半导体激光器(CW振荡,波长:780纳米,单纵模,线宽度:300kHz(1ms),横向模式:TEM00,输出号:高达100mW)被用作光源。此外,从光源发射的激光束通过由EdmundOptics制造的光束扩展器扩大,并且当使用平行光束照射信道时形成幻影(phantom)。
在幻影结构中,作为光漫射剂的氧化铝粒子和作为光吸收剂的红色墨水被混合在紫外线固化树脂中,并且在780纳米的波长的吸收系数和等效散射系数被设置为0.07每毫米和1.08每毫米,与在人体的胃部内壁的吸收系数和等效散射系数相同。
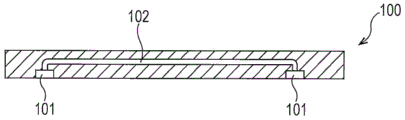
图9A到图9C是示出了使流体循环的工具100的结构的示图。在图9B中示出了沿着图9A的前视图中的线IXB-IXB取得的横截面的视图,以及在图9C中示出了沿着线IXC-IXC取得的横截面的视图。具体地,如在图9A至图9C中所示的,在离观察表面具有200微米的深度的位置形成开口部101和信道102(其横截面具有1毫米角度),并且管连接到相对于观察面设置在后侧的喷射和排放口。此外,用注射泵使人造血液以大约10毫米/秒的速度从开口部101流到信道102。在示例1中,饮用牛奶用作人造血液。参考号码103表示聚光器件。
具体而言,两片具有150毫米的焦距和30毫米的开口直径的球面平凸透镜石英透镜被用作成像光学系统3,光圈32(可变光圈)被布置在其间的傅立叶面上,并且孔的直径在范围3毫米至15毫米内是可调节的。
调整聚焦使得CCD照相机的成像表面与数据获取单元4的图像表面相同。由索尼公司制造的工业CCD照相机(XCD-V60)被用作成像CCD照相机。此外,该照相机具有足够小于散斑颗粒尺寸的像素尺寸,使得散斑图样的强度是足够用于统计处理(其一边是7.4微米的正方形)的分辨率。
来自CCD照相机的信号被输出作为8位、VGA 60帧的位图文件,并且通过根据IEEE1394b的PC获得,以执行统计处理。通过设置用于执行统计处理的图像区域来生成流的图像,为了计算作为分别在水平和垂直方向上具有五个像素的正方形区域的散斑对比度,在该点处设置散斑对比度作为在区域的中央的散斑对比度,并且映射整个图像。
图10A至图10D是示出以这种方式获得的散斑图像的示例的示图。如在图10A至图10D中所示,用在所有图样中交替的长和短的虚线的帧封闭的部分与信道对应。图10A和图10B示出当流体X的流动停止时的散斑,并且图10C和图10D示出流体X的流动。并且,图10A和图10C示出可变光圈(iris diaphragm)的开口直径为12毫米,并且图10B和图10D示出了开口直径为4毫米。从图10A到图10D所示的图像可以观察到的是,散斑图样和对比度根据是否有流体流动或者根据该孔径的尺寸而变的不同。
从图像信息利用上面的方法,参考表达式(9)计算散斑对比度。具体地,相对于其中接近于信道图像的中央的亮度是均匀的区域,可通过获取标准偏差σ和平均<I>,从通过减去对应于各像素的暗电流的值来获取亮度等级的频率分布,来获取孔径的各尺寸的散斑对比度。
图11是表示相对于在图10A到图10D中所示的散斑图像,数值孔径与散斑对比对之间的关系的曲线图。如在图11中所示,在根据示例1的光学系统和样本中,可以发现,当孔径的尺寸为4毫米时,获得为最大值的散斑对比度。也就是说,可以发现,为了将流体的流动可视化,通过将成像光学系统3的数值孔径设置成4毫米,灵敏度和准确度变为最大。以这种方式,可以控制成像光学系统3的数值孔径,使得散斑对比度变成最大。
示例2
在示例2中,除了控制孔径使散斑对比度和非流体X的散斑对比度之间的差变成最大代替控制孔径使得散斑对比度变成最大,用与在示例1中相同的方法执行测试。
图12是示出针对在图10A到10D中所示的散斑图像,数值孔径以及散斑对比度与非流体X的散斑对比度之间的差的曲线图。如在图12中所示,在示例2中,可以发现通过将成像光学系统3的孔径的尺寸设置成大约6毫米,灵敏度和准确度变成最大。以这种方式,可以控制成像光学系统3的数值孔径。
示例3
除了使用在图2中所示的成像光学系统3代替在示例1和2中所使用的成像光学系统3,用在示例1中相同的方法执行测试。具体地,通过液晶透射型空间光调制器实时控制孔径来获取流体的图像,由Holoeye光电制造的该液晶透射型空间光调制器是安装在可变光圈的代替物中。此外,获取孔径(该孔径的散斑图样从颗粒形状变为条纹形状)的尺寸同时控制空间光调制器的孔径,并且获取具有数值孔径的流体的图像以及其形状。因此,可以获得与在示例2中相同的测试结果。
示例4
以在示例1、2和3中相同的方法执行测试,除了使用在图8中所示的流体分析设备11代替在示例1、2和3中使用的流体分析设备1。具体地,基于示例1的光学路径等,旋转斩波器61被设置在光束扩展器21的前方,并且当波长在400纳米至800纳米的范围内是有效的宽频带偏振光束分离器62被设置在光束扩展器21的后方。偏振分束器62被布置成通过780纳米的波长的激光而被穿透。此外,来自Xe灯的平行光可以穿过旋转带通滤波器63,其中,红色、绿色以及蓝色的块在均匀的时间间隔内变化,并且入射并反射在偏振光束分离器62。旋转斩波器61和旋转带通滤波器63是同步的,并且在相同的时间间隔可以用红色、绿色和蓝色的自然发射的光以及近红外激光束照亮样本表面的相同位置。旋转斩波器61和旋转带通滤波器63与成像相机(成像设备41)同步,反复获取用红色、绿色和蓝色的自然发射的光以及近红外激光束照亮的图像,并且将图像数据被发送到PC。
在傅立叶表面上的光圈中,设置了与在示例3中相同的空间光调制器34。当需要空间分辨率用于明场观察时,将数值空间设定的很大,并且当需要在散斑图像中的流动的灵敏度和精确度时,设置数值孔径使得在示例2的方法中的流动检测的灵敏度和精确度变得很高,并且这种孔径控制是重复的。因此,能够实时同步观察在相同观察位置的良好的明场图像和良好的流动图像。此外,在示例4中,Xe灯被用作非相干光照射单元6,但是也可以使用具有充分低的相干性的可见光激光器。
在示例4中,可以发现,当与明场图像、荧光图像等一起使用成像光学系统时,获得最佳的灵敏度、精确度、分辨率以及焦深(focal depth)。
在以上示例1到4中,可以发现,通过调整本公开内容的流体分析设备中的成像光学系统的数值孔径来精确观察血流。
应当由本领域技术人员理解的是,根据设计要求和其它范围内的因素,可以进行各种修改、组合、子组合以及变换,只要它们在所附的权利要求书或其等价物的范围之内。
本领域中普通技术人员应理解的是,只要它们在所附权利要求或其等同物的范围之内,则可根据设计要求和其它因素,进行各种修改,组合,子组合和变更。
参考符号列表
1、11 流体分析设备
2 相干光照射单元
3 成像光学系统
4 数据获取单元
5 控制单元
6 非相干光照射单元
31 第一透镜
32 光圈
33 第二透镜
X 流体(血流)
Claims (18)
1.一种成像装置,包括:
光源,所述光源发射相干光以使物体成像;
光学装置,所述光学装置对来自所述物体的光进行光学处理,所述光学装置具有数值孔径;
成像器,所述成像器接收由所述光学装置光学处理过的光;以及
电路,被配置为基于由所述成像器接收到的光来获取散斑数据并且基于所述散斑数据控制所述光学装置的所述数值孔径;
所述物体包括流体;所述电路被配置为控制所述光学装置的所述数值孔径以增大所述流体的散斑数据与非流体的散斑数据之间的差。
2.根据权利要求1所述的成像装置,其中,所述流体的散斑数据和所述非流体的散斑数据分别是散斑对比度。
3.根据权利要求2所述的成像装置,其中,所述电路被配置为控制所述光学装置的所述数值孔径以增大所述流体的散斑对比度和所述非流体的散斑对比度。
4.根据权利要求3所述的成像装置,其中,所述电路被配置为控制所述光学装置的所述数值孔径以使所述流体的散斑对比度和所述非流体的散斑对比度最大化。
5.根据权利要求4所述的成像装置,其中,所述电路被配置为基于所述流体的散斑对比度和非流体的散斑数据产生图像数据,所述图像数据指示所述流体的位置。
6.根据权利要求1所述的成像装置,其中,所述流体的散斑数据和所述非流体的散斑数据是散斑对比度,并且所述电路被配置为控制所述光学装置的所述数值孔径以使所述流体的散斑对比度与所述非流体的散斑对比度之间的差最大化。
7.根据权利要求1所述的成像装置,其中,所述流体包括血液并且所述成像装置使血液成像。
8.根据权利要求1所述的成像装置,其中,所述电路包括控制器。
9.根据权利要求1所述的成像装置,其中,所述成像器具有小于来自所述物体的光的散斑颗粒尺寸的像素尺寸。
10.根据权利要求1所述的成像装置,其中,所述光源是第一光源,并且所述成像装置进一步包括:
第二光源,所述第二光源发射非相干光以使所述物体成像,其中,
所述成像器使用所述非相干光使所述物体成像。
11.根据权利要求1所述的成像装置,其中,所述电路被配置为通过改变在所述光学装置中的开口的尺寸来控制所述光学装置的所述数值孔径。
12.根据权利要求11所述的成像装置,其中,所述光学装置包括光圈。
13.根据权利要求11所述的成像装置,其中,所述光学装置包括空间光学调制器。
14.一种成像方法,包括:
发射相干光以使物体成像;
使用具有数值孔径的光学装置对来自所述物体的光进行光学处理,所述物体包括流体;
基于由所述光学装置光学处理过的光来获取散斑数据;并且
基于所述散斑数据控制所述光学装置的数值孔径以增大所述流体的散斑数据与非流体的散斑数据之间的差。
15.一种医疗成像系统,包括:
成像装置,包括:
光源,所述光源发射相干光以使物体成像;
光学装置,所述光学装置对来自所述物体的光进行光学处理,所述光学装置具有数值孔径;
成像器,所述成像器接收由所述光学装置光学处理过的光;以及
电路,被配置为基于由所述成像器接收到的光来获取散斑数据并且基于所述散斑数据控制所述光学装置的数值孔径;
所述物体包括流体;所述电路被配置为控制所述光学装置的所述数值孔径以增大所述流体的散斑数据与非流体的散斑数据之间的差。
16.根据权利要求15所述的医疗成像系统,其中,流体是血液并且所述成像装置将所述血液成像。
17.根据权利要求15所述的医疗成像系统,其中,所述医疗成像系统包括显微镜或者内窥镜。
18.根据权利要求15所述的医疗成像系统,进一步包括显示器,所述显示器显示由所述成像装置产生的图像。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2014-112436 | 2014-05-30 | ||
| JP2014112436 | 2014-05-30 | ||
| JP2014260054A JP6394367B2 (ja) | 2014-05-30 | 2014-12-24 | 流体分析装置、流体分析方法、プログラム及び流体分析システム |
| JP2014-260054 | 2014-12-24 | ||
| PCT/JP2015/002521 WO2015182065A1 (en) | 2014-05-30 | 2015-05-20 | Imaging apparatus, imaging method and medical imaging system |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN106413543A CN106413543A (zh) | 2017-02-15 |
| CN106413543B true CN106413543B (zh) | 2020-02-18 |
Family
ID=53404827
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201580026353.1A Expired - Fee Related CN106413543B (zh) | 2014-05-30 | 2015-05-20 | 成像装置、成像方法以及医疗成像系统 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20170188853A1 (zh) |
| EP (1) | EP3148411B1 (zh) |
| JP (1) | JP6394367B2 (zh) |
| CN (1) | CN106413543B (zh) |
| WO (1) | WO2015182065A1 (zh) |
Families Citing this family (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10652444B2 (en) | 2012-10-30 | 2020-05-12 | California Institute Of Technology | Multiplexed Fourier ptychography imaging systems and methods |
| SG11201503293VA (en) | 2012-10-30 | 2015-05-28 | California Inst Of Techn | Fourier ptychographic imaging systems, devices, and methods |
| US9864184B2 (en) | 2012-10-30 | 2018-01-09 | California Institute Of Technology | Embedded pupil function recovery for fourier ptychographic imaging devices |
| WO2015017730A1 (en) | 2013-07-31 | 2015-02-05 | California Institute Of Technoloby | Aperture scanning fourier ptychographic imaging |
| CN110082900B (zh) | 2013-08-22 | 2022-05-13 | 加州理工学院 | 可变照明傅立叶重叠关联成像设备、系统以及方法 |
| US11468557B2 (en) | 2014-03-13 | 2022-10-11 | California Institute Of Technology | Free orientation fourier camera |
| AU2015369663A1 (en) | 2014-12-22 | 2017-05-11 | California Institute Of Technology | Epi-illumination fourier ptychographic imaging for thick samples |
| WO2016118761A1 (en) | 2015-01-21 | 2016-07-28 | California Institute Of Technology | Fourier ptychographic tomography |
| JP2018504628A (ja) | 2015-01-26 | 2018-02-15 | カリフォルニア インスティチュート オブ テクノロジー | マルチウェル・フーリエ・タイコグラフィー撮像及び蛍光撮像 |
| JP6798511B2 (ja) * | 2016-02-18 | 2020-12-09 | ソニー株式会社 | 撮像装置及び撮像システム |
| CN108780035A (zh) * | 2016-03-28 | 2018-11-09 | 索尼公司 | 成像装置以及成像方法 |
| WO2017175470A1 (ja) * | 2016-04-05 | 2017-10-12 | ソニー株式会社 | スペックル測定装置およびスペックル測定方法 |
| US10690904B2 (en) | 2016-04-12 | 2020-06-23 | Stryker Corporation | Multiple imaging modality light source |
| US11092795B2 (en) | 2016-06-10 | 2021-08-17 | California Institute Of Technology | Systems and methods for coded-aperture-based correction of aberration obtained from Fourier ptychography |
| US10568507B2 (en) * | 2016-06-10 | 2020-02-25 | California Institute Of Technology | Pupil ptychography methods and systems |
| US11231436B2 (en) | 2017-05-02 | 2022-01-25 | Sony Corporation | Flow rate measuring method, flow rate measuring device, and program |
| JP7156275B2 (ja) * | 2017-05-16 | 2022-10-19 | ソニーグループ株式会社 | 制御装置、制御方法、及びプログラム |
| US10754140B2 (en) | 2017-11-03 | 2020-08-25 | California Institute Of Technology | Parallel imaging acquisition and restoration methods and systems |
| JP2020163037A (ja) * | 2019-03-29 | 2020-10-08 | ソニー株式会社 | 医療システム、情報処理装置及び情報処理方法 |
| CN111012325B (zh) * | 2019-12-05 | 2022-07-29 | 华中科技大学苏州脑空间信息研究院 | 一种精准光调控系统及光调控方法 |
| WO2023007651A1 (ja) * | 2021-07-29 | 2023-02-02 | 三菱電機株式会社 | 撮像システム及び撮像方法 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7113817B1 (en) * | 2001-10-04 | 2006-09-26 | Wintec, Llc | Optical imaging of blood circulation velocities |
| CN103300841A (zh) * | 2013-06-13 | 2013-09-18 | 上海理工大学 | 一种快速激光散斑血流成像系统和方法 |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH02231673A (ja) * | 1989-03-06 | 1990-09-13 | Kowa Co | 相関関数の評価方法 |
| JPH02232031A (ja) * | 1989-03-06 | 1990-09-14 | Kowa Co | 眼科診断方法 |
| JPH02232028A (ja) * | 1989-03-06 | 1990-09-14 | Kowa Co | 眼科診断装置 |
| US9226661B2 (en) * | 2007-07-06 | 2016-01-05 | Industrial Research Limited | Laser speckle imaging systems and methods |
| JP5087771B2 (ja) | 2007-12-04 | 2012-12-05 | 富士フイルム株式会社 | 撮像システム、内視鏡システム、およびプログラム |
| JP5171564B2 (ja) * | 2008-11-14 | 2013-03-27 | キヤノン株式会社 | 音響光学トモグラフィー測定装置および測定方法 |
| GB0921477D0 (en) * | 2009-12-08 | 2010-01-20 | Moor Instr Ltd | Apparatus for measuring blood parameters |
| CN103857335B (zh) * | 2011-09-26 | 2016-01-27 | 约翰斯.霍普金斯大学 | 激光散斑图像的各向异性处理 |
| CA2863667C (en) * | 2012-02-03 | 2020-04-07 | Oregon Health & Science University | In vivo optical flow imaging |
| US9848787B2 (en) * | 2012-02-07 | 2017-12-26 | Laser Associated Sciences, Inc. | Perfusion assessment using transmission laser speckle imaging |
| WO2013185937A1 (en) * | 2012-06-13 | 2013-12-19 | Koninklijke Philips N.V. | Determining a propagation velocity for a surface wave |
| WO2014081721A1 (en) * | 2012-11-21 | 2014-05-30 | The Board Of Trustees Of The Leland Stanford Junior University | A multi-touch ultrasonic touch screen |
-
2014
- 2014-12-24 JP JP2014260054A patent/JP6394367B2/ja not_active Expired - Fee Related
-
2015
- 2015-05-20 EP EP15729582.5A patent/EP3148411B1/en not_active Not-in-force
- 2015-05-20 WO PCT/JP2015/002521 patent/WO2015182065A1/en active Application Filing
- 2015-05-20 US US15/313,573 patent/US20170188853A1/en not_active Abandoned
- 2015-05-20 CN CN201580026353.1A patent/CN106413543B/zh not_active Expired - Fee Related
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7113817B1 (en) * | 2001-10-04 | 2006-09-26 | Wintec, Llc | Optical imaging of blood circulation velocities |
| CN103300841A (zh) * | 2013-06-13 | 2013-09-18 | 上海理工大学 | 一种快速激光散斑血流成像系统和方法 |
Non-Patent Citations (2)
| Title |
|---|
| Measuring Doppler-like power spectra and dermal perfusion using laser speckle contrast with multiple exposures;O.B.Thompsona ea al.;《Proc.SPIE 7563, Dynamics and Fluctuations in Biomedical Photonics VII》;20100223;第7563卷;第75630N-1至75630N-8页 * |
| Spatiotemporal laser speckle contrast analysis for blood flow imaging with maximized speckle contrast;Jianjun Qiu et al.;《Journal of Biomedical Optics》;20100228;第15卷(第1期);第016003-1至016003-5页 * |
Also Published As
| Publication number | Publication date |
|---|---|
| CN106413543A (zh) | 2017-02-15 |
| EP3148411B1 (en) | 2020-07-22 |
| WO2015182065A1 (en) | 2015-12-03 |
| JP6394367B2 (ja) | 2018-09-26 |
| EP3148411A1 (en) | 2017-04-05 |
| JP2016005525A (ja) | 2016-01-14 |
| US20170188853A1 (en) | 2017-07-06 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN106413543B (zh) | 成像装置、成像方法以及医疗成像系统 | |
| JP5628839B2 (ja) | 眼球表面疾患を検出するシステムおよび眼球表面検査装置 | |
| US8888284B2 (en) | Field of light based device | |
| WO2017168984A1 (ja) | 撮像装置、撮像方法 | |
| KR20210027404A (ko) | 복강경 검사에서 혈류 및 조직 관류의 무염색 가시화를 위한 방법 및 시스템 | |
| US20160157736A1 (en) | System and Methods for Assessment of Relative Fluid Flow Using Laser Speckle Imaging | |
| CN108601505B (zh) | 成像设备、成像方法和成像系统 | |
| US12023128B2 (en) | System and method for eye tracking | |
| JP7053469B2 (ja) | 視線追跡のためのシステムおよび装置 | |
| JP2022062231A (ja) | 内視鏡装置及び内視鏡検査の方法 | |
| WO2017163542A1 (ja) | 画像解析装置、画像解析方法 | |
| AU2015284130B2 (en) | System and method for corneal topography with flat panel display | |
| CN106419890B (zh) | 一种基于时空调制的血流速度测量装置及方法 | |
| US7740356B2 (en) | Monochromatic multi-resolution corneal topography target | |
| US20190059721A1 (en) | Ophthalmologic apparatus and method of controlling the same | |
| US20180249905A1 (en) | System and method for corneal topography with flat panel display | |
| US20180116506A1 (en) | Eye tracking apparatus and image capture module thereof | |
| WO2019195731A1 (en) | Systems and methods for measuring water and lipid content in tissue samples | |
| US20170237885A1 (en) | Method and Apparatus for High Contrast Imaging | |
| WO2021251146A1 (ja) | 瞳孔検出装置 | |
| JP2011083486A (ja) | 生体組織識別装置及び方法 | |
| TW201827914A (zh) | 觀察裝置及觀察方法 | |
| US20190068861A1 (en) | Imaging system, imaging apparatus, and imaging method | |
| US11710236B1 (en) | Variable exposure portable perfusion monitor | |
| JP6480769B2 (ja) | 撮影装置、撮影システム及び撮影装置で用いられる支持部材 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant | ||
| CF01 | Termination of patent right due to non-payment of annual fee | ||
| CF01 | Termination of patent right due to non-payment of annual fee |
Granted publication date: 20200218 |