CN105229159B - 重组多肽生产 - Google Patents
重组多肽生产 Download PDFInfo
- Publication number
- CN105229159B CN105229159B CN201480013725.2A CN201480013725A CN105229159B CN 105229159 B CN105229159 B CN 105229159B CN 201480013725 A CN201480013725 A CN 201480013725A CN 105229159 B CN105229159 B CN 105229159B
- Authority
- CN
- China
- Prior art keywords
- mirna
- mir
- cell
- cells
- antibody
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/42—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against immunoglobulins
- C07K16/4208—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against immunoglobulins against an idiotypic determinant on Ig
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P21/00—Preparation of peptides or proteins
- C12P21/02—Preparation of peptides or proteins having a known sequence of two or more amino acids, e.g. glutathione
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/10—Immunoglobulins specific features characterized by their source of isolation or production
- C07K2317/14—Specific host cells or culture conditions, e.g. components, pH or temperature
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/21—Immunoglobulins specific features characterized by taxonomic origin from primates, e.g. man
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/22—Immunoglobulins specific features characterized by taxonomic origin from camelids, e.g. camel, llama or dromedary
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/31—Immunoglobulins specific features characterized by aspects of specificity or valency multispecific
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/40—Immunoglobulins specific features characterized by post-translational modification
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/622—Single chain antibody (scFv)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/11—Antisense
- C12N2310/113—Antisense targeting other non-coding nucleic acids, e.g. antagomirs
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2330/00—Production
- C12N2330/50—Biochemical production, i.e. in a transformed host cell
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/65—MicroRNA
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2799/00—Uses of viruses
- C12N2799/02—Uses of viruses as vector
- C12N2799/021—Uses of viruses as vector for the expression of a heterologous nucleic acid
- C12N2799/027—Uses of viruses as vector for the expression of a heterologous nucleic acid where the vector is derived from a retrovirus
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/178—Oligonucleotides characterized by their use miRNA, siRNA or ncRNA
Abstract
在此披露了用于在哺乳动物细胞培养物中产生重组多肽的一种方法,在该哺乳动物细胞培养物中,这些哺乳动物细胞具有修饰的微小RNA的活性水平。在一个实施例中,微小RNA活性水平被提高。在另一个实施例中,微小RNA活性水平被降低。在一个更具体的实施例中,这些哺乳动物细胞具有降低的miRNA‑let‑7a活性水平。
Description
1.发明领域
本发明涉及重组多肽的生产。更具体而言,本发明涉及调节miRNA来提高产生重组多肽的细胞系的生产率,例如通过提高或降低一个或多个miRNA的水平。
2.背景
培养的哺乳动物细胞经常用于产生重组多肽。哺乳动物细胞培养提供优于非哺乳动物系统的许多优点,包括例如恰当的蛋白质折叠、组装以及翻译后修饰。然而,在提高大规模哺乳动物培养物的生产率的方面仍然存在挑战,包括例如与生长水平、细胞应激、以及翻译速率有关的挑战。在许多工业细胞培养过程中,在大型生物反应器中作为混悬液高密度地培养细胞,并且细胞往往会增殖超过它们的最优生长条件。在这些条件下,可能会触发细胞凋亡,并且因此细胞活力和生产率可能会降低。因此,许多生产优化策略依赖于防止细胞凋亡,并且通过增强培养基配制和生长条件来改变细胞代谢。最近研究表明细胞生产率可以通过改变调节多个重要细胞路径的关键分子如转录因子的全基因表达模式来提高。
微小RNA(miRNA)是在植物和动物体内发现的具有约22个核苷酸的小的非编码的RNA分子,并且是基因表达的关键的转录和转录后调节剂。miRNA通过与mRNA分子内的互补序列进行碱基配对来起作用,从而经常导致基因沉默,并且这些miRNA涉及动物和植物体内包括与细胞生长、发育以及分化相关的调节功能的各种生物路径。miRNA在维持细胞内环境稳定和调节重要细胞路径如生长和细胞凋亡中发挥关键作用。不合适的miRNA表达与包括癌症的多种疾病相关联,在这些疾病中,它们可能通过同时改变众多蛋白质和路径而形成发病机理。
单个miRNA改变影响多个生理过程的能力表明修饰生产细胞培养物中的miRNA表达可以延迟生产性细胞生长期,产生较高的抗体滴度并且提高生产率(辛普森(Sampson)等人,(2007)“微小RNA Let-7a下调MYC并且使MYC诱导的伯基特氏淋巴瘤细胞的生长恢复原状(MicroRNA Let-7a down-regulates MYC and reverts MYC-induced growth inBurkitt Lymphoma cells.)”癌症研究(Cancer Res)67(20):9762-9770;穆勒(Muller)等人,(2008)“作为用于使CHO细胞工厂工程化的靶标的微小RNA(MicroRNAs as targets forengineering of CHO cell factories.)”生物技术趋势(Trends in Biotechnology)26(7):359-365;以及巴伦(Barron)等人,(2011)“通过miR-7的过表达来使CHO细胞生长和重组多肽生产工程化(Engineering CHO cell growth and recombinant polypeptideproductivity by over expression of miR-7.)”生物技术杂志(Journal ofBiotechnology)151(2):204-11)。因此,研究人员已开始考察微小RNA在哺乳动物细胞培养物中的作用,这主要是通过内源性miRNA在整个生产培养过程中发生的改变的分析来进行(穆勒等人,(2008)“作为用于使CHO细胞工厂工程化的靶标的微小RNA”生物技术趋势26(7):359-365;巴伦等人,(2011)“通过miR-7的过表达来使CHO细胞生长和重组多肽生产工程化”生物技术杂志151(2):204-11;甘默尔(Gammell)等人,(2007)“混悬液CHO-K1细胞中的miRNA表达的低温和培养阶段诱导的初始鉴别(Initial identification of lowtemperature and culture stage induction of miRNA expression in suspensionCHO-K1 cells.)”生物技术杂志130:213-218;以及哈克尔(Hackl)等人,(2010)“中国仓鼠卵巢微小RNA转录组的新一代测序:作为用于细胞工程化的靶标的微小RNA的鉴别、注释以及剖析(Next-generation sequencing of the Chinese hamster ovary microRNAtranscriptome:Identification,annotation and profiling of microRNAs as targetsfor cellular engineering.)”生物技术杂志153(1-2):62-75)。少数研究还探索了异位表达的miR或抗miR对CHO细胞的影响(巴伦等人2011;米尼迪(Meleady)等人2011;德鲁兹(Druz)等人2011)。然而,CHO细胞中改变的miRNA的效果的更精细的表征在这项技术可以按常规实施来提高治疗用生物制剂的生产之前是必要的。
3.概述
在此披露了一种在哺乳动物细胞培养物中产生重组多肽的方法,在该哺乳动物细胞培养物中,哺乳动物细胞具有降低的miRNA-let-7a活性。在一个实施例中,miRNA-let-7a活性被微小RNA抑制剂降低。在一个实施例中,微小RNA抑制剂包括miRNA-let-7a的反义寡核苷酸抑制剂。在另一个实施例中,哺乳动物细胞培养物包括用miRNA-let-7a的合成的反义寡核苷酸抑制剂转染的哺乳动物细胞。在一个实施例中,寡核苷酸抑制剂被化学修饰来改进核酸酶抗性,通过RISC提高对miRNA引导的裂解的抗性和/或提高结合亲和力。在一个实施例中,哺乳动物细胞培养物包括用编码miRNA-let-7a的反义寡核苷酸抑制剂的表达载体转染的哺乳动物细胞。哺乳动物细胞培养物可以用miRNA-let-7a的反义寡核苷酸抑制剂稳定地或瞬时地转染。在另一个实施例中,哺乳动物细胞包括miRNA-let-7a基因敲除。
适合的哺乳动物细胞包括但不限于:例如,中国仓鼠卵巢(CHO)细胞、小鼠骨髓瘤(NS0)、人胚肾(HEK 293和衍生物如293T,293H)、幼仓鼠肾(BHK)细胞、非洲绿猴肾细胞(Vero cells)、人子宫颈癌传代细胞(HeLa cells)、马丁达比犬肾(MDCK)细胞、CV1猴肾细胞、3T3细胞、骨髓瘤细胞系、PC12、WI38细胞、猴肾成纤维细胞的COS-7系、以及C127。
适合的重组多肽包括抗体或它的结合片段以及非抗体蛋白。在一个实施例中,抗体或它的结合片段选自多特异性抗体、完全的人抗体、人源化抗体、骆驼化抗体(camelisedantibodies)、嵌合抗体、CDR移植抗体、单链Fvs(scFv)、二硫键连接的Fvs(sdFv)、Fab片段、F(ab')片段、以及抗独特型(抗Id)抗体。在一个实施例中,抗体或它的结合片段包括选自IgG、IgE、IgM、IgD、IgA以及IgY的同种型。在另一个实施例中,抗体包括选自IgG1、IgG2、IgG3以及IgG4的同种型。
在另一个实施例中,重组多肽包括非抗体蛋白。在一个实施例中,重组多肽包括融合蛋白。在另一个实施例中,重组多肽包括受体。在一个实施例中,重组多肽包括细胞表面蛋白的配体。在另一个实施例中,细胞表面蛋白是受体。在另一个实施例中,重组多肽包括分泌的蛋白。在另一个实施例中,重组多肽包括酶。在另一个实施例中,重组多肽包括支架模拟物。
在一个实施例中,细胞培养物具有与不具有降低的miRNA-let-7a活性的对照细胞培养物相比较增加至少约25%的比生产率。在一个实施例中,细胞培养物具有在峰值活细胞密度(VCD)下确定的,与不具有降低的miRNA-let-7a活性的对照细胞培养物相比较时增加至少约25%的最大生产率。在一个实施例中,细胞培养物在与不具有降低的miRNA-let-7a活性的对照细胞培养物相比较细胞培养物中的每个活细胞的抗体滴度增加情况下具有提高的比生产率。
在一个实施例中,在与不具有降低的miRNA-let-7a活性的对照细胞培养物相比较时,细胞凋亡、蛋白质翻译或细胞代谢中的至少一个介导因子在哺乳动物细胞培养物中的表达增加。在一个实施例中,在与不具有降低的miRNA-let-7a活性的对照细胞培养物相比较时,选自HMGA2、MYC、NF2、NIRF、RAB40C以及eIF4a的miRNA-let-7a的至少一个靶标在细胞培养物中的表达增加。
在一个实施例中,哺乳动物细胞与对照细胞培养物相比较具有选自miR-10a、miR-21以及它们的组合的第二微小RNA的增加的活性。在一个实施例中,哺乳动物细胞用能够表达miR-10a、miR-21或它们的组合的表达载体来转染。在一个实施例中,哺乳动物细胞具有选自miR-16、miR-101、miR-145以及它们的组合的第二微小RNA的降低的活性。在一个实施例中,第二微小RNA的活性被第二微小RNA抑制剂降低。在一个实施例中,第二微小RNA抑制剂包括反义寡核苷酸抑制剂。在一个实施例中,哺乳动物细胞培养物包括用第二反义寡核苷酸抑制剂转染的哺乳动物细胞。在一个实施例中,第二寡核苷酸抑制剂被化学修饰来改进核酸酶抗性,通过RISC提高对miRNA引导的裂解的抗性和/或提高结合亲和力。在一个实施例中,哺乳动物细胞培养物包括用编码第二反义寡核苷酸抑制剂的表达载体转染的哺乳动物细胞。
还披露了被配置成表达重组多肽的哺乳动物细胞系,其中哺乳动物细胞系具有降低的miRNA-let-7a活性;表达系统,这些表达系统包括编码miRNA-let-7a的反义微小RNA抑制剂的一个或多个载体以及编码重组蛋白的核苷酸序列;细胞培养基,这些细胞培养基包括miRNA-let-7a的反义抑制剂;以及重组多肽,这些重组多肽产生自包括用miRNA-let-7a的反义微小RNA抑制剂转染的哺乳动物细胞的哺乳动物细胞培养物。
4.附图简要说明
图1是示出按滴度/累积VCD的积分计算且记录为mg/L/累积细胞天数(CCD)的试验结束比生产率(run specific productivity)(QP)的图。
图2是示出累积QP与最大QP比较的图。
图3是示出每两天测量的抗miR-let-7a、抗miR-143以及miR-10a修饰的CHO细胞系的重组抗体滴度(相对于第2天测量的基线水平)的图。
图4是示出每两天测量的抗miR-let-7a、抗miR-143以及miR-10a修饰的CHO细胞系的VCD(相对于第0天测量的基线水平)的图。
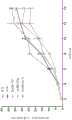
图5是示出用抗miR-let-7a慢病毒载体或载体对照转导的亲本培养物的分批进料测定过程中测量的两种抗体产生细胞系的相对VCD的图。结果示出为相对VCD水平对比基线(第0天)。
图6是示出每两天评价的抗miR-let-7a修饰的培养物和对照的重组抗体滴度(相对于第2天测量的基线)的图。
图7是在产生重组mAb的两个细胞系中相对于对照累积Qp呈%增加的表。
图8是示出在miR-let-7a的抑制之后与对照系相比较的miR或抗miR修饰的细胞系中通过TaqMan定量PCR评价的CHO生产细胞中的多个mRNA靶标的成倍变化的图。条形图表示平均值±SD。
图9A和图9B.(A)示出光密度测量用于计算在miR-let-7a的抑制之后与对照相比较的RAS/GAPDH比的变化%。(B)是示出亲本、对照以及抗miR-let-7a细胞系中的RAS和负载对照GAPDH的蛋白质水平的蛋白质印迹法。
图10是示出靶基因参与多个细胞路径的流程图,这些细胞路径包括因抗体产生细胞系中的miR-let-7a的调控而改变的增殖/细胞周期、细胞凋亡、应激抗性、代谢和转录/翻译。
图11A-C.(A)是用表达抗miR和GFP的慢病毒载体转导的CHO细胞的代表性显微照片,该代表性显微照片指示了接近100%的转导效率。(B)和(C)是示出用慢病毒转导的CHO细胞与亲本细胞相比较荧光值(RFP)出现2 log位移的代表性FACS直方图。
图12A和图12B是以下各项的代表性去卷积ESI质谱:来自亲本系的代表性单克隆抗体–减少的HC和LC质量,LC 22895.9263匹配LC和HC(G0F),50992.2014匹配G0F;51154.2639匹配G1F;和51316.1579匹配G2F;以及(B)来自抗miR-let-7a修饰的系的抗体–减少的HC和LC质量,LC 22895.7493匹配LC和HC(G0F),50992.7636匹配G0F和51154.3954匹配G1F。
5.详细说明
A.综述
在此描述的本发明的实施例涉及用于在哺乳动物细胞培养物中产生重组多肽的方法。在一个实施例中,该方法包括在微小RNA的存在下培养哺乳动物细胞以提高细胞系生产率。在一个更具体的实施例中,哺乳动物细胞系可以被工程化来改变微小RNA活性以便提高重组多肽生产率。
B.定义
除非另外定义,在此使用的科学术语和技术术语应具有本领域普通技术人员普遍理解的含义。另外,除非上下文另有要求,单数术语应包括复数形式,并且复数术语应包括单数形式。一般而言,结合在此描述的细胞和组织培养、分子生物学、以及蛋白质和寡核苷酸或多核苷酸化学连同杂交使用的术语和它们的技术都是本领域熟知的和普遍使用的。
标准技术用于重组DNA、寡核苷酸合成以及组织培养和转化(例如,电穿孔、脂转染、病毒转导)。酶促反应和纯化技术是根据制造商的说明书或本领域常规实行方法或如在此所述进行。这些技术和程序通常是根据本领域中熟知的常规方法和贯穿本说明书中引用且论述的各种通用和更特定的参考文献中所述来进行。参见例如,桑布洛克(Sambrook)等人,分子克隆:实验室手册(Molecular Cloning:A Laboratory Manual)(第3版,冷泉港实验室出版社(Cold Spring Harbor Laboratory Press),冷泉港,纽约(2001)),该实验室手册通过引用结合在此。结合在此描述的分析化学、合成有机化学、以及医学和药物化学使用的术语,它们的实验室方法和技术是本领域熟知的和普遍使用的。标准技术用于化学合成,化学分析,药物制备、配制以及递送,例如以用于治疗患者。
如根据本披露所使用,除非另外指明,以下术语应理解为具有以下含义:
如在此所使用,术语“约”用于修饰例如在描述本发明中采用的组合物中成分的数量、浓度、体积、工艺温度、工艺时间、产率、流速、压力以及它们的范围。术语“约”指代数量的变化,这种变化例如通过制备化合物、组合物、浓缩物或使用配制品所使用的典型的测量和处理程序、通过在这些程序中无意中犯的错误、通过执行方法所使用的起始材料或成分的制备、来源或纯度的差异以及其他类似考虑导致可能发生。术语“约”还涵盖因配制品的老化而与具体起始浓度或混合物不同的量,以及因混合或处理配制品而与具体起始浓度或混合物不同的量。当利用术语“约”修饰时,在此随附的权利要求书包括这些等效量。
如在此所使用,术语“抗体”指代包括通过多肽链的折叠形成的至少一个结合结构域的多肽或一群多肽,这些多肽链具有三维结合空间,其中内表面形状和电荷分布与抗原的抗原决定簇的特征互补。抗体典型地具有四聚体形式,包括两对相同的多肽链,每对具有一个“轻”链和一个“重”链。每个轻/重链对的可变区形成抗原结合位点。抗体可以是寡克隆抗体、多克隆抗体、单克隆抗体、嵌合抗体、骆驼化抗体、CDR移植抗体、多特异性抗体、双特异性抗体、催化性抗体、人源化抗体、完全的人抗体、抗独特型抗体和能够以可溶或结合形式标记的抗体,以及它们的包括表位结合片段的片段、变体或衍生物,它们单独存在或与其他氨基酸序列组合。抗体可以来自任何物种。术语抗体还包括结合片段,包括但不限于:Fv、Fab、Fab'、F(ab')2、单链抗体(svFC)、二聚可变区(二聚抗体)以及二硫键连接的可变区(dsFv)。具体来说,抗体包括免疫球蛋白分子和免疫球蛋白分子的免疫活性片段,即,含有抗原结合位点的分子。抗体片段可以融合或不融合至另一个免疫球蛋白结构域,包括但不限于Fc区域或它的片段。技术人员将进一步了解到,可以生成其他融合产物,包括但不限于:scFv-Fc融合体、可变区(例如,VL和VH)--Fc融合体以及scFv-scFv-Fc融合体。免疫球蛋白分子可以是任何类型(例如IgG、IgE、IgM、IgD、IgA、以及IgY)、类别(例如IgG1、IgG2、IgG3、IgG4、IgA1、以及IgA2)或子类。
如在此所使用的术语“控制序列”指代指影响或影响到与之相连的编码序列的表达和加工的多核苷酸序列。这类控制序列的性质可以因宿主生物而异。在真核生物中,控制序列可以包括启动子、增强子、内含子、转录终止序列、多腺苷酸化信号序列、以及5’和3’非翻译区(UTR)。如在此所使用的术语“控制序列”包括其存在对于表达和加工是必要的所有组分,并且还可以包括其存在并不是必要的但仍然有利的另外的组分,例如前导序列。
术语“基因”广泛用于指代与生物学功能相关联的任何核酸。因此,术语“基因”包括编码序列和/或表达所需的调节序列。术语“基因”还可以适用于特异性基因组序列,以及这些基因组序列所编码的cDNA或mRNA。
术语“异源基因”指代编码自然环境中不存在的生物材料(即,已被人为改变)的基因。例如,异源基因可以包括从一个物种引入到另一个物种中的基因。异源基因还包括生物天然具有的在一定程度上发生改变(例如,突变,添加多个拷贝,连接至非天然启动子或增强子序列等)的基因。异源基因与内源基因的区别在于:异源基因序列可以连接至未发现与基因天然相关联或与自然界中未发现的染色体的部分相关联的调节元件如启动子。
术语“宿主细胞”意指可以或已经吸收核酸如载体并且支持核酸的复制和/或表达以及任选地产生一种或多种编码产物的细胞。在一个实施例中,术语“宿主细胞”指代真核细胞如细胞培养物中的哺乳动物细胞。在一个更具体的实施例中,宿主细胞包括中国仓鼠卵巢(CHO)细胞、人胚肾(HEK 293和衍生物如293T,293H)细胞、非洲绿猴肾细胞、幼仓鼠肾(BHK)细胞、人子宫颈癌传代细胞、CV1猴肾细胞、马丁达比犬肾(MDCK)细胞、3T3细胞、骨髓瘤细胞系、COS细胞(例如,COS1和COS7)、PC12、WI38细胞。术语宿主细胞还涵盖包括例如不同细胞类型或细胞系的混合培养物的细胞的组合或混合物。
在提及异源或分离的核酸时的术语“引入”指代在核酸可以并入到细胞的基因组(例如,染色体、质粒、质体或线粒体DNA)中,转化成自主复制子或瞬时表达(例如,转染的mRNA)的情况下将核酸并入到真核细胞中。术语包括这类方法如“感染”、“转染”、“转化”以及“转导”。各种方法是已知的,并且可以采用于将核酸引入到哺乳动物细胞中。
在此结合生物材料如核酸或蛋白质使用时的术语“分离的”指代已从其天然发生的环境分离的生物材料。“分离的”多核苷酸可以指代基因组、cDNA或合成多核苷酸。分离的多核苷酸可以操作地连接至在自然界中未与之相连的另一个多核苷酸。在此结合蛋白质使用时的术语“分离的”指代已从其天然发生的环境分离的蛋白质。分离的蛋白质可以来源于基因组DNA、cDNA、重组DNA、重组RNA或合成来源或它们的一些组合。
术语“mAb”指代单克隆抗体。
术语“天然发生的”指代生物中存在的生物材料例如多肽、多核苷酸或微小RNA序列,其中该生物材料未被人为故意修饰。术语“外源”指代来源于生物外部或因人为故意修饰而存在于生物中的生物材料,该修饰包括例如用于表达生物材料的生物修饰。
术语“核酸”、“寡核苷酸”和“多核苷酸”指代单链或双链的脱氧核糖核苷酸或核糖核苷酸聚合物,或它们的嵌合体或类似物。除非另外指明,核酸序列涵盖除明确指示的序列之外的互补序列。寡核苷酸是通常具有至多约200个碱基例如约10个到约100个碱基的长度的多核苷酸子集。
如在此所使用的术语“可操作地连接”指代组分位置处于允许它们以它们期望的方式发挥功能的关系中。例如,控制序列“可操作地连接至”编码序列的连接方式使得编码序列的表达在与控制序列相容的条件下实现。
术语“肽”、“多肽”和“蛋白质”在全文中可互换使用,并且指代包括通过肽键彼此连接的两个或更多个氨基酸残基的分子。术语“肽”、“多肽”和“蛋白质”可以指代抗体和非抗体蛋白。非抗体蛋白包括但不限于蛋白质如酶、受体、细胞表面蛋白的配体、分泌的蛋白以及融合蛋白或它们的片段。非抗体蛋白倾向于具有比抗体蛋白更低的分子量。多肽可以是或不是糖基化的。蛋白质可以融合或不融合至另一种蛋白质。肽、多肽和蛋白质还可以包括修饰,例如但不限于糖基化、脂质附着、硫酸盐化、谷氨酸残基的γ-羧化、羟化以及ADP-核糖基化。多肽可以具有科学或商业利益,包括基于蛋白质的药物。多肽包括尤其是抗体和嵌合蛋白或融合蛋白。
“启动子”或“启动子序列”是能够在适当的转录相关的酶例如RNA聚合酶在例如培养或生理条件的条件下存在,借此酶起作用时起始与之可操作地连接的核酸序列的转录的DNA调节区。启动子可以存在于在其中该启动子起始了转录的核酸序列的上游或下游。转录起始位点典型地被发现处于或邻近启动子序列以及蛋白结合结构域(共有序列),该蛋白结合结构域促进、调节、增强或以其他方式负责RNA聚合酶的结合。
术语“重组”指代通过人为介入人为或合成(即,非自然)改变的生物材料例如核酸或蛋白质。
如在此所使用,“基本上纯的”指代为所存在的主要物质(例如,基于摩尔,它比组合物中的任何其他单独的物质更丰富)的生物材料。在一个实施例中,基本上纯化的部分是其中生物材料构成所存在的所有大分子物质的至少约50%(基于摩尔)的组合物。一般而言,基本上纯的组合物将包括组合物中存在的所有大分子物质的多于约80%,或多于约85%,多于约90%,多于约95%,或多于约99%。在一个实施例中,生物材料被纯化为基本上均质(通过常规检测方法无法检测组合物中的污染物质),并且该组合物基本上包括单一的大分子物质。
术语“转染”指代将外来DNA引入到细胞中。术语“转染”和“转化”(以及语法等同物如“转染(transfected)”和“转化(transformed)”)可互换使用。术语“稳定的转染”或“稳定地转染”指代将外来DNA引入和整合到转染细胞的基因组中。术语“瞬时的转染”或“瞬时地转染”指代在外来DNA并不整合到转染细胞的基因组中的情况下将外来DNA引入到细胞中。在瞬时转染中,外来DNA可以在转染细胞的细胞核中持续存在若干天,在这个时间期间,外来DNA经受管理染色体中的内源基因的表达的调节控制。
术语“载体”指代可以用于将异源核酸序列引入到细胞中的核酸例如质粒、病毒载体、重组核酸或cDNA。“表达载体”是能够促进并入在其中的核酸的表达例如转录的载体如质粒。典型地,有待表达的核酸“可操作地连接”至启动子和/或增强子,并且经由启动子和/或增强子而经受转录调节控制。
C.微小RNA
微小RNA(miR,miRNA)是一类在哺乳动物细胞中表达的天然发生的,小的非编码的RNA,这些RNA的长度是在约17个与约27个核苷酸之间,长度是在约19个与约25个核苷酸之间,或长度是在约21个与约23个核苷酸之间,长度经常是22个核苷酸。miRNA可以通过以下内容下调哺乳动物体内的基因表达:结合至靶信使RNA(mRNA)的3’非翻译区(UTR)中的不完全互补的序列,并且抑制mRNA的翻译,例如通过防止核糖体结合,翻译阻遏,脱腺苷酸化或通过诱导或加速mRNA降解(安布罗斯·V.(Ambros,V.)(2001)微小RNA:具有极大潜能的微小调节因子(microRNAs:tiny regulators with great potential.),细胞(Cell)107(7):823-6;白金汉·S.(Buckingham,S.)(2003)微小RNA的大世界、视野论坛:理解RNAissance.(The major world of microRNAs,Horizon Symposia:Understanding theRNAissance.),自然出版集团(Nature Publishing Group),自然(Nature),1-3;何(He)等人(2009)Let-7a通过NIRF的靶向和压制A549肺癌细胞的生长提高p21WAF1水平(Let-7aelevates p21WAF1levels by targeting of NIRF and suppresses the growth of A549lung cancer cells.),欧洲生物化学学会联盟简讯(FEBS Lett.)583:3501-3507)。miRNA调节广泛范围的生物过程,包括发育定时、细胞凋亡、分化、细胞增殖以及代谢,并且miRNA的上调和下调两者均涉及各种病理条件。miRNA经常形成具有常用mRNA靶标的多基因家族。
微小RNA名称使用前缀“mir”或“miR”并且后跟破折号和数字来指定。未大写的“mir”前缀通常指代pre-miRNA,而大写的“miR”前缀通常指代成熟形式。除一个或两个核苷酸之外具有几乎完全相同的序列的miRNA典型地用另外的小写字母注释。
miRNA在细胞核中转录为称为pri-miRNA的大的RNA短发夹前体。pri-miRNA在细胞核中由微处理器复合体加工以生成称为pre-miRNA的双链中间体,这些双链中间体的长度是约70个核苷酸。pre-miRNA之后输出到细胞质中,在细胞质中,它们被组装成称为RNA诱导的沉默复合物(RISC)的胞质内蛋白质-RNA复合物。结合复合物的单链miRNA结合至具有与miRNA至少部分互补的序列的靶mRNA。miRNA靶识别的重要特异性决定簇是基于成熟miRNA中的“种子”区域(例如,成熟miRNA的核苷酸2-7或2-8内)至mRNA的靶3’UTR中,靶5’UTR内或编码区的一部分内的“种子匹配位点”的沃森-克里克配对(Watson-Crick pairing),这使miRNA:靶mRNA相互作用成核。以此方式,每个miRNA可以调节数百种到数千种的mRNA物质。此外,许多miRNA是含有相同种子的高度相关家族的成员。
在一个实施例中,miRNA在哺乳动物细胞培养物中结合重组多肽产生一起使用。在一个实施例中,使用哺乳动物细胞产生重组多肽,这些哺乳动物细胞具有细胞凋亡、蛋白质翻译、细胞代谢、细胞增殖和/或应激反应中涉及的miRNA的修饰的活性。在一个实施例中,哺乳动物细胞或细胞培养物具有细胞凋亡、蛋白质翻译、细胞代谢、细胞增殖和/或应激反应中涉及的特定miRNA的增加的活性或表达。在另一个实施例中,哺乳动物细胞或细胞培养物具有细胞凋亡、蛋白质翻译、细胞代谢、细胞增殖和/或应激反应中涉及的特定miRNA的降低的活性或表达。
在一个实施例中,哺乳动物细胞被工程化以增加或降低miRNA活性。如在此所使用的“miRNA活性”指代miRNA通过结合至靶信使RNA调节生物过程如发育定时、细胞凋亡、分化、细胞增殖以及代谢的能力。可以例如通过增加细胞或细胞培养物中存在的特定miRNA的量来增加该特定miRNA的miRNA活性。例如,用于增加细胞中的miRNA表达的方法是已知的,这些方法包括但不限于:miRNA前体转染,包pri-miRNA或pre-miRNA的转染、miRNA寡核苷酸的转染;以及基于载体的miRNA的过表达,包括使用病毒载体和产生转基因动物。例如,特定miRNA的miRNA活性可以通过用单链miRNA寡核苷酸或用编码miRNA寡核苷酸或它的前体的表达载体转染细胞或细胞培养物来增加。在一个实施例中,细胞是用合成miRNA寡核苷酸转染。在一些实施例中,合成miRNA寡核苷酸包括例如提高核酸酶抗性,通过RISC提高对miRNA引导的裂解的抗性和/或提高结合亲和力的一种或多种化学修饰。在一些实施例中,miRNA寡核苷酸可以缀合至靶抗原以促进细胞对寡核苷酸的吸收。在一个实施例中,细胞被修饰来增加选自miR-10a[SEQ ID NO:1(uacccuguagauccgaauuugug)]、miR-21[SEQ ID NO:2-uagcuuaucagacugauguuga]以及它们的组合的一个或多个miRNA的活性。在另一个实施例中,细胞被修饰来过表达选自miR-10a、miR-21以及它们的组合的一个或多个miRNA。在一个实施例中,细胞被修饰来将选自miR-10a、miR-21以及它们的组合的一个或多个miRNA过表达成为未被修饰来过表达这些miRNA中的一个或多个的细胞系的至少约10倍、25倍、50倍、100倍、200倍、300倍、400倍、500倍、600倍、700倍、800倍、900倍、1000倍以及至多约1100倍、1200倍、1300倍、1400倍、1500倍或更多倍。在一个更具体的实施例中,细胞用能够表达miR-10a和/或miR-21的载体来稳定地或瞬时地转染。
可替代地,可以例如通过降低细胞或细胞培养物中存在的特定miRNA的量来抑制或降低该特定miRNA的miRNA活性。用于降低细胞或细胞培养物中存在的特定miRNA的量的方法包括基因敲除或使用miRNA抑制剂。在一个实施例中,特定miRNA的活性通过培养编码特定miRNA的内源基因已被敲除(即,编码miRNA的基因已被替换或破坏)的一个或多个基因工程化的细胞来降低。用于产生基因敲除的方法是已知的。在另一个实施例中,细胞或细胞培养物中的特定miRNA的活性在miRNA抑制剂的存在下通过培养细胞或细胞培养物来降低。如在此所使用,术语“miRNA抑制剂”指代可以压制靶基因表达的miRNA调节的分子,例如可以压制天然或内源miRNA活性的分子。在一个实施例中,哺乳动物细胞用编码miRNA抑制剂或它的前体的表达载体来稳定地或瞬时地转染。在另一个实施例中,哺乳动物细胞或细胞培养物可以用单链反义miRNA抑制剂寡核苷酸来转染。在一个实施例中,寡核苷酸是合成寡核苷酸。在一些实施例中,合成寡核苷酸包括例如提高核酸酶抗性,通过RISC提高对miRNA引导的裂解的抗性和/或提高结合亲和力的一种或多种化学修饰。在一个实施例中,miRNA寡核苷酸可以缀合至靶抗原以促进细胞对寡核苷酸的吸收。
在一个实施例中,miRNA抑制剂包括抗miRNA反义寡核苷酸(抗miR),该抗miR能够紧密结合至并且从而螯合与细胞靶mRNA竞争的miRNA,从而导致miRNA功能抑制。由于许多miRNA是含有相同种子的高度相关家族的成员,单一的抗miR可以阻断家族中多于一个miRNA的功能。在一个实施例中,抗miR包括单一的反义单元。在另一个实施例中,抗miR包括工程化为能够同时使多个miRNA靶标沉默的单一的寡核苷酸的多个反义单元。在又另一个实施例中,多于一个抗miR可以被共转染成靶向不同同工型或家族成员。仍然在另一个实施例中,多于一个抗miR可以被共转染成靶向多于一个微小RNA。用于提高核酸酶抗性,通过RISC提高对miRNA引导的裂解的抗性和/或提高反义寡核苷酸对miRNA的结合亲和力的化学修饰是已知的,并且包括例如糖、碱基或核苷酸间键的修饰。化学修饰的抗miR的一个实例是含有2’-O-甲基核糖糖的单链抑制剂。2’-O-甲基寡核苷酸对通过RISC和其他核酸酶两者进行的裂解具有抗性,并且形成与未修饰的反义寡核苷酸相比较热力学更稳定的RNA:RNA双链体。在另一个实施例中,抑制剂可以包括具有工程化为能够同时使多个miRNA靶标沉默的单一片段的多个反义单元的单链2’-O-甲基修饰的寡核糖核苷酸。其他化学修饰包括糖部分的2’位置处的2’-O-甲氧基乙基和2’-氟修饰。在另一个实施例中,抗miR可以包括磷酸糖主链中的呋喃糖环(有时称为“锁核酸”)的修饰。核酸酶抗性还可以通过以下内容来提高:硫原子替换磷酸基团中的非桥连氧原子中的一个的亲本磷酸二酯键到硫代磷酸酯(PS)键的主链修饰,或使用六元吗啉环替换糖部分的吗啉代寡聚物。
在另一个实施例中,miRNA抑制剂可以包括miRNA“海绵”技术,它可以用于培养细胞中包括整个miRNA种子家族的miRNA的瞬时和/或稳定抑制。miRNA海绵是可以用于转染哺乳动物细胞并且表达miRNA反义序列的表达载体,这些miRNA反义序列包括与一个或多个靶miRNA互补的多个(即,至少约5个,至少约10个或在约5与约20个之间)miRNA结合位点。在将编码miRNA海绵的载体转染到培养细胞中时,由海绵表达的RNA与用于结合至特定的微小RNA的内源mRNA竞争,从而能够阻抑微小RNAmRNA靶标。在一个实施例中,单个海绵可以用于阻断整个微小RNA种子家族。
在另一个实施例中,miRNA抑制剂包括miRNA掩蔽反义寡核苷酸(miR-mask)。在一个实施例中,miRNA掩蔽反义寡核苷酸包括单链寡核苷酸(例如,化学修饰的2’-O-甲基-修饰的寡核糖核苷酸),该单链寡核苷酸与靶mRNA的3’UTR中的特定miRNA的结合位点完全互补并且结合至该结合位点,而不是直接与靶miRNA相互作用。以此方式,miR-mask阻断靶miRNA进入到结合位点以便阻抑靶基因。在另一个实施例中,抑制剂可以包括前述技术的组合。例如,海绵/miR-mask技术将miRNA海绵的作用原理与用于靶向miRNA的miR-mask技术组合。
在一个实施例中,细胞具有选自miR-let7a[SEQ ID NO:3(ugagguaguagguuguauagu)]、miR-16[SEQ ID NO:4(uagcagcacguaaauauuggcg)]、miR-101[SEQ ID NO:5(uacaguacugugauaacugaa)]、miR-145[SEQ ID NO:6(guccaguuuucccaggaaucccu)]、miR-143[SEQ ID NO:7(ugagaugaagcacuguagcuc)]以及它们的组合的一个或多个miRNA的降低的活性。在一个实施例中,细胞未足够表达选自miR-let-7a、mir-16、miR-101、miR-145、miR-143以及它们的组合的一个或多个miRNA。在一个实施例中,细胞包括选自miR-let-7a、mir-16、miR-101、miR-145、miR-143以及它们的组合的一个或多个miRNA的基因敲除。在另一个实施例中,细胞用能够表达选自抗miR-let7a[SEQID NO:8(ACTATACAACCTACTACCTCA)]、抗miR-16[SEQ ID NO:9(CGCCAATATTTACGTGCTGCTA)]、抗miR-101[SEQ ID NO:10(TTCAGTTATCACAGTACTGTA)]、抗miR-145[SEQ ID NO:11(AGGGATTCCTGGGAAAACTGGAC)guccaguuuucccaggaaucccu]、miR-143[SEQ ID NO:12(GAGCTACAGTGCTTCATCTCA)]以及它们的组合的一种或多种抗miR抑制剂的载体来稳定地或瞬时地转染。miRNA的活性可以通过查看处于蛋白质和RNA水平的miRNA的靶标来量化。例如,可以利用用于miRNA活性的报告子测定,如具有构建体3’UTR中的miRNA位点的GFP或荧光素酶。在一个实施例中,选自抗miR-let7a、抗miR-16、抗miR-101、抗miR-145、miR-143或它们的组合的一种或多种抗miR抑制剂被过表达为未被修饰来表达抑制剂的细胞系的至少约10倍、25倍、50倍、100倍、200倍、300倍、400倍、500倍、600倍、700倍、800倍、900倍、1000倍以及至多约1100倍、1200倍、1300倍、1400倍、1500倍或更多倍。
在另一个实施例中,细胞凋亡、蛋白质翻译和/或细胞代谢中的至少一个介导因子的活性在具有降低的miRNA-let-7a活性的细胞培养物中增加或降低。在一个实施例中,选自miR-10a、miR-21以及它们的组合的一个或多个miRNA的活性在具有降低的miRNA-let-7a活性的细胞培养物中增加,和/或选自mir-16、miR-101、miR-145、miR-143以及它们的组合的一个或多个miRNA的活性在具有降低的miRNA-let-7a活性的细胞培养物中降低。在一个实施例中,miRNA-let-7a的至少一个靶标的表达在具有降低的miRNA-let-7a活性的细胞培养物中增加。在一个实施例中,miRNA-let-7a的至少一个靶标选自HMGA2、MYC、NF2、NIRF、RAB40C、以及eIF4a。用于测量mRNA的表达的方法是已知的,并且包括例如PCR、RN酶保护、DNA印迹、以及原位杂交。
在另一个实施例中,多于一个miR的表达可以发生改变(独立地增加或减少),例如,至少2个、至少3个、至少4个或至多5个miRNA的表达在哺乳动物细胞系中可以发生改变,以通过一次性解决多个区域来提高生产率。在一个实施例中,miR-let-7a活性可以降低,并且第二miR的活性可以发生改变。在一个实施例中,第二miR可以包括miR-21、miR-10a和/或抗miR-143。
D.载体
在一个实施例中,使用哺乳动物细胞产生重组多肽,这些哺乳动物细胞已用能够表达细胞凋亡、蛋白质翻译、细胞代谢、细胞增殖和/或应激反应中涉及的一个或多个miRNA或具有miRNA的抑制剂的载体稳定地或瞬时地转染。如在此所使用,术语“载体”指代可以用于将感兴趣的核酸递送至细胞的内部的物质组分。众多载体是已知的,包括但不限于:线性多核苷酸、与离子化合物或两亲化合物相关联的多核苷酸、质粒、以及病毒。术语“载体”可以包括自主复制的质粒或病毒,或不能自主复制的载体或质粒。在一个实施例中,载体可以是裸露的RNA多核苷酸、裸露的DNA多核苷酸、多聚赖氨酸缀合的DNA或RNA、肽缀合的DNA或RNA、脂质体缀合的DNA,它们不能自主复制。在一个实施例中,载体是合成寡核苷酸。涵盖的是,任何载体都可以用于瞬时转染,只要它被表达在适当的系统中并且在宿主中具有活力。对于稳定的转染,载体在宿主中通常是可复制的。大量合适的载体是已知的,并且是可商购的。
在一个实施例中,载体包括编码miRNA或miRNA抑制剂的至少一个多核苷酸,或其可操作地连接至启动子的前体。短语“可操作地连接”意指启动子相对于多核苷酸处于正确的位置和取向上,以控制通过RNA聚合酶进行的转录的起始以及多核苷酸的表达。如在此所使用,术语“调节序列”指代控制可操作地连接至调节序列的核酸序列的表达的某一方面的核酸序列。在一些情况下,调节序列可以是启动子(即,促进可操作地连接的编码区的转录的起始的调节元件),并且在其他情况下,调节序列可以包括增强子序列和/或其他调节元件,如核糖体结合位点、剪接信号、多腺苷酸化信号、转录终止序列和/或5’侧翼非转录序列。载体中所采用的启动子可以是结构性的或诱导性的。“结构性”启动子是在可操作地连接至编码基因产物的多核苷酸时使得在细胞的大多数或所有生理条件(即,特异性刺激物是不需要的)下能够在细胞中产生基因产物的核苷酸序列。“诱导性”启动子是能够在刺激物(即,热休克、化学品、光等)的存在下引导可操作地连接的多核苷酸序列与在刺激物的不存在下可操作地连接的多核苷酸序列的转录水平不同的转录水平的启动子。调节元件可以是“内源的”或“外源的”或“异源的”。“内源”调节元件是天然连接至特定核酸序列的调节元件。“外源”或“异源”调节元件是通过遗传操纵与核酸序列毗邻放置,这样使得由连接的调节元件来引导核酸序列的转录的调节元件。
合适的启动子的实例包括已知用于控制哺乳动物细胞中的基因的表达的启动子,包括但不限于:病毒启动子如巨细胞病毒(CMV)立即早期启动子、单纯疱疹病毒胸苷激酶(HSV-TK)启动子、猿猴病毒40(SV40)启动子或鲁斯氏肉瘤(RSV)LTR启动子、pMC1、磷酸甘油酸激酶(PGK)启动子、U1启动子、以及H6启动子。
除了编码一个或多个miRNA或miRNA抑制剂之外,载体还可以包括可选择标记基因、报告子基因、或编码感兴趣的重组多肽的基因。另外,用于稳定的转染的表达载体可以包括用于稳定的整合到宿主细胞基因组中的一个或多个位点。
在一个实施例中,表达载体包括用于体外评定载体的递送和作用持续时间的一个或多个可选择标记或报告子基团。术语“可选择标记”指代编码具有活性的,将抗生素或其他药物抗性赋予表达了可选择标记的细胞的酶的基因。可选择标记的实例包括但不限于:腺苷脱氨酶(ADA)、氨基糖苷磷酸转移酶、博来霉素、胞嘧啶脱氨酶、二氢叶酸还原酶、组氨醇脱氢酶、潮霉素-B-磷酸转移酶、嘌呤霉素-N-乙酰转移酶、胸苷激酶、黄嘌呤-鸟嘌呤磷酸核糖转移酶、氨苄青霉素、新霉素、卡那霉素、吉欧霉素(zeocin)、以及羧苄青霉素。
术语“报告子基团”指代编码可以容易地检测其表达(例如,冷光或荧光)的蛋白质的基因。报告子基因的实例包括但不限于:绿色荧光蛋白、萤光素酶、氯霉素乙酰转移酶、β-半乳糖苷酶、碱性磷酸酶、辣根过氧化物酶、RFP、YFP、以及BFP。在一个实施例中,表达载体是病毒载体,包括但不限于:腺病毒载体、腺伴随病毒载体、逆转录病毒载体如慢病毒载体或Moloney鼠白血病病毒、以及来源于痘病毒单纯疱疹病毒I的载体。在另一个实施例中,表达载体是非病毒载体。合适的载体的实例包括但不限于以下真核生物载体:pWLNEO、pSV2CAT、pOG44、PXT1、pSG(Stratagene)、pSVK3、pBPV、pMSG、pSVL(法玛西亚(Pharmacia))、和pCS2载体以及它们的衍生物。
在一个实施例中,使用哺乳动物细胞产生重组多肽,这些哺乳动物细胞已用能够表达选自miR-10a、miR-21以及它们的前体,或它们的组合的一个或多个miRNA的一个或多个载体稳定地或瞬时地转染。在一个更具体的实施例中,使用哺乳动物细胞产生重组多肽,这些哺乳动物细胞已用能够表达选自抗miR-let7a、抗miR-16、抗miR-101、抗miR-145、抗-miR-143以及它们的前体,或它们的组合的一个或多个反义寡核苷酸的一个或多个载体稳定地或瞬时地转染。在一个实施例中,哺乳动物细胞已用能够表达至少一个miRNA和至少一种miRNA抑制剂的一个或多个表达载体稳定地或瞬时地转染。在又另一个实施例中,哺乳动物细胞已用能够表达至少一个miRNA和/或至少一种miRNA抑制剂的一个或多个载体结合编码感兴趣的重组多肽的至少一个多核苷酸来转染。
E.转染
在此描述的载体可以使用本领域已知的方法引入到哺乳动物宿主细胞中。术语“转染”指代将外源基因材料引入到细胞中以产生基因修饰的细胞。例如,载体可以通过物理、化学或生物手段转染到宿主细胞中。用于将多核苷酸引入到宿主细胞中的物理方法包括但不限于:磷酸钙沉淀、脂转染(包括带正电荷的脂质体介导的转染)、粒子轰击、显微注射、DEAE-葡聚糖介导的转染以及电穿孔。用于将载体引入到宿主细胞中的生物方法包括使用DNA和RNA载体,包括例如病毒载体。用于将多核苷酸引入到宿主细胞中的化学手段包括胶体分散体系,如大分子复合物、纳米囊、微球体、珠粒;以及基于脂质的体系,包括水包油型乳剂、胶束、混合型胶束和脂质体。
在一个实施例中,宿主细胞可以用载体稳定地转染。术语“稳定的转染”意指载体中的核苷酸序列能够整合到哺乳动物细胞的全长DNA序列中。典型地,对于稳定的转染,宿主细胞用包括可选择标记的载体转染。在一个实施例中,可选择标记共表达在与miRNA或miRNA抑制剂或它们的前体相同的载体上。在另一个实施例中,可选择标记表达在单独的共转染的载体上。在选择试剂的存在下转染细胞的生长允许外源基因材料已并入到基因组中的细胞的亚群体持续存在。典型地,将选择压力维持至少约1周、至少约2周以及至多约3周或至多约1个月。在选择周期结束时,在选择性培养基中有活力的细胞将从表达质粒整合外源基因材料。外源基因材料的整合可以通过报告子的存在来证实,并且细胞可以被扩增用于大规模培养。
在另一个实施例中,宿主细胞可以用载体瞬时地转染。与稳定的转染相对比,瞬时转染的基因材料仅在转染细胞中表达一段有限的时间,并且不整合到宿主细胞的基因组中。一般而言,瞬时转染使得miRNA、抗miR抑制剂或它们的前体的表达持续至少约24小时、至少约48小时、至少约72小时以及至多约96小时。
F.细胞培养
术语“细胞培养”指代多细胞生物或组织外部的细胞的生长和繁殖。细胞培养条件如pH、温度、湿度、气氛以及搅拌可以改变来改进细胞培养的生长和/或生产率特征。一般而言,哺乳动物细胞培养在约36℃与约38℃之间,典型地在约37℃的温度以及约80%与约95%之间的相对湿度下维持在约6.5与约7.5之间的pH。哺乳动物细胞培养基典型地含有要求约1%与约10%之间,典型地在约5%与约6%之间的二氧化碳(CO2)气氛的缓冲系统。哺乳动物细胞可以在混悬液中或在附接至固体衬底时培养。哺乳动物细胞能够以小规模培养形式培养,例如在实验室中在100ml容器或在250ml容器中培养,该小规模培养形式通常具有容器中不超过容器总体积的40%并且往往是约25%的体积。可替代地,培养可以是大规模的,例如1000ml容器,3000ml容器、8000ml容器以及15000ml容器,或在大规模生物反应器中例如在制造设备中以至多1000L、至多5000L以及至多10,000L的体积培养。通过哺乳动物细胞大规模生产重组多肽可以包括连续的、分批的以及分批补料的培养系统。哺乳动物细胞可以在微载体存在或不存在下,例如在流化床生物反应器、中空纤维生物反应器、滚瓶、摇瓶、或搅拌釜生物反应器中培养,并且以分批、分批补料、连续、半连续或灌注模式操作。大规模细胞培养典型地维持数天,或甚至数周,同时细胞产生一种或多种所希望的蛋白质产物。
在此描述的方法可以用于改进单相和多相培养过程两者中重组多肽的生产。在一个实施例中,细胞培养是多阶段过程,其中细胞首先在最大化细胞增殖和活力的环境条件下以生长相培养,并且之后在最大化多肽生产的条件下转变成生产相。生长相和生产相可以处在一个或多个过渡相之前或与它们分开。在一个实施例中,细胞培养是具有至少一个生长相和至少一个生产相的多阶段过程。在一个实施例中,细胞在生长相期间在比生产相更高的温度下孵育。例如,细胞在生长相期间在约35℃至约38℃之间的第一温度下培养,并且在生产相期间在约29℃至约37℃之间,或在约30℃至约36℃之间,或在约30℃至约34℃之间的第二温度下培养。此外,在生产相期间可以添加蛋白质生产的化学诱导剂例如像咖啡因、丁酸盐、以及六亚甲基二乙酰胺(HMBA)。在一个实施例中,miRNA或miRNA抑制剂的活性在生产相期间增加或降低。在一个实施例中,在生产相期间诱导了编码miRNA或miRNA抑制剂或它们的前体的表达载体的转录。在另一个实施例中,在生产相期间将miRNA或miRNA载体或寡核苷酸,或抑制剂或它们的前体添加至培养基。
哺乳动物细胞系(又称为“宿主细胞”)可以被基因工程化来表达重组多肽例如具有商业或科学利益的多肽。使细胞系基因工程化通常涉及用重组多核苷酸分子转染、转化或转导细胞,和/或以其他方式改变(例如,通过同源重组和基因激活或重组细胞与非重组细胞的融合)以使宿主细胞表达所希望的重组多肽。用于使细胞和/或细胞系基因工程化以表达多肽的方法和载体是已知的。适用于产生重组多肽的哺乳动物细胞的实例包括但不限于:中国仓鼠卵巢(CHO)细胞、小鼠骨髓瘤(NS0)、人胚肾(HEK 293)、幼仓鼠肾(BHK)细胞、非洲绿猴肾细胞、人子宫颈癌传代细胞、马丁达比犬肾(MDCK)细胞、CV1猴肾细胞、3T3细胞、骨髓瘤细胞系如NS0和NS1、PC12、WI38细胞、COS细胞(包括COS-1和COS-7)、以及C127。在一个实施例中,哺乳动物细胞系表达增加的或降低的水平的一个或多个miRNA。在一个实施例中,哺乳动物细胞用如上文更详细描述的异源miRNA或抗miRNA抑制剂来稳定地或瞬时地转染。在一个更具体的实施例中,细胞培养中的哺乳动物细胞具有降低的miRNA-let-7a活性。在一个实施例中,哺乳动物细胞用抗miRNA-let-7a抑制剂转染。
哺乳动物细胞可以维持在多种细胞培养基中。术语“细胞培养基”指代细胞例如哺乳动物细胞在其中生长的营养液。细胞培养基的配制在本领域中是熟知的。典型地,细胞培养基包括缓冲液、盐、碳水化合物、氨基酸、维生素以及必要的微量元素。细胞培养基可以含有或不含有血清、蛋白胨、和/或蛋白质。细胞培养基可以补充有另外的组分或浓度增加的组分,如氨基酸、盐、糖、维生素、激素、生长因子、缓冲液、抗生素、脂质、微量元素等,这取决于有待培养的细胞的要求和/或所希望的细胞培养参数。包括无血清的且限定的培养基的不同培养基是可商购的,并且包括但不限于:最小必需培养基(MEM,西格玛(Sigma),圣路易斯(St.Louis),密苏里州(Mo.));Ham's F10培养基(西格玛);达尔伯克氏改良伊格尔氏培养基(DMEM,西格玛);最小必需培养基(MEM);伊格尔氏基础培养基(BME);RPMI-1640培养基(西格玛);HyClone细胞培养基(HyClone,洛根(Logan),犹他州(Utah));以及化学成分确定的(CD)培养基,它们针对特定细胞类型进行配制,例如CD-CHO培养基(英杰公司(Invitrogen),卡尔斯巴德(Carlsbad),加利福尼亚州(Calif.))。可以将诸如以上所述的那些的补充组分或成分添加至可商购的培养基。在一个实施例中,培养基可以包括miRNA或miRNA抑制剂、寡核苷酸或它们的前体,或编码miRNA或miRNA抑制剂或它们的前体的表达载体。
由哺乳动物细胞培养物表达的重组多肽可以在细胞内产生,或分泌到可以对它们回收和/或收集的培养基中。此外,可以使用已知方法和可从商业厂家获得的产品来从培养物纯化或部分纯化重组多肽。纯化的多肽之后可以被“配制”,例如缓冲液交换、灭菌、成批包装、和/或包装以供最终用户使用。
细胞培养物的产生特征可以通过以下内容确定:测量活细胞密度(VCD)、抗体滴度、以及生产率,该生产率包括比生产率(Qp)、累积生产率以及峰值VCD时评价的最大生产率。
在一个实施例中,细胞培养物包括具有降低的miRNA-let-7a活性的哺乳动物细胞。在一个实施例中,miRNA-let-7a活性被微小RNA抑制剂降低。在一个实施例中,微小RNA抑制剂是miRNA-let-7a的反义寡核苷酸抑制剂。在一个实施例中,哺乳动物细胞用编码miRNA-let-7a的反义抑制剂的可复制表达载体来转染。在另一个实施例中,哺乳动物细胞用miRNA-let-7a的寡核苷酸抑制剂转染。在一个实施例中,寡核苷酸抑制剂被化学修饰例如以改进核酸酶抗性,以通过RISC提高对miRNA引导的裂解的抗性和/或提高结合亲和力。在一个实施例中,具有降低的miRNA-let-7a的哺乳动物细胞包括miRNA-let-7a基因敲除。
在一个实施例中,细胞培养物具有与不具有降低的miRNA-let-7a活性的对照细胞培养物相比较增加至少约25%的生产率。如在此所使用,术语“生产率”指代细胞培养物在一段限定的时间内产生的重组多肽的浓度。生产率可以基于测量结果如滴度、活细胞密度(VCD)以及活力%来评价。用于测量滴度、VCD以及活力%的方法是已知的。在一个实施例中,细胞培养物具有与不具有降低的miRNA-let-7a活性的对照细胞培养物相比较时增加至少约25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%以及至多约100%;约25%到约100%;约50%到约75%的比生产率。
在一个实施例中,生产率指代比生产率(尹(Yoon)等人,(2006)用于增强中国仓鼠卵巢细胞的促红细胞生成素体积生产率的两阶段培养策略(Biphasic culture strategyfor enhancing volumetric erythropoietin productivity of Chinese hamster ovarycells.),酶和微生物技术(Enzyme and Microbial Technology)39:362-365;鲍曼(Baumann)等人,(2008)巴斯德毕赤氏酵母的低氧分批补料培养提高重组蛋白的比生产率和体积生产率(Hypoxic fed-batch cultivation of Pichia pastoris increasesspecific and volumetric productivity of recombinant proteins.),生物技术和生物工程(Biotechnology and Bioengineering)100(1):177-183;布拉辛斯奇(Brezinsky)等人,(2003)用于富集转染CHO细胞的群体以获得较高比生产率的细胞的简单方法(A simplemethod for enriching populations of transfected CHO cells for cells of higherspecific productivity.),免疫学方法杂志(Journal of Immunological Methods)277:141-155;福克斯(Fox)等人,(2003)经由温度变化优化通过中国仓鼠卵巢细胞最大化干扰素-γ生产:实验和建模(Maximizing Interferon-γproduction by Chinese hamsterovary cells through temperature shift optimization:experimental andmodeling.),生物技术和生物工程85(2):177-184;武尔姆(Wurm),(2004)在培养的哺乳动物细胞中产生重组蛋白治疗剂(Production of recombinant protein therapeutics incultivated mammalian cells.),自然生物技术(Nature Biotechnology)22(11):1393-1398;布朗尼(Browne)和艾尔·鲁贝阿(Al-Rubeai),(2009)用于高产哺乳动物细胞系的选择方法(Selection methods for high-producing mammalian cell lines.),由艾尔·鲁贝阿·M编辑,细胞系发展(Cell Line Development),系列:细胞工程6(Series:CellEngineering 6),施普林格科学+商业媒体私人有限公司(Springer Science+BusinessMedia B.V.),第127页-第151页)。如在此所使用,术语“比生产率”指代每天培养中每个活细胞产生的重组蛋白,并且可以计算为产物浓度(滴度)对累积活细胞密度的积分的斜率(mg/L/CCD)。在一个实施例中,细胞培养物具有与不具有降低的miRNA-let-7a活性的对照细胞培养物相比较时增加至少约25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%以及至多约100%;约25%到约100%;约50%到约75%的比生产率。
在一个实施例中,生产率指代峰值活细胞密度(VCD)下确定的“最大生产率”。如在此所使用,术语“最大生产率”指代培养处于其最大VCD时的生产率的水平,并且可以计算为与前一时间点相比较的最大VCD下的滴度的变化除以最大时间点与先前时间点之间的VCD的变化,乘以从第1时间点到第2时间点的培养天数,除以最终VCD相对于最初VCD的自然对数。在一个实施例中,与不具有降低的miRNA-let-7a活性的对照细胞培养物相比较时,最大生产率增加至少约25%。在一个实施例中,细胞培养物具有与不具有降低的miRNA-let-7a活性的对照细胞培养物相比较时为至少约25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、100%、125%、150%、175%或200%或约25%到约200%的最大生产率。
在一个实施例中,生产率指代累积生产率。如在此所使用,术语“累积生产率”指代贯穿整个生长周期的比生产率,并且可以计算为产物浓度(滴度)对累计活细胞密度的积分的斜率(mg/L/CCD)(伦纳德(Renard)等人,(1988)单克隆抗体产生动力学与分批系统中的活细胞曲线的积分相关的证据(Evidence that monoclonal antibody productionkinetics is related to the integral of the viable cells curve in batchsystems.),生物技术通讯(Biotechnology Letters)10(2):91-96;尹等人,(2006)用于增强中国仓鼠卵巢细胞的促红细胞生成素体积生产率的两阶段培养策略,酶和微生物技术39:362-365;李(Li)等人,(2010)用于单克隆抗体生产的细胞培养方法(Cell cultureprocesses for monoclonal antibody production.),单克隆抗体杂志通讯(mAbs),2(5)466-477;布拉辛斯奇等人,(2003)用于富集转染CHO细胞的群体以获得较高比生产率的细胞的简单方法,免疫学方法杂志277:141-155;福克斯等人,(2003)经由温度变化优化通过中国仓鼠卵巢细胞最大化干扰素-γ生产:实验和建模,生物技术和生物工程85(2):177-184)。在一个实施例中,细胞培养物具有与不具有降低的miRNA-let-7a活性的对照细胞培养物相比较时增加至少约25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%以及至多约100%;约25%到约100%;约50%到约75%的累积生产率。
在一个实施例中,生产率指代培养物的比生产率,即,总培养物中的重组多肽细胞的滴度对比对照细胞培养物中的重组多肽的滴度。
G.重组多肽
如在此所使用的术语“重组多肽”指代由培养的宿主细胞产生的基因工程化的多肽或蛋白质。如在此所使用,术语“异源的”指代由宿主细胞产生但不正常表达该多肽的重组多肽。然而,异源多肽可以包括生物天然具有的但已故意以某一方式改变的多肽。例如,异源多肽可以包括由宿主细胞表达的已用表达多核苷酸的载体转染的多肽。
在一个实施例中,多肽是抗体或它的结合片段。抗体可以是寡克隆抗体、多克隆抗体、单克隆抗体、嵌合抗体、骆驼化抗体、CDR移植抗体、多特异性抗体、双特异性抗体、催化性抗体、人源化抗体、完全的人抗体、抗独特型抗体和能够以可溶或结合形式标记的抗体,以及它们的包括表位结合片段的片段、变体或衍生物,它们单独存在或与其他氨基酸序列组合。抗体可以来自任何物种。术语抗体还包括结合片段,包括但不限于:Fv、Fab、Fab'、F(ab')2、单链抗体(svFC)、二聚可变区(二聚抗体)以及二硫键连接的可变区(dsFv)。免疫球蛋白分子可以是任何类型(例如IgG、IgE、IgM、IgD、IgA、以及IgY)、类别(例如IgG1、IgG2、IgG3、IgG4、IgA1、以及IgA2)或子类。
在另一个实施例中,重组多肽是非抗体蛋白。非抗体蛋白的实例包括但不限于:融合蛋白、受体、细胞表面蛋白的配体、分泌的蛋白、以及酶。
H.试剂盒
任何miRNA或抗miRNA寡核苷酸或表达载体以及另外的组分如缓冲液、细胞和培养基可以封装在试剂盒形式中。典型地,试剂盒还含有材料如用于进行本发明的方法的说明书、封装材料、以及容器。在一个实施例中,试剂盒包括编码如上文更详细描述的miRNA基因产物或miRNA抑制剂的至少一个表达载体。在一个实施例中,表达载体可以用于体外转录或转录/翻译系统,或用于瞬时地或稳定地转染细胞。在另一个实施例中,试剂盒包括至少两个表达载体,其中一个编码miRNA基因产物或miRNA抑制剂,并且另一个编码可选择标记、报告子基因或重组多肽。
I.通过引用的结合
在此引用的所有参考文献,包括专利、专利申请、论文、教科书等以及其中引用的参考文献(如同它们还未曾引用过的程度)通过引用以其全部内容结合在此。
J.等效物
前述书面说明书被认为足以使本领域的技术人员能够实践本发明。前述描述和实例详述了本发明的某些优选的实施例,并且描述了诸位发明人所期望的最佳模式。然而,将了解到,无论前述内容以文本形式表现的如何详细,本发明仍可以以多种方式实践,并且应根据随附权利要求书和它的任何等效物来解释本发明。
6.操作实例
为了研究改变的微小RNA表达提高哺乳动物细胞生产率的能力,两个抗体产生CHO细胞系用慢病毒载体稳定地转导,所述慢病毒载体基于涉及重组多肽生产如细胞增殖、应激反应、细胞凋亡以及mRNA翻译的路径中微小RNA的潜在涉及来编码9个不同的微小RNA或反义微小RNA抑制剂(表1)。
A.材料与方法
细胞培养和转导
表达不同单克隆抗体的中国仓鼠卵巢(CHO)细胞(悬浮细胞系)在补充有50uM L-甲硫氨酸亚砜胺(MSX;西格玛奥德里奇(Sigma Aldrich),圣路易斯,密苏里州)和0.5X GS补充剂(SAFC生物科学,雷内克萨(Lenexa),堪萨斯州(KS))的CD CHO培养基(生命技术(Life Technologies),卡尔斯巴德,加利福尼亚州)中生长。将摇瓶培养物维持在120 RPM、37℃、6%CO2以及80%湿度。在2-20的MOI下,用过表达miR-10a、miR-21的慢病毒载体或载体对照(开放生物系统公司(Open Biosystems),亨茨维尔(Huntsville),亚拉巴马州(AL)),或表达抗miR-let7a、-16、-101或-145的那些载体,或载体对照(系统生物科学公司(System Biosciences),山景城(Mountain View),加利福尼亚州)转导25万细胞。将转导细胞扩增并且在5ug/mL嘌呤霉素中选择2周-3周。利用绿色荧光蛋白(GFP)或红色荧光蛋白(RFP)载体组分(分别来自抗miR或miR载体),通过荧光激活细胞分类术(FACS)收集细胞,并且使所述细胞扩增以用于分批补料细胞培养。转导效率逼近100%(图11A)。在使用这些修饰的细胞系的整个过程中监测并证实标记基因表达,并且定量RT-PCR证明了所得的稳定转导的细胞系中miRs和抗miR两者的高水平表达(表2)。
在125mL摇瓶中进行分批补料测定,重复三次。在25mL CD CHO培养基中用上文描述的补充剂接种细胞。在产生稳定的miR-修饰的CHO细胞系之后,持续14天每两天监测细胞的活细胞密度(VCD)(表3),mAb滴度(表4),以及源自改变的miRNA表达的Qp(图1-4)。使用ViCELL细胞活力分析仪(贝克曼库尔特公司(Beckman Coulter),印第安纳波利斯(Indianapolis),印第安纳州(IN))监测活细胞密度(VCD)、活力%(%V)以及细胞大小。使用Octet系统(forteBIO/颇尔生命科学(Pall Life Sciences),门洛帕克(Menlo Park),加利福尼亚州)测量抗体滴度。累积Qp计算为产物浓度(滴度)对累积活细胞密度的积分的斜率(mg/L/CCD)(伦纳德等人,(1988)单克隆抗体产生动力学与分批系统中的活细胞曲线的积分相关的证据,生物技术通讯10(2):91-96;尹等人,(2006)用于增强中国仓鼠卵巢细胞的促红细胞生成素体积生产率的两阶段培养策略,酶和微生物技术39:362-365;李等人,(2010)用于单克隆抗体生产的细胞培养方法,单克隆抗体杂志通讯,2(5)466-477;布拉辛斯奇等人,(2003)用于富集转染CHO细胞的群体以获得较高比生产率的细胞的简单方法,免疫学方法杂志277:141-155;福克斯等人,(2003)经由温度变化优化通过中国仓鼠卵巢细胞最大化干扰素-γ生产:实验和建模,生物技术和生物工程85(2):177-184)。最大QP计算为与前一时间点相比较的最大VCD下的滴度的变化除以最大时间点与先前时间点之间的VCD的变化,乘以从第1时间点到第2时间点的培养天数,除以最终VCD相对于最初VCD的自然对数。滴度、累积Qp和最大Qp与基线相比较都呈现为相对单位。
RNA提取和实时PCR分析
使用miRVana miRNA分离试剂盒(生命技术)根据制造商的说明书从0.5-5x 106个细胞提取总RNA。通过Nanodrop分析来测定浓度,并且在安捷伦2100生物分析仪(Agilent2100 Bioanalyzer)上使用RNA 6000 Nano LabChip评定RNA质量。对于过表达的miRNA的TaqMan分析,使用Multiscribe RT和Megaplex RT引物池(生命技术)根据制造商的说明书将100-300ng总RNA逆转录成cDNA。在含有12.5μL 2X TaqMan预扩增(PreAmp)主要混合物、2.5μL 10X Megaplex预扩增(preamp)引物、7.5μL H2O以及2.5μL RT产物的反应中使用TaqMan预扩增主要混合物和Megaplex预扩增引物池(生命技术)来使所得cDNA预扩增。在循环之后,在DNA悬浮缓冲液(TEKnova,霍利斯特(Hollister),加利福尼亚州)中按1:4稀释扩增的样品,并且保持在-20℃或立即用于PCR。使用特异于miR-10a和miR-21的TaqMan测定(ABI/生命技术,卡尔斯巴德,加利福尼亚州)在预扩增的材料上进行实时PCR。相对于U6snRNA评价每个miRNA的表达。
为了制备用于加载到48x 48动态阵列芯片(富鲁达(Fluidigm),南旧金山,加利福尼亚州)中的样品,反应混合物含有2.5μL 2X通用主要混合物(ABI/生命技术)、0.25μL样品加载缓冲液(富鲁达)以及2.25μL预扩增的cDNA。为了制备引物/探针,反应混合物含有2.5μL 20X TaqMan基因表达测定和2.5μL测定加载缓冲液(富鲁达)。在将样品和测定试剂加载到入口之前,在IFC控制器中引发芯片。将如所述制备的5微升样品加载到动态阵列芯片的每个样品入口中,并且将5μL 10X基因表达测定混合物加载到每个检测器入口中。在完成IFC致敏和加载/混合步骤之后,将芯片加载到用于热循环的BioMarkTM实时PCR系统上。
使用QuantiMiRTM RT试剂盒(系统生物科学公司)根据制造商的说明书来评定抗miR表达。在DNA悬浮缓冲液(TEKnova)中按1:10稀释反应,以用于使用miR-特异性正向引物和通用反向引物(系统生物科学公司)进行SYBR绿色实时PCR。定量PCR反应含有1μL稀释的QuantiMir cDNA、0.5μL 10uM通用反向引物、1μL 10μM miRNA特异性正向引物、15μL 2XSYBR绿色qPCR主要混合物缓冲液以及12.5μL无RNase的H2O。在应用生物系统7900实时PCR仪器上进行热循环。试验结束时包括熔化分析以验证扩增反应特异性。U6snRNA用作内部对照。
对于miR-let7a mRNA靶标的表达分析,使用III第一链合成SuperMix(生命技术)和随机六聚体根据制造商的说明书从500ng提取的总RNA合成cDNA。使用TaqMan基因表达测定和TaqMan预扩增主要混合物进行预扩增。反应含有5μL cDNA、10μL预扩增主要混合物以及5μL 0.2X基因表达测定混合物(包含有待测定的所有引物/探针),最终体积是20μL。通过实时PCR与特异于感兴趣的靶基因的TaqMan基因表达测定以及TaqMan通用主要混合物(生命技术)使用BioMarkTM仪器(富鲁达)测定预扩增的cDNA,如上文针对过表达的miR指示的。β-肌动蛋白和GAPDH用作内部对照,并且使用Δ-ΔCt法来评价数据。
蛋白质印迹
通过具有或不具有miRNA修饰的裂解培养物的蛋白质分析评定靶蛋白改变。在RIPA裂解和提取缓冲液(皮尔斯)中以HALT蛋白酶和磷酸酶抑制剂(皮尔斯(Pierce))制备产生抗体的CHO培养物的细胞裂解液。在还原条件下,在1X MOPS电泳缓冲液(生命技术)中的4%至12%的NuPage凝胶(生命技术)上分辨15微升细胞裂解液,并且将这些细胞裂解液转移至PVDF膜(生命技术)。在无蛋白质T20(PBS)阻断缓冲液(热科学皮尔斯(ThermoScientific Pierce),罗克福德(Rockford)、伊利诺伊州(IL))中将膜阻断1小时,并且在4℃下,用1:500稀释度的兔抗RAS(细胞信号转导技术公司(Cell Signaling),丹弗斯(Danvers),马萨诸塞州(MA))或1:333稀释度的小鼠抗GAPDH(艾博抗(abcam),剑桥(Cambridge),英国)初级抗体孵育过夜。在室温下,在PBST 0.1%+0.02%SDS中荧光标记的二级抗体:分别针对RAS和GAPDH的抗兔800CW(LI-COR,林肯(Lincoln),内布拉斯加州(NE))和抗小鼠680LT(LI-COR)中将印迹孵育30分钟。使用奥德赛(Odyssey)成像系统(LI-COR)和奥德赛软件(LI-COR)捕获和量化荧光信号和带强度。
抗体保真度/完整性分析
生产来自miR或抗miR修饰的系的抗体,并且使用蛋白A亲和色谱法纯化这些抗体。使用配备有安捷伦Zorbax Poroshell SB300 C3 75x 1.0mm的柱的安捷伦1200系列仪器执行反相分离。将2μg蛋白质样品还原并且注入到柱上。用90%溶剂A(0.1%甲酸于H20中)和10%溶剂B(0.1%甲酸的乙腈)平衡柱,并且通过从10%至60%的B的分步梯度(stepgradient)实现洗脱。在整个试验过程中,将流速和温度维持在0.4ml/min和35℃。
在安捷伦6520LC/MS QTOF质谱仪(安捷伦技术,圣塔克拉拉(Santa Clara),加利福尼亚州)上以300-3000m/z的扫描范围在阳离子模式下执行质谱分析。LC与TOF之间的耦合是经由电雾化电离(ESI)源以两个雾化器进行的—一个雾化器用于LC洗脱液,并且一个雾化器用于内部参考质量化合物(m/z 322.0481和m/z 1221.9906)。使用具有用于自动化去卷积的Bioconfirm和蛋白质确认的安捷伦MassHunter定性分析来分析ESI质谱。
B.结果
抗miR-let-7a提高CHO细胞生产率
MiR-10a、抗miR-let-7a和抗miR-143证明累积Qp的最高水平,其中与对照系相比较,生产率分别提高63%、71%以及53%(图1)。除了评价累积Qp之外,我们还评价了这些miR修饰的细胞系中的每一个在峰值VCD下计算的最大Qp。结果显示,与亲本/对照系相比较,miR-10a、抗miR-let-7a和抗miR-143的最大生产率分别增加38%、163%以及64%(图2)。其他miR修饰的CHO细胞系未显示显著变化,或显示了与亲本/对照培养物相比较Qp的降低。
由于重组多肽滴度和VCD是Qp的组分,我们研究了每个miR修饰的细胞系的这些参数上的改变。虽然miR-10a、抗miR-143和抗miR-let-7a显示了与对照相比较增加的Qp,它们的滴度的相对增加类似于在亲本或对照细胞系中观察到的(图3)。此外,产生抗miR-let-7a的修饰的CHO细胞达到亲本或对照系的仅一半的最大VCD(图4)。MiR-10a和抗miR-143修饰的系在第10天以比抗miR-let-7a的那些更高的水平达到VCD峰值,但它们的生长从第12天到第14天发生明显下降,而抗miR-let-7a到第14天仍保持在相对恒定的水平。在降低的细胞密度下的生长可以表明细胞能量有利地重新导向重组多肽合成,而非培养物的增殖(布朗尼和艾尔·鲁贝阿,(2009)用于高产哺乳动物细胞系的选择方法,由艾尔·鲁贝阿·M编辑,细胞系发展,系列:细胞工程6,施普林格科学+商业媒体私人有限公司,第127页-第151页)。总而言之,miR-let-7a的抑制提供Qp的最大增加,评价了所有miR修饰的系的持续时间最长的生长特征。
抑制在另外的mAb产生CHO细胞系中是一致的
为了确定抗miR-let-7a对CHO生长和生产率的影响是否特异于最初测试的生产细胞系,或这种影响是否可以更加泛化到其他生产培养物,选择具有更高的生产能力并产生不同的mAb的另外的CHO细胞系。测试的两个mAb产生细胞系中的结果彼此类似,因为随着时间的推移,抗miR-let-7a细胞系与对照相比较维持类似的或降低的VCD以及类似的最终mAb滴度(图5和图6),从而导致与对照相比较的50%和68%的Qp的增加(图7)。缩减来自miR或抗miR修饰的系的2μg纯化的抗体并且通过反相LC/MS进行评定,使保真度和完整性等同于亲本系。反相LC/MS进一步验证,来自抗miR修饰的细胞系的mAb产物的保真度和完整性等同于亲本系(图12A和图12B)。有趣的是,在亲本细胞系的初始mAb生产能力与引入抗miR-let-7a时Qp的增加百分比之间观察到了逆相关(图7)。具体而言,第二细胞系显示与第一细胞系相比较1.6倍增加的生产能力,并且这翻译为Qp的较低下降(约1.4倍),从而表明miR修饰通常能够以积极的方式影响重组多肽生产,而对于低产细胞系而言可以具有更大的益处。
抗miR-let-7A增加对于CHO细胞生产率而言很重要的靶标
为了理解miR-let-7a抑制的功能效果,检查多个预测的且验证的miR-let-7a的靶标,这些靶标已在无数细胞类型和疾病情况(disease settings)中显示用于调节包括增殖、应激反应、以及蛋白质翻译的多个路径(德·维托(De Vito)等人,(2011)Let-7a是尤因氏肉瘤发展中涉及的直接EWS-FLI-1靶标(Let-7a is direct EWS-FLI-1 targetimplicated in Ewing’s Sarcoma development.),PLoS ONE 6(8):1-11;辛普森等人,(2007)微小RNA Let-7a下调MYC并且使MYC诱导的伯基特氏淋巴瘤细胞的生长恢复原状,癌症研究67(20):9762-9770;约翰逊(Johnson)等人,(2005)RAS由let-7微小RNA家族调节(RAS is regulated by the let-7 microRNA family.),细胞(Cell)120:635-647;马托内(Mathonnet)等人,(2007)通过靶向帽结合复合物eIF4F进行微小RNA体外抑制翻译起始(MicroRNA inhibition of translation initiation in vitro by targeting the cap-binding complex eIF4F),科学(Science)317(5845):1764-7)。
由于先前并未检查出CHO细胞中的miR-let-7a的特异性作用,我们选择了涉及可能与生产培养物特异性相关的路径的一组潜在靶标。在这组miR-let-7a靶标内有三种类别的对于这种miR对CHO细胞生产率的机制而言可能很重要的靶标:(1)先前示出通过mRNA降解调节的mRNA,包括HMGA2、MYC、NF2、NIRF、RAB40C、PRDM1、以及整联蛋白-b3;(2)示出由miR-let-7a翻译抑制调节的mRNA,如RAS、IGF、以及EIF2A;以及(3)根据生物信息预测是miR-let-7a靶标的mRNA,如EIF4A.(穆勒(2008)作为用于使CHO细胞工厂工程化的靶标的微小RNA,生物技术趋势26(7):359-365;德·维托等人,(2011)Let-7a是尤因氏肉瘤发展中涉及的直接EWS-FLI-1靶标,PLoS ONE 6(8):1-11;辛普森等人,(2007)微小RNA Let-7a下调MYC并且使MYC诱导的伯基特氏淋巴瘤细胞的生长恢复原状,癌症研究67(20):9762-9770;孟(Meng)等人,(2007)微小RNA let-7a调节人恶性胆管上皮细胞中的白细胞介素-6-依赖性STAT-3存活信号(The MicroRNA let-7a modulates interleukin-6-dependent STAT-3survival signaling in malignant human cholangiocytes.),生物化学杂志(Journalof Biological Chemistry)282(11):8256-8264;王(Wang)等人,(2012)在结直肠癌中频繁上调NIRF并且它的致癌性可以由let-7a微小RNA压制(NIRF is frequently upregulatedin colorectal cancer and its oncogenicity can be suppressed by let-7amicroRNA.),癌症通讯社(Cancer Letters)314:223-231;杨(Yang)等人,(2011)let-7a在胃癌中的低水平表达以及它通过靶向RAB40C涉及肿瘤发生(Low-level expression oflet-7a in gastric cancer and its involvement in tumorigenesis by targetingRAB40C.),癌发生(Carcinogenesis)32(5):713-722;林(Lin)等人,(2011)小结树突细胞诱导的微小RNA介导的PRDM1的上调以及非霍奇金氏B细胞淋巴瘤中的BCL-6的下调(Follicular dendritic cell-induced microRNA-mediated upregulation of PRDM1and downregulation of BCL-6 in non-Hodgkin’s B-cell lymphomas.),白血病(Leukemia)25(1):145-152;穆勒等人,(2008)作为用于使CHO细胞工厂工程化的靶标的微小RNA,生物技术趋势26(7):359-365;约翰逊等人,(2007)let-7微小RNA抑制人细胞中的细胞增殖路径(The let-7 microRNA represses cell proliferation pathways in humancells.),癌症研究67:7713-7722;陆(Lu)等人,(2011)上皮卵巢癌中let-7a-3的超甲基化与低胰岛素样生长因子-II表达和有利预后相关联(Hypermethylation of let-7a-3 inepithelial ovarian cancer is associated with low insulin-like growth factor-II expression and favorable prognosis.),癌症研究67(21):10117-10122;以及马托内等人,(2007)通过靶向帽结合复合物eIF4F进行微小RNA体外抑制翻译起始,科学317(5845):1764-7)。
结果表明两种不同的mAb产生CHO细胞系中的miR-let-7a的抑制导致包括HMGA2、MYC、NF2、NIRF、RAB40C以及EIF4A的多个miR-let-7a靶标的mRNA水平的提高(图8)。其他基因如PRDM1、整联蛋白-B3、IGF、RAS以及EIF2A在miR-let-7a的抑制之后并未展现出改变的mRNA表达水平(数据未示出)。在先前的操作中,RAS已示出翻译上被抑制而非通过mRNA降解被抑制;因此,我们在miR-let-7a的抑制之后测量RAS蛋白表达并且发现水平提高(图9)。因mAb产生CHO细胞系中源自miR-let-7a抑制的mRNA或蛋白质改变而受影响的关键路径包括增殖、细胞凋亡、应激抗性、细胞代谢、以及翻译和/或分泌机制的调节(穆勒等人,(2008)作为用于使CHO细胞工厂工程化的靶标的微小RNA,生物技术趋势26(7):359-365;巴伦等人,(2011)通过miR-7的过表达来使CHO细胞生长和重组多肽生产工程化,生物技术杂志151(2):204-11;德·维托等人,(2011)Let-7a是尤因氏肉瘤发展中涉及的直接EWS-FLI-1靶标,PLoS ONE 6(8):1-11;辛普森等人,(2007)微小RNA Let-7a下调MYC并且使MYC诱导的伯基特氏淋巴瘤细胞的生长恢复原状,癌症研究67(20):9762-9770;孟等人,(2007)微小RNAlet-7a调节人恶性胆管上皮细胞中的白细胞介素-6-依赖性STAT-3存活信号,生物化学杂志282(11):8256-8264;王等人,(2012)在结直肠癌中频繁上调NIRF并且它的致癌性可以由let-7a微小RNA压制,癌症通讯社314:223-231;杨等人,(2011)let-7a在胃癌中的低水平表达以及它通过靶向RAB40C涉及肿瘤发生,癌发生32(5):713-722)。图10中总结了这些路径以及miR-let-7a的靶标在介导这些路径中的潜在作用。
我们的结果显示CHO细胞中miR-let-7a的抑制导致先前与细胞周期控制/增殖和细胞凋亡、应激反应、细胞代谢、以及蛋白质转录/翻译相关联的多个基因/蛋白质的变化。具体而言,我们的结果表明miR-let-7a改变RAS、MYC、NF2、RAB40C、NIRF以及HMGA2,它们已示出在CHO之外的系统中调节细胞增殖和细胞凋亡(图10)。除了细胞增殖和细胞凋亡之外,MYC和RAS还可以影响适应应激和克服代谢缺陷的能力,这两者对蛋白质的恰当加工和转录因子的调节而言都是很重要的(图10)。eIF4a也由miR-let-7a调节,eIF4a在调节对具有高蛋白质合成速率的细胞而言必要的翻译起始中发挥重要作用。
C.结论
生产细胞培养物中主动使用的多个mAb产生CHO细胞系中的miR-let-7a的抑制通过在对重组多肽生产而言很重要的路径中调节多个mRNA和蛋白靶标来产生提高的比生产率和有利的生长特征。总而言之,这项研究的结果表明调节一个或多个微小RNA可以是将生产能力提高超过它们的当前限制的有效工具。
表2.慢病毒载体转导的细胞系中的miRNA表达的PCR证实。miR修饰的细胞系中相对于亲本细胞系中miR或抗miR表达的水平通过TaqMan或QuantiMir RT PCR来评价。
| miRNA | 过表达倍数 |
| 亲本 | 1 |
| 抗miR-let-7a | 1329 |
| miR-10a | 272 |
| 抗miR-10a | 无可用引物 |
| 抗miR-16 | 1304 |
| miR-21 | 18 |
| 抗miR-21 | 683 |
| 抗miR-101 | 无可用引物 |
| 抗miR-143 | 255 |
| 抗miR-145 | 65 |
表3.所有miR修饰的Ab产生CHO细胞系中的相对VCD。示出了与每个miR修饰的或对照细胞系的基线(第0天)值相比较的三次重复VCD值的平均值±SD。
表4.所有miR修饰的Ab产生CHO细胞系中的相对滴度。示出了与每个miR修饰的或对照细胞系的基线(第2天)值相比较的三次重复滴度值的平均值±SD。
Claims (7)
1.在中国仓鼠卵巢(CHO)细胞培养物中产生重组多肽的一种方法,该方法包括:
(a)培养具有降低的miRNA-let-7a活性的CHO细胞以产生该重组多肽;并且
(b)回收多肽;
其中该CHO细胞培养物与不具有降低的miRNA-let-7a活性的对照细胞培养物相比较时在峰值活细胞密度(VCD)下确定的最大生产率增加至少25%,其中细胞培养物中的CHO细胞具有提高的RAS和MYC;
其中该miRNA-let-7a活性是被微小RNA抑制剂降低,该微小RNA抑制剂是miRNA-let-7a的反义寡核苷酸抑制剂,
其中该重组多肽是抗体或它的结合片段。
2.如权利要求1所述的方法,其中该寡核苷酸抑制剂被化学修饰来改进核酸酶抗性,通过RISC提高对miRNA引导的裂解的抗性和/或提高结合亲和力。
3.如权利要求1-2任一所述的方法,其中用编码该miRNA-let-7a的反义寡核苷酸抑制剂的表达载体转染CHO细胞。
4.如权利要求1所述的方法,其中用miRNA-let-7a的反义寡核苷酸抑制剂稳定或瞬时转染CHO细胞。
5.如权利要求1所述的方法,其中该抗体或它的结合片段选自多特异性抗体、完全的人抗体、人源化抗体、骆驼化抗体、嵌合抗体、CDR移植抗体、单链Fvs(scFv)、二硫键连接的Fvs(sdFv)、Fab片段、F(ab')片段、以及抗独特型(抗Id)抗体。
6.如权利要求1所述的方法,其中该细胞培养物具有与不具有降低的miRNA-let-7a活性的对照细胞培养物相比较处在1%与30%之间的相对活细胞密度。
7.被配置成根据权利要求1所述的方法表达重组多肽的一个CHO细胞系,其中:
该CHO细胞系具有降低的miRNA-let-7a活性;
该CHO细胞的培养物与不具有降低的miRNA-let-7a活性的对照细胞培养物相比较在峰值活细胞密度(VCD)下确定的最大生产率增加至少25%;
所述CHO细胞在细胞培养物中具有提高的RAS和MYC;且
该miRNA-let-7a活性是被微小RNA抑制剂降低,该微小RNA抑制剂是miRNA-let-7a的反义寡核苷酸抑制剂。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201361782180P | 2013-03-14 | 2013-03-14 | |
| US61/782,180 | 2013-03-14 | ||
| PCT/US2014/024512 WO2014159633A1 (en) | 2013-03-14 | 2014-03-12 | Recombinant polypeptide production |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN105229159A CN105229159A (zh) | 2016-01-06 |
| CN105229159B true CN105229159B (zh) | 2021-07-06 |
Family
ID=51625216
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201480013725.2A Active CN105229159B (zh) | 2013-03-14 | 2014-03-12 | 重组多肽生产 |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US10006026B2 (zh) |
| EP (1) | EP2971035B1 (zh) |
| JP (1) | JP6445516B2 (zh) |
| CN (1) | CN105229159B (zh) |
| AU (1) | AU2014244588B2 (zh) |
| CA (1) | CA2902581C (zh) |
| ES (1) | ES2743506T3 (zh) |
| HK (2) | HK1218562A1 (zh) |
| WO (1) | WO2014159633A1 (zh) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AR095196A1 (es) * | 2013-03-15 | 2015-09-30 | Regeneron Pharma | Medio de cultivo celular libre de suero |
| US20170369556A1 (en) * | 2014-12-23 | 2017-12-28 | Ralph A. Tripp | RECOMBINANT CELLS COMPRISING miRNA MIMICS |
| US10383935B2 (en) * | 2015-09-23 | 2019-08-20 | Regents Of The University Of Minnesota | Methods of making and using live attenuated viruses |
| EP3692153A1 (en) * | 2017-10-02 | 2020-08-12 | Astrazeneca AB | Cell lines and methods for increased protein production |
| WO2019227259A1 (zh) * | 2018-05-26 | 2019-12-05 | 深圳市博奥康生物科技有限公司 | 一种基于哺乳动物病毒的介导miRNA过表达方法 |
| WO2019227253A1 (zh) * | 2018-05-26 | 2019-12-05 | 深圳市博奥康生物科技有限公司 | miRNA-21过表达载体的构建及其应用 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN101541972A (zh) * | 2006-08-04 | 2009-09-23 | 都柏林城市大学 | 生产重组生物产品的方法 |
| US20100226884A1 (en) * | 2009-01-20 | 2010-09-09 | Immunomedics, Inc. | Novel Class of Monospecific and Bispecific Humanized Antibodies that Target the Insulin-like Growth Factor Type I Receptor (IGF-1R) |
| WO2010129919A1 (en) * | 2009-05-08 | 2010-11-11 | Research Development Foundation | Mirna expression in allergic disease |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU5898599A (en) | 1998-08-19 | 2000-03-14 | Board Of Trustees Of The Leland Stanford Junior University | Methods and compositions for genomic modification |
| CN101065479A (zh) * | 2004-10-15 | 2007-10-31 | 蒙奈尔化学感觉中心 | 培养哺乳动物味细胞的方法 |
| EP2054529B1 (en) * | 2006-08-25 | 2014-03-26 | Duke University | Methods for in vivo identification of endogenous mrna targets of micrornas |
| EP2291520A4 (en) | 2008-05-19 | 2011-11-30 | Agency Science Tech & Res | NUCLEIC ACID MOLECULE AND METHOD FOR TARGETING GENE EXPRESSION IN GLIOMES |
| US8557786B2 (en) * | 2008-08-19 | 2013-10-15 | Maine Institute of Human Genetics and Health | Micro RNA (MiRNA) and neurofibromatosis type 1: a role in diagnosis and therapy |
| US20110189137A1 (en) * | 2009-11-11 | 2011-08-04 | Sanford-Burnham Medical Research Institute | Method for generation and regulation of ips cells and compositions thereof |
| WO2012092485A1 (en) * | 2010-12-31 | 2012-07-05 | Anthrogenesis Corporation | Enhancement of placental stem cell potency using modulatory rna molecules |
-
2014
- 2014-03-12 ES ES14776495T patent/ES2743506T3/es active Active
- 2014-03-12 EP EP14776495.5A patent/EP2971035B1/en active Active
- 2014-03-12 US US14/775,233 patent/US10006026B2/en active Active
- 2014-03-12 AU AU2014244588A patent/AU2014244588B2/en active Active
- 2014-03-12 CA CA2902581A patent/CA2902581C/en active Active
- 2014-03-12 CN CN201480013725.2A patent/CN105229159B/zh active Active
- 2014-03-12 JP JP2016501560A patent/JP6445516B2/ja active Active
- 2014-03-12 WO PCT/US2014/024512 patent/WO2014159633A1/en active Application Filing
-
2016
- 2016-06-07 HK HK16106504.8A patent/HK1218562A1/zh unknown
- 2016-07-19 HK HK16108512.4A patent/HK1220492A1/zh unknown
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN101541972A (zh) * | 2006-08-04 | 2009-09-23 | 都柏林城市大学 | 生产重组生物产品的方法 |
| US20100226884A1 (en) * | 2009-01-20 | 2010-09-09 | Immunomedics, Inc. | Novel Class of Monospecific and Bispecific Humanized Antibodies that Target the Insulin-like Growth Factor Type I Receptor (IGF-1R) |
| WO2010129919A1 (en) * | 2009-05-08 | 2010-11-11 | Research Development Foundation | Mirna expression in allergic disease |
Non-Patent Citations (5)
| Title |
|---|
| let-7在肿瘤中的研究进展;朱秀明 等;《国际肿瘤学杂志》;20110228;第38卷(第2期);第90页右栏第1段 * |
| MicroRNAs as targets for engineering of CHO cell factories;Müller D 等;《Trends Biotechnol》;20080528;第26卷(第7期);第359页右栏,表1 * |
| Specificity and functionality of microRNA inhibitors;Barbara Robertson 等;《Silence》;20100401;第1卷;第2页左栏,图1 * |
| Stable inhibition of mmu-miR-466h-5p improves apoptosis resistance and protein production in CHO cells;Druz A 等;《Metab Eng》;20130129;第16卷;摘要,第3页第3段、第5页第2节、第6页第5节,图2、6 * |
| The let-7 family of microRNAs;Roush S 等;《Trends Cell Biol》;20080904;第18卷(第10期);第505-516页 * |
Also Published As
| Publication number | Publication date |
|---|---|
| ES2743506T3 (es) | 2020-02-19 |
| WO2014159633A1 (en) | 2014-10-02 |
| AU2014244588A1 (en) | 2015-10-01 |
| JP2016511005A (ja) | 2016-04-14 |
| HK1220492A1 (zh) | 2017-05-05 |
| CA2902581C (en) | 2023-08-08 |
| US10006026B2 (en) | 2018-06-26 |
| EP2971035A1 (en) | 2016-01-20 |
| CN105229159A (zh) | 2016-01-06 |
| EP2971035B1 (en) | 2019-06-12 |
| US20160024502A1 (en) | 2016-01-28 |
| AU2014244588B2 (en) | 2017-11-30 |
| EP2971035A4 (en) | 2016-11-09 |
| HK1218562A1 (zh) | 2017-02-24 |
| CA2902581A1 (en) | 2014-10-02 |
| JP6445516B2 (ja) | 2018-12-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN105229159B (zh) | 重组多肽生产 | |
| EP2937417B1 (en) | MiRNAs enhancing cell productivity | |
| US20220064690A1 (en) | CELL ENGINEERING USING RNAs | |
| EP2430159A1 (en) | Improved cell lines having reduced expression of nocr and use thereof | |
| KR20220097910A (ko) | 세포 선택 방법 | |
| EP4092125A1 (en) | Method for producing a biomolecule by a cell | |
| EP2396404A1 (en) | Rnai based selection system | |
| CN105849265B (zh) | 用于产生供生产重组蛋白的哺乳动物生产细胞的物品和方法 | |
| KR101809594B1 (ko) | 목적 단백질 생산을 위한 발현 벡터 및 이를 이용한 목적 단백질의 과발현 방법 | |
| US20220228110A1 (en) | Expression vectors, methods for screening host cells expressing target proteins, and methods for establishing cell lines stably expressing foreign recombinant genes | |
| WO2023223219A1 (en) | IMPROVED PROTEIN PRODUCTION USING miRNA TECHNOLOGY | |
| WO2024023746A1 (en) | Improved production of cd39 variants | |
| WO2024023580A2 (en) | Stabilizing rnas with mirna-binding motifs | |
| Kelly | Enhancing CHO cell productivity through the stable depletion of microRNA-23 | |
| Greenlees et al. | Inhibition of microRNA-let-7a Increases the Specific Productivity of Antibody-Producing CHO Cell Lines | |
| EP2430165A1 (en) | Combinatorial engineering | |
| WO2014204405A1 (en) | Method for modulating recombinant protein production |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| REG | Reference to a national code |
Ref country code: HK Ref legal event code: DE Ref document number: 1218562 Country of ref document: HK |
|
| GR01 | Patent grant | ||
| GR01 | Patent grant |