CN102718714A - 蒽桥联的四齿咪唑盐及其制备方法与应用 - Google Patents
蒽桥联的四齿咪唑盐及其制备方法与应用 Download PDFInfo
- Publication number
- CN102718714A CN102718714A CN2012102105422A CN201210210542A CN102718714A CN 102718714 A CN102718714 A CN 102718714A CN 2012102105422 A CN2012102105422 A CN 2012102105422A CN 201210210542 A CN201210210542 A CN 201210210542A CN 102718714 A CN102718714 A CN 102718714A
- Authority
- CN
- China
- Prior art keywords
- anthracene
- reaction
- imidazole
- amine methyl
- ethyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Abstract
本发明公开了蒽桥联的四齿咪唑盐的制备方法,并使用合成的
9,10-
二
[
双
(N-1-
取代基
-3-
咪唑乙基
)
胺甲基
]
蒽
盐
与
PdCl
2
原位生成卡宾钯配合物
做催化剂,用于催化多种类型的碳
-
碳键偶联反应。其中制备蒽桥联的四齿咪唑盐的方法,首先用蒽和多聚甲醛反应使蒽的
9,10
位上引入氯甲基,再与二乙醇胺取反应,接着再用
SOCl
2
进行
氯代,得到黄绿色中间物
9,10-
二
[
双
(2-
氯乙基
)
胺甲基
]
蒽
。
9,10-
二
[
双
(2-
氯乙基乙基
)
胺甲基
]
蒽
和
1-
取代基咪唑反应,生成
9,10-
二
[
双
(N-1-
取代基
-3-
咪唑乙基
)
胺甲基
]
蒽氯化物
,继续通过六氟磷酸铵进行阴离子交换反应得到
9,10-
二
[
双
(N-1-
取代基
-3-
咪唑乙基
)
胺甲基
]
蒽
六氟磷酸盐。本发明制备的蒽桥联的四齿咪唑盐主要应用于原位生成催化剂、催化多种类型碳
-
碳键的形成反应。
Description
关于资助研究或开发的声明
本发明是在国家自然科学基金(基金号为21172172)和天津市自然科学基金(基金号为11JCZDJC22000)的资助下进行的。
技术领域
本发明属于有机合成和金属有机化学技术领域,涉及蒽桥联的四齿咪唑盐的合成。更具体的说是9,10-二[双(N-1-取代基-3-咪唑乙基)胺甲基]蒽盐的制备方法以及其在催化领域中的应用。
背景技术
近年来,N-杂环卡宾以其独特的性质引起了化学家们极大的兴趣。自1991年Arduengo第一次分离得到了稳定的游离N-杂环卡宾以后,随着对N-杂环卡宾及其金属络合物研究的不断深入,人们对它的认识也渐渐开阔和系统化。
经过理论化学家和金属有机化学家对N-杂环卡宾性质的研究,发现其虽然类似于富电子的膦配体,但它具有更高的热稳定性,耐水性,空气稳定性,较低的毒性,使均相反应固相化等优点。在一些反应中,N-杂环卡宾的金属配合物比膦配体的金属配合物有更高的催化活性,如高效催化烯烃的复分解反应,烯烃的氢硅化反应,呋喃的合成等,尤其是在与过渡金属形成的配合物催化偶联反应中得到了极大的发展。N-杂环卡宾不仅仅是作为金属有机化合物的前体用于催化反应,还能用作反应底物参与到有机反应中,如亲核Wanzlick型N-杂环卡宾参与的反应,对二氧化碳进行固定而发生的羧化反应以及强亲核N-杂环卡宾作为底物的多组分反应等。因此,N-杂环卡宾以其独特的性能为人们寻找新的性能良好的催化剂以及探索一些新的化学反应开辟了新的视野。随着研究的深入和研究范围的拓展,N-杂环卡宾会在越来越多的领域中显现出其更广泛的应用价值。
发明内容
本发明的目的在于提供蒽桥联的四齿咪唑盐,特别是9,10-二[双(N-1-取代基-3-咪唑乙基)胺甲基]蒽盐。
本发明也涉及制备此类蒽桥联四齿咪唑盐的方法。
本发明涉及此类蒽桥联四齿咪唑盐的氢谱和碳谱标定。
本发明更进一步涉及了通过9,10-二[双(N-1-取代基-3-咪唑乙基)胺甲基]蒽盐与PdCl
2
原位生成卡宾钯配合物做为催化剂应用于催化领域。
为完成上述各项发明目的,本发明提供的技术方案如下:
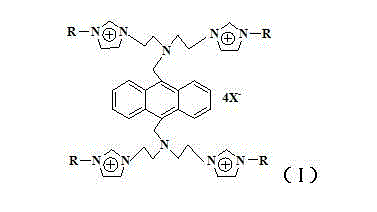
蒽桥联四齿咪唑盐具有如(Ⅰ)所示的结构式:
其中R是独立地或结合起来为氢或C
1
—C
6
有机基,包括烷基、支链烷基、环烷基、链烯基、环烯基、炔基、芳基、芳基烷基、含氮杂环或烷氧基; X为卤素或六氟磷酸根。
其中烷基指的是-C
1
—C
6
烷基;甲基,乙基,丙基,丁基,戊基,己基;
支链烷基指的是C
3
—C
6
支链烷基,例如:异丙基,仲丁基,叔丁基;
环烷基指的是C
3
—C
6
环烷基,例如:环丙基,环丁基,环戊基,环己基;
链烯基指的是:烯丙基,丁烯基等;
环烯基指的是:环戊烯,环己烯等;
炔基指的是:炔丙基,炔丁基等;
芳基指的是:苯基,萘基,蒽基等;
芳基烷基指的是:苄基,萘甲基,蒽甲基等;
含氮杂环或烷氧基指的是:吡啶,咪唑,苯并咪唑,乙氧基,丙氧基等。
本发明优选典型的化合物为:
9,10-二[双(N-1-乙基-3-咪唑乙基)胺甲基]蒽六氟磷酸盐;
9,10-二[双(N-1正丙基-3-咪唑乙基)胺甲基]蒽六氟磷酸盐;
9,10-二[双(N-1-正丁基-3-咪唑乙基)胺甲基]蒽六氟磷酸盐;
9,10-二[双(N-1-仲丁基-3-咪唑乙基)胺甲基]蒽六氟磷酸盐;
9,10-二[双(N-1-苄基-3-咪唑乙基)胺甲基]蒽六氟磷酸盐;
9,10-二[双(N-1-吡啶甲基-3-咪唑乙基)胺甲基]蒽六氟磷酸盐。
本发明进一步公开了蒽桥联四齿咪唑盐的方法,其特征在于按如下的步骤进行:
(1) 首先用蒽和多聚甲醛反应使蒽的9,10位上引入氯甲基,得到9,10-二[双(2-氯甲基)]蒽;其中蒽和多聚甲醛反应的摩尔比为:40-41:24;
(2)9,10-二[双(2-氯甲基)]蒽与二乙醇胺反应,得到9,10-二[双(2-羟乙基)胺甲基]蒽;接着再用SOCl
2
进行氯代,得到黄绿色中间物9,10-二[双(2-氯乙基)胺甲基]蒽;其中9,10-二[双(2-氯甲基)]蒽:二乙醇胺的摩尔比为:18:108-110;9,10-二[双(2-羟乙基)胺甲基]蒽与SOCl
2
的摩尔比为9.7:78-80;
(3)9,10-二[双(2-氯乙基)胺甲基]蒽和1-取代基咪唑反应,生成9,10-二[双(N-1-取代基-3-咪唑乙基)胺甲基]蒽氯化物,继续通过六氟磷酸铵进行阴离子交换反应得到9,10-二[双(N-1-取代基-3-咪唑乙基)胺甲基]蒽六氟磷酸盐;其中9,10-二[双(2-氯乙基)胺甲基]蒽:1-取代基咪唑的摩尔比为3:16-18;9,10-二[双(N-1-乙基-3-咪唑乙基)胺甲基]蒽氯化物:六氟磷酸铵的摩尔比为2.5:10-12。
本发明优选蒽桥联四齿咪唑盐的制备方法,以9,10-二[双(N-1-取代基-3-咪唑乙基)胺甲基]蒽盐为例,其特征在于:
(1) 首先用蒽和多聚甲醛反应使蒽的9,10位上引入氯甲基,再与二乙醇胺取反应,接着再用SOCl
2
进行氯代,得到黄绿色中间物9,10-二[双(2-氯乙基)胺甲基]蒽。
二[双(2-氯乙基)胺甲基]蒽和1-取代基咪唑反应,生成9,10-二[双(N-1-取代基-3-咪唑乙基)胺甲基]蒽氯化物,继续通过六氟磷酸铵进行阴离子交换反应得到9,10-二[双(N-1-取代基-3-咪唑乙基)胺甲基]蒽六氟磷酸盐。
本发明所述的1-取代基苯并咪唑为乙基苯并咪唑、正丁基苯并咪唑、正丙基苯并咪唑、仲丁基苯并咪唑、苄基苯并咪唑或1-吡啶甲基苯并咪唑;
本发明进一步工开了蒽桥联四齿咪唑盐在制备作为催化剂在有机反应中的应用。其中所述的制备作为催化剂在有机反应中的应用,指的是:
原位生成四卡宾钯配合物在催化溴苯和苯乙烯反应中的应用;
原位生成四卡宾钯配合物在催化卤代芳烃和苯乙烯反应中的应用;
原位生成四卡宾钯配合物在催化对溴甲苯和苯硼酸反应中的应用。
其中所述的原位生成指的是:催化剂生成后不用分离直接用于催化反应。
原位生成四卡宾钯配合物在催化卤代芳烃和苯硼酸反应中的应用,典型的为原位生成卡宾钯配合物催化偶联反应的方法,以催化Heck反应为例:
以二氧六环为溶剂,PdCl
2
, 9,10-二[双(N-1-取代基-3-咪唑乙基)胺甲基]蒽盐, K
2
CO
3
,在氮气保护下,30C搅拌1h。然后依次加入芳基卤化物, 苯乙烯和TBAB,在空气条件下,置于110C油浴中反应。用点板跟踪检测反应,硅胶柱层析得产物。
本发明中公开的蒽桥联四齿咪唑盐是并列的关系,无优先主次之分。
本发明进一步公开了蒽桥联四齿咪唑盐在原位生成卡宾钯配合物在催化中的应用。主要是9,10-二[双(N-1-取代基-3-咪唑乙基)胺甲基]蒽盐应用于催化领域。
实验证明:9,10-二[双(N-1-取代基-3-咪唑乙基)胺甲基]蒽盐与PdCl
2
原位生成卡宾钯配合物在一定的条件下对Heck,Suzuki-Miyaura偶联反应有催化性能。如应用实例1和应用实例2在表1、表2、表3、表4中的应用。
具体实施方式:
以下结合较佳实施例,对本发明做进一步的描述,特别加以说明的是,制备本发明化合物的起始物质蒽、多聚甲醛、二乙醇胺、氯化亚砜等均可以从市场上买到或容易地通过已知的方法制得。
制备本发明化合物所用到的试剂全部来源于天津市科威化工有限公司,级别为分析纯。
另外需要加以说明的是:所有的实验操作运用Schlenk技术,溶剂经过标准流程纯化。所有用于合成和分析的试剂都是分析纯,并没有经过进一步的处理。熔点通过Boetius区截机测定。
1
H NMR 和
13
C NMR谱通过汞变量Vx400分光光度计记录,测量区间分别为:400 MHz 和100 MHz。化学位移,δ,参考国际标准的TMS测定。
实施例1
蒽 (7.129 g, 40.4 mmol)和多聚甲醛(7.201 g, 24.0 mmol)加入二氧六环(70 mL)和盐酸(12 mL, 37% (w/w))的混合液中,80C下搅拌6h。抽滤,水洗得到黄色的9,10-二[双(2-氯甲基)]蒽。产率:9.250 g (83%)。熔点:212-214C。(参考文献:M. J. Cloninger, H. W. Whitlock, J. Org. Chem. 1998, 63, 6153-6159)。
乙腈(100 mL)中加入9,10-二[双(2-氯甲基)]蒽(4.950 g, 18.0 mmol),二乙醇胺(11.355 g, 108.0 mmol),K
2
CO
3
(24.840 g, 180.0 mmol),KI (0.896 g, 5.4 mmol),加热回流36 h。抽滤,旋去溶剂,将得到的油用水洗得到黄色9,10-二[双(2-羟乙基)胺甲基]蒽。产率:5.241 g (71%)。熔点:178-180 C 。
将9,10-二[双(2-羟乙基)胺甲基]蒽(3.999 g, 9.7 mmol)溶于30 mL CHCl
3
中,并将其滴加到溶有二氯亚砜(9.234 g, 78.0 mmol)的50 mL CHCl
3
中。混合溶液在60 C下搅拌72h。抽滤得到的粗产物用NaOH水溶液洗涤,CHCl
3
萃取,分液,干燥抽滤,旋干得到黄色的9,10-二[双(2-氯乙基)胺甲基]蒽。产率:3.100 g (77%)。熔点:140-142 C 。
二[双(2-氯乙基)胺甲基]蒽(1.277 g, 3.0 mmol)和1-乙基咪唑(1.560 g, 16.0 mmol)在丙酮中,50C下反应72h,生成黄色粘稠状固体,除去溶液,用丙酮洗两次,得到黄色粘稠状的9,10-二[双(N-1-乙基-3-咪唑乙基)胺甲基]蒽氯化物。产率:2.100 g (85%)。
二[双(N-1-乙基-3-咪唑乙基)胺甲基]蒽氯化物(1.995 g, 2.5 mmol)溶解在30 mL 甲醇,加入30 mL NH
4
PF
6
(1.630 g, 10.0 mmol)的甲醇溶液,室温搅拌72 h。抽滤得到9,10-二[双(N-1-乙基-3-咪唑乙基)胺甲基]蒽六氟磷酸盐淡黄色固体。产率:2.800 g (91%)。M.p.: 162-164 C 。
1
H NMR (400 MH
Z,
DMSO-d
6
): δ 1.31 (t, J = 7.2, 12H, CH
3
), 3.07 (t, J = 5.4, 8H, CH
2
), 4.02 (q, J = 7.2, 8H, CH
2
), 4.34 (t, J = 5.4, 8H, CH
2
), 4.65 (s, 4H, CH
2
), 7.33 (s, 4H, imiH), 7.47 (s, 4H, imiH), 7.51 (q, J = 3.2, 4H, AnH), 8.24 (q, J = 3.3
,
4H, AnH), 8.90 (s, 2H, 2-imiH).
13
C NMR (100 MH
Z,
DMSO-d
6
): δ 14.76 (CH
3
), 44.14 (CH
2
), 46.02 (CH
2
), 49.32 (CH
2
), 51.46 (CH
2
), 121.43 (imiC), 121.95 (imiC), 124.91 (AnC), 125.45 (AnC), 129.67 (AnC), 130.06 (AnC), 135.06 (2-imiC), 141.25 (2-bimiC) (imi = imidazole) (An = Anthracene).
按照上述的实验方法,分别用正丁基苯并咪唑、正丙基苯并咪唑、仲丁基苯并咪唑、苄基苯并咪唑或1-吡啶甲基苯并咪唑代替1-乙基咪唑可以制备相应的9,10-二[双(N-1-取代基-3-咪唑乙基)胺甲基]蒽六氟磷酸盐。
其实验流程如下:
应用实例1
9,10-二[双(N-1-取代基-3-咪唑乙基)胺甲基]蒽盐与PdCl
2
原位生成四卡宾钯配合物催化Heck偶联反应的过程。实施例2中制备的9,10-二[双(N-1-取代基-3-咪唑乙基)胺甲基]蒽盐(0.25 mol %),PdCl
2
(0.5 mol %),K
2
CO
3
(1.0 mmol)和二氧六环(5 mL)加入到25 mL的圆底烧瓶中, 在氮气保护下,室温下搅拌2h。然后依次加入芳基卤化物(0.5 mmol), 苯乙烯(0.75 mmol)和TBAB (10 mol %),在空气条件下,置于110C油浴中反应。用点板跟踪检测反应,至底物与产物的比例不变为止。旋去溶剂,加入水(5 mL),用乙醚(8 mL × 3)萃取,分液,MgSO
4
干燥,抽滤,旋干,过硅胶短柱(400mesh)除去原料,二氯甲烷/正己烷为洗脱剂,硅胶柱层析得产物。通过核磁确定产物。
表1为实施例1中得到的9,10-二[双(N-1-取代基-3-咪唑乙基)胺甲基]蒽盐与PdCl
2
原位生成四卡宾钯配合物在催化溴苯和苯乙烯反应中的反应实例
[a]
。
反应条件:对溴甲苯0.50 mmol,苯乙烯0.75 mmol,碱1.0 mol, 实施例1中制备的蒽桥联的氮杂环四卡宾盐0.25 mol%,PdCl
2
0.5mol%,TBAB 10% mol,溶剂5 mL, 110C。
反应过程中要点板跟踪。
实施例1中制备的蒽桥联的氮杂环四卡宾盐0.15 mol %,PdCl
2
0.3 mol%,其他反应条件与[a]同。
没有加入实施例1中制备的蒽桥联的氮杂环四卡宾盐,其他反应条件与[a]同。
表2为实施例1中得到的9,10-二[双(N-1-取代基-3-咪唑乙基)胺甲基]蒽盐与PdCl
2
原位生成四卡宾钯配合物在催化卤代芳烃和苯乙烯反应中的反应实例
[a]
反应条件:卤代芳烃0.50 mmol,苯乙烯0.75 mmol,碱1.0 mol, 实施例1中制备的蒽桥联的氮杂环四卡宾盐0.25 mol%,PdCl
2
0.5mol%,TBAB 10% mol,溶剂5 mL, 110C。
反应过程中要点板跟踪。
应用实例2
9,10-二[双(N-1-取代基-3-咪唑乙基)胺甲基]蒽盐与PdCl
2
原位生成四卡宾钯配合物催化Suzuki-Miyaura偶联反应的过程: PdCl
2
(0.4 mol %), 9,10-二[双(N-1-取代基-3-咪唑乙基)胺甲基]蒽盐(0.1 mol %), K
2
CO
3
(1.0 mmol)和甲苯(5 mL) 或水(5 mL)加入到 25 mL 的圆底烧瓶中, 在氮气保护下,室温下搅拌 2 h。然后依次加入芳基卤化物 (0.5 mmol), 苯硼酸(0.6 mmol) 和 PEG-400 (0.1 mL) 或TBAB (10 mol %),在空气条件下,置于60C油浴中反应。用点板和气相色谱仪跟踪检测反应,至底物与产物的比例不变为止。旋去溶剂,加入水(5 mL),用乙醚(8 mL × 3)萃取,分液,MgSO
4
干燥,抽滤,旋干,过硅胶短柱(400mesh)除去原料,二氯甲烷/正己烷为洗脱剂,硅胶柱层析得产物。通过核磁确定产物。
表3为实施例1中得到的9,10-二[双(N-1-取代基-3-咪唑乙基)胺甲基]蒽盐与PdCl
2
原位生成四卡宾钯配合物在催化对溴甲苯和苯硼酸反应中的实例
[a]
。
反应条件:对溴甲苯0.50 mmol,苯硼酸0.60 mmol,碱1.0 mmol, 实施例2中制备的9,10-二[双(N-1-取代基-3-咪唑乙基)胺甲基]蒽盐0.1 mol %,PdCl
2
(0.4 mol %),溶剂5 mL,60 C,柱色谱分离。
聚乙二醇-400。
不加入实施例2中制备的9,10-二[双(N-1-取代基-3-咪唑乙基)胺甲基]蒽盐,其它条件均与[a]同。
表4为实施例1中得到的9,10-二[双(N-1-取代基-3-咪唑乙基)胺甲基]蒽盐与PdCl
2
原位生成四卡宾钯配合物在催化卤代芳烃和苯硼酸反应中的实例
[a]
。
反应条件:卤代芳烃0.50 mmol,苯硼酸0.60 mmol,碱1.0 mmol, 实施例2中制备的9,10-二[双(N-1-取代基-3-咪唑乙基)胺甲基]蒽盐0.1 mol %,PdCl
2
(0.4 mol %),溶剂5 mL,60 C,聚乙二醇-400;
反应过程中要点板跟踪;
柱色谱分离产率;
气相色谱检测产率;
不添加聚乙二醇-400。
综上所述,本发明的内容并不局限在实例中,相同领域内的有识之士可以在本发明的技术指导思想之内可以轻易提出其他的实例,但这种实例都包括在本发明的范围之内。
Claims (7)
2.权利要求 1所述蒽桥联的四齿咪唑盐,其典型的化合物为:
9,10-二[双(N-1-乙基-3-咪唑乙基)胺甲基]蒽六氟磷酸盐;
9,10-二[双(N-1正丙基-3-咪唑乙基)胺甲基]蒽六氟磷酸盐;
9,10-二[双(N-1-正丁基-3-咪唑乙基)胺甲基]蒽六氟磷酸盐;
9,10-二[双(N-1-仲丁基-3-咪唑乙基)胺甲基]蒽六氟磷酸盐;
9,10-二[双(N-1-苄基-3-咪唑乙基)胺甲基]蒽六氟磷酸盐;
9,10-二[双(N-1-吡啶甲基-3-咪唑乙基)胺甲基]蒽六氟磷酸盐。
3.一种制备权利要求1所述蒽桥联四齿咪唑盐的方法,其特征在于按如下的步骤进行:
(1) 首先用蒽和多聚甲醛反应使蒽的9,10位上引入氯甲基,得到9,10-二[双(2-氯甲基)]蒽;其中蒽和多聚甲醛反应的摩尔比为:40-41:24;
(2)9,10-二[双(2-氯甲基)]蒽与二乙醇胺反应,得到9,10-二[双(2-羟乙基)胺甲基]蒽;接着再用SOCl2进行氯代,得到黄绿色中间物9,10-二[双(2-氯乙基)胺甲基]蒽;其中9,10-二[双(2-氯甲基)]蒽:二乙醇胺的摩尔比为:18:108-110;9,10-二[双(2-羟乙基)胺甲基]蒽与SOCl2的摩尔比为9.7:78-80;
(3)9,10-二[双(2-氯乙基)胺甲基]蒽和1-取代基咪唑反应,生成9,10-二[双(N-1-取代基-3-咪唑乙基)胺甲基]蒽氯化物,继续通过六氟磷酸铵进行阴离子交换反应得到9,10-二[双(N-1-取代基-3-咪唑乙基)胺甲基]蒽六氟磷酸盐;其中9,10-二[双(2-氯乙基)胺甲基]蒽:1-取代基咪唑的摩尔比为3:16-18;9,10-二[双(N-1-乙基-3-咪唑乙基)胺甲基]蒽氯化物:六氟磷酸铵的摩尔比为2.5:10-12。
4.权利要求3所述的制备方法,其中所述的1-取代基咪唑为:乙基咪唑、正丙基咪唑、正丁基咪唑、仲丁基咪唑、苄基咪唑或1-吡啶甲基咪唑。
5.权利要求 1所述蒽桥联四齿咪唑盐制备作为催化剂在有机反应中的应用。
6.权利要求5所述的应用,其中所述的制备作为催化剂在有机反应中的应用指的是:原位生成四卡宾钯配合物在催化溴苯和苯乙烯反应中的应用;原位生成四卡宾钯配合物在催化卤代芳烃和苯乙烯反应中的应用;原位生成四卡宾钯配合物在催化对溴甲苯和苯硼酸反应中的应用;原位生成四卡宾钯配合物在催化卤代芳烃和苯硼酸反应中的的应用。
7.权利要求6所述的应用,其中所述的原位生成指的是:催化剂生成后不用分离直接用于催化反应。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201210210542.2A CN102718714B (zh) | 2012-06-26 | 2012-06-26 | 蒽桥联的四齿咪唑盐及其制备方法与应用 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201210210542.2A CN102718714B (zh) | 2012-06-26 | 2012-06-26 | 蒽桥联的四齿咪唑盐及其制备方法与应用 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN102718714A true CN102718714A (zh) | 2012-10-10 |
| CN102718714B CN102718714B (zh) | 2014-09-17 |
Family
ID=46944615
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201210210542.2A Expired - Fee Related CN102718714B (zh) | 2012-06-26 | 2012-06-26 | 蒽桥联的四齿咪唑盐及其制备方法与应用 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN102718714B (zh) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN107880079A (zh) * | 2017-11-27 | 2018-04-06 | 天津师范大学 | 环状氮杂环双卡宾钯配合物及其制备方法与用途 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0431794A2 (en) * | 1989-11-21 | 1991-06-12 | Bristol-Myers Squibb Company | 3-Fluorosulfonyloxyceph-3-EM displacement process |
| US20090306414A1 (en) * | 2006-03-02 | 2009-12-10 | Yasuhiro Uozumi | Microchannel Reactor |
-
2012
- 2012-06-26 CN CN201210210542.2A patent/CN102718714B/zh not_active Expired - Fee Related
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0431794A2 (en) * | 1989-11-21 | 1991-06-12 | Bristol-Myers Squibb Company | 3-Fluorosulfonyloxyceph-3-EM displacement process |
| US20090306414A1 (en) * | 2006-03-02 | 2009-12-10 | Yasuhiro Uozumi | Microchannel Reactor |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN107880079A (zh) * | 2017-11-27 | 2018-04-06 | 天津师范大学 | 环状氮杂环双卡宾钯配合物及其制备方法与用途 |
| CN107880079B (zh) * | 2017-11-27 | 2020-05-08 | 天津师范大学 | 环状氮杂环双卡宾钯配合物及其制备方法与用途 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN102718714B (zh) | 2014-09-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Blank et al. | An efficient method for the selective Iridium‐catalyzed monoalkylation of (hetero) aromatic amines with primary alcohols | |
| Yi et al. | Enantioselective Construction of α‐Chiral Silanes by Nickel‐Catalyzed C (sp3)− C (sp3) Cross‐Coupling | |
| CN107880079B (zh) | 环状氮杂环双卡宾钯配合物及其制备方法与用途 | |
| EP2403815A1 (en) | Oxidative homo-coupling reactions of aryl boronic acids using a porous copper metal-organic framework as a highly efficient heterogeneous catalyst | |
| Cesario et al. | Topological enhancement of basicity: Molecular structure and solution study of a monoprotonated catenand | |
| Bernoud et al. | Copper-catalyzed synthesis of alkynylphosphine derivatives: unprecedented use of nucleophilic phosphorus compounds | |
| Liu et al. | A highly active catalyst system for Suzuki–Miyaura coupling of aryl chlorides | |
| CN110105305B (zh) | 过渡金属催化的c-h活化/环合合成1,2-苯并噻嗪衍生物的绿色合成方法 | |
| Huang et al. | Synthesis of Axially Chiral 1, 2, 3-Triazol-5-ylidene–Au (I) Complex and Its Application in Enantioselective [2+ 2] Cycloaddition of Alleneamides with Alkenes | |
| Martín et al. | Ni (II) Precatalysts Enable Thioetherification of (Hetero) Aryl Halides and Tosylates and Tandem C− S/C− N Couplings | |
| Maji et al. | Palladium‐Based Catalysts Supported by Unsymmetrical XYC–1 Type Pincer Ligands: C5 Arylation of Imidazoles and Synthesis of Octinoxate Utilizing the Mizoroki–Heck Reaction | |
| Pandiri et al. | Development of (quinolinyl) amido-based pincer palladium complexes: a robust and phosphine-free catalyst system for C–H arylation of benzothiazoles | |
| CN102584864B (zh) | 氮杂环卡宾金属冠醚及其在识别客体方面的应用 | |
| CN102659622B (zh) | 一种大位阻配体Pd配合物催化剂及其制备方法及应用 | |
| CN109694382A (zh) | 一种室温下制备芳基硼酸酯的方法 | |
| Kato et al. | Iron/photosensitizer hybrid system enables the synthesis of polyaryl-substituted azafluoranthenes | |
| Lin et al. | Ortho‐C–H addition of 2‐substituted pyridines with alkenes and imines enabled by mono (phosphinoamido)‐rare earth complexes | |
| CN102718714B (zh) | 蒽桥联的四齿咪唑盐及其制备方法与应用 | |
| CN102229568A (zh) | 苯基醚桥联的氮杂环卡宾金属配合物的制备与用途 | |
| CN102321104A (zh) | 烷基桥联的氮杂环双卡宾金属配合物及其制备方法与用途 | |
| Tang et al. | The first 4, 4′-imidazolium-tagged C 2-symmetric bis (oxazolines): application in the asymmetric Henry reaction | |
| CN110204580A (zh) | 含镍氮双重键结构的二价镍亚胺配合物及其制备与应用 | |
| WO2000010977A1 (en) | Catalytic asymmetric aminohydroxylation with amino-substituted heterocycles | |
| CN112778272B (zh) | 一种2,2′-联氮杂芳环类双齿配体及其制备方法和应用 | |
| CN102671704B (zh) | 一种Pd配合物催化剂及其制备方法及应用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant | ||
| CF01 | Termination of patent right due to non-payment of annual fee |
Granted publication date: 20140917 Termination date: 20150626 |
|
| EXPY | Termination of patent right or utility model |