CN101410714A - 在克罗恩病患者的外周血白细胞中T细胞受体介导的肿瘤坏死因子超家族与趋化因子mRNA增强的表达 - Google Patents
在克罗恩病患者的外周血白细胞中T细胞受体介导的肿瘤坏死因子超家族与趋化因子mRNA增强的表达 Download PDFInfo
- Publication number
- CN101410714A CN101410714A CNA2007800115431A CN200780011543A CN101410714A CN 101410714 A CN101410714 A CN 101410714A CN A2007800115431 A CNA2007800115431 A CN A2007800115431A CN 200780011543 A CN200780011543 A CN 200780011543A CN 101410714 A CN101410714 A CN 101410714A
- Authority
- CN
- China
- Prior art keywords
- sample
- leucocyte
- ratio
- mrna
- tnfsf
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6883—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/106—Pharmacogenomics, i.e. genetic variability in individual responses to drugs and drug metabolism
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/136—Screening for pharmacological compounds
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/158—Expression markers
Abstract
本发明公开了一种方法,其通过检测应答刺激中某些mRNA的水平,用于确定患有克罗恩病的人是否可能对靶向TNFSF成员或细胞因子的治疗有应答。本发明还公开了一种评估克罗恩病治疗对人的效力的方法。此外,本发明公开了一种筛选用于克罗恩病的治疗中的化合物的方法。本发明还公开了一种随着时间监控克罗恩病患者疾病状态的方法。
Description
本申请要求2006年4月7日提交的美国临时申请No.60/790,354的优先权,该临时申请的标题为在克罗恩病患者的外周血白细胞中T细胞受体介导的肿瘤坏死因子超家族与趋化因子mRNA增强的表达,这里将该临时申请通过参考全部并入,并作为本发明说明书的一部分。
背景
技术领域
本发明涉及一种预测患者对克罗恩病(Crohn’s disease)治疗应答的方法,所述治疗包括拮抗肿瘤坏死因子-α(TNF-α)、肿瘤坏死因子超家族的其他成员或细胞因子;本发明还涉及监控这种治疗效力的方法。本发明还涉及筛选用于治疗克罗恩病的化合物的方法。本发明还涉及监控克罗恩病患者中疾病状态的方法。
相关技术描述
自身免疫性疾病的特征在于产生与宿主细胞反应的抗体或自身反应的免疫效应T细胞。在某些类型的自身免疫性疾病中经常鉴定到自身抗体,例如重症肌无力中的抗乙酰胆碱受体的抗体,以及系统性红斑狼疮中的抗DNA抗体。然而,在许多类型的自身免疫性疾病中没有观察到这类自身抗体。而且,经常在健康个体中检测到自身抗体,但这些抗体不会诱导自身免疫疾病。因此,除了自身抗体外,显然其他未被鉴定的机制参与自身免疫性疾病的发病。
一旦自身抗体与宿主靶细胞结合,则补体级联反应被认为会被激活以形成在靶细胞膜上形成C5-9膜攻击复合体,这会引起宿主细胞的死亡(参见,Esser,毒理学(Toxicology)87,229(1994))。副产物趋化因子例如C3a、C4a或C5a招募更多的白细胞到损伤处(参见Hugli,免疫学关键评论(Crit.Rev.Immunol).1,321(1981))。被招募的白细胞或在损伤处自然存在的白细胞通过Fc受体(“FcR”)识别抗体结合的细胞(免疫复合体)。一旦FcR通过免疫复合体得到交联(cross-bridged),白细胞会释放TNF-α(参见Debets等人,免疫学杂志(J Immunol).141,1197(1998)),TNF-α会结合宿主细胞表面上存在的特异性受体,并诱导细胞凋亡或细胞损伤(参见Micheau等人,细胞(Cell),114,181(2003))。激活的FcR还会启动趋化细胞因子的释放以将不同亚型的白细胞招募到损伤处(参见Chantry等人,欧洲免疫学杂志(Eur.J.Immunol).19,189(1989))。除了FcR外,细胞毒性T细胞上的T细胞受体(“TCR”)也可以识别宿主细胞,并以与交联的FcR相同的方式激活TCR功能(参见Brehm等人,J.Immunol.175,5043(2005))。TCR功能被充分体现在通过与主要组织相容性复合体(MHC)分子的反应呈递抗原上(参见Isaacs等人,炎症性肠病(Inflamm.Bowel Dis).11 Suppl 1,S3(2005);以及Garcia等人,Cell 122,333(2005))。尽管TCR介导的细胞毒性功能没有被充分鉴定,其可能参与没有鉴定到自身抗体的病例中,因为免疫球蛋白和TCR是唯一能够识别靶的特异性结构的分子。这是自身免疫疾病分子机制的全部假设。
克罗恩病(“CD”)是一种包括胃肠道发炎的免疫疾病。尽管在临床上被充分鉴定,但是其发病机理还很少被了解。然而,已知TNF-α(也被称作肿瘤坏死因子超家族成员2(“TNFSF-2)”)的表达在如CD的炎症性肠病中提高。尽管可以使用5-ASA药物如柳氮磺吡啶、糖皮质激素或如硫唑嘌呤或6-巯基嘌呤的嘌呤类似物治疗轻微到中度的CD,但对于标准治疗(例如给药环孢霉素、他克莫司或抗炎性细胞因子)不显疗效的严重CD病例,治疗选择是非常有限的,并且效果会变化。大部分CD患者会需要至少一次外科手术。因为治疗选择依赖于对CD患者疾病状态的评价,因此期望开发评估疾病状态并监控疾病进展的新方法。
发明内容
在一个实施方式中,提供了一种确定患克罗恩病的人是否可能会对治疗应答的方法,其包括:体外刺激第一样品中的白细胞,其中所述第一样品含有来自所述人的白细胞;刺激后,检测第一样品中选自由肿瘤坏死因子亚家族(“TNFSF”)-2、TNFSF-5、TNFSF-6、TNFSF-14、趋化因子(C-C基序)配体(“CCL”)-2、CCL-3、CCL-4和趋化因子(C-X-C基序)配体(“CXCL”)-10所组成的组中的mRNA的量;体外使用对照刺激物刺激第二样品中的白细胞,其中所述第二样品含有来自所述人的白细胞;刺激后,检测第二样品中所述mRNA的量;确定第一样品中mRNA的量与第二样品中mRNA的量的比例,其中如果所述比例为大约1.7∶1或更高,则所述患克罗恩病的人可能会对治疗有应答。
在另一个方面中,刺激所述第一样品中的白细胞包括将抗T细胞受体的抗体与所述第一样品混合。
在另一个方面中,刺激所述第一样品中的白细胞包括将所述第一样品与选自由佛波醇-豆蔻酸酯-乙酸酯(phorbol myristate acetate,PMA)、植物凝血素(phytohemagglutinin,PHA)、麦胚凝集素(wheat germ agglutinin,WGA)、伴刀豆球蛋白-A(concanavalin-A,ConA)、脂多糖(LPS)、木菠萝凝集素(jacalin)、岩藻聚糖(fucoidan)、热聚IgE、热聚IgA和热聚IgM所组成的组中的药物进行混合。
在另一个方面中,所述第一样品和第二样品中的至少一个含有全血。
在另一个方面中,所述对照刺激物包括纯化的对照免疫球蛋白。
在另一个方面中,所述治疗靶向TNF-α活性。
在另一个方面中,所述治疗包括给药因福利美。
在另一个方面中,所述治疗包括给药选自由环孢霉素A和他克莫司所组成的组中的药物。
在一个实施方式中,提供了一种评估克罗恩病治疗对人效力的方法,其包括:体外刺激第一样品中的白细胞,其中所述第一样品含有所述人的白细胞;体外使用对照刺激物刺激第二样品中的白细胞,其中所述第二样品含有所述人的白细胞;刺激后,检测所述第一样品和第二样品中选自由肿瘤坏死因子亚家族(“TNFSF”)-2、TNFSF-5、TNFSF-6、TNFSF-14、趋化因子(C-C基序)配体(“CCL”)-2、CCL-3、CCL-4和趋化因子(C-X-C基序)配体(“CXCL”)-10所组成的组中的mRNA的量;计算所述第一样品中mRNA的量与所述第二样品中mRNA的量的第一比例;为所述人实施治疗;体外刺激第三样品中的白细胞,其中所述第三样品含有从实施治疗后的人获得的白细胞;体外使用对照刺激物刺激第四样品中的白细胞,其中所述第四样品含有从实施治疗后的人获得的白细胞;刺激后,检测所述第三样品和所述第四样品中所述mRNA的水平;计算所述第三样品中所述mRNA的量与所述第四样品中所述mRNA的量的第二比例;以及将所述第一比例和所述第二比例进行比较,其中所述比例的显著差别是有效治疗的指示。
在另一个方面中,刺激所述第一样品和第三样品中的白细胞包括将抗T细胞受体的抗体与所述样品混合。
在另一个方面中,刺激所述第一样品和第三样品中的白细胞包括将所述样品与选自由佛波醇-豆蔻酸酯-乙酸酯(PMA)、植物凝血素(PHA)、麦胚凝集素(WGA)、伴刀豆球蛋白-A(ConA)、脂多糖(LPS)、木菠萝凝集素、岩藻聚糖、热聚IgE、热聚IgA和热聚IgM所组成的组中的药物进行混合。
在另一个方面中,所述对照刺激物包括纯化的对照免疫球蛋白。
在另一个方面中,所述第一样品、第二样品、第三样品和第四样品中的至少一个含有全血。
在另一个方面中,所述比例的显著差别是所述第二比例高于所述第一比例,并且所述治疗包括使肿瘤坏死因子α失活。
在另一个方面中,所述治疗包括给药因福利美。
在另一个方面中,所述比例的显著差别是所述第一比例高于所述第二比例。
在另一个方面中,所述治疗包括给药选自由环孢霉素A和他克莫司所组成的组中的药物。
在一个实施方式中,提供了一种鉴定治疗克罗恩病的假定药物的方法,其包括:获得第一样品、第二样品、第三样品和第四样品,其含有所述人的白细胞,其中在暴露到抗T细胞受体的抗体时,所述人的白细胞显示出选自由肿瘤坏死因子亚家族(“TNFSF”)-2、TNFSF-5、TNFSF-6、TNFSF-14、趋化因子(C-C基序)配体(“CCL”)-2、CCL-3、CCL-4和趋化因子(C-X-C基序)配体(“CXCL”)-10所组成的组中的mRNA转录提高至少1.7倍;体外刺激所述第一样品中的白细胞;体外使用对照刺激物刺激所述第二样品中的白细胞;刺激后,检测所述第一样品和所述第二样品中所述mRNA的量;计算所述第一样品中所述mRNA的量与所述第二样品中所述mRNA的量的第一比例;将所述第三样品和第四样品暴露于所述药物;暴露后,体外刺激所述第三样品中的白细胞;暴露后,使用对照刺激物体外刺激所述第四样品中的白细胞;刺激后,检测所述第三样品和所述第四样品中所述mRNA的水平;计算所述第三样品中所述mRNA的量与所述第四样品中所述mRNA的量的第二比例;以及将所述第一比例和第二比例进行比较,其中所述比例的显著差别是假定药物的指示。
在另一个方面中,刺激所述第一和第三样品中的白细胞包括将抗T细胞受体的抗体与所述样品混合。
在另一个方面中,刺激所述第一和第三样品中的白细胞包括将样品与选自由佛波醇-豆蔻酸酯-乙酸酯(PMA)、植物凝血素(PHA)、麦胚凝集素(WGA)、伴刀豆球蛋白-A(ConA)、脂多糖(LPS)、木菠萝凝集素、岩藻聚糖、热聚IgE、热聚IgA和热聚IgM所组成的组中的药物进行混合。
在另一个方面中,所述对照刺激物包括纯化的对照免疫球蛋白。
在另一个方面中,所述第一样品、第二样品、第三样品和第四样品中的至少一个含有全血。
在另一个方面中,所述比例的显著差别是所述第一比例高于所述第二比例。
在一个实施方式中,提供了一种评估人的克罗恩病状态的方法,其包括:体外刺激第一样品中的白细胞,其中所述第一样品含有白细胞,并且是在第一时间从所述人获得的;刺激后,检测所述第一样品中选自由肿瘤坏死因子亚家族(“TNFSF”)-2、TNFSF-5、TNFSF-6、TNFSF-14、趋化因子(C-C基序)配体(“CCL”)-2、CCL-3、CCL-4和趋化因子(C-X-C基序)配体(“CXCL”)-10所组成的组中的mRNA的量;体外使用对照刺激物刺激第二样品中的白细胞,其中所述第二样品含有在第一时间从所述人获得的白细胞;刺激后,检测所述第二样品中所述mRNA的量;确定所述第一样品中所述mRNA的量与所述第二样品中所述mRNA的量的第一比例;体外刺激第三样品中的白细胞,其中所述第三样品含有白细胞,并且是在第一时间之后的第二时间从所述人获得的;刺激后,检测所述第三样品中所述mRNA的量;使用对照刺激物刺激第四样品中的白细胞,其中所述第四样品含有在第二时间从所述人获得的白细胞;刺激后,检测所述第四样品中所述mRNA的量;确定所述第三样品中所述mRNA的量与所述第四样品中所述mRNA的量的第二比例;以及将第一比例和第二比例进行比较,其中所述第一比例和第二比例的显著差别是疾病状态变化的指示。
在另一个方面中,刺激所述第一和第三样品中的白细胞包括将抗T细胞受体的抗体与所述样品混合。
在另一个方面中,刺激所述第一和第三样品中的白细胞包括将样品与选自由佛波醇-豆蔻酸酯-乙酸酯(PMA)、植物凝血素(PHA)、麦胚凝集素(WGA)、伴刀豆球蛋白-A(ConA)、脂多糖(LPS)、木菠萝凝集素、岩藻聚糖、热聚IgE、热聚IgA和热聚IgM所组成的组中的药物进行混合。
在另一个方面中,所述对照刺激物包括纯化的对照免疫球蛋白。
在另一个方面中,所述第一样品、第二样品、第三样品和第四样品中的至少一个含有全血。
在另一个方面中,所述比例的显著差别是所述第二比例高于所述第一比例,则所述疾病状态的变化是疾病的加重。
在另一个方面中,所述比例的显著差别是所述第一比例高于所述第二比例,则所述疾病状态的变化是疾病的消退。
附图说明
图1显示对来自CD患者和对照外周全血的人白细胞中FcR和TCR介导的TNFSF、CCL、CXCL和白介素mRNA基因表达定量的结果;
图2显示各种HAG诱导的mRNA应答的关联;
图3A-3B显示各种抗TCR诱导的mRNA应答之间的关联;
图4显示热聚IgG(heat aggregated IgG,HAG)对外周血白细胞中TNFSF和趋化因子mRNA表达的影响;
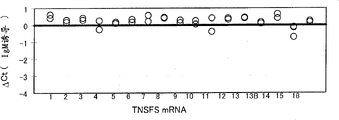
图5显示抗TCR抗体对外周血白细胞中TNFSF和趋化因子mRNA表达的影响;
图6显示使用佛波醇-豆蔻酸酯-乙酸酯(PMA)对健康个体的全血刺激的结果;
图7显示使用植物凝血素(PHA)对健康个体的全血刺激的结果;
图8显示使用麦胚凝集素(WGA)对健康个体的全血刺激的结果;
图9显示使用伴刀豆球蛋白-A(ConA)对健康个体的全血刺激的结果;
图10显示使用脂多糖(LPS)对健康个体的全血刺激的结果;
图11显示使用木菠萝凝集素对健康个体的全血刺激的结果;
图12显示使用岩藻聚糖对健康个体的全血刺激的结果;
图13A-13D显示使用热聚IgG对健康个体的全血刺激的结果;
图14A-14C显示使用热聚IgA对健康个体的全血刺激的结果;
图15A-15C显示使用热聚IgM对健康个体的全血刺激的结果;
图16A-16C显示使用热聚IgE对健康个体的全血刺激的结果。
优选实施方式的详细描述
本发明涉及使用白细胞中应对特异细胞刺激的差异mRNA转录模式(patterns)用于检验是否CD患者是特异治疗的良好候选者,例如使用Remicade的治疗的良好候选者。本发明还涉及使用这类差异转录模式用于评估是否为CD患者施加的治疗例如使用Remicade的治疗是有效的。本发明的公开内容还涉及使用这些差异转录模式用于筛选用于治疗CD的候选药物。本发明的公开内容还涉及使用这些差异转录模式用于评估随着时间患者中CD的状态,并监控该疾病的进展。
如上所述,CD的病理学可能涉及CD患者中免疫细胞中FcR或TCR发挥功能。为了进一步检验FcR或TCR在疾病中的可能作用,有用的是检验是否FcR或TCR在外周血中循环白细胞中的功能在白细胞迁移到自身免疫性疾病患者病理位置之前是正常的,或者在该迁移之前已经被增强。为了分析FcR或TCR的功能在CD患者中的外周血白细胞中是正常的或增强的,将热集结人IgG(“HAG”)或针对α/βT细胞受体的单克隆抗体(“抗TCR”)直接加入到肝素化全血中以分别刺激FcR和TCR中。尽管对于IgG,存在多种FcR(FcγR),例如FcγRI、IIa、IIb和III(GeneBank UniGene数据库),HAG作为能够与所有FcR亚型反应的通用刺激物。对由于使用HAG和抗TCR进行刺激所导致的TNF超家族(“TNFSF”)mRNA(参见,例如GeneBank UniGene数据库)以及选择的CCL和CXCL趋化因子mRNA和趋化白介素mRNA(IL-1β、IL-6和IL-8)的mRNA水平的变化进行定量。由于在与全血混合时,γ/δ抗TCR不会诱导任何TNFSF mRNA,因此选择α/β抗TCR用于刺激。
所采用的方法如下。从GenBank中的UniGene数据库获得各种TNFSF和趋化因子基因的核苷酸序列。通过引物表达(Primer Express)(应用生物系统,福斯特城,加利福尼亚(Applied Biosystem,Foster City,CA))和HYB模拟器(HYBsimulator)(RNAture,欧文(Irvine),CA)设计每个基因的PCR引物(参见Mitsuhashi等人,自然(Nature)367:759(1994)和Hyndman等人,生物技术(BioTechniques),20:1090(1996))。下面的表1中总结了这些序列。通过IDT(Coralville,IA)合成这些寡聚核苷酸。
表1:引物序列
通过在63℃下PBS中加热20mg/mL人IgG(西格玛,圣路易斯州(SigmaSt.Louis))15分钟制备热聚IgG(HAG)(参见Ostreiko等人,Immunol Lett.15,311(1987))。在8孔带状微管中,加入1.2μl HAG或抗TCR抗体(IgG1κ)或对照(HAG的磷酸盐缓冲液或抗TCR的小鼠对照IgG1κ)(BioLegend,圣地亚哥(San Diego)),并存储在-20℃下,直到使用。尽管此处采用小鼠IgG1κ作为抗TCR抗体刺激的对照,但还可以采用其它纯化的对照免疫球蛋白。将60μl新鲜肝素化的全血一式三份(in triplicate)加入到每个孔中,并盖上盖子在37℃下孵育2-8个小时。每次处理后,将50μl全血转移到下面所描述的滤板。将每种血液样品冷冻存储于-80℃直到使用。
根据在Mitsuhashi等人,临床化学(Clin.Chem.)52:4(公开为:doi:10.1373/clinchem.2005.048983)中所描述的方法从全血制备mRNA和cDNA。也可以采用在美国专利申请系列No.10/796,298中所公开的该方法,此处通过参考将其并入。简言之,将96孔滤板置于收集板之上,并施加150μL 5mM Tris(pH 7.4)。接着在4℃下,以120×g离心1分钟,将50μL血样品施加到每个孔,并立即在4℃下120×g离心2分钟,接着使用300μL PBS对每个孔进行清洗一次,并在4℃下2000×g离心5分钟。接着,将60μL裂解缓冲液贮液施加到滤板,接着在37℃下孵育10分钟,其中所述裂解缓冲液贮液补充了1%的2-巯基乙醇(伯乐,赫克尔士,加利福尼亚,美国(Bio Rad,Hercules,CA,USA))、0.5mg/mL蛋白酶K(皮尔斯,洛克福特,伊利诺斯州,美国(Pierce,Rockford,IL,USA))、0.1mg/mL鲑鱼精子DNA(5基本艾芬道夫/布林克曼(Prime Eppendorf/Brinkmann),威斯特伯里,纽约,美国(Westbury,NY,USA))、0.1mg/mL大肠杆菌(E.coli)tRNA(Sigma)、10mmol/L的各种特异性反向引物的混合物以及标准的RNA34寡聚核苷酸。接着将所述滤板置于固定寡聚(dT)的微量培养板(GenePlate,RNAture)上(参见Mitsuhashi等人,Nature357:519(1992)和Hamaguchi等人,Clin.Chem.44,2256(1998),此处通过参考将两者都并入),并在4℃下2000×g离心5分钟。在4℃下存储过夜后,使用100μL单纯裂解缓冲液对微量培养板进行清洗3次,接着在4℃下使用150μL清洗缓冲液(0.5M NaCl,10mM Tris(pH 7.4),1mM EDTA)清洗3次。通过加入30μL含有1×RT-缓冲液、1.25mM的各种dNTP、4单位RNA酶抑制剂(rRNasin)以及80单位莫洛尼氏鼠白血病病毒(MMLV)反转录酶(普洛麦格(Promega))(不含引物)的缓冲液并在37℃下孵育2小时,在每个孔中直接合成cDNA。特异性引物引导的cDNA存在溶液中,寡聚(dT)-引导的cDNA保持固定在微量培养板上(参见Hugli,Crit.Rev.Immunol.1,321(1981))。对于SYBR Green PCR,(参见Morrison等人,生物技术(Biotechniques)24,954(1998),此处通过参考将其并入),将cDNA在水中稀释4倍,并将4μl的cDNA溶液直接转移到384孔PCR板中,向其中加入5μl的iTaq SYBR主体混合物(BioRad,Hercules,CA),并施加1μl寡聚核苷酸混合物(正向和反向引物的每种都为15μM),在PRISM 7900HT(ABI)中进行PCR,其通过一个循环的95℃10分钟,接着45个循环的95℃30秒以及60℃1分钟。还可以采用TaqMan PCR;在这种情况中,直接将cDNA溶液转移到384孔PCR板,向其中施加5μl TaqMan通用主体混合物(ABI)和1μl寡聚核苷酸混合物(正向和反向引物的每种都为15μM以及3-6μM TaqMan探针),在PRISM 7900HT(ABI)中进行PCR其通过一个循环的95℃10分钟,接着45个循环的95℃30秒、55℃30秒以及60℃1分钟。
使用1xRT缓冲液作为阴性对照用于确认在SYBR Green PCR条件下没有产生引物二聚体。而且,分析每种情况的解链曲线,以确认PCR信号是来自单个的PCR产物。通过分析软件(SDS,ABI)确定Ct。通过减去适当对照样品的Ct值计算ΔCt,并通过假设每个PCR循环的效率为100%,将提高的倍数计算为2^(-ΔCt)。
图1显示外周全血的人白细胞中FcR和TCR介导的TNFSF、CCL、CXCL和白介素mRNA基因表达分析结果。图1中的结果被表示为超过对照值提高的倍数。应答者被定义为应答所述刺激显示出mRNA水平提高超过1.7倍的个体。在另一个实施例中,应答者也可以被定义为与对照刺激相比时,显示mRNA水平降低超过1.7倍的个体。每个数据(○代表健康成人,△代表CD患者)是三等份全血的平均值。层垫区域(Blanket area)是外部对照RNA34(R34)数值的平均值±3标准偏差。通过使用上述的应答者和非应答者人群的χ2检验计算图1B中所表示的统计学显著性(*:p<0.05、**:p<0.01、***:p<0.001)。通过使用仅应答者人群的提高的倍数的对数值的t检验,++表示p<0.01。
如图1A所示,HAG主要诱导TNFSF-2、8、15、18、IL-1B、8、CCL-2、3、4、11、20和CXCL-1、2、3,然而抗TCR诱导TNFSF的不同成员(TNFSF-1、2、5、6、9、10、14)和趋化因子(IL-6、CCL-2、3、4、8、20和CXCL-10)的mRNA。图13显示了使用健康个体的全血获得进一步的数据,其中所述健康个体的全血被HAG刺激,并且所述数据表达为循环阈值(Ct)(参见下面)。尽管CD患者不显示任何HAG诱导的活性增强,但是抗TCR诱导的TNFSF-2、5、6、14和CCL-2、3和4的在CD患者中应答者人群(提高>1.7倍)显著大于健康对照中的应答者人群(提高>1.7倍)。令人感兴趣的是CD患者(p<0.001)诱导的TNFSF-2(=TNFα)比TNFSF-14显著地多。这些数据暗示外周血白细胞中TCR功能的损害。该系统将可以用于分析CD和其他自身免疫性疾病中免疫细胞的细胞毒性功能。
图2显示在各种HAG诱导的mRNA应答中的相关性。在图2中,来自图1A的数据被转化成x-y绘图(x-y plots)。分别地,图2A显示IL-1B对比IL-8;图2B显示IL-1B对比CCL-2;图2C显示IL-1B对比CXCL-1;图2D显示CXCL-1对比CXCL-2;图2E显示IL-1B对比TNFSF-15;以及图2F显示TNFSF-15对比TNFSF-8。在图中,○:健康成人;▲:CD。
图3显示在各种抗TCR诱导的mRNA应答中的相关性。在图3中,来自图1A的数据被转化成x-y绘图。分别地,图3A显示TNFSF-2对比TNFSF-14;图3B显示TNFSF-5对比TNFSF-6;图3C显示CCL-2对比CCL-3;图3D显示CCL-2对比CCL-4;图3E显示CCL-2对比CCL-20;以及图3F显示CCL-8对比CXCL-10。在该图中,○:健康成人;▲:CD。在图3A中,画出了对照和CD患者的回归线。
由于个体与个体之间的宽差异以及存在应答者和非应答者人群,因此,标准的研究者t-检验(Student′s t-test)不适合分析这些结果。通过χ2检验,在CD患者中TNFSF-2、5、6、14、CCL-2、3和4的应答者人群(如上所示,提高>1.7倍)分别是92.9%、66.7%、75.0%、82.1%、75.0%、75.0%和83.3%,这显著高于健康对照(分别是38.9%、28.6%、42.9%、44.4%、33.3%、20.0%和20.0%)(参见图1B:*)。当以对数标度对应答者人群的提高的倍数进行比较时,则CD患者显示比对照对象显著(P<0.01)高的数值(参见图1B:++)。而且,与HAG诱导的基因表达的结果类似(图2),某些TNFSF成员和趋化因子的应答者也是其他TNFSF成员和趋化因子的应答者(图3),这暗示抗TCR数据的偏差产生自个体应答,而不是检验技术。令人吃惊的是,抗TCR诱导的TNFSF-2(=TNFα)与TNFSF-14之间的相关性在健康对照和CD患者之间是显著(p<0.001)不同的:CD患者诱导比TNFSF-14多的TNFSF-2,尽管这两种TNFSF应答者在两种情况中都相互关联(图3A)。
所有的情况中外部对照RNA34都没有变化,这暗示该检验进行得适当。尽管这些结果显示个体与个体之间的宽变化,但某种TNFS和趋化因子的应答者也是对其它TNFSF和趋化因子的应答者(参见图2),这暗示数据的偏差是来自于个体的应答,而不是检验技术。令人感兴趣的是,CD患者不显示任何HAG诱导活性的增强,并且一些CD患者确实显示HAG诱导IL-1B、IL-8、CCL-20和CXCL-3mRNA表达的活性降低(图1A)。相反,抗TCR诱导不同的TNFSF(TNFSF-1、2、5、6、9、10和14)以及趋化因子(IL-6、CCL-2、3、4、8、20和CXCL-10)mRNA。抗TCR不诱导IL-1B和IL-8mRNA。
图4显示HAG刺激的剂量应答和动力学研究。图4显示热聚IgG(HAG)对外周血白细胞中TNFSF和趋化因子mRNA表达的影响。图4A显示反应的动力学。将三等份的每种60μl的肝素化全血与PBS混合(○,△),或者与200μg/mL HAG(●,▲)混合,并在37℃下孵育0-12个小时。接着如上所述,对TNFSF-15(○,●)和IL-8(△,▲)的mRNA进行定量。使用在时间=0时的数值作为对照,计算提高的倍数。图4B显示剂量应答。将三等份每种60μl的肝素化全血与各种浓度的HAG混合,并在37℃下孵育2个小时。接着如上所述,对TNFSF-2(●)、TNFSF-15(▲),1L-8(○)、IL-1B(◇)和CXCL-2(△)的mRNA进行定量。使用溶剂(PBS)的数值作为对照计算提高的倍数。每个数据点是三等份全血的平均值±标准偏差(A)或平均值(B)。
图5显示对抗TCR刺激的剂量应答和动力学研究。图5显示抗TCR抗体对外周血白细胞中TNFSF和趋化因子mRNA表达的影响。图5A显示对所述刺激物的剂量应答和动力学。将三等份每种60μl的肝素化全血与10μg/mL(●)、1μg/mL(◆)或0.1μg/mL(▲)的小鼠抗人α/βTCR IgG1κ,PBS(○)或10μg/ml(□)纯化的小鼠IgG1κ混合,并在37℃下孵育0-7个小时。接着如上所述对TNFSF-2mRNA进行定量。图5B显示对刺激物的动力学。将三等份每种60μl的肝素化全血与10μg/ml小鼠抗人α/βTCR IgG1κ或0μg/ml纯化的小鼠IgG1κ混合,并在37℃下孵育2个小时。接着如上所述对TNFSF-2(●)、TNFSF-5(□)、TNFSF-6(▲)、TNFSF-9(◆)、TNFSF-14(○)和CXCL-10(△)mRNA进行定量。通过小鼠IgG1κ作为对照的数值计算提高的倍数。每个数据都是来自三等份全血的平均值±标准偏差(A),或者平均值(B)。
如图6-12和图14-16所示,除了上面描述的抗TCR和HAG外,其他刺激药物例如佛波醇-豆蔻酸酯-乙酸酯(PMA)、植物凝血素(PHA)、麦胚凝集素(WGA)、伴刀豆球蛋白-A(ConA)、脂多糖(LPS)、木菠萝凝集素、岩藻聚糖、热聚IgE、热聚IgA和热聚IgM也诱导从健康个体获取的全血中TNFSF和趋化因子的不同类型亚型。在这些检验中所遵循的方案与上面所提供的相同,除了在每种情况中采用不同的刺激物外。在图6-16中,数据表达为循环阈值(Ct),即产生一定量PCR产物所需要的PCR循环数。通过从被刺激样品的Ct中减去未刺激样品的Ct值,获得ΔCt值。由于Ct是对数标度,因此1个ΔCt单位表示量变化2因素(factor)。由于较高的表达水平会减少产生标准量产物所需要的PCR循环数,因此负的ΔCt值表示表达上的提高。
许多这些药物表现出与抗TCR类似的刺激模式。特别地,如图6和7所示,PMA和PHA与抗TCR在CD患者中刺激相同的TNFSF亚型(TNFSF-2、TNFSF-5、TNFSF-6和TNFSF-14)。此外,如图8-12所示,WGA、ConA、LPS、木菠萝凝集素和岩藻聚糖全部刺激TNFSF-2亚型,已知TNFSF-2亚型与CD相关。如图16所示,热聚IgE刺激TNFSF-2以及CCL-3和CCL-4以及CXCL-10。最后,如图14所示,热聚IgA刺激CCL-2、CCL-3和CCL-4。由于刺激模式与上述抗TCR模式的相似性,因此这些药物也可以用于检验CD患者的治疗选择,以及用于筛选治疗CD的新药物。
通常,细胞毒性检验已经被用于研究由于免疫系统活性所引起的真实的细胞死亡,例如被认为是在CD中所出现的细胞死亡。通常通过将负载51Cr的靶细胞与效应细胞以各种比例孵育进行细胞毒性检验,并对从死细胞或受到损伤的细胞释放的51Cr放射性进行定量(参见Dunkley等人,免疫学方法杂志(JImmunol Methods)6,39(1974))。在某些情况中,放射性材料已经被非放射性材料所替换,例如荧光材料(参见Kruger-Krasagakes等人,J Immunol Methods156,1(1992)),但基本的原理没有变化。因此细胞毒性检验的结果反映真实的细胞死亡。
然而,细胞毒性检验是在非生理实验条件下进行的,因此在这些研究过程中难以检验复杂的细胞与细胞之间相互作用和细胞与血浆的相互作用。而且,细胞毒性检验不显示哪一种TNFSF成员对细胞死亡负责。一旦效应细胞识别靶细胞,则效应细胞的功能不仅是杀死靶细胞,而且还有招募其他效应细胞,因为单个效应细胞不足以杀死众多的靶细胞。这种招募功能被认为是有趋化因子的释放所表示的。效应细胞所释放这些趋化因子的同一性无法被经典的细胞毒性检验所揭示。然而,在本发明中所提出的检验系统能够同时在效应细胞中鉴定许多类型的基因表达。
通常鉴定负责的TNFSF和趋化因子亚型是非常重要的,因为这些分子与靶细胞或白细胞上的特异性受体反应。例如,根据通用基因表达序列标签(UniGene′s Expression Sequence Tag)(EST)布图特征库,TNFSF-2的受体(肿瘤坏死因子受体超家族(TNFRSF)-1A)出现在小肠中,但TNFSF-5、TNFSF-6和TNFSF-14(TNFRSF-5、TNFRSF-6和TNFRSF-14)则不是。因此,CD患者中增强的TNFSF-2(图1B、图3A)可能与小肠的损伤有关,其中小肠是CD疾病的主要位点。此外,已知CCL-2的受体(CCR-2)是单核细胞趋化蛋白-1的受体,以及CXCL-10的受体(CXCR-3)是NK细胞和T细胞迁移的原因(UniGene数据库)。如上所述,所公开的数据显示CD患者的效应白细胞在被刺激时,转录提高量的CCL-2和CXCL-10的mRNA,这可以揭示在CD疾病位置所观察到的各种白细胞浸润。
使用全血优于使用培养基中分离的白细胞,因为前者比后者更符合生理条件,并且可以筛选全部的白细胞种群。较长的孵育全血可能产生额外的假象。因此,理想的方式是通过从体内转换到体外,在短时间孵育过程中鉴定全血中的早期杀伤细胞信号和招募信号。mRNA的转录是在蛋白质合成或者最终生物产物之前的较早事件。因此,mRNA是该研究的合理靶标。在许多TNFSF、CCL、CXCL和白介素的mRNA中,如图1所示,本发明的数据显示FcR和TCR诱导不同亚类的基因。
最近的研究暗示TNFSF-2是CD中的主要因子之一(参见Isaacs等人,Inflamm.Bowel Dis.11 Suppl 1,S3(2005))。事实上,如上所述,针对TNF-α的单克隆抗体Remicade被临床上用于严重CD并使用其他传统治疗效果差的病史的患者。尽管TNF-α在损伤中CD的致病中发挥关键作用,但是,本发明中所列出的数据显示某些TNFSF成员诱导TCR的潜在机能亢进是之前未被发现的,其中所述TNFSF成员包括外周血内循环白细胞中的TNF-α(TNFSF-2)。由于本发明使用全血,而不是肠组织,因此,其可以用作CD的诊断测试用于评估对TNF-α治疗可能的应答,以及监控治疗应答。
具体地,在确定是否患有CD的人可能对靶向TNF-α活性的治疗响应的方法的优选实施方式中,例如采用抗TNF-α单克隆抗体的治疗,如上所述,全血是从CD患者获得的,并且对血液样品施加抗TCR抗体刺激,以及可选择地施加给对照刺激(10mg/ml纯化的小鼠IgG1κ)。根据上述,可以检测样品中TNFSF-2的mRNA水平。在使用抗TCR抗体刺激后TNFSF-2mRNA水平显著提高的CD患者(例如所述,倍数改变超过1.7)是靶向TNF-α的治疗的良好候选者。
可替换地,可以检测应答T细胞刺激,一种或者多种其它mRNA的水平被差异转录,例如可以检测TNFSF-5、TNFSF-6、TNFSF-14、CCL-2、CCL-3、CCL-4或CXCL-10。一种或者多种这些mRNA水平刺激后显著提高(例如1.7倍或更大的变化)的CD患者可以是靶向与这些mRNA相关的蛋白质的治疗的良好候选者。
此外,在评估靶向患者中一种或多种的TNFSF-2、TNFSF-5、TNFSF-6、TNFSF-14、CCL-2、CCL-3、CCL-4和CXCL-10TNF-α的CD治疗功效的方法的优选实施方式中,在开始治疗之前获得体外使用抗TCR抗体或其他刺激物进行T细胞刺激后全血中mRNA的量与体外对照刺激后的量的第一比例。接着开始治疗过程。在治疗过程中或治疗后的某些点,获得体外抗TCR抗体刺激后全血中mRNA的量与体外对照刺激后的量的第二比例。比例中的显著差别可以说明治疗的效力。例如,如果所述治疗是给药因福利美,所检测的mRNA是TNFSF-2,并且所述第二比例大于第一比例,则能够说明治疗的效力。关于与TNF-α相关mRNA的可诱导性得提高的原因是在所分泌的TNF-α被治疗药物如Remicade所成功灭活,在T细胞中有反馈机制发挥作用,通过该机制转录更多的TNFSF-2mRNA。
在其他情况中,关于CD相关mRNA的较小第二比例可以表示成功的治疗。关于治疗后所检测的mRNA,这类结果显示T细胞变得不太可诱导。例如,降低白细胞关于TNFSF-2的诱导性进而减少所释放TNF-α量的治疗,将推测有利于缓解CD的症状。类似地,所转录的CCL-2和CXCL-10的降低将可能会导致白细胞浸润和较不严重的症状。
重要地,该体外方法也可以用于筛选抑制抗TCR介导的TNFα mRNA表达的化合物。这些化合物将是令人感兴趣的药物靶标,因为针对TNF-α的单克隆抗体与损伤处已经释放的TNF-α反应,而这些新药候选物会在转录水平上阻断白细胞产生TNF-α。这是开发针对自身免疫性疾病的药物的新策略。
在使用所公开的系统筛选药物化合物,进而鉴定治疗CD的假定药物的方法的实施方式中,全血是从作为应答者的CD患者中获得的,其中在暴露到如抗TCR的T细胞刺激时,他们的白细胞表现出CD相关mRNA水平的至少1.7倍提高。计算体外使用抗TCR抗体或其他刺激物进行T细胞刺激后的全血中mRNA的量与体外对照刺激后的量的第一比例。进一步,将从这些对象获得的全血样品体外暴露于药物化合物,接着进行上述的差异刺激。接着计算体外T细胞刺激后全血中mRNA的量与体外对照刺激后的量的第二比例。这些比例之间的显著差异可以表示该药物化合物是进行进一步研究作为CD潜在治疗剂的候选化合物。
另外,在通过检测含有从患者获得的白细胞的样品中TNFSF-2、TNFSF-5、TNFSF-6、TNFSF-14、CCL-2、CCL-3、CCL-4和CXCL-10中一种或者多种的mRNA水平监控CD患者疾病状态的方法的优选实施方式中,在第一时间获得使用抗TCR抗体或其他刺激物体外刺激之后全血中mRNA的量,与体外对照刺激之后的量的第一比例。在第一时间之后的第二时间,获得体外T细胞刺激之后全血中mRNA的量与体外对照刺激之后的量的第二比例。比例之间的显著差异可以表示疾病状态的变化。例如,当第二比例高于第一比例时,其能说明疾病加重,而较大的第一比例则说明疾病消退。
序列表
<110>日立化成工业株式会社;日立化成研究中心公司;西塞医疗中心
<120>在克罗恩病患者的外周血白细胞中T细胞受体介导的肿瘤坏死因子超家族与趋化因子mRNA增强的表达
<130>PIJP0811448
<150>60/790,354
<151>2006-04-07
<160>110
<170>FastSEQ for Windows Version 4.0
<210>1
<211>22
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>1
cagctatcca cccacacaga tg 22
<210>2
<211>22
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>2
cgaaggctcc aaagaagaca gt 22
<210>3
<211>20
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>3
tcaatcggcc cgactatctc 20
<210>4
<211>20
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>4
cagggcaatg atcccaaagt 20
<210>5
<211>23
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>5
agggtgtacg tcaacatcag tca 23
<210>6
<211>18
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>6
cacggcccca aagaaggt 18
<210>7
<211>21
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>7
gcccctcttc caactgaaga a 21
<210>8
<211>25
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>8
ggtattgtca gtggtcacat tcaag 25
<210>9
<211>19
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>9
ccacagttcc gccaaacct 19
<210>10
<211>24
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>10
cacctggttg caattcaaat actc 24
<210>11
<211>24
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>11
tggcagcatc ttcacttcta aatg 24
<210>12
<211>24
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>12
gaaatgagtc cccaaaacat ctct 24
<210>13
<211>22
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>13
cacactctgc accaacctca ct 22
<210>14
<211>23
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>14
tgcactccaa agaaggtctc atc 23
<210>15
<211>24
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>15
accaccatat cagtcaatgt ggat 24
<210>16
<211>25
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>16
gaagatggac aacacattct caaga 25
<210>17
<211>23
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>17
agctacaaag aggacacgaa gga 23
<210>18
<211>24
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>18
cgcagctcta gttgaaagaa gaca 24
<210>19
<211>26
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>19
gggaatattt gagcttaagg aaaatg 26
<210>20
<211>20
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>20
aaaaggcccc gaaaaaactg 20
<210>21
<211>30
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>21
gagtatcttc aactaatggt gtacgtcact 30
<210>22
<211>21
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>22
tggtgcttcc tcctttcatc a 21
<210>23
<211>24
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>23
tactgtcagg tgcactttga tgag 24
<210>24
<211>19
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>24
gcagtggctg agaattcct 19
<210>25
<211>22
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>25
atatggtgtc cgaatccagg at 22
<210>26
<211>21
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>26
cctgacccat ggtgaaagtc a 21
<210>27
<211>25
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>27
atgcctgaaa cactacccaa taatt 25
<210>28
<211>24
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>28
gcaagttgga gttcatctcc ttct 24
<210>29
<211>18
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>29
cgtccgtgtg ctggatga 18
<210>30
<211>22
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>30
catgaaagcc ccgaagtaag ac 22
<210>31
<211>23
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>31
tgcgaagtag gtagcaactg gtt 23
<210>32
<211>22
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>32
ccattagctt gtccccttct tg 22
<210>33
<211>26
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>33
cggctgtata aaaacaaaga catgat 26
<210>34
<211>22
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>34
tccccaacat gcaattcata ag 22
<210>35
<211>24
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>35
gaagatggaa aagcgatttg tctt 24
<210>36
<211>21
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>36
gggcatgttt tctgcttgag a 21
<210>37
<211>20
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>37
gctcttggag ctgcctacgt 20
<210>38
<211>24
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>38
aaggtctctt tcaccaatgc actt 24
<210>39
<211>24
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>39
tcatcactgg tcttttggag tttg 24
<210>40
<211>20
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>40
tctgcacagc tctggcttgt 20
<210>41
<211>27
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>41
tgctaaagaa cttagatgtc agtgcat 27
<210>42
<211>23
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>42
tggtccactc tcaatcactc tca 23
<210>43
<211>20
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>43
gcaggccctg aatttcaaca 20
<210>44
<211>29
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>44
gaagtatgca gagcttgatt ttagtttta 29
<210>45
<211>29
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>45
gaagtatgca gagcttgatt ttagtttta 29
<210>46
<211>20
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>46
cccattcgct ccaagatgag 20
<210>47
<211>25
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>47
tgaagtgctt tctcttggag ttaca 25
<210>48
<211>26
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>48
cattcccatt agaagacaaa ctgttg 26
<210>49
<211>22
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>49
aaaacctctt gggaagcatg ag 22
<210>50
<211>20
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>50
gggaccccga ggacagtact 20
<210>51
<211>20
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>51
ccattgtggc caaggagatc 20
<210>52
<211>19
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>52
tgtccaggtg gtccatgga 19
<210>53
<211>28
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>53
cacagaattt catagctgac tactttga 28
<210>54
<211>22
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>54
tcgcttggtt aggaagatga ca 22
<210>55
<211>23
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>55
ggtattccaa accaaaagaa gca 23
<210>56
<211>26
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>56
gttcagttcc aggtcataca cgtact 26
<210>57
<211>21
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>57
agtcgtcttt gtcacccgaa a 21
<210>58
<211>26
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>58
agctcatctc caaagagttg atgtac 26
<210>59
<211>19
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>59
tgtgctgacc ccacacaga 19
<210>60
<211>23
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>60
gctttggagt ttgggttttc ttg 23
<210>61
<211>26
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>61
agagctacac aagaatcacc aacatc 26
<210>62
<211>19
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>62
agacctcctt gccccgttt 19
<210>63
<211>22
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>63
cccagaaagc tgtgatcttc aa 22
<210>64
<211>21
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>64
tcctgcaccc acttcttctt g 21
<210>65
<211>21
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>65
ccaaactggg caaggagatc t 21
<210>66
<211>24
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>66
ggcccaggtg tttcatataa ttct 24
<210>67
<211>27
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>67
tgcttcacct acactaccta caagatc 27
<210>68
<211>18
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>68
gacaattccg ggcttgga 18
<210>69
<211>27
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>69
cagattccac aaaagttcat agttgac 27
<210>70
<211>19
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>70
ccggcctctc ttggttagg 19
<210>71
<211>24
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>71
ctgctgtagt gttcaccaca ctga 24
<210>72
<211>24
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>72
ctgctgtagt gttcaccaca ctga 24
<210>73
<211>28
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>73
gatacacaga ccgtattctt catcctaa 28
<210>74
<211>26
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>74
tgaaagatga tagcattgat gtcaca 26
<210>75
<211>21
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>75
cgctctcagg cagagctatg t 21
<210>76
<211>21
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>76
cttgtccaga tgctgcatca g 21
<210>77
<211>19
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>77
gcgcgtggtg aaacacttc 19
<210>78
<211>22
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>78
atcggcacag atctccttat cc 22
<210>79
<211>20
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>79
cgaagcatcc cgtgttcact 20
<210>80
<211>18
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>80
gatgacaccc ggcttgga 18
<210>81
<211>22
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>81
caggagtgat cttcaccacc aa 22
<210>82
<211>20
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>82
ggcgtccagg ttcttcatgt 20
<210>83
<211>20
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>83
ggcgtccagg ttcttcatgt 20
<210>84
<211>23
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>84
gtagaatatc gcagcaggca gat 23
<210>85
<211>22
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>85
ctgcttccaa tacagccaca ag 22
<210>86
<211>24
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>86
gagcagctgt tactggtgaa ttca 24
<210>87
<211>19
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>87
cgtgcttcac ctggctcaa 19
<210>88
<211>21
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>88
ggtgctcaaa ccactgtgac a 21
<210>89
<211>22
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>89
ggaaatgttt gccacaggaa ga 22
<210>90
<211>21
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>90
tgtttcgtgt ttcccctgat g 21
<210>91
<211>16
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>91
ccactgcgcc caaacc 16
<210>92
<211>20
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>92
gcaggattga ggcaagcttt 20
<210>93
<211>18
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>93
cccctggcca ctgaactg 18
<210>94
<211>23
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>94
tggatgttct tgaggtgaat tcc 23
<210>95
<211>23
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>95
ggaattcacc tcaagaacat cca 23
<210>96
<211>21
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>96
gtggctatga cttcggtttg g 21
<210>97
<211>18
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>97
ccgtcccagg cacatcac 18
<210>98
<211>18
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>98
ccgtcccagg cacatcac 18
<210>99
<211>19
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>99
agagctgcgt tgcgtttgt 19
<210>100
<211>22
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>100
tggcgaacac ttgcagatta ct 22
<210>101
<211>20
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>101
cagagctgcg ttgcacttgt 20
<210>102
<211>23
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>102
acacctgcag tttaccaatc gtt 23
<210>103
<211>22
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>103
tctggaattc atcccaaaaa ca 22
<210>104
<211>22
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>104
tctggaattc atcccaaaaa ca 22
<210>105
<211>25
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>105
ccacctacaa tccttgaaag acctt 25
<210>106
<211>27
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>106
cagtgtagca atgatttcaa ttttctc 27
<210>107
<211>21
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>107
tccacgtgtt gagatcattg c 21
<210>108
<211>21
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>108
tcttgatggc cttcgattct g 21
<210>109
<211>19
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>109
cccacagcca ggacatcag 19
<210>110
<211>22
<212>DNA
<213>人工序列
<220>
<223>PCR引物
<400>110
cttgcacagc acataggaaa gg 22
Claims (30)
1.一种确定患克罗恩病的人是否可能会对治疗应答的方法,其包括:
体外刺激第一样品中的白细胞,其中所述第一样品含有来自所述人的白细胞;
刺激后,检测第一样品中选自由肿瘤坏死因子亚家族(“TNFSF”)-2、TNFSF-5、TNFSF-6、TNFSF-14、趋化因子(C-C基序)配体(“CCL”)-2、CCL-3、CCL-4和趋化因子(C-X-C基序)配体(“CXCL”)-10所组成的组中的mRNA的量;
体外使用对照刺激物刺激第二样品中的白细胞,其中所述第二样品含有来自所述人的白细胞;
刺激后,检测所述第二样品中所述mRNA的量;以及
确定第一样品中所述mRNA的量与第二样品中所述mRNA的量的比例,其中如果所述比例为大约1.7∶1或更高,则所述患克罗恩病的人可能会对治疗有应答。
2.根据权利要求1所述的方法,其中,刺激所述第一样品中的白细胞包括将抗T细胞受体的抗体与所述第一样品混合。
3.根据权利要求1所述的方法,其中,刺激所述第一样品中的白细胞包括将所述第一样品与选自由佛波醇-豆蔻酸酯-乙酸酯(PMA)、植物凝血素(PHA)、麦胚凝集素(WGA)、伴刀豆球蛋白-A(ConA)、脂多糖(LPS)、木菠萝凝集素、岩藻聚糖、热聚IgE、热聚IgA和热聚IgM所组成的组中的药物混合。
4.根据权利要求1所述的方法,其中,所述第一样品和第二样品中的至少一个含有全血。
5.根据权利要求1所述的方法,其中,所述对照刺激物包括纯化的对照免疫球蛋白。
6.根据权利要求1所述的方法,其中,所述治疗靶向TNF-α活性。
7.根据权利要求6所述的方法,其中,所述治疗包括给药因福利美。
8.根据权利要求1所述的方法,其中,所述治疗包括给药选自由环孢霉素A和他克莫司所组成的组中的药物。
9.一种评估克罗恩病治疗对人效力的方法,其包括:
体外刺激第一样品中的白细胞,其中所述第一样品含有来自所述人的白细胞;
体外使用对照刺激物刺激第二样品中的白细胞,其中所述第二样品含有来自所述人的白细胞;
刺激后,检测所述第一样品和第二样品中选自由肿瘤坏死因子亚家族(“TNFSF”)-2、TNFSF-5、TNFSF-6、TNFSF-14、趋化因子(C-C基序)配体(“CCL”)-2、CCL-3、CCL-4和趋化因子(C-X-C基序)配体(“CXCL”)-10所组成的组中的mRNA的量;
计算所述第一样品中所述mRNA的量与所述第二样品中所述mRNA的量的第一比例;
为所述人实施治疗;
体外刺激第三样品中的白细胞,其中所述第三样品含有从实施治疗后的人获得的白细胞;
体外使用对照刺激物刺激第四样品中的白细胞,其中所述第四样品含有从实施治疗后的人获得的白细胞;
刺激后,检测所述第三样品和所述第四样品中所述mRNA的水平;
计算所述第三样品中所述mRNA的量与所述第四样品中所述mRNA的量的第二比例;以及
比较所述第一比例和所述第二比例,其中所述比例的显著差别是有效治疗的指示。
10.根据权利要求9所述的方法,其中,刺激所述第一样品和第三样品中的白细胞包括将抗T细胞受体的抗体与所述样品混合。
11.根据权利要求9所述的方法,其中,刺激所述第一样品和第三样品中的白细胞包括将所述样品与选自由佛波醇-豆蔻酸酯-乙酸酯(PMA)、植物凝血素(PHA)、麦胚凝集素(WGA)、伴刀豆球蛋白-A(ConA)、脂多糖(LPS)、木菠萝凝集素、岩藻聚糖、热聚IgE、热聚IgA和热聚IgM所组成的组中的药物混合。
12.根据权利要求9所述的方法,其中,所述对照刺激物包括纯化的对照免疫球蛋白。
13.根据权利要求9所述的方法,其中,所述第一样品、第二样品、第三样品和第四样品中的至少一个含有全血。
14.根据权利要求9所述的方法,其中,所述比例的显著差别是所述第二比例高于所述第一比例,并且所述治疗包括使肿瘤坏死因子α失活。
15.根据权利要求14所述的方法,其中,所述治疗包括给药因福利美。
16.根据权利要求9所述的方法,其中,所述比例的显著差别是所述第一比例高于所述第二比例。
17.根据权利要求16所述的方法,其中,所述治疗包括给药选自由环孢霉素A和他克莫司所组成的组中的药物。
18.一种鉴定治疗克罗恩病的假定药物的方法,其包括:
获得第一样品、第二样品、第三样品和第四样品,其含有所述人的白细胞,其中在暴露到抗T细胞受体的抗体时,所述人的白细胞显示出选自由肿瘤坏死因子亚家族(“TNFSF”)-2、TNFSF-5、TNFSF-6、TNFSF-14、趋化因子(C-C基序)配体(“CCL”)-2、CCL-3、CCL-4和趋化因子(C-X-C基序)配体(“CXCL”)-10所组成的组中的mRNA转录提高至少1.7倍;
体外刺激所述第一样品中的白细胞;
体外使用对照刺激物刺激所述第二样品中的白细胞;
刺激后,检测所述第一样品和所述第二样品中所述mRNA的量;
计算所述第一样品中所述mRNA的量与所述第二样品中所述mRNA的量的第一比例;
将所述第三样品和第四样品暴露于所述药物;
暴露后,体外刺激所述第三样品中的白细胞;
暴露后,使用对照刺激物体外刺激所述第四样品中的白细胞;
刺激后,检测所述第三样品和所述第四样品中所述mRNA的水平;
计算所述第三样品中所述mRNA的量与所述第四样品中所述mRNA的量的第二比例;以及
比较所述第一比例和第二比例,其中所述比例的显著差别是假定药物的指示。
19.根据权利要求18所述的方法,其中,刺激所述第一和第三样品中的白细胞包括将抗T细胞受体的抗体与所述样品混合。
20.根据权利要求18所述的方法,其中,刺激所述第一和第三样品中的白细胞包括将样品与选自由佛波醇-豆蔻酸酯-乙酸酯(PMA)、植物凝血素(PHA)、麦胚凝集素(WGA)、伴刀豆球蛋白-A(ConA)、脂多糖(LPS)、木菠萝凝集素、岩藻聚糖、热聚IgE、热聚IgA和热聚IgM所组成的组中的药物混合。
21.根据权利要求18所述的方法,其中,所述对照刺激物包括纯化的对照免疫球蛋白。
22.根据权利要求18所述的方法,其中,所述第一样品、第二样品、第三样品和第四样品中的至少一个含有全血。
23.根据权利要求18所述的方法,其中,所述比例的显著差别是所述第一比例高于所述第二比例。
24.一种评估人的克罗恩病状态的方法,其包括:
体外刺激第一样品中的白细胞,其中,所述第一样品含有白细胞,并且是在第一时间从所述人获得的;
刺激后,检测所述第一样品中选自由肿瘤坏死因子亚家族(“TNFSF”)-2、TNFSF-5、TNFSF-6、TNFSF-14、趋化因子(C-C基序)配体(“CCL”)-2、CCL-3、CCL-4和趋化因子(C-X-C基序)配体(“CXCL”)-10所组成的组中的mRNA的量;
体外使用对照刺激物刺激第二样品中的白细胞,其中,所述第二样品含有在所述第一时间从所述人获得的白细胞;
刺激后,检测所述第二样品中所述mRNA的量;
确定所述第一样品中所述mRNA的量与所述第二样品中所述mRNA的量的第一比例;
体外刺激第三样品中的白细胞,其中所述第三样品含有白细胞,并且是在第一时间之后的第二时间从所述人获得的;
刺激后,检测所述第三样品中所述mRNA的量;
使用对照刺激物刺激第四样品中的白细胞,其中所述第四样品含有在所述第二时间从所述人获得的白细胞;
刺激后,检测所述第四样品中所述mRNA的量;
确定所述第三样品中所述mRNA的量与所述第四样品中所述mRNA的量的第二比例;以及
将第一比例和第二比例进行比较,其中,所述第一比例和第二比例的显著差别是疾病状态变化的指示。
25.根据权利要求24所述的方法,其中,刺激所述第一和第三样品中的白细胞包括将抗T细胞受体的抗体与所述样品混合。
26.根据权利要求24所述的方法,其中,刺激所述第一和第三样品中的白细胞包括将样品与选自由佛波醇-豆蔻酸酯-乙酸酯(PMA)、植物凝血素(PHA)、麦胚凝集素(WGA)、伴刀豆球蛋白-A(ConA)、脂多糖(LPS)、木菠萝凝集素、岩藻聚糖、热聚IgE、热聚IgA和热聚IgM所组成的组中的药物混合。
27.根据权利要求24所述的方法,其中,所述对照刺激物包括纯化的对照免疫球蛋白。
28.根据权利要求24所述的方法,其中,所述第一样品、第二样品、第三样品和第四样品中的至少一个含有全血。
29.根据权利要求24所述的方法,其中,所述比例的显著差别是所述第二比例高于所述第一比例,则所述疾病状态的变化是疾病的加重。
30.根据权利要求24所述的方法,其中,所述比例的显著差别是所述第一比例高于所述第二比例,则所述疾病状态的变化是疾病的消退。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US79035406P | 2006-04-07 | 2006-04-07 | |
| US60/790,354 | 2006-04-07 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN101410714A true CN101410714A (zh) | 2009-04-15 |
Family
ID=38581650
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CNA2007800115431A Pending CN101410714A (zh) | 2006-04-07 | 2007-04-05 | 在克罗恩病患者的外周血白细胞中T细胞受体介导的肿瘤坏死因子超家族与趋化因子mRNA增强的表达 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US7838239B2 (zh) |
| EP (1) | EP2005175B1 (zh) |
| JP (1) | JP5027209B2 (zh) |
| CN (1) | CN101410714A (zh) |
| AT (1) | ATE518011T1 (zh) |
| WO (1) | WO2007117611A2 (zh) |
Families Citing this family (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20080261207A1 (en) * | 2004-05-25 | 2008-10-23 | Masato Mitsuhashi | Method of Measuring Cancer Susceptibility |
| EP1802776B1 (en) * | 2004-10-20 | 2013-01-02 | Hitachi Chemical Company, Ltd. | Method for tailoring administration of drugs by quantitation of mrna |
| US11268149B2 (en) | 2004-12-08 | 2022-03-08 | Cedars-Sinai Medical Center | Diagnosis and treatment of inflammatory bowel disease |
| US10544459B2 (en) | 2004-12-08 | 2020-01-28 | Cedars-Sinai Medical Center | Methods of using genetic variants for the diagnosis and treatment of inflammatory bowel disease |
| EP1888089B9 (en) * | 2005-04-28 | 2012-08-08 | Hitachi Chemical Research Center, Inc. | Ex vivo gene expression in whole blood as a model of assessment of individual variation to dietary supplements |
| US8268566B2 (en) | 2006-04-07 | 2012-09-18 | Hitachi Chemical Research Center, Inc. | Enhanced FC receptor-mediated tumor necrosis factor superfamily MRNA expression in peripheral blood leukocytes in patients with rheumatoid arthritis |
| DE102006051628A1 (de) | 2006-11-02 | 2008-05-08 | Daimler Ag | Abgasturbolader für eine Brennkraftmaschine |
| US20100015156A1 (en) * | 2007-03-06 | 2010-01-21 | Cedars-Sinai Medical Center | Diagnosis of inflammatory bowel disease in children |
| US8486640B2 (en) | 2007-03-21 | 2013-07-16 | Cedars-Sinai Medical Center | Ileal pouch-anal anastomosis (IPAA) factors in the treatment of inflammatory bowel disease |
| EP2056110A1 (en) | 2007-10-31 | 2009-05-06 | Max-Planck-Gesellschaft zur Förderung der Wissenschaften e.V. | Biomarker for the prediction of responsiveness to an anti-tumour necrosis factor alpha (TNF) treatment |
| WO2010062960A2 (en) | 2008-11-26 | 2010-06-03 | Cedars-Sinai Medical Center | METHODS OF DETERMINING RESPONSIVENESS TO ANTI-TNFα THERAPY IN INFLAMMATORY BOWEL DISEASE |
| US9580752B2 (en) | 2008-12-24 | 2017-02-28 | Cedars-Sinai Medical Center | Methods of predicting medically refractive ulcerative colitis (MR-UC) requiring colectomy |
| SG189393A1 (en) * | 2010-11-11 | 2013-05-31 | Nestec Sa | Capsule, beverage production machine and system for the preparation of a nutritional product |
| US9902996B2 (en) | 2011-02-11 | 2018-02-27 | Cedars-Sinai Medical Center | Methods of predicting the need for surgery in crohn's disease |
| WO2013012947A1 (en) * | 2011-07-18 | 2013-01-24 | Hitachi Chemical Co., Ltd. | Methods of predicting host responsiveness to cancer immunotherapies by ex vivo induction of leukocyte-function-associated mrnas |
| CN112870368A (zh) | 2013-03-27 | 2021-06-01 | 西达-赛奈医疗中心 | 通过抑制tl1a的功能和相关信号传导途径来减轻并逆转纤维化和炎症 |
| EP3022295A4 (en) | 2013-07-19 | 2017-03-01 | Cedars-Sinai Medical Center | Signature of tl1a (tnfsf15) signaling pathway |
| CN103865998B (zh) * | 2013-12-16 | 2016-04-20 | 周菊华 | 一种肿瘤免疫治疗效果的基因检测方法 |
| US20150257586A1 (en) * | 2014-03-11 | 2015-09-17 | Starbucks Corporation Dba Starbucks Coffee Company | Single-serve beverage production machine |
| US11028443B2 (en) | 2015-08-31 | 2021-06-08 | Showa Denko Materials Co., Ltd. | Molecular methods for assessing urothelial disease |
| WO2017161342A1 (en) | 2016-03-17 | 2017-09-21 | Cedars-Sinai Medical Center | Methods of diagnosing inflammatory bowel disease through rnaset2 |
Family Cites Families (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4925572A (en) | 1987-10-20 | 1990-05-15 | Pall Corporation | Device and method for depletion of the leukocyte content of blood and blood components |
| US4880548A (en) | 1988-02-17 | 1989-11-14 | Pall Corporation | Device and method for separating leucocytes from platelet concentrate |
| US5210015A (en) | 1990-08-06 | 1993-05-11 | Hoffman-La Roche Inc. | Homogeneous assay system using the nuclease activity of a nucleic acid polymerase |
| US5491063A (en) | 1994-09-01 | 1996-02-13 | Hoffmann-La Roche Inc. | Methods for in-solution quenching of fluorescently labeled oligonucleotide probes |
| PT938320E (pt) | 1996-03-26 | 2010-09-22 | Michael S Kopreski | Método que permite a utilização de arn extracelular extraído de plasma ou de soro para detectar, monitorizar ou avaliar o cancro |
| US5683698A (en) | 1996-08-02 | 1997-11-04 | New England Deaconess Hospital | Formulation for alleviating symptoms associated with arthritis |
| US7514232B2 (en) | 1996-12-06 | 2009-04-07 | Becton, Dickinson And Company | Method for detecting T cell response to specific antigens in whole blood |
| US6183951B1 (en) * | 1997-04-11 | 2001-02-06 | Prometheus Laboratories, Inc. | Methods of diagnosing clinical subtypes of crohn's disease with characteristic responsiveness to anti-Th1 cytokine therapy |
| US20020006613A1 (en) | 1998-01-20 | 2002-01-17 | Shyjan Andrew W. | Methods and compositions for the identification and assessment of cancer therapies |
| US6646013B1 (en) | 1999-06-15 | 2003-11-11 | Nutri-Logics | Nutrient formulations for disease reduction |
| US6692916B2 (en) | 1999-06-28 | 2004-02-17 | Source Precision Medicine, Inc. | Systems and methods for characterizing a biological condition or agent using precision gene expression profiles |
| US20020048566A1 (en) | 2000-09-14 | 2002-04-25 | El-Deiry Wafik S. | Modulation of cellular apoptosis and methods for treating cancer |
| US7374881B2 (en) * | 2000-10-31 | 2008-05-20 | Hitachi Chemical Research Center, Inc. | Method for collecting and using nuclear mRNA |
| US20020182274A1 (en) | 2001-03-21 | 2002-12-05 | Kung-Ming Lu | Methods for inhibiting cancer growth, reducing infection and promoting general health with a fermented soy extract |
| US6905827B2 (en) * | 2001-06-08 | 2005-06-14 | Expression Diagnostics, Inc. | Methods and compositions for diagnosing or monitoring auto immune and chronic inflammatory diseases |
| US6964850B2 (en) * | 2001-11-09 | 2005-11-15 | Source Precision Medicine, Inc. | Identification, monitoring and treatment of disease and characterization of biological condition using gene expression profiles |
| US7767390B2 (en) | 2001-11-20 | 2010-08-03 | Oncomedx, Inc. | Methods for evaluating drug-resistance gene expression in the cancer patient |
| US7871619B2 (en) | 2001-11-30 | 2011-01-18 | Chemocentryx, Inc. | Compositions and methods for detecting and treating diseases and conditions related to chemokine receptors |
| FI20020078A (fi) | 2002-01-15 | 2003-07-16 | Danisco | Immuunijärjestelmän stimulointi polydextroosilla |
| US6878518B2 (en) | 2002-01-22 | 2005-04-12 | The Trustees Of The University Of Pennsylvania | Methods for determining steroid responsiveness |
| US7745180B2 (en) | 2002-04-24 | 2010-06-29 | Hitachi Chemical Co., Ltd. | Device and method for high-throughput quantification of mRNA from whole blood |
| EP1507548B1 (en) | 2002-05-27 | 2014-10-01 | CanImGuide Therapeutics AB | Method for determining immune system affecting compounds |
| AU2002953533A0 (en) | 2002-12-24 | 2003-01-16 | Arthron Limited | Fc receptor modulating compounds and compositions |
| US20080261207A1 (en) | 2004-05-25 | 2008-10-23 | Masato Mitsuhashi | Method of Measuring Cancer Susceptibility |
| EP1875246B1 (en) | 2005-04-15 | 2016-10-05 | CanImGuide Therapeutics AB | Diagnostic method for detecting cancer by measuring amount of a cytokine like il-6 |
| EP1888089B9 (en) | 2005-04-28 | 2012-08-08 | Hitachi Chemical Research Center, Inc. | Ex vivo gene expression in whole blood as a model of assessment of individual variation to dietary supplements |
| CA2624359A1 (en) | 2005-09-27 | 2007-04-05 | Source Mdx | Gene expression profiling for identification monitoring and treatment of rheumatoid arthritis |
| US20100190162A1 (en) | 2007-02-26 | 2010-07-29 | Cedars-Sinai Medical Center | Methods of using single nucleotide polymorphisms in the tl1a gene to predict or diagnose inflammatory bowel disease |
-
2007
- 2007-04-05 US US12/296,425 patent/US7838239B2/en not_active Expired - Fee Related
- 2007-04-05 EP EP07755012A patent/EP2005175B1/en not_active Not-in-force
- 2007-04-05 WO PCT/US2007/008597 patent/WO2007117611A2/en active Application Filing
- 2007-04-05 AT AT07755012T patent/ATE518011T1/de not_active IP Right Cessation
- 2007-04-05 CN CNA2007800115431A patent/CN101410714A/zh active Pending
- 2007-04-05 JP JP2009504317A patent/JP5027209B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| ATE518011T1 (de) | 2011-08-15 |
| EP2005175A2 (en) | 2008-12-24 |
| US20090253133A1 (en) | 2009-10-08 |
| US7838239B2 (en) | 2010-11-23 |
| EP2005175B1 (en) | 2011-07-27 |
| WO2007117611A2 (en) | 2007-10-18 |
| JP5027209B2 (ja) | 2012-09-19 |
| EP2005175A4 (en) | 2009-06-03 |
| WO2007117611A3 (en) | 2008-08-07 |
| JP2009535016A (ja) | 2009-10-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN101410714A (zh) | 在克罗恩病患者的外周血白细胞中T细胞受体介导的肿瘤坏死因子超家族与趋化因子mRNA增强的表达 | |
| Sonkoly et al. | IL-31: a new link between T cells and pruritus in atopic skin inflammation | |
| Dos Santos et al. | DNA microarray analysis of gene expression in alveolar epithelial cells in response to TNFα, LPS, and cyclic stretch | |
| de Alcantara et al. | Cytokines in psoriasis | |
| Kunz et al. | Cytokines and cytokine profiles in human autoimmune diseases and animal models of autoimmunity | |
| Mizwicki et al. | Tocilizumab attenuates inflammation in ALS patients through inhibition of IL6 receptor signaling | |
| JP7431812B2 (ja) | 自己免疫疾患における新規な遺伝子分類とその使用 | |
| US8268566B2 (en) | Enhanced FC receptor-mediated tumor necrosis factor superfamily MRNA expression in peripheral blood leukocytes in patients with rheumatoid arthritis | |
| JP5706913B2 (ja) | 攻撃的及び防御的免疫マーカーのexvivo誘導により宿主免疫機能を特徴付けるための方法 | |
| Meugnier et al. | Gene expression profiling in peripheral blood cells of patients with rheumatoid arthritis in response to anti-TNF-α treatments | |
| Shi et al. | Gene expression profiles of peripheral blood monocytes in osteoarthritis and analysis of differentially expressed genes | |
| Hatami et al. | STAT5a and STAT6 gene expression levels in multiple sclerosis patients | |
| Stone et al. | Genomic responses during acute human anaphylaxis are characterized by upregulation of innate inflammatory gene networks | |
| Edwards III et al. | Combined anti-tumor necrosis factor-α therapy and DMARD therapy in rheumatoid arthritis patients reduces inflammatory gene expression in whole blood compared to DMARD therapy alone | |
| Zhang et al. | Identification of key genes and pathways contributing to artery tertiary lymphoid organ development in advanced mouse atherosclerosis | |
| US20090311684A1 (en) | Enhanced fc receptor-mediated tumor necrosis factor superfamily and chemokine mrna expression in peripheral blood leukocytes in patients with rheumatoid arthritis | |
| Mrazek et al. | Expression of the chemokine PARC mRNA in bronchoalveolar cells of patients with sarcoidosis | |
| Lu et al. | Identification of key genes and pathways in Rheumatoid Arthritis gene expression profile by bioinformatics. | |
| Mitsuhashi | Ex vivo simulation of leukocyte function: stimulation of specific subset of leukocytes in whole blood followed by the measurement of function-associated mRNAs | |
| Hamed et al. | Association of interleukin-6 and its-174G/C promoter polymorphism with clinical and laboratory characteristics of non hepatitis C virus rheumatoid arthritis patients | |
| AU2011268223A1 (en) | Method for predicting a therapy response in subjects with multiple sclerosis | |
| Pelosof et al. | Co‐ordinate but disproportionate activation of apoptotic, regenerative and inflammatory pathways characterizes the liver response to acute amebic infection | |
| US20130084577A1 (en) | Methods of characterizing host responsiveness to interferon by ex vivo induction of interferon-responsive markers | |
| Robinson | Transcriptomic evaluation of necrotizing meningoencephalitis and granulomatous meningoencephalomyelitis in dogs | |
| Chen et al. | Pilot Analyses of Interferon Subtype Expression Profiles in Patients with Herpes Zoster or Postherpetic Neuralgia |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C02 | Deemed withdrawal of patent application after publication (patent law 2001) | ||
| WD01 | Invention patent application deemed withdrawn after publication |
Application publication date: 20090415 |