BE1019340A3 - Procede pour nucleer et accelerer la cristallisation du polylactide. - Google Patents
Procede pour nucleer et accelerer la cristallisation du polylactide. Download PDFInfo
- Publication number
- BE1019340A3 BE1019340A3 BE2010/0298A BE201000298A BE1019340A3 BE 1019340 A3 BE1019340 A3 BE 1019340A3 BE 2010/0298 A BE2010/0298 A BE 2010/0298A BE 201000298 A BE201000298 A BE 201000298A BE 1019340 A3 BE1019340 A3 BE 1019340A3
- Authority
- BE
- Belgium
- Prior art keywords
- polylactide
- urethane
- weight
- matrix
- configuration
- Prior art date
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L67/00—Compositions of polyesters obtained by reactions forming a carboxylic ester link in the main chain; Compositions of derivatives of such polymers
- C08L67/04—Polyesters derived from hydroxycarboxylic acids, e.g. lactones
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08J—WORKING-UP; GENERAL PROCESSES OF COMPOUNDING; AFTER-TREATMENT NOT COVERED BY SUBCLASSES C08B, C08C, C08F, C08G or C08H
- C08J5/00—Manufacture of articles or shaped materials containing macromolecular substances
- C08J5/18—Manufacture of films or sheets
-
- D—TEXTILES; PAPER
- D01—NATURAL OR MAN-MADE THREADS OR FIBRES; SPINNING
- D01F—CHEMICAL FEATURES IN THE MANUFACTURE OF ARTIFICIAL FILAMENTS, THREADS, FIBRES, BRISTLES OR RIBBONS; APPARATUS SPECIALLY ADAPTED FOR THE MANUFACTURE OF CARBON FILAMENTS
- D01F6/00—Monocomponent artificial filaments or the like of synthetic polymers; Manufacture thereof
- D01F6/58—Monocomponent artificial filaments or the like of synthetic polymers; Manufacture thereof from homopolycondensation products
- D01F6/62—Monocomponent artificial filaments or the like of synthetic polymers; Manufacture thereof from homopolycondensation products from polyesters
- D01F6/625—Monocomponent artificial filaments or the like of synthetic polymers; Manufacture thereof from homopolycondensation products from polyesters derived from hydroxy-carboxylic acids, e.g. lactones
-
- D—TEXTILES; PAPER
- D01—NATURAL OR MAN-MADE THREADS OR FIBRES; SPINNING
- D01F—CHEMICAL FEATURES IN THE MANUFACTURE OF ARTIFICIAL FILAMENTS, THREADS, FIBRES, BRISTLES OR RIBBONS; APPARATUS SPECIALLY ADAPTED FOR THE MANUFACTURE OF CARBON FILAMENTS
- D01F6/00—Monocomponent artificial filaments or the like of synthetic polymers; Manufacture thereof
- D01F6/88—Monocomponent artificial filaments or the like of synthetic polymers; Manufacture thereof from mixtures of polycondensation products as major constituent with other polymers or low-molecular-weight compounds
- D01F6/92—Monocomponent artificial filaments or the like of synthetic polymers; Manufacture thereof from mixtures of polycondensation products as major constituent with other polymers or low-molecular-weight compounds of polyesters
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08J—WORKING-UP; GENERAL PROCESSES OF COMPOUNDING; AFTER-TREATMENT NOT COVERED BY SUBCLASSES C08B, C08C, C08F, C08G or C08H
- C08J2367/00—Characterised by the use of polyesters obtained by reactions forming a carboxylic ester link in the main chain; Derivatives of such polymers
- C08J2367/04—Polyesters derived from hydroxy carboxylic acids, e.g. lactones
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L75/00—Compositions of polyureas or polyurethanes; Compositions of derivatives of such polymers
- C08L75/04—Polyurethanes
- C08L75/06—Polyurethanes from polyesters
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Textile Engineering (AREA)
- Health & Medical Sciences (AREA)
- General Chemical & Material Sciences (AREA)
- Polymers & Plastics (AREA)
- Organic Chemistry (AREA)
- Manufacturing & Machinery (AREA)
- Materials Engineering (AREA)
- Polyurethanes Or Polyureas (AREA)
- Polyesters Or Polycarbonates (AREA)
- Biological Depolymerization Polymers (AREA)
Abstract
La présente invention se réfère à un procédé pour accélérer la cristallisation du polylactide, caractérisé en ce qu'il comprend l'incorporation dans le polylactide, d'un polyester-uréthane. L'invention se réfère aussi à une composition de polylactide caractérisée en ce qu'elle comprend un polylactide et un polyester-uréthane. L'invention se réfère également à un procédé de fabrication d'un article au départ de ladite compostition ainsi qu'à un article susceptible d'être obtenu par le procédé.
Description
Procédé pour nucléer et accélérer la cristallisation du polvlactide 1. Domaine technique de l'invention : L'invention se rapporte à un procédé pour accélérer la cristallisation du polylactide (PLA), soit du poly-L-lactide (PLLA), soit du poly-D-lactide (PDLA). Le procédé de l'invention se rapporte en particulier à l'utilisation d'un polyester-uréthane obtenu par extension de chaînes de poly-L-lactide ou de poly-D-lactide, oligomère hydroxytéléchélique, par réaction avec des diisocyanates et des allongeurs de chaînes diamine ou dialcool, comme agent accélérateur de cristallisation, ou plus couramment agent nucléant.
2. Etat de la technique :
La faible vitesse de cristallisation du polylactide constitue dans de nombreuses applications potentielles un inconvénient majeur.
L'état de la technique montre, notamment dans les documents suivants : M.Spinu et al ; J.M.S. Pure Appl. Chem. A33(10), 1996 ; H.Li,M. Huneault ; Polymer 48 (2007) 6855-6866 ; M.Salmeron Sanchez et al. ; Macromolecules (2007) 7989-7997 ; H. Tsuji, Y. Itikata ; Polymer 36(14)(1995) 2709-2716 ; M.L. Di Lorenzo ; Eur. Pol. J. 41(2005) 569-575 ; J.Y. Nam et al, ; Polymer 47(2006)1340-1347 ; US200601422505 ; que de nombreux travaux de recherche ont été effectués afin d'accélérer cette cristallisation, soit en favorisant la mobilité des chaînes par l'ajout de plastifiant, soit en favorisant la nucléation de ia cristallisation par ajout de charges, notamment des charges minérales comme le talc ou la montmorillonite, le talc s'étant avéré la charge minérale nucléante la plus efficace mais sans pour autant être totalement satisfaisante du fait notamment que l'additivation par des charges minérales nécessite l'incorporation de quantités importantes de cette charge, qui nuisent aux propriétés optiques du PLA.
On a également proposé la voie de la plastification, mais, si elle permet d'accélérer la cristallisation, elle conduit à une diminution de la température de transition vitreuse, et peut être confrontée à des problèmes d'exsudation du plastifiant hors de la matrice. Les plastifiants les plus souvent mentionnés pour le PLA sont à base de polyéthylèneglycol (PEG). De plus, à l'heure actuelle, et ce quelle que soit la voie choisie, on utilise des additifs d'origine non-renouvelable, ce qui nuit à la valeur ajoutée environnementale du PLA.
Par ailleurs, il est connu depuis plusieurs années que l'association des chaînes de PLLA (poly-L-lactide) et de PDLA (poly-D-lactide) génère des cristaux stéréocomplexes dont la température de complexation et de fusion (> 210 °C) est supérieure de plusieurs dizaines de degrés à la température de fusion des cristaux d'un homopolymère PLLA ou PDLA (< 170 °C). Les stéréocomplexes ont été la plupart du temps étudiés pour leurs propriétés intrinsèques, dans des mélanges équipondérés ou proches de l'équipondération. Cependant, on a déjà décrit dans quelques articles récents, notamment dans H. Yamane, K. Sasai ; Polymer 44 (2003) 2569-2575 ; S.C. Schmidt, M.A. Hillmyer ; J. Pol Sei. Part B : Polym. Phys 39(2001) 300-313 et K.S. Anderson, M.A. Hillmyer ; Polymer 47(2006) 2030-2035 que l'incorporation d'une faible fraction de PDLA (< à 10 % en poids) dans le PLLA permettait la formation de cristaux stéréocomplexes dispersés dans la matrice PLLA qui favorisent la nucléation de l'homocristallisation de cette matrice ; cependant, cette utilisation conduit à de mauvaises propriétés mécaniques de la matrice PLLA.
De plus, les compositions existantes ne présentent que des temps de demi-cristallisation élevés, ce qui conduit à obtenir un polylactide sous sa forme amorphe.
Il existe donc un besoin pour un procédé qui permette d'accélérer la cristallisation du PLA, soit PLLA, soit PDLA, sans rencontrer les inconvénients des solutions connues à ce jour. L e procédé de la présente invention a donc pour but de remédier aux inconvénients mentionnés ci-dessus.
3. Buts de l'invention :
Un des objets du procédé de l'invention est d'utiliser un accélérateur de cristallisation du PLA, soit PLLA, soit PDLA, ou agent nucléant, qui soit issu de ressources renouvelables et présentant une efficacité telle que le temps de demi-cristallisation soit réduit d'au moins 40 % par rapport à celui des meilleures compositions de polylactide existantes.
Un autre objet du procédé de l'invention est d'utiliser un accélérateur de cristallisation ou agent nucléant du PLA, soit PLLA, soit PDLA, en quantités faibles, ne dépassant pas 20 %, et de préférence pas 10 %, en poids par rapport au poids total du mélange agent nucléant et PLA (soit PLLA, soit PDLA).
4. Description détaillée de l'invention :
La présente invention fournit un procédé pour accélérer la cristallisation du polylactide de masse molaire moyenne en nombre comprise entre 30.000 et 200.000 g/mol, caractérisé en ce que l'on incorpore dans ledit polylactide, appelé matrice polylactide, de configuration soit L, soit D, à une température comprise entre 160 °C et 250 °C, de 1 à 20 % en poids par rapport au poids total du mélange, un copolymère de polylactide-uréthane dont la configuration du polylactide est l'inverse de celle de la matrice polylactide.
Dans la présente invention, on entend par matrice polylactide de configuration L, un polymère dans lequel la majorité des unités répétitives sont des monomères de L-lactide (PLLA) et par matrice polylactide de configuration D, un polymère dans lequel la majorité des unités répétitives sont des monomères de D-lactide (PDLA).
Dans la présente invention, on entend par copolymère de polylactide-uréthane dont la configuration du polylactide est l'inverse de celle de la matrice polylactide, un copolymère polylactide-uréthane obtenu par exemple au départ d'un PLLA par réaction avec un diisocyanate en présence d'une diamine ou d'un dialcool alors que la matrice polylactide est un PDLA ou un copolymère polylactide-uréthane obtenu par exemple au départ d'un PDLA par réaction avec un diisocyanate en présence d'une diamine ou d'un dialcool alors que la matrice polylactide est un PLLA.
Suivant un mode de réalisation, la matrice polylactide est de configuration L et le copolymère polylactide-uréthane est obtenu par réaction d'un polylactide de configuration D avec un disocyanate en présence d'une diamine ou d'un diaclool.
Suivant un autre mode de réalisation, la matrice polylactide est de configuration D et le copolymère polylactide-uréthane est obtenu par réaction d'un polylactide de configuration L avec un disocyanate en présence d'une diamine ou d'un dialcool.
La Demanderesse a trouvé, d'une manière inattendue, que l'incorporation de polylactide-uréthane obtenu par réaction de PDLA ou de PLLA préférentiellement de masse molaire moyenne en nombre comprise entre 1.000 et 40.000 g/mol), avec un disocyanate, dans respectivement du PLLA ou du PDLA, permettait d'accélérer la cristallisation de ce PLLA ou PDLA et de répondre ainsi aux besoins énoncés ci-dessus.
De plus, et contrairement à l'enseignement de l'état de la technique, la Demanderesse a maintenant trouvé de manière inattendue que d'une part l'addition d'un poly-D-lactide-uréthane (PDEU) comme agent permettant d'accélérer la cristallisation, dans une matrice PLLA et que d'autre part, l'addition d'un poly-L-lactide-uréthane (PLEU) comme agent permettant d'accélérer la cristallisation, dans une matrice PDLA permettait d'améliorer significativement les propriétés mécaniques respectives des matrices PLLA et PDLA.
La présente invention fournit également une composition de polylactide caractérisée en ce qu'elle comprend de 80 à 99 % en poids de polylactide de masse molaire moyenne en nombre comprise entre 30.000 et 200.000 g/mol, de configuration soit L, soit D, appelé matrice polylactide, et de 1 à 20 % en poids par rapport au poids total de la composition, d'un copolymère polylactide-uréthane dont la configuration du polylactide est l'inverse de celle de la matrice polylactide. Ces compositions se caractérisent par une réduction du temps de demi-cristallisation d'au moins 40 % par rapport à celui des meilleures compositions de PLLA ou PDLA existantes.
La présente invention se réfère également à un procédé de fabrication d'un article caractérisé en ce qu'il comprend la transformation par thermoformage, injection ou extrusion de la composition selon l'invention.
La présente invention se réfère aussi à un article susceptible d'être obtenu selon le procédé de l'invention. L'article peut être un film ou une fibre.
4.1 Obtention de l'additif :
Comme polylactide-uréthane que l'on peut utiliser dans le procédé de l'invention, on peut notamment citer ceux décrits dans le document W02008/037773.
L'additif destiné à nucléer et à accélérer la cristallisation de la matrice PLLA ou PDLA est respectivement un poly-D-lactide-uréthane (PDEU) ou un poly-L-lactide-uréthane (PLEU) élaboré de la manière annoncée précédemment, c'est-à-dire à partir d'un PDLA ou PLLA, oligomère hydroxytéléchélique, présentant préférentiellement une tacticité comprise entre 90 et 100 %, plus préférentiellement entre 95 et 100 %, et préférentiellement une masse molaire moyenne en nombre comprise entre 1.000 et 40.000 g/mol, plus préférentiellement entre 5.000 et 20.000 g/mol.
Le PDEU et le PLEU sont obtenus respectivement à partir de PDLA et de PLLA par une réaction d'extension de chaîne impliquant des diisocyanates aromatiques ou aliphatiques et des diamines ou des dialcools aromatiques ou aliphatiques comme décrit notamment dans les documents W02008/037773 et W02008/037772.
4.2 Composition des formulations :
Bien que l'on puisse ajouter l'agent nucléant du procédé de l'invention à n'importe quel type de PLA, on a cependant remarqué que de meilleurs résultats étaient obtenus lorsque la matrice utilisée est un PLLA ou un PDLA présentant préférentiellement une tacticité comprise entre 90 et 100 %, plus préférentiellement entre 95 et 100 % et une masse molaire moyenne en nombre préférentiellement comprise entre 30.000 et 200.000 g/mol, plus préférentiellement entre 50.000 et 175.000 g/mol, encore plus préférentiellement entre 70.000 et 150.000 g/mol.
On incorpore alors, selon le procédé de l'invention l'additif polylactide-uréthane destiné à nucléer et à accélérer la cristallisation du polylactide à la matrice de PLA à hauteur de 1 à 20 % en poids, préférentiellement à hauteur de 2 à 10 % en poids, plus préférentiellement à hauteur de 3 à 10 % en poids par rapport au poids total du mélange polylactide et polylactide-uréthane. Pour des taux d'incorporation inférieurs à 1 %, l'efficacité de l'additif polylactide-uréthane en tant que promoteur de la nucléation et de la cristallisation du polylactide ne s'exprime pas de manière significative. Pour des taux d'incorporation supérieurs à 20 %, l'efficacité de l'additif polylactide-uréthane en tant que promoteur de la nucléation et de la cristallisation du polylactide reste avérée, mais la fraction stéréocomplexée prend une importance non négligeable, voire prépondérante, au regard de la fraction homocristalline, ce qui conduit à un matériau aux propriétés significativement différentes de celles de la matrice. Les formulations de polylactide à vitesse de cristallisation accélérée peuvent également contenir d'autres additifs, tels que ceux habituellement utilisés pour modifier les propriétés mécaniques, thermiques ou optiques des polyesters, par exemple des plastifiants, des charges minérales, des colorants, des stabilisants, des fibres ou des agents d'aide à la mise en oeuvre, cette liste ne devant pas être considérée comme exhaustive.
4.3 Incorporation de l'additif : L'incorporation de l'additif polylactide-uréthane dans la matrice polylactide peut se faire à l'état fondu, dans un mélangeur interne ou dans une extrudeuse. La température de mise en œuvre du mélange doit être supérieure à la température de fusion de la matrice polylactide, et de préférence supérieure à la température de fusion du stéréocomplexe formé par une fraction de la matrice polylactide et tout ou partie de l'additif polyester-uréthane. Le mélange se fait à une température comprise entre 160 et 250 °C, préférentiellement entre 180 et 230 °C, plus préférentiellement entre 200 et 230 °C.
D'autres ingrédients tels que des antioxydants, colorants, anti-UV, anti-feux et autres analogues peuvent être incorporés à la matrice polylactide lors de l'étape d'incorporation de l'additif polylactide-uréthane ou lors d'une ou plusieurs étapes supplémentaires de formulation, cette ou ces étapes pouvant être réalisées avant ou après l'incorporation de l'additif polyester-uréthane.
Le polylactide et l'additif polylactide-uréthane destiné à nucléer et accélérer sa cristallisation peuvent également être mélangés suivant des modes opératoires différents, comme par exemple par dissolution sous agitation des constituants dans un solvant, par exemple le chloroforme, le toluène, le dichlorométhane, le p-xylène, le dioxane ou l'acétonitrile, suivie d'une évaporation du solvant.
4.4 Synthèse de l'additif :
Le copolymère de poly-D-lactide-uréthane ou de poly-L-lactide-uréthane peut être obtenu par le procédé décrit dans le document W02008/037773.
4.5 Avantages apportés par l'invention :
Le procédé de l'invention, par incorporation de l'additif polylactide-uréthane, permet, à la différence de l'incorporation de la plupart des autres additifs connus aujourd'hui pour cet usage, d'améliorer la nucléation (e.g. charges minérales) ou d'accélérer la cristallisation (e.g. plastifiants) du PLA de manière significative et plus particulièrement de manière à réduire le temps de demi-cristallisation d'au moins 40 % par rapport à celui des compositions de polylactide existantes; de plus le polylactide-uréthane du procédé de l'invention présente l'avantage d'être d'origine renouvelable.
L'additif polylactide-uréthane est un additif de haute masse molaire, qui ne présente donc pas le risque de diminuer les propriétés mécaniques de la matrice PLA ou de favoriser leur détérioration, contrairement à un PDLA de faible masse molaire incorporé dans une matrice PLLA ou un PLLA de faible masse molaire incorporé dans une matrice PDLA. Enfin, l'additif polylactide-uréthane présente, une grande efficacité de nucléation et d'accélération de la cristallisation pour une gamme élargie, en termes de tacticité et de masse molaire moyenne en nombre, de polylactide, là où l'utilisation de PDLA dans une matrice PLLA ou l'utilisation de PLLA dans une matrice PDLA semble nécessiter, d'après la littérature, une optimisation au moins en termes de masse molaire moyenne en nombre dès lors que la nature de la matrice en termes de masse molaire ou de tacticité est modifiée.
5. Exemples :
Exemple 1
Pour la préparation du film de cet exemple, on a utilisé un PLLA commercial de grande pureté optique, le PLA NatureWorks 6201D, qui présente une tacticité de 95% et une masse molaire moyenne en nombre de 93.000 g/mol. Ce PLLA a d'abord subi une étape de précipitation par dissolution dans du chloroforme puis précipitation par addition goutte-à-goutte de méthanol. Après filtration et séchage, le PLLA ainsi obtenu est nommé PLLA-X.
Le PDEU utilisé dans cet exemple est dénommé VALI B140. Il est obtenu par extension de chaîne en mini-extrudeuse au départ d'un PDLA α,ω-dihydroxylé, amorcé par le 1,4-butanediol et stabilisé à l'aide de 0,3 % d'Ultranox 626, de masse moléculaire apparente en standard polystyrène de 7.600 g/mol. Celui-ci est mélangé dans un bêcher à l'aide d'une spatule avec l'agent d'extension de chaîne, c'est-à-dire le 4,4'-méthylène diphénylisocyanate (MDI), et le composé difonctionnel, c'est-à-dire le 4,4'-diaminodiphénylméthane (MDA), ainsi qu'une quantité supplémentaire d'Ultranox 626 à raison de 0,3 % en poids, juste avant introduction dans la mini-extrudeuse. Il est à noter que le PDLA(OH)2 utilisé n'a pas été purifié préalablement et contient donc encore du Sn(Oct)2/PPh3, celui-ci étant également le catalyseur de la réaction d'extension de chaîne. L'introduction du mélange est effectuée à une vitesse de 30 tours/min, avant d'augmenter celle-ci à 75 tours/min. Le temps réactionnel est pris en compte dès que l'introduction de la matière est terminée et est de 5 minutes. La température de mise en œuvre est de 160 °C. Le rapport PLA/composé difonctionnel a été fixé à 60/40 mol/mol et le rapport [NCO] / [OHPLa+NH2] à 1,1.
Le PDLA(OH)2 utilisé (VALI B133b) pour la synthèse de ce PDEU est obtenu par polymérisation du D,D-LA à 160 °C dans un réacteur en verre en présence d'Ultranox 626 comme stabilisant, de 1,4-butanediol comme amorceur et d'un mélange d'octoate d'étain et de triphénylphosphine (1:1 équimolaire) comme solution catalytique dans le toluène. Le lactide, ainsi que l'Ultranox 626 à raison de 0,3 % en poids, sont introduits dans le réacteur sous atmosphère inerte. Le milieu est thermostatisé à 160 °C sous agitation de 50 tours/min à l'aide d'une pâle agitatrice. Lorsque tout le lactide est fondu, on ajoute l'amorceur dans le réacteur, ainsi que la solution catalytique SntOctVPPhs. La polymérisation est arrêtée après 30 min. Le polymère obtenu est dissous dans du chloroforme, précipité dans 10 volumes de méthanol froid, filtré et séché à l'étuve sous vide à 40 °C. Il est à noter que le 1,4-butanediol a été séché sür tamis moléculaire (4Â) durant 48 heures et la triphénylphosphine recristallisée dans l'éther avant d'être séchée par 3 distillations azéotropiques successives au toluène pour être finalement mise en solution dans du toluène sec avec l'octoate d'étain. Afin d'effectuer la caractérisation par chromatographie d'exclusion stérique, le polymère obtenu est débarrassé de ses résidus catalytiques par extraction liquide-liquide. Celui-ci est dissous dans le chloroforme à raison de 1 g de polymère dans 4 ml de chloroforme. Le catalyseur est extrait au moyen d'une solution d'HCI 0,1M d'un volume équivalent. La phase organique est ensuite lavée deux fois par de l'eau déminéralisée. Enfin, le polymère est précipité dans 10 volumes de méthanol, filtré et séché à l'étuve sous vide à 40 °C. Le degré de polymérisation visé de l'échantillon VALI B133b est de 70, pour une masse théorique de 9.600 g/mol. La masse moléculaire apparente en standard polystyrène déterminée par chromatographie d'exclusion stérique est de 18.700 g/mol.
Conformément au procédé de l'invention, on a incorporé 5% en poids de PDEU VALI B140 dans 95 % en poids de PLLA-X. On a dissous 2 g de ce mélange dans 40 ml de chloroforme. Après dissolution complète, le solvant est évaporé à l'air libre, puis pendant une nuit dans une étuve à 50 °C sous vide de pompe à palettes et on a récupéré le film ainsi formé. Ce film sera soumis à un traitement thermique comme décrit ci-après.
Exemple 2 :
On a procédé comme dans l'exemple 1 pour préparer un film contenant 95 % en poids d'un PLLA de très grande pureté optique et 5 % en poids d'un additif polyester-uréthane PDEU.
Cependant, cette fois on a utilisé un PLLA de très grande pureté optique obtenu par un procédé de synthèse par extrusion réactive à partir de L-lactide (L-L-LA). Il présente une tacticité de 99.8 % et une masse molaire moyenne en nombre de 71.000 g/mol. Après une précipitation suivant le mode opératoire décrit à l'exemple 1 pour le cas du PLLA-X, le PLLA précipité est nommé A36.
Le PDEU utilisé dans cet exemple est le PDEU VALI B140, dont l'obtention est décrite dans l'exemple 1.
Le film ainsi obtenu sera soumis à un traitement thermique comme décrit ci-dessous Exemple comparatif 1 :
On a préparé un film comme décrit à l'exemple 1, avec le seul PLLA-X et sans y incorporer quoi que ce soit. Le film obtenu sera soumis à un traitement thermique comme décrit ci-dessous.
Exemple comparatif 2 :
On a préparé un film comme décrit à l'exemple 1 et avec le seul PLLA A36 et sans y incorporer quoi que ce soit. Le film obtenu sera soumis à un traitement thermique comme décrit ci-dessous.
Exemple comparatif 3 :
On a préparé un film comme décrit à l'exemple 1 au départ de 95 % en poids de PLLA-X auquel on a incorporé, 5 % en poids d'un additif PDLA LMW de très grande pureté optique et de basse masse moléculaire élaboré par le procédé décrit dans l'exemple 1. Le PDLA LMW utilisé est le PDLA VALI B133b, qui a servi de base à la synthèse du PDEU VALI B140 et dont l'obtention est décrite dans l'exemple 1.
Exemple comparatif 4 :
On a préparé un film comme décrit à l'exemple 1 au départ de 95 % en poids de PLLA-X auquel on a incorporé, 5 % en poids d'un additif PDLA HMW de très grande pureté optique et de haute masse moléculaire élaboré par le procédé décrit dans l'exemple 1. Le PDLA HMW utilisé est obtenu par polymérisation d'ouverture de cycle de D-lactide (D-D-LA) réalisée en ampoule scellée à 180 °C pendant 45 min amorcée par le 1-heptanol et catalysée par le système catalytique octoate d'étain/triphénylphoshine 1/1 mol/mol. Le PDLA ainsi obtenu est solubilisé dans le chloroforme et reprécipité dans le méthanol afin d'éliminer le monomère résiduel. Il présente une masse moléculaire moyenne en nombre de 96.000 g/mol mesurée par chromatographie d'exclusion stérique (SEC) relative à des standards de polystyrène et est dénommé EMDU D42b.
Le film obtenu sera soumis à un traitement thermique comme décrit ci-dessous. Exemple comparatif 5 :
On a préparé un film comme décrit à l'exemple 1 au départ de 95 % en poids de PLLA A36 auquel on a incorporé 5 % en poids d'un additif PDLA LMW de très grande pureté optique et de basse masse moléculaire dénommé PDLA VALI B133b comme décrit dans l'exemple 1. Le film obtenu sera soumis à un traitement thermique comme décrit ci-dessous.
Exemple comparatif 6 :
On a préparé un film comme dans l'exemple 1 au départ de 95 % en poids de PLLA A36 auquel on a incorporé 5 % en poids d'un additif PDLA HMW de très grande pureté optique et de haute masse moléculaire dénommé PDLA EMDU D42b et élaboré par le procédé décrit dans l'exemple 1. Le film obtenu sera soumis à un traitement thermique comme décrit ci-dessous.
Tous les films obtenus dans les exemples 1 et 2 et dans les exemples comparatifs 1 à 6 sont soumis à une DSC (different scanning calorimetry) sous azote à un traitement thermique comme décrit ci-après. Chauffe de -40 °C à +220 °C à 10 °C/min, trempe (refroidissemnt) de +220 °C à +130 °C à 40 °C/min, isotherme de 30 min à +130 °C, trempe (refroidissement) de +130 °C à -40 °C à 20 °C/min puis chauffe de -40 °C à +220 °C à 10 °C/min. Le temps de demi-cristallisation à 130 °C est estimé conformément à la norme ISO 11357-7 à partir du thermogramme de la phase isotherme du programme de température comme le temps écoulé entre le début de cette phase isotherme et le moment correspondant à la moitié, en termes de surface, du pic de cristallisation observé, en faisant abstraction de l'éventuel début de cristallisation qui a pu avoir lieu pendant la partie de la trempe (refroidissement) précédant l'isotherme. Les résultats ainsi obtenus sont reportés dans le tableau 2, où il apparaît que le gain en termes de vitesse de cristallisation apporté par l'additif PDEU est de loin supérieur à celui apporté par les PDLA LMW ou HMW.
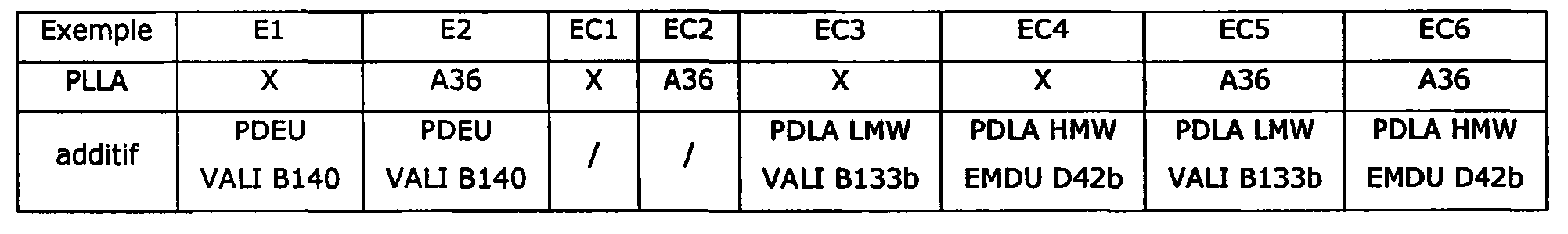
Tableau 1 : Composition des films des exemples 1 et 2 et des exemples comparatifs 1 à 6.
Tableau 2 : Temps de demi-cristallisation en cristallisation isotherme à 130 °C de PLLA, de mélanges PLLA/PDLA et de mélanges PLLA/PDEU obtenus par analyse DSC.
Les exemples El et E2 produits selon le procédé de l'invention présentent un temps de demi-cristallisation réduit par rapport aux temps de demi-cristallisation des meilleures compositions existantes (exemples comparatifs EC3 et EC6).
Claims (10)
1. Procédé pour accélérer la cristallisation du polylactide de masse molaire moyenne en nombre comprise entre 30.000 et 200.000 g/mol, caractérisé en ce que l'on incorpore dans ledit polylactide, appelé matrice polylactide, de configuration soit L, soit D, à une température comprise entre 160 °C et 250 °C, de 1 à 20 % en poids par rapport au poids total du mélange, un copolymère de polylactide-uréthane dont la configuration du polylactide est l'inverse de celle de la matrice polylactide.
2. Procédé selon la revendication 1 caractérisé en ce que la matrice polylactide est de configuration D et en ce que le copolymère polylactide-uréthane est obtenu par réaction d'un polylactide de configuration L avec un disocyanate en présence d'une diamine ou d'un dialcool.
3. Procédé selon la revendication 1 caractérisé en ce que la matrice polylactide est de configuration L et en ce que le polylactide-uréthane est obtenu par réaction d'un polylactide de configuration D avec un disocyanate en présence d'une diamine ou d'un dialcool.
4. Procédé selon l'une quelconque des revendications 1 à 3 caractérisé en ce que l'on incorpore le polylactide-uréthane à raison de 2 à 10 % en poids et de préférence à raison de 3 à 6 % en poids par rapport au poids total du mélange polylactide et polylactide-uréthane.
5. Composition de polylactide caractérisée en ce qu'elle comprend de 80 à 99 % en poids de polylactide de masse molaire comprise entre 30.000 et 200.000 g/mol, de configuration soit L, soit D, appelé matrice polylactide, et de 1 à 20 % en poids par rapport au poids total de la composition, d'un copolymère polylactide-uréthane dont la configuration du polylactide est l'inverse de celle de la matrice polylactide.
6. Composition selon la revendication 5 caractérisée en ce qu'elle comprend de 80 à 99 % en poids de poly-L-lactide et de 1 à 20 % en poids par rapport au poids total de la composition, d'un copolymère polylactide-uréthane dont le polylactide est de configuration D.
7. Composition selon la revendication 5 caractérisée en ce qu'elle comprend de 80 à 99 % en poids de poly-D-lactide et de 1 à 20 % en poids par rapport au poids total de la composition, d'un copolymère polylactide-uréthane dont le polylactide est de configuration L.
8. Procédé de fabrication d'un article caractérisé en ce qu'il comprend la transformation par thermoformage, injection ou extrusion de la composition selon l'une quelconque des revendications 5 à 7.
9. Article susceptible d'être obtenu selon le procédé de la revendication 8.
10. Article selon la revendication 9 caractérisé en ce que l'article est un film ou une fibre.
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| BE2010/0298A BE1019340A3 (fr) | 2010-05-18 | 2010-05-18 | Procede pour nucleer et accelerer la cristallisation du polylactide. |
| PCT/EP2011/057988 WO2011144625A1 (fr) | 2010-05-18 | 2011-05-17 | Procédé pour nucléer et accélérer la cristallisation du polylactide |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| BE201000298 | 2010-05-18 | ||
| BE2010/0298A BE1019340A3 (fr) | 2010-05-18 | 2010-05-18 | Procede pour nucleer et accelerer la cristallisation du polylactide. |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| BE1019340A3 true BE1019340A3 (fr) | 2012-06-05 |
Family
ID=43234215
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BE2010/0298A BE1019340A3 (fr) | 2010-05-18 | 2010-05-18 | Procede pour nucleer et accelerer la cristallisation du polylactide. |
Country Status (2)
| Country | Link |
|---|---|
| BE (1) | BE1019340A3 (fr) |
| WO (1) | WO2011144625A1 (fr) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN104010787B (zh) | 2011-09-09 | 2017-11-21 | 道达尔研究技术弗吕公司 | 包括聚烯烃和聚酯的层的滚塑制品 |
| AU2012306301B2 (en) | 2011-09-09 | 2017-06-01 | Total Research & Technology Feluy | Multilayered rotomoulded articles comprising a layer of polyester |
| AU2014224722B2 (en) | 2013-03-05 | 2018-07-19 | Total Research & Technology Feluy | Rotomoulded articles |
| US9676170B2 (en) | 2013-03-05 | 2017-06-13 | Total Research & Technology Feluy | Multilayered rotomoulded articles |
| US10273356B2 (en) | 2013-06-18 | 2019-04-30 | Total Research & Technology Feluy | Polymer composition |
| JP6628738B2 (ja) | 2014-04-29 | 2020-01-15 | トタル リサーチ アンド テクノロジー フエリユイ | ポリラクチド−ポリブタジエン・ベースのブロック共重合体を含むポリマー組成物 |
| KR20160149249A (ko) | 2014-04-29 | 2016-12-27 | 토탈 리서치 앤드 테크놀로지 펠루이 | 폴리락티드계 조성물 |
| JP6612785B2 (ja) | 2014-06-24 | 2019-11-27 | トタル リサーチ アンド テクノロジー フエリユイ | ポリラクチドをベースにしたポリマーを含む組成物 |
| AU2015314155B2 (en) | 2014-09-11 | 2017-10-12 | Polynt Composites France | Multilayered articles |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0118458A1 (fr) * | 1982-07-16 | 1984-09-19 | Univ Groningen | Materiaux biocompatibles, antithrombogenes appropries pour la chirurgie reconstituante. |
| EP0515203A2 (fr) * | 1991-05-24 | 1992-11-25 | Camelot Technologies Inc. | Compositions de polylactides |
| WO2008037773A1 (fr) * | 2006-09-29 | 2008-04-03 | Futerro S.A. | Copolymères polylactide-uréthane |
| US20080188629A1 (en) * | 2007-02-05 | 2008-08-07 | Nishikawa Rubber Co., Ltd. | Poly-l-lactic acid crystallization accelerator and production method thereof |
| WO2009060959A1 (fr) * | 2007-11-08 | 2009-05-14 | Dainichiseika Color & Chemicals Mfg. Co., Ltd. | Procédé de production d'un article moulé en résine de polyester, inducteur de cristallisation destiné à être utilisé dans le procédé, mélange maître, et article moulé en résine de polyester |
| US20100056700A1 (en) * | 2008-09-02 | 2010-03-04 | Cheil Industries Inc. | Environmentally-Friendly Polylactic Acid Resin Composition |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US1422505A (en) | 1920-11-11 | 1922-07-11 | Weaver Floyd Calvin | Grinding and lapping machine |
| WO2008037772A1 (fr) | 2006-09-29 | 2008-04-03 | Futerro S.A. | Procédé permettant de produire des copolymères polylactide-uréthane |
-
2010
- 2010-05-18 BE BE2010/0298A patent/BE1019340A3/fr not_active IP Right Cessation
-
2011
- 2011-05-17 WO PCT/EP2011/057988 patent/WO2011144625A1/fr active Application Filing
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0118458A1 (fr) * | 1982-07-16 | 1984-09-19 | Univ Groningen | Materiaux biocompatibles, antithrombogenes appropries pour la chirurgie reconstituante. |
| EP0515203A2 (fr) * | 1991-05-24 | 1992-11-25 | Camelot Technologies Inc. | Compositions de polylactides |
| WO2008037773A1 (fr) * | 2006-09-29 | 2008-04-03 | Futerro S.A. | Copolymères polylactide-uréthane |
| US20080188629A1 (en) * | 2007-02-05 | 2008-08-07 | Nishikawa Rubber Co., Ltd. | Poly-l-lactic acid crystallization accelerator and production method thereof |
| WO2009060959A1 (fr) * | 2007-11-08 | 2009-05-14 | Dainichiseika Color & Chemicals Mfg. Co., Ltd. | Procédé de production d'un article moulé en résine de polyester, inducteur de cristallisation destiné à être utilisé dans le procédé, mélange maître, et article moulé en résine de polyester |
| US20100056700A1 (en) * | 2008-09-02 | 2010-03-04 | Cheil Industries Inc. | Environmentally-Friendly Polylactic Acid Resin Composition |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2011144625A1 (fr) | 2011-11-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| BE1019340A3 (fr) | Procede pour nucleer et accelerer la cristallisation du polylactide. | |
| Martínez-Sanz et al. | Characterization of polyhydroxyalkanoates synthesized from microbial mixed cultures and of their nanobiocomposites with bacterial cellulose nanowhiskers | |
| Yang et al. | Two step extrusion process: from thermal recycling of PHB to plasticized PLA by reactive extrusion grafting of PHB degradation products onto PLA chains | |
| Gregorova | Application of differential scanning calorimetry to the characterization of biopolymers | |
| EP2401317B1 (fr) | Procédé de production de stéréocomplexes plla/pdla | |
| FR3036400A1 (fr) | Polyester de haute viscosite aux proprietes choc ameliorees | |
| EP2831136B1 (fr) | Polymères, leur procédé de synthèse et compositions les comprenant | |
| Jeong et al. | Lactide-derived ester oligomers for highly compatible poly (lactide) plasticizer produced through an eco-friendly process: renewable resources, biodegradation, enhanced flexibility, and elastomeric performance | |
| Rizzuto et al. | Plasticization and anti-plasticization effects caused by poly (lactide-ran-caprolactone) addition to double crystalline poly (l-lactide)/poly (ε-caprolactone) blends | |
| EP2294113A2 (fr) | Procede de preparation d'un polyamideimide, polyamideimide et composition comprenant ce polyamideimide | |
| RU2605592C2 (ru) | Биологически разлагаемая полимерная композиция с высокой деформируемостью | |
| Dadras Chomachayi et al. | A comparison of the effect of silk fibroin nanoparticles and microfibers on the reprocessing and biodegradability of PLA/PCL blends | |
| EP2449017A1 (fr) | Composition polyamide modifiee comprenant au moins un compose phenolique | |
| Dominici et al. | Improving the flexibility and compostability of starch/poly (butylene cyclohexanedicarboxylate)-based blends | |
| FR2462454A1 (fr) | Copolycarbonate thermoplastique de poly(tere- ou isophtalate de bisphenol a) et son procede de fabrication | |
| US20210139696A1 (en) | Biobased Additive for Thermoplastic Polyesters | |
| EP3491045B1 (fr) | Composition polymere comprenant un polyester thermoplastique | |
| FR3004188A1 (fr) | Utilisation de polymeres comme additifs dans une matrice de polymere | |
| CN113512281B (zh) | 一种改性pga材料及其制备方法,以及改性pga薄膜 | |
| BE1019289A5 (fr) | Composition de polymeres issus de ressources renouvelables. | |
| KR102350740B1 (ko) | 아세틸화 락타이드 올리고머계 가소제 및 이의 제조방법, 및 아세틸화 락타이드 올리고머계 가소제를 포함하는 pla 수지 조성물 | |
| WO2021005205A1 (fr) | Matiere plastique à haute teneur en pla comprenant du ppgdge | |
| WO2010038860A1 (fr) | Composition d'acide polylactique et son procédé de production | |
| WO2012131252A1 (fr) | Utilisation d'un oligomere de lactide biodegradable comme plastifiant | |
| EP3861050A1 (fr) | Procédé de préparation d'un polyester de type poly(1,4:3,6-dianhydrohexitol-cocyclohexylène téréphtalate) |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| RE | Patent lapsed |
Effective date: 20130531 |