WO2020196323A1 - プログラム、情報処理方法及び情報処理装置 - Google Patents
プログラム、情報処理方法及び情報処理装置 Download PDFInfo
- Publication number
- WO2020196323A1 WO2020196323A1 PCT/JP2020/012464 JP2020012464W WO2020196323A1 WO 2020196323 A1 WO2020196323 A1 WO 2020196323A1 JP 2020012464 W JP2020012464 W JP 2020012464W WO 2020196323 A1 WO2020196323 A1 WO 2020196323A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- information
- exacerbation
- sensor
- acquired
- muscle
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/48—Other medical applications
- A61B5/4842—Monitoring progression or stage of a disease
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/08—Detecting, measuring or recording devices for evaluating the respiratory organs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/02—Detecting, measuring or recording pulse, heart rate, blood pressure or blood flow; Combined pulse/heart-rate/blood pressure determination; Evaluating a cardiovascular condition not otherwise provided for, e.g. using combinations of techniques provided for in this group with electrocardiography or electroauscultation; Heart catheters for measuring blood pressure
- A61B5/0205—Simultaneously evaluating both cardiovascular conditions and different types of body conditions, e.g. heart and respiratory condition
- A61B5/02055—Simultaneously evaluating both cardiovascular condition and temperature
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/02—Detecting, measuring or recording pulse, heart rate, blood pressure or blood flow; Combined pulse/heart-rate/blood pressure determination; Evaluating a cardiovascular condition not otherwise provided for, e.g. using combinations of techniques provided for in this group with electrocardiography or electroauscultation; Heart catheters for measuring blood pressure
- A61B5/021—Measuring pressure in heart or blood vessels
- A61B5/022—Measuring pressure in heart or blood vessels by applying pressure to close blood vessels, e.g. against the skin; Ophthalmodynamometers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/02—Detecting, measuring or recording pulse, heart rate, blood pressure or blood flow; Combined pulse/heart-rate/blood pressure determination; Evaluating a cardiovascular condition not otherwise provided for, e.g. using combinations of techniques provided for in this group with electrocardiography or electroauscultation; Heart catheters for measuring blood pressure
- A61B5/024—Detecting, measuring or recording pulse rate or heart rate
- A61B5/02405—Determining heart rate variability
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/05—Detecting, measuring or recording for diagnosis by means of electric currents or magnetic fields; Measuring using microwaves or radio waves
- A61B5/053—Measuring electrical impedance or conductance of a portion of the body
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/08—Detecting, measuring or recording devices for evaluating the respiratory organs
- A61B5/083—Measuring rate of metabolism by using breath test, e.g. measuring rate of oxygen consumption
- A61B5/0836—Measuring rate of CO2 production
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/103—Detecting, measuring or recording devices for testing the shape, pattern, colour, size or movement of the body or parts thereof, for diagnostic purposes
- A61B5/11—Measuring movement of the entire body or parts thereof, e.g. head or hand tremor, mobility of a limb
- A61B5/1118—Determining activity level
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/103—Detecting, measuring or recording devices for testing the shape, pattern, colour, size or movement of the body or parts thereof, for diagnostic purposes
- A61B5/11—Measuring movement of the entire body or parts thereof, e.g. head or hand tremor, mobility of a limb
- A61B5/113—Measuring movement of the entire body or parts thereof, e.g. head or hand tremor, mobility of a limb occurring during breathing
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/145—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue
- A61B5/1455—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue using optical sensors, e.g. spectral photometrical oximeters
- A61B5/14551—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue using optical sensors, e.g. spectral photometrical oximeters for measuring blood gases
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/24—Detecting, measuring or recording bioelectric or biomagnetic signals of the body or parts thereof
- A61B5/316—Modalities, i.e. specific diagnostic methods
- A61B5/318—Heart-related electrical modalities, e.g. electrocardiography [ECG]
- A61B5/346—Analysis of electrocardiograms
- A61B5/349—Detecting specific parameters of the electrocardiograph cycle
- A61B5/352—Detecting R peaks, e.g. for synchronising diagnostic apparatus; Estimating R-R interval
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/24—Detecting, measuring or recording bioelectric or biomagnetic signals of the body or parts thereof
- A61B5/316—Modalities, i.e. specific diagnostic methods
- A61B5/389—Electromyography [EMG]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/24—Detecting, measuring or recording bioelectric or biomagnetic signals of the body or parts thereof
- A61B5/316—Modalities, i.e. specific diagnostic methods
- A61B5/389—Electromyography [EMG]
- A61B5/397—Analysis of electromyograms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/42—Detecting, measuring or recording for evaluating the gastrointestinal, the endocrine or the exocrine systems
- A61B5/4261—Evaluating exocrine secretion production
- A61B5/4266—Evaluating exocrine secretion production sweat secretion
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/45—For evaluating or diagnosing the musculoskeletal system or teeth
- A61B5/4538—Evaluating a particular part of the muscoloskeletal system or a particular medical condition
- A61B5/4561—Evaluating static posture, e.g. undesirable back curvature
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/68—Arrangements of detecting, measuring or recording means, e.g. sensors, in relation to patient
- A61B5/6801—Arrangements of detecting, measuring or recording means, e.g. sensors, in relation to patient specially adapted to be attached to or worn on the body surface
- A61B5/6813—Specially adapted to be attached to a specific body part
- A61B5/6823—Trunk, e.g., chest, back, abdomen, hip
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/72—Signal processing specially adapted for physiological signals or for diagnostic purposes
- A61B5/7271—Specific aspects of physiological measurement analysis
- A61B5/7275—Determining trends in physiological measurement data; Predicting development of a medical condition based on physiological measurements, e.g. determining a risk factor
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B7/00—Instruments for auscultation
- A61B7/003—Detecting lung or respiration noise
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B7/00—Instruments for auscultation
- A61B7/02—Stethoscopes
- A61B7/04—Electric stethoscopes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B2562/00—Details of sensors; Constructional details of sensor housings or probes; Accessories for sensors
- A61B2562/02—Details of sensors specially adapted for in-vivo measurements
- A61B2562/0271—Thermal or temperature sensors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/02—Detecting, measuring or recording pulse, heart rate, blood pressure or blood flow; Combined pulse/heart-rate/blood pressure determination; Evaluating a cardiovascular condition not otherwise provided for, e.g. using combinations of techniques provided for in this group with electrocardiography or electroauscultation; Heart catheters for measuring blood pressure
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/05—Detecting, measuring or recording for diagnosis by means of electric currents or magnetic fields; Measuring using microwaves or radio waves
- A61B5/053—Measuring electrical impedance or conductance of a portion of the body
- A61B5/0535—Impedance plethysmography
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/08—Detecting, measuring or recording devices for evaluating the respiratory organs
- A61B5/0809—Detecting, measuring or recording devices for evaluating the respiratory organs by impedance pneumography
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/145—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue
- A61B5/14542—Measuring characteristics of blood in vivo, e.g. gas concentration, pH value; Measuring characteristics of body fluids or tissues, e.g. interstitial fluid, cerebral tissue for measuring blood gases
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/24—Detecting, measuring or recording bioelectric or biomagnetic signals of the body or parts thereof
- A61B5/25—Bioelectric electrodes therefor
- A61B5/251—Means for maintaining electrode contact with the body
- A61B5/256—Wearable electrodes, e.g. having straps or bands
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/24—Detecting, measuring or recording bioelectric or biomagnetic signals of the body or parts thereof
- A61B5/25—Bioelectric electrodes therefor
- A61B5/279—Bioelectric electrodes therefor specially adapted for particular uses
- A61B5/296—Bioelectric electrodes therefor specially adapted for particular uses for electromyography [EMG]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/24—Detecting, measuring or recording bioelectric or biomagnetic signals of the body or parts thereof
- A61B5/316—Modalities, i.e. specific diagnostic methods
- A61B5/318—Heart-related electrical modalities, e.g. electrocardiography [ECG]
- A61B5/346—Analysis of electrocardiograms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/72—Signal processing specially adapted for physiological signals or for diagnostic purposes
- A61B5/7235—Details of waveform analysis
- A61B5/7264—Classification of physiological signals or data, e.g. using neural networks, statistical classifiers, expert systems or fuzzy systems
- A61B5/7267—Classification of physiological signals or data, e.g. using neural networks, statistical classifiers, expert systems or fuzzy systems involving training the classification device
Definitions
- the present invention relates to a program, an information processing method, and an information processing device.
- an exacerbation index of a COPD patient is detected by measuring the expression level of the IL-27 protein or a gene encoding the IL-27 protein in a biological sample derived from the COPD patient (for example, blood, serum, etc.). The method of doing so is disclosed.
- Patent Document 1 collects a biological sample to be measured from a COPD patient undergoing an exacerbation test, which may impose a burden on the body of the COPD patient.
- One aspect is to provide a program or the like that can detect abnormalities in respiratory diseases without imposing a burden on the patient's body.
- a program is the activity from an electrocardiogram sensor that acquires the motion information from a detection sensor that detects motion information related to the motion of the respiratory muscle or the respiratory assist muscle, and action potential information for the respiratory muscle or the respiratory assist muscle. It is characterized in that it acquires potential information, detects an abnormality in a respiratory system disease based on the acquired operation information and action potential information, and when the abnormality is detected, causes a computer to execute a process of outputting the abnormality information. To do.
- the first embodiment relates to a mode for detecting an abnormality of a respiratory system disease based on motion information regarding the movement of a respiratory muscle or a respiratory assist muscle and activity potential information for the respiratory muscle or the respiratory assist muscle.
- the detection sensor is used to acquire motion information regarding the movement of the respiratory muscle or the respiratory assist muscle
- the electromyogram sensor is used to acquire the action potential information for the respiratory muscle or the respiratory assist muscle.
- the motion information includes information on the motion of the respiratory muscle or the respiratory assist muscle, the motion of the thorax associated with the motion of the respiratory muscle or the respiratory assist muscle, or the motion associated with the contraction and expansion of the lung or the diaphragm.
- Abnormalities of respiratory diseases are detected based on the acquired motion information and action potential information.
- the detected abnormality can be output to a patient or a doctor.
- COPD which is one of the respiratory diseases
- other types of respiratory diseases for example, asthma, pneumonia, interstitial
- COPD causes chronic inflammation of the airways due to toxic substances and gases (especially smoking) in the air, resulting in airway restriction (sufficient breathing) due to airway narrowing, alveolar wall destruction, and increased sputum. Therefore, it is a disease that causes insufficient ventilation).
- the pathological condition may rapidly worsen due to infection or the like, and these are called exacerbations.
- exacerbation occurs, a significant decrease in respiratory status is observed, and even after recovery, the respiratory status before exacerbation does not return. Each time the exacerbation is repeated, the general condition and prognosis deteriorate.
- FIG. 1 is an explanatory diagram showing an outline of a system for detecting information on exacerbations in COPD.
- the system of this embodiment includes an information processing device 1, an information processing terminal 2, a detection sensor 3, and an electromyogram sensor 4, and each device transmits and receives information via a network N such as the Internet.
- the information processing device 1 is an information processing device that processes, stores, and transmits / receives various information such as motion information related to the movement of the respiratory muscle or the respiratory assist muscle and action potential information for the respiratory muscle or the respiratory assist muscle.
- the information processing device 1 is, for example, a server device, a personal computer, or the like. In the present embodiment, the information processing device 1 is assumed to be a server device, and will be read as a server 1 below for the sake of brevity.
- the information processing terminal 2 is a terminal device that receives and displays the detected abnormality information of the respiratory system disease.
- the information processing terminal 2 is, for example, a wearable device such as a smartphone, a mobile phone, or a wristwatch-type mobile terminal, or an information processing device such as a tablet or a personal computer terminal. In the following, for the sake of brevity, the information processing terminal 2 is read as the terminal 2.
- the detection sensor 3 is a sensor that detects the motion information of the respiratory muscle or the respiratory assist muscle.
- the respiratory muscle is a muscle used to expand and contract the thorax when breathing, and includes the diaphragm, the internal intercostal muscle, the external intercostal muscle, and the like.
- Pectoralis minor muscles anterior oblique muscles, abdominal internal oblique muscles, posterior oblique muscles, serratus anterior muscles, serratus posterior muscles, serratus posterior muscles, broad back muscles, erection muscles, mitral muscles
- It is a muscle group including the lumbar square muscle, pectoralis major muscle, pectoralis minor muscle, abdominal straight muscle, internal oblique muscle, external oblique muscle, transverse abdominal muscle, etc., and is used as an auxiliary when breathing.
- a belt-shaped or tape-shaped detection sensor 3 is attached to the chest of the patient to detect the movement of the patient's respiratory muscles and respiratory assist muscles, or the movement of the thorax based on the movements of the respiratory muscles and respiratory assist muscles.
- the detection sensor 3 for example, a piezoelectric element sensor, an expansion / contraction sensor, a belt-shaped or tape-shaped tape sensor, an echo sensor, a biopotential sensor for measuring bioimpedance, or the like is used.
- the detection sensor 3 is not limited to the above-mentioned sensor, and is, for example, an electrostatic capacity capable of detecting the movement of the respiratory muscle and the respiratory assist muscle, or the movement of the thorax based on the movement of the respiratory muscle and the respiratory assist muscle or the breathing itself without touching the human body. It may be a non-contact sensor of the type.
- the piezoelectric element sensor is a sensor that converts the force applied to the piezoelectric body into a voltage, and may be, for example, a sensor for a breathing monitor that detects a breathing waveform using the piezoelectric element.
- the above-mentioned sensor for respiratory monitor (piezoelectric element sensor) is placed on the thorax, which is the measurement site, and converts the change in pressure applied to the thorax by the respiratory movement of the measurement site into voltage to convert the patient's respiratory muscles and respiratory assist muscles. Detects the movement of and outputs it as waveform data.
- the measurement site described above is not limited to the thorax, and may be, for example, the abdomen, neck, or back.
- the echo sensor is, for example, a sensor that uses ultrasonic waves to measure the flow rate of a liquid, identify the liquid, measure the distance to an object, and the like.
- the echo sensor is used to detect the movement of the ribs, diaphragm, lungs, etc. For example, the movement distance of the ribs or the movement distance of the diaphragm in respiration, the relaxation / contraction information or the movement distance of the lungs, the expansion / contraction information, etc. are detected.
- the biopotential sensor indirectly detects the movement of the thoracic and lungs from the bioimpedance that changes due to changes in lung volume associated with breathing.
- the expansion / contraction sensor is a displacement sensor that expands and contracts like rubber, and monitors the movement of the subject in real time.
- the expansion / contraction sensor is, for example, a thin sheet in which carbon nanotubes having a special structure and an elastomer material are layered.
- the expansion / contraction sensor has elasticity like rubber as well as conductivity, and the capacitance changes according to the amount of expansion / contraction. Since it is possible to measure from small strains to large strains, for example, by attaching a belt-shaped stretch sensor wrapped around the chest or attaching a seal-shaped stretch sensor, joint changes, muscle movements, etc. Alternatively, it accurately measures even small movements that were previously difficult to measure, such as chest movements during breathing and vector changes in chest movements.
- the measurement site described above is not limited to the chest, but may be, for example, the abdomen or the back.
- the electromyogram sensor 4 is a sensor that records the action potential of muscles in a waveform. Depending on the characteristics of the recorded waveform, including the frequency, it is possible to obtain information on the diagnosis of the presence / absence, type, nature, site, etc. of nerve or muscle disorder. Information on exacerbations in COPD can be detected by evaluating the respiratory muscles and respiratory assist muscles involved in COPD using the electromyogram sensor 4.
- the detection sensor 3 and the electromyogram sensor 4 are shown separately, but both may be integrally configured. Further, in the present embodiment, an example in which the terminal 2, the detection sensor 3 and the electromyogram sensor 4 are separated is shown, but the present invention is not limited to this.
- the device configuration may be such that the terminal 2, the detection sensor 3, and the electromyogram sensor 4 are all integrated.
- the terminal 2 uses the detection sensor 3 to acquire motion information regarding the movement of the respiratory muscle or the respiratory assist muscle, and the electrocardiogram sensor 4 to acquire activity potential information for the respiratory muscle or the respiratory assist muscle.
- the motion information acquired by the detection sensor 3 includes, for example, changes in the movement of the thorax and the movement of the thorax due to expansion and contraction of the respiratory muscle or the respiratory assist muscle, the range of movement of the chest, the speed of movement of the chest, and stimulation of the respiratory muscles. Time etc.
- an example of acquiring operation information by using one type of piezoelectric element sensor (for example, a belt in which the piezoelectric element is incorporated) of the detection sensor 3 will be described, but a telescopic sensor or a tape sensor will be described.
- detection sensors 3 such as biopotential sensors.
- the piezoelectric element sensor When the piezoelectric element sensor is attached to the patient's chest, the piezoelectric element sensor generates a voltage according to the movement of the patient's respiratory muscles or respiratory assist muscles, and the piezoelectric element outputs a voltage (operating electrical signal).
- the expansion / contraction sensor When the expansion / contraction sensor is used, the change in the expansion / contraction speed or acceleration may be measured.
- the activity potential information acquired by the electrocardiogram sensor 4 is an activity current signal generated by contraction of a respiratory muscle or a respiratory assist muscle during respiration, and is a duration of the activity potential and a frequency obtained by frequency-converting the activity potential waveform. Also includes waveforms.
- the terminal 2 compares the acquired operation information and action potential information with each predetermined threshold value, and when the condition for detecting the exacerbation in COPD is satisfied, the terminal 2 detects the information on the exacerbation.
- the information regarding the exacerbation in COPD may be, for example, information indicating the presence or absence of exacerbation of COPD, exacerbation level information classified according to the probability value of exacerbation (for example, a value in the range of "0" to "1"), or the like. ..
- the probability value of exacerbation can be determined based on information such as the degree, frequency, and duration of the disease. For example, it may be classified into four exacerbation levels (exacerbation level 1 to exacerbation level 4) according to the exacerbation probability value. Specifically, for example, when the probability value of exacerbation is less than 0.05, exacerbation level 1 (normal) is determined without exacerbation.
- the probability value of exacerbation is 0.05 or more and less than 0.5, it is determined that the exacerbation level 2 has a low risk of developing exacerbation.
- the probability value of exacerbation is 0.5 or more and less than 0.8, it is determined that the exacerbation level 3 has a high risk of developing exacerbation.
- the probability value of exacerbation is 0.8 or more, it is determined that the exacerbation level 4 has been exacerbated.
- the server 1 may detect information on exacerbations based on operation information and activity potential information. In this case, the server 1 transmits the detected exacerbation information to the terminal 2.
- FIG. 2 is a block diagram showing a configuration example of the server 1.
- the server 1 includes a control unit 11, a storage unit 12, a communication unit 13, an input unit 14, a display unit 15, a reading unit 16, and a large-capacity storage unit 17. Each configuration is connected by bus B.
- the control unit 11 includes arithmetic processing units such as a CPU (Central Processing Unit), an MPU (Micro-Processing Unit), and a GPU (Graphics Processing Unit), and reads and executes the control program 1P stored in the storage unit 12. , Performs various information processing, control processing, etc. related to the server 1.
- arithmetic processing units such as a CPU (Central Processing Unit), an MPU (Micro-Processing Unit), and a GPU (Graphics Processing Unit), and reads and executes the control program 1P stored in the storage unit 12. , Performs various information processing, control processing, etc. related to the server 1.
- the control unit 11 is described as a single processor in FIG. 2, it may be a multiprocessor.
- the storage unit 12 includes memory elements such as RAM (RandomAccessMemory) and ROM (ReadOnlyMemory), and stores the control program 1P required for the control unit 11 to execute the process. In addition, the storage unit 12 temporarily stores data and the like necessary for the control unit 11 to execute arithmetic processing.
- the communication unit 13 is a communication module for performing processing related to communication, and transmits / receives information to / from the terminal 2 or the like via the network N.
- the input unit 14 is an input device such as a mouse, a keyboard, a touch panel, and a button, and outputs the received operation information to the control unit 11.
- the display unit 15 is a liquid crystal display, an organic EL (electroluminescence) display, or the like, and displays various information according to the instructions of the control unit 11.
- the reading unit 16 reads a portable storage medium 1a including a CD (Compact Disc) -ROM or a DVD (Digital Versatile Disc) -ROM.
- the control unit 11 may read the control program 1P from the portable storage medium 1a via the reading unit 16 and store it in the large-capacity storage unit 17. Further, the control unit 11 may download the control program 1P from another computer via the network N or the like and store it in the large-capacity storage unit 17. Furthermore, the control unit 11 may read the control program 1P from the semiconductor memory 1b.
- the large-capacity storage unit 17 is a large-capacity storage device including, for example, a hard disk.
- the large-capacity storage unit 17 includes a patient DB 171 and a master DB 172.
- the patient DB 171 stores information about the patient.
- the master DB 172 stores various thresholds for detecting information regarding exacerbations in COPD.
- the storage unit 12 and the large-capacity storage unit 17 may be configured as an integrated storage device. Further, the large-capacity storage unit 17 may be composed of a plurality of storage devices. Furthermore, the large-capacity storage unit 17 may be an external storage device connected to the server 1.
- server 1 is described as one information processing device in the present embodiment, it may be distributed and processed by a plurality of servers, or may be configured by a virtual machine.
- FIG. 3 is an explanatory diagram showing an example of the record layout of the patient DB 171.
- the patient DB 171 includes a patient ID column, a gender column, a name column, an abnormality presence / absence column, an abnormality detail column, a detection date / time column, a sensor column used, and a data column.
- the patient ID column stores a uniquely identified patient ID to identify each patient.
- the gender column remembers the patient's gender.
- the name column remembers the patient's name.
- the abnormality presence / absence column stores information indicating whether or not an abnormality has been detected for the patient.
- the anomaly detail column stores detailed information on the detected anomaly.
- the detection date / time column stores the date / time information when an abnormality is detected.
- the sensor sequence used stores the sensor information used when an abnormality is detected.
- the data string stores sensor data detected by the sensor used.
- the sensor data is, for example, time-series data.
- FIG. 4 is an explanatory diagram showing an example of the record layout of the master DB 172.
- the master DB 172 includes a master ID column, a master name column, a sensor column, and a threshold value column.
- the master ID column stores the ID of the master data uniquely specified in order to identify each master data.
- the master name column stores the name of the master data.
- the sensor sequence stores the name of the sensor to which the threshold is applied.
- the threshold sequence stores reference values for comparison for detecting information on exacerbations.
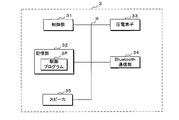
- FIG. 5 is a block diagram showing a configuration example of the terminal 2.
- the terminal 2 includes a control unit 21, a storage unit 22, a communication unit 23, an input unit 24, a display unit 25, and a Bluetooth (registered trademark) communication unit 26. Each configuration is connected by bus B.
- the control unit 21 includes arithmetic processing units such as a CPU and an MPU, and performs various information processing, control processing, and the like related to the terminal 2 by reading and executing the control program 2P stored in the storage unit 22. Although the control unit 21 is described as a single processor in FIG. 5, it may be a multiprocessor.
- the storage unit 22 includes memory elements such as RAM and ROM, and stores the control program 2P required for the control unit 21 to execute the process. In addition, the storage unit 22 temporarily stores data and the like necessary for the control unit 21 to execute arithmetic processing.
- the communication unit 23 is a communication module for performing processing related to communication, and transmits / receives information to / from the server 1 or the like via the network N.
- the input unit 24 may be a keyboard, a mouse, or a touch panel integrated with the display unit 25.
- the display unit 25 is a liquid crystal display, an organic EL display, or the like, and displays various information according to the instructions of the control unit 21.
- the Bluetooth communication unit 26 is a communication module for performing processing related to communication using Bluetooth, and transmits / receives information to / from the detection sensor 3 and the electromyogram sensor 4.
- Bluetooth is illustrated as a short-range wireless communication means in FIG. 5, it is not limited to this, and communication standards such as Zigbee and Wi-Fi may be used. Further, wired communication may be adopted.
- the example of the Bluetooth communication unit 26 has been described with reference to FIG. 5, the present invention is not limited to this. For example, communication may be performed using a public network such as 5G or 4G.
- FIG. 6 is a block diagram showing a configuration example of the detection sensor 3.
- the detection sensor 3 will be described with an example of using the above-mentioned piezoelectric element sensor (for example, a belt or tape in which the piezoelectric element is incorporated).
- the detection sensor 3 includes a control unit 31, a storage unit 32, a piezoelectric element 33, a Bluetooth communication unit 34, and a speaker 35. Each configuration is connected by bus B.
- the control unit 31 includes an arithmetic processing unit such as a CPU and an MPU, and by reading and executing the control program 3P stored in the storage unit 32, the force applied to the piezoelectric body read by the piezoelectric element 33 is applied to the voltage. Performs control processing and the like to convert to.
- the storage unit 32 includes memory elements such as RAM and ROM, and stores the control program 3P required for the control unit 31 to execute the process. In addition, the storage unit 32 temporarily stores data and the like necessary for the control unit 31 to execute arithmetic processing.
- the piezoelectric element 33 is a passive element that utilizes the piezoelectric effect, and converts the force applied to the piezoelectric body into a voltage.
- the Bluetooth communication unit 34 is a communication module for performing communication-related processing using the Bluetooth, and transmits / receives voltage information (for example, time-series data) to / from the terminal 2 or the like.
- Bluetooth is illustrated as a short-range wireless communication means in FIG. 6, it is not limited to this, and communication standards such as Zigbee and Wi-Fi may be used. Further, wired communication may be adopted.
- the speaker 35 is a device that converts an electric signal into sound.
- the speaker 35 may be a headset connected to the detection sensor 3 by a short-range wireless communication method such as Bluetooth.
- FIG. 7 is a block diagram showing a configuration example of the electromyogram sensor 4.
- the EMG sensor 4 includes a control unit 41, a storage unit 42, an EMG measurement unit 43, a Bluetooth communication unit 44, and a speaker 45. Each configuration is connected by bus B.
- the control unit 41 includes an arithmetic processing unit such as a CPU and an MPU, and by reading and executing the control program 4P stored in the storage unit 42, the action potential information (myoelectric potential) read by the myoelectric measurement unit 43.
- Control processing, etc. for The storage unit 42 includes memory elements such as RAM and ROM, and stores a control program 4P required for the control unit 41 to execute processing. In addition, the storage unit 42 temporarily stores data and the like necessary for the control unit 41 to execute arithmetic processing.
- the myoelectric measurement unit 43 measures the activity potential information for the respiratory muscle or the respiratory assist muscle.
- the Bluetooth communication unit 44 is a communication module for performing communication-related processing using the Bluetooth, and transmits / receives active potential information (for example, time-series data) to / from the terminal 2 or the like.
- Bluetooth is illustrated as a short-range wireless communication means, but the present invention is not limited to this, and communication standards such as Zigbee and Wi-Fi may be used. Further, wired communication may be adopted.
- the speaker 45 is a device that converts an electric signal into sound.
- the speaker 45 may be a headset connected to the myocardial diagram sensor 4 by a short-range wireless communication method such as Bluetooth.
- FIG. 8A and 8B are explanatory views for explaining the operation information detected by the detection sensor 3.
- FIG. 8A is an explanatory diagram illustrating respiratory physiology during normal respiration for healthy subjects and COPD patients.
- a person takes in oxygen into the body by breathing exercise and excretes carbon dioxide from the body.
- the lungs are wrapped in the thoracic membrane and are located in the thorax.
- the lung itself has no force to expand and contract, and passively expands and contracts due to the mobility of the ribs that form the thorax and the expansion and contraction movement of the diaphragm and the like.
- the diaphragm is the largest inspiratory muscle of the body, located around the 5th and 6th ribs, has a dome-like shape, and is the muscle used when inhaling.
- the inspiratory muscles including the diaphragm and the inspiratory auxiliary muscles contract in coordination with each other, which expands the thorax and creates negative pressure in the thoracic cavity, causing the lungs to expand and the outside air to be pulmonary.
- the inspiratory muscle / auxiliary inspiratory muscle includes the diaphragm, external intercostal muscle, sternocleidomastoid muscle, anterior scalene muscle, middle scalene muscle, posterior scalene muscle and the like.
- the expiratory muscle / auxiliary expiratory muscle includes the internal intercostal muscle, the rectus abdominis muscle, the internal oblique muscle, the external oblique muscle, the transverse abdominal muscle, and the like.
- FIG. 8B is an image diagram showing motion information of respiratory muscles or respiratory assist muscles for healthy subjects and COPD patients.
- FIG. 8B shows waveform data of operation electrical signals (operation information) of respiratory muscles or respiratory assist muscles.
- the horizontal axis indicates time, and the unit is seconds (sec).
- the vertical axis represents voltage, and the unit is volt (V).
- FIG. 8B The upper part of FIG. 8B is a graph showing the temporal change of the voltage output from the detection sensor 3 attached to a healthy person. In the case of a healthy person, it can be understood that the voltage periodically repeats the maximum and the minimum with little change with time.
- the lower part of FIG. 8B is a graph showing the temporal change of the voltage output from the detection sensor 3 attached to the COPD patient.
- the maximum and minimum with little change over time are periodically repeated.
- the maximal and minimal temporal changes continue to increase, reflecting the progressive increase in residual volume (dynamic hyperinflation) associated with exacerbation of ventilatory impairment during exhalation. Become.
- the control unit 21 when the maximum change in the voltage output from the detection sensor 3 per unit time exceeds a predetermined threshold value (for example, inclination 0.2), it is determined that the first condition is satisfied. Specifically, the control unit 21 performs the following processing. The control unit 21 acquires a voltage from the detection sensor 3 in time series. The control unit 21 obtains the maximum voltage in time series. The control unit 21 extracts the maximum voltage of a predetermined unit time (for example, 60 seconds) and calculates the inclination of the approximate straight line formed by the extracted maximum. When the control unit 21 determines that the inclination exceeds a predetermined threshold value (for example, inclination 0.2), it determines that the first condition is satisfied.
- a predetermined threshold value for example, inclination 0.2
- control unit 21 may further determine that the first condition is satisfied when, for example, the maximum average value per unit time exceeds the threshold value shown by the dotted line in FIG. 8B and the obtained inclination exceeds the threshold value. good. Further, for example, the control unit 21 extracts the maximum and minimum of the voltage for a predetermined unit time (for example, 60 seconds), calculates the maximum inclination of the approximate straight line formed by the extracted maximum, and approximates the extracted minimum. Calculate the minimum slope of the straight line.
- a predetermined unit time for example, 60 seconds
- the maximum inclination exceeds the predetermined maximum inclination threshold
- the minimum inclination exceeds the predetermined minimum inclination threshold
- the minimum inclination exceeds the maximum inclination
- the duration is a predetermined time.
- FIG. 9 is an explanatory diagram for explaining the activity potential information of the respiratory muscles of a healthy person detected by the electromyogram sensor 4.
- the horizontal axis represents time, and the unit is milliseconds (msec).
- the vertical axis represents the potential (active potential), and the unit is microvolt ( ⁇ V).
- the upper part of the graph in FIG. 9 shows the temporal change of the potential of the inspiratory muscle of a healthy person. With respect to the inspiratory muscle, a potential waveform having an amplitude of about 100 ⁇ V is confirmed at regular intervals.
- the lower part of the graph in FIG. 9 shows the temporal change of the potential of the expiratory muscle of a healthy person.
- the expiratory muscles of healthy subjects are not very active, and therefore the corresponding potential waveform is also minute and can hardly be confirmed.
- 10A and 10B are explanatory views for explaining the action potential information of the respiratory muscles of the COPD patient detected by the electromyogram sensor 4. Since the horizontal axis and the vertical axis are the same as those in FIG. 9, the description thereof will be omitted.
- FIG. 10A is an explanatory diagram illustrating action potential information of the respiratory muscles of a COPD patient during normal times.
- the activity of the inspiratory muscles during normal times is stronger than the activity of the inspiratory muscles of healthy subjects (normal time) in FIG. 9, so that the amplitude of the action potential of the inspiratory muscles of COPD patients is the inspiratory muscles of healthy subjects. It becomes larger than the amplitude of the action potential of.
- the amplitude of the active potential of the expiratory muscle becomes larger than that in FIG.
- FIG. 10B is an explanatory diagram for explaining the activity potential information of the respiratory muscles of the COPD patient at the time of exacerbation.
- COPD patients try to get outside air into the lungs by further contracting the inspiratory muscles and widening the thorax.
- the inspiratory muscle contracts more strongly than in the normal state, and the amplitude of the action potential of the inspiratory muscle at the time of exacerbation becomes larger than the amplitude of the action potential of the inspiratory muscle at the time of exacerbation.
- the duration of the action potential of the inspiratory muscle is shorter than the duration of the action potential of the inspiratory muscle at the time of exacerbation.
- these signals are analyzed by Fourier transform, the frequency distribution when exacerbation occurs is different from that in normal times.
- the dotted line in FIG. 10 indicates a predetermined threshold of active potential of the expiratory muscle during normal and exacerbation. Exacerbation can be detected by comparing the peak value of the activity potential of the expiratory muscle of a COPD patient with the threshold value of the active potential of the expiratory muscle during normal and exacerbation.
- thresholds for active potentials during normal and exacerbation may be set, and exacerbation levels may be defined according to the set thresholds.
- the control unit 21 of the terminal 2 compares the peak value of the action potential of the expiratory muscle detected by the electromyogram sensor 4 with the threshold value of the action potential at the time of normal and exacerbation.
- the control unit 21 determines that the peak value of the action potential of the expiratory muscle is less than the threshold value A of the action potential of the expiratory muscle at the normal time, it determines that the exacerbation level 2 has a low risk of developing exacerbation.
- the action potential of the expiratory muscle is equal to or higher than the threshold value A of the action potential of the expiratory muscle at the normal time, and the action potential of the expiratory muscle at the time of exacerbation is increased by 30% of the threshold value B (for example, the threshold value A). If it is determined that the value is less than (value), it is determined that the exacerbation level 3 has a high risk of developing exacerbation.
- control unit 21 determines that the peak value of the active potential of the expiratory muscle is equal to or higher than the threshold value B of the active potential of the expiratory muscle at the time of exacerbation, it determines that the exacerbation level 4 has occurred. For example, when the exacerbation level 4 is determined, the control unit 21 may display information on the exacerbation on the display unit 25.
- the peak values of all action potentials are not limited to being equal to or higher than a predetermined threshold value.
- the terminal 2 may determine the exacerbation level by comparing the number of times the peak value of the activity potential per unit time is equal to or more than a predetermined threshold value with the predetermined number of times.
- the exacerbation level may be determined by the duration of the action potential of the expiratory muscle. For example, for a COPD patient, a threshold value for the duration of each action potential during normal time and exacerbation may be set, and whether or not exacerbation has occurred may be determined according to the set duration threshold value.
- control unit 21 determines that the duration of the action potential of the expiratory muscle is less than the threshold value of the duration of the action potential in the normal state, it determines that the exacerbation level 2 has a low risk of developing exacerbation. ..
- the control unit 21 determines that the duration of the active potential of the expiratory muscle is equal to or greater than the threshold of the duration of the active potential during normal operation and less than the threshold of the duration of the active potential during exacerbation, the exacerbation It is judged to be exacerbation level 3 with a high risk of developing.
- control unit 21 determines that the duration of the active potential of the expiratory muscle is equal to or greater than the threshold value of the duration of the active potential of the expiratory muscle at the time of exacerbation, it determines that the exacerbation level 4 has occurred.
- the exacerbation level may be determined based on both the threshold value of the action potential of the expiratory muscle and the threshold value of the duration. For example, in the control unit 21, the peak value of the action potential of the expiratory muscle is equal to or higher than the threshold value of the action potential at the time of exacerbation, and the duration of the action potential of the expiratory muscle is the duration of the action potential of the expiratory muscle at the time of exacerbation. If it is determined that the value is equal to or higher than the threshold value, it may be determined that the exacerbation level 4 has been exacerbated.
- the exacerbation level may be determined by the frequency distribution of the activity potential of the expiratory muscle.
- a COPD patient may be provided with a threshold value for the average frequency or the central frequency for each of the normal time and the exacerbation, and it may be determined whether or not the exacerbation has occurred according to the provided average frequency or the central frequency threshold. ..
- the exacerbation level may be determined using only the action potential information of both the inspiratory muscle and the expiratory muscle, or the action potential information of the inspiratory muscle.
- FIG. 11 is an explanatory diagram illustrating the operation of the detection process of information regarding exacerbation in COPD.
- the control unit 21 of the terminal 2 transmits the motion information regarding the movement of the respiratory muscle or the respiratory assist muscle from the detection sensor 3 and the action potential information for the respiratory muscle or the respiratory assist muscle from the electromyogram sensor 4 via the Bluetooth communication unit 26. get.
- the operation information and the activity potential information are time-series data measured at predetermined unit times (for example, minute increments, second increments, etc.). Further, the operation information and the activity potential information may be time-series waveform images. Furthermore, the operation information and the activity potential information may be frequency characteristic graphs.
- frequency analysis is performed from time-series data of motion information and activity potential information, and fluctuating waves corresponding to the movement of the thorax and the activity potentials of the respiratory muscles and respiratory assist muscles are extracted.
- frequency analysis for example, discrete Fourier transformation (DFT: Discrete Fourier Transformation) performed on a discrete signal may be used.
- the control unit 21 may store the acquired operation information and action potential information and centrally manage them, for example, using a time-series data infrastructure.
- the control unit 21 acquires various threshold values for detecting information on exacerbations in COPD from the master DB 172 of the large-capacity storage unit 17 of the server 1 via the communication unit 23. It should be noted that various thresholds for detecting information on exacerbations in COPD may be acquired in advance from the server 1 or may be stored in advance in the storage unit 22 of the terminal 2. For example, a predetermined threshold value of the motion electrical signal of the respiratory muscle, a predetermined threshold value of the electric signal of the electromyogram related to each exhaled muscle during normal time and exacerbation, and a predetermined duration of the electric signal of each expiratory muscle during normal time and exacerbation. The threshold value and the like are acquired.
- the control unit 21 determines whether or not the first condition is satisfied based on the operation information detected by the detection sensor 3. When the control unit 21 determines that the first condition is satisfied, the control unit 21 further detects information on exacerbation based on the action potential information related to the expiratory muscle and the predetermined threshold value acquired by the electromyogram sensor 4. The control unit 21 displays information on the detected exacerbation on the display unit 25.
- the control unit 21 may transmit to the detection sensor 3 and the electromyogram sensor 4 to the effect that the exacerbation has been detected via the Bluetooth communication unit 26, respectively.
- the control unit 31 of the detection sensor 3 may receive the fact that the exacerbation transmitted from the terminal 2 has been detected, and notify the COPD patient of an alarm, voice information, or the like by the speaker 35.
- the control unit 41 of the electromyogram sensor 4 may receive the fact that the exacerbation transmitted from the terminal 2 has been detected, and notify the COPD patient of an alarm, voice information, or the like by the speaker 45.
- action potential information related to the expiratory muscle was explained in the above processing, it is not limited to this.
- information on exacerbations may be detected based on action potential information on the inspiratory muscles or action potential information on both the inspiratory and expiratory muscles.
- the control unit 21 transmits the detected exacerbation information to the server 1 by the communication unit 23.
- the control unit 11 of the server 1 receives the information on the exacerbation transmitted from the terminal 2 by the communication unit 13, and stores the received information on the exacerbation in the patient DB 171 of the large-capacity storage unit 17.
- the present invention is not limited to the above-mentioned processing for detecting information on exacerbations.
- the terminal 2 detects information on exacerbations based on the range of movement of the thorax, the speed of movement of the chest, the stimulation time of the respiratory muscles, the frequency change of the action potential of the respiratory muscles, etc. acquired by the detection sensor 3 and the electromyogram sensor 4. You may.
- the terminal 2 measures the power spectrum of the electromyographic signal of the respiratory muscle and performs Fourier transform.
- the power spectrum is obtained by converting the myocardial waveform as the distribution of frequency components on the horizontal axis and the square of the amplitude of each frequency component (signal power) on the vertical axis.
- the terminal 2 calculates a change value of the average frequency (MPF: Mean Power Frequency) or the center frequency (MF: Median Power Frequency) as an index showing the characteristics of the power distribution of the spectrum.
- the average frequency is the average value of each frequency.
- the center frequency is the frequency that divides the area of the power spectrum into two equal areas.
- the terminal 2 determines whether or not it has a tendency of slowing down based on the calculated change value of the average frequency or the center frequency. For example, when gradually shifting from the high frequency band (for example, 86.4 Hz) to the low frequency band (for example, 67.4 Hz), the terminal 2 calculates the change value of the average frequency or the center frequency.
- the terminal 2 When the terminal 2 determines that the calculated change value is equal to or greater than a predetermined threshold value, the terminal 2 outputs information on exacerbation.
- the exacerbation level may be output according to each threshold provided with a plurality of thresholds. For example, when the change value is equal to or more than the first threshold value and less than the second threshold value, the exacerbation level 3 may be set, and when the change value is equal to or higher than the second threshold value, the exacerbation level 4 may be set.
- the electromyographic signal for frequency analysis all data including the expiratory muscle and the inspiratory muscle may be used, or data of either the expiratory muscle or the inspiratory muscle may be utilized.
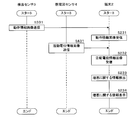
- FIG. 12 is a flowchart showing a processing procedure when detecting information on exacerbations in COPD.
- the control unit 31 of the detection sensor 3 transmits operation information regarding the operation of the respiratory muscle or the respiratory assist muscle to the terminal 2 via the Bluetooth communication unit 34 (step S301).
- the control unit 21 of the terminal 2 receives the operation information transmitted from the detection sensor 3 via the Bluetooth communication unit 26 (step S201).
- the control unit 41 of the electromyogram sensor 4 transmits action potential information for the respiratory muscle or the respiratory assist muscle to the terminal 2 via the Bluetooth communication unit 44 (step S401).
- the control unit 21 of the terminal 2 receives the action potential information transmitted from the electromyogram sensor 4 via the Bluetooth communication unit 26 (step S202).
- the control unit 21 transmits to the server 1 a request for acquiring various threshold values for detecting information on exacerbations in COPD via the communication unit 23 (step S203).
- the control unit 11 of the server 1 receives the threshold value acquisition request transmitted from the terminal 2 via the communication unit 13 (step S101).
- the control unit 11 acquires various thresholds for detecting information on exacerbations in COPD from the master DB 172 of the large-capacity storage unit 17 in response to the received threshold acquisition request (step S102).
- the control unit 11 transmits various acquired threshold values to the terminal 2 via the communication unit 13 (step S103).
- the control unit 21 of the terminal 2 receives various thresholds transmitted from the server 1 via the communication unit 23 (step S204).
- the control unit 21 determines whether or not the first condition is satisfied based on the received threshold value and operation information (step S205). Specifically, for example, the control unit 21 acquires a voltage from the detection sensor 3 in time series, and obtains the maximum of the acquired voltage in time series.
- the control unit 21 extracts the maximum voltage within a predetermined unit time (for example, 60 seconds) and calculates the slope of the approximate straight line formed by the extracted maximum. When the control unit 21 determines that the inclination exceeds a predetermined threshold, it determines that the first condition is satisfied.
- the control unit 21 extracts both the maximum and the minimum of the voltage for a predetermined unit time, calculates the maximum inclination of the approximate straight line formed by the extracted maximum, and minimizes the approximate straight line formed by the extracted minimum. Calculate the slope of.
- the control unit 21 has determined that the maximum tilt exceeds a predetermined maximum tilt threshold, the minimum tilt exceeds a preset minimum tilt threshold, and the duration exceeds a predetermined time (for example, 10 seconds). In this case, it is determined that the first condition is satisfied.
- the minimum tilt threshold value may be a value larger than the maximum tilt threshold value.
- control unit 21 determines that the first condition is not satisfied (NO in step S205)
- the control unit 21 ends the process.
- the control unit 21 executes a subroutine of processing for detecting the exacerbation level (step S206).
- the subroutine of the exacerbation level detection process will be described later.
- the control unit 21 displays the detected exacerbation information (exacerbation level) on the display unit 25 (step S208).
- the control unit 21 transmits the detected exacerbation information to the server 1 by the communication unit 23 (step S209).
- the control unit 11 of the server 1 receives the information regarding the exacerbation transmitted from the terminal 2 by the communication unit 13 (step S104).
- the control unit 11 stores the received information regarding the exacerbation in the patient DB 171 of the large-capacity storage unit 17 (step S105).
- the control unit 11 uses the patient ID, gender, name, abnormality (exacerbation) presence / absence information, abnormality detailed information, detected date / time information, sensor information used when the abnormality is detected, and used.
- the sensor data detected by the sensor is stored in the patient DB 171 as one record.
- the present invention when the first condition is satisfied, an example in which the level of exacerbation is determined by further using the activity potential information has been described, but the present invention is not limited to this. For example, even when the first condition is not satisfied, the level of exacerbation may be determined using the activity potential information.
- exacerbation determination processing (step S205) based on action information and exacerbation determination processing (step S206) based on action potential information
- the present invention is not limited to this.
- the exacerbation determination process (step S206) based on the action potential information may be performed first, and then the exacerbation determination process (step S205) may be performed based on the action potential information.
- the control unit 21 of the terminal 2 detects the exacerbation level by executing a subroutine of the process of detecting the exacerbation level.
- the control unit 21 determines whether or not the first condition is satisfied based on the operation information. When it is determined that the first condition is satisfied, the control unit 21 outputs information on exacerbation.
- the information on the exacerbation is provided. It may be detected. Specifically, the control unit 21 of the terminal 2 determines whether or not the first condition is satisfied based on the operation information. The control unit 21 detects the exacerbation level by executing a subroutine of processing for detecting the exacerbation level. For example, the control unit 21 outputs information on exacerbations when it is determined that the first condition is satisfied and the exacerbation risk is high at exacerbation level 3 or higher.
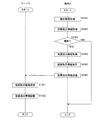
- FIG. 13 is a flowchart showing a processing procedure of a subroutine of processing for detecting an exacerbation level.
- the control unit 21 of the terminal 2 acquires the potential signal acquired from the EMG sensor 4 (step S01).
- the control unit 21 detects a periodic change in the potential of the intake muscle that is equal to or higher than a predetermined potential and exceeds a predetermined duration.
- the control unit 21 monitors the change in the expiratory muscle potential during the change in the inspiratory muscle potential.
- the control unit 21 detects the expiratory muscle potential during changes in the inspiratory muscle potential.
- the detection sensor 3 and the electromyogram sensor 4 may be used in combination to discriminate between the potential of the inspiratory muscle and the potential of the expiratory muscle.
- the detection sensor 3 is a stretch sensor or a tape sensor
- the tape stretches at the time of intake, so that the control unit 21 performs myoelectricity at the timing from the start of the tape stretch to the maximum stretch (MAX: elastic limit stretch).
- MAX elastic limit stretch
- the tape begins to shrink, so that the control unit 21 uses the potential signal acquired from the electromyogram sensor 4 to transmit the potential of the expiratory muscle at the timing from the maximum elongation (MAX) to the minimum elongation (MIN) of the tape. Is determined.
- a learning model learned using training data including a feature amount of activity potential waveform data acquired from the myocardiogram sensor 4 and a label indicating the potential of the inspiratory muscle and a label indicating the potential of the expiratory muscle is used. It may be possible to distinguish between the potential of the inspiratory muscle and the potential of the expiratory muscle. Furthermore, the one with the smaller average value of the amplitude of the action potential acquired from the electromyogram sensor 4 may be determined as the potential of the expiratory muscle.
- the control unit 21 determines whether or not the peak potential of the expiratory muscle is less than the threshold A (normal activity potential of the expiratory muscle) (step S02). When the control unit 21 determines that the peak potential of the expiratory muscle is less than the threshold value A (YES in step S02), the control unit 21 determines the exacerbation level 2 having a low risk of developing exacerbation (step S03). When the control unit 21 determines that the peak potential of the expiratory muscle is equal to or higher than the threshold A (NO in step S02), the peak potential of the expiratory muscle is less than the threshold B (for example, a value increased by 30% of the threshold A). Whether or not it is determined (step S04).
- control unit 21 determines that the peak potential of the expiratory muscle is less than the threshold value B (YES in step S04).
- the control unit 21 determines the exacerbation level 3 having a high risk of developing exacerbation (step S05).
- the control unit 21 determines the exacerbation level 4 in which the exacerbation has occurred (step S06).
- the control unit 21 returns the determination result of the determined exacerbation level (step S07), terminates the subroutine, and returns.
- the exacerbation level may be detected based on the action potential information related to the inspiratory muscle or the action potential information related to both the inspiratory muscle and the expiratory muscle.
- the peak potential of the action potential is used, but the present invention is not limited to this.
- the duration of the action potential, the frequency distribution of the action potential, and the like may be used. An example of using the duration will be described below.
- the control unit 21 detects the start timing and the end timing shown by the dotted line in FIG. 10B based on the change in the potential signal of the expiratory muscle. Specifically, the control unit 21 detects as a start timing the timing at which temporal changes exceeding a predetermined threshold value of the potential signal start to occur continuously. Further, the control unit 21 detects as the end timing the timing at which the temporal change of the potential signal that does not exceed a predetermined threshold value starts to occur continuously after detecting the start timing.
- the control unit 21 outputs information on exacerbation when the time from the start timing to the end timing exceeds a predetermined threshold value.
- a plurality of threshold values may be provided, and the exacerbation level may be set to 3 when the first threshold value or more and less than the second threshold value, and the exacerbation level 4 may be set when the second threshold value or more.
- this embodiment it is possible to detect an abnormality of a respiratory system disease based on the operation information acquired by the detection sensor 3 and the activity potential information acquired by the electromyogram sensor 4. This makes it possible to reduce the burden on the patient's body without collecting biological samples (for example, blood, serum, etc.) from the COPD patient undergoing the exacerbation test.
- biological samples for example, blood, serum, etc.
- the second embodiment relates to a mode in which information on exacerbations in COPD is detected by using an exacerbation detection model constructed by deep learning.
- the description of the contents overlapping with the first embodiment will be omitted.
- FIG. 14 is a block diagram showing a configuration example of the server 1 of the second embodiment.
- the contents overlapping with FIG. 2 are designated by the same reference numerals and the description thereof will be omitted.
- the large-capacity storage unit 17 includes an exacerbation detection model 173.
- the exacerbation detection model 173 is a detector that detects information about exacerbations in COPD, and is a trained model generated by machine learning.
- the trained model is used as a program module that is a part of artificial intelligence software. In the following, a process for detecting information on exacerbations will be described using the exacerbation detection model 173 constructed by deep learning.
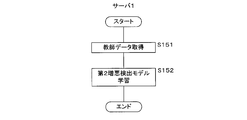
- FIG. 15 is an explanatory diagram relating to the generation process of the exacerbation detection model 173.
- FIG. 15 conceptually illustrates a process of performing machine learning to generate an exacerbation detection model 173. The generation process of the exacerbation detection model 173 will be described with reference to FIG.
- the server 1 in the present embodiment has an image of an electric signal related to the operation information acquired from the detection sensor 3 and a waveform image of the exacerbation portion in the image of the activity potential information acquired from the myocardiogram sensor 4.
- a neural network is constructed (generated) that takes a waveform image as an input and outputs information indicating the presence or absence of information on exacerbation in COPD.
- deep learning may be performed on the image after frequency analysis.
- the neural network is, for example, a CNN (Convolutional Neural Network), and extracts an input layer that accepts input of a waveform image, an output layer that outputs information (identification result) indicating the presence or absence of an abnormality, and an image feature amount of the waveform image. It has an intermediate layer.
- a CNN Convolutional Neural Network
- the input layer has a plurality of neurons that accept the input of the pixel value of each pixel included in the waveform image, and passes the input pixel value to the intermediate layer.
- the intermediate layer has a plurality of neurons for extracting image features of a waveform image, and passes the extracted image features to the output layer.
- the exacerbation detection model 173 is CNN
- the intermediate layer alternates between a convolution layer that convolves the pixel values of each pixel input from the input layer and a pooling layer that maps the pixel values convoluted by the convolution layer. It has a configuration connected to, and finally extracts the feature amount of the image while compressing the pixel information of the waveform image.
- the output layer has one or a plurality of neurons that output identification results that identify the exacerbation points in COPD, and identifies the presence or absence of information on exacerbations based on the image features output from the intermediate layer.
- the exacerbation detection model 173 is described as being a CNN, but the exacerbation detection model 173 is not limited to CNN, and is a neural network other than CNN, SVM (Support Vector Machine), Bayesian network, and regression tree. Etc., it may be a trained model constructed by another learning algorithm.
- the input 1 is a waveform image of the motion information of the respiratory muscles for a predetermined time (for example, 60 seconds) detected by the detection sensor 3, and the input 2 is a predetermined value detected by the electromyogram sensor 4. It is a waveform image of action potential information relating to a respiratory muscle for a time (for example, 60 seconds).
- the waveform image of the operation information (input 1) and the waveform image of the action potential information (input 2) are waveform images showing signals at the same timing.
- the control unit 11 of the server 1 detects and outputs information on the exacerbation from the waveform images of the input operation information and action potential information in accordance with the command from the learned exacerbation detection model 173 stored in the memory.
- the output information regarding the exacerbation may be, for example, information on the presence or absence of exacerbation, an exacerbation probability value, an exacerbation level classified according to the exacerbation probability value, or the like.
- the waveform image (input 2) of the activity potential information related to the respiratory muscle described above is a waveform image showing the change in potential formed by synthesizing the change in the potential of the inspiratory muscle and the change in the potential of the expiratory muscle.
- the input 2 may be a waveform image showing only the change in the expiratory myoelectric potential or only the change in the inspiratory myoelectric potential.
- an image obtained by combining input 1 and input 2 may be input to the exacerbation detection model 173.
- input 1 may be time-series data of motion information of the respiratory muscles
- input 2 may be time-series data of activity potential information related to the respiratory muscles.
- the input 1 and the input 2 may be a combination of the waveform image and the time series data.
- the server 1 performs learning using the teacher data in which the image of the electric signal and the image of the activity potential information related to the operation information and the information related to the exacerbation in each image are associated with each other.
- the teacher data is data in which an image of an electric signal related to operation information, an image of action potential information, and information related to exacerbation are labeled.
- the server 1 inputs a waveform image, which is teacher data, to the input layer, performs arithmetic processing in the intermediate layer, and acquires an identification result indicating the presence or absence of exacerbation in COPD from the output layer.
- the identification result output from the output layer may be a value discretely indicating the presence or absence of exacerbation (for example, a value of "0" or "1"), and a continuous probability value (for example, "0" to "1"). It may be a value in the range up to 1 ”).
- the server 1 acquires, as the identification result output from the output layer, the identification result that identifies the probability value of the exacerbation in addition to the presence or absence of the exacerbation in COPD.
- the probability values of each of a plurality of levels for example, levels 1 to 4, may be output from the output layer.
- the server 1 compares the identification result output from the output layer with the information labeled for the waveform image in the teacher data, that is, the correct answer value, and the intermediate layer so that the output value from the output layer approaches the correct answer value.
- the parameters are, for example, the weight between neurons (coupling coefficient), the coefficient of the activation function used in each neuron, and the like.
- the method of optimizing the parameters is not particularly limited, but for example, the server 1 optimizes various parameters by using the error back propagation method.
- the server 1 performs the above processing on each waveform image included in the teacher data, and generates an exacerbation detection model 173.
- the server 1 acquires an image of an electric signal related to operation information from the detection sensor 3 and an image of action potential information from the electromyogram sensor 4, the server 1 follows a command from the learned exacerbation detection model 173 stored in the memory. Detect information about exacerbations in COPD.
- the server 1 generates the trained exacerbation detection model 173 and then the terminal 2 downloads and installs the trained exacerbation detection model 173, the terminal 2 uses the trained exacerbation detection model 173. Information about exacerbations may be detected.
- the terminal 2 acquires an image of the electric signal related to the operation information from the detection sensor 3 and an image of the action potential information from the electromyogram sensor 4, and detects the information related to the exacerbation using the exacerbation detection model 173.
- the terminal 2 may perform learning or re-learning processing on the exacerbation detection model 173 using the teacher data.
- the waveform image is used as the input value of the exacerbation detection model 173, but the present invention is not limited to this.
- a neural network related to RNN Recurrent Neural Network
- the operation information acquired from the detection sensor 3 and the time-series data of the activity potential information acquired from the electrocardiogram sensor 4 may be used as input values to detect the exacerbation in COPD.
- the learning model is a first learning model learned based on teacher data including motion information and information on exacerbations, and a second learning model learned based on teacher data including activity potential information and information on exacerbations. You may prepare two.
- the first learning model uses the voltage waveform shown in FIG. 8, the voltage waveform image, the frequency waveform obtained by frequency-converting the voltage waveform, or the frequency waveform image as input data, and the probability of exacerbation as output data.
- the server 1 learns the first learning model based on these teacher data.
- the second learning model uses the action potential waveform, the action potential waveform image, the frequency waveform obtained by frequency-converting the action potential waveform, or the frequency waveform image related to the inspiratory muscle and the expiratory muscle shown in FIGS. 10A and 10B as input data, and exacerbates the problem. Let the probability of be the output data.
- the server 1 learns the second learning model based on these teacher data.
- the second learning model may be trained based only on the waveform image of the expiratory muscle or the inspiratory muscle.
- the estimation processing by the second learning model is performed.
- the control unit 21 inputs an action potential waveform, an action potential waveform image, a frequency waveform obtained by frequency-converting the action potential waveform, or the frequency waveform image related to the inspiratory muscle and the expiratory muscle into the second learning model.
- the control unit 21 outputs the probability of exacerbation from the second learning model.
- the order of estimation processing by the first learning model and the second learning model described above is not limited. For example, if the estimation process by the second learning model is performed and the probability of exacerbation output from the second learning model is equal to or greater than a predetermined threshold value, the estimation process by the first learning model may be performed. Alternatively, the estimation process by the first learning model and the estimation process by the second learning model are performed in parallel, and the exacerbation is determined based on the exacerbation probability output by the first learning model and the second learning model. good.
- the first condition may be determined by the method of the first embodiment, and the second learning model may be used for the action potential waveform. Further, the first learning model may be used for the first condition, and the action potential waveform may be determined by the method of the first embodiment.
- FIG. 16 is a flowchart showing an example of the processing procedure of the generation processing of the exacerbation detection model 173. The processing content of the generation process of the exacerbation detection model 173 will be described with reference to FIG.
- the control unit 11 acquires teacher data in which the image of the motion information acquired by the detection sensor 3 and the image of the activity potential information acquired by the electromyogram sensor 4 are associated with the information on the exacerbation in COPD (step). S121).
- the teacher data is data in which, for example, images of motion information and action potential information and information on exacerbations (for example, a probability value of exacerbations) are labeled.
- the control unit 11 outputs information (for example, levels 1 to 4) indicating the presence or absence of information on exacerbations in COPD when waveform images of motion information and action potential information are input using a plurality of teacher data.
- An exacerbation detection model 173 (trained model) is generated (step S122). Specifically, the control unit 11 inputs the waveform image, which is the teacher data, to the input layer of the neural network, and acquires the identification result of identifying the information regarding the exacerbation from the output layer. The control unit 11 compares the acquired identification result with the correct answer value of the teacher data (information labeled for the waveform image), and in the intermediate layer so that the identification result output from the output layer approaches the correct answer value. Optimize the parameters (weights, etc.) used for arithmetic processing. The control unit 11 stores the generated exacerbation detection model 173 in the large-capacity storage unit 17, and ends a series of processes.
- FIG. 17 is an explanatory diagram regarding the detection process of information related to exacerbation using the exacerbation detection model 173.
- FIG. 17 conceptually illustrates how information regarding exacerbations in COPD is detected from a waveform image. The detection process of information regarding exacerbation in COPD will be described with reference to FIG.
- the control unit 21 of the terminal 2 in which the trained exacerbation detection model 173 is installed receives an image of an electric signal related to operation information from the detection sensor 3 and an activity potential information from the myocardiogram sensor 4 via the Bluetooth communication unit 26. Get an image.
- the operation information and action potential information are not limited to the above-mentioned waveform image, but may be time series data.
- the control unit 21 may generate a waveform image based on the acquired time-series data.
- the control unit 21 inputs an image of an electric signal related to the acquired operation information and an image of the activity potential information into the exacerbation detection model 173.
- the control unit 21 performs arithmetic processing for extracting the feature amount of the waveform image in the intermediate layer of the exacerbation detection model 173, inputs the extracted feature amount to the output layer of the exacerbation detection model 173, and determines whether or not there is an exacerbation in COPD. Get the information as output. As shown in the figure, the control unit 21 outputs an exacerbation level information (for example, exacerbation level 1 to exacerbation level 4) classified according to the exacerbation probability value and the exacerbation probability value. When the control unit 21 detects information on the exacerbation from the waveform image using the exacerbation detection model 173, the control unit 21 displays the detection result indicating that the information on the exacerbation in COPD has been detected on the display unit 25.
- an exacerbation level information for example, exacerbation level 1 to exacerbation level 4
- the control unit 21 displays the detection result indicating that the information on the exa
- FIG. 18 is a flowchart showing a processing procedure when detecting information related to exacerbation using the exacerbation detection model 173.
- the control unit 31 of the detection sensor 3 transmits an image of an electric signal related to the operation information to the terminal 2 via the Bluetooth communication unit 34 (step S331).
- the control unit 21 of the terminal 2 in which the trained exacerbation detection model 173 is installed receives an image of an electric signal related to the operation information transmitted from the detection sensor 3 via the Bluetooth communication unit 26 (step S231).
- control unit 21 may receive the raw data of the electric signal related to the operation information from the detection sensor 3 by the Bluetooth communication unit 26.
- the control unit 21 may input the raw data of the received electric signal into the deeply trained image generation model, and output the image of the electric signal by using the image generation model.
- the control unit 41 of the EMG sensor 4 transmits an image of action potential information to the terminal 2 via the Bluetooth communication unit 44 (step S431).
- the control unit 21 of the terminal 2 receives an image of the activity potential information transmitted from the electromyogram sensor 4 via the Bluetooth communication unit 26 (step S232).
- the control unit 21 detects information on the exacerbation in COPD using the exacerbation detection model 173 (step S233), and displays the information on the detected exacerbation on the display unit 25 (step S234).
- the third embodiment relates to a mode for detecting an abnormality of a respiratory system disease by further adding a patient's biological information to the motion information regarding the movement of the respiratory muscle or the respiratory assist muscle and the activity potential information for the respiratory muscle or the respiratory assist muscle. ..
- a mode for detecting an abnormality of a respiratory system disease by further adding a patient's biological information to the motion information regarding the movement of the respiratory muscle or the respiratory assist muscle and the activity potential information for the respiratory muscle or the respiratory assist muscle. ..
- COPD which is one of the respiratory diseases
- the present embodiment includes a second sensor 5 that detects the biological information of the patient.
- the second sensor 5 records, for example, an oximeter for detecting percutaneous arterial blood oxygen saturation, a microphone for collecting biological sounds emitted from the living body, and an active potential or current of the myocardium accompanying the beating of the heart.
- an electrocardiograph capable of analyzing RRI (RR Interval) and CV-RR (Coefficient of Variation RR interval), a blood pressure monitor that detects blood pressure, a body thermometer that detects body temperature, and percutaneous arterial blood carbon dioxide partial pressure (PtcCO2) ), A pulse rate monitor that measures the number of heartbeats, a heart rate variability measuring device that analyzes the frequency of the heartbeat, a biopotential sensor that measures the bioimpedance, a sweating sensor, and the like.
- RRI RR Interval
- CV-RR Coefficient of Variation RR interval
- PtcCO2 percutaneous arterial blood carbon dioxide partial pressure
- the bioelectric potential sensor detects changes in bioelectrical impedance with respiration.
- the change in bioelectrical impedance is the amount of change in thoracic impedance according to the change in lung volume due to ventilation by measuring the thoracic impedance (Z) obtained by energizing a high-frequency current from an electrode placed on the thoracic cavity.
- the ventilation state is grasped by using the sex impedance ( ⁇ Z). That is, the variation of thoracic impedance due to respiration (Z) ( ⁇ Z) is changed according to intrapulmonary air amount variation of the (V L) ( ⁇ V L) .
- [Delta] Z alpha (non-negative proportionality factor) ⁇ [Delta] V L and can be assumed.
- the amount of change in thoracic impedance ⁇ Z increases with inspiration ( ⁇ Z> 0) and decreases with exhalation ( ⁇ Z ⁇ 0). Therefore, the ventilation volume of the lungs can be estimated by measuring the biopotential im
- the second sensor 5 may be a non-contact type vital sensor installed under a bed or bedding without touching the human body.
- the non-contact type vital sensor measures minute movements (heartbeat / breathing) on the body surface accompanying respiratory movements and heartbeats with a small microwave radar, and infrared rays (body temperature) emitted from the body surface with an infrared thermo camera. ) Is measured.
- the biological information is a signal that reflects the state of the biological tissue and information when the tissue is functioning, and is, for example, a signal emitted from the body by a biological phenomenon such as pulse, body movement, or breathing.
- FIG. 19 is an explanatory diagram for explaining the operation of the detection process of information regarding exacerbation by adding the second sensor 5.
- FIG. 19 an example of detecting information on exacerbation in COPD using one type of microphone of the second sensor 5 will be described.
- information on exacerbation may be detected by using, for example, a plurality of second sensors 5.
- a microphone is a sound sensor that collects biological sounds emitted from a living body.
- a microphone can be used to acquire biological sound information including breathing sound, coughing sound, sputum storage sound, lung noise, etc., and frequency analysis can also be performed, and this information is input to a learning model.
- PtcCO2 percutaneous arterial blood carbon dioxide partial pressure
- thermometer When using a thermometer, input the body temperature obtained from the thermometer into the learning model.
- the exacerbation may be triggered by a respiratory infection caused by a bacterium or a virus, and in such a case, an increase in body temperature is observed as an inflammatory finding.
- learning the learning model the learning process is performed using teacher data including motion information, action potential information, body temperature, and exacerbation level obtained based on the history.
- the learning model When using a pulse rate monitor, input the pulse rate per unit time or the temporal change of the pulse rate into the learning model. At the time of exacerbation, the sympathetic nerve becomes dominant as described above, and this causes an increase in the pulse rate.
- the learning process is performed using the teacher data including the motion information, the activity potential information, the pulse rate, and the exacerbation level obtained based on the history.
- the temporal change of the LF (low frequency) / HF (high frequency) ratio or the LF / HF ratio per unit time is input to the learning model.
- the sympathetic nerve becomes dominant as described above, and as a result, an increase in the LF / HF ratio is observed.
- the learning process is performed using the teacher data including the motion information, the activity potential information, the LF / HF ratio, and the exacerbation level obtained based on the history.
- the temporal change of the thoracic impedance change amount ⁇ Z or the thoracic impedance change amount ⁇ Z per unit time is input to the learning model.
- the learning process is performed using the teacher data including the motion information, the activity potential information, the change amount ⁇ Z of the thoracic impedance, and the exacerbation level obtained based on the history.
- the learning model When using a sweating sensor, input the amount of sweating per unit time or the temporal change of the amount of sweating into the learning model. At the time of exacerbation, the sympathetic nerve becomes dominant as described above, and an increase in the amount of sweating is observed.
- the learning process is performed using the teacher data including the motion information, action potential information, sweating amount, and exacerbation level obtained based on the history.
- a plurality of the second sensors described above may be combined and input to the learning model.
- the control unit 21 of the terminal 2 transmits the motion information regarding the movement of the respiratory muscle or the respiratory assist muscle from the detection sensor 3 and the action potential information for the respiratory muscle or the respiratory assist muscle from the electromyogram sensor 4 via the Bluetooth communication unit 26. get.
- the control unit 21 acquires biological sound information from the microphone via the Bluetooth communication unit 26.
- biological sound information such as frequency, intensity, duration or sound quality may be acquired for breathing sound, coughing sound, sputum storage sound, and lung noise.
- the control unit 21 detects information on exacerbations in COPD based on the acquired motion information, action potential information, and biological sound information.
- information on exacerbations may be detected by further adding biological sound information.
- the control unit 21 of the terminal 2 detects information on exacerbation based on operation information and activity potential information, it continuously determines exacerbation based on biological sound information (for example, breathing sound) acquired by a microphone. ..
- biological sound information for example, breathing sound
- the control unit 21 exacerbates based on biological sound information. Detect information about.
- the control unit 21 displays information on the detected exacerbation on the display unit 25.
- the control unit 21 transmits the detected exacerbation information to the server 1 via the communication unit 23.
- the control unit 11 of the server 1 receives the information on the exacerbation transmitted from the terminal 2 by the communication unit 13, and stores the received information on the exacerbation in the patient DB 171 of the large-capacity storage unit 17.
- the second sensor 5, the detection sensor 3, and the electromyogram sensor 4 are shown separately in the present embodiment, they may be integrally configured. Further, the place where the second sensor 5 is arranged is not limited to a specific part of the body, and may be a non-contact type. Further, in the present embodiment, the terminal 2 and the second sensor 5 are shown separately, but the present invention is not limited to this.
- the device configuration may be such that the terminal 2, the detection sensor 3, the electromyogram sensor 4, and the second sensor 5 are all integrated, or the device configuration in which the terminal 2 and the second sensor 5 are integrated (for example, a wristwatch). It may be a wearable device such as a type mobile terminal).
- a clock-type second sensor 5 may be attached to the user, and when an abnormality is detected by the second sensor 5, the detection sensor 3 and the electromyogram sensor 4 may be attached to the user's body. ..
- FIG. 20 is a flowchart showing a processing procedure when a microphone is added to detect information related to exacerbation.
- the contents overlapping with FIG. 12 are designated by the same reference numerals and the description thereof will be omitted.
- the control unit 21 of the terminal 2 acquires biological sound information (for example, breath sounds) from the microphone via the Bluetooth communication unit 26 (step S241).
- biological sound information for example, breath sounds
- the control unit 21 determines whether or not the breath sounds are attenuated (step S242).
- the determination process of the attenuation of the breath sounds for example, the frequency of the breath sounds may be used for the determination.
- step S242 When the control unit 21 determines that the acquired breathing sound is not attenuated (NO in step S242), the control unit 21 ends the process. When the control unit 21 determines that the acquired breathing sound is attenuated (YES in step S242), the control unit 21 executes step S207.
- FIG. 20 has described an example of one breath sound of biological sound information, but the present invention is not limited to this. Information on exacerbations in COPD may be detected by other coughing sounds, sputum storage sounds, lung noise, or a combination of the various sound information described above.
- the above-mentioned process is an example in which an exacerbation determination process based on motion information (step S205) and an exacerbation determination process based on active potential information (step S206) are followed by determination of whether or not the breathing sound is attenuated (step S242).
- it is not limited to this. For example, it is first determined whether or not the breath sounds are attenuated (step S242), then an action potential information exacerbation determination process (step S206), and then an action potential exacerbation determination process (step S205). , Information about exacerbations may be detected.
- step S242 the determination of whether or not the breath sounds are attenuated (step S242), the exacerbation determination process based on the motion information (step S205), and the exacerbation determination process based on the action potential information (step S206) are performed in parallel to perform the three parties.
- Information on the exacerbation may be detected when the exacerbation determination condition derived using the above is satisfied.
- FIG. 21 is a block diagram showing a configuration example of the server 1 of the third embodiment.
- the contents overlapping with FIG. 14 are designated by the same reference numerals and the description thereof will be omitted.
- the large-capacity storage unit 17 includes a second exacerbation detection model 174.
- the second exacerbation detection model 174 is an exacerbation detection model constructed by deep learning.
- the second exacerbation detection model 174 performs deep learning to learn the feature amount of the waveform image of the exacerbation portion in the image of the electric signal related to the operation information, the image of the activity potential information, and the biological signal image acquired by the second sensor 5.
- a neural network is constructed (generated) that takes a waveform image as an input and outputs information indicating the presence or absence of information on exacerbations in COPD. Since the generation process of the second exacerbation detection model 174 is the same as the generation process of the exacerbation detection model 173 of the first embodiment, the description thereof will be omitted.
- FIG. 22 is a flowchart showing a processing procedure when detecting information related to exacerbation using the second exacerbation detection model 174.
- the contents overlapping with FIG. 18 are designated by the same reference numerals and the description thereof will be omitted.
- the second sensor 5 transmits an image of biometric information to the terminal 2 using Bluetooth communication (step S541).
- the control unit 21 of the terminal 2 receives an image of biometric information transmitted from the second sensor 5 via the Bluetooth communication unit 26 (step S243).
- the biological information may be, for example, oxygen dissociation curve data acquired by an oximeter that detects percutaneous arterial oxygen saturation. When a COPD patient has an exacerbation, the percutaneous oxygen concentration decreases, so that information on the exacerbation can be detected based on the image of the oxygen dissociation curve data. It is not limited to percutaneous arterial oxygen saturation.
- the image of the biological information may be, for example, a flag indicating a temporal change of the time series data with respect to the respiratory rate or the heart rate, a waveform data of a microphone, or the like.
- the control unit 21 detects information regarding the exacerbation in COPD using the second exacerbation detection model 174 installed in the terminal 2 (step S244).
- the process of detecting information on exacerbations using the second exacerbation detection model 174 is the same as the process of detecting information on exacerbations using the exacerbation detection model 173 of the first embodiment, and thus the description thereof will be omitted.
- FIG. 23 is a flowchart showing an example of the processing procedure of the learning process of the second exacerbation detection model 174.
- the processing content of the learning process of the second exacerbation detection model 174 will be described with reference to FIG. 23.
- the control unit 11 includes an image of motion information acquired by the detection sensor 3, an image of action potential information acquired by the electromyogram sensor 4, an image of biological information acquired by the second sensor 5, and information on exacerbations in COPD.
- the teacher data is data in which, for example, images of motion information, action potential information, and biological information, and information related to exacerbations (for example, exacerbation probability value, etc.) are labeled.
- the control unit 11 learns the second exacerbation detection model 174 that outputs information regarding the presence or absence of exacerbation when images of motion information, action potential information, and biological information are input using the teacher data (step S152). Specifically, the control unit 11 inputs the waveform image, which is the teacher data, to the input layer of the neural network, and acquires the identification result of identifying the information regarding the exacerbation from the output layer. The control unit 11 compares the acquired identification result with the correct answer value of the teacher data (information labeled for the waveform image), and in the intermediate layer so that the identification result output from the output layer approaches the correct answer value. Optimize the parameters (weights, etc.) used for arithmetic processing. The control unit 11 stores the learned second exacerbation detection model 174 in the large-capacity storage unit 17, and ends a series of processes.
- the abnormality of the respiratory system disease is detected based on the operation information acquired by the detection sensor 3, the action potential information acquired by the electromyogram sensor 4, and the biological information acquired by the second sensor 5. Can be done.
- biometric information is used as an auxiliary means, and information on exacerbations is detected together with motion information and action potential information.
- information on the exacerbation is erroneously detected by the detection process of the first embodiment, the information on the exacerbation can be corrected based on the biological information.
- the fourth embodiment relates to a mode in which an abnormality of a respiratory system disease is detected by using a third sensor that further detects activity (exercise) information based on the third embodiment.
- a third sensor that further detects activity (exercise) information based on the third embodiment.
- the third sensor 6 detects activity information including the patient's momentum, distance traveled, activity amount or posture, and is, for example, an acceleration sensor, a GPS (Global Positioning System / Global Positioning Satellite) sensor, a gyro sensor (angular velocity sensor), or the like. is there.
- activity (exercise) information may be detected by using a plurality of third sensors 6.
- FIG. 24 is a block diagram showing a configuration example of the server 1 of the fourth embodiment.
- the contents overlapping with FIG. 21 are designated by the same reference numerals and the description thereof will be omitted.
- the large-capacity storage unit 17 includes an advice DB 175 and a walking model 176.
- the advice DB 175 stores advice information according to the activity content, information on exacerbation, and the like.
- the activity content includes, for example, walking, biking, climbing stairs, jogging, breathing rehabilitation exercise, etc., and is acquired by the third sensor 6.
- the control unit 21 of the terminal 2 monitors physical activity using an acceleration sensor, acquires acceleration data (activity information) such as posture, speed, and moving distance, and specifies the activity content according to the acquired acceleration data.
- acceleration data activity information
- the identification of the activity content is not limited to the above-mentioned specific processing. For example, when a screen on which the activity content can be selected is displayed to the user, the activity content may be specified by the user's touch operation.
- the walking model 176 is a dedicated exacerbation detection model constructed by deep learning when the activity content is walking. For example, an image of an electric signal related to operation information, an image of action potential information, and a biological signal image acquired by the second sensor 5 are input to the walking model 176.
- the walking model 176 uses the waveform image as an input by performing deep learning to learn the feature amount of the waveform image of the exacerbation part in the input image according to the walking, and provides information indicating the presence or absence of information on the exacerbation in COPD. Build (generate) the neural network to be the output. Since the generation process of the walking model 176 is the same as the generation process of the exacerbation detection model 173 of the first embodiment, the description thereof will be omitted.
- the walking model 176 may be generated based on the motion information and the action potential information without using the biological signal image by the second sensor 5.
- each model for example, a bicycle model, a stair climbing model, a jogging model, a respiratory rehabilitation model, etc.
- each model for example, a bicycle model, a stair climbing model, a jogging model, a respiratory rehabilitation model, etc.
- an activity to be respiratory rehabilitation is specified, an image of an electric signal related to motion information, an image of activity potential information, and a biological signal image acquired by the second sensor 5 are input, and information related to exacerbation in COPD is output.
- a trained respiratory rehabilitation model may be used to detect exacerbation information.
- the respiratory rehabilitation model is an image of motion information during respiratory rehabilitation detected by the detection sensor 3, an image of activity potential information during respiratory rehabilitation detected by the electromyogram sensor 4, and a biological signal image acquired by the second sensor 5.
- information on exacerbation is detected according to the physical reaction status at the time of respiratory rehabilitation.
- FIG. 25 is an explanatory diagram showing an example of the record layout of the master DB 172 of the third embodiment.
- the contents overlapping with FIG. 4 are designated by the same reference numerals and the description thereof will be omitted.
- the master DB 172 includes an activity content column.
- the activity content column remembers the type of action according to the physical activity. For example, the activity content is stair climbing, walking, etc.
- FIG. 26 is an explanatory diagram showing an example of the record layout of the advice DB 175.
- the advice DB 175 includes an advice ID column, an activity content column, an exacerbation information column, and an advice column.
- the advice ID column stores the ID of the advice that is uniquely identified in order to identify each advice.
- the activity content column remembers the type of action according to the physical activity.
- the exacerbation information sequence stores information about exacerbations.
- the advice column stores advice information for the patient according to the activity content and information on exacerbation.
- FIG. 27 is a flowchart showing a processing procedure when transmitting advice information according to the activity content.
- the control unit 21 of the terminal 2 acquires motion information regarding the operation of the respiratory muscle or the respiratory assist muscle from the detection sensor 3 via the bluetooth communication unit 26 (step S261), and the respiratory muscle or the respiratory assist from the electromyogram sensor 4.
- the action potential information for the muscle is acquired (step S262).
- the control unit 21 acquires biometric information by the second sensor 5 (step S263) via the Bluetooth communication unit 26, and acquires the activity information including the patient's exercise amount, movement distance, activity amount or posture by the third sensor 6. (Step S264).
- the control unit 21 specifies the activity content based on the acquired activity information (step S265).
- the control unit 21 detects information on exacerbations based on the acquired motion information, activity potential information, and biological information (step S266). Since the detection process of information related to exacerbation is the same as the detection process in the third embodiment, the description thereof will be omitted.
- the control unit 21 transmits an advice acquisition request to the server 1 via the communication unit 23 based on the detected exacerbation information and the specified activity content (step S267).
- the control unit 11 of the server 1 receives the advice acquisition request transmitted from the terminal 2 via the communication unit 13 (step S161).
- the control unit 11 acquires advice information from the advice DB 175 of the large-capacity storage unit 17 in response to the received advice acquisition request (step S162).
- the control unit 11 transmits the acquired advice information to the terminal 2 via the communication unit 13 (step S163).
- the control unit 21 of the terminal 2 receives the advice information transmitted from the server 1 by the communication unit 23 (step S268), and displays the received advice information by the display unit 25 (step S269).
- the advice information "Let's match the rhythm of breathing! May be displayed to a patient who is jogging at exacerbation level 2 (low risk).
- the advice information "Stop and adjust your breathing! May be displayed to the patient who is climbing the stairs with exacerbation level 3 (high risk).
- the advice information "Use a short-acting inhaled ⁇ 2 stimulant!” May be displayed to a walking patient with exacerbation level 4 (exacerbation).
- the process of detecting information on exacerbations in COPD using a model for each activity constructed by machine learning will be described.
- the description will be based on the walking model 176 that can be used when walking, but the same can be applied to other activity contents. Since the amount of exercise, amount of activity, posture, etc. differ depending on the activity content, it also affects the detection result of detecting information on exacerbation in COPD.
- deep learning for a specific activity for example, walking
- the waveform image is input and the presence or absence of information on exacerbation in COPD is performed. It is possible to construct a neural network that outputs information indicating the above. Therefore, the accuracy of detecting information on the exacerbation of COPD in the specific activity is increased by using the trained dedicated model.
- FIG. 28 is a flowchart showing a processing procedure when detecting information on exacerbation using the walking model 176.
- the contents overlapping with FIG. 27 are designated by the same reference numerals and the description thereof will be omitted.
- the control unit 21 of the terminal 2 specifies a trained activity learning model according to the activity content specified in step S265 (step S270). For example, when the control unit 21 specifies the activity content to be walking from the activity information acquired in step S264, the control unit 21 identifies the walking model 176 installed in advance and detects the information on the exacerbation in COPD. That is, by using the learned activity learning model for each activity content, it is possible to detect highly accurate information on exacerbations in COPD.
- the control unit 21 of the terminal 2 acquires the activity information detected by the third sensor 6 via the Bluetooth communication unit 26.
- the control unit 21 specifies the activity content according to the acquired activity information. Based on the specified activity content, the control unit 21 acquires a predetermined threshold value of an electric signal for determining the activity potential information acquired by the myocardiogram sensor 4 from the master DB 172 of the large-capacity storage unit 17 of the server 1.
- the control unit 21 performs a determination process when detecting information on exacerbation based on the acquired new threshold value. For example, when the control unit 21 of the terminal 2 specifies the activity content as walking, the control unit 21 outputs an action potential information for determining the action potential information corresponding to walking from the master DB 172 of the large-capacity storage unit 17 of the server 1. Acquire a predetermined threshold. In the case of walking, since the amount of exercise increases, the threshold value of the electric signal for detecting information on exacerbation becomes higher than the threshold value at rest.
- the present invention is not limited to this. It is possible to change the first condition for determining the operation information acquired by the detection sensor 3 and the predetermined threshold value of the biological information for determining the biological information acquired by the second sensor 5. For example, when the terminal 2 performs the exacerbation detection process using the detection sensor 3, the operation electric signal threshold value of the expiratory muscle is changed according to the activity content. For example, when the terminal 2 specifies the activity content as walking, the amount of exercise increases, so that the maximum inclination threshold value or the minimum inclination threshold value of the voltage is changed to a high value.
- various threshold values of the second sensor 5 may be changed according to the activity content.
- the control unit 21 of the terminal 2 acquires voice data.
- the control unit 21 frequency-converts the audio data and determines whether or not the power of the specific frequency band exceeds a predetermined threshold value. If the control unit 21 exceeds a predetermined threshold value, it determines that there is a possibility of exacerbation, and makes a determination using the detection sensor 3 and the electromyogram sensor 4.
- the control unit 21 changes the above-mentioned predetermined threshold value according to the activity content.
- the process is not limited to the process of changing the predetermined threshold value according to the activity content described above.
- the predetermined threshold value of the electric signal for determining the action potential information acquired by the electromyogram sensor 4 may be changed according to the output probability value of exacerbation.
- FIG. 29 is a flowchart showing a processing procedure when changing a predetermined threshold value of an electric signal according to a probability value of exacerbation.
- the control unit 21 of the terminal 2 in which the trained exacerbation detection model 173 is installed acquires motion information regarding the motion of the respiratory muscle or the respiratory assist muscle from the detection sensor 3 via the Bluetooth communication unit 26 (step S271).
- the control unit 21 acquires action potential information for the respiratory muscle or the respiratory assist muscle from the electromyogram sensor 4 via the Bluetooth communication unit 26 (step S272).
- the control unit 21 detects information on the exacerbation in COPD using the exacerbation detection model 173 (step S273).
- the control unit 21 acquires an exacerbation probability value from the detected exacerbation information (step S274). For example, if the acquired probability value of exacerbation is 0.3, there is a risk of exacerbation, so it is necessary to change the predetermined threshold value of the electrical signal for determining the action potential information acquired by the electromyogram sensor 4. It becomes.
- the control unit 21 transmits the acquired probability value of exacerbation to the server 1 via the communication unit 23 (step S275).
- the probability value of exacerbation transmitted from the terminal 2 is received via the control unit 11 and the communication unit 13 of the server 1 (step S171).
- the control unit 11 calculates a predetermined threshold value of the electric signal for determining the action potential information acquired by the EMG sensor 4 according to the received probability value of exacerbation (step S172).
- the calculation algorithm for example, when there is a risk of exacerbation, it may be calculated by multiplying a predetermined threshold value of an existing electric signal by a coefficient between 0 and 1. That is, when there is a risk of developing exacerbations, the criteria for detecting exacerbations become strict.
- the control unit 11 updates the calculated predetermined threshold value of the electric signal to the master DB 172 of the large-capacity storage unit 17 (step S173).
- the third sensor 6 is a gyro sensor.
- the terminal 2 uses the detection sensor 3 for motion information regarding the movement of the respiratory muscle or the respiratory assist muscle, the electromyogram sensor 4 for the activity potential information for the respiratory muscle or the respiratory assist muscle, and the gyro sensor for the wobbling of the foot. Get the value.
- the terminal 2 determines whether or not the acquired foot wobble value is equal to or greater than a predetermined threshold value.
- the terminal 2 determines that the acquired foot wobble value is equal to or higher than a predetermined threshold value, the terminal 2 detects information on exacerbation based on the acquired motion information and action potential information by the same processing as in the first embodiment.
- the gyro sensor data acquired by the gyro sensor may be input, and a learned wobbling detection model for detecting the wobbling may be used.
- the process of changing the predetermined threshold value of the electric signal for determining the action potential information acquired by the electromyogram sensor 4 has been described, but the present invention is not limited to this.
- Other threshold values for determination may be changed according to the above-mentioned processing contents.
- each learned activity learning model according to the activity content, activities other than at rest (for example, high-intensity activities such as jogging) in consideration of the actual state of physical activity. Even in the case of, it is possible to detect information on exacerbations in COPD.
- the present embodiment it is possible to appropriately change a predetermined threshold value of an electric signal for determining information regarding the presence or absence of exacerbation according to the activity content or the probability value of exacerbation.
- the fifth embodiment relates to a mode in which, when information on exacerbations in COPD is detected, second advice information other than medication instruction information or medication instruction information is transmitted according to the detected exacerbation information.
- second advice information other than medication instruction information or medication instruction information is transmitted according to the detected exacerbation information.
- FIG. 30 is a block diagram showing a configuration example of the server 1 of the fifth embodiment.
- the contents overlapping with FIG. 24 are designated by the same reference numerals and the description thereof will be omitted.
- the large-capacity storage unit 17 includes medication instruction information DB 177 and treatment result DB 178.
- the medication instruction information DB 177 stores information on medication instructions for a drug prescribed in advance for use at the time of exacerbation for a COPD patient.
- the treatment result DB 178 stores the information on the intake of the medicine prescribed for use at the time of exacerbation and the measurement data after taking the medicine for the patient who has detected the information on the exacerbation.
- FIG. 31 is an explanatory diagram showing an example of the record layout of the medication instruction information DB 177.
- the medication instruction information DB 177 includes a medication instruction ID column, a patient ID column, an exacerbation information sequence, a medication instruction sequence, and an advice sequence.
- the medication instruction ID column stores the ID of the medication instruction uniquely identified in order to identify each medication instruction.
- the patient ID column stores the patient ID that identifies the patient.
- the exacerbation information sequence stores information about exacerbations.
- the medication instruction sequence stores information on medication instructions according to information on exacerbations.
- the advice sequence stores a second piece of advice information other than the medication instruction information, depending on the information about the exacerbation.
- FIG. 32 is an explanatory diagram showing an example of the record layout of the treatment result DB178.
- the treatment result DB 178 includes a management ID column, a patient ID column, a medication instruction ID column, a drug intake status column, and a measurement data string.
- the management ID column stores the ID of the treatment result data uniquely identified in order to identify the data of each treatment result.
- the patient ID column stores the patient ID that identifies the patient.
- the medication instruction ID string stores the medication instruction ID that specifies the medication instruction.
- the drug intake status column remembers the intake status (status) of the drug instructed to be taken by the patient who detected the information on the exacerbation. For example, "ingested”, “ingested”, “not ingested”, etc. may be entered in the drug intake status column.
- the measurement data string includes an action information string, an action potential information string, and a biometric information string.
- the motion information string stores the motion information acquired by the detection sensor 3 for the patient after the patient who has detected the information on the exacerbation has taken the medicine instructed to take the medicine.
- the action potential information sequence stores the action potential information acquired by the electromyogram sensor 4 for the patient after the patient who has detected the information regarding the exacerbation has taken the medicine instructed to take the medicine.
- the biometric information column stores the biometric information acquired by the second sensor 5 for the patient after the patient who has detected the information on the exacerbation has taken the medicine instructed to take the medicine.
- FIG. 33 is a flowchart showing a processing procedure when transmitting medication instruction information for a drug prescribed for use at the time of exacerbation in advance according to the information regarding exacerbation.
- the control unit 21 of the terminal 2 acquires the operation information from the detection sensor 3 (step S281) and the activity potential information from the electromyogram sensor 4 (step S282) via the Bluetooth communication unit 26.
- the control unit 21 determines whether or not to detect information regarding exacerbations in COPD (step S283).
- the process of detecting information on exacerbations is the same as the process of detecting information on exacerbations in the first embodiment, and thus the description thereof will be omitted.
- the control unit 21 determines that the information regarding the exacerbation in COPD has not been detected (NO in step S283), the control unit 21 ends the process.
- the control unit 21 determines that the information on the exacerbation in COPD has been detected (YES in step S283), the control unit 21 acquires the medication instruction information according to the information on the exacerbation (step S284). For example, the control unit 21 may confirm the information regarding the exacerbation by the doctor and receive the direct medication instruction information to be given to the pre-prescribed drug by the communication unit 23 or the input unit 24, or from the storage unit 22. Depending on the information regarding the exacerbation, information on medication instructions for pre-prescribed drugs may be obtained.
- the medication instruction information includes the type of medication (eg, short-acting inhaled ⁇ 2 stimulant, etc.), name (eg, meptin), method of administration, side effects, and the like.
- the control unit 21 displays the acquired medication instruction information on the display unit 25 (step S285).
- the control unit 21 transmits the acquired medication instruction information to the server 1 via the communication unit 23 (step S286).
- the control unit 11 of the server 1 receives the medication instruction information of the medicine corresponding to the information regarding the exacerbation transmitted from the terminal 2 by the communication unit 13 (step S181), and receives the received medication instruction information of the large-capacity storage unit 17. It is stored in the instruction information DB 177 (step S182). Specifically, the control unit 11 allocates a medication instruction ID and stores the patient ID, information on exacerbation, and medication instruction information as one record in the medication instruction information DB 177.
- FIG. 34 is a flowchart showing a processing procedure when transmitting the second advice information according to the information regarding the exacerbation.
- the contents overlapping with FIG. 33 are designated by the same reference numerals and the description thereof will be omitted.
- the control unit 21 of the terminal 2 determines that the information regarding the exacerbation in COPD has been detected in step S283, the control unit 21 acquires the second advice information corresponding to the information regarding the exacerbation (step S291).
- the second advice information is opinions / suggestions and the like other than the above-mentioned medication instruction information, and may be useful information and the like for the treatment of COPD.
- the second piece of advice is information about exercise therapy such as "walk", "basic training", or "be careful not to overeat", "nutrition”.
- the second advice information acquisition process is the same as the above-mentioned medication instruction information acquisition process, and thus the description thereof will be omitted.
- the control unit 21 displays the acquired second advice information on the display unit 25 (step S292).
- the control unit 21 transmits the acquired second advice information to the server 1 via the communication unit 23 (step S293).
- the control unit 11 of the server 1 receives the second advice information corresponding to the information regarding the exacerbation transmitted from the terminal 2 by the communication unit 13 (step S191), and receives the received second advice information in the large-capacity storage unit 17. It is stored in the medication instruction information DB 177 (step S192). Specifically, the control unit 11 allocates a medication instruction ID and stores the patient ID, information on exacerbation, and the second advice information as one record in the medication instruction information DB 177.
- the above-mentioned medication instruction information or the second advice information was transmitted to the terminal 2 respectively, but the present invention is not limited to this.
- the control unit 11 of the server 1 may transmit the medication instruction information to the terminal 2 together with the second advice information according to the detected information on the exacerbation.
- control unit 11 acquires information on the intake of the drug instructed to be taken by the patient who has detected the information on the exacerbation via the communication unit 13 or the input unit 14.
- the control unit 11 transmits the operation information after ingestion of the drug from the detection sensor 3, the action potential information after ingestion of the drug from the electromyogram sensor 4, and the action potential information after ingestion of the drug from the second sensor 5 via the communication unit 13.
- Acquire measurement data including biometric information.
- the control unit 11 stores the acquired information on the intake of the drug and the measurement data after ingesting the drug in the treatment result DB 178 of the large-capacity storage unit 17. Specifically, the control unit 11 allocates a management ID and stores the patient ID, the medication instruction ID, the drug intake status, the operation information, the action potential information, and the biological information as one record in the treatment result DB 178.
- the control unit 11 sent the measurement data including the operation information output from the detection sensor and the activity potential information output from the electromyogram sensor, and the exacerbation.
- the second teacher data associated with the information indicating that it has not occurred (for example, level 1) is acquired.
- the control unit 11 relearns the exacerbation detection model 173 (learned model) that outputs information regarding the presence or absence of exacerbation when motion information and action potential information are input using the second teacher data.
- the control unit 11 stores the relearned exacerbation detection model 173 in the large-capacity storage unit 17, and ends a series of processes.
Abstract
一つの側面に係るプログラムは、呼吸筋または呼吸補助筋の動作に関する動作情報を検出する検出センサ(3)から前記動作情報、及び呼吸筋または呼吸補助筋に対する活動電位情報を取得する筋電図センサ(4)から前記活動電位情報を取得し、取得した前記動作情報及び活動電位情報に基づき呼吸器系疾患の異常を検出し、前記異常を検出した場合に、異常情報を出力する処理をコンピュータ(1)に実行させることを特徴とする。
Description
本発明は、プログラム、情報処理方法及び情報処理装置に関する。
従来、慢性閉塞性肺疾患(Chronic Obstructive Pulmonary Disease:COPD)の増悪の診断において、様々な検出技術がある。例えば、特許文献1には、COPD患者由来の生体試料(例えば、血液、血清等)中のIL-27タンパク質又はそれをコードする遺伝子の発現量を測定することによって、COPD患者の増悪指標を検出する方法が開示されている。
しかしながら、特許文献1に係る発明は、測定に供する生体試料を、増悪検査を行うCOPD患者から採取するため、COPD患者の体に負担をかける恐れがある。
一つの側面では、患者の体への負担をかけずに呼吸器系疾患の異常を検出することが可能なプログラム等を提供することにある。
一つの側面に係るプログラムは、呼吸筋または呼吸補助筋の動作に関する動作情報を検出する検出センサから前記動作情報、及び呼吸筋または呼吸補助筋に対する活動電位情報を取得する筋電図センサから前記活動電位情報を取得し、取得した前記動作情報及び活動電位情報に基づき呼吸器系疾患の異常を検出し、前記異常を検出した場合に、異常情報を出力する処理をコンピュータに実行させることを特徴とする。
一つの側面では、患者の体への負担をかけずに呼吸器系疾患の異常を検出することが可能となる。
以下、本発明をその実施形態を示す図面に基づいて詳述する。
(実施形態1)
実施形態1は、呼吸筋または呼吸補助筋の動作に関する動作情報、及び呼吸筋または呼吸補助筋に対する活動電位情報に基づき、呼吸器系疾患の異常を検出する形態に関する。
実施形態1は、呼吸筋または呼吸補助筋の動作に関する動作情報、及び呼吸筋または呼吸補助筋に対する活動電位情報に基づき、呼吸器系疾患の異常を検出する形態に関する。
本実施形態では、検出センサを用いて呼吸筋または呼吸補助筋の動作に関する動作情報、及び筋電図センサを用いて呼吸筋または呼吸補助筋に対する活動電位情報を取得する。動作情報は、呼吸筋もしくは呼吸補助筋の動作、呼吸筋もしくは呼吸補助筋の動作に伴う胸郭の動作、または肺もしくは横隔膜の収縮膨張に伴う動作に関する情報を含む。取得された動作情報及び活動電位情報に基づき、呼吸器系疾患の異常が検出される。また、呼吸器系疾患の異常が検出された場合、患者または医師宛に検出された異常を出力することができる。なお、以下では、呼吸器系疾患の一つであるCOPDにおける増悪に関する情報を検出する例をあげて説明するが、他の種類の呼吸器系疾患の異常(例えば、喘息、肺炎、間質性肺炎、肺癌等)を検出しても良い。
COPDは、空気中の有毒物質・ガス(特に喫煙)により、気道に慢性的な炎症が起こり、結果、気道狭窄・肺胞壁の破壊・喀痰の増加のために気流制限(息が十分に吐けず、このため十分な換気が行えない)が起きる病気である。またCOPDでは、感染等を契機として急速に病態が悪化することがあり、これらは増悪と呼ばれる。通常、増悪を起こすと呼吸状態の著しい低下が認められ、回復後も増悪前の呼吸状態には戻らない。増悪を繰り返すたびに全身状態ならびに予後が不良となる。
図1は、COPDにおける増悪に関する情報を検出するシステムの概要を示す説明図である。本実施形態のシステムは、情報処理装置1、情報処理端末2、検出センサ3及び筋電図センサ4を含み、各装置はインターネット等のネットワークNを介して情報の送受信を行う。
情報処理装置1は、呼吸筋もしくは呼吸補助筋の動作に関する動作情報、及び呼吸筋もしくは呼吸補助筋に対する活動電位情報等の種々の情報に対する処理、記憶及び送受信を行う情報処理装置である。情報処理装置1は、例えばサーバ装置、パーソナルコンピュータ等である。本実施形態において、情報処理装置1はサーバ装置であるものとし、以下では簡潔のためサーバ1と読み替える。
情報処理端末2は、検出された呼吸器系疾患の異常情報の受信及び表示等を行う端末装置である。情報処理端末2は、例えばスマートフォン、携帯電話、腕時計型携帯端末等のウェアラブルデバイス、タブレット、パーソナルコンピュータ端末等の情報処理機器である。以下では簡潔のため、情報処理端末2を端末2と読み替える。
検出センサ3は、呼吸筋または呼吸補助筋の動作情報を検出するセンサである。呼吸筋は、呼吸をするときに胸郭の拡大、収縮を行うために用いられる筋肉であり、横隔膜、内肋間筋、外肋間筋等を含む。呼吸補助筋は、胸鎖乳突筋、前斜角筋、中斜角筋、後斜角筋、前鋸筋、上後鋸筋、下後鋸筋、広背筋、脊柱起立筋、僧帽筋、腰方形筋、大胸筋、小胸筋、腹直筋、内腹斜筋、外腹斜筋及び腹横筋等を含む筋肉群であり、呼吸の際に補助的に用いる。例えば、ベルト状またはテープ状の検出センサ3を患者の胸部に装着し、患者の呼吸筋及び呼吸補助筋、もしくは呼吸筋、呼吸補助筋の動作に基づく胸郭の動きを検出する。
検出センサ3は、例えば圧電素子センサ、伸縮センサ、ベルト状またはテープ状のテープセンサ、エコーセンサ、生体インピーダンスを計測する生体電位センサ等が用いられる。なお、検出センサ3は、上述したセンサに限らず、例えば人体に触れずに呼吸筋及び呼吸補助筋、もしくは呼吸筋、呼吸補助筋の動作に基づく胸郭の動きまたは呼吸自体を検出できる静電容量型の非接触センサであっても良い。圧電素子センサは、圧電体に加えられた力を電圧に変換するセンサであり、例えば圧電素子を利用して呼吸の波形を検出する呼吸モニター用のセンサであっても良い。例えば上述した呼吸モニター用のセンサ(圧電素子センサ)は、測定部位である胸郭に置かれ、測定部の呼吸運動により胸郭に加わる圧力の変化を電圧に変換し、患者の呼吸筋及び呼吸補助筋の動きを検出して波形データとして出力する。なお、上述した測定部位は、胸郭に限らず、例えば腹部または頚部や背部等であっても良い。エコーセンサは、例えば超音波を利用して液体の流量測定、液体識別、物体との距離の測定等を行うセンサである。エコーセンサを用いて、肋骨、横隔膜、肺等の動きを検出する。例えば呼吸における肋骨の移動距離もしくは横隔膜の移動距離、弛緩・収縮情報もしくは肺の移動距離、膨張・収縮情報等を検出する。生体電位センサは、呼吸に伴う肺容積の変化により変わる生体インピーダンスから、間接的に胸郭及び肺の動きを検出する。
伸縮センサは、ゴムのように伸縮する変位センサであり、対象者の動きをリアルタイムにモニタリングする。伸縮センサは、例えば特殊な構造を持つカーボンナノチューブとエラストマー素材が層になり、薄いシート状のものである。伸縮センサは、導電性とともにゴムのような伸縮性があり、伸縮量に応じて静電容量が変化する。小さな歪みから大きな歪みまで計測をすることが可能であるため、例えば、胸部に巻いたベルト状の伸縮センサを装着、もしくはシール状の伸縮センサを貼付することにより、関節の変化、筋肉の動き、または呼吸時の胸郭の動きや胸郭の動きのベクトル変化等、これまでは計測が難しかった細かな動作でも正確に計測する。なお、上述した測定部位は、胸部に限らず、例えば腹部または背部等であっても良い。
筋電図センサ4は、筋肉の活動電位を波形で記録するセンサである。周波数も含め、記録された波形の特徴によって、神経または筋肉の障害の有無、種類、性質、部位等の診断に関する情報を取得することができる。筋電図センサ4を用いてCOPDに関わる呼吸筋及び呼吸補助筋に対する評価を行うことにより、COPDにおける増悪に関する情報を検出することができる。
なお、本実施形態では、検出センサ3と筋電図センサ4とを分離した形で図示しているが、両者を一体に構成しても良い。また、本実施形態では端末2と、検出センサ3及び筋電図センサ4とを分離した例を示したが、これに限るものではない。例えば、端末2と、検出センサ3及び筋電図センサ4とを全て一体化した装置構成としても良い。
続いて、COPDにおける増悪に関する情報の検出処理について説明する。端末2は、検出センサ3を用いて呼吸筋または呼吸補助筋の動作に関する動作情報、及び筋電図センサ4を用いて呼吸筋または呼吸補助筋に対する活動電位情報を取得する。
検出センサ3によって取得された動作情報は、例えば呼吸筋または呼吸補助筋が伸び縮みすることによる胸郭の動きや胸郭の動きのベクトル変化、胸郭の可動域、胸郭の可動速度及び呼吸筋への刺激時間等である。なお、本実施形態では、検出センサ3の一つの種類の圧電素子センサ(例えば、圧電素子が組み込まれたベルト)を用いて動作情報を取得する例をあげて説明するが、伸縮センサまたはテープセンサ、生体電位センサ等の他種類の検出センサ3にも同様に適用される。圧電素子センサが患者の胸部に装着された場合、患者の呼吸筋または呼吸補助筋の動きに応じて圧電素子センサが電圧を発生し、圧電素子から電圧(動作電気信号)が出力される。なお、伸縮センサを用いる場合、伸縮の速度または加速度の変化を計測するようにしても良い。
筋電図センサ4によって取得された活動電位情報は、呼吸時に呼吸筋または呼吸補助筋の収縮に伴って発生する活動電流信号であり、活動電位の持続時間、及び活動電位波形を周波数変換した周波数波形等も含む。
端末2は、取得した動作情報及び活動電位情報をそれぞれの所定閾値と比較し、COPDにおける増悪に関する情報を検出する条件を満たした場合、端末2は、該増悪に関する情報を検出する。COPDにおける増悪に関する情報は、例えばCOPD増悪の有無を示す情報、または増悪の確率値(例えば「0」から「1」までの範囲の値)に応じて分類する増悪レベル情報等であっても良い。COPD患者の呼吸状態、増悪時のCOPD患者の呼吸に特徴的に認められる動的過膨張(高度の気流閉塞に伴うエアトラッピングのため、呼吸の度ごとに肺内の残気量が増加していく病態)の程度、頻度、持続時間等の情報によって、増悪の確率値を判定することができる。例えば、増悪の確率値に応じて四つの増悪レベル(増悪レベル1~増悪レベル4)に分類しても良い。具体的には、例えば増悪の確率値が0.05未満である場合、増悪を生せず増悪レベル1(正常)と判定する。増悪の確率値が0.05以上、且つ0.5未満である場合、増悪の発症リスクが低い増悪レベル2と判定する。増悪の確率値が0.5以上、かつ0.8未満である場合、増悪の発症リスクが高い増悪レベル3と判定する。増悪の確率値が0.8以上である場合、増悪が生じた増悪レベル4と判定する。
なお、本実施形態では、端末2を用いて増悪に関する情報を検出する処理を説明したが、これに限るものではない。例えば、サーバ1が動作情報及び活動電位情報に基づき、増悪に関する情報を検出しても良い。この場合に、サーバ1は、検出した増悪に関する情報を端末2に送信する。
図2は、サーバ1の構成例を示すブロック図である。サーバ1は、制御部11、記憶部12、通信部13、入力部14、表示部15、読取部16及び大容量記憶部17を含む。
各構成はバスBで接続されている。
各構成はバスBで接続されている。
制御部11はCPU(Central Processing Unit)、MPU(Micro-Processing Unit)、GPU(Graphics Processing Unit)等の演算処理装置を含み、記憶部12に記憶された制御プログラム1Pを読み出して実行することにより、サーバ1に係る種々の情報処理、制御処理等を行う。なお、図2では制御部11を単一のプロセッサであるものとして説明するが、マルチプロセッサであっても良い。
記憶部12はRAM(Random Access Memory)、ROM(Read Only Memory)等のメモリ素子を含み、制御部11が処理を実行するために必要な制御プログラム1Pを記憶している。また、記憶部12は、制御部11が演算処理を実行するために必要なデータ等を一時的に記憶する。通信部13は通信に関する処理を行うための通信モジュールであり、ネットワークNを介して、端末2等との間で情報の送受信を行う。
入力部14は、マウス、キーボード、タッチパネル、ボタン等の入力デバイスであり、受け付けた操作情報を制御部11へ出力する。表示部15は、液晶ディスプレイ又は有機EL(electroluminescence)ディスプレイ等であり、制御部11の指示に従い各種情報を表示する。
読取部16は、CD(Compact Disc)-ROM又はDVD(Digital Versatile Disc)-ROMを含む可搬型記憶媒体1aを読み取る。制御部11が読取部16を介して、制御プログラム1Pを可搬型記憶媒体1aより読み取り、大容量記憶部17に記憶しても良い。また、ネットワークN等を介して他のコンピュータから制御部11が制御プログラム1Pをダウンロードし、大容量記憶部17に記憶しても良い。更にまた、半導体メモリ1bから、制御部11が制御プログラム1Pを読み込んでも良い。
大容量記憶部17は、例えばハードディスク等を含む大容量の記憶装置である。大容量記憶部17は、患者DB171及びマスタDB172を含む。患者DB171は、患者に関する情報を記憶している。マスタDB172は、COPDにおける増悪に関する情報を検出するための各種の閾値を記憶している。
なお、本実施形態において記憶部12及び大容量記憶部17は一体の記憶装置として構成されていても良い。また、大容量記憶部17は複数の記憶装置により構成されていても良い。更にまた、大容量記憶部17はサーバ1に接続された外部記憶装置であっても良い。
なお、本実施形態では、サーバ1は一台の情報処理装置であるものとして説明するが、複数台により分散して処理させても良く、または仮想マシンにより構成されていても良い。
図3は、患者DB171のレコードレイアウトの一例を示す説明図である。患者DB171は、患者ID列、性別列、名前列、異常有無列、異常詳細列、検出日時列、使用されたセンサ列及びデータ列を含む。患者ID列は、各患者を識別するために、一意に特定される患者のIDを記憶している。性別列は、患者の性別を記憶している。名前列は、患者の名前を記憶している。異常有無列は、患者に対する異常が検出されたか否かを示す情報を記憶している。異常詳細列は、検出した異常の詳細情報を記憶している。検出日時列は、異常を検出した日時情報を記憶している。使用されたセンサ列は、異常を検出した際に使用されたセンサ情報を記憶している。データ列は、使用されたセンサにより検出したセンサデータを記憶している。センサデータは、例えば時系列データ等である。
図4は、マスタDB172のレコードレイアウトの一例を示す説明図である。マスタDB172は、マスタID列、マスタ名列、センサ列及び閾値列を含む。マスタID列は、各マスタデータを識別するために、一意に特定されるマスタデータのIDを記憶している。マスタ名列は、マスタデータの名称を記憶している。センサ列は、閾値を適用するセンサの名称を記憶している。閾値列は、増悪に関する情報を検出するための比較用の基準値を記憶している。
図5は、端末2の構成例を示すブロック図である。端末2は、制御部21、記憶部22、通信部23、入力部24、表示部25及びBluetooth(登録商標)通信部26を含む。各構成はバスBで接続されている。
制御部21はCPU、MPU等の演算処理装置を含み、記憶部22に記憶された制御プログラム2Pを読み出して実行することにより、端末2に係る種々の情報処理、制御処理等を行う。なお、図5では制御部21を単一のプロセッサであるものとして説明するが、マルチプロセッサであっても良い。記憶部22はRAM、ROM等のメモリ素子を含み、制御部21が処理を実行するために必要な制御プログラム2Pを記憶している。また、記憶部22は、制御部21が演算処理を実行するために必要なデータ等を一時的に記憶する。
通信部23は通信に関する処理を行うための通信モジュールであり、ネットワークNを介して、サーバ1等と情報の送受信を行う。入力部24は、キーボード、マウスまたは表示部25と一体化したタッチパネルでも良い。表示部25は、液晶ディスプレイ又は有機ELディスプレイ等であり、制御部21の指示に従い各種情報を表示する。
Bluetooth通信部26は、Bluetoothを用いて通信に関する処理を行うための通信モジュールであり、検出センサ3及び筋電図センサ4等との間で情報の送受信を行う。なお、図5では、近距離無線通信手段としてBluetoothを図示しているが、これに限られず、Zigbee、Wi-Fi等の通信規格を用いても良い。また、有線を用いた通信を採用しても良い。なお、図5では、Bluetooth通信部26の例を説明したが、これに限るものではない。例えば、5Gまたは4G等の公衆回線網を用いた通信を行っても良い。
図6は、検出センサ3の構成例を示すブロック図である。なお、検出センサ3は、上述した圧電素子センサ(例えば、圧電素子が組み込まれたベルトまたはテープ)を用いる例をあげて説明する。検出センサ3は、制御部31、記憶部32、圧電素子33、Bluetooth通信部34及びスピーカ35を含む。各構成はバスBで接続されている。
制御部31は、CPU、MPU等の演算処理装置を含み、記憶部32に記憶された制御プログラム3Pを読み出して実行することにより、圧電素子33によって読み取られた圧電体に加えられた力を電圧に変換する制御処理等を行う。記憶部32は、RAM、ROM等のメモリ素子を含み、制御部31が処理を実行するために必要な制御プログラム3Pを記憶している。また、記憶部32は、制御部31が演算処理を実行するために必要なデータ等を一時的に記憶する。
圧電素子33は、圧電効果を利用した受動素子であり、圧電体に加えられた力を電圧に変換する。Bluetooth通信部34は、Bluetoothを用いて通信に関する処理を行うための通信モジュールであり、端末2等との間で電圧情報(例えば、時系列データ等)の送受信を行う。なお、図6では、近距離無線通信手段としてBluetoothを図示しているが、これに限られず、Zigbee、Wi-Fi等の通信規格を用いても良い。また、有線を用いた通信を採用しても良い。スピーカ35は、電気信号を音に変換する装置である。なお、スピーカ35は、Bluetoothのような短距離無線通信方式により検出センサ3に接続されたヘッドセットであっても良い。
図7は、筋電図センサ4の構成例を示すブロック図である。筋電図センサ4は、制御部41、記憶部42、筋電計測部43、Bluetooth通信部44及びスピーカ45を含む。各構成はバスBで接続されている。
制御部41は、CPU、MPU等の演算処理装置を含み、記憶部42に記憶された制御プログラム4Pを読み出して実行することにより、筋電計測部43によって読み取られた活動電位情報(筋電位)に対する制御処理等を行う。記憶部42は、RAM、ROM等のメモリ素子を含み、制御部41が処理を実行するために必要な制御プログラム4Pを記憶している。また、記憶部42は、制御部41が演算処理を実行するために必要なデータ等を一時的に記憶する。
筋電計測部43は、呼吸筋または呼吸補助筋に対する活動電位情報を計測する。Bluetooth通信部44は、Bluetoothを用いて通信に関する処理を行うための通信モジュールであり、端末2等との間で活動電位情報(例えば、時系列データ等)の送受信を行う。なお、図7では、近距離無線通信手段としてBluetoothを図示しているが、これに限られず、Zigbee、Wi-Fi等の通信規格を用いても良い。また、有線を用いた通信を採用しても良い。スピーカ45は、電気信号を音に変換する装置である。なお、スピーカ45は、Bluetoothのような短距離無線通信方式により筋電図センサ4に接続されたヘッドセットであっても良い。
図8A及び図8Bは、検出センサ3により検出した動作情報を説明する説明図である。図8Aは、健常者及びCOPD患者に対する通常呼吸時の呼吸生理を説明する説明図である。人は呼吸運動により体内に酸素を取り入れ、体外に二酸化炭素を排出する。肺は胸膜に包まれ、胸郭内に存在する。肺はそれ自体では伸縮する力がなく、胸郭を形成する肋骨の可動性と横隔膜等の伸縮運動により受動的に膨張・収縮を行う。
横隔膜は体の最大の吸気筋として、肋骨の5番、6番あたりに位置し、ドーム状に横たわる形をし、息を吸うときに使用する筋肉である。人が息を吸うとき、すなわち吸気時には横隔膜を含む吸気筋と吸気補助筋が互いに協調しながら収縮し、これにより胸郭を拡げて胸腔内を陰圧にすることで肺を膨張させ、外気を肺内に取り込む。吸気筋・吸気補助筋は、横隔膜、外肋間筋、胸鎖乳突筋、前斜角筋、中斜角筋、後斜角筋等を含む。
息を吐くとき、すなわち呼気時には、これらの筋肉が収縮を止めて弛緩する。肺は膨らんだゴム風船のように自分で収縮する性質を元々持っているので、胸郭を拡げる筋肉が弛緩することで、肺は自らの縮む力で収縮して呼気を排出する。このため健常者の安静時の呼吸では、呼気筋と呼気補助筋の活動をあまり必要としない。
健常者が呼吸(換気)をするときは、吸気筋と吸気補助筋を収縮させて胸郭を広げることで外気を吸い込み、次にこれらの筋肉を弛緩させることで呼気を排出する。しかしCOPD患者は、呼気時間の延長を伴う呼気での換気機能障害のため、吸い込んだ空気を十分に排出しづらくなる。このため健常人ではあまり使用されない呼気筋と呼気補助筋の収縮を用いることで、呼気の排出を補助することとなる。呼気筋・呼気補助筋は、内肋間筋、腹直筋、内腹斜筋、外腹斜筋、腹横筋等を含む。
図8Bは、健常者及びCOPD患者に対する呼吸筋または呼吸補助筋の動作情報を示すイメージ図である。図8Bでは、呼吸筋または呼吸補助筋の動作電気信号(動作情報)の波形データを示している。横軸は時間を示し、単位は秒(sec)である。縦軸は電圧を示し、単位はボルト(V)である。
図8B上段は健常者に取り付けられた検出センサ3から出力される電圧の時間的変化を示すグラフである。健常者の場合、電圧は時間的変化の少ない極大、極小を周期的に繰り返していることが理解できる。図8B下段はCOPD患者に取り付けられた検出センサ3から出力される電圧の時間的変化を示すグラフである。COPD患者の場合、健常者と同じく通常時は、時間的変化の少ない極大、極小を周期的に繰り返す。しかしながら、増悪に向かう場合、呼気時の換気障害の悪化に伴う進行性の残気量の増加(動的過膨張)を反映して、極大及び極小の時間的変化が継続的に増加することとなる。
本実施形態では一例として、検出センサ3から出力される電圧の極大の単位時間あたりの変化が所定閾値(例えば、傾き0.2)を超えた場合、第1条件を満たすと判断する。具体的には制御部21は以下の処理を行う。制御部21は、検出センサ3から時系列で電圧を取得する。制御部21は、電圧の極大を時系列で求める。制御部21は、所定単位時間(例えば60秒間)の電圧の極大を抽出し、抽出した極大で形成される近似直線の傾きを算出する。制御部21は傾きが予め定めた閾値(例えば、傾き0.2)を超えると判断した場合、第1条件を満たすと判断する。
なお、極小または極大と極小の両方を用いて判断しても良いことはもちろんである。更には、極大極小の差分を用いて判断しても良い。また、制御部21は、更に例えば単位時間あたりの極大の平均値が図8Bの点線で示す閾値を超え、かつ、求めた傾きが閾値を超える場合に、第1条件を満たすと判断しても良い。また例えば制御部21は、所定単位時間(例えば60秒間)の電圧の極大及び極小を抽出し、抽出した極大で形成される近似直線の極大の傾きを算出し、抽出した極小で形成される近似直線の極小の傾きを算出する。制御部21は、極大の傾きが予め定めた極大の傾き閾値を超え、極小の傾きが予め定めた極小の傾き閾値を超え、極小の傾きが極大の傾きを超え、かつ、持続時間が所定時間(例えば10秒)を超えたと判定した場合に、第1条件を満たすと判断しても良い。
図9は、筋電図センサ4により検出した健常者の呼吸筋の活動電位情報を説明する説明図である。横軸は時間を示し、単位はミリ秒(msec)である。縦軸は電位(活動電位)を示し、単位はマイクロボルト(μV)である。図9のグラフ上段は健常者の吸気筋の電位の時間的変化を示す。吸気筋に関しては一定の間隔を置いて約100μVの振幅を有する電位波形が確認される。図9のグラフ下段は健常者の呼気筋の電位の時間的変化を示す。図9から明らかなように、健常者の呼気筋はあまり活動せず、このため対応する電位波形も微小となり、ほとんど確認できない。
図10A及び図10Bは、筋電図センサ4により検出したCOPD患者の呼吸筋の活動電位情報を説明する説明図である。なお、横軸と縦軸については図9と同様であるため、説明を省略する。
図10Aは、通常時のCOPD患者の呼吸筋の活動電位情報を説明する説明図である。COPD患者では、通常時の吸気筋の活動が、図9での健常者(通常時)の吸気筋の活動より強くなるため、COPD患者の吸気筋の活動電位の振幅が、健常者の吸気筋の活動電位の振幅より大きくなる。また、COPD患者では、通常時の呼気においても呼気筋が収縮するため、図9と比較して呼気筋の活動電位の振幅が大きくなる。
図10Bは、増悪時のCOPD患者の呼吸筋の活動電位情報を説明する説明図である。COPD患者は増悪が生じた場合、吸気筋を更に収縮させて胸郭を広げることで外気を肺内に取り込もうとする。これにより吸気筋は、通常時より強く収縮することとなり、増悪時の吸気筋の活動電位の振幅は、通常時の吸気筋の活動電位の振幅より大きくなる。また、増悪時には吸気筋の活動電位の持続時間が、通常時の吸気筋の活動電位の持続時間より短くなる。さらに、これらの信号をフーリエ変換により解析すると、増悪が生じた場合の周波数分布は通常時に比較して異なるものとなる。
COPD患者は増悪が生じた場合、呼気時間の延長を伴う呼気での換気機能障害の増強が認められる。このため、呼気筋には換気をサポートするため通常より更に強く収縮することが求められる。これにより、増悪時の呼気筋の活動電位の振幅が、通常時の呼気筋の活動電位の振幅より大きくなる。また、呼気の排出に時間を要するため増悪時の呼気筋の活動電位の持続時間も、通常時の呼気筋の活動電位の持続時間より長くなる。さらに、これらの信号をフーリエ変換により解析すると、増悪が生じた場合の周波数分布は通常時に比較して異なるものとなる。
図10での点線は、予め定められた呼気筋の通常時と増悪時の活動電位の閾値を示す。COPD患者の呼気筋の活動電位のピーク値と、呼気筋の通常時と増悪時の活動電位の閾値とを比較することにより、増悪を検出することができる。
例えば、COPD患者に対し、通常時、増悪時それぞれの活動電位の閾値が設けられ、設けられた閾値に応じて、増悪レベルが定義されても良い。具体的には、端末2の制御部21は、筋電図センサ4により検出した呼気筋の活動電位のピーク値と、通常時、増悪時それぞれの活動電位の閾値とを比較する。
制御部21は、呼気筋の活動電位のピーク値が、通常時の呼気筋の活動電位の閾値A未満と判定した場合、増悪の発症リスクが低い増悪レベル2と判定する。制御部21は、呼気筋の活動電位が、通常時の呼気筋の活動電位の閾値A以上であり、且つ、増悪時の呼気筋の活動電位の閾値B(例えば、閾値Aの30%増の値)未満であると判定した場合、増悪の発症リスクが高い増悪レベル3と判定する。
制御部21は、呼気筋の活動電位のピーク値が、増悪時の呼気筋の活動電位の閾値B以上であると判定した場合、増悪が生じた増悪レベル4と判定する。例えば増悪レベル4が判定された場合、制御部21は、増悪に関する情報を表示部25により表示しても良い。
なお、すべての活動電位のピーク値が所定閾値以上であることに限るものではない。例えば、端末2は単位時間あたりの活動電位のピーク値が所定閾値以上である回数と、所定回数とを比較し、増悪レベルを判定しても良い。
また、呼気筋の活動電位の持続時間により増悪レベルを判定しても良い。例えばCOPD患者に対し、通常時、増悪時それぞれの活動電位の持続時間の閾値が設けられ、設けられた持続時間の閾値に応じて、増悪が生じたか否かを判定しても良い。
具体的には、制御部21は、呼気筋の活動電位の持続時間が、通常時の活動電位の持続時間の閾値未満であると判定した場合、増悪の発症リスクが低い増悪レベル2と判定する。制御部21は、呼気筋の活動電位の持続時間が、通常時の活動電位の持続時間の閾値以上であり、且つ、増悪時の活動電位の持続時間の閾値未満であると判定した場合、増悪の発症リスクが高い増悪レベル3と判定する。制御部21は、呼気筋の活動電位の持続時間が、増悪時の呼気筋の活動電位の持続時間の閾値以上であると判定した場合、増悪が生じた増悪レベル4と判定する。
更にまた、呼気筋の活動電位の閾値、及び持続時間の閾値の双方に基づき、増悪レベルを判定しても良い。例えば、制御部21は、呼気筋の活動電位のピーク値が増悪時の活動電位の閾値以上であり、且つ、呼気筋の活動電位の持続時間が増悪時の呼気筋の活動電位の持続時間の閾値以上であると判定した場合、増悪が生じた増悪レベル4と判定しても良い。
また、呼気筋の活動電位の周波数分布により増悪レベルを判定しても良い。例えばCOPD患者に対し、通常時、増悪時それぞれの平均周波数または中央周波数の閾値が設けられ、設けられた平均周波数または中央周波数の閾値に応じて、増悪が生じたか否かを判定しても良い。
なお、上述した増悪レベルの判断処理に限るものではない。例えば、吸気筋と呼気筋との両方の活動電位情報、または吸気筋の活動電位情報のみを用いて増悪レベルを判定しても良い。
図11は、COPDにおける増悪に関する情報の検出処理の動作を説明する説明図である。端末2の制御部21は、Bluetooth通信部26を介して、検出センサ3から呼吸筋または呼吸補助筋の動作に関する動作情報、及び筋電図センサ4から呼吸筋または呼吸補助筋に対する活動電位情報を取得する。動作情報及び活動電位情報は、所定の単位時間(例えば、分刻み、秒刻み等)ごとに計測された時系列データである。また、動作情報及び活動電位情報は、時系列の波形画像であっても良い。更にまた、動作情報及び活動電位情報は、周波数特性グラフであっても良い。具体的には、動作情報及び活動電位情報の時系列データから周波数解析を行い、胸郭の動き及び呼吸筋・呼吸補助筋の活動電位に対応する変動波を抽出する。周波数解析に関しては、例えば、離散化された信号に対して行う離散フーリエ変換(DFT:Discrete Fourier Transformation)を利用しても良い。制御部21は、例えば時系列データ基盤を用いて、取得した動作情報及び活動電位情報を記憶して一元管理しても良い。
制御部21は、通信部23を介して、サーバ1の大容量記憶部17のマスタDB172から、COPDにおける増悪に関する情報を検出するための各種の閾値を取得する。なお、COPDにおける増悪に関する情報を検出するための各種の閾値は予めサーバ1から取得されても良く、または端末2の記憶部22に予め記憶されても良い。例えば、呼吸筋の動作電気信号の所定閾値、通常時、増悪時それぞれの呼気筋に係る筋電図の電気信号の所定閾値、通常時、増悪時それぞれの呼気筋の電気信号の持続時間の所定閾値等が取得される。
制御部21は、検出センサ3により検出した動作情報に基づき、第1条件を満たしたか否かを判定する。制御部21は、第1条件を満たしたと判定した場合、制御部21は、更に筋電図センサ4により取得した呼気筋に係る活動電位情報及び所定閾値に基づき、増悪に関する情報を検出する。制御部21は、検出した増悪に関する情報を表示部25により表示する。
なお、増悪に関する情報が検出された場合、制御部21は、Bluetooth通信部26を介して、増悪を検出した旨をそれぞれに検出センサ3、筋電図センサ4に送信しても良い。例えば検出センサ3の制御部31は、端末2から送信された増悪を検出した旨を受信し、スピーカ35によりアラームまたは音声情報等をCOPD患者に通知しても良い。筋電図センサ4の制御部41は、端末2から送信された増悪を検出した旨を受信し、スピーカ45によりアラームまたは音声情報等をCOPD患者に通知しても良い。
なお、上述した処理で呼気筋に係る活動電位情報の例を説明したが、これに限るものではない。例えば、吸気筋に係る活動電位情報、または吸気筋及び呼気筋両方に係る活動電位情報に基づき、増悪に関する情報を検出しても良い。
制御部21は、検出した増悪に関する情報を通信部23によりサーバ1に送信する。サーバ1の制御部11は、端末2から送信された増悪に関する情報を通信部13により受信し、受信した増悪に関する情報を大容量記憶部17の患者DB171に記憶する。なお、上述した増悪に関する情報の検出処理に限るものではない。例えば、端末2は検出センサ3及び筋電図センサ4により取得した胸郭の可動域、胸郭の可動速度及び呼吸筋の刺激時間、呼吸筋の活動電位の周波数変化等に基づき、増悪に関する情報を検出しても良い。
筋疲労の際には筋電図信号の振幅が増え、周波数成分が高周波領域から低周波領域へと移動する徐波化が生じる。徐波化は増悪時の兆候とする。以下では、呼吸筋の活動電位の周波数変化の例を説明する。端末2は、呼吸筋の筋電図信号のパワースペクトルの測定及びフーリエ変換を行う。パワースペクトルは、筋電図波形を横軸に周波数成分の分布、縦軸に各周波数成分の振幅の二乗(信号のパワー)として変換したものである。
端末2は、スペクトルのパワー分布の特徴を表す指標として、平均周波数(MPF : Mean Power Frequency)または中央周波数(MF : Median Power Frequency)の変化値を算出する。平均周波数は、各周波数の平均値である。中央周波数は、パワースペクトルの面積を2つの等しいエリアに分ける周波数である。端末2は、算出した平均周波数または中央周波数の変化値に基づいて、徐波化の傾向を有するか否かを判定する。例えば、高周波帯(例えば、86.4Hz)から徐々に低周波帯(例えば、67.4Hz)に移行している場合、端末2は平均周波数または中央周波数の変化値を算出する。端末2は、算出した変化値が所定閾値以上であると判定した場合、増悪に関する情報を出力する。なお、閾値を複数設けた各閾値に応じて、増悪のレベルを出力するようにしても良い。例えば変化値が第1閾値以上第2閾値未満の場合、増悪レベル3とし、第2閾値以上の場合、増悪レベル4としても良い。また周波数解析を行う筋電図信号は、呼気筋及び吸気筋を含む全てのデータを利用しても良いし、呼気筋または吸気筋のいずれかのデータを活用しても良い。
図12は、COPDにおける増悪に関する情報を検出する際の処理手順を示すフローチャートである。検出センサ3の制御部31は、Bluetooth通信部34を介して、呼吸筋または呼吸補助筋の動作に関する動作情報を端末2に送信する(ステップS301)。端末2の制御部21は、Bluetooth通信部26を介して、検出センサ3から送信された動作情報を受信する(ステップS201)。筋電図センサ4の制御部41は、Bluetooth通信部44を介して、呼吸筋または呼吸補助筋に対する活動電位情報を端末2に送信する(ステップS401)。端末2の制御部21は、Bluetooth通信部26を介して、筋電図センサ4から送信された活動電位情報を受信する(ステップS202)。
制御部21は、通信部23を介して、COPDにおける増悪に関する情報を検出するための各種の閾値を取得するリクエストをサーバ1に送信する(ステップS203)。サーバ1の制御部11は、通信部13を介して、端末2から送信された閾値の取得リクエストを受信する(ステップS101)。制御部11は、受信した閾値の取得リクエストに応じて、大容量記憶部17のマスタDB172から、COPDにおける増悪に関する情報を検出するための各種の閾値を取得する(ステップS102)。制御部11は、通信部13を介して、取得した各種の閾値を端末2に送信する(ステップS103)。
端末2の制御部21は、通信部23を介して、サーバ1から送信された各種の閾値を受信する(ステップS204)。制御部21は、受信した閾値及び動作情報に基づき、第1条件を満たしたか否かを判定する(ステップS205)。具体的には、例えば制御部21は、検出センサ3から時系列で電圧を取得し、取得した電圧の極大を時系列で求める。制御部21は、所定単位時間内(例えば60秒間)の電圧の極大を抽出し、抽出した極大で形成される近似直線の傾きを算出する。制御部21は傾きが予め定めた閾値を超えると判断した場合、第1条件を満たすと判断する。
または、例えば制御部21は、所定単位時間の電圧の極大及び極小両方を抽出し、抽出した極大で形成される近似直線の極大の傾きを算出し、抽出した極小で形成される近似直線の極小の傾きを算出する。制御部21は、極大の傾きが予め定めた極大の傾き閾値を超え、極小の傾きが予め定めた極小の傾き閾値を超え、かつ、持続時間が所定時間(例えば10秒)を超えたと判定した場合に、第1条件を満たすと判断する。なお、極小の傾き閾値は極大の傾き閾値よりも大きい値とすれば良い。
制御部21は、第1条件を満たしていないと判定した場合(ステップS205でNO)、処理を終了する。制御部21は、第1条件を満たしたと判定した場合(ステップS205でYES)、増悪レベルを検出する処理のサブルーチンを実行する(ステップS206)。なお、増悪レベルの検出処理のサブルーチンに関しては後述する。制御部21は、検出した増悪に関する情報(増悪レベル)を表示部25により表示する(ステップS208)。制御部21は、検出した増悪に関する情報を通信部23によりサーバ1に送信する(ステップS209)。
サーバ1の制御部11は、端末2から送信された増悪に関する情報を通信部13により受信する(ステップS104)。制御部11は、受信した増悪に関する情報を大容量記憶部17の患者DB171に記憶する(ステップS105)。具体的には、制御部11は、患者ID、性別、名前、異常(増悪)有無情報、異常の詳細情報、検出した日時情報、異常を検出した際の使用されたセンサ情報、及び使用されたセンサで検出したセンサデータを一つのレコードとして患者DB171に記憶する。
なお、本実施形態では、第1条件を満たした場合、更に活動電位情報を用いて、増悪のレベルを決定した例を説明したが、これに限るものではない。例えば、第1条件を満たしていない場合でも、活動電位情報を用いて、増悪のレベルを決定しても良い。
なお、上述した処理は、動作情報による増悪判定処理(ステップS205)、活動電位情報による増悪判定処理(ステップS206)の順に行った例を説明したが、これに限るものではない。例えば、先に活動電位情報による増悪判定処理(ステップS206)を行い、次に動作情報による増悪判定処理(ステップS205)を行っても良い。具体的には、端末2の制御部21は、増悪レベルを検出する処理のサブルーチンを実行することにより、増悪レベルを検出する。例えば制御部21は、増悪の発症リスクが高い増悪レベル3以上であると判定した場合、動作情報に基づいて第1条件を満たしたか否かを判定する。制御部21は、第1条件を満たしたと判定した場合、増悪に関する情報を出力する。
または、動作情報による増悪判定処理(ステップS205)、及び活動電位情報による増悪判定処理(ステップS206)を並行して行い、両方を用いて導き出される増悪の判定条件を満たした場合、増悪に関する情報を検出しても良い。具体的には、端末2の制御部21は動作情報に基づき、第1条件を満たしたか否かを判定する。制御部21は、増悪レベルを検出する処理のサブルーチンを実行することにより、増悪レベルを検出する。例えば制御部21は、第1条件を満たし、かつ、増悪の発症リスクが高い増悪レベル3以上であると判断した場合、増悪に関する情報を出力する。
図13は、増悪レベルを検出する処理のサブルーチンの処理手順を示すフローチャートである。端末2の制御部21は、筋電図センサ4から取得された電位信号を取得する(ステップS01)。制御部21は、所定電位以上でかつ所定の継続時間を超える吸気筋の周期的な電位の変化を検出する。制御部21は周期的な吸気筋の電位の変化を認識した後に、吸気筋の電位の変化間の呼気筋の電位の変化を監視する。制御部21は、吸気筋の電位の変化間の呼気筋の電位を検出する。
なお、検出センサ3と筋電図センサ4とを併用することにより吸気筋の電位か呼気筋の電位かを識別しても良い。例えば、検出センサ3が伸縮センサやテープセンサである場合、吸気時にはテープが伸びていくため、テープが伸び始めてから最大伸び(MAX:弾性限界伸び)までのタイミングで、制御部21は、筋電図センサ4から取得された電位信号を吸気筋の電位と判定する。呼気時には、逆にテープが縮み始めるため、テープが最大伸び(MAX)から最小伸び(MIN)までのタイミングで、制御部21は、筋電図センサ4から取得された電位信号を呼気筋の電位と判定する。
または、筋電図センサ4から取得された活動電位の波形データの特徴量と、吸気筋の電位を示すラベル及び呼気筋の電位を示すラベルとを含む訓練データを用いて学習した学習モデルを用いて、吸気筋の電位か呼気筋の電位かを識別しても良い。更にまた、筋電図センサ4から取得された活動電位の振幅の平均値が小さい方を呼気筋の電位と判定しても良い。
制御部21は、呼気筋のピーク電位が閾値A(通常時の呼気筋の活動電位)未満であるか否かを判断する(ステップS02)。制御部21は、呼気筋のピーク電位が閾値A未満であると判定した場合(ステップS02でYES)、増悪の発症リスクが低い増悪レベル2を判定する(ステップS03)。制御部21は、呼気筋のピーク電位が閾値A以上であると判定した場合(ステップS02でNO)、呼気筋のピーク電位が閾値B(例えば、閾値Aの30%増の値)未満であるか否かを判定する(ステップS04)。
制御部21は、呼気筋のピーク電位が閾値B未満であると判定した場合(ステップS04でYES)、増悪の発症リスクが高い増悪レベル3を判定する(ステップS05)。制御部21は、呼気筋のピーク電位が閾値B以上であると判定した場合(ステップS04でNO)、増悪が生じた増悪レベル4を判定する(ステップS06)。制御部21は、判定した増悪レベルの判定結果を返却し(ステップS07)、サブルーチンを終了してリターンする。
なお、上述した処理で呼気筋に係る活動電位情報の例を説明したが、これに限るものでもない。例えば、吸気筋に係る活動電位情報、または吸気筋及び呼気筋両方に係る活動電位情報に基づき、増悪レベルを検出しても良い。
また、本実施形態では、活動電位のピーク電位を用いたが、これに限るものではない。例えば、活動電位の持続時間、活動電位の周波数分布等を用いても良い。以下に、持続時間を用いる例を説明する。制御部21は、呼気筋の電位信号の変化に基づき、図10Bの点線で示す開始タイミングと終了タイミングとを検出する。具体的には、制御部21は、電位信号の所定閾値を超える時間的変化が連続して生じ始めたタイミングを開始タイミングとして検出する。また制御部21は、開始タイミングを検出した後に、電位信号の所定閾値を超えない時間的変化が連続して生じ始めたタイミングを終了タイミングとして検出する。制御部21は、開始タイミングから終了タイミングまでの時間が、予め定めた閾値を超える場合に、増悪に関する情報を出力する。なお、複数の閾値を設け、第1の閾値以上第2の閾値未満の場合に増悪レベルを3、第2の閾値以上の場合に増悪レベル4としても良い。
本実施形態によると、検出センサ3により取得した動作情報、及び筋電図センサ4により取得した活動電位情報に基づき、呼吸器系疾患の異常を検出することができる。これにより、増悪検査を行うCOPD患者から生体試料(例えば、血液、血清等)を採取せず、患者の体への負担を軽くすることが可能となる。
(実施形態2)
実施形態2は、ディープラーニングにより構築された増悪検出モデルを用いて、COPDにおける増悪に関する情報を検出する形態に関する。なお、実施形態1と重複する内容については説明を省略する。
実施形態2は、ディープラーニングにより構築された増悪検出モデルを用いて、COPDにおける増悪に関する情報を検出する形態に関する。なお、実施形態1と重複する内容については説明を省略する。
図14は、実施形態2のサーバ1の構成例を示すブロック図である。なお、図2と重複する内容については同一の符号を付して説明を省略する。大容量記憶部17は、増悪検出モデル173を含む。増悪検出モデル173は、COPDにおける増悪に関する情報を検出する検出器であり、機械学習により生成された学習済みモデルである。当該学習済みモデルは、人工知能ソフトウェアの一部であるプログラムモジュールとして利用される。以下では、ディープラーニングにより構築された増悪検出モデル173を用いて、増悪に関する情報を検出する処理を説明する。
図15は、増悪検出モデル173の生成処理に関する説明図である。図15では、機械学習を行って増悪検出モデル173を生成する処理を概念的に図示している。図15に基づき、増悪検出モデル173の生成処理について説明する。
本実施形態でのサーバ1は、増悪検出モデル173として、検出センサ3から取得した動作情報に関する電気信号の画像、及び筋電図センサ4から取得した活動電位情報の画像内における増悪箇所の波形画像の特徴量を学習するディープラーニングを行うことで、波形画像を入力とし、COPDにおける増悪に関する情報の有無を示す情報を出力とするニューラルネットワークを構築(生成)する。なお、上述した波形画像に限らず、周波数を解析した後の画像に対するディープラーニングを行っても良い。ニューラルネットワークは、例えばCNN(Convolutional Neural Network)であり、波形画像の入力を受け付ける入力層と、異常の有無を示す情報(識別結果)を出力する出力層と、波形画像の画像特徴量を抽出する中間層とを有する。
入力層は、波形画像に含まれる各画素の画素値の入力を受け付ける複数のニューロンを有し、入力された画素値を中間層に受け渡す。中間層は、波形画像の画像特徴量を抽出する複数のニューロンを有し、抽出した画像特徴量を出力層に受け渡す。例えば増悪検出モデル173がCNNである場合、中間層は、入力層から入力された各画素の画素値を畳み込むコンボリューション層と、コンボリューション層で畳み込んだ画素値をマッピングするプーリング層とが交互に連結された構成を有し、波形画像の画素情報を圧縮しながら最終的に画像の特徴量を抽出する。出力層は、COPDにおける増悪箇所を識別した識別結果を出力する一又は複数のニューロンを有し、中間層から出力された画像特徴量に基づいて増悪に関する情報の有無を識別する。
なお、本実施の形態では増悪検出モデル173がCNNであるものとして説明するが、増悪検出モデル173はCNNに限定されず、CNN以外のニューラルネットワーク、SVM(Support Vector Machine)、ベイジアンネットワーク、回帰木等、他の学習アルゴリズムで構築された学習済みモデルであっても良い。
図15に示すように、例えば、入力1は検出センサ3により検出した所定時間(例えば、60秒間)の呼吸筋の動作情報の波形画像であり、入力2は筋電図センサ4により検出した所定時間(例えば、60秒間)の呼吸筋に係る活動電位情報の波形画像である。動作情報の波形画像(入力1)及び活動電位情報の波形画像(入力2)は、同じタイミングの信号を示す波形画像である。サーバ1の制御部11が、メモリに記憶された学習済みの増悪検出モデル173からの指令に従って、入力した動作情報及び活動電位情報の波形画像から、増悪に関する情報を検出して出力する。
出力された増悪に関する情報は、例えば増悪の有無の情報、増悪の確率値、増悪の確率値に応じて分類される増悪レベル等であっても良い。上述した呼吸筋に係る活動電位情報の波形画像(入力2)は、吸気筋の電位の変化と呼気筋の電位の変化とを合成して形成した電位の変化を示す波形画像である。なお、入力2は呼気筋電位の変化のみ、もしくは吸気筋電位の変化のみを示す波形画像であっても良い。または、入力1と入力2とを合成した画像を増悪検出モデル173に入力しても良い。または、入力1は呼吸筋の動作情報の時系列データであり、入力2は呼吸筋に係る活動電位情報の時系列データであっても良い。更にまた、入力1及び入力2は、波形画像と時系列データとの組み合わせであっても良い。
サーバ1は、動作情報に関する電気信号の画像及び活動電位情報の画像と、各画像における増悪に関する情報とが対応付けられた教師データを用いて学習を行う。教師データは、動作情報に関する電気信号の画像及び活動電位情報の画像と、増悪に関する情報とがラベル付けされたデータである。サーバ1は、教師データである波形画像を入力層に入力し、中間層での演算処理を経て、出力層からCOPDにおける増悪の有無を示す識別結果を取得する。なお、出力層から出力される識別結果は増悪の有無を離散的に示す値(例えば「0」又は「1」の値)であっても良く、連続的な確率値(例えば「0」から「1」までの範囲の値)であっても良い。例えばサーバ1は、出力層から出力される識別結果として、COPDにおける増悪の有無のほかに、増悪の確率値等を識別した識別結果を取得する。その他、出力層から複数のレベル、例えばレベル1からレベル4それぞれの確率値を出力するようにしても良い。
サーバ1は、出力層から出力された識別結果を、教師データにおいて波形画像に対しラベル付けされた情報、すなわち正解値と比較し、出力層からの出力値が正解値に近づくように、中間層での演算処理に用いるパラメータを最適化する。当該パラメータは、例えばニューロン間の重み(結合係数)、各ニューロンで用いられる活性化関数の係数等である。パラメータの最適化の方法は特に限定されないが、例えばサーバ1は誤差逆伝播法を用いて各種パラメータの最適化を行う。
サーバ1は、教師データに含まれる各波形画像について上記の処理を行い、増悪検出モデル173を生成する。サーバ1は、検出センサ3から動作情報に関する電気信号の画像、及び筋電図センサ4から活動電位情報の画像を取得した場合、メモリに記憶された学習済みの増悪検出モデル173からの指令に従って、COPDにおける増悪に関する情報を検出する。なお、サーバ1が、学習済みの増悪検出モデル173を生成した後に、端末2は当該学習済みの増悪検出モデル173をダウンロードしてインストールした場合、端末2が学習済みの増悪検出モデル173を用いて増悪に関する情報を検出しても良い。この場合、端末2は、検出センサ3から動作情報に関する電気信号の画像、及び筋電図センサ4から活動電位情報の画像を取得し、増悪検出モデル173を用いて増悪に関する情報を検出する。なお、端末2は、増悪検出モデル173に対し、教師データを用いて学習または再学習処理を行っても良い。
なお、本実施形態では、波形画像を増悪検出モデル173の入力値に用いるが、これに限るものではない。例えば、増悪検出モデル173としてRNN(Recurrent Neural Network)に係るニューラルネットワークを用いても良い。この場合に検出センサ3から取得した動作情報、及び筋電図センサ4から取得した活動電位情報の時系列データを入力値として、COPDにおける増悪に関する情報を検出しても良い。
また学習モデルは、動作情報と増悪に関する情報とを含む教師データに基づき学習された第1学習モデル、及び、活動電位情報と増悪に関する情報とを含む教師データに基づき学習された第2学習モデルの2つを用意しても良い。この場合、第1学習モデルは、図8に示す電圧波形、電圧波形画像、当該電圧波形を周波数変換した周波数波形、または当該周波数波形画像を入力データとし、増悪の確率を出力データとする。サーバ1は、これらの教師データを元に第1学習モデルの学習を行う。
第2学習モデルは、図10A及び10Bに示す吸気筋及び呼気筋に係る活動電位波形、活動電位波形画像、当該活動電位波形を周波数変換した周波数波形、または当該周波数波形画像を入力データとし、増悪の確率を出力データとする。サーバ1は、これらの教師データを元に第2の学習モデルの学習を行う。なお、呼気筋もしくは吸気筋に係る波形画像のみに基づいて第2の学習モデルの学習を行っても良い。
推定時において第1学習モデルの出力確率が、所定閾値(例えば80%)以上の場合、またはステップS205でYESの場合、第2学習モデルによる推定処理を行う。制御部21は、第2学習モデルに吸気筋及び呼気筋に係る活動電位波形、活動電位波形画像、当該活動電位波形を周波数変換した周波数波形、または当該周波数波形画像を入力する。制御部21は、第2学習モデルからの増悪の確率を出力する。
なお、上述した第1学習モデル及び第2学習モデルによる推定処理の順序に限るものではない。例えば、第2学習モデルによる推定処理を行い、第2学習モデルから出力された増悪の確率が所定閾値以上である場合、第1学習モデルによる推定処理を行っても良い。または、第1学習モデルによる推定処理及び第2学習モデルによる推定処理を並行して行い、第1学習モデル及び第2学習モデルを用いて出力された増悪の確率に基づいて増悪を判定しても良い。また、第1条件については実施の形態1の方法により判断を行い、活動電位波形に対しては第2学習モデルを利用するようにしても良い。さらに第1条件については第1学習モデルを利用し、活動電位波形については実施の形態1の方法により判断しても良い。
図16は、増悪検出モデル173の生成処理の処理手順の一例を示すフローチャートである。図16に基づき、増悪検出モデル173の生成処理の処理内容について説明する。
制御部11は、検出センサ3により取得した動作情報の画像、及び筋電図センサ4により取得した活動電位情報の画像と、COPDにおける増悪に関する情報とが対応付けられた教師データを取得する(ステップS121)。教師データは、例えば動作情報及び活動電位情報の画像と、増悪に関する情報(例えば、増悪の確率値等)とをラベル付けしたデータである。
制御部11は、複数の教師データを用いて、動作情報及び活動電位情報の波形画像を入力した場合に、COPDにおける増悪に関する情報の有無を示す情報(例えば、レベル1~レベル4)を出力する増悪検出モデル173(学習済みモデル)を生成する(ステップS122)。具体的には、制御部11は、教師データである波形画像をニューラルネットワークの入力層に入力し、増悪に関する情報を識別した識別結果を出力層から取得する。制御部11は、取得した識別結果を教師データの正解値(波形画像に対してラベル付けられた情報)と比較し、出力層から出力される識別結果が正解値に近づくよう、中間層での演算処理に用いるパラメータ(重み等)を最適化する。制御部11は、生成した増悪検出モデル173を大容量記憶部17に格納し、一連の処理を終了する。
図17は、増悪検出モデル173を用いた増悪に関する情報の検出処理に関する説明図である。図17では、波形画像からCOPDにおける増悪に関する情報を検出する様子を概念的に図示している。図17に基づき、COPDにおける増悪に関する情報の検出処理について説明する。
学習済みの増悪検出モデル173がインストールされた端末2の制御部21は、Bluetooth通信部26を介して、検出センサ3から動作情報に関する電気信号の画像、及び筋電図センサ4から活動電位情報の画像を取得する。なお、動作情報及び活動電位情報は、上述した波形画像に限らず、時系列データであっても良い。動作情報及び活動電位情報が時系列データである場合、制御部21は、取得した時系列データに基づいて波形画像を生成しても良い。制御部21は、取得した動作情報に関する電気信号の画像、及び活動電位情報の画像を増悪検出モデル173に入力する。
制御部21は、増悪検出モデル173の中間層にて波形画像の特徴量を抽出する演算処理を行い、抽出した特徴量を増悪検出モデル173の出力層に入力して、COPDにおける増悪の有無に関する情報を出力として取得する。図示のように、制御部21は、増悪の確率値、及び増悪の確率値に応じて分類する増悪レベル情報(例えば、増悪レベル1~増悪レベル4)を出力する。制御部21は、増悪検出モデル173を用いて、波形画像から増悪に関する情報を検出した場合、COPDにおける増悪に関する情報を検出した旨の検出結果を表示部25により表示する。
図18は、増悪検出モデル173を用いて増悪に関する情報を検出する際の処理手順を示すフローチャートである。検出センサ3の制御部31は、Bluetooth通信部34を介して、動作情報に関する電気信号の画像を端末2に送信する(ステップS331)。学習済みの増悪検出モデル173がインストールされた端末2の制御部21は、Bluetooth通信部26を介して、検出センサ3から送信された動作情報に関する電気信号の画像を受信する(ステップS231)。
なお、制御部21は、検出センサ3から動作情報に関する電気信号の生データをBluetooth通信部26により受信しても良い。この場合、例えば制御部21は、受信した電気信号の生データを深層学習済みの画像生成モデルに入力し、該画像生成モデルを用いて、電気信号の画像を出力しても良い。
筋電図センサ4の制御部41は、Bluetooth通信部44を介して、活動電位情報の画像を端末2に送信する(ステップS431)。端末2の制御部21は、Bluetooth通信部26を介して、筋電図センサ4から送信された活動電位情報の画像を受信する(ステップS232)。制御部21は、増悪検出モデル173を用いてCOPDにおける増悪に関する情報を検出し(ステップS233)、検出した増悪に関する情報を表示部25により表示する(ステップS234)。
本実施形態によると、増悪検出モデル173を用いて呼吸器系疾患の異常を検出することにより、速く且つ高精度に診断することが可能となる。
(実施形態3)
実施形態3は、呼吸筋または呼吸補助筋の動作に関する動作情報、及び呼吸筋または呼吸補助筋に対する活動電位情報に、さらに患者の生体情報を加えて、呼吸器系疾患の異常を検出する形態に関する。なお、実施形態3では、呼吸器系疾患の一つであるCOPDにおける増悪に関する情報を検出する例をあげて説明する。
実施形態3は、呼吸筋または呼吸補助筋の動作に関する動作情報、及び呼吸筋または呼吸補助筋に対する活動電位情報に、さらに患者の生体情報を加えて、呼吸器系疾患の異常を検出する形態に関する。なお、実施形態3では、呼吸器系疾患の一つであるCOPDにおける増悪に関する情報を検出する例をあげて説明する。
本実施形態では、患者の生体情報を検出する第2センサ5を含む。第2センサ5は、例えば、経皮的動脈血酸素飽和度を検出するオキシメータ、生体から発せられる生体音を収音するマイク、心臓の拍動に伴う心筋の活動電位または活動電流を記録し、これによりRRI(R-R Interval)及びCV-RR(Coefficient of Variation R-R interval)の解析も可能な心電計、血圧を検出する血圧計、体温を検出する体温計、経皮的動脈血二酸化炭素分圧(PtcCO2)の測定装置、心臓の拍動数を計測する脈拍計、心拍の周波数を解析する心拍変動測定器、生体インピーダンスを計測する生体電位センサ、または発汗センサ等を含む。
生体電位センサは、呼吸に伴う生体電気インピーダンスの変化を検出する。生体電気インピーダンスの変化は、胸郭上に配置した電極から高周波電流を通電して得られる胸郭インピーダンス(Z)を測定することにより、換気に伴う肺容積変化に応じた胸郭インピーダンスの変化量である呼吸性インピーダンス(ΔZ)を利用することで換気状態を把握するものである。即ち、呼吸に伴う胸郭インピーダンス(Z)の変化量(ΔZ)は、肺内気量(VL)の変化量(ΔVL)に応じて変化する。ΔZ = α(非負の比例係数)・ΔVLと仮定できる。胸郭インピーダンスの変化量ΔZは、吸気によって増加し(ΔZ>0)、呼気によって減少する(ΔZ <0)。従って、生体電位インピーダンスを測定することにより、肺の換気量が推定できる。
また、第2センサ5は、人体に触れずにベッド又は寝具下等に設置された非接触型のバイタルセンサであっても良い。非接触型のバイタルセンサは、小型マイクロ波レーダにより呼吸運動と心臓の鼓動に伴う体表面の微小な動き(心拍・呼吸)を計測し、赤外サーモカメラにより体表面から放出される赤外線(体温)を計測する。生体情報は、生体組織の状態及び組織が機能している場合の情報を反映した信号であり、例えば、脈拍、体動、呼吸等の生体現象によって体内から発せられる信号である。
図19は、第2センサ5を加えて増悪に関する情報の検出処理の動作を説明する説明図である。なお、図19では、第2センサ5の一つの種類のマイクを用いてCOPDにおける増悪に関する情報を検出する例をあげて説明する。なお、マイクに限らず、例えば複数の第2センサ5を用いて、増悪に関する情報が検出されても良い。マイクは、生体から発せられる生体音を収音する音センサである。例えばマイクを用いて、呼吸音、咳音、痰の貯留音または肺雑音等を含む生体音情報を取得し、周波数解析も行うことができ、これらの情報を学習モデルに入力する。
経皮的動脈血二酸化炭素分圧(PtcCO2)測定装置を用いる場合、PtcCO2に対応する値を学習モデルに入力する。増悪時にはPtcCO2が増加する傾向にある。またPtcCO2が高度に高くなった場合、呼吸の抑制が認められ、動作情報及び活動電位情報にも変動が生じる。学習モデルの学習の際には、履歴(過去の患者の計測履歴)に基づき得られた動作情報、活動電位情報及びPtcCO2に対応する値と、増悪レベルとを含む教師データを用いて学習処理を行う。
心電図を利用する場合、心電図計から出力される電位を学習モデルに入力する。増悪時には心電図に右心負荷所見が認められ易くなる。また、増悪時には心房細動と呼ばれる不整脈が生じ易く、これに対応した電位の変化が生じる。その他、増悪時には体調不良のため交感神経が副交感神経に比べ優位になり、これに伴いRRI(心電図上のR波とR波の間隔)の短縮ならびにRRIの変動係数であるCV-RRの低下が認められる。学習モデルの学習の際には、履歴に基づき得られた動作情報、活動電位情報及び心電図計の出力電位と、増悪レベルとを含む教師データを用いて学習処理を行う。
血圧計を用いる場合、血圧を学習モデルに入力する。増悪時には、上記のように交感神経が優位となり、この際には血圧が上昇する。学習モデルの学習の際には、履歴に基づき得られた動作情報、活動電位情報及び血圧と、増悪レベルとを含む教師データを用いて学習処理を行う。
体温計を用いる場合、体温計から得られる体温を学習モデルに入力する。増悪は、細菌またはウイルスによる呼吸器感染症が契機となることがあり、このような時には炎症所見として体温の上昇が認められる。学習モデルの学習の際には、履歴に基づき得られた動作情報、活動電位情報及び体温と、増悪レベルとを含む教師データを用いて学習処理を行う。
脈拍計を用いる場合、単位時間あたりの脈拍数または脈拍数の時間的変化を学習モデルに入力する。増悪時には、上記のように交感神経が優位となり、これにより脈拍数の上昇が認められる。学習モデルの学習の際には、履歴に基づき得られた動作情報、活動電位情報及び脈拍数と、増悪レベルとを含む教師データを用いて学習処理を行う。
心拍変動測定器を用いる場合、単位時間あたりのLF(低周波)/HF(高周波)比またはLF/HF比の時間的変化を学習モデルに入力する。増悪時には、上記のように交感神経が優位となり、これによりLF/HF比の上昇が認められる。学習モデルの学習の際には、履歴に基づき得られた動作情報、活動電位情報及びLF/HF比と、増悪レベルとを含む教師データを用いて学習処理を行う。
生体電位センサを用いる場合、単位時間あたりの胸郭インピーダンスの変化量ΔZまたは胸郭インピーダンスの変化量ΔZの時間的変化を学習モデルに入力する。増悪時には、換気障害に伴う肺容積変化の減少が認められ、これにより胸郭インピーダンスの変化量ΔZの低下が認められる。学習モデルの学習の際には、履歴に基づき得られた動作情報、活動電位情報及び胸郭インピーダンスの変化量ΔZと、増悪レベルとを含む教師データを用いて学習処理を行う。
発汗センサを用いる場合、単位時間あたりの発汗量または発汗量の時間的変化を学習モデルに入力する。増悪時には、上記のように交感神経が優位となり、これにより発汗量の上昇が認められる。学習モデルの学習の際には、履歴に基づき得られた動作情報、活動電位情報及び発汗量と、増悪レベルとを含む教師データを用いて学習処理を行う。なお、以上述べた第2センサを複数組み合わせて学習モデルに入力しても良い。
端末2の制御部21は、Bluetooth通信部26を介して、検出センサ3から呼吸筋または呼吸補助筋の動作に関する動作情報、及び筋電図センサ4から呼吸筋または呼吸補助筋に対する活動電位情報を取得する。制御部21は、Bluetooth通信部26を介して、マイクから生体音情報を取得する。例えば、呼吸音、咳音、痰の貯留音、肺雑音に関して周波数、強度、持続時間または音質等の生体音情報が取得されても良い。制御部21は、取得した動作情報、活動電位情報及び生体音情報に基づき、COPDにおける増悪に関する情報を検出する。
例えば、実施形態1で記述した動作情報及び活動電位情報により増悪に関する情報を検出する処理を基にして、更に生体音情報を加えて増悪に関する情報を検出しても良い。具体的には、端末2の制御部21は、動作情報及び活動電位情報に基づき、増悪に関する情報を検出した場合、マイクにより取得した生体音情報(例えば、呼吸音等)により引き続き増悪を判定する。COPD患者は増悪が生じた場合、呼吸音の減弱、呼気の延長、咳または痰の回数の増加、肺雑音の増加等の生体反応が生じるため、制御部21は、生体音情報に基づいて増悪に関する情報を検出する。制御部21は、検出した増悪に関する情報を表示部25により表示する。制御部21は、通信部23を介して、検出した増悪に関する情報をサーバ1に送信する。サーバ1の制御部11は、端末2から送信された増悪に関する情報を通信部13により受信し、受信した増悪に関する情報を大容量記憶部17の患者DB171に記憶する。
なお、本実施形態では、第2センサ5と検出センサ3と筋電図センサ4とを分離した形で図示しているが、両者を一体に構成しても良い。また、第2センサ5の配置場所は体の特定の部位に限定されるものではなく、非接触型であっても構わない。また、本実施形態では端末2と、第2センサ5を分離した形で図示しているが、これに限るものではない。例えば、端末2と、検出センサ3及び筋電図センサ4、第2センサ5とを全て一体化した装置構成としても良いし、端末2と第2センサ5を一体化した装置構成(例えば、腕時計型携帯端末等のウェアラブルデバイス等)であっても構わない。また時計型の第2センサ5をユーザに装着させておき、第2センサ5により異常を検出した場合に、検出センサ3及び筋電図センサ4をユーザの体に取り付けさせる形態であっても良い。
図20は、マイクを加えて増悪に関する情報を検出する際の処理手順を示すフローチャートである。なお、図12と重複する内容については同一の符号を付して説明を省略する。端末2の制御部21は、Bluetooth通信部26を介して、マイクから生体音情報(例えば、呼吸音等)を取得する(ステップS241)。制御部21は、動作情報及び活動電位情報に基づき、COPDにおける増悪に関する情報を検出した場合(ステップ203~206)、呼吸音が減弱しているか否かを判定する(ステップS242)。呼吸音の減弱の判定処理に関しては、例えば呼吸音の周波数を用いて判定しても良い。
制御部21は、取得した呼吸音が減弱していないと判定した場合(ステップS242でNO)、処理を終了する。制御部21は、取得した呼吸音が減弱していると判定した場合(ステップS242でYES)、ステップS207を実行する。なお、図20では、生体音情報の一つの呼吸音の例を説明したが、これに限るものではない。ほかの咳音、痰の貯留音、肺雑音、または上述した各種の音情報の組み合わせにより、COPDにおける増悪に関する情報が検出されても良い。
なお、上述した処理は、動作情報による増悪判定処理(ステップS205)、活動電位情報による増悪判定処理(ステップS206)後に、呼吸音が減弱しているか否かの判定(ステップS242)を行った例を説明したが、これに限るものではない。例えば、先に呼吸音が減弱しているか否かの判定(ステップS242)を行い、その後に活動電位情報による増悪判定処理(ステップS206)、次に動作情報による増悪判定処理(ステップS205)を行い、増悪に関する情報を検出しても良い。
または、呼吸音が減弱しているか否かの判定(ステップS242)、動作情報による増悪判定処理(ステップS205)、及び活動電位情報による増悪判定処理(ステップS206)を並行して行い、三者を用いて導き出される増悪の判定条件を満たした場合、増悪に関する情報を検出しても良い。
続いて、動作情報、活動電位情報及び第2センサ5により取得した生体情報に基づき、ディープラーニングにより構築された学習済みモデルを用いて、増悪に関する情報を検出する処理を説明する。
図21は、実施形態3のサーバ1の構成例を示すブロック図である。なお、図14と重複する内容については同一の符号を付して説明を省略する。大容量記憶部17は、第2増悪検出モデル174を含む。第2増悪検出モデル174は、ディープラーニングにより構築された増悪検出モデルである。第2増悪検出モデル174は、動作情報に関する電気信号の画像、活動電位情報の画像、及び第2センサ5により取得した生体信号画像内における増悪箇所の波形画像の特徴量を学習するディープラーニングを行うことで、波形画像を入力とし、COPDにおける増悪に関する情報の有無を示す情報を出力とするニューラルネットワークを構築(生成)する。なお、第2増悪検出モデル174の生成処理に関しては、実施形態1の増悪検出モデル173の生成処理と同様であるため、説明を省略する。
図22は、第2増悪検出モデル174を用いて増悪に関する情報を検出する際の処理手順を示すフローチャートである。なお、図18と重複する内容については同一の符号を付して説明を省略する。第2センサ5は、Bluetooth通信を利用して生体情報の画像を端末2に送信する(ステップS541)。端末2の制御部21は、Bluetooth通信部26を介して、第2センサ5から送信された生体情報の画像を受信する(ステップS243)。
生体情報は、例えば経皮的動脈血酸素飽和度を検出するオキシメータにより取得した酸素解離曲線データであっても良い。COPD患者は増悪がある場合、経皮的酸素濃度が低下するため、酸素解離曲線データの画像に基づいて増悪に関する情報を検出することができる。なお、経皮的動脈血酸素飽和度に限るものではない。生体情報の画像は、例えば呼吸数または心拍数に対する時系列データの時間的変化を示すフラグ、マイクの波形データ等であっても良い。
制御部21は、端末2にインストールされた第2増悪検出モデル174を用いてCOPDにおける増悪に関する情報を検出する(ステップS244)。なお、第2増悪検出モデル174を用いた増悪に関する情報の検出処理に関しては、実施形態1の増悪検出モデル173を用いた増悪に関する情報の検出処理と同様であるため、説明を省略する。
図23は、第2増悪検出モデル174の学習処理の処理手順の一例を示すフローチャートである。図23に基づき、第2増悪検出モデル174の学習処理の処理内容について説明する。
制御部11は、検出センサ3により取得した動作情報の画像、筋電図センサ4により取得した活動電位情報の画像、及び第2センサ5により取得した生体情報の画像と、COPDにおける増悪に関する情報とが対応付けられた教師データを取得する(ステップS151)。教師データは、例えば動作情報、活動電位情報及び生体情報の画像と、増悪に関する情報(例えば、増悪の確率値等)とをラベル付けしたデータである。
制御部11は、教師データを用いて、動作情報、活動電位情報及び生体情報の画像を入力した場合に増悪の有無に関する情報を出力する第2増悪検出モデル174を学習する(ステップS152)。具体的には、制御部11は、教師データである波形画像をニューラルネットワークの入力層に入力し、増悪に関する情報を識別した識別結果を出力層から取得する。制御部11は、取得した識別結果を教師データの正解値(波形画像に対してラベル付けられた情報)と比較し、出力層から出力される識別結果が正解値に近づくよう、中間層での演算処理に用いるパラメータ(重み等)を最適化する。制御部11は、学習した第2増悪検出モデル174を大容量記憶部17に格納し、一連の処理を終了する。
本実施形態によると、検出センサ3により取得した動作情報、筋電図センサ4により取得した活動電位情報、及び第2センサ5により取得した生体情報に基づき、呼吸器系疾患の異常を検出することができる。
本実施形態によると、生体情報を補助手段とし、動作情報及び活動電位情報と共に増悪に関する情報を検出する。これにより、例えば実施形態1の検出処理によって、増悪に関する情報が誤って検出されても、生体情報に基づいて増悪に関する情報の補正を行うことが可能となる。
(実施形態4)
実施形態4は、実施形態3を基にして、更に活動(労作)情報を検出する第3センサを用いて、呼吸器系疾患の異常を検出する形態に関する。なお、実施形態4では、呼吸器系疾患の一つであるCOPDにおける増悪に関する情報を検出する例をあげて説明する。本実施形態では、第3センサ6を含む。第3センサ6は、患者の運動量、移動距離、活動量または姿勢を含む活動情報を検出し、例えば加速度センサ、GPS(Global Positioning System/Global Positioning Satellite)センサ、またはジャイロセンサ(角速度センサ)等である。なお、複数の第3センサ6を用いて、活動(労作)情報が検出されても良い。
実施形態4は、実施形態3を基にして、更に活動(労作)情報を検出する第3センサを用いて、呼吸器系疾患の異常を検出する形態に関する。なお、実施形態4では、呼吸器系疾患の一つであるCOPDにおける増悪に関する情報を検出する例をあげて説明する。本実施形態では、第3センサ6を含む。第3センサ6は、患者の運動量、移動距離、活動量または姿勢を含む活動情報を検出し、例えば加速度センサ、GPS(Global Positioning System/Global Positioning Satellite)センサ、またはジャイロセンサ(角速度センサ)等である。なお、複数の第3センサ6を用いて、活動(労作)情報が検出されても良い。
図24は、実施形態4のサーバ1の構成例を示すブロック図である。なお、図21と重複する内容については同一の符号を付して説明を省略する。大容量記憶部17は、アドバイスDB175及びウォーキングモデル176を含む。アドバイスDB175は、活動内容、増悪に関する情報等に応じたアドバイス情報を記憶している。
活動内容は、例えばウォーキング、自転車、階段昇降、ジョギング、呼吸リハビリ運動等を含み、第3センサ6により取得する。例えば、端末2の制御部21は、加速度センサを用いて身体活動をモニタリングし、姿勢、速度、移動距離等の加速度データ(活動情報)を取得し、取得した加速度データに応じて活動内容を特定する。なお、活動内容の特定に関しては、上述した特定処理に限るものではない。例えば、活動内容を選択可能な画面がユーザに表示されている場合、ユーザのタッチ操作により活動内容を特定しても良い。
ウォーキングモデル176は、活動内容がウォーキングである場合、ディープラーニングにより構築された専用の増悪検出モデルである。例えば、動作情報に関する電気信号の画像、活動電位情報の画像、及び第2センサ5により取得した生体信号画像がウォーキングモデル176に入力される。ウォーキングモデル176は、ウォーキングに応じて、入力した画像内における増悪箇所の波形画像の特徴量を学習するディープラーニングを行うことで、波形画像を入力とし、COPDにおける増悪に関する情報の有無を示す情報を出力とするニューラルネットワークを構築(生成)する。なお、ウォーキングモデル176の生成処理に関しては、実施形態1の増悪検出モデル173の生成処理と同様であるため、説明を省略する。
また、第2センサ5による生体信号画像を用いずに、動作情報及び活動電位情報に基づき、ウォーキングモデル176が生成されても良い。
なお、本実施形態では、ウォーキングモデル176の例をあげて説明するが、これに限らず、活動内容ごとにそれぞれのモデル(例えば、自転車モデル、階段昇降モデル、ジョギングモデル、呼吸リハビリモデル等)を利用しても良い。例えば、呼吸リハビリとなる活動が特定された場合、動作情報に関する電気信号の画像、活動電位情報の画像、及び第2センサ5により取得した生体信号画像を入力とし、COPDにおける増悪に関する情報を出力する学習済みの呼吸リハビリモデルを用いて増悪に関する情報を検出しても良い。呼吸リハビリモデルは、検出センサ3により検出した呼吸リハビリ時の動作情報の画像、筋電図センサ4により検出した呼吸リハビリ時の活動電位情報の画像、及び第2センサ5により取得した生体信号画像の特徴量を学習することで、呼吸リハビリ時の身体反応状況に応じて、増悪に関する情報を検出する。
図25は、実施形態3のマスタDB172のレコードレイアウトの一例を示す説明図である。なお、図4と重複する内容については同一の符号を付して説明を省略する。マスタDB172は、活動内容列を含む。活動内容列は、身体活動に応じて行動の種類を記憶している。例えば、活動内容が階段昇降、ウォーキング等である。
図26は、アドバイスDB175のレコードレイアウトの一例を示す説明図である。アドバイスDB175は、アドバイスID列、活動内容列、増悪情報列及びアドバイス列を含む。アドバイスID列は、各アドバイスを識別するために、一意に特定されるアドバイスのIDを記憶している。活動内容列は、身体活動に応じて行動の種類を記憶している。増悪情報列は、増悪に関する情報を記憶している。アドバイス列は、活動内容及び増悪に関する情報に応じて、患者に対するアドバイス情報を記憶している。
続いて、活動内容に応じたアドバイス情報の送信処理について説明する。図27は、活動内容に応じたアドバイス情報を送信する際の処理手順を示すフローチャートである。端末2の制御部21は、Bluetooth通信部26を介して、検出センサ3から呼吸筋または呼吸補助筋の動作に関する動作情報を取得し(ステップS261)、筋電図センサ4から呼吸筋または呼吸補助筋に対する活動電位情報を取得する(ステップS262)。制御部21は、Bluetooth通信部26を介して、第2センサ5により生体情報を取得し(ステップS263)、第3センサ6により患者の運動量、移動距離、活動量または姿勢を含む活動情報を取得する(ステップS264)。
制御部21は、取得した活動情報に基づいて活動内容を特定する(ステップS265)。制御部21は、取得した動作情報、活動電位情報及び生体情報に基づき、増悪に関する情報を検出する(ステップS266)。なお、増悪に関する情報の検出処理に関しては、実施形態3での検出処理と同様であるため、説明を省略する。制御部21は、通信部23を介して、検出した増悪に関する情報、及び特定した活動内容に基づき、アドバイスの取得リクエストをサーバ1に送信する(ステップS267)。サーバ1の制御部11は、通信部13を介して、端末2から送信されたアドバイスの取得リクエストを受信する(ステップS161)。
制御部11は、受信したアドバイスの取得リクエストに応じて、大容量記憶部17のアドバイスDB175からアドバイス情報を取得する(ステップS162)。制御部11は、通信部13を介して、取得したアドバイス情報を端末2に送信する(ステップS163)。端末2の制御部21は、サーバ1から送信されたアドバイス情報を通信部23により受信し(ステップS268)、受信したアドバイス情報を表示部25により表示する(ステップS269)。例えば、増悪レベル2(リスクが低い)であるジョギング中の患者に対し、アドバイス情報「呼吸に走るリズムを合わせましょう!」を表示しても良い。また、増悪レベル3(リスクが高い)である階段を上っている患者に対し、アドバイス情報「一旦止まって、呼吸を整えましょう!」を表示しても良い。更にまた、増悪レベル4(増悪)であるウォーキング中の患者に対し、アドバイス情報「短時間作用型吸入β2刺激薬を使用してください!」を表示しても良い。
続いて、機械学習によって構築した活動ごとのモデルを用いてCOPDにおける増悪に関する情報を検出する処理について説明する。なお、本実施形態では、ウォーキングする際に利用可能なウォーキングモデル176に基づいて説明するが、ほかの活動内容でも同様に適用できる。活動内容に応じて、運動量、活動量、姿勢等が異なるため、COPDにおける増悪に関する情報を検出する検出結果にも影響を与える。ある特定の活動(例えば、ウォーキング)に対し、該特定の活動状態から取得した各種の波形画像の特徴量を学習するディープラーニングを行うことで、波形画像を入力とし、COPDにおける増悪に関する情報の有無を示す情報を出力とするニューラルネットワークを構築することができる。よって、該学習済みの専用モデルを用いて、該特定の活動におけるCOPDの増悪に関する情報を検出する精度が高くなる。
図28は、ウォーキングモデル176を用いて増悪に関する情報を検出する際の処理手順を示すフローチャートである。なお、図27と重複する内容については同一の符号を付して説明を省略する。端末2の制御部21は、ステップS265で特定した活動内容に応じて、学習済みの活動学習モデルを特定する(ステップS270)。例えば、制御部21は、ステップS264で取得した活動情報からウォーキングとなる活動内容を特定した場合、予めインストールされたウォーキングモデル176を特定し、COPDにおける増悪に関する情報を検出する。すなわち、活動内容ごとの学習済みの活動学習モデルを利用することにより、COPDにおける精度が高い増悪に関する情報を検出することができる。
続いて、筋電図センサ4により取得した活動電位情報を判定するための電気信号の所定閾値の変更処理を説明する。
活動内容に応じて運動量等が変化するため、これに合わせてCOPDにおける増悪の有無に関する情報の判定基準を変更させる。以下では、活動内容に応じて、筋電図センサ4により取得した活動電位情報を判定するための電気信号の所定閾値変更の例をあげて説明する。端末2の制御部21は、Bluetooth通信部26を介して、第3センサ6により検出した活動情報を取得する。制御部21は、取得した活動情報に応じて、活動内容を特定する。制御部21は、特定した活動内容に基づき、サーバ1の大容量記憶部17のマスタDB172から、筋電図センサ4により取得した活動電位情報を判定するための電気信号の所定閾値を取得する。そして制御部21は、取得した新たな閾値に基づき、増悪に関する情報を検出する際に判定処理を行う。例えば、端末2の制御部21は活動内容をウォーキングと特定した場合、制御部21はサーバ1の大容量記憶部17のマスタDB172から、ウォーキングに対応する活動電位情報を判定するための電気信号の所定閾値を取得する。ウォーキングの場合、運動量がアップするため、増悪に関する情報を検出するための電気信号の閾値は、安静時の閾値より高くなる。
なお、上述した電気信号の閾値の変更処理の例を説明したが、これに限るものではない。検出センサ3により取得した動作情報を判定するための第1条件、第2センサ5により取得した生体情報を判定するための生体情報の所定閾値を変更することができる。例えば、端末2は検出センサ3を用いて増悪の検出処理を行った場合、活動内容に応じて、呼気筋の動作電気信号閾値を変更する。例えば、端末2は活動内容をウォーキングと特定した場合、運動量がアップするため、電圧の極大の傾き閾値または極小の傾き閾値を高く変更する。
また、端末2は第2センサ5を用いて増悪の検出処理を行った場合、活動内容に応じて、第2センサ5の各種の閾値を変更しても良い。例えば第2センサ5がマイクである場合、端末2の制御部21は音声データを取得する。制御部21は音声データを周波数変換し、特定周波数帯のパワーが所定閾値を超えるか否か判断する。制御部21は所定閾値を超える場合、増悪の可能性があると判断し、検出センサ3及び筋電図センサ4を用いた判断を行う。ここで制御部21は活動内容に応じて上述した所定閾値を変化させる。
なお、上述した活動内容に応じた所定閾値を変更する処理に限るものではない。例えば、増悪検出モデル173を用いて、出力した増悪の確率値に応じて、筋電図センサ4により取得した活動電位情報を判定するための電気信号の所定閾値を変更しても良い。
図29は、増悪の確率値に応じた電気信号の所定閾値を変更する際の処理手順を示すフローチャートである。学習済みの増悪検出モデル173がインストールされた端末2の制御部21は、Bluetooth通信部26を介して、検出センサ3から呼吸筋または呼吸補助筋の動作に関する動作情報を取得する(ステップS271)。制御部21は、Bluetooth通信部26を介して、筋電図センサ4から呼吸筋または呼吸補助筋に対する活動電位情報を取得する(ステップS272)。
制御部21は、増悪検出モデル173を用いてCOPDにおける増悪に関する情報を検出する(ステップS273)。制御部21は、検出した増悪に関する情報から増悪の確率値を取得する(ステップS274)。例えば、取得された増悪の確率値が0.3である場合、増悪の発症リスクがあるため、筋電図センサ4により取得した活動電位情報を判定するための電気信号の所定閾値の変更が必要となる。
制御部21は、通信部23を介して、取得した増悪の確率値をサーバ1に送信する(ステップS275)。サーバ1の制御部11、通信部13を介して、端末2から送信された増悪の確率値を受信する(ステップS171)。制御部11は、受信した増悪の確率値に応じて、筋電図センサ4により取得した活動電位情報を判定するための電気信号の所定閾値を算出する(ステップS172)。算出アルゴリズムに関しては、例えば増悪の発症リスクがある場合、既存の電気信号の所定閾値に0~1間の係数を乗じて算出しても良い。すなわち、増悪の発症リスクがある場合、増悪検出の判定基準が厳しくなる。制御部11は、算出した電気信号の所定閾値を大容量記憶部17のマスタDB172に更新する(ステップS173)。
続いて、検出センサ3、筋電図センサ4及び第3センサ6を用いたCOPDにおける増悪に関する情報の検出処理について説明する。例えば、第3センサ6はジャイロセンサである。端末2は、検出センサ3を用いて呼吸筋または呼吸補助筋の動作に関する動作情報、筋電図センサ4を用いて呼吸筋または呼吸補助筋に対する活動電位情報、及びジャイロセンサを用いて足のふらつき値を取得する。端末2は、取得した足のふらつき値が所定閾値以上であるか否かを判定する。端末2は、取得した足のふらつき値が所定閾値以上であると判定した場合、実施形態1と同様の処理により、取得した動作情報及び活動電位情報に基づいて増悪に関する情報を検出する。なお、足のふらつきの検出処理に関しては、ジャイロセンサにより取得したジャイロセンサデータを入力とし、ふらつきを検出する学習済みのふらつき検出モデルを利用しても良い。
なお、本実施形態では、筋電図センサ4により取得した活動電位情報を判定するための電気信号の所定閾値の変更処理を説明したが、これに限るものではない。他の判定用の閾値に対しても、上述した処理内容により変更しても良い。
本実施形態によると、活動内容に応じた呼吸器系疾患の異常を検出することに関し、安静時では発見しにくい増悪に関する症状に対しても、増悪の検出率を高めることが可能となる。
本実施形態によると、活動内容に応じたそれぞれの学習済みの活動学習モデルを利用することにより、身体活動量の実態を考慮して安静時以外の活動(例えば、ジョギング等の高強度の活動)の場合でも、COPDにおける増悪に関する情報を検出することが可能となる。
本実施形態によると、活動内容または増悪の確率値に応じて、増悪の有無に関する情報を判定するための電気信号の所定閾値を適切に変更することが可能となる。
(実施形態5)
実施形態5は、COPDにおける増悪に関する情報を検出した場合、検出した増悪に関する情報に応じて、薬の服薬指示情報または服薬指示情報以外の第2のアドバイス情報を送信する形態に関する。なお、実施形態1~4と重複する内容については説明を省略する。
実施形態5は、COPDにおける増悪に関する情報を検出した場合、検出した増悪に関する情報に応じて、薬の服薬指示情報または服薬指示情報以外の第2のアドバイス情報を送信する形態に関する。なお、実施形態1~4と重複する内容については説明を省略する。
図30は、実施形態5のサーバ1の構成例を示すブロック図である。なお、図24と重複する内容については同一の符号を付して説明を省略する。大容量記憶部17は、服薬指示情報DB177及び治療結果DB178を含む。服薬指示情報DB177は、COPD患者に対して、あらかじめ増悪時に使用するために処方されている薬に対する服薬指示の情報を記憶している。治療結果DB178は、増悪に関する情報を検出した患者に対して、あらかじめ増悪時に使用するために処方されている薬の摂取に関する情報、及び薬を摂取した後の計測データを記憶している。
図31は、服薬指示情報DB177のレコードレイアウトの一例を示す説明図である。服薬指示情報DB177は、服薬指示ID列、患者ID列、増悪情報列、服薬指示列及びアドバイス列を含む。服薬指示ID列は、各服薬指示を識別するために、一意に特定される服薬指示のIDを記憶している。患者ID列は、患者を特定する患者IDを記憶している。増悪情報列は、増悪に関する情報を記憶している。服薬指示列は、増悪に関する情報に応じた薬の服薬指示の情報を記憶している。アドバイス列は、増悪に関する情報に応じて服薬指示の情報以外の第2のアドバイス情報を記憶している。
図32は、治療結果DB178のレコードレイアウトの一例を示す説明図である。治療結果DB178は、管理ID列、患者ID列、服薬指示ID列、薬摂取状況列及び計測データ列を含む。管理ID列は、各治療結果のデータを識別するために、一意に特定される治療結果のデータのIDを記憶している。患者ID列は、患者を特定する患者IDを記憶している。服薬指示ID列は、服薬指示を特定する服薬指示IDを記憶している。薬摂取状況列は、増悪に関する情報を検出した患者に対して服薬指示された薬の摂取の状況(ステータス)を記憶している。例えば、薬摂取状況列に「摂取済み」、「摂取中」または「未摂取」等が記入されても良い。
計測データ列は、動作情報列、活動電位情報列及び生体情報列を含む。動作情報列は、増悪に関する情報を検出した患者が服薬指示された薬を摂取した後に、該患者に対し、検出センサ3により取得した動作情報を記憶している。活動電位情報列は、増悪に関する情報を検出した患者が服薬指示された薬を摂取した後に、該患者に対し、筋電図センサ4により取得した活動電位情報を記憶している。生体情報列は、増悪に関する情報を検出した患者が服薬指示された薬を摂取した後に、該患者に対し、第2センサ5により取得した生体情報を記憶している。
図33は、増悪に関する情報に応じた、あらかじめ増悪時に使用するために処方されている薬に対する服薬指示情報を送信する際の処理手順を示すフローチャートである。端末2の制御部21は、Bluetooth通信部26を介して、検出センサ3から動作情報を取得し(ステップS281)、筋電図センサ4から活動電位情報を取得する(ステップS282)。制御部21は、COPDにおける増悪に関する情報を検出するか否かを判定する(ステップS283)。なお、増悪に関する情報の検出処理に関しては、実施形態1での増悪に関する情報の検出処理と同様であるため、説明を省略する。制御部21は、COPDにおける増悪に関する情報を検出していないと判定した場合(ステップS283でNO)、処理を終了する。
制御部21は、COPDにおける増悪に関する情報を検出したと判定した場合(ステップS283でYES)、増悪に関する情報に応じた薬の服薬指示情報を取得する(ステップS284)。例えば、制御部21は、医師が増悪に関する情報を確認し、 あらかじめ処方していた薬に対して行う直接の服薬指示情報を通信部23若しくは入力部24により受け付けても良く、または記憶部22から増悪に関する情報に応じて、あらかじめ処方されている薬に対する服薬指示の情報を取得しても良い。薬の服薬指示情報は、薬の種類(例えば、短時間作用型吸入β2刺激薬等)、名称(例えば、メプチン)、服用方法及び副作用等を含む。制御部21は、取得した服薬指示情報を表示部25により表示する(ステップS285)。制御部21は、通信部23を介して、取得した服薬指示情報をサーバ1に送信する(ステップS286)。
サーバ1の制御部11は、端末2から送信された増悪に関する情報に応じた薬の服薬指示情報を通信部13により受信し(ステップS181)、受信した服薬指示情報を大容量記憶部17の服薬指示情報DB177に記憶する(ステップS182)。具体的には、制御部11は、服薬指示IDを割り振って、患者ID、増悪に関する情報及び服薬指示情報を一つのレコードとして服薬指示情報DB177に記憶する。
図34は、増悪に関する情報に応じた第2のアドバイス情報を送信する際の処理手順を示すフローチャートである。なお、図33と重複する内容については同一の符号を付して説明を省略する。端末2の制御部21は、ステップS283でCOPDにおける増悪に関する情報を検出したと判定した場合、増悪に関する情報に応じる第2のアドバイス情報を取得する(ステップS291)。第2のアドバイス情報は、上述した服薬指示情報以外の意見・提案等であり、COPDの治療に対する有益な情報等であっても良い。第2のアドバイス情報としては、例えば「ウォーキングをしてください。」、「基礎的なトレーニングをしてください。」等の運動療法に関する情報、または「食べ過ぎに注意してください。」、「栄養管理をしてください。」等の栄養療法に関する情報が含まれる。なお、第2のアドバイス情報の取得処理に関しては、上述した服薬指示情報の取得処理と同様であるため、説明を省略する。制御部21は、取得した第2のアドバイス情報を表示部25により表示する(ステップS292)。制御部21は、通信部23を介して、取得した第2のアドバイス情報をサーバ1に送信する(ステップS293)。
サーバ1の制御部11は、端末2から送信された増悪に関する情報に応じた第2のアドバイス情報を通信部13により受信し(ステップS191)、受信した第2のアドバイス情報を大容量記憶部17の服薬指示情報DB177に記憶する(ステップS192)。具体的には、制御部11は、服薬指示IDを割り振って、患者ID、増悪に関する情報及び第2のアドバイス情報を一つのレコードとして服薬指示情報DB177に記憶する。
なお、上述した服薬指示情報または第2のアドバイス情報がそれぞれに端末2に送信されたが、これに限るものではない。例えば、サーバ1の制御部11は、検出した増悪に関する情報に応じて、服薬指示情報を第2のアドバイス情報と共に端末2に送信しても良い。
また、患者が服薬指示された薬を摂取した後に、薬の摂取に関する情報、及び薬を摂取した後の計測データを記憶することができる。具体的には、制御部11は、通信部13または入力部14を介して、増悪に関する情報を検出した患者に対して服薬指示された薬の摂取に関する情報を取得する。制御部11は、通信部13を介して、検出センサ3から薬の摂取後の動作情報、筋電図センサ4から薬の摂取後の活動電位情報、及び第2センサ5から薬の摂取後の生体情報を含む計測データを取得する。
制御部11は、取得した薬の摂取に関する情報、及び薬を摂取した後の計測データを大容量記憶部17の治療結果DB178に記憶する。具体的には、制御部11は、管理IDを割り振って、患者ID、服薬指示ID、薬の摂取状況、動作情報、活動電位情報及び生体情報を一つのレコードとして治療結果DB178に記憶する。
続いて、薬を摂取した後の計測データを用いて、第2増悪検出モデル174の再学習処理の処理内容について説明する。COPD患者が薬を摂取して所定の時間を経過した後に、制御部11は、検出センサから出力される動作情報、及び筋電図センサから出力される活動電位情報を含む計測データと、増悪が生じていないことを示す情報(例えば、レベル1)とが対応付けられた第2教師データを取得する。制御部11は、第2教師データを用いて、動作情報及び活動電位情報を入力した場合に増悪の有無に関する情報を出力する増悪検出モデル173(学習済みモデル)を再学習する。制御部11は、再学習した増悪検出モデル173を大容量記憶部17に格納し、一連の処理を終了する。
また、患者の薬摂取後の評価、及びその後の対応も行うことが可能となる。例えば、気管支拡張作用のある短時間作用型吸入β2刺激薬の服薬指示を行った患者が、薬を吸入しても、動的過膨張等の増悪状態の改善が認められない場合、病院受診の指示を患者宛に送信する等の対応が可能となる。
本実施形態によると、COPDにおける増悪に関する情報を検出した場合、検出した増悪に関する情報に応じて、薬の服薬指示情報を患者宛に送信することが可能となる。
本実施形態によると、COPDにおける増悪に関する情報を検出した場合、検出した増悪に関する情報に応じて、服薬指示情報以外の第2のアドバイス情報を患者宛に送信することが可能となる。
本実施形態によると、薬を摂取した後の計測データを用いて、第2増悪検出モデルを再学習することにより、増悪に関する情報の検出精度を向上することが可能となる。
今回開示された実施形態はすべての点で例示であって、制限的なものではないと考えられるべきである。本発明の範囲は、上記した意味ではなく、請求の範囲によって示され、請求の範囲と均等の意味及び範囲内でのすべての変更が含まれることが意図される。
1 情報処理装置(サーバ)
11 制御部
12 記憶部
13 通信部
14 入力部
15 表示部
16 読取部
17 大容量記憶部
171 患者DB
172 マスタDB
173 増悪検出モデル
174 第2増悪検出モデル
175 アドバイスDB
176 ウォーキングモデル
177 服薬指示情報DB
178 治療結果DB
1a 可搬型記憶媒体
1b 半導体メモリ
1P 制御プログラム
2 情報処理端末(端末)
21 制御部
22 記憶部
23 通信部
24 入力部
25 表示部
26 Bluetooth通信部
2P 制御プログラム
3 検出センサ
31 制御部
32 記憶部
33 圧電素子
34 Bluetooth通信部
3P 制御プログラム
4 筋電図センサ
41 制御部
42 記憶部
43 筋電計測部
44 Bluetooth通信部
4P 制御プログラム
5 第2センサ
6 第3センサ
11 制御部
12 記憶部
13 通信部
14 入力部
15 表示部
16 読取部
17 大容量記憶部
171 患者DB
172 マスタDB
173 増悪検出モデル
174 第2増悪検出モデル
175 アドバイスDB
176 ウォーキングモデル
177 服薬指示情報DB
178 治療結果DB
1a 可搬型記憶媒体
1b 半導体メモリ
1P 制御プログラム
2 情報処理端末(端末)
21 制御部
22 記憶部
23 通信部
24 入力部
25 表示部
26 Bluetooth通信部
2P 制御プログラム
3 検出センサ
31 制御部
32 記憶部
33 圧電素子
34 Bluetooth通信部
3P 制御プログラム
4 筋電図センサ
41 制御部
42 記憶部
43 筋電計測部
44 Bluetooth通信部
4P 制御プログラム
5 第2センサ
6 第3センサ
Claims (21)
- 呼吸筋または呼吸補助筋の動作に関する動作情報を検出する検出センサから前記動作情報、及び呼吸筋または呼吸補助筋に対する活動電位情報を取得する筋電図センサから前記活動電位情報を取得し、
取得した前記動作情報及び活動電位情報に基づき呼吸器系疾患の異常を検出し、
前記異常を検出した場合に、異常情報を出力する
処理をコンピュータに実行させることを特徴とするプログラム。 - 前記検出センサは、呼吸筋または呼吸補助筋の動作情報を検出する圧電素子センサ、伸縮センサ、エコーセンサまたは生体電位センサを含む
請求項1に記載のプログラム。 - 前記検出センサにより検出した動作情報に基づき、第1条件を満たすか否かを判定し、
前記筋電図センサから取得した活動電位情報の内、呼気筋に対応する電気信号が所定閾値以上か否かを判定し、
前記第1条件を満たし、かつ、呼気筋に対応する電気信号が所定閾値以上である場合に、慢性閉塞性肺疾患における増悪に関する情報を出力する
処理を実行させる請求項1又は2に記載のプログラム。 - 前記検出センサにより検出した動作情報に基づき、第1条件を満たすか否かを判定し、
前記筋電図センサから取得した活動電位情報の内、呼気筋に対応する電気信号の持続時間が所定閾値以上か否かを判定し、
前記第1条件を満たし、かつ、呼気筋に対応する電気信号の持続時間が所定閾値以上である場合に、慢性閉塞性肺疾患における増悪に関する情報を出力する
処理を実行させる請求項1又は2に記載のプログラム。 - 前記検出センサにより検出した動作情報に基づき、第1条件を満たすか否かを判定し、
前記筋電図センサから取得した活動電位情報の内、呼気筋に対応する電気信号の周波数分布の平均周波数または中央周波数の変化値が所定閾値以上か否かを判定し、
前記第1条件を満たし、かつ、呼気筋に対応する電気信号の周波数分布の平均周波数または中央周波数の変化値が所定閾値以上である場合に、慢性閉塞性肺疾患における増悪に関する情報を出力する
処理を実行させる請求項1又は2に記載のプログラム。 - 前記所定閾値は第1閾値、及び、該第1閾値より大きい第2閾値を含み、
呼気筋に対応する電気信号が第1閾値以上第2閾値未満の場合、第1レベルの増悪に関する情報を出力し、
呼気筋に対応する電気信号が第2閾値以上の場合、第2レベルの増悪に関する情報を出力する
処理を実行させる請求項3から5のいずれか一つに記載のプログラム。 - 前記検出センサにより出力される電気信号の極大値及び極小値が所定時間継続して所定量以上増加している場合に第1条件を満たすと判断する
処理を実行させる請求項3から6のいずれか一つに記載のプログラム。 - 患者の生体情報を検出する第2センサにより生体情報を取得し、
取得した前記生体情報、前記検出センサにより取得した動作情報、及び前記筋電図センサにより取得した活動電位情報から、呼吸器系疾患の異常の有無を判断する
処理を実行させる請求項1から7までのいずれかひとつに記載のプログラム。 - マイクを用いて呼吸音、咳音、痰の貯留音または肺雑音を含む生体音情報を取得し、
取得した前記生体音情報、前記動作情報及び活動電位情報から、呼吸器系疾患の異常を検出する
処理を実行させる請求項1から8までのいずれかひとつに記載のプログラム。 - 第2センサは、経皮的動脈血酸素飽和度を検出するオキシメータ、生体から発せられる生体音を収音するマイク、経皮的動脈血二酸化炭素分圧(PtcCO2)測定装置、心臓の拍動に伴う心筋の活動電位または活動電流を記録し、これによりRRI及びCV-RRの解析も可能な心電計、血圧を検出する血圧計、体温を検出する体温計、心臓の拍動数を計測する脈拍計、心拍の周波数を解析する心拍変動測定器、生体インピーダンスを計測する生体電位センサ、または発汗センサを含む
請求項8又は9に記載のプログラム。 - 患者の運動量、移動距離、活動量または姿勢を含む活動情報を検出する第3センサにより前記活動情報を取得する
処理を実行させる請求項1から10までのいずれかひとつに記載のプログラム。 - 前記第3センサにより取得した前記活動情報から所定の活動を検出した場合、検出した前記活動に応じて、前記検出センサにより取得した動作情報を判定するための第1条件、前記筋電図センサにより取得した活動電位情報を判定するための電気信号の所定閾値、または第2センサにより取得した生体情報を判定するための生体情報の所定閾値を変更する
処理を実行させる請求項11に記載のプログラム。 - 前記活動情報に応じて活動内容を特定し、
特定した活動内容、前記検出センサから得られる動作情報、筋電図センサから得られる活動電位情報、及び患者の生体情報を検出する第2センサから得られる生体情報に応じて、アドバイス情報を取得し、
取得した前記アドバイス情報を送信する
処理を実行させる請求項11又は12に記載のプログラム。 - 前記動作情報及び活動電位情報に基づき、慢性閉塞性肺疾患における増悪に関する情報を検出した場合、前記増悪に関する情報に応じて薬の服薬指導情報を取得し、
取得した前記服薬指導情報を送信する
処理を実行させる請求項1から13までのいずれかひとつに記載のプログラム。 - 前記慢性閉塞性肺疾患における増悪に関する情報を検出した場合、前記増悪に関する情報に応じて、前記服薬指導情報以外の第2のアドバイス情報を取得し、
取得した第2のアドバイス情報を送信する
処理を実行させる請求項14に記載のプログラム。 - 前記検出センサから得られる動作情報、及び前記筋電図センサから得られる活動電位情報を取得し、
前記動作情報、活動電位情報及び慢性閉塞性肺疾患における増悪に関する情報を含む複数の教師データに基づき学習された学習モデルに、取得した動作情報及び活動電位情報を入力し、
慢性閉塞性肺疾患における増悪の有無に関する情報を出力する
処理を実行させる請求項1又は2に記載のプログラム。 - 前記動作情報、前記活動電位情報、及び患者の生体情報を検出する第2センサから得られる生体情報を取得し、
前記動作情報、活動電位情報、生体情報及び慢性閉塞性肺疾患における増悪に関する情報を含む複数の教師データに基づき学習された第2学習モデルに、取得した動作情報、活動電位情報及び生体情報を入力し、
慢性閉塞性肺疾患における増悪の有無に関する情報を出力する
処理を実行させる請求項1又は2に記載のプログラム。 - 患者の運動量、移動距離、活動量または姿勢を含む活動情報を検出する第3センサにより取得した前記活動情報に応じて活動内容を特定し、
活動内容ごとに用意された複数の学習モデルから特定した活動情報に対応する学習モデルを選択し、
選択した学習モデルに前記動作情報及び活動電位情報を入力し、
慢性閉塞性肺疾患における増悪の有無に関する情報を出力する
処理を実行させる請求項16又は17に記載のプログラム。 - 薬を摂取して所定の時間を経過した後に、検出センサから出力される動作情報、及び筋電図センサから出力される活動電位情報を取得し、
取得した動作情報、活動電位情報及び増悪が生じていないことを示す情報を用いて学習済みモデルを再学習する
処理を実行させる請求項16から18までのいずれかひとつに記載のプログラム。 - 呼吸筋または呼吸補助筋の動作に関する動作情報を検出する検出センサから前記動作情報、及び呼吸筋または呼吸補助筋に対する活動電位情報を取得する筋電図センサから前記活動電位情報を取得し、
取得した前記動作情報及び活動電位情報に基づき呼吸器系疾患の異常を検出し、
前記異常を検出した場合に、異常情報を出力する
情報処理方法。 - 呼吸筋または呼吸補助筋の動作に関する動作情報を検出する検出センサから前記動作情報、及び呼吸筋または呼吸補助筋に対する活動電位情報を取得する筋電図センサから前記活動電位情報を取得する取得部と、
取得した前記動作情報及び活動電位情報に基づき呼吸器系疾患の異常を検出する検出部と、
前記異常を検出した場合に、異常情報を出力する出力部と
を備えることを特徴とする情報処理装置。
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202080033326.8A CN113939231A (zh) | 2019-03-22 | 2020-03-19 | 程式、资讯处理方法及资讯处理装置 |
| JP2021509339A JP7158783B2 (ja) | 2019-03-22 | 2020-03-19 | プログラム、情報処理方法及び情報処理装置 |
| EP20777852.3A EP3943011A4 (en) | 2019-03-22 | 2020-03-19 | PROGRAM, INFORMATION PROCESSING METHOD AND INFORMATION PROCESSING DEVICE |
| US17/480,262 US20220079518A1 (en) | 2019-03-22 | 2021-09-21 | Program information processing method, and information processing device |
| JP2022160412A JP7321599B2 (ja) | 2019-03-22 | 2022-10-04 | プログラム、情報処理方法及び情報処理装置 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019055536 | 2019-03-22 | ||
| JP2019-055536 | 2019-03-22 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| US17/480,262 Continuation US20220079518A1 (en) | 2019-03-22 | 2021-09-21 | Program information processing method, and information processing device |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2020196323A1 true WO2020196323A1 (ja) | 2020-10-01 |
Family
ID=72611969
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2020/012464 WO2020196323A1 (ja) | 2019-03-22 | 2020-03-19 | プログラム、情報処理方法及び情報処理装置 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20220079518A1 (ja) |
| EP (1) | EP3943011A4 (ja) |
| JP (2) | JP7158783B2 (ja) |
| CN (1) | CN113939231A (ja) |
| WO (1) | WO2020196323A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2023089818A1 (ja) * | 2021-11-22 | 2023-05-25 | 日本電信電話株式会社 | 個人識別装置、方法およびプログラム |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009254611A (ja) * | 2008-04-17 | 2009-11-05 | Konica Minolta Medical & Graphic Inc | 咳検出装置 |
| JP2014010117A (ja) | 2012-07-02 | 2014-01-20 | Institute Of Physical & Chemical Research | 慢性閉塞性肺疾患の増悪指標の検出方法 |
| US20160174903A1 (en) * | 2014-12-23 | 2016-06-23 | Michael Cutaia | System and method for outpatient management of chronic disease |
| JP2017537684A (ja) * | 2014-11-12 | 2017-12-21 | コーニンクレッカ フィリップス エヌ ヴェKoninklijke Philips N.V. | 被験者における慢性閉塞性肺疾患(copd)の重症度を評価するための装置及び方法 |
| JP2018503446A (ja) * | 2015-01-28 | 2018-02-08 | コーニンクレッカ フィリップス エヌ ヴェKoninklijke Philips N.V. | 被験者の呼吸努力を決定及び/又は監視するための装置並びに方法 |
| US20180144465A1 (en) * | 2016-11-23 | 2018-05-24 | General Electric Company | Deep learning medical systems and methods for medical procedures |
| JP2018527069A (ja) * | 2015-08-11 | 2018-09-20 | コーニンクレッカ フィリップス エヌ ヴェKoninklijke Philips N.V. | 呼吸活動に関する筋電図信号を処理するための処理装置及び方法 |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20040230230A1 (en) | 2003-04-11 | 2004-11-18 | Lindstrom Curtis Charles | Methods and systems involving subcutaneous electrode positioning relative to a heart |
| US7787946B2 (en) * | 2003-08-18 | 2010-08-31 | Cardiac Pacemakers, Inc. | Patient monitoring, diagnosis, and/or therapy systems and methods |
| US7510531B2 (en) * | 2003-09-18 | 2009-03-31 | Cardiac Pacemakers, Inc. | System and method for discrimination of central and obstructive disordered breathing events |
| US20120197621A1 (en) * | 2011-01-31 | 2012-08-02 | Fujitsu Limited | Diagnosing Insulin Resistance |
| KR20120113530A (ko) * | 2011-04-05 | 2012-10-15 | 삼성전자주식회사 | 생체 신호의 피크 검출 방법 및 장치 |
| KR101939683B1 (ko) * | 2012-03-29 | 2019-01-18 | 삼성전자 주식회사 | 사용자 행동 실시간 인식장치 및 방법 |
| EP3340876A2 (en) * | 2015-08-26 | 2018-07-04 | ResMed Sensor Technologies Limited | Systems and methods for monitoring and management of chronic disease |
| JP6709116B2 (ja) * | 2016-06-27 | 2020-06-10 | 公立大学法人会津大学 | 呼吸検出装置、呼吸検出方法および呼吸検出用プログラム |
| US10770182B2 (en) * | 2017-05-19 | 2020-09-08 | Boston Scientific Scimed, Inc. | Systems and methods for assessing the health status of a patient |
-
2020
- 2020-03-19 JP JP2021509339A patent/JP7158783B2/ja active Active
- 2020-03-19 WO PCT/JP2020/012464 patent/WO2020196323A1/ja unknown
- 2020-03-19 CN CN202080033326.8A patent/CN113939231A/zh active Pending
- 2020-03-19 EP EP20777852.3A patent/EP3943011A4/en active Pending
-
2021
- 2021-09-21 US US17/480,262 patent/US20220079518A1/en active Pending
-
2022
- 2022-10-04 JP JP2022160412A patent/JP7321599B2/ja active Active
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009254611A (ja) * | 2008-04-17 | 2009-11-05 | Konica Minolta Medical & Graphic Inc | 咳検出装置 |
| JP2014010117A (ja) | 2012-07-02 | 2014-01-20 | Institute Of Physical & Chemical Research | 慢性閉塞性肺疾患の増悪指標の検出方法 |
| JP2017537684A (ja) * | 2014-11-12 | 2017-12-21 | コーニンクレッカ フィリップス エヌ ヴェKoninklijke Philips N.V. | 被験者における慢性閉塞性肺疾患(copd)の重症度を評価するための装置及び方法 |
| US20160174903A1 (en) * | 2014-12-23 | 2016-06-23 | Michael Cutaia | System and method for outpatient management of chronic disease |
| JP2018503446A (ja) * | 2015-01-28 | 2018-02-08 | コーニンクレッカ フィリップス エヌ ヴェKoninklijke Philips N.V. | 被験者の呼吸努力を決定及び/又は監視するための装置並びに方法 |
| JP2018527069A (ja) * | 2015-08-11 | 2018-09-20 | コーニンクレッカ フィリップス エヌ ヴェKoninklijke Philips N.V. | 呼吸活動に関する筋電図信号を処理するための処理装置及び方法 |
| US20180144465A1 (en) * | 2016-11-23 | 2018-05-24 | General Electric Company | Deep learning medical systems and methods for medical procedures |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2023089818A1 (ja) * | 2021-11-22 | 2023-05-25 | 日本電信電話株式会社 | 個人識別装置、方法およびプログラム |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3943011A1 (en) | 2022-01-26 |
| CN113939231A (zh) | 2022-01-14 |
| EP3943011A4 (en) | 2022-12-21 |
| JPWO2020196323A1 (ja) | 2021-11-18 |
| JP2022188188A (ja) | 2022-12-20 |
| JP7158783B2 (ja) | 2022-10-24 |
| JP7321599B2 (ja) | 2023-08-07 |
| US20220079518A1 (en) | 2022-03-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7461072B2 (ja) | 呼吸早期警告スコアリングシステムおよび方法 | |
| CN109996488A (zh) | 呼吸预警评分系统和方法 | |
| JP2023153893A (ja) | 換気療法システムおよび方法 | |
| EP2289402B1 (en) | Method and system for interpretation and analysis of physiological, performance, and contextual information | |
| ES2292755T3 (es) | Presentacion del estado de un paciente. | |
| WO2019212833A1 (en) | System and method to maintain health using personal digital phenotypes | |
| Chen et al. | Machine-learning enabled wireless wearable sensors to study individuality of respiratory behaviors | |
| CN113598726A (zh) | 用于确定和/或监测受试者的呼吸努力的肌电图膜片、装置和方法 | |
| Ostadabbas et al. | A vision-based respiration monitoring system for passive airway resistance estimation | |
| WO2020247940A1 (en) | Device and method for clinical evaluation | |
| Sands et al. | New approaches to diagnosing sleep-disordered breathing | |
| CN111954489A (zh) | 计算和显示由非侵入式基于阻抗的呼吸容积监测获得的连续监测的潮式呼吸流动-容积环(tbfvl)的装置和方法 | |
| JP7321599B2 (ja) | プログラム、情報処理方法及び情報処理装置 | |
| KR20210045163A (ko) | 전기 임피던스 단층촬영을 이용한 심폐기능 모니터링 방법 및 시스템 | |
| McIlwraith et al. | Body sensor networks for sport, wellbeing and health | |
| Li et al. | How do you breathe-a non-contact monitoring method using depth data | |
| Akshay et al. | Design & implementation of real time bio-signal acquisition system for quality health care services for the population of rural India | |
| CN108348175A (zh) | 非侵入性呼吸监测 | |
| Sprowls et al. | Integrated Sensing Systems for Monitoring Interrelated Physiological Parameters in Young and Aged Adults: A Pilot Study | |
| TWI772086B (zh) | 使用全卷積神經網路之呼吸暫停與不足事件偵測方法 | |
| Kanji | Classification of Auscultation Sounds Using a Smart System | |
| US20230263482A1 (en) | Systems, method, and apparatus for providing personalized medical data | |
| Paalvast | Missing data in continuously monitored vital signs of high-risk surgical patients | |
| WO2023164122A2 (en) | Systems, method, and apparatus for providing personalized medical data | |
| Kheirkhah Dehkordi | Assessment of respiratory flow and efforts using upper-body acceleration considering Sleep Apnea Syndrome |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 20777852 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2021509339 Country of ref document: JP Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 2020777852 Country of ref document: EP Effective date: 20211022 |