WO2017195783A1 - アトピー性皮膚炎を治療または予防するための組成物 - Google Patents
アトピー性皮膚炎を治療または予防するための組成物 Download PDFInfo
- Publication number
- WO2017195783A1 WO2017195783A1 PCT/JP2017/017565 JP2017017565W WO2017195783A1 WO 2017195783 A1 WO2017195783 A1 WO 2017195783A1 JP 2017017565 W JP2017017565 W JP 2017017565W WO 2017195783 A1 WO2017195783 A1 WO 2017195783A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- bromide
- acetylcholine
- hydrochloride
- inhibitor
- acetylcholine receptor
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4425—Pyridinium derivatives, e.g. pralidoxime, pyridostigmine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/14—Quaternary ammonium compounds, e.g. edrophonium, choline
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/439—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom the ring forming part of a bridged ring system, e.g. quinuclidine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/46—8-Azabicyclo [3.2.1] octane; Derivatives thereof, e.g. atropine, cocaine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/472—Non-condensed isoquinolines, e.g. papaverine
- A61K31/4725—Non-condensed isoquinolines, e.g. papaverine containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/485—Morphinan derivatives, e.g. morphine, codeine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/55—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole
- A61K31/551—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole having two nitrogen atoms, e.g. dilazep
- A61K31/5513—1,4-Benzodiazepines, e.g. diazepam or clozapine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/43—Enzymes; Proenzymes; Derivatives thereof
- A61K38/46—Hydrolases (3)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
Definitions
- (Item A12) The method of item A10, wherein the three substituents on the nitrogen of the tertiary amino group are methyl groups.
- (Item A13) The method according to Item A1, wherein the inhibitor of acetylcholine is acetylcholinesterase.
- (Item A14) The method according to Item A1, wherein the inhibitor of acetylcholine is an antibody that blocks binding of acetylcholine to an acetylcholine receptor.
- (Item A15) The method according to Item A1, wherein the acetylcholine inhibitor is an acetylcholine receptor gene expression inhibitor.
- (Item A16) The method according to Item A1, wherein the inhibitor of acetylcholine is an inhibitor of choline acetyltransferase.
- FIG. 6B shows test preparation (4. dextromethorphan hydrobromide monohydrate) or 5.
- the photographs of the back of the group of mice coated with physiological saline before (pre), the third day of application (3d), the seventh day of application (7d), and the first day of application (11d) are shown.
- the AD score is shown in the lower left of each photo.
- FIG. 7 shows the weight before application (pre), application start day 3 (3 days), application start day 7 (7 days), and application start day 7 (7 days) when each test preparation is used.
- a graph is shown.
- FIG. 8 shows a graph summarizing the results of AD score and ⁇ AD score (difference between AD scores before and after application) when each test preparation was used.
- siRNA is an RNA molecule having a double-stranded RNA portion consisting of 15 to 40 bases, and mRNA of a target gene having a sequence complementary to the antisense strand of the siRNA. Has a function of suppressing the expression of the target gene.
- the siRNA of the present invention comprises a sense RNA strand comprising a sequence homologous to a continuous RNA sequence in mRNA encoding an acetylcholine receptor and the like, and an antisense RNA strand comprising a sequence complementary to the sense RNA sequence.
- the dose of an anticholinergic substance administered orally or intravenously can vary depending on the subject of administration, the type of substance administered, severity, dosage form, etc., but those skilled in the art will determine an appropriate dosage. It is possible to set appropriately.
- the acetylcholine inhibitor is an acetylcholine receptor gene expression inhibitor.
- An acetylcholine receptor gene expression inhibitor can be used as an active ingredient in the composition of the present invention.
- the acetylcholine receptor gene expression inhibitor include siRNA, antisense nucleic acid and ribozyme against a gene encoding acetylcholine receptor, and siRNA is preferable. If siRNA for a gene encoding an acetylcholine receptor is used, its expression can be knocked down (suppressed).
- Hairpin ribozymes are also useful for the purposes of the present invention.
- This ribozyme is found, for example, in the minus strand of tobacco ring spot virus satellite RNA (Buzyan, JM., Nature, 1986, 323, 349). It has been shown that target-specific RNA-cleaving ribozymes can also be produced from hairpin ribozymes (Kikuchi, Y. & Sasaki, N., Nucl. Acids Res, 1991, 19, 6751., Hiroshi Kikuchi, Chemistry and Biology, 1992, 30, 112.). Thus, the expression of the gene can be inhibited by specifically cleaving the transcript of the gene encoding the acetylcholine receptor using ribozyme.
- the antagonist of nicotinic acetylcholine receptor comprises squismethonium chloride hydrate, decamethonium bromide, vecuronium bromide, pancuronium bromide, d-tubocurarine chloride hydrochloride hydrate, gallamine trietiodide, mecamylamine hydrochloride, cansyl chloride Trimethaphanate, hexamethonium bromide, atracurium besylate, doxacurium chloride, mivacurium chloride, 18-methoxycoronaridine, dextromethorphan hydrobromide hydrate, methyl licacotinine, ⁇ -bungarotoxin, ⁇ -Selected from the group consisting of conotoxin G1, benzoquinonium, and bPiDDB.
- mice Female NC / Nga mice (Nippon Charles River) that induced atopic dermatitis were used.
- the test preparation was applied to the back and left and right auricles 5 times a day (Monday to Friday) once a day for a total of 5 times.
- 100 ⁇ L of the test preparation was applied to the back and 25 ⁇ L was applied to each of the left and right auricles.
- the back was shaved before dosing and the dermatitis score was evaluated.
- Seven days after the first administration the mice were euthanized, and the skin tissue was sampled. The cervical skin was used for various analyses, with the severe skin and the lumbar skin as mild.
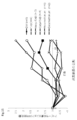
- FIG. 12 shows the average amount of change in the atopic dermatitis score during the test preparation application period. It was confirmed that skisamethonium bromide and decamethonium bromide worsen the atopic dermatitis score more than the solvent administration group (DW).
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Emergency Medicine (AREA)
- Immunology (AREA)
- Dermatology (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Microbiology (AREA)
- Mycology (AREA)
- Molecular Biology (AREA)
- Biotechnology (AREA)
- Genetics & Genomics (AREA)
- Gastroenterology & Hepatology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
Description
(項目1)
アセチルコリンの阻害剤を含む、アトピー性皮膚炎を治療または予防するための組成物。
(項目2)
前記アセチルコリンの阻害剤が、抗コリン作用物質、アセチルコリンエステラーゼ、アセチルコリンエステラーゼをコードする核酸、アセチルコリン受容体へのアセチルコリンの結合を遮断する抗体、アセチルコリン受容体へのアセチルコリンの結合を遮断する抗体をコードする核酸、アセチルコリン受容体に対する抗体、アセチルコリン受容体に対する抗体をコードする核酸、アセチルコリン受容体遺伝子の発現阻害剤、および、コリンアセチルトランスフェラーゼの阻害剤からなる群から選択される、項目1に記載の組成物。
(項目3)
前記アセチルコリンの阻害剤が、抗コリン作用物質である、項目1に記載の組成物。
(項目4)
ピオクタニンを含まない、項目1に記載の組成物。
(項目5)
前記抗コリン作用物質が、アセチルコリン受容体のアンタゴニストである、項目3に記載の組成物。
(項目6)
前記アセチルコリン受容体のアンタゴニストが、トリヘキシフェニジル塩酸塩、ブチルスコポラミン臭化物、ピレンゼピン塩酸水和物、臭化イプラトロピウム、臭化オキシトロピウム、臭化チオトロピウム、アトロピン硫酸塩、トロピカミド、ジフェンヒドラミン塩酸塩、ジシクロベリン、オキシブチニン塩酸塩、シクロペントラート塩酸塩、酒石酸トルテロジン、コハク酸ソリフェナシン、臭化水素酸ダイフェナシン、塩酸メベベリン、塩酸プロシクリジン、アクリジニウム臭化物、プロパンテリン臭化物、スコポラミン臭化水素酸塩水和物、臭化メトスコポラミン、メベンゾラート臭化物、臭化メタンテリニウム、オルフェナドリンクエン酸塩、ホマトロピン臭化物水素塩、プリフィニウム臭化物、メチキセン塩酸塩、臭化エチルピペタナート、塩酸アジフェニン、マザチコール塩酸塩水和物、塩化ユートロピン、イミダフェナシン、フェソテジンフマル酸、スキサメトニウム塩化物水和物、デカメトニウム臭化物、ベクロニウム臭化物、パンクロニウム臭化物、d-ツボクラリン塩化物塩酸水和物、ガラミントリエチオダイド、塩酸メカミラミン、カンシル酸トリメタファン、臭化ヘキサメトニウム、アトラクリウムベシル酸、塩化ドキサクリウム、塩化ミバクリウム、18-メトキシコロナリジン、デキストロメトルファン臭化水素酸塩水和物、メチルリカコチニン、α-ブンガロトキシン、α-コノトキシンG1、ベンゾキノニウム、およびbPiDDBならびに抗コリン作用を有するこれらの物質のアナログ、類似体、または誘導体からなる群から選択される、項目5に記載の組成物。
(項目7)
前記抗コリン作用物質が、アセチルコリン受容体のパーシャルアゴニストまたはインバースアゴニストである、項目3に記載の組成物。
(項目8)
前記抗コリン作用物質が、TAB、Hexyl-TAB、サブコメリンおよびミラメリンならびに抗コリン作用を有するこれらの物質のアナログ、類似体、または誘導体からなる群から選択されるアセチルコリン受容体のパーシャルアゴニストである、項目7に記載の組成物。
(項目9)
前記抗コリン作用物質が、ピレンゼピンおよび抗コリン作用を有するこれらの物質のアナログ、類似体、または誘導体からなる群から選択されるアセチルコリン受容体のインバースアゴニストである、項目7に記載の組成物。
(項目10)
前記抗コリン作用物質が、1~2個以上の第三級アミノ基とこれに結合する炭素数1~9個のアルキル鎖を含む構造を有する化合物である、項目3に記載の組成物。
(項目11)
前記アルキル鎖の炭素数が1~6個である、項目10に記載の組成物。
(項目12)
前記第三級アミノ基の窒素上の3個の置換基がメチル基である、項目10に記載の組成物。
(項目13)
前記アセチルコリンの阻害剤が、アセチルコリンエステラーゼである、項目1に記載の組成物。
(項目14)
前記アセチルコリンの阻害剤が、アセチルコリン受容体へのアセチルコリンの結合を遮断する抗体である、項目1に記載の組成物。
(項目15)
前記アセチルコリンの阻害剤が、アセチルコリン受容体遺伝子の発現阻害剤である、項目1に記載の組成物。
(項目16)
前記アセチルコリンの阻害剤が、コリンアセチルトランスフェラーゼの阻害剤である、項目1に記載の組成物。
(項目A1)被験体におけるアトピー性皮膚炎を治療または予防する方法であって、該被験体にアセチルコリンの阻害剤を投与する工程を包含する、方法。
(項目A2)
前記アセチルコリンの阻害剤が、抗コリン作用物質、アセチルコリンエステラーゼ、アセチルコリンエステラーゼをコードする核酸、アセチルコリン受容体へのアセチルコリンの結合を遮断する抗体、アセチルコリン受容体へのアセチルコリンの結合を遮断する抗体をコードする核酸、アセチルコリン受容体に対する抗体、アセチルコリン受容体に対する抗体をコードする核酸、アセチルコリン受容体遺伝子の発現阻害剤、および、コリンアセチルトランスフェラーゼの阻害剤からなる群から選択される、項目A1に記載の方法。
(項目A3)
前記アセチルコリンの阻害剤が、抗コリン作用物質である、項目A1に記載の方法。
(項目A4)
前記アセチルコリンの阻害剤が、ピオクタニンを含まない、項目A1に記載の方法。
(項目A5)
前記抗コリン作用物質が、アセチルコリン受容体のアンタゴニストである、項目A3に記載の方法。
(項目A6)
前記アセチルコリン受容体のアンタゴニストが、トリヘキシフェニジル塩酸塩、ブチルスコポラミン臭化物、ピレンゼピン塩酸水和物、臭化イプラトロピウム、臭化オキシトロピウム、臭化チオトロピウム、アトロピン硫酸塩、トロピカミド、ジフェンヒドラミン塩酸塩、ジシクロベリン、オキシブチニン塩酸塩、シクロペントラート塩酸塩、酒石酸トルテロジン、コハク酸ソリフェナシン、臭化水素酸ダイフェナシン、塩酸メベベリン、塩酸プロシクリジン、アクリジニウム臭化物、プロパンテリン臭化物、スコポラミン臭化水素酸塩水和物、臭化メトスコポラミン、メベンゾラート臭化物、臭化メタンテリニウム、オルフェナドリンクエン酸塩、ホマトロピン臭化物水素塩、プリフィニウム臭化物、メチキセン塩酸塩、臭化エチルピペタナート、塩酸アジフェニン、マザチコール塩酸塩水和物、塩化ユートロピン、イミダフェナシン、フェソテジンフマル酸、スキサメトニウム塩化物水和物、デカメトニウム臭化物、ベクロニウム臭化物、パンクロニウム臭化物、d-ツボクラリン塩化物塩酸水和物、ガラミントリエチオダイド、塩酸メカミラミン、カンシル酸トリメタファン、臭化ヘキサメトニウム、アトラクリウムベシル酸、塩化ドキサクリウム、塩化ミバクリウム、18-メトキシコロナリジン、デキストロメトルファン臭化水素酸塩水和物、メチルリカコチニン、α-ブンガロトキシン、α-コノトキシンG1、ベンゾキノニウム、およびbPiDDBならびに抗コリン作用を有するこれらの物質のアナログ、類似体、または誘導体からなる群から選択される、項目A5に記載の方法。
(項目A7)
前記抗コリン作用物質が、アセチルコリン受容体のパーシャルアゴニストまたはインバースアゴニストである、項目A3に記載の方法。
(項目A8)
前記抗コリン作用物質が、TAB、Hexyl-TAB、サブコメリンおよびミラメリンならびに抗コリン作用を有するこれらの物質のアナログ、類似体、または誘導体からなる群から選択されるアセチルコリン受容体のパーシャルアゴニストである、項目A7に記載の方法。
(項目A9)
前記抗コリン作用物質が、ピレンゼピンおよび抗コリン作用を有するこれらの物質のアナログ、類似体、または誘導体からなる群から選択されるアセチルコリン受容体のインバースアゴニストである、項目A7に記載の方法。
(項目A10)
前記抗コリン作用物質が、1~2個以上の第三級アミノ基とこれに結合する炭素数1~9個のアルキル鎖を含む構造を有する化合物である、項目A3に記載の方法。
(項目A11)
前記アルキル鎖の炭素数が1~6個である、項目A10に記載の方法。
(項目A12)
前記第三級アミノ基の窒素上の3個の置換基がメチル基である、項目A10に記載の方法。
(項目A13)
前記アセチルコリンの阻害剤が、アセチルコリンエステラーゼである、項目A1に記載の方法。
(項目A14)
前記アセチルコリンの阻害剤が、アセチルコリン受容体へのアセチルコリンの結合を遮断する抗体である、項目A1に記載の方法。
(項目A15)
前記アセチルコリンの阻害剤が、アセチルコリン受容体遺伝子の発現阻害剤である、項目A1に記載の方法。
(項目A16)
前記アセチルコリンの阻害剤が、コリンアセチルトランスフェラーゼの阻害剤である、項目A1に記載の方法。
(項目B1)
ムスカリン性アセチルコリンの阻害剤およびニコチン性アセチルコリンの阻害剤を含む、アトピー性皮膚炎を治療または予防するための組成物または組み合わせ物。
(項目B2)
前記ムスカリン性アセチルコリンの阻害剤が、ムスカリン性アセチルコリン受容体のアンタゴニストであり、前記ニコチン性アセチルコリンの阻害剤が、ニコチン性アセチルコリン受容体のアンタゴニストである、項目B1に記載の組成物または組み合わせ物。
(項目B3)
前記ムスカリン性アセチルコリン受容体のアンタゴニストが、トリヘキシフェニジル塩酸塩、ブチルスコポラミン臭化物、ピレンゼピン塩酸水和物、臭化イプラトロピウム、臭化オキシトロピウム、臭化チオトロピウム、アトロピン硫酸塩、トロピカミド、ジフェンヒドラミン塩酸塩、ジシクロベリン、オキシブチニン塩酸塩、シクロペントラート塩酸塩、酒石酸トルテロジン、コハク酸ソリフェナシン、臭化水素酸ダイフェナシン、塩酸メベベリン、塩酸プロシクリジン、アクリジニウム臭化物、プロパンテリン臭化物、スコポラミン臭化水素酸塩水和物、臭化メトスコポラミン、メベンゾラート臭化物、臭化メタンテリニウム、オルフェナドリンクエン酸塩、ホマトロピン臭化物水素塩、プリフィニウム臭化物、メチキセン塩酸塩、臭化エチルピペタナート、塩酸アジフェニン、マザチコール塩酸塩水和物、塩化ユートロピン、イミダフェナシン、およびフェソテジンフマル酸からなる群から選択され、
前記ニコチン性アセチルコリン受容体のアンタゴニストが、スキサメトニウム塩化物水和物、デカメトニウム臭化物、ベクロニウム臭化物、パンクロニウム臭化物、d-ツボクラリン塩化物塩酸水和物、ガラミントリエチオダイド、塩酸メカミラミン、カンシル酸トリメタファン、臭化ヘキサメトニウム、アトラクリウムベシル酸、塩化ドキサクリウム、塩化ミバクリウム、18-メトキシコロナリジン、デキストロメトルファン臭化水素酸塩水和物、メチルリカコチニン、α-ブンガロトキシン、α-コノトキシンG1、ベンゾキノニウム、およびbPiDDBからなる群から選択される、
項目B2に記載の組成物または組み合わせ物。
(項目B4)
前記ムスカリン性アセチルコリン受容体のアンタゴニストが、コハク酸ソリフェナシン、アクリジニウム臭化物、およびスコポラミン臭化水素酸塩水和物からなる群から選択され、
前記ニコチン性アセチルコリン受容体のアンタゴニストが、d-ツボクラリン塩化物塩酸水和物、ガラミントリエチオダイド、臭化ヘキサメトニウム、デキストロメトルファン臭化水素酸塩水和物、およびα-ブンガロトキシンからなる群から選択される、
項目B3に記載の組成物または組み合わせ物。
(項目B5)
前記ムスカリン性アセチルコリン受容体のアンタゴニストが、スコポラミン臭化水素酸塩水和物であり、前記ニコチン性アセチルコリン受容体のアンタゴニストが、臭化ヘキサメトニウムである、項目B4に記載の組成物または組み合わせ物。
(項目B6)
前記組成物または組み合わせ物が、局所適用、経皮投与、皮内投与、皮下投与、静脈内投与、経口投与、経腸投与、経肺投与、経鼻投与、腹腔内投与、点耳、または点眼により投与されることを特徴とする、項目1~16および項目B1~5のいずれか1項に記載の組成物または組み合わせ物。
(項目B7)
前記ムスカリン性アセチルコリンの阻害剤および前記ニコチン性アセチルコリンの阻害剤が、同時にまたは逐次的に投与されることを特徴とする、項目1B~6Bのいずれか1項に記載の組み合わせ物。
(項目C1)
被験体におけるアトピー性皮膚炎を治療または予防する方法であって、該被験体にムスカリン性アセチルコリンの阻害剤およびニコチン性アセチルコリンの阻害剤を投与する工程を包含する、方法。(項目C2)
前記ムスカリン性アセチルコリンの阻害剤が、ムスカリン性アセチルコリン受容体のアンタゴニストであり、前記ニコチン性アセチルコリンの阻害剤が、ニコチン性アセチルコリン受容体のアンタゴニストである、項目C1に記載の方法。
(項目C3)
前記ムスカリン性アセチルコリン受容体のアンタゴニストが、トリヘキシフェニジル塩酸塩、ブチルスコポラミン臭化物、ピレンゼピン塩酸水和物、臭化イプラトロピウム、臭化オキシトロピウム、臭化チオトロピウム、アトロピン硫酸塩、トロピカミド、ジフェンヒドラミン塩酸塩、ジシクロベリン、オキシブチニン塩酸塩、シクロペントラート塩酸塩、酒石酸トルテロジン、コハク酸ソリフェナシン、臭化水素酸ダイフェナシン、塩酸メベベリン、塩酸プロシクリジン、アクリジニウム臭化物、プロパンテリン臭化物、スコポラミン臭化水素酸塩水和物、臭化メトスコポラミン、メベンゾラート臭化物、臭化メタンテリニウム、オルフェナドリンクエン酸塩、ホマトロピン臭化物水素塩、プリフィニウム臭化物、メチキセン塩酸塩、臭化エチルピペタナート、塩酸アジフェニン、マザチコール塩酸塩水和物、塩化ユートロピン、イミダフェナシン、およびフェソテジンフマル酸からなる群から選択され、
前記ニコチン性アセチルコリン受容体のアンタゴニストが、スキサメトニウム塩化物水和物、デカメトニウム臭化物、ベクロニウム臭化物、パンクロニウム臭化物、d-ツボクラリン塩化物塩酸水和物、ガラミントリエチオダイド、塩酸メカミラミン、カンシル酸トリメタファン、臭化ヘキサメトニウム、アトラクリウムベシル酸、塩化ドキサクリウム、塩化ミバクリウム、18-メトキシコロナリジン、デキストロメトルファン臭化水素酸塩水和物、メチルリカコチニン、α-ブンガロトキシン、α-コノトキシンG1、ベンゾキノニウム、およびbPiDDBからなる群から選択される、
項目C2に記載の方法。
(項目C4)
前記ムスカリン性アセチルコリン受容体のアンタゴニストが、コハク酸ソリフェナシン、アクリジニウム臭化物、およびスコポラミン臭化水素酸塩水和物からなる群から選択され、
前記ニコチン性アセチルコリン受容体のアンタゴニストが、d-ツボクラリン塩化物塩酸水和物、ガラミントリエチオダイド、臭化ヘキサメトニウム、デキストロメトルファン臭化水素酸塩水和物、およびα-ブンガロトキシンからなる群から選択される、
項目C3に記載の方法。
(項目C5)
前記ムスカリン性アセチルコリン受容体のアンタゴニストが、スコポラミン臭化水素酸塩水和物であり、前記ニコチン性アセチルコリン受容体のアンタゴニストが、臭化ヘキサメトニウムである、項目C4に記載の方法。
(項目C6)
前記ムスカリン性アセチルコリンの阻害剤および前記ニコチン性アセチルコリンの阻害剤が、局所適用、経皮投与、皮内投与、皮下投与、静脈内投与、経口投与、経腸投与、経肺投与、経鼻投与、腹腔内投与、点耳、または点眼により投与されることを特徴とする、項目C1~C5のいずれか1項に方法。
(項目C7)
ムスカリン性アセチルコリンの阻害剤およびニコチン性アセチルコリンの阻害剤が、同時にまた逐次的に投与されることを特徴とする、請求項C1~C6のいずれか1項に記載の方法。
「アトピー性皮膚炎」とは、本明細書で使用される場合、痒疹を伴う皮膚炎であり、寛解、憎悪を繰り返す慢性、反復性の経過を特徴とする。多くは、アレルギー性の喘息、アレルギー性鼻炎(花粉症)、アレルギー性結膜炎などを家系に有し、および/またはIgE抗体を産生しやすい素因であるアトピー素因を背景に発症する。
以下に好ましい実施形態の説明を記載するが、この実施形態は本発明の例示であり、本発明の範囲はそのような好ましい実施形態に限定されないことが理解されるべきである。当業者はまた、以下のような好ましい実施例を参考にして、本発明の範囲内にある改変、変更などを容易に行うことができることが理解されるべきである。これらの実施形態について、当業者は適宜、任意の実施形態を組み合わせ得る。
1つの態様において、本発明は、抗コリン作用物質を含む、アトピー性皮膚炎を治療または予防するための組成物を提供する。あるいは、本発明は、抗コリン作用物質を投与する工程を包含する、アトピー性皮膚炎を治療または予防するための方法を提供する。
R1、R2およびR3は炭素数1個以上のアルキル基であり、好ましくは、R1、R2およびR3はそれぞれCH3であり;
R4は、炭素数1~9個のアルキル鎖であり、好ましくは、炭素数1~6個のアルキル基であり、;
X-は、OH-、F-、Cl-、Br-、およびI-からなる群から選択される。
R1、R2およびR3は炭素数1個以上のアルキル基であり、好ましくは、R1、R2およびR3はそれぞれCH3であり;
R4は、炭素数1~9個のアルキル鎖であり、好ましくは、炭素数1~6個のアルキル基であり、;
X-は、OH-、F-、Cl-、Br-、およびI-からなる群から選択され;
R5、R6およびR7は炭素数1個以上のアルキル基であり、好ましくは、R5、R6およびR7はそれぞれCH3である。
本実施例では、ADスコアを用いた目視による検証および組織解析によって、抗コリン薬がAD疾患治療に効果的な薬剤であるかどうかの確認を行った。
アトピー性皮膚炎のモデルマウスの作製:
アトピー性皮膚炎のモデル動物として10週齢のNC/Ngaマウス(日本チャールスリバー)を使用した。皮膚炎の誘発にはダニ(コノヒョウヒダニ)抗原であるビオスタAD(和光純薬)を使用した。モデルマウスの作製は、以下の手順で行った。
1.マウスの背部を剃毛し、初回のみ脱毛クリームを使用した。
2.皮膚バリアを破壊するために、150μLの4%SDSを適用し、2~3時間乾燥した(初回はこの工程を省略した。)。
3.免疫を刺激するために、100mgのビオスタADをマウスの背部および左右耳介に塗布した。
4.これらの工程を週に2回行った。
ムスカリン性アセチルコリン受容体の阻害剤として、アクリジニウム臭化物(和光純薬)およびスコポラミン臭化水素酸塩三水和物(東京化成工業)を使用した。ニコチン性アセチルコリン受容体の阻害剤としては、臭化ヘキサメトニウム(sigma-aldrich)、およびデキストロメトルファン臭化水素酸塩一水和物(和光純薬)を使用した。溶媒にはジメチルスルホオキシド(DMSO、和光純薬)、生理食塩水(大塚製薬)、精製水を使用した。被検製剤の終濃度と溶媒をそれぞれ表2に示す。
アトピー性皮膚炎を誘発した雌性のNC/Ngaマウス(日本チャールスリバー)を使用した。被検製剤は週5日(月から金曜日)で1日1回の計5回、背部および左右耳介に塗布した。背部には被検製剤を100μL、左右耳介にはそれぞれ25μLを塗布した。月曜日と木曜日には投与前に背部を剃毛し、皮膚炎スコアを評価した。初回投与から7日後にマウスを安楽死後、皮膚組織をサンプリングした。頸部皮膚を重症部、腰部皮膚を軽症部として各種解析に供した。
皮膚炎誘発後の薬効評価:
図1Aおよび図1Bに被検製剤を塗布したマウス群の背部の写真を示す。各被検製剤を塗布したマウスの皮膚は、塗布開始7日目には皮膚の損傷が減少しており、回復傾向にあった。また、図2に示されるように、塗布前と塗布開始7日目とでは大きな体重変化が見られず、被検製剤の塗布による副作用がないことが推察される。
本実施例では、炎症や免疫反応に関わる肥満細胞の脱顆粒を抑制する効果があるかどうかを確認した。
被検製剤の調製:
ムスカリン性アセチルコリン受容体の阻害剤として、コハク酸ソリフェナシン(東京化成工業)、アクリジニウム臭化物(和光純薬)、およびスコポラミン臭化水素酸塩三水和物(東京化成工業)を使用した。ニコチン性アセチルコリン受容体の阻害剤としては、ツボクラリンクロリド五水和物(東京化成工業)、ガラミントリエチオジド(sigma-aldrich)、臭化ヘキサメトニウム(sigma-aldrich)、デキストロメトルファン臭化水素酸塩一水和物(和光純薬)、およびα-ブンガロトキシン(alomone labs)を使用した。溶媒にはジメチルスルホオキシド(DMSO、和光純薬)、生理食塩水(大塚製薬)、精製水を使用した。被検製剤の終濃度と溶媒をそれぞれ表3に示す。
図5A~図5Cに、トルイジンブルー染色した組織切片の顕微鏡写真を示している。顕微鏡写真における肥満細胞の染色度に基づいて、活性化していない肥満細胞、脱顆粒した肥満細胞、および中程度に脱顆粒した肥満細胞をカウントした。図5Dは、組織切片における肥満細胞のカウントのグラフを示している。アトピー性皮膚炎を誘導しなかったマウス群(Non-treatment)では、肥満細胞の数が、アトピー性皮膚炎を誘導したマウス(10.Saline)と比べて少なく、脱顆粒した細胞はほとんど見られなかった。生理食塩水を塗布したマウス群(10.Saline)の重症部と比べて、被験製剤を塗布したマウス群の重症部における脱顆粒した肥満細胞(active)の数は少なく、反対に、脱顆粒をしていない肥満細胞(inactive)は多い傾向があることが分かった。また、生理食塩水を塗布したマウス群(10.Saline)において、全肥満細胞に対する脱顆粒した肥満細胞の割合は、約40%であるのに対し、被検製剤を塗布したマウス群においては、脱顆粒した肥満細胞の割合は平均約25%程度であり、高くてもツボクラリン塗布群において約33%であった。これらの結果は、被検製剤を塗布したマウス群では、脱顆粒をある程度抑制していたこと示す。
本実施例では、被検製剤適用期間にもアトピー性皮膚炎誘発処理を並行して行い、被検製剤の薬効評価を行った。
アトピー性皮膚炎のモデルマウスの作製およびスコア化は実施例1と同様に行った。被検製剤は、実施例1と同じものを使用した。
図6Aおよび図6Bに被検製剤を塗布したマウス群の背部の写真を示す。各被検製剤を塗布したマウスの皮膚は、アトピー性皮膚炎誘発処理を並行して行ったが、塗布開始11日目には皮膚の損傷が減少しており、回復傾向にあった。また、図7に示されるように、塗布前から塗布開始11日目にわたって大きな体重変化が見られず、被検製剤の塗布による副作用がないことが推察される。
本実施例では、アトピー性皮膚炎のマウスにおける皮膚内のアセチルコリンの濃度が亢進していることを実証する。
皮膚内アセチルコリン濃度の測定を、アトピー性皮膚炎を誘導して生理食塩水を塗布したマウス群と、アトピー性皮膚炎を誘導しなかったマウス群の皮膚試料を用いて測定し、これらの皮膚内アセチルコリン濃度を比較した。結果を図10に示す。示される通り、アトピー性皮膚炎を誘導したマウス群では、皮膚内アセチルコリンが、アトピー性皮膚炎を誘導していないマウス群と比べて顕著に高かった。この結果から、アトピー性皮膚炎のマウスにおいて、正常のマウスと比べて皮膚内アセチルコリンの濃度が亢進していることが実証された。
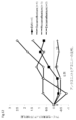
治療効果の比較的高かった臭化ヘキサメトニウムに類似した分子構造を有する化合物において、アゴニストとアンタゴニスト、アミノ基級数、第三級アミノ基の数および炭素鎖数の違いによるアトピー性皮膚炎治療に対する影響の解析を行った。
実施例1と同様に、マウス(NC/Nga、10週齢)にダニ抗原(ビオスタAD)を2回/週、4週間塗布することで、アトピー性皮膚炎発症マウスを作製した。ダニ抗原による誘発(2回/週)と被検製剤塗布(5回/週)を3週間、同時に行い、アトピー性皮膚炎誘発の抑制効果についての解析を行った。被検製剤は1週目では12mMを2週目以降は24mMのものを使用した。ただし、臭化デカメトニウムについては強い毒性が確認されたため、2週目以降も12mMを使用し、最終週では2回/週の投与間隔に変更した。対照として無処置群(誘発なし、被検製剤塗布なし)と溶媒塗布群(誘発あり、精製水塗布)を用意した。スコア化は実施例1と同様に行った。
被検製剤の構造を表4に示す。以下の観点(1)~(4)でアトピー性皮膚炎に対する治療効果を比較した。
(1)アンタゴニストとアゴニスト:ニコチン性アセチルコリン受容体のアンタゴニストとアゴニストを比較するため、臭化ヘキサメトニウムと塩化スキサメトニウム(丸石製薬)及び臭化デカメトニウム(東京化成工業)を使用した。
(2)アミノ基級数:臭化ヘキサメトニウムの第三級アミノ基をそれぞれ第二級アミノ基およびアミノ基に変更したN,N,N’,N’-テトラメチル-1,6-ヘキサンジアミン(和光純薬、以下TMHDAという)およびヘキサメチレンジアミン(和光純薬、以下HMDAという)との比較を行った。
(3)第三級アミノ基の数:臭化ヘキサメトニウムはその分子内に2つの第三級アミノ基を有する。そこで第三級アミノ基を分子内に1つ有し、且つ炭素数6のアルキル基を有する臭化ヘキシルトリメチルアンモニウム(和光純薬、以下Hexyl-TABという)との比較を行った。
(4)炭素鎖長:臭化ヘキサメトニウム(炭素数6)より炭素鎖長の長い臭化デカメトニウム(炭素数10)との比較を行った。また、分子内に第三級アミノ基を1つ有し且つアルキル基炭素鎖長の異なる、臭化テトラメチルアンモニウム(和光純薬、炭素数1、以下TABという)、臭化ヘキシルトリメチルアンモニウム(炭素数6、以下Hexyl-TABという)及び臭化セチルトリメチルアンモニウム(和光純薬、炭素数16、以下Cetyl-TABという)との比較を行った。
被検製剤塗布期間のアトピー性皮膚炎スコア平均変化量を図11に示す。
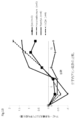
ニコチン性アセチルコリン受容体のアンタゴニストである臭化ヘキサメトニウムと、アゴニストである塩化スキサメトニウム及び臭化デカメトニウムをアトピー性皮膚炎モデルマウスにそれぞれ投与し、皮膚炎スコアの比較を行った。被検製剤塗布期間のアトピー性皮膚炎スコア平均変化量を図12に示す。臭化スキサメトニウムや臭化デカメトニウムは、溶媒投与群(DW)と比較してよりアトピー性皮膚炎スコアを悪化させることが確認された。一方、アンタゴニストである臭化ヘキサメトニウムを投与した群では、溶媒投与群と比較してアトピー性皮膚炎スコアの上昇が抑制されていた。臭化スキサメトニウムや臭化デカメトニウムは生体内でアセチルコリンよりも過剰に受容体を活性化させるアゴニストであるため、アトピー性皮膚炎スコアを悪化させる結果となったと考えられる。以上より、ニコチン性アセチルコリン受容体のアゴニストは、アトピー性皮膚炎を治療する効果を有さないことが示された。また、アンタゴニストでニコチン性アセチルコリン受容体活性を抑制することで、アトピー性皮膚炎の悪化を抑制できることが確認された。
臭化ヘキサメトニウムはその分子内に第三級アミノ基を2つ有する。そこで、このアミノ基が第3級あるいは第1級であるTMHDAとHMDAの比較を行った。その結果を図13に示す。TMHDA及びHMDA共に抑制効果は確認されなかった。以上の結果から、アトピー性皮膚炎の抑制には第三級アミノ基を有する化合物が有効である可能性が示唆された。
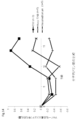
分子内に第三級アミノ基を1つ有するHexyl-TABと2つ有する臭化ヘキサメトニウムの比較を行った。その結果を図14に示す。Hexyl-TABも臭化ヘキサメトニウムよりわずかに弱いながらも、アトピー性皮膚炎抑制効果が確認された。この結果から、第三級アミンであればアトピー性皮膚炎抑制効果を有し、分子内アミノ基数が多い方がより高い抑制効果を持つことが示唆された。
臭化ヘキサメトニウムはアミノ基を炭素数6の炭化水素鎖で結合した構造である。この炭化水素鎖長がより長い臭化デカメトニウム(炭素数10)と比較を行った。臭化デカメトニウムは強い毒性が見られ、投与濃度も回数も低かったものの、アトピー性皮膚炎を悪化させる作用が確認された。
多くの場合、アトピー性皮膚炎患者は鳥肌様皮膚をしている。これは、毛穴周辺のアセチルコリン濃度が高いためだと考えられる。本実施例では、ヘキサメトニウムを塗布したアトピー性皮膚炎患者の毛穴の立ち具合が減少するかどうかを、レプリカ法を使用して検証した。
ヘキサメトニウム(12mM)をアトピー性皮膚炎患者の首(後部)に塗布し、塗布前と塗布後5分~10分経過後の皮膚のレプリカ像を得た。レプリカ像は、アトピー性皮膚炎を発症している皮膚を覆うようにシリコン樹脂(SILFLO)を塗布し、5分後に硬化したシリコンを皮膚からはがすことによって採取した。採取したレプリカに一方向から光を当てて皮膚表面の凹凸の比較検討を行い、写真撮影を行った。
図16にヘキサメトニウム塗布前および塗布後のレプリカ像を示す。へこんだ部分が毛穴に相当し、毛穴入口の漏斗部が盛り上がっていると、毛穴が立った状態を示す。ヘキサメトニウムの塗布後のレプリカ像において、毛穴の立ち具合が治まって、鳥肌様が少なくなっている様子が観察された。したがって、ヘキサメソニウムはアセチルコリンの作用を減弱させる抗コリン作用を発揮し、その結果アトピー性皮膚炎に対する治療効果を発揮していると考えられる。
本実施例では、ニコチン性アセチルコリン受容体阻害剤およびムスカリン性アセチルコリン受容体阻害剤を併用した場合の治療効果について確認した。
アトピー性皮膚炎のモデルマウスの作製:
アトピー性皮膚炎のモデル動物として10週齢のNC/Ngaマウス(日本チャールスリバー)を使用した。皮膚炎の誘発にはダニ抗原(ビオスタAD、和光純薬)を使用した。モデルマウスの作製およびスコア化はビオスタAD添付の説明書記載の方法に従った(実施例1と同様)。
ムスカリン性アセチルコリン受容体の阻害剤として、スコポラミン臭化水素酸塩三水和物(以降スコポラミン、東京化成工業)を使用し、ニコチン性アセチルコリン受容体の阻害剤としては臭化ヘキサメトニウム(以降ヘキサメトニウム、sigma-aldrich)を使用した。それぞれを精製水で溶解し、終濃度で、ヘキサメトニウムとスコポラミンがそれぞれ6mMになる低濃度群(Hexa. & Scop. Lo.)、およびそれぞれ12mMになる高濃度群(Hexa. & Scop. Hi.)を調製した。陰性対照として精製水(DW)を用いた。
アトピー性皮膚炎誘発マウスに対して、低濃度群では1日1回、週5回、計10回、高濃度群では1日1回、週3回、計6回背部に被検製剤を塗布した。背部には被検製剤を100μL、左右耳介にはそれぞれ25μLを塗布した。投与0、7および10日後に皮膚炎スコアを評価し、0日目からの平均変化量を比較した。症状を維持するため、毎週月曜日にのみダニ抗原によるアトピー性皮膚炎誘発処理を行った。
結果を図17に示す。低濃度群においては塗布7日目では皮膚炎の改善効果は認められなかったが、10日目において改善効果が見られた。高濃度群においては被検製剤投与回数が低濃度群より少ないにもかかわらず塗布7日目から皮膚炎の改善が見られ、10日目では7日目より高い改善効果が確認された。これらの結果から、ニコチン性アセチルコリン受容体阻害剤およびムスカリン性アセチルコリン受容体阻害剤の併用はアトピー性皮膚炎に対して治療効果を示すことが確認された。またこれらの効果は濃度依存性があり、高濃度の方がより早く治療効果が表れることが確認された。
本実施例では、全身投与(例えば、経口投与)した場合でも治療効果が発揮されるかどうかを確認した。
アトピー性皮膚炎のモデルマウスの作製:
アトピー性皮膚炎のモデル動物として10週齢のNC/Ngaマウス(日本チャールスリバー)を使用した。皮膚炎の誘発にはダニ抗原(ビオスタAD、和光純薬)を使用した。モデルマウスの作製及びスコア化はビオスタAD添付の説明書記載の方法に従った(実施例1と同様)。
ニコチン性アセチルコリン受容体の阻害剤として臭化ヘキサメトニウム(以降ヘキサメトニウム、sigma-aldrich)を使用した。精製水で溶解し、終濃度が60mMになるよう調製した。陰性対照として精製水(DW)を用いた。
アトピー性皮膚炎誘発マウスに対して、150μLの被検製剤を1日1回、週5回、計10回、経口投与した。投与0および10日後に皮膚炎スコアを評価し、0日目からの平均変化量を比較した。症状を維持するため、毎週月曜日にのみダニ抗原によるアトピー性皮膚炎誘発処理を行った。
結果を図18に示す。投与10日目において皮膚炎スコアの改善が観察された。この結果から、投与経路に拠ることなくヘキサメトニウムはアトピー性皮膚炎の改善効果があることが確認された。
Claims (22)
- アセチルコリンの阻害剤を含む、アトピー性皮膚炎を治療または予防するための組成物。
- 前記アセチルコリンの阻害剤が、抗コリン作用物質、アセチルコリンエステラーゼ、アセチルコリンエステラーゼをコードする核酸、アセチルコリン受容体へのアセチルコリンの結合を遮断する抗体、アセチルコリン受容体へのアセチルコリンの結合を遮断する抗体をコードする核酸、アセチルコリン受容体に対する抗体、アセチルコリン受容体に対する抗体をコードする核酸、アセチルコリン受容体遺伝子の発現阻害剤、および、コリンアセチルトランスフェラーゼの阻害剤からなる群から選択される、請求項1に記載の組成物。
- 前記アセチルコリンの阻害剤が、抗コリン作用物質である、請求項1に記載の組成物。
- ピオクタニンを含まない、請求項1に記載の組成物。
- 前記抗コリン作用物質が、アセチルコリン受容体のアンタゴニストである、請求項3に記載の組成物。
- 前記アセチルコリン受容体のアンタゴニストが、トリヘキシフェニジル塩酸塩、ブチルスコポラミン臭化物、ピレンゼピン塩酸水和物、臭化イプラトロピウム、臭化オキシトロピウム、臭化チオトロピウム、アトロピン硫酸塩、トロピカミド、ジフェンヒドラミン塩酸塩、ジシクロベリン、オキシブチニン塩酸塩、シクロペントラート塩酸塩、酒石酸トルテロジン、コハク酸ソリフェナシン、臭化水素酸ダイフェナシン、塩酸メベベリン、塩酸プロシクリジン、アクリジニウム臭化物、プロパンテリン臭化物、スコポラミン臭化水素酸塩水和物、臭化メトスコポラミン、メベンゾラート臭化物、臭化メタンテリニウム、オルフェナドリンクエン酸塩、ホマトロピン臭化物水素塩、プリフィニウム臭化物、メチキセン塩酸塩、臭化エチルピペタナート、塩酸アジフェニン、マザチコール塩酸塩水和物、塩化ユートロピン、イミダフェナシン、フェソテジンフマル酸、スキサメトニウム塩化物水和物、デカメトニウム臭化物、ベクロニウム臭化物、パンクロニウム臭化物、d-ツボクラリン塩化物塩酸水和物、ガラミントリエチオダイド、塩酸メカミラミン、カンシル酸トリメタファン、臭化ヘキサメトニウム、アトラクリウムベシル酸、塩化ドキサクリウム、塩化ミバクリウム、18-メトキシコロナリジン、デキストロメトルファン臭化水素酸塩水和物、メチルリカコチニン、α-ブンガロトキシン、α-コノトキシンG1、ベンゾキノニウム、およびbPiDDBならびに抗コリン作用を有するこれらの物質のアナログ、類似体、または誘導体からなる群から選択される、請求項5に記載の組成物。
- 前記抗コリン作用物質が、アセチルコリン受容体のパーシャルアゴニストまたはインバースアゴニストである、請求項3に記載の組成物。
- 前記抗コリン作用物質が、TAB、Hexyl-TAB、サブコメリンおよびミラメリンならびに抗コリン作用を有するこれらの物質のアナログ、類似体、または誘導体からなる群から選択されるアセチルコリン受容体のパーシャルアゴニストである、請求項7に記載の組成物。
- 前記抗コリン作用物質が、ピレンゼピンおよび抗コリン作用を有するこれらの物質のアナログ、類似体、または誘導体からなる群から選択されるアセチルコリン受容体のインバースアゴニストである、請求項7に記載の組成物。
- 前記抗コリン作用物質が、1~2個以上の第三級アミノ基とこれに結合する炭素数1~9個のアルキル鎖を含む構造を有する化合物である、請求項3に記載の組成物。
- 前記アルキル鎖の炭素数が1~6個である、請求項10に記載の組成物。
- 前記第三級アミノ基の窒素上の3個の置換基がメチル基である、請求項10に記載の組成物。
- 前記アセチルコリンの阻害剤が、アセチルコリンエステラーゼである、請求項1に記載の組成物。
- 前記アセチルコリンの阻害剤が、アセチルコリン受容体へのアセチルコリンの結合を遮断する抗体である、請求項1に記載の組成物。
- 前記アセチルコリンの阻害剤が、アセチルコリン受容体遺伝子の発現阻害剤である、請求項1に記載の組成物。
- 前記アセチルコリンの阻害剤が、コリンアセチルトランスフェラーゼの阻害剤である、請求項1に記載の組成物。
- ムスカリン性アセチルコリンの阻害剤およびニコチン性アセチルコリンの阻害剤を含む、アトピー性皮膚炎を治療または予防するための組成物または組み合わせ物。
- 前記ムスカリン性アセチルコリンの阻害剤が、ムスカリン性アセチルコリン受容体のアンタゴニストであり、前記ニコチン性アセチルコリンの阻害剤が、ニコチン性アセチルコリン受容体のアンタゴニストである、請求項17に記載の組成物または組み合わせ物。
- 前記ムスカリン性アセチルコリン受容体のアンタゴニストが、トリヘキシフェニジル塩酸塩、ブチルスコポラミン臭化物、ピレンゼピン塩酸水和物、臭化イプラトロピウム、臭化オキシトロピウム、臭化チオトロピウム、アトロピン硫酸塩、トロピカミド、ジフェンヒドラミン塩酸塩、ジシクロベリン、オキシブチニン塩酸塩、シクロペントラート塩酸塩、酒石酸トルテロジン、コハク酸ソリフェナシン、臭化水素酸ダイフェナシン、塩酸メベベリン、塩酸プロシクリジン、アクリジニウム臭化物、プロパンテリン臭化物、スコポラミン臭化水素酸塩水和物、臭化メトスコポラミン、メベンゾラート臭化物、臭化メタンテリニウム、オルフェナドリンクエン酸塩、ホマトロピン臭化物水素塩、プリフィニウム臭化物、メチキセン塩酸塩、臭化エチルピペタナート、塩酸アジフェニン、マザチコール塩酸塩水和物、塩化ユートロピン、イミダフェナシン、およびフェソテジンフマル酸からなる群から選択され、
前記ニコチン性アセチルコリン受容体のアンタゴニストが、スキサメトニウム塩化物水和物、デカメトニウム臭化物、ベクロニウム臭化物、パンクロニウム臭化物、d-ツボクラリン塩化物塩酸水和物、ガラミントリエチオダイド、塩酸メカミラミン、カンシル酸トリメタファン、臭化ヘキサメトニウム、アトラクリウムベシル酸、塩化ドキサクリウム、塩化ミバクリウム、18-メトキシコロナリジン、デキストロメトルファン臭化水素酸塩水和物、メチルリカコチニン、α-ブンガロトキシン、α-コノトキシンG1、ベンゾキノニウム、およびbPiDDBからなる群から選択される、
請求項18に記載の組成物または組み合わせ物。 - 前記ムスカリン性アセチルコリン受容体のアンタゴニストが、コハク酸ソリフェナシン、アクリジニウム臭化物、およびスコポラミン臭化水素酸塩水和物からなる群から選択され、
前記ニコチン性アセチルコリン受容体のアンタゴニストが、d-ツボクラリン塩化物塩酸水和物、ガラミントリエチオダイド、臭化ヘキサメトニウム、デキストロメトルファン臭化水素酸塩水和物、およびα-ブンガロトキシンからなる群から選択される、
請求項19に記載の組成物または組み合わせ物。 - 前記ムスカリン性アセチルコリン受容体のアンタゴニストが、スコポラミン臭化水素酸塩水和物であり、前記ニコチン性アセチルコリン受容体のアンタゴニストが、臭化ヘキサメトニウムである、請求項20に記載の組成物または組み合わせ物。
- 前記組成物または組み合わせ物が、局所適用、経皮投与、皮内投与、皮下投与、静脈内投与、経口投与、経腸投与、経肺投与、経鼻投与、腹腔内投与、点耳、または点眼により投与されることを特徴とする、請求項1~21のいずれか1項に記載の組成物または組み合わせ物。
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP17796144.8A EP3456353A4 (en) | 2016-05-09 | 2017-05-09 | COMPOSITION FOR THE TREATMENT OR PREVENTION OF ATOPIC DERMATITIS |
| JP2018517036A JP6789286B2 (ja) | 2016-05-09 | 2017-05-09 | アトピー性皮膚炎を治療または予防するための組成物 |
| CA3023148A CA3023148A1 (en) | 2016-05-09 | 2017-05-09 | Composition for treating or preventing atopic dermatitis |
| AU2017264119A AU2017264119A1 (en) | 2016-05-09 | 2017-05-09 | Composition for treating or preventing atopic dermatitis |
| US16/099,982 US20190125734A1 (en) | 2016-05-09 | 2017-05-09 | Composition for treating or preventing atopic dermatitis |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2016093918 | 2016-05-09 | ||
| JP2016-093918 | 2016-05-09 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2017195783A1 true WO2017195783A1 (ja) | 2017-11-16 |
Family
ID=60267244
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2017/017565 WO2017195783A1 (ja) | 2016-05-09 | 2017-05-09 | アトピー性皮膚炎を治療または予防するための組成物 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20190125734A1 (ja) |
| EP (1) | EP3456353A4 (ja) |
| JP (2) | JP6789286B2 (ja) |
| AU (1) | AU2017264119A1 (ja) |
| CA (1) | CA3023148A1 (ja) |
| WO (1) | WO2017195783A1 (ja) |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH01151522A (ja) * | 1987-09-16 | 1989-06-14 | Patrick A Beauchamp | 皮膚疾患の局所治療 |
| WO2000010556A1 (de) * | 1998-08-19 | 2000-03-02 | Beiersdorf Ag | Verwendung quaternärer stickstoffverbindungen zur prophylaxe und behandlung des superinfizierten atopischen ekzems |
| JP2000095683A (ja) * | 1998-09-28 | 2000-04-04 | Nof Corp | 皮膚外用剤 |
| KR20150043026A (ko) * | 2013-10-14 | 2015-04-22 | 주식회사 엘지생활건강 | 히오신을 유효 성분으로 함유하는 피부 건조증 또는 피부 장벽 기능 개선용 조성물 |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4902720A (en) * | 1983-01-10 | 1990-02-20 | Baldone Joseph A | Treatment of virus infections with quaternary ammonium compounds |
| DE19626373A1 (de) * | 1996-07-02 | 1998-01-08 | Boehringer Ingelheim Kg | Neuartige Verwendung von Wirkstoffen, welche die Funktion von nichtneuronalem Acetylcholin beeinflussen |
| DE10111843A1 (de) * | 2001-03-13 | 2002-09-19 | Boehringer Ingelheim Pharma | Verbindungen zur Behandlung von inflammatorischen Erkrankungen |
| ES2371026T3 (es) * | 2001-10-19 | 2011-12-26 | Atritech, Inc. | Dispositivo de oclusión ajustable en la orejuela auricular izquierda. |
| GB2419093A (en) * | 2004-10-12 | 2006-04-19 | Ernir Snorrason | Acetylcholinesterase inhibitors for the treatment of skin |
| US20130243888A1 (en) * | 2010-07-27 | 2013-09-19 | Sara Beth Ford | Composition and Method for the Topical Treatment of Dermatitis |
| WO2015168564A1 (en) * | 2014-05-01 | 2015-11-05 | Anterios, Inc. | Methods to treat, prevent, and improve skin conditions |
-
2017
- 2017-05-09 CA CA3023148A patent/CA3023148A1/en not_active Abandoned
- 2017-05-09 JP JP2018517036A patent/JP6789286B2/ja active Active
- 2017-05-09 WO PCT/JP2017/017565 patent/WO2017195783A1/ja unknown
- 2017-05-09 AU AU2017264119A patent/AU2017264119A1/en not_active Abandoned
- 2017-05-09 EP EP17796144.8A patent/EP3456353A4/en active Pending
- 2017-05-09 US US16/099,982 patent/US20190125734A1/en not_active Abandoned
-
2019
- 2019-05-24 JP JP2019097790A patent/JP6883346B2/ja active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH01151522A (ja) * | 1987-09-16 | 1989-06-14 | Patrick A Beauchamp | 皮膚疾患の局所治療 |
| WO2000010556A1 (de) * | 1998-08-19 | 2000-03-02 | Beiersdorf Ag | Verwendung quaternärer stickstoffverbindungen zur prophylaxe und behandlung des superinfizierten atopischen ekzems |
| JP2000095683A (ja) * | 1998-09-28 | 2000-04-04 | Nof Corp | 皮膚外用剤 |
| KR20150043026A (ko) * | 2013-10-14 | 2015-04-22 | 주식회사 엘지생활건강 | 히오신을 유효 성분으로 함유하는 피부 건조증 또는 피부 장벽 기능 개선용 조성물 |
Non-Patent Citations (5)
| Title |
|---|
| GROENE D ET AL.: "Doxepin affects acetylcholine induced cutaneous reactions in atopic eczema", EXP DERMATOL, vol. 10, no. 2, 2001, pages 110 - 117, XP055442500 * |
| SARIDOMICHELAKIS, M N ET AL.: "An update on the treatment of canine atopic dermatitis", THE VETERINARY JOURNAL, vol. 207, January 2016 (2016-01-01), pages 29 - 37, XP029379938 * |
| See also references of EP3456353A4 * |
| TSUKUMO, Y ET AL.: "Pharmacological characterization of itch-associated response induced by repeated application of oxazolone in mice", J PHARMACOL SCI, vol. 113, 2010, pages 255 - 262, XP055442482 * |
| WESSLER, I ET AL.: "Increased acetylcholine levels in skin biopsies of patients with atopic dermatitis", LIFE SCI, vol. 72, no. 18-19, 2003, pages 2169 - 2172, XP055442530 * |
Also Published As
| Publication number | Publication date |
|---|---|
| JPWO2017195783A1 (ja) | 2019-04-04 |
| US20190125734A1 (en) | 2019-05-02 |
| JP6789286B2 (ja) | 2020-11-25 |
| EP3456353A1 (en) | 2019-03-20 |
| CA3023148A1 (en) | 2017-11-16 |
| AU2017264119A1 (en) | 2018-12-06 |
| EP3456353A4 (en) | 2020-09-16 |
| JP6883346B2 (ja) | 2021-06-09 |
| JP2019151663A (ja) | 2019-09-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Hu et al. | Fibronectin type III domain‐containing 5 improves aging‐related cardiac dysfunction in mice | |
| CN102791861B (zh) | 通过调节聚丝蛋白(flg)的表达和活性而治疗flg相关疾病 | |
| US11096926B2 (en) | (3AR)-1,3A,8-trimethyl-1,2,3,3A,8,8A-hexahydropyrrolo[2,3-b]indol-5-yl phenylcarbamate and methods of treating or preventing neurodegeneration | |
| KR20100061616A (ko) | 신경변성 질환 및 장애의 치료 및 예방 방법 | |
| WO2017049157A1 (en) | Methods and compositions for the treatment of steatosis-associated disorders | |
| US20230035892A1 (en) | Methods and compositions for treating cancer | |
| US20220062254A1 (en) | Inhibitors of gangliosides metabolism for the treatment of motor neuron diseases | |
| US20160193143A1 (en) | Medicinal treatment of dermal infectious disorders with norketotifen | |
| EP2928299B1 (en) | Treatment of chronic dermal inflammatory with norketotifen | |
| CN119013027A (zh) | 用于治疗肝脏病症的SSAO抑制剂和THR-β激动剂的组合 | |
| Sekar et al. | Impairing Gasdermin D-mediated pyroptosis is protective against retinal degeneration | |
| EP2764863B1 (en) | Tau aggregation inhibitor | |
| JP6883346B2 (ja) | アトピー性皮膚炎を治療または予防するための組成物 | |
| CN105233286A (zh) | 含酸敏感离子通道调控剂的制剂及其在治疗瘙痒中的用途 | |
| WO2018136933A1 (en) | Inhibition of stromal interaction molecule 1 (stim1) as a co-treatment for adult onset polycystic kidney disease (adpkd) | |
| WO2023154014A1 (en) | Nmdar antagonists prevent ageing and aging-associated conditions and diseases through increasing 20s proteasome activity | |
| WO2023014718A2 (en) | 25-hydroxycholesterol (25hc), cryab aggregation inhibitor to amelioriate vascular stiffness |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| ENP | Entry into the national phase |
Ref document number: 3023148 Country of ref document: CA |
|
| ENP | Entry into the national phase |
Ref document number: 2018517036 Country of ref document: JP Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 17796144 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2017264119 Country of ref document: AU Date of ref document: 20170509 Kind code of ref document: A |
|
| ENP | Entry into the national phase |
Ref document number: 2017796144 Country of ref document: EP Effective date: 20181210 |