WO2007093529A2 - Heteroaroylsubstituierte alanine - Google Patents
Heteroaroylsubstituierte alanine Download PDFInfo
- Publication number
- WO2007093529A2 WO2007093529A2 PCT/EP2007/051144 EP2007051144W WO2007093529A2 WO 2007093529 A2 WO2007093529 A2 WO 2007093529A2 EP 2007051144 W EP2007051144 W EP 2007051144W WO 2007093529 A2 WO2007093529 A2 WO 2007093529A2
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- alkyl
- alkoxy
- phenyl
- heteroaryl
- formula
- Prior art date
Links
- 0 *C(C(C(*)=O)NC(c1c(C(F)(F)F)[o]cc1)=O)N* Chemical compound *C(C(C(*)=O)NC(c1c(C(F)(F)F)[o]cc1)=O)N* 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D231/00—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings
- C07D231/02—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings
- C07D231/10—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D231/12—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D333/00—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom
- C07D333/02—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom not condensed with other rings
- C07D333/04—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom not condensed with other rings not substituted on the ring sulphur atom
- C07D333/06—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom not condensed with other rings not substituted on the ring sulphur atom with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to the ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D407/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00
- C07D407/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00 containing two hetero rings
- C07D407/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
Definitions
- a 5- or 6-membered heteroaryl having one to four nitrogen atoms, or having one to three nitrogen atoms and one oxygen or sulfur atom, or with a
- Oxygen or sulfur atom which may be partially or fully halogenated and / or 1 to 3 radicals from the group cyano, -C 6 alkyl, C 3 -C 6 cycloalkyl, -C 6 -haloalkyl, -C 6 alkoxy, -C 6 haloalkoxy, and CrC can carry 6 -alkoxy-Ci-C4-alkyl;
- R 1 , R 2 are hydrogen, hydroxy or C 1 -C 6 -alkoxy
- R 3 is C 1 -C 6 -alkyl, C 1 -C 4 -cyanoalkyl or C 1 -C 6 -haloalkyl;
- R 4 is hydrogen or C 1 -C 6 -alkyl
- R 5 is hydrogen, Ci-C 6 alkyl, C 2 -C 6 alkenyl, C 2 -C 6 kinyl -alkyl, Ci-C 6 haloalkyl, C 2 - C 6 haloalkenyl, C 2 -C 6 haloalkynyl , Ci-C 6 cyanoalkyl, C 2 -C 6 - cyanoalkenyl, C 2 -C 6 -Cyanoalkinyl, Ci-C 6 hydroxyalkyl, C 2 -C 6 -Hydroxyalkenyl, C 2 -C 6 -Hydroxyalkinyl, C3-C 6 cycloalkyl, C3-C6 cycloalkenyl, 3- to 6-membered
- Heterocyclyl wherein the abovementioned cycloalkyl, cycloalkenyl or 3- to 6-membered heterocyclyl radicals may be partially or completely halogenated and / or one to three radicals from the group consisting of oxo, cyano, nitro, C 1 -C 6 -alkyl, C 1 -C 6 - haloalkyl, hydroxy, Ci-C 6 alkoxy, Ci-C 6 haloalkoxy,
- Ci-C 6 -alkoxycarbonyl hydroxycarbonyl-Ci-C 6 alkoxy, Ci-C 6 alkoxycarbonyl-alkoxy-Ci-C 6, amino, Ci-C6 alkylamino, di (-C 6 - alkyl) amino, Ci-C 6 alkylsulfonylamino, Ci-C ⁇ -haloalkylsulfonylamino, aminocarbonylamino, (CrC 6 alkylamino) carbonylamino, di (CrC 6 - alkyl) aminocarbonylamino aryl, and (CrC 6 alkyl) may bear, aryl;
- C 1 -C 6 -alkoxy amino, C 1 -C 6 -alkylamino, di (C 1 -C 6 -alkyl) amino, C 1 -C 6 -alkylsulfonylamino, C 1 -C 6 -haloalkylsulfonylamino, (C 1 -C 6 -alkylamino) -carbonylamino, di (C 1 -C 6 -alkyl) aminocarbonylamino, aryl and aryl (C 1 -C 6 -alkyl);
- R 7 is hydrogen, CrC ⁇ alkyl, C 3 -C 6 cycloalkyl, C 3 -C 6 alkenyl, C 3 -C 6 kinyl -alkyl, C 3 -C 6 - haloalkenyl, C 3 -C 6 haloalkynyl, hydroxy or C 1 -C 6 -alkoxy;
- R 8 is d-Ce-alkyl, Ci-C 6 -haloalkyl or phenyl, where the phenyl radical may be partially or fully halogenated and / or may carry one to three of the following groups: Ci-C 6 alkyl, d- C ⁇ -haloalkyl or Ci-CrAlkoxy;
- the invention relates to processes and intermediates for the preparation of compounds of formula I, compositions containing them and the use of these derivatives or agents containing them for controlling harmful plants.
- 2, ⁇ -DiaminocarbonylENSen with herbicidal activity are described inter alia in WO 03/045878.
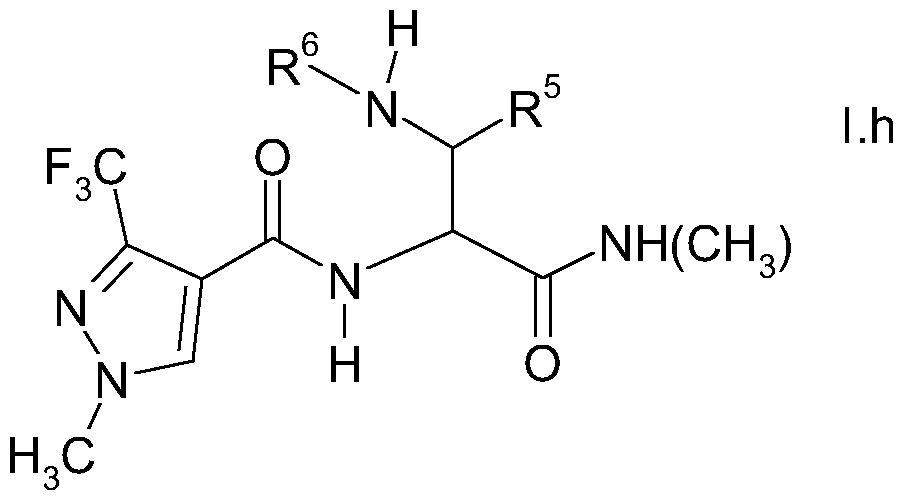
- heteroaroyl-substituted alanines of the formula I and their herbicidal activity were found.
- herbicidal agents were found which contain the compounds I and have a very good herbicidal activity.
- methods for the preparation of these compositions and methods for controlling undesired plant growth with the compounds I have been found.
- the compounds of the formula I contain two or more chiral centers and are then present as enantiomer or diastereomer mixtures.
- the invention provides both the pure enantiomers or diastereomers and mixtures thereof.
- the compounds of the formula I can also be in the form of their agriculturally useful salts, whereby the type of salt generally does not matter.
- the salts of those cations or the acid addition salts of those acids come into consideration whose cations, or anions, do not adversely affect the herbicidal activity of the compounds I.
- the cations used are in particular ions of the alkali metals, preferably lithium, sodium and potassium, the alkaline earth metals, preferably calcium and magnesium, and the transition metals, preferably manganese, copper, zinc and iron, and ammonium, where, if desired, one to four hydrogen atoms are replaced by C 4 -alkyl, hydroxy-C 1 -C 4 -alkyl, C 1 -C 4 -alkoxy-C 1 -C 4 -alkyl, hydroxy-C 1 -C 4 -alkoxy-C 1 -C 4 -alkyl, phenyl or benzyl preferably ammonium, dimethylammonium, diisopropylammonium, tetramethylammonium, tetrabutylammonium, 2- (2-hydroxyeth-1-oxy) eth-1-ylammonium, di- (2-hydroxyeth-1-yl) -ammonium, trimethylbenzylammonium, of further
- Anions of useful acid addition salts are primarily chloride, bromide, fluoride, hydrogen sulfate, sulfate, dihydrogen phosphate, hydrogen phosphate, nitrate, bicarbonate, carbonate, hexafluorosilicate, hexafluorophosphate, benzoate and the anions of Ci-C4-alkanoic acids, preferably formate, acetate, propionate and butyrate.
- substituents R 1 -R 12 or as radicals on phenyl organic moieties mentioned aryl, heteroaryl or Hetrocyclylringen are collective terms for individual enumerations of the individual group members.
- All hydrocarbon chains ie all alkyl, alkylsilyl, alkenyl, Alkynyl, cyanoalkyl, haloalkyl, haloalkenyl, haloalkynyl, alkoxy, haloalkoxy, alkoxyalkyl, alkoxyalkoxyalkyl, alkylcarbonyl, alkenylcarbonyl, alkynecarbonyl, alkoxycarbonyl, alkenyloxycarbonyl, alkynyloxycarbonyl, alkylamino , Alkylsulfonylamino, haloalkylsulfonylamino, alkylalkoxycarbonylamino, alkylaminocarbonyl, alkylamino
- halogenated substituents preferably carry one to five identical or different halogen atoms.
- the meaning halogen in each case represents fluorine, chlorine, bromine or iodine.
- C 1 -C 4 -alkoxy-C 1 -C 4 -alkyl C 2 -C 6 alkenylthio-Ci-C4-alkyl, C2-C6 alkynylthio-Ci-C4-alkyl, Ci-C ⁇ -alkylsulfinyl-Ci-C ⁇ alkyl, Ci-C 6 haloalkyl sulfinyl C 1 -C 4 -alkyl, C 1 -C 6 -alkylsulfonyl-C 1 -C 4 -alkyl, C 1 -C 6 -haloalkylsulfonyl-d- C4-alkyl, amino-Ci-C4-alkyl, Di (C 1 -C 6 -alkyl) amino-C 1 -C 4 -alkyl, formylamino-C 1 -C 4 -alkyl, C 1 -C 6 -alkoxycarbonylamin
- Ci-C4-alkyl as mentioned above, as well as e.g. n-pentyl, 1-methylbutyl, 2-methylbutyl, 3-methylbutyl, 2,2-dimethylpropyl, 1-ethylpropyl, n-hexyl, 1, 1-dimethylpropyl, 1, 2-dimethylpropyl, 1-methylpentyl, 2 Methylpentyl, 3-methylpentyl, 4-methylpentyl, 1, 1-dimethylbutyl, 1, 2-dimethylbutyl, 1, 3-dimethylbutyl, 2,2-dimethylbutyl, 2,3-dimethylbutyl, 3,3-dimethylbutyl, 1 ethyl-butyl,
- C 1 -C 4 -alkylcarbonyl e.g. Methylcarbonyl, ethylcarbonyl, propylcarbonyl, 1-methylethylcarbonyl, butylcarbonyl, 1-methylpropylcarbonyl, 2-methylpropylcarbonyl or
- C 1 -C 4 -alkylcarbonyl as mentioned above, and also, for example, pentylcarbonyl, 1-methylbutylcarbonyl, 2-methylbutylcarbonyl, 3-methylbutylcarbonyl, 2,2- Dimethylpropylcarbonyl, 1-ethylpropylcarbonyl, hexylcarbonyl, 1,1-dimethylpropylcarbonyl, 1,2-dimethylpropylcarbonyl, 1-methylpentylcarbonyl, 2-methylpentylcarbonyl, 3-methylpentylcarbonyl, 4-methylpentylcarbonyl, 1,1-dimethylbutylcarbonyl, 1, 2-Dimethylbutylcarbonyl, 1, 3-dimethylbutylcarbonyl, 2,2-dimethylbutylcarbonyl, 2,3-dimethylbutylcarbonyl, 3,3-dimethylbutylcarbonyl, 1
- Ethylbutylcarbonyl 2-ethylbutylcarbonyl, 1,1,2-trimethylpropylcarbonyl, 1,2,2-trimethylpropylcarbonyl, 1-ethyl-i-methylpropylcarbonyl or 1-ethyl-2-methylpropylcarbonyl;
- C 3 -C 6 -cycloalkyl and the cycloalkyl parts of C 3 -C 6 -cycloalkylcarbonyl monocyclic, saturated hydrocarbon having 3 to 6 ring members, such as cyclopropyl, cyclobutyl, cyclopentyl and cyclohexyl;
- C3-C6 cycloalkenyl e.g. 1-Cyclopropenyl, 2-Cyclopropenyl, 1-Cyclobutenyl, 2-Cyclobutenyl, 1-Cyclopentenyl, 2-Cyclopentenyl, 1, 3-Cyclopentadienyl, 1, 4-
- Alkenyl) -N- (C 1 -C 6 alkoxy) aminocarbonyl e.g. 1-propenyl, 2-propenyl, 1-methyl-ethenyl, 1-butenyl, 2-butenyl, 3-butenyl, 1-methyl-1-propenyl, 2-methyl-1-propenyl, 1-methyl-2-propenyl, 2-methyl-2-propenyl, 1-pentenyl, 2-pentenyl, 3-pentenyl, 4-pentenyl, 1-methyl-1-butenyl, 2-methyl-1-butenyl, 3-methyl-1-butenyl, 1 - Methyl-2-butenyl, 2-methyl-2-butenyl, 3-methyl-2-butenyl, 1-methyl-3-butenyl, 2-methyl-3-butenyl, 3-methyl-3-butenyl, 1, 1- Dimethyl 2-propenyl, 1, 2-dimethyl-1-propenyl, 1, 2-dimethyl-2-propenyl, 1-ethyl-1
- C2-C6-alkenyl and also the alkenyl moieties of C2-C6-alkenylcarbonyl, C2-C6-alkenyloxy Ci-C 4 alkyl, C 2 -C 6 alkenylthio-Ci-C4-alkyl, phenyl-C 2 -C 4 alkenyl, heteroaryl C 2 -C 4 alkenyl: C 3 -C 6 alkenyl as mentioned above and ethenyl; - C3-C6-alkynyl and the alkynyl moieties of Cs-C ⁇ -alkynyloxycarbonyl, C3-C6-alkynylaminocarbonyl, N- (C3-C6-alkynyl) -N- (Ci-C6-alkyl) -aminocarbonyl, N- (C3-C6 Alkynyl) -N- (C 1 -C 6 -alkoxyamin
- cyanoalkyl for example, cyanomethyl, 1-cyanoeth-1-yl, 2-cyanoeth-1-yl, 1-cyano-prop-1-yl, 2-cyanoprop-1-yl, 3-cyanoprop-1 -yl, 1-cyanoprop-2-yl, 2-cyanoprop-2-yl, 1-cyanobut-1-yl, 2-cyanobut-1-yl, 3-cyanobut-1-yl, 4-cyanobut-1-yl , 1-cyano-but-2-yl, 2-cyanobut-2-yl, 1-cyanobut-3-yl, 2-cyanobut-3-yl, 1-cyano-2-methyl-prop-3-yl, 2 Cyano-2-methyl-prop-3-yl, 3-cyano-2-methyl-prop-3-yl and 2-cyano-methyl-prop-2-yl;
- C 1 -C 6 -hydroxyalkyl C 1 -C 4 -hydroxyalkyl as mentioned above, and also, for example, 1-hydroxy-pent-5-yl, 2-hydroxy-pent-5-yl, 3-hydroxy-pent-5-yl, 4 -Hydroxy-pent-5-yl, 5-hydroxy-pent-5-yl, 1-hydroxypent-4-yl, 2-hydroxy-4-yl, 3-hydroxypent-4-yl, 4-
- Hydroxypent-4-yl 1-hydroxy-pent-3-yl, 2-hydroxy-pent-3-yl, 3-hydroxy-pent-3-yl, 1-hydroxy-2-methylbut-3-yl, 2-hydroxy-2-methyl-but-3-yl, 3-hydroxy-2-methyl-but-3-yl, 1-hydroxy-2-methyl-but-4-yl, 2-hydroxy-2-methyl but-4-yl, 3-hydroxy-2-methyl but-4-yl, 4-hydroxy-2-methyl-but-4-yl, 1-hydroxy-3-methyl-but-4-yl, 2-hydroxy-3-methyl-but-4-yl, 3 Hydroxy-3-methylbut-4-yl, 4-hydroxy-3-methyl-but-4-yl, 1-hydroxy-hex-6-yl, 2-hydroxy-hex-6-yl, 3-hydroxy hex-6-yl, 4-hydroxy-hex-6-yl, 5-hydroxy-hex-6-yl, 6-hydroxy-hex-6-yl, 1-hydroxy-2-methyl-pent-5-yl, 2-hydroxy-2-methyl-pent-5-yl, 3-
- C3-C6-haloalkenyl a C3-C6-alkenyl radical as mentioned above which is partially or completely substituted by fluorine, chlorine, bromine and / or iodine, e.g. 2-chloro-prop-2-en-1-yl, 3-chloroprop-2-en-1-yl, 2,3-dichloroprop-2-en-1-yl, 3,3-dichloroprop-2-ene 1-yl, 2,3,3-trichloro-2-en-1-yl, 2,3-dichlorobut-2-en-1-yl, 2-bromoprop-2-en-1-yl, 3
- C2-C6 cyanoalkenyl e.g. 2-cyanovinyl, 2-cyanoallyl, 3-cyanoallyl, 2,3-dicyanoallyl, 3,3-dicyanoallyl, 2,3,3-tricyanoallyl, 2,3-dicyanobut-2-enyl;
- C3-C6-haloalkynyl a C3-C6-alkynyl radical as mentioned above which is partially or completely substituted by fluorine, chlorine, bromine and / or iodine, e.g. 1,1-Difluoro-prop-2-yn-1-yl, 3-iodo-prop-2-yn-1-yl, 4-fluorobut-2-yn-1-yl, 4-chlorobut-2in-1 yl, 1, 1-difluorobut-2-yn-1-yl, 4-iodobut-3-yn-1-yl, 5-fluoropent-3-yn-1-yl, 5-iodopent-4-yn-1 yl, 6-fluorohex-4-yn-1-yl or 6-iodohex-5-yn-1-yl;
- C2-C6 cyanoalkynyl e.g. 1,1-dicyano-prop-2-yn-1-yl, 3-cyano-prop-2-yn-1-yl, A-cyano-but-2-yn-1-yl, 1,1-dicyanobutyl 2-yn-1-yl, 4-cyanobut-3-yn-1-yl, 5-cyanopent-3-yn-1-yl, 5-cyanopent-4-yn-1-yl, 6-cyanohex-4- in-1-yl or 6-cyanohex-5-yn-1-yl;
- C 2 -C 6 -hydroxyalkynyl and the hydroxy parts of phenyl-C 2 -C 4 -hydroxyalkynyl e.g. 1, 1-dihydroxy-prop-2-yn-1-yl, 3-hydroxyprop-2-yn-1-yl, 4-hydroxy-but-2-yn-1-yl, 1, 1-dihydroxybutyl 2-yn-1-yl, 4-hydroxybut-3-yn-1-yl, 5-hydroxypent-3-yn-1-yl, 5-hydroxypent-4-yn-1-yl, 6-hydroxyhex-4 in-1-yl or 6-hydroxyhex-5-yn-1-yl;
- C 1 -C 6 -alkylsulfinyl (C 1 -C 6 -alkyl-S (OO) -) and the C 1 -C 6 -alkylsulfinyl parts of C 1 -C 6 -alkylsulfinyl-C 1 -C 4 -alkyl: for example methylsulfinyl, Ethylsulfinyl, propylsulfinyl, 1-methylethylsulfinyl, butylsulfinyl, 1-methylpropylsulfinyl, 2-methylpropylsulfinyl, 1, 1-dimethylethylsulfinyl, pentylsulfinyl, 1-methylbutylsulfinyl, 2-methylbutylsulfinyl, 3-methylbutylsulfinyl, 2,2-dimethylpropylsulfinyl, 1 - ethylprop
- Ci-C ⁇ -haloalkylsulfinyl and the Ci-C6-Halogenalkylsulfinyl parts of Ci-C ⁇ - haloalkylsulfinyl-Ci-C4-alkyl Ci-C ⁇ -Alkylsulfinylrest as mentioned above, which partially or completely by fluorine, chlorine, bromine and / or iodine is substituted, eg Fluoromethylsulfinyl, difluoromethylsulfinyl, trifluoromethylsulfinyl, chlorodifluoromethylsulfinyl, bromodifluoromethylsulfinyl, 2-fluoroethylsulfinyl, 2-chloroethylsulfinyl, 2-bromoethylsulfinyl, 2-iodoethylsulfinyl, 2, 2-difluoroethylsulf
- C 1 -C 6 -alkylsulfonyl (C 1 -C 6 -alkyl-S (O) 2 -) and the C 1 -C 6 -alkylsulfonyl parts of C 1 -C 6 -alkylsulfonyl-C 1 -C 4 -alkyl, C 1 -C 6 -alkylsulfonylamino, Ci-C 6 - alkylsulfonylamino-Ci-C4-alkyl, Ci-C6-alkylsulfonyl (Ci-C6-alkylamino) -C-C4-alkyl: for example methylsulfonyl, ethylsulfonyl, propylsulfonyl, 1-methylethylsulfonyl, butylsulfonyl, 1-methylpropylsulfonyl, 2-methyl-propylsulfony
- Fluorobutylsulfonyl 4-chlorobutylsulfonyl, 4-bromobutylsulfonyl, nonafluorobutylsulfonyl, 5-fluoropentylsulfonyl, 5-chloropentylsulfonyl, 5-bromo-pentylsulfonyl, 5-iodo-pentylsulfonyl, 6-fluorohexylsulfonyl, 6-bromohexylsulfonyl, 6-iodohexylsulfonyl and tridecafluorohexylsulfonyl;
- C 1 -C 6 -alkoxy and also the alkoxy parts of hydroxycarbonyl-C 1 -C 6 -alkoxy, C 1 -C 6 -alkoxycarbonyl-C 1 -C 6 -alkoxy, N- (C 1 -C 6 -alkoxy) -N- (C 1 -C 6 -alkyl) aminocarbonyl,
- 3-methylpentoxy 4-methylpentoxy, 1, 1-dimethylbutoxy, 1, 2-dimethylbutoxy, 1, 3-dimethylbutoxy, 2,2-dimethylbutoxy, 2,3-dimethylbutoxy, 3,3-dimethylbutoxy, 1-ethylbutoxy, 2-ethylbutoxy, 1, 1, 2-trimethylpropoxy, 1, 2,2-trimethylpropoxy, 1-ethyl-1-methylpropoxy and 1-ethyl-2-methylpropoxy;
- Ci-C4-haloalkoxy a Ci-C4-alkoxy radical as mentioned above, which is partially or completely substituted by fluorine, chlorine, bromine and / or iodine, thus e.g. Fluoromethoxy, difluoromethoxy, trifluoromethoxy, chlorodifluoromethoxy, bromodifluoromethoxy, 2-fluoroethoxy, 2-chloroethoxy, 2-bromomethoxy, 2-iodoethoxy, 2,2-difluoroethoxy, 2,2,2-trifluoroethoxy, 2-chloro 2-fluoroethoxy, 2-chloro-2,2-difluoroethoxy, 2,2-
- Ethylpropoxycarbonyl hexoxycarbonyl, 1,1-dimethylpropoxycarbonyl, 1,2-dimethylpropoxycarbonyl, 1-methylpentoxycarbonyl, 2-methylpentoxycarbonyl, 3-methylpentoxycarbonyl, 4-methylpentoxycarbonyl, 1,1-dimethylbutoxycarbonyl, 1, 2-dimethylbutoxycarbonyl, 1, 3-dimethylbutoxycarbonyl, 2,2-dimethylbutoxycarbonyl, 2,3-dimethylbutoxycarbonyl, 3,3-dimethylbutoxycarbonyl,
- C 1 -C 4 -alkylthio as mentioned above, and also, for example, pentylthio, 1-methylbutylthio, 2 Methylbutylthio, 3-methylbutylthio, 2,2-dimethylpropylthio, 1-ethylpropylthio, hexylthio, 1, 1-dimethylpropylthio, 1, 2-dimethylpropylthio, 1-methylpentylthio, 2-methylpentylthio, 3-methylpentylthio, 4-methylpentylthio, 1 , 1-dimethylbutylthio, 1, 2-dimethylbutylthio, 1, 3-dimethylbutylthio, 2,2-dimethylbutylthio, 2,3-
- Di (C 1 -C 6 -alkyl) aminothiocarbonyl for example N, N-dimethylaminothiocarbonyl, N 1 N-
- three- to six-membered heterocyclyl monocyclic, saturated or partially unsaturated hydrocarbons having three to six ring members as mentioned above which, in addition to carbon atoms, have one to four nitrogen atoms, or one to three nitrogen atoms and one oxygen or sulfur atom, or one to three oxygen atoms, or may contain one to three sulfur atoms, and which may be linked via a C atom or an N atom, eg
- Monocycles such as furyl (eg 2-furyl, 3-furyl), thienyl (eg 2-thienyl, 3-thienyl), pyrrolyl (eg pyrrol-2-yl, pyrrol-3-yl), pyrazolyl (eg pyrazol-3-yl , Pyrazol-4-yl), isoxazolyl (eg isoxazol-3-yl, isoxazol-4-yl, isoxazol-5-yl), isothiazolyl (eg isothiazol-3-yl, isothiazol-4-yl, isothiazol-5-yl ), Imidazolyl (eg imidazol-2-yl, imidazol-4-yl), oxazolyl (eg oxazol-2-yl, oxazol-4-yl, oxazol-5-yl), thiazolyl (eg thiazol-2-yl, thi
- pyridyl eg pyridin-2-yl, pyridin-3-yl, pyridine
- 4-yl pyrazinyl
- pyrimidinyl eg pyrimidin-2-yl, pyrimidin-4-yl, pyrimidin-5-yl
- pyrazine-2-yl Triazinyl (eg, 1, 3,5-triazin-2-yl, 1, 2,4-triazin-3-yl, 1, 2,4-triazin-5-yl, 1, 2,4-triazine-6 yl), tetrazinyl (eg 1, 2,4,5-tetrazine-3-yl); such as
- Bicyclic compounds such as the benzanellated derivatives of the aforementioned monocycles, e.g. Quinolinyl, isoquinolinyl, indolyl, benzthienyl, benzofuranyl, benzoxazolyl, benzothiazolyl, benzisothiazolyl, benzimidazolyl, benzopyrazolyl, benzthiadiazolyl, benzotriazole IyI.
- 5- or 6-membered heteroaryl having one to four nitrogen atoms, or one to three nitrogen atoms and one oxygen or sulfur atom, or with an oxygen or sulfur atom: e.g. C-atom linked aromatic 5-membered heterocycles which may contain, besides carbon atoms, one to four nitrogen atoms, or one to three nitrogen atoms and one sulfur or oxygen atom, or a sulfur or oxygen atom as ring members, e.g.
- Oxadiazol-3-yl 1, 2,4-oxadiazol-5-yl, 1, 2,4-thiadiazol-3-yl, 1, 2,4-thiadiazol-5-yl, 1, 2,4-triazole 3-yl, 1, 3,4-oxadiazol-2-yl, 1, 3,4-thiadiazol-2-yl and 1, 3,4-triazol-2-yl;
- the variables of the heteroaroyl-substituted alanines of the formula I have the following meanings, these being considered singly and in combination with one another in particular embodiments of the compounds of the formula I:
- heteroaroyl-substituted alanines of the formula I in which A is 5-membered heteroaryl having one to four nitrogen atoms, or one to three nitrogen atoms and one oxygen or sulfur atom, or having one oxygen or sulfur atom; particularly preferably 5-membered heteroaryl selected from the group of thienyl, furyl, pyrazolyl, imidazolyl, thiazolyl and oxazolyl; especially preferred 5-membered heteroaryl selected from the group thienyl, furyl, pyrazolyl and imidazolyl; wherein said heteroaryl radicals are substituted by a Ci-C ⁇ -haloalkyl radical, preferably in the 2-position by a Ci-C ⁇ -haloalkyl radical, and 1 to 3 radicals from the group halogen, cyano, Ci-C ⁇ -alkyl, C3 - Can carry C ⁇ -cycloalkyl, Ci-C ⁇ -alkoxy, Ci-C ⁇ -hal
- heteroaroyl-substituted alanines of the formula I in which A 5-membered heteroaryl having one to four nitrogen atoms, or one to three nitrogen atoms and one oxygen or sulfur atom, or with an oxygen or sulfur atom; particularly preferably 5-membered heteroaryl selected from the group of thienyl, furyl, pyrazolyl, imidazolyl, thiazolyl and oxazolyl; especially preferred 5-membered heteroaryl selected from the group thienyl, furyl, pyrazolyl and imidazolyl; where the said heteroaryl radicals can be partially or completely halogenated and / or 1 to 3 radicals from the group cyano, C 1 -C 6 -alkyl, C 3 -C 6 -cycloalkyl, C 1 -C 6 -haloalkyl, C 1 -C 6 -alkoxy, C 1 -C 8 -cycloalkyl Halogenoalkoxy and
- heteroaroyl-substituted alanines of the formula I in which A is 5-membered heteroaryl having one to four nitrogen atoms, or one to three nitrogen atoms and one oxygen or sulfur atom, or having one oxygen atom; particularly preferably 5-membered heteroaryl selected from the group furyl, pyrazolyl, imidazolyl, thiazolyl and oxazolyl; especially preferred 5-membered heteroaryl selected from the group furyl, pyrazolyl and imidazolyl; where the heteroaryl radicals mentioned can be partially or completely halogenated and / or 1 to 3 radicals from the group consisting of cyano, C 1 -C 6 -alkyl, C 3 -C 6 -cycloalkyl, C 1 -C 6 -haloalkyl, C 1 -C 6 -alkoxy, C 1 -C 8 -cycloalkyl, Haloalkoxy and
- Ci-C6-alkoxy-Ci-C4-alkyl can carry; means.
- heteroaroyl-substituted alanines of the formula I in which A is 6-membered heteroaryl having one to four nitrogen atoms; particularly preferably pyridyl or pyrimidyl. especially preferred pyrimidyl; where the said heteroaryl radicals can be partially or completely halogenated and / or 1 to 3 radicals from the group cyano, C 1 -C 6 -alkyl, C 3 -C 6 -cycloalkyl, C 1 -C 6 -haloalkyl, C 1 -C 6 -alkoxy, C 1 -C 8 -cycloalkyl Haloalkoxy and
- Ci-C6-alkoxy-Ci-C4-alkyl can carry; means.
- heteroaroyl-substituted alanines of the formula I in which A is 5- or 6-membered heteroaryl having one to four nitrogen atoms, or having one to three nitrogen atoms and one oxygen or sulfur atom, or an oxygen or sulfur atom which is replaced by a Ci-C ⁇ -haloalkyl radical, preferably in the 2-position by a Ci-C ⁇ -haloalkyl radical, is substituted, and 1 to 3 radicals from the group cyano, Ci-C ⁇ -alkyl, C3-C6-cycloalkyl, ci C 8 haloalkyl, C 1 -C 6 alkoxy, C 1 -C 6 haloalkoxy and C 1 -C 6
- heteroaroyl-substituted alanines of the formula I in which A is 5- or 6-membered heteroaryl selected from the group consisting of pyrrolyl, thienyl,
- heteroaryl radicals mentioned can be partially or completely halogenated and / or 1 to 3 radicals from the group consisting of C 1 -C 6 -alkyl, C 3 -C 6 -alkyl radicals and
- cycloalkyl and Ci-C ⁇ -haloalkyl May carry cycloalkyl and Ci-C ⁇ -haloalkyl; particularly preferably 5-membered heteroaryl selected from the group of thienyl, furyl, pyrazolyl, imidazolyl, thiazolyl and oxazolyl; where said heteroaryl radicals may be partially halogenated and / or may carry from 1 to 2 radicals selected from the group consisting of C 1 -C 6 -alkyl and C 1 -C 4 -haloalkyl;
- heteroaryl radicals may be partially halogenated and / or may carry from 1 to 2 radicals from the group consisting of C 1 -C 6 -alkyl and C 1 -C 4 -haloalkyl.
- heteroaroyl-substituted alanines of the formula I in which A is 5- or 6-membered heteroaryl selected from the group consisting of pyrrolyl, furyl, pyrazolyl, imidazolyl, thiazolyl, oxazolyl, tetrazolyl, pyridyl and pyrimidinyl; where the said heteroaryl radicals can be partially or completely halogenated and / or 1 to 3 radicals from the group cyano, C 1 -C 6 -alkyl, C 3 -C 6 -cycloalkyl, C 1 -C 6 -haloalkyl, C 1 -C 6 -alkoxy, C 1 -C 8 -cycloalkyl Haloalkoxy and can carry;
- heteroaryl radicals mentioned can be partially or completely halogenated and / or 1 to 3 radicals from the group consisting of C 1 -C 6 -alkyl, C 3 -C 6 -alkyl radicals and
- heteroaryl selected from the group furyl, pyrazolyl, imidazolyl, thiazolyl and oxazolyl; wherein said heteroaryl may be partially halogenated and / or may carry from 1 to 2 radicals selected from the group consisting of C 1 -C 6 -alkyl and C 1 -C 4 -haloalkyl;
- heteroaryl radicals may be partially halogenated and / or may carry from 1 to 2 radicals selected from the group consisting of C 1 -C 6 -alkyl and C 1 -C 4 -haloalkyl; means.
- heteroaroyl-substituted alanines of the formula I in which C-linked 5- or 6-membered heteroaryl selected from the group A1 to A14 with
- R 9 is hydrogen, halogen, C 1 -C 6 -alkyl or C 1 -C 6 -haloalkyl; particularly preferably hydrogen, C 1 -C 4 -alkyl or C 1 -C 4 -haloalkyl; particularly preferably hydrogen or C 1 -C 4 -alkyl; most preferably hydrogen;
- R 10 is halogen, C 1 -C 6 -alkyl, C 1 -C 6 -haloalkyl or C 1 -C 6 -haloalkoxy; particularly preferably halogen, C 1 -C 4 -alkyl or C 1 -C 6 -haloalkyl; particularly preferably halogen or Ci-C ⁇ -haloalkyl; very preferably Ci-C ⁇ -haloalkyl; extremely preferably C 1 -C 4 -haloalkyl very particularly preferably CF 3;
- R 11 is hydrogen, halogen, C 1 -C 6 -alkyl or C 1 -C 6 -haloalkyl; particularly preferably hydrogen, halogen or C 1 -C 4 -haloalkyl; especially preferably hydrogen or halogen; most preferably hydrogen; and
- R 12 is hydrogen, C -C alkyl 6 -alkyl, C 3 -C 6 cycloalkyl, Ci-C 6 haloalkyl or C
- C 6 alkoxy-C 1 -C 4 -alkyl particularly preferably C 1 -C 4 -alkyl, C 3 -C 6 -cycloalkyl, C 1 -C 4 -haloalkyl or C 1 -C 4 -alkoxy-C 1 -C 4 -alkyl; particularly preferably C 1 -C 4 -alkyl or C 1 -C 4 -haloalkyl; extremely preferably C 1 -C 4 -alkyl; very preferably CH3;
- R 9 to R 12 are defined as mentioned above;
- heteroaroyl-substituted alanines of the formula I in which
- R 1 is hydrogen
- R 2 is hydrogen or hydroxy; particularly preferably hydrogen; mean.
- heteroaroyl-substituted alanines of the formula I in which
- R 3 is C 1 -C 6 -alkyl or C 1 -C 6 -haloalkyl; particularly preferably C 1 -C 6 -alkyl; especially preferably C 1 -C 4 -alkyl; most preferably CH 3; means.
- R 4 is hydrogen or C 1 -C 4 -alkyl; preferably hydrogen or CH3; especially preferably hydrogen; means.
- C 2 -C 6 -Hydroxyalkinyl, C3-C6 cycloalkyl, C3-C6 cycloalkenyl, 3- to 6-membered heterocyclyl, wherein said precede said cycloalkyl, cycloalkenyl or 3- to 6-membered heterocyclyl radicals may be partially or fully halogenated and / or one to three radicals from the group consisting of oxo, cyano, nitro, CrC 6 -
- Ci-C 6 haloalkyl hydroxy, Ci-C 6 alkoxy, Ci-C 6 haloalkoxy, hydroxycarbonyl, Ci-C 6 -alkoxycarbonyl, hydroxycarbonyl-Ci-C 6 alkoxy, Ci-C 6 alkoxycarbonyl Ci-C 6 alkoxy, amino, Ci-C6 alkylamino, di (-C 6 - alkyl) amino, Ci-C 6 alkylsulfonylamino, Ci-C ⁇ -haloalkylsulfonylamino, aminocarbonylamino, (CrC 6 alkylamino) carbonylamino, di ( C 1 -C 6 alkyl) aminocarbonylamino, aryl and aryl (C 1 -C 6 alkyl); Ci-C 6 alkoxy-Ci-C 4 alkyl, C 2 -C 6 alkenyloxy-CrC 4 alkyl, C 2 -C 6 alkyl
- C -C alkyl are also preferred 6 -alkyl, C 2 -C 6 alkenyl, C 2 -C 6 kinyl -alkyl, Ci-C 6 haloalkyl, C 2 - C ⁇ haloalkenyl, C 2 -C 6 haloalkynyl, Ci-C ⁇ -cyanoalkyl, Ci-C ⁇ -hydroxyalkyl, C 2 -C 6 hydroxyalkenyl, C 2 -C 6 hydroxyalkynyl, C3-C6-cycloalkyl, C3-C6 Cycloalkenyl, 3- to 6-membered heterocyclyl, wherein the above-mentioned cycloalkyl, cycloalkenyl or 3- to 6-membered heterocyclyl radicals may be partially or completely halogenated and / or one to three radicals from the group oxo,
- Phenyl-Ci-C4-alkyl phenyl-C 2 -C 4 -alkenyl, phenyl-C 2 -C 4 -alkynyl, phenyl-Ci-C 4 - haloalkyl, phenyl-C 2 -C 4 haloalkenyl, phenyl-C -C 4 -hydroxyalkyl, phenyl-C 1 -C 4 -alkyl, phenylthio-C 1 -C 4 -alkyl, phenylsulfinyl-C 1 -C 4 -alkyl, phenylsulfonyl-C 1 -C 4 -alkyl; Heteroaryl, heteroaryl-C 1 -C 4 -alkyl, heteroaryl-C 1 -C 4 -hydroxyalkyl, heteroaryloxy
- C 1 -C 6 -alkyl particularly preferably hydrogen, C 1 -C 6 -alkyl, C 2 -C 6 -alkenyl, C 2 -C 6 -alkynyl, C 1 -C 6 -haloalkyl, C 2 -C 6 -haloalkenyl, C 1 -C 6 -hydroxyalkyl, C 1 -C 6 -alkoxy-Ci -C 4 -alkyl, C 1 -C 6 -haloalkoxy-C 1 -C 4 -alkyl, hydroxycarbonyl-C 1 -C 4 -alkyl, C 1 -C 6 -
- C 1 -C 6 -alkyl particularly preferably hydrogen, C 1 -C 6 -alkyl, C 2 -C 6 -alkenyl, C 2 -C 6 -alkynyl, C 1 -C 6 -haloalkyl, C 2 -C 6 -haloalkenyl, C 1 -C 6 -hydroxyalkyl, hydroxycarbonyl-C 1 -C 4 -alkyl, C 1 -C 6 -alkoxycarbonyl-C 1 -C 4 -alkyl, [di (C 1 -C 6 -alkyl) aminocarbonyl-oxy] C 1 -C 4 -alkyl, formylamino-C 1 -C 4 -alkyl;
- Ci-C 6 alkyl extraordinarily preferably hydrogen, Ci-C 6 alkyl, C 2 -C 6 alkenyl, -C 6 -
- Haloalkyl C 2 -C 6 -haloalkenyl, C 1 -C 6 -hydroxyalkyl, formylamino-C 1 -C 4 -alkyl, phenyl-C 1 -C 4 -alkyl or phenyl-C 1 -C 4 -hydroxyalkyl; means.
- C -C alkyl are also preferred 6 -alkyl, C 3 -C 6 cycloalkyl, C 3 -C 6 alkenyl, C 3 -C 6 -alkyl kinyl , C 3 -C 6 - haloalkenyl, C 3 -C 6 -haloalkynyl, formyl, Ci-C 6 alkylcarbonyl, C 3 -C 6 - cycloalkylcarbonyl, C2-C6 alkenylcarbonyl, C2-C6 alkynylcarbonyl, CrC 6 - alkoxycarbonyl, C 3 -C 6 alkenyloxycarbonyl, C 3 -C 6 -alkynyloxycarbonyl, -C 6 - alkylaminocarbonyl, Cs-Ce-alkenylaminocarbonyl, Cs-Ce-alkenylaminocarbonyl, Cs-Ce-alkenylaminocarbony
- Ci-Ce-alkylsulphonylaminocarbonyl di (Ci-C 6 alkyl) aminocarbonyl, N- (C 3 -C 6 - alkenyl) -N- (Ci-C 6 alkyl) aminocarbonyl, N- (C 3 -C 6 alkynyl) -N- (Ci-C 6 alkyl) - aminocarbonyl, N- (Ci-C 6 alkoxy) -N- (Ci-C 6 -alkyl) -amino-carbonyl, N- (C 3 -C 6 - Alkenyl) -N- (C 1 -C 6 -alkoxy) -aminocarbonyl, N- (C 3 -C 6 -alkynyl) -N- (C 1 -C 6 -alkoxy) -aminocarbonyl, di (C 1 -C 6 -alkyl) aminothiocarbonyl, (C 1 -
- C 1 -C 6 -alkyl particularly preferably hydrogen, C 1 -C 6 -alkyl, C 3 -C 6 -alkenyl, C 3 -C 6 -alkynyl, formyl, C 1 -C 6 -alkyl-carbonyl, Ci-C ⁇ -alkoxycarbonyl, di (Ci-Ce-alkylJ-amino-carbonyl, N- (Ci-C6-alkoxy) -N- (Ci-C6-alkyl) -aminocarbonyl,
- the heteroaroyl-substituted alanines of the formula I in which R 6 is hydrogen, Ci-C are also preferred 6 alkyl, C 3 -C 6 alkenyl, C 3 -C 6 kinyl -alkyl, formyl, -C 6 - alkylcarbonyl, Ca -C ⁇ -alkenylcarbonyl, C 3 -C 6 -cycloalkylcarbonyl, C 1 -C 6 -alkoxycarbonyl, C 1 -C 6 -alkylaminocarbonyl, di- (C 1 -C 6 -alkyl) aminocarbonyl, N- (C 1 -C 6 -alkoxy) -N- (C 1 -C 6 -alkyl) aminocarbonyl, di- (C 1 -C 6 -alkyl) aminothiocarbonyl, C 1 -C 6 -alkoxyimino-C 1 -C 6 -alkyl, where the alky
- heteroaroyl-substituted alanines of the formula I in which R 8 is C 1 -C 6 -alkyl, C 1 -C 6 -haloalkyl or phenyl, where the phenyl radical may be partially halogenated and / or represented by C 1 -C 4 -alkyl.
- Alkyl may be substituted; particularly preferably C 1 -C 4 -alkyl, C 1 -C 4 -haloalkyl or phenyl; especially preferably methyl, trifluoromethyl or phenyl. means.
- heteroaroyl-substituted alanines of the formula I in which A is 5- or 6-membered heteroaryl selected from the group consisting of thienyl, furyl, pyrazolyl, imidazolyl, thiazolyl, oxazolyl and pyridyl; wherein said heteroaryl may be partially or completely halogenated and / or 1 to 3 radicals from the group Ci-C ⁇ -alkyl, C3-C6-cycloalkyl and Ci-C ⁇ -haloalkyl may carry; R 1 and R 2 are hydrogen; R 3 is C 1 -C 4 -alkyl, particularly preferably CH 3; R 4 is hydrogen;
- R 5 is hydrogen, Ci-C 6 alkyl, C 2 -C 6 alkenyl, Ci-C 6 haloalkyl, C 2 -C 6 - haloalkenyl, Ci-C 6 hydroxyalkyl, hydroxycarbonyl-d ⁇ alkyl, phenyl C 1 -C 4 -alkyl or phenyl-C 1 -C 4 -hydroxyalkyl;
- R 6 is hydrogen, formyl, C 1 -C 4 -alkylcarbonyl, C 1 -C 4 -alkylaminocarbonyl, di (C 1 -C 4 -alkyl) aminocarbonyl, phenylaminocarbonyl, N- (C 1 -C 4 -alkyl) -N- (phenyl) -aminocarbonyl, SO 2 CH 3 , SO 2 CF 3 or SO 2 (C 6 H 5 ); and R 7 is hydrogen.
- benzoyl-substituted alanines of the formula I are obtainable in various ways, for example by the following processes:
- Alanine derivatives of the formula V are first reacted with heteroaryl acid (derivatives) of the formula IV to give corresponding heteroaroyl derivatives of the formula III, which subsequently react with amines of the formula II to give the desired heteroaroyl-substituted alanines of the formula I:
- L 1 is a nucleophilically displaceable leaving group, for example for hydroxy or C 1 -C 6 -alkoxy.
- L 2 represents a nucleophilic displaceable leaving group, for example for hydroxy, halogen, C 1 -C 6 -alkylcarbonyl, C 1 -C 6 -alkoxycarbonyl, C 1 -C 4 -alkyl, onyl, phosphoryl or iso-ureyl.
- heteroaroyl derivatives of the formula IM is carried out in the presence of an activating reagent and a base usually at temperatures of 0 0 C to the boiling point of the reaction mixture, preferably O 0 C to 11 O 0 C, particularly preferably at room temperature, in an inert organic solvent [cf. KC Nicolaou et al., J. of the Am. Chem. Soc. (2005), 127 (31), 1176-1 1 183; Shu-Sin Chng et al., Tetrahedron Lett.
- Suitable activating reagents are condensing agents, e.g. polystyrene-bonded dicyclohexylcarbodiimide, diisopropylcarbodiimide, carbonyldiimidazole, chlorocarbonic acid esters such as methyl chloroformate, ethyl chloroformate, isoropyl chloroformate, isobutyl chloroformate, sec-butyl chloroformate or allyl chloroformate, pivaloyl chloride, polyphosphoric acid, propanephosphonic anhydride, bis (2-oxo-3-oxazolidinyl) phosphoryl chloride (BOPCI) or Sulfonyl chlorides such as methanesulfonyl chloride, toluenesulfonyl chloride or benzenesulfonyl chloride.
- condensing agents e.g. polystyrene-bonded dicyclohexylcarbodiimi
- Suitable solvents are aliphatic hydrocarbons such as pentane, hexane, cyclohexane and mixtures of Cs-Cs-Al kanen, aromatic hydrocarbons such as benzene, toluene, o-, m- and p-xylene, halogenated hydrocarbons such as methylene chloride, chloroform and chlorobenzene, ethers such as diethyl ether , Diisopropyl ether, tert-butyl methyl ether, dioxane, anisole and tetrahydrofuran (THF), nitriles such as acetonitrile and propionitrile, ketones such as acetone, methyl ethyl ketone, diethyl ketone and tert-butyl methyl ketone, and dimethyl sulfoxide, dimethylformamide (DMF), dimethylacetamide (DMA) and N Methylpyrroli
- Bases generally include inorganic compounds such as alkali metal and alkaline earth metal hydroxides such as lithium hydroxide, sodium hydroxide, potassium hydroxide and calcium hydroxide, alkali metal and alkaline earth metal oxides such as lithium oxide, sodium oxide, calcium oxide and magnesium oxide, alkali metal and alkaline earth metal hydrides such as lithium hydride, sodium hydride, potassium hydride and calcium hydride, Alkali metal and alkaline earth metal carbonates such as lithium carbonate, potassium carbonate and calcium carbonate and alkali metal bicarbonates such as sodium bicarbonate, as well as organic bases, eg tertiary amines such as trimethylamine, triethylamine, diisopropylethylamine, N-
- the bases are generally used in equimolar amounts. But they can also be used in excess or optionally as a solvent.
- the starting materials are generally reacted with one another in equimolar amounts. It may be advantageous to use IV in an excess relative to V.
- reaction mixtures are worked up in the usual way, e.g. by mixing with water, separation of the phases and optionally chromatographic purification of the crude products.
- the intermediate and end products fall z. T. in the form of viscous oils, which are freed or purified under reduced pressure and at moderately elevated temperature of volatile fractions. If the intermediate and end products are obtained as solids, the purification can also be carried out by recrystallization or trituration.
- the reaction of the alanine derivatives of the formula V with heteroaryl acid (derivatives) n of the formula IV in which L 2 is halogen, C 1 -C 6 -alkylcarbonyl, C 1 -C 6 -alkoxycarbonyl, C 1 -C 4 -alkylsulfonyl, phosphoryl or isoureyl, to give heteroaroyl derivatives of the formula IM is carried out in the presence of a base, usually at temperatures from 0 ° C. to the boiling point of the reaction mixture, preferably from 0 ° C. to 100 ° C., more preferably at room temperature in an inert organic solvent [cf. KC Nicolaou et al., J. of the Am.
- Suitable solvents are aliphatic hydrocarbons such as pentane, hexane, cyclohexane and mixtures of Cs-Cs-Al kanen, aromatic hydrocarbons such as benzene, toluene, o-, m- and p-xylene, halogenated hydrocarbons such as methylene chloride, chloroform and chlorobenzene, ethers such as diethyl ether , Diisopropyl ether, tert-butyl methyl ether, dioxane, anisole and tetrahydrofuran (THF), nitriles such as acetonitrile and propionitrile, ketones such as acetone, methyl ethyl ketone, diethyl ketone and tert-butyl methyl ketone, and also dimethyl sulfoxide, dimethylformamide (DMF), dimethylacetamide ( DMA) and N-
- Methylpyrrolidone (NMP) or in water particularly preferred are methylene chloride, THF and water. It is also possible to use mixtures of the solvents mentioned.
- Bases generally include inorganic compounds such as alkali metal and alkaline earth metal hydroxides such as lithium hydroxide, sodium hydroxide, potassium hydroxide and calcium hydroxide, alkali metal and alkaline earth metal oxides such as lithium oxide, sodium oxide, calcium oxide and magnesium oxide, alkali metal and alkaline earth metal hydrides such as lithium hydride, sodium hydride, potassium hydride and calcium hydride, Alkali metal and alkaline earth metal carbonates such as lithium carbonate, potassium carbonate and calcium carbonate and alkali metal bicarbonates such as sodium bicarbonate, as well as organic bases, eg tertiary amines such as trimethylamine, triethylamine, diisopropylethylamine, N-
- Particularly preferred are sodium hydroxide, triethylamine and pyridine.
- the bases are generally used in equimolar amounts. But they can also be used in excess or optionally as a solvent.
- the starting materials are generally reacted with one another in equimolar amounts. It may be advantageous to use IV in an excess relative to V.
- the workup and isolation of the products can be done in a conventional manner.
- the alanine derivatives of the formula V can first be reacted with amines of the formula II to give the corresponding amides, which then react with heteroaryl acid (derivatives) n of the formula IV to give the desired heteroaroyl-substituted alanines of the formula I.
- alanine derivatives of the formula V required for the preparation of the heteroaroyl derivatives of the formula III are known in the literature, even in enantiomerically and diastereomerically pure form, or can be prepared according to the cited literature :
- heteroaryl acid (derivatives) of the formula IV required for the preparation of the heteroaroyl derivatives of the formula III can be purchased or can be prepared analogously to the procedure known from the literature [eg Chang-Ling Liu et al., J. of Fluorine Chem. (2004) , 125 (9), 1287-1290; Manfred Schlosser et al., Europ. J. of Org. Chem. (2002), (17), 2913-2920; Hoh-Gyu Hahn et al., Agricult. Chem. And Biotech. (English Edition) (2002), 45 (1), 37-42; Jonatan O Smith et al., J. of Fluorine Chem. (1997), Vol.
- Suitable activating reagents are condensing agents, e.g. polystyrene-bonded dicyclohexylcarbodiimide, diisopropylcarbodiimide, carbonyldiimidazole, chlorocarbonic acid esters such as methyl chloroformate, ethyl chloroformate, isoropyl chloroformate, isobutyl chloroformate, sec-butyl chloroformate or allyl chloroformate, pivaloyl chloride, polyphosphoric acid,
- Propanephosphonic anhydride bis (2-oxo-3-oxazolidinyl) phosphoryl chloride (BOPCI) or sulfonyl chlorides such as methanesulfonyl chloride, toluenesulfonyl chloride or benzenesulfonyl chloride.
- BOPCI bis (2-oxo-3-oxazolidinyl) phosphoryl chloride
- sulfonyl chlorides such as methanesulfonyl chloride, toluenesulfonyl chloride or benzenesulfonyl chloride.
- Suitable solvents are aliphatic hydrocarbons such as pentane, hexane, cyclohexane and mixtures of Cs-Cs-Al kanen, aromatic hydrocarbons such as benzene, toluene, o-, m- and p-xylene, halogenated hydrocarbons such as methylene chloride, chloroform and chlorobenzene, ethers such as diethyl ether , Diisopropyl ether, tert-butyl methyl ether, dioxane, anisole and tetrahydrofuran (THF), nitriles such as acetonitrile and propionitrile, ketones such as acetone, methyl ethyl ketone, diethyl ketone and tert-butyl methyl ketone, alcohols such as methanol, ethanol, n-propanol, isopropanol, n-butanol and
- Suitable bases are generally inorganic compounds such as alkali metal and alkaline earth metal hydroxides such as lithium hydroxide, sodium hydroxide, potassium hydroxide and calcium hydroxide, alkali metal and alkaline earth metal oxides such as lithium oxide, sodium oxide, calcium oxide and magnesium oxide, alkali metal and alkaline earth metal hydrides such as lithium hydride, sodium hydride, potassium hydride and Calcium hydride, alkali metal and alkaline earth metal carbonates such as lithium carbonate, potassium carbonate and calcium carbonate and alkali metal bicarbonates such as sodium bicarbonate, as well as organic bases, for example tertiary amines such as trimethylamine, triethylamine, diisopropylethylamine, N-methylmorpholine, and N-methylpiperidine, pyridine, substituted pyridines such as collidine Lutidine and 4-dimethylaminopyridine and bicyclic amines into consideration. Especially Preference is given to sodium hydroxide, trieth
- the bases are generally used in catalytic amounts, but they can also be used equimolar, in excess or optionally as solvent.
- the starting materials are generally reacted with one another in equimolar amounts. It may be advantageous to use II in an excess relative to IM.
- the workup and isolation of the products can be done in a conventional manner.
- Suitable solvents are aliphatic hydrocarbons such as pentane, hexane, cyclohexane and mixtures of Cs-Cs-Al kanen, aromatic hydrocarbons such as benzene, toluene, o-, m- and p-xylene, halogenated hydrocarbons such as methylene chloride, chloroform and chlorobenzene, ethers such as diethyl ether , Diisopropyl ether, tert-butyl methyl ether, dioxane, anisole and tetrahydrofuran (THF), nitriles such as acetonitrile and propionitrile, ketones such as acetone, methyl ethyl ketone, diethyl ketone and tert-butyl methyl ketone, alcohols such as methanol, ethanol, n-propanol, isopropanol, n- Butanol and
- the reaction may optionally be carried out in the presence of a base.
- bases are generally inorganic compounds such as alkali metal and alkaline earth metal hydroxides such as lithium hydroxide, sodium hydroxide, potassium hydroxide and calcium hydroxide, alkali metal and alkaline earth metal oxides such as lithium oxide, sodium oxide, calcium oxide and magnesium oxide, alkali metal and alkaline earth metal hydrides such as lithium hydride, sodium hydride, potassium hydride and calcium hydride, alkali metal and alkaline earth metal carbonates such as lithium carbonate, potassium carbonate and calcium carbonate, and alkali metal hydrogen carbonate in addition, organic bases, for example tertiary amines such as trimethylamine, triethylamine, diisopropylethylamine, N-methylmorpholine, and N-methylpiperidine, pyridine, substituted pyridines such as collidine, lutidine and 4-dimethylaminopyridine and bicyclic amines into consideration. Particularly preferred
- the bases are generally used in catalytic amounts, but they can also be used equimolar, in excess or optionally as solvent.
- the starting materials are generally reacted with one another in equimolar amounts. It may be advantageous to use Il in an excess relative to IM.
- the workup and isolation of the products can be done in a conventional manner.
- the amines of the formula II required for the preparation of the heteroaroyl-substituted alanines of the formula I can be purchased.
- R x is R 6 or a removable protecting group such as C 1 -C 6 -alkyloxycarbonyl (eg tert-butyloxycarbonyl), C 1 -C 6 -alkylsulfinyl (eg tert-butylsulfinyl) or optionally C 1 -C 6 -alkyl-substituted arylsulfinyl ( eg toluylsulfinyl).
- C 1 -C 6 -alkyloxycarbonyl eg tert-butyloxycarbonyl
- C 1 -C 6 -alkylsulfinyl eg tert-butylsulfinyl
- optionally C 1 -C 6 -alkyl-substituted arylsulfinyl eg toluylsulfinyl.
- L 1 is a nucleophilically displaceable leaving group, for example for hydroxy or C 1 -C 6 -alkoxy.
- L 2 is a nucleophilically displaceable leaving group, for example hydroxy, halogen, C 1 -C 6 -alkylcarbonyl, C 1 -C 6 -alkoxycarbonyl, C 1 -C 4 -alkyl, onyl, phosphoryl or iso-ureyl.
- Suitable solvents are aliphatic hydrocarbons such as pentane, hexane, cyclohexane and mixtures of Cs-Cs-Al kanen, aromatic hydrocarbons such as toluene, o-, m- and p-xylene, ethers such as diethyl ether, diisopropyl ether, tert-butyl methyl ether, dioxane, anisole and Tetrahydrofuran, as well as dimethyl sulfoxide, dimethylformamide and dimethylacetamide, particularly preferably diethyl ether, dioxane and tetrahydrofuran. It is also possible to use mixtures of the solvents mentioned.
- Suitable bases are generally inorganic compounds such as alkali metal and alkaline earth metal hydrides such as lithium hydride, sodium hydride, potassium hydride and calcium hydride, alkali metal amides such as lithium isopropylamide and lithium hexamethyldisilazide, organometallic compounds, in particular alkali metal alkyls such as methyllithium, butyllithium and phenyllithium, and alkali metal and alkaline earth metal alkoxides such as sodium methoxide, sodium ethanolate, Potassium ethoxide, potassium tert-butoxide, potassium tert-pentoxide and Dimethoxymagnesium, also organic bases, eg tertiary amines such as trimethylamine, triethylamine, diisopropylethylamine and N-methylpiperidine, pyridine, substituted pyridines such as collidine, lutidine and 4-dimethylaminopyridine and bi
- the bases are generally used in equimolar amounts, but they can also be used catalytically, in excess or optionally as a solvent.
- the starting materials are generally reacted with one another in equimolar amounts. It may be advantageous to use the base and / or the imino compounds VII in an excess based on the glycine derivatives VIII.
- the workup and isolation of the products can be done in a conventional manner.
- L 1 is a nucleophilically displaceable leaving group, for example for hydroxy or C 1 -C 6 -alkoxy.
- L 3 is a nucleophilically displaceable leaving group, for example halogen, hydroxy, or C 1 -C 6 -alkoxy.
- Suitable solvents are aliphatic hydrocarbons such as pentane, hexane, cyclohexane and mixtures of Cs-Cs-Al kanen, aromatic hydrocarbons such as toluene, o-, m- and p-xylene, halogenated hydrocarbons such as methylene chloride, chloroform and chlorobenzene, ethers such as diethyl ether, diisopropyl ether , tert-butyl methyl ether, dioxane, anisole and tetrahydrofuran, nitriles such as acetonitrile and propinonitrile, ketones such as acetone, methyl ethyl ketone, diethyl ketone and tert-butyl methyl ketone, alcohols such as methanol, ethanol, n-propanol, isopropanol, n-butanol and tert. Butanol
- Bases generally include inorganic compounds such as alkali metal and alkaline earth metal hydroxides such as lithium hydroxide, sodium hydroxide, potassium hydroxide and calcium hydroxide, alkali metal and alkaline earth metal oxides such as lithium oxide, sodium oxide, calcium oxide and magnesium oxide, alkali metal and alkaline earth metal hydrides such as lithium hydride, sodium hydride, potassium hydride and calcium hydride, Alkali metal amides such as lithium amide, sodium amide and potassium amide, alkali metal and alkaline earth metal carbonates such as lithium carbonate, potassium carbonate and calcium carbonate and also alkali metal hydrogencarbonates such as sodium bicarbonate, organometallic compounds, in particular alkali metal alkyls such as methyllithium, butyllithium and phenyllithium, alkylmagnesium halides such as methylmagnesium chloride and also alkali metal and earth metal halides.
- alkali metal and alkaline earth metal hydroxides such as lithium hydro
- potassium alcoholates such as sodium methoxide, sodium ethanolate, potassium ethanolate, potassium tert-butanolate, potassium tert-pentoxide and dimethoxy magnesium
- organic bases for example tertiary amines such as trimethylamine, triethylamine, diisopropylethylamine and N-methylpiperidine, pyridine, substituted pyridines such as collidine, lutidine and 4-dimethylaminopyridine and bicyclic Amines into consideration.
- tertiary amines such as trimethylamine, triethylamine, diisopropylethylamine and N-methylpiperidine
- pyridine substituted pyridines
- collidine lutidine and 4-dimethylaminopyridine and bicyclic Amines into consideration.
- Particular preference is given to sodium hydroxide, sodium hydride and triethylamine.
- the bases are generally used in equimolar amounts, but they can also be used catalytically, in excess or optionally as a solvent.
- the starting materials are generally reacted with one another in equimolar amounts. It may be advantageous to use the base and / or IX in an excess based on IM or I.
- the workup and isolation of the products can be done in a conventional manner.
- L 1 is a nucleophilically displaceable leaving group, for example hydroxy or C 1 -C 6 -alkoxy.
- L 4 represents a nucleophilically displaceable leaving group, for example halogen, such as chlorine or bromine.
- the reaction of the nitro compound XI with the glycine derivative XM is usually carried out at a temperature of -100 ° C to the boiling point of the reaction mixture, preferably at -80 ° C to 20 ° C, in an inert organic solvent in the presence of a base ( See Vicky A. Burgess et al., Aust. J. of Chem. (1988), 41 (7), 1063-1070).
- Suitable solvents are aliphatic hydrocarbons such as pentane, hexane, cyclohexane and mixtures of Cs-Cs-Al kanen, aromatic hydrocarbons such as toluene, o-, m- and p-xylene, halogenated hydrocarbons such as methylene chloride, chloroform and chlorobenzene, ethers such as diethyl ether, diisopropyl ether , tert-butyl methyl ether, dioxane, anisole and tetrahydrofuran, nitriles such as acetonitrile and propinonitrile, ketones such as acetone, methyl ethyl ketone, diethyl ketone and tert-butyl methyl ketone, alcohols such as methanol, ethanol, n-propanol, isopropanol, n-butanol and tert. Butanol
- Bases generally include inorganic compounds such as alkali metal and alkaline earth metal hydroxides such as lithium hydroxide, sodium hydroxide, potassium hydroxide and calcium hydroxide, alkali metal and alkaline earth metal oxides such as lithium oxide, sodium oxide, calcium oxide and magnesium oxide, alkali metal and alkaline earth metal hydrides such as lithium hydride, sodium hydride, potassium hydride and calcium hydride, Alkali metal amides such as lithium amide, sodium amide and potassium amide, alkali metal and alkaline earth metal carbonates such as lithium carbonate, potassium carbonate and calcium carbonate and also alkali metal hydrogencarbonates such as sodium bicarbonate, organometallic compounds, in particular alkali metal alkyls such as methyllithium, butyllithium and phenyllithium, alkylmagnesium halides such as methylmagnesium chloride and also alkali metal and earth metal halides.
- alkali metal and alkaline earth metal hydroxides such as lithium hydro
- potassium metal alcoholates such as sodium methoxide, sodium ethanolate, potassium ethanolate, potassium tert. Butanolate, potassium tertiary pentoxide and dimethoxy magnesium, as well as organic bases, e.g. tertiary amines such as trimethylamine, triethylamine, Diisopropylethy- lamin and N-methylpiperidine, pyridine, substituted pyridines such as collidine, lutidine and 4-dimethylaminopyridine and bicyclic amines into consideration. Particularly preferred are sodium hydroxide, sodium hydride and triethylamine.
- the bases are generally used in equimolar amounts, but they can also be used catalytically, in excess or optionally as a solvent.
- the starting materials are generally reacted with one another in equimolar amounts. It may be advantageous to use the base and / or XI in an excess based on XII.
- the workup and isolation of the products can be done in a conventional manner.
- the required nitro compound of the formula XI can be purchased.
- the required glycine derivatives of the formula XII can be obtained analogously to methods known from the literature (compare Vicky A. Burgess et al., Aust. J. of Chem. (1988), 41 (7), 1063-1070).
- the reduction of the nitroaniline derivatives of the formula X is usually carried out at a temperature of -100 ° C to the boiling point of the reaction mixture, preferably -80 ° C to 20 ° C, in an inert organic solvent with a reducing agent, (see Vicky A. Burgess et al., Aust. J. of Chem. (1988), 41 (7), 1063-1070).
- Suitable solvents are aliphatic hydrocarbons such as pentane, hexane, cyclohexane and mixtures of Cs-Cs-Al kanen, aromatic hydrocarbons such as toluene, o-, m- and p-xylene, halogenated hydrocarbons such as methylene chloride, chloroform and chlorobenzene, ethers such as diethyl ether, diisopropyl ether , tert-butyl methyl ether, dioxane, anisole and tetrahydrofuran, nitriles such as acetonitrile and propionitrile, ketones such as acetone, methyl ethyl ketone, diethyl ketone and tert-butyl methyl ketone, alcohols such as methanol, ethanol, n-propanol, isopropanol, n-butanol and tert-butanol,
- Suitable reducing agents are transition metal catalysts (e.g., Pd / C or Raney Ni) in combination with hydrogen.
- the workup and isolation of the product can be carried out in a conventional manner.
- A, R 1 and R 4 , R 5 , R 6 and R 7 have the meanings given above and L 1 is a nucleophilically displaceable leaving group, for example hydroxy or C 1 -C 6 alkoxy, are also an object of the present invention.
- L 1 is a nucleophilically displaceable leaving group, for example hydroxy or C 1 -C 6 alkoxy.
- the particularly preferred embodiments of the intermediates with respect to the variables correspond to those of the radicals A, R 1 and R 4 to R 7 of the formula I.
- heteroaroyl derivatives of the formula III in which A is 5- or 6-membered heteroaryl selected from the group consisting of thienyl, furyl, pyrazolyl, imidazolyl, thiazolyl, oxazolyl and pyridyl; wherein said heteroaryl may be partially or fully halogenated and / or 1 to 3 radicals from the group Ci-C ⁇ -alkyl, C3-C6-cycloalkyl, and carry Ci-C ⁇ -haloalkyl; R 1 is hydrogen; R 4 is hydrogen; R 5 is hydrogen, Ci-C 6 alkyl, C 2 -C 6 alkenyl, Ci-C 6 haloalkyl, C 2 -C 6 -
- Haloalkenyl C 1 -C 6 -hydroxyalkyl, hydroxycarbonyl-C 1 -C 4 -alkyl, phenyl-C 1 -C 4 -alkyl or phenyl-C 1 -C 4 -hydroxyalkyl;
- R 6 is hydrogen, formyl, C 1 -C 4 -alkylcarbonyl, C 1 -C 4 -alkylaminocarbonyl, di (C 1 -C 4 -alkyl) aminocarbonyl, phenylaminocarbonyl, N- (C 1 -C 4 -alkyl) -N- (phenyl) -aminocarbonyl, SO 2 CH 31 SO 2 CF 3 or SO 2 (C 6 H 5 ); and
- R 7 is hydrogen; mean.
- the heteroaroyl-substituted alanines of the formula I and their agriculturally useful salts are suitable - both as isomer mixtures and in the form of pure isomers - as herbicides.
- the compounds of the formula I containing herbicidal agents control plant growth on non-crop areas very well, especially at high application rates. In crops such as wheat, rice, corn, soybeans and cotton, they act against weeds and grass weeds without significantly damaging the crops. This effect occurs especially at low application rates.
- the compounds of the formula I or herbicidal compositions containing them can be used in a further number of crop plants for the removal of unwanted plants.
- the following cultures may be considered:
- the compounds of formula I may also be used in cultures tolerant to the action of herbicides by breeding, including genetic engineering.
- the compounds of formula I can also be used in cultures tolerant by breeding including genetic engineering against insect or fungal attack.
- the compounds of the formula I or the herbicidal compositions containing them can be used, for example, in the form of directly sprayable aqueous solutions, powders, suspensions, even high-percentage aqueous, oily or other suspensions or dispersants.
- the forms of application depend on the intended use; In any case, they should ensure the finest possible distribution of the active compounds according to the invention.
- the herbicidal compositions contain a herbicidally effective amount of at least one compound of the formula I or an agriculturally useful salt of I and auxiliaries customary for the formulation of crop protection agents.
- Suitable inert auxiliaries are essentially:
- Mineral oil fractions of medium to high boiling point such as kerosene and diesel oil, coal tar oils and oils of vegetable or animal origin, aliphatic, cyclic and aromatic hydrocarbons, e.g. Paraffins, tetrahydronaphthalene, alkylated naphthalenes and their derivatives, alkylated benzenes and their derivatives, alcohols such as methanol, ethanol, propanol, butanol and cyclohexanol, ketones such as cyclohexanone, strong polar solvents, e.g. Amines such as N-methylpyrrolidone and water.
- Paraffins etrahydronaphthalene
- alkylated naphthalenes and their derivatives alkylated benzenes and their derivatives
- alcohols such as methanol, ethanol, propanol, butanol and cyclohexanol
- ketones such as cyclohexanone
- Aqueous application forms can be prepared from emulsion concentrates, suspensions, pastes, wettable powders or water-dispersible granules by adding
- Water to be prepared Water to be prepared.
- the substrates as such or dissolved in an oil or solvent, can be homogenized in water by means of wetting agents, tackifiers, dispersants or emulsifiers.
- wetting agents wetting, adhesion, dispersing or emulsifying agent and possibly solvent or oil, which are suitable for dilution with water.
- surfactants are the alkali, alkaline earth, ammonium salts of aromatic sulfonic acids, e.g. Lignin, phenol, naphthalene and dibutylnaphthalenesulfonic acid, as well as fatty acids, alkyl and alkylarylsulfonates, alkyl, lauryl ether and fatty alcohol sulfates, as well as salts of sulfated hexa-, hepta- and octadecanols and fatty alcohol glycol ethers, condensation products of sulfonated naphthalene and its derivatives with formaldehyde, condensation products of naphthalene or naphthalenesulfonic acids with phenol and formaldehyde, polyoxyethyl noctylphenol ether, ethoxylated isooctyl, octyl or nonylphenol, alkylphen
- Powders, dispersants and dusts may be prepared by mixing or co-grinding the active substances with a solid carrier.
- Granules for example coated, impregnated and homogeneous granules, can be prepared by binding the active compounds to solid carriers.
- Solid carriers are mineral soils such as silicic acids, silica gels, silicates, talc, kaolin, limestone, lime, chalk, bolus, loess, clay, dolomite, diatomaceous earth, calcium and magnesium sulfate, magnesium oxide, ground plastics, fertilizers such as ammonium sulfate, ammonium phosphate, ammonium nitrate, Ureas and vegetable products such as cereal flour, tree bark, wood and nutshell flour, cellulose powder or other solid carriers.
- mineral soils such as silicic acids, silica gels, silicates, talc, kaolin, limestone, lime, chalk, bolus, loess, clay, dolomite, diatomaceous earth, calcium and magnesium sulfate, magnesium oxide, ground plastics, fertilizers such as ammonium sulfate, ammonium phosphate, ammonium nitrate, Ureas and vegetable products such as cereal flour, tree bark, wood and nutshell flour
- the concentrations of the compounds of the formula I in the ready-to-use formulations can be varied within wide limits.
- the formulations contain from about 0.001 to 98 wt .-%, preferably 0.01 to 95 wt .-%, of at least one active ingredient.
- the active ingredients are used in a purity of 90% to 100%, preferably 95% to 100% (according to NMR spectrum).
- an active compound of the formula I 20 parts by weight of an active compound of the formula I are well mixed with 3 parts by weight of the sodium salt of diisobutylnaphthalenesulfonic acid, 17 parts by weight of the sodium salt of a lignosulfonic acid from a sulfite waste liquor and 60 parts by weight of powdered silica gel and ground in a hammer mill.
- the mixture By finely distributing the mixture in 20,000 parts by weight of water to obtain a spray mixture containing 0.1 wt .-% of the active ingredient of the formula I.
- the application of the compounds of the formula I or of the herbicidal compositions can be carried out in the preemergence or postemergence process. If the active ingredients are less compatible with certain crops, application techniques may be used in which the herbicidal agents are sprayed with the help of the sprayers so as not to hit the leaves of the sensitive crops as far as possible, while the active ingredients on the leaves below grow undesirable plants or the uncovered soil surface (post-directed, lay-by).
- the application rates of compound of the formula I are 0.001 to 3.0, preferably 0.01 to 1.0, kg / ha of active substance (see above).
- the heteroaroyl-substituted alanines of the formula I can be mixed with numerous representatives of other herbicidal or growth-regulating active ingredient groups and applied together.
- the culture vessels used were plastic flower pots with loamy sand with about 3.0% humus as the substrate.
- the seeds of the test plants were sown separately by species.
- the active ingredients suspended or emulsified in water were applied directly after sowing by means of finely distributing nozzles.
- the jars were lightly rained to promote germination and growth and then covered with clear plastic hoods until the plants had grown. This cover causes a uniform germination of the test plants, if it was not affected by the active ingredients.
- the test plants were grown depending on the growth form only to a stature height of 3 to 15 cm and only then treated with the suspended or emulsified in water agents.
- the test plants were either sown directly and grown in the same containers or they were first grown separately as seedlings and transplanted into the test containers a few days before the treatment.
- the application rate for postemergence treatment was 1.0 kg / ha aS (active substance).
- the plants were kept species-specific at temperatures of 10 to 25 0 C and 20 to 35 0 C.
- the trial period lasted for 2 to 4 weeks. During this time, the plants were cared for, and their response to each treatment was evaluated.
- the rating was based on a scale of 0 to 100. 100 means no emergence of the plants or complete destruction of at least the above-ground parts and 0 no damage or normal growth course.
- the plants used in the greenhouse experiments were composed of the following species:
Abstract
Description
Claims
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP07704402A EP1987008A2 (de) | 2006-02-16 | 2007-02-07 | Heteroaroylsubstituierte alanine |
| BRPI0707907-9A BRPI0707907A2 (pt) | 2006-02-16 | 2007-02-07 | composto, processo para preparação de um composto, agente, processos para a preparação de agentes, e para o combate da vegetação indesejada, e, uso de compostos |
| US12/279,425 US20090054240A1 (en) | 2006-02-16 | 2007-02-07 | Heteroaroyl-substituted Alanines |
| JP2008554733A JP2009526804A (ja) | 2006-02-16 | 2007-02-07 | ヘテロアロイル置換アラニン |
| IL192960A IL192960A0 (en) | 2006-02-16 | 2008-07-22 | Heteroaroyl-substituted alanines |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP06110017.8 | 2006-02-16 | ||
| EP06110017 | 2006-02-16 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| WO2007093529A2 true WO2007093529A2 (de) | 2007-08-23 |
| WO2007093529A3 WO2007093529A3 (de) | 2007-12-21 |
Family
ID=38371866
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/EP2007/051144 WO2007093529A2 (de) | 2006-02-16 | 2007-02-07 | Heteroaroylsubstituierte alanine |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20090054240A1 (de) |
| EP (1) | EP1987008A2 (de) |
| JP (1) | JP2009526804A (de) |
| BR (1) | BRPI0707907A2 (de) |
| IL (1) | IL192960A0 (de) |
| WO (1) | WO2007093529A2 (de) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010049405A1 (en) * | 2008-10-31 | 2010-05-06 | Basf Se | Method for improving plant health |
Families Citing this family (29)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8097712B2 (en) | 2007-11-07 | 2012-01-17 | Beelogics Inc. | Compositions for conferring tolerance to viral disease in social insects, and the use thereof |
| US8962584B2 (en) | 2009-10-14 | 2015-02-24 | Yissum Research Development Company Of The Hebrew University Of Jerusalem, Ltd. | Compositions for controlling Varroa mites in bees |
| US9121022B2 (en) | 2010-03-08 | 2015-09-01 | Monsanto Technology Llc | Method for controlling herbicide-resistant plants |
| US10829828B2 (en) | 2011-09-13 | 2020-11-10 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10806146B2 (en) | 2011-09-13 | 2020-10-20 | Monsanto Technology Llc | Methods and compositions for weed control |
| MX348495B (es) | 2011-09-13 | 2017-06-14 | Monsanto Technology Llc | Metodos y composiciones para el control de malezas. |
| AU2012308694B2 (en) | 2011-09-13 | 2018-06-14 | Monsanto Technology Llc | Methods and compositions for weed control |
| AU2012308659B2 (en) | 2011-09-13 | 2017-05-04 | Monsanto Technology Llc | Methods and compositions for weed control |
| UA116090C2 (uk) | 2011-09-13 | 2018-02-12 | Монсанто Текнолоджи Ллс | Спосіб та композиція для боротьби з бур'янами (варіанти) |
| US10760086B2 (en) | 2011-09-13 | 2020-09-01 | Monsanto Technology Llc | Methods and compositions for weed control |
| AU2012308686B2 (en) | 2011-09-13 | 2018-05-10 | Monsanto Technology Llc | Methods and compositions for weed control |
| AR091143A1 (es) | 2012-05-24 | 2015-01-14 | Seeds Ltd Ab | Composiciones y metodos para silenciar la expresion genetica |
| BR112015015975A2 (pt) | 2013-01-01 | 2018-11-06 | A. B. Seeds Ltd. | moléculas de dsrna isoladas e métodos de uso das mesmas para silenciamento das moléculas alvo de interesse. |
| US10683505B2 (en) | 2013-01-01 | 2020-06-16 | Monsanto Technology Llc | Methods of introducing dsRNA to plant seeds for modulating gene expression |
| AU2014249015B2 (en) | 2013-03-13 | 2020-04-16 | Monsanto Technology Llc | Methods and compositions for weed control |
| UY35385A (es) | 2013-03-13 | 2014-09-30 | Monsanto Technology Llc | ?métodos y composiciones para el control de malezas?. |
| US10568328B2 (en) | 2013-03-15 | 2020-02-25 | Monsanto Technology Llc | Methods and compositions for weed control |
| US9850496B2 (en) | 2013-07-19 | 2017-12-26 | Monsanto Technology Llc | Compositions and methods for controlling Leptinotarsa |
| RU2703498C2 (ru) | 2013-07-19 | 2019-10-17 | Монсанто Текнолоджи Ллс | Композиции и способы борьбы с leptinotarsa |
| AU2014341879B2 (en) | 2013-11-04 | 2020-07-23 | Beeologics, Inc. | Compositions and methods for controlling arthropod parasite and pest infestations |
| UA119253C2 (uk) | 2013-12-10 | 2019-05-27 | Біолоджикс, Інк. | Спосіб боротьби із вірусом у кліща varroa та у бджіл |
| AU2015206585A1 (en) | 2014-01-15 | 2016-07-21 | Monsanto Technology Llc | Methods and compositions for weed control using EPSPS polynucleotides |
| WO2015153339A2 (en) | 2014-04-01 | 2015-10-08 | Monsanto Technology Llc | Compositions and methods for controlling insect pests |
| AU2015280252A1 (en) | 2014-06-23 | 2017-01-12 | Monsanto Technology Llc | Compositions and methods for regulating gene expression via RNA interference |
| US11807857B2 (en) | 2014-06-25 | 2023-11-07 | Monsanto Technology Llc | Methods and compositions for delivering nucleic acids to plant cells and regulating gene expression |
| RU2021123470A (ru) | 2014-07-29 | 2021-09-06 | Монсанто Текнолоджи Ллс | Композиции и способы борьбы с насекомыми-вредителями |
| WO2016118762A1 (en) | 2015-01-22 | 2016-07-28 | Monsanto Technology Llc | Compositions and methods for controlling leptinotarsa |
| UY36703A (es) | 2015-06-02 | 2016-12-30 | Monsanto Technology Llc | Composiciones y métodos para la administración de un polinucleótido en una planta |
| WO2016196782A1 (en) | 2015-06-03 | 2016-12-08 | Monsanto Technology Llc | Methods and compositions for introducing nucleic acids into plants |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2003045878A2 (en) * | 2001-11-29 | 2003-06-05 | Basf Aktiengesellschaft | 2,w-diaminocarboxylic acid compounds |
| WO2005061464A1 (de) * | 2003-12-19 | 2005-07-07 | Basf Aktiengesellschaft | Herbizide heteroaroyl-substituierte phenylalanin-amide |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| BRPI0417780B1 (pt) * | 2003-12-19 | 2016-03-01 | Basf Ag | composto, processo para preparar o mesmo, agente, processos para preparar o mesmo, e para combater vegetação indesejada, e, uso de um composto |
-
2007
- 2007-02-07 JP JP2008554733A patent/JP2009526804A/ja not_active Withdrawn
- 2007-02-07 EP EP07704402A patent/EP1987008A2/de not_active Withdrawn
- 2007-02-07 BR BRPI0707907-9A patent/BRPI0707907A2/pt not_active Application Discontinuation
- 2007-02-07 US US12/279,425 patent/US20090054240A1/en not_active Abandoned
- 2007-02-07 WO PCT/EP2007/051144 patent/WO2007093529A2/de active Application Filing
-
2008
- 2008-07-22 IL IL192960A patent/IL192960A0/en unknown
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2003045878A2 (en) * | 2001-11-29 | 2003-06-05 | Basf Aktiengesellschaft | 2,w-diaminocarboxylic acid compounds |
| WO2005061464A1 (de) * | 2003-12-19 | 2005-07-07 | Basf Aktiengesellschaft | Herbizide heteroaroyl-substituierte phenylalanin-amide |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010049405A1 (en) * | 2008-10-31 | 2010-05-06 | Basf Se | Method for improving plant health |
Also Published As
| Publication number | Publication date |
|---|---|
| BRPI0707907A2 (pt) | 2011-05-17 |
| EP1987008A2 (de) | 2008-11-05 |
| IL192960A0 (en) | 2009-02-11 |
| JP2009526804A (ja) | 2009-07-23 |
| WO2007093529A3 (de) | 2007-12-21 |
| US20090054240A1 (en) | 2009-02-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP2121583B1 (de) | Heteroaroylsubstituierte serin-amide | |
| EP1888509B1 (de) | Benzoylsubstituierte serin-amide | |
| US7879761B2 (en) | Heteroaroyl-substituted serineamides | |
| WO2007093529A2 (de) | Heteroaroylsubstituierte alanine | |
| EP1501361B1 (de) | 3-heteroarylsubstituierte 5-methyloxymethyl-isoxazoline als herbizide | |
| EP1987015A2 (de) | Benzoylsubstituierte alanine | |
| US20090186766A1 (en) | Heteroaroyl-Substituted Alanines with a Herbicidal Action | |
| US20090215628A1 (en) | Benzoyl-Substituted Alanines | |
| WO2008084070A1 (de) | Benzoylsubstituierte serin-amide |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 2007704402 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 192960 Country of ref document: IL |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 12279425 Country of ref document: US Ref document number: 2008554733 Country of ref document: JP |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 07704402 Country of ref document: EP Kind code of ref document: A2 |
|
| ENP | Entry into the national phase |
Ref document number: 2008136758 Country of ref document: RU Kind code of ref document: A |
|
| ENP | Entry into the national phase |
Ref document number: PI0707907 Country of ref document: BR Kind code of ref document: A2 Effective date: 20080812 |