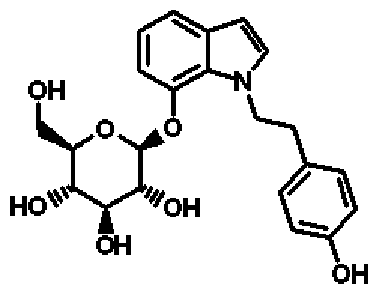
明 細 書
1—置換一 7_ ( j3 _D—グリコピラノシルォキシ)(ァザ)インドールイ匕合 物、及びそれを含有する医薬
技術分野
[0001] 本発明は、 1—置換一 7— ( β—D グリコピラノシルォキシ)(ァザ)インドールイ匕合 物に関するものである。さらに詳しく述べれば、本発明は、糖尿病、耐糖能異常、糖 尿病性合併症又は肥満症等の高血糖症に起因する疾患若しくは血中ガラクトース値 の上昇に起因する疾患の予防又は治療などに用いることができる 1 置換 7— ( β -D-グリコピラノシルォキシ)(ァザ)インドール化合物若しくはそのプロドラッグ又は その薬理学的に許容される塩又はその水和物若しくは溶媒和物、それを含有する医 薬、及びそれと他の医薬との組み合わせ製剤に関するものである。
背景技術
[0002] 単糖とナトリウムとの共輸送担体であるナトリウム依存性糖輸送担体 (以下「SGLT」 という。 )には幾つかのサブタイプの存在が知られている。すなわち、主として小腸や 腎臓の近位尿細管の S3領域にはナトリウム依存性グルコース輸送担体 1 (以下「SG LT1」という。)が存在し、腎臓の近位尿細管の S1領域にはナトリウム依存性ダルコ一 ス輸送担体2 (以下「SGLT2」 t 、う。)が存在して 、る。
[0003] このうち、小腸に存在する SGLT1はグルコース及びガラクトースの消化管からの吸 収に関与している(非特許文献 1及び 2参照)。糖尿病患者では糖質の消化 '吸収が 亢進し、実際、小腸における SGLT1やその mRNAの発現が亢進していることが認 められている(非特許文献 3参照)。したがって、 SGLT1を阻害すれば、小腸でのグ ルコースとガラクトースの吸収を抑えることにより、血糖値の上昇を抑制することができ る (特許文献 1参照)。
[0004] 一方、 SGLT2は糸球体ろ過されたグルコースの再吸収に関与して 、る(非特許文 献 4参照)。したがって、 SGLT2を阻害すれば、グルコースの再吸収を抑えることに より、血糖値を正常化させることができる(特許文献 5参照)。
[0005] SGLT1を阻害する化合物としては、ピラゾール誘導体 (特許文献 1及び 2参照)や
ベンジルフエノール誘導体 (特許文献 3参照)などが知られており、また SGLT2を阻 害する化合物としては、ダルコピラノシルォキシピラゾール誘導体 (特許文献 4参照) 、ダルコピラノシルォキシベンジルベンゼン誘導体 (特許文献 5参照)などが知られて いる。
[0006] 最近、グリコビラノシルォキシ基を有する縮合複素環化合物が優れた SGLT阻害作 用を示すことが報告された (特許文献 6参照)。し力しながら、この報告には、ヘテロ原 子が窒素原子である縮合複素環化合物の窒素原子上に置換基が結合した化合物 に関する記載も示唆もない。
非特許文献 1 :金井好克, 「腎と透析」, 1998年 12月,第 45卷,臨時増刊号, p. 23 2- 237
非特許文献 2 :E. Turk,外 4名, 「Nature」, 1991年 3月,第 350卷, p. 354- 356 非特許文献 3 :J. Dyer、外 4名, 「Am. J. Physiol. J , 2002年 2月,第 282卷,第 2 号, p. G241 -G248
非特許文献 4:Yoshikatsu Kanai、外 4名, 「J. Clin. Invest. J , 1994年 1月,第 93卷, p. 397-404
特許文献 1:国際公開 2004Z014932号パンフレット
特許文献 2 :国際公開 2004Z018491号パンフレット
特許文献 3:特開 2004— 196788号公報
特許文献 4:国際公開 01Z16147号パンフレット
特許文献 5:国際公開 01Z68660号パンフレット
特許文献 6 :国際公開 2004Z087727号パンフレット
発明の開示
発明が解決しょうとする課題
[0007] 本発明は、 SGLT1及び Z又は SGLT2の阻害作用を有する化合物を提供するこ とを課題とする。
課題を解決するための手段
[0008] 本発明者らは、 SGLT1及び Z又は SGLT2の阻害作用を有する化合物について 鋭意検討した結果、下記一般式 (I)で表される 1 置換 7 ( D—グリコピラノ
シルォキシ)(ァザ)インドールイ匕合物力 優れた SGLT1及び Z又は SGLT2阻害活 性を有することを見出し、本発明を完成させた。
[0009] すなわち、本発明の要旨は、下記一般式 (I)で表される 1 置換 7 ( D—グ リコピラノシルォキシ)(ァザ)インドール化合物若しくはそのプロドラッグ又はその薬理 学的に許容される塩、又はその水和物若しくは溶媒和物;それを含有する SGLT阻 害剤;それを含有する医薬及びそれと他の医薬との組み合わせ製剤、に存する。
[0010] [化 1]
(式中、 R1はハロゲン原子、アルキル基、ヒドロキシアルキル基、アルコキシアルキル 基、水酸基、アルコキシ基、シクロアルキルォキシ基、アミノ基、(ジ)アルキルアミノ基 、カルボキシル基又はシァノ基を表し; nは 0〜3の整数を表し; R2は水素原子、ハロ ゲン原子、アルキル基、ヒドロキシアルキル基、アルコキシアルキル基、水酸基、アル コキシ基、シクロアルキルォキシ基、アミノ基、(ジ)アルキルアミノ基、カルボキシル基 又はシァノ基を表し; Xは水素原子若しくはハロゲン原子、アルキル基、ヒドロキシァ ルキル基、アルコキシアルキル基、水酸基、アルコキシ基、シクロアルキルォキシ基、 アミノ基、(ジ)アルキルアミノ基、カルボキシル基及びシァノ基よりなる群力 選択さ れた基が結合した炭素原子又は窒素原子を表し; Qは鎖中に酸素原子又は硫黄原 子を有していてもよいアルキレン基又はァルケ-レン基を表し; Aは置換基を有して いてもよいァリール基又はへテロアリール基を表す。 )
発明の効果
[0011] 本発明に係る 1—置換一 7— ( β—D—グリコピラノシルォキシ)(ァザ)インドールイ匕 合物 (I)若しくはそのプロドラッグ又はその薬理学的に許容される塩又はその水和物 若しくは溶媒和物は、優れた SGLT1及び Ζ又は SGLT2阻害活性を有するので、 血糖値の上昇を抑制し、及び Ζ又は血中ガラクトース値を低下させ、また血糖値を正 常ィ匕することができる。
発明を実施するための最良の形態
本明細書における用語の意味は次のとおりである。
「(ァザ)インドール化合物」とは、環内に他の窒素原子を含んで 、てもよ 、インドー ル化合物であり、具体的にはインドールイ匕合物又はべンズイミダゾールイ匕合物を意 味する。
「ハロゲン」とは、フッ素、塩素、臭素又はヨウ素である。
「アルキル」とは、炭素数 1〜6の分岐して 、てもよ 、低級アルキルを意味する。 「シクロアルキル」とは、 3〜7員のシクロアルキルを意味する。
「ァルケ-ル」とは、炭素数 2〜6の分岐して 、てもよ 、低級ァルケ-ルを意味する。 「アルキニル」とは、炭素数 2〜6の分岐して 、てもよ 、低級アルキニルを意味する。 「アルコキシ」とは、炭素数 1〜6の分岐していてもよい低級アルコキシを意味する。 「(ジ)アルキルァミノ」とは、モノアルキルアミノ又はジアルキルアミノを意味し、ジァ ノレキノレアミノの 2個のァノレキノレは異なって!/、てもよ!/、。
「アルキレン」とは、炭素数 1〜6の分岐して 、てもよ 、低級アルキレンを意味する。 「ァルケ-レン」とは、炭素数 2〜6の分岐して 、てもよ 、低級ァルケ-レンを意味す る。
「鎖中に酸素原子又は硫黄原子を有して 、てもよ 、アルキレン基又はァルケ-レン 基」とは、末端又は中央に酸素原子又は硫黄原子が存在してもよいアルキレン基又 はァルケ-レン基を意味する。
「ァリール」とは、フエ-ル又はナフチルを意味する。
「ヘテロァリール」とは、酸素原子、窒素原子及び硫黄原子よりなる群力も選ばれた ヘテロ原子を 1以上有する単環式又は縮合環式へテロァリールを意味する。
「(ヘテロ)ァリール」とは、ァリール又はへテロアリールを意味する。
「ヘテロシクロアルキル」とは、酸素原子、窒素原子及び硫黄原子よりなる群力も選 ばれたヘテロ原子を 1以上有する 3〜7員環へテロシクロアルキルを意味する。
「(ヘテロ)シクロアルキル」とは、シクロアルキル又はへテロシクロアルキルを意味す る。
「脂環式ァミン」とは、ヘテロ原子が窒素原子であるへテロシクロアルキルを意味す
る。
「ァシル」とは、炭素数 2〜7の分岐していてもよい脂肪族カルボン酸ァシル、(へテ 口)シクロアルキルカルボン酸ァシル又は(ヘテロ)ァリールカルボン酸ァシルを意味 する。
[0013] 一般式 (I)にお 、て、グリコビラノシル基としては、ダルコビラノシル基又はガラクトビ ラノシル基、特にダルコビラノシル基が好まし 、。
R1としては、ハロゲン原子、アルキル基又は水酸基が好ましい。なお、 nが 2又は 3 のとき、複数の R1は異なっていてもよい。
nとしては、 0が好ましい。
R2としては、水素原子、ハロゲン原子、アルキル基又はヒドロキシアルキル基、特に 水素原子が好ましい。
Xとしては、水素原子が結合した炭素原子が好ましい。
Qとしては、アルキレン基、特にメチレン基又はエチレン基が好ましい。
Aとしては、置換基を有して!/、てもよ 、フエ-ル基が好ま U、。
[0014] (ヘテロ)ァリール基が有していてもよい置換基としては、例えば、ハロゲン原子、水 酸基及びシァノ基;それぞれがさらに置換基 α (後述する。以下同じ。)を有していて もよいアルキル基、ァルケ-ル基、アルキ-ル基、アルコキシ基、アルキルチオ基、ァ ルキルスルフィ -ル基及びアルキルスルホ-ル基;それぞれがさらに置換基 aを有し ていてもよぐかつアルキレン基、— O—、—NH—又は— S—を介して置換する(へ テロ)ァリール基と結合して 、てもよ 、他の(ヘテロ)ァリール基又は(ヘテロ)シクロア ルキル基;— U— V— W— N (RA)— Y— Z基並びに— U— V— COO— Y— RB基等 が挙げられる。なお、(ヘテロ)ァリール基が有する置換基が複数の場合、それらは異 なっていてもよい。
[0015] — U— V— W— N (RA)— Y— Z基又は一 U— V— COO— Y— RB基中の Uは、単 結合、— O—又は— S—を表す。
Vは、単結合、それぞれが水酸基を有していてもよいアルキレン基又はァルケ-レ ン基を表す。
Wは、単結合、— CO—、—SO—又は— C ( = NH)—を表す。
RAは、水素原子又はそれぞれが置換基 aを有して 、てもよ 、アルキル基、(ヘテロ )ァリール基若しくは(ヘテロ)シクロアルキル基を表す。
Yは、単結合又はォキソ基を有して 、てもよ 、アルキレン基を表す。
[0016] Zは、水素原子;ホルミル基;それぞれが置換基 aを有して!/ヽてもよ ヽアルキル基、
(ヘテロ)ァリール基又は(ヘテロ)シクロアルキル基;置換基 aを有して!/、てもよ!/ヽァ シル基;それぞれが置換基 aを有して 、てもよ 、アルコキシ又はァリールアルコキシ カルボ-ル基;— CON (RK) (RL)ゝ— CSN (RK) (RL)ゝ—SO N (RK) (RL)又は— C
2
( = NRK) N (RL) (RM)基; 1〜3のアミノ酸残基 [末端のカルボキシル基は水酸基、ァ ルコキシ基、アミノ基若しくは(ジ)アルキルアミノ基を有して 、てもよ 、アルコキシカル ボニル基;それぞれ水酸基、アルコキシ基、アミノ基若しくは (ジ)アルキルアミノ基を 有していてもよいアルキル基、(ヘテロ)シクロアルキル基、アルコキシカルボ-ル基 又はァシル基を有することがある脂環式ァミン又はアルキルァミンのアミド;カルボキ サミド基でもよい。 ];それぞれ水酸基、アルコキシ基、アミノ基若しくは (ジ)アルキル アミノ基を有していてもよいアルキル基、(ヘテロ)シクロアルキル基、アルコキシカル ボニル基又はァシル基を有することがある脂環式ァミンを有する脂肪族、(ヘテロ)シ クロアルキル又は(ヘテロ)ァリールカルボン酸残基を表す。なお、「1〜3のアミノ酸 残基」とは、アミノ酸、ジペプチド又はトリペプチドの N末端力 と結合している基を意 味し、「脂環式ァミンを有する脂肪族、(ヘテロ)シクロアルキル又は(ヘテロ)ァリール カルボン酸残基」とは、脂環式ァミンを有するァシル基を意味する(以下同じ。 ) o
[0017] RK、 RL及び RMは、独立して、水素原子、ニトロ基、シァノ基、スルファモイル基、ァ シル基、アルコキシカルボ-ル基、ァリール基、アルキルスルホ -ル基又は置換基 α を有して!/、てもよ 、アルキル基を表す。
また、窒素原子に結合した RAと Ζを構成する基の一部とが結合して、置換基 αを有 して!/、てもよ!/、脂環式ァミンを形成してもよ!/、。
[0018] RBは、水素原子;カルボキシル基又はアルコキシカルボ-ル基を有するアルコキシ アルキル基;それぞれが置換基 aを有して!/、てもよ 、アルキル基、(ヘテロ)ァリール 基又は(ヘテロ)シクロアルキル基; 1〜3のアミノ酸 [末端のカルボキシル基は水酸基 、アルコキシ基、アミノ基若しくは(ジ)アルキルアミノ基を有していてもよいアルコキシ
カルボニル基;それぞれ水酸基、アルコキシ基、アミノ基若しくは(ジ)アルキルアミノ 基を有していてもよいアルキル基、(ヘテロ)シクロアルキル基、アルコキシカルボ-ル 基又はァシル基を有することがある脂環式ァミン又はアルキルァミンのアミド;力ルバ モイル基でもよい。 ];それぞれ水酸基、アルコキシ基、アミノ基若しくは(ジ)アルキル アミノ基を有していてもよいアルキル基、(ヘテロ)シクロアルキル基、アルコキシカル ボニル基又はァシル基を有することがある脂環式ァミンを有する脂肪族、(ヘテロ)シ クロアルキル又は(ヘテロ)ァリールカルボン酸残基を表す。
[0019] 脂環式ァミンとしては、例えば、ピロリジン、ピぺリジン、ピぺラジン、モルホリン等が 挙げられる。
アミノ酸は、天然アミノ酸、合成アミノ酸のいずれでもよい。合成アミノ酸としては、例 えば、 2—メチルァラニン等のホモアミノ酸、ノルパリン等のノルアミノ酸などが挙げら れる。
なお、 Uがー O 又は S のとき、 V及び Wは同時に単結合とはならない。
[0020] 置換基 αは、ハロゲン原子、アルキル基、ヒドロキシアルキル基、アルコキシアルキ ル基、水酸基、アルコキシ基、アミノ基、(ジ)アルキルアミノ基、シァノ基、カルボキシ ル基、力ルバモイル基、アルコキシカルボ-ル基、ヒドロキシアルコキシカルボ-ル基 、(ヘテロ)ァリール及び (ヘテロ)シクロアルキル基よりなる群カゝら選択された基であり 、これらの基が同一又は異なって複数置換して 、てもよ 、。
[0021] 本発明に係る一般式 (I)で表される 1—置換一 7— ( β—D グリコビラノシルォキ シ)(ァザ)インドールイ匕合物の製造方法の一例を以下に示す。
[0022] [化 2]
5 ( I )
[0023] (式中、
n、 R
2、 X、 Q及び Aは前記と同義であり、 Pは水酸基の保護基を表し、 L 及び! は、独立して、脱離基を表す。 )
[0024] 7 ヒドロキシ (ァザ)インドールイ匕合物 (1)を水酸基が保護された D—グリコビラノシ ル化合物 (2)により配糖ィ匕して 7— ( β—D グリコピラノシルォキシ)(ァザ)インドー ル化合物( )とし、これを (ヘテロ)ァリールアルキル化して 1—置換— 7— ( j8—D— グリコピラノシルォキシ)(ァザ)インドールイ匕合物 ( )とした後、水酸基の保護基を除 去することにより 1—置換一 7— ( D—グリコピラノシルォキシ)(ァザ)インドール 化合物 (I)を製造することができる。
[0025] D—グリコビラノシル化合物 (2)の水酸基の保護基 Pや脱離基 Lには、糖化学の分 野において慣用されているものを用いることができる。このような保護基としては、例 えば、ァセチル基、ビバロイル基等が挙げられる。また、脱離基としては、例えば、臭 素原子、トリクロロアセトイミドイルォキシ基等が挙げられる。
[0026] (ヘテロ)ァリールアルキル化剤 (4)の脱離基! としては、例えば、塩素原子、臭素 原子、メシルォキシ基及びトシルォキシ基等が挙げられる。
[0027] 配糖ィ匕は、脱離基 Lが臭素原子の場合には、炭酸ナトリウム、炭酸カリウム、炭酸セ シゥム、水酸化ナトリウム、水酸ィ匕カリウム又は水素化ナトリウム等の塩基の存在下で 行うのが好ましい。このとき、ベンジルトリブチルアンモ -ゥムクロリド、ベンジルトリブ チルアンモ-ゥムブロミド又はテトラプチルアンモ -ゥム硫酸水素塩等の相間移動触 媒を添加するのが、さらに好ましい。また、脱離基 Lがトリクロロアセトイミドイルォキシ
基の場合には、三フッ化ホウ素'ジェチルエーテル錯体、トリフルォロメタンスルホン 酸トリメチルシリル、四塩ィ匕すず等のルイス酸の存在下で配糖ィ匕するのが好ま 、。
[0028] (ヘテロ)ァリールアルキルィ匕は、水素化ナトリウム、炭酸カリウム、炭酸セシウム、カリ ゥム t—ブトキシド等の塩基の存在下で行うのが好ましい。所望の場合、ヨウ化ナトリウ ムを添カ卩してもよい。
[0029] 水酸基の保護基としてァセチル基又はビバロイル基を用いた場合には、水酸ィ匕ナト リウム、水酸化リチウム、ナトリウムメトキシド又はナトリウムエトキシド等を用いた通常の アルカリ加水分解により除去することができる。
[0030] 1—置換一 7— ( β—D—グリコピラノシルォキシ)(ァザ)インドールイ匕合物 (I)はま た、 7—ヒドロキシ(ァザ)インドール化合物 (丄)の 7位水酸基をベンジル基又はべンズ ヒドリル基等の(置換)ベンジル基で保護した後、上述した (ヘテロ)ァリールアルキル ィ匕、配糖化、脱保護の各工程を経ることによつても製造することができる。なお、(置 換)ベンジル基は、加水素分解や加水分解等の常法に従い、除去することができる。
[0031] 7 ヒドロキシ (ァザ)インドールイ匕合物 (1)や、その 7位水酸基をベンジル基等で保 護した化合物は、市販されているか、又は公知の方法(例えば、 Synthetic Communic ations, Vol.2丄, No.5, pp.611— 617, 1991; Syntheticし ommunications, Vol.33, No.3, p p.507-514, 2003; Heterocycles, Vol.38, No.l l, pp.2415— 2442, 1994; Tetrahedron L etters, Vol.46, pp.1021-1022, 2005等)に準じて製造することができる。
[0032] また、 Xが窒素原子であり、 R2が水素原子である 7— ( β—D グリコビラノシルォキ シ)(ァザ)インドールイ匕合物 ( )、すなわち 7— ( D—グリコピラノシルォキシ)ベ ンズイミダゾール化合物 (al)は、以下に示す方法により製造することができる。
[0033] [化 3]
[0034] (式中、
n、 L及び Pは前記と同義である。 )
すなわち、 2-ァミノ 3 ニトロフエノールイ匕合物 ( )を配糖ィ匕して o ニトロァ-リン
配糖体 (7)とし、この-トロ基を還元して得られる o -フエ-レンジアミン配糖体 (8)を 、オルトギ酸トリメチル等のオルトギ酸エステルと反応させることにより、環化させて 7— ( β—D—グリコピラノシルォキシ)ベンズイミダゾール化合物 ( )を製造することが できる。
[0035] (ヘテロ)ァリールアルキル化剤 (4)は、市販されて!、るものを用いる力、容易に入手 することができる(ヘテロ)ァリールイ匕合物に対して、慣用されているハロゲン化、アミ ノ化、ニトロ化、スルホン化、ジァゾ化、チオール化、エステル化、アミドィ匕、酸化、還 元、脱水縮合、加水分解、カップリング等の反応を適宜組み合わせて行うことにより 調製することができる(例えば、国際公開 2004Z014932号パンフレット及び同 200 4Z018491号パンフレット参照)。また、上述した製造方法で用いる化合物又は生 成する化合物が反応条件で変化したり、反応の進行を阻害する官能基を有するとき には、これを当業者が慣用する適当な保護基を用いて保護し、適当な段階で保護基 を除去すればよい。
[0036] 本発明に係る一般式 (I)で表される 1—置換一 7— ( β—D—グリコビラノシルォキ シ)(ァザ)インドールイ匕合物は、常法により塩ィ匕ェチル又は塩ィ匕べンジル等のハロゲ ン化アルキル;塩化ァセチル又は塩化ベンゾィル等のハロゲン化ァシル;塩化ギ酸ェ チル又は塩化ギ酸べンジル等のハロゲン化ギ酸エステルなどのプロドラッグ化試薬 を反応させることにより、そのカルボキシル基、水酸基及び/又はァミノ基が変換した プロドラッグとすることができる。
[0037] 一般式 (I)で表される 1—置換一 7— ( β—D—グリコピラノシルォキシ)(ァザ)インド 一ルイ匕合物又はそのプロドラッグは、常法により、その薬理学的に許容される塩とす ることができる。このような塩としては、例えば、塩酸及び硝酸等の無機酸塩;酢酸及 びメタンスルホン酸等の有機酸塩、並びにナトリウム塩及びカリウム塩; Ν, N'—ジべ ンジルエチレンジァミン及び 2—アミノエタノール等の有機塩基との付加塩が挙げら れる。
[0038] 一般式 (I)で表される 1—置換— 7— ( β—D—グリコピラノシルォキシ)(ァザ)インド 一ルイ匕合物又はそのプロドラッグは、その精製又は造塩過程において、水和物又は 溶媒和物として得られることがある。本発明に係る医薬には、 1—置換— 7— ( — D
—グリコピラノシルォキシ)(ァザ)インドールイ匕合物若しくはそのプロドラッグ又はその 薬理学的に許容される塩、又はその水和物若しくは溶媒和物のいずれも用いること ができる。
[0039] さらに、一般式 (I)で表される 1—置換一 7— ( β—D—グリコピラノシルォキシ)(ァ ザ)インドールイ匕合物又はそのプロドラッグについて、互変異性体、幾何異性体及び Ζ又は光学異性体が存在することがある力 本発明に係る医薬には、そのいずれの 異性体も用いることができ、またその混合物も用いることができる。
[0040] 本発明に係る医薬は、 1—置換一 7— ( β—D—グリコピラノシルォキシ)(ァザ)イン ドール化合物 (I)若しくはそのプロドラッグ又はその薬理学的に許容される塩、又は その水和物若しくは溶媒和物と慣用されている製剤担体とを混合することにより製造 することができる。
[0041] 製剤担体は、後述する投与形態に応じて、適宜、組み合わせて用いればよぐ例え ば、乳糖等の賦形剤;ステアリン酸マグネシウム等の滑沢剤;カルボキシメチルセル口 ース等の崩壊剤;ヒドロキシプロピルメチルセルロース等の結合剤;マクロゴール等の 界面活性剤;炭酸水素ナトリウム等の発泡剤;シクロデキストリン等の溶解補助剤;ク ェン酸等の酸味剤;ェデト酸ナトリウム等の安定化剤;リン酸塩等の ρΗ調整剤などが 挙げられる。
[0042] 本発明に係る医薬の投与形態としては、例えば、散剤、顆粒剤、細粒剤、ドライシ口 ップ剤、錠剤、カプセル剤等の経口投与剤;注射剤、貼付剤、坐剤等の非経口投与 剤などが挙げられる。
[0043] 一般式 (I)で表される 1—置換一 7— ( β—D—グリコピラノシルォキシ)(ァザ)インド 一ルイ匕合物は、ヒト SGLT1及び SGLT2活性阻害作用確認試験において、強力なヒ ト SGLT1及び Ζ又は SGLT2活性阻害作用を示すので、グルコース又はガラクトー スの吸収を抑制することにより食後血糖値の上昇を抑制し、及び Ζ又は血中ガラタト 一ス値を低下させ、又はグルコースの再吸収を抑制することにより血糖値を正常化さ せることができる。したがって、本発明に係る医薬は、食後高血糖抑制薬として、又は 糖尿病、耐糖能異常、糖尿病性合併症 (例えば、網膜症、神経障害、腎症、潰瘍、 大血管症)、肥満症、高インスリン血症、ガラクトース血症、高脂血症、高コレステロ一
ル血症、高トリグリセリド血症、脂質代謝異常、ァテローム性動脈硬化症、高血圧、メ タボリック症候群、うつ血性心不全、浮腫、高尿酸血症及び痛風よりなる群力 選択さ れる疾患の予防薬又は治療薬として、さらに耐糖能異常から糖尿病への移行を予防 するために用いることができる。
[0044] 上記の予防薬又は治療薬の製造にあたっては、本発明に係る一般式 (I)で表され る 1—置換一 7— ( D グリコピラノシルォキシ)(ァザ)インドールイ匕合物若しくは その薬理学的に許容される塩又はそれらの水和物若しくは溶媒和物力 成人 i日当 たり、経口投与剤では 0. 1〜: LOOOmg、注射剤では 0. 01〜: LOOmgの範囲で投与 されるような製剤とするのが好ましい。
[0045] また、本発明に係る医薬は、他の医薬と組み合わせて用いることができる。このよう な他の医薬としては、例えば、インスリン感受性増強薬、アミラーゼ阻害薬、 α ダル コシダーゼ阻害薬、ビグアナイド薬、インスリン分泌促進薬、インスリン又はインスリン 類縁体、グルカゴン受容体アンタゴ-スト、インスリン受容体キナーゼ刺激薬、トリべ プチジルぺプチダーゼ II阻害薬、ジぺプチジルぺプチダーゼ IV阻害薬、プロテイン チロシンホスファターゼー 1B阻害薬、グリコゲンホスホリラーゼ阻害薬、グルコース 6—ホスファターゼ阻害薬、フルクトース一ビスホスファターゼ阻害薬、ピルビン酸デヒ ドロゲナーゼ阻害薬、肝糖新生阻害薬、 D—カイロイノシトール (D- chiroinositol)、グ リコゲン合成酵素キナーゼ 3阻害薬、 11 j8—ヒドロキシステロイドデヒドロゲナーゼ 阻害薬、グルカゴン様ペプチド 1、グルカゴン様ペプチド 1類縁体、グルカゴン様 ペプチド 1ァゴ-スト、アミリン、アミリン類縁体、アミリンァゴ-スト、アルドース還元 酵素阻害薬、終末糖化産物(advanced glycation endproducts)生成阻害薬、プロティ ンキナーゼ C阻害薬、 γ—ァミノ酪酸受容体アンタゴ-スト、ナトリウムチャンネルアン タゴニスト、転写因子 NF κ Β阻害薬、脂質過酸化酵素阻害薬、 Ν ァセチル化ー α リンクト アシッド シへ °チダー IT (N— acetylated— a—linked— acid— dipeptidase) 阻害薬、インスリン様成長因子 I、血小板由来成長因子 (PDGF)、血小板由来成 長因子(PDGF)類縁体(例えば、 PDGF—AA、 PDGF— BB、 PDGF—AB)、上 皮増殖因子 (EGF)、神経成長因子、カル-チン誘導体、ゥリジン、 5 ヒドロキシー 1 —メチルヒダントイン、 EGB— 761、ビモクロモル(bimoclomol)、スロデキシド(sulodex
ide)、 Y—128、止瀉薬、瀉下薬、ヒドロキシメチルダルタリルコェンザィム Α還元酵素 阻害薬、フイブラート系化合物、 13 アドレナリン受容体ァゴ-スト、ァシルコェンザ
3
ィム A:コレステロールァシル基転移酵素阻害薬、プロブコール、甲状腺ホルモン受 容体ァゴ-スト、コレステロール吸収阻害薬、リパーゼ阻害薬、ミクロソームトリグリセリ ドトランスファープロテイン阻害薬、リポキシゲナーゼ阻害薬、カル-チンパルミトイル トランスフェラーゼ阻害薬、スクアレン合成酵素阻害薬、スクアレンエポキシダーゼ阻 害薬、低比重リポ蛋白受容体増強薬、ニコチン酸誘導体、胆汁酸吸着薬、ナトリウム 共役胆汁酸トランスポーター阻害薬、コレステロールエステル転送タンパク阻害薬、 食欲抑制薬、アンジォテンシン変換酵素阻害薬、中性エンドべプチダーゼ阻害薬、 アンジォテンシン II受容体拮抗薬、エンドセリン変換酵素阻害薬、エンドセリン受容体 アンタゴニスト、利尿薬、カルシウム拮抗薬、血管拡張性降圧薬、交換神経遮断薬、 中枢性降圧薬、 a アドレナリン受容体ァゴニスト、抗血小板薬、尿酸生成阻害薬、
2
尿酸排泄促進薬、尿アルカリ化薬等が挙げられる。
インスリン感受性増強薬としては、例えば、トログリタゾン、塩酸ピオグリタゾン、マレ イン酸ロシグリタゾン、ダルグリタゾンナトリウム、 GI— 262570、ィサグリタゾン(isaglit azon 、 LG— 100641、 NC— 2100、 T— 174、 DRF— 2189、 CLX— 0921、 CS 01 1、 GW— 1929、シグリタゾン、エングリタゾンナトリウム、 NIP— 221等のペルォ キシソーム増殖薬活性化受容体 γァゴ-スト、 GW— 9578、 ΒΜ— 170744等のぺ ルォキシソーム増殖薬活性化受容体 αァゴ-スト、 GW— 409544、 KRP— 297、 Ν Ν— 622、 CLX— 0940、 LR— 90、 SB— 219994、 DRF— 4158、 DRF— MDX8 等のペルォキシソーム増殖薬活性化受容体 α / Ίァゴ-スト、 ALRT— 268、 AGN —4204、 MX— 6054、 AGN— 194204、 LG— 100754、ベクサ口テン(bexarote ne)等のレチノイド X受容体ァゴ-スト、及びレグリキサン、 ONO— 5816、 MBX—1 02、 CRE— 1625、 FK— 614、 CLX— 0901、 CRE— 1633、丽— 2344、 BM— 13125、 BM— 501050、 HQL— 975、 CLX— 0900、 MBX— 668、 MBX— 675 、 S— 15261、 GW— 544、 AZ— 242、 LY— 510929、 AR— H049020、 GW— 5 01516等のその他のインスリン感受性増強薬が挙げられる。インスリン感受性増強薬 は、糖尿病、耐糖能異常、糖尿病性合併症、肥満症、高インスリン血症、高脂血症、
高コレステロール血症、高トリグリセリド血症、脂質代謝異常、ァテローム性動脈硬化 症の予防又は治療、特に、末梢におけるインスリン刺激伝達機構の異常を改善する ことにより血中グルコースの組織への取り込みを亢進し血糖値を低下させることから、 糖尿病、耐糖能異常、高インスリン血症の予防又は治療に好ましい。
[0047] アミラーゼ阻害剤としては、例えば、 RSH— 2083等が挙げられる。
a—ダルコシダーゼ阻害薬としては、例えば、ァカルボース、ボグリボース、ミグリト 一ノレ、 CKD— 711、ェミグ!;テート、 — 25, 637、力ミグジボース、 MDL- 73, 945等の a—ダルコシダーゼ阻害薬、 AZM— 127等が挙げられる。
アミラーゼ阻害剤や α—ダルコシダーゼ阻害薬は、糖尿病、耐糖能異常、糖尿病 性合併症、肥満症、高インスリン血症の予防又は治療に好ましい。食物中に含まれる 炭水化物の消化管における酵素消化を阻害し、体内へのグルコース等の吸収を遅 延又は阻害することから、耐糖能異常の予防又は治療に用いるの力 特に好ましい。
[0048] ビグアナイド薬としては、例えば、フェンホルミン、塩酸ブホルミン、塩酸メトホルミン 等が挙げられる。ビグアナイド薬は、糖尿病、耐糖能異常、糖尿病性合併症、高イン スリン血症の予防又は治療、特に、肝臓における糖新生抑制作用や組織での嫌気 的解糖促進作用又は末梢におけるインスリン抵抗性改善作用などにより血糖値を低 下させることから、糖尿病、耐糖能異常、高インスリン血症の予防又は治療に好まし い。
[0049] インスリン分泌促進薬としては、例えば、トルプタミド、クロルプロパミド、トラザミド、ァ セトへキサミド、グリクロビラミド、グリブリド (ダリベンクラミド)、ダリクラジド、 1—ブチル —3—メタ-リルゥレア、カルプタミド、ダリボルヌリド、グリピジド、グリキドン、ダリソキセ ピド、グリブチアゾール、ダリブゾール、ダリへキサミド、グリミジンナトリウム、グリピナミ ド、フェンブタミド、トルシクラミド、グリメピリド、ナテグリニド、ミチグリニドカルシウム水 和物、レパグリニド等が挙げられ、また RO— 28— 1675等のダルコキナーゼ活性ィ匕 薬も含まれる。インスリン分泌促進薬は、糖尿病、耐糖能異常、糖尿病性合併症の予 防又は治療、特に、脾臓 )8細胞に作用しインスリン分泌を増カロさせることにより血糖 値を低下させることから、糖尿病、耐糖能異常の予防又は治療に好ましい。
[0050] インスリン又はインスリン類縁体としては、ヒトインスリン、動物由来のインスリン、ヒト
又は動物由来のインスリン類縁体が挙げられる。これらの薬剤は、糖尿病、耐糖能異 常、糖尿病性合併症の予防又は治療、特に、糖尿病、耐糖能異常の予防又は治療 に好ましい。
[0051] グルカゴン受容体アンタゴ-ストとしては、例えば、 BAY— 27— 9955、 NNC— 92
— 1687等が挙げられる。インスリン受容体キナーゼ刺激薬としては、例えば、 TER
— 17411、 L— 783281、 KRX— 613等カ挙げられる。トリべプチジルぺプチダーゼ Π阻害薬としては、例えば、 UCL— 1397等が挙げられる。ジぺプチジルぺプチダー ゼ IV阻害薬としては、例えば、 NVP-DPP728A, LAF237, TSL— 225、 P— 32 Z98、 MK— 0431等が挙げられる。プロテインチロシンホスファターゼ— 1B阻害薬 としては、例えば、 PTP— 112、 OC— 86839、 PNU— 177496等が挙げられる。グ リコゲンホスホリラーゼ阻害薬としては、例えば、 NN-4201,イングリフオリブ等が挙 げられる。フルクトース一ビスホスファターゼ阻害薬としては、例えば、 CS— 917等が 挙げられる。ピルビン酸デヒドロゲナーゼ阻害薬としては、例えば、 AZD— 7545等 が挙げられる。肝糖新生阻害薬としては、例えば、 FR— 225659等が挙げられる。 1 1 βーヒドロキシステロイドデヒドロゲナーゼ阻害薬としては、例えば、 BVT— 3498、 ΗΜ— 2002等が挙げられる。グルカゴン様ペプチド— 1類縁体としては、例えば、ェ キセンジン— 4 (exendin- 4)、 CJC— 1131等が挙げられる。グルカゴン様ペプチド— 1ァゴ-ストとしては、例えば、 AZM— 134、 LY— 315902力 S挙げられる。アミリン、 アミリン類縁体又はアミリンァゴニストとしては、例えば、酢酸プラムリンチド等が挙げ られる。これらの薬剤、グルコース一 6—ホスファターゼ阻害薬、 D—カイロイノシトー ル、グリコゲン合成酵素キナーゼ 3阻害薬及びグルカゴン様ペプチド 1類縁体は 、糖尿病、耐糖能異常、糖尿病性合併症、高インスリン血症の予防又は治療、特に、 糖尿病、耐糖能異常の予防又は治療に好ましい。
[0052] アルドース還元酵素阻害薬としては、例えば、ガモレン酸ァスコルビル、トルレスタツ ト、エノ レレスタツト、 ADN— 138、 BAL-ARI8, ZD— 5522、 ADN— 311、 GP 1447、 IDD— 598、フィダレスタツト、ソルビニール、ポナルレスタツト(ponalrestat) 、リサレスタツト (risarestat)、ゼナレスタツト (zenarestat)、ミナノレレスタツト (minalrestat )、メトソルビニール、 AL— 1567、イミレスタツト(imirestat)、 M— 16209、 TAT、 AD
— 5467、ゾポルレスタツト、 AS— 3201、 NZ— 314、 SG— 210、 JTT— 811、リンド ルレスタツ Hlindolrestat)等が挙げられる。アルドース還元酵素阻害薬は、糖尿病性 合併症組織において認められる持続的高血糖状態におけるポリオール代謝経路の 亢進により過剰に蓄積される細胞内ソルビトール量をアルドース還元酵素を阻害する ことにより低下させることから、糖尿病性合併症の予防又は治療に好ましい。
[0053] 終末糖化産物生成阻害薬としては、例えば、ピリドキサミン、 OPB— 9195、 ALT— 946、 ALT— 711、塩酸ピマゲジン等が挙げられる。終末糖化産物生成阻害薬は、 糖尿病状態における持続的高血糖により亢進される終末糖ィ匕産物生成を阻害するこ とにより細胞障害を軽減させるため、糖尿病性合併症の予防又は治療に好ましい。
[0054] プロテインキナーゼ C阻害薬としては、例えば、 LY— 333531、ミドスタウリン等が 挙げられる。プロテインキナーゼ C阻害薬は、糖尿病状態における持続的高血糖に より認められるプロテインキナーゼ c活性の亢進を抑制するため、糖尿病性合併症の 予防又は治療に好ましい。
[0055] γーァミノ酪酸受容体アンタゴニストとしては、例えば、トピラマート等が挙げられる 。ナトリウムチャンネルアンタゴ-ストとしては、例えば、塩酸メキシレチン、オクスカル バゼピン等が挙げられる。転写因子 NF— κ Β阻害薬としては、例えば、デクスリポタ ム(dexlipotam)等が挙げられる。脂質過酸化酵素阻害薬としては、例えば、メシル酸 チリラザド等が挙げられる。 N ァセチノレ化 a リンクトーアシッドージぺプチダー ゼ阻害薬としては、例えば、 GPI— 5693等が挙げられる。カル-チン誘導体としては 、例えば、カル-チン、塩酸レバセカル-ン、塩化レボカル-チン、レボカル-チン、 ST— 261等が挙げられる。これらの薬剤、インスリン様成長因子— I、血小板由来成 長因子、血小板由来成長因子類縁体、上皮増殖因子、神経成長因子、ゥリジン、 5 —ヒドロキシ一 1—メチルヒダントイン、 EGB— 761、ビモクロモル、スロデキシド及び Y— 128は、糖尿病性合併症の予防又は治療に好ましい。
[0056] 止瀉薬又は瀉下薬としては、例えば、ポリカルボフィルカルシウム、タンニン酸アル ブミン、次硝酸ビスマス等が挙げられる。これらの薬剤は、糖尿病等に伴う下痢、便秘 等の予防又は治療に好まし 、。
[0057] ヒドロキシメチルダルタリルコェンザィム A還元酵素阻害薬としては、例えば、セリバ
スタチンナトリウム、プラバスタチンナトリウム、口パスタチン(lovastatin)、シンバスタチ ン、フルパスタチンナトリウム、アトルバスタチンカルシウム水和物、 SC— 45355、 SQ — 33600、 CP— 83101、 BB— 476、 L— 669262、 S— 2468、 DMP— 565、 U— 20685、 BAY-x- 2678, BAY- 10- 2987,ピタノ ス夕チン^ノレシクム、 Pスノ スタチンカルシウム、コレストロン(colestolone)、ダルパスタチン(dalvastatin)、ァシテ メート、メパスタチン、クリルパスタチン(crilvastatin)、: BMS— 180431、 BMY— 219 50、グレンパスタチン、カルパスタチン、 BMY— 22089、ベルパスタチン(bervastati n)等が挙げられる。ヒドロキシメチルダルタリルコェンザィム A還元酵素阻害薬は、高 脂血症、高コレステロール血症、高トリグリセリド血症、脂質代謝異常、ァテローム性 動脈硬化症の予防又は治療、特に、ヒドロキシメチルダルタリルコェンザィム A還元 酵素を阻害することにより血中コレステロールを低下させることから、高脂血症、高コ レステロール血症、ァテローム性動脈硬化症の予防又は治療に好まし 、。
[0058] フイブラート系化合物としては、例えば、ベザフイブラート、ベクロブラート、ビ -フィ ブラート、シプロフイブラート、クリノフイブラート、クロフイブラート、クロフイブラートァノレ ミニゥム、クロフイブリン酸、ェトフイブラート、フエノフイブラート、ゲムフイブ口ジル、二 コフイブラート、ピリフイブラート、ロニフイブラート、シムフイブラート、テオフイブラート、 AHL— 157等が挙げられる。フイブラート系化合物は、高インスリン血症、高脂血症 、高コレステロール血症、高トリグリセリド血症、脂質代謝異常、ァテローム性動脈硬 化症の予防又は治療、特に、肝臓におけるリポ蛋白リパーゼの活性化や脂肪酸酸化 亢進により血中トリグリセリドを低下させることから、高脂血症、高トリグリセリド血症、ァ テローム性動脈硬化症の予防又は治療に好ましい。
[0059] β —アドレナリン受容体ァゴ-ストとしては、例えば、 BRL— 28410、 SR— 58611
3
A、 ICI— 198157、 ZD— 2079、 BMS— 194449、 BRL— 37344、 CP— 331679 、 CP— 114271、 L— 750355、 BMS— 187413、 SR— 59062A、 BMS— 21028 5、 LY— 377604、 SWR— 0342SA、 AZ— 40140、 SB— 226552、 D— 7114、 B RL— 35135、 FR— 149175、 BRL— 26830A、 CL— 316243、 AJ— 9677、 GW —427353、 N— 5984、 GW— 2696、 YM178、 KTO— 7924等力挙げられる。 β
3 アドレナリン受容体ァゴニストは、肥満症、高インスリン血症、高脂血症、高コレステ
ロール血症、高トリグリセリド血症、脂質代謝異常の予防又は治療、特に、脂肪にお ける 13 アドレナリン受容体を刺激し脂肪酸酸化の亢進によりエネルギーを消費さ
3
せることから、肥満症、高インスリン血症の予防又は治療に好ましい。
[0060] ァシルコェンザィム A:コレステロールァシル基転移酵素阻害薬としては、例えば、 NTE— 122、 MCC— 147、 PD— 132301— 2、 DUP— 129、 U— 73482、 U— 76 807、 RP— 70676、 P— 06139、 CP— 113818、 RP— 73163、 FR— 129169、 F Y— 038、 EAB— 309、 KY— 455、 LS— 3115、 FR— 145237、 T— 2591、 J— 10 4127、 R— 755、 FCE— 28654、 YIC— C8— 434、アバシミブ(avasimibe)、 CI— 9 76、 RP— 64477、 F— 1394、エルダシミブ(eldacimibe)、 CS— 505、 CL— 28354 6、 YM— 17E、レシミビデ(lecimibide)、 447C88、 YM— 750、 E— 5324、 KW— 3 033、 HL— 004、エフルシミブ(eflucimibe)等が挙げられる。ァシルコェンザィム A: コレステロールァシル基転移酵素阻害薬は、高脂血症、高コレステロール血症、高ト リグリセリド血症、脂質代謝異常の予防又は治療、特に、ァシルコェンザィム A:コレス テロールァシル基転移酵素を阻害することにより血中コレステロールを低下させること から、高脂血症、高コレステロール血症の予防又は治療に好ましい。
[0061] 甲状腺ホルモン受容体ァゴニストとしては、例えば、リオチロニンナトリウム、レボチ ロキシンナトリウム、 KB— 2611等が挙げられる。コレステロール吸収阻害薬としては 、例えば、ェゼチミブ、 SCH— 48461等が挙げられる。リパーゼ阻害薬としては、例 えば、オルリスタツト、 ATL— 962、 AZM— 131、 RED— 103004等が挙げられる。 カル-チンパルミトイルトランスフェラーゼ阻害薬としては、例えば、エトモキシル等が 挙げられる。スクアレン合成酵素阻害薬としては、例えば、 SDZ— 268— 198、 BMS — 188494、 A— 87049、 RPR— 101821、 ZD— 9720、 RPR— 107393、 ER— 2 7856、 TAK— 475等が挙げられる。ニコチン酸誘導体としては、例えば、ニコチン 酸、ニコチン酸アミド、ニコモール、 -セリトロール、ァシピモクス、ニコランジル等が挙 げられる。胆汁酸吸着薬としては、コレスチラミン、コレスチラン、塩酸コレセベラム、 G T— 102— 279等が挙げられる。ナトリウム共役胆汁酸トランスポーター阻害薬として は、例えば、 264W94, S— 8921、 SD— 5613等力挙げられる。コレステロールエス テル転送タンパク阻害薬としては、例えば、 PNU— 107368E、 SC— 795、JTT— 7
05、 CP— 529414等が挙げられる。これらの薬剤、プロブコール、ミクロソームトリグリ セリドトランスファープロテイン阻害薬、リポキシゲナーゼ阻害薬、スクアレンエポキシ ダーゼ阻害薬及び低比重リポ蛋白受容体増強薬は、高脂血症、高コレステロール血 症、高トリグリセリド血症、脂質代謝異常の予防又は治療に好ましい。
食欲抑制薬としては、例えば、モノアミン再吸収阻害薬、セロトニン再吸収阻害薬、 セロトニン放出刺激薬、セロトニンァゴ-スト(特に 5HT —ァゴ二スト)、ノルアドレナ
2C
リン再吸収阻害薬、ノルアドレナリン放出刺激薬、 a アドレナリン受容体ァゴ-スト
1
、 β —アドレナリン受容体ァゴ-スト、ドーパミンァゴ-スト、カンナピノイド受容体アン
2
タゴニスト、 yーァミノ酪酸受容体アンタゴニスト、 H ヒスタミンアンタゴニスト、 Lーヒ
3
スチジン、レプチン、レプチン類縁体、レプチン受容体ァゴ-スト、メラノコルチン受容 体ァゴ-スト(特に MC3— Rァゴ-スト、 MC4— Rァゴ-スト)、 a—メラニン細胞刺激 ホルモン、コカイン アンドアンフェタミンーレギユレ一テドトランスクリプト、マホガニー タンパク、ェンテロスタチンァゴ-スト、カルシトニン、カルシトニン遺伝子関連べプチ ド、ボンべシン、コレシストキ-ンァゴ-スト(特に CCK— Aァゴ-スト)、コルチコトロピ ン放出ホルモン、コルチコトロピン放出ホルモン類縁体、コルチコトロピン放出ホルモ ンァゴ-スト、ゥロコルチン、ソマトスタチン、ソマトスタチン類縁体、ソマトスタチン受容 体ァゴ-スト、下垂体アデ-レートシクラーゼ活性ィ匕ペプチド、脳由来神経成長因子 、シリアリー-ユートロピックファクター、サイロトロピン放出ホルモン、ニューロテンシン 、ソーバジン、ニューロペプチド Yアンタゴ-スト、 ργγ、ォピオイドペプチドアンタゴ 二スト、ガラニンアンタゴ-スト、メラニン コンセントレイティングホルモン受容体アン タゴニスト、ァグーチ関連蛋白阻害薬、ォレキシン受容体アンタゴニスト等が挙げられ る。具体的には、モノアミン再吸収阻害薬としては、マジンドール等が挙げられ、セロ トニン再吸収阻害薬としては、塩酸デクスフェンフルラミン、フェンフルラミン、塩酸シ ブトラミン、マレイン酸フルボキサミン、塩酸セルトラリン等が挙げられ、セロト-ンァゴ 二ストとしては、イノトリブタン、 (+ )ノルフェンフルラミン等が挙げられ、ノルアドレナリ ン再吸収阻害薬としては、ブプロピオン、 GW— 320659等が挙げられ、ノルアドレナ リン放出刺激薬としては、例えば、ロリプラム、 ΥΜ— 992等が挙げられ、 β —ァドレ
2 ナリン受容体ァゴニストとしては、アンフェタミン、デキストロアンフェタミン、フエンテノレ
ミン、ベンズフエタミン、メタアンフェタミン、フェンジメトラジン、フェンメトラジン、ジェチ ルプロピオン、フエ-ルプロパノールァミン、クロべンゾレックス等が挙げられ、ドーパ ミンァゴ-ストとしては、 ER— 230、ドブレキシン、メシル酸ブロモクリプチンが挙げら れる。カンナピノイド受容体アンタゴ-ストとしては、例えば、リモナバント等が挙げら れる。 y—ァミノ酪酸受容体アンタゴニストとしては、例えば、トピラマート等が挙げら れる。 H—ヒスタミンアンタゴ-ストとしては、例えば、 GT— 2394等が挙げられる。レ
3
プチン、レプチン類縁体又はレプチン受容体ァゴ-ストとしては、例えば、 LY—355 101等が挙げられる。コレシストキニンァゴ-スト(特に CCK— Aァゴ-スト)としては、 例えば、 SR- 146131, SSR- 125180, BP— 3. 200、 A— 71623、 FPL- 158 49、 GI— 248573、 GW— 7178、 GI— 181771、 GW— 7854、 A— 71378等力挙 げられる。ニューロペプチド Yアンタゴ-ストとしては、例えば、 SR— 120819— Α、 Ρ D— 160170、 NGD— 95— 1、 ΒΙΒΡ— 3226、 1229— U— 91、 CGP— 71683、 Β ΙΒΟ— 3304、 CP— 671906— 01、J— 115814等力挙げ、られる。食欲抑帘 U薬 ίま、 糖尿病、耐糖能異常、糖尿病性合併症、肥満症、高脂血症、高コレステロール血症 、高トリグリセリド血症、脂質代謝異常、ァテローム性動脈硬化症、高血圧、うつ血性 心不全、浮腫、高尿酸血症、痛風の予防又は治療、特に、中枢の食欲調節系にお ける脳内モノアミンや生理活性ペプチドの作用を促進又は阻害することによって食欲 を抑制し、摂取エネルギーを減少させることから、肥満症の予防又は治療に好ましい
[0063] アンジォテンシン変換酵素阻害薬としては、例えば、カプトプリル、マレイン酸ェナ ラプリル、ァラセプリル、塩酸デラプリル、ラミプリル、リシノプリル、塩酸イミダプリル、 塩酸べナゼプリル、セロナプリル一水和物、シラザプリル、フオシノプリルナトリウム、 ぺリンドプリルエルプミン、モベルチプリルカルシウム、塩酸キナプリル、塩酸スピラプ リル、塩酸テモカプリル、トランドラプリル、ゾフエノプリルカルシウム、塩酸モエキシプ リル (moexipril)、レンチアプリル等が挙げられる。アンジォテンシン変換酵素阻害薬 は、糖尿病性合併症、高血圧の予防又は治療に好ましい。
[0064] 中性エンドべプチダーゼ阻害薬としては、例えば、ォマパトリラート、 MDL- 1002 40、ファシドトリル (fasidotril)、サムパトリラート、 GW— 660511X、ミキサンプリル(mi
xanpril)、 SA— 7060、 E— 4030、 SLV— 306、ェカド卜リル等力 S挙げられる。中性ェ ンドぺプチダーゼ阻害薬は、糖尿病性合併症、高血圧の予防又は治療に好ましい。
[0065] アンジォテンシン II受容体拮抗薬としては、例えば、カンデサルタンシレキセチル、 カンデサルタンシレキセチル /ヒドロクロ口チアジド、口サルタンカリウム、メシル酸ェ プロサルタン、バルサルタン、テルミサルタン、ィルベサルタン、 EXP— 3174、 L- 1 58809、 EXP— 3312、オルメサルタン、タソサルタン、 KT— 3— 671、 GA— 0113 、 RU— 64276、 EMD— 90423、 BR— 9701等力挙げられる。アンジォテンシン II 受容体拮抗薬は、糖尿病性合併症、高血圧の予防又は治療に好ましい。
[0066] エンドセリン変換酵素阻害薬としては、例えば、 CGS— 31447、 CGS— 35066、 S M— 19712等が挙げられる。エンドセリン受容体アンタゴ-ストとしては、例えば、 L — 749805、 TBC— 3214、 BMS— 182874、 BQ— 610、 TA— 0201、 SB— 215 355、 PD— 180988、シタクセンタンナトリウム(sitaxsentan)、: BMS— 193884、ダ ルセンタン(darusentan)、 TBC— 3711、ボセンタン、テゾセンタンナトリウム(tezosen tan) , J- 104132, YM— 598、 S— 0139、 SB— 234551、 RPR- 118031 A, A TZ— 1993、 RO— 61— 1790、 ABT— 546、ェンラセンタン、 BMS— 207940等 が挙げられる。これらの薬剤は、糖尿病性合併症、高血圧の予防又は治療に好まし ぐ特に、高血圧の予防又は治療に好ましい。
[0067] 利尿薬としては、例えば、クロルタリドン、メトラゾン、シクロペンチアジド、トリクロルメ チアジド、ヒドロクロ口チアジド、ヒドロフルメチアジド、ベンチルヒドロクロ口チアジド、ぺ ンフルチジド、メチクロチアジド、インダパミド、トリバミド、メフルシド、ァゾセミド、ェタク リン酸、トラセミド、ピレタニド、フロセミド、ブメタニド、メチクラン、カンレノ酸カリウム、ス ピロノラタトン、トリアムテレン、アミノフィリン、塩酸シクレタニン、 LLU— a、 PNU- 8 0873A、イソソルビド、 D—マン-トール、 D—ソルビトール、フルクトース、グリセリン 、ァセトゾラミド、メタゾラミド、 FR— 179544、 OPC— 31260、リキシパプタン(lixivap tan)、塩酸コ-パプタンが挙げられる。利尿薬は、糖尿病性合併症、高血圧、うつ血 性心不全、浮腫の予防又は治療に、特に、尿排泄量を増カロさせることにより血圧を低 下させたり、浮腫を改善するため、高血圧、うつ血性心不全、浮腫の予防又は治療に 好ましい。
[0068] カルシウム拮抗薬としては、例えば、ァラ-ジピン、塩酸エホ-ジピン、塩酸二カル ジピン、塩酸ノ ノレニジピン、塩酸べニジピン、塩酸マニジピン、シノレニジピン、ニソノレ ジピン、二トレンジピン、二フエジピン、二ルバジピン、フエロジピン、ベシル酸アムロジ ピン、ブラ-ジピン、塩酸レルカ-ジピン、イスラジピン、ェルゴジピン、ァゼル -ジピ ン、ラシジピン、塩酸バタ-ジピン、レミルジピン、塩酸ジルチアゼム、マレイン酸タレ ンチアゼム、塩酸べラパミール、 S べラパミール、塩酸ファスジル、塩酸べプリジル、 塩酸ガロパミル等が挙げられる。血管拡張性降圧薬としては、例えば、インダパミド、 塩酸トドララジン、塩酸ヒドララジン、力ドララジン、ブドララジン等が挙げられる。交換 神経遮断薬としては、例えば、塩酸ァモスラロール、塩酸テラゾシン、塩酸ブナゾシン 、塩酸プラゾシン、メシル酸ドキサゾシン、塩酸プロプラノロール、ァテノロール、酒石 酸メトプロロール、カルベジロール、二プラジロール、塩酸セリプロロール、ネビボロー ル、塩酸べタキソロール、ピンドロール、塩酸タータトロール、塩酸べバントロール、マ レイン酸チモロール、塩酸カルテオロール、フマル酸ビソプロロール、マロン酸ボピン ドロール、二プラジロール、硫酸ペンブトロール、塩酸ァセブトロール、塩酸チリソロー ル、ナドロール、ゥラピジル、インドラミン等が挙げられる。中枢性降圧薬としては、例 えば、レセルピン等が挙げられる。 アドレナリン受容体ァゴニストとしては、例え
2
ば、塩酸クロ-ジン、メチルドノ CHF— 1035、酢酸グアナベンズ、塩酸グアンファ シン、モクソ-ジン(moxonidine)、口フエキシジン(lofexidine)、塩酸タリぺキソール等 が挙げられる。これらの薬剤は、高血圧の予防又は治療に好ましい。
[0069] 抗血小板薬としては、例えば、塩酸チクロビジン、ジピリダモール、シロスタゾール、 ィコサペント酸ェチル、塩酸サルポダレラート、塩酸ジラゼプ、トラビジル、ベラプロス トナトリウム、アスピリン等が挙げられる。抗血小板薬は、ァテローム性動脈硬化症、う つ血性心不全の予防又は治療に好ま 、。
[0070] 尿酸生成阻害薬としては、例えば、ァロプリノール、ォキシプリノール、フエブキソス タツト等が挙げられる。尿酸排泄促進薬としては、例えば、ベンズブロマロン、プロべ ネシド等が挙げられる。尿アルカリィ匕薬としては、例えば、炭酸水素ナトリウム、クェン 酸カリウム、クェン酸ナトリウム等が挙げられる。これらの薬剤は、高尿酸血症、痛風 の予防又は治療に好まし 、。
[0071] 本発明に係る 1—置換一 7— ( β—D—グリコピラノシルォキシ)(ァザ)インドールイ匕 合物と組み合わせる他の医薬としては、糖尿病の予防又は治療においては、インスリ ン感受性増強薬、アミラーゼ阻害薬、 O ダルコシダーゼ阻害薬、ビグアナイド薬、 インスリン分泌促進薬、インスリン又はインスリン類縁体、グルカゴン受容体アンタゴ- スト、インスリン受容体キナーゼ刺激薬、トリべプチジルぺプチダーゼ II阻害薬、ジぺ プチジルぺプチダーゼ IV阻害薬、プロテインチロシンホスファターゼー 1B阻害薬、グ リコゲンホスホリラーゼ阻害薬、グルコース 6—ホスファターゼ阻害薬、フルクトース ビスホスファターゼ阻害薬、ピルビン酸デヒドロゲナーゼ阻害薬、肝糖新生阻害薬 、 D—力イロイノシトール、グリコゲン合成酵素キナーゼ 3阻害薬、 11 18—ヒドロキシ ステロイドデヒドロゲナーゼ阻害薬、グルカゴン様ペプチド 1、グルカゴン様ぺプチ ド一 1類縁体、グルカゴン様ペプチド一 1ァゴ-スト、アミリン、アミリン類縁体、アミリン ァゴ-スト及び食欲抑制薬よりなる群力 選択される少なくとも 1種の医薬が好ましぐ インスリン感受性増強薬、アミラーゼ阻害薬、 a ダルコシダーゼ阻害薬、ビグアナィ ド薬、インスリン分泌促進薬、インスリン又はインスリン類縁体、グルカゴン受容体アン タゴニスト、インスリン受容体キナーゼ刺激薬、トリべプチジルぺプチダーゼ II阻害薬 、ジぺプチジノレべプチダーゼ IV阻害薬、プロテインチロシンホスファターゼー 1B阻害 薬、グリコゲンホスホリラーゼ阻害薬、グルコース 6—ホスファターゼ阻害薬、フルク トース—ビスホスファターゼ阻害薬、ピルビン酸デヒドロゲナーゼ阻害薬、肝糖新生 阻害薬、 D—力イロイノシトール、グリコゲン合成酵素キナーゼー3阻害薬、 11 —ヒ ドロキシステロイドデヒドロゲナーゼ阻害薬、グルカゴン様ペプチド 1、グルカゴン様 ペプチド— 1類縁体、グルカゴン様ペプチド— 1ァゴニスト、アミリン、アミリン類縁体及 びアミリンァゴニストよりなる群力も選択される少なくとも 1種の医薬がさらに好ましぐ インスリン感受性増強薬、アミラーゼ阻害薬、 a ダルコシダーゼ阻害薬、ビグアナィ ド薬、インスリン分泌促進薬及びインスリン又はインスリン類縁体よりなる群力 選択さ れる少なくとも 1種の医薬が最も好ま 、。
[0072] 糖尿病性合併症の予防又は治療にお!、ては、インスリン感受性増強薬、アミラーゼ 阻害薬、 a—ダルコシダーゼ阻害薬、ビグアナイド薬、インスリン分泌促進薬、インス リン又はインスリン類縁体、グルカゴン受容体アンタゴ-スト、インスリン受容体キナー
ゼ刺激薬、トリべプチジルぺプチダーゼ II阻害薬、ジぺプチジルぺプチダーゼ IV阻 害薬、プロテインチロシンホスファターゼ—IB阻害薬、グリコゲンホスホリラーゼ阻害 薬、グルコース 6—ホスファターゼ阻害薬、フルクトース一ビスホスファターゼ阻害 薬、ピルビン酸デヒドロゲナーゼ阻害薬、肝糖新生阻害薬、 D 力イロイノシトール、 グリコゲン合成酵素キナーゼ 3阻害薬、 11 18—ヒドロキシステロイドデヒドロゲナー ゼ阻害薬、グルカゴン様ペプチド 1、グルカゴン様ペプチド 1類縁体、グルカゴン 様ペプチド— 1ァゴ-スト、アミリン、アミリン類縁体、アミリンァゴ-スト、アルドース還 元酵素阻害薬、終末糖化産物生成阻害薬、プロテインキナーゼ C阻害薬、 γ アミ ノ酪酸受容体アンタゴニスト、ナトリウムチャンネルアンタゴニスト、転写因子 NF— κ Β阻害薬、脂質過酸化酵素阻害薬、 Ν ァセチル化ー a リンクトーアシッドージぺ プチダーゼ阻害薬、インスリン様成長因子 I、血小板由来成長因子、血小板由来 成長因子類縁体、上皮増殖因子、神経成長因子、カル-チン誘導体、ゥリジン、 5— ヒドロキシ一 1—メチルヒダントイン、 EGB— 761、ビモクロモル、スロデキシド、 Y— 12 8、止瀉薬、瀉下薬、アンジォテンシン変換酵素阻害薬、中性エンドべプチダーゼ阻 害薬、アンジォテンシン II受容体拮抗薬、エンドセリン変換酵素阻害薬、エンドセリン 受容体アンタゴニスト及び利尿薬よりなる群力 選択される少なくとも 1種の医薬が好 ましぐアルドース還元酵素阻害薬、アンジォテンシン変換酵素阻害薬、中性エンド ぺプチダーゼ阻害薬及びアンジォテンシン II受容体拮抗薬よりなる群カゝら選択される 少なくとも 1種の医薬がさらに好ましい。
肥満症の予防又は治療においては、インスリン感受性増強薬、アミラーゼ阻害薬、 a ダルコシダーゼ阻害薬、ビグアナイド薬、インスリン分泌促進薬、インスリン又は インスリン類縁体、グルカゴン受容体アンタゴニスト、インスリン受容体キナーゼ刺激 薬、トリべプチジルぺプチダーゼ II阻害薬、ジぺプチジルぺプチダーゼ IV阻害薬、プ ロティンチロシンホスファターゼー 1B阻害薬、グリコゲンホスホリラーゼ阻害薬、ダル コース 6—ホスファターゼ阻害薬、フルクトースービスホスファターゼ阻害薬、ピルビ ン酸デヒドロゲナーゼ阻害薬、肝糖新生阻害薬、 D 力イロイノシトール、グリコゲン 合成酵素キナーゼー 3阻害薬、 11 —ヒドロキシステロイドデヒドロゲナーゼ阻害薬、 グルカゴン様ペプチド 1、グルカゴン様ペプチド 1類縁体、グルカゴン様ペプチド
1ァゴ-スト、アミリン、アミリン類縁体、アミリンァゴ-スト、 β アドレナリン受容体
3
ァゴ-スト及び食欲抑制薬よりなる群力 選択される少なくとも 1種の医薬が好ましぐ アミラーゼ阻害薬、 α ダルコシダーゼ阻害薬、 13 アドレナリン受容体ァゴ-スト
3
及び食欲抑制薬よりなる群力 選択される少なくとも 1種の医薬がさらに好ましい。 実施例
[0074] 本発明の内容を以下に示す参考例、実施例及び試験例により、さらに詳細に説明 する力 本発明はその内容に限定されるものではない。
[0075] 参考例 1 7 -ヒドロキシ 1— (4 メチルベンジル) - 1H—インドール
[0077] 7 ベンジルォキシ— 1H—インドール(0. 3g)の Ν, N ジメチルホルムアミド(5mL )溶液に氷冷下水素化ナトリウム(55% 70mg)を加え 10分間撹拌した。反応混合 物に 4—メチルベンジルクロリド (0. 19mL)を加え室温で 2時間撹拌した。反応混合 物を水中に注ぎ、ジェチルエーテルで抽出した。抽出物を水及び飽和食塩水で洗 浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去して 7—べンジルォキシ —1— (4—メチルベンジル) 1H—インドール(0. 43g)を得た。これをテトラヒドロフ ラン (6mL)に溶解し、 10%パラジウム炭素粉末(50mg)をカ卩え、水素雰囲気下室温 で 5時間撹拌した。不溶物を濾去し、濾液を減圧下濃縮した。残渣をシリカゲルカラ ムクロマトグラフィー精製 (溶出溶媒: キサン Z酢酸ェチル =5Zl)して標記化 合物(86mg)を得た。
一 NMR(CDC1 ) δ ppm: 2.3 (3H, s), 4.68 (1H, s), 5.6 (2H, s), 6.45—6.5 (2H, m
3
), 6.89 (1H, t, J=7.7Hz), 7.0-7.1 (5H, m), 7.15-7.25 (1H, m).
[0078] 参考例 2 7 ヒドロキシー 1 ί2—「4 (3. 3 ジメトキシプロボキシ)フエニル Ίェチ ル}ー111—インドール
[0079] [化 5]

4— (2 ヒドロキシェチル)フエノール( lg) 3 ブロモプロピオンアルデヒドジメチル ァセタール(1. 02mL)、炭酸セシウム(2. 83g)及び触媒量のヨウ化ナトリウムのァセ トン(15mL)混合物を室温で一晩撹拌した。不溶物を濾去し、濾液を減圧下濃縮し た。残渣をァミノプロピルシリカゲルカラムクロマトグラフィー精製 (溶出溶媒: n キ サン Z酢酸ェチル = lZl)して 3— [4一(2 ヒドロキシェチル)フエ-ルォキシ]プロ ピオンアルデヒドジメチルァセタール( 1. 22g)を得た。これを塩化メチレン( 15mL) に溶解し、氷冷下、トリェチルァミン(0. 85mL)及びメタンスルホユルクロリド(0. 43 mL)を加え 1時間撹拌した。反応混合物を水中に注ぎ、酢酸ェチルで抽出した。酢 酸ェチル溶液を 0. 5molZL塩酸、水及び飽和食塩水で順次洗浄後、無水硫酸マ グネシゥムで乾燥し、溶媒を減圧下留去して 3— [4— (2—メタンスルホ -ルォキシェ チル)フエ-ルォキシ]プロピオンアルデヒドジメチルァセタール(1. 49g)を得た。 7 —ベンジルォキシ— 1H—インドール(1. 04g)の N, N ジメチルホルムアミド(10m L)溶液に氷冷下水素化ナトリウム(55% 0. 25g)を加え 10分間撹拌した。反応混 合物に、先の 3— [4一(2 メタンスルホ -ルォキシェチル)フエ-ルォキシ]プロピオ ンアルデヒドジメチルァセタール(1. 49g)及び触媒量のヨウ化ナトリウムを加え室温 で一晩撹拌した。反応混合物を水中に注ぎ、ジェチルエーテルで抽出した。抽出物 を水及び飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留 去した。残渣をシリカゲルカラムクロマトグラフィー精製 (溶出溶媒: n キサン Z酢 酸ェチル=671 571)して7—べンジルォキシー1 {2—[4ー(3, 3 ジメトキシ プロポキシ)フエ-ル]ェチル } 1H—インドールを得た。これをテトラヒドロフラン(10 mL)に溶解し、 10%パラジウム炭素粉末 (0. 5g)をカ卩え、水素雰囲気下室温で 5時 間撹拌した。不溶物を濾去し、濾液を減圧下濃縮して標記化合物(1. 57g)を得た。 一 NMR(CDC1 ) δ ppm: 2.05— 2.1 (2H, m), 3.0—3.1 (2H, m), 3.37 (6H, s), 4.01
(2H, t, J=6.2Hz), 4.5-4.6 (2H, m), 4.63 (IH, t, J=5.9Hz), 4.86 (IH, brs), 6.36 (IH, d, J=3.3Hz), 6.5 (IH, d, J=7.4Hz), 6.75-6.85 (3H, m), 6.89 (IH, t, J=7.4Hz), 6.95-7
.05 (2H, m), 7.15-7.25 (IH, m).
[0081] 参考例 3— 6
対応する原料物質を用いて参考例 1又は 2と同様の方法で表 1に記載の化合物を合 成した。
[0082] [表 1]
[0083] 実施例 1 7—( β—D—ダルコピラノシルォキシ) 1— (4 メチルベンジル) - 1H インドール
[0085] 7 ヒドロキシ一 1— (4—メチルベンジル) IH—インドール(1. 36g)、ァセトブロモ
- a—D グルコース(2. 59g)及びべンジルトリ(n—ブチル)アンモ-ゥムクロリド( 1. 79g)の塩化メチレン(20mL)混合物に 5molZL水酸化ナトリウム水溶液(3. 4m L)をカ卩え、室温で一晩撹拌した。反応混合物をァミノプロピルシリカゲルカラムクロマ トグラフィー精製 (溶出溶媒: n キサン Z酢酸ェチル = 1Z1)し、ついでシリカゲ ルカラムクロマトグラフィー精製 (溶出溶媒: n キサン Z酢酸ェチル =3Zl 2Z 1)して 7— (2, 3, 4, 6—テトラ一 O ァセチルー 13—D—ダルコピラノシルォキシ) —1— (4—メチルベンジル)—1H—インドール(1. 25g)を得た。得られた 7— (2, 3 , 4, 6—テトラ一 O ァセチルー 13—D—ダルコビラノシルォキシ) 1— (4—メチル ベンジル) 1H—インドール(0. 3g)をメタノール(2mL)に溶解し、ナトリウムメトキシ ド(28%メタノール溶液、 0. 05mL)を加え室温で 1時間撹拌した。反応混合物をシリ 力ゲルカラムクロマトグラフィー精製 (溶出溶媒:塩化メチレン Zメタノール =5Zl)し て標記化合物 (0. 19g)を得た。
NMR(CD OD) δ ppm: 2.26 (3Η, s), 3.3—3.5 (4H, m), 3.66 (IH, dd, J=11.9H
3
z, 5.6Hz), 3.86 (IH, dd, J=11.9Hz, 2.2Hz), 5.05 (IH, d, J=7.8Hz), 5.49 (IH, d, J=l 5.6Hz), 5.89 (IH, d, J=15.6Hz), 6.42 (IH, d, J=3.1Hz), 6.85—6.95 (2H, m), 6.95-7.1 5 (5H, m), 7.15-7.25 (IH, m).
[0086] 実施例 2— 5
対応する原料物質を用 ヽて実施例 1と同様の方法で表 2に記載の化合物を合成した
[0087] [表 2]
表 2
[0088] ¾施例 6 1—「2— (4 ヒドロキシフエニル)ェチル Ί— 7— (2. 3. 4. 6—テトラ一 Ο— ピバロイノレー -D-グルコビラノシルォキシ) 1 Η インドール
[0089] [化 7]
[0090] 7 ヒドロキシ— 1— { 2— [4— (3, 3 ジメトキシプロボキシ)フエ-ル]ェチル } 1Η —インドール(1. 57g)、 2, 3, 4, 6—テトラ一 O ピパロイルー a—D—ダルコピラノ シルブロミド(2. 56g)及びべンジルトリ(n—ブチル)アンモ-ゥムクロリド(1. 38g)の 塩化メチレン(15mL)混合物に 5molZL水酸ィ匕ナトリウム水溶液(2. 7mL)をカロえ、 室温で 2日間撹拌した。反応混合物をァミノプロピルシリカゲルカラムクロマトグラフィ
一精製 (溶出溶媒: n キサン Z酢酸ェチル = 1Z1)し、次いでシリカゲルカラムク 口マトグラフィー精製 (溶出溶媒: n へキサン Z酢酸ェチル =6/1 4Z 1 )して 1 {2- [4- (3, 3 ジメトキシプロボキシ)フエ-ル]ェチル } 7—(2, 3, 4, 6—テトラ —O—ビバロイル一 13—D—ダルコピラノシルォキシ) 1H—インドール(1. 05g)を 得た。これをアセトン(12mL)に溶解し、水(6mL)及びシユウ酸 · 2水和物をカ卩ぇ 2時 間加熱還流した。反応混合物にピぺラジン (0. 64g)を加え、室温で 3時間撹拌した 。反応混合物を水中に注ぎ、酢酸ェチルで抽出した。酢酸ェチル溶液を水及び飽和 食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣を シリカゲルカラムクロマトグラフィー精製 (溶出溶媒: n キサン Z酢酸ェチル =4Z 1)ついでァミノプロピルシリカゲルカラムクロマトグラフィー精製 (n キサン/酢酸 ェチル =4Zl 3Zl 2Zl)して標記化合物(0. 31g)を得た。
iH— NMR(CDC1 ) 6 ppm: l.l (9H, s), 1.12 (9H, s), 1.16 (9H, s), 1.18 (9H, s), 2.
3
9—3.05 (2H, m), 3.85—3.95 (1H, m), 4.05-4.2 (2H, m), 4.25-4.4 (1H, m), 4.5-4.65 (
1H, m), 4.7 (1H, s), 5.15-5.25 (1H, m), 5.4-5.55 (3H, m), 6.29 (1H, d, J=2.9Hz), 6.
64 (1H, d, J=2.9Hz), 6.65-6.7 (2H, m), 6.71 (1H, d, J=7.7Hz), 6.8—6.85 (2H, m), 6.
93 (1H, t, J=7.7Hz), 7.25-7.3 (1H, m).
[0091] 実施例 7 7- ( β—D—グルコビラノシルォキシ) 1—「2— (4—ヒドロキシフエニル) ェチル, 1H—インドール
[0092] [化 8]
1— [2— (4 ヒドロキシフエ-ル)ェチル ]—7— (2, 3, 4, 6—テトラ一 O—ビバロイ ルー 13—D—ダルコピラノシルォキシ) 1H—インドール(50mg)のメタノール(lm L)溶液に水(0. lmL)及び水酸化リチウム · 1水和物(1 lmg)を加え室温でー晚撹 拌した。反応混合物をシリカゲルカラムクロマトグラフィー精製 (溶出溶媒:塩化メチレ ン Zメタノール =8Zl 5Zl)して標記化合物(20mg)を得た。
•(ω 'Ηΐ) Z'L-VL '(ω 'Η ) SO •Ζ— S8'9 '(ω Ήε) S8"9-Z"9
'Ρ 'Ηΐ) 6Γ3 '(ω 'Ηΐ) 6· f- L'f '(ω 'Ηΐ) ' - £- '(ZHS 'ΖΗ6·ΐΐ=ί" 'ΡΡ 'Ηΐ) 16'£ '(ω 'Η ) '(ω Ή ΐ) S9"s-ee"s '(ω Ήε) eex-esx '(ω Ήζ) ΐ - 6τ·^^ 9 (ao
sao)H N-H
T — HI (/^^ / έ r= / 一 α— ϋ
'ρ 'ε 'Ζ) - ζ [ ^エ( / ェ ^ΕΗ ー ) " [ェっ(izs= ^エ邈 ベ ^
)マ /^^邈^、(Sraog) /—、ベ tn ( ^: / 3r= / 一 α— ϋ -Λ(
[6^ ] 600] — ^ -ΗΙ Ι ^
8圏第
• (ω 'Ηΐ) Z'L- VL '(ω 'Η ) S6"9-S8"9 '(zH2"S=f 'Ρ 'Ηΐ) S8"9 '( ω 'Η Z"9-9"9
'Ρ 'Ηΐ) 8Γ3 '(ω 'Ηΐ) 6· —3Ζ· '(ω
'Ηΐ)
'ΡΡ 'Ηΐ) ΐ Τ '( ω 'ΗΪ) S9"s-ee"s '(ω Ήε) eex-^x '(ω Ήε) ΐ·ε— 6's:radd§ (ao
sao)H N-H
T C8l7Z0C/900Zdf/X3d ム66磨 900Ζ OAV
[0097] [化 10]
[0098] 1— [2— (4 ヒドロキシフエ-ル)ェチル ]—7— (2, 3, 4, 6—テトラ一 O—ビバロイ ルー 13—D—ダルコピラノシルォキシ) 1H—インドール(0. 2g)、炭酸セシウム(0 . 17g)及び 1ーブロモー 3 クロ口プロパン(0. 05mL)のアセトン(4mL)混合物を 室温で一晩撹拌した。反応混合物をシリカゲルカラムクロマトグラフィー精製 (溶出溶 媒: n へキサン Z酢酸ェチル = 6Z 1 )して 1一 { 2— [4一( 3 クロ口プロポキシ)フ ェ -ル]ェチル }— 7— (2, 3, 4, 6—テトラ一 O—ビバロイル一 13—D—ダルコピラノ シルォキシ)—1H—インドール(0. 21g)を得た。これをァセトニトリル(6mL)に溶解 し、ヨウ化ナトリウム (46mg)をカ卩ぇ一晩加熱還流した。反応混合物にトリス (ヒドロキシ メチル)ァミノメタン (0. 31g)及びエタノール (4mL)をカ卩ぇ 60°Cで 2日間撹拌した。 反応混合物をァミノプロピルシリカゲルカラムクロマトグラフィー精製 (溶出溶媒:塩ィ匕 メチレン Zメタノール = 30Zl〜5Zl)して 1 [2—(4 {3— [2 ヒドロキシー 1, 1 —ビス(ヒドロキシメチル)ェチルァミノ]プロポキシ }フエ-ル)ェチル ]—7— (2, 3, 4 , 6—テトラ一 Ο—ビバロイル一 13—D—ダルコピラノシルォキシ) 1H—インドール( 0. 13g)を得た。これをメタノール(3mL)に溶解し、水(0. 3mL)及び水酸化リチウ ム · 1水和物(24mg)を加え室温で一晩撹拌した。反応混合物を減圧下濃縮し、残 渣を ODS固相抽出法 (洗浄溶媒:蒸留水、溶出溶媒:メタノール)で精製して標記化 合物(71mg)を得た。
一 NMR(CD OD) S ppm: 1.85— 2.0 (2H, m), 2.81 (2H, t, J=7.0Hz), 2.95—3.15 (
3
2H, m), 3.35—3.65 (10H, m), 3.71 (1H, dd, J=11.9Hz, 5.3Hz), 3.9 (1H, dd, J=11.9H z, 2.3Hz), 4.02 (2H, t, J=6.2Hz), 4.4-4.5 (1H, m), 4.75-4.9 (1H, m), 5.18 (1H, d, J =7.8Hz), 6.25 (1H, d, J=3.2Hz), 6.75—6.85 (3H, m), 6.85—6.95 (2H, m), 6.95—7.05 ( 2H, m), 7.1-7.2 (1H, m).
[0099] 実施例 10 7— ( β D—ダルコビラノシルォキシ) 1 (4 メチルベンジル) 1Η ベンズイ^^ゾール,
2 ァミノ一 3 -トロフエノール(0. 5g)、 2, 3, 4, 6—テトラ一 O—ビバロイル一 α —D—ダルコピラノシルブロミド(1. 88g)及びべンジルトリ(n—ブチル)アンモ-ゥム クロリド( 1. 0 lg)の塩化メチレン( 15mL)混合物に 5molZL水酸ィ匕ナトリウム水溶液 (3. 24mL)をカ卩え、室温で 4日間撹拌した。反応混合物を 0. 5molZL塩酸中に注 ぎ、酢酸ェチルで抽出した。抽出物を 0. 5molZL塩酸、水及び飽和食塩水で洗浄 後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラ ムクロマトグラフィー精製 (溶出溶媒: キサン Z酢酸ェチル =4Zl)して 2 アミ ノ一 3 -トロフエ-ル 2, 3, 4, 6—テトラ一 O—ビバロイル一 13—D ダルコピラノ シド (0. 99g)を得た。これをテトラヒドロフラン(15mL)に溶解し、 10%パラジウム炭 素粉末(500mg)を加え、水素雰囲気下室温で一晩撹拌した。不溶物を濾去し、濾 液を減圧下濃縮した。残渣をシリカゲルカラムクロマトグラフィー精製 (溶出溶媒: n— へキサン Z酢酸ェチル =3Zl l. 5Z1)して 2, 3 ジァミノフエ-ル 2, 3, 4, 6 —テトラ一 O—ビバロイル 一 D—ダルコビラノシド (0. 53g)を得た。得られた 2, 3 —ジァミノフエニル 2, 3, 4, 6—テトラ一 O—ビバロイル一 13—D—ダルコビラノシド (0. 2g)にオルトぎ酸トリェチル(0. 24g)及び触媒量の p—トルエンスルホン酸 · 1水 和物をカ卩え、 130°Cで 3分間撹拌した。反応混合物をシリカゲルカラムクロマトグラフ ィー精製 (溶出溶媒: n キサン Z酢酸ェチル = 1Z1 1Z2)して 4ー(2, 3, 4, 6—テトラ一 O—ビバロイル一 13—D—ダルコピラノシルォキシ) 1H ベンズイミダ ゾール(0. 16g)を得た。これに炭酸セシウム(0. 13g)、 4—メチルベンジルクロリド( 40mg)、触媒量のヨウ化ナトリウム及び N, N ジメチルホルムアミド(4mL)をカロえ、 室温で一晩撹拌した。反応混合物を水中に注ぎ析出した結晶を濾取し、水洗後減
圧下乾燥して 1ー(4 メチルベンジル)ー7—(2, 3, 4, 6—テトラー O—ビバロイル - β—D—ダルコピラノシルォキシ) 1H ベンズイミダゾールと 1— (4—メチルベ ンジル) 4— (2, 3, 4, 6—テトラ一 Ο—ビバロイル一 13—D—ダルコビラノシルォキ シ) 1H ベンズイミダゾールとの混合物(0. 16g)を得た。これをメタノール (2mL) に溶解し、水(0. 2mL)及び水酸化リチウム · 1水和物(43mg)を加え室温で 8時間 撹拌した。反応混合物をシリカゲルカラムクロマトグラフィー精製 (溶出溶媒:塩化メチ レン Zメタノール = 5ZD後、フラクションを濃縮して得られた結晶をメタノールで扱う ことにより析出した異性体を濾去し、濾液を減圧下濃縮して標記化合物(12mg)を得 た。
NMR(CD OD) δ ppm: 2.29 (3Η, s), 3.3—3.55 (4H, m), 3.68 (1H, dd, J=12.4
3
Hz, 6.2Hz), 3.88 (1H, dd, J=12.4Hz, 2.2Hz), 5.08 (1H, d, J=7.5Hz), 5.61 (1H, d, J= 15.3Hz), 5.86 (1H, d, J=15.3Hz), 7.05-7.2 (6H, m), 7.33 (1H, d, J=8.0Hz), 8.09 (1H , s).
[0102] (試験例 1)
ヒト SGLT活性阻害作用確認試験
1)ヒト SGLT1のクローユング及び発現ベクターへの組み換え
ヒト小腸由来の総 RNA(Ori gene)を、オリゴ dTをプライマーとして逆転写し、 PC R増幅用 cDNAライブラリーを作成した。この cDNAライブラリーを铸型として、 Hedi gerらにより報告されたヒト SGLT1 (ACCESSION: M24847)の1番から2005番ま での塩基配列を PCR法により増幅し、 pcDNA3. 1 (-) (Invitrogen)のマルチクロ 一ユング部位に挿入した。挿入した DNAの塩基配列は、報告されていた塩基配列と 完全に一致していた。
[0103] 2)ヒト SGLT2のクローユング及び発現ベクターへの組み換え
ヒト腎臓由来の総 RNA(Ori gene)を、オリゴ dTをプライマーとして逆転写し、 PC R増幅用 cDNAライブラリーを作成した。この cDNAライブラリーを铸型として、 R. G . Wellsら【こより報告されたヒト SGLT2 (ACCESSION : M95549, M95299)の 2 番から 2039番までの塩基配列を PCR法により増幅し、 pcDNA3. 1 (一) (Invitrog en)のマルチクローユング部位に挿入した。挿入した DNAの塩基配列は、報告され
て!、た塩基配列と完全に一致して 、た。
[0104] 3)ヒト SGLT1若しくはヒト SGLT2発現細胞の作製
ヒト SGLT1若しくはヒト SGLT2発現ベクターを COS— 7細胞にリポフエクシヨン法( Lipof ectamine2000: Invitrogen)にて導入した。まず、 96穴プレートに COS— 7 細胞を 5 X 104個 ZlOO /z LZ穴で播種し、 37°Cで 2時間静置した。これとは別に、 培地 50 L当たり 0. のヒト SGLT1若しくはヒト SGLT2発現ベクターと 0. 5 L の Lipofectoamine2000を混合し、複合体溶液を調製した。この複合体溶液を先述 の COS— 7細胞に 50 LZ穴ずつ添カ卩して緩やかに撹拌し、 2日間培養した後に 取り込み実験に供した。
[0105] 4)メチル— a—D—ダルコビラノシド MG)取り込み阻害活性の測定
取り込み用緩衝液(140mM塩化ナトリウム、 2mM塩化カリウム、 ImM塩化カルシ ゥム、 ImM塩化マグネシウム、 10mM2 -〔4— (2 ヒドロキシェチル) 1—ピペラ ジ -ル〕エタンスルホン酸、 5mMトリス(ヒドロキシメチル)ァミノメタンを含む緩衝液 p H7. 4)には、非放射ラベル体(Sigma)と14 Cラベル体(Amersham Pharmacia Biotech)の a— MG混合物を最終濃度が ImMとなるように混和して添カ卩した。試 験化合物はジメチルスルホキシドに溶解した後、蒸留水にて適宜希釈して ImM a — MGを含む取り込み用緩衝液に添加し、測定用緩衝液とした。対照群用には試験 化合物を含まない測定用緩衝液を、基礎取り込み測定用には塩ィ匕ナトリウムに替え て 140mMの塩ィ匕コリンを含む基礎取り込み測定用緩衝液を調製した。培養したヒト SGLT1若しくはヒト SGLT2発現細胞の培地を除去し、前処置用緩衝液( a— MG を含まない基礎取り込み用緩衝液)を 1穴あたり 180 L加え、 37°Cで 10分間静置し た。同一操作をもう 1度繰り返した後、前処置用緩衝液を除去し、測定用緩衝液又は 基礎取り込み用緩衝液を 1穴当たり 75 Lずつ加え 37°Cで静置した。 1時間後に測 定用緩衝液を除去し、 1穴当たり 180 Lの洗浄用緩衝液(10mM非ラベル体 a— MGを含む基礎取り込み用緩衝液)で 2回洗浄した。 1穴当たり 75 Lの 0. 2mol/ L水酸ィ匕ナトリウムで細胞を溶解し、その液をピコプレート(Packard)に移した。 150 μ Lのマイクロシンチ 40 (Packard)をカ卩えて混和し、マイクロシンチレーシヨンカウン ター トップカウント (Packard)にて放射活性を計測した。対照群の取り込みから基
礎取り込み量を差し引いた値を 100%として、試験化合物の各濃度におけるメチル a D ダルコビラノシドの取り込み量を算出し、試験化合物がメチルー (X -D- ダルコビラノシドの取り込みを 50%阻害した濃度 (IC 値)を、口ジットプロットにより算
50
出した。結果を表 3に示す。
[0106] [表 3] 表 3
[0107] 表 3に示したとおり、本発明に係る 1—置換一 7— ( β—D グリコピラノシルォキシ)
(ァザ)インドールイ匕合物(I)は、極めて強いヒト SGLT1及び Ζ又はヒト SGLT2阻害 活性を有している。
産業上の利用可能性
[0108] 本発明に係る 1—置換一 7— ( β—D—グリコピラノシルォキシ)(ァザ)インドールイ匕 合物 (I)若しくはそのプロドラッグ又はその薬理学的に許容される塩、又はその水和 物若しくは溶媒和物は、ヒト SGLT活性阻害作用を有するので、小腸でのグルコース 等の糖質吸収を阻害し、又は腎臓でのグルコースの再吸収を抑制することにより、食 後血糖値の上昇を抑制し、及び Ζ又は血糖値を正常化することができる。したがって 、本発明により、糖尿病、食後高血糖、耐糖能異常、糖尿病性合併症又は肥満症等 の予防又は治療薬を提供することができる。