WO2006021378A1 - Dihydropteridinonderivate, verfahren zu deren herstellung und deren verwendung als arzneimittel - Google Patents
Dihydropteridinonderivate, verfahren zu deren herstellung und deren verwendung als arzneimittel Download PDFInfo
- Publication number
- WO2006021378A1 WO2006021378A1 PCT/EP2005/008990 EP2005008990W WO2006021378A1 WO 2006021378 A1 WO2006021378 A1 WO 2006021378A1 EP 2005008990 W EP2005008990 W EP 2005008990W WO 2006021378 A1 WO2006021378 A1 WO 2006021378A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- optionally
- alkylene
- alkyl
- radicals
- group
- Prior art date
Links
- 0 CN1c2cnc(NC(C=C3)=C*(*)C=C3NC(C*)=O)nc2N(*)C(*)(*)C1=O Chemical compound CN1c2cnc(NC(C=C3)=C*(*)C=C3NC(C*)=O)nc2N(*)C(*)(*)C1=O 0.000 description 2
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/14—Drugs for dermatological disorders for baldness or alopecia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/10—Antimycotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/18—Antivirals for RNA viruses for HIV
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P33/00—Antiparasitic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/06—Antianaemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D475/00—Heterocyclic compounds containing pteridine ring systems
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P20/00—Technologies relating to chemical industry
- Y02P20/50—Improvements relating to the production of bulk chemicals
- Y02P20/55—Design of synthesis routes, e.g. reducing the use of auxiliary or protecting groups
Definitions
- DIHYDROPTERIDINONE DERIVATIVES METHOD FOR THEIR PREPARATION AND THEIR USE
- the present invention relates to novel dihydropteridinones of the general formula (I)
- radicals L, R 1 , R 2 , R 3 , R 4 and R 5 have the meanings mentioned in the claims and the description, their isomers, processes for the preparation of these dihydropteridinones and their use as medicaments.
- Pteridinone derivatives are known as agents with antiproliferative action from the prior art.
- WO 01/019825 and WO 03/020722 describe the use of pteridinone derivatives for the treatment of tumor diseases.
- tumor cells partially or completely escape regulation and control by the organism and are characterized by uncontrolled growth. This is due, on the one hand, to the loss of control proteins, e.g. Rb, pl ⁇ , p21 and p53 as well as the activation of so-called accelerators of the cell cycle, the cyclin-dependent kinases (CDK's).
- CDK's cyclin-dependent kinases
- Aurora B has an essential function in entering mitosis.
- Aurora B phosphorylates histone H3 on SerlO and thus initiates chromosome condensation (Hsu et al., 2000, Cell 102: 279-91).
- a specific cell cycle arrest in the G2 / M phase may also be due, for example, to inhibition of specific phosphatases such as Cdc25C (Russell and Nurse 1986, Cell 45: 145-53).
- Cdc25C Yeasts with defective Cdc25 gene arrest in the G2 phase, while overexpression of Cdc25 leads to premature entry into the mitotic phase (Russell and Nurse 1987, Cell 49: 559-67).
- arrest in the G2 / M phase may also be due to inhibition of certain motor proteins, the so-called kinesins such as Eg5 (Mayer et al., 1999, Science 286: 971-4), or microtubule stabilizing or destabilizing agents (eg, colchicine, Taxol, etoposide, vinblastine, vincristine) (Schiff and Horwitz 1980, Proc Natl Acad ScW SA 77: 1561-5).
- kinesins such as Eg5 (Mayer et al., 1999, Science 286: 971-4)
- microtubule stabilizing or destabilizing agents eg, colchicine, Taxol, etoposide, vinblastine, vincristine
- the so-called polo-like kinases a small family of serine / threonine kinases, also play an important role in the regulation of the eukaryotic cell cycle. So far, the polo-like kinases PLK-I, PLK-2, PLK-3 and PLK-4 have been described in the literature. Especially for PLK-I a central role in the regulation of the mitosis phase has been shown.
- PLK-I is responsible for the maturation of the centrosomes, for the activation of the phosphatase Cdc25C, as well as for the activation of the Anaphase Promoting Complex (Glover et al., 1998, Genes Dev. 12: 3777-87, Qian et al., 2001, Mol Biol Cell 12: 1791-9). Injection of PLK-I antibodies results in G2 arrest in untransformed cells while arresting tumor cells in the mitosis phase (Lane and Nigg 1996, J Cell Biol. 135: 1701-13).
- the invention relates to dihydropteridinones of the general formula (I)
- L is a single bond, or a bridging double-bonded group selected from the group consisting of C 1 -C 6 - alkylene, C 2 -C 6 - alkenylene, C 2 - C 6 alkynylene, C 3 -C 7 cycloalkylene, QQ-AIkylen -Ce-Qo-arylene-Ci-Q-alkylene, C 1 -C 4 -alkylene-C 6 -C 10 -arylene, -O-, -O-C 1 -C 6 -alkylene, -O-C 3 - C 6 -
- R 1 and R 2 together are C 2 -C 6 -alkylene, in which optionally one or two methylene groups may be replaced by one of the groups -O- or -NR 7 -, and which may optionally be mono- or polysubstituted by one or more several radicals R 9 ;
- R 3 is hydrogen or a radical selected from C 1 -C 8 -alkyl, C 2 -C 8 -alkenyl, C 2 -C 8 -
- Alkynyl, C 3 -C 8 -cycloalkyl and C 6 -C 14 -aryl which may optionally be monosubstituted or polysubstituted by one or more radicals R 9 ; or
- R 3 and R 2 or R 3 and R 1 together C 2 -C 6 - alkylene, which may optionally be mono- or polysubstituted by one or more radicals R 9 ;
- R 4 is hydrogen, halogen, CN, OH, -NR 7 R 8 or a radical selected from among
- R 5 is phenyl which may optionally be monosubstituted or polysubstituted by one or more radicals R 11 , or
- R 5 is phenyl which is monosubstituted by a radical R 6 , or R 5 C 1 -C 4 -alkyl, which may optionally be mono- or polysubstituted by one or more radicals R 9 , or R 6 -NR 7 R 8 or a 5-10 membered heterocycloalkyl group containing one, two or three heteroatoms selected from the group nitrogen, oxygen and
- Sulfur preferably nitrogen or oxygen, may contain and which may optionally be mono- or polysubstituted by one or more of the radicals R 12 ;
- R 7 and R 8 are hydrogen or C 1 -C 6 -alkyl
- R 9 is halogen, C 1 -C 4 -alkyl, C 1 -C 4 -alkyl, CN, OH or CF 3
- R 10 is halogen, OH, CN, OO, C 1 -C 6 -alkyl, COOR 7 , NR 7 R 8 , CONR 7 R 8 , SO 2 R 7 , CHF 2 or CF 3 ;
- R 1 is halogen, OH, CN, C 1 -C 4 -alkyl, C 1 -C 4 -alkyloxy, COOR 7 , CONR 7 R 8 , SO 2 R 7 ,
- R 12 is halogen, CF 3 , C 1 -C 6 -alkyl, Q-Ce-alkylene-Q-Qo-aryl, C 3 -C 8 -cycloalkyl or
- Ci-Ce-alkylene-Cs-Cs-cycloalkyl optionally, in the form of their Tautonieren, their racemates, their enantiomers, their diastereomers and their mixtures, and optionally in the form of their pharmacologically acceptable acid addition salts, solvates and or hydrates.
- L is a single bond, or a bridging divalent group selected from the group consisting of C 1 -C 6 -alkylene, C 2 -C 6 -alkenylene, C 2 -C 6 -alkynylene, C 3 -C 7 -cycloalkylene, C 1 - C 4 -alkylene-C 6 -C 10 -arylene-C 1 -C 4 -alkylene,
- R 1 and R 2 identical or different, denote hydrogen, or a radical selected from among C 1 -C 6 -alkyl, C 2 -C 6 -alkenyl and C 2 -C 6 -AMnyl, which may be on or can be substituted several times by one or more radicals R 9 , or R 1 and R 2 together C 2 -C 6 - alkylene, in which optionally one or two
- Methylene groups may be replaced by one of the groups -O- or -NR 7 -, and which may optionally be mono- or polysubstituted by one or more radicals R 9 ;
- R 3 is hydrogen or a radical selected from C 1 -C 8 -alkyl, C 2 -C 8 -alkenyl, C 2 -C 8 -
- R 5 Phenyl, which may optionally be mono- or polysubstituted by one or more radicals R 11 , or R 5 is phenyl which is monosubstituted by a radical R 6 , or
- R 5 is C 1 -C 4 -alkyl, which may optionally be monosubstituted or polysubstituted by one or more radicals R 9 , or
- R 6 is a 5-10 membered heterocycloalkyl group which may contain one, two or three heteroatoms selected from the group of nitrogen, oxygen and sulfur, preferably nitrogen or oxygen, and which may optionally be mono- or polysubstituted by one or more of the radicals R 12 ;
- R 7 and R 8 are hydrogen or C 1 -C 6 -alkyl,
- R 9 is halogen, C 1 -C 4 -alkyl, C 1 -C 4 -alkyl, CN, OH or CF 3 ;
- R 11 is halogen, OH, CN, C 1 -C 4 -alkyl, C 1 -C 4 -alkyl, COOR 7 , CONR 7 R 8 , SO 2 R 7 ,
- R 12 is halogen, CF 3 , C 1 -C 6 -alkyl, C 1 -C 6 -alkylene-C 6 -Q 0 -aryl, C 3 -C 8 -cycloalkyl or C 1 -C 6 -alkylene-C 1 -C 8 -cycloalkyl ; optionally, in the form of their tautomers, their racemates, their enantiomers, their diastereomers and their mixtures, and optionally in the form of their pharmacologically acceptable acid addition salts, solvates and or hydrates.
- L is a single bond, -O-, -OQ-Cs-alkylene, -NR 7 -, -NR ⁇ C 1 -C 3 - alkylene or Ci-Q-alkylene, which may optionally be substituted by one or more radicals R 9 ;
- R 1 and R 2 identical or different, denote hydrogen, or a radical selected from the group consisting of C 1 -C 4 -alkyl, C 2 -C 4 -alkenyl and C 2 -C 4 -alkynyl, which may be on or can be substituted several times by one or more radicals R 9 , or R and R together C 2 -C 4 - alkylene, which may optionally be mono- or polysubstituted by one or more radicals R 9 ;
- R 3 is hydrogen or a radical selected from C 1 -C 6 -alkyl, C 3 -C 7 -cycloalkyl and C 6 -C 10 -alkyl which may optionally be monosubstituted or polysubstituted by one or more radicals R 9 ; or R 3 and R 2 or R 3 and R 1 together C 2 -C 4 - alkylene, which may optionally be mono- or polysubstituted by one or more radicals R 9 ;
- Ci-C 4 - alkyl C 1 -C 4 -AIlCyIoXy, C 2 -C 4 - alkenyloxy and C 2 - C 4 alkynyloxy, optionally may be mono- or polysubstituted by one or more radicals R 10 ;
- R 5 is phenyl which may optionally be monosubstituted or disubstituted by one or more radicals R 11 , or
- R 5 is phenyl which is monosubstituted by a radical R 6 , or R 5 is a radical selected from the group consisting of methyl, ethyl, propyl and
- R 6 is a heterocycloalkyl selected from the group consisting of piperidinyl,
- R 7 and R 8 are hydrogen or C 1 -C 4 -alkyl
- R 9 is halogen, C 1 -C 4 -alkyl, QQ-alkyloxy, CN, OH or CF 3
- R 1 J is halogen, OH, CN, C 1 -C 4 -al] CyI, C 1 -C 4 -alkyloxy, COOR 7 , CF 3 , or C 1 -C 4 -
- R 12 is C 1 -C 4 -alkyl, Ci-C 4 -alkylene-phenyl, C 3 -C 6 cycloalkyl or -C 4 -alkylene-C 3 -
- C 6 cycloalkyl optionally, in the form of their tautomers, their racemates, their enantiomers, their diastereomers and their mixtures, and optionally in the form of their pharmacologically acceptable acid addition salts, solvates and or hydrates.
- R 1 and R 2 are hydrogen, or a radical selected from among Group consisting of C 1 -C 4 -alkyl, C 2 -C 4 - alkenyl, and C 2 -C 4 - alkynyl, which optionally may be mono- or disubstituted by a radical selected from the group consisting of fluorine, chlorine, OH and CF 3 ; or R 3 is hydrogen or a radical selected from C 1 -C 6 -alkyl, C 3 -C 7 -cycloalkyl and C 6 -C 1 o-aryl, which may optionally be monosubstituted or disubstituted by a radical selected from the group consisting of fluorine, chlorine, methyl, ethyl, OH, methyloxy, ethyloxy and CF 3 ;
- R 4 is hydrogen, fluorine, chlorine, bromine, -NR 7 R 8 or a radical selected from the group consisting of Ci-C 4 alkyl, C 1 -C 4 -AIlCyIoXy, C 2 -C 4 - alkenyloxy and C 2 -
- C 4 alkynyloxy which may optionally be monosubstituted or disubstituted by a radical selected from the group consisting of fluoro, chloro, OH, methoxy, ethoxy and CF 3 ;
- R 5 is phenyl which may optionally be monosubstituted or disubstituted by a radical selected from the group consisting of methyl, ethyl, OH, fluorine, chlorine,
- R 5 is phenyl which is monosubstituted by a heterocycloalkyl selected from the group consisting of piperidinyl, piperazinyl, pyrrolinyl, pyrrolidinyl, pyrazolinyl, pyrazolidinyl, imidazolinyl, imidazolidinyl and morpholinyl, which may be monosubstituted or disubstituted by methyl, ethyl, benzyl,
- R 5 is a radical selected from the group consisting of methyl, ethyl, propyl and butyl, which may optionally be monosubstituted or disubstituted by one or more radicals selected from among fluorine, chlorine, OH and CF 3 ;
- R 7 and R 8 identical or different, denote hydrogen, methyl or ethyl, optionally in the form of their tautomers, their racemates, their enantiomers, their
- Diastereomers and their mixtures and optionally in the form of their pharmacologically acceptable acid addition salts, solvates and or hydrates.
- R 1 and R 2 identical or different, denote hydrogen or a radical selected from among
- R 3 is hydrogen or a radical selected from the group consisting of methyl
- R 4 is hydrogen, methyl, ethyl, propyl, methyloxy, ethyloxy or propyloxy;
- R 5 is phenyl, which may optionally be monosubstituted or disubstituted by a radical selected from the group consisting of methyl, OH, fluorine, CF 3 , COOH, COOMethyl or COOethyl, or
- R 5 is phenyl which is monosubstituted by a heterocycloalkyl selected from the group consisting of piperidinyl, piperazinyl, pyrrolidinyl and morpholinyl, which may be monosubstituted or disubstituted by methyl, ethyl, benzyl, phenethyl, cyclopropyl or cyclopropylmethyl;
- R 5 is a radical selected from the group consisting of methyl, ethyl, propyl and butyl, which may optionally be monosubstituted or disubstituted by one or more radicals selected from the group of fluorine, chlorine and CF 3 ; optionally, in the form of their tautomers, their racemates, their enantiomers, their diastereomers and their mixtures, and optionally in the form of their pharmacologically acceptable acid addition salts, solvates and or hydrates.
- L is a single bond, or a bridging divalent group selected from the group consisting of -CH 2 -, -CH 2 -CH 2 -, -O-, -O-CH 2 -, -O-CH 2 -CH 2 -, -
- radicals R 1 , R 2 , R 3 , R 4 and R 5 and R 9 may have one of the meanings given above or below, optionally in the form of their tautomers, their racemates, their enantiomers, their diastereomers and their mixtures, and optionally in
- unsymmetrical groups L the bridging, divalent groups can be linked in two different orientations.
- Preference according to the invention is given to those compounds of the formula (I) in which, in the case of an unsymmetrical group L, the heteroatom of the group L is linked to the carbonyl function of the compound of the formula (I).
- L is -NH-, -NH-CH 2 - or -NH-CH 2 -CH 2 -,
- R 4 is hydrogen and the radicals R 1 , R 2 , R 3 and R 5 may have one of the meanings given above or below, optionally in the form of their tautomers, their racemates, their
- Enantiomers their diastereomers and their mixtures, and optionally in the form of their pharmacologically acceptable acid addition salts, solvates and or hydrates.
- R 1 is hydrogen, methyl, ethyl, allyl or propargyl, preferably hydrogen or methyl, more preferably hydrogen and the radicals L, R 2 , R 3 , R 4 and R 5 may have any of the meanings given above, optionally in the form of their tautomers, their racemates, their enantiomers, their diastereomers and their mixtures, and optionally in the form of their pharmacologically acceptable acid addition salts, solvates and or hydrates.
- R 2 is hydrogen, methyl, ethyl, allyl or propargyl, preferably hydrogen, methyl or ethyl, particularly preferably methyl or ethyl
- the radicals L, R 1 , R 3 , R 4 and R 5 may have one of the above or below meanings, optionally in the form of their tautomers, their racemates, their enantiomers, their diastereomers and their mixtures, and optionally in the form of their pharmacologically acceptable acid addition salts, solvates and or hydrates.
- R 3 is methyl, ethyl, propyl, butyl, pentyl, cyclopropyl, cyclopentyl or cyclohexyl are preferably propyl, butyl, pentyl, cyclopentyl or cyclohexyl, particularly preferably propyl, butyl, pentyl, cyclopentyl or cyclohexyl, where propyl, pentyl, cyclopentyl or cyclohexyl in particular cyclopentyl and cyclohexyl are of particular importance, and the radicals L, R 1 , R 2 , R 4 and R 5 may have one of the meanings given above or below, optionally in the form of their tautomers, their racemates, their enantiomers, their Diastereomers and their mixtures, and optionally in
- R 3 is phenyl, which may optionally be one or two times, preferably monosubstituted by fluorine, chlorine, methyl, ethyl, methyloxy, ethyloxy and CF 3 , preferably phenyl, which may optionally be monosubstituted or disubstituted, preferably monosubstituted by fluorine, methyl or methyloxy, and the radicals L, R 1 , R 2 , R 4 and R 5 has one of the meanings given above or below optionally in the form of their tautomers, their racemates, their enantiomers, their diastereomers and their mixtures, and optionally in the form of their pharmacologically acceptable acid addition salts, solvates and or hydrates.
- R 4 is hydrogen, methyl, ethyl, methyloxy or ethyloxy, preferably hydrogen, methyl or methyloxy, particularly preferably hydrogen or methyloxy, and the radicals L, R 1 , R 2 , R 3 and R 5 is one of above or below
- R 5 is phenyl which may optionally be monosubstituted or disubstituted by a radical selected from the group consisting of methyl, OH, fluorine, CF 3 , COOH, COOMethyl or COOethyl, preferably selected from the group consisting of fluorine, CF 3 , COOH , COOMethyl or COOethyl, and the radicals L, R 1 , R 2 , R 3 and R 4 one of the above or mentioned below
- R 5 is phenyl which is monosubstituted by a heterocycloalkyl selected from the group consisting of piperidinyl, piperazinyl, pyrrolidinyl and morpholinyl, which may be monosubstituted or disubstituted by methyl, ethyl, benzyl, phenethyl, cyclopropyl or cyclopropylmethyl and the radicals L , R 1 , R 2 , R 3 and R 4 one of the above or below mentioned
- R 5 is phenyl which is monosubstituted by a heterocycloalkyl selected from the group consisting of piperidinyl, piperazinyl and morpholinyl, which may be monosubstituted or disubstituted by methyl, ethyl, benzyl or
- Cyclopropylmethyl preferably methyl or ethyl
- the radicals L, R 1 , R 2 , R 3 and R 4 may have one of the meanings given above or below, optionally in the form of their tautomers, their racemates, their enantiomers, their diastereomers and their mixtures, and optionally in the form of their pharmacologically acceptable acid addition salts, solvates and or hydrates.
- R 5 is a radical selected from the group consisting of methyl, ethyl, propyl and butyl, which may optionally be substituted one or two times by one or more radicals selected from the group fluorine, chlorine and CF 3 , and the radicals L, R 1 , R 2 , R 3 and R 4 one of the above or below mentioned
- R 5 is a radical selected from the group consisting of methyl, ethyl, propyl and butyl
- the radicals L, R 1 , R 2 , R 3 and R 4 is a may have the meanings given above, optionally in the form of their tautomers, their racemates, their enantiomers, their diastereomers and their mixtures, and optionally in the form of their pharmacologically acceptable acid addition salts, solvates and or hydrates.
- alkyl groups and alkyl groups which are part of other groups are preferably 1 to 6, more preferably 1 to 4 carbon atoms.
- Examples include: methyl, ethyl, propyl, butyl, pentyl, hexyl, heptyl and octyl. Unless otherwise stated, of the abovementioned designations propyl, butyl, pentyl, hexyl, heptyl and octyl, all of the possible isomeric forms are included.
- propyl includes the two isomeric groups n-propyl and iso-propyl, the term butyl n-butyl, iso-butyl, sec-butyl and tert-butyl, the term pentyl, iso-pentyl, neopentyl, etc.
- one or more hydrogen atoms may be replaced by other radicals.
- these alkyl groups may be substituted by fluorine.
- all hydrogen atoms of the alkyl group may also be replaced.
- alkyloxy groups optionally also called alkoxy groups or -O-alkyl groups
- the aforementioned alkyl groups are referred to, which are linked via an oxygen bridge.
- the alkylene bridge or alkylene group are branched and unbranched alkyl groups having 1 to 6 carbon atoms, for example methylene, ethylene, propylene, isopropylene, n-butylene, isobutyl, sec-butyl and tert-butyl, etc. bridges , Particularly preferred are methylene, ethylene, propylene and butylene bridges.
- 1 to 2 C atoms it is possible, if not otherwise stated or supplementarily defined, for 1 to 2 C atoms to be replaced by one or more heteroatoms selected from the group consisting of oxygen, nitrogen or sulfur
- Alkenyl groups are branched and unbranched alkylene groups having 2 to 8 carbon atoms, preferably 2 to 6 carbon atoms, more preferably 2 to 3 carbon atoms, provided they have at least one double bond.
- alkylene groups having 2 to 8 carbon atoms, preferably 2 to 6 carbon atoms, more preferably 2 to 3 carbon atoms, provided they have at least one double bond.
- butenyl includes 1-butenyl, 2-butenyl, 3-butenyl, 1-methyl-1-propenyl, 1-methyl-2-propenyl, 2-methyl-1-propenyl, 2-methyl-2-propenyl and 1 -Ethyl-l -Ethenyl.
- one or more hydrogen atoms in the abovementioned alkenyl groups may optionally be replaced by other radicals.
- these alkyl groups may be substituted by the halogen atoms fluorine. If appropriate, all hydrogen atoms of the alkenyl group may also be replaced.
- alkenyloxy groups optionally also alkenoxy groups or -O-
- Called alkenyl groups referred to above alkenyl groups, which are linked via an oxygen bridge.
- alkenyl groups which are linked via an oxygen bridge.
- oxygen bridge For example: ethyleneoxy, propyleneoxy, butyleneoxy.
- Branched and unbranched, bridging alkylene groups having 2 to 6 carbon atoms, preferably 2 to 4 carbon atoms, particularly preferably 2 to 3, are alkenylene groups (including those which are part of other radicals)
- alkenylene groups including those which are part of other radicals
- ethenylene, propenylene, etc. Unless otherwise stated, are included by the above names propenylene, butenylene, etc. all of the possible isomeric forms.
- Alkynyl groups are branched and unbranched alkynyl groups having 2 to 8 carbon atoms, provided they have at least one triple bond, for example ethynyl, propargyl, butynyl, pentynyl, hexynyl, etc., preferably ethynyl or propynyl.
- one or more hydrogen atoms in the abovementioned alkynyl groups may optionally be replaced by other radicals.
- these alkynyl groups may be fluorine-substituted.
- all hydrogen atoms of the alkynyl group may also be replaced.
- alkynyloxy groups optionally also called alkynoxy groups or -O-alkynyl groups, the abovementioned alkynyl groups are referred to, which are linked via an oxygen bridge.
- Alkynylene groups (including those which are part of other groups) are branched and unbranched, bridging alkynyl groups having 2 to 6
- Carbon atoms provided that they have at least one triple bond, for example, ethynylene, propargylene, etc.
- one or more hydrogen atoms may optionally be replaced by other radicals.
- propargylene, etc. all of the possible isomeric forms are included.
- aryl represents an aromatic ring system having 6 to 14 carbon atoms, preferably 6 or 10 carbon atoms, preferably phenyl or naphthyl, more preferably phenyl.
- Cycloalkyl radicals having 3 to 8 carbon atoms are, for example, cyclopropyl, cyclobutyl, cyclopentyl, cyclohexyl, cycloheptyl or cyclooctyl, preferably cyclopropyl, cyclopentyl or cyclohexyl.
- cycloalkl groups may optionally also be partially unsaturated, that is to say contain at least one double bond such as, for example, cyclohexene.
- cycloalkylene group stands for bridging, divalent cycloalkyl groups.
- heterocycloalkyl which may contain one, two or three heteroatoms selected from the group nitrogen, oxygen and sulfur, preferably nitrogen or oxygen, are, unless otherwise specified in the definitions, for example, tetrahydrofuranyl, tetrahydrofuranonyl, ⁇ Butyrolactonyl, ⁇ -pyranyl, ⁇ -pyranyl, dioxolanyl, tetrahydropyranyl, dioxanyl, dihydrothiophenyl, thiolanyl, dithiolanyl, pyrrolinyl, pyrrolidinyl, pyrazolinyl, pyrazolidinyl, imidazolinyl, imidazolidinyl, piperidinyl, piperazinyl, morpholinyl, thiomorpholinyl, diazepanyl, oxazinyl, tetrahydrooxazinyl, pyrazolidinyl called
- the halogen is generally fluorine, chlorine, bromine or iodine, preferably fluorine, chlorine or bromine, more preferably fluorine or chlorine.
- the compounds according to the invention can be in the form of the individual optical isomers, mixtures of the individual enantiomers, diastereomers or racemates, in the form of the tautomers and in the form of the free bases or the corresponding acid addition salts with pharmacologically acceptable acids.
- Examples of acid addition salts with pharmacologically acceptable acids are salts selected from the group consisting of hydrochloride, hydrobromide, hydroiodide, hydrosulfate, hydrophosphate, hydromethanesulfonate, hydronitrate, hydromlate, hydroacetate, hydrobenzoate, hydrocitrate, hydrofumarate, Hydrotartrate, hydrooxalate, hydrosuccinate, hydrobenzoate and hydro-p-toluenesulfonate, preferably hydrochloride, hydrobromide, hydrosulfate, hydrophosphate, hydrofumarate and hydromethanesulfonate understood.
- the radical R 4 may, unless it is hydrogen, in the compounds of general formula (I) with respect to the attached to the pteridinone skeleton NH group ortho or meta-linked permanently. Particularly preferred are those compounds of general formula (I) in which R 4 is ortho constantly configured to said NH group. These preferred compounds are characterized by the general formula (T)
- radicals L, R 1 , R 2 , R 3 , R 4 and R 5 may have the abovementioned meanings, if appropriate in the form of their tautomers, their racemates, their enantiomers, their diastereomers and their mixtures, and optionally in the form of their pharmacologically acceptable acid addition salts, solvates and or hydrates.
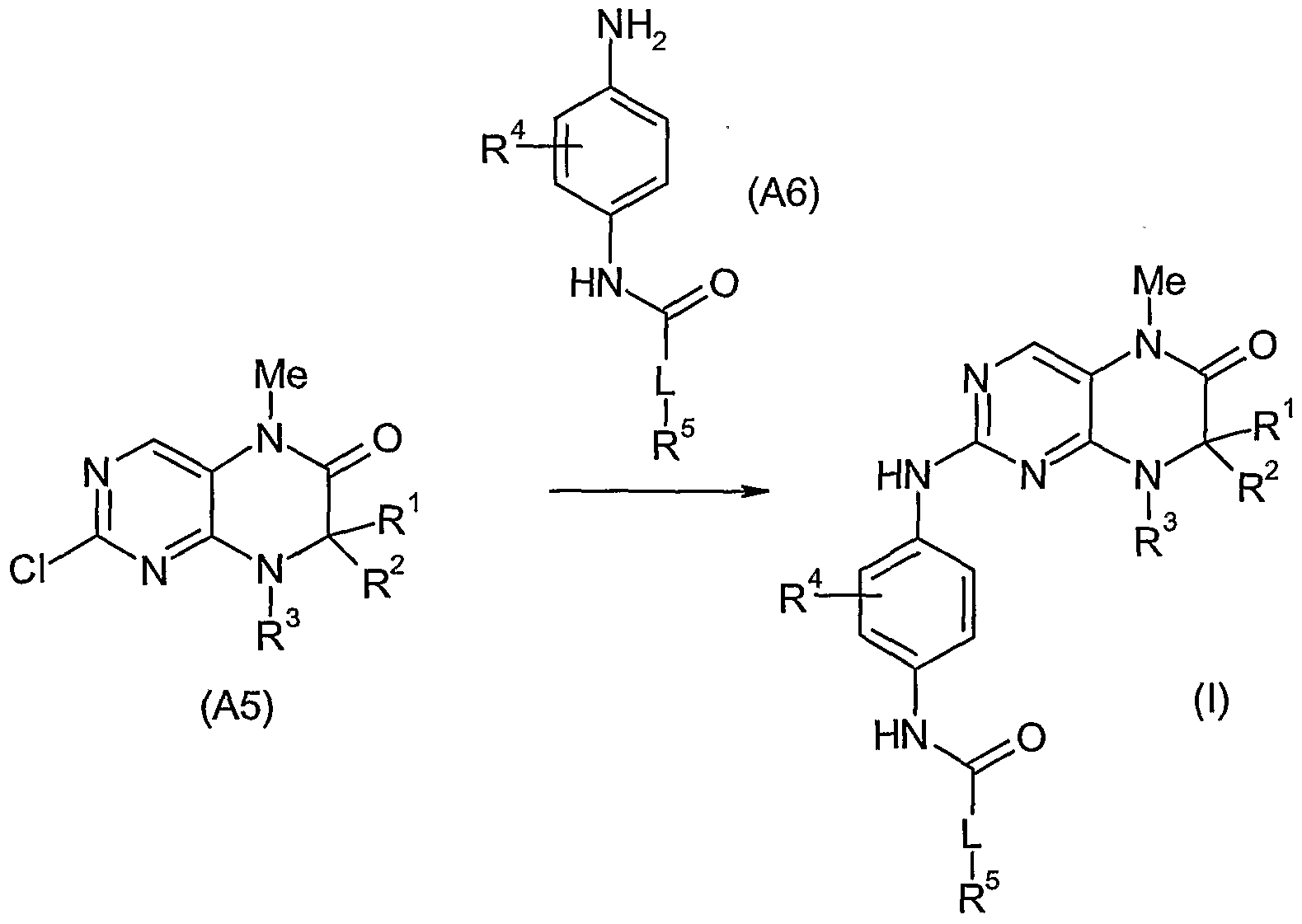
- the compounds according to the invention can be prepared by the synthesis process A described below, the substituents of the general formulas (Al) to (A9) having the abovementioned meanings. This method is to be understood as an explanation of the invention without limiting the same to their subject matter.
- a compound of formula (Al) is reacted with a compound of formula (A2) to give a compound of formula (A3) (Scheme IA).
- This reaction can be carried out according to WO 0043369 or WO 0043372.
- Compound (Al) is commercially available, for example, from City Chemical LLC, 139 Allings Crossing Road, West Haven, CT, 06516, USA.
- Compound (A2) can be used according to literature ( ⁇ ) F. Effenberger, U. Burkhart, J. Willfahrt LiebigsAnn. Chem. 1986, 314-333.
- stage IA 1 equivalent of the compound (A1) and 1 to 1.5 equivalents, preferably 1.1 equivalents of a base, preferably potassium carbonate, potassium bicarbonate, sodium carbonate or sodium bicarbonate, calcium carbonate, more preferably potassium carbonate, are optionally mixed with water in a diluent, for example, acetone, tetrahydrofuran,
- reaction mixture is heated with stirring to a temperature of 18 0 C to 30 0 C, preferably about 22 ° C, and then further stirred for a further 10 to 24 hours, preferably about 12 hours.
- organic solvent for example acetone, tetrahydrofuran, diethyl ether, cyclohexane or dioxane
- step IA The compound (A3) obtained in step IA is reduced at the nitro group and converted to
- Step 2A 1 equivalent of the nitro compound (A3) are dissolved in an acid, preferably glacial acetic acid, formic acid or aqueous hydrochloric acid, preferably glacial acetic acid, and to 50 to 70 ° C, preferably about 60 0 C, warmed.
- a reducing agent for example zinc, tin, or iron, preferably iron powder, is added until the end of the exothermic reaction and 0.2 to 2 hours, preferably 0.5 hours, at 100 to 125 0 C, preferably at about 115 ° C. , touched.
- the iron salt is filtered off and the solvent is distilled off.
- the residue is taken up in a solvent or solvent mixture, for example ethyl acetate or dichloromethane / methanol 9/1 and semisaturated NaCl solution, and filtered through kieselguhr, for example.
- the organic phase is dried and concentrated.
- the residue (compound (A4)) can be purified by chromatography or by crystallization or used as crude product in stage 3 A of the synthesis.
- the compound (A4) obtained in step 2A can be prepared by electrophilic substitution according to
- step 3A 1 equivalent of the amide of formula (A4) is dissolved in an organic solvent, for example dimethylformamide or dimethylacetamide, preferably dimethylacetamide, and cooled to about -5 to 5 ° C., preferably 0 ° C.
- organic solvent for example dimethylformamide or dimethylacetamide, preferably dimethylacetamide
- 1 equivalent of the compound (A5) and 1 to 3 equivalents preferably about 1 equivalent of the compound (A6) without solvent or an organic solvent such as sulfolane, dimethylformamide, dimethylacetamide, toluene, N-methylpyrrolidone, dimethylsulfoxide, or dioxane, preferably sulfolane over 0.1 to 4 hours, preferably 1 hour, at 100 to 220 0 C, preferably heated at about 160 ° C. , After cooling, the addition of org.
- solvent or an organic solvent such as sulfolane, dimethylformamide, dimethylacetamide, toluene, N-methylpyrrolidone, dimethylsulfoxide, or dioxane
- Solvents or solvent mixtures for example diethyl ether / methanol, ethyl acetate, methylene chloride, or diethyl ether, preferably diethyl ether / methanol 9/1, the product (A9) crystallized or purified by chromatography.
- hydrochloric acid and / or an alcohol for example, ethanol, propanol, dioxane,
- Butanol preferably ethanol at reflux for 1 to 48 hours, preferably about 5
- the precipitated product of formula (I) is filtered off and optionally washed with water, dried and from a suitable org. Solvent crystallized.
- radicals R 1 , R 2 and R 3 may have the abovementioned meanings, if appropriate in the form of their tautomers, their racemates, their enantiomers, their diastereomers and their mixtures, and optionally in the form of their acid addition salts, solvates and or hydrates.
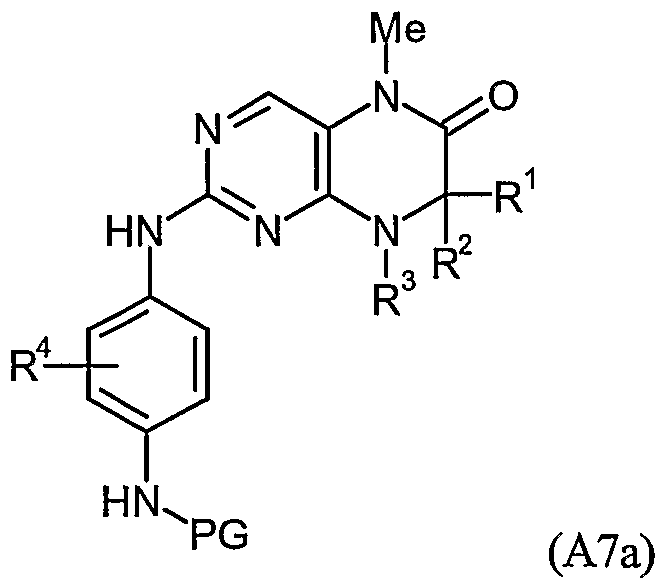
- the products of the formula (A7) are obtained which, after further reaction, are converted into the products of the formula (I) (see Step 5A).
- a group PG as mentioned in the above scheme in the compounds (A7a), come into consideration in the art known amino protecting groups. Suitable methods for the removal of the group PG and thus for the conversion into the compounds of the formula (A8) are known in the prior art (see TW Greene, "Protective Groups in Organic Synthesis", 2nd Edition).
- the products of formula (A9) can also be removed by cleavage of, for example, an acid- or base-labile group of
- a compound (A7a) having an acid-labile protecting group for example, tert-butyloxycarbonyl
- 1-50 equivalents of an acid preferably HCl or trifluoroacetic acid in an organic solvent, eg, methylene chloride, ether, dioxane, tetrahydrofuran, preferably methylene chloride, and at 20-100 ° C, preferably 2O 0 C for 1 to 24h.
- the reaction mixture is separated, for example, over silica gel or obtained by suitable crystallization.
- a solvent e.g. Methanol, ethanol, THF, ethyl acetate, water and dissolved with 0.001 to 0.1
- amides (A9a) For example, 1 equivalent of compound (A8) is reacted with 1 equivalent of an activating reagent, for example, O-benzotriazolyl-N, N, N ', N'-tetramethyluronium tetrafluoroborate (TBTU) and a base, for example, about 1.5 Equivalents, diisopropylethylamine (DIPEA) in an organic diluent, for example, dichloromethane, tetrahydrofuran, dimethylformamide, N-methylpyrrolidione, dimethylacetamide, preferably
- an activating reagent for example, O-benzotriazolyl-N, N, N ', N'-tetramethyluronium tetrafluoroborate (TBTU)
- TBTU O-benzotriazolyl-N, N, N ', N'-tetramethyluronium tetrafluoroborate
- a base for example, about 1.5
- Variant B 1 equivalent of the amine (A8) is dissolved together with 1-3 equivalents of an isocyanate in an organic solvent, for example Dimethylfromamid, THF, dimethylacetamide and stirred at 40-70 0 C for 1-24 h. After removal of the solvent, the product (A9b) is obtained, for example, by crystallization or chromatographic purification.
- an organic solvent for example Dimethylfromamid, THF, dimethylacetamide
- amine (A7) 1 equivalent of the amine (A7) is dissolved in organic solvent, for example dichloromethane, dimethylformamide, THF and mixed with 1-3 equivalents of base, for example diisopropylethylamine, triethylamine. Subsequently, 1-3 equivalents of a chloroformate is added and stirred for 1-24 h at 20-60 ° C. After removal of the solvent, the product (A9c) is obtained, for example, by crystallization or chromatographic purification
- radicals R 1 , R 2 , R 3 and R 4 may have the abovementioned meanings, if appropriate in the form of their tautomers, their racemates, their enantiomers, their diastereomers and their mixtures, and optionally in the form of their acid addition salts, solvates and or hydrates ,
- Suitable acid addition salts are in particular those salts which are listed above for the compounds of the formula (I) as pharmacologically acceptable acid addition salts.
- radicals R 1 , R 2 , R 3 and R 4 may have the abovementioned meanings and in which PG represents an amino protecting group, optionally in the form of their tautomers, their racemates, their enantiomers, their diastereomers and their mixtures, and optionally in the form their acid addition salts, solvates and or hydrates.
- PG is selected from the group consisting of tert-butyloxycarbonyl, acetyl, trifluoromethyl, 9-fluorenylmethyloxycarbonyl, allyloxycarbonyl and Benzyloxycarbonyl, preferably tert-butyloxycarbonyl, acetyl and trifluoromethyl, optionally in the form of their tautomers, their racemates, their enantiomers, their diastereomers and their mixtures, and optionally in the form of their acid addition salts, solvates and or hydrates.
- radicals R 1 , R 2 , R 3 and R 4 may have the abovementioned meanings, if appropriate in the form of their tautomers, their racemates, their enantiomers, their diastereomers and their mixtures, and optionally in the form of their acid addition salts, solvates and or hydrates ,
- novel compounds of the general formula (I) can be synthesized in analogy to the following synthesis examples. However, these examples are to be understood as merely a walkthrough to further explain the invention without limiting it to its subject matter.
- Example 8 0.1 g of 29.19 mg of 4- (4-methylpiperazin-1-yl) benzoic acid chloride, 0.2 ml of triethylamine were stirred for 2 hours in 2 ml of dichloromethane at 20 ° C., then the org phase was taken with 20 mL 5% aqueous potassium carbonate solution extracted. The org. Phase was concentrated and the mixture was separated by silica gel chromatography. The appropriate fractions were combined, concentrated and the residue crystallized from ethyl acetate, diethyl ether and petroleum ether. Yield: 0.095 g of white crystals
- the present invention relates in particularly preferred embodiments, the compounds of formula (I), as mentioned in Table 1, as such, optionally in the form of their tautomers, their racemates, their enantiomers, their diastereomers and their mixtures, and optionally in the form their pharmacologically acceptable acid addition salts, solvates and or hydrates.
- the compounds of general formula (I) are characterized by a variety of therapeutic applications. Worth mentioning are those applications for which the inhibition of specific cell cycle kinases, in particular the inhibitory effect on the proliferation of cultured human tumor cells, but also on the proliferation of other cells, such as. Endothelial cells play a role.
- the proliferation inhibition afforded by the compounds of this invention is mediated by arrest of the cells, especially in the G2 / M phase of the cell cycle.
- the cells arrest for a certain period of time in this cell cycle phase, depending on the cells used, before the programmed cell death is initiated.
- Arrest in the G2 / M phase of the cell cycle is e.g. triggered by the inhibition of specific cell cycle kinases.
- the compounds of the general formula I according to the invention, their isomers and their physiologically tolerable salts are suitable for the treatment of diseases which are characterized by excessive or abnormal cell proliferation.
- Such diseases include, for example: viral infections (eg HIV and Kaposi sarcoma); Inflammation and autoimmune diseases (eg, colitis, arthritis, Alzheimer's disease, glomerulonephritis and wound healing); bacterial, fungal and / or parasitic infections; Leukemia, lymphoma and solid tumors; Skin disorders (eg psoriasis); Bone diseases; cardiovascular diseases (eg restenosis and hypertrophy). Further, they are useful as protection of proliferating cells (eg, hair, intestinal, blood and progenitor cells) against DNA damage by radiation, UV treatment and / or cytostatic treatment (Davis et al., 2001).
- viral infections eg HIV and Kaposi sarcoma
- Inflammation and autoimmune diseases eg, colitis, arthritis, Alzheimer's disease, glomerulonephritis and wound healing
- bacterial, fungal and / or parasitic infections eg, colitis, arthritis, Alzheimer's disease, glomerulonephritis
- novel compounds can be used for the prevention, short-term or long-term treatment of the abovementioned diseases, also in combination with other active substances which are used for the same indications, for example cytostatics, hormones or antibodies.
- the effect of the compounds according to the invention was determined in the PLK1 inhibition assay, in the cytotoxicity test on cultured human tumor cells and / or in a FACS analysis, for example on HeLa S3 cells.
- the compounds showed good to very good activity in both test methods, ie, for example, an EC 50 value in the HeLa S3 cytotoxicity test of less than 5 ⁇ mol / L, generally less than 1 ⁇ mol / L and an IC 50 value in the PLK1 inhibition assay smaller 1 ⁇ mol / L.
- PLK1 Kinase Assay Enzyme Production Recombinant human PLK1 enzyme linked to GST at its N-terminal end is isolated from baculovirus-infected insect cells (Sf21). The purification is carried out by affinity chromatography on glutathione Sepharose columns.
- 4xlO 7 Sf21 cells (Spodoptera frugiperda) in 200 ml of Sf-900 II serum-free insect cell medium (Life Technologies) are seeded in a spinner flask. After 72 hours incubation at 27 ° C. and 70 rpm, IxIO 8 Sf21 cells are seeded in a total of 180 ml of medium in a new spinner flask. After a further 24 hours, 20 ml of recombinant baculovirus stock suspension are added and the cells are cultured for 72 hours at 27 ° C. at 70 rpm. Okadaic acid is added 3 hours before harvest (Calbiochem, final concentration 0.1 ⁇ M) and the suspension is further incubated.
- the cell count is determined, the cells are centrifuged off (5 minutes, 4 ° C, 800 rpm) and Ix with PBS (8 g NaCl / 1, 0.2 g KCl / l, 1.44 g Na 2 HPO 4 / l, 0 , 24 g KH 2 PO4 / 1). After centrifuging again, the pellet is frozen in liquid nitrogen shock.
- the pellet is thawed rapidly and placed in ice-cold lysis buffer (50 mM HEPES pH 7.5, 10 mM MgCfc, 1 mM DTT, 5 ⁇ g / ml leupeptin, 5 ⁇ g / ml aprotinin, 100 ⁇ M NaF, 100 ⁇ M PMSF, 10 mM ⁇ Glycerol phosphate, 0.1 mM Na 3 VO 4 , 30 mM 4-nitro-phenylphosphate) to IxIO 8 cells / 17.5 ml. The cells are lysed for 30 minutes on ice.
- ice-cold lysis buffer 50 mM HEPES pH 7.5, 10 mM MgCfc, 1 mM DTT, 5 ⁇ g / ml leupeptin, 5 ⁇ g / ml aprotinin, 100 ⁇ M NaF, 100 ⁇ M PMSF, 10 mM ⁇ Glycerol phosphate
- ATP solution 45 ⁇ M ATP with 1,1IxIO 6 Bq / ml gamma-P33 ATP.
- the reaction is started and carried out for 45 minutes at 30 ° C with gentle shaking (650 rpm on IKA shaker MTS2).
- the reaction is stopped by addition of 125 ⁇ l of ice-cold 5% TCA per well and incubated on ice for at least 30 minutes.
- the preciptitate is transferred by harvesting to filter plates (96-well microtiter filter plate: UniFilter-96, GF / B, Packard, No. 6005177), then washed four times with 1% TCA and dried at 60 ° C.
- the active substances were added to the cells in different concentrations (dissolved in DMSO; final DMSO concentration: 0.1%) (in triplicate in each case). After 72 hours of incubation, 20 ⁇ l of AlamarBlue reagent (AccuMed International) were added to each well and the cells were incubated for a further 7 hours. For control, 20 ⁇ l of reduced AlamarBlue reagent were added to 3 wells (AlamarBlue reagent, which was autoclaved for 30 min). After 7 h of incubation, the color conversion of the AlamarBlue reagent in the individual wells was determined in a Perkin Elmer fluorescence spectrophotometer (Exitation 530 nm, emission 590 nm, Slits 15, Integrate time 0.1).
- the amount of reacted AlamarBlue reagent represents the metabolic activity of the cells.
- the relative cell activity was calculated as a percentage of the control (HeLa S3 cells without inhibitor) and the drug concentration, which inhibits the cell activity to 50% (IC 50 ) derived.
- the values were calculated from the average of three individual determinations - with correction of the blank value (medium control).
- Propidium iodide (PI) stoichiometrically binds to double-stranded DNA, and is thus capable of determining the proportion of cells in the Gl, S, and G2 / M phase of the cell cycle based on the cellular DNA content.
- Cells in the GO and Gl phases have a diploid DNA content (2N), while cells in G2 or mitosis have a 4N DNA content.
- HeLa S3 cells were seeded onto a 75 cm 2 cell culture flask, after 24 h either 0.1% DMSO was added as a control or the substance was added in different concentrations (in 0.1% DMSO).
- the cells were incubated with the substance or with DMSO for 24 h before the cells were washed twice with PBS and then with trypsin / EDTA.
- the cells were centrifuge (1000 rpm, 5 min, 4 ° C) and wash the cell pellet 2 times with PBS before resuspending the cells in 0.1 ml PBS.
- the cells were fixed for 16 hours at 4 0 C or alternatively for 2 hours at -20 ° C with 80% ethanol.
- the fixed cells (10 6 cells) were centrifuged (1000 rpm, 5 min, 4 ° C), washed with PBS and then centrifuged again.
- the cell pellet was resuspended in 2 ml of Triton X-100 in 0.25% PBS and incubated on ice for 5 min before 5 ml of PBS was added and centrifuged again.
- the cell pellet was resuspended in 350 ⁇ l PI staining solution (0.1 mg / ml KNase A, 10 ⁇ g / ml prodidium iodide in 1 ⁇ PBS).
- the cells were incubated with the staining buffer for 20 min in the dark before being transferred to sample vials for the FACS scan.
- the DNA measurement was carried out in a Becton Dickinson FACS Analyzer, with an argon laser (500 mW, emission 488 nm), and the DNA Cell Quest program (BD).
- the logarithmic PI fluorescence was determined with a band-pass filter (BP 585/42).
- the quantification of the cell populations in the individual cell cycle phases was carried out with the ModFit LT program of Becton Dickinson.
- compounds of the invention were tested on additional tumor cells.
- these compounds are based on carcinomas of various tissues (eg, breast (MCF7), colon (HCT16), head and neck (FaDu), lung (NCI-H460), pancreas (BxPC-3), prostate (DU145)).
- Sarcomas eg, SK-UT-IB
- leukemias and lymphomas eg, HL-60, Jurkat, THP-I
- other tumors eg, melanoma (BRO), gliomas (U-87MG )
- This demonstrates the broad applicability of the compounds according to the invention for the treatment of a wide variety of tumor types.
- the compounds of the general formula (I) can be used alone or in combination with other active compounds according to the invention, if appropriate also in combination with other pharmacologically active substances.
- Suitable application forms are, for example, tablets, capsules, suppositories, solutions, in particular solutions for injection (s.c., i.V., i.m.) and infusion, juices, emulsions or dispersible powders.
- the said doses may, if necessary, be given several times a day.
- Corresponding tablets can be prepared, for example, by mixing the active substance (s) with known auxiliaries, for example inert diluents, such as
- the tablets can also consist of several layers.
- Coated tablets can accordingly be produced by coating cores produced analogously to the tablets with agents normally used in tablet coatings, for example collidone or shellac, gum arabic, talc, titanium dioxide or sugar.
- the core can also consist of several layers consist.
- the dragee sheath to achieve a depot effect of several layers may consist of the above mentioned in the tablets excipients can be used.
- Juices of the active compounds or combinations of active substances according to the invention may additionally contain a sweetening agent, such as saccharin, cyclamate, glycerol or sugar, as well as a taste-improving agent, e.g. Flavorings such as vanillin or orange extract. They may also contain suspending aids or thickening agents, such as sodium carboxymethylcellulose, wetting agents, for example condensation products of fatty alcohols with ethylene oxide, or protective agents, such as p-hydroxybenzoates.
- a sweetening agent such as saccharin, cyclamate, glycerol or sugar
- a taste-improving agent e.g. Flavorings such as vanillin or orange extract.
- suspending aids or thickening agents such as sodium carboxymethylcellulose, wetting agents, for example condensation products of fatty alcohols with ethylene oxide, or protective agents, such as p-hydroxybenzoates.
- Injection and infusion solutions in the usual manner, for example with the addition of isotonic agents, preservatives such as p-hydroxybenzoates, or stabilizers such as alkali metal salts of ethylenediaminetetraacetic acid, optionally with the use of emulsifiers and / or dispersants, for example, in use of water as diluent, if appropriate organic solvents can be used as solubilizers or auxiliary solvents, prepared and filled into injection bottles or ampoules or infusion bottles.
- preservatives such as p-hydroxybenzoates, or stabilizers such as alkali metal salts of ethylenediaminetetraacetic acid
- emulsifiers and / or dispersants for example, in use of water as diluent, if appropriate organic solvents can be used as solubilizers or auxiliary solvents, prepared and filled into injection bottles or ampoules or infusion bottles.
- the capsules containing one or more active ingredients can be prepared, for example, by mixing the active ingredients with inert carriers, such as lactose or sorbitol, and encapsulating them in gelatine capsules.
- suitable suppositories can be prepared, for example, by mixing with suitable carriers, such as neutral fats or polyethylene glycol or its derivatives.
- auxiliaries for example, water, pharmaceutically acceptable organic compounds
- Solvents such as paraffins (e.g., petroleum fractions), oils of vegetable origin (e.g., peanut or sesame oil), mono- or polyfunctional alcohols (e.g., ethanol or glycerin), carriers such as e.g. ground natural minerals (e.g., kaolins, clays, talc, chalk), ground synthetic minerals (e.g., fumed silica and silicates), sugars (e.g., cane, milk and dextrose), emulsifying agents (e.g., lignin, liquor liquors,
- paraffins e.g., petroleum fractions
- oils of vegetable origin e.g., peanut or sesame oil
- mono- or polyfunctional alcohols e.g., ethanol or glycerin
- carriers such as e.g. ground natural minerals (e.g., kaolins, clays, talc, chalk), ground synthetic minerals (e.g., fumed silica and silicates), sugar
- Methyl cellulose, starch and polyvinyl pyrrolidone e.g., magnesium stearate, talc, stearic acid and sodium lauryl sulfate.
- lubricants e.g., magnesium stearate, talc, stearic acid and sodium lauryl sulfate.
- the application is carried out in a customary manner, preferably orally or transdermally, particularly preferably orally.
- the tablets may also contain additives other than those mentioned.
- Sodium citrate, calcium carbonate and dicalcium phosphate together with various additives such as starch, preferably potato starch, gelatin and the like.
- lubricants such as magnesium stearate, sodium lauryl sulfate and talc may be used for tableting.
- the active ingredients may be added to the abovementioned excipients with various flavor enhancers or dyes.
- solutions of the active ingredients may be employed using suitable liquid carrier materials.
- the dosage for intravenous use is 1 - 1000 mg per hour, preferably between 5 - 500 mg per hour. Nevertheless, it may be necessary to deviate from the stated amounts, depending on the body weight or the type of administration route, the individual behavior towards the drug, the nature of its formulation and the time or interval at which it is administered , Thus, in some cases it may be sufficient to manage with less than the aforementioned minimum amount, while in other cases, the said upper limit must be exceeded. In the case of the application of larger quantities, it may be advisable to distribute them in several single doses over the day.
- Another aspect of the present invention relates to pharmaceutical formulations, preferably pharmaceutical formulation of the aforementioned nature, characterized by a content of one or more compounds of general formula (I).
- the finely ground active substance, lactose and part of the corn starch are mixed together.
- the mixture is sieved, then moistened with a solution of polyvinylpyrrolidone in water, kneaded, wet granulated and dried.
- the granules, the remainder of the corn starch and the magnesium stearate are sieved and mixed together.
- the mixture is compressed into tablets of suitable shape and size.
- the finely ground active ingredient, a portion of the corn starch, lactose, microcrystalline cellulose and polyvinylpyrrolidone are mixed together, the mixture is sieved and processed with the remainder of the corn starch and water to a granulate which is dried and sieved. To this is added the sodium carboxymethyl starch and the magnesium stearate, mixed and pressed the mixture into tablets of suitable size.
- Aqua pro inj. 5 ml The active ingredient is dissolved in water at its own pH or optionally at pH 5.5-6.5 and treated with sodium chloride as isotonan. The resulting solution is filtered pyrogen-free and the filtrate filled under aseptic conditions in ampoules, which are then sterilized and sealed.
- the vials contain 5 mg, 25 mg and 50 mg active ingredient.
Landscapes
- Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- General Chemical & Material Sciences (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- General Health & Medical Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Oncology (AREA)
- Communicable Diseases (AREA)
- Immunology (AREA)
- Physical Education & Sports Medicine (AREA)
- Dermatology (AREA)
- Rheumatology (AREA)
- Virology (AREA)
- Cardiology (AREA)
- Neurology (AREA)
- Hematology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Tropical Medicine & Parasitology (AREA)
- Urology & Nephrology (AREA)
- Neurosurgery (AREA)
- Biomedical Technology (AREA)
- Heart & Thoracic Surgery (AREA)
- Hospice & Palliative Care (AREA)
- Vascular Medicine (AREA)
- Psychiatry (AREA)
- Pain & Pain Management (AREA)
- Diabetes (AREA)
- Molecular Biology (AREA)
- AIDS & HIV (AREA)
- Transplantation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
Description
Claims
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CA002578838A CA2578838A1 (en) | 2004-08-25 | 2005-08-19 | Dihydropteridinone derivatives, methods for the production thereof and their use as medicaments |
| EP05775932A EP1786818A1 (de) | 2004-08-25 | 2005-08-19 | Dihydropteridinonderivative, verfahren zu deren herstellung und deren verwendung als arzneimittel |
| JP2007528703A JP2008510750A (ja) | 2004-08-25 | 2005-08-19 | ジヒドロプテリジノン誘導体、その製造方法及び薬物としての使用 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP04020125.3 | 2004-08-25 | ||
| EP04020125A EP1632493A1 (de) | 2004-08-25 | 2004-08-25 | Dihydropteridinonderivative, Verfahren zu deren Herstellung und deren Verwendung als Arzneimittel |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| WO2006021378A1 true WO2006021378A1 (de) | 2006-03-02 |
| WO2006021378A8 WO2006021378A8 (de) | 2006-04-27 |
Family
ID=34926289
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/EP2005/008990 WO2006021378A1 (de) | 2004-08-25 | 2005-08-19 | Dihydropteridinonderivate, verfahren zu deren herstellung und deren verwendung als arzneimittel |
Country Status (7)
| Country | Link |
|---|---|
| US (4) | US7332491B2 (de) |
| EP (2) | EP1632493A1 (de) |
| JP (1) | JP2008510750A (de) |
| AR (1) | AR050611A1 (de) |
| CA (1) | CA2578838A1 (de) |
| TW (1) | TW200621262A (de) |
| WO (1) | WO2006021378A1 (de) |
Cited By (25)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2100894A1 (de) | 2008-03-12 | 2009-09-16 | 4Sc Ag | Pyridopyrimidinone verwendbar als Plk1 (polo-like kinase) Hemmen |
| EP2112152A1 (de) | 2008-04-22 | 2009-10-28 | GPC Biotech AG | Dihydropteridinones als Plk-Inhibitoren |
| US7629460B2 (en) | 2004-08-25 | 2009-12-08 | Boehringer Ingelheim International Gmbh | Dihydropteridione derivatives, process for their manufacture and their use as medicament |
| US20100099680A1 (en) * | 2007-02-01 | 2010-04-22 | Boehringer Ingelheim International Gmbh | Pteridinone derivatives as p13-kinases inhibitors |
| US7728134B2 (en) | 2004-08-14 | 2010-06-01 | Boehringer Ingelheim International Gmbh | Hydrates and polymorphs of 4[[(7R)-8-cyclopentyl-7-ethyl-5,6,7,8-tetrahydro-5-methyl-6-oxo-2-pteridinyl]amino]-3-methoxy-N-(1-methyl-4-piperidinyl)-benzamide, process for their manufacture and their use as medicament |
| US7750152B2 (en) | 2003-02-26 | 2010-07-06 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Intermediate compounds for making dihydropteridinones useful as pharmaceutical compositions and processes of making the same |
| US7759485B2 (en) | 2004-08-14 | 2010-07-20 | Boehringer Ingelheim International Gmbh | Process for the manufacture of dihydropteridinones |
| US7759347B2 (en) | 2004-06-21 | 2010-07-20 | Boehringer Ingelheim International Gmbh | 2-benzylaminodihydropteridinones, process for their manufacture and use thereof as medicaments |
| EP2325185A1 (de) | 2009-10-28 | 2011-05-25 | GPC Biotech AG | Plk-Inhibitor |
| WO2011101369A1 (en) * | 2010-02-17 | 2011-08-25 | Boehringer Ingelheim International Gmbh | Dihydropteridinones, method for production and use thereof |
| US8058270B2 (en) | 2004-08-14 | 2011-11-15 | Boehringer Ingelheim International Gmbh | Dihydropteridinones for the treatment of cancer diseases |
| USRE43115E1 (en) | 2004-12-02 | 2012-01-17 | Boehringer Ingelheim International Gmbh | Process for the manufacture of fused piperazin-2-one derivatives |
| WO2012049153A1 (en) | 2010-10-12 | 2012-04-19 | Boehringer Ingelheim International Gmbh | Process for manufacturing dihydropteridinones and intermediates thereof |
| US8188086B2 (en) | 2006-02-08 | 2012-05-29 | Boehringer Ingelheim International Gmbh | Specific salt, anhydrous and crystalline form of a dihydropteridione derivative |
| US8193188B2 (en) | 2004-07-09 | 2012-06-05 | Boehringer Ingelheim International Gmbh | Methods of using pyridodihydropyrazinones |
| US8329695B2 (en) | 2007-08-03 | 2012-12-11 | Boehringer Ingelheim International Gmbh | Crystalline form of the free base N-[trans-4-[4-(cyclopropylmethyl)-1-piperazinyl]cyclohexyl]-4-[[(7r)-7-ethyl-5,6,7,8-tetrahydro-5-methyl-8-(1-methylethyl)-6-oxo-2-pteridinyl]amino]-3-methoxy-benzamide |
| US8445675B2 (en) | 2004-08-14 | 2013-05-21 | Boehringer Ingelheim International Gmbh | Storage stable perfusion solution for dihydropteridinones |
| US8591895B2 (en) | 2004-08-14 | 2013-11-26 | Boehringer Ingelheim International Gmbh | Combinations for the treatment of diseases involving cell proliferation |
| US9358233B2 (en) | 2010-11-29 | 2016-06-07 | Boehringer Ingelheim International Gmbh | Method for treating acute myeloid leukemia |
| US9370535B2 (en) | 2011-05-17 | 2016-06-21 | Boehringer Ingelheim International Gmbh | Method for treatment of advanced solid tumors |
| DE102017005089A1 (de) | 2016-05-30 | 2017-11-30 | Bayer Pharma Aktiengesellschaft | Substitulerte 3,4-Dihydrochinoxalin-2(1H)-one |
| DE102017005091A1 (de) | 2016-05-30 | 2017-11-30 | Bayer Pharma Aktiengesellschaft | Substituierte 3,4-Dihydropyrido[2,3-b]pyrazin-2(1H)-one |
| US9867831B2 (en) | 2014-10-01 | 2018-01-16 | Boehringer Ingelheim International Gmbh | Combination treatment of acute myeloid leukemia and myelodysplastic syndrome |
| US9956225B2 (en) | 2013-07-26 | 2018-05-01 | Boehringer Ingelheim International Gmbh | Treatment of myelodysplastic syndrome |
| WO2019209757A1 (en) * | 2018-04-24 | 2019-10-31 | Vertex Pharmaceuticals Incorporated | Pteridinone compounds and uses thereof |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1632493A1 (de) * | 2004-08-25 | 2006-03-08 | Boehringer Ingelheim Pharma GmbH & Co.KG | Dihydropteridinonderivative, Verfahren zu deren Herstellung und deren Verwendung als Arzneimittel |
| TW200808325A (en) * | 2006-07-06 | 2008-02-16 | Astrazeneca Ab | Novel compounds |
| CA2665736A1 (en) * | 2006-10-25 | 2008-05-02 | Chroma Therapeutics Ltd. | Pteridine derivatives as polo-like kinase inhibitors useful in the treatment of cancer |
| GB0621203D0 (en) * | 2006-10-25 | 2006-12-06 | Chroma Therapeutics Ltd | PLK inhibitors |
| WO2008130921A1 (en) * | 2007-04-16 | 2008-10-30 | Modgene, Llc | Methods and compositions for diagnosis and treatment of depression and anxiety |
| CA2699607A1 (en) * | 2007-09-25 | 2009-04-02 | Takeda Pharmaceutical Company Limited | Polo-like kinase inhibitors |
| WO2015193228A1 (de) * | 2014-06-19 | 2015-12-23 | Bayer Pharma Aktiengesellschaft | Bet-proteininhibitorische 1,4-dihydropyrido[3,4-b]pyrazinone mit para-substituierter aromatischer amino- oder ethergruppe |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2001019825A1 (en) * | 1999-09-15 | 2001-03-22 | Warner-Lambert Company | Pteridinones as kinase inhibitors |
| WO2003020722A1 (de) * | 2001-09-04 | 2003-03-13 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Neue dihydropteridinone, verfahren zu deren herstellung und deren verwendung als arzneimittel |
Family Cites Families (34)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE3537761A1 (de) * | 1985-10-24 | 1987-04-30 | Bayer Ag | Infusionsloesungen der 1-cyclopropyl-6-fluor-1,4-dihydro-4-oxo-7- (1-piperazinyl)-chinolin-3-carbonsaeure |
| FR2645152B1 (fr) | 1989-03-30 | 1991-05-31 | Lipha | 3h-pteridinones-4, procedes de preparation et medicaments les contenant |
| CA2029651C (en) | 1989-11-17 | 2000-06-06 | David D. Davey | Tricyclic pteridinones and a process for their preparation |
| TW274550B (de) | 1992-09-26 | 1996-04-21 | Hoechst Ag | |
| US5698556A (en) | 1995-06-07 | 1997-12-16 | Chan; Carcy L. | Methotrexate analogs and methods of using same |
| ID27843A (id) * | 1998-08-11 | 2001-04-26 | Pfizer Prod Inc | Substitusi 1, 8-naftiridin-4(ih)-on sebagai penghambat fosfodiesterase 4 |
| US20020183292A1 (en) * | 2000-10-31 | 2002-12-05 | Michel Pairet | Pharmaceutical compositions based on anticholinergics and corticosteroids |
| DE10058119A1 (de) * | 2000-11-22 | 2002-05-23 | Bayer Ag | Pepinotan-Kit |
| US6756374B2 (en) | 2001-01-22 | 2004-06-29 | Hoffmann-La Roche Inc. | Diaminothiazoles having antiproliferative activity |
| WO2002076954A1 (en) | 2001-03-23 | 2002-10-03 | Smithkline Beecham Corporation | Compounds useful as kinase inhibitors for the treatment of hyperproliferative diseases |
| WO2002076985A1 (en) | 2001-03-23 | 2002-10-03 | Smithkline Beecham Corporation | Compounds useful as kinase inhibitors for the treatment of hyperproliferative diseases |
| US20030055026A1 (en) * | 2001-04-17 | 2003-03-20 | Dey L.P. | Formoterol/steroid bronchodilating compositions and methods of use thereof |
| US6806272B2 (en) * | 2001-09-04 | 2004-10-19 | Boehringer Ingelheim Pharma Kg | Dihydropteridinones, processes for preparing them and their use as pharmaceutical compositions |
| PT1463493E (pt) * | 2001-12-14 | 2008-01-04 | Serono Lab | Método para induzir a ovulação utilizando um modulador de nível camp não polipeptídico |
| KR20040106451A (ko) * | 2002-05-03 | 2004-12-17 | 쉐링 악티엔게젤샤프트 | 폴로-유사 키나제 억제제로서의 티아졸리디논 및 그의 용도 |
| CA2493908A1 (en) | 2002-08-08 | 2004-02-19 | Smithkline Beecham Corporation | Thiophene compounds |
| US6861422B2 (en) * | 2003-02-26 | 2005-03-01 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Dihydropteridinones, processes for preparing them and their use as pharmaceutical compositions |
| BR0318145A (pt) | 2003-02-26 | 2006-02-21 | Boehringer Ingelheim Pharma | dihidropteridinonas, processos para a sua preparação e sua aplicação como medicamento |
| CA2552540A1 (en) * | 2004-01-17 | 2005-07-28 | Boehringer Ingelheim International Gmbh | Use of substituted pteridines for the treatment of diseases of the respiratory tract |
| DE102004002557A1 (de) * | 2004-01-17 | 2005-08-04 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Verwendung von substituierten Pyrimido(5,4-d)pyrimidinen zur Behandlung von Atemwegserkrankungen |
| DE102004029784A1 (de) * | 2004-06-21 | 2006-01-05 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Neue 2-Benzylaminodihydropteridinone, Verfahren zur deren Herstellung und deren Verwendung als Arzneimittel |
| DE102004033670A1 (de) * | 2004-07-09 | 2006-02-02 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Neue Pyridodihydropyrazinone, Verfahren zu Ihrer Herstellung und Ihre Verwendung als Arzneimittel |
| DE102004034623A1 (de) * | 2004-07-16 | 2006-02-02 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Neue 6-Formyl-tetrahydropteridine, Verfahren zu ihrer Herstellung und ihre Verwendung als Arzneimittel |
| US20060074088A1 (en) | 2004-08-14 | 2006-04-06 | Boehringer Ingelheim International Gmbh | Dihydropteridinones for the treatment of cancer diseases |
| US20060058311A1 (en) | 2004-08-14 | 2006-03-16 | Boehringer Ingelheim International Gmbh | Combinations for the treatment of diseases involving cell proliferation |
| US20060035903A1 (en) * | 2004-08-14 | 2006-02-16 | Boehringer Ingelheim International Gmbh | Storage stable perfusion solution for dihydropteridinones |
| US7728134B2 (en) * | 2004-08-14 | 2010-06-01 | Boehringer Ingelheim International Gmbh | Hydrates and polymorphs of 4[[(7R)-8-cyclopentyl-7-ethyl-5,6,7,8-tetrahydro-5-methyl-6-oxo-2-pteridinyl]amino]-3-methoxy-N-(1-methyl-4-piperidinyl)-benzamide, process for their manufacture and their use as medicament |
| US7759485B2 (en) * | 2004-08-14 | 2010-07-20 | Boehringer Ingelheim International Gmbh | Process for the manufacture of dihydropteridinones |
| EP1630163A1 (de) * | 2004-08-25 | 2006-03-01 | Boehringer Ingelheim Pharma GmbH & Co.KG | Dihydropteridinonderivative, Verfahren zu deren Herstellung und deren Verwendung als Arzneimittel |
| EP1632493A1 (de) * | 2004-08-25 | 2006-03-08 | Boehringer Ingelheim Pharma GmbH & Co.KG | Dihydropteridinonderivative, Verfahren zu deren Herstellung und deren Verwendung als Arzneimittel |
| JP2008510770A (ja) * | 2004-08-26 | 2008-04-10 | ベーリンガー インゲルハイム インターナショナル ゲゼルシャフト ミット ベシュレンクテル ハフツング | Plk阻害剤としての新規プテリジノン |
| JP2008510771A (ja) * | 2004-08-27 | 2008-04-10 | ベーリンガー インゲルハイム インターナショナル ゲゼルシャフト ミット ベシュレンクテル ハフツング | ジヒドロプテリジノン、その製造方法および医薬薬剤としてのその使用 |
| DE102004058337A1 (de) * | 2004-12-02 | 2006-06-14 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Verfahren zur Herstellung von annelierten Piperazin-2-on Derivaten |
| US7439358B2 (en) * | 2006-02-08 | 2008-10-21 | Boehringer Ingelheim International Gmbh | Specific salt, anhydrous and crystalline form of a dihydropteridione derivative |
-
2004
- 2004-08-25 EP EP04020125A patent/EP1632493A1/de not_active Withdrawn
-
2005
- 2005-08-19 WO PCT/EP2005/008990 patent/WO2006021378A1/de active Application Filing
- 2005-08-19 EP EP05775932A patent/EP1786818A1/de not_active Withdrawn
- 2005-08-19 JP JP2007528703A patent/JP2008510750A/ja not_active Withdrawn
- 2005-08-19 CA CA002578838A patent/CA2578838A1/en not_active Abandoned
- 2005-08-22 AR ARP050103504A patent/AR050611A1/es unknown
- 2005-08-24 TW TW094128936A patent/TW200621262A/zh unknown
- 2005-08-24 US US11/210,951 patent/US7332491B2/en active Active
-
2007
- 2007-12-18 US US11/958,746 patent/US20080113992A1/en not_active Abandoned
- 2007-12-18 US US11/958,750 patent/US7547780B2/en active Active
- 2007-12-18 US US11/958,749 patent/US20080194818A1/en not_active Abandoned
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2001019825A1 (en) * | 1999-09-15 | 2001-03-22 | Warner-Lambert Company | Pteridinones as kinase inhibitors |
| WO2003020722A1 (de) * | 2001-09-04 | 2003-03-13 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Neue dihydropteridinone, verfahren zu deren herstellung und deren verwendung als arzneimittel |
Cited By (43)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7750152B2 (en) | 2003-02-26 | 2010-07-06 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Intermediate compounds for making dihydropteridinones useful as pharmaceutical compositions and processes of making the same |
| US8003786B2 (en) | 2003-02-26 | 2011-08-23 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Dihydropteridinone compounds |
| US7816530B2 (en) | 2003-02-26 | 2010-10-19 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Piperazinyl compounds |
| US7786299B2 (en) | 2003-02-26 | 2010-08-31 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Methods for treating diseases or conditions using dihydropteridinone compounds |
| US7759347B2 (en) | 2004-06-21 | 2010-07-20 | Boehringer Ingelheim International Gmbh | 2-benzylaminodihydropteridinones, process for their manufacture and use thereof as medicaments |
| US8193188B2 (en) | 2004-07-09 | 2012-06-05 | Boehringer Ingelheim International Gmbh | Methods of using pyridodihydropyrazinones |
| US8138341B2 (en) | 2004-08-14 | 2012-03-20 | Boehringer Ingelheim International Gmbh | Intermediate compounds useful for the manufacture of dihydropteridinones |
| US7728134B2 (en) | 2004-08-14 | 2010-06-01 | Boehringer Ingelheim International Gmbh | Hydrates and polymorphs of 4[[(7R)-8-cyclopentyl-7-ethyl-5,6,7,8-tetrahydro-5-methyl-6-oxo-2-pteridinyl]amino]-3-methoxy-N-(1-methyl-4-piperidinyl)-benzamide, process for their manufacture and their use as medicament |
| US8445675B2 (en) | 2004-08-14 | 2013-05-21 | Boehringer Ingelheim International Gmbh | Storage stable perfusion solution for dihydropteridinones |
| US7759485B2 (en) | 2004-08-14 | 2010-07-20 | Boehringer Ingelheim International Gmbh | Process for the manufacture of dihydropteridinones |
| US8138373B2 (en) | 2004-08-14 | 2012-03-20 | Boehringer Ingelheim International Gmbh | Process for the manufacture of dihydropteridinones |
| US8058270B2 (en) | 2004-08-14 | 2011-11-15 | Boehringer Ingelheim International Gmbh | Dihydropteridinones for the treatment of cancer diseases |
| US8591895B2 (en) | 2004-08-14 | 2013-11-26 | Boehringer Ingelheim International Gmbh | Combinations for the treatment of diseases involving cell proliferation |
| US7807831B2 (en) | 2004-08-25 | 2010-10-05 | Boehringer Ingelheim International Gmbh | Dihydropteridione derivatives, process for their manufacture and their use as medicament |
| US7629460B2 (en) | 2004-08-25 | 2009-12-08 | Boehringer Ingelheim International Gmbh | Dihydropteridione derivatives, process for their manufacture and their use as medicament |
| US7700769B2 (en) | 2004-08-25 | 2010-04-20 | Boehringer Ingelheim International Gmbh | Dihydropteridione derivatives, process for their manufacture and their use as medicament |
| US7723517B2 (en) | 2004-08-25 | 2010-05-25 | Boehringer Ingelheim International Gmbh | Dihydropteridione derivatives, process for their manufacture and their use as medicament |
| USRE43115E1 (en) | 2004-12-02 | 2012-01-17 | Boehringer Ingelheim International Gmbh | Process for the manufacture of fused piperazin-2-one derivatives |
| US8664222B2 (en) | 2006-02-08 | 2014-03-04 | Boehringer Ingelheim International Gmbh | Specific salt, anhydrous and crystalline form of a dihydropteridione derivative |
| US8188086B2 (en) | 2006-02-08 | 2012-05-29 | Boehringer Ingelheim International Gmbh | Specific salt, anhydrous and crystalline form of a dihydropteridione derivative |
| US20100099680A1 (en) * | 2007-02-01 | 2010-04-22 | Boehringer Ingelheim International Gmbh | Pteridinone derivatives as p13-kinases inhibitors |
| JP2010517957A (ja) * | 2007-02-01 | 2010-05-27 | ベーリンガー インゲルハイム インターナショナル ゲゼルシャフト ミット ベシュレンクテル ハフツング | Pi3−キナーゼインヒビターとしてのプテリジノン誘導体 |
| US8410100B2 (en) * | 2007-02-01 | 2013-04-02 | Boehringer Ingelheim International Gmbh | Pteridinone derivatives as PI3-kinases inhibitors |
| US8329695B2 (en) | 2007-08-03 | 2012-12-11 | Boehringer Ingelheim International Gmbh | Crystalline form of the free base N-[trans-4-[4-(cyclopropylmethyl)-1-piperazinyl]cyclohexyl]-4-[[(7r)-7-ethyl-5,6,7,8-tetrahydro-5-methyl-8-(1-methylethyl)-6-oxo-2-pteridinyl]amino]-3-methoxy-benzamide |
| EP2100894A1 (de) | 2008-03-12 | 2009-09-16 | 4Sc Ag | Pyridopyrimidinone verwendbar als Plk1 (polo-like kinase) Hemmen |
| EP2112152A1 (de) | 2008-04-22 | 2009-10-28 | GPC Biotech AG | Dihydropteridinones als Plk-Inhibitoren |
| EP2325185A1 (de) | 2009-10-28 | 2011-05-25 | GPC Biotech AG | Plk-Inhibitor |
| WO2011101369A1 (en) * | 2010-02-17 | 2011-08-25 | Boehringer Ingelheim International Gmbh | Dihydropteridinones, method for production and use thereof |
| US8546566B2 (en) | 2010-10-12 | 2013-10-01 | Boehringer Ingelheim International Gmbh | Process for manufacturing dihydropteridinones and intermediates thereof |
| WO2012049153A1 (en) | 2010-10-12 | 2012-04-19 | Boehringer Ingelheim International Gmbh | Process for manufacturing dihydropteridinones and intermediates thereof |
| US9358233B2 (en) | 2010-11-29 | 2016-06-07 | Boehringer Ingelheim International Gmbh | Method for treating acute myeloid leukemia |
| US9370535B2 (en) | 2011-05-17 | 2016-06-21 | Boehringer Ingelheim International Gmbh | Method for treatment of advanced solid tumors |
| US9956225B2 (en) | 2013-07-26 | 2018-05-01 | Boehringer Ingelheim International Gmbh | Treatment of myelodysplastic syndrome |
| US9867831B2 (en) | 2014-10-01 | 2018-01-16 | Boehringer Ingelheim International Gmbh | Combination treatment of acute myeloid leukemia and myelodysplastic syndrome |
| DE102017005091A1 (de) | 2016-05-30 | 2017-11-30 | Bayer Pharma Aktiengesellschaft | Substituierte 3,4-Dihydropyrido[2,3-b]pyrazin-2(1H)-one |
| DE102017005089A1 (de) | 2016-05-30 | 2017-11-30 | Bayer Pharma Aktiengesellschaft | Substitulerte 3,4-Dihydrochinoxalin-2(1H)-one |
| WO2019209757A1 (en) * | 2018-04-24 | 2019-10-31 | Vertex Pharmaceuticals Incorporated | Pteridinone compounds and uses thereof |
| CN112218865A (zh) * | 2018-04-24 | 2021-01-12 | 沃泰克斯药物股份有限公司 | 喋啶酮化合物及其用途 |
| US11059826B2 (en) | 2018-04-24 | 2021-07-13 | Vertex Pharmaceuticals Incorporated | Pteridinone compounds and uses thereof |
| US11572364B2 (en) | 2018-04-24 | 2023-02-07 | Vertex Pharmaceuticals Incorporated | Pteridinone compounds and uses thereof |
| IL278122B1 (en) * | 2018-04-24 | 2023-09-01 | Vertex Pharma | Petridinon compounds and their uses |
| IL278122B2 (en) * | 2018-04-24 | 2024-01-01 | Vertex Pharma | Petridinon compounds and their uses |
| CN112218865B (zh) * | 2018-04-24 | 2024-03-12 | 沃泰克斯药物股份有限公司 | 喋啶酮化合物及其用途 |
Also Published As
| Publication number | Publication date |
|---|---|
| US20080113992A1 (en) | 2008-05-15 |
| CA2578838A1 (en) | 2006-03-02 |
| US20080108812A1 (en) | 2008-05-08 |
| EP1632493A1 (de) | 2006-03-08 |
| US7332491B2 (en) | 2008-02-19 |
| AR050611A1 (es) | 2006-11-08 |
| TW200621262A (en) | 2006-07-01 |
| US20060052383A1 (en) | 2006-03-09 |
| US7547780B2 (en) | 2009-06-16 |
| WO2006021378A8 (de) | 2006-04-27 |
| JP2008510750A (ja) | 2008-04-10 |
| EP1786818A1 (de) | 2007-05-23 |
| US20080194818A1 (en) | 2008-08-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP1786819B1 (de) | Dihydropteridinonderivate, verfahren zu deren herstellung und deren verwendung als arzneimittel | |
| WO2006021378A1 (de) | Dihydropteridinonderivate, verfahren zu deren herstellung und deren verwendung als arzneimittel | |
| EP1761536B1 (de) | Neue 2-benzylaminodihydropteridinone, verfahren zu deren herstellung und deren verwendung als arzneimittel | |
| EP1776363B1 (de) | Neue 6-formyl-tetrahydropteridine, verfahren zu ihrer herstellung und ihre verwendung als arzneimittel u.a. gegen krebs | |
| EP1768981B1 (de) | Neue pyridodihydropyrazinone, verfahren zu ihrer herstellung und ihre verwendung als arzneimittel | |
| EP1427730B1 (de) | Neue dihydropteridinone, verfahren zu deren herstellung und deren verwendung als arzneimittel | |
| EP1599478B1 (de) | Dihydropteridinone, verfahren zu deren herstellung und deren verwendung als arzneimittel | |
| WO2006021548A1 (de) | Dihydropteridinone, verfahren zu deren herstellung und deren verwendung als arzneimittel | |
| WO2006021547A1 (de) | Pteridinone als plk (polo like kinase) inhibitoren | |
| US20040176380A1 (en) | New dihydropteridinones, processes for preparing them and their use as pharmaceutical compositions |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| AK | Designated states |
Kind code of ref document: A1 Designated state(s): AE AG AL AM AT AU AZ BA BB BG BR BW BY BZ CA CH CN CO CR CU CZ DE DK DM DZ EC EE EG ES FI GB GD GE GH GM HR HU ID IL IN IS JP KE KG KM KP KR KZ LC LK LR LS LT LU LV MA MD MG MK MN MW MX MZ NA NG NI NO NZ OM PG PH PL PT RO RU SC SD SE SG SK SL SM SY TJ TM TN TR TT TZ UA UG US UZ VC VN YU ZA ZM ZW |
|
| AL | Designated countries for regional patents |
Kind code of ref document: A1 Designated state(s): BW GH GM KE LS MW MZ NA SD SL SZ TZ UG ZM ZW AM AZ BY KG KZ MD RU TJ TM AT BE BG CH CY CZ DE DK EE ES FI FR GB GR HU IE IS IT LT LU LV MC NL PL PT RO SE SI SK TR BF BJ CF CG CI CM GA GN GQ GW ML MR NE SN TD TG |
|
| CFP | Corrected version of a pamphlet front page | ||
| CR1 | Correction of entry in section i |
Free format text: IN PCT GAZETTE 09/2006 DUE TO A TECHNICAL PROBLEM AT THE TIME OF INTERNATIONAL PUBLICATION, SOME INFORMATION WAS MISSING UNDER (71). THE MISSING INFORMATION NOW APPEARS IN THE CORRECTED VERSION |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application | ||
| WWE | Wipo information: entry into national phase |
Ref document number: 2005775932 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2007528703 Country of ref document: JP Ref document number: 2578838 Country of ref document: CA |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWP | Wipo information: published in national office |
Ref document number: 2005775932 Country of ref document: EP |