PEF-τs-ExpressionseinheitenP EF- τs expression units
Beschreibungdescription
Die vorliegende Erfindung betrifft die Verwendung von Nukleinsäuresequenzen zur Regulation der Transkription und Expression von Genen, die neuen Promotoren und Expressionseinheiten selbst, Verfahren zur Veränderung oder Verursachung der Transkriptionsrate und/oder Expressionsrate von Genen, Expressionskasetten, enthal¬ tend die Expressionseinheiten, genetisch veränderte Mikroorganismen mit veränderter oder verursachter Trankriptionsrate und/oder Expressionsrate sowie Verfahren zurThe present invention relates to the use of nucleic acid sequences for the regulation of the transcription and expression of genes, the novel promoters and expression units themselves, methods for altering or causing the transcription rate and / or expression rate of genes, expression cassettes containing the expression units, genetically modified microorganisms altered or induced rate of transcription and / or rate of expression and methods for
Herstellung von biosynthetischen Produkten durch Kultivierung der genetisch veränder¬ ten Mikroorganismen.Production of biosynthetic products by culturing the genetically modified microorganisms.
Verschiedene biosynthetische Produkte, wie beispielsweise Feinchemikalien, wie unter anderem Aminosäuren, Vitamine aber auch Proteine werden über natürliche Stoff¬ wechselprozesse in Zellen hergestellt und werden in vielen Industriezweigen verwen¬ det, einschließlich der Nahrungsmittel-, Futtermittel-, Kosmetik-, Feed-, Food- und pharmazeutischen Industrie. Diöse Substanzen, die zusammen als Feinchemika¬ lien/Proteine bezeichnet werden, umfassen unter anderem organische Säuren, sowohl proteinogene als auch nicht-proteinogene Aminosäuren, Nukleotide und Nukleoside, Lipide und Fettsäuren, Diole, Kohlenhydrate, aromatische Verbindungen, Vitamine und Cofaktoren, sowie Proteine und Enzyme. Ihre Produktion erfolgt am zweckmäßigsten im Großmaßstab mittels Anzucht von Bakterien, die entwickelt wurden, um große Mengen der jeweils gewünschten Substanz zu produzieren und sezernieren. Für die- sen Zweck besonders geeignete Organismen sind coryneforme Bakterien, gram¬ positive nicht-pathogene Bakterien.Various biosynthetic products, such as, for example, fine chemicals, such as, inter alia, amino acids, vitamins but also proteins, are produced in cells via natural metabolic processes and are used in many branches of industry, including foodstuffs, feedstuffs, cosmetics, feedstuffs and foods and pharmaceutical industry. Diole substances, which are collectively referred to as fine chemicals / proteins, include, among others, organic acids, both proteinogenic and non-proteinogenic amino acids, nucleotides and nucleosides, lipids and fatty acids, diols, carbohydrates, aromatic compounds, vitamins and cofactors, as well as proteins and enzymes. Their production is most conveniently made on a large scale by culturing bacteria that have been developed to produce and secrete large quantities of the desired substance. Particularly suitable organisms for this purpose are coryneform bacteria, gram-positive non-pathogenic bacteria.
Es ist bekannt, dass Aminosäuren durch Fermentation von Stämmen coryneformer Bakterien, insbesondere Corynebacterium glutamicum, hergestellt werden. Wegen der großen Bedeutung wird ständig an .der Verbesserung der Herstellverfahren gearbeitet. Verfahrensverbesserungen können fermentationstechnische Maßnahmen, wie zum Beispiel Rührung und Versorgung mit Sauerstoff, oder die Zusammensetzung der Nährmedien, wie zum Beispiel die Zuckerkonzentration während der Fermentation, oder die Aufarbeitung zum Produkt , beispielsweise durch lonenaustauschchroma- tographie aber auch Sprühtrocknung, oder die intrinsischen Leistungseigenschaften des Mikroorganismus selbst betreffen.It is known that amino acids are produced by fermentation of strains of coryneform bacteria, in particular Corynebacterium glutamicum. Because of the great importance is constantly working. The improvement of the manufacturing process. Process improvements may include fermentation measures, such as stirring and supply of oxygen, or the composition of the nutrient media, such as the sugar concentration during fermentation, or the processing of the product, for example by ion exchange chromatography but also spray-drying, or the intrinsic performance characteristics of the microorganism concern yourself.
Seit einigen Jahren werden ebenfalls Methoden der rekombinanten DNA-Technik zur Stammverbesserung von Feinchemikalien/Proteine produzierender Stämme von Cory- nebacterium eingesetzt, indem man einzelne Gene amplifiziert und die Auswirkung auf die Produktion von Feinchemikalien/Proteine untersucht.
Andere Wege, um ein Verfahren für die Herstellung Feinchemikalien, Aminosäuren oder Proteine zu entwickeln, oder die Produktivität eines bereits existierenden Verfah¬ rens für die Herstellung Feinchemikalien, Aminosäuren oder Proteine zu erhöhen bzw. zu verbessern, sind die Expression eines oder mehrerer Gene zu erhöhen bzw. zu verändern und oder die Translation einer mRNA durch geeignete Polynukleotidse- quenzen zu beeinflussen. Beeinflussung kann in diesem Zusammenhang die Erhö¬ hung, Verringerung, oder auch andere Parameter der Expression von Genen wie zeitli¬ che Expressionsmuster umfassen.For several years, methods of recombinant DNA technology have also been used for strain improvement of fine chemical / protein-producing strains of Corynebacterium by amplifying individual genes and examining the effect on the production of fine chemicals / proteins. Other ways to develop a process for the production of fine chemicals, amino acids or proteins, or to increase or to improve the productivity of an already existing process for the production of fine chemicals, amino acids or proteins, are to increase the expression of one or more genes or to modify and / or to influence the translation of an mRNA by means of suitable polynucleotide sequences. Influencing may in this context include increasing, decreasing, or other parameters of expression of genes such as temporal expression patterns.
Dem Fachmann sind unterschiedliche Bestandteile von bakteriellen Regulationsse¬ quenzen bekannt. Man unterscheidet die Bindungstellen von Regulatoren, auch Opera¬ toren genannt, die Bindungstellen von RNA-Polymerase-Holoenzymen, auch -35 und -10 Regionen genannt, und die Bindungsstelle von Ribosomaler 16S-RNA, auch Ribo- somale Bindungsstelle oder auch Shine-Dalgamo-Sequenz genannt.The skilled worker is aware of various constituents of bacterial regulatory sequences. A distinction is made between the binding sites of regulators, also called operators, the binding sites of RNA polymerase holoenzymes, also called -35 and -10 regions, and the binding site of ribosomal 16S RNA, also ribosomal binding site or Shine-Dalgamo Called sequence.
Als Sequenz einer Ribosomalen Bindungsstelle, auch Shine-Dalgarno-Sequenz ge¬ nannt, im Sinne dieser Erfindung werden Polynukleotidsequenzen verstanden, die sich bis zu 20 Basen stromauf des Initiationskodon der Translation befinden.The sequence of a ribosomal binding site, also called Shine-Dalgarno sequence, for the purposes of this invention is understood to mean polynucleotide sequences which are up to 20 bases upstream of the initiation codon of the translation.
In der Literatur (E. coli und S. typhimurium, Neidhardt F.C. 1995 ASM Press) wird be¬ schrieben, dass sowohl die Zusammensetzung der Polynukletidsequenz der Shine- Delgarno-Sequenz, die Sequenzabfolge der Basen, aber auch der Abstand einer in der Shine-Delgamo-Sequenz enthaltenen Polynukletidsequenz zum einen wesentlichen Einfluss auf die Initiationstionsrate der Translation hat.It is described in the literature (E. coli and S. typhimurium, Neidhardt FC 1995 ASM Press) that both the composition of the polynuclease sequence of the Shine-Delgarno sequence, the sequence sequence of the bases, but also the distance of one in the Shine Delgamo sequence contained polynucleotide sequence has a significant impact on the initiation rate of translation.
Nukleinsäuresequenzen mit Promotoraktivität können die Bildung von mRNA auf un¬ terschiedliche Weise beeinflussen. Promotoren, deren Aktivität unabhängig von der physiologischen Wachstumsphase des Organismus sind, nennt man konstitutiv. Wie¬ derum andere Promotoren reagieren auf externe chemische, wie physikalische Stimuli wie Sauerstoff, Metabolite, Hitze, pH, etc.. Wiederum andere zeigen in unterschiedli¬ chen Wachstumsphasen eine starke Abhängigkeit ihrer Aktivität. Beispielsweise sind in der Literatur Promotoren beschrieben, die während der exponentiellen Wachstums¬ phase von Mikroorganismen eine besonders ausgeprägte Aktivität zeigen, oder aber auch genau in der stationären Phase des mikrobieilen Wachstums. Beide Charakteris- tika von Promotoren können für eine Produktion von Feinchemikalien und Proteine je nach Stoffwechselweg einen günstigen Einfluss auf die Produktivität haben.Nucleic acid sequences with promoter activity can influence the formation of mRNA in different ways. Promoters whose activity is independent of the physiological growth phase of the organism are called constitutive. Again other promoters react to external chemical as well as physical stimuli such as oxygen, metabolites, heat, pH, etc. Still others show a strong dependence of their activity in different growth phases. For example, in the literature promoters are described which show a particularly pronounced activity during the exponential growth phase of microorganisms, or else exactly in the stationary phase of microbial growth. Both characteristics of promoters can have a favorable effect on productivity for the production of fine chemicals and proteins depending on the metabolic pathway.
Zum Beispiel kann man Promotoren die während des Wachstums die Expresssion ei¬ nes Gens ausschalten, diese aber nach einem optimalen Wachstum anschalten dazu nutzen, ein Gen zu regulieren, das die Produktion eines Metaboliten kontrolliert. Der
veränderte Stamm weist dann die gleichen Wachstumsparameter wie der Ausgangs¬ stamm auf, produziert aber mehr Produkt pro Zelle. Diese Art der Modifizierung kann sowohl den Titer (g Produkt/Liter) als auch die C-Ausbeute (g Produkt/g-C-Quelle) er¬ höhen.For example, one may use promoters which, during growth, turn off the expression of a gene, but turn it on after optimal growth, to regulate a gene that controls the production of a metabolite. Of the altered strain then has the same growth parameters as the Ausgangs¬ stem, but produces more product per cell. This type of modification can increase both the titer (g product / liter) and the C yield (g product / gC source).
In Corynebacterium Spezies konnten bereits solche Nukleotidsequenzen isoliert wer¬ den, die für eine Erhöhung bzw. eine Abschwächung der Genexpression genutzt wer¬ den können. Diese regulierten Promotoren können die Rate, mit der ein Gen transkri¬ biert wird, abhängig von den internen und/oder externen Bedingungen der Zelle erhö- hen oder erniedrigen. Zum Teil kann die Anwesenheit eines bestimmten Faktors, be¬ kannt als Inducer, die Rate der Transkrition vom Promotor stimulieren. Inducer können direkt oder aber indirekt die Transkription vom Promotor beeinflussen. Eine andere Klasse von Faktoren, bekannt als Suppressoren ist in der Lage, die Transkription vom Promotor zu reduzieren oder aber zu inhibieren. Wie auch die Inducer, können auch die Suppressoren direkt oder indirekt wirken. Es sind jedoch auch Promotoren bekannt, die über die Temperatur reguliert werden. So kann der Level der Transkription solcher Promotoren zum Beispiel durch eine Erhöhung der Wachstumstemperatur über die normale Wachstumstemperatur der Zelle erhöht oder aber abgeschwächt werden.In Corynebacterium species, it has already been possible to isolate those nucleotide sequences which can be used for increasing or weakening gene expression. These regulated promoters may increase or decrease the rate at which a gene is transcribed, depending on the internal and / or external conditions of the cell. In part, the presence of a particular factor, known as an inducer, may stimulate the rate of transcription from the promoter. Inducers may directly or indirectly affect transcription from the promoter. Another class of factors known as suppressors is capable of reducing or inhibiting transcription from the promoter. Like the inducer, the suppressors can act directly or indirectly. However, there are also promoters known that are regulated by temperature. Thus, for example, the level of transcription of such promoters may be increased or decreased by increasing the growth temperature above the normal growth temperature of the cell.
Eine geringe Anzahl von Promotoren aus C. glutamicum wurden bis zum heutigen Tag beschrieben. Der Promotor des Malatsynthase-Gens aus C. glutamicum wurde im DE 4440118 beschrieben. Dieser Promotor wurde einem für ein Protein kodierendes Struk¬ turgen vorgeschaltet. Nach Transformation eines solchen Konstrukts in ein corynefor- mes Bakterium wird die Expression des dem Promotor nachgeschalteten Strukturgen reguliert. Die Expression des Strukturgens wird induziert sobald dem Medium ein ensprechender Induktor zugesetzt wird.A small number of promoters from C. glutamicum have been described to date. The promoter of the malate synthase gene from C. glutamicum was described in DE 4440118. This promoter was preceded by a structural protein coding for a protein. After transformation of such a construct into a coryneform bacterium, the expression of the downstream structural gene is regulated. The expression of the structural gene is induced as soon as a corresponding inducer is added to the medium.
Reinscheid et al., Microbiology 145:503 (1999) haben eine trankriptionelle Fusion zwi¬ schen dem pta-ack Promotor aus C. glutamicum und einem Reportergen (ChIo- ramphenicol Acetyltransferase) beschrieben. Zellen von C. glutamicum, die eine solche transkriptioneile Fusion enthalten, wiesen eine erhöhte Expression des Reportergenes bei Wachstum auf Acetat haltigem Medium auf. Im Vergleich dazu zeigten transfor¬ mierte Zellen, die auf Glucose wuchsen, keine erhöhte Expression dieses Reporter¬ gens.Reinscheid et al., Microbiology 145: 503 (1999) have described a transcriptional fusion between the pta-ack promoter from C. glutamicum and a reporter gene (chloramphenicol acetyltransferase). Cells of C. glutamicum containing such transcriptional fusion exhibited increased expression of the reporter gene upon growth on acetate-containing medium. In comparison, transformed cells which grew on glucose showed no increased expression of this reporter gene.
In Pa'tek et al., Microbiology 142:1297 (1996) wurden einige DNA Sequenzen aus C. glutamicum beschrieben, die die Expression eines Reportergens in C. glutamicum Zel¬ len verstärken können, beschrieben. Diese Sequenzen wurden miteinander verglichen, um Consensus-Sequenzen für C. glutamicum Promotoren zu definieren.
Weitere DNA-Sequenzen aus C. glutamicum, die zur Regulation der Genexpression genutzt werden können, sind im Patent WO 02/40679 beschrieben worden. Diese iso¬ lierten Polynukleotide stellen Expressionseinheiten aus Corynebakterium glutamicum dar, die entweder zur Erhöhung oder aber zur Verringerung einer Genexpression ge- nutzt werden können. Weiterhin sind in diesem Patent rekombinante Plasmide be¬ schrieben, auf denen die Expressionseinheiten aus Corynebakterium glutamicum mit heterologen Genen assoziiert sind. Die hier beschrieben Methode , Fusion von einem Promotor aus Corynebakterium glutamicum mit einem heterlogen Gen, kann unter an¬ derem zur Regulation der Gene der Aminosäurebiosynthese eingesetzt werden.In Pa 'tek et al, Microbiology 142:. 1297 (1996) described some DNA sequences from C. glutamicum, which can enhance len of a reporter gene in C. glutamicum Zel¬ the expression described. These sequences were compared to define consensus sequences for C. glutamicum promoters. Further DNA sequences from C. glutamicum, which can be used to regulate gene expression, have been described in the patent WO 02/40679. These isolated polynucleotides represent expression units from Corynebacterium glutamicum, which can be used either to increase or to reduce gene expression. Furthermore, recombinant plasmids are described in this patent, on which the expression units from Corynebacterium glutamicum are associated with heterologous genes. The method described here, fusion of a promoter from Corynebacterium glutamicum with a heterologous gene, can be used, inter alia, for regulating the genes of the amino acid biosynthesis.
Der Erfindung lag die Aufgabe zugrunde weitere Promotoren und/oder Expressions¬ einheiten mit vorteilhaften Eigenschaften zur Verfügung zustellen.The object of the invention was to provide further promoters and / or expression units with advantageous properties.
Demgemäß wurde gefunden, dass man Nukleinsäuren mit Promotoraktivität, enthal- tendAccordingly, it has been found that nucleic acids with promoter activity, containing
A) die Nukleinsäuresequenz SEQ. ID. NO. 1 oderA) the nucleic acid sequence SEQ. ID. NO. 1 or
B) eine von dieser Sequenz durch Substitution, Insertion oder Deletion von Nukleo¬ tiden abgeleitete Sequenz, die eine Identität von mindestens 90 % auf Nuklein- säureebene mit der Sequenz SEQ. ID. NO. 1 aufweist oderB) a sequence derived from this sequence by substitution, insertion or deletion of nucleotides which has an identity of at least 90% at the nucleic acid level with the sequence SEQ. ID. NO. 1 or
C) eine Nukleinsäuresequenz, die mit der Nukleinsäuresequenz SEQ. ID. NO. 1 un¬ ter stringenten Bedingungen hybridisiert oderC) a nucleic acid sequence which is linked to the nucleic acid sequence SEQ. ID. NO. 1 hybridized under stringent conditions or
D) funktionell äquivalente Fragmente der Sequenzen unter A), B) oder C)D) functionally equivalent fragments of the sequences under A), B) or C)
zur Transkription von Genen verwenden kann.can use for the transcription of genes.
Unter „Transkription" wird erfindungsgemäß der Prozess verstanden, durch den aus¬ gehend von einer DNA-Matrize ein komplementäres RNA-Molekül hergestellt wird. An diesem Prozess sind Proteine wie die RNA-Polymerase sogenannte Sigma-Faktoren und transkriptionelle Regulatorproteine beteiligt. Die synthetisierte RNA dient dann als Matrize im Prozess der Translation, der dann zum biosynthetisch aktiven Protein führt.According to the invention, "transcription" is understood to mean the process by which a complementary DNA molecule is produced by a DNA template, in which process proteins such as RNA polymerase are involved in so-called sigma factors and transcriptional regulatory proteins then serves as a template in the process of translation, which then leads to the biosynthetically active protein.
Die Bildungsrate, mit der ein biosynthetsich aktives Protein hergestellt wird, ist ein Pro- dukt aus der Rate der Transkription und der Translation. Beide Raten können erfin¬ dungsgemäß beeinflusst werden und damit die Rate der Bildung von Produkten in ei¬ nem Mikroorganismus beeinflussen.
Unter einem „Promotor" oder einer „Nukleinsäure mit Promotoraktivität" wird erfin¬ dungsgemäß eine Nukleinsäure verstanden, die in funktioneller Verknüpfung mit einer zu trankripierenden Nukleinsäure, die Transkription dieser Nukleinsäure reguliert.The rate at which a biosynthetic active protein is produced is a product of the rate of transcription and translation. Both rates can be influenced according to the invention and thus influence the rate of formation of products in a microorganism. A "promoter" or a "nucleic acid with promoter activity" is understood as meaning according to the invention a nucleic acid which, in functional linkage with a nucleic acid to be transected, regulates the transcription of this nucleic acid.
Unter einer „funktionellen Verknüpfung" versteht man in diesem Zusammenhang bei¬ spielsweise die sequentielle Anordnung einer der erfindungsgemäßen Nukleinsäuren mit Promotoraktivität und einer zu transkribierenden Nukleinsäuresequenz und ggf. weiterer regulativer Elemente wie zum Beispiel Nukleinsäureseuqenzen, die die Transkription von Nukleinsäuren gewährleisten, sowie zum Beipsiel einen Terminator derart, dass jedes der regulativen Elemente seine Funktion bei der Transkription der der Nukleinsäuresequenz erfüllen kann. Dazu ist nicht unbedingt eine direkte Verknüp¬ fung im chemischen Sinne erforderlich. Genetische Kontrollsequenzen, wie zum Bei¬ spiel Enhancer-Sequenzen, können ihre Funktion auch von weiter entfernten Positio¬ nen oder gar von anderen DNA-Molekülen aus auf die Zielsequenz ausüben. Bevor- zugt sind Anordnungen, in denen die zu trankribierende Nukleinsäuresequenz hin¬ ter (d.h. am 3'-Ende) der erfindungsgemäßen Promotorsequenz positioniert wird, so dass beide Sequenzen kovalent miteinander verbunden sind. Bevorzugt ist dabei der Abstand zwischen der Promotorsequenz und der transgen zu exprimierende Nuklein¬ säuresequenz geringer als 200 Basenpaare, besonders bevorzugt kleiner als 100 Basenpaare, ganz besonders bevorzugt kleiner als 50 Basenpaare.In this context, a "functional linkage" is understood to mean, for example, the sequential arrangement of one of the nucleic acids according to the invention with promoter activity and a nucleic acid sequence to be transcribed and, if appropriate, further regulatory elements, for example nucleic acid sequences which ensure the transcription of nucleic acids, and for example Terminator such that each of the regulatory elements can fulfill its function in the transcription of the nucleic acid sequence.This does not necessarily require a direct linkage in the chemical sense.Genetic control sequences, such as for example enhancer sequences, can also function Preference is given to arrangements in which the nucleic acid sequence to be transcribed is positioned behind the (ie at the 3 'end) of the promoter sequence according to the invention rd, so that both sequences are covalently linked. The distance between the promoter sequence and the nucleic acid sequence to be expressed transgenically is preferably less than 200 base pairs, more preferably less than 100 base pairs, very particularly preferably less than 50 base pairs.
Unter „Promotoraktivität" wird erfindungsgemäß die in einer bestimmten Zeit durch den Promotor gebildete Menge RNA, also die Trankriptionsrate verstanden.According to the invention, "promoter activity" is understood as meaning the amount of RNA, that is to say the transcription rate, formed by the promoter in a specific time.
Unter „spezifischer Promotoraktivität" wird erfindungsgemäß die in einer bestimmten Zeit durch den Promotor gebildete Menge RNA pro Promotor verstanden.By "specific promoter activity" is meant according to the invention the amount of RNA per promoter formed by the promoter in a certain time.
Unter dem Begriff "Wildtyp" wird erfindungsgemäß der entsprechende Ausgangsmikro¬ organismus verstanden.The term "wild-type" is understood according to the invention as the corresponding starting microorganism.
Je nach Zusammenhang kann unter dem Begriff "Mikroorganismus" der Ausgangsmik¬ roorganismus (Wildtyp) oder ein erfindungsgemäßer, genetisch veränderter Mikroorga¬ nismus oder beides verstanden werden.Depending on the context, the term "microorganism" may be understood as meaning the starting microorganism (wild-type) or a genetically modified microorganism according to the invention or both.
Vorzugsweise und insbesondere in Fällen, in denen der Mikroorganismus oder der Wildtyp nicht eindeutig zugeordnet werden kann, wird unter "Wildtyp" für die Verände¬ rung oder Verursachung der Promotoraktivität oder Trankriptionsrate, für die Verände¬ rung oder Verursachung der Expressionsaktivität oder Expressionsrate und für die Er¬ höhung des Gehalts an biosynthetischen Produkten jeweils ein Referenzorganismus verstanden.
In einer bevorzugten Ausführungsform ist dieser Referenzorganismus Corynebakteri- um glutamicum ATCC 13032.Preferably and in particular in cases in which the microorganism or the wild type can not be unambiguously assigned, the term "wild-type" is used to change or cause the promoter activity or transcription rate, to change or cause the expression activity or expression rate, and for the Er¬ increase the content of biosynthetic products each understood a reference organism. In a preferred embodiment, this reference organism is Corynebacterium glutamicum ATCC 13032.
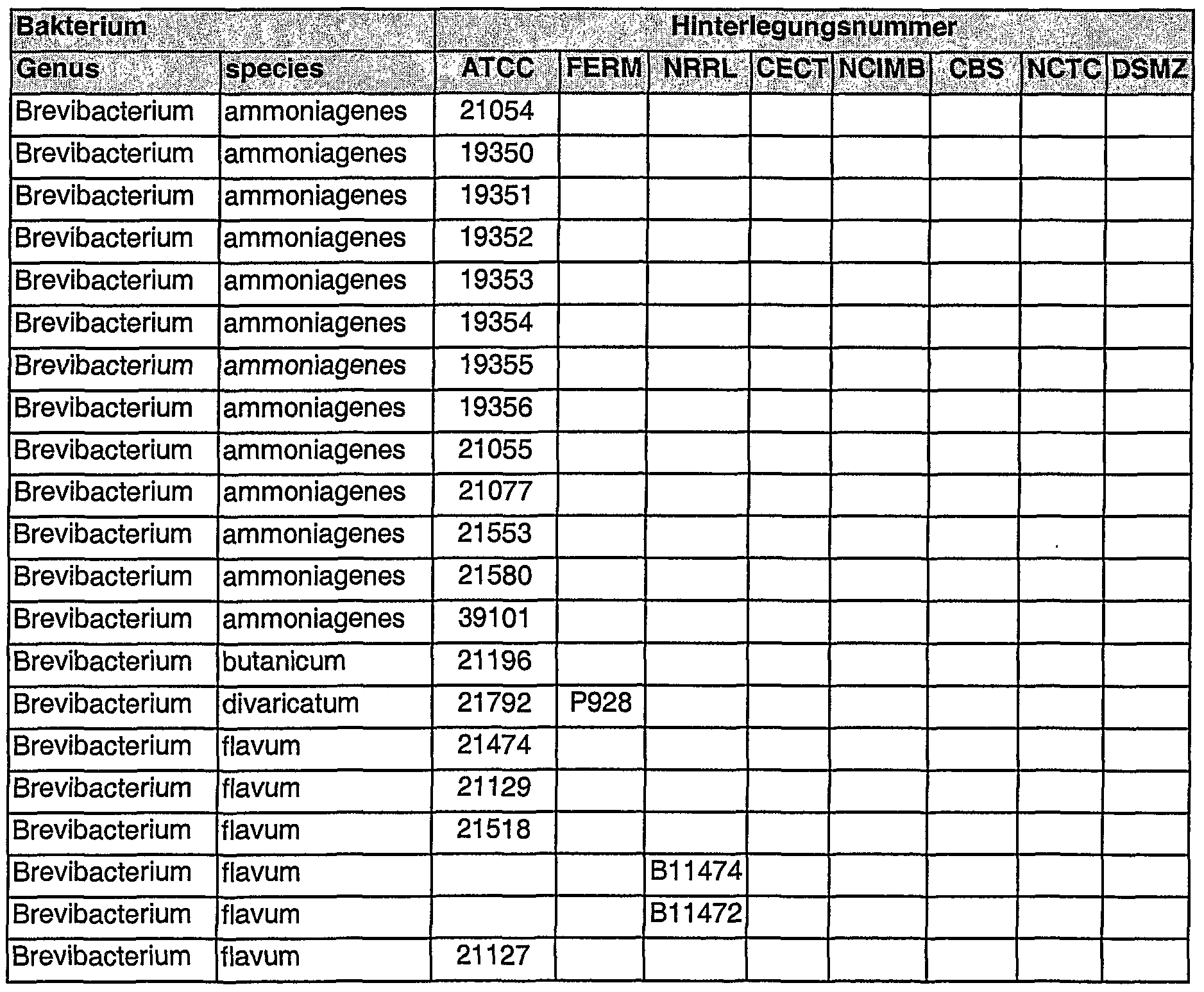
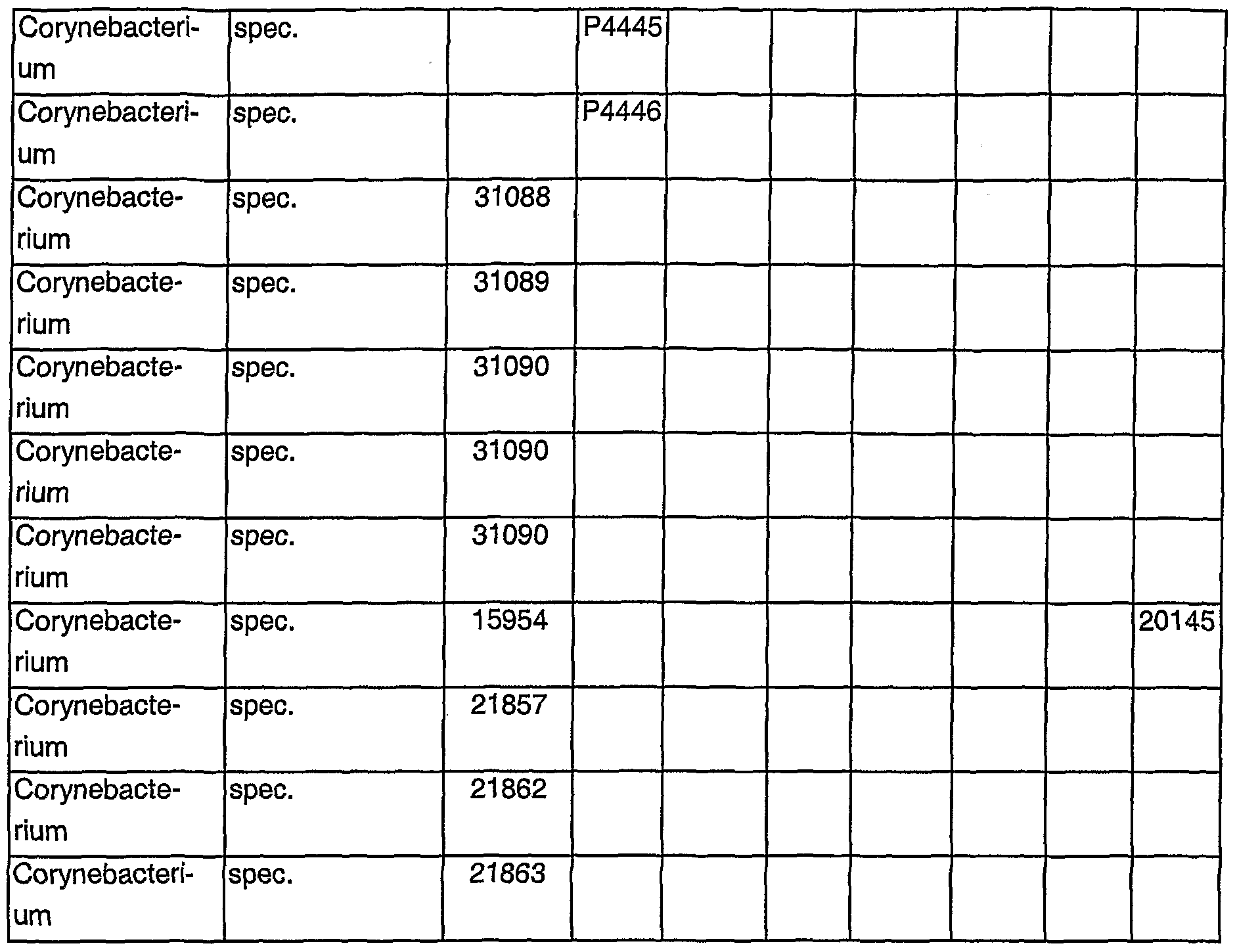
In einer bevorzugten Ausführungsform werden Ausgangsmikroorganismen verwendet die bereits in der Lage sind, die gewünschte Feinchemikalie herzustellen. Besonders bevorzugt sind dabei unter den besonders bevorzugten Mikroorganismen der Bakterien der Gattung Corynebacterien und den besonders bevorzugten Feinchemikalien L- Lysin, L-Methionin und L-Threonin, diejenigen Ausgangsmikroorganismen die bereits in der Lage sind, L-Lysin, L-Methionin und/oder L-Threonin herzustellen. Dies sind be¬ sonderes bevorzugt Corynebakterien bei denen beispielsweise das Gen kodierend für eine Aspartokinase (ask-Gen) dereguliert ist oder die feed-back-lnhibierung aufgeho¬ ben oder reduziert ist. Beispielsweise weisen solche Bakterien im ask-Gen eine Muta¬ tion auf, die zu einer Reduzierung oder Aufhebung der feed-back-lnhibierung führen, wie beispielsweise die Mutation T3111.In a preferred embodiment, starting microorganisms are used which are already capable of producing the desired fine chemical. Among the particularly preferred microorganisms of the bacteria of the genus Corynebacteria and the particularly preferred fine chemicals L-lysine, L-methionine and L-threonine, those starting microorganisms which are already able to produce L-lysine, L-methionine and / or are particularly preferred To produce L-threonine. These are particularly preferably corynebacteria in which, for example, the gene coding for an aspartokinase (ask gene) is deregulated or the feed-back inhibition is stopped or reduced. For example, such bacteria have a mutation in the ask gene which leads to a reduction or abolition of the feedback inhibition, for example the mutation T3111.
Bei einer „verursachten Promotoraktivität" oder Transkriptionsrate im Bezug auf ein Gen im Vergleich zum Wildtyp wird somit im Vergleich zum Wildtyp die Bildung einer RNA verursacht, die im Wildtyp so nicht vorhanden war.With a "caused promoter activity" or transcription rate with respect to a gene compared to the wild type, the formation of a RNA is thus caused in comparison to the wild type, which was thus not present in the wild type.
Bei einer veränderten Promotoraktivität oder Transkriptionsrate im Bezug auf ein Gen im Vergleich zum Wildtyp wird somit im Vergleich zum Wildtyp in einer bestimmten Zeit die gebildete Menge der RNA verändert.In the case of an altered promoter activity or transcription rate with respect to a gene in comparison to the wild type, the amount of RNA formed is thus changed in a certain time compared to the wild type.
Unter „verändert" wird in diesem Zusammenhang bevorzugt erhöht oder erniedrigt ver¬ standen.In this context, "changed" is preferably increased or decreased.
Dies kann beispielsweise durch Erhöhung oder Reduzierung der spezifischen Promo¬ toraktivität des endogenen erfindungsgemäßen Promotors, beispielsweise durch Muta- tion des Promotors oder durch Stimmulierung oder Hemmung des Promotors erfolgen.This can be done, for example, by increasing or reducing the specific promoter activity of the endogenous promoter according to the invention, for example by mutation of the promoter or by stimulation or inhibition of the promoter.
Weiterhin kann die erhöhte Promotoraktivität oder Transkriptionsrate beispielsweise durch Regulation der Transkription von Genen im Mikroorganismus durch erfindungs¬ gemäße Nukleinsäuren mit Promotoraktivität oder durch Nukleinsäuren mit erhöhter spezifischer Prαmotoraktivität erreicht werden, wobei die Gene in Bezug auf die Nuk¬ leinsäuren mit Promotoraktivität heterolog sind.Furthermore, the increased promoter activity or transcription rate can be achieved, for example, by regulating the transcription of genes in the microorganism by nucleic acids according to the invention having promoter activity or by nucleic acids having increased specific promoter activity, the genes being heterologous with respect to the nucleic acids having promoter activity.
Vorzusgweise wird die Regulation der Transkription von Genen im Mikroorganismus durch erfindungsgemäße Nukleinsäuren mit Promotoraktivität oder durch Nukleinsäu- ren mit erhöhter spezifischer Promotoraktivität dadurch erreicht, dass man
eine oder mehrere erfindungsgemäße Nukleinsäuren mit Promotoraktivität, gegebe¬ nenfalls mit veränderter spezifischer Promotoraktivität, in das Genom des Mikroorga¬ nismus einbringt, so dass die Transkription eines oder mehrerer endogenen Gene un- ter der Kontrolle der eingebrachten erfindungsgemäßen Nukleinsäure mit Promotorak¬ tivität gegebenenfalls mit veränderter spezifischer Promotoraktivität, erfolgt oderVorzusgweise the regulation of the transcription of genes in the microorganism by nucleic acids according to the invention with promoter activity or by nucleic acids with increased specific promoter activity is achieved by one or more nucleic acids according to the invention having promoter activity, where appropriate with altered specific promoter activity, are introduced into the genome of the microorganism such that the transcription of one or more endogenous genes under the control of the incorporated nucleic acid according to the invention having promoter activity is optionally altered specific promoter activity, or
ein oder mehrere Gene in das Genom des Mikrorganismus einbringt, so dass die Transkription eines oder mehrerer der eingebrachten Gene unter der Kontrolle der en- dogenen erfindungsgemäßen Nukleinsäuren mit Promotoraktivität, gegebenenfalls mit veränderter spezifischer Promotoraktivität, erfolgt oderintroducing one or more genes into the genome of the microorganism so that the transcription of one or more of the introduced genes takes place under the control of the endogenous nucleic acids according to the invention having promoter activity, optionally with altered specific promoter activity, or
ein oder mehrere Nukleinsäurekonstrukte, enthaltend eine erfindungsgemäße Nuklein¬ säure mit Promotoraktivität, gegebenenfalls mit veränderter spezifischer Promotorakti- vität, und funktionell verknüpft eine oder mehrere, zu transkribierende Nukleinsäuren, in den Mikroorganismus einbringt.one or more nucleic acid constructs comprising a nucleic acid according to the invention having promoter activity, optionally with altered specific promoter activity, and functionally linking one or more nucleic acids to be transcribed into which microorganism introduces.
Die erfindungsgemäßen Nukleinsäuren mit Promotoraktivität enthaltenThe nucleic acids according to the invention with promoter activity contain
A) die Nukleinsäuresequenz SEQ. ID. NO. 1 oder B) eine von dieser Sequenz durch Substitution, Insertion oder Deletion von Nukleo¬ tiden abgeleitete Sequenz, die eine Identität von mindestens 90 % auf Nuklein- säureebene mit der Sequenz SEQ. ID. NO. 1 aufweist oderA) the nucleic acid sequence SEQ. ID. NO. 1 or B) a sequence derived from this sequence by substitution, insertion or deletion of nucleotides which has an identity of at least 90% at the nucleic acid level with the sequence SEQ. ID. NO. 1 or
C) eine Nukleinsäuresequenz, die mit der Nukleinsäuresequenz SEQ. ID. NO. 1 un- ter stringenten Bedingungen hybridisiert oderC) a nucleic acid sequence which is linked to the nucleic acid sequence SEQ. ID. NO. 1 hybridized under stringent conditions or
D) funktionell äquivalente Fragmente der Sequenzen unter A), B) oder C)D) functionally equivalent fragments of the sequences under A), B) or C)
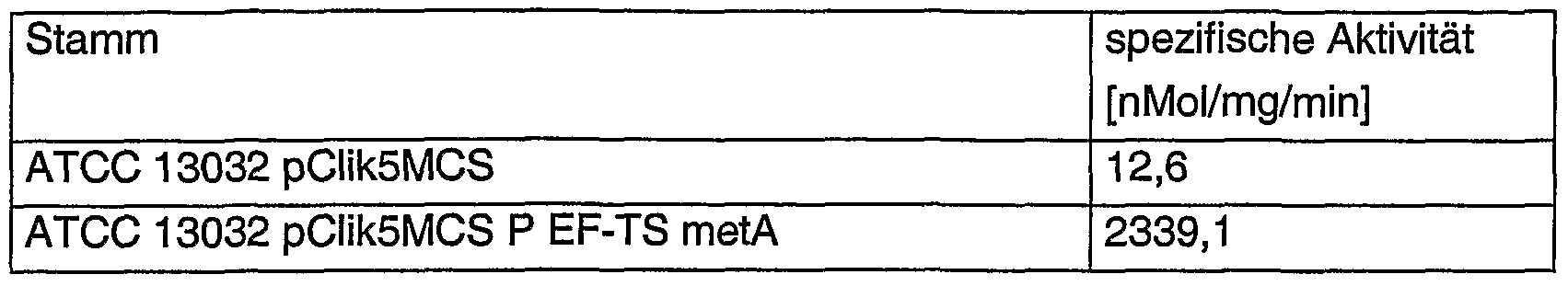
Die Nukleinsäuresequenz SEQ. ID. NO. 1 stellt die Promotorsequenz des Elongations- Faktors TS (PEF-TS) aus Corynebakterium glutamicum dar. SEQ. ID.NO. 1 entspricht der Promotorsequenz des Wildtyps.The nucleic acid sequence SEQ. ID. NO. 1 represents the promoter sequence of the elongation factor TS (PEF-TS) from Corynebacterium glutamicum. SEQ. ID.NO. 1 corresponds to the wild-type promoter sequence.
Die Erfindung betrifft weiterhin Nukleinsäuren mit Promotoraktivität enthaltend eine von dieser Sequenz durch Substitution, Insertion oder Deletion von Nukleotiden abgeleitete Sequenz, die eine Identität von mindestens 90 % auf Nukleinsäureebene mit der Se- quenz SEQ. ID. NO. 1 aufweist.The invention further relates to nucleic acids with promoter activity comprising a sequence derived from this sequence by substitution, insertion or deletion of nucleotides, which has an identity of at least 90% at the nucleic acid level with the sequence SEQ. ID. NO. 1 has.
Weitere natürliche erfindungsgemäße Beispiele für erfindungsgemäße Promotoren lassen sich beispielsweise aus verschiedenen Organismen, deren genomische Se¬ quenz bekannt ist, durch Identitätsvergleiche der Nukleinsäuresequenzen aus Daten-
banken mit der vorstehend beschriebenen Sequenzen SEQ ID NO: 1 leicht auffinden.Further natural examples according to the invention of promoters according to the invention can be prepared, for example, from various organisms whose genomic sequence is known by identity comparisons of the nucleic acid sequences from data Banks with the above-described sequences SEQ ID NO: 1 easily find.
Künstliche erfindungsgemäße Promotor-Sequenzen lassen sich ausgehend von der Sequenz SEQ ID NO: 1 durch künstliche Variation und Mutation, beispielsweise durch Substitution, Insertion oder Deletion von Nukleotiden leicht auffinden.Artificial promoter sequences according to the invention can easily be found starting from the sequence SEQ ID NO: 1 by artificial variation and mutation, for example by substitution, insertion or deletion of nucleotides.
Unter dem Begriff "Substitution" ist in der Beschreibung der Austausch einer oder meh¬ rerer Nukleotide durch ein oder mehrere Nukleotide zu verstehen. „Deletion" ist das Ersetzen eines Nukleotides durch eine direkte Bindung. Insertionen sind Einfügungen von Nukleotiden in die Nukleinsäuresequenz, wobei formal eine direkte Bindung durch ein oder mehrere Nukleotide ersetzt wird.The term "substitution" in the description refers to the replacement of one or more nucleotides by one or more nucleotides. "Deletion" is the replacement of a nucleotide by a direct bond Insertions are insertions of nucleotides into the nucleic acid sequence which formally replaces a direct bond with one or more nucleotides.
Unter Identität zwischen zwei Nukleinsäuren wird die Identität der Nukleotide über die jeweils gesamte Nukleinsäurelänge verstanden, insbesondere die Identität die durch Vergleich mit Hilfe der Vector NTI Suite 7.1 Software der Firma Informax (USA) unter Anwendung der Clustal Methode (Higgins DG, Sharp PM. Fast and sensitive multiple sequence alignments on a microcomputer. Comput Appl. Biosci. 1989 Apr;5(2):151-1) unter Einstellung folgender Parameter berechnet wird:Identity between two nucleic acids is understood to mean the identity of the nucleotides over the entire nucleic acid length, in particular the identity which was determined by comparison with the Vector NTI Suite 7.1 software from Informax (USA) using the Clustal method (Higgins DG, Sharp PM Biosci 1989 Apr; 5 (2): 151-1) is calculated by setting the following parameters: and sensitive multiple sequence alignments on a microcomputer.
Multiple alignment parameter:Multiple alignment parameters:
Gap opening penalty 10Gap opening penalty 10
Gap extension penalty 10Gap extension penalty 10
Gap Separation penalty ränge 8Gap Separation penalty ranks 8
Gap Separation penalty off % identity for alignment deiay 40Gap separation penalty off% identity for alignment deiay 40
Residue specific gaps offResidue specific gaps off
Hydrophilic residue gap offHydrophilic residues gap off
Transition weighing 0Transition weighing 0
Pairwise alignment parameter:Pairwise alignment parameter:
FAST algorithm onFAST algorithm on
K-tuplesize 1K-tuplesize 1
Gap penalty 3Gap penalty 3
Window size 5 Number of best diagonale 5Window size 5 Number of best diagonal 5
Unter einer Nukleinsäuresequenz, die eine Identität von mindestens 90 % mit der Se¬ quenz SEQ ID NO: 1 aufweist, wird dementsprechend eine Nukleinsäuresequenz ver¬ standen, die bei einem Vergleich seiner Sequenz mit der Sequenz SEQ ID NO: 1 , ins-
besondere nach obigen Programmlogarithmus mit obigem Parametersatz eine Identität von mindestens 90 % aufweist.A nucleic acid sequence which has an identity of at least 90% with the sequence SEQ ID NO: 1 is accordingly understood to mean a nucleic acid sequence which, in a comparison of its sequence with the sequence SEQ ID NO: 1, in particular special according to the above program logarithm with the above parameter set has an identity of at least 90%.
Besonders bevorzugte Promotoren weisen mit der Nukleinsäuresequenz SEQ. ID. NO. 1 eine Identität von 91%, bevorzugter 92%, 93%, 94%, 95%, 96%, 97%, 98%, beson¬ ders bevorzugt 99% auf.Particularly preferred promoters have with the nucleic acid sequence SEQ. ID. NO. 1 has an identity of 91%, more preferably 92%, 93%, 94%, 95%, 96%, 97%, 98%, more preferably 99%.
Weitere natürliche Beispiele für Promotoren lassen sich weiterhin ausgehend von den vorstehend beschriebenen Nukleinsäuresequenzen, insbesondere ausgehend von der Sequenz SEQ ID NO: 1 aus verschiedenen Organismen, deren genomische Sequenz nicht bekannt ist, durch Hybridisierungstechniken in an sich bekannter Weise leicht auffinden.Further natural examples of promoters can furthermore readily be found starting from the above-described nucleic acid sequences, in particular starting from the sequence SEQ ID NO: 1 from various organisms whose genomic sequence is unknown, by hybridization techniques in a manner known per se.
Ein weiterer Gegenstand der Erfindung betrifft daher Nukleinsäuren mit Promotoraktivi- tat, enthaltend eine Nukleinsäuresequenz, die mit der Nukleinsäuresequenz SEQ. ID. No. 1 unter stringenten Bedingungen hybridisiert. Diese Nukleinsäuresequenz umfasst mindestens 10, bevorzugter mehr als12,15,30,50 oder besonders bevorzugt mehr als 150 Nukleotide.Another object of the invention therefore relates to nucleic acids with Promotoraktivi- tat, containing a nucleic acid sequence with the nucleic acid sequence SEQ. ID. No. 1 hybridized under stringent conditions. This nucleic acid sequence comprises at least 10, more preferably more than 12, 15, 30, 50, or more preferably more than 150 nucleotides.
Die Hybridisierung erfolgt erfinungsgemäß unter stringenten Bedingungen. SolcheThe hybridization is carried out according to the invention under stringent conditions. Such
Hybridisierungsbedingungen sind beispielsweise bei Sambrook, J., Fritsch, E. F., Mani- atis, T., in: Molecular Cloning (A Laboratory Manual), 2. Auflage, CoId Spring Harbor Laboratory Press, 1989, Seiten 9.31-9.57 oder in Current Protocols in Molecular Biolo- gy, John Wiley & Sons, N. Y. (1989), 6.3.1-6.3.6 beschrieben:Hybridization conditions are described, for example, in Sambrook, J., Fritsch, EF, Maniatis, T., in: Molecular Cloning (A Laboratory Manual), 2nd Edition, ColD Spring Harbor Laboratory Press, 1989, pages 9.31-9.57 or in Current Protocols in Molecular Biolgy, John Wiley & Sons, NY (1989), 6.3.1-6.3.6:
Unter stringenten Hybridisierungs-Bedingungen werden insbesondere verstanden: Die über Nacht Inkubation bei 42°C in einer Lösung bestehend aus 50 % Formamid, 5 x SSC (750 mM NaCI, 75 mM Tri-Natrium Citrat), 50 mM Natrium Phosphat (ph7,6), 5x Denhardt Lösung, 10% Dextransulfat und 20 g/ml denaturierte, gescheerte Lachsspermien-DNA, gefolgt von einem Waschen der Filter mit 0,1x SSC bei 650C.By stringent hybridization conditions are meant in particular: The overnight incubation at 42 ° C in a solution consisting of 50% formamide, 5 x SSC (750 mM NaCl, 75 mM trisodium citrate), 50 mM sodium phosphate (pH 7.6 ), 5x Denhardt solution, 10% dextran sulfate, and 20 g / ml denatured, sheared salmon sperm DNA, followed by washing the filter with 0.1x SSC at 65 0 C.
Unter einem „funktionell äquivalenten Fragment" werden für Nukleinsäuresequenzen mit Promotoraktivität, Fragmente verstanden die im wesentlichen die gleiche oder eine höhere spezifische Promotoraktivität aufweisen wie die Ausgangssequenz.A "functionally equivalent fragment" for nucleic acid sequences with promoter activity, fragments understood that have substantially the same or higher specific promoter activity as the starting sequence.
Unter „im wesentlichen gleich" wird eine spezifische Promotoraktivität verstanden die mindestens 50%, vorzugsweise 60%, bevorzugter 70%, bevorzugter 80%, bevorzugter 90%, besonders bevorzugt 95% der spezifischen Promotoraktivität der Ausgangsse¬ quenz aufweist.
Unter „Fragmente" werden Teilsequenzen der durch Ausführungsform A), B) oder C) beschriebenen Nukleinsäuren mit Promotoraktivität verstanden. Vorzusgweise weisen diese Fragmente mehr als 10, bevorzugter aber mehr als 12,15, 30, 50 oder besonders bevorzugte mehr als 150 zusammenhängende Nukleotide der Nukleinsäuresequenz SEQ. ID. NO. 1 auf.By "substantially the same" is meant a specific promoter activity which has at least 50%, preferably 60%, more preferably 70%, more preferably 80%, more preferably 90%, most preferably 95% of the specific promoter activity of the starting sequence. By "fragments" is meant partial sequences of the nucleic acids having promoter activity described by embodiment A), B) or C. Preferably, these fragments have more than 10, more preferably more than 12, 15, 30, 50 or more preferably more than 150 contiguous nucleotides of the nucleic acid sequence SEQ ID NO: 1.
Besonders bevorzugt ist die Verwendung der Nukleinsäuresequenz SEQ. ID. NO. 1 als Promotor, d.h. zur Transkriptiion von Genen.Particularly preferred is the use of the nucleic acid sequence SEQ. ID. NO. 1 as a promoter, i. for the transcription of genes.
Die SEQ. ID. NO. 1 ist ohne Funktionszuordnung im Genbank-Eintrag AP005283 be¬ schrieben worden. Daher betrifft die Erfindung ferner die neuen, erfindungsgemäßen Nukleinsäuresequenzen mit Promotoraktivität.The SEQ. ID. NO. 1 has been described without function assignment in Genbank entry AP005283. Therefore, the invention further relates to the novel nucleic acid sequences according to the invention with promoter activity.
Insbesondere betrifft die Erfindung eine Nukleinsäure mit Promotoraktivität, enthaltendIn particular, the invention relates to a nucleic acid with promoter activity containing
A) die Nukleinsäuresequenz SEQ. ID. NO. 1 oderA) the nucleic acid sequence SEQ. ID. NO. 1 or
B) eine von dieser Sequenz durch Substitution, Insertion oder Deletion von Nukleotiden abgeleitete Sequenz, die eine Identität von mindestens 90 % auf Nukleinsäureebene mit der Sequenz SEQ. ID. NO. 1 aufweist oderB) a sequence derived from this sequence by substitution, insertion or deletion of nucleotides which has an identity of at least 90% at nucleic acid level with the sequence SEQ. ID. NO. 1 or
C) eine Nukleinsäuresequenz, die mit der Nukleinsäuresequenz SEQ. ID. NO. 1 unter stringenten Bedingungen hybridisiert oderC) a nucleic acid sequence which is linked to the nucleic acid sequence SEQ. ID. NO. 1 hybridized under stringent conditions or
D) funktionell äquivalente Fragmente der Sequenzen unter A), B) oder C),D) functionally equivalent fragments of the sequences under A), B) or C),
mit der Maßgabe, dass die Nukleinsäure mit der Sequenz SEQ. ID. NO. 1 ausgenom¬ men ist.with the proviso that the nucleic acid having the sequence SEQ. ID. NO. 1 is excluded.
Alle vorstehend erwähnten Nukleinsäuren mit Promotoraktivität sind weiterhin in an sich bekannter Weise durch chemische Synthese aus den Nukleotidbausteinen wie beispielsweise durch Fragmentkondensation einzelner überlappender, komplementärer Nukleinsäurebausteine der Doppelhelix herstellbar. Die chemische Synthese von Oli- gonukleotiden kann beispielsweise, in bekannter Weise, nach der Phosphoamidit- methode (Voet, Voet, 2. Auflage, Wiley Press New York, S. 896-897) erfolgen. Die An¬ lagerung synthetischer Oligonukleotide und Auffüllen von Lücken mithilfe des Klenow- Fragmentes der DNA-Polymerase und Ligationsreaktionen sowie allgemeine Klonie- rungsverfahren werden in Sambrook et al. (1989), Molecular cloning: A laboratory manual, CoId Spring Harbor Laboratory Press, beschrieben.All the above-mentioned nucleic acids with promoter activity can furthermore be produced in a manner known per se by chemical synthesis from the nucleotide units, for example by fragment condensation of individual overlapping, complementary nucleic acid units of the double helix. The chemical synthesis of oligonucleotides can be carried out, for example, in a known manner by the phosphoamidite method (Voet, Voet, 2nd edition, Wiley Press New York, pages 896-897). The An¬ storage of synthetic oligonucleotides and filling gaps with the Klenow fragment of the DNA polymerase and ligation reactions and general cloning procedures are in Sambrook et al. (1989), Molecular cloning: A laboratory manual, Col. Spring Harbor Laboratory Press.
Die Erfindung betrifft ferner die Verwendung einer Expressionseinheit, enthaltend eine der erfindungsgemäßen Nukleinsäuren mit Promotoraktivität und zusätzlich funktionell
verknüpft eine Nukleinsäuresequenz, die die Translation von Ribonukleinsäuren ge¬ währleistet, zur Expression von Genen.The invention further relates to the use of an expression unit comprising one of the nucleic acids according to the invention with promoter activity and additionally functional combines a nucleic acid sequence which ensures the translation of ribonucleic acids, for the expression of genes.
Unter einer Expressioneinheit wird erfindungsgemäß eine Nukleinsäure mit Expressi- onsaktivität verstanden, also eine Nukleinsäure verstanden, die in funktioneller Ver¬ knüpfung mit einer zu exprimierenden Nukleinsäure oder Gens, die Expression, also die Transkription und die Translation dieser Nukleinsäure oder dieses Gens reguliert.According to the invention, an expression unit is understood as meaning a nucleic acid with expression activity, ie a nucleic acid which, in functional linkage with a nucleic acid or gene to be expressed, regulates the expression, ie the transcription and the translation of this nucleic acid or gene.
Unter einer „funktionellen Verknüpfung" versteht man in diesem Zusammenhang bei- spielsweise die sequentielle Anordnung einer der erfindungsgemäßen Expressionsein¬ heit und einer transgen zu exprimierenden Nukleinsäuresequenz und ggf. weiterer re¬ gulativer Elemente wie zum Beispiel einem Terminator derart, dass jedes der regulati¬ ven Elemente seine Funktion bei der transgenen Expression der Nukleinsäuresequenz erfüllen kann. Dazu ist nicht unbedingt eine direkte Verknüpfung im chemischen Sinne erforderlich. Genetische Kontrollsequenzen, wie zum Beispiel Enhancer-Sequenzen, können ihre Funktion auch von weiter entfernten Positionen oder gar von anderen DNA-Molekülen aus auf die Zielsequenz ausüben. Bevorzugt sind Anordnungen, in denen die transgen zu exprimierende Nukleinsäuresequenz hinter (d.h. am 3'-Ende) der erfindungsgemäßen Expressionseinheitssequenz positioniert wird, so dass beide Sequenzen kovalent miteinander verbunden sind. Bevorzugt ist dabei der Abstand zwi¬ schen der Expressionseinheitssequenz und der transgen zu exprimierende Nuklein¬ säuresequenz geringer als 200 Basenpaare, besonders bevorzugt kleiner als 100 Basenpaare, ganz besonders bevorzugt kleiner als 50 Basenpaare.In this context, a "functional linkage" is understood to mean, for example, the sequential arrangement of one of the expression units according to the invention and of a nucleic acid sequence to be expressed transgenically and, if appropriate, further regulatory elements such as, for example, a terminator such that each of the regulators regulates This does not necessarily require a direct link in the chemical sense: genetic control sequences, such as enhancer sequences, may also function from more distant locations or even from other DNA molecules Preference is given to arrangements in which the nucleic acid sequence to be transgenically expressed is positioned behind (ie at the 3 'end) of the expression unit sequence according to the invention, so that both sequences are covalently linked to one another between the expression unit sequence and the nucleic acid sequence to be expressed transgene less than 200 base pairs, more preferably less than 100 base pairs, most preferably less than 50 base pairs.
Unter „Expressionsaktivität" wird erfindungsgemäß die in einer bestimmten Zeit durch die Expressionseinheit gebildete Menge Protein, also die Expressionsrate verstanden.According to the invention, "expression activity" is understood to mean the amount of protein formed by the expression unit over a certain period of time, ie the expression rate.
Unter „spezifischer Expressionsaktivität" wird erfindungsgemäß die in einer bestimmten Zeit durch die Expressionseinheit gebildete Menge Protein pro Expressionseinheit ver- standen.According to the invention, "specific expression activity" is understood to mean the amount of protein per expression unit formed by the expression unit in a specific time.
Bei einer „verursachten Expressionsaktivität" oder Expressionsrate im Bezug auf ein Gen im Vergleich zum Wildtyp wird somit im Vergleich zum Wildtyp die Bildung eines Proteins verursacht, das im Wildtyp so nicht vorhanden war.With a "caused expression activity" or expression rate with respect to a gene compared to the wild type, the formation of a protein is thus caused in comparison to the wild type, which was not so present in the wild type.
Bei einer „veränderten Expressionsaktivität" oder Expressionsrate im Bezug auf ein Gen im Vergleich zum Wildtyp wird somit im Vergleich zum Wildtyp in einer bestimm¬ ten Zeit die gebildete Menge des Proteins verändert.
Unter „verändert" wird in diesem Zusammenhang bevorzugt erhöht oder erniedrigt ver¬ standen.In the case of an "altered expression activity" or expression rate with respect to a gene in comparison to the wild type, the amount of protein formed is thus changed in a specific time compared to the wild type. In this context, "changed" is preferably increased or decreased.
Dies kann beispielsweise durch Erhöhung oder Reduzierung der spezifischen Aktivität der endogenen Expressionseinheit, beispielsweise durch Mutation der Expressionsein¬ heit oder durch Stimmulierung oder Hemmung der Expressionseinheit erfolgen.This can be done, for example, by increasing or reducing the specific activity of the endogenous expression unit, for example by mutation of the expression unit or by stimulation or inhibition of the expression unit.
Weiterhin kann die erhöhte Expressionsaktivität oder Expressionsrate beispielsweise durch Regulation der Expression von Genen im Mikroorganismus durch erfindungsge- mäße Expressionseinheiten oder durch Expressionseinheiten mit Erhöhter spezifischer Expressionsaktivität erreicht werden, wobei die Gene im Bezug auf die Expressions¬ einheiten heterolog sind.Furthermore, the increased expression activity or expression rate can be achieved, for example, by regulating the expression of genes in the microorganism by expression units according to the invention or by expression units with increased specific expression activity, wherein the genes are heterologous with respect to the expression units.
Vorzugsweise wird die Regulation der Expression von Genen im Mikroorganismus durch erfindungsgemäße Expressionseinheiten oder durch erfindungsgemäße Expres¬ sionseinheiten mit Erhöhter spezifischer Expressionsaktivitätdadurch erreicht, dass manPreferably, the regulation of the expression of genes in the microorganism by expression units according to the invention or by expression units with increased specific expression activity according to the invention is achieved by
eine oder mehrere erfindungsgemäße Expressionseinheiten, gegebenenfalls mit ver- änderter spezifischer Expressionsaktivität, in das Genom des Mikroorganismus ein¬ bringt, so dass die Expression eines oder mehrerer endogenen Gene unter der Kon¬ trolle der eingebrachten erfindungsgemäßen Expressionseinheiten, gegebenenfalls mit veränderter spezifischer Expressionsaktivität, erfolgt oderone or more expression units according to the invention, optionally with altered specific expression activity, into the genome of the microorganism, so that the expression of one or more endogenous genes takes place under the control of the introduced expression units according to the invention, optionally with altered specific expression activity, or
ein oder mehrere Gene in das Genom des Mikrorganismus einbringt, so dass die Ex¬ pression eines oder mehrerer der eingebrachten Gene unter der Kontrolle der endoge¬ nen, erfindungsgemäßen Expressionseinheiten, gegebenenfalls mit veränderter spezi¬ fischer Expressionsaktivität, erfolgt oderintroducing one or more genes into the genome of the microorganism such that the expression of one or more of the introduced genes takes place under the control of the endogenous expression units according to the invention, optionally with altered specific expression activity, or
ein oder mehrere Nukleinsäurekonstrukte, enthaltend eine erfindungsgemäße Expres¬ sionseinheit, gegebenenfalls mit veränderter spezifischer Expressionsaktivität, und funktionell verknüpft eine oder mehrere, zu exprimierende Nukleinsäuren, in den Mik¬ roorganismus einbringt.one or more nucleic acid constructs containing an expression unit according to the invention, optionally with altered specific expression activity, and functionally linked one or more nucleic acids to be expressed into the microorganism.
Die erfindungsgemäßen Expressionseinheiten, enthalten eine erfindungsgemäße, vor¬ stehend bechriebene Nukleinsäure mit Promotoraktivität und zusätzlich funktionell ver¬ knüpft eine Nukleinsäuresequenz, die die Translation von Ribonukleinsäuren gewährleistet.
Vorzugsweise enthält diese Nukleinsäuresequenz, die die Translation von Ribonuk¬ leinsäuren gewährleistet, die Nukleinsäuresequenz SEQ. ID. NO. 42 als ribosomale Bindungsstelle.The expression units according to the invention contain a nucleic acid according to the invention which is described above with promoter activity and additionally functionally linked to a nucleic acid sequence which ensures the translation of ribonucleic acids. This nucleic acid sequence, which ensures the translation of ribonucleic acids, preferably contains the nucleic acid sequence SEQ. ID. NO. 42 as a ribosomal binding site.
In einer bevorzugten Ausführungsform enthält die erfindungsgemäße Expressionsein¬ heit:In a preferred embodiment, the expression unit according to the invention contains:
E) die Nukleinsäuresequenz SEQ. ID. NO. 2 oderE) the nucleic acid sequence SEQ. ID. NO. 2 or
F) eine von dieser Sequenz durch Substitution, Insertion oder Deletion von Nukleotiden abgeleitete Sequenz, die eine Identität von mindestens 90 % aufF) a sequence derived from this sequence by substitution, insertion or deletion of nucleotides having an identity of at least 90%
Nukleinsäureebene mit der Sequenz SEQ. ID. NO. 2 aufweist oderNucleic acid level with the sequence SEQ. ID. NO. 2 or
G) eine Nukleinsäuresequenz, die mit der Nukleinsäuresequenz SEQ. ID. NO. 2 unter stringenten Bedingungen hybridisiert oderG) a nucleic acid sequence which is linked to the nucleic acid sequence SEQ. ID. NO. 2 hybridized under stringent conditions or
H) funktionell äquivalente Fragmente der Sequenzen unter E), F) oder G).H) functionally equivalent fragments of the sequences under E), F) or G).
Die Nukleinsäuresequenz SEQ. ID. NO. 2 stellt die Nukleinsäuresequenz der Expres¬ sionseinheit des Elongations-Faktors TS (PEF-TS) aus Corynebakterium glutamicum dar. SEQ. ID.NO. 2 entspricht der Sequenz der Expressionseinheit des Wildtyps.The nucleic acid sequence SEQ. ID. NO. 2 represents the nucleic acid sequence of the expression unit of the elongation factor TS (PEF-TS) from Corynebacterium glutamicum. SEQ. ID.NO. 2 corresponds to the sequence of the expression unit of the wild-type.
Die Erfindung betrifft weiterhin Expressionseinheiten, enthaltend eine von dieser Se¬ quenz durch Substitution, Insertion oder Deletion von Nukleotiden abgeleitete Se¬ quenz, die eine Identität von mindestens 90 % auf Nukleinsäureebene mit der Sequenz SEQ. ID. NO. 2 aufweist.The invention furthermore relates to expression units comprising a sequence derived from this sequence by substitution, insertion or deletion of nucleotides which has an identity of at least 90% at the nucleic acid level with the sequence SEQ. ID. NO. 2 has.
Weitere natürliche erfindungsgemäße Beispiele für erfindungsgemäße Expressions¬ einheiten lassen sich beispielsweise aus verschiedenen Organismen, deren genomi¬ sche Sequenz bekannt ist, durch Identitätsvergleiche der Nukleinsäuresequenzen aus Datenbanken mit der vorstehend beschriebenen Sequenzen SEQ ID NO: 2 leicht auf¬ finden.Further natural examples according to the invention for expression units according to the invention can be easily found, for example, from various organisms whose genomic sequence is known by identity comparisons of the nucleic acid sequences from databases with the sequences SEQ ID NO: 2 described above.
Künstliche erfindungsgemäße Sequenzen der Expressionseinheiten lassen sich aus¬ gehend von der Sequenz SEQ ID NO: 2 durch künstliche Variation und Mutation, bei¬ spielsweise durch Substitution, Insertion oder Deletion von Nukleotiden leicht auffin¬ den.Artificial sequences of the expression units according to the invention can be readily ascertained starting from the sequence SEQ ID NO: 2 by artificial variation and mutation, for example by substitution, insertion or deletion of nucleotides.
Unter einer Nukleinsäuresequenz, die eine Identität von mindestens 90 % mit der Se¬ quenz SEQ ID NO: 2 aufweist, wird dementsprechend eine Nukleinsäuresequenz ver¬ standen, die bei einem Vergleich seiner Sequenz mit der Sequenz SEQ ID NO: 2, ins¬ besondere nach obigen Programmlogarithmus mit obigem Parametersatz eine Identität von mindestens 90 % aufweist.
Besonders bevorzugte Expressionseinheiten weisen mit der Nukleinsäuresequenz SEQ. ID. NO. 2 eine Identität von 91%, bevorzugter 92%, 93%, 94%, 95%, 96%, 97%, 98%, besonders bevorzugt 99% auf.A nucleic acid sequence which has an identity of at least 90% with the sequence SEQ ID NO: 2 is accordingly understood to be a nucleic acid sequence which, in a comparison of its sequence with the sequence SEQ ID NO: 2, in particular above program logarithm with the above parameter set has an identity of at least 90%. Particularly preferred expression units have with the nucleic acid sequence SEQ. ID. NO. 2 has an identity of 91%, more preferably 92%, 93%, 94%, 95%, 96%, 97%, 98%, most preferably 99%.
Weitere natürliche Beispiele für Expressionseinheiten lassen sich weiterhin ausgehend von den vorstehend beschriebenen Nukleinsäuresequenzen, insbesondere ausgehend von der Sequenz SEQ ID NO: 2 aus verschiedenen Organismen, deren genomische Sequenz nicht bekannt ist, durch Hybridisierungstechniken in an sich bekannter Weise leicht auffinden.Further natural examples of expression units can furthermore easily be found starting from the above-described nucleic acid sequences, in particular starting from the sequence SEQ ID NO: 2 from various organisms whose genomic sequence is unknown, by hybridization techniques in a manner known per se.
Ein weiterer Gegenstand der Erfindung betrifft daher Expressionseinheiten, enthaltend eine Nukleinsäuresequenz, die mit der Nukleinsäuresequenz SEQ. ID. No. 2 unter stringenten Bedingungen hybridisiert. Diese Nukleinsäuresequenz umfasst mindestens 10, bevorzugter mehr als12,15,30,50 oder besonders bevorzugt mehr als 150 Nukleo¬ tide.A further subject of the invention therefore relates to expression units comprising a nucleic acid sequence which is linked to the nucleic acid sequence SEQ. ID. No. 2 hybridized under stringent conditions. This nucleic acid sequence comprises at least 10, more preferably more than 12, 15, 30, 50 or particularly preferably more than 150 nucleotides.
Unter "hybridisieren" versteht man die Fähigkeit eines PoIy- oder Oligonukleotids unter stringenten Bedingungen an eine nahezu komplementäre Sequenz zu binden, während unter diesen Bedingungen unspezifische Bindungen zwischen nicht-komplementären Partnern unterbleiben. Dazu sollten die Sequenzen vorzugsweise zu 90-100%, kom¬ plementär sein. Die Eigenschaft komplementärer Sequenzen, spezifisch aneinander binden zu können, macht man sich beispielsweise in der Northern- oder Southern-Blot- Technik oder bei der Primerbindung in PCR oder RT-PCR zunutze.By "hybridizing" is meant the ability of a poly or oligonucleotide to bind under stringent conditions to a nearly complementary sequence, while under these conditions nonspecific binding between non-complementary partners is avoided. For this purpose, the sequences should preferably be 90-100%, complementary. The property of complementary sequences to be able to specifically bind to one another, for example, in the Northern or Southern Blot technique or in the primer binding in PCR or RT-PCR advantage.
Die Hybridisierung erfolgt erfinungsgemäß unter stringenten Bedingungen. Solche Hybridisierungsbedingungen sind beispielsweise bei Sambrook, J., Fritsch, E.F., Mani- atis, T., in: Molecular Cloning (A Laboratory Manual), 2. Auflage, CoId Spring Harbor Laboratory Press, 1989, Seiten 9.31-9.57 oder in Current Protocols in Molecular Biolo- gy, John Wiley & Sons, N.Y. (1989), 6.3.1-6.3.6 beschrieben:The hybridization is carried out according to the invention under stringent conditions. Such hybridization conditions are described, for example, in Sambrook, J., Fritsch, EF, Maniatis, T., in: Molecular Cloning (A Laboratory Manual), 2nd Edition, ColD Spring Harbor Laboratory Press, 1989, pages 9.31-9.57 or in Current Protocols in Molecular Biology, John Wiley & Sons, NY (1989), 6.3.1-6.3.6:
Unter stringenten Hybridisierungs-Bedingungen werden insbesondere verstanden: Die über Nacht Inkubation bei 420C in einer Lösung bestehend aus 50 % Formamid, 5 x SSC (750 mM NaCI, 75 mM Tri-Natrium Citrat), 50 mM Natrium Phosphat (ph7,6), 5x Denhardt Lösung, 10% Dextransulfat und 20 g/ml denaturierte, gescheerteUnder stringent hybridization conditions mean in particular: Overnight incubation at 42 0 C in a solution of 50% formamide, 5 x SSC (750 mM NaCl, 75 mM trisodium citrate), 50 mM sodium phosphate (pH 7.6 ), 5x denhardt solution, 10% dextran sulfate and 20 g / ml denatured, seeded
Lachsspermien-DNA, gefolgt von einem Waschen der Filter mit 0,1x SSC bei 65°C.Salmon sperm DNA, followed by washing the filters with 0.1x SSC at 65 ° C.
Die erfindungsgemäß Nukleotidsequenzen ermöglichen ferner die Erzeugung von Sonden und Primern, die zur Identifizierung und/oder Klonierung von homologer Se- quenzen in anderen Zelltypen und Mikroorganismen verwendbar sind. Solche Sonden
bzw. Primer umfassen gewöhnlich einen Nukleotidsequenzbereich, der unter stringen- ten Bedingungen an mindestens etwa 12, vorzugsweise mindestens etwa 25, wie z.B. etwa 40, 50 oder 75 aufeinanderfolgende Nukleotide eines Sense-Stranges einer erfin¬ dungsgemäßen Nukleinsäuresequenz oder eines entsprechenden Antisense-Stranges hybridisiert.The nucleotide sequences according to the invention also allow the generation of probes and primers which are useful for the identification and / or cloning of homologous sequences in other cell types and microorganisms. Such probes or primers usually comprise a nucleotide sequence region which hybridizes under stringent conditions to at least about 12, preferably at least about 25, such as about 40, 50 or 75 consecutive nucleotides of a sense strand of a nucleic acid sequence according to the invention or of a corresponding antisense strand ,
Erfindungsgemäß umfasst sind auch solche Nukleinsäuresequenzen, die sogenannte stumme Mutationen umfassen oder entsprechend der Codon-Nutzung eins speziellen Ursprungs- oder Wirtsorganismus, im Vergleich zu einer konkret genannten Sequenz verändert sind, ebenso wie natürlich vorkommende Varianten, wie z.B. Spleißvarianten oder Allelvarianten, davon.Also included according to the invention are those nucleic acid sequences which comprise so-called silent mutations or are altered according to the codon usage of a specific source or host organism, in comparison with a specifically mentioned sequence, as well as naturally occurring variants, such as e.g. Splice variants or allelic variants, of which
Unter einem „funktionell äquivalenten Fragment" werden für Expressionseinheiten, Fragmente verstanden die im wesentlichen die gleiche oder eine höhere spezifische Expressionsaktivität aufweisen wie die Ausgangssequenz.By a "functionally equivalent fragment" is meant for expression units, fragments having substantially the same or a higher specific expression activity as the starting sequence.
Unter „im wesentlichen gleich" wird eine spezifische Expressionsaktivität verstanden die mindestens 50%, vorzugsweise 60%, bevorzugter 70%, bevorzugter 80%, bevor¬ zugter 90%, besonders bevorzugt 95% der spezifischen Expressionsaktivität der Aus- gangssequenz aufweist.By "substantially the same" is meant a specific expression activity which has at least 50%, preferably 60%, more preferably 70%, more preferably 80%, more preferably 90%, most preferably 95% of the specific expression activity of the starting sequence.
Unter „Fragmente" werden Teilsequenzen der durch Ausführungsform E), F) oder G) beschriebenen Expressionseinheiten verstanden. Vorzusgweise weisen diese Frag¬ mente mehr als 10, bevorzugter aber mehr als 12,15, 30, 50 oder besonders bevor- zugts mehr als 150 zusammenhängende Nukleotide der Nukleinsäuresequenz SEQ. ID. NO. 1 auf."Fragments" are to be understood as meaning partial sequences of the expression units described by embodiment E), F) or G. Preferably, these fragments have more than 10, more preferably more than 12, 15, 30, 50 or, even more preferably, more than 150 contiguous nucleotides of the nucleic acid sequence SEQ ID NO: 1.
Besonders bevorzugt ist die Verwendung der Nukleinsäuresequenz SEQ. ID. NO. 2 als Expressionseinheit, d.h. zur Expression von Genen.Particularly preferred is the use of the nucleic acid sequence SEQ. ID. NO. 2 as expression unit, i. for the expression of genes.
Die Erfindung betrifft ferner die neuen, erfindungsgemäßen Expressionseinheiten.The invention further relates to the new expression units according to the invention.
Insbesondere betrifft die Erfindung eine Expressionseinheit, enthaltend eine erfin¬ dungsgemäße Nukleinsäure mit Promotoraktivität zusätzlich funktionell verknüpft eine Nukleinsäuresequenz, die die Translation von Ribonukleinsäuren gewährleistet.In particular, the invention relates to an expression unit comprising a nucleic acid according to the invention with promoter activity additionally functionally linked to a nucleic acid sequence which ensures the translation of ribonucleic acids.
Besonders bevorzugt betrifft die Erfindung eine Expressionseinheit, enthaltendThe invention particularly preferably relates to an expression unit containing
E) die Nukleinsäuresequenz SEQ. ID. NO. 2 oder
F) eine von dieser Sequenz durch Substitution, Insertion oder Deletion von Nukleotiden abgeleitete Sequenz, die eine Identität von mindestens 90 % auf Nukleinsäureebene mit der Sequenz SEQ. ID. NO. 2 aufweist oderE) the nucleic acid sequence SEQ. ID. NO. 2 or F) a sequence derived from this sequence by substitution, insertion or deletion of nucleotides which has an identity of at least 90% at nucleic acid level with the sequence SEQ. ID. NO. 2 or
G) eine Nukleinsäuresequenz, die mit der Nukleinsäuresequenz SEQ. ID. NO. 2 unter stringenten Bedingungen hybridisiert oderG) a nucleic acid sequence which is linked to the nucleic acid sequence SEQ. ID. NO. 2 hybridized under stringent conditions or
H) funktionell äquivalente Fragmente der Sequenzen unter E), F) oder G),H) functionally equivalent fragments of the sequences under E), F) or G),
mit der Maßgabe, dass die Nukleinsäure mit der Sequenz SEQ. ID. NO. 2 ausgenom¬ men ist.with the proviso that the nucleic acid having the sequence SEQ. ID. NO. 2 is excluded.
Die erfindungsgemäßen Expressionseinheiten umfassen ein oder mehrere der folgen¬ den genetischen Elemente: eine Minus 10 ("-10") Sequenz; eine Minus 35 ("-35") Se¬ quenz; einen Transkriptionsstart, eine Enhancer Region; und eine Operator Region.The expression units according to the invention comprise one or more of the following genetic elements: a minus 10 ("-10") sequence; a minus 35 ("-35") sequence; a transcription start, an enhancer region; and an operator region.
Vorzugsweise sind diese genetischen Elemente spezifisch für die Spezies Corynebak- terien, speziell für Corynbacterium glutamicum.Preferably, these genetic elements are specific for the species Corynebacteria, especially for Corynebacterium glutamicum.
Alle vorstehend erwähnten Expressionseinheiten sind weiterhin in an sich bekannter Weise durch chemische Synthese aus den Nukleotidbausteinen wie beispielsweise durch Fragmentkondensation einzelner überlappender, komplementärer Nukleinsäure- bausteine der Doppelhelix herstellbar. Die chemische Synthese von Oligonukleotiden kann beispielsweise, in bekannter Weise, nach der Phosphoamiditmethode (Voet, Voet, 2. Auflage, Wiley Press New York, S. 896-897) erfolgen. Die Anlagerung synthe¬ tischer Oligonukleotide und Auffüllen von Lücken mithilfe des Klenow-Fragmentes der DNA-Polymerase und Ligationsreaktionen sowie allgemeine Klonierungsverfahren werden in Sambrook et al. (1989), Molecular cloning: A laboratory manual, CoId Spring Harbor Laboratory Press, beschrieben.All of the abovementioned expression units can furthermore be prepared in a manner known per se by chemical synthesis from the nucleotide units, for example by fragment condensation of individual overlapping, complementary nucleic acid building blocks of the double helix. The chemical synthesis of oligonucleotides can be carried out, for example, in a known manner by the phosphoamidite method (Voet, Voet, 2nd edition, Wiley Press New York, p. 896-897). The addition of synthetic oligonucleotides and filling in of gaps using the Klenow fragment of the DNA polymerase and ligation reactions and general cloning methods are described in Sambrook et al. (1989), Molecular cloning: A laboratory manual, Col. Spring Harbor Laboratory Press.
Für die Erfindungen in diesem Patent wurden Methoden und Techniken genutzt, die dem Fachmann, der in mikrobiologischen und rekombinanten DNA-Techniken geübt ist, bekannt sind. Methoden und Techniken für das Wachstum von Bakterienzellen, das Einschleusen von isolierten DNA-Molekülen in die Wirtszelle, und die Isolierung, KIo- nierung und Sequenzierung von isolierten Nukleinsäuremolekülen usw. sind Beispiele für solche Techniken und Methoden. Diese Methoden sind in vielen Standardlitera- turstellen beschrieben: Davis et al., Basic Methods In Molecular Biology (1986); J. H. Miller, Experiments in Molecular Genetics, CoId Spring Harbor Laboratory Press, CoId Spring Harbor, New York (1972); J.H. Miller, A Short Course in Bacterial Genetics, Gold Spring Harbor Laboratory Press, CoId Spring Harbor, New York (1992); M. Singer and P. Berg, Genes & Genomes, University Science Books, MiII Valley, Carlifornia (1991 ); J. Sambrook, E.F. Fritsch and T. Maniatis, Molecular Cloning: A Laboratory
Manual, 2πd ed., CoId Spring Harbor Laboratory Press, CoId Spring Harbor, New York (1989); P.B. Kaufmann et al., Handbook of Molcular and Cellular Methods in Biology and Medicine, CRC Press, Boca Raton, Florida (1995); Methods in Plant Molecular Biology and Biotechnology, B.R. Glick and J.E. Thompson, eds., CRC Press, Boca Raton, Florida (1993); and P.F. Smith-Keary, Molecular Genetics of Escherichia coli, The Guilford Press, New York, NY (1989).For the inventions in this patent, methods and techniques known to those skilled in microbiological and recombinant DNA techniques have been used. Methods and techniques for growth of bacterial cells, introduction of isolated DNA molecules into the host cell, and isolation, isolation, and sequencing of isolated nucleic acid molecules, etc., are examples of such techniques and methods. These methods are described in many standard literature references: Davis et al., Basic Methods In Molecular Biology (1986); JH Miller, Molecular Genetics Experiments, Col. Spring Harbor Laboratory Press, Col. Spring Harbor, New York (1972); JH Miller, A Short Course in Bacterial Genetics, Gold Spring Harbor Laboratory Press, ColD Spring Harbor, New York (1992); M. Singer and P. Berg, Genes & Genomes, University Science Books, Mill Valley, Carlifornia (1991); J. Sambrook, EF Fritsch and T. Maniatis, Molecular Cloning: A Laboratory Manual, 2 πd ed., Colard Spring Harbor Laboratory Press, Col. Spring Harbor, New York (1989); PB Kaufmann et al., Handbook of Molecular and Cellular Methods in Biology and Medicine, CRC Press, Boca Raton, Florida (1995); Methods in Plant Molecular Biology and Biotechnology, BR Glick and JE Thompson, eds., CRC Press, Boca Raton, Florida (1993); and PF Smith-Keary, Molecular Genetics of Escherichia coli, The Guilford Press, New York, NY (1989).
Alle Nukleinsäuremoleküle der vorliegenden Erfindung liegen bevorzugt in Form eines isolierten Nukleinsäuremoleküls vor. Ein "isoliertes" Nukleinsäuremolekül wird von an- deren Nukleinsäuremolekülen abgetrennt, die in der natürlichen Quelle der Nukleinsäu¬ re zugegen sind und kann überdies im wesentlichen frei von anderem zellulären Mate¬ rial oder Kulturmedium sein, wenn es durch rekombinante Techniken hergestellt wird, oder frei von chemischen Vorstufen oder anderen Chemikalien sein, wenn es chemisch synthetisiert wird.All nucleic acid molecules of the present invention are preferably in the form of an isolated nucleic acid molecule. An "isolated" nucleic acid molecule is separated from other nucleic acid molecules present in the natural source of the nucleic acid and, moreover, may be substantially free of other cellular material or culture medium when produced by recombinant techniques or free of chemical precursors or other chemicals when chemically synthesized.
Die Erfindung umfasst weiterhin die zu den konkret beschriebenen Nukleotidsequen- zen komplementären Nukleinsäuremoleküle oder einen Abschnitt davon.The invention further comprises the nucleic acid molecules complementary to the specifically described nucleotide sequences or a portion thereof.
Die erfindungsgemäßen Promotoren und/oder Expressionseinheiten lassen sich bei- spielsweise besonders vorteilhaft in verbesserten Verfahren zur fermentativen Herstel¬ lung von biosynthetischen Produkten wie nachstehend beschrieben verwenden.The promoters and / or expression units according to the invention can be used, for example, with particular advantage in improved processes for the fermentative preparation of biosynthetic products as described below.
Die erfindungsgemäßen Promotoren und/oder Expressionseinheiten weisen insbeson¬ dere den Vorteil auf, dass sie in Mikroorganismen durch Stress induziert werden. Durch geeignete Steuerung des Fermentationsprozesses lässt sich diese Stress¬ induktion gezieit für eine Erhöhung der Trankritptions/Expressionsrate gewünschter Gene steuern. Insbesondere bei der Produktion von L-Lysin wird diese Stressphase sehr früh erreicht, so das hier sehr früh eine erhöhte Transkriptions/Expressionsrate von gewünschten Genen erreicht werden kann.The promoters and / or expression units according to the invention have the particular advantage that they are induced in microorganisms by stress. By suitable control of the fermentation process, this stress induction can be controlled for an increase in the rate of inflammation / expression of desired genes. In particular, in the production of L-lysine, this stress phase is reached very early, so that here very early an increased transcription / expression rate of desired genes can be achieved.
Die erfindungesgemäßen Nukleinsäuren mit Promotoraktivität können zur Verände¬ rung, also zur Erhöhung oder Reduzierung, oder zur Verursachung der Transkriptions¬ rate von Genen in Mikroorganismen im Vergleich zum Wildtyp verwendet werden.The nucleic acids with promoter activity according to the invention can be used for modification, ie for increasing or reducing, or for causing the transcription rate of genes in microorganisms in comparison to the wild type.
Die erfindungsgemäßen Expressionseinheiten können zur Veränderung, also zur Er¬ höhung oder Reduzierung, oder zur Verursachung der Expressionsrate von Genen in Mikroorganismen im Vergleich zum Wildtyp verwendet werden.The expression units according to the invention can be used for altering, that is to say for increasing or reducing, or for causing the expression rate of genes in microorganisms in comparison to the wild type.
Ferner können die erfindungsgemäßen Nukleinsäuren mit Promotoraktivität und die erfindungesgemäßen Expressionseinheiten zur Regulation und Verstärkung der BiI-
düng von verschiedenen biosynthetischen Produkten, wie beispielsweise Feinchemika¬ lien, Proteinen, inbesondere Aminosäuren, in Mikroorganismen, insbsondere in Cory- nebacterium species dienen.Furthermore, the nucleic acids according to the invention with promoter activity and the expression units according to the invention can be used to regulate and enhance the biologic fertil of various biosynthetic products, such as Feinchemika¬ lien, proteins, in particular amino acids, serve in microorganisms, in particular in Corynebacterium species.
Die Erfindung betrifft daher ein Verfahren zur Veränderung oder Verursachung der Transkriptionsrate von Genen in Mikroorganismen im Vergleich zum Wildtyp durchThe invention therefore relates to a method for altering or causing the transcription rate of genes in microorganisms in comparison to the wild type
a) Veränderung der spezifischen Promotoraktivität im Mikroorganismus von endo¬ genen, erfindungsgemäßen Nukleinsäuren mit Promotoraktivität, die die Transkription von endogenen Genen regulieren, im Vergleich zum Wildtyp odera) modification of the specific promoter activity in the microorganism of endogenous nucleic acids according to the invention with promoter activity, which regulate the transcription of endogenous genes, in comparison to the wild-type or
b) Regulation der Transkription von Genen im Mikroorganismus durch erfindungs¬ gemäße Nukleinsäuren mit Promotoraktivität oder durch Nukleinsäuren mit ver¬ änderter spezifischer Promotoraktivität gemäß Ausführungsform a), wobei die Gene in Bezug auf die Nukleinsäuren mit Promotoraktivität heterolog sind.b) Regulation of the transcription of genes in the microorganism by erfindungs¬ according to nucleic acids with promoter activity or by nucleic acids with ver¬ changed specific promoter activity according to embodiment a), wherein the genes are heterologous with respect to the nucleic acids with promoter activity.
Gemäß Ausführungsform a) kann die Veränderung oder Verursachung der Transkripti¬ onsrate von Genen in Mikroorganismen im Vergleich zum Wildtyp dadurch erfolgen, dass im Mikroorganismus die spezifische Promotoraktivität verändert, also erhöht oder erniedrigt wird. Dies kann beispielsweise durch gezielte Mutation der erfindungsgemä¬ ßen Nukleinsäuresequenz mit Promotoraktivität, also durch gezielte Substitution, DeIe- tion oder Insertion von Nukleotiden erfolgen. Eine erhöhte bzw. erniedrigte Promotor¬ aktivität kann dadurch erreicht werden.dass Nukleotide in der Bindungsstelle des RNA- Polymerase-Holoenzym-Bindungsstellen (dem Fachmann auch als -10-Region und - 35 Region bekannt) ausgetauscht werden. Weiterhin dadurch dass der Abstand der beschriebenen RNA-Polymerase-Holoenzym-Bindungsstellen zueinander durch DeIe- tionen von Nukleotiden oder Insertionen von Nukleotiden verkleinert oder vergrößert werden. Weiterhin dadurch dass Bindungsstellen (dem Fachmann auch als - Operatoren bekannt) für Regulatiosproteine (dem Fachmann bekannt als Repressoren und Aktiviatoren) in räumliche Nähe an die Bindungsstellen des RNA-Polymerase- Holoenzyms gebracht werden, dass diese Regulatoren nach Bindung an eine Promo¬ tor-Sequenz die Bindung des und Transkriptionsaktivität des RNA-Polymerase- Holoenzyms abschwächen oder verstärken, oder auch unter einen neuen regulatori¬ schen Einfluss stellen.In accordance with embodiment a), the change or causation of the transcription rate of genes in microorganisms in comparison to the wild type can be achieved by modifying, ie increasing or decreasing, the specific promoter activity in the microorganism. This can be done, for example, by targeted mutation of the nucleic acid sequence according to the invention with promoter activity, that is to say by targeted substitution, de-insertion or insertion of nucleotides. Increased or decreased promoter activity can be achieved by exchanging the nucleotides in the binding site of the RNA polymerase holoenzyme binding sites (also known to the person skilled in the art as the -10 region and the region known). Furthermore, the fact that the distance between the described RNA polymerase holoenzyme binding sites to each other by DeIe- tions of nucleotides or insertions of nucleotides reduced or enlarged. Furthermore, binding sites (also known to the person skilled in the art as regulators) for regulatory proteins (known to the person skilled in the art as repressors and activators) are brought into spatial proximity to the binding sites of the RNA polymerase holoenzyme, that these regulators, after binding to a promotor. Sequence attenuate or enhance the binding and transcriptional activity of the RNA polymerase holoenzyme, or even under a new reguli¬ rule influence.
Die Nukleinsäuresequenz SEQ. ID. NO. 21 stellt vorzugsweise die ribosomale Bin¬ dungsstelle der erfindungsgemäßen Expressionseinheiten, die Sequenzen SEQ. ID. NOs. 19 oder 20 die -10-Region der erfindungsgemäßen Expressionseinheiten dar. Veränderungen der Nukleinsäureaequenz in diesen Regionen führen zu einer Verän- derung der spezifischen Expressionsaktivität.
Die Erfindung betrifft daher die Verwendung der Nukleinsäuresequenz SEQ. ID. NO. 21 als ribosomale Bindungsstelle in Expressionseinheiten, die die Expression von Ge¬ nen in Bakterien der Gattung Corynebacterium oder Brevibacterium ermöglichen.The nucleic acid sequence SEQ. ID. NO. 21 preferably represents the ribosomal binding site of the expression units according to the invention, the sequences SEQ. ID. NOs. 19 or 20 represent the -10 region of the expression units according to the invention. Changes in the nucleic acid sequence in these regions lead to a change in the specific expression activity. The invention therefore relates to the use of the nucleic acid sequence SEQ. ID. NO. 21 as a ribosomal binding site in expression units which enable the expression of genes in bacteria of the genus Corynebacterium or Brevibacterium.
Weiterhin betrifft die Erfindung die Verwendung der Nukleinsäuresequenzen SEQ. ID. NOs. 19 oder 20 als -10-Region in Expressionseinheiten, die die Expression von Ge¬ nen in Bakterien der Gattung Corynebacterium oder Brevibacterium ermöglichen.Furthermore, the invention relates to the use of the nucleic acid sequences SEQ. ID. NOs. 19 or 20 as -10-region in expression units which allow the expression of genes in bacteria of the genus Corynebacterium or Brevibacterium.
Insbesondere betrifft die Erfindung eine Expressionseinheit, die die Expression von Genen in Bakterien der Gattung Corynebacterium oder Brevibacterium ermöglicht, ent¬ haltend die Nukleinsäuresequenz SEQ. ID. NO. 21. Vorzugsweise wird dabei die Nuk¬ leinsäuresequenz SEQ. ID. NO. 21 als ribosomaie Bindungsstelle verwendet .In particular, the invention relates to an expression unit which enables the expression of genes in bacteria of the genus Corynebacterium or Brevibacterium, comprising the nucleic acid sequence SEQ. ID. NO. 21. Preferably, the nucleic acid sequence SEQ. ID. NO. 21 used as a ribosomal binding site.
Weiterhin betrifft die Erfindung eine Expressionseinheit, die die Expression von Genen in Bakterien der Gattung Corynebacterium oder Brevibacterium ermöglicht, enthaltend mindestens eine der Nukleinsäuresequenzen SEQ. ID. NOs. 19 oder 20. Vorzugsweise wird dabei eine der Nukleinsäuresequenzen SEQ. ID. NOs. 19 oder 20 als -10-Region verwendet.Furthermore, the invention relates to an expression unit which allows the expression of genes in bacteria of the genus Corynebacterium or Brevibacterium, containing at least one of the nucleic acid sequences SEQ. ID. NOs. 19 or 20. Preferably, one of the nucleic acid sequences SEQ. ID. NOs. 19 or 20 is used as the -10 region.
In Bezug auf die „spezifische Promotoraktivität" wird unter Erhöhung oder Reduzierung im Vergleich zum Wildtyp eine Erhöhung oder Reduzierung der spezifischen Aktivität gegenüber der erfindungsgemäßen Nukleinsäure mit Promotoraktivität des Wildtyps, also beispielsweise gegenüber der SEQ. ID. NO. 1 verstanden.With regard to the "specific promoter activity", increasing or reducing in comparison with the wild type means an increase or reduction of the specific activity with respect to the nucleic acid according to the invention having promoter activity of the wild-type, that is to say, for example, with reference to SEQ ID NO.
Gemäß Ausführungsform b) kann die Veränderung oder Verursachung der Transkripti¬ onsrate von Genen in Mikroorganismen im Vergleich zum Wildtyp dadurch erfolgen, dass man die Transkription von Genen im Mikroorganismus durch erfindungsgemäße Nukleinsäuren mit Promotoraktivität oder durch Nukleinsäuren mit veränderter spezifi- scher Promotoraktivität gemäß Ausführungsform a) reguliert, wobei die Gene in Bezug auf die Nukleinsäuren mit Promotoraktivität heterolog sind.In accordance with embodiment b), the transcription rate of genes in microorganisms can be changed or caused in comparison to the wild type by transcribing genes in the microorganism by nucleic acids according to the invention having promoter activity or by nucleic acids having modified specific promoter activity according to embodiment a). wherein the genes are heterologous with respect to the nucleic acids having promoter activity.
Dies wird bevorzugt dadurch erreicht, dass manThis is preferably achieved by one
b1) eine oder mehrere erfindungsgemäße Nukleinsäuren mit Promotoraktivität, ge- benenfalls mit veränderter spezifischer Promotoraktivität, in das Genom des Mikroorganismus einbringt, so dass die Transkription eines oder mehrerer en¬ dogenen Gene unter der Kontrolle der eingebrachten Nukleinsäure mit Promo¬ toraktivität, gegebenenfalls mit veränderter spezifischer Promotoraktivität, er-
folgt oderb1) introducing one or more nucleic acids according to the invention with promoter activity, optionally with altered specific promoter activity, into the genome of the microorganism such that the transcription of one or more endogenous genes under the control of the introduced nucleic acid having promoter activity, optionally with altered specific promoter activity, follows or
b2) ein oder mehrere Gene in das Genom des Mikrorganismus einbringt, so dass die Transkription eines oder mehrerer der eingebrachten Gene unter der Kon- trolle der endogenen, erfindungsgemäßen Nukleinsäuren mit Promotoraktivität, gegebenenfalls mit veränderter spezifischer Promotoraktivität, erfolgt oderb2) introducing one or more genes into the genome of the microorganism such that the transcription of one or more of the introduced genes takes place under the control of the endogenous nucleic acids according to the invention having promoter activity, optionally with altered specific promoter activity, or
b3) ein oder mehrere Nukleinsäurekonstrukte, enthaltend eine erfindungsgemäßeb3) one or more nucleic acid constructs containing an inventive
Nukleinsäure mit Promotoraktivität, gegebenenfalls mit veränderter spezifischer Promotoraktivität, und funktionell verknüpft eine oder mehrere, zu transkribie¬ rende Nukleinsäuren, in den Mikroorganismus einbringt.Nucleic acid with promoter activity, optionally with altered specific promoter activity, and functionally linked one or more, to be transkribie¬ rende nucleic acids in the microorganism brings.
Es ist somit möglich, die Transkriptionsrate eines endogenen Gens des Wildtyps zu verändern, also zu erhöhen oder zu erniedrigen indem manIt is thus possible to change the transcription rate of an endogenous gene of the wild-type, ie to increase or decrease it by
gemäß Ausführungsform b1) eine oder mehrere erfindungsgemäße Nukleinsäuren mit Promotoraktivität, gebenenfalls mit veränderter spezifischer Promotoraktivität, in das Genom des Mikroorganismus einbringt, so dass die Transkription eines oder mehrerer endogenen Gene unter der Kontrolle der eingebrachten Nukleinsäure mit Promotorak- tivität, gegebenenfalls mit veränderter spezifischer Promotoraktivität, erfolgt oderAccording to embodiment b1), one or more nucleic acids according to the invention having promoter activity, optionally with altered specific promoter activity, are introduced into the genome of the microorganism such that the transcription of one or more endogenous genes under the control of the introduced nucleic acid with promoter activity, optionally with altered specific promoter activity , or
gemäß Ausführungsform b2) ein oder mehrere endogene Gene in das Genom des Mikrorganismus einbringt, so dass die Transkription eines oder mehrerer der einge¬ brachten, endogenen Gene unter der Kontrolle der endogenen, erfindungsgemäßen Nukleinsäuren mit Promotoraktivität, gegebenenfalls mit veränderter spezifischer Pro¬ motoraktivität, erfolgt oderaccording to embodiment b2) introduces one or more endogenous genes into the genome of the microorganism such that the transcription of one or more of the introduced endogenous genes takes place under the control of the endogenous nucleic acids according to the invention having promoter activity, optionally with altered specific promoter activity or
Gemäß Ausführungsform b3) ein oder mehrere Nukleinsäurekonstrukte, enthaltend eine erfindungsgemäße Nukleinsäure mit Promotoraktivität, gegebenenfalls mit verän- derter spezifischer Promotoraktivität, und funktionell verknüpft eine oder mehrere, zu transkribierende endogene Nukleinsäuren, in den Mikroorganismus einbringt.According to embodiment b3), one or more nucleic acid constructs comprising a nucleic acid according to the invention with promoter activity, optionally with altered specific promoter activity, and functionally linked one or more endogenous nucleic acids to be transcribed, into which microorganism introduces.
Ferner ist es somit möglich, die Transkriptionsrate eines exogenen Gens im Vergleich zum Wildtyps zu verursachen, indem manFurthermore, it is thus possible to cause the transcription rate of an exogenous gene compared to the wild type by
gemäß Ausführungsform b2) ein oder mehrere exogene Gene in das Genom des Mikrorganismus einbringt, so dass die Transkription eines oder mehrerer der einge¬ brachten, exogenen Gene unter der Kontrolle der endogenen, erfindungsgemäßen Nukleinsäuren mit Promotoraktivität, gegebenenfalls mit veränderter spezifischer Pro-
motoraktivität, erfolgt oderin accordance with embodiment b2) introduces one or more exogenous genes into the genome of the microorganism such that the transcription of one or more of the introduced exogenous genes under the control of the endogenous nucleic acids according to the invention having promoter activity, optionally with modified specific pro motor activity, or occurs
Gemäß Ausführungsform b3) ein oder mehrere Nukleinsäurekonstrukte, enthaltend eine erfindungsgemäße Nukleinsäure mit Promotoraktivität, gegebenenfalls mit verän- derter spezifischer Promotoraktivität, und funktionell verknüpft eine oder mehrere, zu transkribierende exogene Nukleinsäuren, in den Mikroorganismus einbringt.According to embodiment b3), one or more nucleic acid constructs comprising a nucleic acid according to the invention with promoter activity, optionally with altered specific promoter activity, and functionally linked one or more exogenous nucleic acids to be transcribed, into which microorganism introduces.
Die Insertion von Genen gemäß Ausführungsform b2) kann dabei so erfolgen, dass das Gen in kodierende Bereiche oder nicht-kodierende Bereiche integriert wird. Vor- zugsweise erfolgt die Insertion in nicht-kodierende Bereiche.The insertion of genes according to embodiment b2) can be carried out so that the gene is integrated into coding regions or non-coding regions. Preferably, the insertion takes place in non-coding regions.
Die Insertion von Nukleinsäurekonstrukten gemäß Ausführungsform b3) kann dabei chromosomal oder extrachromosomal erfolgen. Vorzugsweise erfolgt die Insertion der Nukleinsäurekonstrukte chromosomal. Eine „chromosomale" Integration ist die Inserti- on eines exogenen DNA-Fragmentes in das Chromosom einer Wirtszelle. Dieser Beg¬ riff wird auch für die homologe Rekombination zwischen einem exogenen DNA- Fragment und der entsprechenden Region auf dem Chromosom der Wirtszelle genutzt.The insertion of nucleic acid constructs according to embodiment b3) can be carried out chromosomally or extrachromosomally. Preferably, the insertion of the nucleic acid constructs is chromosomal. A "chromosomal" integration is the insertion of an exogenous DNA fragment into the chromosome of a host cell, which is also used for homologous recombination between an exogenous DNA fragment and the corresponding region on the chromosome of the host cell.
In Ausführungsform b) werden bevorzugt auch erfindungsgemäße Nukleinsäuren mit veränderter spezifischer Promotoraktivität gemäß Ausführungsform a) eingesetzt. Die¬ se können in Ausführungsform b), wie in Ausführungsform a) beschrieben im Mikroor¬ ganismus vorliegen und hergestellt werden oder in isolierter Form in den Mikroorga¬ nismus eingebracht werden.In embodiment b) it is also preferred to use nucleic acids according to the invention with modified specific promoter activity according to embodiment a). These can be present in the microorganism in Example b), as described in embodiment a), and can be prepared or introduced into the microorganism in isolated form.
Unter „endogen" werden genetische Informationen, wie beispielsweise Gene, verstan¬ den, die bereits im Wildtypgenom enthalten sind.By "endogenous" is meant genetic information, such as genes, that are already contained in the wild-type genome.
Unter „exogen" werden genetische Informationen, wie beispielsweise Gene, verstan¬ den, die im Wildtypgenom nicht enthalten sind.By "exogenous" are meant genetic information, such as genes, which are not contained in the wild-type genome.
Unter dem Begriff „Gene" in Bezug auf Regulation der Transkription durch die erfin¬ dungsgemäßen Nukleinsäuren mit Promotoraktivität werden vorzugsweise Nukleinsäu¬ ren verstanden, die einen zu transkripierenden Bereich, also beispielsweise einen Be¬ reich der die Translation reguliert, einen kodierenden Bereich, sowie gegebenenfalls weitere Regulation.selemente, wie beispielsweise einen Terminator, enthalten.The term "genes" with regard to regulation of transcription by the nucleic acids having promoter activity according to the invention are preferably understood to be nucleic acids which have a region to be transcribed, for example a region which regulates translation, a coding region and optionally weitere Regulation.selemente, such as a terminator included.
Unter dem Begriff „Gene" in Bezug auf die nachstehend beschriebene Regulation der Expression durch die erfindungsgemäßen Expressionseinheiten werden vorzugsweise Nukleinsäuren verstanden, die einen kodierenden Bereich, sowie gegebenenfalls wei- tere Regulationselemente, wie beispielsweise einen Terminator, enthalten.
Unter einem „kodierenden Bereich" wird eine Nukleinsäuresequenz verstanden, die ein Protein kodiert.The term "genes" with respect to the expression regulation described below by the expression units according to the invention are preferably understood as meaning nucleic acids which contain a coding region and optionally further regulatory elements, such as, for example, a terminator. By a "coding region" is meant a nucleic acid sequence encoding a protein.
Unter „heterolog" in Bezug auf Nukleinsären mit Promotoraktivität und Gene wird ver¬ standen, dass die verwendeten Gene im Wildtyp nicht unter Regulation der erfin¬ dungsgemäßen Nukleinsäuren mit Promotoraktivität transkribiert werden, sondern das eine neue, im Wildtyp nicht vorkommende funktionelle Verknüpfung entsteht und die funktionelle Kombination aus erfindungsgemäßer Nukleinsäure mit Promotoraktivität und spezifisches Gen im Wildtyp nicht vorkommt.By "heterologous" with reference to nucleic acids with promoter activity and genes is understood that the genes used in the wild type are not transcribed under regulation of the nucleic acids according to the invention with promoter activity, but that a new functional link not occurring in the wild type is produced and the functional combination of inventive nucleic acid with promoter activity and specific gene does not occur in the wild type.
Unter „heterolog" in Bezug auf Expressionseinheiten und Gene wird verstanden, dass die verwendeten Gene im Wildtyp nicht unter Regulation der erfindungsgemäßen Ex¬ pressionseinheiten exprimiert werden, sondern das eine neue, im Wildtyp nicht vor- kommende funktionelle Verknüpfung entsteht und die funktionelle Kombination aus erfindungsgemäßer Expressionseinheit und spezifisches Gen im Wildtyp nicht vor¬ kommt.By "heterologous" in terms of expression units and genes is meant that the genes used are not expressed in the wild-type under regulation of the expression units according to the invention, but that a new, not occurring in the wild type functional linkage is formed and the functional combination of inventive Expression unit and specific gene does not occur in the wild type.
Die Erfindung betrifft femer in einer bevorzugten Ausführungsform ein Verfahren zur Erhöhung oder Verursachung der Transkriptionsrate von Genen in Mikroorganismen im Vergleich zum Wildtyp indem manThe invention further relates in a preferred embodiment to a method for increasing or causing the transcription rate of genes in microorganisms compared to the wild type by
ah) die spezifische Promotoraktivität im Mikroorganismus von erfindungsgemäßen endogenen Nukleinsäuren mit Promotoraktivität , die die Transkription von en- dogenen Genen regulieren, im Vergleich zum Wildtyp erhöht oderah) the specific promoter activity in the microorganism of endogenous nucleic acids with promoter activity according to the invention which regulate the transcription of endogenous genes is increased in comparison to the wild-type or
bh) die Transkription von Genen im Mikroorganismus durch erfindungsgemäße Nukleinsäuren mit Promotoraktivität oder durch Nukleinsäuren mit erhöhter spezifischer Promotoraktivität gemäß Ausführungsform a) reguliert, wobei die Gene in Bezug auf die Nukleinsäuren mit Promotoraktivität heterolog sind.bh) the transcription of genes in the microorganism by nucleic acids according to the invention with promoter activity or by nucleic acids with increased specific promoter activity according to embodiment a) regulated, wherein the genes are heterologous with respect to the nucleic acids with promoter activity.
Vorzugsweise wird die Regulation der Transkription von Genen im Mikroorganismus durch erfindungsgemäße Nukleinsäuren mit Promotoraktivität oder durch erfindungs¬ gemäße Nukleinsäuren mit erhöhter spezifischer Promotoraktivität gemäß Ausfüh- rungsform ah) dadurch erreicht wird, dass manPreferably, the regulation of the transcription of genes in the microorganism is achieved by nucleic acids according to the invention with promoter activity or by nucleic acids according to the invention with increased specific promoter activity according to embodiment (ah) in that
bh1) eine oder mehrere erfindungsgemäße Nukleinsäuren mit Promotoraktivität, gegebenenfalls mit erhöhter spezifischer Promotoraktivität, in das Genom des Mikroorganismus einbringt, so dass die Transkription eines oder mehrerer en- dogenen Gene unter der Kontrolle der eingebrachten erfindungsgemäßen
Nukleinsäure mit Promotoraktivität, gegebenenfalls mit erhöhter spezifischer Promotoraktivität, erfolgt oderbh1) introduces one or more nucleic acids according to the invention with promoter activity, optionally with increased specific promoter activity, into the genome of the microorganism such that the transcription of one or more endogenous genes under the control of the introduced invention Nucleic acid with promoter activity, optionally with increased specific promoter activity, takes place or
bh2) ein oder mehrere Gene in das Genom des Mikrorganismus einbringt, so dass die Transkription eines oder mehrerer der eingebrachten Gene unter der Kon¬ trolle der erfindungsgemäßen, endogenen Nukleinsäuren mit Promotoraktivität, gegebenenfalls mit erhöhter spezifischer Promotoraktivität, erfolgt oderbh2) introduces one or more genes into the genome of the microorganism such that the transcription of one or more of the genes introduced takes place under the control of the endogenous nucleic acids according to the invention with promoter activity, optionally with increased specific promoter activity, or
bh3) ein oder mehrere Nukleinsäurekonstrukte, enthaltend eine erfindungsgemäße Nukleinsäure mit Promotoraktivität, gegebenenfalls mit erhöhter spezifischerbh3) one or more nucleic acid constructs containing a nucleic acid according to the invention with promoter activity, optionally with increased specificity
Promotoraktivität, und funktionell verknüpft eine oder mehrere, zu transkribie¬ rende Nukleinsäuren, in den Mikroorganismus einbringt.Promoter activity, and functionally linked one or more, to transkribie¬ rende nucleic acids, brings in the microorganism.
Die Erfindung betrifft ferner in einer bevorzugten Ausführungsform ein Verfahren zur Reduzierung der Transkriptionsrate von Genen in Mikroorganismen im Vergleich zum Wildtyp, indem manThe invention further relates, in a preferred embodiment, to a method for reducing the transcription rate of genes in microorganisms in comparison to the wild type, by
ar) die spezifische Promotoraktivität im Mikroorganismus von endogenen erfin¬ dungsgemäßen Nukleinsäuren mit Promotoraktivität, die die Transkription der endogenen Gene regulieren, im Vergleich zum Wildtyp reduziert oderar) the specific promoter activity in the microorganism of endogenous nucleic acids according to the invention with promoter activity, which regulate the transcription of the endogenous genes, is reduced in comparison with the wild-type or
br) Nukleinsäuren mit reduzierter spezifischer Promotoraktivität gemäß Ausfüh¬ rungsform a) in das Genom des Mikroorganismus einbringt, so dass die Transkription endogene Gene unter der Kontrolle der eingebrachten Nuklein- säure mit reduzierter Promotoraktivität erfolgt.br) introducing nucleic acids with reduced specific promoter activity according to embodiment a) into the genome of the microorganism, so that the transcription of endogenous genes takes place under the control of the incorporated nucleic acid with reduced promoter activity.
Die Erfindung betrifft ferner ein Verfahren zur Veränderung oder Verursachung der Expressionsrate eines Gens in Mikroorganismen im Vergleich zum Wildtyp durchThe invention further relates to a method for altering or causing the expression rate of a gene in microorganisms compared to the wild type
c) Veränderung der spezifischen Expressionsaktivität im Mikroorganismus von er¬ findungsgemäßen, endogenen Expressionseinheiten, die die Expression der endogenen Gene regulieren, im Vergleich zum Wildtyp oderc) alteration of the specific expression activity in the microorganism of endogenous expression units according to the invention which regulate the expression of the endogenous genes in comparison to the wild-type or
d) Regulation der Expression von Genen im Mikroorganismus durch erfindungs- gemäße Expressionseinheiten oder durch erfindungsgemäße Expressionsein¬ heiten mit veränderter spezifischer Expressionsaktivität gemäß Ausführungs¬ form c), wobei die Gene im Bezug auf die Expressionseinheiten heterolog sind.d) Regulation of the Expression of Genes in the Microorganism by Expression Units According to the Invention or by Expression Units of the Invention with Altered Specific Expression Activity According to Embodiment c), wherein the genes are heterologous with respect to the expression units.
Gemäß Ausführungsform c) kann die Veränderung oder Verursachung der Expressi- onsrate von Genen in Mikroorganismen im Vergleich zum Wildtyp dadurch erfolgen,
dass im Mikroorganismus die spezifische Expressionsaktivität verändert, also erhöht oder erniedrigt wird. Dies kann beispielsweise durch gezielte Mutation der erfindungs¬ gemäßen Nukleinsäuresequenz mit Promotoraktivität, also durch gezielte Substitution, Deletion oder Insertion von Nukleotiden erfolgen. Beispielsweise führt die Verlänge- rung des Abstandes zwischen Shine-Dalgamo-Sequenz und dem translationellen Startcodon in der Regel zu einer Änderung, einer Verkleinerung oder aber auch einer Verstärkung der spezifischen Expressionsaktivität. Eine Veränderung der der spezifi¬ schen Expressionsaktivität kann auch dadurch erreicht werden, dass die Sequenz der Shine-Dalgamo-Region (Ribosomale Bindungsstelle) in seinem Abstand zum translati- onellen Startcodon durch Deletionen oder Insertionen von Nukleotiden entweder ver¬ kürzt oder verlängert wird. Aber auch dadurch dass die Sequenz der Shine-Dalgamo- Region so verändert wird, dass die Homologie zu komplementären 3' Seite 16S rRNA entweder verstärkt oder aber auch verringert wird.According to embodiment c), the change or causation of the expression rate of genes in microorganisms can take place in comparison to the wild type, that in the microorganism, the specific expression activity is changed, that is increased or decreased. This can be done, for example, by targeted mutation of the nucleic acid sequence according to the invention with promoter activity, ie by targeted substitution, deletion or insertion of nucleotides. For example, the extension of the distance between the Shine-Dalgamo sequence and the translational start codon usually leads to a change, a reduction or else an increase in the specific expression activity. A change in the specific expression activity can also be achieved by shortening or lengthening the sequence of the Shine-Dalgamo region (ribosomal binding site) in its distance from the translational start codon by deletions or insertions of nucleotides. But also by the fact that the sequence of the Shine-Dalgamo region is changed so that the homology to complementary 3 'Page 16S rRNA either increased or decreased.
In Bezug auf die „spezifische Expressionsaktivität" wird unter Erhöhung oder Reduzie¬ rung im Vergleich zum Wildtyp eine Erhöhung oder Reduzierung der spezifischen Akti¬ vität gegenüber der erfindungsgemäßen Expressionseinheit des Wildtyps, also bei¬ spielsweise gegenüber der SEQ. ID. NO. 2 verstanden.With regard to the "specific expression activity", an increase or reduction in the specific activity relative to the wild-type expression unit according to the invention, ie with respect to SEQ ID NO.
Gemäß Ausführungsform d) kann die Veränderung oder Verursachung der Expressi¬ onsrate von Genen in Mikroorganismen im Vergleich zum Wildtyp dadurch erfolgen, dass man die Expression von Genen im Mikroorganismus durch erfindungsgemäße Expressionseinheiten oder durch erfindungsgemäße Expressionseinheiten mit verän¬ derter spezifischer Expressionsaktivität gemäß Ausführungsform c) reguliert, wobei die Gene in Bezug auf die Expressionseinheiten heterolog sind.In accordance with embodiment d), the change or causation of the expression rate of genes in microorganisms in comparison to the wild type can be effected by regulating the expression of genes in the microorganism by expression units according to the invention or by expression units according to the invention with altered specific expression activity according to embodiment c) wherein the genes are heterologous with respect to the expression units.
Dies wird bevorzugt dadurch erreicht, dass manThis is preferably achieved by one
d1) eine oder mehrere erfindungsgemäße Expressionseinheiten, gegebenenfalls mit veränderter spezifischer Expressionsaktivität, in das Genom des Mikroorga¬ nismus einbringt, so dass die Expression eines oder mehrerer endogenen Gene unter der Kontrolle der eingebrachten Expressionseinheiten erfolgt oderd1) introducing one or more expression units according to the invention, optionally with altered specific expression activity, into the genome of the microorganism such that the expression of one or more endogenous genes takes place under the control of the introduced expression units or
d2) ein oder mehrere Gene in das Genom des Mikrorganismus einbringt, so dass die Expression eines oder mehrerer der eingebrachten Gene unter der Kontrolle der erfindungsgemäßen, endogenen Expressionseinheiten, gegebenenfalls mit veränderter spezifischer Expressionsaktivität, erfolgt oderd2) introducing one or more genes into the genome of the microorganism, so that the expression of one or more of the genes introduced takes place under the control of the endogenous expression units according to the invention, optionally with altered specific expression activity, or
d3) ein oder mehrere Nukleinsäurekonstrukte, enthaltend eine erfindungsgemäße Expressionseinheit, gegebenenfalls mit veränderter spezifischer Expressionsak-
tivität, und funktionell verknüpft eine oder mehrere, zu exprimierende Nuklein¬ säuren, in den Mikroorganismus einbringt.d3) one or more nucleic acid constructs containing an expression unit according to the invention, optionally with modified specific expression activity, and functionally linked to one or more nucleic acids to be expressed, into which microorganisms are introduced.
Es ist somit möglich, die Expressionsrate eines endogenen Gens des Wildtyps zu ver- ändern, also zu erhöhen oder zu erniedrigen indem manIt is thus possible to change the expression rate of an endogenous gene of the wild-type, ie to increase or decrease it by
gemäß Ausführungsform d1) eine oder mehrere erfindungsgemäße Expressionseinhei¬ ten, gegebenenfalls mit veränderter spezifischer Expressionsaktivität, in das Genom des Mikroorganismus einbringt, so dass die Expression eines oder mehrerer endoge- nen Gene unter der Kontrolle der eingebrachten Expressionseinheiten erfolgt oderAccording to embodiment d1), one or more expression units according to the invention, optionally with altered specific expression activity, are introduced into the genome of the microorganism such that expression of one or more endogenous genes takes place under the control of the introduced expression units or
gemäß Ausführungsform d2) ein oder mehrere Gene in das Genom des Mikrorganis- mus einbringt, so dass die Expression eines oder mehrerer der eingebrachten Gene unter der Kontrolle der erfindungsgemäßen, endogenen Expressionseinheiten, gege- benenfalls mit veränderter spezifischer Expressionsaktivität, erfolgt oderaccording to embodiment d2) introduces one or more genes into the genome of the microorganism such that the expression of one or more of the introduced genes takes place under the control of the endogenous expression units according to the invention, optionally with altered specific expression activity, or
gemäß Ausführungsform d3) ein oder mehrere Nukleinsäurekonstrukte, enthaltend eine erfindungsgemäße Expressionseinheit, gegebenenfalls mit veränderter spezifi¬ scher Expressionsaktivität, und funktionell verknüpft eine oder mehrere, zu exprimie- rende Nukleinsäuren, in den Mikroorganismus einbringt.according to embodiment d3) one or more nucleic acid constructs containing an expression unit according to the invention, optionally with modified specific expression activity, and functionally linked one or more nucleic acids to be expressed, into which microorganism introduces.
Ferner ist es somit möglich, die Expressionssrate eines exogenen Gens im Vergleich zum Wildtyps zu verursachen, indem manFurthermore, it is thus possible to cause the expression rate of an exogenous gene compared to the wild type by
gemäß Ausführungsform d2) ein oder mehrere exogene Gene in das Genom desaccording to embodiment d2) one or more exogenous genes into the genome of the
Mikrorganismus einbringt, so dass die Expression eines oder mehrerer der eingebrach¬ ten Gene unter der Kontrolle der erfindungsgemäßen, endogenen Expressionseinhei¬ ten, gegebenenfalls mit veränderter spezifischer Expressionsaktivität, erfolgt oderIntroduces microorganism, so that the expression of one or more of the incorporated genes takes place under the control of the endogenous expression units according to the invention, optionally with altered specific expression activity, or
gemäß Ausführungsform d3) ein oder mehrere Nukleinsäurekonstrukte, enthaltend eine erfindungsgemäße Expressionseinheit, gegebenenfalls mit veränderter spezifi¬ scher Expressionsaktivität, und funktionell verknüpft eine oder mehrere, zu exprimie¬ rende, exogene Nukleinsäuren, in den Mikroorganismus einbringt.according to embodiment d3), one or more nucleic acid constructs comprising an expression unit according to the invention, optionally with altered specific expression activity, and functionally linked one or more exogenous nucleic acids to be expressed, into which microorganism introduces.
Die Insertion von Genen gemäß Ausführungsform d2) kann dabei so erfolgen, dass das Gen in kodierende Bereiche oder nicht-kodierende Bereiche integriert wird. Vor¬ zugsweise erfolgt die Insertion in nicht-kodierende Bereiche.
6The insertion of genes according to embodiment d2) can be carried out so that the gene is integrated into coding regions or non-coding regions. Vor¬ preferably the insertion into non-coding regions. 6
Die Insertion von Nukleinsäurekonstrukten gemäß Ausführungsform d3) kann dabei chromosomal oder extrachromosomal erfolgen. Vorzugsweise erfolgt die Insertion der Nukleinsäurekonstrukte chromosomal.The insertion of nucleic acid constructs according to embodiment d3) can be effected chromosomally or extrachromosomally. Preferably, the insertion of the nucleic acid constructs is chromosomal.
Die Nukleinsäurekonstrukte werden im folgenden auch als Expressionskasetten be¬ zeichnet.The nucleic acid constructs are also referred to below as expression cassettes.
In Ausführungsform d) werden bevorzugt auch erfindungsgemäße Expressionseinhei¬ ten mit veränderter spezifischer Expressionsaktivität gemäß Ausführungsform c) ein- gesetzt. Diese können in Ausführungsform d), wie in Ausführungsform d) beschrieben im Mikroorganismus vorliegen und hergestellt werden oder in isolierter Form in den Mikroorganismus eingebracht werden.In embodiment d) it is also preferred to use expression units according to the invention with modified specific expression activity according to embodiment c). These can be present in the microorganism and prepared in embodiment d), as described in embodiment d), or introduced into the microorganism in isolated form.
Die Erfindung betrifft ferner in einer bevorzugten Ausführungsform ein Verfahren zur Erhöhung oder Verursachung der Expressionsrate eines Gens in Mikroorganismen im Vergleich zum Wildtyp indem manThe invention further relates in a preferred embodiment to a method for increasing or causing the expression rate of a gene in microorganisms compared to the wild type by
ch) die spezifische Expressionsaktivität im Mikroorganismus von erfindungsgemäßen, endogenen Expressionseinheiten, die die Expression der endogenen Gene regulieren, im Vergleich zum Wildtyp erhöht oderch) the specific expression activity in the microorganism of endogenous expression units according to the invention which regulate the expression of the endogenous genes is increased in comparison to the wild-type or
dh) die Expression von Genen im Mikroorganismus durch erfindungsgemäße Expres¬ sionseinheiten oder durch Expressionseinheiten mit erhöhter spezifischer Expressi¬ onsaktivität gemäß Ausführungsform c) reguliert, wobei die Gene im Bezug auf die Expressionseinheiten heterolog sind.ie) the expression of genes in the microorganism by expression units according to the invention or by expression units with increased specific expression activity on the basis of embodiment c), the genes being heterologous with respect to the expression units.
Vorzugsweise wird die Regulation der Expression von Genen im Mikroorganismus durch erfindungsgemäße Expressionseinheiten oder durch Expressionseinheiten mit erhöhter spezifischer Expressionsaktivität gemäß Ausführungsform c) dadurch erreicht, dass manPreferably, the regulation of the expression of genes in the microorganism by expression units according to the invention or by expression units with increased specific expression activity according to embodiment c) is achieved by
dh1 ) eine oder mehrere erfindungsgemäße Expressionseinheiten, gegebenenfalls mit erhöhter spezifischer Expressionsaktivität, in das Genom des Mikroorga¬ nismus einbringt, so dass die Expression eines oder mehrerer endogenen Gene unter der Kontrolle der eingebrachten Expressionseinheiten, gegebe¬ nenfalls mit erhöhter spezifischer Expressionsaktivität, erfolgt oderdh1) introduces one or more expression units according to the invention, optionally with increased specific expression activity, into the genome of the microorganism such that the expression of one or more endogenous genes takes place under the control of the introduced expression units, if appropriate with increased specific expression activity, or
dh2) ein oder mehrere Gene in das Genom des Mikrorganismus einbringt, so dass die Expression eines oder mehrerer der eingebrachten Gene unter der Kon- trolle der erfindungsgemäßen, endogenen Expressionseinheiten, gegebenen-
falls mit erhöhter spezifischer Expressionsaktivität, erfolgt oderdh2) introduces one or more genes into the genome of the microorganism, so that the expression of one or more of the genes introduced under the control of the endogenous expression units according to the invention, given if increased specific expression activity, or
dh3) ein oder mehrere Nukleinsäurekonstrukte, enthaltend eine erfindungsgemäße Expressionseinheit, gegebenenfalls mit erhöhter spezifischer Expressionsak- tivität, und funktionell verknüpft eine oder mehrere, zu exprimierende Nuklein¬ säuren, in den Mikroorganismus einbringt.ie3) one or more nucleic acid constructs containing an expression unit according to the invention, optionally with increased specific expression activity, and functionally linked one or more nucleic acids to be expressed, into which microorganism introduces.
Die Erfindung betrifft ferner ein Verfahren zur Reduzierung der Expressionsrate von Genen in Mikroorganismen im Vergleich zum Wildtyp, indem manThe invention further relates to a method for reducing the expression rate of genes in microorganisms compared to the wild type by
er) die spezifische Expressionsaktivität im Mikroorganismus von endogenen, erfin¬ dungsgemäßen Expressionseinheiten, die die Expression der endogenen Gene regu¬ lieren, im Vergleich zum Wildtyp reduziert oderhe) reduces the specific expression activity in the microorganism of endogenous expression units according to the invention which regulate the expression of the endogenous genes in comparison to the wild type or
dr) Expressionseinheiten mit reduzierter spezifischer Expressionsaktivität gemäß Aus¬ führungsform er) in das Genom des Mikroorganismus einbringt, so dass die Expression endogener Gene unter der Kontrolle der eingebrachten Expressionseinheiten mit redu¬ zierter Expressionsaktivität erfolgt.dr) introduces expression units with reduced specific expression activity according to embodiment (s) into the genome of the microorganism, so that expression of endogenous genes takes place under the control of the introduced expression units with reduced expression activity.
In einer bevorzugten Ausführungsform der vorstehend beschriebenen erfindungsge¬ mäßen Verfahren zur Veränderung oder Verursachung der Transkriptionsrate und/oder Expressionsrate von Genen in Mikroorganismen sind die Gene ausgewählt aus der Gruppe Nukleinsäuren kodierend ein Protein aus den Biosyntheseweg von Feinchemi¬ kalien, wobei die Gene gegebenenfalls weitere Regulationselemente enthalten können.In a preferred embodiment of the inventive method described above for altering or causing the transcription rate and / or expression rate of genes in microorganisms, the genes are selected from the group nucleic acids encoding a protein from the biosynthetic pathway of Feinchemi¬ kalien, wherein the genes optionally further regulatory elements can contain.
In einer besonders bevorzugten Ausführungsform der vorstehend beschriebenen erfin¬ dungsgemäßen Verfahren zur Veränderung oder Verursachung der Transkriptionsrate und/oder Expressionsrate von Genen in Mikroorganismen sind die Gene ausgewählt aus der Gruppe Nukleinsäuren kodierend ein Protein aus den Biosyntheseweg von proteinogenen und nicht-proteinogenen Aminosäuren, Nukleinsäuren kodierend ein Protein aus dem Biosyntheseweg von Nukleotiden und Nukleosiden, Nukleinsäuren kodierend ein Protein aus dem Biosyntheseweg von organischen Säuren, Nukleinsäu¬ ren kodierend ein Protein aus dem Biosyntheseweg von Lipiden und Fettsäuren, Nuk¬ leinsäuren kodierend ein Protein aus dem Biosyntheseweg von Diolen, Nukleinsäuren kodierend ein Protein aus dem Biosyntheseweg von Konhlenhydraten, Nukleinsäuren kodierend ein Protein aus dem Biosyntheseweg von aromatischen Verbindung, Nuk¬ leinsäuren kodierend ein Protein aus dem Biosyntheseweg von Vitaminen, Nukleinsäu¬ ren kodierend ein Protein aus dem Biosyntheseweg von Cofaktoren und Nukleinsäuren kodierend ein Protein aus dem Biosyntheseweg von Enzymen, wobei die Gene gege- benenfalls weitere Regulationselemente enthalten können.
In einer besondere bevorzugten Ausführungsform sind die Proteine aus dem Biosyn¬ theseweg von Aminosäuren ausgewählt aus der Gruppe Aspartatkinase, Aspartat-Semialdehyd-Dehydrogenase, Diaminopimelat- Dehydrogenase, Diaminopimelat-Decarboxylase, Dihydrodipicolinate-Synthetase, Di- hydrodipicolinate-Reduktase, Glycerinaldehyd-3-Phosphat-Dehydrogenase, 3- Phosphoglycerat-Kinase, Pyruvat-Carboxylase, Triosephosphat-Isomerase, Transkrip- tioneller Regulator LuxR, Transkriptioneller Regulator LysR1 , Transkriptioneller Regulator LysR2, Malat-Quinon-Oxidoreduktase, Glucose-6-Phosphat-Deydrogenase, 6-Phosphogluconat-Dehydrognease, Transketolase, Transaldolase, Homoserin-O- Acetyltransferase, Cystahionin-gamma-Synthase, Cystahionin-beta-Lyase, Serin- Hydroxymethyltransferase, O-Acetylhomoserin-Sulfhydrylase, Methylen- Tetrahydrofolat-Reduktase, Phosphoserin-Aminotransferase, Phosphoserin- Phosphatase, Serin-Acetyl-Transferase, Homoserin-Dehydrogenase, Homoserin- Kinase, Threonin-Synthase, Threonin-Exporter-Carrier, Threonin-Dehydratase, Pyru- vat-Oxidase, Lysin-Exporter, Biotin-Ligase, Cystein-Synthasel, Cystein-Synthase II, Coenzym B12-abhängige Methionin-Synthase, Coenzym B12-unabhängige Methionin- Synthase-Aktivität, Sulfatadenyltransferase Untereinheit 1 und 2, Phosphoadenosin Phosphosulfat Reduktase, Ferredoxin-sulfit-reductase, Ferredoxin NADP Reduktase, 3-Phosphoglycerat Dehydrogenase, RXA00655 Regulator, RXN2910-Regulator, Argi- nyl-t-RNA-Synthetase, Phosphoenolpyruvat-Carboxylase, Threonin Efflux-Protein, Se- rinhydroxymethyltransferase, Fruktose-1 ,6-bisphosphatase, Protein der Sulfat- Reduktion RXA077, Protein der Sulfat-Reduktion RXA248, Protein der Sulfat- Reduktion RXA247, Protein OpcA, 1 -Phosphof ruktokinase und 6-Phosphof ruktokinase.In a particularly preferred embodiment of the inventive method described above for altering or causing the transcription rate and / or expression rate of genes in microorganisms, the genes are selected from the group nucleic acids encoding a protein from the biosynthetic pathway of proteinogenic and non-proteinogenic amino acids, encoding nucleic acids a protein from the biosynthetic pathway of nucleotides and nucleosides, nucleic acids encoding a protein from the biosynthetic pathway of organic acids, nucleic acids encoding a protein from the biosynthetic pathway of lipids and fatty acids, nucleic acids encoding a protein from the biosynthetic pathway of diols, encoding nucleic acids Protein from the biosynthetic pathway of carbohydrate hydrates, nucleic acids encoding a protein from the biosynthetic pathway of aromatic compound, nucleic acids encoding a protein from the biosynthetic pathway of vitamins, encoding nucleic acids a protein from the biosynthetic pathway of cofactors and nucleic acids encoding a protein from the biosynthetic pathway of enzymes, wherein the genes may optionally contain further regulatory elements. In a particularly preferred embodiment, the proteins from the biosynthesis path of amino acids are selected from the group aspartate kinase, aspartate semialdehyde dehydrogenase, diaminopimelate dehydrogenase, diaminopimelate decarboxylase, dihydrodipicolinate synthetase, dihydrodipicolinate reductase, glyceraldehyde-3-phosphate Dehydrogenase, 3-phosphoglycerate kinase, pyruvate carboxylase, triosephosphate isomerase, transcriptional regulator LuxR, transcriptional regulator LysR1, transcriptional regulator LysR2, malate-quinone oxidoreductase, glucose-6-phosphate dehydrogenase, 6-phosphogluconate dehydrognease , Transketolase, transaldolase, homoserine O-acetyltransferase, cystahionine gamma synthase, cystahionine beta-lyase, serine hydroxymethyltransferase, O-acetylhomoserine sulfhydrylase, methylenetetrahydrofolate reductase, phosphoserine aminotransferase, phosphoserine phosphatase, serine acetyl Transferase, homoserine dehydrogenase, homoserine kinase, threonine synthase, T hreonine export carrier, threonine dehydratase, pyruvate oxidase, lysine exporter, biotin ligase, cysteine synthase, cysteine synthase II, coenzyme B12-dependent methionine synthase, coenzyme B12-independent methionine synthase activity , Sulfatadenyltransferase subunits 1 and 2, phosphoadenosine phosphosulfate reductase, ferredoxin sulfite reductase, ferredoxin NADP reductase, 3-phosphoglycerate dehydrogenase, RXA00655 regulator, RXN2910 regulator, arginyl t-RNA synthetase, phosphoenolpyruvate carboxylase, threonine efflux Protein, serine hydroxymethyltransferase, fructose-1, 6-bisphosphatase, sulfate reduction protein RXA077, sulfate reduction protein RXA248, sulfate reduction protein RXA247, protein OpcA, 1-phosphofructokinase and 6-phosphofructokinase.
Bevorzugte Proteine und Nukleinsäuren kodierend diese Proteine der vorstehend be¬ schriebenen Proteine aus dem Biosyntheseweg von Aminosäuren sind Proteinsequen¬ zen bzw. Nukleinsäuresequenzen mikrobiellen Ursprungs, vorzusgweise aus Bakterien der Gattung Corynebacterium oder Brevibacterium, bevorzugt aus coryneformen Bak- terien, besonders bevorzugt aus Corynebakterium glutamicum.Preferred proteins and nucleic acids encoding these proteins of the above-described proteins from the biosynthetic pathway of amino acids are protein sequences or nucleic acid sequences of microbial origin, preferably from bacteria of the genus Corynebacterium or Brevibacterium, preferably from coryneform bacteria, particularly preferably from Corynebacterium glutamicum.
Beispiele für besonders bevorzugte Proteinsequenzen und die entsprechenden Nuk¬ leinsäuresequenzen kodierend diese Proteine aus dem Biosyntheseweg von Amino¬ säuren, deren Bezugsdokument, sowie deren Bezeichnung im Bezugsdokument sind in Tabelle 1 aufgelistet:
Tabelle 1Examples of particularly preferred protein sequences and the corresponding nucleic acid sequences encoding these proteins from the biosynthetic pathway of amino acids, their reference document, as well as their name in the reference document are listed in Table 1: Table 1
Ein weiteres Beispiel für eine besonders bevorzugte Proteinsequenz und die entspre¬ chenden Nukleinsäuresequenz kodierend dieses Protein aus dem Biosyntheseweg von Aminosäuren, ist die Sequenz der Fructose-1 ,6-bisphosphatase 2, oder auch fbr2 ge- nannt, (SEQ. ID. NO. 23) und die entsprechenden Nukleinsäuresequenz kodierend eine Fructose-1 ,6-bisphosphatase 2 (SEQ. ID. NO. 22).Another example of a particularly preferred protein sequence and the corresponding nucleic acid sequence encoding this protein from the biosynthetic pathway of amino acids is the sequence of the fructose-1,6-bisphosphatase 2, or also called fbr2, (SEQ ID NO. 23) and the corresponding nucleic acid sequence encoding a fructose-1, 6-bisphosphatase 2 (SEQ ID NO: 22).
Ein weiteres Beispiel für eine besonders bevorzugte Proteinsequenz und die entspre¬ chenden Nukleinsäuresequenz kodierend dieses Protein aus dem Biosyntheseweg von Aminosäuren, ist die Sequenz des Proteins in Sulfat-Reduktion, oder auch RXA077 genannt, (SEQ. ID. NO. 3) und die entsprechenden Nukleinsäuresequenz kodierend ein Protein in Sulfat-Reduktion (SEQ, ID. NO. 4)Another example of a particularly preferred protein sequence and the corresponding nucleic acid sequence encoding this protein from the biosynthetic pathway of amino acids is the sequence of the protein in sulfate reduction, or else called RXA077, (SEQ ID NO: 3) and the corresponding Nucleic acid sequence encoding a protein in sulfate reduction (SEQ ID NO: 4)
Weitere besonders bevorzugte Proteinsequenzen aus dem Biosyntheseweg von Ami- nosäuren, weisen jeweils die in Tabelle 1 für dieses Protein angegebene Aminosäure¬ sequenz auf, wobei das jeweilige Protein jeweils an mindestens einer der in Tabelle 2/Spalte2 für diese Aminosäuresequenz angegebenen Aminosäurepositionen eine andere proteinogene Aminosäure aufweist als die jeweilige in Tabelle2/Spalte3 in der gleichen Zeile angegebene Aminosäure. In einer weiter bevorzugten Ausführungsform, weisen die Proteine an mindestens einer der in Tabelle 2/Spalte 2 für die Aminosäure¬ sequenz angegebenenen Aminosäureposition die in Tabelle2/Spalte4 in der gleichen Zeile angegebene Aminosäure auf. Es handelt sich bei den in Tabelle 2 angegebenen Proteine um mutierte Proteine des Biosyntheseweges von Aminosäuren, die beson¬ ders vorteilhafte Eigenschaften aufweisen und sich deshalb insbesondere zur Expres-
sion der entsprechenden Nukleinsäuren durch den erfinungsgemäßen Promotor und zur Herstellung von Aminosäuren eignen. Beispielsweise führt die Mutation T3111 zu einem Ausschalten der feedback-lnhibierung von ask.Further particularly preferred protein sequences from the biosynthesis pathway of amino acids each have the amino acid sequence given in Table 1 for this protein, the respective protein in each case at least one of the amino acid positions indicated in Table 2 / column 2 for this amino acid sequence another proteinogenic amino acid than the respective amino acid indicated in Table 2 / Column 3 in the same line. In a further preferred embodiment, the proteins have the amino acid indicated in Table 2 / Column 4 in the same row on at least one of the amino acid positions indicated in Table 2 / Column 2 for the amino acid sequence. The proteins indicated in Table 2 are mutated proteins of the biosynthetic pathway of amino acids which have particularly advantageous properties and are therefore particularly suitable for expression. sion of the corresponding nucleic acids by the promoter according to the invention and for the production of amino acids. For example, the T3111 mutation results in switching off the feedback inhibition from ask.
Die entsprechenden Nukleinsäuren, die ein vorstehend beschriebenes mutiertes Prote¬ in aus Tabelle 2 kodieren, lassen sich durch übliche verfahren herstellen.The corresponding nucleic acids which encode a mutated protein from Table 2 described above can be prepared by conventional methods.
Als Ausgangspunkt zur Herstellung der Nukleinsäuresequenzen kodierend ein mutier¬ tes Protein eignet sich beispielsweise das Genom eines Corynebactθrium glutamicum- Stammes, der von der American Type Culture Collection unter der Bezeichnung ATCC 13032 erhältlich ist oder die in Tabelle 1 in Bezug genommenen Nukleinsäuresequen¬ zen. Für die Rückübersetzung der Aminosäuresequenz der mutierten Proteine in die Nukleinsäuresequenzen kodierend diese Proteine ist es vorteilhaft, die codon usage desjenigen Organismus zu verwenden, in den die Nukleinsäuresequenz eingebracht werden soll oder in der die Nukleinsäuresequenz vorliegt. Beispielsweise ist es vortei- haft für Corynebakterium glutamicum die codon usage von Corynebakterium glutami- cum zu verwenden. Die codon usage des jeweiligen Organismus lässt sich in an sich bekannter Weise aus Datenbanken oder Patentanmeldungen ermitteln, die zumindest ein Protein und ein Gen, das dieses Protein kodiert, aus dem gewünschten Organis- mus beschreiben.The starting point for the preparation of the nucleic acid sequences encoding a mutated protein is, for example, the genome of a Corynebacterium glutamicum strain which is obtainable from the American Type Culture Collection under the name ATCC 13032 or the nucleic acid sequences referred to in Table 1. For the back translation of the amino acid sequence of the mutated proteins into the nucleic acid sequences encoding these proteins, it is advantageous to use the codon usage of the organism into which the nucleic acid sequence is to be introduced or in which the nucleic acid sequence is present. For example, it is preferable for Corynebacterium glutamicum to use the codon usage of Corynebacterium glutamicum. The codon usage of the particular organism can be determined in a manner known per se from databases or patent applications which describe at least one protein and a gene which codes for this protein from the desired organism.
Die Angaben in Tabelle 2 sind folgendermassen zu verstehen:The data in Table 2 are to be understood as follows:
In Spalte 1 "Identifikation" wird eine eindeutige Bezeichnung für jede Sequenz in Bezug auf Tabelle 1 aufgeführt.Column 1 "Identification" lists a unique name for each sequence in relation to Table 1.
In Spalte 2 "AS-POS" bezieht sich die jeweilige Zahl auf die Aminosäureposition der entsprechenden Polypeptidsequenz aus Tabelle 1. Eine "26" in der Spalte "AS-POS" bedeutet demzufolge die Aminosäureposition 26 der entsprechend angegebenen PoIy- peptidsequenz. Die Zählung der Position beginnt N-Terminal bei +1.In column 2 "AS-POS" the respective number refers to the amino acid position of the corresponding polypeptide sequence from Table 1. A "26" in the column "AS-POS" therefore means the amino acid position 26 of the corresponding indicated polypeptide sequence. The counting of the position starts N-terminal at +1.
In Spalte 3 "AS-Wildtyp" bezeichnet der jeweilige Buchstabe die Aminosäure - darge¬ stellt im Ein-Buchstaben-Code- an der in Spalte 2 angegebenen Position beim ent¬ sprechenden Wildtyp-Stamm der Sequenz aus Tabelle 1.In column 3 "AS wild type" the respective letter designates the amino acid - represents in the one-letter code at the position indicated in column 2 at the ent speaking wild-type strain of the sequence from Table 1.
In Spalte 4 "AS-Mutante" bezeichnet der jeweilige Buchstabe die Aminosäure - darge¬ stellt im Ein-Buchstaben-Code- an der in Spalte 2 angegebenen Position beim ent¬ sprechenden Mutanten-Stamm.
In Spalte 5 "Funktion" wird die physiologische Funktion der entsprechenden Polypep- tidsequenz aufgeführt.In column 4 "AS mutant" the respective letter designates the amino acid - represents in the one-letter code- at the position indicated in column 2 in the corresponding mutant strain. Column 5 "Function" lists the physiological function of the corresponding polypeptide sequence.
Für ein mutiertes Protein mit einer bestimmten Funktion (Spalte 5) und einer bestimm- ten Ausgangsaminosäuresequenz (Tabelle 1) werden in den Spalten 2,3 und 4 min¬ destens eine Mutation, bei einigen Sequenzen auch mehrere Mutationen beschrieben. Diese mehreren Mutationen beziehen sich immer auf die jeweils obenstehende, nächstliegendste Ausgangsaminosäuresequenz (Tabelle 1). Unter dem Begriff „min¬ destens eine der Aminsäurepositionen" einer bestimmten Aminosäuresequenz wird vorzugsweise mindestens eine der für diese Aminosäuresequenz in Spalte 2, 3 und 4 beschriebenen Mutationen verstanden.For a mutated protein with a specific function (column 5) and a specific starting amino acid sequence (table 1), at least one mutation is described in columns 2, 3 and 4, and several mutations are also described for some sequences. These multiple mutations always refer to the above-mentioned, closest starting amino acid sequence (Table 1). The term "at least one of the amino acid positions" of a particular amino acid sequence is preferably understood to mean at least one of the mutations described for this amino acid sequence in columns 2, 3 and 4.
Ein-Buchstaben-Code der proteinogenen Aminosäuren:One-letter code of proteinogenic amino acids:
A AlaninA Alanine
C CysteinC Cysteine
D AspartatD aspartate
E GlutamatE glutamate
FPhenylalanin G GlycinFPhenylalanine G glycine
H HisH His
I lsoleucinI isoleucine
K LysinK lysine
LLeucin M MethioninLLeucine M methionine
N AsparaginN asparagine
P ProlinP proline
Q GlutaminQ Glutamine
R Arginin S SerinR arginine S serine
TThreoninTThreonin
V ValinV Valin
W TryptophanW tryptophan
Y Tyrosin
Tabelle 2Y tyrosine Table 2
In den vorstehend beschriebenen erfindungsgemäßen Verfahren zur Veränderung o- der Verursachung der Transkriptionsrate und/oder Expressionsrate von Genen in Mik¬ roorganismen sowie den nachstehend beschriebenen Verfahren zur Herstellung von genetisch veränderten Mikroorganismen, den nachstehend beschriebenen genetisch veränderten Mikroorganoismen und den nachstehend beschriebenen Verfahren zur Herstellung von biosynthetischen Produkten erfolgt das Einbringen der erfindungsge¬ mäßen Nukleinsäuren mit Promotoraktivität, der erfindungsgemäßen Expressionsein¬ heiten, der vorstehend beschriebenen Gene und der vorstehend beschriebnen Nuk- leinsäurekonstrukte oder Expressionskasetten in den Mikroorganismus, insbeondere in corynefome Bakterien, vorzugsweise durch die SacB-Methode.In the above-described method according to the invention for altering or causing the transcription rate and / or expression rate of genes in microorganisms and the methods for the production of genetically modified microorganisms described below, the genetically modified microorganisms described below and the methods for the preparation of biosynthetic products, the incorporation of the erfindungsge¬ according to nucleic acids with promoter activity, the expression units of the invention, the genes described above and the above-described Nucleic acid constructs or expression cassettes in the microorganism, in particular in corynefome bacteria, preferably by the SacB method.
Die SacB-Methode ist dem Fachmann bekannt und beispielsweise in Schäfer A, Tauch A, Jäger W, Kalinowski J, Thierbach G, Pühler A.; Small mobilizable multi-purpose clo- ning vectors derived f rom the Escherichia coli plasmids pK18 and pK19: selection of def ined deletions in the chromosome of Corynebacterium glutamicum, Gene. 1994 JuI 22;145(1):69-73 und Blomfield IC, Vaughn V, Rest RF1 Eisenstein Bl.; Allelic exchange in Escherichia coli using the Bacillus subtilis sacB gene and a temperature-sensitive pSC-101 replicon; Mol Microbiol. 1991 Jun;5(6): 1447-57 beschrieben.The SacB method is known to the person skilled in the art and is described, for example, in Schäfer A, Tauch A, Jäger W, Kalinowski J, Thierbach G, Pühler A .; Small mobilizable multi-purpose cloning vectors derived from the Escherichia coli plasmids pK18 and pK19: selection of deficient deletions in the chromosomes of Corynebacterium glutamicum, Gene. 1994 JuI 22; 145 (1): 69-73 and Blomfield IC, Vaughn V, remainder RF 1 Eisenstein Bl .; Allelic exchange in Escherichia coli using the Bacillus subtilis sacB gene and a temperature-sensitive pSC-101 replicon; Mol Microbiol. 1991 Jun; 5 (6): 1447-57.
In einer bevorzugten Ausführungsform der vorstehend beschriebenen erfindungsge¬ mäßen Verfahren erfolgt die Veränderung oder Verursachung der Transkriptionsrate und/oder Expressionsrate von Genen in Mikroorganismen durch Einbringen von erfin¬ dungsgemäßen Nukleinsäuren mit Promotoraktivität bzw. erfindungsgemäßen Expres- sionseinheiten in den Mikroorganismus.In a preferred embodiment of the method according to the invention described above, the change or causation of the transcription rate and / or expression rate of genes in microorganisms is effected by introducing nucleic acids according to the invention having promoter activity or inventive expression units into the microorganism.
In einer weiteren bevorzugten Ausführungsform der vorstehend beschriebenen erfin¬ dungsgemäßen Verfahren erfolgt die Veränderung oder Verursachung der Transkripti¬ onsrate und/oder Expressionsrate von Genen in Mikroorganismen durch Einbringen der vorstehend beschriebenen Nukleinsäurekonstrukte oder Expressionskasetten in den Mikroorganismus.
Die Erfindung betrifft daher ferner eine Expressionskassette, umfassendIn a further preferred embodiment of the methods according to the invention described above, the change or causation of the transcription rate and / or expression rate of genes in microorganisms takes place by introduction of the above-described nucleic acid constructs or expression cassettes into the microorganism. The invention therefore further relates to an expression cassette comprising
mindestens eine erfindungsgemäße Expressionseinheitat least one expression unit according to the invention
mindestens eine weitere, zu exprimierende Nukleinsäuresequenz, also ein zu exprimie- rendes Gen undat least one further nucleic acid sequence to be expressed, ie a gene to be expressed, and
gegebenenfalls weitere genetische Kontrollelemente, wie beispielsweise einen Termi¬ nator,optionally further genetic control elements, such as a terminator,
wobei mindestens eine Expressionseinheit und eine weitere, zu exprimierende, Nuk¬ leinsäuresequenz funktionell miteinander verknüpft sind und die weitere, zu exprimie¬ rende, Nukleinsäuresequenz in Bezug auf die Expressionseinheit heterolog ist.wherein at least one expression unit and another nucleic acid sequence to be expressed are functionally linked to one another and the further nucleic acid sequence to be expressed is heterologous with respect to the expression unit.
Vorzugsweise ist die zu exprimierende Nukleinsäuresequenz mindestens eine Nuklein¬ säuren kodierend ein Protein aus den Biosyntheseweg von Feinchemikalien.Preferably, the nucleic acid sequence to be expressed is at least one nucleic acid encoding a protein from the biosynthetic pathway of fine chemicals.
Besonders bevorzugt ist die zu exprimierende Nukleinsäuresequenz ausgewählt aus der Gruppe Nukleinsäuren kodierend ein Protein aus den Biosyntheseweg von protei- nogenen und nicht-proteinogenen Aminosäuren, Nukleinsäuren kodierend ein Protein aus dem Biosyntheseweg von Nukleotiden und Nukleosiden, Nukleinsäuren kodierend ein Protein aus dem Biosyntheseweg von organischen Säuren, Nukleinsäuren kodie¬ rend ein Protein aus dem Biosyntheseweg von Lipiden und Fettsäuren, Nukleinsäuren kodierend ein Protein aus dem Biosyntheseweg von Diolen, Nukleinsäuren kodierend ein Protein aus dem Biosyntheseweg von Konhlenhydraten, Nukleinsäuren kodierend ein Protein aus dem Biosyntheseweg von aromatischen Verbindung, Nukleinsäuren kodierend ein Protein aus dem Biosyntheseweg von Vitaminen, Nukleinsäuren kodie¬ rend ein Protein aus dem Biosyntheseweg von Cofaktoren und Nukleinsäuren kodie¬ rend ein Protein aus dem Biosyntheseweg von Enzymen.The nucleic acid sequence to be expressed is particularly preferably selected from the group of nucleic acids encoding a protein from the biosynthesis pathway of proteinogenic and non-proteinogenic amino acids, nucleic acids encoding a protein from the biosynthetic pathway of nucleotides and nucleosides, nucleic acids encoding a protein from the biosynthetic pathway of organic acids , Nucleic acids encoding a protein from the biosynthetic pathway of lipids and fatty acids, nucleic acids encoding a protein from the biosynthetic pathway of diols, nucleic acids encoding a protein from the biosynthetic pathway of carbohydrates, nucleic acids encoding a protein from the biosynthetic pathway of aromatic compound, nucleic acids encoding a protein from the biosynthetic pathway of vitamins, nucleic acids encoding a protein from the biosynthetic pathway of cofactors and nucleic acids encoding a protein from the biosynthetic pathway of enzymes.
Bevorzugte Proteine aus dem Biosyntheseweg von Aminosäuren sind vorstehend und deren Beispiele in Tabelle 1 und 2 beschrieben.Preferred proteins from the biosynthetic pathway of amino acids are described above and their examples in Tables 1 and 2.
In den erfindungsgemäßen Expressionskassetten ist die physikalische Lage der Ex- pressionseinheit relativ zum zu exprimierenden Gen so gewählt, daß die Expressio¬ neinheit die Transkription und vorzugsweise auch die Translation des zu exprimieren¬ den Gens reguliert und damit die Bildung eines oder mehrerer Proteine ermöglicht. Die "Bildung ermöglichen" beinhaltet dabei die konstitutive Steigerung der Bildung, Abschwächung bzw. Blockierung der Bildung unter spezifischen Bedingungen und oder die Steigerung der Bildung unter spezifischen Bedingungen. Die "Bedingungen" umfassen dabei: (1 ) Zugabe einer Komponente zum Kulturmedium, (2) Entfernen einer
fassen dabei: (1) Zugabe einer Komponente zum Kulturmedium, (2) Entfernen einer Komponente vom Kulturmedium, (3) Austausch einer Komponente im Kulturmedium durch eine zweite Komponente, (4) Erhöhung der Temperatur des Kulturmediums, (5) Erniedrigung der Temperatur des Kulturmediums, und (6) Regulierung der atmosphäri- sehen Bedingungen, wie z.B. die Sauerstoff- oder Stickstoffkonzentration, in der das Kulturmedium gehalten wird.In the expression cassettes according to the invention, the physical position of the expression unit relative to the gene to be expressed is selected so that the expression unit regulates the transcription and preferably also the translation of the gene to be expressed and thus enables the formation of one or more proteins. The "enabling education" involves constitutively increasing the formation, weakening or blocking the formation under specific conditions and / or increasing the formation under specific conditions. The "conditions" include: (1) adding a component to the culture medium, (2) removing one (1) adding a component to the culture medium, (2) removing a component from the culture medium, (3) replacing a component in the culture medium with a second component, (4) increasing the temperature of the culture medium, (5) lowering the temperature of the culture medium Culture medium, and (6) regulation of atmospheric conditions, such as oxygen or nitrogen concentration, in which the culture medium is maintained.
Die Erfindung betrifft ferner einen Expressionsvektor enthaltend eine vorstehend be¬ schriebene, erfindungsgemäße Expressionskassette.The invention furthermore relates to an expression vector comprising an above-described expression cassette according to the invention.
Vektoren sind dem Fachmann wohl bekannt und können beispielsweise aus "Cloning Vectors" (Pouwels P. H. et al., Hrsg, Elsevier, Amsterdam-New York-Oxford, 1985) entnommen werden. Unter Vektoren sind außer Plasmiden auch alle anderen dem Fachmann bekannten Vektoren, wie beispielsweise Phagen, Transposons, IS- Elemente, Phasmide, Cosmide, und lineare oder zirkuläre DNA zu verstehen. Diese Vektoren können autonom im Wirtsorganismus repliziert oder chromosomal repliziert werden.Vectors are well known to those skilled in the art and can be found, for example, in "Cloning Vectors" (Pouwels P.H. et al., Eds. Elsevier, Amsterdam-New York-Oxford, 1985). Vectors other than plasmids are also to be understood as meaning all other vectors known to the person skilled in the art, such as, for example, phages, transposons, IS elements, phasmids, cosmids, and linear or circular DNA. These vectors can be autonomously replicated in the host organism or replicated chromosomally.
Als Plasmide eignen sich solche besonders bevorzugt, die in coryneformen Bakterien repliziert werden. Zahlreiche bekannte Plasmidvektoren, wie z. B. pZ1 (Menkel et al., Applied and Environmental Microbiology (1989) 64: 549-554), pEKExi (Eikmanns et al., Gene 102: 93-98 (1991)) oder pHS2-1 (Sonnen et al., Gene 107: 69-74 (1991)) beruhen auf den kryptischen Plasmiden pHM1519, pBL1 oder pGA1. Andere Plasmid¬ vektoren, wie z. B. pCLiK5MCS, oder solche, die auf pCG4 (US-A 4,489,160) oder pNG2 (Serwold-Davis et al., FEMS Microbiology Letters 66, 119-124 (1990)) oder pAG1 (US-A 5,158,891) beruhen, können in gleicher Weise verwendet werden.Particularly suitable plasmids are those which are replicated in coryneform bacteria. Numerous known plasmid vectors, such. PZKE (Menkel et al., Applied and Environmental Microbiology (1989) 64: 549-554), pEKExi (Eikmanns et al., Gene 102: 93-98 (1991)) or pHS2-1 (Sonnen et al. Gene 107: 69-74 (1991)) are based on the cryptic plasmids pHM1519, pBL1 or pGA1. Other Plasmid¬ vectors, such as. B. pCLiK5MCS, or those based on pCG4 (US-A 4,489,160) or pNG2 (Serwold-Davis et al., FEMS Microbiology Letters 66, 119-124 (1990)) or pAG1 (US-A 5,158,891), can be in be used in the same way.
Weiterhin eignen sich auch solche Plasmidvektoren mit Hilfe derer man das Verfahren der Genamplifikation durch Integration in das Chromosom anwenden kann, so wie es beispielsweise von Remscheid et al. (Applied and Environmental Microbiology 60,126- 132 (1994)) zur Duplikation bzw. Amplif ikation des hom-thrB-Operons beschrieben wurde. Bei dieser Methode wird das vollständige Gen in einen Plasmidvektor Moniert, der in einem Wirt (typischerweise E. coli), nicht aber in C. glutamicum replizieren kann. Als Vektoren kommen beispielsweise pSUP301 (Simon et al., Bio/ Technology 1 ,784- 791 (1983)), pK18mob oder pK19mob (Schäfer et al., Gene 145,69-73 (1994)), Ber¬ nard et al., Journal ofMolecular Biology, 234: 534-541 (1993)), pEM1 (Schrumpf et al. 1991 , Journal of Bacteriology 173: 4510-4516) oder pBGS8 (Spratt et al.,1986, Gene 41 : 337-342) in Frage. Der Plasmidvektor, der das zu amplifizierende Gen enthält, wird anschließend durch Transformation in den gewünschten Stamm von C. glutamicum überführt. Methoden zur Transformation sind beispielsweise bei Thierbach et al. (Ap-
plied Microbiology and Biotechnology 29, 356-362 (1988)), Dunican und Shivnan (Bio- technology 7, 1067-1070 (1989)) und Tauch et al. (FEMS Microbiological Letters 123,343-347 (1994)) beschrieben.Furthermore, those plasmid vectors by means of which one can apply the method of gene amplification by integration into the chromosome, as described for example by Remscheid et al. (Applied and Environmental Microbiology 60, 126-132 (1994)) for the duplication or amplification of the hom-thrB operon. In this method, the complete gene is cloned into a plasmid vector that can replicate in a host (typically E. coli) but not in C. glutamicum. Examples of vectors which are used are pSUP301 (Simon et al., Bio / Technology 1, 784-791 (1983)), pK18mob or pK19mob (Schäfer et al., Gene 145, 69-73 (1994)), Berard et al. , Journal of Molecular Biology, 234: 534-541 (1993)), pEM1 (Schrumpf et al., 1991, Journal of Bacteriology 173: 4510-4516) or pBGS8 (Spratt et al., 1986, Gene 41: 337-342) Question. The plasmid vector containing the gene to be amplified is then transformed into the desired strain of C. glutamicum by transformation. Methods for transformation are described by Thierbach et al. (Ap Plied Microbiology and Biotechnology 29, 356-362 (1988)), Dunican and Shivnan (Biotechnology 7, 1067-1070 (1989)) and Tauch et al. (FEMS Microbiological Letters 123,343-347 (1994)).
Die Erfindung betrifft ferner einen genetisch verändertem Mikroorganismus, wobei die genetische Veränderung zu einer Veränderung oder Verursachung der Transkriptions¬ rate von mindestens einem Gen im Vergleich zum Wildtyp führt und bedingt ist durchThe invention further relates to a genetically modified microorganism, wherein the genetic modification leads to a change or causation of the transcription rate of at least one gene in comparison to the wild type and is conditioned by
a) Veränderung der spezifischen Promotoraktivität im Mikroorganismus von mindes- tens einer endogenen Nukleinsäure mit Promotoraktivität gemäß Anspruch 1 , die diea) modification of the specific promoter activity in the microorganism of at least one endogenous nucleic acid with promoter activity according to claim 1, which
Transkription mindestens eines endogenen Gens reguliert oderRegulated transcription of at least one endogenous gene or
b) Regulation der Transkription von Genen im Mikroorganismus durch Nukleinsäuren mit Promotoraktivität gemäß Anspruch 1 oder durch Nukleinsäuren mit Promotoraktivi- tat gemäß Anspruch 1 mit veränderter spezifischer Promotoraktivität gemäß Ausfüh¬ rungsform a), wobei die Gene in Bezug auf die Nukleinsäuren mit Promotoraktivität heterolog sind.b) Regulation of the transcription of genes in the microorganism by nucleic acids with promoter activity according to claim 1 or by nucleic acids with promoter activity according to claim 1 with modified specific promoter activity according to embodiment a), wherein the genes are heterologous with respect to the nucleic acids with promoter activity.
Wie vorstehend bei den Verfahren beschrieben, wird die Regulation der Transkription von Genen im Mikroorganismus durch Nukleinsäuren mit Promotoraktivität gemäß An¬ spruch 1 oder durch Nukleinsäuren mit Promotoraktivität gemäß Anspruch 1 mit verän¬ derter spezifischer Promotoraktivität gemäß Ausführungsform a) dadurch erreicht, dass manAs described above in the methods, the regulation of the transcription of genes in the microorganism by nucleic acids with promoter activity according to claim 1 or by nucleic acids with promoter activity according to claim 1 with altered specific promoter activity according to embodiment a) is achieved by
b1 ) eine oder mehrere Nukleinsäuren mit Promotoraktivität gemäß Anspruch 1 , gebe- nenfalls mit veränderter spezifischer Promotoraktivität, in das Genom des Mikroorga¬ nismus einbringt, so dass die Transkription eines oder mehrerer endogenen Gene un¬ ter der Kontrolle der eingebrachten Nukleinsäure mit Promotoraktivität gemäß An¬ spruch 1 , gegebenenfalls mit veränderter spezifischer Promotoraktivität, erfolgt oderb1) introduces one or more nucleic acids with promoter activity according to claim 1, optionally with modified specific promoter activity, into the genome of the microorganism such that the transcription of one or more endogenous genes under the control of the introduced nucleic acid with promoter activity according to An ¬ Speech 1, optionally with altered specific promoter activity, takes place or
b2) ein oder mehrere Gene in das Genom des Mikrorganismus einbringt, so dass die Transkription eines oder mehrerer der eingebrachten Gene unter der Kontrolle der en¬ dogenen Nukleinsäuren mit Promotoraktivität gemäß Anspruch 1, gegebenenfalls mit veränderter spezifischer Promotoraktivität, erfolgt oderb2) introducing one or more genes into the genome of the microorganism such that the transcription of one or more of the introduced genes takes place under the control of the endogenous nucleic acids with promoter activity according to claim 1, optionally with altered specific promoter activity, or
b3) ein oder mehrere Nukleinsäurekonstrukte, enthaltend eine Nukleinsäure mit Pro¬ motoraktivität gemäß Anspruch 1 , gegebenenfalls mit veränderter spezifischer Promo¬ toraktivität, und funktionell verknüpft eine oder mehrere, zu transkribierende Nuklein¬ säuren, in den Mikroorganismus einbringt.
Die Erfindung betrifft ferner eine genetisch verändertem Mikroorganismus mit erhöhter oder verursachter Transkriptionsrate von mindestens einem Gen im Vergleich zum Wildtyp, wobeib3) one or more nucleic acid constructs containing a nucleic acid with Pro¬ motor activity according to claim 1, optionally with altered specific Promo¬ toraktivität, and functionally linked one or more nucleic acids to be transcribed into the microorganism brings. The invention further relates to a genetically modified microorganism having an increased or caused transcription rate of at least one gene in comparison to the wild type, wherein
ah) die spezifische Promotoraktivität im Mikroorganismus von endogenen Nukleinsäu¬ ren mit Promotoraktivität gemäß Anspruch 1 , die die Transkription von endogenen Ge¬ nen regulieren, im Vergleich zum Wildtyp erhöht ist oderah) the specific promoter activity in the microorganism of endogenous nucleic acids having promoter activity according to claim 1, which regulate the transcription of endogenous genes, is increased in comparison with the wild-type, or
bh) die Transkription von Genen im Mikroorganismus durch Nukleinsäuren mit Promo- toraktivität gemäß Anspruch 1 oder durch Nukleinsäuren mit erhöhter spezifischerbh) the transcription of genes in the microorganism by nucleic acids with promoter activity according to claim 1 or by nucleic acids with increased specific
Promotoraktivität gemäß Ausführungsform ah) reguliert wird, wobei die Gene in Bezug auf die Nukleinsäuren mit Promotoraktivität heterolog sind.Promoter activity according to embodiment ah), wherein the genes are heterologous with respect to the nucleic acids having promoter activity.
Wie vorstehend bei den Verfahren beschrieben, wird die Regulation der Transkription von Genen im Mikroorganismus durch Nukleinsäuren mit Promotoraktivität gemäß An¬ spruch 1 oder durch Nukleinsäuren mit Promotoraktivität gemäß Anspruch 1 mit verän¬ derter spezifischer Promotoraktivität gemäß Ausführungsform a) dadurch erreicht, dass manAs described above in the methods, the regulation of the transcription of genes in the microorganism by nucleic acids with promoter activity according to claim 1 or by nucleic acids with promoter activity according to claim 1 with altered specific promoter activity according to embodiment a) is achieved by
bh1) eine oder mehrere Nukleinsäuren mit Promotoraktivität gemäß Anspruch 1 , ge¬ gebenenfalls mit erhöhter spezifischer Promotoraktivität, in das Genom des Mikroorga¬ nismus einbringt, so dass die Transkription eines oder mehrerer endogenen Gene un¬ ter der Kontrolle der eingebrachten Nukleinsäure mit Promotoraktivität, gegebenenfalls mit erhöhter spezifischer Promotoraktivität, erfolgt oderbh1) introduces one or more nucleic acids with promoter activity according to claim 1, where appropriate with increased specific promoter activity, into the genome of the microorganism such that the transcription of one or more endogenous genes under control of the introduced nucleic acid with promoter activity, optionally with increased specific promoter activity, or
bh2) ein oder mehrere Gene in das Genom des Mikrorganismus einbringt, so dass die Transkription eines oder mehrerer der eingebrachten Gene unter der Kontrolle der en¬ dogenen Nukleinsäuren mit Promotoraktivität gemäß Anspruch 1 , gegebenenfalls mit erhöhter spezifischer Promotoraktivität, erfolgt oderbh2) introduces one or more genes into the genome of the microorganism such that the transcription of one or more of the introduced genes takes place under the control of the endogenous nucleic acids with promoter activity according to claim 1, optionally with increased specific promoter activity, or
bh3) ein oder mehrere Nukleinsäurekonstrukte, enthaltend eine Nukleinsäure mit Promotoraktivität gemäß Anspruch 1 , gegebenenfalls mit erhöhter spezifischer Promo¬ toraktivität, und funktionell verknüpft eine oder mehrere, zu transkribierende Nuklein¬ säuren, in den Mikroorganismus einbringt.bh3) one or more nucleic acid constructs containing a nucleic acid with promoter activity according to claim 1, optionally with increased specific promoter activity, and functionally linked one or more nucleic acids to be transcribed into the microorganism.
Die Erfindung betrifft ferner einen genetisch verändertem Mikroorganismus mit redu¬ zierter Transkriptionsrate von mindetstens einem Gen im Vergleich zum Wildtyp, wobeiThe invention further relates to a genetically modified microorganism having a reduced transcription rate of at least one gene in comparison to the wild type, wherein
ar)die spezifische Promotoraktivität im Mikroorganismus von mindestens einer endo- genen Nukleinsäure mit Promotoraktivität gemäß Anspruch 1 , die die Transkription von
mindestens einem, endogenen Gen reguliert, im Vergleich zum Wildtyp reduziert ist oderar) the specific promoter activity in the microorganism of at least one endogenous nucleic acid with promoter activity according to claim 1, the transcription of or at least one endogenous gene is reduced compared to the wild type or
br)eine oder mehrere Nukleinsäuren mit reduzierter Promotoraktivität gemäßAusfüh- rungsform a) in das Genom des Mikrorganismus eingebracht wurden, so dass diebr) one or more nucleic acids with reduced promoter activity according to embodiment a) have been introduced into the genome of the microorganism, so that the
Transkription mindestens eines endogenen Gens unter der Kontrolle der eingebrachten Nukleinsäure mit reduzierter Promotoraktivität erfolgt.Transcription of at least one endogenous gene under the control of the introduced nucleic acid with reduced promoter activity takes place.
Die Erfindung betrifft ferner einen genetisch verändertem Mikroorganismus, wobei die genetische Veränderung zu einer Veränderung oder Verursachung der Expressionsra¬ te mindestens eines Gens im Vergleich zum Wildtyp führt und bedingt ist durchThe invention further relates to a genetically modified microorganism, wherein the genetic modification leads to a change or causation of the Expressionsra¬ te of at least one gene in comparison to the wild type and is caused by
c) Veränderung der spezifischen Expressionsaktivität im Mikroorganismus von mindes¬ tens einer endogenen Expressionseinheiten gemäß Anspruch 2 oder 3, die die Ex- pression mindestens eines endogenen Gens reguliert, im Vergleich zum Wildtyp oderc) alteration of the specific expression activity in the microorganism of at least one endogenous expression unit according to claim 2 or 3, which regulates the expression of at least one endogenous gene, in comparison to the wild-type or
d) Regulation der Expression von Genen im Mikroorganismus durch Expressionsein¬ heiten gemäß Anspruch 2 oder 3 oder durch Expressionseinheiten gemäß Anspruch 2 oder 3 mit veränderter spezifischer Expressionsaktivität gemäß Ausführungsform a), wobei die Gene im Bezug auf die Expressionseinheiten heterolog sind.d) Regulation of the expression of genes in the microorganism by Expressionsein¬ units according to claim 2 or 3 or by expression units according to claim 2 or 3 with altered specific expression activity according to embodiment a), wherein the genes are heterologous with respect to the expression units.
Wie vorstehend bei den Verfahren beschrieben, wird die Regulation der Expression von Genen im Mikroorganismus durch Expressionseinheiten gemäß Anspruch 2 oder 3 oder durch Expressionseinheiten gemäß Anspruch 2 oder 3 mit veränderter spezifi- scher Expressionsaktivität gemäß Ausführungsform a) dadurch erreicht, dass manAs described above in the methods, the regulation of the expression of genes in the microorganism by expression units according to claim 2 or 3 or by expression units according to claim 2 or 3 with altered specific expression activity according to embodiment a) is achieved by
d1 ) eine oder mehrere Expressionseinheiten gemäß Anspruch 2 oder 3, gegebenen¬ falls mit veränderter spezifischer Expressionsaktivität, in das Genom des Mikroorga¬ nismus einbringt, so dass die Expression eines oder mehrerer endogenen Gene unter der Kontrolle der eingebrachten Expressionseinheiten gemäß Anspruch 2 oder 3, ge¬ gebenenfalls mit veränderter spezifischer Expressionsaktivität, erfolgt oderd1) introduces one or more expression units according to claim 2 or 3, optionally with altered specific expression activity, into the genome of the microorganism such that the expression of one or more endogenous genes under the control of the introduced expression units according to claim 2 or 3, optionally with altered specific expression activity, or
d2) ein oder mehrere Gene in das Genom des Mikrorganismus einbringt, so dass die Expression eines oder mehrerer der eingebrachten Gene unter der Kontrolle der endo- genen Expressipnseinheiten gemäß Anspruch 2 oder 3, gegebenenfalls mit veränder¬ ter spezifischer Expressionsaktivität, erfolgt oderd2) introduces one or more genes into the genome of the microorganism such that the expression of one or more of the genes introduced takes place under the control of the endogenous expressing units according to claim 2 or 3, optionally with altered specific expression activity, or
d3) ein oder mehrere Nukleinsäurekonstrukte, enthaltend eine Expressionseinheit ge¬ mäß Anspruch 2 oder 3, gegebenenfalls mit veränderter spezifischer Expressionsakti-
vität, und funktionell verknüpft eine oder mehrere, zu exprimierende Nukleinsäuren, in den Mikroorganismus einbringt.d3) one or more nucleic acid constructs containing an expression unit according to claim 2 or 3, optionally with modified specific expression and functionally links one or more nucleic acids to be expressed, into which microorganisms are introduced.
Die Erfindung betrifft ferner einen genetisch verändertem Mikroorganismus mit erhöh- ter oder verursachter Expressionsrate mindestens eines Gens im Vergleich zum Wild¬ typ, wobei manThe invention further relates to a genetically modified microorganism having an increased or caused expression rate of at least one gene in comparison to the wild type, wherein
ch) die spezifische Expressionsaktivität im Mikroorganismus von mindestens einer endogenen Expressionseinheiten gemäß Anspruch 2 oder 3, die die Expression der endogenen Gene reguliert, im Vergleich zum Wildtyp erhöht oderch) the specific expression activity in the microorganism of at least one endogenous expression units according to claim 2 or 3, which regulates the expression of the endogenous genes, compared to the wild type increased or
dh) die Expression von Genen im Mikroorganismus durch Expressionseinheiten ge¬ mäß Anspruch 2 oder 3 oder durch Expressionseinheiten gemäß Anspruch 2 oder 3 mit erhöhter spezifischer Expressionsaktivität gemäß Ausführungsform a) reguliert, wobei die Gene im Bezug auf die Expressionseinheiten heterolog sind.ie) the expression of genes in the microorganism by expression units according to claim 2 or 3 or by expression units according to claim 2 or 3 with increased specific expression activity according to embodiment a), wherein the genes are heterologous with respect to the expression units.
Wie vorstehend bei den Verfahren beschrieben, wird die Regulation der Expression von Genen im Mikroorganismus durch Expressionseinheiten gemäß Anspruch 2 oder 3 oder durch Expressionseinheiten gemäß Anspruch 2 oder 3 mit erhöhter spezifischer Expressionsaktivität gemäß Ausführungsform a) dadurch erreicht, dass manAs described above in the methods, the regulation of the expression of genes in the microorganism by expression units according to claim 2 or 3 or by expression units according to claim 2 or 3 with increased specific expression activity according to embodiment a) is achieved by
dh1 ) eine oder mehrere Expressionseinheiten gemäß Anspruch 2 oder 3, gegebenen¬ falls mit erhöhter spezifischer Expressionsaktivität, in das Genom des Mikroorganismus einbringt, so dass die Expression eines oder mehrerer endogenen Gene unter der Kon- trolle der eingebrachten Expressionseinheiten gemäß Anspruch 2 oder 3, gegebenen¬ falls mit erhöhter spezifischer Expressionsaktivität, erfolgt oderdh1) introduces one or more expression units according to claim 2 or 3, optionally with increased specific expression activity, into the genome of the microorganism, so that the expression of one or more endogenous genes under the control of the introduced expression units according to claim 2 or 3, if appropriate with increased specific expression activity, takes place or
dh2) ein oder mehrere Gene in das Genom des Mikrorganismus einbringt, so dass die Expression eines oder mehrerer der eingebrachten Gene unter der Kontrolle der endo- genen Expressionseinheiten gemäß Anspruch 2 oder 3, gegebenenfalls mit erhöhter spezifischer Expressionsaktivität, erfolgt oderdh2) introduces one or more genes into the genome of the microorganism such that the expression of one or more of the introduced genes takes place under the control of the endogenous expression units according to claim 2 or 3, optionally with increased specific expression activity, or
dh3) ein oder mehrere Nukleinsäurekonstrukte, enthaltend eine Expressionseinheit gemäß Anspruch 2 oder 3, gegebenenfalls mit erhöhter spezifischer Expressionsaktivi- tat, und funktionell verknüpft eine oder mehrere, zu exprimierende Nukleinsäuren, in den Mikroorganismus einbringt.ie3) one or more nucleic acid constructs containing an expression unit according to claim 2 or 3, optionally with increased specific expression activity, and functionally linked to one or more nucleic acids to be expressed, into which microorganism introduces.
Die Erfidnung betrifft ferner einen genetisch verändertem Mikroorganismus mit redu¬ zierter Expressionsrate von mindetstens einem Gen im Vergleich zum Wildtyp, wobei,
er) die spezifische Expressionsaktivität im Mikroorganismus von mindestens einer en¬ dogenen Expressionseinheit gemäß Anspruch 2 oder 3, die die Expression von min¬ destens einem edogenen Gen reguliert, im Vergleich zum Wildtyp reduziert ist oderThe invention further relates to a genetically modified microorganism having a reduced expression rate of at least one gene in comparison to the wild type, wherein it) the specific expression activity in the microorganism of at least one endogenous expression unit according to claim 2 or 3, which regulates the expression of at least one edogenic gene, is reduced in comparison with the wild-type or
dr)eine oder mehrere Expressionseinheiten gemäß Anspruch 2 oder 3 mit reduzierter Expressionsaktivität in das Genom des Mikrorganismus eingebracht wurden, so dass die Expression mindestens eines Gens unter der Kontrolle der eingebrachten Expres¬ sionseinheit gemäß Anspruch 2 oder 3 mit reduzierter Expressionsaktivität erfolgt.dr) one or more expression units according to claim 2 or 3 were introduced with reduced expression activity in the genome of the microorganism, so that the expression of at least one gene under the control of the introduced expression unit according to claim 2 or 3 takes place with reduced expression activity.
Ferner betrifft die Erfindung einen genetisch veränderter Mikroorganismus, enthaltend eine Expressionseinheit gemäß Anspruch 2 oder 3 und funktionell verknüpft ein zu eprimierendes Gen, wobei das Gen im Bezug auf die Expressionseinheit heterolog ist.Furthermore, the invention relates to a genetically modified microorganism containing an expression unit according to claim 2 or 3 and functionally linked to a gene to be expressed, wherein the gene is heterologous with respect to the expression unit.
Besonders bevorzugt enthält dieser genetisch veränderte Mikroorganismus eine erfin¬ dungsgemäße Expressionskasette.This genetically modified microorganism particularly preferably contains an expression cassette according to the invention.
Besonders bevorzugt betrifft die vorliegende Erfindung gentisch veränderte Mikroor- gansismen, insbesondere coryneforme Bakterien, die einen Vektor, insbesondereThe present invention particularly preferably relates to genetically modified microorganisms, in particular coryneform bacteria, which contain a vector, in particular
Pendelvektor oder Plasmidvektor, der wenigstens ein rekombinantes Nukleinsäurekon- strukt erfindungsgemäßer Definition trägt, enthalten.Shuttle vector or plasmid vector carrying at least one recombinant nucleic acid of the invention definition.
In einer bevorzugten Ausführungsform der genetisch veränderten Mikroorganismen sind die vorstehend beschriebenen Gene mindestens eine Nukleinsäuren kodierend ein Protein aus den Biosyntheseweg von Feinchemikalien.In a preferred embodiment of the genetically modified microorganisms, the genes described above are at least one nucleic acid encoding a protein from the biosynthetic pathway of fine chemicals.
In einer besonders bevorzugten Ausführungsform der genetisch veränderten Mikroor¬ ganismen sind die vorstehend beschriebenen Gene ausgewählt sind aus der Gruppe Nukleinsäuren kodierend ein Protein aus den Biosyntheseweg von proteinogenen und nicht-proteinogenen Aminosäuren, Nukleinsäuren kodierend ein Protein aus dem Bio¬ syntheseweg von Nukleotiden und Nukleosiden, Nukleinsäuren kodierend ein Protein aus dem Biosyntheseweg von organischen Säuren, Nukleinsäuren kodierend ein Pro¬ tein aus dem Biosyntheseweg von Lipiden und Fettsäuren, Nukleinsäuren kodierend ein Protein aus dem Biosyntheseweg von Diolen, Nukleinsäuren kodierend ein Protein aus dem Biosyntheseweg von Konhlenhydraten, Nukleinsäuren kodierend ein Protein aus dem Biosyntheseweg von aromatischen Verbindung, Nukleinsäuren kodierend ein Protein aus dem Biosyntheseweg von Vitaminen, Nukleinsäuren kodierend ein Protein aus dem Biosyntheseweg von Cofaktoren und Nukleinsäuren kodierend ein Protein
aus dem Biosyntheseweg von Enzymen, wobei die Gene gegebenenfalls weitere Re¬ gulationselemente enthalten können.In a particularly preferred embodiment of the genetically modified microorganisms, the genes described above are selected from the group consisting of nucleic acids encoding a protein from the biosynthetic pathway of proteinogenic and non-proteinogenic amino acids, nucleic acids encoding a protein from the biosynthesis pathway of nucleotides and nucleosides, Nucleic acids encoding a protein from the biosynthetic pathway of organic acids, nucleic acids encoding a protein from the biosynthetic pathway of lipids and fatty acids, nucleic acids encoding a protein from the biosynthetic pathway of diols, nucleic acids encoding a protein from the biosynthesis pathway of carbohydrates, nucleic acids encoding a protein the biosynthetic pathway of aromatic compound, nucleic acids encoding a protein from the biosynthetic pathway of vitamins, nucleic acids encoding a protein from the biosynthetic pathway of cofactors and nucleic acids encoding a protein from the biosynthetic pathway of enzymes, which genes may optionally contain further regulatory elements.
Bevorzugte Proteine aus dem Biosyntheseweg von Aminosäuren sind ausgewählt aus der Gruppe Aspartatkinase, Aspartat-Semialdehyd-Dehydrogenase, Diaminopimelat- Dehydrogenase, Diaminopimelat-Decarboxylase, Dihydrodipicolinate-Synthetase, Di- hydrodipicolinate-Reduktase, Glycerinaldehyd-3-Phosphat-Dehydrogenase, 3- Phosphoglycerat-Kinase, Pyruvat-Carboxylase, Triosephosphat-Isomerase, Transkrip- tioneller Regulator LuxR, Transkriptioneller Regulator LysR1 , Transkriptioneller Regulator LysR2, Malat-Quinon-Oxidoreduktase, Glucose-6-Phosphat-Deydrogenase, 6-Phosphogluconat-Dehydrognease, Transketolase, Transaldolase, Homoserin-O- Acetyltransferase, Cystahionin-gamma-Synthase, Cystahionin-beta-Lyase, Serin- Hydroxymethyltransferase, O-Acetylhomoserin-Sulfhydrylase, Methylen- Tetrahydrofolat-Reduktase, Phosphoserin-Aminotransferase, Phosphoserin- Phosphatase, Serin-Acetyl-Transferase, Homoserin-Dehydrogenase, Homoserin- Kinase, Threonin-Synthase, Threonin-Exporter-Carrier, Threonin-Dehydratase, Pyru- vat-Oxidase, Lysin-Exporter, Biotin-Ligase, Cystein-Synthasel, Cystein-Synthase Il Coenzym B12-abhängige Methionin-Synthase, Coenzym B12-unabhängige Methionin- Synthase-Aktivität, Sulfatadenyltransferase Untereinheit 1 und 2, Phosphoadenosin Phosphosulfat Reduktase, Ferredoxin-sulfit-reductase, Ferredoxin NADP Reduktase, 3-Phosphoglycerat Dehydrogenase, RXA00655 Regulator, RXN2910-Regulator, Argi- nyl-t-RNA-Synthetase, Phosphoenolpyruvat-Carboxylase, Threonin Efflux-Protein, Se¬ rin hydroxymethyltransferase, Fruktose-1 ,6-bisphosphatase, Protein der Sulfat- Reduktion RXA077, Protein der Sulfat-Reduktion RXA248, Protein der Sulfat- Reduktion RXA247, Protein OpcA, 1 -Phosphofruktokinase und 6-PhosphofruktokinasePreferred proteins from the biosynthetic pathway of amino acids are selected from the group aspartate kinase, aspartate-semialdehyde dehydrogenase, diaminopimelate dehydrogenase, diaminopimelate decarboxylase, dihydrodipicolinate synthetase, dihydrodipicolinate reductase, glyceraldehyde-3-phosphate dehydrogenase, 3-phosphoglycerate Kinase, pyruvate carboxylase, triosephosphate isomerase, transcriptional regulator LuxR, transcriptional regulator LysR1, transcriptional regulator LysR2, malate quinone oxidoreductase, glucose-6-phosphate dehydrogenase, 6-phosphogluconate dehydrognease, transketolase, transaldolase, homoserine O-acetyltransferase, cystahionine gamma synthase, cystahionine beta-lyase, serine hydroxymethyltransferase, O-acetylhomoserine sulfhydrylase, methylenetetrahydrofolate reductase, phosphoserine aminotransferase, phosphoserine phosphatase, serine acetyltransferase, homoserine dehydrogenase, Homoserine kinase, threonine synthase, threonine-exporter-carrier, threonine-dehydrata se, pyruvate oxidase, lysine exporter, biotin ligase, cysteine synthase, cysteine synthase II coenzyme B12-dependent methionine synthase, coenzyme B12-independent methionine synthase activity, sulfate adenyltransferase subunit 1 and 2, phosphoadenosine phosphosulfate Reductase, ferredoxin sulfite reductase, ferredoxin NADP reductase, 3-phosphoglycerate dehydrogenase, RXA00655 regulator, RXN2910 regulator, Arginyl t-RNA synthetase, phosphoenolpyruvate carboxylase, threonine efflux protein, serine hydroxymethyltransferase, fructose 1, 6-bisphosphatase, sulfate reduction protein RXA077, sulfate reduction protein RXA248, sulfate reduction protein RXA247, protein OpcA, 1-phosphofructokinase and 6-phosphofructokinase
Besonders bevorzugte Beispiele der Proteine und Gene aus dem Biosyntheseweg von Aminosäuren sind vorstehend in Tabelle 1 und Tabelle 2 beschrieben.Particularly preferred examples of the proteins and genes from the biosynthetic pathway of amino acids are described above in Table 1 and Table 2.
Bevorzugte Mikroorganismen oder genetisch veränderte Mikroorganismen sind Bakte¬ rien, Algen, Pilze oder Hefen.Preferred microorganisms or genetically modified microorganisms are bacteria, algae, fungi or yeasts.
Besonders bevorzugte Mikroorgansimen sind insbeondere coryneforme Bakterien.Particularly preferred microorganisms are, in particular, coryneform bacteria.
Bevorzugte coryneforme Bakterien sind Bakterien der Gattung Corynebacterium, ins¬ besondere der Arten Corynebacterium glutamicum, Corynebacterium acetoglutami- cum, Corynebacterium acetoacidophilum, Corynebacterium thermoaminogenes, Cory¬ nebacterium melassecola und Corynebacterium efficiens oder der Gattung Brevibacte- rium, insbesondere der Arten Brevibacterium flavum, Brevibacterium lactofermentum und Brevibacterium divaricatum.
Besonders bevorzugte Bakterien der Gattungen Corynebacterium und Brevibacterium sind ausgewählt aus der Gruppe Corynebacterium glutamicum ATCC 13032, Coryne- bacterium acetoglutamicum ATCC 15806, Corynebacterium acetoacidophilum ATCC 13870, Corynebacterium thermoaminogenes FERM BP-1539, Corynebacterium me- lassecola ATCC 17965, Corynebacterium efficiens DSM 44547, Corynebacterium effi- ciens DSM 44548. Corynebacterium efficiens DSM 44549, Brevibacterium flavum ATCC 14067, Brevibacterium lactofermentum ATCC 13869, Brevibacterium divarica- tum ATCC 14020, Corynebacterium glutamicum KFCC10065 und Corynebacterium glutamicum ATCC21608.Preferred coryneform bacteria are bacteria of the genus Corynebacterium, in particular of the species Corynebacterium glutamicum, Corynebacterium acetoglutamicum, Corynebacterium acetoacidophilum, Corynebacterium thermoaminogenes, Corynebacterium melassecola and Corynebacterium efficiens or of the genus Brevibacterium, in particular of the species Brevibacterium flavum, Brevibacterium lactofermentum and Brevibacterium divaricatum. Particularly preferred bacteria of the genera Corynebacterium and Brevibacterium are selected from the group Corynebacterium glutamicum ATCC 13032, Corynebacterium acetoglutamicum ATCC 15806, Corynebacterium acetoacidophilum ATCC 13870, Corynebacterium thermoaminogenes FERM BP-1539, Corynebacterium melassecola ATCC 17965, Corynebacterium efficiens DSM 44547, Corynebacterium efficiens DSM 44548. Corynebacterium efficiens DSM 44549, Brevibacterium flavum ATCC 14067, Brevibacterium lactofermentum ATCC 13869, Brevibacterium divarica- tum ATCC 14020, Corynebacterium glutamicum KFCC10065 and Corynebacterium glutamicum ATCC21608.
Mit der Abkürzung KFCC ist die Korean Federation of Culture Collection gemeint, mit der Abkürzung ATCC die American type strain culture collection, mit der Abkürzung DSM die Deutsche Sammlung von Mikroorganismen.The abbreviation KFCC means the Korean Federation of Culture Collection, the abbreviation ATCC means the American strain strain culture collection, with the abbreviation DSM the German Collection of Microorganisms.
Weitere besonders bevorzugte Bakterien der Gattungen Corynebacterium und Brevi¬ bacterium sind in Tabelle 3 aufgelistet:Further particularly preferred bacteria of the genera Corynebacterium and Brevibacterium are listed in Table 3:
Die Abkürzungen haben folgende Bedeutung:The abbreviations have the following meaning:
ATCC: American Type Culture Collection, Rockville, MD1 USAATCC: American Type Culture Collection, Rockville, MD 1 USA
FERM: Fermentation Research Institute, Chiba, JapanFERM: Fermentation Research Institute, Chiba, Japan
NRRL: ARS Culture Collection, Northern Regional Research Laboratory, Peoria, IL,NRRL: ARS Culture Collection, Northern Regional Research Laboratory, Peoria, IL
USAUSA
CECT: Coleccion Espanola de Cultivos Tipo, Valencia, SpainCECT: Coleccion Espanola de Cultivos Tipo, Valencia, Spain
NCIMB: National Collection of Industrial and Marine Bacteria Ltd., Aberdeen, UKNCIMB: National Collection of Industrial and Marine Bacteria Ltd., Aberdeen, UK
CBS: Centraalbureau voor Schimmelcultures, Baarn, NLCBS: Centraalbureau voor Schimmelcultures, Baarn, NL
NCTC: National Collection of Type Cultures, London, UKNCTC: National Collection of Type Cultures, London, UK
DSMZ: Deutsche Sammlung von Mikroorganismen und Zellkulturen, Braunschweig,DSMZ: German Collection of Microorganisms and Cell Cultures, Braunschweig,
Germanygermany
Durch die erfindungsgemäßen Nukleinsäuren mit Promotoraktivität und den erfin¬ dungsgemäßen Expressionseinheiten ist es mit Hilfe der vorstehend beschriebenen, erfindungsgemäßen Verfahren möglich in den vorstehend beschriebenen, erfindungs¬ gemäßen genetisch veränderten Mikroorganismen die Stoffwechselwege zu spezifi¬ schen biosynthetischen Produkten zu regulieren.
Dazu werden beispielsweise Stoffwechselwege die zu einem spezifischen biosyntheti¬ schen Produkt führen durch Verursachung oder Erhöhung der Transkriptionrate bzw. Expressionsrate von Genen dieses Biosyntheseweges verstärkt in dem die erhöhte Proteinmenge zu einer erhöhten Gesamtaktivität dieser Proteine des gewünschten Biosyntheseweges und damit zu einem verstärkten Stoffwechselfluß zu dem gewün- schen biosynthetischen Produkt führt.The inventive nucleic acids with promoter activity and the expression units according to the invention make it possible with the aid of the above-described inventive methods to regulate the metabolic pathways to specific biosynthetic products in the above-described inventive genetically modified microorganisms. For this purpose, for example, metabolic pathways which lead to a specific biosynthetic product by causing or increasing the transcription rate or expression rate of genes of this biosynthetic pathway in which the increased protein amount to increased total activity of these proteins of the desired biosynthetic pathway and thus to an increased metabolic flux to the gewün - leads biosynthetic product.
Weiterhin können Stoffwechselwege die von einem spezifischen biosynthetischen Pro¬ dukt wegführen durch Reduzierung der Transkriptionrate bzw. Expressionsrate von Genen dieses wegführenden Biosyntheseweges abgeschwächt werden in dem die reduzierte Proteinmenge zu einer reduzierten Gesamtaktivität dieser Proteine des un¬ erwünschten Biosyntheseweges und damit zusätzlich zu einem verstärkten Stoffwech¬ selfluß zu dem gewünschen biosynthetischen Produkt führt.Furthermore, metabolic pathways which lead away from a specific biosynthetic product can be attenuated by reducing the transcription rate or expression rate of genes of this pathway leading to reduced total protein activity of these proteins of the unwanted biosynthetic pathway and thus in addition to increased metabolic activity selfluß leads to the desired biosynthetic product.
Die erfindungsgemäßen genetisch veränderten Mikroorganismen sind beispielsweise in der Lage aus Glucose, Saccharose, Lactose, Fructose, Maltose, Melasse, Stärke, Cellulose oder aus Glycerin und Ethanol biosynthetische Produkte herzustellen.The genetically modified microorganisms according to the invention are, for example, able to produce biosynthetic products from glucose, sucrose, lactose, fructose, maltose, molasses, starch, cellulose or from glycerol and ethanol.
Die Erfindung betrifft daher ein Verfahren zur Herstellung von biosynthetischen Produk- ten durch Kultivierung von erfindungsgemäßen, genetisch veränderten Mikroorganis¬ men.The invention therefore relates to a process for the production of biosynthetic products by culturing genetically modified microorganisms according to the invention.
Je nach gewünschtem biosynthetischen Produkt muss die Transkriptionsrate bzw. Ex¬ pressionsrate verschiedener Gene erhöht bzw. reduziert werden. In der Regel ist es vorteilhaft die Transkrioptionsrate bzw. Expressionsrate mehrere Gene zu verändern, d.h. die Transkrioptionsrate bzw. Expressionsrate einer Kombination von Gene zu Er¬ höhen und/oder die Transkrioptionsrate bzw. Expressionsrate einer Kombination von Gene zu reduzieren.Depending on the desired biosynthetic product, the transcription rate or expression rate of different genes must be increased or reduced. In general, it is advantageous to change the transcription rate or expression rate of several genes, i. to reduce the transcription rate or expression rate of a combination of genes to erhe and / or to reduce the transcription rate or expression rate of a combination of genes.
In den erfindungsgemäßen genetisch veränderten Mikroorganismen ist mindestens eine veränderte, dass heißt erhöhte oder reduzierte Transkriptionsrate bzw. Expressi¬ onsrate eines Gens auf eine erfindungsgemäße Nukleinsäure mit Promotoraktivität bzw. erfindungsgemäße Expressionseinheit zurückzuführen.In the genetically modified microorganisms according to the invention, at least one altered, that is to say increased or reduced, transcription rate or expression rate of a gene can be attributed to a nucleic acid according to the invention having promoter activity or the expression unit according to the invention.
Weitere, zusätzliche veränderte, d.h. zusätzlich erhöhte oder zusätzlich reduzierteFurther, additional modified, i. additionally increased or additionally reduced
Transkriptionsraten bzw. Expressionsraten von weiteren Genen im genetisch veränder¬ ten Mikroorganismus können, müssen aber nicht auf die erfindungsgemäßen Nuklein¬ säuren mit Promotoraktivität bzw. die erfindungsgemäßen Expressionseinheiten zurück gehen.
Die Erfindung betrifft deshalb weiterhin ein Verfahren zur Herstellung von biosyntheti¬ schen Produkten durch Kultivierung von erfindungsgemäßen, genetisch veränderten Mikroorganismen.Transcription rates or expression rates of further genes in the genetically modified microorganism can, but need not, go back to the nucleic acids according to the invention with promoter activity or the expression units according to the invention. The invention therefore furthermore relates to a process for the preparation of biosynthetic products by culturing genetically modified microorganisms according to the invention.
Bevorzugte biosynthetische Produkte sind Feinchemikalien.Preferred biosynthetic products are fine chemicals.
Der Begriff "Feinchemikalie" ist im Fachgebiet bekannt und beinhaltet Verbidnungen, die von einem Organismus produziert werden und in verschiedenen Industriezweigen Anwendungen finden, wie bspw., jedoch nicht beschränkt auf die pharmazeutische Industrie, die Landwirtschafts-, Kosmetik , Food und Feed-Industrie. Diese Verbindun¬ gen umfassen organische Säuren, wie beispielsweise Weinsäure, Itaconsäure und Diaminopimelinsäure, sowohl proteinogene als auch nicht-proteinogene Aminosäuren, Purin- und Pyrimidinbasen, Nukleoside und Nukleotide (wie bspw. beschrieben in Ku- ninaka, A. (1996) Nucleotides and related Compounds, S. 561-612, in Biotechnology Bd. 6, Rehm et al., Hrsg. VCH: Weinheim und den darin enthaltenen Zitaten), Lipide, gesättigte und ungesättigte Fettsäuren (bspw. Arachidonsäure), Diole (bspw. Propan- diol und Butandiol), Kohlenhydrate (bspw. Hyaluronsäure und Trehalose), aromatische Verbindungen (bspw. aromatische Amine, Vanillin und Indigo), Vitamine und Cofakto- ren (wie beschrieben in Ullmann's Encyclopedia of Industrial Chemistry, Bd. A27, "Vitamins", S. 443-613 (1996) VCH: Weinheim und den darin enthaltenen Zitaten; und Ong, A.S., Niki, E. und Packer, L. (1995) "Nutrition, Lipids, Health and Disease" Proceedings of the UNESCO/Confederation of Scientific and Technological Associations in Malaysia and the Society for Free Radical Research - Asien, abgehalten am 1.-3. Sept. 1994 in Penang, Malysia, AOCS Press (1995)), Enzyme und sämtliche anderen von Gutcho (1983) in Chemicals by Fermentation, Noyes Data Cor¬ poration, ISBN: 0818805086 und den darin angegebenen Literaturstellen, beschriebe¬ nen Chemikalien. Der Metabolismus und die Verwendungen bestimmter Feinchemika¬ lien sind nachstehend weiter erläutert.The term "fine chemical" is well known in the art and includes compounds produced by an organism and used in various industries, such as, but not limited to, the pharmaceutical, agricultural, cosmetics, food and feed industries. These compounds include organic acids such as tartaric acid, itaconic acid and diaminopimelic acid, both proteinogenic and non-proteinogenic amino acids, purine and pyrimidine bases, nucleosides and nucleotides (as described for example in Kuinaka, A. (1996) Nucleotides and Related Compounds, pp. 561-612, Biotechnology Vol. 6, Rehm et al., ed. VCH: Weinheim and the citations contained therein), lipids, saturated and unsaturated fatty acids (for example arachidonic acid), diols (for example propane). diol and butanediol), carbohydrates (for example hyaluronic acid and trehalose), aromatic compounds (for example aromatic amines, vanillin and indigo), vitamins and cofactors (as described in Ullmann's Encyclopedia of Industrial Chemistry, Vol. A27, "Vitamins", Pp. 443-613 (1996) VCH: Weinheim and the citations therein; and Ong, AS, Niki, E. and Packer, L. (1995) "Nutrition, Lipids, Health and Disease" Proceedings of the UNESCO / Confederation of Scientific and Technological Gical Associations in Malaysia and the Society for Free Radical Research - Asia, held on 1-3 May. Enzymes and all others by Gutcho (1983) in Chemicals by Fermentation, Noyes Data Corporation, ISBN: 0818805086 and the references cited therein. The metabolism and the uses of certain fine chemicals are further elucidated below.
I. Aminosäure-Metabolismus und VerwendungenI. Amino Acid Metabolism and Uses
Die Aminosäuren umfassen die grundlegenden Struktureinheiten sämtlicher Proteine und sind somit für die normalen Zellfunktionen essentiell. Der Begriff "Aminosäure" ist im Fachgebiet bekannt. Die proteinogenen Aminosäuren, von denen es 20 Arten gibt, dienen als Struktureinheiten für Proteine, in denen sie über Peptidbindungen miteinan¬ der verknüpft sind, wohingegen die nicht-proteinogenen Aminosäuren (von denen Hunderte bekannt sind) gewöhnlich nicht in Proteinen vorkommen (siehe Ullmann's Encyclopedia of Industrial Chemistry, Bd. A2, S. 57-97 VCH: Weinheim (1985)). Die Aminosäuren können in der D- oder L-Konfiguration vorliegen, obwohl L-Aminosäuren gewöhnlich der einzige Typ sind, den man in natürlich vorkommenden Proteinen vor-
findet. Biosynthese- und Abbauwege von jeder der 20 proteinogenen Aminosäuren sind sowohl bei prokaryotischen als auch eukaryotischen Zellen gut charakterisiert (siehe bspw. Stryer, L. Biochemistry, 3. Auflage, S. 578-590 (1988)). Die "essentiellen" Aminosäuren (Histidin, Isoleucin, Leucin, Lysin, Methionin, Phenylalanin, Threonin, Tryptophan und Valin), so bezeichnet, da sie aufgrund der Komplexität ihrer Biosyn¬ these mit der Ernährung aufgenommen werden müssen, werden durch einfache Bio¬ syntheseswege in die übrigen 11 "nichtessentiellen" Aminosäuren (Alanin, Arginin, Asparagin, Aspartat, Cystein, Glutamat, Glutamin, Glycin, Prolin, Serin und Tyrosin) umgewandelt. Höhere Tiere besitzen die Fähigkeit, einige dieser Aminosäuren zu syn- thetisieren, jedoch müssen die essentiellen Aminosäuren mit der Nahrung aufgenom¬ men werden, damit eine normale Proteinsynthese stattfindet.The amino acids comprise the basic structural units of all proteins and are therefore essential for normal cell function. The term "amino acid" is known in the art. The proteinogenic amino acids, of which there are 20 species, serve as structural units for proteins in which they are linked via peptide bonds, whereas the non-proteinogenic amino acids (of which hundreds are known) usually do not occur in proteins (see Ullmann's Encyclopedia of Industrial Chemistry, Vol. A2, pp. 57-97 VCH: Weinheim (1985)). The amino acids may be in the D or L configuration, although L-amino acids are usually the only type found in naturally occurring proteins. place. Biosynthesis and degradation pathways of each of the 20 proteinogenic amino acids are well characterized in both prokaryotic and eukaryotic cells (see, for example, Stryer, L. Biochemistry, 3rd Edition, pp. 578-590 (1988)). The "essential" amino acids (histidine, isoleucine, leucine, lysine, methionine, phenylalanine, threonine, tryptophan and valine), referred to as having to be taken up with the nutrition due to the complexity of their biosynthesis, are synthesized by simple synthetic routes converted into the remaining 11 "nonessential" amino acids (alanine, arginine, asparagine, aspartate, cysteine, glutamate, glutamine, glycine, proline, serine and tyrosine). Higher animals have the ability to synthesize some of these amino acids, however, the essential amino acids must be taken up with food for normal protein synthesis to take place.
Abgesehen von ihrer Funktion bei der Proteinbiosynthese sind diese Aminosäuren inte¬ ressante Chemikalien an sich, und man hat entdeckt, daß viele bei verschiedenen An- Wendungen in der Nahrungsmittel-, Futter-, Chemie-, Kosmetik-, Landwirtschafts- und pharmazeutischen Industrie zum Einsatz kommen. Lysin ist nicht nur für die Ernährung des Menschen eine wichtige Aminosäure, sondern auch für monogastrische Tiere, wie Geflügel und Schweine. Glutamat wird am häufigsten als Geschmacksadditiv (Mono- natriumglutamat, MSG) sowie weithin in der Nahrungsmittelindustrie verwendet, wie auch Aspartat, Phenylalanin, Glycin und Cystein. Glycin, L-Methionin und Tryptophan werden sämtlich in der pharmazeutischen Industrie verwendet. Glutamin, Valin, Leucin, Isoleucin, Histidin, Arginin, Prolin, Serin und Alanin werden in der pharmazeutischen Industrie und der Kosmetikindustrie verwendet. Threonin, Tryptophan und D-/L- Methionin sind weitverbreitete Futtermittelzusätze (Leuchtenberger, W. (1996) Amino acids - technical production and use, S. 466-502 in Rehm et al., (Hrsg.) Biotechnology Bd. 6, Kapitel 14a, VCH: Weinheim). Man hat entdeckt, daß sich diese Aminosäuren außerdem als Vorstufen für die Synthese von synthetischen Aminosäuren und Protei¬ nen, wie N-Acetylcystein, S-Carboxymethyl-L-cystein, (S)-5-Hydroxytryptophan und anderen, in Ullmann's Encyclopedia of Industrial Chemistry, Bd. A2, S. 57-97, VCH, Weinheim, 1985 beschriebenen Substanzen eignen.Apart from their function in protein biosynthesis, these amino acids are interesting chemicals in themselves, and it has been discovered that many are used in various applications in the food, feed, chemical, cosmetic, agricultural and pharmaceutical industries come. Lysine is an important amino acid not only for human nutrition, but also for monogastric animals such as poultry and pigs. Glutamate is most commonly used as a flavor additive (monosodium glutamate, MSG) as well as widely used in the food industry, as are aspartate, phenylalanine, glycine and cysteine. Glycine, L-methionine and tryptophan are all used in the pharmaceutical industry. Glutamine, valine, leucine, isoleucine, histidine, arginine, proline, serine and alanine are used in the pharmaceutical and cosmetics industries. Threonine, tryptophan and D- / L-methionine are widely used feed additives (Leuchtenberger, W. (1996) Amino acids - technical production and use, pp. 466-502 in Rehm et al., (Ed.) Biotechnology Vol. 6, chapters 14a, VCH: Weinheim). It has also been discovered that these amino acids are also useful as precursors for the synthesis of synthetic amino acids and proteins such as N-acetylcysteine, S-carboxymethyl-L-cysteine, (S) -5-hydroxytryptophan and others in Ullmann's Encyclopedia of Industrial Chemistry, Vol. A2, pp. 57-97, VCH, Weinheim, 1985.
Die Biosynthese dieser natürlichen Aminosäuren in Organismen, die sie produzieren können, bspw. Bakterien, ist gut charakterisiert worden (für einen Überblick der bakte¬ riellen Aminosäure-Biosynthese und ihrer Regulation, s. Umbarger, H.E. (1978) Ann. Rev. Biochem. 47: 533 - 606). Glutamat wird durch reduktive Aminierung von α-The biosynthesis of these natural amino acids in organisms which they can produce, for example bacteria, has been well characterized (for a review of bacterial amino acid biosynthesis and its regulation, see Umbarger, HE (1978) Ann. Rev. Biochem. 47: 533-606). Glutamate is produced by reductive amination of α-
Ketoglutarat, einem Zwischenprodukt im Citronensäure-Zyklus, synthetisiert. Glutamin, Prolin und Arginin werden jeweils nacheinander aus Glutamat erzeugt. Die Biosynthe¬ se von Serin erfolgt in einem Dreischritt-Verfahren und beginnt mit 3-Phosphoglycerat (einem Zwischenprodukt bei der Glykolyse), und ergibt nach Oxidations-, Transaminie- rungs- und Hydrolyseschritten diese Aminosäure. Cystein und Glycin werden jeweils
aus Serin produziert, und zwar die erstere durch Kondensation von Homocystein mit Serin, und die letztere durch Übertragung des Seitenketten-ß-Kohlenstoffatoms auf Tetrahydrofolat, in einer durch Serintranshydroxymethylase katalysierten Reaktion. Phenylalanin und Tyrosin werden aus den Vorstufen des Glycolyse- und Pento- sephosphatweges, Erythrose-4-phosphat und Phosphoenolpyruvat in einem 9-Schritt- Biosyntheseweg synthetisiert, der sich nur in den letzten beiden Schritten nach der Synthese von Prephenat unterscheidet. Tryptophan wird ebenfalls aus diesen beiden Ausgangsmolekülen produziert, jedoch erfolgt dessen Synthese in einem 11 -Schritt- Weg. Tyrosin läßt sich in einer durch Phenylalaninhydroxylase katalysierten Reaktion auch aus Phenylalanin herstellen. Alanin, Valin und Leucin sind jeweils Biosynthese¬ produkte aus Pyruvat, dem Endprodukt der Glykolyse. Aspartat wird aus Oxalacetat, einem Zwischenprodukt des Citratzyklus, gebildet. Asparagin, Methionin, Threonin und Lysin werden jeweils durch Umwandlung von Aspartat produziert. Isoleucin wird aus Threonin gebildet. In einem komplexen 9-Schritt-Weg erfolgt die Bildung von Histidin aus 5-Phosphoribosyl-1 -pyrophosphat, einem aktivierten Zucker.Ketoglutarate, an intermediate in the citric acid cycle. Glutamine, proline and arginine are each produced sequentially from glutamate. The biosynthesis of serine takes place in a three-step process and begins with 3-phosphoglycerate (an intermediate in glycolysis), and after oxidation, transamination and hydrolysis steps yields this amino acid. Cysteine and Glycine are each from serine, the former by condensation of homocysteine with serine, and the latter by transfer of the side-chain β-carbon atom to tetrahydrofolate, in a serine transhydroxymethylase catalyzed reaction. Phenylalanine and tyrosine are synthesized from the precursors of the glycolysis and pentose phosphate pathway, erythrose 4-phosphate and phosphoenolpyruvate in a 9-step biosynthetic pathway that differs only in the last two steps after the synthesis of prephenate. Tryptophan is also produced from these two starting molecules, but its synthesis takes place in an 11-step pathway. Tyrosine can also be prepared from phenylalanine in a reaction catalyzed by phenylalanine hydroxylase. Alanine, valine and leucine are each biosynthesis products from pyruvate, the end product of glycolysis. Aspartate is formed from oxalacetate, an intermediate of the citrate cycle. Asparagine, methionine, threonine and lysine are each produced by conversion of aspartate. Isoleucine is formed from threonine. In a complex 9-step pathway, histidine is formed from 5-phosphoribosyl-1-pyrophosphate, an activated sugar.
Aminosäuren, deren Menge den Proteinbiosynthesebedarf der Zelle übersteigt, können nicht gespeichert werden, und werden stattdessen abgebaut, so daß Zwischenproduk¬ te für die Haupt-Stoffwechselwege der Zelle bereitgestellt werden (für einen Überblick siehe Stryer, L., Biochemistry, 3. Aufl. Kap. 21 "Amino Acid Degradation and the Urea Cycle"; S 495-516 (1988)). Die Zelle ist zwar in der Lage, ungewünschte Aminosäuren in nützliche Stoffwechsel-Zwischenprodukte umzuwandeln, jedoch ist die Aminosäure¬ produktion hinsichtlich der Energie, der Vorstufenmoleküle und der für ihre Synthese nötigen Enzyme aufwendig. Es überrascht daher nicht, daß die Aminosäure- Biosynthese durch Feedback-Hemmung reguliert wird, wobei das Vorliegen einer be¬ stimmten Aminosäure ihre eigene Produktion verlangsamt oder ganz beendet (für ei¬ nen Überblick über den Rückkopplungs-Mechanismus bei Aminosäure- Biosynthesewegen, siehe Stryer, L., Biochemistry, 3. Aufl., Kap. 24, "Biosynthesis of Amino Acids and Heme", S. 575-600 (1988)). Der Ausstoß einer bestimmten Amino- säure wird daher durch die Menge dieser Aminosäure in der Zelle eingeschränkt.Amino acids whose amount exceeds the protein biosynthetic needs of the cell can not be stored, and are instead degraded to provide intermediates for the cell's major metabolic pathways (for review, see Stryer, L., Biochemistry, 3rd Ed. Chapter 21 "Amino Acid Degradation and the Urea Cycle", S 495-516 (1988)). While the cell is capable of converting unwanted amino acids into useful metabolic intermediates, amino acid production is expensive in terms of energy, precursor molecules and the enzymes necessary for their synthesis. It is therefore not surprising that the amino acid biosynthesis is regulated by feedback inhibition, wherein the presence of a certain amino acid slows down or completely stops its own production (for a review of the feedback mechanism in amino acid biosynthetic pathways, see Stryer , L., Biochemistry, 3rd Ed., Chapter 24, "Biosynthesis of Amino Acids and Heme", pp. 575-600 (1988)). The release of a particular amino acid is therefore limited by the amount of this amino acid in the cell.
II. Vitamine, Cofaktoren und Nutrazeutika-Metabolismus sowie VerwendungenII. Vitamins, cofactors and nutraceutical metabolism and uses
Vitamine, Cofaktoren und Nutrazeutika umfassen eine weitere Gruppe von Molekülen. Höhere Tiere haben die Fähigkeit verloren, diese zu synthetisieren und müssen sie somit aufnehmen, obwohl sie leicht durch andere Organismen, wie Bakterien, syntheti¬ siert werden. Diese Moleküle sind entweder biologisch aktive Moleküle an sich oder Vorstufen von biologisch aktiven Substanzen, die als Elektronenträger oder Zwischen¬ produkte bei einer Reihe von Stoffwechselwegen dienen. Diese Verbindungen haben neben ihrem Nährwert auch einen signifikanten industriellen Wert als Farbstoffe, Antio-
xidantien und Katalysatoren oder andere Verarbeitungs-Hilfsstoffe. (Für einen Über¬ blick über die Struktur, Aktivität und die industriellen Anwendungen dieser Verbindun¬ gen siehe bspw. Ullmann's Encyclopedia of Industrial Chemistry, "Vitamins", Bd. A27, S. 443-613, VCH: Weinheim, 1996). Der Begriff "Vitamin" ist im Fachgebiet bekannt und umfaßt Nährstoffe, die von einem Organismus für eine normale Funktion benötigt werden, jedoch nicht von diesem Organismus selbst synthetisiert werden können. Die Gruppe der Vitamine kann Cofaktoren und nutrazeutische Verbindungen umfassen. Der Begriff "Cofaktor" umfaßt nicht-proteinartige Verbindungen, die für das Auftreten einer normalen Enzymaktivität nötig sind. Diese Verbindungen können organisch oder anorganisch sein; die erfindungsgemäßen Cofaktor-Moleküle sind vorzugsweise orga¬ nisch. Der Begriff "Nutrazeutikum" umfaßt Nahrungsmittelzusätze, die bei Pflanzen und Tieren, insbesondere dem Menschen, gesundheitsfördernd sind. Beispiele solcher Mo¬ leküle sind Vitamine, Antioxidantien und ebenfalls bestimmte Lipide (z.B. mehrfach ungesättigte Fettsäuren).Vitamins, cofactors and nutraceuticals comprise another group of molecules. Higher animals have lost the ability to synthesize them and thus need to ingest them, although they are readily synthesized by other organisms, such as bacteria. These molecules are either biologically active molecules per se or precursors of biologically active substances which serve as electron carriers or intermediates in a number of metabolic pathways. In addition to their nutritional value, these compounds also have a significant industrial value as dyes, xidants and catalysts or other processing aids. (For an overview of the structure, activity and industrial applications of these compounds see, for example, Ullmann's Encyclopedia of Industrial Chemistry, "Vitamins", Vol. A27, pp. 443-613, VCH: Weinheim, 1996). The term "vitamin" is known in the art and includes nutrients that are needed by an organism for normal function, but can not be synthesized by that organism itself. The group of vitamins may include cofactors and nutraceutical compounds. The term "cofactor" includes non-proteinaceous compounds that are necessary for the occurrence of normal enzyme activity. These compounds may be organic or inorganic; the cofactor molecules according to the invention are preferably organic. The term "nutraceutical" includes food additives that are beneficial to the health of plants and animals, especially humans. Examples of such molecules are vitamins, antioxidants and also certain lipids (eg polyunsaturated fatty acids).
Die Biosynthese dieser Moleküle in Organismen, die zu ihrer Produktion befähigt sind, wie Bakterien, ist umfassend charakterisiert worden (Ullmann's Encyclopedia of Indus¬ trial Chemistry, "Vitamins", Bd. A27, S. 443-613, VCH: Weinheim, 1996, Michal, G. (1999) Biochemical Pathways: An Atlas of Biochemistry and Molecular Biology, John Wiley & Sons; Ong, A.S., Niki, E. und Packer, L. (1995) "Nutrition, Lipids, Health and Disease" Proceedings of the UNESCO/Confederation of Scientific and Technological Associations in Malaysia and the Society for free Radical Research - Asien, abgehalten am 1.-3. Sept. 1994 in Penang, Malaysia, AOCS Press, Champaign, IL X, 374 S).The biosynthesis of these molecules in organisms capable of producing them, such as bacteria, has been extensively characterized (Ullmann's Encyclopedia of Industrial Chemistry, "Vitamins", Vol. A27, pp. 443-613, VCH: Weinheim, 1996). Michal, G. (1999) Biochemical Pathways: An Atlas of Biochemistry and Molecular Biology, John Wiley, Ong, AS, Niki, E. and Packer, L. (1995) Nutrition, Lipids, Health and Disease Proceedings of the UNESCO / Confederation of Scientific and Technological Associations of Malaysia and the Society for Free Radical Research - Asia, held Sept. 1-3, 1994 in Penang, Malaysia, AOCS Press, Champaign, IL X, 374 S).
Thiamin (Vitamin B1) wird durch chemisches Kuppeln von Pyrimidin und Thiazol-Thiamine (vitamin B 1 ) is produced by chemical coupling of pyrimidine and thiazole
Einheiten gebildet. Riboflavin (Vitamin B2) wird aus Guanosin-5'-triphosphat (GTP) und Ribose-5'-phosphat synthetisiert. Riboflavin wiederum wird zur Synthese von Flavin- mononukleotid (FMN) und Flavinadenindinukleotid (FAD) eingesetzt. Die Familie von Verbindungen, die gemeinsam als "Vitamin B6" bezeichnet werden (bspw. Pyridoxin, Pyridoxamin, Pyridoxal-5'-phosphat und das kommerziell verwendete Pyridoxin- hydrochlorid), sind alle Derivate der gemeinsamen Struktureinheit 5-Hydroxy-6- methylpyridin. Panthothenat (Pantothensäure, R-(+)-N-(2,4-Dihydroxy-3,3-dimethyl-1 - oxobutyl)-ß-alanin) kann entweder durch chemische Synthese oder durch Fermentation hergestellt werden. Die letzten Schritte bei der Pantothenat-Biosynthese bestehen aus der ATP-getriebenen Kondensation von ß-Alanin und Pantoinsäure. Die für die Biosyn¬ theseschritte für die Umwandlung in Pantoinsäure, in ß-Alanin und zur Kondensation in Pantothensäure verantwortlichen Enzyme sind bekannt. Die metabolisch aktive Form von Pantothenat ist Coenzym A, dessen Biosynthese über 5 enzymatische Schritte verläuft. Pantothenat, Pyridoxal-5'-phosphat, Cystein und ATP sind die Vorstufen von Coenzym A. Diese Enzyme katalysieren nicht nur die Bildung von Pantothenat, son-
dem auch die Produktion von (R)-Pantoinsäure, (R)-Pantolacton, (R)-Panthenol (Provi¬ tamin B5), Pantethein (und seinen Derivaten) und Coenzym A.Formed units. Riboflavin (vitamin B 2 ) is synthesized from guanosine 5'-triphosphate (GTP) and ribose 5'-phosphate. In turn, riboflavin is used to synthesize flavin mononucleotide (FMN) and flavin adenine dinucleotide (FAD). The family of compounds collectively referred to as "vitamin B6" (eg, pyridoxine, pyridoxamine, pyridoxal-5'-phosphate and the commercially used pyridoxine hydrochloride) are all derivatives of the common structural unit 5-hydroxy-6-methylpyridine. Panthothenate (pantothenic acid, R - (+) - N- (2,4-dihydroxy-3,3-dimethyl-1-oxobutyl) -β-alanine) can be prepared either by chemical synthesis or by fermentation. The last steps in pantothenate biosynthesis consist of the ATP-driven condensation of β-alanine and pantoic acid. The enzymes responsible for the biosynthesis steps for the conversion into pantoic acid, into β-alanine and for the condensation in pantothenic acid are known. The metabolically active form of pantothenate is coenzyme A, whose biosynthesis proceeds through 5 enzymatic steps. Pantothenate, pyridoxal-5'-phosphate, cysteine and ATP are the precursors of coenzyme A. These enzymes not only catalyze the formation of pantothenate, but also also the production of (R) -pantoic acid, (R) -pantolactone, (R) -panthenol (provitamin B 5 ), pantethein (and its derivatives) and coenzyme A.
Die Biosynthese von Biotin aus dem Vorstufenmolekül Pimeloyl-CoA in Mikroorganis- men ist ausführlich untersucht worden, und man hat mehrere der beteiligten Gene i- dentifiziert. Es hat sich herausgestellt, daß viele der entsprechenden Proteine an der Fe-Cluster-Synthese beteiligt sind und zu der Klasse der nifS-Proteine gehören. Die Liponsäure wird von der Octanonsäure abgeleitet und dient als Coenzym beim Ener¬ gie-Metabolismus, wo sie Bestandteil des Pyruvatdehydrogenasekomplexes und des oc-Ketoglutaratdehydrogenasekomplexes wird. Die Folate sind eine Gruppe von Sub¬ stanzen, die alle von der Folsäure abgeleitet werden, die wiederum von L- Glutaminsäure, p-Aminobenzoesäure und 6-Methylpterin hergeleitet ist. Die Biosynthe¬ se der Folsäure und ihrer Derivate, ausgehend von den metabolischen Stoffwechsel¬ zwischenprodukten Guanosin-5'-triphosphat (GTP), L-Glutaminsäure und p- Aminobenzoesäure ist in bestimmten Mikroorganismen eingehend untersucht worden.The biosynthesis of biotin from the precursor molecule pimeloyl-CoA in microorganisms has been extensively studied, and several of the genes involved have been identified. It has been found that many of the corresponding proteins are involved in Fe cluster synthesis and belong to the class of nifS proteins. The lipoic acid is derived from octanoic acid and serves as a coenzyme in energy metabolism, where it becomes part of the pyruvate dehydrogenase complex and of the α-ketoglutarate dehydrogenase complex. The folates are a group of substances which are all derived from folic acid, which in turn is derived from L-glutamic acid, p-aminobenzoic acid and 6-methylpterin. The biosynthesis of folic acid and its derivatives, starting from the metabolic intermediates guanosine 5'-triphosphate (GTP), L-glutamic acid and p-aminobenzoic acid, has been extensively studied in certain microorganisms.
Corrinoide (wie die Cobalamine und insbesondere Vitamin Bi2) und die Porphyrine gehören zu einer Gruppe von Chemikalien, die sich durch ein Tetrapyrrol-Ringsystem auszeichnen. Die Biosynthese von Vitamin B12 ist hinreichend komplex, daß sie noch nicht vollständig charakterisiert worden ist, jedoch ist inzwischen ein Großteil der betei¬ ligten Enzyme und Substrate bekannt. Nikotinsäure (Nikotinat) und Nikotinamid sind Pyridin-Derivate, die auch als "Niacin" bezeichnet werden. Niacin ist die Vorstufe der wichtigen Coenzyme NAD (Ntkotinamidadenindinukleotid) und NADP (Nikotinamidade- nindinukleotidphosphat) und ihrer reduzierten Formen.Corrinoids (such as the Cobalamine and especially Vitamin Bi 2 ) and the porphyrins belong to a group of chemicals that are characterized by a tetrapyrrole ring system. The biosynthesis of vitamin B 12 is sufficiently complex that it has not yet been fully characterized, however, a large part of the participating enzymes and substrates is now known. Nicotinic acid (nicotinate) and nicotinamide are pyridine derivatives, also referred to as "niacin". Niacin is the precursor of the important coenzymes NAD (Ntkotinamidadenine dinucleotide) and NADP (Nicotinamide Nadeinucleotide Phosphate) and their reduced forms.
Die Produktion dieser Verbindungen im Großmaßstab beruht größtenteils auf zellfreien chemischen Synthesen, obwohl einige dieser Chemikalien ebenfalls durch großange¬ legte Anzucht von Mikroorganismen produziert worden sind, wie Riboflavin, Vitamin B6, Pantothenat und Biotin. Nur Vitamin Bi2 wird aufgrund der Komplexität seiner Synthese lediglich durch Fermentation produziert. In-vitro-Verfahren erfordern einen erheblichen Aufwand an Materialien und Zeit und häufig an hohen Kosten.The large scale production of these compounds relies largely on cell-free chemical syntheses, although some of these chemicals have also been produced by the large-scale growth of microorganisms such as riboflavin, vitamin B 6 , pantothenate and biotin. Only Vitamin Bi 2 is only produced by fermentation due to the complexity of its synthesis. In vitro methods require a considerable expenditure of materials and time and often at high costs.
III. Purin-, Pyrimidin-, Nukleosid- und Nukleotid-Metabolismus und VerwendungenIII. Purine, pyrimidine, nucleoside and nucleotide metabolism and uses
Gene für den Purin- und Pyrimidin-Stoffwechsel und ihre entsprechenden Proteine sind wichtige Ziele für die Therapie von Tumorerkrankungen und Virusinfektionen. Der Beg¬ riff "Purin" oder "Pyrimidin" umfaßt stickstoffhaltige Basen, die Bestandteil der Nuklein¬ säuren, Coenzyme und Nukleotide sind. Der Begriff "Nukleotid" beinhaltet die grundle¬ genden Struktureinheiten der Nukleinsäuremoleküle, die eine stickstoffhaltige Base, einen Pentose-Zucker (bei RNA ist der Zucker Ribose, bei DNA ist der Zucker D-
Desoxyribose) und Phosphorsäure umfassen. Der Begriff "Nukleosid" umfaßt Moleküle, die als Vorstufen von Nukleotiden dienen, die aber im Gegensatz zu den Nukleotiden keine Phosphorsäureeinheit aufweisen. Durch Hemmen der Biosynthese dieser Mole¬ küle oder ihrer Mobilisation zur Bildung von Nukleinsäuremolekülen ist es möglich, die RNA- und DNA-Synthese zu hemmen; wird diese Aktivität zielgerichtet bei kanzeroge¬ nen Zellen gehemmt, läßt sich die Teilungs- und Replikations-Fähigkeit von Tumorzel¬ len hemmen.Genes for purine and pyrimidine metabolism and their corresponding proteins are important targets for the treatment of tumors and viral infections. The term "purine" or "pyrimidine" includes nitrogen-containing bases which are part of the nucleic acids, coenzymes and nucleotides. The term "nucleotide" includes the basic structural units of the nucleic acid molecules which comprise a nitrogen-containing base, a pentose sugar (in the case of RNA, the sugar is ribose, in the case of DNA the sugar D is Deoxyribose) and phosphoric acid. The term "nucleoside" includes molecules which serve as precursors of nucleotides, but unlike the nucleotides have no phosphoric acid moiety. By inhibiting the biosynthesis of these molecules or mobilizing them to form nucleic acid molecules, it is possible to inhibit RNA and DNA synthesis; If this activity is purposefully inhibited in cancerous cells, the ability to divide and replicate tumor cells can be inhibited.
Es gibt zudem Nukleotide, die keine Nukleinsäuremoleküle bilden, jedoch als Energie- Speicher (d.h. AMP) oder als Coenzyme (d.h. FAD und NAD) dienen.There are also nucleotides that do not form nucleic acid molecules but serve as energy stores (i.e., AMPs) or coenzymes (i.e., FAD and NAD).
Mehrere Veröffentlichungen haben die Verwendung dieser Chemikalien für diese me¬ dizinischen Indikationen beschrieben, wobei der Purin- und/oder Pyrimidin- Metabolismus beeinflußt wird (bspw. Christopherson, R.l. und Lyons, S.D. (1990) "Po- tent inhibitors of de novo pyrimidine and purine biosynthesis as chemotherapeutic a- gents", Med. Res. Reviews 10: 505-548). Untersuchungen an Enzymen, die am Purin- und Pyrimidin-Metabolismus beteiligt sind, haben sich auf die Entwicklung neuer Medi¬ kamente konzentriert, die bspw. als Immunsuppressionsmittel oder Antiproliferantien verwendet werden können (Smith, J.L "Enzymes in Nucleotide Synthesis" Curr. Opin. Struct. Biol. 5 (1995) 752-757; Biochem. Soc. Transact. 23 (1995) 877-902). Die Purin- und Pyrimidinbasen, Nukleoside und Nukleotide haben jedoch auch andere Einsatz¬ möglichkeiten: als Zwischenprodukte bei der Biosysnthese verschiedener Feinchemi¬ kalien (z.B. Thiamin, S-Adenosyl-methionin, Folate oder Riboflavin), als Energieträger für die Zelle (bspw. ATP oder GTP) und für Chemikalien selbst, werden gewöhnlich als Geschmacksverstärker verwendet (bspw. IMP oder GMP) oder für viele medizinische Anwendungen (siehe bspw. Kuninaka, A., (1996) "Nucleotides and Related Com¬ pounds in Biotechnology Bd. 6, Rehm et al., Hrsg. VCH: Weinheim, S. 561-612). En¬ zyme, die am Purin-, Pyrimidin-, Nukleosid- oder Nukleotid-Metabolismus beteiligt sind, dienen auch immer stärker als Ziele, gegen die Chemikalien für den Pflanzenschutz, einschließlich Fungiziden, Herbiziden und Insektiziden entwickelt werden.Several publications have described the use of these chemicals for these medical indications, whereby the purine and / or pyrimidine metabolism is influenced (for example Christopherson, Rl and Lyons, SD (1990) "Potential inhibitors of de novo pyrimidines and purine biosynthesis as chemotherapeutic agents ", Med. Res. Reviews 10: 505-548). Studies on enzymes involved in purine and pyrimidine metabolism have focused on the development of new medicaments which may be used, for example, as immunosuppressants or antiproliferants (Smith, JL "Enzymes in Nucleotide Synthesis" Curr. Opin. Struct. Biol. 5 (1995) 752-757; Biochem. Soc. Transact. 23 (1995) 877-902). The purine and pyrimidine bases, nucleosides and nucleotides, however, also have other possibilities of use: as intermediates in the biosynthesis of various fine chemicals (eg thiamine, S-adenosylmethionine, folates or riboflavin), as energy carrier for the cell (for example ATP or GTP) and chemicals themselves are commonly used as flavor enhancers (eg, IMP or GMP) or for many medical applications (see, for example, Kuninaka, A. (1996) Nucleotides and Related Compounds in Biotechnology Vol. Weinheim, pages 561-612). Enzymes involved in purine, pyrimidine, nucleoside or nucleotide metabolism are also increasingly serving as targets against which chemicals are used plant protection, including fungicides, herbicides and insecticides.
Der Metabolismus dieser Verbindungen in Bakterien ist charakterisiert worden (für Ü- bersichten siehe bspw. Zalkin, H. und Dixon, J.E. (1992) "De novo purin nucleotide biosynthesis" in Progress in Nucleic Acids Research and Molecular biology, Bd. 42, Academic Press, S. 259-287; und Michal, G. (1999) "Nucleotides and Nucleosides"; Kap. 8 in : Biochemical Pathways: An Atlas of Biochemistry and Molecular Biology, Wiley, New York). Der Purin-Metabolismus, das Objekt intesiver Forschung, ist für das normale Funktionieren der Zelle essentiell. Ein gestörter Purin-Metabolismus in höhe¬ ren Tieren kann schwere Erkrankungen verursachen, bspw. Gicht. Die Purinnukleotide werden über eine Reihe von Schritten über die Zwischenverbindung lnosin-5'-phosphat
(IMP) aus Ribose-5-phosphat synthetisiert, was zur Produktion von Guanosin-5'- monophosphat (GMP) oder Adenosin-5'-monophosphat (AMP) führt, aus denen sich die als Nukleotide verwendeten Triphosphatformen leicht herstellen lassen. Diese Ver¬ bindungen werden auch als Energiespeicher verwendet, so daß ihr Abbau Energie für viele verschiedene biochemische Prozesse in der Zelle liefert. Die Pyrimidinbiosynthe- se erfolgt über die Bildung von Uridin-5'-monophosphat (UMP) aus Ribose-5-phosphat. UMP wiederum wird in Cytidin-5'-triphosphat (CTP) umgewandelt. Die Desoxyformen sämtlicher Nukleotide werden in einer Einschritt-Reduktionsreaktion aus der Diphosphat-Riboseform des Nukleotides zur Diphosphat-Desoxyriboseform des Nukle- otides hergestellt. Nach der Phosphorylierung können diese Moleküle an der DNA- Synthese teilnehmen.The metabolism of these compounds in bacteria has been characterized (for reviews, see, for example, Zalkin, H. and Dixon, JE (1992) "De novo purin nucleotide biosynthesis" in Progress in Nucleic Acids Research and Molecular Biology, Vol. 42, Academic Press, pp. 259-287; and Michal, G. (1999) "Nucleotides and Nucleosides", Chap. 8 in: Biochemical Pathways: An Atlas of Biochemistry and Molecular Biology, Wiley, New York). Purine metabolism, the object of intesive research, is essential to the normal functioning of the cell. Disturbed purine metabolism in higher animals can cause severe diseases, for example gout. The purine nucleotides are made via a series of steps via the intermediate lnosine 5'-phosphate (IMP) from ribose-5-phosphate, resulting in the production of guanosine 5'-monophosphate (GMP) or adenosine 5'-monophosphate (AMP), from which the triphosphate forms used as nucleotides can be easily prepared. These compounds are also used as energy stores, so that their degradation provides energy for many different biochemical processes in the cell. The Pyrimidinbiosynthe- se via the formation of uridine 5'-monophosphate (UMP) from ribose-5-phosphate. In turn, UMP is converted to cytidine 5'-triphosphate (CTP). The deoxy forms of all nucleotides are prepared in a one-step reduction reaction from the diphosphate ribose form of the nucleotide to the diphosphate-deoxyribose form of the nucleotide. After phosphorylation, these molecules can participate in DNA synthesis.
IV. Trehalose-Metabolismus und VerwendungenIV. Trehalose Metabolism and Uses
Trehalose besteht aus zwei Glucosemolekülen, die über α,α-1 , 1 -Bindung miteinander verknüpft sind. Sie wird gewöhnlich in der Nahrungsmittelindustrie als Süßstoff, als Additiv für getrocknete oder gefrorene Nahrungsmittel sowie in Getränken verwendet. Sie wird jedoch auch in der pharmazeutischen Industrie, der Kosmetik- und Biotechno¬ logie-Industrie angewendet (s. bspw. Nishimoto et al., (1998) US-Patent Nr. 5 759 610; Singer, M.A. und Lindquist, S. Trends Biotech. 16 (1998) 460-467; Paiva, C.L.A. und Panek, A.D. Biotech Ann. Rev. 2 (1996) 293-314; und Shiosaka, M. J. Japan 172 (1997) 97-102). Trehalose wird durch Enzyme von vielen Mikroorganismen produziert und auf natürliche Weise in das umgebende Medium abgegeben, aus dem sie durch im Fachgebiet bekannte Verfahren gewonnen werden kann.Trehalose consists of two molecules of glucose linked together by α, α-1, 1 bonding. It is commonly used in the food industry as a sweetener, as an additive for dried or frozen foods, and in beverages. However, it is also used in the pharmaceutical, cosmetics and biotechnology industries (see, for example, Nishimoto et al., (1998) US Patent No. 5,759,610; Singer, MA and Lindquist, S. Trends Biotech 16 (1998) 460-467; Paiva, CLA and Panek, AD Biotech Ann. Rev. 2 (1996) 293-314; and Shiosaka, MJ Japan 172 (1997) 97-102). Trehalose is produced by enzymes from many microorganisms and naturally released into the surrounding medium from which it can be recovered by methods known in the art.
Besonders bevorzugte biosynthetische Produkte sind ausgewählt aus der Gruppe or¬ ganische Säuren, Proteine, Nukleotide und Nukleoside, sowohl proteinogene als auch nicht-proteinogene Aminosäuren, Lipide und Fettsäuren, Diole, Kohlehydrate, aromati¬ sche Verbindungen, Vitamine und Cofaktoren, Enzyme und Proteine.Particularly preferred biosynthetic products are selected from the group of organic acids, proteins, nucleotides and nucleosides, both proteinogenic and non-proteinogenic amino acids, lipids and fatty acids, diols, carbohydrates, aromati cal compounds, vitamins and cofactors, enzymes and proteins.
Bevorzugte organische Säuren sind Weinsäure, Itaconsäure und DiaminopimelinsäurePreferred organic acids are tartaric acid, itaconic acid and diaminopimelic acid
Bevorzugte Nukleoside und Nukleotide sind beispielsweise beschrieben in Kuninaka, A. (1996) Nucleotides and related Compounds, S. 561-612, in Biotechnology Bd. 6, Rehm et al., Hrsg. VCH: Weinheim und den darin enthaltenen Zitaten.Preferred nucleosides and nucleotides are described, for example, in Kuninaka, A. (1996) Nucleotides and Related Compounds, pp. 561-612, Biotechnology Vol. 6, Rehm et al., Ed. VCH: Weinheim and the citations contained therein.
Bevorzugte biosynthetische Produkte sind weiterhin Lipide, gesättigte und ungesättigte Fettsäuren, wie beispielsweise Arachidonsäure, Diole wie beispielsweise Propandiol und Butandiol, Kohlenhydrate, wie beispielsweise Hyaluronsäure und Trehalose, aro- matische Verbindungen, wie beispielsweise aromatische Amine, Vanillin und Indigo,
Vitamine und Cofaktoren, wie beispielsweise beschrieben in Ullmann's Encyclopedia of Industrial Chemistry, Bd. A27, "Vitamins", S. 443-613 (1996) VCH: Weinheim und den darin enthaltenen Zitaten; und Ong, A.S., Niki, E. und Packer, L. (1995) "Nutrition, Lip- ids, Health and Disease" Proceedings of the UNESCO/Confederation of Scientific and Technological Associations in Malaysia and the Society for Free Radical Research - Asien, abgehalten am 1.-3. Sept. 1994 in Penang, Malysia, AOCS Press (1995)), En¬ zyme Polyketide (Cane et al. (1998) Science 282: 63-68), und sämtliche anderen von Gutcho (1983) in Chemicals by Fermentation, Noyes Data Corporation, ISBN: 0818805086 und den darin angegebenen Literaturstellen, beschriebenen Chemikalien.Preferred biosynthetic products are also lipids, saturated and unsaturated fatty acids, such as, for example, arachidonic acid, diols, for example propanediol and butanediol, carbohydrates, for example hyaluronic acid and trehalose, aromatic compounds, for example aromatic amines, vanillin and indigo, Vitamins and cofactors as described, for example, in Ullmann's Encyclopedia of Industrial Chemistry, Vol. A27, "Vitamins", pp. 443-613 (1996) VCH: Weinheim and the citations contained therein; and Ong, AS, Niki, E. and Packer, L. (1995) "Nutrition, Lipids, Health and Disease" Proceedings of the UNESCO / Confederation of Scientific and Technological Associations in Malaysia and the Society for Free Radical Research - Asia , held on 1.-3. Sept. 1994 in Penang, Malysia, AOCS Press (1995)), Enzyme Polyketides (Cane et al. (1998) Science 282: 63-68), and all others by Gutcho (1983) in Chemicals by Fermentation, Noyes Data Corporation, ISBN: 0818805086 and the references cited therein.
Besonders bevorzugte biosynthetische Produkte sind Aminosäuren, besonders bevor¬ zugt essentielle Aminosäuren, insbeondere L-Glycin, L-Alanin, L-Ieucin, L-Methionin, L- Phenylalanin, L-Tryptophan, L-Lysin, L-Glutamin, L-Glutaminsäure, L-Serin, L-Prolin, L- Valin, L-Isoleucin, L-Cystein, L-Tyrosin, L-Histidin, L-Arginin, L-Asparagin, L- Asparaginsäure und L-Threonin, L-Homoserin, insbesondere L-Lysin, L-Methionin und L-Threonin. Im folgenden wird unter unter einer Aminosäure, wie beispielsweise Lysin, Methionin und Threonin, sowohl jeweils die L- und die D-Form der Aminosäure, vor¬ zugsweise die L-Form, also beispielsweise L-Lysin, L-Methionin und L-Threonin ver¬ standen.Particularly preferred biosynthetic products are amino acids, more preferably essential amino acids, in particular L-glycine, L-alanine, L-leucine, L-methionine, L-phenylalanine, L-tryptophan, L-lysine, L-glutamine, L-glutamic acid , L-serine, L-proline, L-valine, L-isoleucine, L-cysteine, L-tyrosine, L-histidine, L-arginine, L-asparagine, L-aspartic acid and L-threonine, L-homoserine, in particular L-lysine, L-methionine and L-threonine. In the following, among an amino acid such as lysine, methionine and threonine, both the L and the D form of the amino acid, preferably the L-form, that is, for example, L-lysine, L-methionine and L-threonine stood.
Die Erfindung betrifft insbesondere ein Verfahren zur Herstellung von Lysin durch Kul¬ tivierung von genetisch veränderten Mikroorganismen mit erhöhter oder verursachter Expressionsrate mindestens eines Gens im Vergleich zum Wildtyp, wobei manThe invention relates in particular to a process for the preparation of lysine by cultivating genetically modified microorganisms with an increased or caused expression rate of at least one gene in comparison to the wild type, wherein
ch) die spezifische Expressionsaktivität im Mikroorganismus von mindestens einer endogenen, erfindungsgemäßen Expressionseinheit, die die Expression der endoge¬ nen Gene reguliert, im Vergleich zum Wildtyp erhöht oderch) the specific expression activity in the microorganism of at least one endogenous expression unit according to the invention which regulates the expression of the endogenous genes is increased in comparison to the wild type or
dh) die Expression von Genen im Mikroorganismus durch erfindungsgemäße Expres- sionseinheiten oder durch erfindungsgemäße Expressionseinheiten mit erhöhter spezi¬ fischer Expressionsaktivität gemäß Ausführungsform ch) reguliert, wobei die Gene im Bezug auf die Expressionseinheiten heterolog sind,ie) the expression of genes in the microorganism is regulated by expression units according to the invention or by expression units according to the invention with increased specific expression activity according to embodiment (ch), whereby the genes are heterologous with respect to the expression units,
und wobei die Gene ausgewählt sind aus der Gruppe Nukleinsäuren kodierend eine Aspartatkinase, Nukleinsäuren kodierend eine Aspartat-Semialdehyd-Dehydrogenase, Nukleinsäuren kodierend eine Diaminopimelat- Dehydrogenase, Nukleinsäuren kodie¬ rend eine Diaminopimelat- Decarboxylase, Nukleinsäuren kodierend eine Dihydrodipi- colinate-Synthetase, Nukleinsäuren kodierend eine Dihydridipicolinate-Reduktase, Nukleinsäuren kodierend eine Glycerinaldehyd-3-Phosphat Dehydrogenase, Nuklein- säuren kodierend eine 3-Phosphoglycerat-Kinase, Nukleinsäuren kodierend eine Pyru-
vat Carboxylase, Nukleinsäuren kodierend eine Triosephosphat-Isomerase, Nuklein¬ säuren kodierend einen Transkriptionellen Regulator LuxR, Nukleinsäuren kodierend einen Transkriptionellen Regulator LysR1 , Nukleinsäuren kodierend einen Transkripti¬ onellen Regulator LysR2, Nukleinsäuren kodierend eine Malat-Quinon- Oxodoreduktase, Nukleinsäuren kodierend eine Glucose-6-Phosphat-Deydrognease, Nukleinsäuren kodierend eine 6-Phosphogluconat-Dehydrognease, Nukleinsäuren kodierend eine Transketolase, Nukleinsäuren kodierend eine Transaldolase, Nuklein¬ säuren kodierend einen Lysin Exporter, Nukleinsäuren kodierend eine Biotin-Ligase, Nukleinsäuren kodierend eine Arginyl-t-RNA-Synthetase, Nukleinsäuren kodierend eine Phosphoenolpyruvat-Carboxylase, Nukleinsäuren kodierend eine Fruktose-1 ,6- bisphosphatase, Nukleinsäuren kodierend ein Protein OPCA, Nukleinsäuren kodierend eine 1 -Phosphof ructokinase und Nukleinsäuren kodierend eine 6-Phosphofructokinase.and wherein the genes are selected from the group consisting of nucleic acids encoding an aspartate kinase, nucleic acids encoding an aspartate semialdehyde dehydrogenase, nucleic acids encoding a diaminopimelate dehydrogenase, nucleic acids encoding a diaminopimelate decarboxylase, nucleic acids encoding a dihydrodipicolinate synthetase, encoding nucleic acids a dihydridipicolinate reductase, nucleic acids encoding a glyceraldehyde-3-phosphate dehydrogenase, nucleic acids encoding a 3-phosphoglycerate kinase, nucleic acids encoding a pyruvic acid vat carboxylase, nucleic acids encoding a triosephosphate isomerase, nucleic acids encoding a transcriptional regulator LuxR, nucleic acids encoding a transcriptional regulator LysR1, nucleic acids encoding a transcriptional regulator LysR2, nucleic acids encoding a malate quinone oxodoreductase, nucleic acids encoding a glucose-6 Phosphate de-dehydrogenase, nucleic acids encoding a 6-phosphogluconate dehydrognease, nucleic acids encoding a transketolase, nucleic acids encoding a transaldolase, nucleic acids encoding a lysine exporter, nucleic acids encoding a biotin ligase, nucleic acids encoding an arginyl t-RNA synthetase, Nucleic acids encoding a phosphoenolpyruvate carboxylase, nucleic acids encoding a fructose-1,6-bisphosphatase, nucleic acids encoding an OPCA protein, nucleic acids encoding a 1-phosphofructokinase and nucleic acids encoding a 6-phosphofructokinase.
Wie vorstehend bei den Verfahren beschrieben, wird die Regulation der Expression dieser Genen im Mikroorganismus durch erfindungsgemäße Expressionseinheiten o- der durch erfindungsgemäße Expressionseinheiten mit erhöhter spezifischer Expressi¬ onsaktivität gemäß Ausführungsform ch) dadurch erreicht, dass manAs described above in the methods, the regulation of the expression of these genes in the microorganism by expression units according to the invention or by expression units according to the invention with increased specific expression activity according to embodiment ch) is achieved by
dh1) eine oder mehrere erfindungsgemäße Expressionseinheiten, gegebenenfalls mit erhöhter spezifischer Expressionsaktivität, in das Genom des Mikroorganismus ein¬ bringt, so dass die Expression eines oder mehrerer dieser endogenen Gene unter der Kontrolle der eingebrachten, erfindungsgemäßen Expressionseinheiten, gegebenen¬ falls mit erhöhter spezifischer Expressionsaktivität, erfolgt oderdh1) brings one or more expression units according to the invention, optionally with increased specific expression activity, into the genome of the microorganism such that the expression of one or more of these endogenous genes under the control of the introduced expression units according to the invention, if appropriate with increased specific expression activity, done or
dh2) ein oder mehrere dieser Gene in das Genom des Mikrorganismus einbringt, so dass die Expression eines oder mehrerer der eingebrachten Gene unter der Kontrolle der endogenen, erfindungsgemäßen Expressionseinheiten, gegebenenfalls mit erhöh¬ ter spezifischer Expressionsaktivität, erfolgt oderdh2) introduces one or more of these genes into the genome of the microorganism, so that the expression of one or more of the introduced genes takes place under the control of the endogenous expression units according to the invention, optionally with increased specific expression activity, or
dh3) ein oder mehrere Nukleinsäurekonstrukte, enthaltend eine erfindungsgemäße Expressionseinheit, gegebenenfalls mit erhöhter spezifischer Expressionsaktivität, und funktionell verknüpft eine oder mehrere, zu exprimierende Nukleinsäuren, in den Mik¬ roorganismus einbringt.ie3) one or more nucleic acid constructs containing an expression unit according to the invention, optionally with increased specific expression activity, and functionally linked one or more nucleic acids to be expressed, into which microorganisms are introduced.
Eine weiter bevorzugte Ausführungsform des vorstehend beschriebenen Verfahrens zur Herstellung von Lysin ist dadurch gekennzeichnet, dass die genetisch veränderten Mikroorganismen im Vergleich zum Wildtyp zusätzlich eine erhöhte Aktivität, mindes¬ tens einer der Aktivitäten, ausgewählt aus der Gruppe Aspartatkinase-Aktivität, Aspartat-Semialdehyd-Dehydrogenase-Aktivität, Diaminopi- melat- Dehydrogenase-Aktivität, Diaminopimelat-Decarboxylase-Aktivität, Dihydrodipi-
colinate-Synthetase-Aktivität, Dihydridipicolinate-Rθduktase-Aktivität, Glycerinaldehyd- 3-Phosphat Dehydrogenase-Aktivität, 3-Phosphoglycerat-Kinase-Aktivität, Pyruvat Carboxylase-Aktivität, Triosephosphat-Isomerase-Aktivität, Aktivität des Transkriptio¬ nellen Regulators LuxR, Aktivität des Transkriptionellen Regulators LysR1 , Aktivität des Transkriptionellen Regulators LysR2, Malat-Quinon-Oxodoreduktase-Aktivität, Glucose-6-Phosphat-Deydrognease-Aktivität, 6-Phosphogluconat~Dehydrognease- Aktivität, Transketolase-Aktivität, Transaldolase-Aktivität, Lysin-Exporter-Aktivität, Argi- nyl-t-RNA-Synthetase-Aktivität, Phosphoenolpyruvat-Carboxylase-Aktivität, Fruktose- 1 ,6-bisphosphatase-Aktivität, Protein OpcA-Aktivität, 1-Phosphofructokinase-Aktivität, 6-Phosphofructokinase-Aktivität und Biotiri-Ligase-Aktivität aufweisen.A further preferred embodiment of the process for the preparation of lysine described above is characterized in that the genetically modified microorganisms in addition to the wild type additionally an increased activity, at least one of the activities selected from the group aspartate kinase activity, aspartate semialdehyde dehydrogenase Activity, diaminopilate dehydrogenase activity, diaminopimelate decarboxylase activity, dihydrodipic colinate synthetase activity, dihydridipicolinate Rductase activity, glyceraldehyde-3-phosphate dehydrogenase activity, 3-phosphoglycerate kinase activity, pyruvate carboxylase activity, triosephosphate isomerase activity, activity of the transcriptional regulator LuxR, activity of the Transcriptional Regulators LysR1, Transcriptional Regulators Activity LysR2, Malate Quinone Oxodoreductase Activity, Glucose-6-phosphate Deydrognease Activity, 6-Phosphogluconate Dehydrognease Activity, Transketolase Activity, Transaldolase Activity, Lysine Exporter Activity, Arginol t-RNA synthetase activity, phosphoenolpyruvate carboxylase activity, fructose 1, 6-bisphosphatase activity, protein OpcA activity, 1-phosphofructokinase activity, 6-phosphofructokinase activity and biotiri ligase activity exhibit.
Eine weiter besonders bevorzugte Ausführungsform des vorstehend beschriebenen Verfahrens zur Herstellung von Lysin ist dadurch gekennzeichnet, dass die genetisch veränderten Mikroorganismen im Vergleich zum Wildtyp zusätzlich eine reduzierte Ak- tivität, mindestens einer der Aktivitäten, ausgewählt aus der Gruppe Threonin Dehydra- tase-Aktivität, Homoserin O-Acetyltransferase-Aktivität, O-Acetylhomoserin- Sulfhydrylase-Aktivität, Phosphoenolpyruvat-Carboxykinase-Aktivität, Pyruvat-Oxidase- Aktivität, Homoserine-Kinase-Aktivität, Homoserin-Dehydrogenase-Aktivität, Threonin- Exporter-Aktivität, Threonin-Efflux-Protein-Aktivität, Asparaginase-Aktivität, Aspartat- Decarboxylase-Aktivität und Threonin-Synthase-Aktivität aufweisen.A further particularly preferred embodiment of the process for the preparation of lysine described above is characterized in that the genetically modified microorganisms in addition to the wild type additionally a reduced activity, at least one of the activities selected from the group threonine dehydratase activity, homoserine O-acetyltransferase activity, O-acetyl homoserine sulfhydrylase activity, phosphoenolpyruvate carboxykinase activity, pyruvate oxidase activity, homoserine kinase activity, homoserine dehydrogenase activity, threonine exporter activity, threonine efflux protein Activity, asparaginase activity, aspartate decarboxylase activity and threonine synthase activity.
Diese zusätzlichen, erhöhten oder reduzierten Aktivitäten mindestens einer der vorste¬ hend beschriebenen Aktivitäten können, müssen aber nicht durch eine erfindungsge¬ mäße Nukleinsäure mit Promotoraktivität und/oder eine erfindungsgemäße Expressi- onseinheit verursacht sein.These additional, increased or reduced activities of at least one of the above-described activities may, but need not, be caused by a nucleic acid according to the invention having promoter activity and / or an expression unit according to the invention.
Die Erfindung betrifft ferner ein Verfahren zur Herstellung von Methionin durch Kultivie¬ rung von genetisch veränderten Mikroorganismen mit erhöhter oder verursachter Ex¬ pressionsrate mindestens eines Gens im Vergleich zum Wildtyp, wobei manThe invention further relates to a process for the production of methionine by cultivating genetically modified microorganisms having an increased or caused expression rate of at least one gene in comparison to the wild type, wherein
ch) die spezifische Expressionsaktivität im Mikroorganismus von mindestens einer endogenen, erfindungsgemäßen Expressionseinheit, die die Expression der endoge¬ nen Gene reguliert, im Vergleich zum Wildtyp erhöht oderch) the specific expression activity in the microorganism of at least one endogenous expression unit according to the invention which regulates the expression of the endogenous genes is increased in comparison to the wild type or
dh) die Expression von Genen im Mikroorganismus durch erfindungsgemäße Expres¬ sionseinheiten oder durch erfindungsgemäße Expressionseinheiten mit erhöhter spezi¬ fischer Expressionsaktivität gemäß Ausführungsform ch) reguliert, wobei die Gene im Bezug auf die Expressionseinheiten heterolog sind,
und wobei die Gene ausgewählt sind aus der Gruppe Nukleinsäuren kodierend eine Aspartatkinase, Nukleinsäuren kodierend eine Aspartat-Semialdehyd-Dehydrogenase, Nukleinsäuren kodierend eine Homoserin Dehydrogenase, Nukleinsäuren kodierend eine Glycerinaldehyd-3-Phosphat Dehydrogenase, Nukleinsäuren kodierend eine 3- Phosphoglycerat Kinase, Nukleinsäuren kodierend eine Pyruvat Carboxylase, Nuklein¬ säuren kodierend eine Triosephosphat Isomerase, Nukleinsäuren kodierend eine Ho¬ moserin O-Acetyltransferase, Nukleinsäuren kodierend eine Cystahionin-gamma- Synthase, Nukleinsäuren kodierend eine Cystahionin-beta-Lyase, Nukleinsäuren ko¬ dierend eine Serin-Hydroxymethyltransferase, Nukleinsäuren kodierend eine O- Acetylhomoserin-Sulfhydrylase, Nukleinsäuren kodierend eine Methylen- Tetrahydrofolat-Reduktase, Nukleinsäuren kodierend eine Phosphoserin- Aminotransferase, Nukleinsäuren kodierend eine Phosphoserin-Phosphatase, Nuklein¬ säuren kodierend eine Serine Acetyl-TransferaseNukleinsäuren kodierend eine Cystein-Synthase Aktivität I1 Nukleinsäuren kodierend eine Cystein-Synthase Aktivität Il , Nukleinsäuren kodierend eine Coenzym B12-abhängige Methionin-Synthase- Aktivität, Nukleinsäuren kodierend eine Coenzym B12-unabhängige Methionin- Synthase-Aktivität, Nukleinsäuren kodierend eine Sulfat-Adenylyltransferase-Aktivität, Nukleinsäuren kodierend eine Phosphoadenosin-Phosphosulfat-Reductase-Aktivität, Nukleinsäuren kodierend eine Ferredoxin-Sulfit-Reduktase-Aktivität, Nukleinsäuren kodierend eine Ferredoxin NADPH-Reduktase Aktivität, Nukleinsäuren kodierend eine Ferredoxin-Aktivität, Nukleinsäuren kodierend ein Protein der Sulfat-Reduktion RXA077, Nukleinsäuren kodierend ein Protein der Sulfat-Reduktion RXA248, Nuklein¬ säuren kodierend ein Protein der Sulfat-Reduktion RXA247, Nukleinsäuren kodierend eine, RXA0655 Regulator undNukleinsäuren kodierend einen RXN2910 Regulator.ie) the expression of genes in the microorganism by expression units according to the invention or by expression units according to the invention with increased specific expression activity according to embodiment ch), the genes being heterologous with respect to the expression units, and wherein the genes are selected from the group of nucleic acids encoding an aspartate kinase, nucleic acids encoding an aspartate semialdehyde dehydrogenase, nucleic acids encoding a homoserine dehydrogenase, nucleic acids encoding a glyceraldehyde-3-phosphate dehydrogenase, nucleic acids encoding a 3-phosphoglycerate kinase, encoding nucleic acids Pyruvate carboxylase, nucleic acids encoding a triosephosphate isomerase, nucleic acids encoding a homologous O-acetyltransferase, nucleic acids encoding a cystahionin gamma synthase, nucleic acids encoding a cystahionin beta-lyase, nucleic acids encoding a serine hydroxymethyltransferase, encoding nucleic acids an O-acetylhomoserine sulfhydrylase, nucleic acids encoding a methylene tetrahydrofolate reductase, nucleic acids encoding a phosphoserine aminotransferase, nucleic acids encoding a phosphoserine phosphatase, nucleic acids encoding a serine acetyl trans ferase nucleic acids encoding a cysteine synthase activity I 1 nucleic acids encoding a cysteine synthase activity II, nucleic acids encoding a coenzyme B12-dependent methionine synthase activity, nucleic acids encoding a coenzyme B12-independent methionine synthase activity, nucleic acids encoding a sulfate adenylyltransferase Activity, nucleic acids encoding a phosphoadenosine phosphosulfate reductase activity, nucleic acids encoding a ferredoxin sulfite reductase activity, nucleic acids encoding a ferredoxin NADPH reductase activity, nucleic acids encoding a ferredoxin activity, nucleic acids encoding a protein of sulfate reduction RXA077 , Nucleic acids encoding a protein of the sulfate reduction RXA248, nucleic acids encoding a protein of the sulfate reduction RXA247, nucleic acids encoding a, RXA0655 regulator and nucleic acids encoding a RXN2910 regulator.
Wie vorstehend bei den Verfahren beschrieben, wird die Regulation der Expression dieser Genen im Mikroorganismus durch erfindungsgemäße Expressionseinheiten o- der durch erfindungsgemäße Expressionseinheiten mit erhöhter spezifischer Expressi¬ onsaktivität gemäß Ausführungsform ch) dadurch erreicht, dass manAs described above in the methods, the regulation of the expression of these genes in the microorganism by expression units according to the invention or by expression units according to the invention with increased specific expression activity according to embodiment ch) is achieved by
dh1) eine oder mehrere erfindungsgemäße Expressionseinheiten, gegebenenfalls mit erhöhter spezifischer Expressionsaktivität, in das Genom des Mikroorganismus ein¬ bringt, so dass die Expression eines oder mehrerer dieser endogenen Gene unter der Kontrolle der eingebrachten, erfindungsgemäßen Expressionseinheiten, gegebenen- falls mit erhöhter spezifischer Expressionsaktivität, erfolgt oderdh1) brings one or more expression units according to the invention, optionally with increased specific expression activity, into the genome of the microorganism so that the expression of one or more of these endogenous genes under the control of the incorporated expression units according to the invention, optionally with increased specific expression activity, done or
dh2) ein oder mehrere dieser Gene in das Genom des Mikrorganismus einbringt, so dass die Expression eines oder mehrerer der eingebrachten Gene unter der Kontrolle der endogenen, erfindungsgemäßen Expressionseinheiten, gegebenenfalls mit erhöh- ter spezifischer Expressionsaktivität, erfolgt oder
dh3) ein oder mehrere Nukleinsäurekonstrukte, enthaltend eine erfindungsgemäße Expressionseinheit, gegebenenfalls mit erhöhter spezifischer Expressionsaktivität, und funktionell verknüpft eine oder mehrere, zu exprimierende Nukleinsäuren, in den Mik- roorganismus einbringt.dh2) introduces one or more of these genes into the genome of the microorganism, so that the expression of one or more of the genes introduced takes place under the control of the endogenous expression units according to the invention, optionally with increased specific expression activity, or ie3) one or more nucleic acid constructs containing an expression unit according to the invention, optionally with increased specific expression activity, and functionally linked to one or more nucleic acids to be expressed, into which microorganism introduces.
Eine weiter bevorzugte Ausführungsform des vorstehend beschriebenen Verfahrens zur Herstellung von Methionin ist dadurch gekennzeichnet, dass die genetisch verän¬ derten Mikroorganismen im Vergleich zum Wildtyp zusätzlich eine erhöhte Aktivität, mindestens einer der Aktivitäten, ausgewählt aus der Gruppe Aspartatkinase-Aktivität, Aspartat-Semialdehyd-Dehydrogenase-Aktivität, Homoserin Dehydrogenase-Aktivität, Glycerinaldehyd-3-Phosphat Dehydrogenase-Aktivität, 3-Phosphoglycerat Kinase- Aktivität, Pyruvat Carboxyiase-Aktivität, Triosephosphat Isomerase-Aktivität, Homose¬ rin O-Acetyltransferase-Aktivität, Cystahionin-gamma-Synthase-Aktivität, Cystahionin- beta-Lyase-Aktivität Serin-Hydroxymethyltransferase-Aktivität, O-Acetylhomoserin- Sulfhydrylase-Aktivität, Methylen-Tetrahydrofolat-Reduktase-Aktivität, Phosphoserin- Aminotransferase-Aktivität, Phosphoserin-Phosphatase-Aktivität, Serine Acetyl- Transferase-Aktivität, Cystein-Synthase-Aktivität, Cystein-Synthase Il -Aktivität, Coen- zym B12-abhängige Methionin-Synthase-Aktivität, Coenzym B12-unabhängige Methio- nin-Synthase-Aktivität, Sulfat-Adenylyltransferase-Aktivität, Phosphoadenosin-A further preferred embodiment of the method for producing methionine described above is characterized in that the genetically modified microorganisms in comparison to the wild type additionally an increased activity, at least one of the activities selected from the group aspartate kinase activity, aspartate semialdehyde dehydrogenase Activity, homoserine dehydrogenase activity, glyceraldehyde-3-phosphate dehydrogenase activity, 3-phosphoglycerate kinase activity, pyruvate carboxyiase activity, triosephosphate isomerase activity, homosein O-acetyltransferase activity, cystahionine gamma synthase activity , Cystahionin beta-lyase activity, serine hydroxymethyltransferase activity, O-acetyl homoserine sulfhydrylase activity, methylene tetrahydrofolate reductase activity, phosphoserine aminotransferase activity, phosphoserine phosphatase activity, serine acetyltransferase activity, cysteine Synthase activity, cysteine syntha se II activity, coenzyme B12-dependent methionine synthase activity, coenzyme B12-independent methionine synthase activity, sulfate adenylyltransferase activity, phosphoadenosine
Phosphosulfat-Reductase-Aktivität, Ferredoxin-Sulfit-Reduktase-Aktivität, Ferredoxin NADPH-Reduktase Aktivität, Ferredoxin-Aktivität Aktivität Proteins der Sulfat- Reduktion RXA077, Aktivität eines Proteins der Sulfat-Reduktion RXA248, Aktivität eines Proteins der Sulfat-Reduktion RXA247, Aktivität eines RXA655-Regulators und Aktivität eines RXN2910-Regulators aufweisenPhosphosulfate reductase activity, ferredoxin sulfite reductase activity, ferredoxin NADPH reductase activity, ferredoxin activity activity protein of sulfate reduction RXA077, activity of a sulfate-reducing protein RXA248, activity of a protein of sulfate reduction RXA247, activity an RXA655 regulator and activity of an RXN2910 regulator
Eine weiter besonders bevorzugte Ausführungsform des vorstehend beschriebenen Verfahrens zur Herstellung von Methionin ist dadurch gekennzeichnet, dass die gene¬ tisch veränderten Mikroorganismen im Vergleich zum Wildtyp zusätzlich eine reduzier- te Aktivität, mindestens einer der Aktivitäten, ausgewählt aus der Homoserine-Kinase- Aktivität, Threonin-Dehydratase-Aktivität, Threonin Synthase-Aktivität, Meso- Diaminopimelat D-Dehydrogenase-Aktivität, Phosphoenolpyruvat-Carboxykinase- Aktivität, Pyruvat-Oxidase-Aktivität, Dihydrodipicolinat Synthase-Aktivität, Dihydrodipi- colinat Reduktase-Aktivität, und Diaminopicolinat Decarboxylase-Aktivität aufweisen.A further particularly preferred embodiment of the method for the production of methionine described above is characterized in that the genetically modified microorganisms in addition to the wild type additionally a reduced activity, at least one of the activities selected from the homoserine kinase activity, threonine Dehydratase activity, threonine synthase activity, meso-diaminopimelate D-dehydrogenase activity, phosphoenolpyruvate carboxykinase activity, pyruvate oxidase activity, dihydrodipicolinate synthase activity, dihydrodipicolinate reductase activity, and diaminopicolinate decarboxylase activity.
Diese zusätzlichen, erhöhten oder reduzierten Aktivitäten mindestens einer der vorste¬ hend beschriebenen Aktivitäten können, müssen aber nicht durch eine erfindungsge¬ mäße Nukleinsäure mit Promotoraktivität und/oder eine erfindungsgemäße Expressi¬ onseinheit verursacht sein.
Die Erfindung betrifft ferner ein Verfahren zur Herstellung von Threonin durch Kultivie¬ rung von genetisch veränderten Mikroorganismen mit erhöhter oder verursachter Ex¬ pressionsrate mindestens eines Gens im Vergleich zum Wildtyp, wobei manThese additional, increased or reduced activities of at least one of the above-described activities can, but need not, be caused by a nucleic acid according to the invention having promoter activity and / or an expression unit according to the invention. The invention further relates to a process for the production of threonine by cultivating genetically modified microorganisms having an increased or caused expression rate of at least one gene in comparison to the wild type, wherein
ch) die spezifische Expressionsaktivität im Mikroorganismus von mindestens einer endogenen, erfindungsgemäßen Expressionseinheit, die die Expression der endoge¬ nen Gene reguliert, im Vergleich zum Wildtyp erhöht oderch) the specific expression activity in the microorganism of at least one endogenous expression unit according to the invention which regulates the expression of the endogenous genes is increased in comparison to the wild type or
dh) die Expression von Genen im Mikroorganismus durch erfindungsgemäße Expres- sionseinheiten oder durch erfindungsgemäße Expressionseinheiten mit erhöhter spezi¬ fischer Expressionsaktivität gemäß Ausführungsform ch) reguliert, wobei die Gene im Bezug auf die Expressionseinheiten heterolog sind,ie) the expression of genes in the microorganism is regulated by expression units according to the invention or by expression units according to the invention with increased specific expression activity according to embodiment (ch), whereby the genes are heterologous with respect to the expression units,
und wobei die Gene ausgewählt sind aus der Gruppe Nukleinsäuren kodierend eine Aspartatkinase, Nukleinsäuren kodierend eine Aspartat-Semialdehyd-Dehydrogenase, Nukleinsäuren kodierend eine Glycerinaldehyd-3-Phosphat Dehydrogenase, Nuklein¬ säuren kodierend eine 3-Phosphoglycerat Kinase, Nukleinsäuren kodierend eine Pyru- vat Carboxylase, Nukleinsäuren kodierend eine Triosephosphat Isomerase, Nuklein¬ säuren kodierend eine Homoserin-Kinase, Nukleinsäuren kodierend eine Threonin Synthase, Nukleinsäuren kodierend einen Threonin Exporter Carrier, Nukleinsäuren kodierend eine Glucose-6-Phosphat-Dehydrogenase, Nukleinsäuren kodierend eine Transaldolase, Nukleinsäuren kodierend eine Transketolase, Nukleinsäuren kodierend einer Malat-Quinon-Oxidoreductase, Nukleinsäuren kodierend eine 6- Phosphogluconat-Dehydrogenase, Nukleinsäuren kodierend einen Lysin-Exporter, Nukleinsäuren kodierend eine Biotin-Ligase, Nukleinsäuren kodierend eine Phosphoe- nolpyruvat-Carboxylase, Nukleinsäuren kodierend ein Threonin Efflux-Protein, Nuklein¬ säuren kodierend eine Fruktose-1 ,6-bisphosphatase, Nukleinsäuren kodierend ein Op- cA Protein, Nukleinsäuren kodierend eine 1 -Phosphof ructokinase, Nukleinsäuren ko¬ dierend eine 6-Phosphofructokinase, und Nukleinsäuren kodierend eine Homoserin- Dehydrogenaseand wherein the genes are selected from the group of nucleic acids encoding an aspartate kinase, nucleic acids encoding an aspartate semialdehyde dehydrogenase, nucleic acids encoding a glyceraldehyde-3-phosphate dehydrogenase, nucleic acids encoding a 3-phosphoglycerate kinase, nucleic acids encoding a pyruvate carboxylase , Nucleic acids encoding a triosephosphate isomerase, nucleic acids encoding a homoserine kinase, nucleic acids encoding a threonine synthase, nucleic acids encoding a threonine exporter carrier, nucleic acids encoding a glucose-6-phosphate dehydrogenase, nucleic acids encoding a transaldolase, nucleic acids encoding a transketolase, Nucleic acids encoding a malate quinone oxidoreductase, nucleic acids encoding a 6-phosphogluconate dehydrogenase, nucleic acids encoding a lysine exporter, nucleic acids encoding a biotin ligase, nucleic acids encoding a phosphoenolpyruvate carboxylase, nucleus encoding a threonine efflux protein, nucleic acids encoding a fructose-1,6-bisphosphatase, nucleic acids encoding an OpcA protein, nucleic acids encoding a 1-phosphofructokinase, nucleic acids encoding a 6-phosphofructokinase, and nucleic acids encoding one Homoserine dehydrogenase
Wie vorstehend bei den Verfahren beschrieben, wird die Regulation der Expression dieser Genen im Mikroorganismus durch erfindungsgemäße Expressionseinheiten o- der durch erfindungsgemäße Expressionseinheiten mit erhöhter spezifischer Expressi- onsaktivität gemäß Ausführungsform ch) dadurch erreicht, dass manAs described above in the methods, the regulation of the expression of these genes in the microorganism by expression units according to the invention or by expression units according to the invention with increased specific expression activity according to embodiment ch) is achieved by
dh1) eine oder mehrere erfindungsgemäße Expressionseinheiten, gegebenenfalls mit erhöhter spezifischer Expressionsaktivität, in das Genom des Mikroorganismus ein¬ bringt, so dass die Expression eines oder mehrerer dieser endogenen Gene unter der Kontrolle der eingebrachten, erfindungsgemäßen Expressionseinheiten, gegebenen-
falls mit erhöhter spezifischer Expressionsaktivität, erfolgt oderie1) one or more expression units according to the invention, optionally with increased specific expression activity, into the genome of the microorganism ein¬, so that the expression of one or more of these endogenous genes under the control of the introduced expression units according to the invention, given if increased specific expression activity, or
dh2) ein oder mehrere dieser Gene in das Genom des Mikrorganismus einbringt, so dass die Expression eines oder mehrerer der eingebrachten Gene unter der Kontrolle der endogenen, erfindungsgemäßen Expressionseinheiten, gegebenenfalls mit erhöh¬ ter spezifischer Expressionsaktivität, erfolgt oderdh2) introduces one or more of these genes into the genome of the microorganism, so that the expression of one or more of the introduced genes takes place under the control of the endogenous expression units according to the invention, optionally with increased specific expression activity, or
dh3) ein oder mehrere Nukleinsäurekonstrukte, enthaltend eine erfindungsgemäße Expressionseinheit, gegebenenfalls mit erhöhter spezifischer Expressionsaktivität, und funktionell verknüpft eine oder mehrere, zu exprimierende Nukleinsäuren, in den Mik¬ roorganismus einbringt.ie3) one or more nucleic acid constructs containing an expression unit according to the invention, optionally with increased specific expression activity, and functionally linked one or more nucleic acids to be expressed, into which microorganisms are introduced.
Eine weiter bevorzugte Ausführungsform des vorstehend beschriebenen Verfahrens zur Herstellung von Threonin ist dadurch gekennzeichnet, dass die genetisch veränderten Mikroorganismen im Vergleich zum Wildtyp zusätzlich eine erhöhte Aktivität, mindestens einer der Aktivitäten, ausgewählt aus der Gruppe Aspartatkinase-Aktivität, Aspartat-Semialdehyd-Dehydrogenase-Aktivität, Glycerinal- dehyd-3-Phosphat Dehydrogenase-Aktivität, 3-Phosphoglycerat Kinase-Aktivität, Pyru- vat Carboxylase-Aktivität, Triosephosphat Isomerase-Aktivität, Threonin Synthase- Aktivität, Aktivität eines Threonin Export-Carriers, Transaldolase-Aktivität, Transketola- se-Aktivität, Glucose-6-Phosphat-dehydrogenase-Aktivität, Malat-Qinon- Oxidoreductase-Aktivität, Homoserin-Kinase-Aktivität, Biotin-Ligase-Aktivität, Phosphoenolpyruvat-Carboxylase-Aktivität, Threonin-Efflux-Protein-Aktivität, Protein OpcA-Aktivität, 1-Phosphofructokinase-Aktivität, 6-Phosphofructokinase-Aktivität, Fruk- tose 1 ,6 bisphosphatase-Aktivität, 6-Phosphogluconat-Dehydrogenase und Homoserin- Dehydrogenase-Aktivität aufweisen.A further preferred embodiment of the method for the production of threonine described above is characterized in that the genetically modified microorganisms in addition to the wild type additionally an increased activity, at least one of the activities selected from the group aspartate kinase activity, aspartate semialdehyde dehydrogenase activity , Glyceraldehyde-3-phosphate dehydrogenase activity, 3-phosphoglycerate kinase activity, pyruvate carboxylase activity, triosephosphate isomerase activity, threonine synthase activity, threonine export carrier activity, transaldolase activity, transketolase Activity, glucose-6-phosphate dehydrogenase activity, malate-quinone oxidoreductase activity, homoserine kinase activity, biotin ligase activity, phosphoenolpyruvate carboxylase activity, threonine efflux protein activity, protein OpcA- Activity, 1-phosphofructokinase activity, 6-phosphofructokinase activity, fructose 1 , 6-bisphosphatase activity, 6-phosphogluconate dehydrogenase and homoserine dehydrogenase activity.
Eine weiter besonders bevorzugte Ausführungsform des vorstehend beschriebenen Verfahrens zur Herstellung von Threonin ist dadurch gekennzeichnet, dass die gene- tisch veränderten Mikroorganismen im Vergleich zum Wildtyp zusätzlich eine reduzier¬ te Aktivität, mindestens einer der Aktivitäten, ausgewählt aus der Gruppe Threonin Dehydratase-Aktivität, Homoserin O-Acetyltransferase-Aktivität, Serin- Hydroxymethyltransferase-Aktivität, O-Acetylhomoserin-Sulfhydrylase-Aktivität, Meso- Diaminopimelat D-Dehydrogenase-Aktivität, Phosphoenolpyruvat-Carboxykinase- Aktivität, Pyruvat-Oxidase-Aktivität, Dihydrodipicolinat Synthetase-Aktivität, Dihydrodi- picolinat Reduktase-Aktivität, Asparaginase-Aktivität, Aspartat-Decarboxylase-Aktivität, Lysin-Exporter-Aktivität, Acetolactat-Synthase-Aktivität , Ketol-Aid-Reductoisomerase- Aktivität , Branched chain aminotransferase- Aktivität , Coenzym B12-abhängige Methionin Synthase- Aktivität , Coenzym B12-unabhängige Methion Synthase- Aktivi-
tät, Dihydroxy-acid Dehydratase- Aktivität und Diaminopicolinat Decarboxylase-Aktivität aufweisen.A further particularly preferred embodiment of the above-described method for the production of threonine is characterized in that the genetically modified microorganisms in addition to the wild type additionally a reduced activity, at least one of the activities selected from the group threonine dehydratase activity, homoserine O-acetyltransferase activity, serine hydroxymethyltransferase activity, O-acetylhomoserine sulfhydrylase activity, meso-diaminopimelate D-dehydrogenase activity, phosphoenolpyruvate carboxykinase activity, pyruvate oxidase activity, dihydrodipicolinate synthetase activity, dihydrodipolinate reductase Activity, asparaginase activity, aspartate decarboxylase activity, lysine exporter activity, acetolactate synthase activity, ketol-Aid reductoisomerase activity, branched chain aminotransferase activity, coenzyme B12-dependent methionine synthase activity, coenzyme B12 independent methion synth ase- having dihydroxy-acid dehydratase activity and diaminopicolinate decarboxylase activity.
Diese zusätzlichen, erhöhten oder reduzierten Aktivitäten mindestens einer der vorste- hend beschriebenen Aktivitäten können, müssen aber nicht durch eine erfindungsge¬ mäße Nukleinsäure mit Promotoraktivität und/oder eine erfindungsgemäße Expressi¬ onseinheit verursacht sein.These additional, increased or reduced activities of at least one of the above-described activities may, but need not, be caused by a nucleic acid according to the invention having promoter activity and / or an expression unit according to the invention.
Unter dem Begriff der „Aktivität" eines Proteins wird bei Enzymen die Enzymaktivität des entsprechenden Proteins, bei anderen Proteinen, beispielsweise Struktur oder Transport-Proteinen die physiologische Aktivität der Proteine verstanden.The term "activity" of a protein in enzymes means the enzyme activity of the corresponding protein, in other proteins, for example structure or transport proteins, the physiological activity of the proteins.
Die Enzyme sind in der Regel in der Lage ein Substrat in ein Produkt umzuwandeln bzw. diesen Umwandlunsgschritt zu katalysieren.The enzymes are usually able to convert a substrate into a product or to catalyze this conversion step.
Dementsprechend wird unter der „Aktivität" eines Enzyms die in einer bestimmten Zeit durch das Enzym umgesetzte Menge Substrat bzw. gebildete Menge Produkt verstan¬ den.Accordingly, the "activity" of an enzyme is understood to mean the amount of substrate or amount of product converted by the enzyme in a specific time.
Bei einer erhöhten Aktivität im Vergleich zum Wildtyp wird somit im Vergleich zum Wildtyp in einer bestimmten Zeit durch das Enzym die umgesetzte Menge Substrat bzw. die gebildete Menge Produkt erhöht.With an increased activity in comparison to the wild type, the amount of substrate or the amount of product formed is thus increased by the enzyme compared to the wild type in a certain time.
Vorzugsweise beträgt diese Erhöhung der „Aktivität" bei allen vorstehend und nachste- hend beschriebenen Aktivitäten mindestens 5 %, weiter bevorzugt mindestens 20 %, weiter bevorzugt mindestens 50 %, weiter bevorzugt mindestens 100 %, bevorzugter mindestens 300 %, noch bevorzugter mindestens 500 %, insbesondere mindestens 600 % der „Aktivität des Wildtyps".Preferably, this increase in "activity" in all the activities described above and below is at least 5%, more preferably at least 20%, more preferably at least 50%, more preferably at least 100%, more preferably at least 300%, even more preferably at least 500%, in particular at least 600% of the "wild-type activity".
Bei einer reduzierten Aktivität im Vergleich zum Wildtyp wird somit im Vergleich zum Wildtyp in einer bestimmten Zeit durch das Enzym die umgesetzte Menge Substrat bzw. die gebildete Menge Produkt reduziert.With a reduced activity in comparison to the wild type, the amount of substrate or the amount of product formed is thus reduced by the enzyme compared to the wild type in a certain time.
Unter einer reduzierten Aktivität wird vorzugsweise die teilweise oder im wesentlichen vollständige, auf unterschiedliche zellbiologische Mechanismen beruhende Unterbin¬ dung oder Blockierung der Funktionalität diese Enzyms in einem Mikroorganismus ver¬ standen.A reduced activity is preferably understood to mean the partial or substantially complete interruption or blocking of the functionality of this enzyme in a microorganism based on different cell biological mechanisms.
Eine Reduzierung der Aktivität umfasst eine mengenmäßige Verringerung eines En- zyms bis hin zu einem im wesentlichen vollständigen Fehlen des Enzyms (d.h. fehlen¬ de Nachweisbarkeit der entsprechenden Aktivität oder fehlende immunologische
Nachweisbarkeit des Enzyms). Vorzugsweise wird diß Aktivität im Mikroorganismus im Vergleich zum Wildtyp um mindestens 5 %, weiter bevorzugt um mindestens 20 %, weiter bevorzugt um mindestens 50 %, weiter bevorzugt um 100 % reduziert. Insbe¬ sondere meint "Reduzierung" auch das vollständigen Fehlen der entsprechenden Akti- vität.A reduction in activity includes a reduction in the amount of an enzyme to a substantially complete absence of the enzyme (ie lack of detectability of the corresponding activity or lack of immunological Detectability of the enzyme). Preferably, the activity in the microorganism is reduced by at least 5%, more preferably by at least 20%, more preferably by at least 50%, more preferably by 100%, compared to the wild type. In particular, "reduction" also means the complete absence of the corresponding activity.
Die Aktivität bestimmter Enzyme in genetisch veränderten Mikroorganismen sowie im Wildtyp und damit die Erhöhung oder Reduzierung der Enzymaktivität lassen sich nach bekannten Verfahren, wie beispielsweise Enzymassays ermitteln.The activity of certain enzymes in genetically modified microorganisms and in the wild type and thus the increase or reduction of the enzyme activity can be determined by known methods, such as enzyme assays.
Beispielsweise wird unter eine Pyruvatcarboxylase ein Protein verstanden, das die enzymatische Aktivität aufweist, Pyruvat in Oxaloacetat umzuwandeln.For example, a pyruvate carboxylase is understood as meaning a protein which has the enzymatic activity of converting pyruvate into oxaloacetate.
Dementsprechend wird unter einer Pyruvatcarboxylase-Aktivität die in einer bestimm- ten Zeit durch das Protein Pyruvatcarboxylase umgesetzte Menge Pyruvat bzw. gebil¬ dete Menge Oxaloacetat verstanden.Accordingly, a pyruvate carboxylase activity is understood as meaning the amount of pyruvate or amount of oxaloacetate converted in a certain time by the protein pyruvate carboxylase.
Bei einer erhöhten Pyruvatcarboxylase-Aktivität gegenüber dem Wildtyp wird somit im Vergleich zum Wildtyp in einer bestimmten Zeit durch das Protein Pyruvatcarboxylase die umgesetzte Menge Pyruvat bzw. die gebildete Menge Oxaloacetat erhöht.In the case of an increased pyruvate carboxylase activity compared to the wild type, the amount of pyruvate reacted or the amount of oxaloacetate formed is thus increased by the protein pyruvate carboxylase compared to the wild type in a specific time.
Vorzugsweise beträgt diese Erhöhung der Pyruvatcarboxylase-Aktivität mindestens 5 %, weiter bevorzugt mindestens 20 %, weiter bevorzugt mindestens 50 %, weiter bevorzugt mindestens 100 %, bevorzugter mindestens 300 %, noch bevorzugter min- destens 500 %, insbesondere mindestens 600 % der Pyruvatcarboxylase -Aktivität des Wildtyps.Preferably, this increase in pyruvate carboxylase activity is at least 5%, more preferably at least 20%, more preferably at least 50%, even more preferably at least 100%, more preferably at least 300%, even more preferably at least 500%, especially at least 600% of the pyruvate carboxylase. Activity of the wild type.
Weiterhin wir beispielsweise unter eine Phosphoenolpyruvat-Carboxykinase-Aktivität die Enzymaktivität einer Phosphoenolpyruvat-Carboxykinase-verstanden.Furthermore, we understand, for example, a phosphoenolpyruvate carboxykinase activity as the enzyme activity of a phosphoenolpyruvate carboxykinase.
Unter einer Phosphoenolpyruvat-Carboxykinase wird ein Protein verstanden, das die enzymatische Aktivität aufweist, Oxaloacetat in Phosphoenolpyruvat umzuwandeln.By a phosphoenolpyruvate carboxykinase is meant a protein having the enzymatic activity of converting oxaloacetate to phosphoenolpyruvate.
Dementsprechend wird unter Phosphoenolpyruvat-Carboxykinase-Aktivität die in einer bestimmten Zeit durch das Protein Phosphoenolpyruvat umgesetzte Menge Oxaloace¬ tat bzw. gebildete Menge Phosphoenolpyruvat verstanden.Accordingly, phosphoenolpyruvate-carboxykinase activity is understood as meaning the amount of oxaloacetate reacted or the amount of phosphoenolpyruvate formed in a certain time by the protein phosphoenolpyruvate.
Bei einer reduzierten Phosphoenolpyruvat-Carboxykinase-Aktivität gegenüber dem Wildtyp wird somit im Vergleich zum Wildtyp in einer bestimmten Zeit durch das Protein
Phosphoenolpyruvat-Carboxykinase die umgesetzte Menge Oxaloacetat bzw. die gebildete Menge Phosphoenolpyruvat reduziert.With a reduced phosphoenolpyruvate carboxykinase activity compared to the wild type is thus compared to the wild type in a certain time by the protein Phosphoenolpyruvat carboxykinase reduces the reacted amount of oxaloacetate or the amount of phosphoenolpyruvate formed.
Eine Reduzierung der Phosphoenolpyruvat-Carboxykinase-Aktivität umfasst eine men- genmäßige Verringerung einer Phosphoenolpyruvat-Carboxykinase bis hin zu einem im wesentlichen vollständigen Fehlen der Phosphoenolpyruvat-Carboxykinase (d.h. fehlende Nachweisbarkeit von Phosphoenolpyruvat-Carboxykinase-Aktivität oder feh¬ lende immunologische Nachweisbarkeit der Phosphoenolpyruvat-Carboxykinase). Vorzugsweise wird die Phosphoenolpyruvat-Carboxykinase-Aktivität im Vergleich zum Wildtyp um mindestens 5 %, weiter bevorzugt um mindestens 20 %, weiter bevorzugt um mindestens 50 %, weiter bevorzugt um 100 % reduziert. Insbesondere meint "Re¬ duzierung" auch das vollständigen Fehlen der Phosphoenolpyruvat-Carboxykinase - Aktivität.A reduction in phosphoenolpyruvate carboxykinase activity includes a quantitative reduction of a phosphoenolpyruvate carboxykinase to an essentially complete absence of phosphoenolpyruvate carboxykinase (ie, lack of detectability of phosphoenolpyruvate carboxykinase activity or lack of immunological detectability of phosphoenolpyruvate carboxykinase ). Preferably, the phosphoenolpyruvate carboxykinase activity is reduced by at least 5%, more preferably by at least 20%, more preferably by at least 50%, more preferably by 100% as compared to the wild-type. In particular, "reduction" also means the complete absence of the phosphoenolpyruvate carboxykinase activity.
Die zusätzliche Erhöhung von Aktivitäten kann durch verschiedene Wege erfolgen, beispielsweise durch Ausschalten von hemmenden Regulationsmechanismen auf Expressions- und Proteinebene oder durch Erhöhung der Genexpression von Nuk¬ leinsäuren kodierend die vorstehend beschriebenen Proteine gegenüber dem Wildtyp.The additional increase of activities can take place by different ways, for example by switching off inhibitory regulation mechanisms on expression and protein level or by increasing the gene expression of nucleic acids coding the proteins described above against the wild type.
Die Erhöhung der Genexpression der Nukleinsäuren kodierend die vorstehend be¬ schriebenen Proteine gegenüber dem Wildtyp kann ebenfalls durch verschiedene We¬ ge erfolgen, beispielsweise durch Induzierung des Gens durch Aktivatoren oder wie vorstehend beschrieben durch Erhöhung der Promotoraktivität oder Erhöhung der Ex¬ pressionsaktivität oder durch Einbringen von einer oder mehrerer Genkopien in den Mikroorganismus.The increase in the gene expression of the nucleic acids encoding the above-described proteins relative to the wild-type can also be effected by various means, for example by inducing the gene by activators or as described above by increasing the promoter activity or increasing the expression activity or by introducing one or more gene copies into the microorganism.
Unter Erhöhung der Genexpression einer Nukleinsäure codierend ein Protein wird er¬ findungsgemäß auch die Manipulation der Expression der Mikroorganismus eigenen, endogenen Proteine verstanden.By increasing the gene expression of a nucleic acid encoding a protein, the manipulation of the expression of the microorganism's own endogenous proteins is also understood according to the invention.
Dies kann beispielsweise, wie vorstehend beschrieben durch Veränderung der Promo¬ tor- und/oder Expressionseinheits-Sequenzen der Gene erreicht werden. Eine solche Veränderung, die eine erhöhte Expressionsrate des Gens zur Folge hat, kann bei¬ spielsweise durch Deletion oder Insertion von DNA Sequenzen erfolgen.This can be achieved, for example, as described above by changing the promoter and / or expression unit sequences of the genes. Such a change, which results in an increased expression rate of the gene, can take place, for example, by deletion or insertion of DNA sequences.
Es ist, wie vorstehend beschrieben, möglich, die Expression der endogenen Proteine durch die Applikation exogener Stimuli zu verändern. Dies kann durch besondere phy¬ siologische Bedingungen, also durch die Applikation von Fremdsubstanzen erfolgen.
Zur Erzielung einer Erhöhung der Genexpression kann der Fachmann weitere unter¬ schiedliche Maßnahmen einzeln oder in Kombination ergreifen. So kann beispielsweise die Kopienzahl der entsprechenden Gene erhöht werden, oder es kann die Promotor- und Regulationsregion oder die Ribosomenbindungsstelle, die sich stromaufwärts des Strukturgens befindet, mutiert werden. Durch induzierbare Promotoren ist es zusätzlich möglich, die Expression im Verlaufe der fermentativen Produktion zu steigern. Durch Maßnahmen zur Verlängerung der Lebensdauer der mRNA wird ebenfalls die Expres¬ sion verbessert. Weiterhin wird durch Verhinderung des Abbaus des Enzymproteins ebenfalls die Enzymaktivität verstärkt. Die Gene oder Genkonstrukte können entweder in Plasmiden mit unterschiedlicher Kopienzahl vorliegen oder im Chromosom integriert und amplifiziert sein. Alternativ kann weiterhin eine Überexpression der betreffenden Gene durch Veränderung der Medienzusammensetzung und Kulturführung erreicht werden.It is possible, as described above, to alter the expression of the endogenous proteins by the application of exogenous stimuli. This can be done by special physiological conditions, ie by the application of foreign substances. To achieve an increase in gene expression, the person skilled in the art can take further different measures individually or in combination. For example, the copy number of the respective genes can be increased, or the promoter and regulatory region or ribosome binding site located upstream of the structural gene can be mutated. By inducible promoters it is additionally possible to increase the expression in the course of fermentative production. Measures to extend the lifetime of the mRNA also improve the expression. Furthermore, by preventing degradation of the enzyme protein, enzyme activity is also enhanced. The genes or gene constructs may either be present in different copy number plasmids or be integrated and amplified in the chromosome. Alternatively, overexpression of the genes in question can be achieved by changing the composition of the medium and culture.
Anleitungen hierzu findet der Fachmann unter anderem bei Martin et al. (Biontechnolo- gy 5, 137-146 (1987)), bei Guerrero et al. (Gene 138, 35-41 (1994)), Tsuchiya und Mo- rinaga (Bio/Technology 6, 428-430 (1988)), bei Eikmanns et al. (Gene 102, 93-98 (1991)), in der Europäischen Patentschrift 0472869, im US Patent 4,601 ,893, bei Schwarzer und Pühler (Biotechnology 9, 84-87 (1991), bei Remscheid et al. (Applied and Environmental Microbiology 60,126-132 (1994), bei LaBarre et al. (Journal of Bac- teriology 175, 1001-1007 (1993)), in der Patentanmeldung WO 96/15246, bei Ma- lumbres et al. (Gene 134, 15-24 (1993)), in der japanischen Offenlegungsschrift JP-A- 10-229891 , bei Jensen und Hammer (Biotechnology and Bioengineering 58,.191 -195 (1998)), bei Makrides (Microbiological Reviews 60 : 512-538 (1996) und in bekannten Lehrbüchern der Genetik und Molekularbiologie.For instructions on this, the skilled person will find, inter alia, in Martin et al. (Biontechnolgy 5, 137-146 (1987)), Guerrero et al. (Gene 138, 35-41 (1994)), Tsuchiya and Morinaga (Bio / Technology 6, 428-430 (1988)), in Eikmanns et al. (Gene 102, 93-98 (1991)), European Patent 0472869, U.S. Patent 4,601,893, Schwarzer and Pühler (Biotechnology 9, 84-87 (1991), Remscheid et al. (Applied and Environmental Microbiology 60,126-132 (1994), in LaBarre et al., (Journal of Bacteriology 175, 1001-1007 (1993)), in the patent application WO 96/15246, in Malumbres et al., (Gene 134, 15-24 (1993)), Japanese Laid-Open Patent Publication JP-A-10-229891, Jensen and Hammer (Biotechnology and Bioengineering 58, 1991-195 (1998)), Makrides (Microbiological Reviews 60: 512-538 (1996) and in well-known textbooks of genetics and molecular biology.
Weiterhin kann es für die Produktion von biosynthetischen Produkten, insbesondere L- Lysin, L-Methionin und L-Threonin, vorteilhaft sein, neben der Expression bzw. Ver¬ stärkung eines Gens unerwünschte Nebenreaktionen auszuschalten (Nakayama: "Breeding of Amino Acid Producing Microorganisms", in: Overproduction of Microbial Products, Krumphanzl, Sikyta, Vanek (eds.), Academic Press, London, UK, 1982).Furthermore, it may be advantageous for the production of biosynthetic products, in particular L-lysine, L-methionine and L-threonine, to eliminate unwanted side reactions in addition to the expression or amplification of a gene (Nakayama: "Breeding of Amino Acid Producing Microorganisms". , in: Overproduction of Microbial Products, Krumphanzl, Sikyta, Vanek (eds.), Academic Press, London, UK, 1982).
In einer bevorzugten Ausführungsform erfolgt die Erhöhung der Genexpression einer Nukleinsäure kodierend eines der vorstehend beschriebenen Proteine durch Einbrin- gen von mindestens einer Nukleinsäure kodierend ein entsprechendes Protein in den Mikroorganismus. Das Einbringen der Nukleinsäure kann chromsomal oder extrachro¬ mosomal erfolgen, also durch Erhöhung der Kopienzahl auf dem Chromosom und oder eine Kopie des Gens auf einem sich replizierenden Plasmid in dem Wirtsmikroorga¬ nismus.
Vorzugsweise erfolgt das Einbringen der Nukleinsäure, beispielsweise in Form einer Expressionskassete, enthaltend die Nukleinsäure, chromosomal, insbesondere durch die vorstehend beschriebene SacB-Methode.In a preferred embodiment, the gene expression of a nucleic acid encoding one of the proteins described above is increased by introducing at least one nucleic acid encoding a corresponding protein into the microorganism. Introduction of the nucleic acid can be chromosomally or extrachromosomally, ie by increasing the copy number on the chromosome and / or a copy of the gene on a replicating plasmid in the host microorganism. The introduction of the nucleic acid, for example in the form of an expression cassette containing the nucleic acid, preferably takes place chromosomally, in particular by the SacB method described above.
Dazu kann prinzipiell jedes Gen, das eines der vorstehend beschriebenen Proteine kodiert verwendet werden.In principle, any gene encoding one of the proteins described above can be used for this purpose.
Bei genomischen Nukleinsäure-Sequenzen aus eukaryontischen Quellen, die Introns enthalten, sind für den Fall das der Wirtsmikroorganismus nicht in der Lage ist oder nicht in die Lage versetzt werden kann, die entsprechenden Proteine zu exprimieren, bevorzugt bereits prozessierte Nukleinsäuresequenzen, wie die entsprechenden cDNAs zu verwenden.For genomic nucleic acid sequences from eukaryotic sources containing introns, in the event that the host microorganism is unable or unable to express the corresponding proteins, preferably already processed nucleic acid sequences, such as the corresponding cDNAs to use.
Beispiele für die entsprechenden Gene sind in Tabelle 1 und 2 aufgelistet.Examples of the corresponding genes are listed in Tables 1 and 2.
Vorzugsweise erfolgt die Reduzierung der vorstehend beschriebenen Aktivitäten in Mikroorganismen durch mindestens eines der nachfolgenden Verfahren:Preferably, the reduction of the above-described activities in microorganisms is carried out by at least one of the following processes:
• Einbringen mindestens einer sense-Ribonukleinsäuresequenz zur Induktion ei- ner Kosuppression oder einer deren Expression gewährleistenden Expressi¬ onskassetteIntroducing at least one sense ribonucleic acid sequence for inducing a cosuppression or an expression cassette ensuring its expression
• Einbringen mindestens eines DNA- oder Protein-bindenden Faktors gegen das entsprechede -Gen, -RNA oder -Protein oder einer dessen Expression gewähr- leistenden ExpressionskassetteIntroducing at least one DNA- or protein-binding factor against the corresponding gene, RNA or protein or an expression cassette ensuring its expression
• Einbringen mindestens einer den RNA-Abbau bewirkenden viralen Nukleinsäu- resequenz oder einer deren Expression gewährleistenden ExpressionskassetteIntroducing at least one viral nucleic acid sequence causing RNA degradation or an expression cassette ensuring its expression
• Einbringen mindestens eines Konstruktes zur Erzeugung eines Funktionsver¬ lustes, wie beispielsweise die Generierung von Stopp-Kodons oder eine Ver¬ schiebungen im Leseraster, an einem Gen beispielsweise durch Erzeugung ei¬ ner Insertion, Deletion, Inversion oder Mutation in einem Gen. Bevorzugt kön¬ nen Knockout-Mutanten mittels gezielter Insertion in das gewünschte Zielgen durch homologe Rekombination oder Einbringen von sequenzspezifischenIntroducing at least one construct for generating a loss of function, for example the generation of stop codons or a shift in the reading frame, on a gene, for example by generating an insertion, deletion, inversion or mutation in a gene. Knockout mutants can preferably be obtained by targeted insertion into the desired target gene by homologous recombination or introduction of sequence-specific
Nukleasen gegen das Zielgen generiert werden.Nucleases are generated against the target gene.
• Einbringen eines Promotors mit reduzierter Promotoraktivität oder einer Ex¬ pressionseinheit mit reduzierter Expressionsaktivität.
Dem Fachmann ist bekannt, dass auch weitere Verfahren im Rahmen der vorliegenden Erfindung zur Reduzierung seiner Aktivität oder Funktion eingesetzt werden können. Beispielsweise kann auch das Einbringen einer dominant-negativen Variante eines Proteins oder einer deren Expression gewährleistenden Expressionskassette vorteil- haft sein.Introducing a promoter with reduced promoter activity or an expression unit with reduced expression activity. It is known to the person skilled in the art that other methods within the scope of the present invention can also be used to reduce its activity or function. For example, the introduction of a dominant-negative variant of a protein or of an expression cassette which ensures its expression can also be advantageous.
Dabei kann jedes einzelne dieser Verfahren eine Verminderung der Proteinmenge, mRNA-Menge und/oder Aktivität eines Proteins bewirken. Auch eine kombinierte An¬ wendung ist denkbar. Weitere Methoden sind dem Fachmann bekannt und können die Behinderung oder Unterbindung der Prozessierung des Proteins, des Transports des Proteins oder dessen mRNA, Hemmung der Ribosomenanlagerung, Hemmung des RNA-Spleißens, Induktion eines RNA abbauenden Enzyms und/oder Hemmung der Translationselongation oder -termination umfassen.Each of these methods can cause a reduction in the amount of protein, mRNA amount and / or activity of a protein. A combined application is also conceivable. Other methods are known in the art and may include inhibiting or inhibiting processing of the protein, transport of the protein or its mRNA, inhibition of ribosome attachment, inhibition of RNA splicing, induction of an RNA degrading enzyme and / or inhibition of translation elongation or termination ,
Im erfindungsgemäßen Verfahren zur Herstellung von biosynthetischen Produkten wird vorzugsweise dem Kultivierungsschritt der genetisch veränderten Mikroorganismen ein Isolieren von biosynthetischen Produkten aus den Mikroorganismen oder/oder aus der Fermentationsbrühe angeschlossen. Diese Schritte können gleichzeitig und/oder vor- zugsweisie nach dem Kultivierungsschritt stattfinden.In the method according to the invention for the production of biosynthetic products, the step of cultivating the genetically modified microorganisms is preferably followed by isolating biosynthetic products from the microorganisms or from the fermentation broth. These steps may take place simultaneously and / or preferably after the culturing step.
Die erfindungsgemäßen genetisch veränderten Mikroorganismen können kontinuierlich oder diskontinuierlich im batch- Verfahren (Satzkultivierung) oder im fed batch (Zulauf¬ verfahren) oder repeated fed batch Verfahren (repetitives Zulaufverfahren) zur Produk¬ tion von biosynthetischen Produkten, insbesondere L-Lysin, L-Methionin und L- Threonin, kultiviert werden. Eine Zusammenfassung über bekannte Kultivierungsme¬ thoden ist im Lehrbuch von Chmiel (Bioprozeßtechnik 1. Einführung in die Bioverfah¬ renstechnik (Gustav Fischer Verlag, Stuttgart, 1991)) oder im Lehrbuch von Storhas (Bioreaktoren und periphere Einrichtungen (Vieweg Verlag, Braunschweig/Wiesbaden, 1994)) zu finden.The genetically modified microorganisms according to the invention can be used continuously or discontinuously in the batch process (batch culturing) or in the fed batch (feed process) or repeated fed batch process (repetitive feed process) for the production of biosynthetic products, in particular L-lysine, L-methionine and L-threonine, to be cultured. A summary of known cultivation methods is in the textbook by Chmiel (Bioprozesstechnik 1. Introduction to the bioprocess engineering (Gustav Fischer Verlag, Stuttgart, 1991)) or in the textbook by Storhas (bioreactors and peripheral facilities (Vieweg Verlag, Braunschweig / Wiesbaden, 1994)).
Das zu verwendende Kulturmedium hat in geeigneter Weise den Ansprüchen der je¬ weiligen Stämme zu genügen. Beschreibungen von Kulturmedien verschiedener Mik¬ roorganismen sind im Handbuch "Manual of Methods für General Bacteriology" der American Society für Bacteriology (Washington D. C1 USA, 1981) enthalten.The culture medium to be used must suitably satisfy the requirements of the respective strains. Descriptions of culture media for various-organisms Mik¬ contained in the handbook "Manual of Methods for General Bacteriology" of the American Society for Bacteriology (Washington DC USA 1, 1981).
Diese erfindungsgemäß einsetzbaren Medien umfassen gewöhnlich eine oder mehrere Kohlenstoffquellen, Stickstoffquellen, anorganische Salze, Vitamine und/oder Spuren¬ elemente.
Bevorzugte Kohlenstoffquellen sind Zucker, wie Mono-, Di- oder Polysaccharide. Sehr gute Kohlenstoffquellen sind beispielsweise Glucose, Fructose, Mannose, Galactose, Ribose, Sorbose, Ribulose, Lactose, Maltose, Saccharose, Raffinose, Stärke oder CeI- lulose. Man kann Zucker auch über komplexe Verbindungen, wie Melassen, oder an- dere Nebenprodukte der Zucker-Raffinierung zu den Medien geben. Es kann auch vor¬ teilhaft sein, Gemische verschiedener Kohlenstoffquellen zuzugeben. Andere mögliche Kohlenstoffquellen sind Öle und Fette wie z. B. Sojaöl. Sonnenblumenöl. Erdnußöl und Kokosfett, Fettsäuren wie z. B. Palmitinsäure, Stearinsäure oder Linolsäure, Alkohole wie z. B. Glycerin, Methanol oder Ethanol und organische Säuren wie z. B. Essigsäure oder Milchsäure.These media which can be used according to the invention usually comprise one or more carbon sources, nitrogen sources, inorganic salts, vitamins and / or trace elements. Preferred carbon sources are sugars, such as mono-, di- or polysaccharides. Very good sources of carbon are, for example, glucose, fructose, mannose, galactose, ribose, sorbose, ribulose, lactose, maltose, sucrose, raffinose, starch or cellulose. Sugar can also be added to the media via complex compounds such as molasses or other by-products of sugar refining. It may also be advantageous to add mixtures of different carbon sources. Other possible sources of carbon are oils and fats such. B. soybean oil. Sunflower oil. Peanut oil and coconut fat, fatty acids such. As palmitic acid, stearic acid or linoleic acid, alcohols such. As glycerol, methanol or ethanol and organic acids such. As acetic acid or lactic acid.
Stickstoffquellen sind gewöhnlich organische oder anorganische Stickstoffverbindun¬ gen oder Materialien, die diese Verbindungen enthalten. Beispielhafte Stickstoffquellen umfassen Ammoniak-Gas oder Ammoniumsalze, wie Ammoniumsulfat, Ammoniumch- lorid, Ammoniumphosphat, Ammoniumcarbonat oder Ammoniumnitrat, Nitrate, Harn¬ stoff, Aminosäuren oder komplexe Stickstoffquellen, wie Maisquellwasser, Sojamehl, Sojaprotein, Hefeextrakt, Fleischextrakt und andere. Die Stickstoffquellen können ein¬ zeln oder als Mischung verwendet werden.Nitrogen sources are usually organic or inorganic nitrogen compounds or materials containing these compounds. Exemplary nitrogen sources include ammonia gas or ammonium salts such as ammonium sulfate, ammonium chloride, ammonium phosphate, ammonium carbonate or ammonium nitrate, nitrates, urea, amino acids or complex nitrogen sources such as corn steep liquor, soybean meal, soy protein, yeast extract, meat extract and others. The nitrogen sources can be used singly or as a mixture.
Anorganische Salzverbindungen, die in den Medien enthalten sein können, umfassen die Chlorid-, Phosphor- oder Sulfatsalze von Calcium, Magnesium, Natrium, Kobalt, Molybdän, Kalium, Mangan, Zink, Kupfer und EisenInorganic salt compounds which may be included in the media include the chloride, phosphorus or sulfate salts of calcium, magnesium, sodium, cobalt, molybdenum, potassium, manganese, zinc, copper and iron
Als Schwefelquelle für die Herstellung von Feinchemikalien, insbesondere von Methio- nin, können anorganische Verbindungen wie beispielsweise Sulfate, Sulfite, Dithionite, Tetrathionate, Thiosulfate, Sulfide aber auch organische Schwefelverbindungen, wie Mercaptane und Thiole, verwendet werden.As sulfur source for the production of fine chemicals, in particular of methionine, it is possible to use inorganic compounds such as, for example, sulfates, sulfites, dithionites, tetrathionates, thiosulfates, sulfides, but also organic sulfur compounds, such as mercaptans and thiols.
Als Phosphorquelle können Phosphorsäure, Kaliumdihydrogenphosphat oder Dikali- umhydrogenphosphat oder die entsprechenden Natrium haltigen Salze verwendet werden.Phosphoric acid, potassium dihydrogen phosphate or dipotassium hydrogen phosphate or the corresponding sodium-containing salts can be used as the phosphorus source.
Chelatbildner können zum Medium gegeben werden, um die Metallionen in Lösung zu halten. Besonders geeignete Chelatbildner umfassen Dihydroxyphenole, wie Catechol oder Protocatechuat, oder organische Säuren, wie Citronensäure.Chelating agents can be added to the medium to keep the metal ions in solution. Particularly suitable chelating agents include dihydroxyphenols, such as catechol or protocatechuate, or organic acids, such as citric acid.
Die erfindungsgemäß eingesetzten Fermentationsmedien enthalten üblicherweise auch andere Wachstumsfaktoren, wie Vitamine oder Wachstumsförderer, zu denen bei¬ spielsweise Biotin, Riboflavin, Thiamin, Folsäure, Nikotinsäure, Panthothenat und Pyri- doxin gehören. Wachstumsfaktoren und Salze stammen häufig von komplexen Me-
dienkomponenten, wie Hefeextrakt, Melassen, Maisquellwasser und dergleichen. Dem Kulturmedium können überdies geeignete Vorstufen zugesetzt werden. Die genaue Zusammensetzung der Medienverbindungen hängt stark vom jeweiligen Experiment ab und wird für jeden spezifischen Fall individuell entschieden. Information über die Me- dienoptimierung ist erhältlich aus dem Lehrbuch "Applied Microbiol. Physiology, A Practical Approach" (Hrsg. P.M. Rhodes, P.F. Stanbury, IRL Press (1997) S. 53-73, ISBN 0 19 963577 3). Wachstumsmedien lassen sich auch von kommerziellen Anbie¬ tern beziehen, wie Standard 1 (Merck) oder BHI (Brain heart infusion, DIFCO) und der¬ gleichen.The fermentation media used according to the invention usually also contain other growth factors, such as vitamins or growth promoters, which include, for example, biotin, riboflavin, thiamine, folic acid, nicotinic acid, panthothenate and pyridoxine. Growth factors and salts are often derived from complex me- serving components such as yeast extract, molasses, corn steep liquor and the like. In addition, suitable precursors can be added to the culture medium. The exact composition of the media compounds will depend heavily on the particular experiment and will be decided on a case by case basis. Information about the media optimization is available from the textbook "Applied Microbiol Physiology, A Practical Approach" (Ed PM Rhodes, PF Stanbury, IRL Press (1997) pp 53-73, ISBN 0 19 963577 3). Growth media can also be obtained from commercial suppliers, such as Standard 1 (Merck) or BHI (Brain heart infusion, DIFCO) and the like.
Sämtliche Medienkomponenten werden, entweder durch Hitze (20 min bei 1 ,5 bar und 1210C) oder durch Sterilfiltration, sterilisiert. Die Komponenten können entweder zu¬ sammen oder nötigenfalls getrennt sterilisiert werden. Sämtliche Medienkomponenten können zu Beginn der Anzucht zugegen sein oder wahlfrei kontinuierlich oder char- genweise hinzugegeben werden.All media components are sterilized either by heat (20 min at 1, 5 bar and 121 0 C) or by sterile filtration. The components can either be sterilized together or, if necessary, sterilized separately. All media components may be present at the beginning of the culture or added randomly or in batches as desired.
Die Temperatur der Kultur liegt normalerweise zwischen 15°C und 45°C, vorzugsweise bei 25°C bis 400C und kann während des Experimentes konstant gehalten oder verän¬ dert werden. Der pH-Wert des Mediums sollte im Bereich von 5 bis 8,5, vorzugsweise um 7,0 liegen. Der pH-Wert für die Anzucht läßt sich während der Anzucht durch Zu¬ gabe von basische Verbindungen wie Natriumhydroxid, Kaliumhydroxid, Ammoniak bzw. Ammoniakwasser oder saure Verbindungen wie Phosphorsäure oder Schwefel¬ säure kontrollieren. Zur Kontrolle der Schaumentwicklung können Antischaummittel, wie z. B. Fettsäurepolyglykolester, eingesetzt werden. Zur Aufrechterhaltung der Stabi- lität von Plasmiden können dem Medium geeignete selektiv wirkende Stoffe, wie z. B. Antibiotika, hinzugefügt werden. Um aerobe Bedingungen aufrechtzuerhalten, werden Sauerstoff oder Sauerstoff haltige Gasmischungen, wie z. B. Umgebungsluft, in die Kultur eingetragen. Die Temperatur der Kultur liegt normalerweise bei 2O0C bis 45°C. Die Kultur wird solange fortgesetzt, bis sich ein Maximum des gewünschten Produktes gebildet hat. Dieses Ziel wird normalerweise innerhalb von 10 Stunden bis 160 Stun¬ den erreicht.The temperature of the culture is normally between 15 ° C and 45 ° C, preferably at 25 ° C to 40 0 C and can be kept constant or changed during the experiment. The pH of the medium should be in the range of 5 to 8.5, preferably around 7.0. The pH for cultivation can be controlled during cultivation by addition of basic compounds such as sodium hydroxide, potassium hydroxide, ammonia or ammonia water or acidic compounds such as phosphoric acid or sulfuric acid. To control the development of foam anti-foaming agents, such as. As fatty acid polyglycol, are used. In order to maintain the stability of plasmids, suitable selective substances, such as e.g. As antibiotics, are added. In order to maintain aerobic conditions, oxygen or oxygen-containing gas mixtures, such. B. ambient air, registered in the culture. The temperature of the culture is usually 2O 0 C to 45 ° C. The culture is continued until a maximum of the desired product has formed. This goal is usually reached within 10 hours to 160 hours.
Die so erhaltenen Fermentationsbrühen haben üblicherweise eine Trockenmasse von 7,5 bis 25 Gew.-%.The fermentation broths thus obtained usually have a dry matter content of 7.5 to 25% by weight.
Vorteilhaft ist außerdem auch, wenn die Fermentation zumindest am Ende, insbeson¬ dere jedoch über mindestens 30% der Fermentationsdauer zuckerlimitiert gefahren wird. Das heißt, dass während dieser Zeit die Konzentration an verwertbarem Zucker im Fermentationsmedium auf 0 bis 3 g/l gehalten, beziehungsweise abgesenkt wird.
Die Isolierung von biosynthetischen Produkten aus der Fermentationsbrühe und/oder den Mikroorganismen erfolgt in an sich bekannter Weise entsprechend den physika¬ lisch-chemischen Eigenschaften des biosynthetischen Wertprodukts und den biosyn¬ thetischen Nebenprodukten.In addition, it is also advantageous if the fermentation is driven sugar-limited at least at the end, but in particular over at least 30% of the fermentation time. This means that during this time the concentration of utilizable sugar in the fermentation medium is maintained at 0 to 3 g / l, or lowered. The isolation of biosynthetic products from the fermentation broth and / or the microorganisms takes place in a manner known per se in accordance with the physicochemical properties of the biosynthetic desired product and the biosynthetic by-products.
Die Fermentationsbrühe kann anschließend beispielsweise weiterverarbeitet werden. Je nach Anforderung kann die Biomasse ganz oder teilweise durch Separationsmetho¬ den, wie z. B. Zentrifugation, Filtration, Dekantieren oder einer Kombination dieser Me¬ thoden aus der Fermentationsbrühe entfernt oder vollständig in ihr belassen werden.The fermentation broth can then be further processed, for example. Depending on the requirement, the biomass may be wholly or partly by Separationsmetho¬ the, such. As centrifugation, filtration, decantation or a combination of these methods from the fermentation broth or be completely left in it.
Anschließend kann die Fermentationsbrühe mit bekannten Methoden, wie z. B. mit Hilfe eines Rotationsverdampfers, Dünnschichtverdampfers, Fallfilmverdampfers, durch Umkehrosmose, oder durch Nanofiltration, eingedickt beziehungsweise aufkon¬ zentriert werden. Diese aufkonzentrierte Fermentationsbrühe kann anschließend durch Gefriertrocknung, Sprühtrocknung, Sprühgranulation oder durch anderweitige Verfah¬ ren aufgearbeitet werden.Subsequently, the fermentation broth with known methods, such as. B. with the aid of a rotary evaporator, thin film evaporator, falling film evaporator, by reverse osmosis, or by nanofiltration, thickened or aufkon¬ centered. This concentrated fermentation broth can then be worked up by freeze drying, spray drying, spray granulation or by other methods.
Es ist aber auch möglich die biosynthetischen Produkte, insbesonder L-Lysin, L- Methionin und L-Threonin, weiter aufzureinigen. Hierzu wird die produkthaltige Brühe nach dem Abtrennen der Biomasse einer Chromatographie mit einem geeigneten Harz unterworfen, wobei das gewünschte Produkt oder die Verunreinigungen ganz oder teilweise auf dem Chromatographieharz zurückgehalten werden. Diese Chroma¬ tographieschritte können nötigenfalls wiederholt werden, wobei die gleichen oder ande¬ re Chromatographieharze verwendet werden. Der Fachmann ist in der Auswahl der geeigneten Chromatographieharze und ihrer wirksamsten Anwendung bewandert. Das gereinigte Produkt kann durch Filtration oder Ultrafiltration konzentriert und bei einer Temperatur aufbewahrt werden, bei der die Stabilität des Produktes maximal ist.However, it is also possible to further purify the biosynthetic products, in particular L-lysine, L-methionine and L-threonine. For this purpose, after separation of the biomass, the product-containing broth is subjected to chromatography with a suitable resin, the desired product or impurities being wholly or partially retained on the chromatography resin. If necessary, these chromatographic steps can be repeated using the same or different chromatography resins. The person skilled in the art is familiar with the choice of suitable chromatography resins and their most effective use. The purified product may be concentrated by filtration or ultrafiltration and stored at a temperature at which the stability of the product is maximized.
Die biosynthetischen Produkte können in unterschiedlichen Formen anfallen, bei- spielsweise in Form ihrer Salze oder Ester.The biosynthetic products can be obtained in different forms, for example in the form of their salts or esters.
Die Identität und Reinheit der isolierten Verbindung(en) kann durch Techniken des Standes der Technik bestimmt werden. Diese umfassen Hochleistungs- Flüssigkeitschromatographie (HPLC), spektroskopische Verfahren, Färbeverfahren, Dünnschichtchromatographie, NIRS, Enzymtest oder mikrobiologische Tests. Diese Analyseverfahren sind zusammengefaßt in: Patek et al. (1994) Appl. Environ. Micro- biol. 60:133-140; Malakhova et al. (1996) Biotekhnologiya 11 27-32; und Schmidt et al. (1998) Bioprocess Engineer. 19:67-70. Ulmann's Encyclopedia of Industrial Chemistry (1996) Bd. A27, VCH: Weinheim, S. 89-90, S. 521-540, S. 540-547, S. 559-566, 575- 581 und S. 581-587; Michal, G (1999) Biochemical Pathways: An Atlas of Biochemistry
and Molecular Biology, John Wiley and Sons; Fallon, A. et al. (1987) Applications of HPLC in Biochemistry in: Laboratory Techniques in Biochemistry and Molecular Biol¬ ogy, Bd. 17.The identity and purity of the isolated compound (s) can be determined by techniques of the prior art. These include high performance liquid chromatography (HPLC), spectroscopic methods, staining procedures, thin layer chromatography, NIRS, enzyme assay or microbiological assays. These analytical methods are summarized in: Patek et al. (1994) Appl. Environ. Microbiol. 60: 133-140; Malakhova et al. (1996) Biotekhnologiya 11 27-32; and Schmidt et al. (1998) Bioprocess Engineer. 19: 67-70. Ulmann's Encyclopedia of Industrial Chemistry (1996) Vol. A27, VCH: Weinheim, pp. 89-90, pp. 521-540, pp. 540-547, pp. 559-566, pp. 575-581 and pp. 581-587; Michal, G (1999) Biochemical Pathways: An Atlas of Biochemistry and Molecular Biology, John Wiley and Sons; Fallon, A. et al. (1987) Applications of HPLC in Biochemistry in: Laboratory Techniques in Biochemistry and Molecular Biology, Vol. 17.
Die Erfindung wird nun anhand der folgenden nicht-limitierenden Beispiele näher be¬ schrieben:The invention will now be described in more detail by means of the following non-limiting examples:
Beispiel 1example 1
Herstellung des Vektors pCUK5MCSPreparation of vector pCUK5MCS
Zunächst wurden Ampicillinresistenz und Replikationsursprung des Vektors pBR322 mit den Oligonukleotidprimern SEQ ID NO 5: und SEQ ID NO 6:mit Hilfe der Polyme- rase-Kettenreaktion (PCR) amplifiziert.First, ampicillin resistance and origin of replication of the vector pBR322 with the oligonucleotide primers SEQ ID NO 5: and SEQ ID NO 6: were amplified by means of the polymerase chain reaction (PCR).
SEQ ID NO 5:SEQ ID NO 5:
5'-CCCGGGATCCGCTAGCGGCGCGCCGGCCGGCCCGGTGTGAAATACCGCACA G-3'5'-CCCGGGATCCGCTAGCGGCGCGCCGGCCGGCCCGGTGTGAAATACCGCACA G-3 '
SEQ ID NO 6: 5'-TCTAGACTCGAGCGGCCGCGGCCGGCCTTTAAATTGAAGACGAAAGGGCCTC G-3'SEQ ID NO 6: 5'-TCTAGACTCGAGCGGCCGCGGCCGGCCTTTAAATTGAAGACGAAAGGGCCTC G-3 '
Neben den zu pBR322 komplementären Sequenzen, enthält der Oligonukleotidprimer SEQ ID NO 5: in 5'-3' Richtung die Schnittstellen für die Restriktionsendonukleasen Smal, BamHI, Nhel und Ascl und der Oligonukleotidprimer SEQ ID NO 6: in 5'-3' Richtung die Schnittstellen für die Restriktionsendonukleasen Xbal, Xhol, Notl und Dral. Die PCR Reaktion wurde nach Standardmethode wie Innis et al. (PCR Protocols. A Guide to Methods and Applications, Academic Press (1990)) mit PfuTurbo Poly¬ merase (Stratagene, La JoIIa, USA) durchgeführt. Das erhaltene DNA Fragment mit einer Größe von ungefähr 2,1 kb wurde mit dem GFX™PCR, DNA and Gel Band Puri- fication Kit (Amersham Pharmacia, Freiburg) nach Angaben des Herstellers gereinigt. Die stumpfen Enden des DNA-Fragmentes wurden mit dem Rapid DNA Ligation Kit (Roche Diagnostics, Mannheim) nach Angaben des Hersteilers miteinander ligiert und der Ligationsansatz nach Standardmethoden wie in Sambrook et al. (Molecular CIo- ning. A Laboratory Manual, CoId Spring Harbor, beschrieben (1989)), in kompetente E.coli XL-1 Blue (Stratagene, La JoIIa, USA) transformiert. Eine Selektion auf Plasmid tragende Zellen wurde durch das Ausplattieren auf Ampicillin (50μg/ml) haltigen LB Agar (Lennox, 1955, Viroiogy, 1 :190) erreicht.
Die Plasmid-DNA eines individuellen Klons wurde mit dem Qiaprep Spin Miniprep Kit (Qiagen, Hilden) nach Angaben des Herstellers isoliert und über Restriktionsverdaus überprüft. Das so erhaltene Plasmid erhält den Namen pCLiKI .In addition to the sequences complementary to pBR322, the oligonucleotide primer SEQ ID NO 5: contains in 5'-3 'direction the sites for the restriction endonucleases Smal, BamHI, Nhel and Ascl and the oligonucleotide primer SEQ ID NO 6: in 5'-3' direction Interfaces for the restriction endonucleases Xbal, Xhol, Notl and Dral. The PCR reaction was carried out by standard method as Innis et al. (PCR Protocols, A Guide to Methods and Applications, Academic Press (1990)) with PfuTurbo polymerase (Stratagene, La JoIIa, USA). The resulting DNA fragment, approximately 2.1 kb in size, was purified using the GFX ™ PCR, DNA and Gel Band Purification Kit (Amersham Pharmacia, Freiburg) according to the manufacturer's instructions. The blunt ends of the DNA fragment were ligated together with the Rapid DNA Ligation Kit (Roche Diagnostics, Mannheim) according to the Hersteilers and the ligation mixture by standard methods as in Sambrook et al. (Molecular Corning, A Laboratory Manual, ColD Spring Harbor, described (1989)), transformed into competent E. coli XL-1 Blue (Stratagene, La JoIIa, USA). Selection for plasmid-carrying cells was achieved by plating on ampicillin (50 μg / ml) -containing LB agar (Lennox, 1955, Viroiogy, 1: 190). The plasmid DNA of an individual clone was isolated with the Qiaprep Spin Miniprep Kit (Qiagen, Hilden) according to the manufacturer and checked by restriction digests. The resulting plasmid is named pCLiKI.
Ausgehend vom Plasmid pWLT1 (Liebl et al.,1992) als Template für eine PCR Reakti¬ on wurde mit den Oligonukleotidprimem SEQ ID NO:7 und SEQ ID NO:8 eine Kana- mycin-Resistenzcassette amplifiziert.Starting from the plasmid pWLT1 (Liebl et al., 1992) as a template for a PCR reaction, a kanamycin resistance cassette was amplified using the oligonucleotide primers SEQ ID NO: 7 and SEQ ID NO: 8.
SEQ ID NO:7: 5'-GAGATCTAGACCCGGGGATCCGCTAGCGGGCTGCTAAAGGAAGCGGA-S'SEQ ID NO: 7: 5'-GAGATCTAGACCCGGGGATCCGCTAGCGGGCTGCTAAAGGAAGCGGA-S '
SEQ ID NO:8 5'-GAGAGGCGCGCCGCTAGCGTGGGCGAAGAACTCCAGCA-S'SEQ ID NO: 8 5'-GAGAGGCGCGCCGCTAGCGTGGGCGAAGAACTCCAGCA-S '
Neben den zu pWLT1 komplementären Sequenzen, enthält der Oligonukleotidprimer SEQ ID NO: 7 in 5'-3' Richtung die Schnittsteilen für die Restriktionsendonukleasen Xbal, Smal, BamHI, Nhel und der Oligonukleotidprimer SEQ ID NO:8 in 5'-3' Richtung die Schnittstellen für die Restriktionsendonukleasen Ascl und Nhel. Die PCR Reaktion wurde nach Standardmethode wie Innis et al. (PCR Protocols. A Guide to Methods and Applications, Academic Press (1990)) mit Pf uTurbo Polymerase (Stratagene, La JoIIa, USA) durchgeführt. Das erhaltene DNA Fragment mit einer Größe von ungefähr 1 ,3 kb wurde mit dem GFX™PCR, DNA and Gel Band Purification Kit (Amersham Pharmacia, Freiburg) nach Angaben des Herstellers gereinigt. Das DNA-Fragment wurde mit den Restriktionsendonukleasen Xbal und Ascl (New England Biolabs, Beverly, USA) ge- schnitten und im Anschluß daran erneut mit dem GFX™PCR, DNA and Gel Band Puri¬ fication Kit (Amersham Pharmacia, Freiburg) nach Angaben des Herstellers gereinigt. Der Vektor pCLJKI wurde ebenfalls mit den Restriktionsendonukleasen Xbal und Ascl geschnitten und mit alkalischer Phosphatase (I (Roche Diagnostics, Mannheim)) nach Angaben des Herstellers dephosphoryliert. Nach Elektrophorese in einem 0,8%igen Agarosegel wurde der linearisierte Vektor (ca. 2,1 kb) mit dem GFX™PCR, DNA and Gel Band Purification Kit (Amersham Pharmacia, Freiburg) nach Angaben des Herstel¬ lers isoliert. Dieses Vektor-Fragment wurde mit Hilfe des Rapid DNA Ligation Kit (Ro¬ che Diagnostics, Mannheim) nach Angaben des Herstellers mit dem geschnittenen PCR Fragment ligiert und der Ligationsansatz nach Standardmethoden wie in Sambrook et al. (Molecular Cloning. A Laboratory Manual, CoId Spring Harbor, be- schrieben(1989)), in kompetente E.coli XL-1 Blue (Stratagene, La JoIIa, USA) transfor¬ miert. Eine Selektion auf Plasmid tragende Zellen wurde durch das Ausplattieren auf Ampicillin (50μg/ml) und Kanamycin (20μg/ml) haltigen LB Agar (Lennox, 1955, Virolo- gy, 1 :190) erreicht.
Die Plasmid-DNA eines individuellen Klons wurde mit dem Qiaprep Spin Miniprep Kit (Qiagen, Hilden) nach Angaben des Herstellers isoliert und über Restriktionsverdaus überprüft. Das so erhaltene Plasmid erhält den Namen pCLiK2.In addition to the pWLT1 complementary sequences, the oligonucleotide primer SEQ ID NO: 7 in 5'-3 'direction contains the cut portions for the restriction endonucleases Xbal, Smal, BamHI, NheI and the oligonucleotide primer SEQ ID NO: 8 in 5'-3' direction the Interfaces for the restriction endonucleases Ascl and Nhel. The PCR reaction was carried out by standard method as Innis et al. (PCR Protocols, A Guide to Methods and Applications, Academic Press (1990)) with Pf uTurbo polymerase (Stratagene, La JoIIa, USA). The resulting DNA fragment, approximately 1.3 kb in size, was purified using the GFX ™ PCR, DNA and Gel Band Purification Kit (Amersham Pharmacia, Freiburg) according to the manufacturer's instructions. The DNA fragment was cut with the restriction endonucleases XbaI and AscI (New England Biolabs, Beverly, USA) and then again with the GFX ™ PCR, DNA and Gel Band Purification Kit (Amersham Pharmacia, Freiburg) according to cleaned by the manufacturer. The vector pCLJKI was also cut with the restriction endonucleases XbaI and AscI and dephosphorylated with alkaline phosphatase (I (Roche Diagnostics, Mannheim)) according to the manufacturer's instructions. After electrophoresis in a 0.8% agarose gel, the linearized vector (about 2.1 kb) was isolated using the GFX ™ PCR, DNA and Gel Band Purification Kit (Amersham Pharmacia, Freiburg) according to the manufacturer's instructions. This vector fragment was ligated with the aid of the Rapid DNA Ligation Kit (Rosche Diagnostics, Mannheim) according to the manufacturer with the cut PCR fragment and the ligation mixture according to standard methods as in Sambrook et al. (Molecular Cloning, A Laboratory Manual, ColD Spring Harbor, described (1989)), transformed into competent E. coli XL-1 Blue (Stratagene, La JoIIa, USA). Selection for plasmid-carrying cells was achieved by plating on ampicillin (50 μg / ml) and kanamycin (20 μg / ml) -containing LB agar (Lennox, 1955, Virolgy, 1: 190). The plasmid DNA of an individual clone was isolated with the Qiaprep Spin Miniprep Kit (Qiagen, Hilden) according to the manufacturer and checked by restriction digests. The resulting plasmid is named pCLiK2.
Der Vektor pCLiK2 wurde mit der Restriktionsendonuklease Dral (New England Bio¬ labs, Beverly, USA) geschnitten. Nach Elektrophorese in einem 0,8%igen Agarosegel wurde ein ca. 2,3 kb großes Vektorfragment mit dem GFX™PCR, DNA and Gel Band Purification Kit (Amersham Pharmacia, Freiburg) nach Angaben des Herstellers isoliert. Dieses Vektor-Fragment wurde mit Hilfe des Rapid DNA Ligation Kit (Roche Di- agnostics, Mannheim) nach Angaben des Herstellers religiert und der Ligationsansatz nach Standardmethoden wie in Sambrook et al. (Molecular Cloning. A Laboratory Ma¬ nual, CoId Spring Harbor, beschrieben^ 989)), in kompetente E.coli XL-1 Blue (Strata- gene, La JoIIa, USA) transformiert. Eine Selektion auf Plasmid tragende Zellen wurde durch das Ausplattieren auf Kanamycin (20μg/ml) haltigen LB Agar (Lennox, 1955, Virology, 1 : 190) erreicht.The vector pCLiK2 was cut with the restriction endonuclease Dral (New England Biolabs, Beverly, USA). After electrophoresis in a 0.8% agarose gel, a ca. 2.3 kb vector fragment was isolated using the GFX ™ PCR, DNA and Gel Band Purification Kit (Amersham Pharmacia, Freiburg) according to the manufacturer's instructions. This vector fragment was religated using the Rapid DNA Ligation Kit (Roche Diagnostics, Mannheim) according to the manufacturer's instructions and the ligation mixture was purified by standard methods as described in Sambrook et al. (Molecular Cloning, A Laboratory Manual, Colard Spring Harbor, supra; 989)), transformed into competent E. coli XL-1 Blue (Stratagene, La JoIIa, USA). Selection for plasmid-carrying cells was achieved by plating on kanamycin (20 μg / ml) -containing LB agar (Lennox, 1955, Virology, 1: 190).
Die Plasmid-DNA eines individuellen Klons wurde mit dem Qiaprep Spin Miniprep Kit (Qiagen, Hilden) nach Angaben des Herstellers isoliert und über Restriktionsverdaus überprüft. Das so erhaltene Plasmid erhält den Namen pCLiK3.The plasmid DNA of an individual clone was isolated with the Qiaprep Spin Miniprep Kit (Qiagen, Hilden) according to the manufacturer and checked by restriction digests. The resulting plasmid is named pCLiK3.
Ausgehend vom Plasmid pWLQ2 (Liebl et al., 1992) als Template für eine PCR Reak¬ tion wurde mit den Oligonukleotidprimem SEQ ID NO:9 und SEQ ID NO:10 der Repli- kationsursprung pHM1519 amplifiziert.Starting from the plasmid pWLQ2 (Liebl et al., 1992) as a template for a PCR reaction, the replication origin pHM1519 was amplified using the oligonucleotide primers SEQ ID NO: 9 and SEQ ID NO: 10.
SEQ ID NO:9: δ'-GAGAGGGCGGCCGCGCAAAGTCCCGCTTCGTGAA-S'SEQ ID NO: 9: δ'-GAGAGGGCGGCCGCGCAAAGTCCCGCTTCGTGAA-S '
SEQ ID NO:10: 5'-GAGAGGGCGGCCGCTCAAGTCGGTCAAGCCACGC-S'SEQ ID NO: 10: 5'-GAGAGGGCGGCCGCTCAAGTCGGTCAAGCCACGC-S '
Neben den zu pWLQ2 komplementären Sequenzen, enthalten die Oligonukleotidpri- mer SEQ ID NO:9 und SEQ ID NO:10 Schnittstellen für die Restriktionsendonuklease Notl. Die PCR Reaktion wurde nach Standardmethode wie Innis et al. (PCR Protocols. A Guide to Methods and Applications, Academic Press (1990)) mit PfuTurbo PoIy- merase (Stratagene, La JoIIa, USA) durchgeführt. Das erhaltene DNA Fragment mit einer Größe von ungefähr 2,7 kb wurde mit dem GFX™PCR, DNA and Gel Band Puri¬ fication Kit (Amersham Pharmacia, Freiburg) nach Angaben des Herstellers gereinigt. Das DNA-Fragment wurde mit der Restriktionsendonuklease Notl (New England Bio¬ labs, Beverly, USA) geschnitten und im Anschluß daran erneut mit dem GFX™PCR, DNA and Gel Band Purification Kit (Amersham Pharmacia, Freiburg) nach Angaben
des Herstellers gereinigt. Der Vektor pCLiK3 wurde ebenfalls mit der Restriktionsendo- nuklease Notl geschnitten und mit alkalischer Phosphatase (I (Roche Diagnostics, Mannheim)) nach Angaben des Herstellers dephosphoryliert. Nach Elektrophorese in einem 0,8%igen Agarosegel wurde der linearisierte Vektor (ca. 2,3kb) mit dem GFX™PCR, DNA and Gel Band Purification Kit (Amersham Pharmacia, Freiburg) nach Angaben des Herstellers isoliert. Dieses Vektor-Fragment wurde mit Hilfe des Rapid DNA Ligation Kit (Roche Diagnostics, Mannheim) nach Angaben des Herstellers mit dem geschnittenen PCR Fragment ligiert und der Ligationsansatz nach Standardme¬ thoden wie in Sambrook et al. (Molecular Cloning. A Laboratory Manual, CoId Spring Harbor, beschrieben(1989)), in kompetente E.coli XL-1 Blue (Stratagene, La JoIIa1 In addition to the sequences complementary to pWLQ2, the oligonucleotide primers SEQ ID NO: 9 and SEQ ID NO: 10 contain cleavage sites for the restriction endonuclease NotI. The PCR reaction was carried out by standard method, such as Innis et al. (PCR Protocols, A Guide to Methods and Applications, Academic Press (1990)) with PfuTurbo polymerase (Stratagene, La JoIIa, USA). The resulting 2.7 kb DNA fragment was purified using the GFX ™ PCR, DNA and Gel Band Purification Kit (Amersham Pharmacia, Freiburg) according to the manufacturer's instructions. The DNA fragment was cleaved with the restriction endonuclease Notl (New England Bio¬ labs, Beverly, USA) and subsequently again with the GFX ™ PCR, DNA and Gel Band Purification Kit (Amersham Pharmacia, Freiburg) according to cleaned by the manufacturer. The vector pCLiK3 was likewise cut with the restriction endonuclease NotI and dephosphorylated with alkaline phosphatase (I (Roche Diagnostics, Mannheim)) according to the manufacturer's instructions. After electrophoresis in a 0.8% agarose gel, the linearized vector (approximately 2.3 kb) was isolated using the GFX ™ PCR, DNA and Gel Band Purification Kit (Amersham Pharmacia, Freiburg) according to the manufacturer's instructions. This vector fragment was ligated with the aid of the Rapid DNA Ligation Kit (Roche Diagnostics, Mannheim) according to the manufacturer with the cut PCR fragment and the ligation mixture by standard methods as in Sambrook et al. (Molecular Cloning, A Laboratory Manual, Colard Spring Harbor, described (1989)), in competent E. coli XL-1 Blue (Stratagene, La JoIIa 1
USA) transformiert. Eine Selektion auf Plasmid tragende Zellen wurde durch das Aus¬ plattieren auf Kanamycin (20μg/ml) haltigen LB Agar (Lennox, 1955, Virology, 1 :190) erreicht.USA). Selection for plasmid-carrying cells was achieved by Aus¬ plating on kanamycin (20 ug / ml) containing LB agar (Lennox, 1955, Virology, 1: 190).
Die Plasmid-DNA eines individuellen Klons wurde mit dem Qiaprep Spin Miniprep Kit (Qiagen, Hilden) nach Angaben des Herstellers isoliert und über Restriktionsverdaus überprüft. Das so erhaltene Plasmid erhält den Namen pCLiKδ.The plasmid DNA of an individual clone was isolated with the Qiaprep Spin Miniprep Kit (Qiagen, Hilden) according to the manufacturer and checked by restriction digests. The resulting plasmid is named pCLiKδ.
Für die Erweiterung von pCLiKδ um eine „multiple cloning Site" (MCS) wurden die bei¬ de synthetischen, weitestgehend komplementären Oligonukleotide SEQ ID NO:11und SEQ ID NO:12, die Schnittstellen für die Restriktionsendonukleasen Swal, Xhol, Aatl, Apal, Asp718, MIuI, Ndel, Spei, EcoRV, Sali, CIaI, BamHI, Xbal und Smal enthalten, durch gemeinsames erhitzen auf 950C und langsames abkühlen zu einem dop- pelsträngigen DNA-Fragment vereinigt.For the extension of pCLiKδ by a multiple cloning site (MCS), the two synthetic, largely complementary oligonucleotides SEQ ID NO: 11 and SEQ ID NO: 12, the restriction endonuclease sites Swal, Xhol, Aatl, Apal, Asp718 containing MluI, NdeI, SpeI, EcoRV, SalI, ClaI, BamHI, XbaI and SmaI, by heating together at 95 0 C and cooling slowly to a double-stranded DNA fragment pooled.
SEQ ID NO:11 : 5'-TCGAATTTAAATCTCGAGAGGCCTGACGTCGGGCCCGGTACCACGCGTCATATSEQ ID NO: 11: 5'-TCGAATTTAAATCTCGAGAGGCCTGACGTCGGGCCCGGTACCACGCGTCATAT
GACTAGTTCGGACCTAGGGATATCGTCGACATCGATGCTCTTCTGCGTTAATTAA- CAATTGGGATCCTCTAGACCCGGGATTTAAAT-3'GACTAGTTCGGACCTAGGGATATCGTCGACATCGATGCTCTTCTGCGTTAATTAA- CAATTGGGATCCTCTAGACCCGGGATTTAAAT-3 '
SEQ ID NO:12: 5'-GATCATTTAAATCCCGGGTCTAGAGGATCCCAATTGTTAATTAACGCAGAAGAGSEQ ID NO: 12: 5'-GATCATTTAAATCCCGGGTCTAGAGGATCCCAATTGTTAATTAACGCAGAAGAG
CATCGATGTCGACGATATCCCTAGGTCCGAACTAGTCATATGACGCGTGG- TACCGGGCCCGACGTCAGGCCTCTCGAGATTTAAAT-3'CATCGATGTCGACGATATCCCTAGGTCCGAACTAGTCATATGACGCGTGG- TACCGGGCCCGACGTCAGGCCTCTCGAGATTTAAAT-3 '
Der Vektor pCLiKδ wurde mit den Restriktionsendonuklease Xhol und BamHI (New England Biolabs, Beverly, USA) geschnitten und mit alkalischer Phosphatase (I (Roche Diagnostics, Mannheim)) nach Angaben des Herstellers dephosphoryliert. Nach E- lektrophorese in einem 0,8%igen Agarosegel wurde der linearisierte Vektor (ca. 5,0 kb)
mit dem GFX™PCR, DNA and Gel Band Purification Kit (Amersham Pharmacia, Frei¬ burg) nach Angaben des Herstellers isoliert. Dieses Vektor-Fragment wurde mit Hilfe des Rapid DNA Ligation Kit (Roche Diagnostics, Mannheim) nach Angaben des Her¬ stellers mit dem synthetischen Doppelsträngigen DNA-Fragment ligiert und der Ligati- onsansatz nach Standardmethoden wie in Sambrook et al. (Molecular Cloning. A Labo- ratory Manual, CoId Spring Harbor, beschrieben(1989)), in kompetente E.coli XL-1 Blue (Stratagene, La JoIIa, USA) transformiert. Eine Selektion auf Plasmid tragende Zellen wurde durch das Ausplattieren auf Kanamycin (20μg/ml) haltigen LB Agar (Lennox, 1955, Virology, 1 :190) erreicht.The vector pCLiKδ was cut with the restriction endonuclease Xhol and BamHI (New England Biolabs, Beverly, USA) and dephosphorylated with alkaline phosphatase (I (Roche Diagnostics, Mannheim)) according to the manufacturer's instructions. After electrophoresis in a 0.8% agarose gel, the linearized vector (about 5.0 kb) was isolated with the GFX ™ PCR, DNA and Gel Band Purification Kit (Amersham Pharmacia, Freiburg) according to the manufacturer's instructions. This vector fragment was ligated with the aid of the Rapid DNA Ligation Kit (Roche Diagnostics, Mannheim) according to the manufacturer with the synthetic double-stranded DNA fragment and the ligation onsansatz according to standard methods as in Sambrook et al. (Molecular Cloning, A Laboratory Manual, ColD Spring Harbor, described (1989)), transformed into competent E. coli XL-1 Blue (Stratagene, La JoIIa, USA). Selection for plasmid-carrying cells was achieved by plating on kanamycin (20 μg / ml) -containing LB agar (Lennox, 1955, Virology, 1: 190).
Die Plasmid-DNA eines individuellen Klons wurde mit dem Qiaprep Spin Miniprep Kit (Qiagen, Hilden) nach Angaben des Herstellers isoliert und über Restriktionsverdaus überprüft. Das so erhaltene Plasmid erhält den Namen pCLiK5MCS.The plasmid DNA of an individual clone was isolated with the Qiaprep Spin Miniprep Kit (Qiagen, Hilden) according to the manufacturer and checked by restriction digests. The resulting plasmid is named pCLiK5MCS.
Sequenzierungsreaktionen wurden nach Sanger et al. (1977) Proceedings of the Na¬ tional Academy of Sciences USA 74:5463-5467 durchgeführt. Die Sequenzierreaktio¬ nen wurden mittels ABI Prism 377 (PE Applied Biosystems, Weiterstadt) aufgetrennt und ausgewertet.Sequencing reactions were performed according to Sanger et al. (1977) Proceedings of the National Academy of Sciences USA 74: 5463-5467. The sequencing reactions were separated and evaluated by means of ABI Prism 377 (PE Applied Biosystems, Weiterstadt).
Das entstandene Plasmid pCLiK5MCS ist als SEQ ID NO: 13 aufgeführt.The resulting plasmid pCLiK5MCS is listed as SEQ ID NO: 13.
Beispiel 2Example 2
Herstellung des Plasmids P EF-TS metAPreparation of the plasmid P EF-TS metA
Chromosomale DNA aus C. glutamicum ATCC 13032 wurde nach Tauch et al. (1995) Plasmid 33:168-179 oder Eikmanns et al. (1994) Microbiology 140:1817-1828 präpa¬ riert. Mit den Oligonukleotidprimer BK 1849 SEQ ID NO 14 und BK 1862 SEQ ID NO 15 33, der chromosomalen DNA als Template und Pfu Turbo Polymerase (Fa. Strata¬ gene) wurde mit Hilfe der Polymerase-Kettenreaktion (PCR) nach Standardmethoden, wie in Innis et al. (1990) PCR Protocols. A Guide to Methods and Applications, Acade- mic Press beschrieben, das metA Gen, das für die Homoserin-O-Acetyltransferase kodiert, amplifiziert.Chromosomal DNA from C. glutamicum ATCC 13032 was isolated according to Tauch et al. (1995) Plasmid 33: 168-179 or Eikmanns et al. (1994) Microbiology 140: 1817-1828. With the oligonucleotide primers BK 1849 SEQ ID NO 14 and BK 1862 SEQ ID NO 15 33, the chromosomal DNA as template and Pfu Turbo Polymerase (Strata genes) was using the polymerase chain reaction (PCR) by standard methods, as described in Innis et al. (1990) PCR Protocols. A Guide to Methods and Applications, Acadic Press, amplified the metA gene encoding homoserine O-acetyltransferase.
BK 1849 SEQ ID NO 14 5'- gtgtgtcgacttagatgtagaactcgatgtag -3' undBK 1849 SEQ ID NO 14 5'- gtgtgtcgacttagatgtagaactcgatgtag -3 'and
BK 1862 SEQ ID NO 15 5'-atgcccaccctcgcgcc -3'
Das erhaltene DNA Fragment von ca. 1134 bp Größe wurde mit dem GFX™PCR, DNA and Gel Band Purification Kit (Amersham Pharmacia, Freiburg) nach Angaben des Herstellers gereinigt.BK 1862 SEQ ID NO 15 5'-atgcccaccctcgcgcc -3 ' The obtained DNA fragment of about 1134 bp size was purified using the GFX ™ PCR, DNA and Gel Band Purification Kit (Amersham Pharmacia, Freiburg) according to the manufacturer's instructions.
Mit den Oligonukleotidprimer Haf 26 SEQ ID NO 16 und Haf 27 SEQ ID NO 17, der chromosomalen DNA als Template und Pfu Turbo Polymerase (Fa. Stratagene) wurde mit Hilfe der Polymerase-Kettenreaktion (PCR) nach Standardmethoden, wie in Innis et al. (1990) PCR Protocols. A Guide to Methods and Applications, Academic Press beschrieben, die Expressioneinheit des Gens (SEQ ID 2), das für den Elongationsfak- tor TS kodiert, amplif iziert.The oligonucleotide primers Haf 26 SEQ ID NO 16 and Haf 27 SEQ ID NO 17, the chromosomal DNA as template and Pfu Turbo Polymerase (Stratagene) were amplified by polymerase chain reaction (PCR) according to standard methods as described in Innis et al. (1990) PCR Protocols. A Guide to Methods and Applications, Academic Press, the expression unit of the gene (SEQ ID 2), which codes for the elongation factor TS, amplified.
Haf 26 SEQ ID NO 16 5'-gagaggatcccccccacgacaatggaac-3' und Haf 27 SEQ ID NO 17Haf 26 SEQ ID NO 16 5'-gagaggatcccccccacgacaatggaac-3 'and Haf 27 SEQ ID NO 17
5'-cctgaaggcgcgagggtgggcattacggggcgatcctccttatg -3'5'-cctgaaggcgcgagggtgggcattacggggcgatcctccttatg -3 '
Das erhaltene DNA Fragment von ca. 195 bp Größe wurde mit dem GFX™PCR, DNA and Gel Band Purification Kit (Amersham Pharmacia, Freiburg) nach Angaben des Herstellers gereinigt.The obtained DNA fragment of about 195 bp size was purified with the GFX ™ PCR, DNA and Gel Band Purification Kit (Amersham Pharmacia, Freiburg) according to the manufacturer's instructions.
Die Primer Haf 27 und BK 1862 enthalten eine überlappende Sequenz und sind an ihren 5'-Enden homolog zueinander.The primers Haf 27 and BK 1862 contain an overlapping sequence and are homologous to each other at their 5 'ends.
Die oben erhaltenen PCR-Produkte wurden als Template für eine weitere PCR ein- setzt, in der die Primer BK 1849 (SEQ. ID. NO. 14) und Haf 26 (SEQ. ID. NO. 16) ge¬ nutzt wurden.The PCR products obtained above were used as templates for a further PCR in which the primers BK 1849 (SEQ ID NO 14) and Haf 26 (SEQ ID NO 16) were used.
Mit diesem Ansatz konnte ein DNA-Fragment amplifiziert werden, das der erwarteten Größe von 1329 bp entsprach. Diese P EF-TS/metA-Fusion wurde dann über die Restriktionschnittstellen BamHI und Sali in den Vektor pClik 5a MCS (SEQ. ID. NO. 13)kloniert.With this approach, a DNA fragment corresponding to the expected size of 1329 bp could be amplified. This P EF-TS / metA-fusion was then cloned via the restriction sites BamHI and Sali into the vector pClik 5a MCS (SEQ ID NO: 13).
Das Vektorfragment wurde zusammen mit dem PCR-Fragment mit Hilfe des Rapid DNA Ligation Kit (Roche Diagnostics, Mannheim) nach Angaben des Herstellers ligiert und der Ligationsansatz nach Standardmethoden wie in Sambrook et al. (Molecular Cloning. A Laboratory Manual, CoId Spring Harbor, beschrieben(1989)), in kompetente E.coli XL-1 Blue (Stratagene, La JoIIa, USA) transformiert. Eine Selektion auf Plasmid tragende Zellen wurde durch das Ausplattieren auf Kanamycin (20μg/ml) haltigen LB Agar (Lennox, 1955, Virology, 1 :190) erreicht.
Die Präparation der Plasmid DNA wurde nach Methoden und mit Materialien der Fa. Quiagen durchgeführt. Sequenzierungsreaktionen wurden nach Sanger et al. (1977) Proceedings of the National Academy of Sciences USA 74:5463-5467 durchgeführt. Die Sequenzierreaktionen wurden mittels ABI Prism 377 (PE Applied Biosystems, Wei¬ terstadt) aufgetrennt und ausgewertet.The vector fragment was ligated together with the PCR fragment using the Rapid DNA Ligation Kit (Roche Diagnostics, Mannheim) according to the manufacturer's instructions and the ligation mixture according to standard methods as in Sambrook et al. (Molecular Cloning, A Laboratory Manual, ColD Spring Harbor, described (1989)), transformed into competent E. coli XL-1 Blue (Stratagene, La JoIIa, USA). Selection for plasmid-carrying cells was achieved by plating on kanamycin (20 μg / ml) -containing LB agar (Lennox, 1955, Virology, 1: 190). The preparation of the plasmid DNA was carried out by methods and materials of Fa. Quiagen. Sequencing reactions were performed according to Sanger et al. (1977) Proceedings of the National Academy of Sciences USA 74: 5463-5467. The sequencing reactions were separated and evaluated by ABI Prism 377 (PE Applied Biosystems, Wei¬ terstadt).
Das resultierende Plasmid wurde mit pClik 5a MCS P EF-TS metA (SEQ. ID. NO. 18) bezeichnet.The resulting plasmid was designated pClik 5a MCS P EF-TS metA (SEQ ID NO: 18).
Beispiel 3 MetA-AktivitätenExample 3 MetA activities
Der Stamm Corynebacterium glutamicum ATCC13032 wurde jeweils mit den Plasmi¬ den pClikδ MCS, pClik MCS EF-TS metA nach der beschriebenen Methode (Liebl, et al. (1989) FEMS Microbiology Letters 53:299-303) transformiert. Die Transformations¬ mischung wurde auf CM-Platten plattiert, die zusätzlich 20mg/l Kanamycin enthielten, um eine Selektion auf Plasmid-haltige Zellen zu erreichen. Erhaltene Kan-resistente Klone wurden gepickt und vereinzelt.The strain Corynebacterium glutamicum ATCC13032 was in each case transformed with the plasmids pClikδ MCS, pClik MCS EF-TS metA according to the method described (Liebl, et al. (1989) FEMS Microbiology Letters 53: 299-303). The transformation mixture was plated on CM plates which additionally contained 20 mg / l kanamycin to achieve selection for plasmid-containing cells. Obtained Kan-resistant clones were picked and separated.
C. glutamicum Stämme, die eines dieser Plasmidkonstrukte enthielten, wurden in MMA-Medium ((40 g/l Saccharose, 20 g/l (NH4)2SO4, 1 g/l KH2PO4, 1 g/l K2HPO4, 0,25g/l MgSO4 x 7H2O, 54 g Aces, 1 ml CaCI2 (10 g/l), 1 ml Protocatechoat (300 mg/10 ml), 1 ml Spurenelementelösung (10 g/l FeSO4 x /H20, 10 g/l MnSO4 x H20, 2 g/l ZnSO4 x 7 H2O, 0,2 g/l CuSO4, 0,02 g/l NiCI2 x 6 H2O)1IOO //g/l Vitamin B12, 0,3 mg/l Thiamin, 1mM Leucin, 1 mg/l Pyridoxal HCl, 1 ml Biotin ( 100 mg/l), pH7,0) bei 300C über Nacht angezogen. Die Zellen wurden bei 4°C abzentrifugiert und das zweimal mit kaltem Tris-HCI-Puffer (0,1 %, pH 8,0) gewaschen. Nach erneuter Zentrifugation wur- den die Zellen in kalten Tris-HCI-Puffer ( 0,1 %, pH 8,0) aufgenommen und eine OD600 von 160 eingestellt. Für den Zellaufschluß wurden 1 ml dieser Zellsuspension in 2 ml Ribolyserröhrchen der Fa. Hybaid überführt und in einem Ribolyser der Fa. Hybaid bei einer Rotationseinstellung von 6,0 dreimal für jeweils 30 sec lysiert. Das Lysat wur¬ de durch 30minütige Zentrifugation bei 15.000 rpm bei 40C in einer Eppendorfzentrif u- ge geklärt und der Überstand in ein neues Eppendororfcup überführt. Der Proteingehalt wurde nach Bradford, M.M. (1976) Anal. Biochem. 72:248-254 bestimmt.C. glutamicum strains containing one of these plasmid constructs were dissolved in MMA medium (40 g / l sucrose, 20 g / l (NH 4 ) 2 SO 4 , 1 g / l KH 2 PO 4 , 1 g / l K 2 HPO 4 , 0.25 g / l MgSO 4 x 7H 2 O, 54 g aces, 1 ml CaCl 2 (10 g / l), 1 ml protocatechoate (300 mg / 10 ml), 1 ml of trace element solution (10 g / l FeSO 4) 4 x / H 2 0, 10 g / l MnSO 4 × H 2 0, 2 g / l ZnSO 4 × 7 H 2 O, 0.2 g / l CuSO 4 , 0.02 g / l NiCl 2 × 6 H 2 O) 1 IOO // g / l vitamin B 12, 0.3 mg / l thiamine, 1 mM leucine, 1 mg / l pyridoxal HCl, 1 ml of biotin (100 mg / l), pH 7.0) at 30 0 C. The cells were removed by centrifugation at 4 ° C. and washed twice with cold Tris-HCl buffer (0.1%, pH 8.0) After renewed centrifugation, the cells were poured into cold Tris-HCl buffer (0.1%, pH 8.0) and set an OD 600 of 160. For the cell disruption, 1 ml of this cell suspension was transferred to 2 ml Ribolyser tubes from Hybaid and incubated in a Ribolyser from Hybaid at a rotation setting of 6 , Three lysed for each 30 sec. The lysate wur¬ de by 30 min centrifugation at 15,000 rpm at 4 0 C in a Eppendorfzentrif u- ge clarified and the supernatant into a new Eppendororfcup transferred. The protein content was determined by Bradford, MM (1976) Anal. Biochem. 72: 248-254.
Die Messung der enzymatischen Aktivität von MetA wurde wie folgt durchgeführt. Die Reaktionsansätze von 1 ml enthielten 100 mM Kaliumphosphatpuffer (pH 7,5), 5mM MgCI2, 100 //M Acetyl CoA, 5mM L-Homoserine, 500 μM DTNB (Ellmans Reagenz)
und Zellextrakt. Der Test wurde durch Zugabe von dem jeweiligen Proteinlysat gestar¬ tet und bei Raumtemperatur inkubiert. Es wurde dann eine Kinetik bei 412 nm über 10 min aufgenommen.The measurement of the enzymatic activity of MetA was carried out as follows. Reactions of 1 ml contained 100 mM potassium phosphate buffer (pH 7.5), 5 mM MgCl 2, 100 mM acetyl CoA, 5 mM L-homoserines, 500 μM DTNB (Ellman's reagent). and cell extract. The test was started by addition of the respective protein lysate and incubated at room temperature. Kinetics were then recorded at 412 nm for 10 min.
Die Ergebnisse sind in Tabelle 4 gezeigt.The results are shown in Table 4.
Tabelle 4Table 4
Die Aktivität von MetA konnte durch die Verwendung der heterologen Expressionsein¬ heit PEF.TS erheblich gesteigert werden.
The activity of MetA could be improved by the use of the heterologous expression unit P EF . TS are significantly increased.