RU2723548C1 - Method of producing high-octane additive by hydrogenation of furfural and furfuryl alcohol - Google Patents
Method of producing high-octane additive by hydrogenation of furfural and furfuryl alcohol Download PDFInfo
- Publication number
- RU2723548C1 RU2723548C1 RU2019144465A RU2019144465A RU2723548C1 RU 2723548 C1 RU2723548 C1 RU 2723548C1 RU 2019144465 A RU2019144465 A RU 2019144465A RU 2019144465 A RU2019144465 A RU 2019144465A RU 2723548 C1 RU2723548 C1 RU 2723548C1
- Authority
- RU
- Russia
- Prior art keywords
- furfural
- methylfuran
- furfuryl alcohol
- hydrogenation
- catalyst
- Prior art date
Links
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J37/00—Processes, in general, for preparing catalysts; Processes, in general, for activation of catalysts
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/02—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings
- C07D307/34—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D307/36—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with only hydrogen atoms or radicals containing only hydrogen and carbon atoms, directly attached to ring carbon atoms
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Catalysts (AREA)
Abstract
Description
Изобретение относится к области разработки способа получения высокооктановой добавки - 2-метилфурана путем гидрирования фурфурола и/или фурфурилового спирта.The invention relates to the field of development of a method for producing high-octane additives - 2-methylfuran by hydrogenation of furfural and / or furfuryl alcohol.
При мировом производстве 300 тыс. тонн/г фурфурол является исходным сырьем для получения многих химических веществ. Одним из наиболее распространенных продуктов переработки фурфурола методом селективного гидрирования является фурфуриловый спирт.With world production of 300 thousand tons / g, furfural is the feedstock for many chemicals. One of the most common products of furfural processing by selective hydrogenation is furfuryl alcohol.
В последнее время фурановые производные рассматриваются как альтернативное «био»-сырье с широким спектром использования. Одним из компонентов, получаемых при гидрировании фурфурола или фурфурилового спирта может быть 2-метилфуран (метилфуран, сильван), который образуется при гидрогенолизе гидроксильной группы фурфурилового спирта или альдегидной группы фурфурола.Recently, furan derivatives are considered as an alternative “bio” raw material with a wide range of uses. One of the components obtained by hydrogenation of furfural or furfuryl alcohol can be 2-methylfuran (methylfuran, sylvan), which is formed during the hydrogenolysis of the hydroxyl group of furfuryl alcohol or the aldehyde group of furfural.
Сильван уже нашел широкое применение в качестве растворителя и в производстве противомалярийных препаратов (хлорохин), N- и S- гетероциклов и функционально замещенных алифатических соединений. Поскольку электронодонорная метальная группа метилфурана увеличивает реакционную способность фуранового кольца, то в положении 5 оно легко алкилируется и позволяет использовать его в качестве исходного сырья для создания длинных углеводородных цепей при производстве дизельного или реактивного топлива.Sylvan has already found widespread use as a solvent in the manufacture of antimalarial drugs (chloroquine), N- and S-heterocycles, and functionally substituted aliphatic compounds. Since the electron-donating methyl group of methylfuran increases the reactivity of the furan ring, in position 5 it is easily alkylated and allows it to be used as a feedstock to create long hydrocarbon chains in the production of diesel or jet fuel.
К тому же метилфуран рассматривается в качестве перспективной высокооктановой добавки к бензину [ЕР 0082689, C10L 1/02, 17.12.1982], поскольку имеет сопоставимые значения по химмотологическим свойствам с традиционным бензином, при этом его производство является возобновляемым, а применение в смеси с ископаемым топливом позволяет снизить количество выбросов в атмосферу.In addition, methylfuran is considered as a promising high-octane additive to gasoline [EP 0082689,
В патенте [ЕР 0082689, C10L 1/02, 17.12.1982] используется бензин с исследовательским октановым числом выше 85, подходящим для использования в двигателях внутреннего сгорания. Результаты показали, что добавление 10 об. % 2-метилфурана повышает исследовательское октановое число бензина, содержащего олефины с 92,7 до 96,3 пунктов.In the patent [EP 0082689,
Традиционные способы приготовления катализаторов получения метилфурана в процессе гидрирования водородом включают в себя использование в качестве прекурсоров соединения меди и хрома.Conventional methods for preparing methylfuran production catalysts during hydrogenation with hydrogen include the use of copper and chromium compounds as precursors.
Промьшшенный газофазный процесс, осуществляется путем подачи фурфурола в систему испарителя при 120°С, с последующим гидрированием газообразного фурфурола водородом на CuCr катализаторах и конденсацией получаемого фурфурилового спирта с последующим повышением температуры реакции от 120°С (температура производства фурфурилового спирта) до 250°С, что позволяет получить 2-метилфуран с выходом до 90%.An advanced gas-phase process is carried out by feeding furfural to the evaporator system at 120 ° С, followed by hydrogenation of furfural gas with hydrogen on CuCr catalysts and condensation of the resulting furfuryl alcohol with a subsequent increase in the reaction temperature from 120 ° С (furfuryl alcohol production temperature) to 250 ° С, which allows to obtain 2-methylfuran with a yield of up to 90%.
В патенте 1948 года [US 2456187, С07С 29/145, 14.12.1948] гидрирование фурфурола ос уществляли при температуре 170°С и давлении 0,4 МПа с о скоростью подачи фурфурола 90 л/час с использованием чистой меди, полученной восстановлением оксида меди при 140°С. Конверсия составила 100%, выход 2-метилфурана - 40%, выход фурфурилового спирта - 60%. При более низкой температуре (140°С) метилфуран не образовывался. В случае, если в качестве исходного сырья использовался фурфуриловый спирт вместо фурфурола, наблюдалась его полная конверсия в метилфуран при 170°С.In the 1948 patent [US 2456187, С07С 29/145, 12/14/1948] furfural was hydrogenated at a temperature of 170 ° C and a pressure of 0.4 MPa with a furfural feed rate of 90 l / h using pure copper obtained by reduction of copper oxide at 140 ° C. The conversion was 100%, the yield of 2-methylfuran was 40%, the yield of furfuryl alcohol was 60%. At a lower temperature (140 ° C), methylfuran did not form. If furfuryl alcohol was used as the feedstock instead of furfural, its complete conversion to methylfuran at 170 ° C was observed.
Manly с соавт. [D.G. Manly, А.Р. Dunlop, Catalytic Hydrogenation. I. Kinetics and Catalyst Composition in the Preparation of 2-Methylfuran, The Journal of Organic Chemistry, 23 (1958) 1093-1095] для жидкофазного процесса использовали способ модификации хромита меди оксидом кальция по методу Адкинса [R. Connor, K. Folkers, Н. Adkins, The preparation of copper-chromium oxide catalysts for hydrogenation, Journal of the American Chemical Society, 54 (1932) 1138-1145.]. Катализатор CuO(46%)-Cr2O3(50%)-CaO(4%) позволил получить 93,1% метилфурана в гидрировании фурфурола при температуре 200°С.Manly et al. [DG Manly, A.R. Dunlop, Catalytic Hydrogenation. I. Kinetics and Catalyst Composition in the Preparation of 2-Methylfuran, The Journal of Organic Chemistry, 23 (1958) 1093-1095] for the liquid-phase process used the method of modifying copper chromite with calcium oxide according to the Adkins method [R. Connor, K. Folkers, N. Adkins, The preparation of copper-chromium oxide catalysts for hydrogenation, Journal of the American Chemical Society, 54 (1932) 1138-1145.]. The CuO catalyst (46%) - Cr 2 O 3 (50%) - CaO (4%) allowed to obtain 93.1% methylfuran in the hydrogenation of furfural at a temperature of 200 ° C.
При температуре 250°С, объемной скорости фурфурола 0,13 ч-1, соотношении водород/альдегид равном 7,8, продолжительности эксперимента 5,5 часа с использованием катализатора с атомным соотношением Cu:Cr:Mg равным 1:1,05:0,04 [J.G.M. Bremner, R.K.F. Keeys, 202. The hydrogenation of furfuraldehyde to furfuryl alcohol and sylvan (2-methylfuran), Journal of the Chemical Society (Resumed), (1947) 1068-1080] наблюдалось образование до 87% сильвана.At a temperature of 250 ° C, a furfural volumetric rate of 0.13 h -1 , a hydrogen / aldehyde ratio of 7.8, an experiment duration of 5.5 hours using a catalyst with a Cu: Cr: Mg atomic ratio of 1: 1.05: 0 04 [JGM Bremner, RKF Keeys, 202. The hydrogenation of furfuraldehyde to furfuryl alcohol and sylvan (2-methylfuran), Journal of the Chemical Society (Resumed), (1947) 1068-1080], up to 87% sylvan was observed.
В газофазных реакциях метилфуран можно получить с выходом до 69,7% с использованием катализатора CuO(46,9%)-Cr2O3(46%)-MnO2(3,3%)-BaCrO4(3,6%) [US 6479677, C07D 307/06, 12.11.2002], полученного по методу Адкинса при проведении гидрирования фурфурола при температуре 175°С, скорость подачи газовой смеси фурфурол-водород составила 1,5 мл/мин, мольное соотношение водород к фурфуролу равнялось 2.In gas-phase reactions, methylfuran can be obtained with a yield of up to 69.7% using the catalyst CuO (46.9%) - Cr 2 O 3 (46%) - MnO 2 (3.3%) - BaCrO 4 (3.6%) [US 6479677, C07D 307/06, 11/12/2002], obtained by the Adkins method for hydrogenation of furfural at a temperature of 175 ° C, the feed rate of the furfural-hydrogen gas mixture was 1.5 ml / min, the molar ratio of hydrogen to furfural was 2 .
В гидрировании фурфурилового спирта при 200°С, скорости подачи водорода 20 л/час и скорости подачи фурфурола 0,5 моль/час было получено 80% метилфурана с использованием Fe(10%)-Cu(90%) катализатора [R.M. Lukes, C.L. Wilson, Reactions of Furan Compounds. XI. Side Chain Reactions of Furfural and Furfuryl Alcohol over Nickel-Copper and Iron-Copper Catalysts 1, Journal of the American Chemical Society, 73 (1951) 4790-4794].In the hydrogenation of furfuryl alcohol at 200 ° C, a hydrogen feed rate of 20 l / h and a furfural feed rate of 0.5 mol / h, 80% methylfuran was obtained using Fe (10%) - Cu (90%) catalyst [R.M. Lukes, C.L. Wilson, Reactions of Furan Compounds. Xi. Side Chain Reactions of Furfural and Furfuryl Alcohol over Nickel-Copper and Iron-
Метилфуран с 87% выходом был получен с использованием коммерческого катализатора Cu(59):Zn(33):Al(6):Ca(1):Na(1) (атомное соотношение), восстановленного при 270°С, [H.-Y. Zheng, Y.-L. Zhu, В.-Т. Teng, Z.-Q. Bai, C.-H. Zhang, H.-W. Xiang, Y.-W. Li, Towards understanding the reaction pathway in vapour phase hydrogenation of furfural to 2-methylfuran, Journal of Molecular Catalysis A: Chemical, 246 (2006) 18-23] при гидрировании фурфурола. В реакции использовалось давление 0,1 МПа, нагрузка на катализатор 0,3 ч-1, мольное соотношение водорода к фурфуролу равное 25 и температура процесса 250°С. При тех же условиях, но с использованием фурфурилового спирта в качестве реагента выход 2-метилфурана составил 92,7%.Methylfuran in 87% yield was obtained using a commercial catalyst Cu (59): Zn (33): Al (6): Ca (1): Na (1) (atomic ratio), reduced at 270 ° C, [H.- Y. Zheng, Y.-L. Zhu, V.-T. Teng, Z.-Q. Bai, C.-H. Zhang, H.-W. Xiang, Y.-W. Li, Towards understanding the reaction pathway in vapour phase hydrogenation of furfural to 2-methylfuran, Journal of Molecular Catalysis A: Chemical, 246 (2006) 18-23] in the hydrogenation of furfural. The reaction used a pressure of 0.1 MPa, a catalyst load of 0.3 h −1 , a molar ratio of hydrogen to furfural equal to 25, and a process temperature of 250 ° C. Under the same conditions, but using furfuryl alcohol as a reagent, the yield of 2-methylfuran was 92.7%.
Однако стоит отметить, что рассмотренные катализаторы дезактивируются в условиях процесса. Одними из основных причин дезактивации катализаторов на основе меди и хрома в процессе гидрирования фурфурола являются образование коксовых отложений, сильная адсорбция продуктов реакции на поверхности катализатора, изменение степени окисления активных центров и спекание частиц металла. Кроме того, соединения на основе хрома токсичны, что является еще одним фактором для отказа от их использования в конверсии фурфурола.However, it is worth noting that the considered catalysts are deactivated under process conditions. One of the main reasons for the deactivation of copper and chromium catalysts during furfural hydrogenation is the formation of coke deposits, strong adsorption of reaction products on the catalyst surface, change in the oxidation state of active centers and sintering of metal particles. In addition, chromium-based compounds are toxic, which is another factor for not using them in furfural conversion.
Способы приготовления катализаторов на основе благородных металлов позволяют получить каталитические системы, лишенные недостатков катализаторов на основе меди. Однако благородные металлы менее селективны в образовании 2-метилфурана, и зачастую приводят к образованию фурфурилового спирта или продуктов гидрирования фуранового кольца. В работе [С. Nguyen-Huy, J.S. Kim, S. Yoon, E. Yang, J.H. Kwak, M.S. Lee, K. An, Supported Pd nanoparticle catalysts with high activities and selectivities in liquid-phase furfural hydrogenation, Fuel 226 (2018) 607-617] в результате проведения реакции в реакторе высокого давления из нержавеющей стали на 100 мл, содержащего 1 г фурфурола и 20 мл изопропанола при давлении водорода 2 МПа, температуре реактора 180°С и со скоростью перемешивания 600 об/мин в течение 5 часов было установлено, что нанесенный на углерод образец Pd(5%)/C приводит к образованию лишь 44% 2-метилфурана.Methods for preparing noble metal catalysts make it possible to obtain catalyst systems devoid of the disadvantages of copper based catalysts. However, noble metals are less selective in the formation of 2-methylfuran, and often lead to the formation of furfuryl alcohol or hydrogenation products of the furan ring. In the work [S. Nguyen-Huy, J.S. Kim, S. Yoon, E. Yang, J.H. Kwak, M.S. Lee, K. An, Supported Pd nanoparticle catalysts with high activities and selectivities in liquid-phase furfural hydrogenation, Fuel 226 (2018) 607-617] by reaction in a 100 ml stainless steel high pressure reactor containing 1 g furfural and 20 ml of isopropanol at a hydrogen pressure of 2 MPa, a reactor temperature of 180 ° C and a stirring speed of 600 rpm for 5 hours, it was found that a Pd (5%) / C sample deposited on carbon leads to the formation of only 44% 2- methylfuran.
В то же время было показано, что Pd, нанесенный на другие носители, не образует 2-метилфуран даже в малых количествах. Подобное поведение катализаторов на основе Pt и Ru наблюдалось в работе [Е. Makela, R. Lahti, S. Jaatinen, Н. Romar, Т. Hu, R.L. Риигипеп, U. Lassi, R. Karinen, Study of Ni, Pt, and Ru Catalysts on Wood-based Activated Carbon Supports and their Activity in Furfural Conversion to 2-Methylfuran, ChemCatChem, 10 (2018) 3269-3283]. Было обнаружено, что максимальный выход 2-метилфурана при гидрировании фурфурола при 230°С и давлении 4 МПа на катализаторах Pt(3%)/C и Ru(3%)/C составил 48% и 40%, соответственно.At the same time, it was shown that Pd, supported on other carriers, does not form 2-methylfuran even in small amounts. A similar behavior of catalysts based on Pt and Ru was observed in [E. Makela, R. Lahti, S. Jaatinen, H. Romar, T. Hu, R.L. Riigipep, U. Lassi, R. Karinen, Study of Ni, Pt, and Ru Catalysts on Wood-based Activated Carbon Supports and their Activity in Furfural Conversion to 2-Methylfuran, ChemCatChem, 10 (2018) 3269-3283]. It was found that the maximum yield of 2-methylfuran upon hydrogenation of furfural at 230 ° C and a pressure of 4 MPa on Pt (3%) / C and Ru (3%) / C catalysts was 48% and 40%, respectively.
Таким образом, использование катализаторов на основе благородных металлов малоэффективно для производства сильвана. Кроме того, высокая стоимость благородных металлов делает применение этих каталитических систем менее экономически целесообразным.Thus, the use of noble metal catalysts is ineffective for the production of sylvan. In addition, the high cost of precious metals makes the use of these catalytic systems less economically feasible.
В последнее время для получения 2-метилфурана разрабатываются безхромные катализаторы на основе переходных металлов. Полученные такими способами катализаторы имеют низкую стоимость, хорошую каталитическую активность и низкую токсичность. Так, жидкофазное гидрирование фурфурола до 2-метилфурана при 230°С и давлении водорода 4 МПа позволяет получить до 48,9% 2-метилфурана при использовании Ni(10%)/C катализатора [S.K. Jaatinen, R.S. Karinen, J.S. Lehtonen, Liquid Phase Furfural Hydrotreatment to 2-Methylfuran with Carbon Supported Copper, Nickel, and Iron Catalysts, ChemistrySelect, 2 (2017) 51-60].Recently, chromium-free transition metal catalysts have been developed to produce 2-methylfuran. The catalysts obtained by such methods have a low cost, good catalytic activity and low toxicity. Thus, liquid-phase hydrogenation of furfural to 2-methylfuran at 230 ° C and a hydrogen pressure of 4 MPa allows to obtain up to 48.9% of 2-methylfuran using a Ni (10%) / C catalyst [S.K. Jaatinen, R.S. Karinen, J.S. Lehtonen, Liquid Phase Furfural Hydrotreatment to 2-Methylfuran with Carbon Supported Copper, Nickel, and Iron Catalysts, ChemistrySelect, 2 (2017) 51-60].
Гидрирование 10% раствора фурфурола в изопропаноле в интервале температур 100-200°С и давлении водорода 6 МПа изучалось в работе [А.А. Смирнов, И.Н. Шилов, М.В. Алексеева, С.А. Селищева, В.А. Яковлев, Исследование влияние состава модифицированных молибденом NiCu-содержащих катализаторов на их активность и селективность в гидрировании фурфурола с получением различных ценных химических веществ, Катализ в промышленности, 17 (2017) 517-526] с использованием золь-гель катализаторов на основе Ni, полученных золь-гель методом. Хотя выход 2-метилфурана не превышал 45% даже при температуре 200°С, было обнаружено, что введение в катализатор молибдена приводит к образованию никель-молибденовых сплавов, которые увеличивают выход сильвана в условиях жидкофазного гидрирования фурфурола.Hydrogenation of a 10% solution of furfural in isopropanol in the temperature range of 100-200 ° C and a hydrogen pressure of 6 MPa was studied in [A.A. Smirnov, I.N. Shilov, M.V. Alekseeva, S.A. Selishcheva, V.A. Yakovlev, Investigation of the effect of the composition of molybdenum-modified NiCu-containing catalysts on their activity and selectivity in the hydrogenation of furfural to produce various valuable chemicals, Industrial Catalysis, 17 (2017) 517-526] using sol-gel Ni-based catalysts prepared by sol gel method. Although the yield of 2-methylfuran did not exceed 45% even at a temperature of 200 ° C, it was found that the introduction of molybdenum into the catalyst leads to the formation of nickel-molybdenum alloys, which increase the yield of sylvan in the conditions of liquid-phase hydrogenation of furfural.
Влияние состава нанопористых сплавов Cu-Al-Со было изучено в газофазном гидрировании фурфурола [G.S. Hutchings, W. Luc, Q. Lu, Y. Zhou, D.G. Vlachos, F. Jiao, Nanoporous Cu-Al-Со Alloys for Selective Furfural Hydrodeoxygenation to 2-Methylfuran, Industrial & Engineering Chemistry Research, 56 (2017) 3866-3872]. Показано, что, несмотря на слабую дезактивацию катализатора, связанную с коксованием, была достигнута общая конверсия фурфурола 98,2% с выходом 2-метилфурана 64,9% при 240°С с использованием нанопористого катализатора Cu-Al-Со с содержанием кобальта приблизительно 5%.The effect of the composition of nanoporous Cu-Al-Co alloys was studied in the gas-phase hydrogenation of furfural [G.S. Hutchings, W. Luc, Q. Lu, Y. Zhou, D.G. Vlachos, F. Jiao, Nanoporous Cu-Al-Co Alloys for Selective Furfural Hydrodeoxygenation to 2-Methylfuran, Industrial & Engineering Chemistry Research, 56 (2017) 3866-3872]. It was shown that, despite weak catalyst deactivation associated with coking, a total conversion of furfural of 98.2% was achieved with a yield of 2-methylfuran of 64.9% at 240 ° C using a Cu-Al-Co nanoporous catalyst with a cobalt content of approximately 5 %
Выход сильвана, равный 78%, был получен при гидрировании фурфурола при 220°С и 4,0 МПа над катализатором Cu-Co, полученным методом пропитки оксида алюминия растворами нитратов соответствующих металлов [S. Srivastava, G.C. Jadeja, J. Parikh, A versatile bi-metallic copper-cobalt catalyst for liquid phase hydrogenation of furfural to 2-methylfuran, RSC Advances, 6 (2016) 1649-1658]. Однако такой катализатор привел к низким значениям выходов 2-метилфурана при повторном использовании.The sylvan yield of 78% was obtained by hydrogenation of furfural at 220 ° C and 4.0 MPa over a Cu-Co catalyst obtained by impregnating alumina with solutions of nitrates of the corresponding metals [S. Srivastava, G.C. Jadeja, J. Parikh, A versatile bi-metallic copper-cobalt catalyst for liquid phase hydrogenation of furfural to 2-methylfuran, RSC Advances, 6 (2016) 1649-1658]. However, such a catalyst resulted in low yields of 2-methylfuran when reused.
В последнее время стали популярными катализаторы на основе карбида молибдена. Важной особенностью этих катализаторов является их способность гидрогенизировать спиртовые и карбонильные группы без восстановления ненасыщенных углеродных связей и ароматических систем.Recently, molybdenum carbide catalysts have become popular. An important feature of these catalysts is their ability to hydrogenate alcohol and carbonyl groups without reducing unsaturated carbon bonds and aromatic systems.
Наиболее близким по своей технической сущности к заявляемому способу получения 2-метилфурана является способ селективного гидрирования фурфурола, описанный в работе [K. Xiong, W.-S. Lee, A. Bhan, J.G. Chen, Molybdenum Carbide as a Highly Selective Deoxygenation Catalyst for Converting Furfural to 2-Memylfuran, 7 (2014) 2146-2149]. Селективное гидрирование фурфурола проводилось в проточном кварцевом реакторе (внутренний диаметр 10 мм) при атмосферном давлении с использованием 0,64 г Мо2С катализатора фракцией 0,42-0,177 мм. Температура реакции составляла 150°С. Перед реакцией катализатор обрабатывали водородом с общей скоростью потока 60 мл/мин при 477°С в течение 1 ч (со скоростью нагрева 0,185°С/с от комнатной температуры). Затем температуру реактора охлаждали до 150°С и поток газа переключали с чистого Н2 на реакционную смесь (1,67 см3/с), состоящую из 0,24/2,50/97,26 об. % фурфурола, CH4, и Н2. Данный катализатор позволяет достичь 60% селективности по образованию 2-метилфурана. Начальная степень конверсии фурфурола 87%, выход 2-метилфурана 83%.Closest in technical essence to the claimed method for producing 2-methylfuran is the method of selective hydrogenation of furfural, described in [K. Xiong, W.-S. Lee, A. Bhan, JG Chen, Molybdenum Carbide as a Highly Selective Deoxygenation Catalyst for Converting Furfural to 2-Memylfuran, 7 (2014) 2146-2149]. Selective hydrogenation of furfural was carried out in a flowing quartz reactor (internal diameter 10 mm) at atmospheric pressure using 0.64 g of Mo 2 C catalyst with a fraction of 0.42-0.177 mm. The reaction temperature was 150 ° C. Before the reaction, the catalyst was treated with hydrogen with a total flow rate of 60 ml / min at 477 ° C for 1 h (with a heating rate of 0.185 ° C / s from room temperature). Then the temperature of the reactor was cooled to 150 ° C and the gas flow was switched from pure H 2 to the reaction mixture (1.67 cm 3 / s), consisting of 0.24 / 2.50 / 97.26 vol. % furfural, CH 4 , and H 2 . This catalyst allows to achieve 60% selectivity for the formation of 2-methylfuran. The initial degree of furfural conversion is 87%, the yield of 2-methylfuran is 83%.
Общим недостатком для прототипа и всех вышеперечисленных способов получения 2-метилфурана является то, что при их использовании не удается достичь высокого выхода фурфурилового спирта, и, кроме того, наблюдается снижение активности катализатора за счет образования углеродных отложений на его поверхности.A common disadvantage for the prototype and all of the above methods for producing 2-methylfuran is that when using them it is not possible to achieve a high yield of furfuryl alcohol, and, in addition, a decrease in the activity of the catalyst due to the formation of carbon deposits on its surface is observed.
Технической проблемой, на решение которой направлено заявляемое изобретение, является разработка высокопроизводительного способа получения 2-метилфурана путем селективного гидрирования фурфурола и/или фурфурилового спирта, позволяющего достичь высоких значений конверсии исходного сырья и выхода 2-метилфурана.The technical problem to which the claimed invention is directed is the development of a high-performance method for producing 2-methylfuran by selective hydrogenation of furfural and / or furfuryl alcohol, which allows to achieve high values of the conversion of the feedstock and the yield of 2-methylfuran.
Технический результат - получение 2-метилфурана с выходом свыше 90% при селективном гидрировании фурфурола и/или фурфурилового спирта, как в случае проведения процесса в периодическом режиме, так и в случае проведения процесса в проточной установке без использования растворителя.EFFECT: obtaining 2-methylfuran with a yield of over 90% by selective hydrogenation of furfural and / or furfuryl alcohol, both in the case of a process in a batch mode and in the case of a process in a flow unit without using a solvent.
Задача решается способом получения 2-метилфурана путем гидрирования фурфурола и/или фурфурилового спирта в присутствии катализатора, содержащего карбид молибдена, причем катализатор содержит 15 мас. % активного компонента в виде молибдена в карбидной форме, модифицированного металлическим никелем с мольным соотношением Ni/Mo от 0,1 до 0,5, остальное - углеродный носитель типа Сибунит, Гидрирование проводят на установке периодического действия при температуре 150°С, давлении водорода 6,0 МПа, скорости перемешивания 1800 об/мин, времени реакции 4 ч с использованием раствора с объемным содержанием фурфурола или фурфурилового спирта в изопропаноле 3,5 об. % или на установке проточного типа в отсутствии растворителя при температуре 160-200°С, давлении водорода 5,0 МПа, скорости подачи сырья 3-6 мл/ч и объемной скорости водорода 300-600 мл/мин в присутствии указанного катализатора.The problem is solved by the method of producing 2-methylfuran by hydrogenation of furfural and / or furfuryl alcohol in the presence of a catalyst containing molybdenum carbide, and the catalyst contains 15 wt. % of the active component in the form of molybdenum in carbide form, modified with metallic nickel with a Ni / Mo molar ratio of 0.1 to 0.5, the rest is a carbon carrier of the Sibunit type. Hydrogenation is carried out on a batch unit at a temperature of 150 ° C, a hydrogen pressure of 6 , 0 MPa, stirring speed 1800 rpm, reaction time 4 hours using a solution with a volumetric content of furfural or furfuryl alcohol in isopropanol 3.5 vol. % or in a flow-type installation in the absence of a solvent at a temperature of 160-200 ° C, a hydrogen pressure of 5.0 MPa, a feed rate of 3-6 ml / h and a volumetric hydrogen rate of 300-600 ml / min in the presence of said catalyst.
Для получения 2-метилфурана используемый катализатор перед проведением селективного гидрирования фурфурола и/или фурфурилового спирта восстанавливают в токе водорода, подаваемого со скоростью 100 мл/мин, при температуре 350°С, давлении 0,1 МПа в течение 1 часа.To obtain 2-methylfuran, the used catalyst before reducing the selective hydrogenation of furfural and / or furfuryl alcohol is reduced in a stream of hydrogen supplied at a rate of 100 ml / min, at a temperature of 350 ° C, a pressure of 0.1 MPa for 1 hour.
Отличиями предлагаемого способа получения 2-метилфурана по сравнению с прототипом является то, что в качестве исходного реагента может быть использован фурфуриловый спирт, а процесс селективного гидрирования можно проводить в двух режимах: в периодическом режиме при температуре 150-200°С, давлении 6,0 МПа с использованием растворителя либо в проточном жидкофазном режиме при температуре 160-200°С, давлении 5,0 МПа, скорости подачи фурфурола 3-6 мл/ч, скорости подачи водорода 300-600 мл/мин в присутствии 3 мл катализатора фракцией 0,25-0,5 мм, содержащего 15 мас. % активного компонента, представляющего собой молибден в карбидной форме, модифицированный металлическим никелем с мольным соотношением Ni/Mo от 0,1 до 0,5 и 85 мас. % носитель - углеродный носитель типа Сибунит.The differences of the proposed method for producing 2-methylfuran in comparison with the prototype is that furfuryl alcohol can be used as the initial reagent, and the selective hydrogenation process can be carried out in two modes: in a batch mode at a temperature of 150-200 ° C, a pressure of 6.0 MPa using a solvent or in a flowing liquid-phase mode at a temperature of 160-200 ° C, a pressure of 5.0 MPa, a feed rate of furfural of 3-6 ml / h, a feed rate of hydrogen of 300-600 ml / min in the presence of 3 ml of catalyst fraction 0, 25-0.5 mm containing 15 wt. % of the active component, which is molybdenum in carbide form, modified with metallic nickel with a molar ratio of Ni / Mo from 0.1 to 0.5 and 85 wt. % carrier is a carbon carrier of the Sibunit type.
Технический результат предлагаемого способа получения 2-метилфурана путем селективного гидрирования фурфурола и/или фурфурилового спирта обеспечивается следующим:The technical result of the proposed method for producing 2-methylfuran by selective hydrogenation of furfural and / or furfuryl alcohol is provided by the following:
1. Высокая селективность в образовании 2-метилфурана обеспечивается наличием в составе катализатора для селективного гидрирования фурфурола/фурфурилового спирта, двух типов карбида молибдена: кубической fcc-MoC1-x и гексагональной hcp-Mo2C формы карбида молибдена. Такой химический состав карбида молибдена формируется после прокалки исходного образца в токе аргона при температуре 400°С за счет взаимодействия оксидной формы молибдена с источником углерода - лимонной кислотой, а также за счет влияния углеродного носителя. Наличие двух фаз карбида молибдена было подтверждено рентгенодифракционным анализом (фиг. 1)1. High selectivity in the formation of 2-methylfuran is ensured by the presence of two types of molybdenum carbide in the catalyst for selective hydrogenation of furfural / furfuryl alcohol: cubic fcc-MoC 1-x and hexagonal hcp-Mo 2 C form of molybdenum carbide. Such a chemical composition of molybdenum carbide is formed after calcining the initial sample in an argon stream at a temperature of 400 ° C due to the interaction of the oxide form of molybdenum with a carbon source - citric acid, and also due to the influence of a carbon carrier. The presence of two phases of molybdenum carbide was confirmed by x-ray diffraction analysis (Fig. 1)
На фиг. 1 показана рентгенограмма катализатора на основе карбида молибдена, модифицированного никелем и нанесенного на Сибунит.In FIG. 1 shows an X-ray diffraction pattern of a catalyst based on molybdenum carbide modified with nickel and deposited on Sibunit.
2. Высокая активность в гидрировании фурфурола/фурфурилового спирта обусловлена наличием в составе используемого для селективного гидрирования фурфурола/фурфурилового спирта катализатора монометаллических частиц никеля, при этом соблюдение мольного соотношения Ni/Mo от 0,1 до 0,5 обеспечивает оптимальное распределение частиц металлического никеля по поверхности карбида молибдена при восстановлении образца в водороде при 600°С, что приводит к синергетическому эффекту высокой активности никеля в реакциях гидрирования и высокой селективности карбида молибдена в образовании 2-метилфурана. Наличие металлического никеля было подтверждено методом рентгеновской фотоэлектронной спектроскопии. Распределение металлических частиц никеля на поверхности карбида молибдена и носителя по данным просвечивающей электронной микроскопии (ПЭМ) представлено на фиг. 2 (снимок ПЭМ катализатора на основе карбида молибдена, модифицированного никелем и нанесенного на Сибунит).2. The high activity in the hydrogenation of furfural / furfuryl alcohol is due to the presence of nickel monometallic particles in the composition used for selective hydrogenation of furfural / furfuryl alcohol, while observing a molar ratio of Ni / Mo from 0.1 to 0.5 ensures an optimal distribution of metallic nickel particles over the surface of molybdenum carbide upon reduction of the sample in hydrogen at 600 ° C, which leads to a synergistic effect of high nickel activity in hydrogenation reactions and high selectivity of molybdenum carbide in the formation of 2-methylfuran. The presence of metallic nickel was confirmed by x-ray photoelectron spectroscopy. The distribution of nickel metal particles on the surface of molybdenum carbide and the carrier according to transmission electron microscopy (TEM) is shown in FIG. 2 (TEM image of a nickel-modified molybdenum carbide catalyst deposited on Sibunit).
3. Использование Сибунита в качестве носителя 85 мас. % приводит к повышению общей поверхности карбидных катализаторов с 11 м2/г без носителя до 148-175 м2/г с использованием Сибунита, что также способствует повышению активности катализатора.3. The use of Sibunit as a carrier of 85 wt. % leads to an increase in the total surface of carbide catalysts from 11 m 2 / g without support to 148-175 m 2 / g using Sibunit, which also increases the activity of the catalyst.
Селективное гидрирование фурфурола/фурфурилового спирта проводят, в частности, на установке периодического действия при температуре 150-200°С, давлении 6,0 МПа, скорости перемешивания 1800 об/мин, времени реакции 4 ч, в присутствии 60 мл раствора с объемным содержанием фурфурол/фурфурилового спирта в изопропаноле 3,5 об. % в присутствии 1 г карбидного катализатора.Selective hydrogenation of furfural / furfuryl alcohol is carried out, in particular, at a batch unit at a temperature of 150-200 ° C, a pressure of 6.0 MPa, a stirring speed of 1800 rpm, a reaction time of 4 hours, in the presence of 60 ml of a solution with a volumetric content of furfural / furfuryl alcohol in isopropanol 3.5 vol. % in the presence of 1 g of carbide catalyst.
Селективное гидрирование также проводят на установке проточного типа при температуре 160-200°С, давлении 5,0 МПа, скорости подачи фурфурола/фурфурилового спирта 3-6 мл/ч, скорости подачи водорода 300-600 мл/мин в присутствии карбидного катализатора.Selective hydrogenation is also carried out on a flow-through installation at a temperature of 160-200 ° C, a pressure of 5.0 MPa, a feed rate of furfural / furfuryl alcohol of 3-6 ml / h, a hydrogen supply of 300-600 ml / min in the presence of a carbide catalyst.
Карбидный катализатор содержит 15 мас. % активного компонента, представляющего собой молибден в карбидной форме, модифицированный металлическим никелем с мольным соотношением Ni/Mo от 0,1 до 0,5; и 85 мас. % носитель - углеродный носитель типа Сибунит. Перед реакцией катализатор активируют в токе водорода, подаваемого со скоростью 100 мл/мин, при температуре 350°С в течение 1 часа, что приводит к дополнительному восстановлению металлических частиц никеля.The carbide catalyst contains 15 wt. % of the active component, which is molybdenum in carbide form, modified with metallic nickel with a molar ratio of Ni / Mo from 0.1 to 0.5; and 85 wt. % carrier is a carbon carrier of the Sibunit type. Before the reaction, the catalyst is activated in a stream of hydrogen supplied at a rate of 100 ml / min, at a temperature of 350 ° C for 1 hour, which leads to an additional reduction of metal particles of Nickel.
Пример 1.Example 1
Получение 2-метилфурана проводили в реакторе периодического действия (автоклаве) при постоянном давлении водорода 6 МПа и температуре 150°С, скорости перемешивания 1800 об/мин, времени реакции 4 ч, с использованием 60 мл раствора реагента с объемным содержанием фурфурола в изопропаноле 3,5 об. % в присутствии 1 г катализатора.The preparation of 2-methylfuran was carried out in a batch reactor (autoclave) at a constant hydrogen pressure of 6 MPa and a temperature of 150 ° C, a stirring speed of 1800 rpm, a reaction time of 4 hours, using 60 ml of a reagent solution with a volume content of furfural in isopropanol 3, 5 vol. % in the presence of 1 g of catalyst.
Для приготовления катализатора NiMoC/Сибунит требуемое количество молибдата аммония, нитрата никеля, лимонной кислоты и дистиллированной воды для обеспечения мольного соотношения Ni/Mo от 0,1 до 0,5 (мольное соотношение молибдена и никеля к количеству углерода в лимонной кислоте равно 1:1) интенсивно перемешивают при нагреве до 100°С до полного растворения компонентов. Доводят раствор до нужной концентрации дистиллированной водой. Полученным пропиточным раствором по влагоемкости пропитывают углеродный носитель - Сибунит, который затем сушат на воздухе при 100°С и прокаливают в токе Ar при 400°С (при этом осуществляется термический распад органической матрицы с образованием карбидных фаз). Полученный композит охлаждают в токе Ar, восстанавливают при 600°С в токе водорода, что приводит к образованию металлических частиц никеля, повторно охлаждают и пассивируют 1% O2 в аргоне при комнатной температуре. Перед реакцией катализатор восстанавливают в токе водорода при температуре 350°С в течение 1 ч со скоростью подачи водорода 300 мл/мин и давлении 0,1 МПа.To prepare the NiMoC / Sibunit catalyst, the required amount of ammonium molybdate, nickel nitrate, citric acid and distilled water to provide a Ni / Mo molar ratio of 0.1 to 0.5 (the molar ratio of molybdenum and nickel to carbon in the citric acid is 1: 1 ) are intensively mixed when heated to 100 ° C until the components are completely dissolved. Bring the solution to the desired concentration with distilled water. A carbon carrier, Sibunit, is impregnated with the obtained impregnation solution for moisture capacity, which is then dried in air at 100 ° C and calcined in a stream of Ar at 400 ° C (the thermal decomposition of the organic matrix is carried out with the formation of carbide phases). The resulting composite is cooled in a stream of Ar, reduced at 600 ° C in a stream of hydrogen, which leads to the formation of metallic particles of nickel, re-cooled and passivated with 1% O 2 in argon at room temperature. Before the reaction, the catalyst is reduced in a stream of hydrogen at a temperature of 350 ° C for 1 h with a flow rate of hydrogen of 300 ml / min and a pressure of 0.1 MPa.
Показатели процесса селективного гидрирования фурфурола при температуре процесса 150°С приведены в таблице 1. Состав катализаторов приведен без учета карбидного углерода и углерода, оставшегося после разложения лимонной кислоты.The performance of the selective hydrogenation of furfural at a process temperature of 150 ° C is shown in table 1. The composition of the catalysts is given without taking into account carbide carbon and carbon remaining after the decomposition of citric acid.
Оценить их содержание невозможно, поскольку невозможно определить точное соотношение кубической fcc-MoC1-x и гексагональной hcp-Мо2С форм молибдена, а также отличить свободный углерод от Сибунита. При расчете состава катализатора учитывалось количество металлов при пропитке и количество используемого носителя.It is impossible to evaluate their content, since it is impossible to determine the exact ratio of cubic fcc-MoC 1-x and hexagonal hcp-Mo 2 C forms of molybdenum, and to distinguish free carbon from Sibunit. When calculating the composition of the catalyst, the amount of metals impregnated and the amount of carrier used were taken into account.
Пример 2.Example 2
Аналогичен примеру 1. Катализатор содержит мольное соотношение Ni/Mo равное 1. Величина площади удельной поверхности по БЭТ составляет 181 м2/г. Однако выход 2-метилфурана составляет всего 63% с конверсией фурфурола близкой к 100%. Низкий выход 2-метилфурана обусловлен высоким содержанием металлического никеля, который способствует протеканию реакций гидрирования фуранового кольца с образованием тетрагидрофурфурилового спирта и метилтетрагидрофурана.Similar to example 1. The catalyst contains a molar ratio of Ni / Mo equal to 1. The specific surface area according to BET is 181 m 2 / year However, the yield of 2-methylfuran is only 63% with a furfural conversion close to 100%. The low yield of 2-methylfuran is due to the high content of metallic nickel, which promotes the hydrogenation of the furan ring to form tetrahydrofurfuryl alcohol and methyltetrahydrofuran.
Пример 3.Example 3
Аналогичен примеру 1. Катализатор содержит мольное соотношение Ni/Mo равное 0,1. Величина удельной поверхности смешанного оксида по БЭТ составляет 148 м2/г и средний размер пор 11 нм. Процесс гидрирования фурфурола проводился аналогично примеру 1, отличающийся температурой процесса 150-200°С. Результаты проведения процесса гидрирования фурфурола представлены в Таблице 2.Similar to example 1. The catalyst contains a molar ratio of Ni / Mo equal to 0.1. The BET specific surface area of the mixed oxide is 148 m 2 / g and the average pore size is 11 nm. The process of hydrogenation of furfural was carried out analogously to example 1, characterized by a process temperature of 150-200 ° C. The results of the process of hydrogenation of furfural are presented in Table 2.
При повышении температуры реакции появляются продукты гидрирования фуранового кольца с образованием метилтетрагидрофурана.With increasing reaction temperature, hydrogenation products of the furan ring appear with the formation of methyltetrahydrofuran.
Пример 4.Example 4
Аналогичен примеру 1. Катализатор содержит мольное соотношение Ni/Mo равное 0,1. Катализатор после реакции отделялся фильтрованием, промывался и использовался повторно в реакции гидрирования фурфурола при условиях согласно примеру 1. Конверсия фурфурола и выход 2-метилфурана после каждого повторного цикла представлены в таблице 3. Согласно полученным данным примененный катализатор обладает высокой стабильностью в условиях процесса и может быть использован повторно.Similar to example 1. The catalyst contains a molar ratio of Ni / Mo equal to 0.1. The catalyst after the reaction was separated by filtration, washed and reused in the hydrogenation reaction of furfural under the conditions according to example 1. The conversion of furfural and the yield of 2-methylfuran after each repeated cycle are presented in table 3. According to the data obtained, the used catalyst has high stability under process conditions and can be reused.
Пример 5.Example 5
Аналогичен примеру 1, отличающийся тем, что вместо фурфурола используется фурфуриловый спирт в исходном растворе. Катализатор содержит мольное соотношение Ni/Mo равное 0,1. Конверсия фурфурилового спирта составила 100%, а выход 2-метилфурана достиг 97,1%, что превышает выход 2-метилфурана при использовании фурфурола при тех же условиях. Вероятно, это связанно с тем, что фурфурол является более реакционноспособным по маршрутам гидрирования фуранового кольца, чем фурфуриловый спирт.Similar to example 1, characterized in that instead of furfural, furfuryl alcohol is used in the initial solution. The catalyst contains a molar ratio of Ni / Mo equal to 0.1. The conversion of furfuryl alcohol was 100%, and the yield of 2-methylfuran reached 97.1%, which exceeds the yield of 2-methylfuran when using furfural under the same conditions. This is probably due to the fact that furfural is more reactive along the hydrogenation routes of the furan ring than furfuryl alcohol.
Пример 6.Example 6
В качестве сравнения был приготовлен катализатор МоС без никеля, не содержащий носитель. Способ приготовления аналогичен примеру 1, но отсутствует стадия пропитки. Полученный раствор упаривают при 100°С до вязкого состояния. Сушат при 100°С в течение 24 часов. И подвергают термической обработке согласно примеру 1.As a comparison, a nickel-free MoC catalyst was prepared without a carrier. The preparation method is similar to example 1, but there is no stage of impregnation. The resulting solution was evaporated at 100 ° C to a viscous state. Dried at 100 ° C for 24 hours. And subjected to heat treatment according to example 1.
Удельная поверхность полученного катализатора составляет 11 м2/г. Процесс гидрирования фурфурола проводился согласно примеру 1. Конверсия фурфурола составила 3%, продуктом являлся фурфуриловый спирт.The specific surface area of the resulting catalyst is 11 m 2 / g. The process of hydrogenation of furfural was carried out according to example 1. The conversion of furfural was 3%, the product was furfuryl alcohol.
Пример 7.Example 7
В качестве сравнения был приготовлен нанесенный катализатор МоС/Сибунит без никеля. Способ приготовления аналогичен примеру 1, но отсутствует стадия введения нитрата никеля (мольное соотношение молибдена к углероду в лимонной кислоте соответствует 1:1). Удельная поверхность полученного катализатора составляет 11 м2/г. Процесс гидрирования фурфурола проводился согласно примеру 1. Полученный композит представляет собой смесь двух типов карбида молибдена кубической fcc-MoC1-x и гексагональной hcp-Мо2С формы. После 4 ч проведения процесса по аналогии с Примером 1 конверсия фурфурола составляет 11 мол. %, селективность образования 2-метилфурана - 98 мол. %, что подтверждает высокую селективность карбидных форм молибдена в образовании 2-метилфурана, но и свидетельствует о низкой активности карбид молибдена без металлических частиц никеля.As a comparison, a supported MoC / Sibunit catalyst without nickel was prepared. The preparation method is similar to example 1, but there is no stage of the introduction of nickel nitrate (the molar ratio of molybdenum to carbon in citric acid corresponds to 1: 1). The specific surface area of the resulting catalyst is 11 m 2 / g. The process of hydrogenation of furfural was carried out according to example 1. The resulting composite is a mixture of two types of molybdenum carbide cubic fcc-MoC 1-x and hexagonal hcp-Mo 2 C form. After 4 hours of carrying out the process, by analogy with Example 1, the conversion of furfural is 11 mol. %, the selectivity of the formation of 2-methylfuran - 98 mol. %, which confirms the high selectivity of the carbide forms of molybdenum in the formation of 2-methylfuran, but also indicates a low activity of molybdenum carbide without metal particles of nickel.
Пример 8.Example 8
Предварительно готовят катализатор по способу, аналогичному примеру 1. В результате получают катализатор Ni0.1MoC/Сибунит, содержащий 15 мас. % активного компонента, представляющего собой молибден в карбидной форме, модифицированный металлическим никелем с мольным соотношением Ni/Mo равным 0,1 и 85 мас. % носитель - углеродный носитель типа Сибунит.The catalyst is preliminarily prepared according to a method analogous to Example 1. The result is a Ni 0.1 MoC / Sibunit catalyst containing 15 wt. % of the active component, which is molybdenum in carbide form, modified with metallic nickel with a molar ratio of Ni / Mo equal to 0.1 and 85 wt. % carrier is a carbon carrier of the Sibunit type.
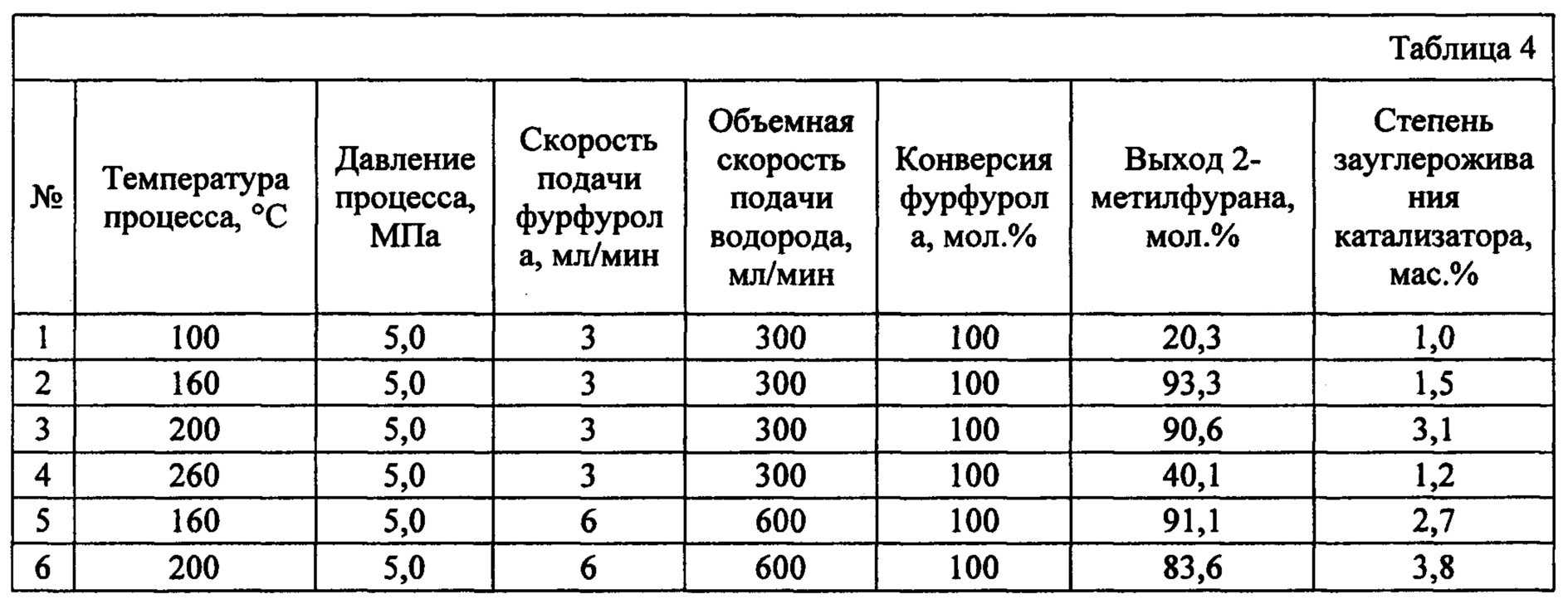
Процесс селективного гидрирования фурфурола проводят на установке проточного типа в отсутствии растворителя при температуре 100-260°С, давлении водорода 5,0 МПа, скорости подачи сырья 3-6 мл/ч и водорода 300-600 мл/мин, для соблюдения постоянного соотношения сырья к водороду, массе катализатора 1,7 г (3 мл, размер фракции 0,25-0,5 мм). Данные по выходу 2-метилфурана представлены в таблице 4. Перед реакцией катализатор восстанавливают аналогично примеру 1. Содержание углерода рассчитывалось как разница между исходным содержанием углерода в катализаторе и содержанием углерода после проведения реакции в течение 7 часов. Анализ углерода проводился с использованием CHNS-анализатора.The process of selective hydrogenation of furfural is carried out on a flow-through installation in the absence of solvent at a temperature of 100-260 ° C, a hydrogen pressure of 5.0 MPa, a feed rate of 3-6 ml / h and a hydrogen of 300-600 ml / min, to maintain a constant ratio of raw materials to hydrogen, the mass of the catalyst is 1.7 g (3 ml, fraction size 0.25-0.5 mm). The yield data of 2-methylfuran are presented in table 4. Before the reaction, the catalyst is reduced analogously to example 1. The carbon content was calculated as the difference between the initial carbon content in the catalyst and the carbon content after the reaction for 7 hours. Carbon analysis was performed using a CHNS analyzer.
Как видно из полученных данных оптимальными условиями получения 2-метилфурана является температуре 160-200°С, давлении водорода 5,0 МПа, скорости подачи сырья 3-6 мл/ч и водорода 300-600 мл/мин.As can be seen from the data obtained, the optimal conditions for the production of 2-methylfuran is a temperature of 160-200 ° C, a hydrogen pressure of 5.0 MPa, a feed rate of 3-6 ml / h and a hydrogen of 300-600 ml / min.
При повышении температуры процесса выше 200 градусов во время гидрирования фурфурола происходит целый ряд побочных процессов, в частности образование 2-метилтетрагидфурана как главного продукта, а также раскрытие фуранового кольца с появлением таких соединений как 1-пентанол, 2-пентанол и пентан. Также стоит отметить высокую стабильность катализатора, который не теряет своей активности в течение 7 часов работы, по сравнению с прототипом.When the process temperature rises above 200 degrees during the hydrogenation of furfural, a number of side processes occur, in particular the formation of 2-methyltetrahydrofuran as the main product, as well as the opening of the furan ring with the appearance of compounds such as 1-pentanol, 2-pentanol and pentane. It is also worth noting the high stability of the catalyst, which does not lose its activity during 7 hours of operation, compared with the prototype.
Пример 9.Example 9
Аналогичен примеру 8, отличающийся тем, что вместо фурфурола используется фурфуриловый спирт. Процесс селективного гидрирования фурфурилового спирта проводят на установке проточного типа в отсутствии растворителя при температуре 100-260°С, давлении водорода 5,0 МПа, скорости подачи сырья 3 мл/ч и водорода 300 мл/мин, массе катализатора 1,7 г (размер фракции 0,25-0,5 мм). Данные по гидрированию фурфурилового спирта представлены в таблице 5.Similar to example 8, characterized in that instead of furfural, furfuryl alcohol is used. The process of selective hydrogenation of furfuryl alcohol is carried out on a flow-through installation in the absence of solvent at a temperature of 100-260 ° C, a hydrogen pressure of 5.0 MPa, a feed rate of 3 ml / h and a hydrogen of 300 ml / min, a catalyst weight of 1.7 g (size fractions 0.25-0.5 mm). Data on the hydrogenation of furfuryl alcohol are presented in table 5.
В случае использования в качестве исходного сырья фурфурилового спирта выход 2-метилфурана ниже, чем при использовании фурфурола. Кроме того, наблюдается более высокое содержание углеродистых отложений. Вероятно, это связано с тем, что используемый фурфуриловый спирт при хранении полимеризуется и образующиеся полимерные молекулы блокируют активные центры катализатора, снижая выход 2-метилфурана.In the case of using furfuryl alcohol as the starting material, the yield of 2-methylfuran is lower than when using furfural. In addition, there is a higher content of carbon deposits. This is probably due to the fact that the used furfuryl alcohol polymerizes during storage and the resulting polymer molecules block the active sites of the catalyst, reducing the yield of 2-methylfuran.
Пример 10Example 10
Полученный 2-метилфуран может быть использован в качестве высокооктановой добавки (ВОД) для автомобильных топлив, в частности, бензина. В таблице 6 представлены данные о влиянии 2-метилфурана на химмотологические свойства бензинов, марок АИ-80 и АИ-92. Доля метилфурана может составлять от 1 до 15 об. % в бензине.The obtained 2-methylfuran can be used as a high-octane additive (WAT) for automotive fuels, in particular gasoline. Table 6 presents data on the effect of 2-methylfuran on the chemical properties of gasolines, grades AI-80 and AI-92. The proportion of methylfuran can be from 1 to 15 vol. % in gasoline.
Данные дистилляционных характеристик бензина и соответствующей смеси бензин и 2-метилфуран (2-МФ) приведены в таблице 6. Как видно, добавление 2-метилфурана к бензину АИ-92 не оказало значительного влияния на характеристики дистилляции, в то время как добавление 5 об. % 2-метилфурана к бензину АИ-80 позволило снизить максимальную температуру кипения с 215,30 до 159,53°С.The distillation characteristics of gasoline and the corresponding mixture of gasoline and 2-methylfuran (2-MF) are shown in Table 6. As can be seen, the addition of 2-methylfuran to AI-92 gasoline did not significantly affect the distillation characteristics, while the addition of 5 vol. % 2-methylfuran to AI-80 gasoline allowed to reduce the maximum boiling point from 215.30 to 159.53 ° С.
Анализ бензинов и смеси бензинов с 2-метилфураном на содержание моноароматики и полиароматики высокоэффективной жидкостной хроматографией на приборе Agilent 1260 согласно методике ASTM 6591-11 показало, что в составе АИ-80 топлива и его смесей с ВОД содержится 6-7% моноароматических соединений, тогда как бензин АИ-92 и его смеси с 2-метилфураном, содержат до 28,5% моноароматики. Несмотря на то, что 2-метилфуран имеет ароматическое кольцо, оно не относится к бензольному кольцу, а значит сильван имеет преимущества перед ВОД на основе бензольных колец, на содержание которых в топливе существует ограничение. Кроме того, стоит отметить, что метилфурана содержит в своем составе кислород, который способствует дожиганию углеводородов и СО, что способствует снижению этих вредных веществ в выхлопных газах, а значит делает топливо более экологичным.Analysis of gasolines and a mixture of gasolines with 2-methylfuran for the content of monoaromatics and polyaromatics by high-performance liquid chromatography on an Agilent 1260 instrument according to ASTM 6591-11 showed that AI-80 fuel and its mixtures with water contain 6-7% of monoaromatic compounds, then like AI-92 gasoline and its mixtures with 2-methylfuran, contain up to 28.5% of monoaromatics. Despite the fact that 2-methylfuran has an aromatic ring, it does not belong to the benzene ring, which means that sylvan has advantages over water based on benzene rings, the content of which in the fuel is limited. In addition, it is worth noting that methylfuran contains oxygen in its composition, which contributes to the afterburning of hydrocarbons and CO, which helps to reduce these harmful substances in the exhaust gases, which makes the fuel more environmentally friendly.
Значения октанового число по исследовательскому методу (ОЧИ) полученных смесей бензинов с 2-метилфураном определяли согласно ГОСТ 8226 на установке УИТ-65. Значения исследовательского октанового числа смешения рассчитывали из измеренных значений ОЧИ бензинов и смесей 2-метилфуран с бензином, используя формулу:The octane values according to the research method (OCI) of the obtained mixtures of gasoline with 2-methylfuran were determined according to GOST 8226 at the UIT-65 installation. The research octane mixing values were calculated from the measured values of the OCI of gasolines and mixtures of 2-methylfuran with gasoline using the formula:
где ОЧИсм - исследовательское октановое число смешения для высокооктановой добавки;where OCH cm - research octane mixing for high-octane additives;
ОЧИбензин+ВОД - исследовательское октановое число топлива, полученного при смешении бензина и высокооктановой добавки;OCHI gasoline + WATER - research octane number of fuel obtained by mixing gasoline and high-octane additives;
ОЧИбензина - исследовательское октановое число исходного бензина;OCHI gasoline - research octane of the source gasoline;
ωбензин и ωВОД - процентные содержания бензина и высокооктановой добавки в полученном бленде,ω gasoline and ω WATER - percentage of gasoline and high-octane additives in the resulting blend,
ВОД - высокооктановая добавка.WATER is a high octane additive.
Из полученных данных видно, что наилучшие результаты получаются при смешении низкооктанового бензина с 2-метилфураном, что позволяет повысить значения октанового числа на 7-8 пунктов. Вероятно, низкое влияние добавки на бензин АИ-92 обусловлено тем, что в нем уже содержатся ароматические добавки, влияние которых на свойства топлива гораздо сильнее влияния 2-метилфурана.From the data obtained, it is seen that the best results are obtained by mixing low-octane gasoline with 2-methylfuran, which makes it possible to increase the octane number by 7-8 points. Probably, the low effect of the additive on AI-92 gasoline is due to the fact that it already contains aromatic additives, the effect of which on the fuel properties is much stronger than the effect of 2-methylfuran.
Таким образом, как видно из приведенных примеров, предлагаемый способ получения 2-метилфурана путем селективного гидрирования фурфурола и/или фурфурилового спирта позволяет получать целевой продукт с высоким выходом (более 90 мол. %) в жидкофазном процессе как в присутствии растворителя, так и без использования растворителя, с высокой стабильностью катализатора к отложению углерода. Полученный 2-метилфуран может использоваться в качестве высокооктановой добавки для бензинов. Причем наиболее эффективен он для бензинов с низким начальным значением октанового числа.Thus, as can be seen from the above examples, the proposed method for producing 2-methylfuran by selective hydrogenation of furfural and / or furfuryl alcohol allows to obtain the target product with a high yield (more than 90 mol.%) In the liquid phase process both in the presence of a solvent and without using solvent, with high stability of the catalyst to carbon deposition. The resulting 2-methylfuran can be used as a high-octane gasoline additive. Moreover, it is most effective for gasolines with a low initial value of the octane number.
Claims (2)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2019144465A RU2723548C1 (en) | 2019-12-27 | 2019-12-27 | Method of producing high-octane additive by hydrogenation of furfural and furfuryl alcohol |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2019144465A RU2723548C1 (en) | 2019-12-27 | 2019-12-27 | Method of producing high-octane additive by hydrogenation of furfural and furfuryl alcohol |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2723548C1 true RU2723548C1 (en) | 2020-06-16 |
Family
ID=71095948
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2019144465A RU2723548C1 (en) | 2019-12-27 | 2019-12-27 | Method of producing high-octane additive by hydrogenation of furfural and furfuryl alcohol |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2723548C1 (en) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN113145146A (en) * | 2021-03-05 | 2021-07-23 | 广东工业大学 | Molybdenum carbide-molybdenum oxide catalyst and preparation method and application thereof |
| CN116273173A (en) * | 2022-12-08 | 2023-06-23 | 东南大学 | COF supported Ni-based catalyst and preparation and application thereof |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SU694509A1 (en) * | 1978-06-09 | 1979-10-30 | Уфимский Нефтяной Институт | Method of preparing 2-methylfuran |
| US6479677B1 (en) * | 2000-10-26 | 2002-11-12 | Pure Energy Corporation | Processes for the preparation of 2-methylfuran and 2-methyltetrahydrofuran |
| RU2660439C1 (en) * | 2017-12-28 | 2018-07-06 | Федеральное государственное автономное образовательное учреждение высшего образования "Новосибирский национальный исследовательский государственный университет" (Новосибирский государственный университет, НГУ) | Furfural hydrogenation catalyst |
-
2019
- 2019-12-27 RU RU2019144465A patent/RU2723548C1/en active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SU694509A1 (en) * | 1978-06-09 | 1979-10-30 | Уфимский Нефтяной Институт | Method of preparing 2-methylfuran |
| US6479677B1 (en) * | 2000-10-26 | 2002-11-12 | Pure Energy Corporation | Processes for the preparation of 2-methylfuran and 2-methyltetrahydrofuran |
| RU2660439C1 (en) * | 2017-12-28 | 2018-07-06 | Федеральное государственное автономное образовательное учреждение высшего образования "Новосибирский национальный исследовательский государственный университет" (Новосибирский государственный университет, НГУ) | Furfural hydrogenation catalyst |
Non-Patent Citations (2)
| Title |
|---|
| K.XIONG et al. ChemSusChem, vol. 7, 2014, pp. 2146-2149. * |
| СМИРНОВ А.А. и др. Катализ в промышленности, 17, 2017, стр. 517-526. * |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN113145146A (en) * | 2021-03-05 | 2021-07-23 | 广东工业大学 | Molybdenum carbide-molybdenum oxide catalyst and preparation method and application thereof |
| CN113145146B (en) * | 2021-03-05 | 2023-03-07 | 广东工业大学 | Molybdenum carbide-molybdenum oxide catalyst and preparation method and application thereof |
| CN116273173A (en) * | 2022-12-08 | 2023-06-23 | 东南大学 | COF supported Ni-based catalyst and preparation and application thereof |
| CN116273173B (en) * | 2022-12-08 | 2024-04-19 | 东南大学 | COF supported Ni-based catalyst and preparation and application thereof |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Liu et al. | Selective hydrogenation of furfural over Pt based and Pd based bimetallic catalysts supported on modified multiwalled carbon nanotubes (MWNT) | |
| Seemala et al. | Support induced control of surface composition in Cu–Ni/TiO2 catalysts enables high yield co-conversion of HMF and furfural to methylated furans | |
| Madduluri et al. | Rice husk-derived carbon-silica supported Ni catalysts for selective hydrogenation of biomass-derived furfural and levulinic acid | |
| JP4625582B2 (en) | Two-stage hydrodesulfurization method using bulk composite metal catalyst | |
| EP1440046B1 (en) | Hydrogenolysis of sugars, sugar alcohols and glycerol | |
| Wang et al. | Highly stable and selective Ru/NiFe2O4 catalysts for transfer hydrogenation of biomass-derived furfural to 2-methylfuran | |
| EP1942092A1 (en) | Preparation of propylene glycol by hydrogenating lactate or lactic acid | |
| RU2722837C1 (en) | Method of preparing a hydrogenation catalyst for furfurol and furfuryl alcohol to 2-methylfuran | |
| RU2723548C1 (en) | Method of producing high-octane additive by hydrogenation of furfural and furfuryl alcohol | |
| Lan et al. | Furfural hydrodeoxygenation (HDO) over silica-supported metal phosphides–The influence of metal–phosphorus stoichiometry on catalytic properties | |
| RU2639159C2 (en) | Catalyst, method of producing carrier, method of producing catalyst and method of hydrofining hydrocarbon feedstock | |
| Umasankar et al. | Effect of copper on NiCu bimetallic catalyst supported on SBA-16 for the catalytic hydrogenation of 5-hydroxymethylfurfural to 2, 5-dimethylfuran | |
| RU2660439C1 (en) | Furfural hydrogenation catalyst | |
| US20080015267A1 (en) | Fischer-tropsch catalysts incorporating promoter for increasing yields of c5+ hydrocarbons and methods for making and using same | |
| Shen et al. | Biomass-derived 2-methyltetrahydrofuran platform: a focus on precious and non-precious metal-based catalysts for the biorefinery | |
| Shao et al. | Importance of oxyphilic FeNi alloy in NiFeAl catalysts for selective conversion of biomass-derived 5-hydroxymethylfurfural to 2, 5-dimethylfuran | |
| Smirnov et al. | Study of the Composition Effect of Molybdenum-Modified Nickel–Copper Catalysts on Their Activity and Selectivity in the Hydrogenation of Furfural to Different Valuable Chemicals | |
| CN114144257A (en) | Catalyst comprising an active nickel phase in the form of small particles and a nickel-copper alloy | |
| KR20200015663A (en) | Method of preparing light oil from extra heavy oil using unsupported NiMoW sulfide dispersed catalyst | |
| Sreenavya et al. | Hydrogenation of biomass derived furfural using Ru-Ni-Mg–Al-hydrotalcite material | |
| CN104549318A (en) | Catalyst for preparing furfuryl alcohol through hydrogenating furfural liquid phase and preparation method of catalyst | |
| Singh et al. | Hydrogenation of lignin-derived feedstocks and bio-oil using active and stable ruthenium catalyst | |
| RU2722836C1 (en) | Catalyst for hydrogenation of furfurol and furfuryl alcohol to 2-methylfuran | |
| Hwang et al. | Production of Middle Distillate Through Hydrocracking of Paraffin Wax over NiMo/SiO 2–Al 2 O 3 Catalysts: Effect of SiO 2–Al 2 O 3 Composition on Acid Property and Catalytic Performance of NiMo/SiO 2–Al 2 O 3 Catalysts | |
| US4483943A (en) | Gas conversion catalysts |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PC41 | Official registration of the transfer of exclusive right |
Effective date: 20200923 |