RU2688165C1 - Способ повышения чувствительности холерных вибрионов к антибактериальным препаратам - Google Patents
Способ повышения чувствительности холерных вибрионов к антибактериальным препаратам Download PDFInfo
- Publication number
- RU2688165C1 RU2688165C1 RU2018124130A RU2018124130A RU2688165C1 RU 2688165 C1 RU2688165 C1 RU 2688165C1 RU 2018124130 A RU2018124130 A RU 2018124130A RU 2018124130 A RU2018124130 A RU 2018124130A RU 2688165 C1 RU2688165 C1 RU 2688165C1
- Authority
- RU
- Russia
- Prior art keywords
- diclofenac
- day
- cholerae
- agar
- mouse
- Prior art date
Links
- 230000035945 sensitivity Effects 0.000 title claims abstract description 21
- 206010008631 Cholera Diseases 0.000 title claims abstract description 20
- 238000002360 preparation method Methods 0.000 title claims abstract description 11
- 241000607598 Vibrio Species 0.000 title claims abstract description 9
- 238000000034 method Methods 0.000 title claims description 31
- 206010047400 Vibrio infections Diseases 0.000 title abstract description 6
- 230000000844 anti-bacterial effect Effects 0.000 title abstract description 3
- DCOPUUMXTXDBNB-UHFFFAOYSA-N diclofenac Chemical compound OC(=O)CC1=CC=CC=C1NC1=C(Cl)C=CC=C1Cl DCOPUUMXTXDBNB-UHFFFAOYSA-N 0.000 claims abstract description 58
- 229960001259 diclofenac Drugs 0.000 claims abstract description 58
- 230000003115 biocidal effect Effects 0.000 claims abstract description 27
- 229940124350 antibacterial drug Drugs 0.000 claims abstract description 24
- 239000003814 drug Substances 0.000 claims abstract description 14
- 238000000338 in vitro Methods 0.000 claims abstract description 5
- 108090000623 proteins and genes Proteins 0.000 claims abstract description 4
- 239000003795 chemical substances by application Substances 0.000 claims abstract 3
- 241000607626 Vibrio cholerae Species 0.000 claims description 31
- 229920001817 Agar Polymers 0.000 claims description 22
- 241000699666 Mus <mouse, genus> Species 0.000 claims description 22
- 239000008272 agar Substances 0.000 claims description 22
- MYSWGUAQZAJSOK-UHFFFAOYSA-N ciprofloxacin Chemical compound C12=CC(N3CCNCC3)=C(F)C=C2C(=O)C(C(=O)O)=CN1C1CC1 MYSWGUAQZAJSOK-UHFFFAOYSA-N 0.000 claims description 20
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 claims description 18
- 239000000725 suspension Substances 0.000 claims description 18
- 230000001580 bacterial effect Effects 0.000 claims description 12
- 239000003242 anti bacterial agent Substances 0.000 claims description 11
- 229940088710 antibiotic agent Drugs 0.000 claims description 11
- 229940079593 drug Drugs 0.000 claims description 11
- 229960001625 furazolidone Drugs 0.000 claims description 11
- PLHJDBGFXBMTGZ-WEVVVXLNSA-N furazolidone Chemical compound O1C([N+](=O)[O-])=CC=C1\C=N\N1C(=O)OCC1 PLHJDBGFXBMTGZ-WEVVVXLNSA-N 0.000 claims description 11
- 241001465754 Metazoa Species 0.000 claims description 10
- WIIZWVCIJKGZOK-RKDXNWHRSA-N chloramphenicol Chemical compound ClC(Cl)C(=O)N[C@H](CO)[C@H](O)C1=CC=C([N+]([O-])=O)C=C1 WIIZWVCIJKGZOK-RKDXNWHRSA-N 0.000 claims description 10
- 229960003405 ciprofloxacin Drugs 0.000 claims description 10
- 238000011282 treatment Methods 0.000 claims description 10
- 229960005091 chloramphenicol Drugs 0.000 claims description 9
- 238000013207 serial dilution Methods 0.000 claims description 9
- 229960005322 streptomycin Drugs 0.000 claims description 9
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 claims description 8
- VAAUVRVFOQPIGI-SPQHTLEESA-N ceftriaxone Chemical compound S([C@@H]1[C@@H](C(N1C=1C(O)=O)=O)NC(=O)\C(=N/OC)C=2N=C(N)SC=2)CC=1CSC1=NC(=O)C(=O)NN1C VAAUVRVFOQPIGI-SPQHTLEESA-N 0.000 claims description 8
- 229960004755 ceftriaxone Drugs 0.000 claims description 8
- 235000015097 nutrients Nutrition 0.000 claims description 8
- 229940118696 vibrio cholerae Drugs 0.000 claims description 8
- 241000699670 Mus sp. Species 0.000 claims description 7
- 238000009792 diffusion process Methods 0.000 claims description 7
- 238000001727 in vivo Methods 0.000 claims description 7
- 241000894006 Bacteria Species 0.000 claims description 6
- 230000002401 inhibitory effect Effects 0.000 claims description 5
- 239000011780 sodium chloride Substances 0.000 claims description 5
- 239000000243 solution Substances 0.000 claims description 5
- 230000000721 bacterilogical effect Effects 0.000 claims description 4
- 238000010790 dilution Methods 0.000 claims description 4
- 239000012895 dilution Substances 0.000 claims description 4
- 208000015181 infectious disease Diseases 0.000 claims description 4
- 230000003287 optical effect Effects 0.000 claims description 4
- 238000011160 research Methods 0.000 claims description 4
- 238000012360 testing method Methods 0.000 claims description 4
- 238000011156 evaluation Methods 0.000 claims description 3
- 238000005303 weighing Methods 0.000 claims description 3
- 241000282342 Martes americana Species 0.000 claims description 2
- 230000005764 inhibitory process Effects 0.000 claims description 2
- 238000009331 sowing Methods 0.000 claims description 2
- 230000000694 effects Effects 0.000 abstract description 6
- 239000000126 substance Substances 0.000 abstract description 3
- 206010034133 Pathogen resistance Diseases 0.000 description 4
- 230000036541 health Effects 0.000 description 4
- HZZVJAQRINQKSD-UHFFFAOYSA-N Clavulanic acid Natural products OC(=O)C1C(=CCO)OC2CC(=O)N21 HZZVJAQRINQKSD-UHFFFAOYSA-N 0.000 description 3
- 206010035148 Plague Diseases 0.000 description 3
- HZZVJAQRINQKSD-PBFISZAISA-N clavulanic acid Chemical compound OC(=O)[C@H]1C(=C/CO)/O[C@@H]2CC(=O)N21 HZZVJAQRINQKSD-PBFISZAISA-N 0.000 description 3
- 239000003112 inhibitor Substances 0.000 description 3
- 230000009916 joint effect Effects 0.000 description 3
- 244000052769 pathogen Species 0.000 description 3
- WZRJTRPJURQBRM-UHFFFAOYSA-N 4-amino-n-(5-methyl-1,2-oxazol-3-yl)benzenesulfonamide;5-[(3,4,5-trimethoxyphenyl)methyl]pyrimidine-2,4-diamine Chemical compound O1C(C)=CC(NS(=O)(=O)C=2C=CC(N)=CC=2)=N1.COC1=C(OC)C(OC)=CC(CC=2C(=NC(N)=NC=2)N)=C1 WZRJTRPJURQBRM-UHFFFAOYSA-N 0.000 description 2
- 208000035143 Bacterial infection Diseases 0.000 description 2
- 229930186147 Cephalosporin Natural products 0.000 description 2
- 206010059866 Drug resistance Diseases 0.000 description 2
- ULGZDMOVFRHVEP-RWJQBGPGSA-N Erythromycin Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)C(=O)[C@H](C)C[C@@](C)(O)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 ULGZDMOVFRHVEP-RWJQBGPGSA-N 0.000 description 2
- 238000000692 Student's t-test Methods 0.000 description 2
- 208000022362 bacterial infectious disease Diseases 0.000 description 2
- 229940124587 cephalosporin Drugs 0.000 description 2
- 150000001780 cephalosporins Chemical class 0.000 description 2
- 229940090805 clavulanate Drugs 0.000 description 2
- 229940047766 co-trimoxazole Drugs 0.000 description 2
- 230000001419 dependent effect Effects 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 244000005700 microbiome Species 0.000 description 2
- 230000001717 pathogenic effect Effects 0.000 description 2
- 238000012545 processing Methods 0.000 description 2
- FKENQMMABCRJMK-RITPCOANSA-N sulbactam Chemical compound O=S1(=O)C(C)(C)[C@H](C(O)=O)N2C(=O)C[C@H]21 FKENQMMABCRJMK-RITPCOANSA-N 0.000 description 2
- 229960005256 sulbactam Drugs 0.000 description 2
- 238000002560 therapeutic procedure Methods 0.000 description 2
- GSDSWSVVBLHKDQ-UHFFFAOYSA-N 9-fluoro-3-methyl-10-(4-methylpiperazin-1-yl)-7-oxo-2,3-dihydro-7H-[1,4]oxazino[2,3,4-ij]quinoline-6-carboxylic acid Chemical compound FC1=CC(C(C(C(O)=O)=C2)=O)=C3N2C(C)COC3=C1N1CCN(C)CC1 GSDSWSVVBLHKDQ-UHFFFAOYSA-N 0.000 description 1
- 241000193738 Bacillus anthracis Species 0.000 description 1
- 206010006500 Brucellosis Diseases 0.000 description 1
- 206010069747 Burkholderia mallei infection Diseases 0.000 description 1
- 206010069748 Burkholderia pseudomallei infection Diseases 0.000 description 1
- 208000035473 Communicable disease Diseases 0.000 description 1
- 108090000204 Dipeptidase 1 Proteins 0.000 description 1
- 241001050985 Disco Species 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 229930182566 Gentamicin Natural products 0.000 description 1
- CEAZRRDELHUEMR-URQXQFDESA-N Gentamicin Chemical compound O1[C@H](C(C)NC)CC[C@@H](N)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](NC)[C@@](C)(O)CO2)O)[C@H](N)C[C@@H]1N CEAZRRDELHUEMR-URQXQFDESA-N 0.000 description 1
- 201000003641 Glanders Diseases 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- 229930182555 Penicillin Natural products 0.000 description 1
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 1
- 208000034784 Tularaemia Diseases 0.000 description 1
- 241000607479 Yersinia pestis Species 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 229940038195 amoxicillin / clavulanate Drugs 0.000 description 1
- 229960000723 ampicillin Drugs 0.000 description 1
- AVKUERGKIZMTKX-NJBDSQKTSA-N ampicillin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)=CC=CC=C1 AVKUERGKIZMTKX-NJBDSQKTSA-N 0.000 description 1
- 229940043312 ampicillin / sulbactam Drugs 0.000 description 1
- 230000003616 anti-epidemic effect Effects 0.000 description 1
- 230000003110 anti-inflammatory effect Effects 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 102000006635 beta-lactamase Human genes 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- GCFBRXLSHGKWDP-XCGNWRKASA-N cefoperazone Chemical compound O=C1C(=O)N(CC)CCN1C(=O)N[C@H](C=1C=CC(O)=CC=1)C(=O)N[C@@H]1C(=O)N2C(C(O)=O)=C(CSC=3N(N=NN=3)C)CS[C@@H]21 GCFBRXLSHGKWDP-XCGNWRKASA-N 0.000 description 1
- 229960004682 cefoperazone Drugs 0.000 description 1
- -1 ciprofloxacinol Chemical compound 0.000 description 1
- 229960003324 clavulanic acid Drugs 0.000 description 1
- 238000003759 clinical diagnosis Methods 0.000 description 1
- 230000002301 combined effect Effects 0.000 description 1
- 238000010835 comparative analysis Methods 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- NWOYIVRVSJDTLK-YSDBFZIDSA-L disodium;(2s,5r,6r)-6-[[(2r)-2-amino-2-phenylacetyl]amino]-3,3-dimethyl-7-oxo-4-thia-1-azabicyclo[3.2.0]heptane-2-carboxylate;(1r,4s)-3,3-dimethyl-2,2,6-trioxo-2$l^{6}-thiabicyclo[3.2.0]heptane-4-carboxylate Chemical compound [Na+].[Na+].O=S1(=O)C(C)(C)[C@H](C([O-])=O)C2C(=O)C[C@H]21.C1([C@@H](N)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C([O-])=O)(C)C)=CC=CC=C1 NWOYIVRVSJDTLK-YSDBFZIDSA-L 0.000 description 1
- 229960003276 erythromycin Drugs 0.000 description 1
- 229940124307 fluoroquinolone Drugs 0.000 description 1
- 229960002518 gentamicin Drugs 0.000 description 1
- 230000003308 immunostimulating effect Effects 0.000 description 1
- 238000011835 investigation Methods 0.000 description 1
- 229960000318 kanamycin Drugs 0.000 description 1
- 229930027917 kanamycin Natural products 0.000 description 1
- SBUJHOSQTJFQJX-NOAMYHISSA-N kanamycin Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CN)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](N)[C@H](O)[C@@H](CO)O2)O)[C@H](N)C[C@@H]1N SBUJHOSQTJFQJX-NOAMYHISSA-N 0.000 description 1
- 229930182823 kanamycin A Natural products 0.000 description 1
- 229960002422 lomefloxacin Drugs 0.000 description 1
- ZEKZLJVOYLTDKK-UHFFFAOYSA-N lomefloxacin Chemical compound FC1=C2N(CC)C=C(C(O)=O)C(=O)C2=CC(F)=C1N1CCNC(C)C1 ZEKZLJVOYLTDKK-UHFFFAOYSA-N 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 201000004015 melioidosis Diseases 0.000 description 1
- 230000000813 microbial effect Effects 0.000 description 1
- 239000004570 mortar (masonry) Substances 0.000 description 1
- 229940021182 non-steroidal anti-inflammatory drug Drugs 0.000 description 1
- 229960001180 norfloxacin Drugs 0.000 description 1
- OGJPXUAPXNRGGI-UHFFFAOYSA-N norfloxacin Chemical compound C1=C2N(CC)C=C(C(O)=O)C(=O)C2=CC(F)=C1N1CCNCC1 OGJPXUAPXNRGGI-UHFFFAOYSA-N 0.000 description 1
- 238000010899 nucleation Methods 0.000 description 1
- 229960001699 ofloxacin Drugs 0.000 description 1
- 230000008520 organization Effects 0.000 description 1
- 229960004236 pefloxacin Drugs 0.000 description 1
- FHFYDNQZQSQIAI-UHFFFAOYSA-N pefloxacin Chemical compound C1=C2N(CC)C=C(C(O)=O)C(=O)C2=CC(F)=C1N1CCN(C)CC1 FHFYDNQZQSQIAI-UHFFFAOYSA-N 0.000 description 1
- 229940049954 penicillin Drugs 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 229930192033 plastin Natural products 0.000 description 1
- 108010049148 plastin Proteins 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 238000009155 rehydration therapy Methods 0.000 description 1
- JQXXHWHPUNPDRT-WLSIYKJHSA-N rifampicin Chemical compound O([C@](C1=O)(C)O/C=C/[C@@H]([C@H]([C@@H](OC(C)=O)[C@H](C)[C@H](O)[C@H](C)[C@@H](O)[C@@H](C)\C=C\C=C(C)/C(=O)NC=2C(O)=C3C([O-])=C4C)C)OC)C4=C1C3=C(O)C=2\C=N\N1CC[NH+](C)CC1 JQXXHWHPUNPDRT-WLSIYKJHSA-N 0.000 description 1
- 229960001225 rifampicin Drugs 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 238000007619 statistical method Methods 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- LPQZKKCYTLCDGQ-WEDXCCLWSA-N tazobactam Chemical compound C([C@]1(C)S([C@H]2N(C(C2)=O)[C@H]1C(O)=O)(=O)=O)N1C=CN=N1 LPQZKKCYTLCDGQ-WEDXCCLWSA-N 0.000 description 1
- 229960003865 tazobactam Drugs 0.000 description 1
- OHKOGUYZJXTSFX-KZFFXBSXSA-N ticarcillin Chemical compound C=1([C@@H](C(O)=O)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)C=CSC=1 OHKOGUYZJXTSFX-KZFFXBSXSA-N 0.000 description 1
- 229960004659 ticarcillin Drugs 0.000 description 1
- 231100000820 toxicity test Toxicity 0.000 description 1
- 238000011269 treatment regimen Methods 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
- 230000036642 wellbeing Effects 0.000 description 1
- 150000003952 β-lactams Chemical class 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/195—Carboxylic acids, e.g. valproic acid having an amino group
- A61K31/196—Carboxylic acids, e.g. valproic acid having an amino group the amino group being directly attached to a ring, e.g. anthranilic acid, mefenamic acid, diclofenac, chlorambucil
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Hematology (AREA)
- Immunology (AREA)
- Molecular Biology (AREA)
- Urology & Nephrology (AREA)
- Food Science & Technology (AREA)
- General Physics & Mathematics (AREA)
- Cell Biology (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Biochemistry (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- Pathology (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
Изобретение относится к области медицины, а именно к медицинской микробиологии, и предназначено для лабораторных или экспериментальных исследований при изучении антибиотикочувствительности холерных вибрионов. Для повышения чувствительности холерных вибрионов к антибактериальным препаратам используют средство, снижающее экспрессию генов к антибиотикорезитентности. В качестве экспрессирующего средства применяют диклофенак в количестве 500 мг/л. Использование изобретения позволяет повысить чувствительность холерных вибрионов к антибактериальным препаратам при их совместном применении с диклофенаком в отношении антибиотикорезистентных штаммов холерных вибрионов in vitro и vivo. 4 з.п. ф-лы, 3 табл., 3 пр.
Description
Изобретение относится к медицине, а именно к медицинской микробиологии и может быть использовано в лабораторных или экспериментальных исследованиях при изучении антибиотикочувствительности холерных вибрионов.
В основе лечения холеры лежит патогенетическая терапия. Наряду с этим, использование антибактериальных препаратов позволяет сократить продолжительность заболевания, уменьшить объемы регидратационной терапии, предупредить формирование вибриононосительства. В инструктивно-методических документах (1-6) для лечения и профилактики холеры рекомендуется использовать фуразолидон, триметоприм / сульфаметоксазол, эритромицин, хлорамфеникол, фторхинолоны (ципрофлоксацин, офлоксацин, пефлоксацин, норфлоксацин, ломефлоксацин (с 18 лет)), тетрациклин и доксициклин (у лиц старше 8 лет), рифампицин, канамицин.
Однако, в настоящее время повсеместно распространены штаммы Vibrio cholerae, устойчивые к вышеперечисленным препаратам и обладающие множественной антибиотикорезистентностью. Последняя резко ограничивает выбор эффективных средств этиотропной терапии холеры и требует поиска веществ, повышающих антибиотикочувствительность возбудителя.
Известен способ преодоления лекарственной устойчивости бактерий (7), заключающийся в применении антибиотиков в комбинации с ингибиторами бактериальных ферментов: клавулановая кислота (клавуланат), сульбактам и тазобактам, на их основе созданы комбинированные препараты, содержащие аминопенициллиновый или цефалоспориновый антибиотик и один из ингибиторов бета-лактамаз (амоксициллин/клавуланат, ампициллин/ сульбактам, цефоперазон/ сульбактам, тикарциллин / клавуланат).
Недостатком данного способа является то, что указанные комбинации препаратов преодолевают резистентность микробов, обусловленную только выработкой бета-лактамаз.
Известен способ повышения чувствительности микроорганизмов к антибиотикам (8), основанный на воздействии препарата бактериального происхождения. В качестве активного вещества, оказывающего одновременно бактерицидное, противовоспалительное и
иммуностимулирующее действие, используют водный раствор пиластина. Однако использование пиластина может привести к развитию аллергических реакций.
Известен способ преодоления лекарственной устойчивости бактерий, включающий комбинированное применение двух антибиотиков с различным механизмом действия: пенициллина и стрептомицина, гентамицина и ампициллина (9).
Недостаток этого способа - ограниченный спектр активности данных комбинаций в отношении антибиотикорезистентных штаммов V. cholerae.
За прототип выбран способ повышения антибиотикочувствительности микроорганизмов, включающий комбинированное воздействие антибактериального препарата и нестероидного противовоспалительного средства диклофенака в субингибирующей концентрации (10)
Недостатком этого способа является использование диклофенака в концентрации 80 мг/л, что не обеспечивает статистически значимое повышение антибиотикочувствительности.
Техническим результатом предполагаемого изобретения является разработка нового эффективного способа, позволяющего повысить чувствительность холерных вибрионов к антибактериальным препаратам при их совместном применении с диклофенаком в отношении антибиотикорезистентных штаммов холерных вибрионов Эль Top in vitro и vivo.
Технический результат достигается за счет того, что в способе повышения чувствительности холерных вибрионов к антибактериальным препаратам, включающем использование препаратов снижающих экспрессию генов антибиотикорезитентности, в качестве экспрессирующего препарата, применяют диклофенак в количестве 500 мг/л, при этом исследования осуществляют in vivo и in vitro, причем в последнем случае используют метод серийных разведений и диско- диффузионный метод, а затем проводят оценку результатов исследований, соответствующую проведенным методам.
Кроме того при методе серийных разведений готовят два ряда чашек с питательной средой Мюллера-Хинтона с двукратными разведениями выбранного антибиотика, а именно левомицетина, стрептомицина, фуразолидона - 1-2-4-8-16-32-64-128-256-512 мг/л среды; цефтриаксона - 0,5-1-2-4 мг/л среды; ципрофлоксацина - 0,0001-0,00025-0,0005-0,001-0,0025-0,005-0,01-0,025-0,05-0,1-0,25-0,5-1-2-4 мг/л среды, при этом во второй ряд чашек дополнительно вводят диклофенак в концентрации 500 мг/л, затем на все чаши засевают 0,05 мл исследуемого штамма V. cholerae из предварительно подготовленной бактериальной взвеси, содержащей 106 м.кл по оптическому стандарту мутности в количестве 5 ед., в качестве контроля используют среду Мюллера-Хинтона без антибиотика и диклофенака, посевы инкубируют при 37 С в течение 16-18 часов, учет результатов проводят по величине минимальной подавляющей концентрации (МПК), которая полностью подавляет рост культуры V. cholerae при обязательном росте бактерий на контрольных чашках, уменьшение значений МПК в присутствии диклофенака, в сравнении со значениями МПК этих препаратов без воздействия диклофенака, свидетельствует о его способности повышать чувствительность V. cholerae к антибиотикам.
При этом для диско-диффузионного метода готовят чашки с агаром Мюллера-Хинтона в два ряда, в один из которых добавляют 500 мг/л диклофенака, затем на поверхность агара засевают бактерии исследуемых штаммов V.cholerae из предварительно подготовленной суспензии, содержащей n×106 м.кл/мл посев производят в объеме 0,2-0,3 мл, равномерно распределяя шпателем, после впитывания суспензии в агар на его поверхность накладывают диски с отобранным антибиотиком, а на контрольные чашки с 500 мг/л диклофенака и без него диски не накладывают, посевы инкубируют в течение 16-18 часов при 37°C, оценку результатов проводят визуально по размеру зон подавления роста бактерий на среде, содержащей диклофенак или без него.
Для проведения in vivo белых мышей массой 18-20 г. заражают внутрибрюшинно взвесью 18 часовой агаровой культуры 37°С холерного вибриона в 0,3% агаризованном 0,9% растворе хлорида натрия в дозе 108 м.кл в объеме 0,2 мл, лечение антибактериальными препаратами и диклофенаком начинают сразу после заражения и проводят по отдельности либо одновременно в течение 3-х дней (один раз в сутки) в дозах, соответствующих среднесуточным человекодозам, а именно диклофенаком в дозе 0,25 мг/мышь/сут, ципрофлоксацином - 2,0 мг/мышь/сут, стрептомицином - 2,0 мг/мышь/сут, цефтриаксоном 10,0 мг/мышь/сут, фуразолидоном - 4,0 мг/мышь/сут, левомицетином - 10,0 мг/мышь/сут, наблюдают животных в течение 10 суток, результаты оценивают по числу выживших животных, выраженному в процентах.
Предварительную подготовку при методе серийных разведений исследуемых штаммов проводят по следующей технологии: готовят бактериальную взвесь из 18 часовой агаровой культуры V. cholerae, выращенной на агаре Мартена при рН 7,6 затем готовят 1 млрд. взвесь по отраслевому стандарту мутности, для этого в стерильной бактериологической пробирке суспендируют культуру в 5 мл физиологического раствора.
Способ осуществляется следующим образом
В работе используют 4 штамма V. cholerae El Tor: 19191, 18826, 19242, 19667. Все штаммы получены из музея живых культур ФКУЗ Ростовского-на-Дону противочумного института Роспотребнадзора, где они хранятся в лиофилизированном состоянии.
Культуры выращивают на среде Мюллера-Хинтона (Himedia, Индия).
В исследовании использован диклофенак (производства ООО «Хемофарм», Россия).
Определение минимальной подавляющей концентрации (МПК) диклофенака проводят методом двукратных серийных разведений этого препарата в плотной питательной среде (агар Мюллера-Хинтона). МПК определяют по минимальной концентрации вещества, подавляющей рост микробов.
За субингибирующую дозу принимают максимальную концентрацию диклофенака, не приводящую к подавлению роста бактерий исследуемых штаммов. Посевы инкубируют при 37°С в течение 18-24 ч. Учет результатов проводят при наличии роста культуры на контрольных чашках (без диклофенака).
Способ реализуют путем совместного действия на штаммы V. cholerae, в том числе антибиотикоустойчивые, диклофенака в концентрации 500 мг/л и двукратных разведений антибактериальных препаратов.
Способ повышения чувствительности V. cholerae к антибактериальным препаратам реализуется по общепринятой методике определения чувствительности возбудителей опасных бактериальных инфекций к антибактериальным препаратам методом серийных разведений в плотной питательной среде или диско-диффузионным методом в соответствии с МУК 4.2.2495-09 (11). Отличием является добавление в среды с антибактериальными препаратами раствора диклофенака до конечной концентрации 500 мг/л
В основу заявленного способа положено обнаружение повышения чувствительности к антибактериальным препаратам V. cholerae, в том числе антибиотикоустойчивых штаммов, при совместном действии антибиотика и диклофенака. Данный эффект связан со способностью диклофенака снижать экспрессию бактериальных генов антибиотикорезистентности (10).
1. Метод серийных разведений в плотной питательной среде.
1.1 Подготовка чашек Петри с питательной средой.
Для метода серийных разведений в плотной питательной среде готовят два ряда чашек с питательной средой Мюллера-Хинтона: 1-й ряд содержит двукратные разведения исследуемого антибиотика (левомицетина, стрептомицина, фуразолидона - 1-2-4-8-16-32-64-128-256-512 мг/л среды; цефтриаксона - 0,5-1-2-4 мг/л среды; ципрофлоксацина - 0,0001-0,00025-0,0005-0,001-0,0025-0,005-0,01-0,025-0,05-0,1-0,25-0,5-1-2-4 мг/л среды). Параллельно готовят такой же ряд чашек, но в среду дополнительно вводят диклофенак в концентрации 500 мг/л.
1.2 Подготовка культуры
Из 18 часовой агаровой культуры V. cholerae, выращенной на агаре Мартена (рН 7,6±0,1) либо щелочном агаре (рН 7,8±0,1), готовят 1 млрд. взвесь по отраслевому стандарту мутности ФГБУ «НЦЭСМП» (ОСО-42-28-86). Для этого в стерильной бактериологической пробирке суспендируют культуру в 5 мл физиологического раствора.
На чашки засевают по 0,05 мл (капля) исследуемого штамма из бактериальной взвеси, содержащей 106 м.кл./мл по оптическому стандарту мутности 5 ед. либо используют для этого штамп-репликатор (при большом количестве исследуемых культур). В качестве контроля используют среду Мюллера-Хинтона (без антибиотика и диклофенака). Посевы инкубируют при 37°С в течение 16-18 ч. Результаты учитывают по величине МПК (минимальная подавляющая концентрация) при обязательном росте бактерий на контрольных чашках.
1.3 Учет результатов.
Результат учитывают по величине минимальной подавляющей концентрации (МПК) антибактериального препарата, которая полностью подавляет рост культуры V. cholerae. Уменьшение значений МПК антибактериальных препаратов в присутствии диклофенака, в сравнении со значениями МПК этих препаратов без воздействия диклофенака, свидетельствуют о его способности повышать чувствительность V. cholerae к антибиотикам.
2. Диско-диффузонный метод.
2.1 Подготовка сред.
Для диско-диффузионного метода готовят чашки с агаром Мюллера-Хинтона в два ряда, в один из которых добавляют 500 мг/л диклофенака,
2.2 Подготовка культуры.
Для определения уровня устойчивости исследуемого штамма Vibrio cholerae готовят суспензию, соответствующую n×109 м.кл./мл по оптическому стандарту мутности ФГБУ «НЦЭСМП» (ОСО-42-28-86). Из суспензии n×107 м.кл./мл производят посев в объеме 0,2-0,3 мл, равномерно распределяя шпателем. После впитывания суспензии в агар на его поверхность накладывают диски с левомицетином, цефтриаксоном, ципрофлоксацинолл, стрептомицином, фуразолидоном. На контрольные чашки с 500 мг/л диклофенака и без него диски не накладывают. Посевы инкубируют в течение 16-18 часов при 37°С, оценку результатов проводят визуально по размеру зон подавления роста бактерий на среде, содержащей диклофенак или без него.
Статистическую обработку полученных результатов проводят с использованием парного t-критерия Стьюдента для зависимых совокупностей (12).
Варианты примеров, проведенных in vitro и in vivo подтверждающих возможность использования диклофенака для повышения
чувствительности холерных вибрионов к антибактериальным препаратам. Пример 1.
Изучены значения МПК антибактериальных препаратов в присутствии диклофенака (500 мг/л) и без него в отношении 4 клинических изолятов V. cholerae El Tor: 19191, 18826, 19242, 19667, полученных из музея живых культур ФКУЗ Ростовского-на-Дону противочумного института Роспотребнадзора.
Таким образом, в присутствии диклофенака в отношении штаммов V. cholerae El Tor наблюдают снижение значений МПК в 2-4 раза левомицетина, ципрофлоксацина, фуразолидона, триметоприма/ сульфаметоксазола.
Пример 2.
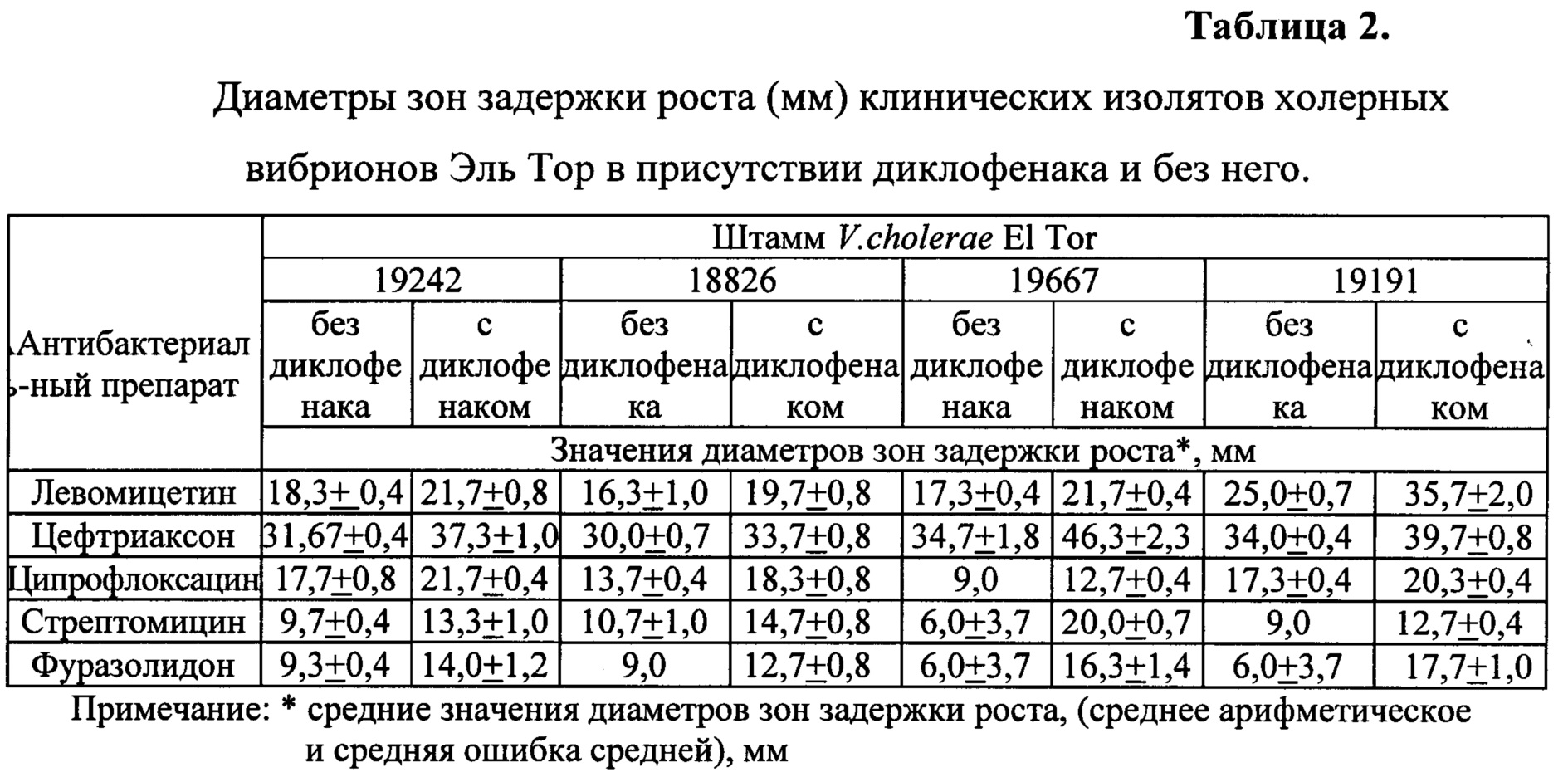
Проверяют действие диклофенака на антибиотикочувствительность штаммов V. cholerae El Tor 18826, 19667, 19242, 19191 диско-диффузионным методом (таблица 2).
Результаты учитывают по увеличению диаметров зон задержки роста V. cholerae вокруг дисков с антибиотиками на среде с диклофенаком (500 мг/л) в сравнении с диаметрами зон задержки роста вокруг таких же дисков с антибиотиками на среде, не содержащей диклофенак. Достоверность различий полученных результатов определяют с использованием парного t-критерия Стьюдента для зависимых совокупностей (12).
В сравнении с диаметрами зон задержки роста вокруг дисков с антибиотиками (левомицетином, цефтриаксоном, ципрофлоксацином, стрептомицином, фуразолидоном) на среде без диклофенака (500 мг/л), наблюдается достоверное увеличение диаметров зон задержки роста вокруг дисков с этими же антибиотиками в отношении всех изученных штаммов V. cholerae El Tor (18826, 19667, 19242, 19191) на среде, содержащей диклофенак (500 мг/л).
Пример 3.
Для сравнительной оценки эффективности антибактериальных препаратов, действующих самостоятельно, а так же совестно с диклофенаком, в опытах in vivo используют модель генерализованной формы холеры у беспородных белых мышей массой 18-20 г, которых заражают с помощью шприца внутрибрюшинно взвесью 18-часовой агаровой культуры (37°С) холерного вибриона в 0,3% агаризованном 0,9% растворе хлорида натрия в дозе 108 м.к. в объеме 0,2 мл. Диклофенак и антибиотики вводят перорально каплями (0.05 мл), для этого таблетки растирают в ступке и смешивают с растительным маслом до требуемой концентрации. Препараты вводимые внутримышечно разводят физ. раствором до требуемой концентрации (см. таблицу 3).
Для исследования проводят три схемы лечения:
1) применяют диклофенак в дозе 0,25 мг/мышь/сут
2) антибиотик в расчетной дозе (см.таблицу 3).
3) -антибиотик плюс диклофенак (в тех же дозах).
Лечение антибактериальными препаратами и диклофенаком по отдельности либо одновременно антибактериальными препаратами и диклофенаком начинают сразу после заражения и проводят в течение 3-х дней, один раз в сутки, в дозах, рассчитанных по формуле J.E. Paget, J.M. Barnes (13), исходя из среднесуточных человекодоз:
Дч(мг) - суточная доза для человека в мг;
Дм (мг/мышь) - суточная доза для мышей в мг/мышь;
50 - количество мышиных доз на 1 кг массы тела животного;
70 - масса тела человека;
Км - коэффициент для мышей (=3);
Кч - коэффициент для человека (=37).
Проводят не менее двух опытов при числе животных в группе не менее 10. Наблюдают за животными в течение 10 дней. Осуществляют бактериологический контроль заражения и эффективности лечения. Опыт учитывают по числу выживших животных, выраженному в процентах, при 100% гибели контрольных (нелеченых) животных. Для статистической обработки данных по сравнительному изучению эффективности антибактериальных препаратов использовали таблицы А.Я. Боярского (1955), вычисляя доверительный интервал I95 для р=0,05 для группы белых мышей не менее 20 для каждого препарата [14].
Из таблицы 3 видно, что при лечении животных только диклофенаком в дозе 0,25 мг/мышь/сут, либо только ципрофлоксацином - 2,0 мг/мышь/сут, или стрептомицином - 2,0 мг/мышь/сут, или цефтриаксоном 10,0 мг/мышь/сут, или фуразолидоном - 4,0 мг/мышь/сут, или левомицетином - 10,0 мг/мышь/сут, их выживаемость составила 50% и менее. При одновременном использовании таких же доз ципрофлоксацина, стрептомицина, цефтриаксона, фуразолидона, левомицетина и диклофенака, процент выживших белых мышей составил 80-100%, что свидетельствует о повышении эффективности антибактериальных препаратов при совместном действии с диклофенаком.
Использование предполагаемого изобретения позволяет при совместном действии антибиотика и диклофенака, повышать эффективность антибактериальных препаратов за счет повышения их чувствительности в отношении антибиотикорезистентных штаммов холерных вибрионов Эль Тор в опытах in vitro и in vivo.
Источники информации
1. Организация и проведение первичных противоэпидемических мероприятий в случаях выявления больного (трупа), подозрительного на заболевания инфекционными болезнями, вызывающими чрезвычайные ситуации в области санитарно-эпидемиологического благополучия населения. МУК 3.4.2552-09.
2. Стандарт специализированной медицинской помощи детям при холере легкой степени тяжести. Приложение к приказу Министерства здравоохранения Российской Федерации от 9 ноября 2012 г. N 809н.
3. Стандарт специализированной медицинской помощи детям при холере средней степени тяжести. Приложение к приказу Министерства здравоохранения Российской Федерации от 9 ноября 2012 г. N 808н.
4. Стандарт специализированной медицинской помощи детям при холере тяжелой степени тяжести. Приложение к приказу Министерства здравоохранения Российской Федерации от 9 ноября 2012 г. N 810н.
5. Клинические рекомендации (протокол лечения) оказания медицинской помощи детям, больным холерой ФГБУ НИИДИ ФМБА России. Утверждено на заседании Профильной комиссии 9 октября 2015 г.
6. Клинический протокол диагностики и лечения. Холера. Одобрено Объединенной комиссией по качеству медицинских услуг Министерства здравоохранения и социального развития Республики Казахстан от «16» августа 2016 года. Протокол №9.
7. Friese S. Prophylaxin in gynaecological surgery: a prospective randomized comparision between single dose profilaxis with amoxicillin clavulanate and the combination of cefuroxime and metronidazole. // Antimicrob. Chemother. - 1989. - V.24, Suppl. В. - P. 213-6.
8. Патент RU на изобретение №2052198. Анисимова Т.И., Попова А.Е., Наумов А.В., Шведун Г.П., Майскова Т.С., Попов В.И., Никитина Г.А., Кривошеев В.А. Способ повышения чувствительности микроорганизмов к антибиотикам.
9. Навашин С.М. и Фомина И.П. Рациональная антибиотикотерапия. Справочник., 4-е изд., перераб. и доп., М., Медицина, 2002, 496 с.
10. Riordan J.Т., Dupre J M., Cantore-Matyi S.A., Kumar-Singh A., Song Y., Zaman Sh., Horan S., Helal N.S., Nagarajan V., Elasri M.O., Wilkinson B.J., Gustafson J.E. Alterations in the transcriptome and antibiotic susceptibility of Staphylococcus aureus grown in the presence of diclofenac // Ann Clin Microbiol Antimicrob. 2011; 10: 30.
11. Определение чувствительности возбудителей опасных бактериальных инфекций (чума, сибирская язва, холера, туляремия, бруцеллез, сап, мелиоидоз) к антибактериальным препаратам МУК 4.2.2495-09. - М., 2009. - 59 с.
12. http://www.medstatistic.ru/calculators/calcpars.html
13. Paget J.E., Barnes Y.M. Toxicity tests // Evaluation of drug activities pharmacometric. - London, 1964. - Vol.1. - P. 135-167.
14. Боярский А.Я. Статистические методы в экспериментальных медицинских исследованиях. - М.: Медицина, 1955. - 262 с.
Claims (5)
1. Способ повышения чувствительности холерных вибрионов к антибактериальным препаратам, включающий использование средств снижающих экспрессию генов к антибиотикорезитентности, отличающийся тем, что в качестве экспрессирующего средства, применяют диклофенак в количестве 500 мг/л, при этом исследования осуществляют in vivo и in vitro, причем в последнем случае используют метод серийных разведений и диско-диффузионный метод, а затем проводят оценку результатов исследований, соответствующую проведенным методам.
2. Способ по п. 1, отличающийся тем, что при методе серийных разведений готовят два ряда чашек с питательной средой Мюллера-Хинтона с двукратными разведениями выбранного антибиотика, а именно левомицетина, стрептомицина, фуразолидона - 1-2-4-8-16-32-64-128-256-512 мг/л среды; цефтриаксона - 0,5-1-2-4 мг/л среды; ципрофлоксацина - 0,0001-0,00025-0,0005-0,001-0,0025-0,005-0,01-0,025-0,05-0,1-0,25-0,5-1-2-4 мг/л среды, при этом во второй ряд чашек дополнительно вводят диклофенак в концентрации 500 мг/л, затем на все чаши засевают 0,05 мл исследуемого штамма V.cholerae из предварительно подготовленной бактериальной взвеси, содержащей 106 м.кл по оптическому стандарту мутности в количестве 5 ед., в качестве контроля используют среду Мюллера-Хинтона без антибиотика и диклофенака, посевы инкубируют при 37°С в течение 16-18 часов, учет результатов проводят по величине минимальной подавляющей концентрации (МПК), которая полностью подавляет рост культуры V. cholerae при обязательном росте бактерий на контрольных чашках, уменьшение значений МПК в присутствии диклофенака, в сравнении со значениями МПК этих препаратов без воздействия диклофенака, свидетельствует о его способности повышать чувствительность V.cholerae к антибиотикам.
3. Способ по п. 1, отличающийся тем, что для диско-диффузионного метода готовят чашки с агаром Мюллера-Хинтона в два ряда, в один из которых добавляют 500 мг/л диклофенака, затем на поверхность агара засевают бактерии исследуемых штаммов V.cholerae из предварительно подготовленной суспензии, содержащей n×1O7 м.кл/мл посев производят в объеме 0,2-0,3 мл, равномерно распределяя шпателем, после впитывания суспензии в агар на его поверхность накладывают диски с отобранным антибиотиком, а на контрольные чашки с 500 мг/л диклофенака и без него диски не накладывают, посевы инкубируют в течение 16-18 часов при 37°С, оценку результатов проводят визуально по размеру зон подавления роста бактерий на среде, содержащей диклофенак или без него.
4. Способ по п. 1, отличающийся тем, что для проведения in vivo белых мышей массой 18-20 г. заражают внутрибрюшинно взвесью 18 часовой агаровой культуры 37°С холерного вибриона в 0,3% агаризованном 0,9% растворе хлорида натрия в дозе 108 м.кл в объеме 0,2 мл, лечение антибактериальными препаратами и диклофенаком начинают сразу после заражения и проводят по отдельности либо одновременно в течение 3-х дней, дин раз в сутки, в дозах соответствующих среднесуточным человекодозам, а именно диклофенаком в дозе 0,25 мг/ мышь/ сут, ципрофлоксацином - 2,0 мг/ мышь/ сут, стрептомицином - 2,0 мг/ мышь/ сут, цефтриаксоном 10,0 мг/ мышь/ сут, фуразолидоном - 4,0 мг/ мышь/ сут, левомицетином - 10,0 мг/ мышь/ сут, наблюдают животных в течение 10 суток, результаты оценивают по числу выживших животных, выраженному в процентах.
5. Способ по п. 2, отличающийся тем, что предварительную подготовку исследуемых штаммов проводят по следующей технологии: из 18 часовой агаровой культуры V. cholerae, выращенной на агаре Мартена при рН 7,6 готовят 1 млрд. взвесь по отраслевому стандарту мутности, для этого в стерильной бактериологической пробирке суспендируют культуру в 5 мл физиологического раствора.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2018124130A RU2688165C1 (ru) | 2018-07-02 | 2018-07-02 | Способ повышения чувствительности холерных вибрионов к антибактериальным препаратам |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2018124130A RU2688165C1 (ru) | 2018-07-02 | 2018-07-02 | Способ повышения чувствительности холерных вибрионов к антибактериальным препаратам |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2688165C1 true RU2688165C1 (ru) | 2019-05-20 |
Family
ID=66578853
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2018124130A RU2688165C1 (ru) | 2018-07-02 | 2018-07-02 | Способ повышения чувствительности холерных вибрионов к антибактериальным препаратам |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2688165C1 (ru) |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2529367C1 (ru) * | 2013-04-19 | 2014-09-27 | Федеральное государственное бюджетное учреждение "Саратовский научно-исследовательский институт травматологии и ортопедии" Министерства здравоохранения Российской Федерации (ФГБУ "СарНИИТО" Минздрава России) | Способ повышения чувствительности микроорганизмов к антимикробным препаратам |
| RU2630645C1 (ru) * | 2016-03-31 | 2017-09-11 | Федеральное казенное учреждение здравоохранения "Ростовский-на-Дону ордена Трудового Красного Знамени научно-исследовательский противочумный институт" Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека | Способ снижения резистентности возбудителя туляремии к цефалоспоринам (варианты) |
-
2018
- 2018-07-02 RU RU2018124130A patent/RU2688165C1/ru active
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2529367C1 (ru) * | 2013-04-19 | 2014-09-27 | Федеральное государственное бюджетное учреждение "Саратовский научно-исследовательский институт травматологии и ортопедии" Министерства здравоохранения Российской Федерации (ФГБУ "СарНИИТО" Минздрава России) | Способ повышения чувствительности микроорганизмов к антимикробным препаратам |
| RU2630645C1 (ru) * | 2016-03-31 | 2017-09-11 | Федеральное казенное учреждение здравоохранения "Ростовский-на-Дону ордена Трудового Красного Знамени научно-исследовательский противочумный институт" Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека | Способ снижения резистентности возбудителя туляремии к цефалоспоринам (варианты) |
Non-Patent Citations (2)
| Title |
|---|
| PONGKORPSAKOL P et al. Inhibition of cAMP-activated intestinal chloride secretion by diclofenac: cellular mechanism and potential application in cholera. PLoS Negl Trop Dis., 2014, 4; 8(9), p.e3119. * |
| RIORDAN JT et al. Alterations in the transcriptome and antibiotic susceptibility of Staphylococcus aureus grown in the presence of diclofenac. Ann Clin Microbiol Antimicrob., 2011, 21, 10:30. * |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Michalopoulos et al. | The revival of fosfomycin | |
| Chetchotisakd et al. | Maintenance therapy of melioidosis with ciprofloxacin plus azithromycin compared with cotrimoxazole plus doxycycline. | |
| Kuriyama et al. | Antimicrobial chemotherapy: significance to healthcare | |
| Kim et al. | Scrub typhus meningoencephalitis occurring during doxycycline therapy for Orientia tsutsugamushi | |
| CN110124012B (zh) | 一种颗粒溶素作为多粘菌素类抗生素增效剂的应用 | |
| Ferris | Current understanding of bacterial biofilms and latent infections: A clinical perspective | |
| Koley et al. | Genetic basis of biofilm formation and spread of nosocomial infections | |
| CA2693544A1 (en) | Antibacterial combination therapy | |
| RU2688165C1 (ru) | Способ повышения чувствительности холерных вибрионов к антибактериальным препаратам | |
| CN102099027B (zh) | 富里酸及抗生素组合物 | |
| Stryjewski et al. | Pseudomonas aeruginosa infections in specific types of patients and clinical settings | |
| Park et al. | Identification and antimicrobial susceptibility of bacteria isolated from dogs with chronic otitis externa | |
| Rodrigo et al. | Melioidosis as a cause of femoral osteomyelitis and multifocal intramuscular abscess around the hip joint in a farmer: a case report | |
| RU2614730C1 (ru) | Антибактериальное средство и способ лечения кишечного иерсиниоза, или псевдотуберкулеза, или эшерихиоза | |
| Pius et al. | Levels of biofilm expression in Klebsiella pneumoniae isolates exposed to herbal drugs | |
| Khan et al. | Dual infection by Burkholderia Cepacia and Pseudomonas Putida in an infective endocarditis case | |
| Amangeldykyzy et al. | The effect of a combined choline salicylate and cetalkonium chloride gel on particular strains of Pseudomonas aeruginosa, Staphylococcus spp. and Streptococcus spp. | |
| Hussein | Antibacterial Activity of Lantana camara Flower Extracts Against Growth of Pathogenic Bacteria Isolated from Wounds and Burns Infections | |
| Shewly et al. | Antibiotic Susceptibility of Bacterial Isolates from Pus Specimens Collected from a General Hospital in Dhaka, Bangladesh | |
| Al-Dahmoshi et al. | Virulence and Antibiotic Resistance of Acinetobacter baumannii among Urinary Tract Infections | |
| AU2018285342B2 (en) | Antibiotic composition for the treatment of infections with resistent microorganism | |
| Kadhum | Antibiotic sensitivity tests of Klebsiella pneumonia isolated from different clinical specimens in Hilla city | |
| Strazdins et al. | Soluble Nitrofurans in Recurrent Urinary Tract Infections: Unexpected Findings from 2014 Latvian Study | |
| Salahuddin | Combined effect of Cefixime and Azithromycin against multiple antibiotics resistant Klebsiella pneumoniae and Pseudomonas aeruginosa | |
| Drum et al. | Hospital-onset bloodstream infection rates after discontinuing active surveillance cultures for methicillin-resistant Staphylococcus aureus in a regional burn center |