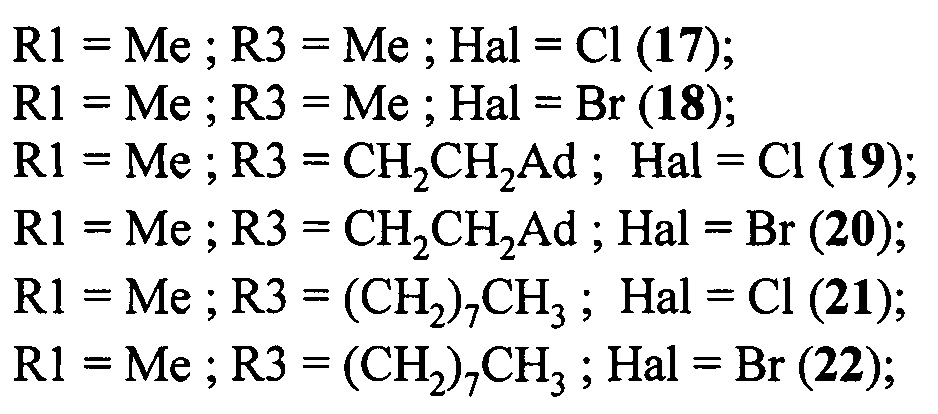RU2677337C2 - N-замещенные N'-(1-алкилтетразол-5-ил)-тринитроацетимидамиды и способ их получения - Google Patents
N-замещенные N'-(1-алкилтетразол-5-ил)-тринитроацетимидамиды и способ их получения Download PDFInfo
- Publication number
- RU2677337C2 RU2677337C2 RU2016150796A RU2016150796A RU2677337C2 RU 2677337 C2 RU2677337 C2 RU 2677337C2 RU 2016150796 A RU2016150796 A RU 2016150796A RU 2016150796 A RU2016150796 A RU 2016150796A RU 2677337 C2 RU2677337 C2 RU 2677337C2
- Authority
- RU
- Russia
- Prior art keywords
- substituted
- trinitroacetimidamides
- alkyltetrazol
- alkyltetrazole
- trinitromethyltetrazolo
- Prior art date
Links
- 238000004519 manufacturing process Methods 0.000 title description 2
- 238000000034 method Methods 0.000 claims abstract description 13
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 claims abstract description 3
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 claims description 10
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims description 7
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 6
- SCYULBFZEHDVBN-UHFFFAOYSA-N 1,1-Dichloroethane Chemical compound CC(Cl)Cl SCYULBFZEHDVBN-UHFFFAOYSA-N 0.000 claims description 4
- 150000001298 alcohols Chemical class 0.000 claims description 3
- 230000003993 interaction Effects 0.000 claims description 3
- 150000001875 compounds Chemical class 0.000 abstract description 5
- 230000001472 cytotoxic effect Effects 0.000 abstract description 5
- 239000000126 substance Substances 0.000 abstract description 3
- 239000003814 drug Substances 0.000 abstract description 2
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 abstract 1
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 abstract 1
- 230000000694 effects Effects 0.000 abstract 1
- UHCBBWUQDAVSMS-UHFFFAOYSA-N fluoroethane Chemical compound CCF UHCBBWUQDAVSMS-UHFFFAOYSA-N 0.000 abstract 1
- 125000006412 propinylene group Chemical group [H]C#CC([H])([H])* 0.000 abstract 1
- 230000015572 biosynthetic process Effects 0.000 description 8
- 238000003786 synthesis reaction Methods 0.000 description 7
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 6
- 238000006243 chemical reaction Methods 0.000 description 6
- ULRPISSMEBPJLN-UHFFFAOYSA-N 2h-tetrazol-5-amine Chemical compound NC1=NN=NN1 ULRPISSMEBPJLN-UHFFFAOYSA-N 0.000 description 4
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 4
- 125000000623 heterocyclic group Chemical group 0.000 description 3
- 239000000543 intermediate Substances 0.000 description 3
- 150000002825 nitriles Chemical class 0.000 description 3
- 229910052757 nitrogen Inorganic materials 0.000 description 3
- 239000011541 reaction mixture Substances 0.000 description 3
- 239000007858 starting material Substances 0.000 description 3
- 238000003756 stirring Methods 0.000 description 3
- 239000013543 active substance Substances 0.000 description 2
- 150000001409 amidines Chemical class 0.000 description 2
- HUMNYLRZRPPJDN-UHFFFAOYSA-N benzaldehyde Chemical compound O=CC1=CC=CC=C1 HUMNYLRZRPPJDN-UHFFFAOYSA-N 0.000 description 2
- 229960004592 isopropanol Drugs 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- WBHFVXWMMICZCD-UHFFFAOYSA-N n'-(2h-tetrazol-5-yl)benzenecarboximidamide Chemical compound C=1C=CC=CC=1C(N)=NC=1N=NNN=1 WBHFVXWMMICZCD-UHFFFAOYSA-N 0.000 description 2
- 125000004433 nitrogen atom Chemical group N* 0.000 description 2
- 229920006395 saturated elastomer Polymers 0.000 description 2
- 159000000000 sodium salts Chemical class 0.000 description 2
- WBEARYVZUXYDAU-UHFFFAOYSA-N 2,2-dinitroethanimidamide Chemical class NC(=N)C([N+]([O-])=O)[N+]([O-])=O WBEARYVZUXYDAU-UHFFFAOYSA-N 0.000 description 1
- GPEZBOYWAXXHJE-UHFFFAOYSA-N 3-(2h-tetrazol-5-yl)quinazolin-4-one Chemical compound C1=NC2=CC=CC=C2C(=O)N1C=1N=NNN=1 GPEZBOYWAXXHJE-UHFFFAOYSA-N 0.000 description 1
- PQOXFEBQGPWGNW-UHFFFAOYSA-N 3-methyl-5-(trinitromethyl)tetrazolo[1,5-a][1,3,5]triazin-7-one Chemical compound Cn1nnn2c1nc(nc2=O)C([N+]([O-])=O)([N+]([O-])=O)[N+]([O-])=O PQOXFEBQGPWGNW-UHFFFAOYSA-N 0.000 description 1
- -1 5-tetrazolyl Chemical group 0.000 description 1
- ATTYXXTUSGOJNS-UHFFFAOYSA-N N'-(1-methyltetrazol-5-yl)-2,2,2-trinitroethanimidamide Chemical compound Cn1nnnc1\N=C(/N)C([N+]([O-])=O)([N+]([O-])=O)[N+]([O-])=O ATTYXXTUSGOJNS-UHFFFAOYSA-N 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- 238000005804 alkylation reaction Methods 0.000 description 1
- 239000012736 aqueous medium Substances 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 230000002238 attenuated effect Effects 0.000 description 1
- 238000001460 carbon-13 nuclear magnetic resonance spectrum Methods 0.000 description 1
- 210000004027 cell Anatomy 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 238000000921 elemental analysis Methods 0.000 description 1
- 239000002360 explosive Substances 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 238000002329 infrared spectrum Methods 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- AICOOMRHRUFYCM-ZRRPKQBOSA-N oxazine, 1 Chemical compound C([C@@H]1[C@H](C(C[C@]2(C)[C@@H]([C@H](C)N(C)C)[C@H](O)C[C@]21C)=O)CC1=CC2)C[C@H]1[C@@]1(C)[C@H]2N=C(C(C)C)OC1 AICOOMRHRUFYCM-ZRRPKQBOSA-N 0.000 description 1
- QNGNSVIICDLXHT-UHFFFAOYSA-N para-ethylbenzaldehyde Natural products CCC1=CC=C(C=O)C=C1 QNGNSVIICDLXHT-UHFFFAOYSA-N 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 1
- NXONKORUAPPSHC-UHFFFAOYSA-N sodium;2h-tetrazol-5-amine Chemical compound [Na].NC=1N=NNN=1 NXONKORUAPPSHC-UHFFFAOYSA-N 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 125000004299 tetrazol-5-yl group Chemical group [H]N1N=NC(*)=N1 0.000 description 1
- 150000003536 tetrazoles Chemical class 0.000 description 1
- GKASDNZWUGIAMG-UHFFFAOYSA-N triethyl orthoformate Chemical compound CCOC(OCC)OCC GKASDNZWUGIAMG-UHFFFAOYSA-N 0.000 description 1
- 210000004881 tumor cell Anatomy 0.000 description 1
- 238000009281 ultraviolet germicidal irradiation Methods 0.000 description 1
- 238000012800 visualization Methods 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D257/00—Heterocyclic compounds containing rings having four nitrogen atoms as the only ring hetero atoms
- C07D257/02—Heterocyclic compounds containing rings having four nitrogen atoms as the only ring hetero atoms not condensed with other rings
- C07D257/04—Five-membered rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/12—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a chain containing hetero atoms as chain links
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
Abstract
Description
Изобретение относится к области химии нитрометильных производных ацетимидамидов, замещенных по одному из атомов азота гетероциклом тетразолом и по другому атому азота различными группами, и способу их получения.
N-Замещенные N'-(1-алкилтетразол-5-ил)-тринитроацетимидамиды могут использоваться в качестве энергонасыщенных материалов, полупродуктов в синтезе энергонасыщенных материалов (наличие эксплозофорной тринитрометильной группы и цикла тетразола), биологически активных веществ, обладающих цитотоксической активностью, и полупродуктов в синтезе биологически активных веществ, также обладающих цитотоксической активностью (см. приложение 1). Это свидетельствует о возможном практическом применении изобретения: изготовление на основе N-замещенных N'-(1-алкилтетразол-5-ил)-тринитроацетимидамидов компонентов взрывчатых веществ и лекарственных препаратов.
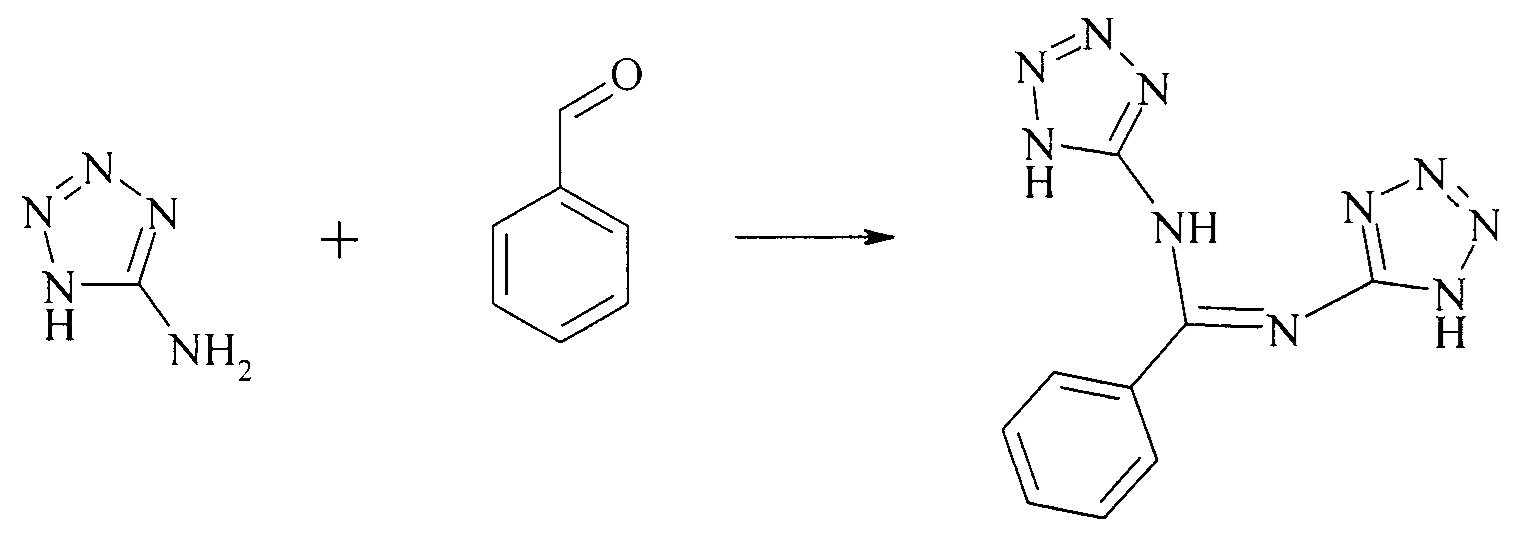
Известно три способа (способы-аналоги) построения структуры N-замещенных N'-(тетразол-5-ил)имидамидов. Первый заключается во взаимодействии 5-аминотетразола и бензальдегидом с образованием N,N'-ди(тетразол-5-ил)бензимидамида [1] [1. Henry R.A., Finnegan W.G. Mono-alkylation of Sodium 5-Aminotetrazole in Aqueous Medium.// J. Am. Chem. Soc. - 1954. - Vol. 76. №3. - P. 923-926]:
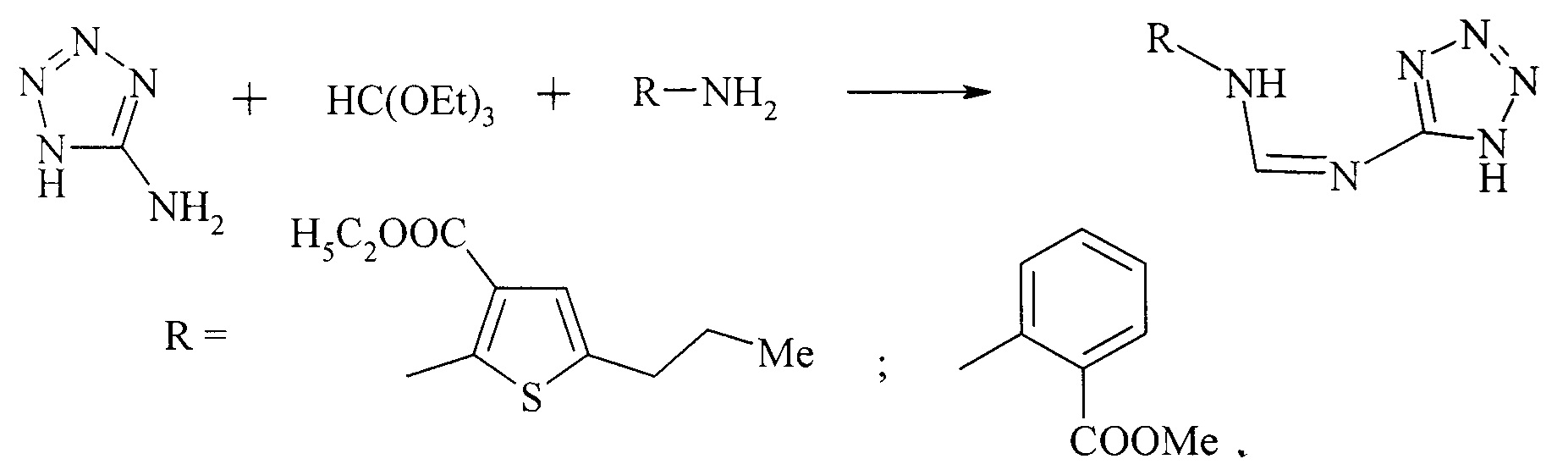
Второй основан на реакции 5-аминотетразола с триэтилортоформиатом и арил- или гетериламинами [2] [2. Vinogradoff А.Р., Peet N.P. Development of a new synthesis of 3-(1H-tetrazol-5-yl)-4(3H)-quinazolinone, sodium salt via an amidine intermediate // Journal of Heterocyclic Chemistry. - 1989. - Vol. 26. - №1. - P. 97-103; Patent US 4761474, date of patent 02.08.1988]:
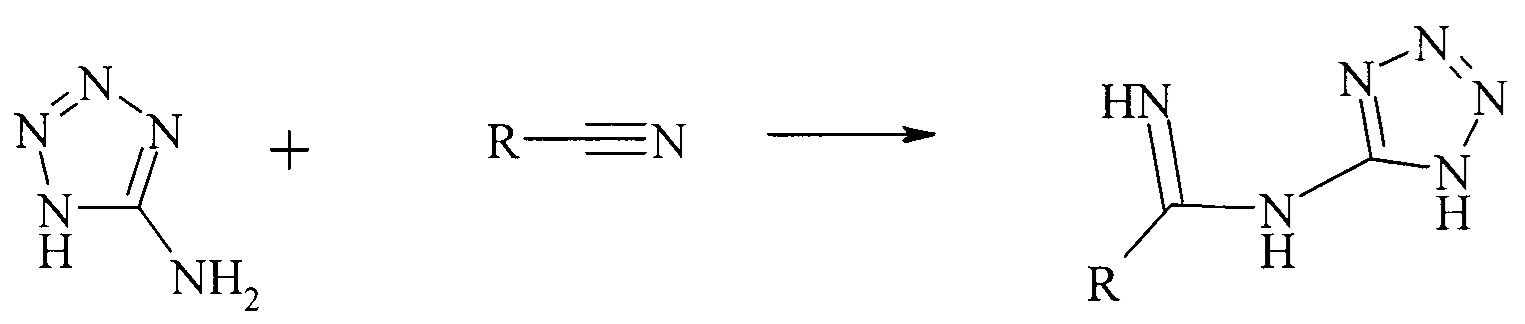
В основе третьего способа лежит реакция 5-аминотетразола с нитрилами [3] [3. V.A. Dorokhov, A.R. Amamchyan, V.S. Bogdanov, Т.A. Shchegoleva Synthesis of N-(5-tetrazolyl)amidines from 5-aminotetrazole and nitriles using organoboranes // Bulletin of the Academy of Sciences of the USSR, Division of chemical science. - 1987. - Vol. 36. - №11. - P. 2436-2438]:
R = Me; Ph
Все вышеперерчисленные способы-аналоги не позволяют получать N-замещенные N'-(1-алкилтетразол-5-ил)-тринитроацетимидамиды. Способ-прототип получения N-замещенных N'-(1-алкилтетразол-5-ил)-тринитроацетимидамидов не обнаружен. Это свидетельствует о научной новизне и изобретательском уровне предполагаемого изобретения.
Техническим результатом изобретения являются: создание новых веществ, к которым не выработана резистентность опухолевых клеток.
Исходные 3-алкил-5-тринитрометилтетразоло[1,5-а]-1,3,5-триазин-7-оны получают по методике [4] [4. Бахарев В.В., Гидаспов А.А. Конденсированные тетразоло-1,3,5-триазины. 3. Синтез 3-R-5-тринитрометилтетразоло[1,5-а]-1,3,5-триазин-7-онов // Химия гетероцикл. соединений. - 2006. - №3. - С. 466-467].
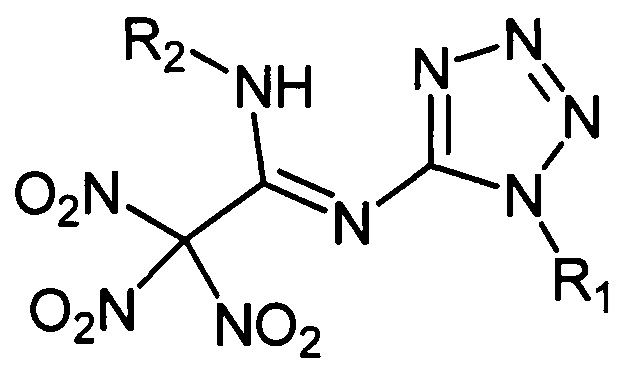
Технический результат достигается тем, что N-замещенные N'-(1-алкилтетразол-5-ил)-тринитроацетимидамиды обладают общей формулой:
где R1 = СН3; СН2-СН=СН2; Ad
R2 = Н; COOR3
R3 = Alk; замещенный Alk, a
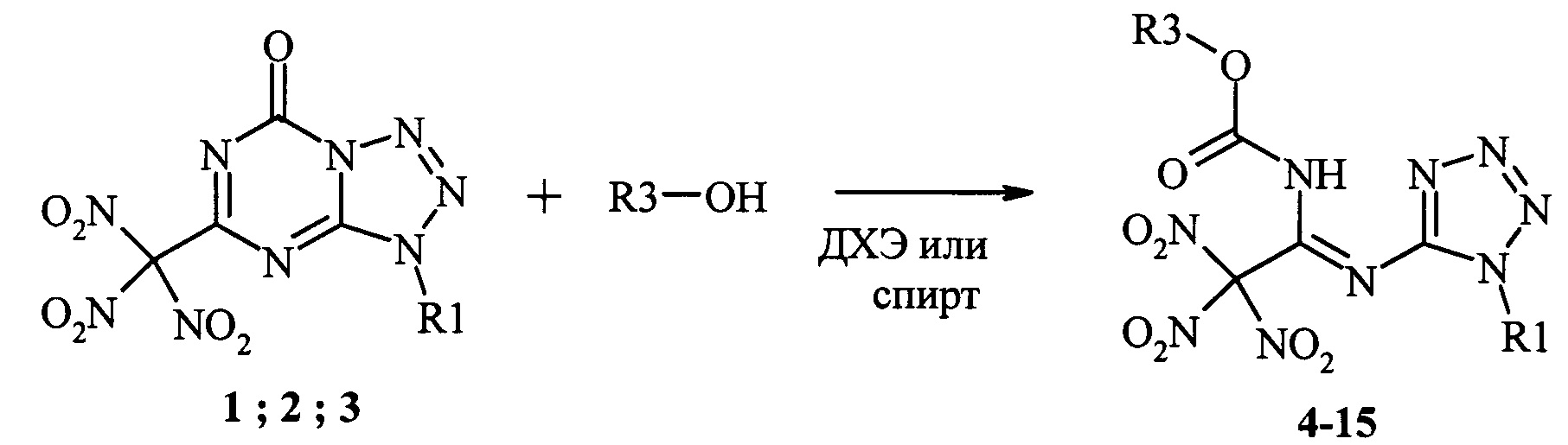
способ получения N-замещенных N'-(1-алкилтетразол-5-ил)-тринитроацетимидамидов по п. 1, заключающийся во взаимодействии 3-алкил-5-тринитрометилтетразоло[1,5-а]-1,3,5-триазин-7-онов с водой в среде ацетона или спиртами в среде дихлорэтана или самого спирта.
Исходные 3-алкил-5-тринитрометилтетразоло[1,5-а]-1,3,5-триазин-7-оны получают по методике [4] [4. Бахарев В.В., Гидаспов А.А. Конденсированные тетразоло-1,3,5-триазины. 3. Синтез 3-R-5-тринитрометилтетразоло[1,5-а]-1,3,5-триазин-7-онов // Химия гетероцикл. соединений. - 2006. - №3. - С. 466-467].
Для лучшего понимания предлагаемого способа рассмотрим несколько примеров синтеза N-(1-метилтетразол-5-ил)-2,2,2-тринитроацетимидамида и N-замещенных N'-(1-алкилтетразол-5-ил)-тринитроацетимидамидов.
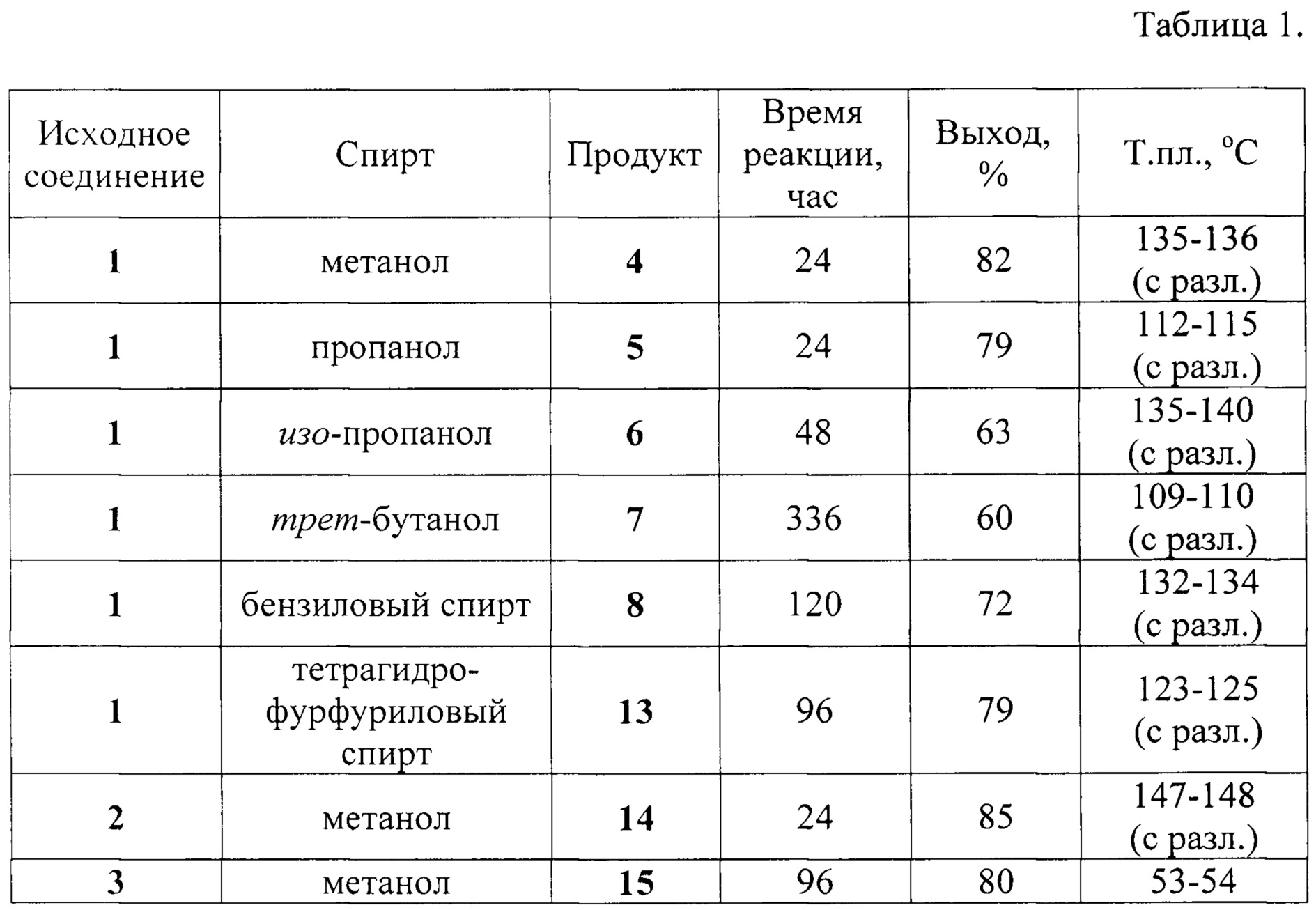
Пример 1. К 10 мл соответствующего спирта при перемешивании и температуре 20-25°С присыпали порциями в течение 10 минут 0,003 моль 3-алкил-5-тринитрометилтетразоло[1,5-а]-1,3,5-триазин-7-она 1, 2 или 3. Реакционную смесь перемешивали при температуре 20-25°С до окончания реакции, которое фиксировали по данным ТСХ на исходные соединения 1, 2 или 3 (см. табл. 1). Избыток спирта удаляли при пониженном давлении, остаток обрабатывали 2 раза по 4 мл изо-пропанолом и 2 раза по 4 мл диэтиловым эфиром. Нерастворившийся продукт отфильтровывали и сушили на воздухе. Выход продуктов 4-8 и 13-15 представлены в табл. 1. ИК, ЯМР 1Н и 13С представлены в таблице (см. приложение 2).
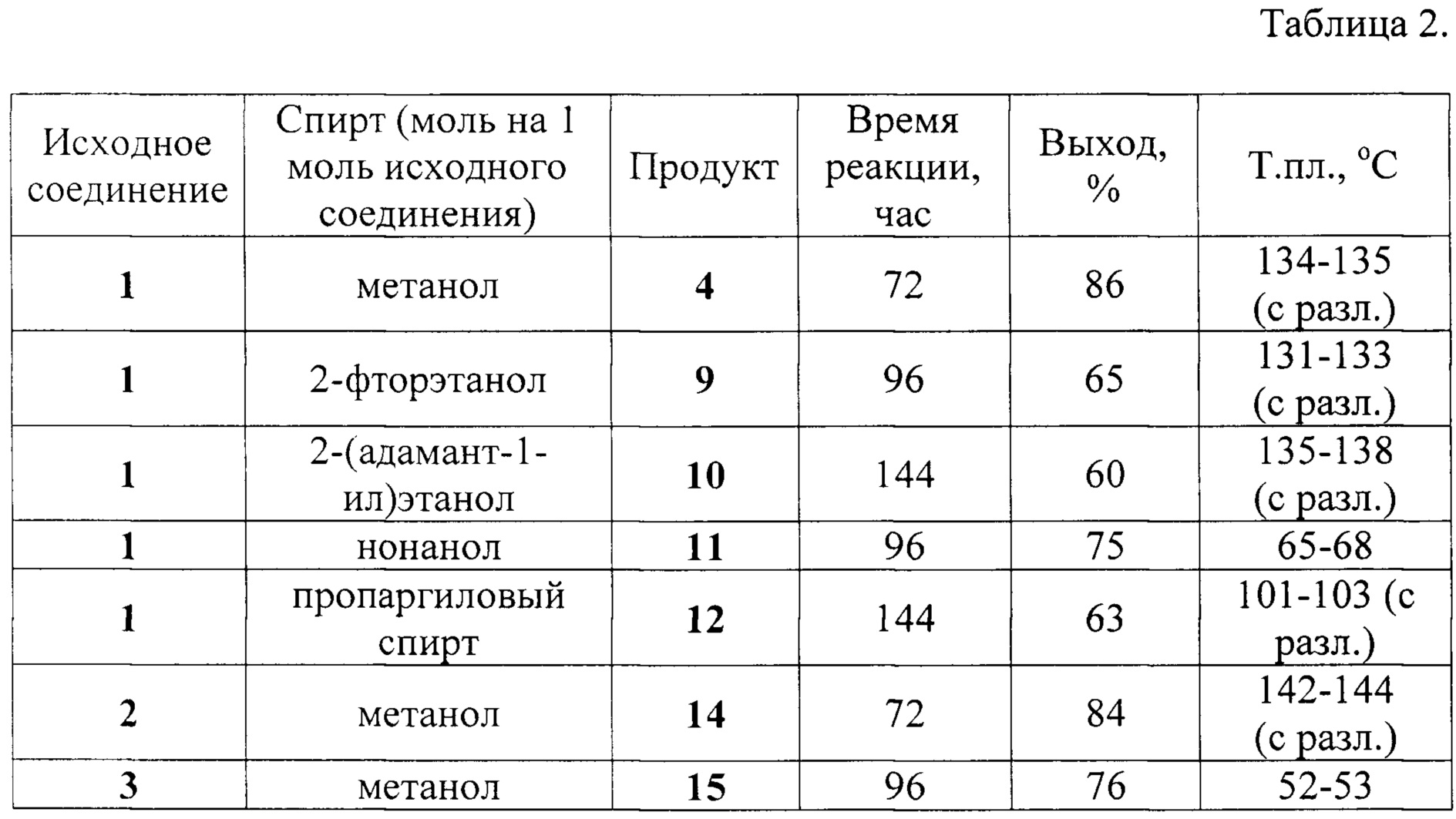
Пример 2. К 10 мл дихлорэтана и определенному количеству соответствующего спирта (см. табл. 2) при перемешивании и температуре 20-25°С присыпали порциями в течении 10 минут 0,003 моль 3-алкил-5-тринитрометилтетразоло[1,5-а]-1,3,5-триазин-7-она 1, 2 или 3. Реакционную смесь перемешивали при температуре 30-35°С до окончания реакции, которое фиксировали по данным ТСХ на исходные соединения 1, 2 или 3 (см. табл. 2). Дихлорэтан и избыток спирта удаляли при пониженном давлении, остаток обрабатывали 2 раза по 4 мл изо-пропанолом и 2 раза по 4 мл диэтиловым эфиром. Нерастворившийся продукт отфильтровывали и сушили на воздухе. Продукт 11 после промывки растворителями вакуумировали до постоянного веса. Выход продуктов 4, 9-12, 14-15 представлены в табл. 2. ИК, ЯМР 1Н и 13С представлены в таблице (см. приложение 2).
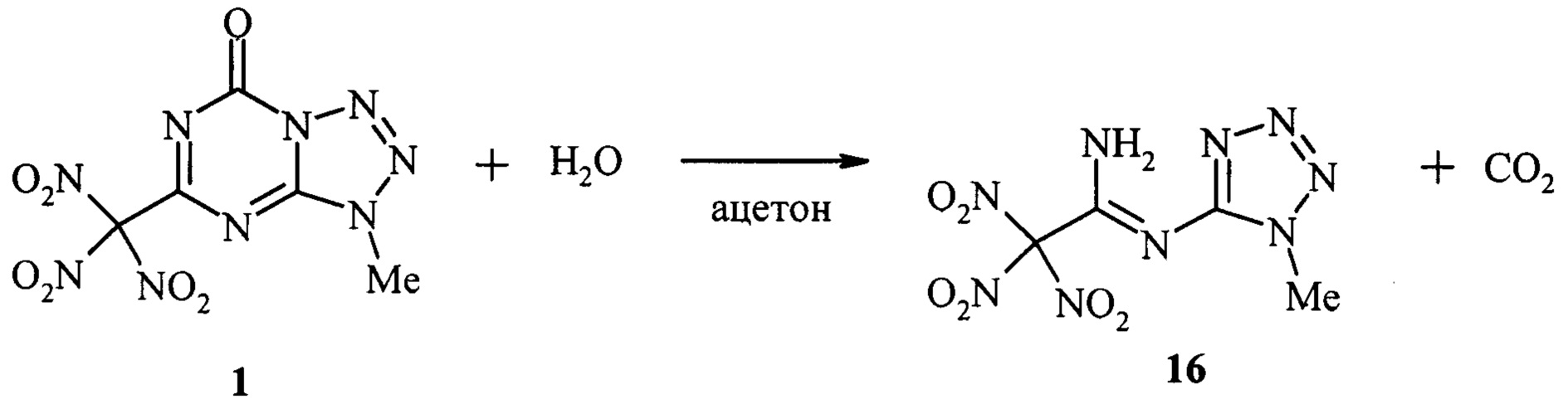
Пример 3. К 10 мл ацетона и 1,1 мл (0,06 моль) воды при перемешивании и температуре 20-25°С присыпали порциями в течение 10 минут 0,003 моль 3-метил-5-тринитрометилтетразоло[1,5-а]-1,3,5-триазин-7-она 1. Реакционную смесь перемешивали при температуре 40-45°С в течение 24 часов, добавляли еще 2,2 мл (0,12 моль) воды и выдерживали до окончания реакции, которое фиксировали по данным ТСХ на исходное соединение 1. Избыток ацетона испаряли при пониженном давлении, остаток обрабатывали 2 раза по 10 мл воды. Нерастворившийся продукт отфильтровывали и сушили на воздухе. Выход 16 - 80%, Т.пл. = 127-128°С (с разл.). ИК, ЯМР 1Н и 13С представлены в таблице (см. приложение 2).
ИК спектры зарегистрированы на фурье-спектрофотометре Avatar 360ESP с использованием приставки нарушенного полного внутреннего отражения (НПВО). Спектры ЯМР 1Н и 13С зарегистрированы на спектрометре JEOL JNM ЕСХ-400 (400 и 100 МГц соответственно) в ДМСО-d6, внутренний стандарт ТМС. Элементный анализ выполнен на приборе Eurovector ЕА 3000. Температуры плавления определены на приборе Gallenkamp и не исправлены. Контроль за ходом реакций и чистотой полученных соединений осуществлен методом ТСХ на пластинах Silufol UV-254 (визуализация хроматограмм УФ облучением при 254 нм).
Таким образом, предлагаемый способ позволяет получать N-замещенные N'-(1-алкилтетразол-5-ил)-тринитроацетимидамиды взаимодействием 3-алкил-5-тринитрометилтетразоло[1,5-а]-1,3,5-триазин-7-онов с водой в среде ацетона или спиртами в среде ДХЭ или самого спирта.
Объединенная формула для соединений 16 и 4-15 имеет вид
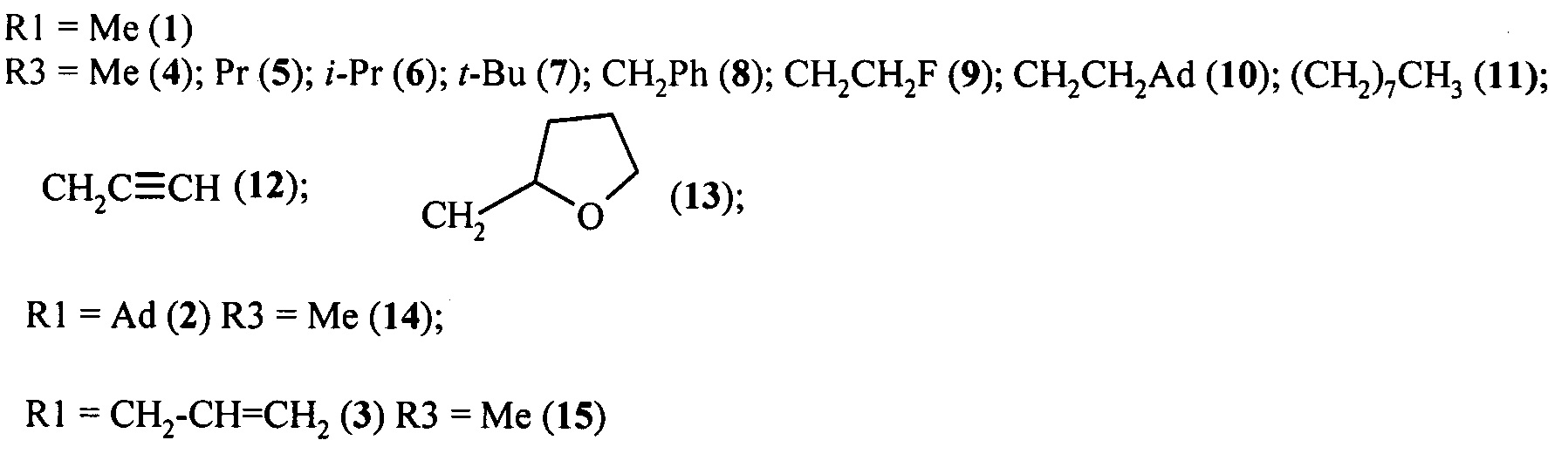
где R1=СН3; СН2-СН=СН2; Ad
R2=Н; COOR3
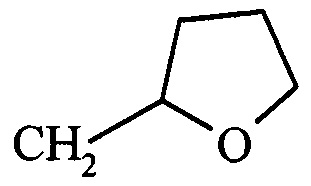
R3=Me; Pr; i-Pr; t-Bu; CH2Ph; CH2CH2F; CH2CH2Ad; (CH2)7CH3;
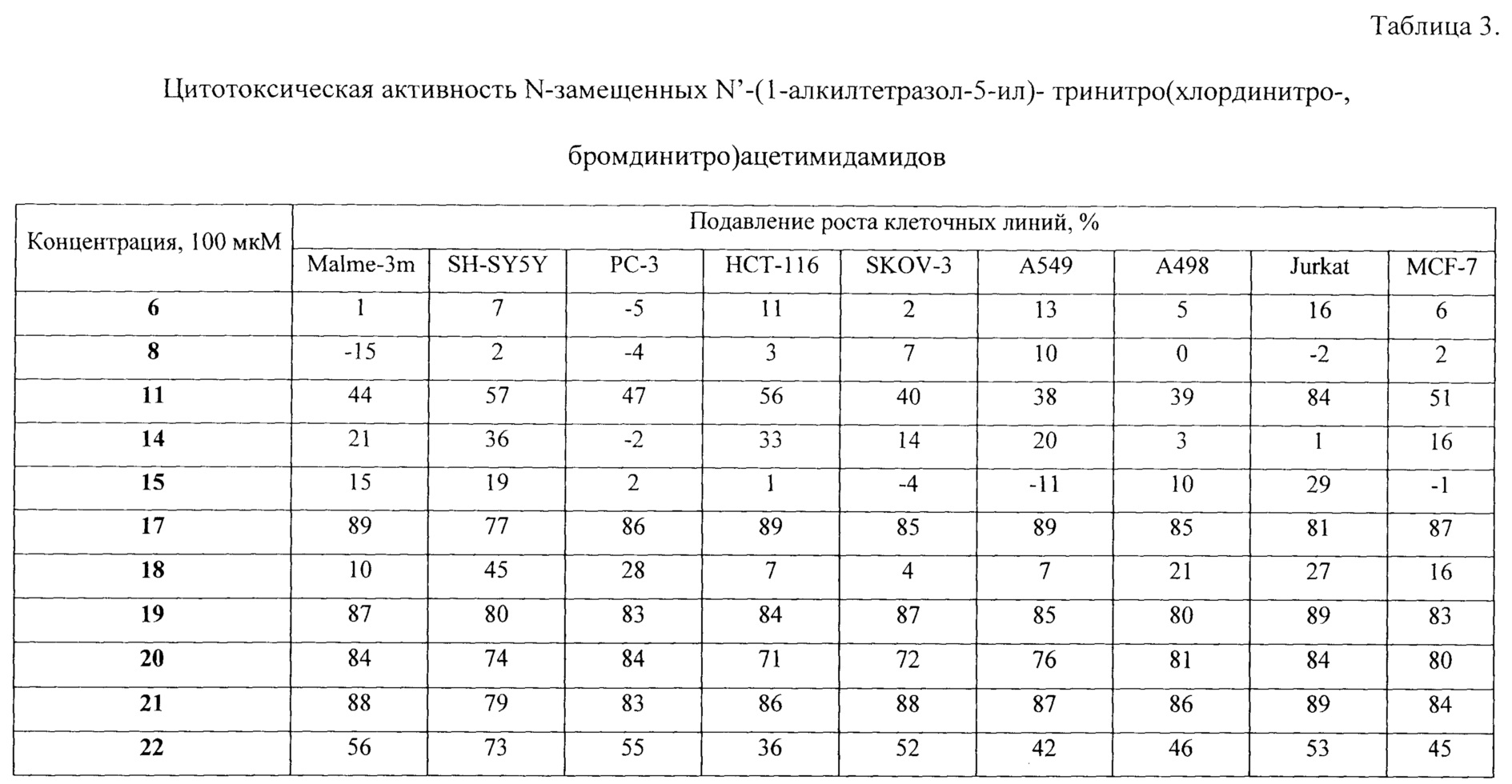
Приложение 1.
Цитотоксическая активность N-замещенных N'-(1-алкилтетразол-5-ил)-тринитроацетимидамидов и их производных.
На основе N-замещенных N'-(1-алкилтетразол-5-ил)-тринитроацетимидамидов получен ряд производных, которые обладают цитотоксической активностью на некоторых клеточных линиях опухолей человека in vitro.
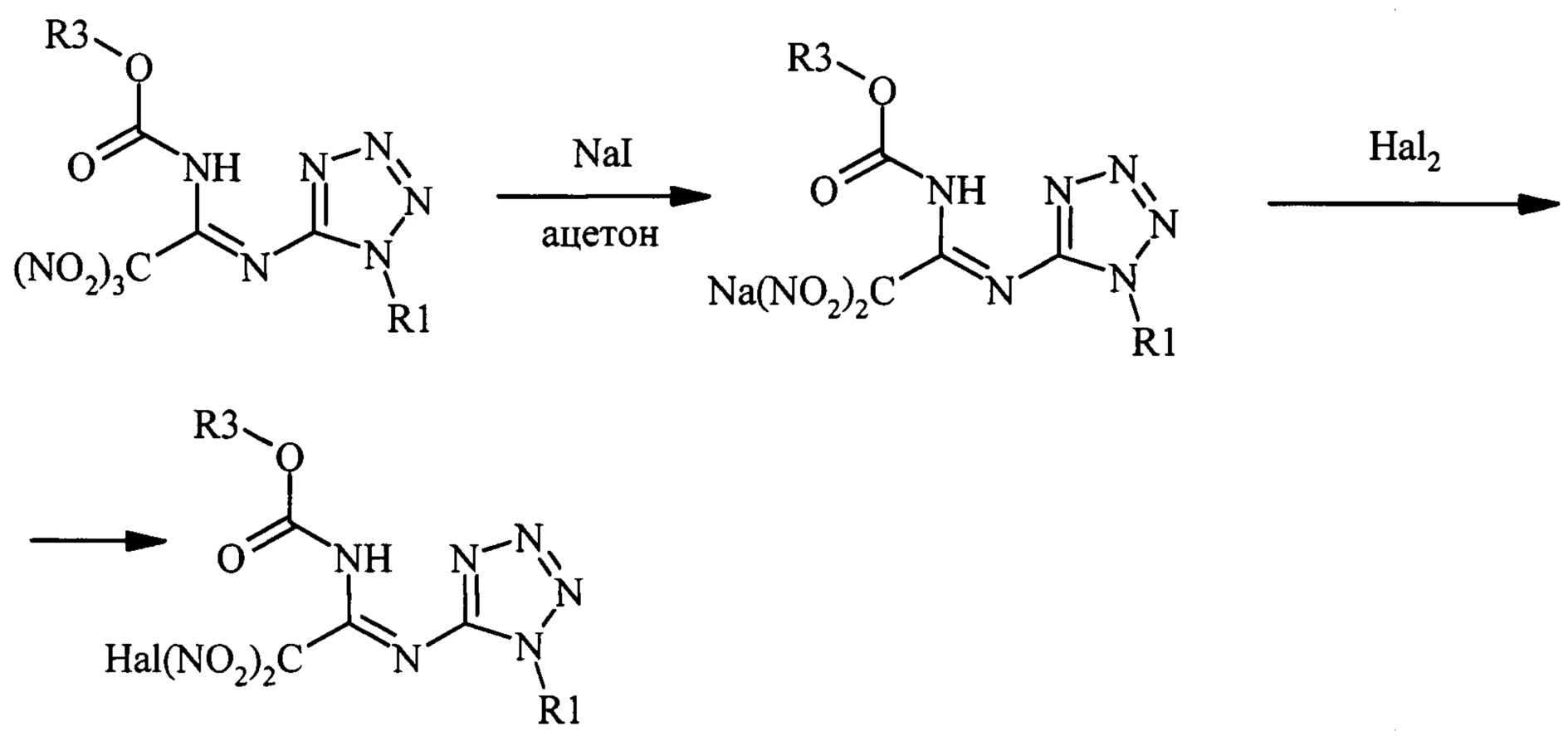
Денитрованием N-замещенных N'-(1-алкилтетразол-5-ил)-тринитроацетимидамидов синтезированы натриевые соли N-замещенных N'-(1-алкилтетразол-5-ил)-динитроацетимидамидов, из которые получены N-замещенные N'-(1-алкилтетразол-5-ил)-хлор(бром)динитроацетимидамиды.
Claims (7)
1. N-Замещенные N'-(1-алкилтетразол-5-ил)-тринитроацетимидамиды общей формулы:
где R1=СН3; СН2-СН=СН2; Ad;
R2=Н; COOR3;
R3=Me; Pr; i-Pr; t-Bu; CH2Ph; CH2CH2F; CH2CH2Ad; (CH2)7CH3;
2. Способ получения N-замещенных N'-(1-алкилтетразол-5-ил)-тринитроацетимидамидов по п. 1, заключающийся во взаимодействии 3-алкил-5-тринитрометилтетразоло[1,5-а]-1,3,5-триазин-7-онов с водой в среде ацетона или спиртами в среде дихлорэтана или самого спирта.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2016150796A RU2677337C2 (ru) | 2016-12-22 | 2016-12-22 | N-замещенные N'-(1-алкилтетразол-5-ил)-тринитроацетимидамиды и способ их получения |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2016150796A RU2677337C2 (ru) | 2016-12-22 | 2016-12-22 | N-замещенные N'-(1-алкилтетразол-5-ил)-тринитроацетимидамиды и способ их получения |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| RU2016150796A RU2016150796A (ru) | 2018-06-26 |
| RU2016150796A3 RU2016150796A3 (ru) | 2018-08-31 |
| RU2677337C2 true RU2677337C2 (ru) | 2019-01-16 |
Family
ID=62713129
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2016150796A RU2677337C2 (ru) | 2016-12-22 | 2016-12-22 | N-замещенные N'-(1-алкилтетразол-5-ил)-тринитроацетимидамиды и способ их получения |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2677337C2 (ru) |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0234557A1 (en) * | 1986-02-25 | 1987-09-02 | Merrell Dow Pharmaceuticals Inc. | 3-(1H-Tetrazol-5-yl)thieno[2,3-d]pyrimidin-4(3H)-ones |
| RU2522437C2 (ru) * | 2012-07-23 | 2014-07-10 | Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования "Астраханский государственный университет" | Способ получения гидразонов нитро-тетразол-5-карбальдегида |
-
2016
- 2016-12-22 RU RU2016150796A patent/RU2677337C2/ru not_active IP Right Cessation
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0234557A1 (en) * | 1986-02-25 | 1987-09-02 | Merrell Dow Pharmaceuticals Inc. | 3-(1H-Tetrazol-5-yl)thieno[2,3-d]pyrimidin-4(3H)-ones |
| RU2522437C2 (ru) * | 2012-07-23 | 2014-07-10 | Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования "Астраханский государственный университет" | Способ получения гидразонов нитро-тетразол-5-карбальдегида |
Non-Patent Citations (1)
| Title |
|---|
| Дорохов В.А. и др. "Синтез N-(тетразол-5-ил)амидинов из 5-аминотетразола и нитрилов с использованием органоборанов" Известия Академии наук СССР, Серия Химическая, N11, 1987, 2622-2624. R.A. Henry et al. "Mono-alkylation of Sodium 5-Aminotetrazole in Aqueous Medium" Journal of the American Chemical Society, vol.76, N3, 1954, 923-926. A.P. Vinogradoff et al. "Development of a New Synthesis of 3-(1H-Tetrazol-5-yl)-4-(3H)-quinazolinone, Sodium Salt via an Amidine Intermediate" Journal of Heterocyclic Chemistry, vol.26, N1, 1989, 97-103. * |
Also Published As
| Publication number | Publication date |
|---|---|
| RU2016150796A3 (ru) | 2018-08-31 |
| RU2016150796A (ru) | 2018-06-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Sączewski et al. | Synthesis, structure and anticancer activity of novel 2, 4-diamino-1, 3, 5-triazine derivatives | |
| JP2016519653A (ja) | Ido阻害剤 | |
| US4900836A (en) | (3-amino-1H-pyrazol-4-yl) (aryl)methanones | |
| Wang et al. | One-pot synthesis of 1 H-isochromenes and 1, 2-dihydroisoquinolines by a sequential isocyanide-based multicomponent/Wittig reaction | |
| CA2769474A1 (fr) | Derives d'acyl-guanidines modulateurs de la voie de signalisation des proteines hedgehog | |
| JP5529843B2 (ja) | 置換シクロヘキシルジアミン | |
| RU2707197C1 (ru) | 9-Ароил-8-гидрокси-6-(2-гидроксиэтил)-1,3,6-триазаспиро[4,4]нон-8-ен-2,4,7-трионы, обладающие анальгетической активностью, и способ их получения | |
| CN102838571A (zh) | 含γ-亚基丁烯内酯穿心莲内酯衍生物、其合成方法和用途 | |
| JP6190067B2 (ja) | フルオロフェニルピラゾール化合物 | |
| Gein et al. | Synthesis and Antiinflammatory and Analgesic Activity of 1-(2-aminoethyl)-5-aryl-4-acyl-3-hydroxy-3-pyrrolin-2-ones | |
| Voitekhovich et al. | Synthesis of new functionally substituted 1-R-tetrazoles and their 5-amino derivatives | |
| RU2677337C2 (ru) | N-замещенные N'-(1-алкилтетразол-5-ил)-тринитроацетимидамиды и способ их получения | |
| Nesterkina et al. | Synthesis and anticonvulsant activity of menthyl γ-aminobutyrate | |
| RU2607920C2 (ru) | Этиловые эфиры 2-амино-1-бензоиламино-4-оксо-5-(2-оксо-2-арил-этилиден)-4,5-дигидро-1h-пирролидин-3-карбоновых кислот, проявляющие противоопухолевую активность, и способ их получения | |
| RU2503671C1 (ru) | (Z)-2-[(3-КАРБАМОИЛ-4,5,6,7-ТЕТРАГИДРОБЕНЗО[b]ТИЕН-2-ИЛ)АМИНО]-4-(4-R-ФЕНИЛ)-4-ОКСОБУТ-2-ЕНОВЫЕ КИСЛОТЫ, ОБЛАДАЮЩИЕ АНАЛЬГЕТИЧЕСКОЙ АКТИВНОСТЬЮ | |
| RU2404987C2 (ru) | Антинеоплазические соединения и фармацевтические композиции на их основе | |
| CN114206904B (zh) | 选择性bcrp/abcg2转运蛋白抑制剂作为消除抗癌药物耐药性的药物 | |
| Efimova et al. | Reactions of 1-Amino-2-nitroguanidine with 2-Aryl (hetaryl)-1-nitro-1-ethoxycarbonyl (benzoyl) ethenes | |
| JP5715146B2 (ja) | 5−(2−アミノ−ピリミジン−4−イル)−2−アリール−1h−ピロール−3−カルボキサミドの調製方法 | |
| RU2396263C2 (ru) | Бис{3-фенил-1-[2-(5-метил-1,3,4-тиадиазолил)]карбоксамидо-1,3-пропандионато}марганец, обладающий противовоспалительной и анальгетической активностью | |
| RU2824814C2 (ru) | [1,2,4]Триазоло[3,4-b][1,3,4]тиадиазины, проявляющие активность против вируса гриппа А, и способ их получения | |
| CN101314603B (zh) | 缬氨酸保护的咪唑并[1,2-a]嘌呤三环碱基开环核苷类化合物、其制备方法和用途 | |
| RU2598607C1 (ru) | Способ получения 5-гетарилметиленпиримидин-2,4,6-трионов | |
| CN101225049A (zh) | β-榄香烯氨基酸衍生物及其合成方法和用途 | |
| RU2404978C2 (ru) | Калиевые или гидразиниевые соли 4-динитрометил-1,2,3-триазолов, обладающие гербицидной активностью |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20191223 |