RU2668373C1 - Композиции, содержащие аминокислоты для применения при лечении инсульта у пациентов с дисфагией - Google Patents
Композиции, содержащие аминокислоты для применения при лечении инсульта у пациентов с дисфагией Download PDFInfo
- Publication number
- RU2668373C1 RU2668373C1 RU2017112492A RU2017112492A RU2668373C1 RU 2668373 C1 RU2668373 C1 RU 2668373C1 RU 2017112492 A RU2017112492 A RU 2017112492A RU 2017112492 A RU2017112492 A RU 2017112492A RU 2668373 C1 RU2668373 C1 RU 2668373C1
- Authority
- RU
- Russia
- Prior art keywords
- patients
- stroke
- amino acids
- dysphagia
- active substance
- Prior art date
Links
- 239000000203 mixture Substances 0.000 title claims abstract description 75
- 208000019505 Deglutition disease Diseases 0.000 title claims abstract description 73
- 150000001413 amino acids Chemical class 0.000 title claims abstract description 57
- 208000006011 Stroke Diseases 0.000 title description 81
- 229940024606 amino acid Drugs 0.000 claims abstract description 56
- 230000004054 inflammatory process Effects 0.000 claims abstract description 40
- 239000013543 active substance Substances 0.000 claims abstract description 28
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 claims abstract description 27
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 claims abstract description 27
- 230000009885 systemic effect Effects 0.000 claims abstract description 19
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 claims abstract description 17
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 claims abstract description 17
- 239000004472 Lysine Substances 0.000 claims abstract description 17
- 229960000310 isoleucine Drugs 0.000 claims abstract description 17
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 claims abstract description 17
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 claims abstract description 16
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical compound CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 claims abstract description 16
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 claims abstract description 16
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Natural products CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 claims abstract description 16
- 229930182817 methionine Natural products 0.000 claims abstract description 16
- 239000004474 valine Substances 0.000 claims abstract description 16
- QIVBCDIJIAJPQS-VIFPVBQESA-N L-tryptophane Chemical compound C1=CC=C2C(C[C@H](N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-VIFPVBQESA-N 0.000 claims abstract description 15
- AYFVYJQAPQTCCC-UHFFFAOYSA-N Threonine Natural products CC(O)C(N)C(O)=O AYFVYJQAPQTCCC-UHFFFAOYSA-N 0.000 claims abstract description 15
- 239000004473 Threonine Substances 0.000 claims abstract description 15
- QIVBCDIJIAJPQS-UHFFFAOYSA-N Tryptophan Natural products C1=CC=C2C(CC(N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-UHFFFAOYSA-N 0.000 claims abstract description 15
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 claims abstract description 14
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 claims abstract description 13
- AYFVYJQAPQTCCC-GBXIJSLDSA-N L-threonine Chemical compound C[C@@H](O)[C@H](N)C(O)=O AYFVYJQAPQTCCC-GBXIJSLDSA-N 0.000 claims abstract description 13
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 claims abstract description 13
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 claims abstract description 13
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 claims abstract description 12
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 claims abstract description 12
- 239000002562 thickening agent Substances 0.000 claims abstract description 11
- 229960003067 cystine Drugs 0.000 claims abstract description 9
- 239000000126 substance Substances 0.000 claims abstract description 5
- LEVWYRKDKASIDU-QWWZWVQMSA-N D-cystine Chemical compound OC(=O)[C@H](N)CSSC[C@@H](N)C(O)=O LEVWYRKDKASIDU-QWWZWVQMSA-N 0.000 claims abstract 3
- 235000001014 amino acid Nutrition 0.000 claims description 55
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 claims description 8
- 229920002752 Konjac Polymers 0.000 claims description 6
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 claims description 6
- 235000004279 alanine Nutrition 0.000 claims description 6
- 150000001720 carbohydrates Chemical class 0.000 claims description 6
- 235000014633 carbohydrates Nutrition 0.000 claims description 6
- 239000000252 konjac Substances 0.000 claims description 6
- -1 methylhydroxypropyl Chemical group 0.000 claims description 5
- 239000004471 Glycine Substances 0.000 claims description 4
- 239000000654 additive Substances 0.000 claims description 4
- 239000000230 xanthan gum Substances 0.000 claims description 4
- 229920001285 xanthan gum Polymers 0.000 claims description 4
- 235000010493 xanthan gum Nutrition 0.000 claims description 4
- 229940082509 xanthan gum Drugs 0.000 claims description 4
- LUEWUZLMQUOBSB-FSKGGBMCSA-N (2s,3s,4s,5s,6r)-2-[(2r,3s,4r,5r,6s)-6-[(2r,3s,4r,5s,6s)-4,5-dihydroxy-2-(hydroxymethyl)-6-[(2r,4r,5s,6r)-4,5,6-trihydroxy-2-(hydroxymethyl)oxan-3-yl]oxyoxan-3-yl]oxy-4,5-dihydroxy-2-(hydroxymethyl)oxan-3-yl]oxy-6-(hydroxymethyl)oxane-3,4,5-triol Chemical compound O[C@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@@H](O[C@@H]2[C@H](O[C@@H](OC3[C@H](O[C@@H](O)[C@@H](O)[C@H]3O)CO)[C@@H](O)[C@H]2O)CO)[C@H](O)[C@H]1O LUEWUZLMQUOBSB-FSKGGBMCSA-N 0.000 claims description 3
- RBCOYOYDYNXAFA-UHFFFAOYSA-L (5-hydroxy-4,6-dimethylpyridin-3-yl)methyl phosphate Chemical compound CC1=NC=C(COP([O-])([O-])=O)C(C)=C1O RBCOYOYDYNXAFA-UHFFFAOYSA-L 0.000 claims description 3
- 244000247812 Amorphophallus rivieri Species 0.000 claims description 3
- 235000001206 Amorphophallus rivieri Nutrition 0.000 claims description 3
- 229920002581 Glucomannan Polymers 0.000 claims description 3
- 229920000084 Gum arabic Polymers 0.000 claims description 3
- 229920000881 Modified starch Polymers 0.000 claims description 3
- 239000000205 acacia gum Substances 0.000 claims description 3
- 235000010489 acacia gum Nutrition 0.000 claims description 3
- 239000001913 cellulose Substances 0.000 claims description 3
- 229920002678 cellulose Polymers 0.000 claims description 3
- 229940046240 glucomannan Drugs 0.000 claims description 3
- 235000010485 konjac Nutrition 0.000 claims description 3
- 235000019823 konjac gum Nutrition 0.000 claims description 3
- 235000019426 modified starch Nutrition 0.000 claims description 3
- JZRWCGZRTZMZEH-UHFFFAOYSA-N thiamine Chemical compound CC1=C(CCO)SC=[N+]1CC1=CN=C(C)N=C1N JZRWCGZRTZMZEH-UHFFFAOYSA-N 0.000 claims description 3
- 235000013343 vitamin Nutrition 0.000 claims description 3
- 239000011782 vitamin Substances 0.000 claims description 3
- 229930003231 vitamin Natural products 0.000 claims description 3
- 229940088594 vitamin Drugs 0.000 claims description 3
- 235000019156 vitamin B Nutrition 0.000 claims description 3
- 239000011720 vitamin B Substances 0.000 claims description 3
- MTCFGRXMJLQNBG-REOHCLBHSA-N (2S)-2-Amino-3-hydroxypropansäure Chemical compound OC[C@H](N)C(O)=O MTCFGRXMJLQNBG-REOHCLBHSA-N 0.000 claims description 2
- 239000004475 Arginine Substances 0.000 claims description 2
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 claims description 2
- ONIBWKKTOPOVIA-BYPYZUCNSA-N L-Proline Chemical compound OC(=O)[C@@H]1CCCN1 ONIBWKKTOPOVIA-BYPYZUCNSA-N 0.000 claims description 2
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 claims description 2
- ONIBWKKTOPOVIA-UHFFFAOYSA-N Proline Natural products OC(=O)C1CCCN1 ONIBWKKTOPOVIA-UHFFFAOYSA-N 0.000 claims description 2
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 claims description 2
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 claims description 2
- 235000013922 glutamic acid Nutrition 0.000 claims description 2
- 239000004220 glutamic acid Substances 0.000 claims description 2
- 210000004698 lymphocyte Anatomy 0.000 abstract description 26
- 206010061218 Inflammation Diseases 0.000 abstract description 23
- 210000004369 blood Anatomy 0.000 abstract description 21
- 239000008280 blood Substances 0.000 abstract description 21
- 238000000034 method Methods 0.000 abstract description 16
- 230000007423 decrease Effects 0.000 abstract description 13
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 abstract description 9
- 239000008103 glucose Substances 0.000 abstract description 9
- 210000002381 plasma Anatomy 0.000 abstract description 9
- 210000002966 serum Anatomy 0.000 abstract description 9
- 102000006395 Globulins Human genes 0.000 abstract description 8
- 108010044091 Globulins Proteins 0.000 abstract description 8
- 210000000440 neutrophil Anatomy 0.000 abstract description 8
- 230000000694 effects Effects 0.000 abstract description 7
- 238000011084 recovery Methods 0.000 abstract description 7
- 102000014702 Haptoglobin Human genes 0.000 abstract description 5
- 108050005077 Haptoglobin Proteins 0.000 abstract description 5
- 230000008569 process Effects 0.000 abstract description 5
- 102000011767 Acute-Phase Proteins Human genes 0.000 abstract description 2
- 108010062271 Acute-Phase Proteins Proteins 0.000 abstract description 2
- 238000010606 normalization Methods 0.000 abstract description 2
- 230000008092 positive effect Effects 0.000 abstract description 2
- 239000003814 drug Substances 0.000 abstract 2
- 235000020776 essential amino acid Nutrition 0.000 description 79
- 239000003797 essential amino acid Substances 0.000 description 79
- 210000003205 muscle Anatomy 0.000 description 54
- 108090000623 proteins and genes Proteins 0.000 description 31
- 235000018102 proteins Nutrition 0.000 description 30
- 102000004169 proteins and genes Human genes 0.000 description 30
- 230000014616 translation Effects 0.000 description 26
- 238000001243 protein synthesis Methods 0.000 description 24
- 229960003136 leucine Drugs 0.000 description 19
- 235000005772 leucine Nutrition 0.000 description 19
- 239000000902 placebo Substances 0.000 description 18
- 229940068196 placebo Drugs 0.000 description 18
- 230000002829 reductive effect Effects 0.000 description 17
- 230000006872 improvement Effects 0.000 description 15
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 15
- 102000008934 Muscle Proteins Human genes 0.000 description 14
- 108010074084 Muscle Proteins Proteins 0.000 description 14
- 230000001154 acute effect Effects 0.000 description 14
- 230000017854 proteolysis Effects 0.000 description 14
- 150000005693 branched-chain amino acids Chemical class 0.000 description 13
- 235000018977 lysine Nutrition 0.000 description 12
- 229960004799 tryptophan Drugs 0.000 description 12
- 230000022558 protein metabolic process Effects 0.000 description 11
- 229960002898 threonine Drugs 0.000 description 11
- 235000008521 threonine Nutrition 0.000 description 11
- 230000001195 anabolic effect Effects 0.000 description 10
- 235000013305 food Nutrition 0.000 description 10
- 229960002885 histidine Drugs 0.000 description 10
- 235000014304 histidine Nutrition 0.000 description 10
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 10
- 235000016709 nutrition Nutrition 0.000 description 10
- 229960005190 phenylalanine Drugs 0.000 description 10
- 230000009747 swallowing Effects 0.000 description 10
- XOAAWQZATWQOTB-UHFFFAOYSA-N taurine Chemical compound NCCS(O)(=O)=O XOAAWQZATWQOTB-UHFFFAOYSA-N 0.000 description 10
- 229960004441 tyrosine Drugs 0.000 description 10
- 206010049645 Hypercatabolism Diseases 0.000 description 9
- 235000005911 diet Nutrition 0.000 description 9
- 230000037213 diet Effects 0.000 description 9
- 230000001976 improved effect Effects 0.000 description 9
- 239000007788 liquid Substances 0.000 description 9
- 230000035764 nutrition Effects 0.000 description 9
- 238000012360 testing method Methods 0.000 description 9
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 9
- 230000015572 biosynthetic process Effects 0.000 description 8
- 230000015556 catabolic process Effects 0.000 description 8
- 230000007246 mechanism Effects 0.000 description 8
- 238000004458 analytical method Methods 0.000 description 7
- 230000003247 decreasing effect Effects 0.000 description 7
- 229960004452 methionine Drugs 0.000 description 7
- 238000007619 statistical method Methods 0.000 description 7
- DCXYFEDJOCDNAF-UHFFFAOYSA-N Asparagine Natural products OC(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-N 0.000 description 6
- DCXYFEDJOCDNAF-REOHCLBHSA-N L-asparagine Chemical compound OC(=O)[C@@H](N)CC(N)=O DCXYFEDJOCDNAF-REOHCLBHSA-N 0.000 description 6
- LEVWYRKDKASIDU-IMJSIDKUSA-N L-cystine Chemical compound [O-]C(=O)[C@@H]([NH3+])CSSC[C@H]([NH3+])C([O-])=O LEVWYRKDKASIDU-IMJSIDKUSA-N 0.000 description 6
- 229960001230 asparagine Drugs 0.000 description 6
- 235000009582 asparagine Nutrition 0.000 description 6
- 210000004556 brain Anatomy 0.000 description 6
- 230000002596 correlated effect Effects 0.000 description 6
- 238000009826 distribution Methods 0.000 description 6
- 238000005259 measurement Methods 0.000 description 6
- 208000010125 myocardial infarction Diseases 0.000 description 6
- 230000004044 response Effects 0.000 description 6
- 238000002560 therapeutic procedure Methods 0.000 description 6
- 108010088751 Albumins Proteins 0.000 description 5
- 102000009027 Albumins Human genes 0.000 description 5
- 102000004127 Cytokines Human genes 0.000 description 5
- 108090000695 Cytokines Proteins 0.000 description 5
- 102000004877 Insulin Human genes 0.000 description 5
- 108090001061 Insulin Proteins 0.000 description 5
- 206010022489 Insulin Resistance Diseases 0.000 description 5
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 5
- 229920002774 Maltodextrin Polymers 0.000 description 5
- 108010071690 Prealbumin Proteins 0.000 description 5
- 102000007584 Prealbumin Human genes 0.000 description 5
- 102000004338 Transferrin Human genes 0.000 description 5
- 108090000901 Transferrin Proteins 0.000 description 5
- 229960003767 alanine Drugs 0.000 description 5
- 230000037396 body weight Effects 0.000 description 5
- 230000006378 damage Effects 0.000 description 5
- 210000003414 extremity Anatomy 0.000 description 5
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 5
- 235000004554 glutamine Nutrition 0.000 description 5
- 229940125396 insulin Drugs 0.000 description 5
- 230000000302 ischemic effect Effects 0.000 description 5
- 238000004519 manufacturing process Methods 0.000 description 5
- 239000000463 material Substances 0.000 description 5
- 230000002503 metabolic effect Effects 0.000 description 5
- 230000004060 metabolic process Effects 0.000 description 5
- 210000002027 skeletal muscle Anatomy 0.000 description 5
- 238000003786 synthesis reaction Methods 0.000 description 5
- 229960003080 taurine Drugs 0.000 description 5
- 239000012581 transferrin Substances 0.000 description 5
- 208000001072 type 2 diabetes mellitus Diseases 0.000 description 5
- 102000004889 Interleukin-6 Human genes 0.000 description 4
- 108090001005 Interleukin-6 Proteins 0.000 description 4
- JVTAAEKCZFNVCJ-UHFFFAOYSA-M Lactate Chemical compound CC(O)C([O-])=O JVTAAEKCZFNVCJ-UHFFFAOYSA-M 0.000 description 4
- 239000005913 Maltodextrin Substances 0.000 description 4
- 210000005006 adaptive immune system Anatomy 0.000 description 4
- 210000000577 adipose tissue Anatomy 0.000 description 4
- 230000008859 change Effects 0.000 description 4
- 239000003246 corticosteroid Substances 0.000 description 4
- 238000006731 degradation reaction Methods 0.000 description 4
- 210000004185 liver Anatomy 0.000 description 4
- 229940035034 maltodextrin Drugs 0.000 description 4
- 235000021075 protein intake Nutrition 0.000 description 4
- 239000013589 supplement Substances 0.000 description 4
- 238000011870 unpaired t-test Methods 0.000 description 4
- 102100030840 AT-rich interactive domain-containing protein 4B Human genes 0.000 description 3
- 101000792935 Homo sapiens AT-rich interactive domain-containing protein 4B Proteins 0.000 description 3
- 206010061216 Infarction Diseases 0.000 description 3
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 3
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 3
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 description 3
- 235000003704 aspartic acid Nutrition 0.000 description 3
- 229960005261 aspartic acid Drugs 0.000 description 3
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 3
- 206010008118 cerebral infarction Diseases 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- 210000003743 erythrocyte Anatomy 0.000 description 3
- 239000000796 flavoring agent Substances 0.000 description 3
- 235000019634 flavors Nutrition 0.000 description 3
- 230000037406 food intake Effects 0.000 description 3
- 230000006870 function Effects 0.000 description 3
- 229960002743 glutamine Drugs 0.000 description 3
- 210000002865 immune cell Anatomy 0.000 description 3
- 210000000987 immune system Anatomy 0.000 description 3
- 230000007574 infarction Effects 0.000 description 3
- 230000003993 interaction Effects 0.000 description 3
- 208000028867 ischemia Diseases 0.000 description 3
- 210000000265 leukocyte Anatomy 0.000 description 3
- 230000033001 locomotion Effects 0.000 description 3
- 235000012054 meals Nutrition 0.000 description 3
- 208000015380 nutritional deficiency disease Diseases 0.000 description 3
- 230000036961 partial effect Effects 0.000 description 3
- 210000005105 peripheral blood lymphocyte Anatomy 0.000 description 3
- 239000000047 product Substances 0.000 description 3
- 238000004062 sedimentation Methods 0.000 description 3
- 239000000758 substrate Substances 0.000 description 3
- 230000009469 supplementation Effects 0.000 description 3
- 238000012549 training Methods 0.000 description 3
- 208000016261 weight loss Diseases 0.000 description 3
- 230000004580 weight loss Effects 0.000 description 3
- OCUSNPIJIZCRSZ-ZTZWCFDHSA-N (2s)-2-amino-3-methylbutanoic acid;(2s)-2-amino-4-methylpentanoic acid;(2s,3s)-2-amino-3-methylpentanoic acid Chemical compound CC(C)[C@H](N)C(O)=O.CC[C@H](C)[C@H](N)C(O)=O.CC(C)C[C@H](N)C(O)=O OCUSNPIJIZCRSZ-ZTZWCFDHSA-N 0.000 description 2
- 102000004506 Blood Proteins Human genes 0.000 description 2
- 108010017384 Blood Proteins Proteins 0.000 description 2
- 201000006474 Brain Ischemia Diseases 0.000 description 2
- 108010074051 C-Reactive Protein Proteins 0.000 description 2
- 102100032752 C-reactive protein Human genes 0.000 description 2
- 206010008120 Cerebral ischaemia Diseases 0.000 description 2
- 108010049003 Fibrinogen Proteins 0.000 description 2
- 102000008946 Fibrinogen Human genes 0.000 description 2
- 206010019468 Hemiplegia Diseases 0.000 description 2
- 101000795167 Homo sapiens Tumor necrosis factor receptor superfamily member 13B Proteins 0.000 description 2
- 208000032382 Ischaemic stroke Diseases 0.000 description 2
- 206010025327 Lymphopenia Diseases 0.000 description 2
- 208000002720 Malnutrition Diseases 0.000 description 2
- 208000010428 Muscle Weakness Diseases 0.000 description 2
- 206010028289 Muscle atrophy Diseases 0.000 description 2
- 206010028372 Muscular weakness Diseases 0.000 description 2
- 206010028980 Neoplasm Diseases 0.000 description 2
- 206010033799 Paralysis Diseases 0.000 description 2
- 102100029675 Tumor necrosis factor receptor superfamily member 13B Human genes 0.000 description 2
- 230000003044 adaptive effect Effects 0.000 description 2
- 230000004721 adaptive immunity Effects 0.000 description 2
- 238000013528 artificial neural network Methods 0.000 description 2
- 229940009098 aspartate Drugs 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 239000000090 biomarker Substances 0.000 description 2
- 201000011510 cancer Diseases 0.000 description 2
- 210000004027 cell Anatomy 0.000 description 2
- 208000026106 cerebrovascular disease Diseases 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 238000000546 chi-square test Methods 0.000 description 2
- 238000002591 computed tomography Methods 0.000 description 2
- 229960001334 corticosteroids Drugs 0.000 description 2
- DDRJAANPRJIHGJ-UHFFFAOYSA-N creatinine Chemical compound CN1CC(=O)NC1=N DDRJAANPRJIHGJ-UHFFFAOYSA-N 0.000 description 2
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 2
- 235000018417 cysteine Nutrition 0.000 description 2
- 229960002433 cysteine Drugs 0.000 description 2
- 230000001419 dependent effect Effects 0.000 description 2
- 238000003745 diagnosis Methods 0.000 description 2
- 201000010099 disease Diseases 0.000 description 2
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 2
- 238000001962 electrophoresis Methods 0.000 description 2
- 230000007717 exclusion Effects 0.000 description 2
- 229940012952 fibrinogen Drugs 0.000 description 2
- 238000002594 fluoroscopy Methods 0.000 description 2
- 235000012631 food intake Nutrition 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 239000003102 growth factor Substances 0.000 description 2
- 230000036541 health Effects 0.000 description 2
- 230000002008 hemorrhagic effect Effects 0.000 description 2
- 230000002157 hypercatabolic effect Effects 0.000 description 2
- 208000019016 inability to swallow Diseases 0.000 description 2
- 230000006698 induction Effects 0.000 description 2
- 239000004615 ingredient Substances 0.000 description 2
- 210000005007 innate immune system Anatomy 0.000 description 2
- 210000000936 intestine Anatomy 0.000 description 2
- 210000003734 kidney Anatomy 0.000 description 2
- 210000003127 knee Anatomy 0.000 description 2
- 231100001023 lymphopenia Toxicity 0.000 description 2
- 235000021073 macronutrients Nutrition 0.000 description 2
- 235000000824 malnutrition Nutrition 0.000 description 2
- 230000001071 malnutrition Effects 0.000 description 2
- 230000020763 muscle atrophy Effects 0.000 description 2
- 210000000663 muscle cell Anatomy 0.000 description 2
- 201000000585 muscular atrophy Diseases 0.000 description 2
- 230000000926 neurological effect Effects 0.000 description 2
- 230000036542 oxidative stress Effects 0.000 description 2
- 230000037361 pathway Effects 0.000 description 2
- 230000036470 plasma concentration Effects 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 230000002797 proteolythic effect Effects 0.000 description 2
- LXNHXLLTXMVWPM-UHFFFAOYSA-N pyridoxine Chemical compound CC1=NC=C(CO)C(CO)=C1O LXNHXLLTXMVWPM-UHFFFAOYSA-N 0.000 description 2
- QZAYGJVTTNCVMB-UHFFFAOYSA-N serotonin Chemical compound C1=C(O)C=C2C(CCN)=CNC2=C1 QZAYGJVTTNCVMB-UHFFFAOYSA-N 0.000 description 2
- 230000011664 signaling Effects 0.000 description 2
- 238000002630 speech therapy Methods 0.000 description 2
- 150000003431 steroids Chemical class 0.000 description 2
- 230000004936 stimulating effect Effects 0.000 description 2
- 230000002123 temporal effect Effects 0.000 description 2
- 230000001228 trophic effect Effects 0.000 description 2
- QDGAVODICPCDMU-UHFFFAOYSA-N 2-amino-3-[3-[bis(2-chloroethyl)amino]phenyl]propanoic acid Chemical compound OC(=O)C(N)CC1=CC=CC(N(CCCl)CCCl)=C1 QDGAVODICPCDMU-UHFFFAOYSA-N 0.000 description 1
- WBZFUFAFFUEMEI-UHFFFAOYSA-M Acesulfame k Chemical compound [K+].CC1=CC(=O)[N-]S(=O)(=O)O1 WBZFUFAFFUEMEI-UHFFFAOYSA-M 0.000 description 1
- 208000004476 Acute Coronary Syndrome Diseases 0.000 description 1
- 206010048998 Acute phase reaction Diseases 0.000 description 1
- 206010001497 Agitation Diseases 0.000 description 1
- 108010011485 Aspartame Proteins 0.000 description 1
- 206010003504 Aspiration Diseases 0.000 description 1
- 206010003694 Atrophy Diseases 0.000 description 1
- 239000004135 Bone phosphate Substances 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 102000007590 Calpain Human genes 0.000 description 1
- 108010032088 Calpain Proteins 0.000 description 1
- 206010007558 Cardiac failure chronic Diseases 0.000 description 1
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 1
- 238000002965 ELISA Methods 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 241001125671 Eretmochelys imbricata Species 0.000 description 1
- 102000003676 Glucocorticoid Receptors Human genes 0.000 description 1
- 108090000079 Glucocorticoid Receptors Proteins 0.000 description 1
- 206010020100 Hip fracture Diseases 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- XUJNEKJLAYXESH-REOHCLBHSA-N L-Cysteine Chemical compound SC[C@H](N)C(O)=O XUJNEKJLAYXESH-REOHCLBHSA-N 0.000 description 1
- 235000019766 L-Lysine Nutrition 0.000 description 1
- 240000008790 Musa x paradisiaca Species 0.000 description 1
- 235000018290 Musa x paradisiaca Nutrition 0.000 description 1
- 208000008238 Muscle Spasticity Diseases 0.000 description 1
- 208000029549 Muscle injury Diseases 0.000 description 1
- 206010029164 Nephrotic syndrome Diseases 0.000 description 1
- 208000001132 Osteoporosis Diseases 0.000 description 1
- 208000004210 Pressure Ulcer Diseases 0.000 description 1
- 208000037169 Retrograde Degeneration Diseases 0.000 description 1
- 238000000692 Student's t-test Methods 0.000 description 1
- 239000004376 Sucralose Substances 0.000 description 1
- 102000013530 TOR Serine-Threonine Kinases Human genes 0.000 description 1
- 108010065917 TOR Serine-Threonine Kinases Proteins 0.000 description 1
- 229930003451 Vitamin B1 Natural products 0.000 description 1
- 238000002835 absorbance Methods 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 235000010358 acesulfame potassium Nutrition 0.000 description 1
- 229960004998 acesulfame potassium Drugs 0.000 description 1
- 239000000619 acesulfame-K Substances 0.000 description 1
- 239000012190 activator Substances 0.000 description 1
- 208000038016 acute inflammation Diseases 0.000 description 1
- 208000012764 acute weight loss Diseases 0.000 description 1
- 230000004658 acute-phase response Effects 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 239000003263 anabolic agent Substances 0.000 description 1
- 238000000540 analysis of variance Methods 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 230000008321 arterial blood flow Effects 0.000 description 1
- 239000000605 aspartame Substances 0.000 description 1
- 235000010357 aspartame Nutrition 0.000 description 1
- IAOZJIPTCAWIRG-QWRGUYRKSA-N aspartame Chemical compound OC(=O)C[C@H](N)C(=O)N[C@H](C(=O)OC)CC1=CC=CC=C1 IAOZJIPTCAWIRG-QWRGUYRKSA-N 0.000 description 1
- 229960003438 aspartame Drugs 0.000 description 1
- 230000037444 atrophy Effects 0.000 description 1
- 210000003403 autonomic nervous system Anatomy 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 230000002146 bilateral effect Effects 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 235000019577 caloric intake Nutrition 0.000 description 1
- 230000001925 catabolic effect Effects 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 208000020832 chronic kidney disease Diseases 0.000 description 1
- 208000022831 chronic renal failure syndrome Diseases 0.000 description 1
- 230000004087 circulation Effects 0.000 description 1
- 230000003920 cognitive function Effects 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 238000013170 computed tomography imaging Methods 0.000 description 1
- 238000004590 computer program Methods 0.000 description 1
- 238000012937 correction Methods 0.000 description 1
- 238000010219 correlation analysis Methods 0.000 description 1
- 229940109239 creatinine Drugs 0.000 description 1
- 230000002638 denervation Effects 0.000 description 1
- 238000001212 derivatisation Methods 0.000 description 1
- 230000001627 detrimental effect Effects 0.000 description 1
- 206010012601 diabetes mellitus Diseases 0.000 description 1
- 230000029087 digestion Effects 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 230000004064 dysfunction Effects 0.000 description 1
- 230000002526 effect on cardiovascular system Effects 0.000 description 1
- 210000003038 endothelium Anatomy 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 239000003925 fat Substances 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 210000002950 fibroblast Anatomy 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- IRXSLJNXXZKURP-UHFFFAOYSA-N fluorenylmethyloxycarbonyl chloride Chemical compound C1=CC=C2C(COC(=O)Cl)C3=CC=CC=C3C2=C1 IRXSLJNXXZKURP-UHFFFAOYSA-N 0.000 description 1
- 230000005714 functional activity Effects 0.000 description 1
- 238000012812 general test Methods 0.000 description 1
- 238000010353 genetic engineering Methods 0.000 description 1
- 229960002449 glycine Drugs 0.000 description 1
- 230000002975 glyconeogenic effect Effects 0.000 description 1
- 210000003714 granulocyte Anatomy 0.000 description 1
- 208000037907 haemorrhagic injury Diseases 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 230000003054 hormonal effect Effects 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 1
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 1
- 230000003166 hypermetabolic effect Effects 0.000 description 1
- 230000028993 immune response Effects 0.000 description 1
- 230000036039 immunity Effects 0.000 description 1
- 208000015181 infectious disease Diseases 0.000 description 1
- 230000002757 inflammatory effect Effects 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 235000001705 insufficient nutrition Nutrition 0.000 description 1
- 229940100601 interleukin-6 Drugs 0.000 description 1
- 230000003585 interneuronal effect Effects 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 230000003447 ipsilateral effect Effects 0.000 description 1
- 208000037906 ischaemic injury Diseases 0.000 description 1
- 210000002414 leg Anatomy 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 210000005228 liver tissue Anatomy 0.000 description 1
- 238000011068 loading method Methods 0.000 description 1
- 238000007477 logistic regression Methods 0.000 description 1
- 210000003141 lower extremity Anatomy 0.000 description 1
- 210000001165 lymph node Anatomy 0.000 description 1
- 210000003712 lysosome Anatomy 0.000 description 1
- 230000001868 lysosomic effect Effects 0.000 description 1
- 210000002540 macrophage Anatomy 0.000 description 1
- 238000002595 magnetic resonance imaging Methods 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 108020004999 messenger RNA Proteins 0.000 description 1
- 230000004066 metabolic change Effects 0.000 description 1
- 235000020938 metabolic status Nutrition 0.000 description 1
- 239000011785 micronutrient Substances 0.000 description 1
- 235000013369 micronutrients Nutrition 0.000 description 1
- 210000001616 monocyte Anatomy 0.000 description 1
- 230000001095 motoneuron effect Effects 0.000 description 1
- 210000002161 motor neuron Anatomy 0.000 description 1
- 208000018731 motor weakness Diseases 0.000 description 1
- 230000004770 neurodegeneration Effects 0.000 description 1
- 230000002232 neuromuscular Effects 0.000 description 1
- 230000035771 neuroregeneration Effects 0.000 description 1
- 108020004707 nucleic acids Proteins 0.000 description 1
- 150000007523 nucleic acids Chemical class 0.000 description 1
- 102000039446 nucleic acids Human genes 0.000 description 1
- 235000008935 nutritious Nutrition 0.000 description 1
- 238000001584 occupational therapy Methods 0.000 description 1
- 229940127017 oral antidiabetic Drugs 0.000 description 1
- 230000000242 pagocytic effect Effects 0.000 description 1
- 239000000137 peptide hydrolase inhibitor Substances 0.000 description 1
- 210000005259 peripheral blood Anatomy 0.000 description 1
- 239000011886 peripheral blood Substances 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 230000002085 persistent effect Effects 0.000 description 1
- 210000001539 phagocyte Anatomy 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- ZWLUXSQADUDCSB-UHFFFAOYSA-N phthalaldehyde Chemical compound O=CC1=CC=CC=C1C=O ZWLUXSQADUDCSB-UHFFFAOYSA-N 0.000 description 1
- 238000000554 physical therapy Methods 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 238000004393 prognosis Methods 0.000 description 1
- 230000000750 progressive effect Effects 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- RADKZDMFGJYCBB-UHFFFAOYSA-N pyridoxal hydrochloride Natural products CC1=NC=C(CO)C(C=O)=C1O RADKZDMFGJYCBB-UHFFFAOYSA-N 0.000 description 1
- 210000003314 quadriceps muscle Anatomy 0.000 description 1
- 210000002321 radial artery Anatomy 0.000 description 1
- 230000007420 reactivation Effects 0.000 description 1
- 108020003175 receptors Proteins 0.000 description 1
- 102000005962 receptors Human genes 0.000 description 1
- 230000008929 regeneration Effects 0.000 description 1
- 238000011069 regeneration method Methods 0.000 description 1
- 230000014493 regulation of gene expression Effects 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 230000008439 repair process Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000000241 respiratory effect Effects 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 239000000523 sample Substances 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 229940076279 serotonin Drugs 0.000 description 1
- 230000019491 signal transduction Effects 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- IFGCUJZIWBUILZ-UHFFFAOYSA-N sodium 2-[[2-[[hydroxy-(3,4,5-trihydroxy-6-methyloxan-2-yl)oxyphosphoryl]amino]-4-methylpentanoyl]amino]-3-(1H-indol-3-yl)propanoic acid Chemical compound [Na+].C=1NC2=CC=CC=C2C=1CC(C(O)=O)NC(=O)C(CC(C)C)NP(O)(=O)OC1OC(C)C(O)C(O)C1O IFGCUJZIWBUILZ-UHFFFAOYSA-N 0.000 description 1
- 208000018198 spasticity Diseases 0.000 description 1
- 208000020431 spinal cord injury Diseases 0.000 description 1
- 210000000952 spleen Anatomy 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
- 235000019408 sucralose Nutrition 0.000 description 1
- BAQAVOSOZGMPRM-QBMZZYIRSA-N sucralose Chemical compound O[C@@H]1[C@@H](O)[C@@H](Cl)[C@@H](CO)O[C@@H]1O[C@@]1(CCl)[C@@H](O)[C@H](O)[C@@H](CCl)O1 BAQAVOSOZGMPRM-QBMZZYIRSA-N 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 229960003495 thiamine Drugs 0.000 description 1
- DPJRMOMPQZCRJU-UHFFFAOYSA-M thiamine hydrochloride Chemical compound Cl.[Cl-].CC1=C(CCO)SC=[N+]1CC1=CN=C(C)N=C1N DPJRMOMPQZCRJU-UHFFFAOYSA-M 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 238000012876 topography Methods 0.000 description 1
- 238000013518 transcription Methods 0.000 description 1
- 230000035897 transcription Effects 0.000 description 1
- 230000001052 transient effect Effects 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- 238000013519 translation Methods 0.000 description 1
- 238000012762 unpaired Student’s t-test Methods 0.000 description 1
- 210000001364 upper extremity Anatomy 0.000 description 1
- 230000002792 vascular Effects 0.000 description 1
- 210000004509 vascular smooth muscle cell Anatomy 0.000 description 1
- 210000001835 viscera Anatomy 0.000 description 1
- 235000010374 vitamin B1 Nutrition 0.000 description 1
- 239000011691 vitamin B1 Substances 0.000 description 1
- 235000019158 vitamin B6 Nutrition 0.000 description 1
- 239000011726 vitamin B6 Substances 0.000 description 1
- 229940011671 vitamin b6 Drugs 0.000 description 1
- 239000002023 wood Substances 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/195—Carboxylic acids, e.g. valproic acid having an amino group
- A61K31/197—Carboxylic acids, e.g. valproic acid having an amino group the amino and the carboxyl groups being attached to the same acyclic carbon chain, e.g. gamma-aminobutyric acid [GABA], beta-alanine, epsilon-aminocaproic acid or pantothenic acid
- A61K31/198—Alpha-amino acids, e.g. alanine or edetic acid [EDTA]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/403—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil condensed with carbocyclic rings, e.g. carbazole
- A61K31/404—Indoles, e.g. pindolol
- A61K31/405—Indole-alkanecarboxylic acids; Derivatives thereof, e.g. tryptophan, indomethacin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
- A61K31/4172—Imidazole-alkanecarboxylic acids, e.g. histidine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4415—Pyridoxine, i.e. Vitamin B6
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/506—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim not condensed and containing further heterocyclic rings
- A61K31/51—Thiamines, e.g. vitamin B1
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/66—Phosphorus compounds
- A61K31/675—Phosphorus compounds having nitrogen as a ring hetero atom, e.g. pyridoxal phosphate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Chemistry (AREA)
- Heart & Thoracic Surgery (AREA)
- Cardiology (AREA)
- Vascular Medicine (AREA)
- Urology & Nephrology (AREA)
- Rheumatology (AREA)
- Neurology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Physical Education & Sports Medicine (AREA)
- Pain & Pain Management (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
Abstract
Группа изобретений относится к медицине и касается применения композиции при лечении системного воспалительного процесса у пациентов после инсульта с дисфагией. Причем композиция содержит активное вещество, при этом упомянутое активное вещество состоит из аминокислот лейцин, изолейцин, валин, лизин, треонин, гистидин, фенилаланин, метионин, триптофан, тирозин, цистин, при этом композиция содержит один или более загустителей в количестве от 10 до 50 масс. % относительно массы активного вещества. Также предложено применение композиции при лечении системного воспалительного процесса у пациентов после инсульта. Группа изобретений обеспечивает лечение системного воспалительного процесса у указанных пациентов за счет снижения сывороточного уровня альфа-1 глобулина, гаптоглобулина и повышения сывороточных концентраций циркулирующих отрицательных белков острой фазы. Также группа изобретений обеспечивает нормализацию и снижение содержания глюкозы в плазе крови и усиливает восстановительные процессы по сравнению с процессами воспаления путем положительного влияния на соотношение нейтрофилов к лимфоцитам в циркулирующей крови. 2 н. и 9 з.п. ф-лы, 3 ил., 11 табл., 2 пр.
Description
Область техники
Настоящее изобретение относится к композициям для применения при лечении инсульта у пациентов, в частности пациентов с дисфагией.
Предшествующий уровень техники
Во всем мире инсульты являются ведущей причиной инвалидности. Приблизительно одна треть переживших инсульт являются постоянно нетрудоспособными в течение одного года после острого инсульта. Приблизительно две трети пациентов не полностью восстанавливаются после инсультов, при этом одна треть не может передвигаться без помощника. Более того, у полупарализованных субъектов, которые все еще могут передвигаться сами, способность к ходьбе понижена и энергетические затраты на ходьбу повышены по сравнению с эффективностью симметричной ходьбы. Помимо утраты центральных трофических эффектов и транссинаптической дегенерации нижних мотонейронов, изменения скелетных мышц после инсульта также могут потенциально способствовать инвалидности. Эти изменения включают изменение типа волокон в паретической (контралатеральной) стороне, повышенное замещение мышечной ткани жировой (миостеатоз), спастичность, неиспользование, недостаточное питание и незагруженность мышц. Предыдущее исследование показало, что скелетные мышцы пациентов после подострого инсульта подвержены постоянному системному воспалительному процессу, который может привести к гиперкатаболизму (разрушение белка выше, чем синтез белка). Данный воспалительный процесс неповрежденной стороны может способствовать инвалидизации пациента за счет инициации потери, как мышечной массы, так и силы, что приводит к инвалидности пациента. Данная проблема особо касается пациентов с дисфагией. Поэтому существует необходимость идентификации новых композиций, способных уменьшить вышеупомянутую проблему.
Краткое описание изобретения
Целью настоящего изобретения является предложить композиции, для применения при лечении инсульта у пациентов, в частности у пациентов с дисфагией, которые способны ослаблять вышеупомянутый постоянный системный воспалительный процесс, и таким образом ослаблять или даже превращать мышечный гиперкатаболизм (МН) в сбалансированный белковый обмен или мышечный анаболизм анаболической активности.
Перед употреблением, композиции, описанные в данном документе, диспергируют в жидкости, предпочтительно воде, которая приобретает идеальную вязкость и консистенцию для перорального приема пациентом с дисфагией.
Согласно настоящему описанию вышеупомянутой цели достигают за счет объекта изобретения, названного конкретно в следующей формуле изобретения, которую следует понимать как формирующую составную часть данного раскрытия.
Воплощение настоящего описания предлагает композицию для применения при лечении системного воспалительного процесса, ассоциированного после инсульта у пациентов, в частности у пациентов с дисфагией, причем композиция содержит активное вещество, при этом активное вещество содержит аминокислоты лейцин, изолейцин, валин, лизин, треонин и по меньшей мере одну из аминокислот гистидин, фенилаланин, метионин, триптофан, тирозин, цистин, композицию, дополнительно содержащую один или более загустителей в количестве от 10 масс. % до 50 масс. %, более предпочтительно от 20 масс. % до 30 масс. % активного вещества.
Загустители могут быть выбраны из ксантановой камеди, метилгидроксипропилцеллюлозы, камеди конжака, глюкоманнана конжака, аравийской камеди (камедь акации), модифицированных крахмалов.
Присутствие таких веществ в композиции позволяет сгустить жидкость, предпочтительно воду, в которой композицию диспергируют перед употреблением.
В некоторых воплощениях композиция, раскрытая в данном документе, дополнительно содержит витамины, предпочтительно выбранные из группы витаминов В, таких как витамин B1 и/или витамин В6.
В дальнейшем воплощении композиция также включает углеводы, добавки и/или вкусоароматические вещества.
Авторы изобретения обнаружили, что композиции, раскрытые в данном документе, способны превращать мышечный гиперкатаболизм в анаболизм ипсилатеральной (здоровой) руки пациентов после инсульта с дисфагией. Таким образом, может происходить лучшее восстановление физической независимости.
Дальнейшее воплощение настоящего описания предлагает композицию для применения при лечении системного воспалительного процесса, причем композиция содержит активное вещество, при этом активное вещество содержит аминокислоты лейцин, изолейцин, валин, лизин, треонин и по меньшей мере одну из аминокислот гистидин, фенилаланин, метионин, триптофан, тирозин, цистин.
Преимущество, связанное с применением композиций, описанных в данном документе, заключается в высокой переносимости композиций, которые можно вводить постоянно. В предпочтительном воплощении введение может осуществляться через достаточно длительный период для по меньшей мере частичного восстановления после инсульта.
Другое преимущество, связанное с применением композиций, описанных в данном документе, заключается в том факте, что применение аминокислот в свободном виде, содержащихся в активном веществе, позволяет получать такие композиции при сравнительно крайне низкой стоимости в отношении синтеза белков и факторов роста, посредством по существу известных и широкого применяемых в области получения композиций способов производства, основанных на свободных аминокислотах. Однако область применения изобретения также может быть распространена на аминокислоты, получаемые при помощи генетической инженерии или любого другого искусственного способа.
Краткое описание графических материалов
Изобретение в настоящем будет описано только посредством примеров, со ссылкой на прилагаемые фигуры, где:
- Фиг. 1 представляет собой схему исследуемой добавки с композицией, описанной в данном документе, по сравнению с плацебо в течение лечения пациентов после инсульта с дисфагией. Схема включает число пациентов, анализируемых в отношении основного итога (мышечный гиперкатаболизм здоровой руки); и
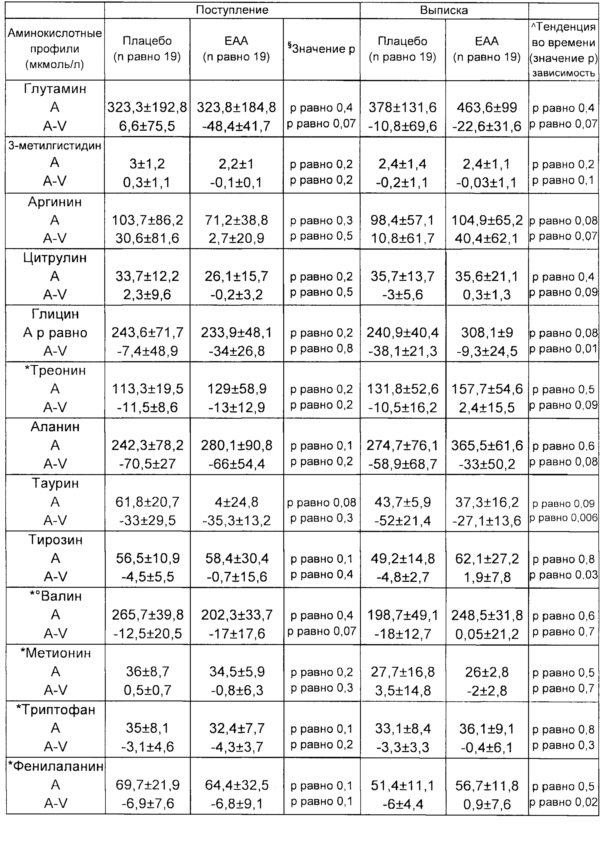
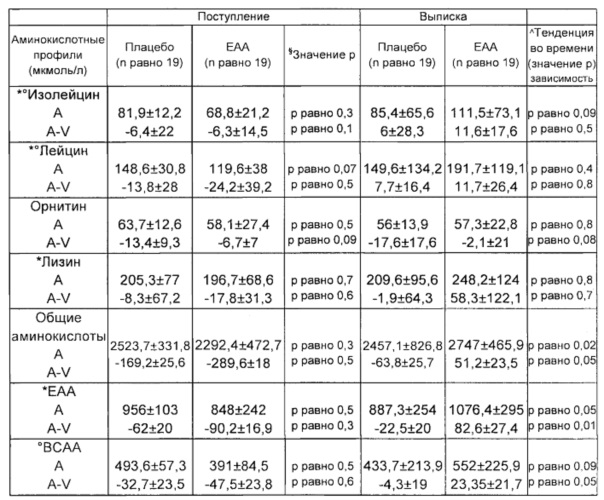
- Фиг. 2 представляет различия во временной динамике фенила, общих незаменимых аминокислот, общих аминокислот (А - V), и уровней общих аминокислот в артериальной крови в группе после инсульта. Точка 0 означает отсутствие захвата/высвобождения.
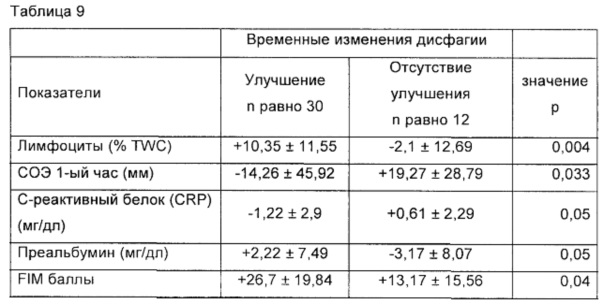
- Фиг. 3 представляет взаимосвязь между изменением со временем лимфоцитов периферической крови в виде % всех белых клеток и способности к глотанию (DOSS) во всей группе после инсульта (график а), у субъектов с плацебо (график b) и с лечением незаменимыми аминокислотами (график с). Число точек, наблюдаемых на графике, является меньшим, чем реальное число исследованных пациентов, из-за перекрывания значений в ряде случаев.
Подробное описание изобретения
В следующем описании многочисленные конкретные детали приведены для полного понимания воплощений. Воплощения могут быть реализованы на практике без одной или более конкретных деталей или при помощи других способов, компонентов, материалов и т.д. В других случаях хорошо известные структуры, материалы или операции не показаны или не описаны детально для того, чтобы избежать неясности воплощений.
Ссылка везде в данном описании на «одно воплощение» или «воплощение» означает, что отдельная черта, структура или характеристика, описанная в связи с воплощением, включена в по меньшей мере одно воплощение. Таким образом, фразы «в одном воплощении» или «в воплощении» в различных местах данного описания не обязательно все относятся к одному и тому же воплощению. Более того, отдельные черты, структуры или характеристики могут быть скомбинированы любым приемлемым способом в одном или более воплощении. Заголовки приведены в данном документе для удобства и не отражают объем и значение воплощений.
Раскрытая в данном документе композиция для применения в лечении инсульта у пациентов с дисфагией, а именно системного воспалительного процесса, ассоциированного с инсультом, содержит активное вещество, причем активное вещество содержит аминокислоты лейцин, изолейцин, валин, лизин, треонин и по меньшей мере одну из следующих аминокислот: гистидин, фенилаланин, метионин, триптофан, тирозин, цистеин. Композиция дополнительно содержит один или более загуститель в количестве от 10 масс. % до 50 масс. %, более предпочтительно от 20 масс. % до 30 масс. % по отношению к массе активного вещества.
Загустители могут быть выбраны из ксантановой камеди, метилгидроксипропилцеллюлозы, камеди конжака, глюкоманнана конжака, аравийской камеди (камеди акации), модифицированных крахмалов. Присутствие таких веществ, предпочтительно ксантановой камеди, метилгидроксипропилцеллюлозы, позволяет загустить жидкость, предпочтительно воду, в которой композицию диспергируют перед употреблением.
Известно, что люди с дисфагией обычно не обладают должным мышечным контролем и координацией для закрытия дыхательного горла должным образом, или они не обладают способностью должного продвижения целых пищевых комков и/или питья в желудок. Поэтому очень важно, чтобы продукты питания, потребляемые пациентами с дисфагией, имели надлежащую вязкость и консистенцию.
При растворении композиции, раскрытой в данном документе, в жидкости, предпочтительно воде, консистенция конечного продукта приобретает идеальную вязкость для пищеварения пациента с дисфагией.
В некоторых воплощениях один или более загустителей присутствуют в количестве от 2 масс. % до 30 масс. %, предпочтительно от 4 масс. % до 15 масс. % относительно массы сухой композиции.
После получения дисперсию выдерживают в течение 5 минут при комнатной температуре с целью достижения желаемой консистенции и вязкости.
Количество жидкости, добавляемое к композиции, раскрытой в данном документе, зависит, например, от консистенции, которую необходимо получить. Данный параметр оценивают и определяют специалисты в области техники, также принимая во внимание степень дисфагии пациента.
В одном или более воплощениях композиция может быть добавлена в жидкость, предпочтительно в воду. Выбранная концентрация зависит от консистенции получаемого геля.
В некоторых воплощениях, композиция, раскрытая в данном документе, дополнительно содержит витамины, предпочтительно выбранные из группы витаминов В, таких как витамин B1 и/или витамин В6. В дальнейшем воплощении настоящего раскрытия, композиция также включает углеводы, добавки и/или вкусоароматические вещества.
Предпочтительные углеводы могут быть выбраны среди мальтодекстринов. Добавка может быть выбрана среди натрия цитрат дегидрата трехосновного, порошка аспартама, ацесульфама калия, сукралозы. Предпочтительным вкусоароматическим веществом является ароматизатор «банан».
Согласно некоторым воплощениям настоящего раскрытия предпочтительно соотношение по массе изолейцин:лейцин находится в диапазоне 0,2-0,7, предпочтительно 0,4-0,6 и/или предпочтительно соотношение по массе валин: лейцин находится в диапазоне 0,2-0,8, предпочтительно в диапазоне 0,4-0,7.
В дальнейшем воплощении соотношение по массе треонин:лейцин находится в диапазоне 0,15-0,50, предпочтительно 0,20-0,45 и/или соотношение по массе лизин:лейцин находится в диапазоне 0,15-0,60, предпочтительно 0,30-0,55.
В другом воплощении соотношение по массе лейцин:изолейцин:валин эквивалентно 2:1:1.
В дальнейшем воплощении, учитывая, что сумма лейцина, изолейцина, валина, треонина и лизина эквивалентна 1, общее количество дополнительных незаменимых аминокислот может варьировать от 0,02 до 0,25 (т.е. 1:0,02-0,25), предпочтительно от 0,05 до 0,15 (т.е. 1:0,05-0,15), приведенное в виде отношения масс.
В дальнейшем воплощении цистеин присутствует в количестве от 150 масс. % до 350 масс. % метионина.
В некоторых воплощениях активное вещество содержит заменимую аминокислоту тирозин в количестве от 15 масс. % до 50 масс. %, предпочтительно от 20 масс. % до 35 масс. % относительно массы фенилаланина.
В дальнейшем воплощении активное вещество состоит из аминокислот лейцина, изолейцина, валина, лизина, треонина в сочетании с гистидином, фенилаланином, метионином, триптофаном, тирозином, цистином, и композиция в дальнейшем содержит один или более загуститель в количестве от 10 масс. % до 50 масс. %, более предпочтительно от 20 масс. % до 30 масс. % относительно массы активного вещества.
В некоторых воплощениях композиция также может быть введена пациенту после инсульта без дисфагии для лечения системного воспалительного процесса, ассоциированного с инсультом. В таких случаях композиция может содержать активное вещество (лейцин, изолейцин, валин, лизин, треонин и по меньшей мере одно из гистидина, фенилаланина, метионина, триптофана, тирозина, цистина) без загустителей.
В дальнейших воплощениях композиция может быть введена для применения при лечении системного воспалительного процесса, причем композиция содержит активное вещество, при этом активное вещество содержит аминокислоты лейцин, изолейцин, валин, лизин, треонин и по меньшей мере одну из аминокислот: гистидин, фенилаланин, метионин, триптофан, тирозин, цистин.
Более того, в частности, при получении композиций согласно настоящему раскрытию и конкретно активного вещества, предпочтительно избегают таких аминокислот, как серии, пролин, глицин, аланин, глутаминовая кислота и главным образом аргинин, поскольку они могут быть контрпродуктивными или даже вредными в некоторых концентрациях или стехиометрических соотношениях с упомянутым составом.
Вышеупомянутые аминокислоты могут быть замещены соответствующими фармацевтически приемлемыми производными, а именно солями.
Предпочтительно, композиция находится в виде сухого порошка, который с целью введения пациенту диспергируют в жидкости, предпочтительно воде.
Дальнейшие описания, относительно количеств и соотношений среди различных аминокислот, предложенных для композиций с целью применения при лечении инсульта у пациентов с дисфагией, приведены в прилагаемой формуле изобретения, которая представляет неотъемлемую часть технического описания, приведенного в данном документе относительно данного изобретения.
Результаты, приведенные в данном документе, демонстрируют, что метаболизм мышечных белков здоровой руки индивидуумов с подострым инсультом и дисфагией может быть охарактеризован как МН, который может быть скорректирован при помощи введения композиции, описанной в данном документе.
Пример 1
Материалы и методы
Группа. Шестьдесят семь пациентов с дисфагией и после подострого инсульта (менее 3 месяцев после острого цереброваскулярного нарушения) (Guidelines of the Ministry of Health for rehabilitation activities. National Health Plan 1998-2000), поступивших в наш реабилитационный центр, подпали под исследование. 11 субъектов были исключены из-за ассоциированной хронической сердечной недостаточности, 1 из-за острого коронарного синдрома, 4 из-за острой хронической почечной недостаточности (клиренс креатинина менее 30 мг/100 мл), 1 из-за онкологической операции, 2 из-за пролежня, 7 из-за диабета (пероральное антидиабетическое лечение или инсулинотерапия), 2 из-за дистиреоза и наконец 1 из-за стероидной терапии. Причина исключения данных заболеваний была тесно связана с их сильным влиянием на метаболизм мышечных белков.
Оставшиеся тридцать восемь пациентов (29 мужчин и 9 женщин; 69,7±11,4 лет) были включены в данное рандомизированное двойное слепое плацебо-контролируемое исследование. Основанием для включения пациента была реабилитация по поводу дисфагии и одностороннего паралича. Все пациенты были лежачими больными и поступили из нейрохирургического (34,2%), неврологического или инсультного отделений (52,6%) или других реабилитационных отделений (13,2%). Острое нарушение мозгового кровообращения, задокументированное посредством компьютерной томографии было ишемическим повреждением в 57,9% или геморрагическим повреждением (42,1%). Индивидуумов с ишемическими и геморрагическими повреждениями объединяли, поскольку в фазе реабилитации инсульта, эти две группы имеют схожие метаболический, трофический и функциональный профили (Aquilani с соавт., 2014).
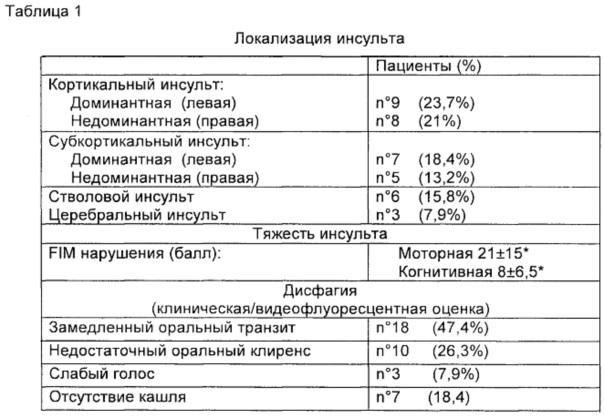
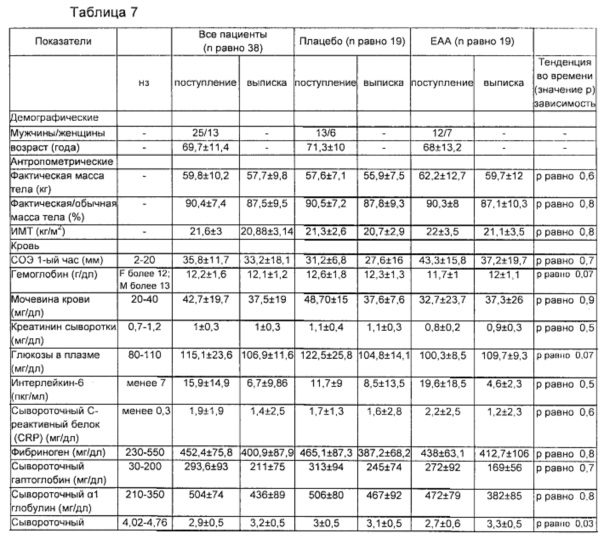
На основании картины компьютерной томографии или магнитного резонанса области повреждения после инсульта классифицировали относительно расположения ишемической деструкции в виде PACI (частичный инфаркт бассейна сонной артерии; 23,7%), TACI (общий инфаркт бассейна сонной артерии; 50%) или POCI (инфаркт в вертебрально-базилярном бассейне; 26,3%). Эти данные приведены в табл. 1, которая также показывает тяжесть инсульта и определенные механизмы, лежащие в основе нарушений глотания.
При допуске все пациенты получали питание посредством чрескожной эндоскопической гастростомии (ЧЭГ; n равно 30) или посредством пероральной модифицированной диеты (n равно 8).
Порядок выполнения. Не позднее двух дней с момента допуска после ночного голодания в 8 ч утра брали образцы крови от каждого пациента для определения следующего:
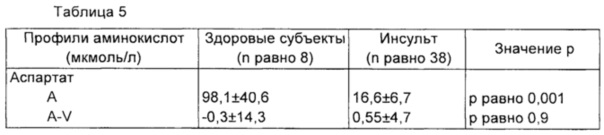
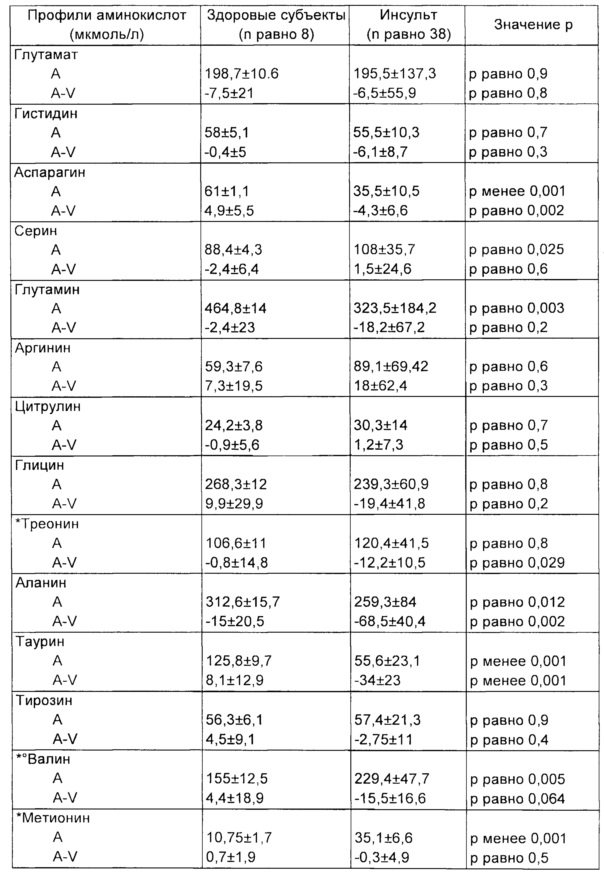
1) Аминокислоты в плазме
Данные субстраты определяли как в артериальной (лучевая артерия), так и в венозной крови здоровой руки. Концентрации свободных аминокислот в плазме измеряли при помощи анализатора аминокислот AminoQuant II на основе системы ВЭЖХ HP 1090 с полностью автоматизированной предколоночной дериватизацией при помощи химизма реакции орто-фталевого альдегида и 9-фторенил-метил-хлорформата согласно протоколу производителя. Результаты получали при введении 1 мкл дереватизированной смеси и измерения абсорбции одновременно при 338 и 262 нм. Концентрации в плазме выражали в виде мкмоль/л. Измерение аминокислот проводили в сравнении с восьмью здоровыми субъектами подходящими по возрасту (71±4,5 лет), распределению по полу (6 М/2 Ж), индексу массы тела (22,3±3,5 кг/м2).
Вычисления
a) Метаболизм мышечных белков. Как описано в другом документе (Aquilani с соавт., 2012), повышенную деградацию мышечных белков оценивали посредством мышечного высвобождения незаменимой аминокислоты фенилаланина (фенил-), при этом синтез мышечных белков определяли посредством захвата фенила мышцами. Учитывая, что фенил не синтезируется и не деградирует в мышечной ткани, любые изменения в мышечном захвате/высвобождении отражают общий белковый баланс (Liu и Barret, 2002).
Отрицательное фенил A-V (высвобождение) означало несбалансированный белковый метаболизм с преобладанием деградации белка над синтезом белка, в свою очередь положительное фенил A-V (захват) свидетельствовало о преобладании синтеза белка. Фенил A-V, равное нулю (нет захвата/нет высвобождения), означало сбалансированный метаболизм мышечных белков.
b) A-V различия других аминокислот, общее содержание аминокислот (ТАА), общее содержание незаменимых аминокислот (ЕАА: валин, изолейцин, лейцин, треонин, фенил, триптофан, метионин, лизин), аминокислот с разветвленной цепью (ВСАА: валин, изолейцин, лейцин).
2) Биомаркеры воспалительного процесса тела
i) Сывороточные уровни интерлейкина 6 (IL-6; нормальное значение менее 7 пг/мл), определяли в дупликатах при помощи высокочувствительного коммерческого набора для «сэндвич» твердофазного иммуноферментного анализа (ELISA) от Mabtech (Agilent Technologies GmbH, Boblingen, Германия);
ii) С-реактивный белок (CRP; нормальное значение менее 0,3 мг/дл) определяли при помощи иммунотурбодиметрического метода;
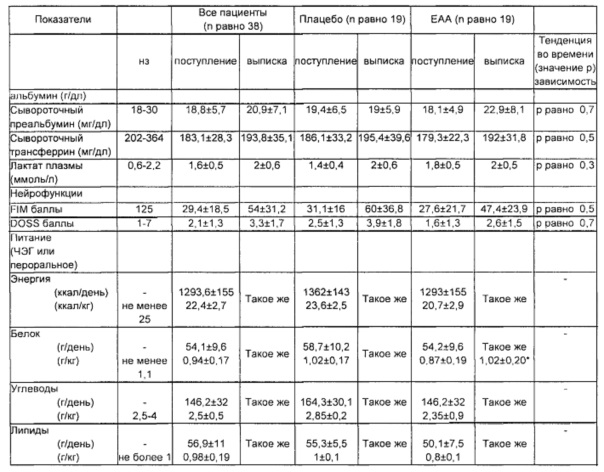
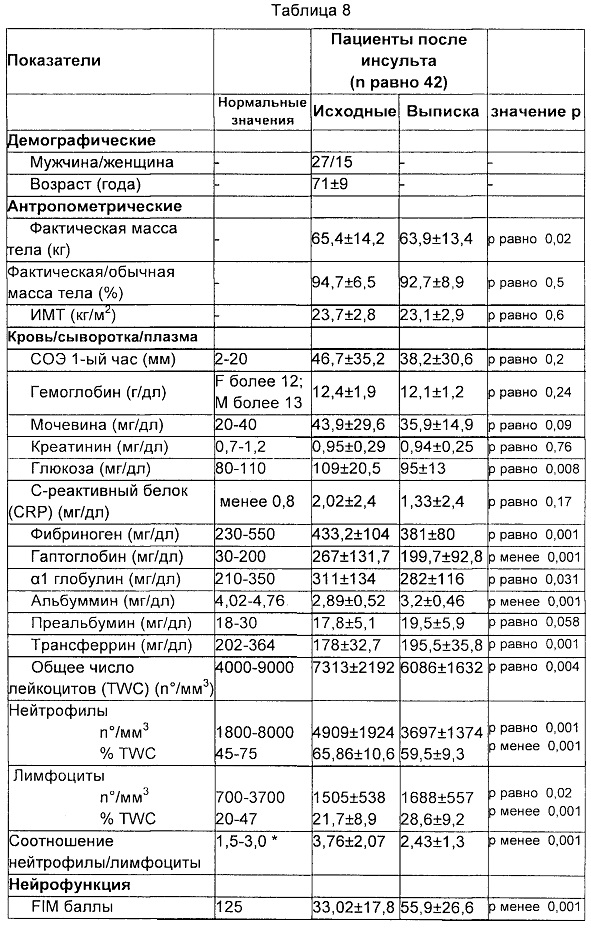
iii) белки острой фазы воспаления (гаптоглобин, нормальные значения 30-200 мг/дл; α-1 глобулиновая система, нормальное значение 0,21-0,35 г/дл; нереактивные белки (альбумин, нормальные значения 4,02-4,76 г/дл; преальбумин, нормальные значения 18-30 мг/дл и трансферрин, нормальные значения 202-364 мг/дл).
3) Концентрации лактата в плазме
Данные концентрации измеряли при помощи ферментных тестов, следуя порядку выполнения, рекомендованному производителем (Siemens Diagnostic, Германия). Нормальное значение 0,6-2,2 ммоль/л.
4) В качестве части рутинной оценки, у пациентов измеряли следующие показатели:
i) антропометрические характеристики: масса тела (МТ, кг), определенная при помощи механического весового подъемника; рост (м), вычисленный исходя из высоты колена (Chumlea с соавт., 1985). Индекс массы тела (ИМТ) вычисляли в виде кг/м2. Пациентов опрашивали (или лиц, осуществляющих уход за ними) в отношении их прединсультной МТ. Потерю фактической МТ относительно обычной (предострой) МТ более 5%, т.е. фактическую/обычную МТ менее 95%, рассматривали в качестве числового показателя существенно пониженного питания;
ii) биогуморальные параметры: обычные показатели, включая электрофорез сывороточных белков.
5) Функциональный статус
Данный статус оценивали при помощи меры функциональной независимости (FIM) (Keith с соавт., 1987). Данный тест обычно применяют врачи в нейро-реабилитационном центре. FIM представляет собой 18 пунктов, которые оценивают независимость пациента в отношении питания, ухода, одевания, пользования туалетом, подвижности, когнитивных функций. 126 баллов свидетельствуют о полной функциональной независимости.
6) Дисфагия
Дисфагию определяли клинически во всей группе. В случае положительного или неопределенного диагноза, пациентов подвергали видео-флуоресцентному исследованию. Тяжесть дисфагии оценивали при помощи шкалы для оценки результата и тяжести дисфагии (Dysphagia Outcome и Severity Scale, DOSS), семибалльная шкала, разработанная для систематической оценки функциональной тяжести дисфагии (O'Neil с соавт., 1999). Диапазон баллов составляет 1-7, где уровень 1 означает тяжелую дисфагию, уровень 2 дисфагию средней тяжести, уровень 3 умеренную дисфагию, уровень 4 дисфагию легкой-умеренной тяжести, уровень 5 легкую дисфагию, уровень 6 внутри функционального предела/модифицированная независимость и уровень 7 - норма при всех ситуациях.
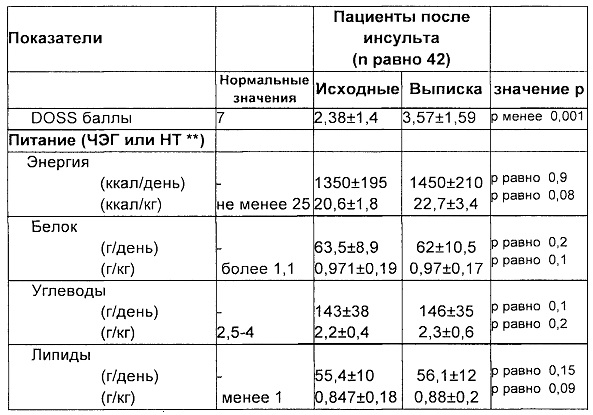
7) Прием пищи
Для пациентов, самостоятельно принимающих пищу (n равно 8), на модифицированной диете, трехдневный дневник питания вели медицинские сестры, которые предварительно специально для этого обучались. Сестры записывали тип и массу приготовленной и неприготовленной пищи, выбранной пациентами на диете из госпитального меню в течение 3 дней как до, так и после приема пищи пациентом. Фактически поглощаемое количество пищи переводили в ее сырой эквивалент при необходимости при помощи соответствующих таблиц (Carnevale с соавт., 1989). Анализ на питательную ценность, выполненный при помощи компьютерной программы, разработанной данной группой (Aquilani с соавт., 1999), применяли для вычисления фактически потребленных калорий и макро/микро питательных веществ. Получение пищи из фармацевтического препарата пациентами при помощи ЧЭГ (n равно 30) вычисляли исходя из пищевой композиции, описанной на этикетке.
8) Реабилитационная терапия
Все пациенты получали реабилитационное лечение, адаптированное для каждого отдельного пациента. Кратко, реабилитация заключалась в лечебной гимнастике с персональным физиотерапевтом в течение 60 минут, пять дней в неделю. Тренировка включала упражнения на координацию с объемом пассивных, активных и активно-вспомогательных движений, техники улучшения контралатеральных конечностей, упражнения для развития мышц туловища, активные тренировки здоровых конечностей и ходьбу при помощи вспомогательных устройств или помощи. Число или повторы упражнений и дистанцию для передвижения увеличивали по мере прогресса физического состояние пациентов. В зависимости от индивидуальных потребностей также проводили логопедическое лечение, реабилитационную терапию (элементарное самообслуживание, тренировка профессиональной, перцептивной и функциональной активности), организацию досуга.
Для реабилитации дисфагии пациентов с уровнями DOSS не менее 3 обеспечивали модифицированной диетой, а также обучали перемене положения тела для благополучного глотания. Во время диеты сначала давали пюреобразную, гомогенную, вязкую пищу с постепенным переходом к пище с почти нормальной текстурой для пациентов, чьи дисфункции глотания постепенно улучшаются.
Перемена положения тела во время приема пищи обычно состояла из адаптивных техник пациента, которые снижали риск аспирации. Они включали, например, поворот головы на пораженную сторону, наклон головы к более сильной стороне, подбирание подбородка, подтягивания.
В случае с пациентами с DOSS менее 3 предпринимали попытки орального транзита после видеофлюороскопии и/или после оценки логопедом. Если пациенты могли благополучно съесть по меньшей мере две трети предписанных им калорий (1500 ккал/д), зондовое кормление прерывали.
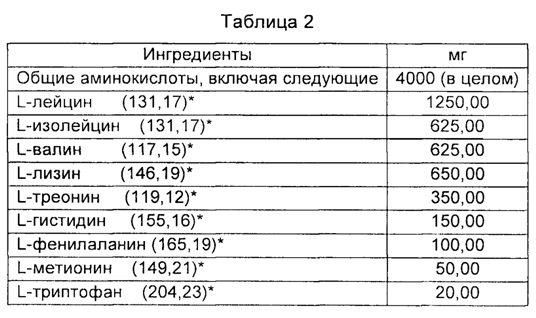
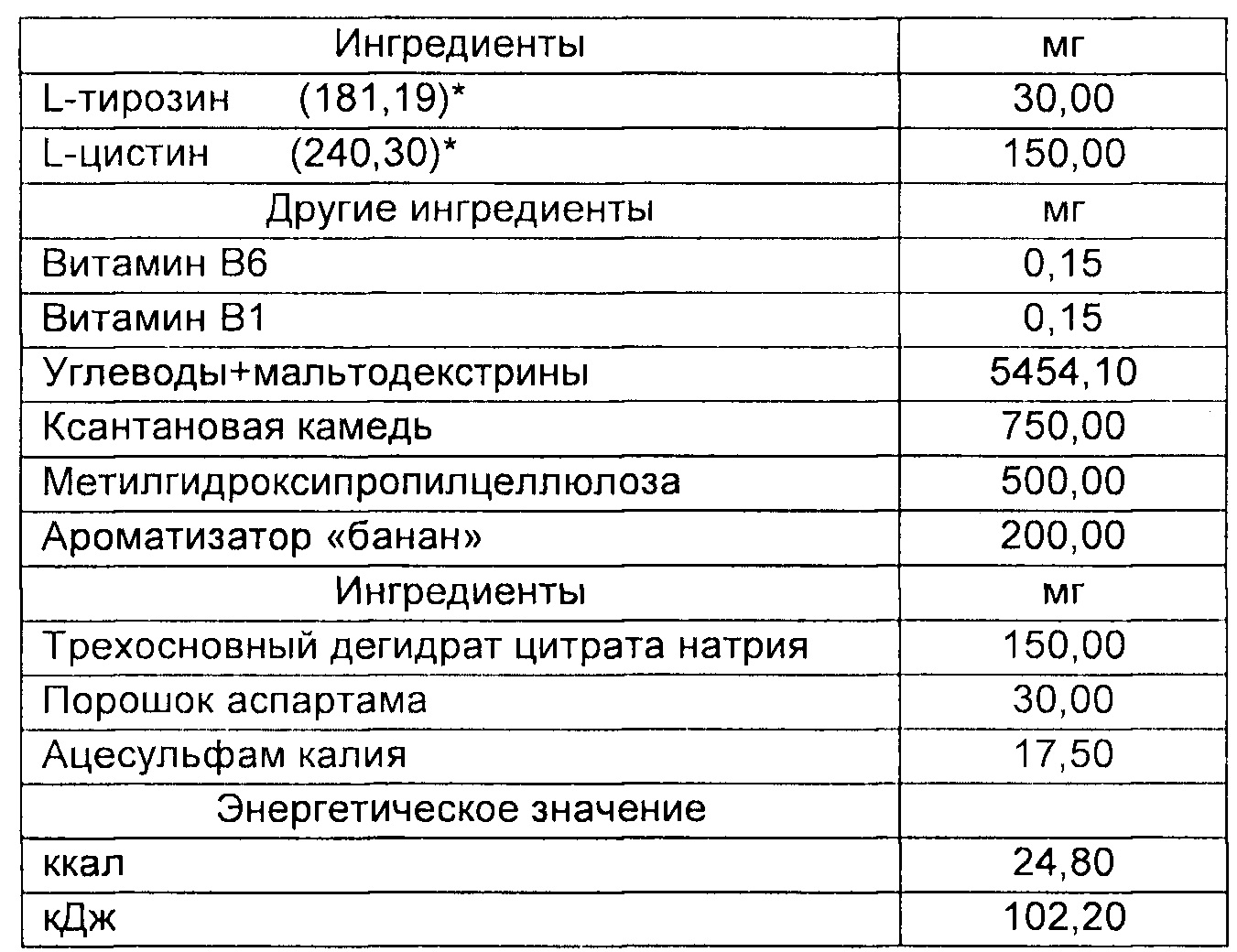
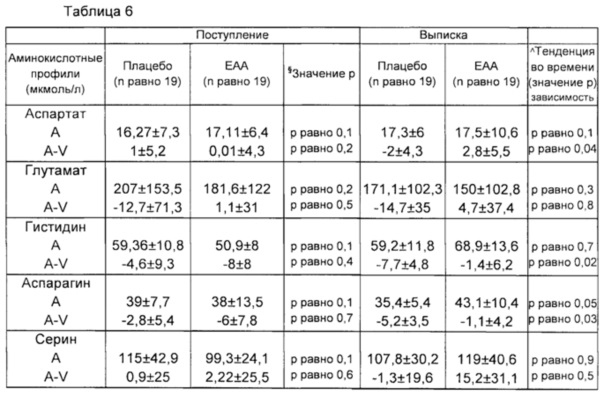
Рандомизация пациентов. После выполнения всех данных процедур пациентам назначали лечение согласно рандомизированному распределению (Фиг. 1). Лист рандомизации получали при помощи статистического программного обеспечения SAS (SAS Institute, штат Северная Каролина). А и В представляли собой идентификаторы лечения в слепом режиме. Лист был доступен как врачам, так и клиническим фармацевтам. Врач последовательно распределял пациентов для лечения А или В согласно листу рандомизации. Первый исследователь, кто интерпретировал все результаты, не знал распределения пациентов. Экспериментальная группа (группа ЕАА) принимала композицию, раскрытую в данном документе, что обеспечивало 8 г незаменимых аминокислот/день (табл. 2; 4 г утром плюс 4 г вечером, разведенные приблизительно половиной стакана воды до выписки пациента).
* молекулярная масса из "Amino Acid, Nucleic Acids & Related Compounds - Specification/General Tests", издание 8, Kyowa Hakko Kogyo Co., Ltd.
Как видно из табл. 2, отношения по массе лейцина, изолейцина и валина предпочтительно эквивалентны 2:1:1. Табл. 1 также показывает, что отдельные количества гистидина, фенилаланина, метионина и триптофана предпочтительно являются понижающимися (т.е. количество гистидина выше, чем фенилаланина, которое выше, чем метионина, которое выше, чем триптофана) и количество (масса в граммах или молях) цистина предпочтительно выше, чем тирозина.
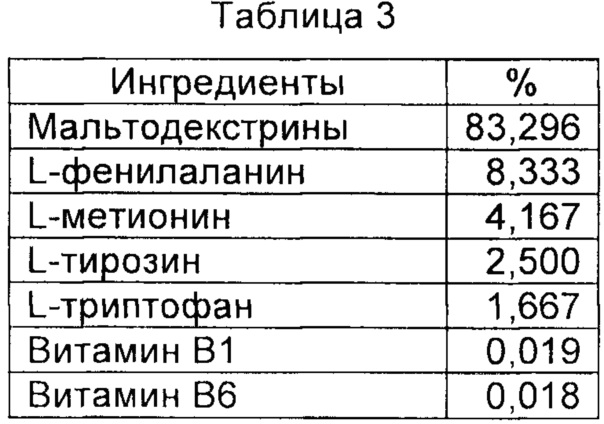
Композицию, показанную в табл. 2, получают, во-первых, посредством загрузки в барабанный смеситель со спиральными перегородками L-фенилаланина, L-тирозина, L-триптофана, витамина В1 и витамина В6 вместе с L-лизином с целью получения предварительной смеси. Процентный состав предварительной смеси представлен в табл. 3.
Ингредиенты смешивают в течение 10 минут с целью получения гомогенной предварительной смеси.
Оставшиеся ингредиенты, приведенные в табл. 1, загружают в барабанный смеситель со спиральными перегородками и перемешивают в течение 20 минут для получения гомогенной конечной композиции.
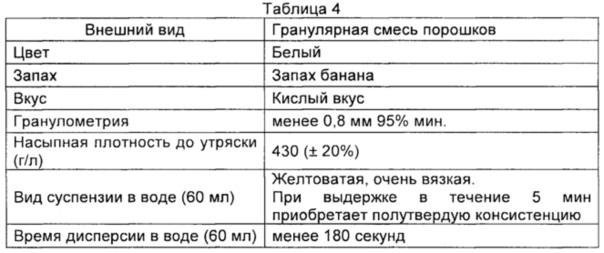
Табл. 4 содержит характеристики композиции, полученной как описано выше:
Композицию по настоящему описанию добавляют и диспергируют в жидкости, предпочтительно воде. Количество жидкости, добавляемой к композиции, описанной в данном документе, зависит, например, от консистенции, которую необходимо получить. Данный параметр оценивают и определяют специалисты в области техники, также принимая во внимание степень дисфагии пациента.
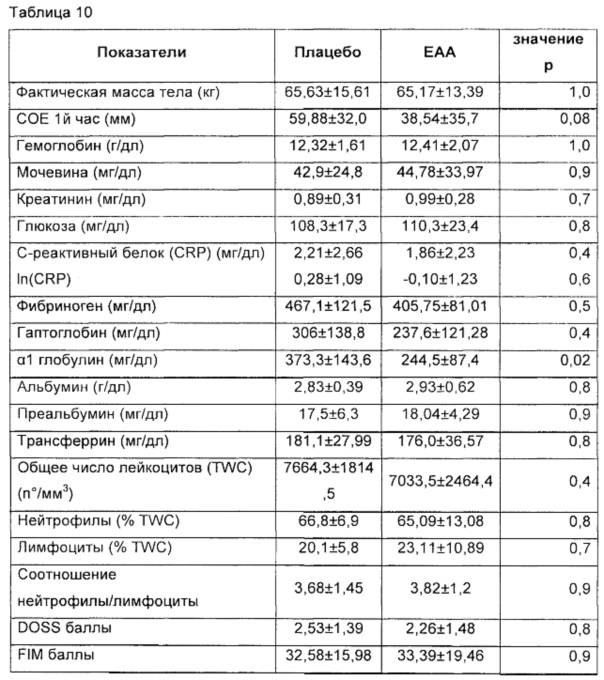
Группа-плацебо (Plac) получала сходный изокалорийный продукт, содержащий мальтодекстрин вместо активного вещества, содержащего аминокислоты.
Медицинские сестры помогали каждому пациенту в его оральной диете во время принятия плацебо или композиции (ЕАА), раскрытой в данном документе, чтобы быть уверенными в соблюдении больным режима лечения.
Сестры не знали о типе добавки (Plac или ЕАА), упаковки, содержащие продукты, были идентичны, пронумерованы как 1 или 2. Содержимое было известно только лечащему врачу и фармацевтам (1-плацебо; 2-ЕАА). Продукт, содержащийся в пакете 1 и 2, имел сходный цвет и вкус. Для пациентов, принимающих энтеральное питание (ЭП), водный раствор композиции, раскрытой в данном документе, подавали через трубку для кормления (чрескожная эндоскопическая гастростомия). Исследование длилось 38±4 дня от процедуры рандомизации. Измерения аминокислот, маркеров воспаления, а также антропометрического и функционального статуса все повторяли при завершении реабилитации пациента (42±4 дня после поступления). Исследование было одобрено этическим научно-техническим комитетом института. Письменное информированное согласие получали от участников или когда требовалось от лиц, осуществляющих уход за ними, после полного разъяснения сути исследования.
Статистический анализ. Описательную статистику выполняли для всех регистрируемых показателей, описывая средние и стандартные отклонения для количественных показателей и частоты распределения для качественных показателей. Критерий Хи-квадрата применяли для категориальных показателей. Дисперсионный анализ повторных измерений применяли для оценки каких-либо тенденций различий с течением времени между пациентами, получавшими ЕАА или Plac. Базовые отличия между группами (ЕАА и Plac) и различия в профилях аминокислот между всей группой после инсульта при поступлении на реабилитацию и здоровой контрольной группой оценивали при помощи непарного t-критерия Стьюдента. Статистическую значимость устанавливали при р менее 0,05.
Результаты
Все пациенты, вошедшие в данное исследование, были рандомизированы для получения композиции, раскрытой в данном документе (ЕАА), или плацебо (Plac) (Фиг. 1).
1) Белковый обмен в мышцах здоровой руки
Табл. 5 показывает артериальные концентрации аминокислот и артерио-венозные различия мышечных аминокислот (A-V), обнаруженные как у пациентов после инсульта при поступлении на реабилитацию, так и у здоровых субъектов.
Данные выражены в виде среднего значения ± стандартное отклонение (СО). Статистический анализ: непарный t-критерий. "Незаменимые аминокислоты (ЕАА); ° Аминокислоты с разветвленной цепью (ВСАА)
Результаты показали, что метаболизм мышечных белков здоровой стороны преимущественно был в гиперкатаболическом состоянии (МН) из-за преобладания белкового катаболизма над синтезом белка, о чем свидетельствует высвобождение мышцами фенила. Это существенно отличается (р менее 0,03) от здоровых субъектов, чей мышечный белковый метаболизм был в равновесии. Помимо фенила, у пациентов высвобождалось существенное количество аспарагина, треонина, лейцина, аланина и таурина.
В отношении артериальных концентраций аминокислот, у пациентов после инсульта наблюдались более высокие уровни серина, метионина, фенила, изолейцина, лейцина, лизина, но более низкие концентрации аспарагиновой кислоты, аспарагина, глутамина, аланина, таурина, триптофана. Субанализ пациентов, разделенных по типу острого нарушения мозгового кровообращения (ишемическое или геморагичесое), выявил сходные результаты.
Табл. 6 показывает аминокислотные профили двух подгрупп пациентов, рандомизированных по приему композиции, раскрытой в данном документе (табл. 2, ЕАА) или Plac, как при поступлении, так и при выписке из реабилитации. При поступлении две подгруппы не имели существенной разницы в степени МН (равно высвобождению фенила), различий по другим аминокислотам и A-V различий по общим аминокислотам (ТАА). Артериальные концентрации отдельных аминокислот, TAAs и ЕАА были сходны у обеих подгрупп, как ЕАА, так и Plac.
При выписке, у пациентов, которые принимали композицию, раскрытую в данном документе (ЕАА), но не у пациентов, принимающих Plac, нормализовался их белковый метаболизм в здоровой руке. Более того, высвобождение фенила переходило в захват мышцами у пациентов, получивших лечение, но осталось фактически неизменным у пациентов, получивших Plac. Эта разница во времени (A-V) фенила была существенной (зависимость, р равно 0,02).
Данные приведены в виде среднего значения ± стандартное отклонение (СО). Статистический анализ: §непарный t-тест; ∧анализ повторных измерений показателей. Тенденция во времени: тенденции различий зависимости между группами. *Незаменимые аминокислоты (ЕАА); °аминокислоты с разветвленной цепью (ВСАА).
Фиг. 2 показывает расхождение между двумя подгруппами, также подразумевающее артериальные ТАА (р равно 0,02), ТАА (A-V) (р равно 0,05), ЕАА (A-V) (р равно 0,01), ВСАА (A-V) (р равно 0,05, не показано на фигуре).
Более того, из всех измеренных аминокислот 49% из них принимали субъекты, принимающие ЕАА (субъект, который принимал композицию, раскрытую в данном документе), в тоже время только 23,2% - субъекты, принимающие Plac (р менее 0,001). A-V разница по времени между двумя группами также отличалась по аспарагиновой кислоте, гистидину, аспарагину, глицину, таурину, тирозину, высвобождаемым более в группе Plac, чем в группах ЕАА. У последних пациентов аспарагиновая кислота не высвобождалась и не захватывалась.
2) Другие показатели анализа
Табл. 7 показывает демографические, антропометрические, нейрофункциональные, биогуморальные характеристики, а также потребление пищи пациентами после инсульта как целой группы, так и двух групп после рандомизации как при поступлении, так и при выписке. При поступлении все пациенты имели недостаточное питание, судя по постинсультной потере массы по сравнению с их обычной МТ (-9,7%). У пациентов было воспаление, о чем свидетельствовали высокие сывороточные уровни IL-6 и CRP с последующими пониженными концентрациями отрицательных реагентов острой фазы ответа (альбумин, преальбумин, трансферрин) и повышенными концентрациями положительных реагентов (гаптоглобиин, α1 глобулин).
Данные приведены в виде среднего значения ± стандартное отклонение (СО). Статистический анализ: анализ повторных измерений показателей. Тенденция во времени: тенденция различий зависимости между группами. ИМТ: индекс массы тела; СОЕ: скорость оседания эритроцитов; FIM: функциональная мера независимости; DOSS: шкала оценки результата и тяжести дисфагии *Данное количество представляет собой сумму вводимого/проглоченного белка (54,2 г) и белка (6,9 г), обеспеченного добавкой ЕАА [41].
Пациенты также имели повышенные концентрации в крови глюкозы и нормальные концентрации лактата. Исходя из функциональной точки зрения, у пациентов была тяжелая форма инвалидности (FIM -76,7% от нормального значения). При оценке DOSS, девятнадцать пациентов имели серьезную дисфагию (DOSS равно 1,21±0,88) и девятнадцать имели умеренную дисфагию (DOSS равно 3,07±1,76). Ежедневные калории и макронутриенты, введенные или проглоченные, составляли 22,4±2,7 ккал/кг, 0,94±0,17 г/кг белка, 2,5±0,5 г/кг углеводов, 0,98±0,19 г/кг липидов. После рандомизации подгруппы ЕАА и Plac были схожи по всем измеренным показателям на исходном уровне.
При выписке обе группы имели сходное снижение массы тела, которое существенно не отличалось от исходного уровня и сходные улучшения степени дисфагии, физической недееспособности, воспаления, циркулирующих белков ответа острой фазы воспаления. Уровни глюкозы в крови улучшались в группе, принимающей Plac. Обе группы имели сходные концентрации лактата в плазме, которые с течением времени не отличались от значений на исходном уровне. Добавление 8 г/день ЕАА к общему белку, введенному/проглоченному (54,2 г/день) обеспечивало 6,9 г белкового субстрата, так что при выписке группа, получавшая лечение, получала 1,02 кг белка.
Приведенные в данном документе результаты подтверждают, что в мышцах здоровой руки пациентов после подострого инсульта катаболическая активность может преобладать над анаболической.
Композиция, раскрытая в данном документе, имела тенденцию к улучшению степени воспаления, таким образом, преобразуя мышечный гиперкатаболизм (МН) в анаболический/сбалансированный белковый метаболизм у пациентов после инсульта с дисфагией через месяц после острого инсульта.
Постоянное воспаление тела, иммобилизация/неиспользование, недостаточное питание, это все являлось факторами, присутствующими в испытуемой группе, которые могли повышать МН в здоровой руке. Воспалительный статус, инициированный острым нарушением мозгового кровообращения и возможно сохраняющийся в течение времени за счет постинсультных инфарктных осложнений, снижал синтез белка и повышал его распад, а также через IL-6 стимулировал гипоталамо-гипофизарно-адренокортикальную систему. Степень протеолиза возможно усугублялась резистентностью к инсулину как показано в испытуемой группе на основании концентраций глюкозы в крови выше нормальных значений. Воспаление обусловливает восстановление печенью синтеза белка, наблюдаемого у исследуемых пациентов.
Неиспользование из-за иммобилизации, денервация, отсутствие мышечной нагрузки, приводят к повышенному протеолизу и в меньшей степени, пониженному синтезу белка.
Отсутствие нагрузки per se может приводить к протеолизу мышц из-за индукции окислительного стресса в скелетной мышце, что запускает повышенную деградацию белка.
Неадекватное постинсультное питание, в частности потребление белка, способствует протеолизу.
О том факте, что пациенты получали длительное неадекватное питание до их поступления на реабилитацию, свидетельствуют ассоциированная потеря массы тела и дисфагия.
По всей видимости, МН контрастирует с нормальными уровнями циркулирующих незаменимых аминокислот у пациентов. Данное расхождение может быть связано с двумя факторами: во-первых, недостаточное питание при интенсивной терапии из-за неадекватного потребления энергии, но не потребления белка, учитывая, что вышеупомянутое составляет 89,6% потребностей тела в энергии, поскольку последние составляют 99% рекомендованного количества. Количества потребляемых энергии и белка были сходны и соответственно выше, чем таковые, описанные в предыдущем исследовании у пациентов после инсульта в сходный период после острого инсульта (21 день). Нормальные уровни ЕАА подтверждают, что 1 г/кг/день белка поставляемый/потребляемый пациентами после подострого инсульта на этапе реабилитации заболевания может быть питательным, но метаболически недостаточным для снижения мышечного гиперкатаболизма. Это подтверждает, что здоровая мышца является местом значительных метаболических изменений, перекрывающих анаболическую активность, обеспеченную ЕАА.
Неиспользование, отсутствие нагрузки, повышенное содержание цитокина в мышцах являются некоторыми факторами, приводящими к МН. Неиспользование активирует потенциальную протеолитическую активность АТФ-зависимого убиквитин-протеосомного пути, лизосомы, кальций-зависимую кальпаиновую систему. Отсутствие нагрузки является потенциальным фактором, способствующим мышечному протеолизу посредством индукции окислительного стресса. Повышенное содержание цитокина в мышцах может оказывать протеолитический эффект, в частности миофибриллярного белка. Интересно, что цитокины, оказывающие действие на функцию мышечных клеток, могут быть продуцированы по сути внутри мышечных или немышечных клеток, таких как нейтрофилы и макрофаги. В течение воспаления данные фагоциты инфильтруют мышечную ткань. Другие нерезидентные клетки, такие как фибробласты, клетки гладкой мускулатуры сосудов, мышечного эндотелия могут продуцировать цитокины.
Кроме того, достаточное потребление белка снижает метаболический клиренс циркулирующих ВСАА за счет жировой ткани, что может способствовать нормальным артериальным уровням незаменимых аминокислот (ЕАА). Более того, жировая ткань модулирует уровни циркулирующих ВСАА, но не в случае устойчивости к инсулину, как в нашей испытуемой группе, снижает или препятствует захвату ВСАА.
Предыдущие исследования касались скорости наступления постинсультной потери мышечной массы в здоровой конечности. В течение первой недели после инсульта одно исследование выявило мышечную слабость в здоровой четерехглавой мышце пациентов с гемиплегией после инсульта и корреляцию между изменением силы четырехглавой мышцы и острой потерей массы. Другое исследование сообщило об отсутствии данных о потере мышечной силы в какой-либо конечности. Другие исследования документировали пониженную мышечную массу и силу спустя шесть месяцев после инсульта. Это в большей степени наблюдалось в паретической по сравнению с непаретической нижней конечностью и верхней конечностью. Исследования продемонстрировали пониженную мышечную силу в обеих ногах у пациентов спустя год после инсульта по сравнению с нормальными субъектами.
Результаты, описанные в данном документе, предоставляют информацию о времени наступления атрофии мышечной ткани здоровой конечности, поскольку описывают мышечный гиперкатаболизм у пациентов после инсульта спустя месяц после инсульта. Это подтверждает, что в случае подострого инсульта системные воспалительно-метаболические изменения могут быть важным фактором, способствующим мышечной атрофии, в дополнение к другим механизмам слабости здоровой стороны тела. Данные механизмы включают мышечное повреждение в результате постинсультного поражения из-за билатеральных проекций каждого полушария мозга, физической неактивности, сниженного питания и возможной моторной слабости вследствие сопутствующей патологии в предынсультный период. Разумно предположить, что системные факторы также отрицательно влияют на поврежденные контралатеральные мышцы. По сравнению со здоровыми субъектами, у пациентов, участвующих в настоящем исследовании, также высвобождались существенные количества аминокислот аспарагина, треонина и ВСАА. Это подтверждает прогрессирующее истощение содержания аминокислот в здоровой мышце.
Другими чертами, отличающими постинсультных и здоровых субъектов, является концентрация определенных аминокислот в артериальной крови. Пациенты после инсульта имеют пониженные уровни аспартата, аспарагина, глутамина, аланина, таурина и триптофана, но повышенные уровни ВСАА, метионина, фенила, лизина. При воспалении и мышечном протеолизе эти уменьшения подтверждают повышенный метаболический клиренс аминокислот за счет висцеральных органов, включая печень, кишечник, почки, которые будут находиться в гиперметаболическом состоянии. Например, для печени характерно высокое потребление гликонеогенного аспартата, аспарагина, аланина и глутамина, для кишечника и почек - глутамина, для иммунной системы - глутамина, для мозга - всех аминокислот, в частности предшественника серотонина триптофана.
Повышения артериальных концентраций аминокислот в основном имеют мышечное происхождение, учитывая, что помимо высвобождения фенила, чрезмерному высвобождению подвергаются ВСАА, метионин, лизин. Нормальные уровни лактата подтверждают, что в мышцах здоровой руки имеет место сбалансированный аэробно-анаэробный путь образования энергии. Интересно, что как деградация белка, так и синтез требуют для своего осуществления больших количеств энергии.
Таким образом, исследование показывает, что мышцы здоровой руки пациентов после инсульта с гемиплегией и дисфагией являются участками гиперкатаболической активности, которая без коррекции приведет к мышечной слабости.
Более того, инсульты, вызывающие дисфагию, вызывают изменения в артериальном аминокислотном профиле. Потеря мышечной массы и силы оказывает существенное влияние на функциональность и жизненный прогноз пациентов после инсульта. Субъекты с истощенными мышцами имеют пониженный метаболический контроль глюкозы, повышенный риск остеопороза, который может быть ответственен за перелом шейки бедра и падения, дезадаптацию сердечно-сосудистой системы и более сильную недееспособность, в частности неспособность к передвижению.
Поэтому распознавание и лечение мышечной атрофии так рано, как только возможно, имеет первостепенное значение для исхода реабилитации пациентов после инсульта, в частности, если мы учитываем, что 80% общего нейромоторного восстановления происходит в течение первого месяца после острого инсульта.
Исследование ясно показывает, что введение композиции, раскрытой в данном документе, может корректировать повышенную деградацию белка в здоровой мышце у пациентов после инсульта с подострой дисфагией.
Напротив, без применения таких композиций, пациенты продолжали терять мышечную массу спустя семьдесят дней после острого инсульта. После реабилитации преобладание анаболической активности в группе ЕАА сопровождалось захватом в здоровой мышце 49% аминокислот из артериальной крови и общих артериальных аминокислот в плазме, подтверждая анаболический белковый обмен в мышцах.
Это подтверждается более низким высвобождением гистидина, глицина, таурина по сравнению с таковым в группе-плацебо, а также повышенной доступностью артериальной ТАА.
В отношении синтеза белка незаменимые аминокислоты с разветвленной цепью действуют как активатор и анаболические сигналы в мышцах человека. Постоянная добавка лейцина, как в данном документе, стимулирует синтез белка после приема пищи в соответствующих тканях, включая скелетные мышцы, печень, жировую ткань. Показано, что пероральный прием 2,5 г лейцина стимулирует синтез мышечных белков после упражнений или ночного голодания.
В отношении протеолиза лейцин является регулирующим фактором деградации миофибриллярного белка, поскольку он подавляет деградацию миофибрилярного белка вскоре после орального введения. Инфузия ВСАА человеку явно уменьшает деградацию белков скелетных мышц, но стимулирует синтез белка в сердце. Показано, что эффективное использование белка определяется изменчивостью чувствительности протеолиза до аминокислот в отличие от синтеза белка. Небольшие количества аминокислот достаточны для уменьшения протеолиза в отличие от синтеза белка.
Несколько механизмов лежат в основе синтеза белка и в то же время снижают протеолиз за счет незаменимых аминокислот. Один механизм представляет собой достаточную доступность незаменимых аминокислот per se. Более того, незаменимые аминокислоты могут стимулировать синтез белка вне зависимости от гормонов. Другие механизмы включают регуляцию генной экспрессии, модуляцию активности анаболических гормонов, улучшенный аэробный метаболизм энергообразования и пониженное соотношение циркулирующих TNFα/IGF-1. И наконец, аминокислоты влияют на мишенные гены при транскрипции, стабильность мРНК и трансляцию. Аминокислоты и в частности ЕАА, обеспечивают синтез белка за счет стимулирования инсулинового фактора роста 1 (IGF-1) и модулирования инсулинового сигналинга. Более того, они играют роль в регуляции инсулинового сигналинга через mTOR сигнальный путь. Инсулин (и IGF-1) не может стимулировать синтез белка, если концентрации аминокислот не поддерживаются.
Более того, незаменимые аминокислоты также могут снижать резистентность к инсулину. Незаменимые аминокислоты индуцируют анаболическую активность непосредственно за счет стимулирования клеточного аэробного метаболизма к получению энергии, доступность которой необходима для синтеза белка. Особенно важно при процессе системного воспаления, что незаменимые аминокислоты могут обеспечить синтез мышечных белков за счет снижения циркулирующего цитокина TNFα, так что снижается числовой показатель TNFα/IGF-1.
Различия, наблюдаемые в данном документе между нормальными уровнями незаменимых аминокислот в плазме и мышечным гиперкатаболизмом, подтверждают, что постоянная добавка свободных незаменимых аминокислот может быть лучше, чем незаменимые аминокислоты в белках в отношении обеспечения мышечного анаболизма. Более того, для того, чтобы происходил синтез мышечных белков, быстрое повышение уровней незаменимых аминокислот в плазме вследствие потребления незаменимых аминокислот является более важным, чем внутримышечная доступность аминокислот. Это обусловлено тем, что аппарат синтеза белка в мышцах не чувствителен после 2,5 часов. Скорость, с которой достигаются пиковые концентрации в крови, является более высокой после потребления свободных незаменимых аминокислот, чем после ЕАА из белка, поскольку скорость абсорбции последних замедлена из-за сопутствующей диеты из комплекса углеводов и жиров.
Кроме того, модулирование синтеза мышечных белков за счет повышения в крови незаменимых аминокислот может объяснить, почему в данном документе две группы пациентов после инсульта имели сходные уровни ЕАА в плазме, но различные ответы метаболизма мышечных белков.
Необходимо, чтобы пациентам с дисфагией после инсульта вводили соответствующее количество белка высокого качества. Пониженное потребление белка, приводящее к низким уровням незаменимых аминокислот в крови, может способствовать драматическому увеличению МН.
Результаты, описанные в данном документе, предоставляют полезную информацию для клинической практики, поскольку показано, что композиция, раскрытая в данном документе, способна снижать системный воспалительный процесс у пациентов после инсульта и, таким образом, преобразовывать гиперкатаболизм в анаболизм, который даст возможность лучшего восстановления физической независимости пациентов.
Пример 2
Материалы и методы
Группа. Сорок два пациента с дисфагией вследствие ишемического инсульта последовательно поступившие в Институт Реабилитации (Rehab) (Nervi, Генуя, Италия), были включены в течение 37±12 дней после острого инсульта.
Пациенты поступили из следующих мест: инсультные отделения (14,3%), дома (61,9%), неврологические отделения (23,8%). Ни один из пациентов не был на стероидной терапии, не имел рака, нефротического синдрома, всех случаев, которые составляли критерии исключения из исследования, при которых действовали компоненты острой фазы ответа.
Топографию васкулярного церебрального инсульта устанавливали при помощи изображения компьютерной томографии или магнитного резонанса.
Поврежденные инсультом области классифицировали в отношении расположения ишемической обструкции в виде PACI (частичный инфаркт бассейна сонной артерии; 45,2%), TACI (общий инфаркт бассейна сонной артерии; 30,95%), POCI (инфаркт в вертебрально-базилярном бассейне; 23,8%).
Письменное информированное согласие получали от участников или при необходимости от лиц, осуществляющих уход за ними, после полного объяснения сути исследования. Исследование утверждалось научным и этическим комитетами института.
Порядок действий. В течение первых трех дней поступления в Институт реабилитации, измеряли следующие исходные показатели:
a) антропометрические показатели: масса тела (МТ, кг), измеренная при помощи механического весового подъемника; рост (м), вычисленный исходя из высоты колена (Chumlea с соавт., 1985). Индекс массы тела вычисляли в виде кг⋅м-2. Фактическую массу тела соотносили с обычной (прединсультной) МТ. Фактическую/обычную МТ не более 95% рассматривали в качестве существенной потери МТ;
b) биогуморальные показатели: 1) обычные показатели, включая электрофорез белков сыворотки и соотношение нейтрофилы/лимфоциты (Нф/Лф) периферической крови (в лаборатории данное соотношение у здоровых индивидуумов варьирует от 1 до 3); 2) биомаркеры воспаленного процесса тела: С-реактивный белок (CRP; нормальное значение менее 0,8 мг⋅дл-1, определенное посредством иммунотурбидиметрического метода); скорость оседания эритроцитов (СОЭ; нормальное значение 2-20 мм в первый час); 3) реагенты острой фазы: положительные белки (α-1 глобулиновая система, нормальные значения 210-350 мг⋅дл-1; гаптоглобин 30-200 мг⋅дл-1; фибриноген, нормальные значения 230-550 мг⋅дл-1); отрицательные белки (альбумин, нормальные значения 4,02-4,76 г⋅дл-1; преальбумин, нормальные значения 18-30 мг⋅дл-1 и трансферрин, нормальные значения 202-364 мг⋅дл-1);
c) функциональный статус: оценивали при помощи Меры функциональной независимости (FIM), как описано в другом документе [Keith с соавт. 1987];
d) дисфагия: все пациенты поступали с диагнозом дисфагия. Наличие дисфагии исследователи контролировали при помощи видеофлюороскопического исследования. Тяжесть дисфагии оценивали при помощи шкалы для оценки результата и тяжести дисфагии (DOSS), семибалльная шкала, разработанная для систематической оценки функциональной тяжести дисфагии [O'Neil с соавт 1999]. Диапазон оценки составлял 1-7, уровень 1 означает тяжелую дисфагию, уровень 2 умеренно тяжелую дисфагию, уровень 3 умеренную дисфагию, уровень 4 легкоумеренную дисфагию, уровень 5 легкую дисфагию, уровень 6 внутри функциональное ограничение/измененную самостоятельность и уровень 7 - норма во всех ситуациях.
При поступлении 21,4% всех пациентов были на модифицированной диете, в тоже время 78,6% получали питание при помощи назогастральной трубки или трубки чрескожной эндоскопической гастростомии.
Рандомизация пациентов. После завершения данных действий, пациентов рандомизировали по получению незаменимых аминокислот (ЕАА; группа ЕАА, n равно 21) или плацебо (мальтодекстрин; группа плацебо, n равно 21). Лист рандомизации получали при помощи статистического программного обеспечения SAS (SAS Institute, Кэри, штат Северная Каролина). А и В представляли собой идентификаторы лечения в слепом режиме. Лист был доступен как врачам, так и клиническим фармацевтам. Врач последовательно распределял пациентов на лечение А или В согласно листу рандомизации. Первый исследователь, кто интерпретировал все результаты, не знал о распределении пациентов. Экспериментальная группа (ЕАА группа) принимала 8 г/день ЕАА (табл. 2), 4 г утром плюс 4 г днем, разведенные в половине стакана воды. Группа плацебо получала изокалорийную смесь, содержащую мальтодекстрин.
Пациенты на искусственном питании получали добавку плацебо или ЕАА через питающую трубку. Субъекты на модифицированной диете получали ЕАА в виде гелеобразной смеси.
Продолжительность лечения (ЕАА или мальтодекстрин) составила 35 дней. На 38±1 день от поступления на реабилитацию все показатели от а) до d) повторяли.
Реабилитационная терапия. Все пациенты, следовавшие протоколу реабилитации центра, состоящему из выполнения упражнений на координацию из объема пассивных, активных и активно-вспомогательных движений, ходьбы с помощью устройств или поддержки. Период, в течение которого проводилось лечение одним и тем же терапевтом, составлял 60 мин в день в течение пяти дней в неделю. Более того, все пациенты получали логопедическое лечение и трудовую терапию.
Статистический анализ. Все показатели анализировали, сообщая среднее значение и стандартное отклонение для количественных показателей и частоты распределения для качественных показателей.
Критерий Хи-квадрата применяли для категориальных показателей. Впоследствии, CRP переводили в значения натурального логарифма (In CRP).
В целой группе различия в показателях между исходными значениями и значениями при выписке тестировали при помощи парного t-критерия Стьюдента.
Взаимосвязь между циркуляцией лимфоцитов, соотношением Нф/Лф и нейрофункциональным тестом в течение реабилитации исследовали при помощи простого корреляционного анализа.
Группу пациентов разделяли на две группы, с улучшенным DOSS по меньшей мере на один балл, и группу со стабильным DOSS. Исходные различия в показателях между указанными группами тестировали при помощи непарного t-критерия. Анализ повторных измерений показателей применяли для оценки любых различий по тенденции во времени между двумя группами пациентов.
Линейные множественные регрессионные анализы проводили для того, чтобы продемонстрировать показатели с высокой ассоциацией с DOSS в двух подгруппах пациентов.
Исходные различия в показателях пациентов при ЕАА и плацебо тестировали при помощи непарного t-критерия и анализ повторных измерений показателей применяли для оценки различий по тенденции во времени. И в этом случае проводили линейные множественные регрессионные анализы, чтобы продемонстрировать показатели с высокой ассоциацией с DOSS.
Уровень статистической значимости устанавливали при р менее 0,05.
Результаты
а) Группа пациентов
В табл. 8 приведены как исходные демографические, антропометрические, биогуморальные, клинические и нейрофункциональные характеристики, так и таковые при выписке и потребление питания.
На исходном уровне, пациенты имели нормальную массу тела (МТ) (ИМТ равно 23,7±2,8 кг/м2), но со средней потерей массы 5,3% относительно прединсультной МТ. У субъектов наблюдалась тяжелая утрата физической способности (FIM: -74% от нормального значения, в среднем) и способность к глотанию (средний DOSS: -71% в среднем). Умеренная и тяжелая дисфагия (DOSS не более 3) наблюдалась у 38% субъектов. Присутствовало легкое системное воспаление (средние уровни CRP в 2,5 раза выше, чем нормальное значение). Воспаление было ассоциировано с пониженными уровнями циркулирующих отрицательных белков (альбумин, преальбумин, трансферрин) острой фазы ответа и с повышенными сывороточными концентрациями положительных белков (альфа-1 глобулиновая система, гаптоглобулин, фибриноген) и с глюкозой в крови на верхнем пределе нормальных значений (табл. 8).
При выписке МТ в дальнейшем уменьшилась (среднее снижение: -1,5 кг, р менее 0,02). Это соответствовало существенным улучшениям как физической недееспособности (среднее увеличение FIM: +69%, р менее 0,001), так и дисфагии (среднее увеличение DOSS: +1,19 балл; р менее 0,001). Улучшение дисфагии наблюдалось у 30 пациентов (71,4%) (16 у плацебо и 14 у ЕАА субъектов), в тоже время стабильная дисфагия была выявлена у 28,6% пациентов.
Воспаление еще присутствовало, но было ассоциировано с существенно пониженными сывороточными уровнями антипротеазной системы (альфа-1 глобулин от 311 мг⋅дл-1 до 282 мг⋅дл-1 в среднем; р равно 0,031), гаптоглобин (р менее 0,001) и повышенными сывороточными концентрациями циркулирующих отрицательных белков острой фазы ответа (табл. 8). Глюкоза в плазме существенно снизилась и нормализовалась (р равно 0,008).
В течение реабилитации субъекты с улучшением и те, у кого не было улучшения дисфагии, имели сходное число случаев инфекции (1,8±0,4 против 1,6±0,5, соответственно; незначимо).
Данные приведены в виде среднего значения ± стандартное отклонение (СО).
Статистический анализ: парный t-критерий Стьюдента.
ИМТ: Индекс Массы Тела; СОЕ: скорость оседания эритроцитов; FIM: Мера функциональной независимости; DOSS: шкала оценки результата и тяжести дисфагии
b) Циркулирующие лимфоциты, число Нф и соотношение Нф/Лф
Табл. 8 показывает, что на исходном уровне пациенты имели нормальное общее число лейкоцитов (TWC), лимфоцитов и Нф, не имели системного воспаления, однако соотношение Нф/Лф было выше (3,76±2,07), чем нормальное значение нашей лаборатории (не более 3).
При выписке существенные снижения исходных чисел TWC (р равно 0,004) и Нф (р равно 0,001) были обнаружены, при этом число лимфоцитов было повышено (р равно 0,02). Таким образом, соотношение Нф/Лф существенно понижалось до 2,43±1,3 (р менее 0,001) и нормализовалось.
c) Взаимосвязь между циркулирующими лимфоцитами, соотношением Нф/Лф и нейрофункциональными тестами в течение реабилитации
Абсолютные количества лимфоцитов и % лимфоцитов положительно коррелировали с DOSS (r равно +0,235, р равно 0,04 и г равно +0,224, р равно 0,05, соответственно) и отрицательно коррелировали с маркером воспаления In CRP (r равно -0,265, р равно 0,02 и r равно -0,484, р равно 0,0001 соответственно). Число Нф было положительно связано с In CRP (r равно +0,37, р равно 0,001) и показывало слабую негативную ассоциацию с физической способностью (FIM, г равно -0,20, р равно 0,07). Корреляции между Нф и DOSS обнаружено не было. Лимфоциты и нейтрофилы сильно отрицательно коррелировали (r равно - 0,926, р менее 0,001). Соотношение Нф/Лф было обратно пропорционально физической способности (r равно -0,262, р равно 0,02) и способности к глотанию (r равно -0,279, р равно 0,01), но было положительно ассоциировано с In CRP (r равно +0,514, р равно 0,0001). Результаты показывают положительную корреляцию между FIM и DOSS (r равно +0,78, р менее 0,0001).
С целью лучшего понимания взаимосвязи между временными изменениями циркулирующих иммунных клеток и дисфагией, всю группу после инсульта разделяли на первую группу, которая после реабилитации, проявляла улучшение дисфагии (n равно 30 субъектов) и вторую группу, которая не имела улучшения дисфагии (n равно 12 субъектов). Табл. 9 показывает изменения некоторых показателей между субъектами с улучшением и без улучшения дисфагии.
Данные показатели одновременно тестировали в регрессионной логистической модели, наконец, показывая, что только % лимфоцитов был значимо ассоциирован с улучшенной способностью к глотанию (р равно 0,01). Наряду с этим открытием, временные изменения в % лимфоцитов и DOSS были положительно скоррелированы (р равно 0,015; Фиг. 3, график а).
d) Влияние добавки ЕАА на лимфоциты и дисфагию
На исходном уровне, группы ЕАА и плацебо были сходны по всем рассматриваемым показателям, за исключением сывороточных концентраций альфа-1 глобулина, которая была выше в группе плацебо, чем в группе ЕАА (р менее 0,02) (табл. 10). В течение периода реабилитации временные изменения всех рассматриваемых показателей (табл. 11) были сходными между двумя группами пациентов за исключением альфа-1 глобулина, который снижался у пациентов плацебо группы (взаимодействие р равно 0,01), и соотношения Нф/Лф снижение которого было более выражено в группе ЕАА (взаимодействие р равно 0,04).
Значения выражены в виде среднего ± стандартное отклонение. Статистический анализ: анализ повторных измерений показателей. Описан только уровень р взаимодействия (время*лечение). Уровень значимости установлен при р менее 0,05
В обеих группах улучшения дисфагии были положительно связаны с улучшениями в % лимфоцитов (Фиг. 3, графики b и с), но ассоциация была более явной в группе ЕАА, подтверждая, что ассоциация, наблюдаемая у всей группы пациентов после инсульта (Фиг. 3, график а) в основном обусловлена лечением ЕАА.
Исследование показывает, что в течение подострой стадии ишемического инсульта пациенты при поступлении в институт реабилитации имели нормальные количества лимфоцитов и нейтрофилов периферической крови, но высокое соотношение Нф/Лф. После реабилитации соотношение Нф/Лф нормализовалось, из-за понижения числа Нф и повышения числа Лф. Более того, исследование показывает, что повышенный % лимфоцитов в периферической крови в значительной степени ассоциирован с улучшенной дисфагией и что эта взаимосвязь усилена добавкой незаменимых аминокислот (ЕАА) пациенту.
1) Количества циркулирующих лимфоцитов и нейтрофилов, соотношение Нф/Лф
Исследование показывает нормальный профиль общего числа лейкоцитов крови, числа лимфоцитов и нейтрофилов со слегка повышенным соотношением Нф/Лф.
В течение реабилитации происходило снижение степени постострого воспаления с положительным влиянием на клинико-метаболический статус пациента. Фактически, снижение соотношения Нф/Лф было ассоциировано с улучшениями в физической недееспособности и неспособности к глотанию пациента, уровней циркулирующих отрицательных белков острой фазы ответа, потенциально влияющих на восстановление мозга. Более того, у пациентов улучшалась концентрация глюкозы в крови, свидетельствуя о снижении устойчивости к инсулину.
Профиль иммунных клеток в крови в течение подострого инсульта противоположен таковому, описанному при острой или непосредственно постострой фазы церебральной ишемии. При острой ишемии общее число лейкоцитов и число нейтрофилов повышены, а число лимфоцитов понижено, и в течение дней после инсульта происходит ингибирование пролиферации/активности лимфоцитов, за счет как супрессивного эффекта в результате чрезмерно активированной вегетативной нервной системы в селезенке и лимфоузлах, так и прямой ингибиторной активности, оказываемой Нф на лимфоциты.
По сравнению с острой стадией инсульта, при которой снижение адаптивной иммунной системы является полезным для пациента, в течение подострого инсульта улучшение адаптивной иммунной системы не только неблагоприятно, но также может способствовать нейродегенерации. Настоящее исследование показывает, что восстановление функции иммунной системы связано с улучшением в FIM как у пациентов после инсульта, так и с повреждением спинного мозга.
Возможно, что повышение циркулирующих лимфоцитов, наблюдаемое у пациентов с подострым инсультом, может быть обусловлено пониженной продукцией кортикостероидов, вследствие сниженного воспаления, поскольку повышенные уровни кортикостероида (или метанефрина) ассоциированы с лимфопенией после обширного инфаркта головного мозга. Лимфоциты экспрессируют больше глюкокортикоидных рецепторов, чем гранулоциты и моноциты. Блокада данных рецепторов предотвращает лимфопению. Даже если уровни циркулирующих кортикостероидов не определены в настоящем исследовании, нормализация глюкозы в крови в течение реабилитации, свидетельствующая о пониженной устойчивости к инсулину, подтверждает снижение продукции кортикостероидов. Поскольку при острой ишемии Нф влияют на тяжесть инсульта, снижение Нф в течение реабилитации может способствовать процессам нейрорепарации и нейрорегенерации. В настоящем исследовании это косвенно подтверждается отрицательной корреляцией, выявленной между соотношением Нф/Лф и восстановлением обеих физической недееспособности (FIM) и неспособности к глотанию (DOSS). Это подтверждает, что чем меньше воспаление, тем более высока способность к глотанию.
Даже если врожденные и адаптивные иммунные системы совместно кооперируются для обеспечения лучшего иммунного ответа после воспаления, индуцированного церебральной ишемией, Нф и лимфоциты обратно скоррелированы, поскольку Нф могут ингибировать число и активность лимфоцитов.
Таки образом, исследование подтверждает, что в течение подострого инсульта адаптивный иммунитет может преобладать над врожденной иммунной системой и может быть ассоциирован с нейрофункциональным восстановлением пациента, при этом постоянный более высокий уровень воспаления может быть пагубным для восстановления глотания.
2) Добавка ЕАА и взаимосвязь между адаптивной иммунной системой и нейрофункцией
Исследование показывает, что ЕАА ассоциированы со значительным снижением соотношения Нф/Лф в крови и усилением взаимосвязи между улучшенной временной динамикой % лимфоцитов и DOSS. Таким образом, ЕАА влияют как на сывороточный иммунитет, так и на нейрорепаративные процессы. Учитывая метаболическую активность ЕАА, данные субстраты обеспечивают эти процессы посредством нескольких механизмов.
Во-первых, ЕАА могут непосредственно индуцировать синтез белка в иммунных клетках для пролиферации и дупликации лимфоцитов.
В случае, когда Нф преобладают над Лф, как в случае острой ишемии и при поступлении пациента на реабилитацию, фагоцитарная активность циркулирующих Нф может отрицательно влиять на восстановление глотания. В данном исследовании об этом свидетельствует отрицательная корреляция, обнаруженная между соотношением Нф/Лф и способностью к глотанию. Таким образом, исследование подтверждает, что ЕАА изменяют иммунный профиль в пользу адаптивного иммунитета по сравнению с паттерном воспаления.
Во-вторых, ЕАА-индуцированный синтез белка непосредственно улучшает способность к глотанию за счет механизмов, лежащих в основе нормального глотания, таких как межнейронная активность и/или центр глотания и/или периферическая нейромышечная функция глотания.
В-третьих, ЕАА-индуцированный анаболический статус тела имеет первостепенное значение для восстановления и функционирования мозга. В данном исследовании на улучшенный анаболический статус, несмотря на небольшую потерю исходной массы тела, указывает восстановление синтеза печенью отрицательных белков острой фазы ответа, таких как альбумин, трансферрин, преальбумин. Следует отметить, что данные белки per se могут играть роль в восстановлении/регенерации мозга и реактивации нейронных сетей.
Исследование показывает, что более чем у 28% пациентов не происходило улучшения дисфагии при реабилитации. Это может быть обусловлено отсутствием возбудимости коры в неповрежденном полушарии. Данная гипотеза основана на следующем: 1) глотательная мускулатура представлена в каждом полушарии, но с заметной межполушарной ассиметрией; 2) возникновение дисфагии связано с размером фарингеальной проекции в неповрежденном полушарии.
Исследование показывает, что физическая дееспособность (FIM) и способность к глотанию (DOSS) взаимосвязаны. Тот факт, что при логистическом регрессионном анализе исход дисфагии в основном ассоциирован с % лимфоцитов, а не с FIM, подтверждает, что улучшение дисфагии зависит не только от общего улучшения нейронных сетей, как в случае пациентов с плацебо, но и также опосредовано повышенной активностью адаптивной иммунной системы при восстановлении мозга, как в случае с пациентами ЕАА.
Более того экспериментальные данные свидетельствуют о наличии положительной корреляции между значением соотношения Нф/Лф и концентрацией ЕАА в артериальной крови, в основном незаменимых аминокислот с разветвленной цепью (лейцин, изолейцин и валин).
С другой стороны, корреляции между значением соотношения Нф/Лф и общей концентрацией аминокислот в артериальной крови, а также корреляция между значением соотношения Нф/Лф и общей концентрацией аминокислот в венозной крови не существенны.
Физиопатологическим объяснением вышеупомянутого является тот факт, что более высокие воспалительные процессы (высокое соотношение Нф/Лф) представляют собой более высокий белковый обмен (синтезируются высокие количества белковых медиаторов воспаления, например, цитокинов) и поэтому выше потребность в соответствующей концентрации, в частности незаменимых аминокислот, в системном артериальном кровотоке, для синтеза белка, в тоже время венозная кровь отражает мышечный катаболизм.
СПИСОК ССЫЛОК
1. R. Aquilani, М. Boselli, P. Baiardi, с соавт., "Is stroke rehabilitation a metabolic problem?" Brain Inj, т. 28, №2, стр. 161-173, 2014.
2. R. Aquilani, M.T. La Rovere, O. Febo, с соавт., "Preserved muscle protein metabolism in obese patients with chronic heart failure" Int J Cardiol, т. 160, №2, стр. 102-108, 2012.
3. Z. Liu и E.J. Barrett, "Human protein metabolism: its measurement и regulation" Am J Physiol Endocrinol Metab, т. 283, №6, стр. E1105-E1112, 2002.
4. W.С. Chumlea, A.F. Roche, и M.L. Steinbaugh, "Estimating stature from knee height for persons 60 to 90 years of age" J Am Geriatr Soc, т. 33, №2, стр. 116-120, 1985.
5. R.A. Keith, С.V. Granger, В.B. Hamilton и F.S. Sherwin, "The functional independence measure: a new tool for rehabilitation" В: M.G. Eisenberg, R.C. Grzesiak, eds. Advances in Clinical Rehabilitation, т. I. New York: Springer-Verlag, стр. 6-18, 1987.
6. К.H. O'Neil, M. Purdy, J. Falk, и L. Gallo, "The Dysphagia Outcome and Severity Scale" Dysphagia, т. 14, №3, стр. 139-145, 1999.
7. E. Carnevale и L. Marietta. Istituto Nazionale di Ricerca per gli Alimenti e la Nutrizione, INRAN. Tabelle di composizione degli alimenti. Roma, Italy: Istituto Superiore Nazionale della Nutrizione; 1989.
8. R. Aquilani, R. Tramarin, R.F. Pedretti с соавт., "Despite good compliance, very low fat diet alone does not achieve recommended cholesterol goals in outpatients with coronary heart disease" Eur Heart J, т. 20, №14, стр. 1020-1029, 1999.
Claims (15)
1. Применение композиции при лечении системного воспалительного процесса у пациентов после инсульта с дисфагией, причем композиция содержит активное вещество, при этом упомянутое активное вещество состоит из аминокислот лейцин, изолейцин, валин, лизин, треонин, гистидин, фенилаланин, метионин, триптофан, тирозин, цистин, при этом композиция содержит один или более загустителей в количестве от 10 до 50 масс. % относительно массы активного вещества.
2. Применение по п. 1, где количество загустителей составляет от 20 до 30 масс. % относительно массы активного вещества.
3. Применение по п. 1 или 2, где загустители выбраны из ксантановой камеди, метилгидроксипропилцеллюлозы, камеди конжака, глюкоманнана конжака, аравийской камеди (камеди акации), модифицированных крахмалов.
4. Применение по п. 1 или 2, где массовое отношение лейцин : изолейцин : валин эквивалентно 2:1:1.
5. Применение по п. 1 или 2, где
- массовое отношение изолейцин : лейцин находится в диапазоне 0,2-0,7, предпочтительно в диапазоне 0,4-0,6, и/или
- массовое отношение валин : лейцин находится в диапазоне 0,2-0,8, предпочтительно в диапазоне 0,4-0,7.
6. Применение по п. 1 или 2, где
- массовое отношение треонин : лейцин находится в диапазоне 0,15-0,50, предпочтительно в диапазоне 0,20-0,45, и/или
- массовое отношение лизин : лейцин находится в диапазоне 0,15-0,60, предпочтительно в диапазоне 0,30-0,55.
7. Применение по п. 1 или 2, где упомянутое активное вещество не содержит аргинин.
8. Применение по п. 1 или 2, где упомянутое активное вещество не содержит серин, пролин, глицин, аланин, глутаминовую кислоту.
9. Применение по п. 1 или 2, где композиция дополнительно содержит один или более витаминов, предпочтительно выбранных из группы витаминов В, таких как витамин B1 и/или витамин В6.
10. Применение по п. 1 или 2, где композиция дополнительно содержит углеводы, добавки и/или вкусоароматические вещества.
11. Применение композиции при лечении системного воспалительного процесса у пациентов после инсульта, причем композиция содержит активное вещество, при этом упомянутое активное вещество состоит из аминокислот лейцин, изолейцин, валин, лизин, треонин, гистидин, фенилаланин, метионин, триптофан, тирозин, цистин.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| ITTO2014A000806 | 2014-10-08 | ||
| ITTO20140806 | 2014-10-08 | ||
| PCT/IB2015/057662 WO2016055948A1 (en) | 2014-10-08 | 2015-10-07 | Compositions comprising amino acids for use in the treatment of stroke in patients with dysphagia |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2668373C1 true RU2668373C1 (ru) | 2018-09-28 |
Family
ID=52101507
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2017112492A RU2668373C1 (ru) | 2014-10-08 | 2015-10-07 | Композиции, содержащие аминокислоты для применения при лечении инсульта у пациентов с дисфагией |
Country Status (14)
| Country | Link |
|---|---|
| US (1) | US9707198B2 (ru) |
| EP (1) | EP3006027B1 (ru) |
| JP (1) | JP6447716B2 (ru) |
| KR (1) | KR102077374B1 (ru) |
| AU (1) | AU2015329581B2 (ru) |
| CA (1) | CA2958033C (ru) |
| DK (1) | DK3006027T3 (ru) |
| ES (1) | ES2651903T3 (ru) |
| HU (1) | HUE035699T2 (ru) |
| NO (1) | NO3006027T3 (ru) |
| NZ (1) | NZ728962A (ru) |
| PL (1) | PL3006027T3 (ru) |
| RU (1) | RU2668373C1 (ru) |
| WO (1) | WO2016055948A1 (ru) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP6773269B2 (ja) * | 2015-05-14 | 2020-10-21 | プロフェッショナル ダイエテティクス エス.ピー.エー. | 放射線療法および/または化学療法を受けている腫瘍患者における粘膜炎の治療における使用のためのアミノ酸を備える組成物 |
| IT201700087376A1 (it) * | 2017-07-28 | 2019-01-28 | Professional Dietetics Spa | Composizioni comprendenti amino acidi per l'uso nel trattamento di malattie associate a disfunzione mitocondriale |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2275084A1 (en) * | 2009-07-15 | 2011-01-19 | Unilever PLC | Oral care composition |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4780475A (en) * | 1986-02-03 | 1988-10-25 | Cerra Frank B | Preparation for the prevention of catabolism |
| US5276018A (en) * | 1992-07-17 | 1994-01-04 | Brigham And Women's Hospital | Composition comprising amino acids and methods for decreasing muscle breakdown |
| IT1320783B1 (it) * | 2000-07-04 | 2003-12-10 | Professional Dietetics Srl | Composizioni a base di aminoacidi, atte al miglioramento delleprestazioni muscolari. |
| US20030060421A1 (en) * | 2001-07-19 | 2003-03-27 | Neuron Therapeutics, Inc. | Kits and compositions supporting intracranial perfusions |
| RU2012105901A (ru) * | 2009-07-20 | 2013-08-27 | Нестек С.А. | Способы снижения потери функционального состояния |
| WO2012117065A1 (en) * | 2011-03-01 | 2012-09-07 | Nestec S.A. | Extensional viscosity to promote safe swallowing of food boluses |
| JP2012214451A (ja) * | 2011-03-25 | 2012-11-08 | En Otsuka Pharmaceutical Co Ltd | 炎症性疾患用アミノ酸組成物 |
| JP5837315B2 (ja) * | 2011-03-25 | 2015-12-24 | イーエヌ大塚製薬株式会社 | 炎症性疾患用栄養組成物 |
| WO2012133198A1 (ja) * | 2011-03-25 | 2012-10-04 | イーエヌ大塚製薬株式会社 | 炎症性疾患用栄養組成物 |
| WO2012142678A1 (en) * | 2011-04-21 | 2012-10-26 | Fit-Bioceuticals Limited | Weight loss composition |
| RU2526826C2 (ru) * | 2012-10-24 | 2014-08-27 | Николай Владимирович Соловьёв | Композиция для парентерального введения, способ получения и применение композиции |
-
2015
- 2015-10-01 NO NO15187946A patent/NO3006027T3/no unknown
- 2015-10-01 ES ES15187946.7T patent/ES2651903T3/es active Active
- 2015-10-01 PL PL15187946T patent/PL3006027T3/pl unknown
- 2015-10-01 EP EP15187946.7A patent/EP3006027B1/en active Active
- 2015-10-01 HU HUE15187946A patent/HUE035699T2/en unknown
- 2015-10-01 DK DK15187946.7T patent/DK3006027T3/en active
- 2015-10-07 AU AU2015329581A patent/AU2015329581B2/en not_active Ceased
- 2015-10-07 JP JP2017511782A patent/JP6447716B2/ja not_active Expired - Fee Related
- 2015-10-07 KR KR1020177009224A patent/KR102077374B1/ko not_active Expired - Fee Related
- 2015-10-07 WO PCT/IB2015/057662 patent/WO2016055948A1/en not_active Ceased
- 2015-10-07 NZ NZ728962A patent/NZ728962A/en not_active IP Right Cessation
- 2015-10-07 CA CA2958033A patent/CA2958033C/en active Active
- 2015-10-07 RU RU2017112492A patent/RU2668373C1/ru active
- 2015-10-08 US US14/878,100 patent/US9707198B2/en not_active Expired - Fee Related
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2275084A1 (en) * | 2009-07-15 | 2011-01-19 | Unilever PLC | Oral care composition |
Non-Patent Citations (7)
| Title |
|---|
| AXEL G. FELLER. Nutrition Support in the Stroke Patient. Nutrition and Stroke, edited by Pierre Guesry, Michael Hennerici, and Gerhard Sitzer. Nestle Nutrition Workshop Series, Supplement. Nestec Ltd., Vevey/Lippincott-Raven Publishers, Philadelphia 1997 р.159-169 DISCUSSION р.170. * |
| DIOGUARDI F. S. Clinical use of amino acids as dietary supplement: pros and cons. Journal of Cachexia, Sarcopenia and Muscle, 2011vol. 2, no. 2, pp. 75-80, с. 78, фиг.1. * |
| DIOGUARDI F. S. Clinical use of amino acids as dietary supplement: pros and cons. Journal of Cachexia, Sarcopenia and Muscle, 2011vol. 2, no. 2, pp. 75-80, с. 78, фиг.1. AXEL G. FELLER. Nutrition Support in the Stroke Patient. Nutrition and Stroke, edited by Pierre Guesry, Michael Hennerici, and Gerhard Sitzer. Nestle Nutrition Workshop Series, Supplement. Nestec Ltd., Vevey/Lippincott-Raven Publishers, Philadelphia 1997 р.159-169 DISCUSSION р.170. WILFRED DRUML. Amino acid kinetics in patients with sepsis. Am J Clin Nutr 2001;73:908-13. Printed in USA. American Society for Clinical Nutrition 1-3. SHIN-JOE YEH. Dysphagia screening decreases pneumonia in acute stroke patients admitted to the stroke intensive care unit. Journal of the Neurological Sciences 306 (2011) 38-41 doi:10.1016/j.jns.2011.04.001. DIOGUARDI F. S. Clinical use of amino acids as dietary supplement: pros and cons. Journal of Cachexia, Sarcopenia and Muscle, 2011vol. 2, no. 2, pp. 75-80. * |
| DIOGUARDI F. S. Clinical use of amino acids as dietary supplement: pros and cons. Journal of Cachexia, Sarcopenia and Muscle, 2011vol. 2, no. 2, pp. 75-80. * |
| SHIN-JOE YEH. Dysphagia screening decreases pneumonia in acute stroke patients admitted to the stroke intensive care unit. Journal of the Neurological Sciences 306 (2011) 38-41 doi:10.1016/j.jns.2011.04.001. * |
| WILFRED DRUML. Amino acid kinetics in patients with sepsis. Am J Clin Nutr 2001;73:908-13. Printed in USA. American Society for Clinical Nutrition 1-3. * |
| РУМЯНЦЕВА С.А. Алгоритмы терапии острого инсульта. пункт 9. Новости медицины и фармации: всеукр. спец. мед.-фармац. изд. - Кихв. Неврология (328) 2010 (тематический номер) с.25-30. * |
Also Published As
| Publication number | Publication date |
|---|---|
| DK3006027T3 (en) | 2017-12-18 |
| NO3006027T3 (ru) | 2018-04-14 |
| KR102077374B1 (ko) | 2020-02-13 |
| KR20170057308A (ko) | 2017-05-24 |
| NZ728962A (en) | 2019-05-31 |
| EP3006027A1 (en) | 2016-04-13 |
| CA2958033A1 (en) | 2016-04-14 |
| JP6447716B2 (ja) | 2019-01-09 |
| CA2958033C (en) | 2019-07-16 |
| ES2651903T3 (es) | 2018-01-30 |
| HUE035699T2 (en) | 2018-05-28 |
| US9707198B2 (en) | 2017-07-18 |
| EP3006027B1 (en) | 2017-11-15 |
| AU2015329581A1 (en) | 2017-03-02 |
| PL3006027T3 (pl) | 2018-02-28 |
| US20160101078A1 (en) | 2016-04-14 |
| AU2015329581B2 (en) | 2019-02-07 |
| JP2017530103A (ja) | 2017-10-12 |
| WO2016055948A1 (en) | 2016-04-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Bo et al. | A high whey protein, vitamin D and E supplement preserves muscle mass, strength, and quality of life in sarcopenic older adults: A double-blind randomized controlled trial | |
| Viana et al. | Impact of β− hydroxy-β− methylbutyrate (HMB) on muscle loss and protein metabolism in critically ill patients: A RCT | |
| Ferrando et al. | International Society of Sports Nutrition Position Stand: Effects of essential amino acid supplementation on exercise and performance | |
| May et al. | Reversal of cancer-related wasting using oral supplementation with a combination of β-hydroxy-β-methylbutyrate, arginine, and glutamine | |
| Symons et al. | Aging does not impair the anabolic response to a protein-rich meal | |
| Breen et al. | Skeletal muscle protein metabolism in the elderly: Interventions to counteract the'anabolic resistance'of ageing | |
| Børsheim et al. | Essential amino acids and muscle protein recovery from resistance exercise | |
| Irving et al. | Effect of insulin sensitizer therapy on amino acids and their metabolites | |
| Adachi et al. | Effects of ghrelin administration after total gastrectomy: a prospective, randomized, placebo-controlled phase II study | |
| Rondanelli et al. | Effect of essential amino acid supplementation on quality of life, amino acid profile and strength in institutionalized elderly patients | |
| Aquilani et al. | Unaffected arm muscle hypercatabolism in dysphagic subacute stroke patients: the effects of essential amino acid supplementation | |
| RU2668373C1 (ru) | Композиции, содержащие аминокислоты для применения при лечении инсульта у пациентов с дисфагией | |
| Kawahara et al. | Anti-sarcopenic effects of active vitamin D through modulation of anabolic and catabolic signaling pathways in human skeletal muscle: a randomized controlled trial | |
| Wicks et al. | Sarcopenia, diabetes, and nutritional intervention | |
| Cao et al. | Intensive versus conventional insulin therapy in nondiabetic patients receiving parenteral nutrition after D2 gastrectomy for gastric cancer: a randomized controlled trial | |
| Jirka et al. | Effect of oral citrulline supplementation on whole body protein metabolism in adult patients with short bowel syndrome: A pilot, randomized, double-blind, cross-over study | |
| JP7789007B2 (ja) | アミノ酸を含有する組成物及びサルコペニアを治療するためにかかる組成物を使用する方法 | |
| Jourdan et al. | O025 CITRULLINE STIMULATES MUSCLE PROTEIN SYNTHESIS AT THE POST-ABSORPTIVE STATE IN HEALTHY SUBJECTS FED A LOW-PROTEIN DIET | |
| Takiguchi et al. | Clinical trial of ghrelin synthesis administration for upper GI surgery | |
| Ertuglu et al. | Protein–Energy Wasting and Nutritional Interventions in Chronic Kidney Disease | |
| Kawano et al. | Successful treatment of heart failure in an adult patient with Prader-Willi syndrome | |
| Deger et al. | Nutritional Management of Hemodialysis Patients | |
| Oyama et al. | Jelly-type carbohydrate supplement in healthy subjects suppresses the catabolism of adipose tissue and muscle protein and improves their satisfactions | |
| Lyon et al. | 12 Metabolic Interventions for Sarcopenic Obesity | |
| Fitschen | Efficacy of beta-hydroxy-beta-methylbutyrate (HMB) supplementation in hemodialysis patients |