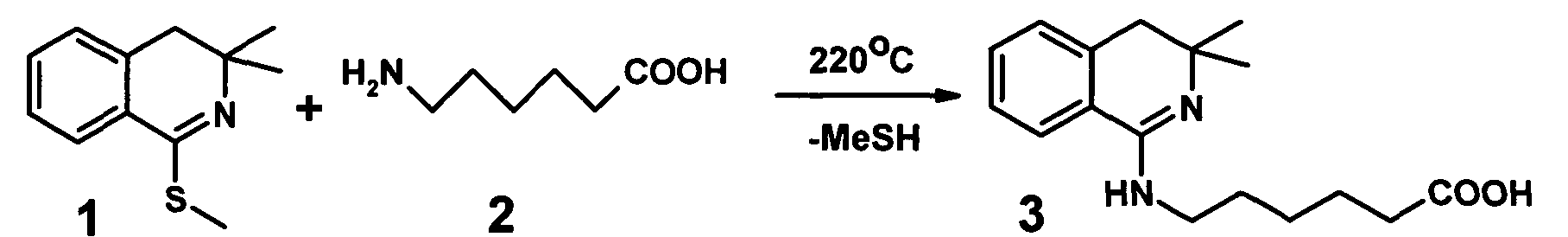RU2563244C1 - Способ получения n-(3,3-диметил-3,4-дигидроизохинолил-1)-6-аминокапроновой кислоты - Google Patents
Способ получения n-(3,3-диметил-3,4-дигидроизохинолил-1)-6-аминокапроновой кислоты Download PDFInfo
- Publication number
- RU2563244C1 RU2563244C1 RU2014142439/04A RU2014142439A RU2563244C1 RU 2563244 C1 RU2563244 C1 RU 2563244C1 RU 2014142439/04 A RU2014142439/04 A RU 2014142439/04A RU 2014142439 A RU2014142439 A RU 2014142439A RU 2563244 C1 RU2563244 C1 RU 2563244C1
- Authority
- RU
- Russia
- Prior art keywords
- dimethyl
- aminocaproic acid
- dihydroisoquinolyl
- producing
- dihydroisoquinoline
- Prior art date
Links
- SLXKOJJOQWFEFD-UHFFFAOYSA-N 6-aminohexanoic acid Chemical compound NCCCCCC(O)=O SLXKOJJOQWFEFD-UHFFFAOYSA-N 0.000 title claims abstract description 19
- 238000000034 method Methods 0.000 title claims abstract description 18
- IAYIROUIYOEEAO-UHFFFAOYSA-N 3,3-dimethyl-1-methylsulfanyl-4h-isoquinoline Chemical compound C1=CC=C2C(SC)=NC(C)(C)CC2=C1 IAYIROUIYOEEAO-UHFFFAOYSA-N 0.000 claims abstract description 10
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims abstract description 9
- 229960002684 aminocaproic acid Drugs 0.000 claims abstract description 8
- 238000002425 crystallisation Methods 0.000 claims abstract description 5
- 239000002904 solvent Substances 0.000 claims abstract description 5
- 230000003993 interaction Effects 0.000 claims description 6
- 230000008025 crystallization Effects 0.000 claims description 4
- 239000000463 material Substances 0.000 abstract description 2
- 238000000746 purification Methods 0.000 abstract description 2
- 238000001953 recrystallisation Methods 0.000 abstract description 2
- 239000007795 chemical reaction product Substances 0.000 abstract 1
- 238000010438 heat treatment Methods 0.000 abstract 1
- 239000000047 product Substances 0.000 abstract 1
- 239000000126 substance Substances 0.000 abstract 1
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 8
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 6
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 4
- LSDPWZHWYPCBBB-UHFFFAOYSA-N Methanethiol Chemical compound SC LSDPWZHWYPCBBB-UHFFFAOYSA-N 0.000 description 4
- 235000019441 ethanol Nutrition 0.000 description 4
- 238000004519 manufacturing process Methods 0.000 description 4
- 150000001412 amines Chemical class 0.000 description 3
- 229910052786 argon Inorganic materials 0.000 description 3
- 230000001760 anti-analgesic effect Effects 0.000 description 2
- 230000003110 anti-inflammatory effect Effects 0.000 description 2
- 150000002391 heterocyclic compounds Chemical class 0.000 description 2
- RPMSUIMQCCQJDX-UHFFFAOYSA-N 1-methylsulfanyl-3,4-dihydroisoquinoline Chemical class C1=CC=C2C(SC)=NCCC2=C1 RPMSUIMQCCQJDX-UHFFFAOYSA-N 0.000 description 1
- FXQNTOHRTXRWTM-UHFFFAOYSA-N 3,3-dimethyl-4h-isoquinoline Chemical class C1=CC=C2C=NC(C)(C)CC2=C1 FXQNTOHRTXRWTM-UHFFFAOYSA-N 0.000 description 1
- 229910000831 Steel Inorganic materials 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 230000000202 analgesic effect Effects 0.000 description 1
- 239000000730 antalgic agent Substances 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 239000012153 distilled water Substances 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 239000000203 mixture Substances 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 238000010992 reflux Methods 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 239000010959 steel Substances 0.000 description 1
Landscapes
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
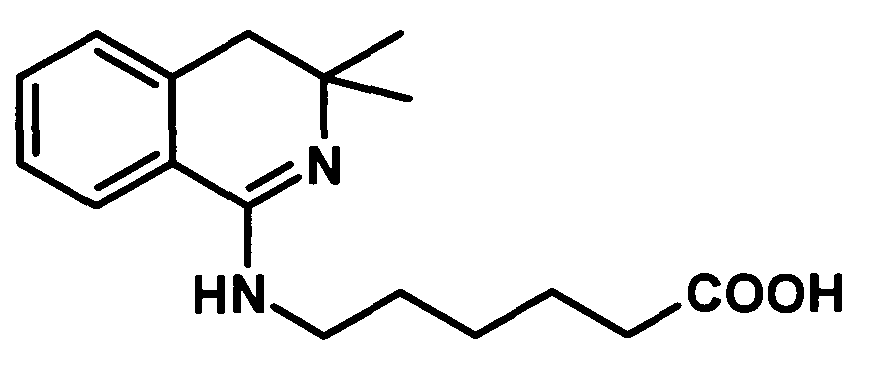
Изобретение относится к области органической химии, а именно к способу получения N-(3,3-диметил-3,4-дигидроизохинолил-1)-6-аминокапроновой кислоты, заключающийся во взаимодействии 1-метилтио-3,3-диметил-3,4-дигидроизохинолина с ε-аминокапроновой кислотой при нагревании в автоклаве без растворителя с последующей очисткой продукта кристаллизацией из воды. Технический результат: предлагаемый способ получения позволяет существенно увеличить выход целевого продукта, сократить время проведения процесса, а также снизить пожароопасность и материальные затраты за счет использования для перекристаллизации воды. 1 з.п. ф-лы, 2 пр.
Description
Изобретение относится к области химии гетероциклических соединений, а именно к способу получения N-(3,3-диметил-3,4-дигидроизохинолил-1)-6-аминокапроновой кислоты, являющейся ненаркотическим анальгезирующим средством [Патент RU №2223763. Анальгезирующее средство. Опубл. 20.02.2004. БИ №5].
Известен способ получения 1-N-замещенных производных 3,3-диметил-3,4-дигидроизохинолина взаимодействием 1-метилтио-3,3-диметил-3,4-дигидроизохинолина с аминами при температуре 150°С с выделением продуктов известными способами [Взаимодействие 1-метилтио-3,4-дигидроизохинолинов с аминами / Шкляев Ю.В.; Глушков В.А.; Белогуб Н.Б.; Мисюра И.Л. // Химия гетероциклических соединений. - 1996. - №6. - С. 800-806]. К недостаткам указанного способа относится сравнительно низкая температура проведения реакции, которая не позволяет проводить реакцию в гомогенных условиях, поскольку т.пл. ε-аминокапроновой кислоты равна 210-212°С и, кроме того, в реакции используется избыток амина, что в данном случае затрудняет выделение целевого продукта.
Наиболее близким по технической сущности, принятым за прототип, является способ получения N-(3,3-диметил-3,4-дигидроизохинолил-1)-6-аминокапроновой кислоты взаимодействием 1-метилтио-3,3-диметил-3,4-дигидроизохинолина с ε-аминокапроновой кислотой в среде этилового спирта при нагревании [Противоспалительная и анальгетическая активность N-(3,3-диметил-3,4-дигидроизохинолил-1)-аминокислот / Л.В. Аникина, Ю.Б. Вихарев, В.А. Сафин, А.А. Горбунов, Ю.В. Шкляев, В.И. Карманов. // Хим. - фарм. журнал. - 2002. - Т. 36.- №2. - С. 19-23].
К недостаткам данного способа следует отнести сравнительно низкий выход (71%) целевого продукта, большую длительность процесса (4 ч) и использование пожароопасного этилового спирта.
Задачей предлагаемого изобретения является увеличение выхода целевого продукта, сокращение времени реакции и уменьшение пожароопасности при проведении процесса.
1. Для решения поставленной задачи предлагается способ получения N-(3,3-диметил-3,4-дигидроизохинолил-1)-6-аминокапроновой кислоты
взаимодействием 1-метилтио-3,3-диметил-3,4-дигидроизохинолина с ε-аминокапроновой кислотой при нагревании, где реакцию проводят в автоклаве без растворителя.
2. Способ получения N-(3,3-диметил-3,4-дигидроизохинолил-1)-6-аминокапроновой кислоты по п. 1 отличается тем, что очистку продукта проводят кристаллизацией из воды.
Указанная задача решается взаимодействием смеси эквимолярных количеств 1-метилтио-3,3-диметил-3,4-дигидроизохинолина и ε-аминокапроновой кислоты при повышенном давлении и температуре.
Повышение давления за счет выделения метилмеркаптана повышает т. кип. 1-метилтио-3,3-диметил-3,4-дигидроизохинолина, что способствует протеканию реакции в гомогенной фазе, а повышение температуры способствует увеличению скорости реакции. В совокупности данные факторы приводят к увеличению выхода целевого продукта и уменьшению времени проведения процесса. Использование воды вместо этилового спирта на стадии очистки N-(3,3-диметил-3,4-дигидроизохинолил-1)-6-аминокапроновой кислоты снижает пожароопасность процесса.
Предлагаемый способ отличается от выбранного прототипа тем, что реакцию проводят в автоклаве без растворителя, а очистку продукта проводят кристаллизацией из воды. Это позволяет сделать вывод о соответствии заявляемого решения критерию "новизна".
Достижение указанного технического результата возможно только при использовании всех существенных признаков предлагаемого технического решения в совокупности, что обеспечивает соответствие его критерию "изобретательский уровень".
Возможность осуществления предлагаемого способа подтверждается примерами.
Пример 1 (прототип)
В двугорлую круглодонную колбу емкостью 50 мл, снабженную трубкой для ввода аргона, помещают 6.55 г (0.05 моля) 6-аминокапроновой кислоты и 10.25 г (0.05 моля) 1-метилтио-3,3-диметил-3,4-дигидроизохинолина. Колбу закрывают обратным холодильником, снабженным ловушкой для поглощения выделяющегося метилмеркаптана, подают ток аргона (1-2 пузырька в сек) и помещают на металлическую баню, нагретую до 180°С. Температуру постепенно поднимают до 220°С и выдерживают в течение 30 мин. Колбу охлаждают, добавляют 2 г активированного угля и 100 мл дистиллированной воды, после чего кипятят в течение 10 мин. Раствор фильтруют горячим через складчатый фильтр и охлаждают. Выделившиеся кристаллы отделяют и сушат при 200°С. Получают 21.6 г (75%) N-(3,3-диметил-3,4-дигидроизохинолил-1)-6-аминокапроновой кислоты, т.пл. 210-214°С. Найдено, %: С 71.03; Н 8.54; N 9.75. С17Н24N2O2. Вычислено, %: С 70.80; Н 8.39; N 9.71.
В литературе [Противоспалительная и анальгетическая активность N-(3,3-диметил-3,4-дигидроизохинолил-1)-аминокислот / Л.В. Аникина, Ю.Б. Вихарев, В.А. Сафин, А.А. Горбунов, Ю.В. Шкляев, В.И. Карманов. // Хим. - фарм. журнал. - 2002. - Т. 36. - №2. - С. 19-23] т.пл. 179-182°С, что связано с кристаллизацией продукта из другого растворителя. Сравнительно низкий выход целевого продукта объясняется тем, что его т.пл. значительно выше, чем т.кип. 1-метилтио-3,3-диметил-3,4-дигидроизохинолина, и часть исходного не вступает в реакцию.
Пример 2
В стальной вращающийся автоклав емкостью 500 мл помещают 13.1 г (0.1 моля) 6-аминокапроновой кислоты и 20.5 г (0.1 моля) 1-метилтио-3,3-диметил-3,4-дигидроизохинолина. Автоклав продувают аргоном, закрывают, включают вращение, нагревают до 220°С и выдерживают до прекращения повышения давления (~30 мин). Давление сбрасывают, содержимое автоклава обрабатывают, как описано в примере 1, используя 4 г активированного угля и 200 мл воды. Получают 25 г (~87%) N-(3,3-диметил-3,4-дигидроизохинолил-1)-6-аминокапроновой кислоты, константы которой совпадают с описанными в примере 1.
Таким образом, применение предлагаемого способа позволяет существенно увеличить выход целевого продукта, сократить время проведения процесса, а также снизить пожароопасность и материальные затраты за счет использования для перекристаллизации воды вместо этилового спирта.
Claims (2)
2. Способ получения N-(3,3-диметил-3,4-дигидроизохинолил-1)-6-аминокапроновой кислоты по п. 1, отличающийся тем, что очистку продукта проводят кристаллизацией из воды.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2014142439/04A RU2563244C1 (ru) | 2014-10-21 | 2014-10-21 | Способ получения n-(3,3-диметил-3,4-дигидроизохинолил-1)-6-аминокапроновой кислоты |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2014142439/04A RU2563244C1 (ru) | 2014-10-21 | 2014-10-21 | Способ получения n-(3,3-диметил-3,4-дигидроизохинолил-1)-6-аминокапроновой кислоты |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2563244C1 true RU2563244C1 (ru) | 2015-09-20 |
Family
ID=54147748
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2014142439/04A RU2563244C1 (ru) | 2014-10-21 | 2014-10-21 | Способ получения n-(3,3-диметил-3,4-дигидроизохинолил-1)-6-аминокапроновой кислоты |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2563244C1 (ru) |
-
2014
- 2014-10-21 RU RU2014142439/04A patent/RU2563244C1/ru not_active IP Right Cessation
Non-Patent Citations (1)
| Title |
|---|
| Аникина Л.В. и др.: "Противовоспалительная и анальгетическая активность N-(3,3-диметил-3,4-дигидроизохинолин-1-)-аминокислот", Химико-фармацевтическая журнал, 36(2), стр.19-23, 2002. Сыропятов Б.Я. и др.: "Синтез и антиаритмическая и антиагрегационная активность 3,4-дигидроизохинолинаминокислот", Химико-фармацевтическая журнал, 30(11), стр.13-14, 1996 * |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Moriarty et al. | Preparation of methyl carbamates from primary alkyl-and arylcarboxamides using hypervalent iodine | |
| JP7236433B2 (ja) | Lfa-1拮抗薬リフィテグラストを調製および精製するためのプロセス | |
| JPWO2014157612A1 (ja) | (1s,4s,5s)−4−ブロモ−6−オキサビシクロ[3.2.1]オクタン−7−オンの製造方法 | |
| AU2009309378A1 (en) | Acrylamido derivatives useful as inhibitors of the mitochondrial permeability transition | |
| RU2593752C1 (ru) | Соединения, пригодные для синтеза бензамидных соединений | |
| CA3100715A1 (en) | Inhibitors of integrated stress response pathway | |
| JP6370316B2 (ja) | エナンチオマー濃縮された3−アミノピペリジンの調製のためのプロセス | |
| RU2563244C1 (ru) | Способ получения n-(3,3-диметил-3,4-дигидроизохинолил-1)-6-аминокапроновой кислоты | |
| JP2016537396A5 (ru) | ||
| Valiveti et al. | Synthesis and in vitro kinetic evaluation of N-thiazolylacetamido monoquaternary pyridinium oximes as reactivators of sarin, O-ethylsarin and VX inhibited human acetylcholinesterase (hAChE) | |
| Liu et al. | Diastereoselective Synthesis of Arylidene Bis (3‐arylaminoacrylates) via One‐pot Domino Reactions | |
| JP4463209B2 (ja) | 光学活性アミン化合物の製造方法 | |
| UA113281C2 (xx) | Поліпшений спосіб отримання 1-заміщених 2-трифторметил-5-алкілпіридинів | |
| US6825353B2 (en) | Process for producing quinolonecarboxylic acids and intermediates thereof | |
| JP2018520134A (ja) | オルチプラズを調製する方法 | |
| JP6763401B2 (ja) | ベンズオキサゾール化合物の製造方法 | |
| ES2322500T3 (es) | Proceso para la preparacion de derivados del acido 2-azabiciclo(3.3.0)-octano-3-carboxilico. | |
| Coffey et al. | 197. Ethyl esters of β-arylaminocrotonic acids | |
| RU2461545C1 (ru) | Способ получения 2-метилпиримидин-4,6-(3н,5н)-диона | |
| RU2653511C2 (ru) | 4-метил-n-2,4-диметилфенил-6-(3-фторфенил)-2-тиоксо-1,2,3,6-тетрагидропиримидин-5-карбоксамид, проявляющий анальгетическое действие | |
| RU2663899C1 (ru) | Способ получения 1-карбамоилметил-4-фенил-2-пирролидона | |
| JP2016539185A (ja) | N−ベンジル−2−(2−ニトロ−1h−イミダゾール−1−イル)アセトアミドを得るための製造工程 | |
| RU2649141C2 (ru) | 3,4-диметил-6-(3-пиридил)-N-фенил-2-оксо-1,2,3,6-тетрагидропиримидин-5-карбоксамид, проявляющий противогрибковое действие в отношении штамма Candida albicans | |
| US9758488B2 (en) | Method for preparing phenyloxymethyl-nitro-imidazole derivatives and use of same | |
| EP1258478A1 (en) | Process for producing quinolonecarboxylic acids and intermediates thereof |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20161022 |