RU2557927C1 - Способ диагностики фиброза печени при хроническом вирусном гепатите с - Google Patents
Способ диагностики фиброза печени при хроническом вирусном гепатите с Download PDFInfo
- Publication number
- RU2557927C1 RU2557927C1 RU2014123015/15A RU2014123015A RU2557927C1 RU 2557927 C1 RU2557927 C1 RU 2557927C1 RU 2014123015/15 A RU2014123015/15 A RU 2014123015/15A RU 2014123015 A RU2014123015 A RU 2014123015A RU 2557927 C1 RU2557927 C1 RU 2557927C1
- Authority
- RU
- Russia
- Prior art keywords
- stage
- fibrosis
- hcv
- timp
- liver
- Prior art date
Links
Landscapes
- Investigating Or Analysing Biological Materials (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Abstract
Изобретение относится к области медицины, а именно к инфекционным болезням и гастроэнтерологии. Способ диагностики наличия и стадии фиброза печени при хроническом вирусном гепатите С заключается в том, что определяют концентрации ГГТ, ТФР-β1, ТИМП-1 и комплекс ММП-9/ТИМП-2 в сыворотке крови, на 1-м этапе рассчитывают вероятность наличия HCV-ассоциированного фиброза печени (РНФП) по формуле: РНФП=(ey/(1+ey))×100%, где y=-13,6+3,78·X1-0,1·X2 где X1 - сывороточное значение прогностического фактора ММП-9/ТИМП-2, X2 - сывороточное значение прогностического фактора ТИМП-1, ey - экспоненциальная функция. При значении РНФП>50% прогнозируют наличие HCV-ассоциированных фиброзных изменений в печени. Далее на 2-м этапе рассчитывают вероятность стадии HCV-ассоциированного фиброза печени (РСФП) по формуле: РСФП=(ey/(1+ey))×100%, где y=-12+0,134317·X1+0,527778·X2-0,05·X3, где X1 - сывороточное значение прогностического фактора ММП-9/ТИМП-2, X2 - сывороточное значение прогностического фактора ТФР-β1; X3 - сывороточное значение прогностического фактора ГГТ. При значении РСФП>50% диагностируют наличие предцирротической стадии фиброза и цирроза печени при ХВГС (F3-4 ст.), при РСФП<50% - HCV-ассоциированного фиброза печени начальной стадии (F0-2 ст.). Заявленный способ является простым в исполнении, доступным для практических медицинских учреждений здравоохранения, неинвазивным и безопасным для пациентов, экономичным по стоимости и времени, эффективным для скрининга предцирротической стадии фиброза и цирроза печени. 3 пр., 3 табл.
Description
Изобретение относится к области медицины, а именно к инфекционным болезням и гастроэнтерологии, и может использоваться для неинвазивной диагностики фиброза печени при хроническом вирусном гепатите С (ХВГС) с целью скрининга предцирротической стадии фиброза и цирроза печени.
Хронические заболевания печени вирусной этиологии являются одной из наиболее актуальных и серьезных медико-социальных и экономических проблем современной мировой медицины [10]. Лидирующее место среди ХЗП занимает вирусный гепатит С. По последним данным Всемирной организации здравоохранения на земном шаре насчитывают около 500 млн. человек, инфицированных вирусом гепатита С, при этом ряд авторов отмечают, что 170-180 млн. человек из них, около 2,6% населения мира, - это пациенты с хронической HCV-инфекцией [6].
Прогноз заболевания и тактика ведения пациентов с ХВГС зависят от своевременной диагностики фиброза печени на начальной стадии (F0-2 ст.), которая позволяет определить показания и характер проводимого лечения, вероятность успеха и потенциальный риск развития нежелательных явлений противовирусной терапии и, конечно же, предотвратить дальнейшее прогрессирование фиброза и связанные с ним неблагоприятные последствия [1].
В настоящее время пункционная биопсия печени с морфологическим исследованием биоптата, позволяющим с помощью различных полуколичественных индексов (Knodell, Ishak, METAVIR, Desmet) установить степень воспалительной активности и стадию фиброзирования, остается основным методом («золотым стандартом») определения выраженности фиброзных изменений печеночной паренхимы [10]. Однако более широкое внедрение методики в клиническую практику специализированных отделений ограничивается наличием некоторых проблем: инвазивный характер процедуры и потенциальный риск развития осложнений, наличие противопоказаний. А также существенен риск недооценки или переоценки гистологической картины при нарушении стандартной техники выполнения процедуры, включая «ошибки попадания», нехватка квалифицированных морфологов, способных объективно описать и дать количественную оценку морфологическим признакам, несовершенство предложенной системы полуколичественной оценки индекса гистологической активности и стадии фиброза, отсутствие возможности регулярного динамического исследования и т.д. [9].
Существует способ диагностики фиброза печени с помощью Фибротеста (Biopredictive, Франция) [1]. Исследование основывается на определении в сыворотке крови по стандартной методике 6 специфических протеинов: гаптоглобулин, альфа-2-макроглобулин, аполипопротеин А1, ГГТ, АЛТ и общий билирубин, которые измеряются от 0,00 до 1,00. По полученным данным, а также учитывая пол и возраст пациента, с помощью программы вычисляется результирующая величина, позволяющая установить степень активности гепатита и стадию фиброзных изменений в органе-мишени от F0 до F4. Недостатками применения теста является возрастание показателей билирубина и/или уменьшение уровня гаптоглобина, не связанное с печеночной недостаточностью (гемолиз, функциональные гипербилирубинемии), ограничение его доступности для медицинских учреждений здравоохранения и стоимость для пациентов [9].
Известен способ оценки выраженности фиброзных изменений в печени при ХВГС, заключающийся в определении фенотипа CD56+ лимфоцитов крови и по диапазону значений процентного содержания CD3+/CD56+, CD3+/CD56+/CD4+, CD3+/CD56+/CD8+, CD56+/CD94+, CD56+/NKG2D+, CD56+/CD107a+ клеток в крови устанавливают третью стадию фиброза или цирроз печени [3]. Трудоемкий процесс выполнения исследования, определенные сложности в интерпретации результатов диагностики, ограничение внедрения методики в клиническую практику являются недостатками данного метода.
На сегодняшний день признано, что иммунологические механизмы являются одними из ведущих в патогенезе ХВГС и его исходах. Имеются убедительные данные о роли дисбаланса цитокинов на системном и локальном уровнях в вирусной персистенции и хронизации HCV-инфекции. Определение содержания цитокинов в биологических средах может свидетельствовать о функциональной активности различных иммунокомпетентных клеток, а следовательно, о патологическом процессе в целом, его течении и исходе [5]. Важное значение в прогрессирование ХВГС имеет трансформирующий фактор роста-β1 (ТФР-β1), что обусловлено его биологическими эффектами, а именно, иммуносупрессивным, провоспалительным и, конечно же, профиброгенным [8].
В качестве прототипа выбран способ диагностики фиброза печени при ХВГС, основанный на исследовании венозной крови пациента и определении сывороточной концентрации ТФР-β1 методом твердофазного иммуноферментного анализа, и при значении концентрации ТФР-β1 более 400 пг/мл диагностируют слабовыраженный или умеренный фиброз печени, а при значении ТФР-β1 менее 400 пг/мл - выраженный фиброз или цирроз печени [2].
Фиброз печени - это универсальный патофизиологический процесс, характеризующий нарушением равновесия между синтезом и разрушением компонентов экстрацеллюлярного матрикса [8]. Следовательно, недостатком прототипа следует считать то, что не учитывается процесс фибролиза, поскольку ТФР-β1 может свидетельствовать только о фиброгенезе печени.
В настоящее время известно, что ведущую роль в иммунопатогенезе фиброза печени играет дисбаланс в системе ММП/ТИМП, которая является ключевым эффектором процесса ремоделирования соединительной ткани, и отражает структурные изменения внеклеточного матрикса печеной ткани [7].
Таким образом, углубленное исследование недостаточно изученных механизмов иммунопатогенеза фиброза печени при ХВГС будет способствовать созданию новых и/или усовершенствованию имеющихся методов диагностики фиброзных изменений в органе-мишени.
Задача настоящего изобретения заключается в разработке неинвазивного способа диагностики HCV-ассоциированного фиброза печени с учетом иммунных нарушений при данной патологии.
Поставленная задача достигается тем, что определяют концентрации ГГТ, ТФР-β1, ТИМП-1 и комлекс ММП-9/ТИМП-2 в сыворотке крови, на 1-м этапе рассчитывают вероятность наличия HCV-ассоциированного фиброза печени (РНФП) по формуле:
РНФП=(ey(1+ey))×100%,
где y=-13,6+3,78·X1-0,1·X2, где
X1 - сывороточное значение прогностического фактора ММП-9/ТИМП-2, X2 - сывороточное значение прогностического фактора ТИМП-1, ey - экспоненциальная функция,
и при значении РНФП>50% прогнозируют наличие HCV-ассоциированных фиброзных изменений в печени; на 2-м этапе рассчитывают вероятность стадии HCV-ассоциированного фиброза печени (РСФП) по формуле:
РСФП=(ey/(1+ey)×100%,
где y=-12+0,134317·X1+0,527778·X2-0,05·X3, где
X1 - сывороточное значение прогностического фактора ММП-9/ТИМП-2, Х2 - сывороточное значение прогностического фактора ТФР-β1; Х3 - сывороточное значение прогностического фактора ГГТ,
и при значении РСФП>50% диагностируют наличие предцирротической стадии фиброза и цирроза печени при ХВГС (F3-4 ст.), при РСФП<50% - HCV-ассоциированного фиброза печени начальной стадии (F0-2 ст.).
Технический результат заявляемого способа заключается в следующем: простота технического выполнения, а также интерпретации результатов исследования; доступность применения в клинической практике медицинских учреждений здравоохранения; неинвазивность; безопасность для пациентов, а именно отсутствие противопоказаний и потенциального риска развития осложнений; низкая стоимость; короткая продолжительность во времени от момента диагностики до получения заключения; возможность проведения повторного исследования с необходимой частотой в динамике; применение не только «рутинных» биохимических, но и специфических иммунологических показателей в качестве маркеров фиброзного поражения печени; высокая точность дифференциальной диагностики начального (F0-2 ст.) и выраженного (F3-4 ст.) фиброза печени; возможность своевременной коррекции тактики ведения пациента и, следовательно, предотвратить прогрессирование фиброза печени и связанные с ним неблагоприятные последствия.
Заявленный способ диагностики осуществляется следующим образом.
Обследована группа пациентов численностью 103 человека, самостоятельно обратившихся за медицинской помощью в лечебно-профилактические учреждения. Случайность выборки исследуемой группы обеспечивает максимальное соответствие ее основных свойств генеральной совокупности пациентов, которые обращаются в медицинские организации по поводу ХВГС.
Все пациенты подверглись комплексному обследованию, по результатам которого было выявлено, что 22 чел. (21,4%) - практически здоровые пациенты, 81 чел. (78,6%) - HCV-инфицированные пациенты с разной степенью выраженности фиброзных изменений в печени. В связи с чем исследуемые пациенты были распределены на четыре группы: I-я - HCV-инфицированные пациенты, у которых признаки фиброза отсутствуют (F0 ст.) - 24 чел. (23,3% от общей численности обследованных лиц), II-я - HCV-инфицированные пациенты со слабовыраженным и умеренным фиброзом печени (F1-2 ст.) - 26 чел. (25,2%), III-я - HCV-инфицированные пациенты с тяжелой стадией фиброза и циррозом печени (F3-4 ст.) - 31 чел. (30,1%), IV-я - практически здоровые пациенты - 22 чел. (21,4%).
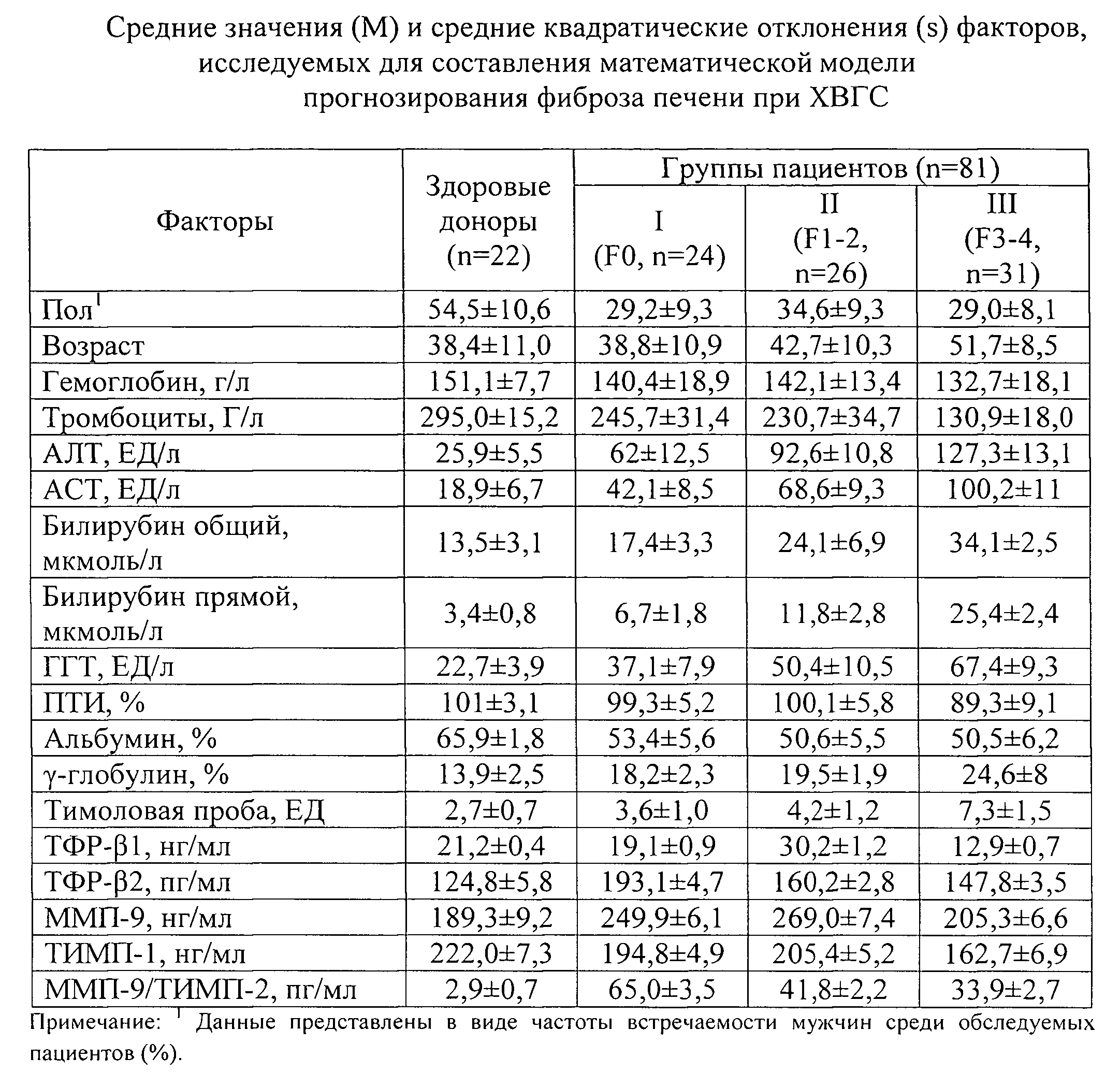
Для сформированной когорты пациентов была собрана база данных по факторам, описывающие значения которых представлены в таблице 1.
Первым этапом для достижения поставленной задачи являлось составление математической формулы, позволяющей определить наличие фиброзных изменений в печени при ХВГС. Для этого первоначально выявляли наличие и силу статистической связи между факторами и HCV-ассоциированным фиброзом печени, который представляет собой двоичный ряд чисел, где 1 - наличие фиброза печени, 0 - его отсутствие [4]. Так как заболевание представляет собой двоичный числовой ряд, то в качестве метода исследования был выбран коэффициент корреляции для непараметрических данных Спирмена. Оценка корреляционной связи показала наличие статистически значимой (р<0,05) взаимосвязи между факторами и фиброзом печени у 17 факторов из 18, исключение составил показатель сывороточного уровня ТФР-β1.
Далее определяли линейно-независимые друг от друга факторы, которые имеют статистически значимую корреляцию (р<0,05) с HCV-ассоциированным фиброзом печени, используя непараметрический коэффициент корреляции Спирмена (табл. 2).
Учитывая полученные данные, были выбраны два независимых друг от друга прогностических фактора: ММП-9/ТИМП-2 и ТИМП-1, которые в то же время статистически значимо коррелировали с наличием HCV-ассоциированного фиброза печени (rS=0,71 и rS=-0,34 соответственно, р<0,05).
Заключительная часть первого этапа - построение математической формулы для вычисления вероятности наличия фиброза печени (РНПФ) при ХВГС с помощью логистического регрессионного анализа:
РНПФ=(ey/(1+ey)×100%,
где y=-13,6+3,78·X1-0,1·Х2, где
X1 - сывороточное значение прогностического фактора ММП-9/ТИМП-2, Х2 - сывороточное значение прогностического фактора ТИМП-1, ey - экспоненциальная функция.
Полученную РНПФ соотносят с граничным значением 50%. При РНПФ>50% прогнозируют наличие HCV-ассоциированных фиброзных изменений в печени, при РНПФ<50% - отсутствие фиброза печени при ХВГС.
Диагностическая точность разработанной математической формулы проверили на исследуемой группе пациентов (103 чел.). Анализ полученных данных показал совпадение прогнозных и фактических результатов отсутствия/наличия HCV-ассоциированного фиброза печени в 100% случаев, а именно во всех случаях наличия фиброза печени прогнозное значение было равно 100%, при отсутствии - 0%.
Второй этап реализации поставленной задачи - построение математической формулы, позволяющей у пациентов ХВГС с фиброзом печени определить стадию патологических изменений в органе-мишени.
Для выполнения этой части работы были использованы данные HCV-инфицированных пациентов с разной степенью выраженности фиброзных изменений в печени из предыдущего этапа исследования. Пациенты данной категории (81 чел.) по результатам эластографии печени и/или гистологического исследования гепатобиоптатов были распределены в зависимости от стадии фиброза печени на три группы: I-я - пациенты, у которых признаки фиброза отсутствуют (F0 ст.) - 24 чел. (29,6% от общей численности данной выборки), II-я - пациенты со слабовыраженной и умеренной стадией фиброза (F1-2 ст.) - 26 чел. (32,1%), III-я - пациенты с тяжелой стадией фиброза и циррозом печени (F3-4 ст.) - 31 чел. (38,3%).
База данных по факторам, исследуемым для составления математической модели прогнозирования фиброза печени при ХВГС, с их основными характеристиками значений представлена в таблице 1.
Первоначально необходимо было выявить наличие и силу статистической связи между факторами и 3-4 стадией HCV-ассоциированного фиброза печени, которая представляет собой двоичный ряд чисел, где 1 - наличие выраженного фиброза печени (F3-4 ст.), 0 - наличие HCV-ассоциированного фиброза печени начальной стадии (F0-2 ст.) [4]. Поскольку предцирротическая стадия фиброза и цирроза печени имели бинарный характер, то для изучения вышеуказанной корреляционной связи использовали непараметрический коэффициент корреляции Спирмена. Полученные результаты указали с уровнем значимости р<0,05 на наличие корреляционной связи у 16 из 18 изучаемых факторов.
Далее выявляли линейно-независимые друг от друга факторы, у которых обнаружена статистически значимая (р<0,05) корреляционная связь с 3-4 стадией HCV-ассоциированного фиброза печени, используя коэффициент корреляции для непараметрических данных Спирмена, а также параметрических данных Пирсона, поскольку показатели гемоглобина и тромбоцитов имели нормальное распределение (табл. 3). С учетом полученных результатов нами были выбраны три независимых друг от друга прогностических фактора: ММП-9/ТИМП-2, ТФР-β1 и ГГТ, которые при этом имели статистически значимые корреляционные связи с предцирротической стадией фиброза и циррозом печени (rS=-0,41, rS=-0,71 и rS=0,34 соответственно, р<0,05).
Используя логистический регрессионный анализ, построена математическая формула, позволяющая определить вероятность стадии HCV-ассоциированного фиброза печени (РСФП):
РСФП=(ey/(1+ey))×100%,
где y=-12+0,134317·X1+0,527778·X2-0,05·X3, где
X1 - сывороточное значение прогностического фактора ММП-9/ТИМП-2, Х2 - сывороточное значение прогностического фактора ТФР-β1; Х3 - сывороточное значение прогностического фактора ГГТ, ey - экспоненциальная функция.
Полученную вероятность РСФП соотносят с граничным значением 50%. При РСФП>50% определяют наличие предцирротической стадии фиброза и цирроза печени при ХВГС, а при РСФП<50% - HCV-ассоциированного фиброза печени начальной стадии (F0-2 ст.).
Диагностическая точность прогнозирования разработанной формулы проверили на группе пациентов (81 чел.). Оценка полученных данных свидетельствовала о совпадении прогнозных и фактических результатов отсутствия/наличия HCV-ассоциированного фиброза печени 3-4 стадии в 92,6% случаев. И только у 6 из 81 обследованных нами пациентов стадия фиброза печени при ХВГС, определенная с помощью математической формулы, не согласовалась с фактическими данными. Из них 5 случаев приходились на ложноотрицательные (гиподиагностика) результаты и один - ложноположительный (гипердиагностика). В разрезе по исследуемым группам совпадение прогнозного и фактического результата в когорте пациентов с начальными фиброзными изменениями в печени при ХВГС (F0-2 ст.) составило 49 случаев из 50 (98% совпадений), а в группе HCV-инфицированных пациентов с выраженной стадией фиброза печени (F3-4 ст.) совпадение зарегистрировано в 26 случаях из 31 (83,9% совпадений).
Таким образом, на 1-м этапе формула РНФП=(ey/(1+ey))×100% позволяет выявить у обследуемых лиц наличие HCV-ассоциированного фиброза печени, а на 2-м этапе формула РСФП=(ey/(1+ey)×100% - отсутствие или наличие предцирротической стадии фиброза и цирроза печени (F0-2 ст. или F3-4 ст. соответственно), что способствует своевременной коррекции тактики ведения пациента, и, конечно же, предотвращению дальнейшего прогрессирования фиброзных изменений в органе-мишени.
Сущность изобретения продемонстрирована следующими примерами.
Клинический пример 1.
Пациентка Ф., 28 лет. Клинический диагноз: Основной: Хронический вирусный гепатит С, минимальная степень активности (по клинико-лабораторным данным), генотип 1в, высокая вирусная нагрузка (2,4×105 МЕ/мл), F0 по Metavir при ПБП. Осложнения основного: нет. Сопутствующий: нет. Жалобы на момент осмотра на общую слабость, повышенную утомляемость и снижение работоспособности. Из анамнеза: впервые маркеры вирусного гепатита С выявлены при скрининговом обследовании во время беременности в 2010 г. На «Д» учете у инфекциониста не состоит, специфического лечения не получала. При объективном обследовании: состояние удовлетворительное, размеры печени по Курлову 10-8-7 см, печень и селезенка не пальпируются. По другим органам и системам без особенностей. Биохимический анализ крови: общий билирубин - 24,3. мкмоль/л (прямой - 5 мкмоль/л), ACT - N, АЛТ - N, тимоловая проба - 2 ЕД, ЩФ - 120 ЕД/л, ГГТ - 37 ЕД/л, общий белок - 68,8 г/л, глюкоза - 4,7 ммоль/л. УЗИ органов брюшной полости. Печень: контуры ровные, эхоструктура мелкозернистая, эхогенность обычная. Нижний край не выступает из-под реберной дуги. Правая доля - 10,0 см. Левая доля - 6,8 см. Диаметр портальной вены - 0,9 см. Желчный пузырь 8,2×2,3 см. Стенка не изменена, содержимое однородное, деформации нет, конкрементов нет. Поджелудочная железа: 2,3×1,8×2,3 см. Контуры неровные, эхоплотность нормальная. Структура обычная, вирсунгов проток нормальный. Селезенка: 8,6×3,8 см. Структура обычная. ФГДС: Слизистая пищевода розовая, блестящая, сосуды не выражены, розетки кардии смыкаются полностью. Слизистая в желудке розовая, блестящая, цельная. Привратник свободно проходим. Луковица 12-перстной кишки обычной формы, слизистая розовая. Эластометрии печени с перерасчетом по шкале Метавир: проведено обследование на аппарате FibroScan 502. Медиана эластичности печени по 11 измерениям составляет 6,3 КРа; IQR 1,4 КРа, размах значений 4,3-8,0 КПа. Общий результат измерений может соответствовать фиброзу стадии F1 по METAVIR. Гистологическое исследование печени: в половине портальных трактов умеренная мононуклеарная инфильтрация, не распространяющаяся за пределы пограничной пластинки. Встречаются единичные внутридольковые некрозы. В гепатоцитах умеренная белковая и рассеянная жировая (в немногочисленных клетках) дистрофия. Ядерный полиморфизм выражен умеренно, встречаются двухядерные элементы. Активность купферовских клеток повышена незначительно. Заключение: описанная морфологическая картина не противоречит диагнозу вирусного гепатита С минимальной активности. ИГА по Knodell = 4 балла. METAVIR: А-1, F-0.
Исследуемые прогностические показатели: ГГТ - 37 ЕД/л, ТФР-β1 - 23,96 нг/мл, ТИМП-1 - 248,47 нг/мл, ММП-9/ТИМП-2 - 92,75 пг/мл. РНФП=100%, РСФП=100%. Таким образом, применяя математическую модель, у пациентки диагностирован фиброз печени начальной стадии (F0-2 ст.), что совпадает с данными гистологического исследования печени.
Клинический пример 2.
Пациентка З., 48 лет. Клинический диагноз: Основной: Хронический вирусный гепатит С, умеренная степень активности (по клинико-лабораторным данным), генотип 1в, высокая вирусная нагрузка (4,8×106 МЕ/мл), F2 по Metavir при ПБП. Осложнения основного: Синдром печеночно-клеточной недостаточности: латентная печеночная энцефалопатия. Сопутствующий: Дискинезия желчевыводящих путей. Гипертоническая болезнь II ст., риск 3. ХСН IIA, ФК III. Жалобы при поступлении на периодический дискомфорт в правом подреберье, возникающий после погрешности в диете, общую слабость, повышенную утомляемость. Считает себя больной с июня 2006 г., когда впервые выявлены маркеры вирусного гепатита С. В анамнезе неоднократная экстракция зубов. Употребление наркотических веществ и алкоголя отрицает. Объективно: состояние удовлетворительное, субиктеричность склер, отмечается увеличение печени - выступает из-под правого края реберной дуги на 1-2 см (размеры по Курлову 12-10-8 см), при пальпации печень: плотно-эластической консистенции, с гладкой поверхностью, чувствительна. Селезенка не пальпируется. По другим органам и системам без особенностей. Биохимический анализ крови: общий билирубин - 15,3 мкмоль/л (прямой - 3,7 мкмоль/л), ACT-2N, АЛТ-3N, тимоловая проба - 2 ЕД, ЩФ - 245 ЕД/л, ГГТ - 43 ЕД/л, общий белок - 68,6 г/л, глюкоза - 4,4 ммоль/л. УЗИ органов брюшной полости. Печень: контуры ровные, эхоструктура мелко- и среднезернистая, эхогенность повышена с линейной эхогенной исчерченностью. Нижний край острый, выступает из-под реберной дуги на 1,0 см. Правая доля - 11,9 см. Левая доля - 7,3 см. Диаметр портальной вены - 1,0. Желчный пузырь 7,7×2,7 см. Стенка уплотнена, содержимое однородное, деформации нет, конкрементов нет. Поджелудочная железа: 2,4×1,8×2,3 см. Контуры ровные, эхоплотность диффузно усилена. Структура изменена, вирсунгов проток нормальный. Селезенка: 8,6×4,2 см. Структура обычная. ФГДС: Слизистая пищевода не изменена, кардия сомкнута. В желудке небольшое количество жидкости. Складки в желудке обычной высоты, расправляются воздухом. Слизистая желудка бледно-розовая. Привратник округлый. Луковица 12 перст. кишки обычной формы, слизистая ее истончена, сосудистый рисунок усилен. Заключение: косвенные признаки дискинезии желчевыводящих путей. Эластометрии печени с перерасчетом по шкале Метавир: проведено обследование на аппарате FibroScan 502. Медиана эластичности печени по 12 измерениям составляет 8,7 КРа; IQR 1,5 КРа, размах значений 5,5-11,6 КПа. Общий результат измерений может соответствовать фиброзу стадии F2 по METAVIR. Гистологическое исследование печени: гепатоциты с умеренной белковой дистрофией и внутридольковыми некрозами. Портальные тракты коллагенезированы, встречаются неполные септы. В портальных трактах лимфоцитарная инфильтрация с единичными ступенчатыми некрозами. Ядерный полиморфизм в гапатоцитах не выражен. Активность купферовских клеток повышена умеренно. Заключение: описанная морфологическая картина не противоречит диагнозу хронического вирусного гепатита С со слабовыраженной активностью. ИГА по Knodell = 7 баллов. METAVIR : А-1, F-2.
Исследуемые прогностические показатели: ГГТ - 43 ЕД/л, ТФР-β1 - 36,7 нг/мл, ТИМП-1 - 237,6 нг/мл, ММП-9/ТИМП-2 - 24,8 пг/мл. РНФП=100%, РСФП=0,01 %. Следовательно, с помощью предлагаемого способа у пациентки исключен HCV-ассоциированный фиброз печени 3-4 стадии, что совпадает с данными гистологического исследования печени.
Клинический пример 3.
Пациент С., 49 лет. Клинический диагноз: Основной: Цирроз печени в исходе хронического вирусного гепатита С, генотип 1в, низкая вирусная нагрузка (7,5×104 МЕ/мл). F4 по Metavir при ПБП. Класс А по Чайлд-Пью (5 баллов). Осложнения основного: Гепатоспленомегалия с синдромом гиперспленизма (тромбоцитопения). Синдром печеночно-клеточной недостаточности: латентная печеночная энцефалопатия. Синдром холестаза. Сопутствующий: Хронический панкреатит с внешнесекреторной недостаточностью, ремиссия. Гипертоническая болезнь II ст., риск 3. ХСН IIA, ФК II. Жалобы на момент осмотра на дискомфорт и чувство тяжести в правом подреберье, не связанные с приемом пищи, выраженную слабость, повышенную утомляемость и снижение работоспособности. Из анамнеза: Считает себя больной с сентября 2008 г., когда впервые выявлены маркеры вирусного гепатита С при плановом медицинском обследовании. Работает врачом. Холецистэктомия в 2006 г. При объективном обследовании: состояние удовлетворительное, субиктеричность склер, отмечается увеличение печени - выступает из-под правого края реберной дуги на 2-3 см (размеры по Курлову 13-11-9 см), при пальпации печень: плотно-эластической консистенции, с гладкой поверхностью, безболезненна. Размеры селезенки 10×4 см. По другим органам и системам без особенностей. Клинический анализ крови: Нв - 139 г/л; тромбоциты 135×109; Биохимический анализ крови: общий билирубин - 24,5 мкмоль/л (прямой - 9,7 мкмоль/л), ACT - 1,5N, АЛТ - 3,5N, тимоловая проба - 3,8 ЕД, ЩФ - 200 ЕД/л, ГГТ - 116 ЕД/л, общий белок - 75,5 г/л, глюкоза - 5,5 ммоль/л. САСС: ПТИ - 93%, фибриноген - 4,4 г/л. УЗИ органов брюшной полости. Печень: контуры ровные, эхоструктура среднезернистая, эхогенность повышена. Нижний край острый, выступает из-под реберной дуги на 2 см. Правая доля - 12,0 см. Левая доля - 8,8 см. Диаметр портальной вены - 0,8 см. Желчный пузырь отсутствует. Поджелудочная железа: 2,2×2,0×2,1 см. Контуры ровные, эхоплотность диффузно усилена. Структура изменена, вирсунгов проток нормальный. Селезенка: 12,0×3,5 см. Структура обычная. ФГДС: Слизистая пищевода розовая, блестящая, сосуды не видны. Розетка кардии сомкнута. Слизистая в желудке розовая, эластичная. Привратник свободно проходим. В 12-перстной кишке слизистая белесая, с умеренно выраженным феноменом «манной крупы». Заключение: косвенные признаки хронического панкреатита. Эластометрии печени с перерасчетом по шкале Метавир: проведено обследование на аппарате FibroScan 502. Медиана эластичности печени по 15 измерениям составляет 16 КРа; IQR 2,6 КРа, размах значений 12,0-21,8 КПа. Общий результат измерений может соответствовать фиброзу стадии F4 по METAVIR. Гистологическое исследование печени: биоптат состоит из узлов - регенератов разделенных прослойками соединительной ткани со слабо выраженной лимфоидно-фибропластической реакцией и ступенчатыми некрозами. Гепатоциты с явлениями умеренной жировой дистрофии. Ядерный полиморфизм не выражен, встречаются немногочисленные двухядерные элементы. Заключение: описанная морфологическая картина не противоречит диагнозу вирусного гепатита С с исходом в цирроз печени умеренной активности. ИГА по Knodell = 11 баллов. METAVIR : А - 1, F - 4.
Исследуемые прогностические показатели: ГГТ - 116 ЕД/л, ТФР-β1 - 13,21 нг/мл, ТИМП-1 - 155,5 нг/мл, ММП-9/ТИМП-2 - 47,06 пг/мл. РНФП=100%, РСФП=97%. Таким образом, математическая модель позволила установить у пациента выраженный фиброз печени (F3-4 ст.), что совпадает с данными гистологического исследования печени.
Источники информации
1. Павлов Ч.С. Современные возможности эластометрии, Фибро- и АктиТеста в диагностике фиброза печени / Ч.С. Павлов, Д.В. Глушенков, В.Т. Ивашкин // Рос. журн. гастроэнтерологии, гепатологии, колопроктологии. - 2008. - Т. 18, № 4. - С. 43-52.
2. Пат. 2408289 RU, МПК A61B 10/02, G01N 33/50. Способ дифференциальной диагностики фиброза печени при хроническом вирусном гепатите С / А.В. Баранов; заявитель и патентообладатель Баранов Александр Викторович. - №2009133379/14; заявл. 07.09.2009; опубл. 10.01.2011, Бюл. № 1. - 11 с. (прототип).
3. Пат. 2416794 RU, МПК G01N 33/48. Способ оценки фиброза печени у больных хроническим вирусным гепатитом С / Н.Д. Ющук, И.П. Балмасова, О.О. Знойко [и др.]; заявитель и патентообладатель ГОУ ВПО "Московский государственный медико-стоматологический университет Федерального агентства по здравоохранению и социальному развитию", Федеральное агентство по науке и инновациям. - №2009144106/15; заявл. 30.11.2009; опубл. 20.04.2011, Бюл. №11. - 16 с.
4. Реброва, О.Ю. Статистический анализ медицинских данных. Применение пакета прикладных программ STATISTICA / О.Ю. Реброва. - М.: МедиаСфера, 2002. - 312 с.
5. Системный и локальный цитокиновый профиль при хроническом гепатите С / Л.Ф. Скляр, Н.Д. Никифоров, Е.В. Маркелова [и др.] // Клин. лабораторная диагностика. - 2005. - №12. - С. 42-44.
6. Современные эпидемиологические особенности хронических гепатитов В и С / И.В. Шахгильдян, М.И. Михайлов, А.А. Ясинский [и др.] // Гепатология сегодня : мат. 16-го Рос. конгр., г. Москва 21-23 марта. - (Прил. №37 к Рос. журн. гастроэнтерол., гепатол., колопроктол. - 2011. - № 1. - С. 135-136.
7. Altered pattern of circulating matrix metalloproteinases-2,-9 and tissue inhibitor of metalloproteinase-2 in patients with HCV-related chronic hepatitis. Relationship to histological features / С.M. Bruno, M. Valenti, G. Bertino [et al.] // Panminerva Med. - 2009. - Vol. 51, 4. - P. 191-196.
8. Lee, U.E. Mechanisms of Hepatic Fibrogenesis / U.E. Lee, S.L. Friedman // Best Pract. Res. Clin. Gastroenterol. - 2011. - Vol. 25, №2. - P. 195-206.
9. Non-Invasive markers for hepatic fibrosis / А. Baranova, P. Lal, A. Birerdinc, Z.M. Younossi // BMC Gastroenterol. - 2011 - Vol. 11, № 91. - P. 1-15.
10. The role of serum biomarkers in predicting fibrosis progression in pediatric and adult hepatitis С virus chronic infection / P. Valva, P. Casciato, J.M. Diaz Carrasco [et al.] // PLoS One. - 2011. - Vol. 6, № 8. - P. 1-10.
Claims (1)
- Способ диагностики наличия и стадии фиброза печени при хроническом вирусном гепатите С, включающий определение концентрации ГГТ и ТФР-β1 в сыворотке крови, отличающийся тем, что для диагностики используют иммунологические показатели регуляции фиброгенеза и фибринолиза, такие как ТИМП-1 и комплекс ММП-9/ТИМП-2, и на 1-м этапе рассчитывают вероятность наличия HCV-ассоциированного фиброза печени (РНФП) по формуле:
РНФП=(ey/(1+ey))×100%,
где y=-13,6+3,78·X1-0,1·X2,
где X1 - сывороточное значение прогностического фактора ММП-9/ТИМП-2, X2 - сывороточное значение прогностического фактора ТИМП-1, ey - экспоненциальная функция,
и при значении РНФП>50% прогнозируют наличие HCV-ассоциированных фиброзных изменений в печени;
на 2-м этапе рассчитывают вероятность стадии HCV-ассоциированного фиброза печени (РСПФ) по формуле:
РСФП=(ey/(1+ey))×100%,
где y=-12+0,134317·X1+0,527778·X2-0,05·X3,
где X1 - сывороточное значение прогностического фактора ММП-9/ТИМП-2, X2 - сывороточное значение прогностического фактора ТФР-β1; X3 - сывороточное значение прогностического фактора ГГТ,
и при значении РСФП>50% диагностируют наличие предцирротической стадии фиброза и цирроза печени при ХВГС (F3-4 ст.), при РСФП<50% - HCV-ассоциированного фиброза печени начальной стадии (F0-2 ст.).
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2014123015/15A RU2557927C1 (ru) | 2014-06-05 | 2014-06-05 | Способ диагностики фиброза печени при хроническом вирусном гепатите с |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2014123015/15A RU2557927C1 (ru) | 2014-06-05 | 2014-06-05 | Способ диагностики фиброза печени при хроническом вирусном гепатите с |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2557927C1 true RU2557927C1 (ru) | 2015-07-27 |
Family
ID=53762588
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2014123015/15A RU2557927C1 (ru) | 2014-06-05 | 2014-06-05 | Способ диагностики фиброза печени при хроническом вирусном гепатите с |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2557927C1 (ru) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2623151C2 (ru) * | 2015-11-03 | 2017-06-22 | Федеральное государственное казенное учреждение Главный клинический военный госпиталь ФСБ России | Способ прогнозирования динамики фиброза печени у пациентов с хроническим гепатитом С, генотипом 1, не ответивших на лечение пегилированными интерферонами и рибавирином |
| RU2763257C1 (ru) * | 2021-05-14 | 2021-12-28 | Федеральное государственное бюджетное учреждение "Детский научно-клинический центр инфекционных болезней Федерального медико-биологического агентства" | Способ диагностики стадии фиброза печени при хронических заболеваниях печени у детей |
| RU2827360C1 (ru) * | 2024-03-12 | 2024-09-24 | Федеральное государственное бюджетное образовательное учреждение высшего образования "Ставропольский государственный медицинский университет" Министерства здравоохранения Российской Федерации | Способ диагностики фиброза F4 у пациентов с хроническими заболеваниями печени |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2261441C2 (ru) * | 2003-10-06 | 2005-09-27 | Ягода Александр Валентинович | Способ неинвазивной диагностики степени выраженности фиброза печени у больных хроническим вирусным гепатитом |
| WO2006082522A1 (en) * | 2005-02-03 | 2006-08-10 | Assistance Publique - Hopitaux De Paris | Diagnosis method of hepatic steatosis using biochemical markers |
| RU2408289C1 (ru) * | 2009-09-07 | 2011-01-10 | Александр Викторович Баранов | Способ дифференциальной диагностики фиброза печени при хроническом вирусном гепатите с |
| RU2482792C1 (ru) * | 2011-12-27 | 2013-05-27 | Государственное бюджетное образовательное учреждение высшего профессионального образования "Смоленская государственная медицинская академия" Министерства здравоохранения и социального развития Российской Федерации | Способ дифференциальной диагностики диффузных заболеваний печени |
| RU2516970C1 (ru) * | 2012-12-18 | 2014-05-20 | Государственное Образовательное Учреждение Высшего Профессионального Образования "Кубанский государственный медицинский университет" (ГОУ ВПО КубГМУ Минздрава России) | Способ дифференциальной диагностики гепатита и цирроза печени |
-
2014
- 2014-06-05 RU RU2014123015/15A patent/RU2557927C1/ru not_active IP Right Cessation
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2261441C2 (ru) * | 2003-10-06 | 2005-09-27 | Ягода Александр Валентинович | Способ неинвазивной диагностики степени выраженности фиброза печени у больных хроническим вирусным гепатитом |
| WO2006082522A1 (en) * | 2005-02-03 | 2006-08-10 | Assistance Publique - Hopitaux De Paris | Diagnosis method of hepatic steatosis using biochemical markers |
| RU2408289C1 (ru) * | 2009-09-07 | 2011-01-10 | Александр Викторович Баранов | Способ дифференциальной диагностики фиброза печени при хроническом вирусном гепатите с |
| RU2482792C1 (ru) * | 2011-12-27 | 2013-05-27 | Государственное бюджетное образовательное учреждение высшего профессионального образования "Смоленская государственная медицинская академия" Министерства здравоохранения и социального развития Российской Федерации | Способ дифференциальной диагностики диффузных заболеваний печени |
| RU2516970C1 (ru) * | 2012-12-18 | 2014-05-20 | Государственное Образовательное Учреждение Высшего Профессионального Образования "Кубанский государственный медицинский университет" (ГОУ ВПО КубГМУ Минздрава России) | Способ дифференциальной диагностики гепатита и цирроза печени |
Non-Patent Citations (1)
| Title |
|---|
| ОСТАНИН А.А. и др. Прогностическая модель неинвазивной диагностики фиброза печени у больных хроническими вирусными гепатитами. Неинвазивная диагностика фиброза печени. 2008, Т. 10, N 4-5, с. 405-414 * |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2623151C2 (ru) * | 2015-11-03 | 2017-06-22 | Федеральное государственное казенное учреждение Главный клинический военный госпиталь ФСБ России | Способ прогнозирования динамики фиброза печени у пациентов с хроническим гепатитом С, генотипом 1, не ответивших на лечение пегилированными интерферонами и рибавирином |
| RU2763257C1 (ru) * | 2021-05-14 | 2021-12-28 | Федеральное государственное бюджетное учреждение "Детский научно-клинический центр инфекционных болезней Федерального медико-биологического агентства" | Способ диагностики стадии фиброза печени при хронических заболеваниях печени у детей |
| RU2827360C1 (ru) * | 2024-03-12 | 2024-09-24 | Федеральное государственное бюджетное образовательное учреждение высшего образования "Ставропольский государственный медицинский университет" Министерства здравоохранения Российской Федерации | Способ диагностики фиброза F4 у пациентов с хроническими заболеваниями печени |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Pare et al. | Point-of-care lung ultrasound is more sensitive than chest radiograph for evaluation of COVID-19 | |
| EP2409154B1 (en) | Non-invasive method for assessing liver fibrosis progression | |
| CN106462666A (zh) | 肝病的预诊检测 | |
| EP3296744A1 (en) | Method of diagnosis of non-alcoholic fatty liver diseases | |
| EP2872031B1 (en) | Method for providing reliable non-invasive diagnostic tests | |
| Ramu et al. | A prospective study on the diagnostic value of hyperbilirubinemia as a predictive factor for appendicular perforation in acute appendicitis | |
| RU2583939C1 (ru) | Способ лабораторной диагностики стадии фиброза печени при хроническом вирусном гепатите с | |
| Trevisani et al. | Recommendations from the Brazilian society of rheumatology for the diagnosis of Sjögren's syndrome (Part I): glandular manifestations (systematic review) | |
| Shaoul et al. | An overview of tools to score severity in pediatric inflammatory bowel disease | |
| Duyan et al. | Assessment of the diagnostic value of novel biomarkers in adult patients with acute appendicitis: a cross-sectional study | |
| Huang et al. | Optimal timing of contrast‑enhanced computed tomography in an evaluation of severe acute pancreatitis‑associated complications | |
| Rodriguez-Lopez et al. | Impaired immune reaction and increased lactate and C-reactive protein for early prediction of severe morbidity and pancreatic fistula after pancreatoduodenectomy | |
| RU2557927C1 (ru) | Способ диагностики фиброза печени при хроническом вирусном гепатите с | |
| Lappharat et al. | A model for predicting gestational diabetes mellitus in early pregnancy: a prospective study in Thailand | |
| JP7007361B2 (ja) | 複数標的線維症検査 | |
| Taşçı et al. | Impact of COVID-19 pandemic on pediatric appendicitis hospital admission time and length of hospital stay | |
| Tsvetkov et al. | Machine learning model for diagnosing the stage of liver fibrosis in patients with chronic viral hepatitis C | |
| Du et al. | Predicting the risk of acute kidney injury in patients after percutaneous coronary intervention (PCI) or cardiopulmonary bypass (CPB) surgery: development and assessment of a nomogram prediction model | |
| Yan et al. | ClinicalLab: Aligning Agents for Multi-Departmental Clinical Diagnostics in the Real World | |
| RU2763257C1 (ru) | Способ диагностики стадии фиброза печени при хронических заболеваниях печени у детей | |
| RU2563129C1 (ru) | Способ диагностики цирротической стадии хронического вирусного гепатита с | |
| RU2723891C1 (ru) | Способ определения риска развития гепатоцеллюлярной карциномы у больных хроническим гепатитом с | |
| Verbrugge et al. | Lymph node biopsies in a general internal medicine department: algorithm or individualized decision-making? | |
| RU2721689C1 (ru) | Способ оценки риска развития атеросклероза на основании определения сывороточного уровня интерлейкина-33 | |
| Al Gohary et al. | Comparison of hepatic and splenic stiffness in chronic hepatitis C infection with and without schistosomal infection; correlation with hepatic histopathological changes |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20170606 |