RU2553372C1 - Способ профилактики постинфекционного синдрома раздраженной кишки - Google Patents
Способ профилактики постинфекционного синдрома раздраженной кишки Download PDFInfo
- Publication number
- RU2553372C1 RU2553372C1 RU2014102545/15A RU2014102545A RU2553372C1 RU 2553372 C1 RU2553372 C1 RU 2553372C1 RU 2014102545/15 A RU2014102545/15 A RU 2014102545/15A RU 2014102545 A RU2014102545 A RU 2014102545A RU 2553372 C1 RU2553372 C1 RU 2553372C1
- Authority
- RU
- Russia
- Prior art keywords
- enterococcus faecium
- enterococcus
- clones
- ibs
- bowel syndrome
- Prior art date
Links
Abstract
Изобретение относится к медицине и предназначено для профилактики постинфекционного синдрома раздраженной кишки (ПИ-СРК). Назначают пероральный прием аутопробиотика, представляющего собой индивидуальный молочнокислый продукт, приготовленный на основе штамма Enterococcus faecium и содержащий 108 KOE в 1 мл продукта. Осуществляют посев бактерий из фекалий пациента на селективную питательную среду с последующим выращиванием культуры в селективной питательной среде, идентификацией и отбором типичных для Enterococcus faecium колоний, получением чистой культуры Enterococcus faecium и уточнением видовой принадлежности и содержания факторов патогенности методом полимеразной цепной реакции, отбором апатогенных клонов Enterococcus faecium, соответствующих стандартам генетической безопасности и физиологической функциональности, из которых готовят молочнокислую закваску. Аутопробиотик вводят в дозе не менее 100 мл/сутки курсом не менее 10 дней. Отобранные апатогенные клоны Enterococcus faecium депонируют в криохранилище при температуре не выше -75°C со сроком хранения не более 1 года. В качестве селективной питательной среды используют энтерококк-агар. Способ позволяет повысить эффективность профилактики больных с ПИ-СРК за счет уменьшении частоты его развития. 2 з.п. ф-лы, 1 табл., 1 пр.
Description
Изобретение относится к медицине, а именно к гастроэнтерологии, и может быть использовано для профилактики постинфекционного синдрома раздраженной кишки (СРК).
Синдром раздраженного кишечника является хроническим функциональным расстройством желудочно-кишечного тракта (ЖКТ), поражающий 5-20% населения. Наряду с психосоматическими изменениями в настоящее время большая роль отводится инфекционному агенту как пусковому фактору. Значение этого фактора в настоящее время весьма значимо, так как в целом в мире сохраняется неблагоприятная эпидемиологическая ситуация и, по данным ВОЗ, ежегодно регистрируется около 500000 случаев острой диареи. Обычно для обозначения данного варианта СРК используется термин «постинфекционный СРК» (ПИ-СРК). Впервые ПИ-СРК описали Chaudhary N.А. и Truetove S.С. более 50 лет назад, после изучения 130 случаев «синдрома раздраженной толстой кишки» они выявили 26% пациентов, у которых СРК стало следствием перенесенной дизентерии. У большинства людей, которые заболевают острой бактериальной диареей, самопроизвольное исчезновение симптомов наступает в течение 5 дней, однако у части больных развивается неспецифическая кишечная симптоматика, которая может проявляться в течение многих лет. Постинфекционный СРК развивается у 4-32% пациентов после перенесенного бактериального гастроэнтерита как ответ на неспецифические инфекции, вызванные различными кишечными возбудителями. Факторами риска развития постинфекционных функциональных кишечных нарушений являются:
- женский пол;
- лечение инфекционной диареи антибиотиками;
- наличие органического заболевания пищеварительной системы;
- признаки социально-психологической дезадаптации (тревожность, депрессия, склонность к соматизации, хронический стресс, диссомнические расстройства).
Известно использование пробиотиков в комплексном лечении СРК. Пробиотики оказывают положительное воздействие на выраженность вздутия и других симптомов СРК посредством коррекции состава и метаболической активности кишечной микрофлоры, что обеспечивает улучшение пищеварения и моторики кишечника, а также уменьшение газообразования. Эти клинические эффекты характерны для использования пробиотиков в схемах лечения ПИ-СРК [Guyonnet D, Chassany О, Ducrotte Р et al. Effect of a fermented milk containing Bifidobacterium animalis dn-173010 on the health-related quality of life and symptoms in irritable bowel syndrome in adults in primary care: a multicentre, randomized, double-blind, controlled trial. Aliment Pharmacol Ther 2005; 26: 475-86; Moayyedi P, Ford AC, Talley NJ et al. The efficacy of probiotics in the treatment of irritable bowel syndrome: a systematic review. Gut. 2010 Mar; 59(3): 325-32]. Пробиотики рекомендованы Всемирной гастроэнтерологической организацией для лечения СРК (WGO, Global Guideline IBS, 2009).
Во всех встречаемых в литературе источниках в качестве пробиотиков для лечения СРК (в том числе и ПИ-СРК) использовались промышленные пробиотические штаммы, что является серьезным недостатком, ограничивающим возможности их применения. Наряду с расширением сферы применения пробиотиков накапливаются данные о негативных проявлениях терапии препаратами или продуктами, содержащими промышленные штаммы микроорганизмов.
В настоящее время полагают, что оральный прием живых бактерий теоретически может быть ответственен за четыре типа побочных эффектов (Шендеров Б., Осипенко М., 2003; Salminen М., 2006):
- развитие инфекционных процессов, обусловленных штаммами, входящими в состав пробиотиков;
- развитие метаболических расстройств;
- чрезмерная иммуностимуляция лимфатического аппарата кишечника;
- формирование новых клонов бактериальных штаммов за счет передачи генов, ответственных за экспрессию факторов патогенности.
Микробы, выращенные искусственно, являются инородными для организма определенного человека и отторгаются вследствие биологической несовместимости. Биотехнологические пробиотики не имеют возможности внедряться внутрь биопленки кишечника и поэтому пребывают в нем транзиторно, как микрофлора пищи. Это признают производители пробиотиков, подтверждая, что их добавки не восполняют дефицит соответствующих содержимому пробиотика микроорганизмов, но стимулируют рост облигатной микрофлоры. Все это не позволяет получить высоких и стабильных клинических результатов при лечении больных с СРК.
Аутопробиотики лишены вышеперечисленных недостатков, так как они производятся на основе субстратов, полученных от макроорганизма, для которого они предназначены, и обладают сродством к биопленке кишечника.
В качестве прототипа по наиболее близкой технической сущности нами выбран способ профилактики постинфекционного синдрома раздраженной кишки, включающий пероральный прием пробиотика, включающий промышленный пробиотический штамм Enterococcus faecium L3 в виде молочнокислой закваски, содержащей 108 KOE в 1 мл продукта [Симаненков В.И., Шумихина И.А. Постинфекционный синдром раздраженной толстой кишки: частота развития и возможности профилактики. / Сборник материалов II Всероссийской конференции с международным участием. «Профилактическая медицина - 2012». - СПб. - С.78-79].
По мнению авторов заявляемого изобретения, способ-прототип не обладает достаточно высокой эффективностью.
Технический результат, достигаемый изобретением, заключается в повышении эффективности профилактики больных с ПИ-СРК за счет уменьшении частоты развития этого страдания.
Сущность изобретения заключается в том, что для профилактики постинфекционного синдрома раздраженной кишки осуществляют пероральный прием аутопробиотика, представляющего собой индивидуальный молочнокислый продукт, приготовленный на основе штамма Enterococcus faecium и содержащий 108 KOE в 1 мл продукта. Осуществляют посев бактерий из фекалий пациента на селективную питательную среду с последующим выращиванием культуры в селективной питательной среде, идентификацией и отбором типичных для Enterococcus faecium колоний, получением чистой культуры Enterococcus faecium и уточнением видовой принадлежности и содержания факторов патогенности методом полимеразной цепной реакции, отбором апатогенных клонов Enterococcus faecium, соответствующих стандартам генетической безопасности и физиологической функциональности, из которых готовят молочнокислую закваску. Аутопробиотик вводят в дозе не менее 100 мл/сутки курсом не менее 10 дней. Отобранные апатогенные клоны Enterococcus faecium депонируют в криохранилище при температуре не выше -75°C со сроком хранения не более 1 года. В качестве селективной питательной среды используют энтерококк-агар.
Способ осуществляется следующим образом.
Способ получения аутопробиотика на основе Enterococcus faecium, представителя индигенной микрофлоры кишечника-хозяина, был защищен патентом RU №2460778.
Суспензию фекалий пациента высевают на селективную среду для энтерококков (Питательная агаризованная среда с азидом натрия, НИЦФ, Санкт-Петербург). Культивируют в течение 24-48 часов при температуре 37°C. Учитывая особенности культуральных свойств Enterococcus faecium, проводят ориентировочную идентификацию энтерококков до вида. Чистые культуры направляют на генетический анализ. Из индивидуальных колоний энтерококков экспресс-методом выделяют хромосомную ДНК, после чего производят полимеразную цепную реакцию (ПЦР).
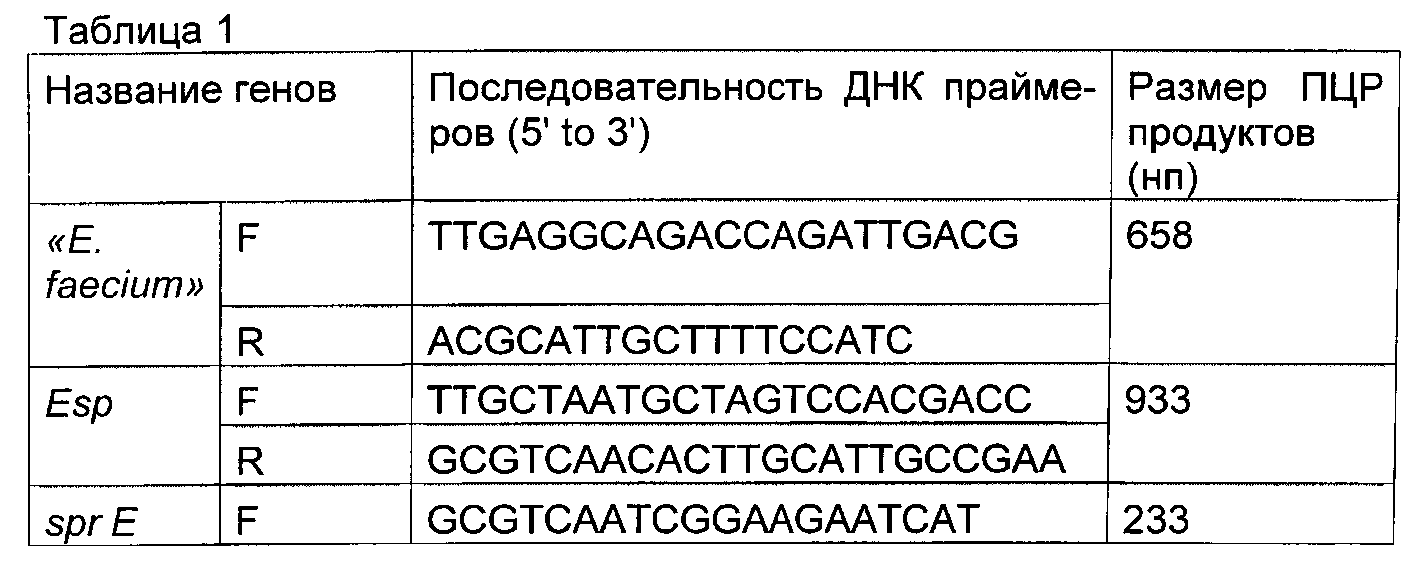
Для приготовления индивидуального молочнокислого продукта отбирают бактериальные клоны, относящиеся к Е. faecium (продукт 658 нп) и не содержащие ни одного из генов патогенности. В таблице 1 приведены последовательность ДНК-праймеров и размеры продуктов ПЦР для детекции видовой принадлежности и генов патогенности энтерококков.
Полученный молочнокислый продукт с содержанием выделенного штамма Enterococcus faecium не менее 1×108 KOE/мл пациент принимает в дозе не менее 100 мл/сутки не менее 10 дней.
Отобранные апатогенные клоны Enterococcus faecium депонируют в криохранилище при температуре не выше -75°C со сроком хранения не более 1 года. В качестве селективной питательной среды используют энтерококк-агар.
Отличительные существенные признаки заявляемого способа и причинно-следственная связь между ними и достигаемым результатом:
больному вводят аутопробиотик, представляющий собой индивидуальный молочнокислый продукт, приготовленный на основе штамма Enferococcus faecium и содержащий не менее 1×108 KOE/мл;
осуществляют посев бактерий из фекалий пациента на селективную питательную среду с последующим выращиванием культуры в селективной питательной среде, идентификацией и отбором типичных для Enterococcus faecium колоний, получением чистой культуры Enterococcus faecium и уточнением видовой принадлежности и содержания факторов патогенности методом полимеразной цепной реакции, отбором апатогенных клонов Enterococcus faecium, соответствующих стандартам генетической безопасности и физиологической функциональности, из которых готовят молочнокислую закваску. Аутопробиотик вводят в дозе не менее 100 мл/сутки курсом не менее 10 дней. Отобранные апатогенные клоны Enterococcus faecium депонируют в криохранилище при температуре не выше -75°C со сроком хранения не более 1 года. В качестве селективной питательной среды используют энтерококк-агар.
Для изучения эффективности заявленного изобретения было проведено слепое рандомизированное сравнительное плацебоконтролируемое клиническое исследование.
В исследование было включено 50 пациентов с верифицированной острой кишечной инфекцией (ОКИ) бактериальной и вирусной этиологии. Все пациенты получали терапию для лечения ОКИ: антибактериальное средство (ципрофлоксацин), симптоматическое лечение. По окончании проводимой антибактериальной терапии пациенты методом случайной выборки были рандомизированы на 3 группы:
- первая группа пациентов (20 человек) - апробация персонифицированной профилактики постинфекционного синдрома раздраженной кишки по заявляемому способу. Пациенты принимали молочнокислый продукт, содержащий 108 KOE/мл аутоэнтерококков, в дозе 100 мл/сутки - по 50 мл 2 раза в день в течение 10 дней;
- вторая группа пациентов (20 человек) - способ-прототип;
- третья группа пациентов (10 человек) - контрольная - получала молочный продукт без пробиотических добавок (автоклавированное молоко) в суточной дозе 100 мл - по 50 мл 2 раза в день в течение 10 дней.
Исходно по изучаемым параметрам все группы были сравнимы. Перед приемом, непосредственно после курсового приема и через шесть месяцев после лечения проводилось изучение кишечного микробиоценоза методом ПЦР-RT. Контрольный осмотр пациентов проводился через полгода. Во время визитов проводилось обследование для выявления признаков, характерных для наличия синдрома раздраженной кишки. Клиническая оценка проводилась на основании динамики выраженности таких симптомов, как выраженность боли в животе, дискомфорт в эпигастральной области, метеоризм, характеристика стула по Бристольской шкале (БШ). В течение исследования пациенты вели дневник, в котором ежедневно отмечали жалобы, самочувствие, характер стула.
При осмотре через полгода после проведения профилактических курсов пробиотической терапии оказалось, что симптомы, характерные для ПИ-СРК, выявлялись у 8 человек (80%) в группе, получавшей плацебо, у 6 человек (30%) в группе, получавшей промышленный пробиотик, и у 3 человек (15%) в группе, получавшей аутопробиотик на основе Enterococcus faecium. Различия в группах достоверны (p<0,01).
Таким образом, предложенный способ профилактики ПИ-СРК с применением пробиотика на основе аутоштамма энтерококка позволяет достоверно уменьшить частоту развития этого страдания на 15% по сравнению с прототипом.
Примеры из клинической практики.
Пример 1. Пациентка С., 24 года. Находилась на лечении в КИБ №30 им. С.П. Боткина с диагнозом: сальмонеллез группы D enteritidis средней степени тяжести (бактериальный рост от 21.11.11 позитивный, ПЦР положительна от 22.11.2011). Аденовирусная инфекция (ПЦР положительна от 22.11.2011 г.). При поступлении предъявляла жалобы на боли в животе, жидкий стул до 10 раз в сутки (7 тип по Бристольской шкале стула) без патологических примесей, повышение температуры тела до 39°С, тошнота без рвоты. Было назначено лечение: ципрофлоксацин 1000 мг в сутки: в/в + per os; солевые растворы (дисоль, трисоль); ферменты (мезим-форте), сорбенты. На фоне терапии самочувствие несколько улучшилось: уменьшилась частота стула до 3-4 раза в сутки, изменилась его форма (5 тип по Бристольской шкале стула); сохранялись боли в животе. Общее самочувствие пациентка оценила на два балла (по 3-балльной шкале). В клиническом анализе крови наблюдался лейкоцитоз до 11,3·109/л, лимфопения до 2·109/л, повышение СОЭ до 14 мм/ч. В биохимическом анализе крови отклонений от нормы выявлено не было. После окончания курса антибактериальной терапии пациентке было выполнено количественное определение микробиоты толстого кишечника в режиме «ПЦР - Real time», где найдены следующие изменения: уменьшение количества бифидобактерий до 107, кишечной палочки - до 106. Одновременно с забором фекалий для молекулярно-генетического исследования состава кишечной микрофлоры, после подписания пациенткой Информированного согласия на участие в клиническом исследовании, был произведен забор образца кала для выделения аутоштаммов Enterococcus faecium. По описанной выше методике для пациентки был приготовлен индивидуальный молочнокислый продукт, содержащий не менее 1×108 KOE/мл выделенного аутоштамма Enterococcus faecium. Пациентка принимала аутопробиотик в дозе 100 мл/сутки - по 50 мл 2 раза в день в течение 10 дней. На 6-е сутки лечения было отмечено снижение выраженности болей в животе, появилась тенденция к нормализации стула. Через 10 дней лечения было отмечено значительное улучшение общего самочувствия (хорошее - 0 баллов), исчезновение абдоминального болевого синдрома (0 баллов), нормализовалась частота стула (1-2 раза в сутки) и его форма (4 тип по Бристольской шкале). При исследовании кишечной микрофлоры выявлено увеличение количества бифидобактерий (до 109 KOE/мл). Пациентка отметила приятный вкус и консистенцию аутопробиотического продукта, что повысило ее приверженность к лечению.
Через три месяца пациентка была приглашена на контрольный визит. При опросе отмечала хорошее общее самочувствие (по шкале 0 баллов), отсутствие жалоб со стороны желудочно-кишечного тракта, стул нормальный (4 тип по Бристольской шкале), 1 раз в сутки, без патологических примесей. В клиническом анализе крови отклонений от нормы не было выявлено. За 7 дней до контрольного визита пациентке был выполнен анализ: посев кала на кишечную микрофлору. В результатах анализа отклонений от нормы не было выявлено.
Через 6 месяцев после окончания курса аутопробиотической терапии пациентка была опрошена по телефону. Ей было предложено ответить на вопросы, позволяющие выявить симптомы, подозрительные на СРК. Пациентка ответила на предложенные вопросы, сформулированные в опроснике пациента, о наличии симптомов, характерных для постинфекционного синдрома раздраженной кишки. Признаков, подозрительных на СРК, выявлено не было.
Таким образом, как уже было указано выше, заявляемый способ профилактики ПИ-СРК с применением пробиотика на основе аутоштамма энтерококка позволяет достоверно уменьшить частоту развития этого страдания на 15% по сравнению с прототипом.
Claims (3)
- Способ профилактики постинфекционного синдрома раздраженной кишки, включающий пероральный прием пробиотика, представляющего собой молочнокислый продукт, приготовленный на основе штамма Enterococcus faecium и содержащий 108 КОЕ в 1 мл продукта, отличающийся тем, что осуществляют посев бактерий из фекалий пациента на селективную питательную среду с последующим выращиванием культуры в селективной питательной среде, идентификацией и отбором типичных для Enterococcus faecium колоний, получением чистой культуры Enterococcus faecium и уточнением видовой принадлежности и содержания факторов патогенности методом полимеразной цепной реакции, отбором апатогенных клонов Enterococcus faecium, соответствующих стандартам генетической безопасности и физиологической функциональности, из которых готовят молочнокислую закваску.
- 2. Способ по п.1, отличающийся тем, что отобранные апатогенные клоны Enterococcus faecium депонируют в криохранилище при температуре не выше -75°C со сроком хранения не более 1 года.
- 3. Способ по п.1, отличающийся тем, что в качестве селективной питательной среды используют энтерококк-агар.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2014102545/15A RU2553372C1 (ru) | 2014-01-27 | 2014-01-27 | Способ профилактики постинфекционного синдрома раздраженной кишки |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2014102545/15A RU2553372C1 (ru) | 2014-01-27 | 2014-01-27 | Способ профилактики постинфекционного синдрома раздраженной кишки |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2553372C1 true RU2553372C1 (ru) | 2015-06-10 |
Family
ID=53295326
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2014102545/15A RU2553372C1 (ru) | 2014-01-27 | 2014-01-27 | Способ профилактики постинфекционного синдрома раздраженной кишки |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2553372C1 (ru) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2688921C2 (ru) * | 2017-06-27 | 2019-05-23 | Российская Федерация, от имени которой выступает Министерство обороны Российской Федерации | Способ измерения дальности и радиальной скорости в РЛС с зондирующим составным псевдослучайным ЛЧМ импульсом |
| RU2734896C2 (ru) * | 2018-12-28 | 2020-10-26 | Федеральное государственное бюджетное научное учреждение "Институт экспериментальной медицины" (ФГБНУ "ИЭМ") | Способ приготовления аутопробиотика на основе анаэробного консорциума бактерий |
| RU2766765C1 (ru) * | 2021-05-25 | 2022-03-15 | Федеральное государственное бюджетное учреждение "Детский научно-клинический центр инфекционных болезней Федерального медико-биологического агентства" | Способ лечения функциональных заболеваний желудочно-кишечного тракта у детей |
| US11878039B1 (en) | 2023-03-01 | 2024-01-23 | King Faisal University | Composition for treating Irritable Bowel Syndrome |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN102438637A (zh) * | 2009-03-05 | 2012-05-02 | 益生菌股份公司 | 具有高抗炎活性的细菌菌株 |
| RU2460778C1 (ru) * | 2010-12-30 | 2012-09-10 | Александр Николаевич Суворов | Способ получения аутопробиотика на основе enterocuccus faecium, представителя индигенной микрофлоры кишечника хозяина |
-
2014
- 2014-01-27 RU RU2014102545/15A patent/RU2553372C1/ru active
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN102438637A (zh) * | 2009-03-05 | 2012-05-02 | 益生菌股份公司 | 具有高抗炎活性的细菌菌株 |
| RU2460778C1 (ru) * | 2010-12-30 | 2012-09-10 | Александр Николаевич Суворов | Способ получения аутопробиотика на основе enterocuccus faecium, представителя индигенной микрофлоры кишечника хозяина |
Non-Patent Citations (1)
| Title |
|---|
| СОЛОВЬЕВА О.И. и др., Постинфекционный синдром раздраженной кишки: частота возникновения и возможность профилактики, Здоровье - основа человеческого потенциала - проблемы и пути их решения, N 2, том 7, 2012. онлайн [найдено 18.02.2015], найдено из Интернет http://cyberleninka.ru/. ГРИГОРЬЕВ П.Я. и др., Справочное руководство по гастроэнтерологии, Москва - МИА - 2003, с. 364-366, 382-387. САМСОНОВ А.А. и др., Постинфекционный синдром раздраженной кишки — особая форма функциональной кишечной патологии, Лечащий врач N7, 2012, онлайн [найдено 03.11.2014], найдено из Интернет http://www.lvrach.ru/2012/07/15435466/. IL'IN VK et al, Autochthonous probiotics in prevention of infectious and inflammatory diseases of a human in the altered habitats Vestn Ross Akad Med Nauk. 2013;(2):56-62. онлайн [найдено 03.11.2014], найдено из Интернет PMID:23819330 * |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2688921C2 (ru) * | 2017-06-27 | 2019-05-23 | Российская Федерация, от имени которой выступает Министерство обороны Российской Федерации | Способ измерения дальности и радиальной скорости в РЛС с зондирующим составным псевдослучайным ЛЧМ импульсом |
| RU2734896C2 (ru) * | 2018-12-28 | 2020-10-26 | Федеральное государственное бюджетное научное учреждение "Институт экспериментальной медицины" (ФГБНУ "ИЭМ") | Способ приготовления аутопробиотика на основе анаэробного консорциума бактерий |
| RU2766765C1 (ru) * | 2021-05-25 | 2022-03-15 | Федеральное государственное бюджетное учреждение "Детский научно-клинический центр инфекционных болезней Федерального медико-биологического агентства" | Способ лечения функциональных заболеваний желудочно-кишечного тракта у детей |
| US11878039B1 (en) | 2023-03-01 | 2024-01-23 | King Faisal University | Composition for treating Irritable Bowel Syndrome |
| US11883442B1 (en) | 2023-03-01 | 2024-01-30 | King Faisal University | Composition for treating irritable bowel syndrome |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Suez et al. | Post-antibiotic gut mucosal microbiome reconstitution is impaired by probiotics and improved by autologous FMT | |
| EP3639834B1 (en) | Use of microbial communities for human and animal health | |
| JP6978463B2 (ja) | 相乗的細菌組成物並びにその生成及び使用の方法 | |
| US20210106629A1 (en) | Compositions and Methods for Treating Inflammatory Bowel Diseases (IBDs) and Other Disorders | |
| RU2617952C2 (ru) | Композиция, содержащая N-ацетилцистеин в сочетании с пробиотическими бактериями, способная восстанавливать собственный барьерный эффект желудка, который утрачивается во время фармалогического лечения желудочной гиперацидности | |
| Sanders | How do we know when something called “probiotic” is really a probiotic? A guideline for consumers and health care professionals | |
| US9255246B2 (en) | Use of lactobacilli inhibiting gas producing coliform bacterial isolated from infants affected by colic | |
| CN109562134B (zh) | 用于维持和/或恢复健康女性微生物群的阴道制剂 | |
| BR112020013712A2 (pt) | composições anidras compreendendo uma microbiota co-selecionada, método de uso das mesmas e medicamento | |
| RU2460778C1 (ru) | Способ получения аутопробиотика на основе enterocuccus faecium, представителя индигенной микрофлоры кишечника хозяина | |
| CN108135948A (zh) | 用于治疗和预防肠感染和炎症的组合物和方法 | |
| RU2580002C1 (ru) | Способ получения аутопробиотика, содержащего живые бифидобактерии и лактобактерии | |
| RU2553372C1 (ru) | Способ профилактики постинфекционного синдрома раздраженной кишки | |
| Mansour et al. | Inhibition of Clostridium difficile in mice using a mixture of potential probiotic strains Enterococcus faecalis NM815, E. faecalis NM915, and E. faecium NM1015: novel candidates to control C. difficile infection (CDI) | |
| Xu et al. | Lactobacillus casei JY300-8 generated by 12C6+ beams mutagenesis inhibits tumor progression by modulating the gut microbiota in mice | |
| RU2546253C2 (ru) | Способ получения персонифицированного аутопробиотического продукта и способ лечения синдрома раздраженной кишки с использованием этого продукта | |
| JP6005041B2 (ja) | プレバイオティック組成物の製造のための大豆発酵抽出物の使用 | |
| TWI600758B (zh) | 具免疫調節機能的植物乳桿菌及其用途 | |
| Anjum et al. | Potentially probiotic Limosilactobacillus reuteri from human milk strengthens the gut barrier in T84 cells and a murine enteroid model | |
| RU2528867C2 (ru) | Способ оценки выживаемости бифидо- и лактобактерий в желудочно-кишечном тракте экспериментальных животных | |
| TWI827293B (zh) | 羅伊氏乳桿菌tci850及其提高免疫力及抗發炎用途 | |
| RU2589843C2 (ru) | Средство для лечения кишечных инфекций и состояний, вызванных дисбактериозом, "биобаланс а" | |
| RU2734896C2 (ru) | Способ приготовления аутопробиотика на основе анаэробного консорциума бактерий | |
| Fiore | Overall Assessment of a Model Probiotic Bacterium: from Gut Colonization to Clinical Efficacy | |
| RU2405546C1 (ru) | Способ профилактики и лечения энтеропатий, развивающихся на фоне полихимиотерапии |