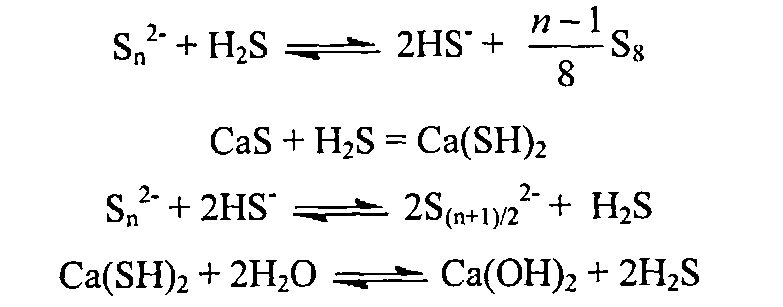RU2523478C1 - Method of obtaining calcium polysulphide solutions - Google Patents
Method of obtaining calcium polysulphide solutions Download PDFInfo
- Publication number
- RU2523478C1 RU2523478C1 RU2012153109/05A RU2012153109A RU2523478C1 RU 2523478 C1 RU2523478 C1 RU 2523478C1 RU 2012153109/05 A RU2012153109/05 A RU 2012153109/05A RU 2012153109 A RU2012153109 A RU 2012153109A RU 2523478 C1 RU2523478 C1 RU 2523478C1
- Authority
- RU
- Russia
- Prior art keywords
- calcium
- stage
- suspension
- aqueous
- carried out
- Prior art date
Links
Landscapes
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Compounds Of Alkaline-Earth Elements, Aluminum Or Rare-Earth Metals (AREA)
- Solid-Sorbent Or Filter-Aiding Compositions (AREA)
Abstract
Description
Изобретение относится к способу получения растворов полисульфида кальция (CaSn) в форме водных, водно-спиртовых и спиртовых (метанол, этанол) растворов, которые находят применение в качестве инсектицидно-фунгицидно-акарицидных средств (пестицидов) в сельскохозяйственной практике, для защиты лесных насаждений, реагентов для делигнификации древесины, модификаторов цементного бетона, средств для дезинсекции и санитарии в бытовой практике, препаратов для лечения кожных заболеваний, реагентов в химической промышленности и т.д. Перспективно применение водных растворов полисульфида кальция в качестве высокоэкологичных серосодержащих жидких удобрений.The invention relates to a method for producing solutions of calcium polysulfide (CaS n ) in the form of aqueous, aqueous-alcoholic and alcoholic (methanol, ethanol) solutions, which are used as insecticidal-fungicidal-acaricidal agents (pesticides) in agricultural practice, for the protection of forest stands reagents for delignification of wood, cement concrete modifiers, disinsection and sanitation products in domestic practice, preparations for treating skin diseases, reagents in the chemical industry, etc. The use of aqueous solutions of calcium polysulfide as highly environmentally friendly sulfur-containing liquid fertilizers is promising.
Полисульфиды щелочных и щелочно-земельных металлов и в первую очередь полисульфиды кальция играют важную роль в решении актуальной экономической и экологической проблемы мирового масштаба - расширении областей практического применения элементной серы.Polysulfides of alkali and alkaline-earth metals and primarily calcium polysulfides play an important role in solving the urgent economic and environmental problems on a global scale - expanding the areas of practical application of elemental sulfur.
Современный нефте- и газокомплекс характеризуются постоянным увеличением доли перерабатываемого высокосернистого сырья и, как следствие, производством возрастающих объемов элементной серы как ассоциированного продукта. Количество накапливаемой серы неуклонно возрастает из-за растущих требований к защите окружающей среды от серосодержащих промышленных выбросов и повышения качества продуктов за счет снижения в них содержания серы. Между тем, потребление серы по традиционным направлениям (производство серной кислоты, целлюлозно-бумажная промышленность, техника) достигло определенного предела, а в ряде направлений имеет тенденцию к сокращению из-за внедрения новых экологически чистых технологий и материалов. Возникший в мировой практике дисбаланс производства и потребления серы имеет место и в России. Порожденная сложившейся ситуацией практика вынужденного долговременного хранения серы порождает серьезные проблемы экологического и правового характера (вероятный перевод серы из разряда побочных продуктов в разряд отходов производства).The modern oil and gas complex is characterized by a constant increase in the share of processed high-sulfur raw materials and, as a result, the production of increasing volumes of elemental sulfur as an associated product. The amount of accumulated sulfur is steadily increasing due to growing requirements to protect the environment from sulfur-containing industrial emissions and to improve the quality of products by reducing their sulfur content. Meanwhile, sulfur consumption in traditional areas (production of sulfuric acid, pulp and paper industry, machinery) has reached a certain limit, and in some areas has a tendency to decrease due to the introduction of new environmentally friendly technologies and materials. The imbalance in sulfur production and consumption that has arisen in world practice also occurs in Russia. The practice of forced long-term storage of sulfur generated by this situation gives rise to serious environmental and legal problems (the probable transfer of sulfur from the category of by-products to the category of production waste).
Выход из создавшегося положения связывают с расширением практики применения серы в новых и еще неизвестных направлениях, практическими мерами по ограничению производства излишней серы. Другими словами, речь идет о создании новых или усовершенствовании известных форм серосодержащих материалов, предусматривающих использование не только серы, но и ее предшественников, главным из которых является сероводород. Актуальность такого подхода связана и с тем, что возможности традиционного промышленного метода утилизации сероводорода - процесса Клауса мало применимы для малотоннажных объектов.The way out of this situation is associated with the expansion of the practice of using sulfur in new and still unknown directions, with practical measures to limit the production of excess sulfur. In other words, we are talking about creating new or improving known forms of sulfur-containing materials, involving the use of not only sulfur, but also its predecessors, the main of which is hydrogen sulfide. The relevance of this approach is also related to the fact that the possibilities of the traditional industrial method of utilizing hydrogen sulfide, the Klaus process, are of little use for small-capacity facilities.
В связи с вышеизложенным первостепенное значение приобретает разработка современных практически удобных способов синтеза полисульфидных соединений, содержащих значительное количество серы (до 80%). Преимуществом полисульфидов щелочных и щелочно-земельных металлов, в частности полисульфидов кальция, является высокая растворимость в воде, что делает их максимально адаптированными к природным объектам.In connection with the foregoing, the development of modern practically convenient methods for the synthesis of polysulfide compounds containing a significant amount of sulfur (up to 80%) is of paramount importance. The advantage of polysulfides of alkali and alkaline earth metals, in particular calcium polysulfides, is their high solubility in water, which makes them as adaptable to natural objects as possible.
Известны следующие методы синтеза полисульфидов щелочных металлов: прямым взаимодействием металла с элементной серой при температуре выше 250°С [Авт.св. СССР №1129186, МПК С01В 17/22, оп. 15.12.84], взаимодействием серы с водными растворами щелочей при 100°С с образованием сульфитов и тиосульфатов металлов в качестве побочных продуктов (их образование и количества определяются стехиометрией реакций) или взаимодействием серы с сульфидами металлов в тех же условиях без образования побочных сульфитов и тиосульфатов [Синтетический каучук / Под ред. И.В.Гармонова. Л.: Химия. 1983. 560 с.]. Для двух последних реакций катализ водорастворимыми аминами позволяет ускорить процесс и снизить температуру процесса до 60°С [Авт.св. СССР №1137075, МПК С01В 17/22, оп. 30.01.85].The following methods are known for the synthesis of alkali metal polysulfides: by direct interaction of the metal with elemental sulfur at temperatures above 250 ° C [Auth. USSR No. 1129186, IPC СВВ 17/22, op. 12.15.84], by the interaction of sulfur with aqueous alkali solutions at 100 ° C with the formation of metal sulfites and thiosulfates as by-products (their formation and quantities are determined by reaction stoichiometry) or by the interaction of sulfur with metal sulfides under the same conditions without the formation of side sulfites and thiosulfates [Synthetic rubber / Ed. I.V. Garmonova. L .: Chemistry. 1983. 560 p.]. For the last two reactions, catalysis by water-soluble amines allows to accelerate the process and reduce the process temperature to 60 ° C [Auth. USSR No. 1137075, IPC С01В 17/22, op. 01/30/85].
Для полисульфидов щелочно-земельных металлов, в частности кальция, вышеназванные простые методы синтеза ограничены в применении. Прямое взаимодействие кальция и серы невозможно из-за недостаточно высокой устойчивости полисульфидов кальция при повышенных температурах. Реакция серы с сульфидом кальция также трудноосуществима: промышленный синтез исходного CaS восстановлением сульфата кальция представляет энергетически затратный высокотемпературный процесс (800-1000°С) [Авт.св. СССР №1528724, МПК С01В 17/44, оп. 15.12.89], а сам CaS плохо растворим в воде и к тому же разлагается на воздухе.For polysulfides of alkaline earth metals, in particular calcium, the above simple synthesis methods are limited in application. Direct interaction of calcium and sulfur is impossible due to the insufficiently high stability of calcium polysulfides at elevated temperatures. The reaction of sulfur with calcium sulfide is also difficult: the industrial synthesis of the initial CaS by reduction of calcium sulfate is an energy-intensive high-temperature process (800-1000 ° C) [Auth. USSR No. 1528724, IPC С01В 17/44, op. 12.15.89], and CaS itself is poorly soluble in water and also decomposes in air.
Известен способ получения полисульфида кальция взаимодействием окиси кальция с серой в воде при 100°С и соотношении компонентов по массе S:CaO:H2O=10:5:85 [Позин М.Е. Технология минеральных солей (удобрений, пестицидов, промышленных солей, окислов и кислот). 4.1. М.: Химия. 1974. С.502]. Процесс начинают взаимодействием СаО с частью воды (гашение извести и образование гидроокиси кальция - Са(ОН)2), а затем добавляют серу в виде пасты (измельчение с добавлением воды) или сухом молотом виде. Вместо СаО можно использовать «готовую» гидроокись кальция. В результате реакции образуется смесь полисульфидов CaSn со средним значением степени сульфидности n до 4,5 и концентрацией основного вещества до 20-22%. Концентрация побочного продукта - тиосульфата кальция (CaS2O3) в растворе - до 10%. Отходами процесса являются нерастворимые сульфит кальция (CaSO3), непрореагировавшая элементная сера и карбонат кальция (СаСО3), обычно присутствующий в качестве примеси в исходном СаО и образующийся в результате реакции гидроокиси кальция с углекислым газом воздуха при открытом способе варки.A known method of producing calcium polysulfide by the interaction of calcium oxide with sulfur in water at 100 ° C and the ratio of components by weight S: CaO: H 2 O = 10: 5: 85 [Pozin M.E. The technology of mineral salts (fertilizers, pesticides, industrial salts, oxides and acids). 4.1. M .: Chemistry. 1974. S. 502]. The process is started by the interaction of CaO with part of the water (slaking lime and the formation of calcium hydroxide - Ca (OH) 2 ), and then sulfur is added in the form of a paste (grinding with the addition of water) or in dry ground form. Instead of CaO, you can use "prepared" calcium hydroxide. As a result of the reaction, a mixture of CaSn polysulfides is formed with an average value of the degree of sulfide n up to 4.5 and the concentration of the basic substance up to 20-22%. The concentration of the by-product calcium thiosulfate (CaS 2 O 3 ) in solution is up to 10%. The process wastes are insoluble calcium sulfite (CaSO 3 ), unreacted elemental sulfur and calcium carbonate (CaCO 3 ), usually present as an impurity in the initial CaO and formed as a result of the reaction of calcium hydroxide with carbon dioxide in an open cooking process.
Недостатками известного способа являются длительность процесса (несколько часов), высокая температура (100°С), большое количество побочных продуктов и трудноутилизируемых отходов, невысокая концентрация раствора по целевому веществу (до 20-22%).The disadvantages of this method are the duration of the process (several hours), high temperature (100 ° C), a large number of by-products and difficult to recycle waste, a low concentration of the solution for the target substance (up to 20-22%).
Недостатки вышеуказанного применяемого на практике метода устранены в способе получения растворов полисульфида кальция [Пат. РФ №2256602, МПК С01В 17/43, оп. 20.07.2005], принятом за прототип.The disadvantages of the above practical method are eliminated in the method for producing calcium polysulfide solutions [US Pat. RF №2256602, IPC СВВ 17/43, op. July 20, 2005] adopted as a prototype.
Согласно этому способу получение CaSn ведут при непрерывном барботировании газообразного сероводорода в реакционную массу, содержащую окись или гидроокись кальция и молотую элементную серу при соотношении CaO:S:H2S=1:(1÷3):избыток. Использование H2S обеспечивает образование CaS, который, находясь в активной мелкодисперсной форме, взаимодействует с серой в мягких условиях с образованием CaSn с выходом (90-92%). Использование сероводорода позволяет также снизить температуру процесса до 50-80°С и сократить время реакции до 30-90 мин. В результате образуется раствор CaSn со средней степенью сульфидности n - до 3,5 для водных растворов и до 4,4 - для спиртовых, с концентрацией основного вещества до 34% - для водных и до 36% - для спиртовых растворов.According to this method, CaSn is produced by continuously sparging gaseous hydrogen sulfide into a reaction mass containing calcium oxide or hydroxide and ground elemental sulfur at a ratio of CaO: S: H 2 S = 1: (1 ÷ 3): excess. The use of H 2 S provides the formation of CaS, which, being in the active finely dispersed form, interacts with sulfur under mild conditions with the formation of CaS n with a yield (90-92%). The use of hydrogen sulfide also reduces the process temperature to 50-80 ° C and reduces the reaction time to 30-90 minutes. As a result, a CaS n solution is formed with an average degree of sulfidity n of up to 3.5 for aqueous solutions and up to 4.4 for alcoholic solutions, with a basic substance concentration of up to 34% for aqueous and up to 36% for alcoholic solutions.
Недостатками известного способа-прототипа являются высокие энергетические затраты, связанные с нагревом реакционной массы, низкий выход целевого продукта и пониженное (относительно заложенного стехиометрией исходных реагентов) значение средней степени сульфидности n. Кроме того, серьезным недостатком известного способа является наличие в продукте растворенного сероводорода, неустранимого обычными приемами продувки инертным газом, что обуславливает неудовлетворительные органолептические свойства готового продукта (запах «тухлых яиц»). Это связано с протеканием во время синтеза вторичных процессов, главным образом, в результате накапливания избыточного гидросульфида кальция (Ca(SH)2) в продукте в результате взаимодействия сероводорода с сульфидом кальция (CaS) и целевым полисульфидом кальция (CaSn). Равновесные гидролиз гидросульфидов или их реакция с полисульфидом определяет постоянное присутствие «неустраняемого» сероводорода в продукте:The disadvantages of the known prototype method are the high energy costs associated with heating the reaction mass, low yield of the target product and low (relative to the stoichiometry of the starting reagents) value of the average degree of sulfidity n. In addition, a serious drawback of the known method is the presence of dissolved hydrogen sulfide in the product, which cannot be eliminated by conventional inert gas purging methods, which causes unsatisfactory organoleptic properties of the finished product (the smell of “rotten eggs”). This is due to the secondary processes occurring during the synthesis, mainly as a result of the accumulation of excess calcium hydrosulfide (Ca (SH) 2 ) in the product as a result of the interaction of hydrogen sulfide with calcium sulfide (CaS) and the target calcium polysulfide (CaS n ). The equilibrium hydrolysis of hydrosulfides or their reaction with polysulfide determines the constant presence of “unremovable” hydrogen sulfide in the product:
Этим также объясняется и далекий от теоретического выход целевого продукта и пониженное значение средней степени сульфидности n.This also explains the yield of the target product that is far from theoretical and the low value of the average degree of sulfidity n.
Задачей настоящего изобретения является снижение энергетических затрат процесса, повышение выхода целевого продукта, существенное повышение (максимизация) значений средней степени сульфидности водных растворов CaSn, исключение примесных продуктов, особенно гидросульфида, ответственного за наличие постоянных примесей сероводорода в растворе и обуславливающего органолептические недостатки целевого продукта.The objective of the present invention is to reduce the energy costs of the process, increase the yield of the target product, significantly increase (maximize) the average degree of sulfide content of aqueous CaS n solutions, eliminate impurity products, especially hydrosulfide, which is responsible for the presence of constant impurities of hydrogen sulfide in the solution and causes organoleptic disadvantages of the target product.
Указанная задача решается способом получения растворов полисульфида кальция из гидроокиси или окиси кальция, сероводорода и элементной серы постадийно: на первой стадии получают раствор или суспензию гидросульфида кальция путем насыщения водной, водно-спиртовой или спиртовой суспензии гидроокиси или окиси кальция сероводородом, на второй стадии - водную, водно-спиртовую или спиртовую суспензию сульфида кальция смешением раствора или суспензии гидросульфида кальция, полученной на первой стадии, с водной, водно-спиртовой или спиртовой суспензией гидроокиси или окиси кальция и на третьей стадии получают целевой продукт - полисульфид кальция в виде водного, водно-спиртового или спиртового раствора смешением суспензии сульфида кальция, полученной на второй стадии, с элементной серой, при этом первую стадию процесса проводят в двух последовательно расположенных поглотительных колоннах при температуре 5-70°C и мольном отношении гидроокиси или окиси кальция к сероводороду в первой поглотительной колонне от 1:1 до 1:3, вторую стадию процесса проводят при температуре 5-40°C и мольном отношении гидроокиси или окиси кальция к гидросульфиду кальция от 1:1 до 1,2:1, а третью стадию процесса проводят при температуре 5-40°C и мольном отношении сульфида кальция к элементной сере от 1:1 до 1:5.This problem is solved by the method of producing solutions of calcium polysulfide from calcium hydroxide or calcium oxide, hydrogen sulfide and elemental sulfur in stages: in the first stage, a solution or suspension of calcium hydrosulfide is obtained by saturating an aqueous, aqueous-alcoholic or alcohol suspension of hydroxide or calcium oxide with hydrogen sulfide, in the second stage - aqueous , an aqueous-alcoholic or alcoholic suspension of calcium sulfide by mixing a solution or suspension of calcium hydrosulfide obtained in the first stage, with an aqueous, aqueous-alcoholic or alcohol with a suspension of hydroxide or calcium oxide and in the third stage, the target product is obtained — calcium polysulfide in the form of an aqueous, aqueous-alcohol or alcohol solution by mixing the suspension of calcium sulfide obtained in the second stage with elemental sulfur, while the first stage of the process is carried out in two sequentially absorbing columns at a temperature of 5-70 ° C and a molar ratio of hydroxide or calcium oxide to hydrogen sulfide in the first absorption column from 1: 1 to 1: 3, the second stage of the process is carried out at a temperature of 5-40 ° C and mol SG respect hydroxide or calcium oxide to calcium hydrogen sulphide from 1: 1 to 1.2: 1, and the third process step is carried out at a temperature of 5-40 ° C and a molar ratio of calcium sulfide to elemental sulfur of from 1: 1 to 1: 5.
Целесообразно процесс проводить по полунепрерывной схеме, причем в первой поглотительной колонне процесс проводят в течение 0,1-24 часов, а во второй поглотительной колонне проводят улавливание избытка сероводорода, не поглощенного в первой колонне, и в следующем технологическом цикле последовательность работы колонн меняется на обратную.It is advisable to carry out the process according to a semicontinuous scheme, and in the first absorption column the process is carried out for 0.1-24 hours, and in the second absorption column the excess hydrogen sulfide that is not absorbed in the first column is captured, and in the next process cycle the sequence of columns is reversed .
Целесообразно вторую стадию процесса проводить в реакторе с мешалкой в течение 0,1-2,0 часов.It is advisable to carry out the second stage of the process in a reactor with a stirrer for 0.1-2.0 hours.
Целесообразно третью стадию процесса проводить в реакторе с мешалкой после окончания второй стадии процесса в течение 0,1-5 часов.It is advisable to carry out the third stage of the process in a reactor with a stirrer after the end of the second stage of the process within 0.1-5 hours.
На первой и/или второй стадиях можно применять водную, водно-спиртовую или спиртовую суспензию гидроокиси или окиси кальция с содержанием гидроокиси или окиси кальция 5-70% масс.In the first and / or second stages, you can apply an aqueous, aqueous-alcoholic or alcoholic suspension of hydroxide or calcium oxide with a content of hydroxide or calcium oxide of 5-70% of the mass.
На первой стадии можно применять сероводород, содержащий инертные в отношении сырьевых компонентов примеси, например азот и легкие углеводороды.At the first stage, hydrogen sulfide containing inert impurities in relation to the raw material components, for example nitrogen and light hydrocarbons, can be used.
На третьей стадии можно применять молотую серу в виде суспензии в водной, водно-спиртовой или спиртовой среде с содержанием серы 10-99% масс.In the third stage, ground sulfur can be used in the form of a suspension in an aqueous, aqueous-alcoholic or alcoholic medium with a sulfur content of 10-99% by weight.
Целесообразно все стадии процесса проводить под азотной подушкой.It is advisable to carry out all stages of the process under a nitrogen blanket.
Поясняющая схема превращений сырьевых компонентов в целевой продукт приведена ниже.An explanatory diagram of the conversion of raw materials into the target product is given below.
Суммарно: Total:
Как следует из схемы реакций, сероводород принимает участие только в реакциях (1) и после удаления избытка продувкой азотом не фигурирует в дальнейших процессах. Благодаря высокой активности образующегося в реакции (2) высокодисперсного сульфида кальция (CaS) следующая реакция (3) протекает практически количественно при нормальной температуре с небольшой экзотермией и обеспечивает селективное образование стандартного полисульфида кальция (CaSn) с n до 5,0, в т.ч. для водных растворов. Концентрации основного вещества - до 40% (большие концентрации ограничены растворимостью полисульфида), т.е. на уровне прототипа и выше. Уровень примесей в продукте в пересчете на CaS2O3 не превышает 0,7% масс. Выход целевого продукта от теоретической массы полисульфида - более 98%.As follows from the reaction scheme, hydrogen sulfide takes part only in reactions (1) and does not appear in further processes after removal of the excess by nitrogen purge. Due to the high activity of the finely dispersed calcium sulfide (CaS) formed in reaction (2), the following reaction (3) proceeds almost quantitatively at normal temperature with a small exotherm and ensures the selective formation of standard calcium polysulfide (CaS n ) from n to 5.0, in t. hours for aqueous solutions. The concentration of the basic substance is up to 40% (large concentrations are limited by the solubility of the polysulfide), i.e. at prototype level and above. The level of impurities in the product in terms of CaS 2 O 3 does not exceed 0.7% of the mass. The yield of the target product from the theoretical mass of polysulfide is more than 98%.
Содержание свободного H2S в продукте не обнаруживается органолептически (по запаху). Известно, что человек чувствует запах сероводорода при концентрации в несколько ppm, а при содержании его на уровне 10 ppm и выше необходима химическая защита от него с использованием специальных картриджей.The content of free H 2 S in the product is not detected organoleptically (by smell). It is known that a person smells hydrogen sulfide at a concentration of several ppm, and if it is kept at 10 ppm or higher, chemical protection against it is necessary using special cartridges.
Предлагаемое изобретение иллюстрируют следующие примеры.The invention is illustrated by the following examples.
Пример №1 (типовой экспериментальный)Example No. 1 (typical experimental)
В качестве исходного сырья используют водную суспензию гидроокиси кальция. Стехиометрия реакции рассчитана на получение CaSn со средней степенью сульфидности n=4,5. В суспензию 50,0 г Са(ОН)2 (99%) в 306,4 дистиллированной воды, помещенную в высокий цилиндр (500 мл), через мелкопористый рассекатель барботируют газообразный сероводород. Мольное отношение гидроокиси кальция к сероводороду, достаточное для полной конверсии гидроокиси кальция в гидросульфид, - 1:2. Тепло реакции снимают водяным охлаждением. Проскок сероводорода, свидетельствующий о скором завершении процесса образования Ca(SH)2, фиксируют любой подходящей качественной реакцией. Подавая заведомый избыток сероводорода, гарантируют полную конверсию сырья в гидросульфид кальция. Избыточный растворенный сероводород выдувают током азота.An aqueous suspension of calcium hydroxide is used as a feedstock. The stoichiometry of the reaction is designed to produce CaS n with an average degree of sulfidity of n = 4.5. In a suspension of 50.0 g of Ca (OH) 2 (99%) in 306.4 distilled water, placed in a tall cylinder (500 ml), gaseous hydrogen sulfide is bubbled through a finely porous divider. The molar ratio of calcium hydroxide to hydrogen sulfide, sufficient for the complete conversion of calcium hydroxide to hydrosulfide, is 1: 2. The heat of reaction is removed by water cooling. A breakdown of hydrogen sulfide, indicating the imminent completion of the process of formation of Ca (SH) 2 , is fixed by any suitable qualitative reaction. By submitting a known excess of hydrogen sulfide, they guarantee the complete conversion of the feed to calcium hydrosulfide. Excess dissolved hydrogen sulfide is blown out by a stream of nitrogen.
Полученную суспензию Са(SH)2 в собственном насыщенном растворе количественно переносят (омывая стенки цилиндра 50 мл воды, т.е. общее количество воды на первой стадии 356,4 г) в литровую четырехгорлую колбу, снабженную перемешивающим устройством, термометром и капилляром для подачи азота. При перемешивании в колбу вносят 50,5 г Са(ОН)2 (мольное отношение гидроокиси кальция к гидросульфиду кальция - 1,01:1). Небольшую экзотермию реакции снимают с помощью холодной водяной бани. Эту и последующие стадии проводят под азотной подушкой. После 30 мин перемешивания (достаточно для полного образования суспензии CaS) в колбу порционно вносят 151,4 г молотой элементной серы (мольное отношение сульфида кальция к сере - 1:3,5), не прекращая перемешивания и охлаждения реакционной массы, поддерживая температуру смеси не выше 30°С. Перемешивание продолжают в течение 1-2 часов. Продукт фильтруют через бумажный фильтр («белая лента») под вакуумом и хранят в герметичной таре под слоем индустриального масла (изолирующий слой). Промытый и высушенный осадок в количестве 4,5 г представляет собой смесь в основном непрореагировавшей серы и карбоната кальция.The resulting suspension of Ca (SH) 2 in its own saturated solution is quantitatively transferred (washing the walls of the cylinder with 50 ml of water, i.e., the total amount of water in the first stage 356.4 g) into a liter four-necked flask equipped with a mixing device, a thermometer and a capillary for feeding nitrogen. With stirring, 50.5 g of Ca (OH) 2 is added to the flask (the molar ratio of calcium hydroxide to calcium hydrosulfide is 1.01: 1). A small exotherm of the reaction is removed using a cold water bath. This and subsequent steps are carried out under a nitrogen blanket. After 30 minutes of stirring (sufficient for the complete formation of a CaS suspension), 151.4 g of ground elemental sulfur (molar ratio of calcium sulfide to sulfur is 1: 3.5) are portioned into the flask, without stopping mixing and cooling of the reaction mass, while maintaining the temperature of the mixture above 30 ° C. Stirring is continued for 1-2 hours. The product is filtered through a paper filter ("white tape") under vacuum and stored in a sealed container under a layer of industrial oil (insulating layer). The washed and dried precipitate in an amount of 4.5 g is a mixture of mainly unreacted sulfur and calcium carbonate.
Полученный водный раствор CaSn - прозрачная подвижная жидкость насыщенного оранжевого цвета. По результатам йодометрического титрования вычислено: средняя степень сульфидности CaSn n=4,46, содержание основного вещества CaSn - 37,4% масс. (при вычисленном n), доля примесей в пересчете на CaS2O3 - 0,6% масс. Плотность - 1,339 г/см3. Выход (от теоретической массы полисульфида) - 98,4%.The resulting aqueous solution of CaS n is a clear mobile liquid of a saturated orange color. According to the results of iodometric titration it was calculated: the average degree of sulfide CaS n n = 4.46, the content of the basic substance CaS n - 37.4% of the mass. (when calculated n), the proportion of impurities in terms of CaS 2 O 3 - 0.6% of the mass. Density - 1,339 g / cm 3 . The output (from the theoretical mass of polysulfide) is 98.4%.
Пример №2Example No. 2
Процесс ведут в соответствии с примером №1 со следующими изменениями загрузок компонентов: вода на первой стадии - 712,8 г (общее количество). В этом случае воды достаточно для полного растворения гидросульфида кальция, получаемого на первой стадии, и дальнейшие операции проводят с раствором гидросульфида. В итоге получают продукт со средней степенью сульфидности CaSn n=4,49 и содержанием основного вещества CaSn - 24,3% масс. (при вычисленном n).The process is carried out in accordance with example No. 1 with the following changes in component loading: water in the first stage - 712.8 g (total amount). In this case, there is enough water to completely dissolve the calcium hydrosulfide obtained in the first stage, and further operations are carried out with a hydrosulfide solution. The result is a product with an average degree of sulfidity CaS n n = 4.49 and a basic substance content of CaS n - 24.3% of the mass. (with calculated n).
Пример №3Example No. 3
В качестве исходного сырья используют свежепрокаленную окись кальция (800°С, 8 ч, охлаждают в эксикаторе над хлористым кальцием) вместо гидроокиси кальция. Процесс ведут в соответствии с примером №1 со следующими изменениями загрузок компонентов: окись кальция - 37,8 г на первой стадии и 38,2 г - на второй, вода - 380,8 г (общее количество). Получают продукт, аналогичный продукту примера №1.Freshly calcined calcium oxide (800 ° C, 8 hours, cooled in a desiccator over calcium chloride) is used as feedstock instead of calcium hydroxide. The process is carried out in accordance with example No. 1 with the following changes in component loads: calcium oxide - 37.8 g in the first stage and 38.2 g in the second, water - 380.8 g (total amount). Get a product similar to the product of example No. 1.
Пример №4Example No. 4
В качестве элементной серы на третьей стадии используют молотую серу в виде 70% (масс.) водной суспензии (густая влажная масса). Процесс ведут в соответствии с примером №1 со следующими изменениями загрузок компонентов: общее количество воды на первой стадии - 291,5 г. Получают продукт, аналогичный продукту примера №1.As elemental sulfur in the third stage, ground sulfur is used in the form of 70% (mass.) Aqueous suspension (thick wet mass). The process is carried out in accordance with example No. 1 with the following changes in component loadings: the total amount of water in the first stage is 291.5 g. A product similar to that of example No. 1 is obtained.
Пример №5Example No. 5
В качестве элементной серы на третьей стадии используют высокодисперсную серу, механоактивированную с использованием интенсивного механического воздействия, например в устройстве типа дезинтегратора. Процесс ведут в соответствии с примером №1 с получением аналогичного продукта.As elemental sulfur in the third stage, finely dispersed sulfur mechanically activated using intense mechanical action, for example, in a device such as a disintegrator, is used. The process is carried out in accordance with example No. 1 to obtain a similar product.
Пример №6Example No. 6
В качестве исходного сырья на третьей стадии вместо молотой серы используют жидкую серу, которую вводят с одновременным диспергированием в суспензию сульфида кальция, циркулирующую в выносном контуре реакционного сосуда, при охлаждении. Диспергирование и циркуляцию осуществляют с помощью насоса типа роторно-пульсационного аппарата. В остальном процесс ведут в соответствии с примером №1 с получением аналогичного продукта.Instead of ground sulfur, liquid sulfur is used as the feedstock in the third stage, which is introduced while dispersing into a suspension of calcium sulfide circulating in the external circuit of the reaction vessel under cooling. Dispersion and circulation is carried out using a pump of the rotary pulsation apparatus type. The rest of the process is carried out in accordance with example No. 1 to obtain a similar product.
Водные растворы полисульфидов могут быть использованы в различных отраслях народного хозяйства: сельскохозяйственной практике (микроудобрение, препарат с инсектицидно-фунгицидно-акарицидной активностью для защиты растений), лесном хозяйстве и садоводстве (экологически чистое профилактическое средство для защиты лесных и культурных растений от вредителей широкого спектра действия), строительной практике (компонент композиций строительного назначения, гидрофобизатор каменных материалов), технике (реагент-аналог полисульфида натрия), а также в сфере экологии (дезактивация токсичных промышленных отходов и сточных вод, содержащих тяжелые металлы). Особо перспективно использование полисульфида кальция в качестве серосодержащего удобрения, т.к. общепризнана проблема дефицита серы в почвах. Потенциальное использование водных растворов CaSn в качестве удобрения может составить конкуренцию традиционным сульфатным формам за счет большей доли серы и пролонгированного характера действия.Aqueous solutions of polysulfides can be used in various sectors of the national economy: agricultural practice (microfertilizer, a drug with insecticidal-fungicidal-acaricidal activity for plant protection), forestry and horticulture (environmentally friendly prophylactic for protecting forest and cultivated plants from broad spectrum pests ), construction practice (component of compositions for construction purposes, water-repellent stone materials), engineering (reagent-analogue of sodium polysulfide ), as well as in the field of ecology (decontamination of toxic industrial waste and wastewater containing heavy metals). Especially promising is the use of calcium polysulfide as a sulfur-containing fertilizer, because The problem of sulfur deficiency in soils is widely recognized. The potential use of aqueous CaS n solutions as a fertilizer can compete with traditional sulfate forms due to a greater proportion of sulfur and a prolonged action.
Пример №7Example No. 7
В качестве исходного сырья используют спиртовую суспензию гидроокиси кальция. Процесс ведут в соответствии с типовым примером №1 с заменой воды на метиловый спирт (99,9%). Дополнительно на стадии барботажа сероводорода цилиндр снабжают эффективным обратным холодильником для улавливания паров спирта.As a feedstock, an alcoholic suspension of calcium hydroxide is used. The process is carried out in accordance with model example No. 1 with the replacement of water with methyl alcohol (99.9%). Additionally, at the stage of bubbling of hydrogen sulfide, the cylinder is equipped with an effective reflux condenser for trapping alcohol vapor.
Полученный стартовый раствор CaSn - прозрачная подвижная жидкость насыщенного оранжевого цвета. По результатам йодометрического титрования вычислено: средняя степень сульфидности CaSn n=4,48, содержание основного вещества CaSn - 37,8% масс. (при вычисленном n), доля примесей в пересчете на CaS2O3 - 0,3% масс. Плотность - 1,164 г/см3. Выход (от теоретической массы полисульфида) - 99,4%.The resulting CaS n starter solution is a clear mobile liquid of a saturated orange color. According to the results of iodometric titration it was calculated: the average degree of sulfide CaS n n = 4.48, the content of the basic substance CaS n - 37.8% of the mass. (when calculated n), the proportion of impurities in terms of CaS 2 O 3 - 0.3% of the mass. Density - 1.164 g / cm 3 . The output (from the theoretical mass of polysulfide) is 99.4%.
Пример №8Example No. 8
В качестве исходного сырья используют водно-спиртовую суспензию гидроокиси кальция. Процесс ведут в соответствии с типовым примером №1 с заменой воды на 50%-ный метиловый спирт. Дополнительно на стадии барботажа сероводорода цилиндр снабжают эффективным обратным холодильником для улавливания паров спирта.As a feedstock, a water-alcohol suspension of calcium hydroxide is used. The process is carried out in accordance with model example No. 1 with the replacement of water with 50% methyl alcohol. Additionally, at the stage of bubbling of hydrogen sulfide, the cylinder is equipped with an effective reflux condenser for trapping alcohol vapor.
Полученный спиртовой раствор CaSn - прозрачная подвижная жидкость насыщенного оранжевого цвета. По результатам йодометрического титрования вычислено: средняя степень сульфидности CaSn n=4,49, содержание основного вещества CaSn - 37,7% масс. (при вычисленном n), доля примесей в пересчете на CaS2O3 - 0,3% масс. Плотность - 1,250 г/см3. Выход (от теоретической массы полисульфида) - 99,3%.The resulting alcoholic solution CaS n is a clear mobile liquid of a saturated orange color. According to the results of iodometric titration it was calculated: the average degree of sulfide CaS n n = 4.49, the content of the basic substance CaS n - 37.7% of the mass. (when calculated n), the proportion of impurities in terms of CaS 2 O 3 - 0.3% of the mass. Density - 1,250 g / cm 3 . The yield (from the theoretical mass of polysulfide) is 99.3%.
Пример №9Example No. 9
В качестве исходного сырья используют спиртовую суспензию гидроокиси кальция. Процесс ведут в соответствии с типовым примером №7 с заменой метилового спирта на этиловый спирт (96%) со следующими изменениями загрузок компонентов: общее количество этилового спирта на первой стадии - 526,4 г.As a feedstock, an alcoholic suspension of calcium hydroxide is used. The process is carried out in accordance with model example No. 7 with the replacement of methyl alcohol with ethyl alcohol (96%) with the following changes in component loads: the total amount of ethyl alcohol in the first stage is 526.4 g.
Полученный спиртовой раствор CaSn - прозрачная подвижная жидкость насыщенного оранжевого цвета. По результатам йодометрического титрования вычислено: средняя степень сульфидности CaSn n=4,50, содержание основного вещества CaSn - 30,2% масс. (при вычисленном n), доля примесей в пересчете на CaS2O3 - 0,2% масс. Плотность - 1,141 г/см3. Выход (от теоретической массы полисульфида) - 99,5%.The resulting alcoholic solution CaS n is a clear mobile liquid of a saturated orange color. According to the results of iodometric titration it was calculated: the average degree of sulfidity CaS n n = 4,50, the content of the basic substance CaS n - 30.2% of the mass. (when calculated n), the proportion of impurities in terms of CaS 2 O 3 - 0.2% of the mass. Density - 1,141 g / cm 3 . The output (from the theoretical mass of polysulfide) is 99.5%.
Пример №10Example No. 10
В качестве исходного сырья используют спиртовую суспензию свежепрокаленной окиси кальция (готовят, как в примере №3). Процесс ведут в соответствии с примером №3 с заменой части воды на метиловый спирт при следующих загрузках этих компонентов: спирт - 355,8 г, вода - 25,0 г, причем вода вводится в суспензию окиси кальция в спирте при активном перемешивании и охлаждении. Дополнительно на стадии барботажа сероводорода цилиндр снабжают эффективным обратным холодильником для улавливания паров спирта. Получают продукт, аналогичный продукту примера №7.As a starting material, an alcohol suspension of freshly calcined calcium oxide is used (prepared as in Example No. 3). The process is carried out in accordance with example No. 3 with the replacement of part of the water with methyl alcohol at the following downloads of these components: alcohol - 355.8 g, water - 25.0 g, and water is introduced into the suspension of calcium oxide in alcohol with vigorous stirring and cooling. Additionally, at the stage of bubbling of hydrogen sulfide, the cylinder is equipped with an effective reflux condenser for trapping alcohol vapor. Get a product similar to the product of example No. 7.
Спиртовый и водно-спиртовый раствор полисульфида кальция может использоваться в качестве реагента (в основном - источника полисульфидного синтона или мягкого восстанавливающего или окисляющего агента) в процессах химической технологии и органическом синтезе, в частности для получения мономерных диорганополисульфидов, полимерных полиорганополисульфидов (тиоколов), когда процесс целесообразнее проводить в неводных средах.An alcoholic and aqueous-alcoholic solution of calcium polysulfide can be used as a reagent (mainly a source of polysulfide synthon or a mild reducing or oxidizing agent) in chemical processes and organic synthesis, in particular for the preparation of monomeric diorganopolysulfides, polymeric polyorganopolysulfides (thiocol), when more expediently carried out in non-aqueous environments.
Технологическая схема полунепрерывного процесса на примере синтеза водного раствора полисульфида кальция приведена на прилагаемом чертеже и включает следующие узлы:The flow diagram of a semi-continuous process on the example of the synthesis of an aqueous solution of calcium polysulfide is shown in the attached drawing and includes the following nodes:
- узел приготовления водной суспензии гидроксида кальция в реакторе-смесителе 1 с линиями подвода исходного сырья - воды через расходомер 2 по линии 3 и гидроокиси кальция из бункера 4 по линии 5;- site for the preparation of an aqueous suspension of calcium hydroxide in the reactor-mixer 1 with lines for supplying the feedstock — water through the flow meter 2 through line 3 and calcium hydroxide from the hopper 4 through line 5;
- узел синтеза суспензии гидросульфида кальция в колоннах 6 и 7, оснащенных линией подвода суспензии гидроксида кальция 8 насосом 9, линией подвода сероводорода 10, абсорбером 11 (для улавливания следов не поглотившегося сероводорода), связанным с колоннами 6 и 7 линией 12, линией подвода азота 13 (для выдувания растворенного в гидросульфиде сероводорода и продувки системы азотом);- a unit for synthesizing a suspension of calcium hydrosulfide in columns 6 and 7, equipped with a supply line for the suspension of calcium hydroxide 8 with a pump 9, a supply line for hydrogen sulfide 10, an absorber 11 (for tracing traces of non-absorbed hydrogen sulfide), connected to columns 6 and 7 with a line 12, a nitrogen supply line 13 (for blowing hydrogen sulfide dissolved in hydrosulfide and purging the system with nitrogen);
- узел приготовления суспензии сульфида кальция и раствора полисульфида кальция в реакторе 14, оснащенном линией подвода суспензии гидроокиси кальция 15 насосом 9, линий подвода суспензии гидросульфида кальция 16 насосом 17, системой подачи молотой серы из бункера 18 по линии 19, линией вывода готового раствора полисульфида кальция 20 насосом 21 на фильтрацию;- a unit for preparing a suspension of calcium sulfide and a solution of calcium polysulfide in a reactor 14 equipped with a line for supplying a suspension of calcium hydroxide 15 with a pump 9, lines for supplying a suspension of calcium hydrosulfide 16 with a pump 17, a feed system for ground sulfur from the hopper 18 along line 19, an output line for the finished solution of calcium polysulfide 20 pump 21 to filter;
- узел фильтрации раствора полисульфида кальция на фильтре 22 и подачи готового продукта по линии 23 насосом 24 на фасовочную линию 25, на которой продукт затаривается под слоем масла из емкости 26 по линии 27 или под азотом из линии 28.- site filtering the solution of calcium polysulfide on the filter 22 and supplying the finished product through line 23 with a pump 24 to the packaging line 25, on which the product is packed under a layer of oil from the tank 26 along line 27 or under nitrogen from line 28.
Установка работает следующим образом.Installation works as follows.
I стадия - приготовление суспензии гидросульфида кальцияStage I - preparation of a suspension of calcium hydrosulfide
В реактор-смеситель 1 через расходомер 2 по линии 3 подают водопроводную воду, включают перемешивающее устройство и постепенно из бункера 4 по линии 5 подают отмеренное количество гидроокиси кальция. Суспензию перемешивают до однородного состояния. Получают суспензию гидроокиси кальция - состав А (20,0%-ный), которую подают в колонны 6 и 7 по линии 8 насосом 9. Загрузив в обе колонны расчетное количество состава А, начинают подавать сероводород по линии 10 последовательно. Сначала в колонну 6, а из нее - в колонну 7. В случае проскока сероводород улавливается абсорбером 11, куда отводится по линии 12 из обеих колонн. Абсорбер 11 содержит водный раствор гипохлорита и гидроокиси натрия.To the reactor-mixer 1 through the flow meter 2 through line 3 serves tap water, turn on the mixing device and gradually from the hopper 4 through line 5 serves a measured amount of calcium hydroxide. The suspension is stirred until smooth. A suspension of calcium hydroxide is obtained — composition A (20.0%), which is supplied to columns 6 and 7 via line 8 by pump 9. After loading the calculated amount of composition A into both columns, hydrogen sulfide is fed through line 10 sequentially. First, to column 6, and from it to column 7. In the event of a breakthrough, hydrogen sulfide is trapped by the absorber 11, where it is discharged along line 12 from both columns. The absorber 11 contains an aqueous solution of hypochlorite and sodium hydroxide.
В колоне 6 реакцию ведут до полного поглощения сероводорода (контролируется газоанализатором на выходе из колонны). Полное насыщение суспензии гидроокиси кальция сероводородом наступает при мольном отношении гидроокиси кальция к сероводороду 1:2. Избыток сероводорода, гарантирующий полную конверсию сырья, из колонны 6 подают в колонну 7. Растворенный в полупродукте избыточный сероводород выдувается по линии 13 током азота из колонны 6 в колонну 7 и далее - на абсорбер 11. Температура реакционной массы в колоннах 6 и 7 должна находиться в интервале 5-70°С. Избыточное тепло снимается холодной водой через змеевики охлаждения и рекуперируется для внутренних нужд.In column 6, the reaction is conducted until complete absorption of hydrogen sulfide (controlled by a gas analyzer at the outlet of the column). Full saturation of the suspension of calcium hydroxide with hydrogen sulfide occurs when the molar ratio of calcium hydroxide to hydrogen sulfide is 1: 2. The excess hydrogen sulfide, guaranteeing a complete conversion of the feedstock, is sent from column 6 to column 7. The excess hydrogen sulfide dissolved in the intermediate product is blown through line 13 by a stream of nitrogen from column 6 to column 7 and then to the absorber 11. The temperature of the reaction mixture in columns 6 and 7 should be in the range of 5-70 ° C. Excessive heat is removed by cold water through cooling coils and recovered for internal needs.
Следующая партия гидросульфида кальция готовится подачей сероводорода в колонну 7, а из нее - в колонну 6, в которую предварительно загружен новый состав А. Производственный цикл повторяется для колонны 7, как это описано для колонны 6.The next batch of calcium hydrosulfide is prepared by supplying hydrogen sulfide to column 7, and from it to column 6, into which the new composition A is preloaded. The production cycle is repeated for column 7, as described for column 6.
II стадия - приготовление суспензии сульфида кальцияStage II - preparation of a suspension of calcium sulfide
В реактор-смеситель 1 через расходомер 2 по линии 3 подают водопроводную воду, включают перемешивающее устройство и постепенно из бункера 4 по линии 5 подают отмеренное количество гидроокиси кальция. Суспензию перемешивают до однородного состояния. Получают суспензию гидроокиси кальция - состав В (25,8%-ный), который подают в по линии 15 насосом 9 в реактор 14. Включают перемешивающее устройство реактора 14, и суспензия гидросульфида кальция подается в реактор 14 из колонн 6 или 7 по линии 16 насосом 17 в таком количестве, чтобы мольное отношение гидроокиси кальция к гидросульфиду кальция составляло от 1:1 до 1,1:1. Процесс получения суспензии сульфида кальция ведут в течение 0,1-1,0 часа с постоянным контролем температуры. Температура в реакторе должна быть в диапазоне 5-40°С, регулировка температуры достигается вводом в рубашку реактора 14 холодной воды (которая впоследствии будет использована для приготовления составов А или В в реакторе-смесителе 1).To the reactor-mixer 1 through the flow meter 2 through line 3 serves tap water, turn on the mixing device and gradually from the hopper 4 through line 5 serves a measured amount of calcium hydroxide. The suspension is stirred until smooth. A suspension of calcium hydroxide is obtained - composition B (25.8%), which is fed in line 15 by pump 9 to reactor 14. The mixing device of reactor 14 is turned on and the suspension of calcium hydrosulfide is supplied to reactor 14 from columns 6 or 7 via line 16 pump 17 in such an amount that the molar ratio of calcium hydroxide to calcium hydrosulfide is from 1: 1 to 1.1: 1. The process of obtaining a suspension of calcium sulfide is carried out for 0.1-1.0 hours with constant temperature control. The temperature in the reactor should be in the range of 5-40 ° C, temperature control is achieved by introducing cold water into the jacket of the reactor 14 (which will subsequently be used to prepare compositions A or B in the mixing reactor 1).
III стадия - получение полисульфида кальцияStage III - production of calcium polysulfide
В реактор 14 (в котором находится готовая суспензия сульфида кальция после стадии II) при работающей мешалке, порциями из бункера 18 по линии 19 загружают расчетное количество молотой серы. Расчет ведут на требуемое значение средней степени сульфидности n в CaSn. Например, для получения n=4,5 мольное отношение сульфида кальция к сере должно равняться 3,5. После загрузки процесс ведут в течение 0,1-3 часов с постоянным контролем температуры. Температура в реакторе должна быть в диапазоне 5-40°С, регулировка температуры достигается вводом в рубашку реактора 15 холодной воды (которая впоследствии будет использована для приготовления составов А или В в реакторе-смесителе 1).In the reactor 14 (in which the finished suspension of calcium sulfide is located after stage II) with the stirrer operating, the calculated amount of ground sulfur is loaded in portions from hopper 18 along line 19. The calculation is carried out on the required value of the average degree of sulfidity n in CaS n . For example, to obtain n = 4.5, the molar ratio of calcium sulfide to sulfur should be 3.5. After loading, the process is conducted for 0.1-3 hours with constant temperature control. The temperature in the reactor should be in the range of 5-40 ° C, temperature control is achieved by introducing cold water into the jacket of the reactor 15 (which will subsequently be used to prepare formulations A or B in the mixing reactor 1).
Из реактора 14 реакционная масса (раствор полисульфида кальция) по линии 20 насосом 21 поступает на фильтр 22, откуда ее по линии 23 насосом 24 подают на фасовочный узел 25. Фильтрованный продукт с добавлением из емкости 26 по линии 27 индустриального масла (для предотвращения контакта продукта с кислородом и углекислым газом воздуха) фасуют в тару. Другой вариант фасовки - в герметичную тару с продувкой азотом по линии 28.From the reactor 14, the reaction mass (calcium polysulfide solution) is pumped through line 20 to filter 22, from where it is pumped to line 24 via line 23 to packing unit 25. Filtered product with industrial oil added from tank 26 through line 27 (to prevent product contact with oxygen and carbon dioxide) is packaged in containers. Another packaging option is in sealed containers with nitrogen purge along line 28.
Водный раствор полисульфида кальция принимают партиями. Партией считается количество выгруженного готового продукта из реактора 15.An aqueous solution of calcium polysulfide is taken in batches. A batch is the amount of unloaded finished product from the reactor 15.
В таблице представлен ориентировочный материальный баланс производства из расчета на тонну продукта.The table shows the approximate material balance of production per ton of product.
Предлагаемое изобретение по сравнению с прототипом позволяет получить полисульфиды кальция с низкими энергетическими затратами, повышенным выходом целевого продукта, высоким (максимальным) значением средней степени сульфидности, хорошими органолептическими свойствами, позволяющими применять полученный раствор в самых разнообразных отраслях народного хозяйства. При этом для получения полисульфидов кальция могут быть использованы различные сорта серы, в том числе техническая, сероводород - индивидуальный или в составе смесей с углеводородами и другими инертными в отношении сырьевых компонентов газами, гидроокись кальция, окись кальция или техническая гашеная известь.The present invention, in comparison with the prototype, allows to obtain calcium polysulfides with low energy costs, increased yield of the target product, high (maximum) value of the average degree of sulfide, good organoleptic properties that allow the solution to be used in a wide variety of sectors of the national economy. At the same time, various types of sulfur can be used to produce calcium polysulfides, including industrial, hydrogen sulfide - individual or in mixtures with hydrocarbons and other gases inert with respect to raw materials, calcium hydroxide, calcium oxide, or hydrated lime.
Таким образом, предлагаемое изобретение позволяет расширить область применения серы и сероводорода и способствовать их утилизации.Thus, the present invention allows to expand the scope of sulfur and hydrogen sulfide and facilitate their disposal.
Claims (10)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2012153109/05A RU2523478C1 (en) | 2012-12-07 | 2012-12-07 | Method of obtaining calcium polysulphide solutions |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2012153109/05A RU2523478C1 (en) | 2012-12-07 | 2012-12-07 | Method of obtaining calcium polysulphide solutions |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2523478C1 true RU2523478C1 (en) | 2014-07-20 |
| RU2012153109A RU2012153109A (en) | 2014-07-20 |
Family
ID=51214865
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2012153109/05A RU2523478C1 (en) | 2012-12-07 | 2012-12-07 | Method of obtaining calcium polysulphide solutions |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2523478C1 (en) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2742990C1 (en) * | 2020-05-12 | 2021-02-12 | Открытое акционерное общество "Научно-исследовательский и проектный институт обогащения и механической обработки полезных ископаемых "Уралмеханобр" (ОАО "Уралмеханобр") | Method for producing calcium hydrosulfide |
| RU2777173C1 (en) * | 2021-11-24 | 2022-08-01 | Общество с ограниченной ответственностью инновационное предприятие "Сульфидные технологии" | Method for obtaining calcium polysulfide |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0349671A1 (en) * | 1988-07-07 | 1990-01-10 | PAN-CHEMIE Dr. J. Fülöp | Process for separating heavy metals from waste water by sulfide precipitation using calcium polysulfide |
| SU1740314A1 (en) * | 1989-12-07 | 1992-06-15 | Институт проблем технологии микроэлектроники и особо чистых материалов АН СССР | Method of alkaline-earth metal sulfides preparation |
| RU2256602C1 (en) * | 2003-12-22 | 2005-07-20 | Общество с ограниченной ответственностью "Башкирский инновационный центр "Содействие" | Method for preparing calcium polysulfide solution |
| JP2009209231A (en) * | 2008-03-03 | 2009-09-17 | Koda Tooru | Method for producing polysulfide chemical agent for heavy metal fixation |
-
2012
- 2012-12-07 RU RU2012153109/05A patent/RU2523478C1/en not_active IP Right Cessation
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0349671A1 (en) * | 1988-07-07 | 1990-01-10 | PAN-CHEMIE Dr. J. Fülöp | Process for separating heavy metals from waste water by sulfide precipitation using calcium polysulfide |
| SU1740314A1 (en) * | 1989-12-07 | 1992-06-15 | Институт проблем технологии микроэлектроники и особо чистых материалов АН СССР | Method of alkaline-earth metal sulfides preparation |
| RU2256602C1 (en) * | 2003-12-22 | 2005-07-20 | Общество с ограниченной ответственностью "Башкирский инновационный центр "Содействие" | Method for preparing calcium polysulfide solution |
| JP2009209231A (en) * | 2008-03-03 | 2009-09-17 | Koda Tooru | Method for producing polysulfide chemical agent for heavy metal fixation |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2742990C1 (en) * | 2020-05-12 | 2021-02-12 | Открытое акционерное общество "Научно-исследовательский и проектный институт обогащения и механической обработки полезных ископаемых "Уралмеханобр" (ОАО "Уралмеханобр") | Method for producing calcium hydrosulfide |
| RU2777173C1 (en) * | 2021-11-24 | 2022-08-01 | Общество с ограниченной ответственностью инновационное предприятие "Сульфидные технологии" | Method for obtaining calcium polysulfide |
Also Published As
| Publication number | Publication date |
|---|---|
| RU2012153109A (en) | 2014-07-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2377388B2 (en) | PROCEDURE FOR THE PREPARATION OF LIQUID DISSOLUTION OF CALCIUM TIOSULFATE FROM LIME, SULFUR AND SULFUR DIOXIDE. | |
| EA038027B1 (en) | Oxidation process for producing potassium thiosulfate | |
| CN104672206A (en) | Preparation process of ethylene sulfide | |
| FI78846B (en) | FOERFARANDE FOER AVLAEGSNANDE AV GASFORMIGA SVAVELFOERENINGAR OCH SVAVELDIOXID UR ROEKGASER I EN PANNA. | |
| CN100390061C (en) | Method for preparing anhydrous sodium sulfite using industrial by-product anhydrous sodium sulfate | |
| RU2523478C1 (en) | Method of obtaining calcium polysulphide solutions | |
| CN115814580A (en) | Carbide slag modified desulfurizer composition, desulfurizer, preparation method and application thereof | |
| CN108800147A (en) | Low NOx burning process and its device | |
| CN109110859A (en) | A kind of coking desulfurization waste liquor advanced treatment process | |
| CN103551027A (en) | Sulfur dioxide absorbent prepared from lime-flue gas secondary salt slurry | |
| CN103551015A (en) | Sulfur dioxide absorbent prepared from two-alkali salt slurry | |
| KR20150042281A (en) | Preparation method for organic thiosulfate | |
| KR100568336B1 (en) | A preparing method of compound fertilizer by using sewage sludge dehydrated cake and the compound fertilizer thereby | |
| FI78845B (en) | FOERFARANDE FOER AVLAEGSNANDE AV GASFORMIGA SVAVELFOERENINGAR, SAOSOM SVAVELDIOXID FRAON ROEKGASERNA FRAON EN PANNA. | |
| CN103772315A (en) | Method for synthesizing ethyl 4-methylthiazole-5-formate employing single step | |
| RU2777173C1 (en) | Method for obtaining calcium polysulfide | |
| CN110330468A (en) | A kind of synthetic method of 4,4 '-dithio morpholines | |
| RU2339610C2 (en) | Method of production of formic acid formates | |
| CN102408391A (en) | Production method of thiazolidine | |
| KR102506565B1 (en) | Method and apparatus for preparing calcium formate | |
| CA1143539A (en) | Process for preparing stable copper (ii)- sulfate monohydrate to be used as trace- element additive for animal feeds | |
| US1374889A (en) | Process of destructively decomposing liquids of high organic content and product of such process | |
| JP2011036854A (en) | Method for desulfurizing fluid and method for operating coal combustion system | |
| JPS5825492B2 (en) | Iousankabutsunojiyokiyohouhou | |
| CN105664692B (en) | SO in flue gas is removed in depth in a kind of calcium and magnesium fusion method2The method of coproduction crystal whisker of gypsum |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PC43 | Official registration of the transfer of the exclusive right without contract for inventions |
Effective date: 20190531 |
|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20191208 |