RU2496501C2 - Композиции, включающие антибиотик и кортикостероид - Google Patents
Композиции, включающие антибиотик и кортикостероид Download PDFInfo
- Publication number
- RU2496501C2 RU2496501C2 RU2010154083/15A RU2010154083A RU2496501C2 RU 2496501 C2 RU2496501 C2 RU 2496501C2 RU 2010154083/15 A RU2010154083/15 A RU 2010154083/15A RU 2010154083 A RU2010154083 A RU 2010154083A RU 2496501 C2 RU2496501 C2 RU 2496501C2
- Authority
- RU
- Russia
- Prior art keywords
- composition
- infection
- composition according
- acid
- treating
- Prior art date
Links
- 239000000203 mixture Substances 0.000 title claims abstract description 133
- 239000003246 corticosteroid Substances 0.000 title description 30
- 230000003115 biocidal effect Effects 0.000 title description 27
- 239000012453 solvate Substances 0.000 claims abstract description 34
- 235000014113 dietary fatty acids Nutrition 0.000 claims abstract description 29
- 239000000194 fatty acid Substances 0.000 claims abstract description 29
- 229930195729 fatty acid Natural products 0.000 claims abstract description 29
- 150000004665 fatty acids Chemical class 0.000 claims abstract description 28
- 241001465754 Metazoa Species 0.000 claims abstract description 25
- QIPQASLPWJVQMH-DTORHVGOSA-N Orbifloxacin Chemical compound C1[C@@H](C)N[C@@H](C)CN1C1=C(F)C(F)=C2C(=O)C(C(O)=O)=CN(C3CC3)C2=C1F QIPQASLPWJVQMH-DTORHVGOSA-N 0.000 claims abstract description 17
- 208000015181 infectious disease Diseases 0.000 claims abstract description 17
- 229960004780 orbifloxacin Drugs 0.000 claims abstract description 14
- 239000000725 suspension Substances 0.000 claims abstract description 13
- 125000004432 carbon atom Chemical group C* 0.000 claims abstract description 12
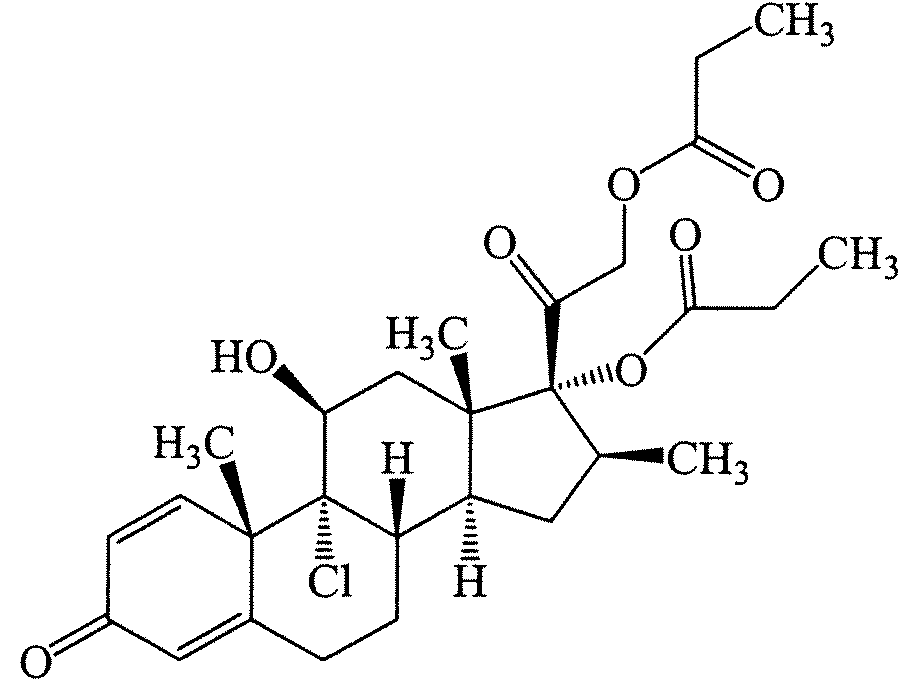
- WOFMFGQZHJDGCX-ZULDAHANSA-N mometasone furoate Chemical compound O([C@]1([C@@]2(C)C[C@H](O)[C@]3(Cl)[C@@]4(C)C=CC(=O)C=C4CC[C@H]3[C@@H]2C[C@H]1C)C(=O)CCl)C(=O)C1=CC=CO1 WOFMFGQZHJDGCX-ZULDAHANSA-N 0.000 claims abstract description 11
- 238000000034 method Methods 0.000 claims abstract description 10
- 229960002744 mometasone furoate Drugs 0.000 claims abstract description 10
- 239000008194 pharmaceutical composition Substances 0.000 claims abstract description 6
- 230000001225 therapeutic effect Effects 0.000 claims abstract description 6
- 239000003814 drug Substances 0.000 claims abstract description 5
- 238000002844 melting Methods 0.000 claims abstract description 5
- 230000008018 melting Effects 0.000 claims abstract description 5
- 150000003839 salts Chemical class 0.000 claims description 68
- -1 triazole salt Chemical class 0.000 claims description 41
- POULHZVOKOAJMA-UHFFFAOYSA-N dodecanoic acid Chemical compound CCCCCCCCCCCC(O)=O POULHZVOKOAJMA-UHFFFAOYSA-N 0.000 claims description 31
- 229940121375 antifungal agent Drugs 0.000 claims description 22
- 239000003429 antifungal agent Substances 0.000 claims description 19
- WRIDQFICGBMAFQ-UHFFFAOYSA-N (E)-8-Octadecenoic acid Natural products CCCCCCCCCC=CCCCCCCC(O)=O WRIDQFICGBMAFQ-UHFFFAOYSA-N 0.000 claims description 17
- LQJBNNIYVWPHFW-UHFFFAOYSA-N 20:1omega9c fatty acid Natural products CCCCCCCCCCC=CCCCCCCCC(O)=O LQJBNNIYVWPHFW-UHFFFAOYSA-N 0.000 claims description 17
- QSBYPNXLFMSGKH-UHFFFAOYSA-N 9-Heptadecensaeure Natural products CCCCCCCC=CCCCCCCCC(O)=O QSBYPNXLFMSGKH-UHFFFAOYSA-N 0.000 claims description 17
- 239000005642 Oleic acid Substances 0.000 claims description 17
- ZQPPMHVWECSIRJ-UHFFFAOYSA-N Oleic acid Natural products CCCCCCCCC=CCCCCCCCC(O)=O ZQPPMHVWECSIRJ-UHFFFAOYSA-N 0.000 claims description 17
- QXJSBBXBKPUZAA-UHFFFAOYSA-N isooleic acid Natural products CCCCCCCC=CCCCCCCCCC(O)=O QXJSBBXBKPUZAA-UHFFFAOYSA-N 0.000 claims description 17
- 239000005639 Lauric acid Substances 0.000 claims description 15
- RAGOYPUPXAKGKH-XAKZXMRKSA-N posaconazole Chemical compound O=C1N([C@H]([C@H](C)O)CC)N=CN1C1=CC=C(N2CCN(CC2)C=2C=CC(OC[C@H]3C[C@@](CN4N=CN=C4)(OC3)C=3C(=CC(F)=CC=3)F)=CC=2)C=C1 RAGOYPUPXAKGKH-XAKZXMRKSA-N 0.000 claims description 15
- 150000003852 triazoles Chemical class 0.000 claims description 15
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 claims description 14
- 239000002480 mineral oil Substances 0.000 claims description 13
- 235000010446 mineral oil Nutrition 0.000 claims description 13
- 229960001589 posaconazole Drugs 0.000 claims description 13
- 238000004140 cleaning Methods 0.000 claims description 9
- 208000005141 Otitis Diseases 0.000 claims description 8
- 208000019258 ear infection Diseases 0.000 claims description 8
- 241000282472 Canis lupus familiaris Species 0.000 claims description 7
- RFHAOTPXVQNOHP-UHFFFAOYSA-N fluconazole Chemical compound C1=NC=NN1CC(C=1C(=CC(F)=CC=1)F)(O)CN1C=NC=N1 RFHAOTPXVQNOHP-UHFFFAOYSA-N 0.000 claims description 4
- BLSQLHNBWJLIBQ-OZXSUGGESA-N (2R,4S)-terconazole Chemical compound C1CN(C(C)C)CCN1C(C=C1)=CC=C1OC[C@@H]1O[C@@](CN2N=CN=C2)(C=2C(=CC(Cl)=CC=2)Cl)OC1 BLSQLHNBWJLIBQ-OZXSUGGESA-N 0.000 claims description 3
- 238000004519 manufacturing process Methods 0.000 claims description 3
- 229960000580 terconazole Drugs 0.000 claims description 3
- VHVPQPYKVGDNFY-DFMJLFEVSA-N 2-[(2r)-butan-2-yl]-4-[4-[4-[4-[[(2r,4s)-2-(2,4-dichlorophenyl)-2-(1,2,4-triazol-1-ylmethyl)-1,3-dioxolan-4-yl]methoxy]phenyl]piperazin-1-yl]phenyl]-1,2,4-triazol-3-one Chemical compound O=C1N([C@H](C)CC)N=CN1C1=CC=C(N2CCN(CC2)C=2C=CC(OC[C@@H]3O[C@](CN4N=CN=C4)(OC3)C=3C(=CC(Cl)=CC=3)Cl)=CC=2)C=C1 VHVPQPYKVGDNFY-DFMJLFEVSA-N 0.000 claims description 2
- 229960004884 fluconazole Drugs 0.000 claims description 2
- 229960004130 itraconazole Drugs 0.000 claims description 2
- 150000004682 monohydrates Chemical class 0.000 claims description 2
- BCEHBSKCWLPMDN-MGPLVRAMSA-N voriconazole Chemical compound C1([C@H](C)[C@](O)(CN2N=CN=C2)C=2C(=CC(F)=CC=2)F)=NC=NC=C1F BCEHBSKCWLPMDN-MGPLVRAMSA-N 0.000 claims description 2
- HUADITLKOCMHSB-AVQIMAJZSA-N 2-butan-2-yl-4-[4-[4-[4-[[(2s,4r)-2-(2,4-difluorophenyl)-2-(1,2,4-triazol-1-ylmethyl)-1,3-dioxolan-4-yl]methoxy]phenyl]piperazin-1-yl]phenyl]-1,2,4-triazol-3-one Chemical compound O=C1N(C(C)CC)N=CN1C1=CC=C(N2CCN(CC2)C=2C=CC(OC[C@H]3O[C@@](CN4N=CN=C4)(OC3)C=3C(=CC(F)=CC=3)F)=CC=2)C=C1 HUADITLKOCMHSB-AVQIMAJZSA-N 0.000 claims 1
- 229950005137 saperconazole Drugs 0.000 claims 1
- 229960004740 voriconazole Drugs 0.000 claims 1
- 230000000694 effects Effects 0.000 abstract description 7
- 238000009472 formulation Methods 0.000 abstract description 3
- 238000003860 storage Methods 0.000 abstract description 2
- 239000000126 substance Substances 0.000 abstract description 2
- 208000001860 Eye Infections Diseases 0.000 abstract 1
- 229940079593 drug Drugs 0.000 abstract 1
- 208000011323 eye infectious disease Diseases 0.000 abstract 1
- 239000003242 anti bacterial agent Substances 0.000 description 33
- BYZXOYSEYWCLOK-UHFFFAOYSA-N 6-fluoro-1h-quinolin-4-one Chemical class C1=C(F)C=C2C(O)=CC=NC2=C1 BYZXOYSEYWCLOK-UHFFFAOYSA-N 0.000 description 22
- 229940088710 antibiotic agent Drugs 0.000 description 21
- 150000001875 compounds Chemical class 0.000 description 20
- 229960001664 mometasone Drugs 0.000 description 19
- 239000002253 acid Substances 0.000 description 17
- QLIIKPVHVRXHRI-CXSFZGCWSA-N mometasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(Cl)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CCl)(O)[C@@]1(C)C[C@@H]2O QLIIKPVHVRXHRI-CXSFZGCWSA-N 0.000 description 17
- 239000004615 ingredient Substances 0.000 description 15
- 239000000047 product Substances 0.000 description 15
- LKKVDASEMCCQFX-UHFFFAOYSA-N 6-fluoro-1h-1,8-naphthyridin-4-one Chemical class N1C=CC(=O)C2=CC(F)=CN=C21 LKKVDASEMCCQFX-UHFFFAOYSA-N 0.000 description 12
- 239000004480 active ingredient Substances 0.000 description 11
- 150000007524 organic acids Chemical class 0.000 description 11
- 229960001334 corticosteroids Drugs 0.000 description 10
- 239000000243 solution Substances 0.000 description 10
- 150000002460 imidazoles Chemical class 0.000 description 9
- 229960004123 mometasone furoate monohydrate Drugs 0.000 description 9
- 229920002125 Sokalan® Polymers 0.000 description 8
- 229940124307 fluoroquinolone Drugs 0.000 description 8
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 7
- 150000007513 acids Chemical class 0.000 description 7
- 239000002585 base Substances 0.000 description 7
- MYSWGUAQZAJSOK-UHFFFAOYSA-N ciprofloxacin Chemical compound C12=CC(N3CCNCC3)=C(F)C=C2C(=O)C(C(=O)O)=CN1C1CC1 MYSWGUAQZAJSOK-UHFFFAOYSA-N 0.000 description 7
- WVDDGKGOMKODPV-UHFFFAOYSA-N Benzyl alcohol Chemical compound OCC1=CC=CC=C1 WVDDGKGOMKODPV-UHFFFAOYSA-N 0.000 description 6
- 239000004215 Carbon black (E152) Substances 0.000 description 6
- BPFYOAJNDMUVBL-UHFFFAOYSA-N LSM-5799 Chemical compound C1CN(C)CCN1C1=C(F)C=C2C(=O)C(C(O)=O)=CN3N(C)COC1=C32 BPFYOAJNDMUVBL-UHFFFAOYSA-N 0.000 description 6
- 241000124008 Mammalia Species 0.000 description 6
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 6
- VNFPBHJOKIVQEB-UHFFFAOYSA-N clotrimazole Chemical compound ClC1=CC=CC=C1C(N1C=NC=C1)(C=1C=CC=CC=1)C1=CC=CC=C1 VNFPBHJOKIVQEB-UHFFFAOYSA-N 0.000 description 6
- 229930195733 hydrocarbon Natural products 0.000 description 6
- 150000002430 hydrocarbons Chemical class 0.000 description 6
- 235000005985 organic acids Nutrition 0.000 description 6
- 239000003755 preservative agent Substances 0.000 description 6
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 6
- GSDSWSVVBLHKDQ-UHFFFAOYSA-N 9-fluoro-3-methyl-10-(4-methylpiperazin-1-yl)-7-oxo-2,3-dihydro-7H-[1,4]oxazino[2,3,4-ij]quinoline-6-carboxylic acid Chemical compound FC1=CC(C(C(C(O)=O)=C2)=O)=C3N2C(C)COC3=C1N1CCN(C)CC1 GSDSWSVVBLHKDQ-UHFFFAOYSA-N 0.000 description 5
- NIXOWILDQLNWCW-UHFFFAOYSA-N Acrylic acid Chemical compound OC(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 5
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 5
- GSDSWSVVBLHKDQ-JTQLQIEISA-N Levofloxacin Chemical compound C([C@@H](N1C2=C(C(C(C(O)=O)=C1)=O)C=C1F)C)OC2=C1N1CCN(C)CC1 GSDSWSVVBLHKDQ-JTQLQIEISA-N 0.000 description 5
- 239000004698 Polyethylene Substances 0.000 description 5
- 230000015572 biosynthetic process Effects 0.000 description 5
- 239000003795 chemical substances by application Substances 0.000 description 5
- 239000000499 gel Substances 0.000 description 5
- 229960002531 marbofloxacin Drugs 0.000 description 5
- VQOXZBDYSJBXMA-NQTDYLQESA-N nystatin A1 Chemical compound O[C@H]1[C@@H](N)[C@H](O)[C@@H](C)O[C@H]1O[C@H]1/C=C/C=C/C=C/C=C/CC/C=C/C=C/[C@H](C)[C@@H](O)[C@@H](C)[C@H](C)OC(=O)C[C@H](O)C[C@H](O)C[C@H](O)CC[C@@H](O)[C@H](O)C[C@](O)(C[C@H](O)[C@H]2C(O)=O)O[C@H]2C1 VQOXZBDYSJBXMA-NQTDYLQESA-N 0.000 description 5
- 230000001717 pathogenic effect Effects 0.000 description 5
- 239000000546 pharmaceutical excipient Substances 0.000 description 5
- 229920000573 polyethylene Polymers 0.000 description 5
- XOFYZVNMUHMLCC-ZPOLXVRWSA-N prednisone Chemical compound O=C1C=C[C@]2(C)[C@H]3C(=O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 XOFYZVNMUHMLCC-ZPOLXVRWSA-N 0.000 description 5
- 239000011734 sodium Substances 0.000 description 5
- 235000015424 sodium Nutrition 0.000 description 5
- 229910052708 sodium Inorganic materials 0.000 description 5
- PHYFQTYBJUILEZ-IUPFWZBJSA-N triolein Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC(OC(=O)CCCCCCC\C=C/CCCCCCCC)COC(=O)CCCCCCC\C=C/CCCCCCCC PHYFQTYBJUILEZ-IUPFWZBJSA-N 0.000 description 5
- SPFYMRJSYKOXGV-UHFFFAOYSA-N Baytril Chemical compound C1CN(CC)CCN1C(C(=C1)F)=CC2=C1C(=O)C(C(O)=O)=CN2C1CC1 SPFYMRJSYKOXGV-UHFFFAOYSA-N 0.000 description 4
- KUVIULQEHSCUHY-XYWKZLDCSA-N Beclometasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(Cl)[C@@H]1[C@@H]1C[C@H](C)[C@@](C(=O)COC(=O)CC)(OC(=O)CC)[C@@]1(C)C[C@@H]2O KUVIULQEHSCUHY-XYWKZLDCSA-N 0.000 description 4
- WHNWPMSKXPGLAX-UHFFFAOYSA-N N-Vinyl-2-pyrrolidone Chemical compound C=CN1CCCC1=O WHNWPMSKXPGLAX-UHFFFAOYSA-N 0.000 description 4
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 4
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid group Chemical group C(C1=CC=CC=C1)(=O)O WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 4
- 229960001631 carbomer Drugs 0.000 description 4
- 229910052799 carbon Inorganic materials 0.000 description 4
- 239000001768 carboxy methyl cellulose Substances 0.000 description 4
- 239000007857 degradation product Substances 0.000 description 4
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 description 4
- 239000000945 filler Substances 0.000 description 4
- WMWTYOKRWGGJOA-CENSZEJFSA-N fluticasone propionate Chemical compound C1([C@@H](F)C2)=CC(=O)C=C[C@]1(C)[C@]1(F)[C@@H]2[C@@H]2C[C@@H](C)[C@@](C(=O)SCF)(OC(=O)CC)[C@@]2(C)C[C@@H]1O WMWTYOKRWGGJOA-CENSZEJFSA-N 0.000 description 4
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 4
- VMPHSYLJUKZBJJ-UHFFFAOYSA-N lauric acid triglyceride Natural products CCCCCCCCCCCC(=O)OCC(OC(=O)CCCCCCCCCCC)COC(=O)CCCCCCCCCCC VMPHSYLJUKZBJJ-UHFFFAOYSA-N 0.000 description 4
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 4
- 239000011976 maleic acid Substances 0.000 description 4
- 229940021182 non-steroidal anti-inflammatory drug Drugs 0.000 description 4
- OGJPXUAPXNRGGI-UHFFFAOYSA-N norfloxacin Chemical compound C1=C2N(CC)C=C(C(O)=O)C(=O)C2=CC(F)=C1N1CCNCC1 OGJPXUAPXNRGGI-UHFFFAOYSA-N 0.000 description 4
- 239000003883 ointment base Substances 0.000 description 4
- 150000002889 oleic acids Chemical class 0.000 description 4
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 4
- 244000052769 pathogen Species 0.000 description 4
- 230000002335 preservative effect Effects 0.000 description 4
- 239000000018 receptor agonist Substances 0.000 description 4
- 229940044601 receptor agonist Drugs 0.000 description 4
- HEMHJVSKTPXQMS-UHFFFAOYSA-M sodium hydroxide Substances [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 4
- 239000003381 stabilizer Substances 0.000 description 4
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 4
- XBHBWNFJWIASRO-UHFFFAOYSA-N 6-fluoro-1-(4-fluorophenyl)-4-oxo-7-(1-piperazinyl)-3-quinolinecarboxylic acid Chemical compound C12=CC(N3CCNCC3)=C(F)C=C2C(=O)C(C(=O)O)=CN1C1=CC=C(F)C=C1 XBHBWNFJWIASRO-UHFFFAOYSA-N 0.000 description 3
- 244000215068 Acacia senegal Species 0.000 description 3
- VOVIALXJUBGFJZ-KWVAZRHASA-N Budesonide Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@@H]2[C@@H]1[C@@H]1C[C@H]3OC(CCC)O[C@@]3(C(=O)CO)[C@@]1(C)C[C@@H]2O VOVIALXJUBGFJZ-KWVAZRHASA-N 0.000 description 3
- QMLVECGLEOSESV-RYUDHWBXSA-N Danofloxacin Chemical compound C([C@@H]1C[C@H]2CN1C)N2C(C(=CC=1C(=O)C(C(O)=O)=C2)F)=CC=1N2C1CC1 QMLVECGLEOSESV-RYUDHWBXSA-N 0.000 description 3
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 3
- 241000282326 Felis catus Species 0.000 description 3
- 229920000084 Gum arabic Polymers 0.000 description 3
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 3
- BYBLEWFAAKGYCD-UHFFFAOYSA-N Miconazole Chemical compound ClC1=CC(Cl)=CC=C1COC(C=1C(=CC(Cl)=CC=1)Cl)CN1C=NC=C1 BYBLEWFAAKGYCD-UHFFFAOYSA-N 0.000 description 3
- PWNMXPDKBYZCOO-UHFFFAOYSA-N Prulifloxacin Chemical compound C1=C2N3C(C)SC3=C(C(O)=O)C(=O)C2=CC(F)=C1N(CC1)CCN1CC=1OC(=O)OC=1C PWNMXPDKBYZCOO-UHFFFAOYSA-N 0.000 description 3
- 229920002472 Starch Polymers 0.000 description 3
- 229920001615 Tragacanth Polymers 0.000 description 3
- 235000010489 acacia gum Nutrition 0.000 description 3
- 239000000205 acacia gum Substances 0.000 description 3
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 3
- 230000000843 anti-fungal effect Effects 0.000 description 3
- 230000003110 anti-inflammatory effect Effects 0.000 description 3
- 239000004599 antimicrobial Substances 0.000 description 3
- 235000010233 benzoic acid Nutrition 0.000 description 3
- CIWBQSYVNNPZIQ-XYWKZLDCSA-N betamethasone dipropionate Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@H](C)[C@@](C(=O)COC(=O)CC)(OC(=O)CC)[C@@]1(C)C[C@@H]2O CIWBQSYVNNPZIQ-XYWKZLDCSA-N 0.000 description 3
- 230000015556 catabolic process Effects 0.000 description 3
- 238000000354 decomposition reaction Methods 0.000 description 3
- NOCJXYPHIIZEHN-UHFFFAOYSA-N difloxacin Chemical compound C1CN(C)CCN1C(C(=C1)F)=CC2=C1C(=O)C(C(O)=O)=CN2C1=CC=C(F)C=C1 NOCJXYPHIIZEHN-UHFFFAOYSA-N 0.000 description 3
- IDYZIJYBMGIQMJ-UHFFFAOYSA-N enoxacin Chemical compound N1=C2N(CC)C=C(C(O)=O)C(=O)C2=CC(F)=C1N1CCNCC1 IDYZIJYBMGIQMJ-UHFFFAOYSA-N 0.000 description 3
- 238000002474 experimental method Methods 0.000 description 3
- FEBLZLNTKCEFIT-VSXGLTOVSA-N fluocinolone acetonide Chemical compound C1([C@@H](F)C2)=CC(=O)C=C[C@]1(C)[C@]1(F)[C@@H]2[C@@H]2C[C@H]3OC(C)(C)O[C@@]3(C(=O)CO)[C@@]2(C)C[C@@H]1O FEBLZLNTKCEFIT-VSXGLTOVSA-N 0.000 description 3
- 229920001903 high density polyethylene Polymers 0.000 description 3
- 239000004700 high-density polyethylene Substances 0.000 description 3
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 3
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- ZEKZLJVOYLTDKK-UHFFFAOYSA-N lomefloxacin Chemical compound FC1=C2N(CC)C=C(C(O)=O)C(=O)C2=CC(F)=C1N1CCNC(C)C1 ZEKZLJVOYLTDKK-UHFFFAOYSA-N 0.000 description 3
- DMKSVUSAATWOCU-HROMYWEYSA-N loteprednol etabonate Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@@](C(=O)OCCl)(OC(=O)OCC)[C@@]1(C)C[C@@H]2O DMKSVUSAATWOCU-HROMYWEYSA-N 0.000 description 3
- 229920001684 low density polyethylene Polymers 0.000 description 3
- 239000004702 low-density polyethylene Substances 0.000 description 3
- 229910052751 metal Inorganic materials 0.000 description 3
- 239000002184 metal Substances 0.000 description 3
- 229920000609 methyl cellulose Polymers 0.000 description 3
- 235000010981 methylcellulose Nutrition 0.000 description 3
- 239000001923 methylcellulose Substances 0.000 description 3
- LXCFILQKKLGQFO-UHFFFAOYSA-N methylparaben Chemical compound COC(=O)C1=CC=C(O)C=C1 LXCFILQKKLGQFO-UHFFFAOYSA-N 0.000 description 3
- FABPRXSRWADJSP-MEDUHNTESA-N moxifloxacin Chemical compound COC1=C(N2C[C@H]3NCCC[C@H]3C2)C(F)=CC(C(C(C(O)=O)=C2)=O)=C1N2C1CC1 FABPRXSRWADJSP-MEDUHNTESA-N 0.000 description 3
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 3
- VHSIAYLBCLUAFT-UHFFFAOYSA-N n-[3-acetyl-6-(4-chlorophenyl)-7-(2,4-dichlorophenyl)-1-methyl-2-oxo-1,8-naphthyridin-4-yl]acetamide Chemical compound C=1C=C(Cl)C=CC=1C=1C=C2C(NC(=O)C)=C(C(C)=O)C(=O)N(C)C2=NC=1C1=CC=C(Cl)C=C1Cl VHSIAYLBCLUAFT-UHFFFAOYSA-N 0.000 description 3
- JYJTVFIEFKZWCJ-UHFFFAOYSA-N nadifloxacin Chemical compound FC1=CC(C(C(C(O)=O)=C2)=O)=C3N2C(C)CCC3=C1N1CCC(O)CC1 JYJTVFIEFKZWCJ-UHFFFAOYSA-N 0.000 description 3
- 229960003808 nadifloxacin Drugs 0.000 description 3
- 239000000041 non-steroidal anti-inflammatory agent Substances 0.000 description 3
- 229960000988 nystatin Drugs 0.000 description 3
- 229960001699 ofloxacin Drugs 0.000 description 3
- 150000007530 organic bases Chemical class 0.000 description 3
- 229940056360 penicillin g Drugs 0.000 description 3
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 3
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 3
- 229940069328 povidone Drugs 0.000 description 3
- QELSKZZBTMNZEB-UHFFFAOYSA-N propylparaben Chemical compound CCCOC(=O)C1=CC=C(O)C=C1 QELSKZZBTMNZEB-UHFFFAOYSA-N 0.000 description 3
- 150000007660 quinolones Chemical class 0.000 description 3
- 229960004889 salicylic acid Drugs 0.000 description 3
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 3
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 3
- 235000019698 starch Nutrition 0.000 description 3
- 239000008107 starch Substances 0.000 description 3
- 239000002562 thickening agent Substances 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- 229920001285 xanthan gum Polymers 0.000 description 3
- 235000010493 xanthan gum Nutrition 0.000 description 3
- 239000000230 xanthan gum Substances 0.000 description 3
- 229940082509 xanthan gum Drugs 0.000 description 3
- XMAYWYJOQHXEEK-ZEQKJWHPSA-N (2S,4R)-ketoconazole Chemical compound C1CN(C(=O)C)CCN1C(C=C1)=CC=C1OC[C@H]1O[C@](CN2C=NC=C2)(C=2C(=CC(Cl)=CC=2)Cl)OC1 XMAYWYJOQHXEEK-ZEQKJWHPSA-N 0.000 description 2
- LNAZSHAWQACDHT-XIYTZBAFSA-N (2r,3r,4s,5r,6s)-4,5-dimethoxy-2-(methoxymethyl)-3-[(2s,3r,4s,5r,6r)-3,4,5-trimethoxy-6-(methoxymethyl)oxan-2-yl]oxy-6-[(2r,3r,4s,5r,6r)-4,5,6-trimethoxy-2-(methoxymethyl)oxan-3-yl]oxyoxane Chemical compound CO[C@@H]1[C@@H](OC)[C@H](OC)[C@@H](COC)O[C@H]1O[C@H]1[C@H](OC)[C@@H](OC)[C@H](O[C@H]2[C@@H]([C@@H](OC)[C@H](OC)O[C@@H]2COC)OC)O[C@@H]1COC LNAZSHAWQACDHT-XIYTZBAFSA-N 0.000 description 2
- XUBOMFCQGDBHNK-JTQLQIEISA-N (S)-gatifloxacin Chemical compound FC1=CC(C(C(C(O)=O)=CN2C3CC3)=O)=C2C(OC)=C1N1CCN[C@@H](C)C1 XUBOMFCQGDBHNK-JTQLQIEISA-N 0.000 description 2
- LEZWWPYKPKIXLL-UHFFFAOYSA-N 1-{2-(4-chlorobenzyloxy)-2-(2,4-dichlorophenyl)ethyl}imidazole Chemical compound C1=CC(Cl)=CC=C1COC(C=1C(=CC(Cl)=CC=1)Cl)CN1C=NC=C1 LEZWWPYKPKIXLL-UHFFFAOYSA-N 0.000 description 2
- JLGKQTAYUIMGRK-UHFFFAOYSA-N 1-{2-[(7-chloro-1-benzothiophen-3-yl)methoxy]-2-(2,4-dichlorophenyl)ethyl}imidazole Chemical compound ClC1=CC(Cl)=CC=C1C(OCC=1C2=CC=CC(Cl)=C2SC=1)CN1C=NC=C1 JLGKQTAYUIMGRK-UHFFFAOYSA-N 0.000 description 2
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 2
- SMNDYUVBFMFKNZ-UHFFFAOYSA-N 2-furoic acid Chemical compound OC(=O)C1=CC=CO1 SMNDYUVBFMFKNZ-UHFFFAOYSA-N 0.000 description 2
- CDOUZKKFHVEKRI-UHFFFAOYSA-N 3-bromo-n-[(prop-2-enoylamino)methyl]propanamide Chemical compound BrCCC(=O)NCNC(=O)C=C CDOUZKKFHVEKRI-UHFFFAOYSA-N 0.000 description 2
- VHRSUDSXCMQTMA-PJHHCJLFSA-N 6alpha-methylprednisolone Chemical compound C([C@@]12C)=CC(=O)C=C1[C@@H](C)C[C@@H]1[C@@H]2[C@@H](O)C[C@]2(C)[C@@](O)(C(=O)CO)CC[C@H]21 VHRSUDSXCMQTMA-PJHHCJLFSA-N 0.000 description 2
- 244000144927 Aloe barbadensis Species 0.000 description 2
- 235000002961 Aloe barbadensis Nutrition 0.000 description 2
- RUXPNBWPIRDVTH-UHFFFAOYSA-N Amifloxacin Chemical compound C1=C2N(NC)C=C(C(O)=O)C(=O)C2=CC(F)=C1N1CCN(C)CC1 RUXPNBWPIRDVTH-UHFFFAOYSA-N 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- 241000416162 Astragalus gummifer Species 0.000 description 2
- 239000005711 Benzoic acid Substances 0.000 description 2
- 0 C[C@@]1C(C2)N(C)CC1*2c(cc(*(C1CC1)C=C(C(O)=O)C1=O)c1c1)c1F Chemical compound C[C@@]1C(C2)N(C)CC1*2c(cc(*(C1CC1)C=C(C(O)=O)C1=O)c1c1)c1F 0.000 description 2
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 2
- GNWUOVJNSFPWDD-XMZRARIVSA-M Cefoxitin sodium Chemical compound [Na+].N([C@]1(OC)C(N2C(=C(COC(N)=O)CS[C@@H]21)C([O-])=O)=O)C(=O)CC1=CC=CS1 GNWUOVJNSFPWDD-XMZRARIVSA-M 0.000 description 2
- LUKZNWIVRBCLON-GXOBDPJESA-N Ciclesonide Chemical compound C1([C@H]2O[C@@]3([C@H](O2)C[C@@H]2[C@@]3(C[C@H](O)[C@@H]3[C@@]4(C)C=CC(=O)C=C4CC[C@H]32)C)C(=O)COC(=O)C(C)C)CCCCC1 LUKZNWIVRBCLON-GXOBDPJESA-N 0.000 description 2
- ULGZDMOVFRHVEP-RWJQBGPGSA-N Erythromycin Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)C(=O)[C@H](C)C[C@@](C)(O)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 ULGZDMOVFRHVEP-RWJQBGPGSA-N 0.000 description 2
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 2
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical compound C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 description 2
- 241000233866 Fungi Species 0.000 description 2
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 2
- AIJTTZAVMXIJGM-UHFFFAOYSA-N Grepafloxacin Chemical compound C1CNC(C)CN1C(C(=C1C)F)=CC2=C1C(=O)C(C(O)=O)=CN2C1CC1 AIJTTZAVMXIJGM-UHFFFAOYSA-N 0.000 description 2
- 229920002907 Guar gum Polymers 0.000 description 2
- XAGMUUZPGZWTRP-ZETCQYMHSA-N LSM-5745 Chemical compound C([C@@H](N1C2=C(C(C(C(O)=O)=C1)=O)C=C1F)C)OC2=C1C1(N)CC1 XAGMUUZPGZWTRP-ZETCQYMHSA-N 0.000 description 2
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 2
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 2
- MBBZMMPHUWSWHV-BDVNFPICSA-N N-methylglucamine Chemical compound CNC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO MBBZMMPHUWSWHV-BDVNFPICSA-N 0.000 description 2
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 2
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 2
- NJCJBUHJQLFDSW-UHFFFAOYSA-N Rufloxacin Chemical compound C1CN(C)CCN1C1=C(F)C=C2C(=O)C(C(O)=O)=CN3CCSC1=C32 NJCJBUHJQLFDSW-UHFFFAOYSA-N 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- 125000001931 aliphatic group Chemical group 0.000 description 2
- 235000011399 aloe vera Nutrition 0.000 description 2
- 229910052782 aluminium Inorganic materials 0.000 description 2
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 2
- 229950009484 amifloxacin Drugs 0.000 description 2
- AVKUERGKIZMTKX-NJBDSQKTSA-N ampicillin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)=CC=CC=C1 AVKUERGKIZMTKX-NJBDSQKTSA-N 0.000 description 2
- RWZYAGGXGHYGMB-UHFFFAOYSA-N anthranilic acid Chemical compound NC1=CC=CC=C1C(O)=O RWZYAGGXGHYGMB-UHFFFAOYSA-N 0.000 description 2
- 230000001139 anti-pruritic effect Effects 0.000 description 2
- 229940125715 antihistaminic agent Drugs 0.000 description 2
- 239000000739 antihistaminic agent Substances 0.000 description 2
- 239000003908 antipruritic agent Substances 0.000 description 2
- 235000019445 benzyl alcohol Nutrition 0.000 description 2
- 229960001102 betamethasone dipropionate Drugs 0.000 description 2
- 239000011230 binding agent Substances 0.000 description 2
- 150000001649 bromium compounds Chemical class 0.000 description 2
- OSGAYBCDTDRGGQ-UHFFFAOYSA-L calcium sulfate Chemical compound [Ca+2].[O-]S([O-])(=O)=O OSGAYBCDTDRGGQ-UHFFFAOYSA-L 0.000 description 2
- 229960003669 carbenicillin Drugs 0.000 description 2
- FPPNZSSZRUTDAP-UWFZAAFLSA-N carbenicillin Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)C(C(O)=O)C1=CC=CC=C1 FPPNZSSZRUTDAP-UWFZAAFLSA-N 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- NBFNMSULHIODTC-CYJZLJNKSA-N cefadroxil monohydrate Chemical compound O.C1([C@@H](N)C(=O)N[C@H]2[C@@H]3N(C2=O)C(=C(CS3)C)C(O)=O)=CC=C(O)C=C1 NBFNMSULHIODTC-CYJZLJNKSA-N 0.000 description 2
- SNBUBQHDYVFSQF-HIFRSBDPSA-N cefmetazole Chemical compound S([C@@H]1[C@@](C(N1C=1C(O)=O)=O)(NC(=O)CSCC#N)OC)CC=1CSC1=NN=NN1C SNBUBQHDYVFSQF-HIFRSBDPSA-N 0.000 description 2
- AZZMGZXNTDTSME-JUZDKLSSSA-M cefotaxime sodium Chemical compound [Na+].N([C@@H]1C(N2C(=C(COC(C)=O)CS[C@@H]21)C([O-])=O)=O)C(=O)\C(=N/OC)C1=CSC(N)=N1 AZZMGZXNTDTSME-JUZDKLSSSA-M 0.000 description 2
- 238000002512 chemotherapy Methods 0.000 description 2
- 229960005091 chloramphenicol Drugs 0.000 description 2
- WIIZWVCIJKGZOK-RKDXNWHRSA-N chloramphenicol Chemical compound ClC(Cl)C(=O)N[C@H](CO)[C@H](O)C1=CC=C([N+]([O-])=O)C=C1 WIIZWVCIJKGZOK-RKDXNWHRSA-N 0.000 description 2
- OSASVXMJTNOKOY-UHFFFAOYSA-N chlorobutanol Chemical compound CC(C)(O)C(Cl)(Cl)Cl OSASVXMJTNOKOY-UHFFFAOYSA-N 0.000 description 2
- 229960003405 ciprofloxacin Drugs 0.000 description 2
- QGPKADBNRMWEQR-UHFFFAOYSA-N clinafloxacin Chemical compound C1C(N)CCN1C1=C(F)C=C2C(=O)C(C(O)=O)=CN(C3CC3)C2=C1Cl QGPKADBNRMWEQR-UHFFFAOYSA-N 0.000 description 2
- 229950001320 clinafloxacin Drugs 0.000 description 2
- 238000001816 cooling Methods 0.000 description 2
- 229920001577 copolymer Polymers 0.000 description 2
- 229960004385 danofloxacin Drugs 0.000 description 2
- 229950001733 difloxacin Drugs 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 2
- 235000019329 dioctyl sodium sulphosuccinate Nutrition 0.000 description 2
- 239000007884 disintegrant Substances 0.000 description 2
- 210000000613 ear canal Anatomy 0.000 description 2
- 229960002549 enoxacin Drugs 0.000 description 2
- 229960000740 enrofloxacin Drugs 0.000 description 2
- 239000000796 flavoring agent Substances 0.000 description 2
- 235000019634 flavors Nutrition 0.000 description 2
- 229960003306 fleroxacin Drugs 0.000 description 2
- XBJBPGROQZJDOJ-UHFFFAOYSA-N fleroxacin Chemical compound C1CN(C)CCN1C1=C(F)C=C2C(=O)C(C(O)=O)=CN(CCF)C2=C1F XBJBPGROQZJDOJ-UHFFFAOYSA-N 0.000 description 2
- XTULMSXFIHGYFS-VLSRWLAYSA-N fluticasone furoate Chemical compound O([C@]1([C@@]2(C)C[C@H](O)[C@]3(F)[C@@]4(C)C=CC(=O)C=C4[C@@H](F)C[C@H]3[C@@H]2C[C@H]1C)C(=O)SCF)C(=O)C1=CC=CO1 XTULMSXFIHGYFS-VLSRWLAYSA-N 0.000 description 2
- 229960000289 fluticasone propionate Drugs 0.000 description 2
- NJDRXTDGYFKORP-LLVKDONJSA-N garenoxacin Chemical compound N([C@@H](C1=CC=2)C)CC1=CC=2C(C=1OC(F)F)=CC=C(C(C(C(O)=O)=C2)=O)C=1N2C1CC1 NJDRXTDGYFKORP-LLVKDONJSA-N 0.000 description 2
- 229960001430 garenoxacin Drugs 0.000 description 2
- XUBOMFCQGDBHNK-UHFFFAOYSA-N gatifloxacin Chemical compound FC1=CC(C(C(C(O)=O)=CN2C3CC3)=O)=C2C(OC)=C1N1CCNC(C)C1 XUBOMFCQGDBHNK-UHFFFAOYSA-N 0.000 description 2
- 229960003923 gatifloxacin Drugs 0.000 description 2
- 235000010417 guar gum Nutrition 0.000 description 2
- 239000000665 guar gum Substances 0.000 description 2
- 229960002154 guar gum Drugs 0.000 description 2
- 229940071676 hydroxypropylcellulose Drugs 0.000 description 2
- DXKRGNXUIRKXNR-UHFFFAOYSA-N ibafloxacin Chemical compound C1CC(C)N2C=C(C(O)=O)C(=O)C3=C2C1=C(C)C(F)=C3 DXKRGNXUIRKXNR-UHFFFAOYSA-N 0.000 description 2
- 229950007954 ibafloxacin Drugs 0.000 description 2
- 150000004694 iodide salts Chemical class 0.000 description 2
- 239000004310 lactic acid Substances 0.000 description 2
- 235000014655 lactic acid Nutrition 0.000 description 2
- 229960003376 levofloxacin Drugs 0.000 description 2
- 229960002422 lomefloxacin Drugs 0.000 description 2
- 239000000314 lubricant Substances 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 235000010270 methyl p-hydroxybenzoate Nutrition 0.000 description 2
- 239000004292 methyl p-hydroxybenzoate Substances 0.000 description 2
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 2
- 239000008108 microcrystalline cellulose Substances 0.000 description 2
- 229940016286 microcrystalline cellulose Drugs 0.000 description 2
- 150000007522 mineralic acids Chemical class 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- VWOIKFDZQQLJBJ-DTQAZKPQSA-N neticonazole Chemical compound CCCCCOC1=CC=CC=C1\C(=C/SC)N1C=NC=C1 VWOIKFDZQQLJBJ-DTQAZKPQSA-N 0.000 description 2
- 239000003921 oil Substances 0.000 description 2
- 235000019198 oils Nutrition 0.000 description 2
- 239000002674 ointment Substances 0.000 description 2
- QRJJEGAJXVEBNE-HKOYGPOVSA-N oxiconazole Chemical compound ClC1=CC(Cl)=CC=C1CO\N=C(C=1C(=CC(Cl)=CC=1)Cl)/CN1C=NC=C1 QRJJEGAJXVEBNE-HKOYGPOVSA-N 0.000 description 2
- 229960002625 pazufloxacin Drugs 0.000 description 2
- 230000000704 physical effect Effects 0.000 description 2
- WCMIIGXFCMNQDS-IDYPWDAWSA-M piperacillin sodium Chemical compound [Na+].O=C1C(=O)N(CC)CCN1C(=O)N[C@H](C=1C=CC=CC=1)C(=O)N[C@@H]1C(=O)N2[C@@H](C([O-])=O)C(C)(C)S[C@@H]21 WCMIIGXFCMNQDS-IDYPWDAWSA-M 0.000 description 2
- 229910052700 potassium Inorganic materials 0.000 description 2
- 239000011591 potassium Substances 0.000 description 2
- 229960004618 prednisone Drugs 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 235000010232 propyl p-hydroxybenzoate Nutrition 0.000 description 2
- 239000004405 propyl p-hydroxybenzoate Substances 0.000 description 2
- 229960001224 prulifloxacin Drugs 0.000 description 2
- LISFMEBWQUVKPJ-UHFFFAOYSA-N quinolin-2-ol Chemical compound C1=CC=C2NC(=O)C=CC2=C1 LISFMEBWQUVKPJ-UHFFFAOYSA-N 0.000 description 2
- 229960004062 rufloxacin Drugs 0.000 description 2
- 229950007734 sarafloxacin Drugs 0.000 description 2
- 229920006395 saturated elastomer Polymers 0.000 description 2
- 235000011121 sodium hydroxide Nutrition 0.000 description 2
- 235000010199 sorbic acid Nutrition 0.000 description 2
- 239000004334 sorbic acid Substances 0.000 description 2
- 229940075582 sorbic acid Drugs 0.000 description 2
- WSWCOQWTEOXDQX-MQQKCMAXSA-N sorbic acid group Chemical group C(\C=C\C=C\C)(=O)O WSWCOQWTEOXDQX-MQQKCMAXSA-N 0.000 description 2
- DZZWHBIBMUVIIW-DTORHVGOSA-N sparfloxacin Chemical compound C1[C@@H](C)N[C@@H](C)CN1C1=C(F)C(N)=C2C(=O)C(C(O)=O)=CN(C3CC3)C2=C1F DZZWHBIBMUVIIW-DTORHVGOSA-N 0.000 description 2
- 239000005720 sucrose Substances 0.000 description 2
- 239000004094 surface-active agent Substances 0.000 description 2
- OTVAEFIXJLOWRX-NXEZZACHSA-N thiamphenicol Chemical compound CS(=O)(=O)C1=CC=C([C@@H](O)[C@@H](CO)NC(=O)C(Cl)Cl)C=C1 OTVAEFIXJLOWRX-NXEZZACHSA-N 0.000 description 2
- 229960003053 thiamphenicol Drugs 0.000 description 2
- 235000010487 tragacanth Nutrition 0.000 description 2
- 239000000196 tragacanth Substances 0.000 description 2
- 229940116362 tragacanth Drugs 0.000 description 2
- YNDXUCZADRHECN-JNQJZLCISA-N triamcinolone acetonide Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@H]3OC(C)(C)O[C@@]3(C(=O)CO)[C@@]1(C)C[C@@H]2O YNDXUCZADRHECN-JNQJZLCISA-N 0.000 description 2
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical class [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 2
- GETQZCLCWQTVFV-UHFFFAOYSA-N trimethylamine Chemical compound CN(C)C GETQZCLCWQTVFV-UHFFFAOYSA-N 0.000 description 2
- 229960000497 trovafloxacin Drugs 0.000 description 2
- WVPSKSLAZQPAKQ-CDMJZVDBSA-N trovafloxacin Chemical compound C([C@H]1[C@@H]([C@H]1C1)N)N1C(C(=CC=1C(=O)C(C(O)=O)=C2)F)=NC=1N2C1=CC=C(F)C=C1F WVPSKSLAZQPAKQ-CDMJZVDBSA-N 0.000 description 2
- JETQIUPBHQNHNZ-NJBDSQKTSA-N (2s,5r,6r)-3,3-dimethyl-7-oxo-6-[[(2r)-2-phenyl-2-sulfoacetyl]amino]-4-thia-1-azabicyclo[3.2.0]heptane-2-carboxylic acid Chemical compound C1([C@H](C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)S(O)(=O)=O)=CC=CC=C1 JETQIUPBHQNHNZ-NJBDSQKTSA-N 0.000 description 1
- DAVPSCAAXXVSFU-ALEPSDHESA-N (2s,5r,6r)-6-bromo-3,3-dimethyl-7-oxo-4-thia-1-azabicyclo[3.2.0]heptane-2-carboxylic acid Chemical compound OC(=O)[C@H]1C(C)(C)S[C@@H]2[C@H](Br)C(=O)N21 DAVPSCAAXXVSFU-ALEPSDHESA-N 0.000 description 1
- ALYUMNAHLSSTOU-CIRGZYLNSA-N (6r,7r)-7-[[(2r)-2-amino-2-(4-hydroxyphenyl)acetyl]amino]-8-oxo-3-[(e)-prop-1-enyl]-5-thia-1-azabicyclo[4.2.0]oct-2-ene-2-carboxylic acid;hydrate Chemical compound O.C1([C@@H](N)C(=O)N[C@H]2[C@@H]3N(C2=O)C(=C(CS3)/C=C/C)C(O)=O)=CC=C(O)C=C1 ALYUMNAHLSSTOU-CIRGZYLNSA-N 0.000 description 1
- WKJGTOYAEQDNIA-IOOZKYRYSA-N (6r,7r)-7-[[(2r)-2-amino-2-phenylacetyl]amino]-3-chloro-8-oxo-5-thia-1-azabicyclo[4.2.0]oct-2-ene-2-carboxylic acid;hydrate Chemical compound O.C1([C@H](C(=O)N[C@@H]2C(N3C(=C(Cl)CS[C@@H]32)C(O)=O)=O)N)=CC=CC=C1 WKJGTOYAEQDNIA-IOOZKYRYSA-N 0.000 description 1
- MMRINLZOZVAPDZ-LSGRDSQZSA-N (6r,7r)-7-[[(2z)-2-(2-amino-1,3-thiazol-4-yl)-2-methoxyiminoacetyl]amino]-3-[(1-methylpyrrolidin-1-ium-1-yl)methyl]-8-oxo-5-thia-1-azabicyclo[4.2.0]oct-2-ene-2-carboxylic acid;chloride Chemical compound Cl.S([C@@H]1[C@@H](C(N1C=1C([O-])=O)=O)NC(=O)\C(=N/OC)C=2N=C(N)SC=2)CC=1C[N+]1(C)CCCC1 MMRINLZOZVAPDZ-LSGRDSQZSA-N 0.000 description 1
- YWKJNRNSJKEFMK-PQFQYKRASA-N (6r,7r)-7-[[(2z)-2-(2-amino-1,3-thiazol-4-yl)-2-methoxyiminoacetyl]amino]-8-oxo-3-(5,6,7,8-tetrahydroquinolin-1-ium-1-ylmethyl)-5-thia-1-azabicyclo[4.2.0]oct-2-ene-2-carboxylate Chemical compound N([C@@H]1C(N2C(=C(C[N+]=3C=4CCCCC=4C=CC=3)CS[C@@H]21)C([O-])=O)=O)C(=O)\C(=N/OC)C1=CSC(N)=N1 YWKJNRNSJKEFMK-PQFQYKRASA-N 0.000 description 1
- GPYKKBAAPVOCIW-HSASPSRMSA-N (6r,7s)-7-[[(2r)-2-amino-2-phenylacetyl]amino]-3-chloro-8-oxo-1-azabicyclo[4.2.0]oct-2-ene-2-carboxylic acid;hydrate Chemical compound O.C1([C@H](C(=O)N[C@@H]2C(N3C(=C(Cl)CC[C@@H]32)C(O)=O)=O)N)=CC=CC=C1 GPYKKBAAPVOCIW-HSASPSRMSA-N 0.000 description 1
- SYVFBJQHOGXAMY-XUCMERPOSA-N (8s,9s,10r,13s,14s,17s)-10,13-dimethyl-17-propanoyl-6,7,8,9,11,12,14,15,16,17-decahydrocyclopenta[a]phenanthren-3-one Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H](C(=O)CC)[C@@]1(C)CC2 SYVFBJQHOGXAMY-XUCMERPOSA-N 0.000 description 1
- MPIPASJGOJYODL-SFHVURJKSA-N (R)-isoconazole Chemical compound ClC1=CC(Cl)=CC=C1[C@@H](OCC=1C(=CC=CC=1Cl)Cl)CN1C=NC=C1 MPIPASJGOJYODL-SFHVURJKSA-N 0.000 description 1
- QKDHBVNJCZBTMR-LLVKDONJSA-N (R)-temafloxacin Chemical compound C1CN[C@H](C)CN1C(C(=C1)F)=CC2=C1C(=O)C(C(O)=O)=CN2C1=CC=C(F)C=C1F QKDHBVNJCZBTMR-LLVKDONJSA-N 0.000 description 1
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- RKDVKSZUMVYZHH-UHFFFAOYSA-N 1,4-dioxane-2,5-dione Chemical compound O=C1COC(=O)CO1 RKDVKSZUMVYZHH-UHFFFAOYSA-N 0.000 description 1
- QKDHBVNJCZBTMR-UHFFFAOYSA-N 1-(2,4-difluorophenyl)-6-fluoro-7-(3-methylpiperazin-1-yl)-4-oxo-1,4-dihydroquinoline-3-carboxylic acid Chemical compound C1CNC(C)CN1C(C(=C1)F)=CC2=C1C(=O)C(C(O)=O)=CN2C1=CC=C(F)C=C1F QKDHBVNJCZBTMR-UHFFFAOYSA-N 0.000 description 1
- VFWCMGCRMGJXDK-UHFFFAOYSA-N 1-chlorobutane Chemical class CCCCCl VFWCMGCRMGJXDK-UHFFFAOYSA-N 0.000 description 1
- VUQPJRPDRDVQMN-UHFFFAOYSA-N 1-chlorooctadecane Chemical class CCCCCCCCCCCCCCCCCCCl VUQPJRPDRDVQMN-UHFFFAOYSA-N 0.000 description 1
- IXPNQXFRVYWDDI-UHFFFAOYSA-N 1-methyl-2,4-dioxo-1,3-diazinane-5-carboximidamide Chemical compound CN1CC(C(N)=N)C(=O)NC1=O IXPNQXFRVYWDDI-UHFFFAOYSA-N 0.000 description 1
- OVYMWJFNQQOJBU-UHFFFAOYSA-N 1-octanoyloxypropan-2-yl octanoate Chemical compound CCCCCCCC(=O)OCC(C)OC(=O)CCCCCCC OVYMWJFNQQOJBU-UHFFFAOYSA-N 0.000 description 1
- MPIPASJGOJYODL-UHFFFAOYSA-N 1-{2-[(2,6-dichlorobenzyl)oxy]-2-(2,4-dichlorophenyl)ethyl}imidazole Chemical compound ClC1=CC(Cl)=CC=C1C(OCC=1C(=CC=CC=1Cl)Cl)CN1C=NC=C1 MPIPASJGOJYODL-UHFFFAOYSA-N 0.000 description 1
- QXHHHPZILQDDPS-UHFFFAOYSA-N 1-{2-[(2-chloro-3-thienyl)methoxy]-2-(2,4-dichlorophenyl)ethyl}imidazole Chemical compound S1C=CC(COC(CN2C=NC=C2)C=2C(=CC(Cl)=CC=2)Cl)=C1Cl QXHHHPZILQDDPS-UHFFFAOYSA-N 0.000 description 1
- AFNXATANNDIXLG-UHFFFAOYSA-N 1-{2-[(4-chlorobenzyl)sulfanyl]-2-(2,4-dichlorophenyl)ethyl}-1H-imidazole Chemical compound C1=CC(Cl)=CC=C1CSC(C=1C(=CC(Cl)=CC=1)Cl)CN1C=NC=C1 AFNXATANNDIXLG-UHFFFAOYSA-N 0.000 description 1
- SMZOUWXMTYCWNB-UHFFFAOYSA-N 2-(2-methoxy-5-methylphenyl)ethanamine Chemical compound COC1=CC=C(C)C=C1CCN SMZOUWXMTYCWNB-UHFFFAOYSA-N 0.000 description 1
- KGWHMDCQVDMTNZ-UHFFFAOYSA-N 2-(butylcarbamoylamino)acetic acid Chemical compound CCCCNC(=O)NCC(O)=O KGWHMDCQVDMTNZ-UHFFFAOYSA-N 0.000 description 1
- TWJNQYPJQDRXPH-UHFFFAOYSA-N 2-cyanobenzohydrazide Chemical compound NNC(=O)C1=CC=CC=C1C#N TWJNQYPJQDRXPH-UHFFFAOYSA-N 0.000 description 1
- NFIHXTUNNGIYRF-UHFFFAOYSA-N 2-decanoyloxypropyl decanoate Chemical compound CCCCCCCCCC(=O)OCC(C)OC(=O)CCCCCCCCC NFIHXTUNNGIYRF-UHFFFAOYSA-N 0.000 description 1
- SMNDYUVBFMFKNZ-UHFFFAOYSA-M 2-furoate Chemical compound [O-]C(=O)C1=CC=CO1 SMNDYUVBFMFKNZ-UHFFFAOYSA-M 0.000 description 1
- WMPPDTMATNBGJN-UHFFFAOYSA-N 2-phenylethylbromide Chemical class BrCCC1=CC=CC=C1 WMPPDTMATNBGJN-UHFFFAOYSA-N 0.000 description 1
- 229940090248 4-hydroxybenzoic acid Drugs 0.000 description 1
- UHPMCKVQTMMPCG-UHFFFAOYSA-N 5,8-dihydroxy-2-methoxy-6-methyl-7-(2-oxopropyl)naphthalene-1,4-dione Chemical compound CC1=C(CC(C)=O)C(O)=C2C(=O)C(OC)=CC(=O)C2=C1O UHPMCKVQTMMPCG-UHFFFAOYSA-N 0.000 description 1
- WNPVZANXRCPJPW-UHFFFAOYSA-N 5-[isocyano-(4-methylphenyl)sulfonylmethyl]-1,2,3-trimethoxybenzene Chemical compound COC1=C(OC)C(OC)=CC(C([N+]#[C-])S(=O)(=O)C=2C=CC(C)=CC=2)=C1 WNPVZANXRCPJPW-UHFFFAOYSA-N 0.000 description 1
- KNWODGJQLCISLC-UHFFFAOYSA-N 6-fluoro-1-(4-fluorophenyl)-4-oxo-7-piperazin-1-ylquinoline-3-carboxylic acid;hydron;chloride Chemical compound Cl.C12=CC(N3CCNCC3)=C(F)C=C2C(=O)C(C(=O)O)=CN1C1=CC=C(F)C=C1 KNWODGJQLCISLC-UHFFFAOYSA-N 0.000 description 1
- WUWFMDMBOJLQIV-UHFFFAOYSA-N 7-(3-aminopyrrolidin-1-yl)-1-(2,4-difluorophenyl)-6-fluoro-4-oxo-1,4-dihydro-1,8-naphthyridine-3-carboxylic acid Chemical compound C1C(N)CCN1C(C(=C1)F)=NC2=C1C(=O)C(C(O)=O)=CN2C1=CC=C(F)C=C1F WUWFMDMBOJLQIV-UHFFFAOYSA-N 0.000 description 1
- MPORYQCGWFQFLA-ONPDANIMSA-N 7-[(7s)-7-amino-5-azaspiro[2.4]heptan-5-yl]-8-chloro-6-fluoro-1-[(1r,2s)-2-fluorocyclopropyl]-4-oxoquinoline-3-carboxylic acid;trihydrate Chemical compound O.O.O.C([C@H]1N)N(C=2C(=C3C(C(C(C(O)=O)=CN3[C@H]3[C@H](C3)F)=O)=CC=2F)Cl)CC11CC1.C([C@H]1N)N(C=2C(=C3C(C(C(C(O)=O)=CN3[C@H]3[C@H](C3)F)=O)=CC=2F)Cl)CC11CC1 MPORYQCGWFQFLA-ONPDANIMSA-N 0.000 description 1
- 241000251468 Actinopterygii Species 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- 239000005995 Aluminium silicate Substances 0.000 description 1
- 244000144725 Amygdalus communis Species 0.000 description 1
- 235000011437 Amygdalus communis Nutrition 0.000 description 1
- BSYNRYMUTXBXSQ-UHFFFAOYSA-N Aspirin Chemical compound CC(=O)OC1=CC=CC=C1C(O)=O BSYNRYMUTXBXSQ-UHFFFAOYSA-N 0.000 description 1
- BHELIUBJHYAEDK-OAIUPTLZSA-N Aspoxicillin Chemical compound C1([C@H](C(=O)N[C@@H]2C(N3[C@H](C(C)(C)S[C@@H]32)C(O)=O)=O)NC(=O)[C@H](N)CC(=O)NC)=CC=C(O)C=C1 BHELIUBJHYAEDK-OAIUPTLZSA-N 0.000 description 1
- 241000972773 Aulopiformes Species 0.000 description 1
- 241000271566 Aves Species 0.000 description 1
- MGQLHRYJBWGORO-LLVKDONJSA-N Balofloxacin Chemical compound C1[C@H](NC)CCCN1C1=C(F)C=C2C(=O)C(C(O)=O)=CN(C3CC3)C2=C1OC MGQLHRYJBWGORO-LLVKDONJSA-N 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- COVZYZSDYWQREU-UHFFFAOYSA-N Busulfan Chemical compound CS(=O)(=O)OCCCCOS(C)(=O)=O COVZYZSDYWQREU-UHFFFAOYSA-N 0.000 description 1
- 239000004322 Butylated hydroxytoluene Substances 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 241000222120 Candida <Saccharomycetales> Species 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 1
- UQLLWWBDSUHNEB-CZUORRHYSA-N Cefaprin Chemical compound N([C@H]1[C@@H]2N(C1=O)C(=C(CS2)COC(=O)C)C(O)=O)C(=O)CSC1=CC=NC=C1 UQLLWWBDSUHNEB-CZUORRHYSA-N 0.000 description 1
- NCFTXMQPRQZFMZ-WERGMSTESA-M Cefoperazone sodium Chemical compound [Na+].O=C1C(=O)N(CC)CCN1C(=O)N[C@H](C=1C=CC(O)=CC=1)C(=O)N[C@@H]1C(=O)N2C(C([O-])=O)=C(CSC=3N(N=NN=3)C)CS[C@@H]21 NCFTXMQPRQZFMZ-WERGMSTESA-M 0.000 description 1
- QYQDKDWGWDOFFU-IUODEOHRSA-N Cefotiam Chemical compound CN(C)CCN1N=NN=C1SCC1=C(C(O)=O)N2C(=O)[C@@H](NC(=O)CC=3N=C(N)SC=3)[C@H]2SC1 QYQDKDWGWDOFFU-IUODEOHRSA-N 0.000 description 1
- REACMANCWHKJSM-DWBVFMGKSA-M Cefsulodin sodium Chemical compound [Na+].C1=CC(C(=O)N)=CC=[N+]1CC1=C(C([O-])=O)N2C(=O)[C@@H](NC(=O)[C@@H](C=3C=CC=CC=3)S([O-])(=O)=O)[C@H]2SC1 REACMANCWHKJSM-DWBVFMGKSA-M 0.000 description 1
- HOKIDJSKDBPKTQ-GLXFQSAKSA-N Cephalosporin C Natural products S1CC(COC(=O)C)=C(C(O)=O)N2C(=O)[C@@H](NC(=O)CCC[C@@H](N)C(O)=O)[C@@H]12 HOKIDJSKDBPKTQ-GLXFQSAKSA-N 0.000 description 1
- 241000282994 Cervidae Species 0.000 description 1
- 239000004099 Chlortetracycline Substances 0.000 description 1
- HZZVJAQRINQKSD-UHFFFAOYSA-N Clavulanic acid Natural products OC(=O)C1C(=CCO)OC2CC(=O)N21 HZZVJAQRINQKSD-UHFFFAOYSA-N 0.000 description 1
- 229920002261 Corn starch Polymers 0.000 description 1
- 241000252210 Cyprinidae Species 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- ZZZCUOFIHGPKAK-UHFFFAOYSA-N D-erythro-ascorbic acid Natural products OCC1OC(=O)C(O)=C1O ZZZCUOFIHGPKAK-UHFFFAOYSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- APFDJSVKQNSTKF-FXMYHANSSA-N Danofloxacin mesylate Chemical compound CS(O)(=O)=O.C([C@@H]1C[C@H]2CN1C)N2C(C(=CC=1C(=O)C(C(O)=O)=C2)F)=CC=1N2C1CC1 APFDJSVKQNSTKF-FXMYHANSSA-N 0.000 description 1
- 206010012438 Dermatitis atopic Diseases 0.000 description 1
- 108090000204 Dipeptidase 1 Proteins 0.000 description 1
- OVBJJZOQPCKUOR-UHFFFAOYSA-L EDTA disodium salt dihydrate Chemical compound O.O.[Na+].[Na+].[O-]C(=O)C[NH+](CC([O-])=O)CC[NH+](CC([O-])=O)CC([O-])=O OVBJJZOQPCKUOR-UHFFFAOYSA-L 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- YAVZHCFFUATPRK-YZPBMOCRSA-N Erythromycin stearate Chemical compound CCCCCCCCCCCCCCCCCC(O)=O.O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)C(=O)[C@H](C)C[C@@](C)(O)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 YAVZHCFFUATPRK-YZPBMOCRSA-N 0.000 description 1
- 239000001856 Ethyl cellulose Substances 0.000 description 1
- ZZSNKZQZMQGXPY-UHFFFAOYSA-N Ethyl cellulose Chemical compound CCOCC1OC(OC)C(OCC)C(OCC)C1OC1C(O)C(O)C(OC)C(CO)O1 ZZSNKZQZMQGXPY-UHFFFAOYSA-N 0.000 description 1
- PIICEJLVQHRZGT-UHFFFAOYSA-N Ethylenediamine Chemical compound NCCN PIICEJLVQHRZGT-UHFFFAOYSA-N 0.000 description 1
- 241000282324 Felis Species 0.000 description 1
- YCKRFDGAMUMZLT-UHFFFAOYSA-N Fluorine atom Chemical compound [F] YCKRFDGAMUMZLT-UHFFFAOYSA-N 0.000 description 1
- 241000223218 Fusarium Species 0.000 description 1
- 241000287828 Gallus gallus Species 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 241000699694 Gerbillinae Species 0.000 description 1
- 229920000569 Gum karaya Polymers 0.000 description 1
- 239000004354 Hydroxyethyl cellulose Substances 0.000 description 1
- 229920000663 Hydroxyethyl cellulose Polymers 0.000 description 1
- 206010062767 Hypophysitis Diseases 0.000 description 1
- HEFNNWSXXWATRW-UHFFFAOYSA-N Ibuprofen Chemical compound CC(C)CC1=CC=C(C(C)C(O)=O)C=C1 HEFNNWSXXWATRW-UHFFFAOYSA-N 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 239000004166 Lanolin Substances 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- RJQXTJLFIWVMTO-TYNCELHUSA-N Methicillin Chemical compound COC1=CC=CC(OC)=C1C(=O)N[C@@H]1C(=O)N2[C@@H](C(O)=O)C(C)(C)S[C@@H]21 RJQXTJLFIWVMTO-TYNCELHUSA-N 0.000 description 1
- 229920000881 Modified starch Polymers 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- 235000021360 Myristic acid Nutrition 0.000 description 1
- TUNFSRHWOTWDNC-UHFFFAOYSA-N Myristic acid Natural products CCCCCCCCCCCCCC(O)=O TUNFSRHWOTWDNC-UHFFFAOYSA-N 0.000 description 1
- 229910002651 NO3 Inorganic materials 0.000 description 1
- CMWTZPSULFXXJA-UHFFFAOYSA-N Naproxen Natural products C1=C(C(C)C(O)=O)C=CC2=CC(OC)=CC=C21 CMWTZPSULFXXJA-UHFFFAOYSA-N 0.000 description 1
- NHNBFGGVMKEFGY-UHFFFAOYSA-N Nitrate Chemical compound [O-][N+]([O-])=O NHNBFGGVMKEFGY-UHFFFAOYSA-N 0.000 description 1
- VJRRJXHSVNQVOL-UHFFFAOYSA-N OC(C(C(c1c2)=O)=CN(C3CC3)c1cc(N1C=CNCC1)c2F)=O Chemical compound OC(C(C(c1c2)=O)=CN(C3CC3)c1cc(N1C=CNCC1)c2F)=O VJRRJXHSVNQVOL-UHFFFAOYSA-N 0.000 description 1
- 239000004100 Oxytetracycline Substances 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 239000004186 Penicillin G benzathine Substances 0.000 description 1
- 239000004105 Penicillin G potassium Substances 0.000 description 1
- 239000004107 Penicillin G sodium Substances 0.000 description 1
- 229930195708 Penicillin V Natural products 0.000 description 1
- 241000286209 Phasianidae Species 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 229920001214 Polysorbate 60 Polymers 0.000 description 1
- 201000004681 Psoriasis Diseases 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 241000277331 Salmonidae Species 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- 241000934878 Sterculia Species 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- 239000004098 Tetracycline Substances 0.000 description 1
- 229930003268 Vitamin C Natural products 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
- 229960001138 acetylsalicylic acid Drugs 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 229940007526 advocin Drugs 0.000 description 1
- 239000000443 aerosol Substances 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 150000001346 alkyl aryl ethers Chemical class 0.000 description 1
- 235000020224 almond Nutrition 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 229940060610 alrex Drugs 0.000 description 1
- 235000012211 aluminium silicate Nutrition 0.000 description 1
- 229940009868 aluminum magnesium silicate Drugs 0.000 description 1
- WMGSQTMJHBYJMQ-UHFFFAOYSA-N aluminum;magnesium;silicate Chemical compound [Mg+2].[Al+3].[O-][Si]([O-])([O-])[O-] WMGSQTMJHBYJMQ-UHFFFAOYSA-N 0.000 description 1
- 229940099032 alvesco Drugs 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- 229960003022 amoxicillin Drugs 0.000 description 1
- LSQZJLSUYDQPKJ-NJBDSQKTSA-N amoxicillin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)=CC=C(O)C=C1 LSQZJLSUYDQPKJ-NJBDSQKTSA-N 0.000 description 1
- 229960000723 ampicillin Drugs 0.000 description 1
- 229960001931 ampicillin sodium Drugs 0.000 description 1
- KLOHDWPABZXLGI-YWUHCJSESA-M ampicillin sodium Chemical compound [Na+].C1([C@@H](N)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C([O-])=O)(C)C)=CC=CC=C1 KLOHDWPABZXLGI-YWUHCJSESA-M 0.000 description 1
- 229960003311 ampicillin trihydrate Drugs 0.000 description 1
- 229940121363 anti-inflammatory agent Drugs 0.000 description 1
- 239000002260 anti-inflammatory agent Substances 0.000 description 1
- 229940124599 anti-inflammatory drug Drugs 0.000 description 1
- 229960005475 antiinfective agent Drugs 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 235000006708 antioxidants Nutrition 0.000 description 1
- 229950001979 apalcillin Drugs 0.000 description 1
- XMQVYNAURODYCQ-SLFBBCNNSA-N apalcillin Chemical compound C1([C@@H](NC(=O)C=2C(=C3N=CC=CC3=NC=2)O)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)=CC=CC=C1 XMQVYNAURODYCQ-SLFBBCNNSA-N 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 229960000202 aspoxicillin Drugs 0.000 description 1
- 239000000305 astragalus gummifer gum Substances 0.000 description 1
- 201000008937 atopic dermatitis Diseases 0.000 description 1
- 229940062316 avelox Drugs 0.000 description 1
- 229960004099 azithromycin Drugs 0.000 description 1
- MQTOSJVFKKJCRP-BICOPXKESA-N azithromycin Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)N(C)C[C@H](C)C[C@@](C)(O)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 MQTOSJVFKKJCRP-BICOPXKESA-N 0.000 description 1
- 229960003623 azlocillin Drugs 0.000 description 1
- JTWOMNBEOCYFNV-NFFDBFGFSA-N azlocillin Chemical compound N([C@@H](C(=O)N[C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C=1C=CC=CC=1)C(=O)N1CCNC1=O JTWOMNBEOCYFNV-NFFDBFGFSA-N 0.000 description 1
- 229960002699 bacampicillin Drugs 0.000 description 1
- PFOLLRNADZZWEX-FFGRCDKISA-N bacampicillin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@@H]3N(C2=O)[C@H](C(S3)(C)C)C(=O)OC(C)OC(=O)OCC)=CC=CC=C1 PFOLLRNADZZWEX-FFGRCDKISA-N 0.000 description 1
- 229950000805 balofloxacin Drugs 0.000 description 1
- 229940105596 baytril Drugs 0.000 description 1
- 229950000210 beclometasone dipropionate Drugs 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 229960000686 benzalkonium chloride Drugs 0.000 description 1
- JUHORIMYRDESRB-UHFFFAOYSA-N benzathine Chemical compound C=1C=CC=CC=1CNCCNCC1=CC=CC=C1 JUHORIMYRDESRB-UHFFFAOYSA-N 0.000 description 1
- WPYMKLBDIGXBTP-VQEHIDDOSA-N benzoic acid Chemical compound OC(=O)C1=CC=C[13CH]=C1 WPYMKLBDIGXBTP-VQEHIDDOSA-N 0.000 description 1
- CKNWWFLJDPCURW-UHFFFAOYSA-N benzoic acid;2-phenylphenol Chemical compound OC(=O)C1=CC=CC=C1.OC1=CC=CC=C1C1=CC=CC=C1 CKNWWFLJDPCURW-UHFFFAOYSA-N 0.000 description 1
- 150000001559 benzoic acids Chemical class 0.000 description 1
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 1
- CADWTSSKOVRVJC-UHFFFAOYSA-N benzyl(dimethyl)azanium;chloride Chemical compound [Cl-].C[NH+](C)CC1=CC=CC=C1 CADWTSSKOVRVJC-UHFFFAOYSA-N 0.000 description 1
- BVGLIYRKPOITBQ-ANPZCEIESA-N benzylpenicillin benzathine Chemical compound C=1C=CC=CC=1C[NH2+]CC[NH2+]CC1=CC=CC=C1.N([C@H]1[C@H]2SC([C@@H](N2C1=O)C([O-])=O)(C)C)C(=O)CC1=CC=CC=C1.N([C@H]1[C@H]2SC([C@@H](N2C1=O)C([O-])=O)(C)C)C(=O)CC1=CC=CC=C1 BVGLIYRKPOITBQ-ANPZCEIESA-N 0.000 description 1
- 102000006635 beta-lactamase Human genes 0.000 description 1
- UREBDLICKHMUKA-DVTGEIKXSA-N betamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-DVTGEIKXSA-N 0.000 description 1
- 229960004311 betamethasone valerate Drugs 0.000 description 1
- SNHRLVCMMWUAJD-SUYDQAKGSA-N betamethasone valerate Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@H](C)[C@@](C(=O)CO)(OC(=O)CCCC)[C@@]1(C)C[C@@H]2O SNHRLVCMMWUAJD-SUYDQAKGSA-N 0.000 description 1
- 229960004436 budesonide Drugs 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 235000010354 butylated hydroxytoluene Nutrition 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910000019 calcium carbonate Inorganic materials 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 229910000389 calcium phosphate Inorganic materials 0.000 description 1
- 235000011010 calcium phosphates Nutrition 0.000 description 1
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 1
- 229920003090 carboxymethyl hydroxyethyl cellulose Polymers 0.000 description 1
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 1
- 229960000717 carindacillin Drugs 0.000 description 1
- JIRBAUWICKGBFE-MNRDOXJOSA-N carindacillin Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)C(C(=O)OC=1C=C2CCCC2=CC=1)C1=CC=CC=C1 JIRBAUWICKGBFE-MNRDOXJOSA-N 0.000 description 1
- 235000010418 carrageenan Nutrition 0.000 description 1
- 239000000679 carrageenan Substances 0.000 description 1
- 229920001525 carrageenan Polymers 0.000 description 1
- 229940113118 carrageenan Drugs 0.000 description 1
- 229960005361 cefaclor Drugs 0.000 description 1
- 229960004841 cefadroxil Drugs 0.000 description 1
- 229960001065 cefadroxil monohydrate Drugs 0.000 description 1
- CZTQZXZIADLWOZ-CRAIPNDOSA-N cefaloridine Chemical compound O=C([C@@H](NC(=O)CC=1SC=CC=1)[C@H]1SC2)N1C(C(=O)[O-])=C2C[N+]1=CC=CC=C1 CZTQZXZIADLWOZ-CRAIPNDOSA-N 0.000 description 1
- 229960000603 cefalotin Drugs 0.000 description 1
- XIURVHNZVLADCM-IUODEOHRSA-N cefalotin Chemical compound N([C@H]1[C@@H]2N(C1=O)C(=C(CS2)COC(=O)C)C(O)=O)C(=O)CC1=CC=CS1 XIURVHNZVLADCM-IUODEOHRSA-N 0.000 description 1
- 229960003012 cefamandole Drugs 0.000 description 1
- OLVCFLKTBJRLHI-AXAPSJFSSA-N cefamandole Chemical compound CN1N=NN=C1SCC1=C(C(O)=O)N2C(=O)[C@@H](NC(=O)[C@H](O)C=3C=CC=CC=3)[C@H]2SC1 OLVCFLKTBJRLHI-AXAPSJFSSA-N 0.000 description 1
- OJMNTWPPFNMOCJ-CFOLLTDRSA-M cefamandole sodium Chemical compound [Na+].CN1N=NN=C1SCC1=C(C([O-])=O)N2C(=O)[C@@H](NC(=O)[C@H](O)C=3C=CC=CC=3)[C@H]2SC1 OJMNTWPPFNMOCJ-CFOLLTDRSA-M 0.000 description 1
- 229960004350 cefapirin Drugs 0.000 description 1
- 229960001817 cefbuperazone Drugs 0.000 description 1
- SMSRCGPDNDCXFR-CYWZMYCQSA-N cefbuperazone Chemical compound O=C1C(=O)N(CC)CCN1C(=O)N[C@H]([C@H](C)O)C(=O)N[C@]1(OC)C(=O)N2C(C(O)=O)=C(CSC=3N(N=NN=3)C)CS[C@@H]21 SMSRCGPDNDCXFR-CYWZMYCQSA-N 0.000 description 1
- 229960002100 cefepime Drugs 0.000 description 1
- 229960004041 cefetamet Drugs 0.000 description 1
- MQLRYUCJDNBWMV-GHXIOONMSA-N cefetamet Chemical compound N([C@@H]1C(N2C(=C(C)CS[C@@H]21)C(O)=O)=O)C(=O)\C(=N/OC)C1=CSC(N)=N1 MQLRYUCJDNBWMV-GHXIOONMSA-N 0.000 description 1
- 229960002129 cefixime Drugs 0.000 description 1
- OKBVVJOGVLARMR-QSWIMTSFSA-N cefixime Chemical compound S1C(N)=NC(C(=N\OCC(O)=O)\C(=O)N[C@@H]2C(N3C(=C(C=C)CS[C@@H]32)C(O)=O)=O)=C1 OKBVVJOGVLARMR-QSWIMTSFSA-N 0.000 description 1
- 229950001334 cefluprenam Drugs 0.000 description 1
- XAKKNLNAJBNLPC-MAYKBZFQSA-N cefluprenam Chemical compound N([C@H]1[C@@H]2N(C1=O)C(=C(CS2)/C=C/C[N+](C)(CC)CC(N)=O)C([O-])=O)C(=O)C(=N/OCF)\C1=NSC(N)=N1 XAKKNLNAJBNLPC-MAYKBZFQSA-N 0.000 description 1
- 229960003791 cefmenoxime Drugs 0.000 description 1
- HJJDBAOLQAWBMH-YCRCPZNHSA-N cefmenoxime Chemical compound S([C@@H]1[C@@H](C(N1C=1C(O)=O)=O)NC(=O)\C(=N/OC)C=2N=C(N)SC=2)CC=1CSC1=NN=NN1C HJJDBAOLQAWBMH-YCRCPZNHSA-N 0.000 description 1
- 229960003585 cefmetazole Drugs 0.000 description 1
- 229960002676 cefmetazole sodium Drugs 0.000 description 1
- 229960002025 cefminox Drugs 0.000 description 1
- JSDXOWVAHXDYCU-VXSYNFHWSA-N cefminox Chemical compound S([C@@H]1[C@@](C(N1C=1C(O)=O)=O)(NC(=O)CSC[C@@H](N)C(O)=O)OC)CC=1CSC1=NN=NN1C JSDXOWVAHXDYCU-VXSYNFHWSA-N 0.000 description 1
- 229960001958 cefodizime Drugs 0.000 description 1
- XDZKBRJLTGRPSS-BGZQYGJUSA-N cefodizime Chemical compound S([C@@H]1[C@@H](C(N1C=1C(O)=O)=O)NC(=O)\C(=N/OC)C=2N=C(N)SC=2)CC=1CSC1=NC(C)=C(CC(O)=O)S1 XDZKBRJLTGRPSS-BGZQYGJUSA-N 0.000 description 1
- 229960004682 cefoperazone Drugs 0.000 description 1
- GCFBRXLSHGKWDP-XCGNWRKASA-N cefoperazone Chemical compound O=C1C(=O)N(CC)CCN1C(=O)N[C@H](C=1C=CC(O)=CC=1)C(=O)N[C@@H]1C(=O)N2C(C(O)=O)=C(CSC=3N(N=NN=3)C)CS[C@@H]21 GCFBRXLSHGKWDP-XCGNWRKASA-N 0.000 description 1
- 229960002417 cefoperazone sodium Drugs 0.000 description 1
- 229960004292 ceforanide Drugs 0.000 description 1
- SLAYUXIURFNXPG-CRAIPNDOSA-N ceforanide Chemical compound NCC1=CC=CC=C1CC(=O)N[C@@H]1C(=O)N2C(C(O)=O)=C(CSC=3N(N=NN=3)CC(O)=O)CS[C@@H]21 SLAYUXIURFNXPG-CRAIPNDOSA-N 0.000 description 1
- 229950001580 cefoselis Drugs 0.000 description 1
- ZINFAXPQMLDEEJ-GFVOIPPFSA-N cefoselis Chemical compound S([C@@H]1[C@@H](C(N1C=1C(O)=O)=O)NC(=O)\C(=N/OC)C=2N=C(N)SC=2)CC=1CN1C=CC(=N)N1CCO ZINFAXPQMLDEEJ-GFVOIPPFSA-N 0.000 description 1
- 229960004261 cefotaxime Drugs 0.000 description 1
- 229960002727 cefotaxime sodium Drugs 0.000 description 1
- 229960005495 cefotetan Drugs 0.000 description 1
- SRZNHPXWXCNNDU-RHBCBLIFSA-N cefotetan Chemical compound N([C@]1(OC)C(N2C(=C(CSC=3N(N=NN=3)C)CS[C@@H]21)C(O)=O)=O)C(=O)C1SC(=C(C(N)=O)C(O)=O)S1 SRZNHPXWXCNNDU-RHBCBLIFSA-N 0.000 description 1
- 229960001242 cefotiam Drugs 0.000 description 1
- 229960002682 cefoxitin Drugs 0.000 description 1
- 229960003016 cefoxitin sodium Drugs 0.000 description 1
- DKOQGJHPHLTOJR-WHRDSVKCSA-N cefpirome Chemical compound N([C@@H]1C(N2C(=C(C[N+]=3C=4CCCC=4C=CC=3)CS[C@@H]21)C([O-])=O)=O)C(=O)\C(=N/OC)C1=CSC(N)=N1 DKOQGJHPHLTOJR-WHRDSVKCSA-N 0.000 description 1
- 229960000466 cefpirome Drugs 0.000 description 1
- 229960005090 cefpodoxime Drugs 0.000 description 1
- WYUSVOMTXWRGEK-HBWVYFAYSA-N cefpodoxime Chemical compound N([C@H]1[C@@H]2N(C1=O)C(=C(CS2)COC)C(O)=O)C(=O)C(=N/OC)\C1=CSC(N)=N1 WYUSVOMTXWRGEK-HBWVYFAYSA-N 0.000 description 1
- 229960002580 cefprozil Drugs 0.000 description 1
- 229950009592 cefquinome Drugs 0.000 description 1
- 229960002588 cefradine Drugs 0.000 description 1
- 229960003202 cefsulodin Drugs 0.000 description 1
- SYLKGLMBLAAGSC-QLVMHMETSA-N cefsulodin Chemical compound C1=CC(C(=O)N)=CC=[N+]1CC1=C(C([O-])=O)N2C(=O)[C@@H](NC(=O)[C@@H](C=3C=CC=CC=3)S(O)(=O)=O)[C@H]2SC1 SYLKGLMBLAAGSC-QLVMHMETSA-N 0.000 description 1
- 229960001281 cefsulodin sodium Drugs 0.000 description 1
- 229960000484 ceftazidime Drugs 0.000 description 1
- 229960003547 ceftazidime pentahydrate Drugs 0.000 description 1
- NMVPEQXCMGEDNH-TZVUEUGBSA-N ceftazidime pentahydrate Chemical compound O.O.O.O.O.S([C@@H]1[C@@H](C(N1C=1C([O-])=O)=O)NC(=O)\C(=N/OC(C)(C)C(O)=O)C=2N=C(N)SC=2)CC=1C[N+]1=CC=CC=C1 NMVPEQXCMGEDNH-TZVUEUGBSA-N 0.000 description 1
- 229960004086 ceftibuten Drugs 0.000 description 1
- UNJFKXSSGBWRBZ-BJCIPQKHSA-N ceftibuten Chemical compound S1C(N)=NC(C(=C\CC(O)=O)\C(=O)N[C@@H]2C(N3C(=CCS[C@@H]32)C(O)=O)=O)=C1 UNJFKXSSGBWRBZ-BJCIPQKHSA-N 0.000 description 1
- 229960001991 ceftizoxime Drugs 0.000 description 1
- NNULBSISHYWZJU-LLKWHZGFSA-N ceftizoxime Chemical compound N([C@@H]1C(N2C(=CCS[C@@H]21)C(O)=O)=O)C(=O)\C(=N/OC)C1=CSC(N)=N1 NNULBSISHYWZJU-LLKWHZGFSA-N 0.000 description 1
- 229960004755 ceftriaxone Drugs 0.000 description 1
- VAAUVRVFOQPIGI-SPQHTLEESA-N ceftriaxone Chemical compound S([C@@H]1[C@@H](C(N1C=1C(O)=O)=O)NC(=O)\C(=N/OC)C=2N=C(N)SC=2)CC=1CSC1=NC(=O)C(=O)NN1C VAAUVRVFOQPIGI-SPQHTLEESA-N 0.000 description 1
- 229960000479 ceftriaxone sodium Drugs 0.000 description 1
- 229960001668 cefuroxime Drugs 0.000 description 1
- JFPVXVDWJQMJEE-IZRZKJBUSA-N cefuroxime Chemical compound N([C@@H]1C(N2C(=C(COC(N)=O)CS[C@@H]21)C(O)=O)=O)C(=O)\C(=N/OC)C1=CC=CO1 JFPVXVDWJQMJEE-IZRZKJBUSA-N 0.000 description 1
- 229950000807 cefuzonam Drugs 0.000 description 1
- CXHKZHZLDMQGFF-ZSDSSEDPSA-N cefuzonam Chemical compound S([C@@H]1[C@@H](C(N1C=1C(O)=O)=O)NC(=O)\C(=N/OC)C=2N=C(N)SC=2)CC=1CSC1=CN=NS1 CXHKZHZLDMQGFF-ZSDSSEDPSA-N 0.000 description 1
- 229940087110 celestone Drugs 0.000 description 1
- 229920003086 cellulose ether Polymers 0.000 description 1
- 229940106164 cephalexin Drugs 0.000 description 1
- AVGYWQBCYZHHPN-CYJZLJNKSA-N cephalexin monohydrate Chemical compound O.C1([C@@H](N)C(=O)N[C@H]2[C@@H]3N(C2=O)C(=C(CS3)C)C(O)=O)=CC=CC=C1 AVGYWQBCYZHHPN-CYJZLJNKSA-N 0.000 description 1
- HOKIDJSKDBPKTQ-GLXFQSAKSA-M cephalosporin C(1-) Chemical compound S1CC(COC(=O)C)=C(C([O-])=O)N2C(=O)[C@@H](NC(=O)CCC[C@@H]([NH3+])C([O-])=O)[C@@H]12 HOKIDJSKDBPKTQ-GLXFQSAKSA-M 0.000 description 1
- VUFGUVLLDPOSBC-XRZFDKQNSA-M cephalothin sodium Chemical compound [Na+].N([C@H]1[C@@H]2N(C1=O)C(=C(CS2)COC(=O)C)C([O-])=O)C(=O)CC1=CC=CS1 VUFGUVLLDPOSBC-XRZFDKQNSA-M 0.000 description 1
- VGEOUKPOQQEQSX-OALZAMAHSA-M cephapirin sodium Chemical compound [Na+].N([C@H]1[C@@H]2N(C1=O)C(=C(CS2)COC(=O)C)C([O-])=O)C(=O)CSC1=CC=NC=C1 VGEOUKPOQQEQSX-OALZAMAHSA-M 0.000 description 1
- RDLPVSKMFDYCOR-UEKVPHQBSA-N cephradine Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@@H]3N(C2=O)C(=C(CS3)C)C(O)=O)=CCC=CC1 RDLPVSKMFDYCOR-UEKVPHQBSA-N 0.000 description 1
- 229960001927 cetylpyridinium chloride Drugs 0.000 description 1
- NFCRBQADEGXVDL-UHFFFAOYSA-M cetylpyridinium chloride monohydrate Chemical compound O.[Cl-].CCCCCCCCCCCCCCCC[N+]1=CC=CC=C1 NFCRBQADEGXVDL-UHFFFAOYSA-M 0.000 description 1
- 239000002738 chelating agent Substances 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 235000013330 chicken meat Nutrition 0.000 description 1
- 229960004926 chlorobutanol Drugs 0.000 description 1
- VDANGULDQQJODZ-UHFFFAOYSA-N chloroprocaine Chemical compound CCN(CC)CCOC(=O)C1=CC=C(N)C=C1Cl VDANGULDQQJODZ-UHFFFAOYSA-N 0.000 description 1
- 229960002023 chloroprocaine Drugs 0.000 description 1
- CYDMQBQPVICBEU-UHFFFAOYSA-N chlorotetracycline Natural products C1=CC(Cl)=C2C(O)(C)C3CC4C(N(C)C)C(O)=C(C(N)=O)C(=O)C4(O)C(O)=C3C(=O)C2=C1O CYDMQBQPVICBEU-UHFFFAOYSA-N 0.000 description 1
- 229960004475 chlortetracycline Drugs 0.000 description 1
- 235000019365 chlortetracycline Nutrition 0.000 description 1
- CYDMQBQPVICBEU-XRNKAMNCSA-N chlortetracycline Chemical compound C1=CC(Cl)=C2[C@](O)(C)[C@H]3C[C@H]4[C@H](N(C)C)C(O)=C(C(N)=O)C(=O)[C@@]4(O)C(O)=C3C(=O)C2=C1O CYDMQBQPVICBEU-XRNKAMNCSA-N 0.000 description 1
- 229940088516 cipro Drugs 0.000 description 1
- 229960002626 clarithromycin Drugs 0.000 description 1
- AGOYDEPGAOXOCK-KCBOHYOISA-N clarithromycin Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)C(=O)[C@H](C)C[C@](C)([C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)OC)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 AGOYDEPGAOXOCK-KCBOHYOISA-N 0.000 description 1
- 229960003324 clavulanic acid Drugs 0.000 description 1
- HZZVJAQRINQKSD-PBFISZAISA-N clavulanic acid Chemical compound OC(=O)[C@H]1C(=C/CO)/O[C@@H]2CC(=O)N21 HZZVJAQRINQKSD-PBFISZAISA-N 0.000 description 1
- 229960004022 clotrimazole Drugs 0.000 description 1
- 238000002648 combination therapy Methods 0.000 description 1
- 230000002301 combined effect Effects 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 239000013068 control sample Substances 0.000 description 1
- 239000008120 corn starch Substances 0.000 description 1
- 239000006184 cosolvent Substances 0.000 description 1
- 229940111134 coxibs Drugs 0.000 description 1
- 239000006071 cream Substances 0.000 description 1
- 229960000913 crospovidone Drugs 0.000 description 1
- 229960004244 cyclacillin Drugs 0.000 description 1
- HGBLNBBNRORJKI-WCABBAIRSA-N cyclacillin Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)C1(N)CCCCC1 HGBLNBBNRORJKI-WCABBAIRSA-N 0.000 description 1
- 239000003255 cyclooxygenase 2 inhibitor Substances 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 229940026692 decadron Drugs 0.000 description 1
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 229960001145 deflazacort Drugs 0.000 description 1
- FBHSPRKOSMHSIF-GRMWVWQJSA-N deflazacort Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@@H]2[C@@H]1[C@@H]1C[C@H]3OC(C)=N[C@@]3(C(=O)COC(=O)C)[C@@]1(C)C[C@@H]2O FBHSPRKOSMHSIF-GRMWVWQJSA-N 0.000 description 1
- 229940027008 deltasone Drugs 0.000 description 1
- 229960003957 dexamethasone Drugs 0.000 description 1
- 150000008050 dialkyl sulfates Chemical class 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- ZBCBWPMODOFKDW-UHFFFAOYSA-N diethanolamine Chemical compound OCCNCCO ZBCBWPMODOFKDW-UHFFFAOYSA-N 0.000 description 1
- 229940043237 diethanolamine Drugs 0.000 description 1
- 125000004177 diethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- HPNMFZURTQLUMO-UHFFFAOYSA-N diethylamine Chemical compound CCNCC HPNMFZURTQLUMO-UHFFFAOYSA-N 0.000 description 1
- 229940063123 diflucan Drugs 0.000 description 1
- FSBVERYRVPGNGG-UHFFFAOYSA-N dimagnesium dioxido-bis[[oxido(oxo)silyl]oxy]silane hydrate Chemical compound O.[Mg+2].[Mg+2].[O-][Si](=O)O[Si]([O-])([O-])O[Si]([O-])=O FSBVERYRVPGNGG-UHFFFAOYSA-N 0.000 description 1
- 125000000118 dimethyl group Chemical group [H]C([H])([H])* 0.000 description 1
- GAFRWLVTHPVQGK-UHFFFAOYSA-N dipentyl sulfate Chemical class CCCCCOS(=O)(=O)OCCCCC GAFRWLVTHPVQGK-UHFFFAOYSA-N 0.000 description 1
- 229940074639 diprolene Drugs 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- FDRNWTJTHBSPMW-GNXCPKRQSA-L disodium;(6r,7r)-7-[[(2e)-2-(2-amino-1,3-thiazol-4-yl)-2-methoxyiminoacetyl]amino]-3-[(2-methyl-6-oxido-5-oxo-1,2,4-triazin-3-yl)sulfanylmethyl]-8-oxo-5-thia-1-azabicyclo[4.2.0]oct-2-ene-2-carboxylate Chemical compound [Na+].[Na+].S([C@@H]1[C@@H](C(N1C=1C([O-])=O)=O)NC(=O)/C(=N/OC)C=2N=C(N)SC=2)CC=1CSC1=NC(=O)C([O-])=NN1C FDRNWTJTHBSPMW-GNXCPKRQSA-L 0.000 description 1
- FDRNWTJTHBSPMW-BBJOQENWSA-L disodium;(6r,7r)-7-[[(2z)-2-(2-amino-1,3-thiazol-4-yl)-2-methoxyimino-1-oxidoethylidene]amino]-3-[(2-methyl-5,6-dioxo-1h-1,2,4-triazin-3-yl)sulfanylmethyl]-8-oxo-5-thia-1-azabicyclo[4.2.0]oct-2-ene-2-carboxylate Chemical compound [Na+].[Na+].S([C@@H]1[C@@H](C(N1C=1C([O-])=O)=O)NC(=O)\C(=N/OC)C=2N=C(N)SC=2)CC=1CSC1=NC(=O)C([O-])=NN1C FDRNWTJTHBSPMW-BBJOQENWSA-L 0.000 description 1
- 208000032625 disorder of ear Diseases 0.000 description 1
- 125000003438 dodecyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 210000005069 ears Anatomy 0.000 description 1
- 229960003913 econazole Drugs 0.000 description 1
- 229940073610 elocon Drugs 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 239000003623 enhancer Substances 0.000 description 1
- 229940002671 entocort Drugs 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 229940041693 ertaczo Drugs 0.000 description 1
- 229960003276 erythromycin Drugs 0.000 description 1
- AWMFUEJKWXESNL-JZBHMOKNSA-N erythromycin estolate Chemical compound CCCCCCCCCCCCOS(O)(=O)=O.O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)C(=O)[C@H](C)C[C@@](C)(O)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)OC(=O)CC)[C@H]1C)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 AWMFUEJKWXESNL-JZBHMOKNSA-N 0.000 description 1
- 229960003203 erythromycin estolate Drugs 0.000 description 1
- 229960000741 erythromycin ethylsuccinate Drugs 0.000 description 1
- NSYZCCDSJNWWJL-YXOIYICCSA-N erythromycin ethylsuccinate Chemical compound O1[C@H](C)C[C@H](N(C)C)[C@@H](OC(=O)CCC(=O)OCC)[C@@H]1O[C@H]1[C@@](O)(C)C[C@@H](C)C(=O)[C@H](C)[C@@H](O)[C@](C)(O)[C@@H](CC)OC(=O)[C@H](C)[C@@H](O[C@@H]2O[C@@H](C)[C@H](O)[C@](C)(OC)C2)[C@@H]1C NSYZCCDSJNWWJL-YXOIYICCSA-N 0.000 description 1
- 229960004142 erythromycin stearate Drugs 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 229940031098 ethanolamine Drugs 0.000 description 1
- BEFDCLMNVWHSGT-UHFFFAOYSA-N ethenylcyclopentane Chemical compound C=CC1CCCC1 BEFDCLMNVWHSGT-UHFFFAOYSA-N 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- 235000019325 ethyl cellulose Nutrition 0.000 description 1
- 229920001249 ethyl cellulose Polymers 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 229940012017 ethylenediamine Drugs 0.000 description 1
- 229940085379 exelderm Drugs 0.000 description 1
- 239000004744 fabric Substances 0.000 description 1
- 229940107247 factive Drugs 0.000 description 1
- 239000003925 fat Substances 0.000 description 1
- 235000019197 fats Nutrition 0.000 description 1
- 235000019688 fish Nutrition 0.000 description 1
- 229940085861 flovent Drugs 0.000 description 1
- 229940072686 floxin Drugs 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 229960001347 fluocinolone acetonide Drugs 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 229940060037 fluorine Drugs 0.000 description 1
- 229960001469 fluticasone furoate Drugs 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 239000012458 free base Substances 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- JIYMVSQRGZEYAX-CWUUNJJBSA-N gemifloxacin mesylate Chemical compound CS(O)(=O)=O.C1C(CN)C(=N/OC)/CN1C(C(=C1)F)=NC2=C1C(=O)C(C(O)=O)=CN2C1CC1 JIYMVSQRGZEYAX-CWUUNJJBSA-N 0.000 description 1
- 239000003862 glucocorticoid Substances 0.000 description 1
- 235000011187 glycerol Nutrition 0.000 description 1
- 150000002334 glycols Chemical class 0.000 description 1
- LHGVFZTZFXWLCP-UHFFFAOYSA-N guaiacol Chemical class COC1=CC=CC=C1O LHGVFZTZFXWLCP-UHFFFAOYSA-N 0.000 description 1
- 150000004820 halides Chemical group 0.000 description 1
- 125000000623 heterocyclic group Chemical group 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 210000003630 histaminocyte Anatomy 0.000 description 1
- 229920001519 homopolymer Polymers 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 235000019447 hydroxyethyl cellulose Nutrition 0.000 description 1
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 1
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 1
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 1
- UFVKGYZPFZQRLF-UHFFFAOYSA-N hydroxypropyl methyl cellulose Chemical compound OC1C(O)C(OC)OC(CO)C1OC1C(O)C(O)C(OC2C(C(O)C(OC3C(C(O)C(O)C(CO)O3)O)C(CO)O2)O)C(CO)O1 UFVKGYZPFZQRLF-UHFFFAOYSA-N 0.000 description 1
- 229960001680 ibuprofen Drugs 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 229940060367 inert ingredients Drugs 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 150000007529 inorganic bases Chemical class 0.000 description 1
- 238000010255 intramuscular injection Methods 0.000 description 1
- 239000007927 intramuscular injection Substances 0.000 description 1
- 238000010253 intravenous injection Methods 0.000 description 1
- 229960004849 isoconazole Drugs 0.000 description 1
- VHVPQPYKVGDNFY-ZPGVKDDISA-N itraconazole Chemical compound O=C1N(C(C)CC)N=CN1C1=CC=C(N2CCN(CC2)C=2C=CC(OC[C@@H]3O[C@](CN4N=CN=C4)(OC3)C=3C(=CC(Cl)=CC=3)Cl)=CC=2)C=C1 VHVPQPYKVGDNFY-ZPGVKDDISA-N 0.000 description 1
- 229960004144 josamycin Drugs 0.000 description 1
- XJSFLOJWULLJQS-NGVXBBESSA-N josamycin Chemical compound CO[C@H]1[C@H](OC(C)=O)CC(=O)O[C@H](C)C\C=C\C=C\[C@H](O)[C@H](C)C[C@H](CC=O)[C@@H]1O[C@H]1[C@H](O)[C@@H](N(C)C)[C@H](O[C@@H]2O[C@@H](C)[C@H](OC(=O)CC(C)C)[C@](C)(O)C2)[C@@H](C)O1 XJSFLOJWULLJQS-NGVXBBESSA-N 0.000 description 1
- NLYAJNPCOHFWQQ-UHFFFAOYSA-N kaolin Chemical compound O.O.O=[Al]O[Si](=O)O[Si](=O)O[Al]=O NLYAJNPCOHFWQQ-UHFFFAOYSA-N 0.000 description 1
- 235000010494 karaya gum Nutrition 0.000 description 1
- 239000000231 karaya gum Substances 0.000 description 1
- 229940039371 karaya gum Drugs 0.000 description 1
- 229960004125 ketoconazole Drugs 0.000 description 1
- JJTUDXZGHPGLLC-UHFFFAOYSA-N lactide Chemical compound CC1OC(=O)C(C)OC1=O JJTUDXZGHPGLLC-UHFFFAOYSA-N 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 229940039717 lanolin Drugs 0.000 description 1
- 235000019388 lanolin Nutrition 0.000 description 1
- 229940094522 laponite Drugs 0.000 description 1
- 229940089519 levaquin Drugs 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- XCOBTUNSZUJCDH-UHFFFAOYSA-B lithium magnesium sodium silicate Chemical compound [Li+].[Li+].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[Na+].[Na+].[Mg+2].[Mg+2].[Mg+2].[Mg+2].[Mg+2].[Mg+2].[Mg+2].[Mg+2].[Mg+2].[Mg+2].[Mg+2].[Mg+2].[Mg+2].[Mg+2].[Mg+2].[Mg+2].O1[Si](O2)([O-])O[Si]3([O-])O[Si]1([O-])O[Si]2([O-])O3.O1[Si](O2)([O-])O[Si]3([O-])O[Si]1([O-])O[Si]2([O-])O3.O1[Si](O2)([O-])O[Si]3([O-])O[Si]1([O-])O[Si]2([O-])O3.O1[Si](O2)([O-])O[Si]3([O-])O[Si]1([O-])O[Si]2([O-])O3.O1[Si](O2)([O-])O[Si]3([O-])O[Si]1([O-])O[Si]2([O-])O3.O1[Si](O2)([O-])O[Si]3([O-])O[Si]1([O-])O[Si]2([O-])O3 XCOBTUNSZUJCDH-UHFFFAOYSA-B 0.000 description 1
- 244000144972 livestock Species 0.000 description 1
- 229960001977 loracarbef Drugs 0.000 description 1
- 229940080267 lotemax Drugs 0.000 description 1
- 229960003744 loteprednol etabonate Drugs 0.000 description 1
- 239000006210 lotion Substances 0.000 description 1
- 229940063175 lotrimin Drugs 0.000 description 1
- 229940080290 lotrimin af Drugs 0.000 description 1
- 239000003120 macrolide antibiotic agent Substances 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 239000000391 magnesium silicate Substances 0.000 description 1
- 229910052919 magnesium silicate Inorganic materials 0.000 description 1
- 235000019792 magnesium silicate Nutrition 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 229940103196 maxaquin Drugs 0.000 description 1
- 229940064748 medrol Drugs 0.000 description 1
- 229960003194 meglumine Drugs 0.000 description 1
- 229960003806 metampicillin Drugs 0.000 description 1
- FZECHKJQHUVANE-MCYUEQNJSA-N metampicillin Chemical compound C1([C@@H](N=C)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)=CC=CC=C1 FZECHKJQHUVANE-MCYUEQNJSA-N 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 229960002900 methylcellulose Drugs 0.000 description 1
- 229960002216 methylparaben Drugs 0.000 description 1
- 229960004584 methylprednisolone Drugs 0.000 description 1
- 229960003085 meticillin Drugs 0.000 description 1
- 229960002509 miconazole Drugs 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 229940000973 monistat Drugs 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 229960003702 moxifloxacin Drugs 0.000 description 1
- 125000001421 myristyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- GPXLMGHLHQJAGZ-JTDSTZFVSA-N nafcillin Chemical compound C1=CC=CC2=C(C(=O)N[C@@H]3C(N4[C@H](C(C)(C)S[C@@H]43)C(O)=O)=O)C(OCC)=CC=C21 GPXLMGHLHQJAGZ-JTDSTZFVSA-N 0.000 description 1
- 229960000515 nafcillin Drugs 0.000 description 1
- OCXSDHJRMYFTMA-KMFBOIRUSA-M nafcillin sodium monohydrate Chemical compound O.[Na+].C1=CC=CC2=C(C(=O)N[C@@H]3C(N4[C@H](C(C)(C)S[C@@H]43)C([O-])=O)=O)C(OCC)=CC=C21 OCXSDHJRMYFTMA-KMFBOIRUSA-M 0.000 description 1
- 229960002009 naproxen Drugs 0.000 description 1
- CMWTZPSULFXXJA-VIFPVBQESA-N naproxen Chemical compound C1=C([C@H](C)C(O)=O)C=CC2=CC(OC)=CC=C21 CMWTZPSULFXXJA-VIFPVBQESA-N 0.000 description 1
- 229940002297 nasacort Drugs 0.000 description 1
- 229920001206 natural gum Polymers 0.000 description 1
- 229950010757 neticonazole Drugs 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- UEHLXXJAWYWUGI-UHFFFAOYSA-M nitromersol Chemical compound CC1=CC=C([N+]([O-])=O)C2=C1O[Hg]2 UEHLXXJAWYWUGI-UHFFFAOYSA-M 0.000 description 1
- 229940118238 nitromersol Drugs 0.000 description 1
- 229940064438 nizoral Drugs 0.000 description 1
- 229960001180 norfloxacin Drugs 0.000 description 1
- 229940064764 noroxin Drugs 0.000 description 1
- 229940099075 noxafil Drugs 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 229940087154 omnaris Drugs 0.000 description 1
- 229940001566 orbax Drugs 0.000 description 1
- UWYHMGVUTGAWSP-JKIFEVAISA-N oxacillin Chemical compound N([C@@H]1C(N2[C@H](C(C)(C)S[C@@H]21)C(O)=O)=O)C(=O)C1=C(C)ON=C1C1=CC=CC=C1 UWYHMGVUTGAWSP-JKIFEVAISA-N 0.000 description 1
- 229960001019 oxacillin Drugs 0.000 description 1
- 229960003483 oxiconazole Drugs 0.000 description 1
- 229940105627 oxistat Drugs 0.000 description 1
- 229960000625 oxytetracycline Drugs 0.000 description 1
- 235000019366 oxytetracycline Nutrition 0.000 description 1
- IWVCMVBTMGNXQD-PXOLEDIWSA-N oxytetracycline Chemical compound C1=CC=C2[C@](O)(C)[C@H]3[C@H](O)[C@H]4[C@H](N(C)C)C(O)=C(C(N)=O)C(=O)[C@@]4(O)C(O)=C3C(=O)C2=C1O IWVCMVBTMGNXQD-PXOLEDIWSA-N 0.000 description 1
- LSQZJLSUYDQPKJ-UHFFFAOYSA-N p-Hydroxyampicillin Natural products O=C1N2C(C(O)=O)C(C)(C)SC2C1NC(=O)C(N)C1=CC=C(O)C=C1 LSQZJLSUYDQPKJ-UHFFFAOYSA-N 0.000 description 1
- IPCSVZSSVZVIGE-UHFFFAOYSA-N palmitic acid group Chemical group C(CCCCCCCCCCCCCCC)(=O)O IPCSVZSSVZVIGE-UHFFFAOYSA-N 0.000 description 1
- 229920001277 pectin Polymers 0.000 description 1
- 229960004236 pefloxacin Drugs 0.000 description 1
- FHFYDNQZQSQIAI-UHFFFAOYSA-N pefloxacin Chemical compound C1=C2N(CC)C=C(C(O)=O)C(=O)C2=CC(F)=C1N1CCN(C)CC1 FHFYDNQZQSQIAI-UHFFFAOYSA-N 0.000 description 1
- YCOFRPYSZKIPBQ-UHFFFAOYSA-N penicillic acid Natural products COC1=CC(=O)OC1(O)C(C)=C YCOFRPYSZKIPBQ-UHFFFAOYSA-N 0.000 description 1
- 235000019371 penicillin G benzathine Nutrition 0.000 description 1
- 235000019368 penicillin G potassium Nutrition 0.000 description 1
- 235000019369 penicillin G sodium Nutrition 0.000 description 1
- VOUGEZYPVGAPBB-UHFFFAOYSA-N penicillin acid Natural products OC(=O)C=C(OC)C(=O)C(C)=C VOUGEZYPVGAPBB-UHFFFAOYSA-N 0.000 description 1
- 229940056365 penicillin g benzathine Drugs 0.000 description 1
- 229940056367 penicillin v Drugs 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 229940127557 pharmaceutical product Drugs 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- ORMNNUPLFAPCFD-DVLYDCSHSA-M phenethicillin potassium Chemical compound [K+].N([C@@H]1C(N2[C@H](C(C)(C)S[C@@H]21)C([O-])=O)=O)C(=O)C(C)OC1=CC=CC=C1 ORMNNUPLFAPCFD-DVLYDCSHSA-M 0.000 description 1
- BPLBGHOLXOTWMN-MBNYWOFBSA-N phenoxymethylpenicillin Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)COC1=CC=CC=C1 BPLBGHOLXOTWMN-MBNYWOFBSA-N 0.000 description 1
- WVDDGKGOMKODPV-ZQBYOMGUSA-N phenyl(114C)methanol Chemical compound O[14CH2]C1=CC=CC=C1 WVDDGKGOMKODPV-ZQBYOMGUSA-N 0.000 description 1
- WLJVXDMOQOGPHL-UHFFFAOYSA-N phenylacetic acid Chemical compound OC(=O)CC1=CC=CC=C1 WLJVXDMOQOGPHL-UHFFFAOYSA-N 0.000 description 1
- XEBWQGVWTUSTLN-UHFFFAOYSA-M phenylmercury acetate Chemical compound CC(=O)O[Hg]C1=CC=CC=C1 XEBWQGVWTUSTLN-UHFFFAOYSA-M 0.000 description 1
- 235000011007 phosphoric acid Nutrition 0.000 description 1
- 150000003016 phosphoric acids Chemical class 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 239000000049 pigment Substances 0.000 description 1
- 229960002292 piperacillin Drugs 0.000 description 1
- 210000003635 pituitary gland Anatomy 0.000 description 1
- 229960003342 pivampicillin Drugs 0.000 description 1
- ZEMIJUDPLILVNQ-ZXFNITATSA-N pivampicillin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@@H]3N(C2=O)[C@H](C(S3)(C)C)C(=O)OCOC(=O)C(C)(C)C)=CC=CC=C1 ZEMIJUDPLILVNQ-ZXFNITATSA-N 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- 235000013809 polyvinylpolypyrrolidone Nutrition 0.000 description 1
- 229920000523 polyvinylpolypyrrolidone Polymers 0.000 description 1
- ABVRVIZBZKUTMK-JSYANWSFSA-M potassium clavulanate Chemical compound [K+].[O-]C(=O)[C@H]1C(=C/CO)/O[C@@H]2CC(=O)N21 ABVRVIZBZKUTMK-JSYANWSFSA-M 0.000 description 1
- 229940119343 potassium phenethicillin Drugs 0.000 description 1
- 229960001248 pradofloxacin Drugs 0.000 description 1
- LZLXHGFNOWILIY-APPDUMDISA-N pradofloxacin Chemical compound C12=C(C#N)C(N3C[C@H]4NCCC[C@H]4C3)=C(F)C=C2C(=O)C(C(=O)O)=CN1C1CC1 LZLXHGFNOWILIY-APPDUMDISA-N 0.000 description 1
- OIGNJSKKLXVSLS-VWUMJDOOSA-N prednisolone Chemical compound O=C1C=C[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 OIGNJSKKLXVSLS-VWUMJDOOSA-N 0.000 description 1
- MFDFERRIHVXMIY-UHFFFAOYSA-N procaine Chemical compound CCN(CC)CCOC(=O)C1=CC=C(N)C=C1 MFDFERRIHVXMIY-UHFFFAOYSA-N 0.000 description 1
- 229960004919 procaine Drugs 0.000 description 1
- 235000019260 propionic acid Nutrition 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 229960003415 propylparaben Drugs 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 150000003218 pyrazolidines Chemical class 0.000 description 1
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 1
- 239000003306 quinoline derived antiinfective agent Substances 0.000 description 1
- 229940014063 qvar Drugs 0.000 description 1
- 238000005057 refrigeration Methods 0.000 description 1
- 239000011347 resin Substances 0.000 description 1
- 229920005989 resin Polymers 0.000 description 1
- 229940061341 retisert Drugs 0.000 description 1
- 150000003873 salicylate salts Chemical class 0.000 description 1
- 235000019515 salmon Nutrition 0.000 description 1
- 239000000523 sample Substances 0.000 description 1
- 229960005429 sertaconazole Drugs 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 229960003177 sitafloxacin Drugs 0.000 description 1
- 208000017520 skin disease Diseases 0.000 description 1
- 229940083542 sodium Drugs 0.000 description 1
- 235000010413 sodium alginate Nutrition 0.000 description 1
- 239000000661 sodium alginate Substances 0.000 description 1
- 229940005550 sodium alginate Drugs 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- 229940037001 sodium edetate Drugs 0.000 description 1
- 229940023144 sodium glycolate Drugs 0.000 description 1
- 239000001488 sodium phosphate Substances 0.000 description 1
- 229910000162 sodium phosphate Inorganic materials 0.000 description 1
- 235000011008 sodium phosphates Nutrition 0.000 description 1
- SFKUIGDOGVNRJK-UHFFFAOYSA-N sodium;3-sulfanylpropane-1,2-diol Chemical class [Na].OCC(O)CS SFKUIGDOGVNRJK-UHFFFAOYSA-N 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 229960004954 sparfloxacin Drugs 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 229940063138 sporanox Drugs 0.000 description 1
- 230000006641 stabilisation Effects 0.000 description 1
- 238000011105 stabilization Methods 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 238000005556 structure-activity relationship Methods 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 229960005256 sulbactam Drugs 0.000 description 1
- FKENQMMABCRJMK-RITPCOANSA-N sulbactam Chemical compound O=S1(=O)C(C)(C)[C@H](C(O)=O)N2C(=O)C[C@H]21 FKENQMMABCRJMK-RITPCOANSA-N 0.000 description 1
- 229960004932 sulbenicillin Drugs 0.000 description 1
- 229960002780 talampicillin Drugs 0.000 description 1
- SOROUYSPFADXSN-SUWVAFIASA-N talampicillin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(=O)OC2C3=CC=CC=C3C(=O)O2)(C)C)=CC=CC=C1 SOROUYSPFADXSN-SUWVAFIASA-N 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 235000012222 talc Nutrition 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- LPQZKKCYTLCDGQ-WEDXCCLWSA-N tazobactam Chemical compound C([C@]1(C)S([C@H]2N(C(C2)=O)[C@H]1C(O)=O)(=O)=O)N1C=CN=N1 LPQZKKCYTLCDGQ-WEDXCCLWSA-N 0.000 description 1
- 229960003865 tazobactam Drugs 0.000 description 1
- 229960004576 temafloxacin Drugs 0.000 description 1
- 229940061354 tequin Drugs 0.000 description 1
- IWVCMVBTMGNXQD-UHFFFAOYSA-N terramycin dehydrate Natural products C1=CC=C2C(O)(C)C3C(O)C4C(N(C)C)C(O)=C(C(N)=O)C(=O)C4(O)C(O)=C3C(=O)C2=C1O IWVCMVBTMGNXQD-UHFFFAOYSA-N 0.000 description 1
- 235000019364 tetracycline Nutrition 0.000 description 1
- 150000003522 tetracyclines Chemical class 0.000 description 1
- 229940040944 tetracyclines Drugs 0.000 description 1
- RTKIYNMVFMVABJ-UHFFFAOYSA-L thimerosal Chemical compound [Na+].CC[Hg]SC1=CC=CC=C1C([O-])=O RTKIYNMVFMVABJ-UHFFFAOYSA-L 0.000 description 1
- 229940033663 thimerosal Drugs 0.000 description 1
- 229960004659 ticarcillin Drugs 0.000 description 1
- OHKOGUYZJXTSFX-KZFFXBSXSA-N ticarcillin Chemical compound C=1([C@@H](C(O)=O)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)C=CSC=1 OHKOGUYZJXTSFX-KZFFXBSXSA-N 0.000 description 1
- 229960000223 tilmicosin Drugs 0.000 description 1
- JTSDBFGMPLKDCD-XVFHVFLVSA-N tilmicosin Chemical compound O([C@@H]1[C@@H](C)[C@H](O)CC(=O)O[C@@H]([C@H](/C=C(\C)/C=C/C(=O)[C@H](C)C[C@@H]1CCN1C[C@H](C)C[C@H](C)C1)CO[C@H]1[C@@H]([C@H](OC)[C@H](O)[C@@H](C)O1)OC)CC)[C@@H]1O[C@H](C)[C@@H](O)[C@H](N(C)C)[C@H]1O JTSDBFGMPLKDCD-XVFHVFLVSA-N 0.000 description 1
- 229950008187 tosufloxacin Drugs 0.000 description 1
- 231100000583 toxicological profile Toxicity 0.000 description 1
- 229960002117 triamcinolone acetonide Drugs 0.000 description 1
- JEJAMASKDTUEBZ-UHFFFAOYSA-N tris(1,1,3-tribromo-2,2-dimethylpropyl) phosphate Chemical compound BrCC(C)(C)C(Br)(Br)OP(=O)(OC(Br)(Br)C(C)(C)CBr)OC(Br)(Br)C(C)(C)CBr JEJAMASKDTUEBZ-UHFFFAOYSA-N 0.000 description 1
- RYFMWSXOAZQYPI-UHFFFAOYSA-K trisodium phosphate Chemical compound [Na+].[Na+].[Na+].[O-]P([O-])([O-])=O RYFMWSXOAZQYPI-UHFFFAOYSA-K 0.000 description 1
- DYNZICQDCVYXFW-AHZSKCOESA-N trovafloxacin mesylate Chemical compound CS(O)(=O)=O.C([C@H]1[C@@H]([C@H]1C1)N)N1C(C(=CC=1C(=O)C(C(O)=O)=C2)F)=NC=1N2C1=CC=C(F)C=C1F DYNZICQDCVYXFW-AHZSKCOESA-N 0.000 description 1
- 229940055820 trovan Drugs 0.000 description 1
- 229940029469 vagistat Drugs 0.000 description 1
- 230000003639 vasoconstrictive effect Effects 0.000 description 1
- 239000005526 vasoconstrictor agent Substances 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
- 229940110854 veramyst Drugs 0.000 description 1
- 229940034215 vigamox Drugs 0.000 description 1
- 239000011718 vitamin C Substances 0.000 description 1
- 235000019154 vitamin C Nutrition 0.000 description 1
- 229940049589 zagam Drugs 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
- 239000011701 zinc Substances 0.000 description 1
- UHVMMEOXYDMDKI-JKYCWFKZSA-L zinc;1-(5-cyanopyridin-2-yl)-3-[(1s,2s)-2-(6-fluoro-2-hydroxy-3-propanoylphenyl)cyclopropyl]urea;diacetate Chemical compound [Zn+2].CC([O-])=O.CC([O-])=O.CCC(=O)C1=CC=C(F)C([C@H]2[C@H](C2)NC(=O)NC=2N=CC(=CC=2)C#N)=C1O UHVMMEOXYDMDKI-JKYCWFKZSA-L 0.000 description 1
- 229940109235 zymar Drugs 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/496—Non-condensed piperazines containing further heterocyclic rings, e.g. rifampin, thiothixene or sparfloxacin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/58—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids containing heterocyclic rings, e.g. danazol, stanozolol, pancuronium or digitogenin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/12—Carboxylic acids; Salts or anhydrides thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0046—Ear
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/16—Otologicals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/10—Antimycotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Epidemiology (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Engineering & Computer Science (AREA)
- Oncology (AREA)
- Communicable Diseases (AREA)
- Dispersion Chemistry (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
Abstract
Предложены: фармацевтическая композиция для лечения инфекции, включающая мометазона фуроат или его сольват, орбифлоксацин, жирную кислоту, содержащую от 3 до 18 атомов углерода и имеющую температуру плавления не более примерно 60°С; способ лечения инфекции у животного, включающий ее введение, применение указанной композиции для получения лекарственного средства для лечения инфекции у животного и терапевтический набор для лечения инфекции, включающий эту композицию. Показана устойчивость хранения заявленного состава при комнатной температуре. Приведены примеры стабильного состава суспензий, предназначенных, например, для лечения ушных инфекций. 4 н. и 10 з.п. ф-лы, 11 табл., 3 пр.
Description
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к композициям, включающим антибиотик (как правило, хинолон или нафтиридинон), кортикостероид и органическую кислоту (как правило, жирную кислоту). Кроме того, настоящее изобретение относится к способам лечения, в которых применяются эти композиции, применению этих композиций для изготовления лекарственных средств, а также к терапевтическим наборам, включающим эти композиции.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
В опубликованной заявке на патент США № 2006-0122159 обсуждаются фармацевтические составы, пригодные для лечения инфекций у животных, в частности ушных инфекций. Эти композиции, как правило, включают кортикостероид, антибиотик и триазол. В число этих составов входят, например, суспензии, содержащие мометазона фуроата моногидрат, орбифлоксацин и позаконазол. Конкретный состав, приведенный в качестве иллюстрации в опубликованной заявке на патент США № 2006-0122159, показан в таблице 1.
| Таблица 1 Состав примера 1 опубликованной заявки на патент США № 2006-0122159 |
|
| Ингредиент | мг/г |
| Тонкоизмельченный орбифлоксацин | 10,0 |
| Тонкоизмельченный мометазона фуроата моногидрат | 1,0 |
| Тонкоизмельченный позаконазол | 1,0 |
| Минеральное масло USP (40 сантистокс) | 685,0 |
| Основа мази - пластифицированный углеводородный гель (Plastibase® 50W, содержащий 5% полиэтилена и 95% минерального масла) | количество, достаточное для доведения общей массы до 1 г |
Авторы изобретения наблюдали увеличение содержания по меньшей мере одного продукта разрушения мометазона с течением времени, если приведенный выше состав хранился при комнатной температуре. Кроме того, авторы заявки установили, что наличие в составе орбифлоксацина ускоряет образование этого продукта разрушения. Как правило, образование продукта разрушения может быть сведено к минимум в случае хранении состава при пониженных температурах (например, 5°C). Однако существует потребность в составах, которые могут оставаться устойчивыми при более высоких температурах (например, при комнатной температуре). Такой состав предложен в настоящем изобретении.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Вкратце, настоящее изобретение в основном относится к композициям (например, суспензиям), которые включают кортикостероид и антибиотик. Эти композиции, как правило, устойчивы при комнатной или более высокой температуре (например, при 50°C) в течение продолжительного периода времени (например, 5 месяцев). Преимущества таких стабильных композиций, как правило, включают, например, устранение расходов и трудозатрат, связанных с охлаждением, устранение риска разрушения продукта из-за отказа холодильного оборудования, а также отсутствие опасности введения разложившегося продукта пациенту после небрежного хранения без охлаждения.
Таким образом, настоящее изобретение относится в том числе к фармацевтической композиции. Эта композиция включает кортикостероид, антибиотик и органическую кислоту. В число органических кислот в основном входят жирные кислоты, которые, в свою очередь, включают от примерно 3 до примерно 18 атомов углерода и имеют температуру плавления, не превышающую примерно 60°C. В некоторых вариантах осуществления в число антибиотиков входят хинолоны (в частности, фторхинолон, соль фторхинолона, сольват фторхинолона или его соли). В других вариантах осуществления антибиотики включают нафтиридинон (в частности, фторнафтиридинон, соль фторнафтиридинона, сольват фторнафтиридинона или его соли).
Также настоящее изобретение относится, в числе прочего, к способу лечения инфекции у животного путем введения животному описанной выше композиции.
Кроме того, настоящее изобретение относится в том числе к применению описанной выше композиции для получения лекарственного средства для лечения инфекции у животного.
Помимо этого, настоящее изобретение относится, в числе прочего, к терапевтическому набору. Этот набор включает описанную выше композицию и дополнительный компонент. Этот дополнительный компонент может являться, например, средством диагностики, раствором для очистки слуховых путей, устройством для очистки слуховых путей, инструкциями по введению композиции животному или устройством для введения композиции животному.
Другие преимущества изобретения авторов настоящей заявки будут ясны специалисту в данной области техники при прочтении настоящего описания.
ПОДРОБНОЕ ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНЫХ ВАРИАНТОВ
ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Настоящее подробное описание предпочтительных вариантов осуществления изобретения предназначено только для ознакомления специалистов в данной области техники с изобретением заявителей, с его основными идеями и практическим применением, с тем чтобы специалисты в данной области могли адаптировать и применить изобретение в его многочисленных формах, так чтобы эти формы могли наилучшим образом соответствовать требованиям того или иного конкретного применения. Это подробное описание и приведенные конкретные примеры, хотя и демонстрируют предпочтительные варианты осуществления настоящего изобретения, предназначены только для иллюстративных целей. Следовательно, настоящее изобретение не ограничено предпочтительными вариантами осуществления, раскрытыми в данном описании, и может подвергаться различным модификациям.
I. Композиция
Фармацевтическая композиция по настоящему изобретению, как правило, включает кортикостероид, антибиотик и органическую кислоту. Прежде всего, необходимо отдавать себе отчет, что этот перечень ингредиентов не является исчерпывающим. Следовательно, композиция по настоящему изобретению может (и, как правило, будет) содержать дополнительные ингредиенты. Эти дополнительные ингредиенты могут включать, например, один или несколько дополнительных кортикостероидов, антибиотиков и/или органических кислот. Кроме того, как будет обсуждаться более подробно далее по тексту, эти дополнительные ингредиенты могут включать один или несколько других действующих ингредиентов. И, как также будет обсуждаться ниже, эти дополнительные ингредиенты могут (и, как правило, будут) включать один или несколько наполнителей.
Композиции по настоящему изобретению в основном могут принимать различные формы, в частности нетвердые формы. Например, эти композиции могут иметь форму суспензии, раствора, эмульсии, мази и т.д. В некоторых вариантах осуществления композиция по настоящему изобретению имеет форму суспензии.
A. Кортикостероид
Кортикостероиды, как правило, являются природными и синтетическими аналогами гормонов, секретируемых системой гипоталамус - передняя доля гипофиза - кора надпочечников (известной также как гипофиз). Общеизвестно, что кортикостероиды (в частности, глюкокортикостероиды), являются мощными противовоспалительными агентами. Кроме того, они, как правило, демонстрируют противозудное и сосудосуживающее действие. Различные кортикостероиды применяют, например, местно для лечения дерматозов, восприимчивых к их действию, таких как псориаз и атопический дерматит.
Примеры кортикостероидов включают соединения, показанные в таблице 2 (а также соли этих соединений и сольваты соединений и их солей).
| Таблица 2 Примеры кортикостероидов |
||
| Кортикостероид | Примеры опубликованных торговых наименований продуктов, содержащих данный кортикостероид | Структура |
| беклометазона дипропионат | Beclovent® QVAR® Vanceril |
|
| бетаметазона дипропионат | Diprosone Diprolene® |
|
| бетаметазона валерат | Celestone® M Bentovate® |
|
| будесонид | Entocort® EC Rhinocort Aqua® |
|
| циклесонид | Alvesco® Omnaris® |
|
| дефлазакорд | Calcort | |
| дексаметазон | Azium® Dexacort Decadron® |
| флуоцинолона ацетонид | Derma-Smoothe/FS Retisert® |
|
| флутиказона пропионат | Flixotide Flovent® Flixonase |
|
| флутиказона фуроат | Veramyst® | |
| лотепреднола этабонат | Alrex® Lotemax® |
| метилпреднизолон | Medrol® | |
| преднизолон | Prelon® Meti-Derm |
|
| преднизон | Deltasone Orasone® Meticorten |
|
| рофлепонид | ||
| триамцинолона ацетонид | Nasacort® Tricortone |
В некоторых вариантах осуществления кортикостероиды в композиции по настоящему изобретению включают кортикостероид, выбранный из группы, состоящей из соединений таблицы 2, их солей, а также сольватов соединений и их солей.
В других вариантах осуществления кортикостероид включает мометазон, соль мометазона или сольват мометазона или соли мометазона. Мометазон является синтетическим глюкокортикостероидом и имеет следующую структуру:
В других вариантах осуществления в число кортикостероидов входят сложный эфир мометазона, соль сложного эфира мометазона или сольват сложного эфира мометазона или соли сложного эфира мометазона.
В некоторых из таких вариантов осуществления сложный эфир мометазона включает мометазона фуроат. Мометазона фуроат имеет следующую структуру:
Химическое наименование этого соединения: 9,21-дихлор-11(бета),17-дигидрокси-16(альфа)-метилпрегна-1,4-диен-3,20-диона 17-(2-фуроат). Мометазона фуроат является, например, действующим компонентом крема, лосьона и мази Elocon®, и его можно приобрести у Schering-Plough Corporation (Kenilworth, NJ).
Кортикостероиды могут существовать в различных энантиомерных формах. Кроме того, они могут существовать в различных кристаллических формах. Например, как указано выше, может применяться сольват мометазона фуроата. В некоторых вариантах осуществления этот сольват включает, например, гидрат. Гидрат может представлять собой, например, моногидрат.
В некоторых вариантах осуществления кортикостероид включает моментазон, мометазона фуроат или сольват мометазона или мометазона фуроата (например, моногидрат мометазаона фуроата).
Как правило, общее содержание кортикостероида в композиции по настоящему изобретению достаточно для того, чтобы кортикостероид являлся терапевтически эффективным при той дозировке, в которой вводят композицию. В некоторых вариантах осуществления общая концентрация кортикостероида (например, мометазона, мометазона фуроата и/или сольвата мометазона или мометазона фуроата) в композиции составляет как минимум примерно 0,01% (по массе). В некоторых из таких вариантов осуществления, например, общая концентрация составляет от примерно 0,01 до примерно 1% (по массе).
B. Антибиотик
В некоторых вариантах осуществления настоящего изобретения в число антибиотиков входят хинолоны. Как правило, хинолоны включают фторхинолон, соль фторхинолона или сольват фторхинолона или его соли. Фторхинолоновые антибиотики включают, например, 6-фторхинолин-4(1H)-оны соли 6-фторхинолин-4(1H)-онов и сольваты 6-фторхинолин-4(1H)-онов и их солей. Примеры 6-фторхинолин-4(1H)-онов включают соединения, показанные в таблице 3.
| Таблица 3 Примеры 6-фторхинолин-4(1H)-онов |
||
| 6-фторхинолин-4(1H)-он | Примеры опубликованных торговых наименований продуктов, содержащих данный 6-фторхинолин-4(1H)-он | Структура |
| амифлоксацин | ||
| балофлоксацин | ||
| ципрофлоксацин | Cipro®, Ciprobay, и Ciproxin | |
| клинафлоксацин | ||
| данофлоксацин | Advocin и Advocid | |
| дифлоксацин | Dicural® и Vetequinon | |
| энрофлоксацин | Baytril® | |
| флероксацин | Megalone |
| флумеквин | Flubactin | |
| гареноксацин | ||
| гатифлоксацин | Tequin® и Zymar® | |
| грепафлоксацин | Raxar | |
| ибафлоксацин | ||
| левофлоксацин | Levaquin®, Gatigol, Tavanic, Lebact, Levox и Cravit |
| ломефлоксацин | Maxaquin® | |
| марбофлоксацин | Marbocyl® и Zenequin | |
| моксифлоксацин | Avelox® и Vigamox® | |
| надифлоксацин | Acuatin, Nadoxia и Nadixa | |
| норфлоксацин | Noroxin®, Lexinor, Quinabic и Janacin | |
| офлоксацин | Floxin®, Oxaldin и Tarivid |
| руфлоксацин | Uroflox | |
| сарафлоксацин | Floxasol, Saraflox, Sarafin | |
| ситафлоксацин | ||
| спарфлоксацин | Zagam | |
| темафлоксацин | Omniflox |
Другие примеры 6-фторхинолин-4(1H)-онов включают соединения, показанные в таблице 4.
Смотрите Chu et al., “Minireview: Structure-Activity Relationships of the Fluoroquinolones”, Antimicrobial Agents and Chemotherapy, 33(2), pp.131-135 (Feb.1989).
В некоторых вариантах осуществления, антибиотики включают антибиотик, выбранный из группы, состоящей из 6-фторхинолин-4(1H)-онов, показанных в таблице 3, солей этих 6-фторхинолин-4(1H)-онов, а также сольватов этих 6-фторхинолин-4(1H)-онов и их солей.
В некоторых вариантах осуществления антибиотики включают антибиотик, выбранный из группы, состоящей из амифлоксацина, балофлоксацина, ципрофлоксацина, клинафлоксацина, флекроксацина, гареноксацина, гатифлоксацина, грепафлоксацина, ломефлоксацина, моксифлоксацина, норфлоксацина, пефлоксацина, прадофлоксацина, ситафлоксацина, спарфлоксацина и темафлоксацина; солей этих 6-фторхинолин-4(1H)-онов; а также сольватов этих 6-фторхинолин-4(1H)-онов и их солей.
В некоторых вариантах осуществления антибиотики включают антибиотик, выбранный из группы, состоящей из данофлоксацина, дифлоксацина, энрофлоксацина и сарафлоксацина; солей этих 6-фторхинолин-4(1H)-онов; а также сольватов этих 6-фторхинолин-4(1H)-онов и их солей.
В некоторых вариантах осуществления антибиотики включают антибиотик, выбранный из группы, состоящей из 6-фторхинолин-4(1H)-онов, показанных в таблице 4, солей этих 6-фторхинолин-4(1H)-онов, а также сольватов этих 6-фторхинолин-4(1H)-онов и их солей.
В некоторых вариантах осуществления антибиотики включают орбифлоксацин, соль орбифлоксацина или сольват орбифлоксацина или соли орбифлоксацина. Орбифлоксацин представляет собой известный эффективный антибактериальный агент широкого спектра действия, безопасный и эффективный для лечения различных заболеваний, в частности у собак и кошек.
В некоторых вариантах осуществления антибиотики включают 6-фторхинолин-4(1H)-он, который содержит три цикла, конденсированных друг с другом. В некоторых из этих вариантов осуществления, например, в число антибиотиков входит антибиотик, выбранный из группы, состоящей из флумеквина, ибафлоксацина, левофлоксацина, надифлоксацина, офлоксацина, пазуфлоксацина, прулифлоксацина и руфлоксацина; солей этих 6-фторхинолин-4(1H)-онов; а также сольватов этих 6-фторхинолин-4(1H)-онов и их солей. В других вариантах осуществления антибиотик включает марбофлоксацин, соль марбофлоксацина или сольват марбофлоксацина или соли марбофлоксацина.
В других вариантах осуществления в число антибиотиков входят нафтиридиноны. Как правило, нафтиридиноны включают фторнафтиридиноны, соли фторнафтиридинонов или сольваты фторнафтиридинонов или их солей. Фторнафтиридиноновые антибиотики включают, например, 6-фтор-1,8-нафтиридин-4(1H)-оны, соли 6-фтор-1,8-нафтиридин-4(1H)-онов и сольваты 6-фтор-1,8-нафтиридин-4(1H)онов и их солей. Примеры 6-фтор-1,8-нафтиридин-4(1H)-онов включают соединения, показанные в таблице 5.
| Таблица 5 Примеры 6-фтор-1,8-нафтиридин-4(1H)-онов |
||
| 6-фтор-1,8-нафтиридин-4(1H)-он | Примеры опубликованных торговых наименований продуктов, содержащих данный 6-фтор-1,8-нафтиридин-4(1H)-он | Структура |
| эноксацин | Penetrex и Enroxil | |
| гемифлоксацин | Factive | |
| тозуфлоксацин | ||
| тровафлоксацин | Trovan | |
В некоторых вариантах осуществления в число антибиотиков входит антибиотик, выбранный из группы, состоящей из 6-фтор-1,8-нафтиридин-4(1H)-онов, показанных в таблице 5, солей этих 6-фтор-1,8-нафтиридин-4(1H)-онов и сольватов этих 6-фтор-1,8-нафтиридин-4(1H)-онов и их солей.
В некоторых вариантах осуществления в число антибиотиков входит антибиотик, выбранный из группы, состоящей из эноксацина, гемифлоксацина, тозуфлоксацина и тровафлоксацина; солей этих 6-фтор-1,8-нафтиридин-4(1H)-онов; и сольватов этих 6-фтор-1,8-нафтиридин-4(1H)-онов и их солей.
Другие примеры 6-фтор-1,8-нафтиридин-4(1H)-онов включают:
Смотрите Chu et al., Antimicrobial Agents and Chemotherapy, на стр. 132. В некоторых вариантах осуществления антибиотик включает это соединение, его соль или сольват этого соединения или его соли.
Как правило, концентрация антибиотика в композиции по настоящему изобретению достаточна для того, чтобы антибиотик являлся терапевтически эффективным при той дозировке, в которой вводят композицию. В некоторых вариантах осуществления концентрация антибиотика в композиции (т.е. общая концентрация всех антибиотиков в композиции) составляет как минимум примерно 0,01% (по массе). В некоторых вариантах осуществления эта концентрация составляет от примерно 0,01 до примерно 30% (по массе), от примерно 0,1 до примерно 10% (по массе) или от примерно 0,5 до примерно 5% (по массе).
C. Органическая кислота
Органические кислоты, как правило, включают жирные кислоты. Эти жирные кислоты предпочтительно содержат как минимум примерно 3 атома углерода. В некоторых вариантах осуществления жирная кислота содержит например, от примерно 3 до примерно 18 атомов углерода. В других вариантах осуществления жирная кислота содержит, от примерно 4 до примерно 18 атомов углерода. В еще одной группе вариантов осуществления эта жирная кислота содержит от примерно 7 до примерно 18 атомов углерода.
Жирная кислота может быть природной жирной кислотой или синтетической кислотой. Кроме того, она может быть насыщенной или ненасыщенной. В некоторых вариантах осуществления жирная кислота включает неразветвленную алифатическую цепь, которая содержит не менее примерно 4 атомов углерода и является насыщенной или ненасыщенной. Предпочтительно эта жирная кислота имеет температуру плавления более примерно 60°C.
Эта жирная кислота предпочтительно растворяет или смешивается с носителем, присутствующим в композиции, при тех температурах, при которых применяется композиция. Кроме того, жирная кислота предпочтительно растворяет или смешивается с носителем, присутствующим в композиции, при тех температурах, при которых осуществляется хранение композиции. Так, например, в некоторых вариантах осуществления, в которых композиция представляет собой суспензию, включающую носитель на основе минерального масла, жирная кислота способна смешиваться с минеральным маслом при комнатной температуре (т.е. от примерно 20 до примерно 25°C). В таких вариантах осуществления жирная кислота также предпочтительно способна смешиваться с минеральным маслом при более низких или более высоких температурах, при которых композиция может применяться или храниться.
В некоторых вариантах осуществления в число жирных кислот входит пропионовая кислота (которая содержит 3 атома углерода). В других вариантах осуществления в число жирных кислот входит миристиновая кислота (которая содержит 14 атомов углерода). В других вариантах осуществления в число жирных кислот входит лауриновая кислота (которая содержит 12 атомов углерода). В еще одной группе вариантов осуществления в число жирных кислот входит олеиновая кислота (которая содержит 18 атомов углерода). Следует понимать, что композиция по настоящему изобретению может включать более чем одну жирную кислоту. Например, в некоторых вариантах осуществления композиция включает как олеиновую, так и лауриновую кислоту.
Как правило, концентрация жирной кислоты в композиции достаточная для эффективного уменьшения (и предпочтительно частичного или полного подавления) образования продукта распада как минимум одного кортикостероида (например, мометазона или момметазона фуроата) в течение как минимум 1 месяца, как минимум 2 месяцев, как минимум 5 месяцев при хранении в пластиковых бутылках, изготовленных из полиэтилена высокой плотности (“HDPE”), c крышками, изготовленными из полиэтилена низкой плотности (“LDPE”) при температуре не менее 15°C, не менее 20°C, не менее 25°C, не менее 40°C или не менее 50°C. В некоторых вариантах осуществления концентрация жирной кислоты составляет не менее примерно 0,01% (по массе). В некоторых из таких вариантов осуществления, например, концентрация составляет от примерно 0,01 до примерно 5,0% (по массе). В других вариантах осуществления концентрация составляет от примерно 0,1 до примерно 2,0% (по массе). В некоторых вариантах осуществления композиция по настоящему изобретению включает олеиновую кислоту, и концентрация олеиновой кислоты в композиции составляет от примерно 0,1 до примерно 2,0% (по массе). В других вариантах осуществления композиция включает лауриновую кислоту, и концентрация лауриновой кислоты составляет от примерно 0,1 до примерно 1,0% (по массе).
D. Дополнительные ингредиенты, входящие в композицию
Как было отмечено выше, композиция по настоящему изобретению может (и, как правило, будет) включать и другие ингредиенты. Эти ингредиенты могут представлять собой, например, один или несколько других действующих ингредиентов и/или один или несколько наполнителей.
i. Другие действующие ингредиенты
Предполагается, что в состав композиции по настоящему изобретению можно включить целый ряд других действующих ингредиентов, помимо кортикостероида и антибиотика. Любые из таких действующих ингредиентов предпочтительно являются подходящими для тех ситуаций, в которых применяются композиции по настоящему изобретению, и не оказывают значительного отрицательного воздействия на активность кортикостероида и антибиотика.
В некоторых вариантах осуществления композиция по настоящему изобретению включает противогрибковое средство. В некоторых из таких вариантов осуществления в число противогрибковых средств входят, например, имидазолы, соли имидазолов или сольваты имидазолов или их солей. Имидазолы включают, например, соединения, показанные в таблице 6.
| Таблица 6 Примеры противогрибковых имидазолов |
||
| Имидазол | Примеры опубликованных торговых наименований продуктов, содержащих данный имидазол | Структура |
| клотримазол | Canesten®, MyCelex®, Lotrimin®, Lotrimin AF®, Agisten, Clotrimaderm и Clotrimazole-Teva | |
| эконазол | Spectazole® | |
| изоконазол | Travogen | |
| кетоконазол | Nizoral® | |
| миконазол | Monistat® | |
| нетиконазол | Atolant | |
| оксиконазол | Oxistat® |
В некоторых вариантах осуществления противогрибковые средства включают противогрибковое средство, выбранное из группы, состоящей из имидазолов, показанных в таблице 6, солей этих имидазолов и сольватов этих имидазолов и их солей.
В других вариантах осуществления в число противогрибковых средств входят триазолы, соли триазолов или сольваты триазолов или их солей. Триазолы включают, например, соединения, показанные в таблице 7.
| Таблица 7 Примеры противогрибковых триазолов |
||
| Триазол | Примеры опубликованных торговых наименований продуктов, содержащих данный триазол | Структура |
| флуконазол | Diflucan® и Trican |
|
| итраконазол | Sporanox® | |
| позаконазол | Noxafil® | |
| саперконазол | ||
В некоторых вариантах осуществления противогрибковые средства включают противогрибковые средства, выбранные из группы, состоящей из триазолов, показанных в таблице 7, солей этих триазолов и сольватов этих триазолов и их солей.
В некоторых вариантах осуществления в число противогрибковых средств входит позаконазол, соль позаконазола или сольват позаконазола или его соли. В некоторых из таких вариантов осуществления антибиотики включают, например, позаконазол. Известно, что позаконазол обладает противогрибковой активностью в отношении широкого спектра грибков, включая Aspergillis, Candida, Cryptoccoccus, Fusarium и других условно-патогенных грибков. Обсуждения, связанные с позаконазолом, могут быть найдены, например, в патентах США 5661151; 5834472 и 5846971.
В некоторых вариантах осуществления в число противогрибковых средств входит нистатин, соль нистатина или сольват нистатина или соли нистатина. Нистатин имеет следующую структуру:
Как правило, концентрация противогрибкового средства в композиции является достаточной для того, чтобы это противогрибковое средство являлось терапевтически эффективным при той дозировке, в которой вводится композиция. Если в композиции имеется более одного противогрибкового средства, общая концентрация всех противогрибковых средств является достаточной для того, чтобы комбинация противогрибковых средств была терапевтически эффективной при той дозировке, в которой вводят композицию. В некоторых вариантах осуществления концентрация противогрибкового средства в композиции (т.е. общая концентрация всех противогрибковых средств в композиции) составляет как минимум примерно 0,01% (по массе). В некоторых вариантах осуществления концентрация составляет, например, от приблизительно 0,01 до приблизительно 1,0% (по массе).
В некоторых вариантах осуществления композиция по настоящему изобретению включает один или несколько антибиотиков (в дополнение к хинолоновому или нафтиридиноновому антибиотику (антибиотикам)). Эти антибиотики могут включать, например, перечисленные ниже антибиотики (а также их соли, их сольваты и сольваты их солей).
A. Хлорамфеникол, тиамфеникол и фторсодержащие аналоги хлорамфеникола и тиамфеникола (например, фторфеникол или D-(трео)-1-п-метилсульфонил фенил-2-дифторацетамидо-3-фтор-1-пропанол).
B. Тетрациклины, например хлортетрациклин и окситетрациклин.
C. Амоксициллин, ампициллин, ампициллина тригидрат, ампициллин натрия, апалциллин, аспоксициллин, азлоциллин, бакампициллин, карбенициллин, карбенициллин натрия, карфециллин, кариндациллин, циклациллин, клоксациллин натрия, клоксациллин бензатин, диклоксациллин, диклоксациллин натрия, флуклоксациллин, гетациллин, ленампициллин, мециллинам, метампициллин, метициллин, мезлоциллин, нафциллин, нафциллин натрия, оксациллин, пеницилловую кислоту, пенициллин G, пенициллин G бензатин, пенициллин G калий, пенициллин G натрий, пенициллин V, фенетициллин, фенетициллин калия, пиперациллин, пиперациллин натрия, пивампициллин, сулбенициллин, султамициллин, талампициллин, тикарциллин, цефаклор, цефадроксил, цефадроксила моногидрат, цефамандол, цефамандол лития, цефамандола нанфат, цефамандол натрия, цефазафлур, цефазедон, цефазолин, цефазолин натрия, цефклидин, цефдинир, цефепим, цефетамет, цефиксим, цефлупренам, цефменоксим, цефметазол натрия, цефодизим, цефоницид, цефоперазон, цефоперазон натрия, цефоранид, цефоселис, цефотаксим, цефотаксим натрия, цефотиам, цефозопран, цефпимизол, цефпимизол натрия, цефпирамид, цефпиром, цефподоксим, цефпрозил, цефхином, цефроксадин, цефсулодин, цефсулодина натрия гидрат, цефтазидим, цефтазидима пентагидрат, цефтезол, цефтибутен, цефтиолен, цефтизоксим, цефтриаксон, динатриевую соль цефтриаксона, цефтриаксон натрия, цефуроксим, цефузонам, цефацетрил, цефалексин, цефалоридин, цефалоспорин C, цефалотин, цефалотин натрия, цефапирин, цефапирин натрия, цефрадин, лоракарбеф, цефбуперазон, цефокситин, цефокситин натрия, цефминокс, цефметазол, цефотетан, сами по себе, либо в комбинации с ингибиторами β-лактамазы, например, клавулановой кислотой, калия клавуланатом, сульбактам йодпенициллановой кислотой, 6-бромпенициллановой кислотой, оливановой кислотой и тазобактамом.
D. Макролидные антибиотики, например азитромицин, брефелдин, кларитромицин, эритромицин, эритромицина эстолат, эритромицина этилсукцинат, эритромицина стеарат, йозамицин, китазамицин, тулатромицин и тилмикозин.
В некоторых вариантах осуществления композиция по настоящему изобретению включает один или несколько противовоспалительных ингредиентов, помимо кортикостероида(ов). В число этих противовоспалительных ингредиентов могут входить, например, одно или несколько нестероидных противовоспалительных средств (“NSAIDs”). NSAIDs включают, например, салицилаты, арилалкановые кислоты, 2-арилпропионовые кислоты (или «профены»), N-арилантраниловые кислоты, производные пиразолидина, оксикамы, ингибиторы COX-2, сульфонанилиды и ликофелон. В некоторых вариантах осуществления NSAID включают аспирин, ибупрофен или напроксен. Противовоспалительные ингредиенты могут включать также, например, антигистаминные препараты. В число антигистаминных препаратов входят, например, агонисты рецептора H1, агонисты рецептора H2, агонисты рецептора H3, агонисты рецептора H4, стабилизаторы мастоцитов и витамин C.
ii. Наполнители
Подходящие наполнители композиций по настоящему изобретению включают, например, жидкие носители, средства для улучшения вязкости, поверхностно-активные вещества (ПАВ), консерванты, стабилизаторы, смолы, наполнители, связующие средства, смазывающие средства, средства для улучшения скольжения, дезинтегрирующие средства, сорастворители, а также красители или пигменты фармацевтической категории.
В некоторых вариантах осуществления композиции по настоящему изобретению имеют форму суспензий. Эти композиции обычно включают жидкую основу (или «носитель»), например воду, углеводород, животные жиры, растительные масла, минеральное масло или синтетическое масло. Также в число носителей могут быть включены физиологический солевой раствор или гликоли (например, этиленгликоль, пропиленгликоль или полипропиленгликоль). В некоторых вариантах осуществления жидкий носитель включает минеральное масло.
Композиции по настоящему изобретению, как правило, включают одно или несколько средств для увеличения вязкости (или «загустителей»). Концентрация средства для увеличения вязкости в композиции обычно составляет не менее примерно 0,1% (по массе). Например, в некоторых вариантах осуществления эта концентрация составляет от примерно 0,1 до примерно 15% (по массе). В некоторых из таких вариантов осуществления концентрация составляет, например, от приблизительно 0,1 до приблизительно 5%. В других вариантах осуществления эта концентрация составляет от примерно 2 до примерно 10% (по массе) или от примерно 4 до примерно 8% (по массе). В некоторых вариантах осуществления средство для увеличения вязкости включает полиэтилен. Полиэтилен представляет собой инертный углеводород с высокой молекулярной массой и высокой температурой плавления. Его можно применять в качестве загустителя для повышения вязкости, например минерально-масляной основы. В некоторых вариантах осуществления полиэтилен вводят в композицию в форме Plastibase® 50W (можно приобрести у Bristol-Myers Squibb). Plastibase® 50W содержит 5% полиэтилена в 95% минерального масла. Кроме того (или в качестве альтернативы), могут применяться и другие предполагаемые средства для увеличения вязкости. В некоторых вариантах осуществления в число средств для увеличения вязкости входят, например, метилцеллюлоза, карбоксиметилцеллюлоза натрий, гидроксипропил-метилцеллюлоза, гидроксипропилцеллюлоза, альгинат натрия, карбомер, повидон, гуммиарабик, гуаровая камедь, ксантановая камедь или трагакант. В других вариантах осуществления средство для увеличения вязкости включает метилцеллюлозу, карбомер, ксантановую камедь, гуаровую камедь, повидон, натрий карбоксиметилцеллюлозу или силикат магния алюминия. В других вариантах осуществления средство для улучшения вязкости включает карбоксивиниловые полимеры; каррагинан; гидроксиэтилцеллюлозу; лапонит; а также водорастворимые соли и простые эфиры целлюлозы, например, натрий карбоксиметилцеллюлозу и натрий карбоксиметил гидроксиэтил целлюлозу. В еще одной группе вариантов осуществления средство для улучшения вязкости может представлять собой природные камеди, например камедь карайи, ксантановая камедь, гуммиарабик или камедь трагаканта. В следующей группе вариантов осуществления средства для увеличения вязкости включают коллоидный силикат магния алюминия или тонкоизмельченный оксид кремния, который может применяться в качестве составной части загустителя для дополнительного улучшения текстуры. В других вариантах осуществления средства для улучшения вязкости включают гомополимеры акриловой кислоты, поперечно сшитые алкиловым эфиром пентаэритрита или алкиловым эфиром сахарозы, или карбомеры. Карбомеры можно приобрести у B.F. Goodrich, как продукты серии Carbopol®. В некоторых вариантах осуществления карбомер представляет собой Carbopol® 934, 940, 941, 956 или их смесь. Сополимеры лактидных и гликолидных мономеров могут применяться для доставки действующих веществ, в частности, если этот сополимер имеет молекулярную массу от примерно 1000 до примерно 120000 (среднечисловая молекулярная масса). Эти полимеры описаны в патентах США 5198220; 5242910 и 4443430.
Подходящие ПАВ включают, например, сложные эфиры полиоксиэтиленсорбитана и жирных кислот; моноалкиловые простые эфиры полиоксиэтилена; сложные моноэфиры сахарозы; сложные и простые эфиры ланолина; соли алкилсульфатов; а также натриевые, калиевые и аммониевые соли жирных кислот.
Подходящие консерванты включают, например, фенол; алкиловые эфиры парагидроксибензойной кислоты (например, метил п-гидроксибензоат (или «метилпарабен») и пропил п-гидроксибензоат (или «пропилпарабен»)); сорбиновую кислоту; о-фенилфенол бензойную кислоту и ее соли; хлорбутанол; бензиловый спирт; тимеросал; ацетат и нитрат фенилртути; нитромерсол; бензалкония хлорид; и цетилпиридиния хлорид. Особенно подходящим консервантом является сорбиновая кислота. Если композиция по настоящему изобретению включает консервант, концентрация консерванта в этой композиции, как правило, не превышает примерно 5% (по массе). В некоторых вариантах осуществления концентрация консерванта составляет, например, от приблизительно 0,01 до приблизительно 5% (по массе).
Подходящие стабилизаторы включают, например, хелатообразующие агенты, такие как, эдетат натрия. Кроме того, подходящие стабилизаторы включают, например, антиоксиданты, такие как бутилзамещенный гидроксианизол и монотиоглицерин натрий.
Подходящие связующие вещества включают, например, желатин, гуммиарабик и карбоксиметилцеллюлозу.
Подходящие смазывающие вещества включают, например, стеарат магния, стеариновую кислоту и тальк.
Подходящие дезинтегрирующие средства включают, например, кукурузный крахмал и альгиновую кислоту.
В композицию по настоящему изобретению при желании можно добавлять другие инертные ингредиенты. Предполагается, что эти ингредиенты могут включать, например, лактозу, маннит, сорбит, карбонат кальция, карбонат натрия, тризамещенный фосфат кальция, дизамещенный фосфат кальция, фосфат натрия, каолин, прессуемый сахар, крахмал, сульфат кальция, декстро или микрокристаллическую целлюлозу, коллоидный диоксид кремния, крахмал, крахмал гликолят натрия, кроссповидон, кросскармелозу натрия, микрокристаллическую целлюлозу, трагакант, гидроксипропилцеллюлозу, прежелатинированный крахмал, повидон, этилцеллюлозу, гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу и метилцеллюлозу.
E. Соли
Как было отмечено выше, многие соединения, присутствующие в композициях по настоящему изобретению, могут входить в ее состав в форме солей. Например, форму солей могут иметь многие из описанных выше антибиотиков, кортикостероидов и противогрибковых средств. Соль может иметь преимущество благодаря одному или нескольким из своих физических свойств, например фармацевтической устойчивости при различных значениях температуры и влажности; кристаллическим свойствам; и/или желаемой растворимости в воде, масле или другом растворителе. Соли кислот и оснований чаще всего можно получить, например, смешивая соединение, соответственно, с кислотой или основанием и применяя различные методики, известные в технике. Как правило, если соединение по настоящему изобретению предполагается вводить in vivo (т.е. животным) для достижения терапевтического результата, все соли в составе композиции предпочтительно являются фармацевтически приемлемыми.
Кислотно-аддитивные соли, как правило, можно получать взаимодействием соединения в форме свободного основания с приблизительно стехиометрическим количеством неорганической или органической кислоты. Примеры распространенных неорганических кислот, подходящих для получения фармацевтически приемлемых солей, включают хлористоводородную, бромистоводородную, йодистоводородную, азотную, угольную, серную и фосфорную кислоты. Примеры распространенных органических кислот, подходящих для получения фармацевтически приемлемых солей, в основном включают, например, алифатические, циклоалифатические, ароматические, аралифатические, гетероциклические, карбоновые и сульфоновые органические кислоты. Конкретные примеры подходящих распространенных органических кислот включают холевую, сорбиновую, лауриновую, уксусную, трифторуксусную, муравьиную, пропионовую, янтарную, гликолевую, глюконовую, диглюконовую, молочную, яблочную, винную, лимонную, аскорбиновую, глюкуроновую, малеиновую, фумаровую, пировинную, аспарагиновую, глутаминовую кислоты, арилкарбоновые кислоты (например, бензойную), антраниловую кислоту, метансульфоновую, стеариновую, салициловую, п-гидроксибензойную, фенилуксусную, миндальную, эмбоновую (памовую), алкилсульфоновую (например, этансульфоновую), арилсульфоновую (например, бензолсульфоновую), пантотеновую, 2-гидроксиэтансульфоновую, сульфаниловую, циклогексиламиносульфоновую, β-гидроксимасляную, галактаровую, галактуроновую, адипиновую, альгиновую, масляную, камфорную, камфорсульфоновую, циклопентанпропионовую, додецилсерную, глюкогептановую, глицерофосфорную, гептановую, гексановую, никотиновую, 2-нафталинсульфоновую, щавелевую, пальмитиновую, пектиновую, 3-фенилпропионовую, пикриновую, пивалиновую, тиоциановую, толуолсульфоновую и ундекановую кислоты.
Основно-аддитивные соли, как правило, можно получить взаимодействием соединения в форме свободной кислоты с приблизительно стехиометрическим количеством неорганического или органического основания. Примеры основно-аддитивных солей могут включать, например, соли металлов и соли органических оснований. Соли металлов включают, например, соли щелочных металлов (группы Ia), соли щелочноземельных металлов (группы IIa) и другие физиологически приемлемые соли металлов. Такие соли могут быть получены из алюминия, кальция, лития, магния, калия, натрия и цинка. Например, соединение в форме свободной кислоты можно смешать с гидроксидом натрия с получением подобной основно-аддитивной соли. Соли органических оснований можно получать из аминов, например триметиламина, диэтиламина, N,N'-дибензилэтилендиамина, хлорпрокаина, этаноламина, диэтаноламина, этилендиамина, меглумина (N-метилглюкамина) и прокаина. Основные азотсодержащие группы могут быть кватернизованы такими реагентами, как C1-C6 алкилгалогениды (например, метил, этил, пропил и бутил хлориды, бромиды и йодиды), диалкилсульфаты (например, диметил, диэтил, дибутил и диамил сульфаты), галогениды с длинными цепями (например, децил, лаурил, миристил и стеарил хлориды, бромиды и йодиды), арилалкилгалогениды (например, бензил и фенэтил бромиды), и другими соединениями.
II. Получение композиций по настоящему изобретению
Композиции по настоящему изобретению чаще всего можно получать, например, с использованием методик, хорошо известных в технике. Как правило, какой-либо носитель (носители), который предполагается использовать в композиции (или часть такого носителя (носителей)), добавляют в сосуд для приготовления смеси, после чего добавляют оставшиеся наполнители, действующие вещества и жирную кислоту. Как правило, порядок добавления компонентов в сосуд не имеет решающего значения.
III. Способы лечения с применением композиций по настоящему изобретению
Композиции по настоящему изобретению в основном могут применяться для лечения инфекций у животных. Предусматривается, что композиция может применяться для лечения целого ряда животных, в особенности млекопитающих. Эти млекопитающие включают, например, людей. Другие млекопитающие включают, например, сельскохозяйственных животных и домашний скот (например, свиней, коров, овец, коз и т.д.), лабораторных млекопитающих (например, мышей, крыс, песчанок и т.д.), домашних млекопитающих (например, собак, кошек, лошадей и т.д.), а также диких млекопитающих и обитателей зоопарков (буйволов, оленей и т.д.). В некоторых вариантах осуществления композиции по настоящему изобретению применимы для лечения псовых (например, собак). В других вариантах осуществления композиции применимы для лечения кошачьих (например, домашних кошек). Предусматривается, что композиции подходят также для лечения животных, не являющихся млекопитающими, например, птиц (например, индеек, кур и т.д.) и рыб (например, лосося, форели, декоративных карпов и т.д.).
Композиции по настоящему изобретению, как правило, вводят в такой дозировке, которая обеспечивает наличие терапевтически эффективного количества композиции (и в частности, действующих ингредиентов) в месте инфекции. Для противовоспалительных средств (например, кортикостероидов, таких как мометазона фуроата моногидрат) «терапевтически эффективное количество» представляет собой такое количество, которого достаточно для облегчения, подавления или устранения целевого воспаления или проявления противозудного или сосудосуживающего действия в целевой ткани. Для противоинфекционных средств (например, антибиотика или противогрибкового средства) «терапевтически эффективное количество», представляет собой такое количество, которого достаточно для облегчения, подавления или уничтожения целевой патогенной инфекции. В некоторых вариантах осуществления вводят достаточное количество композиции для достижения концентрации антибиотика, которая эквивалентна, как минимум, уровню MIC90 (минимальной ингибирующей концентрации, т.е. концентрации, которая ингибирует рост 90% целевого патогена) антибиотика для целевого патогена. Если композиция по настоящему изобретению включает несколько действующих ингредиентов, обеспечивающих комбинированное воздействие на желаемую целевую ткань или патоген, количество каждого ингредиента, который составляет «терапевтически эффективное количество» представляет собой такое количество, которое при совместном действии с другими активными ингредиентами, вызывает желаемое воздействие на целевую ткань или патоген.
Предусматривается, что композицию по настоящему изобретению можно вводить ректально, вагинально, с помощью ингаляции (например, в форме аэрозоля), трансдермально, например с помощью трансдермального пластыря, или парентерально (например, с помощью подкожной инъекции, внутривенной инъекции, внутримышечной инъекции и т.д.). Также предусмотрено, что композиции можно вводить перорально. Например, композиции можно добавлять в пищу намеченного животного реципиента либо непосредственно, либо в виде части заранее приготовленной смеси; или в виде отдельной дозированной лекарственной формы.
В некоторых вариантах осуществления композицию по настоящему изобретению применяют для лечения ушной инфекции. В некоторых из таких вариантов осуществления ушная инфекция имеется у собаки. В других вариантах осуществления ушная инфекция имеется у кошки. В случае применения для лечения ушной инфекции, композицию по настоящему изобретению, как правило, вводят в инфицированное ухо (уши) животного. Хотя предпочтительно введение единой дневной дозы, предусмотрено, что композиция может быть введена в виде нескольких доз в течение дня. Во многих случаях для лечения инфекции достаточно одной дозы, особенно, если композиция включает, например, мометазона фуроата моногидрат, орбифлоксацин и позаконазол. Однако в других ситуациях может оказаться желательным (или необходимым) ввести вторую дозу, например, через 48 часов после первой дозы для полного излечения животного (или гарантии того, что излечение является полным). В других случаях композицию можно вводить ежедневно до 7 дней (или более).
Определение надлежащей дозировки, как правило, находится в компетенции специалиста в данной области. Точная дозировка будет зависеть от различных факторов. Эти факторы могут включать, например, тип (например, вид или породу), возраст, размеры, пол, рацион питания, активность и состояние предполагаемого реципиента; фармакологические соображения, такие как активность, эффективность, фармакокинетика и токсикологический профиль конкретной вводимой композиции; а также является ли вводимая композиция частью комбинированной терапии совместно с одним или несколькими действующими ингредиентами. Например, в некоторых вариантах осуществления, где композиция по настоящему изобретению применяется для лечения ушных инфекций у собак, дозировка составляет от примерно 1 до примерно 10 капель. В других вариантах осуществления, в которых композицию по настоящему изобретению применяют для лечения ушных инфекций у собак, эта дозировка составляет от примерно 25 до примерно 500 мг. В некоторых из этих вариантов осуществления дозировка составляет, например, от приблизительно 25 до приблизительно 250 мг.
IV. Терапевтические наборы
Настоящее изобретение направлено также на наборы, которые подходят, например, для применения при реализации описанных выше способов лечения. Как правило, такой набор будет включать терапевтически эффективное количество композиции по настоящему изобретению, а также дополнительный компонент (компоненты). Этот дополнительный компонент (компоненты) может представлять собой, например, одну или несколько позиций из следующего списка: средство диагностики, инструкции по введению композиции или устройство для введения композиции (например, шприц или мягкую бутыль). В некоторых вариантах осуществления для лечения ушных заболеваний, набор может включать композицию по настоящему изобретению, в комбинации, например, с устройством для чистки ушей и/или раствором для чистки ушей. Примеры подходящих устройств для чистки ушей включают чистящие куски материи (например, сухие тряпочки или мягкие прокладки, пропитанные спиртом) или средства для очистки ушей повышенной эффективности (например, систему Auriflush®, продаваемую Schering-Plough Corp.). Примеры подходящих растворов для чистки ушей включают раствор Virbac Animal Health's Cerulytic® Solution (содержащий пропиленгликоля дикаприлат/дикапрат, бензиловый спирт, ароматизатор и бутилзамещенный гидрокситолуол), раствор Pfizeer Inc.,s Oti-Clens® Solution (включающий производные пропиленгликоля и яблочной кислоты, бензойной кислоты и салициловой кислоты), раствор Vet Solutions Ear Cleaning Solution (содержащий пропиленгликоль, гель алоэ вера, SD (особой очистки) спирт 40-2, молочную кислоту, глицерин, диоктил натрий сульфосукцинат, салициловую кислоту, ароматизатор, бензойную кислоту и бензиловый спирт) и раствор IVX Animal Health's OtiRinse® Solution (включающий диоктилнатрий сульфосукцинат, салициловую кислоту, молочную кислоту, бензойную кислоту и алоэ вера).
ПРИМЕРЫ
Приведенные ниже примеры являются лишь иллюстрациями и никоим образом не ограничивают остальное содержание настоящей заявки.
Пример 1. Стабилизация суспензии с применением олеиновой кислоты или лауриновой кислоты
Цель настоящего эксперимента заключалась в демонстрации того факта, что олеиновая или лауриновая кислота может уменьшать образование как минимум одного продукта разрушения мометазона в суспензии, включающей мометазона фуроата моногидрат в комбинации с орбифлоксацином. В данном эксперименте суспензия имела состав, показанный в таблице 8:
| Таблица 8 Суспензия, включающая производное мометазона и фторхинолоновый антибиотик |
|
| Компонент | Концентрация (мг/г) |
| Тонкоизмельченный орбифлоксацин | 10,0 |
| Тонкоизмельченный мометазона фуроата моногидрат | 1,0 |
| Тонкоизмельченный позаконазол | 1,0 |
| Минеральное масло | 685,0 |
| Основа мази - пластифицированный углеводородный гель (Plastibase® 50W) | количество, достаточное для доведения общей массы до 1 г (после добавления соответствующего количества олеиновой или лауриновой кислоты) |
Эту суспензию разделяли на несколько образцов меньшей массы. Каждый образец смешивали с олеиновой кислотой для достижения определенной концентрации олеиновой кислоты (равной 0,1%, 0,2%, 0,5%, 1,0% или 2,0%), с лауриновой кислотой для достижения определенной концентрации лауриновой кислоты (0,1%, 0,2%, 0,5% или 1,0%) или не смешивали с олеиновой или лауриновой кислотами (в контрольном образце). Образцы упаковывали в 7,5 г бутылки из HDPE с крышками из LDPE и помещали на хранение для исследования устойчивости в вертикальном положении. Во избежание появления каких-либо загрязнений от этикеток, ни одна из упаковок не имела коммерческой этикетки. Каждую из бутылок хранили при одной из следующих комбинаций условий окружающей среды: (a) температура 40°C и относительная влажность 75% или (b) 50°C при естественной влажности.
Образцы исследовали с помощью ВЭЖХ в начале эксперимента и затем через промежутки времени, равные 1 месяцу, 2 месяцам и 5 месяцам, для определения концентрации продуктов разложения мометазона. Наблюдавшиеся концентрации продуктов разложения мометазона показаны в таблице 9.
| Таблица 9 Наблюдаемая концентрация продукта распада мометазона с течением времени при различных условиях и различных концентрациях олеиновой кислоты и лауриновой кислоты |
|||||||
| Добавл. кислота | Прошедшее время (в месяцах) и условия | ||||||
| исх. | 1 | 1 | 2 | 2 | 5 | 5 | |
| 40°C 75% отн. вл. |
50°C естеств. влажн. |
40°C 75% отн. вл. |
50°C естеств. влажн. |
40°C 75% отн. вл. |
50°C естеств. влажн. |
||
| контроль (нет) | ND | 0,35% | 0,26% | 0,46% | 0,30% | 0,60% | 0,25% |
| 0,1% олеин. к-та |
ND | ND | ND | ND | ND | ND | ND |
| 0,2% олеин. к-та |
ND | ND | ND | ND | ND | ND | ND |
| 0,5% олеин. к-та |
ND | ND | ND | ND | ND | ND | ND |
| 1,0% олеин. к-та |
ND | ND | ND | ND | ND | ND | ND |
| 2,0% олеин. к-та |
ND | ND | ND | ND | ND | ND | ND |
| 0,1% лаурин. к-та |
ND | ND | ND | ND | ND | ND | ND |
| 0,2% лаурин. к-та |
ND | ND | ND | ND | ND | ND | ND |
| 0,5% лаурин. к-та |
ND | ND | ND | ND | ND | ND | ND |
| 1,0% лаурин. к-та |
ND | ND | ND | ND | ND | ND | ND |
В таблице 9 сокращение «ND» означает «не обнаружено». Как можно видеть из приведенных данных, наличие обеих кислот при всех исследованных концентрациях ингибировало образование продукта распада мометазона в течение 5 месяцев при 40°C и относительной влажности 75%, а также при 50°C и естественной относительной влажности. Авторы заявки также не наблюдали каких-либо изменений в физических свойствах образцов и не обнаружили новых продуктов распада в результате добавления олеиновой или лауриновой кислоты.
Пример 2. Иллюстративный ушной состав, содержащий олеиновую кислоту
В приведенной ниже таблице 10 показана композиция по настоящему изобретению, включающая олеиновую кислоту.
| Таблица 10 Иллюстративный ушной состав, включающий олеиновую кислоту |
|
| Компонент | Концентрация (мг/г) |
| Тонкоизмельченный орбифлоксацин | 10,0 |
| Тонкоизмельченный мометазона фуроата моногидрат | 1,0 |
| Тонкоизмельченный позаконазол | 1,0 |
| Минеральное масло | 685,0 |
| Олеиновая кислота | 20 |
| Основа мази - пластифицированный углеводородный гель (Plastibase® 50W) | количество, достаточное для доведения общей массы до 1 г |
Пример 3. Иллюстративный ушной состав, содержащий олеиновую кислоту
В приведенной ниже таблице 11 показана композиция по настоящему изобретению, включающая лауриновую кислоту.
| Таблица 11 Иллюстративный ушной состав, включающий лауриновую кислоту |
|
| Компонент | Концентрация (мг/г) |
| Тонкоизмельченный орбифлоксацин | 10,0 |
| Тонкоизмельченный мометазона фуроата моногидрат | 1,0 |
| Тонкоизмельченный позаконазол | 1,0 |
| Минеральное масло | 685,0 |
| Лауриновая кислота | 20 |
| Основа мази - пластифицированный углеводородный гель (Plastibase® 50W) | количество, достаточное для доведения общей массы до 1 г |
Слова «включать», «включает» и «включающий» следует понимать во включающем, а не исключающем смысле. Предполагается, что интерпретация этих слов такая же, как и интерпретация, данная в патентном законодательстве Соединенных Штатов.
Термин «фармацевтически приемлемый» используется в качестве прилагательного для обозначения того, что определяемое им существительное подходит для применения в фармацевтическом продукте. Когда этот термин применяется, например, для описания соли или наполнителя, он характеризует эту соль или наполнитель как совместимые с другими ингредиентами композиции и не приносящие вреда предполагаемому животному реципиенту в такой степени, чтобы отрицательное действие (действия) превзошли полезное действие (действия) указанной соли или наполнителя.
Все литературные источники, приведенные в данной заявке на патент, включены в заявку с помощью ссылок.
Приведенное выше подробное описание предпочтительных вариантов осуществления предназначено только для знакомства других специалистов в данной области с настоящим изобретением, его основными идеями и его практическим применением, с тем чтобы другие специалисты в данной области могли адаптировать и применить это изобретение в его многочисленных формах, так чтобы оно наилучшим образом подходило к требованиям практического применения. Следовательно, настоящее изобретение не ограничено приведенными выше вариантами осуществления и может быть модифицировано различными путями.
Claims (14)
1. Фармацевтическая композиция для лечения инфекции, где указанная композиция включает: мометазона фуроат или его сольват, орбифлоксацин, жирную кислоту, содержащую от примерно 3 до примерно 18 атомов углерода и имеющую температуру плавления не более примерно 60°С.
2. Композиция по п.1, где композиция имеет форму суспензии.
3. Композиция по п.1, включающая моногидрат мометазона фуроата.
4. Композиция по п.1, где композиция дополнительно включает противогрибковое средство.
5. Композиция по п.4, где противогрибковое средство включают триазол, соль триазола или сольват триазола или его соли.
6. Композиция по п.5, где триазолы включают триазол, выбранный из группы, состоящей из флуконазола, итраконазола, саперконазола, терконазола и вориконазола.
7. Композиция по п.5, где триазолы включают позаконазол.
8. Композиция по п.1, где жирные кислоты включают лауриновую кислоту.
9. Композиция по п.1, где жирная кислота включает олеиновую кислоту.
10. Композиция по п.1, где композиция дополнительно включает минеральное масло.
11. Способ лечения инфекции у животного, где указанный способ включает введение животному композиции, определенной в п.1.
12. Способ по п.11, где инфекции включают ушную инфекцию у собак.
13. Применение композиции по п.1 для получения лекарственного средства для лечения инфекции у животного.
14. Терапевтический набор для лечения инфекции, где набор включает:
композицию по любому из пп.1-10, а также
дополнительный компонент, выбранный из группы, состоящей из:
средства диагностики,
раствора для чистки ушей,
устройства для чистки ушей,
инструкции по введению композиции животному и
устройства для введения композиции животному.
композицию по любому из пп.1-10, а также
дополнительный компонент, выбранный из группы, состоящей из:
средства диагностики,
раствора для чистки ушей,
устройства для чистки ушей,
инструкции по введению композиции животному и
устройства для введения композиции животному.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US5794008P | 2008-06-02 | 2008-06-02 | |
| US61/057,940 | 2008-06-02 | ||
| PCT/EP2009/056751 WO2009147144A2 (en) | 2008-06-02 | 2009-06-02 | Composition comprising an antibiotic and a corticosteroid |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2010154083A RU2010154083A (ru) | 2012-07-20 |
| RU2496501C2 true RU2496501C2 (ru) | 2013-10-27 |
Family
ID=41278754
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2010154083/15A RU2496501C2 (ru) | 2008-06-02 | 2009-06-02 | Композиции, включающие антибиотик и кортикостероид |
Country Status (13)
| Country | Link |
|---|---|
| US (2) | US20100087409A1 (ru) |
| EP (1) | EP2293778B1 (ru) |
| JP (1) | JP5674648B2 (ru) |
| CN (1) | CN102083414B (ru) |
| AR (1) | AR071988A1 (ru) |
| AU (1) | AU2009253956B2 (ru) |
| BR (1) | BRPI0913297B8 (ru) |
| CA (1) | CA2726074C (ru) |
| ES (1) | ES2436193T3 (ru) |
| HK (1) | HK1156876A1 (ru) |
| RU (1) | RU2496501C2 (ru) |
| TW (1) | TW201010708A (ru) |
| WO (1) | WO2009147144A2 (ru) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4792032B2 (ja) | 2004-08-13 | 2011-10-12 | シェーリング−プラウ・リミテッド | 抗生物質、トリアゾールおよびコルチコステロイドを含む薬学的処方物 |
| BR112013015572A2 (pt) | 2010-12-20 | 2016-09-27 | Colgate Palmolive Co | composição para cuidado oral de gelatina encapsulada contendo hidrofílico ativo, agente de estruturação hidrofóbico e transportador de óleo |
| EP2502616A1 (fr) * | 2011-03-21 | 2012-09-26 | Matthew Krayenbuhl | Composition pharmaceutique nasale |
| ES2845948T3 (es) * | 2012-01-10 | 2021-07-28 | Entrx LLC | Formulaciones óticas |
| US9849126B2 (en) | 2013-01-03 | 2017-12-26 | Entrx LLC | Sterile otic formulations |
| MX2018015475A (es) * | 2016-06-13 | 2019-07-12 | Vyome Therapeutics Ltd | Composiciones antifungicas sinérgicas y métodos de las mismas. |
| WO2017216722A2 (en) * | 2016-06-13 | 2017-12-21 | Vyome Biosciences Pvt. Ltd. | Synergistic antifungal compositions and methods thereof |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2000068243A1 (en) * | 1999-05-07 | 2000-11-16 | Smithkline Beecham Corporation | Methods using mechanisms of action of aroa |
| WO2003000175A2 (en) * | 2001-06-20 | 2003-01-03 | Bristol-Myers Squibb Company | Pediatric formulation of gatifloxacin |
| RU2201219C2 (ru) * | 2001-04-24 | 2003-03-27 | Макаров Константин Алексеевич | Фармакологическая композиция пролонгированного действия |
| RU2267491C1 (ru) * | 2004-07-14 | 2006-01-10 | Общество с ограниченной ответственностью "Исследовательский Институт Химического Разнообразия" (ООО "Исследовательский Институт Химического Разнообразия") | Физиологически активная композиция, замещенные 1-оксо-1,2-дигидро[2,7]-нафтиридины, способ их получения, применения и набор |
| US20060122159A1 (en) * | 2004-08-13 | 2006-06-08 | Huq Abu S | Pharmaceutical formulation |
| US20070196398A1 (en) * | 2006-02-17 | 2007-08-23 | Murthy Yerramilli V S | Fluoroquinolone fatty acid salt compositions |
Family Cites Families (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS6013711A (ja) * | 1983-06-21 | 1985-01-24 | ザ、プロクタ−、エンド、ギヤンブル、カンパニ− | コルチコステロイドを含有する浸透局所製薬組成物 |
| NZ243062A (en) * | 1991-06-10 | 1993-09-27 | Schering Corp | Aerosol containing medicament and 1,1,1,2-tetrafluoroethane |
| US7917386B2 (en) * | 1995-06-16 | 2011-03-29 | Catalina Marketing Corporation | Virtual couponing method and apparatus for use with consumer kiosk |
| US5710886A (en) * | 1995-06-16 | 1998-01-20 | Sellectsoft, L.C. | Electric couponing method and apparatus |
| GB9620187D0 (en) * | 1996-09-27 | 1996-11-13 | Minnesota Mining & Mfg | Medicinal aerosol formulations |
| US20080052169A1 (en) * | 2000-03-29 | 2008-02-28 | O'shea Deirdre | Method and apparatus for providing a coupon offer having a variable value |
| WO2003025822A1 (en) * | 2001-09-19 | 2003-03-27 | Matsushita Electric Corporation Of America | Adaptive electronic coupon |
| ATE442146T1 (de) * | 2003-11-07 | 2009-09-15 | Senju Pharma Co | Pharmazeutische zusammensetzung mit prostaglandin |
| US20050118206A1 (en) * | 2003-11-14 | 2005-06-02 | Luk Andrew S. | Surfactant-based gel as an injectable, sustained drug delivery vehicle |
| US20060041469A1 (en) * | 2004-08-18 | 2006-02-23 | Torrance Mathis | Marketing system employing electronically generated discount coupons |
| EP1968548A2 (en) * | 2005-12-02 | 2008-09-17 | Elan Pharma International Limited | Mometasone compositions and methods of making and using the same |
| US8268347B1 (en) * | 2006-10-24 | 2012-09-18 | Aradigm Corporation | Dual action, inhaled formulations providing both an immediate and sustained release profile |
| US20080253970A1 (en) * | 2007-02-09 | 2008-10-16 | Schering Corporation | Stable Pharmaceutical Drug Products |
| CA2720851A1 (en) * | 2008-04-15 | 2009-10-22 | Schering Corporation | Oral pharmaceutical compositions in a molecular solid dispersion |
-
2009
- 2009-05-27 TW TW098117771A patent/TW201010708A/zh unknown
- 2009-06-02 JP JP2011512100A patent/JP5674648B2/ja active Active
- 2009-06-02 BR BRPI0913297A patent/BRPI0913297B8/pt active IP Right Grant
- 2009-06-02 RU RU2010154083/15A patent/RU2496501C2/ru active
- 2009-06-02 AU AU2009253956A patent/AU2009253956B2/en active Active
- 2009-06-02 ES ES09757525T patent/ES2436193T3/es active Active
- 2009-06-02 WO PCT/EP2009/056751 patent/WO2009147144A2/en active Application Filing
- 2009-06-02 CA CA2726074A patent/CA2726074C/en active Active
- 2009-06-02 US US12/476,783 patent/US20100087409A1/en not_active Abandoned
- 2009-06-02 CN CN2009801255946A patent/CN102083414B/zh active Active
- 2009-06-02 EP EP09757525.2A patent/EP2293778B1/en active Active
- 2009-06-02 AR ARP090101978A patent/AR071988A1/es not_active Application Discontinuation
-
2011
- 2011-10-20 HK HK11111313.4A patent/HK1156876A1/xx unknown
- 2011-11-01 US US13/286,747 patent/US10045940B2/en active Active
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2000068243A1 (en) * | 1999-05-07 | 2000-11-16 | Smithkline Beecham Corporation | Methods using mechanisms of action of aroa |
| RU2201219C2 (ru) * | 2001-04-24 | 2003-03-27 | Макаров Константин Алексеевич | Фармакологическая композиция пролонгированного действия |
| WO2003000175A2 (en) * | 2001-06-20 | 2003-01-03 | Bristol-Myers Squibb Company | Pediatric formulation of gatifloxacin |
| RU2267491C1 (ru) * | 2004-07-14 | 2006-01-10 | Общество с ограниченной ответственностью "Исследовательский Институт Химического Разнообразия" (ООО "Исследовательский Институт Химического Разнообразия") | Физиологически активная композиция, замещенные 1-оксо-1,2-дигидро[2,7]-нафтиридины, способ их получения, применения и набор |
| US20060122159A1 (en) * | 2004-08-13 | 2006-06-08 | Huq Abu S | Pharmaceutical formulation |
| US20070196398A1 (en) * | 2006-02-17 | 2007-08-23 | Murthy Yerramilli V S | Fluoroquinolone fatty acid salt compositions |
Non-Patent Citations (4)
| Title |
|---|
| [Найдено из базы данных PatSearch (DWPI)]. * |
| TSUJI Y et al. Pharma-ceutical properties of freeze-dried formulations of egg albumin, several drugs and ovile oil. Biol. Pharm.Bull. 1996 Apr; 19(4):636-40. Реферат [online] [Найдено из базы данных PubMed PMID: 9132174] [найдено 04.03.2013]. * |
| TSUJI Y et al. Pharma-ceutical properties of freeze-dried formulations of egg albumin, several drugs and ovile oil. Biol. Pharm.Bull. 1996 Apr; 19(4):636-40. Реферат [online] [Найдено из базы данных PubMed PMID: 9132174] [найдено 04.03.2013]. [Найдено из базы данных PatSearch (DWPI)]. * |
| ОЛИВКОВОЕ МАСЛО (Olea europaea) [online] [Найдено из Интернета://forum.aromarti.ru/showthread.pdp?t=109] [найдено 04.03.2013] § Жирнокислотный состав. * |
Also Published As
| Publication number | Publication date |
|---|---|
| US10045940B2 (en) | 2018-08-14 |
| AR071988A1 (es) | 2010-07-28 |
| BRPI0913297B8 (pt) | 2020-09-15 |
| AU2009253956A1 (en) | 2009-12-10 |
| EP2293778A2 (en) | 2011-03-16 |
| AU2009253956B2 (en) | 2016-05-12 |
| HK1156876A1 (en) | 2012-06-22 |
| WO2009147144A2 (en) | 2009-12-10 |
| CN102083414B (zh) | 2013-10-23 |
| BRPI0913297B1 (pt) | 2019-01-29 |
| RU2010154083A (ru) | 2012-07-20 |
| CN102083414A (zh) | 2011-06-01 |
| ES2436193T3 (es) | 2013-12-27 |
| US20100087409A1 (en) | 2010-04-08 |
| EP2293778B1 (en) | 2013-09-18 |
| TW201010708A (en) | 2010-03-16 |
| WO2009147144A3 (en) | 2010-09-16 |
| JP2011521999A (ja) | 2011-07-28 |
| US20120046259A1 (en) | 2012-02-23 |
| JP5674648B2 (ja) | 2015-02-25 |
| BRPI0913297A2 (pt) | 2016-01-26 |
| CA2726074C (en) | 2016-07-19 |
| CA2726074A1 (en) | 2009-12-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2394573C2 (ru) | Фармацевтическая композиция | |
| RU2496501C2 (ru) | Композиции, включающие антибиотик и кортикостероид | |
| JP2008522998A (ja) | 耳内部での衛生的使用のための薬剤 | |
| JP2021121608A (ja) | 抗菌剤及び抗炎症剤を含む眼内投与のための医薬組成物 | |
| JP2007534717A (ja) | 獣医学におけるメロキシカム製剤の使用 | |
| CN113559264A (zh) | 治疗包括乳房炎的微生物感染的方法 | |
| TWI433691B (zh) | 苯并咪唑之非水性組合物 | |
| US20220401457A1 (en) | Use of Deoxycholic Acid, Derivatives, or Salts Thereof in Managing Bacterial Infections and Compositions Related Thereto | |
| EP2934524B1 (en) | Penethamate veterinary injectable formulations |