RU202193U1 - Устройство для иммунохроматографической высокочувствительной и внелабораторной детекции фитопатогенной бактерии Clavibacter michiganensis, основанное на повышении интенсивности регистрируемого колориметрического сигнала за счет каталитических свойств наномаркера - Google Patents
Устройство для иммунохроматографической высокочувствительной и внелабораторной детекции фитопатогенной бактерии Clavibacter michiganensis, основанное на повышении интенсивности регистрируемого колориметрического сигнала за счет каталитических свойств наномаркера Download PDFInfo
- Publication number
- RU202193U1 RU202193U1 RU2020119108U RU2020119108U RU202193U1 RU 202193 U1 RU202193 U1 RU 202193U1 RU 2020119108 U RU2020119108 U RU 2020119108U RU 2020119108 U RU2020119108 U RU 2020119108U RU 202193 U1 RU202193 U1 RU 202193U1
- Authority
- RU
- Russia
- Prior art keywords
- michiganensis
- membrane
- sample
- nanoparticles
- porous
- Prior art date
Links
- 241001136168 Clavibacter michiganensis Species 0.000 title claims abstract description 46
- 238000001514 detection method Methods 0.000 title claims abstract description 27
- 230000003197 catalytic effect Effects 0.000 title claims abstract description 10
- 230000003032 phytopathogenic effect Effects 0.000 title claims abstract description 10
- 238000012360 testing method Methods 0.000 claims abstract description 51
- 239000002105 nanoparticle Substances 0.000 claims abstract description 49
- 239000012528 membrane Substances 0.000 claims abstract description 39
- 239000000758 substrate Substances 0.000 claims abstract description 18
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 claims abstract description 14
- 241000283973 Oryctolagus cuniculus Species 0.000 claims abstract description 10
- 238000006243 chemical reaction Methods 0.000 claims abstract description 10
- 239000000020 Nitrocellulose Substances 0.000 claims abstract description 9
- 229920001220 nitrocellulos Polymers 0.000 claims abstract description 9
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 claims abstract description 9
- 229920000036 polyvinylpyrrolidone Polymers 0.000 claims abstract description 9
- 239000001267 polyvinylpyrrolidone Substances 0.000 claims abstract description 9
- 230000001580 bacterial effect Effects 0.000 claims abstract description 8
- 239000003365 glass fiber Substances 0.000 claims abstract description 7
- 239000007788 liquid Substances 0.000 claims abstract description 6
- 238000010186 staining Methods 0.000 claims abstract description 6
- HSTOKWSFWGCZMH-UHFFFAOYSA-N 3,3'-diaminobenzidine Chemical compound C1=C(N)C(N)=CC=C1C1=CC=C(N)C(N)=C1 HSTOKWSFWGCZMH-UHFFFAOYSA-N 0.000 claims abstract description 5
- 238000009825 accumulation Methods 0.000 claims abstract description 5
- 102000028557 immunoglobulin binding proteins Human genes 0.000 claims abstract description 5
- 108091009323 immunoglobulin binding proteins Proteins 0.000 claims abstract description 5
- 238000013508 migration Methods 0.000 claims abstract description 5
- 230000005012 migration Effects 0.000 claims abstract description 5
- 239000004793 Polystyrene Substances 0.000 claims abstract description 4
- 239000003463 adsorbent Substances 0.000 claims abstract description 4
- 229920002223 polystyrene Polymers 0.000 claims abstract description 4
- 238000007254 oxidation reaction Methods 0.000 claims abstract description 3
- 230000003647 oxidation Effects 0.000 claims abstract 2
- 241000894006 Bacteria Species 0.000 claims description 7
- 238000010521 absorption reaction Methods 0.000 claims description 5
- 238000011161 development Methods 0.000 claims description 4
- 238000000926 separation method Methods 0.000 claims description 3
- VEQPNABPJHWNSG-UHFFFAOYSA-N Nickel(2+) Chemical compound [Ni+2] VEQPNABPJHWNSG-UHFFFAOYSA-N 0.000 claims description 2
- 238000012423 maintenance Methods 0.000 claims description 2
- 229910001453 nickel ion Inorganic materials 0.000 claims description 2
- 239000011152 fibreglass Substances 0.000 claims 1
- 238000004458 analytical method Methods 0.000 abstract description 29
- 239000002245 particle Substances 0.000 abstract description 19
- 235000002595 Solanum tuberosum Nutrition 0.000 abstract description 18
- 244000061456 Solanum tuberosum Species 0.000 abstract description 18
- 239000000284 extract Substances 0.000 abstract description 18
- 239000011258 core-shell material Substances 0.000 abstract description 14
- PXIPVTKHYLBLMZ-UHFFFAOYSA-N Sodium azide Chemical compound [Na+].[N-]=[N+]=[N-] PXIPVTKHYLBLMZ-UHFFFAOYSA-N 0.000 abstract description 12
- 230000003321 amplification Effects 0.000 abstract description 11
- 238000003199 nucleic acid amplification method Methods 0.000 abstract description 11
- 230000000694 effects Effects 0.000 abstract description 8
- 102000003992 Peroxidases Human genes 0.000 abstract description 7
- 239000000203 mixture Substances 0.000 abstract description 6
- 239000002131 composite material Substances 0.000 abstract description 4
- 108040007629 peroxidase activity proteins Proteins 0.000 abstract description 4
- 235000012015 potatoes Nutrition 0.000 abstract description 4
- 108700020962 Peroxidase Proteins 0.000 abstract description 3
- 150000002500 ions Chemical class 0.000 abstract description 3
- 230000003287 optical effect Effects 0.000 abstract description 3
- 239000007787 solid Substances 0.000 abstract description 3
- 238000010915 one-step procedure Methods 0.000 abstract description 2
- 239000000427 antigen Substances 0.000 abstract 1
- 102000036639 antigens Human genes 0.000 abstract 1
- 108091007433 antigens Proteins 0.000 abstract 1
- 239000013000 chemical inhibitor Substances 0.000 abstract 1
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Substances [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 55
- 230000015572 biosynthetic process Effects 0.000 description 17
- 229910052697 platinum Inorganic materials 0.000 description 15
- 239000000243 solution Substances 0.000 description 10
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical group [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 8
- 238000003786 synthesis reaction Methods 0.000 description 7
- 241000196324 Embryophyta Species 0.000 description 6
- 229910052737 gold Inorganic materials 0.000 description 6
- 239000010931 gold Substances 0.000 description 6
- 238000000034 method Methods 0.000 description 6
- 229910000510 noble metal Inorganic materials 0.000 description 5
- 238000011896 sensitive detection Methods 0.000 description 5
- 208000032420 Latent Infection Diseases 0.000 description 4
- 230000009471 action Effects 0.000 description 4
- 238000013459 approach Methods 0.000 description 4
- 239000011248 coating agent Substances 0.000 description 4
- 238000000576 coating method Methods 0.000 description 4
- 238000003018 immunoassay Methods 0.000 description 4
- 244000005700 microbiome Species 0.000 description 4
- 239000000047 product Substances 0.000 description 4
- 238000002965 ELISA Methods 0.000 description 3
- 238000006555 catalytic reaction Methods 0.000 description 3
- 230000018109 developmental process Effects 0.000 description 3
- 208000015181 infectious disease Diseases 0.000 description 3
- 239000003550 marker Substances 0.000 description 3
- 238000002360 preparation method Methods 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 238000012216 screening Methods 0.000 description 3
- 238000001179 sorption measurement Methods 0.000 description 3
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 239000003054 catalyst Substances 0.000 description 2
- 238000006911 enzymatic reaction Methods 0.000 description 2
- 230000000984 immunochemical effect Effects 0.000 description 2
- 239000010410 layer Substances 0.000 description 2
- 229910052751 metal Inorganic materials 0.000 description 2
- 239000002184 metal Substances 0.000 description 2
- PXHVJJICTQNCMI-UHFFFAOYSA-N nickel Substances [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 2
- 239000008363 phosphate buffer Substances 0.000 description 2
- 239000000419 plant extract Substances 0.000 description 2
- 238000003752 polymerase chain reaction Methods 0.000 description 2
- 230000001105 regulatory effect Effects 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 239000002356 single layer Substances 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- UAIUNKRWKOVEES-UHFFFAOYSA-N 3,3',5,5'-tetramethylbenzidine Chemical compound CC1=C(N)C(C)=CC(C=2C=C(C)C(N)=C(C)C=2)=C1 UAIUNKRWKOVEES-UHFFFAOYSA-N 0.000 description 1
- 241001646719 Escherichia coli O157:H7 Species 0.000 description 1
- 241000526118 Fusarium solani f. radicicola Species 0.000 description 1
- 229940123742 Peroxidase inhibitor Drugs 0.000 description 1
- 102000007066 Prostate-Specific Antigen Human genes 0.000 description 1
- 108010072866 Prostate-Specific Antigen Proteins 0.000 description 1
- 229910018885 Pt—Au Inorganic materials 0.000 description 1
- 241000607479 Yersinia pestis Species 0.000 description 1
- 239000002250 absorbent Substances 0.000 description 1
- 230000002745 absorbent Effects 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 239000007979 citrate buffer Substances 0.000 description 1
- 238000004040 coloring Methods 0.000 description 1
- 239000000356 contaminant Substances 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 230000006866 deterioration Effects 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 208000037771 disease arising from reactivation of latent virus Diseases 0.000 description 1
- 239000002532 enzyme inhibitor Substances 0.000 description 1
- 150000002343 gold Chemical class 0.000 description 1
- 238000003306 harvesting Methods 0.000 description 1
- 230000002779 inactivation Effects 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 229910052741 iridium Inorganic materials 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 239000002082 metal nanoparticle Substances 0.000 description 1
- 238000001000 micrograph Methods 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 239000011943 nanocatalyst Substances 0.000 description 1
- LGQLOGILCSXPEA-UHFFFAOYSA-L nickel sulfate Chemical compound [Ni+2].[O-]S([O-])(=O)=O LGQLOGILCSXPEA-UHFFFAOYSA-L 0.000 description 1
- 229910000363 nickel(II) sulfate Inorganic materials 0.000 description 1
- 229910052763 palladium Inorganic materials 0.000 description 1
- KDLHZDBZIXYQEI-UHFFFAOYSA-N palladium Substances [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 150000003057 platinum Chemical class 0.000 description 1
- 229920001992 poloxamer 407 Polymers 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 238000004445 quantitative analysis Methods 0.000 description 1
- 238000013102 re-test Methods 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 235000010378 sodium ascorbate Nutrition 0.000 description 1
- 229960005055 sodium ascorbate Drugs 0.000 description 1
- PPASLZSBLFJQEF-RKJRWTFHSA-M sodium ascorbate Substances [Na+].OC[C@@H](O)[C@H]1OC(=O)C(O)=C1[O-] PPASLZSBLFJQEF-RKJRWTFHSA-M 0.000 description 1
- PPASLZSBLFJQEF-RXSVEWSESA-M sodium-L-ascorbate Chemical compound [Na+].OC[C@H](O)[C@H]1OC(=O)C(O)=C1[O-] PPASLZSBLFJQEF-RXSVEWSESA-M 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 238000004627 transmission electron microscopy Methods 0.000 description 1
- 230000017260 vegetative to reproductive phase transition of meristem Effects 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M1/00—Apparatus for enzymology or microbiology
- C12M1/26—Inoculator or sampler
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M1/00—Apparatus for enzymology or microbiology
- C12M1/34—Measuring or testing with condition measuring or sensing means, e.g. colony counters
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/543—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/558—Immunoassay; Biospecific binding assay; Materials therefor using diffusion or migration of antigen or antibody
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Immunology (AREA)
- Biomedical Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biotechnology (AREA)
- Molecular Biology (AREA)
- Microbiology (AREA)
- Urology & Nephrology (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Hematology (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- Analytical Chemistry (AREA)
- Cell Biology (AREA)
- Genetics & Genomics (AREA)
- General Engineering & Computer Science (AREA)
- Sustainable Development (AREA)
- Food Science & Technology (AREA)
- Physics & Mathematics (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
Abstract
Заявленное устройство предназначено для иммунохроматографической высокочувствительной, внелабораторной и экспрессной детекции фитопатогенной бактерии Clavibacter michiganensis в экстрактах листьев и клубней картофеля. Устройство представляет собой мультимембранный композит с предварительно нанесенными и высушенными иммунореагентами (тест-полоску). В состав мультимембранного композита входят рабочая нитроцеллюлозная мембрана с предварительно нанесенными иммунореагентами, закрепленная на твердой полистироловой основе, стекловолоконная мембрана с нанесенными конъюгатом пористых наночастиц типа ядро-оболочка - Au-Pt, стабилизированных поливинилпирролидоном с кроличьими поликлональными антителами, специфичными к бактериальным клеткам С.michiganensis, мембрана для впитывания и сепарации компонентов исследуемой пробы и конечной адсорбирующей мембраны для впитывания компонентов пробы после прохождения реакции и поддержания миграции жидкости по тест-полоске за счет капиллярных сил. Отличительной особенностью заявленного устройства является то, что в качестве метки использован конъюгат пористых наночастиц ядро-оболочка - Au-Pt, стабилизированных поливинилпирролидоном с поликлональными антителами против С.michiganensis. Частицы Au-Pt обладают как оптическими, так и каталитическими (пероксидаза-подобными свойствами), что позволяет использовать их в иммунохроматографическом анализе (ИХА) как наноразмерную метку с собственным оптическими сигналом, так и для снижения предела обнаружения ИХА, основанного на повышении интенсивности окрашивания при низких концентрациях антигена в пробе за счет пероксидаза-подобных свойств наночастиц, приводящих к накоплению окрашенных продуктов окисления субстрата. Высокая устойчивость частиц к химическим ингибиторам пероксидаз (азид натрия) и температуре (до 100°С) позволяет использовать наночастицы Au-Pt для амплификации сигнала даже в пробах с высокой эндогенной пероксидазной активностью после ее нивелирования. В контрольную зону (К.З.) нанесен иммуноглобулин-связывающий белок А. В тестовую зону (Т.З.) нанесены кроличьи поликлональные антитела, специфичные к бактериальным клеткам С.michiganensis. На стекловолоконную мембрану нанесен конъюгат поликлональных кроличьих антител, специфичных к детектируемым бактериальным клеткам, с пористыми наночастицами типа ядро-оболочка Au-Pt, стабилизированных поливинилпирролидоном. Для проведения анализа не требуется никаких дополнительных стационарных устройств. Продолжительность анализа составляет 15 мин, включает в себя стадии подготовки анализируемой пробы, проведение иммунохроматографического анализа с использованием тест-полоски, добавления субстратного раствора для повышения интенсивности регистрируемого колориметрического сигнала. Технической задачей заявленной полезной модели является повышение интенсивности регистрируемого окрашивания Т.З. за счет реакции, катализируемой пористыми наночастицами типа ядро-оболочка Au-Pt непосредственно на тест-полоске. Технический результат заявленной полезной модели заключается в снижении предела обнаружения фитопатогенной бактерии С.michiganensis за счет использования простой одностадийной процедуры, обеспечиваемой за счет добавления на тест-полоску субстратного раствора, содержащего смесь 3,3'-диаминобензидина, пероксида водорода и ионов Ni2+. 4 табл., 3 пр., 2 ил.
Description
Полезная модель относится к детекции фитопатогенной бактерии Clavibacter michiganensis (С michiganensis) и может быть использована как экспрессное лабораторное и внелабораторное средство для проведения фитосанитарного контроля специализированными службами, таможенного контроля посевного материала, мониторинга зараженности фермерскими хозяйствами.
Фитопатогенные микроорганизмы поражают широкий спектр сельскохозяйственных культур. Заражение фитопатогенными микроорганизмами приводит к существенным экономическим потерям за счет снижения урожайности растений (до 100%), ухудшению их хранимости и устойчивости к вредителям.
Широко распространенным на территории Российской Федерации является бактериальный фитопатоген С.michiganensis, аэробная, неспорообразующая грамположительная бактерия. Основным растением, поражаемым С.michiganensis, является картофель. Поражение картофеля приводит к загниванию его клубней (т.н. кольцевая гниль картофеля) и возникновению очагов ямчатой гнили. Заражение может происходить в период уборки урожая за счет проникновения бактерий через участки с поврежденной кожурой. Детекция низких концентраций бактерий, не вызывающих развития выраженных симптомов (латентная инфекция), представляет особый интерес для практического использования, поскольку при посадке клубней с низкой концентрацией бактерий развитие симптомов наблюдается только в процессе цветения. Таким образом, изолирование зараженных растений приведет к существенным экономическим потерям. Для предотвращения больших потерь урожая и существенных убытков необходимо диагностировать латентные инфекции в семенном материале. Согласно нормативной документации - ГОСТ 33996-2016 «Картофель семенной. Технические условия и методы определения качества» - С.michiganensis входит в список контролируемых фитопатогенных микроорганизмов картофеля. Согласно рекомендациям нормативной документации предел обнаружения для иммунохимических методов анализа составляет 104 клеток/мл. Однако для диагностики латентных инфекций необходимо достижение меньших пределов обнаружения.
Для детекции С.michiganensis используются различные вариации метода полимеразной цепной реакции, иммуноферментный анализ, иммунохроматографический анализ. Несмотря на такие преимущества, как специфичность и низкий предел обнаружения, для применения методов, основанных на полимеразной цепной реакции, необходимо дорогостоящее стационарное оборудование, условия, обеспечивающие отсутствие контаминации, квалифицированный персонал. Продолжительность анализа (минимум один час без учета подготовки проб) также ограничивает применимость данных методов во внелабораторных условиях.
Для высокочувствительной детекции С.michiganensis могут быть также использованы активно развивающиеся методы иммунохимического анализа - иммуноферментный (ИФА) и иммунохроматографический (ИХА) анализ. Возможности иммуноанализа связаны с его методической простотой, а также высокой производительностью, обеспечивающей одновременное тестирование множества проб в течение 2-3 часов. Однако выполнение ИФА включает несколько дополнительных стадий (внесение реагентов и отмывка), сопряжено с необходимостью дополнительных расходных материалов (микропланшеты, наконечники пипеток, и др.) и оборудования для регистрации результатов анализа. ИХА, в отличие от ИФА, не требует дополнительного оборудования и позволяет проводить массовый скрининг в нестерильных внелабораторных условиях с использованием минимальной подготовки проб. В классическом формате ИХА является одностадийным анализом и позволяет проводить качественный (наличие/отсутствие окрашенной Т.З.) и количественный анализ (регистрация интенсивности колориметрического сигнала в Т.З., определение количества бактерий путем сравнения интенсивности колориметрического сигнала пробы и образцов с известным количеством бактерий) по накоплению окрашенного маркера.
Однако предел обнаружения одностадийного ИХА зачастую оказывается недостаточным для высокочувствительной детекции. Один из подходов для снижения предела обнаружения ИХА основан на повышении интенсивности регистрируемого колориметрического сигнала за счет каталитической конверсии молекул субстрата в окрашенный продукт. Амплификация сигнала достигается за счет того, что единичная наночастица-катализатор приводит к конверсии большого количества молекул субстрата в регистрируемый продукт.
Увеличение регистрируемой интенсивности окрашивания связано с накоплением продукта ферментативной реакции на тест-полоске. В качестве каталитической метки могут быть использованы наночастицы металлов, поскольку они обладают уникальными оптическими свойствами, могут быть легко сконъюгированы с рецепторными молекулами, показывают высокую каталитическую активность и стабильность в присутствии ингибиторов ферментов. Наиболее широко в качестве каталитически активных нанометок используются частицы Au, Pt, Pd, Ir различной формы и морфологии. Однако высокая стоимость благородных металлов-катализаторов ограничивает их применение в аналитических тест-системах.
Особенностью катализа с использованием наночастиц является множество активных центров, расположенных на поверхности частиц. Таким образом, большая часть атомов благородных металлов оказывается экранированной (внутри частиц) и не участвует в катализе. Для снижения расхода благородных металлов при синтезе каталитически активных частиц предложен подход, основанный на формировании тонкого слоя каталитически-активного металла на наночастицах носителях, благодаря чему все поверхностно экспонированные атомы металла оказываются доступны для субстрата и каталитической конверсии. Данный подход был использован в ряде работ для получения каталитически активных наночастиц Au-Pt. Например, Zhang и соавторы использовали конъюгат наночастиц Au-Pt с антителами против IgG кролика для ИХА. Gao и соавторы использовали наночастицы, состоящие из золотого ядра и монослойного платинового покрытия в качестве метки в ИХА простатического специфического антигена.
Использованные протоколы синтеза основаны на формировании платинового покрытия на наночастицах золота, однако не позволяют достичь максимального экспонирования каталитически активного платинового покрытия. Формирование пористого платинового покрытия на затравочных наночастицах золота позволит увеличить площадь поверхности каталитически-активных частиц. В литературе описан синтез пористых наночастиц Au-Pt. Так, Loynachan и соавторы для формирования пористой платиновой оболочки в качестве затравочных частиц использовали наночастицы золота, стабилизированные поливинилпирролидоном. Для синтеза пористых использовали высокие концентрации платины (до 3 мМ), высокая стоимость частиц ограничивает их применение для рутинного скрининга. Jiang и соавторы для синтеза пористых платиновых частиц использовали реакцию совместного восстановления солей платины и золота в присутствии полимера Pluronic F127. Однако в данном случае также были использованы высокие концентрации солей благородных металлов (10 мМ), а совместное восстановление не позволяет достигнуть экспонирования каталитически активных платиновых частиц на поверхности.
Таким образом, известные разработки иммунохроматографических тест-систем сфокусированы на использовании неоптимальных с точки зрения катализа непористых частиц типа ядро-оболочка, а протоколы синтеза пористых частиц требуют высоких концентраций дорогостоящих солей благородных металлов, и также не позволяют достигнуть максимального экспонирования каталитически-активных платиновых частиц на поверхности.
Отличительной особенностью предлагаемой полезной модели является использование для ИХА наночастиц типа ядро-оболочка - Au-Pt, обладающих пористой структурой каталитически активной платиновой оболочки и требующих в 3-10 раз меньшего (1 мМ) количества дорогостоящей платины для синтеза. Поливинилпирролидон (молекулярная масса 10 кДа) формирует плотный адсорбционный слой вокруг наночастиц золота (20 нм) и приводит к формированию пористой платиновой оболочки при восстановлении соли платины (Na2PtCl6, 1 мМ) в присутствии аскорбата натрия (10 мМ). Полученные пористые наночастицы Au-Pt могут быть связаны с антителами за счет физической адсорбции.
ИХА основан на миграции жидкой пробы вдоль тест-полоски под действием капиллярных сил без использования дополнительного оборудования. При прохождении пробы через иммобилизованные на тест-полоске иммуннореагенты на разных участках мембраны происходит формирование двойных иммунных комплексов при контакте пробы с конъюгатом (клетки С.michiganensis с конъюгатом антител с пористыми наночастицами Au-Pt), тройных иммунных комплексов при прохождении пробы через тестовую зону (Т.З.) (клетки С.michiganensis с конъюгатом антител с пористыми наночастицами Au-Pt - иммобилизованные в Т.З. антитела) и связывания избытка свободного конъюгата в контрольной зоне (К.З.) (конъюгат антител с пористыми наночастицами Au-Pt - иммуноглобулин-связывающий белок А в К.З.) Конъюгированный со специфическими антителами маркер (пористые наночастицы Au-Pt) распределяется по рабочей мембране за счет формирования иммунных комплексов, и его наличие или отсутствие в определенных участках мембраны приводит к возникновению окрашивания. Для снижения предела обнаружения ИХА на тест-полоску наносится субстратный раствор (10 мкл), состоящий из 0,05% 3,3'-диаминобензидина, 0,03% пероксида водорода и 0,05% сульфата никеля в 50 мМ фосфатном буфере (рН=7,2). После пятиминутной инкубации субстратного раствора н тест-полоски под действием наночастиц Au-Pt происходит конверсия неокрашенного субстрата в нерастворимый продукт, накопление которого в Т.З. и К.З. существенно увеличивает интенсивность колориметрического сигнала.
Использование ИХА для детекции фитопатогенных микроорганизмов обеспечивает достижение ряда преимуществ - проведение эффективного параллельного скрининга большого количества проб во внелабораторных условиях, экспрессность анализа (15-20 мин) при минимальной подготовке проб, простота детектирования и интерпретации результатов.
Несмотря на то, что ИХА активно разрабатывается и применяется для диагностики фитопатогенов и других токсичных контаминантов, разработка иммунохроматографических тест-систем для высокочувствительной детекции С.michiganensis с целью внелабораторного выявления латентных инфекций кольцевой гнили картофеля не описана.
Наиболее близкими аналогами заявляемой полезной модели являются иммунохроматографические тест-системы с использованием наночастиц ядро-оболочка Au-Pt, представленные в работах:
Jiang и соавторов « Sensitive detection of Escherichia coli 0157:H7 using Pt-Au bimetal nanoparticles with peroxidase-like amplification)), Biosensors and Bioelectronics, 2016, v. 77, p. 687-694.;
Loynachan и соавторов «Platinum nanocatalyst amplification: redefining the gold standard for lateral flow immunoassays with ultrabroad dynamic range)). ACS Nano, 2018, V. 12, p. 279-288.
Технической задачей заявленной полезной модели является повышение интенсивности окрашивания Т.З. посредством реакции, катализируемой пористыми наночастицами типа ядро-оболочка Au-Pt на тест-полоске.
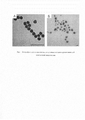
Технический результат заявленной полезной модели заключается в снижении предела обнаружения фитопатогенной бактерии С.michiganensis за счет использованием простой одностадийной процедуры, обеспечиваемой добавлением на тест-полоску субстратного раствора, содержащего смесь 3 3'-диаминобензидина, пероксида водорода и ионов Ni2+. Пористая структура наночастиц ядро-оболочка Au-Pt (Рис 1 А), отличающая их от стандартных частиц ядро-оболочка (Рис 1 Б), достигается за счет адсорбции поливинилпирролидона на поверхности затравочных наночастиц золота, что препятствует формированию монослоя плагины вокруг затравочных частиц. Пористая морфология обеспечивает большую площадь поверхности активных частиц, существенно увеличивая их удельную каталитическую активность по сравнению с непористыми частицами ядро-оболочка. Пористые наночастицы Au-Pt сохраняют до 80% пероксидазо-подобной активности в присутствии азида натрия - ингибитора пероксидаз, что позволяет использовать предложенную схему для повышения интенсивности колориметрического сигнала даже в растительных пробах с высокой эндогенной пероксидазной активностью.
Предлагается устройство для иммунохроматографической экспрессной лабораторной и внелабораторной высокочувствительной детекции С.michiganensis в экстрактах листьев и клубней картофеля. Устройство представляет собой мультимембранный композит с предварительно нанесенными и высушенными иммунореагентами (тест-полоску). В состав композита (рис. 2) входят рабочая нитроцеллюлозная мембрана с предварительно нанесенными иммунореагентами, закрепленная на твердой полистироловой основе, стекловолоконная мембрана с нанесенными конъюгатом пористых наночастиц типа ядро-оболочка - Au-Pt. стабилизированных поливинилпирролидоном с кроличьими поликлональными антителами специфичными к бактериальным клеткам С.michiganensis, мембрана для впитывания и сепарации компонентов исследуемой пробы и конечной адсорбирующей мембраны для впитывания компонентов пробы после прохождения реакции и поддержания миграции жидкости по тест-полоске за счет капиллярных сил.
Указанный технический результат достигается тем, что:
- в контрольную зону (К.З.) нанесен иммуноглобулин-связывающий белок А;
- в тестовую зону (Т.З.) нанесены кроличьи поликлональные антитела специфичные к клеткам С.michiganensis;
- на стекловолоконную мембрану нанесен конъюгат пористых наночастиц Au-Pt с поликлональиыми кроличьими антителами, специфичными к С.michiganensis
- при добавлении смеси субстратного раствора, содержащего смесь 3,3'-диаминобензидина, пероксида водорода и ионов Ni2+ наночастицы Au-Pt катализируют реакцию окисления 3,3'-диаминобензидина пероксидом водорода, ионы никеля обеспечивают формирование нерастворимого темноокрашенного продукта реакции, прецицитирующего на рабочей нитроцеллюлозной мембране.
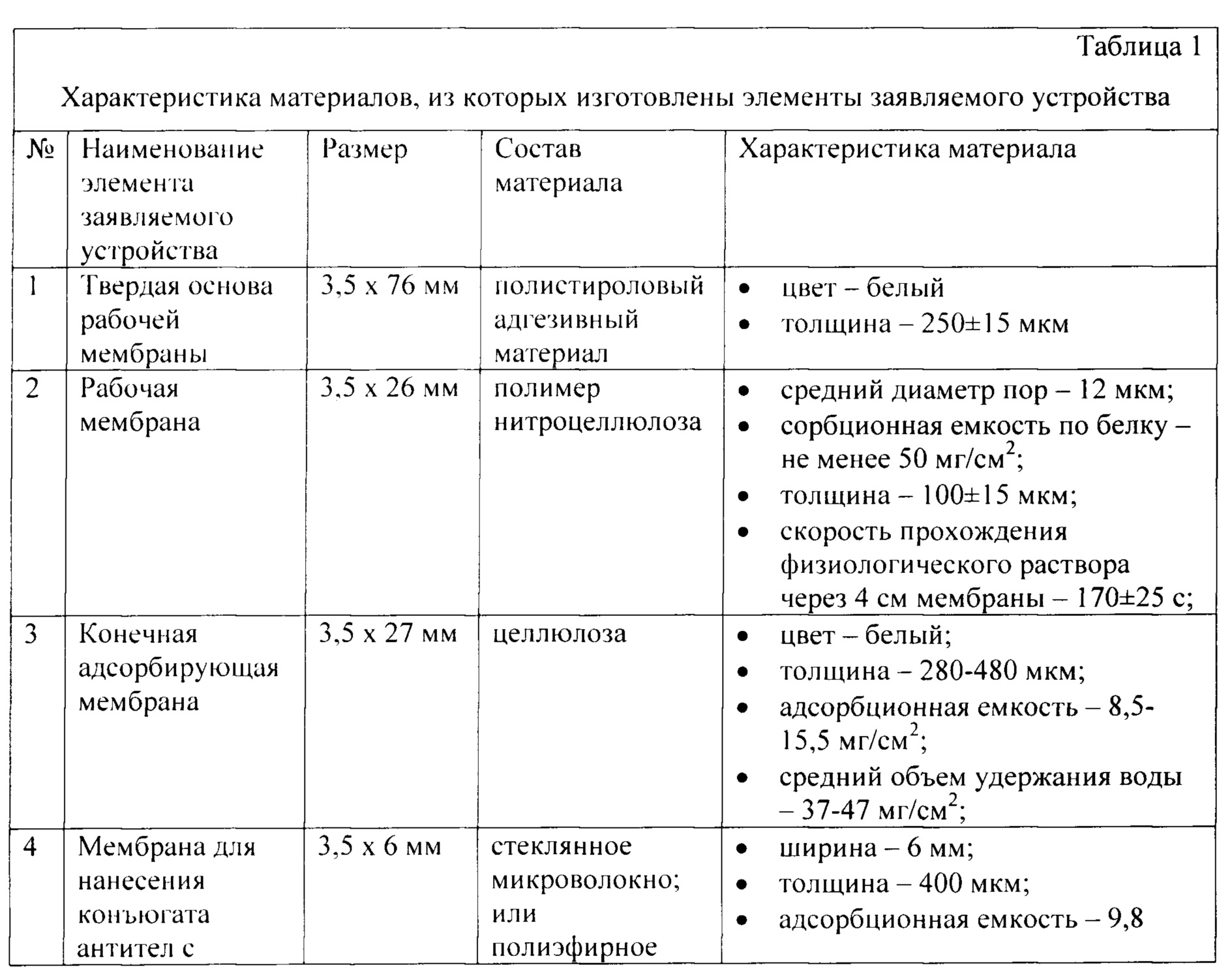
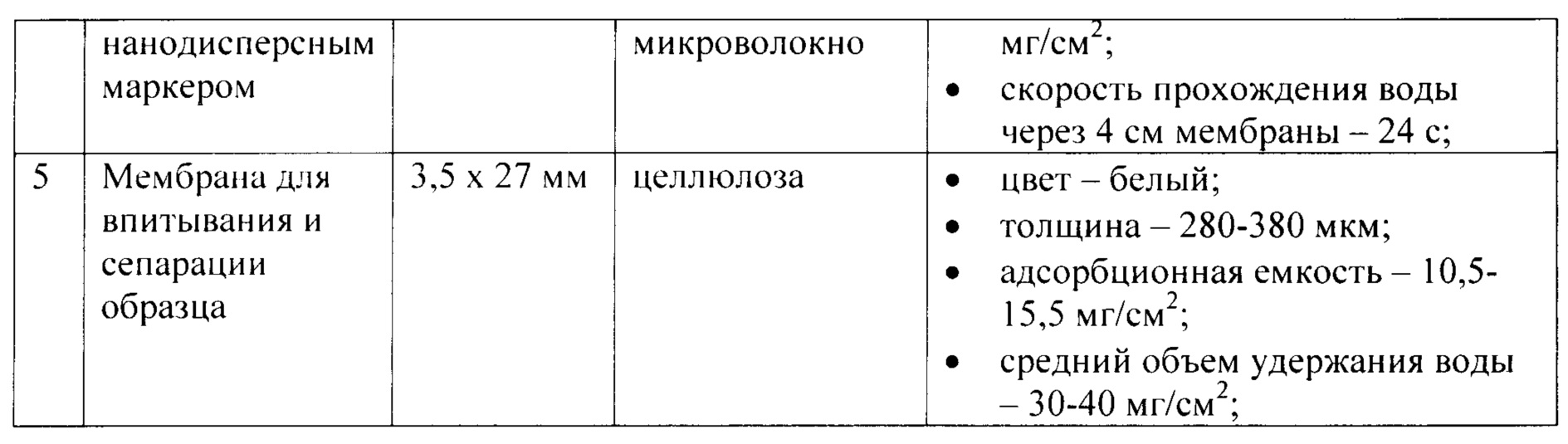
В таблице 1 приведена характеристика материалов, из которых изготовлены элементы заявляемого устройства.
Анализ проводят следующим образом:
1. 100 мкл анализируемого растительного экстракта (экстракт листьев или клубней картофеля) вносят в пластиковую пробирку вместимостью 1,5 мл.
2. Тест-полоску погружают вертикально нижним концом мембраны для впитывания образца в анализируемый экстракт и выдерживают при комнатной температуре в течение 5 мин.
3. Вынимают тест-полоску и помещают ее на сухую горизонтальную поверхность на 5 мин.
4. Через 10 мин после начала движения жидкости по тест-полоске результат анализа фиксируют визуально или с использованием детектора с видеоцифровой регистрацией.
5. Добавляют 20 мкл субстратного раствора, и выдерживают в течение 3 мин. Результат анализа фиксируют визуально или с использованием детектора с видеоцифровой регистрацией.
Заявляемое устройство функционирует следующим образом (см. рис. 1). Если в образце присутствуют клетки С.michiganensis, то под действием капиллярных сил они с потоком жидкости перемещаются по впитывающей мембране (5), доходят до стекловолоконной мембраны (4) и вступают в реакцию с поликлональными антителами на поверхности конъюгатов пористых наночастиц Au-Pt с образованием двойных иммунных комплексов (клетки С.michiganensis - антитела, меченные пористыми наночастицами Au-Pt). Образовавшиеся двойные иммунные комплексы под действием капиллярных сил движутся вдоль рабочей нитроцеллюлозной мембраны (2) и взаимодействуют с иммобилизованными в Т.З. поликлональными антителами к С.michiganensis с образованием тройных комплексов (иммобилизованные на мембране в Т.З. антитела - клетки С.michiganensis - антитела, меченные пористыми наночастицами Au-Pt). Избыток несвязавшихся в Т.З. конъюгатов пористых наночастиц с антителами продолжает двигаться вдоль рабочей нитроцеллюлозной мембраны (2) и взаимодействует с белком А, иммобилизованными в К.З. (А), с образованием двойных комплексов (иммобилизованные на мембране антивидовые антитела - антитела, меченные коллоидным золотом).
Интерпретация результатов анализа производится на основании наличия окрашенных Т.З. и К.З.:
1. Если через 10 мин на рабочей мембране тест-полоски появляются две темноокрашенные зоны (Т.З. и К.З.), то результат анализа считается положительным, т.е. в растительной пробе присутствуют клетки С.michiganensis. Проведения дополнительной стадии усиления сигнала в таком случае не требуется.
2. Если через 10 мин на рабочей мембране тест-полоски появляется одна темноокрашенная К.З. при этом окрашивание Т.З. не наблюдается, то результат анализа считается отрицательным, т.е. в растительной пробе не содержится клеток С.michiganensis или их количество оказывается меньше предела обнаружения ИХА. В таком случае проводится дополнительная стадия усиления сигнала. Для этого на тест-полоску добавляют 20 мкл субстратного раствора. После добавления субстрата полоска выдерживается в течение 3 мин в вертикальном положении. Наличие темноокрашенной Т.З. свидетельствует о присутствии бактериальных клеток С.michiganensis в анализируемой пробе, отсутствие окрашенной Т.З. и наличие окрашенной К.З. свидетельствует об отсутствии С.michiganensis в анализируемой пробе.
3. Если через 10 мин на рабочей мембране тест-полоски не образуется ни одной окрашенной линии или происходит окрашивание только Т.З. (без формирования окраски К.З.), то результат анализа считается недействительным (рис. 2д). В таком случае необходимо повторное тестирование с использованием новой тест-полоски.
Эффективность данного подхода подтверждается следующими примерами:
Пример 1 (влияние азида натрия на пероксидазную активность экстрактов клубней картофеля и конъюгата пористых наночастиц Ai-Pt с поликлональными антителами против клеток С.michiganensis)
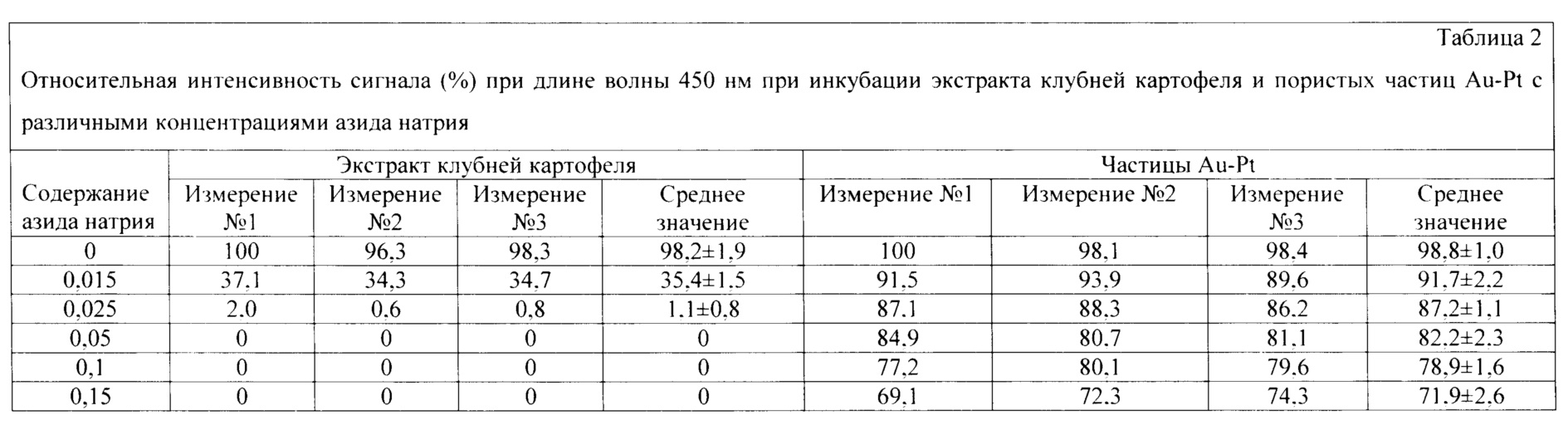
Выбор концентрации азида натрия, обеспечивающей ингибирование эндогенных пероксидаз в растительном экстракте с сохранением высокой перикосидаза-подобной активности пористых наночастиц Au-Pt, позволяет использовать данный наноразмерный маркер для ИХА без дополнительных отмывок. В течение 5 мин инкубировали различные концентрации азида натрия (0-0,15%) с 100 мкл экстракта клубней картофеля и 95 мкл фосфатного буфера, содержащего 5 мкл пористых наночастиц. Далее добавляли 100 мкл субстратного раствора, содержащего 50 мМ 3,3'5,5'-тетраметилбензидин, 3 мМ пероксид водорода в 50 мМ цитратном буфере, рН=5,0, и выдерживали в течение 10 мин. Ферментативную реакцию останавливали добавлением 50 мкл 1 М серной кислоты. Интенсивность окрашивания при длине волны 450 нм фиксировали с помощью фотометра в трех повторностях. Результаты представлены в таблице 2.
Наночастицы Au-Pt сохраняют до 82% пероксидаза-подобной активности в условиях, обеспечивающих полную инактивацию эндогенных пероксидаз. Таким образом, добавление 0,05% азида натрия позволяет проводить амплификацию сигнала с использованием каталитической активности пористых наночастиц даже при анализе проб с высокой эндогенной пероксидазной активностью.
Пример 2 (выявление клеток С.michiganensis в экстракте клубней картофеля без проведения стадии амплификации сигнала).
С использованием заявляемого устройства проводят анализ экстрактов клубней картофеля, с добавлением 103- 106 клеток/мл (кл/мл) С.michiganensis и экстракта клубней картофеля, не содержащего бактериальных клеток. Анализируемую аликвоту (100 мкл экстракта) вносят в пробирку, после чего тест-полоску погружают вертикально нижним концом мембраны для впитывания образца на глубину 0,5 см в образец и инкубируют при комнатной температуре в течение 5 мин. Вынимают тест-полоску и помещают ее на горизонтальную поверхность. Результат анализа оценивают через 5 мин с помощью программного обеспечения видеоцифрового детектора. Анализ проводят в трех повторностях, используя тест-полоски разных серий. Результаты анализа приведены в таблице 3.
Пределом обнаружения ИХА считали количество клеток С.michiganensis, обеспечивающих колориметрический сигнал в Т.З. превосходящий сумму среднего значения колориметрического сигнала и трех стандартных отклонений для отрицательной пробы (здоровый экстракт). Для ИХА без проведения амплификации сигнала сумма среднего значения колориметрического сигнала и трех стандартных отклонений для отрицательной пробы была равна 0,85. Таким образом, предел обнаружения для данной системы составлял 104 кл/мл С.michiganensis. Из приведенных данных видно, что регистрируемая интенсивность колориметрического сигнала в тестовой зоне позволяет достоверно детектировать 104 кл/мл С.michiganensis в экстракте клубней картофеля в рамках заявленного времени анализа (10 мин).
Пример 3 (выявление клеток С.michiganensis в экстракте клубней картофеля без проведения стадии амплификации сигнала).
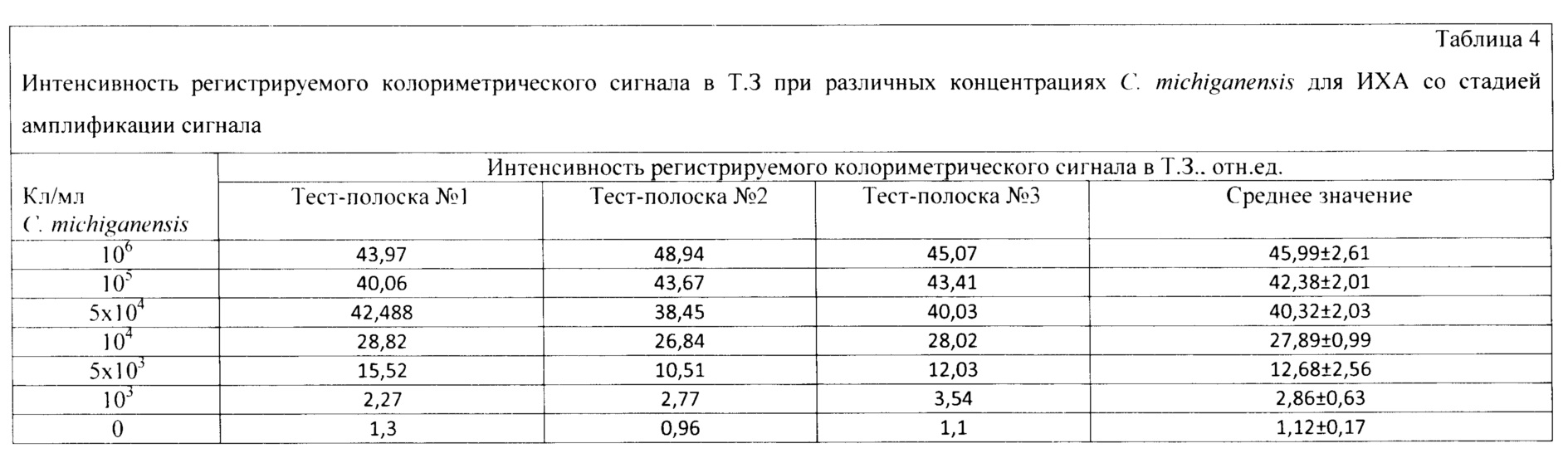
С использованием заявляемого устройства проводят анализ экстрактов клубней картофеля, с добавлением 103-106 клеток/мл (кл/мл) С.michiganensis и экстракта клубней картофеля, не содержащего бактериальных клеток. Анализируемую аликвоту (100 мкл экстракта) вносят в пробирку, после чего тест-полоску погружают вертикально нижним концом мембраны для впитывания образца на глубину 0,5 см в образец и инкубируют при комнатной температуре в течение 5 мин. Вынимают тест-полоску и помещают ее на горизонтальную поверхность. Спустя 5 мин добавляют 20 мкл субстратного раствора. Результат анализа оценивают через 5 мин с помощью видеоцифрового детектора. Анализ проводят в трех повторностях, используя тест-полоски разных серий. Результаты анализа приведены в таблице 4.
Пределом обнаружения ИХА считали количество клеток С.michiganensis, обеспечивающих колориметрический сигнал в Т.З. превосходящий сумму среднего значения колориметрического сигнала и трех стандартных отклонений для отрицательной пробы (здоровый экстракт). Для ИХА без проведения амплификации сигнала сумма среднего значения колориметрического сигнала и трех стандартных отклонений для отрицательной пробы была равна 1,63. Таким образом, предел обнаружения для данной системы составлял 103 кл/мл С.michiganensis. Из приведенных экспериментальных данных видно, что регистрируемая интенсивность колориметрического сигнала в тестовой зоне позволяет достоверно детектировать 103 кл/мл С.michiganensis в экстракте клубней картофеля в рамках заявленного времени анализа (10 мин).
По сравнению с системой без амплификации сигнала получено десятикратное снижение предела обнаружения, достигаемое за короткое время (дополнительных 5 мин), и не требующее сложных методических решений (добавление капли готового к использованию субстратного раствора на тест-полоску).
Краткое описание чертежей.
На рис. 1 представлены микрофотографии наночастиц, полученные методом просвечивающей электронной микроскопии. А - наночастицы типа ядро-оболочка Au-Pt. Б - пористые наночастицы типа ядро-оболочка Au-Pt, стабилизированные поливинилпирролидоном.
На рис. 2 изображена схема заявляемого устройства для иммунохроматографической экспрессной лабораторной и внелабораторной детекции С.michiganensis. 1 - твердая полистирольная основа рабочей нитроцеллюлозной мембраны; 2 - рабочая нитроцеллюлозная мембрана; 3 - конечная адсорбирующая мембрана для впитывания компонентов образца после прохождения реакции; 4 - стекловолоконная мембрана с нанесенным и высушенным конъюгатом пористых наночастиц Au-Pt с поликлональными кроличьими антителами, специфичными к С.michiganensis; 5 - мембрана для впитывания и сепарации исследуемого образца; 6 - Т.З. с нанесенными поликлональными кроличьими антителами к С.michiganensis; 7 - К.З. с нанесенным иммуноглобулин-связывающим белком А.
Claims (1)
- Устройство для иммунохроматографической экспрессной внелабораторной детекции фитопатогенной бактерии - Clavibacter michiganensis, включающее в себя тест-полоску, состоящую из полистироловой подложки, на которую закреплены нитроцеллюлозная мембрана с предварительно нанесенными и высушенными антителами, стекловолоконная мембрана с нанесенными и высушенными конъюгатом антител с пористыми наночастицами ядро-оболочка - Au-Pt, стабилизированных поливинилпирролидоном, мембрана для впитывания и сепарации исследуемой пробы и конечная адсорбирующая мембрана для впитывания компонентов пробы после прохождения реакции и поддержания миграции жидкости по тест-полоске за счет капиллярных сил, на нитроцеллюлозную мембрану нанесены контрольная и тестовые зоны, в контрольную зону иммобилизован иммуноглобулин-связывающий белок А, в тестовую зону иммобилизованы поликлональные кроличьи антитела, специфичные к бактериальным клеткам С.michiganensis, на стекловолоконную мембрану нанесен конъюгат поликлональных кроличьих антител, специфичных к С.michiganensis, с пористыми наночастицами Au-Pt, формирующие в результате миграции пробы в тестовой зоне иммунные комплексы приводят к развитию окрашивания, и интенсивность которого пропорциональна количеству клеток С.michiganensis в пробе, повышение интенсивности окрашивания при низких концентрациях С.michiganensis основано на накоплении нерастворимого продукта каталитической реакции окисления 3,3'-диаминобензидина в присутствии пероксида водорода и ионов никеля и достигается за счет пероксидазо-подобных свойств пористых наночастиц Au-Pt, используемых в качестве каталитической и колориметрической метки.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2020119108U RU202193U1 (ru) | 2020-06-09 | 2020-06-09 | Устройство для иммунохроматографической высокочувствительной и внелабораторной детекции фитопатогенной бактерии Clavibacter michiganensis, основанное на повышении интенсивности регистрируемого колориметрического сигнала за счет каталитических свойств наномаркера |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2020119108U RU202193U1 (ru) | 2020-06-09 | 2020-06-09 | Устройство для иммунохроматографической высокочувствительной и внелабораторной детекции фитопатогенной бактерии Clavibacter michiganensis, основанное на повышении интенсивности регистрируемого колориметрического сигнала за счет каталитических свойств наномаркера |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU202193U1 true RU202193U1 (ru) | 2021-02-05 |
Family
ID=74550983
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2020119108U RU202193U1 (ru) | 2020-06-09 | 2020-06-09 | Устройство для иммунохроматографической высокочувствительной и внелабораторной детекции фитопатогенной бактерии Clavibacter michiganensis, основанное на повышении интенсивности регистрируемого колориметрического сигнала за счет каталитических свойств наномаркера |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU202193U1 (ru) |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2523393C1 (ru) * | 2013-03-19 | 2014-07-20 | Федеральное государственное бюджетное учреждение науки Институт биохимии имени А.Н. Баха РАН Российской академии наук (ИНБИ РАН) | Тест-полоска для высокочувствительного иммунохроматографического анализа |
| US9739773B1 (en) * | 2010-08-13 | 2017-08-22 | David Gordon Bermudes | Compositions and methods for determining successful immunization by one or more vaccines |
| RU2642588C1 (ru) * | 2017-03-14 | 2018-01-25 | Федеральное государственное бюджетное образовательное учреждение высшего образования "Вятский государственный университет" | Иммунохроматографическая тест-система для выявления патогенных штаммов helicobacter pylori |
| RU192778U1 (ru) * | 2018-12-26 | 2019-10-01 | Федеральное государственное учреждение "Федеральный исследовательский центр "Фундаментальные основы биотехнологии" Российской академии наук" (ФИЦ Биотехнологии РАН) | Устройство для иммунохроматографической экспрессной внелабораторной диагностики заболевания винограда, вызываемого вирусом скручивания листьев |
-
2020
- 2020-06-09 RU RU2020119108U patent/RU202193U1/ru active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9739773B1 (en) * | 2010-08-13 | 2017-08-22 | David Gordon Bermudes | Compositions and methods for determining successful immunization by one or more vaccines |
| RU2523393C1 (ru) * | 2013-03-19 | 2014-07-20 | Федеральное государственное бюджетное учреждение науки Институт биохимии имени А.Н. Баха РАН Российской академии наук (ИНБИ РАН) | Тест-полоска для высокочувствительного иммунохроматографического анализа |
| RU2642588C1 (ru) * | 2017-03-14 | 2018-01-25 | Федеральное государственное бюджетное образовательное учреждение высшего образования "Вятский государственный университет" | Иммунохроматографическая тест-система для выявления патогенных штаммов helicobacter pylori |
| RU192778U1 (ru) * | 2018-12-26 | 2019-10-01 | Федеральное государственное учреждение "Федеральный исследовательский центр "Фундаментальные основы биотехнологии" Российской академии наук" (ФИЦ Биотехнологии РАН) | Устройство для иммунохроматографической экспрессной внелабораторной диагностики заболевания винограда, вызываемого вирусом скручивания листьев |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Dehghani et al. | Colorimetric aptasensor for Campylobacter jejuni cells by exploiting the peroxidase like activity of Au@ Pd nanoparticles | |
| CA1251382A (en) | Use of substituted quinone electron transfer agents in analytical determinations | |
| DE3785499T2 (de) | Verwendung von Phenolen und Anilinen zur Erhöhung der Rate von peroxidase-katalysierter Oxydation der Leucofarbstoffe. | |
| EP2574926B1 (en) | Chromatographic kit and chromatography method | |
| WO1986004421A1 (en) | Enzyme immunoassay with two-part solution of tetramethylbenzidine as chromogen | |
| CH627281A5 (ru) | ||
| JPS63271160A (ja) | 糞便試料のイムノアツセイの組成物および方法 | |
| KR101990301B1 (ko) | 광학 바이오센서 | |
| DE68924272T2 (de) | Verfahren zur vorbehandlung von mustern bei peroxidase-katalysierten enzymtestverfahren. | |
| Siegmann-Thoss et al. | Enzyme immunosensor for diagnosis of myocardial infarction | |
| Salimi et al. | Electrochemical immunosensor based on carbon nanofibers and gold nanoparticles for detecting anti-Toxoplasma gondii IgG antibodies | |
| Głowacka et al. | Photometric flow system for the determination of serum lactate dehydrogenase activity | |
| RU202193U1 (ru) | Устройство для иммунохроматографической высокочувствительной и внелабораторной детекции фитопатогенной бактерии Clavibacter michiganensis, основанное на повышении интенсивности регистрируемого колориметрического сигнала за счет каталитических свойств наномаркера | |
| Slama et al. | Simultaneous mixture analysis using a dynamic microbial sensor combined with chemometrics | |
| Fernandez-Baldo et al. | Microfluidic immunosensor with micromagnetic beads coupled to carbon-based screen-printed electrodes (SPCEs) for determination of Botrytis cinerea in tissue of fruits | |
| US20100209941A1 (en) | Method, device and kit for determining conditions related to a dysfunction of the renal proximal tubule | |
| Vinicius Foguel et al. | Amperometric Immunosensor for Chagas’ Disease Using Gold CD‐R Transducer | |
| US20090053694A1 (en) | Photochemically Amplified Bioassay | |
| Patra et al. | Biosensors involved in dairy industries | |
| EP4127719B1 (en) | Method for detection of cd16b | |
| RU201487U1 (ru) | Устройство для мультиплексного иммунохроматографического анализа патогенов вирусной и бактериальной природы с дополнительной стадией усиления сигнала | |
| Monroe | Amperometric immunoassay | |
| EP0903410B1 (de) | Verfahren zum Nachweis und zur Bestimmung enzymatischer Reaktionen in Urin | |
| Tasaki et al. | Hyporesponsiveness against donor’s ABO antigens of renal grafts after ABO-incompatible kidney transplantation | |
| CN110296972B (zh) | 一种基于sers技术的金黄色葡萄球菌定量检测方法 |