KR20210053881A - 살리노마이신을 포함하는 폴리머 나노입자 - Google Patents
살리노마이신을 포함하는 폴리머 나노입자 Download PDFInfo
- Publication number
- KR20210053881A KR20210053881A KR1020217004716A KR20217004716A KR20210053881A KR 20210053881 A KR20210053881 A KR 20210053881A KR 1020217004716 A KR1020217004716 A KR 1020217004716A KR 20217004716 A KR20217004716 A KR 20217004716A KR 20210053881 A KR20210053881 A KR 20210053881A
- Authority
- KR
- South Korea
- Prior art keywords
- peg
- cancer
- poly
- pharmaceutical composition
- pla
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/51—Nanocapsules; Nanoparticles
- A61K9/5107—Excipients; Inactive ingredients
- A61K9/513—Organic macromolecular compounds; Dendrimers
- A61K9/5146—Organic macromolecular compounds; Dendrimers obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyethylene glycol, polyamines, polyanhydrides
- A61K9/5153—Polyesters, e.g. poly(lactide-co-glycolide)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/35—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having six-membered rings with one oxygen as the only ring hetero atom
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7048—Compounds having saccharide radicals and heterocyclic rings having oxygen as a ring hetero atom, e.g. leucoglucosan, hesperidin, erythromycin, nystatin, digitoxin or digoxin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y5/00—Nanobiotechnology or nanomedicine, e.g. protein engineering or drug delivery
Abstract
본 발명은 살리노마이신을 포함하는 폴리머 나노입자, 및 특정 질병의 치료를 필요로 하는 대상체에 이러한 폴리머 나노입자를 투여하는 것을 포함하는 특정 질병을 치료하는 방법에 관한 것이다.
Description
관련 출원
본 출원은 2018년 7월 18일에 출원된 미국 가출원 제62/699,963호에 대한 우선권의 혜택을 주장한다. 상기 출원의 내용은 전문이 본원에 참고로 포함된다.
분야
본 발명은 나노기술 분야, 구체적으로, 살리노마이신과 같은 치료제의 전달을 위한 생분해성 폴리머 나노입자의 용도에 관한 것이다.
스트렙토마이세스 알부스(Streptomyces albus)로부터 단리된 모노카복실 폴리에테르 항생제인 살리노마이신은 전통적으로, 항생제로서 사용되고 있다. 살리노마이신은 최근에, 세포 주기 정지, 아폽토시스를 야기시키고 다중-약물 내성을 극복하는 것을 포함하는, 여러 방식으로 암 세포 및 암 줄기 세포에 영향을 미치는 것으로 밝혀졌다. 시험관내 증거에서는 살리노마이신이 유방암, 난소암, 및 췌장암을 포함하는 여러 암 타입에 영향을 미치는 것으로 나타났다. 살리노마이신으로의 치료는 신경독성을 포함하는 독성을 유발할 수 있으며, 살리노마이신의 유효 용량을 여전히 유지하면서 이러한 독성을 줄일 필요성이 존재한다.
본 개시는 부분적으로, 살리노마이신을 포함하는 나노입자가 암을 치료하는 데 동일한 용량으로 투여될 때 살리노마이신 단독보다 덜 독성적이라는 발견을 기초로 한 것이다. 따라서, 일 양태에서, 본 발명은 폴리(락트산)(PLA) 및 폴리(에틸렌 글리콜)(PEG)을 포함하는 블록 코폴리머를 포함하는 폴리머 나노입자; 및 살리노마이신을 포함하는 조성물을 제공한다.
본 개시는 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG) 테트라블록 코폴리머를 포함하는 폴리머 나노입자 및 살리노마이신을 포함하는 조성물을 제공한다.
조성물의 다양한 구현예에서, PLA-PEG-PPG-PEG 테트라블록 코폴리머는 PEG-PPG-PEG 트리블록 코폴리머와 PLA의 컨쥬게이션으로부터 형성된다. 예를 들어, 컨쥬게이션은 화학적 컨쥬게이션이다.
다른 양태에서, 본원에는 빠르게 증식하는 세포의 증식, 생존, 이동, 또는 콜로니 형성 능력의 감소를 필요로 하는 대상체에서 빠르게 증식하는 세포의 증식, 생존, 이동, 또는 콜로니 형성 능력을 감소시키는 방법으로서, 세포를, 치료학적 유효량의 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG) 테트라블록 코폴리머를 포함하는 폴리머 나노입자, 및 살리노마이신을 포함하는 조성물과 접촉시키는 것을 포함하며, 치료학적 유효량은 대상체 체중 1 kg 당 약 0.025 mg(mg/kg) 내지 약 5 mg/kg의 살리노마이신인 방법이 제공된다.
방법의 일부 구현예에서, 세포는 암 세포이다. 방법의 다른 구현예에서, 세포는 암 줄기 세포이다.
다른 양태에서, 본원에는 암 치료를 필요로 하는 대상체에서 암을 치료하는 방법으로서, 대상체에, 치료학적 유효량의 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG) 테트라블록 코폴리머를 포함하는 폴리머 나노입자, 및 살리노마이신을 포함하는 조성물을 투여하는 것을 포함하며, 치료학적 유효량은 약 0.025 mg/kg 내지 약 5 mg/kg인 방법이 제공된다.
방법의 일부 구현예에서, 암은 유방암, 난소암, 췌장암, 백혈병, 림프종, 골육종, 위암, 전립선암, 결장암, 폐암, 간암, 신장암, 두경부암, 및 자궁경부암으로 이루어진 군으로부터 선택된다. 일 구현예에서, 암은 전이성이다.
다른 구현예에서, 방법은 대상체에 추가 항암 요법을 투여하는 것을 추가로 포함한다. 방법의 일 구현예에서, 추가 항암 요법은 수술, 화학요법, 방사선, 호르몬 요법, 면역요법, 또는 이들의 조합이다.
방법의 일부 구현예에서, 암은 화학치료제에 내성이 있거나 불응성이다.
방법의 특정 구현예에서, 대상체는 인간이다.
다른 양태에서, 본원에는 암 줄기 세포의 증식, 생존, 이동, 또는 콜로니 형성 능력의 감소를 필요로 하는 대상체에서 암 줄기 세포의 증식, 생존, 이동, 또는 콜로니 형성 능력을 감소시키는 방법으로서, 대상체에, 치료학적 유효량의, 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG) 테트라블록 코폴리머를 포함하는 폴리머 나노입자 및 살리노마이신을 포함하는 조성물을 투여하는 것을 포함하며, 치료학적 유효량은 약 0.025 mg/kg 내지 약 5 mg/kg인 방법이 제공된다.
방법의 구현예에서, 치료학적 유효량은 약 0.03 mg/kg 내지 약 0.5 mg/kg이다.
방법의 다른 구현예에서, 치료학적 유효량은 약 0.05 mg/kg 내지 약 0.8 mg/kg이다.
방법의 구현예에서, 치료학적 유효량은 약 0.08 mg/kg 내지 약 1.1 mg/kg이다.
방법의 구현예에서, 조성물은 정맥내로, 종양내로, 또는 피하로 투여된다.
방법의 일부 구현예에서, 조성물은 적어도 하루에 1회, 격일에 1회, 1주일에 1회, 1주일에 2회, 1개월에 1회, 또는 1개월에 2회 투여된다.
방법의 일 구현예에서, 조성물은 3주의 기간 동안 1주일에 1회 또는 1주일에 2회 투여된다.
방법의 일 구현예에서, PLA의 분자량은 약 10,000 내지 약 100,000 달톤이다.
방법의 다른 구현예에서, PLA의 분자량은 약 20,000 내지 90,000 달톤이다.
방법의 다른 구현예에서, PLA의 분자량은 약 30,000 내지 80,000 달톤이다.
방법의 다른 구현예에서, PLA의 분자량은 약 50,000 내지 80,000 달톤이다.
방법의 다른 구현예에서, PEG-PPG-PEG의 분자량은 약 2,000 달톤 내지 18,000 달톤이다.
방법의 다른 구현예에서, PEG-PPG-PEG의 분자량은 약 10,000 달톤 내지 15,000 달톤이다.
방법의 다른 구현예에서, 코폴리머에서 PLA의 분자량은 72,000이며, PEG-PPG-PEG의 분자량은 12,500 달톤이다.
방법의 다른 구현예에서, 코폴리머에서 PLA의 분자량은 35,000이며, PEG-PPG-PEG의 분자량은 12,500 달톤이다.
방법의 일 구현예에서, 조성물은 제2 치료제 또는 타겟팅된 항암제를 추가로 포함한다.
방법의 다른 구현예에서, 코폴리머에서 PLA의 분자량은 20,000이며, PEG-PPG-PEG의 분자량은 2,000 달톤이다.
다른 양태에서, 본원에는 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG) 테트라블록 코폴리머를 포함하는 폴리머 나노입자, 및 살리노마이신, 및 약제학적으로 허용되는 담체를 포함하는 약제 조성물이 제공된다.
약제 조성물의 일 구현예에서, 폴리머 나노입자는 폴리머 나노입자의 외측에 부착된 타겟팅 모이어티를 추가로 포함한다.
다른 양태에서, 본원에는 약 12.5 mg 내지 약 500 mg의, 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG) 테트라블록 코폴리머를 포함하는 폴리머 나노입자, 및 살리노마이신, 및 약제학적으로 허용되는 담체를 포함하는 약제 조성물을 포함하는 제형(dosage form)이 제공된다.
조성물의 다양한 구현예에서, PLA의 분자량은 약 10,000 내지 약 100,000 달톤; 약 20,000 내지 90,000 달톤; 약 30,000 내지 80,000 달톤; 약 8,000 달톤 내지 18,000 달톤; 또는 약 10,000 달톤 내지 15,000이다. 예를 들어, PLA의 분자량은 약 10,000; 20,000; 30,000; 40,000; 50,000; 60,000; 70,000; 80,000; 90,000, 또는 100,000 달톤이다. 추가 구현예에서, PLA의 분자량은 약 12,500 달톤(즉, 12.5 kDA) 또는 약 72,000 달톤(즉, 72 kDA)이다. 일 구현예에서, A-B 구조, 즉, A 및 B 서브유닛이 규칙적으로 교대하는 교대 코폴리머에서 테트라 블록을 생성하기 위한 2,000 내지 12,5000의 PEG-PPG-PEG의 분자량은 12.5 kDa이다.
조성물의 다양한 구현예에서, 폴리머 나노입자는 폴리(락트산)-폴리(에틸렌 글리콜)(PLA-PEG) 디-블록 코폴리머를 본질적으로 포함하는 폴리머로 형성된다.
조성물의 다양한 구현예에서, 폴리머 나노입자는 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG) 테트라블록 코폴리머를 본질적으로 포함하는 폴리머로 형성된다.
조성물의 다양한 구현예에서, 폴리머 나노입자는 폴리머 나노입자의 외측에 부착된 타겟팅 모이어티를 추가로 포함하며, 여기서, 타겟팅 모이어티는 항체, 펩타이드, 또는 아프타머이다. 다양한 구현예에서, 타겟팅 모이어티는 면역글로불린 분자, scFv, 모노클론 항체, 인간화된 항체, 키메라 항체, 인간화된 항체, Fab 단편, Fab' 단편, F(ab')2, Fv, 및 디설파이드 결합된 Fv를 포함한다.
본원에 제공된 임의의 조성물 또는 방법의 다양한 구현예에서, 나노입자는 폴리(락트산)(PLA) 및 폴리(에틸렌 글리콜)(PEG)을 포함하는 블록 코폴리머; 및 살리노마이신으로부터 형성된다. 일 구현예에서, 나노입자는 소정 기간 동안 살리노마이신을 방출시킨다. 추가 구현예에서, 기간은 적어도 1일 내지 20일이다. 방법의 다양한 구현예에서, 기간은 약 5일 내지 10일이다.
다른 양태에서, 본원에는 빠르게 증식하는 세포의 증식, 생존, 이동, 또는 콜로니 형성 능력의 감소를 필요로 하는 대상체에서 빠르게 증식하는 세포의 증식, 생존, 이동, 또는 콜로니 형성 능력을 감소시키는 데 사용하기 위한 약제 조성물로서, 약제 조성물은 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG) 테트라블록 코폴리머, 및 살리노마이신을 포함하며, 치료학적 유효량의 약제 조성물이 대상체에 투여되며, 치료학적 유효량은 약 0.025 mg/kg 내지 약 5 mg/kg인, 약제 조성물이 제공된다.
사용하기 위한 약제 조성물의 일부 구현예에서, 세포는 암 세포이다. 사용하기 위한 약제 조성물의 다른 구현예에서, 세포는 암 줄기 세포이다.
다른 양태에서, 본원에는 암의 치료를 필요로 하는 대상체에서 암을 치료하는 데 사용하기 위한 약제 조성물로서, 약제 조성물은 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG) 테트라블록 코폴리머, 및 살리노마이신을 포함하며, 치료학적 유효량의 약제 조성물이 대상체에 투여되며, 치료학적 유효량은 약 0.025 mg/kg 내지 약 5 mg/kg인 약제 조성물이 제공된다.
사용하기 위한 약제 조성물의 일부 구현예에서, 암은 유방암, 난소암, 췌장암, 백혈병, 림프종, 골육종, 위암, 전립선암, 결장암, 폐암, 간암, 신장암, 두경부암, 및 자궁경부암으로 이루어진 군으로부터 선택된다. 일 구현예에서, 암은 전이성이다.
다른 구현예에서, 사용하기 위한 약제 조성물은 대상체에 추가 항암 요법을 투여하는 것을 추가로 포함한다. 사용하기 위한 약제 조성물의 일 구현예에서, 추가 항암 요법은 수술, 화학요법, 방사선, 호르몬 요법, 면역요법, 또는 이들의 조합이다.
사용하기 위한 약제 조성물의 일부 구현예에서, 암은 화학치료제에 내성이 있거나 불응성이다.
사용하기 위한 약제 조성물의 특정 구현예에서, 대상체는 인간이다.
다른 양태에서, 본원에는 암 줄기 세포의 증식, 생존, 이동, 또는 콜로니 형성 능력의 감소를 필요로 하는 대상체에서 암 줄기 세포의 증식, 생존, 이동, 또는 콜로니 형성 능력을 감소시키는 데 사용하기 위한 약제 조성물로서, 약제 조성물은 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG) 테트라블록 코폴리머, 및 살리노마이신을 포함하며, 치료학적 유효량의 약제 조성물이 대상체에 투여되며, 치료학적 유효량은 약 0.025 mg/kg 내지 약 5 mg/kg인 약제 조성물이 제공된다.
사용하기 위한 약제 조성물의 구현예에서, 치료학적 유효량은 약 0.03 mg/kg 내지 약 0.5 mg/kg이다.
사용하기 위한 약제 조성물의 다른 구현예에서, 치료학적 유효량은 약 0.05 mg/kg 내지 약 0.8 mg/kg이다.
사용하기 위한 약제 조성물의 구현예에서, 치료학적 유효량은 약 0.08 mg/kg 내지 약 1.1 mg/kg이다.
사용하기 위한 약제 조성물의 구현예에서, 조성물은 정맥내로, 종양내로, 또는 피하로 투여된다.
사용하기 위한 약제 조성물의 일부 구현예에서, 조성물은 적어도 하루에 1회, 격일에 1회, 1주일에 1회, 1주일에 2회, 1개월에 1회, 또는 1개월에 2회 투여된다.
사용하기 위한 약제 조성물의 일 구현예에서, 조성물은 3주의 기간 동안 1주일에 1회 또는 1주일에 2회 투여된다.
사용하기 위한 약제 조성물의 일 구현예에서, PLA의 분자량은 약 10,000 내지 약 100,000 달톤이다.
사용하기 위한 약제 조성물의 다른 구현예에서, PLA의 분자량은 약 20,000 내지 90,000 달톤이다.
사용하기 위한 약제 조성물의 다른 구현예에서, PLA의 분자량은 약 30,000 내지 80,000 달톤이다.
사용하기 위한 약제 조성물의 다른 구현예에서, PLA의 분자량은 약 50,000 내지 80,000 달톤이다.
사용하기 위한 약제 조성물의 다른 구현예에서, PEG-PPG-PEG의 분자량은 약 8,000 달톤 내지 18,000 달톤이다.
사용하기 위한 약제 조성물의 다른 구현예에서, PEG-PPG-PEG의 분자량은 약 10,000 달톤 내지 15,000 달톤이다.
사용하기 위한 약제 조성물의 다른 구현예에서, 코폴리머에서 PLA의 분자량은 72,000이며, PEG-PPG-PEG의 분자량은 12,500 달톤이다.
사용하기 위한 약제 조성물의 다른 구현예에서, 코폴리머에서 PLA의 분자량은 35,000이며, PEG-PPG-PEG의 분자량은 12,500 달톤이다.
사용하기 위한 약제 조성물의 일 구현예에서, 조성물은 제2 치료제 또는 타겟팅된 항암제를 추가로 포함한다.
당업자는 본원에 기술되는 본 발명이 구체적으로 기술된 것 이외에 변경되고 개질될 수 있음을 인지할 것이다. 본원에 기술되는 본 발명이 이러한 모든 변형예 및 개질예를 포함하는 것으로 이해되어야 한다. 본 발명은 또한, 본 명세서에 개별적으로 또는 집합적으로 지칭되거나 명시된 이러한 모든 단계, 특징, 조성물 및 화합물, 및 임의의 2 이상의 단계 또는 특징의 임의의 및 모든 조합을 포함한다.
하기 도면은 본 명세서의 일부를 형성하고, 본 발명의 양태를 추가로 예시하기 위해 포함된다.
도 1a, 도 1b, 및 도 1c는 대조군의 마우스로부터의 건강한 간 섹션(도 1a), SAL 12.5 mg/kg 그룹의 마우스로부터의 지방 변화와 세포질 글리코겐의 혼합물(도 1b), 및 SAL 12.5 mg/kg 그룹의 마우스로부터의 건 지방증(tension lipidosis)(도 1c)을 나타낸 H&E로 염색된 마우스 간 섹션의 현미경 이미지이다.
도 2a 및 도 2b는 대조군의 마우스로부터의 정상 가수체(G), 근위 세뇨관(PT) 및 원위 세뇨관(DT)을 갖는 건강한 신장 섹션(도 2a), 및 12.5 mg/kg SAL 그룹의 마우스의 피복 상피의 위축증과 함께 세뇨관의 이격(별표), 관내강 내의 망상조직의 캐스트(화살표), 및 신소체의 뚜렷한 위축증(도 2b)을 도시한 H&E로 염색된 마우스 신장 섹션의 현미경 이미지이다.
도 3a 및 도 3b는 대조군으로부터의 마우스의 건강한 고환(도 3a) 및 12.5 mg/kg SAL 그룹으로부터의 마우스에서 수축된 정세관 및 생식 상피의 액포화(도 3b)를 나타낸 H&E로 염색된 마우스 고환 섹션의 현미경 이미지이다.
도 4a 및 도 4b는 대조군으로부터의 마우스의 건강한 부고환(도 4a) 및 12.5 mg/kg SAL 그룹으로부터의 마우스에서 액포화 및 괴저성 세포의 발생과 함께 상피의 파괴(도 4b)를 나타낸 H&E로 염색된 마우스 부고환 섹션의 현미경 이미지이다.
도 5a 및 도 5b는 살리노마이신-나노입자의 전자 현미경 사진이다. 도 5a는 살리노마이신-나노입자의 주사 전자 현미경 사진을 도시한 것이다. 도 5b는 살리노마이신-나노입자의 주사 전자 현미경 사진을 도시한 것이다. 도 6a 및 도 6b는 살리노마이신-나노입자의 크기 분포(도 6a) 및 제타 전위(도 6b)를 도시한 것이다.
도 7은 살리노마이신-나노입자로부터 살리노마이신의 방출을 나타낸 그래프이다.
도 8은 살리노마이신-나노입자로의 처리 후 H358 세포의 세포 생존의 용량 반응 곡선이다.
도 9a 및 도 9b는 살리노마이신-나노입자로의 처리 후 NCI-H526 세포의 세포 생존의 용량 반응 곡선이다(도 9a). 도 9b는 살리노마이신-나노입자의 2가지 상이한 제형으로의 처리 후 용량 반응 곡선이다.
도 10은 살리노마이신-나노입자로의 처리 후 NCI-H69 세포의 세포 생존의 용량 반응 곡선이다.
도 11은 살리노마이신-나노입자로의 처리 후 MDA-MB-231 세포의 세포 생존의 용량 반응 곡선이다.
도 12는 살리노마이신-나노입자로의 처리 후 SUM149 세포의 세포 생존의 용량 반응 곡선이다.
도 13은 살리노마이신-나노입자로의 처리 후 MCF7 세포의 세포 생존의 용량 반응 곡선이다.
도 14는 살리노마이신-나노입자로의 처리 후 MDA-MB-468 세포의 세포 생존의 용량 반응 곡선이다.
도 15a 및 도 15b는 살리노마이신 나노입자 또는 비히클 대조군으로의 처리 후 마우스에서 H69 세포의 종양 용적(도 15a) 및 동일한 마우스의 체중(도 15b)을 나타낸 그래프이다.
도 16a, 도 16b, 도 16c, 도 16d, 및 도 16e는 5 mg/kg(도 16a), 7.5 mg/kg(도 16b), 10 mg/kg(도 16c), 12.5 mg/kg(도 16d), 및 15 mg/kg(도 16e)의 살리노마이신 단독 또는 살리노마이신-나노입자로의 처리 후 야생형 마우스의 체중 및 사망률을 나타낸 그래프이다.
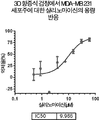
도 17a, 도 17b 및 도 17c는 3D 항-증식 검정에서 MDA-MB 231 세포에 대한 살리노마이신(도 17a), 살리노마이신 나노입자(도 17b)의 억제율(percentage inhibition)을 나타낸 용량 반응 곡선이다. 도 17c는 도 17a 및 도 17b의 데이터를 비교한 것이다.
도 18은 CD44+/CD24low 세포의 정량화와 함께, TNBC 환자로부터 단리되고 PBS, 살리노마이신, 살리노마이신-NP, 또는 파클리탁셀로 처리된 암 줄기 세포의 사진을 도시한 것이다.
도 1a, 도 1b, 및 도 1c는 대조군의 마우스로부터의 건강한 간 섹션(도 1a), SAL 12.5 mg/kg 그룹의 마우스로부터의 지방 변화와 세포질 글리코겐의 혼합물(도 1b), 및 SAL 12.5 mg/kg 그룹의 마우스로부터의 건 지방증(tension lipidosis)(도 1c)을 나타낸 H&E로 염색된 마우스 간 섹션의 현미경 이미지이다.
도 2a 및 도 2b는 대조군의 마우스로부터의 정상 가수체(G), 근위 세뇨관(PT) 및 원위 세뇨관(DT)을 갖는 건강한 신장 섹션(도 2a), 및 12.5 mg/kg SAL 그룹의 마우스의 피복 상피의 위축증과 함께 세뇨관의 이격(별표), 관내강 내의 망상조직의 캐스트(화살표), 및 신소체의 뚜렷한 위축증(도 2b)을 도시한 H&E로 염색된 마우스 신장 섹션의 현미경 이미지이다.
도 3a 및 도 3b는 대조군으로부터의 마우스의 건강한 고환(도 3a) 및 12.5 mg/kg SAL 그룹으로부터의 마우스에서 수축된 정세관 및 생식 상피의 액포화(도 3b)를 나타낸 H&E로 염색된 마우스 고환 섹션의 현미경 이미지이다.
도 4a 및 도 4b는 대조군으로부터의 마우스의 건강한 부고환(도 4a) 및 12.5 mg/kg SAL 그룹으로부터의 마우스에서 액포화 및 괴저성 세포의 발생과 함께 상피의 파괴(도 4b)를 나타낸 H&E로 염색된 마우스 부고환 섹션의 현미경 이미지이다.
도 5a 및 도 5b는 살리노마이신-나노입자의 전자 현미경 사진이다. 도 5a는 살리노마이신-나노입자의 주사 전자 현미경 사진을 도시한 것이다. 도 5b는 살리노마이신-나노입자의 주사 전자 현미경 사진을 도시한 것이다. 도 6a 및 도 6b는 살리노마이신-나노입자의 크기 분포(도 6a) 및 제타 전위(도 6b)를 도시한 것이다.
도 7은 살리노마이신-나노입자로부터 살리노마이신의 방출을 나타낸 그래프이다.
도 8은 살리노마이신-나노입자로의 처리 후 H358 세포의 세포 생존의 용량 반응 곡선이다.
도 9a 및 도 9b는 살리노마이신-나노입자로의 처리 후 NCI-H526 세포의 세포 생존의 용량 반응 곡선이다(도 9a). 도 9b는 살리노마이신-나노입자의 2가지 상이한 제형으로의 처리 후 용량 반응 곡선이다.
도 10은 살리노마이신-나노입자로의 처리 후 NCI-H69 세포의 세포 생존의 용량 반응 곡선이다.
도 11은 살리노마이신-나노입자로의 처리 후 MDA-MB-231 세포의 세포 생존의 용량 반응 곡선이다.
도 12는 살리노마이신-나노입자로의 처리 후 SUM149 세포의 세포 생존의 용량 반응 곡선이다.
도 13은 살리노마이신-나노입자로의 처리 후 MCF7 세포의 세포 생존의 용량 반응 곡선이다.
도 14는 살리노마이신-나노입자로의 처리 후 MDA-MB-468 세포의 세포 생존의 용량 반응 곡선이다.
도 15a 및 도 15b는 살리노마이신 나노입자 또는 비히클 대조군으로의 처리 후 마우스에서 H69 세포의 종양 용적(도 15a) 및 동일한 마우스의 체중(도 15b)을 나타낸 그래프이다.
도 16a, 도 16b, 도 16c, 도 16d, 및 도 16e는 5 mg/kg(도 16a), 7.5 mg/kg(도 16b), 10 mg/kg(도 16c), 12.5 mg/kg(도 16d), 및 15 mg/kg(도 16e)의 살리노마이신 단독 또는 살리노마이신-나노입자로의 처리 후 야생형 마우스의 체중 및 사망률을 나타낸 그래프이다.
도 17a, 도 17b 및 도 17c는 3D 항-증식 검정에서 MDA-MB 231 세포에 대한 살리노마이신(도 17a), 살리노마이신 나노입자(도 17b)의 억제율(percentage inhibition)을 나타낸 용량 반응 곡선이다. 도 17c는 도 17a 및 도 17b의 데이터를 비교한 것이다.
도 18은 CD44+/CD24low 세포의 정량화와 함께, TNBC 환자로부터 단리되고 PBS, 살리노마이신, 살리노마이신-NP, 또는 파클리탁셀로 처리된 암 줄기 세포의 사진을 도시한 것이다.
본 개시는 그 중에서도, 암을 치료하거나 예방하는 데 유용한 살리노마이신을 포함하는 나노입자를 제공한다. 나노입자는 살리노마이신의 독성을 감소시킨다.
정의
편의상, 본 발명의 추가 설명 전에, 본 명세서, 실시예 및 첨부된 청구범위에서 사용되는 특정 용어들이 본원에 기술된다. 이러한 정의는 본 개시의 나머지 부분을 고려하여 읽혀져야 하고, 당업자에 의해서 이해되어야 한다. 달리 규정하지 않는 한, 본원에서 사용되는 모든 기술 용어 및 과학 용어는 당업자에 의해 일반적으로 이해되는 것과 동일한 의미를 갖는다. 본 명세서 전반에 걸쳐 사용되는 용어는 특정 경우에서 달리 제한되지 않는 한, 하기와 같이 규정된다.
단수 형태("a," "an" 및 "the")는 하나의 물품의 문법적 대상 또는 하나 초과(즉, 적어도 하나)의 물품의 문법적 대상을 지칭하기 위해 사용된다.
용어 "포함하다(comprise)" "포함하는(comprising, including)" "함유하는" "...에 의해 특징되는" 및 이의 문법적 등가물은 포괄적, 개방형 의미로 사용되는 것으로서, 추가적인 요소가 포함될 수 있음을 의미한다. 이는 "...로만 이루어진" 것으로서 해석되는 것으로 의도되지 않는다.
본원에서 사용되는 "...로 이루어진" 및 이의 문법적 등가물은 청구범위에 기술되지 않은 임의의 요소, 단계 또는 구성성분을 배제한다.
본원에서 사용되는 용어 "약" 또는 "대략"은 제공된 값 또는 범위의 5% 이내를 의미한다.
본원에서 사용되는 용어 "생분해성"은 폴리머 구조의 효소적 및 비-효소적 파괴 또는 분해 둘 모두를 지칭한다.
용어 "양이온성"은 개개 환경 조건 하에서 순 양전하 또는 양의 제타 전위를 갖는 임의의 제제, 조성물, 분자 또는 물질을 지칭한다. 다양한 구현예에서, 본원에 기술된 나노입자는 양이온성 폴리머, 펩타이드, 단백질 담체, 또는 지질을 포함한다.
본원에서 사용되는 용어 "다중-약물 내성"은 둘 이상의 화학요법 약물에 대한 내성을 나타낸 암 세포를 지칭한다. 암 세포는 약물 흡수 감소 및 약물 유출 증가를 포함하는 여러 메커니즘에 의해 다중-약물 내성이 될 수 있다.
암 환자를 언급할 때 본원에서 사용되는 용어 치료제에 대한 "내성" 또는 "불응성"은 암이 치료제와의 접촉의 결과로서 치료제의 효과에 대한 내성을 선천적으로 갖거나 이에 대한 내성을 달성하였음을 의미한다. 대안적으로 기술하면, 암은 특정 치료제와 관련된 일반적인 치료 표준에 대해 내성이 있다.
본원에서 사용되는 용어 "나노입자"는 직경이 10 nm 내지 1000 nm 범위인 입자를 지칭하며, 여기서, 직경은 입자와 동일한 용적을 갖는 완전 구체의 직경을 지칭한다. 용어 "나노입자"는 "나노입자(들)"와 교환 가능하게 사용된다. 일부 경우에, 입자의 직경은 약 1 내지 1000 nm, 10 내지 500 nm, 20 내지 300 nm, 또는 100 내지 300 nm의 범위이다. 다양한 구현예에서, 직경은 약 30 내지 170 nm이다. 특정 구현예에서, 나노입자의 직경은 약 1, 5, 10, 25, 50, 75, 100, 125, 150, 175, 200, 225, 250, 275, 300, 325, 350, 375, 400, 425, 450, 475, 500, 525, 550, 575, 600, 625, 650, 675, 700, 725, 750, 775, 800, 825, 850, 875, 900, 925, 950, 975, 또는 1000 nm이다. 다른 구현예에서, 나노입자의 직경은 1, 5, 10, 25, 50, 75, 100, 125, 150, 175, 200, 225, 250, 275, 300, 325, 350, 375, 400, 425, 450, 475, 500, 525, 550, 575, 600, 625, 650, 675, 700, 725, 750, 775, 800, 825, 850, 875, 900, 925, 950, 975, 또는 1000 nm이다.
일부 경우에, 입자의 집단이 존재할 수 있다. 본원에서 사용되는, 나노입자의 직경은 특정 집단의 분포의 평균치이다.
본원에서 사용되는 용어 "폴리머"는 당해 분야에서 사용되는 바와 같은 이의 일반적인 의미, 즉, 공유 결합에 의해 연결된, 하나 이상의 반복 단위(모노머)를 포함하는 분자 구조를 제공한다. 반복 단위는 모두 동일할 수 있거나, 일부 경우에, 폴리머 내에 한 타입을 초과하는 반복 단위가 존재할 수 있다.
"화학치료제," "치료제," 및 "약물"은 작용 메커니즘과는 무관하게, 암의 치료에서 유용한 생물학적(대분자) 또는 화학적(소분자) 화합물이다. 화학치료제의 부류는 알킬화제, 항대사물질, 방추체 저해제 식물 알칼로이드, 세포독성/항종양 항생제, 토포이소머라아제 억제제, 단백질, 항체, 광민감제, 및 키나아제 억제제를 포함하지만, 이로 제한되지 않는다. 화학치료제는 "타겟팅된 치료법" 및 비-타겟팅된, 통상적인 화학요법에서 유용한 화합물을 포함한다.
"타겟팅 모이어티"는 타겟팅된 세포의 표면에 선택적으로 결합하는 분자이다. 예를 들어, 타겟팅 모이어티는 특정 타입의 세포 상에서 발견되거나 다른 세포보다 타겟 세포 상에서 더 높은 빈도로 발현되는 세포 표면 수용체에 결합하는 리간드일 수 있다.
타겟팅 모이어티 또는 치료제는 펩타이드 또는 단백질일 수 있다. "단백질" 및 "펩타이드"는 당해 분야에 널리 공지된 용어로서, 본원에서 사용되는 이러한 용어는 당해 분야에서 이의 일반적인 의미로 제공된다. 일반적으로, 펩타이드는 길이가 약 100개의 아미노산 미만인 아미노산 서열이며, 단백질은 일반적으로, 적어도 100개의 아미노산의 분자인 것으로 간주된다. 아미노산은 D- 또는 L-배열로 존재할 수 있다. 단백질은 예를 들어, 단백질 약물, 항체, 재조합 항체, 재조합 단백질, 또는 효소, 등일 수 있다. 일부 경우에, 펩타이드 또는 단백질의 아미노산 중 하나 이상은 화학적 독립체, 예를 들어, 탄수화물 기, 포스페이트 기, 파르네실 기, 이소파르네실 기, 지방산 기, 컨쥬게이션, 작용화, 또는 다른 개질, 예를 들어, 환형화, 바이-환형화(by-cyclization), 및 펩타이드 및 단백질에 더욱 유리한 성질을 부여하도록 의도된 임의의 여러 다른 개질을 위한 링커의 첨가에 의해 변형될 수 있다. 다른 경우에, 펩타이드 또는 단백질의 아미노산 중 하나 이상은 하나 이상의 비-천연 발생 아미노산으로의 치환에 의해 변형될 수 있다. 펩타이드 또는 단백질은 조합 라이브러리, 예를 들어, 파지 라이브러리, 효모 라이브러리, 또는 시험관내 조합 라이브러리로부터 선택될 수 있다.
본원에서 사용되는 용어 "조합," "치료 조합," 또는 "약제학적 조합"은 둘 이상의 치료제의 조합된 투여(예를 들어, 동시-전달)를 지칭한다. 병용 요법의 성분들은 동시에 또는 순차적으로 투여될 수 있으며, 즉, 조합물의 적어도 하나의 성분은 다른 성분(들)과 시간적으로 구별되는 소정 시간에 투여된다. 구현예에서, 성분(들)은 다른 성분(들)과 1개월, 1주, 1 내지 6일, 18, 12, 10, 9, 8, 7, 6, 5, 4, 3, 2, 1시간, 또는 30, 20, 15, 10, 또는 5분 이내에 투여된다.
본원에서 사용되는 용어 "약제학적으로 허용되는"은 건전한 의학적 판단의 범위 내에서, 과도한 독성, 자극성 알레르기 반응 및 합리적인 이익/위험 비율에 상응하는 다른 문제 합병증 없이, 온혈 동물, 예를 들어, 포유동물 또는 인간의 조직과 접촉하기에 적합한, 그러한 화합물, 물질, 조성물 및/또는 제형을 지칭한다.
하나 이상의 치료제를 포함하는 폴리머 나노입자의 "치료학적 유효량"은 조합물로 치료되는 장애의 임상적으로 관찰 가능한 징후 및 증상의 기준선에 비해 관찰 가능하거나 임상적으로 유의미한 개선을 제공하기에 충분한 양이다.
본원에서 사용되는 용어 "대상체" 또는 "환자"는 암 또는 암과 직접적으로 또는 간접적으로 관련된 임의의 장애를 앓거나 앓을 수 있는 동물을 포함하는 것으로 의도된다. 대상체의 예는 포유동물, 예를 들어, 인간, 유인원, 원숭이, 개, 소, 말, 돼지, 양, 염소, 고양이, 마우스, 토끼, 래트, 및 비-인간 형질 전환 동물을 포함한다. 일 구현예에서, 대상체는 인간, 예를 들어, 암을 앓고 있는 인간이다.
본원에서 사용되는 용어 "치료하는" 또는 "치료"는 대상체에서 적어도 하나의 증상을 완화, 감소 또는 개선시키거나 질병 진행의 지연을 형성시키는 치료를 포함한다. 예를 들어, 치료는 장애의 하나 또는 여러 증상의 감소 또는 암과 같은 장애의 완전한 박멸일 수 있다. 본 개시의 의미 내에서, 용어 "치료하다"는 또한, 질병을 악화시킬 위험을 억제하고/거나 감소시키는 것을 나타낸다. 본원에서 사용되는 용어 "예방하다," "예방하는" 또는 "예방"은 예방될 상태, 질병 또는 장애와 관련되거나 이에 의해 야기된 적어도 하나의 증상의 예방을 포함한다.
본원에서 사용되는 용어 "인간 등가 용량"은 동물 연구에서 사용되는 특정 용량으로부터 계산되는 인간에게 투여되는 조성물의 용량을 지칭한다.
본원에서 사용되는 용어 "빠르게 증식하는 세포"는 자율적 성장에 대한 능력을 갖는 세포(예를 들어, 암 세포)를 지칭한다.
본원에서 사용되는 용어 "암 줄기 세포"는 특정 종양 타입 및 자가-재생 능력 내에서 모든 세포 타입을 발생시키는 것과 같은 줄기 세포의 특징을 갖는 암 세포를 지칭한다. 일부 구현예에서, 암 줄기 세포는 화학요법에 내성이 있거나 불응성이다.
살리노마이신을 포함하는
폴리머
나노입자
본원에는 살리노마이신의 전달을 위한 생분해성 폴리머 나노입자가 제공된다. 살리노마이신을 포함하는 나노입자는 예를 들어, US 2015-0353676 A1호; PCT/US2016/060276호(2017년 5월 11일에 공개됨); 및 PCT/US2017/059542호(2017년 11월 1일에 출원됨)에 기술된 방법을 이용하여 제조될 수 있다.
일 구현예에서, 본원에 제공되는 폴리머 나노입자는 폴리(락트산)(PLA) 및 폴리(에틸렌 글리콜)(PEG)을 포함하는 블록 코폴리머를 포함한다. 폴리(락트산)(PLA)은 소수성 폴리머이고, 폴리머 나노입자의 합성을 위한 바람직한 폴리머이다. 그러나, 폴리(글리콜산)(PGA) 및 폴리 락트산-코-글리콜산(PLGA)의 블록 코폴리머가 또한 사용될 수 있다. 소수성 폴리머는 또한, 생물학적으로 유도될 수 있거나, 바이오폴리머일 수 있다. 사용되는 PLA의 분자량은 일반적으로 약 2,000 g/mol 내지 80,000 g/mol의 범위이다. 이에 따라, 일 구현예에서, 사용되는 PLA는 약 10,000 g/mol 내지 80,000 g/mol의 범위이다. PLA의 평균 분자량은 또한, 약 70,000 g/mol일 수 있다.
PEG는 친수성, 대식 세포에 대한 항-식균 작용, 및 면역학적 인식에 대한 내성을 부여하기 때문에, 폴리머 나노입자를 형성하기 위해 사용되는 폴리머에 대한 다른 바람직한 성분이다. 폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PEG-PPG-PEG)과 같은 블록 코폴리머는 본 발명에서 사용될 수 있는 친수성 또는 친수성-소수성 코폴리머이다. 블록 코폴리머는 2, 3, 4, 또는 그 초과의 수의 별개의 블록을 가질 수 있다.
본원에서 사용되는 1 g/mole은 1 "달톤"과 등가이다(즉, 달톤 및 g/mol은 폴리머의 분자량을 지칭할 때 상호 교환 가능함). 본원에서 사용되는 "킬로달톤"은 1,000 달톤을 지칭한다.
추가 구현예에서, 본원에 제공되는 폴리머 나노입자는 폴리(락트산)-폴리(에틸렌 글리콜)(PLA-PEG) 디-블록 코폴리머를 포함한다.
또 다른 구현예에서, 본원에 제공되는 폴리머 나노입자는 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG) 테트라블록 코폴리머를 포함한다. 다양한 구현예에서, 나노입자는 NANOPRO™를 포함하는데, 이는 생분해성, 긴 혈액 순환, 스텔스(stealth), 테트라-블록 폴리머 나노입자 플랫폼(NanoProteagen Inc.; Massachusetts)이다. PLA-PEG-PPG-PEG 테트라블록 코폴리머는 PEG-PPG-PEG 트리블록 코폴리머와 PLA의 화학적 컨쥬게이션으로부터 형성될 수 있다.
폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG) 테트라블록 코폴리머를 포함하는 나노입자의 합성 및 특징분석은 PCT 공개 WO2013/160773호에 기술되어 있으며, 이러한 문헌은 전문이 본원에 참고로 포함된다. 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG) 테트라블록 코폴리머를 포함하는 폴리머 나노입자는 안전하고, 안정적이고, 비-독성인 것으로 나타났다.
이러한 테트라블록 코폴리머를 형성하기 위해 사용되는 공정은 폴리-락트산(PLA) 매트릭스에 PEG-PPG-PEG를 공유 결합시켜, 블록 코폴리머를 매트릭스, 즉, 나노입자 전달 시스템의 일부가 되게 하는 것을 포함한다. 이는 에멀젼화제에서 배지로의 침출을 방지한다.
특정 구현예에서, 분자량은 수평균 분자량 또는 중량평균 분자량으로서 표현될 수 있다.
수평균 분자량(Mn)은 하기 수학식에 의해 규정된다:
[수학식]
[상기 식에서, Mi는 사슬의 분자량이며, Ni는 그러한 분자량의 사슬의 수임]. 중량평균 분자량(Mw)은 하기 수학식에 의해 규정된다:
[수학식]
Mn과 비교하면, Mw는 분자량 평균에 대한 기여도를 결정하는 데 사슬의 분자량을 고려한다. 사슬의 질량이 클수록, 사슬이 Mw에 더 많이 기여한다.
일부 구현예에서, 친수성-소수성 블록 코폴리머(예를 들어, PEG-PPG-PEG)의 수평균 분자량(Mn)은 일반적으로, 1,000 내지 20,000 g/mol의 범위이다. 추가 구현예에서, 친수성-소수성 블록 코폴리머의 평균 분자량(Mn)은 약 4,000 g/mol 내지 15,000 g/mol이다. 일부 경우에, 친수성-소수성 블록 코폴리머의 평균 분자량(Mn)은 4,400 g/mol, 8,400 g/mol, 또는 14,600 g/mol이다. 특정 구현예에서, PEG-PPG-PEG의 Mn은 1,100 내지 15,000 g/mol, 예를 들어, 4,000 내지 13,000 g/mol이다. 특정 구현예에서, PEG-PPG-PEG의 Mn은 10,000 내지 13,000 g/mol이다. 다른 구현예에서, PEG-PPG-PEG의 Mn은 약 12,500 g/mol이다.
일부 구현예에서, 본 발명의 블록 코폴리머는 폴리(락트산)(PLA)의 세그먼트 및 폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PEG-PPG-PEG)의 세그먼트를 본질적으로 포함한다.
일 구현예에서, 특정 생분해성 폴리머 나노입자는 블록 코폴리머 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG)로 형성된다.
본 발명의 다른 특정 생분해성 폴리머 나노입자는 블록 코폴리머 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)-폴리(락트산)(PLA-PEG-PPG-PEG-PLA)으로 형성된다.
본 발명의 생분해성 폴리머는 공유 결합을 이용하여 PLA를 친수성-소수성 블록 코폴리머로 화학적으로 개질시킴으로써 형성될 수 있다.
본 발명의 생분해성 폴리머 나노입자는 다양한 구현예에서, 약 1 내지 1000 nm 범위의 크기, 약 30 내지 300 nm 범위의 크기, 약 100 내지 300 nm 범위의 크기, 또는 약 100 내지 250 nm 범위의 크기, 또는 적어도 약 100 nm의 크기를 갖는다.
본 발명의 생분해성 폴리머 나노입자는 다양한 구현예에서, 약 30 내지 120 nm 범위의 크기, 약 120 내지 200 nm의 크기, 또는 약 200 내지 260 nm의 크기, 또는 적어도 약 260 nm의 크기를 갖는다.
일 구현예에서, 본 발명의 생분해성 폴리머에는 에멀젼화제가 실질적으로 존재하지 않거나, 이는 외부 에멀젼화제를 약 0.5 중량% 내지 5 중량% 양으로 포함할 수 있다.
일 구현예에서, 본 발명의 생분해성 폴리머 나노입자는 PLA-PEG-PPG-PEG이며, 폴리(락트산) 블록의 평균 분자량은 약 60,000 g/mol이며, PEG-PPG-PEG 블록의 평균 중량은 약 8,400 또는 약 14,600 g/mol이며, 외부 에멀젼화제는 약 0.5 중량% 내지 5 중량%이다.
다른 구현예에서, 본 발명의 생분해성 폴리머 나노입자는 PLA-PEG-PPG-PEG이며, 폴리(락트산) 블록의 평균 분자량은 대략 16,000 g/mol 이하이며, PEG-PPG-PEG 블록의 평균 중량은 약 8,400 g/mol 또는 약 14,600 g/mol이며, 여기서, 조성물에는 에멀젼화제가 실질적으로 존재하지 않는다.
일 구현예에서, 생분해성 폴리머 나노입자는 PLA-PEG-PPG-PEG이며, 폴리(락트산) 블록의 평균 분자량은 약 10,000 내지 약 100,000 달톤, 약 20,000 내지 90,000 달톤, 약 30,000 내지 80,000 달톤, 약 50,000 내지 80,000 달톤, 및 약 72,000 달톤이며, PEG-PPG-PEG 블록의 평균 중량은 약 8,000 달톤 내지 18,000 달톤, 약 12,000 달톤 내지 17,000 달톤 및 약 8,400 내지 약 14,600 g/mol이며, 외부 에멀젼화제는 약 0.5 중량% 내지 5 중량%이다.
다른 구현예에서, 생분해성 폴리머 나노입자는 PLA-PEG-PPG-PEG이며, 폴리(락트산) 블록의 평균 분자량은 대략 100,000 달톤 이하이며, PEG-PPG-PEG 블록의 평균 중량은 약 12,000 달톤 또는 약 17,000 달톤이며, 여기서, 조성물에는 에멀젼화제가 실질적으로 존재하지 않는다.
다른 구현예에서, 본원에 제공되는 폴리머 나노입자는 양이온성 펩타이드를 추가로 포함한다.
다른 양태에서, 본원에는 PLA-PEG-PPG-PEG 테트라블록 코폴리머 또는 PLA-PEG 디-블록 코폴리머를 본질적으로 포함하는 폴리머로 형성된 폴리머 나노입자가 제공되며, 여기서, 폴리머 나노입자에는 살리노마이신, 및 선택적으로, 제2 치료제가 로딩된다.
나노입자(또한, 본원에서 "NP"로도 지칭됨)는 나노캡슐 또는 나노구체로서 형성될 수 있다. 나노입자에 살리노마이신 로딩은 흡착 공정 또는 캡슐화 공정에 의해 수행될 수 있다[Spada et al., 2011; Protein delivery of polymeric nanoparticles; World Academy of Science, Engineering and Technology: 76, 이러한 문헌은 전문이 본원에 참고로 포함됨]. 나노입자는, 수동 및 능동 타겟팅 전략 둘 모두를 이용함으로써, 정상 세포에서 독성을 피하면서 암 세포에서 약물의 세포내 농도를 향상시킬 수 있다. 나노입자가 특정 수용체에 결합하고 세포로 들어갈 때, 이러한 것은 대개 수용체-매개 엔도시토시스를 통해 엔도솜에 의해 둘러싸여져서, 주요 약물 내성 메커니즘 중 하나인 P-당단백질의 인식을 우회한다[Cho et al., 2008, Therapeutic Nanoparticles for Drug Delivery in Cancer, Clin. Cancer Res.,2008, 14:1310-1316, 이러한 문헌은 전문이 본원에 참고로 포함됨]. 나노입자는 옵소닌화 및 식균 작용에 의해 신체로부터 제거된다[Sosnik et al., 2008; Polymeric Nanocarriers: New Endeavors for the Optimization of the Technological Aspects of Drugs; Recent Patents on Biomedical Engineering, 1: 43-59, 이러한 문헌은 전문이 본원에 참고로 포함됨]. 나노담체 기반 시스템이 세포내 침투 개선, 국부 전달, 조기 분해에 대한 약물의 보호, 약동학 및 약물 조직 분포 프로파일의 조절, 낮은 용량 요건 및 비용 효율성의 장점을 갖는 효과적인 약물 전달을 위해 사용될 수 있다[Farokhzad OC, et al.; Targeted nanoparticle-aptamer bioconjugates for cancer chemotherapy in vivo. Proc. Natl. Acad. Sci. USA 2006,103 (16): 6315-20; Fonseca C, et al., Paclitaxel-loaded PLGA nanoparticles: preparation, physicochemical characterization and in vitro anti-tumoral activity. J. Controlled Release 2002; 83 (2): 273-86; Hood et al., Nanomedicine, 2011, 6(7):1257-1272, 이러한 문헌은 전문이 본원에 참고로 포함됨].
나노입자의 흡수는 이의 작은 치수에 간접적으로 비례한다. 이의 작은 크기로 인해, 폴리머 나노입자는 망상-내피계(RES)에 의한 인식 및 흡수를 회피하며, 따라서 오랜 기간 동안 혈류 내에서 순환할 수 있는 것으로 밝혀졌다[Borchard et al., 1996, Pharm. Res. 7: 1055-1058, 이러한 문헌은 전문이 본원에 참고로 포함됨]. 나노입자는 또한, 고형 종양의 누출 맥관구조와 같은 병리학적 부위에서 유출하여, 수동적 타겟팅 메커니즘을 제공할 수 있다. 더 빠른 가용화 속도를 초래하는 더 높은 표면적으로 인해, 나노-크기의 구조는 일반적으로, 더 높은 혈장 농도 및 곡선 아래 면적(AUC) 값을 나타낸다. 입자 크기가 작으면, 숙주 방어 메커니즘을 회피하고 혈액 순환 시간을 증가시키는 데 도움이 된다. 나노입자 크기는 약물 방출에 영향을 미친다. 입자가 크면, 계 내로의 약물의 확산이 느려진다. 입자가 작을수록 더 큰 표면적을 제공하지만, 빠른 약물 방출을 야기시킨다. 작은 입자는 나노입자 분산물의 저장 및 수송 동안 응집되는 경향이 있다. 이에 따라, 나노입자의 작은 크기와 최대 안정성 간의 절충안이 요구된다. 약물 전달 시스템에서 사용되는 나노입자의 크기는 혈액 모세혈관으로의 빠른 누출을 막기에 충분히 크지만, 간 및 비장과 같은 망상내피계에 제공된 고정된 대식 세포에 의한 포획을 피할 수 있기에 충분히 작아야 한다.
이의 크기 이외에, 나노입자의 표면 특징은 또한, 순환 동안 수명 및 운명을 결정하는 데 중요한 인자이다. 나노입자는 이상적으로, 대식 세포 포획을 피하기 위한 친수성 표면을 가져야 한다. 친수성 도메인 및 소수성 도메인을 갖는 블록 코폴리머로부터 형성된 나노입자는 이러한 기준을 충족시킨다. 제어된 폴리머 분해는 또한, 병든 상태로의 작용제 전달 수준을 증가시킬 수 있다. 폴리머 분해는 또한, 입자 크기에 영향을 받을 수 있다. 분해율은 시험관내에서 입자 크기가 증가함에 따라 증가한다[Biopolymeric nanoparticles; Sundar et al., 2010, Science and Technology of Advanced Materials; doi:10.1088/1468-6996/11/1/014104, 이러한 문헌은 전문이 본원에 참고로 포함됨].
폴리(락트산)(PLA)은 조직 공학, 의료용 소재 및 약물 담체에 적용하기 위해 미국 FDA로부터 승인받았으며, 폴리(락트산)-폴리(에틸렌 글리콜) PLA-PEG 기반 약물 전달 시스템은 당해 분야에 알려져 있다. US2006/0165987A1호(전문이 본원에 참고로 포함됨)에는 폴리(에스테르)-폴리(에틸렌) 다중블록 코폴리머, 및 나노구체에 강성을 부여하고 약제학적 화합물을 도입하기 위한 선택적 성분들을 포함하는 스텔스 폴리머 생분해성 나노구체가 기술되어 있다. US2008/0081075A1호(전문이 본원에 참고로 포함됨)에는 그라프트 거대 분자 및 하나 이상의 블록 코폴리머로부터 자가-조립된, 기능성 내부 코어 및 친수성 외부 쉘을 갖는 신규한 혼합된 마이셀 구조가 개시되어 있다. US2010/0004398A1호(전문이 본원에 참고로 포함됨)에는 중간상 영역을 갖는 쉘/코어 구성의 폴리머 나노입자, 및 이를 제조하는 공정이 기술되어 있다.
다양한 구현예에서, 본 발명은 안정한 나노복합체를 형성하고/거나 세포 침투 펩타이드로서 역할을 하기 위해 치료 분자와 상호작용하는 양이온성 분자를 추가로 포함한다. 다양한 구현예에서, 양이온성 분자 세포는 침투 펩타이드 또는 단백질 형질 전환 도메인을 포함한다. 다양한 구현예에서, 양이온성 분자는 핵으로의 치료제의 형질 도입을 용이하게 하는 양이온성 펩타이드이다.
본원에는 살리노마이신 및 추가 치료제를 포함하는 폴리머 나노입자를 제조하는 방법이 제공된다. 얻어진 폴리머 나노입자는 비-독성이고, 안전하고, 생분해성일 뿐만 아니라 높은 저장 안정성과 함께 생체내에서 안정적이고, 의약 분야의 나노담체 시스템 또는 약물 전달 시스템에서 안전하게 사용될 수 있다. 구현예에서, 본원에서 사용되는 폴리머 나노입자는 생체내에서 전달 가능한 약물 또는 치료제의 반감기를 증가시킬 수 있다.
제조 공정은 살리노마이신을 제공하고, 용매 중에 블록 폴리머를 용해시켜 블록 코폴리머 용액을 형성하고, 블록 코폴리머 용액에 복합물을 첨가하여 복합물 및 블록 코폴리머를 포함하는 용약을 형성하는 것을 포함할 수 있다.
일 구현예에서, 블록 코폴리머는 PLA-PEG 디-블록 코폴리머이다.
일 구현예에서, 블록 코폴리머는 PLA-PEG-PPG-PEG 테트라블록 코폴리머이다.
일 구현예에서, 블록 코폴리머 용액은 약 2 mg/ml 내지 10 mg/ml의 농도로 제조된다. 추가 구현예에서, 블록 코폴리머 용액은 약 6 mg/ml의 농도로 제조된다.
일 구현예에서, 공정은 살리노마이신을 포함하는 용액을 계면활성제를 포함하는 용액에 첨가하는 것을 추가로 포함한다. 추가 구현예에서, 살리노마이신과 블록 폴리머 용액을 합하여 얻어진 용액은 안정한 나노입자가 형성될 때까지 교반된다.
다양한 구현예에서, 폴리머 나노입자는 팽창 또는 수축 시에 비-구형 구성을 채택할 수 있다.
나노입자는 다양한 구현예에서, 성질상 양친매성이다.
나노입자의 제타 전위 PDI(다분산도 지수)가 계산될 수 있다[미국특허 제9,149,426호 참조, 이러한 문헌은 전문이 본원에 참고로 포함됨].
폴리머 나노입자는 투과 전자 현미경을 이용하여 측정될 수 있는 치수를 갖는다. 적합한 구현예에서, 본원에 제공되는 폴리머 나노입자의 직경은 약 100 내지 350 nm의 직경, 또는 약 100 내지 30 nm의 직경, 또는 약 100 내지 250 nm의 직경일 것이다. 추가 구현예에서, 본원에서 제공되는 폴리머 나노입자의 직경은 약 100 nm, 110 nm, 120, nm, 130 nm, 140 nm, 150 nm, 160 nm, 170 nm, 180 nm, 190 nm, 200 nm, 210 nm, 220 nm, 230 nm, 240 nm, 또는 250 nm이다.
일 구현예에서, 복합물을 포함하는 폴리머 나노입자는 약 +5 내지 -90 mV, 예를 들어, +4 내지 -75 mV, +3 내지 -30 mV, +2 내지 -25mV, +1 내지 -40 mV의 제타-전위를 갖는다. 추가 구현예에서, 복합물은 약 -30 mV의 제타-전위를 갖는다.
폴리머 나노입자 형성을 위한 특정 공정 및 약제 조성물에서의 용도는 참조 목적으로 본원에 제공된다. 이러한 공정 및 용도는 당업자에게 명백한 다양한 방법을 통해 수행될 수 있다.
약제
조성물
또한, 본원에는 의약에서 및 나노입자의 담체 시스템 또는 저장소 또는 데폿(depot)을 사용하는 다른 분야에서 사용하기 위한 살리노마이신 폴리머 나노입자를 포함하는 약제 조성물이 제공된다. 나노입자는 예후, 치료, 진단 및/또는 치료진단 조성물에서 사용될 수 있다. 적합하게, 본 발명의 나노입자는 약물 및 작용제 전달(예를 들어, 종양 세포 내로)뿐만 아니라 인간 및 동물에서 질병 진단 및 의료학적 영상화를 위해 사용된다. 이에 따라, 본 발명은 본원에 기술된 바와 같은 치료제를 추가로 포함하는 나노입자를 사용하여 질병을 치료하는 방법을 제공한다. 본 발명의 나노입자는 또한, 저장소 또는 데폿이 필요한 경우 화학적 또는 생물학적 반응과 같은 다른 적용에서, 바이오센서로서, 고정된 효소를 위한 작용제로서, 등으로 사용될 수 있다.
이에 따라, 일 양태에서, 본원에는,
a) 폴리(락트산)(PLA) 및 폴리(에틸렌 글리콜)(PEG)을 포함하는 블록 코폴리머를 포함하는 폴리머 나노입자; 및
b) 살리노마이신을 포함하는 약제 조성물이 제공된다.
일 구현예에서, 폴리머 나노입자는 폴리(락트산)-폴리(에틸렌 글리콜)(PLA-PEG) 디-블록 코폴리머를 포함한다.
일 구현예에서, 폴리머 나노입자는 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG) 테트라블록 코폴리머를 포함한다.
추가 구현예에서, PLA-PEG-PPG-PEG 테트라블록 코폴리머는 PEG-PPG-PEG 트리블록 코폴리머와 PLA의 화학적 컨쥬게이션으로부터 형성된다.
일 구현예에서, PLA의 분자량은 약 10,000 내지 약 100,000 달톤이다.
본원에 제공되는 조성물의 일 구현예에서, 폴리머 나노입자는 폴리(락트산)-폴리(에틸렌 글리콜)(PLA-PEG) 디-블록 코폴리머를 본질적으로 포함하는 폴리머로 형성된다.
본원에 제공되는 조성물의 일 구현예에서, 폴리머 나노입자는 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG) 테트라블록 코폴리머를 본질적으로 포함하는 폴리머로 형성된다.
본원에 제공되는 조성물의 일 구현예에서, 폴리머 나노입자는 폴리머 나노입자 외측에 부착된 타겟팅 모이어티를 추가로 포함하며, 여기서, 타겟팅 모이어티는 항체, 펩타이드, 또는 아프타머이다.
적합한 약제 조성물 또는 제형은 예를 들어, 약 0.1% 내지 약 99.9%, 바람직하게는, 약 1% 내지 약 60%의 활성 성분(들)을 함유할 수 있다. 장내 또는 비경구 투여를 위한 약제학적 제형은 예를 들어, 단위 제형, 예를 들어, 당-코팅된 정제, 정제, 캡슐 또는 좌제, 또는 앰플의 약제학적 제형이다. 달리 명시하지 않는 경우에, 이러한 것은 예를 들어, 통상적인 혼합, 과립화, 당-코팅, 용해 또는 동결건조 공정에 의해 그 자체로 공지된 방식으로 제조된다. 필요한 유효량이 복수의 투약 단위의 투여에 의해 도달될 수 있기 때문에, 개별 용량의 각 제형에 함유된 조합 파트너의 단위 함량이 그 자체로 유효량을 구성할 필요가 없다는 것이 인식될 것이다.
약제 조성물은 활성 성분으로서, 하나 이상의 약제학적으로 허용되는 담체(부형제)와 함께 나노입자 중 하나 이상을 함유할 수 있다. 본 발명의 조성물을 제조할 때, 활성 성분은 통상적으로, 부형제와 혼합되거나, 부형제에 의해 희석되거나, 예를 들어, 캡슐, 사세(sachet), 페이퍼, 또는 다른 용기 형태의 이러한 담체 내에 동봉된다. 부형제가 희석제로서 역할을 할 때, 이는 고체, 반-고체, 또는 액체 물질일 수 있으며, 이는 활성 성분을 위한 비히클, 담체 또는 매질로서 작용한다. 이에 따라, 조성물은 예를 들어, 최대 10 중량%의 활성 화합물을 함유한 정제, 환제, 분말, 로젠지, 사세, 카시에(cachet), 엘릭시르(elixir), 현탁액, 에멀젼, 용액, 시럽, 에어로졸(고체로서 또는 액체 매질 중), 연고, 연질 및 경질 젤라틴 캡슐, 좌제, 멸균 주사액, 및 멸균 패키징된 분말 형태일 수 있다.
적합한 부형제의 일부 예는 락토오스(예를 들어, 락토오스 일수화물), 덱스트로오스, 수크로오스, 소르비톨, 만니톨, 전분(예를 들어, 나트륨 전분 글리콜레이트), 검 아카시아, 칼슘 포스페이트, 알기네이트, 트래거캔스, 젤라틴, 칼슘 실리케이트, 콜로이드성 이산화규소, 미정질 셀룰로오스, 폴리비닐피롤리돈(예를 들어, 포비돈), 셀룰로오스, 물, 시럽, 메틸 셀룰로오스, 및 하이드록시프로필 셀룰로오스를 포함한다. 제형은 추가적으로, 윤활제, 예를 들어, 탈크, 마그네슘 스테아레이트, 및 미네랄 오일; 습윤제; 에멀젼화 및 현탁제; 보존제, 예를 들어, 메틸- 및 프로필하이드록시-벤조에이트; 감미제; 및 착향제를 포함할 수 있다.
본 발명의 화합물 및 조성물이 경구로 또는 주사에 의해 투여하기 위해 도입될 수 있는 액체 형태는 면실유, 참기름, 코코넛 오일, 또는 땅콩유와 같은 식용 오일뿐만 아니라 엘릭시르 및 유사한 약제학적 비히클을 갖는 수용액, 적합하게, 향미 시럽(flavored syrup), 수성 또는 오일 현탁액, 및 향미 에멀젼을 포함한다.
치료 방법
본원에 개시된 나노입자는 살리노마이신으로의 치료로 혜택을 입을 것으로 알려지거나 이러한 혜택을 가질 것으로 예상되는 임의의 질환 또는 장애를 치료하거나 예방하기 위해 사용될 수 있다.
일 양태에서, 살리노마이신-함유 나노입자는 암 또는 전암 상태를 치료하거나 예방하기 위해 사용된다. 일부 구현예에서, 암은 유방암, 난소암, 췌장암, 백혈병, 림프종, 골육종, 위암, 전립선암, 결장암, 폐암, 간암, 신장암, 두경부암, 및 자궁경부암으로 이루어진 군으로부터 선택된다.
일 구현예에서, 암은 유방암이다. 다른 구현예에서, 유방암은 삼중 음성 유방암이다. 다른 구현예에서, 유방암 호르몬-의존성 유방암이다.
일 구현예에서, 암은 폐암이다. 다른 구현예에서, 폐암은 비소세포 폐암이다. 다른 구현예에서, 폐암은 소세포 폐암이다.
일 구현예에서, 암은 화학치료제에 내성이 있거나 불응성이다. 다른 구현예에서, 암은 다중-약물 내성이다.
일 양태에서, 본원에는 질병의 치료를 필요로 하는 대상체에서 질병을 치료하는 방법으로서, 대상체에, 치료학적 유효량의, a) PLA-PEG 디-블록 코폴리머를 포함하는 폴리머로 형성된 폴리머 나노입자; 및 살리노마이신을 포함하는 약제 조성물을 투여하는 것을 포함하는 방법이 제공된다.
본원에 제공되는 방법의 일 구현예에서, 약제 조성물은 레날리도마이드, 크리조티닙, 글리벡, 헤르셉틴, 아브스틴, PD-1 관문 억제제, PDL-1 관문 억제제, CTLA-4 관문 억제제, 독소루비신, 다우노루비신, 데시타빈, 이리노테칸, SN-38, 시타라빈, 도세탁셀, 트립톨라이드, 겔다나마이신, 17-AAG, 5-FU, 옥살리플라틴, 카르보플라틴, 탁소테레, 메토트렉세이트, 파클리탁셀, 및 인데노이소퀴놀린으로 이루어진 군으로부터 선택된 화학치료제 또는 타겟팅된 항암제를 추가로 포함한다.
본원에 제공되는 방법의 일 구현예에서, 질병은 암, 자가면역 질환, 염증 질병, 대사 장애, 발달 장애, 심혈관 질병, 간 질병, 장 질병, 감염 질병, 내분비 질병, 및 신경 장애이다.
본원에 제공되는 방법의 일 구현예에서, 나노입자는 PLA-PEG 디-블록 코폴리머를 본질적으로 포함하는 폴리머로 형성된다.
본원에 제공되는 방법의 일 구현예에서, 나노입자는 PLA-PEG-PPG-PEG 테트라블록 코폴리머를 본질적으로 포함하는 폴리머로 형성된다.
일 구현예에서, 폴리머 나노입자는 PLA-PEG 디-블록 코폴리머를 본질적으로 포함하는 폴리머로 형성된다.
일 구현예에서, 폴리머 나노입자는 PLA-PEG-PPG-PEG 테트라블록 코폴리머를 본질적으로 포함하는 폴리머로 형성된다.
본원에 제공되는 약제 조성물의 투여는 질병 또는 장애를 개선시키거나 이의 진행을 지연시키거나, 이의 증상을 억제하는 것과 관련하여 유익한 효과를 야기시킬 뿐만 아니라, 향후 놀라운 유익한 효과, 예를 들어, 본원에 기술된 폴리머 나노입자 시스템을 사용하지 않거나 임의의 다른 통상적인 수단에 의해 작용제를 전달하는 것과 비교하여, 예를 들어, 더 적은 부작용, 더욱 지속 가능한 반응, 개선된 삶의 질 또는 감소된 사망률을 초래할 수 있다.
투여량 및 투여
일 양태에서, 본 개시는 암 치료를 필요로 하는 대상체에서 암을 치료하는 방법으로서, 대상체에, 치료학적 유효량의, 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG) 테트라블록 코폴리머를 포함하는 폴리머 나노입자, 및 살리노마이신을 포함하는 조성물을 투여하는 것을 포함하며, 치료학적 유효량은 약 0.025 mg/kg 내지 약 5 mg/kg인 방법에 관한 것이다.
다른 양태에서, 본원에는 대상체에서 암 줄기 세포의 증식, 생존, 이동, 또는 콜로니 형성 능력을 감소시키는 방법으로서, 대상체에, 치료학적 유효량의, 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG) 테트라블록 코폴리머를 포함하는 폴리머 나노입자, 및 살리노마이신을 포함하는 조성물을 투여하는 것을 포함하며, 치료학적 유효량은 약 0.025 mg/kg 내지 약 5 mg/kg인 방법이 제공된다.
방법의 구현예에서, 치료학적 유효량은 약 0.1 mg/kg 내지 약 2.5 mg/kg이다. 방법의 구현예에서, 치료학적 유효량은 약 0.5 mg/kg 내지 약 5 mg/kg이다. 방법의 구현예에서, 치료학적 유효량은 약 1 mg/kg 내지 약 5 mg/kg이다. 방법의 구현예에서, 치료학적 유효량은 약 2.5 mg/kg 내지 약 5 mg/kg이다. 방법의 구현예에서, 치료학적 유효량은 약 0.025 mg/kg 내지 약 0.5 mg/kg이다. 방법의 구현예에서, 치료학적 유효량은 약 0.025 mg/kg 내지 약 0.1 mg/kg이다.
방법의 다른 구현예에서, 치료학적 유효량은 약 0.025 mg/kg 내지 약 1 mg/kg이다. 방법의 구현예에서, 치료학적 유효량은 약 1 mg/kg 내지 약 2 mg/kg이다. 방법의 구현예에서, 치료학적 유효량은 약 2 mg/kg 내지 약 3 mg/kg이다. 방법의 구현예에서, 치료학적 유효량은 약 3 mg/kg 내지 약 4 mg/kg이다. 방법의 구현예에서, 치료학적 유효량은 약 4 mg/kg 내지 약 5 mg/kg이다.
방법의 구현예에서, 치료학적 유효량은 약 0.03 mg/kg 내지 약 0.5 mg/kg이다. 방법의 일 구현예에서, 치료학적 유효량은 약 0.35 mg/kg이다. 방법의 일 구현예에서, 치료학적 유효량은 약 0.4 mg/kg이다. 방법의 다른 구현예에서, 치료학적 유효량은 약 0.05 mg/kg 내지 약 0.8 mg/kg이다. 방법의 일 구현예에서, 치료학적 유효량은 약 0.61 mg/kg이다. 방법의 일 구현예에서, 치료학적 유효량은 약 0.69 mg/kg이다.
방법의 구현예에서, 치료학적 유효량은 약 0.08 mg/kg 내지 약 1.1 mg/kg이다. 방법의 일 구현예에서, 치료학적 유효량은 약 0.89 mg/kg이다. 방법의 일 구현예에서, 치료학적 유효량은 약 1.0 mg/kg이다.
방법의 구현예에서, 조성물은 정맥내로, 종양내로, 또는 피하로 투여된다.
방법의 일부 구현예에서, 조성물은 적어도 하루에 1회, 격일에 1회, 1주일에 1회, 1주일에 2회, 1개월에 1회, 또는 1개월에 2회 투여된다. 방법의 일 구현예에서, 조성물은 적어도 하루에 1회 투여된다. 방법의 일 구현예에서, 조성물은 적어도 격일에 1회 투여된다. 방법의 일 구현예에서, 조성물은 적어도 1주일에 1회 투여된다. 방법의 일 구현예에서, 조성물은 적어도 1주일에 2회 투여된다. 방법의 일 구현예에서, 조성물은 적어도 1개월에 1회 투여된다. 방법의 일 구현예에서, 조성물은 적어도 1개월에 2회 투여된다. 다른 구현예에서, 조성물은 하루에 1회 넘게 투여된다.
방법의 일부 구현예에서, 조성물은 3주의 기간 동안 투여된다. 방법의 다른 구현예에서, 조성물은 30일의 기간 동안 투여된다. 방법의 다른 구현예에서, 조성물은 60일의 기간 동안 투여된다. 방법의 다른 구현예에서, 조성물은 90일의 기간 동안 투여된다. 방법의 다른 구현예에서, 조성물은 120일의 기간 동안 투여된다. 방법의 다른 구현예에서, 조성물은 150일의 기간 동안 투여된다. 방법의 다른 구현예에서, 조성물은 6개월의 기간 동안 투여된다. 방법의 다른 구현예에서, 조성물은 약 6개월 내지 약 1년의 기간 동안 투여된다. 방법의 다른 구현예에서, 조성물은 약 1년 내지 약 2년의 기간 동안 투여된다.
본원에 개시된 방법 및 투여량은 생체내에서 살리노마이신의 독성을 감소시키는 것으로 확인되었다. 또한, 본원에 기술된 조성물은 살라노마이신 나노입자가 살리노마이신 단독보다 더 높은 용량으로 대상체에 투여될 수 있게 한다.
특정 구현예에서, 치료학적 유효량은 동물 실험으로부터 결정된 인간 등가 용량이다.
약제 조성물의 일 구현예에서, 폴리머 나노입자는 폴리머 나노입자의 외측에 부착된 타겟팅 모이어티를 추가로 포함한다.
다른 양태에서, 본원에는 약 12.5 mg 내지 약 500 mg의, 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG) 테트라블록 코폴리머를 포함하는 폴리머 나노입자, 및 살리노마이신을 포함하는 약제 조성물, 및 약제학적으로 허용되는 담체를 포함하는 제형이 제공된다.
본원에 제공된 폴리머 나노입자의 유효 투여량은 사용되는 특정 단백질, 핵산, 및/또는 다른 치료제, 투여 모드, 치료되는 질환, 및 치료되는 질환의 중증도에 따라 달라질 수 있다. 이에 따라, 폴리머 나노입자의 투약 요법은 투여 경로 및 환자의 신장 및 간 기능을 포함하는 다양한 인자에 따라 선택된다.
효능을 결정하기 위해, 치료는 하나 이상의 치료전 또는 치료후 표현형을 표준 표현형과 비교하는 것을 추가로 포함할 수 있다. 표준 표현형은 참조 세포 또는 세포의 집단에서 상응하는 표현형이다. 참조 세포는 단백질 분해 장애가 의심되지 않는 사람 또는 대상체로부터의 세포, 대상체로부터의 세포, 배양된 세포, 대상체로부터의 배양된 세포, 또는 치료전 대상체로부터의 세포 중 하나 이상이다. 대상체로부터의 세포는 예를 들어, 골수 기질 세포(BMSC), 말초 혈액 단핵 세포(PBMC), 림프구, 모낭, 혈액 세포, 다른 상피 세포, 골수 혈장 세포, 원발성 암 세포, 환자 유래 종양 세포, 정상 또는 암성 조혈 줄기 세포, 신경 줄기 세포, 고형 종양 세포, 성상 세포, 및 암 줄기 세포, 등을 포함할 수 있다.
병용 치료
본원에 제공되는 조성물은 추가 치료 양식, 예를 들어, 살리노마이신과 함께 대상체에 투여되는 치료제(예를 들어, 화학치료제), 방사선 작용제, 호르몬제, 생물학적 작용제, 또는 함염증제를 선택적으로 추가로 포함한다.
살리노마이신과 병용 요법으로 사용될 수 있는 치료제는 예를 들어, 레날리도마이드, 크리조티닙 또는 히스톤 데아세틸라아제 억제제(HDAC), 예를 들어, 미국특허 제8,883,842호에 개시된 것을 포함할 수 있으며, 이러한 문헌은 전문이 본원에 참고로 포함된다. 추가 치료제는 예를 들어, 글리벡, 헤르셉틴, 아브스틴, PD-1 관문 억제제, PDL-1 관문 억제제, CTLA-4 관문 억제제, 타목시펜, 트라스투자맙, 랄록시펜, 독소루비신, 플루오로우라실/5-fu, 파리드로네이트, 디나트륨, 아나스트로졸, 엑세메스탄, 사이클로포스파미드, 에피루비신, 레트로졸, 토레미펜, 풀베스트란트, 플루옥시메스테론, 트라스투주맙, 메토트렉세이트, 메가스트롤 아세테이트, 도세탁셀, 파클리탁셀, 테스토락톤, 아지리딘, 빈블라스틴, 카페시타빈, 고셀레린 아세테이트, 졸레드론산, 탁솔, 빈블라스틴, 및/또는 빈크리스틴을 포함한다. 유용한 비-스테로이드성 항염증제는 아스피린, 이부프로펜, 디클로페낙, 나프록센, 베녹사프로펜, 플루르비프로펜, 페노프로펜, 플루부펜, 케토프로펜, 인도프로펜, 피로프로펜, 카르프로펜, 옥사프로진, 프라모프로펜, 무로프로펜, 트리옥사프로펜, 수프로펜, 아미노프로펜, 티아프로펜산, 플루프로펜, 부클록스산, 인도메타신, 술린닥, 톨메틴, 조메피락, 티오피낙, 지도메타신, 아세메타신, 펜티아작, 클리다낙, 옥스피낙, 메페남산, 메클로페남산, 플루페남산, 니플룸산, 톨페남산, 디플루리살, 플루페니살, 피록시캄, 수독시캄, 이속시캄; 아스피린, 나트륨 살리실레이트, 콜린 마그네슘 트리살리실레이트, 살살레이트, 디플루니살, 살리실살리실산, 술파살라진, 및 올살라진을 포함하는 살리실산 유도체; 아세트아미노펜 및 페나세틴을 포함하는 파라-아미노페놀 유도체; 인도메타신, 술리낙, 및 에토돌락을 포함하는 인돌 및 인덴 아세트산; 톨레틴, 디클로페낙, 및 케토롤락을 포함하는 헤테로아릴 아세트산; 메페남산, 및 메클로페남산을 포함하는 안트라닐산(페나메이트); 옥시캄(피록시캄, 테녹시캄), 및 피라졸리딘디온(페닐부타존, 옥시펜타르타존)을 포함하는 에놀산; 및 나부메톤을 포함하는 알카논, 및 이의 약제학적으로 허용되는 염 및 이들의 혼합물을 포함하지만, 이로 제한되지 않는다. NSAID의 더욱 상세한 설명을 위해 문헌[Paul A. Insel, Analgesic-Antipyretic and Antiinflammatory Agents and Drugs Employed in the Treatment of Gout, in Goodman & Gilman's The Pharmacological Basis of Therapeutics 617-57 Perry B. Molinhoff and Raymond W. Ruddon eds., 9th ed 1996, Glen R. Hanson, Analgesic, Antipyretic and Anti-Inflammatory Drugs in Remington: The Science and Practice of Pharmacy Vol II 1196-1221 and A. R. Gennaro ed. 19th ed. 1995]을 참조하며, 이러한 문헌은 전문이 본원에 참고로 포함된다.
일 구현예에서, 추가 화학치료제 또는 타겟팅된 항암제는 독소루비신, 다우노루비신, 데시타빈, 이리노테칸, SN-38, 시타라빈, 도세탁셀, 트립톨라이드, 겔다나마이신, 17-AAG, 5-FU, 옥살리플라틴, 카르보플라틴, 탁소테레, 메토트렉세이트, 파클리탁셀, 및 인데노이소퀴놀린으로 이루어진 군으로부터 선택된다.
이의 특정 구현예를 참조하여 대상이 상당히 상세히 설명되었지만, 다른 구현예가 가능하다. 이와 같이, 첨부된 청구범위의 사상 및 범위는 그 안에 포함된 특정 구현예의 설명으로 제한되지 않아야 한다.
실시예
본 개시는 하기에서 실시예로 예시될 것이며, 이는 본 개시의 실행을 예시하기 위해 의도되고, 본 개시의 범위를 제한적으로 임의의 한정하는 것으로 의도되지 않는다. 달리 규정하지 않는 한, 본원에 사용되는 모든 기술 용어 및 과학 용어는 본 개시가 속하는 당업자에게 통상적으로 이해되는 것과 동일한 의미를 갖는다. 본원에 기술된 것과 유사하거나 동등한 방법 및 물질이 개시된 방법 및 조성물의 실행에서 사용될 수 있지만, 예시적인 방법, 장치, 및 물질이 본원에 기술된다.
실시예
1.
PLA
-PEG-
PPG
-PEG 블록
코폴리머의
폴리머
나노입자의 제조
폴리(락트산)(MW. 약 45,000 내지 60,000 g/mol), PEG-PPG-PEG 및 조직 배양 시약을 Sigma-Aldrich(St. Louis, MO)로부터 획득하였다. 달리 기술하지 않는 한, 모든 시약은 분석 등급 이상이었고, 받은 상태로 사용하였다. 세포주를 NCCS Pune(India) 또는 ATCC(Maryland, USA)로부터 획득하였다.
250 ml 둥근 바닥 플라스크에서 5 gm의, 60,000 g/mol의 평균 분자량을 갖는 폴리(락트산)(PLA)을 100 ml CH2Cl2(디클로로메탄) 중에 용해하였다. 이러한 용액에, 0.7 g의 PEG-PPG-PEG 폴리머(1100 내지 8400 Mn의 분자량 범위)를 첨가하였다. 용액을 0℃에서 10 내지 12시간 동안 교반하였다. 이러한 반응 혼합물에, 5 ml의 1% N,N-디사이클로헥실카보디이미드(DCC) 용액을 첨가하고, 이후에 -4℃ 내지 0℃/영하온도에서 5 ml의 0.1% 4-디메틸아미노피리딘(DMAP)을 서서히 첨가하였다. 반응 혼합물을 다음 24시간 동안 교반하고, 이후에 PLA-PEG-PPG-PEG 블록 코폴리머를 디에틸 에테르로 침전시키고, Whatman 필터지 No. 1을 이용하여 여과하였다. 이에 따라 수득된 PLA-PEG-PPG-PEG 블록 코폴리머 침전물을 저 진공 하에서 건조시키고, 추가로 사용할 때까지 2℃ 내지 8℃에서 저장하였다.
PLA-PEG-PPG-PEG 나노입자를 에멀젼 침전 방법에 의해 제조하였다. 100 mg의, 상기에 언급된 공정에 의해 수득된 PLA-PEG-PPG-PEG 코폴리머를 유기 용매, 예를 들어, 아세토니트릴, 디메틸 포름아미드(DMF) 또는 디클로로메탄 중에 별도로 용해시켜 폴리머 용액을 수득하였다.
이러한 폴리머 용액을 20 ml 증류수의 수성상에 적가함으로서 나노입자를 제조하였다. 용액을 실온에서 10 내지 12시간 동안 자석으로 교반하여 잔류 용매를 증발시키고 나노입자를 안정화시켰다. 이후에, 나노입자를 10분 동안 25,000 rpm에서의 원심분리에 의해 수집하고, 증류수를 사용하여 3회 세척하였다. 나노입자를 추가로 동결건조시키고, 추가로 사용할 때까지 2℃ 내지 8℃에서 저장하였다.
상기에 언급된 공정에 의해 수득된 나노입자의 형상은 본질적으로 구형이다. 입자 크기 범위는 약 30 내지 120 nm이었다. 나노입자의 유체역학적 반경을 동적 광산란(DLS) 기기를 이용하여 측정하였고, 이는 110 내지 120 nm의 범위이다.
실시예
2. 살리노마이신-캡슐화된 나노입자의 제조
본 발명의 나노입자는 성질상 양친매성으로서, 여기에는 소수성 및 친수성 약물 둘 모두가 로딩될 수 있다.
100 mg의, 실시예 1의 공정을 이용하여 제조된 PLA-PEG-PPG-PEG 나노입자를 5 ml의 유기 용매, 예를 들어, 아세토니트릴(CH3CN), 디메틸 포름아미드(DMF; C3H7NO), 아세톤 또는 디클로로메탄(CH2Cl2) 중에 용해하였다.
1 내지 10 mg의 살리노마이신을 수용액 중에 용해하고, 상기 폴리머 용액에 첨가하였다. 살리노마이신을 통상 폴리머의 약 10 내지 20 중량%의 중량 범위로 사용하였다. 이러한 용액을 10 내지 15초 동안 250 내지 400 rpm으로 잠시 초음파처리하여 미세한 1차 에멀젼을 생성하였다.
미세한 1차 에멀젼을 시린지/마이크로피펫을 이용하여 F-127 폴록소머를 함유한 20 ml 증류수의 수성상에 적가하고, 용매를 증발시키고 나노입자를 안정화시키기 위해 25℃ 내지 30℃에서 10 내지 12시간 동안 250 내지 400 rpm으로 자석으로 교반하였다. 수성상은 당 첨가제를 추가로 포함한다. 얻어진 나노입자 현탁액을 개방된, 덮혀지지 않은 조건에서 밤새 교반하여 잔류 유기 용매를 증발시켰다. 살리노마이신 캡슐화된 폴리머 나노입자를 10분 동안 10,000 g에서 원심분리에 의해 또는 15분 동안 3000 g에서 한외여과에 의해 수집하였다(Amicon Ultra, 100,000 NMWL을 갖는 Ultracel 막, Millipore, USA). 나노입자를 증류수 중에 재현탁시키고, 3회 세척하고, 동결건조하였다. 이러한 것을 추가로 사용할 때까지 2℃ 내지 8℃에서 저장하였다. 폴리머 나노입자는 매우 안정적이다.
실시예
3. CD2 수컷 마우스에서 살리노마이신-나노입자(
SAL
-NP) 예비 독성 연구의 개념 증명 및 동일한 용량의 SAL과 일대일 비교
3가지 상이한 농도에서 살리노마이신(SAL)의 효과를 평가하고 비교하기 위한 연구를 야생형 CD2 수컷 마우스에서 수행하였고, 생분해성 테트라-블록 폴리머 나노입자 중의 SAL의 제형과 비교하였다.
마우스
Taconic으로부터의 6 내지 8주령의 20 내지 25 g 수컷 CD2 마우스를 사용하였다. 연구를 시작하기 전에 5일 동안 동물을 순응시켰다.
용량
동물에 하기 표 1에 따라, 5.0 mg/kg, 8.5 mg/kg, 또는 12.5 mg/kg의 SAL 또는 SAL-NP를 정맥내로 1회 주사하였다. 대조군 동물을 PBS로 처리하였다.
표 1. 실험 설계
방법
모든 동물을 7일 동안 매일 변화(체중, 음식 및 물 섭취)에 대해 관찰하였다. 동물의 내약성을 임상, 체중 및 행동 변화를 통해 측정하였다. 화합물을 1일째에 1회 투여하였다. 투여 후 7일째에, 모든 동물을 마취시키고, 완전 혈액 화학 및 혈액학 분석을 위해 혈액을 수집하였다(하기 표 2 및 표 3 참조). 모든 동물을 검사하기 위해 사후 검사를 수행하였다. 상이한 장기(뇌, 심장, 폐, 간, 비장, 위, 장, 신장 및 피부)를 H & E 염색에 의한 조직-병리학적 평가를 위해 단리하였다.
표 2. 완전 혈액 화학 분석
표 3. 혈액학 분석
결과
각 실험 동물을 물 및 음식 섭취, 배뇨, 배변 및 연구 과정에서 임의의 관찰 가능한 변화를 포함하여, 임의의 임상 및 행동 변화에 대해 개별적으로 및 면밀히 관찰하였다.
12.5 mg/kg SAL을 투여받은 그룹의 체중 변화를 관찰할 수 있었다. 또한, 8.5 mg/kg SAL이 투여된 동물의 그룹에서 또한 체중의 약간의 감소가 관찰되었다. 5 mg/kg SAL 그룹에서는 변화를 관찰할 수 없었다. 흥미롭게도, 모든 용량에서 SAL-NP가 투여된 그룹의 동물의 체중 변화를 관찰할 수 없었다. 7일째에 12.5 mg/kg SAL 그룹을 제외하고, 모든 그룹에서 음식 및 물 섭취는 일정한 수준이었다. 체중 데이터는 하기 표 4를 참조하고, 사후 검사 소견은 표 5를 참조한다.
표 4. 체중 관찰
표 5. 사후 관찰
모든 그룹으로부터의 동물에서 배뇨 및 배변의 변화가 관찰되지 않았다. 6일째에 12.5 mg/kg SAL 그룹의 동물 번호 2 및 3에서 약간의 거친 털이 관찰되었다. 털의 거칠기는 7일째에 이러한 동물 그룹에서 약간 악화되었다.
12.5 mg/kg SAL 그룹의 동물 번호 1에서 6일째 뒷다리 지체(hind leg lagging) 및 움직임 감소의 징후가 명확하였으며, 이는 7일째에 악화되었다. 이러한 뒷다리의 지체는 7일째에 동물 2 및 3(12.5 mg/kg의 SAL 그룹)에서도 관찰되었다. 뒷다리 지체는 SAL 8.5 mg/kg 그룹에서 더 낮은 정도로 보였다. 12.5 mg/kg SAL, 8.5 mg/kg SAL 및 5 mg/kg SAL 그룹의 모든 동물은 움직임이 활발하지 못하였다.
중요하게, SAL-NP를 투여받은 그룹의 동물은 어떠한 뒷다리 지체 증상을 나타내지 않았고, 움직임의 장애가 없었다. 이러한 데이터에서는, 나노입자 및 살리노마이신의 제형이 놀랍게도 살리노마이신 단독보다 더 낮은 독성이 있다는 것을 나타낸다.
연구 7일째에, 각 및 모든 동물에 대해 사후 검사를 수행하였다. 5 mg/kg SAL을 투여받은 그룹은 검사한 임의의 11개의 장기에서 해부 현미경으로 관찰 가능한 어떠한 변화도 나타내지 않았다. 8.5 mg/kg SAL 그룹의 동물 번호 2에서는 고환이 약간 붉고 약간 비대되었다. 이러한 그룹의 모든 동물은 정상 동물에 비해 고환 중량이 감소되었다. 고환 주변 근막의 약간의 비대가 관찰되었다. 외상이 관찰되지 않았으며, 부고환은 어떠한 변화도 없는 것으로 확인되었다. 12.5 mg/kg SAL을 투여받은 그룹의 모든 동물은 고환 및 부고환의 중량 감소, 고환을 둘러싸는 근막의 발적(reddening)을 나타내어, 비대된 것처럼 보였다. 이러한 동물들에서는 외상의 어떠한 징후도 나타내지 않았다. SAL-NP(5 mg/kg, 8.5 mg/kg 및 12.5 mg/kg)를 투여받은 그룹의 모든 동물은 이러한 임의의 변화를 보이지 않았고, 정상으로 보였다.
살리노마이신 12.5 mg/kg 그룹을 제외한 모든 동물은 본 연구에서 잘 수행되었다. H & E 염색에 의해 뇌, 심장, 폐, 간, 비장, 위, 장, 신장, 근육, 및 피부 조직에 대한 조직병리학적 연구를 수행하였다. 7일째에 조직을 수집하였고, 상승하는 농도의 알코올로 통과시키고, 이후에 섹션화를 위해 Buoyins 용액 중에 보존하였다.
모든 조직의 현미경 검사 시에, SAL-NP를 투여받은 연구에서 모든 동물의 뇌, 심장, 폐, 비장, 위, 고환, 부고환, 좌골 신경, 장, 근육 및 피부에서 어떠한 변화도 관찰되지 않았다. 그러나, 12.5 mg/kg의 SAL을 투여받은 그룹의 신장, 간, 고환 및 부고환에서 변화가 관찰되었다.
12.5 mg/kg SAL을 투여받은 동물의 간에서 지방 혼합물 변화, 세포질 글리코겐 및 건 지방증(tension lipidosis)이 존재하였다. 이러한 변화는 12.5 mg/kg SAL 용량에서 세 마리 동물 모두에서 나타났다. 12.5 mg/kg SAL-NP를 투여받은 동물에서 간의 변화는 관찰되지 않았다.
12.5 mg/kg의 SAL을 투여받은 세 마리의 동물 모두의 고환은 정세관이 수축되었고 생식 상피의 액포화가 발생하였다. 12.5 mg/kg SAL을 투여받은 동물의 부고환의 단면에서 액포화 및 괴저성 세포의 발생과 함께 상피의 파괴가 관찰되었다. 이러한 치료는 고환의 정세관 및 간질에서 다양한 구조적 변화(수축)를 유발하였다. 상피 틈새, 상피 탈피 및 생식 세포 퇴화가 또한 관찰되었다. 놀랍게도, 12.5 mg/kg의 SAL-NP로 처리된 동물에서는 이의 부고환이 변하지 않았다.
12.5 mg/kg SAL이 투여된 세 마리 동물 모두에서는 신장의 피복 상피의 위축증과 함께 세뇨관의 이격을 나타내었다. 관내강 내의 망상조직의 캐스트(reticulated cast)가 관찰되었으며, 신소체의 뚜렷한 위축증이 나타났다. 12.5 mg/kg의 SAL-NP로 처리된 동물은 신장의 변화를 나타내지 않았다.
결론
SAL로 처리된 동물이 간, 신장, 고환 및 부고환에 독성을 갖는 것으로 명확히 나타내었지만, SAL-NP 그룹의 최고 농도에서도 어떠한 변화도 관찰되지 않았다. 이러한 연구에서는 동물에서 모두 3가지 농도의 SAL-NP가 잘 용인됨을 나타낸다.
실시예
4.
살리노마이신-나노입자(SAL-NP)의 인간 등가 용량(HED)의 계산
마우스 연구에서 사용된 용량의 살리노마이신-나노입자(SAL-NP)의 인간 등가 용량(HED)을 문헌[Nair and Jacob, "A simple practice guide for dose conversion between animals and human" (2016) 및 J. Basic Clin. Pharma. 27-31; 및 또한 FDA's "Guidance for Industry" (July 2005)]에 개시된 2개 다른 방정식에 의해 계산하였으며, 이러한 문헌은 전문이 본원에 참고로 포함된다. SAL-NP에 대한 HED의 특정 구현예는 하기 표 6에 개시되어 있다.
표
6. 실시예 3에서 사용된 SAL-NP 용량의 HED
본원에 인용된 각 및 모든 특허, 특허 출원, 및 공개문의 개시는 전문이 본원에 참고로 포함된다.
본 발명이 특정 구현예를 참조하여 개시되었지만, 본 발명의 다른 구현예 및 변형예가 본 발명의 실제 사상 및 범위를 벗어나지 않고 당업자에 의해 고안될 수 있다는 것이 명백하다. 첨부된 청구범위는 이러한 모든 구현예 및 동등한 변형예를 포함하는 것으로 해석되도록 의도된다.
실시예
5. 여러 암 세포주의 세포 생존에 대한 살리노마이신-함유 나노입자
의 효과
암 세포 생존에 대한 살리노마이신-함유 나노입자의 효과를 Alamar Blue 검정을 이용하여 평가하였다. 각 세포주의 성장률을 기반으로 하여, 1500 내지 4000개의 세포/웰을 96 웰 플레이트에 플레이팅하고, 37℃, 5% CO2에서 밤새 성장시켰다. 세포를 5일 동안 8가지 농도로 3배 연속 희석으로 상이한 농도의 살리노마이신-함유 나노입자로 처리하였다.
Alamar Blue 시약(배양 배지 중 1:10 희석)을 이후에 웰에 첨가하고, 2 내지 4시간 동안 인큐베이션하였다. 흡수 변화를 570 nM에서의 여기 및 600 nM에서의 방출로 측정하였다. 생존 백분율을 100%로서의 미처리된 대조군과 비교하여 계산하였다.
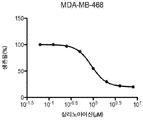
세기관지폐포 암종(비소세포 폐암) 세포주의 결과는 도 8(NCI-H358)에 도시되어 있다. 소세포 폐암 세포주의 결과는 도 9a(NCI-H526), 도 9b(NCI-H526, 2개의 상이한 SAL-NP 제형) 및 도 10(NCI-H69)에 도시되어 있다. 삼중 음성 유방암 세포주의 결과는 도 11(MDA-MB-231), 도 12(SUM149), 및 도 14(MDA-MB-468)에 도시되어 있다. 호르몬-의존성 유방 암종 세포에 대한 결과는 도 13(MCF-7)에 도시되어 있다. 모든 그래프에는 나노입자 농도(x-축)에 대한 생존률(y-축)이 나타나 있다. 각 세포주의 IC50 값을 세포 생존 데이터로부터 계산하였다(하기 표 7 참조).
표 7. 암 세포주에서 SAL-NP의 IC
50
값
실시예 6. 맘모스피어에 대한 살리노마이신-함유 나노입자의 효과
3D 배양물로서 MDA-MB-231 삼중 음성 유방암(TNBC) 세포로부터의 무혈청 종양구 성장 특수 배지 중에서 암 줄기 세포-매개 맘모스피어를 생성하였다. 성공적인 생성 후에, 맘모스피어를 72시간 동안 듀플리케이트 웰(duplicate well)을 이용하여 8가지의 상이한 농도의 살리노마이신 또는 살리노마이신-NP로 처리하였다. 인큐베이션 후에, WST-1 시약을 첨가하고, 플레이트를 추가 60분 동안 인큐베이션하고, 630 nm에서 발광도 또는 흡광도를 판독하였다. SAL 및 SAL-NP로의 3D 맘모스피어에서의 항-증식 검정의 결과는 도 17a 내지 도 17c에 도시되어 있다.
실시예 7. TNBC 환자로부터 단리된 암 줄기 세포에 대한 살리노마이신-함유 나노입자의 효과
구상체 배양물로서 배양된 삼중 음성 유방암(TNBC) 환자 종양 유래 세포에서 CD24-PE & CD44-FITC 항체 염색에 의해 암 줄기 세포(CSC)를 유세포 분석하고, 이후에 72시간 동안 명시된 약물로 처리하였다. 72시간의 맘모스피어의 처리 후에, 세포를 Acutase 처리로 분리하였다. 세척 후에, 세포를 CD24-PE & CD44-FITC 항체로 염색시키고, 세척하고, FACS에 의해 분석하였다. CD44+/CD24-low 세포의 하위집단을 게이팅하고, 정량화하였다. 살리노마이신 및 살리노마이신-NP를 사용한 경우 CD44+/CD24low 세포에서 유의미한 효과가 관찰되었으며, 파클리탁셀을 사용한 경우에는 효과가 크게 관찰되지 않았다(도 18 참조).
실시예
8. 동물 이종이식 마우스 모델에서 종양 성장 억제에 대한 살리노마
이신-NP의 효과
마우스에 이식된 H69 소세포 폐 암종 세포의 성장을 억제하는 살리노마이신-함유 나노입자의 능력을 검사하였다.
4주령 내지 6주령 Balb/c nu/nu 마우스의 왼쪽 옆구리에 5×106개의 H69 소세포 폐 암종 세포를 피하 주사하였다. 확립된 H69 종양(90 내지 120 mm3)을 가진 마우스를 각각 6마리 마우스의 그룹으로 무작위화하고, 3주 동안 (i) 매일 비히클 대조군을, 또는 (ii) 1주일에 1회 5 mg/kg 살리노마이신-나노입자로 i.p. 치료하였다. 종양을 캘리퍼를 이용하여 격일로 측정하였으며, 종양 용적을 수학식 (A×B2)/0.5를 이용하여 계산하였으며, 상기 식에서, A 및 B는 각각 최장 종양 직경 및 최단 종양 직경이다. 종양 용적의 통계학적 분석을 일원 ANOVA(one-way ANOVA) 및 Origin 8.0(Origin Lab)을 이용한 Dunnett 테스트에 의해 수행하였다.
결과는 도 15a에 도시되어 있다. 시간(x-축)에 대한 종양 용적(y-축)으로 도시되어 있다. 비히클 대조군으로 처리된 마우스의 종양 용적은 2000 mm3에 도달하였다. 반대로, 살리노마이신-함유 나노입자로 처리된 마우스의 종양 용적은 1000 mm3을 초과하지 않았다.
실시예
9:
살리노마이신-함유 나노입자로 처리된 H69 이종이식 마우스의 체중 평가
상기 실시예 6에서 논의된 바와 같은, 살리노마이신-나노입자로 처리된 H69 이종이식 마우스 및 대조군 마우스의 체중을 21일의 기간 동안 검사하였고 비히클로 처리된 마우스의 체중과 비교하였다.
결과는 도 15b에 도시되어 있다. 연구 기간 동안 두 그룹 모두에서 체중이 안정적으로 유지되거나 약간 증가하였다. 이러한 결과는, 살리노마이신-함유 나노입자가 체중에 악영향을 미치지 않음을 입증하는 것이다.
실시예
10. 야생형 마우스에서 다양한 용량의
살리노마이신 및 살리노마이신-함유 나노입자의 비교 독성
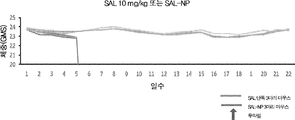
살리노마이신의 독성을 완화시키는 나노입자의 효과를 야생형 마우스에서 검사하였다. 상이한 용량의 살리노마이신 단독(5, 7.5, 10, 12.5 및 15 mg/kg) 또는 살리노마이신-나노입자(SAL-NP)(5, 7.5, 10, 12.5 및 15 mg/kg)를 야생형 마우스에 주사하였다. 살리노마이신 단독 및 살리노마이신-NP 그룹의 각 그룹에서 3마리의 마우스를 사용하였으며, 체중, 음식 및 물 섭취를 22일 동안 매일 측정하였다.
결과는 도 16a 내지 도 16e에 도시되어 있다. 결과는 살리노마이신 단독 및 살리노마이신-NP로 처리된 마우스의 체중 변화 또는 치사율을 나타낸 것이다. 최저 용량에서, 체중은 연구 마지막에 살리노마이신 단독으로 처리된 마우스에 비해 살리노마이신-나노입자로 처리된 마우스에서 유의미하게 더 높았다(도 16a 및 도 16b; 각각 5 및 7.5 mg/kg 용량).
검사된 다음으로 더 높은 2개의 용량에서, 살리노마이신 단독으로 처리된 마우스에서 치사율이 관찰되었으며; 살리노마이신 단독으로 처리된 마우스에서는 5일(도 16c; 10 mg/kg 용량) 또는 3일(도 16d; 12.5 mg/kg 용량) 넘게 생존하지 못하였다. 반대로, 이러한 농도의 살리노마이신-함유 나노입자로 처리된 마우스는 본 연구 기간 동안 생존하였으며, 체중은 본질적으로 변하지 않았다.
두 그룹 모두에서 최고 농도의 살리노마이신(도 16e; 15 mg/kg)에서 치사율이 관찰되었다. 그러나, 살리노마이신-함유 나노입자 그룹의 마우스는 연구 10 내지 12일까지 생존한 반면, 살리노마이신 단독으로 처리된 그룹의 모든 구성원은 3일 후에 사망하였다.
이러한 결과는, 나노입자가 마우스에서 살리노마이신의 용량 증가로 인한 독성 효과를 완화시킴을 입증하는 것이다.
실시예
11.
살리노마이신-함유 나노입자의 특징분석
도 5a 및 도 5b는 상기 실시예에서 사용된 살리노마이신-나노입자의 크기 및 형상을 제공하는 투과 전자 현미경 사진을 제공한 것이다. 도 7은 시험관내 무세포 완충 시스템에서 30일 동안 나노입자로부터 살리노마이신의 느리고 지속적인 방출을 도시한 그래프이다.
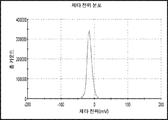
도 6a 및 도 6b는 살리노마이신-나노입자의 크기 분포 및 제타 전위 분포를 도시한 그래프이다. 살리노마이신-나노입자의 물리화학적 특징은 하기 표 8에서 상세히 설명되며, 사용된 코폴리머의 겔 투과 크로마토그래피(GPC)는 하기 표 9에 개시되어 있다.
표 8. SAL-NP의 물리화학적 특징
표 9. 나노입자의
GPC
Claims (59)
- 빠르게 증식하는 세포의 증식, 생존, 이동, 또는 콜로니 형성 능력의 감소를 필요로 하는 대상체에서 빠르게 증식하는 세포의 증식, 생존, 이동, 또는 콜로니 형성 능력을 감소시키는 방법으로서,
세포를, 치료학적 유효량의
a) 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG) 테트라블록 코폴리머를 포함하는 폴리머 나노입자, 및;
b) 살리노마이신을 포함하는 조성물과 접촉시키는 것을 포함하며,
치료학적 유효량은 약 0.025 mg/kg 내지 약 5 mg/kg인 방법. - 제1항에 있어서, 세포가 암세포인 방법.
- 제1항 또는 제2항에 있어서, 세포가 암 줄기 세포인 방법.
- 암 치료를 필요로 하는 대상체에서 암을 치료하는 방법으로서,
대상체에, 치료학적 유효량의,
a) 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG) 테트라블록 코폴리머를 포함하는 폴리머 나노입자; 및
b) 살리노마이신을 포함하는 조성물을 투여하는 것을 포함하며,
치료학적 유효량은 약 0.025 mg/kg 내지 약 5 mg/kg인 방법. - 제4항에 있어서, 암이 유방암, 난소암, 췌장암, 백혈병, 림프종, 골육종, 위암, 전립선암, 결장암, 비소세포 폐암 및 소세포 폐암, 간암, 신장암, 두경부암, 및 자궁경부암으로 이루어진 군으로부터 선택되는 방법.
- 제4항에 있어서, 암이 전이성인 방법.
- 제4항에 있어서, 추가 항암 요법을 대상체에 투여하는 것을 추가로 포함하는 방법.
- 제7항에 있어서, 추가 항암 요법이 수술, 화학요법, 방사선, 호르몬 요법, 면역요법, 또는 이들의 조합인 방법.
- 제4항에 있어서, 암이 화학치료제에 내성이 있거나 불응성인 방법.
- 제4항에 있어서, 대상체가 인간인 방법.
- 암 줄기 세포의 증식, 생존, 이동, 또는 콜로니 형성 능력의 감소를 필요로 하는 대상체에서 암 줄기 세포의 증식, 생존, 이동, 또는 콜로니 형성 능력을 감소시키는 방법으로서,
대상체에, 치료학적 유효량의
a) 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG) 테트라블록 코폴리머를 포함하는 폴리머 나노입자, 및;
b) 살리노마이신을 포함하는 조성물을 투여하는 것을 포함하며,
치료학적 유효량은 약 0.025 mg/kg 내지 약 5 mg/kg인 방법. - 제1항 내지 제11항 중 어느 한 항에 있어서, 치료학적 유효량이 약 0.03 mg/kg 내지 약 0.5 mg/kg인 방법.
- 제1항 내지 제11항 중 어느 한 항에 있어서, 치료학적 유효량이 약 0.5 mg/kg 내지 약 0.8 mg/kg인 방법.
- 제1항 내지 제11항 중 어느 한 항에 있어서, 치료학적 유효량이 약 0.8 mg/kg 내지 약 1.1 mg/kg인 방법.
- 제1항 내지 제14항 중 어느 한 항에 있어서, 조성물이 정맥내로, 종양내로, 또는 피하로 투여되는 방법.
- 제1항 내지 제15항 중 어느 한 항에 있어서, 조성물이 적어도 하루에 1회, 격일에 1회, 1주일에 1회, 1주일에 2회, 1개월에 1회, 또는 1개월에 2회 투여되는 방법.
- 제1항 내지 제16항 중 어느 한 항에 있어서, 조성물이 3주의 기간 동안 1주일에 1회 또는 1주일에 2회 투여되는 방법.
- 제1항 내지 제17항 중 어느 한 항에 있어서, PLA-PEG-PPG-PEG 테트라블록 코폴리머가 PEG-PPG-PEG 트리블록 코폴리머와 PLA의 화학적 컨쥬게이션으로부터 형성되는 방법.
- 제1항 내지 제17항 중 어느 한 항에 있어서, PLA의 분자량이 약 10,000 내지 약 100,000 달톤인 방법.
- 제1항 내지 제17항 중 어느 한 항에 있어서, PLA의 분자량이 약 20,000 내지 90,000 달톤인 방법.
- 제1항 내지 제17항 중 어느 한 항에 있어서, PLA의 분자량이 약 30,000 내지 80,000 달톤인 방법.
- 제1항 내지 제17항 중 어느 한 항에 있어서, PEG-PPG-PEG의 분자량이 약 8,000 달톤 내지 18,000 달톤인 방법.
- 제1항 내지 제17항 중 어느 한 항에 있어서, PEG-PPG-PEG의 분자량이 약 12,000 달톤 내지 17,000 달톤인 방법.
- 제1항 내지 제17항 중 어느 한 항에 있어서, 코폴리머에서 PLA의 분자량이 약 30,000 내지 80,000 달톤이며, PEG-PPG-PEG의 분자량이 12,000 달톤 내지 17,000 달톤인 방법.
- 제1항 내지 제17항 중 어느 한 항에 있어서, 폴리머 나노입자의 평균 직경이 80 내지 120 nm인 방법.
- 제1항 내지 제17항 중 어느 한 항에 있어서, 폴리머 나노입자의 평균 직경이 90 내지 110 nm인 방법.
- 제1항 내지 제17항 중 어느 한 항에 있어서, 폴리머 나노입자의 평균 직경이 95 내지 105 nm인 방법.
- 제1항 내지 제17항 중 어느 한 항에 있어서, 제2 치료제 또는 타겟팅된 항암제를 추가로 포함하는 방법.
- a) 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG) 테트라블록 코폴리머를 포함하는 폴리머 나노입자;
b) 살리노마이신; 및
c) 약제학적으로 허용되는 담체를 포함하는 약제 조성물. - 제29항에 있어서, 폴리머 나노입자가 폴리머 나노입자의 외측에 부착된 타겟팅 모이어티를 추가로 포함하는 약제 조성물.
- 약 12.5 mg 내지 약 500 mg의 제25항의 약제 조성물을 포함하는 제형.
- 빠르게 증식하는 세포의 증식, 생존, 이동, 또는 콜로니 형성 능력의 감소를 필요로 하는 대상체에서 빠르게 증식하는 세포에서 증식, 생존, 이동, 또는 콜로니 형성 능력을 감소시키는 데 사용하기 위한 약제 조성물로서,
약제 조성물은
a) 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG) 테트라블록 코폴리머를 포함하는 폴리머 나노입자, 및;
b) 살리노마이신을 포함하며,
치료학적 유효량의 약제 조성물은 대상체에 투여되며, 치료학적 유효량은 약 0.025 mg/kg 내지 약 5 mg/kg인, 약제 조성물. - 제32항에 있어서, 세포가 암 세포인, 사용하기 위한 약제 조성물.
- 제32항 또는 제33항에 있어서, 세포가 암 줄기 세포인, 사용하기 위한 약제 조성물.
- 암 치료를 필요로 하는 대상체에서 암의 치료에서 사용하기 위한 약제 조성물로서,
약제 조성물은
a) 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG) 테트라블록 코폴리머를 포함하는 폴리머 나노입자, 및;
b) 살리노마이신을 포함하며,
치료학적 유효량의 약제 조성물은 대상체에 투여되며, 치료학적 유효량은 약 0.025 mg/kg 내지 약 5 mg/kg인, 약제 조성물. - 제35항에 있어서, 암이 유방암, 난소암, 췌장암, 백혈병, 림프종, 골육종, 위암, 전립선암, 결장암, 비소세포 폐암 및 소세포 폐암, 간암, 신장암, 두경부암, 및 자궁경부암으로 이루어진 군으로부터 선택되는, 사용하기 위한 약제 조성물.
- 제35항에 있어서, 암이 전이성인, 사용하기 위한 약제 조성물.
- 제35항에 있어서, 추가 항암 요법을 대상체에 투여하는 것을 추가로 포함하는, 사용하기 위한 약제 조성물.
- 제38항에 있어서, 추가 항암 요법이 수술, 화학요법, 방사선, 호르몬 요법, 면역요법, 또는 이들의 조합인, 사용하기 위한 약제 조성물.
- 제35항에 있어서, 암이 화학치료제에 내성이 있거나 불응성인, 사용하기 위한 약제 조성물.
- 제35항에 있어서, 대상체가 인간인, 사용하기 위한 약제 조성물.
- 암 줄기 세포의 증식, 생존, 이동, 또는 콜로니 형성 능력의 감소를 필요로 하는 대상체에서 암 줄기 세포의 증식, 생존, 이동, 또는 콜로니 형성 능력을 감소시키는 데 사용하기 위한 약제 조성물로서,
약제 조성물은
a) 폴리(락트산)-폴리(에틸렌 글리콜)-폴리(프로필렌 글리콜)-폴리(에틸렌 글리콜)(PLA-PEG-PPG-PEG) 테트라블록 코폴리머를 포함하는 폴리머 나노입자, 및;
b) 살리노마이신을 포함하며;
치료학적 유효량의 약제 조성물은 대상체에 투여되며, 치료학적 유효량은 약 0.025 mg/kg 내지 약 5 mg/kg인 약제 조성물. - 제32항 내지 제42항 중 어느 한 항에 있어서, 치료학적 유효량이 약 0.03 mg/kg 내지 약 0.5 mg/kg인, 사용하기 위한 약제 조성물.
- 제32항 내지 제42항 중 어느 한 항에 있어서, 치료학적 유효량이 약 0.5 mg/kg 내지 약 0.8 mg/kg인, 사용하기 위한 약제 조성물.
- 제32항 내지 제42항 중 어느 한 항에 있어서, 치료학적 유효량이 약 0.8 mg/kg 내지 약 1.1 mg/kg인, 사용하기 위한 약제 조성물.
- 제32항 내지 제45항 중 어느 한 항에 있어서, 조성물이 정맥내로, 종양내로, 또는 피하로 투여되는, 사용하기 위한 약제 조성물.
- 제32항 내지 제46항 중 어느 한 항에 있어서, 조성물이 적어도 하루에 1회, 격일에 1회, 1주일에 1회, 1주일에 2회, 1개월에 1회, 또는 1개월에 2회 투여되는, 사용하기 위한 약제 조성물.
- 제32항 내지 제47항 중 어느 한 항에 있어서, 조성물이 3주의 기간 동안 1주일에 1회 또는 1주일에 2회 투여되는, 사용하기 위한 약제 조성물.
- 제32항 내지 제48항 중 어느 한 항에 있어서, PLA-PEG-PPG-PEG 테트라블록 코폴리머가 PEG-PPG-PEG 트리블록 코폴리머와 PLA의 화학적 컨쥬게이션으로부터 형성되는, 사용하기 위한 약제 조성물.
- 제32항 내지 제48항 중 어느 한 항에 있어서, PLA의 분자량이 약 10,000 내지 약 100,000 달톤인, 사용하기 위한 약제 조성물.
- 제32항 내지 제48항 중 어느 한 항에 있어서, PLA의 분자량이 약 20,000 내지 90,000 달톤인, 사용하기 위한 약제 조성물.
- 제32항 내지 제48항 중 어느 한 항에 있어서, PLA의 분자량이 약 30,000 내지 80,000 달톤인, 사용하기 위한 약제 조성물.
- 제32항 내지 제48항 중 어느 한 항에 있어서, PEG-PPG-PEG의 분자량이 약 8,000 달톤 내지 18,000 달톤인, 사용하기 위한 약제 조성물.
- 제32항 내지 제48항 중 어느 한 항에 있어서, PEG-PPG-PEG의 분자량이 약 12,000 달톤 내지 17,000 달톤인, 사용하기 위한 약제 조성물.
- 제32항 내지 제48항 중 어느 한 항에 있어서, 코폴리머에서 PLA의 분자량이 약 30,000 내지 80,000 달톤이며, PEG-PPG-PEG의 분자량이 12,000 달톤 내지 17,000 달톤인, 사용하기 위한 약제 조성물.
- 제32항 내지 제48항 중 어느 한 항에 있어서, 폴리머 나노입자의 평균 직경이 80 내지 120 nm인, 사용하기 위한 약제 조성물.
- 제32항 내지 제48항 중 어느 한 항에 있어서, 폴리머 나노입자의 평균 직경이 90 내지 110 nm인, 사용하기 위한 약제 조성물.
- 제32항 내지 제48항 중 어느 한 항에 있어서, 폴리머 나노입자의 평균 직경이 95 내지 105 nm인, 사용하기 위한 약제 조성물.
- 제32항 내지 제48항 중 어느 한 항에 있어서, 제2 치료제 또는 타겟팅된 항암제를 추가로 포함하는, 사용하기 위한 약제 조성물.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201862699963P | 2018-07-18 | 2018-07-18 | |
| US62/699,963 | 2018-07-18 | ||
| PCT/US2019/042382 WO2020018778A1 (en) | 2018-07-18 | 2019-07-18 | Polymeric nanoparticles comprising salinomycin |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20210053881A true KR20210053881A (ko) | 2021-05-12 |
Family
ID=67704555
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020217004716A KR20210053881A (ko) | 2018-07-18 | 2019-07-18 | 살리노마이신을 포함하는 폴리머 나노입자 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US20200046648A1 (ko) |
| EP (1) | EP3823589A1 (ko) |
| JP (1) | JP2021530504A (ko) |
| KR (1) | KR20210053881A (ko) |
| CN (1) | CN113164375A (ko) |
| AU (1) | AU2019307629A1 (ko) |
| CA (1) | CA3105731A1 (ko) |
| WO (1) | WO2020018778A1 (ko) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2022251844A1 (en) * | 2021-05-25 | 2022-12-01 | Hillstream Biopharma, Inc. | Polymeric nanoparticles comprising chemotherapeutic compounds and related methods |
| CN116570584A (zh) * | 2023-05-08 | 2023-08-11 | 广州白云山医药集团股份有限公司白云山制药总厂 | 盐霉素在制备降尿酸和/或治疗高尿酸血症的药物中的应用 |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU2003227147A1 (en) | 2002-04-05 | 2003-10-27 | Universite De Montreal | Stealthy polymeric biodegradable nanospheres and uses thereof |
| HUE028025T2 (en) | 2005-08-03 | 2016-11-28 | Novartis Ag | Use of Panobinostat HDAC inhibitor to treat myeloma |
| EP2046575A4 (en) | 2006-07-28 | 2010-01-13 | Bridgestone Corp | POLYMERS CORE SHELL NANOPARTICLES WITH AN INTERPHASE AREA |
| US20080081075A1 (en) | 2006-10-02 | 2008-04-03 | National Tsing Hua University | Multifunctional mixed micelle of graft and block copolymers and preparation thereof |
| US9149426B2 (en) | 2012-02-15 | 2015-10-06 | University Of Tennessee Research Foundation | Nanoparticle composition and methods to make and use the same |
| WO2013160773A2 (en) | 2012-04-23 | 2013-10-31 | Nanogen Pharmaceuticals | Polymeric nanoparticles and a process of preparation thereof |
| WO2018049155A1 (en) * | 2016-09-08 | 2018-03-15 | Dana-Farber Cancer Institute, Inc. | Compositions comprising polymeric nanoparticles and mcl-1 antagonists |
| US20190105261A1 (en) * | 2017-10-11 | 2019-04-11 | Illustris Pharmaceuticals, Inc. | Methods and compositions for topical delivery |
| CA3079751A1 (en) * | 2017-11-22 | 2019-05-31 | Hillstream Biopharma Inc. | Polymeric nanoparticles comprising bortezomib |
-
2019
- 2019-07-18 AU AU2019307629A patent/AU2019307629A1/en not_active Abandoned
- 2019-07-18 EP EP19756447.9A patent/EP3823589A1/en active Pending
- 2019-07-18 CA CA3105731A patent/CA3105731A1/en active Pending
- 2019-07-18 KR KR1020217004716A patent/KR20210053881A/ko unknown
- 2019-07-18 US US16/515,405 patent/US20200046648A1/en not_active Abandoned
- 2019-07-18 JP JP2021501041A patent/JP2021530504A/ja active Pending
- 2019-07-18 CN CN201980047686.0A patent/CN113164375A/zh active Pending
- 2019-07-18 WO PCT/US2019/042382 patent/WO2020018778A1/en active Application Filing
Also Published As
| Publication number | Publication date |
|---|---|
| EP3823589A1 (en) | 2021-05-26 |
| WO2020018778A1 (en) | 2020-01-23 |
| CN113164375A (zh) | 2021-07-23 |
| JP2021530504A (ja) | 2021-11-11 |
| US20200046648A1 (en) | 2020-02-13 |
| AU2019307629A1 (en) | 2021-02-18 |
| CA3105731A1 (en) | 2020-01-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20220175874A1 (en) | Polymeric nanoparticles and a process of preparation thereof | |
| JP2019537600A (ja) | ポリマーナノ粒子 | |
| WO2018049155A1 (en) | Compositions comprising polymeric nanoparticles and mcl-1 antagonists | |
| US20220175688A1 (en) | Polymeric nanoparticles | |
| KR20210053881A (ko) | 살리노마이신을 포함하는 폴리머 나노입자 | |
| US10695427B2 (en) | Shape memory particles for biomedical uses | |
| US20190151340A1 (en) | Polymeric nanoparticles comprising bortezomib | |
| JP7158450B2 (ja) | ポリマーナノ粒子およびその調整のプロセス | |
| WO2022251844A1 (en) | Polymeric nanoparticles comprising chemotherapeutic compounds and related methods |