KR20210003813A - IL-15/IL-15Rα Fc-융합 단백질 및 LAG-3 항원 결합 도메인을 함유하는 LAG-3 표적화 이종이량체 융합 단백질 - Google Patents
IL-15/IL-15Rα Fc-융합 단백질 및 LAG-3 항원 결합 도메인을 함유하는 LAG-3 표적화 이종이량체 융합 단백질 Download PDFInfo
- Publication number
- KR20210003813A KR20210003813A KR1020207033040A KR20207033040A KR20210003813A KR 20210003813 A KR20210003813 A KR 20210003813A KR 1020207033040 A KR1020207033040 A KR 1020207033040A KR 20207033040 A KR20207033040 A KR 20207033040A KR 20210003813 A KR20210003813 A KR 20210003813A
- Authority
- KR
- South Korea
- Prior art keywords
- domain
- variant
- lag
- terminus
- monomer
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/52—Cytokines; Lymphokines; Interferons
- C07K14/54—Interleukins [IL]
- C07K14/5443—IL-15
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/715—Receptors; Cell surface antigens; Cell surface determinants for cytokines; for lymphokines; for interferons
- C07K14/7155—Receptors; Cell surface antigens; Cell surface determinants for cytokines; for lymphokines; for interferons for interleukins [IL]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
- A61K2039/507—Comprising a combination of two or more separate antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
- C07K2317/524—CH2 domain
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
- C07K2317/526—CH3 domain
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
- C07K2317/53—Hinge
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/622—Single chain antibody (scFv)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/66—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising a swap of domains, e.g. CH3-CH2, VH-CL or VL-CH1
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/30—Non-immunoglobulin-derived peptide or protein having an immunoglobulin constant or Fc region, or a fragment thereof, attached thereto
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Immunology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Toxicology (AREA)
- Zoology (AREA)
- Gastroenterology & Hepatology (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Epidemiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Cell Biology (AREA)
- Peptides Or Proteins (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
Abstract
본 발명은 IL-15/IL-15Rα Fc-융합 단백질 및 LAG-3 항체 단편-Fc 융합 단백질을 포함하는 신규한 표적화 이종이량체 융합 단백질에 관한 것이다.
Description
관련 출원의 교차 참조
본 출원은 2018년 4월 18일자 출원된 미국 가출원 제62/659,624호 및 2018년 12월 20일자 출원된 미국 가출원 제62/783,107호를 우선권 주장하며, 상기 문헌들은 그 전문이, 특히 그 안의 도면, 범례 및 청구범위가 본원에 명백하게 참조로서 인용된다.
암 면역요법에서 매우 유망한 두 가지 접근법에는, 사이토카인 기반 치료와 PD-1과 같은 면역 체크포인트 단백질의 차단이 포함된다.
IL-2 및 IL-15와 같은 사이토카인은 B세포, T세포 및 NK세포의 증식 및 분화를 돕는 기능을 한다. 두 가지 사이토카인은 모두 2개의 공유된 수용체인 공통 감마 사슬(γc; CD132) 및 IL-2 수용체 베타 사슬(IL-2Rβ; CD122)과, 각각의 사이토카인에 고유한 알파 사슬 수용체인 IL-2 수용체 알파(IL-2Rα; CD25) 또는 IL-15 수용체 알파(IL-15Rα; CD215)로 이루어진 삼량체성 복합체에의 결합을 통해 이의 세포 신호전달 기능을 발휘한다. 두 가지 사이토카인은 모두 종양학에서 잠재적으로 유용한 치료제로서 간주되며, IL-2는 전이성 신장세포암종 및 악성 흑색종을 앓고 있는 환자에 사용하도록 승인되어 있다. 현재, 몇몇 임상 시험이 진행 중이지만, 재조합 IL-15의 사용은 승인되어 있지 않다. 하지만, 잠재적인 약물로서, 두 가지 사이토카인은 모두 반감기가 수분 내로 측정되는 매우 빠른 제거로 인해 불리하다. IL-2 면역요법은 빠른 제거를 극복하기 위해 고용량으로 투여되는 경우 전신 독성과 관련이 있었다. 이러한 전신 독성은 또한 최근 임상 시험에서 IL-15 면역요법을 이용한 경우에도 보고되었다(문헌[Guo et al., J Immunol, 2015, 195(5):2353-64]).
PD-1과 같은 면역 체크포인트 단백질은 T세포 활성화 후 상향조절되어, PD-L1과 같은 면역 체크포인트 리간드에의 결합 시 활성화된 T세포를 고갈시킴으로써 자가면역을 불가능하게 한다. 하지만, 면역 체크포인트 단백질은 또한 종양 침윤 림프구(TIL: tumor-infiltrating lymphocyte)에서도 상향조절되며, 면역 체크포인트 리간드는 종양세포에서 과발현되어 종양세포에 의한 면역 회피에 기여한다. Opdivo®(니볼루맙(nivolumab)) 및 Keytruda®(펨브롤리주맙(pembrolizumab))과 같은 약물을 이용한 면역 체크포인트 상호작용의 차단에 의한 TIL의 억제 해제는, 암의 치료에서 매우 효과적인 것으로 입증되었다. 니볼루맙 및 펨브롤리주맙과 같은 체크포인트 차단 요법의 가능성에도 불구하고, 많은 환자들은 여전히 체크포인트 차단 단독에 대해 충분한 반응을 달성하지 못하고 있다.
따라서, 고용량을 필요로 하지 않으며 전신 독성을 회피하기 위해 종양을 표적으로 하는 사이토카인을 이용한 치료 전략에 대한 종양 치료에는 충족되지 않은 요구가 남아있다. 나아가, 환자 반응률을 증가시킬 수 있는, 체크포인트 차단과 조합할 추가적인 치료 방식을 규명하는 것이 필요하다.
이러한 요구와 주의사항을 해결하기 위해, 본원에는 체크포인트 차단 항체와 상조적으로 조합되며, 안전성 프로파일을 개선시키기 위해 반감기가 증강되고 TIL을 보다 선택적으로 표적화하는 신규한 LAG-3 표적화 IL-15 이종이량체 융합 단백질이 제공된다(도 1).
하나의 양태에서, 본 발명은 표적화 IL-15/IL-15Rα 이종이량체 단백질로서, (a) 제1 단량체로서, N-말단에서 C-말단으로, i) IL-15 스시(sushi) 도메인; ii) 제1 도메인 링커; iii) 변이체 IL-15 도메인; iv) 제2 도메인 링커; v) CH2-CH3을 포함하는 제1 변이체 Fc 도메인을 포함하는 제1단량체; 및 (b) 제2 단량체로서, N-말단에서 C-말단으로, i) scFv 도메인; ii) 제3 도메인 링커; iii) CH2-CH3을 포함하는 제2 변이체 Fc 도메인을 포함하는 제2 단량체를 포함하며, 여기서 scFv 도메인은 제1 가변 중쇄 도메인, scFv 링커 및 제1 가변 경쇄 도메인을 포함하고, 인간 LAG-3에 결합하는, 표적화 IL-15/IL-15Rα 이종이량체 단백질을 제공한다.
본 발명의 다른 양태에서, 본원에는 표적화 IL-15/IL-15Rα 이종이량체 단백질로서, (a) 제1 단량체로서, N-말단에서 C-말단으로, i) IL-15 스시 도메인; ii) 제1 도메인 링커; iii) CH2-CH3을 포함하는 제1 변이체 Fc 도메인을 포함하는 제1 단량체; (b) 제2 단량체로서, N-말단에서 C-말단으로, i) scFv 도메인; ii) 제3 도메인 링커; iii) CH2-CH3을 포함하는 제2 변이체 Fc 도메인을 포함하는 제2 단량체(여기서 scFv 도메인은 제1 가변 중쇄 도메인, scFv 링커 및 제1 가변 경쇄 도메인을 포함함); 및 (c) 변이체 IL-15 도메인을 포함하는 제3 단량체를 포함하며, 여기서 scFv 도메인은 인간 LAG-3에 결합하는, 표적화 IL-15/IL-15Rα 이종이량체 단백질이 제공된다.
하나의 양태에서, "scIL-15/Rα X Fab" 형식 이종이량체 단백질이 제공된다. 상기와 같은 "scIL-15/Rα X Fab" 형식 이종이량체 단백질은, a) 제1 단량체로서, N-말단에서 C-말단으로, i) IL-15Rα(스시) 도메인; ii) 제1 도메인 링커; iii) IL-15 변이체; iv) 제2 도메인 링커; v) CH2-CH3을 포함하는 제1 변이체 Fc 도메인을 포함하는 제1 단량체; b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) VL-CL을 포함하는 제3 단량체를 포함한다. 상기 VH 및 VL은, 각각, 인간 LAG-3 항원 결합 도메인을 형성하는 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 일부 구현예에서, 상기 제2 도메인 링커는 항체 힌지이다.
"scIL-15/Rα X Fab" 형식 이종이량체 단백질의 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 EU 넘버링에 따라 S267K/L368D/K370S : S267K/S364K/E357Q; S364K/E357Q : L368D/K370S; L368D/K370S : S364K; L368E/K370S : S364K; T411E/K360E/Q362E : D401K; L368D/K370S : S364K/E357L 및 K370S : S364K/E357Q 중 하나의 비대칭(skew) 변이체 세트를 포함한다. 예시적인 구현예에서, 상기 비대칭 변이체 세트는 S364K/E357Q : L368D/K370S이다.
"scIL-15/Rα X Fab" 형식 이종이량체 단백질의 예시적인 구현예에서, "scIL-15/Rα X Fab" 형식 이종이량체 단백질은, a) 제1 단량체로서, N-말단에서 C-말단으로, i) IL-15Rα(스시) 도메인; ii) 제1 도메인 링커; iii) IL-15 변이체; iv) 힌지; v) CH2-CH3을 포함하는 제1 변이체 Fc 도메인을 포함하는 제1 단량체; b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) VL-CL을 포함하는 제3 단량체를 포함한다. 상기 VH 및 VL은, 각각, 인간 LAG-3 항원 결합 도메인을 형성하는 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 상기와 같은 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 상기 제1 변이체 Fc 도메인은 pI 변이체 Q295E/N384D/Q418E/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따른다. 일부 구현예에서, 상기 제1 단량체의 힌지는 아미노산 치환 C220S를 포함하며, 여기서 넘버링은 EU 넘버링에 따른다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428:/N434S를 추가로 포함한다.
"scIL-15/Rα X Fab" 형식 이종이량체 단백질의 일부 구현예에서, 본원에 제공된 이종이량체 단백질의 IL-15 변이체는 N1D, N4D, D8N, D30N, D61N, E64Q, N65D, Q108E, N4D/N65D, D30N/N65D 및 D30N/E64Q/N65D로 이루어지는 군으로부터 선택되는 아미노산 치환(들)을 포함한다. 예시적인 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함한다.
예시적인 구현예에서, "scIL-15/Rα X Fab" 형식 이종이량체 단백질은 XENP27972, XENP27973, XENP27977, XENP27978, XENP029486, XENP029487, XENC1000, XENC1001, XENC1002, XENC1003, XENC1004 또는 XENC1005이다.
특정 구현예에서, 본원에 제공된 "scIL-15/Rα X Fab" 형식 이종이량체 단백질의 VH 및 VL은 도 12 및 도 13의 임의의 LAG-3 항원 결합 도메인의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 예시적인 구현예에서, 상기 LAG-3 항원 결합 도메인은 2A11_H1.144_L2.142 및 7G8_H3.30_L1.34이다.
하나의 양태에서, 본원에는 "scIL-15/Rα X scFv" 형식을 갖는 이종이량체 단백질이 제공된다. 하나의 구현예에서, 상기 이종이량체 단백질은, a) 제1 단량체로서, N-말단에서 C-말단으로, i) IL-15Rα(스시) 도메인; ii) 제1 도메인 링커; iii) IL-15 변이체; iv) 제2 도메인 링커; 및 v) CH2-CH3을 포함하는 제1 변이체 Fc 도메인을 포함하는 제1 단량체; 및 b) 제2 단량체로서, N-말단에서 C-말단으로, i) scFv 도메인; ii) 제3 도메인 링커; 및 iii) CH2-CH3을 포함하는 제2 변이체 Fc 도메인을 포함하는 제2 단량체를 포함한다. 일부 구현예에서, 상기 scFv 도메인은 가변 중쇄 도메인(VH), scFv 링커 및 가변 경쇄 도메인(VL)을 포함하고, 인간 LAG-3에 결합한다. "scIL-15/Rα X scFv" 형식 이종이량체 단백질의 일부 구현예에서, 상기 제2 도메인 링커와 제3 도메인 링커는 각각 항체 힌지이다.
특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 EU 넘버링에 따라 S267K/L368D/K370S : S267K/S364K/E357Q; S364K/E357Q : L368D/K370S; L368D/K370S : S364K; L368E/K370S : S364K; T411E/K360E/Q362E : D401K; L368D/K370S : S364K/E357L 및 K370S : S364K/E357Q 중 하나의 비대칭 변이체 세트를 포함한다. 예시적인 구현예에서, 상기 비대칭 변이체 세트는 S364K/E357Q : L368D/K370S이다.
"scIL-15/Rα X scFv" 형식의 일부 구현예에서, 상기 이종이량체 단백질은, a) 제1 단량체로서, N-말단에서 C-말단으로, i) IL-15Rα(스시) 도메인; ii) 제1 도메인 링커; iii) IL-15 변이체; iv) 힌지; 및 v) CH2-CH3을 포함하는 제1 변이체 Fc 도메인을 포함하는 제1 단량체; 및 b) 제2 단량체로서, N-말단에서 C-말단으로, i) scFv 도메인; ii) 힌지; 및 iii) CH2-CH3을 포함하는 제2 변이체 Fc 도메인을 포함하는 제2 단량체를 포함한다. 일부 구현예에서, 상기 scFv 도메인은 가변 중쇄 도메인(VH), scFv 링커 및 가변 경쇄 도메인(VL)을 포함하고, 인간 LAG-3에 결합한다. 상기와 같은 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 상기 제1 변이체 Fc 도메인은 pI 변이체 Q295E/N384D/Q418E/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따른다. 특정 구현예에서, 상기 제1 힌지와 제2 힌지는 각각 아미노산 치환 C220S를 포함하며, 여기서 넘버링은 EU 넘버링에 따른다. 하나의 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428:/N434S를 추가로 포함한다.
또 다른 양태에서, 본원에는 "scFv X ncIL-15/Rα" 형식 이종이량체 단백질이 제공된다. 상기와 같은 이종이량체 단백질은, a) 제1 단량체로서, N-말단에서 C-말단으로, i) scFv 도메인; ii) 제1 도메인 링커; 및 iii) CH2-CH3을 포함하는 제1 변이체 Fc 도메인을 포함하는 제1 단량체; b) 제2 단량체로서, N-말단에서 C-말단으로, i) IL-15Rα(스시) 도메인; ii) 제2 도메인 링커; 및 iii) CH2-CH3을 포함하는 제2 변이체 Fc 도메인을 포함하는 제2 단량체; 및 c) IL-15 변이체를 포함하는 제3 단량체를 포함한다. 상기 scFv 도메인은 가변 중쇄 도메인(VH), scFv 링커 및 가변 경쇄 도메인(VL)을 포함하고, 인간 LAG-3에 결합한다. 하나의 구현예에서, 상기 제1 도메인 링커와 제2 도메인 링커는 각각 항체 힌지이다.
"scFv X ncIL-15/Rα" 형식 이종이량체 단백질의 일부 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 EU 넘버링에 따라 S267K/L368D/K370S : S267K/S364K/E357Q; S364K/E357Q : L368D/K370S; L368D/K370S : S364K; L368E/K370S : S364K; T411E/K360E/Q362E : D401K; L368D/K370S : S364K/E357L 및 K370S : S364K/E357Q 중 하나의 비대칭 변이체 세트를 포함한다. 예시적인 구현예에서, 상기 비대칭 변이체 세트는 S364K/E357Q : L368D/K370S이다.
예시적인 구현예에서, "scFv X ncIL-15/Rα" 형식 이종이량체 단백질은, a) 제1 단량체로서, N-말단에서 C-말단으로, i) scFv 도메인; ii) 힌지; 및 iii) CH2-CH3을 포함하는 제1 변이체 Fc 도메인을 포함하는 제1 단량체; b) 제2 단량체로서, N-말단에서 C-말단으로, i) IL-15Rα(스시) 도메인; ii) 힌지; 및 iii) CH2-CH3을 포함하는 제2 변이체 Fc 도메인을 포함하는 제2 단량체; 및 c) IL-15 변이체를 포함하는 제3 단량체를 포함한다. 나아가, 상기 scFv 도메인은 가변 중쇄 도메인(VH), scFv 링커 및 가변 경쇄 도메인(VL)을 포함하고, 인간 LAG-3에 결합한다. 상기와 같은 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 상기 제1 변이체 Fc 도메인은 pI 변이체 Q295E/N384D/Q418E/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따른다. 특정 구현예에서, 상기 제1 힌지와 제2 힌지는 각각 아미노산 치환 C220S를 포함하며, 여기서 넘버링은 EU 넘버링에 따른다. 하나의 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428:/N434S를 추가로 포함한다.
또 다른 양태에서, 본원에는 "scFv x dsIL-15/Rα" 형식 이종이량체 단백질이 제공된다. "scFv x dsIL-15/Rα" 형식 이종이량체 단백질은, a) 제1 단량체로서, N-말단에서 C-말단으로, i) 시스테인 잔기 대신 치환된 아미노산을 포함하는 변이체 IL-15Rα(스시) 도메인; ii) 제1 도메인 링커; 및 iii) CH2-CH3을 포함하는 제1 변이체 Fc 도메인을 포함하는 제1 단량체; b) 제2 단량체로서, N-말단에서 C-말단으로, i) scFv 도메인; ii) 제2 도메인 링커; iii) CH2-CH3을 포함하는 제2 변이체 Fc 도메인을 포함하는 제2 단량체; 및 c) 시스테인 잔기 대신 치환된 아미노산을 포함하는 IL-15 변이체를 포함하는 제3 단량체를 포함한다. 상기 scFv 도메인은 가변 중쇄 도메인(VH), scFv 링커 및 가변 경쇄 도메인(VL)을 포함하고, 여기서 상기 변이체 IL-15Rα(스시) 도메인의 시스테인 잔기와 IL-15 변이체의 시스테인 잔기는 다이설파이드 결합을 형성하며, 상기 scFv 도메인은 인간 LAG-3에 결합한다. 특정 구현예에서, 상기 제1 도메인 링커와 제2 도메인 링커는 각각 항체 힌지이다.
"scFv x dsIL-15/Rα" 형식 이종이량체 단백질의 일부 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 EU 넘버링에 따라 S267K/L368D/K370S : S267K/S364K/E357Q; S364K/E357Q : L368D/K370S; L368D/K370S : S364K; L368E/K370S : S364K; T411E/K360E/Q362E : D401K; L368D/K370S : S364K/E357L 및 K370S : S364K/E357Q 중 하나의 비대칭 변이체 세트를 포함한다. 예시적인 구현예에서, 상기 비대칭 변이체 세트는 S364K/E357Q : L368D/K370S이다.
예시적인 구현예에서, "scFv x dsIL-15/Rα" 형식 이종이량체 단백질은, a) 제1 단량체로서, N-말단에서 C-말단으로, i) 시스테인 잔기 대신 치환된 아미노산을 포함하는 변이체 IL-15Rα(스시) 도메인; ii) 힌지; 및 iii) CH2-CH3을 포함하는 제1 변이체 Fc 도메인을 포함하는 제1 단량체; b) 제2 단량체로서, N-말단에서 C-말단으로, i) scFv 도메인; ii) 힌지; iii) CH2-CH3을 포함하는 제2 변이체 Fc 도메인을 포함하는 제2 단량체; 및 c) 시스테인 잔기 대신 치환된 아미노산을 포함하는 IL-15 변이체를 포함하는 제3 단량체를 포함한다. 상기 scFv 도메인은 가변 중쇄 도메인(VH), scFv 링커 및 가변 경쇄 도메인(VL)을 포함하고, 여기서 상기 변이체 IL-15Rα(스시) 도메인의 시스테인 잔기와 IL-15 변이체의 시스테인 잔기는 다이설파이드 결합을 형성하며, 상기 scFv 도메인은 인간 LAG-3에 결합한다. 상기와 같은 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 상기 제1 변이체 Fc 도메인은 pI 변이체 Q295E/N384D/Q418E/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따른다. 특정 구현예에서, 상기 제1 단량체의 힌지와 제2 단량체의 힌지는 각각 아미노산 치환 C220S를 포함하며, 여기서 넘버링은 EU 넘버링에 따른다. 일부 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428:/N434S를 포함한다.
하나의 양태에서, 본원에는 "Fab X ncIL-15/Rα" 형식 이종이량체 단백질이 제공된다. 상기와 같은 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) 제2 단량체로서, N-말단에서 C-말단으로, i) IL-15Rα(스시) 도메인; ii) 제1 도메인 링커; iii) CH2-CH3을 포함하는 제1 변이체 Fc 도메인을 포함하는 제2 단량체; c) VL-CL을 포함하는 경쇄를 포함하는 제3 단량체; 및 d) IL-15 변이체를 포함하는 제4 단량체를 포함한다. 상기 VH 및 VL은, 각각, 인간 LAG-3 항원 결합 도메인을 형성하는 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 일부 구현예에서, 상기 제1 도메인 링커는 항체 힌지이다.
"Fab X ncIL-15/Rα" 형식 이종이량체 단백질의 일부 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 EU 넘버링에 따라 S267K/L368D/K370S : S267K/S364K/E357Q; S364K/E357Q : L368D/K370S; L368D/K370S : S364K; L368E/K370S : S364K; T411E/K360E/Q362E : D401K; L368D/K370S : S364K/E357L 및 K370S : S364K/E357Q 중 하나의 비대칭 변이체 세트를 포함한다. 예시적인 구현예에서, 상기 비대칭 변이체 세트는 S364K/E357Q : L368D/K370S이다.
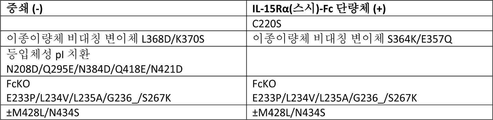
예시적인 구현예에서, "Fab X ncIL-15/Rα" 형식 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) 제2 단량체로서, N-말단에서 C-말단으로, i) IL-15Rα(스시) 도메인; ii) 힌지; iii) CH2-CH3을 포함하는 제1 변이체 Fc 도메인을 포함하는 제2 단량체; c) VL-CL을 포함하는 경쇄를 포함하는 제3 단량체; 및 d) IL-15 변이체를 포함하는 제4 단량체를 포함한다. 상기 VH 및 VL은, 각각, 인간 LAG-3 항원 결합 도메인을 형성하는 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 상기와 같은 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 상기 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 변이체 N208D/Q295E/N384D/Q418E/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따른다. 일부 구현예에서, 상기 제2 단량체의 힌지는 아미노산 치환 C220S를 포함하며, 여기서 넘버링은 EU 넘버링에 따른다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428:/N434S를 추가로 포함한다.
또 다른 양태에서, 본원에는 "Fab X dsIL-15/Rα" 형식 이종이량체 단백질이 제공된다. 상기와 같은 "Fab X dsIL-15/Rα" 형식 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) 제2 단량체로서, N-말단에서 C-말단으로, i) 시스테인 잔기 대신 치환된 아미노산을 포함하는 변이체 IL-15Rα(스시) 도메인; ii) 제1 도메인 링커; 및 iii) CH2-CH3을 포함하는 제1 변이체 Fc 도메인을 포함하는 제2 단량체; c) N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체; 및 d) 시스테인 잔기 대신 치환된 아미노산을 포함하는 IL-15 변이체를 포함하는 제4 단량체를 포함한다. 나아가, 상기 변이체 IL-15Rα(스시) 도메인의 시스테인 잔기와 IL-15 변이체의 시스테인 잔기는 다이설파이드 결합을 형성하고, 상기 VH 및 VL은, 각각, 인간 LAG-3 항원 결합 도메인을 형성하는 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 일부 구현예에서, 상기 제1 도메인 링커는 항체 힌지이다.
"Fab X dsIL-15/Rα" 형식 이종이량체 단백질의 일부 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 EU 넘버링에 따라 S267K/L368D/K370S : S267K/S364K/E357Q; S364K/E357Q : L368D/K370S; L368D/K370S : S364K; L368E/K370S : S364K; T411E/K360E/Q362E : D401K; L368D/K370S : S364K/E357L 및 K370S : S364K/E357Q 중 하나의 비대칭 변이체 세트를 포함한다. 예시적인 구현예에서, 상기 비대칭 변이체 세트는 S364K/E357Q : L368D/K370S이다.
예시적인 구현예에서, "Fab X dsIL-15/Rα" 형식 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) 제2 단량체로서, N-말단에서 C-말단으로, i) 시스테인 잔기 대신 치환된 아미노산을 포함하는 변이체 IL-15Rα(스시) 도메인; ii) 힌지; 및 iii) CH2-CH3을 포함하는 제1 변이체 Fc 도메인을 포함하는 제2 단량체; c) N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체; 및 d) 시스테인 잔기 대신 치환된 아미노산을 포함하는 IL-15 변이체를 포함하는 제4 단량체를 포함한다. 나아가, 상기 변이체 IL-15Rα(스시) 도메인의 시스테인 잔기와 IL-15 변이체의 시스테인 잔기는 다이설파이드 결합을 형성하고, 상기 VH 및 VL은, 각각, 인간 LAG-3 항원 결합 도메인을 형성하는 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 상기와 같은 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 상기 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 변이체 N208D/Q295E/N384D/Q418E/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따른다. 특정 구현예에서, 상기 제2 단량체의 힌지는 아미노산 치환 C220S를 포함하며, 여기서 넘버링은 EU 넘버링에 따른다. 일부 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428:/N434S를 추가로 포함한다.
하나의 양태에서, 본원에는 "mAb-scIL-15/Rα" 형식 이종이량체 단백질이 제공된다. "mAb-scIL-15/Rα" 형식 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3-도메인 링커-IL-15Rα(스시) 도메인-도메인 링커-IL-15 변이체를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함한다. 나아가, 상기 제1 단량체의 VH와 제3 단량체의 VL은 제1 인간 LAG-3 결합 도메인을 형성하고, 상기 제2 단량체의 VH와 제4 단량체의 VL은 제2 인간 LAG-3 결합 도메인을 형성한다.
"mAb-scIL-15/Rα" 형식 이종이량체 단백질의 일부 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 EU 넘버링에 따라 S267K/L368D/K370S : S267K/S364K/E357Q; S364K/E357Q : L368D/K370S; L368D/K370S : S364K; L368E/K370S : S364K; T411E/K360E/Q362E : D401K; L368D/K370S : S364K/E357L 및 K370S : S364K/E357Q 중 하나의 비대칭 변이체 세트를 포함한다. 예시적인 구현예에서, 상기 비대칭 변이체 세트는 S364K/E357Q : L368D/K370S이다.
"mAb-scIL-15/Rα" 형식 이종이량체 단백질의 일부 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하며, 여기서 넘버링은 EU 넘버링에 따른다. 특정 구현예에서, a) 상기 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 N208D/Q295E/N384D/Q418D/N421D를 추가로 포함하고, 상기 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 Q196K/I199T/P271R/P228R/N276K를 추가로 포함하거나; b) 상기 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 N208D/Q295E/N384D/Q418D/N421D를 추가로 포함하거나; 또는 c) 상기 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 Q196K/I199T/P271R/P228R/N276K를 추가로 포함하며, 여기서 넘버링은 EU 넘버링에 따른다.
"mAb-scIL-15/Rα" 형식 이종이량체 단백질의 일부 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하며, 여기서 넘버링은 EU 넘버링에 따른다. 상기와 같은 구현예에서, a) 상기 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 Q196K/I199T/P271R/P228R/N276K를 추가로 포함하고, 상기 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 N208D/Q295E/N384D/Q418D/N421D를 추가로 포함하거나; b) 상기 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 Q196K/I199T/P271R/P228R/N276K를 추가로 포함하거나; 또는 c) 상기 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 N208D/Q295E/N384D/Q418D/N421D를 추가로 포함하며, 여기서 넘버링은 EU 넘버링에 따른다.
"mAb-scIL-15/Rα" 형식 이종이량체 단백질의 일부 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428:/N434S를 추가로 포함한다.
또 다른 양태에서, 본원에는 "mAb-ncIL-15/Rα" 형식 이종이량체 단백질이 제공된다. 상기와 같은 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3-도메인 링커-IL-15Rα(스시) 도메인을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); c) IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체를 포함한다. 상기 제1 단량체의 VH와 제4 단량체의 VL은 제1 인간 LAG-3 결합 도메인을 형성하고, 상기 제2 단량체의 VH와 제5 단량체의 VL은 제2 인간 LAG-3 결합 도메인을 형성한다.
"mAb-ncIL-15/Rα" 형식 이종이량체 단백질의 일부 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 EU 넘버링에 따라 S267K/L368D/K370S : S267K/S364K/E357Q; S364K/E357Q : L368D/K370S; L368D/K370S : S364K; L368E/K370S : S364K; T411E/K360E/Q362E : D401K; L368D/K370S : S364K/E357L 및 K370S : S364K/E357Q 중 하나의 비대칭 변이체 세트를 포함한다. 예시적인 구현예에서, 상기 비대칭 변이체 세트는 S364K/E357Q : L368D/K370S이다.
"mAb-ncIL-15/Rα" 형식 이종이량체 단백질의 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하며, 여기서 넘버링은 EU 넘버링에 따른다. 일부 구현예에서, a) 상기 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 N208D/Q295E/N384D/Q418D/N421D를 추가로 포함하고, 상기 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 Q196K/I199T/P271R/P228R/N276K를 추가로 포함하거나; b) 상기 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 N208D/Q295E/N384D/Q418D/N421D를 추가로 포함하거나; 또는 c) 상기 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 Q196K/I199T/P271R/P228R/N276K를 추가로 포함하며, 여기서 넘버링은 EU 넘버링에 따른다.
"mAb-ncIL-15/Rα" 형식 이종이량체 단백질의 또 다른 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하며, 여기서 넘버링은 EU 넘버링에 따른다. 특정 구현예에서, a) 상기 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 Q196K/I199T/P271R/P228R/N276K를 추가로 포함하고, 상기 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 N208D/Q295E/N384D/Q418D/N421D를 추가로 포함하거나; b) 상기 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 Q196K/I199T/P271R/P228R/N276K를 추가로 포함하거나; 또는 c) 상기 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 N208D/Q295E/N384D/Q418D/N421D를 추가로 포함하며, 여기서 넘버링은 EU 넘버링에 따른다.
특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428:/N434S를 추가로 포함한다.
또 다른 양태에서, 본원에는 "mAb-dsIL-15/Rα" 이종이량체 단백질이 제공된다. 상기와 같은 "mAb-dsIL-15/Rα" 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3-도메인 링커-변이체 IL-15Rα(스시) 도메인을 포함하는 제2 단량체(여기서 변이체 IL-15Rα(스시) 도메인은 시스테인 잔기 대신 치환된 아미노산이고, CH2-CH3은 제2 변이체 Fc 도메인임); c) 시스테인 잔기 대신 치환된 아미노산을 포함하는 IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체를 포함한다. 상기 변이체 IL-15Rα(스시) 도메인의 시스테인 잔기와 IL-15 변이체의 시스테인 잔기는 다이설파이드 결합을 형성하고, 상기 제1 단량체의 VH와 제4 단량체의 VL은 제1 인간 LAG-3 결합 도메인을 형성하고, 상기 제2 단량체의 VH와 제5 단량체의 VL은 제2 인간 LAG-3 결합 도메인을 형성한다.
일부 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 EU 넘버링에 따라 S267K/L368D/K370S : S267K/S364K/E357Q; S364K/E357Q : L368D/K370S; L368D/K370S : S364K; L368E/K370S : S364K; T411E/K360E/Q362E : D401K; L368D/K370S : S364K/E357L 및 K370S : S364K/E357Q 중 하나의 비대칭 변이체 세트를 포함한다. 예시적인 구현예에서, 상기 비대칭 변이체 세트는 S364K/E357Q : L368D/K370S이다.
"mAb-dsIL-15/Rα" 이종이량체 단백질의 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하며, 여기서 넘버링은 EU 넘버링에 따른다. 일부 구현예에서, a) 상기 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 N208D/Q295E/N384D/Q418D/N421D를 추가로 포함하고, 상기 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 Q196K/I199T/P271R/P228R/N276K를 추가로 포함하거나; b) 상기 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 N208D/Q295E/N384D/Q418D/N421D를 추가로 포함하거나; 또는 c) 상기 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 Q196K/I199T/P271R/P228R/N276K를 추가로 포함하며, 여기서 넘버링은 EU 넘버링에 따른다.
"mAb-dsIL-15/Rα" 이종이량체 단백질의 또 다른 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하며, 여기서 넘버링은 EU 넘버링에 따른다. 특정 구현예에서, a) 상기 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 Q196K/I199T/P271R/P228R/N276K를 추가로 포함하고, 상기 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 N208D/Q295E/N384D/Q418D/N421D를 추가로 포함하거나; b) 상기 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 Q196K/I199T/P271R/P228R/N276K를 추가로 포함하거나; 또는 c) 상기 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 N208D/Q295E/N384D/Q418D/N421D를 추가로 포함하며, 여기서 넘버링은 EU 넘버링에 따른다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428:/N434S를 추가로 포함한다.
하나의 양태에서, 본원에는 "central-IL-15/Rα" 형식 이종이량체 단백질이 제공된다. 상기와 같은 "central-IL-15/Rα" 형식 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-CH1-도메인 링커-IL-15 변이체-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-CH1-도메인 링커-IL-15Rα(스시) 도메인-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함한다. 상기 제1 단량체의 VH와 제3 단량체의 VL은 제1 인간 LAG-3 결합 도메인을 형성하고, 상기 제2 단량체의 VH와 제4 단량체의 VL은 제2 인간 LAG-3 결합 도메인을 형성한다.
"central-IL-15/Rα" 형식 이종이량체 단백질의 일부 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 EU 넘버링에 따라 S267K/L368D/K370S : S267K/S364K/E357Q; S364K/E357Q : L368D/K370S; L368D/K370S : S364K; L368E/K370S : S364K; T411E/K360E/Q362E : D401K; L368D/K370S : S364K/E357L 및 K370S : S364K/E357Q 중 하나의 비대칭 변이체 세트를 포함한다. 예시적인 구현예에서, 상기 비대칭 변이체 세트는 S364K/E357Q : L368D/K370S이다.
예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q를 포함하고, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 상기 제1 변이체 Fc 도메인은 pI 치환 Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따른다.
"central-IL-15/Rα" 형식 이종이량체 단백질의 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 L368D/K370S를 포함하고, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 상기 제2 단량체의 제2 변이체 Fc 도메인은 pI 치환 Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따른다. "central-IL-15/Rα" 형식 이종이량체 단백질의 일부 구현예에서, 상기 제1 단량체의 힌지와 제2 단량체의 힌지는 각각 아미노산 치환 C220S를 포함하며, 여기서 넘버링은 EU 넘버링에 따른다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428:/N434S를 추가로 포함한다.
또 다른 양태에서, 본원에는 "central-scIL-15/Rα" 형식 이종이량체 단백질이 제공된다. 상기와 같은 "central-scIL-15/Rα" 형식 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-CH1-도메인 링커-IL-15Rα(스시) 도메인-도메인 링커-IL-15 변이체-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함한다. 상기 제1 단량체의 VH와 제3 단량체의 VL은 제1 인간 LAG-3 결합 도메인을 형성하고, 상기 제2 단량체의 VH와 제4 단량체의 VL은 제2 인간 LAG-3 결합 도메인을 형성한다.
"central-scIL-15/Rα" 형식 이종이량체 단백질의 일부 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 EU 넘버링에 따라 S267K/L368D/K370S : S267K/S364K/E357Q; S364K/E357Q : L368D/K370S; L368D/K370S : S364K; L368E/K370S : S364K; T411E/K360E/Q362E : D401K; L368D/K370S : S364K/E357L 및 K370S : S364K/E357Q 중 하나의 비대칭 변이체 세트를 포함한다. 예시적인 구현예에서, 상기 비대칭 변이체 세트는 S364K/E357Q : L368D/K370S이다.
예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 상기 제1 변이체 Fc 도메인은 pI 변이체 Q295E/N384D/Q418E/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따른다. 일부 구현예에서, 상기 제1 단량체의 힌지는 아미노산 치환 C220S를 포함하며, 여기서 넘버링은 EU 넘버링에 따른다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428:/N434S를 추가로 포함한다.
특정 구현예에서, 본원에 제공된 임의의 이종이량체 단백질의 VH 및 VL은 도 12 및 도 13의 임의의 LAG-3 항원 결합 도메인의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 예시적인 구현예에서, 상기 LAG-3 항원 결합 도메인은 2A11_H1.144_L2.142 및 7G8_H3.30_L1.34이다.
일부 구현예에서, 본원에 제공된 이종이량체 단백질의 IL-15 변이체는 N1D, N4D, D8N, D30N, D61N, E64Q, N65D, Q108E, N4D/N65D, D30N/N65D 및 D30N/E64Q/N65D로 이루어지는 군으로부터 선택되는 아미노산 치환(들)을 포함한다. 예시적인 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함한다.
하나의 양태에서, 본원에는 본원에 개시된 임의의 이종이량체 단백질 및 약학적으로 허용 가능한 담체를 포함하는 약학적 조성물이 제공된다.
또 다른 양태에서, 본원에는 본원에 개시된 이종이량체 단백질 또는 약학적 조성물 중 어느 하나를 환자에게 투여하는 것을 포함하는, 이를 필요로 하는 환자를 치료하는 방법이 제공된다. 일부 구현예에서, 상기 방법은 항체를 투여하는 것을 추가로 포함하며, 여기서 항체는 항-PD-1 항체, 항-PD-L1 항체, 항-CTLA-4 항체, 항-TIM-3 항체 또는 항-TIGIT 항체이다.
또 다른 양태에서, 본원에는 본원에 개시된 임의의 이종이량체 단백질을 인코딩하는 하나 이상의 핵산을 포함하는 핵산 조성물, 상기 핵산을 포함하는 발현 벡터, 상기 핵산 또는 발현 벡터를 포함하는 숙주세포가 제공된다. 또한, 본원에는 적합한 조건 하에서 숙주세포를 배양하고 이종이량체 단백질을 회수함으로써, 본 발명의 이종이량체 단백질을 제조하는 방법이 제공된다.
도 1은, PD-1을 발현하는 종양 반응성 종양 침윤 림프구에 대한 LAG-3 표적화 IL-15/Rα-Fc 융합 단백질의 선택성, 및 상기 융합 단백질과 PD-1 차단 항체의 조합을 도시한 것이다.
도 2a 및 도 2b는, IL-15 및 이의 수용체의 서열을 도시한 것이다.
도 3은, 임상 개발의 용이성을 위해 둘 모두에 결합하는 항원 결합 도메인의 개발을 용이하게 하는, 인간 및 시노몰구스 원숭이(예측)에 대한 LAG-3의 서열을 도시한 것이다.
도 4a 내지 도 4e는, 유용한 Fc 이종이량체화 변이체 세트(비대칭 변이체 및 pI 변이체를 포함함)의 쌍을 도시한 것이다. 상응하는 "단량체 2" 변이체가 없는 변이체가 존재하며; 이는 어느 쪽의 단량체에도 단독으로 사용될 수 있는 pI 변이체이다.
도 5는, 등입체성(isosteric) 변이체 항체 불변 영역 및 이의 각각의 치환의 목록을 도시한 것이다. pI_(-)는 보다 낮은 pI를 갖는 변이체를 나타내고, pI_(+)는 보다 높은 pI를 갖는 변이체를 나타낸다. 이는 본 발명의 다른 이종이량체화 변이체 (및 또한 본원에 개괄된 바와 같은 다른 변이체 유형)와 선택적으로 및 독립적으로 조합될 수 있다.
도 6은, FcγR 결합을 절제하는 유용한 절제 변이체(때때로 "녹아웃(knock out)" 또는 "KO" 변이체로 지칭됨)를 도시한 것이다. 일반적으로, 절제 변이체는 두 가지 단량체 모두에서 발견되지만, 일부 경우에 하나의 단량체에만 존재할 수도 있다.
도 7a 내지 도 7f는, 본 발명의 LAG-3 표적화 IL-15/Rα-Fc 융합 단백질의 "비(非)사이토카인"/"비(非)Fv" 구성요소의 특히 유용한 구현예를 보여준다.
도 8은, IL-15/Rα-Fc 융합 단백질에 사용되는 다수의 예시적인 가변 길이 링커를 도시한 것이다. 일부 구현예에서, 이러한 링커는 IL-15 및/또는 IL-15Rα(스시)의 C-말단을 Fc 영역의 N-말단에 연결하는 데 사용된다. 일부 구현예에서, 이러한 링커는 IL-15를 IL-15Rα(스시)에 융합시키는 데 사용된다.
도 9a 내지 도 9c는, 구성요소로서 하나 이상의 scFv를 이용하는 이종이량체 항체의 pI를 증가시키거나 감소시키는 데 사용되는 다수의 하전된 scFv 링커를 도시한 것이다. (+H) 양성 링커가 특히 본원에서 사용된다. 단일 전하를 갖는 하나의 선행 기술 scFv 링커는, 문헌[Whitlow et al., Protein Engineering 6(8):989-995 (1993)]에 "Whitlow"로 언급되어 있다. 이러한 링커가 scFv에서 응집을 감소시키고 단백질 분해 안정성을 증강시키는 데 사용되었다는 점에 주목해야 한다.
도 10은, 사이토카인 서열(예를 들어, IL-15 및/또는 IL-15Rα(스시)) 또는 VH를 갖지 않고, 추가로 도 11에 도시된 경쇄 백본을 제외한, 인간 IgG1을 기반으로 하는 몇 가지 유용한 LAG-3 표적화 IL-15/Rα-Fc 융합체 형식 백본의 서열을 보여준다. 백본 1은 인간 IgG1(356E/358M 알로타입(allotype))을 기반으로 하며, S364K/E357Q : L368D/K370S 비대칭 변이체, C220S, L368D/K370S 비대칭 변이체를 갖는 사슬 상의 Q295E/N384D/Q418E/N421D pI 변이체, 및 양쪽 사슬 상의 E233P/L234V/L235A/G236del/S267K 절제 변이체를 포함한다. 백본 2는 인간 IgG1(356E/358M 알로타입)을 기반으로 하며, S364K/E357Q : L368D/K370S 비대칭 변이체, L368D/K370S 비대칭 변이체를 갖는 사슬 상의 N208D/Q295E/N384D/Q418E/N421D pI 변이체, S364K/E357Q 변이체를 갖는 사슬 상의 C220S, 및 양쪽 사슬 상의 E233P/L234V/L235A/G236del/S267K 절제 변이체를 포함한다. 백본 3은 인간 IgG1(356E/358M 알로타입)을 기반으로 하며, S364K/E357Q : L368D/K370S 비대칭 변이체, L368D/K370S 비대칭 변이체를 갖는 사슬 상의 N208D/Q295E/N384D/Q418E/N421D pI 변이체, S364K/E357Q 변이체를 갖는 사슬 상의 Q196K/I199T/P217R/P228R/N276K pI 변이체, 및 양쪽 사슬 상의 E233P/L234V/L235A/G236del/S267K 절제 변이체를 포함한다. 상기와 같은 백본 서열은, 예를 들어 본원에 기재된 "scIL-15/Rα X Fab" 형식 이종이량체 단백질에 포함될 수 있다. ). 일부 구현예에서, "scIL-15/Rα X Fab" 형식 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(힌지)-CH2-CH3을 포함하는 제1 단량체(여기서 힌지-CH2-CH3은 도 10의 임의의 백본 서열의 "사슬 2"의 아미노산 서열(서열번호 XXX-XXX)을 가짐); b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 VH는 가변 중쇄 도메인이고, CH1-힌지-CH2-CH3은 도 10의 임의의 백본 서열의 사슬 1의 아미노산 서열(서열번호 XXX-XXX)을 가짐); 및 c) N-말단에서 C-말단으로, VL-VC를 포함하는 경쇄(여기서 VL은 가변 경쇄 도메인이고, VC는 도 11의 "불변 경쇄-카파" 또는 "불변 경쇄-람다"의 서열(서열번호 XXX-XXX)을 가짐)를 포함한다. 예시적인 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함한다. 예시적인 구현예에서, 상기 VH 및 VL은, 각각, 도 12 및 도 13a 내지 도 13c에 제공된 임의의 LAG-3 ABD의 가변 중쇄 도메인 및 가변 경쇄 도메인이다.
특정 구현예에서, 이러한 서열은 356D/358L 알로타입일 수 있다. 다른 구현예에서, 이러한 서열은 N297A 또는 N297S 치환 중 어느 하나를 포함할 수 있다. 일부 다른 구현예에서, 이러한 서열은 M428L/N434S Xtend 돌연변이를 포함할 수 있다. 또 다른 구현예에서, 이러한 서열은 대신 인간 IgG4를 기반으로 하며, 양쪽 사슬 상에 S228P(EU 넘버링, 이는 Kabat에서 S241P임) 변이체(이는 당업계에 공지된 바와 같이 Fab 아암(arm) 교환을 제거함)를 포함한다. 추가의 구현예에서, 이러한 서열은 대신 인간 IgG2를 기반으로 할 수 있다. 나아가, 이러한 서열은 대신 도면에 도시된 다른 비대칭 변이체, pI 변이체 및 절제 변이체를 이용할 수 있다.
당업자가 이해하고 하기에 개괄되는 바와 같이, 이러한 서열은 도 21에 개략적으로 도시된 바와 같이, 비제한적으로 scIL-15/Rα, ncIL-15/Rα 및 dsIL-15Rα를 포함하는, 본원에 개괄된 임의의 IL-15와 IL-15Rα(스시)의 쌍과 함께 사용될 수 있다. 나아가, 당업자가 이해하고 하기에 개괄되는 바와 같이, 임의의 IL-15 및/또는 IL-15Rα(스시) 변이체가 이러한 백본에 혼입될 수 있다. 나아가, 당업자가 이해하고 하기에 개괄되는 바와 같이, 이러한 서열은 scFv 또는 Fab을 포함하는, 본원에 개괄된 임의의 VH와 VL의 쌍과 함께 사용될 수 있다.
이러한 각각의 백본 내에는, (본원에 정의된 바와 같이) 인용된 서열과 90%, 95%, 98% 및 99% 동일하고/하거나 (당업자가 이해하는 바와 같이, 도면의 "모(parent)" 서열과 비교하여) 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개 또는 10개의 추가 아미노산 치환을 함유하는(모 인간 IgG1 (또는 백본에 따라, IgG2 또는 IgG4)과 비교하여 이미 다수의 아미노산 변형을 함유하는) 서열이 포함되어 있다. 즉, 인용된 백본은 이러한 도면의 백본 내에 함유된 비대칭 변이체, pI 변이체 및 절제 변이체에 더하여, 추가의 아미노산 변형(일반적으로 아미노산 치환)을 함유할 수 있다.
도 11은, 본 발명의 LAG-3 표적화 IL-15/Rα-Fc 융합 단백질에 사용되는 경쇄의 "비Fv" 백본(즉, 불변 경쇄)을 도시한 것이다.
도 12는, 선택된 수의 항-LAG-3 항체 결합 도메인에 대한 가변 영역 서열을 도시한 것이다. CDR에는 밑줄이 그어져 있다. 본원에 표시되고, CDR을 함유하는 본원의 모든 서열에 대하여 적용되는 바와 같이, CDR 위치의 정확한 식별은 표 2에 제시된 바와 같이 사용되는 넘버링에 따라 약간 상이할 수 있기 때문에, 밑줄 그어진 CDR뿐 아니라 다른 넘버링 시스템을 사용하여 VH 및 VL 도메인 내에 포함되는 CDR도 본원에 포함된다. 나아가, 도면의 모든 서열에 대하여, 이러한 VH 및 VL 서열은 scFv 형식 또는 Fab 형식 중 어느 하나로 사용될 수 있다.
도 13a 내지 도 13c는, 본 발명의 LAG-3 표적화 IL-15/Rα-Fc 융합 단백질에 사용될 수 있는 추가의 LAG-3 ABD의 가변 영역을 도시한 것이다. CDR에는 밑줄이 그어져 있다. 본원에 표시되고, CDR을 함유하는 본원의 모든 서열에 대하여 적용되는 바와 같이, CDR 위치의 정확한 식별은 표 2에 제시된 바와 같이 사용되는 넘버링에 따라 약간 상이할 수 있기 때문에, 밑줄 그어진 CDR뿐 아니라 다른 넘버링 시스템을 사용하여 VH 및 VL 도메인 내에 포함되는 CDR도 본원에 포함된다. 나아가, 도면의 모든 서열에 대하여, 이러한 VH 및 VL 서열은 scFv 형식 또는 Fab 형식 중 어느 하나로 사용될 수 있다.
도 14는, 조작된 다이설파이드 결합 쌍의 위치를 보여주는 IL-15/Rα 이종이량체의 구조 모델을 도시한 것이다.
도 15는, 시스테인 잔기를 조작하기 위한 스캐폴드로서 작용하도록 C-말단에서 추가의 잔기로 조작된 예시적인 IL-15Rα(스시) 변이체의 서열을 도시한 것이다.
도 16은, 시스테인으로 조작된 IL-15Rα(스시) 변이체와 공유결합형 다이설파이드 결합을 형성하기 위해 시스테인으로 조작된 예시적인 IL-15 변이체의 서열을 도시한 것이다.
도 17은, 시스테인으로 조작된 IL-15 변이체와 공유결합형 다이설파이드 결합을 형성하기 위해 시스테인으로 조작된 예시적인 IL-15Rα(스시) 변이체의 서열을 도시한 것이다.
도 18은, IL-15Rα, IL-2Rβ 및 공통 감마 사슬과 복합체화된 IL-15의 구조를 도시한 것이다. 역가를 감소시키기 위해 설계된 치환의 위치가 제시되어 있다.
도 19a 내지 도 19c는, 역가 감소를 위해 조작된 예시적인 IL-15 변이체의 서열을 도시한 것이다. 각각의 이러한 변이체 IL-15 서열 내에는, (본원에 정의된 바와 같이) 인용된 서열과 90%, 95%, 98% 및 99% 동일하고/하거나 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개 또는 10개의 추가의 아미노산 치환을 함유하는 서열이 포함되어 있다. 비제한적인 예에서, 인용된 서열은 도 14, 도 16 및 도 17에 제시된 바와 같이 공유결합형 다이설파이드 결합의 형성에 기여하는 것들과 같은 추가의 아미노산 변형을 함유할 수 있다.
도 20은, 변이체 IL-15/Rα-Fc 융합 단백질에 의한 NK세포 및 CD8+ T세포 증식의 유도에 대한 EC50, 및 야생형인 XENP20818과 비교한 EC50의 감소 배수를 도시한 것이다. 이러한 융합 단백질은 LAG-3 ABD를 함유하지 않는다.
도 21a 내지 도 21k는, 본 발명의 LAG-3 표적화 IL-15/Rα-Fc 융합 단백질에 대한 몇 가지 형식을 도시한 것이다. "scIL-15/Rα x scFv" 형식(도 21a)은 가변 길이 링커에 의해 IL-15에 융합된 IL-15Rα(스시)("scIL-15/Rα"로 지칭됨)(이는 이후에 이종이량체 Fc 영역의 N-말단에 융합됨)와, 이종이량체 Fc의 다른 쪽에 융합된 scFv를 포함한다. "scFv x ncIL-15/Rα" 형식(도 21b)은 이종이량체 Fc 영역의 N-말단에 융합된 scFv와 이종이량체 Fc의 다른 쪽에 융합된 IL-15Rα(스시)를 포함하지만, IL-15는 비공유결합형 IL-15/Rα 복합체가 형성되도록 별도로 트랜스펙션된다. "scFv x dsIL-15/Rα" 형식(도 21c)은 "scFv x ncIL-15/Rα" 형식과 동일하지만, 여기서 IL-15Rα(스시)와 IL-15는 조작된 시스테인의 결과로서 공유결합으로 연결된다. "scIL-15/Rα x Fab" 형식(도 21d)은 가변 길이 링커에 의해 IL-15에 융합된 IL-15Rα(스시)("scIL-15/Rα"로 지칭됨)(이는 이후에 이종이량체 Fc 영역의 N-말단에 융합됨)와, 이종이량체 Fc의 다른 쪽에 융합된 가변 중쇄(VH)를 포함하며, 상응하는 경쇄는 VH와 Fab을 형성하도록 별도로 트랜스펙션된다. "ncIL-15/Rα x Fab" 형식(도 21e)은 이종이량체 Fc 영역의 N-말단에 융합된 VH와 이종이량체 Fc의 다른 쪽에 융합된 IL-15Rα(스시)를 포함하며, 상응하는 경쇄는 VH와 Fab을 형성하도록 별도로 트랜스펙션되고, IL-15는 비공유결합형 IL-15/Rα 복합체가 형성되도록 별도로 트랜스펙션된다. "dsIL-15/Rα x Fab" 형식(도 21f)은 "ncIL-15/Rα x Fab" 형식과 동일하지만, 여기서 IL-15Rα(스시)와 IL-15는 조작된 시스테인의 결과로서 공유결합으로 연결된다. "mAb-scIL-15/Rα" 형식(도 21g)은 제1 이종이량체 Fc와 제2 이종이량체 Fc의 N-말단에 융합된 VH와, IL-15Rα(스시)에 융합된 IL-15(이는 이후에 이종이량체 Fc 영역 중 하나의 C-말단에 추가로 융합됨)를 포함하며, 상응하는 경쇄는 VH와 Fab을 형성하도록 별도로 트랜스펙션된다. "mAb-ncIL-15/Rα" 형식(도 21h)은 제1 이종이량체 Fc와 제2 이종이량체 Fc의 N-말단에 융합된 VH와, 이종이량체 Fc 영역 중 하나의 C-말단에 융합된 IL-15Rα(스시)를 포함하며, 상응하는 경쇄는 VH와 Fab을 형성하도록 별도로 트랜스펙션되고, IL-15는 비공유결합형 IL-15/Rα 복합체가 형성되도록 별도로 트랜스펙션된다. "mAb-dsIL-15/Rα" 형식(도 21i)은 "mAb-ncIL-15/Rα" 형식과 동일하지만, 여기서 IL-15Rα(스시)와 IL-15는 조작된 시스테인의 결과로서 공유결합으로 연결된다. "central-IL-15/Rα" 형식(도 21j)은 IL-15의 N-말단에 재조합적으로 융합된 VH(이는 이후에 이종이량체 Fc의 한쪽에 추가로 융합됨)와, IL-15Rα(스시)의 N-말단에 재조합적으로 융합된 VH(이는 이후에 이종이량체 Fc의 다른 한쪽에 추가로 융합됨)를 포함하며, 상응하는 경쇄는 VH와 Fab을 형성하도록 별도로 트랜스펙션된다. "central-scIL-15/Rα" 형식(도 21k)은 IL-15에 융합된 IL-15Rα(스시)의 N-말단에 융합된 VH(이는 이후에 이종이량체 Fc의 한쪽에 추가로 융합됨)와, 이종이량체 Fc의 다른 한쪽에 융합된 VH를 포함하며, 상응하는 경쇄는 VH와 Fab을 형성하도록 별도로 트랜스펙션된다.
도 22a 및 도 22b는, "scIL-15/Rα x Fab" 형식의 예시적인 LAG-3 표적화 IL-15/Rα-Fc 융합 단백질인 XENP27972 및 XENP27973의 서열을 도시한 것이다. CDR은 볼드체로 표시되어 있다. 본원에 표시되고, CDR을 함유하는 본원의 모든 서열에 대하여 적용되는 바와 같이, CDR 위치의 정확한 식별은 표 2에 제시된 바와 같이 사용되는 넘버링에 따라 약간 상이할 수 있기 때문에, 밑줄 그어진 CDR뿐 아니라 다른 넘버링 시스템을 사용하여 VH 및 VL 도메인 내에 포함되는 CDR도 본원에 포함된다. IL-15 및 IL-15Rα(스시)에는 밑줄이 그어져 있고, 링커에는 이중 밑줄이 그어져 있으며(당업자가 이해하는 바와 같이, 링커는 다른 링커로 대체될 수 있으며, 이 중 일부는 도면에 도시되어 있음), 슬래시(/)는 IL-15, IL-15Rα, 링커, 가변 영역 및 불변/Fc 영역 사이의 경계(들)을 나타낸다.
도 23은, 절제 변이체 (E233P/L234V/L235A/G236del/S267K, "IgG1_PVA_/S267k")를 갖는 2가 항-PD-1 mAb인 XENP16432의 서열을 도시한 것이다. CDR에는 밑줄이 그어져 있다. 본원에 표시되고, CDR을 함유하는 본원의 모든 서열에 대하여 적용되는 바와 같이, CDR 위치의 정확한 식별은 표 2에 제시된 바와 같이 사용되는 넘버링에 따라 약간 상이할 수 있기 때문에, 밑줄 그어진 CDR뿐 아니라 다른 넘버링 시스템을 사용하여 VH 및 VL 도메인 내에 포함되는 CDR도 본원에 포함된다.
도 24a 및 도 24b는, 표시된 시험 물품의 첫 번째 투여 후, 6일차(도 24a) 및 10일차(도 24b)에서의 PBMC 이식된 NSG 마우스의 전혈 중 CD8+ T세포 수를 도시한 것이다.
도 25a 및 도 25b는, 표시된 시험 물품의 첫 번째 투여 후, 6일차(도 25a) 및 10일차(도 25b)에서의 PBMC 이식된 NSG 마우스의 전혈 중 CD4+ T세포 수를 도시한 것이다.
도 26a 및 도 26b는, 표시된 시험 물품의 첫 번째 투여 후, 6일차(도 26a) 및 10일차(도 26b)에서의 PBMC 이식된 NSG 마우스의 전혈 중 CD45+ T세포 수를 도시한 것이다.
도 27a 및 도 27b는, 표시된 시험 물품의 첫 번째 투여 후, 6일차(도 27a) 및 10일차(도 27b)에서의 PBMC 이식된 NSG 마우스의 전혈 중 CD16+CD56+ NK세포 수를 도시한 것이다.
도 28은, 표시된 시험 물품의 투여 후, PBMC 이식된 NSG 마우스의 체중 변화(초기 체중의 백분율로서)를 도시한 것이다.
도 29a 및 도 29b는, 양쪽 Fc 도메인에 M428L/N434S 변이체를 포함하는 XENP27977 및 XENP27978의 서열을 도시한 것이다.
도 30은, 세포 증식률(CFSE 희석법에 기반하여 결정됨)로 표시되는, LAG-3 표적화 IL-15/Rα-Fc 융합체 (및 대조군)에 의한 CD8+ T세포(도 30a) 및 CD4+ T세포(도 30b) 증식의 유도를 도시한 것이다. 데이터는, LAG-3 표적화 IL-15/Rα-Fc 융합체가 비(非)표적화 IL-15(D30N/E64Q/N65D)/Rα-Fc 융합체 (및 대조군인 RSV 표적화 IL-15/Rα-Fc 융합체)에 비해 CD8+ T세포의 증식을 유도하는 데 더 강력함을 보여준다.
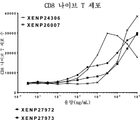
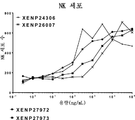
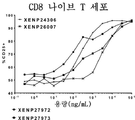
도 31은, 세포 증식률(CFSE 희석법에 기반하여 결정됨)로 표시되는, LAG-3 표적화 IL-15/Rα-Fc 융합체 (및 대조군)에 의한 CD8 기억T세포(도 31a) 및 CD8 나이브(naive) T세포(도 31b) 증식의 유도를 도시한 것이다. 데이터는, LAG-3 표적화 IL-15/Rα-Fc 융합체가 비표적화 IL-15(D30N/E64Q/N65D)/Rα-Fc 융합체 (및 대조군인 RSV 표적화 IL-15/Rα-Fc 융합체)에 비해 CD8 기억T세포의 증식을 유도하는 데 훨씬 더 강력함을 보여준다.
도 32는, 세포 수로 표시되는, LAG-3 표적화 IL-15/Rα-Fc 융합체 (및 대조군)에 의한 CD8 기억T세포(도 32a) 및 CD8 나이브 T세포(도 32b) 증식의 유도를 도시한 것이다. 데이터는, LAG-3 표적화 IL-15/Rα-Fc 융합체가 비표적화 IL-15(D30N/E64Q/N65D)/Rα-Fc 융합체 (및 대조군인 RSV 표적화 IL-15/Rα-Fc 융합체)에 비해 CD8 기억T세포를 확장시키는 데 훨씬 더 강력함을 보여준다.
도 33은, 세포 증식률(CFSE 희석법에 기반하여 결정됨)로 표시되는, LAG-3 표적화 IL-15/Rα-Fc 융합체 (및 대조군)에 의한 CD4 기억T세포(도 33a) 및 CD4 나이브 T세포(도 33b) 증식의 유도를 도시한 것이다. 데이터는, LAG-3 표적화 IL-15/Rα-Fc 융합체가 비표적화 IL-15(D30N/E64Q/N65D)/Rα-Fc 융합체 (및 대조군인 RSV 표적화 IL-15/Rα-Fc 융합체)에 비해 CD4 기억T세포를 확장시키는 데 더 강력함을 보여준다.
도 34는, 세포 수로 표시되는, LAG-3 표적화 IL-15/Rα-Fc 융합체 (및 대조군)에 의한 CD4 기억T세포(도 34a) 및 CD4 나이브 T세포(도 34b) 증식의 유도를 도시한 것이다.
도 35는, 세포 증식률(CFSE 희석법에 기반하여 결정됨)(도 35a) 및 세포 수(도 35b)로 표시되는, LAG-3 표적화 IL-15/Rα-Fc 융합체 (및 대조군)에 의한 NK세포 증식의 유도를 도시한 것이다.
도 36은, LAG-3 표적화 IL-15/Rα-Fc 융합체 (및 대조군)와 함께 인큐베이션한 후, CD8 기억T세포의 CD25 발현율(도 36a), CD8 나이브 T세포의 CD25 발현율(도 36b), CD4 기억T세포의 CD25 발현율(도 36c) 및 CD4 나이브 T세포의 CD25 발현율(도 36d)로 표시되는 CD8+ T세포의 활성화를 도시한 것이다. 데이터는, LAG-3 표적화 IL-15/Rα-Fc 융합체, 특히 XENP27972가 비표적화 IL-15(D30N/E64Q/N65D)/Rα-Fc 융합체 (및 대조군인 RSV 표적화 IL-15/Rα-Fc 융합체)에 비해 CD8 기억T세포 및 CD4 기억T세포 둘 모두에서 CD25를 상향조절함을 보여준다.
도 37은, LAG-3 표적화 IL-15/Rα-Fc 융합체 (및 대조군)와 함께 인큐베이션한 후, CD8 기억T세포에서의 HLA-DR MFI(도 37a), CD8 기억T세포의 HLA-DR 발현율(도 37b), CD8 나이브 T세포에서의 HLA-DR MFI(도 37c) 및 CD8 나이브 T세포의 HLA-DR 발현율(도 37d)로 표시되는 CD8+ T세포의 활성화를 도시한 것이다. 데이터는, LAG-3 표적화 IL-15/Rα-Fc 융합체가 비표적화 IL-15(D30N/E64Q/N65D)/Rα-Fc 융합체 (및 대조군인 RSV 표적화 IL-15/Rα-Fc 융합체)에 비해 CD8 기억T세포에서 HLA-DR를 더 강력하게 상향조절함을 보여준다.
도 38은, LAG-3 표적화 IL-15/Rα-Fc 융합체 (및 대조군)와 함께 인큐베이션한 후, CD4 기억T세포에서의 HLA-DR MFI(도 38a), CD4 기억T세포의 HLA-DR 발현율(도 38b), CD4 나이브 T세포에서의 HLA-DR MFI(도 38c) 및 CD4 나이브 T세포의 HLA-DR 발현율(도 38d)로 표시되는 CD4+ T세포의 활성화를 도시한 것이다.
도 39는, 야생형 IL-15 및 Xtend Fc(M428L/N434S) 변이체를 포함하는 IL-15/Rα-heteroFc 융합체인 XENP22853의 서열을 도시한 것이다. IL-15 및 IL-15Rα(스시)에는 밑줄이 그어져 있고, 링커에는 이중 밑줄이 그어져 있으며(당업자가 이해하는 바와 같이, 링커는 다른 링커로 대체될 수 있으며, 이 중 일부는 도면에 도시되어 있음), 슬래시(/)는 IL-15, IL-15Rα, 링커 및 불변/Fc 영역 사이의 경계(들)을 나타낸다.
도 40은, IL-15(N4D/N65D) 변이체 및 Xtend Fc(M428L/N434S) 변이체를 포함하는 IL-15/Rα-heteroFc 융합체인 XENP24113의 서열을 도시한 것이다. IL-15 및 IL-15Rα(스시)에는 밑줄이 그어져 있고, 링커에는 이중 밑줄이 그어져 있으며(당업자가 이해하는 바와 같이, 링커는 다른 링커로 대체될 수 있으며, 이 중 일부는 도면에 도시되어 있음), 슬래시(/)는 IL-15, IL-15Rα, 링커 및 불변/Fc 영역 사이의 경계(들)을 나타낸다.
도 41은, IL-15(N4D/N65D) 변이체 및 Xtend Fc(M428L/N434S) 치환을 포함하는 scIL-15/Rα-Fc 융합체인 XENP24294의 서열을 도시한 것이다. IL-15 및 IL-15Rα(스시)에는 밑줄이 그어져 있고, 링커에는 이중 밑줄이 그어져 있으며(당업자가 이해하는 바와 같이, 링커는 다른 링커로 대체될 수 있으며, 이 중 일부는 도면에 도시되어 있음), 슬래시(/)는 IL-15, IL-15Rα, 링커 및 불변/Fc 영역 사이의 경계(들)을 나타낸다.
도 42는, IL-15(D30N/E64Q/N65D) 변이체 및 Xtend Fc (M428L/N434S) 치환을 포함하는 IL-15/Rα-heteroFc 융합체인 XENP24306의 서열을 도시한 것이다. IL-15 및 IL-15Rα(스시)에는 밑줄이 그어져 있고, 링커에는 이중 밑줄이 그어져 있으며(당업자가 이해하는 바와 같이, 링커는 다른 링커로 대체될 수 있으며, 이 중 일부는 도면에 도시되어 있음), 슬래시(/)는 IL-15, IL-15Rα, 링커 및 불변/Fc 영역 사이의 경계(들)을 나타낸다.
도 43은, 표시된 상대 농도로의 첫 번째 투여 후, 시노몰구스 원숭이에서 시간 경과에 따른 표시된 시험 물품의 혈청 농도를 도시한 것이다.
도 44a 내지 도 44c는, 추가의 IL-15 역가 변이체를 포함하는 예시적인 scIL-15/Rα-Fc 융합체의 서열을 도시한 것이다. IL-15 및 IL-15Rα(스시)에는 밑줄이 그어져 있고, 링커에는 이중 밑줄이 그어져 있으며(당업자가 이해하는 바와 같이, 링커는 다른 링커로 대체될 수 있으며, 이 중 일부는 도 9 및 도 10에 도시되어 있음), 슬래시(/)는 IL-15, IL-15Rα, 링커, 가변 영역 및 불변/Fc 영역 사이의 경계(들)을 나타낸다.
도 45a 내지 도 45g는, PBMC를 표시된 시험 물품과 함께 3일 동안 인큐베이션한 후, CD4+CD45RA-(도 45a), CD4+CD45RA+(도 45b), CD8+CD45RA-(도 45c), CD8+CD45RA+(도 45d), CD16+ NK세포(도 45e), CD56+ NK세포(도 45f) 및 γδ 세포(도 45g)의 Ki67 발현율을 도시한 것이다.
도 46a 및 도 46b는, IL-15(D30N/N65D) 변이체를 포함하는 예시적인 LAG-3 표적화 IL-15/Rα-Fc 융합체의 서열을 도시한 것이다. CDR은 볼드체로 표시되어 있다. 본원에 표시되고, CDR을 함유하는 본원의 모든 서열에 대하여 적용되는 바와 같이, CDR 위치의 정확한 식별은 표 2에 제시된 바와 같이 사용되는 넘버링에 따라 약간 상이할 수 있기 때문에, 밑줄 그어진 CDR뿐 아니라 다른 넘버링 시스템을 사용하여 VH 및 VL 도메인 내에 포함되는 CDR도 본원에 포함된다. IL-15 및 IL-15Rα(스시)에는 밑줄이 그어져 있고, 링커에는 이중 밑줄이 그어져 있으며(당업자가 이해하는 바와 같이, 링커는 다른 링커로 대체될 수 있으며, 이 중 일부는 도 9 및 도 10에 도시되어 있음), 슬래시(/)는 IL-15, IL-15Rα, 링커, 가변 영역 및 불변/Fc 영역 사이의 경계(들)을 나타낸다.
도 47a 및 도 47b는, IL-15(D30N/E64Q/N65D) 변이체를 포함하는 예시적인 LAG-3 표적화 IL-15/Rα-Fc 융합체의 서열을 도시한 것이다. CDR은 볼드체로 표시되어 있다. 본원에 표시되고, CDR을 함유하는 본원의 모든 서열에 대하여 적용되는 바와 같이, CDR 위치의 정확한 식별은 표 2에 제시된 바와 같이 사용되는 넘버링에 따라 약간 상이할 수 있기 때문에, 밑줄 그어진 CDR뿐 아니라 다른 넘버링 시스템을 사용하여 VH 및 VL 도메인 내에 포함되는 CDR도 본원에 포함된다. IL-15 및 IL-15Rα(스시)에는 밑줄이 그어져 있고, 링커에는 이중 밑줄이 그어져 있으며(당업자가 이해하는 바와 같이, 링커는 다른 링커로 대체될 수 있으며, 이 중 일부는 도 9 및 도 10에 도시되어 있음), 슬래시(/)는 IL-15, IL-15Rα, 링커, 가변 영역 및 불변/Fc 영역 사이의 경계(들)을 나타낸다.
도 48a 내지 도 48d는, 혈청 반감기를 증강시키기 위한 Xtend(M428L/N434S) 치환을 포함하는 예시적인 LAG-3 표적화 IL-15/Rα-Fc 융합체의 서열을 도시한 것이다. CDR은 볼드체로 표시되어 있다. 본원에 표시되고, CDR을 함유하는 본원의 모든 서열에 대하여 적용되는 바와 같이, CDR 위치의 정확한 식별은 표 2에 제시된 바와 같이 사용되는 넘버링에 따라 약간 상이할 수 있기 때문에, 밑줄 그어진 CDR뿐 아니라 다른 넘버링 시스템을 사용하여 VH 및 VL 도메인 내에 포함되는 CDR도 본원에 포함된다. IL-15 및 IL-15Rα(스시)에는 밑줄이 그어져 있고, 링커에는 이중 밑줄이 그어져 있으며(당업자가 이해하는 바와 같이, 링커는 다른 링커로 대체될 수 있으며, 이 중 일부는 도 9 및 도 10에 도시되어 있음), 슬래시(/)는 IL-15, IL-15Rα, 링커, 가변 영역 및 불변/Fc 영역 사이의 경계(들)을 나타낸다. 본원에 도시된 임의의 서열이 M428L/N434S 치환을 포함하거나 이를 배제할 수 있다는 점에 주목해야 한다.
도 49a 및 도 49b는, 대조군인 RSV 표적화 IL-15/Rα-Fc 융합체, XENP26007, XENP29481 및 XENP30432의 서열을 도시한 것이다. CDR에는 밑줄이 그어져 있다. 본원에 표시되고, CDR을 함유하는 본원의 모든 서열에 대하여 적용되는 바와 같이, CDR 위치의 정확한 식별은 표 2에 제시된 바와 같이 사용되는 넘버링에 따라 약간 상이할 수 있기 때문에, 밑줄 그어진 CDR뿐 아니라 다른 넘버링 시스템을 사용하여 VH 및 VL 도메인 내에 포함되는 CDR도 본원에 포함된다. IL-15 및 IL-15Rα(스시)는 이탤릭체로 표시되어 있고, 링커에는 이중 밑줄이 그어져 있으며(당업자가 이해하는 바와 같이, 링커는 다른 링커로 대체될 수 있으며, 이 중 일부는 도 9 및 도 10에 도시되어 있음), 슬래시(/)는 IL-15, IL-15Rα, 링커, 가변 영역 및 불변/Fc 영역 사이의 경계(들)을 나타낸다.
도 2a 및 도 2b는, IL-15 및 이의 수용체의 서열을 도시한 것이다.
도 3은, 임상 개발의 용이성을 위해 둘 모두에 결합하는 항원 결합 도메인의 개발을 용이하게 하는, 인간 및 시노몰구스 원숭이(예측)에 대한 LAG-3의 서열을 도시한 것이다.
도 4a 내지 도 4e는, 유용한 Fc 이종이량체화 변이체 세트(비대칭 변이체 및 pI 변이체를 포함함)의 쌍을 도시한 것이다. 상응하는 "단량체 2" 변이체가 없는 변이체가 존재하며; 이는 어느 쪽의 단량체에도 단독으로 사용될 수 있는 pI 변이체이다.
도 5는, 등입체성(isosteric) 변이체 항체 불변 영역 및 이의 각각의 치환의 목록을 도시한 것이다. pI_(-)는 보다 낮은 pI를 갖는 변이체를 나타내고, pI_(+)는 보다 높은 pI를 갖는 변이체를 나타낸다. 이는 본 발명의 다른 이종이량체화 변이체 (및 또한 본원에 개괄된 바와 같은 다른 변이체 유형)와 선택적으로 및 독립적으로 조합될 수 있다.
도 6은, FcγR 결합을 절제하는 유용한 절제 변이체(때때로 "녹아웃(knock out)" 또는 "KO" 변이체로 지칭됨)를 도시한 것이다. 일반적으로, 절제 변이체는 두 가지 단량체 모두에서 발견되지만, 일부 경우에 하나의 단량체에만 존재할 수도 있다.
도 7a 내지 도 7f는, 본 발명의 LAG-3 표적화 IL-15/Rα-Fc 융합 단백질의 "비(非)사이토카인"/"비(非)Fv" 구성요소의 특히 유용한 구현예를 보여준다.
도 8은, IL-15/Rα-Fc 융합 단백질에 사용되는 다수의 예시적인 가변 길이 링커를 도시한 것이다. 일부 구현예에서, 이러한 링커는 IL-15 및/또는 IL-15Rα(스시)의 C-말단을 Fc 영역의 N-말단에 연결하는 데 사용된다. 일부 구현예에서, 이러한 링커는 IL-15를 IL-15Rα(스시)에 융합시키는 데 사용된다.
도 9a 내지 도 9c는, 구성요소로서 하나 이상의 scFv를 이용하는 이종이량체 항체의 pI를 증가시키거나 감소시키는 데 사용되는 다수의 하전된 scFv 링커를 도시한 것이다. (+H) 양성 링커가 특히 본원에서 사용된다. 단일 전하를 갖는 하나의 선행 기술 scFv 링커는, 문헌[Whitlow et al., Protein Engineering 6(8):989-995 (1993)]에 "Whitlow"로 언급되어 있다. 이러한 링커가 scFv에서 응집을 감소시키고 단백질 분해 안정성을 증강시키는 데 사용되었다는 점에 주목해야 한다.
도 10은, 사이토카인 서열(예를 들어, IL-15 및/또는 IL-15Rα(스시)) 또는 VH를 갖지 않고, 추가로 도 11에 도시된 경쇄 백본을 제외한, 인간 IgG1을 기반으로 하는 몇 가지 유용한 LAG-3 표적화 IL-15/Rα-Fc 융합체 형식 백본의 서열을 보여준다. 백본 1은 인간 IgG1(356E/358M 알로타입(allotype))을 기반으로 하며, S364K/E357Q : L368D/K370S 비대칭 변이체, C220S, L368D/K370S 비대칭 변이체를 갖는 사슬 상의 Q295E/N384D/Q418E/N421D pI 변이체, 및 양쪽 사슬 상의 E233P/L234V/L235A/G236del/S267K 절제 변이체를 포함한다. 백본 2는 인간 IgG1(356E/358M 알로타입)을 기반으로 하며, S364K/E357Q : L368D/K370S 비대칭 변이체, L368D/K370S 비대칭 변이체를 갖는 사슬 상의 N208D/Q295E/N384D/Q418E/N421D pI 변이체, S364K/E357Q 변이체를 갖는 사슬 상의 C220S, 및 양쪽 사슬 상의 E233P/L234V/L235A/G236del/S267K 절제 변이체를 포함한다. 백본 3은 인간 IgG1(356E/358M 알로타입)을 기반으로 하며, S364K/E357Q : L368D/K370S 비대칭 변이체, L368D/K370S 비대칭 변이체를 갖는 사슬 상의 N208D/Q295E/N384D/Q418E/N421D pI 변이체, S364K/E357Q 변이체를 갖는 사슬 상의 Q196K/I199T/P217R/P228R/N276K pI 변이체, 및 양쪽 사슬 상의 E233P/L234V/L235A/G236del/S267K 절제 변이체를 포함한다. 상기와 같은 백본 서열은, 예를 들어 본원에 기재된 "scIL-15/Rα X Fab" 형식 이종이량체 단백질에 포함될 수 있다. ). 일부 구현예에서, "scIL-15/Rα X Fab" 형식 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(힌지)-CH2-CH3을 포함하는 제1 단량체(여기서 힌지-CH2-CH3은 도 10의 임의의 백본 서열의 "사슬 2"의 아미노산 서열(서열번호 XXX-XXX)을 가짐); b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 VH는 가변 중쇄 도메인이고, CH1-힌지-CH2-CH3은 도 10의 임의의 백본 서열의 사슬 1의 아미노산 서열(서열번호 XXX-XXX)을 가짐); 및 c) N-말단에서 C-말단으로, VL-VC를 포함하는 경쇄(여기서 VL은 가변 경쇄 도메인이고, VC는 도 11의 "불변 경쇄-카파" 또는 "불변 경쇄-람다"의 서열(서열번호 XXX-XXX)을 가짐)를 포함한다. 예시적인 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함한다. 예시적인 구현예에서, 상기 VH 및 VL은, 각각, 도 12 및 도 13a 내지 도 13c에 제공된 임의의 LAG-3 ABD의 가변 중쇄 도메인 및 가변 경쇄 도메인이다.
특정 구현예에서, 이러한 서열은 356D/358L 알로타입일 수 있다. 다른 구현예에서, 이러한 서열은 N297A 또는 N297S 치환 중 어느 하나를 포함할 수 있다. 일부 다른 구현예에서, 이러한 서열은 M428L/N434S Xtend 돌연변이를 포함할 수 있다. 또 다른 구현예에서, 이러한 서열은 대신 인간 IgG4를 기반으로 하며, 양쪽 사슬 상에 S228P(EU 넘버링, 이는 Kabat에서 S241P임) 변이체(이는 당업계에 공지된 바와 같이 Fab 아암(arm) 교환을 제거함)를 포함한다. 추가의 구현예에서, 이러한 서열은 대신 인간 IgG2를 기반으로 할 수 있다. 나아가, 이러한 서열은 대신 도면에 도시된 다른 비대칭 변이체, pI 변이체 및 절제 변이체를 이용할 수 있다.
당업자가 이해하고 하기에 개괄되는 바와 같이, 이러한 서열은 도 21에 개략적으로 도시된 바와 같이, 비제한적으로 scIL-15/Rα, ncIL-15/Rα 및 dsIL-15Rα를 포함하는, 본원에 개괄된 임의의 IL-15와 IL-15Rα(스시)의 쌍과 함께 사용될 수 있다. 나아가, 당업자가 이해하고 하기에 개괄되는 바와 같이, 임의의 IL-15 및/또는 IL-15Rα(스시) 변이체가 이러한 백본에 혼입될 수 있다. 나아가, 당업자가 이해하고 하기에 개괄되는 바와 같이, 이러한 서열은 scFv 또는 Fab을 포함하는, 본원에 개괄된 임의의 VH와 VL의 쌍과 함께 사용될 수 있다.
이러한 각각의 백본 내에는, (본원에 정의된 바와 같이) 인용된 서열과 90%, 95%, 98% 및 99% 동일하고/하거나 (당업자가 이해하는 바와 같이, 도면의 "모(parent)" 서열과 비교하여) 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개 또는 10개의 추가 아미노산 치환을 함유하는(모 인간 IgG1 (또는 백본에 따라, IgG2 또는 IgG4)과 비교하여 이미 다수의 아미노산 변형을 함유하는) 서열이 포함되어 있다. 즉, 인용된 백본은 이러한 도면의 백본 내에 함유된 비대칭 변이체, pI 변이체 및 절제 변이체에 더하여, 추가의 아미노산 변형(일반적으로 아미노산 치환)을 함유할 수 있다.
도 11은, 본 발명의 LAG-3 표적화 IL-15/Rα-Fc 융합 단백질에 사용되는 경쇄의 "비Fv" 백본(즉, 불변 경쇄)을 도시한 것이다.
도 12는, 선택된 수의 항-LAG-3 항체 결합 도메인에 대한 가변 영역 서열을 도시한 것이다. CDR에는 밑줄이 그어져 있다. 본원에 표시되고, CDR을 함유하는 본원의 모든 서열에 대하여 적용되는 바와 같이, CDR 위치의 정확한 식별은 표 2에 제시된 바와 같이 사용되는 넘버링에 따라 약간 상이할 수 있기 때문에, 밑줄 그어진 CDR뿐 아니라 다른 넘버링 시스템을 사용하여 VH 및 VL 도메인 내에 포함되는 CDR도 본원에 포함된다. 나아가, 도면의 모든 서열에 대하여, 이러한 VH 및 VL 서열은 scFv 형식 또는 Fab 형식 중 어느 하나로 사용될 수 있다.
도 13a 내지 도 13c는, 본 발명의 LAG-3 표적화 IL-15/Rα-Fc 융합 단백질에 사용될 수 있는 추가의 LAG-3 ABD의 가변 영역을 도시한 것이다. CDR에는 밑줄이 그어져 있다. 본원에 표시되고, CDR을 함유하는 본원의 모든 서열에 대하여 적용되는 바와 같이, CDR 위치의 정확한 식별은 표 2에 제시된 바와 같이 사용되는 넘버링에 따라 약간 상이할 수 있기 때문에, 밑줄 그어진 CDR뿐 아니라 다른 넘버링 시스템을 사용하여 VH 및 VL 도메인 내에 포함되는 CDR도 본원에 포함된다. 나아가, 도면의 모든 서열에 대하여, 이러한 VH 및 VL 서열은 scFv 형식 또는 Fab 형식 중 어느 하나로 사용될 수 있다.
도 14는, 조작된 다이설파이드 결합 쌍의 위치를 보여주는 IL-15/Rα 이종이량체의 구조 모델을 도시한 것이다.
도 15는, 시스테인 잔기를 조작하기 위한 스캐폴드로서 작용하도록 C-말단에서 추가의 잔기로 조작된 예시적인 IL-15Rα(스시) 변이체의 서열을 도시한 것이다.
도 16은, 시스테인으로 조작된 IL-15Rα(스시) 변이체와 공유결합형 다이설파이드 결합을 형성하기 위해 시스테인으로 조작된 예시적인 IL-15 변이체의 서열을 도시한 것이다.
도 17은, 시스테인으로 조작된 IL-15 변이체와 공유결합형 다이설파이드 결합을 형성하기 위해 시스테인으로 조작된 예시적인 IL-15Rα(스시) 변이체의 서열을 도시한 것이다.
도 18은, IL-15Rα, IL-2Rβ 및 공통 감마 사슬과 복합체화된 IL-15의 구조를 도시한 것이다. 역가를 감소시키기 위해 설계된 치환의 위치가 제시되어 있다.
도 19a 내지 도 19c는, 역가 감소를 위해 조작된 예시적인 IL-15 변이체의 서열을 도시한 것이다. 각각의 이러한 변이체 IL-15 서열 내에는, (본원에 정의된 바와 같이) 인용된 서열과 90%, 95%, 98% 및 99% 동일하고/하거나 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개 또는 10개의 추가의 아미노산 치환을 함유하는 서열이 포함되어 있다. 비제한적인 예에서, 인용된 서열은 도 14, 도 16 및 도 17에 제시된 바와 같이 공유결합형 다이설파이드 결합의 형성에 기여하는 것들과 같은 추가의 아미노산 변형을 함유할 수 있다.
도 20은, 변이체 IL-15/Rα-Fc 융합 단백질에 의한 NK세포 및 CD8+ T세포 증식의 유도에 대한 EC50, 및 야생형인 XENP20818과 비교한 EC50의 감소 배수를 도시한 것이다. 이러한 융합 단백질은 LAG-3 ABD를 함유하지 않는다.
도 21a 내지 도 21k는, 본 발명의 LAG-3 표적화 IL-15/Rα-Fc 융합 단백질에 대한 몇 가지 형식을 도시한 것이다. "scIL-15/Rα x scFv" 형식(도 21a)은 가변 길이 링커에 의해 IL-15에 융합된 IL-15Rα(스시)("scIL-15/Rα"로 지칭됨)(이는 이후에 이종이량체 Fc 영역의 N-말단에 융합됨)와, 이종이량체 Fc의 다른 쪽에 융합된 scFv를 포함한다. "scFv x ncIL-15/Rα" 형식(도 21b)은 이종이량체 Fc 영역의 N-말단에 융합된 scFv와 이종이량체 Fc의 다른 쪽에 융합된 IL-15Rα(스시)를 포함하지만, IL-15는 비공유결합형 IL-15/Rα 복합체가 형성되도록 별도로 트랜스펙션된다. "scFv x dsIL-15/Rα" 형식(도 21c)은 "scFv x ncIL-15/Rα" 형식과 동일하지만, 여기서 IL-15Rα(스시)와 IL-15는 조작된 시스테인의 결과로서 공유결합으로 연결된다. "scIL-15/Rα x Fab" 형식(도 21d)은 가변 길이 링커에 의해 IL-15에 융합된 IL-15Rα(스시)("scIL-15/Rα"로 지칭됨)(이는 이후에 이종이량체 Fc 영역의 N-말단에 융합됨)와, 이종이량체 Fc의 다른 쪽에 융합된 가변 중쇄(VH)를 포함하며, 상응하는 경쇄는 VH와 Fab을 형성하도록 별도로 트랜스펙션된다. "ncIL-15/Rα x Fab" 형식(도 21e)은 이종이량체 Fc 영역의 N-말단에 융합된 VH와 이종이량체 Fc의 다른 쪽에 융합된 IL-15Rα(스시)를 포함하며, 상응하는 경쇄는 VH와 Fab을 형성하도록 별도로 트랜스펙션되고, IL-15는 비공유결합형 IL-15/Rα 복합체가 형성되도록 별도로 트랜스펙션된다. "dsIL-15/Rα x Fab" 형식(도 21f)은 "ncIL-15/Rα x Fab" 형식과 동일하지만, 여기서 IL-15Rα(스시)와 IL-15는 조작된 시스테인의 결과로서 공유결합으로 연결된다. "mAb-scIL-15/Rα" 형식(도 21g)은 제1 이종이량체 Fc와 제2 이종이량체 Fc의 N-말단에 융합된 VH와, IL-15Rα(스시)에 융합된 IL-15(이는 이후에 이종이량체 Fc 영역 중 하나의 C-말단에 추가로 융합됨)를 포함하며, 상응하는 경쇄는 VH와 Fab을 형성하도록 별도로 트랜스펙션된다. "mAb-ncIL-15/Rα" 형식(도 21h)은 제1 이종이량체 Fc와 제2 이종이량체 Fc의 N-말단에 융합된 VH와, 이종이량체 Fc 영역 중 하나의 C-말단에 융합된 IL-15Rα(스시)를 포함하며, 상응하는 경쇄는 VH와 Fab을 형성하도록 별도로 트랜스펙션되고, IL-15는 비공유결합형 IL-15/Rα 복합체가 형성되도록 별도로 트랜스펙션된다. "mAb-dsIL-15/Rα" 형식(도 21i)은 "mAb-ncIL-15/Rα" 형식과 동일하지만, 여기서 IL-15Rα(스시)와 IL-15는 조작된 시스테인의 결과로서 공유결합으로 연결된다. "central-IL-15/Rα" 형식(도 21j)은 IL-15의 N-말단에 재조합적으로 융합된 VH(이는 이후에 이종이량체 Fc의 한쪽에 추가로 융합됨)와, IL-15Rα(스시)의 N-말단에 재조합적으로 융합된 VH(이는 이후에 이종이량체 Fc의 다른 한쪽에 추가로 융합됨)를 포함하며, 상응하는 경쇄는 VH와 Fab을 형성하도록 별도로 트랜스펙션된다. "central-scIL-15/Rα" 형식(도 21k)은 IL-15에 융합된 IL-15Rα(스시)의 N-말단에 융합된 VH(이는 이후에 이종이량체 Fc의 한쪽에 추가로 융합됨)와, 이종이량체 Fc의 다른 한쪽에 융합된 VH를 포함하며, 상응하는 경쇄는 VH와 Fab을 형성하도록 별도로 트랜스펙션된다.
도 22a 및 도 22b는, "scIL-15/Rα x Fab" 형식의 예시적인 LAG-3 표적화 IL-15/Rα-Fc 융합 단백질인 XENP27972 및 XENP27973의 서열을 도시한 것이다. CDR은 볼드체로 표시되어 있다. 본원에 표시되고, CDR을 함유하는 본원의 모든 서열에 대하여 적용되는 바와 같이, CDR 위치의 정확한 식별은 표 2에 제시된 바와 같이 사용되는 넘버링에 따라 약간 상이할 수 있기 때문에, 밑줄 그어진 CDR뿐 아니라 다른 넘버링 시스템을 사용하여 VH 및 VL 도메인 내에 포함되는 CDR도 본원에 포함된다. IL-15 및 IL-15Rα(스시)에는 밑줄이 그어져 있고, 링커에는 이중 밑줄이 그어져 있으며(당업자가 이해하는 바와 같이, 링커는 다른 링커로 대체될 수 있으며, 이 중 일부는 도면에 도시되어 있음), 슬래시(/)는 IL-15, IL-15Rα, 링커, 가변 영역 및 불변/Fc 영역 사이의 경계(들)을 나타낸다.
도 23은, 절제 변이체 (E233P/L234V/L235A/G236del/S267K, "IgG1_PVA_/S267k")를 갖는 2가 항-PD-1 mAb인 XENP16432의 서열을 도시한 것이다. CDR에는 밑줄이 그어져 있다. 본원에 표시되고, CDR을 함유하는 본원의 모든 서열에 대하여 적용되는 바와 같이, CDR 위치의 정확한 식별은 표 2에 제시된 바와 같이 사용되는 넘버링에 따라 약간 상이할 수 있기 때문에, 밑줄 그어진 CDR뿐 아니라 다른 넘버링 시스템을 사용하여 VH 및 VL 도메인 내에 포함되는 CDR도 본원에 포함된다.
도 24a 및 도 24b는, 표시된 시험 물품의 첫 번째 투여 후, 6일차(도 24a) 및 10일차(도 24b)에서의 PBMC 이식된 NSG 마우스의 전혈 중 CD8+ T세포 수를 도시한 것이다.
도 25a 및 도 25b는, 표시된 시험 물품의 첫 번째 투여 후, 6일차(도 25a) 및 10일차(도 25b)에서의 PBMC 이식된 NSG 마우스의 전혈 중 CD4+ T세포 수를 도시한 것이다.
도 26a 및 도 26b는, 표시된 시험 물품의 첫 번째 투여 후, 6일차(도 26a) 및 10일차(도 26b)에서의 PBMC 이식된 NSG 마우스의 전혈 중 CD45+ T세포 수를 도시한 것이다.
도 27a 및 도 27b는, 표시된 시험 물품의 첫 번째 투여 후, 6일차(도 27a) 및 10일차(도 27b)에서의 PBMC 이식된 NSG 마우스의 전혈 중 CD16+CD56+ NK세포 수를 도시한 것이다.
도 28은, 표시된 시험 물품의 투여 후, PBMC 이식된 NSG 마우스의 체중 변화(초기 체중의 백분율로서)를 도시한 것이다.
도 29a 및 도 29b는, 양쪽 Fc 도메인에 M428L/N434S 변이체를 포함하는 XENP27977 및 XENP27978의 서열을 도시한 것이다.
도 30은, 세포 증식률(CFSE 희석법에 기반하여 결정됨)로 표시되는, LAG-3 표적화 IL-15/Rα-Fc 융합체 (및 대조군)에 의한 CD8+ T세포(도 30a) 및 CD4+ T세포(도 30b) 증식의 유도를 도시한 것이다. 데이터는, LAG-3 표적화 IL-15/Rα-Fc 융합체가 비(非)표적화 IL-15(D30N/E64Q/N65D)/Rα-Fc 융합체 (및 대조군인 RSV 표적화 IL-15/Rα-Fc 융합체)에 비해 CD8+ T세포의 증식을 유도하는 데 더 강력함을 보여준다.
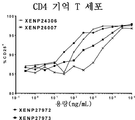
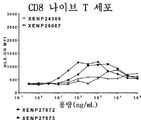
도 31은, 세포 증식률(CFSE 희석법에 기반하여 결정됨)로 표시되는, LAG-3 표적화 IL-15/Rα-Fc 융합체 (및 대조군)에 의한 CD8 기억T세포(도 31a) 및 CD8 나이브(naive) T세포(도 31b) 증식의 유도를 도시한 것이다. 데이터는, LAG-3 표적화 IL-15/Rα-Fc 융합체가 비표적화 IL-15(D30N/E64Q/N65D)/Rα-Fc 융합체 (및 대조군인 RSV 표적화 IL-15/Rα-Fc 융합체)에 비해 CD8 기억T세포의 증식을 유도하는 데 훨씬 더 강력함을 보여준다.
도 32는, 세포 수로 표시되는, LAG-3 표적화 IL-15/Rα-Fc 융합체 (및 대조군)에 의한 CD8 기억T세포(도 32a) 및 CD8 나이브 T세포(도 32b) 증식의 유도를 도시한 것이다. 데이터는, LAG-3 표적화 IL-15/Rα-Fc 융합체가 비표적화 IL-15(D30N/E64Q/N65D)/Rα-Fc 융합체 (및 대조군인 RSV 표적화 IL-15/Rα-Fc 융합체)에 비해 CD8 기억T세포를 확장시키는 데 훨씬 더 강력함을 보여준다.
도 33은, 세포 증식률(CFSE 희석법에 기반하여 결정됨)로 표시되는, LAG-3 표적화 IL-15/Rα-Fc 융합체 (및 대조군)에 의한 CD4 기억T세포(도 33a) 및 CD4 나이브 T세포(도 33b) 증식의 유도를 도시한 것이다. 데이터는, LAG-3 표적화 IL-15/Rα-Fc 융합체가 비표적화 IL-15(D30N/E64Q/N65D)/Rα-Fc 융합체 (및 대조군인 RSV 표적화 IL-15/Rα-Fc 융합체)에 비해 CD4 기억T세포를 확장시키는 데 더 강력함을 보여준다.
도 34는, 세포 수로 표시되는, LAG-3 표적화 IL-15/Rα-Fc 융합체 (및 대조군)에 의한 CD4 기억T세포(도 34a) 및 CD4 나이브 T세포(도 34b) 증식의 유도를 도시한 것이다.
도 35는, 세포 증식률(CFSE 희석법에 기반하여 결정됨)(도 35a) 및 세포 수(도 35b)로 표시되는, LAG-3 표적화 IL-15/Rα-Fc 융합체 (및 대조군)에 의한 NK세포 증식의 유도를 도시한 것이다.
도 36은, LAG-3 표적화 IL-15/Rα-Fc 융합체 (및 대조군)와 함께 인큐베이션한 후, CD8 기억T세포의 CD25 발현율(도 36a), CD8 나이브 T세포의 CD25 발현율(도 36b), CD4 기억T세포의 CD25 발현율(도 36c) 및 CD4 나이브 T세포의 CD25 발현율(도 36d)로 표시되는 CD8+ T세포의 활성화를 도시한 것이다. 데이터는, LAG-3 표적화 IL-15/Rα-Fc 융합체, 특히 XENP27972가 비표적화 IL-15(D30N/E64Q/N65D)/Rα-Fc 융합체 (및 대조군인 RSV 표적화 IL-15/Rα-Fc 융합체)에 비해 CD8 기억T세포 및 CD4 기억T세포 둘 모두에서 CD25를 상향조절함을 보여준다.
도 37은, LAG-3 표적화 IL-15/Rα-Fc 융합체 (및 대조군)와 함께 인큐베이션한 후, CD8 기억T세포에서의 HLA-DR MFI(도 37a), CD8 기억T세포의 HLA-DR 발현율(도 37b), CD8 나이브 T세포에서의 HLA-DR MFI(도 37c) 및 CD8 나이브 T세포의 HLA-DR 발현율(도 37d)로 표시되는 CD8+ T세포의 활성화를 도시한 것이다. 데이터는, LAG-3 표적화 IL-15/Rα-Fc 융합체가 비표적화 IL-15(D30N/E64Q/N65D)/Rα-Fc 융합체 (및 대조군인 RSV 표적화 IL-15/Rα-Fc 융합체)에 비해 CD8 기억T세포에서 HLA-DR를 더 강력하게 상향조절함을 보여준다.
도 38은, LAG-3 표적화 IL-15/Rα-Fc 융합체 (및 대조군)와 함께 인큐베이션한 후, CD4 기억T세포에서의 HLA-DR MFI(도 38a), CD4 기억T세포의 HLA-DR 발현율(도 38b), CD4 나이브 T세포에서의 HLA-DR MFI(도 38c) 및 CD4 나이브 T세포의 HLA-DR 발현율(도 38d)로 표시되는 CD4+ T세포의 활성화를 도시한 것이다.
도 39는, 야생형 IL-15 및 Xtend Fc(M428L/N434S) 변이체를 포함하는 IL-15/Rα-heteroFc 융합체인 XENP22853의 서열을 도시한 것이다. IL-15 및 IL-15Rα(스시)에는 밑줄이 그어져 있고, 링커에는 이중 밑줄이 그어져 있으며(당업자가 이해하는 바와 같이, 링커는 다른 링커로 대체될 수 있으며, 이 중 일부는 도면에 도시되어 있음), 슬래시(/)는 IL-15, IL-15Rα, 링커 및 불변/Fc 영역 사이의 경계(들)을 나타낸다.
도 40은, IL-15(N4D/N65D) 변이체 및 Xtend Fc(M428L/N434S) 변이체를 포함하는 IL-15/Rα-heteroFc 융합체인 XENP24113의 서열을 도시한 것이다. IL-15 및 IL-15Rα(스시)에는 밑줄이 그어져 있고, 링커에는 이중 밑줄이 그어져 있으며(당업자가 이해하는 바와 같이, 링커는 다른 링커로 대체될 수 있으며, 이 중 일부는 도면에 도시되어 있음), 슬래시(/)는 IL-15, IL-15Rα, 링커 및 불변/Fc 영역 사이의 경계(들)을 나타낸다.
도 41은, IL-15(N4D/N65D) 변이체 및 Xtend Fc(M428L/N434S) 치환을 포함하는 scIL-15/Rα-Fc 융합체인 XENP24294의 서열을 도시한 것이다. IL-15 및 IL-15Rα(스시)에는 밑줄이 그어져 있고, 링커에는 이중 밑줄이 그어져 있으며(당업자가 이해하는 바와 같이, 링커는 다른 링커로 대체될 수 있으며, 이 중 일부는 도면에 도시되어 있음), 슬래시(/)는 IL-15, IL-15Rα, 링커 및 불변/Fc 영역 사이의 경계(들)을 나타낸다.
도 42는, IL-15(D30N/E64Q/N65D) 변이체 및 Xtend Fc (M428L/N434S) 치환을 포함하는 IL-15/Rα-heteroFc 융합체인 XENP24306의 서열을 도시한 것이다. IL-15 및 IL-15Rα(스시)에는 밑줄이 그어져 있고, 링커에는 이중 밑줄이 그어져 있으며(당업자가 이해하는 바와 같이, 링커는 다른 링커로 대체될 수 있으며, 이 중 일부는 도면에 도시되어 있음), 슬래시(/)는 IL-15, IL-15Rα, 링커 및 불변/Fc 영역 사이의 경계(들)을 나타낸다.
도 43은, 표시된 상대 농도로의 첫 번째 투여 후, 시노몰구스 원숭이에서 시간 경과에 따른 표시된 시험 물품의 혈청 농도를 도시한 것이다.
도 44a 내지 도 44c는, 추가의 IL-15 역가 변이체를 포함하는 예시적인 scIL-15/Rα-Fc 융합체의 서열을 도시한 것이다. IL-15 및 IL-15Rα(스시)에는 밑줄이 그어져 있고, 링커에는 이중 밑줄이 그어져 있으며(당업자가 이해하는 바와 같이, 링커는 다른 링커로 대체될 수 있으며, 이 중 일부는 도 9 및 도 10에 도시되어 있음), 슬래시(/)는 IL-15, IL-15Rα, 링커, 가변 영역 및 불변/Fc 영역 사이의 경계(들)을 나타낸다.
도 45a 내지 도 45g는, PBMC를 표시된 시험 물품과 함께 3일 동안 인큐베이션한 후, CD4+CD45RA-(도 45a), CD4+CD45RA+(도 45b), CD8+CD45RA-(도 45c), CD8+CD45RA+(도 45d), CD16+ NK세포(도 45e), CD56+ NK세포(도 45f) 및 γδ 세포(도 45g)의 Ki67 발현율을 도시한 것이다.
도 46a 및 도 46b는, IL-15(D30N/N65D) 변이체를 포함하는 예시적인 LAG-3 표적화 IL-15/Rα-Fc 융합체의 서열을 도시한 것이다. CDR은 볼드체로 표시되어 있다. 본원에 표시되고, CDR을 함유하는 본원의 모든 서열에 대하여 적용되는 바와 같이, CDR 위치의 정확한 식별은 표 2에 제시된 바와 같이 사용되는 넘버링에 따라 약간 상이할 수 있기 때문에, 밑줄 그어진 CDR뿐 아니라 다른 넘버링 시스템을 사용하여 VH 및 VL 도메인 내에 포함되는 CDR도 본원에 포함된다. IL-15 및 IL-15Rα(스시)에는 밑줄이 그어져 있고, 링커에는 이중 밑줄이 그어져 있으며(당업자가 이해하는 바와 같이, 링커는 다른 링커로 대체될 수 있으며, 이 중 일부는 도 9 및 도 10에 도시되어 있음), 슬래시(/)는 IL-15, IL-15Rα, 링커, 가변 영역 및 불변/Fc 영역 사이의 경계(들)을 나타낸다.
도 47a 및 도 47b는, IL-15(D30N/E64Q/N65D) 변이체를 포함하는 예시적인 LAG-3 표적화 IL-15/Rα-Fc 융합체의 서열을 도시한 것이다. CDR은 볼드체로 표시되어 있다. 본원에 표시되고, CDR을 함유하는 본원의 모든 서열에 대하여 적용되는 바와 같이, CDR 위치의 정확한 식별은 표 2에 제시된 바와 같이 사용되는 넘버링에 따라 약간 상이할 수 있기 때문에, 밑줄 그어진 CDR뿐 아니라 다른 넘버링 시스템을 사용하여 VH 및 VL 도메인 내에 포함되는 CDR도 본원에 포함된다. IL-15 및 IL-15Rα(스시)에는 밑줄이 그어져 있고, 링커에는 이중 밑줄이 그어져 있으며(당업자가 이해하는 바와 같이, 링커는 다른 링커로 대체될 수 있으며, 이 중 일부는 도 9 및 도 10에 도시되어 있음), 슬래시(/)는 IL-15, IL-15Rα, 링커, 가변 영역 및 불변/Fc 영역 사이의 경계(들)을 나타낸다.
도 48a 내지 도 48d는, 혈청 반감기를 증강시키기 위한 Xtend(M428L/N434S) 치환을 포함하는 예시적인 LAG-3 표적화 IL-15/Rα-Fc 융합체의 서열을 도시한 것이다. CDR은 볼드체로 표시되어 있다. 본원에 표시되고, CDR을 함유하는 본원의 모든 서열에 대하여 적용되는 바와 같이, CDR 위치의 정확한 식별은 표 2에 제시된 바와 같이 사용되는 넘버링에 따라 약간 상이할 수 있기 때문에, 밑줄 그어진 CDR뿐 아니라 다른 넘버링 시스템을 사용하여 VH 및 VL 도메인 내에 포함되는 CDR도 본원에 포함된다. IL-15 및 IL-15Rα(스시)에는 밑줄이 그어져 있고, 링커에는 이중 밑줄이 그어져 있으며(당업자가 이해하는 바와 같이, 링커는 다른 링커로 대체될 수 있으며, 이 중 일부는 도 9 및 도 10에 도시되어 있음), 슬래시(/)는 IL-15, IL-15Rα, 링커, 가변 영역 및 불변/Fc 영역 사이의 경계(들)을 나타낸다. 본원에 도시된 임의의 서열이 M428L/N434S 치환을 포함하거나 이를 배제할 수 있다는 점에 주목해야 한다.
도 49a 및 도 49b는, 대조군인 RSV 표적화 IL-15/Rα-Fc 융합체, XENP26007, XENP29481 및 XENP30432의 서열을 도시한 것이다. CDR에는 밑줄이 그어져 있다. 본원에 표시되고, CDR을 함유하는 본원의 모든 서열에 대하여 적용되는 바와 같이, CDR 위치의 정확한 식별은 표 2에 제시된 바와 같이 사용되는 넘버링에 따라 약간 상이할 수 있기 때문에, 밑줄 그어진 CDR뿐 아니라 다른 넘버링 시스템을 사용하여 VH 및 VL 도메인 내에 포함되는 CDR도 본원에 포함된다. IL-15 및 IL-15Rα(스시)는 이탤릭체로 표시되어 있고, 링커에는 이중 밑줄이 그어져 있으며(당업자가 이해하는 바와 같이, 링커는 다른 링커로 대체될 수 있으며, 이 중 일부는 도 9 및 도 10에 도시되어 있음), 슬래시(/)는 IL-15, IL-15Rα, 링커, 가변 영역 및 불변/Fc 영역 사이의 경계(들)을 나타낸다.
I. 정의
본 출원을 보다 완벽하게 이해할 수 있도록 하기 위해, 몇 가지 정의가 하기에 제시된다. 이러한 정의는 문법적 등가물을 포함하는 것으로 의도된다.
본원에서 "절제"란 활성의 감소 또는 제거를 의미한다. 따라서, 예를 들어, "FcγR 결합의 절제"는 Fc 영역 아미노산 변이체가 이러한 특정 변이체를 포함하지 않는 Fc 영역과 비교하여 50% 미만의 출발 결합을 갖는 것을 의미하며, 이때 70-80-90-95-98% 미만의 활성 손실이 바람직하고, 일반적으로 상기 활성은 Biacore 검정에서 검출 가능한 결합 수준 미만이다. 특히, FcγR 결합의 절제에 사용되는 것은 도 6에 제시된 것들이다. 하지만, 달리 언급되지 않는 한, 본 발명의 Fc 단량체는 FcRn 수용체에 대한 결합을 유지한다.
본원에 사용된 "ADCC" 또는 "항체 의존적 세포 매개 세포독성"이란, FcγR을 발현하는 비(非)특이적 세포독성 세포가 표적세포 상의 결합된 항체를 인식하고, 이어서 표적세포의 용해를 유발하는 세포 매개 반응을 의미한다. ADCC는 FcγRIIIa에 대한 결합과 상관관계가 있고, FcγRIIIa에 대한 결합 증가는 ADCC 활성을 증가시킨다. 본원에 논의된 바와 같이, 본 발명의 다수의 구현예는 ADCC 활성을 완전히 제거한다.
본원에 사용된 "ADCP" 또는 항체 의존적 세포 매개 포식작용(phagocytosis)이란, FcγR을 발현하는 비특이적 세포독성 세포가 표적세포 상의 결합된 항체를 인식하고, 이어서 표적세포의 포식작용을 유발하는 세포 매개 반응을 의미한다.
본원에서 "항원 결합 도메인" 또는 "ABD"란, 폴리펩타이드 서열의 일부로 존재할 때, 본원에 논의된 바와 같이 표적 항원에 특이적으로 결합하는 6개 상보성 결정 영역(Complementary Determining Regions: CDR)의 세트를 의미한다. 따라서, "LAG-3 항원 결합 도메인"은 본원에 개괄된 바와 같이 인간 LAG-3 항원에 결합한다. 당업계에 공지된 바와 같이, 이러한 CDR은 일반적으로, 각각이 3개의 CDR(중쇄의 경우 vhCDR1, vhCDR2, vhCDR3, 및 경쇄의 경우 vlCDR1, vlCDR2 및 vlCDR3)을 포함하는, 제1 가변 중쇄 CDR 세트(vhCDR 또는 VHCDR) 및 제2 가변 경쇄 CDR 세트(vlCDR 또는 VLCDR)로 존재한다. CDR은 가변 중쇄 도메인 및 가변 경쇄 도메인에 각각 존재하며, 함께 Fv 영역을 형성한다. 따라서, 일부 경우에, 항원 결합 도메인의 6개의 CDR은 가변 중쇄 및 가변 경쇄에 의해 제공된다. "Fab" 형식에서, 6개 CDR의 세트는 2개의 상이한 폴리펩타이드 서열, 가변 중쇄 도메인(VH 또는 vh 또는 VH; vhCDR1, vhCDR2 및 vhCDR3을 함유함) 및 가변 경쇄 도메인(VL 또는 vl 또는 VL; vlCDR1, vlCDR2 및 vlCDR3을 함유함)에 의해 제공되며, 여기서 VH 도메인의 C-말단은 중쇄의 CH1 도메인의 N-말단에 부착되고, VL 도메인의 C-말단은 불변 경쇄 도메인의 N-말단에 부착된다(따라서 경쇄를 형성함). scFv 형식에서, VH 도메인과 VL 도메인은 일반적으로 본원에 개괄된 바와 같은 링커의 사용을 통해 단일 폴리펩타이드 서열에 공유결합으로 부착되고, 이는 (N-말단에서 시작하여) VH-링커-VL 또는 VL-링커-VH일 수 있으며, 일반적으로 전자가 바람직하다(사용된 형식(예를 들어, 미국 특허 제62/353,511호의 도 1 참조)에 따라 각 측면에 선택적 도메인 링커를 포함함).
본원에서 "변형"이란, 폴리펩타이드 서열에서의 아미노산 치환, 삽입 및/또는 결실, 또는 단백질에 화학적으로 연결된 모이어티로의 변경을 의미한다. 예를 들어, 변형은 단백질에 부착된 변경된 탄수화물 또는 PEG 구조일 수 있다. 본원에서 "아미노산 변형"이란, 폴리펩타이드 서열에서의 아미노산 치환, 삽입 및/또는 결실을 의미한다. 명확성을 위해, 달리 언급되지 않는 한, 아미노산 변형은 항상 DNA에 의해 코딩된 아미노산, 예를 들어 DNA 및 RNA에 코돈을 갖는 20개의 아미노산에 대한 것이다.
본원에서 "아미노산 치환" 또는 "치환"이란, 모 폴리펩타이드 서열에서 특정 위치의 아미노산을 상이한 아미노산으로 대체하는 것을 의미한다. 특히, 일부 구현예에서, 치환은 특정 위치에서 자연적으로 발생하지 않는(유기체 내에서 또는 임의의 유기체에서 자연적으로 발생하지 않는) 아미노산에 대한 것이다. 예를 들어, 치환 E272Y는 변이체 폴리펩타이드, 이러한 경우 272번 위치의 글루탐산이 티로신으로 대체된 Fc 변이체를 나타낸다. 명확성을 위해, 핵산 코딩 서열은 변경하지만, 출발 아미노산은 변경하지 않도록 조작된 단백질(예를 들어, 숙주 유기체 발현 수준을 증가시키 위해 CGG(아르기닌을 인코딩함)를 CGA(여전히 아르기닌을 인코딩함)으로 교환함)은 "아미노산 치환"이 아니며; 즉, 동일한 단백질을 인코딩하는 새로운 유전자의 생성에도 불구하고, 단백질이 시작된 특정 위치에서 동일한 아미노산을 갖는 경우, 이는 아미노산 치환이 아니다.
본원에 사용된 "아미노산 삽입" 또는 "삽입"이란, 모 폴리펩타이드 서열의 특정 위치에 아미노산 서열을 부가하는 것을 의미한다. 예를 들어, -233E 또는 233E는 233번 위치 이후 및 234번 위치 이전에 글루탐산의 삽입을 나타낸다. 또한, -233ADE 또는 A233ADE는 233번 위치 이후 및 234번 위치 이전에 AlaAspGlu의 삽입을 나타낸다.
본원에 사용된 "아미노산 결실" 또는 "결실"이란, 모 폴리펩타이드 서열의 특정 위치에서 아미노산 서열을 제거하는 것을 의미한다. 예를 들어, E233- 또는 E233#, E233() 또는 E233del은 233번 위치에 있는 글루탐산의 결실을 나타낸다. 또한, EDA233- 또는 EDA233#은 233번 위치에서 시작하는 GluAspAla 서열의 결실을 나타낸다.
본원에 사용된 "변이체 단백질", "단백질 변이체" 또는 "변이체"란, 적어도 하나의 아미노산 변형에 의해 모 단백질과 다른 단백질을 의미한다. 단백질 변이체는 단백질 자체, 단백질을 포함하는 조성물, 또는 이를 인코딩하는 아미노산 서열을 나타낼 수 있다. 바람직하게는, 단백질 변이체는 모 단백질과 비교하여 적어도 하나의 아미노산 변형, 예를 들어 모 단백질과 비교하여 약 1 내지 약 70개의 아미노산 변형, 바람직하게는 약 1개 내지 약 5개의 아미노산 변형을 갖는다. 하기에 기재되는 바와 같이, 일부 구현예에서, 모 폴리펩타이드, 예를 들어 Fc 모 폴리펩타이드는 IgG1, IgG2, IgG3 또는 IgG4의 Fc 영역과 같은, 인간 야생형 서열이다. 본원의 단백질 변이체 서열은 바람직하게는 모 단백질 서열과 적어도 약 80%의 동일성, 가장 바람직하게는 적어도 약 90%의 동일성, 더욱 바람직하게는 적어도 약 95-98-99%의 동일성을 보유할 것이다. 변이체 단백질은 변이체 단백질 자체, 단백질 변이체를 포함하는 조성물, 또는 이를 인코딩하는 DNA 서열을 나타낼 수 있다.
본원에 사용된 "변이체"란, 또한 하기 섹션 II.C.에 개시된 바와 같은, 변이체 단백질(예를 들어, 변이체 Fc 도메인)에서의 특정 아미노산 변형(예를 들어, 치환, 결실, 삽입), 예를 들어 이종이량체화 변이체, 절제 변이체, FcKO 변이체 등을 나타낼 수 있다.
따라서, 본원에 사용된 "Fc 변이체" 또는 "변이체 Fc"란, Fc 도메인에 아미노산 변형을 포함하는 단백질을 의미한다. 본 발명의 Fc 변이체는 이를 구성하는 아미노산 변형에 따라 정의된다. 따라서, 예를 들어 N434S 또는 434S는 모 Fc 폴리펩타이드와 비교하여 434번 위치에 세린 치환을 갖는 Fc 변이체이며, 여기서 넘버링은 EU 인덱스에 따른다. 마찬가지로, M428L/N434S는 모 Fc 폴리펩타이드와 비교하여 치환 M428L 및 N434S를 갖는 Fc 변이체로 정의된다. WT 아미노산의 정체가 명시되지 않을 수 있으며, 이러한 경우 상기 언급된 변이체는 428L/434S로 지칭된다. 치환이 제공되는 순서는 임의적이며, 즉, 예를 들어 428L/434S는 M428L/N434S 등과 동일한 Fc 변이체이라는 점에 주목해야 한다. 항체와 관련하여 본 발명에서 논의된 모든 위치에 대하여, 달리 언급되지 않는 한, 아미노산 위치 넘버링은 EU 인덱스에 따른다. EU 인덱스, 또는 Kabat 또는 EU 넘버링 체계에서와 같은 EU 인덱스는 EU 항체의 넘버링을 나타낸다(문헌[Edelman et al., 1969, Proc Natl Acad Sci USA 63: 78-85](이는 그 전문이 본원에 참조로서 인용됨)). 이러한 변형은 부가, 결실 또는 치환일 수 있다. 치환은 자연 발생 아미노산, 및 일부 경우에 합성 아미노산을 포함할 수 있다. 이의 예에는, 미국 특허 제6,586,207호; WO 98/48032; WO 03/073238; US2004-0214988A1; WO 05/35727A2; WO 05/74524A2; 문헌[J. W. Chin et al., (2002), Journal of the American Chemical Society 124:9026-9027]; 문헌[J. W. Chin, & P. G. Schultz, (2002), ChemBioChem 11:1135-1137]; 문헌[J. W. Chin, et al., (2002), PICAS United States of America 99:11020-11024]; 및 문헌[L. Wang, & P. G. Schultz, (2002), Chem. 1-10]이 포함되며, 이들은 모두 그 전문이 본원에 참조로서 인용된다.
본원에 사용된 "단백질"이란, 적어도 2개의 공유결합으로 부착된 아미노산을 의미하며, 이에는 단백질, 폴리펩타이드, 올리고펩타이드 및 펩타이드가 포함된다.
본원에 사용된 "잔기"란, 단백질 및 이의 관련 아미노산 정체의 위치를 의미한다. 예를 들어, 297번 아스파라긴(Asn297 또는 N297로도 지칭됨)은 인간 항체 IgG1에서 297번 위치의 잔기이다.
본원에 사용된 "Fab" 또는 "Fab 영역"이란, VH, CH1, VL 및 CL 면역글로불린 도메인을 포함하는 폴리펩타이드를 의미한다. Fab은 단리된 이러한 영역, 또는 전장 항체, 항체 단편 또는 Fab 융합 단백질의 맥락에서의 이러한 영역을 나타낼 수 있다.
본원에 사용된 "Fv" 또는 "Fv 단편" 또는 "FV 영역"이란, 단일 항체의 VL 도메인 및 VH 도메인을 포함하는 폴리펩타이드를 의미한다. 당업자가 이해하는 바와 같이, 이는 일반적으로 2개의 사슬로 이루어져 있거나, (일반적으로 본원에 논의된 바와 같은 링커를 이용하여) 조합되어 scFv를 형성할 수 있다.
본원에서 "단일 사슬 Fv" 또는 "scFv"란, 일반적으로 본원에 논의된 바와 같은 scFv 링커를 사용하여 scFv 또는 scFv 도메인을 형성하는, 가변 경쇄 도메인에 공유결합으로 부착된 가변 중쇄 도메인을 의미한다. ScFv 도메인은 N 말단에서 C 말단으로의 배향(VH-링커-VL 또는 VL-링커-VH)으로 있을 수 있다.
본원에 사용된 "IgG 서브클래스 변형" 또는 "아이소타입(isotype) 변형"이란, 하나의 IgG 아이소타입의 하나의 아미노산을 상이한 정렬된 IgG 아이소타입의 상응하는 아미노산으로 전환시키는 아미노산 변형을 의미한다. 예를 들어, EU 296번 위치에 IgG1은 티로신을 포함하고 IgG2는 페닐알라닌을 포함하기 때문에, IgG2에서의 F296Y 치환은 IgG 서브클래스 변형으로 간주된다.
본원에 사용된 "비(非)자연 발생 변형"이란, 아이소타입이 아닌 아미노산 변형을 의미한다. 예를 들어, IgG 중 어느 것도 434번 위치에 세린을 포함하지 않기 때문에, IgG1, IgG2, IgG3 또는 IgG4 (또는 이들의 혼성체)에서의 434S 치환은 비자연 발생 변형으로 간주된다.
본원에 사용된 "아미노산" 및 "아미노산 정체"란, DNA 및 RNA에 의해 코딩되는 20개의 자연 발생 아미노산 중 하나를 의미한다.
본원에 사용된 "효과기 기능"이란, 항체 Fc 영역과 Fc 수용체 또는 리간드의 상호작용으로부터 유도된 생화학적 사건을 의미한다. 효과기 기능에는, 비제한적으로, ADCC, ADCP 및 CDC가 포함된다.
본원에 사용된 "Fc 감마 수용체", "FcγR" 또는 "Fc감마R"이란, IgG 항체 Fc 영역에 결합하고 FcγR 유전자에 의해 인코딩되는 단백질 패밀리의 임의의 구성원을 의미한다. 인간에서, 이러한 패밀리에는, 비제한적으로, 동형(isoform) FcγRIa, FcγRIb 및 FcγRIc를 포함하는 FcγRI(CD64); 동형 FcγRIIa(알로타입 H131 및 R131을 포함함), FcγRIIb(FcγRIIb-1 및 FcγRIIb-2를 포함함) 및 FcγRIIc를 포함하는 FcγRII(CD32); 및 동형 FcγRIIIa(알로타입 V158 및 F158을 포함함) 및 FcγRIIIb(알로타입 FcγRIIb-NA1 및 FcγRIIb-NA2를 포함함)를 포함하는 FcγRIII(CD16)(문헌[Jefferis et al., 2002, Immunol Lett 82:57-65](이는 그 전문이 본원에 참조로서 인용됨)), 및 임의의 발견되지 않은 인간 FcγR 또는 FcγR 동형 또는 알로타입이 포함된다.
본원에 사용된 "FcRn" 또는 "신생아 Fc 수용체"란, IgG 항체 Fc 영역에 결합하고 적어도 부분적으로 FcRn 유전자에 의해 인코딩되는 단백질을 의미한다. 당업계에 공지된 바와 같이, 기능성 FcRn 단백질은 종종 중쇄 및 경쇄로 지칭되는 2개의 폴리펩타이드를 포함한다. 여기서 경쇄는 베타-2-마이크로글로불린이고, 중쇄는 FcRn 유전자에 의해 인코딩된다. 본원에서 달리 언급되지 않는 한, FcRn 또는 FcRn 단백질은 FcRn 중쇄와 베타-2-마이크로글로불린의 복합체를 나타낸다. 다양한 FcRn 변이체는 FcRn 수용체에 대한 결합을 증가시키고, 일부 경우에서 혈청 반감기를 증가시키는 데 사용될 수 있다. 일반적으로, 달리 언급되지 않는 한, 본 발명의 Fc 단량체는 FcRn 수용체에 대한 결합을 유지한다(하기 언급되는 바와 같이, FcRn 수용체에 대한 결합을 증가시키는 아미노산 변이체를 포함할 수 있음).
본원에 사용된 "모 폴리펩타이드"란, 변이체를 생성하기 위해 후속으로 변형되는 출발 폴리펩타이드를 의미한다. 모 폴리펩타이드는 자연 발생 폴리펩타이드, 또는 자연 발생 폴리펩타이드의 변이체 또는 조작된 버전일 수 있다. 모 폴리펩타이드는 폴리펩타이드 자체, 모 폴리펩타이드를 포함하는 조성물, 또는 이를 인코딩하는 아미노산 서열을 나타낼 수 있다.
본원에 사용된 "Fc" 또는 "Fc 영역" 또는 "Fc 도메인"이란, 항체의 불변 영역을 포함하며, 제1 불변 영역 면역글로불린 도메인(예를 들어, CH1)을 제외한, 일부 경우에는 힌지의 일부를 제외한 폴리펩타이드를 의미한다. IgG의 경우, Fc 도메인은 면역글로불린 도메인 CH2 및 CH3(Cγ2 및 Cγ3), 및 CH1(Cγ1)과 CH2(Cγ2) 사이의 하부 힌지 영역을 포함한다. 따라서, 일부 경우에, Fc 도메인은, N-말단에서 C-말단으로, CH2-CH3 및 힌지-CH2-CH3을 포함한다. 일부 구현예에서, Fc 도메인은 IgG1, IgG2, IgG3 또는 IgG4에서 유래된 것이며, 여기서 IgG1 힌지-CH2-CH3 및 IgG4 힌지-CH2-CH3이 특히 다수의 구현예에서 사용된다. 또한, 특정 구현예에서, Fc 도메인은 인간 IgG1 Fc 도메인이고, 힌지는 C220S 아미노산 치환을 포함한다. 나아가, 일부 구현예에서, Fc 도메인은 인간 IgG4 Fc 도메인이고, 힌지는 S228P 아미노산 치환을 포함한다. Fc 영역의 경계는 달라질 수 있지만, 인간 IgG 중쇄 Fc 영역은 통상적으로 이의 카르복실 말단에 잔기 C226 또는 P230을 포함하는 것으로 정의되며, 여기서 넘버링은 Kabat에서와 같이 EU 인덱스에 따른다. 따라서, IgG의 맥락에서 "CH" 도메인은 다음과 같다: "CH1"은 Kabat에서와 같이 EU 인덱스에 따라 118번 내지 215번 위치를 나타낸다. "힌지"는 Kabat에서와 같이 EU 인덱스에 따라 216번 내지 230번 위치를 나타낸다. "CH2"는 Kabat에서와 같이 EU 인덱스에 따라 231번 내지 340번 위치를 나타내고, "CH3"은 Kabat에서와 같이 EU 인덱스에 따라 341번 내지 447번 위치를 나타낸다. 따라서, "Fc 도메인"은 -CH2-CH3 도메인 및 선택적으로 힌지 도메인을 포함한다(힌지-CH2-CH3).
당업자가 이해하는 바와 같이, 중쇄 불변 영역 도메인의 정확한 넘버링 및 배치는 상이한 넘버링 시스템들 간에 상이할 수 있다. EU 및 Kabat에 따른 중쇄 불변 영역 넘버링의 유용한 비교는 문헌[Edelman et al., 1969, Proc Natl Acad Sci USA 63:78-85], 및 문헌[Kabat et al., 1991, Sequences of Proteins of Immunological Interest, 5th Ed., United States Public Health Service, National Institutes of Health, Bethesda]를 참조한다(상기 문헌들은 그 전문이 본원에 참조로서 인용됨).
본원의 구현예에서, scFv 또는 IL-15 복합체가 Fc 도메인에 부착되는 경우, 도메인 링커, 예를 들어 도 8에 도시된 바와 같은 힌지 도메인을 통해 Fc 도메인에 부착되는 것은 scFv, IL-15 또는 IL-15Rα 구조체의 C-말단이다. 일부 구현예에서, 하기에 보다 충분히 기재되어 있는 바와 같이, 예를 들어 하나 이상의 FcγR 수용체 또는 FcRn 수용체에 대한 결합을 변경시키고, 본원에 개괄된 바와 같이 이종이량체의 형성 및 정제를 가능하게 하기 위해 Fc 영역에 대한 아미노산 변형이 이루어진다.
본원에서 "중쇄 불변 영역"이란, 항체의 CH1-힌지-CH2-CH3 부분을 의미한다.
본원에서 "Fc 융합 단백질" 또는 "면역부착소(immunoadhesin)"란, 본원에 기재된 바와 같이, 일반적으로 IL-15 및/또는 IL-15R과 같은 상이한 단백질에 (선택적으로 본원에 기재된 바와 같은 링커 모이어티를 통해) 연결되는 Fc 영역을 포함하는 단백질을 의미한다. 일부 경우에서, 2개의 Fc 융합 단백질은 동종이량체 Fc 융합 단백질 또는 이종이량체 융합 단백질을 형성할 수 있으며, 여기서 후자가 바람직하다. 일부 경우에, 이종이량체 융합 단백질 중 하나의 단량체는 Fc 도메인 단독(예를 들어, 빈(empty) Fc 도메인)을 포함하고, 다른 하나의 단량체는 변이체 Fc 도메인과, 수용체, 리간드 또는 다른 결합 파트너와 같은 단백질 도메인을 포함하는 Fc 융합체이다.
본원에 사용된 "위치"란, 단백질 서열 내 위치를 의미한다. 위치는 순차적으로, 또는 확립된 형식, 예를 들어 항체 넘버링에 대한 EU 인덱스에 따라 넘버링될 수 있다.
본 발명의 이종이량체 항체의 단량체의 맥락에서 "가닥 배열(strandedness)"이란, "매칭"되는 DNA의 2개의 가닥과 유사하게, 이종이량체화 변이체가 이종이량체를 형성하기 위해 "매칭"되는 능력을 보존하도록 각각의 단량체에 혼입됨을 의미한다. 예를 들어, 일부 pI 변이체가 단량체 A로 조작되는 경우(예를 들어, pI를 더 높게 만드는 경우), 또한 이용될 수 있는 "전하 쌍"인 입체 변이체는 pI 변이체를 방해하지 않으며, 예를 들어 pI 를 더 높게 만드는 전하 변이체는 두 가지 기능을 모두 보존하기 위해 동일한 "가닥" 또는 "단량체"에 배치된다. 유사하게는, 하기에 보다 충분히 개괄되는 바와 같이 세트의 쌍으로 된 "비대칭" 변이체의 경우, 당업자는, pI 분리가 비대칭체의 pI를 사용하여 최대화되도록, 한 쌍의 세트를 포함하는 어떠한 가닥 또는 단량체가 들어갈 것인지를 결정하는 데 pI를 고려할 것이다.
본원에 사용된 "표적세포"란, 표적 항원을 발현하는 세포, 이 경우 LAG-3을 의미한다.
본원에 사용된 "가변 영역"이란, 카파, 람다 및 중쇄 면역글로불린 유전자 좌위를 각각 구성하는 Vκ, Vλ 및/또는 VH 유전자 중 임의의 것에 의해 실질적으로 인코딩되는 하나 이상의 Ig 도메인을 포함하는 면역글로불린의 영역을 의미한다.
본원에서 "야생형 또는 WT"란, 대립유전자 변이를 포함하는, 자연에서 발견되는 아미노산 서열 또는 뉴클레오타이드 서열을 의미한다. WT 단백질은 의도적으로 변형되지 않은 아미노산 서열 또는 뉴클레오타이드 서열을 갖는다.
본 발명의 LAG-3 표적화 이종이량체 단백질은 일반적으로 단리되거나 재조합된다. 본원에 개시된 다양한 폴리펩타이드를 기재하는 데 사용될 때 "단리된"은, 발현된 세포 또는 세포 배양물로부터 식별되고, 분리 및/또는 회수된 폴리펩타이드를 의미한다. 통상적으로, 단리된 폴리펩타이드는 적어도 하나의 정제 단계에 의해 제조될 것이다. "단리된 단백질"은 상이한 결합 특이성을 갖는 다른 단백질이 실질적으로 없는 단백질을 나타낸다. "재조합"은 외인성 숙주세포에서 재조합 핵산 기법을 이용하여 단백질이 생성되는 것을 의미한다.
단백질 서열에 대한 "아미노산 서열 동일성 백분율(%)"은 서열을 정렬하고, 필요한 경우 갭을 도입하여 최대 서열 동일성%를 달성하고, 임의의 보존적 치환을 서열 동일성의 일부로서 간주하지 않은 후, 특정(모) 서열의 아미노산 잔기와 동일한 후보 서열 내 아미노산 잔기의 백분율(%)로 정의된다. 아미노산 서열 동일성%를 결정하기 위한 정렬은, 예를 들어 BLAST, BLAST-2, ALIGN 또는 Megalign(DNASTAR) 소프트웨어와 같은 공개적으로 이용 가능한 컴퓨터 소프트웨어를 사용하여 당업계의 기술에 속하는 다양한 방식으로 달성될 수 있다. 당업자는, 비교되는 서열의 전체 길이에 대하여 최대 정렬을 달성하는 데 필요한 임의의 알고리즘을 포함하여, 정렬 측정을 위한 적절한 매개변수를 결정할 수 있다. 하나의 특정한 프로그램은 미국 특허출원공개 제20160244525호의 단락 [0279] 내지 [0280]에 개괄된 ALIGN-2 프로그램이며, 상기 문헌은 본원에 참조로서 인용된다.
본 발명의 아미노산 서열("발명 서열")과 모 아미노산 서열 사이의 동일성 정도는, 2개 서열의 정렬에서 정확한 매칭의 수를, "발명 서열"의 길이 또는 모 서열의 길이(어느 것이든 가장 짧은 쪽)로 나눈 값으로 계산된다. 결과는 동일성%로 표현된다.
일부 구현예에서, 2개 이상의 아미노산 서열은 적어도 50%, 60%, 70%, 80% 또는 90% 동일하다. 일부 구현예에서, 2개 이상의 아미노산 서열은 적어도 95%, 97%, 98%, 99% 또는 심지어 100% 동일하다.
특정 항원 또는 에피토프(이 경우, 인간 LAG-3)에 대해 "특이적으로 결합하는" 또는 "특이적으로 결합한다" 또는 "특이적인"은, 비특이적 상호작용과 측정 가능하게 상이한 결합을 의미한다. 특이적 결합은, 예를 들어 분자의 결합을 일반적으로 결합 활성을 갖지 않는 유사한 구조의 분자인 대조군 분자의 결합과 비교하여 결정함으로써 측정될 수 있다. 예를 들어, 특이적 결합은 표적과 유사한 대조군 분자와의 경쟁에 의해 측정될 수 있다.
특정 항원 또는 에피토프에 대한 특이적 결합은, 예를 들어 항체가 항원 또는 에피토프에 대하여, 적어도 약 10-4 M, 적어도 약 10-5 M, 적어도 약 10-6 M, 적어도 약 10-7 M, 적어도 약 10-8 M, 적어도 약 10-9 M, 대안적으로 적어도 약 10-10 M, 적어도 약 10-11 M, 적어도 약 10-12 M 또는 그 이상의 KD를 갖는 것으로 나타날 수 있으며, 여기서 KD는 특정 항체-항원 상호작용의 해리 속도를 나타낸다. 전형적으로, 항원에 특이적으로 결합하는 항체는 항원 또는 에피토프에 비해 대조군 분자에 대하여 20배, 50배, 100배, 500배, 1000배, 5,000배, 10,000배 또는 그 이상의 KD를 가질 것이다.
또한, 특정 항원 또는 에피토프에 대한 특이적 결합은, 예를 들어 항체가 대조군에 비해 에피토프에 대하여 적어도 20배, 50배, 100배, 500배, 1000배, 5,000배, 10,000배 또는 그 이상의 항원 또는 에피토프에 대한 KA 또는 Ka를 갖는 것으로 나타날 수 있으며, 여기서 KA 또는 Ka는 특정 항체-항원 상호작용의 해리 속도를 나타낸다. 결합 친화성은 일반적으로 Biacore 검정을 사용하여 측정된다.
II. 도입
본 발명은 한쪽에 IL-15 복합체 및 다른 한쪽에 항-인간 LAG-3 항원 결합 도메인을 함유하는 이종이량체 융합 단백질을 제공한다. 따라서, 본 발명의 이종이량체 융합 단백질은 체크포인트 LAG-3 항원에 결합할 수 있고, 공통 감마 사슬(γc; CD132) 및/또는 IL-2 수용체 β-사슬(IL-2Rβ; CD122)과 복합체를 형성할 수 있다. 일반적으로, 본 발명의 이종이량체 융합 단백질은 IL-15/IL-15Rα(스시) 구성요소(일반적으로 "IL-15 복합체"로 지칭됨), 융합 단백질을 LAG-3을 발현하는 세포에 제공함으로써 "표적화" 모이어티로서 작용하는 항-LAG-3 ABD 구성요소, 및 Fc 구성요소의 세 가지 기능성 구성요소를 가지며, 이들은 각각 상이한 형태를 취할 수 있고, 임의의 입체구조로 다른 구성요소와 조합될 수 있다.
일반적으로, 본원에 보다 충분히 기재된 바와 같이, 본 발명의 융합 단백질은 항체 Fc 도메인의 회합을 기반으로 하는 이종이량체 단백질이다. 즉, 동종이량체보다 이종이량체의 형성이 선호되도록 조작된 두 가지 상이한 변이체 Fc 도메인을 사용하면, 이종이량체 단백질이 형성된다. 이러한 경우, 상기 변이체 Fc 도메인 중 하나는 IL-15/Rα 복합체에 융합되고, 다른 하나는 본원에 보다 충분히 개괄된 바와 같은 LAG-3 ABD이다. 선택적 pI 변이체를 포함시키면, 이종이량체는 동종이량체로부터 더 용이하게 정제될 수 있다. 또한, 절제 변이체의 포함은 Fc 도메인의 효과기 기능을 제거한다.
A. IL-15/IL-15Rα(스시) 도메인
도면에 제시된 바와 같이, IL-15 복합체는 몇 가지 형태를 취할 수 있다. 상기 언급된 바와 같이, IL-15 단백질 자체는 IL-15Rα 단백질과 복합체를 형성할 때 덜 안정하다. 당업계에 공지된 바와 같이, IL-15Rα 단백질은 IL-15 결합 활성을 보유하는 수용체의 가장 짧은 영역인 "스시 도메인"을 함유한다. 따라서, 전체 IL-15Rα 단백질을 포함하는 이종이량체 융합 단백질이 만들어질 수 있지만, 본원의 바람직한 구현예는 스시 도메인만을 사용하는 복합체를 포함하며, 이의 서열은 도면에 제시되어 있다.
따라서, IL-15 복합체는 일반적으로 IL-15 단백질 및 IL-15Rα의 스시 도메인을 포함한다(전장 서열이 사용된다고 달리 언급되지 않는 한, "IL-15Rα", "IL-15Rα(스시)", "IL-15RA" 및 "스시"는 명세서 전반에 걸쳐 상호교환적으로 사용됨).
중요하게는, IL-15 구성요소는 일반적으로 이의 역가가 감소되도록 조작된다. 다수의 구현예에서, 야생형 IL-15는 너무 강력하여, 바람직하지 않은 독성을 유발할 수 있다. 따라서, IL-15 복합체의 IL-15 구성요소는 활성을 감소시키는 하나 이상의 아미노산 치환을 가질 수 있다. 다양한 아미노산 치환이 만들어지고(도 19 참조), 시험되었다(도 20 참조). 일부 구현예에서 특히 관심있는 것은, 이중 변이체인 N4D/N65D 또는 D30N/N65D, 또는 삼중 변이체인 D30N/E64Q/N65D이다.
본 발명의 표적화 IL-15/IL-15Rα 이종이량체 융합 단백질은 IL-15/IL-15 수용체 알파(IL-15Rα)-Fc 융합 단량체를 포함하며; 이는 2017년 10월 16일자 출원된 US2018/0118828, 2016년 10월 14일자 출원된 미국 특허출원 제62/408,655호, 2016년 11월1일자 출원된 미국 특허출원 제62/416,087호, 2017년 1월 6일자 출원된 미국 특허출원 제62/443,465호, 2017년 3월 28일자 출원된 미국 특허출원 제62/477,926호, 및 2018년 4월 18일자 출원된 미국 특허출원 제62/659,571호에 기재되어 있으며, 상기 문헌들은 그 전문이, 특히 그 안에 개괄된 서열이 본원에 참조로서 인용된다. 일부 경우에, IL-15 단백질 도메인과 IL-15 수용체 알파(IL-15Rα) 단백질 도메인은 상이한 배향으로 존재한다. IL-15/IL-15Rα-Fc 융합 단량체의 예시적인 구현예는, 예를 들어 US 2018/0118828에 기재된 바와 같이 XENP21480(사슬 1; 도 64a), XENP22022(사슬 1, 도 64d), XENP22112(사슬 1 및 사슬 3; 도 64e), XENP22641(사슬 2 및 사슬 4; 도 64f), XENP22642(사슬 1 및 사슬 4; 도 64h) 및 XENP22644(사슬 1 및 사슬 4; 도 64i)에 제시되어 있다.
1. IL-15 변이체
일부 구현예에서, 인간 IL-15 단백질은 도 2에 제시된 바와 같이 NCBI 기준 서열번호 NP_000576.1에 기재된 아미노산 서열을 갖는다. 일부 경우에, 인간 IL-15의 코딩 서열은 NCBI 기준 서열번호 NM_000585에 기재되어 있다. 본원에 개괄된 Fc 융합 이종이량체 단백질의 예시적인 IL-15 단백질은 서열번호 2의 아미노산 서열 또는 서열번호 1의 49번 내지 162번의 아미노산을 가질 수 있다. 일부 구현예에서, IL-15 단백질은 서열번호 2와 적어도 90%, 예를 들어 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 그 이상의 동일성을 갖는다. 일부 구현예에서, IL-15 단백질은 아미노산 치환 N72D를 갖는 것을 제외하고는, 서열번호 2에 기재되어 있는 아미노산 서열을 갖는다. 다른 구현예에서, IL-15 단백질은 C42S, L45C, Q48C, V49C, L52C, E53C, E87C 및 E89C로 이루어진 군으로부터 선택되는 하나 이상의 아미노산 치환을 제외하고는, 서열번호 2의 아미노산 서열을 갖는다. 일부 양태에서, IL-15 단백질은 N1D, N4D, D8N, D30N, D61N, E64Q, N65D 및 Q108E로 이루어지는 군으로부터 선택되는 하나 이상의 아미노산 치환을 갖는다. 다른 구현예에서, 아미노산 치환은 N4D/N65D이다. 특정 구현예에서, 아미노산 치환은 D30N/N65D이다. 일부 구현예에서, 아미노산 치환은 Q108E이다. 특정 구현예에서, 아미노산 치환은 N65D이다. 다른 구현예에서, 아미노산 치환은 D30N/E64Q/N65D이다. 특정 구현예에서, 아미노산 치환은 N65D이다. 일부 경우에, 아미노산 치환은 N1D/N65D이다. 일부 경우에, 아미노산 치환은 D30N/N65D이다. 선택적으로, IL-15 단백질은 또한 N72D 치환을 갖는다. Fc 융합 단백질의 IL-15 단백질은 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개 또는 9개의 아미노산 치환을 가질 수 있다. 일부 구현예에서, Fc 융합 단백질의 IL-15 단백질은 D30N 치환을 갖는다. 일부 구현예에서, Fc 융합 단백질의 IL-15 단백질은 N65D 치환을 갖는다. 일부 구현예에서, Fc 융합 단백질의 IL-15 단백질은 IL-15:CD132 인터페이스에 하나 이상의 아미노산 치환을 갖는다. 특정 구현예에서, 본원에 기재된 Fc 융합 단백질은 NK세포 및 CD8+ T세포의 증식을 유도한다. 또한, 본 발명의 표적화 IL-15/IL-15Rα 이종이량체 단백질과 함께 사용될 수 있는 IL-15 변이체는 도 19a 내지 도 19c에 포함되어 있다.
일부 구현예에서, 인간 IL-15 수용체 알파(IL-15Rα) 단백질은 NCBI 기준 서열번호 NP_002180.1 또는 서열번호 3에 기재된 아미노산 서열을 갖는다. 일부 경우에, 인간 IL-15Rα의 코딩 서열은 NCBI 기준 서열번호 NM_002189.3에 기재되어 있다. 본원에 개괄된 Fc 융합 이종이량체 단백질의 예시적인 IL-15Rα 단백질은 서열번호 3의 스시 도메인(예를 들어, 서열번호 3의 31번 내지 95번의 아미노산), 또는 다르게 말하면 서열번호 4의 아미노산 서열을 포함하거나 이로 이루어질 수 있다. 일부 구현예에서, IL-15Rα 단백질은 서열번호 4의 아미노산 서열, 및 D96, P97, A98, D96/P97, D96/C97, D96/P97/A98, D96/P97/C98 및 D96/C97/A98로 이루어지는 군으로부터 선택되는 아미노산 삽입을 가지며, 여기서 아미노산 위치는 전장 인간 IL-15Rα 단백질 또는 서열번호 3을 기준으로 한 것이다. 예를 들어, D(예를 들어, Asp), P(예를 들어, Pro), A(예를 들어, Ala), DP(예를 들어, Asp-Pro), DC(예를 들어, Asp-Cys), DPA(예를 들어, Asp-Pro-Ala), DPC(예를 들어, Asp-Pro-Cys) 또는 DCA(예를 들어, Asp-Cys-Ala)와 같은 아미노산(들)이 서열번호 4의 IL-15Rα 단백질의 C-말단에 부가될 수 있다. 일부 구현예에서, IL-15Rα 단백질은 서열번호 4의 아미노산 서열, 및 K34C, A37C, G38C, S40C 및 L42C로 이루어지는 군으로부터 선택되는 하나 이상의 아미노산 치환을 가지며, 여기서 아미노산 위치는 서열번호 4를 기준으로 한 것이다. IL-15Rα 단백질은 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개 또는 그 이상의 아미노산 돌연변이(예를 들어, 치환, 삽입 및/또는 결실)를 가질 수 있다.
2. IL-15/Rα 복합체
본원에 개괄된 바와 같이, IL-15 변이체 및 스시 도메인은 IL-15 복합체를 형성하기 위해 적어도 3가지 상이한 방식으로 복합체화될 수 있다.
일부 구현예에서, 도 21b에 제시된 바와 같이, IL-15 단백질과 IL-15Rα(스시)는 공유결합으로 부착되는 것이 아니라, 규칙적인 리간드-리간드 상호작용을 통해 자가 조립된다. 본원에 보다 충분히 기재된 바와 같이, 이는 (일반적으로 선택적 도메인 링커를 사용하여) Fc 도메인에 공유결합으로 연결된 스시 도메인 또는 IL-15 도메인일 수 있다. 다시 말하면, 이러한 구현예서 특히 사용되는 것은, 야생형 스시 도메인과 함께 사용되는, 이중 변이체인 N4D/N65D 또는 D30N/N65D, 또는 삼중 변이체인 D30N/E64Q/N65D이다.
대안적인 구현예에서, 변이체 IL-15는 일반적으로 도 21d에 제시된 바와 같이 공유결합으로 부착되도록 도메인 링커를 사용하여 스시 도메인에 복합체화될 수 있으며; 상기 도면에는 스시 도메인이 N-말단 도메인으로 도시되어 있지만, 이는 역전될 수 있다. 다시 말하면, 이러한 구현예서 특히 사용되는 것은, 야생형 스시 도메인과 함께 사용되는, 이중 변이체인 N4D/N65D 또는 D30N/N65D, 또는 삼중 변이체인 D30N/E64Q/N65D이다. IL-15 변이체를 스시 도메인에 부착시키는 데 사용될 수 있는 예시적인 도메인 링커는 도 8에 도시되어 있다.
대안적으로, IL-15 및 스시 도메인은 각각 일반적으로 도 21c에 제시된 바와 같이 다이설파이드 결합을 형성하여 복합체를 형성하는 시스테인 아미노산을 함유하도록 조작될 수 있으며, 다시 말하면, IL-15 도메인 또는 스시 도메인은 (선택적 도메인 링커를 사용하여) Fc 도메인에 공유결합으로 부착된다. 다시 말하면, 이러한 구현예서 특히 사용되는 것은, 시스테인을 제공하기 위해 또한 아미노산 치환을 포함하는 스시 도메인과 함께 사용되는, 이중 변이체인 N4D/N65D 또는 D30N/N65D(추가로 시스테인에 대한 아미노산 치환을 포함함), 또는 삼중 변이체인 D30N/E64Q/N65D(추가로 시스테인에 대한 아미노산 치환을 포함함)이다.
추가의 특정 구현예가 하기에 개괄된다.
B. 항-LAG-3 구성요소
일부 구현예에서, 본원에 제공된 이종이량체 융합 단백질은 일부 항체 구성요소를 포함한다.
전형적인 항체 구조 단위는 전형적으로 사량체를 포함한다. 각각의 사량체는 전형적으로 2개의 동일한 폴리펩타이드 사슬의 쌍으로 구성되어 있으며, 각각의 쌍은 하나의 "경쇄"(전형적으로 분자량이 약 25 kDa임)와 하나의 "중쇄"(전형적으로 분자량이 약 50 내지 70 kDa임)를 갖는다. 인간 경쇄는 카파 경쇄와 람다 경쇄로 분류된다. 본 발명은, 비제한적으로, IgG1, IgG2, IgG3 및 IgG4를 포함하여 몇 가지 서브클래스를 갖는, 일반적으로 IgG 클래스를 기반으로 하는 항체 또는 항체 단편(항체 단량체)에 관한 것이다. 일반적으로, IgG1, IgG2 및 IgG4가 IgG3보다 자주 사용된다. IgG1이 356(D 또는 E) 및 358(L 또는 M)에서 다형성을 갖는 상이한 알로타입을 갖는다는 점에 주목해야 한다. 본원에 도시된 서열은 356D/358M 알로타입을 사용하지만, 다른 알로타입도 본원에 포함된다. 즉, 본원에 포함된 IgG1 Fc 도메인을 포함하는 임의의 서열은 356D/358M 알로타입 대신 356E/358L을 가질 수 있다.
또한, 본원의 다수의 단량체 서열은 다이설파이드 형성을 감소시키기 위해 220번 위치에서 세린으로 대체되는 적어도 하나의 시스테인을 갖는다. 대체된 이러한 시스테인(C220S) 중 하나 또는 둘 모두는 특히 본원의 서열 내에 포함된다.
따라서, 본원에 사용된 "아이소타입"은 이들의 불변 영역의 화학적 및 항원적 특징에 의해 정의된 면역글로불린의 임의의 서브클래스를 의미한다.
각 사슬의 아미노-말단 부분은 주로 항원 인식을 담당하는 약 100개 내지 110개 또는 그 이상의 아미노산의 가변 영역을 포함하며, 이는 일반적으로 당업계 및 본원에서 "Fv 도메인"또는 "Fv 영역"으로 지칭된다. 가변 영역에서, 중쇄 및 경쇄의 V 도메인 각각에 대하여 3개의 루프가 모여서 항원 결합 부위를 형성한다. 각각의 루프는 아미노산 서열의 변화가 가장 유의한, 상보성 결정 영역(이하, "CDR"로 지칭됨)으로 지칭된다. "가변"은, 가변 영역의 특정 분절이 항체들 간 서열에서 광범위하게 상이하다는 사실을 나타낸다. 가변 영역 내 가변성은 균일하게 분포되어 있지 않다. 대신, V 영역은 각각 9개 내지 15개의 아미노산 또는 그 이상의 길이인 "초가변 영역"으로 불리는 극심한 가변성의 더 짧은 영역에 의해 분리된, 15개 내지 30개 아미노산의 프레임워크 영역(FR)으로 불리는 비교적 불변의 스트레치로 이루어진다.
각각의 VH 및 VL은 다음의 순서로 아미노-말단에서 카르복시-말단으로 배열된, 3개의 초가변 영역("상보성 결정 영역", "CDR") 및 4개의 FR로 구성된다: FR1-CDR1-FR2-CDR2-FR3-CDR3-FR4.
초가변 영역은 일반적으로 경쇄 가변 영역에서 약 24번 내지 34번(LCDR1; "L"은 경쇄를 나타냄), 50번 내지 56번(LCDR2) 및 89번 내지 97번(LCDR3)의 아미노산 잔기로부터의 아미노산 잔기, 및 중쇄 가변 영역에서 약 31번 내지 35B번(HCDR1; "H"는 중쇄를 나타냄), 50번 내지 65번(HCDR2) 및 95번 내지 102번(HCDR3)의 아미노산 잔기로부터의 아미노산 잔기(문헌[Kabat et al., SEQUENCES OF PROTEINS OF IMMUNOLOGICAL INTEREST, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, Md. (1991)]) 및/또는 초가변 루프를 형성하는 잔기(예를 들어, 경쇄 가변 영역에서 26번 내지 32번(LCDR1), 50번 내지 52번(LCDR2) 및 91번 내지 96번(LCDR3)의 잔기, 및 중쇄 가변 영역에서 26번 내지 32번(HCDR1), 53번 내지 55번(HCDR2) 및 96번 내지 101번(HCDR3))의 잔기(문헌[Chothia and Lesk (1987) J. Mol. Biol. 196:901-917])를 포함한다. 본 발명의 특정 CDR이 하기에 기재된다.
당업자가 이해하는 바와 같이, CDR의 정확한 넘버링 및 배치는 상이한 넘버링 시스템들 간에 상이할 수 있다. 하지만, 가변 중쇄 및/또는 가변 경쇄 서열의 개시내용이 관련된(고유한) CDR의 개시내용을 포함한다는 것을 이해해야 한다. 따라서, 각각의 가변 중쇄 영역의 개시내용은 vhCDR(예를 들어, vhCDR1, vhCDR2 및 vhCDR3)의 개시내용이며, 각각의 가변 경쇄 영역의 개시내용은 vlCDR(예를 들어, vlCDR1, vlCDR2 및 vlCDR3)의 개시내용이다.
CDR 넘버링의 유용한 비교는 문헌[Lafranc et al., Dev. Comp. Immunol. 27(1):55-77 (2003)]를 참조한다.
본 명세서 전반에 걸쳐, Kabat 넘버링 시스템은 일반적으로 가변 도메인의 잔기(대략, 경쇄 가변 영역의 1번 내지 107번 잔기 및 중쇄 가변 영역의 1번 내지 113번 잔기)를 언급할 때 사용되고, EU 넘버링 시스템은 Fc 영역에 대하여 사용된다(예를 들어, 상기 Kabat 등의 문헌(1991) 참조).
본 발명은 다수의 상이한 CDR 세트를 제공한다. 이러한 경우, "완전 CDR 세트"는 3개의 가변 경쇄 CDR과 3개의 가변 중쇄 CDR, 예를 들어 vlCDR1, vlCDR2, vlCDR3, vhCDR1, vhCDR2 및 vhCDR3을 포함한다. 이들은 각각 더 큰 가변 경쇄 도메인 또는 가변 중쇄 도메인의 일부일 수 있다. 또한, 본원에 보다 충분히 개괄된 바와 같이, 가변 중쇄 도메인 및 가변 경쇄 도메인은 중쇄 및 경쇄가 사용되는 경우(예를 들어, Fab이 사용되는 경우) 별개의 폴리펩타이드 사슬에 존재하거나, scFv 서열의 경우에는 단일 폴리펩타이드 사슬에 존재할 수 있다.
CDR은 항원 결합, 또는 보다 구체적으로 항체의 에피토프 결합 부위의 형성에 기여한다. "에피토프"는 파라토프로 공지된 항체 분자의 가변 영역에서 특이적 항원 결합 부위와 상호작용하는 결정기를 나타낸다. 에피토프는 아미노산 또는 당 측쇄와 같은 분자의 그룹이며, 통상적으로 특정한 구조 특징 및 특정한 전하 특징을 갖는다. 단일 항원은 하나 초과의 에피토프를 가질 수 있다.
에피토프는 결합에 직접 관여하는 아미노산 잔기(에피토프의 면역우세 구성요소로도 불림) 및 결합에 직접 관여하지 않는 다른 아미노산 잔기, 예컨대 특이적인 항원 결합 펩타이드에 의해 효과적으로 차단되는 아미노산 잔기(즉, 상기 아미노산 잔기는 특이적인 항원 결합 펩타이드의 풋프린트 내에 있음)를 포함할 수 있다.
에피토프는 입체구조 또는 선형일 수 있다. 입체구조 에피토프는 선형 폴리펩타이드 사슬의 상이한 분절로부터 공간적으로 병치된 아미노산에 의해 생성된다. 선형 에피토프는 폴리펩타이드 사슬의 인접한 아미노산 잔기에 의해 생성된 것이다. 입체구조 및 비(非)입체구조 에피토프는, 변성 용매의 존재 하에서 비입체구조 에피토프에 대한 결합이 아닌 입체구조 에피토프에 대한 결합이 손실된다는 점에서 구별될 수 있다.
에피토프는 전형적으로 고유한 공간 입체구조에서 적어도 3개, 보다 일반적으로 적어도 5개, 또는 8개 내지 10개의 아미노산을 포함한다. 동일한 에피토프를 인식하는 항체는 단순한 면역검정에서 입증될 수 있는데, 이는 표적 항원에 대한 또 다른 항체의 결합을 차단하는 하나의 항체의 능력, 예를 들어 "비닝(binning)"을 보여준다. 하기에 개괄되는 바와 같이, 본 발명은 본원에 열거된 항원 결합 도메인 및 항체를 포함할 뿐 아니라, 열거된 항원 결합 도메인에 의해 결합된 에피토프와의 결합에서 경쟁하는 것들을 포함한다.
각 사슬의 카르복시-말단 부분은 주로 효과기 기능을 담당하는 불변 영역을 정의한다. Kabat 등은 중쇄 및 경쇄의 가변 영역의 수많은 1차 서열을 수집하였다. 서열의 보존 정도에 기반하여, 이들은 각각의 1차 서열을 CDR 및 프레임워크로 분류하고 이의 목록을 작성하였다(문헌[SEQUENCES OF IMMUNOLOGICAL INTEREST, 5th edition, NIH publication, No. 91-3242, E.A. Kabat et al.](이는 그 전문이 본원에 참조로서 인용됨) 참조).
면역글로불린의 IgG 서브클래스에는, 중쇄에 몇몇 면역글로불린 도메인이 존재한다. 본원에서 "면역글로불린(Ig) 도메인"이란, 별개의 3차 구조를 갖는 면역글로불린의 영역을 의미한다. 본 발명에서 관심있는 것은 불변 중쇄(CH) 도메인 및 힌지 도메인을 포함하는 중쇄 도메인이다. IgG 항체의 맥락에서, IgG 아이소타입은 각각 3개의 CH 영역을 갖는다. 따라서, IgG의 맥락에서 "CH" 도메인은 다음과 같다: "CH1"은 Kabat에서와 같이 EU 인덱스에 따라 118번 내지 220번 위치를 나타낸다. "CH2"는 Kabat에서와 같이 EU 인덱스에 따라 237번 내지 340번 위치를 나타내고, "CH3"은 Kabat에서와 같이 EU 인덱스에 따라 341번 내지 447번 위치를 나타낸다. 본원에 제시되고 하기에 기재되는 바와 같이, pI 변이체는 하기 논의되는 힌지 영역뿐 아니라 하나 이상의 CH 영역에 있을 수 있다.
중쇄의 또 다른 유형의 Ig 도메인은 힌지 영역이다. 본원에서 "힌지" 또는 "힌지 영역" 또는 "항체 힌지 영역" 또는 "면역글로불린 힌지 영역"이란, 항체의 제1 불변 도메인과 제2 불변 도메인 사이에 아미노산을 포함하는 가요성 폴리펩타이드를 의미한다. 구조적으로, IgG CH1 도메인은 EU 220번 위치에서 종결되고, IgG CH2 도메인은 EU 237번 위치의 잔기에서 시작된다. 따라서, IgG의 경우, 항체 힌지는 본원에서 221번(IgG1에서 D221) 내지 236번(IgG1에서 G236) 위치를 포함하도록 정의되며, 여기서 넘버링은 Kabat에서와 같이 EU 인덱스에 따른다. 일부 구현예에서, 예를 들어 Fc 영역의 맥락에서, 하부 힌지가 포함되며, 여기서 "하부 힌지"는 일반적으로 226번 또는 230번 위치를 나타낸다. 본원에 언급된 바와 같이, pI 변이체는 또한 힌지 영역에서 만들어질 수 있다.
경쇄는 일반적으로 2개의 도메인, 즉 가변 경쇄 도메인(경쇄 CDR을 함유하고, 가변 중쇄 도메인과 함께 Fv 영역을 형성함) 및 불변 경쇄 영역(종종 CL 또는 Cκ로 지칭됨)을 포함한다.
본원에 개괄된 추가 치환을 위해 관심있는 또 다른 영역은 Fc 영역이다.
따라서, 본원에 제공된 본 발명의 이종이량체 융합 단백질은 하나 이상의 항체 도메인을 포함한다. 본원에 기재되고 당업계에 공지된 바와 같이, 본원에 제공된 이종이량체 항체는 중쇄 및 경쇄 내에 상이한 도메인을 포함하며, 이들은 또한 중첩될 수 있다. 이러한 도메인에는, 비제한적으로, Fc 도메인, CH1 도메인, CH2 도메인, CH3 도메인, 힌지 도메인, 중쇄 불변 도메인(CH1-힌지-Fc 도메인 또는 CH1-힌지-CH2-CH3), 가변 중쇄 도메인, 가변 경쇄 도메인, 경쇄 불변 도메인, Fab 도메인 및 scFv 도메인이 포함된다.
일반적으로 본원에 개괄된 바와 같이, 본 발명의 이종이량체 단백질은 인간 LAG-3에 결합하는 하나 이상의 LAG-3 항원 결합 도메인(예를 들어, Fv)을 포함한다. 본원에 사용된 "림프구 활성화 유전자 3", "LAG-3", "LAG3", "CD223" 및 "분화 클러스터 3"(예를 들어, Genebank 수탁번호 NM_002286 및 NP_002277(인간))은, 4개의 세포외 Ig 유사 도메인을 갖는 제1형 막관통 단백질인 면역글로불린(Ig) 수퍼패밀리의 구성원을 의미한다. LAG-3은 T세포의 음성 조절자이며, CTLA-4 및 PD-1을 포함하는 다른 체크포인트 분자와 함께 작동하는 것으로 보인다. 1990년에, Triebel등은 LAG3을 활성화된 인간 자연 살해(NK)세포주 및 T세포주에 의해 발현되는 막관통 단백질로서 발견하였지만, 이는 또한 B세포에서도 발현될 수 있다. 인간 LAG3 유전자는 인간 CD4 유전자와 20% 동일성을 갖기 때문에, 표면 발현된 LAG-3 단백질은 높은 친화성으로 주요 조직적합성 복합체(MHC) 클래스 II 분자에 결합할 수 있다. LAG-3은 막 근위 연결 펩타이드의 단백질분해 절단을 통해 인터페론-감마 생성 CD4 양성 T세포에 의해 방출되는 가용성 형태 또는 세포 표면 이량체로 존재한다. 예시적인 LAG-3 서열은 도 3에 도시되어 있다.
본 발명의 이종이량체 융합 단백질의 Fv 또는 항-LAG-3 구성요소(항-LAG-3 항원 결합 도메인 또는 LAG-3 ABD)는, 일반적으로 인간 LAG-3와 결합할 수 있는 Fv 도메인을 형성하는 6개 CDR의 세트 및/또는 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 본원에 기재된 바와 같이, 일반적으로 본원에 개괄된 바와 같이 scFv 또는 Fab을 사용함으로써 사용될 수 있는 다수의 상이한 형식이 존재한다.
특정 구현예에서, 본 발명의 ABD는 특정 생식계열 중쇄 면역글로불린 유전자로부터의 프레임워크를 갖는 중쇄 가변 영역 및/또는 특정 생식계열 경쇄 면역글로불린 유전자로부터의 경쇄 가변 영역을 포함한다. 예를 들어, 이러한 ABD는 특정 생식계열 서열의 "산물"이거나 "이에서 유도된" 중쇄 가변 영역 또는 경쇄 가변 영역을 포함하는 인간 ABD를 포함하거나 이로 이루어질 수 있다. 인간 생식계열 면역글로불린 서열의 "산물"이거나 "이에서 유래된" ABD는 ABD의 아미노산 서열을 인간 생식계열 면역글로불린의 아미노산 서열과 비교하고, ABD의 서열과 가장 가까운 서열(즉, 가장 높은 동일성%)의 인간 생식계열 면역글로불린 서열을 선택함으로써 식별될 수 있다. 특정 인간 생식계열 면역글로불린 서열의 "산물"이거나 "이에서 유도된" ABD는, 예를 들어 ABD, 자연 발생 체세포 돌연변이 또는 부위 특이적 돌연변이의 의도적인 도입으로 인해, 생식계열 서열과 비교하여 아미노산 차이를 함유할 수 있다. 하지만, 인간화 ABD는 전형적으로 인간 생식계열 면역글로불린 유전자에 의해 인코딩된 아미노산 서열과 아미노산 서열이 적어도 90% 동일하며, 다른 종의 생식계열 면역글로불린 아미노산 서열(예를 들어, 쥣과 생식계열 서열)과 비교할 때 ABD를 인간 서열에서 유도된 것으로서 식별하는 아미노산 잔기를 함유한다. 특정 경우에, 인간화 ABD는 생식계열 면역글로불린 유전자에 의해 인코딩되는 아미노산 서열과, 아미노산 서열에 있어, 적어도 95%, 96%, 97%, 98% 또는 99%, 또는 심지어 적어도 96%, 97%, 98% 또는 99% 동일할 수 있다. 전형적으로, 특정 인간 생식계열 서열에서 유도된 인간화 ABD는 인간 생식계열 면역글로불린 유전자에 의해 인코딩된 아미노산 서열로부터 최대 10개 내지 20개의 아미노산 차이를 나타낼 것이다(본원에서 임의의 비대칭 변이체, pI 변이체 및 절제 변이체의 도입 이전에; 즉, 본 발명의 변이체의 도입 이전에 변이체의 수는 일반적으로 적음). 특정 경우에, 인간화 ABD는 생식계열 면역글로불린 유전자에 의해 인코딩된 아미노산 서열로부터 5개 이하, 또는 심지어 4개, 3개, 2개 또는 1개 이하의 아미노산 차이를 나타낼 수 있다(다시 말하면, 본원에서 임의의 비대칭 변이체, pI 변이체 및 절제 변이체의 도입 이전에, 즉, 본 발명의 변이체를 도입하기 이전에 변이체의 수는 일반적으로 적음). 하나의 구현예에서, 모 ABD는 당업계에 공지된 바와 같이 친화성이 성숙되어 있다. 구조 기반 방법은, 예를 들어 미국 특허출원 USSN 제11/004,590호에 기재된 바와 같이 인간화 및 친화성 성숙을 위해 이용될 수 있다. 선택 기반 방법은 항체 가변 영역을 인간화하고/하거나 이의 친화성을 성숙시키기 위해 이용될 수 있으며, 이에는, 비제한적으로, 문헌[Wu et al., 1999, J. Mol. Biol. 294:151-162]; 문헌[Baca et al., 1997, J. Biol. Chem. 272(16):10678-10684]: 문헌[Rosok et al., 1996, J. Biol. Chem. 271(37): 22611-22618]; 문헌[Rader et al., 1998, Proc. Natl. Acad. Sci. USA 95: 8910-8915]; 문헌[Krauss et al., 2003, Protein Engineering 16(10):753-759](이들은 모두 그 전문이 본원에 참조로서 인용됨)에 기재된 방법이 포함된다. 다른 인간화 방법은 CDR의 일부만 이식하는 것을 포함할 수 있으며, 이에는, 비제한적으로, 미국 특허출원 USSN 제09/810,510호; 문헌[Tan et al., 2002, J. Immunol. 169:1119-1125]; 문헌[De Pascalis et al., 2002, J. Immunol. 169:3076-3084](이들은 모두 그 전문이 본원에 참조로서 인용됨)에 기재된 방법이 포함된다.
본원에 제시된 바와 같이, 항-LAG-3 ABD는 Fab 또는 scFv의 형태일 수 있다.
일부 구현예에서, 예를 들어 도 21b 및 도 21c에 도시된 바와 같이, 항-LAG-3 ABD는 scFv이며, 여기서 VH 도메인과 VL 도메인은 선택적으로 하전된 scFv 링커일 수 있는 scFv 링커를 사용하여 연결된다. 당업자가 이해하는 바와 같이, scFv는, N-말단에서 C-말단으로, N-VH-scFv 링커-VL-C 또는 N-VL-scFv 링커-VH-C로 조립될 수 있으며, 여기서 scFv 도메인의 C-말단은 일반적으로 힌지-CH2-CH3 Fc 도메인에 연결되고, 이러한 경우 힌지는 도메인 링커로 작용한다. 적합한 Fv(CDR 세트, 및 가변 중쇄 도메인/가변 경쇄 도메인 포함)는 도면에 제시된, 및 WO2017/218707에 개시된 scFv 형식 또는 Fab 형식으로 사용될 수 있으며, 상기 문헌은 모든 목적을 위하여 그 전문이, 특히 LAG-3 ABD에 대하여, 도 11, 도 18, 도 55, 도 56, 도 63의 데이터, 서열목록의 서열번호 36819-36962, 서열번호 35417-35606, 서열번호 25914-32793 및 서열번호 32794-33002의 서열이 본원에 참조로서 인용된다.
나아가 당업자가 이해하는 바와 같이, 힌지(이는 또한 IgG1, IgG2 또는 IgG4의 야생형 힌지, 또는 이의 변이체, 예컨대 모 IgG4 힌지 폴리펩타이드를 기준으로 228번 위치에서 프롤린 치환을 갖는 IgG4 S241P 또는 S228P 힌지 변이체(여기서 넘버링 S228P는 EU 인덱스에 따른 것이고, S241P는 Kabat 넘버링에 따른 것임)일 수 있음)의 일부 또는 전부가 scFv와 CH2-CH3 도메인 사이의 도메인 링커로서 사용될 수 있거나, 또는 도면에 도시된 바와 같은 상이한 도메인 링커가 사용될 수 있다.
대안적으로, LAG-3 ABD는 Fab 단편의 형태일 수 있다. 이러한 구현예에서, ABD는 중쇄에 의해 제공되는 가변 중쇄 도메인, 및 경쇄에 의해 제공되는 가변 경쇄 도메인으로 구성된다. 적합한 Fv(CDR 세트, 및 가변 중쇄 도메인/가변 경쇄 도메인 포함)는 도면에 제시된, 및 WO2017/218707에 개시된 scFv 형식 또는 Fab 형식으로 사용될 수 있으며, 상기 문헌은 모든 목적을 위하여 그 전문이, 특히 LAG-3 ABD에 대하여, 도 11, 도 18, 도 55, 도 56, 도 63의 데이터, 서열목록의 서열번호 36819-36962, 서열번호 35417-35606, 서열번호 25914-32793 및 서열번호 32794-33002의 서열이 본원에 참조로서 인용된다.
당업자가 이해하는 바와 같이, 적합한 LAG-3 결합 도메인은 서열목록 및 도면(예를 들어, 도 12 및 도 13)도시된 바와 같은 6개 CDR의 세트를 포함할 수 있으며, 이는 밑줄이 그어져 있거나/볼드체로 표시되어 있거나, 또는 본원에 기재된 바 및 표 2에 제시된 바와 같이 상이한 넘버링 체계가 사용되는 경우에는, 도면(예를 들어, 도 12 및 도 13a 내지 도 13c) 및 서열목록에 도시된 것들의 가변 중쇄(VH) 도메인 및 가변 경쇄 도메인(VL) 서열 내 다른 정렬을 사용하여 식별되는 CDR로 표시되어 있다. 본 발명의 표적화 IL-15/IL-15Rα 이종이량체 융합 단백질에 사용되는 적합한 LAG-3 ABD는 또한, scFv 또는 Fab로 사용되는, 이러한 서열 및 도면에 도시된 바와 같은 전체 VH 서열 및 VL 서열을 포함할 수 있다.
하나의 구현예에서, LAG-3 항원 결합 도메인은 도 12 및 도 13a 내지 도 13c, 또는 서열목록에 기재된 임의의 LAG-3 결합 도메인의 6개의 CDR(즉, vhCDR1 내지 vhCDR3 및 vlCDR1 내지 vlCDR3)을 포함한다.
LAG-3에 대한 ABD를 형성하는 도면 및 서열목록에 개시된 모 CDR 세트에 더하여, 본원에는 본원에(예를 들어, 도 12 및 도 13a 내지 도 13c) 개시된 LAG-3 ABD CDR의 적어도 하나의 변형을 포함하는 CDR을 갖는 변이체 LAG-3 ABD가 제공된다. 하나의 구현예에서, 이종이량체 융합 단백질은 도 12 및 도 13a 내지 도 13c, 또는 서열목록에 도시된 바와 같은 LAG-3 ABD의 6개의 CDR과 비교하여, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개 10개의 아미노산 변형을 갖는 6개 CDR의 세트를 포함하는 LAG-3 ABD를 포함한다. 특정 구현예에서, LAG-3 ABD는 Biacore 검정, 표면 플라즈몬 공명(SPR: surface plasmon resonance) 및/또는 BLI 검정(생체층 간섭법, 예를 들어 Octet 검정)에 의해 측정되는 바와 같이, LAG-3 항원에 결합할 수 있으며, 여기서 특히 후자가 다수의 구현예에서 사용된다.
하나의 구현예에서, 본 발명의 표적화 IL-15/IL-15Rα 이종이량체 융합 단백질의 LAG-3 ABD는, 도 12 및 도 13a 내지 도 13c 또는 서열목록에 도시된 바와 같은 LAG-3 ABD의 6개의 CDR과 적어도 90%, 95%, 97%, 98% 또는 99% 동일한 6개의 CDR을 포함한다. 특정 구현예에서, LAG-3 ABD는 Biacore 검정, 표면 플라즈몬 공명(SPR) 및/또는 BLI 검정(생체층 간섭법, 예를 들어 Octet 검정)에 의해 측정되는 바와 같이, LAG-3에 결합할 수 있으며, 여기서 특히 후자가 다수의 구현예에서 사용된다.
본 발명의 표적화 IL-15/IL-15Rα 이종이량체 융합 단백질의 하나의 구현예에서, LAG-3 항원 결합 도메인은 하기 LAG-3 ABD 중 하나의 6개의 CDR(즉, vhCDR1 내지 vhCDR3 및 vlCDR1 내지 vlCDR3)을 포함한다: 7G8[LAG-3]_H0_L0, 7G8[LAG-3]_H3_L1, 7G8[LAG-3]_H3.30_L1.34, 2A11[LAG-3]_H0_L0, 2A11[LAG-3]_H1_L2, 2A11[LAG-3]_H1.44_L2.142, BMS-986016[LAG-3], IMP731[LAG-3], 13E2[LAG-3], 34F4[LAG-3], IMP761[LAG-3], H5L7[LAG-3], hu22D2[LAG-3], H4sH15482P[LAG-3], L35D4[LAG-3], L35G6[LAG-3], L33H11[LAG-3], L32A9[LAG-3], L32D10[LAG-3], L32A4[LAG-3], L3A1[LAG-3], L3A10[LAG-3], L3C5[LAG-3] 및 L3E3[LAG-3](예를 들어, 도 12 및 도 13a 내지 도 13c 참조). 예시적인 구현예에서, LAG-3 ABD는 7G8[LAG-3]_H3.30_L1.34 또는 2A11[LAG-3]_H1.144_L2.142 LAG-3 ABD이다(예를 들어, 도 12 참조).
하나의 구현예에서, LAG-3 항원 결합 도메인은 하기 LAG-3 ABD 중 하나의 6개의 CDR과 비교하여 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개 10개의 아미노산 변형을 포함하는 6개의 CDR(즉, vhCDR1 내지 vhCDR3 및 vlCDR1 내지 vlCDR3)을 포함하는 변이체 LAG-3 항원 결합 도메인이다: 7G8[LAG-3]_H0_L0, 7G8[LAG-3]_H3_L1, 7G8[LAG-3]_H3.30_L1.34, 2A11[LAG-3]_H0_L0, 2A11[LAG-3]_H1_L2, 2A11[LAG-3]_H1.44_L2.142, BMS-986016[LAG-3], IMP731[LAG-3], 13E2[LAG-3], 34F4[LAG-3], IMP761[LAG-3], H5L7[LAG-3], hu22D2[LAG-3], H4sH15482P[LAG-3], L35D4[LAG-3], L35G6[LAG-3], L33H11[LAG-3], L32A9[LAG-3], L32D10[LAG-3], L32A4[LAG-3], L3A1[LAG-3], L3A10[LAG-3], L3C5[LAG-3] 및 L3E3[LAG-3] (예를 들어, 도 12 및 도 13a 내지 도 13c 참조). 예시적인 구현예에서, LAG-3 ABD는 7G8[LAG-3]_H3.30_L1.34 또는 2A11[LAG-3]_H1.144_L2.142 LAG-3 ABD이다(예를 들어, 도 12 참조).
하나의 구현예에서, IL-15/IL-15Rα 이종이량체 융합 단백질의 LAG-3 항원 결합 도메인은 하기 LAG-3 ABD 중 하나의 6개의 CDR과 비교하여 적어도 90%, 95%, 97%, 98% 또는 99% 동일한 6개의 CDR(즉, vhCDR1 내지 vhCDR3 및 vlCDR1 내지 vlCDR3)을 포함하는 변이체 LAG-3 항원 결합 도메인이다: 7G8[LAG-3]_H0_L0, 7G8[LAG-3]_H3_L1, 7G8[LAG-3]_H3.30_L1.34, 2A11[LAG-3]_H0_L0, 2A11[LAG-3]_H1_L2, 2A11[LAG-3]_H1.44_L2.142, BMS-986016[LAG-3], IMP731[LAG-3], 13E2[LAG-3], 34F4[LAG-3], IMP761[LAG-3], H5L7[LAG-3], hu22D2[LAG-3], H4sH15482P[LAG-3], L35D4[LAG-3], L35G6[LAG-3], L33H11[LAG-3], L32A9[LAG-3], L32D10[LAG-3], L32A4[LAG-3], L3A1[LAG-3], L3A10[LAG-3], L3C5[LAG-3] 및 L3E3[LAG-3] (예를 들어, 도 12 및 도 13a 내지 도 13c 참조). 예시적인 구현예에서, LAG-3 ABD는 7G8[LAG-3]_H3.30_L1.34 또는 2A11[LAG-3]_H1.144_L2.142 LAG-3 ABD이다(예를 들어, 도 12 참조).
일부 구현예에서, IL-15/IL-15Rα 이종이량체 융합 단백질의 LAG-3 ABD는, 비제한적으로, 도 12 및 도 13a 내지 도 13c에 개시된 것들을 포함하여, 본원에 개시된 임의의 LAG-ABD의 가변 중쇄 도메인(VH) 및 가변 경쇄 도메인(VL)을 포함한다. 본원에 개시된 모 LAG-3 가변 중쇄 도메인 및 가변 경쇄 도메인에 더하여, 본원에는 본원에 개시된 LAG-3 ABD VH 도메인 및 VL 도메인의 변이체인 가변 중쇄 도메인 및/또는 가변 경쇄 도메인을 포함하는 하나 이상의 LAG-3 ABD를 갖는 본 발명의 표적화 IL-15/IL-15Rα 이종이량체 융합 단백질이 제공된다. 하나의 구현예에서, 변이체 VH 도메인 및/또는 변이체 VL 도메인은 도 12, 도 13a 내지 도 13c, 도 29a 및 도 29b, 또는 서열목록에 도시된 LAG-3 ABD의 VH 도메인 및/또는 VL 도메인으로부터의 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개 또는 10개의 아미노산 변경을 갖는다. 특정 구현예에서, LAG-3 ABD는 Biacore 검정, 표면 플라즈몬 공명(SPR) 및/또는 BLI 검정(생체층 간섭법, 예를 들어 Octet 검정)에 의해 측정되는 바와 같이, LAG-3에 결합할 수 있으며, 여기서 특히 후자가 다수의 구현예에서 사용된다.
하나의 구현예에서, IL-15/IL-15Rα 이종이량체 융합 단백질의 변이체 VH 도메인 및/또는 VL 도메인은, 도 12 및 도 13a 내지 도 13c 또는 서열목록에 도시된 바와 같은 LAG-3 ABD의 VH 및/또는 VL과 적어도 90%, 95%, 97%, 98% 또는 99% 동일하다. 특정 구현예에서, LAG-3 ABD는 Biacore 검정, 표면 플라즈몬 공명(SPR) 및/또는 BLI 검정(생체층 간섭법, 예를 들어 Octet 검정)에 의해 측정되는 바와 같이, LAG-3에 결합할 수 있으며, 여기서 특히 후자가 다수의 구현예에서 사용된다.
일부 구현예에서, LAG-3 ABD는 하기 LAG-3 ABD 중 하나의 VH 및 VL을 포함한다: 7G8[LAG-3]_H0_L0, 7G8[LAG-3]_H3_L1, 7G8[LAG-3]_H3.30_L1.34, 2A11[LAG-3]_H0_L0, 2A11[LAG-3]_H1_L2, 2A11[LAG-3]_H1.44_L2.142, BMS-986016[LAG-3], IMP731[LAG-3], 13E2[LAG-3], 34F4[LAG-3], IMP761[LAG-3], H5L7[LAG-3], hu22D2[LAG-3], H4sH15482P[LAG-3], L35D4[LAG-3], L35G6[LAG-3], L33H11[LAG-3], L32A9[LAG-3], L32D10[LAG-3], L32A4[LAG-3], L3A1[LAG-3], L3A10[LAG-3], L3C5[LAG-3] 및 L3E3[LAG-3](예를 들어, 도 12 및 도 13a 내지 도 13c 참조). 예시적인 구현예에서, LAG-3 ABD는 7G8[LAG-3]_H3.30_L1.34 또는 2A11[LAG-3]_H1.144_L2.142 LAG-3 ABD이다(예를 들어, 도 12 참조).
일부 구현예에서, LAG-3 ABD는, VH 및/또는 VL이 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142 LAG-3 ABD의 VH 및/또는 VL(예를 들어, 도 12 참조)과 비교하여 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개 또는 10개의 아미노산 변경을 포함하는 VH 및 VL를 포함한다.
특정 구현예에서, LAG-3 ABD는 하기 LAG-3 ABD 중 하나의 VH 및 VL과 비교하여 적어도 90%, 95%, 97%, 98% 또는 99% 동일한 VH 및 VL를 포함한다: 7G8[LAG-3]_H0_L0, 7G8[LAG-3]_H3_L1, 7G8[LAG-3]_H3.30_L1.34, 2A11[LAG-3]_H0_L0, 2A11[LAG-3]_H1_L2, 2A11[LAG-3]_H1.44_L2.142, BMS-986016[LAG-3], IMP731[LAG-3], 13E2[LAG-3], 34F4[LAG-3], IMP761[LAG-3], H5L7[LAG-3], hu22D2[LAG-3], H4sH15482P[LAG-3], L35D4[LAG-3], L35G6[LAG-3], L33H11[LAG-3], L32A9[LAG-3], L32D10[LAG-3], L32A4[LAG-3], L3A1[LAG-3], L3A10[LAG-3], L3C5[LAG-3] 및 L3E3[LAG-3](예를 들어, 도 12 및 도 13a 내지 도 13c 참조). 예시적인 구현예에서, LAG-3 ABD는 7G8[LAG-3]_H3.30_L1.34 또는 2A11[LAG-3]_H1.144_L2.142 LAG-3 ABD이다(예를 들어, 도 12 참조).
C. Fc 도메인
본원에 기재된 바와 같이 일반적으로 비대칭 변이체 및/또는 선택적 pI 변이체 및/또는 절제 변이체를 함유하는 본 발명의 Fc 도메인 구성요소가 본원에 개괄된다. 예를 들어, "IV Heterodimeric Antibodies"라는 제목의 WO2017/218707의 개시내용(섹션 IV.A, IV.B, IV.C, IV.D, IV.E, IV.F, IV.G, IV.H 및 IV.I 포함)을 참조하며, 상기 문헌은 그 전문이 본원에 명백하게 참조로서 인용된다. 본 발명의 이종이량체 단백질에서 특히 사용되는 것은, 본원에 개괄된 "비대칭 변이체", "pI 변이체", "절제 변이체" 및 FcRn 변이체를 함유하는 Fc 도메인이다. 이러한 변이체의 특히 유용한 조합은, 예를 들어 도 7a 내지 도 7f에 도시되어 있다.
Fc 도메인은 IgG Fc 도메인, 예를 들어 IgG1, IgG2, IgG3 또는 IgG4 Fc 도메인에서 유도될 수 있다. 예시적인 구현예에서, 본원에 제공된 본 발명의 이종이량체 융합 단백질은 IgG1 Fc 도메인을 포함한다. 하기에는 표적화 IL-15/IL-15Rα 이종이량체 융합 단백질의 IL-15/IL-15Rα Fc 융합 단량체 및 항-LAG-3 항체 단편에 유용한 Fc 도메인이 기재된다.
따라서, "Fc 도메인"은 -CH2-CH3 도메인 및 선택적으로 힌지 도메인을 포함하며, 이는 IgG1에서 유도된 Fc 도메인을 포함하여, 인간 IgG1, IgG2, IgG3 또는 IgG4에서 유래될 수 있다. 본원의 일부 구현예에서, 단백질 단편, 예를 들어 IL-15 또는 IL-15Rα가 Fc 도메인에 부착되는 경우, Fc 도메인의 힌지의 전부 또는 일부에 부착되는 것은 IL-15 또는 IL-15Rα 구조체의 C-말단이다. 다른 구현예에서, 단백질 단편, 예를 들어 IL-15 또는 IL-15Rα가 Fc 도메인에 부착되는 경우, Fc 도메인의 CH1 도메인에 부착되는 것은 IL-15 또는 IL-15Rα 구조체의 C-말단이다.
본원에 개괄된 Fc 도메인 단백질의 일부 구조체 및 서열에서, IL-15 또는 IL-15Rα 단백질 단편의 C-말단은 도메인 링커의 N-말단에 부착되고, 이의 C-말단은 불변 Fc 도메인의 N-말단에 부착에 부착되지만(N-IL-15 또는 IL-15Rα 단백질 단편-링커-Fc 도메인-C), 이는 전환될 수 있다(N-Fc 도메인-링커-IL-15 또는 IL-15Rα 단백질 단편-C). 본원에 개괄된 다른 구조체 및 서열에서, 제1 단백질 단편의 C-말단은 선택적으로 도메인 링커를 통해 제2 단백질 단편의 N-말단에 부착되고, 제2 단백질 단편의 C-말단은 선택적으로 도메인 링커를 통해 불변 Fc 도메인의 N-말단에 부착된다. 본원에 개괄된 또 다른 구조체 및 서열에서, 제1 단백질 단편 또는 제2 단백질 단편에 부착되지 않은 불변 Fc 도메인이 제공된다. 이종이량체 융합 단백질은 본원에 기재된 예시적인 단량체 Fc 도메인 단백질 중 2종 이상을 함유할 수 있다. 임의의 도메인 링커를 사용하여, 본원에 제공된 이종이량체 융합 단백질의 Fc 도메인에 IL-15 단백질 단편 또는 IL-15Rα 단백질 단편을 부착시킬 수 있다. 일부 구현예에서, 링커는 도 8의 링커 중 임의의 것이다.
일부 구현예에서, 링커는 본원에 개괄된 바와 같은 임의의 2개의 도메인을(예를 들어, IL-15 단백질 단편 또는 IL-15Rα 단백질 단편을 Fc 도메인에, 또는 scFv를 Fc 도메인에) 함께 연결하는 데 사용되는 "도메인 링커"이며, 이의 일부는 도 8에 도시되어 있다. 임의의 적합한 링커가 사용될 수 있지만, 다수의 구현예는, 예를 들어 (GS)n, (GSGGS)n, (GGGGS)n 및 (GGGS)n(여기서 n은 적어도 1의 정수(일반적으로 1에서 2, 3, 4 내지 5까지)임)을 포함하는 글리신-세린 중합체뿐 아니라, 각 도메인이 이의 생물학적 기능을 유지하도록 충분한 길이 및 가요성을 갖는 2개의 도메인의 재조합 부착을 가능하게 하는 임의의 펩타이드 서열을 이용한다. 일부 경우에, 하기에 개괄되는 바와 같이, "가닥 배열"에 주목하면, 링커는 하전된 도메인 링커이다.
하나의 구현예에서, 이종이량체 융합 단백질은 pI 조작과 같이 이종이량체를 생성하도록 조작될 수 있는 적어도 2개의 불변 도메인을 포함한다. 사용될 수 있는 다른 Fc 도메인은 pI 조작된 본 발명의 CH1, CH2, CH3 및 힌지 도메인 중 하나 이상을 함유하는 단편을 포함한다. 특히, 도 21에 도시된 형식은 이종이량체 Fc 융합 단백질이며, 이는 하기에 보다 충분히 기재되는 바와 같이 단백질이 이종이량체 Fc 도메인 및 적어도 하나의 융합 단백질(예를 들어, 1개, 2개 또는 그 이상의 융합 단백질)로 자가 조립되는 2개의 관련된 Fc 서열을 갖는다는 것을 의미한다. 일부 경우에, 제1 융합 단백질은 제1 Fc에 연결되고, 제2 융합 단백질은 제2 Fc에 연결된다. 다른 경우에, 제1 융합 단백질은 제1 Fc에 연결되고, 제1 융합 단백질은 Fc에 연결되지 않은 제2 융합 단백질에 비공유결합으로 부착된다. 일부 경우에, 이종이량체 Fc 융합 단백질은 제1 Fc 서열에 연결된 제2 융합 단백질에 연결된 제1 융합 단백질, 및 제1 융합 단백질 또는 제2 융합 단백질에 연결되지 않은 제2 Fc 서열을 함유한다.
따라서, 일부 구현예에서, 본 발명은 자가 조립되어 이종이량체 Fc 도메인 융합 폴리펩타이드를 형성하는, 2개의 상이한 중쇄 변이체 Fc 서열의 사용에 의존하는 이종이량체 Fc 융합 단백질을 제공한다.
본 발명은 하나 이상의 결합 파트너, 리간드 또는 수용체에 대한 결합을 가능하게 하는 이종이량체 융합 단백질을 제공하는 신규한 구조체에 관한 것이다. 이종이량체 융합 구조체는 항체의 중쇄의 2개 Fc 도메인, 예를 들어 "이량체"로 조립되는 2개의 "단량체"의 자가 조립 특성을 기반으로 한다. 이종이량체 Fc 융합체는 하기에 보다 충분히 논의되는 바와 같이 각각의 단량체의 아미노산 서열을 변경함으로써 만들어진다. 따라서, 본 발명은 일반적으로 결합 파트너(들), 리간드(들) 또는 수용체(들)를 몇 가지 방식으로 공동 결합시킬 수 있는 이종이량체 융합 단백질의 생성에 관한 것으로, 이는 이종이량체의 형성을 촉진시키고/시키거나 동종이량체보다 이종이량체의 정제를 용이하게 하도록 각각의 사슬 상의 상이한 불변 영역 내 아미노산 변이체에 의존한다. 본 발명의 이종이량체 융합 단백질의 특정 구현예의 Fc 도메인에 포함되는 특정 변이체가 하기에 보다 상세하게 기재된다.
1. 이종이량체화 변이체
본 발명은 다양한 형식의 이종이량체 Fc 융합 단백질을 포함하는 이종이량체 단백질을 제공한다. 본원에서 총괄하여 "이종이량체화 변이체"로 지칭되는, 상기와 같은 이종이량체 단백질은 제1 단량체와 제2 단량체의 이종이량체화를 용이하게 하고/하거나 동종이량체보다 이종이량체의 정제를 용이하게 하는 변형을 포함하는 2개의 상이한 Fc 도메인(제1 단량체 및 제2 단량체 각각에 하나씩)을 포함한다. 하기에 논의되는 바와 같이, 이종이량체화 변이체는 비대칭 변이체(예를 들어, 하기에 기재되는 "놉 앤 홀(knobs and holes)" 및 "전하 쌍" 변이체), 및 "pI 변이체"를 포함할 수 있으며, 이는 이종이량체로부터 동종이량체의 정제를 용이하게 한다. 미국 특허 US 9,605,084호(이는 그 전문이 본원에 참조로서 인용됨)에 일반적으로 기재되고, 구체적으로 이종이량체화 변이체에 대하여 하기에 논의되는 바와 같이, 이종이량체화에 유용한 메커니즘에는, 미국 특허 US 9,605,084호에 기재된 바와 같은 "놉 앤 홀"("KIH"), 미국 특허 US 9,605,084호에 기재된 바와 같은 "정전기 스티어링(electrostatic steering)" 또는 "전하 쌍", 미국 특허 US 9,605,084호에 기재된 바와 같은 pI 변이체, 및 미국 특허 US 9,605,084호 및 하기에 개괄된 바와 같은 일반적인 추가의 Fc 변이체가 포함된다.
a. 비대칭 변이체
일부 구현예에서, 본 발명의 이종이량체 단백질은 Fc 동종이량체(2개의 제1 Fc 도메인 또는 2개의 제2 Fc 도메인을 포함하는 Fc 이량체; A-A 또는 B-B)보다 Fc 이종이량체(제1 Fc 도메인과 제2 Fc 도메인을 포함하는 Fc 이량체; A-B)의 형성을 유리하게 하는, 제1 Fc 도메인(A) 및/또는 제2 Fc 도메인(B) 내 하나 이상의 아미노산 변형인 비대칭 변이체를 포함한다. 적합한 비대칭 변이체는 미국 특허출원공개 제2016/0355608호의 도 4 뿐 아니라 도 29에 포함되어 있으며, 상기 문헌은 그 전문이, 구체적으로 비대칭 변이체의 개시내용이 본원에 참조로서 인용된다.
비대칭 변이체에 대한 하나의 메커니즘은 일반적으로 당업계에서 이종이량체 형성을 유리하게 하고 동종이량체 형성을 불리하게 하는 입체적 영향을 생성하는 아미노산 조작을 나타내는, "놉 앤 홀"로 지칭되며, 이는 미국 특허출원 USSN 제61/596,846호, 문헌[Ridgway et al., Protein Engineering 9(7):617 (1996)]; 문헌[Atwell et al., J. Mol. Biol. 1997 270:26]; 미국 특허 제8,216,805호(이들은 모두 그 전문이, 구체적으로 "놉 앤 홀" 돌연변이의 개시내용이 본원에 참조로서 인용됨)에 기재되어 있다. 이는 때때로 본원에서 "입체 변이체"로 지칭된다. 도면은 "놉 앤 홀"에 의존하는 다수의 "단량체 A - 단량체 B" 쌍을 식별한다. 또한, 문헌[Merchant et al., Nature Biotech. 16:677 (1998)]에 기재된 바와 같이, 이러한 "놉 앤 홀" 돌연변이는 다이설파이드 결합과 조합되어 Fc 이종이량체의 형성을 추가로 유리하게 할 수 있다.
이종이량체의 생성에 사용되는 비대칭 변이체에 대한 추가의 메커니즘은 때때로 문헌[Gunasekaran et al., J. Biol. Chem. 285(25):19637 (2010)](이는 그 전문이 본원에 참조로서 인용됨)에 기재된 바와 같이 "정전기 스티어링"으로 지칭된다. 이는 때때로 본원에서 "전하 쌍"으로 지칭된다. 이러한 구현예에서, 정전기는 형성을 이종이량체화로 편향되게 하는 데 사용된다. 당업자가 이해하는 바와 같이, 이는 또한 pI, 및 이에 따른 정제에 영향을 미칠 수 있기 때문에, 일부 경우에 이는 또한 pI 변이체로 간주될 수 있다. 하지만, 이는 이종이량체화를 강제하기 위해 생성되었고 정제 도구로서 사용되지 않았기 때문에, 이들은 "비대칭 변이체"로 분류된다. 이에는, 비제한적으로, D221R/P228R/K409R과 쌍을 이루는 D221E/P228E/L368E(예를 들어, 이들은 "단량체" 상응 세트임) 및 C220R/E224R/P228R/K409R과 쌍을 이루는 C220E/P228E/368E가 포함된다.
일부 구현예에서, 비대칭 변이체는 유리하게 및 동시에 상기 기재된 "놉 앤 홀" 메커니즘뿐 아니라 "정전기 스티어링" 메커니즘에 기반하여 이종이량체화를 유리하게 한다. 일부 구현예에서, 이종이량체 단백질은 상기와 같은 이종이량체화 비대칭 변이체의 하나 이상의 세트를 포함한다. 이러한 변이체는 "세트"의 "쌍"으로 도입된다. 즉, 한 세트의 쌍은 제1 단량체에 혼입되고, 다른 한 세트의 쌍은 제2 단량체에 혼입된다. 이러한 범주의 예시적인 "비대칭 변이체"에는, S364K/E357Q : L368D/K370S; L368D/K370S : S364K; L368E/K370S : S364K; T411T/E360E/Q362E : D401K; L368D/K370S : S364K/E357L; K370S : S364K/E357Q; 또는 T366S/L368A/Y407V : T366W (선택적으로 브릿징 다이설파이드, T366S/L368A/Y407V/Y349C : T366W/S354C를 포함함) "비대칭" 변이체 아미노산 치환 세트가 포함된다. 명명법에 관하여, 쌍 "S364K/E357Q : L368D/K370S"는 단량체 중 하나가 아미노산 치환 S364K 및 E357Q를 포함하는 Fc 도메인을 포함하고, 다른 하나의 단량체가 아미노산 치환 L368D 및 K370S를 포함하는 Fc 도메인을 포함한다는 것을 의미하며; 상기와 같이 이러한 쌍의 "가닥 배열"은 출발 pI에 따라 달라진다. 이러한 세트가 반드시 하나의 단량체 상의 잔기와 다른 하나의 단량체 상의 잔기 사이에서 일대일 대응을 갖는 "놉 인 홀(knob in hole)" 변이체로서 거동할 필요가 없다는 점에 주목해야 한다. 즉, 이러한 세트의 쌍은 이종이량체 형성을 유리하게 하고 동종이량체 형성을 불리하게 하는 2개의 단량체 사이의 인터페이스를 형성함으로써, 생물학적 조건 하에 자발적으로 형성되는 이종이량체의 백분율이 예상되는 50%(25%의 동종이량체 A/A: 50%의 이종이량체 A/B: 25%의 동종이량체 B/B)가 아니라 90%를 초과하는 것을 가능하게 한다.
예시적인 구현예에서, 이종이량체 융합 단백질은 S364K/E357Q : L368D/K370S; L368D/K370S : S364K; L368E/K370S : S364K; T411T/E360E/Q362E : D401K; L368D/K370S : S364K/E357L; K370S : S364K/E357Q; 또는 T366S/L368A/Y407V : T366W (선택적으로 브릿징 다이설파이드, T366S/L368A/Y407V/Y349C : T366W/S354C를 포함함) "비대칭" 변이체 아미노산 치환 세트를 포함한다. 예시적인 구현예에서, 이종이량체 융합 단백질은 "S364K/E357Q : L368D/K370S" 아미노산 치환 세트를 포함한다.
일부 구현예에서, 본원에 제공된 비대칭 변이체는 독립적으로, 비제한적으로, 다른 비대칭 변이체(예를 들어, 미국 특허출원공개 제2012/0149876호의 도 37 참조(상기 문헌은 특히 비대칭 변이체의 개시내용이 본원에 참조로서 인용됨)), pI 변이체, 아이소타입 변이체, FcRn 변이체, 절제 변이체 등을 포함하는 다른 변형과 함께, 이종이량체 융합 단백질의 제1 Fc 도메인 및 제2 Fc 도메인 중 하나 또는 둘 모두에 혼입된다. 나아가, 개별 변형은 또한 독립적으로 및 선택적으로 본 발명의 이종이량체 융합 단백질에 포함되거나 이로부터 배제될 수 있다.
b. 이종이량체를 위한 pI(등전점) 변이체
일부 구현예에서, 이종이량체 융합 단백질은 유리하게는 동종이량체 단백질로부터 이종이량체 융합 단백질의 분리를 가능하게 하는 정제 변이체("pI 변이체")를 포함한다.
일반적으로, 당업자가 이해하는 바와 같이, 단백질의 pI를 증가시키는(염기성 변경) pI 변이체 및 단백질의 pI를 감소시키는(산성 변경) pI 변이체의 두 가지 일반적인 범주가 존재한다. 본원에 기재된 바와 같이, 이러한 변이체의 모든 조합이 이루어질 수 있으며, 하나의 단량체는 야생형, 또는 야생형과 유의하게 상이한 pI를 나타내지 않는 변이체일 수 있고, 다른 하나의 단량체는 더 염기성이거나 더 산성일 수 있다. 대안적으로, 각각의 단량체는 하나가 더 염기성으로 하나가 더 산성으로 변경된다.
이종이량체 단백질의 정제를 용이하게 할 수 있는 몇 가지 기본 메커니즘이 존재한다. 하나의 이러한 메커니즘은, 융합 단백질의 단량체 중 하나 또는 둘 모두의 등전점에 영향을 미치는 하나 이상의 변형을 포함하는 pI 변이체를 사용하는 것으로, 각각의 단량체, 및 후속으로 각각의 이량체 종이 상이한 pI를 갖도록 함으로써 A-A, A-B 및 B-B 이량체 단백질의 등전위 정제를 가능하게 하는 것이다. 대안적으로, 일부 형식은 또한 크기를 기준으로 한 분리를 가능하게 한다. 상기에 추가로 개괄된 바와 같이, 또한 비대칭 변이체를 사용하여 동종이량체에 비해 이종이량체의 형성을 "비대칭화"시킬 수 있다. 따라서, 특히 이종이량체화 비대칭 변이체와 pI 변이체의 조합이 본원에 제공된 본 발명의 이종이량체 융합 단백질에 사용된다.
또한, 하기에 보다 충분히 개괄되는 바와 같이, 이종이량체 Fc 융합 단백질의 형식에 따라, pI 변이체가 단량체의 불변 영역 및/또는 Fc 도메인 내에 포함될 수 있고/있거나, 도메인 링커가 사용될 수 있다. 일부 구현예에서, 이종이량체 융합 단백질은 Fc 변이체, FcRn 변이체 및 KO 변이체와 같은, pI 를 변경시킬 수 있는 대안적인 기능에 대한 추가의 변형을 포함한다.
이종이량체 융합 단백질의 정제를 가능하게 하는 분리 메커니즘으로서 pI를 이용하는 구현예에서, 이종이량체 융합 단백질의 단량체 중 하나 또는 둘 모두에 아미노산 변형이 도입될 수 있다. 즉, 하나의 단량체(본원에서 간단히 "단량체 A"로 지칭됨)의 pI가 단량체 B로부터 멀어지게 조작될 수 있거나, 단량체 A의 pI는 증가하고 단량체 B의 pI는 감소하도록 단량체 A 및 단량체 B 둘 모두가 변경될 수 있다. 논의된 바와 같이, 한쪽 또는 양쪽 단량체의 pI 변경은, 하전된 잔기를 제거 또는 부가하거나(예를 들어, 중성 아미노산이 양 또는 음으로 하전된 아미노산 잔기로, 예를 들어 글루타민에서 글루탐산으로 대체됨), 양 또는 음으로 하전된 잔기를 반대 전하로 변경하거나(예를 들어, 아스파르트산에서 리신으로), 또는 하전된 잔기를 중성 잔기로 변경함(예를 들어, 전하 손실, 리신에서 세린으로)으로써 수행될 수 있다. 다수의 이러한 변이체들이 도 4 및 도 5를 포함하는 도면에 도시되어 있다.
이종이량체가 동종이량체로부터 분리될 수 있도록 적어도 하나의 단량체에서 pI를 충분히 변경시키는 것은, "야생형" 중쇄 불변 영역과 이의 pI를 증가 또는 감소시키도록 조작된 변이체 영역을 사용하거나(야생형 A : B+ 또는 야생형 A : B-), 하나의 영역을 증가시키고 다른 하나의 영역을 감소시킴(A+ : B- 또는 A- : B+)으로써 수행될 수 있다.
따라서, 일반적으로, 본 발명의 융합 단백질의 일부 구현예의 구성요소는 아미노산 치환("pI 변이체" 또는 "pI 치환체")을 단량체 중 하나 또는 둘 모두에 혼입시킴으로써 이량체 단백질의 단량체 중 적어도 하나(둘 모두가 아닌 경우)의 등전점(pI: isoelectric point)을 변경시키는 Fc 도메인 또는 불변 도메인 영역의 아미노산 변이체이다. 2개의 동종이량체로부터 이종이량체를 분리시키는 것은, 2개의 단량체의 pI가 0.2, 0.3, 0.4, 0.5 또는 그 이상으로 0.1 pH 단위만큼 차이가 나는 경우에 달성될 수 있으며, 이들은 모두 본 발명에 사용된다.
당업자가 이해하는 바와 같이, 양호한 분리를 달성하기 위해 이종이량체 융합 단백질의 각각의 또는 양쪽 단량체(들)에 포함되는 pI 변이체의 수는 부분적으로 구성요소의 출발 pI에 따라 달라질 것이다. 즉, 조작하고자 하는 단량체 또는 이의 "방향"(예를 들어, 더 양으로 또는 더 음으로)을 결정하기 위해, Fc 도메인, 및 각각의 단량체에 포함된 임의의 IL-15, IL-15Rα 또는 링커의 서열이 계산되고, 이로부터 단량체의 pI를 기준으로 결정이 이루어진다. 당업계에 공지된 바와 같이, 상이한 Fc 도메인, 링커, IL-15 및 IL-15Rα는 상이한 출발 pI를 가질 것이다. 일반적으로, 본원에 개괄된 바와 같이, pI는 각각의 단량체의 총 pI 차이가 적어도 약 0.1 로그가 되도록 조작되며, 이러한 차이는 본원에 개괄된 바와 같이 0.2 내지 0.5가 바람직하다.
일반적으로, 당업자가 이해하는 바와 같이, 단백질의 pI를 증가시키는 pI 변이체(염기성 변경) 및 단백질의 pI를 감소시키는 pI 변이체(산성 변경)와 같은 pI에 영향을 미치는 아미노산 변형의 두 가지 일반적인 범주가 존재한다. 본원에 기재된 바와 같이, 이러한 변이체의 모든 조합이 사용될 수 있으며, 하나의 단량체는 야생형 Fc 도메인, 또는 야생형과 유의하게 상이한 pI를 나타내지 않는 변이체 Fc 도메인을 포함할 수 있고, 다른 하나의 단량체는 더 염기성이거나 더 산성인 Fc 도메인을 포함한다. 대안적으로, 각각의 단량체는 하나가 더 염기성으로 하나가 더 산성으로 변경될 수 있다.
이종이량체화를 달성하기 위해 pI 변이체가 사용되는 경우, 이종이량체 융합 단백질을 설계하고 정제하는 보다 모듈식인 접근법이 제공된다. 따라서, 일부 구현예에서, 이종이량체화 변이체(비대칭 이종이량체화 변이체 및 pI 변이체를 포함함)는 조작되어야 한다. 또한, 일부 구현예에서, pI 변이체에서 기인한 면역원성의 가능성은, pI가 유의한 면역원성의 도입없이 변경되도록 상이한 IgG 아이소타입으로부터의 pI 변이체를 이입함으로써 유의하게 감소된다(하기 아이소타입 변이체 참조). 따라서, 해결하고자 하는 추가적인 문제는 높은 인간 서열 함량을 갖는 낮은 pI 불변 도메인의 규명, 예를 들어 임의의 특정한 위치에서의 비(非)인간 잔기의 최소화 또는 회피이다. 아이소타입 치환에 대안적으로 또는 이에 더하여, pI 변이체에서 기인한 면역원성의 가능성은 등입체성 치환(예를 들어, Asn에서 Asp로; 및 Gln에서 Glu로)을 이용하여 유의하게 감소된다.
이러한 pI 조작으로 발생할 수 있는 부수적 이점은 또한 혈청 반감기의 연장 및 FcRn 결합의 증가이다. 즉, 미국 특허출원공개 US 2012/0028304호(이는 그 전문이, 구체적으로 추가의 기능을 제공하는 pI 변이체의 개시내용이 본원에 참조로서 인용됨)에 기재된 바와 같이, 항체 불변 도메인(Fc 융합체에서 발견되는 것들 포함)의 pI를 낮추면, 생체내에서 더 긴 혈청 보유를 유도할 수 있다. 혈청 반감기 증가를 위한 이러한 pI 변이체는 또한 정제를 위한 pI 변경을 가능하게 한다.
또한, 이종이량체화 변이체의 pI 변이체는, 동종이량체가 존재하는 경우 제거, 최소화 및 구별하는 능력이 중요하기 때문에, Fc 융합 단백질의 분석 및 품질 관리 과정에 추가적인 이점을 제공한다는 점에 주목해야 한다. 유사하게, 이종이량체 융합 단백질 생산의 재현성을 신뢰성 있게 시험하는 능력이 중요하다.
pI 변이체의 예시적인 조합은 미국 특허출원공개 제2016/0355608호의 도 4 및 도 5, 및 도 30에 제시되어 있으며, 상기 문헌은 그 전문이, 구체적으로 pI 변이체의 개시내용이 본원에 참조로서 인용된다. 본원에 개괄되고 도면에 제시된 바와 같이, 이러한 변경은 IgG1과 관련하여 표시되어 있지만, 모든 아이소타입뿐 아니라 아이소타입 혼성체도 이러한 방식으로 변경될 수 있다. 중쇄 불변 도메인이 IgG2 내지 IgG4 유래인 경우, R133E 및 R133Q가 또한 사용될 수 있다.
일부 구현예에서, 변형은 EU 넘버링을 기준으로 208번, 216번, 217번, 218번, 219번, 220번, 221번, 222번, 223번, 224번, 225번, 226번, 227번, 228번, 229번 및 230번의 위치를 포함하는 Fc 도메인의 힌지에서 만들어진다. 따라서, pI 돌연변이, 특히 치환은 216번 내지 230번의 위치 중 하나 이상에서 만들어질 수 있으며, 여기서 1개, 2개, 3개, 4개 또는 5개의 돌연변이가 사용된다. 다시 말하면, 모든 가능한 조합이, 단독으로 또는 다른 도메인의 다른 pI 변이체와 함께, 고려된다.
힌지 도메인의 pI를 저하시키는 데 사용되는 특정한 치환에는, 비제한적으로, 221번 위치에서의 결실, 222번 위치에서의 비(非)천연 발린 또는 트레오닌, 223번 위치에서의 결실, 224번 위치에서의 비천연 글루탐산, 225번 위치에서의 결실, 235번 위치에서의 결실, 및 236번 위치에서의 결실 또는 비천연 알라닌이 포함된다. 일부 경우에, 힌지 도메인에는 pI 치환만이 일어나고, 다른 것들의 경우에는, 이러한 치환(들)이 다른 도메인의 다른 pI 변이체에 임의의 조합으로 부가된다.
일부 구현예에서, 돌연변이는 EU 넘버링을 기준으로 233번, 234번, 235번, 236번, 274번, 296번, 300번, 309번, 320번, 322번, 326번, 327번, 334번 및 339번의 위치를 포함하는 CH2 영역에서 만들어 질 수 있다. IgG2 백본에서 (327A와 함께) 효과기 기능을 증가시키기 위해 233번 내지 236번에서 변경이 만들어질 수 있다는 점에 주목해야 한다. 다시 말하면, 이러한 14가지 위치의 모든 가능한 조합이 이루어질 수 있으며; 예를 들어, 이종이량체 융합 단백질은 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개 또는 10개의 CH2 pI 치환을 갖는 변이체 Fc 도메인을 포함할 수 있다.
CH2 도메인의 pI를 저하시키는 데 사용되는 특정한 치환에는, 비제한적으로, 274번 위치에서의 비천연 글루타민 또는 글루탐산, 296번 위치에서의 비천연 페닐알라닌, 300번 위치에서의 비천연 페닐알라닌, 309번 위치에서의 비천연 발린, 320번 위치에서의 비천연 글루탐산, 322번 위치에서의 비천연 글루탐산, 326번 위치에서의 비천연 글루탐산, 327번 위치에서의 비천연 글리신, 334번 위치에서의 비천연 글루탐산, 339번 위치에서의 비천연 트레오닌, 및 CH2 내 및 다른 도메인과의 모든 가능한 조합이 포함된다.
이러한 구현예에서, 변형은 독립적으로 및 선택적으로 CH3 영역의 (EU 넘버링) 355번, 359번, 362번, 384번, 389번, 392번, 397번, 418번, 419번, 444번 및 447번의 위치로부터 선택될 수 있다. CH3 도메인의 pI를 저하시키는 데 사용되는 특정한 치환에는, 비제한적으로, 355번 위치에서의 비천연 글루타민 또는 글루탐산, 384번 위치에서의 비천연 세린, 392번 위치에서의 비천연 아스파라긴 또는 글루탐산, 397번 위치에서의 비천연 메티오닌, 419번 위치에서의 비천연 글루탐산, 359번 위치에서의 비천연 글루탐산, 362번 위치에서의 비천연 글루탐산, 389번 위치에서의 비천연 글루탐산, 418번 위치에서의 비천연 글루탐산, 444번 위치에서의 비천연 글루탐산, 및 447번 위치에서의 결실 또는 비천연 아스파르트산이 포함된다. pI 변이체의 예시적인 구현예는 도 5에 제공된다.
하나의 구현예에서, 이종이량체 융합 단백질은 pI 변이체 변형 295E/384D/418E/421D(인간 IgG1를 기준으로 하는 경우 Q295E/N384D/Q418E/N421D)을 갖는 변이체 Fc 도메인을 갖는 단량체를 포함한다. 하나의 구현예에서, 이종이량체 융합 단백질은 pI 변이체 변형 208D/295E/384D/418E/421D(인간 IgG1를 기준으로 하는 경우 N208D/Q295E/N384D/Q418E/N421D)를 갖는 변이체 Fc 도메인을 갖는 단량체를 포함한다. 일부 구현예에서, 이종이량체 융합 단백질은 pI 변이체 변형 295E/384D/418E/421D(인간 IgG1를 기준으로 하는 경우 Q295E/N384D/Q418E/N421D)를 갖는 변이체 Fc 도메인을 갖는 단량체를 포함한다. 하나의 구현예에서, 이종이량체 융합 단백질은 pI 변이체 변형 196K/199T/217R/228R/276K(인간 IgG1를 기준으로 하는 경우 Q196K/I199T/P217R/P228R/N276K)를 갖는 변이체 Fc 도메인을 갖는 단량체를 포함한다.
하나의 구현예에서, 이종이량체 융합 단백질은 pI 변이체 변형 217R/228R/276K(인간 IgG1를 기준으로 하는 경우 P217R/P228R/N276K)를 갖는 변이체 Fc 도메인을 갖는 단량체를 포함한다. 본 발명의 Fc 도메인에 혼입될 수 있는 추가의 예시적인 pI 변이체 변형은 도 5에 도시되어 있다.
c. 아이소타입 변이체
또한, 본 발명의 다수의 구현예는 특정 위치에서 하나의 IgG 아이소타입으로부터 또 다른 IgG 아이소타입으로의 pI 아미노산의 "이입"에 의존하기 때문에, 원치 않는 면역원성이 변이체에 도입될 가능성이 감소되거나 제거된다. 다수의 이러한 것들이 미국 특허출원공개 제2014/0370013호의 도 21에 제시되어 있으며, 상기 문헌은 본원에 참조로서 인용된다. 즉, IgG1은 높은 효과기 기능을 포함하는 다양한 이유에서 치료용 항체를 위한 통상의 아이소타입이다. 하지만, IgG1의 중쇄 불변 영역은 IgG2보다 높은 pI를 갖는다(8.10 대 7.31). 특정 위치의 IgG2 잔기를 IgG1 골격에 도입하면, 생성된 단량체의 pI는 저하되고 (또는 증가하고), 추가로 더 긴 혈청 반감기를 나타낸다. 예를 들어, IgG1은 137번 위치에서 글리신(pI 5.97)을 갖고, IgG2는 글루탐산(pI 3.22)을 가지며, 글루탐산을 이입하는 것은 생성되는 단백질의 pI에 영향을 미칠 것이다. 하기에 기재되는 바와 같이, 다수의 아미노산 치환은 일반적으로 변이체 Fc 융합 단백질의 pI에 유의한 영향을 미치는 데 필요하다. 하지만, 하기에 논의되는 바와 같이, IgG2 분자의 변경도 혈청 반감기를 증가시킬 수 있다는 점에 주목해야 한다.
다른 구현예에서, 비(非)아이소타입 아미노산 변경은 하기에 추가로 기재되는 바와 같이, (예를 들어, 더 높은 pI 아미노산을 더 낮은 pI 아미노산으로 변경시킴으로써) 생성되는 단백질의 전반적인 전하 상태를 감소시키거나, 안정성을 위해 구조의 조정을 가능하게 하도록 이루어진다.
또한, 중쇄 불변 도메인과 경쇄 불변 도메인 둘 모두를 pI 조작하면, 이종이량체 각각의 단량체에서 유의한 변화를 확인할 수 있다. 본원에 논의된 바와 같이, 2개의 단량체의 pI를 적어도 0.5만큼 차이나게 하면, 이온 교환 크로마토그래피, 등전점 전기영동(isoelectric focusing) 또는 등전점에 민감한 다른 방법에 의한 분리를 가능하게 할 수 있다.
d. pI 계산
각각의 단량체의 pI는 변이체 중쇄 불변 도메인의 pI와, 변이체 중쇄 불변 도메인 및 융합 파트너를 포함하는 전체 단량체의 pI에 따라 달라질 수 있다. 따라서, 일부 구현예에서, pI의 변화는 US2014/0370013호의 도 19에서의 도표를 사용하여 변이체 중쇄 불변 도메인을 기준으로 계산된다. 본원에 논의된 바와 같이, 어떤 단량체를 조작할 것인지는 일반적으로 각각의 단량체의 고유의 pI에 의해 결정된다.
2. 추가적인 기능을 위한 추가의 Fc 변이체
pI 아미노산 변이체에 더하여, 비제한적으로, 하나 이상의 FcγR 수용체에 대한 결합 변경, FcRn 수용체에 대한 결합 변경 등을 포함하는 다양한 이유로 이루어질 수 있는 다수의 유용한 Fc 아미노산 변형이 존재한다.
따라서, 본 발명의 단백질은 pI 변이체 및 입체 변이체를 포함하는 본원에 개괄된 이종이량체화 변이체를 비롯한 아미노산 변형을 포함할 수 있다. 각각의 변이체 세트는 독립적으로 및 선택적으로 임의의 특정한 이종이량체 단백질에 포함되거나 이로부터 배제될 수 있다.
a. FcγR 변이체
따라서, 하나 이상의 FcγR 수용체에 대한 결합을 변경하기 위해 이루어질 수 있는 다수의 유용한 Fc 치환이 존재한다. 결합을 증가시킬뿐 아니라 결합을 감소시키는 치환이 유용할 수 있다. 예를 들어, FcγRIIIa에 대한 결합 증가는 ADCC(항체 의존적 세포 매개 세포독성; FcγR을 발현하는 비특이적 세포독성 세포가 표적세포 상의 결합된 항체를 인식하고, 이어서 표적세포의 용해를 유발하는 세포 매개 반응)의 증가를 유도하는 것으로 공지되어 있다. 유사하게, FcγRIIb(억제 수용체)에 대한 결합 감소는 일부 상황에서 마찬가지로 유익할 수 있다. 본 발명에 사용되는 아미노산 치환에는, 미국 특허출원 USSN 제11/124,620호(특히 도 41), 제11/174,287호, 제11/396,495호, 제11/538,406호(이들은 모두 그 전문이, 구체적으로 본원에 개시된 변이체에 대한 것이 본원에 명백하게 참조로서 인용됨)에 기재된 것들이 포함된다. 본원에 사용되는 특정한 변이체에는, 비제한적으로, 236A, 239D, 239E, 332E, 332D, 239D/332E, 267D, 267E, 328F, 267E/328F, 236A/332E, 239D/332E/330Y, 239D, 332E/330L, 243A, 243L, 264A, 264V 및 299T가 포함된다.
또한, FcγRIIc에 대한 친화성을 증가시키는 아미노산 치환도 본원에 개괄된 Fc 도메인 변이체에 포함될 수 있다. 예를 들어, 미국 특허출원 USSN 제11/124,620호 및 제14/578,305호에 기재된 치환이 유용하다.
또한, 미국 특허출원 USSN 제12/341,769호(이는 그 전문이 본원에 참조로서 인용됨)에 구체적으로 개시된 바와 같은, FcRn 수용체에 대한 결합 증가 및 혈청 반감기 증가에 사용되는 추가적인 Fc 치환이 존재하며, 이에는, 비제한적으로, 434S, 434A, 428L, 308F, 259I, 428L/434S, 259I/308F, 436I/428L, 436I 또는 V/434S, 436V/428L, 및 259I/308F/428L이 포함된다.
b. 절제 변이체
유사하게, 기능성 변이체의 또 다른 범주는 "FcγR 절제 변이체" 또는 "Fc 녹아웃(FcKO 또는 KO) 변이체"이다. 이러한 구현예에서, 일부 치료적 적용을 위해, Fcγ 수용체(예를 들어, FcγR1, FcγRIIa, FcγRIIb, FcγRIIIa 등) 중 하나 이상 또는 전부에 대한 Fc 도메인의 정상적인 결합을 감소시키거나 제거하여, 추가적인 작용 메커니즘을 회피하는 것이 바람직하다. 즉, 예를 들어, 다수의 구현예에서, 특히 이중특이적 면역조절 항체의 사용에 있어서, 하나의 Fc 도메인이 하나 이상의 Fcγ 수용체 절제 변이체를 포함하도록 ADCC 활성을 제거하거나 유의하게 감소시키기 위해 FcγRIIIa 결합을 절제하는 것이 바람직하다. 이러한 절제 변이체는 미국 특허출원 USSN 제15/141,350호(이는 그 전문이 본원에 참조로서 인용됨)의 도 31에 도시되어 있고, 이들 각각은 독립적으로 및 선택적으로 포함되거나 배제될 수 있으며, 여기서 바람직한 양태는 EU 인덱스에 따라 G236R/L328R, E233P/L234V/L235A/G236del/S239K, E233P/L234V/L235A/G236del/S267K, E233P/L234V/L235A/G236del/S239K/A327G, E233P/L234V/L235A/G236del/S267K/A327G 및 E233P/L234V/L235A/G236del로 이루어지는 군으로부터 선택되는 절제 변이체를 이용하는 것이다. 본원에 언급된 절제 변이체는 FcγR 결합을 절제하지만, 일반적으로 FcRn 결합은 절제하지 않는다는 점에 주목해야 한다.
예시적인 절제 변이체는 도 5에 제시되어 있다.
c. 이종이량체 변이체와 Fc 변이체의 조합
당업자가 이해하는 바와 같이, 모든 언급된 이종이량체화 변이체(비대칭 변이체 및/또는 pI 변이체를 포함함)는, 이들이 "가닥 배열" 또는 "단량체 분할"을 유지하는 한, 선택적으로 및 독립적으로 임의의 방식으로 조합될 수 있다. 또한, 모든 이러한 변이체는 임의의 이종이량체화 형식으로 조합될 수 있다.
pI 변이체의 경우에, 특히 사용되는 구현예가 도면에 도시되어 있지만, 정제를 용이하게 하기 위해 2개의 단량체 사이의 pI 차이를 변경하는 기본 규칙에 따라 다른 조합이 생성될 수 있다.
또한, 임의의 이종이량체화 변이체, 비대칭 변이체 및 pI 변이체는 또한 본원에 일반적으로 개괄된 바와 같이 Fc 절제 변이체, Fc 변이체, FcRn 변이체와 독립적으로 및 선택적으로 조합된다.
또한, 단량체 Fc 도메인은 C220S/S267K/L368D/K370S 또는 C220S/S267K/S364K/E357Q를 포함하는 아미노산 치환 세트를 포함할 수 있다.
또한, 이종이량체 융합 단백질은 비대칭 변이체(예를 들어, 미국 특허출원 USSN 제15/141,350호의 도 1a 내지 도 1c에 제시된 바와 같은 아미노산 치환 세트, 상기 문헌은 그 전문이 본원에 참조로서 인용됨)(특히 유용한 비대칭 변이체는 S364K/E357Q : L368D/K370S; L368D/K370S : S364K; L368E/K370S : S364K; T411E/K360E/Q362E : D401K; L368D/K370S : S364K/E357L; K370S : S364K/E357Q; 및T366S/L368A/Y407V/Y349C : T366W/S354C로 이루어지는 군으로부터 선택됨), 선택적으로 절제 변이체, 선택적으로 하전된 도메인 링커, 및 pI 변이체를 포함하는 중쇄를 포함할 수 있다.
일부 구현예에서, Fc 도메인은 236R, 239D, 239E, 243L, M252Y, V259I, 267D, 267E, 298A, V308F, 328F, 328R, 330L, 332D, 332E, M428L, N434A, N434S, 236R/328R, 239D/332E, M428L, 236R/328F, V259I/V308F, 267E/328F, M428L/N434S, Y436I/M428L, Y436V/M428L, Y436I/N434S, Y436V/N434S, 239D/332E/330L, M252Y/S254T/T256E, V259I/V308F/M428L, E233P/L234V/L235A/G236del/S267K, G236R/L328R 및 PVA/S267K로 이루어지는 군으로부터 선택되는 아미노산 치환을 포함한다. 일부 경우에, Fc 도메인은 아미노산 치환 239D/332E를 포함한다. 다른 경우에, Fc 도메인은 아미노산 치환 G236R/L328R 또는 PVA/S267K를 포함한다.
하나의 구현예에서, 본 발명에서 사용되는 비대칭 변이체와 pI 변이체의 특정한 조합은 T366S/L368A/Y407V : T366W(선택적으로 브릿징 다이설파이드, T366S/L368A/Y407V/Y349C : T366W/S354C를 포함함)이며, 여기서 하나의 단량체는 Q295E/N384D/Q418E/N481D를 포함하고, 다른 하나는 양으로 하전된 도메인 링커이다. 당업계에서 이해되는 바와 같이, "놉 인 홀" 변이체는 pI를 변경시키지 않기 때문에, 어느 단량체에도 사용될 수 있다. 본 발명의 특정 형식에 사용될 수 있는 변이체의 유용한 조합은 도 7a 내지 도 7f에 포함되어 있다.
III. IL-15/IL-15Rα Fc 융합체 x LAG-3 ABD 이종이량체 단백질
본원에는 체크포인트 저해제 LAG-3 항원에 결합할 수 있고, 공통 감마 사슬(γc; CD132) 및/또는 IL-2 수용체 β-사슬(IL-2Rβ; CD122)과 복합체를 형성할 수 있는 이종이량체 융합 단백질이 제공된다. 이종이량체 융합 단백질은 IL-15/IL-15Rα-Fc 융합 단백질과 항체 융합 단백질을 함유할 수 있다. IL-15/IL-15Rα-Fc 융합 단백질은 IL-15Rα에 공유결합으로 부착된 IL-15 단백질(일반적으로 아미노산 치환을 포함함), 및 Fc 도메인을 포함할 수 있다. 선택적으로, IL-15 단백질과 IL-15Rα 단백질은 비공유결합으로 부착된다.
IV. 본 발명의 유용한 형식
도 21에 제시된 바와 같이, 본 발명의 표적화 IL-15/IL-15Rα 이종이량체 융합 단백질의 다수의 유용한 형식이 존재한다. 일반적으로, 본원에 제공된 이종이량체 융합 단백질은 IL-15/IL-15Rα(스시) 구성요소, 항-LAG-3 구성요소(또한 "LAG-3 결합 도메인" 또는 "LAG-3 항원 결합 도메인"으로 지칭됨), 및 제1 Fc 도메인 및 제2 Fc 도메인을 포함하는 Fc 구성요소의 세 가지 기능성 구성요소를 가지며, 이들은 각각 본원에 개괄된 바와 같이 상이한 형태를 취할 수 있고, 임의의 입체구조로 다른 구성요소와 조합될 수 있다.
제1 Fc 도메인 및 제2 Fc 도메인은, EU 넘버링에 따라 a) S267K/L368D/K370S : S267K/S364K/E357Q; b) S364K/E357Q : L368D/K370S; c) L368D/K370S : S364K; d) L368E/K370S : S364K; e) T411E/K360E/Q362E : D401K; f) L368D/K370S : S364K/E357L 및 g) K370S : S364K/E357Q의 비대칭 변이체로부터 선택되는 아미노산 비대칭 치환 세트를 가질 수 있다. 예시적인 구현예에서, 비대칭 변이체는 S364K/E357Q : L368D/K370S이다.
일부 구현예에서, 제1 Fc 도메인 및/또는 제2 Fc 도메인은, EU 넘버링에 따라 Q295E/N384D/Q418E/N421D, N208/Q295E/N384D/Q418E/N421D 또는 Q196K/I199T/P217R/P228R/N276K의 pI 변이체로부터 선택되는 추가의 pI 아미노산 치환 세트를 갖는다.
선택적으로, 제1 Fc 도메인 및/또는 제2 Fc 도메인은, EU 넘버링에 따라 G236R/L328R, E233P/L234V/L235A/G236del/S239K, E233P/L234V/L235A/G236del/S267K, E233P/L234V/L235A/G236del/S239K/A327G, E233P/L234V/L235A/G236del/S267K/A327G 및 E233P/L234V/L235A/G236del의 FcKO 변이체로부터 선택되는 추가의 절제("FcKO") 변이체 세트를 갖는다.
선택적으로, 제1 Fc 도메인 및/또는 제2 Fc 도메인은 반감기 연장을 위한 428L/434S 변이체를 갖는다.
힌지 또는 부분 힌지가 Fc 도메인을 scFv, IL-15 또는 IL-15Rα 도메인에 연결하는 데 사용되는 구현예에서, 힌지는 선택적으로 힌지가 임의의 경쇄와 바람직하지 않은 다이설파이드 결합을 형성하는 것을 방지하기 위해 C220S 치환을 포함할 수 있다.
본 발명의 이종이량체 융합 단백질의 예시적인 형식이 하기에 제공된다.
A. scIL-15/Rα X scFv
하나의 구현예는 도 21a에 제시되어 있으며, 이는 2개의 단량체를 포함한다. 제1 단량체는, N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하고, 여기서 제2 도메인 링커는 종종 힌지 도메인이며, 제2 단량체는 VH-scFv 링커-VL-힌지-CH2-CH3 또는 VL-scFv 링커-VH-힌지-CH2-CH3을 포함하지만, 어느 배향으로도 도메인 링커는 힌지로 대체될 수 있다. 이는 일반적으로 "scIL-15/Rα X scFv"로 지칭되며, 여기서 "sc"는 공유결합 링커를 사용한 IL-15 변이체와 IL-15Rα(스시) 도메인의 부착을 나타내는 "단일 사슬"을 의미한다. 이러한 구현예에 대한 변이체의 바람직한 조합은 도 21a 및 도 21b에 제시되어 있다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); 및 b) N-말단에서 C-말단으로, 항-LAG-3 scFv-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임)를 포함하는, "scIL-15/Rα X scFv" 형식 이종이량체 단백질이다. 비제한적으로, 도 8 및 도 9a 내지 도 9c의 링커를 포함하는 임의의 유용한 도메인 링커가 상기 이종이량체 단백질의 다양한 구성요소를 부착시키는 데 사용될 수 있다. 예시적인 구현예에서, 상기 IL-15 변이체를 제1 Fc 도메인에 부착시키고 항-LAG-3 scFv를 제2 Fc 도메인에 부착시키는 도메인 링커는, 각각 항체 힌지 도메인이다.
일부 구현예에서, 상기 항-LAG-3 scFv는 scFv 링커(예를 들어, 도 9a 내지 도 9c)에 의해 가변 경쇄 도메인(VL)에 공유결합으로 부착된 가변 중쇄 도메인(VH)을 포함한다. 하나의 구현예에서, 상기 항-LAG-3 scFv는, N-말단에서 C-말단으로, VH-scFv 링커-VL이다. 또 다른 구현예에서, 상기 항-LAG-3 scFv는, N-말단에서 C-말단으로, VL-scFv 링커-VH이다. 상기 항-LAG-3 scFv의 C-말단은 도메인 링커(예를 들어, 항체 힌지 도메인)에 의해 제1 Fc 도메인의 N-말단에 부착된다.
scIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 도 12 및 도 13a 내지 도 13c에 제시된 바와 같은 임의의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다.
scIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, "scIL-15/Rα X scFv" 형식 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(힌지)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); 및 b) N-말단에서 C-말단으로, 항-LAG-3 scFv-(힌지)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인이고, 항-LAG-3 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인을 포함함)를 포함한다. 하나의 구현예에서, "scIL-15/Rα X scFv" 형식 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(힌지)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); 및 b) N-말단에서 C-말단으로, 항-LAG-3 scFv-(힌지)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인이고, 항-LAG-3 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인을 포함함)를 포함한다.
scIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는 IL-15 변이체를 이용한다. 하나의 구현예에서, "scIL-15/Rα X scFv" 형식 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(힌지)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); 및 b) N-말단에서 C-말단으로, 항-LAG-3 scFv-(힌지)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임)를 포함하며, 여기서 IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함한다. 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
scIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 IL-15 N4D/N65D 변이체 또는 IL-15 D30N/N65D 변이체 또는 IL-15 D30N/E64Q/N65D 변이체와 함께, 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, "scIL-15/Rα X scFv" 형식 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(힌지)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); 및 b) N-말단에서 C-말단으로, 항-LAG-3 scFv-(힌지)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인이고, 항-LAG-3 scFv는 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인을 포함함)를 포함하며, 여기서 IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함한다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. scIL-15/Rα X scFv 형식 이종이량체 단백질의 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. scIL-15/Rα X scFv 형식 이종이량체 단백질의 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 IL-15 D30N/E64Q/N65D 변이체이고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다.
scIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); 및 b) N-말단에서 C-말단으로, 항-LAG-3 scFv-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임)를 포함하며, 여기서 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "scIL-15/Rα X scFv" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); 및 b) N-말단에서 C-말단으로, 항-LAG-3 scFv-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임)를 포함하며, 여기서 IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "scIL-15/Rα X scFv" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함한다. 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
scIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 및 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, "scIL-15/Rα X scFv" 형식 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(힌지)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); 및 b) N-말단에서 C-말단으로, 항-LAG-3 scFv-(힌지)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인이고, 항-LAG-3 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인을 포함함)를 포함하며, 여기서 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함한다. 하나의 구현예에서, "scIL-15/Rα X scFv" 형식 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(힌지)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); 및 b) N-말단에서 C-말단으로, 항-LAG-3 scFv-(힌지)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인이고, 항-LAG-3 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인을 포함함)를 포함하며, 여기서 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함한다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함한다.
scIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 IL-15 N4D/N65D 변이체 또는 IL-15 D30N/N65D 변이체 또는 IL-15 D30N/E64Q/N65D 변이체와 함께, 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 및 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, "scIL-15/Rα X scFv" 형식 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(힌지)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); 및 b) N-말단에서 C-말단으로, 항-LAG-3 scFv-(힌지)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인이고, 항-LAG-3 scFv는 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인을 포함함)를 포함하며, 여기서 IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함한다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함한다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. scIL-15/Rα X scFv 형식 이종이량체 단백질의 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 IL-15 D30N/E64Q/N65D 변이체이고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다.
scIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 비대칭 변이체 세트 S364K/E357Q : L368D/K370S, pI 변이체 Q295E/N384D/Q418E/N421D, 제1 단량체와 제2 단량체 양쪽 상의 절제 변이체 E233P/L234V/L235A/G236_/S267K, 및 선택적으로 제1 단량체와 제2 단량체 양쪽 상의 428L/434S 변이체를 이용한다.
하나의 구현예에서, "scIL-15/Rα X scFv" 형식 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); 및 b) N-말단에서 C-말단으로, 항-LAG-3 scFv-(힌지)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임)를 포함하며, 여기서 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 변이체 Fc 도메인은 pI 변이체 Q295E/N384D/Q418E/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따른다. 일부 구현예에서, 상기 제1 단량체의 힌지와 제2 단량체의 힌지는 또한 각각 아미노산 치환 C220S를 포함한다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 예시적인 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함한다. 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함한다. 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
scIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 도 21a 형식으로 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 비대칭 변이체 세트 S364K/E357Q : L368D/K370S, pI 변이체 Q295E/N384D/Q418E/N421D, 제1 단량체와 제2 단량체 양쪽 상의 절제 변이체 E233P/L234V/L235A/G236_/S267K, 및 선택적으로 제1 단량체와 제2 단량체 양쪽 상의 428L/434S 변이체를 갖는 항-LAG-3 ABD를 이용한다.
하나의 구현예에서, "scIL-15/Rα X scFv" 형식 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); 및 b) N-말단에서 C-말단으로, 항-LAG-3 scFv-(힌지)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인이고, 항-LAG-3 scFv는 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인을 포함함)를 포함하며, 여기서 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 변이체 Fc 도메인은 pI 변이체 Q295E/N384D/Q418E/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따른다. 일부 구현예에서, 상기 제1 단량체의 힌지와 제2 단량체의 힌지는 또한 각각 아미노산 치환 C220S를 포함한다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. scIL-15/Rα X scFv 형식 이종이량체 단백질의 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다.
B. scFv X ncIL-15/Rα
이 구현예는 도 21b에 제시되어 있으며, 이는 3개의 단량체를 포함한다. 제1 단량체는, N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-도메인 링커-CH2-CH3을 포함하고, 제2 단량체는 VH-scFv 링커-VL-힌지-CH2-CH3 또는 VL-scFv 링커-VH-힌지-CH2-CH3을 포함하지만, 어느 배향으로도 도메인 링커는 힌지로 대체될 수 있다. 제3 단량체는 변이체 IL-15 도메인이다. 이는 일반적으로 "ncIL-15/Rα X scFv" 또는 "scFv X ncIL-15/Rα"로 지칭되며, 여기서 "nc"는IL-15 변이체와 IL-15Rα(스시) 도메인의 비공유결합형 부착의 자가 조립을 나타내는 "비공유결합"을 의미한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, 항-LAG-3 scFv-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); 및 c) IL-15 변이체를 포함하며, 여기서 IL-15 변이체와 IL-15Rα(스시) 도메인이 IL-15 복합체를 형성하는, "scFv X ncIL-15/Rα" 형식 이종이량체 단백질이다. 비제한적으로, 도 8 및 도 9a 내지 도 9c의 링커를 포함하는 임의의 유용한 도메인 링커가 상기 이종이량체 단백질의 다양한 구성요소를 부착시키는 데 사용될 수 있다. 예시적인 구현예에서, 상기 항-LAG-3 scFv를 제1 Fc 도메인에 부착시키고 IL-15Rα(스시) 도메인을 제2 Fc 도메인에 부착시키는 도메인 링커는, 각각 항체 힌지 도메인이다.
일부 구현예에서, 상기 항-LAG-3 scFv는 scFv 링커(예를 들어, 도 9a 내지 도 9c)에 의해 가변 경쇄 도메인(VL)에 공유결합으로 부착된 가변 중쇄 도메인(VH)을 포함한다. 하나의 구현예에서, 상기 항-LAG-3 scFv는, N-말단에서 C-말단으로, VH-scFv 링커-VL이다. 또 다른 구현예에서, 상기 항-LAG-3 scFv는, N-말단에서 C-말단으로, VL-scFv 링커-VH이다. 상기 항-LAG-3 scFv의 C-말단은 도메인 링커(예를 들어, 항체 힌지 도메인)에 의해 제1 Fc 도메인의 N-말단에 부착된다.
ncIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 도 12 및 도 13a 내지 도 13c에 제시된 바와 같은 임의의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다.
ncIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, 항-LAG-3 scFv-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); 및 c) IL-15 변이체를 포함하며, 여기서 IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 항-LAG-3 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인을 포함하는, "scFv X ncIL-15/Rα" 형식 이종이량체 단백질이다. 또 다른 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, 항-LAG-3 scFv-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); 및 c) IL-15 변이체를 포함하며, 여기서 IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 항-LAG-3 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인을 포함하는, "scFv X ncIL-15/Rα" 형식 이종이량체 단백질이다.
ncIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는 IL-15 변이체를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, 항-LAG-3 scFv-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); 및 c) IL-15 변이체를 포함하며, 여기서 IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는, "scFv X ncIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
ncIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 IL-15 N4D/N65D 변이체 또는 IL-15 D30N/N65D 변이체 또는 IL-15 D30N/E64Q/N65D 변이체와 함께, 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, 항-LAG-3 scFv-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); 및 c) IL-15 변이체를 포함하며, 여기서 IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 항-LAG-3 scFv는 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인을 포함하고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는, "scFv X ncIL-15/Rα" 형식 이종이량체 단백질이다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다.
ncIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, 항-LAG-3 scFv-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) IL-15 변이체를 포함하며, 여기서 IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "scFv X ncIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, 항-LAG-3 scFv-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) IL-15 변이체를 포함하며, 여기서 IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "scFv X ncIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함한다. 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
ncIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 및 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, 항-LAG-3 scFv-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) IL-15 변이체를 포함하며, 여기서 IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 항-LAG-3 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인을 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "scFv X ncIL-15/Rα" 형식 이종이량체 단백질이다. 또 다른 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, 항-LAG-3 scFv-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) IL-15 변이체를 포함하며, 여기서 IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 항-LAG-3 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인을 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "scFv X ncIL-15/Rα" 형식 이종이량체 단백질이다.
ncIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 IL-15 N4D/N65D 변이체 또는 IL-15 D30N/N65D 변이체 또는 IL-15 D30N/E64Q/N65D 변이체와 함께, 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 및 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 갖는 항-LAG-3 ABD를 이용한다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, 항-LAG-3 scFv-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) IL-15 변이체를 포함하며, 여기서 IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 항-LAG-3 scFv는 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인을 포함하고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "scFv X ncIL-15/Rα" 형식 이종이량체 단백질이다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다.
ncIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 비대칭 변이체 세트 S364K/E357Q : L368D/K370S, pI 변이체 Q295E/N384D/Q418E/N421D, 제1 단량체와 제2 단량체 양쪽 상의 절제 변이체 E233P/L234V/L235A/G236_/S267K, 및 선택적으로 제1 단량체와 제2 단량체 양쪽 상의 428L/434S 변이체를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, 항-LAG-3 scFv-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) IL-15 변이체를 포함하며, 여기서 IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 변이체 Fc 도메인은 pI 변이체 Q295E/N384D/Q418E/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "scFv X ncIL-15/Rα" 형식 이종이량체 단백질이다. 일부 구현예에서, 상기 제1 단량체의 힌지와 제2 단량체의 힌지는 또한 각각 아미노산 치환 C220S를 포함한다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 예시적인 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함한다. 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함한다. 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
ncIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 도 21b 형식으로 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 비대칭 변이체 세트 S364K/E357Q : L368D/K370S, pI 변이체 Q295E/N384D/Q418E/N421D, 제1 단량체와 제2 단량체 양쪽 상의 절제 변이체 E233P/L234V/L235A/G236_/S267K, 및 선택적으로 제1 단량체와 제2 단량체 양쪽 상의 428L/434S 변이체를 갖는 항-LAG-3 ABD를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, 항-LAG-3 scFv-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) IL-15 변이체를 포함하며, 여기서 IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 항-LAG-3 scFv는 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인을 포함하고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 변이체 Fc 도메인은 pI 변이체 Q295E/N384D/Q418E/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "scFv X ncIL-15/Rα" 형식 이종이량체 단백질이다. 일부 구현예에서, 상기 제1 단량체의 힌지와 제2 단량체의 힌지는 또한 각각 아미노산 치환 C220S를 포함한다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. scIL-15/Rα X scFv 형식 이종이량체 단백질의 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다.
C. scFv X dsIL-15/Rα
이 구현예는 도 21c에 제시되어 있으며, 이는 3개의 단량체를 포함한다. 제1 단량체는, N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-도메인 링커-CH2-CH3을 포함하고, 여기서 IL-15Rα(스시) 도메인은 조작된 시스테인 잔기를 가지며, 상기 제2 단량체는 VH-scFv 링커-VL-힌지-CH2-CH3 또는 VL-scFv 링커-VH-힌지-CH2-CH3을 포함하지만, 어느 배향으로든 도메인 링커는 힌지로 대체될 수 있다. 제3 단량체는 또한 시스테인 변이체 아미노산을 갖도록 조작되어 IL-15Rα(스시) 도메인과 변이체 IL-15 도메인 사이에 다이설파이드 브릿지가 형성되도록 하는 변이체 IL-15 도메인이다. 이는 일반적으로 "scFv X dsIL-15/Rα" 또는 dsIL-15/Rα X scFv로 지칭되며, 여기서 "ds"는 "다이설파이드"를 의미한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, 항-LAG-3 scFv-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인이고, IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함함); 및 c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하며, 여기서 IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기가 다이설파이드 결합을 형성하는, "scFv X dsIL-15/Rα" 형식 이종이량체 단백질이다. 비제한적으로, 도 8 및 도 9a 내지 도 9c의 링커를 포함하는 임의의 유용한 도메인 링커가 상기 이종이량체 단백질의 다양한 구성요소를 부착시키는 데 사용될 수 있다. 예시적인 구현예에서, 상기 항-LAG-3 scFv를 제1 Fc 도메인에 부착시키고 IL-15Rα(스시) 도메인을 제2 Fc 도메인에 부착시키는 도메인 링커는, 각각 항체 힌지 도메인이다.
비제한적으로, 도 8 및 도 9a 내지 도 9c의 링커를 포함하는 임의의 유용한 도메인 링커가 상기 이종이량체 단백질의 다양한 구성요소를 부착시키는 데 사용될 수 있다. 예시적인 구현예에서, 상기 항-LAG-3 scFv를 제1 Fc 도메인에 부착시키고 IL-15Rα(스시) 도메인을 제2 Fc 도메인에 부착시키는 도메인 링커는, 각각 항체 힌지 도메인(예를 들어, 항체 힌지 도메인)이다.
일부 구현예에서, 상기 항-LAG-3 scFv는 scFv 링커(예를 들어, 도 9a 내지 도 9c)에 의해 가변 경쇄 도메인(VL)에 공유결합으로 부착된 가변 중쇄 도메인(VH)을 포함한다. 하나의 구현예에서, 상기 항-LAG-3 scFv는, N-말단에서 C-말단으로, VH-scFv 링커-VL이다. 또 다른 구현예에서, 상기 항-LAG-3 scFv는, N-말단에서 C-말단으로, VL-scFv 링커-VH이다. 상기 항-LAG-3 scFv의 C-말단은 도메인 링커(예를 들어, 항체 힌지 도메인)에 의해 제1 Fc 도메인의 N-말단에 부착된다.
dsIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 도 12 및 도 13a 내지 도 13c에 제시된 바와 같은 임의의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다.
dsIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, 항-LAG-3 scFv-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인이고, IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함함); 및 c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하며, 여기서 IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, 항-LAG-3 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인을 포함하는, "scFv X dsIL-15/Rα" 형식 이종이량체 단백질이다. 또 다른 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, 항-LAG-3 scFv-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인이고, IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함함); 및 c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하며, 여기서 IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, 항-LAG-3 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인을 포함하는, "scFv X dsIL-15/Rα" 형식 이종이량체 단백질이다.
dsIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 IL-15 N4D/N65D 변이체 또는 IL-15 D30N/N65D 변이체 또는 IL-15 D30N/E64Q/N65D 변이체 뿐 아니라, 적절한 시스테인 치환을 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, 항-LAG-3 scFv-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인이고, IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함함); 및 c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하며, 여기서 IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는, "scFv X dsIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
dsIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 IL-15 N4D/N65D 변이체 또는 IL-15 D30N/N65D 변이체 또는 IL-15 D30N/E64Q/N65D 변이체, 및 적절한 시스테인 치환과 함께, 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, 항-LAG-3 scFv-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인이고, IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함함); 및 c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하며, 여기서 IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, 항-LAG-3 scFv는 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인을 포함하고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는, "scFv X dsIL-15/Rα" 형식 이종이량체 단백질이다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다.
dsIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, 항-LAG-3 scFv-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인이고, IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함함); 및 c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하며, 여기서 IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "scFv X dsIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, 항-LAG-3 scFv-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인이고, IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함함); 및 c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하며, 여기서 IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "scFv X dsIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함한다. 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
dsIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 및 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, 항-LAG-3 scFv-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인이고, IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함함); 및 c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하며, 여기서 IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, 항-LAG-3 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인을 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "scFv X dsIL-15/Rα" 형식 이종이량체 단백질이다. 또 다른 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, 항-LAG-3 scFv-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인이고, IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함함); 및 c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하며, 여기서 IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, 항-LAG-3 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인을 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "scFv X dsIL-15/Rα" 형식 이종이량체 단백질이다.
dsIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 IL-15 N4D/N65D 변이체 또는 IL-15 D30N/N65D 변이체 또는 IL-15 D30N/E64Q/N65D 변이체, 및 적절한 시스테인 치환과 함께, 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 및 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 갖는 항-LAG-3 ABD를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, 항-LAG-3 scFv-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인이고, IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함함); 및 c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하며, 여기서 IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, 항-LAG-3 scFv는 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인을 포함하고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "scFv X dsIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함한다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다.
dsIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 비대칭 변이체 세트 S364K/E357Q : L368D/K370S, pI 변이체 Q295E/N384D/Q418E/N421D, 제1 단량체와 제2 단량체 양쪽 상의 절제 변이체 E233P/L234V/L235A/G236_/S267K, 및 선택적으로 제1 단량체와 제2 단량체 양쪽 상의 428L/434S 변이체를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, 항-LAG-3 scFv-(힌지)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인이고, IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함함); 및 c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하며, 여기서 IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 변이체 Fc 도메인은 pI 변이체 Q295E/N384D/Q418E/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "scFv X dsIL-15/Rα" 형식 이종이량체 단백질이다. 일부 구현예에서, 상기 제1 단량체의 힌지와 제2 단량체의 힌지는 또한 각각 아미노산 치환 C220S를 포함한다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 예시적인 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함한다. 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함한다. 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 예시적인 구현예에서, 상기 LAG-3 scFv는 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL을 포함하고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
dsIL-15/Rα X scFv 형식에서, 하나의 바람직한 구현예는 도 21c 형식으로 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 비대칭 변이체 세트 S364K/E357Q : L368D/K370S, pI 변이체 Q295E/N384D/Q418E/N421D, 제1 단량체와 제2 단량체 양쪽 상의 절제 변이체 E233P/L234V/L235A/G236_/S267K, 및 선택적으로 제1 단량체와 제2 단량체 양쪽 상의 428L/434S 변이체를 갖는 항-LAG-3 ABD를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, 항-LAG-3 scFv-(힌지)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인이고, IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함함); 및 c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하며, 여기서 IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, 항-LAG-3 scFv는 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인을 포함하고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 변이체 Fc 도메인은 pI 변이체 Q295E/N384D/Q418E/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "scFv X dsIL-15/Rα" 형식 이종이량체 단백질이다. 일부 구현예에서, 상기 제1 단량체의 힌지와 제2 단량체의 힌지는 또한 각각 아미노산 치환 C220S를 포함한다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. scIL-15/Rα X scFv 형식 이종이량체 단백질의 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다.
D. scIL-15/Rα X Fab
이 구현예는 도 21d에 제시되어 있으며, 이는 3개의 단량체를 포함한다. 제1 단량체는, N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-변이체 IL-15-도메인 링커-CH2-CH3을 포함하고, 제2 단량체는 중쇄 VH-CH1-힌지-CH2-CH3을 포함한다. 제3 단량체는 경쇄인 VL-CL이다. 이는 일반적으로 "scIL-15/Rα X Fab"로 지칭되며, 여기서 "sc"는 "단일 사슬"을 의미한다. scIL-15/Rα x Fab 형식(도 21d 참조)은 가변 길이 링커에 의해 변이체 IL-15에 융합된 IL-15Rα(스시)("scIL-15/Rα"로 지칭됨)를 포함하며, 이는 이후에 이종이량체 Fc-영역(힌지 포함)의 N-말단에 융합된다. 제2 단량체는 중쇄인 VH-CH1-힌지-CH2-CH3이며, 상응하는 경쇄(제3 단량체)는 VH와 Fab을 형성하도록 별도로 트랜스펙션된다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제2 Fc 도메인임), 및 c) N-말단에서 C-말단으로, VL-VC를 포함하는 경쇄(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 VH와 VL이 LAG-3 결합 도메인을 형성하는, "scIL-15/Rα X Fab" 형식 이종이량체 단백질이다. 비제한적으로, 도 8 및 도 9a 내지 도 9c의 링커를 포함하는 임의의 유용한 도메인 링커가 상기 이종이량체 단백질의 다양한 구성요소를 부착시키는 데 사용될 수 있다. 예시적인 구현예에서, 상기 IL-15 변이체를 제1 Fc 도메인에 부착시키는 도메인 링커는 항체 힌지 도메인(예를 들어, 항체 힌지 도메인)이다.
scIL-15/Rα X Fab 형식에서, 하나의 바람직한 구현예는 도 12 및 도 13a 내지 도 13c에 제시된 바와 같은 임의의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다.
scIL-15/Rα X Fab 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 융합 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제2 Fc 도메인임), 및 c) N-말단에서 C-말단으로, VL-VC를 포함하는 경쇄(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 VH 및 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인인, "scIL-15/Rα X Fab" 형식 이종이량체 단백질이다. 또 다른 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제2 Fc 도메인임), 및 c) N-말단에서 C-말단으로, VL-VC를 포함하는 경쇄(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 VH 및 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인인, "scIL-15/Rα X Fab" 형식 이종이량체 단백질이다.
scIL-15/Rα X Fab 형식에서, 하나의 바람직한 구현예는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는 IL-15 변이체를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제2 Fc 도메인임), 및 c) N-말단에서 C-말단으로, VL-VC를 포함하는 경쇄(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 VH와 VL이 LAG-3 결합 도메인을 형성하고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는, "scIL-15/Rα X Fab" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
scIL-15/Rα X Fab 형식에서, 하나의 바람직한 구현예는 IL-15 N4D/N65D 변이체 또는 IL-15 D30N/N65D 변이체 또는 IL-15 D30N/E64Q/N65D 변이체와 함께, 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제2 Fc 도메인임), 및 c) N-말단에서 C-말단으로, VL-VC를 포함하는 경쇄(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는, "scIL-15/Rα X Fab" 형식 이종이량체 단백질이다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다.
scIL-15/Rα X Fab 형식에서, 하나의 바람직한 구현예는 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제2 변이체 Fc 도메인임), 및 c) N-말단에서 C-말단으로, VL-VC를 포함하는 경쇄(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 VH와 VL은 LAG-3 결합 도메인을 형성하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "scIL-15/Rα X Fab" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제2 변이체 Fc 도메인임), 및 c) N-말단에서 C-말단으로, VL-VC를 포함하는 경쇄(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 VH와 VL은 LAG-3 결합 도메인을 형성하고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "scIL-15/Rα X Fab" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함한다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
scIL-15/Rα X Fab 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 및 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제2 변이체 Fc 도메인임), 및 c) N-말단에서 C-말단으로, VL-VC를 포함하는 경쇄(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 VH 및 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "scIL-15/Rα X Fab" 형식 이종이량체 단백질이다. 또 다른 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제2 변이체 Fc 도메인임), 및 c) N-말단에서 C-말단으로, VL-VC를 포함하는 경쇄(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 VH 및 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "scIL-15/Rα X Fab" 형식 이종이량체 단백질이다.
scIL-15/Rα X Fab 형식에서, 하나의 바람직한 구현예는 IL-15 N4D/N65D 변이체 또는 IL-15 D30N/N65D 변이체 또는 IL-15 D30N/E64Q/N65D 변이체와 함께, 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 및 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제2 변이체 Fc 도메인임), 및 c) N-말단에서 C-말단으로, VL-VC를 포함하는 경쇄(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "scIL-15/Rα X Fab" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함한다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다.
scIL-15/Rα X Fab 형식에서, 하나의 바람직한 구현예는 비대칭 변이체 세트 S364K/E357Q : L368D/K370S, pI 변이체 Q295E/N384D/Q418E/N421D, 제1 단량체와 제2 단량체 양쪽 상의 절제 변이체 E233P/L234V/L235A/G236_/S267K, 및 선택적으로 제1 단량체와 제2 단량체 양쪽 상의 428L/434S 변이체를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제2 변이체 Fc 도메인임), 및 c) N-말단에서 C-말단으로, VL-VC를 포함하는 경쇄(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 VH와 VL은 LAG-3 결합 도메인을 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 변이체 Fc 도메인은 pI 변이체 Q295E/N384D/Q418E/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "scIL-15/Rα X Fab" 형식 이종이량체 단백질이다. 일부 구현예에서, 상기 제1 단량체의 힌지는 또한 아미노산 치환 C220S를 포함한다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 예시적인 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함한다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
scIL-15/Rα X Fab 형식에서, 하나의 바람직한 구현예는 도 21d 형식으로 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 비대칭 변이체 세트 S364K/E357Q : L368D/K370S, pI 변이체 Q295E/N384D/Q418E/N421D, 제1 단량체와 제2 단량체 양쪽 상의 절제 변이체 E233P/L234V/L235A/G236_/S267K, 및 선택적으로 제1 단량체와 제2 단량체 양쪽 상의 428L/434S 변이체를 갖는 항-LAG-3 ABD를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제2 변이체 Fc 도메인임), 및 c) N-말단에서 C-말단으로, VL-VC를 포함하는 경쇄(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 변이체 Fc 도메인은 pI 변이체 Q295E/N384D/Q418E/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "scIL-15/Rα X Fab" 형식 이종이량체 단백질이다. 일부 구현예에서, 상기 제1 단량체의 힌지는 또한 아미노산 치환 C220S를 포함한다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. scIL-15/Rα X scFv 형식 이종이량체 단백질의 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 scFv는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다.
E. Fab X ncIL-15/Rα
이 구현예는 도 21e에 제시되어 있으며, 이는 4개의 단량체를 포함한다. 제1 단량체는, N-말단에서 C-말단으로, IL-15Rα(스시)도메인-(도메인 링커)-CH2-CH3을 포함하고, 제2 단량체는 중쇄인 VH-CH1-힌지-CH2-CH3을 포함한다. 제3 단량체는, N-말단에서 C-말단으로, 가변 경쇄 도메인(VL) 및 경쇄 불변 도메인(CL)을 포함하는 경쇄이다. 제4 단량체는 변이체 IL-15 도메인이다. 이는 일반적으로 "Fab X ncIL-15/Rα"로 지칭되며, 여기서 "nc"는IL-15 변이체와 IL-15Rα(스시) 도메인의 비공유결합형 부착의 자가 조립을 나타내는 "비공유결합"을 의미한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); c) N-말단에서 C-말단으로, VL-VC를 포함하는 제3 단량체(여기서 VL은 가변 경쇄 도메인임); 및 d) IL-15 변이체를 포함하는 제4 단량체를 포함하며, 여기서 VH와 VL은 LAG-3 결합 도메인을 형성하고, IL-15 도메인과 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하는, "Fab X ncIL-15/Rα" 형식 이종이량체 단백질이다. 비제한적으로, 도 8 및 도 9a 내지 도 9c의 링커를 포함하는 임의의 유용한 도메인 링커가 상기 이종이량체 단백질의 다양한 구성요소를 부착시키는 데 사용될 수 있다. 예시적인 구현예에서, 상기 IL-15Rα(스시) 도메인을 제2 Fc 도메인에 부착시키는 도메인 링커는 항체 힌지 도메인(예를 들어, 항체 힌지 도메인)이다.
Fab X ncIL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 임의의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다.
Fab X ncIL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); c) N-말단에서 C-말단으로, VL-VC를 포함하는 제3 단량체(여기서 VL은 가변 경쇄 도메인임); 및 d) IL-15 변이체를 포함하는 제4 단량체를 포함하며, 여기서 VH 및 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 도메인과 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하는, "Fab X ncIL-15/Rα" 형식 이종이량체 단백질이다. 또 다른 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); c) N-말단에서 C-말단으로, VL-VC를 포함하는 제3 단량체(여기서 VL은 가변 경쇄 도메인임); 및 d) IL-15 변이체를 포함하는 제4 단량체를 포함하며, 여기서 VH 및 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 도메인과 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하는, "Fab X ncIL-15/Rα" 형식 이종이량체 단백질이다.
Fab X ncIL-15/Rα 형식에서, 하나의 바람직한 구현예는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는 IL-15 변이체를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); c) N-말단에서 C-말단으로, VL-VC를 포함하는 제3 단량체(여기서 VL은 가변 경쇄 도메인임); 및 d) IL-15 변이체를 포함하는 제4 단량체를 포함하며, 여기서 VH와 VL은 LAG-3 결합 도메인을 형성하고, IL-15 도메인과 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는, "Fab X ncIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
Fab X ncIL-15/Rα 형식에서, 하나의 바람직한 구현예는 IL-15 N4D/N65D 변이체 또는 IL-15 D30N/N65D 변이체 또는 IL-15 D30N/E64Q/N65D 변이체와 함께, 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); c) N-말단에서 C-말단으로, VL-VC를 포함하는 제3 단량체(여기서 VL은 가변 경쇄 도메인임); 및 d) IL-15 변이체를 포함하는 제4 단량체를 포함하며, 여기서 VH와 VL은 LAG-3 결합 도메인을 형성하고, IL-15 도메인과 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는, "Fab X ncIL-15/Rα" 형식 이종이량체 단백질이다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다.
Fab X ncIL-15/Rα 형식에서, 하나의 바람직한 구현예는 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); c) N-말단에서 C-말단으로, VL-VC를 포함하는 제3 단량체(여기서 VL은 가변 경쇄 도메인임); 및 d) IL-15 변이체를 포함하는 제4 단량체를 포함하며, 여기서 VH와 VL은 LAG-3 결합 도메인을 형성하고, IL-15 도메인과 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "Fab X ncIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); c) N-말단에서 C-말단으로, VL-VC를 포함하는 제3 단량체(여기서 VL은 가변 경쇄 도메인임); 및 d) IL-15 변이체를 포함하는 제4 단량체를 포함하며, 여기서 VH와 VL은 LAG-3 결합 도메인을 형성하고, IL-15 도메인과 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "Fab X ncIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함한다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
Fab X ncIL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 및 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); c) N-말단에서 C-말단으로, VL-VC를 포함하는 제3 단량체(여기서 VL은 가변 경쇄 도메인임); 및 d) IL-15 변이체를 포함하는 제4 단량체를 포함하며, 여기서 VH 및 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 도메인과 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "Fab X ncIL-15/Rα" 형식 이종이량체 단백질이다. 또 다른 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); c) N-말단에서 C-말단으로, VL-VC를 포함하는 제3 단량체(여기서 VL은 가변 경쇄 도메인임); 및 d) IL-15 변이체를 포함하는 제4 단량체를 포함하며, 여기서 VH 및 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 도메인과 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "Fab X ncIL-15/Rα" 형식 이종이량체 단백질이다.
Fab X ncIL-15/Rα 형식에서, 하나의 바람직한 구현예는 IL-15 N4D/N65D 변이체 또는 IL-15 D30N/N65D 변이체 또는 IL-15 D30N/E64Q/N65D 변이체와 함께, 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 및 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 갖는 항-LAG-3 ABD를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); c) N-말단에서 C-말단으로, VL-VC를 포함하는 제3 단량체(여기서 VL은 가변 경쇄 도메인임); 및 d) IL-15 변이체를 포함하는 제4 단량체를 포함하며, 여기서 VH와 VL은 LAG-3 결합 도메인을 형성하고, IL-15 도메인과 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "Fab X ncIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함한다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다.
Fab X ncIL-15/Rα 형식에서, 하나의 바람직한 구현예는 비대칭 변이체 세트 S364K/E357Q : L368D/K370S, pI 변이체 Q295E/N384D/Q418E/N421D, 제1 단량체와 제2 단량체 양쪽 상의 절제 변이체 E233P/L234V/L235A/G236_/S267K, 및 선택적으로 제1 단량체와 제2 단량체 양쪽 상의 428L/434S 변이체를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); c) N-말단에서 C-말단으로, VL-VC를 포함하는 제3 단량체(여기서 VL은 가변 경쇄 도메인임); 및 d) IL-15 변이체를 포함하는 제4 단량체를 포함하며, 여기서 VH와 VL은 LAG-3 결합 도메인을 형성하고, IL-15 도메인과 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 변이체 N208D/Q295E/N384D/Q418E/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "Fab X ncIL-15/Rα" 형식 이종이량체 단백질이다. 일부 구현예에서, 상기 제2 단량체의 힌지는 또한 아미노산 치환 C220S를 포함한다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 예시적인 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함한다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
Fab X ncIL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 21e 형식으로 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 비대칭 변이체 세트 S364K/E357Q : L368D/K370S, pI 변이체 Q295E/N384D/Q418E/N421D, 제1 단량체와 제2 단량체 양쪽 상의 절제 변이체 E233P/L234V/L235A/G236_/S267K, 및 선택적으로 제1 단량체와 제2 단량체 양쪽 상의 428L/434S 변이체를 갖는 항-LAG-3 ABD를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); c) N-말단에서 C-말단으로, VL-VC를 포함하는 제3 단량체(여기서 VL은 가변 경쇄 도메인임); 및 d) IL-15 변이체를 포함하는 제4 단량체를 포함하며, 여기서 VH와 VL은 LAG-3 결합 도메인을 형성하고, IL-15 도메인과 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 변이체 N208D/Q295E/N384D/Q418E/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "Fab X ncIL-15/Rα" 형식 이종이량체 단백질이다. 일부 구현예에서, 상기 제2 단량체의 힌지는 또한 아미노산 치환 C220S를 포함한다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 scFv는 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 포함한다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다.
F. Fab X dsIL-15/Rα
이 구현예는 도 21f에 제시되어 있으며, 이는 4개의 단량체를 포함한다. 제1 단량체는, N-말단에서 C-말단으로, IL-15Rα(스시)도메인-도메인 링커-CH2-CH3을 포함하고, 여기서 IL-15Rα(스시)도메인은 시스테인 잔기를 함유하도록 조작되어 있으며, 제2 단량체는 중쇄인 VH-CH1-힌지-CH2-CH3을 포함한다. 제3 단량체는, N-말단에서 C-말단으로, 가변 경쇄 도메인(VL) 및 불변 경쇄 도메인(CL)을 포함하는 경쇄이다. 제4 단량체는 나이브 세포 조건 하에서 다이설파이드 브릿지가 형성되도록, 시스테인 잔기를 갖도록 조작된 변이체 IL-15 도메인이다. 이는 일반적으로 "Fab x dsIL-15/Rα"로 지칭되며, 여기서 "ds"는 "다이설파이드"를 의미한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인이고, IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함함); c) N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체(여기서 VL은 가변 경쇄 도메인임); 및 d) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하며, 여기서 VH와 VL은 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하는, "Fab X dsIL-15/Rα" 형식 이종이량체 단백질이다. 비제한적으로, 도 8 및 도 9a 내지 도 9c의 링커를 포함하는 임의의 유용한 도메인 링커가 상기 이종이량체 단백질의 다양한 구성요소를 부착시키는 데 사용될 수 있다. 예시적인 구현예에서, 상기 IL-15Rα(스시) 도메인을 제2 Fc 도메인에 부착시키는 도메인 링커는 항체 힌지 도메인(예를 들어, 항체 힌지 도메인)이다.
Fab X dsIL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 임의의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다.
Fab X dsIL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인이고, IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함함); c) N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체(여기서 VL은 가변 경쇄 도메인임); 및 d) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하며, 여기서 VH 및 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하는, "Fab X dsIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인이고, IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함함); c) N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체(여기서 VL은 가변 경쇄 도메인임); 및 d) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하며, 여기서 VH 및 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하는, "Fab X dsIL-15/Rα" 형식 이종이량체 단백질이다.
Fab X dsIL-15/Rα 형식에서, 하나의 바람직한 구현예는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D, 및 적절한 시스테인 아미노산 치환을 포함하는 IL-15 변이체를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인이고, IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함함); c) N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체(여기서 VL은 가변 경쇄 도메인임); 및 d) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하며, 여기서 VH와 VL은 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는, "Fab X dsIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
Fab X dsIL-15/Rα 형식에서, 하나의 바람직한 구현예는 IL-15 N4D/N65D 변이체 또는 IL-15 D30N/N65D 변이체 또는 IL-15 D30N/E64Q/N65D 변이체, 및 적절한 시스테인 아미노산 치환과 함께, 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인이고, IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함함); c) N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체(여기서 VL은 가변 경쇄 도메인임); 및 d) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하며, 여기서 VH와 VL은 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는, "Fab X dsIL-15/Rα" 형식 이종이량체 단백질이다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다.
Fab X dsIL-15/Rα 형식에서, 하나의 바람직한 구현예는 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인이고, IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함함); c) N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체(여기서 VL은 가변 경쇄 도메인임); 및 d) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하며, 여기서 VH와 VL은 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "Fab X dsIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인이고, IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함함); c) N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체(여기서 VL은 가변 경쇄 도메인임); 및 d) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하며, 여기서 VH와 VL은 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "Fab X dsIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함한다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
Fab X dsIL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 및 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인이고, IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함함); c) N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체(여기서 VL은 가변 경쇄 도메인임); 및 d) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하며, 여기서 VH 및 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "Fab X dsIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인이고, IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함함); c) N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체(여기서 VL은 가변 경쇄 도메인임); 및 d) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하며, 여기서 VH 및 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "Fab X dsIL-15/Rα" 형식 이종이량체 단백질이다.
Fab X dsIL-15/Rα 형식에서, 하나의 바람직한 구현예는 IL-15 N4D/N65D 변이체 또는 IL-15 D30N/N65D 변이체 또는 IL-15 D30N/E64Q/N65D 변이체, 및 적절한 시스테인 치환과 함께, 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 및 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인이고, IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함함); c) N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체(여기서 VL은 가변 경쇄 도메인임); 및 d) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하며, 여기서 VH와 VL은 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "Fab X dsIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함한다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다.
Fab X dsIL-15/Rα 형식에서, 하나의 바람직한 구현예는 비대칭 변이체 세트 S364K/E357Q : L368D/K370S, pI 변이체 Q295E/N384D/Q418E/N421D, 제1 단량체와 제2 단량체 양쪽 상의 절제 변이체 E233P/L234V/L235A/G236_/S267K, 및 선택적으로 제1 단량체와 제2 단량체 양쪽 상의 428L/434S 변이체를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인이고, IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함함); c) N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체(여기서 VL은 가변 경쇄 도메인임); 및 d) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하며, 여기서 VH와 VL은 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 변이체 N208D/Q295E/N384D/Q418E/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "Fab X dsIL-15/Rα" 형식 이종이량체 단백질이다. 일부 구현예에서, 상기 제2 단량체의 힌지는 또한 아미노산 치환 C220S를 포함한다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 예시적인 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함한다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
Fab X dsIL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 21f 형식으로 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 비대칭 변이체 세트 S364K/E357Q : L368D/K370S, pI 변이체 Q295E/N384D/Q418E/N421D, 제1 단량체와 제2 단량체 양쪽 상의 절제 변이체 E233P/L234V/L235A/G236_/S267K, 및 선택적으로 제1 단량체와 제2 단량체 양쪽 상의 428L/434S 변이체를 갖는 항-LAG-3 ABD를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인이고, IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함함); c) N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체(여기서 VL은 가변 경쇄 도메인임); 및 d) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하며, 여기서 VH와 VL은 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 변이체 N208D/Q295E/N384D/Q418E/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "Fab X dsIL-15/Rα" 형식 이종이량체 단백질이다. 일부 구현예에서, 상기 제2 단량체의 힌지는 또한 아미노산 치환 C220S를 포함한다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다.
G. mAb-scIL-15/Rα
이 구현예는 도 21g에 제시되어 있으며, 이는 (융합 단백질은 사량체이지만) 3개의 단량체를 포함한다. 제1 단량체는 중쇄인 VH-CH1-힌지-CH2-CH3을 포함한다. 제2 단량체는 scIL-15 복합체를 갖는 중쇄인, VH-CH1-힌지-CH2-CH3-도메인 링커-IL-15Rα 스시 도메인-도메인 링커-IL-15 변이체를 포함한다. 제3 단량체 (및 제4 단량체)는 경쇄인 VL-CL이다. 이는 일반적으로 "mAb-scIL-15/Rα"로 지칭되며, 여기서 "sc"는 "단일 사슬"을 의미한다. 이는 LAG-3 분자에 2가로(bivalently) 결합한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); 및 c) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하는, "mAb-scIL-15/Rα" 형식 이종이량체 단백질이다. 비제한적으로, 도 8 및 도 9a 내지 도 9c의 링커를 포함하는 임의의 유용한 도메인 링커가 상기 이종이량체 단백질의 다양한 구성요소를 부착시키는 데 사용될 수 있다.
mAb-scIL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 임의의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다.
mAb-scIL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); 및 c) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH 및 제3 단량체의 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제2 단량체의 VH 및 제4 단량체의 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하는, "mAb-scIL-15/Rα" 형식 이종이량체 단백질이다. 또 다른 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); 및 c) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH 및 제3 단량체의 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제2 단량체의 VH 및 제4 단량체의 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하는, "mAb-scIL-15/Rα" 형식 이종이량체 단백질이다.
mAb-scIL-15/Rα 형식에서, 하나의 바람직한 구현예는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는 IL-15 변이체를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); 및 c) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는, "mAb-scIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
mAb-scIL-15/Rα 형식에서, 하나의 바람직한 구현예는 IL-15 N4D/N65D 변이체 또는 IL-15 D30N/N65D 변이체 또는 IL-15 D30N/E64Q/N65D 변이체와 함께, 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); 및 c) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는, "mAb-scIL-15/Rα" 형식 이종이량체 단백질이다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다.
mAb-scIL-15/Rα 형식에서, 하나의 바람직한 구현예는 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "mAb-scIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D 및 K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K 및 E357Q를 포함한다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 S364K 및 E357Q를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 L368D 및 K370S를 포함한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "mAb-scIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D 및 K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K 및 E357Q를 포함한다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 S364K 및 E357Q를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 L368D 및 K370S를 포함한다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
mAb-scIL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 및 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH 및 제3 단량체의 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제2 단량체의 VH 및 제4 단량체의 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "mAb-scIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH 및 제3 단량체의 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제2 단량체의 VH 및 제4 단량체의 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "mAb-scIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D 및 K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K 및 E357Q를 포함한다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 S364K 및 E357Q를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 L368D 및 K370S를 포함한다.
mAb-scIL-15/Rα 형식에서, 하나의 바람직한 구현예는 IL-15 N4D/N65D 변이체 또는 IL-15 D30N/N65D 변이체 또는 IL-15 D30N/E64Q/N65D 변이체와 함께, 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 및 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "mAb-scIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D 및 K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K 및 E357Q를 포함한다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D 및 K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K 및 E357Q를 포함한다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 S364K 및 E357Q를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 L368D 및 K370S를 포함한다.
mAb-scIL-15/Rα 형식에서, 하나의 바람직한 구현예는 비대칭 변이체 세트 S364K/E357Q : L368D/K370S, pI 변이체 N208D/Q295E/N384D/Q418D/N421D 및/또는 Q196K/I199T/P271R/P228R/N276K, 제1 단량체와 제2 단량체 양쪽 상의 절제 변이체 E233P/L234V/L235A/G236_/S267K, 및 선택적으로 제1 단량체와 제2 단량체 양쪽 상의 428L/434S 변이체를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 N208D/Q295E/N384D/Q418D/N421D를 포함하고, 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 Q196K/I199T/P271R/P228R/N276K를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-scIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 N208D/Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-scIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 Q196K/I199T/P271R/P228R/N276K를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-scIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 L368D/K370S를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 Q196K/I199T/P271R/P228R/N276K를 포함하고, 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 N208D/Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-scIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 L368D/K370S를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 Q196K/I199T/P271R/P228R/N276K를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-scIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 L368D/K370S를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제2 단량체의 힌지-제2 변이체 Fc 도메인의 힌지-제1 변이체 Fc 도메인은 pI 변이체 N208D/Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-scIL-15/Rα" 형식 이종이량체 단백질이다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 예시적인 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함한다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
mAb-scIL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 21g 형식으로 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 비대칭 변이체 세트 S364K/E357Q : L368D/K370S, pI 변이체 N208D/Q295E/N384D/Q418D/N421D 및/또는 Q196K/I199T/P271R/P228R/N276K, 제1 단량체와 제2 단량체 양쪽 상의 절제 변이체 E233P/L234V/L235A/G236_/S267K, 및 선택적으로 제1 단량체와 제2 단량체 양쪽 상의 428L/434S 변이체를 갖는 항-LAG-3 ABD를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 N208D/Q295E/N384D/Q418D/N421D를 포함하고, 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 Q196K/I199T/P271R/P228R/N276K를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-scIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 N208D/Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-scIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 Q196K/I199T/P271R/P228R/N276K를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-scIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 L368D/K370S를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 Q196K/I199T/P271R/P228R/N276K를 포함하고, 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 N208D/Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-scIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 L368D/K370S를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 Q196K/I199T/P271R/P228R/N276K를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-scIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 L368D/K370S를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제2 단량체의 힌지-제2 변이체 Fc 도메인의 힌지-제1 변이체 Fc 도메인은 pI 변이체 N208D/Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-scIL-15/Rα" 형식 이종이량체 단백질이다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다.
H. mAb-ncIL-15/Rα
이 구현예는 도 21h에 제시되어 있으며, 이는 (이종이량체 융합 단백질은 오량체이지만) 4개의 단량체를 포함한다. 제1 단량체는 중쇄인 VH-CH1-힌지-CH2-CH3을 포함한다. 제2 단량체는 scIL-15α(스시) 도메인을 갖는 중쇄인, 예를 들어 VH-CH1-힌지-CH2-CH3-도메인 링커-IL-15Rα(스시) 도메인을 포함한다. 제3 단량체는 변이체 IL-15 도메인이다. 제4 단량체 (및 제5 단량체)는 경쇄인 VL-CL이다. 이는 일반적으로 "mAb-ncIL-15/Rα"로 지칭되며, 여기서 "nc"는 "비공유결합"을 의미한다. 이는 또한 LAG-3에 2가로 결합한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); c) IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하는, "mAb-ncIL-15/Rα" 형식 이종이량체 단백질이다. 비제한적으로, 도 8 및 도 9a 내지 도 9c의 링커를 포함하는 임의의 유용한 도메인 링커가 상기 이종이량체 단백질의 다양한 구성요소를 부착시키는 데 사용될 수 있다.
mAb-ncIL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 임의의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다.
mAb-ncIL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); c) IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH 및 제4 단량체의 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제2 단량체의 VH 및 제5 단량체의 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하는, "mAb-ncIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); c) IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH 및 제4 단량체의 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제2 단량체의 VH 및 제5 단량체의 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하는, "mAb-ncIL-15/Rα" 형식 이종이량체 단백질이다.
mAb-ncIL-15/Rα 형식에서, 하나의 바람직한 구현예는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는 IL-15 변이체를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); c) IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는, "mAb-ncIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
mAb-ncIL-15/Rα 형식에서, 하나의 바람직한 구현예는 IL-15 N4D/N65D 변이체 또는 IL-15 D30N/N65D 변이체 또는 IL-15 D30N/E64Q/N65D 변이체와 함께, 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); c) IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는, "mAb-ncIL-15/Rα" 형식 이종이량체 단백질이다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다.
mAb-ncIL-15/Rα 형식에서, 하나의 바람직한 구현예는 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); c) IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "mAb-ncIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함한다. 또 다른 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); c) IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "mAb-ncIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함한다. 또 다른 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함한다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
mAb-ncIL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 및 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); c) IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH 및 제4 단량체의 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제2 단량체의 VH 및 제5 단량체의 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "mAb-ncIL-15/Rα" 형식 이종이량체 단백질이다. 또 다른 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); c) IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH 및 제4 단량체의 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제2 단량체의 VH 및 제5 단량체의 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "mAb-ncIL-15/Rα" 형식 이종이량체 단백질이다.
mAb-ncIL-15/Rα 형식에서, 하나의 바람직한 구현예는 IL-15 N4D/N65D 변이체 또는 IL-15 D30N/N65D 변이체 또는 IL-15 D30N/E64Q/N65D 변이체와 함께, 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 및 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); c) IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "mAb-ncIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함한다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함한다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다.
mAb-ncIL-15/Rα 형식에서, 하나의 바람직한 구현예는 비대칭 변이체 세트 S364K/E357Q : L368D/K370S, pI 변이체 N208D/Q295E/N384D/Q418D/N421D 및/또는 Q196K/I199T/P271R/P228R/N276K, 제1 단량체와 제2 단량체 양쪽 상의 절제 변이체 E233P/L234V/L235A/G236_/S267K, 및 선택적으로 제1 단량체와 제2 단량체 양쪽 상의 428L/434S 변이체를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 N208D/Q295E/N384D/Q418D/N421D를 포함하고, 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 Q196K/I199T/P271R/P228R/N276K를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-ncIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 N208D/Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-ncIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 Q196K/I199T/P271R/P228R/N276K를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-ncIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 L368D/K370S를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 Q196K/I199T/P271R/P228R/N276K를 포함하고, 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 N208D/Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-ncIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 L368D/K370S를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 Q196K/I199T/P271R/P228R/N276K를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-ncIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 L368D/K370S를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 N208D/Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-ncIL-15/Rα" 형식 이종이량체 단백질이다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 예시적인 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함한다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
mAb-ncIL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 21h 형식으로 도 12에 제시된 바와 같은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 비대칭 변이체 세트 S364K/E357Q : L368D/K370S, pI 변이체 N208D/Q295E/N384D/Q418D/N421D 및/또는 Q196K/I199T/P271R/P228R/N276K, 제1 단량체와 제2 단량체 양쪽 상의 절제 변이체 E233P/L234V/L235A/G236_/S267K, 및 선택적으로 제1 단량체와 제2 단량체 양쪽 상의 428L/434S 변이체를 갖는 항-LAG-3 ABD를 이용한다. 예시적인 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 N208D/Q295E/N384D/Q418D/N421D를 포함하고, 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 Q196K/I199T/P271R/P228R/N276K를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-ncIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 N208D/Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-ncIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 Q196K/I199T/P271R/P228R/N276K를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-ncIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 L368D/K370S를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 Q196K/I199T/P271R/P228R/N276K를 포함하고, 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 N208D/Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-ncIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 L368D/K370S를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 Q196K/I199T/P271R/P228R/N276K를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-ncIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 c) IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 L368D/K370S를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 N208D/Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-ncIL-15/Rα" 형식 이종이량체 단백질이다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다.
I. mAb-dsIL-15/Rα
이 구현예는 도 21i에 제시되어 있으며, 이는 (이종이량체 융합 단백질은 오량체이지만) 4개의 단량체를 포함한다. 제1 단량체는 중쇄인 VH-CH1-힌지-CH2-CH3을 포함한다. 제2 단량체는 IL-15Rα(스시) 도메인을 갖는 중쇄인, 예를 들어 VH-CH1-힌지-CH2-CH3-도메인 링커-IL-15Rα(스시) 도메인을 포함하며, 여기서 IL-15Rα(스시) 도메인은 시스테인 잔기를 함유하도록 조작되었다. 제3 단량체는 생리학적 조건 하에서 IL-15 복합체가 형성되도록, 시스테인 잔기를 함유하도록 조작된 변이체 IL-15 도메인이다. 제4 단량체 (및 제5 단량체)는 경쇄인 VL-CL이다. 이는 일반적으로 "mAb-dsIL-15/Rα"로 지칭되며, 여기서 "ds"는 "다이설파이드"를 의미하고, 이는 LAG-3에 2가로 결합한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함하고, CH2-CH3은 제2 Fc 도메인임); c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하는, "mAb-dsIL-15/Rα" 형식 이종이량체 단백질이다. 비제한적으로, 도 8 및 도 9a 내지 도 9c의 링커를 포함하는 임의의 유용한 도메인 링커가 상기 이종이량체 단백질의 다양한 구성요소를 부착시키는 데 사용될 수 있다.
mAb-dsIL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 임의의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다.
mAb-dsIL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함하고, CH2-CH3은 제2 Fc 도메인임); c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제2 단량체의 VH와 제5 단량체의 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하는, "mAb-dsIL-15/Rα" 형식 이종이량체 단백질이다. 또 다른 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함하고, CH2-CH3은 제2 Fc 도메인임); c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제2 단량체의 VH와 제5 단량체의 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하는, "mAb-dsIL-15/Rα" 형식 이종이량체 단백질이다.
mAb-dsIL-15/Rα 형식에서, 하나의 바람직한 구현예는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D, 및 적절한 시스테인 아미노산 치환을 포함하는 IL-15 변이체를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함하고, CH2-CH3은 제2 Fc 도메인임); c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는, "mAb-dsIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
mAb-dsIL-15/Rα 형식에서, 하나의 바람직한 구현예는 IL-15 N4D/N65D 변이체 또는 IL-15 D30N/N65D 변이체 또는 IL-15 D30N/E64Q/N65D 변이체, 및 적절한 시스테인 아미노산 치환과 함께, 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함하고, CH2-CH3은 제2 Fc 도메인임); c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는, "mAb-dsIL-15/Rα" 형식 이종이량체 단백질이다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다.
mAb-dsIL-15/Rα 형식에서, 하나의 바람직한 구현예는 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함하고, CH2-CH3은 제2 변이체 Fc 도메인임); c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "mAb-dsIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함한다. 또 다른 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함하고, CH2-CH3은 제2 변이체 Fc 도메인임); c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "mAb-dsIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함한다. 또 다른 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함한다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
mAb-dsIL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 및 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함하고, CH2-CH3은 제2 변이체 Fc 도메인임); c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제2 단량체의 VH와 제5 단량체의 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "mAb-dsIL-15/Rα" 형식 이종이량체 단백질이다. 또 다른 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함하고, CH2-CH3은 제2 변이체 Fc 도메인임); c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제2 단량체의 VH와 제5 단량체의 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "mAb-dsIL-15/Rα" 형식 이종이량체 단백질이다.
mAb-dsIL-15/Rα 형식에서, 하나의 바람직한 구현예는 IL-15 N4D/N65D 변이체 또는 IL-15 D30N/N65D 변이체 또는 IL-15 D30N/E64Q/N65D 변이체, 및 적절한 시스테인 치환과 함께, 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 및 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함하고, CH2-CH3은 제2 Fc 도메인임); c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "mAb-dsIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함한다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함한다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다.
mAb-dsIL-15/Rα 형식에서, 하나의 바람직한 구현예는 비대칭 변이체 세트 S364K/E357Q : L368D/K370S, pI 변이체 N208D/Q295E/N384D/Q418D/N421D 및/또는 Q196K/I199T/P271R/P228R/N276K, 제1 단량체와 제2 단량체 양쪽 상의 절제 변이체 E233P/L234V/L235A/G236_/S267K, 및 선택적으로 제1 단량체와 제2 단량체 양쪽 상의 428L/434S 변이체를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함하고, CH2-CH3은 제2 Fc 도메인임); c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 N208D/Q295E/N384D/Q418D/N421D를 포함하고, 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 Q196K/I199T/P271R/P228R/N276K를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-dsIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함하고, CH2-CH3은 제2 Fc 도메인임); c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 N208D/Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-dsIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함하고, CH2-CH3은 제2 Fc 도메인임); c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 Q196K/I199T/P271R/P228R/N276K를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-dsIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함하고, CH2-CH3은 제2 Fc 도메인임); c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 L368D/K370S를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 Q196K/I199T/P271R/P228R/N276K를 포함하고, 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 N208D/Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-dsIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함하고, CH2-CH3은 제2 Fc 도메인임); c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 L368D/K370S를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 Q196K/I199T/P271R/P228R/N276K를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-dsIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함하고, CH2-CH3은 제2 Fc 도메인임); c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 L368D/K370S를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 N208D/Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-dsIL-15/Rα" 형식 이종이량체 단백질이다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 예시적인 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함한다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
mAb-dsIL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 21i 형식으로 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 비대칭 변이체 세트 S364K/E357Q : L368D/K370S, pI 변이체 N208D/Q295E/N384D/Q418D/N421D 및/또는 Q196K/I199T/P271R/P228R/N276K, 제1 단량체와 제2 단량체 양쪽 상의 절제 변이체 E233P/L234V/L235A/G236_/S267K, 및 선택적으로 제1 단량체와 제2 단량체 양쪽 상의 428L/434S 변이체를 갖는 항-LAG-3 ABD를 이용한다. 예시적인 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함하고, CH2-CH3은 제2 Fc 도메인임); c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 N208D/Q295E/N384D/Q418D/N421D를 포함하고, 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 Q196K/I199T/P271R/P228R/N276K를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-dsIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함하고, CH2-CH3은 제2 Fc 도메인임); c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 N208D/Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-dsIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함하고, CH2-CH3은 제2 Fc 도메인임); c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 Q196K/I199T/P271R/P228R/N276K를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-dsIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함하고, CH2-CH3은 제2 Fc 도메인임); c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 L368D/K370S를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 Q196K/I199T/P271R/P228R/N276K를 포함하고, 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 N208D/Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-dsIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함하고, CH2-CH3은 제2 Fc 도메인임); c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 L368D/K370S를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 단량체의 힌지-제1 변이체 Fc 도메인은 pI 치환 Q196K/I199T/P271R/P228R/N276K를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-dsIL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)를 포함하는 제2 단량체(여기서 IL-15Rα(스시) 도메인은 시스테인 잔기에 대한 아미노산 치환을 포함하고, CH2-CH3은 제2 Fc 도메인임); c) 시스테인 잔기에 대한 아미노산 치환을 포함하는 IL-15 변이체를 포함하는 제3 단량체; 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제4 단량체 및 제5 단량체(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 제1 단량체의 VH와 제4 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제5 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체 상의 시스테인 잔기와 IL-15Rα(스시) 도메인 상의 시스테인 잔기는 다이설파이드 결합을 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 L368D/K370S를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제2 단량체의 힌지-제2 변이체 Fc 도메인은 pI 변이체 N208D/Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "mAb-dsIL-15/Rα" 형식 이종이량체 단백질이다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다.
J. central-IL-15/Rα
이 구현예는 도 21j에 제시되어 있으며, 이는 사량체를 형성하는 4개의 단량체를 포함한다. 제1 단량체는 VH-CH1-[선택적 도메인 링커]-IL-15 변이체-[선택적 도메인 링커]-CH2-CH3을 포함하며, 여기서 제2 선택적 도메인 링커는 때때로 힌지 도메인이다. 제2 단량체는 VH-CH1-[선택적 도메인 링커]-IL-15Rα(스시) 도메인-[선택적 도메인 링커]-CH2-CH3을 포함하며, 여기서 제2 선택적 도메인 링커는 때때로 힌지 도메인이다. 제3 단량체 (및 제4 단량체)는 경쇄인 VL-CL이다. 이는 일반적으로 "central-IL-15/Rα"로 지칭된다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하는, "central-IL-15/Rα" 형식 이종이량체 단백질이다. 비제한적으로, 도 8 및 도 9a 내지 도 9c의 링커를 포함하는 임의의 유용한 도메인 링커가 상기 이종이량체 단백질의 다양한 구성요소를 부착시키는 데 사용될 수 있다. 예시적인 구현예에서, 상기 IL-15 변이체를 제1 Fc 도메인에 부착시키고 IL-15Rα(스시) 도메인을 제2 Fc 도메인에 부착시키는 도메인 링커는, 각각 항체 힌지 도메인이다.
central-IL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 임의의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다.
central-IL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH 및 제3 단량체의 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제2 단량체의 VH 및 제4 단량체의 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하는, "central-IL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH 및 제3 단량체의 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제2 단량체의 VH 및 제4 단량체의 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하는, "central-IL-15/Rα" 형식 이종이량체 단백질이다.
"central-IL-15/Rα" 형식에서, 하나의 바람직한 구현예는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는 IL-15 변이체를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는, "central-IL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
central-IL-15/Rα 형식에서, 하나의 바람직한 구현예는 IL-15 N4D/N65D 변이체 또는 IL-15 D30N/N65D 변이체 또는 IL-15 D30N/E64Q/N65D 변이체와 함께, 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는, "central-IL-15/Rα" 형식 이종이량체 단백질이다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다.
central-IL-15/Rα 형식에서, 하나의 바람직한 구현예는 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "central-IL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 S364K 및 E357Q를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 L368D 및 K370S를 포함한다. 또 다른 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D 및 K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K 및 E357Q를 포함한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "central-IL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 S364K 및 E357Q를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 L368D 및 K370S를 포함한다. 또 다른 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D 및 K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K 및 E357Q를 포함한다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
central-IL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 및 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH 및 제3 단량체의 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제2 단량체의 VH 및 제4 단량체의 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "central-IL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH 및 제3 단량체의 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제2 단량체의 VH 및 제4 단량체의 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "central-IL-15/Rα" 형식 이종이량체 단백질이다.
central-IL-15/Rα 형식에서, 하나의 바람직한 구현예는 IL-15 N4D/N65D 변이체 또는 IL-15 D30N/E64Q/N65D 변이체, 및 적절한 시스테인 치환과 함께, 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 및 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "central-IL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 S364K 및 E357Q를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 L368D 및 K370S를 포함한다. 또 다른 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D 및 K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K 및 E357Q를 포함한다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다.
central-IL-15/Rα 형식에서, 하나의 바람직한 구현예는 비대칭 변이체 세트 S364K/E357Q : L368D/K370S, pI 변이체 Q295E/N384D/Q418E/N421D, 제1 단량체와 제2 단량체 양쪽 상의 절제 변이체 E233P/L234V/L235A/G236_/S267K, 및 선택적으로 제1 단량체와 제2 단량체 양쪽 상의 428L/434S 변이체를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15 변이체-(힌지)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(힌지)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 변이체 Fc 도메인은 pI 치환 Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "central-IL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15 변이체-(힌지)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(힌지)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 L368D/K370S를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제2 단량체의 제2 변이체 Fc 도메인은 pI 치환 Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "central-IL-15/Rα" 형식 이종이량체 단백질이다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 예시적인 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함한다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
central-IL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 21k 형식으로 도 12에 제시된 바와 같은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 비대칭 변이체 세트 S364K/E357Q : L368D/K370S, pI 변이체 Q295E/N384D/Q418E/N421D, 제1 단량체와 제2 단량체 양쪽 상의 절제 변이체 E233P/L234V/L235A/G236_/S267K, 및 선택적으로 제1 단량체와 제2 단량체 양쪽 상의 428L/434S 변이체를 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15 변이체-(힌지)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(힌지)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 변이체 Fc 도메인은 pI 치환 Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "central-IL-15/Rα" 형식 이종이량체 단백질이다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15 변이체-(힌지)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(힌지)-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 L368D/K370S를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제2 단량체의 제2 변이체 Fc 도메인은 pI 치환 Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "central-IL-15/Rα" 형식 이종이량체 단백질이다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다.
K. central scIL-15/Rα
이 구현예는 도 21k에 제시되어 있으며, 이는 사량체를 형성하는 4개의 단량체를 포함한다. 제1 단량체는 VH-CH1-[선택적 도메인 링커]-IL-15Rα(스시) 도메인-도메인 링커-IL-15 변이체-[선택적 도메인 링커]-CH2-CH3을 포함하며, 여기서 제2 선택적 도메인 링커는 때때로 힌지 도메인이다. 제2 단량체는 VH-CH1-힌지-CH2-CH3을 포함한다. 제3 단량체 (및 제4 단량체)는 경쇄인 VL-CL이다. 이는 일반적으로 "central-scIL-15/Rα"로 지칭되며, 여기서 "sc"는 "단일 사슬"을 의미한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하는, "central-scIL-15/Rα" 형식 이종이량체 단백질이다. 비제한적으로, 도 8 및 도 9a 내지 도 9c의 링커를 포함하는 임의의 유용한 도메인 링커가 상기 이종이량체 단백질의 다양한 구성요소를 부착시키는 데 사용될 수 있다. 예시적인 구현예에서, 상기 IL-15 변이체를 제1 Fc 도메인에 부착시키는 도메인 링커는 항체 힌지 도메인이다.
central-scIL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 임의의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다.
central-scIL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH 및 제3 단량체의 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제2 단량체의 VH 및 제4 단량체의 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하는, "central-scIL-15/Rα" 형식 이종이량체 단백질이다. 또 다른 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-(도메인 링커)-IL-15 변이체-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH 및 제3 단량체의 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제2 단량체의 VH 및 제4 단량체의 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하는, "central-scIL-15/Rα" 형식 이종이량체 단백질이다.
central-scIL-15/Rα 형식에서, 하나의 바람직한 구현예는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는 IL-15 변이체를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는, "central-scIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
central-scIL-15/Rα 형식에서, 하나의 바람직한 구현예는 IL-15 N4D/N65D 변이체 또는 IL-15 D30N/N65D 변이체 또는 IL-15 D30N/E64Q/N65D 변이체와 함께, 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍을 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는, "central-scIL-15/Rα" 형식 이종이량체 단백질이다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다.
central-scIL-15/Rα 형식에서, 하나의 바람직한 구현예는 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "central-scIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D 및 K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K 및 E357Q를 포함한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "central-scIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D 및 K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K 및 E357Q를 포함한다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
central-scIL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 및 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH 및 제3 단량체의 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제2 단량체의 VH 및 제4 단량체의 VL은, 각각, 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "central-scIL-15/Rα" 형식 이종이량체 단백질이다. 또 다른 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH 및 제3 단량체의 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제2 단량체의 VH 및 제4 단량체의 VL은, 각각, 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "central-scIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D 및 K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K 및 E357Q를 포함한다.
central-scIL-15/Rα 형식에서, 하나의 바람직한 구현예는 IL-15 N4D/N65D 변이체 또는 IL-15 D30N/N65D 변이체 또는 IL-15 D30N/E64Q/N65D 변이체와 함께, 도 12에 제시된 바와 같은 7G8_H3.30_L1.34의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 및 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 갖는 항-LAG-3 ABD를 이용한다. 하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 비대칭 변이체 쌍 S364K/E357Q : L368D/K370S를 포함하는, "central-scIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 상기 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함한다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다.
central-scIL-15/Rα 형식에서, 하나의 바람직한 구현예는 비대칭 변이체 세트 S364K/E357Q : L368D/K370S, pI 변이체 Q295E/N384D/Q418E/N421D, 제1 단량체와 제2 단량체 양쪽 상의 절제 변이체 E233P/L234V/L235A/G236_/S267K, 및 선택적으로 제1 단량체와 제2 단량체 양쪽 상의 428L/434S 변이체를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(힌지)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 변이체 Fc 도메인은 pI 변이체 Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "central-scIL-15/Rα" 형식 이종이량체 단백질이다. 예시적인 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함한다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
central-scIL-15/Rα 형식에서, 하나의 바람직한 구현예는 도 21k 형식으로 도 12에 제시된 바와 같은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인과 가변 경쇄 도메인의 쌍, 비대칭 변이체 세트 S364K/E357Q : L368D/K370S, pI 변이체 Q295E/N384D/Q418E/N421D, 제1 단량체와 제2 단량체 양쪽 상의 절제 변이체 E233P/L234V/L235A/G236_/S267K, 및 선택적으로 제1 단량체와 제2 단량체 양쪽 상의 428L/434S 변이체를 갖는 항-LAG-3 ABD를 이용한다.
하나의 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, VH-(도메인 링커)-IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(힌지)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및 d) 각각, N-말단에서 C-말단으로, VL-CL을 포함하는 제3 단량체 및 제4 단량체를 포함하며, 여기서 제1 단량체의 VH와 제3 단량체의 VL은 제1 LAG-3 결합 도메인을 형성하고, 제2 단량체의 VH와 제4 단량체의 VL은 제2 LAG-3 결합 도메인을 형성하고, IL-15 변이체와 IL-15Rα(스시) 도메인은 IL-15 복합체를 형성하고, VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 변이체 Fc 도메인은 pI 변이체 Q295E/N384D/Q418D/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "central-scIL-15/Rα" 형식 이종이량체 단백질이다. 특정 구현예에서, 상기 제1 단량체의 힌지는 변이체 C220S를 추가로 포함한다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 특정 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 하나의 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 7G8_H3.30_L1.34의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 또 다른 구현예에서, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함하고, 상기 VH 및 VL은 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다.
V. 본 발명의 특히 유용한 구현예
본 발명은 적어도 2개의 단량체, 즉 항-LAG-3 ABD를 포함하는 하나의 단량체, 및 이종이량체 Fc 도메인을 사용하여 연결된 IL-15/Rα 복합체를 함유하는 다른 하나의 단량체를 포함하는 표적화 IL-15/IL-15Rα 이종이량체 단백질을 제공한다.
일부 구현예에서, 제1 Fc 도메인과 제2 Fc 도메인은 EU 넘버링에 따라 S267K/L368D/K370S : S267K/S364K/E357Q; S364K/E357Q : L368D/K370S; L368D/K370S : S364K; L368E/K370S : S364K; T411E/K360E/Q362E : D401K; L368D/K370S : S364K/E357L 및 K370S : S364K/E357Q로 이루어지는 군으로부터 선택되는 아미노산 치환 세트를 갖는다.
일부 경우에, 제1 Fc 도메인 및/또는 제2 Fc 도메인은 EU 넘버링에 따라 Q295E/N384D/Q418E/N421D를 포함하는 추가의 아미노산 치환 세트를 갖는다. 일부 경우에, 제1 Fc 도메인 및/또는 제2 Fc 도메인은 EU 넘버링에 따라 G236R/L328R, E233P/L234V/L235A/G236del/S239K, E233P/L234V/L235A/G236del/S267K, E233P/L234V/L235A/G236del/S239K/A327G, E233P/L234V/L235A/G236del/S267K/A327G 및 E233P/L234V/L235A/G236del로 이루어지는 추가의 아미노산 치환 세트를 갖는다.
일부 구현예에서, IL-15 단백질은 서열번호 1(전장의 인간 IL-15) 및 서열번호 2(절단된 인간 IL-15)로 이루어지는 군으로부터 선택되는 폴리펩타이드 서열을 갖고, IL-15Rα 단백질은 서열번호 3(전장의 인간 IL-15Rα) 및 서열번호 4(인간 IL-15Rα의 스시 도메인)로 이루어지는 군으로부터 선택되는 폴리펩타이드 서열을 갖는다.
구현예에서, IL-15 단백질 및 IL-15Rα 단백질은, 각각, E87C : D96/P97/C98; E87C : D96/C97/A98; V49C : S40C; L52C : S40C; E89C : K34C; Q48C : G38C; E53C : L42C; C42S : A37C; 및 L45C : A37C로 이루어지는 군으로부터 선택되는 아미노산 치환 세트를 가질 수 있다.
일부 구현예에서, IL-15 단백질은 역가를 감소시키기 위해 도 19 및 도 20으로부터 선택되는 서열을 갖는 변이체 단백질이다. 일부 구현예에서, IL-15 단백질은 IL-15:CD132 인터페이스에 하나 이상의 아미노산 치환을 갖는 변이체 단백질이다.
일부 구현예에서, LAG-3 항원 결합 도메인은 항-LAG-3 scFv 또는 항-LAG-3 Fab을 포함한다. 예시적인 구현예에서, LAG-3 ABD는 도 12 및 도 13a 내지 도 13c에 도시된 임의의 LAG-3 ABD의 VH 및 VL을 포함한다.
예시적인 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제2 변이체 Fc 도메인임), 및 c) N-말단에서 C-말단으로, VL-VC를 포함하는 경쇄(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 VH와 VL은 LAG-3 결합 도메인을 형성하고, IL-15 변이체는 IL-15 N4D/N65D 변이체이고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 변이체 Fc 도메인은 pI 변이체 Q295E/N384D/Q418E/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "scIL-15/Rα X Fab" 형식 이종이량체 단백질이다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 특정 구현예에서, 상기 제1 단량체의 힌지는 또한 아미노산 치환 C220S를 포함하고, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 일부 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 일부 구현예에서, 상기 VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다(도 12).
예시적인 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제2 변이체 Fc 도메인임), 및 c) N-말단에서 C-말단으로, VL-VC를 포함하는 경쇄(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 VH와 VL은 LAG-3 결합 도메인을 형성하고, IL-15 변이체는 IL-15 D30N/N65D 변이체이고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 변이체 Fc 도메인은 pI 변이체 Q295E/N384D/Q418E/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "scIL-15/Rα X Fab" 형식 이종이량체 단백질이다. 일부 구현예에서, 상기 제1 단량체의 힌지는 또한 아미노산 치환 C220S를 포함한다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 특정 구현예에서, 상기 제1 단량체의 힌지는 또한 아미노산 치환 C220S를 포함하고, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 일부 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 일부 구현예에서, 상기 VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다(도 12).
예시적인 구현예에서, 상기 표적화 IL-15/IL-15Rα 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(도메인 링커)-CH2-CH3을 포함하는 제1 단량체(여기서 CH2-CH3은 제1 변이체 Fc 도메인임); b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 VH는 가변 중쇄 도메인이고, CH2-CH3은 제2 변이체 Fc 도메인임), 및 c) N-말단에서 C-말단으로, VL-VC를 포함하는 경쇄(여기서 VL은 가변 경쇄 도메인임)를 포함하며, 여기서 VH와 VL은 LAG-3 결합 도메인을 형성하고, IL-15 변이체는 IL-15 D30N/E64Q/N65D 변이체이고, 제1 변이체 Fc 도메인은 비대칭 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고, 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고, 제1 변이체 Fc 도메인은 pI 변이체 Q295E/N384D/Q418E/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, "scIL-15/Rα X Fab" 형식 이종이량체 단백질이다. 일부 구현예에서, 상기 제1 단량체의 힌지는 또한 아미노산 치환 C220S를 포함한다. 특정 구현예에서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 특정 구현예에서, 상기 제1 단량체의 힌지는 또한 아미노산 치환 C220S를 포함하고, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 반감기 연장 변이체 M428L/N434S를 추가로 포함한다. 일부 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 가변 중쇄 도메인 및 가변 경쇄 도메인이다. 일부 구현예에서, 상기 VH 및 VL은 7G8_H3.30_L1.34 또는 2A11_H1.144_L2.142의 가변 중쇄 도메인 및 가변 경쇄 도메인이다(도 12).
"scIL-15/Rα X Fab" 형식 이종이량체 단백질에 포함될 수 있는 유용한 "백본" 서열은 도 10에 도시되어 있다. 일부 구현예에서, "scIL-15/Rα X Fab" 형식 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(힌지)-CH2-CH3을 포함하는 제1 단량체(여기서 힌지-CH2-CH3은 도 10의 "백본 1"의 사슬 2의 아미노산 서열(서열번호 XXX)을 가짐); b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 VH는 가변 중쇄 도메인이고, CH1-힌지-CH2-CH3은 도 10의 "백본 1"의 사슬 1의 아미노산 서열(서열번호 XXX)을 가짐); 및 c) N-말단에서 C-말단으로, VL-VC를 포함하는 경쇄(여기서 VL은 가변 경쇄 도메인이고, VC는 도 11의 "불변 경쇄-카파"의 서열(서열번호 XXX)을 가짐)를 포함한다. 특정 구현예에서, "scIL-15/Rα X Fab" 형식 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(힌지)-CH2-CH3을 포함하는 제1 단량체(여기서 힌지-CH2-CH3은 도 10의 "백본 2"의 사슬 2의 아미노산 서열(서열번호 XXX)을 가짐); b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 VH는 가변 중쇄 도메인이고, CH1-힌지-CH2-CH3은 도 10의 "백본 2"의 사슬 1의 아미노산 서열(서열번호 XXX)을 가짐); 및 c) N-말단에서 C-말단으로, VL-VC를 포함하는 경쇄(여기서 VL은 가변 경쇄 도메인이고, VC는 도 11의 "불변 경쇄-카파"의 서열(서열번호 XXX)을 가짐)를 포함한다. 일부 구현예에서, "scIL-15/Rα X Fab" 형식 이종이량체 단백질은, a) N-말단에서 C-말단으로, IL-15Rα(스시) 도메인-(도메인 링커)-IL-15 변이체-(힌지)-CH2-CH3을 포함하는 제1 단량체(여기서 힌지-CH2-CH3은 도 10의 "백본 3"의 사슬 2의 아미노산 서열(서열번호 XXX)을 가짐); b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 VH는 가변 중쇄 도메인이고, CH1-힌지-CH2-CH3은 도 10의 "백본 3"의 사슬 1의 아미노산 서열(서열번호 XXX)을 가짐); 및 c) N-말단에서 C-말단으로, VL-VC를 포함하는 경쇄(여기서 VL은 가변 경쇄 도메인이고, VC는 도 11의 "불변 경쇄-카파"의 서열(서열번호 XXX)을 가짐)를 포함한다. 예시적인 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함한다. 예시적인 구현예에서, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함한다. 예시적인 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 N4D/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/N65D를 포함한다. 또 다른 구현예에서, 상기 VH 및 VL은 도 12 및 도 13a 내지 도 13c의 임의의 LAG-3 ABD의 VH 및 VL이고, 상기 IL-15 변이체는 아미노산 치환 D30N/E64Q/N65D를 포함한다.
특히 바람직한 LAG-3 표적화 IL-15/IL-15Rα-Fc 이종이량체 융합 단백질에는, XENP27972, XENP27973, XENP27977, XENP27978, XENP029486, XENP029487, XENC1000, XENC1001, XENC1002, XENC1003, XENC1004 및 XENC1005의 "scIL-15/Rα X Fab" 형식 이종이량체 단백질이 포함된다. LAG-3 표적화 IL-15/IL-15Rα-Fc 이종이량체 융합 단백질의 예시적인 구현예는, 도 22a 및 도 22b, 도 29a 및 도 29b, 도 46a 및 도 46b, 도 47a 및 도 47b, 및 도 48a 내지 도 48d에 제시되어 있다.
VI. 본 발명의 핵산
또 다른 양태에서, 본원에는 표적화 이종이량체 융합 단백질을 인코딩하는 핵산 조성물 (또는, 단량체 Fc 도메인 단백질의 경우, 이를 인코딩하는 핵산)이 제공된다.
당업자가 이해하는 바와 같이, 이러한 핵산 조성물은 상기 표적화 이종이량체 융합 단백질의 형식에 따라 달라질 것이다. 따라서, 예를 들어 상기 형식이 3개의 아미노산 서열을 필요로 하는 경우, 3개의 핵산 서열은 발현을 위해 하나 이상의 발현 벡터에 혼입될 수 있다. 유사하게, 일부 형식은 2개의 핵산만을 필요로 하며; 다시 말하면, 이들은 1개 또는 2개의 발현 벡터, 또는 4개 또는 5개의 발현 벡터에 도입될 수 있다. 본원에 제시된 바와 같이, 일부 구조체는, 예를 들어 2개의 경쇄 카피를 갖는다.
당업계에 공지된 바와 같이, 본 발명의 구성요소를 인코딩하는 핵산은 당업계에 공지된 바와 같이, 및 본 발명의 표적화 이종이량체 융합 단백질을 생산하는 데 사용되는 숙주세포에 따라 발현 벡터에 혼입될 수 있다. 일반적으로, 핵산은 임의의 수의 조절 요소(프로모터, 복제 기점, 선택 가능한 마커, 리보솜 결합 부위, 유도제 등)에 작동 가능하게 연결된다. 발현 벡터는 염색체외 벡터 또는 통합 벡터일 수 있다.
이어서, 본원에 제공된 핵산 및/또는 발현 벡터는 포유류, 박테리아, 효모, 곤충 세포 및/또는 진균 세포를 포함하는 당업계에 널리 공지된 바와 같은 임의의 수의 상이한 유형의 숙주세포로 형질전환되며, 여기서 포유류 세포(예를 들어, CHO 세포)가 다수의 구현예에서 사용된다.
일부 구현예에서, 형식에 따라 적용 가능한 각각의 단량체를 인코딩하는 핵산은, 일반적으로 상이하거나 동일한 프로모터 제어 하에서 단일 발현 벡터 내에 각각 함유되어 있다. 본 발명의 특정 용도의 구현예에서, 이들 2개 또는 3개의 핵산은 각각 상이한 발현 벡터에 함유되어 있다.
본 발명의 표적화 이종이량체 융합 단백질은 당업계에 공지된 바와 같이 발현 벡터(들)를 포함하는 숙주세포를 배양함으로써 제조된다. 생산되면, 이온 교환 크로마토그래피 단계를 포함하는 통상적인 융합 단백질 또는 항체 정제 단계가 수행된다. 본원에 논의된 바와 같이, 2개의 단량체의 pI를 적어도 0.5만큼 차이나게 하면, 이온 교환 크로마토그래피, 등전점 전기영동 또는 등전점에 민감한 다른 방법에 의한 분리를 가능하게 할 수 있다. 즉, pI 치환의 포함은 각각의 단량체가 상이한 pI를 갖고 이종이량체가 또한 별개의 pI를 갖도록 각각의 단량체의 등전점(pI)을 변경시키며, 따라서 이종이량체의 등전위 정제(예를 들어 음이온 교환 컬럼, 양이온 교환 컬럼)를 용이하게 한다. 이러한 치환은 또한 정제 후 임의의 오염된 동종이량체의 측정 및 모니터링을 돕는다(예를 들어 IEF 겔, cIEF 및 분석용 IEX 컬럼).
VII. 표적화 LAG-3 항체 x IL-15/IL-15Rα 이종이량체 면역조절 융합 단백질의 생물학적 및 생화학적 기능성
일반적으로, 본 발명의 표적화 융합 단백질이 암을 앓고 있는 환자에게 투여되고, 본원에 기재된 바와 같은 다수의 방식으로 효능이 평가된다. 따라서, 암 부하, 종양의 크기, 전이의 존재 또는 정도의 평가 등과 같은 효능의 표준 검정이 수행될 수 있으나, 면역종양학 치료는 또한 면역 상태 평가에 기초하여 평가될 수 있다. 이는 시험관내 검정 및 생체내 검정을 포함하는 다수의 방식으로 수행될 수 있다. 예를 들어, 종양 부하, 크기, 침윤성, LN 침범, 전이 등과 같은 "전형적인" 측정과 함께 면역 상태의 변화가 평가될 수 있다. 따라서, 다음 중 임의의 것 또는 전부가 평가될 수 있다: CD4+ T세포 활성화 또는 증식, CD8+ T(CTL) 세포 활성화 또는 증식, CD8+ T세포 매개 세포독성 활성 및/또는 CTL 매개 세포 고갈, NK세포 활성 및 NK 매개 세포 고갈에 대한 이종이량체 단백질의 저해 효과; Treg 세포 분화 및 증식, 및 Treg 또는 골수 유래 억제 세포(MDSC) 매개 면역억제 또는 면역 내성에 대한 이종이량체 단백질의 강화 효과; 및/또는 면역세포에 의한 전염증성 사이토카인 생산, 예를 들어 T세포 또는 다른 면역세포에 의한 IL-2, IFN-γ 또는 TNF-α 생산에 대한 이종이량체 단백질의 효과.
일부 구현예에서, 치료의 평가는, 예를 들어 CFSE 희석 방법, 면역 효과기 세포의 Ki67 세포내 염색 및 3H-티미딘 혼입 방법을 사용하여 면역세포 증식을 평가함으로써 수행된다.
일부 구현예에서, 치료의 평가는 CD25, CD69, CD137, ICOS, PD1, GITR, OX40 중 하나 이상을 포함하는 활성화 관련 마커의 단백질 수준 증가 또는 유전자 발현 증가, 및 CD107A의 표면 발현에 의해 측정되는 세포 탈과립화를 평가함으로써 수행된다.
일반적으로, 유전자 발현 검정은 당업계에 공지된 바와 같이 수행된다.
일반적으로, 단백질 발현 측정은 또한 당업계에 공지된 바와 같이 유사하게 수행된다.
일부 구현예에서, 치료의 평가는 효소 활성(프로테아제 활성 포함), 세포막 투과성, 세포 부착성, ATP 생산, 조효소 생산 및 뉴클레오타이드 흡수 활성과 같은 다수의 세포 매개변수의 추정을 통한 표적세포 생존력 검출에 의해 측정된 세포독성 활성을 평가함으로써 수행된다. 이러한 검정의 특정 예에는, 비제한적으로, 트립판 블루(Trypan Blue) 또는 PI 염색, 51Cr 또는 35S 방출 방법, LDH 활성, MTT 및/또는 WST 검정, 칼세인(Calcein)-AM 검정, 발광 기반의 검정 등이 포함된다.
일부 구현예에서, 치료의 평가는 사이토카인 생산에 의해 측정되는 T세포의 활성을 평가함으로써 수행되며, 여기서 측정은 널리 공지된 기술을 사용하여, 비제한적으로, IFNγ, TNFα, GM-CSF, IL2, IL6, IL4, IL5, IL10, IL13을 포함하는 사이토카인을 사용하여 배양 상청액에서 세포내 측정으로 수행된다.
따라서, 치료의 평가는 다음 중 하나 이상을 평가하는 검정을 사용하여 수행될 수 있다: (i) 면역 반응의 증가, (ii) αβT세포 및/또는 γδT세포의 활성화 증가, (iii) 세포독성 T세포 활성의 증가, (iv) NK세포 및/또는 NKT세포 활성의 증가, (v) αβT세포 및/또는 γδT세포 억제의 완화, (vi) 전염증성 사이토카인 분비의 증가, (vii) IL-2 분비의 증가, (viii) 인터페론-γ 생산의 증가, (ix) Th1 반응의 증가, (x) Th2 반응의 감소, (xi) 조절 T세포(Treg)의 세포 수 및/또는 적어도 하나의 조절 T세포(Treg)의 활성의 감소 또는 제거.
A. 효능 측정을 위한 검정
일부 구현예에서, T세포 활성화는 당업계에 공지된 바와 같은 혼합 림프구 반응(MLR: Mixed Lymphocyte Reaction) 검정을 사용하여 평가된다. 활성의 증가는 면역자극 활성을 나타낸다. 활성의 적절한 증가는 하기에 개괄되어 있다.
하나의 구현예에서, 신호전달 경로 검정은, 예를 들어 상이한 인자의 인산화 또는 탈인산화에 의해, 또는 다른 번역후 변형을 측정함으로써 측정되는 면역 반응의 증가 또는 감소를 측정한다. 활성의 증가는 면역자극 활성을 나타낸다. 활성의 적절한 증가는 하기에 개괄되어 있다.
하나의 구현예에서, 신호전달 경로 검정은, 예를 들어 사이토카인 분비에 의해, 증식에 의해, 또는 예를 들어 CD137, CD107a, PD1 등과 같은 활성화 마커의 발현 변화에 의해 측정되는, αβT세포 및/또는 γδT세포 활성화의 증가 또는 감소를 측정한다. 활성의 증가는 면역자극 활성을 나타낸다. 활성의 적절한 증가는 하기에 개괄되어 있다.
하나의 구현예에서, 신호전달 경로 검정은, 예를 들어 암세포와 같은 표적세포의 직접 사멸에 의해, 사이토카인 분비에 의해, 증식에 의해, 또는 예를 들어 CD137, CD107a, PD1 등과 같은 활성화 마커의 발현 변화에 의해 측정되는, 세포독성 T세포 활성의 증가 또는 감소를 측정한다. 활성의 증가는 면역자극 활성을 나타낸다. 활성의 적절한 증가는 하기에 개괄되어 있다.
하나의 구현예에서, 신호전달 경로 검정은, 예를 들어 암세포와 같은 표적세포의 직접 사멸에 의해, 사이토카인 분비에 의해, 또는 예를 들어 CD107a 등과 같은 활성화 마커의 발현 변화에 의해 측정되는, NK세포 및/또는 NKT세포 활성의 증가 또는 감소를 측정한다. 활성의 증가는 면역자극 활성을 나타낸다. 활성의 적절한 증가는 하기에 개괄되어 있다.
하나의 구현예에서, 신호전달 경로 검정은, 예를 들어 사이토카인 분비에 의해, 증식에 의해, 또는 예를 들어 CD137, CD107a, PD1 등과 같은 활성화 마커의 발현 변화에 의해 측정되는, αβT세포 및/또는 γδT세포 억제의 증가 또는 감소를 측정한다. 활성의 증가는 면역자극 활성을 나타낸다. 활성의 적절한 증가는 하기에 개괄되어 있다.
하나의 구현예에서, 신호전달 경로 검정은, 예를 들어 ELISA에 의해, Luminex에 의해, 멀티플렉스(multiplex) 비드 기반 방법에 의해, 세포내 염색 및 FACS 분석에 의해, 또는 Alispot 등에 의해 측정되는, 전염증성 사이토카인 분비의 증가 또는 감소를 측정한다. 활성의 증가는 면역자극 활성을 나타낸다. 활성의 적절한 증가는 하기에 개괄되어 있다.
하나의 구현예에서, 신호전달 경로 검정은, 예를 들어 ELISA에 의해, Luminex에 의해, 멀티플렉스 비드 기반 방법에 의해, 세포내 염색 및 FACS 분석에 의해, 또는 Alispot 등에 의해 측정되는, IL-2 분비의 증가 또는 감소를 측정한다. 활성의 증가는 면역자극 활성을 나타낸다. 활성의 적절한 증가는 하기에 개괄되어 있다.
하나의 구현예에서, 신호전달 경로 검정은, 예를 들어 ELISA에 의해, Luminex에 의해, 멀티플렉스 비드 기반 방법에 의해, 세포내 염색 및 FACS 분석에 의해, 또는 Alispot 등에 의해 측정되는, 인터페론-γ 생산의 증가 또는 감소를 측정한다. 활성의 증가는 면역자극 활성을 나타낸다. 활성의 적절한 증가는 하기에 개괄되어 있다.
하나의 구현예에서, 신호전달 경로 검정은, 예를 들어 사이토카인 분비에 의해 또는 활성화 마커의 발현 변화에 의해 측정되는, Th1 반응의 증가 또는 감소를 측정한다. 활성의 증가는 면역자극 활성을 나타낸다. 활성의 적절한 증가는 하기에 개괄되어 있다.
하나의 구현예에서, 신호전달 경로 검정은, 예를 들어 사이토카인 분비에 의해 또는 활성화 마커의 발현 변화에 의해 측정되는, Th2 반응의 증가 또는 감소를 측정한다. 활성의 증가는 면역자극 활성을 나타낸다. 활성의 적절한 증가는 하기에 개괄되어 있다.
하나의 구현예에서, 신호전달 경로 검정은, 예를 들어 유세포 분석법에 의해 또는 IHC에 의해 측정되는, 조절 T세포(Treg)의 세포 수 및/또는 적어도 하나의 조절 T세포(Treg)의 활성의 증가 또는 감소를 측정한다. 반응의 감소는 면역자극 활성을 나타낸다. 적절한 감소는 하기에 개괄되는 증가의 경우와 동일하다.
하나의 구현예에서, 신호전달 경로 검정은, 예를 들어 유세포 분석법 또는 IHC에 의해 측정되는, M2 대식세포 수의 증가 또는 감소를 측정한다. 반응의 감소는 면역자극 활성을 나타낸다. 적절한 감소는 하기에 개괄되는 증가의 경우와 동일하다.
하나의 구현예에서, 신호전달 경로 검정은, 예를 들어 사이토카인 분비에 의해 또는 활성화 마커의 발현 변화에 의해 측정되는, M2 대식세포 친종양형성 활성의 증가 또는 감소를 측정한다. 반응의 감소는 면역자극 활성을 나타낸다. 적절한 감소는 하기에 개괄되는 증가의 경우와 동일하다.
하나의 구현예에서, 신호전달 경로 검정은, 예를 들어 유세포 분석법 또는 IHC에 의해 측정되는, N2 호중구 수의 증가 또는 감소를 측정한다. 반응의 감소는 면역자극 활성을 나타낸다. 적절한 감소는 하기에 개괄되는 증가의 경우와 동일하다.
하나의 구현예에서, 신호전달 경로 검정은, 예를 들어 사이토카인 분비에 의해 또는 활성화 마커의 발현 변화에 의해 측정되는, N2 호중구 친종양형성 활성의 증가 또는 감소를 측정한다. 반응의 감소는 면역자극 활성을 나타낸다. 적절한 감소는 하기에 개괄되는 증가의 경우와 동일하다.
하나의 구현예에서, 신호전달 경로 검정은, 예를 들어 사이토카인 분비에 의해, 증식에 의해, 또는 예를 들어 CD137, CD107a, PD1 등과 같은 활성화 마커의 발현 변화에 의해 측정되는, T세포 활성화 저해의 증가 또는 감소를 측정한다. 활성의 증가는 면역자극 활성을 나타낸다. 활성의 적절한 증가는 하기에 개괄되어 있다.
하나의 구현예에서, 신호전달 경로 검정은, 예를 들어 암세포와 같은 표적세포의 직접 사멸에 의해, 사이토카인 분비에 의해, 증식에 의해, 또는 예를 들어 CD137, CD107a, PD1 등과 같은 활성화 마커의 발현 변화에 의해 측정되는, CTL 활성화 저해의 증가 또는 감소를 측정한다. 활성의 증가는 면역자극 활성을 나타낸다. 활성의 적절한 증가는 하기에 개괄되어 있다.
하나의 구현예에서, 신호전달 경로 검정은, 예를 들어 활성화 마커의 발현 변화에 의해 측정되는, αβT세포 및/또는 γδT세포 고갈의 증가 또는 감소를 측정한다. 반응의 감소는 면역자극 활성을 나타낸다. 적절한 감소는 하기에 개괄되는 증가의 경우와 동일하다.
하나의 구현예에서, 신호전달 경로 검정은, 예를 들어 사이토카인 분비에 의해, 증식에 의해, 또는 예를 들어 CD137, CD107a, PD1 등과 같은 활성화 마커의 발현 변화에 의해 측정되는, αβT세포 및/또는 γδT세포 반응의 증가 또는 감소를 측정한다. 활성의 증가는 면역자극 활성을 나타낸다. 활성의 적절한 증가는 하기에 개괄되어 있다.
하나의 구현예에서, 신호전달 경로 검정은, 예를 들어 사이토카인 분비에 의해, 증식에 의해, 또는 예시적인 CD45RA, CCR7 등과 같은 활성화 마커의 발현 변화에 의해 측정되는, 항원 특이적 기억 반응 자극의 증가 또는 감소를 측정한다. 활성의 증가는 면역자극 활성을 나타낸다. 활성의 적절한 증가는 하기에 개괄되어 있다.
하나의 구현예에서, 신호전달 경로 검정은, 예를 들어 MTT, Cr 방출, 칼세인 AM과 같은 세포독성 검정에 의해, 또는 예를 들어 CFSE 희석 또는 프로피듐 요오다이드 염색 등과 같은 유세포 분석법 기반의 검정에 의해 측정되는, 암세포의 세포자멸사 또는 용해의 증가 또는 감소를 측정한다. 활성의 증가는 면역자극 활성을 나타낸다. 활성의 적절한 증가는 하기에 개괄되어 있다.
하나의 구현예에서, 신호전달 경로 검정은, 예를 들어 MTT, Cr 방출, 칼세인 AM과 같은 세포독성 검정에 의해, 또는 예를 들어 CFSE 희석 또는 프로피듐 요오다이드 염색 등과 같은 유세포 분석법 기반 검정에 의해 측정되는, 암세포에 대한 세포독성 또는 세포증식억제 효과 자극의 증가 또는 감소를 측정한다. 활성의 증가는 면역자극 활성을 나타낸다. 활성의 적절한 증가는 하기에 개괄되어 있다.
하나의 구현예에서, 신호전달 경로 검정은, 예를 들어 MTT, Cr 방출, 칼세인 AM과 같은 세포독성 검정에 의해, 또는 예를 들어 CFSE 희석 또는 프로피듐 요오다이드 염색 등과 같은 유세포 분석법 기반 검정에 의해 측정되는, 암세포 직접 사멸의 증가 또는 감소를 측정한다. 활성의 증가는 면역자극 활성을 나타낸다. 활성의 적절한 증가는 하기에 개괄되어 있다.
하나의 구현예에서, 신호전달 경로 검정은, 예를 들어 사이토카인 분비에 의해, 증식에 의해, 또는 활성화 마커의 발현 변화에 의해 측정되는, Th17 활성의 증가 또는 감소를 측정한다. 활성의 증가는 면역자극 활성을 나타낸다. 활성의 적절한 증가는 하기에 개괄되어 있다.
하나의 구현예에서, 신호전달 경로 검정은, 예를 들어 MTT, Cr 방출, 칼세인 AM과 같은 세포독성 검정에 의해, 또는 예를 들어 CFSE 희석 또는 프로피듐 요오다이드 염색 등과 같은 유세포 분석법 기반 검정에 의해 측정되는, 보체 의존적 세포독성 및/또는 항체 의존적 세포 매개 세포독성 유도의 증가 또는 감소를 측정한다. 활성의 증가는 면역자극 활성을 나타낸다. 활성의 적절한 증가는 하기에 개괄되어 있다.
하나의 구현예에서, T세포 활성화는, 예를 들어 암세포와 같은 표적세포의 직접 사멸에 의해, 사이토카인 분비에 의해, 증식에 의해, 또는 예를 들어 CD137, CD107a, PD1 등과 같은 활성화 마커의 발현 변화에 의해 측정된다. T-세포의 경우, 증식, 세포 표면 마커(예를 들어, CD25, CD69, CD137, PD1)의 활성화, 세포독성(표적세포 사멸 능력) 및 사이토카인(예를 들어, IL-2, IL-4, IL-6, IFNγ, TNF-a, IL-10, IL-17A) 생산의 증가는, 면역 조절을 나타낼 수 있으며, 이는 암세포의 증강된 사멸과 일치할 수 있다.
하나의 구현예에서, NK세포 활성화는, 예를 들어 암세포와 같은 표적세포의 직접 사멸에 의해, 사이토카인 분비에 의해, 또는 예를 들어CD107a 등과 같은 활성화 마커의 발현 변화에 의해 측정된다. NK 세포의 경우, 증식, 세포독성(표적세포 사멸 능력, 및 CD107a, 그랜자임 및 퍼포린 발현의 증가), 사이토카인(예를 들어, IFNγ 및 TNF) 생산, 및 세포 표면 수용체(예를 들어, CD25) 발현의 증가는, 면역 조절을 나타낼 수 있으며, 이는 암세포의 증강된 사멸과 일치할 수 있다.
하나의 구현예에서, γδ T세포 활성화는, 예를 들어 사이토카인 분비에 의해, 증식에 의해, 또는 활성화 마커의 발현 변화에 의해 측정된다.
하나의 구현예에서, Th1 세포 활성화는, 예를 들어 사이토카인 분비에 의해 또는 활성화 마커의 발현 변화에 의해 측정된다.
적절한 활성 또는 반응의 증가 (또는, 상기 개괄된 바와 같이 적절한 경우, 감소)는 참조 샘플 또는 대조군 샘플, 예를 들어 본 발명의 이종이량체 단백질을 함유하지 않는 시험 샘플에서의 신호에 비해 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95%, 또는 98% 내지 99%의 증가이다. 유사하게, 참조 샘플 또는 대조군 샘플과 비교하여 적어도 1배, 2배, 3배, 4배 또는 5배의 증가는 효능을 나타낸다.
VIII. 치료
일단 제조되면, 본 발명의 조성물은 일반적으로 본 발명의 이종이량체 Fc 융합 단백질의 결합으로 T세포 활성화를 촉진시키는 것에 의해(예를 들어, T세포가 더 이상 억제되지 않음) 암을 치료함으로써 다수의 종양학 적용에 사용된다.
따라서, 본 발명의 표적화 이종이량체 조성물은 이러한 암의 치료에 유용하다.
A. 생체내 투여를 위한 표적화 이종이량체 단백질 조성물
본 발명에 따라 사용되는 항체의 제형은 보관을 위해 동결건조된 제형 또는 수용액의 형태로, 목적하는 정도의 순도를 갖는 항체와 선택적인 약학적으로 허용 가능한 담체, 부형제 또는 안정화제를 혼합함으로써(일반적으로 문헌[Remington's Pharmaceutical Sciences 16th edition, Osol, A. Ed. [1980]]에 개괄된 바와 같음) 제조된다. 허용 가능한 담체, 완충제, 부형제 또는 안정화제는 이용되는 투여량 및 농도에서 수용자에게 비독성이며, 이에는, 포스페이트, 시트레이트 및 다른 유기산과 같은 완충제; 아스코르브산 및 메티오닌을 포함하는 항산화제; 보존제(예컨대, 옥타데실디메틸벤질 암모늄 클로라이드; 헥사메토늄 클로라이드; 벤즈알코늄 클로라이드, 벤즈에토늄 클로라이드; 페놀, 부틸 또는 벤질 알코올; 메틸 또는 프로필 파라벤과 같은 알킬 파라벤; 카테콜; 레조르시놀; 사이클로헥산올; 3-펜탄올; 및 m-크레졸); 저분자량(약 10개 미만의 잔기) 폴리펩타이드; 혈청 알부민, 젤라틴 또는 면역글로불린과 같은 단백질; 폴리비닐피롤리돈과 같은 친수성 중합체; 글리신, 글루타민, 아스파라긴, 히스티딘, 아르기닌 또는 리신과 같은 아미노산; 단당류, 이당류, 및 글루코오스, 만노오스 또는 덱스트린을 포함하는 다른 탄수화물; EDTA와 같은 킬레이트제; 수크로오스, 만니톨, 트레할로오스 또는 소르비톨과 같은 당류; 소듐과 같은 염 형성 반대 이온; 금속 복합체(예를 들어, Zn-단백질 복합체); 및/또는 TWEENTM, PLURONICSTM 또는 폴리에틸렌글리콜(PEG)과 같은 비이온성 계면활성제가 포함된다.
B. 병용요법
일부 구현예에서, 본 발명의 이종이량체 단백질은, 예를 들어 LAG-3 항체가 아닌 상이한 체크포인트 단백질에 결합하는 항체와 병용요법으로 사용될 수 있다. 이러한 방식으로, 추가 항체의 항원 결합 도메인은 표적화 이종이량체 단백질과 결합을 위해 경쟁하지 않는다. 이러한 방식으로, 3개의 수용체(표적화 이종이량체 단백질에서 2개 및 추가 항체에서 1개)가 관여하기 때문에, 일종의 "삼중 병용" 요법이 달성된다. 본원에 논의된 바와 같이, 이종이량체 단백질은 본원에 개괄된 바와 같은 상이한 원자가 및 특이성을 가질 수 있다.
놀랍게도, 본원에 제시된 바와 같이, 이러한 조합은 병용투여되는 경우 상조적 효과를 유도할 수 있다. 이러한 맥락에서, "병용투여"는, 2개의 모이어티가 동시에 또는 순차적으로 투여될 수 있다는 것을 의미한다. 즉, 일부 경우에, 약물은 동시에 투여될 수 있지만, 이는 일반적으로 2회의 별도의 IV 주입을 통해 이루어지며; 즉, 약물은 일반적으로 단일 투여 단위로 조합되지 않는다. 대안적으로, 병용투여는 두 가지 별개의 약물의 하루 또는 별도의 날(시간 경과에 따른 별도의 날 포함)에의 순차적 투여를 포함한다.
1. 병용투여 요법에 사용되는 항-PD-1 항체
당업계에 공지된 바와 같이, 현재 승인된 두 가지 항-PD-1 항체 및 임상 시험 중인 다수의 항-PD-1 항체가 존재한다. 따라서, 본원에 개괄된 바와 같은 병용요법에 사용하기에 적합한 항-PD-1 항체에는, 비제한적으로, 현재 FDA에서 승인된 두 가지 항체인 펨브롤리주맙 및 니볼리주맙(nivolizumab); 및, 비제한적으로, 티스렐리주맙(tislelizumab), Sym021, REGN2810(Rengeneron에서 개발됨), JNJ-63723283(J and J에서 개발됨), SHR-1210, 피딜리주맙, AMP-224, MEDIo680, PDR001 및 CT-001을 포함하는 현재 임상 시험 중인 것들뿐 아니라, 문헌[Liu et al., J. Hemat. & Oncol. (2017)10:136]에 개괄된 것들(상기 문헌의 항체는 명백하게 본원에 참조로서 인용됨)이 포함된다. 상기와 같이, 항-PD-1 항체는 본 발명의 표적화 이종이량체 단백질이 PD-1에 결합하는 항원 결합 도메인을 갖지 않는 경우에 조합으로 사용된다.
2. 병용투여 요법에 사용되는 항-PD-L1 항체
일부 구현예에서, 항-PD-L1 항체가 병용된다. 당업계에 공지된 바와 같이, 현재 승인된 세 가지 항-PD-L1 항체 및 임상 시험 중인 다수의 항-PD-L1 항체가 존재한다. 따라서, 본원에 개괄된 바와 같은 병용요법에 사용하기에 적합한 항-PD-L1 항체에는, 현재 FDA에서 승인된 세 가지 항체인 아테졸리주맙(atezolizumab), 아벨루맙(avelumab), 두르발루맙(durvalumab), 및 비제한적으로, LY33000054 및 CS1001을 포함하는 현재 임상 중인 것들뿐 아니라, 문헌[Liu et al., J. Hemat. & Oncol. (2017)10:136]에 개괄된 것들(상기 문헌의 항체는 명백하게 본원에 참조로서 인용됨)이 포함된다. 상기와 같이, 항-PD-L1 항체는 본 발명의 표적화 이종이량체 단백질이 PD-L1에 결합하는 항원 결합 도메인을 갖지 않는 경우에 조합으로 사용된다.
3. 병용투여 요법에 사용되는 항-TIM-3 항체
일부 구현예에서, 항-TIM-3 항체는 본 발명의 표적화 이종이량체 단백질과 조합으로 사용될 수 있다. MBG453 및 TSR-022를 포함하여, 임상 개발 중에 있는 몇 가지 TIM-3 항체가 존재한다. 상기와 같이, 항-TIM-3 항체는 본 발명의 표적화 이종이량체 단백질이 TIM-3에 결합하는 항원 결합 도메인을 갖지 않는 경우에 조합으로 사용된다.
4. 병용투여 요법에 사용되는 항-TIGIT 항체
일부 구현예에서, 항-TIGIT 항체는 본 발명의 표적화 이종이량체 단백질과 조합으로 사용될 수 있다. BMS-986207, OMP-313M32 및 MTIG7192A를 포함하여, 임상 개발 중에 있는 몇 가지 TIGIT 항체가 존재한다. 상기와 같이, 항-TIGIT 항체는 본 발명의 표적화 이종이량체 단백질이 TIGIT에 결합하는 항원 결합 도메인을 갖지 않는 경우에 조합으로 사용된다.
5. 병용투여 요법에 사용되는 항-CTLA-4 항체
일부 구현예에서, 항-CTLA-4 항체는 본 발명의 표적화 이종이량체 단백질과 조합으로 사용될 수 있다. 이필리무맙이 승인되어 있으며, CP-675,206 및 AGEN-1884를 포함하여 개발 중에 있는 몇 가지가 더 존재한다. 상기와 같이, 항-CTLA-4 항체는 본 발명의 표적화 이종이량체 단백질이 CTLA-4에 결합하는 항원 결합 도메인을 갖지 않는 경우에 조합으로 사용된다.
C. 투여 방식
본 발명의 표적화 이종이량체 단백질 및 화학요법제는 볼루스로서의 정맥내 투여 또는 일정 기간에 걸친 연속 주입과 같은 공지된 방법에 따라 대상에게 투여된다.
D. 치료 방식
본 발명의 방법에서, 요법은 질환 또는 병태에 대하여 긍정적인 치료 반응을 제공하기 위해 사용된다. "긍정적인 치료 반응"은 질환 또는 병태의 개선, 및/또는 질환 또는 병태와 관련된 증상의 개선을 의미한다. 예를 들어, 긍정적인 치료 반응은 질환에서 다음 개선 중 하나 이상을 나타낼 수 있다: (1) 신생물 세포 수의 감소; (2) 신생물 세포 사멸의 증가; (3) 신생물 세포 생존의 저해; (5) 종양 성장의 저해(예를 들어, 어느 정도의 지연, 바람직하게는 중단); (6) 환자 생존율의 증가; 및 (7) 질환 또는 병태와 관련된 하나 이상의 증상의 어느 정도 경감.
임의의 주어진 질환 또는 병태에서 긍정적인 치료 반응은 해당 질환 또는 병태에 대하여 특정한 표준화된 반응 기준에 따라 결정될 수 있다. 종양 반응은 자기 공명 영상화(MRI) 스캔, x-선 촬영 영상화, 전산화 단층촬영(CT) 스캔, 뼈 스캔 영상화, 내시경검사, 및 골수 흡인(BMA) 및 순환하는 종양 세포의 계수를 포함하는 종양 생검 샘플링과 같은 스크리닝 기법을 사용하여, 종양 형태(즉, 전체적인 종양 부담, 종양 크기 등)의 변화로 평가될 수 있다.
이러한 긍정적인 치료 반응에 더하여, 요법을 받는 대상은 질환과 관련된 증상의 유익한 개선 효과를 경험할 수 있다.
본 발명에 따른 치료는 사용된 약제의 "치료적 유효량"을 포함한다. "치료적 유효량"은 목적하는 치료 결과를 달성하는 데 필요한 투여량으로 필요한 기간 동안 효과적인 양을 나타낸다.
치료적 유효량은 개체의 질환 상태, 연령, 성별 및 체중, 및 개체에서 목적하는 반응을 이끌어내는 약제의 능력과 같은 요인에 따라 달라질 수 있다. 치료적 유효량은 치료적으로 유익한 효과가 항체 또는 항체 부분의 임의의 독성 또는 유해한 효과를 능가하는 양이다.
종양 치료를 위한 "치료적 유효량"은 또한 질환의 진행을 안정화시키는 능력으로 측정될 수 있다. 암을 저해하는 화합물의 능력은 인간 종양에서의 효능을 예측하는 동물 모델 시스템에서 평가될 수 있다.
대안적으로, 조성물의 이러한 특성은 숙련된 의사에게 공지된 시험관내 검정에 의해 세포 성장을 저해하거나 세포자멸사를 유도하는 화합물의 능력을 조사함으로써 평가될 수 있다. 치료적 유효량의 치료용 화합물은 종양 크기를 감소시키거나, 다르게는 대상의 증상을 개선시킬 수 있다. 당업자는 대상의 크기, 대상의 증상의 중증도, 및 선택된 특정 조성물 또는 투여 경로와 같은 이러한 요인을 기반으로 이러한 양을 결정할 수 있을 것이다.
투여 방식은 최적의 목적하는 반응(예를 들어, 치료 반응)을 제공하도록 조정된다. 예를 들어, 단일 볼루스가 투여될 수 있으며, 여러 번으로 분할된 용량이 시간에 걸쳐 투여될 수 있거나, 또는 치료 상황의 긴급성에 의해 지시된 바와 같이 용량이 비례적으로 감소되거나 증가될 수 있다. 비경구 조성물은 투여의 용이성 및 투여량의 균일성을 위해 단위 투여 형태로 제형화될 수 있다. 본원에 사용된 단위 투여 형태는 치료하고자 하는 대상을 위한 단일 투여량으로서 적합한 물리적으로 구분된 단위를 나타내며; 각각의 단위는 필요한 약학적 담체와 함께 목적하는 치료 효과를 생성하도록 계산된 선결된 양의 활성 화합물을 함유한다.
본 발명의 단위 투여 형태에 대한 사양은 (a) 활성 화합물의 고유한 특성 및 달성하고자 하는 특정 치료 효과, 및 (b) 개체의 감수성 치료를 위해 이러한 활성 화합물을 컴파운딩하는 기술에 내재된 한계에 의해 결정되고, 이에 직접적으로 의존한다.
본 발명에 사용되는 표적화 이종이량체 단백질에 대한 효율적인 투여량 및 투여 방식은 치료하고자 하는 질환 또는 병태에 따라 달라지며, 당업자에 의해 결정될 수 있다.
본 발명에 사용되는 표적화 이종이량체 단백질의 치료적 유효량의 예시적인 비제한적인 범위는 약 0.1 내지 100 mg/kg이다.
모든 인용된 참고문헌은 그 전문이 명백하게 본원에 참조로서 인용된다.
본 발명의 특정 구현예가 예시의 목적으로 상기 기재되었지만, 당업자는 첨부된 청구범위에 기재된 바에서 벗어나지 않는 한 세부 사항에 대한 다수의 변형이 이루어질 수 있다는 것을 이해할 것이다.
IX. 실시예
하기 실시예는 본 발명을 예시하기 위해 제공된다. 이러한 실시예는 본 발명을 임의의 특정한 적용 또는 작동 이론으로 제한하고자 하는 것이 아니다. 본 발명에서 논의된 모든 불변 영역 위치에 있어서, 넘버링은 Kabat에서와 같이 EU 인덱스에 따른다(문헌[Kabat et al., 1991, Sequences of Proteins of Immunological Interest, 5th Ed., United States Public Health Service, National Institutes of Health, Bethesda], 이는 그 전문이 본원에 참조로서 인용됨). 항체 분야의 당업자는 이러한 협약이 면역글로불린 서열의 특정 영역에서의 비(非)순차적인 넘버링으로 이루어지며, 이는 면역글로불린 패밀리의 보존된 위치에 대한 정규화된 참조를 가능하게 한다는 점을 이해할 것이다. 따라서, EU 인덱스에 의해 정의된 임의의 주어진 면역글로불린의 위치는 반드시 이의 순차적 서열에 상응하지 않을 것이다.
일반적인 및 특정한 과학적 기법은 미국 특허출원공개 제2015/0307629호, 제2014/0288275호 및 WO2014/145806에 개괄되어 있으며, 이들은 모두 그 전문이, 특히 본원에 개괄된 기법에 대하여 참조로서 인용된다. 2016년 11월 1일자 출원된 미국 특허출원 제62,416,087호의 실시예 1 및 2는 상응하는 도면을 포함하여 그 전문이 명백하게 본원에 참조로서 인용된다. 또한, 미국 특허출원 USSN 제62/408,655호, 제62/443,465호, 제62/477,926호, 제15/785,401호, 제62/416,087호 및 제15/785,393호는, 그 전문이, 구체적으로 그 안의 서열, 도면 및 도면 범례가 명백하게 본원에 참조로서 인용된다.
A. 실시예 1: 항-LAG-3 ABD
LAG-3에 결합하는 항원 결합 도메인의 예는 WO2017/218707에 기재되어 있으며, 상기 문헌은 모든 목적을 위하여 그 전문이, 특히 LAG-3 ABD에 대하여, 도 11, 도 18, 도 55, 도 56, 도 63의 데이터, 서열목록의 서열번호 36819-36962, 서열번호 35417-35606, 서열번호 25914-32793 및 서열번호 32794-33002의 서열이 본원에 참조로서 인용된다.
B. 실시예 2: LAG-3 표적화 IL-15/Rα-Fc 융합체
ABD를 함유하지 않는 IL-15/Rα-Fc 융합체가 기재되어 있는 WO2018/071919(일반적으로 도 9a 내지 도 9g 및 도 39a 내지 도 39d에 도시되어 있음)를 참조한다. WO2018/071919는 그 전문이, 구체적으로 그 안의 서열, 형식, 도면 및 도면 범례가 명백하게 본원에 참조로서 인용된다.
2A: LAG-3 표적화 IL-15/Rα-Fc 융합체의 생성
IL-15, IL-15Rα 스시 도메인 또는 항-LAG-3 가변 영역을 코딩하는 플라스미드를 표준 유전자 합성에 의해 구축한 후, Fc 융합 파트너(예들 들어, 도면에 도시된 바와 같은 불변 영역)를 함유하는 pTT5 발현 벡터에 서브클로닝하였다. 예시적인 LAG-3 표적화 IL-15/Rα-Fc 융합체의 카툰식 개략도는 도 21에 도시되어 있다.
"scIL-15/Rα x scFv" 형식(도 21a)은 가변 길이 링커에 의해 IL-15에 융합된 IL-15Rα(스시)("scIL-15/Rα"로 지칭됨)(이는 이후에 이종이량체 Fc 영역의 N-말단에 융합됨)와, 이종이량체 Fc의 다른 쪽에 융합된 scFv를 포함한다.
"scFv x ncIL-15/Rα" 형식(도 21b)은 이종이량체 Fc 영역의 N-말단에 융합된 scFv와 이종이량체 Fc의 다른 쪽에 융합된 IL-15Rα(스시)를 포함하지만, IL-15는 비공유결합형 IL-15/Rα 복합체가 형성되도록 별도로 트랜스펙션된다.
"scFv x dsIL-15/Rα" 형식(도 21c)은 "scFv x ncIL-15/Rα" 형식과 동일하지만, 여기서 IL-15Rα(스시)와 IL-15는 조작된 시스테인의 결과로서 공유결합으로 연결된다.
"scIL-15/Rα x Fab" 형식(도 21d)은 가변 길이 링커에 의해 IL-15에 융합된 IL-15Rα(스시)("scIL-15/Rα"로 지칭됨)(이는 이후에 이종이량체 Fc 영역의 N-말단에 융합됨)와, 이종이량체 Fc의 다른 쪽에 융합된 가변 중쇄(VH)를 포함하며, 상응하는 경쇄는 VH와 Fab을 형성하도록 별도로 트랜스펙션된다. 이러한 형식의 예시적인 LAG-3 표적화 IL-15/Rα-Fc 융합 단백질의 서열은 도면에 도시되어 있다.
"ncIL-15/Rα x Fab" 형식(도 21e)은 이종이량체 Fc 영역의 N-말단에 융합된 VH와 이종이량체 Fc의 다른 쪽에 융합된 IL-15Rα(스시)를 포함하며, 상응하는 경쇄는 VH와 Fab을 형성하도록 별도로 트랜스펙션되고, IL-15는 비공유결합형 IL-15/Rα 복합체가 형성되도록 별도로 트랜스펙션된다.
"dsIL-15/Rα x Fab" 형식(도 21f)은 "ncIL-15/Rα x Fab" 형식과 동일하지만, 여기서 IL-15Rα(스시)와 IL-15는 조작된 시스테인의 결과로서 공유결합으로 연결된다.
"mAb-scIL-15/Rα" 형식(도 21g)은 제1 이종이량체 Fc와 제2 이종이량체 Fc의 N-말단에 융합된 VH와, IL-15Rα(스시)에 융합된 IL-15(이는 이후에 이종이량체 Fc 영역 중 하나의 C-말단에 추가로 융합됨)를 포함하며, 상응하는 경쇄는 VH와 Fab을 형성하도록 별도로 트랜스펙션된다.
"mAb-ncIL-15/Rα" 형식(도 21h)은 제1 이종이량체 Fc와 제2 이종이량체 Fc의 N-말단에 융합된 VH와, 이종이량체 Fc 영역 중 하나의 C-말단에 융합된 IL-15Rα(스시)를 포함하며, 상응하는 경쇄는 VH와 Fab을 형성하도록 별도로 트랜스펙션되고, IL-15는 비공유결합형 IL-15/Rα 복합체가 형성되도록 별도로 트랜스펙션된다.
"mAb-dsIL-15/Rα" 형식(도 21i)은 "mAb-ncIL-15/Rα" 형식과 동일하지만, 여기서 IL-15Rα(스시)와 IL-15는 조작된 시스테인의 결과로서 공유결합으로 연결된다.
"central-IL-15/Rα" 형식(도 21j)은 IL-15의 N-말단에 재조합적으로 융합된 VH(이는 이후에 이종이량체 Fc의 한쪽에 추가로 융합됨)와, IL-15Rα(스시)의 N-말단에 재조합적으로 융합된 VH(이는 이후에 이종이량체 Fc의 다른 한쪽에 추가로 융합됨)를 포함하며, 상응하는 경쇄는 VH와 Fab을 형성하도록 별도로 트랜스펙션된다.
"central-scIL-15/Rα" 형식(도 21k)은 IL-15에 융합된 IL-15Rα(스시)의 N-말단에 융합된 VH(이는 이후에 이종이량체 Fc의 한쪽에 추가로 융합됨)와, 이종이량체 Fc의 다른 한쪽에 융합된 VH를 포함하며, 상응하는 경쇄는 VH와 Fab을 형성하도록 별도로 트랜스펙션된다.
2B: LAG-3 표적화 IL-15/Rα-Fc 융합체는 GVHD를 증강시키며, 항-PD-1 항체와 상조적으로 조합됨
예시적인 LAG-3 표적화 IL-15/Rα-Fc 융합 단백질인 XENP27972 및 XENP27973을, 단독으로 또는 XENP016432(효과기 기능이 절제된 니볼루맙을 기반으로 하는 2가 항-PD-1 mAb; 이의 서열은 도 23에 도시되어 있음)와 조합으로, NSG(NOD-SCID-감마) 면역 결핍 마우스에서 수행된 이식편대숙주병(GVHD) 모델에서 평가하였다. NSG 마우스에 인간 PBMC가 주입될 때, 인간 PBMC는 마우스 세포에 대한 자가면역 반응을 나타낸다. NSG 마우스에게 인간 PBMC를 주사하고, 이어서 LAG-3 표적화 IL-15/Rα-Fc 융합 단백질을 투여하면, 생착된 T세포가 증식하여 생착이 증강된다.
-1일차에 천만 개의 인간 PBMC를 IV-OSP를 통해 NSG 마우스에게 이식한 후, 0일차, 7일차, 14일차 및 21일차에 표시된 시험 물품을 표시된 농도로 투여하였다. 다양한 림프구 집단의 수를 6일차 및 10일차에 계수하였고, 이의 데이터를 도면에 도시하였다. 마우스의 체중을 시간의 경과에 따라 측정하고, 초기 체중의 백분율로서 도면에 도시하였다. 데이터는, 인간 PBMC를 이식한 후 XENP27972 또는 XENP27973의 투여가, PBMC만 이식한 것에 비해 증가된 T세포(CD8+ 및 CD4+), NK세포 및 CD45+ 세포의 세포 수, 및 감소된 체중으로 표시되는 바와 같이 GVHD를 증강시켰음을 보여준다. 특히, XENP27972 및 XENP27973은 모두 XENP16432 단독 투여보다 큰 정도로 GVHD를 증강시켰다. 또한, 데이터는, XENP27972와 XENP16432의 조합을 투여한 후 19일차에 모든 마우스가 죽은 것으로 표시되고, XENP27973과 XENP16432의 조합을 투여한 후 19일차에 한 마리를 제외한 모든 마우스가 죽은 것으로 표시된 바와 같이, XENP27972와 XENP27973이 GVHD를 증강시키는 데 있어서 XENP16432와 상조적으로 조합함을 보여준다. 이는, 면역종양학 설정에서, LAG-3 표적화 IL-15/Rα-Fc 융합 단백질의 단독 또는 체크포인트 차단 항체와 조합으로의 치료가, 종양 침윤 림프구를 증식시키고 항종양 활성을 증강시킬 것임을 시사한다.
2C: LAG-3 표적화 IL-15/Rα-Fc 융합체의 시험관내 특징분석
LAG-3 표적화 IL-15/Rα-Fc 융합체를 세포 증식 검정으로 추가로 특징분석하였다. 인간 PBMC를 500 ng/ml 플레이트 결합된 항-CD3(OKT3)으로 48시간 동안 자극한 후, CFSE로 표지하고, 하기 시험 물품과 함께 37℃에서 4일 동안 인큐베이션하였다: XENP27972(항-LAG-3 클론 7G8을 기반으로 하는 LAG-3 표적화 IL-15/Rα-Fc 융합체); XENP27973(항-LAG-3 클론 2A11을 기반으로 하는 LAG-3 표적화 IL-15/Rα-Fc 융합체); XENP24306(대조군인 D30N/E64Q/N65D IL-15 변이체를 갖는 비표적화 IL-15(D30N/E64Q/N65D)/Rα-Fc 융합체); 및 XENP26007(대조군인 N4D/N65D IL-15 변이체를 갖는 RSV 표적화 IL-15/Rα-Fc 융합체). 세포를 항-CD8-PerCP-Cy5.5(SK1), 항-CD3-PE-Cy7(OKT3), 항-CD45RO-APC-Fire750(UCHL1), 항-HLA-DR-Alexa700(L243), 항-CD16-BV605(3G6), 항-CD56-BV605(HCD56), 항-CD25-BV711(M-A251), 항-CD45RA-BV785(HI100), 항-CD4-BUV395(SK3) 및 Zombie Aqua-BV510의 항체로 염색하고, 다양한 세포 집단에 대하여 흐름으로 분석하였다.
CFSE 희석(사멸한 세포를 제외하기 위해 Zombie Aqua)을 기반으로 다양한 T세포 및 NK세포 집단의 증식을 조사하고, 이의 데이터를 도 30 내지 도 35에 도시하였다. 데이터는, LAG-3 표적화 IL-15/Rα-Fc 융합체, 특히 XENP27972가, CD8+ T세포에 대한 선호를 갖는 비표적화 IL-15(D30N/E64Q/N65D)/Rα-Fc 융합체 (및 대조군인 RSV 표적화 IL-15/Rα-Fc 융합체)에 비해 CD8+ T세포 및 CD4+ T세포 둘 모두의 증식을 유도하는 데 있어서 더 강력함을 보여준다. 특히, LAG-3 표적화 IL-15/Rα-Fc 융합체는 기억T세포를 우선적으로 표적화하며, 이는 임상 설정에서, LAG-3 표적화 IL-15/Rα-Fc 융합체가 종양 환경에서 활성화된 종양 침윤 림프구에 대하여 선택성을 가질 수 있음을 시사한다.
CD25(후기 T세포 활성화 마커) 및 HLA-DR(또 다른 활성화 마커)의 발현을 기반으로 한 다양한 T세포 집단의 활성화를 또한 조사하고, 이의 데이터를 도 36 내지 도 38에 도시하였다. 데이터는, LAG-3 표적화 IL-15/Rα-Fc 융합체가 일반적으로 비표적화 IL-15(D30N/E64Q/N65D)/Rα-Fc 융합체 (및 대조군인 RSV 표적화 IL-15/Rα-Fc 융합체)에 비해 CD8 기억T세포 집단의 활성화를 유도하는 데 더 강력함을 보여준다.
C. 실시예 3: IL-15 역가가 조정된 LAG-3 표적화 IL-15/Rα-Fc 융합체
3A: IL-15(D30N/N65D) 변이체
Xtend를 갖는 IL-15-Fc 역가 변이체의 약동학을 조사하기 위한 연구에서, 시노몰구스 원숭이에게 다양한 농도로의 XENP22853(Xtend를 갖는 WT IL-15/Rα-heteroFc, 서열은 도 39에 도시되어 있음), XENP24306(Xtend를 갖는 IL-15(D30N/E64Q/N65D)/Rα-heteroFc, 서열은 도 42에 도시되어 있음), XENP24113(Xtend를 갖는 IL-15(N4D/N65D)/Rα-heteroFc, 서열은 도 40에 도시되어 있음) 및 XENP24294(Xtend를 갖는 scIL-15(N4D/N65D)/Rα-Fc, 서열은 도 41에 도시되어 있음)의 첫 번째 단일 정맥내(i.v.) 용량을 투여하였다.
도 43은, 첫 번째 투여 후 시간 경과에 따른 시험 물품의 혈청 농도를 도시한 것이다. 예측한 바와 같이, (XENP24306 및 XENP24113에서와 같이) Xtend 치환에 더하여 역가 변이체를 혼합시키면 (XENP22583에 비해) IL-15-Fc 융합체의 약동학이 크게 개선된다. 하지만, 예상치 못하게, IL-15/Rα-heteroFc 융합체인 XENP24113 및 scIL-15/Rα-Fc 융합체인 XENP24294(이들은 동일한 IL-15(N4D/N65D) 역가 변이체를 가짐)는 XENP24306에 비해 감소된 약동학을 나타냈다. 이는, 약동학의 감소가 IL-15-Fc 융합체의 형식이 아닌 특정한 IL-15 역가 변이체로 인한 것임을 시사한다. XENP24113 및 XENP24294에 대한 약동학의 감소는, IL-15(N4D/N65D) 변이체를 갖는 IL-15-Fc 융합체가 IL-15(D30N/E64Q/N65D) 변이체를 갖는 IL-15-Fc 융합체보다 큰 시험관내 역가를 가짐이 입증되었던 이전 발견에 기반하여 예측되었지만, 약동학의 감소는 예상치 못하게 역가의 증가와 균형이 맞지 않았다. 따라서, 본 발명의 LAG-3 표적화 IL-15-Fc 융합체에 사용하기 위한 대안적인 IL-15 역가 변이체의 동정을 수행하였다.
IL-15(N4D/N65D)는 CD122에의 결합을 담당하는 IL-15 인터페이스에 이의 2개의 치환을 모두 갖는 반면, IL-15(D30N/E64Q/N65D)는 IL-15:CD122 인터페이스에 2개의 치환(E64Q 및 N65D)을 가지며, 여기서 IL-15 인터페이스에 있는 하나의 치환(D30N)이 CD132에 대한 결합을 담당한다는 점에 주목해야 한다. 따라서, IL-15:CD132 인터페이스에서의 변형이 XENP24306에 대하여 관찰된 우수한 약동학에 기여할 수 있다고 여겨진다. 특히, IL-15(N4D/N65D) 변이체 및 IL-15(D30N/N65D) 변이체를 포함하는 scIL-15/Rα-Fc 융합체가 도 45에 도시된 바와 같이 시험관내에서 매우 유사한 역가를 나타내는 것으로 결정되었다. 상기를 고려하여, IL-15(D30N/N65D) 변이체를 포함하는 예시적인 LAG-3 표적화 IL-15-Fc 융합체를 구상하였으며, 이의 서열을 도 46에 도시하였다. 대조군인 IL-15(D30N/N65D) 변이체를 갖는 RSV 표적화 IL-15/Rα-Fc 융합 단백질 XENP29481을 또한 생성하고, 이의 서열을 도 49에 도시하였다.
3B: IL-15(D30N/E64Q/N65D) 변이체
LAG-3 표적화 IL-15/Rα-Fc 융합체는 LAG-3 표적화 아암을 통해 종양 환경을 표적화하기 위한 목적으로 설계되었지만, 사이토카인 모이어티는 여전히 종양 부위에 도달하기 전 신호전달을 할 수 있고, 전신 독성에 기여할 수 있다. 따라서, IL-15 역가를 추가로 감소시키기 위해 IL-15(D30N/E64Q/N65D) 변이체를 갖는 LAG-3 표적화 IL-15/Rα-Fc 융합체를 구축하였고, 이는 실시예 2C 및 도 45에 예시된 바와 같이 극적으로 활성이 감소되었다. IL-15(D30N/E64Q/N65D) 변이체를 포함하는 예시적인 LAG-3 표적화 IL-15/Rα-Fc 융합체에 대한 서열은 도 47에 도시되어 있다. 또한, 종양 환경 외부에서 IL-15(D30N/E64Q/N65D) 변이체를 포함하는 LAG-3 표적화 IL-15/Rα-Fc 융합체의 거동을 조사하기 위한 대용물로서의 역할을 위해, IL-15(D30N/E64Q/N65D) 변이체를 포함하는 RSV 표적화 IL-15/Rα-Fc 융합체인XENP30432(이의 서열은 도 49에 도시되어 있음)를 구축하였다.
SEQUENCE LISTING
<110> XENCOR, INC.
<120> LAG-3 TARGETED HETERODIMERIC FUSION PROTEINS CONTAINING
IL-15/IL-15RA FC-FUSION PROTEINS AND LAG-3 ANTIGEN BINDING
DOMAINS
<130> 067461-5222-WO
<140> PCT/US2019/028180
<141> 2019-04-18
<150> 62/783,107
<151> 2018-12-20
<150> 62/659,624
<151> 2018-04-18
<160> 383
<170> PatentIn version 3.5
<210> 1
<211> 162
<212> PRT
<213> Homo sapiens
<400> 1
Met Arg Ile Ser Lys Pro His Leu Arg Ser Ile Ser Ile Gln Cys Tyr
1 5 10 15
Leu Cys Leu Leu Leu Asn Ser His Phe Leu Thr Glu Ala Gly Ile His
20 25 30
Val Phe Ile Leu Gly Cys Phe Ser Ala Gly Leu Pro Lys Thr Glu Ala
35 40 45
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
50 55 60
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
65 70 75 80
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
85 90 95
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
100 105 110
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
115 120 125
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
130 135 140
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
145 150 155 160
Thr Ser
<210> 2
<211> 114
<212> PRT
<213> Homo sapiens
<400> 2
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 3
<211> 267
<212> PRT
<213> Homo sapiens
<400> 3
Met Ala Pro Arg Arg Ala Arg Gly Cys Arg Thr Leu Gly Leu Pro Ala
1 5 10 15
Leu Leu Leu Leu Leu Leu Leu Arg Pro Pro Ala Thr Arg Gly Ile Thr
20 25 30
Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val Lys Ser
35 40 45
Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly Phe Lys
50 55 60
Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn Lys Ala
65 70 75 80
Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile Arg Asp
85 90 95
Pro Ala Leu Val His Gln Arg Pro Ala Pro Pro Ser Thr Val Thr Thr
100 105 110
Ala Gly Val Thr Pro Gln Pro Glu Ser Leu Ser Pro Ser Gly Lys Glu
115 120 125
Pro Ala Ala Ser Ser Pro Ser Ser Asn Asn Thr Ala Ala Thr Thr Ala
130 135 140
Ala Ile Val Pro Gly Ser Gln Leu Met Pro Ser Lys Ser Pro Ser Thr
145 150 155 160
Gly Thr Thr Glu Ile Ser Ser His Glu Ser Ser His Gly Thr Pro Ser
165 170 175
Gln Thr Thr Ala Lys Asn Trp Glu Leu Thr Ala Ser Ala Ser His Gln
180 185 190
Pro Pro Gly Val Tyr Pro Gln Gly His Ser Asp Thr Thr Val Ala Ile
195 200 205
Ser Thr Ser Thr Val Leu Leu Cys Gly Leu Ser Ala Val Ser Leu Leu
210 215 220
Ala Cys Tyr Leu Lys Ser Arg Gln Thr Pro Pro Leu Ala Ser Val Glu
225 230 235 240
Met Glu Ala Met Glu Ala Leu Pro Val Thr Trp Gly Thr Ser Ser Arg
245 250 255
Asp Glu Asp Leu Glu Asn Cys Ser His His Leu
260 265
<210> 4
<211> 65
<212> PRT
<213> Homo sapiens
<400> 4
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg
65
<210> 5
<211> 175
<212> PRT
<213> Homo sapiens
<400> 5
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Asp Pro Ala Leu Val His Gln Arg Pro Ala Pro Pro Ser Thr Val
65 70 75 80
Thr Thr Ala Gly Val Thr Pro Gln Pro Glu Ser Leu Ser Pro Ser Gly
85 90 95
Lys Glu Pro Ala Ala Ser Ser Pro Ser Ser Asn Asn Thr Ala Ala Thr
100 105 110
Thr Ala Ala Ile Val Pro Gly Ser Gln Leu Met Pro Ser Lys Ser Pro
115 120 125
Ser Thr Gly Thr Thr Glu Ile Ser Ser His Glu Ser Ser His Gly Thr
130 135 140
Pro Ser Gln Thr Thr Ala Lys Asn Trp Glu Leu Thr Ala Ser Ala Ser
145 150 155 160
His Gln Pro Pro Gly Val Tyr Pro Gln Gly His Ser Asp Thr Thr
165 170 175
<210> 6
<211> 551
<212> PRT
<213> Homo sapiens
<400> 6
Met Ala Ala Pro Ala Leu Ser Trp Arg Leu Pro Leu Leu Ile Leu Leu
1 5 10 15
Leu Pro Leu Ala Thr Ser Trp Ala Ser Ala Ala Val Asn Gly Thr Ser
20 25 30
Gln Phe Thr Cys Phe Tyr Asn Ser Arg Ala Asn Ile Ser Cys Val Trp
35 40 45
Ser Gln Asp Gly Ala Leu Gln Asp Thr Ser Cys Gln Val His Ala Trp
50 55 60
Pro Asp Arg Arg Arg Trp Asn Gln Thr Cys Glu Leu Leu Pro Val Ser
65 70 75 80
Gln Ala Ser Trp Ala Cys Asn Leu Ile Leu Gly Ala Pro Asp Ser Gln
85 90 95
Lys Leu Thr Thr Val Asp Ile Val Thr Leu Arg Val Leu Cys Arg Glu
100 105 110
Gly Val Arg Trp Arg Val Met Ala Ile Gln Asp Phe Lys Pro Phe Glu
115 120 125
Asn Leu Arg Leu Met Ala Pro Ile Ser Leu Gln Val Val His Val Glu
130 135 140
Thr His Arg Cys Asn Ile Ser Trp Glu Ile Ser Gln Ala Ser His Tyr
145 150 155 160
Phe Glu Arg His Leu Glu Phe Glu Ala Arg Thr Leu Ser Pro Gly His
165 170 175
Thr Trp Glu Glu Ala Pro Leu Leu Thr Leu Lys Gln Lys Gln Glu Trp
180 185 190
Ile Cys Leu Glu Thr Leu Thr Pro Asp Thr Gln Tyr Glu Phe Gln Val
195 200 205
Arg Val Lys Pro Leu Gln Gly Glu Phe Thr Thr Trp Ser Pro Trp Ser
210 215 220
Gln Pro Leu Ala Phe Arg Thr Lys Pro Ala Ala Leu Gly Lys Asp Thr
225 230 235 240
Ile Pro Trp Leu Gly His Leu Leu Val Gly Leu Ser Gly Ala Phe Gly
245 250 255
Phe Ile Ile Leu Val Tyr Leu Leu Ile Asn Cys Arg Asn Thr Gly Pro
260 265 270
Trp Leu Lys Lys Val Leu Lys Cys Asn Thr Pro Asp Pro Ser Lys Phe
275 280 285
Phe Ser Gln Leu Ser Ser Glu His Gly Gly Asp Val Gln Lys Trp Leu
290 295 300
Ser Ser Pro Phe Pro Ser Ser Ser Phe Ser Pro Gly Gly Leu Ala Pro
305 310 315 320
Glu Ile Ser Pro Leu Glu Val Leu Glu Arg Asp Lys Val Thr Gln Leu
325 330 335
Leu Leu Gln Gln Asp Lys Val Pro Glu Pro Ala Ser Leu Ser Ser Asn
340 345 350
His Ser Leu Thr Ser Cys Phe Thr Asn Gln Gly Tyr Phe Phe Phe His
355 360 365
Leu Pro Asp Ala Leu Glu Ile Glu Ala Cys Gln Val Tyr Phe Thr Tyr
370 375 380
Asp Pro Tyr Ser Glu Glu Asp Pro Asp Glu Gly Val Ala Gly Ala Pro
385 390 395 400
Thr Gly Ser Ser Pro Gln Pro Leu Gln Pro Leu Ser Gly Glu Asp Asp
405 410 415
Ala Tyr Cys Thr Phe Pro Ser Arg Asp Asp Leu Leu Leu Phe Ser Pro
420 425 430
Ser Leu Leu Gly Gly Pro Ser Pro Pro Ser Thr Ala Pro Gly Gly Ser
435 440 445
Gly Ala Gly Glu Glu Arg Met Pro Pro Ser Leu Gln Glu Arg Val Pro
450 455 460
Arg Asp Trp Asp Pro Gln Pro Leu Gly Pro Pro Thr Pro Gly Val Pro
465 470 475 480
Asp Leu Val Asp Phe Gln Pro Pro Pro Glu Leu Val Leu Arg Glu Ala
485 490 495
Gly Glu Glu Val Pro Asp Ala Gly Pro Arg Glu Gly Val Ser Phe Pro
500 505 510
Trp Ser Arg Pro Pro Gly Gln Gly Glu Phe Arg Ala Leu Asn Ala Arg
515 520 525
Leu Pro Leu Asn Thr Asp Ala Tyr Leu Ser Leu Gln Glu Leu Gln Gly
530 535 540
Gln Asp Pro Thr His Leu Val
545 550
<210> 7
<211> 214
<212> PRT
<213> Homo sapiens
<400> 7
Ala Val Asn Gly Thr Ser Gln Phe Thr Cys Phe Tyr Asn Ser Arg Ala
1 5 10 15
Asn Ile Ser Cys Val Trp Ser Gln Asp Gly Ala Leu Gln Asp Thr Ser
20 25 30
Cys Gln Val His Ala Trp Pro Asp Arg Arg Arg Trp Asn Gln Thr Cys
35 40 45
Glu Leu Leu Pro Val Ser Gln Ala Ser Trp Ala Cys Asn Leu Ile Leu
50 55 60
Gly Ala Pro Asp Ser Gln Lys Leu Thr Thr Val Asp Ile Val Thr Leu
65 70 75 80
Arg Val Leu Cys Arg Glu Gly Val Arg Trp Arg Val Met Ala Ile Gln
85 90 95
Asp Phe Lys Pro Phe Glu Asn Leu Arg Leu Met Ala Pro Ile Ser Leu
100 105 110
Gln Val Val His Val Glu Thr His Arg Cys Asn Ile Ser Trp Glu Ile
115 120 125
Ser Gln Ala Ser His Tyr Phe Glu Arg His Leu Glu Phe Glu Ala Arg
130 135 140
Thr Leu Ser Pro Gly His Thr Trp Glu Glu Ala Pro Leu Leu Thr Leu
145 150 155 160
Lys Gln Lys Gln Glu Trp Ile Cys Leu Glu Thr Leu Thr Pro Asp Thr
165 170 175
Gln Tyr Glu Phe Gln Val Arg Val Lys Pro Leu Gln Gly Glu Phe Thr
180 185 190
Thr Trp Ser Pro Trp Ser Gln Pro Leu Ala Phe Arg Thr Lys Pro Ala
195 200 205
Ala Leu Gly Lys Asp Thr
210
<210> 8
<211> 369
<212> PRT
<213> Homo sapiens
<400> 8
Met Leu Lys Pro Ser Leu Pro Phe Thr Ser Leu Leu Phe Leu Gln Leu
1 5 10 15
Pro Leu Leu Gly Val Gly Leu Asn Thr Thr Ile Leu Thr Pro Asn Gly
20 25 30
Asn Glu Asp Thr Thr Ala Asp Phe Phe Leu Thr Thr Met Pro Thr Asp
35 40 45
Ser Leu Ser Val Ser Thr Leu Pro Leu Pro Glu Val Gln Cys Phe Val
50 55 60
Phe Asn Val Glu Tyr Met Asn Cys Thr Trp Asn Ser Ser Ser Glu Pro
65 70 75 80
Gln Pro Thr Asn Leu Thr Leu His Tyr Trp Tyr Lys Asn Ser Asp Asn
85 90 95
Asp Lys Val Gln Lys Cys Ser His Tyr Leu Phe Ser Glu Glu Ile Thr
100 105 110
Ser Gly Cys Gln Leu Gln Lys Lys Glu Ile His Leu Tyr Gln Thr Phe
115 120 125
Val Val Gln Leu Gln Asp Pro Arg Glu Pro Arg Arg Gln Ala Thr Gln
130 135 140
Met Leu Lys Leu Gln Asn Leu Val Ile Pro Trp Ala Pro Glu Asn Leu
145 150 155 160
Thr Leu His Lys Leu Ser Glu Ser Gln Leu Glu Leu Asn Trp Asn Asn
165 170 175
Arg Phe Leu Asn His Cys Leu Glu His Leu Val Gln Tyr Arg Thr Asp
180 185 190
Trp Asp His Ser Trp Thr Glu Gln Ser Val Asp Tyr Arg His Lys Phe
195 200 205
Ser Leu Pro Ser Val Asp Gly Gln Lys Arg Tyr Thr Phe Arg Val Arg
210 215 220
Ser Arg Phe Asn Pro Leu Cys Gly Ser Ala Gln His Trp Ser Glu Trp
225 230 235 240
Ser His Pro Ile His Trp Gly Ser Asn Thr Ser Lys Glu Asn Pro Phe
245 250 255
Leu Phe Ala Leu Glu Ala Val Val Ile Ser Val Gly Ser Met Gly Leu
260 265 270
Ile Ile Ser Leu Leu Cys Val Tyr Phe Trp Leu Glu Arg Thr Met Pro
275 280 285
Arg Ile Pro Thr Leu Lys Asn Leu Glu Asp Leu Val Thr Glu Tyr His
290 295 300
Gly Asn Phe Ser Ala Trp Ser Gly Val Ser Lys Gly Leu Ala Glu Ser
305 310 315 320
Leu Gln Pro Asp Tyr Ser Glu Arg Leu Cys Leu Val Ser Glu Ile Pro
325 330 335
Pro Lys Gly Gly Ala Leu Gly Glu Gly Pro Gly Ala Ser Pro Cys Asn
340 345 350
Gln His Ser Pro Tyr Trp Ala Pro Pro Cys Tyr Thr Leu Lys Pro Glu
355 360 365
Thr
<210> 9
<211> 240
<212> PRT
<213> Homo sapiens
<400> 9
Leu Asn Thr Thr Ile Leu Thr Pro Asn Gly Asn Glu Asp Thr Thr Ala
1 5 10 15
Asp Phe Phe Leu Thr Thr Met Pro Thr Asp Ser Leu Ser Val Ser Thr
20 25 30
Leu Pro Leu Pro Glu Val Gln Cys Phe Val Phe Asn Val Glu Tyr Met
35 40 45
Asn Cys Thr Trp Asn Ser Ser Ser Glu Pro Gln Pro Thr Asn Leu Thr
50 55 60
Leu His Tyr Trp Tyr Lys Asn Ser Asp Asn Asp Lys Val Gln Lys Cys
65 70 75 80
Ser His Tyr Leu Phe Ser Glu Glu Ile Thr Ser Gly Cys Gln Leu Gln
85 90 95
Lys Lys Glu Ile His Leu Tyr Gln Thr Phe Val Val Gln Leu Gln Asp
100 105 110
Pro Arg Glu Pro Arg Arg Gln Ala Thr Gln Met Leu Lys Leu Gln Asn
115 120 125
Leu Val Ile Pro Trp Ala Pro Glu Asn Leu Thr Leu His Lys Leu Ser
130 135 140
Glu Ser Gln Leu Glu Leu Asn Trp Asn Asn Arg Phe Leu Asn His Cys
145 150 155 160
Leu Glu His Leu Val Gln Tyr Arg Thr Asp Trp Asp His Ser Trp Thr
165 170 175
Glu Gln Ser Val Asp Tyr Arg His Lys Phe Ser Leu Pro Ser Val Asp
180 185 190
Gly Gln Lys Arg Tyr Thr Phe Arg Val Arg Ser Arg Phe Asn Pro Leu
195 200 205
Cys Gly Ser Ala Gln His Trp Ser Glu Trp Ser His Pro Ile His Trp
210 215 220
Gly Ser Asn Thr Ser Lys Glu Asn Pro Phe Leu Phe Ala Leu Glu Ala
225 230 235 240
<210> 10
<211> 525
<212> PRT
<213> Homo sapiens
<400> 10
Met Trp Glu Ala Gln Phe Leu Gly Leu Leu Phe Leu Gln Pro Leu Trp
1 5 10 15
Val Ala Pro Val Lys Pro Leu Gln Pro Gly Ala Glu Val Pro Val Val
20 25 30
Trp Ala Gln Glu Gly Ala Pro Ala Gln Leu Pro Cys Ser Pro Thr Ile
35 40 45
Pro Leu Gln Asp Leu Ser Leu Leu Arg Arg Ala Gly Val Thr Trp Gln
50 55 60
His Gln Pro Asp Ser Gly Pro Pro Ala Ala Ala Pro Gly His Pro Leu
65 70 75 80
Ala Pro Gly Pro His Pro Ala Ala Pro Ser Ser Trp Gly Pro Arg Pro
85 90 95
Arg Arg Tyr Thr Val Leu Ser Val Gly Pro Gly Gly Leu Arg Ser Gly
100 105 110
Arg Leu Pro Leu Gln Pro Arg Val Gln Leu Asp Glu Arg Gly Arg Gln
115 120 125
Arg Gly Asp Phe Ser Leu Trp Leu Arg Pro Ala Arg Arg Ala Asp Ala
130 135 140
Gly Glu Tyr Arg Ala Ala Val His Leu Arg Asp Arg Ala Leu Ser Cys
145 150 155 160
Arg Leu Arg Leu Arg Leu Gly Gln Ala Ser Met Thr Ala Ser Pro Pro
165 170 175
Gly Ser Leu Arg Ala Ser Asp Trp Val Ile Leu Asn Cys Ser Phe Ser
180 185 190
Arg Pro Asp Arg Pro Ala Ser Val His Trp Phe Arg Asn Arg Gly Gln
195 200 205
Gly Arg Val Pro Val Arg Glu Ser Pro His His His Leu Ala Glu Ser
210 215 220
Phe Leu Phe Leu Pro Gln Val Ser Pro Met Asp Ser Gly Pro Trp Gly
225 230 235 240
Cys Ile Leu Thr Tyr Arg Asp Gly Phe Asn Val Ser Ile Met Tyr Asn
245 250 255
Leu Thr Val Leu Gly Leu Glu Pro Pro Thr Pro Leu Thr Val Tyr Ala
260 265 270
Gly Ala Gly Ser Arg Val Gly Leu Pro Cys Arg Leu Pro Ala Gly Val
275 280 285
Gly Thr Arg Ser Phe Leu Thr Ala Lys Trp Thr Pro Pro Gly Gly Gly
290 295 300
Pro Asp Leu Leu Val Thr Gly Asp Asn Gly Asp Phe Thr Leu Arg Leu
305 310 315 320
Glu Asp Val Ser Gln Ala Gln Ala Gly Thr Tyr Thr Cys His Ile His
325 330 335
Leu Gln Glu Gln Gln Leu Asn Ala Thr Val Thr Leu Ala Ile Ile Thr
340 345 350
Val Thr Pro Lys Ser Phe Gly Ser Pro Gly Ser Leu Gly Lys Leu Leu
355 360 365
Cys Glu Val Thr Pro Val Ser Gly Gln Glu Arg Phe Val Trp Ser Ser
370 375 380
Leu Asp Thr Pro Ser Gln Arg Ser Phe Ser Gly Pro Trp Leu Glu Ala
385 390 395 400
Gln Glu Ala Gln Leu Leu Ser Gln Pro Trp Gln Cys Gln Leu Tyr Gln
405 410 415
Gly Glu Arg Leu Leu Gly Ala Ala Val Tyr Phe Thr Glu Leu Ser Ser
420 425 430
Pro Gly Ala Gln Arg Ser Gly Arg Ala Pro Gly Ala Leu Pro Ala Gly
435 440 445
His Leu Leu Leu Phe Leu Ile Leu Gly Val Leu Ser Leu Leu Leu Leu
450 455 460
Val Thr Gly Ala Phe Gly Phe His Leu Trp Arg Arg Gln Trp Arg Pro
465 470 475 480
Arg Arg Phe Ser Ala Leu Glu Gln Gly Ile His Pro Pro Gln Ala Gln
485 490 495
Ser Lys Ile Glu Glu Leu Glu Gln Glu Pro Glu Pro Glu Pro Glu Pro
500 505 510
Glu Pro Glu Pro Glu Pro Glu Pro Glu Pro Glu Gln Leu
515 520 525
<210> 11
<211> 422
<212> PRT
<213> Homo sapiens
<400> 11
Val Pro Val Val Trp Ala Gln Glu Gly Ala Pro Ala Gln Leu Pro Cys
1 5 10 15
Ser Pro Thr Ile Pro Leu Gln Asp Leu Ser Leu Leu Arg Arg Ala Gly
20 25 30
Val Thr Trp Gln His Gln Pro Asp Ser Gly Pro Pro Ala Ala Ala Pro
35 40 45
Gly His Pro Leu Ala Pro Gly Pro His Pro Ala Ala Pro Ser Ser Trp
50 55 60
Gly Pro Arg Pro Arg Arg Tyr Thr Val Leu Ser Val Gly Pro Gly Gly
65 70 75 80
Leu Arg Ser Gly Arg Leu Pro Leu Gln Pro Arg Val Gln Leu Asp Glu
85 90 95
Arg Gly Arg Gln Arg Gly Asp Phe Ser Leu Trp Leu Arg Pro Ala Arg
100 105 110
Arg Ala Asp Ala Gly Glu Tyr Arg Ala Ala Val His Leu Arg Asp Arg
115 120 125
Ala Leu Ser Cys Arg Leu Arg Leu Arg Leu Gly Gln Ala Ser Met Thr
130 135 140
Ala Ser Pro Pro Gly Ser Leu Arg Ala Ser Asp Trp Val Ile Leu Asn
145 150 155 160
Cys Ser Phe Ser Arg Pro Asp Arg Pro Ala Ser Val His Trp Phe Arg
165 170 175
Asn Arg Gly Gln Gly Arg Val Pro Val Arg Glu Ser Pro His His His
180 185 190
Leu Ala Glu Ser Phe Leu Phe Leu Pro Gln Val Ser Pro Met Asp Ser
195 200 205
Gly Pro Trp Gly Cys Ile Leu Thr Tyr Arg Asp Gly Phe Asn Val Ser
210 215 220
Ile Met Tyr Asn Leu Thr Val Leu Gly Leu Glu Pro Pro Thr Pro Leu
225 230 235 240
Thr Val Tyr Ala Gly Ala Gly Ser Arg Val Gly Leu Pro Cys Arg Leu
245 250 255
Pro Ala Gly Val Gly Thr Arg Ser Phe Leu Thr Ala Lys Trp Thr Pro
260 265 270
Pro Gly Gly Gly Pro Asp Leu Leu Val Thr Gly Asp Asn Gly Asp Phe
275 280 285
Thr Leu Arg Leu Glu Asp Val Ser Gln Ala Gln Ala Gly Thr Tyr Thr
290 295 300
Cys His Ile His Leu Gln Glu Gln Gln Leu Asn Ala Thr Val Thr Leu
305 310 315 320
Ala Ile Ile Thr Val Thr Pro Lys Ser Phe Gly Ser Pro Gly Ser Leu
325 330 335
Gly Lys Leu Leu Cys Glu Val Thr Pro Val Ser Gly Gln Glu Arg Phe
340 345 350
Val Trp Ser Ser Leu Asp Thr Pro Ser Gln Arg Ser Phe Ser Gly Pro
355 360 365
Trp Leu Glu Ala Gln Glu Ala Gln Leu Leu Ser Gln Pro Trp Gln Cys
370 375 380
Gln Leu Tyr Gln Gly Glu Arg Leu Leu Gly Ala Ala Val Tyr Phe Thr
385 390 395 400
Glu Leu Ser Ser Pro Gly Ala Gln Arg Ser Gly Arg Ala Pro Gly Ala
405 410 415
Leu Pro Ala Gly His Leu
420
<210> 12
<211> 533
<212> PRT
<213> Macaca fascicularis
<220>
<221> MOD_RES
<222> (74)..(74)
<223> Any amino acid
<400> 12
Met Trp Glu Ala Gln Phe Leu Gly Leu Leu Phe Leu Gln Pro Leu Trp
1 5 10 15
Val Ala Pro Val Lys Pro Pro Gln Pro Gly Ala Glu Ile Ser Val Val
20 25 30
Trp Ala Gln Glu Gly Ala Pro Ala Gln Leu Pro Cys Ser Pro Thr Ile
35 40 45
Pro Leu Gln Asp Leu Ser Leu Leu Arg Arg Ala Gly Val Thr Trp Gln
50 55 60
His Gln Pro Asp Ser Gly Pro Pro Ala Xaa Ala Pro Gly His Pro Pro
65 70 75 80
Val Pro Gly His Arg Pro Ala Ala Pro Tyr Ser Trp Gly Pro Arg Pro
85 90 95
Arg Arg Tyr Thr Val Leu Ser Val Gly Pro Gly Gly Leu Arg Ser Gly
100 105 110
Arg Leu Pro Leu Gln Pro Arg Val Gln Leu Asp Glu Arg Gly Arg Gln
115 120 125
Arg Gly Asp Phe Ser Leu Trp Leu Arg Pro Ala Arg Arg Ala Asp Ala
130 135 140
Gly Glu Tyr Arg Ala Thr Val His Leu Arg Asp Arg Ala Leu Ser Cys
145 150 155 160
Arg Leu Arg Leu Arg Val Gly Gln Ala Ser Met Thr Ala Ser Pro Pro
165 170 175
Gly Ser Leu Arg Thr Ser Asp Trp Val Ile Leu Asn Cys Ser Phe Ser
180 185 190
Arg Pro Asp Arg Pro Ala Ser Val His Trp Phe Arg Ser Arg Gly Gln
195 200 205
Gly Arg Val Pro Val Gln Gly Ser Pro His His His Leu Ala Glu Ser
210 215 220
Phe Leu Phe Leu Pro His Val Gly Pro Met Asp Ser Gly Leu Trp Gly
225 230 235 240
Cys Ile Leu Thr Tyr Arg Asp Gly Phe Asn Val Ser Ile Met Tyr Asn
245 250 255
Leu Thr Val Leu Gly Leu Glu Pro Ala Thr Pro Leu Thr Val Tyr Ala
260 265 270
Gly Ala Gly Ser Arg Val Glu Leu Pro Cys Arg Leu Pro Pro Ala Val
275 280 285
Gly Thr Gln Ser Phe Leu Thr Ala Lys Trp Ala Pro Pro Gly Gly Gly
290 295 300
Pro Asp Leu Leu Val Ala Gly Asp Asn Gly Asp Phe Thr Leu Arg Leu
305 310 315 320
Glu Asp Val Ser Gln Ala Gln Ala Gly Thr Tyr Ile Cys His Ile Arg
325 330 335
Leu Gln Gly Gln Gln Leu Asn Ala Thr Val Thr Leu Ala Ile Ile Thr
340 345 350
Val Thr Pro Lys Ser Phe Gly Ser Pro Gly Ser Leu Gly Lys Leu Leu
355 360 365
Cys Glu Val Thr Pro Ala Ser Gly Gln Glu His Phe Val Trp Ser Pro
370 375 380
Leu Asn Thr Pro Ser Gln Arg Ser Phe Ser Gly Pro Trp Leu Glu Ala
385 390 395 400
Gln Glu Ala Gln Leu Leu Ser Gln Pro Trp Gln Cys Gln Leu His Gln
405 410 415
Gly Glu Arg Leu Leu Gly Ala Ala Val Tyr Phe Thr Glu Leu Ser Ser
420 425 430
Pro Gly Ala Gln Arg Ser Gly Arg Ala Pro Gly Ala Leu Arg Ala Gly
435 440 445
His Leu Pro Leu Phe Leu Ile Leu Gly Val Leu Phe Leu Leu Leu Leu
450 455 460
Val Thr Gly Ala Phe Gly Phe His Leu Trp Arg Arg Gln Trp Arg Pro
465 470 475 480
Arg Arg Phe Ser Ala Leu Glu Gln Gly Ile His Pro Pro Gln Ala Gln
485 490 495
Ser Lys Ile Glu Glu Leu Glu Gln Glu Pro Glu Leu Glu Pro Glu Pro
500 505 510
Glu Leu Glu Arg Glu Leu Gly Pro Glu Pro Glu Pro Gly Pro Glu Pro
515 520 525
Glu Pro Glu Gln Leu
530
<210> 13
<211> 422
<212> PRT
<213> Macaca fascicularis
<220>
<221> MOD_RES
<222> (46)..(46)
<223> Any amino acid
<400> 13
Ile Ser Val Val Trp Ala Gln Glu Gly Ala Pro Ala Gln Leu Pro Cys
1 5 10 15
Ser Pro Thr Ile Pro Leu Gln Asp Leu Ser Leu Leu Arg Arg Ala Gly
20 25 30
Val Thr Trp Gln His Gln Pro Asp Ser Gly Pro Pro Ala Xaa Ala Pro
35 40 45
Gly His Pro Pro Val Pro Gly His Arg Pro Ala Ala Pro Tyr Ser Trp
50 55 60
Gly Pro Arg Pro Arg Arg Tyr Thr Val Leu Ser Val Gly Pro Gly Gly
65 70 75 80
Leu Arg Ser Gly Arg Leu Pro Leu Gln Pro Arg Val Gln Leu Asp Glu
85 90 95
Arg Gly Arg Gln Arg Gly Asp Phe Ser Leu Trp Leu Arg Pro Ala Arg
100 105 110
Arg Ala Asp Ala Gly Glu Tyr Arg Ala Thr Val His Leu Arg Asp Arg
115 120 125
Ala Leu Ser Cys Arg Leu Arg Leu Arg Val Gly Gln Ala Ser Met Thr
130 135 140
Ala Ser Pro Pro Gly Ser Leu Arg Thr Ser Asp Trp Val Ile Leu Asn
145 150 155 160
Cys Ser Phe Ser Arg Pro Asp Arg Pro Ala Ser Val His Trp Phe Arg
165 170 175
Ser Arg Gly Gln Gly Arg Val Pro Val Gln Gly Ser Pro His His His
180 185 190
Leu Ala Glu Ser Phe Leu Phe Leu Pro His Val Gly Pro Met Asp Ser
195 200 205
Gly Leu Trp Gly Cys Ile Leu Thr Tyr Arg Asp Gly Phe Asn Val Ser
210 215 220
Ile Met Tyr Asn Leu Thr Val Leu Gly Leu Glu Pro Ala Thr Pro Leu
225 230 235 240
Thr Val Tyr Ala Gly Ala Gly Ser Arg Val Glu Leu Pro Cys Arg Leu
245 250 255
Pro Pro Ala Val Gly Thr Gln Ser Phe Leu Thr Ala Lys Trp Ala Pro
260 265 270
Pro Gly Gly Gly Pro Asp Leu Leu Val Ala Gly Asp Asn Gly Asp Phe
275 280 285
Thr Leu Arg Leu Glu Asp Val Ser Gln Ala Gln Ala Gly Thr Tyr Ile
290 295 300
Cys His Ile Arg Leu Gln Gly Gln Gln Leu Asn Ala Thr Val Thr Leu
305 310 315 320
Ala Ile Ile Thr Val Thr Pro Lys Ser Phe Gly Ser Pro Gly Ser Leu
325 330 335
Gly Lys Leu Leu Cys Glu Val Thr Pro Ala Ser Gly Gln Glu His Phe
340 345 350
Val Trp Ser Pro Leu Asn Thr Pro Ser Gln Arg Ser Phe Ser Gly Pro
355 360 365
Trp Leu Glu Ala Gln Glu Ala Gln Leu Leu Ser Gln Pro Trp Gln Cys
370 375 380
Gln Leu His Gln Gly Glu Arg Leu Leu Gly Ala Ala Val Tyr Phe Thr
385 390 395 400
Glu Leu Ser Ser Pro Gly Ala Gln Arg Ser Gly Arg Ala Pro Gly Ala
405 410 415
Leu Arg Ala Gly His Leu
420
<210> 14
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 14
Gly Gly Gly Gly Ser
1 5
<210> 15
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 15
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10
<210> 16
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 16
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 17
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 17
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser
20
<210> 18
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 18
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser
20 25
<210> 19
<211> 30
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 19
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
20 25 30
<210> 20
<211> 35
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 20
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
20 25 30
Gly Gly Ser
35
<210> 21
<211> 30
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 21
Asp Pro Ala Leu Val His Gln Arg Pro Ala Pro Pro Gly Gly Gly Gly
1 5 10 15
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
20 25 30
<210> 22
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 22
Gly Lys Pro Gly Ser
1 5
<210> 23
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 23
Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly
1 5 10 15
Lys Pro Gly Ser Gly Lys Pro Gly Ser
20 25
<210> 24
<211> 30
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 24
Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly
1 5 10 15
Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser
20 25 30
<210> 25
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 25
Gly Gly Gly Glu Ser
1 5
<210> 26
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 26
Lys Thr His Thr Cys Pro Pro Cys Pro
1 5
<210> 27
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 27
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro
1 5 10 15
<210> 28
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 28
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Lys Thr His Thr Cys Pro
1 5 10 15
Pro Cys Pro
<210> 29
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 29
Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Lys Thr His Thr Cys Pro
1 5 10 15
Pro Cys Pro
<210> 30
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 30
Gly Lys Pro Gly Ser Lys Thr His Thr Cys Pro Pro Cys Pro
1 5 10
<210> 31
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 31
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 32
<211> 18
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 32
Gly Ser Thr Ser Gly Ser Gly Lys Pro Gly Ser Gly Glu Gly Ser Thr
1 5 10 15
Lys Gly
<210> 33
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 33
Ile Arg Pro Arg Ala Ile Gly Gly Ser Lys Pro Arg Val Ala
1 5 10
<210> 34
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 34
Gly Lys Gly Gly Ser Gly Lys Gly Gly Ser Gly Lys Gly Gly Ser
1 5 10 15
<210> 35
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 35
Gly Gly Lys Gly Ser Gly Gly Lys Gly Ser Gly Gly Lys Gly Ser
1 5 10 15
<210> 36
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 36
Gly Gly Gly Lys Ser Gly Gly Gly Lys Ser Gly Gly Gly Lys Ser
1 5 10 15
<210> 37
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 37
Gly Lys Gly Lys Ser Gly Lys Gly Lys Ser Gly Lys Gly Lys Ser
1 5 10 15
<210> 38
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 38
Gly Gly Gly Lys Ser Gly Gly Lys Gly Ser Gly Lys Gly Gly Ser
1 5 10 15
<210> 39
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 39
Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser
1 5 10 15
<210> 40
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 40
Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly
1 5 10 15
Lys Pro Gly Ser
20
<210> 41
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 41
Gly Lys Gly Lys Ser Gly Lys Gly Lys Ser Gly Lys Gly Lys Ser Gly
1 5 10 15
Lys Gly Lys Ser
20
<210> 42
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 42
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser
20
<210> 43
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 43
Ser Thr Ala Gly Asp Thr His Leu Gly Gly Glu Asp Phe Asp
1 5 10
<210> 44
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 44
Gly Glu Gly Gly Ser Gly Glu Gly Gly Ser Gly Glu Gly Gly Ser
1 5 10 15
<210> 45
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 45
Gly Gly Glu Gly Ser Gly Gly Glu Gly Ser Gly Gly Glu Gly Ser
1 5 10 15
<210> 46
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 46
Gly Gly Gly Glu Ser Gly Gly Gly Glu Ser Gly Gly Gly Glu Ser
1 5 10 15
<210> 47
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 47
Gly Glu Gly Glu Ser Gly Glu Gly Glu Ser Gly Glu Gly Glu Ser
1 5 10 15
<210> 48
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 48
Gly Gly Gly Glu Ser Gly Gly Glu Gly Ser Gly Glu Gly Gly Ser
1 5 10 15
<210> 49
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 49
Gly Glu Gly Glu Ser Gly Glu Gly Glu Ser Gly Glu Gly Glu Ser Gly
1 5 10 15
Glu Gly Glu Ser
20
<210> 50
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 50
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 51
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 51
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser
20
<210> 52
<211> 18
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 52
Gly Ser Thr Ser Gly Ser Gly Lys Pro Gly Ser Gly Glu Gly Ser Thr
1 5 10 15
Lys Gly
<210> 53
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 53
Pro Arg Gly Ala Ser Lys Ser Gly Ser Ala Ser Gln Thr Gly Ser Ala
1 5 10 15
Pro Gly Ser
<210> 54
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 54
Gly Thr Ala Ala Ala Gly Ala Gly Ala Ala Gly Gly Ala Ala Ala Gly
1 5 10 15
Ala Ala Gly
<210> 55
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 55
Gly Thr Ser Gly Ser Ser Gly Ser Gly Ser Gly Gly Ser Gly Ser Gly
1 5 10 15
Gly Gly Gly
<210> 56
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 56
Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly
1 5 10 15
Lys Pro Gly Ser
20
<210> 57
<211> 329
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 57
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
115 120 125
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
130 135 140
Val Val Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
145 150 155 160
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
165 170 175
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
180 185 190
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
195 200 205
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
210 215 220
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met
225 230 235 240
Thr Lys Asn Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
245 250 255
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
260 265 270
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
275 280 285
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
290 295 300
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
305 310 315 320
Lys Ser Leu Ser Leu Ser Pro Gly Lys
325
<210> 58
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 58
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
130 135 140
Asn Gln Val Ser Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 59
<211> 329
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 59
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asp Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
115 120 125
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
130 135 140
Val Val Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
145 150 155 160
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
165 170 175
Glu Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
180 185 190
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
195 200 205
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
210 215 220
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met
225 230 235 240
Thr Lys Asn Gln Val Ser Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro
245 250 255
Ser Asp Ile Ala Val Glu Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn
260 265 270
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
275 280 285
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Glu Gln Gly Asp Val
290 295 300
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
305 310 315 320
Lys Ser Leu Ser Leu Ser Pro Gly Lys
325
<210> 60
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 60
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys
130 135 140
Asn Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 61
<211> 329
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 61
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asp Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
115 120 125
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
130 135 140
Val Val Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
145 150 155 160
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
165 170 175
Glu Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
180 185 190
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
195 200 205
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
210 215 220
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met
225 230 235 240
Thr Lys Asn Gln Val Ser Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro
245 250 255
Ser Asp Ile Ala Val Glu Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn
260 265 270
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
275 280 285
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Glu Gln Gly Asp Val
290 295 300
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
305 310 315 320
Lys Ser Leu Ser Leu Ser Pro Gly Lys
325
<210> 62
<211> 329
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 62
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Arg Lys Ser Cys Asp Lys Thr His Thr Cys Pro Arg Cys
100 105 110
Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
115 120 125
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
130 135 140
Val Val Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Lys Trp Tyr
145 150 155 160
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
165 170 175
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
180 185 190
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
195 200 205
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
210 215 220
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met
225 230 235 240
Thr Lys Asn Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
245 250 255
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
260 265 270
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
275 280 285
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
290 295 300
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
305 310 315 320
Lys Ser Leu Ser Leu Ser Pro Gly Lys
325
<210> 63
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 63
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 64
<211> 106
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 64
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro
35 40 45
Val Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Thr Glu Cys Ser
100 105
<210> 65
<211> 121
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 65
Glu Val Lys Leu Glu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Met Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Ala
20 25 30
Trp Met Asp Trp Val Arg Gln Ser Pro Glu Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Arg Thr Lys Ala Asn Asn His Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Ser
65 70 75 80
Val Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Gly Ile Tyr
85 90 95
Tyr Cys Thr Arg Leu Ala Asn Trp Asp Trp Tyr Phe Asp Val Trp Gly
100 105 110
Ala Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 66
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 66
Asp Ala Trp Met Asp
1 5
<210> 67
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 67
Glu Ile Arg Thr Lys Ala Asn Asn His Ala Thr Tyr Tyr Ala Glu Ser
1 5 10 15
Val Lys Gly
<210> 68
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 68
Leu Ala Asn Trp Asp Trp Tyr Phe Asp Val
1 5 10
<210> 69
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 69
Asp Thr Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Lys Ala Ser Gln Ser Val Asp Tyr Asp
20 25 30
Gly Asp Ser Tyr Met Asn Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Leu Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Asn Ile His
65 70 75 80
Pro Val Glu Glu Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Asp Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Val Lys
100 105 110
<210> 70
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 70
Lys Ala Ser Gln Ser Val Asp Tyr Asp Gly Asp Ser Tyr Met Asn
1 5 10 15
<210> 71
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 71
Ala Ala Ser Asn Leu Glu Ser
1 5
<210> 72
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 72
Gln Gln Ser Asn Glu Asp Pro Phe Thr
1 5
<210> 73
<211> 121
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 73
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Ala
20 25 30
Trp Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Arg Thr Lys Ala Asn Asn His Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Ser
65 70 75 80
Val Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Thr Arg Leu Ala Asn Trp Asp Trp Tyr Phe Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 74
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 74
Asp Ala Trp Met Asp
1 5
<210> 75
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 75
Glu Ile Arg Thr Lys Ala Asn Asn His Ala Thr Tyr Tyr Ala Glu Ser
1 5 10 15
Val Lys Gly
<210> 76
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 76
Leu Ala Asn Trp Asp Trp Tyr Phe Asp Val
1 5 10
<210> 77
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 77
Asp Thr Val Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Val Asp Tyr Asp
20 25 30
Gly Asp Ser Tyr Met Asn Trp Tyr Gln Gln Lys Pro Gly Lys Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Leu Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Asp Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 78
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 78
Arg Ala Ser Gln Ser Val Asp Tyr Asp Gly Asp Ser Tyr Met Asn
1 5 10 15
<210> 79
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 79
Ala Ala Ser Asn Leu Glu Ser
1 5
<210> 80
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 80
Gln Gln Ser Asn Glu Asp Pro Phe Thr
1 5
<210> 81
<211> 121
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 81
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Ala
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Ser Thr Lys Ala Asn Asn His Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Ser
65 70 75 80
Val Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Thr Arg Leu Ala Thr Trp Asp Trp Tyr Phe Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 82
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 82
Asp Ala Trp Met Ser
1 5
<210> 83
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 83
Glu Ile Ser Thr Lys Ala Asn Asn His Ala Thr Tyr Tyr Ala Glu Ser
1 5 10 15
Val Lys Gly
<210> 84
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 84
Leu Ala Thr Trp Asp Trp Tyr Phe Asp Val
1 5 10
<210> 85
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 85
Asp Ile Val Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Val Asp Tyr Asp
20 25 30
Gly Asp Ser Tyr Met Asn Trp Tyr Gln Gln Lys Pro Gly Lys Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Glu Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Asp Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 86
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 86
Arg Ala Ser Gln Ser Val Asp Tyr Asp Gly Asp Ser Tyr Met Asn
1 5 10 15
<210> 87
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 87
Ala Ala Ser Glu Leu Glu Ser
1 5
<210> 88
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 88
Gln Gln Ser Asn Glu Asp Pro Phe Thr
1 5
<210> 89
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 89
Glu Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Val Arg Ser Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Thr Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Lys Gln Arg Pro Glu Gln Gly Leu Glu Trp Ile
35 40 45
Gly Trp Ile Asp Pro Glu Asn Gly Asp Thr Glu Tyr Ala Pro Lys Phe
50 55 60
Gln Gly Lys Ala Thr Met Thr Ala Asp Thr Ser Ser Asn Thr Ala Tyr
65 70 75 80
Leu Gln Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Tyr Ala Arg Gly Val Arg Gln Ala Leu Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Ser Val Thr Val Ser Ser
115
<210> 90
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 90
Asp Tyr Tyr Met His
1 5
<210> 91
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 91
Trp Ile Asp Pro Glu Asn Gly Asp Thr Glu Tyr Ala Pro Lys Phe Gln
1 5 10 15
Gly
<210> 92
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 92
Arg Gly Val Arg Gln Ala Leu Asp Tyr
1 5
<210> 93
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 93
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Gly Asn Tyr
20 25 30
Leu Asn Trp Phe Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 94
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 94
Arg Ala Ser Gln Asp Ile Gly Asn Tyr Leu Asn
1 5 10
<210> 95
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 95
Tyr Thr Ser Arg Leu His Ser
1 5
<210> 96
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 96
Gln Gln Gly Asn Thr Leu Pro Tyr Thr
1 5
<210> 97
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 97
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Gln Gln Ala Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Pro Glu Asn Gly Asp Thr Glu Tyr Ala Pro Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Tyr Ala Arg Gly Val Arg Gln Ala Leu Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 98
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 98
Asp Tyr Tyr Met His
1 5
<210> 99
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 99
Trp Ile Asp Pro Glu Asn Gly Asp Thr Glu Tyr Ala Pro Lys Phe Gln
1 5 10 15
Gly
<210> 100
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 100
Arg Gly Val Arg Gln Ala Leu Asp Tyr
1 5
<210> 101
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 101
Asp Ile Gln Met Thr Gln Ser Pro Ala Phe Leu Ser Val Thr Pro Gly
1 5 10 15
Glu Lys Val Thr Ile Thr Cys Gln Ala Ser Gln Asp Ile Gly Asn Tyr
20 25 30
Leu Asn Trp Phe Gln Gln Lys Pro Asp Gln Thr Val Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Phe Thr Ile Ser Ser Leu Glu Ala
65 70 75 80
Glu Asp Ala Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 102
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 102
Gln Ala Ser Gln Asp Ile Gly Asn Tyr Leu Asn
1 5 10
<210> 103
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 103
Tyr Thr Ser Arg Leu His Ser
1 5
<210> 104
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 104
Gln Gln Gly Asn Thr Leu Pro Tyr Thr
1 5
<210> 105
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 105
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Phe Met His Trp Val Gln Gln Ala Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Pro Glu Leu Gly Asp Thr Glu Tyr Ala Pro Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Tyr Ala Arg Gly Val Tyr Gln Ala Leu Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 106
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 106
Asp Tyr Phe Met His
1 5
<210> 107
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 107
Trp Ile Asp Pro Glu Leu Gly Asp Thr Glu Tyr Ala Pro Lys Phe Gln
1 5 10 15
Gly
<210> 108
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 108
Arg Gly Val Tyr Gln Ala Leu Asp Tyr
1 5
<210> 109
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 109
Asp Ile Gln Met Thr Gln Ser Pro Ala Phe Leu Ser Val Thr Pro Gly
1 5 10 15
Glu Lys Val Thr Ile Thr Cys Gln Ala Ser Gln Asp Ile Gly Asn Tyr
20 25 30
Leu Asn Trp Phe Gln Gln Lys Pro Gly Gln Thr Val Lys Leu Leu Ile
35 40 45
Tyr Phe Thr Ser Tyr Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Phe Thr Ile Ser Ser Leu Glu Ala
65 70 75 80
Glu Asp Ala Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 110
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 110
Gln Ala Ser Gln Asp Ile Gly Asn Tyr Leu Asn
1 5 10
<210> 111
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 111
Phe Thr Ser Tyr Leu His Ser
1 5
<210> 112
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 112
Gln Gln Gly Asn Thr Leu Pro Tyr Thr
1 5
<210> 113
<211> 120
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 113
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Asp Tyr
20 25 30
Tyr Trp Asn Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asn His Arg Gly Ser Thr Asn Ser Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Leu Ser Leu Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Arg Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Phe Gly Tyr Ser Asp Tyr Glu Tyr Asn Trp Phe Asp Pro Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 114
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 114
Asp Tyr Tyr Trp Asn
1 5
<210> 115
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 115
Glu Ile Asn His Arg Gly Ser Thr Asn Ser Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 116
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 116
Gly Tyr Ser Asp Tyr Glu Tyr Asn Trp Phe Asp Pro
1 5 10
<210> 117
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 117
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Asn Leu Glu Ile Lys
100 105
<210> 118
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 118
Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Ala
1 5 10
<210> 119
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 119
Asp Ala Ser Asn Arg Ala Thr
1 5
<210> 120
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 120
Gln Gln Arg Ser Asn Trp Pro Leu Thr
1 5
<210> 121
<211> 116
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 121
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ala Tyr
20 25 30
Gly Val Asn Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Met Ile Trp Asp Asp Gly Ser Thr Asp Tyr Asn Ser Ala Leu Lys
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Arg Tyr Tyr Cys Ala
85 90 95
Arg Glu Gly Asp Val Ala Phe Asp Tyr Trp Gly Gln Gly Thr Thr Leu
100 105 110
Thr Val Ser Ser
115
<210> 122
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 122
Ala Tyr Gly Val Asn
1 5
<210> 123
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 123
Met Ile Trp Asp Asp Gly Ser Thr Asp Tyr Asn Ser Ala Leu Lys Ser
1 5 10 15
<210> 124
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 124
Glu Gly Asp Val Ala Phe Asp Tyr
1 5
<210> 125
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 125
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Ala Val Ser Val Gly
1 5 10 15
Gln Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Gly
20 25 30
Ser Asn Gln Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Ser Pro Lys Leu Leu Val Tyr Phe Ala Ser Thr Arg Asp Ser Gly Val
50 55 60
Pro Asp Arg Phe Ile Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Asp Tyr Phe Cys Leu Gln
85 90 95
His Phe Gly Thr Pro Pro Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
100 105 110
Lys Arg
<210> 126
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 126
Lys Ser Ser Gln Ser Leu Leu Asn Gly Ser Asn Gln Lys Asn Tyr Leu
1 5 10 15
Ala
<210> 127
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 127
Phe Ala Ser Thr Arg Asp Ser
1 5
<210> 128
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 128
Leu Gln His Phe Gly Thr Pro Pro Thr
1 5
<210> 129
<211> 123
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 129
Gln Val Thr Leu Lys Glu Ser Gly Pro Gly Ile Leu Gln Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ser Phe Ser Gly Phe Ser Leu Ser Thr Ser
20 25 30
Gly Met Gly Leu Gly Trp Ile Arg Gln Pro Ser Gly Lys Gly Leu Glu
35 40 45
Trp Leu Thr His Ile Trp Trp Asp Asp Ile Lys Arg Tyr Asn Pro Asp
50 55 60
Leu Arg Ser Arg Leu Thr Ile Ser Lys Asp Thr Ser Ser Ser Gln Ile
65 70 75 80
Phe Leu Lys Ile Ala Ser Val Asp Thr Ala Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Ala Arg Ile Val Glu Gly Ser Tyr Ser Ser Ser Tyr Phe Asp Val
100 105 110
Trp Gly Ala Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 130
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 130
Thr Ser Gly Met Gly Leu Gly
1 5
<210> 131
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 131
His Ile Trp Trp Asp Asp Ile Lys Arg Tyr Asn Pro Asp Leu Arg Ser
1 5 10 15
<210> 132
<211> 13
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 132
Ile Val Glu Gly Ser Tyr Ser Ser Ser Tyr Phe Asp Val
1 5 10
<210> 133
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 133
Asp Ile Val Met Thr Gln Pro His Lys Phe Met Ser Thr Ser Val Glu
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ile Phe Asp
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Ser Arg Val Ser Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Val Gln Ala
65 70 75 80
Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln His Tyr Ser Thr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Thr Leu Glu Ile Lys
100 105
<210> 134
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 134
Lys Ala Ser Gln Asp Val Ile Phe Asp Val Ala
1 5 10
<210> 135
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 135
Ser Ala Ser Ser Arg Val Ser
1 5
<210> 136
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 136
Gln Gln His Tyr Ser Thr Pro Tyr Thr
1 5
<210> 137
<211> 123
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 137
Gln Val Thr Leu Lys Glu Ser Gly Pro Gly Ile Leu Gln Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ser Phe Ser Gly Phe Ser Leu Asn Thr Ser
20 25 30
Gly Met Gly Val Gly Trp Ile Arg Gln Pro Ser Gly Lys Gly Leu Glu
35 40 45
Trp Leu Thr His Ile Trp Trp Asp Asp Val Lys Arg Tyr Asn Pro Ala
50 55 60
Leu Lys Ser Arg Leu Thr Ile Ser Lys Asp Thr Ser Ser Ser Gln Val
65 70 75 80
Phe Leu Lys Ile Ala Ser Val Asp Thr Ala Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Ala Arg Ile Glu Gly Asp Thr Tyr Tyr Asp Tyr Tyr Phe Asp Tyr
100 105 110
Trp Gly Gln Gly Val Thr Leu Thr Val Ser Ser
115 120
<210> 138
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 138
Thr Ser Gly Met Gly Val Gly
1 5
<210> 139
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 139
His Ile Trp Trp Asp Asp Val Lys Arg Tyr Asn Pro Ala Leu Lys Ser
1 5 10 15
<210> 140
<211> 13
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 140
Ile Glu Gly Asp Thr Tyr Tyr Asp Tyr Tyr Phe Asp Tyr
1 5 10
<210> 141
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 141
Asp Ile Val Met Thr Gln Ser His Lys Leu Met Ser Thr Ser Val Gly
1 5 10 15
Asp Gly Leu Ser Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Ile Ala
20 25 30
Val Val Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Arg Tyr Thr Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Val Gln Ala
65 70 75 80
Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln His Tyr Ser Ile Pro Trp
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 142
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 142
Lys Ala Ser Gln Asp Val Ser Ile Ala Val Val
1 5 10
<210> 143
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 143
Ser Ala Ser Phe Arg Tyr Thr
1 5
<210> 144
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 144
Gln Gln His Tyr Ser Ile Pro Trp Thr
1 5
<210> 145
<211> 123
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 145
Gln Ile Thr Leu Lys Glu Ser Gly Pro Thr Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Ser Thr Ser
20 25 30
Gly Met Gly Leu Gly Trp Ile Arg Gln Pro Pro Gly Lys Thr Leu Glu
35 40 45
Trp Leu Thr His Ile Trp Trp Asp Asp Ile Lys Arg Tyr Asn Pro Asp
50 55 60
Leu Arg Ser Arg Leu Ser Ile Thr Lys Asp Thr Ser Lys Asn Gln Val
65 70 75 80
Val Leu Thr Met Thr Asn Met Asp Pro Leu Asp Thr Gly Thr Tyr Tyr
85 90 95
Cys Ala Arg Ile Val Glu Gly Ser Tyr Ser Ser Ser Tyr Phe Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 146
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 146
Thr Ser Gly Met Gly Leu Gly
1 5
<210> 147
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 147
His Ile Trp Trp Asp Asp Ile Lys Arg Tyr Asn Pro Asp Leu Arg Ser
1 5 10 15
<210> 148
<211> 13
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 148
Ile Val Glu Gly Ser Tyr Ser Ser Ser Tyr Phe Asp Val
1 5 10
<210> 149
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 149
Asp Ile Val Met Thr Gln Thr Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Ile Phe Asp
20 25 30
Val Ala Trp Tyr Gln Gln Arg Pro Gly Gln Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Ser Arg Val Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Ser Thr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Asp Ile Lys
100 105
<210> 150
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 150
Lys Ala Ser Gln Asp Val Ile Phe Asp Val Ala
1 5 10
<210> 151
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 151
Ser Ala Ser Ser Arg Val Ser
1 5
<210> 152
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 152
Gln Gln His Tyr Ser Thr Pro Tyr Thr
1 5
<210> 153
<211> 116
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 153
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ala Tyr
20 25 30
Gly Val Asn Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Met Ile Trp Asp Asp Gly Ser Thr Asp Tyr Asp Ser Ala Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Glu Gly Asp Val Ala Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 154
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 154
Ala Tyr Gly Val Asn
1 5
<210> 155
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 155
Met Ile Trp Asp Asp Gly Ser Thr Asp Tyr Asp Ser Ala Leu Lys Ser
1 5 10 15
<210> 156
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 156
Glu Gly Asp Val Ala Phe Asp Tyr
1 5
<210> 157
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 157
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ser Ser Gln Ser Leu Leu Asn Pro
20 25 30
Ser Asn Gln Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys
35 40 45
Ala Pro Lys Leu Leu Val Tyr Phe Ala Ser Thr Arg Asp Ser Gly Val
50 55 60
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln
85 90 95
His Phe Gly Thr Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile
100 105 110
Lys Arg
<210> 158
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 158
Lys Ser Ser Gln Ser Leu Leu Asn Pro Ser Asn Gln Lys Asn Tyr Leu
1 5 10 15
Ala
<210> 159
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 159
Phe Ala Ser Thr Arg Asp Ser
1 5
<210> 160
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 160
Leu Gln His Phe Gly Thr Pro Pro Thr
1 5
<210> 161
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 161
Gln Met Gln Leu Val Gln Ser Gly Pro Glu Val Lys Lys Pro Gly Thr
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Val Asp Trp Val Arg Gln Ala Arg Gly Gln Arg Leu Glu Trp Ile
35 40 45
Gly Asp Ile Asn Pro Asn Asn Gly Gly Thr Ile Tyr Ala Gln Lys Phe
50 55 60
Gln Glu Arg Val Thr Ile Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Tyr Arg Trp Phe Gly Ala Met Asp His Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 162
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 162
Asp Tyr Asn Val Asp
1 5
<210> 163
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 163
Asp Ile Asn Pro Asn Asn Gly Gly Thr Ile Tyr Ala Gln Lys Phe Gln
1 5 10 15
Glu
<210> 164
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 164
Asn Tyr Arg Trp Phe Gly Ala Met Asp His
1 5 10
<210> 165
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 165
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ala Ser Gln Ser Leu Asp Tyr Glu
20 25 30
Gly Asp Ser Asp Met Asn Trp Tyr Leu Gln Lys Pro Gly Gln Pro Pro
35 40 45
Gln Leu Leu Ile Tyr Gly Ala Ser Asn Leu Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser
65 70 75 80
Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gln Gln Ser Thr
85 90 95
Glu Asp Pro Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 166
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 166
Lys Ala Ser Gln Ser Leu Asp Tyr Glu Gly Asp Ser Asp Met Asn
1 5 10 15
<210> 167
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 167
Gly Ala Ser Asn Leu Glu Ser
1 5
<210> 168
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 168
Gln Gln Ser Thr Glu Asp Pro Arg Thr
1 5
<210> 169
<211> 123
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 169
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Val Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ile Ile Trp Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Gln Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Val Ala Thr Ser Gly Asp Phe Asp Tyr Tyr Gly Met Asp Val
100 105 110
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 170
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 170
Ser Tyr Gly Met His
1 5
<210> 171
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 171
Ile Ile Trp Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 172
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 172
Val Ala Thr Ser Gly Asp Phe Asp Tyr Tyr Gly Met Asp Val
1 5 10
<210> 173
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 173
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Thr Thr Leu Ser Cys Arg Ala Ser Gln Arg Ile Ser Thr Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Lys Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Gly Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 174
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 174
Arg Ala Ser Gln Arg Ile Ser Thr Tyr Leu Ala
1 5 10
<210> 175
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 175
Asp Ala Ser Lys Arg Ala Thr
1 5
<210> 176
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 176
Gln Gln Arg Ser Asn Trp Pro Leu Thr
1 5
<210> 177
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 177
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Ala Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Leu Met Ala Thr Gly Gly Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 178
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 178
Ser Tyr Tyr Met His
1 5
<210> 179
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 179
Ile Ile Asn Pro Ser Ala Gly Ser Thr Ser Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 180
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 180
Glu Leu Met Ala Thr Gly Gly Phe Asp Tyr
1 5 10
<210> 181
<211> 112
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 181
Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Val Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln Tyr Pro Gly Lys Ala Pro Arg Leu
35 40 45
Met Ile Phe Glu Val Thr Glu Arg Ala Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Val Ser Gly Leu
65 70 75 80
Gln Thr Glu Asp Glu Ala Val Tyr Phe Cys Ser Ser Tyr Ser Gly Ser
85 90 95
Asn Asn Pro Gly Ala Met Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 182
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 182
Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr Asn Tyr Val Ser
1 5 10
<210> 183
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 183
Glu Val Thr Glu Arg Ala Ser
1 5
<210> 184
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 184
Ser Ser Tyr Ser Gly Ser Asn Asn Pro Gly Ala Met
1 5 10
<210> 185
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 185
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Ala Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Leu Met Ala Thr Gly Gly Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 186
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 186
Ser Tyr Tyr Met His
1 5
<210> 187
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 187
Ile Ile Asn Pro Ser Ala Gly Ser Thr Ser Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 188
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 188
Glu Leu Met Ala Thr Gly Gly Phe Asp Tyr
1 5 10
<210> 189
<211> 110
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 189
Gln Ala Gly Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Ser Ser Ser Asp Val Gly Gly Tyr
20 25 30
Ser Tyr Val Ser Trp Tyr Gln Lys His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Thr Asn Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Thr Tyr Thr Arg Ser
85 90 95
Asn Thr Leu Val Phe Gly Pro Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 190
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 190
Thr Gly Ser Ser Ser Asp Val Gly Gly Tyr Ser Tyr Val Ser
1 5 10
<210> 191
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 191
Asp Val Thr Asn Arg Pro Ser
1 5
<210> 192
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 192
Ser Thr Tyr Thr Arg Ser Asn Thr Leu Val
1 5 10
<210> 193
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 193
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Ala Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Leu Met Ala Thr Gly Gly Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 194
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 194
Ser Tyr Tyr Met His
1 5
<210> 195
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 195
Ile Ile Asn Pro Ser Ala Gly Ser Thr Ser Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 196
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 196
Glu Leu Met Ala Thr Gly Gly Phe Asp Tyr
1 5 10
<210> 197
<211> 110
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 197
Leu Pro Val Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Thr Asn Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Asn Thr Leu Leu Phe Gly Gly Gly Thr Gln Leu Thr Val Leu
100 105 110
<210> 198
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 198
Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr Asn Tyr Val Ser
1 5 10
<210> 199
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 199
Asp Val Thr Asn Arg Pro Ser
1 5
<210> 200
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 200
Ser Ser Tyr Thr Ser Ser Asn Thr Leu Leu
1 5 10
<210> 201
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 201
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Ala Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Leu Met Ala Thr Gly Gly Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 202
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 202
Ser Tyr Tyr Met His
1 5
<210> 203
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 203
Ile Ile Asn Pro Ser Ala Gly Ser Thr Ser Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 204
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 204
Glu Leu Met Ala Thr Gly Gly Phe Asp Tyr
1 5 10
<210> 205
<211> 110
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 205
Gln Ser Val Val Thr Gln Pro Pro Ser Val Ser Ala Ala Pro Gly Gln
1 5 10 15
Lys Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn
20 25 30
Tyr Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Asp Asn Asn Lys Arg His Ser Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Thr Ser Asp Thr Ser Ala Thr Leu Gly Ile Thr Arg Leu Gln
65 70 75 80
Thr Gly Asp Glu Ala Asp Tyr Tyr Cys Gly Thr Trp Asp Ser Ser Leu
85 90 95
Ser Ala Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 206
<211> 13
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 206
Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn Tyr Val Ser
1 5 10
<210> 207
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 207
Asp Asn Asn Lys Arg His Ser
1 5
<210> 208
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 208
Gly Thr Trp Asp Ser Ser Leu Ser Ala Tyr Val
1 5 10
<210> 209
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 209
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Ala Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Leu Met Ala Thr Gly Gly Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 210
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 210
Ser Tyr Tyr Met His
1 5
<210> 211
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 211
Ile Ile Asn Pro Ser Ala Gly Ser Thr Ser Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 212
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 212
Glu Leu Met Ala Thr Gly Gly Phe Asp Tyr
1 5 10
<210> 213
<211> 110
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 213
Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Val Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asp Tyr Val Ser Trp Tyr Gln Gln His Gln Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Thr Thr Leu Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 214
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 214
Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr Asp Tyr Val Ser
1 5 10
<210> 215
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 215
Asp Val Ser Asn Arg Pro Ser
1 5
<210> 216
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 216
Ser Ser Tyr Thr Ser Ser Thr Thr Leu Val
1 5 10
<210> 217
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 217
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Ala Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Leu Met Ala Thr Gly Gly Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 218
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 218
Ser Tyr Tyr Met His
1 5
<210> 219
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 219
Ile Ile Asn Pro Ser Ala Gly Ser Thr Ser Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 220
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 220
Glu Leu Met Ala Thr Gly Gly Phe Asp Tyr
1 5 10
<210> 221
<211> 110
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 221
Gln Ser Val Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Ile Gly Ala Tyr
20 25 30
Asn Phe Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Asn Arg Pro Ser Gly Val Ser Ser Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Ser Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Thr Ser
85 90 95
Gly Ser Ala Val Phe Gly Thr Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 222
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 222
Thr Gly Thr Ser Ser Asp Ile Gly Ala Tyr Asn Phe Val Ser
1 5 10
<210> 223
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 223
Gly Val Ser Asn Arg Pro Ser
1 5
<210> 224
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 224
Ser Ser Tyr Thr Thr Ser Gly Ser Ala Val
1 5 10
<210> 225
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 225
Glu Val Gln Leu Leu Glu Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Ala Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Leu Met Ala Thr Gly Gly Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 226
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 226
Ser Tyr Tyr Met His
1 5
<210> 227
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 227
Ile Ile Asn Pro Ser Ala Gly Ser Thr Ser Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 228
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 228
Glu Leu Met Ala Thr Gly Gly Phe Asp Tyr
1 5 10
<210> 229
<211> 110
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 229
Gln Ser Val Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Ile Gly Ala Tyr
20 25 30
Asn Phe Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Gly Val Ser Asn Arg Pro Ser Gly Val Ser Ser Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Ser Thr Ala Ser Leu Thr Ile Thr Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Thr Ser
85 90 95
Gly Ser Ala Val Phe Gly Thr Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 230
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 230
Thr Gly Thr Ser Ser Asp Ile Gly Ala Tyr Asn Phe Val Ser
1 5 10
<210> 231
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 231
Gly Val Ser Asn Arg Pro Ser
1 5
<210> 232
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 232
Ser Ser Tyr Thr Thr Ser Gly Ser Ala Val
1 5 10
<210> 233
<211> 121
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 233
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Val Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn His
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Ser Lys Lys Phe Tyr Ser Asp Ser Val
50 55 60
Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Gly Ala His Gly Tyr Thr Ser Gly Trp His Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 234
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 234
Asn His Ala Met His
1 5
<210> 235
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 235
Val Ile Ser Tyr Asp Gly Ser Lys Lys Phe Tyr Ser Asp Ser Val Arg
1 5 10 15
Gly
<210> 236
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 236
Gly Ala His Gly Tyr Thr Ser Gly Trp His Asp Tyr
1 5 10
<210> 237
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 237
Asp Val Val Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Ser Ile Thr Cys Arg Ala Ser Gln Asn Ile Gly Arg Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Val
35 40 45
Ser Ala Ala Ser Ser Leu Gln Gly Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Phe Cys Gln Gln Thr Tyr Ser Ser Pro Gln
85 90 95
Cys Thr Phe Gly Gln Gly Thr Lys Val Asp Ile Lys
100 105
<210> 238
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 238
Arg Ala Ser Gln Asn Ile Gly Arg Tyr Leu Asn
1 5 10
<210> 239
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 239
Ala Ala Ser Ser Leu Gln Gly
1 5
<210> 240
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 240
Gln Gln Thr Tyr Ser Ser Pro Gln Cys Thr
1 5 10
<210> 241
<211> 121
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 241
Gln Val Gln Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ala Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ser Gly Tyr Asp Leu Gly Tyr Gly Met Asp Val Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 242
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 242
Asn Tyr Tyr Met His
1 5
<210> 243
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 243
Ile Ile Asn Pro Ser Gly Gly Ala Thr Asn Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 244
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 244
Asp Ser Gly Tyr Asp Leu Gly Tyr Gly Met Asp Val
1 5 10
<210> 245
<211> 110
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 245
Gln Ser Val Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Pro Ser Gly Ala Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Asn Arg
85 90 95
Asn Thr Leu Leu Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 246
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 246
Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr Asn Tyr Val Ser
1 5 10
<210> 247
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 247
Asp Val Ser Asn Arg Pro Ser
1 5
<210> 248
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 248
Ser Ser Tyr Thr Asn Arg Asn Thr Leu Leu
1 5 10
<210> 249
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 249
Glu Val Gln Leu Leu Glu Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Ala Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Leu Met Ala Thr Gly Gly Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 250
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 250
Ser Tyr Tyr Met His
1 5
<210> 251
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 251
Ile Ile Asn Pro Ser Ala Gly Ser Thr Ser Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 252
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 252
Glu Leu Met Ala Thr Gly Gly Phe Asp Tyr
1 5 10
<210> 253
<211> 110
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 253
Gln Ser Val Leu Thr Gln Pro Ala Ser Ala Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asn Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Thr Asn Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 254
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 254
Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr Asn Tyr Val Ser
1 5 10
<210> 255
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 255
Asp Val Ser Asn Arg Pro Ser
1 5
<210> 256
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 256
Ser Ser Tyr Thr Ser Ser Ser Thr Asn Val
1 5 10
<210> 257
<211> 66
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 257
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Asp
65
<210> 258
<211> 67
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 258
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Asp Pro
65
<210> 259
<211> 68
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 259
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Asp Pro Ala
65
<210> 260
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 260
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Cys Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 261
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 261
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Cys Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 262
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 262
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Cys Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 263
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 263
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Cys Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 264
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 264
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Cys
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 265
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 265
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Cys Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 266
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 266
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Ser Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 267
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 267
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Cys Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 268
<211> 67
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 268
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Asp Cys
65
<210> 269
<211> 68
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 269
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Asp Pro Cys
65
<210> 270
<211> 68
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 270
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Asp Cys Ala
65
<210> 271
<211> 65
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 271
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Cys Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg
65
<210> 272
<211> 65
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 272
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Cys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg
65
<210> 273
<211> 65
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 273
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Cys Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg
65
<210> 274
<211> 65
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 274
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Cys Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg
65
<210> 275
<211> 65
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 275
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Cys Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg
65
<210> 276
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 276
Asp Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 277
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 277
Asn Trp Val Asp Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 278
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 278
Asn Trp Val Asn Val Ile Ser Asn Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 279
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 279
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asn Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 280
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 280
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asn Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 281
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 281
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Gln
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 282
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 282
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asp Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 283
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 283
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Glu Met Phe Ile Asn
100 105 110
Thr Ser
<210> 284
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 284
Asp Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asn Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 285
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 285
Asp Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Gln
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 286
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 286
Asn Trp Val Asp Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asn Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 287
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 287
Asn Trp Val Asp Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Gln
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 288
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 288
Asn Trp Val Asn Val Ile Ser Asn Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asn Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 289
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 289
Asn Trp Val Asn Val Ile Ser Asn Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Gln
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 290
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 290
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asn Thr Val Gln
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 291
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 291
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Gln
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Glu Met Phe Ile Asn
100 105 110
Thr Ser
<210> 292
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 292
Asp Trp Val Asp Val Ile Ser Asn Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 293
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 293
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asn Thr Val Gln
50 55 60
Asp Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 294
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 294
Asp Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asn Thr Val Gln
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Glu Met Phe Ile Asn
100 105 110
Thr Ser
<210> 295
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 295
Asn Trp Val Asp Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asn Thr Val Gln
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Glu Met Phe Ile Asn
100 105 110
Thr Ser
<210> 296
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 296
Asp Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asp Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 297
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 297
Asp Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Glu Met Phe Ile Asn
100 105 110
Thr Ser
<210> 298
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 298
Asn Trp Val Asp Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asp Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 299
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 299
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asn Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asp Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 300
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 300
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asn Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Glu Met Phe Ile Asn
100 105 110
Thr Ser
<210> 301
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 301
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asp Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Glu Met Phe Ile Asn
100 105 110
Thr Ser
<210> 302
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 302
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Gln
50 55 60
Asp Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 303
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 303
Asp Trp Val Asp Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asp Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 304
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 304
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asn Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Gln
50 55 60
Asp Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 305
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 305
Asn Trp Val Asp Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asn Thr Val Glu
50 55 60
Asp Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 306
<211> 435
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 306
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
65 70 75 80
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asn Trp Val Asp Val Ile
85 90 95
Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile Gln Ser Met His Ile Asp
100 105 110
Ala Thr Leu Tyr Thr Glu Ser Asp Val His Pro Ser Cys Lys Val Thr
115 120 125
Ala Met Lys Cys Phe Leu Leu Glu Leu Gln Val Ile Ser Leu Glu Ser
130 135 140
Gly Asp Ala Ser Ile His Asp Thr Val Glu Asp Leu Ile Ile Leu Ala
145 150 155 160
Asn Asn Ser Leu Ser Ser Asn Gly Asn Val Thr Glu Ser Gly Cys Lys
165 170 175
Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser
180 185 190
Phe Val His Ile Val Gln Met Phe Ile Asn Thr Ser Glu Pro Lys Ser
195 200 205
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
210 215 220
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
225 230 235 240
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
245 250 255
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
260 265 270
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
275 280 285
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
290 295 300
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
305 310 315 320
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
325 330 335
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
340 345 350
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
355 360 365
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
370 375 380
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
385 390 395 400
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
405 410 415
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
420 425 430
Pro Gly Lys
435
<210> 307
<211> 65
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 307
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg
65
<210> 308
<211> 114
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 308
Asn Trp Val Asp Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asp Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 309
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 309
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
130 135 140
Asn Gln Val Ser Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 310
<211> 450
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 310
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Ala
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Ser Thr Lys Ala Asn Asn His Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Ser
65 70 75 80
Val Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Thr Arg Leu Ala Thr Trp Asp Trp Tyr Phe Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn Gln Val Lys Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 311
<211> 121
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 311
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Ala
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Ser Thr Lys Ala Asn Asn His Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Ser
65 70 75 80
Val Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Thr Arg Leu Ala Thr Trp Asp Trp Tyr Phe Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 312
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 312
Asp Ala Trp Met Ser
1 5
<210> 313
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 313
Glu Ile Ser Thr Lys Ala Asn Asn His Ala Thr Tyr Tyr Ala Glu Ser
1 5 10 15
Val Lys Gly
<210> 314
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 314
Leu Ala Thr Trp Asp Trp Tyr Phe Asp Val
1 5 10
<210> 315
<211> 218
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 315
Asp Ile Val Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Val Asp Tyr Asp
20 25 30
Gly Asp Ser Tyr Met Asn Trp Tyr Gln Gln Lys Pro Gly Lys Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Glu Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Asp Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 316
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 316
Asp Ile Val Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Val Asp Tyr Asp
20 25 30
Gly Asp Ser Tyr Met Asn Trp Tyr Gln Gln Lys Pro Gly Lys Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Glu Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Asp Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 317
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 317
Arg Ala Ser Gln Ser Val Asp Tyr Asp Gly Asp Ser Tyr Met Asn
1 5 10 15
<210> 318
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 318
Ala Ala Ser Glu Leu Glu Ser
1 5
<210> 319
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 319
Gln Gln Ser Asn Glu Asp Pro Phe Thr
1 5
<210> 320
<211> 435
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 320
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
65 70 75 80
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asn Trp Val Asp Val Ile
85 90 95
Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile Gln Ser Met His Ile Asp
100 105 110
Ala Thr Leu Tyr Thr Glu Ser Asp Val His Pro Ser Cys Lys Val Thr
115 120 125
Ala Met Lys Cys Phe Leu Leu Glu Leu Gln Val Ile Ser Leu Glu Ser
130 135 140
Gly Asp Ala Ser Ile His Asp Thr Val Glu Asp Leu Ile Ile Leu Ala
145 150 155 160
Asn Asn Ser Leu Ser Ser Asn Gly Asn Val Thr Glu Ser Gly Cys Lys
165 170 175
Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser
180 185 190
Phe Val His Ile Val Gln Met Phe Ile Asn Thr Ser Glu Pro Lys Ser
195 200 205
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
210 215 220
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
225 230 235 240
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
245 250 255
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
260 265 270
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
275 280 285
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
290 295 300
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
305 310 315 320
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
325 330 335
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
340 345 350
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
355 360 365
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
370 375 380
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
385 390 395 400
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
405 410 415
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
420 425 430
Pro Gly Lys
435
<210> 321
<211> 447
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 321
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Phe Met His Trp Val Gln Gln Ala Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Pro Glu Leu Gly Asp Thr Glu Tyr Ala Pro Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Tyr Ala Arg Gly Val Tyr Gln Ala Leu Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Lys His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Glu Gln Met Thr Lys Asn Gln Val Lys Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 322
<211> 214
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 322
Asp Ile Gln Met Thr Gln Ser Pro Ala Phe Leu Ser Val Thr Pro Gly
1 5 10 15
Glu Lys Val Thr Ile Thr Cys Gln Ala Ser Gln Asp Ile Gly Asn Tyr
20 25 30
Leu Asn Trp Phe Gln Gln Lys Pro Gly Gln Thr Val Lys Leu Leu Ile
35 40 45
Tyr Phe Thr Ser Tyr Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Phe Thr Ile Ser Ser Leu Glu Ala
65 70 75 80
Glu Asp Ala Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 323
<211> 442
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 323
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Asp Cys Lys Ala Ser Gly Ile Thr Phe Ser Asn Ser
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Lys Arg Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Thr Asn Asp Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
100 105 110
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
115 120 125
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
130 135 140
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
145 150 155 160
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
165 170 175
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
180 185 190
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
195 200 205
Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
210 215 220
Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro
225 230 235 240
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
245 250 255
Val Val Val Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp
260 265 270
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
275 280 285
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
290 295 300
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
305 310 315 320
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
325 330 335
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu
340 345 350
Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
355 360 365
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
370 375 380
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
385 390 395 400
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
405 410 415
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
420 425 430
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440
<210> 324
<211> 214
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 324
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Ser Asn Trp Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 325
<211> 435
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 325
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
65 70 75 80
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asn Trp Val Asp Val Ile
85 90 95
Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile Gln Ser Met His Ile Asp
100 105 110
Ala Thr Leu Tyr Thr Glu Ser Asp Val His Pro Ser Cys Lys Val Thr
115 120 125
Ala Met Lys Cys Phe Leu Leu Glu Leu Gln Val Ile Ser Leu Glu Ser
130 135 140
Gly Asp Ala Ser Ile His Asp Thr Val Glu Asp Leu Ile Ile Leu Ala
145 150 155 160
Asn Asn Ser Leu Ser Ser Asn Gly Asn Val Thr Glu Ser Gly Cys Lys
165 170 175
Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser
180 185 190
Phe Val His Ile Val Gln Met Phe Ile Asn Thr Ser Glu Pro Lys Ser
195 200 205
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
210 215 220
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
225 230 235 240
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
245 250 255
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
260 265 270
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
275 280 285
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
290 295 300
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
305 310 315 320
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
325 330 335
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
340 345 350
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
355 360 365
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
370 375 380
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
385 390 395 400
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Leu
405 410 415
His Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
420 425 430
Pro Gly Lys
435
<210> 326
<211> 450
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 326
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Ala
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Ser Thr Lys Ala Asn Asn His Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Ser
65 70 75 80
Val Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Thr Arg Leu Ala Thr Trp Asp Trp Tyr Phe Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn Gln Val Lys Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Leu His
420 425 430
Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 327
<211> 218
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 327
Asp Ile Val Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Val Asp Tyr Asp
20 25 30
Gly Asp Ser Tyr Met Asn Trp Tyr Gln Gln Lys Pro Gly Lys Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Glu Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Asp Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 328
<211> 435
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 328
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
65 70 75 80
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asn Trp Val Asp Val Ile
85 90 95
Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile Gln Ser Met His Ile Asp
100 105 110
Ala Thr Leu Tyr Thr Glu Ser Asp Val His Pro Ser Cys Lys Val Thr
115 120 125
Ala Met Lys Cys Phe Leu Leu Glu Leu Gln Val Ile Ser Leu Glu Ser
130 135 140
Gly Asp Ala Ser Ile His Asp Thr Val Glu Asp Leu Ile Ile Leu Ala
145 150 155 160
Asn Asn Ser Leu Ser Ser Asn Gly Asn Val Thr Glu Ser Gly Cys Lys
165 170 175
Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser
180 185 190
Phe Val His Ile Val Gln Met Phe Ile Asn Thr Ser Glu Pro Lys Ser
195 200 205
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
210 215 220
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
225 230 235 240
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
245 250 255
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
260 265 270
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
275 280 285
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
290 295 300
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
305 310 315 320
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
325 330 335
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
340 345 350
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
355 360 365
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
370 375 380
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
385 390 395 400
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Leu
405 410 415
His Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
420 425 430
Pro Gly Lys
435
<210> 329
<211> 447
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 329
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Phe Met His Trp Val Gln Gln Ala Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Pro Glu Leu Gly Asp Thr Glu Tyr Ala Pro Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Tyr Ala Arg Gly Val Tyr Gln Ala Leu Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Lys His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Glu Gln Met Thr Lys Asn Gln Val Lys Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Leu His Glu Ala Leu
420 425 430
His Ser His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 330
<211> 214
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 330
Asp Ile Gln Met Thr Gln Ser Pro Ala Phe Leu Ser Val Thr Pro Gly
1 5 10 15
Glu Lys Val Thr Ile Thr Cys Gln Ala Ser Gln Asp Ile Gly Asn Tyr
20 25 30
Leu Asn Trp Phe Gln Gln Lys Pro Gly Gln Thr Val Lys Leu Leu Ile
35 40 45
Tyr Phe Thr Ser Tyr Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Phe Thr Ile Ser Ser Leu Glu Ala
65 70 75 80
Glu Asp Ala Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 331
<211> 350
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 331
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser Ser Asp Lys Thr His
115 120 125
Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe
130 135 140
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
145 150 155 160
Glu Val Thr Cys Val Val Val Asp Val Lys His Glu Asp Pro Glu Val
165 170 175
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
180 185 190
Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
195 200 205
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
210 215 220
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
225 230 235 240
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
245 250 255
Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Asp Val
260 265 270
Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asp Gly
275 280 285
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
290 295 300
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
305 310 315 320
Glu Gln Gly Asp Val Phe Ser Cys Ser Val Leu His Glu Ala Leu His
325 330 335
Ser His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
340 345 350
<210> 332
<211> 301
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 332
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Gly Gly Gly Gly Ser Glu Pro Lys Ser Ser Asp Lys Thr His Thr
65 70 75 80
Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu
85 90 95
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
100 105 110
Val Thr Cys Val Val Val Asp Val Lys His Glu Asp Pro Glu Val Lys
115 120 125
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
130 135 140
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
145 150 155 160
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
165 170 175
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
180 185 190
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
195 200 205
Arg Glu Gln Met Thr Lys Asn Gln Val Lys Leu Thr Cys Leu Val Lys
210 215 220
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
225 230 235 240
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
245 250 255
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
260 265 270
Gln Gly Asn Val Phe Ser Cys Ser Val Leu His Glu Ala Leu His Ser
275 280 285
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
290 295 300
<210> 333
<211> 350
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 333
Asn Trp Val Asp Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asp Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser Ser Asp Lys Thr His
115 120 125
Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe
130 135 140
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
145 150 155 160
Glu Val Thr Cys Val Val Val Asp Val Lys His Glu Asp Pro Glu Val
165 170 175
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
180 185 190
Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
195 200 205
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
210 215 220
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
225 230 235 240
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
245 250 255
Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Asp Val
260 265 270
Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asp Gly
275 280 285
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
290 295 300
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
305 310 315 320
Glu Gln Gly Asp Val Phe Ser Cys Ser Val Leu His Glu Ala Leu His
325 330 335
Ser His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
340 345 350
<210> 334
<211> 301
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 334
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Gly Gly Gly Gly Ser Glu Pro Lys Ser Ser Asp Lys Thr His Thr
65 70 75 80
Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu
85 90 95
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
100 105 110
Val Thr Cys Val Val Val Asp Val Lys His Glu Asp Pro Glu Val Lys
115 120 125
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
130 135 140
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
145 150 155 160
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
165 170 175
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
180 185 190
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
195 200 205
Arg Glu Gln Met Thr Lys Asn Gln Val Lys Leu Thr Cys Leu Val Lys
210 215 220
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
225 230 235 240
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
245 250 255
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
260 265 270
Gln Gly Asn Val Phe Ser Cys Ser Val Leu His Glu Ala Leu His Ser
275 280 285
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
290 295 300
<210> 335
<211> 435
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 335
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
65 70 75 80
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asn Trp Val Asp Val Ile
85 90 95
Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile Gln Ser Met His Ile Asp
100 105 110
Ala Thr Leu Tyr Thr Glu Ser Asp Val His Pro Ser Cys Lys Val Thr
115 120 125
Ala Met Lys Cys Phe Leu Leu Glu Leu Gln Val Ile Ser Leu Glu Ser
130 135 140
Gly Asp Ala Ser Ile His Asp Thr Val Glu Asp Leu Ile Ile Leu Ala
145 150 155 160
Asn Asn Ser Leu Ser Ser Asn Gly Asn Val Thr Glu Ser Gly Cys Lys
165 170 175
Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser
180 185 190
Phe Val His Ile Val Gln Met Phe Ile Asn Thr Ser Glu Pro Lys Ser
195 200 205
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
210 215 220
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
225 230 235 240
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
245 250 255
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
260 265 270
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
275 280 285
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
290 295 300
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
305 310 315 320
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
325 330 335
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
340 345 350
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
355 360 365
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
370 375 380
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
385 390 395 400
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Leu
405 410 415
His Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
420 425 430
Pro Gly Lys
435
<210> 336
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 336
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys
130 135 140
Asn Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Leu His Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 337
<211> 350
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 337
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asn Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Gln
50 55 60
Asp Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser Ser Asp Lys Thr His
115 120 125
Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe
130 135 140
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
145 150 155 160
Glu Val Thr Cys Val Val Val Asp Val Lys His Glu Asp Pro Glu Val
165 170 175
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
180 185 190
Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
195 200 205
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
210 215 220
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
225 230 235 240
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
245 250 255
Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Asp Val
260 265 270
Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asp Gly
275 280 285
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
290 295 300
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
305 310 315 320
Glu Gln Gly Asp Val Phe Ser Cys Ser Val Leu His Glu Ala Leu His
325 330 335
Ser His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
340 345 350
<210> 338
<211> 301
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 338
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Gly Gly Gly Gly Ser Glu Pro Lys Ser Ser Asp Lys Thr His Thr
65 70 75 80
Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu
85 90 95
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
100 105 110
Val Thr Cys Val Val Val Asp Val Lys His Glu Asp Pro Glu Val Lys
115 120 125
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
130 135 140
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
145 150 155 160
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
165 170 175
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
180 185 190
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
195 200 205
Arg Glu Gln Met Thr Lys Asn Gln Val Lys Leu Thr Cys Leu Val Lys
210 215 220
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
225 230 235 240
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
245 250 255
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
260 265 270
Gln Gly Asn Val Phe Ser Cys Ser Val Leu His Glu Ala Leu His Ser
275 280 285
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
290 295 300
<210> 339
<211> 435
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 339
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
65 70 75 80
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asn Trp Val Asn Val Ile
85 90 95
Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile Gln Ser Met His Ile Asp
100 105 110
Ala Thr Leu Tyr Thr Glu Ser Asp Val His Pro Ser Cys Lys Val Thr
115 120 125
Ala Met Lys Cys Phe Leu Leu Glu Leu Gln Val Ile Ser Leu Glu Ser
130 135 140
Gly Asp Ala Ser Ile His Asp Thr Val Glu Asn Leu Ile Ile Leu Ala
145 150 155 160
Asn Asn Ser Leu Ser Ser Asn Gly Asn Val Thr Glu Ser Gly Cys Lys
165 170 175
Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser
180 185 190
Phe Val His Ile Val Gln Met Phe Ile Asn Thr Ser Glu Pro Lys Ser
195 200 205
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
210 215 220
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
225 230 235 240
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
245 250 255
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
260 265 270
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
275 280 285
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
290 295 300
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
305 310 315 320
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
325 330 335
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
340 345 350
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
355 360 365
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
370 375 380
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
385 390 395 400
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
405 410 415
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
420 425 430
Pro Gly Lys
435
<210> 340
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 340
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys
130 135 140
Asn Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 341
<211> 435
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 341
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
65 70 75 80
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asn Trp Val Asp Val Ile
85 90 95
Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile Gln Ser Met His Ile Asp
100 105 110
Ala Thr Leu Tyr Thr Glu Ser Asp Val His Pro Ser Cys Lys Val Thr
115 120 125
Ala Met Lys Cys Phe Leu Leu Glu Leu Gln Val Ile Ser Leu Glu Ser
130 135 140
Gly Asp Ala Ser Ile His Asp Thr Val Glu Asp Leu Ile Ile Leu Ala
145 150 155 160
Asn Asn Ser Leu Ser Ser Asn Gly Asn Val Thr Glu Ser Gly Cys Lys
165 170 175
Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser
180 185 190
Phe Val His Ile Val Gln Met Phe Ile Asn Thr Ser Glu Pro Lys Ser
195 200 205
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
210 215 220
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
225 230 235 240
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
245 250 255
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
260 265 270
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
275 280 285
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
290 295 300
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
305 310 315 320
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
325 330 335
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
340 345 350
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
355 360 365
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
370 375 380
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
385 390 395 400
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
405 410 415
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
420 425 430
Pro Gly Lys
435
<210> 342
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 342
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys
130 135 140
Asn Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 343
<211> 435
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 343
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
65 70 75 80
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asn Trp Val Asn Val Ile
85 90 95
Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile Gln Ser Met His Ile Asp
100 105 110
Ala Thr Leu Tyr Thr Glu Ser Asn Val His Pro Ser Cys Lys Val Thr
115 120 125
Ala Met Lys Cys Phe Leu Leu Glu Leu Gln Val Ile Ser Leu Glu Ser
130 135 140
Gly Asp Ala Ser Ile His Asp Thr Val Glu Asn Leu Ile Ile Leu Ala
145 150 155 160
Asn Asn Ser Leu Ser Ser Asn Gly Asn Val Thr Glu Ser Gly Cys Lys
165 170 175
Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser
180 185 190
Phe Val His Ile Val Gln Met Phe Ile Asn Thr Ser Glu Pro Lys Ser
195 200 205
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
210 215 220
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
225 230 235 240
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
245 250 255
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
260 265 270
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
275 280 285
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
290 295 300
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
305 310 315 320
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
325 330 335
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
340 345 350
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
355 360 365
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
370 375 380
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
385 390 395 400
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
405 410 415
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
420 425 430
Pro Gly Lys
435
<210> 344
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 344
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys
130 135 140
Asn Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 345
<211> 435
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 345
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
65 70 75 80
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asn Trp Val Asn Val Ile
85 90 95
Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile Gln Ser Met His Ile Asp
100 105 110
Ala Thr Leu Tyr Thr Glu Ser Asn Val His Pro Ser Cys Lys Val Thr
115 120 125
Ala Met Lys Cys Phe Leu Leu Glu Leu Gln Val Ile Ser Leu Glu Ser
130 135 140
Gly Asp Ala Ser Ile His Asp Thr Val Glu Asp Leu Ile Ile Leu Ala
145 150 155 160
Asn Asn Ser Leu Ser Ser Asn Gly Asn Val Thr Glu Ser Gly Cys Lys
165 170 175
Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser
180 185 190
Phe Val His Ile Val Gln Met Phe Ile Asn Thr Ser Glu Pro Lys Ser
195 200 205
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
210 215 220
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
225 230 235 240
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
245 250 255
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
260 265 270
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
275 280 285
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
290 295 300
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
305 310 315 320
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
325 330 335
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
340 345 350
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
355 360 365
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
370 375 380
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
385 390 395 400
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
405 410 415
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
420 425 430
Pro Gly Lys
435
<210> 346
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 346
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys
130 135 140
Asn Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 347
<211> 435
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 347
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
65 70 75 80
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asn Trp Val Asn Val Ile
85 90 95
Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile Gln Ser Met His Ile Asp
100 105 110
Ala Thr Leu Tyr Thr Glu Ser Asn Val His Pro Ser Cys Lys Val Thr
115 120 125
Ala Met Lys Cys Phe Leu Leu Glu Leu Gln Val Ile Ser Leu Glu Ser
130 135 140
Gly Asp Ala Ser Ile His Asp Thr Val Gln Asp Leu Ile Ile Leu Ala
145 150 155 160
Asn Asn Ser Leu Ser Ser Asn Gly Asn Val Thr Glu Ser Gly Cys Lys
165 170 175
Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser
180 185 190
Phe Val His Ile Val Gln Met Phe Ile Asn Thr Ser Glu Pro Lys Ser
195 200 205
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
210 215 220
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
225 230 235 240
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
245 250 255
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
260 265 270
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
275 280 285
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
290 295 300
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
305 310 315 320
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
325 330 335
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
340 345 350
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
355 360 365
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
370 375 380
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
385 390 395 400
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
405 410 415
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
420 425 430
Pro Gly Lys
435
<210> 348
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 348
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys
130 135 140
Asn Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 349
<211> 435
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 349
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
65 70 75 80
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asn Trp Val Asn Val Ile
85 90 95
Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile Gln Ser Met His Ile Asp
100 105 110
Ala Thr Leu Tyr Thr Glu Ser Asn Val His Pro Ser Cys Lys Val Thr
115 120 125
Ala Met Lys Cys Phe Leu Leu Glu Leu Gln Val Ile Ser Leu Glu Ser
130 135 140
Gly Asp Ala Ser Ile His Asp Thr Val Glu Asp Leu Ile Ile Leu Ala
145 150 155 160
Asn Asn Ser Leu Ser Ser Asn Gly Asn Val Thr Glu Ser Gly Cys Lys
165 170 175
Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser
180 185 190
Phe Val His Ile Val Gln Met Phe Ile Asn Thr Ser Glu Pro Lys Ser
195 200 205
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
210 215 220
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
225 230 235 240
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
245 250 255
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
260 265 270
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
275 280 285
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
290 295 300
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
305 310 315 320
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
325 330 335
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
340 345 350
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
355 360 365
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
370 375 380
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
385 390 395 400
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
405 410 415
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
420 425 430
Pro Gly Lys
435
<210> 350
<211> 450
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 350
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Ala
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Ser Thr Lys Ala Asn Asn His Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Ser
65 70 75 80
Val Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Thr Arg Leu Ala Thr Trp Asp Trp Tyr Phe Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn Gln Val Lys Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 351
<211> 218
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 351
Asp Ile Val Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Val Asp Tyr Asp
20 25 30
Gly Asp Ser Tyr Met Asn Trp Tyr Gln Gln Lys Pro Gly Lys Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Glu Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Asp Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 352
<211> 435
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 352
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
65 70 75 80
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asn Trp Val Asn Val Ile
85 90 95
Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile Gln Ser Met His Ile Asp
100 105 110
Ala Thr Leu Tyr Thr Glu Ser Asn Val His Pro Ser Cys Lys Val Thr
115 120 125
Ala Met Lys Cys Phe Leu Leu Glu Leu Gln Val Ile Ser Leu Glu Ser
130 135 140
Gly Asp Ala Ser Ile His Asp Thr Val Glu Asp Leu Ile Ile Leu Ala
145 150 155 160
Asn Asn Ser Leu Ser Ser Asn Gly Asn Val Thr Glu Ser Gly Cys Lys
165 170 175
Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser
180 185 190
Phe Val His Ile Val Gln Met Phe Ile Asn Thr Ser Glu Pro Lys Ser
195 200 205
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
210 215 220
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
225 230 235 240
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
245 250 255
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
260 265 270
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
275 280 285
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
290 295 300
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
305 310 315 320
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
325 330 335
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
340 345 350
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
355 360 365
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
370 375 380
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
385 390 395 400
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
405 410 415
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
420 425 430
Pro Gly Lys
435
<210> 353
<211> 447
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 353
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Phe Met His Trp Val Gln Gln Ala Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Pro Glu Leu Gly Asp Thr Glu Tyr Ala Pro Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Tyr Ala Arg Gly Val Tyr Gln Ala Leu Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Lys His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Glu Gln Met Thr Lys Asn Gln Val Lys Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 354
<211> 214
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 354
Asp Ile Gln Met Thr Gln Ser Pro Ala Phe Leu Ser Val Thr Pro Gly
1 5 10 15
Glu Lys Val Thr Ile Thr Cys Gln Ala Ser Gln Asp Ile Gly Asn Tyr
20 25 30
Leu Asn Trp Phe Gln Gln Lys Pro Gly Gln Thr Val Lys Leu Leu Ile
35 40 45
Tyr Phe Thr Ser Tyr Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Phe Thr Ile Ser Ser Leu Glu Ala
65 70 75 80
Glu Asp Ala Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 355
<211> 435
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 355
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
65 70 75 80
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asn Trp Val Asn Val Ile
85 90 95
Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile Gln Ser Met His Ile Asp
100 105 110
Ala Thr Leu Tyr Thr Glu Ser Asn Val His Pro Ser Cys Lys Val Thr
115 120 125
Ala Met Lys Cys Phe Leu Leu Glu Leu Gln Val Ile Ser Leu Glu Ser
130 135 140
Gly Asp Ala Ser Ile His Asp Thr Val Gln Asp Leu Ile Ile Leu Ala
145 150 155 160
Asn Asn Ser Leu Ser Ser Asn Gly Asn Val Thr Glu Ser Gly Cys Lys
165 170 175
Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser
180 185 190
Phe Val His Ile Val Gln Met Phe Ile Asn Thr Ser Glu Pro Lys Ser
195 200 205
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
210 215 220
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
225 230 235 240
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
245 250 255
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
260 265 270
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
275 280 285
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
290 295 300
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
305 310 315 320
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
325 330 335
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
340 345 350
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
355 360 365
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
370 375 380
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
385 390 395 400
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
405 410 415
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
420 425 430
Pro Gly Lys
435
<210> 356
<211> 450
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 356
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Ala
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Ser Thr Lys Ala Asn Asn His Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Ser
65 70 75 80
Val Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Thr Arg Leu Ala Thr Trp Asp Trp Tyr Phe Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn Gln Val Lys Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 357
<211> 218
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 357
Asp Ile Val Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Val Asp Tyr Asp
20 25 30
Gly Asp Ser Tyr Met Asn Trp Tyr Gln Gln Lys Pro Gly Lys Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Glu Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Asp Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 358
<211> 435
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 358
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
65 70 75 80
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asn Trp Val Asn Val Ile
85 90 95
Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile Gln Ser Met His Ile Asp
100 105 110
Ala Thr Leu Tyr Thr Glu Ser Asn Val His Pro Ser Cys Lys Val Thr
115 120 125
Ala Met Lys Cys Phe Leu Leu Glu Leu Gln Val Ile Ser Leu Glu Ser
130 135 140
Gly Asp Ala Ser Ile His Asp Thr Val Gln Asp Leu Ile Ile Leu Ala
145 150 155 160
Asn Asn Ser Leu Ser Ser Asn Gly Asn Val Thr Glu Ser Gly Cys Lys
165 170 175
Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser
180 185 190
Phe Val His Ile Val Gln Met Phe Ile Asn Thr Ser Glu Pro Lys Ser
195 200 205
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
210 215 220
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
225 230 235 240
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
245 250 255
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
260 265 270
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
275 280 285
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
290 295 300
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
305 310 315 320
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
325 330 335
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
340 345 350
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
355 360 365
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
370 375 380
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
385 390 395 400
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
405 410 415
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
420 425 430
Pro Gly Lys
435
<210> 359
<211> 447
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 359
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Phe Met His Trp Val Gln Gln Ala Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Pro Glu Leu Gly Asp Thr Glu Tyr Ala Pro Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Tyr Ala Arg Gly Val Tyr Gln Ala Leu Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Lys His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Glu Gln Met Thr Lys Asn Gln Val Lys Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 360
<211> 214
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 360
Asp Ile Gln Met Thr Gln Ser Pro Ala Phe Leu Ser Val Thr Pro Gly
1 5 10 15
Glu Lys Val Thr Ile Thr Cys Gln Ala Ser Gln Asp Ile Gly Asn Tyr
20 25 30
Leu Asn Trp Phe Gln Gln Lys Pro Gly Gln Thr Val Lys Leu Leu Ile
35 40 45
Tyr Phe Thr Ser Tyr Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Phe Thr Ile Ser Ser Leu Glu Ala
65 70 75 80
Glu Asp Ala Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 361
<211> 435
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 361
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
65 70 75 80
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asn Trp Val Asn Val Ile
85 90 95
Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile Gln Ser Met His Ile Asp
100 105 110
Ala Thr Leu Tyr Thr Glu Ser Asn Val His Pro Ser Cys Lys Val Thr
115 120 125
Ala Met Lys Cys Phe Leu Leu Glu Leu Gln Val Ile Ser Leu Glu Ser
130 135 140
Gly Asp Ala Ser Ile His Asp Thr Val Glu Asp Leu Ile Ile Leu Ala
145 150 155 160
Asn Asn Ser Leu Ser Ser Asn Gly Asn Val Thr Glu Ser Gly Cys Lys
165 170 175
Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser
180 185 190
Phe Val His Ile Val Gln Met Phe Ile Asn Thr Ser Glu Pro Lys Ser
195 200 205
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
210 215 220
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
225 230 235 240
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
245 250 255
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
260 265 270
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
275 280 285
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
290 295 300
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
305 310 315 320
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
325 330 335
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
340 345 350
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
355 360 365
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
370 375 380
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
385 390 395 400
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Leu
405 410 415
His Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
420 425 430
Pro Gly Lys
435
<210> 362
<211> 450
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 362
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Ala
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Ser Thr Lys Ala Asn Asn His Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Ser
65 70 75 80
Val Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Thr Arg Leu Ala Thr Trp Asp Trp Tyr Phe Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn Gln Val Lys Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Leu His
420 425 430
Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 363
<211> 218
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 363
Asp Ile Val Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Val Asp Tyr Asp
20 25 30
Gly Asp Ser Tyr Met Asn Trp Tyr Gln Gln Lys Pro Gly Lys Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Glu Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Asp Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 364
<211> 435
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 364
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
65 70 75 80
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asn Trp Val Asn Val Ile
85 90 95
Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile Gln Ser Met His Ile Asp
100 105 110
Ala Thr Leu Tyr Thr Glu Ser Asn Val His Pro Ser Cys Lys Val Thr
115 120 125
Ala Met Lys Cys Phe Leu Leu Glu Leu Gln Val Ile Ser Leu Glu Ser
130 135 140
Gly Asp Ala Ser Ile His Asp Thr Val Glu Asp Leu Ile Ile Leu Ala
145 150 155 160
Asn Asn Ser Leu Ser Ser Asn Gly Asn Val Thr Glu Ser Gly Cys Lys
165 170 175
Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser
180 185 190
Phe Val His Ile Val Gln Met Phe Ile Asn Thr Ser Glu Pro Lys Ser
195 200 205
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
210 215 220
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
225 230 235 240
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
245 250 255
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
260 265 270
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
275 280 285
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
290 295 300
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
305 310 315 320
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
325 330 335
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
340 345 350
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
355 360 365
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
370 375 380
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
385 390 395 400
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Leu
405 410 415
His Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
420 425 430
Pro Gly Lys
435
<210> 365
<211> 447
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 365
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Phe Met His Trp Val Gln Gln Ala Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Pro Glu Leu Gly Asp Thr Glu Tyr Ala Pro Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Tyr Ala Arg Gly Val Tyr Gln Ala Leu Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Lys His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Glu Gln Met Thr Lys Asn Gln Val Lys Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Leu His Glu Ala Leu
420 425 430
His Ser His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 366
<211> 214
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 366
Asp Ile Gln Met Thr Gln Ser Pro Ala Phe Leu Ser Val Thr Pro Gly
1 5 10 15
Glu Lys Val Thr Ile Thr Cys Gln Ala Ser Gln Asp Ile Gly Asn Tyr
20 25 30
Leu Asn Trp Phe Gln Gln Lys Pro Gly Gln Thr Val Lys Leu Leu Ile
35 40 45
Tyr Phe Thr Ser Tyr Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Phe Thr Ile Ser Ser Leu Glu Ala
65 70 75 80
Glu Asp Ala Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 367
<211> 435
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 367
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
65 70 75 80
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asn Trp Val Asn Val Ile
85 90 95
Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile Gln Ser Met His Ile Asp
100 105 110
Ala Thr Leu Tyr Thr Glu Ser Asn Val His Pro Ser Cys Lys Val Thr
115 120 125
Ala Met Lys Cys Phe Leu Leu Glu Leu Gln Val Ile Ser Leu Glu Ser
130 135 140
Gly Asp Ala Ser Ile His Asp Thr Val Gln Asp Leu Ile Ile Leu Ala
145 150 155 160
Asn Asn Ser Leu Ser Ser Asn Gly Asn Val Thr Glu Ser Gly Cys Lys
165 170 175
Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser
180 185 190
Phe Val His Ile Val Gln Met Phe Ile Asn Thr Ser Glu Pro Lys Ser
195 200 205
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
210 215 220
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
225 230 235 240
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
245 250 255
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
260 265 270
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
275 280 285
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
290 295 300
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
305 310 315 320
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
325 330 335
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
340 345 350
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
355 360 365
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
370 375 380
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
385 390 395 400
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Leu
405 410 415
His Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
420 425 430
Pro Gly Lys
435
<210> 368
<211> 450
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 368
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Ala
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Ser Thr Lys Ala Asn Asn His Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Ser
65 70 75 80
Val Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Thr Arg Leu Ala Thr Trp Asp Trp Tyr Phe Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn Gln Val Lys Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Leu His
420 425 430
Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 369
<211> 218
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 369
Asp Ile Val Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Val Asp Tyr Asp
20 25 30
Gly Asp Ser Tyr Met Asn Trp Tyr Gln Gln Lys Pro Gly Lys Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Glu Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Asp Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 370
<211> 435
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 370
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
65 70 75 80
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asn Trp Val Asn Val Ile
85 90 95
Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile Gln Ser Met His Ile Asp
100 105 110
Ala Thr Leu Tyr Thr Glu Ser Asn Val His Pro Ser Cys Lys Val Thr
115 120 125
Ala Met Lys Cys Phe Leu Leu Glu Leu Gln Val Ile Ser Leu Glu Ser
130 135 140
Gly Asp Ala Ser Ile His Asp Thr Val Gln Asp Leu Ile Ile Leu Ala
145 150 155 160
Asn Asn Ser Leu Ser Ser Asn Gly Asn Val Thr Glu Ser Gly Cys Lys
165 170 175
Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser
180 185 190
Phe Val His Ile Val Gln Met Phe Ile Asn Thr Ser Glu Pro Lys Ser
195 200 205
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
210 215 220
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
225 230 235 240
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
245 250 255
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
260 265 270
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
275 280 285
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
290 295 300
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
305 310 315 320
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
325 330 335
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
340 345 350
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
355 360 365
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
370 375 380
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
385 390 395 400
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Leu
405 410 415
His Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
420 425 430
Pro Gly Lys
435
<210> 371
<211> 447
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 371
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Phe Met His Trp Val Gln Gln Ala Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Pro Glu Leu Gly Asp Thr Glu Tyr Ala Pro Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Tyr Ala Arg Gly Val Tyr Gln Ala Leu Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Lys His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Glu Gln Met Thr Lys Asn Gln Val Lys Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Leu His Glu Ala Leu
420 425 430
His Ser His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 372
<211> 214
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 372
Asp Ile Gln Met Thr Gln Ser Pro Ala Phe Leu Ser Val Thr Pro Gly
1 5 10 15
Glu Lys Val Thr Ile Thr Cys Gln Ala Ser Gln Asp Ile Gly Asn Tyr
20 25 30
Leu Asn Trp Phe Gln Gln Lys Pro Gly Gln Thr Val Lys Leu Leu Ile
35 40 45
Tyr Phe Thr Ser Tyr Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Phe Thr Ile Ser Ser Leu Glu Ala
65 70 75 80
Glu Asp Ala Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 373
<211> 435
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 373
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
65 70 75 80
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asn Trp Val Asp Val Ile
85 90 95
Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile Gln Ser Met His Ile Asp
100 105 110
Ala Thr Leu Tyr Thr Glu Ser Asp Val His Pro Ser Cys Lys Val Thr
115 120 125
Ala Met Lys Cys Phe Leu Leu Glu Leu Gln Val Ile Ser Leu Glu Ser
130 135 140
Gly Asp Ala Ser Ile His Asp Thr Val Glu Asp Leu Ile Ile Leu Ala
145 150 155 160
Asn Asn Ser Leu Ser Ser Asn Gly Asn Val Thr Glu Ser Gly Cys Lys
165 170 175
Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser
180 185 190
Phe Val His Ile Val Gln Met Phe Ile Asn Thr Ser Glu Pro Lys Ser
195 200 205
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
210 215 220
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
225 230 235 240
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
245 250 255
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
260 265 270
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
275 280 285
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
290 295 300
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
305 310 315 320
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
325 330 335
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
340 345 350
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
355 360 365
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
370 375 380
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
385 390 395 400
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
405 410 415
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
420 425 430
Pro Gly Lys
435
<210> 374
<211> 449
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 374
Gln Val Thr Leu Arg Glu Ser Gly Pro Ala Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Ser Thr Ala
20 25 30
Gly Met Ser Val Gly Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu
35 40 45
Trp Leu Ala Asp Ile Trp Trp Asp Asp Lys Lys His Tyr Asn Pro Ser
50 55 60
Leu Lys Asp Arg Leu Thr Ile Ser Lys Asp Thr Ser Lys Asn Gln Val
65 70 75 80
Val Leu Lys Val Thr Asn Met Asp Pro Ala Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Ala Arg Asp Met Ile Phe Asn Phe Tyr Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn Gln Val Lys Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 375
<211> 213
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 375
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Ala Ser Ser Arg Val Gly Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp
65 70 75 80
Asp Phe Ala Thr Tyr Tyr Cys Phe Gln Gly Ser Gly Tyr Pro Phe Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 376
<211> 435
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 376
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
65 70 75 80
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asn Trp Val Asn Val Ile
85 90 95
Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile Gln Ser Met His Ile Asp
100 105 110
Ala Thr Leu Tyr Thr Glu Ser Asn Val His Pro Ser Cys Lys Val Thr
115 120 125
Ala Met Lys Cys Phe Leu Leu Glu Leu Gln Val Ile Ser Leu Glu Ser
130 135 140
Gly Asp Ala Ser Ile His Asp Thr Val Glu Asp Leu Ile Ile Leu Ala
145 150 155 160
Asn Asn Ser Leu Ser Ser Asn Gly Asn Val Thr Glu Ser Gly Cys Lys
165 170 175
Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser
180 185 190
Phe Val His Ile Val Gln Met Phe Ile Asn Thr Ser Glu Pro Lys Ser
195 200 205
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
210 215 220
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
225 230 235 240
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
245 250 255
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
260 265 270
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
275 280 285
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
290 295 300
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
305 310 315 320
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
325 330 335
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
340 345 350
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
355 360 365
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
370 375 380
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
385 390 395 400
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
405 410 415
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
420 425 430
Pro Gly Lys
435
<210> 377
<211> 449
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 377
Gln Val Thr Leu Arg Glu Ser Gly Pro Ala Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Ser Thr Ala
20 25 30
Gly Met Ser Val Gly Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu
35 40 45
Trp Leu Ala Asp Ile Trp Trp Asp Asp Lys Lys His Tyr Asn Pro Ser
50 55 60
Leu Lys Asp Arg Leu Thr Ile Ser Lys Asp Thr Ser Lys Asn Gln Val
65 70 75 80
Val Leu Lys Val Thr Asn Met Asp Pro Ala Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Ala Arg Asp Met Ile Phe Asn Phe Tyr Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn Gln Val Lys Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 378
<211> 213
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 378
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Ala Ser Ser Arg Val Gly Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp
65 70 75 80
Asp Phe Ala Thr Tyr Tyr Cys Phe Gln Gly Ser Gly Tyr Pro Phe Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 379
<211> 435
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 379
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
65 70 75 80
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asn Trp Val Asn Val Ile
85 90 95
Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile Gln Ser Met His Ile Asp
100 105 110
Ala Thr Leu Tyr Thr Glu Ser Asn Val His Pro Ser Cys Lys Val Thr
115 120 125
Ala Met Lys Cys Phe Leu Leu Glu Leu Gln Val Ile Ser Leu Glu Ser
130 135 140
Gly Asp Ala Ser Ile His Asp Thr Val Gln Asp Leu Ile Ile Leu Ala
145 150 155 160
Asn Asn Ser Leu Ser Ser Asn Gly Asn Val Thr Glu Ser Gly Cys Lys
165 170 175
Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser
180 185 190
Phe Val His Ile Val Gln Met Phe Ile Asn Thr Ser Glu Pro Lys Ser
195 200 205
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
210 215 220
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
225 230 235 240
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
245 250 255
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
260 265 270
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
275 280 285
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
290 295 300
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
305 310 315 320
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
325 330 335
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
340 345 350
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
355 360 365
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
370 375 380
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
385 390 395 400
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
405 410 415
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
420 425 430
Pro Gly Lys
435
<210> 380
<211> 449
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 380
Gln Val Thr Leu Arg Glu Ser Gly Pro Ala Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Ser Thr Ala
20 25 30
Gly Met Ser Val Gly Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu
35 40 45
Trp Leu Ala Asp Ile Trp Trp Asp Asp Lys Lys His Tyr Asn Pro Ser
50 55 60
Leu Lys Asp Arg Leu Thr Ile Ser Lys Asp Thr Ser Lys Asn Gln Val
65 70 75 80
Val Leu Lys Val Thr Asn Met Asp Pro Ala Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Ala Arg Asp Met Ile Phe Asn Phe Tyr Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn Gln Val Lys Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 381
<211> 213
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 381
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Ala Ser Ser Arg Val Gly Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp
65 70 75 80
Asp Phe Ala Thr Tyr Tyr Cys Phe Gln Gly Ser Gly Tyr Pro Phe Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 382
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 382
Gly Ser Gly Gly Ser
1 5
<210> 383
<211> 4
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 383
Gly Gly Gly Ser
1
Claims (12)
- 이종이량체 융합 단백질로서,
a) 제1 단량체로서, N-말단에서 C-말단으로,
i) IL-15Rα(스시) 도메인;
ii) 제1 도메인 링커;
iii) IL-15 변이체;
iv) 힌지; 및
v) CH2-CH3을 포함하는 제1 변이체 Fc 도메인을 포함하는 제1 단량체;
b) N-말단에서 C-말단으로, VH-CH1-힌지-CH2-CH3을 포함하는 제2 단량체(여기서 CH2-CH3은 제2 변이체 Fc 도메인임); 및
c) VL-CL을 포함하는 제3 단량체를 포함하며,
여기서 VH 및 VL은, 각각, 인간 LAG-3 항원 결합 도메인을 형성하는 가변 중쇄 도메인 및 가변 경쇄 도메인이고,
제1 변이체 Fc 도메인은 비대칭(skew) 변이체 L368D/K370S를 포함하고, 제2 변이체 Fc 도메인은 비대칭 변이체 S364K/E357Q를 포함하고,
제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인은 각각 FcKO 변이체 E233P/L234V/L235A/G236del/S267K를 포함하고,
제1 변이체 Fc 도메인은 pI 변이체 Q295E/N384D/Q418E/N421D를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, 이종이량체 융합 단백질. - 제1항에 있어서, 상기 제1 단량체의 힌지가 아미노산 치환 C220S를 포함하며, 여기서 넘버링은 EU 넘버링에 따르는, 이종이량체 융합 단백질.
- 제1항 또는 제2항에 있어서, 상기 제1 변이체 Fc 도메인 및 제2 변이체 Fc 도메인이 각각 반감기 연장 변이체 M428:/N434S를 추가로 포함하는, 이종이량체 융합 단백질.
- 제1항 내지 제3항 중 어느 한 항에 있어서, 상기 IL-15 변이체가 N1D, N4D, D8N, D30N, D61N, E64Q, N65D, Q108E, N4D/N65D, D30N/N65D 및 D30N/E64Q/N65D로 이루어지는 군으로부터 선택되는 아미노산 치환(들)을 포함하는, 이종이량체 융합 단백질.
- 제4항에 있어서, 상기 IL-15 변이체가 아미노산 치환 N4D/N65D, D30N/N65D 또는 D30N/E64Q/N65D를 포함하는, 이종이량체 융합 단백질.
- 제1항 내지 제5항 중 어느 한 항에 있어서, 상기 VH 및 VL이 도 12 및 도 13의 임의의 LAG-3 항원 결합 도메인의 가변 중쇄 도메인 및 가변 경쇄 도메인인, 이종이량체 융합 단백질.
- 제6항에 있어서, 상기 LAG-3 항원 결합 도메인이 2A11_H1.144_L2.142 및 7G8_H3.30_L1.34로부터 선택되는, 이종이량체 융합 단백질.
- 제1항에 있어서, XENP27972, XENP27973, XENP27977, XENP27978, XENP029486, XENP029487, XENC1000, XENC1001, XENC1002, XENC1003, XENC1004 및 XENC1005로 이루어지는 군으로부터 선택되는, 이종이량체 융합 단백질.
- 핵산 조성물로서,
a) 제1항 내지 제8항 중 어느 한 항의 상기 제1 단량체를 인코딩하는 제1 핵산;
b) 제1항 내지 제8항 중 어느 한 항의 상기 제2 단량체를 인코딩하는 제2 핵산; 및
c) 제1항 내지 제8항 중 어느 한 항의 상기 제3 단량체를 인코딩하는 제3 핵산을 각각 포함하는 핵산 조성물. - 발현 벡터 조성물로서,
a) 제9항의 상기 제1 핵산을 포함하는 제1 발현 벡터;
b) 제9항의 상기 제2 핵산을 포함하는 제2 발현 벡터; 및
c) 제9항의 상기 제3 핵산을 포함하는 제3 발현 벡터를 포함하는 발현 벡터 조성물. - 제10항에 따른 발현 벡터 조성물을 포함하는 숙주세포.
- 제11항의 숙주세포를 배양하는 단계 및 세포 배양물로부터 이종이량체 융합 단백질을 회수하는 단계를 포함하는, 이종이량체 융합 단백질을 제조하는 방법.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201862659624P | 2018-04-18 | 2018-04-18 | |
| US62/659,624 | 2018-04-18 | ||
| US201862783107P | 2018-12-20 | 2018-12-20 | |
| US62/783,107 | 2018-12-20 | ||
| PCT/US2019/028180 WO2019204646A1 (en) | 2018-04-18 | 2019-04-18 | Lag-3 targeted heterodimeric fusion proteins containing il-15/il-15ra fc-fusion proteins and lag-3 antigen binding domains |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20210003813A true KR20210003813A (ko) | 2021-01-12 |
Family
ID=66429614
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020207033040A KR20210003813A (ko) | 2018-04-18 | 2019-04-18 | IL-15/IL-15Rα Fc-융합 단백질 및 LAG-3 항원 결합 도메인을 함유하는 LAG-3 표적화 이종이량체 융합 단백질 |
Country Status (9)
| Country | Link |
|---|---|
| US (2) | US20190352362A1 (ko) |
| EP (1) | EP3781597A1 (ko) |
| JP (1) | JP7366056B2 (ko) |
| KR (1) | KR20210003813A (ko) |
| CN (1) | CN113195534A (ko) |
| AU (1) | AU2019256520A1 (ko) |
| CA (1) | CA3097649A1 (ko) |
| IL (1) | IL278088A (ko) |
| WO (1) | WO2019204646A1 (ko) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| TW202128757A (zh) | 2019-10-11 | 2021-08-01 | 美商建南德克公司 | 具有改善之特性的 PD-1 標靶 IL-15/IL-15Rα FC 融合蛋白 |
| WO2021092719A1 (zh) * | 2019-11-11 | 2021-05-20 | 王盛典 | 一种靶向抗原特异性t细胞诱导其向记忆干性细胞分化的融合蛋白 |
| CN113135996A (zh) * | 2019-12-09 | 2021-07-20 | 启愈生物技术(上海)有限公司 | 一种双特异抗体及其应用 |
| KR102313505B1 (ko) * | 2020-06-30 | 2021-10-18 | (주)지아이이노베이션 | 항-lag-3 항체 및 il-2를 포함하는 융합단백질 및 이의 용도 |
| CA3206844A1 (en) * | 2021-02-05 | 2022-08-11 | John Li | Il-15 fusion proteins and methods of making and using same |
| CN115925967A (zh) * | 2021-04-22 | 2023-04-07 | 广东菲鹏制药股份有限公司 | 双特异性多功能融合多肽 |
| WO2023196905A1 (en) | 2022-04-07 | 2023-10-12 | Xencor, Inc. | Lag-3 targeted heterodimeric fusion proteins containing il-15/il-15ra fc-fusion proteins and lag-3 antigen binding domains |
| CN115806627A (zh) * | 2022-08-03 | 2023-03-17 | 深圳市先康达生命科学有限公司 | 一种自分泌IL-15与anti-LAG3结合的融合蛋白及其应用 |
Family Cites Families (25)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5731168A (en) | 1995-03-01 | 1998-03-24 | Genentech, Inc. | Method for making heteromultimeric polypeptides |
| EP0915987A2 (en) | 1997-04-21 | 1999-05-19 | Donlar Corporation | POLY-($g(a)-L-ASPARTIC ACID), POLY-($g(a)-L-GLUTAMIC ACID) AND COPOLYMERS OF L-ASP AND L-GLU, METHOD FOR THEIR PRODUCTION AND THEIR USE |
| US7449443B2 (en) | 2000-03-23 | 2008-11-11 | California Institute Of Technology | Method for stabilization of proteins using non-natural amino acids |
| US6586207B2 (en) | 2000-05-26 | 2003-07-01 | California Institute Of Technology | Overexpression of aminoacyl-tRNA synthetases for efficient production of engineered proteins containing amino acid analogues |
| WO2003073238A2 (en) | 2002-02-27 | 2003-09-04 | California Institute Of Technology | Computational method for designing enzymes for incorporation of amino acid analogs into proteins |
| EP2322569B1 (en) | 2003-10-09 | 2020-08-26 | Ambrx, Inc. | Polymer derivatives for the selective modification of proteins |
| CA2553040A1 (en) | 2004-02-02 | 2005-08-18 | Ambrx, Inc. | Modified human four helical bundle polypeptides and their uses |
| US20100226925A1 (en) * | 2007-09-14 | 2010-09-09 | Amgen Inc. | Homogeneous Antibody Populations |
| CA2806252C (en) | 2010-07-29 | 2019-05-14 | Xencor, Inc. | Antibodies with modified isoelectric points |
| KR102070098B1 (ko) * | 2010-09-21 | 2020-01-28 | 알토 바이오사이언스 코포레이션 | 다량체성 아이엘 15 용해성 융합 분자 및 그의 제조 및 사용 방법 |
| AU2011325833C1 (en) | 2010-11-05 | 2017-07-13 | Zymeworks Bc Inc. | Stable heterodimeric antibody design with mutations in the Fc domain |
| EA201892619A1 (ru) * | 2011-04-29 | 2019-04-30 | Роше Гликарт Аг | Иммуноконъюгаты, содержащие мутантные полипептиды интерлейкина-2 |
| US9605084B2 (en) | 2013-03-15 | 2017-03-28 | Xencor, Inc. | Heterodimeric proteins |
| EP3620473A1 (en) | 2013-01-14 | 2020-03-11 | Xencor, Inc. | Novel heterodimeric proteins |
| JP6594855B2 (ja) | 2013-03-15 | 2019-10-23 | ゼンコア インコーポレイテッド | ヘテロ二量体タンパク質 |
| AU2014232416B2 (en) * | 2013-03-15 | 2017-09-28 | Xencor, Inc. | Modulation of T Cells with Bispecific Antibodies and FC Fusions |
| MX2016001555A (es) * | 2013-08-08 | 2016-08-03 | Cytune Pharma | Modulocinas basadas en dominio sushi de interleucina-15 (il-15) y receptor alfa de interleucina-15 (il-15ra). |
| EP3093295B1 (en) * | 2014-01-08 | 2020-05-27 | Shanghai Hengrui Pharmaceutical Co., Ltd. | Il-15 heterogeneous dimer protein and uses thereof |
| CN111410691B (zh) | 2014-03-28 | 2024-02-13 | Xencor公司 | 结合至cd38和cd3的双特异性抗体 |
| RU2017119185A (ru) | 2014-11-05 | 2018-12-05 | Дженентек, Инк. | Антитела против fgfr2/3 и способы их применения |
| US10259887B2 (en) * | 2014-11-26 | 2019-04-16 | Xencor, Inc. | Heterodimeric antibodies that bind CD3 and tumor antigens |
| US10787518B2 (en) | 2016-06-14 | 2020-09-29 | Xencor, Inc. | Bispecific checkpoint inhibitor antibodies |
| WO2018045110A1 (en) * | 2016-08-30 | 2018-03-08 | Xencor, Inc. | Bispecific immunomodulatory antibodies that bind costimulatory and checkpoint receptors |
| AU2017342560B2 (en) | 2016-10-14 | 2022-03-17 | Xencor, Inc. | IL15/IL15Ralpha heterodimeric Fc-fusion proteins |
| JP2020529832A (ja) * | 2017-06-30 | 2020-10-15 | ゼンコア インコーポレイテッド | IL−15/IL−15Rαおよび抗原結合ドメインを含む標的化ヘテロダイマーFc融合タンパク質 |
-
2019
- 2019-04-18 WO PCT/US2019/028180 patent/WO2019204646A1/en unknown
- 2019-04-18 KR KR1020207033040A patent/KR20210003813A/ko active Search and Examination
- 2019-04-18 CA CA3097649A patent/CA3097649A1/en active Pending
- 2019-04-18 US US16/388,646 patent/US20190352362A1/en not_active Abandoned
- 2019-04-18 CN CN201980032099.4A patent/CN113195534A/zh active Pending
- 2019-04-18 JP JP2020556942A patent/JP7366056B2/ja active Active
- 2019-04-18 AU AU2019256520A patent/AU2019256520A1/en active Pending
- 2019-04-18 EP EP19722389.4A patent/EP3781597A1/en active Pending
-
2020
- 2020-10-15 IL IL278088A patent/IL278088A/en unknown
-
2023
- 2023-04-28 US US18/309,303 patent/US20230279071A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| WO2019204646A9 (en) | 2019-11-28 |
| US20190352362A1 (en) | 2019-11-21 |
| EP3781597A1 (en) | 2021-02-24 |
| JP7366056B2 (ja) | 2023-10-20 |
| AU2019256520A1 (en) | 2020-11-26 |
| CN113195534A (zh) | 2021-07-30 |
| JP2021521779A (ja) | 2021-08-30 |
| IL278088A (en) | 2020-11-30 |
| WO2019204646A1 (en) | 2019-10-24 |
| US20230279071A1 (en) | 2023-09-07 |
| CA3097649A1 (en) | 2019-10-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11584794B2 (en) | Bispecific heterodimeric fusion proteins containing IL-15-IL-15Ralpha Fc-fusion proteins and immune checkpoint antibody fragments | |
| US11524991B2 (en) | PD-1 targeted heterodimeric fusion proteins containing IL-15/IL-15Ra Fc-fusion proteins and PD-1 antigen binding domains and uses thereof | |
| US20220073588A1 (en) | TARGETED HETERODIMERIC Fc FUSION PROTEINS CONTAINING IL-15 IL-15alpha AND ANTIGEN BINDING DOMAINS | |
| KR102523402B1 (ko) | 이중특이적 체크포인트 억제제 항체 | |
| US20230055445A1 (en) | Pd-1 targeted il-15/il-15ralpha fc fusion proteins and uses in combination therapies thereof | |
| US11505595B2 (en) | TIM-3 targeted heterodimeric fusion proteins containing IL-15/IL-15RA Fc-fusion proteins and TIM-3 antigen binding domains | |
| US20230279071A1 (en) | LAG-3 TARGETED HETERODIMERIC FUSION PROTEINS CONTAINING IL-15/IL-15RA Fc-FUSION PROTEINS AND LAG-3 ANTIGEN BINDING DOMAINS | |
| US12006345B2 (en) | Untargeted and targeted IL-10 Fc-fusion proteins | |
| US11932675B2 (en) | PD-1 targeted IL-15/IL-15Rα Fc fusion proteins with improved properties | |
| US20220227867A1 (en) | ICOS TARGETED HETERODIMERIC FUSION PROTEINS CONTAINING IL-15/IL-15RA Fc-FUSION PROTEINS AND ICOS ANTIGEN BINDING DOMAINS | |
| US20240025968A1 (en) | LAG-3 TARGETED HETERODIMERIC FUSION PROTEINS CONTAINING IL-15/IL-15RA Fc-FUSION PROTEINS AND LAG-3 ANTIGEN BINDING DOMAINS |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination |