본 발명은 링커 및 메디토프를 포함하는 자가-가교결합 메디토프-이용가능 재조합 항체 또는 이들의 항원 결합 단편을 제공한다. 본 발명의 링커는 메디토프-링커가 메디토프 활성화된 항체 또는 항원 결합의 상호 작용 또는 가교 결합을 용이하게 하는 항체 또는 이의 항원 결합 단편상의 위치에서, 메디토프가 부착된 항체에 존재하는 메디토프 결합 부위에 메디토프가 결합하는 것을 허용하지 않으면서, 메디토프 및 항체 또는 항원 결합 단편에 부착된다. 자가 가교-결합 항체 또는 이의 단편은 링커 및 메디토프를 통해 다른 메디토프-이용가능 항체와 복합체를 형성할 수 있다. 일 실시 양태에서, 상기 메디토프-이용가능 항체 또는 이의 항원 결합 단편은 세포 표면 상에 존재하는 하나 이상의 에피토프에 결합한다. 상술한 자가-가교결합 항체 또는 이의 항원 결합 단편의 복합체 형성은 이들 항체 또는 항원 결합 단편이 다수의 항체 또는 이의 항원 결합 단편이 결합하는 세포 표면 항원의 분포를 변경한다. 자가-가교결합 항체와 표적 항원 상의 동족 에피토프의 상호 작용을 통한 복합체 형성은 복합체의 내재화를 증가시키거나 촉진시킬 수 있는 세포 표면 항원의 클러스터링 또는 공동-편재화(co-localization)을 증가 또는 촉진시킬 수 있다. 다음으로, 증가된 내재화는 표적 세포의 표면으로부터 세포 표면 항원의 농도를 제거 또는 감소시키고 표적 세포로의 복합체의 내재화 속도를 증가시키는 데 사용될 수 있다. 내재화 속도의 증가는 특정 치료법의 효능을 증가 시키거나 특정 치료 효과를 얻기 위해 필요한 약물의 양을 감소시킬 수 있다. 세포 표면 항원의 클러스터링을 증가시키거나 촉진시키는 방법은 세포-표면 항원에 특이적으로 결합하는 하나 이상의 자가 가교결합 항체를 세포에 투여함으로써 표적 세포의 표면상의 세포 표면 항원의 클러스터링을 촉진시키는 것을 포함할 수 있다. 특정 실시 양태에서, 자가-가교결합 항체는 하나 이상의 약제에 접합된다.
Ⅰ. 자가-가교결합 항체
자가-가교결합 메디토프-이용가능 항체 또는 이의 항원 결합 단편은 링커, 메디토프 및 메디토프-이용가능 항체 또는 이의 항원 결합 단편을 포함한다. 링커는 강성 세그먼트 및 가요성 세그먼트를 포함하며, 메디토프와 결합하도록 되어 있다.
본원발명의 링커는 이에 부착된 메디토프가 일반적으로 동일한 항체 내에 함유된 메디토프 결합 부위에 결합하지 않고, 다른 메디토프-이용가능 항체 또는 이의 항원 결합 단편상의 메디토프 결합 부위에 우선적으로 결합하도록 설계된다. 전형적으로 상기 링커는 아미노산과 같은 반복 단위로 구성되며, 조립시 상이한 구조적 특징을 포함할 수 있다. 예를 들어, 일부 실시 양태에서, 링커는 제한되거나 감소된 운동 범위를 갖는 강성 세그먼트를 포함한다. 일부 실시 양태에서, 상기 강성(rigidity)은 메디토프-이용가능 항체에 융합된 메디토프가 동일한 항체 또는 그의 항원 결합 단편상의 메디토프 결합 부위에 결합하는 것을 방지 또는 감소시킬 수 있다.
일부 실시 양태에서, 링커는 가요성(flexible) 및/또는 비구조적(unstructured) 세그먼트를 포함한다. 일부 실시양태에서, 가요성 및/또는 비구조적 세그먼트는 링커가 구부려지거나 회전 할 수 있도록 하여 메디토프가 다른 항체의 메디토프 결합 부위에 결합할 수 있게 한다.
일부 실시양태에서, 링커가 펩타이드 일 때, 강성 세그먼트는 전형적으로 구부리고 및/또는 회전하는 능력을 제한하기에 충분한 강성을 갖는 펩타이드를 제공하는 아미노산 서열을 포함한다. 일 실시 양태에서, 강성 세그먼트는 알파 나선형 구조를 갖는 펩타이드를 생산하는 아미노산 서열을 포함한다. 또 다른 실시 양태에서, 가요성 및/또는 비구조적 세그먼트는 가요성 영역이 구부러지거나 및/또는 회전할 수 있을 정도로 충분한 유연성을 갖는 펩타이드를 생산하는 아미노산 서열을 포함하여 메디토프가 메디토프 결합 부위에 결합하기에 충분한 유연성을 갖도록 한다.
A. 링커
본 발명은 자가-가교결합 메디토프-이용가능 항체 또는 항원 결합 단편의 일 구성요소인 링커를 제공한다. 본원에서 사용된 용어 "링커"는 메디토프가 활성화된 항체 또는 이의 항원 결합 단편을 포함하여 항체 또는 이의 항원 결합 단편에 메디토프가 연결되거나 연결된 구조를 나타낸다. 대표적인 링커는 펩타이드, 일부 실시양태에서 변형된 펩타이드 골격, 작은 화학 스캐폴드, 비오틴-스트렙타비딘, 유기 또는 무기 나노입자, 폴리뉴클레오타이드 서열, 펩타이드-핵산 또는 유기 중합체를 갖는 펩타이드를 형성하는 데 사용될 수 있는 하나 이상의 천연 또는 비천연 아미노산을 포함할 수 있다.
링커는 메디토프-이용가능 항체 또는 이의 항원 결합 단편의 임의의 부분에 부착될 수 있다. 일 실시 양태에서, 링커는 메디토프-이용가능 항체 또는 이의 항원 결합 단편의 중쇄 또는 중쇄의 아미노 말단에 부착된다. 일부 실시 양태에서, 메디토프를 갖는 링커는 자가-가교결합 항체 또는 단편의 각각의 중쇄 또는 각각의 경쇄에 부착된다. 일부 실시양태에서, 메디토프를 갖는 갖는 링커는 자가-가교결합 항체의 중쇄 및 경쇄 중 하나 이상 또는 전부에 부착된다. 링커는 공유 결합 및/또는 비공유 결합을 통해 항체에 부착될 수 있다.
1. 링커의 구조
링커는 다양한 기능 또는 특성을 제공하는 다양한 서열 또는 다른 구조적 특징을 포함할 수 있다. 예를 들어, 일부 실시양태에서, 링커의 일 말단에서의 메디토프는 동일한 메디토프-이용가능 항체 또는 이의 항원 결합 단편 상의 메디토프 결합 부위에 결합하는 것을 감소시키거나 저해할 수 있다. 일부 실시양태에서, 링커는 강성, 구조적, 순서화된, 또는 상대적으로 강성, 구조적, 순서화된 세그먼트를 하나 이상 포함할 수 있다. 예를 들어, 강성 세그먼트는 링커가 구부리거나 움직일 수 있는 능력을 감소시킬 수 있어, 링커의 일 달단에 있는 메디토프가 동일한 또는 다른 메디토프-이용가능 항체 또는 이의 항원 결합 단편상의 메디토프 결합 부위와 접촉하는 방식으로 구부러지거나, 회전하거나 또는 접히는 능력을 감소시킨다.
바람직한 실시 양태에서, 링커는 메디토프-이용가능 항체 또는 이의 항원 결합 단편의 동일한 측면(예를 들어, 동측) 또는 반대 측면(예를 들어, 대측성) 상의 메디토프 결합 부위에 메디토프가 결합하는 것을 방지할 수 있을 정도로 충분한 강성을 갖는다. 이러한 메디토프 자가-결합의 감소는 다른 메디토프-이용가능 항체에 결합하는 자가-가교결합 항체의 능력을 향상시킬 수 있는데, 예를 들어, 그의 메디토프 결합 사이트를 자유롭게 하여 다른 메디토프-이용가능 항체 또는 이의 항원 결합 단편에 연결된 메디토프를 결합시킬 수 있다.
링커의 견고하고 구조화된 세그먼트은 임의의 펩타이드 서열 또는 화합물을 포함할 수 있어, 링커의 구부러지거나, 방향 전환 또는 접히는 능력을 감소시켜, 링커의 일 말단에 있는 메디토프가 항체의 동일 또는 다른 Fab 영역에 있는 메디토프 결합 부위에 접촉할 수 있게 한다. 일부 실시양태에서, 입체구조적 강성 세그먼트는 펩타이드를 포함한다. 일부 실시양태에서, 링커는 알파 나선을 형성하는 경향이 있는 아미노산 잔기의 서열을 포함할 수 있는 강성 알파 나선형 세그먼트, 영역(region), 도메인 또는 펩타이드를 포함하는 하나 이상의 구조적 요소를 함유할 수 있다. 일부 실시양태에서, 이들 서열은 알파 나선형 구조를 촉진시키는 역할을 할 수 있는 Met, Ala, Leu, Lys, Gln, Arg, Glu, Ser, 및 Pro 아미노산을 포함할 수 있다.
일부 실시양태에서, 소수성 잔기는 단백질의 상이한 세그먼트 또는 도메인 사이의 상호 작용을 증가시킬 수 있다. 소수성 잔기는 Gly, Ala, Val, Leu, Ile, Pro, Phe, Met, 및 Trp을 포함한다. 따라서, 일부 실시양태에서, 링커 세그먼트는 링커 세그먼트 사이 및/또는 링커와 메디토프 또는 항체 사이의 상호 작용을 감소시키기 위해 소수성 잔기를 포함하지 않거나 적게 포함한다. 일부 실시양태에서, 링커의 강성 세그먼트를 포함하는 다수의 알파 나선 간의 상호 작용을 증가시키기 위해 링커의 강성 세그먼트는 소수성 잔기를 포함하는 것이 유리할 수 있다. 다수의 알파 나선을 포함하는 강성 세그먼트의 예는 1FHA(four helix bundle; 서열번호 272) 및 미오글로빈 3RGK(서열번호 273)을 포함한다.
일부 실시양태에서, 입체구조적 강성 세그먼트는 2, 3, 4, 5, 6, 7, 8 또는 그 이상의 알파 나선형 세그먼트를 포함하는 다수의 알파 나선 세그먼트, 영역, 도메인 또는 펩타이드를 포함한다. 일부 실시양태에서, 복수의 알파 나선형 세그먼트는 턴(turns), 루프(loops) 및/또는 헤어핀(hairpins)을 통해 연결된다. 예를 들어, 턴(turns)은 하나 이상의 α-턴, β-턴, γ-턴, δ-턴 및 π-턴을 포함한다. 헤어핀에는 베타 헤어핀이 포함된다. 상기 턴, 루프 및 헤어핀은 복수의 강성 알파 나선형 세그먼트 사이에서 구부러짐을 허용할 수 있다. 구부러짐은 알파 나선형 도메인 사이의 상호 작용을 허용할 수 있으며, 이러한 상호 작용은 강성 세그먼트의 강성을 향상시킬 수 있다. 일부 실시양태에서, 입체구조적 강성 단편은 예를 들어, 알파 나선의 카르복시 또는 아미노 말단을 포함하는 310-나선 또는 파이-나선을 포함한다.
일부 실시양태에서, 다른 메디토프-이용가능 항체의 메디토프 결합 부위에 결합하기 위해 링커를 통해 항체에 연결된 메디토프의 능력을 증가시키는 것이 유리할 수 있다. 따라서, 일부 실시양태에서, 링커는 이러한 결합을 강화시키는 구조적 특징을 포함한다. 예를 들어, 일부 실시양태에서, 링커는 임의로 구조화되지 않거나, 가요성이거나, 무질서하거나, 또는 상대적으로 비구조적이거나, 가요성이거나 또는 무질서한 하나 이상의 세그먼트를 포함한다. 예를 들어, 가요성 또는 무질서한 세그먼트는 링커 또는 링커의 일부분의 구부리거나 움직일 수 있는 능력을 증가시킬 수 있어, 링커의 일 말단에 있는 메디토프가 다른 메디토프-이용가능 항체 상의 메디토프 결합 부위와 접촉 및/또는 결합된 채로 있게 하는 방식으로 링커의 구부리거나, 방향 전환하거나, 접히는 능력을 증가시킨다.
일부 실시양태에서, 링커의 가요성 세그먼트는 펩타이드 골격의 큰 구조적 자유가 있는 것과 같은 생리적 조건 하에서 변성된 펩타이드 서열처럼 거동하도록 디자인 될 수 있다. 일부 예에서, 이들 세그먼트는 본질적으로 생리학적 조건 또는 수용액에서 2차 구조를 갖지 않는다. 일부 구체예에서, 가요성 세그먼트는 하나 이상의 연속 글리신 잔기를 포함하는 하나 이상의 글리신 잔기를 포함할 수 있다. 글리신 잔기는 알파 나선을 포함하여 단백질 구조를 파괴할 수 있다. 이러한 붕괴는 부분적으로 글리신의 최소 측쇄 때문에 생길 수 있는데, 이는 유연성을 증가시킬 수 있다. 따라서, 일부 실시양태에서, 링커의 가요성 단편은 1,2 3, 4, 5, 6 이상의 글리신 잔기를 포함한다. 일부 구체예에서, 가요성 세그먼트는 하나 이상의 글리신 잔기 및 하나 이상의 프롤린 잔기를 포함할 수 있다. 일부 실시양태에서, 링커의 가요성 단편은 서열번호 265의 아미노산 서열을 포함한다.
일부 측면에서, 링커는 하기의 속성 중 하나 이상을 갖는다: 구조적 유연성, 향상된 수용성, 높은 수준의 프로테아제 내성, 낮은 면역원성, 포유류 수용체에 대한 낮은 결합력, 한정된 전하량 및 증가된 유체 역학(또는 스톡스) 반경을 포함한다. 일부 실시양태에서, 링커는 항체/에피토프 상호 작용, 항체/항체 상호작용 또는 항체/메디토프 상호 작용의 입체적 방해를 방지하거나 일으키도록 체계적으로 또는 무작위로 설계된다. 예시적인 변형은 아미노산 치환, 첨가, 결실 또는 변형을 포함한다. 일부 실시양태에서, 입체 장애는 수용체가 클러스터링, 신호 전달 또는 수용체-매개 엔도시토시스를 못하게 할 수 있다. 일부 실시양태에서, 입체 장애를 방지함으로써 수용체가 클러스터링, 신호 전달 또는 수용체-매개 엔도시토시스를 야기할 수 있다.
가요성 세그먼트는 단독으로 사용될 수 있거나 본 명세서에서 기재된 바와 같이 하나 이상의 강성 세그먼트와 결합될 수 있다. 예를 들어, 일부 실시양태에서, 링커는 하기 화학식을 갖는 하나 이상의 사슬(예를 들어, 폴리펩타이드 사슬)을 갖는 화합물이다:
L1A-L2A (화학식 I)
여기서, L1A 는 견고하고 구조화된 세그먼트이고, L2A는 링커의 유연하고 비구조적인 세그먼트이다.
일부 실시양태에서, 링커는 하기 화학식을 갖는 하나 이상의 사슬(예를 들어, 폴리펩타이드 사슬)을 갖는 화합물이다:
L2A-L1A (화학식 Ⅱ)
여기서, L2A 는 링커의 유연하고 비구조적인 세그먼트이고, L1A 는 견고하고 구조화된 세그먼트이다.
일부 실시양태에서, 링커는 하나 이상의 가요성 비구조적인 세그먼트를 포함할 수 있다. 예를 들어, 일부 실시양태에서, 링커는 하기 화학식을 갖는 하나 이상의 사슬(예를 들어, 폴리펩타이드 사슬)을 갖는 화합물이다:
L2B-L1A-L2A (화학식 Ⅲ)
여기서, L1A 는 링커의 견고하고 구조화된 세그먼트이고, L2A 및 L2B는 링커의 유연하고 비구조적인 세그먼트이다.
일부 실시양태에서, 링커는 하기 화학식을 갖는 하나 이상의 사슬 (예를 들어, 폴리펩타이드 사슬)을 갖는 화합물이다:
L1A-L2A-L1B (화학식 Ⅳ)
여기서 L1A 및 L1B는 링커의 견고하고 구조화된 세그먼트이고 L2A는 링커의 유연하고 비구조적인 세그먼트이다. 예시적인 강성 링커 세그먼트는 서열번호: 266 내지 274에 의해 코딩되는 펩타이드 서열을 포함하나, 이에 한정되는 것은 아니다.
2. 링커 및 세그먼트의 길이
링커의 강성 및 가요성 세그먼트의 길이는 링커에 부착된 메디토프가 다른 항체의 메디토프 결합 부위에 결합할 수 있도록 충분히 길어야 한다. 또한 동일한 메디토프-이용가능 항체 또는 항원 결합 단편 상의 메디토프 결합 부위에 대한 상기 메디토프의 결합을 방지 또는 감소시킬 수 있도록 충분히 짧아야 한다. 일부 실시양태에서, 링커의 길이는 적어도 10 Å 일 수 있다. 일부 실시양태에서, 링커의 길이는 적어도 10 Å이고, 바람직하게는 80 Å 미만이다.
일부 실시양태에서, 동일한 항체에서 하나의 Fab 영역의 중쇄의 아미노 말단과 대측성(contralateral) Fab 영역의 중용자 결합 부위 사이의 거리는 약 80 Å이다. 상기 거리는 항체의 순서, 구조 및 유연성에 따라 다를 수 있다. 일부 실시양태에서, 링커의 카르복시 말단 및 메디토프는 10-80, 10-70, 15-60, 20-50, 또는 25-40 Å의 거리만큼 분리되어 있다. 일부 실시양태에서, 링커의 카르복시 말단 및 메디토프 말단은 10-80, 10-70, 15-60, 20-50, 또는 25-40 Å의 거리만큼 분리되어 있다. 일부 실시양태에서, 링커 또는 링커 세그먼트의 길이는 적절한 펩타이드 서열을 적절한 펩타이드 선택에 따라 다양해질 수 있다.
일부 실시양태에서, 링커의 길이는 링커 또는 링커 세그먼트를 포함하는 아미노산의 수에 의해 결정될 수 있다. 후술하는 바와 같이, 알파 나선형 세그먼트는 일련의 회전(turn)을 구성한다. 나선의 각 회전은 약 5.4 Å의 피치(pitch)를 가질 수 있고, 약 3.6 아미노산 잔기를 포함할 수 있다. 이에, 아미노산을 첨가하거나 제거함으로써 링커의 길이를 조절할 수 있다. 일부 실시양태에서, 링커 또는 링커 세그먼트의 길이는 링커의 2차 또는 3차 구조에 의해 결정 될 수 있다. 후술하는 바와 같이, 일부 실시양태에서, 링커 또는 세그먼트는 다수의 구부러진 알파 나선을 포함하는 펩타이드 서열을 포함한다. 일부 실시양태에서, 링커의 길이는 상기 펩타이드의 2차 또는 3차 구조를 변형시킴으로서 조정될 수 있다.
일부 실시예에서, 메디토프의 위치 및 다른 메디토프-이용가능 항체상의 메디토프 결합 부위에 결합하는 능력을 조절하는 것은 링커의 길이를 변화시키거나 또는 링커의 일 말단과 링커의 다른 말단 사이의 거리를 변화시킴으로써 강화될 수 있다. 예를 들어, 일부 실시양태에서, 링커의 길이는 링커가 연결되는 항체 사슬의 아미노 말단과 링커가 결합된 메디토프-이용가능 항체 또는 이의 항원 결합 단편의 동일한 측면상(the same side)의 메디토프 결합 부위 사이의 거리보다 짧다. 일부 실시양태에서, 링커의 길이는 링커가 연결된 항체 사슬의 아미노 말단과 링커가 결합된 메디토프-이용가능 항체 또는 이의 항원 결합 단편의 다른 쪽(the other side)에 있는 메디토프 결합 부위 사이의 거리보다 작다.
또한, 일부 실시양태에서, 세그먼트의 길이 및 링커 조성을 변화시킴으로써 메디토프의 위치 제어를 강화시킬 수 있다. 예를 들어, 일부 실시양태에서, 하나 이상의 강성 세그먼트의 길이는 하나 이상의 가요성 세그먼트의 길이보다 길다. 이렇게 하면, 메디토프는 가요성 영역보다 길이가 긴 강성 영역을 갖는 항체 Fab 영역으로부터 멀어짐으로써 같은 항체의 메디토프 결합 부위에 결합할 가능성을 낮출 수 있다.
링커의 길이는 클러스터링의 기하학을 변경시킬 수 있다. 예를 들어, 2개의 수용체를 근접하게 가지고 오면 잠재적으로 세포 내 신호전달 분자의 보다 높은 활성을 유도한다. 여기서, 항체와 메디토프 사이의 링커는 약 10 Å 이상일 수 있다. 대안으로 수용체를 멀리 유지하는 것이 유리할 수 있다. 여기서, 강성 링커 및/또는 항체와 메디토프 사이의 더 긴 링커는 특정 수용체를 "밀어내는"데 사용될 수 있다.
일부 측면에서, 링커는 표적화 될 세포 표면상의 2개의 수용체 사이의 거리와 동일하거나 대략 동일한 길이를 갖도록 설계된다. 일부 실시양태에서, 수용체는 동일하거나 상이할 수 있다. 예를 들어, 두 수용체는 상이한 아미노산 서열 및/또는 상이한 에피토프를 포함할 수 있다. 일부 상황에서는, 단일 항원에서 상이한 에피토프를 인식하는 2개의 mAb가 상승적으로 작용한다(see Kamat, V. et al., Cancer Biol Ther 7, 726-733 (2008)). 일부 예에서, 자가-가교결합 항체는 어떤 메디토프-이용가능 항체와도 짝을 이룰 수 있는 유연함이 있다. 일부 실시양태에서 자가-가교결합 항체 변이체(예를 들어, 링커 기하 구조를 변화시킴으로써 생성됨)는 특이성 및 상승 효과를 추가로 강화시킨다. 따라서, 일부 실시양태에서, 링커의 길이는 세포 표면 항원에 결합된 자가-가교결합 항체와 세포 표면 항원에 결합된 또 다른 항체의 메디토프 결합 부위 사이의 거리를 모방하거나 비슷하게 설계된다.
주어진 폴리펩타이드에서 2차 및 3차 구조의 존재 또는 부존재를 분별하기 위한 다양한 방법이 당업계에 수립되어 있다. 특히, 2차 구조는 "원-자외선" 스펙트럼 영역(190-250 nm)에서 원편광 이색성(Circular dichroism) 분광법에 의해, 분광분석적으로 측정될 수 있다. 2차 구조 요소, 예를 들어 알파-나선 및 베타-병풍 구조 각각은 CD 스펙트럼의 특징적인 모양과 크기가 생기게 한다. 또한, 2차 구조는 미국특허출원공보 제20030228309 A1호에 기재된 바와 같이, 특정 컴퓨터 프로그램 또는 알고리즘, 예를 들어 잘 알려진 초우 파스만(Chou-Fasman) 알고리즘(Chou, P Y, et al (1974) Biochemistry, 13:222-45) 및 "GOR"(Garnier-Osguthorpe-Robson) 알고리즘 (Garnier J, Gibrat J F, Robson B (1996), GOR method for predicting protein secondary structure scondary structure from amino acid sequence Methods Enzymol 266:540-553)을 통해 폴리펩타이드 서열로부터 예측될 수 있다. 주어진 서열에 대해, 알고리즘은, 예를 들어, 알파-나선 또는 베타-병풍구조를 형성하는 서열의 잔기의 전체 및/또는 퍼센트, 또는 결과적으로 무작위 코일(2차 구조가 결여됨)을 형성할 것으로 예측되는 서열의 잔기의 퍼센트로 표현되는 2차 구조가 존재하는지 전혀 존재하지 않는 지를 예측할 수 있다.
일 실시양태에서, 링커는 초우 파스만 알고리즘에 의해 결정된 바와 같이, 50% 내지 약 95% 초과의 알파-나선 비율을 갖는다. 또 다른 실시 양태에서, 링커는 초우 파스만 알고리즘에 의해 결정된 바와 같이 0% 내지 약 5% 미만 범위의 베타-병풍구조 비율을 갖는다. 일부 실시양태에서, 링커는 초우 파스만 알고리즘에 의해 결정된 바와 같이, 50% 내지 약 95% 초과 범위의 알파-나선 비율 및 0% 내지 약 5% 미만 범위의 베타-병풍구조 비율을 갖는다. 일부 실시양태에서, 링커는, 약 60% 초과, 약 65% 초과, 약 70% 초과, 약 75% 초과, 약 90% 초과 또는 약 95% 초과의 알파 나선 비율을 갖는다. 일부 측면에서, 링커는 혈청 프로테아제(들)에 의한 절단 부위 및/또는 면역원성을 피하기 위한 특정 프로테아제 절단 부위의 존재를 피하도록 설계된다.
본원에서 제공하는 링커는 서열번호 262, 263 및 264의 아미노산 서열을 갖는 것, 또는 1개, 2개, 3개 또는 4개의 임의의 잔기가 임의로 리신 잔기 대신 공액 아미노산으로 치환 된 그의 변형된 변이체를 포함한다.
3. 변형(Modification)
링커는 링커가 유도체화 되도록 다양한 기능 또는 특성을 제공하는 다양한 서열 또는 다른 구조적 특징을 포함할 수 있다. 대표적인 구조적 요소는 프로테아제 절단 부위, 면역원성 서열, 및 예를 들어, 치료제 또는 진단제의 접합에 사용될 수 있는, 예를 들어 포르밀글리신-생성 효소(FGE: formylglycine generating enzyme)와 적합한 알데히드 태그, 리신, 티로신, 글루탐산, 아스파트산 및 비천연 아미노산을 포함한 잔기, 부위 또는 태그가 존재하거나 없을 때를 포함한다.
일부 측면에서, 제공된 화합물의 링커, 예를 들어 프로테아제는 예컨대 MMP 절단 부위, ADAM 절단 부위 및/또는 카텝신 절단 부위와 같은 리소좀성 구획에 존재할 수 있다.
일부 측면에서, 링커는 아미노산이 세린 또는 글리세린이 아니거나, 10, 9, 8, 7, 6, 5, 4, 3, 또는 2 미만의 부분서열 점수를 갖지 않거나, 글리신 및 세린 이외에 적어도 하나의 잔기를 포함하지 않는다면 동일한 3개의 인접한 아미노산을 포함하지 않는다. 일부 측면에서, 링커는 임의의 혈청 프로테아제, 또는 하기 중 하나 이상 또는 어느 하나의 절단 부위를 포함하지 않는다(또는 그에 의해 절단되지 않는다): 혈액 응고 경로 패밀리의 단백질, 인자 XIIIa, XIIa, XIa, Xa, IXa, 및 VIIa, 트롬빈, 혈장 칼리크레인, 활성화된 PC, 프로트롬비나제, hK1, PSA/hK3, hK10, hK15, 활성화된 단백질 C(APC), 하게만 인자(응고 인자 XII), 인자 Xa, ADAMTS13, 폰빌레브란트인자-절단 프로테아제(VWFCP), 프로테아제 넥신 2, 플라스민, 트립신, α-키모트립신, 기질 금속단백분해효소-2, 기질 금속단백분해효소-9, 엘라스타제, MASP-1(만노스 결합 렉티 관련 세린 프로테아제-1), MASP-2, MASP-3, 카텝신 K, 카텝신 B, 스트렙토키나아제, 혈장 프로카르복시펩티다아제 B, 트롬빈-활성화 가능한 피브린 용해 억제제(TAFI), 플라스미노겐 플라스미노겐 활성화 인자 패밀리(예를 들어 조직 플라스미노겐 활성화 인자, 비뇨기 플라스미노겐 활성화 인자(uPA)), 유로키나아제, 보체 전환효소 패밀리 단백질, 인자 C1r, C1s, 인자 D, 및 C3 전환효소, 예를 들어 C4bㆍ2a, C3bㆍBb, 및 C3bㆍBbㆍC3b.
일부 실시양태에서, 링커는, 예를 들어 T 세포 에피토프(들)의 가능성을 최소화하여, 가능한 면역원성을 피하거나 감소하도록 설계된다. 항원 제시 세포(APC: antibody presenting cell)의 표면에 제시하기 위해, 주어진 MHC II형 분자에 펩타이드의 결합능은 펩타이드의 1차 서열을 포함한 많은 인자에 따라 결정된다. 일 측면에서, 본원의 펩타이드 또는 링커는 APC에서 항원 프로세싱에 내성이 있는 그의 서열로 인해 낮은 정도의 면역원성을 갖는다. 또 다른 측면에서, 본원의 펩타이드 또는 링커는 MHC 수용체에 실질적으로 결합하지 않거나, 면역 반응을 유발하기에 충분한 정도로 MHC 수용체에 결합하지 않는 서열을 갖는다. 본 발명은 링커 및 링커를 포함하는 펩타이드로서, 링커 및 펩타이드가 1차 서열에서 실질적으로 비반복적이고 MHC II 수용체와 결합을 감소시키도록 설계된 것인 링커 또는 펩타이드를 제공한다. 다른 측면에서, 본원의 펩타이드 및 링커는 T 세포 수용체 또는 항체 결합을 위한 에피토프를 형성하지 않고, 결과적으로 면역원성의 정도가 낮다. 일 측면에서, 면역원성의 회피는 적어도 부분적으로 링커 서열의 입체구조적 가요성의 결과, 즉, 아미노산 잔기의 선택 및 순서로 인한 2차 구조의 결여의 결과에 기인할 수 있다. 예를 들어, 수용액에서 또는 생리 조건하에서 치밀하게 접힌 입체구조를 적응시키는 경향을 가진 서열은 수용액에서 또는 생리 조건하에서 치밀하게 접힌 입체구조를 적응시키는 경향이 상대적으로 낮은 서열보다 결과적으로 입체구조적 에피토프를 가져올 가능성이 더 크다. 통상적인 치료 관례 및 복용법을 이용하여 본 개시의 링커를 포함하는 융합 단백질의 투여는 일반적으로 링커 서열에 대해 중화 항체의 형성을 일으키지 않는다. 일 측면에서, 면역원성이 낮은 링커 서열은 링커는, 예를 들어 메디토프에 융합되거나 연결될 때, 융합 파트너의 면역원성을 감소시킨다.
일 실시양태에서, 링커는 인간 T 세포에 의해 인식되는 에피토프를 포함하거나 실질적으로 포함하지 않을 수 있다. 면역원성이 낮은 단백질을 생성하기 위해 이러한 에피토프의 제거는 이전에 개시되었다. 예를 들어 본원에서 참고로 포함되는 WO 98/52976, WO 02/079232, 및 WO 00/3317을 참조한다. 동일한 원리, 예를 들어 에피토프의 확인은 상기 에피토프를 링커에 도입하는데 이용될 수 있다. 인간 T 세포 에피토프의 분석은 문헌(Stickler, M, et al (2003) J Immunol Methods, 281: 95-108)에 기재되었다 T 세포 에피토프 또는 비-인간 서열을 생성하거나 생성하지 않고 올리고머화될 수 있는 펩타이드 서열이 특히 관심 받고 있다. 이는 T-세포 에피
토프의 존재에 의해, 및 6 내지 15-mer, 특히 인간이 아닌 9-mer 서열의 존재에 대해 상기 서열의 직접적인 반복을 시험한 후, 링커 서열의 설계를 에피토프 서열을 포함 또는 제거 또는 파괴하도록 변경하여 달성된다. 일부 실시양태에서, 링커 서열은 MHC 수용체에 결합할 것으로 예측되는 링커의 에피토프의 개수를 제한함으로써 실질적으로 비면역원성이다. MHC 수용체에 결합할 수 있는 에피토프의 개수의 감소로, T 세포 활성화에 대한 포텐셜뿐만 아니라 T 세포 보조 기능이 동시에 감소하고, B 세포 활성화 또는 상향 조절이 감소하고 항체 생산이 감소한다. 낮은 정도의 예측된 T 세포 에피토프는 예를 들어, 테피토프(TEPITOPE)(Sturniolo, T, et al(1999) Nat Biotechnol, 17: 555-61)와 같은 에피토프 예측 알고리즘에 의해 결정될 수 있다. 단백질 내에 주어진 펩타이드 프레임의 테피토프 점수는 문헌(Sturniolo, T et al (1999) Nature Biotechnology 17:555)에 개시된 바와 같이, 가장 보편적인 다수의 인간 MHC 대립유전자에 그 펩타이드 프레임의 결합의 Kd(해리 상수, 친화도)의 로그이다. 점수는 적어도 20 로그 초과, 약 10 내지 약 -10(10e10Kd 내지 10e-10Kd의 결합 제약에 상응) 범위이고, MHC상 펩타이드 디스플레이 과정에서 고정(anchor) 잔기로서 역할을 하는 소수성 아미노산, 예를 들어 M, I, L, V, F를 피함으로써 감소될 수 있다. 일부 실시양태에*, 링커 서열은 약 -5, 또는 -6, 또는 -7, 또는 -8, 또는 -9의 테피토프 역치 점수에서 또는 테피토프 점수 -10에서 예측되는 T-세포 에피토프를 갖지 않는다. 본원에서 사용되는 바와 같이, 점수 "-9"는 점수 -5보다 더 엄격한 테피토프 역치이다.
9-mer 펩타이드 서열의 테피토프 점수는 문헌(Sturniolo, T, et al (1999) Nat Biotechnol, 17: 555)에 기재된 바와 같이 포켓 포텐셜을 더하여 계산될 수 있다. 테피토프 점수는 대략 -10 내지 +10 범위의 상기 방법에 의해 계산될 수 있다. 그러나 P1 위치에서 하나의 소수성 아미노산이 결여된 9-mer 펩타이드(FKLMVWY)(서열 번호 240)는 -1009 내지 -989 범위에서 테피토프 점수를 계산하였다. 이 값은 생물학적으로 무의미하며 하나의 소수성 아미노산이 HLA 결합을 위한 고정 잔기로 작용하는 것을 반영하고, P1에서 하나의 소수성 잔기가 결여된 펩타이드는 HLA에 결합하지 않는 것으로 생각된다.
일부 실시양태에서, 링커는, 예를 들어, 에피토프-확인 프로그램 또는 알고리즘에 예측되는 바와 같이, 임의의 MHC II형 에피토프를 포함하거나 포함하지 않는 것으로 예측된다. 일 실시양태에서, 본원의 링커는 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 또는 30개의 MHC II형 에피토프를 갖거나 가질 것으로 예측된다. 또 다른 실시양태에서, 본원에 개시된 링커는 약 2개 이하, 약 3개 이하, 약 4개 이하, 약 5개 이하, 약 6개 이하, 약 7개 이하, 약 8개 이하, 약 9개 이하, 약 10개 이하, 약 11개 이하, 약 12개 이하, 약 13개 이하, 약 14개 이하, 약 15개 이하, 약 16개 이하, 약 17개 이하, 약 18개 이하, 약 19개 이하, 약 20개 이하, 약 21개 이하, 약 22개 이하, 약 23개 이하, 약 24개 이하, 약 25개 이하, 약 26개 이하, 약 27개 이하, 약 28개 이하, 약 29개 이하, 또는 약 30개 이하의 MHC II형 에피토프를 갖거나 가질 것으로 예측된다.
일부 실시양태에서, 링커는 문헌(Singh, H and Raghava, GPS (2001), ProPred: Prediction [0133] of HLA-DR binding sites, Bioinformatics, 17(12):1236-37)에 기재된 프로프레드 툴(ProPred tool)에 의해 예측되는 바 와 같이, 예측된 임의의 MHC II형 에피토프를 포함할 수 있거나 포함하지 않을 수 있다.프로프레드는 항원 단백질 서열에서 MHC II형 결합 영역을 예측하기 위한 그래픽 웹 툴이다. 일 측면에서, 프로프레드 툴을 이용하여 MHC II형 에피토프의 예측은 문헌(Sturniolo, T, et al (1999), Nat Biotechnol, 17: 555)으로부터 유래한 정량적인 매트릭스를 이용한다.
추가로, 링커 서열에서 비반복적인 서열과 상응하는 에피토프의 결여는 B 세포가 링커에 결합하거나 그에 의해 활성화될 수 있는 능력을 제한하거나 향상시킨다 반복적인 서열은 인식되고 심지어 소수의 B 세포와 다가 접촉을 형성할 수 있으며, 다수의 T 세포 비의존 수용체의 가교 결합의 결과로서, B 세포 증식 및 항체 생산을 자극할 수 있다. 대조적으로, 링커는 그의 연장된 서열에 대해 다양한 많은 B 세포와 접촉할 수 있지만, 각 개별 B세포는 서열 반복성의 결여로 인해 개별 링커와 하나 또는 소수의 접촉만 할 수 있다. 일 실시양태에서, 본 개시의 링커는 전형적으로 B 세포의 증식, 따라서 면역 반응을 자극하는 경향이 훨씬 낮다 한 실시양태에서, 링커에 융합된 메디토프는 링커에 융합되지 않은 상응하는 메디토프와 비교하여 면역원성이 감소된다.
일 실시양태에서, 비반복적인 링커는 전형적으로 높은 정도의 반복성을 가진 링커보다 항체와 더 약한 접촉을 형성한다. 항체는 다가 분자이고, 예를 들어, IgG는 2개의 동일한 결합 부위를 가지고 IgM은 10개의 동일한 결합 부위를 가진다. 따라서, 반복적인 서열에 대한 항체는 높은 결합활성을 가진 상기 반복적인 서열과 다가 접촉을 형성할 수 있으며, 이는 상기 반복적인 서열의 효능 및/또는 제거에 영향을 줄 수 있다. 반면에, 비반복적인 링커에 대한 항체는 아마도 단지 1가 상호작용을 일으켜, 결과적으로 비반복적인 링커를 포함하는 펩타이드가 늘어난 기간 동안에 순환에 남아있을 수 있도록 면역 청소의 가능성이 더 낮아지게 한다.
링커 서열은, 예를 들어 MHC I형 에피토프의 예측을 위한 알고리즘을 이용하여, 후보 MHC I형 에피토프를 확인하기 위해 평가될 수 있다. 가능한 MHC I형 에피토프, 즉, 주어진 폴리펩타이드에서 MHC I 형 분자에 디스플레이 될 수 있는 에피토프의 확인을 위해 다양한 많은 예측 프로그램이 이용 가능하다. 다수의 대표적인 알고리즘이 WO 2009/051555호에 기재되어 있으며, 그 개시내용은 본원에서 모든 목적에 참고로 포함된다. 에피토프-확인 프로그램의 예는 하기 기관 및 시설의 웹사이트에서 찾아볼 수 있다: Institute of Microbial Technology(India), 문헌(Singh, H and Raghava, G P S Bioinformatics 22;19(8):1009-14 (2003))에 기재된 프로프레드-I 툴 문헌(Hans-Georg Rammensee, et al, Immunogenetics (1999) 50: 213-219)에 기재된 SYFPEITHI 면역 에피토프 데이터베이스 예를 들어 문헌(Kim Y, Sidney J, Pinilla C, Sette A, Peters B, BMC Bioinformatics 10:394 (2009)) 참조 Max-Planck-Institute for Infection Biology 예를 들어 문헌(J Hakenberg, A Nussbaum, H Schild, H-G Rammensee, C Kuttler, H-G Holzhutter, P-M Kloetzel, SHE Kaufmann, H-J Mollenkopf (2003) MAPPP - MHC-I Antigenic Peptide Processing Prediction Applied Bioinformatics 2(3):155-158)) 참조 문헌(Nielsen M, Lundegaard C, Lund O, Kesmir C Immunogenetics57(1-2): 33-41, 2005)에 기재된 넷찹(NetChop) 서버(Technical University of Denmark).
상기 예측 웹 사이트에서 사용된 알고리즘은 동일한 사이트에서 찾아볼 수 있다. 하기는 적합한 예측 알고리즘을 기재하는 총망라한 것은 아닌 참고문헌의 목록이다: Parker et al (1994) Scheme for ranking potential HLA-A2 binding peptides based on independent binding of individual peptide side-chains, J Immunol, 152, 163-175; Hans-Georg Rammensee et al (1999) SYFPEITHI: database for MHC ligands and peptide motifs, Immunogenetics 50: 213-219; Reche et al (2002) Prediction of MHC Class I binding peptides using profile motifs Hum Immunol 63 (9):701-9; Greenbaum et al (2007) Journal of Molecular Recognition 20 (2):75-82.
일 실시양태에서, 본원의 링커는 MHC 수용체에 대한 에피토프를 전혀 포함하지 않는다. 일 실시양태에서, 본원의 링커는 MHC I형 또는 II형 에피토프를 전혀 포함하지 않는다. 또 다른 실시양태, 본원에 개시된 링커는, 예를 들어, 에피토프-확인 프로그램 또는 알고리즘에 의해 예측된 바와 같이 예측된 MHC I형 에피토프를 전혀 포함하지 않는다. 일 실시양태에서, 본 개시의 링커는 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 또는 30개의 MHC I형 에피토프를 갖거나 가질 것으로 예측된다. 또 다른 실시양태, 본원에 개시된 링커는 약 2개 이하, 약 3개 이하, 약 4개 이하, 약 5개 이하, 약 6개 이하, 약 7개 이하, 약 8개 이하, 약 9개 이하, 약 10개 이하, 약 11개 이하, 약 12개 이하, 약 13개 이하, 약 14개 이하, 약 15개 이하, 약 16개 이하, 약 17개 이하, 약 18개 이하, 약 19개 이하, 약 20개 이하, 약 21개 이하, 약 22개 이하, 약 23개 이하, 약 24개 이하, 약 25개 이하, 약 26개 이하, 약 27개 이하, 약28개 이하, 약 29개 이하, 또는 약 30개 이하의 MHC I형 에피토프를 갖거나 가질 것으로 예측된다.
일부 실시양태에서, 링커는, 예를 들어, 진단제, 예를 들어 영상화제, 또는 치료제와 같은 제제에, 예를 들어, 스캐폴드 또는 링커를 통하여, 유도체화, 예를 들어 다가 메디토프의 접합에 사용될 수 있는 반응 작용기를 포함한다. 일부 실시양태에서, 링커는, 예를 들어, 리신, 티로신, 글루탐산, 아스파트산, FGE 서열, 또는 스캐폴드, 링커 또는 제제를 접합하는데 유용한 비천연 아미노산을 포함한 하나 이상의 접합 부위를 포함한다. 일부 실시양태에서, 접합 부위의 개수 및 위치는 접합 부위를 첨가 또는 제거하여 조절함으로써 후속적으로 접합되는 제제의 양 또는 위치를 조절할 수 있다. 일부 실시양태에서, 파실화 서열, 소르타아제 서열, 또는 인테인 서열을 포함하는 링커는 하나 이상의 접합 부위를 더 포함한다. 예를 들어, 일부 실시양태에서, 메디토프는, 예를 들어 링커 내를 포함하여, 하나 이상의 파실화 서열을 포함한다. 파실화 서열은 정해진 또는 무작위 서열 내에 프롤린, 알라닌, 및 세린을 포함할 수 있다. 따라서, 파실화 서열은 중성의 소수성 아미노산을 포함하는 펩타이드를 포함할 수 있다. 서열 번호 231은 대표적인 3가 메디토프를 개시한다. 서열은 파실화를 포함하며 문헌(Morath, et al Mol Pharm 2015 May 4;12(5):1431-42)에 기재되어 있다. 파실화는 약물 전달을 개선하고 혈장 반감기를 연장시킬 수 있다. 예를 들어 파실화는 단백질의 유체역학적 부피를 증가시켜서 순환을 연장시키고/거나 신장 여과 전에 생물활성을 촉진할 수 있다.
일부 실시양태에서, 티올 작용기는 링커에 임의의 적합한 위치에 도입될 수 있고, 진단제 또는 치료제, 예를 들어 영상화제, 기타 단백질 및 펩타이드, 금속 킬레이트제, siRNA, 나노입자, 세포 독성제 등을 포함한 다수의 외부 시약을 이용하여 선택적으로 변형될 수 있다.
예를 들어, 일부 실시양태에서, 메디토프, 이의 변형된 변이체, 또는 링커는 임의의 1, 2, 3, 또는 4개의 잔기가 임의로 접합된 아미노산, 예를 들어 라이신에서, 치환된 서열을 포함한다. 일부 실시양태에서 쇄(chain)는 금속 이온에 결합된 금속 킬레이트제, 소분자, 화학치료제, 치료 항체 또는 이의 기능적 단편, 독소, 방사성 동위원소, 효소, 뉴클레아제, 호르몬, 면역조절제, 올리고뉴클레오티드, 유기 또는 무기 나노입자, RNAi 분자, siRNA, 킬레이트제, 붕소 화합물, 광활성제, 염료, 형광 또는 발광 물질, 효소, 상승제, 방사성 물질, 또는 킬레이트제를 포함하는 접합된 펩티딜 모이어티이다.
B. 메디토프
본 발명은 세포 표면 항원의 분포를 변경하는 개시된 방법과 함께 사용하기 위한 메디토프 뿐 아니라 상기를 포함하는 벡터, 세포, 라이브러리 및 기타 시스템을 제공한다.
본원에서 사용되는 용어 "메디토프"는 메디토프-이용가능 항체 또는 이의 항원 결합 단편의 중앙 캐비티 예를 들어 메디토프 결합 부위에 결합하는 펩타이드 또는 펩타이드들을 지칭하며, 여기서 항체 또는 이의 항원 결합 단편은 카밧(Kabat) 넘버링에 따라, 이의 경쇄의 위치 40에서 트레오닌, 위치 41에서 아스파라긴, 및 위치 85에서 아스파테이트를 갖거나, 본원에 개시된 세툭시맙, 메디토프 이용가능 트라스투주맙, 또는 메디토프 이용가능 M5A의 메디토프 결합 부위 내의 잔기에 상응하는 잔기를 포함하는 메디토프 결합 부위를 포함한다. 일부 실시양태에*, 상술한 바와 같이, 메디토프는 링커를 통해 항체에 융합될 수 있다. 일부 실시양태에서, 상기 메디토프는 자유 메디토프이다. 대표적인 메디토프는 cQFD(서열 번호 1) 및 cQYN(서열 번호 2) 펩타이드 및 이의 변이체("메디토프 변이체" 또는 "변이체 메디토프")를 포함하나 이에 제한되지 않는다. 기타 분자들은 또한 메디토프-이용가능 항체의 메디토프 결합 부위에 결합할 수 있으며, 메디토프의 특성과 유사한 기능적 특성을 갖는다. "메디토프 유사체"로 정의되는 상기 분자는 소분자, 앱타머, 핵산 분자, 펩티바디 및 메디토프와 동일한 메디토프 결합 부위에 결합할 수 있는 기타 임의의 물질을 포함할 수 있으나 이에 제한되지 않는다. 일부 실시양태에서, 메디토프 서열은 본원에 개시된 바와 같이 고리화된다(예를 들어 말단 (또는 말단 가까운) 시스테인 잔기는 다이설파이드 결합을 형성함).
제공되는 메디토프 중에, 메디토프 1 또는 2(서열 번호 1 또는 2의 메디토프)와 비교하여, 하나 이상의 변형, 예를 들어, 구조적 변형을 갖는 메디토프 변이체(변이체 메디토프로 불림)가 있으며, 이들의 제조 방법도 제공된다. 일부 실시양태에*, cQFD 및 cQYN 메디토프가 메디토프 변이체의 설계에서 출발점으로 사용된다. 일부 측면에서, 메디토프 변이체는 예를 들어 비변형된 메디토프, cQFD 및 cQYN과 비교하여, 상이한 생리 조건하에서 세툭시맙과 본원에 기재된 기타 항체들을 포함한 하나 이상의 제공된 메디토프-이용가능 항체에 대해 변경된 특성, 예를 들어 증가 또는 변경된 친화도, 변경된 pH 의존성, 또는 상이한 친화도를 갖도록 설계된다. 메디토프 변이체는 다양한 화학적 및 생물물리학적 방법을 이용하여 설계되고 제조된다.
메디토프 변이체는 메디토프, 예를 들어 cQFD 및 cQYN에 변형을 편입시키는 변이체 및 본원에 기재된 기타를 포함하나 이에 제한되지 않는다. 적합한 변형은 당업계에 공지된 임의의 펩타이드 변형, 예를 들어, 제한 없이 펩타이드 고리화 방식 및/또는 위치의 변형, 환형 펩타이드의 하나 이상의 아미노산 성분의 변형, 또는 환형 펩타이드로부터 하나 이상의 아미노산의 첨가 또는 결실을 포함하나 이에 제한되지 않는다: 특정 예에서, cQFD는 하기 변형 중 하나 이상으로 변경될 수 있다: Arg8의 변형, Phe3의 변형, Leu5의 변형, Leu10의 변형, 펩타이드 고리화 방식의 변화, 및/또는 하나 이상의 위치에서 수화 가능한 카보닐 작용기의 편입, 및 하나 이상의 아미노산 결실 또는 첨가 cQYN의 경우, 적합한 변형은 다음 중 하나 이상을 포함할 수 있다: Arg8의 변형, Leu5의 변형, Leu10의 변형, 펩타이드 고리화 방식의 변화, 및/또는 하나 이상의 위치에서 수화 가능한 카보닐 작용기의 편입, 및 하나 이상의 아미노산 결실 또는 첨가 메디토프내의 특정 아미노산 위치는 결실되거나 상이한 천연 아미노산 또는 비천연 아미노산으로 대체될 수 있거나, 메디토프는, 예를 들어 "클릭 화학"을 이용하여, 단편과 화학적으로 접합될 수 있다. 본원에서 서열 번호 1의 Arg9가 시트룰린으로 돌연변이된 메디토프는 세툭시맙에 결합한다는것을 보여준다 또한, 아미노 및 카르복시말단은 Fab에 추가로 접촉하기 위해서 메디토프 변이체의 환형 부분 이외에(추가로) 추가의 아미노산으로 연장될 수 있다. 예를 들어, 단백질 L은 cQFD 메디토프의 C-말단에 첨가되었으며 예비 데이터는 이것이 훨씬 더 높은 친화도로 결합한다는 것을 보여준다.
또한, 본 발명은 메디토프-이용가능 항체의 메디토프 결합 부위에 특이적 친화력을 갖는 메디토프를 포함하는 자가-가교결합 항체를 제공한다. 일부 실시양태에서, 자가-가교결합 항체는 예를들어 서열번호 1 또는 서열번호 2와 비교하여, 메디토프 결합 부위에 대해 낮거나 감소된 결합 친화성을 갖는 메디토프 또는 변이체를 포함한다. 일부 실시양태에서, 낮거나 감소된 결합 친화도를 갖는 메디토프 또는 변이체를 포함하는 자가-가교결합 항체는 특정 조건 하에서 자가-가교결합을 감소시키거나 제거할 수 있다. 예를 들어, 더 높은 농도에서 감소된 자가-가교결합 능력 및/또는 추가적인 자유 메디토프가 필요없이 자가-가교결합 항체를 사용하거나 저장할 수 있다. 이러한 항체는 생성 또는 저장 중에 큰 응집체를 형성하거나 용액으로부터 침전될 가능성이 적지만, 항원의 농도가 항체-항체 자가-가교결합 상호 작용을 촉진시키기에 충분히 높으면 항체 또는 항원 내재화를 향상시킨다.
일부 실시양태에서, 자가-가교결합 항체는 예를 들어 서열번호 1 또는 서열번호 2와 비교하여 메디토프 결합 부위에 대해 높거나 증가된 결합 친화성을 갖는 메디토프 또는 이의 변이체를 포함한다. 일부 실시양태에서 높거나 증가된 결합 친화력을 갖는 메디토프 또는 변이체를 포함하는 자가-가교결합 항체는 특정 조건 하에서 자가-가교결합을 증가시킬 수 있다. 예를 들어, 항원의 농도가 특정 세포 표면에서 낮거나 감소할 때 항체 또는 항원의 내부화를 증가시키는 데 유리할 수 있다. 이는 또는 적은 양 또는 적은 농도의 자가-가교결합 항체가 요구되는 경우에 유리할 수 있다.
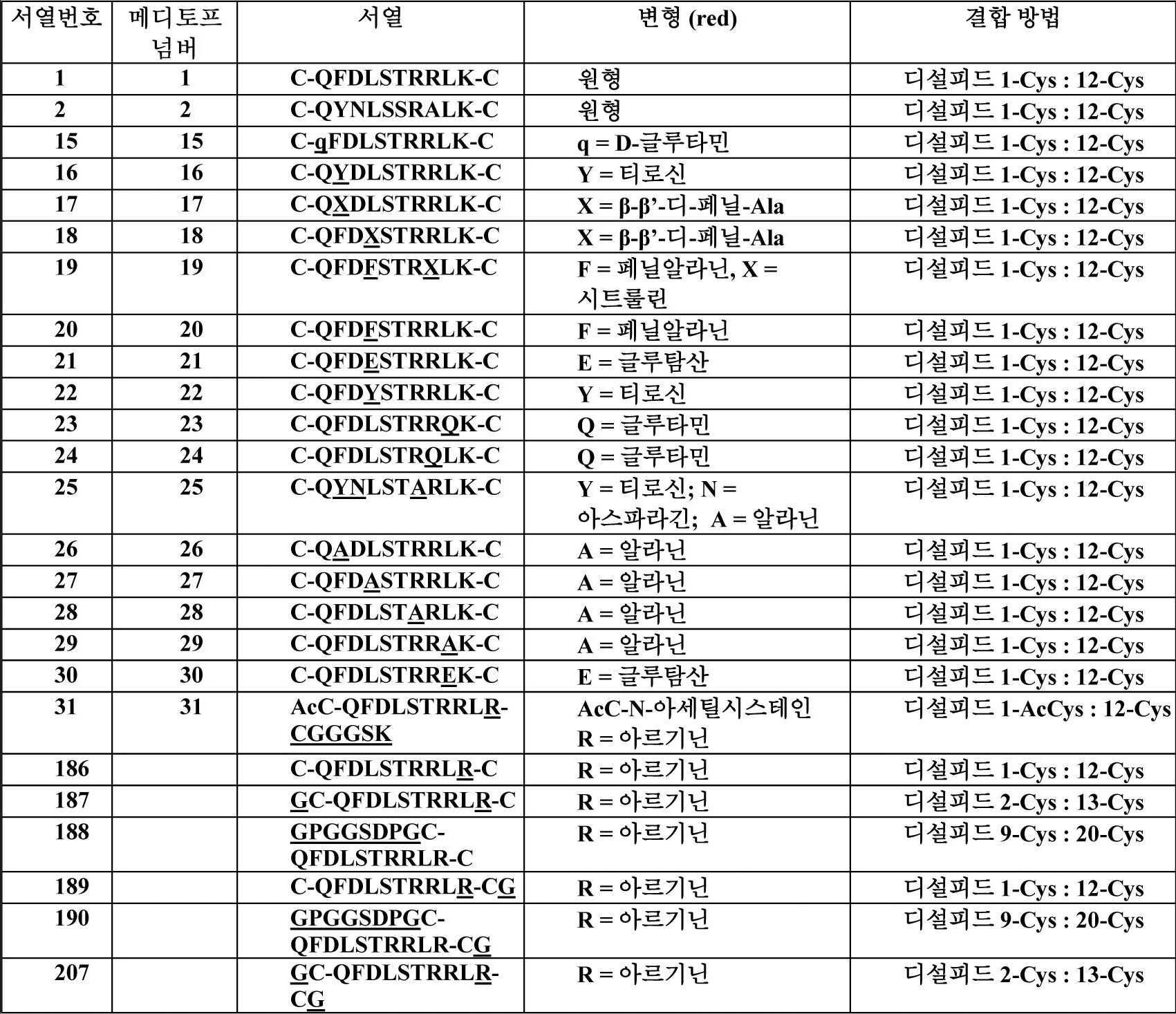
일부 실시양태에서, 메디토프는 [표 1] 및 [표 2]에 열거된 것들뿐만 아니라 추가의 아미노산을 갖는 상기 메디토프, 예를 들어 최대 16개 아미노산 길이를 갖는 것을 포함한다. 예를 들어, 일부 측면에서, 메디토프는 첫째 잔기 앞, 즉 위치 0에서 세린을 추가로 포함하는 메디토프 1, 2, 또는 15-55 중 하나이다. [표 1]에 열거된 메디토프는 C와 N 말단을 연결하는 다이설파이드 결합을 이용하는데, 단, 특정 메디토프가 두 말단 잔기 사이에 결합이 없도록 하기 위해 추가 서열, 예를 들어 꼬리 또는 리더를 포함하는 경우는 제외한다. 대표적인 꼬리 및 선도 서열은 1 내지 50개 아미노산 길이, 예를 들어 1 내지 40, 1 내지 30, 1 내지 25, 1 내지 20, 1 내지 15, 1 내지 10, 9, 8, 7, 6, 5, 4, 3, 또는 2개 아미노산 길이를 갖는 것, 예를 들어 본원에서 R5A 및 R5B로 개시된 꼬리이다. 대표적인 꼬리 및 선도 서열은 임의의 하나 이상의 G, S, P, K, 및/또는 D 잔기(들)을 포함한다. 대표적인 꼬리 및 선도 서열은 GGGSK, G, GPGGSDPG, 및 GPGGSDPG를 포함한다. 예를 들어, 서열 번호 31을 갖는 메디토프는 추가 꼬리를 포함하였으며, 이는 두 말단 잔기 사이에 다이설파이드 결합이 없다는 것을 의미한다. 유사하게, 표에서 다른 특정 메디토프(서열 번호 187-190, 207)는 꼬리 및/또는 선도 서열을 포함하며, 결과적으로 말단 잔기 이외에 잔기들 사이에 결합을 일으킨다. [표 2]의 펩타이드 경우, 다이설파이드 이외의 결합인 락탐 가교(예를 들어 [3+2] 고리화 첨가반응)가 사용되거나 결합이 사용되지 않는다(예를 들어, 비환형 또는 선형 변이체). 본원에 기재된 실시 양태에 따라서 사용될 수 있는 추가의 메디토프는 세툭시맙 또는 임의의 기타 치료 항체의 항체 골격 결합 계면(즉, Fab 경쇄와 중쇄 사이)에 결합하는 펩타이드인, 본원에 정의된 임의의 메디토프를 포함한다. 예를 들어, 환형 펩타이드 cQFD와 cQYN 외에, 일부 실시양태는 cQFD와 cQYN의 하나 이상의 변이체를 포함한다.
[표 1]
[표 2]
메디토프 변이체는 전형적으로 5 내지 16개 아미노산, 예를 들어, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 또는 16개 아미노산 길이, 예를 들어 8 내지 13개 아미노산 길이, 예를 들어, 9 내지 12 아미노산 길이의 아미노산 서열 길이를 갖는다. 메디토프는 추가로 링커 또는 제제를 포함한 또 다른 분자, 예를 들어 또 다른 펩타이드와 (예를 들어, 융합 단백질 또는 펩타이드의 일부로서) 접합되거나 결합될 수 있다. 따라서, 이 경우에, 메디토프를 포함하는 화합물은 상기 문단에 기재된 길이 이상의 추가의 아미노산 잔기를 포함할 수 있으며, 여기서 메디토프 부분은 5 내지 16개 아미노산을 포함하고 복합체 또는 화합물은 추가의 아미노산을 포함한다. 예로서, 예를 들어 상기 서열 번호 31이 본원에 기재되어 있다.
일부 실시양태에서, 변이체 메디토프는 환형 펩타이드이다 기타 실시양태에*,이들은 선형 또는 비환형 펩타이드이다.
메디토프는 예를 들어 하기 식을 갖는 펩타이드 또는 상기 펩타이드로부터 유도된 환형 펩타이드를 포함할 수 있다:
X1-X2-X3-X4-X5-X6-X7-X8-X9-X10-X11-X12 (화학식 VI),
예를 들어, 상기 식에서,
X1 = Cys, Gly, β-알라닌, 디아미노프로피온산, β-아지도알라닌이거나, 존재하지 않고;
X2 = Gln이거나 존재하지 않고;
X3 = Phe, Tyr, β-β'-디페닐-Ala, His, Asp, 2-브로모-L-페닐알라닌, 3-브로모-L-페닐알라닌, 또는 4-브로모-L-페닐알라닌, Asn, Gln, 변형된 Phe, 수화 가능한 카보닐 함유 잔기; 또는 보론산 함유 잔기이고;
X4 = Asp 또는 Asn이고;
X5 = Leu; β-β'-디페닐-Ala; Phe; Trp; Tyr; 페닐알라닌, 트립토판, 또는 티로신의 비천연 유사체; 수화 가능한 카보닐 함유 잔기; 또는 보론산 함유 잔기이고;
X6 = Ser이고;
X7 = Thr 또는 Ser이고;
X8 = Arg, Ser, 변형된 Arg, 또는 수화 가능한 카보닐 또는 보론산 함유 잔기이고;
X9 = Arg, Ala이고;
X10 = Leu, Gln, Glu, β-β'-디페닐-Ala; Phe; Trp; Tyr; 페닐알라닌, 트립토판, 또는 티로신의 비천연 유사체; 수화 가능한 카보닐 함유 잔기; 또는 보론산 함유 잔기이고;
X11 = Lys이고;
X12 = Cys, Gly, 7-아미노헵탄산, β-알라닌, 디아미노프로피온산, 프로파르길글리신, 이소아스파트산이거나, 존재하지 않는다.
일부 측면에서, 변형된 Arg는 도 6에 나타낸 화학식의 구조를 갖는다. 일부 측면에서, 변형된 Phe은 페닐 고리로 편입된 하나 이상의 할로겐을 가진 Phe이다.일부 측면에서, 화학식 VI는 서열 번호 1 또는 서열 번호 2가 아니다.
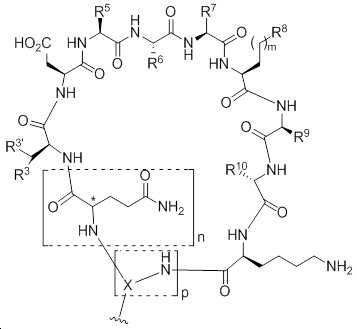
일부 실시양태에서, 메디토프는 화학식 VII의 구조를 갖는 펩타이드 또는 이의 약학적으로 허용 가능한 염이다:
<화학식 VI>
상기 식에서,
"*"로 표시된 중심은 "R" 또는 "S" 배열이고;
R3 및 R3'는 각각 독립적으로, H이거나, C1-4 알킬, -OH, 플루오로, 클로로, 브로모, 및 요오도로부터 독립적으로 선택된 1, 2 또는 3개의 치환기로 경우에 따라 치환된 페닐이고;
R5는:
(A) 옥소, 아세탈, 케탈, -B(OH)2, 보론산 에스테르, 포스포네이트 에스테르, 오르토 에스테르, -CO2C1-4 알킬,-CH=CH-CHO, -CH=CH-C(O)C1-4알킬,-CH=CH-CO2C1-4알킬, -CO2H, 및 -CONH2 기로 이루어진 군으로부터 선택된 하나 이상의 치환기로 경우에 따라 치환된 C1-8 알킬이거나;
(B) 하기로 치환된 C1-4 알킬 기이고:
a) 각 페닐이 -OH, 플루오로, 클로로, 브로모, 및 요오도로부터 독립적으로 선택된 1, 2 또는 3개의 치환기로 경우에 따라 치환된 1 또는 2개의 페닐 기; 또는
b) 나프틸, 이미다졸, 또는 인돌 기
R6은 -C1-4알킬-OH 또는 -C1-4알킬-SH이고;
R7은 -C1-4알킬-OH 또는 -C1-4알킬-SH이고;
m은 0, 1, 2, 3, 4, 또는 5이고;
R8은:
(a) -OH, -NRaRb, -N(Rc)C(O)Re, 또는 -N(Rc)C(=NRd)Re이고;
여기서,
Ra는 H이고;
Rb는 H이거나, 옥소, 아세탈, 및 케탈, -B(OH)2, -SH, 보론산 에스테르, 포스포네이트 에스테르, 오르토 에스테르,-CH=CH-CHO, -CH=CH-C(O)C1-4알킬, -CH=CH-CO2C1-4알킬, -CO2H, 또는 -CO2C1-4알킬 기로 이루어진 군으로부터 선택된 하나 이상의 치환기로 경우에 따라 치환된 C1-8 알킬이고;
Rc는 H, C1-8알킬, C3-8시클로알킬, 분지형 알킬, 또는 아릴이고;
Rd는 H이거나, 각각이 -N3, -NH2, -OH, -SH, 할로겐, 옥소, 아세탈, 케탈, -B(OH)2, 보론산 에스테르, 포스포네이트 에스테르, 오르토 에스테르, -CH=CH-CHO, -CH=CH-C(O)C1-4알킬, -CH=CH-CO2C1-4알킬, -CO2H, 및 -CO2C1-4알킬기로 이루어진 군으로부터 선택된 1개 이상의 치환기로 경우에 따라 치환된 C1-8 알킬, C2-8 알케닐, C2-8 알키닐, C3-8시클로알킬, 분지형 알킬, 또는 아릴 기이고;
Re는 H; -NHRd; 또는 각각 -N3, -NH2, -OH, -SH, 옥소, C2-4아세탈, C2-4케탈, -B(OH)2, 보론산 에스테르, 포스포네이트 에스테르, 오르토 에스테르, -CH=CH-CHO, -CH=CH-C(O)C1-4알킬, -CH=CH-CO2C1-4알킬, 및 -CO2C1-4알킬 기로 이루어진 군으로부터 선택된 하나 이상의 치환기로 경우에 따라 치환된 C1-12알킬, C3-8시클로알킬, C2-12알케닐, C2-8알키닐, 또는 아릴 기이거나; 또는
(b) 옥소, 아세탈, 케탈, -B(OH)2, 보론산 에스테르, -SH, -OH, 포스포네이트 에스테르, 오르토 에스테르, -CH=CH-CHO, -CH=CH-C(O)C1-4알킬, -CH=CH-CO2C1-4알킬, 또는 -CO2C1-4알킬 기로 치환된 C1-12 알킬이고;
R9는 C1-4알킬 또는 -C1-2알킬렌- Rx이며;
여기서 Rx는 -CO2H, -CONH2, -CH2NHC(O)NH2, 또는 -CH2NHC(=NH)NH2이고;
R10은:
(1) 옥소, 아세탈, 케탈, -B(OH)2, 보론산 에스테르, 포스포네이트 에스테르, 오르토 에스테르, -CH=CHCHO, -CH=CH-C(O)C1-4알킬, -CH=CH-CO2C1-4알킬, -CO2C1-4알킬, -CO2H, 및 -CONH2 기로 이루어진 군으로부터 선택된 하나 이상의 치환기로 경우에 따라 치환된 C1-8 알킬; 또는
(2) 1 또는 2개의 페닐 기, 또는 1개의 나프틸, 이미다졸, 또는 인돌 기로 치환된 C1-4 알킬 기이고, 여기서, 각 페닐은 -OH, 플루오로, 클로로, 브로모, 및 요오도로부터 독립적으로 선택된 1, 2, 또는 3개의 치환기로 경우에 따라 치환되고;
n은 0 또는 1이고;
p는 0 또는 1이고;
X는 각각의 탄소가 옥소, -C(O)-, -NHC(O)-, -CO2H, -NH2, 또는 -NHC(O) Ry로 경우에 따라 치환된 C1-8 알킬렌 또는 C2-8 알케닐렌이며;
여기서 상기 알킬렌의 1개의 탄소는 -C(O)NH-, 5원 헤테로아릴 고리, 또는 -S-S-로 경우에 따라 치환되고;
Ry는 -C1-4알킬, -CH(Rz)C(O)-, 또는-CH(Rz)CO2H이고,
여기서 Rz는 -H이거나 -OH, -SH, 또는 -NH2로 경우에 따라 치환된 C1-4알킬이다.
일부 경우에, X는 각각의 탄소가 -CO2H, -NH2, 또는 -NHC(O)Ry로 경우에 따라 치환된 C1-8 알킬렌 또는 C2-8 알케닐렌이며, 여기서 상기 알킬렌의 1개의 탄소는 -C(O)NH-, 5원 헤테로아릴 고리, 또는 -S-S-로 경우에 따라 치환되고; Ry는 -C1-4알킬 또는 -CH(Rz)CO2H이고; 여기서 Rz는 -H이거나 -OH, -SH, 또는 -NH2로 임의로 치환된 C1-4알킬인 것; 또는 이의 약학적으로 허용가능한 염이다.
일부 경우에, 상기 메디토프는 서열 번호 1 또는 2가 아니거나, 상기 서열로부터 유래된 환형 펩타이드가 아니고/거나 메디토프 1 또는 2가 아니다.
[화학식 VI]의 메디토프의 일부 실시양태에서, m은 0, 1, 또는 2이다. 기타 실시양태에서, R3은 H 또는 페닐이고 R3'는 페닐, 2-브로모페닐, 3-브로모페닐, 또는 4-브로모페닐이다. 또 다른 실시양태에서, R5는 메틸, 에틸, 프로필, 이소프로필, 부틸, 이소부틸, sec-부틸, 또는 tert-부틸이며, 이들은 각각 옥소, -B(OH)2, -CO2H, 또는 -CONH2 기로, 또는 각각 브로모 또는 클로로 치환기로 경우에 따라 치환된 1 또는 2개의 페닐 기로 경우에 따라 치환된다. 또 다른 실시양태에*, R8은 -OH, -NH2, -N(Rc)C(O) Re, 또는 -N(Rc)C(=N Rd)Re이다. 또 다른 실시양태에서, Rc는 H 또는 메틸이고, Rd는 H 또는 C1-4알킬이고, Re는 C1-4알킬, 또는 -NH(C1-4알킬)이다. 다른 실시양태에서, R9는 -CO2H, -CONH2, -CH2NHC(O)NH2, 또는 -CH2NHC(=NH)NH2로 경우에 따라 치환된 메틸 또는 에틸이다. 또 다른 실시양태에서, R10은 각각 옥소, -B(OH)2, -CO2H, 또는 -CONH2 기로 임의로 치환된 메틸, 에틸, 프로필, 이소프로필, 부틸, 이소부틸, sec-부틸, 또는 tert-부틸이다. 또 다른 실시양태에서, -X-NH가 -Cys-Cys-, -Gly-Gly-, -C(O)(CH2)6-NH-, -β-Ala-β-Ala-, -C(O)CH(NH2)CH2CH=CHCH2CH(CO2H)-NH-, -C(O)CH(NH2)CH2NHC(O)CH2CH(CO2H)-NH-, -β-Ala-C(O)CH2CH(CO2H)-NH-, 또는 -C(O)CH(NH2)CH2-트리아지닐-CH2-CH(CO2H)-NH-이다.
일부 실시양태에서, 메디토프는 [화학식 VII]의 구조를 갖는 펩타이드이다:
[화학식 VII]
"*"로 표시된 중심은 "R" 또는 "S" 배열이다. 기호 는 L1A에 R1A의 부착 지점을 나타낸다.
R3 및 R3'는 각각 독립적으로, H이거나, C1-4 알킬, -OH, 플루오로, 클로로, 브로모, 및 요오도로부터 독립적으로 선택된 1, 2 또는 3개의 치환기로 경우에 따라 치환된 페닐이고;
R5는: (A) 옥소, 아세탈, 케탈, -B(OH)2, 보론산 에스테르, 포스포네이트 에스테르, 오르토 에스테르, -CO2C1-4 알킬,-CH=CH-CHO, -CH=CH-C(O)C1-4알킬,-CH=CH-CO2C1-4알킬, -CO2H, 및 -CONH2 기로 이루어진 군으로부터 선택된 하나 이상의 치환기로 경우에 따라 치환된 C1-8 알킬이거나; (B) 하기로 치환된 C1-4 알킬 기이고: a) 각 페닐이 -OH, 플루오로, 클로로, 브로모, 및 요오도로부터 독립적으로 선택된 1, 2 또는 3개의 치환기로 경우에 따라 치환된 1 또는 2개의 페닐 기; 또는 b) 나프틸, 이미다졸, 또는 인돌 기.
R6은 -C1-4알킬-OH 또는 -C1-4알킬-SH이다. R7은 -C1-4알킬-OH 또는 -C1-4알킬-SH이다. m은 0, 1, 2, 3, 4, 또는 5이다.
R8은 -OH, -NRaRb, -N(Rc)C(O)Re, 또는 -N(Rc)C(=NRd)Re이다. 여기서, Ra는 H이다. Rb는 H이거나, 옥소, 아세탈, 및 케탈, -B(OH)2, -SH, 보론산 에스테르, 포스포네이트 에스테르, 오르토 에스테르,-CH=CH-CHO, -CH=CH-C(O)C1-4알킬, -CH=CH-CO2C1-4알킬, -CO2H, 또는 -CO2C1-4알킬 기로 이루어진 군으로부터 선택된 하나 이상의 치환기로 경우에 따라 치환된 C1-8 알킬이다. Rc는 H, C1-8알킬, C3-8시클로알킬, 분지형 알킬, 또는 아릴이다. Rd는 H이거나, 각각이 -N3, -NH2, -OH, -SH, 할로겐, 옥소, 아세탈, 케탈, -B(OH)2, 보론산 에스테르, 포스포네이트 에스테르, 오르토 에스테르, -CH=CH-CHO, -CH=CH-C(O)C1-4알킬, -CH=CH-CO2C1-4알킬, -CO2H, 및 -CO2C1-4알킬기로 이루어진 군으로부터 선택된 1개 이상의 치환기로 경우에 따라 치환된 C1-8 알킬, C2-8 알케닐, C2-8 알키닐, C3-8시클로알킬, 분지형 알킬, 또는 아릴 기이다. Re는 H; -NHRd; 또는 각각 -N3, -NH2, -OH, -SH, 옥소, C2-4아세탈, C2-4케탈, -B(OH)2, 보론산 에스테르, 포스포네이트 에스테르, 오르토 에스테르, -CH=CH-CHO, -CH=CH-C(O)C1-4알킬, -CH=CH-CO2C1-4알킬, 및 -CO2C1-4알킬 기로 이루어진 군으로부터 선택된 하나 이상의 치환기로 경우에 따라 치환된 C1-12알킬, C3-8시클로알킬, C2-12알케닐, C2-8알키닐, 또는 아릴 기이다. 대안적으로, R8은 옥소, 아세탈, 케탈, -B(OH)2, 보론산 에스테르, -SH, -OH, 포스포네이트 에스테르, 오르토 에스테르, -CH=CH-CHO, -CH=CH-C(O)C1-4알킬, -CH=CH-CO2C1-4알킬, 또는 -CO2C1-4알킬 기로 치환된 C1-12 알킬이다.
R9는 C1-4알킬 또는 -C1-2알킬렌- Rx이다. 여기서 Rx는 -CO2H, -CONH2, -CH2NHC(O)NH2, 또는 -CH2NHC(=NH)NH2이다.
R10은: (1) 옥소, 아세탈, 케탈, -B(OH)2, 보론산 에스테르, 포스포네이트 에스테르, 오르토 에스테르, -CH=CHCHO, -CH=CH-C(O)C1-4알킬, -CH=CH-CO2C1-4알킬, -CO2C1-4알킬, -CO2H, 및 -CONH2 기로 이루어진 군으로부터 선택된 하나 이상의 치환기로 경우에 따라 치환된 C1-8 알킬; 또는 (2) 1 또는 2개의 페닐 기, 또는 1개의 나프틸, 이미다졸, 또는 인돌 기로 치환된 C1-4 알킬 기이고, 여기서, 각 페닐은 -OH, 플루오로, 클로로, 브로모, 및 요오도로부터 독립적으로 선택된 1, 2, 또는 3개의 치환기로 경우에 따라 치환된다.
n은 0 또는 1이다. p는 0 또는 1이다.
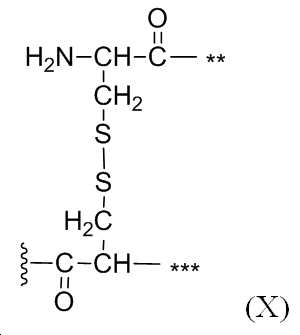
X는 (1) 본원에서 논의된 임의의 메디토프 고리화 전략으로부터 생성된 링커; (2) 치환된 알킬렌, 치환된 헤테로알킬렌, 치환된 시클로알킬렌, 치환된 헤테로시클로알킬렌, 치환된 아릴렌 또는 치환된 헤테로아릴렌 또는 (3) 각 탄소가 옥소, -C(O)-, NH2, -NHC(O)- 또는 -NHC(O)Ry로 경우에 따라 치환된 C1-8 알킬렌 또는 C2-8알킬렌이다. X C1-8의 한 개의 탄소는 -C(O)NH-, 5원 헤테로아릴 고리, 또는 -S-S-로 경우에 따라 치환된다. Ry는 -C1-4알킬 또는 -CH(Rz)C(O)- 또는 -CH(Rz)CO2H이다. Rz는 -H이거나, -OH, -SH, 또는 -NH2로 경우에 따라 치환된 -C1-4알킬이다. 화학식 VII은 모두 적합한 약학적으로 허용 가능한 염을 포함한다. (1)에서, X는 그의 화학적 3가성 때문에, 그리고 X가 경우에 따라 상기에 개시된 추가의 치환기(예를 들어 -NH2 및 옥소)를 포함할 수 있기 때문에 치환된 링커로 생각된다. 일부 실시양태에*, X는:
[화학식 VII]에서, **는 X에 부착된 글루타민에의 부착 지점을 나타내고 ***은 [화학식 VII]에서 X 및 라이신에 부착된 질소에의 부착 지점을 나타낸다. 기호
는 분자의 나머지 부분에 X가 부착하는 지점을 나타낸다.
[화학식 VII]의 메디토프의 일부 실시양태에서, m은 0, 1, 또는 2이다. 기타 실시양태에서, R3은 H 또는 페닐이고 R3'는 페닐, 2-브로모페닐, 3-브로모페닐, 또는 4-브로모페닐이다. 또 다른 실시양태에서, R5는 메틸, 에틸, 프로필, 이소프로필, 부틸, 이소부틸, sec-부틸, 또는 tert-부틸이며, 이들은 각각 옥소, -B(OH)2, -CO2H, 또는 -CONH2 기로, 또는 각각 브로모 또는 클로로 치환기로 경우에 따라 치환된 1 또는 2개의 페닐 기로 경우에 따라 치환된다. 또 다른 실시양태에*, R8은 -OH, -NH2, -N(Rc)C(O) Re, 또는 -N(Rc)C(=N Rd)Re이다. 또 다른 실시양태에서, Rc는 H 또는 메틸이고, Rd는 H 또는 C1-4알킬이고, Re는 C1-4알킬, 또는 -NH(C1-4알킬)이다. 다른 실시양태에서, R9는 -CO2H, -CONH2, -CH2NHC(O)NH2, 또는 -CH2NHC(=NH)NH2로 경우에 따라 치환된 메틸 또는 에틸이다. 또 다른 실시양태에서, R10은 각각 옥소, -B(OH)2, -CO2H, 또는 -CONH2 기로 임의로 치환된 메틸, 에틸, 프로필, 이소프로필, 부틸, 이소부틸, sec-부틸, 또는 tert-부틸이다. 또 다른 실시양태에서, -X-NH가 -Cys-Cys-, -Gly-Gly-, -C(O)(CH2)6-NH-, -β-Ala-β-Ala-, -C(O)CH(NH2)CH2CH=CHCH2CH(CO2H)-NH-, -C(O)CH(NH2)CH2NHC(O)CH2CH(CO2H)-NH-, -β-Ala-C(O)CH2CH(CO2H)-NH-, 또는 -C(O)CH(NH2)CH2-트리아지닐-CH2-CH(CO2H)-NH-이다.
1. 변형
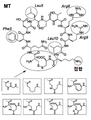
구조적 및 열역학적 데이터를 기초로 하여, 본원에 기재된 메디토프 1 및 2 내에 다수의 위치가, 전체 결합 친화도를 향상시키고/거나 본원에 기재된 또 다른 특성을 변경하기 위한, 예를 들어 상이한 천연 또는 비-천연 아미노산을 갖는, 변형을 위한 표적 부위로서 확인되었다. 이러한 변형은 헤드-투-테일(head-to-tail) 환형 락탐 펩타이드를 생성하기 위한 cQFD 또는 cQYN의 변형, Arg8의 변형, 위치 3의 변형(예를 들어, cQFD 또는 이의 변이체의 Phe3)의 변형, Leu5의 변형, Leu10의 변형, 및/또는 수화 가능한 카보닐 작용기의 편입(도 2 참조)을 포함하나 이에 제한되지 않는다. 본원에서 증명되는 바와 같이, cQFD의 원래 메디토프에서 Phe3, Leu5, 및 Arg8 각각의 알라닌으로의 돌연변이는 생성 화합물의 메디토프-이용가능 항체 결합 계면에 대한 친화도를 10-140배 감소시킨다. 일부 측면에서, 변이체 메디토프는 서열번호 1 또는 2의 메디토프 또는 [표 1] 또는 [표 2]에 열거된 기타 메디토프의 위치 1, 3, 5, 8, 10, 및 12 중 하나 이상에서 변형을 갖는 것들을 포함한다.
a. 위치 8
일부 실시양태에서, 메디토프 변이체는 메디토프 1 또는 2의 위치 8(Arg8)에 상응하는 위치에서 변형을 포함한다. 변형되지 않은 메디토프(cQFD; 서열번호 1)에서, Arg8은 연장되어, 메디토프-이용가능 항체 중쇄의 Q105의 중쇄 카보닐과 수소결합한다. 상기 잔기 가까이에 인접한 영역은 소수성이지만 용매에 노출된다. 일부 측면에서, 메디토프는 이 위치에서 변형된 잔기를 포함한다(예를 들어, 변형된 Arg8). 일부 예에서, 변형된 잔기는 메디토프-이용가능 항체 H-결합에 유용한 Arg8 잔기의 면역 작용성을 유지하며, 치환 또는 비치환된 소수성 아암(arm)을 도입시켜 캐비티를 채운다. 이러한 변형은 리간드 도킹 계산에 의해 지지되는 바와 같이, 엔트로피 증가로 인하여, 결과적으로 결합을 상당히 증가시킨다. 이러한 변형은 N-알킬 구아니디늄기, 또는 알킬-아미딘 작용기를 사용하여 편입할 수 있다. 다른 경우에, 말단 N-원자의 치환된 기는 알킬 또는 아릴일 수 있으며, 여기서 알킬 또는 아릴 기의 각 위치는 말단 위치를 포함하여 기 내에서 추가의 작용기로 경우에 따라 치환될 수 있다. 한 예로, 도 1에 나타낸 구조를 갖는 변형된 아르기닌(변형된 Arg8)으로 메디토프의, 예를 들어 NH2(도 1에서 NHR로 나타냄)상에 부틸 기를 가진 서열번호 1 또는 2의 메디토프의 Arg8을 치환한다. 일부 측면에서, 변이체 메디토프는 위치 8에서 n-부틸 아르기닌 또는 부틸아미딘 변형을 포함한다.
b. 위치 3
일부 실시양태에서, 메디토프 변이체는 메디토프 1의 위치 3, 예를 들어 Phe3에 상응하는 위치에서 변형을 포함한다. 메디토프 변이체 Phe3Tyr cQYN (서열번호 2)의 히드록실 기는 cQFD(서열번호 1)와 비교하여 Arg8 측쇄의 연장된 입체구조에서 변경을 갖는다. 본원에서 데이터는 Fab에 결합된 물과 유리한 수소 결합 네트워크의 형성을 시사한다. 엔탈피-유도된 최적화는 약물 설계에 있어서 수많은 소분자 접근법에서 성공적인 것으로 입증하였고 제공된 메디토프에서 엔트로피 증가를 조작하기 위한 기회가 있다. 일부 실시양태에서, 메디토프 설계에서 결과적으로 엔탈피 및/또는 엔트로피를 증가시키는 접근법은, 예를 들어, 결합을 최적화하는, 변이체 메디토프를 생성하는데 사용된다.
예를 들어, 메디토프-이용가능 항체에 결합된 경우, Phe3의 소수성 페닐 고리는 메디토프-이용가능 항체 Fab의 측쇄 잔기의 상당한 극성의 배열로 둘러싸이게 된다. 일부 실시양태에서, 하나 이상의 할로겐이 상기 잔기의 페닐 고리에 도입되어, 극성 측쇄 잔기와 할로겐 결합 상호작용을 가능하게 한다. 할로겐 결합은 수소 결합과 유사하지만, 산소 원자와, 브롬 또는 염소(또는 기타 할로겐)와 같은 할로겐의 상호작용을 수반하는 비교적 강한 비-공유결합이다. 일부 측면에서, 상기 위치의 잔기는 할로겐 치환기를 편입하도록 변형된다. 일부 측면에서, 메디토프-이용 가능 항체와 할로겐 결합에 적합한 위치에, 예를 들어, 각각, 메디토프-이용가능 항체의 Tyr87(경쇄), Gln38, 및/또는 Tyr91(중쇄) 위치에 브롬 원자가 위치하도록 하기 위해서 Phe3은 2-브로모-, 3-브로모-, 또는 4-브로모페닐알라닌으로 치환된다. 이러한 페닐알라닌 유도체는 구입가능하며 일부 측면에서 고상 펩타이드 합성법(SPPS)에 의해 환형 펩타이드 메디토프 변이체에 편입된다. 대표적인 변이체 메디토프는 메디토프 1의 Phe3에 상응하는 위치에 2-브로모-L-페닐알라닌, 3-브로모-L-페닐알라닌, 또는 4-브로모-L-페닐알라닌을 포함하는 것들을 포함한다.
또 다른 예에서, 메디토프는 예를 들어, Phe3을 β,β'-디페닐알라닌으로 치환시켜 상기 위치에 추가의 페닐기를 편입시킨다.
c. 위치 5 및 10(예를 들어, 메디토프 1 또는 2의 Leu5, Leu10)
일부 실시양태에서, 메디토프 변이체는 메디토프 1 또는 2의 위치 5 또는 10 (Leu5 또는 Leu10)에 상응하는 위치에서 변형을 포함한다. 본원에 나타낸 바와 같이, 메디토프 1의 Leu5 및 Leu10의 측쇄는 메디토프 이용 가능 Fab, 세툭시맙에 소수성으로 접촉한다. 특정 실시양태에서, 메디토프의 한 가지 이상의 특성, 예를 들어, 친화도는 이들 위치중 하나 또는 둘 다에 상이한 천연 아미노산, 또는 비-천연 아미노산을 편입시켜, 예를 들어, 연장될 수 있는 표면 영역의 양을 변화시킴으로써, 변경된다. 한 실시양태에서, 천연 아미노산(Phe/Tyr/Trp) 및 비-천연 유사체 (예를 들어, β,β'-디페닐-L-알라닌, 또는 분지형 알킬, 나프틸과 같은 연장된 방향족, 또는 기타 소수성 기를 포함하는 측쇄를 편입시키는 아미노산)가 상기 위치중 하나 또는 둘 다에 SPPS를 통하여 체계적으로 도입된다.
2. 접합
특정 실시양태에서, 메디토프는 치료제, 진단 제제 또는 검출 가능한 제제와 같은 제제에 접합된다. 펩타이드는 임의의 적합한 수단, 예컨대 화학적 링커를 통해 작용제에 접합 될 수 있다. 특정 실시양태에서, 화학적 링커는 공유결합 링커이다. 일부 실시양태에서, 화학적 링커는 치환 또는 비치환 알킬렌, 치환 또는 비치환 헤테로 알킬렌, 치환 또는 비치환 시클로 알킬렌, 치환 또는 비치환 헤테로 시클로 알킬렌, 치환 또는 비치환 아릴렌 및/또는 치환 또는 비치환 헤테로 아릴렌을 포함한다.
특정 실시양태에서, 화학적 링커는 PEG 링커를 포함한다. 특정 실시양태에*, 화학적 링커는 펩타이드 링커(예를 들어, 글리신, 라이신, 티로신, 글루탐산, 아스파르트산 등과 같은 하나 이상의 천연 또는 비천연 아미노산)을 포함한다.
화학적 링커는 N-말단, C-말단 및/또는 측쇄와 같은 임의의 적합한 위치에서 메디토프와 결합 할 수 있다. 특정 실시양태에서, 화학적 링커는 N-말단에 결합한다. 또 다른 실시양태에서, 화학적 링커는 C-말단에 결합한다. 또 다른 실시양태에서, 메디토프는 화학적 링커가 N-말단 및 C-말단에 결합되는 하나 이상의 화학적 링커를 포함한다. 일부 실시양태에서, 화학적 링커는 아미노산 서열 -GGGK를 포함한다.
본원에 개시된 특정 실시양태에서, 화학적 링커는 항체-약물 접합체를 형성하기 위해 당업계에 알려지고 시판되는 링커를 추가로 포함할 수 있다. 따라서, 특정 실시양태에서, 화학적 링커는 Ala-Ala-Asn-PAB, ALD-BZ-OSu, ALD-di-EG-OPFP, ALD-di-EG-OSu, ALD-mono-EG-OPFP, ALD-mono-EG-OSu, ALD-tetra-EG-OPFP, ALD-tetra-EG-OSu, ALD-tri-EG-OPFP, ALD-tri-EG-OSu, BCOT-di-EG-OPFP, BCOT-di-EG-Osu, BCOT-tetra-EG-OPFP, BCOT-tetra-EG-OSu, BCOT-tri-EG-OPFP, BCOT-tri-EG-Osu, Boc-NMe-DAE, BrAH, Br-di-EG-OSu, Br-tetra-EG-OSu, Br-tri-EG-OSu, COT-acetic acid, COT-di-EG-OPFP, COT-di-EG-OSu, COT-tetra-EG-OPFP, COT-tetra-EG-OSu, COT-tri-EG-OPFP, COT-tri-EG-OSu, DHA, DHH, Fmoc-Ala-Ala-Asn-PAB-PNP, Fmoc-Phe-Lys(Trt)-PAB-PNP, Fmoc-Val-Cit-PAB, Fmoc-Val-Cit-PAB-PNP, HAC, MAH, MAL-di-EG-OPFP, MAL-di-EG-OSu, MAL-HA-OSu, MAL-tetra-EG-OPFP, MAL-tetra-EG-OSu, MAL-tri-EG-OPFP, MAL-tri-EG-OSu, MBA, MC-Val-Cit-PAB-PNP, MDB, MEL-di-EG-OPFP, MEL-di-EG-OSu, MEL-tetra-EG-OPFP, MEL-tetra-EG-OSu, MEL-tri-EG-OPFP, MEL-tri-EG-OSu, MMC, N3BA, N3-di-EG-OPFP, N3-di-EG-OSu, N3-tetra-EG-OPFP, N3-tetra-EG-OSu, N3-tri-EG-OPFP, N3-tri-EG-OSu, PAB, PHA-di-EG-OPFP, PHA-di-EG-OSu, PHA-tetra-EG-OPFP, PHA-tetra-EG-OSu, PHA-tri-EG-OPFP, PHA-tri-EG-OSu, Phe-Lys(Fmoc)-PAB, Phe-Lys(Trt)-PAB, Py-ds-But-OPFP, Py-ds-But-OSu, Py-ds-dmBut-OPFP, Py-ds-dmBut-OSu, Py-ds-Prp-OPFP, Py-ds-Prp-OSu, and Val-Cit-PAB (ALB Materials Inc, Nevada, U.S.)로 이루어진 군에서 선택되는 것을 포함할 수 있다.
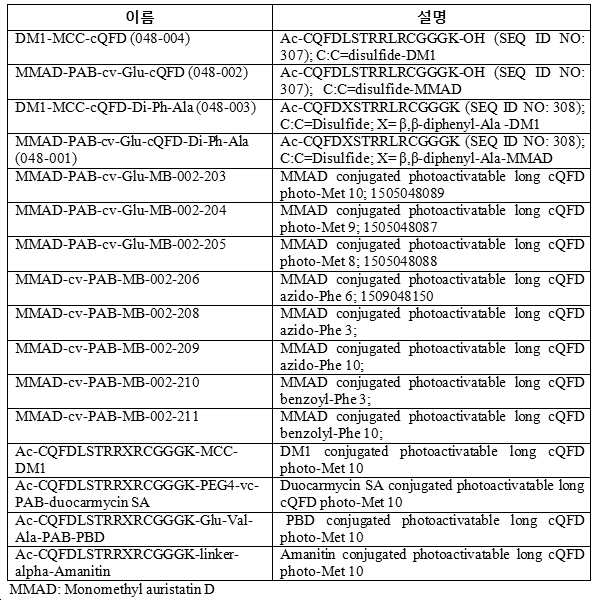
접합된 메디토프 펩타이드의 비제한적인 예를 하기 표에 나타내었다.
3. 대안적인 고리화 전략 및 다이설파이드 가교의 대체
특정의 실시양태에서, 변이체 메디토프는 cQFD 및 cQYN에서와 같이, 다이설파이드 가교를 포함한다. 디설파이드 가교는 2개의 시스테인 잔기의 측쇄 반응에 의해 형성될 수 있다. 특정의 실시양태에서, 메디토프, 예를 들어, 메디토프 1 또는 2에서 다이설파이드 가교는 대안적인 결합으로 대체되거나 제거된다. 따라서, 변이체 메디토프중에는 또 다른 결합을 갖거나 본래 메디토프의 다이설파이드 가교가 결여되어 있는 것들이 있다.
일부 측면에서, 아미노산 쇄(chain) 내에 하나 이상의 비천연 아미노산 사이에 결합이 만들어 진다. 비천연 아미노산으로 만들어질 수 있는 결합의 예는 (i) 알데히드 또는 케톤을 포함하는 잔기와 아민 기를 포함하는 잔기의 반응(여기서 아민 질소는 -NH2 또는 알킬옥시 기로 치환됨)의 반응(예를 들어, p-아세틸페닐알라닌, m-아세틸페닐알라닌, 또는 p-(3-옥소부타노일)-L-페닐알라닌 잔기와 p-(2-아미노-3-히드록시에틸)-페닐알라닌 잔기의 반응)으로 만들어지는 안정한 히드라존 또는 옥심-기반 결합, (ii) 페닐셀레니딜알라닌의 편입에 의한 반응성인 티올, (iii) p-벤조일-L-페닐알라닌의 편입에 의한 벤조페논을 함유하는 UV 가교 결합제, (iv) p-이소프로필티오카보닐-페닐알라닌 또는 p-에틸티오카보닐-페닐알라닌의 편입에 의한 반응성인 아민, (v) 예를 들어, 아지드 기를 포함하는 잔기를 알킨 기를 포함하는 잔기와 후이스겐(Huisgen) 고리화 첨가반응을 통하여 반응시켜(예를 들어, p-프로파르길옥시페닐알라닌 잔기와 p-아지도페닐알라닌 잔기의 반응) 만들어진 헤테로시클릭 결합, 예를 들어 트리아진, 티아졸, 티아졸리딘, 또는 옥사졸 결합; (v) 한 잔기 내 산 기와 또 다른 잔기 내 아민 기의 반응에 의해 만들어진 아미드 결합; (vi) 한 잔기 내 산 기와 또 다른 잔기 내 세린과 같은 알코올과의 반응에 의해 만들어진 에스테르 결합; (vii) 각각 말단 올레핀을 포함하는 2개 잔기의 반응, 예를 들어, 올레핀 복분해 반응(예를 들어, 2개의 알릴 글리신 잔기 또는 2개의 N-알릴 치환된 아미노산의 반응)에 의해 만들어진 이중결합, 또는 (VII) 당 업계에 공지된 적합한 잔기의 임의의 기타 쌍의 반응에 의해 만들어진 것을 포함하는 결합을 포함한다. 리뷰를 위하여, 예를 들어 문헌(Davies, J.S., "The Cyclization of Peptides and Depsipeptides," J. Peptide Sci. 2003, 9, 471-501)을 참고한다. 일 실시양태에서, 메디토프는 반응성 기를 Fab에 편입된 비천연 아미노산, 예를 들어 p-아세틸페닐알라닌으로 향하도록 할 수 있다.
메디토프의 다양한 고리화 방법을 이용하여, 예를 들어, 생체 내 안정성을 제공하고 후속되는 접합 화학을 화학선택적으로 제어할 수 있다. 일부 실시양태에*?*, 고리화 전략은 헤드-투-테일 락탐 고리화(비환형 펩타이드의 말단 잔기 사이에서) 및/또는 다른 잔기 사이의 락탐 결합을 포함한 락탐 고리화 전략이다. 락탐 형성은 또한 글리신, β-Ala, 7-아미노헵탄산 등과 같은 잔기를 비환형 메디토프 고리화 전구체에 편입시켜 상이한 락탐 고리 크기와 연결 방식을 생성시킬 수 있다. "클릭" 화학 및 올레핀 복분해와 같은 추가적인 고리화 전략이 또한 사용될 수 있다(도 2의 오른쪽 박스 참조). 이 같은 펩타이드와 펩타이드 모방체 고리화 방법은 당 업계에 잘 알려져 있다.
일부 실시양태에서, 락탐 결합을 포함하는 메디토프는 생체 내에서 더욱 안정한데, 예를 들어 다른 결합을 갖는 메디토프와 비교하여 생체 내에서 더욱 안정한 결합을 갖는다.
일부 실시양태에서, 비환형 펩타이드의 말단 잔기는 반응하여 환형 메디토프, 예를 들어, 환형 메디토프 변이체를 형성한다. 기타 실시양태에서, 잔기 3과 11 및 4와 11 사이를 포함하여, 다른 위치는 고리화가 일어나기 쉽다. 따라서, 일부 측면에서, 메디토프는 예를 들어, 12개-아미노산 펩타이드의 잔기 3과 11 사이 및/또는 4와 11 사이와 같이, N-말단 및 C-말단을 제외한 잔기 사이에서 형성된 결합을 포함한다.
일부 실시양태에서, 메디토프, 예를 들어, 변이체 메디토프는 반응성 아민 작용기(예를 들어, Lys11)를 포함하며, 이는 예를 들어, 스캐폴드 또는 링커 또는 제제, 예를 들어 진단제, 예를 들어 영상화제, 또는 본원에 기재된 치료제에 메디토프 변이체의 후속되는 접합에 사용될 수 있다. 예를 들어, 도 3은 FACS 분석을 위해 플루오레세인을 메디토프 변이체에 접합시키는 절차를 나타내며; 이 전략은 생체 내 PET 영상화를 위한 DOTA를 포함한, 기타 영상화제 및 기타 제제에 적용될 수 있다.
C. 메디토프-이용가능 항체
본 발명은 메디토프 결합 부위를 통하여 하나 이상의 메디토프에 결합할 수 있는 메디토프-이용가능 항체 및 이의 항원 결합 단편을 제공한다. 일부 경우에, 메디토프-이용가능 항체는 서열번호 1 또는 2(메디토프 1 또는 2)의 환형 펩타이드 및/또는 이들의 하나 이상의 변이체, 예를 들어 메디토프 1, 2, 16-18, 23, 29, 31, 32, 36, 39, 42, 43, 45, 46, 51, 52, 54, 또는 55(서열 번호 1, 2, 16-18, 23, 29, 31, 32, 36, 39, 42, 43, 45, 46, 51, 52, 54, 또는 55에 개시된 서열을 갖는 펩타이드를 기본으로 하는 메디토프), 또는 일부 경우에는, 메디토프 1, 2 또는 15-55 중 임의의 메디토프 및/또는 서열번호 186-190 및 207 중 임의의 서열의 메디토프에 결합한다. 제공된 메디토프-이용가능 항체 중에는 세툭시맙의 친화도와 유사한 친화도로 메디토프 또는 메디토프들에 결합하는 것들이 있다. 예를 들어, 특정의 측면에서, 항체는 약 10 μM 이하, 약 5 μM 이하, 또는 약 2 μM 이하, 약 1 μM 이하, 약 500, 400, 300, 200, 100 nM 이하 또는 그 미만, 예를 들어 약 200 피코몰 이하의 해리 상수로 메디토프(들)에 결합한다. 일부 경우에, 해리 상수, 예를 들어 본원에 열거된 임의의 해리 상수는 특정 기술, 예를 들어 표면 플라즈몬 공명(SPR), 등온 적정 열량측정법(ITC), 형광, 형광 편광, NMR, IR, 열량측정 적정법; 동역학 배제법(Kinetic exclusion); 원이색성(Circular dichroism), 시차 주사 열량측정법, 또는 기타 공지의 방법을 이용하여 측정된다. 예를 들어, 일부 경우에, 유사체 또는 메디토프는 SPR로 측정된바 또는 ITC로 측정된바 또는 이들 방법들 중 임의의 방법에 의해 측정된바, 약 10 μM 이하, 약 5 μM 이하, 또는 약 2 μM 이하, 약 1 μM 이하, 약 500, 400, 300, 200, 100 nM 이하, 또는 그 미만의 결합 상수를 나타낸다.
일부 예에서, 메디토프 결합 부위는 단클론 항체 세툭시맙의 구조적 특징이다. 따라서, 일부 경우에, 메디토프 결합 부위는 세툭시맙의 메디토프 결합 부위 내에 잔기에 상응하는 잔기를 포함한다. x-선 결정학 분석은 서열번호 1의 펩타이드가 중쇄 및 경쇄의 다양한 잔기에 의해 정의된(도 4a 및 도 5 참조), 세툭시맙 Fab 단편의 중앙 캐비티 내의 메디토프 결합 부위에 ~ 700 nM의 결합 상수로 결합한다는 것을 밝혔다.
특정의 실시양태에서, 메디토프와 세툭시맙 결합 부위 사이의 고유 상호작용을 이용하여 추가의 메디토프-이용가능 항체를 생성한다. 일부 실시양태에서, 메디토프-이용가능 항체는 세툭시맙(때로는 주형 항체로 언급됨) 이외의 항체, 예를 들어 세툭시맙의 CDR과 구별되는 적어도 하나의 CDR을 갖는 항체를 변형시켜, 하나 이상의 제공된 메디토프, 예를 들어 서열번호 1 또는 2의 메디토프, 또는 이의 변이체에 결합하는 능력을 부여하여 생성된다.
주형 항체는 인간 또는 인간화 항체 또는 생쥐 항체일 수 있다. 일 측면에서, 변형은 주형 항체를 메디토프-이용가능하게 만들기 위해서 Fab 단편의 중앙 캐비티 내, 전형적으로 중쇄 및 경쇄 가변 영역 및/또는 불변 영역 내 골격 영역(FR) 내에 잔기를 치환하는 단계를 포함한다. 예를 들어, 주형 항체가 인간 또는 인간화 항체일 경우, 변형은 일반적으로 중쇄 및 경쇄 가변 영역 FR 내 잔기에서 치환을 포함한다. 일부 실시양태에서, 상기 잔기는 세툭시맙에 존재하는 상응하는 잔기 또는 비슷한 아미노산으로 치환된다. 따라서, 특정 실시양태에서, 인간 또는 인간화 항체의 FR 내 잔기는 상응하는 쥣과(murine) 잔기로 치환된다; 특정 실시양태에서, 이들은 기타 잔기, 예를 들어 메디토프와 상호작용하기 위한 유사한 작용기를 갖는 잔기로 치환된다. 전형적으로, 상응하는 쥣과(또는 기타) 잔기로 치환된 잔기는 중심 Fab 캐비티 내에서 발견되고, 따라서 면역계에 노출되지 않는다. 이와 같이, 일부 실시양태에서, 인간 또는 인간화 항체에서 아미노산 치환의 도입은 인간 피험체로 전달과 관련하여 변형된 주형 항체의 항원성을 증가시키지 못하거나 실질적으로 증가시키지 못한다. 게다가, 항원성 예측 알고리즘을 추가로 사용하여 점 돌연변이를 가진 인간 서열이 항원성을 갖지 않는다는 것을 나타낼 수 있다.
일부 실시양태에서, 메디토프 결합 부위에서 치환되는 하나 이상의 잔기는 자가-가교결합 항체에 특정 메디토프, 즉, 자유 메디토프, 링커를 통해 항체에 결합된 메디토프, 또는 둘 모두에 대한 특이적 결합 친화력을 부여하도록 선택된다. 예를 들어, 자가-가교결합 항체의 일부 실시양태는 제1 메디토프에 대해 높거나 증가된 친화력 및 제2 메디토프에 대해 낮거나 감소된 친화력을 나타내는 메디토프 결합 부위를 포함한다. 일부 실시양태에서, 제1 메디토프는 자유 메디토프이고, 제2 메디토프는 본원에 기술된 바와 같이 링커를 통해 자가-가교결합 항체에 부착된다. 이러한 실시 양태는 예를 들어 자유 메디토프를 사용하여 항체의 자가-가교결합을 제어하거나 변조할 때 유리할 수 있다. 다른 실시양태에서, 제1 메디토프는 링커를 통해 자가-가교결합 항체에 부착되고, 제2 메디토프는 자유 메디토프이다. 이러한 실시 양태는, 예를 들어 고농축 자유 메디토프를 사용할 때 및/또는 항원 수준 또는 농도가 낮거나 감소될 때 유리할 수 있다.
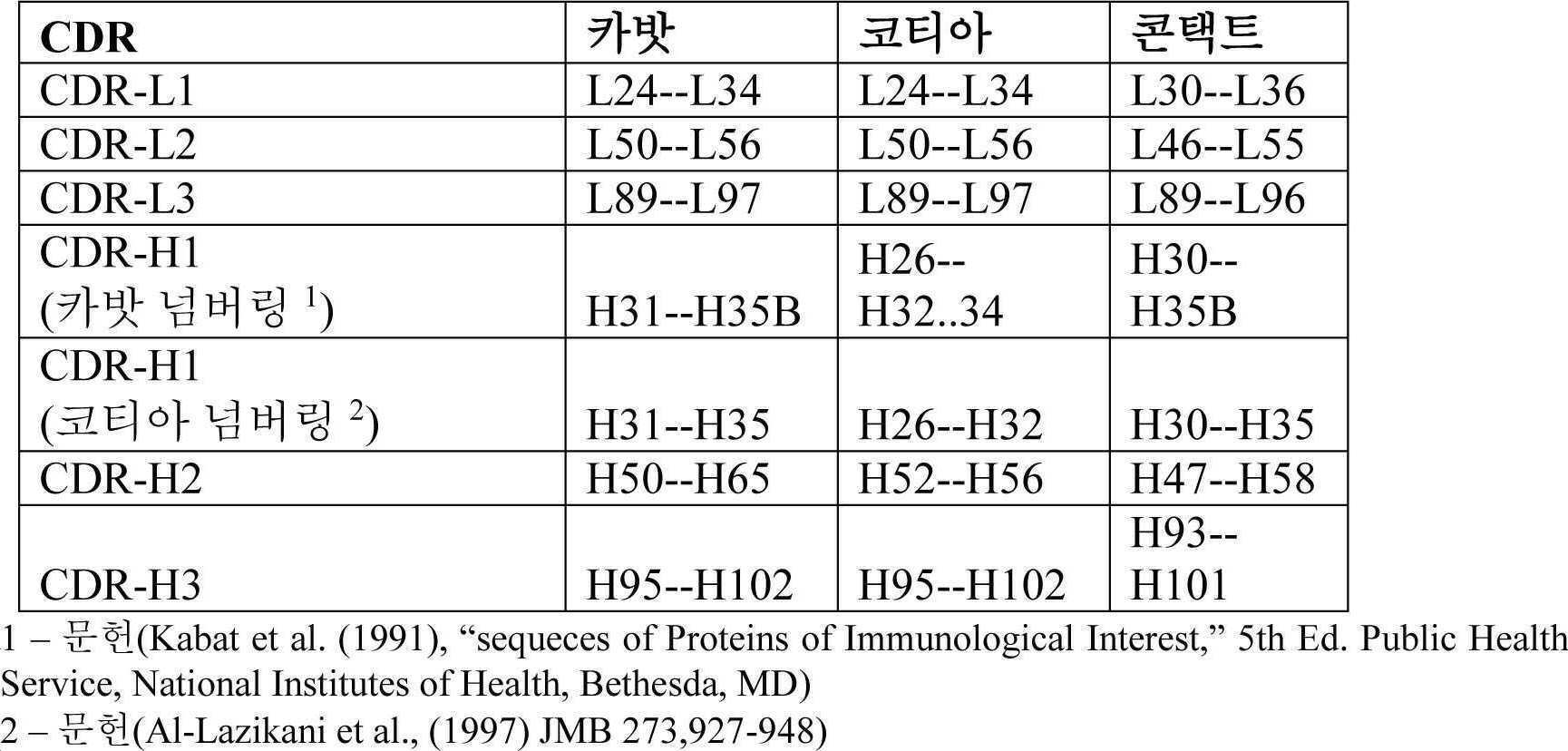
일부 실시양태에서, 대체되는 하나 이상의 잔기는 카밧 넘버링(그 전문이 본원에 참고로 포함된 문헌(Kabat E.A., et al. (1991) Sequences of Proteins of Immunological Interest, Fifth Edition. NIH Publication No. 91-3242) 참조)에 따라, 경쇄 골격 잔기 10, 39-43, 83, 85, 100 및/또는 104, 및/또는 카밧 넘버링에 따라, 중쇄 골격 잔기 번호 40, 89 및 105로부터 선택된다. 일반적으로, 달리 명시되지 않는다면, 항체의 중쇄 또는 경쇄 내 아미노산 위치는 카밧 넘버링을 참고한다. 또한, 본원에 기재된 세툭시맙의 잔기에 상응하는 기타 항체 내 잔기, 예를 들어 세툭시맙 메디토프 결합 부위 내 잔기는 본 개시내용 안에 포함된다. 일부 실시양태에서, 경쇄 잔기 9, 10, 39, 40, 41, 42, 43, 83, 85, 100, 및/또는 104, 및/또는 중쇄 잔기 40, 89, 및/또는 105에 상응하는 주형 항체 내 잔기는 예를 들어, 세툭시맙 내 이들 위치에 존재하는 아미노산으로 대체된다. 일부 실시양태에서, 메디토프-이용가능 항체는 이의 경쇄 골격 영역 내에서(또는 하나 이상의 상기 FR, 예를 들어, FR-L1, FR-L2, FR-L3, 및/또는 FR-L4 내에서) 주형 항체의 경쇄 골격 영역(또는 각각의 하나 이상의 FR-L(들))과 적어도 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99% 동일성을 포함하고/거나; 이의 중쇄 골격 영역 내에서(또는 하나 이상의 상기 FR, 예를 들어, FR-H1, FR-H2, FR-H3, 및/또는 FR-H4 내에서) 주형 항체의 중쇄 골격 영역(또는 각각의 하나 이상의 FR-H(들))과 적어도 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99% 동일성을 포함하고/거나; 이의 VH 영역 내에서, 주형 항체의 VH 영역과 적어도 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99% 동일성을 포함하고/거나; 이의 VL 영역 내에서, 주형 항체의 VL 영역과 적어도 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99% 동일성을 포함한다. 일부 실시양태에서, 항체는 주형 항체와 비교하여 중쇄 및/또는 경쇄 내 하나 이상, 예를 들어 전체 CDR 내에서 전부 또는 적어도 95, 96, 97, 98, 또는 99% 동일성을 포함한다. 일부 측면에서, 항체는 주형 항체와 비교하여 경쇄(예를 들어, FR-L) 내에 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20개의 변형을 포함하고/거나 주형 항체와 비교하여 중쇄(예를 들어, FR-H) 내에 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20개의 변형을 포함한다.
일 실시양태에서, 대체된 하나 이상의 잔기는 카밧 넘버링에 따라 40, 41, 83 및 85를 포함하는, 그러나 이에 제한되지 않는, 경쇄 골격 잔기이다. 일 실시양태에서, 경쇄 잔기 40은 트레오닌으로 대체되고; 경쇄 잔기 41은 아스파라긴으로 대체되며, 경쇄 잔기 83은 이소류신 또는 발린으로 대체되고/거나 경쇄 잔기 85는 아스파테이트로 대체된다. 한 실시양태에서, 경쇄 잔기 40은 트레오닌으로 대체되고; 경쇄 잔기 41은 아스파라긴으로 대체되며, 경쇄 잔기 83은 글루타메이트로 대체되고/거나 경쇄 잔기 85는 아스파테이트로 대체된다. 특정 예에서, 경쇄 골격 Pro40은 Thr(P40T) 또는 Ser(P40S)으로 대체되고, 경쇄 골격 Gly41은 Asn(G41N)으로 대체되며, 경쇄 골격 잔기 Phe83은 Ile(F83I) 또는 Val(F83V) 또는 글루타메이트(F83E)로 대체되고 경쇄 골격 Thr85는 Asp(T85D) 또는 Asn(T85N)으로 대체된다. 예를 들어, 세툭시맙을 포함하는 일부 실시양태에서, 경쇄 골격 골격 잔기 Ile83은 글루타메이트(I83E)로 대체된다.
따라서, 제공된 메디토프-이용가능 항체 중에는 세툭시맙 또는 기타 메디토프-이용가능 항체, 예를 들어 메디토프-이용가능 트라스투주맙 및 메디토프-이용가능 M5A를 포함하여 본원에 기재된 것의 메디토프 결합 부위 내 위치에 상응하는 잔기에서 하나 이상의 변형, 전형적으로 아미노산 치환을 갖는 항체가 있다. 상기 항체 중에는 카밧 넘버링에 따라, 위치 40에서 트레오닌, 세린 또는 아스파테이트, 위치 41에서 글리신 이외의 잔기, 및 위치 85에서 아스파테이트 또는 아스파라긴이 있는 VL 영역을 갖는 것들, 예를 들어, 위치 40에서 트레오닌, 위치 41에서 아스파라긴, 및 위치 85에서 아스파테이트를 갖는 VL 영역을 갖는 항체가 있다. 일부 실시양태에서, 항체는 카밧 넘버링에 따라, 위치 40에서 세린과 위치 89에서 이소류신을 갖는 VH 영역 및/또는 위치 40에서 세린 또는 프롤린과 위치 89에서 이소류신, 티로신, 메티오닌, 페닐알라닌, 또는 트립토판을 갖는 VH 영역을 갖는다. 일부 실시양태에서, VL 영역은 위치 10에서 이소류신 또는 류신, 및/또는 위치 83에서 이소류신 또는 위치 83에서 글루타메이트를 갖는다. 일부 실시양태에서, VL 영역은 위치 9에서 발린 또는 이소류신 및/또는 위치 100에서 글루타민 이외의 잔기를 갖는다.
일부 실시예에서, VL 영역은 카밧 넘버링에 따라, 위치 9에서 발린 또는 이소류신, 위치 10에서 이소류신 또는 류신, 위치 39에서 아르기닌, 위치 40에서 트레오닌, 위치 41에서 아스파라긴, 위치 42에서 글리신, 위치 43에서 세린, 위치 83에서 이소류신 또는 글루타메이트, 위치 85에서 아스파테이트, 및 위치 100에서 알라닌을 가지며; VH 영역은 위치 40에서 세린 및 위치 89에서 이소류신을 갖는다. 일부 실시예에서, VL 영역은 카밧 넘버링에 따라, 위치 40에서 프롤린, 위치 41에서 글리신, 또는 위치 85치에서 트레오닌을 포함하지 않고/거나 VH 영역은 카밧 넘버링에 따라, 위치 40에서 아스파라긴 또는 알라닌 또는 위치 89에서 발린을 포함하지 않는다. 일부 실시예에서, VL 영역은 카밧 넘버링에 따라, 위치 10에서 세린, 위치 40에서 프롤린, 위치 41에서 글리신, 위치 83에서 페닐알라닌, 또는 위치 85에서 트레오닌을 포함하지 않고/거나 VH 영역은 위치 40에서 아스파라긴 또는 알라닌 또는 위치 89에서 발린을 포함하지 않는다.
일부 측면에서, 항체는 카밧 넘버링에 따라, P8, V9 또는 I9, I10 또는 L10, Q38, R39, T40, N41, G42, S43, P44, R45, D82, I83, A84, D85, Y86, Y87, G99, A100, G101, T102, K103, L104, E105, R142, S162, V163, T164, E165, Q166, D167, S168, 및 Y173을 갖는 경쇄, 및/또는 카밧 넘버링에 따라, Q6, P9, R38, Q39, S40, P41, G42, K43, G44, L45, S84, D86, T87, A88, I89, Y90, Y91, W103, G104, Q105, G106, T107, L108, V109, T110, V111, Y147, E150, P151, V152, T173, F174, P175, A176, V177, Y185, S186, 및 L187을 갖는 중쇄를 갖는다.
일부 측면에서, 항체는 카밧 넘버링에 따라, P8 , V9 또는 I9, I10 또는 L10, Q38, R39, T40, N41, G42, S43, P44, R45, D82, E83, A84, D85, Y86, Y87, G99, A100, G101, T102, K103, L104, E105, R142, S162, V163, T164, E165, Q166, D167, S168, 및 Y173을 갖는 경쇄, 및/또는 카밧 넘버링에 따라 Q6, P9, R38, Q39, S40, P41, G42, K43, G44, L45, S84, D86, T87, A88, I89, Y90, Y91, W103, G104, Q105, G106, T107, L108, V109, T110, V111, Y147, E150, P151, V152, T173, F174, P175, A176, V177, Y185, S186, 및 L187을 갖는 중쇄를 갖는다.
일부 실시양태에서, 메디토프-이용가능 항체는 항체, 예를 들어 인간 또는 인간화 항체, 예를 들어, 트라스투주맙의 경쇄 내 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 또는 11개 잔기를 예를 들어 세툭시맙 내 상응하는 위치(카밧 넘버링기준)와 유사하도록, 변이시켜 생성된다. 일부 측면에서, 상기 항체는 인간 또는 인간화 서열에 비해, 카밧 넘버링을 기준으로 하여, 경쇄의 위치 9, 10, 39, 40, 41, 42, 43, 45, 83, 85, 및 100에서 돌연변이된 잔기를 포함한다. 한 측면에서, 메디토프-이용가능 항체의 경쇄는 카밧 넘버링을 기준으로 V9 또는 I9, I10 또는 L10, R39, T40, N41, G42, S43, R45, I83 또는 E83, D85, 및 A100, 예를 들어: V9, I10, R39, T40, N41, G42, S43, R45, I83, D85, 및 A100을 포함한다. 일부 실시양태에서, 항체는 그 외 인간 또는 인간화 항체이다.
일부 실시양태에서, 메디토프-이용가능 항체는 항체, 예를 들어 인간 또는 인간화 항체, 예를 들어, 트라스투주맙의 중쇄 내 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 또는 11개 잔기, 예를 들어 1 또는 2개 잔기를, 예를 들어 세툭시맙 내 상응하는 위치(카밧 넘버링기준)와 유사하도록, 변이시켜 생성된다. 일부 측면에서, 상기 항체는 인간 또는 인간화 서열에 비해, 카밧 넘버링을 기준으로 하여, 중쇄 내 위치 40 및 89에서 돌연변이된 잔기를 포함한다. 한 측면에서, 중쇄는 카밧 넘버링을 기준으로 S40 및 I89를 포함한다. 일부 실시양태에서, 항체는 그 외 인간 또는 인간화 항체이다.
일부 실시양태에서 메디토프-이용가능 항체는, 예를 들어 인간화 또는 인간 서열과 비교하여 13개의 돌연변이를 포함한다. 한 측면에서, 메디토프-이용가능 항체는 인간화 또는 인간 서열과 비교하여 11개의 돌연변이를 갖는 경쇄 및 2개의 돌연변이를 갖는 중쇄를 포함한다. 일부 측면에서, 항체는 카밧 넘버링을 기준으로 경쇄 내 V9 또는 I9, I10 또는 L10, R39, T40, N41, G42, S43, R45, I83, D85, 및 A100 및 중쇄 내 S40 및 I89를 포함한다. 일부 측면에서, 항체는 카밧을 기준으로 경쇄 내 V9 또는 I9, I10 또는 L10, R39, T40, N41, G42, S43, R45, E83, D85, 및 A100 및 중쇄 내 S40 및 I89를 포함한다. 일부 측면에서, 항체는 카밧 넘버링을 기준으로 경쇄 내 V9, I10, R39, T40, N41, G42, S43, R45, I83, D85, 및 A100 및 중쇄 내 S40 및 I89를 포함한다. 일부 측면에서, 항체는 카밧 넘버링을 기준으로 경쇄 내 V9, I10, R39, T40, N41, G42, S43, R45, E83, D85, 및 A100 및 중쇄 내 S40 및 I89를 포함한다. 일부 측면에서, 항체는 카밧 넘버링을 기준으로 경쇄 내 V9, I10, R39, T40, N41, G42, S43, R45, E83, D85, 및 A100 및 중쇄 내 S40 및 I89를 포함한다. 일부 실시양태에서, 항체 및/또는 이의 골격 영역은 그 외 인간 또는 인간화 항체이다.
다른 실시양태에서, 메디토프-이용가능 항체는 전형적으로 메디토프-이용가능 항체, 예를 들어 본원에 기재된 임의의 메디토프-이용가능 항체의 중쇄 및/또는 경쇄의 하나 이상의 상보성 결정 영역(CDR)(예를 들어, 하나 이상의 CDR 1-3)을 기타 CDR, 예를 들어 기존의 또는 신규 항체의 CDR로 대체하도록 변형시킴에 의한 CDR 이식(grafting)을 통하여 생성된다. CDR 이식은, 예를 들어, 생쥐와 같은 비-인간 종에서 생성된 항체의 CDR을 인간 항체 골격에 이식하여, 인간화 단클론 항체를 제조하기 위한 표준 실시법이다. 미국 특허 제5,558,864호 및 제8,133,982호; 문헌(Kettleborough et al., "Humanization of a mouse monoclonal antibody by CDR-grafting: the importance of framework residues on loop conformation, "Protein Eng., 4:773-783 (1991))을 참조한다. 따라서, 특정 실시양태에서, 메디토프-이용가능 항체의 항원 특이성은 기존의 또는 신규 생성된 관심 항체의 CDR을 이식하여 변경된다. 또한, 제공된 메디토프-이용가능 항체 중에 상기 CDR-이식된 메디토프-이용가능 항체가 있다.
일부 실시양태에서, 메디토프-이용가능 항체는 본원에 기재된 항체 중 하나(예를 들어, 세툭시맙, 메디토프-이용가능 트라스투맙, 또는 메디토프-이용가능 M5A(항-CEA) 항체)를 주형 서열로 사용하고, 이를 변경, 예를 들어, 이의 항원-결합 특징을 변경하는 공지된 하나 이상의 항체 조작법을 수행하고, 독특한 특징을 갖는 메디토프-이용가능 항체를 생산하여 생성된다. 항원 결합 및 기타 특성을 변경하는데 전형적으로 이용되는 공지된 항체 조작법은 오류유발(error-prone) PCR, 스파이크(spiked) PCR, 부위-지정 돌연변이 유발법, 파아지 디스플레이 및 기타 선별 방법을 포함한, 다양한 시험관 내 무작위 배정(in vitro randomization), 친화도 성숙, 및 선별 방법을 포함한다. 상기 방법을 수행하기 위한, 구조물, 라이브러리, 및 GPI-연관 발현 시스템을 포함한 발현 시스템이 또한 제공된다. 따라서, 특정의 실시양태에서, 제공된 메디토프-이용가능 항체는 메디토프-이용가능 항체, 예를 들어 세툭시맙, 메디토프-이용가능 트라스투주맙, 또는 메디토프-이용가능 M5A의 골격 영역 또는 영역들(FR)(또는 상기 항체의 FR(들)과 적어도 대략 75, 80, 85, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99% 동일성을 갖는 FR(들)을 갖는 경쇄 및/또는 중쇄 가변 영역을 갖는다. 일부 측면에서, 상기 항체는 메디토프-이용가능 항체의 CDR과 구별되는 하나 이상의 CDR을 갖는다.
예를 들어, 일부 실시양태에서, VL 영역은 서열번호 71에 개시된 경쇄 서열의 경쇄 골격 영역(FR) 1(FR-L1), FRL2, FR-L3, 및/또는 FR-L4(또는 서열 번호 71의 FR-L1, FR-L2, FR-L3, 및/또는 FR-L4와 적어도 대략 75, 80, 85, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99% 동일한 FR-L1, FR-L2, FR-L3, 및/또는 FR-L4), 및 일부 측면에서, 서열번호 71에 개시된 경쇄 서열의 CDR과 구별되는 적어도 하나의 CDR을 포함하는 아미노산 서열을 갖고/거나; VH 영역은 서열 번호 72에 개시된 중쇄 서열의 중쇄 FR1(FR-H1), FR-H2, FR-H3, 및/또는 FRH4(또는 서열 번호 72의 FR-H1, FR-H2, FR-H3, 및/또는 FR-H4와 적어도 대략 75, 80, 85, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99% 동일한 FR-H1, FR-H2, FR-H3, 및/또는 FR-H4), 및 일부 측면에서 서열번호 72에 개시된 중쇄 서열의 CDR과 구별되는 적어도 하나의 CDR을 갖는 아미노산 서열을 갖는다.
일부 실시양태에서, VL 영역은 서열번호 9에 개시된 경쇄 서열의 경쇄 골격 영역(FR) 1(FR-L1), FRL2, FR-L3, 및/또는 FR-L4(또는 서열번호 9의 FR-L1, FR-L2, FR-L3, 및/또는 FR-L4와 적어도 대략 75, 80, 85, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99% 동일한 FR-L1, FR-L2, FR-L3, 및/또는 FR-L4), 및 일부 측면에서, 서열번호 9에 개시된 경쇄 서열의 CDR과 구별되는 적어도 하나의 CDR을 포함하는 아미노산 서열을 갖고/거나; VH 영역은 서열번호 6에 개시된 중쇄 서열의 중쇄 FR1(FR-H1), FR-H2, FR-H3, 및/또는 FRH4(또는 서열번호 6의 FR-H1, FR-H2, FR-H3, 및/또는 FR-H4와 적어도 대략 75, 80, 85, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99% 동일한 FR-H1, FR-H2, FR-H3, 및/또는 FR-H4), 및 일부 측면에서 서열 번호 6에 개시된 중쇄 서열의 CDR과 구별되는 적어도 하나의 CDR을 갖는 아미노산 서열을 갖는다.
일부 실시양태에서, VL 영역은 서열번호 68에 개시된 경쇄 서열의 경쇄 골격 영역(FR) 1(FR-L1), FRL2, FR-L3, 및/또는 FR-L4(또는 서열번호 68의 FR-L1, FR-L2, FR-L3, 및/또는 FR-L4와 적어도 대략 75, 80, 85, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99% 동일한 FR-L1, FR-L2, FR-L3, 및/또는 FR-L4), 및 일부 측면에서, 서열번호 68에 개시된 경쇄 서열의 CDR과 구별되는 적어도 하나의 CDR을 포함하는 아미노산 서열을 갖고/거나; VH 영역은 서열번호 70에 개시된 중쇄 서열의 중쇄 FR1(FR-H1), FR-H2, FR-H3, 및/또는 FRH4(또는 서열 번호 70의 FR-H1, FR-H2, FR-H3, 및/또는 FR-H4와 적어도 대략 75, 80, 85, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99% 동일한 FR-H1, FR-H2, FR-H3, 및/또는 FR-H4), 및 일부 측면에서 서열번호 70에 개시된 중쇄 서열의 CDR과 구별되는 적어도 하나의 CDR을 갖는 아미노산 서열을 갖는다.
일부 실시양태에서, VL 영역은 서열 번호 61에 개시된 경쇄 서열의 경쇄 골격 영역(FR) 1(FR-L1), FRL2, FR-L3, 및/또는 FR-L4(또는 서열 번호 61의 FR-L1, FR-L2, FR-L3, 및/또는 FR-L4와 적어도 약 75, 80, 85, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99% 동일한 FR-L1, FR-L2, FR-L3, 및/또는 FR-L4), 및 일부 측면에서, 서열 번호 61에 개시된 경쇄 서열의 CDR과 구별되는 적어도 하나의 CDR을 포함하는 아미노산 서열을 갖고/거나; VH 영역은 서열 번호 63에 개시된 중쇄 서열의 중쇄 FR1(FR-H1), FR-H2, FR-H3, 및/또는 FRH4(또는 서열 번호 63의 FR-H1, FR-H2, FR-H3, 및/또는 FR-H4와 적어도 약 75, 80, 85, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99% 동일한 FR-H1, FR-H2, FR-H3, 및/또는 FR-H4), 및 일부 측면에서 서열 번호 63에 개시된 중쇄 서열의 CDR과 구별되는 적어도 하나의 CDR을 포함하는 아미노산 서열을 갖는다. 일부 실시양태에서, 메디토프-이용가능 항체는 서열번호 6, 7, 9, 10, 12, 14, 61, 63, 68, 69, 70, 71 및/또는 72에 개시된 CDR과 구별되는 하나 이상의 CDR을 갖는다.
일부 실시양태에서, 메디토프는 세툭시맙 이외의 항체이고/거나, EGFR에 특이적으로 결합하지 않고/거나, EGFR 이외의 항원에 결합하고/거나 세툭시맙에 의해 특이적으로 결합된 EGFR 상의 에피토프에 특이적으로 결합하지 않는다.
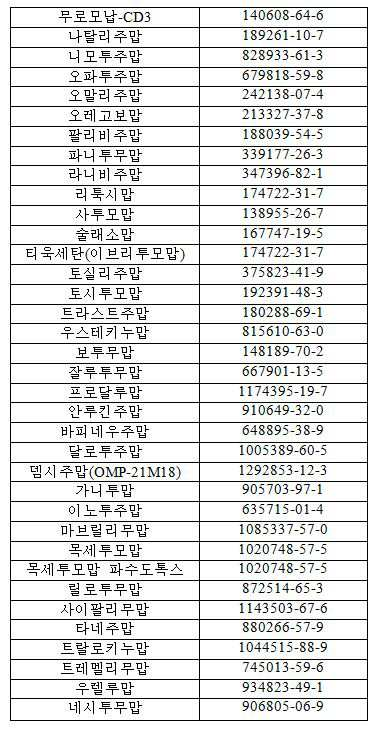
일부 실시예에서, 메디토프-이용가능 항체는 주형 항체를 기본으로 하여 생성되는데, 주형 항체는 아바고보맙, 아브식시맙, 아달리무맙, 아데카투무맙, 알렘투주맙, 알투모맙, 알투모맙 펜테테이트, 아나투모맙, 아나투모맙 마페나톡스, 아르시투모맙, 아틀리주맙, 바실릭시맙, 벡투모맙, 엑투모맙, 벨리무맙, 벤랄리주맙, 베바시주맙, 브렌툭시맙, 카나키누맙, 카프로맙, 카프로맙 펜데티드, 카투막소맙, 세르톨리주맙, 클리바투주맙 테트락세탄, 다클리주맙, 데노수맙, 에쿨리주맙, 에드레콜로맙, 에팔리주맙, 에타라시주맙, 에르투막소맙, 파놀레소맙, Fbta05, 폰톨리주맙, 젬투주맙, 지렌툭시맙, 골리무맙, 이브리투모맙, 이고보맙, 인플릭시맙, 이필리무맙, 라베투주맙, 메폴리주맙, 무로모납, 무로모맙-CD3, 나탈리주맙, 네시투무맙, 니모투주맙, 오파투무맙, 오말리주맙, 오레고보맙, 팔리비주맙, 파니투무맙, 라니비주맙, 리툭시맙, 사투모맙, 술레소맙, 이브리투모맙, 이브리투모맙 티욱세탄, 토실리주맙, 토시투모맙, 트라스투주맙, Trbs07, 우스테키누맙, 비실리주맙, 보투무맙, 잘루투무맙, 브로달루맙, 안루킨주맙, 바피네우주맙, 달로투주맙, 뎀시주맙, 가니투맙, 이노투주맙, 마브릴리무맙, 목세투모맙 파수도톡스, 릴로투무맙, 시팔리무맙, 타네주맙, 트랄로키누맙, 트레멜리무맙, 하이브리도마 10B5에 의해 생산된 항체, B6H12.2, 및 우렐루맙, 이들의 단편, CDR을 갖는 항체 및/또는 이의 항원-결합 영역, 및/또는 상기 항체와의 결합에 대해 경쟁하는 항체; 및/또는 서열번호 78-124, 및/또는 125-170 중 어느 하나에 개시된 서열을 갖는 항체, 이의 단편, CDR을 갖는 항체 및/또는 이의 항원-결합 영역, 및/또는 상기 항체와의 결합에 대해 경쟁하는 항체로부터 선택된다. [표 3]은 특정 항체에 대한 CAS® 등록 번호를 열거한다.
[표 3]
(이어서)
다른 실시예에서, 주형 항체는 하기 중에서 선택된다: 아바고보맙, 아브식시맙, 아달리무맙, 아데카투무맙, 알렘투주맙, 알투모맙, 알투모맙 펜테테이트, 아나투모맙, 아나투모맙 마페나톡스, 아르시투모맙, 아틀리주맙, 바실릭시맙, 벡투모맙, 엑투모맙, 벨리무맙, 벤랄리주맙, 베바시주맙, 브렌툭시맙, 카나키누맙, 카프로맙, 카프로맙 펜데티드, 카투막소맙, 세르톨리주맙, 클리바투주맙 테트락세탄, 다클리주맙, 데노수맙, 에쿨리주맙, 에드레콜로맙, 에팔리주맙, 에타라시주맙, 에르투막소맙, 파놀레소맙, Fbta05, 폰톨리주맙, 젬투주맙, 지렌툭시맙, 골리무맙, 이브리투모맙, 이고보맙, 인플릭시맙, 이필리무맙, 라베투주맙, 메폴리주맙, 무로모납, 무로모맙-CD3, 나탈리주맙, 네시투무맙, 니모투주맙, 오파투무맙, 오말리주맙, 오레고보맙, 팔리비주맙, 파니투무맙, 라니비주맙, 리툭시맙, 사투모맙, 술레소맙, 이브리투모맙, 이브리투모맙 티욱세탄, 토실리주맙, 토시투모맙, 트라스투주맙, Trbs07, 우스테키누맙, 비실리주맙, 보투무맙, 잘루투무맙, 하이브리도마 10B5에 의해 생산된 항체, 및 브로달루맙, 또는 티우제단. 일부 상기 예에서, 하나 이상의 CDR은 이들 주형 항체에 존재하는 CDR이고/거나, 항체는 상기 항체와 동일한 항원 또는 에피토프에 결합하고/거나, 이들 항원에 대한 상기 항체와의 결합에 대해 경쟁한다.
따라서, 일부 경우에, 메디토프-이용가능 항체(이들의 단편을 포함하여)는 하기로 이루어진 군으로부터 선택되는 항원에 특이적으로 결합한다: CA-125, 당단백질(GP) IIb/IIIa 수용체, TNF-알파, CD52, TAG-72, 암배아성 항원(CEA), 인터류킨-6 수용체(IL-6R), IL-2, 인터류킨-2 수용체 a-쇄(CD25), CD22, CD23(CD23A, Fc 엡실론 RII, FcεRII, FCE2, CLEC4J, C형 렉틴 도메인 패밀리 4 일원 J, 면역글로불린 E-결합 인자, 림프구 IgE 수용체, BLAST-2, 또는 IGEBF로도 알려짐), CD37 (테트라스패닌-26, TSPAN26, tspan-26, 또는 GP52-40으로도 알려짐), 뮤신-1, 프로락틴 수용체(PRL-R로도 알려짐), SDC-1(CD138, 신데칸, 프로테오글리칸 1, 신데칸 1, 또는 헤파란 설페이트 프로테오글리칸 섬유아세포 성장 인자 수용체로도 알려짐), B-세포 활성화 인자, 인터류킨-5 수용체(CD125), VEGF, VEGF-A, CD30, IL-1 베타, 전립선 특이적 막 항원(PSMA), CD3, EpCAM, EGF 수용체(EGFR), MUC1, 인간 인터류킨-2 수용체, Tac, RANK 리간드, 보체 단백질, 예를 들어, C5, EpCAM, CD11a, 예를 들어, 인간 CD11a, 인테그린, 예를 들어, 알파-v 베타-3 인테그린, 비트로넥틴 수용체 알파 v 베타 3 인테그린, HER2, neu, CD3, CD15, CD20(소루프 및/또는 대루프), 인터페론 감마, CD33, CA-IX, TNF 알파, CTLA-4, 암배아성 항원, IL-5, CD3 엡실론, CAM, 알파-4-인테그린, IgE, 예를 들어, IgE Fc 영역, RSV 항원, 예를 들어, 호흡기 세포융합 바이러스(RSV)의 융합 단백질, TAG-72, NCA-90(과립구 세포 항원), IL-6, GD2, GD3, IL-12, IL-23, IL-17, CTAA16.88, IL13, 인터류킨-1 베타, 베타-아밀로이드, IGF-1 수용체(IGF-1R), 델타-유사 리간드 4(DLL4), 과립구 대식세포 콜로니 자극 인자 수용체의 알파 서브유닛, 간세포 성장 인자, IFN-알파, 신경 성장 인자, IL-13, PD-L1, CD326, CD47, 및 CD137. 일부 실시예에서, 메디토프-이용가능 항원은 암 또는 기타 질환과 같은, 관심 질환 또는 병태에서 표적으로 확인되는 또 다른 항원에 결합한다.
1. CD19
일 실시양태에서, 주형 항체는 항-CD19 항체, 예를 들어, CD19에 대한 인간 또는 인간화 항체 또는 생쥐 항체, 예를 들어 MOR208, 또는 상기 항체의 중쇄, 경쇄, VH, 또는 VL을 갖는 항체, 또는 이의 기능적 단편이다. 일부 실시양태에서, 메디토프-이용가능 항체는 CD19에 특이적으로 결합한다. CD19(또는 분화 클러스터-19)는 예를 들어, NCBI 승인번호 NP_001171569 또는 유니프롯 식별자(UuniProt Identifier) P15391로 확인된다. 한 측면에서, CD19는 B-세포 모세포로의 발생 과정 중 가장 초기에 인식할 수 있는 B-계통 세포로부터 B 세포 표면에서 발견되지만 혈장세포로의 성숙 시 사라진다. 특정 측면에서, CD19는 항원 수용체-의존성 자극에 대한 역치를 감소시키는 조절 분자이다.
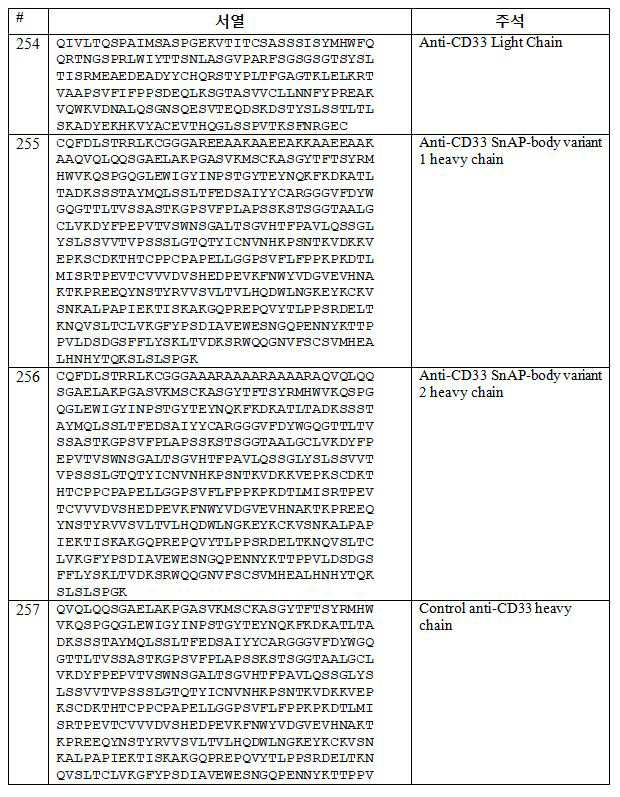
일부 실시양태에서, 주형 항체는 MOR208(XmAb®5574)(CD19, 예를 들어, 미성숙, 성숙 및 악성 종양 B 세포의 CD19에 특이적으로 결합하는 단클론 항체)의 경쇄 및 중쇄 아미노산 서열을 각각 개시하는 서열번호 226 및/또는 서열번호 227(선도 서열을 포함 또는 미포함)의 아미노산 서열을 포함하고/거나, MOR208의 VL 및 VH 아미노산 서열을 각각 개시하는 서열번호 245 및/또는 246(선도 서열 포함 또는 미포함)의 아미노산 서열을 포함한다.
일부 측면에서, 메디토프-이용가능 항체 또는 단편은 서열번호 226에 개시된 경쇄 서열 또는 MOR208의 경쇄 또는 VL의 CDR(즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2, 및/또는 CDR3), 및/또는 서열번호 227에 개시된 중쇄 서열 또는 MOR208의 중쇄 또는 VH의 CDR(즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2, 및/또는 CDR3)을 갖는다.
일부 측면에서, 메디토프-이용가능 항체의 VL 영역은 선도 서열을 포함 또는 미포함하는 서열번호 245에 개시된 아미노산 서열과 비교하여 하나 이상, 일반적으로 다수의 변형(일반적으로 골격 영역에 존재), 예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20개 변형을 포함하고/거나, 메디토프-이용가능 항체의 VH 영역은 선도 서열을 포함 또는 미포함하는 서열번호 246에 개시된 아미노산 서열의 VH 영역의 아미노산 서열과 비교하여 하나 이상, 예를 들어, 다수의 변형(일반적으로 골격 영역에 존재), 예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20개 변형을 포함한다.
일부 실시양태에서, 메디토프-이용가능 항체는 이의 경쇄 골격 영역 내에서(또는 하나 이상의 상기 영역 내에서, 예를 들어, FR-L1, FR-L2, FR-L3, 및/또는 FR-L4 내에서), MOR208, 또는 서열번호 226의 경쇄 골격 영역(또는 각각의 하나 이상의 FR-L(들))과 적어도 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99% 동일성을 포함하고/거나; 이의 중쇄 골격 영역 내에서(또는 하나 이상의 상기 영역 내에서, 예를 들어, FR-H1, FR-H2, FR-H3, 및/또는 FR-H4 내에서), MOR208, 또는 서열번호 227의 중쇄 골격 영역(또는 각각의 하나 이상의 FR-H)과 적어도 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99% 동일성을 포함하고/거나; 이의 VH 영역 내에서, MOR208, 또는 서열번호 246의 VH 영역과 적어도 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99% 동일성을 포함하고/거나; 이의 VL 영역 내에서, MOR208, 또는 서열 번호 245의 VL 영역과 적어도 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99% 동일성을 포함한다. 일부 실시양태에서, 항체는 MOR208과 비교하여(예를 들어, 서열번호 226 또는 227의 CDR(들)과 비교하여) 중쇄 및/또는 경쇄 내 하나 이상, 예를 들어 모든 CDR 내에서 전부 또는 적어도 95, 96, 97, 98, 또는 99% 동일성을 포함한다.
일부 측면에서, 메디토프-이용가능 항체는 MOR208에 의해 특이적으로 결합된 CD19의 에피토프에 특이적으로 결합하지 않지만, CD19에 특이적으로 결합하거나, MOR208의 CDR을 포함하지 않고/거나, MOR208과 항원 결합에 대해 경쟁하지 않지만, CD19에 특이적으로 결합한다.
일부 실시양태에서, 메디토프-이용가능 항체 또는 단편은 서열번호 305의 아미노산 서열을 포함하는 경쇄를 포함하고/거나 서열번호 306의 아미노산 서열을 포함하는 중쇄를 포함한다. 일부 실시양태에서, 메디토프-이용가능 항체 또는 단편은 cQFD 메디토프, 변이체 3 링커를 포함하고/거나 메디토프-이용가능 항 CD19 항체(예를 들어, 서열번호 306)의 중쇄에 융합된다.
2. CD22
일부 실시양태에서, 주형 항체(template antibody)는 항-CD22 항체이다. 예를 들어, 에프라투주맙, 또는 목세투모맙 또는 이러한 항체의 중쇄, 경쇄, VH 또는 VL를 갖는 항체 또는 이의 기능적 단편과 같은, CD22에 대한 인간 또는 인간화 항체 또는 마우스 항체이다. 일부 실시양태에서, 상기 메디토프-이용가능 항체는 CD22에 특이적으로 결합한다. CD22 (또는 분화 클러스터-22)는 예를 들어, NCBI Accession No. NP_001762 또는 UniProt Identifier P20273에 의해 확인된, SIGLEC 계열의 렉틴(lectins)에 속하는 분자이다. 일 측면에서, CD22는 성숙 B 세포(mature B cells)의 표면에서 발견되며, 일부 미성숙 B 세포에서는 보다 적게 발견된다. 특정 측면에서, CD22는 면역계의 과다 활성화 및 자가 면역 질환의 발병을 예방하는 조절 분자이다. 일 실시 양태에서, CD22에 대한 주형 항체는 서열번호 175의 아미노산 서열을 갖는 폴리 펩타이드 또는 단백질, 또는 서열번호 176의 핵산 서열을 포함하는 폴리뉴클레오티드에 의해 코딩되는 아미노산 서열을 갖는 폴리펩타이드 또는 단백질 상의 하나 이상의 에피토프와 특이적으로 결합한다.
일부 실시양태에서, 주형 항체는 각각 에프라투주맙(예를 들어 성숙 및 악성 B 세포의 CD22와 같은 CD22에 특이적으로 결합하는 인간화 단일클론 항체)의 경쇄 및 중쇄 아미노산 서열을 기재하는(set forth) 서열번호 177 및/또는 서열번호 178의 아미노산 서열 (각 서열에서 서열 내의 아미노산 위치에 의해 식별되는 리더 서열을 갖거나 갖지 않음)을 포함하고/포함하거나, 각각 에프라투주맙의 VL 및 VH 아미노산 서열을 기재하는 서열번호 179 및/또는 183(각 서열에서 서열 내의 아미노산 위치에 의해 동정되는 리더 서열을 갖거나 갖지 않음)의 아미노산 서열을 포함한다.
에프라투주맙 경쇄 서열은 서열번호 177에 기재되어 있으며, 이는 서열번호 177의 아미노산 1 내지 20 위치에 기재된 리더 서열을 포함한다. 에프라투주맙 중쇄 서열은 서열번호 178에 기재되어 있으며, 이는 서열 번호 178의 아미노산 위치 1 내지 19에 기재된 리더 서열을 포함한다. 에프라투주맙 경쇄 가변 (VL) 영역 서열은 서열 번호 179에 기재되어 있으며, 이는 서열 번호 179의 아미노산 1-20 위치에 기재된 리더 서열을 포함한다. 에프라투주맙 중쇄 가변 (VH) 영역 서열은 서열번호 183에 기재되어 있으며, 이는 서열번호 183의 아미노산 위치 1 내지 19에 기재된 리더 서열을 포함한다.
일부 측면에서, 상기 메디토프-이용가능 항체 또는 단편은 서열번호 177 또는 서열번호 179에 기재된 경쇄 또는 VL 서열, 또는 에프라투주맙의 경쇄 또는 VL 의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3) 및/또는 서열번호 178 또는 183에 기재된 중쇄 또는 VH 서열, 또는 에프라투주맙의 중쇄 또는 VH 의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3)을 갖는다.
일부 측면에서, 메디토프-이용가능 항체의 VL 영역은, 리더 서열을 갖거나 갖지 않는, 서열번호 179로 기재되는 아미노산 서열과 비교하여, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20 개의 변이(modifications)와 같은, 하나 이상의, 일반적으로 다수의 변이(일반적으로 골격 영역에 존재하는)를 포함하고/포함하거나, meditope-enabled antibody의 VH 영역은, 리더 서열을 갖거나 갖지 않는, 서열번호 183의 아미노산 서열과 비교하여, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20 개의 변이와 같은, 하나 이상의, 예를 들어 다수의 변이(일반적으로 골격 영역에 존재하는)를 포함한다.
일부 실시양태에서, 메디토프-이용가능 항체는, 그의 경쇄 골격 영역(light chain framework) 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어, FR-L1, FR-L2, FR-L3 및/또는 FR-L4 내에), 에프라투주맙, 서열번호 178 또는 183의 경쇄 골격 영역(또는 각각의 하나 이상의 FR-L (s))과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성을 포함한다; 그리고/또는 그의 중쇄 골격 영역 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어 FR-H1, FR-H2, FR-H3 및/또는 FR-H4 내에), 에프라투주맙, 서열번호 178 또는 183의 중쇄 골격 영역 (또는 각각 하나 이상의 FR-H)과 적어도 또는 대략 75, 76, 77 , 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성을 포함한다; 그리고/또는 그것의 VH 영역 내에, 에프라투주맙의 VH 영역 (예를 들어, 서열번호 183의 아미노산 서열)과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99%의 동일성을 포함한다; 그리고/또는 그것의 VL 영역 내에, 에프라투주맙의 VL 영역(예를 들어, 서열번호 179의 아미노산 서열)과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99 %의 동일성을 포함한다; 일부 실시양태에서, 상기 항체는 에프라투주맙과 비교하여(예를 들어 서열번호 177 또는 179 또는 서열번호 178 또는 183의 CDR(S)과 비교하여) 상기 중쇄 및/또는 경쇄 내의 CDR 중 하나 이상, 예를 들어 모두 내에, 모든 또는 적어도 95, 96, 97, 98, 또는 99 %의 동일성을 포함한다.
일부 측면에서, 상기 메디토프-이용가능 항체는 에프라투주맙에 특이적으로 결합되는 CD22의 에피토프에 특이적으로 결합하지 않으나, CD22에 특이적으로 결합하거나, 또는 에프라투주맙의 CDR을 포함하지 않고/않거나 항원 결합을 위해 에프라투주맙과 경쟁하지 않지만, CD22에 특이적으로 결합한다.
일부 실시양태에서, 주형 항체는, 목세투모맙(항-CD22 마우스 단일클론 항체)의 VL 및 VH 아미노산 서열을 기재하는, 서열번호 65 및/또는 서열번호 67의 아미노산 서열 (서열번호 67의 N-말단 메티오닌인 리더 서열/잔기를 갖거나 갖지 않음)을 포함하고/하거나, 목세투모맙의 중쇄 아미노산 서열을 기재하는 서열번호 66의 아미노산 서열(서열번호 66의 N-말단 메티오닌인 리더 서열을 갖거나 갖지 않음)을 포함한다.
일부 측면에서, 상기 메디토프-이용가능 항체 또는 단편은 서열번호 65에 기재된 VL 서열, 또는 목세투모맙의 경쇄 또는VL의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3) 및/또는 서열번호 66 또는 67에 기재된 중쇄 또는 VH 서열, 또는 목세투모맙의 중쇄 또는 VH 의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3)을 갖는다.
일부 측면에서, 메디토프-이용가능 항체의 VL 영역은, 리더 서열을 갖거나 갖지 않는 서열번호 65로 기재되는 아미노산 서열 또는 목세투모맙의 VL과 비교하여, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20 개의 변이와 같은, 하나 이상의, 일반적으로 다수의 변이(일반적으로 골격 영역에 존재하는)를 포함하고/포함하거나, 메디토프-이용가능 항체의 VH 영역은, 리더 서열을 갖거나 갖지 않는, 서열번호: 67의 아미노산 서열 또는 목세투모맙의 VH와 비교하여, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20 개의 변이와 같은, 하나 이상의, 예를 들어 다수의 변이(일반적으로 골격 영역에 존재하는)를 포함한다.
일부 실시양태에서, 메디토프-이용가능 항체는, 그것의 경쇄 골격 영역 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어, FR-L1, FR-L2, FR-L3 및/또는 FR-L4 내에), 목세투모맙 또는 서열번호 65의 경쇄 골격 영역(또는 각각의 하나 이상의 FR-L (s))과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성을 포함한다; 그리고/또는 그것의 중쇄 골격 영역 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어 FR-H1, FR-H2, FR-H3 및/또는 FR-H4 내에), 목세투모맙, 서열번호 66 또는 67의 중쇄 골격 영역 (또는 각각 하나 이상의 FR-H)과 적어도 또는 대략 75, 76, 77 , 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성을 포함한다; 그리고/또는 그것의 VH 영역 내에, 목세투모맙의 VH 영역 (예를 들어, 서열번호 67의 아미노산 서열)과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99%의 동일성을 포함한다; 그리고/또는 그것의 VL 영역 내에, 목세투모맙의 VL 영역(예를 들어, 서열번호 65의 아미노산 서열)과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99 %의 동일성을 포함한다; 일부 실시양태에서, 상기 항체는 목세투모맙과 비교하여(예를 들어 서열번호 65또는 66 또는 67의 CDR(S)과 비교하여) 상기 중쇄 및/또는 경쇄 내의 CDR 중 하나 이상 (예를 들어, 모두) 내에, 모든 또는 적어도 95, 96, 97, 98, 또는 99 % 의 동일성을 포함한다.
일부 측면에서, 상기 메디토프-이용가능 항체는 목세투모맙에 특이적으로 결합되는 CD22의 에피토프에 특이적으로 결합하지 않으나, CD22에 특이적으로 결합하거나, 또는 목세투모맙의 CDR을 포함하지 않고/않거나 항원 결합을 위해 목세투모맙과 경쟁하지 않지만, CD22에 특이적으로 결합한다.
3. CD23
일부 실시양태에서, 주형 항체는 항-CD23 항체이다. 예를 들어, 루밀릭시맙(lumiliximab) 또는 이러한 항체의 중쇄, 경쇄, VH 또는 VL을 갖는 항체 또는 이의 기능적 단편과 같은, CD23에 대한 인간 또는 인간화 항체또는 마우스 항체이다
일부 실시양태에서, 상기 메디토프-이용가능 항체는 CD23에 특이적으로 결합한다. CD23은 Fc 엡실론(epsilon) RII 또는 FcεRII로 알려져 있으며, 기생충에 대한 알러지 및 내성에 관여하는 항체 이소 타입인 IgE에 대한 "낮은 친화성 "수용체이며, IgE 수준의 조절에 있어서 중요하다.
CD23은, 예를 들어 NCBI Accession No. NP_001193948.2 또는 UniProt Identifier P06734에 의해 확인된 바와 같이, C-형 렉틴 (lectin)이다. CD23 항원은 여러 조혈 세포(hematopoietic cell) 유형에서 발현되는 45kDa 타입 II 막 관통성 당 단백질(transmembrane glycoprotein) 이다. 일부 측면에서, CD23은 성숙 B 세포, 활성화된 대식세포(activated macrophages), 호산구(eosinophils), 낭포 수지상 세포(follicular dendritic cells) 및 혈소판(platelets)에서 발현된다. CD23은 면역 글로불린 유전자 수퍼패밀리 (immunoglobulin gene superfamily)에 속하지 않는 유일한 FcR입니다. CD23의 기능은 B 세포에 의한 IgE 생산의 조절 및 배중심-유래(germinal center-derived) B 세포의 생존 촉진을 포함한다. CD23의 발현은 정상적으로 활성화된 낭포(follicular) B 세포 및 CLL 세포에서 고도로 상향 조절된다.
일 실시 양태에서, CD23에 대한 주형 항체는 서열번호 172의 아미노산 서열을 갖는 폴리펩타이드 또는 단백질, 또는 서열번호 184의 핵산 서열을 포함하는 폴리뉴클레오티드에 의해 코딩되는 아미노산 서열을 갖는 폴리펩타이드 또는 단백질 상의 하나 이상의 에피토프와 특이적으로 결합한다.
일 실시 양태에서, 주형 항체는 각각 루밀릭시맙(lumiliximab)의 VL 및 VH 아미노산 서열을 나타내는 서열번호 185 및/또는 서열번호 190의 아미노산 서열(적용가능한 경우, 서열번호 185의 아미노산 1-22 및 서열번호 190의 아미노산 1-19에 상응하는 리더서열/잔기를 갖거나 갖지 않음)을 포함한다.
루밀릭시맙(Lumiliximab) (IDEC-152, P5E8, gomiliximab으로도 알려짐; Biogen Idec)은 긴꼬리 원숭이 가변 영역 (cynomolgus macaque variable regions) 및 인간 불변 영역(human constant regions)(IgG1-κ)을 포함하는 영장류화된 (primatized) 항-CD23 mAb이다. 이것은 원래 활성화된 인간 말초 혈액 B 세포(activated human peripheral blood B cells)에 의한 IgE 생산을 억제하기 위해 개발되었다; 그러나, 나중에 그것은 강력한 항-CD23 mAb로서의 인식을 얻었다. 전임상 데이터(Preclinical data)는 루밀릭시맙(Lumiliximab)이 세포 자멸(apoptosis)(즉, 항-세포 자멸 단백질 Bcl-2, Bcl-XL 및 XIAP의 하향 조절, Bax의 활성화 및 미토콘드리아 시토크롬 c의 방출을 유도함)의 고유 경로(intrinsic pathway)에 의해 주로 CLL 세포와 CD23-발현 B-세포에 대한 항 종양 효과를 매개한다는 것을 시사한다. 상승적 세포 독성(Synergistic cytotoxicity)은 또한 루밀릭시맙(Lumiliximab)이 이종 이식 모델 (xenograft models)에서 리투시맙(rituximab) 또는 플루다라빈(fludarabine)과 결합하였을 때 CD23-발현 B-세포주(CD23-expressing B-cell lines) 및 원발성 CLL 세포(primary CLL cells )에서 입증되었다. 46명의 헤비하게 전처리된(heavily pretreated) CLL 환자에 대한 제1 임상 실험에서, 루밀릭시맙(Lumiliximab)은 단일 약제로서 적당한 임상 활성(modest clinical activity)을 보였다.
객관적인 CRs (Complete Responses) 또는 PRs (Partial Responses)는 관찰되지 않았지만, 루밀릭시맙(Lumiliximab)은 환자의 52 %에서 확대된 림프절 크기를 감소시켰으며 환자의 91 %에서 말초 혈액 림프구 수를 감소시켰다. 루밀릭시맙(Lumiliximab)의 안전성 프로파일(safety profile)은 대부분의 부작용(adverse events, AEs)이 1/2 등급으로 제한된다는 것을 입증하였다. 루밀릭시맙(Lumiliximab)은 면역억제성(immunosuppressive)이 아니었고 MTD (maximum tolerated dose)에 도달하지 못했다
일부 측면에서, 상기 메디토프-이용가능 항체 또는 단편은 서열번호 185에 기재된 VL 서열, 또는 루밀릭시맙(Lumiliximab)의 경쇄 또는VL의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3), 및/또는 서열번호 190에 기재된 VH 서열, 또는 루밀릭시맙(Lumiliximab)의 중쇄 또는 VH 의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3)을 갖는다.
일부 측면에서, 메디토프-이용가능 항체의 VL 영역은, 리더 서열을 갖거나 갖지 않는 서열번호 185로 기재되는 아미노산 서열 또는 루밀릭시맙(Lumiliximab)의 VL과 비교하여, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또 20 개의 변이(modifications)와 같은, 하나 이상의, 일반적으로 다수의 변이(일반적으로 골격(framework) 영역에 존재하는)를 포함하고/포함하거나, 메디토프-이용가능 항체의 VH 영역은, 리더 서열을 갖거나 갖지 않는, 서열번호 190의 아미노산 서열 또는 루밀릭시맙(Lumiliximab)의 VH와 비교하여, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20 개의 변이와 같은, 하나 이상의, 예를 들어 다수의 변이(일반적으로 골격 영역에 존재하는)를 포함한다.
일부 실시양태에서, 메디토프-이용가능 항체는, 그것의 경쇄 골격 영역(light chain framework) 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어, FR-L1, FR-L2, FR-L3 및/또는 FR-L4 내에), 루밀릭시맙(Lumiliximab) 또는 서열번호 185의 경쇄 골격 영역(또는 각각의 하나 이상의 FR-L (s))과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성(identity)을 포함한다; 그리고/또는 그것의 중쇄 골격 영역(heavy chain framework) 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어 FR-H1, FR-H2, FR-H3 및/또는 FR-H4 내에), 루밀릭시맙(Lumiliximab), 서열번호 190의 중쇄 골격 영역 (또는 각각 하나 이상의 FR-H)과 적어도 또는 대략 75, 76, 77 , 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성을 포함한다; 그리고/또는 그것의 VH 영역 내에, 루밀릭시맙(Lumiliximab)의 VH 영역 (예를 들어, 서열번호 190의 아미노산 서열)과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99%의 동일성을 포함한다; 그리고/또는 그것의 VL 영역 내에, 루밀릭시맙(Lumiliximab)의 VL 영역(예를 들어, 서열번호 185의 아미노산 서열)과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99 %의 동일성을 포함한다; 일부 실시양태에서, 상기 항체는 루밀릭시맙(Lumiliximab)과 비교하여(예를 들어 서열번호 185또는 190의 CDR(S)과 비교하여) 상기 중쇄 및/또는 경쇄 내의 CDR 중 하나 이상, 예를 들어, 모두 내에, 모든 또는 적어도 95, 96, 97, 98, 또는 99 % 의 동일성을 포함한다.
일부 측면에서, 상기 메디토프-이용가능 항체는 루밀릭시맙(Lumiliximab)에 특이적으로 결합되는 CD23의 에피토프에 특이적으로 결합하지 않으나, CD23에 특이적으로 결합하거나, 또는 루밀릭시맙(Lumiliximab)의 CDR을 포함하지 않고/않거나 항원 결합을 위해 루밀릭시맙(Lumiliximab)과 경쟁하지 않지만, CD23에 특이적으로 결합한다
4. CD33
일 실시 양태에서, 주형 항체(template antibody)는 항-CD33 항체이다. 예를 들어, 젬투주맙 (gemtuzumab) 또는 이러한 항체의 중쇄, 경쇄, VH 또는 VL을 갖는 항체 또는 이의 기능적 단편과 같은, CD33에 대한 인간 또는 인간화 항체(humanized antibody) 또는 마우스 항체이다. 일부 실시양태에서, 상기 메디토프-이용가능 항체는 항체는 CD33에 특이 적으로 결합한다. CD33 (또는 분화 클러스터-33)은 UniProt Identifier P20138에 의해 확인된다. 일 측면에서, CD33은 골수 세포의 표면에서 발견된다.
일부 실시양태에서, 주형 항체는 젬투주맙(Mylotarg)(미성숙, 성숙 및 악성 B 세포의 CD33과 같은 CD33에 특이적으로 결합하는 단일 클론 항체)의 경쇄 및 중쇄 아미노산 서열을 각각 나타내는 서열번호 224 및/또는 서열번호 225의 아미노산 서열(리더 서열을 갖거나 갖지 않음)을 포함하고/포함하거나, 각각 젬투주맙(gemtuzumab)의 VL 및 VH 아미노산 서열을 기재하는 서열번호 243 및/또는 245의 아미노산 서열(리더 서열을 갖거나 갖지 않음)을 포함한다.
일부 실시양태에서, 상기 메디토프-이용가능 항체 또는 단편(fragment) 은 서열번호 293의 아미노산 서열을 포함하는 경쇄를 갖고/갖거나 서열번호 294의 아미노산 서열을 포함하는 중쇄를 갖는다. 일부 실시양태에서, 상기 메디토프-이용가능 항체 또는 단편은 cQFD 메디토프, 변이형 1 링커(variant 1 linker)를 포함하고/포함하거나 메디토프 인에이블된(meditope enabled) 젬투주맙(gemtuzumab)(예를 들어, 서열번호 294)의 중쇄에 융합된다.
일부 실시양태에서, 상기 메디토프-이용가능 항체 또는 단편(fragment) 은 서열번호 295의 아미노산 서열을 포함하는 경쇄를 갖고/갖거나 서열번호 296의 아미노산 서열을 포함하는 중쇄를 갖는다. 일부 실시양태에서, 상기 메디토프-이용가능 항체 또는 단편은 cQFD 메디토프, 변이형 2 링커(variant 2 linker)를 포함하고/포함하거나 메디토프 인에이블된(meditope enabled) 젬투주맙(예를 들어, 서열번호 296)의 중쇄에 융합된다.
일부 실시양태에서, 상기 메디토프-이용가능 항체 또는 단편(fragment) 은 서열번호 297의 아미노산 서열을 포함하는 경쇄를 갖고/갖거나 서열번호 298의 아미노산 서열을 포함하는 중쇄를 갖는다. 일부 실시양태에서, 상기 메디토프-이용가능 항체 또는 단편은 cQFD 메디토프, 변이형 3 링커(variant 3 linker)를 포함하고/포함하거나 메디토프 인에이블된(meditope enabled) 젬투주맙(gemtuzumab)(예를 들어, 서열번호 298)의 중쇄에 융합된다.
일부 측면에서, 상기 메디토프-이용가능 항체 또는 단편은 서열번호 177 또는 서열번호 224에 기재된 경쇄 서열, 또는 젬투주맙(gemtuzumab)의 경쇄 또는 VL 의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3) 및/또는 서열번호 225에 기재된 중쇄, 또는 젬투주맙의 중쇄 또는 VH 의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3)을 갖는다.
일부 측면에서, 메디토프-이용가능 항체의 VL 영역은, 리더 서열을 갖거나 갖지 않는 서열번호 243으로 기재되는 아미노산 서열과 비교하여, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20 개의 변이(modifications)와 같은, 하나 이상의, 일반적으로 다수의 변이(일반적으로 골격(framework) 영역에 존재하는)를 포함하고/포함하거나, 메디토프-이용가능 항체의 VH 영역은, 리더 서열을 갖거나 갖지 않는, 서열번호 244로 기재되는 아미노산 서열의 VH영역의 아미노산 서열과 비교하여, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20 개의 변이와 같은, 하나 이상의, 예를 들어 다수의 변이(일반적으로 골격 영역에 존재하는)를 포함한다.
일부 실시양태에서, 상기 메디토프-이용가능 항체는, 그것의 경쇄 골격 영역 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어, FR-L1, FR-L2, FR-L3 및/또는 FR-L4 내에), 젬투주맙(gemtuzumab) 또는 서열번호 224의 경쇄 골격 영역(또는 각각의 하나 이상의 FR-L (s))과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성(identity)을 포함한다; 그리고/또는 그것의 중쇄 골격 영역(heavy chain framework) 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어 FR-H1, FR-H2, FR-H3 및/또는 FR-H4 내에), 젬투주맙(gemtuzumab), 또는 서열번호 225의 중쇄 골격 영역 (또는 각각 하나 이상의 FR-H)과 적어도 또는 대략 75, 76, 77 , 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성을 포함한다; 그리고/또는 그것의 VH 영역 내에, 젬투주맙(gemtuzumab) 또는 서열번호 244의 VH 영역과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99%의 동일성을 포함한다; 그리고/또는 그것의 VL 영역 내에, 젬투주맙(gemtuzumab) 또는 서열번호 243의 VL 영역과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99 %의 동일성을 포함한다; 일부 실시양태에서, 상기 항체는 젬투주맙(gemtuzumab)과 비교하여(예를 들어, 서열번호 224 또는 225의 CDR(S)과 비교하여), 상기 중쇄 및/또는 경쇄 내의 CDR 중 하나 이상 (예를 들어, 모두) 내에, 모든 또는 적어도 95, 96, 97, 98, 또는 99 % 의 동일성을 포함한다.
일부 측면에서, 상기 메디토프-이용가능 항체는 젬투주맙(gemtuzumab)에 특이적으로 결합되는 CD33의 에피토프에 특이적으로 결합하지 않으나, CD33에 특이적으로 결합하거나, 또는 젬투주맙(gemtuzumab)의 CDRs을 포함하지 않고/않거나 항원 결합을 위해 젬투주맙(gemtuzumab)과 경쟁하지 않지만, CD33에 특이적으로 결합한다.
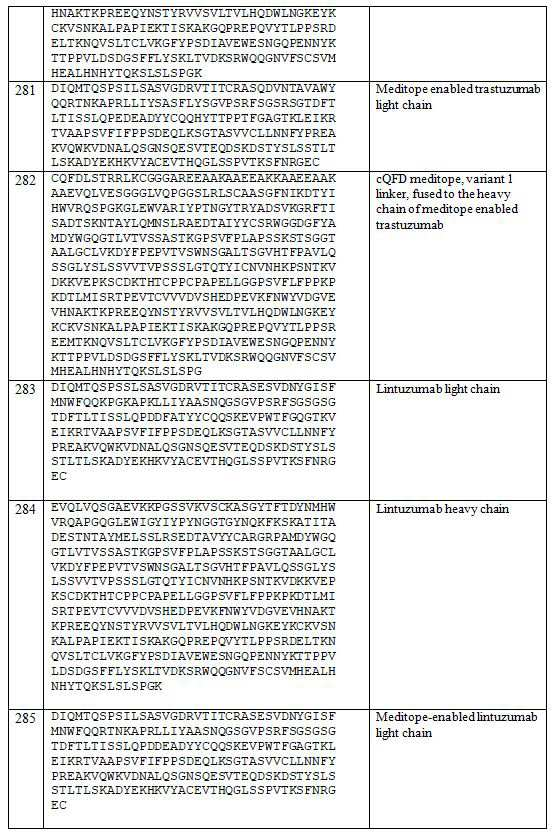
일 실시 양태에서, 본 명세서(disclosure)는 메디토프-이용가능 린투주맙(meditope-enabled lintuzumab)을 제공한다. 일 실시 양태에서, 메디토프-이용가능 린투주맙은 서열번호 289, 290, 291 또 는292의 중쇄를 포함한다. 일 실시 양태에서, 메디토프-이용가능 린투주맙은 서열번호 285, 286, 287 또는 288의 경쇄를 포함한다. 린투주맙(lintuzumab)의 본래의(original) 아미노산 서열은 참조로서 서열번호 284 (중쇄) 및 283 (경쇄)에 제공된다.
일 실시 양태에서, 주형 항체(template antibody)는 항-CD33 항체이다. 예를 들어, 린투주맙(lintuzumab)또는 이러한 항체의 중쇄, 경쇄, VH 또는 VL을 갖는 항체 또는 이의 기능적 단편과 같은, CD33에 대한 인간 또는 인간화 항체(humanized antibody) 또는 마우스 항체이다. 일부 실시양태에서, 상기 메디토프-이용가능 항체는 항체는 CD33에 특이 적으로 결합한다. CD33(또는 분화 클러스터-33)은 UniProt Identifier P20138에 의해 확인된다. 일 측면에서, CD33은 골수 세포(myeloid cells)의 표면에서 발견된다.
일부 실시양태에서, 주형 항체는 린투주맙(lintuzumab)(미성숙, 성숙 및 악성 B 세포의 CD33과 같은 CD33에 특이적으로 결합하는 단일 클론 항체)의 경쇄 및 중쇄 아미노산 서열을 각각 나타내는 서열번호 285-288 및/또는 서열번호 289-292의 아미노산 서열(밑줄 친 잔기로 표시된 리더 서열을 갖거나 갖지 않음)을 포함한다.
일부 측면에서, 상기 메디토프-이용가능 항체 또는 단편은 서열번호 284에 기재된 경쇄 서열, 또는 린투주맙(lintuzumab)의 경쇄 또는 VL 의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3) 및/또는 서열번호 283에 기재된 중쇄 또는 VH 서열, 또는 린투주맙(lintuzumab)의 중쇄 또는 VH 의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3)을 갖는다.
일부 측면에서, 상기 메디토프-이용가능 항체의 VL 영역은 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20 개의 변이(modifications)와 같은, 하나 이상의, 일반적으로 다수의 변이(일반적으로 골격(framework) 영역에 존재하는)를 포함하고/포함하거나, 상기 메디토프-이용가능 항체의 VH 영역은 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20 개의 변이와 같은, 하나 이상의, 예를 들어 다수의 변이(일반적으로 골격 영역에 존재하는)를 포함한다.
일부 실시양태에서, 상기 메디토프-이용가능 항체는, 그것의 경쇄 골격 영역(light chain framework) 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어, FR-L1, FR-L2, FR-L3 및/또는 FR-L4 내에), 린투주맙(lintuzumab) 또는 서열번호 285-288의 경쇄 골격 영역(또는 각각의 하나 이상의 FR-L(s))과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성(identity)을 포함한다; 그리고/또는 그것의 중쇄 골격 영역(heavy chain framework) 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어 FR-H1, FR-H2, FR-H3 및/또는 FR-H4 내에), 린투주맙(lintuzumab), 또는 서열번호 289-292의 중쇄 골격 영역 (또는 각각 하나 이상의 FR-H)과 적어도 또는 대략 75, 76, 77 , 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성을 포함한다; 그리고/또는 그것의 VH 영역 내에, 린투주맙(lintuzumab) 또는 서열번호 289-292의 VH 영역과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99%의 동일성을 포함한다; 그리고/또는 그것의 VL 영역 내에, 린투주맙(lintuzumab) 또는 서열번호 285-288의 VL 영역과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99 %의 동일성을 포함한다; 일부 실시양태에서, 상기 항체는 린투주맙(lintuzumab) 과 비교하여(예를 들어, 서열번호 285-288 또는 289-292의 CDR(S)과 비교하여), 상기 중쇄 및/또는 경쇄 내의 CDR 중 하나 이상 (예를 들어, 모두) 내에, 모든 또는 적어도 95, 96, 97, 98, 또는 99 % 의 동일성을 포함한다.
일부 측면에서, 상기 메디토프-이용가능 항체는 린투주맙(lintuzumab)에 특이적으로 결합되는 CD33의 에피토프에 특이적으로 결합하지 않으나, CD33에 특이적으로 결합하거나, 또는 린투주맙(lintuzumab) 의 CDRs을 포함하지 않고/않거나 항원 결합을 위해 린투주맙(lintuzumab) 과 경쟁하지 않지만, CD33에 특이적으로 결합한다.
5. CD37
일 실시 양태에서, 주형 항체(template antibody)는 항-CD37 항체이다. 예를 들어, 오틀레투주맙(otlertuzumab) 또는 이러한 항체의 중쇄, 경쇄, VH 또는 VL을 갖는 항체 또는 이의 기능적 단편과 같은, CD33에 대한 인간 또는 인간화 항체(humanized antibody) 또는 마우스 항체이다
일부 실시양태에서, 상기 메디토프-이용가능 항체는 는 CD37에 특이 적으로 결합한다. CD37은 GP52-40 또는 TSPAN26으로도 알려져 있으며, 테트라스파닌 패밀리(tetraspanin family)라고도 알려진 막 관통성 4 수퍼패밀리(transmembrane 4 superfamily)의 멤버이다. WO 2011112978은 CD37- 결합 분자 및 이의 면역 접합체(immunoconjugates)를 개시하는데, 이의 개시 내용은 모든 목적을 위해 그 전체가 본원에 참고로 포함된다.
일 실시 양태에서, CD37에 대한 주형 항체는 서열번호 191의 아미노산 서열을 갖는 폴리펩타이드 또는 단백질, 또는 서열번호 192의 핵산 서열을 포함하는 폴리뉴클레오티드에 의해 코딩되는 아미노산 서열을 갖는 폴리펩타이드 또는 단백질 상의 하나 이상의 에피토프와 특이적으로 결합한다
일부 실시양태에서, 주형 항체는 오틀레투주맙(otlertuzumab)의 VL 및 VH 아미노산 서열을 각각 나타내는 서열번호 193 및/또는 서열번호 194의 아미노산 서열을 포함한다. 오틀레투주맙(Betalutin 또는 IMGN529라고도 함)은 NHL 서브타입(subtypes) 상의 CD20과 유사한 발현 프로파일을 갖는 CD37을 타겟으로 한다.
일부 측면에서, 상기 메디토프-이용가능 항체 또는 단편은 서열번호 193에 기재된 VL 서열, 또는 오틀레투주맙(otlertuzumab)의 경쇄 또는 VL 의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3) 및/또는 서열번호 194에 기재된 VH 서열, 또는 오틀레투주맙(otlertuzumab)의 중쇄 또는 VH 의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3)을 갖는다.
일부 측면에서, 메디토프-이용가능 항체의 VL 영역은, 서열번호 193으로 기재되는 아미노산 서열, 또는 오틀레투주맙(otlertuzumab)의 VL과 비교하여, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20 개의 변이(modifications)와 같은, 하나 이상의, 일반적으로 다수의 변이(일반적으로 골격(framework) 영역에 존재하는)를 포함하고/포함하거나, 메디토프-이용가능 항체의 VH 영역은, 서열번호 194로 기재되는 아미노산 서열 또는 오틀레투주맙(otlertuzumab)의 VH와 비교하여, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20 개의 변이와 같은, 하나 이상의, 예를 들어 다수의 변이(일반적으로 골격 영역에 존재하는)를 포함한다.
일부 실시양태에서, 상기 메디토프-이용가능 항체는, 그것의 경쇄 골격 영역 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어, FR-L1, FR-L2, FR-L3 및/또는 FR-L4 내에), 오틀레투주맙(otlertuzumab) 또는 서열번호 193의 경쇄 골격 영역(또는 각각의 하나 이상의 FR-L(s))과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성(identity)을 포함한다; 그리고/또는 그것의 중쇄 골격 영역(heavy chain framework) 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어 FR-H1, FR-H2, FR-H3 및/또는 FR-H4 내에), 오틀레투주맙(otlertuzumab), 서열번호 194의 중쇄 골격 영역 (또는 각각 하나 이상의 FR-H)과 적어도 또는 대략 75, 76, 77 , 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성을 포함한다; 그리고/또는 그것의 VH 영역 내에, 오틀레투주맙(otlertuzumab)의 VH 영역(예를 들어, 서열번호 194의 아미노산 서열)과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99%의 동일성을 포함한다; 그리고/또는 그것의 VL 영역 내에, 오틀레투주맙(otlertuzumab)의 VL 영역(예를 들어, 서열번호 193의 아미노산 서열)과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99 %의 동일성을 포함한다; 일부 실시양태에서, 상기 항체는 오틀레투주맙(otlertuzumab)과 비교하여(예를 들어, 서열번호 193 또는 194의 CDR(s)과 비교하여), 상기 중쇄 및/또는 경쇄 내의 CDR 중 하나 이상, 예를 들어 모두, 내에 모든 또는 적어도 95, 96, 97, 98, 또는 99 % 의 동일성을 포함한다.
일부 측면에서, 상기 메디토프-이용가능 항체는 오틀레투주맙(otlertuzumab)에 특이적으로 결합되는 CD37의 에피토프에 특이적으로 결합하지 않으나, CD37에 특이적으로 결합하거나, 또는 오틀레투주맙(otlertuzumab)의 CDRs을 포함하지 않고/않거나 항원 결합을 위해 오틀레투주맙(otlertuzumab)과 경쟁하지 않지만, CD37에 특이적으로 결합한다.
6. 뮤신-1
일 실시 양태에서, 주형 항체(template antibody)는 항-뮤신-1(anti-Mucin-1) 항체이다. 예를 들어, hPAM4-Cide(클리바투주맙 테트락세탄(clivatuzumab tetraxetan)으로도 알려짐) 또는 이러한 항체의 중쇄, 경쇄, VH 또는 VL을 갖는 항체 또는 이의 기능적 단편과 같은, 뮤신-1에 대한 인간 또는 인간화 항체(humanized antibody) 또는 마우스 항체이다.
일부 실시양태에서, 상기 메디토프-이용가능 항체는 뮤신- 1에 특이적으로 결합한다. Mucin-1은 또한 Mucin 1, 세포 표면 결합 (MUC1) 또는 다형성 상피 점액 (polymorphic epithelial mucin, PEM)으로 알려져 있으며, NCBI Accession No. NP_001018021 또는 UniProt Identifier P15941에 의해 확인된 바와 같이 인간의 MUC1 유전자에 의해 코딩되는 점액이다. 일 실시 양태에서, 뮤신-1에 대한 주형 항체는 서열번호 195의 아미노산 서열을 갖는 폴리펩타이드 또는 단백질, 또는 서열번호 196의 핵산 서열을 포함하는 폴리뉴클레오티드에 의해 코딩되는 아미노산 서열을 갖는 폴리펩타이드 또는 단백질 상의 하나 이상의 에피토프와 특이적으로 결합한다.
일부 실시양태에서, 주형 항체는 hPAM4-Cide(클리바투주맙 테트락세탄(clivatuzumab tetraxetan)으로도 알려짐)의 VL과 VH 아미노산 서열을 각각 나타내는 서열번호 197및/또는 서열번호 198의 아미노산 서열을 포함한다. WO 201004256는 추가의 뮤신-1(additional Mucin-1) 항체를 개시하는데, 이의 개시 내용은 모든 목적을 위해 본원에 참고로 포함된다.
일부 측면에서, 상기 메디토프-이용가능 항체 또는 단편은 서열번호 197에 기재된 VL 서열, 또는 hPAM4-Cide의 경쇄 또는VL의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3), 및/또는 서열번호 198에 기재된 VH 서열, 또는 hPAM4-Cide 의 중쇄 또는 VH 의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3)을 갖는다.
일부 측면에서, 상기 메디토프-이용가능 항체의 VL 영역은, 리더 서열을 갖거나 갖지 않는 서열번호 197로 기재되는 아미노산 서열, 또는 hPAM4-Cide 의 VL과 비교하여, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20 개의 변이(modifications)와 같은, 하나 이상의, 일반적으로 다수의 변이(일반적으로 골격(framework) 영역에 존재하는)를 포함하고/포함하거나, 상기 메디토프-이용가능 항체의 VH 영역은, 리더 서열을 갖거나 갖지 않는, 서열번호 198로 기재되는 아미노산 서열, 또는 hPAM4-Cide 의 VH와 비교하여, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20 개의 변이와 같은, 하나 이상의, 예를 들어 다수의 변이(일반적으로 골격 영역에 존재하는)를 포함한다.
일부 실시양태에서, 상기 메디토프-이용가능 항체는, 그것의 경쇄 골격 영역 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어, FR-L1, FR-L2, FR-L3 및/또는 FR-L4 내에), hPAM4-Cide 또는 서열번호 197의 경쇄 골격 영역(또는 각각의 하나 이상의 FR-L(s))과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성(identity)을 포함한다; 그리고/또는 그것의 중쇄 골격 영역(heavy chain framework) 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어 FR-H1, FR-H2, FR-H3 및/또는 FR-H4 내에), hPAM4-Cide, 서열번호 198의 중쇄 골격 영역 (또는 각각 하나 이상의 FR-H)과 적어도 또는 대략 75, 76, 77 , 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성을 포함한다; 그리고/또는 그것의 VH 영역 내에, hPAM4-Cide 의 VH 영역(예를 들어, 서열번호 198의 아미노산 서열)과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99%의 동일성을 포함한다; 그리고/또는 그것의 VL 영역 내에, hPAM4-Cide 의 VL 영역(예를 들어, 서열번호 197의 아미노산 서열)과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99 %의 동일성을 포함한다; 일부 실시양태에서, 상기 항체는 hPAM4-Cide 과 비교하여(예를 들어, 서열번호 197 또는 198의 CDR(s)과 비교하여), 상기 중쇄 및/또는 경쇄 내의 CDR 중 하나 이상, 예를 들어 모두, 내에 모든 또는 적어도 95, 96, 97, 98, 또는 99 % 의 동일성을 포함한다. 서열번호 197은 hPAM4-Cide 경쇄 가변 (VL) 영역 서열을 나타내고, 서열번호 198은 hPAM4-Cide 중쇄 가변 (HL) 영역 서열을 나타낸다.
일부 측면에서, 상기 메디토프-이용가능 항체는 hPAM4-Cide에 특이적으로 결합되는 뮤신1(Mucin1)의 에피토프에 특이적으로 결합하지 않으나, 뮤신1에 특이적으로 결합하거나, 또는 hPAM4-Cide 의 CDRs을 포함하지 않고/않거나 항원 결합을 위해 hPAM4-Cide과 경쟁하지 않지만, 뮤신1 에 특이적으로 결합한다.
7. 프롤락틴 수용체
일 실시 양태에서, 주형 항체(template antibody)는 항-프롤락틴 수용체(anti- prolactin receptor, PRLR) 항체이다. 예를 들어, LFA-102 또는 002-H08, 또는 이러한 항체의 중쇄, 경쇄, VH 또는 VL을 갖는 항체, 또는 이의 기능적 단편과 같은, 프롤락틴 수용체에 대한 인간 또는 인간화 항체(humanized antibody) 또는 마우스 항체이다.
일부 실시양태에서, 상기 메디토프-이용가능 항체는 프롤락틴 수용체에 특이적으로 결합한다. 일 측면에서, 프롤락틴 수용체는 염색체 5p13-14상의 유전자에 의해 코딩되고, 막 관통성 수용체로서 프롤락틴 분자와 상호작용한다. 상기 프롤락틴 수용체는 프롤락틴, 막 관통성 (transmembrane) 영역 및 세포질 영역(cytoplasmic region) 결합하는 세포외 영역(extracellular region)을 포함한다.
일부 실시양태에서, 주형 항체는 IgG1 카파 서브타입 (kappa subtype)의 인간화된 단일클론 항체인 LFA-102의 VL 및/또는 VH 아미노산 서열의 아미노산 서열을 포함하고, 비-리간드 경쟁 방식(non-ligand competitive manner)으로 PRLR의 추정 이합체 영역(putative dimerization region)에 결합하고 PRL -유도 신호를 억제한다.
일부 측면에서, 상기 메디토프-이용가능 항체 또는 단편은 LFA-102의 VL의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3) 및/또는 LFA-102의 VH의 의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3)를 갖는다.
일부 측면에서, 상기 메디토프-이용가능 항체의 VL 영역은, LFA-102의 VL과 비교하여, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20 개의 변이(modifications)와 같은, 하나 이상의, 일반적으로 다수의 변이(일반적으로 골격(framework) 영역에 존재하는)를 포함하고/포함하거나, 상기 메디토프-이용가능 항체의 VH 영역은, LFA-102의 VH와 비교하여, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20 개의 변이와 같은, 하나 이상의, 예를 들어 다수의 변이(일반적으로 골격 영역에 존재하는)를 포함한다.
일부 실시양태에서, 상기 메디토프-이용가능 항체는, 그것의 경쇄 골격 영역 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어, FR-L1, FR-L2, FR-L3 및/또는 FR-L4 내에), LFA-102의 경쇄 골격 영역(또는 각각의 하나 이상의 FR-L(s))과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성(identity)을 포함한다; 그리고/또는 그것의 중쇄 골격 영역(heavy chain framework) 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어 FR-H1, FR-H2, FR-H3 및/또는 FR-H4 내에), LFA-102의 중쇄 골격 영역 (또는 각각 하나 이상의 FR-H)과 적어도 또는 대략 75, 76, 77 , 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성을 포함한다; 그리고/또는 그것의 VH 영역 내에, LFA-102의 VH 영역과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99%의 동일성을 포함한다; 그리고/또는 그것의 VL 영역 내에, LFA-102의 VL 영역과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99 %의 동일성을 포함한다; 일부 실시양태에서, 상기 항체는 LFA-102와 비교하여, 상기 중쇄 및/또는 경쇄 내의 CDRs 중 하나 이상, 예를 들어 모두, 내에 모든 또는 적어도 95, 96, 97, 98, 또는 99 % 의 동일성을 포함한다.
일부 측면에서, 상기 메디토프-이용가능 항체는 LFA-102에 특이적으로 결합되는 프롤락틴 수용체의 에피토프에 특이적으로 결합하지 않으나, 프롤락틴 수용체에 특이적으로 결합하거나, 또는 LFA-102의 CDRs을 포함하지 않고/않거나 항원 결합을 위해 LFA-102와 경쟁하지 않지만, 프롤락틴 수용체에 특이적으로 결합한다.
일부 실시양태에서, 주형 항체는 각각 002-H08의 VL 및 VH 아미노산 서열을 기재하는 서열번호 208 및/또는 서열번호 209의 아미노산 서열을 포함한다. 출원 공개 공보 No. US 20120315276는 002-H08을 포함하는 프로락틴 수용체 항체를 개시하고, 그 개시 내용은 모든 목적을 위해 본원에 참고로 인용된다.
일부 측면에서, 상기 메디토프-이용가능 항체 또는 단편은 서열번호 208에 기재된VL 서열, 또는 002-H08의 경쇄 또는 VL 의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3), 및/또는 서열번호 209에 기재된 VH 서열, 또는 002-H08의 중쇄 또는 VH 의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3)을 갖는다.
일부 측면에서, 상기 메디토프-이용가능 항체의 VL 영역은, 서열번호 208에 기재된 아미노산 서열, 또는002-H08 의 VL과 비교하여, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20 개의 변이(modifications)와 같은, 하나 이상의, 일반적으로 다수의 변이(일반적으로 골격(framework) 영역에 존재하는)를 포함하고/포함하거나, 상기 메디토프-이용가능 항체의 VH 영역은, 서열번호 209의 아미노산 서열, 또는 002-H08의 VH와 비교하여, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20 개의 변이와 같은, 하나 이상의, 예를 들어 다수의 변이(일반적으로 골격 영역에 존재하는)를 포함한다.
일부 실시양태에서, 상기 메디토프-이용가능 항체는, 그것의 경쇄 골격 영역 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어, FR-L1, FR-L2, FR-L3 및/또는 FR-L4 내에), 002-H08또는 서열번호 208의 경쇄 골격 영역(또는 각각의 하나 이상의 FR-L(s))과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성(identity)을 포함한다; 그리고/또는 그것의 중쇄 골격 영역(heavy chain framework) 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어 FR-H1, FR-H2, FR-H3 및/또는 FR-H4 내에), 002-H08, 서열번호 209의 중쇄 골격 영역 (또는 각각 하나 이상의 FR-H)과 적어도 또는 대략 75, 76, 77 , 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성을 포함한다; 그리고/또는 그것의 VH 영역 내에, 002-H08의 VH 영역(서열번호 209의 아미노산 서열)과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99%의 동일성을 포함한다; 그리고/또는 그것의 VL 영역 내에, 002-H08의 VL 영역(서열번호 208의 아미노산 서열)과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99 %의 동일성을 포함한다; 일부 실시양태에서, 상기 항체는 002-H08과 비교하여(서열번호 208 또는 209의 CDR(s)와 비교하여), 상기 중쇄 및/또는 경쇄 내의 CDRs 중 하나 이상, 예를 들어 모두, 내에 모든 또는 적어도 95, 96, 97, 98, 또는 99 %의 동일성을 포함한다.
일부 측면에서, 상기 메디토프-이용가능 항체는 002-H08에 특이적으로 결합되는 프롤락틴 수용체의 에피토프에 특이적으로 결합하지 않으나, 프롤락틴 수용체에 특이적으로 결합하거나, 또는 002-H08의 CDRs을 포함하지 않고/않거나 항원 결합을 위해 002-H08와 경쟁하지 않지만, 프롤락틴 수용체에 특이적으로 결합한다.
8. SDC-1
일 실시 양태에서, 주형 항체(template antibody)는 항-SDC-1(anti-SDC-1) 항체이다. 예를 들어, 인다툭시맙 라브탄신(indatuximab ravtansine), 또는 이러한 항체의 중쇄, 경쇄, VH 또는 VL을 갖는 항체, 또는 이의 기능적 단편과 같은, SDC-1(Syndecan 1, 또는 CD138으로도 알려짐)에 대한 인간 또는 인간화 항체(humanized antibody) 또는 마우스 항체이다.
일부 실시양태에서, 상기 메디토프-이용가능 항체는 SDC-1에 특이적으로 결합한다. 일 측면에서, SDC-1는 막관통성(타입 I) 헤파린 설페이트 프로테오글리칸(transmembrane (type I) heparan sulfate proteoglycan)이며, 신데칸 프로테오글리칸 패밀리(syndecan proteoglycan family)의 멤버이다. 신데칸은 세포 결합, 세포 신호전달, 및 세포골격형성을 매개하며, 신데칸 수용체는 HIV-1 tat 단백질의 내재화(internalization)에 필요하다. 신데칸-1 단백질은 내재성 막 단백질(integral membrane protein)로서 기능하며 세포 외 기질 단백질에 대한 수용체를 통해 세포 증식, 세포 이동 및 세포 - 매트릭스 상호 작용에 참여한다.
변이된 신데칸-1 발현(altered syndecan-1 expression)이 여러 가지 종양 유형에서 발견되었다. 이 유전자에 대해 여러 가지 전사 변이체가 존재할 수 있지만, 현재까지 2종의 전장(full-length)의 자연물(natures)이 기술되어 졌다. 이러한 두 가지는 이 유전자의 주요 변종을 나타내며 동일한 단백질을 코딩한다. 일 실시 양태에서, SDC-1에 대한 주형 항체는 서열번호 210의 아미노산 서열을 갖는 폴리펩타이드 또는 단백질 상의 하나 이상의 에피토프에 특이적으로 결합한다
일부 실시양태에서, 주형 항체는 각각 인다툭시맙 라브탄신(indatuximab ravtansine)의 VL 및 VH 아미노산 서열을 기재한 서열번호 211 및/또는 서열번호 212의 아미노산 서열을 포함한다. 인다툭시맙 라브탄신(BT-062, BT062, 또는 B-B4로도 알려짐)은 SDC-1 항체이다.
일부 측면에서, 상기 메디토프-이용가능 항체 또는 단편은 서열번호 211에 기재된VL 서열, 또는 인다툭시맙 라브탄신(indatuximab ravtansine)의 경쇄 또는 VL 의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3), 및/또는 서열번호 212에 기재된 VH 서열, 또는 인다툭시맙 라브탄신(indatuximab ravtansine)의 중쇄 또는 VH 의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3)을 갖는다.
일부 측면에서, 상기 메디토프-이용가능 항체의 VL 영역은, 서열번호 211에 기재된 아미노산 서열, 또는 인다툭시맙 라브탄신(indatuximab ravtansine)의 VL과 비교하여, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20 개의 변이(modifications)와 같은, 하나 이상의, 일반적으로 다수의 변이(일반적으로 골격(framework) 영역에 존재하는)를 포함하고/포함하거나, 상기 메디토프-이용가능 항체의 VH 영역은, 리더 서열을 갖거나 갖지 않은, 서열번호 212의 아미노산 서열, 또는 인다툭시맙 라브탄신(indatuximab ravtansine)의 VH와 비교하여, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20 개의 변이와 같은, 하나 이상의, 예를 들어 다수의 변이(일반적으로 골격 영역에 존재하는)를 포함한다.
일부 실시양태에서, 상기 메디토프-이용가능 항체는, 그것의 경쇄 골격 영역(light chain framework) 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어, FR-L1, FR-L2, FR-L3 및/또는 FR-L4 내에), 인다툭시맙 라브탄신(indatuximab ravtansine), 또는 서열번호 211의 경쇄 골격 영역(또는 각각의 하나 이상의 FR-L(s))과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성(identity)을 포함한다; 그리고/또는 그것의 중쇄 골격 영역(heavy chain framework) 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어 FR-H1, FR-H2, FR-H3 및/또는 FR-H4 내에), 인다툭시맙 라브탄신(indatuximab ravtansine), 서열번호 212의 중쇄 골격 영역 (또는 각각 하나 이상의 FR-H)과 적어도 또는 대략 75, 76, 77 , 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성을 포함한다; 그리고/또는 그것의 VH 영역 내에, 인다툭시맙 라브탄신(indatuximab ravtansine)의 VH 영역(예를 들어 서열번호 212의 아미노산 서열)과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99%의 동일성을 포함한다; 그리고/또는 그것의 VL 영역 내에, 인다툭시맙 라브탄신(indatuximab ravtansine)의 VL 영역(예를 들어 서열번호 211아미노산 서열)과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99 %의 동일성을 포함한다; 일부 실시양태에서, 상기 항체는 인다툭시맙 라브탄신(indatuximab ravtansine)과 비교하여(예를 들어 서열번호 211 또는 212의 CDR(s)과 비교하여), 상기 중쇄 및/또는 경쇄 내의 CDRs 중 하나 이상, 예를 들어 모두, 내에 모든 또는 적어도 95, 96, 97, 98, 또는 99 %의 동일성을 포함한다.
일부 측면에서, 상기 메디토프-이용가능 항체는 인다툭시맙 라브탄신(indatuximab ravtansine)에 특이적으로 결합되는 SDC-1의 에피토프에 특이적으로 결합하지 않으나, SDC-1 에 특이적으로 결합하거나, 또는 인다툭시맙 라브탄신의 CDRs을 포함하지 않고/않거나 항원 결합을 위해 인다툭시맙 라브탄신과 경쟁하지 않지만, SDC-1 에 특이적으로 결합한다.
9. HER-2
일 실시 양태에서, 주형 항체(template antibody)는 항-HER-2 (anti-HER-2) 항체이다. 예를 들어, 트라스투주맙(trastuzumab)(Herceptin®, 또는 이러한 항체의 중쇄, 경쇄, VH 또는 VL을 갖는 항체, 또는 이의 기능적 단편과 같은, HER-2 (ERBB2으로도 알려짐)에 대한 인간 또는 인간화 항체 또는 마우스 항체이다.
일부 실시양태에서, 메디토프-이용가능 항체는 HER-2에 특이적으로 결합한다. 일부 측면에서, 상기 메디토프-이용가능 항체 또는 단편은 서열번호 303에 기재된VL 서열, 또는 트라스투주맙(trastuzumab)의 경쇄 또는 VL 의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3), 및/또는 서열번호 304에 기재된 VH 서열, 또는 트라스투주맙(trastuzumab)의 중쇄 또는 VH 의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3)을 갖는다.
일부 측면에서, 상기 메디토프-이용가능 항체의 VL 영역은, 트라스투주맙(trastuzumab)의 아미노산 서열과 비교하여, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20 개의 변이(modifications)와 같은, 하나 이상의, 일반적으로 다수의 변이(일반적으로 골격(framework) 영역에 존재하는)를 포함하고/포함하거나, 상기 메디토프-이용가능 항체의 VH 영역은, 트라스투주맙(trastuzumab)의 아미노산 서열과 비교하여, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20 개의 변이와 같은, 하나 이상의, 예를 들어 다수의 변이(일반적으로 골격 영역에 존재하는)를 포함한다.
일부 실시양태에서, 상기 메디토프-이용가능 항체는, 그것의 경쇄 골격 영역(light chain framework) 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어, FR-L1, FR-L2, FR-L3 및/또는 FR-L4 내에), 트라스투주맙(trastuzumab)의 경쇄 골격 영역(또는 각각의 하나 이상의 FR-L(s))과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성(identity)을 포함한다; 그리고/또는 그것의 중쇄 골격 영역(heavy chain framework) 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어 FR-H1, FR-H2, FR-H3 및/또는 FR-H4 내에), 트라스투주맙(trastuzumab)의 중쇄 골격 영역 (또는 각각 하나 이상의 FR-H)과 적어도 또는 대략 75, 76, 77 , 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성을 포함한다; 그리고/또는 그것의 VH 영역 내에, 트라스투주맙(trastuzumab)의 VH 영역과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99%의 동일성을 포함한다; 그리고/또는 그것의 VL 영역 내에, 트라스투주맙(trastuzumab)의 VL 영역과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99 %의 동일성을 포함한다; 일부 실시양태에서, 상기 항체는 트라스투주맙(trastuzumab)과 비교하여, 상기 중쇄 및/또는 경쇄 내의 CDRs 중 하나 이상, 예를 들어 모두, 내에 모든 또는 적어도 95, 96, 97, 98, 또는 99 %의 동일성을 포함한다.
일부 측면에서, 상기 메디토프-이용가능 항체는 트라스투주맙(trastuzumab)에 특이적으로 결합되는 HER-2의 에피토프에 특이적으로 결합하지 않으나, HER-2에 특이적으로 결합하거나, 또는 트라스투주맙(trastuzumab)의 CDRs을 포함하지 않고/않거나 항원 결합을 위해 트라스투주맙(trastuzumab)과 경쟁하지 않지만, HER-2에 특이적으로 결합한다.
일부 실시양태에서, 상기 메디토프-이용가능 항체 (meditope-enabled antibody) 또는 단편(fragment) 은 서열번호 303의 아미노산 서열을 포함하는 경쇄를 갖고/갖거나 서열번호 304의 아미노산 서열을 포함하는 중쇄를 갖는다. 일부 실시양태에서, 상기 메디토프-이용가능 항체 또는 단편은 cQFD 메디토프, 변이형 3 링커(variant 3 linker)를 포함하고/포함하거나 메디토프 인에이블된(meditope enabled) 트라스투주맙(trastuzumab) (예를 들어, 서열번호 304)의 중쇄에 융합된다.
10. EGFR
일 실시 양태에서, 주형 항체(template antibody)는 항-EGFR (anti-EGFR) 항체이다. 예를 들어, ABT-806, 자툭시맙(zatuximab), 또는 이러한 항체의 중쇄, 경쇄, VH 또는 VL을 갖는 항체, 또는 이의 기능적 단편과 같은, EGFR 대한 인간 또는 인간화 항체(humanized antibody) 또는 마우스 항체이다. 일부 측면에서, 항- EGFR 주형 항체는 세툭시맙(cetuximab)이 아니며 세툭시맙(cetuximab)의 전부 또는 일부 CDRs을 포함하지 않고/않거나 결합을 위해 세툭시맙(cetuximab)과 경쟁하지 않는다.
일 실시 양태에서, EGFR에 대한 주형 항체는 서열번호 213의 아미노산 서열을 갖는 폴리펩타이드 또는 단백질, 또는 서열번호 214의 핵산 서열을 포함하는 폴리뉴클레오티드에 의해 코딩되는 아미노산 서열을 갖는 폴리펩타이드 또는 단백질 상의 하나 이상의 에피토프와 특이적으로 결합한다.
일부 실시 형태에서, 주형 항체는 EGFR 항체인, ABT-806 (mAb806/414로도 알려진)의 VL 및 VH 아미노산 서열을 각각 기재한 서열번호 215 및/또는 서열번호 216의 아미노산 서열을 포함하고/포함하거나 각각 ABT-806의 경쇄 및 중쇄 서열을 기재한 서열번호 217 및 서열번호 218의 아미노산 서열을 포함한다.
일부 측면에서, 상기 메디토프-이용가능 항체 또는 단편은 서열번호 215에 기재된VL 서열, 또는 ABT-806의 경쇄 또는 VL 의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3), 및/또는 서열번호 216에 기재된 VH 서열, 또는 ABT-806의 중쇄 또는 VH 의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3)을 갖는다.
일부 측면에서, 상기 메디토프-이용가능 항체의 VL 영역은, 서열번호 215로 기재된 아미노산 서열, 또는ABT-806의 VL과 비교하여, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20 개의 변이(modifications)와 같은, 하나 이상의, 일반적으로 다수의 변이(일반적으로 골격(framework) 영역에 존재하는)를 포함하고/포함하거나, 상기 메디토프-이용가능 항체의 VH 영역은, 서열번호 216으로 기재된 아미노산 서열, 또는 ABT-806의 VH와 비교하여, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20 개의 변이와 같은, 하나 이상의, 예를 들어 다수의 변이(일반적으로 골격 영역에 존재하는)를 포함한다.
일부 실시양태에서, 상기 메디토프-이용가능 항체는, 그것의 경쇄 골격 영역(light chain framework) 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어, FR-L1, FR-L2, FR-L3 및/또는 FR-L4 내에), ABT-806, 또는 서열번호 215의 경쇄 골격 영역(또는 각각의 하나 이상의 FR-L(s))과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성(identity)을 포함한다; 그리고/또는 그것의 중쇄 골격 영역(heavy chain framework) 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어 FR-H1, FR-H2, FR-H3 및/또는 FR-H4 내에), ABT-806, 서열번호 216의 중쇄 골격 영역 (또는 각각 하나 이상의 FR-H)과 적어도 또는 대략 75, 76, 77 , 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성을 포함한다; 그리고/또는 그것의 VH 영역 내에, ABT-806의 VH 영역(예를 들어 서열번호 216의 아미노산 서열)과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99%의 동일성을 포함한다; 그리고/또는 그것의 VL 영역 내에, ABT-806의 VL 영역(예를 들어서열번호 215의 아미노산 서열)과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99 %의 동일성을 포함한다; 일부 실시양태에서, 상기 항체는 ABT-806과 비교하여(예를 들어, 서열번호 215 또는 216의 CDR(s) 과 비교하여), 상기 중쇄 및/또는 경쇄 내의 CDRs 중 하나 이상, 예를 들어 모두, 내에 모든 또는 적어도 95, 96, 97, 98, 또는 99 %의 동일성을 포함한다.
일부 측면에서, 상기 메디토프-이용가능 항체는 ABT-806에 특이적으로 결합되는 EGFR의 에피토프에 특이적으로 결합하지 않으나, EGFR에 특이적으로 결합하거나, 또는 ABT-806의 CDRs을 포함하지 않고/않거나 항원 결합을 위해 ABT-806과 경쟁하지 않지만, EGFR에 특이적으로 결합한다.
일부 실시 형태에서, 주형 항체는 각각 자툭시맙(zatuximab)의VL 및 VH 아미노산 서열을 기재한 서열번호 219 및/또는 서열번호 220의 아미노산 서열을 포함하고/포함하거나 EGFR 항체인, 자툭시맙(zatuximab)의 경쇄 및 중쇄 서열을 각각 기재한 서열번호 221및/또는 서열번호 222의 아미노산 서열을 포함한다.
일부 측면에서, 상기 메디토프-이용가능 항체 또는 단편은 서열번호 219에 기재된VL 서열, 또는 자툭시맙(zatuximab)의 경쇄 또는 VL 의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3), 및/또는 서열번호 220에 기재된 VH 서열, 또는 자툭시맙(zatuximab)의 중쇄 또는 VH 의 CDR (즉, 하나 이상의 CDR, 예를 들어, CDR1, CDR2 및/또는 CDR3)을 갖는다.
일부 측면에서, 상기 메디토프-이용가능 항체의 VL 영역은, 서열번호 219로 기재된 아미노산 서열, 또는 자툭시맙(zatuximab)의 VL과 비교하여, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는20 변이(modifications)와 같은, 하나 이상의, 일반적으로 다수의 변이(일반적으로 골격(framework) 영역에 존재하는)를 포함하고/포함하거나, 상기 메디토프-이용가능 항체의 VH 영역은, 서열번호 220으로 기재된 아미노산 서열, 또는 자툭시맙(zatuximab)의 VH와 비교하여, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20 변이와 같은, 하나 이상의, 예를 들어 다수의 변이(일반적으로 골격 영역에 존재하는)를 포함한다.
일부 실시양태에서, 상기 메디토프-이용가능 항체는, 그것의 경쇄 골격 영역(light chain framework) 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어, FR-L1, FR-L2, FR-L3 및/또는 FR-L4 내에), 자툭시맙(zatuximab), 또는 서열번호 219의 경쇄 골격 영역(또는 각각의 하나 이상의 FR-L(s))과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성(identity)을 포함한다; 그리고/또는 그것의 중쇄 골격 영역(heavy chain framework) 내에(또는 하나 이상의 그러한 영역 내에, 예를 들어 FR-H1, FR-H2, FR-H3 및/또는 FR-H4 내에), 자툭시맙(zatuximab), 서열번호 220의 중쇄 골격 영역 (또는 각각 하나 이상의 FR-H)과 적어도 또는 대략 75, 76, 77 , 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 %의 동일성을 포함한다; 그리고/또는 그것의 VH 영역 내에, 자툭시맙(zatuximab)의 VH 영역(예를 들어 서열번호 220의 아미노산 서열)과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99%의 동일성을 포함한다; 그리고/또는 그것의 VL 영역 내에, 자툭시맙(zatuximab)의 VL 영역(예를 들어서열번호 220의 아미노산 서열)과 적어도 또는 대략 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 또는 99 %의 동일성을 포함한다; 일부 실시양태에서, 상기 항체는 자툭시맙(zatuximab)과 비교하여(예를 들어, 서열번호 219 또는 220의 CDR(s) 과 비교하여), 상기 중쇄 및/또는 경쇄 내의 CDRs 중 하나 이상, 예를 들어 모두, 내에 모든 또는 적어도 95, 96, 97, 98, 또는 99 %의 동일성을 포함한다.
일부 측면에서, 상기 메디토프-이용가능 항체는 자툭시맙(zatuximab)에 특이적으로 결합되는 EGFR의 에피토프에 특이적으로 결합하지 않으나, EGFR에 특이적으로 결합하거나, 또는 자툭시맙(zatuximab)의 CDRs을 포함하지 않고/않거나 항원 결합을 위해 자툭시맙(zatuximab)과 경쟁하지 않지만, EGFR에 특이적으로 결합한다.
일부 실시양태에서, 상기 메디토프-이용가능 항체 또는 단편(fragment)은 서열번호 299의 아미노산 서열을 포함하는 경쇄를 갖고/갖거나 서열번호 300의 아미노산 서열을 포함하는 중쇄를 갖는다. 일부 실시양태에서, 상기 메디토프-이용가능 항체 (meditope-enabled antibody) 또는 단편은 cQFD 메디토프, 변이형 1 링커(variant 1 linker)를 포함하고/포함하거나 세툭시맙(cetuximab)에 융합된다.
일부 실시양태에서, 메디토프-이용가능 항체 또는 단편(fragment)은 서열번호 301의 아미노산 서열을 포함하는 경쇄를 갖고/갖거나 서열번호 302의 아미노산 서열을 포함하는 중쇄를 갖는다. 일부 실시양태에서, 상기 메디토프-이용가능 항체 (meditope-enabled antibody) 또는 단편은 cQFD 메디토프, 변이형 3 링커(variant 3 linker)를 포함하고/포함하거나 I83E (Kabat numbering), 예를 들어 서열번호 302 로 치환된 세툭시맙(cetuximab)에 융합된다.
메디토프-이용가능 항체는 일반적으로 불변 영역(constant region), 전형적으로 중쇄 및 경쇄 불변 영역을 추가로 포함하는데, 이는 일반적으로 인간 또는 부분적으로 인간 불변 영역 (partially human constant regions)이다. 일부 측면에서, 중쇄 불변 영역은 CH1 또는 그의 일부를 포함한다. 일부 측면에서, 경쇄 불변 영역은 CL 또는 그의 일부를 포함한다. 일부 실시양태에서, 불변 영역의 일부는 예를 들어 필수 결합 친화도(requisite binding affinity)를 갖는 메디토프에 항체가 결합할 수 있도록 하기에 충분하다. 일부 측면에서, 불변 영역은 세툭시맙(cetuximab) 또는 트라스투주맙(trastuzumab)의 불변 영역이다. 따라서, 일부 측면에서, 중쇄 불변 영역은 하나 이상의 인간 IgG1 불변 영역이고; 일부 측면에서, 경쇄 불변 영역은 카파 불변 사슬 영역(kappa constant chain regions)이다. 다른 예에서, 불변 영역은 인간 (또는 기타 생물체, 예를 들어 쥐 또는 닭) IgG1, IgG2, IgG3, IgG4, IgEs, IgA1, IgA2, IgD 또는 IgM을 포함하는 다른 아이소 타입(isotypes)의 것들을 포함할 수 있으며, 카파 또는 람다(lambda) 불변 영역을 포함할 수 있다. 따라서, 제공되는 메디토프-이용가능 항체 중 인간, 쥐 또는 닭과 같은 다른 IgGs 또는 다른 면역 글로불린의 잔기의 돌연변이에 의해 생성된 항체가 있다. 환원하면, 본원에서 제공되는 메디토프-인에이블링 법 (meditope-enabling methods)은 IgA, IgE, IgD 및 IgM을 포함하는 임의의 항체 및, 닭, 쥐, 쥐, 소, 토끼, 영장류 및 염소를 포함하는 하나 이에 한정되지 않는, 항체를 생산하는 임의의 유기체 유래의 임의의 항체에 사용될 수 있다.
예를 들어, 인간 IgG1, IgG2, IgG3 및 IgG4의 제 1 불변 영역 (CH1)의 서열은 세툭시맙(cetuximab)의 메디토프-결합 영역(meditope-binding region) 내에 존재하지 않는 잔기에서 상이하고, 이는 메디토프-인에이블링(meditope-enabling) 기술이 세툭시맙(cetuximab)의 IgG1 이외의 아이소타입(isotypes)에 적용 가능하다는 것을 확인해준다. 다른 예로서, IgG1 및 IgE Fab 도메인의 서열 및 구조적 배열(structural alignment)은 메디토프 결합 자리(meditope binding site) 근처의 IgE 상의 잔기를 나타낸다.
단일 클론 항체 내에서 Fab 캐비티(cavity)의 메디토프-사이트-그래프팅(meditope-site grafting)을 위해 제공되는 방법은 메디토프 결합(meditope binding)을 위한 유니크한 핸들(unique handle)을 만드는 데 사용할 수 있으며 이전에 공개된 기술과 함께 사용될 수 있고 새로 생성된 항체에 사용될 수 있다. 특정 실시 양태에서, 상기 메디토프 결합 자리(meditope binding site)는 기존의 및 미래의 모든 단일 클론 항체 상에 생성될 수 있다.
또한, 상기 메디토프-이용가능 항체를 변형시키는 방법, 예를 들어, 친화도(affinity), 결합력(avidity), pH-의존성(pH-dependence)을 포함하는, 메디토프와의 상호작용 측면뿐만 아니라 항체의 약물동태학 (pharmacokinetics, PK), 약력학(pharmacodynamics, PD)을 포함한 다른 측면을 포함하여, 메디토프와의 상호작용 측면을 포함하여, 메디토프-이용가능 항체의 다양한 특성을 변경하기 위한 방법이 제공된다.
따라서, 제공된 메디토프-이용가능 항체 중에서도, 예를 들어, 아래의 섹션 F에 기술된 임의의 하나 이상의 변이(modifications)를 갖는 항체를 포함하는, 예를 들어 파마코포어(pharmacophore) 결합 모델을 생성함으로써, 이들 방법에 따라 생성된, 변이된(modified) 항체들이 있다.
또한 메디토프-이용가능 항체를 생성하기 위한 주형 항체로 사용되는 항체 중에는 CovX-BodyTM과 같은 변이된 항체 및 그것의 일부가 있다. 따라서, 제공된 메디토프-이용가능 항체 중 하나 이상은 제공된 메디토프 중 하나 이상에, 예를 들어 본원에서 기재된 바와 같이 친화도(affinity)에 의해 그것들이 결합할 수 있도록 변이된 CovX-바디이다.
또한, 본원에 기재된 임의의 항체와 같이, 메디토프-이용가능 항체에 결합 된 하나 이상의 메디토프를 포함하는 복합체가 제공된다.
또한, 메디토프-이용가능 항체를 코딩하는cDNA 및 RNA 분자와 같은 핵산, 이를 포함하는 벡터 및 라이브러리 및, 선택 및 발현 방법(selection and expression methods) 및 그러한 컨스트럭(constructs)을 사용하여 형질전환 동물(transgenic animals)을 생산하는 방법을 포함하는, 이들의 사용 방법이 제공된다.
아래의 표는 본원에서 언급된 추가 링커 및 메디토프-이용가능 항체의 서열을 나타낸다.
(이어서)
(이어서)
(이어서)
(이어서)
(이어서)
(이어서)
(이어서)
(이어서)
Ⅱ. 자가-가교결합 항체의 생산을 위한 조성물 및 방법.
A. 핵산, 벡터, 및 이를 포함하는 세포
또한, 본원에 기재된 임의의 항체를 코딩하는 분리된 핵산이 제공된다. 일부 실시양태에서, 핵산은 이전에 기술된 자가-가교결합 항체 중 임의의 것을 코딩하는 핵산의 발현에 적합한 벡터를 추가로 포함한다. 또 다른 특정 측면에서, 상기 벡터는 핵산의 발현에 적합한 숙주 세포 내에 존재한다. 또 다른 특정 측면에서, 숙주 세포는 진핵 세포 또는 원핵 세포이다. 또 다른 특정 측면에서, 진핵 세포는 포유 동물 세포, 예를 들면, 차이니즈 햄스터 오바리 (Chinese Hamster Ovary, CHO) 또는 HEK-293 및 그의 변이체이다.
일부 실시양태에서, 상기 핵산은 자유 메디토프(free meditope)를 코딩하는 뉴클레오타이드 서열을 추가로 포함한다. 일부 실시양태에서, 제1 핵산은 자가-가교결합 항체를 코딩하는 뉴클레오타이드 서열을 포함하고, 제2 핵산은 자유 메디토프(free meditope)를 코딩하는 뉴클레오타이드 서열을 포함한다. 상기 자유 메디토프는 본원에 기재된, 예를 들어 서열번호서열번호 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 186, 187, 188, 189, or 207 중 어느 하나를 포함하는 임의의 환형 펩타이드 또는 그로부터 유래된 환상 펩타이드를 포함할 수 있다. 일부 실시양태에서, 자유 메디토프(free meditope)는 핵산에 의해 코딩되는 자가-가교결합 항체 상의 메디토프 결합 자리(meditope binding site) 에 결합할 수 있다.
상기 항체 또는 이의 항원 결합 단편은 당업계에 공지 된 방법을 사용하여, 예를 들어, 이러한 항체 또는 단편을 생산하기에 적합한 조건 하에서, 발현이 적합한 형태의 전술한 자가-가교결합 항체 또는 항원 결합 단편 중 임의의 것을 코딩하는 핵산을 함유하는 숙주 세포를 배양하는 단계, 및 상기 항체 또는 단편을 회수하는 단계를 포함하는 방법에 의해 제조될 수 있다.
일부 실시양태에서, 자가-가교결합 항체는 재조합 방법을 사용하여 제조될 수 있다. 항-항원 항체(anti-antigen antibody)의 재조합 생산을 위해, 항체를 코딩하는 핵산을 분리할 수 있고 추가 복제 (DNA의 증폭) 또는 발현을 위해 복제 가능한 벡터에 삽입할 수 있다. 항체를 암호화하는 DNA는 통상적인 절차 (예를 들어, 항체의 중쇄 및 경쇄를 코딩하는 유전자에 특이적으로 결합할 수 있는 올리고 뉴클레오타이드 프로브를 사용함으로써)를 이용하여 용이하게 분리(단리) 및 시퀀싱될 수 있다. 예를 들어 pCEP4 벡터, 바이러스 벡터, 레트로 바이러스 벡터, 렌티 바이러스 벡터 또는 감마 레트로 바이러스 벡터를 비롯한 많은 벡터가 이용 가능하다. 벡터 성분은 일반적으로 다음 중 하나 이상을 포함하지만, 이에 한정되지는 않는다: 신호 서열, 복제 원점, 하나 이상의 마커 유전자, 인핸서 요소, 프로모터, 및 전사 종결 서열.
1. 폴리시스트론성 발현 벡터
일부 실시양태에서, 발현 벡터는 자가-가교결합 항체(self-crosslinking antibody) 및 자유 메디토프(free meditope)를 동시에 발현할 수 있는 바이시스트론성(bicistronic), 트리시스 트론성(tricistronic) 또는 폴리시스트론성 (polycistronic) 벡터 (멀티시스트론성 벡터라고도 함)이다. 일부 실시양태에서, 자유 메디토프를 코딩하는 뉴클레오타이드의 서열 및 자가-가교결합 항체를 코딩하는 뉴클레오타이드의 서열은 작동 가능하게 연결되거나 자가-절단 펩타이드(self-cleaving peptide)를 코딩하는 뉴클레오타이드의 서열에 의해 분리된다. 일부 실시양태에서, 이들은 피코르나바이러스 2A 리보좀 스킵 펩타이드(picornavirus 2A ribosomal skip peptide) 또는 T2A 펩타이드와 같은, 리보솜 스키핑(ribosome skipping)을 유발하는 펩타이드를 코딩하는 뉴클레오타이드 서열에 의해 분리된다.
일부 실시양태에서, 자유 메디토프를 코디하는 일련의 핵산 및 자가-가교결합 항체를 코딩하는 일련의 핵산은 작동 가능하게 연결되거나 내부 리보솜 유입점(internal ribosome entry site, IRES)에 의해 분리된다. 일부 실시양태에서, IRES 서열 이전의 유전자는 IRES 서열 이후의 유전자보다 높은 수준으로 발현된다. 일부 실시양태에서, IRES 서열 전에 자유 메디토프를 코딩하는 뉴클레오타이드 서열 및 IRES 서열 후에 자가-가교결합 항체를 코딩하는 뉴클레오타이드의 서열을 위치시키는 것이 유리할 수 있다. 이러한 배열은 자가-가교결합 항체와 비교하여 과량의 자유-메디토프 펩타이드의 발현을 허용하여 생산, 분리 동안, 및/또는 저장 동안 항체가 자가-가교결합되는 것을 감소시키거나 방지한다.
2. 신호 서열 구성 요소
일부 실시양태에서, 자가-가교결합 항체는 직접적으로 뿐만 아니라 이종 (heterologous) 폴리펩타이드와의 융합 폴리펩타이드로서 재조합적으로 생산될 수 있으며, 이는 성숙 단백질 또는 폴리펩타이드의 N- 말단에 특이적 절단 부위 (specific cleavage site)를 갖는 신호 서열 또는 다른 폴리펩타이드일 수 있다. 바람직하게 선택된 이종 신호 서열은 숙주 세포에 의해 인식되고 처리 (예를 들어, 신호 펩티다아제에 의해 절단)되는 것이다. 천연 항체 신호 서열(native antibody signal sequence)을 인식 및 처리하지 않는 원핵 숙주 세포에 대하여, 신호 서열은 예를 들어 알칼리성 포스파타아제 (alkaline phosphatase), 페니실리나아제(penicillinase), lpp, 또는 열-안정성엔테로톡신 II 리더(heat-stable enterotoxin II leaders)의 그룹(군)으로부터 선택된 원핵 세포 신호 서열로 치환된다. 효모 분비(yeast secretion)의 경우, 천연 신호 서열(native signal sequence)은 예를 들어 효모 인버타아제 리더(yeast invertase leader), 인자 리더(factor leader)(Saccharomyces 및 Kluyveromyces α- 인자 리더 포함), 또는 산 포스 파타아제 리더(acid phosphatase leader), C. albicans 글루코아밀라아제 리더(albicans glucoamylase leader), 또는 WO 90/13646에 기재된 신호로 대체 될 수 있다. 포유동물 세포 발현에서, 포유류 신호 서열뿐만 아니라 바이러스성 분비 리더(viral secretory leaders), 예를 들어 헤르페스 심플렉스gD 신호(herpes simplex gD signal)가 이용 가능하다.
3. 복제 원점
발현 및 클로닝 벡터 모두는 일반적으로 벡터가 하나 이상의 선택된 숙주 세포에서 복제할 수 있게 하는 핵산 서열을 포함한다. 클로닝 벡터에서 이러한 서열은 벡터가 숙주 염색체 DNA와 독립적으로 복제할 수 있게 할 수 있으며, 복제원점 또는 자율적으로 복제하는 서열을 포함할 수 있다. 이러한 서열은 다양한 박테리아, 효모 및 바이러스에서 잘 알려져 있다. 플라스미드 pBR322의 복제원점은 대부분의 그람 음성 박테리아에 적합하며, 2μ 플라스미드 원점(Origin)은 효모에 적합하고, 다양한 바이러스 원점(SV40, 폴리오마(polyoma), 아데노바이러스(adenovirus), VSV 또는 BPV)은 포유류 세포에서 벡터를 클로닝하는데 유용하다. 초기 프로모터를 함유하고 있기 때문에 SV40 원점은 초기 프로모터(early promoter)를 함유하고 있기 때문에 사용될 수 있기는 하지만, 일반적으로 복제원점의 성분(component)은 포유류 발현 벡터에 필요하지 않다.
4. 선택 구성요소
발현 벡터 및 클로닝 벡터는 선택 마커(selectable marker)라고도하는 선택 유전자(selection gene)를 포함할 수 있다. 전형적인 선택 유전자는 (a) 암피실린(ampicillin), 네오마이신(neomycin), 메토트렉세이트(methotrexate) 또는 테트라사이클린(tetracycline)과 같은 항생제 또는 다른 독소에 대한 내성을 부여하거나, (b) 영양요구성(auxotrophic) 결핍을 보충하거나, (c) 복합 매개체(complex media), 예를 들어 Bacilli에 대한 D-알라닌 라세마아제(racemase)를 코딩하는(암호화하는) 유전자에서 얻을 수 없는 중요한 영양소를 공급하는 단백질을 코딩한다.
선택 체계(selection scheme)의 한 예는 숙주 세포의 성장을 억제하기 위해 약물을 이용한다. 이종 유전자로 성공적으로 형질 전환된 세포는 약물 내성을 부여하는 단백질을 생성하여 선택 요법(selection regimen)에서 살아남는다. 이러한 지배적인 선택(dominant selection)의 예는 약물 네오마이신(neomycin), 마이코페놀산(mycophenolic acid) 및 히그로마이신(hygromycin)을 사용한다.
포유류 세포에 대한 적절한 선택 마커(selectable markers)의 또 다른 예는 DHFR, 글루타민 신타아제 (glutamine synthetase, GS), 티미딘 키나아제(thymidine kinase) 메탈로티오네인(metallothionein)-I 및 -II, 바람직하게는 영장류 메탈로티오네인, 아네노신 디아미나아제(adenosine deaminase), 오르니틴 디카르복실라아제(ornithine decarboxylase) 등과 같은 항체-코딩 핵산(antibody-encoding nucleic acid)을 취할 능력이 있는 세포의 동정을 가능하게 하는 것이다.
예를 들어, DHFR의 경쟁적 길항제(competitive antagonist)인 메토트렉세이트 (methotrexate, Mtx)를 포함하는 배양 배지에서 형질전환체를 배양함으로써 DHFR 유전자로 형질전환된 세포를 동정할 수 있다. 이러한 조건 하에서, DHFR 유전자는 임의의 다른 공동-형질전환된(co-transformed) 핵산과 함께 증폭된다. 내인성(endogenous) DHFR 활성이 결핍된 차이니즈 햄스터 오바리(Chinese hamster ovary, CHO) 세포주 (예 : ATCC CRL-9096)가 사용될 수 있다.
또는, GS 유전자로 형질전환된 세포는 형질전환체를 GS의 억제제인 L- 메티오닌 설폭시민(methionine sulfoximine)(Msx)을 포함하는 배양 배지에서 배양함으로써 동정된다. 이러한 조건 하에서, GS 유전자는 임의의 다른 공동-형질전환된 핵산과 함께 증폭된다. GS 선별/증폭 시스템은 전술한 DHFR 선별/증폭 시스템과 조합하여 사용될 수 있다.
또한, 목적 항체, 야생형 DHFR 유전자, 및 APH(aminoglycoside 3'-phosphotransferase)와 같은 또 다른 선택가능한 마커를 코딩하는 DNA 서열로 형질전환되거나 공동-형질전환된 숙주 세포(특히 내인성 DHFR을 포함하는 야생형 숙주)는, 예를 들어 카나마이신, 네오마이신 또는 G418과 같은 아미노글리코시딕 항생제와 같은 선택가능한 마커에 대한 선택제(selection agent)를 함유하는 배지에서의 세포 성장에 의해 선택될 수 있다. U.S. Pat. No. 4,965,199를 참조한다.
효모에서 사용하기에 적합한 선택 유전자는 효모 플라스미드 YRp7에 존재하는 trp1 유전자이다 (Stinchcomb et al., Nature, 282 : 39 (1979)). trp1 유전자는 트립토판에서 자라는 능력이 결여된 효모의 돌연변이 균주, 예를 들어 ATCC No. 44076 또는 PEP4-1에 대한 선택 마커를 제공한다. Jones, Genetics, 85:12 (1977). 효모 숙주 세포 게놈에서 trp1 병변의 존재는 트립토판의 부재 하에서의 성장에 의한 형질전환을 검출하기 위한 효과적인 환경을 제공한다. 유사하게, Leu2- 결핍 효모 균주 (ATCC 20,622 또는 38,626)는 Leu2 유전자를 갖는 공지된 플라스미드에 의해 보완된다.
또한, 1.6 μm 원형 플라스미드 pKD1으로부터 유래된 벡터는 클루 베로마이세스(Kluyveromyces) 효모의 형질 전환에 사용될 수 있다. 또한 재조합 칼프 키모신(calf chymosin)의 대량 생산을 위한 발현 시스템이 K. lactis에 대해 보고되었다. Van den Berg, Bio / Technology, 8 : 135 (1990). 클루베로 마이세스(Kluyveromyces)의 산업 균주(industrial strains)에 의한 성숙한 재조합 인간 혈청 알부민의 분비를 위한 안정한 다중 - 복제(Stable multi-copy) 발현 벡터가 또한 공개되었다. Fleer 등, Bio / Technology, 9 : 968-975 (1991)]에 기재되어 있다.
5. 프로모터 구성 요소
발현 및 클로닝 벡터는 일반적으로 숙주 유기체에 의해 인식되고, 항체를 코딩하는 핵산에 작동 가능하게 연결된 프로모터를 함유한다. 일부 실시양태에서, 상기 벡터는 자가 -가교결합 항체의 전사를 제어하는 하나의 프로모터를 포함한다. 일부 실시양태에서, 벡터는 자기 가교 항체 및 하나 이상의 자유 메디토프를 모두 코딩하는 핵산 서열에 작동 가능하게 연결된 하나의 프로모터를 포함한다. 또 다른 실시 양태에서, 상기 벡터는 제 1 프로모터에 작동 가능하게 연결된 재조합 메디토프 이용가능 항체 또는 이의 항원 결합 단편을 코딩하는 뉴클레오타이드 서열 및 제 2 프로모터에 작동 가능하게 연결된 자유 메디토프를 코딩하는 뉴클레오티드의 서열을 포함한다. 제 1 및 제 2 프로모터는 동일하거나 상이할 수있다.
일부 실시양태에서, 상이한 수준에서 자유 메디토프 및 자가-가교결합 항체를 발현하는 것이 유리할 수 있다. 예를 들어, 생산, 분리 (isolation) 또는 저장 중에 자가-가교결합을 방지하기 위해, 자가-가교결합 항체보다 높은 수준에서 자유 메디토프를 발현하는 것이 유리할 수 있다. 따라서, 일부 실시양태에서, 하나의 프로모터는 보다 강한 프로모터일 수 있고, 보다 높은 전사 개시 속도를 유도하거나, 다른 것보다 RNA 폴리머라제에 대해 더 높은 친 화성을 가질 수 있다. 일부 실시양태에서, 프로모터 중 하나 또는 둘 모두는 조건부 프로모터(conditional promoters )이다.
원핵 생물 숙주와 함께 사용하기에 적합한 프로모터는 phoA 프로모터, β- 락타 마아제 및 락토오즈 프로모터 시스템, 알칼리 포스파타아제 프로모터, 트립토판 (trp) 프로모터 시스템 및 하이브리드 프로모터, 예컨대 tac 프로모터를 포함한다. 그러나, 다른 공지된 박테리아 프로모터가 적합하다. 박테리아 시스템에서의 사용을 위한 프로모터는 항체를 코딩하는 DNA에 작동 가능하게 연결된 Shine-Dalgarno (S.D.) 서열을 포함할 수 있다.
진핵 생물에 대하여 프로모터 서열을 알려져 있다. 실제로 모든 진핵 생물 유전자는 전사가 시작되는 부위로부터 약 25 내지 30 염기 상류( upstream) 에 위치하는 AT가 풍부한 영역 (AT-rich region)을 갖는다. 많은 유전자의 전사 시작 (the tart of transcription) 으로부터 70-80 염기 상류에서 발견되는 또 다른 서열은 N이 임의의 뉴클레오티드일 수 있는 CNCAAT 영역이다. 대부분의 진핵 생물 유전자의 3 '말단에는 코딩 서열의 3'말단에 폴리 (A) 꼬리의 첨가를 위한 신호 일 수있는 AATAAA 서열이 있다. 이들 모든 서열은 진핵 생물 발현 벡터에 적합하게 삽입된다.
효모 숙주와 함께 사용하기에 적합한 프로모터 서열의 예는 3- 포스포 글리세레이트 키나아제 또는 해당 효소(glycolytic enzymes), 예를 들어 에놀라아제, 글리세르 알데히드-3-포스페이트 디하이드로게나아제, 헥소키나아제, 피루베이트 디카르 복실라아제, 포스포프룩토키나아제 (phosphofructokinase), 글루코스-6-포스페이트 이소머라아제, 3- 포스포글리세레이트 뮤타아제, 피루베이트 키나아제, 트리오스 포스페이트 이소머라아제, 포스포글루코오스 이소머라아제 및 글루코키나아제를 포함한다.
성장 조건에 의해 제어되는 전사의 추가 이점을 갖는 유도성 프로모터인 다른 효모 프로모터는, 알코올 디하이드로게나아제 2, 이소시토크롬 C, 산 포스파타아제(acid phosphatase), 질소 대사와 관련된 분해 효소, 메탈로티오네인, 글리세르알데하이드-3-포스페이트 디하이드로게나아제, 및 말토오스 및 갈락토오즈 이용에 관여하는 효소를 위한 프로모터 영역이 있다. 효모 발현에 사용하기에 적합한 벡터 및 프로모터는 EP 73,657에 추가로 기재되어 있다. 효모 인핸서는 또한 효모 프로모터와 함께 유리하게 사용된다.
포유 동물 숙주 세포에서의 벡터로부터의 항체 전사는, 예를 들어, 폴리오마 바이러스( polyoma virus), 계두 바이러스( fowlpox virus), 아데노바이러스 (아데노 바이러스 2와 같은), 소유두종바이러스(bovine papilloma virus), 조류육종바이러스(avian sarcoma virus) , CMV (cytomegalovirus), 레트로바이러스, B형 간염 바이러스(hepatitis-B virus), SV40(Simian Virus 40)와 같은 바이러스 게놈으로부터 수득된 프로모터에 의해, 또는 이종 프로모터가 숙주 세포 시스템과 양립 할 수 있다면, 이종 포유 동물 프로모터 (예를 들어 액틴 프로모터 또는 면역글로블린 프로모터), 열 충격 프로모터로부터 제어될 수 있다.
SV40 바이러스의 초기(early) 및 후기(late) 프로모터는 SV40 바이러스 복제원점을 포함하는 SV40 제한 단편으로서 편리하게 수득된다. 인간 사이토메갈로바이러스(human cytomegalovirus)의 직접적인 초기 프로모터는 HindIII E 제한 단편으로서 편리하게 얻어진다. 소유두종 바이러스 (bovine papilloma virus)를 벡터로 사용하여 포유류 숙주에서 DNA를 발현시키는 시스템은 미국 제 4,419,446 호 에 개시되어 있다. 이 시스템의 변형 예가 미국 특허 제 4,601,978 호에 기술되어 있다. 헤르페스 심플렉스 바이러스로부터의 티미딘 키나아제 프로모터의 조절 하에 마우스 세포에서 인간 β- 인터페론 cDNA의 발현에 대한 문헌 [Reyes et al., Nature 297 : 598-601 (1982)] 참조. 또는, 라우스 육종바이러스(Rous Sarcoma Virus) 긴말단반복 (long terminal repeat), PGK, EF1α, NSE, UBC, CAGG, 시냅신, β- 액틴 또는 GFAP가 프로모터로 사용될 수 있다.
일부 실시양태에서, 발현은 조건부 프로모터(conditional promoter), 인핸서 또는 트랜스작용인자(transactivator)의 제어 하에 있다. 일부 실시양태에서, 자가-가교결합 항체의 발현은 조건부 프로모터, 인핸서 또는 트랜스작용인자의 제어 하에 있으며, 자유 메디토프의 발현은 구조적으로 액티브한 프로모터 (constitutively active promoter) 의 제어 하에 있다. 예시적인 이점으로서, 그러한 양태는 생성된 자가-가교결합 항체의 양, 발현의 시기, 및 자가-가교결합 항체 및 자유 메디토프의 비율을 제어할 수 있다. 일부 실시양태에서, 자가-가교결합 항체의 발현은 구조적으로 액티브한 프로모터, 인핸서 또는 트랜스작용인자의 제어 하에 있으며, 자유 메디토프의 발현은 조건부 프로모터의 제어 하에 있다. 예시적인 이점으로서, 그러한 양태는 생산, 분리(단리) 또는 저장 중에 항체 자가-가교결합을 조절할 필요가 있을 때만 자유 메디토프의 발현을 허용할 수 있다. 일부 실시양태에서, 조건부 프로모터, 인핸서 또는 트랜스작용인자는 유도성 프로모터, 인핸서 또는 트랜스작용인자, 억제 가능한 프로모터, 인핸서 또는 트랜스작용인자, 또는 조직-특이적 프로모터, 인핸서 또는 트랜스작용인자이다.
일부 실시양태에서, 본원에 기재된 임의의 펩타이드 또는 핵산의 발현은, 예를 들어 독시사이클린(doxycycline), 테트라사이틀린 또는 그의 유사체와 같은 조절인자로 세포를 처리함으로써 외부적으로 조절될 수 있다. 테트라 사이클린의 유사체는 예를 들어 클로르테트라사이클린, 옥시테트라 사이클린, 디메틸클로로-테트라사이클린, 메타사이클린, 독시사이클린 및 미노사이클린을 포함한다.
일부 실시양태에서, 유도성 전사 및/또는 발현은 트랜스작용인자 유도 프로모터와 함께 트랜스작용인자를 사용하여 수행될 수 있다. 일부 실시양태에서, 이러한 트랜스작용인자 유도된 프로모터는 목적하는 트랜스진 또는 핵산(transgene or nucleic acid of interest)의 전사의 증강 또는 억제를 위한 조절 요소를 포함한다. 조절 요소에는, 제한없이, 오퍼레이터, 인핸서 및 프로모터가 포함된다. 일부 실시양태에서, 트랜스작동인자 유도성 프로모터는 트랜스작동인자에 결합 될 때 전사 활성을 가지며, 이는 차례로, 특정 세트의 조건 하에서 예를 들어 화학 신호의 특정 조합의 존재 또는 비존재 하에서 활성화되며, 예를 들어 이전의 리스트로부터 선택된 조절 인자에 의해 결정된다.
상기 트랜스작동인자 유도된 프로모터는, 여러가지 tet- 오페론 서열과 같은 트랜스작동인자 결합 서열, 예를 들어 3, 4, 5, 6, 7, 8, 9 또는 10 tet-오페론 서열을 통합하도록 변이된, 본원에 언급된 임의의 프로모터일 수 있다. 일부 실시양태에서, tet- 오페론 서열은 직렬로 존재한다.
조절 인자의 존재 하에 발현을 유도하는 전사 조절 도메인(transcription modulator domains)의 특정 예는 하기 전사 조절기(transcription modulator)에서 발견되는 전사 조절 도메인을 포함하나, 이에 한정되지 않는다: Tet-On 전사 조절기; 및 Tet-On 고급(advanced) 전사 조절기 및 Tet-On 3G 전사 조절기; 이들 모두는 Clontech Laboratories, Mountain View, CA로부터 입수 가능하다. 조절 인자의 부재 하에 발현을 유도하는 전사 조절 도메인의 구체적인 예로는 하기 전사 조절기(transcription modulator)에서 발견되는 전사 조절 도메인을 포함하나, 이에 한정되지 않는다: Tet-off 전사 조절기 및 Tet-Off 고급 전사 조절기는 모두 Clontech Laboratories, Mountain View, CA로부터 입수가능하다. 이러한 시스템은 당업계에 공지되어 있고 당업자에게 익숙한 절차에 따라 적용되고 사용될 수 있다.
일부 실시양태에서, 트랜스작동인자 유도된 프로모터는 억제 핵산 분자 (inhibitory nucleic acid molecule)에 작동 가능하게 연결된 다수의 트랜스작동인자 결합 서열을 포함한다.
트랜스작동인자는, 트랜스작동인자를 코딩하는 서열에 작동 가능하게 연결된 조절 인자-의존 프로모터를 포함하는 동일한 발현 벡터 또는 상이한 발현 벡터에서 핵산 서열에 의해 제공 될 수 있다. 용어 "상이한 발현 벡터(different expression vector)"는 핵산, 예를 들어, 바이러스, 플라스미드, 코스미드 또는 트랜스포존의 전달을 위한 임의의 비히클을 포함하는 것으로 의도된다. 상기 핵산 서열에서 사용하기에 적합한 프로모터는, 예를 들어 세포, 바이러스 또는, 예를 들어 CMV, RSV, PGK, EF1α, NSE, 시냅신(synapsin), β-액틴, GFAP 과 같은 합성원점일 수 있는, 구성적(constitutive), 조절된(regulated), 조직-특이적(tissue-specific) 또는 유비쿼터스 (ubiquitous) 프로모터를 포함한다.
일부 실시양태에 따른 예시적인 트랜스작동인자는 rtTA2-M2 및 Oct-2Q (Q → A) 활성화 도메인의 DNA 결합 도메인으로 구성된 rtTA-Oct.2 트랜스작동인자이다. 일부 실시양태에 따른 또 다른 예시적인 트랜스작동인자는 Tet- 리프레서 단백질 (E.coli) 및 Oct-2Q (Q → A) 활성화 도메인의 DNA 결합 도메인으로 구성된 rtTA-Oct.3 트랜스작동인자다. 둘 모두 특허 출원 WO 2007/004062에 기술되어 있다.
6. 인핵서 인자 구성 요소
고등 진핵 생물에 의한 본 발명의 항체를 코딩하는 DNA의 전사는 종종 벡터에 인핸서 서열을 삽입함으로써 증가된다. 포유류 유전자 (글로빈, 엘라스타아제, 알부민, α- 페토프로틴(fetoprotein) 및 인슐린)로부터 많은 인핸서 서열이 알려졌 있다. 그러나 전형적으로, 하나는 진핵 세포 바이러스로부터의 인핸서를 사용할 것이다. 예를 들어, 복제원점의 후기 (late side) (bp 100-270)의 SV40 인핸서, 사이토메갈로바이러스 초기(early) 프로모터 인핸서, 복제원점의 후기(late side)의 폴리오마 인핸서 및 아데노바이러스 인핸서를 들 수 있다. 진핵 세포 프로모터의 활성화 요소를 향상시키기 위한 인핸싱 요소에 대해서는Yaniv, Nature 297 : 17-18 (1982) 참조. 인핸서는 항체 코딩 서열의 5 '또는 3'위치에서 벡터로 스플라이싱될 수 있지만, 바람직하게는 프로모터로부터 5 '부위에 위치한다.
7. 전사 종결 구성 요소
진핵 생물 숙주 세포 (효모, 균류, 곤충, 식물, 동물, 인간 또는 다른 다세포 생물로부터 유래된 유핵 세포)에서 사용되는 발현 벡터는 또한 전사 종결 및 mRNA 안정화에 필요한 서열을 포함할 수 있다. 이러한 서열은 일반적으로 5 '및 때로는 3'의 진핵 또는 바이러스 DNA 또는 cDNA의 비번역 영역으로부터 이용 가능하다. 이 영역은 항체를 코딩하는 mRNA의 번역되지 않은 부분에서의 폴리아데닐화된 단편으로 전사된 뉴클레오티드 분절(nucleotide segments)을 포함한다. 하나의 유용한 전사 종결 성분은 소성장호르몬(bovine growth hormone) 폴리아데닐화 영역이다. WO94/11026 및 그 문헌에 개시된 발현 벡터를 참조한다.
8. 숙주 세포의 선택과 형질 전환
본 발명의 벡터에서 DNA를 클로닝 또는 발현시키기에 적합한 숙주 세포는 상기 기술된 원핵 세포, 효모 또는 고등 진핵 세포이다. 이러한 목적을 위한 적절한 원핵 생물은 그람-음성 또는 그람-양성 유기체와 같은 진균 (eubacteria), 에스 케리치아 (Escherichia)와 같은 장내 세균 류(Enterobacteriaceae), 예컨대 대장균 (E. coli,), 엔테로박터(Enterobacter), 에르위니아(Erwinia), 클렙시엘라 (Klebsiella) , 프로테우스(Proteus), 살모넬라(Salmonella), 예를 들어, 살모넬라 티피뮤륨(Salmonella typhimurium), 세라티아(Serratia), 예를 들어, Serratia marcescans, 및 시겔라(Shigella), B. 서브틸리스 (B. subtilis) 및 B. 리첸니포미스 (예, B. licheniformis 41P disclosed in DD 266,710 published 12 Apr. 1989)와 같은 바실러스(Bacilli), P. 에루기노사(P. aeruginosa)와 같은 슈도모나스(Pseudomonas), 및 스테렙토마이세스(Streptomyces)를 포함한다. 대장균 B, 대장균 X1776(ATCC 31,537), 및 대장균 W3110(ATCC 27,325)과 같은 다른 균주가 적합하지만, 바람직한 대장균 복제 호스트는 대장균 294(ATCC 31,446)이다. 이러한 예는 제한적인 것이라기 보다는 예시적인 것이다.
전장 항체(Full length antibody), 항체 융합 단백질 및 항체 단편은, 박테리아에서, 특히 글리코실화 및 Fc 효과기 기능이 필요하지 않은 경우, 예를 들어 치료 항체가 세포 독성 (예 : 독소)에 접합된 경우, 그 자체로 종양 세포 파괴에 효과를 보인다. 전장 항체는 서큘레이션 (circulation)에서 보다 큰 반감기를 갖는다. E. coli에서의 생산은 보다 빠르고 비용 효율적이다. 박테리아에서의 항체 단편 및 폴리펩타이드의 발현을 위해, 예를 들어, U.S. 특허 No. 미국 특허 제 5,648,237 호 (Carter et al.), 미국 특허 제 5,789,199 호 (Joly et al.), U.S. 특허 No. 5,840,523 (Simmons et al.)를 참조한다. 여기서 발현 및 분비를 최적화하기 위한 번역 개시 영역(translation initiation region, TIR) 및 신호 서열에 대해 개시한다. E. coli 에서의 항체 단편의 발현을 개시하는, Charlton, Methods in Molecular Biology, Vol. 248 (B. K. C. Lo, ed., Humana Press, Totowa, N.J., 2003), 245-254 페이지를 참조한다. 발현 후, 항체는 가용성 분획에서 대장균 세포 페이스트로부터 분리(단리) 될 수 있고, 이 타입에 따라 예를 들어 단백질 A 또는 G 컬럼을 통해 정제될 수 있다. 최종 정제는 예를 들어 CHO 세포에서 발현된 항체를 정제하는 공정과 유사하게 수행 될 수 있다. 원핵 생물 이외에, 사상균(filamentous fungi) 또는 효모와 같은 진핵 세포는 항체 -인코딩 벡터에 적합한 클로닝 또는 발현 숙주이다. 사카로마이세스 세레비시애(Saccharomyces cerevisiae) 또는 일반 베이커 효모(baker's yeast)는 하등 진핵 (lower eukaryotic) 생물 숙주 미생물 중에서 가장 일반적으로 사용된다. 그러나, 스키조사카로마이세스 폼베(Schizosaccharomyces pombe)와 같은 다수의 다른 속 (genus), 종 (species) 및 균주가 일반적으로 이용가능하고 유용하다; 예를 들어, K. lactis, K. fragilis (ATCC 12,424), K. bulgaricus (ATCC 16,045), K. wickeramii (ATCC 24,178), K. waltii (ATCC 56,500), K. drosophilarum (ATCC 36,906), K. thermotolerans, and K. marxianus; yarrowia (EP 402,226)와 같은 클루이베로마이세스(Kluyveromyces) 숙주; 네우로스포라 크라사(Neurospora crassa); 쉬반니오마이세스 오시덴탈리스(Schwanniomyces occidentalis)와 같은 쉬반니오마이세스(Schwanniomyces); 및 네우로스포라(Neurospora), 페니실륨(Penicillium), 톨리포클라듐(Tolypocladium)과 같은 사상균(filamentous fungi), 및 A.니둘란스(A. nidulans) 및 A. 나이거(A. niger)와 같은 아스퍼질러스(Aspergillus) 숙주. 치료용 단백질의 생산을위한 효모 및 사상 균류의 사용에 대해 검토하는 경우, 예를 들어, Gerngross, Nat. Biotech. 22 : 1409-1414 (2004)]를 참조한다.
글리코실화 경로(glycosylation pathways)가 "인간화된(humanized)" 특정 곰팡이 및 효모 균주를 선택하여 부분적으로 또는 완전히 인간의 글리코실화 패턴을 갖는 항체를 생성시킬 수 있다. 예를 들어, Li 등, Nat. Biotech. 24 : 210-215 (2006)] (피키아 파스토리스 (Pichia pastoris)에서 글리코실화 경로의 인간화를 기술 함); 및 Gerngross et al., supra.를 참조한다.
글리코실화 항체의 발현에 적합한 숙주 세포는 또한 다세포 생물(무척추 동물 및 척추 동물) 유래이다. 무척추 동물 세포의 예는 식물 및 곤충 세포를 포함한다.
Spodoptera frugiperda (애벌레)), Aedes aegypti (모기)), Aedes albopictus (모기), Drosophila melanogaster (과실파리), 및 Bombyx mori와 같은 숙주로부터 수많은 배큘러 바이러스 균주 및 변이체 및 상응하는 허용(permissive) 곤충 숙주 세포가 동정되었다. 형질감염(transfection)을 위하 다양한 바이러스 균주, 예를 들어 Autographa californica NPV의 L-1 변이체 및 Bombyx mori NPV의 Bm-5 균주 가 공개적으로 입수 가능하며, 그러한 바이러스는 본 발명에 따른 본 발명에 따른 바이러스로, 특히 스포도프테라 프루기페르다(Spodoptera frugiperda) 세포의 형질감염을 위해 사용될 수 있다.
면(cotton), 옥수수, 감자, 콩, 피튜니아(petunia), 토마토, 우엉(Leninaceae), 알팔파 (M. truncatula) 및 담배(tobacco)의 식물 세포 배양물도 숙주로서 이용 될 수 있다. 예를 들어, U.S. Pat. Nos. 5,959,177, 6,040,498, 6,420,548, 7,125,978, 및 6,417,429 (트랜스제닉 식물에서 항체를 생산하기 위한 PLANTIBODIESTM 기술을 개시함)를 참조한다.
척추동물 세포는 숙주로서 사용될 수 있고, 배양(조직 배양)에서의 척추동물 세포의 증식은 일상적인 절차가 되었다. 유용한 포유류 숙주 세포주의 예는 SV40 (COS-7, ATCC CRL 1651)에 의해 형질전환된 원숭이 신장 CV1 계통; 인간 배아 신장 세포주(293 세포 또는 HEK-293 세포 (현탁 배양에서 성장을 위해 서브 클로닝 된 세포 포함), Graham et al., J. Gen Virol. 36:59 (1977), FREESTYLE™ 293-F 세포(Invitrogen, Carlsbad, CA)를 포함하는 다른 변이체); 베이비 햄스터 신장 세포 (BHK, ATCC CCL 10); 마우스 세르톨리(sertoli) 세포 (TM4, Mather, Biol. Reprod., 23 : 243-251 (1980)); 원숭이 신장 세포 (CV1 ATCC CCL 70); 아프리카 녹색 원숭이 신장 세포 (VERO-76, ATCC CRL-1587); 인간 자궁 경부암 세포 (HELA, ATCC CCL 2); 개(canine) 신장 세포 (MDCK, ATCC CCL 34); 버팔로 쥐 간세포 (BRL 3A, ATCC CRL 1442); 인간 폐 세포 (W138, ATCC CCL 75); 인간 간세포 (Hep G2, HB 8065); 마우스 유방 종양 (MMT 060562, ATCC CCL51); TRI 세포 (Mather 등, Annals N.Y. Acad. Sci. 383 : 44-68 (1982)); MRC 5 세포; FS4 세포; 및 인간 간암 세포주 (human hepatoma line) (Hep G2)을 포함한다.
다른 유용한 포유 동물 숙주 세포주는 DHFR-CHO 세포 (Urlaub 등, Proc. Natl. Acad. Sci. USA 77 : 4216 (1980))를 포함하는 차이니즈 햄스터 오바리(CHO) 세포; 및 NS0 및 Sp2/0과 같은 골수종 세포주를 포함한다. 항체 생산에 적합한 특정 포유 동물 숙주 세포주의 리뷰는 예를 들어, Yazaki and Wu, Methods in Molecular Biology, Vol. 248 (B. K. C. Lo, ed., Humana Press, Totowa, N.J., 2003), pp. 255-268을 참조한다.
숙주 세포는 항체 생산을 위하여 상기 발현 또는 클로닝 벡터로 형질 전환되고, 프로모터 유도, 형질전환체 선택, 또는 원하는 서열을 코딩하는 유전자의 증폭을 위해 적절하게 변이된 통상적인 영양 배지에서 배양된다.
9. 숙주 세포 배양
자가-가교결합 항체를 생산하는데 사용되는 숙주 세포는 다양한 배지에서 배양 될 수 있다. Ham 's F10 (Sigma), Minimal Essential Medium (MEM), (Sigma), RPMI-1640 (Sigma) 및 Dulbecco 's Modified Eagle 's Medium ((DMEM), Sigma) 과 같은 상업적으로 이용 가능한 배지가 숙주 세포 배양에 적합하다. 또한, Ham et al., Meth. Enz. 58:44 (1979), Barnes et al., Anal. Biochem. 102:255 (1980), U.S. Pat. Nos. 4,767,704; 4,657,866; 4,927,762; 4,560,655; 또는 5,122,469; WO 90/03430; WO 87/00195; or U.S. Pat. Re. 30,985 에 개시된 임의의 배지가 숙주 세포를 위한 배양 배지로 사용될 수 있다. 이 배지는 필요에 따라 호르몬 및/또는 다른 성장 인자 (인슐린, 트랜스페린 또는 표피 성장 인자), 염 (예 : 소듐 클로라이드, 칼슘, 마그네슘 및 포스페이트), 완충액 (예 : HEPES), 뉴클레오타이드(예 : 아데노신 및 티미딘), 항생제 (GENTAMYCINTM 약물과 같은), 미량 원소 (일반적으로 마이크로 몰 범위의 최종 농도로 존재하는 무기 화합물로 정의됨) 및 글루코오스 또는 등가의 에너지 원을 포함할 수 있다. 당업자에게 공지된 임의의 다른 필요한 보충물도 적절한 농도로 포함될 수 있다. 온도, pH 등과 같은 배양 조건은 발현을 위해 선택된 숙주 세포와 함께 이전에 사용된 것들이며, 이는 통상의 기술자에게 명백할 것이다.
B. 항체의 정제
재조합 기술을 사용할 때, 항체는 세포 내, 주변세포질 공간(periplasmic space)에서 생성되거나, 배지(medium)로 직접 분비 될 수 있다. 항체가 세포 내에서 생성되면, 제1 단계로서, 예를 들어 원심 분리 또는 한외 여과에 의해 숙주 세포 또는 용해된 단편의 미립자 잔해를 제거한다. Carter et al., Bio / Technology 10 : 163-167 (1992)은 대장균의 세포질 주위 공간으로 분비되는 항체를 분리(단리)하기 위한 절차를 기술한다. 간략하게, 세포 페이스트는 약 30 분에 걸쳐 아세트산 나트륨 (pH 3.5), EDTA 및 페닐메틸 술포닐플루오라이드(PMSF)의 존재 하에서 녹는다. 세포 잔해(debris)은 원심 분리로 제거 할 수 있다. 항체가 배지로 분비되는 경우, 이러한 발현 시스템으로부터의 상청액은 일반적으로 시판되는 단백질 농축 필터, 예를 들어, Amicon 또는 Millipore Pellicon 한외 여과 유닛을 사용하여 먼저 농축된다. PMSF와 같은 프로테아제 억제제는 단백질 분해를 억제하기 위한 전술한 단계들 중 임의의 단계에 포함될 수 있고, 항생제가 우발적인 오염물의 성장을 방지하기 위해 포함될 수 있다.
세포로부터 제조된 항체 조성물은 예를 들어 히드록실아파타이트 크로마토 그래피, 소수성 상호 작용 크로마토그래피, 겔 전기 영동, 투석 및 친화성 크로마토그래피를 사용하여 정제할 수 있으며, 친화 크로마토그래피는 통상적으로 바람직한 정제 단계 중 하나이다. 친화성 리간드로서의 단백질 A의 적합성은 항체에 존재하는 임의의 면역 글로불린 Fc 도메인의 종(species) 및 이소타입(isotype)에 의존한다. 단백질 A는 인간 γ1, γ2 또는 γ4 중쇄를 기반으로 하는 항체를 정제하는데 사용될 수 있다(Lindmark et al., J. Immunol. Meth. 62 : 1-13 (1983)). 단백질 G는 모든 마우스 이소타입 및 인간 γ3에 대해 권장된다(Guss et al., EMBO J. 5 : 15671575 (1986)). 친화성 리간드가 부착된 매트릭스는 가장 흔히 아가로오스이지만, 다른 매트릭스도 이용 가능하다. 제어된 포어 글래스 (controlled pore glass) 또는 폴리(다이스티렌디비닐)벤젠과 같은 기계적으로 안정한 매트릭스는 아가로오스로 달성할 수 있는 것보다 빠른 유속 및 짧은 처리 시간을 허용한다. 항체가 CH3도메인을 포함하는 경우, Bakerbond ABXTM 수지 (J. T. Baker, Phillipsburg, NJ)가 정제에 유용하다. 다른 단백질 정제 기술, 예를 들어 이온 교환 컬럼, 에탄올 침전, 역상 (Reverse Phase) HPLC, 실리카 상의 크로마토 그래피, 음이온 또는 양이온 교환 수지 (예: 폴리아스파르트산 (polyaspartic acid) 칼럼) 상의 헤파린 SEPHAROSETM 크로마토 그래피 상의 크로마토그래피, 크로마토포커싱, SDS-PAGE, 및 황산 암모늄 침전은 또한 회수될 항체에 따라 이용 가능하다. 일반적으로, 연구, 시험 및 임상에서 사용하기 위한 항체를 제조하기 위한 다양한 방법론은 상기에서 기술한 방법론과 일치하고/하거나 목적하는 특정 항체에 대해 당업자에 의해 적절하게 고려되는 바와 같이 당업계에 잘 확립되어 있다.
C. 자가-가교결합 항체 접합체(Self-Crosslinking Antibody-Agent Conjugates) 를 포함하는 조성물
특정 실시 양태에서, 자가-가교결합 항체는 하나 이상의 치료제 또는 진단 제제, 예를 들어, 영상화제, 치료 유효성 제제(therapeutically effective agents) 또는 화합물을 치료 유효량의 화합물 또는 둘 모두에 접합된다. 제공된 복합체는, 일부 실시양태에서는 복수의 메디토프, 하나 이상의 링커 및 하나 이상의 제제(agent)를 포함한다.
본 발명은 질환 또는 상태를 치료, 예방, 진단 또는 모니터링하기 위해, 치료 또는 진단 (예 : 이미징) 제제 또는 화합물과, 메디토프 또는 그의 변이체, 링커, 및/또는 항체를 접합시키는 것을 고려한다. 일 측면에서, 자가-가교결합 결합 항체와 제제(agent)의 그러한 접합은 질환을 치료 및 검출하기 위한 단일클론 항체(mAb) 기반 치료법 및 이미징 방법을 현저히 향상시킬 고도의 다용도의 플랫폼(versatile platform) 기술을 제공한다.
제제(agent)는 당업계에 공지된 임의의 수단에 의해 접합될 수 있다. 일부 실시양태에서, 상기 제제는 라이신 (lysine), 티로신 (tyrosine), 글루탐산(glutamic acid), 아스파르트산 (aspartic acid), 포르밀글리신 (formylglycine) 또는 알데히드 태그 (aldehyde tag), 비 천연 아미노산 (unnatural amino acid) 등에 접합된다. 포르밀글리신 또는 알데히드 태그는, 반응성 알데히드 그룹을 생성시키는 포르밀글리신-생성 효소 (FGE)에 의해 인식되고 표적화될 수 있는 6-아미노산 (LCTPSR; 서열번호 247) 또는 13- 아미노산 (LCTPSRGSLFTGR, 서열번호 248) 서열을 포함할 수 있다. 반응성 알데히드 그룹은 메디토프와 제제의 접합을 포함하는 서브시퀀스 반응 (subsequence reactions)에 유용 할 수 있다. Carrico 등, Nature Chemical Biology 3, 321-322 (2007) 참조.
진단 및 치료제에는 관련 기술 분야에 공지된 임의의 이러한 제제가 포함된다. 영상화제(imaging agent) 중에는 형광 및 발광 물질이 있고, 이들은 염료", "표지 (labels)" 또는 "표지자 (indicators)"로 흔히 칭하는 다양한 유기 또는 무기 소분자를 포함하되 이들로 제한되지는 않는다. 예로는 플루오레세인, 로다민, 아크리딘 염료, Alexa 염료 및 시아닌 염료를 들 수 있다. 본원의 실시 양태에 따라 영상화제로 사용될 수 있는 효소로는 겨자무 과산화효소(horseradish peroxidase), 알칼리 포스파타제, 산 포스파타아제, 글루코오스 옥시다아제, β-갈락토시다아제, β-글루코로니다아제 또는 β-락타마아제를 들 수 있지만, 이들로 제한되지는 않는다. 이러한 효소는 검출 가능한 신호를 생성하는 발색체, 형광성 화합물 또는 발광성 화합물과 조합되어 사용될 수 있다.
본원의 실시 양태에 따라 영상화제로서 사용될 수 있는 방사성 물질은, 18F, 32P, 33P, 45Ti, 47Sc, 52Fe, 59Fe, 62Cu, 64Cu, 67Cu, 67Ga, 68Ga, 77As, 86Y, 90Y. 89Sr, 89Zr, 94Tc, 94Tc, 99mTc, 99Mo, 105Pd, 105Rh, 111Ag, 111In, 123I, 124I, 125I, 131I, 142Pr, 143Pr, 149Pm, 153Sm, 154-1581Gd, 161Tb, 166Dy, 166Ho, 169Er, 175Lu, 177Lu, 186Re, 188Re, 189Re, 194Ir, 198Au, 199Au, 211At, 211Pb, 212Bi, 212Pb, 213Bi, 223Ra 또는 225Ac를 포함하지만, 이들로 제한되는 것은 아니다. 본원 실시 양태에 따라 추가의 영상화제로서 사용될 수 있는 상자성 이온 (Paramagnetic ions)은 전이 금속 및 란탄족 금속(예를 들어, 21-29, 42, 43, 44 또는 57-71의 원자 번호를 갖는 금속) 이온을 포함하지만, 이에 제한되는 것은 아니다. 이들 금속은 Cr, V, Mn, Fe, Co, Ni, Cu, La, Ce, Pr, Nd, Pm, Sm, Eu, Gd, Tb, Dy, Ho, Er, Tm, Yb 및 Lu의 이온을 포함한다.
영상화제가 방사성 금속 또는 상자성 이온일 때, 상기 제제는 이러한 이온을 결합시키기 위한 긴 꼬리에 부착된 1개 이상의 킬레이팅 기를 갖는 긴 꼬리를 갖는 다른 긴 꼬리 시약과 반응할 수 있다. 긴 꼬리는, 예를 들어 폴리리신, 폴리사카라이드, 또는 금속 또는 이온에 결합하기 위해 첨가될 수 있는 펜던트 기를 갖는 다른 유도된(derivatized) 또는 유도체화 쇄 (derivatizable chain)와 같은 중합체일 수 있다. 본 개시내용에 따라 사용될 수 있는 킬레이팅 기의 예로는 에틸렌디아민테트라아세트산(EDTA), 디에틸렌트리아민펜타아세트산(DTPA), DOTA, NOTA, NETA, 포르피린, 폴리아민, 크라운 에테르, 비스-티오세미카르바존, 폴리옥심 및 유사 기를 들 수 있지만, 이들로 제한되지는 않는다. 킬레이트는 면역 반응성의 최소 손실 및 최소 응집으로 분자에 대한 결합 형성 및/또는 내부 가교결합을 가능하게 하는 기(group)에 의해 PSMA 항체 또는 기능성 항체 단편에 통상 연결된다. 동일한 킬레이트는, 망간, 철 및 가돌리늄과 같은 비 방사성 금속과 복합체될 때, 본원에 기재된 항체 및 담체와 함께 사용될 때, MRI에 유용하다. NOTA, DOTA, 및 TETA와 같은 거대고리 킬레이트는 각각 갈륨, 이트륨 및 구리의 방사성 핵종(이들로 제한되지는 않음)을 비롯한 다양한 금속 및 방사성 금속을 사용한다. RAIT에 대한 223Ra와 같은 안정하게 결합하는 핵종에 중요한 거대고리 폴리에테르와 같은 다른 고리 유형의 킬레이트를 사용할 수 있다. 특정 실시양태에서, 킬레이팅 모이어티는 PET 분석에 사용하기 위한 표적 분자에 AI-18F 복합체와 같은 PET 영상화제를 부착시키기 위해 사용될 수 있다.
예시적인 치료제로는 약물, 화학치료제, 치료학적 항체 및 항체 단편, 독소, 방사성 동위원소, 효소(예를 들면, 종양의 자리에서 프로드럭을 세포독성 물질로 분할하는 효소), 뉴클레아제, 호르몬, 면역조절제, 안티센스 올리고뉴클레오타이드, RNAi 분자(예를 들면, siRNA 또는 shRNA), 킬레이터, 붕소 화합물, 광활성제 및 염료를 들 수 있지만, 이들로 제한되지는 않는다. 치료제는 또한 표적된 세포가 건강한 세포와 비교하여 방사선 치료에 더 민감하게 되도록 방사선증감제로서 작용하는 킬레이터에 결합된 코어-셀 나노입자, 금속간 화합물, 금속 합금 또는 금속을 포함할 수 있다. 추가로, 치료제는 MRI 조영제를 위한 상자성 나노입자(예를 들면, 자철석 또는 Fe3O4)를 포함할 수 있고, 다른 유형의 치료(예를 들면, 광역학 및 고열발생 치료) 및 영상화(예를 들면, 형광 영상화(Au 및 CdSe))와 사용될 수 있다.
화학치료제는 종종 세포 독성 또는 세포 증식억제성이 있으며, 알킬화제, 대사길항제, 항-종양 항생제, 토포아이소머라제 억제제, 핵분열 억제제 호르몬 치료제, 표적 치료제 및 면역 치료제를 포함할 수 있다. 일부 실시양태에서 본 개시내용의 실시양태에 따라 치료제로서 사용될 수 있는 화학치료제로는 13-시스-레티노산, 2-클로로데옥시아데노신, 5-아자시티딘, 5-플루오로우라실, 6-머캅토푸린, 6-티오구아닌, 악티노마이신-D, 아드리아마이신, 알데스류킨, 알렘투주맙, 알리트레티노인, 올-트랜스레티노산, 알파 인터페론, 알트레타민, 아메톱테린, 아미포스틴, 아나그렐리드, 아나스트로졸, 아라비노실시토신, 삼산화비소, 암사크린, 아미노캄프토테신, 아미노글루테티미드, 아스파라기나제, 아우리스타틴, AFP(dimethylvaline-valine-dolaisoleuine-dolaproine-phenylalanine-p-phenylenediamine), MMAF(dovaline-valine-dolaisoleuine-dolaproine-phenylalanine), MMAE(monomethyl auristatin E), 오레오마이신(auromycins), 아자시티딘, 바실루스 칼메트-게렝(BCG), 벤다무스틴, 베바시주맙, 에타너셉트(etanercept), 벡사로텐, 비칼루타미드, 비스무트, 보르테조밉, 블레오마이신, 부술판, 칼슘 류코보린, 시트로보룸 인자, 카페시타빈, 카네르티닙, 카르보플라틴, 카르무스틴, 세툭시맙, 클로람부실, 시스플라틴, 클라드리빈, 코티손, 시클로포스파미드, 시타라빈, cc1065, 다르베포에틴 알파, 다사티닙, 다우노마이신, 데시타빈, 데닐류킨 디프티톡스, 덱사메타손, 덱사손, 덱스라족산, 닥티노마이신, 다우노루비신, 데카르바진, 도세탁셀, 돌라스타틴(dolostatins), 독소루비신, 독시플루리딘, 에닐우라실, 에피루비신, 에포에틴 알파, 에를로티닙, 에버롤리무스, 엑세메스탄, 에스트라무스틴, 브롬화 에티듐, 에토포사이드, 필그라스팀, 플루옥시메스테론, 풀베스트란트, 플라보피리돌, 플록수리딘, 플루다라빈, 플루오로우라실, 플루타미드, 게피티닙, 겜시타빈, 겜투주맙 오조가마이신, 고세렐린, 과립구-콜로니 자극 인자, 과립구 대식세포-콜로니 자극 인자, 헥사메틸멜라민, 히드로코티손 히드록시우레아, 이브리투모맙, 인터페론 알파, 인터류킨-2, 인터류킨-11, 이소트레티노인, 익사베필론, 이다루비신, 이마티닙 메실레이트, 이포스파미드, 이리노테칸, 라파티닙, 레날리도마이드, 레트로졸, 류코보린, 류프롤라이드, 리포솜 Ara-C, 로무스틴, 메클로레타민, 메게스트롤, 멜팔란, 머캅토푸린, 메스나, 메토트렉세이트, 메틸프레드니솔론, 미토마이신 C, 미토탄, 미톡산트론, 메이톤시노이드(maytonsinoids), 넬라라빈, 닐루타미드, 옥트레오타이드, 오프렐베킨, 옥살리플라틴, 파클리탁셀, 파미드로네이트, 페메트렉세드, 파니투무맙, PEG 인터페론, 페가스파르가세, 페그필그라스팀, PEG-L-아스파라기나제, 펜토스타틴, 플리카마이신, 프레드니솔론, 프레드니손, 프로카르바진, 랄록시펜, 리신, 리신A-쇄, 리툭시맙, 로미플로스팀, 랄리트렉세드, 사파시타빈, 사르그라모스팀, 사트라플라틴, 소라페닙, 수니티닙, 세무스틴, 스트렙토조신, 택솔, 타목시펜, 테가푸르, 테가푸르-우라실, 템시롤리무스, 테모졸라미드, 테니포사이드, 탈리도마이드, 티오구아닌, 티오테파, 토포테칸, 토레미펜, 토시투모맙, 트라스투주맙, 트레티노인, 트리미트렉세이트, 알루비신, 빈크리스틴, 빈블라스틴, 빈데스틴, 비노렐빈, 보리노스타트, yttrieum, 또는 졸레드론산을 들 수 있지만, 이들로 제한되지는 않는다.
본 개시 내용의 실시 양태에 따라 치료제로서 사용될 수 있는 치료용 항체 및 이의 기능성 단편으로는 알렘투주맙, 베바시주맙, 세툭시맙, 에드레콜로맙, 겜투주맙, 이브리투모맙 티욱세탄, 파니투무맙, 리툭시맙, 토시투모맙, 및 트라스투주맙 및 본원에 기재된 특정 질환과 관련된 다른 항체를 들 수 있지만, 이들로 제한되지는 않는다.
본 개시 내용의 실시 양태에 따라 치료제로서 사용될 수 있는 독소로는 리신, 아브린, 리보뉴클레아제(RNase), DNase I, 스타필로코커스 장내독소-A, 포크위드(pokeweed) 항바이러스 단백질, 젤로닌, 디프테리아 독소, 슈도모나스 외독소 및 슈도모나스 내독소를 들 수 있지만, 이들로 제한되지는 않는다. 본 개시 내용의 실시 양태에 따라 치료제로서 사용될 수 있는 방사성 동위원소로는 32P, 89Sr, 90Y. 99mTc, 99Mo, 131I, 153Sm, 177Lu, 186Re, 213Bi, 223Ra 및 225Ac를 들 수 있지만 이에 제한되지 않는다.
D. 자가-가교결합 항체 및 자유 메디토프(Free Meditope)를 포함하는 조성물
또한, 본원에서는 자가-가교결합 항체 및 자유 메디토프를 포함하는 조성물이 제공된다. 본원에 기재된 바와 같이, 이러한 조성물은 발현, 제형 및 저장 동안 에 자가-가교결합을 조절하거나 제어하는데 유리할 수 있으며, 또는 본원에 기술된 임의의 방법과 함께 사용할 수 있다. 자유 메디토프는 자가-가교결합 항체와 동시에 발현될 수 있지만, 전술 한 바와 같이, 또는 조성물에 별도로 첨가될 수 있다.
일부 실시양태에서, 상기 조성물은 자가-가교결합 항체에 비해 고농도의 자유 메디토프를 포함한다. 예를 들어, 일부 실시양태에서, 자가-가교결합 항체와 자유 메디토프의 비율은 1:1 내지 1:1,000이고, 약 1:2, 1:3, 1:4, 1:5, 1:6, 1:7, 1:8, 1:10, 1:15, 1:20, 1:25, 1:50, 1:75, 1:100, 1:150, 1:200, 1:250, 1:300, 1:400, 1:500, 및 1:750을 포함한다.
일부 실시양태에서, 상기 조성물은 링커를 통해 자가-가교결합 항체에 결합된 메디토프보다 자가-가교결합 항체의 메디토프 결합 부위에 대해 더 높은 친화도를 갖는 자유 메디토프를 포함한다. 일부 실시양태에서, 상기 조성물은 링커를 통해 자가-가교결합 항체에 부착된 메디토프보다 자가-가교결합 항체의 메디토프 결합 부위에 대해 낮은 친화도를 갖는 자유 메디토프를 포함한다. 일부 실시양태에서, 상기 자가-가교결합 항체의 메디토프 결합 부위는, 상기 기재된 바와 같이 하나 이상의 메디토프에 대해 결합 친화도를 변경하는 하나 이상의 치환을 포함한다. 예를 들어, 상기 메디토프 결합 부위는 자가-가교결합 항체에 융합된 메디토프보다 자유 메디토프에 대해 더 높은 친화도를 나타내거나, 또는 그 반대일 수 있다.
농도 및 친화도의 다양한 조합이 또한 고려된다. 저농도의 자가-가교결합 항체와 고농도의 자유 메디토프를 포함하는 조성물이 일부 실시양태에서 유리할 수 있으며, 이때, 상기 자유 메디토프는 상기 자가-가교결합 항체의 메디토프 결합 부위에 대해 높은 친화도를 갖는다. 예를 들어, 이러한 구현예는 자가-가교결합 항체의 생산 또는 저장 동안 자가-가교결합을 최소화할 수 있고, 또는 더 높은 자가-가교결합 능력을 갖는 자가-가교결합 항체의 생산, 저장, 및 사용을 가능하게 할 수 있다. 일부 실시양태에서, 상기 조성물은 고농도의 자가-가교결합 항체 및 상기 자가-가교결합 항체의 메디토프 결합 부위에 대해 높은 결합도를 갖는 고농도의 자유 메디토프를 포함한다. 예시적인 이점으로, 이러한 구현예는 더 농축된 자가-가교결합 항체의 조성물을 가능하게 할 수 있다.
전술한 바와 같이, 일부 실시양태에서 상기 제형은 자유 메디토프가 제1 자가-가교결합 또는 메디토프-이용가능 항체의 메디토프 결합 부위에 대해 증가된 결합도를 갖는 pH를 갖는다. 일부 실시양태에서, 선택된 pH에서의 자유 메디토프의 증가된 친화도는 제1 자가-가교결합 또는 메디토프-이용가능 항체의 메디토프 결합 부위에 대해 제2 자가-가교결합 항체의 메디토프의 친화도보다 더 높다. 일부 실시양태에서, 이러한 친화도의 차이는 항체의 자가-가교결합 활성을 방지하거나 감소시키는데 유리할 수 있다.
또한, 일부 실시양태에서 자가-가교결합 항체의 메디토프는 동족 항원의 부위에 존재하는 pH에서 메디토프 결합 부위에 대해 자유 메디토프보다 더 높은 친화도를 나타낸다. 일부 실시양태에서, 상기 동족 항원의 부위는 암을 포함하는 질환 또는 장애를 갖는 세포 또는 조직을 포함하는 표적화된 세포 또는 조직이다.
E. 자가-가교결합 항체의 특성
메디토프-이용가능한 항체에 대한 메디토포의 결합 특성은, 예를 들어 자가-가교결합 항체와의 결합이 메디토프-Ig 상호작용에 영향을 미치지 않도록 하기 위해, SPR 및 ITC를 포함하는 수많은 공지된 임의의 방법으로 특징지어질 수 있다. 일부의 경우, 이러한 접근법은 일반적으로 세포 표면 (예를 들어 종양 세포의 표면) 상에 존재하는 항원을 포함하지 않기 때문에, 그러한 측정법은 상승효과에 대한 능력이 제한될 수 있다. 따라서, 일부 측면에서, FACS 분석 및/또는 세포 생존능 분석는 항체에 의해 인식되는 항원을 발현하는 세포 (예를 들어, 세툭시맙에서 EGFR을 과발현하는 세포) 상에서 직접적으로 자가-가교결합 항체의 효과를 정량화하는데 사용된다. 일반적으로, 자가-가교결합 항체에 의해 인식되는 항원을 발현하는 (예를 들어, 과발현하는) 세포주는 상기 항체가 상기 세포 상에서 발현되는 항원에 결합하는 조건 하에서 자가-가교결합 항체와 함께 배양된다. 일부의 경우, 다양한 농도의 항체가 사용된다. 적절한 배양 시간과 세척이 수행된다. 다가 또는 1가 메디토프에 결합된 비-자가-가교결합 메디토프-이용가능한 항체는 각각 양성 및 음성 대조군으로 사용될 수 있다. 상기 항체와 메디토프는 공지된 유세포 분석 또는 현미경으로 검출가능한 제제로 표지될 수 있다. 일부 실시양태에서, 자가-가교결합 항체의 존재 하에서 (FACS의 경우) 시프트 또는 증가된 신호는, 예를 들어 비-자가-가교결합 항체에 비해, 상승효과 또는 상가효과를 나타낸다. 또 다른 실시예에서, 자가-가교결합 항체의 상가효과를 추가로 확인하기 위해, 비-표지된, 1가 메디토프는 경쟁 분석에서 다른 항원-결합 자가-가교결합 항체에 대한 결합을 위한 표지된 자가-가교결합 항체와 경쟁할 수 있는지 결정하는데 사용된다.
다른 실시예에서, 세포 생존능 분석는 자가-가교결합 항체가 세포-사멸 효과를 증가시키는 능력을 결정하는데 사용된다. 예를 들어, 관심있는 항원을 발현하는 세포는 다양한 농도의 자가-가교결합 항체와 함께 배양될 수 있다. 비-자가-가교결합 메디토프-이용가능 항체에 결합된 다가 메디토프 및 1가 메디토프는 다시 대조군으로 유용하다. 일부 실시양태에서, MTT (3-(4,5-디메틸티아졸-2-일)-2,5-디페닐테트라졸리움 브로마이드)는, 살아있는 세포의 수 또는 백분율을 정량화하는데 사용된다. 세포 생존력, 증식, 및/또는 사멸을 측정하기 위한 다른 접근법은 당해 기술분야에 공지되어 있고 사용될 수 있다.
다른 일 실시예에서, 이러한 분석에서 활성을 보여주는 자가-가교결합 항체의 경우, 웨스턴 블랏 분석 또는 다른 생화학적 또는 신호전달 접근법이 세포 표면 수용체와 같은 특정 항원과 연관된 신호전달의 억제를 조사하기 위해 수행된다 (예를 들어, 세툭시맙의 경우, EGFR 신호전달 경로의 일부인 EGFR, AKT, MAP의 인산화 상태를 추적하기 위해). 그러한 연구로부터의 데이터는 메디토프-이용가능 항체 (즉, 메디토프가 없음), 1가 메디토프, 다가 메디토프, 및/또는 티로신 키나아제 또는 다른 공지된 억제제(AG1478 등)로만 처리되는 세포로부터의 데이터와 비교될 수 있다. 일부 실시양태에서, 자가-가교결합 항체 농도의 기능으로서 세포 사멸의 증가가 관찰되며, 이는 자가-가교결합 항체의 상승적인 세포 사멸 효과를 입증한다.
F. 생물학적으로 활성인 항체의 선별
전술한 바와 같이 제조된 항체는 치료학적 관점으로부터 유익한 특성을 갖는 항체를 선별하는 하나 이상의 "생물학적 활성" 분석 또는 상기 항체의 생물학적 활성을 보유하는 제형 및 조건을 선택하는데 적용될 수 있다. 상기 항체는 항원에 결합하는 능력에 대해 테스트될 수 있다. 일부 실시양태에서, 상기 항체의 결합은 예를 들어 포화 결합; ELISA; 및/또는 경쟁 분석 (예를 들어, RIA's)로 결정될 수 있다. 또한, 상기 항체는 예를 들어, 치료법으로서 효율성을 평가하기 위해 다른 생물학적 활성 분석에 적용될 수 있다. 이러한 분석은 당해 기술분야에 공지되어 있으며 표적 항원 및 항체에 대해 의도된 용도에 따라 달라진다.
관심있는 항원에서 특정 에피토프에 결합하는 항체를 스크리닝하기 위해, 문헌 [Antibodies, A Laboratory Manual, Cold Spring Harbor Laboratory, Ed Harlow and David Lane (1988)]에 기재된 바와 같은 통상적인 교차-차단 분석이 수행될 수 있다. 다르게는, 예를 들어, Champe 등의 [J. Biol. Chem. 270:1388-1394 (1995)]에 기재된 바와 같은 에피토프 맵핑은 상기 항체가 관심있는 에피토프에 결합하는지 결정하기 위해 수행될 수 있다.
G. 제형의 제조
관심 있는 항체의 제조 후 (예를 들어, 본원에 기재된 바와 같이 제형화될 수 있는 항체를 제조하기 위한 기술은 하기에 기술되며 당해 기술분야에 공지되어 있다), 이를 포함하는 약학적 제형이 제조된다. 특정 실시양태에서, 제형화 되는 항체는 사전에 동결건조를 거치지 않았으며 본원에서 관심있는 제형은 수용성 제형이다. 특정 실시양태에서, 상기 항체는 전장 항체이다. 일 실시양태에서, 상기 제형에서 항체는 F(ab')2와 같은 항체 단편이고, 이 경우 전장 항체에 발생하지 않을 수 있는 문제 (예를 들어, 항체의 Fab로의 클리핑(clipping))가 다루어질 필요가 있다. 상기 제형에 존재하는 항체의 치료학적으로 유효한 양은 예를 들어 바람직한 투여량 및 투여 방식(들)을 고려하여 결정된다. 약 25 mg/mL 내지 약 150 mg/mL, 또는 약 30 mg/mL 내지 약 140 mg/mL, 또는 약 35 mg/mL 내지 약 130 mg/mL, 또는 약 40 mg/mL 내지 약 120 mg/mL, 또는 약 50 mg/mL 내지 약 130 mg/mL, 또는 약 50 mg/mL 내지 약 125 mg/mL, 또는 약 50 mg/mL 내지 약 120 mg/mL, 또는 약 50 mg/mL 내지 약 110 mg/mL, 또는 약 50 mg/mL 내지 약 100 mg/mL, 또는 약 50 mg/mL 내지 약 90 mg/mL, 또는 약 50 mg/mL 내지 약 80 mg/mL, 또는 약 54 mg/mL 내지 약 66 mg/mL은 상기 제형에서 예시적인 항체의 농도이다.
일부 실시양태에서, 상기 제형은 추가로 자유 메디토프를 포함한다. 상기 자유 메디토프는 자가-가교결합 항체가 생산, 분리, 및/또는 저장 동안 자가-가교결합하는 것을 감소 또는 방지할 수 있다. 이러한 자유 메디토프는 전술한 바와 같이, 자가-가교결합 항체와 함께 발현 및 분리되거나, 생성된 다음 조성물 및 제형에 개별적으로 첨가될 수 있다. 일부 구현예는 과량의 자유-메디토프 펩타이드를 함유한다. 일부 실시양태에서, 자유 메디토프의 양은 자가-가교결합 항체의 양에 화학량론적으로 관련될 수 있다. 예를 들어, 일부 실시양태에서, 자가-가교결합 항체와 자유 메디토프의 비율은 1:1 내지 1:1,000이고, 약 1:2, 1:3, 1:4, 1:5, 1:6, 1:7, 1:8, 1:10, 1:15, 1:20, 1:25, 1:50, 1:75, 1:100, 1:150, 1:200, 1:250, 1:300, 1:400, 1:500, 및 1:750을 포함한다. 일부 실시양태에서, 메디토프 펩타이드의 유리된 양은, 예를 들어 약 0.1 mg/mL 내지 약 150 mg/mL를 포함하는 농도로 결정된다.
수용성 제형은 pH-완충된 용액에서 항체를 포함하는 것으로 제조된다. 본 발명의 버퍼는 약 5.0 내지 약 7.0 범위 내의 pH를 갖는다. 특정 실시양태에서, 상기 pH는 약 5.0 내지 약 6.5 범위 내이고, 상기 pH 약 5.0 내지 약 6.4 범위 내이며, 약 5.0 내지 약 6.3 범위 내이고, 상기 pH는 약 5.0 내지 약 6.2 범위 내이며, 상기 pH는 약 5.0 내지 약 6.1 범위 내이고, 상기 pH는 약 5.5 내지 약 6.1 범위 내이며, 상기 pH는 약 5.0 내지 약 6.0 범위 내이고, 상기 pH는 약 5.0 내지 약 5.9 범위 내이며, 상기 pH는 약 5.0 내지 약 5.8 범위 내이고, 상기 pH는5.1 내지 약 6.0 범위 내이며, 상기 pH는 약 5.2 내지 약 6.0 범위 내이고, 상기 pH는 약 5.3 내지 약 6.0 범위 내이며, 상기 pH는 약 5.4 내지 약 6.0 범위 내이고, 상기pH는 약 5.5 내지 약 6.0 범위 내이며, 상기 pH는 약 5.6 내지 약 6.0 범위 내이고, 상기 pH는 약 5.7 내지 약 6.0 범위 내이며, 또는 상기 pH는 약 5.8 내지 약 6.0 범위 내이다. 본 발명의 특정 실시양태에서, 상기 제형은 6.0 또는 약 6.0의 pH를 갖는다. 본 발명의 특정 실시양태에서, 상기 제형은 5.9 또는 약 5.9의 pH를 갖는다. 본 발명의 특정 실시양태에서, 상기 제형은 5.8 또는 약 5.8의 pH를 갖는다. 본 발명의 특정 실시양태에서, 상기 제형은 5.7 또는 약 5.7의 pH를 갖는다. 본 발명의 특정 실시양태에서, 상기 제형은 5.6 또는 약 5.6의 pH를 갖는다. 본 발명의 특정 실시양태에서, 상기 제형은 5.5 또는 약 5.5의 pH를 갖는다. 본 발명의 특정 실시양태에서, 상기 제형은5.4 또는 약 5.4의 pH를 갖는다. 본 발명의 특정 실시양태에서, 상기 제형은 5.3 또는 약 5.3의 pH를 갖는다. 본 발명의 특정 실시양태에서, 상기 제형은 5.2 또는 약 5.2의 pH를 갖는다.
이러한 범위 내에서 pH를 조절하는 버퍼의 예는 히스티딘 (예를 들어, L-히스티딘) 또는 아세트산나트륨을 포함한다. 특정 실시양태에서, 상기 버퍼는 약 15 mM 내지 약 25 mM 농도의 히스티딘 아세테이트 또는 아세트산나트륨을 함유한다. 본 발명의 특정 실시양태에서, 상기 버퍼는 약 15 mM 내지 약 25 mM, 약 16 mM 내지 약 25 mM, 약 17 mM 내지 약 25 mM, 약 18 mM 내지 약 25 mM, 약 19 mM 내지 약 25 mM, 약 20 mM 내지 약 25 mM, 약 21 mM 내지 약 25 mM, 약 22 mM 내지 약 25 mM, 약 15 mM, 약 16 mM, 약 17 mM, 약 18 mM, 약 19 mM, 약 20 mM, 약 21 mM, 약 22 mM, 약 23 mM, 약 24 mM, 또는 약 25 mM 농도의 히스티딘 아세테이트 또는 아세트산나트륨을 함유한다. 일 실시양태에서, 상기 버퍼는 pH 5.0, 약 20 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다. 일 실시양태에서, 상기 버퍼는 pH 5.1, 약 20 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다. 일 실시양태에서, 상기 버퍼는 pH 5.2, 약 20 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다. 일 실시양태에서, 상기 버퍼는 pH 5.3, 약 20 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다. 일 실시양태에서, 상기 버퍼는 pH 5.4, 약 20 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다. 일 실시양태에서, 상기 버퍼는 pH 5.5, 약 20 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다. 일 실시양태에서, 상기 버퍼는 pH 5.6, 약 20 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다. 일 실시양태에서, 상기 버퍼는 pH 5.7, 약 20 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다. 일 실시양태에서, 상기 버퍼는 pH 5.8, 약 20 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다. 일 실시양태에서, 상기 버퍼는 pH 5.9, 약 20 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다. 일 실시양태에서, 상기 버퍼는 pH 6.0, 약 20 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다. 일 실시양태에서, 상기 버퍼는 pH 6.1, 약 20 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다. 일 실시양태에서, 상기 버퍼는 pH 6.2, 약 20 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다. 일 실시양태에서, 상기 버퍼는 pH 6.3, 약 20 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다. 일 실시양태에서, 상기 버퍼는 pH 5.2, 약 25 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다. 일 실시양태에서, 상기 버퍼는 pH 5.3, 약 25 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다. 일 실시양태에서, 상기 버퍼는 pH 5.4, 약 25 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다. 일 실시양태에서, 상기 버퍼는 pH 5.5, 약 25 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다. 일 실시양태에서, 상기 버퍼는 pH 5.6, 약 25 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다. 일 실시양태에서, 상기 버퍼는 pH 5.7, 약 25 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다. 일 실시양태에서, 상기 버퍼는 pH 5.8, 약 25 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다. 일 실시양태에서, 상기 버퍼는 pH 5.9, 약 25 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다. 일 실시양태에서, 상기 버퍼는 pH 6.0, 약 25 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다. 일 실시양태에서, 상기 버퍼는 pH 6.1, 약 25 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다. 일 실시양태에서, 상기 버퍼는 pH 6.2, 약 25 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다. 일 실시양태에서, 상기 버퍼는 pH 6.3, 약 25 mM 양의 히스티딘 아세테이트 또는 아세트산나트륨이다.
상기 제형은 약 60 mM 내지 약 240 mM 양의 수크로스를 추가로 포함할 수 있다. 일부 실시양태에서, 상기 제형의 수크로스는 약 60 mM 내지 약 230 mM, 약 60 mM 내지 약 220 mM, 약 60 mM 내지 약 210 mM, 약 60 mM 내지 약 200 mM, 약 60 mM 내지 약 190 mM, 약 60 mM 내지 약 180 mM, 약 60 mM 내지 약 170 mM, 약 60 mM 내지 약 160 mM, 약 60 mM 내지 약 150 mM, 약 60 mM 내지 약 140 mM, 약 80 mM 내지 약 240 mM, 약 90 mM 내지 약 240 mM, 약 100 mM 내지 약 240 mM, 약 110 mM 내지 약 240 mM, 약 120 mM 내지 약 240 mM, 약 130 mM 내지 약 240 mM, 약 140 mM 내지 약 240 mM, 약 150 mM 내지 약 240 mM, 약 160 mM 내지 약 240 mM, 약 170 mM 내지 약 240 mM, 약 180 mM 내지 약 240 mM, 약 190 mM 내지 약 240 mM, 약 200 mM 내지 약 240 mM, 약 80 mM 내지 약 160 mM, 약 100 mM 내지 약 140 mM, 또는 약 110 mM 내지 약 130 mM이다. 일부 실시양태에서, 상기 제형의 수크로스는 약 60 mM, 약 70 mM, 약 80 mM, 약 90 mM, 약 100 mM, 약 110 mM, 약 120 mM, 약 130 mM, 약 140 mM, 약 150 mM, 약 160 mM, 약 170 mM, 약 180 mM, 약 190 mM, 약 200 mM, 약 210 mM, 약 220 mM, 약 230 mM, 또는 약 240 mM이다.
일부 실시양태에서, 상기 제형의 항체 농도는 약 40 mg/ml 내지 약 125 mg/ml이다. 일부 실시양태에서, 상기 제형의 항체 농도는 약40 mg/ml 내지 약 120 mg/ml, 약 40 mg/ml 내지 약 110 mg/ml, 약 40 mg/ml 내지 약 100 mg/ml, 약 40 mg/ml 내지 약 90 mg/ml, 약 40 mg/ml 내지 약 80 mg/ml, 약 40 mg/ml 내지 약 70 mg/ml, 약 50 mg/ml 내지 약 120 mg/ml, 약 60 mg/ml 내지 약 120 mg/ml, 약 70 mg/ml 내지 약 120 mg/ml, 약 80 mg/ml 내지 약 120 mg/ml, 약 90 mg/ml 내지 약 120 mg/ml, 또는 약 100 mg/ml 내지 약 120 mg/ml이다. 일부 실시양태에서, 상기 제형의 항체 농도는 약 60 mg/ml이다. 일부 실시양태에서, 상기 제형의 항체 농도는 약 65 mg/ml이다. 일부 실시양태에서, 상기 제형의 항체 농도는 약 70 mg/ml이다. 일부 실시양태에서, 상기 제형의 항체 농도는 약 75 mg/ml이다. 일부 실시양태에서, 상기 제형의 항체 농도는 약 80 mg/ml이다. 일부 실시양태에서, 상기 제형의 항체 농도는 약 85 mg/ml이다. 일부 실시양태에서, 상기 제형의 항체 농도는 약 90 mg/ml이다. 일부 실시양태에서, 상기 제형의 항체 농도는 약 95 mg/ml이다. 일부 실시양태에서, 상기 제형의 항체 농도는 약 100 mg/ml이다. 일부 실시양태에서, 상기 제형의 항체 농도는 약 110 mg/ml이다. 일부 실시양태에서, 상기 제형의 항체 농도는 약 125 mg/ml이다.
일부 실시양태에서, 계면활성제가 상기 항체 제형에 첨가된다. 예시적인 계면활성제는 폴리소르베이트 (예를 들어, 폴리소르베이트 20, 80 등) 또는 폴록사머 (예를 들어, 폴록사머 188 등)와 같은 비이온성 계면활성제를 포함한다. 계면활성제의 양은 제형화된 항체의 응집을 감소시키고/감소시키거나 제형 내 미립자의 형성을 최소화하고/최소화하거나 흡착을 감소시키는 정도로 첨가된다. 예를 들어, 상기 계면활성제는 약 0.001% 내지 약 0.5% (w/v)의 양으로 제형 내에 존재할 수 있다. 일부 실시양태에서, 상기 계면활성제는 (예를 들어, 폴리소르베이트 20) 약 0.005% 내지 약 0.2%, 약 0.005% 내지 약 0.1%, 약 0.005% 내지 약 0.09%, 약 0.005% 내지 약 0.08%, 약 0.005% 내지 약 0.07%, 약 0.005% 내지 약 0.06%, 약 0.005% 내지 약 0.05%, 약 0.005% 내지 약 0.04%, 약 0.008% 내지 약 0.06%, 약 0.01% 내지 약 0.06%, 약 0.02% 내지 약 0.06%, 약 0.01% 내지 약 0.05%, 또는 약 0.02% 내지 약 0.04%이다. 특정 실시양태에서, 상기 계면활성제는 (예를 들어, 폴리소르베이트 20) 0.005% 또는 약 0.005%의 양으로 제형 내에 존재한다. 특정 실시양태에서, 상기 계면활성제는 (예를 들어, 폴리소르베이트 20) 0.006% 또는 약 0.006%의 양으로 제형 내에 존재한다. 특정 실시양태에서, 상기 계면활성제는 (예를 들어, 폴리소르베이트 20) 0.007% 또는 약 0.007%의 양으로 제형 내에 존재한다. 특정 실시양태에서, 상기 계면활성제는 (예를 들어, 폴리소르베이트 20) 0.008% 또는 약 0.008%의 양으로 제형 내에 존재한다. 특정 실시양태에서, 상기 계면활성제는 (예를 들어, 폴리소르베이트 20) 0.009% 또는 약 0.009%의 양으로 제형 내에 존재한다. 특정 실시양태에서, 상기 계면활성제는 (예를 들어, 폴리소르베이트 20) 0.01% 또는 약 0.01%의 양으로 제형 내에 존재한다. 특정 실시양태에서, 상기 계면활성제는 (예를 들어, 폴리소르베이트 20) 0.02% 또는 약 0.02%의 양으로 제형 내에 존재한다. 특정 실시양태에서, 상기 계면활성제는 (예를 들어, 폴리소르베이트 20) 0.03% 또는 약 0.03%의 양으로 제형 내에 존재한다. 특정 실시양태에서, 상기 계면활성제는 (예를 들어, 폴리소르베이트 20) 0.04% 또는 약 0.04%의 양으로 제형 내에 존재한다. 특정 실시양태에서, 상기 계면활성제는 (예를 들어, 폴리소르베이트 20) 0.05% 또는 약 0.05%의 양으로 제형 내에 존재한다. 특정 실시양태에서, 상기 계면활성제는 (예를 들어, 폴리소르베이트 20) 0.06% 또는 약 0.06%의 양으로 제형 내에 존재한다. 특정 실시양태에서, 상기 계면활성제는 (예를 들어, 폴리소르베이트 20) 0.07% 또는 약 0.07%의 양으로 제형 내에 존재한다. 특정 실시양태에서, 상기 계면활성제는 (예를 들어, 폴리소르베이트 20) 0.08% 또는 약 0.08%의 양으로 제형 내에 존재한다. 특정 실시양태에서, 상기 계면활성제는 (예를 들어, 폴리소르베이트 20) 0.1% 또는 약 0.1%의 양으로 제형 내에 존재한다. 특정 실시양태에서, 상기 계면활성제는 (예를 들어, 폴리소르베이트 20) 0.2% 또는 약 0.2%의 양으로 제형 내에 존재한다. 특정 실시양태에서, 상기 계면활성제는 (예를 들어, 폴리소르베이트 20) 0.3% 또는 약 0.3%의 양으로 제형 내에 존재한다. 특정 실시양태에서, 계면활성제는 (예를 들어, 폴리소르베이트 20) 0.4% 또는 약 0.4%의 양으로 제형 내에 존재한다. 특정 실시양태에서, 계면활성제는 (예를 들어, 폴리소르베이트 20) 0.5% 또는 약 0.5%의 양으로 제형 내에 존재한다.
일 실시양태에서, 상기 제형은 상기 확인된 제제 (예를 들어, 항체, 버퍼, 수크로스, 및/또는 계면활성제)를 함유하고, 벤질 알코올, 페놀, m-크레솔, 클로로부탄올 및 염화 벤제토늄과 같은 하나 이상의 방부제를 필수적으로 포함하지 않는다. 다른 일 실시양태에서, 방부제는 상기 제혀에 포함될 수 있으며, 특히 제형이 다중-투여 제형인 경우에 포함될 수 있다. 방부제의 농도는 약 0.1% 내지 약 2%, 바람직하게는 약0.5% 내지 약 1% 범위 내일 수 있다. 제형의 바람직한 특성에 악영향을 미치지 않는다면, Remington 의 문헌 [Pharmaceutical Sciences 16th edition, Osol, A. Ed. (1980)]에 기재된 것과 같은 하나 이상의 다른 약학적으로 허용가능한 담체, 부형제 또는 안정화제가 제형에 포함될 수 있다. 허용가능한 담체, 부형제 또는 안정화제는 적용되는 투여량 및 농도에서 수혜자에게 비독성이고; 추가의 완충제 (buffering agent); 공-용매; 아스코르빈산 및 메티오닌을 포함하는 항산화제; EDTA와 같은 킬레이트제; 금속 착물 (예를 들어, Zn-단백질 착물); 폴리에스테르와 같은 생분해성 폴리머; 및/또는 염 형성 반대이온 (salt-forming counterions)을 포함한다. 본원에서 예시적인 약학적으로 허용가능한 담체는 수용성 중성-활성 히알루로니다아제 글리코단백질 (sHASEGP)와 같은 간질성 (interstitial) 약물 분산제, 예를 들어, rHuPH20 (HYLENEX®, Baxter International, Inc.)과 같은 인간 수용성 PH-20 히알루로니다아제 글리코단백질를 추가로 포함한다. 특정 예시적인 sHASEGP 및 rHuPH20를 포함하는 사용 방법은 미국 특허공보 제 2005/0260186 호 및 제 2006/0104968 호에 기재되어 있다. 일 측면에서, sHASEGP는 콘드로이티나아제와 같은 하나 이상의 추가적인 글리코사미노글리카네이즈 (glycosaminoglycanases)와 조합된다.
본원에서 상기 제형은 또한 치료되는 특정 적응증에 필요한 하나 이상의 단백질, 바람직하게는 다른 단백질에 악영향을 미치지 않는 상보적인 활성을 갖는 단백질을 함유할 수 있다. 예를 들어, 자가-가교결합 항체는 하나 이상의 추가적인 제제 (예를 들어, 화학요법제, 항-신생물제 또는 조영제)와 함께 조합될 수 있다.일부 실시양태에서, 상기 제형 내에서 항체의 물리적 안정성, 화학적 안정성, 또는 생물학적 활성이 평가되거나 측정된다. 당해 기술분야에 공지되고 본원의 실시예에 기재된 임의의 방법은 상기 제형에서 항체의 안정성과 생물학적 활성을 평가하는데 사용될 수 있다. 예를 들어, 상기 제형 내의 항체의 안정성은, 이로 한정되지 않지만, 크기 배제 크로마토그래피 (SEC 또는 SE-HPLC), 영상화 모세관 등전점전기영동 (ICIEF), 펩타이드 맵핑, 소부피 빛 차광 (volume light obscuration; HIAC) 분석, 및 CE-소듐 도데실 설페이트 (CE-SDS) 및 CE-글리칸 분석과 같은 모세관 전기이동 (CE)으로 측정될 수 있지만, 이로 한정되지 않는다. 일부 실시양태에서, 상기 제형의 항체는 -20°C에서 적어도 약 6개월, 적어도 약 8개월, 적어도 약 10개월, 적어도 약 12개월, 적어도 약 14개월, 적어도약 16 개월, 적어도 약 18개월, 적어도 약 20 개월, 적어도 약 21개월, 적어도 약 22개월, 적어도 약 23개월, 적어도 약 24 개월, 적어도 약 3년, 또는 적어도 약 4년 동안 안정하다. 일부 실시양태에서, 상기 제형의 항체는 2℃ 내지 8℃ (예를 들어, 5℃)에서 적어도 약 6개월, 적어도 약 8개월, 적어도 약 10개월, 적어도 약 12개월, 적어도 약 14개월, 적어도 약 16개월, 적어도 약 18개월, 적어도 약 20개월, 적어도 약 21개월, 적어도 약 22개월, 적어도 약 23개월, 적어도 약 24개월 동안 안정하다. 일부 실시양태에서, 상기 항체의 안정성 (즉, 항체 모노머)은 저장 후 상기 제형에서 크기 배제 크로마토그래피로 측정된다. 일부 실시양태에서, 상기 항체의 안정성은 (즉, 항체 모노머) 보관 후 제형에서 이미지화된 모세관 등전점 전기영동에 의해 측정된다. 일부 실시양태에서, 총 단백질 (예를 들어, 항체 및 응집체를 포함함)과 비교하여 상기 제형에서 항체 모노머의 퍼센트는 -20℃에서 적어도 약 6개월, 적어도 약 12개월, 적어도 약 18개월, 또는 적어도 약 24개월 동안 저장한 후에 약 60%, 약 65%, 약 70%, 약 75%, 약 80%, 약 85%, 약 86%, 약 87%, 약 88%, 약 89%, 약 90%, 약 91%, 약 92%, 약 93%, 약 94% 또는 약 95%를 초과한다. 일부 실시양태에서, 총 단백질 (예를 들어, 항체 및 응집체를 포함함)과 비교하여 상기 제형에서 항체 모노머의 퍼센트는 2℃ 내지 8℃ (예를 들어, 5℃)에서 적어도 약 6개월, 적어도 약 12개월, 적어도 약 18개월, 또는 적어도 약 24개월 저장 후에 약 60%, 약 65%, 약 70%, 약 75%, 약 80%, 약 85%, 약 86%, 약 87%, 약 88%, 약 89%, 약 90%, 약 91%, 약 92%, 약 93%, 약 94% 또는 약 95%를 초과한다. 일부 실시양태에서, 총 단백질 (예를 들어, 항체 및 응집체를 포함함)과 비교하여 상기 제형에서 항체 모노머의 퍼센트는 실온 (예를 들어, 약 15℃ 내지 25℃)에서 적어도 약 2시간, 적어도 약 4시간, 적어도 약 6시간, 적어도 약 8시간, 적어도 약 10시간, 적어도 약 12시간, 적어도 약 14시간, 적어도 약 16시간, 적어도 약 18시간, 적어도 약 20시간, 또는 적어도 약 24시간 동안 교반 후에 약 60%, 약 65%, 약 70%, 약 75%, 약 80%, 약 85%, 약 86%, 약 87%, 약 88%, 약 89%, 약 90%, 약 91%, 약 92%, 약 93%, 약 94% 또는 약 95%를 초과한다.
일부 실시양태에서, 상기 제형에서 총 응집체 (예를 들어, 고분자량 종 및 저분자량 종)의 퍼센트는 -20℃에서 적어도 약 6개월, 적어도 약 12개월, 적어도 약 18개월, 또는 적어도 약 24개월 동안 저장한 후에 약 0.1%, 약 0.2%, 약 0.3%, 약 0.4%, 약 0.5%, 약 0.6%, 약 0.7%, 약 0.8%, 약 0.9%, 약 1%, 약 2%, 약 3%, 약 4%, 약 5%, 약 6%, 약 7%, 약 8%, 약 9%, 또는 약 10% 중 어느 하나 보다 작다. 일부 실시양태에서, 상기 제형에서 총 응집체 (예를 들어, 고분자량 종 및 저분자량 종)의 퍼센트는 2℃ 내지 5℃ (예를 들어, 5℃)에서 적어도 약 6개월, 적어도 약 12개월, 적어도 약 18개월, 또는 적어도 약 24개월 동안 저장한 후에 약 0.1%, 약 0.2%, 약 0.3%, 약 0.4%, 약 0.5%, 약 0.6%, 약 0.7%, 약 0.8%, 약 0.9%, 약 1%, 약 2%, 약 3%, 약 4%, 약 5%, 약 6%, 약 7%, 약 8%, 약 9%, 또는 약 10% 중 어느 하나 보다 작다. 일부 실시양태에서, 상기 제형에서 총 응집체 (예를 들어, 고분자량 종 및 저분자량 종)의 퍼센트는 실온 (예를 들어, 약 15℃ 내지 25℃)에서 적어도 약 2시간, 적어도 약 4시간, 적어도 약 6시간, 적어도 약 8시간, 적어도 약 10시간, 적어도 약 12시간, 적어도 약 14시간, 적어도 약 16시간, 적어도 약 18시간, 적어도 약 20시간, 또는 적어도 약 24시간 동안 교반 후에 약 0.1%, 약 0.2%, 약 0.3%, 약 0.4%, 약 0.5%, 약 0.6%, 약 0.7%, 약 0.8%, 약 0.9%, 약 1%, 약 2%, 약 3%, 약 4%, 약 5%, 약 6%, 약 7%, 약 8%, 약 9%, 또는 약 10% 중 어느 하나 보다 작다. 본원의 임의의 실시예에 있어서, 상기 안정한 제형은 유리병, 금속 합금 용기, 또는 정맥 내 (IV) 백(bag)에 저장될 수 있다. 일부 실시양태에서, 상기 금속 합금은 316L 스테인리스 스틸 또는 하스텔로이이다.
생체 내 투여를 위해 사용되는 제형은 무균이어야 한다. 이는 제형의 제조 전 또는 제조 후에 무균 여과막을 통한 여과에 의해 용이하게 달성된다.
Ⅲ. 사용 방법
본원에서는 또한 자가-가교결합 항체의 방법 및 용도가 제공된다. 제공된 방법 중에는 선택적으로 제제가 결합된 것을 포함하는 자가-가교결합 항체 및 이의 항원 결합 단편을 자가-가교결합 항체에 의해 인식되는 항원을 발현하는 세포 및 조직으로 전달하는 방법이 있다. 일부 실시양태에서, 상기 자가-가교결합 항체는 메디토프-이용가능 자가-가교결합 항체를 포함하여 메디토프-이용가능 항체를 가교결합 시킨다. 일부 실시양태에서, 상기 항체는 세포 표면 항원을 표적화 한다. 예시적인 항원은 이의 세포 또는 조직의 질환 또는 질병에 의해, 또는 수용체 매개 엔도시토시스가 가능한 세포 표면 수용체에 의해 발현된 항원을 포함한다.
A. 세포 표면 항원의 분포를 변경하기 위한 방법
세포 표면 항원을 표적화 하고 숙주 세포의 표면상에 이들 항원의 분포 변화를 생성하기 위해, 메디토프 이용가능 자가-가교결합 항체를 포함하는 자가-가교결합 항체를 이용하는 방법이 제공된다. 예를 들어, 종양 관련 항원과 같은 세포 표면 항원, GPCR과 같은 수용체, 수용체 티로신 키나아제, CTLA4와 같은 다른 신호전달 분자, 및 세포 표면 단백질 상에 존재하는 다른 에피토프의 표시는 이들 항원 상의 에피토프를 인식하는 자가-가교결합 항체의 사용을 통해 조작되고 그리고/또는 재구성될 수 있다. 수용체와 신호전달 분자의 재구성은 신호전달 경로와 세포 반응에 중대한 영향을 미칠 수 있다.
생체 내에서, 이러한 유형의 재구성은 하나의 세포로부터의 리간드가 다른 세포 상의 수용체와 결합하여 효과적으로 다가 상호작용을 일으키는 경우, 세포-세포 접촉을 통해 발생한다. 이러한 접촉점을 통해, 수용체/리간드는 국소화되거나 서로 근접하게 되어, 신호전달 "시냅스"를 생성한다. 신호전달 시냅스는 세포 내에서 번역 후 변형을 일으키며, 예를 들어, 액틴 및 미세소관 구성 또는 단백질 인산화를 변형시켜, 궁극적으로 특정 전사 현상(event)을 유도할 수 있다.
자가-가교결합 항체는 세표 표면 항원의 분포를 변경하는 유사한 방식으로 이용될 수 있다. 일부 실시양태에서, 상기 방법은 표적 세포 상의 세포 표면 항원의 공동-편재화, 응집, 또는 클러스터링을 개선 또는 증가시킨다. 일부 측면에서, 상기 증가는 자가-가교결합 항체를 첨가하기 전 또는 첨가하지 않을 때, 또는 메디토프 가교제없이 항체의 존재 하에 관찰된 것과 비교하여 정도(degree), 속도, 및/또는 기간의 증가이다. 구체적으로, 하나 이상의 자가-가교결합 항체가 투여되어 결합 시 세포의 표면 상의 표적화된 항원에 결합시킬 수 있다. 이러한 효과는 2개 자가-가교결합 메디토프-이용가능 항체의 사용으로 설명된다. 이러한 조합은 제1 메디토프-이용가능 항체의 Fab 암(arm)에 링커를 통해 융합된 하나의 메디토프가 제2 메디토프-이용가능 항체의 Fab 암과 결합하도록 한다. 상기 결합은 동족 항원에 결합된 연결 항체의 복합체 형성을 가능하게 한다. 이 시나리오에서, 당업자는 세포 표면 항원에 결합된 2개의 자가-가교결합 메디토프-이용가능 항체의 "선형" 배열을 예상할 것이다.
일부 측면에서, 메디토프는 인접한 항체, 예를 들어, IgG에 "달라붙어" 세포 표면 항원에 결합한 자가-결합 항체의 "데이지-체인" 유사 또는 웹 유사 배열을 형성할 수 있다. 상기 항체는 서로 결합되고, 서로를 향해 표면 항원을 끌어당기거나 (drawing) 가교결합하여, 효과적으로 세포의 표면에 이들 항원의 표시를 변경한다. 따라서, 종양 세포의 높은 항원 밀도를 고려하여, 더 많은 수의 자가-가교결합 항체의 적용이 예를 들어, 종양 항원을 표적화하는 항체에 사용될 수 있다.
일부 실시양태에서, 자가-가교결합 항체 또는 이의 항원 결합 단편의 각 암(arm)은 상기 항체 또는 이의 단편에 결합되는 메디토프를 포함한다. 전술한 바와 같이, 일부 실시양태에서 상기 링커는 하나 또는 둘 다의 중쇄, 하나 또는 둘 다의 경쇄, 또는 하나 이상의 중쇄 및 경쇄의 조합에 결합 될 수 있다. 따라서, 일부 실시양태에서, 상기 자가-가교결합 항체의 각 메디토프는 하나 이상의 항체의 메디토프 결합 부위에 독립적으로 결합할 수 있다. 예를 들어, 일부 실시양태에서, 상기 자가-가교결합 항체는 또 다른 메디토프-이용가능 항체의 각 암(arm)에서 메디토프 결합 부위에 결합할 수 있다. 일부 실시양태에서, 이는 다른 나머지 항체에 대한 자가-가교결합 항체의 결합 친화도를 변경 또는 증가시킨다. 또 다른 일례로, 일부 실시양태에서, 자가-가교결합 항체의 각 메디토프는 상이한 항체의 메디토프 결합 부위에 결합할 수 있다. 이러한 결합은 결합 기하학, 표면 항원 분포, 또는 항체-항원 복합체를 추가로 변경할 수 있는 상호연결된 자가-가교결합 항체의 수를 증가시킬 수 있다.
다른 일 실시양태에서, 상기 자가-가교결합 항체는 면역 반응에 대해 특이적인 세포를 표시하는데 사용될 수 있다. 이 경우, 자가-가교결합 항체와 결합된 수용체의 클러스터링은 T 세포 상의 FcR에 대해 "고" 농도의 Fc 도메인을 나타낼 것이다. 다수의 조사는 Fc 도메인이 적절한 반응을 유도하는 제한된 수의 점 돌연변이를 통해 특이적으로 조정될 수 있다는 것을 입증하였다.
표적 세포상의 세포 표면 항원의 내재화 및/또는 분해를 향상 또는 증가시키기 위한 항체 전달 방법이 제공된다. 일부 실시양태에서, 상기 방법은 세포 표면 항원(들)에 특이적으로 결합하는 하나 이상의 자가-가교결합 항체를 세포에 투여함으로써 수행되고 링커를 통해 상기 항체에 결합된 메디토프를 포함한다. 일부 실시양태에서, 항원의 내재화 및/또는 분해는 촉진, 향상 또는 증가된다. 일부 실시양태에서, 상기 내재화의 증가는 자가-가교결합 항체의 첨가 전에 또는 첨가하지 않을 때, 또는 메디포트가 없는 항체의 존재 하에 관찰되는 것과 비교하여 수준, 속도, 및/또는 기간의 증가이다. 일부 실시양태에서, 상기 방법은 내재화 또는 세포내 교환(trafficking)을 변경시킨다. 일부 실시양태에서, 상기 방법은 세포간 또는 세포내 신호전달을 변경시킨다.
내재화 속도를 촉진 또는 변경하기 위한 대안적인 접근법이 본원에서 제공된 특정 실시양태에서와 같이 세포 결합 수용체의 응집을 촉진 또는 제어함으로써 이루어진다. 본원의 일부 실시양태에서, 공동-편재화, 클러스터링, 응집, 내재화, 및/또는 세포내 교환 또는 선별이 자가-가교결합 항체를 이용하여 수행, 재현, 또는 개선 또는 변경된다. 링커를 통해 융합된 메디토프를 포함하지 않는 항체를 포함하는, 비-자가-가교결합 항체의 투여에 비해 그러한 수용체 항원을 인식하는 자가-가교결합 항체의 세포로의 투여 후 그러한 표면 수용체의 클러스터링 및/또는 내재화의 차이가 관찰된다. 제공된 구현예 중에는 메디토프-이용가능 항체에 의해 인식되는 표면 항원의 공동-편재화 및 클러스터링 및/또는 수용체를 포함하는, 세포 표면 항원을 포함하는 그러한 항원의 내재화/교환/선별을 촉진하는 자가-가교결합 항체가 있다. 내재화되어야 하는 숙주 세포 상의 세포 표면 단백질은 이의 동족 리간드와의 상호 작용에 덜 이용될 수 있으며, 이는 그 리간드에 대해 숙주 세포가 반응하는 능력에 영향을 미칠 수 있다.
연구는 세포막에 국한된 입자의 크기가 내재화 메커니즘에 중요하다는 것을 입증하였으며 (문헌 [Biochem J. 2004 Jan 1;377(Pt 1):159-69; J Nanobiotechnology. 2014 Feb 3;12:5. doi: 10.1186/1477-3155-12-5] 참조), 이는 관련된 리간드의 크기가 일부 내재화 경로에 영향을 줄 수 있다는 것을 시사한다. 자가-가교결합 항체의 사용은 세포 표면 항원에 결합한 단일 항체와 비교하여 더 큰 입자 크기를 갖는 리간드의 외관을 형성한다. 일부 실시양태에서, 상기 더 큰 입자 크기는 항원 또는 세포 표면 수용체 내재화를 향상시킬 수 있다.
또 다른 일 실시양태에서, 항체 치료의 효능은 i) 메디토프-이용가능 항체의 메디토프 결합 부위에 대한 항체에 결합된 메디토프의 결합 친화도를 조작함으로써, ii) 표적 항원 상의 이의 동족 에피토프에 대한 바람직한 결합 친화도를 갖는 메디토프-이용가능 항체를 선택함으로써, 또는 iii) 자가-가교결합 메디토프-이용가능 항체 복합체를 표적화하는 특이성 뿐만 아니라 수명을 최적화 화는 두 가지 특성 모두를 조작함으로써, 변경 및 개선될 수 있다. 구체적으로, 상호작용의 수명은 동력학 제거 속도 (off-rate)와 관련된다. 일부 경우에, 가능한 최장 수명이 유리할 것으로 생각될 수 있다. 다른 경우에, 적당한 수명 (tau = 10초 내지 10분)이 유리할 것이다. 후자의 경우, 종양 조직에서 과발현되지만, 낮은 수준 (10, 100 or 1000배)이지만 건강한 특정 조직에서도 발현되는 특이적인 수용체 (예를 들어, EGFR 또는 Her2)가 있다. 임상적으로, 종양에 결합하지만 건강한 조직에는 결합하지 않는 것이 바람직할 수 있다. 적당한 수명을 가진 자가-가교결합 항체의 조합을 사용하여 선택성을 향상시킨다. 구체적으로, 정상 세포에서 발견되는 것과 같은 항원의 낮은 농도에서, 메디토프-이용가능 항체는 항원에 결합할 수 있다. 그러나, 제2 메디토프-이용가능 항체가 항원에 결합할 가능성이 낮으면, 이는 항체 가교결합을 막는다. 일부 질환 상태를 포함하는, 고농도의 항원을 갖는 상태에서, 인접한 메디토프-이용가능 항체가 항원에 결합할 가능성이 높을수록, 둘 이상의 자가-가교결합 항체 결합 항원들 사이의 가교를 가능하게 한다.
전술한 바와 같이, 일부 실시양태에서, 상기 방법은 세포 표면 항원의 내재화의 증가된 정도 및/또는 속도를 제공한다. 증가되거나 또는 더 신속한 내재화는 항체가 항체가 질환의 진행과 관련되거나 원인이 되는 표면 수용체 또는 다른 표면 항원의 하향 조절을 촉진시키기 위해 전달되는 경우 유리할 수 있다. 또한, 예를 들어, 세포 표면 상의 수용체 또는 다른 표면 항원의 양을 감소시킴으로써, 예를 들어, 분해를 위해 이를 표적화함으로써 유리하게 될 수 있다. 공동-수용체를 포함하는 일부 그러한 수용체는 세포 신호전달을 달성하거나 매개할 수 있다.
따라서, 본원에 기재된 방법은 일부 실시양태에서 유해한 세포 신호전달 경로를 감소, 방해 또는 제거할 수 있다. 일부 실시양태에서, 본원에 기재된 조성물 및 방법은 항원 내재화를 1.5-, 2-, 3-, 4-, 5-, 6-, 7-, 8-, 9-, 10-, 20-, 30-, 40-, 50-, 75-, 100-, 200-, 300-, 400-, 500-배 또는 그 이상 증가시킬 수 있다. 일부 실시양태에서, 본원에 기재된 조성물 및 방법은 세포의 표면상에 존재하는 항원의 양을 1.5-, 2-, 3-, 4-, 5-, 6-, 7-, 8-, 9-, 10-, 20-, 30-, 40-, 50-, 75-, 100-, 200-, 300-, 400-, 500-배 또는 그 이상 감소시킬 수 있다. 일부 실시양태에서, 본원에 기재된 조성물 및 방법은, 낮은 내재화율을 갖는 항체의 내재화를 포함하여, 항체 내재화를 1.5-, 2-, 3-, 4-, 5-, 6-, 7-, 8-, 9-, 10-, 20-, 30-, 40-, 50-, 75-, 100-, 200-, 300-, 400-, 500-배 또는 그 이상 증가시킬 수 있다.
더 느린 정도 또는 덜 신속한 내재화는 항체가 전달되어 효과기 기능, 예를 들어 ADCC 및/또는 보체 매개 용해를 촉진하고/촉진하거나 세포 표면 수용체 항원을 통해 신호전달에 관여하거나 이를 촉진하기 위해 전달되는 것과 같은 일부의 경우에서 바람직할 수 있다. 일부 실시양태에서, 상기 방법은 세포 표면 항원을 통한 신호의 정도 및/또는 결합된 항체를 통해 매개된 효과기 기능의 정도를 촉진하거나 향상시킨다.
일부 실시양태에서, 비 내재화 항원은 링커를 통해 결합된 메디토프 없이 단일 특이적인 2가 항체의 결합이 상기 항원의 내재화를 야기하지 않거나, 대사 회전으로 인한 정도 또는 항원 특이적인 항체의 부재의 정도보다 크지 않거나 대사 회전으로 인한 정도 또는 항원 특이적인 항체의 부재의 정도보다 2배 이상 크지 않은 내재화를 일으키는 항원이다. 일부 실시양태에서, 단일 특이적 2가 항체와 배양 후 항원은 대사 회전으로 인한 정도 또는 항원 특이적 항체의 부재의 정도 보다 3-, 4-, 5-, 6-, 7-, 8-, 또는 9-배 더 큰 속도로 내재화하지 않는다.
일부 실시양태에서, 비내재화 항원은 세포 표면 항원 단독에 대한 자연 결합 파트너 또는 리간드의 결합이 결과적으로 항원 내재화를 일으키지 않거나, 대사 되전으로 인한 정도, 또는 결합 파트너 또는 리간드의 부재의 정도보다 크지 않거나, 대사 회전으로 인한 정도 또는 리간드/결합 파트너의 부재의 정도보다 2배 더 큰 내재화 정도를 일으키지 않는 항원이다. 일부 실시양태에서, 항원에 대한 자연 리간드 또는 결합 파트너와 세포를 배양한 후 항원은 대사 회전으로 인한 비율 또는 리간드 또는 결합 파트너의 부재의 속도보다 3-, 4-, 5-, 6-,7-, 8-, 또는 9-배 더 큰 비율로 내재화하지 않는다. 일부 실시양태에서, 항원은 링커를 통해 결합된 메디토프가 없는 단일 특이적 2가 항체 또는 자연 리간드 또는 결합 파트너에 결합한 후 적어도 10, 11, 12, 13, 14, 15, 또는 16시간 이상의 반감기로 내재화된다.
B. 항체 치료의 효능을 증가시키기 위한 방법
결합된 제제를 포함하는 항체를 비롯한 세포에 항체를 전달하기 위한 방법이 또한 제공된다. 일부 실시양태에서, 상기 방법은 세포 표면 항원(들)에 특이적으로 결합하는 하나 이상의 자가-가교결합 항체를 세포에 투여함으로써 수행되고, 링커를 통해 항체에 결합되는 메디토프를 포함한다.
일부 실시양태에서, 상기 방법은 세포에 의한 항체 내재화를 증가시킨다. 증가되거나 또는 보다 신속한 내재화는, 예를 들어, ADC 또는 항체가 세포에 제제를 전달하는데 사용되거나 항체가 암과 같은 질환의 진행과 관련되거나 원인이 되는 표면 수용체 또는 표면 항원의 하향조절을 촉진하기 위해, 예를 들어 분해를 위해 이를 표적화 함으로써 전달되는 다른 용도와 관련하여 유리할 수 있다.
다른 실시예에서, 제공된 방법은 세포의 특성을 이용하고, 자가-가교결합 항체와 결합된 제제를 효율적으로 방출하기 위해 결합된 생물학적 제제의 내재화 및 선별 경로를 변경한다. 앞서 논의된 바와 같이, 연구들은 세포막에 국한된 입자의 크기가 일부 내재화 메커니즘에 중요하다는 것을 입증하며, 이는 결합된 리간드의 크기가 일부 내재화 경로에 영향을 미칠 수 있음을 시사한다. 자가-가교결합 항체의 사용은 세포 표면 항원에 결합된 단일 항체와 비교하여 더 큰 입자 크기를 갖는 리간드의 외관을 생성할 것이다.
또한, 다가 메디토프 및 다른 단백질 또는 단백질 도메인에 융합된 메디토프를 포함하는, 자유 메디토프를 포함하는, 메디토프를 전달하는데 있어서 그러한 자가-가교결합 항체의 방법 및 사용을 제공한다. 일부 메디토프는 예를 들어, 치료학적 방법 및 영상화 방법의 제제에 결합 될 수 있다. 예시적인 방법은 선택적으로 링커를 통해 항체에 융합되지 않은 메디토프를 포함하는, 다가 메디토프를 포함하는, 메디토프에 결합된 치료제 또는 조영제와 같은 제제의 전달을 달성하는 것이다.
표적 세포의 표면에 풍부한 특이적 항원을 인식하는 일부 잠재적으로 유용한 항체는 "내재화 가능성이 저조하다" (Matzku et al. Int.J. Cancer. 1988 2:11-14; Reilly et al. Clin. Pharmacokinet. 1995 28:126-142). 저조하거나 차선의 내재화는 표적 기관 또는 조직에서 세포내 전달 및 축척화를 감소시킨다 (Matzku et al. Int. J. Cancer. 1988 2:11-14; Reilly et al. Clin. Pharmacokinet. 1995 28:126-142). 따라서, 상기 "내재화 가능성이 저조한" 항체는 세포내 표적화에 최적화되지 않는다. 이에 따라, 항체 표적화 및 세포에 의한 내재화를 향상시키는 항체 시스템이 요구된다.
일부 항체는 세포에 들어간 후 치료 효과를 나타낸다. 일부 실시양태에서, 증가되거나 또는 더 신속한 내재화는 항체의 효능 또는 효율을 증가시킬 수 있다. 따라서, 일부 실시양태에서, 동일한 치료효과를 달성하는데 더 낮은 투여량이 사용될 수 있다. 일부 실시양태에서, 자가-가교결합 항체의 투여는 1.5-, 2-, 3-, 4-, 5-, 6-,7-, 8-, 9-, 10-, 20-, 30-, 40-, 50-, 75-, 100-, 200-, 300-, 400-, 또는 500-배 낮은 약물을 이용하여 항체 단독 투여로서 동일한 치료효과를 달성할 수 있다.
일부 실시양태에서, 증가되거나 또는 더 신속한 내재화는 항체의 엔도솜으로의 전달을 증가시키거나 더 신속하게 한다. 일부 항체는 단백질 분해 절단 부위를 포함하는 링커를 포함한다. 링커는 조영제 또는 치료제를 포함하는, 제제에 결합될 수 있으며, 이는 그 후 내재화에 따라 항체에 의해 방출된다. 일부 실시양태에서, 링커 절단은 엔도솜 또는 리소좀에서 발생한다. 따라서, 항체의 엔도솜 또는 리소좀으로의 증가되거나 더 신속한 전달은 항체의 효능 또는 효율을 증가시킬 수 있다.
일부 실시양태에서, 메디토프, 링커, 또는 항체는 화학요법, 세포독성 또는 ADC 또는 방사성면역요법 (RIT)에 사용하기 위한 방사성 표지된 제제와 같은 치료제 또는 진단제에 결합된다. 일부 실시양태에서, 본원에 기재된 방법은 제제의 전달을 향상시키거나 항체에 의해 표적화되는 항원을 발현하는 세포 또는 조직에 항체-매개 전달을 위한 다른 방법을 향상시키는데 유용하다. 일부 실시양태에서, 상기 방법은 비내재화 항원, 예를 들어 암배아 항원 (CEA), 종양 관련 당단백질 (TAG-72), KS1/4의 경우에, 항원, 항원에 결합된 항원, 및 항체와 결합된 제제의 클러스터링 및 이에 따라 내재화를 촉진한다는 점에서 유리하다 (문헌 [Schmidt et al., Cancer Immunol Immunother. Dec 2008; 57(12): 1879-1890; Myer et al. Cancer Res 1993;53:3956-3963] 참조).
유사하게, 다양한 제제, 예를 들어 조영제에 결합된 항체를 이용하여, 세포를 클러스터하거나 공동-편재화하고/하거나 표면 항원을 내재화하는 능력은 중요할 수 있다. 예를 들어, 항체-약물 접합체 (ADC)와 같은 약물 접합된 생물학적 제제는 일반적으로 표적화된 조직, 대개 표적화된 조직 또는 표적화된 세포, 예를 들어 종양 세포 내에서 제제, 예를 들어, 활성 약물을 선택적으로 전달하는 목적으로 설계된다. 표적화 생물학적 제제, 예를 들어, 항체는 일반적으로 관심 세포에 우선적으로 결합하도록 설계되고; 표적 세포 또는 조직에만 존재하고/존재하거나 다른 조직에 매우 적은 양 또는 드물게 존재하는 항원에 선택적인 결합이 특히 바람직할 수 있다. 질환 세포, 예를 들어 종양 세포를 직접적으로 표적화 하는 약물 접합 항체의 경우 특히, 제제 결합 항체는 세포 표면상 표적 항원에 결합한 후에 표적 세포 내에서 내재화되는 것이 바람직하거나 중요할 수 있. 예를 들어, 문헌 [Trail et al., Antibodies 2013, 2, 113-129; H.L. Perez, et al., Drug Discov Today (2013)]을 참조한다. 일부의 경우에서, 결과적으로 항원의 내재화를 일으키는 항체는 또한 방사성 면역요법 (RI)의 경우에 바람직하다. 문헌 [Boudousq V et al., PLoS ONE 8(7): e69613 (2013)]을 참조한다. 일반적으로, 접합된 제제, 예를 들어, 약물은 표적 세포 내에서 방출되어 활성을 나타낸다. 일부의 경우, 예를 들어, 특정 세포외 기질 성분 및/또는 종양 환경에 특이적인 항원을 표적화하는데 있어서, 내재화는 필수적이지 않을 수 있다. 문헌 [Ackerman et al., Cancer Immunol Immunother. Jul 2008; 57(7): 1017-1027]을 참조한다.
일부 실시양태에서, 제공된 방법은 종양 세포의 특성을 이용하고 제제를 효율적으로 방출하기 위한 결합된 생물학적 제제의 내재화 및 선별 경로를 변경한다. 일부 실시양태에서, 상기 방법은 항원 및/또는 메디토프-이용가능 항체의 공동-편재화, 클러스터링, 내재화, 및/또는 세포내 교환 또는 선별 및/또는 재현 또는 이의 향상 또는 변경을 달성한다. 본원에서 세포로 투여한 후 비-자가-가교결합 항체에 비해 자가-가교결합 항체의 클러스터링 및/또는 내재화에 차이가 관찰된다.
캐싸일라® (KADCYLA®)로 판매되는 항- Her2 ADC, TDM1의 성공적인 개발에도 불구하고, 접합된 약물의 단지 적은 부분 (~2%)만이 종양에 전달된다. 이 같은 낮은 전달 수율의 정확한 이유는 분명하지 않지만, 아마도 세포에 의해 이용되는 다른 내재화 경로 (예를 들어, 클라트린 매개 엔도시토시스 및/또는 소포 매개 엔도사이토시트 및/또는 대음세포작용 (macropinocytosis))뿐만 아니라 일단 세포 안으로 엔도시토시스된 물질의 경로 (재순환 엔도솜 또는 후기 엔도솜 또는 리소좀)에 기인한다. 다이설파이드 링커를 통해 항체에 결합된 약물은 세포성 세포질의 환원 환경으로 인해 방출될 수 있다. 다르게는, 오리스타틴과 같은 일부 약물 접합체가 엔도솜 비히클에 활성인 특이적 프로테아제에 의해 방출될 수 있다. 상이한 링커를 이용한 다른 연구는 리소좀이 결합 화학과 무관하게 약물을 방출하는데 효과적인 수단이라는 것을 나타낸다. 그러나 다이설파이드는 혈청에서 환원될 수 있고 프로테아제는 건강한 조직에서 활성일 수 있다. 일부 실시양태에서, 제공된 방법, 항체 (자가-가교결합 항체 포함), 및 메디토프는 질환을 치료하기 위한 독소와 같은 제제의 개선 예를 들어 특이적으로 효과적인 전달을 제공한다.
종양 면역요법에서, 많은 항원은 종양 특이적 이라기 보다 종양 세포/환경에서 단지 종양과 관련되거나 높은 수준으로 발현된다. 예를 들어, 예를 들어, Her2 및 EGFR은 종양 조직 예를 들어 Her2+ 유방암 및 직장결장암에서 상당히 과발현되지만, 이들은 건강한 조직에서도 발현되고, 이는 결과적으로 표적에 (on target), 조직 이탈 (off-tissue) 독성을 가져올 수 있다. 기타 유형의 항원 (예를 들어 종양 특이적 항원 및 종양태아성 항원, 예를 들어, 암배아성 항원 (CEA))은 종양 조직에서만 그리고/또는 그렇지 않으면 최소한으로 또는 발생의 특정 단계에서만 발현된다. 동일한 항원 상 고유 에피토프를 인식하는 모노클로날 항체 (mAb)의 조합은 여러 항체 효과기 기능 (예를 들어, ADCC, 보체 의존성 용해, 신호전달 억제)의 향상, 세포 사멸의 향상, 및 암 표적화 항체의 경우, 종양 성장 억제의 향상을 포함한 상승작용 효과를 가져 올 수 있다. 예를 들어, 문헌 [Dechant M et al., "Complement-dependent tumor cell lysis triggered by combinations of epidermal growth factor receptor antibodies," Cancer Res, 2008 Jul 1;68(13):4998-5003; Scheuer W et al., "Strongly enhanced antitumor activity of trastuzumab and pertuzumab combination treatment on HER2-positive human xenograft tumor models," Cancer Res, 2009 Dec 15;69(24):9330-6; Cardarelli PM et al., "Binding to CD20 by anti-B1 antibody or F(ab')(2) is sufficient for induction of apoptosis in B-cell lines," Cancer Immunol Immunother, 2002 Mar;51(1):15-24. Epub 2001 Dec 18]을 참조한다.
일부 측면에서, 자가-가교결합 항체는 이중 특이성 항체 대신에, 예를 들어 메디토프-이용가능 항체와 함께 상승작용을 달성하기 위해 사용된다. 일부 측면에서, 자가-가교결합 항체는 동일한 항원 상 2개의 개별적인 에피토프를 인식하는 이중 특이성 항체의 사용과 비교하여 장점을 제공한다. 예를 들어, 자가-가교결합 항체의 생성은 이중 특이적 항체를 제조하는 것과 비교할 때 보다 효과적이고 비용 효율적일 수 있다. 일부 측면에서, 자가-가교결합 항체는 또한 종양과 같은 질환 부위에 비교적 더 쉽게 표적화된다. 메디토프 결합 부위 (항체 CDR로부터 분리된 메디토프 결합 부위 내에)의 특성, 및 선택된 메디토프-이용가능한 임의의 항체에 대해 본원에서 제공된 광범위하게 적용가능한 방법이 고려되는 경우, 자가-가교결합 항체와 메디토프-이용가능 항체는 또한 치료학적으로 허용가능한 특성을 갖는 이중 특이성 항체를 제조할 필요없이, 그리고 관련된 상당한 이의 개발 비용없이, 광범위한 치료학적 항체에 쉽게 적용가능하다는 장점을 갖는다.
일부 실시양태에서, 상기 화합물 및 방법은 트라스투주맙-퍼투주맙 조합에서 관찰되는 바와 같이 (문헌 [Baselga J, et al. (2012). N Engl J Med 366(2):109-119]), 상승작용적 종양를 유도하는데 유용하다 (문헌 [Kamat, V., et al., Cancer Biol Ther 7, 726-733 (2008); Koefoed K, et al. (2011) MAbs 3(6):584-595; Spangler JB, et al. (2010) Proc Natl Acad Sci USA 107(30):13252-13257]). 일부 실시양태에서, 자가-가교결합 항체는 제2 "mAb"-유사 분자로서 기능하지만, 임의의 양립 가능한 메디토프-이용가능 항체와 짝을 이룰 수 있는 유연성을 갖는다. 일부 측면에서, 이는 제2 치료학적 mAb를 확인 및 개발하는 비용을 감소시킨다. 일부 실시양태에서, 다가 메디토프 변이체 (예를 들어 원자가 및/또는 링커 기하학적 구조를 변경함으로써 제조됨)는 추가로 특이성 및 상승작용 효과를 향상시킨다.
유사하게, 일부 실시양태에서, 2개의 자가-가교결합 메디토프-이용가능 항체, 동일한 세포의 표면상에 발현된 상이한 항원에 특이적으로 결합하는 각 항체는 2가 항체 대신에 사용된다. 일부 실시양태에서, 상기 방법은 세포 표면상의 서로에 대한 2개의 항원의 밀도 또는 존재 비율과 관계없이 향상된 항원 (예를 들어, 수용체), 응집, 및/또는 특정 수준의 응집을 제공한다. 일부 측면에서, 상기 방법은 항원의 세포 표면 클러스터링 및/또는 공동-편재화를 향상시킨다. 일 실시양태에서, 둘 이상의 자가-가교결합 항체는 다수의 상이한 항원을 인식하는 것과 함께 그러한 클러스터링을 달성하기 위해 사용된다. 따라서, 일부 실시양태에서, 항체의 각 암이 이의 각 항원에 결합하는 경우에만 클러스터링이 발생하는 이중 특이성 항체와 비교하여, 그러한 구현예에서 클러스터링은 항체 중 하나에 결합된 항원이 다른 결합된 항원과 비교하여 세포 표면에 훨씬 더 높은 밀도로 존재하는 경우에도 달성될 수 있다. 또한, 일부 실시양태에서, 두 개의 자가-가교결합 항체의 사용은 2개의 세포 표면 항원 사이의 거리가 이중 특이적 항체의 두 개의 암 사이의 거리를 초과하는 경우에도 효능을 향상시킬 수 있다. 그러한 구현예에서, 상기 링커 길이는 전술한 바와 같이, 세포 표면 항원 사이의 실제 또는 예상 거리를 수용하도록 변화될 수 있다.
일부 실시양태에서, 상기 자가-가교결합 항체는 2가 항체를 능가하는 이점 및/또는 개선점을 제공한다. 일부 실시양태에서, 상기 자가-가교결합 항체는, 이중 특이성 항체를 단독으로 사용하는 것에 비해, 예를 들어 두 개의 항원, 예를 들어, 세포 표면 항원의 응집을 향상시키기 위해 이중 특이적 항체의 상이한 암에 의해 결합된, 예를 들어, 친화도, 항체에 의해 유도된 신호절달, 효과기 기능, 및/또는 내재화를 향상시키기 위한 이중 특이성 메디토프-이용가능 항체이다. 따라서, 일부 측면에서, 상기 자가-가교결합 이중 특이성 메디토프-이용가능 항체는 이중 특이성 항체 단독과 비교하여 예를 들어, 클러스터링의 추가적인 수준을 야기함으로써 증가된 수준의 효능을 제공한다.
제공된 항체 및 결합 화합물 (예를 들어, 메디토프)은 실질적인 용도를 가지며, 일부 실시양태에서 이용 가능한 mAb-기반 기술과 관련된 장애를 극복할 수 있다. 일부 실시양태에서, 제공된 화합물과 방법은 예를 들어 항원성을 나타낼 수 있는 새로운 표면을 노출시키는, 비천연 시약으로부터 발생할 수 있는 항원성의 문제를 다루고/다루거나 그러한 분자의 제조에서 안정성 및 확작성과 관련된다 (문헌 [Nelson AL (2010) Antibody fragments: hope and hype. MAbs 2(1):77-83]). 세툭시맙은 임상에서 성공적으로 사용되고 안정하며 규모에 따라 생산된다. 일부 실시양태에서, 메디토프 결합 부위에 정렬한 잔기의 고유한 조합은 서열이 떨어져 있으며 (즉, 펩타이드 T 세포 에피토프가 될 가능성이 없음) 깊은 공동 내에 위치한다 (즉, 표면 노출된 B 세포 에피토프가 될 가능성이 없음). 따라서, 일부 실시양태에서, 메디토프 결합 부위를 함유하는 mAbs는 면역원성이 아니다.
일부 실시양태에서, 상기 메디토프 결합 부위는 이용가능 방법에 의해 효과적인 ADC의 발달에 전형적으로 영향을 미치는 이종성 및 결합 효율의 문제를 회피하는데 유용한 결합의 특정 지점으로 사용된다. 일부 실시양태에서 독소를 포함하는 메디토프는 반응성 화학물질을 Fab 공동으로 전달할 수 있으며, 이는 특이성 및 단위 화학량론을 유리하게 한다.
일부 측면에서, 보통 친화도의 메디토프 (예를 들어, cQFD 및 cQYN 메디토프)는 예를 들어 다가 접근법을 고려할 때와 같이 유리하며 (문헌 [Mammen M, Choi S, & Whitesides G (1998) Polyvalent interactions in biological systems: Implications for design and use of multivalent ligands and inhibitor. Angew. Chem., Int. Ed. Eng 37:2755]), 일부 실시양태에서, 상이한 비천연 아미노산, 고리화 전략, 및/또는 스크리닝 방법을 이용하여 친화도 및/또는 약동학/약력학/독성을 향상시킨다. 본원에서 입증된 바와 같이, 일부 실시양태에서, 메디토프에서 변화를 제공하는 메디토프 결합 부위를 조정하는 것도 마찬가지로 가능하다.
C. 치료학적 및 진단학적 용도와 약학적 조성물
일 실시양태에서, 자가-가교결합 항체는 치료제, 진단제 (예를 들어, 조영제), 또는 질병 또는 질환의 치료, 진단 (예를 들어, 영상화)을 위한 이의 조합을 전달하는데 사용된다. 자가-가교결합 항체-약물 접합체는 치료학적 항체에 의해 표적화될 수 있는 질환 또는 질병에서 세포의 특성 유형 또는 세포 집단에 치료를 유도하기 위한 방법에 사용될 수 있다. 그러한 치료의 방법은 치료학적으로 유효한 양의 약학적 조성물을 임의의 적합한 투여 경로를 통해 상기 질환 및 질병을 가진 개체에게 투여하는 것을 포함할 수 있다. 상기 약학적 조성물은 자가-가교결합 항체 또는 이의 기능적 단편을 포함할 수 있다.
일부 실시양태에서, 제공된 자가-가교결합 항체와 이의 복합체는 치료학적 항체를 이용하여 치료 또는 표적화 될 수 있는 임의의 암, 질환 또는 기타 질병을 포함하는 질환 또는 질병의 치료, 진단 또는 영상화에 사용된다. 암은 면역계를 적극적으로 억제함으로써 면역감시를 회피한다. 이러한 면역억제에 대응하기 위해 고려되는 하나의 방법은 종양 세포에 의해 독특하게 발현되거나 과발현되는 항원의 에피토프를 이용한 백신화를 통한 것이다. 예를 들어, 신호전달 경로를 차단하여 성장인자를 격리시키고/격리시키거나 면역 반응을 유도하는 자가-가교결합 항체가 암 및 기타 질환을 치료하기 위한 임상에서 성공적으로 시행되었다.
따라서, 상기 질환 및 질병은 백혈병 및 림프종 (예를 들어, 알렘투주맙, 베크투모맙, 젬투주맙, 린투주맙, FBTA05, 이브리투모맙 튜세탄, 오파투무맙, 리툭시맙, 토시투모맙의 자가-가교결합 버전을 이용하여 치료 또는 영상화될 수 있음), 유방암 (예를 들어, 트라스투주맙, 아데카투무맙, 에르투막소맙의 자가-가교결합 버전을 이용하여 치료 또는 영상화될 수 있음), 전립선암 (예를 들어, 아데카투무맙, 카프로맙 펜데티드, 에타라시주맙의 자가-가교결합 버전을 이용하여 치료 또는 영상화될 수 있음), 대장암 (예를 들어, 라베투주맙, 파니투무맙, 알투무맙 펜테테이트, 보투무맙의 자가-가교결합 버전을 이용하여 치료 또는 영상화될 수 있음), 위장암 (예를 들어, 아르시투무맙, 카투막소맙의 자가-가교결합 버전을 이용하여 치료 또는 영상화될 수 있음), 난소암 (예를 들어, 아바고보맙, 카투막소맙, 에타라시주맙, 이고보맙, 오레고보맙의 자가-가교결합 버전을 이용하여 치료 또는 영상화될 수 있음), 폐암 (예를 들어, 아나투무맙 마페나톡스의 자가-가교결합 버전을 이용하여 치료 또는 영상화될 수 있음), 췌장암 (예를 들어, 클리바투주맙 테트락세탄의 자가-가교결합 버전을 이용하여 치료 또는 영상화될 수 있음), 신장암 (예를 들어, 지렌툭시맙의 자가-가교결합 버전을 이용하여 치료 또는 영상화될 수 있음), 흑색종암(예를 들어, 에타라시주맙, 이필리무맙, TRBS07의 자가-가교결합 버전을 이용하여 치료 또는 영상화될 수 있음), 신경교종 (예를 들어, 니모투주맙의 자가-가교결합 버전을 이용하여 치료 또는 영상화될 수 있음), 골전이(예를 들어, 데노수맙의 자가-가교결합 버전을 이용하여 치료 또는 영상화될 수 있음), 두경부암 (예를 들어, 자루투무맙의 자가-가교결합 버전을 이용하여 치료 또는 영상화될 수 있음), 심혈관계질환 (예를 들어, 압식시맙의 자가-가교결합 버전을 이용하여 치료 또는 영상화될 수 있음), 자가면역질환 (예를 들어, 아달리무맙, 인플릭시맙의 자가-가교결합 버전을 이용하여 치료 또는 영상화될 수 있음), 류마티스 관절염 (예를 들어, 아틀리주맙, 골리무맙, 인플릭시맙의 자가-가교결합 버전을 이용하여 치료 또는 영상화될 수 있음), 이식거부 (예를 들어, 바실릭시맙, 다클리주맙, 무로모납-CD3의 자가-가교결합 버전을 이용하여 치료 또는 영상화될 수 있음), 크론병 (예를 들어, 세르톨리주맙, 폰톨리주맙, 나탈리주맙, 인플릭시맙, 비실리주맙의 자가-가교결합 버전을 이용하여 치료 또는 영상화될 수 있음), 헤모글로빈 요증 (에쿨리주맙의 자가-가교결합 버전을 이용하여 치료 또는 영상화될 수 있음), 건선 (예를 들어, 에팔리주맙, 인플릭시맙, 우스테키누맙의 자가-가교결합 버전을 이용하여 치료 또는 영상화될 수 있음), 다발성 경화증 (예를 들어, 나탈리주맙, 우스테키누맙의 자가-가교결합 버전을 이용하여 치료 또는 영상화될 수 있음), 천식 (예를 들어, 벤랄리주맙, 메폴리주맙, 오말리주맙의 자가-가교결합 버전을 이용하여 치료 또는 영상화될 수 있음), 호흡기 세포융합 바이러스 (RSV) (예를 들어, 팔리비주맙의 자가-가교결합 버전을 이용하여 치료 또는 영상화될 수 있음), 황반변성 (예를 들어, 라니비주맙의 자가-가교결합 버전을 이용하여 치료 또는 영상화될 수 있음), 맹장염 (예를 들어, 파놀레소맙의 자가-가교결합 버전을 이용하여 치료 또는 영상화될 수 있음), 및 항체로 표적화 또는 치료될 수 있는 기타 다른 임의의 질병을 포함하지만 이에 한정되지 않는, 임의의 암, 치료학적 모노클로날 항체 (mAbs)를 이용하여 표적화되는 것을 포함하는 다른 질환 및 질병을 포함한다. 상기 기재된 항체 및 관련 질환 또는 장애는 단지 예시일 뿐이며, 상기 플랫폼을 제한하지 않는다.
특정 실시양태에서, 상기 메디토프-이용가능 자가-가교결합 항체는 하나 이상의 자유 메디토프, 메디토프 변이체, 다가 메티토프 테더링제 또는 다가 메디토프 변이체 테더링제에 의해 결합될 수 있다. 이러한 메디토프는 하나 이상의 조영제, 치료학적으로 유효한 양의 치료학적으로 유효한 제제 또는 화합물 또는 이 둘 다에 결합될 수 있다. 치료학적으로 유효한 화합물을 갖는 메디토프 또는 이의 변이체에 의해 결합된 메디토프-이용가능 자가-가교결합 항체의 투여는 질환 또는 질병의 치료, 예방, 진단 또는 모니터링을 할 수 있다. 그러한 높은 친화도의 접합체 및/또는 메디토프-이용가능 mAb에 결합된 다가 메디토프는 질환을 치료 및 검출하기 위한 mAb 기반 치료제 및 영상화 방법을 현저하게 개선하는 매우 다기능적인 플랫폼 기술을 제공한다.
일부 실시양태에서, 제공된 방법 및 화합물은 항체 조작, 항체-약물 접합체(ADC), 항체-지시된 효소 전구 약물요법(ADEPT: antibody-directed enzyme produg theraphy), 면역계 관여(예를 들어, Fc 변형 (문헌 [Desjarlais JR & Lazar GA (2011) Modulation of antibody effector function. Exp Cell Res 317(9):1278-1285]), 케모카인 융합, 이중 특이적 T 세포 관여항체(engager) (문헌 [Wolf E, Hofmeister R, Kufer P, Schlereth B, & Baeuerle PA (2005) BiTEs: bispecific antibody constructs with unique anti-tumor activity. Drug Discov Today 10(18):1237-1244]) 및 질환 영상화 (예를 들어, 면역PET 및 예비 표적화 방사성 핵종 영상화 (문헌 [Goldenberg DM, et al. (2012) Pretargeted molecular imaging and radioimmunotherapy. Theranostics 2(5):523-540; Pagel JM, et al. (2006) Comparison of a tetravalent single-chain antibody-streptavidin fusion protien and an antibody-streptavidin chemical conjugate for pretargeted anti-CD20 radioimmunotherapy of B-cell lymphomas. Blood 108(1):328-336])에 유용하다.
일부 측면에서, 제공된 방법 및 화합물은, 예를 들어 치료 및 영상화 적용에 유해한 바람직하지 않은 결과를 초래할 수 있는, 상기 이용가능한 방법, 예를 들어 유전자 서열의 번역 후 화학적 변형 또는 조작을 이용하는 방법에서 관찰되는 문제점을 극복한다. 예를 들어, 이용가능한 방법을 사용하여 질환 부위에 대한 세포독소를 표적화하는 ADC의 경우, 독소의 화학적 결합 (전형적으로 mAb 상의 라이신, 감소된 시스테인, 또는 당을 수반함)이 이종의 혼합물을 생성할 수 있고, 이는 mAb의 특이성 및 안정성에 악영향을 미칠 수 있으며, 이의 생체-분포를 변화시킬 수 있다.
다른 실시양태에서, 종양 또는 다른 조직을 영상화하는 방법이 제공된다. 이러한 방법에서, 조영제로 표지된 자가-가교결합 항체는 임의의 적합한 투여 경로를 통해 투여되고 표적 종양 또는 조직에 결합된 치료용 항체에 결합할 것이다. 조영제의 예로는 방사성 표지 (예를 들어, 3H, 14C, 35S, 90Y, 99mTc, 125I, 131I, 177Lu, 166Ho, 및 153Sm), 금속 또는 자성 표지 (예를 들어, 금, 철, 가돌리늄), 비오틴, 킬레이팅제 (예를 들어, 1,4,7,10-테트라아자사이클로도데칸-N,N',N'',N'''-테트라아세트산 ("DOTA")) 또는 전술한 임의의 제제를 포함하지만 이에 한정되지 않는다. 일 실시양태에서, 본원에 기재된 방법과 함께 사용된 조영제는 DOTA이다.
또 다른 양태로, 종양 침투를 촉진하고 이용가능한 방법을 사용하여 영상화를 향상시키기 위해, mAb의 크기를 Fab 단편 (예를 들어, 단일 사슬 Fab 가변 도메인 (scFvs))으로 감소시키는 것은 원자가를 감소시킬 수 있고 따라서 본래의 mAb에 비해 친화도 및 조직 특이성에 모두 영향을 미칠 수 있다. 다른 경우, 검출을 개선하기 위한 예비-표적화된 영상화 프로토콜의 일부로서, 이용가능한 방법을 사용하여, 스트렙타비딘과 접합된 mAb 또는 스캐폴드를 통해 서로 묶인 (stiched) 다수의 Fab/scFv (예를 들어, "락 앤 도크(lock-and-dock)")는 혈청에서 면역원성을 가지며 불안정하고, 특히 임상의 용도에 필수적인 규모로 생산하기에 기술적으로 어렵고 비용이 많이 들 수 있다. 일부 실시양태에서 제공된 화합물 및 방법은 암 및 기타 질환 및 질병을 위한 대항적인 mAb 플랫폼 및 향상된 mAb-기반 전달 시스템을 제공함으로써 상기 어려움을 극복하는데 유용하다.
D. 자가-가교결합 항체의 효과 조절
또한, 자유 메디토프를 갖는 자가-가교결합 항체의 효과를 변경하는 방법이 제공된다. 일부 실시양태에서, 자유 메디토프는 메디토프 결합 부위에 결합하기 위한 자가-가교결합 항체에 융합된 메디토프와 경쟁할 수 있다. 일반적으로, 상기 방법은 메디토프-이용가능 항체의 메디토프 결합 부위를 자유 메디토프와 접촉하는 것을 포함한다. 상기 메디토프 결합 부위와 자유 메디토프 사이의 결합은 메디토프 결합 부위를 차지할 수 있게 함으로써, 상기 메디토프 결합 부위에 접촉하거나 결합하는 것으로부터 자가-가교결합 항체로부터의 메디토프를 억제, 감소, 또는 방지할 수 있다. 일부 실시양태에서, 상기 자유 메디토프는 링커를 통해 자가-가교결합 항체에 융합된 메디토프를 대체하거나 방해할 수 있다. 메디토프와 메디토프 결합 부위 사이의 결합이 일반적으로 비공유적이기 때문에, 이러한 결합은 일시적이거나 가역적일 수 있다.
일부 실시양태에서, 상기 방법은 자가-가교결합 항체의 효과를 역전시키거나 감소시킨다. 이러한 효과는, 예를 들어, 자가-가교결합 항체가 세포 표면 항원의 분포, 공동-편재화, 또는 내재화를 변경하는 능력을 역전시키거나 감소시키는 것을 포함한다. 이러한 효과는 또한, 예를 들어, 자가-가교결합 항체가 항체 내재화의 속도, 항체 효능을 변화 또는 증가시키거나, 바람직한 치료학적 효과를 달성하는데 필요한 항체 요법의 투여량을 감소시키는 능력을 역전시키거나 감소시키는 것을 포함한다.
예시적인 이점으로, 이러한 방법은 시간에 따른 측정 치료의 조절을 가능하게 할 수 있다. 예를 들어, 일부 실시양태에서, 긴 반감기를 갖는 자가-가교결합 항체가 투여되지만, 상기 항체의 효과는 더 짧은 반감기를 갖는 자유 메디토프의 투여에 의해 조절된다. 일부 실시양태에서, 자유 메디토프의 더 짧은 반감기는 상기 자유 메디토프 수준이 분해 또는 제거로 인해 떨어질 때까지 항체 자가-가교결합의 일시적인 억제를 허용한다. 자유 메디토프 수준이 떨어지는 경우, 펩타이드는 자가-결합을 억제하는데 덜 효과적이며, 자가-가교결합이 재개될 수 있다. 그러한 반감기는 자유 메디토프의 구조와 그것이 사용되는 조건에 따라 수 분, 수 시간, 수 일, 또는 수 주가 될 수 있다.
일 실시양태에서, 자유 메디토프는 자가-가교결합 항체의 투여와 동시에, 직전에, 또는 직후에 투여된다. 일부 실시양태에서, 상기 방법은 자가-가교결합 항체와 자유 메디토프 둘 다를 포함하는 조성물, 또는 상기 자가-가교결합 항체를 포함하는 제1 조성물과 상기 자유 메디토프를 포함하는 제2 조성물을 이용하는 것을 포함한다. 일부 실시양태에서, 상기 자유 메디토프는 자가-가교결합을 감소 또는 방지하고, 따라서 항체가 이의 동종 항원에 결합하기 전에 응집한다. 일부 실시양태에서, 이는 혈액에서 발생하는 자가-가교결합의 양을 감소시킬 수 있어, 모세혈관에 침착될 수 있는 자가-가교결합 항체의 양을 감소시킬 수 있다. 일부 실시양태에서, 자가-가교결합 및 응집을 감소시키는 것은 신장 또는 간에 의해 제거된 항체의 양을 감소시킨다. 따라서, 예를 들어, 자가-가교결합 항체보다 더 짧은 반감기를 갖는 자유-메디토프 펩타이드를 포함하는 자유 메디토프를 갖는 자가-가교결합 항체의 투여는 자가-가교결합을 일시적으로 감소 또는 지연시킬 수 있다. 이러한 감소 또는 지연은 자가-가교결합 항체가 다른 항체와 자가-가교결합하기 전에 이의 동족 항원에 결합하도록 함으로써, 항체 표적으로서 의도되지 않은 혈관, 조직 또는 기관에서 자가-가교결합 또는 응집을 감소시킨다.
또 다른 하나의 예시적인 방법에서, 자유 메디토프는 자가-가교결합 항체를 이미 투여받은 개체에게 자가-가교결합 항체의 효과를 역전, 감소, 또는 변경시키기 위해 투여될 수 있다.
이러한 방법은 자가-가교결합 항체에 의해 야기되는 치료학적 효과 또는 부작용을 감소시키는데 유용할 수 있다. 일부 실시양태에서, 이는 자가-가교결합을 일시적으로 제어하는데 유용할 수 있다. 전술한 바와 같이, 자가-가교결합 항체는 세포의 표면 상에서 항원의 분포를 변화시키거나 또는 항체 또는 항원 내재화의 속도를 증가시키는데 사용될 수 있다. 일부 실시양태에서, 이는 자가-가교결합을 감소 또는 억제함으로써 이들 효과를 제어 또는 감소시키는데 유리할 수 있다. 이러한 방법은 자유 메디토프의 투여를 포함할 수 있다.
일부 실시양태에서, 상기 자유 메디토프는 긴 반감기를 가짐으로써, 자가-가교결합을 영구적으로 또는 반-영구적으로 변화시킨다. 일부 실시양태에서, 자가-가교결합 항체의 반감기보다 짧은 반감기를 갖는 자유 메디토프가 투여된다. 일부 실시양태에서, 짧은 반감기를 갖는 자유 메디토프의 투여는 자가-가교결합의 일시적인 감소 또는 억제를 야기한다. 일부 실시양태에서, 개체는 다수의 자유 메디토프 투여를 받는다. 이러한 투여는 상기 자유 메디토프의 억제 또는 감소 효과를 연장하거나 확장하기 위한 "부스터 용량 (booster dose)"으로 전달될 수 있다. 대안적으로, 그러한 투여는 장시간에 걸쳐 전달될 수 있고, 그렇게 함으로써 항체의 자가-가교결합이 시간이 지남에 따라 억제 및 복원되도록 하게 한다. 그러한 실시양태에서, 높은 수준의 자유 메디토프는 자가-가교결합을 억제할 수 있다. 자유 메디토프가 제거 또는 분해됨에 따라, 자가-가교결합 항체의 메디토프 결합 부위를 덜 자치할 수 있게 되고, 그렇게 함으로써 항체 자가-가교결합이 복원된다. 추가적인 자유-메디토프 펩타이드의 후속 투여는 항체 자가-가교결합을 다시 한번 감소 또는 억제시킬 수 있다.
자가-가교결합의 억제 또는 감소 정도는 일부 실시양태에서 자유 메디토프를 보다 많은 용량 또는 보다 적은 용량으로 투여함으로써 조절된다. 일부 실시양태에서, 자유 메디토프의 보다 많은 용량의 투여는 보다 적은 용량보다 더 큰 억제 효과를 나타낼 것이다. 이러한 투여량은, 예를 들어, 자가-가교결합 항체에 대한 자유 메디토프의 비율로서, 바람직한 시간 동안 치료학적 효과를 생성하기 위해 필요한 양으로서, 상대적 또는 절대적 IC50으로서, 또는 중량 또는 부피에 의해 계산되는 양으로서 계산될 수 있다.
일부 실시양태에서, 자가-가교결합의 억제 또는 감소의 정도는 메디토프 결합 부위에 특이적인 친화도를 갖는 자유 메디토프를 투여함으로써 조절될 수 있다. 예를 들어, 일부 실시양태에서, 높은 친화도를 갖는 자유 메디토프는 낮은 친화도를 갖는 자유 메디토프보다 자가-가교결합을 억제 또는 감소시키는데 더 높고, 더 강력하고, 더 긴 효과를 나타낸다. 일부 실시양태에서, 높은 친화도를 갖는 자유 메디토프는 낮은 친화도를 갖는 자유 메디토프보다 더 강하게 메디토프 결합 부위에 결합하거나 또는 더 긴 제거 속도(off-rate)를 갖는다. 일부 실시양태에서, 항체 자가-가교결합은 동일한 효과를 달성하는데 필요한 낮은 친화도를 갖는 자유 메디토프의 양에 비해 높은 친화도를 갖는 자유 메디토프의 더 적은 양으로 감소 또는 억제될 수 있다.
일부 실시양태에서, 낮은 친화도를 갖는 자유 메디토프는 자가-가교결합에 더 적당하거나 일시적인 효과를 나타내는데 사용될 수 있다. 일부 실시양태에서, 그러한 메디토프는 특정 항체 요법의 효능을 조정하는데 사용될 수 있다.
일부 실시양태에서, 상기 자유 메디토프는, 예를 들어, 선택적으로 2, 3, 4, 5, 6, 7, 8, 9, 10 또는 그 이상의 회수를 포함하는 복수의 회수로 투여된다. 일부 실시양태에서, 상기 투여는 수분, 수시간, 수일, 수개월, 또는 수년의 기간 동안 일어난다. 일부 실시양태에서, 다수의 자유 메디토프가 투여되며, 상기 다수는 동일하거나 상이한 자유 메디토프를 포함할 수 있다. 예를 들어, 일부 실시양태에서, 제1 자유 메디토프는 메디토프 결합 부위에 대해 제1 친화도를 포함할 수 있고, 제2 자유 메디토프는 상기 메디토프 결합 부위에 대해 제2 친화도를 포함할 수 있다. 상기 제1 및 제2 자유 메디토프는 반감기 또는 IC50이 상이할 수 있다. 제1 및/또는 제2 자유 메디토프를 투여하는 것은 메디토프 자가-가교결합을 변경하기 위한 추가의 메커니즘을 가능하게 할 수 있다.
Ⅳ. 투여 방법
상기 제형은 항체로 치료되는 것이 요구되는 포유동물, 바람직하게는 인간에게, 정맥내 투여 (예를 들어, 환약 또는 일정 시간에 걸친 연속 투입), 근육내, 복강내, 뇌척수내, 피하, 관절내, 활막내, 척추 강내, 경구, 국소, 또는 흡입 경로와 같이 공지된 방법에 따라 투여된다. 일 실시양태에서, 상기 제형은 포유동물에게 정맥내 투여로 투여된다. 이를 위해, 상기 제형은 예를 들어, 주사기를 이용하여 또는 IV 라인을 통해 주입될 수 있다. 일 실시양태에서, 상기 제형은 포유동물에게 피하 투여에 의해 투여된다.
항체의 적절한 투여량 ("치료학적으로 유효한 양")은, 예를 들어, 치료되는 질병, 질병의 심각도 및 경과, 항체가 예방 또는 치료 목적으로 투여되는지의 여부, 이전의 치료, 환자의 병력 및 항체에 대한 반응, 사용된 항체의 종류, 및 주치의의 재량에 따라 달라질 수 있다. 항체는 한번에 또는 일련의 치료 동안 환자에게 적합하게 투여되고 진단 이후부터 계속 임의의 시간에 환자에게 투여될 수 있다. 항체는 단독의 치료로서 또는 문제의 질병을 치료하는데 유용한 다른 약물 또는 치료법과 함께 투여될 수 있다.
일반적인 제안으로, 인간에게 투여되는 항체의 치료학적으로 유효한 양은 하나 또는 그 이상의 투여에 관계없이 환자의 체중 kg 당 약 0.01 내지 약 50 mg/kg의 범위 내일 수 있다. 일부 실시양태에서, 사용되는 항체는 예를 들어 약 0.01 내지 약 45 mg/kg, 약 0.01 내지 약 40 mg/kg, 약 0.01 내지 약 35 mg/kg, 약 0.01 내지 약 30 mg/kg, 약 0.01 내지 약 25 mg/kg, 약 0.01 내지 약 20 mg/kg, 약 0.01 내지 약 15 mg/kg, 약 0.01 내지 약 10 mg/kg, 약 0.01 내지 약 5 mg/kg, 또는 약 0.01 내지 약 1 mg/kg으로 매일 투여된다. 일부 실시양태에서, 항체는 15 mg/kg으로 투여된다. 그러나, 다른 용량 요법이 유용할 수 있다. 일 실시양태에서, 본원에 기재된 자가-가교결합 항체는 21일 주기 중 1일에 약 100 mg, 약 200 mg, 약 300 mg, 약 400 mg, 약 500 mg, 약 600 mg, 약 700 mg, 약 800 mg, 약 900 mg, 약 1000 mg, 약 1100 mg, 약 1200 mg, 약 1300 mg 또는 약 1400 mg의 투여량으로 인간에게 투여된다. 상기 투여량은 주입과 같이 단일 투여 또는 다중 투여 (예를 들어, 2 또는 3회 투여)로 투여될 수 있다. 치료와 함께 투여되는 항체의 용량은 단일 치료와 비교하여 감소될 수 있다. 이러한 치료법의 과정은 통상적인 기술로 용이하게 모니터링될 수 있다.
일부 실시양태에서, 질환 또는 장애는 암이다. 일부 실시양태에서, 상기 암은 국소적으로 진행되거나 전이성이다. 일부 실시양태에서, 상기 암은 고형 종양, 혈액암, 방광암, 뇌암, 유방암, 대장암, 결장암, 위암, 신경교종, 두부암, 백혈병, 간암, 폐암 (예를 들어, 비-소세포 폐암), 림프종, 골수종, 경부암, 난소암, 흑색종, 췌장암, 신장암, 타액암 (salivary cancer), 위암, 흉선 상피암, 갑상선암 및 두경부의 평편상피세포 암종으로 이루어진 군으로부터 선택된 것이다.
일부 실시양태에서, 질병 또는 장애는 감염이다. 일부 실시양태에서, 상기 감염은 지속적인 감염이다. 일부 실시양태에서, 상기 감염은 바이러스 감염, 박테리아 감염, 진균 감염, 기생충 감염 또는 원충 감염이다. 일부 실시양태에서, 상기 바이러스 감염은 사이토메갈로바이러스 엡스타인-바 바이러스, B형 간염, C형 간염 바이러스, 헤르페스 바이러스, 홍역 바이러스, 인플루엔자, 인간 면역결핍 바이러스, 인간 T 림프친화 바이러스, 림프구성 맥락수막염 바이러스, 호흡기 세포융합 바이러스, 및/또는 리노바이러스로 이루어진 군으로부터 선택된 것이다. 일부 실시양태에서, 상기 박테리아 감염은 헬리코박터 종 (Helicobacter spp.), 마이코박테리움 종 (Mycobacterium spp.), 포르피로모나스 종 (Porphyromonas spp.), 클라미디아 종 (Chlamydia spp.), 살모넬라 종 (Salmonella spp.), 리스테리아 종 (Listeria spp.), 스트렙토코커스 종 (Streptococcus spp.), 헤모필루스 종 (Haemophilus spp.), 나이세리아 종 (Neisseria spp.), 클렙시엘라 종 (Klebsiella spp.), 보렐리아 종 (Borrelia spp.), 박테로이데스 종 (Bacterioides spp.), 및 트레포네마 종 (Treponema spp.)으로 이루어진 군으로부터 선택된 것이다. 일부 실시양태에서, 상기 원충 감염은 리슈마니아 종 (Leishmania spp.), 열대말라리아 원충 (Plasmodium falciparum), 주혈흡충 종(Schistosoma spp.), 톡소플라스마 종 (Toxoplasma spp.), 트리파노소마 종 (Trypanosoma spp.), 및 테니아 종 (Taenia spp.)으로 이루어진 군으로부터 선택된 것이다. 일부 실시양태에서, 상기 진균 감염은 블라스토마이코시스, 콕시디오이데스증 (coccidioiodmycosis), 히스토플라즈마증, 칸디다증, 크립토콕쿠스증, 아스페르길루스증, 털곰팡이증 및 뉴모시스티스증으로 이루어진 군으로부터 선택된 것이다.
일부 실시양태에서, 상기 질환 또는 장애는 염증성 질환이다. 일부 실시양태에서, 상기 염증성 질환은 급성 파종성 뇌척수염, 에디슨병, 알츠하이머병, 강직성 척추염, 항인지질 항체 증후군, 죽상동맥경화증, 자가면역성 용혈성 빈혈, 자가면역성 간염, 관절염, 베체트병, 버거씨병, 수포성 유사천포창, 셀리악병, 샤가스병, 담관염, 크론병, 피부근염, 제1 형 당뇨병, 사구체신염, 굿파스쳐증후군, 이식편대숙주병, 그레이브스병, 귈랑-바레 증후군, 하시모토병, 두드러기, 고 IgE 증후군, 특발성 혈소판 감소성 자반증, 홍반성 루푸스, 루푸스 콩팥염, 다발성 경화증, 중증 근무력증, 기관 이식 거부 (organ transplant rejection), 파킨슨병, 천포창, 악성 빈혈, 다발성 근염, 원발성 담즙성 경변증, 건선, 레이노 증후군, 류마티스 관절염, 피부경화증, 쇼그렌 증후군, 측두동맥염, 갑상선염, 궤양성 대장염, 포도막염, 혈관염, 및 베게너 육아종증으로 이루어진 군으로부터 선택된 것이다.
일부 실시양태에서, 상기 항체를 함유하는 제형은 또 다른 치료학적 제제와 함께 개체 또는 개인에게 질환 또는 장애를 치료하기 위해 투여될 수 있다. 예를 들어, 암을 치료하기 위해, 본원에 기재된 자가-가교결합 항체 제형이 다른 하나의 항암 치료 (예를 들어, 화학요법 또는 상이한 항체 치료)와 함께 투여될 수 있다.
Ⅴ. 제조 물품 또는 키트
본원에 기재된 실시양태 중 임의의 수용성 약학적 제형을 보유하는 용기를 포함하는 제조 물품 또는 키트가 본원에서 또한 제공되고 이의 사용을 위한 설명서를 선택적으로 제공한다. 적합한 용기는, 예를 들어, 병, 바이알, 백(bag) 및 주사기를 포함한다. 상기 용기는 유리, 플라스틱 (예를 들어, 폴리비닐 클로라이드 또는 폴리올레핀), 또는 금속 합금 (예를 들어, 스테인리스 스틸 또는 하스텔로이)과 같은 다양한 물질로부터 형성될 수 있다. 예시적인 용기는 300 cc 금속 합금 용기 (예를 들어, -20℃에서 저장하기 위한)이다. 다른 하나의 예시적인 용기는 10-50 cc 유리 바이알 (예를 들어, 2-8℃에서 저장하기 위한)일 수 있다. 예를 들어, 상기 용기는 10 cc, 15 cc, 20 cc, 또는 50 cc 유리 바이알일 수 있다. 상기 용기는 제형을 보유하며, 용기 상에, 또는 용기와 결합된 라벨은 사용을 위한 지시를 나타낼 수 있다. 상기 제조 물품은 다른 버퍼, 희석제, 필터, 바늘, 주사기, 및 사용을 위한 지시사항이 있는 포장 삽입물을 포함하여, 상업적 및 사용자 입장에서 바람직한 다른 물질을 추가로 포함할 수 있다. 일부 실시양태에서, 상기 제조 물품은 하나 이상의 다른 제제 (예를 들어, 화학요법제, 및 항-신생물제)를 추가로 포함한다. 하나 이상의 제제를 위한 적합한 용기는, 예를 들어, 병, 바이알, 백 및 주사기를 포함한다.
실시양태 및 실례가 되는 예와 관련하여 본 발명을 설명하였지만, 당업자는 명세서에 개시된 본 발명의 취지 및 범위를 벗어나지 않는, 기재되고 설명된 본 발명의 변형을 인식할 수 있다. 실시예는 본 발명을 이해를 돕고자 개시하며 어떤 방법으로든 그 범위를 제한하고자 한 것이 아니며 그렇게 해석되어서는 안 된다. 실시예는 통상적인 방법에 대해 상세한 설명을 포함하지 않는다. 이러한 방법은 당 업자에게 잘 알려져 있으며 여러 출판물에도 기재되어 있다. 게다가, 상기 및 하기 실시예에서 인용된 모든 참고문헌은 본원에서 완전히 개시된 것과 마찬가지로 그 전문이 참고로 포함된다.
다음의 문서는 모든 목적을 위해 그 전문이 참고로 포함된다: 2012년 2월 10일에 출원된 미국 출원 제61/597,708호; 2011년 10월 10일에 출원된 미국 출원 제13/270,207호, 현재 미국 특허 제8,658,774호; 2011년 10월 10일에 출원된 국제 출원 PCT/US2011/055656호; 2012년 4월 10일에 출원된 국제 출원 PCT/US12/32938; 2012년 4월 10일에 출원된 미국 출원 제13/443,804호, 현재 미국 특허 제8,962,804호; 2012년 2월 10일에 출원된 미국 출원 61/749,830호, 및 2013년 2월 11일에 출원된 13/764,762호.
Ⅵ. 정의
본원에 사용된 "항체"는 항원 또는 에피토프에 특이적으로 결합하거나, 또는 면역학적으로 반응하는 면역글로불린 분자를 의미하며, 단편 항원 결합 (Fab) 단편, F(ab')2 단편, Fab' 단편, Fv 단편, 재조합 IgG (rIgG) 단편, 단일 사슬 가변 단편 (scFv) 및 단일 도메인 항체 (예를 들어, sdAb, sdFv, 나노바디) 단편을 포함하지만, 이로 한정되는 것은 아닌 기능적 항체 단편뿐만 아니라 폴리클로날 및 모노클로날 항체 모두를 포함한다. 상기 용어 "항체"는 인트라바디, 펩티바디, 키메릭 항체, 완전 인간 항체, 인간화 항체, 메디토프-이용가능한 항체 및 이종결합 (heteroconjugate) 항체 (예를 들어, 이중 특이성 항체, 디아바디, 트리아바디, 테트라바디, 탠덤 디-scFv, 탠덤 트리-scFv)와 같은 면역글로불린의 유전자 조작된 형태, 또는 다른 방법으로 변형된 형태를 포함한다. 다르게 설명되지 않는 한, 상기 용어 "항체"는 그의 기능적 항체 단편을 포함하는 것으로 이해되어야 한다.
용어 "상보성 결정 영역 (complementarity determining region)", 및 "CDR"은 항원 특이성 및 결합 친화도를 부여하는 항체 가변 영역 내 아미노산의 비-인접 서열을 지칭하는 것으로 당해 기술분야에 공지되어 있다. 일반적으로, 각 중쇄 가변 영역에 3 종의 CDR (CDR-H1, CDR-H2, CDR-H3)이 있고 각 경쇄 가변 영역에 3 종의 CDR (CDR-L1, CDR-L2, CDR-L3)이 있다. "프레임워크 영역" 및 "FR"은 당해 기술분야에 중쇄 및 경쇄의 가변 영역의 비-CDR 부분을 지칭하는 것으로 공지되어 있다. 일반적으로, 각 중쇄 가변 영영에 4종의 FR (FR-H1, FR-H2, FR-H3, and FR-H4)이 있고, 각 경쇄 가변 영역에 4 종의 FR (FR-L1, FR-L2, FR-L3, and FR-L4)이 있다.
주어진 CDR 또는 FR의 정확한 아미노산 서열 경계는 하기 문헌에 의해 기재된 것을 포함하여, 잘 알려져 있는 다수의 체계 중 하나를 사용하여 쉽게 결정될 수 있다 (Kabat et al. (1991), "Sequences of Protein of Immunological Interest," 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD ("카밧" 넘버링 체계), Al-Lazikani et al., (1997) JMB 273,927-948 ("코티아(Chothia)" 넘버링 체계), MacCallum et al., J. Mol. Biol. 262:732-745 (1996), "Antibody-antigen interations: Contact Analysis and binding site topography," J. Mol. Biol. 262, 732-745." ("콘택트(Contact)" 넘버링 체계), Lefranc MP et al., "IMGT unique numbering for immunoglobuline and T cell receptor variable domains and Ig superfamily V-like domains," Dev Comp Immunol, 2003 Jan;27(1):55-77 ("IMGT" 넘버링 체계), and Honegger A and Pluckthun A, "Yet another numbering scheme for immunoglobuline variable domains: an automatic modeling and analysis tool," J Mol Biol, 2001 Jun 8;309(3):657-70, (AHo 넘버링 체계)).
주어진 CDR 또는 FR의 경계는 확인에 사용되는 체계에 따라 변할 수 있다. 예를 들어, 카밧 체계는 구조적 정렬을 기본으로 하는 반면, 코티아 체계는 구조적 정보를 기본으로 한다. 카밧 및 코티아 체계 두 가지 넘버링은 가장 통상적인 항체 영역 서열 길이를 기본으로 하며, 일부 항체에서 나타나는 삽입 문자, 예를 들어, "30a"로 제공되는 삽입과 삭제 부분을 갖는다. 상기 두 체계는 상이한 위치에 특정 삽입과 결실("삽입 결실(indel)")을 배치하기 때문에 결과적으로 넘버링이 차이난다. 콘택트 체계는 복합 결정 구조의 분석을 기본으로 하며 코티아 넘버링 체계와 많은 면에서 유사하다.
하기 [표 4]는 각각, 카밧, 코티아 및 콘택드 체계에 의해 확인되는 CDR-L1, CDR-L2, CDR-L3 및 CDR-H1, CDR-H2, CDR-H3의 위치를 열거한다. CDR-H1 경우, 잔기 넘버링은 카밧 및 코티아 넘버링 체계 둘 다를 사용하여 열거된다. 카밧 넘버링 체계는 H35A와 H35B에 삽입을 배치하기 때문에, 카밧 넘버링 규정을 사용하여 넘버링될 때 코티아 CDR-H1 루프의 말단이 루프의 길이에 따라서 H32와 H34 사이에서 변한다는 것에 주의한다.
[표 4]
따라서, 달리 명시되지 않는다면, 주어진 항체 또는 이의 영역, 예를 들어 이의 가변 영역의 "CDR" 또는 "상보성 결정 영역", 또는 각각의 명시된 CDR(예를 들어, "CDR-H1, CDR-H2)은 공지된 임의의 체계에 의해 정의된 하나의(또는 특정) 상보성 결정 영역을 포함하는 것으로 이해되어야 한다. 마찬가지로, 달리 명시되지 않는다면, 주어진 항체 또는 이의 영역, 예를 들어 이의 가변 영역의 "FR" 또는 "골격 영역", 또는 각각의 명시된 FR(예를 들어, "FR-H1, FR-H2)은 공지된 임의의 체계에 의해 정의된 하나의(또는 특정) 골격 영역을 포함하는 것으로 이해되어야 한다. 일부 경우에, 카밧, 코티아, 또는 콘택트 방법에 의해 정의된 CDR과 같이, 특정의 CDR, FR, 또는 FR들 또는 CDR들의 확인을 위한 체계가 명시된다. 다른 경우에, CDR 또는 FR의 특정의 아미노산 서열이 주어진다.
용어 "메디토프-이용가능(meditope-enabled)" 항체 및 "메디토프 이용가능 항체 (meditope enabled antibody)" 및 "메디토프 이용가능 항체"는 메디토프 결합 부위를 통해 메디토프에 결합할 수 있는 항체 또는 이의 기능적 단편을 의미한다. 메디토프-이용가능 항체의 예는 세툭시맙 및 본원에 기재된 다른 항체를 포함하지만, 이에 제한되는 것은 아니다. "메디토프 결합 부위"는 결합된 메디토프와 상호작용하는 아미노산 잔기를 함유하는 메디토프 이용 가능 항체의 영역으로, 이들 잔기는 중쇄 및 경쇄의 골격 영역(FR) 잔기를 포함한다. 항체의 Fab 단편 또는 Fab 부분과 관련하여, 메디토프 결합 부위는 Fab 단편 또는 일부의 중심 공동 내에 위치한다.
Fab의 3차원 구조에 대한 "중심 공동"은 중쇄 및 경쇄 가변과 불변 영역의 부분에 의해 줄지어 있는, Fab의 내부 공동을 의미한다. 따라서 상기 중심 공동은 VH, VL, CH1, 및 CL 영역의 잔기에 의해 정렬되지만 항원 결합 부위를 포함하지 않는다.
일부 실시양태에서, 상기 메디토프 결합 부위는 Kabat 넘버링에 따라 메디토프-이용가능한 항체의 경쇄의 잔기 40, 41, 83, 및 85를 포함하고/포함하거나 kabat 넘버링에 따라 상기 메디토프-이용가능한 항체의 중쇄의 잔기 39, 89, 105, 및 108을 포함한다.
일부 실시양태에서, 상기 메디토프 결합 부위는 Kabat 넘버링에 따른, 항체의 경쇄의 잔기 8, 9, 10, 38, 39, 40, 41 42, 43, 44, 45, 82, 83, 84, 85, 86, 87, 99, 100, 101, 102, 103, 104, 105, 142, 162, 163, 164, 165, 166, 167, 168, 및 173, 그리고 항체의 중쇄의 잔기6, 9, 38, 39, 40, 41, 42, 43, 44, 45, 84, 86, 87, 88, 89, 90, 91, 103, 104, 105, 106, 107, 108, 111, 110, 147, 150, 151, 152, 173, 174, 175, 176, 177, 185, 186, 및 187에 의해 형성된 공동 내 위치한다.
메디토프-이용가능 항체의 Fab 부분에 대해, 상기 메디토프 결합 부위는 중심 공동 내 잔기를 포함한다. 상기 메디토프 결합 부위는 전형적으로 불변 영역 잔기를 추가로 포함한다.
본원에 사용된 "치료학적 제제"는 질환 또는 질병의 치료에 유용한 원자, 분자, 또는 화합물이다.
"치료학적으로 유효한 양", "치료학적으로 유효한 농도" 또는 "치료학적으로 유효한 투여량"은 표적 질병을 예방 또는 치료하거나, 상기 질병과 관련된 증상을 완화시키거나, 바람직한 생리학적 효과를 생성시키거나, 또는 질환 또는 질병의 치료를 유도하는 상태의 영상화 또는 진단을 가능하게 하는 것과 같이, 개체에서 바람직한 치료학적 효과를 생성하는 화합물의 양이다. 정확한 치료학적 유효량은 주어진 개체에서 치료의 효능 측면에서 가장 효과적인 결과를 야기하게 되는 조성물의 양이다. 이러한 양은 치료학적 화합물의 특성 (활성, 약동학, 약력학, 및 생체이용률을 포함함), 개체의 생리학적 상태 (나이, 성별, 질환 유형과 단계, 일반적인 물리적 상태, 주어진 투여량에 대한 반응성, 및 약물의 유형을 포함함), 제형 내에서 약학적으로 허용가능한 담체 또는 담체들의 특성, 및 투여 경로를 포함하지만, 이로 한정되지 않는 다양한 요인에 따라 달라진다.
임상 및 약리학 분야의 숙련된 기술자는 통상적인 실험을 통해, 즉 화합물 투여에 대한 개체의 반응을 모니터링하고 이에 따라 투여량을 조절함으로써 치료학적으로 유효한 양을 결정할 수 있을 것이다. 예를 들어, 일부 실시양태에서, 항체의 치료학적으로 유효한 양은 약 1 내지 약 1000 mg/m², 또는 다르게는 1 내지 약 1000 mg/m², 1 내지 약 1000 mg/m², 1 내지 약 1000 mg/m², 10 내지 약 900 mg/m², 20 내지 약 800 mg/m², 30 내지 약 700 mg/m², 40 내지 약 600 mg/m², 50 내지 약 500 mg/m², 100 내지 약 400 mg/m², 1 내지 약 500 mg/m², 10 내지 약 400 mg/m², 50 내지 약 300 mg/m², 100 내지 약 1000 mg/m², 150 내지 약 900 mg/m², 200 내지 약 800 mg/m², 250 내지 약 700 mg/m²이다. 추가 안내는 문헌 [Remington: The Science and Practice of Pharmacy 21st Edition, Univ. of Sciences in Philadelphia (USIP), Lippincott Williams & Wilkins, Philadelphia, PA, 2005]를 참고한다.
"약학적으로 허용가능한 담체"는 관심있는 화합물을 하나의 조직, 기관 또는 신체의 일부에서 다른 조직, 기관, 또는 신체의 일부로 운반 또는 전송하는 것과 관련된 약학적으로 허용가능한 물질, 조성물, 또는 비히클을 의미한다. 예를 들어, 상기 담체는 액체 또는 고체 충진제, 희석제, 부형제, 용매, 또는 캡슐화 물질, 또는 이들의 일부 조합일 수 있다. 담체의 각 성분은 제형의 다른 성분과 양립가능한 것이어야 한다는 점에서 "약학적으로 허용가능한" 것이어야 한다. 또한, 마주칠 수 있는 임의의 조직, 기관 또는 신체의 일부와 접촉하는데 적합해야하고, 이는 독성, 자극, 알러지 반응, 면역원성, 또는 치료학적 이점을 능가하는 임의의 다른 합병증의 위험이 따르지 않아야함을 의미한다.
"투여 경로"는 당해 기술분야에 공지된 임의의 투여 경로를 의미할 수 있고, 에어로졸, 장, 코, 안구, 경구, 비경구, 직장, 경피, 또는 질을 포함하지만 이로 한정되는 것은 아니다. "경피" 투여는 국소 크림 또는 연고를 사용하거나 경피 패치를 사용하여 이루어질 수 있다. "비경구적"은 일반적으로 주입과 관련된 투여 경로를 의미하며, 안와하 (infraorbital), 주입 (infusion), 동맥내, 피막내, 심장내, 피내, 근육내, 복강내, 폐내, 척수내, 흉골내 (intrasternal), 척추강내, 자궁내, 정맥내, 지주막하, 피막하, 피하, 점막경유, 또는 기관경유를 포함한다.
본원에서 다수의 제제, 치료제 또는 치료와 관련하여 사용되는 "조합된" 또는 "와 조합된"은 동일한 질환 또는 병태를 치료하는 과정에서 두 가지 이상의 제제, 약물, 치료 요법, 치료 양식 또는 이들의 조합(예를 들어, 메디토프와 조합된 항체 또는 메디토프)을 임의의 순서로 피험체에게 투여하는 것을 의미한다. 이는 동시 투여(또는 "공동투여"), 제2 제제의 투여 전 또는 후뿐만 아니라 며칠까지 떨어진 일시적으로 간격이 있는 순서의, 제1 제제의 투여를 포함한다. 이러한 병용 치료는 또한 임의의 하나 이상의 제제, 약물, 치료 요법 또는 치료 양식의 단일 투여 이상을 포함할 수 있다. 또한, 두 가지 이상의 제제, 약물, 치료 요법, 치료 양식 또는 이들의 조합의 투여는 동일하거나 상이한 투여 경로에 의할 수 있다.
"치료학적 항체"는 암, 자가면역질환, 이식 거부, 심혈관 질환 또는 본원에 기재된 것과 같은 다른 질환 또는 질병을 치료하는데 사용되는 임의의 항체 또는 이의 기능적 단편을 의미할 수 있다. 본원에 기재된 실시양태에 따라 사용될 수 있는 치료학적 항체의 예는 뮤린 항체, 뮤린화 또는 인간화 키메라 항체, 또는 에르비툭스 (세툭시맙), 리오프로 (압식시맙), 시뮬렉트 (바실릭시맙), 레미케이드 (인플릭시맙); 오르쏘클론 OKT3 (무로모납-CD3); 리툭산 (리툭시맙), 벡사 (토시투모맙), 휴미라 (아달리무맙), 캄파스 (알렘투주맙), 시뮬렉트 (바실릭시맙), 아바스틴 (베바시주맙), 심지아 (세르톨리주맙 페골), 제나팍스 (다클리주맙), 솔리리스 (에쿨리주맙), 랩티바 (에팔리주맙), 마이로타그 (젬투주맙), 린투주맙, 제발린 (이브리투모맙 튜세탄), 타이사브리 (나탈리주맙), 졸레어 (오말리주맙), 시나지스 (팔리비주맙), 벡티빅스 (파니투무맙), 루센티스 (라니비주맙), 및 허셉틴 (트라스투주맙)을 포함하지만, 이에 한정되지 않는 인간 항체를 포함하지만, 이에 한정되지 않는다.
질병을 "치료하는" 또는 질병의 "치료"는 질병의 예방, 병태의 발병 또는 발전의 속도의 지연, 질병의 발생 위험의 감소, 질병 관련 증상 발생의 예방 또는 지연, 질병 관련 증상의 감소 또는 종료, 질병의 완전 또는 부분 퇴행, 또는 이들의 일부 조합을 언급할 수 있다.
본원에 사용된 용어 "포괄하는 (including)", "함유하는 (containing), 및 "포함하는 (comprising)"은 이들의 개방적이고, 비제한적인 의미로 사용된다.
본원에 사용된 단수 형태 "a", "an", 및 "the"는 문맥상 명확하게 다르게 지시하지 않는한 복수의 대상을 포함한다.
보다 간결한 설명을 제공하기 위해, 본원에 제시된 일부 정량적인 표현은 "약"이라는 용어로 자격이 부여되지 않는다. 용어 "약"이 명시적으로 사용되는지의 여부에 관계없이, 본원에 주어진 모든 수량은 실제 주어진 값을 의미하는 것으로 이해되며, 또한 실험 및/또는 측정 조건으로 인해 주어진 값에 대한 등가물 및 근사값을 포함하는 당해 기술분야의 통상적 지식을 바탕으로 합리적으로 유추될 수 있는 그러한 주어진 값에 대한 근사값을 의미하기도 한다.
본원에서 사용된 "알킬"은 1 내지 12개의 탄소 원자를 갖는 포화된, 직쇄 또는 분지쇄 탄화수소기를 의미한다. 대표적인 알킬기는 메틸, 에틸, n-프로필, 이소프로필, 2-메틸-1프로필, 2-메틸-2-프로필, 2-메틸-1-부틸, 3-메틸-1-부틸, 2-메틸-3-부틸, 2,2-디메틸-1-프로필, 2-메틸-1-펜틸, 3-메틸-1-펜틸, 4-메틸-1-펜틸, 2-메틸-2-펜틸, 3-메틸-2-펜틸, 4-메틸-2-펜틸, 2,2-디메틸-1-부틸, 3,3-디메틸-1-부틸, 2-에틸-1-부틸, 부틸, 이소부틸, t-부틸, n-펜틸, 이소펜틸, 네오펜틸, n-헥실 등, 그리고 헵틸, 옥틸 등과 같이 더 긴 알킬기를 포함하지만 이에 한정되지 않는다. 용어 "Cx-y알킬" 은 x-y개의 탄소 원자를 갖는 알킬기를 의미하고, 여기서 x와 y는 정수이다.
본원에 사용된 "알켄닐 (alkenyl)"은 하나 이상의 이중 결합을 가지며 2 내지 12개의 탄소 원자를 갖는 직쇄 또는 분지쇄 탄화수소기를 의미한다. 예시적인 알케닐기는 에틸레닐 (ethylenyl), 비닐, 알릴, 부테닐, 펜테닐, 헥세닐, 부타디에닐 (butadienyl), 펜타디에닐, 헥사디에닐, 2-에틸헥세닐, 2-프로필-2-부테닐, 4-(2-메틸-3-부텐)-펜테닐 등을 포함하지만, 이에 한정되지 않는다. 용어 "Cx-y알케닐"은 x-y개의 탄소 원자를 갖는 알케닐을 의미하고, 여기서 x와 y는 정수이다.
용어 "알킬렌일 (alkylenyl)" 또는 "알킬렌"은 2가의 알킬기를 의미한다. 용어 "알케닐레닐" 또는 "알케닐렌"은 2가의 알케닐기를 의미한다.
본원에 사용된 "알키닐 (alkynyl)"은 하나 이상의 삼중 결합을 가지며 2 내지 10개의 탄소 원자를 갖는 직쇄 또는 분지쇄 탄화수소기를 의미한다. 예시적인 알키닐기는 에티닐, 프로피닐, 부티닐, 펜티닐, 헥시닐, 메틸프로피닐, 4-메틸-1-부티닐, 4-프로필-2-펜티닐, 4-부틸-2-헥시닐 등을 포함하지만, 이에 제한되지 않는다.
그 자체로 또는 다른 용어와 조합하여 용어 "헤테로알킬"은, 달리 언급되지 않는다면, 적어도 하나의 탄소 원자와 O, N, P, Si, 및 S로 이루어진 군으로부터 선택된 적어도 하나의 헤테로원자를 포함하며, 여기서 상기 질소 및 황 원자는 선택적으로 산화될 수 있고, 질소 헤테로원자는 선택적으로 4차화될 수 있는 것을 포함하는 안정한 직쇄 또는 분지쇄, 또는 이의 조합을 의미한다. 헤테로 원자(들) O, N, P, S, 및 Si는 헤테로알킬기의 임의의 내부 위치 또는 알킬기가 분자의 나머지 부분에 결합되는 위치에 배치될 수 있다. 예는 다음을 포함하지만 이로 한정되지 않는다: -CH2-CH2-O-CH3, -CH2-CH2-NH-CH3, -CH2-CH2-N(CH3)-CH3, -CH2-S-CH2-CH3, -CH2-CH2, -S(O)-CH3, -CH2-CH2-S(O)2-CH3, -CH=CH-O-CH3, -Si(CH3)3, -CH2-CH=N-OCH3, -CH=CH-N(CH3)-CH3, -O-CH3, -O-CH-2-CH3, 및 -CN. 예를 들어, -CH2-NH-OCH3 및 -CH2-O-Si(CH3)3와 같이 최대 2개 또는 3개의 헤테로원자가 연속될 수 있다.
유사하게, 그 자체 또는 또 다른 치환기의 일부로서, 용어 "헤테로알킬렌"은, 달리 언급되지 않는다면, 헤테로일킬로부터 유리한 2가 라디칼을 의미하며, -CH2-CH2-S-CH2-CH2- 및 -CH2-S-CH2-CH2-NH-CH2-로 예시될 수 있지만, 이에 제한되지 않는다. 헤테로알킬렌기의 경우, 헤테로원자는 또한 사슬 말단의 한쪽 또는 양쪽을 차지할 수 있다 (예를 들어, 알킬렌옥시, 알킬렌디옥시, 알킬렌아미노, 알킬렌디아미노 등). 또한, 알킬렌 및 헤테로알킬렌 연결기 (linking group)의 경우, 연결기의 배향이 연결기의 화학식이 기재된 방향을 의미하지 않는다. 예를 들어, 화학식 -C(O)2R'-는 -C(O)2R'- 및 -R'C(O)2- 둘 다를 나타낸다. 상기에 기재된 바와 같이, 본원에서 사용되는 헤테로알킬기는 헤테로원자를 통해 분자의 나머지 부분에 결합되는 기, 예를 들어, -C(O)R', -C(O)NR', -NR'R'', -OR', -SR', 및/또는 -SO2R'을 포함한다. "헤테로알킬"이 열거되고, 이어서 -NR'R'' 등과 같은 특정 헤테로알킬기가 열거될 경우, 용어 헤테로알킬 및 -NR'R''는 중복되거나 상호 배타적이지 않다는 것으로 이해될 것이다. 오히려, 특정 헤테로알킬기는 명확히 하기 위해 열거된다. 따라서, 용어 "헤테로알킬"은 본원에서 -NR'R'' 등과 같은 특정 헤테로알킬기를 배재하는 것으로 해석되어서는 안된다.
용어 "사이클로알킬" 및 "헤테로사이클로알킬"은 그 자체로 또는 다른 용어와 함께, 달리 언급되지 않는다면, 각각 "알킬" 및 "헤테로알킬"의 환형이다. 추가로, 헤테로사이클로알킬의 경우, 헤테로원자는 헤테로사이클이 분자의 나머지 부분에 결합되는 위치를 차지할 수 있다. 사이클로알킬의 예는 사이클로프로필, 사이클로부틸, 사이클로펜틸, 사이클로헥실, 1-사이클로헥세닐, 3-사이클로헥세닐, 사이클로헵틸 등을 포함하나 이에 제한되지 않는다. 헤테로사이클로알킬의 예는 1-(1,2,5,6-테트라하이드로피리딜), 1-피페리디닐, 2-피페리디닐, 3-피페리디닐, 4-모르폴리닐, 3-모르폴리닐, 테트라하이드로푸란-2-일, 테트라하이드로푸란-3-일, 테트라하이드로티엔-2-일, 테트라하이드로티엔-3-일, 1-피페라지닐, 2-피페라지닐 등을 포함하지만 이에 제한되지 않는다. "사이클로알킬렌" 및 "헤테로사이클로알킬렌"은 단독 또는 또 다른 치환기의 일부로서, 각각 사이클로알킬 및 헤테로사이클로알킬로부터 유도된 2가 라디칼을 의미한다.
용어 "아릴"은, 달리 언급되지 않는다면, 단일 고리 또는 서로 융합되거나 (즉, 융합된 고리형 아릴) 또는 공유 결합된 다수의 고리 (바람직하게는 1 내지 3개의 고리)일 수 있는 다불포화 방향족 탄화수소 치환기를 의미한다. 융합된 고리형 아릴은 적어도 하나의 융합된 고리가 아릴 고리인, 서로 융합된 다수의 고리를 지칭한다. 용어 "헤테로아릴"은 N, O, 또는 S와 같은 적어도 하나의 헤테로원자를 함유하는 아릴기 (또는 아릴 고리)를 지칭하며, 여기서 상기 질소 및 황 원자는 선택적으로 산화되고, 상기 질소 원자(들)은 선택적으로 4차화된다. 따라서, 용어 "헤테로아릴"은 융합된 고리형 헤테로아릴기 (즉, 적어도 하나의 융합된 고리가 헤테로 방향족 고리인 서로 융합된 다수의 고리)를 포함한다. 5,6-융합된 고리형 헤테로아릴렌은 두 개의 고리가 서로 융합된 것을 의미하며, 여기서 하나의 고리는 5원의 고리이고 다른 고리는 6원의 고리이다. 유사하게, 6,6-융합된 고리형 헤테로아릴렌은 두 개의 고리가 서로 융합된 것을 의미하며, 여기서 하나의 고리는 6원의 고리이고 다른 고리는 6원의 고리이며, 이때 적어도 하나의 고리가 헤테로아릴 고리이다. 6,5-융합된 고리형 헤테로아릴렌은 두 개의 고리가 서로 융합된 것을 의미하며, 여기서 하나의 고리는 6원의 고리이고 다른 고리는 5원의 고리이며, 이때 적어도 하나의 고리가 헤테로아릴 고리이다. 헤테로아릴기는 탄소 또는 헤테로원자를 통해 분자의 나머지 부분에 결합될 수 있다. 아릴 및 헤테로아릴기의 비제한적인 예는 페닐, 1-나프틸, 2-나프틸, 4-비페닐, 1-피롤일, 2-피롤일, 3-피롤일, 3-피라졸일, 2-이미다졸일, 4-이미다졸일, 피라진일, 2-옥사졸일, 4-옥사졸일, 2-페닐-4-옥사졸일, 5-옥사졸일, 3-이소옥사졸릴, 4-이소옥사졸릴, 5-이소옥사졸릴, 2-티아졸일, 4-티아졸일, 5-티아졸일, 2-푸릴(furyl), 3-푸릴, 2-티에닐, 3-티에닐, 2-피리딜, 3-피리딜, 4-피리딜, 2-피리미딜, 4-피리미딜, 5-벤조티아졸일, 퓨리닐(purinyl), 2-벤즈이미다졸일, 5-인돌일, 1-이소퀴놀릴, 5-이소퀴놀릴, 2-퀴녹살린일, 5-퀴녹살린일, 3-퀴놀릴, 및 6-퀴놀릴을 포함하나 이에 제한되지 않는다. 상기에 나타낸 아릴 및 헤테로아릴 고리계 각각에 대한 치환기는 하기에 기재된 허용가능한 치환기의 군으로부터 선택된다. "아릴렌 (arylene)" 및 "헤테로아릴렌,"은, 단독 또는 또 다른 치환기의 일부로서, 각각 아릴 및 헤테로아릴로부터 유도된 2가 라디칼을 의미한다. 헤테로아릴기의 비제한적인 예는 피리딘일, 피리미딘일, 티오페닐, 푸라닐(furanyl), 인돌일, 벤즈옥사디아졸일, 벤조디옥솔일 (benzodioxolyl), 벤조디옥사닐, 티아나프탄일, 피롤로피리딘일, 인다졸일, 퀴놀린일, 퀴녹살린일, 피리도피라진일, 퀴나졸리논일 (quinazolinonyl), 벤조이소옥사졸일, 이미다조피리딘일, 벤조푸라닐, 벤조티오페닐, 페닐, 나프틸, 비페닐, 피롤일, 피라졸일, 이미다졸일, 피라진일, 옥사졸릴, 이소옥사졸릴, 티아졸일, 푸릴티에닐, 피리딜, 피리미딜, 벤조티아졸일, 퓨리닐, 벤즈이미다졸일, 이소퀴놀릴, 티아디아졸일, 옥사디아졸일, 피롤일, 디아졸일, 트리아졸일, 테트라졸일, 벤조티아디아졸일, 이소티아졸일, 피라졸로피리미딘일, 피롤로피리미딘일, 벤조트리아졸일, 벤조옥사졸릴, 또는 퀴놀릴을 포함한다. 상기 예는 치환 또는 비치환될 수 있고, 상기 각 헤테로아릴 예시의 2가 라디칼은 헤테로아릴렌의 비제한적인 예이다.
용어 "보론산 에스테르 (boronic ester)"는 치환기 -B(OR)2를 지칭하는 것으로, 여기서 각 R기는 독립적으로 C1-4알킬기이거나, 2개의 R기는 함께 C2-6알킬렌을 형성한다.
용어 "아세탈"은 -CH(OR)2기를 지칭하며, 여기서 각 R기는 독립적으로 C1-4알킬이거나, 2개의 R기는 함께 C2-6알킬렌을 형성한다. 예시적인 아세탈기는 디메틸아세탈 또는 디에틸아세탈, 또는 사이클릭 아세탈을 포함한다. 용어 "케탈"은 -C(OR)2-기를 지칭하는 것으로, 여기서 각 R기는 독립적으로 C1-4알킬이거나, 2개의 R기는 함께 C2-6알킬렌을 형성한다. 예시적인 케탈은 디메틸케탈 또는 디에틸케탈, 또는 사이클릭 케탈을 포함한다.
용어 "할로"는 클로로, 플루오로, 브로모, 또는 아이오도를 나타낸다. 일부 실시양태에서, 할로는 클로로, 플루오로, 또는 브로모이다. 본원에서 사용된 용어 "할로겐"은 플루오린, 염소, 브로민, 또는 아이오딘을 지칭한다. 용어 "오르쏘 에스테르"는 -C(OR)3 기를 지칭하며, 여기서 각 R기는 독립적으로 C1-4알킬이거나, R기들 중 2개는 함께 C2-6알킬렌을 형성한다. 용어 "옥소"는 =O 기를 의미하며 탄소 원자 또는 황 원자에 결합될 수 있다. 용어 "포스포네이트 에스테르"는 -P(O)(OR)2 기를 지칭하며, 여기서 각 R기는 독립적으로 C1-4알킬이거나, 2개의 R기는 함께 C2-6알킬렌을 형성한다.
본원에 사용되는 용어 "사이클로알킬"은 3 내지 15개의 고리 탄소 원자를 갖는, 포화된 또는 부분적으로 포화된, 모노사이클릭, 융합된 폴리사이클릭, 가교된 폴리사이클릭, 또는 스피로 폴리사이클릭 카보사이클을 지칭한다. 사이클로알킬기의 비제한적인 카테고리는 3 내지 6개의 탄소 원자를 갖는, 포화된 또는 부분적으로 포화된, 모노사이클릭 카보사이클이다.
사이클로알킬기의 실례는 하기 모이어티(moiety)를 포함하지만 이에 제한되지 않는다:
본원에서 사용되는 용어 "5원 헤테로아릴"은 탄소, 산소, 질소 및 황으로부터 선택되는 5개의 고리 원자를 갖는 모노사이클릭, 방향족 헤테로사이클을 지칭한다. 5원 헤테로아릴기의 예는 이미다졸릴, 피라졸릴, 트리아졸릴, 테트라졸릴, 푸라닐, 티에닐, 이소옥사졸릴, 티아졸릴, 옥사졸릴, 이소티아졸릴, 피롤릴, 및 티아디아졸릴을 포함하지만 이에 제한되지 않는다. 5원 헤테로아릴의 특정 예는 아지드와 프로파르길기 사이의 후이겐 반응과 같은 1,3-고리화 첨가반응에 의해 형성될 수 있는 것을 포함한다.
본원에서 사용되는 용어 "치환된"은 특정된 기 또는 모이어티가 하나 이상의 적합한 치환기를 포함한다는 것을 의미한다. 본원에 사용되는 용어 "비치환된"은 특정된 기가 치환기를 포함하지 않는다는 것을 의미한다. 본원에 사용되는 용어 "선택적으로 치환된"은 특정된 기가 비치환되거나 특정된 개수의 치환기로 치환되는 것을 의미한다. 용어 "치환된"이 구조 시스템을 설명하기 위해 사용되는 경우, 치환은 시스템 상의 원자가가 허용되는 임의의 위치에서 발생하는 것을 의미한다. 본원에 사용되는 표현 "하나 이상의 치환기"는 상기 시스템 상의 원자가가 허용되는 임의의 위치에서 발생할 수 있는 1 내지 가능한 최대의 치환기 개수를 나타낸다. 특정 실시양태에서, "하나 이상의 치환기"는 1, 2, 3, 4, 또는 5개의 치환기를 의미한다. 또 다른 일 실시양태에서, 하나 이상의 치환기는 1, 2, 또는 3개의 치환기를 의미한다.
본원에서 사용되는 "치환기 (substituent group)" 또는 "치환체 (substituent group)"은 다음의 모이어티로부터 선택된 기를 의미한다:
(A) 옥소, 할로겐, -CF3, -CN, -OH, -NH2, -COOH, -CONH2, -NO2, -SH, -SO2Cl, -SO3H, -SO4H, -SO2NH2, -NHNH2, -ONH2, -NHC=(O)NHNH2, -NHC=(O) NH2, -NHSO2H, -NHC= (O)H, -NHC(O)-OH, -NHOH, -OCF3, -OCHF2, 비치환된 알킬, 비치환된 헤테로알킬, 비치환된 사이클로알킬, 비치환된 헤테로사이클로알킬, 비치환된 아릴, 비치환된 헤테로아릴, 및
(B) 하기로부터 선택된 적어도 하나의 치환기로 치환된 알킬, 헤테로알킬, 사이클로알킬, 헤테로사이클로알킬, 아릴, 및 헤테로아릴:
i. 옥소, 할로겐, -CF3, -CN, -OH, -NH2, -COOH, -CONH2, -NO2, -SH, -SO2Cl, -SO3H, -SO4H, -SO2NH2, -NHNH2, -ONH2, -NHC=(O)NHNH2, -NHC=(O) NH2, -NHSO2H, -NHC= (O)H, -NHC(O)-OH, -NHOH, -OCF3, -OCHF2, 비치환된 알킬, 비치환된 헤테로알킬, 비치환된 사이클로알킬, 비치환된 헤테로사이클로알킬, 비치환된 아릴, 비치환된 헤테로아릴, 및
ii. 하기로부터 선택된 적어도 하나의 치환기로 치환된 알킬, 헤테로알킬, 사이클로알킬, 헤테로사이클로알킬, 아릴, 및 헤테로아릴:
1. 옥소, 할로겐, -CF3, -CN, -OH, -NH2, -COOH, -CONH2, -NO2, -SH, -SO2Cl, -SO3H, -SO4H, -SO2NH2, -NHNH2, -ONH2, -NHC=(O)NHNH2, -NHC=(O) NH2, -NHSO2H, -NHC= (O)H, -NHC(O)-OH, -NHOH, -OCF3, -OCHF2, 비치환된 알킬, 비치환된 헤테로알킬, 비치환된 사이클로알킬, 비치환된 헤테로사이클로알킬, 비치환된 아릴, 비치환된 헤테로아릴, 및
2. 옥소, 할로겐, -CF3, -CN, -OH, -NH2, -COOH, -CONH2, -NO2, -SH, -SO2Cl, -SO3H, -SO4H, -SO2NH2, -NHNH2, -ONH2, -NHC=(O)NHNH2, -NHC=(O) NH2, -NHSO2H, -NHC= (O)H, -NHC(O)-OH, -NHOH, -OCF3, 비치환된 알킬, 비치환된 헤테로알킬, 비치환된 사이클로알킬, 비치환된 헤테로사이클로알킬, 비치환된 아릴, 및 비치환된 헤테로아릴로부터 선택된 적어도 하나의 치환기로 치환된 알킬, 헤테로알킬, 사이클로알킬, 헤테로사이클로알킬, 아릴, 또는 헤테로아릴.
본원에서 사용되는 "크기 제한 치환체" 또는 "크기 제한 치환기"는 "치환기"에 대해 상기 기재된 모든 치환제로부터 선택된 기를 의미하며, 여기서 각 치환된 또는 비치환된 알킬은 치환된 또는 비치환된 C1-C20 알킬이고, 각 치환된 또는 비치환된 헤테로알킬은 치환된 또는 비치환된 2 내지 20원 헤테로알킬이며, 각 치환된 또는 비치환된 사이클로알킬은 치환된 또는 비치환된 C3-C8 사이클로알킬이고, 각 치환된 또는 비치환된 헤테로사이클로알킬은 치환된 또는 비치환된 3 내지 8원의 헤테로사이클로알킬이며, 각 치환된 또는 비치환된 아릴은 치환된 또는 비치환된 C6-C10 아릴이고, 각 치환된 또는 비치환된 헤테로아릴은 5 내지 10원의 헤테로아릴이다. 본원에서 사용되는 "저급 치환체" 또는 "저급 치환기"는 "치환기"에 대해 상기 기재된 모든 치환체로부터 선택된 기를 의미하며, 여기서 각 치환된 또는 비치환된 알킬은 치환된 또는 비치환된 C1-C8 알킬이고, 각 치환된 또는 비치환된 헤테로알킬은 치환된 또는 비치환된 2 내지 8원의 헤테로알킬이며, 각 치환된 또는 비치환된 사이클로알킬은 치환된 또는 비치환된 C3-C7 사이클로알킬이고, 각 치환된 또는 비치환된 헤테로사이클로알킬은 치환된 또는 비치환된 3 내지 7원의 헤테로사이클로알킬이며, 각 치환된 또는 비치환된 아릴은 치환된 또는 비치환된 C6-C10 아릴이고, 각 치환된 또는 비치환된 헤테로아릴은 치환된 또는 비치환된 5 내지 9원의 헤테로아릴이다.
일부 실시양태에서, 본원의 화합물에 기재된 각 치환된 기는 적어도 하나의 치환기로 치환된다. 보다 구체적으로, 일부 실시양태에서, 본원의 화합물에 기재된 각 치환된 알킬, 치환된 헤테로알킬, 치환된 사이클로알킬, 치환된 헤테로사이클로알킬, 치환된 아릴, 치환된 헤테로아릴, 치환된 알킬렌, 치환된 헤테로알킬렌, 치환된 사이클로알킬렌, 치환된 헤테로사이클로알킬렌, 치환된 아릴렌, 및/또는 치환된 헤테로아릴렌은 적어도 하나의 치환기로 치환된다. 다른 실시양태에서, 적어도 하나 또는 모든 이러한 기는 적어도 하나의 크기 제한 치환기로 치환된다. 다른 실시양태에서, 적어도 하나 또는 모든 이러한 기는 적어도 하나의 저급 치환기로 치환된다.
본원의 다른 실시양태에서, 각 치환된 또는 비치환된 알킬은 치환된 또는 비치환된 C1-C20 알킬일 수 있고, 각 치환된 또는 비치환된 헤테로알킬은 치환된 또는 비치환된 2 내지 20원의 헤테로알킬이며, 각 치환된 또는 비치환된 사이클로알킬은 치환된 또는 비치환된 C3-C8 사이클로알킬이고, 각 치환된 또는 비치환된 헤테로사이클로알킬은 치환된 또는 비치환된 3 내지 8원의 헤테로사이클로알킬이며, 각 치환된 또는 비치환된 아릴은 치환된 또는 비치환된 C6-C10 아릴이고, 그리고/또는 각 치환된 또는 비치환된 헤테로아릴은 치환된 또는 비치환된 5 내지 10원의 헤테로아릴이다. 본원의 화합물의 일부 실시양태에서, 각 치환된 또는 비치환된 알킬렌은 치환된 또는 비치환된 C1-C20 알킬렌이고, 각 치환된 또는 비치환된 헤테로알킬렌은 치환된 또는 비치환된 2 내지 20원의 헤테로알킬렌이며, 각 치환된 또는 비치환된 사이클로알킬렌은 치환된 또는 비치환된 C3-C8 사이클로알킬렌이고, 각 치환된 또는 비치환된 헤테로사이클로알킬렌은 치환된 또는 비치환된 3 내지 8원의 헤테로사이클로알킬렌이며, 각 치환된 또는 비치환된 아릴렌은 치환된 또는 비치환된 C6-C10 아릴렌이고, 그리고/또는 각 치환된 또는 비치환된 헤테로아릴렌은 치환된 또는 비치환된 5 내지 10원의 헤테로아릴렌이다.
일부 실시양태에서, 각 치환된 또는 비치환된 알킬은 치환된 또는 비치환된 C1-C8 알킬이고, 각 치환된 또는 비치환된 헤테로알킬은 치환된 또는 비치환된 2 내지 8원의 헤테로알킬이며, 각 치환된 또는 비치환된 사이클로알킬은 치환된 또는 비치환된 C3-C7 사이클로알킬이고, 각 치환된 또는 비치환된 헤테로사이클로알킬은 치환된 또는 비치환된 3 내지 7원의 헤테로사이클로알킬이며, 각 치환된 또는 비치환된 아릴은 치환된 또는 비치환된 C6-C10 아릴이고, 그리고/또는 각 치환된 또는 비치환된 헤테로아릴은 치환된 또는 비치환된 5 내지 9원의 헤테로아릴이다. 일부 실시양태에서, 각 치환된 또는 비치환된 알킬렌은 치환된 또는 비치환된 C1-C8 알킬렌이고, 각 치환된 또는 비치환된 헤테로알킬렌은 치환된 또는 비치환된 2 내지 8원의 헤테로알킬렌이며, 각 치환된 또는 비치환된 사이클로알킬렌은 치환된 또는 비치환된 C3-C7 사이클로알킬렌이고, 각 치환된 또는 비치환된 헤테로사이클로알킬렌은 치환된 또는 비치환된 3 내지 7원의 헤테로사이클로알킬렌이며, 각 치환된 또는 비치환된 아릴렌은 치환된 또는 비치환된 C6-C10 아릴렌이고, 그리고/또는 각 치환된 또는 비치환된 헤테로아릴렌은 치환된 또는 비치환된 5 내지 9원의 헤테로아릴렌이다.
불충족된 원자가를 갖는 본원에 나타낸 임의의 원자는 원자의 원자가를 충족시키기에 충분한 개수의 수소 원자를 갖는 것으로 추정된다. 알킬, R3, 또는 R5와 같은 임의의 변수가 임의의 화학식 또는 본원에 제공된 설명에 하나 이상의 위치에서 나타날 경우, 각 경우의 변수의 정의는 모든 다른 경우의 이의 정의와는 독립적이다. 본원에서 사용되는 수의 범위는 연속되는 전체 수를 포함고자 한다. 예를 들어, "0 내지 4" 또는 "0-4"와 같이 표현된 범위는 0, 1, 2, 3 및 4를 포함한다. 다작용성 모이어티를 나타내는 경우, 중심부에 부착 지점은 선 또는 하이픈(hyphen)으로 나타낸다. 예를 들어, -OH는 산소 원자가 분자의 나머지 부분에 히드록실 기를 부착하는 지점인 모이어티를 나타낸다.
본원에 주어진 임의의 화학식은 구조식으로 도식되는 구조를 갖는 화합물 뿐만 아니라 특정의 변이 또는 형태를 나타내고자 한다. 예를 들어, 본원에서 임의의 화학식의 화합물은 비대칭 또는 키랄 중심을 가질 수 있어서, 상이한 입체이성체 형태로 존재할 수 있다. 일반식의 화합물의 광학이성체, 거울상 이성체, 및 부분입체이성체를 포함한, 모든 입체이성체, 및 이의 혼합물은 그 화학식의 범위 내에 속하는 것으로 간주된다. 또한, 특정 구조는 기하학적 이성체로서(즉, 시스 및 트랜스 이성체), 호변이성체로서, 또는 아트로프이성체(atropisomer)로서 존재할 수 있다. 상기 모든 이성체 형태, 및 이의 혼합물은 본원에서 본 발명의 일부로 고려된다. 따라서, 본원에 주어진 임의의 화학식은 라세미체, 하나 이상의 거울상 이성체 형태, 하나 이상의 부분입체이성체 형태, 하나 이상의 호변이성체 또는 아트로프이성체 형태, 및 이들의 혼합물을 나타내고자 한다.
부분입체이성체 혼합물은 이들의 물리화학적 차이를 기본으로 하여 당업자에게 잘 알려져 있는 방법, 예를 들어, 크로마토그래피 및/또는 분별 결정에 의해 이들 각각의 부분입체이성체로 분리될 수 있다. 거울상 이성체는 적절한 광학 활성 화합물(예를 들어, 키랄 알코올 또는 모셔(Mosher)의 산 클로라이드와 같은 키랄 보조제, 또는 부분입체이성체 염의 혼합물의 형성)과의 반응에 의해 거울상 이성체 혼합물을 부분입체이성체 혼합물로 전환하고, 상기 부분입체이성체를 분리하여 각각의 부분입체이성체를 상응하는 순수한 거울상 이성체로 전환(예를 들어, 가수분해 또는 탈염)시킴으로써 분리될 수 있다. 또한, 거울상 이성체는 키랄 HPLC 컬럼을 사용하여 분리시킬 수 있다. 본 발명의 화합물의 키랄 중심은 IUPAC 1974 권고사항에 의해 정의되는 "R" 또는 "S"로, 또는 펩타이드 문헌과 일치하는 "D" 또는 "L"로 지정할 수 있다.
본원에서 사용되는 바와 같이, 아래 첨자와 함께 도시된 구조의 일부분에 둘러진 박스는 박스 내에 나타나는 구조적 단편이 첨자에 따라 반복되는 것을 나타낸다. 예를 들어, 하위구조 (여기서 x는 0, 1, 또는 2임)는 단편이 구조에 존재하지 않거나 -단편- 또는 -단편-단편인 것을 나타낸다:
예를 들어, 식 VII 내에서, 하기 하위구조 (여기서 p는 0 또는 1임)는 박스 내의 X-NH-기가 구조에 존재하지 않거나 (p는 0임), 한번 존재하는 것(p는 1임)을 의미한다:
본 발명의 화합물은 약학적으로 허용 가능한 염을 형성할 수 있으며, 이 또한 본 발명의 범위 내에 있다. "약학적으로 허용 가능한 염"이란 비독성이고, 생리학적으로 내성을 가질 수 있으며, 제제화되는 약학 조성물과 적합성이고, 그 외 제제 및/또는 피험체에 대한 투여에 적합한 본원에 기재된 화합물의 유리산 또는 유리 염기의 염을 의미한다. 본원에서 화합물의 언급은 달리 명시되지 않는 한 상기 화합물의 약학적으로 허용 가능한 염의 언급도 포함하는 것으로 이해되어야 한다.
화합물 염은 무기 및/또는 유기산으로 형성된 산성 염, 뿐만 아니라 무기 및/또는 유기 염기로 형성된 염기성 염을 포함한다. 또한, 주어진 화합물은 염기성 모이어티, 예를 들어, 비제한적으로, 피리딘 또는 이미다졸, 및 산성 잔기, 예를 들어, 비제한적으로, 카복실산을 둘 다 함유하는 경우, 당 업자는 상기 화합물이 양쪽성 이온("내부 염")으로 존재할 수 있다는 것을 인식할 될 것이며; 상기 염은 본원에 사용되는 용어 "염"에 포함된다. 본 발명의 화합물의 염은 염이 침전되는 것과 같은 매질 또는 수성 매질에서 예를 들어, 화합물을 등가량과 같은 양의 적합한 산 또는 염기와, 반응시킨 다음 동결건조시켜 제조할 수 있다.
대표적인 염은 설페이트, 시트레이트, 아세테이트, 옥살레이트, 염소, 브롬, 요오드, 니트레이트, 비설페이트, 포스페이트, 산 포스페이트, 이소니코티네이트, 락테이트, 살리실레이트, 산 시트레이트, 타르트레이트, 올레에이트, 탄네이트, 판토테네이트, 비타르트레이트, 아스코르베이트, 숙시네이트, 말레에이트, 겐티시네이트, 푸마레이트, 글루코네이트, 글루쿠로네이트, 사카레이트, 포르메이트, 벤조에이트, 글루타메이트, 메탄설포네이트("메실레이트"), 에탄설포네이트, 벤젠설포네이트, p-톨루엔설포네이트, 및 파모에이트(즉, 1,1'-메틸렌-비스(2-히드록시-3-나프토에이트))염을 포함하나 이에 제한되지 않는다. 약학적으로 허용 가능한 염은 아세테이트 이온, 숙시네이트 이온 또는 다른 카운터 이온과 같은 또 다른 분자의 포집(inclusion)을 수반할 수 있다. 카운터 이온은 모체 화합물 상에서 전하를 안정화시키는 임의의 유기 또는 무기 모이어티일 수 있다. 또한, 약학적으로 허용 가능한 염은 이의 구조 내에 하전된 하나 이상의 원자를 가질 수 있다. 다수의 하전된 원자가 약학적으로 허용 가능한 염의 일부일 경우 다수의 카운터 이온을 가질 수 있다. 따라서, 약학적으로 허용 가능한 염은 하나 이상의 하전된 원자 및/또는 하나 이상의 카운터 이온을 가질 수 있다.
대표적인 산부가염은 아세테이트, 아스코르베이트, 벤조에이트, 벤젠설포네이트, 비설페이트, 보레이트, 부티레이트, 시트레이트, 캄포레이트, 캄포르설포네이트, 푸마레이트, 히드로클로라이드, 히드로브로마이드, 히드로요오다이드, 락테이트, 말레에이트, 메탄설포네이트, 나프탈렌설포네이트, 니트레이트, 옥살레이트, 포스페이트, 프로피오네이트, 살리실레이트, 숙시네이트, 설페이트, 타르타레이트, 티오시아네이트, 톨루엔설포네이트(토실레이트로도 알려져 있음) 등을 포함한다.
대표적인 염기성 염은 암모늄 염, 알칼리 금속염, 예를 들어 나트륨, 리튬, 및 칼륨염, 알칼리 토금속염, 예를 들어 칼슘 및 마그네슘염, 유기 염기 (예를 들어, 유기 아민)와의 염, 예를 들어 디시클로헥실아민, t-부틸 아민, 및 아르기닌, 리신 등과 같은 아미노산과의 염을 포함한다. 염기성 질소-함유 기는 저급 알킬 할라이드(예를 들어, 메틸, 에틸, 및 부틸 클로라이드, 브로마이드 및 요오다이드), 디알킬 설페이트(예를 들어, 디메틸, 디에틸, 및 디부틸 설페이트), 장쇄 할라이드 (예를 들어, 데실, 라우릴, 및 스테아릴 클로라이드, 브로마이드 및 요오다이드), 아르알킬 할라이드(예를 들어, 벤질 및 펜에틸 브로마이드), 및 기타의 것들과 같은 제제와 4차화 될 수 있다.
일반적으로 약학 화합물로부터 약학적으로 유용한 염의 형성은 적합하다고 고려되는 산 및 염기는 예를 들어 문헌(P. Stahl et al, Camille G. (eds.) Handbook of Pharmaceutical Salts. Properties, Selection and Use. (2002) Zurich: Wiley-VCH; S. Berge et al, Journal of Pharmaceutical Sciences (1977) 66(1) 1-19; P. Gould, International J. of Pharmaceutics (1986) 33 201-217; Anderson et al, The Practice of Medicinal Chemistry (1996), Academic Press, New York; and in The Orange Book (Food & Drug Administration, MD, FDA로부터 이용가능함))에서 논의된다. 이들 개시내용은 본원에서 참고로 포함된다.
또한, 본원에 기재된 임의의 화합물은 형태가 명백하게 게시되지 않는다 하더라도 임의의 비용매화된 형태, 또는 수화물, 용매화물, 또는 상기 화합물의 다형체, 및 이들의 혼합물을 언급하고자 한다. "용매화물"은 본 발명의 화합물과 하나 이상의 용매 분자와 물리적 결합을 의미한다. 이런 물리적 결합은 수소 결합을 포함한, 이온성 및 공유결합의 정도 변화를 수반한다. 특정 경우에, 예를 들어, 하나 이상의 용매 분자가 결정성 고체의 결정 격자에 용매화물에 편입될 때, 용매화물은 분리될 수 있다. "용매화물"은 용액 상태 및 분리 가능한 용매화물 둘 다를 포함한다. 적합한 용매화물은 물, 에탄올 등과 같은 약학적으로 허용 가능한 용매와 형성되는 것들이다. 일부 실시양태로, 용매는 물이며 용매화물은 수화물이다.
또한, 본원에 주어진 임의의 화학식은 비표지된 형태 뿐만 아니라 동위원소 표지된 형태의 화합물을 나타내고자 한다. 동위원소 표지된 화합물은 하나 이상의 원자가 선택된 원자량 또는 질량수를 갖는 원자로 대체된 것을 제외하고는 본원에 주어진 화학식으로 도시되는 구조를 갖는다. 본 발명의 화합물에 포함될 수 있는 동위원소의 예는 수소, 탄소, 질소, 산소, 인, 불소, 염소, 및 요오드의 동위원소, 예를 들어 각각 2H, 3H, 11C, 13C, 14C, 15N, 18O, 17O, 31P, 32P, 35S, 18F, 36Cl, 및 125I를 포함한다. 상기 동위원소 표지된 화합물은 대사연구(예를 들어, 14C를 사용), 반응 동역학 연구(예를 들어, 2H, 또는 3H를 사용), 약물 또는 기질 조직 분포 분석법을 포함하여 검출 또는 영상화 기술[예를 들어 양전자방출 단층촬영술(PET) 또는 단일광자방출 단층촬영술(SPECT)], 또는 환자의 방사선 치료에 유용하다. 특히, 18F 또는 11C 표지된 화합물은 PET 또는 SPECT 연구에 특히 적합할 수 있다. 또한, 중수소(즉, 2H)와 같이 중동위원소로 치환은 더 커진 대사 안정성 예를 들어, 증가된 생체 내 반감기 또는 감소된 투여량 요건으로 인한 특정의 치료적 장점을 얻을 수 있다. 본 발명의 동위원소 표지된 화합물과 이들의 전구 약물은 일반적으로 동위원소로 표지되지 않은 시약을 쉽게 이용 가능한 동위원소 표지된 시약으로 치환하여 하기에 기재된 반응 개요에 또는 실시예 및 제조에 개시되어 있는 절차를 수행함으로써 제조될 수 있다.
VII. 실시예
하기 실시예는 본 발명을 설명하기 위한 것으로 본 발명의 범위를 제한하려는 것은 아니다.
실시예 1: 메디토프 Fc 결합
메디토프-Fc 구조물은 메디토프를 Fc 도메인의 N-말단에 폴리-글리신-세린 링커를 통해 융합하여 생성하였다. 상기 메디토프-Fc 구조물의 유전자는 DNA2.0(인간 IgG 감마 중쇄 3(승인번호# AAW65947) 잔기 22-241에 37-잔기 링커를 통해 연결된 cQFD 메디토프)에 의해 제작하고, pAcGP67A 벡터(BD Biosciences)에 클로닝하고 Sf9 세포에서 생산하였다. 단백질은 단백질 A 및 크기 배제 크로마토그래피를 이용하여 정제하였다. 메디토프-Fc는 서열번호 57에 개시된 아미노산 서열을 갖는 폴리펩타이드를 포함하였다(위치 1에 선도서열("G"), 메디토프는 볼드체, 링커는 이탤릭체, Fc 부분은 일반 텍스트로 하기 나타냄).
GCQFDLSTRRLRC GGSRSGGTSGGGSVPGSGSSGSTSGSGKSSEGSGQASTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK (서열번호 57).
상기 구조물을 이용하여, 크기 배제 크로마토그래피(SEC)에 의해 세툭시맙 Fab, EGFRdIII과 메디토프가 복합체를 형성한다는 것을 증명하였다. 메디토프-Fc 구조물을 EGFRdIII과 세툭시맙 Fab의 화학양론적 복합체에 첨가하고 Fab-EGFRdIII 복합체보다 훨씬 일찍 용리되는 새로운 피크를 관찰하였으며, 이는 유체역학적 질량의 증가와 일치한다. 상기 새로운 피크는 세 가지 단백질 모두가 존재한다는 것을 보였다. 또한, 본 연구는 메디토프가 항원 인식을 크게 방해하지 않았다는 것을 확인하였다.
실시예 2: 메디토프-이용가능 트라스투주맙의 생성
메디토프 결합 부위는 인간 mAb 골격에 이식하여 메디토프 이용 가능 항체(메디토프 이용 가능 항체), 특히, 메디토프-이용가능 항체 트라스투주맙을 생성하였다. 세툭시맙과 트라스투주맙의 서열을 정렬하여 서열 동일성을 트라스투주맙의 원자 모델에 맵핑하였다(1N8Z, 문헌(Cho et al., Nature 421, 756-760(2003)) 참조). cQFD-세툭시맙과 트라스투주맙 구조의 상기 맵핑 및 중첩을 기초로 하여, 13개 잔기가 세툭시맙과 트라스투주맙 사이에 차이가 있으며, 그 측쇄는 메디토프와 직접 접촉하거나 메디토프 결합에 간접적으로 영향을 줄 수 있다는것을 확인하였다. 상기 잔기는 다음과 같다: 경쇄에서 Thr40, Asn41, Asp85(상기 참조), 결합되지 않은 인산 기를 배위 결합하고, 일부 실시예에서, 경쇄의 Thr40 및 Asn41를 포함하는 루프를 안정화시키는 경쇄에서 Arg39, 및 Arg45, 메디토프 내 Leu10의 측쇄 가까이 얕은 소수성 표면을 형성하는데 관여하는 Val9 및 Ile10, 경쇄에서 Gly42, Ser43, Ile83 및 Ala100, 게다가 중쇄에서 Ser40 및 Ile89. 메디토프-이용가능 항체의 경쇄 서열은 서열번호 303에 개시되어 있고, 중쇄는 서열번호 304에 개시되어 있다(메디토프 펩타이드 서열과 링커 서열은 포함하지 않음).
트라스투주맙 서열에서 등가 위치를 변이시키고(카밧 넘버링을 기준으로 경쇄에서 Thr40, Asn41, Asp85, Arg39, Arg45, Ile9, Leu10, Gly42, Ser43, Ile83 및 Ala100, 및 중쇄에서 Ser40 및 Ile89로), 단백질을 생산하고 정제하였다. SPR을 이용하여, cQFD 메디토프가 이식된 트라스투주맙 Fab에 세툭시맙과 유사한 친화도(KD = 1.2 μM)로 결합한다는 것을 보였다. 또한, 메디토프 이용 가능 트라스투주맙 Fab가 가용성 HER2에 시판되는 것으로부터 단리된 Fab와 유사한 친화도로 결합한다는 것을 관찰하였으며, 이는 돌연변이가 항원 결합에 해로운 영향을 주지 않는다는 것을 확인해 주었다. 메디토프 이용 가능 트라스투주맙, sHER2, 및 메디토프-Fc가 동시에 용리되었다는 것을 크기 배제 크로마토그래피에 의해 증명하였다.
점 돌연변이가 Fab의 전체 구조를 크게 방해하지 않는다는 것을 추가로 확인하기 위하여, 트라스투주맙 메디토프-이용가능 항체의 Fab를 cQFD 메디토프와 함께 또는 없이 결정화하였다. 잘 회절하는 결정은 결정화를 돕는 단백질 A 및 단백질 L의 존재하에서 얻었다. 아포(apo)-메디토프 이용가능 항체 트라스투주맙 및 메디토프-포함 복합체의 구조는 각각 1.95와 2.0Å에서 해석하였다. 또한, 단백질 A 및 단백질 L에 결합된 부모 트라스투주맙 Fab를 결정화하여 2.08Å 해상도로 해석하였다. "아포"-메디토프 이용가능 항체 트라스투주맙에 아포-부모 트라스투주맙 Fab 또는 HER2-결합된 부모 트라스투주맙 Fab(22)의 중첩은 전체 구조에서 약간의 변화만을 밝혔다(433 및 431 Cα 원자에 대해 각각 RMSD = 0.22Å 및 0.56Å). "아포"-와 메디토프-리간드화된 메디토프 이용가능 항체 트라스투주맙의 중첩은 메디토프 점유가 세툭시맙에 대해 관찰된 것과 유사하게 개방 입체구조 내 중쇄 루프(잔기 39-44)를 안정화시킨다는 것을 보였으며, 약간 더 높은 RMSD를 부분적으로 설명해 주었다. 더 중요하게도, "아포"-와 메디토프-리간드화된 메디토프 이용가능 항체의 서열 맵핑에 의해 확인된 잔기(Thr40, Asn41 및 Asp85)는 세툭시맙에서 이들의 대응물과 동일한 위치에 필수적이었으며 메디토프와 유사한 상호작용을 형성하였다. 또한, 메디토프의 중요한 측쇄 회전 이성체는 이들이 cQFD-세툭시맙 구조에 존재하는 것과 본질적으로 동일하였다. 세툭시맙과 관련하여, CDR 루프 내 유의한 변경은 관찰되지 않았다.
상기 데이터는 항원 결합에 유의하게 영향을 주지 않으면서 인간 Fab 골격에 메디토프 결합부위를 성공적으로 이식하였음을 증명해준다. 게다가, 메디토프 부위의 성공적인 이식은 회절 데이터 및 상호작용의 특이성을 통해 얻은 초기 세툭시맙-메디토프를 입증한다. 데이터는 또한 결합활성을 통해 메디토프 결합 친화도를 향상시킬 실행 가능성을 확인하고, 2가 메디토프가 항원을 과발현하는 세포에 특이적이며 높은 친화도로, 그러나 동족 메디토프 이용가능 항체의 존재 하에서만 결합한다는 것을 보여준다.
실시예 3: 메디토프 융합 항체 가교 결합을 이용한 항체 내재화의 증가
SnAP-바디(링커를 통해 중쇄의 N 말단에 융합된 메디토프를 포함하는 메디토프 이용가능 항체)가 표적 항원을 발현하는 세포에 의해 내재화 될 수 있는 능력을 평가하였다.
A. 항체 생산
세 가지 다른 종류를 포유류 발현 시스템에서 생산하였다. 각각의 항체는 서열번호 254의 아미노산 서열을 포함하는 경쇄를 갖는 메디토프-이용가능 젬투주맙 를 포함하였다. SnAP-바디 변이체 1은 링커(서열번호 255)를 통해 메디토프에 융합된 메디토프-이용가능 젬투주맙 IgG1 중쇄 서열을 포함하는 중쇄를 가진다. SnAP-바디 변이체 2는 링커(서열번호 256)을 통해 메디토프에 융합된 메디토프 이용가능 젬투주맙 IgG1 중쇄 서열을 포함하는 중쇄를 가진다. 대조군 항체는 메디토프가 활성화된 젬투주맙 IgG1 중쇄 아미노산 서열(서열번호 257)을 가지지만 메디토프 또는 N-터미너스에 융합된 링커는 없다.
서열번호 254-257을 코딩하는 핵산을 EBV 복제 기점을 함유하는 CMV-기재 pCEP4 발현 벡터(Invitrogen)에 클로닝 하였다. 발현 벡터를 폴리에틸렌 이민 형질 전환제 (FuGENE® HD, Promega)를 사용하여 1μg 내 독소가없는 DNA/106 세포에서 엡스타인-바 바이러스(EBV)를 포함하는 인간 배아 신장 293세포주(HEK-293)에 형질 감염시켰다. 세포를 25 μg/ml Hygromycin B (Thermo Fischer Scientific) 및 0.1 % Pluronic® F68(Thermo Fischer Scientific)이 보충된 FREESTYLE ™ 293 발현 배지(Invitrogen, Carlsbad, CA)에서 6-7 일 동안 배양 하였다. 세포 배양 상등액을 0.22 μM 필터를 사용하여 멸균하고 정제 할 때까지 4 ℃에서 보관했다.
항체는 단백질 A 칼럼과 크기 배제 크로마토그래피(SEC) 칼럼으로 순도를 정제하여 순도 95 %, 내 독소 농도 ≤ 1EU/mg을 산출했다. 항체를 최종 농도 5 mg/ml의 20 mM 히스티딘 및 5 % 수크로오스를 함유하는 멸균 완충액에 제형화 하였다. 농도는 분광 광도계 (Nanodrop 2000c; Thermo Fisher)로 측정 하였다. 손상되지 않은 항체의 생산은 표준 단백질 겔에서의 시각화에 의해 확인되었다.
B. 항체 표지
SnAP- 바디 변이체 1, SnAP- 바디 변이체 2 및 대조군 항체는 pHrodo™ Red SE(ThermoFisher Scientific, Waltham, MA)로 제조사의 지시에 따라 표지하였다. pHrodo™ 염료는 pH에 민감하다; 이의 형광도는 pH가 감소하면서 증가한다. 따라서, pHrodo™-표지된 항체의 형광도의 정량은 항체 엔도시토시스의 비율을 나타낸다. 간략하게, pHrodo™을 2-5 μM의 염료의 최종 농도를 달성하도록 건조 디메틸설폭시드(DMSO)(Invitrogen) 중에 제조하였다. 2mg의 항체를 2mL의 인산 완충 식염수(PBS), pH 9에 용해하였다. 그 후, 형광 프로브를 4번의 50㎕ 증가량으로 항체 용액에 서서히 첨가하고 실온에서 흔들어주면서 각 첨가물과 15분간 인큐베이션하였다.
C. 형광 현미경법
CD33을 발현하는 HL-60 세포를 항체를 첨가하기 전에 얼음으로 배양 하였다. SnAP 바디 변형 1, SnAP 바디 변형 2, 또는 컨트롤 항체를 형광 현미경법을 위해 염색하여 pHrodo™-표지된 항체의 수용체 매개 엔도시토시스 속도를 결정하였다. 표지 된 세포를 37 ℃의 수조에서 15 분 동안 배양 하였다. 세포를 빙냉 완충액(1 % BSA가 보충된 PBS)으로 세척하고, 완충액 100μl에 재현탁시키고 4 % 파라 포름 알데히드 100μl를 가하여 고정시켰다. 그런 다음 세포를 Nunc® Lab-Tek® II 챔버 슬라이드 시스템에 슬라이드 당 8 개의 웰 (0.7 cm2 / 웰)을 사용하여 영상화 하였다. 이어서, 슬라이드를 플루오로마운트(Fluoromount) G (Southern Biotechnology, Birmingham, AL)에 고정하였다.
도 7a에 나타낸 바와 같이, 세포를 pHrodo™-표지된 항체에 적합한 파장 설정을 이용하여 공초점 현미경으로 영상화하였다. Z 절편은 내재화된 물질의 가시화를 허용하고 모든 정량적 측정은 정해진 동일한 절편 높이에서 이루어졌다. 30 개 이상의 세포가 각 영상화에 대해 3 개의 초점 필드로 각 시점에서 영상화되고 정량화되었다. 영상화된 세포(n=9)의 각 염색의 총 형광도를 이미지J 분석을 이용하여 계산하고, 각 조건에 대해 평균을 취하여 대조군에 대해 표준화하였다. SnAP- 바디 변이체 1의 총 염색은 대조군보다 2.5 배 이상 높았다. 도 7b에 나타낸 바와 같이, SnAP-바디 변이체 2에 대한 총 염색은 대조군보다 2.0 배 이상 크다. 결과는 HL-60 세포가 비 가교결합 항체의 2 배 이상의 속도로 자가-가교결합 SnAP 개체를 내재화하였다는 것을 나타낸다.
실시예 4. 메디토프 융합 항체 가교결합을 사용하여 항체 내재화 증가
CD33을 발현하는 HL-60 세포를 항체를 첨가하기 전에 얼음으로 배양 하였다.항체의 수용체 매개-엔도시토시스 비율을 결정하기 위해, 실시예 1에 기술 된 바와 같이, pHrodoTM-표지된 SnAP-바디 변이체 1, SnAP- 바디 변이체 2 또는 대조군 항체를 사용하여 유동 세포 계측 분석을 위해 세포를 염색 하였다. 표지된 세포를 37 ℃의 수조에서 15 분 동안 배양 하였다. 세포를 빙냉 완충액 (1 % BSA가 보충 된 PBS)으로 세척하고 100㎕ 완충액에 재현탁시켰다.
CytoFLEX 유동 세포 계측기(Becton Dickinson)를 사용하여 세포를 분석하고 FloJo, 버전 9를 사용하여 히스토그램으로 분석 하였다. 자가-가교결합 항체(SnAP 바디 변이체 1 및 2)에 대한 데이터는 대조군과 비교하여 증가된 강도를 갖는 추가 피크를 나타내며, 이는 HL-60 세포가 대조군에 비해 증가된 속도로 자가-가교결합 항체를 내재화한다는 것을 나타낸다(도 8).
실시예 5. 메디토프-항체 융합체를 이용한 항체 가교결합의 증가
포유류 발현 시스템에서 4 가지 항체를 생산하였다. 각각의 항체는 서열번호 254로 개시되는 아미노산 서열을 포함하는 메디토프-이용가능 젬투주맙 경쇄를 포함한다. 실시예 1에 개시된 바와 같이 SnAP-바디 변이체 1 및 2를 제조 하였다. SnAP-바디 변이체 3은 링커(서열번호 279)를 통해 메디토프에 연결되는 메디토프-이용가능 젬투주맙 IgG1 중쇄 서열을 포함하는 중쇄를 갖는다. 대조군 항체는 메디토프-이용가능 젬투주맙 IgG1 중쇄 아미노산 서열 (서열 번호 : 257)을 가지지만 메디토프 또는 N-터미너스에 융합된 링커는 없다. 서열은 발현 벡터로 클로닝되고 실시예 1에 개시된 바와 같이 발현된다.
이어서 항체를 정제하고 Sepax 기술의 SRT-10C SEC 컬럼을 사용하여 크기 배제 크로마토그래피로 분석했다. 컬럼은 친수성 및 중성 나노미터 두께의 필름으로 코팅된 5-10μm 실리카 입자를 함유하고 있다. 입자는 또한 100A의 기공을 함유하고 있다. 컬럼을 먼저 히스티딘 - 수크로오스 완충액 (히스티딘 20mM pH6, 수크로스 5 %)로 평형화시켰다. 샘플을 로드하고 동일 완충액에서 1 ㎖/분으로 용출시켰다. 크로마토그램은 UV 검출기를 280nM으로 설정하여 기록 하였다.
데이터는 젬투주맙 대조군 항체가 단일 단량체 피크로서 용출(도 9A)되는 반면, 자가-가교결합 SnAP-바디 변이체 1, 2 및 3은 작은 초기 피크에 의해 입증되는 바와 같이 이량체 및 다량체를 형성 할 수 있음을 보여준다(각각도 9b-9d).
실시예 6. 항체 자가-가교결합은 농도 의존적일 수 있다.
실시예 1의 SnAP-바디 변이체 1, SnAP-바디 변이체 2 및 대조군 젬투주맙 항체는 각각 인산염 완충 식염수 용액에서 1nM 및 100nM 샘플로 제조 하였다. PBS는 137 nM의 NaCl, 2.7 mM의 KCl, 10 mM의 Na2HPO4 및 1.8 mM의 KH2PO4를 함유 하였다. 각각의 샘플을 62.5 mM TrisHCl, pH 6.8, 25 % 글리세롤 및 1 % 브로모 페놀 블루로 제조된 2 x 샘플 버퍼와 혼합 하였다. 샘플을 실행 버퍼 (50 MM BisTris, 50 MM Tricine, pH 6.8)가 들어있는 겔 전기영동 챔버에서 폴리아크릴아마이드 겔(3-12 % 폴리아크릴아마이드 그래디언트 네이티브페이지(® 비스-트리스 겔 (Thermo Fisher))에 넣었다. 겔은 일정한 150V에서 90-115 분 동안 작동시켰다. 겔을 제조자의 지시에 따라 Thermo Scientific (cat # 24612)의 피어스 실버 스테이닝 키트로 염색 하였다.
그 결과 자가-가교결합 항체는 농도 의존적으로 이량체, 삼량체 및 사량체를 포함하는 다량체를 형성함을 보였다(도 10). 대조군 젬투주맙 항체는 단지 단량체를 형성하고 자가-가교결합을 일으키지 않았다.
실시예 7. 항체 자가-가교결합은 자유-메디토프 펩타이드에 의해 조절 될 수 있다.
실시예 1 및 3의 SnAP-바디 변이체 1, SnAP-바디 변이체 2, SnAP-바디 변이체 3 및 대조군 젬투주맙 항체 각각을 100nM 샘플로 인산 완충 식염수 용액으로 제조 하였다. 다음으로, 자유 메디토프(cQFD, 서열 번호 1)를 1μM의 최종 농도로 샘플 중 하나에 첨가하고 30 분 동안 배양했다. 각각의 샘플을 62.5 mM TrisHCl, pH 6.8, 25 % 글리세롤 및 1 % 브로모페놀 블루로 제조된 2x 샘플 버퍼와 혼합 하였다. 샘플을 실행 버퍼 (50 MM BisTris, 50 MM Tricine, pH 6.8)가 들어있는 겔 전기 영동 챔버에서 폴리아크릴아마이드 겔 (3-12 % polyacrylamide gradient NativePAGE® Bis-Tris Gels (Thermo Fisher))에 넣었다. 겔은 일정한 150V에서 90-115 분 동안 작동시켰다. 겔을 제조자의 지시에 따라 Thermo Scientific (cat # 24612)의 Pierce silver staining kit로 염색 하였다.
그 결과는 자유 메디토프가 자가-가교결합 항체의 자가-가교결합 능력을 방해할 수 있음을 보여준다. SnAP- 바디 변이체 1, 2 및 3 각각은 자유 메디토프의 부재하에 이량체, 삼량체 및 사량체를 형성하는 능력을 나타낸다(도 11). 그러나, 자유 메디토프가 과량 추가되었을 때는 검출할 수 있는 다량체가 거의 또는 전혀 존재하지 않는다.
실시예 8. 누드 마우스의 난소 이종 이식 모델에서 SnAP-바디의 효능
본 실시예는 생물 발광 영상과 전통적인 종양 캘리퍼스 측정을 사용하여 HER2 발현 SK-OV-3-Luc 난소 이식편 피하 모델에 대한 ADC 구조의 효능을 평가하기 위해 수행하였다. 생후 4 주령의 흉선이 제거된 누드 마우스(athymic nudes)를 찰스 리버 (Charles River)에서 65마리 구입하였다. SK-OV-3-Luc 세포는 표준 조직 배양 기술을 사용하여 확장시켰다. 이식 당일에, 30 % 마트리글 (matrigel)을 갖는 불완전 배지에서 2.5x106 세포를 각 마우스의 우측 하부(right lower flank)에 이식 하였다. 동물을 10 일 째에 총 플럭스 (Perkin Elmer IVIS Lumina XRMS II)에 기초한 치료를 위해 8 마리의 마우스를 7 개 그룹으로 계층화 하였다. 종양 측정과 함께 주 2 회 동물의 무게를 측정했다. Bioluminescent 영상은 일주일에 한 번 수행하였다. 종양 질량은 다음 공식을 사용하여 계산되었다:
질량(mg)= 종양 부피(mm3)= d2xD/2, 여기에서 d와 D는 각각 가장 짧은 직경과 가장 긴 직경 (mm)이다.
동물을 하기 표에 따라 처리 하였다(BIW: 주2회, QW: 주 1 회, DM1: 메르탄신, MMAD : 모노메틸 아우리스타틴(Monomethyl auristatin) D, ADC : 항체 약물 접합체(antibody-drug conjugate)).
MBI Her2 Snap바디의 서열은 서열번호 303 및 304로 제공된다. MBI Her2 항체의 경쇄 및 중쇄는 Snap바디와 동일하지만 Her2 항체는 메디토프 및 링커 서열을 포함하지 않는다(실시예 2의 설명 참조). 결과를 도 1에 나타내었다. 종양은 10 일 째에 생체 발광 (bioluminescence)에 의해 검출 가능 하였다. 비히클 군의 종양 양은 연구가 끝날 때까지 계속 증가했다. 66 일 pi에서 비히클 군과 비교했을 때, 2 군(G2, 트라스트주맙 9mg/kg으로 치료)의 HER2 발현 종양은 완전한 회귀를 보였다. 캐싸일라(maytansinoid 독소에 접합된 트라스투주맙)는 3 mg/kg에서 효능을 보였다. 모든 ADC 및 Snap-바디 치료 그룹은 종양 성장 감소 또는 억제를 나타냈다. 종양은 초기에 파클리탁셀 (20 mg/kg)에 반응하였으나, 전반적으로 최소 (2.80 % TGI, 52 일 pi) 저해를 보였다. 대부분의 동물은 연구 전반에 걸쳐 각 치료에 악영향을 주지 않았으며 모든 그룹의 체중은 연구가 끝날 때까지 계속 증가했다 (도 13).
이 연구는 HER2 발현 난소 이종이식 피하 모델에 대한 ADC 구조의 효능을 증명한다. 개별 항체 및 ADC는 예상된 효능을 나타내었다. 모든 MBI ADC 및 Snap-바디 치료 그룹은 종양성장 감소 또는 억제를 나타냈다. 캐싸일라(전통적인 ADC 접합)와 MBI DM1 접합 ADC는 SnAP-바디 기술이 항체의 활성을 유지한다는 것을 입증하는 유사한 결과를 나타냈다.
본 발명은 예를 들어 본 발명의 다양한 양태를 설명하기 위해 제공되는 특정 개시된 실시예에 대한 범위를 제한하려는 의도는 아니다. 기술된 조성물 및 방법에 대한 다양한 변형은 본원의 설명 및 교시로부터 명백해질 것이다. 이러한 변형은 본 개시물의 진정한 범위 및 사상을 벗어나지 않고 실시 될 수 있고 본 개시물의 범위 내에 포함되도록 의도된다.