KR20180098402A - 전기 자극에 의한 혈소판의 칼슘 제어 활성화 - Google Patents
전기 자극에 의한 혈소판의 칼슘 제어 활성화 Download PDFInfo
- Publication number
- KR20180098402A KR20180098402A KR1020187022044A KR20187022044A KR20180098402A KR 20180098402 A KR20180098402 A KR 20180098402A KR 1020187022044 A KR1020187022044 A KR 1020187022044A KR 20187022044 A KR20187022044 A KR 20187022044A KR 20180098402 A KR20180098402 A KR 20180098402A
- Authority
- KR
- South Korea
- Prior art keywords
- sample
- prp
- calcium ion
- calcium
- platelet
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K41/00—Medicinal preparations obtained by treating materials with wave energy or particle radiation ; Therapies using these preparations
- A61K41/0004—Homeopathy; Vitalisation; Resonance; Dynamisation, e.g. esoteric applications; Oxygenation of blood
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N13/00—Treatment of microorganisms or enzymes with electrical or wave energy, e.g. magnetism, sonic waves
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/14—Blood; Artificial blood
- A61K35/19—Platelets; Megacaryocytes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/18—Growth factors; Growth regulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K41/00—Medicinal preparations obtained by treating materials with wave energy or particle radiation ; Therapies using these preparations
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
- C12N5/0644—Platelets; Megakaryocytes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/56—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving blood clotting factors, e.g. involving thrombin, thromboplastin, fibrinogen
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/15—Medicinal preparations ; Physical properties thereof, e.g. dissolubility
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/86—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving blood coagulating time or factors, or their receptors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K33/00—Medicinal preparations containing inorganic active ingredients
- A61K33/06—Aluminium, calcium or magnesium; Compounds thereof, e.g. clay
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Zoology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Hematology (AREA)
- Biomedical Technology (AREA)
- Immunology (AREA)
- Medicinal Chemistry (AREA)
- Organic Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Biotechnology (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Wood Science & Technology (AREA)
- Epidemiology (AREA)
- Genetics & Genomics (AREA)
- Biochemistry (AREA)
- Microbiology (AREA)
- Cell Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- General Engineering & Computer Science (AREA)
- Gastroenterology & Hepatology (AREA)
- Molecular Biology (AREA)
- Developmental Biology & Embryology (AREA)
- Virology (AREA)
- Analytical Chemistry (AREA)
- Physics & Mathematics (AREA)
- Food Science & Technology (AREA)
- General Physics & Mathematics (AREA)
- Biophysics (AREA)
- Urology & Nephrology (AREA)
- Pathology (AREA)
- Alternative & Traditional Medicine (AREA)
- Dermatology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
Abstract
Description
도 1은 본 발명의 양태들에 따른 펄스 생성 시스템의 개략도이다.
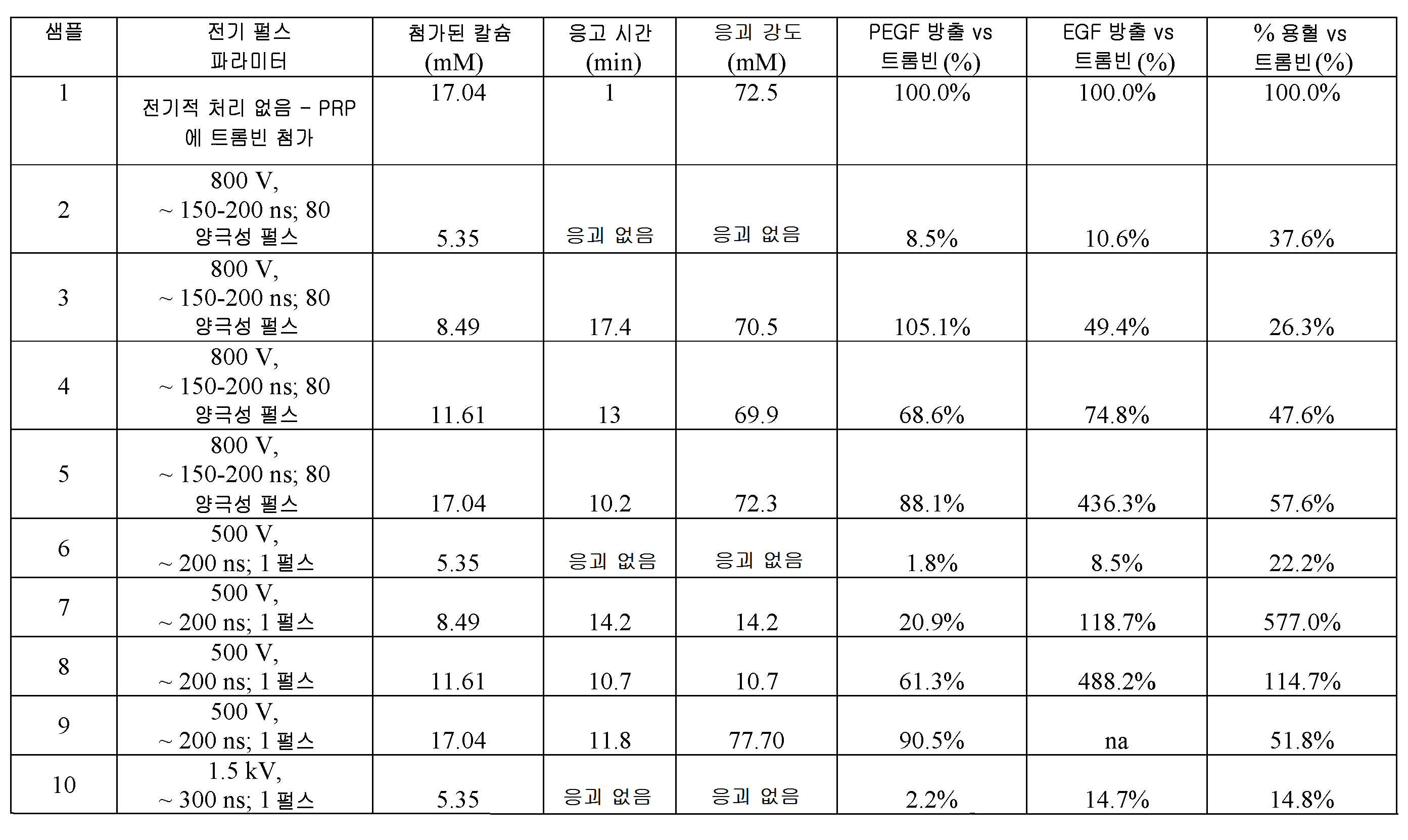
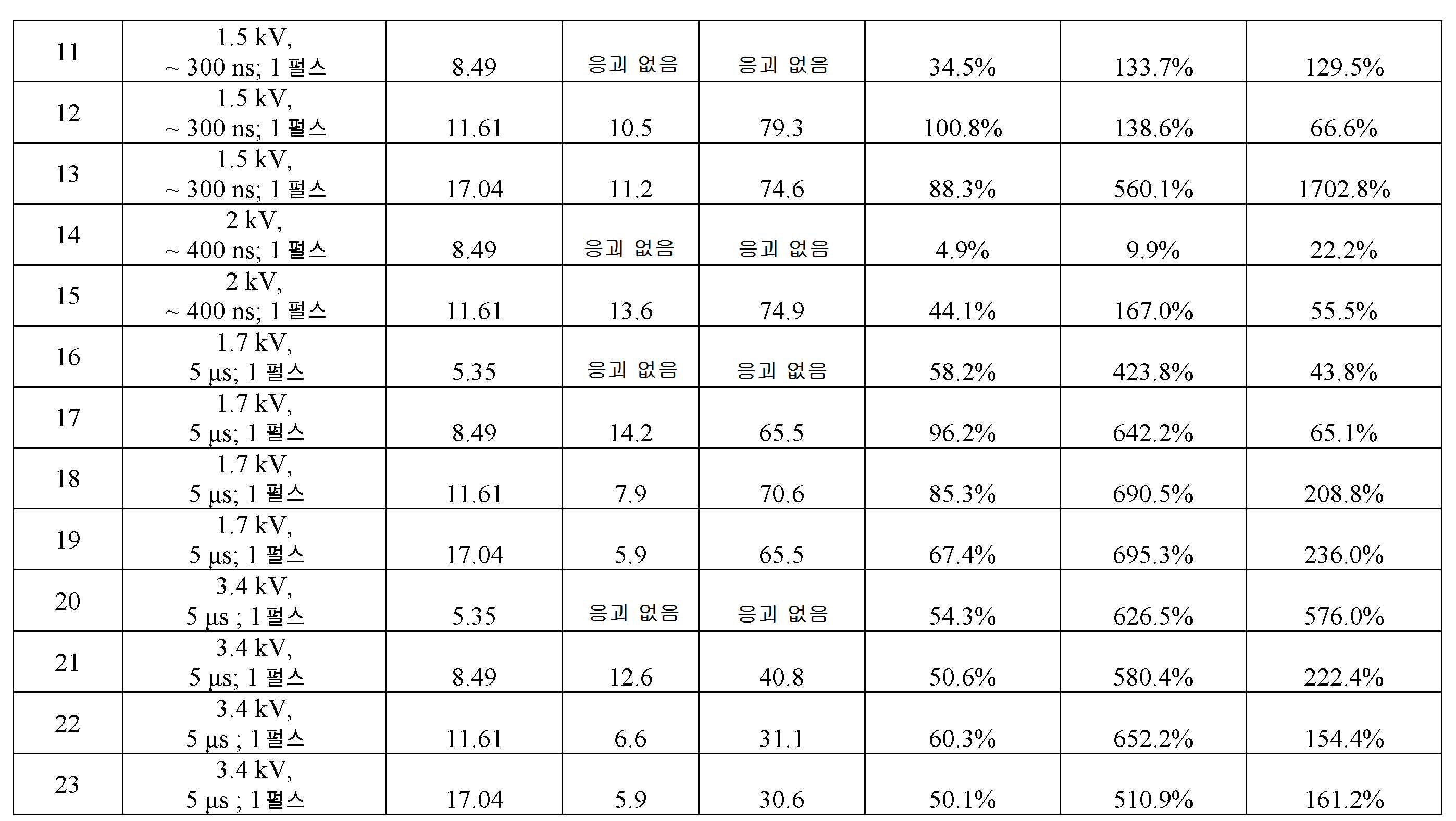
도 2는, 본 발명의 양태들에 따른, 연구 결과의 세트에 대한 초기 응괴 형성까지의 시간(응고 시간)을 그래프로 도시한다.
도 3은, 본 발명의 양태들에 따른, 연구 결과의 세트에 대한 응고 키네틱(응고 속도)을 그래프로 도시한다.
도 4는, 본 발명의 양태들에 따른, 연구 결과의 세트에 대한 피브리노겐 수준을 그래프로 도시한다.
도 5는, 본 발명의 양태들에 따른, 연구 결과의 세트에 대한 응괴 강도를 그래프로 도시한다.
도 6은, 본 발명의 양태들에 따른, 한 연구 참여자에 대한 시간에 따라 관찰한 응괴의 기계적 강도(MA)를 보여주는 대표적인 TEG 트레이싱을 도시한다.
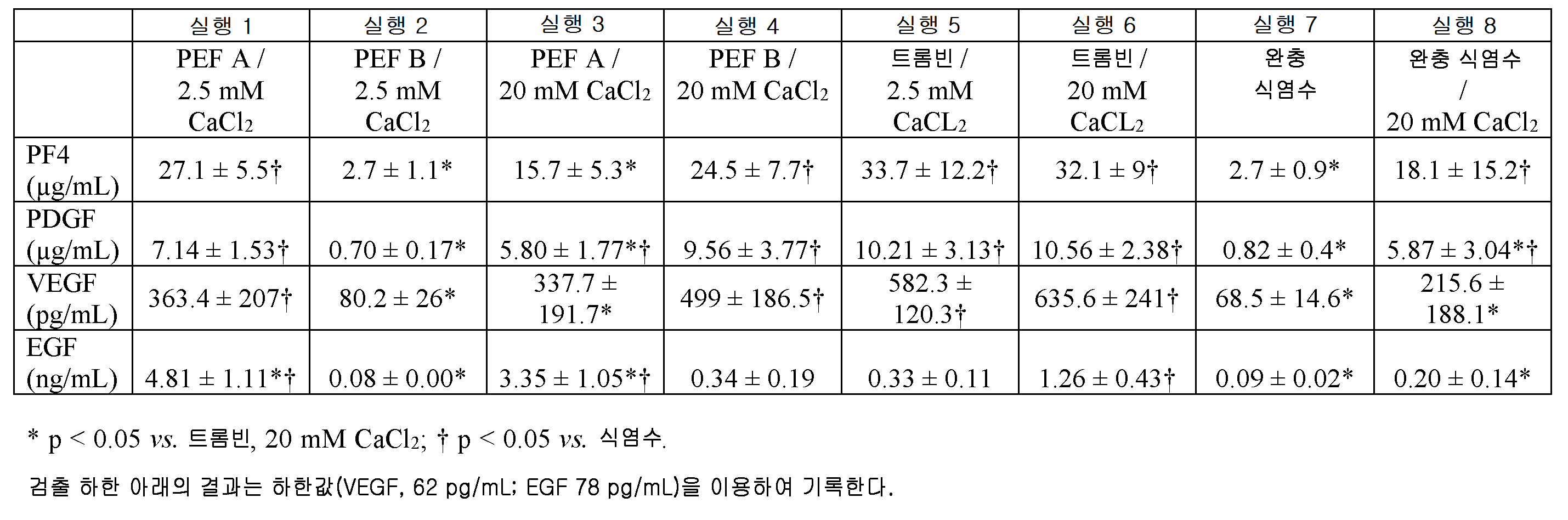
도 7은, 본 발명의 양태들에 따른, 연구 결과의 세트에 대한 PF4 수준을 그래프로 도시한다.
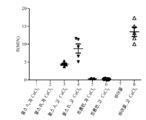
도 8은, 본 발명의 양태들에 따른, 연구 결과의 세트에 대한 PDGF 수준을 그래프로 도시한다.
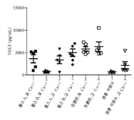
도 9는, 본 발명의 양태들에 따른, 연구 결과의 세트에 대한 VEGF 수준을 그래프로 도시한다.
도 10은, 본 발명의 양태들에 따른, 연구 결과의 세트에 대한 EGF 수준을 도시한다.
Claims (20)
- 활성화를 위해 혈소판 농축 혈장(platelet-rich plasma; PRP) 샘플을 제조하는 단계로서, 상기 PRP 샘플은, 칼슘 이온을 각각의 농도로 첨가함으로써 제조하고, 상기 각각의 농도는, PRP 샘플을 사용하여 생성한 활성화된 생성물 조성물 중에 응괴가 존재해야 하는지 여부와, 응고가 존재해야 한다면, 응괴 형성까지의 시간 또는 응괴의 기계적 강도 중 하나 이상을 기초로 선택되는 것인 단계;
전자기 자극 장치의 전극에 대해 PRP 샘플을 위치시키는 단계;
전기 펄스 파라미터의 세트를 지정하는 단계; 및
파라미터 값에 따라 생성된 하나 이상의 전기 펄스에 상기 PRP 샘플을 노출시키는 단계로서, 상기 PRP 샘플은, 하나 이상의 전기 펄스에 노출될 경우, 1종 이상의 성장 인자를 포함하며 지정된 응고 특성을 갖는 활성화된 생성물 조성물을 산출하는 것인 단계
를 포함하는, 활성화된 생성물을 생성하는 방법. - 제1항에 있어서, 상기 전기 펄스 파라미터의 세트는, 적어도 부분적으로, 선택된 칼슘 이온 농도를 기초로 선택되는 것인 방법.
- 제1항에 있어서, 전기 펄스 파라미터는 동일하지만 칼슘 이온 농도는 상이한 것이, 활성화된 생성물 조성물에서 상이한 응고 특성을 산출하는 것인 방법.
- 제1항에 있어서, 상기 샘플이 혈소판 농축 혈장 샘플, 혈소판 현탁액, 또는 전혈 샘플 중 하나를 포함하는 것인 방법.
- 제1항에 있어서, 1종 이상의 성장 인자의 상대 수준은, 전기 펄스 파라미터의 세트 또는 첨가된 칼슘 이온 중 하나 또는 둘 다에 의해 결정되는 것인 방법.
- 제1항에 있어서, 전극 사이에 샘플을 위치시키는 것은, 전극 사이의 도관을 통해 샘플을 흘려 보내는 것을 포함하고, 상기 활성화된 생성물 조성물은, 도관 직경 또는 도관을 통한 샘플의 유량 중 하나 또는 둘 다에 의해 적어도 부분적으로 결정되는 하나 이상의 인자의 상대 수준을 갖는 것인 방법.
- 제1항에 있어서, 항응고제 처리된 PRP 샘플에 약 2.5 mM 내지 약 20 mM 범위의 농도로 CaCl2를 첨가하는 것을 포함하는 방법.
- 제1항에 있어서, 칼슘 이온의 농도는, 항응고제 처리된 PRP 샘플에 첨가되는 2.5 mM, 5.0 mM, 7.5 mM, 10 mM, 15 mM, 20 mM, 또는 25 mM CaCl2에 상응하는 복수의 가능한 농도로부터 선택되는 것인 방법.
- 제1항에 있어서, 제2 칼슘 이온 농도보다 낮은 제1 칼슘 농도는, 제2 칼슘 이온 농도에서 관찰되는 것보다 초기 응괴 형성을 늦추는 것인 방법.
- 제1항에 있어서, 제2 칼슘 이온 농도보다 낮은 제1 칼슘 농도는, 제2 칼슘 이온 농도에서 관찰되는 것보다 응괴의 기계적 강도를 감소시키는 것인 방법.
- 활성화를 위해, 항응고제 처리된 혈소판 농축 혈장(PRP) 샘플을 제조하는 단계;
다양한 가능한 농도로부터 선택되는 칼슘 이온 농도에 도달하도록, PRP 샘플에 칼슘 이온을 첨가하는 단계로서, 상기 농도는, PRP 샘플을 사용하여 생성한 활성화된 생성물 조성물 중에 존재하는 1종 이상의 성장 인자의 목표 수준을 기초로 선택되는 것인 단계;
PRP 샘플을 전기적 활성화 자극에 노출시키는 단계로서, 상기 PRP 샘플은, 전기적 활성화 자극에 노출될 경우, 1종 이상의 성장 인자를 목표 수준으로 포함하는 활성화된 생성물 조성물을 산출하며, 전기적 활성화 자극을 변경하지 않고 칼슘 이온 농도를 변경하는 것이 1종 이상의 성장 인자의 절대 또는 상대 수준 중 하나 또는 둘 다를 변화시키는 것인 단계
를 포함하는, 활성화된 생성물을 생성하는 방법. - 제11항에 있어서, 하나 이상의 응고 특성이 또한 칼슘 이온 농도에 의해 결정되는 것인 방법.
- 제11항에 있어서, PRP 샘플에 칼슘 이온을 첨가하는 단계가, PRP 샘플에 약 2.5 mM 내지 약 20 mM 범위의 농도로 CaCl2를 첨가하는 것을 포함하는 것인 방법.
- 제11항에 있어서, 칼슘 이온의 농도는, PRP 샘플에 첨가되는 2.5 mM, 5.0 mM, 7.5 mM, 10 mM, 15 mM, 20 mM, 또는 25 mM CaCl2에 상응하는 복수의 가능한 농도로부터 선택되는 것인 방법.
- 제11항에 있어서, 제2 칼슘 이온 농도보다 낮은 제1 칼슘 농도는, 제2 칼슘 이온 농도에서 관찰되는 것보다 초기 응괴 형성을 빠르게 하는 것인 방법.
- 제11항에 있어서, 제2 칼슘 이온 농도보다 낮은 제1 칼슘 농도는, 제2 칼슘 이온 농도에서 관찰되는 것보다 응괴의 기계적 강도를 감소시키는 것인 방법.
- 혈소판 겔에서 생성되는 하나 이상의 응괴의 잠재적 기계적 강도를 결정하는 단계로서, 잠재적 기계적 강도는 트롬빈만을 사용하여 혈소판 겔을 생성함으로써 관찰되어지는 강도보다 큰 것인 단계;
잠재적 기계적 강도를 기초로, 복수의 칼슘 이온 농도 중에서 잠재적 기계적 강도에 상응하는 칼슘 이온 농도를 선택하는 단계;
선택된 칼슘 이온 농도로 칼슘 이온을 포함하는 혈소판 농축 혈장(PRP) 샘플을 활성화시킴으로써 혈소판 겔을 생성하는 단계로서, PRP 샘플은 전기 자극을 이용하여 활성화시키고, 혈소판 겔은, 형성되면, 잠재적 기계적 강도를 갖는 응괴를 포함하는 것인 단계
를 포함하는, 혈소판 겔의 응괴의 기계적 강도를 제어하는 방법. - 제17항에 있어서, 복수의 칼슘 이온 농도에 있어서, 더 높은 칼슘 이온 농도가 응괴의 더 큰 기계적 강도에 상응하는 것인 방법.
- 제17항에 있어서, 복수의 칼슘 이온 농도는, PRP 샘플에 약 2.5 mM 내지 약 20 mM의 CaCl2를 첨가함으로써 생성된 것에 상응하는 범위 내에 있는 것인 방법.
- 제17항에 있어서, 칼슘 이온 농도는, PRP 샘플에 첨가되는 2.5 mM, 5.0 mM, 7.5 mM, 10 mM, 15 mM, 20 mM, 또는 25 mM CaCl2에 상응하는 복수의 가능한 농도로부터 선택되는 것인 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US14/984,988 | 2015-12-30 | ||
| US14/984,988 US10633645B2 (en) | 2015-12-30 | 2015-12-30 | Calcium controlled activation of platelets via electrical stimulation |
| PCT/US2016/069197 WO2017117385A2 (en) | 2015-12-30 | 2016-12-29 | Calcium controlled activation of platelets via electrical stimulation |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20180098402A true KR20180098402A (ko) | 2018-09-03 |
| KR102722475B1 KR102722475B1 (ko) | 2024-10-25 |
Family
ID=57868356
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020187022044A Active KR102722475B1 (ko) | 2015-12-30 | 2016-12-29 | 전기 자극에 의한 혈소판의 칼슘 제어 활성화 |
Country Status (10)
| Country | Link |
|---|---|
| US (2) | US10633645B2 (ko) |
| EP (2) | EP3397268B1 (ko) |
| JP (1) | JP7050680B2 (ko) |
| KR (1) | KR102722475B1 (ko) |
| CN (2) | CN108697763B (ko) |
| AU (1) | AU2016380342B2 (ko) |
| BR (1) | BR112018013444A2 (ko) |
| MX (1) | MX392919B (ko) |
| RU (1) | RU2742937C2 (ko) |
| WO (1) | WO2017117385A2 (ko) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2021137358A1 (ko) * | 2020-01-02 | 2021-07-08 | 주식회사 엠엔 | 펄스 미세 전자기장 방식의 키성장 보조장치 및 그 장치의 구동방법 |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10968423B2 (en) | 2018-02-26 | 2021-04-06 | General Electric Company | System and method for electric pulse based activation of biological samples |
| TW202527970A (zh) * | 2024-01-05 | 2025-07-16 | 艾瑞生醫股份有限公司 | 以人類血小板製備外泌體的方法 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015108778A1 (en) * | 2014-01-17 | 2015-07-23 | General Electric Company | Platelet activation and growth factor release using electric pulses |
| WO2015168015A1 (en) | 2014-04-28 | 2015-11-05 | T2 Biosystems, Inc. | Systems and methods for identifying coagulopathies |
Family Cites Families (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP3180824B2 (ja) * | 1991-08-30 | 2001-06-25 | シスメックス株式会社 | 血液凝固試薬 |
| US5293772A (en) * | 1992-01-17 | 1994-03-15 | Center For Innovative Technology | Instrumentation and method for evaluating platelet performance during clotting and dissolution of blood clots and for evaluating erythrocyte flexibility |
| US6322785B1 (en) | 1999-03-02 | 2001-11-27 | Natrex Technologies | Methods and compositions for bone graft implants |
| US6326711B1 (en) | 1999-09-07 | 2001-12-04 | Tokyo Parts Industrial Co., Ltd. | DC brushless motor having eccentric rotor |
| DK1504269T3 (da) * | 2002-05-01 | 2007-12-03 | Synapse Bv | Diagnostisk test til bestemmelse af koncentrationen af forbigående proteolytisk aktivitet i sammensatte biologiske medier |
| US7565201B2 (en) | 2004-12-17 | 2009-07-21 | Eastern Virginia Medical School | Activation of calcium-mediated cell functions in cells and tissues, including aggregation of human platelets. by nanosecond pulsed electric fields |
| WO2006110393A1 (en) * | 2005-04-04 | 2006-10-19 | The Regents Of The University Of California | Inorganic materials for hemostatic modulation and therapeutic wound healing |
| EP1717588A1 (en) * | 2005-04-29 | 2006-11-02 | Synapse B.V. | Measuring thrombin activity in whole blood |
| US7837941B2 (en) * | 2006-04-07 | 2010-11-23 | Agamatrix, Inc. | Method and apparatus for monitoring alteration of flow characteristics in a liquid sample |
| US8034014B2 (en) | 2007-03-06 | 2011-10-11 | Biomet Biologics, Llc | Angiogenesis initation and growth |
| WO2010042658A1 (en) | 2008-10-07 | 2010-04-15 | Bioparadox, Llc | Use of platelet rich plasma composition in the treatment of cardiac conduction abnormalities |
| EP2364155B1 (en) | 2008-11-13 | 2017-06-28 | Eastern Virginia Medical School | Activation and aggregation of human platelets and formation of platelet gels by nanosecond pulsed electric fields |
| KR101114712B1 (ko) * | 2009-10-23 | 2012-02-29 | 세원셀론텍(주) | 염화칼슘용액과 제1형 콜라겐으로 혈소판풍부혈장(prp)을 활성화하여 조직재생을 유도하는 조성물의 제조방법 |
| EP2389942B1 (en) * | 2010-05-25 | 2013-01-23 | GwoWei Technology Co., Ltd. | Virally-inactivated growth factors-containing platelet lysate depleted of PDGF and VEGF and preparation method thereof |
| US9314609B2 (en) | 2011-10-28 | 2016-04-19 | Martin Brown | Device for providing electrical stimulation of a human knee |
| CN103110947A (zh) * | 2011-11-16 | 2013-05-22 | 玛旺干细胞医学生物科技股份有限公司 | 用以活化血小板的添加剂 |
| US10493134B2 (en) * | 2013-03-21 | 2019-12-03 | Collplant Ltd. | Compositions comprising collagen and PRP for tissue regeneration |
| US9078862B2 (en) | 2013-06-06 | 2015-07-14 | General Electric Company | Platelet activation using long electric field pulses |
| US9238808B2 (en) | 2013-06-06 | 2016-01-19 | General Electric Company | Modular adjustable pulse generator |
| US9708597B2 (en) | 2014-01-17 | 2017-07-18 | General Electric Company | Electric pulse generation systems using capacitive coupling |
| EP3107590B1 (en) | 2014-02-20 | 2021-11-17 | Ortho Regenerative Technologies Inc. | Freeze-dried polymer compositions for mixing with platelet rich plasma to form implants for tissue repair and/or compositions for therapeutic intra-articular injections |
| US9752120B2 (en) | 2015-03-31 | 2017-09-05 | General Electric Company | Activated platelet composition with tunable growth factor level |
-
2015
- 2015-12-30 US US14/984,988 patent/US10633645B2/en active Active
-
2016
- 2016-12-29 BR BR112018013444-9A patent/BR112018013444A2/pt not_active Application Discontinuation
- 2016-12-29 MX MX2018008146A patent/MX392919B/es unknown
- 2016-12-29 RU RU2018121952A patent/RU2742937C2/ru active
- 2016-12-29 EP EP16829375.1A patent/EP3397268B1/en active Active
- 2016-12-29 WO PCT/US2016/069197 patent/WO2017117385A2/en not_active Ceased
- 2016-12-29 CN CN201680082886.6A patent/CN108697763B/zh active Active
- 2016-12-29 KR KR1020187022044A patent/KR102722475B1/ko active Active
- 2016-12-29 JP JP2018533697A patent/JP7050680B2/ja active Active
- 2016-12-29 CN CN202211454001.4A patent/CN115873793A/zh active Pending
- 2016-12-29 AU AU2016380342A patent/AU2016380342B2/en active Active
- 2016-12-29 EP EP20184433.9A patent/EP3738604B1/en active Active
-
2020
- 2020-04-16 US US16/850,727 patent/US11591590B2/en active Active
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015108778A1 (en) * | 2014-01-17 | 2015-07-23 | General Electric Company | Platelet activation and growth factor release using electric pulses |
| WO2015168015A1 (en) | 2014-04-28 | 2015-11-05 | T2 Biosystems, Inc. | Systems and methods for identifying coagulopathies |
Non-Patent Citations (1)
| Title |
|---|
| ZHANG et al., Archives of Biochemistry and Biophysics, Academic Press, 2007, 471, 240-248. * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2021137358A1 (ko) * | 2020-01-02 | 2021-07-08 | 주식회사 엠엔 | 펄스 미세 전자기장 방식의 키성장 보조장치 및 그 장치의 구동방법 |
Also Published As
| Publication number | Publication date |
|---|---|
| RU2018121952A (ru) | 2020-01-30 |
| EP3738604A3 (en) | 2021-01-13 |
| US20200239868A1 (en) | 2020-07-30 |
| RU2742937C2 (ru) | 2021-02-11 |
| US11591590B2 (en) | 2023-02-28 |
| EP3738604A2 (en) | 2020-11-18 |
| US10633645B2 (en) | 2020-04-28 |
| KR102722475B1 (ko) | 2024-10-25 |
| AU2016380342B2 (en) | 2023-04-13 |
| MX2018008146A (es) | 2018-12-06 |
| MX392919B (es) | 2025-03-24 |
| WO2017117385A2 (en) | 2017-07-06 |
| CN108697763B (zh) | 2022-12-09 |
| BR112018013444A2 (pt) | 2019-02-12 |
| CA3009523A1 (en) | 2017-07-06 |
| WO2017117385A3 (en) | 2017-08-10 |
| CN108697763A (zh) | 2018-10-23 |
| RU2018121952A3 (ko) | 2020-04-08 |
| JP2019501911A (ja) | 2019-01-24 |
| EP3397268A2 (en) | 2018-11-07 |
| CN115873793A (zh) | 2023-03-31 |
| EP3738604B1 (en) | 2023-09-13 |
| EP3397268B1 (en) | 2020-07-08 |
| JP7050680B2 (ja) | 2022-04-08 |
| AU2016380342A1 (en) | 2018-07-12 |
| US20170191052A1 (en) | 2017-07-06 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| AU2020207831B2 (en) | Platelet activation and growth factor release using electric pulses | |
| US11591590B2 (en) | Calcium controlled activation of platelets via electrical stimulation | |
| JP2013536841A (ja) | インターロイキン−1受容体アンタゴニストを送達するための方法および組成物 | |
| JP2014012703A (ja) | インターロイキン−1受容体アンタゴニストを送達するための方法および組成物 | |
| JP2013503182A (ja) | 骨溶解治療 | |
| CA3009523C (en) | Calcium controlled activation of platelets via electrical stimulation | |
| US20160289664A1 (en) | Activated platelet composition with tunable growth factor level | |
| KR102516995B1 (ko) | 조정가능한 성장 인자 레벨을 가진 활성화된 혈소판 조성 | |
| RU2790831C2 (ru) | Способ получения гемостатического состава | |
| JP7248721B2 (ja) | 成長因子レベルを調節可能な活性化血小板組成物 | |
| Caloprisco et al. | New method to produce hemocomponents for regenerative use from peripheral blood: Integration among platelet growth factors monocytes and stem cells | |
| CA3018505C (en) | Activated platelet composition with tunable growth factor level | |
| Grewal et al. | Perioperative Fibrinogen Supplementation: Safety and Efficacy | |
| Siegemund et al. | Individual Therapy of Hemophilia—New Laboratory Methods Considering Platelets |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
St.27 status event code: A-0-1-A10-A15-nap-PA0105 |
|
| PG1501 | Laying open of application |
St.27 status event code: A-1-1-Q10-Q12-nap-PG1501 |
|
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| E13-X000 | Pre-grant limitation requested |
St.27 status event code: A-2-3-E10-E13-lim-X000 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
St.27 status event code: A-1-2-D10-D22-exm-PE0701 |
|
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment |
St.27 status event code: A-2-4-F10-F11-exm-PR0701 |
|
| PR1002 | Payment of registration fee |
St.27 status event code: A-2-2-U10-U12-oth-PR1002 Fee payment year number: 1 |
|
| PG1601 | Publication of registration |
St.27 status event code: A-4-4-Q10-Q13-nap-PG1601 |
|
| R18 | Changes to party contact information recorded |
Free format text: ST27 STATUS EVENT CODE: A-5-5-R10-R18-OTH-X000 (AS PROVIDED BY THE NATIONAL OFFICE) |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |