KR20170017996A - 암을 치료하고 암 약물 내성을 예방하는 방법 - Google Patents
암을 치료하고 암 약물 내성을 예방하는 방법 Download PDFInfo
- Publication number
- KR20170017996A KR20170017996A KR1020177000139A KR20177000139A KR20170017996A KR 20170017996 A KR20170017996 A KR 20170017996A KR 1020177000139 A KR1020177000139 A KR 1020177000139A KR 20177000139 A KR20177000139 A KR 20177000139A KR 20170017996 A KR20170017996 A KR 20170017996A
- Authority
- KR
- South Korea
- Prior art keywords
- cancer
- antagonist
- antibody
- therapy
- agent
- Prior art date
Links
- GPXBXXGIAQBQNI-UHFFFAOYSA-N CCCS(Nc(c(F)c1C(c(c2c3)c[nH]c2ncc3-c(cc2)ccc2Cl)=O)ccc1F)(=O)=O Chemical compound CCCS(Nc(c(F)c1C(c(c2c3)c[nH]c2ncc3-c(cc2)ccc2Cl)=O)ccc1F)(=O)=O GPXBXXGIAQBQNI-UHFFFAOYSA-N 0.000 description 1
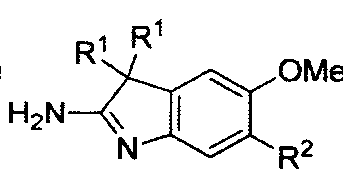
- 0 COc(c(*)c1)cc(C2(*)*)c1N=C2N Chemical compound COc(c(*)c1)cc(C2(*)*)c1N=C2N 0.000 description 1
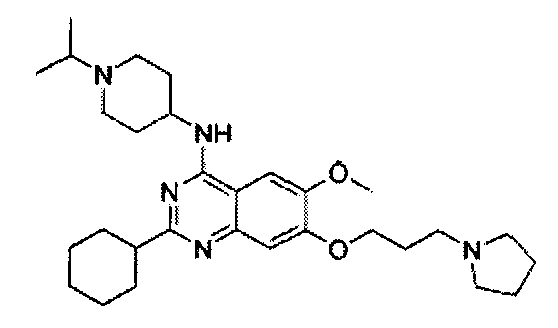
- BKCDJTRMYWSXMC-UHFFFAOYSA-N COc(cc(C1(CCC1)C(N)=N1)c1c1)c1OCCCN1CCCC1 Chemical compound COc(cc(C1(CCC1)C(N)=N1)c1c1)c1OCCCN1CCCC1 BKCDJTRMYWSXMC-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/337—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having four-membered rings, e.g. taxol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/403—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil condensed with carbocyclic rings, e.g. carbazole
- A61K31/404—Indoles, e.g. pindolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/4353—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems
- A61K31/437—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems the heterocyclic ring system containing a five-membered ring having nitrogen as a ring hetero atom, e.g. indolizine, beta-carboline
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/517—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with carbocyclic ring systems, e.g. quinazoline, perimidine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
G9a의 길항제를 사용하는 방법 (예를 들어 개체에서 암을 치료하고/하거나 약물 내성을 예방하기 위한) 방법이 본원에 제공된다. 예를 들어, 개체에서 암을 치료하는 방법은 G9a의 길항제 단독으로, 또는 암 요법 제제와 조합하여 상기 개체에게 투여하는 단계를 포함한다. 일부 구현예에서, G9a의 길항제는 암 민감도의 기간을 증가시키고/시키거나 암 내성의 진행을 지연시킨다.
Description
관련 출원(들)의 상호 참조
본원은 본원에 참고로 인용된 2014년 6월 23일 출원된 미국 출원 번호 제62/015,932호를 우선권으로 주장한다.
분야
본원에 기술된 G9a의 길항제를 사용하여 암 약물 내성을 치료 및/또는 예방하는 방법이 본원에 제공된다.
암 약물에 대한 내성의 상대적으로 빠른 획득은 성공적인 암 요법에 주요 장애물로 남아있다. 상기 약물 내성에 대한 분자 기반을 자세히 설명하고자 하는 실질적인 노력은 하기를 포함하는 다양한 기전을 드러냈다: 약물 방출, 표적의 약물 결합-결핍 돌연변이의 획득, 대안적인 생존 경로의 계합, 및 후성적 변경. 그러한 기전은 일반적으로 약물 치료 동안 선택된 종양 세포 집단 내의 드물고, 확률적이고, 내성-부여의 유전적 변경을 반영한다고 여겨졌다. 참고: Sharma et al., Cell 141(1):69-80 (2010). 암 요법 내의 증가 추세로 관찰된 현상은 소위 “재-치료 반응”이다. 예를 들어, 일부 비-소세포 폐암 (NSCLC) 환자 (EGFR (상피 성장 인자 수용체) 티로신 키나아제 억제제로의 치료에 잘 반응하고, 이후 요법 실패를 경험함)는 “약물-휴지기” 후 EGFR TKI 재-치료에 제2의 반응을 예증한다. 참고: Kurata et al., Ann. Oncol . 15:173-174 (2004); Yano et al., Oncol . Res. 15:107-111 (2005). 몇몇 기타 암 요법 제제에 대한 유사한 재-치료 반응은 잘 확립되어 있다. 참고: Cara and Tannock, Ann. Oncol . 12:23-27 (2001). 그러한 발건은, 암 약물에 대한 획득된 내성이, 가역적 “약물-내성” 상태를 포함할 수 있고, 이의 기전 기반이 확립될 필요가 아직 남아있다는 것을 시사한다.
일부 특정 내성-부여 돌연변이는, 획득된 약물 내성을 나타내는 많은 암 환자에서 식별되었고, 약물 내성에 대한 돌연변이성 및 비돌연변이성 기전 및 종양 세포 아집단의 역할은 다소 명확하지 않는 채로 남아있다. 암 세포 집단 내에 이종성 및 약물 치료에 대해 내성인 암 세포의 발생을 성공적으로 해결하는 새로운 치료 방법이 필요하다.
요약
G9a의 길항제를 사용하는 방법 (예를 들어 개체에서 암을 치료하고/하거나 약물 내성을 예방하기 위한) 방법이 본원에 제공된다. 예를 들어, 개체에서 암을 치료하는 방법은 G9a의 길항제 단독으로, 또는 암 요법 제제와 조합하여 상기 대상체에게 투여하는 단계를 포함한다. 일부 구현예에서, 상기 개체는 암 요법 제제에 의한 치료 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)을 위하여 선택된다. 일부 구현예에서, 상기 개체는 암 요법 제제에 의한 치료 전에 G9a의 길항제의 투여를 포함하는 치료를 개시한다. 일부 구현예에서, 상기 개체는 암 요법 제제 및 G9a의 길항제를 포함하는 치료를 동시에 수용한다. 일부 구현예에서, G9a의 길항제는 암 민감도의 기간을 증가시키고/시키거나 암 내성의 진행을 지연시킨다.
또한, G9a의 길항제 및 암 요법 제제를 사용하는 조합 요법 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)이 본원에 제공된다.
특히, 개체에서 암을 치료하는 방법으로서, 상기 개체에게 (a) G9a의 길항제 및 (b) 암 요법 제제를 투여하는 단계 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)를 포함하는 방법이 본원에 제공된다. 일부 구현예에서, G9a의 길항제 및 암 요법 제제의 각각의 양은 암 민감도의 기간을 증가시키고/시키거나 암 요법 제제에 대한 암 세포 내성의 진행을 지연시키는데 유효하다. 일부 구현예에서, G9a의 길항제 및 암 요법 제제의 각각의 양은 암 요법 제제를 포함하는 암 치료의 효능을 증가시키는데 유효하다. 예를 들어, 일부 구현예에서, G9a의 길항제 및 암 요법 제제의 각각의 양은 G9a의 길항제 없이 (이의 부재하에) 암 요법 제제의 유효량을 투여하는 것을 포함하는 치료 (예컨대, 표준 돌봄 치료) (예컨대, 표준 돌봄 치료)와 비교하여, 암 요법 제제를 포함하는 암 치료의 효능을 증가시키는데 유효하다. 일부 구현예에서, G9a의 길항제 및 암 요법 제제의 각각의 양은 G9a의 길항제 없이 (이의 부재하에) 암 요법 제제의 유효량을 투여하는 것을 포함하는 치료 (예컨대, 표준 돌봄 치료)와 비교하여, 반응을 증가시키는데 (예컨대, 완전한 반응) 유효하다.
또한, 개체에서 암 요법 제제를 포함하는 암 치료의 효능을 증가시키는 방법으로서, 상기 개체에 하기를 투여하는 단계를 포함하는 방법이 본원에 제공된다: (a) 유효량의 G9a의 길항제 및 (b) 유효량의 암 요법 제제.
개체에서 암을 치료하는 방법이 본원에 제공되고, 여기서 암 치료는 상기 개체에 (a) 유효량의 G9a의 길항제 및 (b) 유효량의 암 요법 제제를 투여하는 것을 포함하고, 상기 암 치료는 G9a의 길항제 없이 (이의 부재하에) 암 요법 제제의 유효량을 투여하는 것을 포함하는 치료 (예컨대, 표준 돌봄 치료)와 비교하여, 증가된 효능을 갖는다.
또한, 개체에서 암 요법 제제에 내성인 암의 발병을 진행을 지연시키고/시키거나 예방하는 방법으로서, 상기 개체에 하기를 투여하는 단계를 포함하는 방법이 본원에 제공된다: (a) 유효량의 G9a의 길항제 및 (b) 유효량의 암 요법 제제.
암 요법 제제에 내성이 진행될 증가된 공산을 갖는, 암을 갖는 개체를 치료하는 방법으로서, 상기 개체에 하기를 투여하는 단계를 포함하는 방법이 본원에 제공된다: (a) 유효량의 G9a의 길항제 및 (b) 유효량의 암 요법 제제.
추가로, 암을 갖는 개체에서 암 요법 제제의 민감도를 증가시키는 방법으로서, 상기 개체에 하기를 투여하는 단계를 포함하는 방법이 본원에 제공된다: (a) 유효량의 G9a의 길항제 및 (b) 유효량의 암 요법 제제.
또한, 암을 갖는 개체에서 암 요법 제제의 민감도의 기간을 연장시키는 방법으로서, 상기 개체에 하기를 투여하는 단계를 포함하는 방법이 본원에 제공된다: (a) 유효량의 G9a의 길항제 및 (b) 유효량의 암 요법 제제.
또한, 암을 갖는 개체에서 암 요법 제제에 대한 반응 기간을 연장시키는 방법으로서, 상기 개체에 하기를 투여하는 단계를 포함하는 방법이 본원에 제공된다: (a) 유효량의 G9a의 길항제 및 (b) 유효량의 암 요법 제제.
상기 방법들의 일부 구현예에서, 암 요법 제제는 표적화된 요법이다. 일부 구현예에서, 표적화된 요법은 EGFR 길항제, RAF 억제제, 및/또는 PI3K 억제제 중 하나 이상이다.
상기 방법들의 일부 구현예에서, 표적화된 요법은 EGFR 길항제이다. 상기 방법들의 일부 구현예에서, EGFR 길항제는 N-(3-에틸페닐)-6,7-비스(2-메톡시에톡시)-4-퀴나졸린아민 및/또는 약제학적으로 허용가능한 염이다. 일부 구현예에서, EGFR 길항제는 N-(3-에틸페닐)-6,7-비스(2-메톡시에톡시)-4-퀴나졸린아민이다. 일부 구현예에서, EGFR 길항제는 N-(4-(3-플루오로벤질옥시)-3-클로로페닐)-6-(5-((2-(메틸설포닐)에틸아미노)메틸)푸란-2-일)퀴나졸린-4-아민,디4-메틸벤젠설포네이트 또는 이의 약제학적으로 허용가능한 염 (예컨대, 라파티닙)이다.
상기 방법들의 일부 구현예에서, 표적화된 요법은 RAF 억제제이다. 일부 구현예에서, RAF 억제제는 BRAF 억제제이다. 일부 구현예에서, RAF 억제제는 CRAF 억제제이다. 일부 구현예에서, BRAF 억제제는 베무라페닙이다. 일부 구현예에서, RAF 억제제는 3-(2-시아노프로판-2-일)-N-(4-메틸-3-(3-메틸-4-옥소-3,4-디하이드로퀴나졸린-6-일아미노)페닐)벤즈아미드 또는 이의 약제학적으로 허용가능한 염 (예컨대, AZ628 (CAS# 878739-06-1) 이다.
상기 방법들의 일부 구현예에서, 표적화된 요법은 PI3K 억제제이다.
상기 방법들의 일부 구현예에서, 암 요법 제제는 화학요법이다. 상기 방법들의 일부 구현예에서, 화학요법은 탁산이다. 일부 구현예에서, 탁산은 파클리탁셀이다. 일부 구현예에서, 탁산은 도세탁셀이다.
상기 방법들의 일부 구현예에서, 화학요법은 백금 제제이다. 일부 구현예에서, 백금 제제는 카보플라틴이다. 일부 구현예에서, 백금 제제는 시스플라틴이다. 상기 방법들의 일부 구현예에서, 화학요법은 탁산 및 백금 제제이다. 일부 구현예에서, 탁산은 파클리탁셀이다. 일부 구현예에서, 탁산은 도세탁셀이다. 일부 구현예에서, 백금 제제는 카보플라틴이다. 일부 구현예에서, 백금 제제는 시스플라틴이다.
상기 방법들의 일부 구현예에서, 화학요법은 빈카 알칼로이드이다. 일부 구현예에서, 빈카 알칼로이드는 비노렐빈이다. 상기 방법들의 일부 구현예에서, 화학요법은 뉴클레오시드 유사체이다. 일부 구현예에서, 뉴클레오시드 유사체는 젬시타빈이다.
상기 방법들의 일부 구현예에서, 암 요법 제제는 방사성요법이다.
상기 방법들의 일부 구현예에서, G9a의 길항제는 G9a 소분자 길항제이다.
특정 구현예의 실시에 유용할 수 있는 소분자 G9a의 길항제의 예시는 하기를 포함한다: 화학식 I의 화합물, 이의 이성질체, 또는 이의 이성질체의 혼합물 또는 이의 약제학적으로 허용가능한 염, 이의 용매화물 또는 전구약물. UNC0638로 또한 공지되고, 본원에서 G9ai-2로 지칭되는 화학식 I의 화합물은 농도 의존적 방식으로 H3K9me2 수준을 감소시키는 G9a 및 GLP에 대한 강력하고, 선택적이고, 그리고 세포 침투적 화학 프로브이다. 상기 화합물 및 상기 화합물을 제조하는게 유용한 방법 및 중간체는 하기에 기술된다: Vedadi et al., Nat. Chem . Biol ., 7, 566-574 (2011) 및 Sweis et al., ACS Med. Chem. Lett., 5, 205-209 (2014).
화학식 I
일부 구현예에서, G9a 억제제는 Bix-01294, UNC0321, UNC0646, 및/또는 UNC0224이다 (참고: Vedadi et al., Nat. Chem . Biol ., 7, 566-574 (2011)). Bix-01294는 또한 본원에서 G9ai-2로 지칭된다.
일부 구현예에서, G9a 억제제는 2-(헥사하이드로-4-메틸-1H-1,4-디아제핀-1-일)-6,7-디메톡시-[1-(페닐메틸)-4-피페리딘일]-4-퀴나졸린아민 또는 이의 염을 포함한다. 일부 구현예에서, G9a 억제제는 2-(헥사하이드로-4-메틸-1H-1,4-디아제핀-1-일)-6,7-디메톡시-[1-(페닐메틸)-4-피페리딘일]-4-퀴나졸린아민 트리하이드로클로라이드를 포함한다. 일부 구현예에서, G9a 억제제는 7-[3-(디메틸아미노)프로폭시]-2-(헥사하이드로-4-메틸-1H-1,4-디아제핀-1-일)-6-메톡시-N-(1-메틸-4-피페리딘일)-4-퀴나졸린아민 또는 이의 염을 포함한다.
일부 구현예에서, G9a 억제제는
일부 구현예에서, G9a 억제제는 하기를 포함하고:
일부 구현예에서, G9A 억제제는 하기에 기술되고: the world wide web site sciencedirect.com/science/article/pii/S0960894X12015399, (Fujishiro et al., Bioorganic & Medicinal Chemistry Letters, 23, 733-736 (2013)), 이의 전문은 본원에서 참조로 포함된다.
상기 방법들의 일부 구현예에서, G9a의 길항제는 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)와 동시에 투여된다. 일부 구현예에서, G9a의 길항제는 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법) 이전에 및/또는 이와 동시에 투여된다.
상기 방법들의 일부 구현예에서, 암은 폐암, 유방암, 췌장암, 결장직장암, 및/또는 흑색종이다. 일부 구현예에서, 암은 폐암이다. 일부 구현예에서, 폐암은 NSCLC이다. 일부 구현예에서, 암은 유방암이다. 일부 구현예에서, 상기 암은 흑색종이다.
도 1A-C | (A) 하기의 도식: 히스톤 3 (H3) 꼬리 및 번역-후 변형의 아미노산 위치. G9a/EHMT2는 H3의 리신 9를 메틸화할 수 있는 메틸전이효소(emethytransferase)이다. (B) G9a는, 친계 PC9 세포와 비교하여, 인간 소-세포-폐 암 세포주 PC9 약물 내성 존속성균 (DTP) 내에서 상향조절된다. (C) 3’-UTR-GFP 녹다운을 갖는 G9a 짧은 헤어핀의 발현은 PC9 약물 내성 세포를 제거하는 것으로 나타났다.
도 2A-C | (A) 하기의 도식: 친계 PC9 세포와 비교하여, 인간 소-세포-폐 암 세포주 PC9 약물 내성 존속성균 (DTP) 내의 H3 메틸화 변화. (B) H3K4 me2 및 me3 이, PC9 친계 세포와 비교하여, PC9 DTP 내에서 감소된다 (웨스턴 블랏 및 MSD ELISA로 나타낼 경우). (C) H3K9 me3 이, PC9 친계 세포와 비교하여, PC9 DTP 내에서 증가된다 (웨스턴 블랏 및 MSD ELISA로 나타낼 경우). H3K9 아세틸화는, PC9 친계 세포와 비교하여, PC9 DTP에서 감소된다.
도 3A-B | (A) 소분자 G9a 길항제 UNC0638는, 웨스턴 블랏 및 질량 분광측정으로 관찰 시, H3K9의 메틸화를 억제할 수 있었다. (B) 소분자 G9a 길항제는 자가-메틸화 G9aK185me3를 억제한다.
도 4 | G9A-K185me 0/1/2/3 펩티드 풀다운 질량 분광측정 데이터를 사용하여, CDYL1 및 LRWD1를 H3K9 또는 G9aK185 메틸화된 펩티드로 풀다운하였다.
도 5 | UNC0638 (G9ai-2)는 타세바(Tarceva)로의 치료를 통하여 생성된 PC9 DTP의 생존력을 감소시켰다.
도 6 | (A) UNC0638 (G9ai-2)는 용량 의존적 방식으로 H3K9 메틸화 (예컨대, me1, me2, 및 me3)를 감소시킨다. (B) G9A 억제제는 DTP 형성을 억제한다. UNC0638 (G9ai-2)의 가변 용량으로 사전-투여 후 형성된 DTP 수의 용량 의존적 감소를 나타내는 히스토그램. 나타난 농도는 친계 PC9 세포의 생존력에는 영향을 주지 않는다.
도 7 | (A-C) UNC0638 (G9ai-2)는 타세바(Tarceva)로의 치료를 통하여 생성된 PC9 DTP의 생존력을 감소시켰다.
도 8 | (A) UNC0638 (G9ai-2)는 인간 유방암 세포주 EVSA-T 내에서 용량 의존적 방식으로 H3K9 메틸화 (예컨대, me1, me2, 및 me3)를 감소시킨다 (B) G9A 억제제는 GDC-0980에 의한 치료 상에서의 DTP 형성을 억제한다. UNC0638 (G9ai-2)의 가변 용량으로 사전-투여 후 형성된 EVSA-T DTP 수의 용량 의존적 감소를 나타내는 히스토그램. 나타난 농도는 친계 EVSA-T 세포의 생존력에는 영향을 주지 않는다.
도 9 | (A) UNC0638 (G9ai-2)는 인간 유방 선암종 암 세포주 SKBR3 내에서 용량 의존적 방식으로 H3K9 메틸화 (예컨대, me1, me2, 및 me3)를 감소시킨다. (B) G9A 억제제는 라파티닙에 의한 치료 상에서 DTP 형성을 억제한다. UNC0638 (G9ai-2)의 가변 용량으로 사전-투여 후 형성된 SKBR3 DTP 수의 용량 의존적 감소를 나타내는 히스토그램. 나타난 농도는 친계 SKBR3 세포의 생존력에는 영향을 주지 않는다.
도 10 | (A) UNC0638 (G9ai-2)는 인간 흑색종 암 세포주 M14 내에서 용량 의존적 방식으로 H3K9 메틸화 (예컨대, me1, me2, 및 me3)를 감소시킨다. (B) G9A 억제제는 GDC0973에 의한 치료 상에서 DTP 형성을 억제한다. UNC0638 (G9ai-2)의 가변 용량으로 사전-투여 후 형성된 M14 DTP 수의 용량 의존적 감소를 나타내는 히스토그램. 나타난 농도는 친계 M14 세포의 생존력에는 영향을 주지 않는다.
도 11 | (A) UNC0638 (G9ai-2)는 인간 결장암 세포주 Colo205 내에서 용량 의존적 방식으로 H3K9 메틸화 (예컨대, me1, me2, 및 me3)를 감소시킨다. (B) G9A 억제제는 AZ628에 의한 치료 상에서 DTP 형성을 억제한다. UNC0638 (G9ai-2)의 가변 용량으로 사전-투여 후 형성된 Colo205 DTP 수의 용량 의존적 감소를 나타내는 히스토그램. 나타난 농도는 친계 Colo205 세포의 생존력에는 영향을 주지 않는다.
도 2A-C | (A) 하기의 도식: 친계 PC9 세포와 비교하여, 인간 소-세포-폐 암 세포주 PC9 약물 내성 존속성균 (DTP) 내의 H3 메틸화 변화. (B) H3K4 me2 및 me3 이, PC9 친계 세포와 비교하여, PC9 DTP 내에서 감소된다 (웨스턴 블랏 및 MSD ELISA로 나타낼 경우). (C) H3K9 me3 이, PC9 친계 세포와 비교하여, PC9 DTP 내에서 증가된다 (웨스턴 블랏 및 MSD ELISA로 나타낼 경우). H3K9 아세틸화는, PC9 친계 세포와 비교하여, PC9 DTP에서 감소된다.
도 3A-B | (A) 소분자 G9a 길항제 UNC0638는, 웨스턴 블랏 및 질량 분광측정으로 관찰 시, H3K9의 메틸화를 억제할 수 있었다. (B) 소분자 G9a 길항제는 자가-메틸화 G9aK185me3를 억제한다.
도 4 | G9A-K185me 0/1/2/3 펩티드 풀다운 질량 분광측정 데이터를 사용하여, CDYL1 및 LRWD1를 H3K9 또는 G9aK185 메틸화된 펩티드로 풀다운하였다.
도 5 | UNC0638 (G9ai-2)는 타세바(Tarceva)로의 치료를 통하여 생성된 PC9 DTP의 생존력을 감소시켰다.
도 6 | (A) UNC0638 (G9ai-2)는 용량 의존적 방식으로 H3K9 메틸화 (예컨대, me1, me2, 및 me3)를 감소시킨다. (B) G9A 억제제는 DTP 형성을 억제한다. UNC0638 (G9ai-2)의 가변 용량으로 사전-투여 후 형성된 DTP 수의 용량 의존적 감소를 나타내는 히스토그램. 나타난 농도는 친계 PC9 세포의 생존력에는 영향을 주지 않는다.
도 7 | (A-C) UNC0638 (G9ai-2)는 타세바(Tarceva)로의 치료를 통하여 생성된 PC9 DTP의 생존력을 감소시켰다.
도 8 | (A) UNC0638 (G9ai-2)는 인간 유방암 세포주 EVSA-T 내에서 용량 의존적 방식으로 H3K9 메틸화 (예컨대, me1, me2, 및 me3)를 감소시킨다 (B) G9A 억제제는 GDC-0980에 의한 치료 상에서의 DTP 형성을 억제한다. UNC0638 (G9ai-2)의 가변 용량으로 사전-투여 후 형성된 EVSA-T DTP 수의 용량 의존적 감소를 나타내는 히스토그램. 나타난 농도는 친계 EVSA-T 세포의 생존력에는 영향을 주지 않는다.
도 9 | (A) UNC0638 (G9ai-2)는 인간 유방 선암종 암 세포주 SKBR3 내에서 용량 의존적 방식으로 H3K9 메틸화 (예컨대, me1, me2, 및 me3)를 감소시킨다. (B) G9A 억제제는 라파티닙에 의한 치료 상에서 DTP 형성을 억제한다. UNC0638 (G9ai-2)의 가변 용량으로 사전-투여 후 형성된 SKBR3 DTP 수의 용량 의존적 감소를 나타내는 히스토그램. 나타난 농도는 친계 SKBR3 세포의 생존력에는 영향을 주지 않는다.
도 10 | (A) UNC0638 (G9ai-2)는 인간 흑색종 암 세포주 M14 내에서 용량 의존적 방식으로 H3K9 메틸화 (예컨대, me1, me2, 및 me3)를 감소시킨다. (B) G9A 억제제는 GDC0973에 의한 치료 상에서 DTP 형성을 억제한다. UNC0638 (G9ai-2)의 가변 용량으로 사전-투여 후 형성된 M14 DTP 수의 용량 의존적 감소를 나타내는 히스토그램. 나타난 농도는 친계 M14 세포의 생존력에는 영향을 주지 않는다.
도 11 | (A) UNC0638 (G9ai-2)는 인간 결장암 세포주 Colo205 내에서 용량 의존적 방식으로 H3K9 메틸화 (예컨대, me1, me2, 및 me3)를 감소시킨다. (B) G9A 억제제는 AZ628에 의한 치료 상에서 DTP 형성을 억제한다. UNC0638 (G9ai-2)의 가변 용량으로 사전-투여 후 형성된 Colo205 DTP 수의 용량 의존적 감소를 나타내는 히스토그램. 나타난 농도는 친계 Colo205 세포의 생존력에는 영향을 주지 않는다.
I. 정의
관심 폴리펩티드의 “길항제” (상호교환적으로 “억제제”로 지칭됨)는 관심 폴리펩티드의 활성화 또는 기능을 저해하며, 예를 들어 관심 폴리펩티드에 의해 매개된 생물학적 활성을 부분적으로 또는 완전하게 차단, 억제, 또는 중화하는 제제이다. 예를 들어, 폴리펩티드 X의 길항제는 폴리펩티드 X에 의하여 매개된 생물학적 활성을 부분적으로 또는 완전하게 차단, 억제, 또는 중화하는 임의의 분자를 지칭할 수 있다. 억제제의 예시는 하기를 포함한다: 항체; 리간드 항체; 소분자 길항제; 안티센스 및 억제적 RNA (예컨대, shRNA) 분자. 바람직하게는, 억제제는 관심 폴리펩티드에 결합하는 항체 또는 소분자이다. 특정 구현예에서, 억제제는 약 1,000 nM 이하의 관심 폴리펩티드에 대한 결합 친화도(해리 상수)를 갖는다. 또 다른 구현예에서, 억제제는 약 100 nM 이하의 관심 폴리펩티드에 대한 결합 친화도를 갖는다. 또 다른 구현예에서, 억제제는 약 50 nM 이하의 관심 폴리펩티드에 대한 결합 친화도를 갖는다. 특정 구현예에서, 억제제는 관심 폴리펩티드에 공유결합된다. 특정 구현예에서, 억제제는 약 1,000 nM 이하의 IC50 으로 관심 폴리펩티드 신호전달을 억제한다. 또 다른 구현예에서, 억제제는 약 500 nM 이하의 IC50 으로 관심 폴리펩티드 신호전달을 억제한다. 또 다른 구현예에서, 억제제는 약 50 nM 이하의 IC50 으로 관심 폴리펩티드 신호전달을 억제한다. 특정 구현예에서, 길항제는 관심 폴리펩티드의 발현 수준 또는 생물학적 활성을, 적어도 약 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% 또는 그 이상 만큼 감소시키거나 억제한다. 일부 구현예에서, 관심 폴리펩티드는 G9a이다. 본원에 사용된 바와 같이, 용어 “폴리펩티드”는, 달리 지적되지 않는 경우 영장류 (예컨대, 인간) 및 설치류 (예컨대, 마우스 및 래트)와 같은 포유동물을 포함하는 임의의 척추동물 공급원 기원의 임의의 천연 관심 폴리펩티드를 지칭한다. 상기 용어는 세포내 처리로 유발된 임의의 형태의 폴리펩티드 뿐만 아니라 “전장”의 비처리된 폴리펩티드를 포괄한다. 상기 용어는 또한, 폴리펩티드의 자연 발생 변이체, 예를 들면, 스플라이스 변이체 또는 대립형질 변이체를 포괄한다.
본원에서 상호교환적으로 사용되는 바와 같이 "폴리뉴클레오타이드," 또는 "핵산,"은 임의의 길이의 뉴클레오타이드의 폴리머를 언급하고, 그리고 DNA 및 RNA를 포함한다. 상기 뉴클레오티드는 데옥시리보뉴클레오티드, 리보뉴클레오티드, 변형된 뉴클레오티드 또는 염기, 및/또는 그들의 유사체, 또는 DNA 또는 RNA 폴리머라아제에 의하여, 또는 합성 반응에 의하여, 폴리머로 포함될 수 있는 임의의 기질일 수 있다. 폴리뉴클레오타이드는 변형된 뉴클레오타이드, 예컨대 메틸화된 뉴클레오타이드 및 그 유사체를 포함할 수 있다. 존재한다면, 뉴클레오타이드 구조에 대한 변형은 폴리머의 조립 이전 또는 이후 부여될 수 있다. 뉴클레오타이드의 서열은 비-뉴클레오타이드 성분에 의해 방해될 수 있다. 폴리뉴클레오티드는 합성 후에 예를 들어 표지로의 콘주케이션에 의하여 추가적으로 변형될 수 있다. 다른 유형의 변형은, 예를 들면, "캡(cap)", 천연 발생 뉴클레오타이드 중 하나 이상의 유사체로의 치환, 뉴클레오타이드간 변형 예컨대, 예를 들면, 미하전된 연결기 (예를 들면, 메틸 포스포네이트, 포스포트리에스테르, 포스포아미데이트, 카바메이트 등) 및 하전된 연결기 (예를 들면, 포스포로티오에이트, 포스포로디티오에이트 등)를 갖는 것, 현수 모이어티, 예컨대, 예를 들면, 단백질 (예를 들면, 뉴클레아제, 독소, 항체, 신호 펩티드, ply-L-라이신 등)을 함유하는 것, 삽입제 (예를 들면, 아크리딘, 소랄렌, 등)를 갖는 것, 킬레이터 (예를 들면, 금속, 방사성 금속, 붕소, 산화적 금속, 등)를 함유하는 것, 알킬화제를 함유하는 것, 변형된 연결기 (예를 들면, 알파 아노머성 핵산, 등)를 갖는 것, 뿐만 아니라 비변형된 형태의 폴리뉴클레오타이드(들)를 포함한다. 더욱이, 당에 보통 존재하는 히드록실 기의 임의의 것은 예를 들어 포스포네이트 기, 포스페이트 기로 대체될 수 있으며, 표준 보호기에 의하여 보호되거나, 또는 부가적인 뉴클레오티드들로 부가적인 결합을 제조하기 위하여 활성화될 수 있으며, 또는 고형 지지체로 콘주게이트될 수 있다. 5’ 및 3’ 말단 OH는 1 내지 20의 탄소 원자들의 아민 또는 유기 캡핑(capping) 기 모이어티로 포스포릴화 또는 치환될 수 있다. 다른 하이드록실은 또한 표준 보호기로 유도될 수 있다. 폴리뉴클레오타이드는 또한, 예를 들면, 2'-O-메틸-, 2'-O-알릴, 2'-플루오로- 또는 2'-아지도-리보오스, 카보사이클릭 당 유사체, α-아노머성 당, 에피머 당류 예컨대 아라비노오스, 자일로스 또는 릭소스, 파이라노스 당, 푸라노스 당, 세도헵툴로스, 비환식 유사체 및 무염기성 뉴클레오시드 유사체 예컨대 메틸 리보사이드를 포함하여, 당해기술에 일반적으로 공지되는 리보오스 또는 데옥시리보스 당류의 유사 형태를 함유할 수 있다. 하나 이상의 포스포디에스테르 연결기는 대안적인 연결기에 의해 대체될 수 있다. 이러한 대안적인 결합기는, 비제한적으로 구현예들을 포함하며, 여기서 포스페이트는 P(O)S (“티오에이트”), P(S)S ("디티오에이트"), (O)NR2 ("아미데이트"), P(O)R, P(O)OR', CO 또는 CH2 ("폼아세탈(formacetal)")로 교체될 수 있으며, 여기서 각 R 또는 R'은 독립적으로 H 또는 임의로 에터 (-O-) 결합, 아릴,. 알케닐, 시클로알킬, 시클로알케닐, 또는 아랄딜을 함유하는 치환된 또는 비치환된 알킬 (1-20 C)이다. 폴리뉴클레오타이드에서 모든 연결기가 동일할 필요는 없다. 이전의 설명은 RNA 및 DNA를 포함하여 본원에서 언급되는 모든 폴리뉴클레오타이드에 적용한다.
용어 “소분자”는 2000 달톤 이하, 바람직하게는 약 500 달톤 이하의 분자량을 갖는 임의의 분자를 지칭한다.
"단리된" 항체는 그 자연 환경의 성분으로부터 분리되는 것이다. 일부 구현예에서, 항체는 다음 기술에 의한 측정시 95% 또는 99% 초과의 순도로 정제된다: 예를 들어, 전기영동 (예를 들어, SDS-PAGE, 등전점 포커싱 (IEF), 모세관 전기영동) 또는 크로마토그래피(예를 들어, 이온 교환 또는 역상 HPLC). 항체 순도의 평가 방법의 검토를 위해, 참고: 예를 들면, Flatman et al., J. Chromatogr . B 848:79-87 (2007).
본원에서 용어 "항체"는 가장 넓은 의미로 사용되고 이들이 목적 항원-결합 활성을 나타내는 동안, 비제한적으로 단클론성 항체, 다클론성 항체, 다중특이적 항체 (예를 들면, 이중특이적 항체)를 포함하여, 다양한 항체 구조, 및 항체 단편을 포함한다.
용어 "항-폴리펩티드 관심 항체" 및 "관심 폴리펩티드에 결합하는 항체"는 상기 항체가 관심 폴리펩티드를 표적으로 할 때 진단 및/또는 치료 제제로서 유용하도록 충분한 친화도로 관심 폴리펩티드와 결합할 수 있는 항체를 지칭한다. 일 구현예에서, 관심 항체의 항-폴리펩티드의, 무관한 관심 단백질의 비-폴리펩티드에 결합하는 정도는 예컨대, 방사면역검정(RIA)에 의해 측정시, 상기 항체가 관심 폴리펩티드에 결합하는 경우의 약 10% 미만이다. 특정 구현예에서, 관심 폴리펩티드에 결합하는 항체는 ≤ 1μM, ≤ 100 nM, ≤ 10 nM, ≤ 1 nM, ≤ 0.1 nM, ≤ 0.01 nM, 또는 ≤ 0.001 nM (예를 들면, 10-8 M 이하, 예를 들면, 10-8 M 내지 10-13 M, 예를 들면, 10-9 M 내지 10-13 M)의 해리 상수 (Kd)를 갖는다. 특정 구현예에서, 관심 항체의 항-폴리펩티드는 상이한 종 유래의 관심 폴리펩티드 중 보존된 관심 폴리펩티드의 에피토프에 결합한다. 일부 구현예에서, 관심 폴리펩티드는 G9a이다.
"차단 항체” 또는 "길항제" 항체는 이 항체가 결합하는 항원의 생물학적 활성을 억제하거나 감소시키는 것이다. 바람직한 차단 항체 또는 길항제 항체는 항원의 생물학적 활성을 실질적으로 또는 완전히 억제한다.
"친화도"은 분자 (예를 들면, 항체)의 단일 결합 부위와 그 결합 파트너 (예를 들면, 항원) 사이의 비공유 상호작용의 총계의 강도를 언급한다. 다르게 명시되지 않으면, 본원에서 사용된 바와 같이, "결합 친화도"은 결합 쌍 (예를 들면, 항체 및 항원)의 구성원 사이의 1:1 상호작용을 반영하는 고유 결합 친화도을 언급한다. 그 파트너 Y에 대한 분자 X의 친화도은 일반적으로 해리 상수 (Kd)로 나타낼 수 있다. 친화도은 본원에서 기재된 것을 포함하여 당해분야에서 공지된 공통의 방법으로 측정될 수 있다. 결합 친화도 측정을 위한 구체적인 예증적 및 예시적 구현예는 하기에 기재된다.
"항체 단편"은 온전한 항체가 결합하는 항원과 결합하는 온전한 항체의 일부분을 포함하는 온전한 항체가 아닌 분자를 가리킨다. 항체 단편들의 예시들은 비제한적으로 Fv, Fab, Fab', Fab'-SH, F(ab')2; 디아바디; 선형 항체; 단일-쇄 항체 분자 (예컨대, scFv); 및 항체 단편으로부터 형성된 다중특이적 항체를 포함한다.
표준 항체와 “동일한 에피토프에 결합하는 항체”는 경쟁 검정에서 표준 항체의 이의 항원으로의결합을 50% 이상 차단하는 항체를 언급하고, 역으로, 표준 항체는 경쟁 검정에서 50% 이상으로 항체의 이의 항원으로의 결합을 차단한다.
용어 "키메라" 항체는 중쇄 및/또는 경쇄의 일부분이 특정 공급원 또는 특정 종에서 유도된 반면, 상기 중쇄 및/또는 경쇄의 나머지 부분이 상이한 공급원 또는 상이한 종에서 유도된 것인 항체를 가리킨다.
용어 "전장 항체", "온전한 항체" 및 "전체 항체"는 본원에서 상호교환적으로 사용되어 천연 항체 작제물와 실질적으로 유사한 작제물를 갖거나 또는 Fc 영역을 함유하는 중쇄를 갖는 항체를 가리킨다.
본원에서 사용된 바와 같이 용어 "단클론성 항체"는 실질적으로 균질 항체의 동원단으로부터 수득된 항체를 언급한다, 즉, 동원단을 포함하는 개별 항체는, 예를 들면, 천연 발생 돌연변이를 함유하거나 또는 단클론성 항체 제제의 생산 동안 발생하는 가능한 변이체 항체 (상기 변이체는 일반적으로 소량으로 존재한다)를 제외하고, 동일하고/하거나 동일한 에피토프를 결합한다. 전형적으로 상이한 결정인자 (에피토프)에 대하여 유도된 상이한 항체를 포함하는 다클론성 항체와 대조로, 단클론성 항체 제제의 각각의 단클론성 항체는 항원에서 단일 결정인자에 대해서 유도된다. 따라서, 형용사 "단클론"은 항체가 실질적으로 균일한 항체 집단에서 수득된 것이라는 속성을 명시하고, 어떤 특정한 방법에 의한 상기 항체의 생산을 요구하는 것으로 간주되지 않는다. 예를 들어, 본 발명에 따라 사용되는 단클론 항체는 다양한 기법, 예를 들면 비제한적으로 융합세포법, 재조합 DNA법, 파지-현시법 및 인간 면역글로불린 자리의 전부 또는 일부를 함유하는 형질 전환 동물을 활용하는 방법, 예컨대 단클론 항체를 제조하기 위한 방법들 및 기타 예시적 방법들에 의해 제조될 수 있다.
"인간 항체"는 인간 또는 인간 세포에 의해 생성되거나 또는 인간 항체 목록 또는 기타 인간 항체-암호화 서열을 활용하는 비-인간 공급원에서 유도된 항체의 아미노산 서열에 해당하는 것을 포함하는 것이다. 인간 항체의 이러한 정의는 특이적으로 비인간 항원-결합 잔기를 포함하는 인간화 항체를 배제한다.
"인간화된" 항체는 비-인간 HVR에서 유래된 아미노산 잔기와 인간 FR에서 유래된 아미노산 잔기를 포함하는 키메라 항체를 가리킨다. 특정 구현예에서, 인간화 항체는 적어도 1개, 및 전형적으로 2개의 가변 도메인의 실질적으로 모두를 포함할 것이고, 여기에서 HVR (예를 들면, CDR)의 실질적으로 모두는 비인간 항체의 것에 일치하고, 그리고 FR의 모두 또는 실질적으로 모두는 인간 항체의 것에 일치한다. 인간화 항체는 임의로 인간 항체로부터 유도된 항체 불변 영역의 적어도 일부를 포함할 수 있다. 항체, 예를 들면, 비인간 항체의 "인간화 형태"는 인간화처리되는 항체를 언급한다.
본원에서 사용된 바와 같이, 용어 "표적화된 치료제”는 특정 관심 폴리펩티드(들)의 활성 및/또는 활성화를 억제하고, 관심 폴리펩티드(들)에 결합하는 치료적 제제를 지칭한다. 상기 제제의 예는 관심 폴리펩티드에 결합하는 항체 및 소분자를 포함한다.
“화학요법”은 암의 치료에 유용한 화학적 화합물을 지칭한다. 화학 요법의 예에는 알킬화제, 예컨대 티오테파 및 사이클로포스파마이드(CYTOXAN®); 알킬 설포네이트, 예컨대 부설판, 임프로설판 및 피포설판; 아지리딘, 예컨대 벤조도파, 카보쿠온, 메투레도파, 및 우레도파; 에틸렌이민 및 메틸아멜라민, 예컨대 알트레타민, 트리에틸렌멜라민, 트리에틸렌포스포르아미드, 트리에틸렌티오포스포르아미드 및 트리메틸롤로멜라민; 아세토게닌(특히 불라타신 및 불라타시논); 델타-9-테트라하이드로칸나비놀(드로나비놀, MARINOL®); 베타-라파콘; 라파콜; 콜히친; 베툴린산; 캄프토테신(합성 유사체 토포테칸(HYCAMTIN® 포함); CPT-11 (이리노테칸, CAMPTOSAR®), 아세틸캄프토테신, 스코폴렉틴, 및 9-아미노캄프토테신); 브리오스타틴; 칼리스타틴; CC-1065(그 아도젤레신, 카르젤레신 및 바이젤레신 합성 유사체 포함); 포도필로톡신; 포도필린산; 테니포사이드; 크립토파이신(특히 크립토파이신 1 및 크립토파이신 8); 돌라스타틴; 듀오카르마이신(합성 유사체, KW-2189 및 CB1-TM1 포함); 엘류테로빈; 판크라티스타틴; 사르코딕티인; 스폰지스타틴; 질소 머스타드, 예컨대 클로르암부실, 클로르나파진, 콜로포스파마이드, 에스트라무스틴, 이포스파마이드, 메클로르에타민, 메클로르에타민 옥사이드 하이드로클로라이드, 멜팔란, 노벰비친, 펜에스테린, 프레드니무스틴, 트로포스파마이드, 우라신 머스타드; 나이트로스우레아, 예컨대 카르무스틴, 클로로조토신, 포테무스틴, 로무스틴, 니무스틴, 및 라님누스틴; 항생제, 예컨대 엔디인 항생제(예를 들면, 칼리키아마이신, 특히 칼리키아마이신 감마1I 및 칼리키아마이신 오메가I1 (예를 들어, 참고: Nicolaou et al., Angew . Chem Intl . Ed. Engl ., 33: 183-186(1994) 참고); CDP323, 경구 알파-4 인테그린 억제제; 다이네마이신, 다이네마이신 A 포함; 에스페라마이신뿐만 아니라 네오카르지노스타틴 발색단 및 관련된 색소단백질 엔디인 항생제 발색단), 아클라시노마이신, 악티노마이신, 오트라마이신, 아자세린, 블레오마이신, 칵티노마이신, 카라비신, 카미노마이신, 카르지노필린, 크로모마이시니스, 닥티노마이신, 다우노루비신, 데토루비신, 6-디아조-5-옥소-L-노르류신, 독소루비신(ADRIAMYCIN®, 모폴리노-독소루비신, 시아노모폴리노-독소루비신, 2-피롤리노-독소루비신, 독소루비신 HCl 리포좀 주사(DOXIL®) 리포좀 독소루비신 TLC D-99 (MYOCET®), 페길화된 리포좀l 독소루비신 (CAELYX®) 및 데옥시독소루비신 포함), 에피루비신, 에소루비신, 아이다루비신, 마르셀로마이신, 미토마이신, 예컨대 미토마이신 C, 마이코페놀산, 노갈라마이신, 올리보마이신, 페플로마이신, 포트피로마이신, 퓨로마이신, 쿠엘라마이신, 로도루비신, 스트렙토니그린, 스트렙토조신, 투베르시딘, 우베니멕스, 지노스타틴, 조루비신; 항-대사물질, 예컨대 메토트렉세이트, 젬시타빈(GEMZAR®), 테가푸르(UFTORAL®), 카페시타빈(XELODA®), 에포틸론, 및 5-플루오로우라실(5-FU); 엽산 유사체, 예컨대 데노프테린, 메토트렉세이트, 프테로프테린, 트리메트렉세이트; 퓨린 유사체, 예컨대 플루다라빈, 6-머캅토퓨린, 티아미프린, 티오구아닌; 피리미딘 유사체, 예컨대 안시타빈, 아자시티딘, 6-아자우리딘, 카모푸르, 사이타라빈, 디데옥시우리딘, 독시플루리딘, 에노시타빈, 플록수리딘; 안드로겐, 예컨대 칼루스테론, 드로모스타놀론 프로피오네이트, 에피티오스탄올, 메피티오스탄, 테스토락톤; 항-부신물질, 예컨대 아미노글루테티미드, 미토탄, 트릴로스탄; 엽산 보충물, 예컨대 프롤린산; 아세글라톤; 알도포스파미드 글리코사이드; 아미노레불린산; 에닐우라실; 암사크린; 베스트라부실; 비스안트렌; 에다트락세이트; 데포파민; 데메콜신; 디아지쿠온; 엘포르미틴; 엘립티늄 아세테이트; 아네포틸론; 에토글루시드; 갈륨 니트레이트; 하이드록시우레아; 렌티난; 로니다이닌; 메이탄시노이드, 예컨대 메이탄신 및 안사미토신; 미토구아존; 미톡산트론; 모피단몰; 니트라에린; 펜토스타틴; 페나메트; 피라루비신; 로속산트론; 2-에틸하이드라자이드; 프로카바진; PSK® 다당류 복합체(JHS Natural Products, Eugene, OR); 라족산; 라이족신; 시조푸란; 스피로게르마늄; 테누아진산; 트리아지쿠온; 2,2',2’-트리클로로트리에틸아민; 트리코테센(특히 T-2 독소, 베라쿠린 A, 로리딘 A 및 안구이딘); 우레탄; 빈데신(ELDISINE®, FILDESIN®); 다카르바진; 만노무스틴; 미토브로니톨; 미토락톨; 피포브로만; 가시토신; 아라바이노사이드("Ara-C"); 티오테파; 탁소이드, 예를 들면, 파클리탁셀(TAXOL®), 파클리탁셀의 알부민-가공된 나노입자 제형(ABRAXANE™), 및 독세탁셀(TAXOTERE®); 클로란부실; 6-티오구아닌; 머캅토퓨린; 메토트렉세이트; 백금 제제 예컨대 시스플라틴, 옥살리플라틴 (예컨대, ELOXATIN®), 및 카보플라틴; 빈카 (튜불린 중합이 빈블라스틴을 포함하는 미세소관을 형성하는 것을 방지 (VELBAN®)), 빈크리스틴 (ONCOVIN®), 빈데신 (ELDISINE®, FILDESIN®), 및 비노렐빈 (NAVELBINE®); 에토포시드 (VP-16); 이포스파미드; 미톡산트론; 류코보린; 노반트론; 에다트렉세이트; 다우노마이신; 아미노프테린; 이반드로네이트; 토포이소머라제 억제제 RFS 2000; 디플루오로메틸오미틴 (DMFO); 레티노산 유도체 예컨대 벡사로텐 (TARGRETIN®); 비스포스포네이트, 예컨대 클로드로네이트 (예를 들어, BONEFOS® 또는 OSTAC®), 에티드로네이트 (DIDROCAL®), NE-58095, 졸레드론 산/졸레드로네이트 (ZOMETA®), alendronate (FOSAMAX®), 파미드로네이트 (AREDIA®), 티루드로네이트 (SKELID®), 또는 리세드로네이트 (ACTONEL®); 트록사시타빈 (1,3-디옥솔란 뉴클레오시드 시토신 유사체); 및 임의의 상기의 약제학적으로 허용가능한 염, 산 또는 유도체뿐만 아니라 상기의 2 이상의 조합, 예컨대 CHOP(사이클로포스파마이드, 독소루비신, 빈크리스틴, 및 프레드니솔론의 병용 요법에 대한 약어), 및 FOLFOX(5-FU 및 류코보빈과 조합된 옥살리플라틴(ELOXATIN™)을 이용한 치료 레지멘에 대한 약어)를 포함한다.
본원에서 사용된 바와 같이 용어 "세포독성제"는 세포성 기능을 억제 또는 예방하고/하거나 세포사 또는 파괴를 일으키는 물질을 언급한다. 세포독성제는, 비제한적으로, 방사성 동위원소 (예를 들면, At211, I131, I125, Y90, Re186, Re188, Sm153, Bi212, P32, Pb212 및 Lu의 방사성 동위원소); 화학치료제 또는 약물 (예를 들면, 메토트렉세이트, 아드리아마이신, 빈카 알칼로이드 (빈크리스틴, 빈블라스틴, 에토포시드), 독소루비신, 멜팔란, 미토마이신 C, 클로르암부실, 다우노루비신 또는 다른 개재 약물); 성장 억제성 제제; 효소 및 그 단편 예컨대 핵산분해 효소; 항생제; 독소 예컨대 소분자 독소 또는 박테리아, 진균, 식물 또는 동물 기원의 효소적으로 활성 독소, 단편 및/또는 그 변이체 포함; 및 아래 개시된 다양한 항종양 또는 항암제를 포함한다. 다른 세포독성 제제는 아래에 기재되어 있다. 살종양제는 종양 세포의 파괴를 유도한다.
"면역접합체"는 하나 이상의 이종 분자(들), 예를 들면 비제한적으로 세포독성 제제에 콘주게이트되는 항체이다.
“개체 반응” 또는 “반응”은 상기 개체에 대한 이점을 표지하는 임의의 종료점을 사용하여 평가될 수 있으며, 이는 비제한적으로 하기를 포함한다: (1) 지연 및 완전한 정지를 포함하는, 질병 진행 (예컨대, 암 진행)의, 일정 정도까지의, 억제; (2) 종양 크기의 감소; (3) 인접 말초 기관 및/또는 조직으로 암 세포 침윤의 억제 (즉, 감소, 지연, 또는 완전한 정지); (4) 전이의 억제 (즉, 감소, 지연 또는 완전한 정지); (5) 질환 또는 장애 (예컨대, 암)과 연관된 하나 이상의 증상의, 일정 정도까지의, 완화 ; (6) 진행 무생존의 길이 증가; 및/또는 (7) 치료 후 소정의 시간에서 감소된 사망률.
본원에 사용되는 용어 "실질적으로 동일한"은 두 개의 수치 값 사이에 충분히 높은 정도의 유사성이 있어서, 당해기술의 숙련가가 두 값 사이의 차이가 상기 값들에 의해 측정되는 생물학적 특징(예컨대, Kd 값 또는 발현)의 상황 내에서 생물학적 및/또는 통계학적 유의성이 거의 또는 전혀 없는 것으로 간주하는 것을 의미한다. 상기 두 값의 차이는, 예를 들어, 기준/비교 값의 함수로서 약 50% 미만, 약 40% 미만, 약 30% 미만, 약 20% 미만, 및/또는 약 10% 미만이다.
본원에 사용된 구문 "실질적으로 상이한"은 두 개의 수치 값 사이에 충분히 높은 정도의 상이성이 있어서, 당해기술의 숙련가가 두 값 사이의 차이를 상기 값들에 의해 측정되는 생물학적 특징(예컨대, Kd 값)들이 상황 내에서 통계학적 유의성이 있다고 간주하는 것을 의미힌다. 상기 두 값의 차이는, 예를 들어, 기준/비교 분자에 대한 값의 함수로서 약 10% 초과, 약 20% 초과, 약 30% 초과, 약 40% 초과, 및/또는 약 50% 초과이다.
물질/분자, 예를 들면, 약제학적 조성물의 "효과적인 양"은 목적 치료 또는 예방 결과를 달성하기 위해 필요한 복용량에서 시간의 기간동안 효과적인 양을 언급한다.
물질/분자의 “치료적 유효량”은 개체의 질환 단계, 연령, 성별 및 체중과 같은 요인, 및 개체에서의 목적 반응을 일으키는 물질/분자의 능력에 따라 가변될 수 있다. 치료 유효량은 또한 물질/분자의 임의의 독성 또는 유해 효과가 치료적 유익 효과를 능가하는 것이다. "예방적 유효량"은 목적 예방 결과를 달성하기 위해 필요한 기간 동안 그러한 투여량에서, 유효한 양을 나타낸다. 초기 질환 병기 전에 또는 이 병기에서 대상체에서 예방학적 용량을 사용할 수 있으므로, 반드시 그런 것은 아니지만 통상적으로 예방학적 유효량은 치료학적 유효량보다 적다.
용어 "약제학적 제형"은 그안에 함유된 활성 성분의 생물학적 활성이 효과적이도록 하기 위한 형태인, 그리고 제형이 투여되는 대상체에 허용불가능하게 독성인 추가의 성분을 함유하지 않는 제제를 언급한다.
"약제학적으로 허용가능한 담체"는 대상체에 비독성인, 활성 성분 이외의, 약제학적 제형에서의 성분을 언급한다. 약제학적으로 허용가능한 담체는, 비제한적으로, 완충제, 부형제, 안정제, 또는 보존제를 포함한다.
본 명세서에서 이용된 바와 같이, 구절 "약제학적으로 허용가능한 염"이란 화합물의 약제학적으로 허용가능한 유기 또는 무기 염을 지칭한다.
본원에서 사용된 바와 같이, "치료" (및 이의 문법적 변화 예컨대 "치료한다" 또는 "치료하는")는 치료받는 개체의 당연한 과정을 변경하기 위한 시도로 임상 중재를 언급하고, 예방을 위해 또는 임상 병리학의 과정 동안 수행될 수 있다. 바람직한 치료 효과에는 비제한적으로 하기를 포함한다: 질환 발생 또는 재발의 방지, 증상의 완화, 질환의 임의의 직접적 또는 간접적 병리 결과의 약화, 전이의 방지, 질환 진행 속도의 감소, 질환 상태의 개선 또는 경감, 및 차도 또는 향상된 예후. 일부 구현예에서, 본 발명의 항체는 질환의 발달을 지연하기 위해 또는 질환의 진행을 늦추게 하기 위해 사용된다.
"개체" 또는 "대상체"는 포유동물이다. 포유동물은, 비제한적으로, 사육된 동물 (예를 들면, 소, 양, 고양이, 개, 및 말), 영장류 (예를 들면, 인간 및 비인간 영장류 예컨대 원숭이), 토끼, 및 설치류 (예를 들면, 마우스 및 랫트)를 포함한다. 특정 구현예에서, 개체 또는 대상체는 인간이다.
본원에 사용된 용어 "동시에"는 둘 이상의 치료 제제의 투여를 지칭하며, 이는 개별 치료 효과가 시간적으로 중첩되는, 충분한 시간적 근접성을 부여한다. 따라서, 동시 투여에는 하나 이상의 다른 제제(들)의 투여를 중단한 후 하나 이상의 제제(들)의 투여가 이어질 때의 투여 레지멘이 포함된다. 일부 구현예에서, 동시 투여는 동시, 순차, 및/또는 동시간의 것이다.
“감소 또는 억제”는 20%, 30%, 40%, 50%, 60%, 70%, 75%, 80%, 85%, 90%, 95%, 또는 그 이상의 전체적 감소를 유발하는 능력을 의미한다. 감소 또는 억제는 원발 종양의 크기, 전이의 크기 또는 존재, 또는 치료될 장애의 증상을 감소 또는 억제시키는 것을 지칭한다.
용어 "팩키지 삽입물"은 치료학적 제품의 상업 팩키지에 통상적으로 포함되는 지침서를 언급하기 위해 사용되고 이는 상기 치료학적 제품의 사용에 관한 지적사항, 용도, 투여량, 투여, 조합 치료요법, 사용금지 사항 및/또는 경고에 관한 정보를 함유한다.
“제조 물품”은 적어도 하나의 시약, 예를 들면 본 발명의 바이오마커 유전자 또는 단백질을 특이적으로 검출하기 위한 프로브 또는 질환 또는 장애 (예를 들면, 암)의 치료를 위한 약제를 포함하는 임의의 제조물 또는 키트 (예를 들면, 패키지 또는 용기)이다. 특정 구현예에서, 상기 제조물 또는 키트는 바람직하게는 본 발명의 방법들을 수행하기 위한 단위로서 선전, 유통 또는 판매된다.
본 분야의 숙련가에 의하여 이해되는 바와 같이, 본원에서 "약" 값 또는 파라미터에 대한 언급은 상기 값 또는 파라미터 그 자체에 관한 구현예를 포함한다 (그리고 기재한다). 예를 들면, "약 X"를 언급하는 기술은 "X"의 언급을 포함한다.
본원에 기재된 발명의 측면 및 구현예는 "구성되는(consisting) 및/또는 "~로 본질적으로 구성되는"의 측면 및 구현예를 포함하는 것으로 이해된다. 본원에 사용된 것으로서, 단수 용어("a," "an" 및 "the")는, 내용이 달리 명확하게 표지되지 않는 한 다수의 지시대상을 포함한다.
II. 방법 및 용도
G9a의 길항제를 사용하는 방법 (예를 들어 암을 치료하고/하거나 약물 내성을 예방하기 위한 (예컨대, 단일 제제 및/또는 조합 요법으로)) 방법이 본원에 제공된다. 예를 들어, 개체에서 암을 치료하는 방법은 G9a의 길항제 단독으로, 또는 암 요법 제제와 조합하여 상기 대상체에게 투여하는 단계를 포함한다. 일부 구현예에서, 상기 개체는 암 요법 제제에 의한 치료 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)을 위하여 선택된다. 일부 구현예에서, 상기 개체는 암 요법 제제에 의한 치료 전에 G9a의 길항제의 투여를 포함하는 치료를 개시한다. 일부 구현예에서, 상기 개체는 암 요법 제제 및 G9a의 길항제를 포함하는 치료를 동시에 수용한다. 일부 구현예에서, G9a의 길항제는 암 민감도의 기간을 증가시키고/시키거나 암 내성의 진행을 지연시킨다.
또한, G9a의 길항제 및 암 요법 제제를 이용하는 방법 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)이 본원에 제공된다.
특히, 개체에서 암을 치료하는 방법으로서, 상기 개체에게 (a) G9a의 길항제 및 (b) 암 요법 제제를 투여하는 단계 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)를 포함하는 방법이 본원에 제공된다. 일부 구현예에서, G9a의 길항제 및 암 요법 제제의 각각의 양은 암 민감도의 기간을 증가시키고/시키거나 암 요법 제제에 대한 세포 내성의 진행을 지연시키는데 유효하다. 일부 구현예에서, G9a의 길항제 및 암 요법 제제의 각각의 양은 암 요법 제제를 포함하는 암 치료의 효능을 증가시키는데 유효하다. 예를 들어, 일부 구현예에서, G9a의 길항제 및 암 요법 제제의 각각의 양은 G9a의 길항제 없이 (이의 부재하에) 암 요법 제제의 유효량을 투여하는 것을 포함하는 치료 (예컨대, 표준 돌봄 치료)와 비교하여, 암 요법 제제를 포함하는 암 치료의 효능을 증가시키는데 유효하다. 일부 구현예에서, G9a의 길항제 및 암 요법 제제의 각각의 양은 G9a의 길항제 없이 (이의 부재하에) 암 요법 제제의 유효량을 투여하는 것을 포함하는 치료 (예컨대, 표준 돌봄 치료)와 비교하여, 반응을 증가시키는데 (예컨대, 완전한 반응) 유효하다. 일부 구현예에서, G9a의 길항제 및 암 요법 제제는 동시에 투여된다. 일부 구현예에서, 암 요법 제제는, 표적화된 요법, 화학요법, 및/또는 방사성요법이다. 일부 구현예에서, 표적화된 요법 및/또는 화학요법은 EGFR 길항제, RAF 억제제, PI3K 억제제, 탁산, 및 백금 제제 중 하나 이상이다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) EGFR 길항제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) RAF 억제제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) PI3K 억제제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) 탁산 (예컨대, 파클리탁셀)을 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) 백금 제제 (예컨대, 카보플라틴 또는 시스플라틴)을 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제, (b) 탁산 (예컨대, 파클리탁셀), (c) 백금 제제 (예컨대, 카보플라틴 또는 시스플라틴)을 포함한다. 일부 구현예에서, 탁산은 파클리탁셀이다.
또한, 개체에서 암 요법 제제를 포함하는 암 치료 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)의 효능을 증가시키는 방법으로서, 상기 개체에 하기를 투여하는 단계를 포함하는 방법이 추가로 본원에 제공된다: (a) 유효량의 G9a의 길항제 및 (b) 유효량의 암 요법 제제. 일부 구현예에서, G9a의 길항제 및 암 요법 제제는 동시에 투여된다. 일부 구현예에서, 암 요법 제제는, 표적화된 요법, 화학요법, 및/또는 방사성요법이다. 일부 구현예에서, 표적화된 요법 및/또는 화학요법은 EGFR 길항제, RAF 억제제, PI3K 억제제, 탁산, 및 백금 제제 중 하나 이상이다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) EGFR 길항제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) RAF 억제제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) PI3K 억제제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) 탁산 (예컨대, 파클리탁셀)을 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) 백금 제제 (예컨대, 카보플라틴 또는 시스플라틴)을 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제, (b) 탁산 (예컨대, 파클리탁셀), (c) 백금 제제 (예컨대, 카보플라틴 또는 시스플라틴)을 포함한다. 일부 구현예에서, 탁산은 파클리탁셀이다.
개체에서 암을 치료하는 방법이 본원에 제공되고, 여기서 암 치료는 상기 개체에 (a) 유효량의 G9a의 길항제 및 (b) 유효량의 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)를 투여하는 것을 포함하고, 상기 암 치료는 G9a의 길항제 없이 (이의 부재하에) 암 요법 제제의 유효량을 투여하는 것을 포함하는 치료 (예컨대, 표준 돌봄 치료)와 비교하여, 증가된 효능을 갖는다. 일부 구현예에서, G9a의 길항제 및 암 요법 제제는 동시에 투여된다. 일부 구현예에서, 암 요법 제제는, 표적화된 요법, 화학요법, 및/또는 방사성요법이다. 일부 구현예에서, 표적화된 요법 및/또는 화학요법은 EGFR 길항제, RAF 억제제, PI3K 억제제, 탁산, 및 백금 제제 중 하나 이상이다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) EGFR 길항제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) RAF 억제제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) PI3K 억제제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) 탁산 (예컨대, 파클리탁셀)을 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) 백금 제제 (예컨대, 카보플라틴 또는 시스플라틴)을 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제, (b) 탁산 (예컨대, 파클리탁셀), (c) 백금 제제 (예컨대, 카보플라틴 또는 시스플라틴)을 포함한다. 일부 구현예에서, 탁산은 파클리탁셀이다.
또한, 개체에서 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)에 내성인 암의 진행을 지연시키고/시키거나 예방하는 방법으로서, 상기 개체에 하기를 투여하는 단계를 포함하는 방법이 추가로 본원에 제공된다: (a) 유효량의 G9a의 길항제 및 (b) 유효량의 암 요법 제제. 일부 구현예에서, G9a의 길항제 및 암 요법 제제는 동시에 투여된다. 일부 구현예에서, 암 요법 제제는, 표적화된 요법, 화학요법, 및/또는 방사성요법이다. 일부 구현예에서, 표적화된 요법 및/또는 화학요법은 EGFR 길항제, RAF 억제제, PI3K 억제제, 탁산, 및 백금 제제 중 하나 이상이다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) EGFR 길항제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) RAF 억제제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) PI3K 억제제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) 탁산 (예컨대, 파클리탁셀)을 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) 백금 제제 (예컨대, 카보플라틴 또는 시스플라틴)을 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제, (b) 탁산 (예컨대, 파클리탁셀), (c) 백금 제제 (예컨대, 카보플라틴 또는 시스플라틴)을 포함한다. 일부 구현예에서, 탁산은 파클리탁셀이다.
암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)에 내성이 진행될 증가된 공산을 갖는, 암을 갖는 개체를 치료하는 방법으로서, 상기 개체에 하기를 투여하는 단계를 포함하는 방법이 본원에 제공된다: (a) 유효량의 G9a의 길항제 및 (b) 유효량의 암 요법 제제. 일부 구현예에서, G9a의 길항제 및 암 요법 제제는 동시에 투여된다. 일부 구현예에서, 암 요법 제제는, 표적화된 요법, 화학요법, 및/또는 방사성요법이다. 일부 구현예에서, 표적화된 요법 및/또는 화학요법은 EGFR 길항제, RAF 억제제, PI3K 억제제, 탁산, 및 백금 제제 중 하나 이상이다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) EGFR 길항제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) RAF 억제제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) PI3K 억제제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) 탁산 (예컨대, 파클리탁셀)을 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) 백금 제제 (예컨대, 카보플라틴 또는 시스플라틴)을 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제, (b) 탁산 (예컨대, 파클리탁셀), (c) 백금 제제 (예컨대, 카보플라틴 또는 시스플라틴)을 포함한다. 일부 구현예에서, 탁산은 파클리탁셀이다.
또한, 암을 갖는 개체에서 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)에 대한 민감도를 증가시키는 방법으로서, 상기 개체에 하기를 투여하는 단계를 포함하는 방법이 추가로 본원에 제공된다: (a) 유효량의 G9a의 길항제 및 (b) 유효량의 암 요법 제제. 일부 구현예에서, G9a의 길항제 및 암 요법 제제는 동시에 투여된다. 일부 구현예에서, 암 요법 제제는, 표적화된 요법, 화학요법, 및/또는 방사성요법이다. 일부 구현예에서, 표적화된 요법 및/또는 화학요법은 EGFR 길항제, RAF 억제제, PI3K 억제제, 탁산, 및 백금 제제 중 하나 이상이다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) EGFR 길항제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) RAF 억제제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) PI3K 억제제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) 탁산 (예컨대, 파클리탁셀)을 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) 백금 제제 (예컨대, 카보플라틴 또는 시스플라틴)을 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제, (b) 탁산 (예컨대, 파클리탁셀), (c) 백금 제제 (예컨대, 카보플라틴 또는 시스플라틴)을 포함한다. 일부 구현예에서, 탁산은 파클리탁셀이다.
또한, 암을 갖는 개체에서 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법) 민감도의 기간을 연장시키는 방법으로서, 상기 개체에 하기를 투여하는 단계를 포함하는 방법이 추가로 본원에 제공된다: (a) 유효량의 G9a의 길항제 및 (b) 유효량의 암 요법 제제. 일부 구현예에서, G9a의 길항제 및 암 요법 제제는 동시에 투여된다. 일부 구현예에서, 암 요법 제제는, 표적화된 요법, 화학요법, 및/또는 방사성요법이다. 일부 구현예에서, 표적화된 요법 및/또는 화학요법은 EGFR 길항제, RAF 억제제, PI3K 억제제, 탁산, 및 백금 제제 중 하나 이상이다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) EGFR 길항제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) RAF 억제제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) PI3K 억제제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) 탁산 (예컨대, 파클리탁셀)을 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) 백금 제제 (예컨대, 카보플라틴 또는 시스플라틴)을 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제, (b) 탁산 (예컨대, 파클리탁셀), (c) 백금 제제 (예컨대, 카보플라틴 또는 시스플라틴)을 포함한다. 일부 구현예에서, 탁산은 파클리탁셀이다.
또한, 암을 갖는 개체에서 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)에 대한 반응 기간을 연장시키는 방법으로서, 상기 개체에 하기를 투여하는 단계를 포함하는 방법이 추가로 본원에 제공된다: (a) 유효량의 G9a의 길항제 및 (b) 유효량의 암 요법 제제. 일부 구현예에서, G9a의 길항제 및 암 요법 제제는 동시에 투여된다. 일부 구현예에서, 암 요법 제제는, 표적화된 요법, 화학요법, 및/또는 방사성요법이다. 일부 구현예에서, 표적화된 요법 및/또는 화학요법은 EGFR 길항제, RAF 억제제, PI3K 억제제, 탁산, 및 백금 제제 중 하나 이상이다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) EGFR 길항제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) RAF 억제제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) PI3K 억제제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) 탁산 (예컨대, 파클리탁셀)을 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) 백금 제제 (예컨대, 카보플라틴 또는 시스플라틴)을 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제, (b) 탁산 (예컨대, 파클리탁셀), (c) 백금 제제 (예컨대, 카보플라틴 또는 시스플라틴)을 포함한다. 일부 구현예에서, 탁산은 파클리탁셀이다.
암에 대한 개선된 치료를 제공하는 것에 더하여, 본원에 기술된 특정 구현예의 투여는, 상이한 치료를 수용하는 상동한 환자에 의하여 경험된 삶의 질과 비교하여, 환자의 삶의 질을 개선할 수 있다. 예를 들어, 개체에 본원에 기술된 G9a의 길항제 및 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)의 조합을 투여하는 것은, 암 요법 제제를 단독으로 수용할 경우 상동한 환자에 의하여 경험된 삶의 질과 비교하여, 환자의 삶의 질을 개선할 수 있다. 예를 들어, 본원에 기술된 상기 조합에 의한 조합 요법은 필요한 암 요법 제제의 투여량을 낮추어, 이로써 치료제와 연관된 부작용 (예컨대, 구역질, 구토, 탈모, 발진, 식욕 감퇴, 체중 감소 등)을 경화시킬 수 있다. 상기 조합은 또한 종양 부하 및 연관된 부작용, 예컨대 통증, 기관 기능부전, 체중 감소 등을 감소하는 것을 야기할 수 있다. 따라서, 일 양태는 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)로 암에 대한 치료를 받는 환자의 삶의 질을 개선시키기 위한 치료적 용도를 위한 G9a의 길항제를 제공한다. 일부 구현예에서, G9a의 길항제 및 암 요법 제제는 동시에 투여된다. 일부 구현예에서, 암 요법 제제는, 표적화된 요법, 화학요법, 및/또는 방사성요법이다. 일부 구현예에서, 표적화된 요법 및/또는 화학요법은 EGFR 길항제, RAF 억제제, PI3K 억제제, 탁산, 및 백금 제제 중 하나 이상이다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) EGFR 길항제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) RAF 억제제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) PI3K 억제제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) 탁산 (예컨대, 파클리탁셀)을 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) 백금 제제 (예컨대, 카보플라틴 또는 시스플라틴)을 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제, (b) 탁산 (예컨대, 파클리탁셀), (c) 백금 제제 (예컨대, 카보플라틴 또는 시스플라틴)을 포함한다. 일부 구현예에서, 탁산은 파클리탁셀이다.
상기 방법들의 일부 구현예에서, G9a의 길항제는 천연 또는 합성 기원이다. 상기 방법들의 일부 구현예에서, G9a의 길항제는 항체, 결합 폴리펩티드, 결합 소분자, 또는 폴리뉴클레오티드이다.
상기 방법들의 일부 구현예에서, 암 요법 제제는 표적화된 요법이다. 상기 방법들의 일부 구현예에서, 암 요법 제제는 화학요법이다. 상기 방법들의 일부 구현예에서, 암 요법 제제는 방사성요법이다.
본원에 사용된 바와 같이, 요법에 대해 내성을 갖는 암은, 상기 요법에 대해 현저한 반응 (예컨대, 부분적 반응 및/또는 완전한 반응)을 생성할 능력이 감소되고/되거나 비-반응성인 암을 포함한다. 내성은 치료 방법의 절차 내에서 발생하는 획득된 내성일 수 있다. 일부 구현예에서, 획득된 약물 내성은 일시적 및/또는 가역적 약물 내성이다. 요법에 대한 일시적 및/또는 가역적 약물 내성은, 치료 방법의 휴지기 후 상기 요법에 대한 민감도를 다시 얻을 수 있는 것을 포함한다. 일부 구현예에서, 획득된 내성은 영구적인 내성이다. 요법에 대한 영구적인 내성은 약물 내성을 부여하는 유전적 변화를 포함한다.
본원에 사용된 바와 같이, 요법에 대해 민감도를 갖는 암은, 상기 요법에 대해 현저한 반응 (예컨대, 부분적 반응 및/또는 완전한 반응)을 생성할 수 있고/있거나 반응성인 암을 포함한다.
요법에 대한 민감도의 유지 및/또는 내성 획득을 측정하거나 평가하는 방법은 당해기술에 공지되어 있고 실시예에 기술된다. 약물 내성 및/또는 민감도는 하기에 의하여 측정될 수 있다: (a) 참조 암 세포 또는 세포 집단을, G9a의 길항제의 존재 및/또는 부재 하에서 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)에 노출시키는 단계; 및/또는 (b) 예를 들어, 하기 중 하나 이상을 검정하는 단계: 암 세포 성장, 세포 생존력, 세포사멸 수준 및/또는 백분율, 히스톤 3 리신 9 (H3K9) 메틸화 수준 (예컨대, 모노메틸화, 디메틸화, 및/또는 트리메틸화), 및/또는 반응.
일부 구현예에서, 약물 내성 및/또는 민감도는 G9a의 길항제의 양 및/또는 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)의 다양한 농도에서, 및/또는 시간에 걸쳐 측정될 수 있다. 약물 내성 및/또는 민감도는 추가로, 하기를 포함하는 참조 세포주 (예컨대, PC9 및/또는 H1299)와 비교하여 측정 및/또는 비교될 수 있다: 상기 세포주의 친계 세포, 약물 내성 존속성균 세포, 및/또는약물 내성 증식된 존속성균 세포. 일부 구현예에서, 세포 생존력은 CyQuant 직접 세포 증식 검정에 의하여 검정될 수 있다. 내성의 획득 및/또는 민감도 유지에서의 변화, 예컨대 약물 내성은 실시예 및 Sharma et al에서 기술된 바와 같이 약물 내성 존속성균의 성장을 검정함으로써 평가될 수 있다. 내성의 획득 및/또는 민감도 유지에서의 변화, 예컨대 영구 내성 및/또는 증식된 내성체(resisters)는 실시예 및 Sharma et al에서 기술된 바와 같이 약물 내성 증식된 존속성균의 성장을 검정함으로써 평가될 수 있다. 일부 구현예에서, 내성은 약물 내성 존속성균 및/또는 약물 내성 증식된 존속성균에서의 종양 성장의 IC50, EC50 변화 또는 감소에 의해 표지될 수 있다. 일부 구현예에서, 상기 변화는 약 50%, 100%, 및/또는 200% 중 임의의 것의 초과이다. 추가로, 내성 획득 및/또는 민감도 유지는, 예를 들어 반응, 반응의 기간, 및/또는 요법에 대한 진행 시간 (예컨대, 부분적 반응 및 완전한 반응)을 평가함에 의하여 생체내 평가될 수 있다. 내성 획득 및/또는 민감도 유지의 변화는, 하기에 대한 변화를 기반으로 할 수 있다: 반응, 반응의 기간, 및/또는 개체 집단에서의 요법에 대한 진행 시간 (예컨대, 부분적 반응 및 완전한 반응의 수).
상기 방법들의 일부 구현예에서, 암은 고형 종양 암이다. 일부 구현예에서, 암은 폐암, 유방암, 결장직장암, 결장암, 흑색종 및/또는 췌장암이다. 일부 구현예에서, 암은 폐암(예컨대, 비-소세포 폐암(NSCLC))이다. 일부 구현예에서, 암은 유방암이다. 일부 구현예에서, 암은 고수준의 H3K9 트리메틸화를 갖는다. 일부 구현예에서, 암은 고수준의 H3K9 디메틸화를 갖는다. 일부 구현예에서, 암은 고수준의 H3K9 모노메틸화를 갖는다. 일부 구현예에서, 암은 증가하는 수준의 H3K9 트리메틸화가 발병될 위험에 처해있다. 일부 구현예에서, 암은 증가하는 수준의 H3K9 디메틸화가 발병될 위험에 처해있다. 일부 구현예에서, 암은 증가하는 수준의 H3K9 모노메틸화가 발병될 위험에 처해있다.
G9a의 길항제 및 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)을 포함하는 치료 방법을 개시할 경우, 본원에 기술된 조합 요법 방법 중 임의의 것에서의 암은 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)만을 포함하는 치료 방법과 비교하여 민감할 수 있다 (민감성의 예시는 비제한적으로 하기를 포함한다: 현저한 반응 (예컨대, 부분적 반응 및/또는 완전한 반응)을 생성할 수 있고/있거나 반응성임). G9a의 길항제 및 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)을 포함하는 치료 방법을 개시할 경우, 본원에 기술된 조합 요법 방법 중 임의의 것에서의 암은 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)만을 포함하는 치료 방법과 비교하여 비-내성일 수 있다 (비-내성의 예시는 비제한적으로 하기를 포함한다: 현저한 반응 (예컨대, 부분적 반응 및/또는 완전한 반응)을 생성할 수 없고/없거나, 이의 감소된 능력을 갖고/갖거나 비-반응성임).
상기 방법들의 일부 구현예에서, 상기 구현예 중 임의의 것에 따른 "개체"는 인간일 수 있다.
상기 방법들의 일부 구현예에서, 조합 요법은 동시에 투여될 수 있다. 상기 방법들의 일부 구현예에서, 조합 요법은 병용 투여 (2 또는 그 초과 치료제가 동일 또는 개별의 제형에 포함되는 경우), 및 개별 투여를 포함하고, 이 경우에, 본 발명의 항체 또는 G9a의 길항제 및 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)의 투여는 추가 치료제 및/또는 보조제의 투여 이전에, 동시간에, 순차로, 동시에, 및/또는 이후에 발생할 수 있다. 일부 구현예에서, G9a의 길항제는 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법) 이전에 및/또는 이와 동시에 투여된다. 일부 구현예에서, 조합 요법은 추가로 방사성 요법 및/또는 추가의 치료 제제를 포함한다.
상기 방법들의 일부 구현예에서, G9a의 길항제 및 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)은 경우, 비경구, 폐내 및 비강내 및 경우에 따라 국소 치료를 위해, 병변내 투여를 포함하는 임의의 적합한 수단에 의해 투여될 수 있다. 비경구 주입은 근육내, 정맥내, 동맥내, 복강내, 또는 피하 투여를 포함한다. 복용은 모든 적합한 경로, 예컨대 부분적으로 상기 투여가 간단한 것이냐 또는 만성적인 것이냐에 따라, 주사, 예컨대 정맥내 또는 피하 주사에 의해 이루어진다. 비제한적으로 다양한 시점에 걸친 단일 또는 다중 투여, 볼루스 투여 및 펄스 주입을 비롯한 다양한 복용 스케줄이 본원에 고안되었다.
상기 방법들의 일부 구현예에서, 본원에 기술된 G9a의 길항제 (예컨대, 항체, 결합 폴리펩티드, 및/또는 결합 소분자) 및 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)는 양호한 의학적 실시와 일치하는 방식으로 제형화, 복용, 및 투여될 수 있다. 이러한 맥락에서 고려 요인은 치료되는 특정한 장애, 치료되는 특정한 포유동물, 개별적인 환자의 임상적 조건, 장애의 원인, 제제의 전달 부위, 투여 방법, 투여 계획, 및 의료 종사자에게 공지인 다른 요인을 포함한다. G9a의 길항제 및 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)은, 그럴 필요는 없지만, 해당 장애를 예방 또는 치료하기 위하여 현재 사용되는 하나 이상의 제제와 함께 임의로 제형화된다. 유효량의 그러한 다른 제제는 제형에 존재하는 G9a의 길항제 및 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)의 양, 장애 또는 치료의 유형, 및 위에서 논의된 다른 요인에 의존한다. 이들은 일반적으로 본원에 기재된 바와 같은 투여 경로, 또는 본원에 기재된 용량의 약 1 내지 99% 또는 경험적으로/임상적으로 적당한 것으로 결정된 임의의 용량 및 임의의 경로와 함께 동일한 용량으로 사용된다.
질환의 예방 또는 치료를 위해, (단독으로 또는 하나 또는 그 초과 다른 추가 치료제와 병용하여 사용될 때) 본원에 기술된 G9a의 길항제 및 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)의 적절한 복용량은 치료받는 질환의 유형, G9a의 길항제 및 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)의 유형, 중증도 및 질환의 추이, 항체 또는 면역접합체가 예방적 또는 치료적 목적으로 투여되는지 여부, 이전의 요법, G9a의 길항제 및 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)에 대한 환자의 임상 이력 및 반응, 및 주치의의 재량에 의존할 것이다. G9a의 길항제 및 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)은 한 번에 또는 일련의 치료에 걸쳐 환자에게 적당하게 투여된다. 여러 날 또는 더 길게 반복적인 투여를 하는 경우, 상태에 따라, 상기 치료는 일반적으로 질병의 증상의 바람직한 억제가 일어날 때까지 지속될 것이다. 그러한 용량은 간헐적으로, 예를 들어, 매주마다 또는 3주마다 투여될 수 있다 (예컨대, 따라서 환자가 약 2 회 내지 약 20 회, 또는 예컨대 약 6 회 용량의 G9a의 길항제 및 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)를 투여받는다). 최초의 더 많은 로딩 용량에 이어, 하나 이상의 더 적은 용량이 투여될 수 있다. 예시적인 투여 레지멘은 투여를 포함한다. 그러나, 다른 투여 레지멘이유용할 수 있다. 이러한 요법의 진행은 전통적인 기술과 검정에 의해 쉽게 모니터링된다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) EGFR 길항제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) RAF 억제제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) PI3K 억제제를 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) 탁산 (예컨대, 파클리탁셀)을 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제 및 (b) 백금 제제 (예컨대, 카보플라틴 또는 시스플라틴)을 포함한다. 일부 구현예에서, 조합 요법은 (a) G9a 길항제, (b) 탁산 (예컨대, 파클리탁셀), (c) 백금 제제 (예컨대, 카보플라틴 또는 시스플라틴)을 포함한다.
임의의 상기 제형 또는 치료 방법이 G9a의 길항제 및 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)로서의 면역접합체를 사용하여 수행될 수 있음이 이해된다.
III. 치료 조성물
본원에 제공된 방법에서의 사용을 위하여 G9a의 길항제 및 암 요법 제제를 사용하는 조합 요법 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)를 포함하는 조합이 본원에 제공된다. 특정 구현예에서, 상기 조합은 단독으로 투여된 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)의 효능을 증가시킨다. 특정 구현예에서, 상기 조합은 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)에 대해 내성인 암의 진행을 지연하고/하거나 예방한다. 특정 구현예에서, 상기 조합은 암을 갖는 개체에서의 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)의 민감도의 기간을 연장시킨다. 일부 구현예에서, G9a의 길항제 및/또는 암 요법 제제를 사용하는 조합 요법 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법) (예컨대, EGFR 길항제, PI3K 길항제, 및/또는 RAF 억제제)는 항체, 결합 폴리펩티드, 결합 소분자 및/또는 폴리뉴클레오티드이다. G9A는 진정염색질 내에서 히스톤 H3 (H3K9me1 및 H3K9me2 각각)의 'Lys-9’를 특이적으로 모노- 및 디메틸화하는 히스톤 메틸전달효소이다. H3K9me는, HP-1 단백질을 메틸화된 히스톤으로 동원함으로써 후성적 전사 억제에 대한 특정 태그를 나타낸다. G9a는 또한, 라민 관련 도메인에 대한 동원을 매개하고/하거나 DNA 메틸화를 개시하는 이질염색질에서 기능할 수 있다.
G9a의 길항제의 임의의 일부 구현예에서, G9a의 길항제는 약 4 μM, 2 μM, 1 μM, 500 nM, 250 nM, 200 nM, 150 nM, 100 nM, 75 nM, 50 nM, 및/또는 30 nM 중 임의의 것보다 양호 (예컨대, 이의 미만)의 G9a IC50 를 갖는다. 화합물에 대한 G9a IC50 를 측정하는 방법은 당해 분야에 공지되어 있다.
G9a의 길항제의 임의의 일부 구현예에서, G9a의 길항제는 약 5 μM, 7.5 μM, 10 μM, 15 μM, 및/또는 20 μM 중 임의의 것보다 초과의 IC50 를 갖는다.
G9a의 길항제의 임의의 일부 구현예에서, G9a의 길항제는 약 25 μM, 15 μM, 10 μM, 7.5 μM, 5 μM, 4 μM, 3.5 μM, 3 μM, 2.5 μM, 2 μM, 및/또는 1 μM 중 임의의 것보다 양호 (예컨대, 이의 미만)의 H3K9me (예컨대, me1, me2, 및/또는 me3) EC50 를 갖는다. 화합물에 대한 H3K9me EC50 를 측정하는 방법은 당해 분야에 공지되어 있다 (참고: Sayegh et al. JBC Manuscript M112.419861 (2013), 하기의 다국적 웹사이트에서 이용가능함: jbc.org/cgi/doi/10.1074/jbc.M112.419861 및 Kristensen et al. FEBS J. 279:1905-1914 (2012), 이는 전문이 본원에 참고로 인용되고 기술됨).
펩티드-의존적 교체 백분율은, 펩티드의 부재하의 교체 백분율을 기질 펩티드 존재하의 교체 백분율로부터 감함으로써 산출한다. 백분율 억제 및 IC50 를 소정의 억제제 농도에서 펩티드-의존적 교체 백분율을 사용하여 산출한다. 각 억제제에 대한 IC50 값의 산출을, GraFit 소프트웨어 (Erithacus Software Ltd., Surrey UK) 를 사용하여 수행하였다.
본원에 기술된 방법에서 사용하기 위한 EGFR 길항제를 또한 제공한다. EGFR는 하기에 기술된 수용체 티로신 키나아제 폴리펩티드 표피 성장 인자 수용체를 의미하며 (하기에 기술됨: Ullrich et al, Nature (1984) 309:418425), 이는 대안적으로 Her-1 및 c-erbB 유전자 산물, 뿐만 아니라 이의 변이체 예컨대 EGFRvIII 로 지칭된다. EGFR 변이체는 또한 결실형, 치환형, 및 삽입형 변이체, 예를 들어, 하기에 기술된 것들을 포함한다: Lynch et al. (NEJM 2004, 350:2129), Paez et al. (Science 2004, 304:1497), Pao et al. (PNAS 2004, 101:13306). 일부 구현예에서, EGFR은 일반적으로 자연발생적 EGFR 단백질의 아미노산 서열을 포함하는 폴리펩티드를 지칭하는 야생헝 EGFR이다. 상기 방법들의 일부 구현예에서, EGFR의 길항제는 항체, 결합 폴리펩티드, 결합 소분자, 및/또는 폴리뉴클레오티드이다.
예시적인 EGFR 길항제 (항-EGFR 항체)는 하기를 포함한다: 항체 예컨대 인간화된 단클론성 항체 (니모투주맙으로 공지됨) (YM Biosciences), 완전 인간 ABX-EGF (파니투무맙, Abgenix Inc.) 뿐만 아니라 완전 인간 항체 (E1.1, E2.4, E2.5, E6.2, E6.4, E2.11, E6. 3 및 E7.6 3으로 공지되고, US 6,235,883; MDX-447 (Medarex Inc)에 기술됨). 퍼투주맙 (2C4)은 HER2에 직접 결합하지만, HER2-EGFR 이량체화를 저해하며, 이로써 EGFR 신호전달을 억제하는 인간화된 항체이다. EGFR에 결합하는 항체의 기타 예시는 하기를 포함한다: GA201 (RG7160; Roche Glycart AG), MAb 579 (ATCC CRL HB 8506), MAb 455 (ATCC CRL HB8507), MAb 225 (ATCC CRL 8508), MAb 528 (ATCC CRL 8509) (참고, US 특허 번호 4,943, 533, Mendelsohn et al) 및 이의 변이체, 예컨대 키메라화된 225 (C225 또는 세툭시맙; ERBUTIX®) 및 재형상화된 인간 225 (H225) (참고, WO 96/40210, Imclone Systems Inc.); IMC-11F8, 완전 인간, EGFR-표적 항체 (Imclone); 유형 II 돌연변이체 EGFR에 결합하는 항체 (US 특허 번호 5,212,290); US 특허 번호 5,891,996에 기재된, EGFR에 결합하는 인간화되고 키메라성인 항체; 및 EGFR에 결합하는 인간 항체, 예컨대 ABX-EGF (참고 WO98/50433, Abgenix); EMD 55900 (Stragliotto et al. Eur . J. Cancer 32A:636-640 (1996)); EMD7200 (마투주맙) EGFR 결합을 위하여 EGF 및 TGF-알파 둘 모두와 경쟁하는 EGFR에 대하여 지향된, 인간화된 EGFR 항체; 및 mAb 806 또는 인간화된 mAb 806 (Johns et al., J. Biol . Chem. 279(29):30375-30384 (2004)). 항-EGFR 항체는 세포독성 제제와 콘주게이트되어 이로써 면역접합체를 생성할 수 있다 (참고: 예를 들어 EP659,439A2, Merck Patent GmbH). 일부 구현예에서, 항-EGFR 항체 세툭시맙이다. 일부 구현예에서, 항-EGFR 항체 파니투무맙이다. 일부 구현예에서, 항-EGFR 항체 자루투무맙, 니모투주맙, 및/또는 마투주맙이다.
상기 방법에 유용한 항-EGFR 항체에는 충분한 친화도 및 특이성으로 EGFR에 결합하고 EGFR의 활성을 감소시키거나 억제할 수 있는 임이의 항체를 포함된다. 선택된 항체는 일반적으로 EGFR에 대한 충분히 강한 결합 친화도를 갖는데, 예를 들어, 상기 항체는 100 nM 내지 1 pM의 Kd 값을 갖는 인간 c-met와 결합할 수 있다. 항체 친화도는, 예를 들면 표면 플라즈몬 공명 기반 분석(예컨대 PCT 출원 공개 번호 WO2005/012359에 기재된 BIAcore 분석); 효소-결합 면역흡착제 분석(ELISA); 및 경쟁 분석(예를 들면 RIA)에 의해 결정될 수 있다. 바람직하게는, 본 발명의 항-EGFR 항체는 질병 또는 질환을 표적으로 삼을 때 및 방해할 때 치료 제제로서 사용될 수 있되, EGFR/EGFR 리간드 활성이 수반된다. 또한 상기 항체는 예컨대, 치료로서 효과성을 평가하기 위해 기타 생물학적 활성 분석을 받을 수 있다. 이와 같은 분석은 당해기술에 알려져 있고 표적 항원 및 상기 항체에 대한 의도된 사용에 의존한다. 일부 구현예에서, EGFR 아암은 T 세포 수용체 분자 (예를 들어, CD2 또는 CD3), 또는 IgG (FcγR)에 대한 Fc 수용체 예컨대 FcγRI (CD64), FcγRII (CD32) 및 FcγRIII (CD16)의 백혈구 상에서 특정 항원을 발현하는 세포에 세포 방어 기전을 집중시키기 위하여 촉발 분자에 결합하는 아암과 조합될 수 있다. 이중특이적 항체는 또한 EGFR를 발현하는 세포에 세포독성제를 국소화하는데 사용될 수 있다. 이러한 항체는 항원-결합 아암 및 세포독성 제제 (예컨대. 사포린, 항-인터페론-α, 빈카 알칼로이드, 리신 A 쇄, 메토트렉세이트 또는 방사성 동위원소 합텐)에 결합하는 아암을 갖는다. 이중특이성 항체는 전장 항체 또는 항체 단편 (예컨대, F(ab')2 이중특이적 항체)으로 제조될 수 있다.
예시적인 EGFR 길항제는 또한 하기에 기술된 화합물과 같은 결합 소분자를 포함한다: US5616582, US5457105, US5475001, US5654307, US5679683, US6084095, US6265410, US6455534, US6521620, US6596726, US6713484, US5770599, US6140332, US5866572, US6399602, US6344459, US6602863, US6391874, WO9814451, WO9850038, WO9909016, WO9924037, WO9935146, WO0132651, US6344455, US5760041, US6002008, 및/또는 US5747498. 특정한 결합 소분자 EGFR 길항제는 하기를 포함한다: OSI-774 (CP-358774, 에를로티닙, OSI 의약품); PD 183805 (CI 1033, 2-프로펜아미드, N-[4-[(3-클로로-4-플루오로페닐)아미노]-7-[3-(4-모폴리닐)프로폭시]-6-퀴나졸리닐]-, 디하이드로클로라이드, Pfizer Inc.); Iressa® (ZD1839, 게피티닙, AstraZeneca); ZM 105180 ((6-아미노-4-(3-메틸페닐-아미노)-퀴나졸린, Zeneca); BIBX-1382 (N8-(3-클로로-4-플루오로-페닐)-N2-(1-메틸-피페리딘-4-일)-피리미도[5,4-d]피리미딘-2,8-디아민, Boehringer Ingelheim); PKI-166 ((R)-4-[4-[(1-페닐에틸)아미노]-1H-피롤로[2,3-d]피리미딘-6-일]-페놀); (R)-6-(4-하이드록시페닐)-4-[(1-페닐에틸)아미노]-7H-피롤로[2,3-d]피리미딘); CL-387785 (N-[4-[(3-브로모페닐)아미노]-6-퀴나졸리닐]-2-부틴아미드(butynamid)); EKB-569 (N-[4-[(3-클로로-4-플루오로페닐)아미노]-3-시아노-7-에톡시-6-퀴놀리닐]-4-(디메틸아미노)-2-부텐아미드); 라파티닙 (Tykerb, GlaxoSmithKline); ZD6474 (Zactima, AstraZeneca); CUDC-101 (Curis); 카네르티닙 (CI-1033); AEE788 (6-[4-[(4-에틸-1-피페라지닐)메틸]페닐]-N-[(1R)-1-페닐에틸]-7H-피롤로[2,3-d]피리미딘-4-아민, WO2003013541, Novartis) 및 PKI166 4-[4-[[(1R)-1-페닐에틸]아미노]-7H-피롤로[2,3-d]피리미딘-6-일]-페놀, WO9702266 Novartis). 일부 구현예에서, EGFR 길항제는 N-(3-에틸페닐)-6,7-비스(2-메톡시에톡시)-4-퀴나졸린아민 및/또는 약제학적으로 허용가능한 염 (예컨대, N-(3-에틸페닐l)-6,7-비스(2-메톡시에톡시)-4-퀴나졸린아민-HCl)이다. 일부 구현예에서, EGFR 길항제는 제피티닙, 및/또는 이의 약제학적으로 허용가능한 염이다. 일부 구현예에서, EGFR 길항제는 라파티닙, 및/또는 이의 약제학적으로 허용가능한 염이다. 일부 구현예에서, EGFR 길항제는 제피티닙 및/또는 엘로티닙이다.
일부 구현예에서, EGFR 길항제는 EGFR에 대한 특이적 억제제일 수 있다. 일부 구현예에서, 억제제는 이중 억제제 또는 판(pan) 억제제일 수 있고, EGFR 길항제는 EGFR 및 하나 이상의 표적 폴리펩티드를 억제한다.
포스파티딜이노시톨 3-키나아제 (PI3K)는 포스파티딜이노시톨의 3-하이드록실기를 인산화하는 1차 생화학적 기능을 갖는 지질 키나아제 패밀리에 속한다. PI3K 억제제의 예시는 당해 분야에 공지되어 있으며 비제한적으로 하기를 포함한다: Wortmannin, LY294002, SF1126 (소분자 전구약물, 인테그린-결합 성분에 결합하는 Ly294002의 콘주게이트), NVP-BEZ235 (이미다조퀴놀린(midazoquionline) 유도체), NVP-BGT226, XL765, GDC-0980, PF-04691502, PF-05212384, PKI-587, NVP-BKM120, XL147, PX-866, GDC-0941, GSK615, 및/또는 CAL-101. 일부 구현예에서, PI3K 억제제는 하기에 기술된 화합물이며: WO2009/114874, WO2009/088990, US7511041, US7666901, US7662977, WO2010/046639, US20100105711, WO2010/037765, US20100087440, WO2010034414, US20100075965, US20100075951, US20100075947, WO2010/038165, WO2010/036380, WO2010/059788, WO2010/049481, WO2009/134825, WO2009/123971, WO2009/099163, 및/또는 WO2009/042607, 이의 전체 내용은 본원에 참조로 편입된다.
본원에 기술된 방법에서 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)으로서 유용한 RAF 억제제가 본원에 제공된다. 일부 구현예에서, RAF 억제제는 BRAF 억제제이다. 일부 구현예에서, RAF 억제제는 CRAF 억제제이다. 예시적인 BRAF 키나아제 억제제는 당해 분야에 공지되어 있으며 이는 하기를 포함한다: 예를 들어, 소라페닙, PLX4720, PLX-3603, 다브라페닙 (GSK2118436), GDC-0879, RAF265 (Novartis), XL281, AZ628, ARQ736, BAY73-4506, 베무라페닙 및 하기에 기술된 것들: WO2007/002325, WO2007/002433, WO2009111278, WO2009111279, WO2009111277, WO2009111280 및 미국 특허 번호 7,491,829. 일부 구현예에서, BRAF 억제제는 선택적 BRAF 억제제이다. 일부 구현예에서, BRAF 억제제는 BRAF V600의 선택적 억제제이다. 일부 구현예에서, BRAF V600은 BRAF V600E, BRAF V600K, 및/또는 V600D이다. 일부 구현예에서, BRAF V600는 BRAF V600R이다. 일부 구현예에서, BRAF 억제제는 베무라페닙이다. 일부 구현예에서, BRAF 억제제는 베무라페닙이다.
베무라페닙 (RG7204, PLX-4032, CAS Reg. No. 1029872-55-5)은 다양한 암 세포주(call lines), 예를 들어, 흑색종 세포주에서의 프로그램된 세포사를 야기하는 것으로 나타났다. 베무라페닙은, BRAF가 통상적 V600E 돌연변이를 갖는 경우, BRAF/MEK/ERK 경로 상에서의 BRAF/MEK 단계를 저해한다. 베무라페닙은 환자, 예를 들어 암이 V600E BRAF 돌연변이 (즉, BRAF 단백질 상의 아미노산 위치 번호 600에서, 정상 발린이 글루탐산으로 교체되는, FDA에 의하여 승인된 흑색종 환자 내에서 작용한다. 흑색종의 약 60%가 V600E BRAF 돌연변이를 갖는다. V600E 돌연변이는 하기를 포함하는 다양한 암에 존재한다: 림프종, 결장암, 흑색종, 갑상선압 및 폐암. 베무라페닙은 하기 구조를 갖는다:
ZELBORAF® (베무라페닙) (Genentech, Inc.)는 미국에서 승인되고, FDA-승인된 시험으로 검출 시, BRAF V600E 돌연변이로 절제불가능한 또는 전이성의 흑색종을 갖는 환자를 치료하기 위해 표지된 약물 생성물이다. ZELBORAF® (베무라페닙)은 BRAF V600E 돌연변이 (야생형 BRAF 흑색종)이 없는 흑색종 환자에서의 용도로는 비추천된다.
본원에 기술된 방법에서 백금계 제제의 길항제 및 암 요법 제제를 사용하는 조합 요법 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)으로서 유용한 백금계 제제가 본원에 제공된다. 백금계 제제의 예시는 비제한적으로 하기를 포함한다: 시스플라틴, 카보플라틴, 옥살리플라틴, 사트라플라틴, 피코플라틴, 네다플라틴, 및/또는 트리플라틴. 일부 구현예에서, 백금계 제제는 시스플라틴이다. 일부 구현예에서, 백금계 제제는 카보플라틴이다.
본원에 기술된 방법에서 탁산의 길항제 및 암 요법 제제를 사용하는 조합 요법 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)으로서 유용한 탁산이 또한 본원에 제공된다. 탁산은, 미세소관 조립 및 안정화를 촉진하는 튜불린에 결합할 수 있고/있거나 미세소관 탈폴리머화를 예방할 수 있는 디터펜이다. 본원에서 탁산은 탁소이드 10-데아세틸바카틴 III 및/또는 이의 유도체를 포함한다. 탁산의 예시는, 비제한적으로 하기를 포함한다: 파클리탁셀 (즉, 탁솔, CAS # 33069-62-4), 도세탁셀 (즉, 탁소테르, CAS #114977-28-5), 라로탁셀, 카바지탁셀, 밀라탁셀, 테세탁셀, 및/또는 오라탁셀. 일부 구현예에서, 탁산은 파클리탁셀이다. 일부 구현예에서, 탁산은 도세탁셀이다. 일부 구현예에서, 탁산 is 제형화된 in 크레모포어 (예를 들면, Taxol®) 내에서 Tween 예컨대 폴리소르베이트 80 (예를 들면, Taxotere®)로 제형화된다. 일부 구현예에서, 탁산은 리포좀 봉입된 탁산이다. 일부 구현예에서, 탁산은 탁산의 전구약물 형태 및/또는 콘주게이트된 형태이다 (예컨대, 파클리탁셀, 파클리탁셀 폴리글루멕스, 및/또는 리놀레일 카보네이트-파클리탁셀에 공유적으로 콘주게이트된 DHA). 일부 구현예에서, 파클리탁셀은 실질적으로 계면활성제의 부재하에서 (예컨대, 크레모포어 및/또는 Tween-예컨대 토코솔 파클리탁셀의 부재 하에서) 제형화된다. 일부 구현예에서, 탁산은 알부민-코팅된 나노입자 (예컨대, 아브락산 및/또는 ABI-008)이다. 일부 구현예에서, 탁산은 Taxol®이다.
본원에 기술된 방법에서 빈카 알칼로이드의 길항제 및 암 요법 제제를 사용하는 조합 요법 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)으로서 유용한 빈카 알칼로이드가 본원에 제공된다. 빈카 알칼로이드는 협죽도과(Periwinkle) 식물 일일초(Catharanthus roseus)로부터 원래 유래되었던 항-유사분열 및 항-미세소관 제제의 세트이다. 빈카 알칼로이드의 예는 비제한적으로, 빈블라스틴, 빈크리스틴, 빈데신, 및 비노렐빈을 포함한다. 일부 구현예에서, 빈카 알칼로이드는 비노렐빈이다.
본원에 기술된 방법에서 뉴클레오시드의 길항제 및 암 요법 제제를 사용하는 조합 요법 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)으로서 유용한 뉴클레오시드 유사체가 본원에 제공된다. 뉴클레오시드 유사체의 예시는 비제한적으로 하기를 포함하고: 젬시타빈, 플루다라빈, 6-머캅토퓨린, 티아미프린, 티오구아닌, 안시타빈, 아자시티딘, 6-아자우리딘, 카모푸르, 사이타라빈, 디데옥시우리딘, 독시플루리딘, 에노시타빈, 및/또는 플록수리딘; 일부 구현예에서, 뉴클레오시드 유사체는 젬시타빈이다.
A.항체
본원에 기술된 방법에서의 사용을 위한, 관심 폴리펩티드, 예컨대 G9a에 결합하는 단리된 항체가 본원에 제공된다. 임의의 상기 구현예에서, 항체는 인간화된 것이다. 추가로, 임의의 상기 구현예에 따른 항체는, 키메라성, 인간화, 또는 인간 항체를 포함하여, 단클론성 항체이다. 일 구현예에서, 항체는 항체 단편, 예를 들면, Fv, Fab, Fab', scFv, 디아바디, 또는 F(ab')2 단편이다. 또 다른 구현예에서, 상기 항체는 전장 항체, 예컨대, “온전한 IgG1” 항체 또는 본원에서 정의된 기타 항체 부류 또는 이소형이다.
추가의 측면에서, 상기 임의의 양태에 따른 항체는 하기 섹션에 기재된 바와 같이 단독으로 또는 조합적으로 임의의 특징을 혼입할 수 있다.
1.항체 친화도
특정 구현예에서, 본원에서 제공된 항체는 ≤ 1μM, ≤ 100 nM, ≤ 10 nM, ≤ 1 nM, ≤ 0.1 nM, ≤ 0.01 nM, 또는 ≤ 0.001 nM (예를 들면, 10-8 M 또는 그 미만, 예를 들면, 10-8 M 내지 10-13 M, 예를 들면, 10-9 M 내지 10-13 M)의 해리 상수 (Kd)를 갖는다. 한 구현예에서, Kd는 방사성표지된 항원 결합 검정 (RIA)으로 측정된다. 한 구현예에서, RIA는 해당 항체 및 그 항원의 Fab 버전으로 수행된다. 예를 들어, 항원에 대한 Fab의 용액 결합 친화도은 일련의 적정된 비표지된 항원의 존재하에 최소 농도의 (125I)-표지된 항원으로 Fab를 평형화시키고 이어서 결합된 항원을 항-Fab 항체 코팅된 플레이트로 포획함에 의해 측정된다 (예를 들어, 참고: Chen et al., J. Mol . Biol . 293:865-881(1999)). 검정용 조건을 수립하기 위해, MICROTITER® 다중-웰 플레이트 (Thermo Scientific)는 50 mM 탄산나트륨 (pH 9.6)에서 포착 항-Fab 항체 (Cappel Labs)의 5 μg/ml로 밤새 코팅되고, 그리고 그 뒤에 2 내지 5 시간동안 실온 (대략 23℃)에서 PBS내 2% (w/v) 소 혈청 알부민으로 차단된다. 비-흡착제 플레이트 (Nunc #269620)에서, 100 pM 또는 26 pM [125I]-항원은 해당 Fab의 연속 희석으로 혼합된다 (예를 들면, 항-VEGF 항체, Fab-12의 평가와 일치, Presta et al., Cancer Res. 57:4593-4599 (1997)). 그 다음 해당 Fab는 밤새 항온처리되지만; 그러나, 항온처리는 평형이 달성됨을 확인하기 위해 더 오랜 기간 (예를 들면, 약 65 시간)동안 계속할 수 있다. 그 후에, 혼합물은 실온에서 (예를 들면, 1 시간 동안) 항온처리를 위해 포착 플레이트로 이동된다. 이어서, 상기 용액을 제거하고 플레이트는 PBS 중에서 0.1% 폴리소르베이트 20 (TWEEN-20®)으로 8회 세척하였다. 플레이트를 건조시키는 경우, 150 μl/웰의 섬광제 (MICROSCINT-20 TM; Packard)를 첨가하고 플레이트는 10분 동안 TOPCOUNT TM 감마 카운터 (Packard) 상에서 계수한다. 최대 결합의 20% 이하를 제공하는 각각의 Fab의 농도는 경쟁 결합 검정에 사용하기 위해 선택한다.
또 다른 구현예에 따르면, Kd는 BIACORE® 표면 플라즈몬 공명 검정을 이용하여 측정된다. 예를 들면, BIACORE®-2000 또는 BIACORE®-3000 (BIAcore, Inc., Piscataway, NJ)을 이용한 검정은 ~10 반응 유니트 (RU)에서 고정된 항원 CM5 칩으로 25 ℃에서 수행된다. 한 구현예에서, 카복시메틸화된 덱스트란 바이오센서 칩 (CM5, BIACORE, Inc.)은 공급자의 설명서에 따라 N-에틸-N'-(3-디메틸아미노프로필)-카보디이미드 하이드로클로라이드 (EDC) 및 N-하이드록시석신이미드 (NHS)로 활성화된다. 항원은 pH 4.8, 10 mM 아세트산나트륨으로 5 μg/ml (~0.2 μM)까지 희석되고, 그 다음 5 μl/분의 유속으로 주입되어 커플링된 단백질의 대략 10 반응 유니트 (RU)를 달성한다. 항원 주사 후, 1 M 에탄올아민을 주사하여 미반응된 그룹을 차단시킨다. 역학적 측정을 위해, 2배 연속 희석된 Fab (0.78 nM 내지 500 nM)를 대략 25 μl/min의 유속으로 25°C 에서 PBS 중에서 0.05% 폴리소르베이트 20 (TWEEN-20TM) 계면활성제 (PBST)와 함께 사용한다. 결합율 (kon) 및 해리율 (koff)은 결합 및 해리 센서그램을 동시에 피팅함에 의해 단순한 1 대 1 랑무이르 결합 모델 (BIACORE® 평가 소프트웨어 버젼 3.2)을 사용하여 계산한다. 평형 해리 상수 (Kd)는 비율 koff/kon로서 계산한다. 참고, 예를 들면, Chen et al., J. Mol . Biol . 293:865-881 (1999). 만일 가역속도(on-rate)가 상기 표면 플라즈몬 공명 검정에 의해 106 M- 1 s-1 를 초과하면, 분광기, 예컨대 정지-유동 구비된 분광광도계 (Aviv Instruments) 또는 교반된 큐벳을 갖춘 8000-시리즈 SLM-AMINCOTM 분광광도계 (ThermoSpectronic)에서 측정된 바와 같이 항원의 증가 농도의 존재하에 25 ℃에서 pH 7.2, PBS 내 20 nM 항-항원 항체 (Fab 형태)의 형광 방출 세기 (여기 = 295 nm; 방출 = 340 nm, 16 nm 대역통과)에서의 증가 또는 감소를 측정하는 형광성 켄칭 기술을 이용함으로써 가역 속도는 측정될 수 있다.
2.항체
단편
특정 구현예에서, 본원에 제공된 항체는 항체 단편이다. 항체 단편은 Fab, Fab’, Fab’-SH, F(ab’)2, Fv, 및 scFv 단편, 및 하기된 다른 단편을 포함하지만 이에 제한되지 않는다. 특정 항체 단편의 검토를 위해, 참고 Hudson et al. Nat. Med. 9:129-134 (2003). scFv 단편의 검토를 위하여, 예를 들면, 다음을 참고하며: The Pharmacology of Monoclonal Antibodies, vol. 113, Rosenburg and Moore eds., (Springer-Verlag, New York), pp. 269-315 (1994); 또한 다음을 참고한다: WO 93/16185; 및 미국 특허 번호 5,571,894 및 5,587,458. 에피토프 잔기를 결합하는 회수 수용체를 포함하고 증가된 생체내 반감기를 갖는 Fab 및 F(ab')2 단편의 논의를 위해, 참고 미국 특허 번호 5,869,046.
디아바디는 2가 또는 이중특이적일 수 있는 2개의 항원 결합 부위를 갖는 항체 단편이다. 참고, 예를 들면, EP 404,097; WO 1993/01161; Hudson et al., Nat. Med. 9:129-134 (2003); 및 Hollinger et al., Proc . Natl . Acad . Sci . USA 90: 6444-6448 (1993). 트리아바디 및 테트라바디가 또한 하기에 기술된다: Hudson et al., Nat. Med. 9:129-134 (2003).
단일 도메인 항체는 항체의 중쇄 가변 도메인의 전부 또는 일부를, 또는 항체의 경쇄 가변 도메인의 전부 또는 일부를 포함하는 항체 단편이다. 특정 구현예에서, 단일 도메인 항체는 인간 단일 도메인 항체(Domantis, Inc., Waltham, MA; 예컨대, 미국 특허 제6,248,516호 참조)이다.
항체 단편은, 본원에 기술된 온전한 항체의 단백질분해 소화 뿐만 아니라 재조합 숙주 세포에 의한 생산 (예컨대 이. 콜라이 또는 파지)를 비제한적으로 포함하는 다양한 기술에 의해 제조될 수 있다. 이.
3.키메라 및 인간화된 항체
특정 구현예에서, 본원에 제공되는 항체는 키메라 항체이다. 특정 키메라성 항체는, 예를 들면 하기에 기재되어 있다: 미국 특허 번호 4,816,567 및 Morrison et al., Proc . Natl . Acad . Sci . USA, 81:6851-6855 (1984)). 일 예에서, 키메라 항체는 비-인간 가변 영역(예컨대, 마우스, 래트, 햄스터, 토끼, 또는 비-인간 영장류, 예컨대 원숭이에서 유도된 가변 영역)과 인간 불변영역을 포함한다. 추가의 예에서, 키메라 항체는 부류 또는 하위부류가 모 항체의 부류로부터 변화된 “부류 스위칭된” 항체이다. 키메라 항체는 이의 항원 결합 단편을 포함한다.
특정 구현예에서, 키메라 항체는 인간화된 항체이다. 전형적으로, 비-인간 항체는 인간화되어 인간에 대한 면역원성이 감소되어 있고 모 비-인간 항체의 특이성 및 친화도을 보유한다. 일반적으로, 인간화 항체는, HVR, 예를 들면, CDR, (또는 그 일부)가 비인간 항체로부터 유도되고, FR (또는 그 일부)가 인간 항체 서열로부터 유도되는 하나 또는 그 초과 가변 도메인을 포함한다. 인간화된 항체는 임의로 또한 인간 불변 영역의 적어도 일부를 포함한다. 일부 구현예에서, 인간화 항체에서 일부 FR 잔기는 비인간 항체 (예를 들면, HVR 잔기가 유도되는 항체)로부터 상응하는 잔기로 치환되어, 예를 들면, 항체 특이성 또는 친화도을 회복 또는 개선한다.
인간화 항체 및 이의 제조 방법은, 예를 들면, 하기에 고찰되고: Almagro and Fransson, Front. Biosci . 13: 1619-1633 (2008)에서 검토되었고, 추가로 예컨대, Riechmann et al., Nature 332:323-329 (1988); Queen et al., Proc . Nat’l Acad. Sci . USA 86:10029-10033 (1989); 미국 특허 번호 5,821,337, 7,527,791, 6,982,321, 및 7,087,409; Kashmiri et al., Methods 36:25-34 (2005) (특이성 결정 영역 (SDR) 그라프팅 기재); Padlan, Mol . Immunol . 28:489-498 (1991) ("재표면화" 기재); Dall’Acqua et al., Methods 36:43-60 (2005) ("FR 셔플링" 기재); 및 Osbourn et al., Methods 36:61-68 (2005) 및 Klimka et al., Br. J. Cancer, 83:252-260 (2000) (FR 셔플링에 대한 "유도된 선택" 접근법을 기재함).
인간화를 위해 사용될 수 있는 인간 프레임워크 영역에는 비제한적으로 하기: "최적-피팅" 방법을 이용해서 선택된 프레임워크 영역(예를 들면, 참고: Sims et al. J. Immunol . 151:2296 (1993)); 특정 하위그룹의 경쇄 또는 중쇄 가변 영역의 인간 항체의 공통 서열로부터 유래된 프레임워크 영역 (참고: 예를 들어, Carter et al. Proc . Natl . Acad . Sci . USA, 89:4285 (1992); 및 Presta et al. J. Immunol., 151:2623 (1993)); 인간 성숙(체세포적으로 돌연변이된) 프레임워크 영역 또는 인간 생식선 프레임워크 영역(예를 들면, 참고: Almagro and Fransson, Front. Biosci . 13:1619-1633 (2008)); 및 스크리닝 FR 라이브러리로부터 유래된 프레임워크 영역 (참고: 예를 들어, Baca et al., J. Biol . Chem . 272:10678-10684 (1997) 및 Rosok et al., J. Biol. Chem. 271:22611-22618 (1996)).
4.인간 항체
특정 구현예에서, 본원에 제공된 항체는 인간 항체이다. 인간 항체는 당해기술에 공지된 다양한 기술을 이용하여 생산될 수 있다. 인간 항체는 일반적으로 다음 문헌에 기재되어 있다: van Dijk and van de Winkel, Curr . Opin . Pharmacol. 5: 368-74 (2001) 및 Lonberg, Curr . Opin . Immunol . 20:450-459 (2008).
인간 항체는 항원 자극(challenge)에 반응하여 인간 가변 영역과 온전한 인간 항체 또는 온전한 항체를 만들기 위해 변형된 형질 전환 동물에 면역원을 투여함으로써 제조될 수 있다. 상기 동물은 전형적으로 내인성 면역글로불린 유전자좌를 대체하거나 염색체외적으로 존재하거나 동물의 염색체에 무작위로 통합된 인간 면역글로불린 유전자좌 모두 또는 일부를 함유한다. 상기 형질전환 마우스에서, 내인성 면역글로불린 유전자좌는 일반적으로 불활성화되어 있다. 형질전환 동물로부터 인간 항체를 수득하는 방법의 검토를 위해, 하기를 참조한다: Lonberg, Nat. Biotech. 23:1117-1125 (2005). 또한, 예컨대, 미국 특허 제6,075,181호 및 제6,150,584호(XENOMOUSETM 기술을 설명함); 미국 특허 제 5,770,429호(HuMab® 기술을 설명함); 미국 특허 제7,041,870호(K-M MOUSE® 기술을 설명함), 및 미국 특허 출원 공보 번호 US 2007/0061900(VelociMouse® 기술을 설명함)를 참조한다. 이와 같은 동물에 의해 생성된 온전한 항체의 인간 가변 영역은, 예컨대 상이한 인간 불변영역과 조합함으로써, 추가로 변형될 수 있다.
인간 항체는 또한 하이브리도마 기반 방법에 의해 제조될 수 있다. 인간 단클론성 항체의 제조를 위한 인간 골수종 및 마우스-인간 이종골수종 세포주가 기재되었다. (참고: 예를 들어, Kozbor J. Immunol ., 133: 3001 (1984); Brodeur et al., Monoclonal Antibody Production Techniques and Applications, pp. 51-63 (Marcel Dekker, Inc., New York, 1987); and Boerner et al., J. Immunol., 147: 86 (1991).) 인간 B 세포 하이브리도마 기술을 통해 제조된 인간 항체가 또한 다음 문헌에 기재되어 있다: Li et al., Proc. Natl. Acad. Sci. USA, 103:3557-3562 (2006). 추가의 방법은, 예를 들면, 미국 특허 번호 7,189,826 (하이브리도마 세포주로부터 단클론성 인간 IgM 항체의 생산 기재) 및 Ni, Xiandai Mianyixue, 26(4):265-268 (2006) (인간-인간 하이브리도마 기재)에 기재된 것을 포함한다. 인간 하이브리도마 기술 (Trioma technology)은 또한 다음 문헌에 기재되어 있다: Vollmers and Brandlein, Hist . & Histopath., 20(3):927-937 (2005) 및 Vollmers and Brandlein, Methods Find Exp. Clin. Pharmacol., 27(3):185-91 (2005).
인간 항체는 또한 인간-유도 파지 현시 라이브러리에서 선택된 Fv 클론 가변 도메인 서열을 단리함으로써 생성될 수 있다. 상기 가변 도메인 서열은 이어서 목적하는 인간 불변 도메인과 조합될 수 있다. 항체 라이브러리로부터 인간 항체를 선택하기 위한 기술은 하기에 기재되어 있다.
5.라이브러리-
유래된
항체
항체는 목적 활성 또는 활성들을 갖는 항체를 위한 조합 라이브러리를 가려냄으로써 단리될 수 있다. 예를 들어, 파지 현시 라이브러리를 생성하고 목적 결합 특성을 갖는 항체용 라이브러리를 가려내기 위한 다양한 방법이 당해기술에 알려져 있다. 그러한 방법은 하기에 검토되며: 예컨대, Hoogenboom et al. Methods Mol. Biol . 178:1-37 (O’Brien et al., ed., Human Press, Totowa, NJ, 2001) 추가로 하기에 검토된다: 예를 들어, McCafferty et al., Nature 348:552-554; Clackson et al., Nature 352: 624-628 (1991); Marks et al., J. Mol . Biol . 222: 581-597 (1992); Marks and Bradbury, Methods Mol . Biol . 248:161-175 (Lo, ed., Human Press, Totowa, NJ, 2003); Sidhu et al., J. Mol. Biol. 338(2): 299-310 (2004); Lee et al., J. Mol . Biol . 340(5): 1073-1093 (2004); Fellouse, Proc . Natl. Acad . Sci . USA 101(34): 12467-12472 (2004); 및 Lee et al., J. Immunol . Methods 284(1-2): 119-132(2004).
일부 파아지 현시 방법에서, VH 및 VL 유전자 레퍼토리는 폴리머라제 연쇄 반응(PCR)에 의해 별도로 클로닝되고 파아지 라이브러리에서 무작위로 재조합되며, 이어서 Winter et al., Ann. Rev. Immunol., 12: 433-455 (1994)에 기술된 항원-결합 파아지에 대해 스크리닝된다. 파아지는 전형적으로 단일쇄 Fv (scFv) 단편 또는 Fab 단편으로서 항체 단편을 현시한다. 면역화된 공급원으로부터의 라이브러리는 하이브리도마를 작제할 필요 없이 면역원에 대한 고친화도 항체를 제공한다. 대안적으로, 단순 레퍼토리는 (예를 들면, 인간으로부터) 클로닝되어 Griffiths et al., EMBO J, 12: 725-734 (1993)에 기재된 바와 같이 임의의 면역화 없이 광범위한 비자가 및 또한 자가 항원에 항체의 단일 공급원을 제공할 수 있다. 최종적으로, 순수 라이브러리는 또한 줄기 세포로부터 비재배열된 V-유전자 분절을 클로닝하고 고도의 가변성 CDR3 영역을 암호화하고 시험관내 재배열을 성취하기 위해 무작위 서열을 함유하는 PCR 프라이머를 사용함에 의해 합성적으로 제조될 수 있고, 이는 다음 문헌에 기재된 바와 같다: Hoogenboom and Winter, J. Mol . Biol., 227: 381-388 (1992). 인간 항체 파아지 라이브러리를 기재하는 특허 공보는 예를 들어, 다음의 문헌을 포함한다: 미국 특허 번호 5,750,373, 및 미국 특허 공개 번호 2005/0079574, 2005/0119455, 2005/0266000, 2007/0117126, 2007/0160598, 2007/0237764, 2007/0292936, 및 2009/0002360.
인간 항체 라이브러리에서 단리된 항체 또는 항체 단편은 본원의 인간 항체 또는 인간 항체 단편으로 간주된다.
6.다중특이적 항체
특정 구현예에서, 본원에서 제공된 항체는 다중특이적 항체, 예를 들면, 이중특이적 항체이다. 다중특이적 항체는 최소한 두 개의 상이한 부위에 대해 결합 특이성을 갖는 단클론 항체이다. 특정 구현예에서, 결합 특이성들 중 하나는 관심 폴리펩티드, 예컨대 G9a에 대한 것이고 다른 하나는 임의의 다른 항원에 대한 것이다. 특정 구현예에서, 이중특이적 항체는 관심 폴리펩티드, 예컨대 G9a의 2개의 상이한 에피토프에 결합할 수 있다. 이중특이적 항체는 또한 관심 폴리펩티드, 예컨대 G9a를 발현하는 세포에 세포독성제를 국소화하는데 사용될 수 있다. 이중특이성 항체는 전장 항체 또는 항체 단편으로 제조될 수 있다.
다중특이적 항체를 제조하기 위한 기술은 상이한 특이성을 갖는 2개의 면역글로불린 중쇄-경쇄 쌍의 재조합 공발현 (참조: Milstein and Cuello, Nature 305: 537 (1983)), WO 93/08829, 및 Traunecker et al., EMBO J. 10: 10: 3655 (1991)), 및 "크놉-인-홀" 가공 (참고, 예를 들면, 미국 특허 번호 5,731,168). 다중 특이적 항체는 또한 다음과 같이 제조될 수 있다: 항체 Fc-이종이량체 분자를 제조하기 위한 정전기 스티어링 효과를 가공함에 의해 (WO 2009/089004A1); 2개 이상의 항체 또는 단편을 가교 결합시킴에 의해 (참고, 예를 들면, 미국 특허 번호 4,676,980, 및 Brennan et al., Science, 229: 81 (1985)); 이중특이적 항체를 생산하기 위하여 류신 지퍼(leucine zipper)를 사용함으로써 (참고: 예를 들어, Kostelny et al., J. Immunol ., 148(5):1547-1553 (1992)); 이중특이적 항체 단편을 제조하디 위한 "디아바디" 기술을 사용함으로써 (참고: 예를 들어, Hollinger et al., Proc . Natl . Acad . Sci . USA, 90:6444-6448 (1993)); 및 단일쇄 Fv(sFv) 이량체를 사용함에 의해 (참고: 예를 들어, Gruber et al., J. Immunol., 152:5368 (1994)); 및 다음 문헌에 기재된 바와 같이 3특이적 항체를 제조함에 의해: 예를 들어, Tutt et al. J. Immunol. 147: 60 (1991).
"옥토퍼스 항체"를 포함하는, 3개 이상의 기능성 항원 결합 부위를 갖는 가공된 항체는 또한 본원에 포함된다(문헌참조: 예를 들어 US 2006/0025576A1).
본원에서 항체 또는 단편은 또한 관심 폴리펩티드, 예컨대 G9a 및 또 다른 상이한 항원에 결합하는 항원 결합 부위를 포함하는 "이원 작용 Fab" 또는 "DAF"를 포함한다(문헌참조: 예를 들어 US 2008/0069820).
7.항체 변이체
a)
당화
변이체
특정 구현예에서, 본원에서 제공된 항체는 항체가 당화되는 범위를 증가 또는 감소하기 위해 변경된다. 항체에 대한 당화 부위의 부가 또는 결실은 아미노산 서열을 변경시킴으로써 편리하게 달성될 수 있어서 하나 또는 그 초과 당화 부위는 제조 또는 제거된다.
항체가 Fc 영역을 포함하는 경우, 여기에 부착된 탄수화물은 변경될 수 있다. 포유동물 세포에 의해 생산된 천연 항체는 전형적으로 Fc 영역의 CH2 도메인의 Asn297에 대한 N-연결부에 의해 일반적으로 부착되는 분지형, 2원 올리고당을 포함한다. 참고: 예를 들어, Wright et al. TIBTECH 15:26-32 (1997). 올리고당은 다양한 탄수화물, 예를 들면, 만노스, N-아세틸 글루코사민 (GlcNAc), 갈락토오스, 및 시알산, 뿐만 아니라 2원 올리고당 구조의 "줄기"에서 GlcNAc에 부착된 푸코오스를 포함할 수 있다. 일부 구현예에서, 본 발명의 항체에서 올리고당의 변형은 특정 개선된 특성을 갖는 항체 변이체를 제조하기 위해 실시될 수 있다.
한 구현예에서, Fc 영역에 (직접적으로 또는 간접적으로) 부착된 푸코오스가 부족한 탄수화물 구조를 갖는 항체 변이체가 제공된다. 예를 들면, 상기 항체에서 푸코오스의 양은 1% 내지 80%, 1% 내지 65%, 5% 내지 65% 또는 20% 내지 40%일 수 있다. 푸코오스의 양은, 예를 들어, WO 2008/077546에 기술된 바와 같이, MALDI-TOF 질량 분광측정에 의하여 측정 시, Asn 297에 부착된 모든 당구조(glycostructure) (예를 들어, 복합체, 혼성체 및 고 만노스 구조)의 총합과 비교하여, Asn297에서의 당 쇄 내의 푸코오스의 평균 양을 산출함으로써 측정될 수 있다. Asn297은 Fc 영역에서의 약 위치 297 (Fc 영역 잔기의 Eu 넘버링)에 배치된 아스파라긴 잔기를 언급하지만; 그러나, Asn297은, 항체내 작은 서열 변이로 인해, 위치 297의 약 ± 3 아미노산 업스트림 또는 다운스트림, 즉, 위치 294 와 300 사이에 또한 배치될 수 있다. 이와 같은 푸코실화 변이체은 ADCC 작용을 향상시킬 가능성이 있다. 예컨대, 미국 특허 공보 번호 US 2003/0157108(Presta, L.); US 2004/0093621(Kyowa Hakko Kogyo Co., Ltd)를 참조한다. “탈푸코실화된” 또는 “푸코스-결핍” 항체 변이체와 관련된 공보의 예는 다음을 포함한다: US 2003/0157108; WO 2000/61739; WO 2001/29246; US 2003/0115614; US 2002/0164328; US 2004/0093621; US 2004/0132140; US 2004/0110704; US 2004/0110282; US 2004/0109865; WO 2003/085119; WO 2003/084570; WO 2005/035586; WO 2005/035778; WO2005/053742; WO2002/031140; Okazaki et al. J. Mol . Biol. 336:1239-1249 (2004); Yamane-Ohnuki et al., Biotech. Bioeng. 87: 614 (2004). 탈푸코실화된 항체를 생성할 수 있는 세포주의 예시는 단백질 푸코실화가 결핍된 Lec13 CHO 세포를 포함한다 (Ripka et al. Arch. Biochem . Biophys . 249:533-545 (1986); 미국 특허 출원 번호 US 2003/0157108 A1, Presta, L; 및 WO 2004/056312 A1, Adams et al., 특히 실시예 11), 및 녹아웃 세포주, 예컨대 알파-1,6-푸코실전달효소 유전자, FUT8, 녹아웃 CHO 세포 (참고, 예를 들면, Yamane-Ohnuki et al. Biotech. Bioeng. 87: 614 (2004); Kanda, Y. et al., Biotechnol . Bioeng., 94(4):680-688 (2006); 및 WO2003/085107).
항체 변이체는 이등분한 올리고당으로 추가 제공되고, 예를 들면, 여기에서 항체의 Fc 영역에 부착된 2원 올리고당은 GlcNAc에 의해 이등분된다. 상기 항체 변이체는 푸코실화를 감소시킬 수 있고/있거나 ADCC 기능을 개선시킬 수 있다. 상기 항체 변이체의 예는, 예를 들면, WO 2003/011878 (Jean-Mairet et al.); 미국 특허 번호 6,602,684 (Umana et al.); 및 US 2005/0123546 (Umana et al.)에 기재된다. Fc 영역에 부착된 올리고당에서 적어도 하나의 갈락토오스 잔기를 갖는 항체 변이체가 또한 제공된다. 상기 항체 변이체는 CDC 기능을 개선시킬 수 있다. 상기 항체 변이체는, 예를 들면, WO 1997/30087 (Patel et al.); WO 1998/58964 (Raju, S..); 및 WO 1999/22764 (Raju, S.)에 기재된다.
b)
Fc
영역
변이체
특정 구현예에서, 하나 또는 그 초과 아미노산 변형은 본원에 제공된 항체의 Fc 영역속에 도입될 수 있고, 그렇게 함으로써 Fc 영역 변이체를 발생시킨다. Fc 영역 변이체는 하나 이상의 아미노산 위치에서 아미노산 변형 (예를 들어, 치환)을 포함하는 인간 Fc 영역 서열 (예를 들어, 인간 IgG1, IgG2, IgG3 또는 IgG4 Fc 영역)을 포함할 수 있다.
특정 구현예에서, 본 발명은 모든 효과기 작용은 아니지만 일부 효과기 작용을 지니는 항체 변이체를 고려하며, 이 기능은 상기 항체 변이체를 생체내 항체 반감기가 중요하지만 특정 반응기 기능(예컨대 보체 및 ADCC)은 불필요하거나 해로운 용도에 바람직한 후보로 만든다. 시험관내 및/또는 생체내 세포독성 검정은 CDC 및/또는 ADCC 활성의 경감/고갈을 확인하기 위해 수행될 수 있다. 예를 들면, Fc 수용체 (FcR) 결합 검정은 항체가 FcγR 결합이 부재하지만 (따라서 유사하게 ADCC 활성 부재), FcRn 결합 능력을 보유하는 것을 확보하기 위해 수행될 수 있다. ADCC, NK 세포 매개용 1차 세포는 Fc(RIII) 만을 발현하고, 반면에 단핵구는 Fc(RI), Fc(RII) 및 Fc(RIII)을 발현한다. 조혈 세포상의 FcR 발현은 다음 문헌의 464 페이지 상의 표 3에 요약되어 있다: Ravetch and Kinet, Annu . Rev. Immunol . 9:457-492 (1991). 해당 분자의 ADCC 활성을 평가하기 위한 시험관내 검정의 비-제한적인 예는 하기에 기재된다: 미국 특허 번호 5,500,362 (참고, 예를 들면 Hellstrom, I. et al. Proc . Nat’l Acad . Sci . USA 83:7059-7063 (1986)) 및 Hellstrom, I et al., Proc . Nat’l Acad . Sci . USA 82:1499-1502 (1985); 5,821,337 (참고 Bruggemann, M. et al., J. Exp . Med . 166:1351-1361 (1987)). 대안적으로, 하기와 같은 비-방사능활성 검정 방법이 사용될 수 있다: 예를 들어 하기 참조: 유동 세포측정을 위한 ACTI™ 비-방사능활성 세포독성 검정 (CellTechnology, Inc. Mountain View, CA); 및 CytoTox 96® 비 방사성 세포독성 검정 (Promega, Madison, WI). 그와 같은 분석을 위해 유용한 효과기 세포에는 말초 혈액 단핵구(PBMC) 및 자연 살해(NK) 세포가 포함된다. 대안적으로, 또는 부가적으로, 해당 분자의 ADCC 활성은 하기와 같이 생체내 평가될 수 있다: 예를 들면, 하기에 기술된 바와 같은 동물 모델: Clynes et al. Proc . Nat’l Acad . Sci . USA 95:652-656 (1998). C1q 결합 검정은 또한 항체가 C1q를 결합할 수 없음에 따라서 CDC 활성이 부재임을 확인하기 위해 수행될 수 있다. 참고, 예를 들면, WO 2006/029879 및 WO 2005/100402에서 C1q 및 C3c 결합 ELISA. 보체 활성화를 평가하기 위해, CDC 검정이 수행될 수 있다 (참고, 예를 들면, Gazzano-Santoro et al., J. Immunol . Methods 202:163 (1996); Cragg, M.S. et al., Blood 101:1045-1052 (2003); 및 Cragg, M.S. and M.J. Glennie, Blood 103:2738-2743 (2004)). FcRn 결합 및 생체내 제거/반감기 결정은 또한 당업계에 공지된 방법을 사용하여 수행될 수 있다 (참조: 예를 들어, Petkova, S.B. et al., Int’l. Immunol. 18(12):1759-1769 (2006)).
감소된 효과기 기능을 갖는 항체는 Fc 영역 잔기 238, 265, 269, 270, 297, 327 및 329 중 하나 이상의 치환을 갖는 것을 포함한다 (미국 특허 번호 6,737,056). 상기 Fc 돌연변이체는, 알라닌에 대해 잔기 265 및 297의 치환을 갖는 소위 "DANA" Fc 돌연변이체를 포함하여, 2 또는 그 초과의 아미노산 위치 265, 269, 270, 297 및 327에서 치환을 갖는 Fc 돌연변이체를 포함한다 (미국 특허 번호 7,332,581).
FcRs로의 개선되거나 감소된 결합을 갖는 특정 항체 변이체가 기재되어 있다. (예를 들어, 참고: 미국 특허 번호 6,737,056; WO 2004/056312, 및 Shields et al., J. Biol . Chem . 9(2): 6591-6604 (2001).) 특정 구현예에서, 항체 변이체은 ADCC를 향상시키는 하나 이상의 아미노산 치환, 예컨대, Fc 영역의 위치 298, 333 및/또는 334에서의 치환을 갖는 Fc 영역을 포함한다(잔기의 EU 넘버링). 일부 구현예에서, 변경은 예를 들어 하기에 기술된 바와 같이, 변경된 (즉, 개선되거나 감소된) C1q 결합 및/또는 보체 의존적 세포독성 (CDC)을 유발하는 Fc 영역 내에서 제조된다: 미국 특허 번호 6,194,551, WO 99/51642, 및 Idusogie et al. J Immunol . 164: 4178-4184 (2000).
증가된 반감기 및 태아로의 모체 IgG의 이동에 원인으로 작용하는, 신생아 Fc 수용체 (FcRn)로의 개선된 결합을 갖는 항체 (Guyer et al., J. Immunol . 117:587 (1976) 및 Kim et al., J. Immunol . 24:249 (1994))가 US2005/0014934A1 (Hinton et al.)에 기재된다. 상기 항체는 FcRn에 대한 Fc 영역의 결합을 개선하는 그안에 하나 또는 그 초과 치환을 갖는 Fc 영역을 포함한다. 상기 Fc 변이체는 Fc 영역 잔기: 238, 256, 265, 272, 286, 303, 305, 307, 311, 312, 317, 340, 356, 360, 362, 376, 378, 380, 382, 413, 424 또는 434의 하나 이상에서 치환, 예를 들면, Fc 영역 잔기 434의 치환을 갖는 것을 포함한다 (미국 특허 번호 7,371,826). Fc 영역 변이체의 다른 예에 관하여 또한 하기 참고: Duncan & Winter, Nature 322:738-40 (1988); 미국 특허 번호 5,648,260; 미국 특허 번호 5,624,821; 및 WO 94/29351.
c)시스테인 가공된 항체
변이체
특정 구현예에서, 시스테인 가공된 항체, 예를 들면, 항체의 하나 또는 그 초과 잔기가 시스테인 잔기로 치환되는 "thioMAb,"를 제조하는 것이 바람직할 수 있다. 특정 구현예에서, 치환된 잔기는 항체의 접근가능한 부위에서 발생한다. 상기 잔기를 시스테인으로 치환시킴으로써, 반응성 티올기는 그렇게 함으로써 항체의 접근가능한 부위에 배치되고, 다른 모이어티, 예컨대 약물 모이어티 또는 링커-약물 모이어티에 항체를 콘주게이트하는데 사용되어, 본원에서 추가로 기재된 바와 같이, 면역접합체를 제조할 수 있다. 특정 구현예에서, 하기의 잔기들 중 임의의 하나 이상은 시스테인으로 치환될 수 있다: 경쇄의 V205 (카밧 넘버링); 중쇄의 A118 (EU 넘버링); 및 중쇄 Fc 영역의 S400 (EU 넘버링). 시스테인이 가공된 항체는 예컨대, 미국 특허 제7,521,541호에 기술된 바와 같이 생성될 수 있다.
B.면역접합체
추가로, 본원에 기술된 방법에서 사용하기 위한, 하나 이상의 세포독성 제제, 예컨대 화학요법 제제 또는 약물, 성장 억제제, 독소(예컨대, 단백질 독소, 세균, 곰팡이, 식물 또는 동물에서 유래된 효소차원의 활성 독소, 또는 이것의 단편), 또는 방사성 활성 동위원소에 콘주게이트된 관심 폴리펩티드, 예컨대 G9a 또는 EGFR에 결합하는 항체를 포함하는 면역접합체가 본원에 제공된다.
일 구현예에서, 면역접합체는 항체가 비제한적으로 하기를 포함하는 하나 이상 상의 약물에 콘주게이트되는 항체-약물 콘주게이트 (ADC)이다: 메이탄시노이드(미국 특허 제5,208,020호, 제5,416,064호 및 유럽 특허 EP 0 425 235 참조); 아우리스타틴, 예컨대 모노메틸아우리스타틴 약물 모이어티 DE 및 DF(MMAE 및 MMAF)(미국 특허 제5,635,483호 및 제5,780,588호, 및 제7,498,298호 참조); 돌라스타틴; 칼리케아미신 또는 이것의 유도체(미국 특허 제5,712,374호, 제5,714,586호, 제5,739,116호, 제5,767,285호, 제5,770,701호, 제5,770,710호, 제5,773,001호, 및 제5,877,296호 참조; Hinman et al., Cancer Res. 53:3336-3342 (1993); 및 Lode et al., Cancer Res. 58:2925-2928 (1998)); 안스라시클린, 예컨대 다우노마이신 또는 독소루비신(참고: Kratz et al., Current Med . Chem . 13:477-523 (2006); Jeffrey et al., Bioorganic & Med . Chem . Letters 16:358-362 (2006); Torgov et al., Bioconj . Chem . 16:717-721 (2005); Nagy et al., Proc . Natl . Acad . Sci . USA 97:829-834 (2000); Dubowchik et al., Bioorg . & Med . Chem . Letters 12:1529-1532 (2002); King et al., J. Med . Chem . 45:4336-4343 (2002); 및 미국 특허 번호 6,630,579); 메토트렉세이트; 빈데신; 탁산 예컨대 도세탁셀, 파클리탁셀, 라로탁셀, 테세탁셀, 및 오르타탁셀; 트리코테센; 및 CC1065.
또 다른 구현예에서, 면역접합체는 본원에 기술된 바와 같이, 효소차원의 활성 독소 또는 이것의 단편, 예를 들면 비제한적으로 디프테리아 A 쇄, 디프테리아 독소의 비결합 활성 단편, 엑소독소 A 쇄(Pseudomonas aeruginosa 유래), 리신 A 쇄, 아브린 A 쇄, 모데신 A 쇄, 알파-사르신, Aleurites fordii 단백질, 디안틴 단백질, 파이토라카 아메리카나 단백질(PAPI, PAPII 및 PAP-S), 모모르디카 차란티아 억제제, 쿠르신, 크로틴, 사파오나리아 오피시날리스 억제제, 겔로닌, 미토겔린, 레스트릭토신, 페노마이신, 에노마이신 및 트리코테센에 콘주게이트된 항체를 포함한다.
또 다른 구현예에서, 면역접합체는 본원에 기술된 바와 같이, 방사성 활성 원자에 콘주게이트되어 방사성 접합체를 형성하는 항체를 포함한다. 다양한 방사성 활성 동위원소가 방사성 접합체의 생산을 위해 사용가능하다. 예시는 하기를 포함한다: At211, I131, I125, Y90, Re186, Re188, Sm153, Bi212, P32, Pb212 및 Lu의 방사성 동위원소. 방사성 접합체가 검출을 위해 사용되는 경우, 이것은 섬광조영 구를 위한 방사성 활성 원자, 예를 들어 Tc99m 또는 I123를, 또는 핵자기공명(NMR) 영상(자기공명영상(mri)로도 알려짐)을 위한 스핀 표지, 예컨대 다시 한 번 요오드-123, 요오드-131, 인듐-111, 불소-19, 탄소-13, 질소-15, 산소-17, 가돌리늄, 망간 또는 철을 포함할 수 있다.
항체 및 세포독성제의 콘주게이트는 다양한 이작용성 단백질 커플링제 예컨대 N-석신이미딜-3-(2-피리딜디티오) 프로피오네이트 (SPDP), 석신이미딜-4-(N-말레이미도메틸) 사이클로헥산-1-카복실레이트 (SMCC), 이미노티올란 (IT), 이미도에스테르의 이작용성 유도체 (예컨대 디메틸 아디프이미데이트 HCl), 활성 에스테르 (예컨대 디석신이미딜 우베레이트), 알데하이드 (예컨대 글루타르알데하이드), 비스-아지도 화합물 (예컨대 비스(p-아지도벤조일)헥산디아민), 비스-디아조늄 유도체 (예컨대 비스-(p-디아조늄벤조일)-에틸렌디아민), 디이소시아네이트 (예컨대 톨루엔 2,6-디이소시아네이트), 및 비스-활성 불소 화합물 (예컨대 1,5-디플루오로-2,4-디나이트로벤젠) 을 이용하여 제조될 수 있다. 예를 들어, 리신 면역독소는 Vitetta et al., Science 238:1098 (1987)에 기술된 바와 같이 제조될 수 있다. 탄소-14-표지된 1-이소티오시아네이토벤질-3-메틸디에틸렌 트리아민펜타아세트산 (MX-DTPA)은 항체에 방사성뉴클레오티드의 콘주게이트를 위한 예시적인 킬레이트제이다. 참고 WO94/11026. 상기 링커는 상기 세포에서 세포독성 약물의 방출을 용이하게 하는 "절단가능한 링커"일 수 있다. 예를 들어, 산-불안정 링커, 펩티다아제-민감성 링커, 광불안정성 링커, 디메틸 링커 또는 디설피드-함유 링커(Chari et al., Cancer Res. 52: 127-131 (1992); 미국 특허 제5,208,020호)가 사용될 수 있다.
본원의 면역접합체 또는 ADC는 본원에서 명백히 고안되는데, 비제한적으로 이와 같은 콘주게이트는 가교 링커 시약, 비제한적으로, BMPS, EMCS, GMBS, HBVS, LC-SMCC, MBS, MPBH, SBAP, SIA, SIAB, SMCC, SMPB, SMPH, 술포-EMCS, 술포-GMBS, 술포-KMUS, 술포-MBS, 술포-SIAB, 술포-SMCC 및 술포-SMPB 및 SVSB(숙신이미딜-(4-비닐술폰)벤조에이트)(예컨대, Pierce Biotechnology, Inc., Rockford, IL., U.S.A에서 상업적으로 확보 가능함)으로 제조된다.
C.결합 폴리펩티드
결합 폴리펩티드는 본원에 기술된 방법에서의 사용을 위한, 관심 폴리펩티드, 예컨대 G9a에 결합하는 폴리펩티드이다. 일부 구현예에서, 결합 폴리펩티드는 G9a 길항제 길항제이다. 결합 폴리펩티드는 공지된 폴리펩티드 합성 방법을 사용하여 화학적으로 합성될 수 있거나, 재조합 기술을 사용하여 제조 및 정제될 수 있다. 결합 폴리펩티드 보통 아미노산 길이가 적어도 약 5개 아미노산, 대안적으로 길이가 적어도 약 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 또는 100개 아미노산이고, 여기서 상기 결합 폴리펩티드는 표적, 본원에 기술된, 예컨대 G9a 또는 EGFR에 바람직하게 특이적으로 결합할 수 있다. 일부 구현예에서, 결합 폴리펩티드는 G9a 메틸전달효소 활성을 억제한다.
결합 폴리펩티드는 잘 알려진 기술을 사용하여 과도한 실험 없이 식별될 수 있다. 이것에 관하여, 폴리펩티드 표적에 특이적으로 결합할 수 있는 결합 폴리펩티드에 대한 폴리펩티드 라이브러리를 스크리닝하기 위한 방법이 본 분야에 잘 알려져 있다는 것이 언급된다 (참고, 예를 들어, 미국 특허 번호 5,556,762, 5,750,373, 4,708,871, 4,833,092, 5,223,409, 5,403,484, 5,571,689, 5,663,143; PCT 공보 번호 WO 84/03506 및 WO84/03564; Geysen et al., Proc . Natl . Acad . Sci. U.S.A ., 81:3998-4002 (1984); Geysen et al., Proc . Natl . Acad . Sci . U.S.A., 82:178-182 (1985); Geysen et al., in Synthetic Peptides as Antigens, 130-149 (1986); Geysen et al., J. Immunol . Meth ., 102:259-274 (1987); Schoofs et al., J. Immunol., 140:611-616 (1988), Cwirla, S. E. et al. (1990) Proc . Natl. Acad . Sci . USA, 87:6378; Lowman, H.B. et al. (1991) Biochemistry, 30:10832; Clackson, T. et al. (1991) Nature, 352: 624; Marks, J. D. et al. (1991), J. Mol . Biol ., 222:581; Kang, A.S. et al. (1991) Proc . Natl . Acad . Sci. USA, 88:8363, and Smith, G. P. (1991) Current Opin. Biotechnol., 2:668).
펩티드 라이브러리를 생성하고, 이러한 라이브러리를 스크리닝하는 방법은 또한 하기에 개시된다: 미국 특허 번호 5,723,286, 5,432,018, 5,580,717, 5,427,908, 5,498,530, 5,770,434, 5,734,018, 5,698,426, 5,763,192, 및 5,723,323.
D.결합 소분자
상기 기술된 방법에서의 사용을 위한, 관심 폴리펩티드, 예컨대 G9a의 결합 소분자 길항제로서의 용도를 위한 결합 소분자가 본원에 제공된다. 일부 구현예에서, 결합 소분자 길항제는 G9a 메틸전달효소 활성을 억제한다.
결합 소분자는 본원에 기술된 G9a 및/또는 EGFR에, 바람직하게는 특이적으로 결합하는, 본원에 정의된 결합 폴리펩티드 또는 항체 이외에, 바람직하게는 유기 분자이다.
특정 구현예의 실시에 유용할 수 있는 소분자 G9a의 길항제의 예시는 하기를 포함한다: 화학식 I의 화합물, 이의 이성질체, 또는 이의 이성질체의 혼합물 또는 이의 약제학적으로 허용가능한 염, 이의 용매화물 또는 전구약물. UNC0638로 또한 공지되고, 본원에서 G9ai-2로 지칭되는 화학식 I의 화합물은 농도 의존적 방식으로 H3K9me2 수준을 감소시키는 G9a 및 GLP에 대한 강력하고, 선택적이고, 그리고 세포 침투적 화학 프로브이다. 상기 화합물 및 상기 화합물을 제조하는게 유용한 방법 및 중간체는 하기에 기술된다: Vedadi et al., Nat. Chem . Biol ., 7, 566-574 (2011) 및 Sweis et al., ACS Med. Chem. Lett., 5, 205-209 (2014).
화학식 I
일부 구현예에서, G9a 억제제는 Bix-01294, UNC0321, UNC0646, 및/또는 UNC0224이다 (참고: Vedadi et al., Nat. Chem . Biol ., 7, 566-574 (2011). Bix-01294는 또한 본원에서 G9ai-2로 지칭된다.
일부 구현예에서, G9a 억제제는 2-(헥사하이드로-4-메틸-1H-1,4-디아제핀-1-일)-6,7-디메톡시-[1-(페닐메틸)-4-피페리딘일]-4-퀴나졸린아민 또는 이의 염을 포함한다. 일부 구현예에서, G9a 억제제는 2-(헥사하이드로-4-메틸-1H-1,4-디아제핀-1-일)-6,7-디메톡시-[1-(페닐메틸)-4-피페리딘일]-4-퀴나졸린아민 트리하이드로클로라이드를 포함한다. 일부 구현예에서, G9a 억제제는 7-[3-(디메틸아미노)프로폭시]-2-(헥사하이드로-4-메틸-1H-1,4-디아제핀-1-일)-6-메톡시-N-(1-메틸-4-피페리딘일)-4-퀴나졸린아민 또는 이의 염을 포함한다.
일부 구현예에서, G9a 억제제는
일부 구현예에서, G9a 억제제는 하기를 포함하고:
일부 구현예에서, G9A 억제제는 하기에 기술되고: the world wide web site sciencedirect.com/science/article/pii/S0960894X12015399, (Fujishiro et al., Bioorganic & Medicinal Chemistry Letters, 23, 733-736 (2013)), 이의 전문은 본원에서 참조로 포함된다.
결합 소분자는 공지된 방법을 사용하여 식별 및 화학적 합성될 수 있다 (참고: 예를 들어, PCT 공보 번호 WO00/00823 및 WO00/39585). 결합 소분자는 보통 크기가 약 2000 달톤 미만이며, 대안적으로는 크기가 약 1500, 750, 500, 250 또는 200 달톤 미만이고, 여기서 본원에 기술된 폴리펩티드에 바람직하게는 특이적으로 결합할 수 있는 소분자는 잘 알려진 기술을 사용하여 과도한 실험 없이 식별될 수 있다. 이것에 관하여, 관심 폴리펩티드에 결합할 수 있는 분자에 대한 유기 소분자 라이브러리를 스크리닝하기 위한 방법이 본 분야에 잘 알려져 있다는 것이 언급된다 (참고, 예를 들어, PCT 공보 번호 WO00/00823 및 WO00/39585). 결합 유기 소분자 예를 들면, 하기일 수 있다: 알데하이드, 케톤, 옥심, 하이드라존, 세미카바존, 카바자이드, 1차 아민, 2차 아민, 3차 아민, N-치환된 하이드라진, 하이드라자이드, 알코올, 에테르, 티올, 티오에테르, 디설파이드, 카복실산, 에스테르, 아미드, 우레아, 카바메이트, 카보네이트, 케탈, 티오케탈, 아세탈, 티오아세탈, 아릴 할라이드, 아릴 설포네이트, 알킬 할라이드, 알킬 설포네이트, 방향족 화합물, 헤테로사이클릭 화합물, 아닐린, 알켄, 알킨, 디올, 아미노 알코올, 옥사졸리딘, 옥사졸린, 티아졸리딘, 티아졸린, 엔아민, 설폰아미드, 에폭사이드, 아지리딘, 이소시아네이트, 설포닐 클로라이드, 디아조 화합물, 산 클로라이드, 등.
E.길항제 폴리뉴클레오티드
본원에 기술된 방법에서 사용하기 위한 폴리뉴클레오티드 길항제를 또한 제공한다. 폴리뉴클레오티드는 안티센스 핵산 및/또는 리보자임일 수 있다. 안티센스 핵산은 본원에 기술된 관심 유전자, 예컨대 G9a 유전자의 RNA 전사체의 적어도 하나의 부분에 상보적인 서열을 포함한다 (예컨대, 하기의 아미노산 서열: UNIPROT 번호 Q96KQ7-1, Q96KQ7-2, 및/또는 Q96KQ7-3, 이는 그 전체가 본원에 참조로 편입됨). 그러나, 절대 상보성은, 바람직하더라도, 요구되지 않는다.
본원에 지칭된, RNA의 적어도 하나의 부분에 대한 서열 “상보성”은 안정한 이중나성을 형성하는 RNA와 혼성화될 수 있는 충분한 상보성을 갖는 서열을 의미하며, 이중 가닥 안티센스 핵산의 경우, 이중나선 DNA의 단일 가닥은 따라서 시험될 수 있으며, 또는 삼중가닥 형성이 검정될 수 있다. 혼성화 능력은 안티센스 핵산의 길이 및 상보성의 정도, 둘 모두에 의존적일 것이다. 일반적으로, 핵산 혼성화가 클 수록, RNA와의 더욱 많은 염기 미스매치가 발생하며, 이는 안정한 이중가닥 (또는 있다면 삼중가닥)을 함유하고 여전히 형성할 수 있다. 본 분야의 숙련가는 표준 절차에 의하여 미스매치의 허용가능한 수준을 특정하여 혼성화된 복합체의 용융점을 측정할 수 있다.
메세지, 예를 들어, 5’ 비번역된 서열의 5’ 말단에 상보적이고, AUG 개시 코돈을 포함하는 폴리뉴클레오티드는 번역을 억제하는데 있어 가장 효율적으로 작용할 것이다. 그러나, mRNA의 3’ 비번역된 서열에 상보적인 서열은 mRNA의 번역을 또한 억제하는데 유효한 것으로 나타났다. 전반적으로, Wagner, R., 1994, Nature 372:333-335를 참조한다. 유전자의 5’- 또는 3’ 비-번역된, 비-암호화 영역에 상보적인 올리고뉴클레오티드는 내인성 mRNA의 번역을 억제하는 안티센스 접근에 사용될 수 있다. mRNA의 5’ 비번역된 영역에 상보적인 폴리뉴클레오티드는 AUG 개시 코돈의 보체를 포함할 것이다. mRNA 암호화 영역에 상보적인 안티센스 폴리뉴클레오티드는 보다 덜 효과적인 번역 억제제이지만, 본 발명에 따라 사용될 수 있다. mRNA, 안티센스 핵산의 5’, 3’, 또는 앙호화 영역에 혼성화되도록 설계되는지 여부는 길이가 적어도 6개인 뉴클레오티드일 것이고, 이는 바람직하게는 길이가 6개 내지 약 50개 뉴클레오티드 범위의 올리고뉴클레오티드이다. 특정 구현예에서, 올리고뉴클레오티드는 적어도 10개 뉴클레오티드, 적어도 17개 뉴클레오티드, 적어도 25개 뉴클레오티드, 또는 적어도 50개 뉴클레오티드이다.
F.항체 및 결합 폴리펩티드 변이체
특정 구현예에서, 본원에 제공되는 항체 및/또는 결합 폴리펩티드의 아미노산 서열 변이체이 고안되었다. 예를 들어, 상기 항체 및/또는 결합 폴리펩티드의 결합 친화도 및/또는 기타 생물학적 특성들을 향상시키는 것이 바람직한 일일 수 있다. 항체 및/또는 결합 폴리펩티드의 아미노산 서열 변이체은 상기 항체 및/또는 결합 폴리펩티드를 암호화하는 뉴클레오티드 서열에 적절할 변형을 도입시킴으로써, 또는 펩티드 합성에 의해 제조될 수 있다. 이와 같은 변형에는 예를 들어, 상기 항체 및/또는 결합 폴리펩티드의 아미노산 서열 내에서 잔기에서 결실, 및/또는 잔기로의 삽입 및/또는 잔기의 치환이 포함된다. 결실, 삽입 및 치환의 어떠한 조합이 이루어져서 최종 작제물에 도달할 수 있는데, 단, 상기 최종 작제물는 바람직한 특징, 예컨대, 항원-결합을 갖는다.
특정 구현예에서, 하나 이상의 아미노산 치환을 갖는 항체 변이체 및/또는 결합 폴리펩티드가 제공된다. 치환성 돌연변이 유발을 위한 관심대상 부위에는 HVR 및 FR가 포함된다. 보존적 치환은 "보존적 치환"이라는 표제하에 표 1에 나타낸다. 보다 실질적 변화는 "예시적 치환"의 표제하에 표 1에 제공되고, 추가로 아미노산 측쇄 부류를 참조로 하기에 기재된 바와 같다. 아미노산 치환은 관심 항체 및/또는 결합 폴리펩티드, 및 목적 활성, 예컨대 유지된/향상된 항원 결합, 감소된 면역원성, 또는 향상된 ADCC 또는 CDC에 대해 스크리닝된 생성물에 도입될 수 있다.
표 1
아미노산은 통상의 측쇄 성질에 따라 분류될 수 있다:
(1) 소수성: 노르류신, Met, Ala, Val, Leu, Ile;
(2) 중성 친수성: Cys, Ser, Thr, Asn, Gln;
(3) 산성: Asp, Glu;
(4) 염기성: His, Lys, Arg;
(5) 쇄 배향에 영향을 주는 잔기: Gly, Pro;
(6) 방향족: Trp, Tyr, Phe.
비-보존적 치환은 이들 부류 중 하나의 구성원을 또 다른 부류의 구성원으로 교환시킬 필요가 있다.
G.항체 및 결합 폴리펩티드 유도체
특정 구현예에서, 본원에 제공되는 항체 및/또는 결합 폴리펩티드는 추가로 변형되어 당해기술에 알려져 있고 쉽게 확보가능한 추가적인 비단백질성 모이어티를 함유할 수 있다. 상기 항체 및/또는 결합 폴리펩티드의 유도에 적합한 모이어티에는 비제한적으로 수용성 중합체가 포함된다. 수용성 중합체의 비제한적 예에는, 비제한적으로, 폴리에틸렌 글리콜(PEG), 에틸렌 글리콜/프로필렌 글리콜의 공중합체, 카복시메틸셀룰로오스, 덱스트란, 폴리비닐 알코올, 폴리비닐 피롤리돈, 폴리-1, 3-디옥솔란, 폴리-1,3,6-트리옥산, 에틸렌/말레이 무수물 공중합체, 폴리아미노산(동종중합체 또는 랜덤 공중합체), 및 덱스트란 또는 폴리(n-비닐피롤리돈)폴리에틸렌 글리콜, 프로프로필렌 글리콜 동종중합체, 프롤리프로필렌 옥사이드/에틸렌 옥사이드 공중합체, 폴리옥시에틸화된 폴리올(예컨대, 글리세롤), 폴리비닐 알코올 및 이들의 혼합물이 포함된다. 폴리에틸렌 글리콜 프로피온알데하이드는 물에서 그 안정성 때문에 제조시 이점을 가질 수 있다. 폴리머는 임의의 분자량일 수 있고, 그리고 분지형 또는 비분지형일 수 있다. 항체 및/또는 결합 폴리펩티드에 부착된 폴리머의 수는 다양할 수 있고, 만일 1 초과 폴리머가 부착되면, 이들은 동일 또는 상이한 분자일 수 있다. 일반적으로, 유도를 위해 사용되는 중합체의 개수 및/또는 유형은 비제한적으로, 향상될 대상인 항체 및/또는 결합 폴리펩티드의 특정 속성 또는 작용, 상기 항체 유도체 및/또는 결합 폴리펩티드 유도체가 규정된 조건 하에서 치료에 사용될 것인지 여부 등을 비롯한 고려사항들을 기반으로 결정될 수 있다.
또 다른 구현예에서, 방사성 노출에 의해 선택적으로 가열될 수 있는 비단백질성 모이어티에 대한 항체 및/또는 결합 폴리펩티드의 콘주게이트가 제공된다. 일 구현예에서, 비단백질성 모이어티는 탄소 나노튜브이다 (참고: Kam et al., Proc . Natl. Acad . Sci . USA 102: 11600-11605 (2005)). 방사성은 어떤 파장이든 가질 수 있는데, 상기 방사성에는 비제한적으로, 일반적인 세포를 해치지 않지만, 항체-비단백질성 모이어티의 중심에 가까이 있는 세포가 사멸되는 온도로 비단백질성 모이어티를 가열하는 파장이 포함된다.
IV. 목적 기능을 갖는 G9a의 길항제의 스크리닝 및/또는 식별 방법
항체, 결합 폴리펩티드, 및/또는 소분자를 포함하는, 본원에 기술된 방법에서의 사용을 위한 관심 폴리펩티드, 예컨대 G9a의 추가적 길항제가 상기 기술되었다. 본원에서 제공된, 예컨대 항-G9a 항체, 결합 폴리펩티드, 및/또는 결합 소분자의 추가적 길항제는 당해기술에서 공지된 다양한 검정에 의해 그 물리적/화학 특성 및/또는 생물학적 활성으로 식별, 스크리닝, 또는 특징화될 수 있다.
특정 구현예에서, G9a 폴리펩티드의 분좌적 좌표를 포함하는 메모리를 포함하는 컴퓨터 시스템이, G9a의 리간드 결합 부위에서 화합물을 합리적으로 식별하기 위한 모델로서 유용하다. 그러한 화합물은 예를 들어, 새롭게 또는 공지된 화합물의 변형에 의하여 설계될 수 있다. 다른 경우에서, 결합 화합물은 알려진 화합물을 시험함으로써 식별되어 “도크(dock)”가 G9a 분자 모델을 갖는지 여부를 측정할 수 있다. 그와 같은 도킹(docking) 방법은 일반적으로 당해기술에서 공지되어 있다.
G9a 결정 구조 데이터는, 상기 결정 구조 데이터의 분석에 의한 다양한 G9a-결합 화합물의 결합 모델을 발전시키는 컴퓨터-모델링 기술과 연합하여 사용될 수 있다. 부위 모델은, 반데르발스 접촉, 정전 상호작용 및 수소-결합 경우를 포함하는 인자뿐만 아니라, 부위 표면의 3-차원 지형을 특징화한다. 컴퓨터 시뮬레이션 기술은 이후 하기를 비제한적으로 포함하는 작용기에 대한 상호작용 위치를 맵핑하는데 사용된다: 양성자, 하이드록실기, 아민기, 2가 양이온, 방향족 및 지방족 작용기, 아미드기, 알코올기 등 (모델 부위와 상호작용하도록 설계됨). 이러한 기들은 상기 후보 화합물이 상기 부위에 특이적으로 결합할 것이라는 예상으로 약물특이분자단 또는 후보 화합물로 설계될 수 있다. 약물특이분자단 설계는 따라서, 수소 결합, 반데르발스 결합, 정전 및 공유적 상호작용을 포함하는 화학적 상호작용의 이용가능한 유형 중 임의의 것 또는 전체를 통하여 부위와 상호작용하는 약물특이분자단 내에 속하는 후보 화합물의 능력의 고려를 포함하며, 그러나 일반적으로 약물특이분자단은 비-공유적 기전을 통하여 부위와 상호작용한다.
G9a 폴리펩티드와 결합하는 약물특이분자단 또는 후보 화합물의 능력을, 컴퓨터 모델링 기술을 사용하여 실제적 합성에 부가하여 분석하였다. 충분한 결합 에너지 (일 예에서, 10-2 M 또는 더 긴밀한 순서 상의 표적을 갖는 해리 상수에 상응한 결합 에너지)를 갖는 표적 (예컨대, G9a 폴리펩티드 결합 부위)에 결합하는 컴퓨터 모델링에 의하여 표지된 상기 후보 만이 합성될 수 있고, G9a 폴리펩티드에 결합하고, 적용가능할 경우, 본 분야의 숙련가에게 알려진 효소 검정 및/또는 본원에 기술된 효소 검정을 사용하여 G9a 효소적 기능을 억제하는 그들의 능력에 대해 시험될 수 있었다. 컴퓨터 평가 단계는 따라서 적당한 친화도를 갖는 G9a 폴리펩티드에 결합하지 않을 것 같은 화합물의 불필요한 합성을 회피한다.
G9a 약물특이분자단 또는 후보 화합물은, 화학적 단위체 또는 단편이 G9a 폴리펩티드 상에서 개별 결합 표적 부위와 결합하는 그들의 능력에 대해 스크리닝되고 선택되는 일련의 단계에 의하여 컴퓨터 상에서 평가 및 설계될 수 있다. 본 분야의 숙련가는 G9a 폴리펩티드와, 더욱 특히는 G9a 폴리펩티드드 상의 표적 부위와 결합하는 그들의 능력에 대해 화학적 단위체 또는 단편을 스크리닝하는 몇몇의 방법 중 하나를 사용할 수 있다. 상기 처리는 예를 들어, 컴퓨터 스크린 상에서, G9a 폴리펩티드 좌표를 기반으로, 또는 본 분야에 알려진 좌표의 하위세트를 기반으로 육안 검사에 의하여 시작될 수 있다.
암 세포사를 유도하는 길항제에 대한 선택을 위하여, 막 온전성의 손실이 참조군과 비요하여 평가될 수 있다 (예컨대, 프로피디움 요오드화물 (PI), 트리판 블루 또는 7AAD 흡수량에 의하여 표지 시). PI 흡수량 검정이, 보체 및 면역 효과기 세포의 부재 하에서 수행될 수 있다. 종양 세포를 적절한 조합 요법을 함유하는 배지로 또는 배지 단독으로 항온처리하였다. 세포를 3-일 시간 기간 동안 항온처리하였다. 각 처리 후, 세포를 세정하고, 세포 무리의 제거를 위하여 35 mm 스트레이너-캡핑된 12 x 75 튜브 (튜브 당 1 ml, 처리 군 당 3개 튜브)로 분취하였다. 튜브에 이후 PI (10 μg/ml)를 수용시킨다. 샘플은 FACSCAN® 유동 세포분석기 및 FACSCONVERT® CellQuest 소프트웨어 (Becton Dickinson)을 사용하여 분석될 수 있다. PI 흡수량으로 측정시, 배지 단독 및/또는 단일요법과 비교하여, 통계적으로 현저한 수준의 세포사를 유도하는 상기 길항제가 세포-유도 항체, 결합 폴리펩티드, 또는 결합 소분자로서 선택될 수 있다.
상기 스크리닝 및/또는 식별 방법 중 일부 구현예에서, G9a의 후보 길항제는 항체, 결합 폴리펩티드, 결합 소분자, 또는 폴리뉴클레오티드이다. 일부 구현예에서, G9a의 길항제는 항체이다. 일부 구현예에서, G9a의 길항제는 결합 소분자이다. 일부 구현예에서, G9a 길항제는 G9a 메틸전달효소 활성을 억제한다.
V. 약제학적 제형
본원에 기재된 바와 같은 G9a의 길항제 및/또는 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)의 약제학적 제형은 상기 항체 또는 목적하는 정도의 순도를 갖는 면역접합체를 하나 이상의 임의의 약제학적으로 허용되는 담체와 혼합함에 의해 제조되고 (Remington's Pharmaceutical Sciences 16th edition, Osol, A. Ed. (1980)), 동결건조된 제형 또는 수용액 형태이다. 일부 구현예에서, G9a의 길항제 및/또는 표적화된 요법은 결합 소분자, 항체, 결합 폴리펩티드, 및/또는 폴리뉴클레오티드이다. 일부 구현예에서, 암 요법 제제는 EGFR 길항제이다. 일부 구현예에서, 암 요법 제제는 탁산이다. 일부 구현예에서, 탁산은 파클리탁셀이다. 일부 구현예에서, 탁산은 도세탁셀이다.
약제학적으로 허용가능한 담체는 이용된 복용량 및 농도에서 수령체에 일반적으로 비독성이고, 비제한적으로 하기를 포함한다: 완충제 예컨대 포스페이트, 시트레이트, 및 다른 유기 산; 아스코르브산 및 메티오닌을 포함하는 항산화제; 보존제 (예컨대 옥타데실디메틸벤질 염화암모늄; 헥사메토늄 클로라이드; 벤즈알코늄 클로라이드; 벤즈에토늄 클로라이드; 페놀, 부틸 또는 벤질 알코올; 알킬 파라벤 예컨대 메틸 또는 프로필 파라벤; 카테콜; 레조르시놀; 사이클로헥산올; 3-펜타놀; 및 m-크레졸); 저분자량 (약 10 미만 잔기) 폴리펩티드; 단백질, 예컨대 혈청 알부민, 젤라틴, 또는 면역글로불린; 친수성 폴리머 예컨대 폴리비닐피롤리돈; 아미노산 예컨대 글리신, 글루타민, 아스파라긴, 히스티딘, 아르기닌, 또는 라이신; 모노사카라이드, 디사카라이드, 및 글루코오스, 만노스, 또는 덱스트린을 포함하는 다른 탄수화물; 킬레이트제 예컨대 EDTA; 당류 예컨대 수크로오스, 만니톨, 트레할로오스 또는 소르비톨; 염 형성 반대 이온 예컨대 나트륨; 금속 복합체 (예를 들면 Zn-단백질 복합체); 및/또는 비-이온성 계면활성제 예컨대 폴리에틸렌 글리콜 (PEG). 본원에서 예시적 약제학적으로 허용되는 담체는 간질 약물 분산제, 예를 들어, 가용성 중성-활성 하이알루로니다제 당단백질 (sHASEGP), 예를 들어, 인간 가용성 PH-20 하이알루로니다제 당단백질, 예를 들어, rHuPH20 (HYLENEX®, Baxter International, Inc.)을 추가로 포함한다. rHuPH20을 포함하는, 특정 예시적인 sHASEGP 및 사용 방법이 미국 특허 공개 번호 2005/0260186 및 2006/0104968에 기재된다. 일 측면에서, sHASEGP는 하나 이상의 추가의 글리코사미노글리카나제, 예를 들어, 콘드로이티나제와 조합된다.
예시적인 동결건조된 제형이 미국 특허 번호 6,267,958에 기재된다. 수성 항체 제형은 미국 특허 번호 6,171,586 및 WO2006/044908에 기재된 것을 포함하고, 후자 제형은 히스티딘-아세테이트 완충제를 포함한다.
본원에서의 상기 제형은 또한 시험된 특정 징후에 필요한 만큼 하나 이상의 활성 성분들을 함유할 수 있고, 바람직하게는 서로 안좋은 영향을 주지 않는 상보적 활성을 갖는 것들을 포함한다. 상기 활성 성분은 적합하게는, 의도된 목적을 위해 효과적인 양으로 조합되어 존재한다.
활성 성분들은 예를 들어, 코나세르베이션 기술에 의해 또는 계면 중합화에 의해 제조된 마이크로캡슐, 예를 들어, 콜로이드성 약물 전달 시스템(예를 들어, 리포좀, 알부민 미소구, 나노입자 및 나노캡슐) 중에 또는 마크로에멀젼 중에 하이드록시메틸셀룰로스 또는 겔라틴-마이크로캡슐 및 폴리-(메틸메타크릴레이트) 마이크로캡슐 중에 포집될 수 있다. 상기 기술은 하기에서 개시되어 있다: Remington's Pharmaceutical Sciences 16th edition, Osol, A. Ed. (1980).
지속-방출 제제는 제조될 수 있다. 지속-방출 제제의 적합한 예는, 매트릭스가 형상화된 물품, 예를 들면 필름, 또는 마이크로캡슐의 형태인, G9a의 길항제 및/또는 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)를 함유하는 고체 소수성 폴리머의 반투과성 매트릭스를 포함한다.
생체내 투여용으로 사용될 제형은 일반적으로 멸균성이다. 멸균은, 예를 들면, 멸균된 여과 막을 통한 여과에 의해 쉽게 달성될 수 있다.
VI. 제조 물품
본 발명의 다른 양상에서, 전술한 장애의 치료, 예방 및/또는 진단에 유용한 물질을 내포하는 제조 물품이 제시된다. 제조 물품은 용기 및 그 용기에 또는 관련된 표지 또는 포장 삽입물을 포함한다. 적절한 용기에는 예로서, 병, 바이알, 주사기, IV 용액 백 등이 포함된다. 상기 용기는 다양한 재료, 예컨대 유리 또는 플라스틱으로 형성될 수 있다. 용기는 그것만으로 있거나 또는 장애의 치료, 예방 및/또는 진단에 효과적인 또 다른 조성물과 조합되고 그리고 멸균된 접근 포트를 가질 수 있는 조성물을 수용한다 (예를 들면 용기는 피하 주사 바늘에 의해 뚫을 수 있는 스토퍼를 갖춘 정맥내 용액 백 또는 바이알일 수 있다). 상기 조성물 내의 적어도 하나의 활성 제제는 본원에 기술된 G9a의 길항제이다. 표지 또는 포장 삽입물은 조성물이 선택 질환의 치료에 사용됨을 나타낸다. 더욱이, 제품은 (a) 조성물이 여기에 함유된 제1 컨테이너(여기서, 상기 조성물은 본 발명의 G9a의 길항제를 포함한다); 및 (b) 조성물이 여기에 함유된 제2 컨테이너(여기서, 상기 조성물은 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법)를 포함한다)를 포함할 수 있다.
일부 구현예에서, 제조물품은 용기, 상기 용기 상의 표지, 및 상기 용기 내에에 함유된 조성물을 포함하며, 여기서 상기 조성물은 하기를 포함한다: 하나 이상의 시약 (예컨대, 본원에 기술된 하나 이상의 바이오마커 또는 상기 바이오마커 중 하나 이상에 대한 프로브 및/또는 프라이머에 결합하는 1차 항체); 상기 조성물이 샘플 내 하나 이상의 바이오마커의 존재를 평가하는데 사용될 수 있다고 표지하는 , 상기 용기 상의 표지; 및 상기 샘플 내 하나 이상의 바이오마커를 평가하기 위한 시약을 사용하기 위한 설명서. 제조 물품은 추가로, 샘플을 제조하고 시약을 이용하기 위한 설명서 및 재료의 세트를 포함할 수 있다. 일부 구현예에서, 제조물품은 시약 예컨대 1차 및 2차 항체 둘 모두를 포함할 수 있으며, 여기서 상기 2차 항체는 표지, 예를 들어 효소적 표지에 콘주게이트된다. 일부 구현예에서, 제조 물품은 본원에 기술된 바이오마커 중 하나 이상에 대한 하나 이상의 프로브 및/또는 프라이머를 포함한다.
상기 방법들의 일부 구현예에서, 제조물품, G9a의 길항제, 및/또는 암 요법 제제는 항체, 결합 폴리펩티드, 결합 소분자, 또는 폴리뉴클레오티드이다. 일부 구현예에서, 암 요법 제제는 탁산이다. 일부 구현예에서, 탁산은 파클리탁셀이다. 일부 구현예에서, 암 요법 제제는 EGFR 길항제이다. 일부 구현예에서, G9a 길항제의 길항제는 결합 소분자이다. 일부 구현예에서, EGFR 결합 소분자 길항제는 엘로티닙이다. 일부 구현예에서, G9a 길항제의 길항제는 항체이다. 일부 구현예에서, 항체는 단클론성 항체이다. 일부 구현예에서, 항체는 인간, 인간화된, 또는 키메라 항체이다. 일부 구현예에서, 항체는 G9a 및/또는 억제제에 결합하는 항체 및 항체 단편이다. 일부 구현예에서, G9a 길항제는 G9a 메틸전달효소 활성을 억제한다.
본 발명의 이러한 구체예에서, 제조 물품은 조성물이 특정 질환을 치료하는데 이용될 수 있다는 것을 표시하는 포장 삽입물을 더욱 포함할 수도 있다. 일부 구현예에서, 포장 삽입물은 G9a의 길항제를 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법) 이전에 및/또는 이와 동시에 투여하기 위한 설명서를 포함한다. 대안적으로, 또는 부가적으로, 제조 물품은 추가로, 약제학적으로-허용가능한 완충제, 예컨대 정균 주사용 물 (BWFI), 포스페이트-완충된 염수, 링거액 및 덱스트로오스 용액을 포함하는 제2 (또는 제3) 용기를 포함할 수 있다. 다른 완충제, 희석제, 필터, 바늘, 및 주사기를 포함하여, 상업적 및 사용자 관점으로부터 바람직한 다른 물질을 추가로 포함할 수 있다.
제조 물품 중 기타 임의의 성분은 하기를 포함한다: 하나 이상의 완충제 (예를 들면, 블록 완충제, 세척 완충제, 기질 완충제, 등), 다른 시약 예컨대 기질 (예를 들면, 색원체) (효소 표지, 에피토프 회수 용액, 대조군 샘플 (양성 및/또는 음성 대조군)에 의하여 화학적으로 변경됨), 대조군 슬라이드(들) 등.
상기 임의의 제조물품은 G9a의 길항제 및 암 요법 제제 (예컨대, 표적화된 요법, 화학요법, 및/또는 방사성요법) 대신에 또는 이에 추가로 본 발명의 면역접합체를 포함할 수있는 것으로 이해된다.
실시예
하기는 본 발명의 방법 및 조성물의 실시예이다. 상기 제공된 일반적인 설명이 주어지면, 다양한 다른 구현예가 실시될 수 있음이 이해된다. 결과가 또한 제시되며 표 및 범례에서 기술된다.
실시예 1
재료 및 방법
세포 배양
전체 세포를 5% CO2 및 37°C 하에서 5% 우태 혈청 (FBS), L-글루타민으로 보강된 RPMI 배지 (고 글루코스) 내에서 유지시켰다.
세포 생존 검정
2×105 의 세포를 6-웰 클러스터 접시 내 각 웰에 플레이팅하였다. 플레이팅 24시간 후, 배지를 제거하고 약물을 함유한 배지로 교체하였다. 새로운 배지를, 비처리된 세포가 합류에 도달할 때까지 매 2일마다 교체하였다. 배지를 이후 제거하고, 세포를 인산염 완충 식염수 (PBS)로 세정하고, 이후 PBS 중 4% 포름알데히드로 15분간 고정시켰다. 세포를 이후 PBS로 세정하고, 형광 핵산 염색 Syto60 (PBS 중 1 nM; 분자 프로브)로 15분간 염색하였다. 염색을 제거하고, 세포 단일층을 PBS로 세정하고, 형광 정량화를 Odyssey 적외선 영상화 장치 (Li-Cor Biosciences)로 700nm에서 수행하였다. 일부 세팅에서, RFP 핵산 세포를 Syto60 대신 사용하였다.
약물-내성
존속성균
형성 (DTP)
약물-민감성 세포를, 72시간 지속되는 각 치료로, 3회 동안, 확립된 IC50 값으로 100회 초과의 농도에서의 본원에 기술된 관련 약물로 처리하였다. 관련 약물 처리의 제3회 말에 접시 상에 부착된 잔여 생세포를 DTP로 고려하였고, 이를 분석을 위하여 수집하였다.
특히 타세바, GDC-0980, GDC-0973, AZ628, 및 라파티닙 DTP에 대하여, 세포를 플레이팅하고 60-70% 합치성으로 성장시켰고, 이후 타세바 (0.1, 0.2, 0.5, 및/또는 1 uM), GDC-0980 (2 uM), GDC-0973 (1 uM), AZ628 (2 uM) 및 라파티닙 (1 uM)로 처리하였다. DTP를 수집하고, 화학요법 최종 투여 1주 후 분석하였다.
siRNA 및 shRNA 녹다운
siRNA 녹다운에 대하여, 세포를 0.0625 ul 의 DharmaFECT 1 형질감염 지질 (Dharmacon, 카탈로그 #T-2001) 및 단일 siRNA (Dharmacon siGENOME) (12.5 nM 최종 농도에서)를 사용하여 웰당 1000개 세포로 흑색 96 웰 투명 바닥 플레이트 (Corning, 카탈로그 #3603) 내에 역-형질감염시켰다. 세포를, 형질감염 배지를 배지 내의 1 uM 관련 약물 처리하거나 배지 단독으로 교체하기 전에 48-72 시간 동안 형질감염시켰다. 72시간의 항온처리 후 배지 +/- 약물을 이후 새로운 배지로 교체하여 관련 약물 처리 (회수 단계) 후 생존한 약물 내성 존속성균의 회수를 가능케하였다. 회수 단계 3일 후, 최종 세포 생존력을 제조사 프로토콜에 따라 CyQUANT 직접 세포 증식 검정 (분자 프로브)을 사용하여 측정하였다. CyQUANT 형광 신호를 GE IN 세포 분석기 2000 (4X 배율)을 사용하여 검출하고, GE 개발자 툴박스 1.9.1 을 사용하여 개발된 이미지 분석 알고리즘를 사용하여 웰당 세포 수로서 정량화하였다. 데이터를 이후 마이크로소프트 엑셀로 처리하였고, 각 세포주를 완전히 독립적인 조건 하에서 2회 구동하였다.
결합 소분자 억제제 실험
일반적으로, G9a 억제제 실험에 대하여, 세포를 G9a 억제제 UNC0638 0.1, 0.2, 0.5 및/또는 1 uM에서의 활성 화합물로 화학요법 전 3-5일 동안 처리하였고, 연구 기간 동안 약물 상에서 유지하였다.
세포 수확 및 단백질 검정
세포 용해물을 레밀리(Laemmli) 샘플 완충제 내에서 제조하고, 이전에 기술된 면역블랏팅에 의하여 분석하였다. 세포 용해물을 H3 상의 변형에 대한 상업적 항체를 사용하여 분석하였다 (Abcam, 활성 모티프, 및 세포 신호전달 기술).
질량 분광측정 샘플 제조
1000만개 세포를 갖는 샘플을 용해시켰고, 히스톤을 활성 모티프 히스톤 정제 키트 (world wide web activemotif.com/catalog/171.html)를 사용하여 세포 용해물로부터 단리시켰다. 단리-후 단백질 정량화를 Qubit 형광 플랫폼 (Invitrogen)을 사용하여 수행하였다. 표적 산출량은 500만 세포 당 적어도 20 μg 이상의 정제된 히스톤이었다. 샘플을 이후 유도체화하고, d0/d10 프로피온산 무수물 및 트립신 소화를 사용하여 2원 비교를 수행하였다. 구체적으로, 각 샘플의 5 μg 분취량을 d0 프로피온산 무수물로 유도체화하여 리신 및 모노-메틸화된 리신 잔여물을 차단하였다. 대조군 샘플 15 μg를 이용하였다. 샘플을 트립신으로 소화시켰다. 대조군 샘플을 d0 프로피온산 무수물로 재-유도체화하였다 (노출된 펩티드 N-말단 상에서). 시험 샘플을 d10 프로피온산 무수물로 재-유도체화하였다 (노출된 N-말단 상에서). 각 시험 샘플을 독립적으로 대조군 샘플과 1:1 풀링하였다. 이후 샘플을 다중-효소 소화에 편입시켰다. 샘플 당 3개 효소의 세트를 이용하여 특징화될 PTM 부위 주위의, 그리고 전체 부위 주위의 동시적 중첩 서열 범위로 대형 펩티드를 생성하였다.
질량 분광측정
펩티드 소화물을 나노 LC/MS/MS로 LTQ Orbitrap Velos 탠덤 질량 분광계 상에서 데이터-의존적 방식으로 분석하였다. 데이터를 CID, HCD 및 ETD 단편화 체계를 사용하여 획득하였다. 데이터 획득 시에, Mascot (Matrix Science)을 사용하여 검색한 데이터베이스를 사용하여 아세틸화, 메틸화, 디메틸화, 트리메틸화, 인산화, 및 유비퀴틴화를 측정하였다. 드노보 서열분석을 포함하는 매뉴얼 데이터 분석을 사용하여 추정 인-실리코 배분을 확인하고, Mascot 내에 비매칭된 변형된 펩티드에 대한 원 데이터를 얻었다. 정확한 질량 전체 스캔 LC/MS 데이터를 통합하여 샘플 간 변형된 폴리펩티드의 상대적 존재비를 측정하였다. 트립신 소화된 프로피오닐화된 샘플을 d0/d5 쌍을 비교함으로써 각 LC/MS 구동 내에서 정량화하였다 (하기 문헌에 따라: Garcia et al., JPR, 8, 5367-5374 (2009)). 대안적인 효소 샘플을 LC/MS 구동 사이에서 표지 없이 정량화하였다.
결과
G9a는 히스톤 H3의 모노- 및 디메틸레이트 리신 9을 특이적으로 촉매하는 히스톤 메틸전달효소이다. G9a는 또한 EHMT2, BAT8, GAT8, KMT1C, 및 NG36 로 공지된다. H3K9 KMT G9a (KMT1C)는 H3K27을 시험관내 및 생체내에서 메틸화하는 것으로 나타났다. G9a 및 G9a-유사 단백질 (GLP 또는 KMT1D)은 G9a-GLP 이종이량체 복합체로서 우세하게 존재하고, 이는 생체내 기능적 H3K9 메틸전달효소인 것으로 나타난다. 상승된 수준의 G9A 발현은 많은 유형의 인간 암에서 관찰되었다.
표 1B에서 나타난 바와 같이, G9a는, 친계 PC9 세포와 비교하여, 인간 소-세포-폐 암 세포주 PC9 약물 내성 존속성균 (DTP) 내에서 상향조절된다. G9a 메틸화 활성이 약물-내성의 확립을 위하여 요구된다는 것을 확인하기 위하여, 3’-UTR-GFP 녹다운을 갖는 G9a 짧은 헤어핀의 발현이 PC9 약물 내성 세포를 제거하는 것으로 나타났다. 참고: 도 1C. G9a의 발현 수준 변화와 일치하게, 도 2C에 나타난 바와 같이, 웨스턴 블랏팅 및 질량 분광측정에 의하여 측정시, H3K9me3는, PC9 친계 세포와 비교하여, PC9 DTP 내에서 증가된다.
도 3A에 나타난 소분자 G9a 길항제 UNC0638 및 비도시된 데이터는, 웨스턴 블랏팅 및 질량 분광측정에 의하여 측정시, H3K9의 메틸화를 억제할 수 있었다. 추가로, 도 3B에 나타난 소분자 G9a 길항제 UNC0638는 자가-메틸화 G9aK185me3를 억제한다. 도 4에 나타난 G9A-K185me 0/1/2/3 펩티드 풀다운 질량 분광측정 데이터를 사용하여, CDYL1 및 LRWD1를 H3K9 또는 G9aK185 메틸화된 펩티드로 풀다운하였고, 이는 메틸화된 K9 또는 메틸화된 G9a가 단백질을 동원하고, 이의 기능은 이러한 집단에 대한 이질염색질에 대해 중요할 수 있다는 것을 시사한다.
소분자 G9a 길항제 UNC0638 (G9ai-2)는 암 세포 유형의 범위에 걸쳐, 그리고 다양한 약물을 사용하여 생성된 DTP에 걸쳐 H3K9의 메틸화 및 감소된 DTP 형성을 억제할 수 있었다는 것이 도면에 예증된다. 도 5 및 7에 나타난 바와 같이, UNC0638 (G9ai-2)에 의한 치료는 타세바(Tarceva)로의 치료를 통하여 생성된 비-소세포 폐암 세포주, PC9, DTP의 수를 감소시킨다. 추가로, UNC0638 (G9ai-2)는, 웨스턴 블랏으로 측정 시, H3K9의 메틸화를 감소시키고, 또한 PC9 DTP의 수를 감소시켰다 (참고: 도 6). DTP 형성 뿐만 아니라, UNC0638 (G9ai-2)에 의한 H3K9의 메틸화 감소는 하기에 나타난 바와 같은 다중 세포주 및 치료 레지멘에 걸쳐 나타난다: 도 8 (유방암 세포주 EVSA-T/GDC-0980), 도 9 (유방암 세포주 SKBR3/Lapatnib), 도 10 (흑색종 암 세포주 M14/GDC-0973), 및 도 11 (결장직장암 세포주 Colo205/AZ628).
앞서 발명의 이해를 명확히 하기 위한 목적으로 그림 및 예의 방식으로 상세히 기술된 바 있으나, 본 설명 및 예는 본 발명의 범위를 제한하는 것으로 여겨져서는 안 된다. 본원에서 인용된 모든 특허 및 과학적 문헌의 개시내용은 명확히 그 전체가 참고로 편입된다.
Claims (27)
- 개체에서 암을 치료하는 방법으로서,
(a) G9a의 길항제, 및
(b) 암 요법 제제를 상기 개체에게 투여하는 단계를 포함하는, 방법. - 청구항 1에 있어서, 상기 G9a의 길항제 및 상기 암 요법 제제의 각각의 양은 암 민감도의 기간을 증가시키고/시키거나 상기 암 요법 제제에 대한 세포 내성의 진행을 지연시키는데 유효한, 방법.
- 암 요법 제제를 포함하는 암 치료의 효능을 증가시키는 방법으로서,
(a) 유효량의 G9a의 길항제를 상기 개체에게 투여하는 단계를 포함하는, 방법. - 개체에서 암을 치료하는 방법으로서,
암 치료는 상기 개체에 (a) 유효량의 G9a의 길항제 및 (b) 암 요법을 투여하는 것을 포함하고,
상기 암 치료는 상기 G9a의 길항제 없이 (이의 부재하에) 상기 암 요법 제제의 유효량을 투여하는 것을 포함하는 치료 (예컨대, 표준 돌봄 치료)와 비교하여, 증가된 효능을 갖는, 방법. - 개체에서 암 요법 제제에 내성인 암의 진행을 지연시키고/시키거나 예방하는 방법으로서,
상기 개체에 (a) 유효량의 G9a의 길항제를 투여하는 단계를 포함하는, 방법. - 암 요법 제제에 내성이 진행될 증가된 공산을 갖는, 암을 갖는 개체를 치료하는 방법으로서,
상기 개체에 (a) 유효량의 G9a의 길항제 및 (b) 유효량의 암 요법 제제를 투여하는 단계를 포함하는, 방법. - 암을 갖는 개체에서 암 요법 제제에 대한 민감도를 증가시키는 방법으로서,
상기 개체에 (a) 유효량의 G9a의 길항제를 투여하는 단계를 포함하는, 방법. - 암을 갖는 개체에서 암 요법 제제 민감도의 기간을 연장시키는 방법으로서,
상기 개체에 (a) 유효량의 G9a의 길항제를 투여하는 단계를 포함하는, 방법. - 암을 갖는 개체에서 암 요법에 대한 반응 기간을 연장시키는 방법으로서,
상기 개체에 (a) 유효량의 G9a의 길항제를 투여하는 단계를 포함하는, 방법. - 청구항 3, 5, 7, 8 및 9 중 어느 한 항에 있어서, 상기 방법은, (b) 상기 개체에게 유효량의 상기 암 요법 제제를 투여하는 단계를 추가로 포함하는, 방법.
- 청구항 1 내지 10 중 어느 한 항에 있어서, 상기 G9a의 길항제는 항체 억제제, 결합 소분자 억제제, 결합 폴리펩티드 억제제 및/또는 폴리뉴클레오티드 길항제인, 방법.
- 청구항 11에 있어서, 상기 G9a의 길항제는 G9a에 결합하고, G9a 메틸전달효소 활성을 억제하는, 방법.
- 청구항 1 내지 12 중 어느 한 항에 있어서, 상기 암 요법 제제는 화학요법인, 방법.
- 청구항 13에 있어서, 상기 암 요법 제제는 화학요법이고, 그리고 상기 화학요법은 탁산을 포함하는, 방법.
- 청구항 14 에 있어서, 상기 탁산은 파클리탁셀 또는 도세탁셀인, 방법.
- 청구항 1 내지 15 중 어느 한 항에 있어서, 상기 암 요법 제제는 화학요법이고, 그리고 상기 화학요법은 백금 제제를 포함하는, 방법.
- 청구항 1 내지 12 중 어느 한 항에 있어서, 상기 암 요법 제제는 표적화된 요법인, 방법.
- 청구항 17에 있어서, 상기 암 요법 제제는 표적화된 요법이고, 그리고 상기 표적화된 요법은 EGFR의 길항제를 포함하는, 방법.
- 청구항 18에 있어서, 상기 EGFR의 길항제는, N-(3-에틸페닐)-6,7-비스(2-메톡시에톡시)퀴나졸린-4-아민 또는 이의 약제학적으로 허용가능한 염 (예컨대, 엘로티닙)인, 방법.
- 청구항 17에 있어서, 상기 암 요법 제제는 표적화된 요법이고, 그리고 상기 표적화된 요법은 RAF 억제제인, 방법.
- 청구항 20에 있어서, 상기 RAF 억제제는 BRAF 억제제 및/또는 CRAF 억제제인, 방법.
- 청구항 21에 있어서, 상기 RAF 억제제는 베무라페닙인, 방법.
- 청구항 17에 있어서, 상기 암 요법 제제는 표적화된 요법이고, 그리고 상기 표적화된 요법은 PI3K 억제제인, 방법.
- 청구항 1 내지 23 중 어느 한 항에 있어서, 상기 G9a의 길항제는 소분자 G9a 길항제인, 방법.
- 청구항 1 내지 24 중 어느 한 항에 있어서, 상기 G9a의 길항제 및 상기 암 요법 제제는 동시에 투여되는, 방법.
- 청구항 1 내지 청구항 25 중 어느 한 항에 있어서, 상기 G9a의 길항제는 상기 암 요법 제제 이전에 및/또는 이와 동시에 투여되는, 방법.
- 청구항 1 내지 청구항 26 중 어느 한 항에 있어서, 상기 암은 폐암 (예컨대, 비-소세포 폐암 (NSCLC)), 흑색종, 결장직장암, 췌장암, 및/또는 유방암인, 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201462015932P | 2014-06-23 | 2014-06-23 | |
| US62/015,932 | 2014-06-23 | ||
| PCT/US2015/037189 WO2015200329A1 (en) | 2014-06-23 | 2015-06-23 | Methods of treating cancer and preventing cancer drug resistance |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20170017996A true KR20170017996A (ko) | 2017-02-15 |
Family
ID=54938739
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020177000139A KR20170017996A (ko) | 2014-06-23 | 2015-06-23 | 암을 치료하고 암 약물 내성을 예방하는 방법 |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US20170209444A1 (ko) |
| EP (1) | EP3157524A4 (ko) |
| JP (1) | JP2017519017A (ko) |
| KR (1) | KR20170017996A (ko) |
| CN (1) | CN106456627A (ko) |
| BR (1) | BR112016030064A2 (ko) |
| CA (1) | CA2952474A1 (ko) |
| MX (1) | MX2016016667A (ko) |
| RU (1) | RU2017101809A (ko) |
| WO (1) | WO2015200329A1 (ko) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3519393B1 (en) | 2016-09-30 | 2022-05-18 | Epizyme Inc | Substituted fused bi- or tri- heterocyclic compounds as ehmt2 inhibitors |
| JP7300394B2 (ja) | 2017-01-17 | 2023-06-29 | ヘパリジェニックス ゲーエムベーハー | 肝再生の促進又は肝細胞死の低減もしくは予防のためのプロテインキナーゼ阻害 |
| US11672800B2 (en) | 2017-04-21 | 2023-06-13 | Epizyme, Inc. | Combination therapies with EHMT2 inhibitors |
| SG11202003225YA (en) * | 2017-10-18 | 2020-05-28 | Epizyme Inc | Amine-substituted heterocyclic compounds as ehmt2 inhibitors, salts thereof, and methods of synthesis thereof |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20090137516A1 (en) * | 2007-11-05 | 2009-05-28 | Wyeth | Compositions and methods of treating dyslipidemia |
-
2015
- 2015-06-23 KR KR1020177000139A patent/KR20170017996A/ko unknown
- 2015-06-23 RU RU2017101809A patent/RU2017101809A/ru not_active Application Discontinuation
- 2015-06-23 WO PCT/US2015/037189 patent/WO2015200329A1/en active Application Filing
- 2015-06-23 CN CN201580033855.7A patent/CN106456627A/zh active Pending
- 2015-06-23 JP JP2016573937A patent/JP2017519017A/ja active Pending
- 2015-06-23 MX MX2016016667A patent/MX2016016667A/es unknown
- 2015-06-23 CA CA2952474A patent/CA2952474A1/en not_active Abandoned
- 2015-06-23 EP EP15810899.3A patent/EP3157524A4/en not_active Withdrawn
- 2015-06-23 US US15/321,625 patent/US20170209444A1/en not_active Abandoned
- 2015-06-23 BR BR112016030064A patent/BR112016030064A2/pt not_active Application Discontinuation
Also Published As
| Publication number | Publication date |
|---|---|
| BR112016030064A2 (pt) | 2017-08-22 |
| JP2017519017A (ja) | 2017-07-13 |
| CA2952474A1 (en) | 2015-12-30 |
| EP3157524A1 (en) | 2017-04-26 |
| US20170209444A1 (en) | 2017-07-27 |
| EP3157524A4 (en) | 2017-12-06 |
| RU2017101809A (ru) | 2018-07-23 |
| CN106456627A (zh) | 2017-02-22 |
| WO2015200329A1 (en) | 2015-12-30 |
| MX2016016667A (es) | 2017-08-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20160160213A1 (en) | Methods of treating cancer and preventing cancer drug resistance | |
| US9925240B2 (en) | Methods of treating and preventing cancer drug resistance | |
| US20160143910A1 (en) | Methods of treating cancer and preventing cancer drug resistance | |
| KR20150118159A (ko) | 암의 치료 방법 및 약물 내성의 예방 방법 | |
| EP2536748B1 (en) | Neuregulin antagonists and use thereof in treating cancer | |
| US20170204187A1 (en) | Methods of treating and preventing cancer drug resistance | |
| WO2013025853A1 (en) | Neuregulin antibodies and uses thereof | |
| KR20170017996A (ko) | 암을 치료하고 암 약물 내성을 예방하는 방법 | |
| US20230190750A1 (en) | Methods of treating and preventing cancer drug resistance |