KR20140143655A - 모링가 잎의 수용성 추출물을 유효성분으로 포함하는 암 치료 또는 예방용 조성물 및 모링가 잎의 추출물의 제조방법 - Google Patents
모링가 잎의 수용성 추출물을 유효성분으로 포함하는 암 치료 또는 예방용 조성물 및 모링가 잎의 추출물의 제조방법 Download PDFInfo
- Publication number
- KR20140143655A KR20140143655A KR1020130065519A KR20130065519A KR20140143655A KR 20140143655 A KR20140143655 A KR 20140143655A KR 1020130065519 A KR1020130065519 A KR 1020130065519A KR 20130065519 A KR20130065519 A KR 20130065519A KR 20140143655 A KR20140143655 A KR 20140143655A
- Authority
- KR
- South Korea
- Prior art keywords
- cancer
- extract
- moringa
- water
- pharmaceutical composition
- Prior art date
Links
- 235000011347 Moringa oleifera Nutrition 0.000 title claims abstract description 175
- 239000000284 extract Substances 0.000 title claims abstract description 174
- 206010028980 Neoplasm Diseases 0.000 title claims abstract description 81
- 201000011510 cancer Diseases 0.000 title claims abstract description 77
- 239000000203 mixture Substances 0.000 title claims abstract description 57
- 238000011282 treatment Methods 0.000 title claims abstract description 19
- 238000000034 method Methods 0.000 title claims abstract description 17
- 230000002265 prevention Effects 0.000 title claims description 6
- 244000179886 Moringa oleifera Species 0.000 title abstract description 164
- 238000002360 preparation method Methods 0.000 title description 16
- 239000004480 active ingredient Substances 0.000 claims abstract description 25
- 230000001093 anti-cancer Effects 0.000 claims abstract description 11
- 238000004519 manufacturing process Methods 0.000 claims abstract description 8
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 64
- 108090000623 proteins and genes Proteins 0.000 claims description 61
- 102000004169 proteins and genes Human genes 0.000 claims description 48
- 238000000605 extraction Methods 0.000 claims description 41
- 239000008194 pharmaceutical composition Substances 0.000 claims description 35
- 239000002904 solvent Substances 0.000 claims description 27
- 239000000843 powder Substances 0.000 claims description 13
- 235000013305 food Nutrition 0.000 claims description 12
- 206010058467 Lung neoplasm malignant Diseases 0.000 claims description 11
- 239000002537 cosmetic Substances 0.000 claims description 11
- 238000007654 immersion Methods 0.000 claims description 11
- 201000007270 liver cancer Diseases 0.000 claims description 11
- 208000014018 liver neoplasm Diseases 0.000 claims description 11
- 201000005202 lung cancer Diseases 0.000 claims description 11
- 208000020816 lung neoplasm Diseases 0.000 claims description 11
- 239000006286 aqueous extract Substances 0.000 claims description 8
- 239000000243 solution Substances 0.000 claims description 6
- 241001641404 Meringa Species 0.000 claims description 5
- 239000002775 capsule Substances 0.000 claims description 5
- 238000001914 filtration Methods 0.000 claims description 5
- 239000003826 tablet Substances 0.000 claims description 5
- 206010006187 Breast cancer Diseases 0.000 claims description 4
- 208000026310 Breast neoplasm Diseases 0.000 claims description 4
- 208000000453 Skin Neoplasms Diseases 0.000 claims description 4
- 239000008187 granular material Substances 0.000 claims description 4
- 201000010260 leiomyoma Diseases 0.000 claims description 4
- 201000000849 skin cancer Diseases 0.000 claims description 4
- 206010041823 squamous cell carcinoma Diseases 0.000 claims description 4
- 239000000725 suspension Substances 0.000 claims description 4
- 239000006188 syrup Substances 0.000 claims description 4
- 235000020357 syrup Nutrition 0.000 claims description 4
- 239000003937 drug carrier Substances 0.000 claims description 3
- 239000000839 emulsion Substances 0.000 claims description 3
- 239000006187 pill Substances 0.000 claims description 3
- 208000017572 squamous cell neoplasm Diseases 0.000 claims description 3
- 206010046798 Uterine leiomyoma Diseases 0.000 claims description 2
- 241000220215 Moringa Species 0.000 claims 12
- 231100000331 toxic Toxicity 0.000 abstract description 8
- 230000002588 toxic effect Effects 0.000 abstract description 8
- 239000003814 drug Substances 0.000 abstract description 6
- 239000003795 chemical substances by application Substances 0.000 abstract description 4
- 239000005445 natural material Substances 0.000 abstract 1
- 210000004027 cell Anatomy 0.000 description 145
- 230000000694 effects Effects 0.000 description 28
- 239000012510 hollow fiber Substances 0.000 description 16
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 15
- 238000004458 analytical method Methods 0.000 description 14
- 239000012153 distilled water Substances 0.000 description 14
- 230000014509 gene expression Effects 0.000 description 14
- 238000009472 formulation Methods 0.000 description 12
- 239000012528 membrane Substances 0.000 description 12
- 239000000499 gel Substances 0.000 description 11
- 231100000419 toxicity Toxicity 0.000 description 11
- 230000001988 toxicity Effects 0.000 description 11
- AOJJSUZBOXZQNB-TZSSRYMLSA-N Doxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-TZSSRYMLSA-N 0.000 description 10
- 238000002474 experimental method Methods 0.000 description 10
- 230000001105 regulatory effect Effects 0.000 description 10
- 238000002493 microarray Methods 0.000 description 9
- 238000001262 western blot Methods 0.000 description 9
- 239000002246 antineoplastic agent Substances 0.000 description 8
- 238000003556 assay Methods 0.000 description 8
- 239000002299 complementary DNA Substances 0.000 description 8
- 238000011534 incubation Methods 0.000 description 8
- 230000002401 inhibitory effect Effects 0.000 description 8
- 239000003642 reactive oxygen metabolite Substances 0.000 description 8
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 7
- 230000008859 change Effects 0.000 description 7
- 238000002347 injection Methods 0.000 description 7
- 239000007924 injection Substances 0.000 description 7
- 239000000523 sample Substances 0.000 description 7
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 6
- 238000012413 Fluorescence activated cell sorting analysis Methods 0.000 description 6
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 6
- 241000699670 Mus sp. Species 0.000 description 6
- 238000006731 degradation reaction Methods 0.000 description 6
- 230000003828 downregulation Effects 0.000 description 6
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 6
- 239000000126 substance Substances 0.000 description 6
- 238000000134 MTT assay Methods 0.000 description 5
- 231100000002 MTT assay Toxicity 0.000 description 5
- 230000015556 catabolic process Effects 0.000 description 5
- 230000022131 cell cycle Effects 0.000 description 5
- 230000012292 cell migration Effects 0.000 description 5
- 230000007423 decrease Effects 0.000 description 5
- 229960004679 doxorubicin Drugs 0.000 description 5
- 238000009396 hybridization Methods 0.000 description 5
- 108020004999 messenger RNA Proteins 0.000 description 5
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 5
- 108010085238 Actins Proteins 0.000 description 4
- 102000007469 Actins Human genes 0.000 description 4
- 206010014733 Endometrial cancer Diseases 0.000 description 4
- 206010014759 Endometrial neoplasm Diseases 0.000 description 4
- 229940041181 antineoplastic drug Drugs 0.000 description 4
- 230000006907 apoptotic process Effects 0.000 description 4
- 230000000052 comparative effect Effects 0.000 description 4
- 201000010099 disease Diseases 0.000 description 4
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 4
- 229940079593 drug Drugs 0.000 description 4
- 230000006870 function Effects 0.000 description 4
- 230000001939 inductive effect Effects 0.000 description 4
- 239000002609 medium Substances 0.000 description 4
- 230000005012 migration Effects 0.000 description 4
- 238000013508 migration Methods 0.000 description 4
- 239000003960 organic solvent Substances 0.000 description 4
- 239000000546 pharmaceutical excipient Substances 0.000 description 4
- 239000011148 porous material Substances 0.000 description 4
- 239000002994 raw material Substances 0.000 description 4
- 230000004083 survival effect Effects 0.000 description 4
- 238000012546 transfer Methods 0.000 description 4
- 108020004463 18S ribosomal RNA Proteins 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- 102000003952 Caspase 3 Human genes 0.000 description 3
- 108090000397 Caspase 3 Proteins 0.000 description 3
- 102000004142 Trypsin Human genes 0.000 description 3
- 108090000631 Trypsin Proteins 0.000 description 3
- 238000002835 absorbance Methods 0.000 description 3
- 238000010521 absorption reaction Methods 0.000 description 3
- 210000003050 axon Anatomy 0.000 description 3
- 235000013361 beverage Nutrition 0.000 description 3
- 150000001720 carbohydrates Chemical class 0.000 description 3
- 235000014633 carbohydrates Nutrition 0.000 description 3
- 230000030833 cell death Effects 0.000 description 3
- 210000003169 central nervous system Anatomy 0.000 description 3
- 238000005119 centrifugation Methods 0.000 description 3
- 239000003153 chemical reaction reagent Substances 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 238000001035 drying Methods 0.000 description 3
- 239000012091 fetal bovine serum Substances 0.000 description 3
- 239000000796 flavoring agent Substances 0.000 description 3
- 235000019634 flavors Nutrition 0.000 description 3
- 238000000338 in vitro Methods 0.000 description 3
- 238000001727 in vivo Methods 0.000 description 3
- 230000003834 intracellular effect Effects 0.000 description 3
- 230000002147 killing effect Effects 0.000 description 3
- 235000019359 magnesium stearate Nutrition 0.000 description 3
- -1 maltose and sucrose Chemical compound 0.000 description 3
- 238000000386 microscopy Methods 0.000 description 3
- 239000006228 supernatant Substances 0.000 description 3
- 238000012360 testing method Methods 0.000 description 3
- 239000012588 trypsin Substances 0.000 description 3
- 239000011782 vitamin Substances 0.000 description 3
- 235000013343 vitamin Nutrition 0.000 description 3
- 229940088594 vitamin Drugs 0.000 description 3
- 229930003231 vitamin Natural products 0.000 description 3
- QAPSNMNOIOSXSQ-YNEHKIRRSA-N 1-[(2r,4s,5r)-4-[tert-butyl(dimethyl)silyl]oxy-5-(hydroxymethyl)oxolan-2-yl]-5-methylpyrimidine-2,4-dione Chemical compound O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](CO)[C@@H](O[Si](C)(C)C(C)(C)C)C1 QAPSNMNOIOSXSQ-YNEHKIRRSA-N 0.000 description 2
- VFNKZQNIXUFLBC-UHFFFAOYSA-N 2',7'-dichlorofluorescein Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC(Cl)=C(O)C=C1OC1=C2C=C(Cl)C(O)=C1 VFNKZQNIXUFLBC-UHFFFAOYSA-N 0.000 description 2
- XDFNWJDGWJVGGN-UHFFFAOYSA-N 2-(2,7-dichloro-3,6-dihydroxy-9h-xanthen-9-yl)benzoic acid Chemical compound OC(=O)C1=CC=CC=C1C1C2=CC(Cl)=C(O)C=C2OC2=CC(O)=C(Cl)C=C21 XDFNWJDGWJVGGN-UHFFFAOYSA-N 0.000 description 2
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 2
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 2
- 201000009030 Carcinoma Diseases 0.000 description 2
- 241000282552 Chlorocebus aethiops Species 0.000 description 2
- 102000006311 Cyclin D1 Human genes 0.000 description 2
- 108010058546 Cyclin D1 Proteins 0.000 description 2
- 108020004414 DNA Proteins 0.000 description 2
- 241000196324 Embryophyta Species 0.000 description 2
- 239000004606 Fillers/Extenders Substances 0.000 description 2
- ZHNUHDYFZUAESO-UHFFFAOYSA-N Formamide Chemical compound NC=O ZHNUHDYFZUAESO-UHFFFAOYSA-N 0.000 description 2
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 2
- 102000002812 Heat-Shock Proteins Human genes 0.000 description 2
- 108010004889 Heat-Shock Proteins Proteins 0.000 description 2
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 2
- 108010055717 JNK Mitogen-Activated Protein Kinases Proteins 0.000 description 2
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 2
- 241000699660 Mus musculus Species 0.000 description 2
- 102100038895 Myc proto-oncogene protein Human genes 0.000 description 2
- 101710135898 Myc proto-oncogene protein Proteins 0.000 description 2
- 108091034117 Oligonucleotide Proteins 0.000 description 2
- 241000700159 Rattus Species 0.000 description 2
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- 101710150448 Transcriptional regulator Myc Proteins 0.000 description 2
- GLNADSQYFUSGOU-GPTZEZBUSA-J Trypan blue Chemical compound [Na+].[Na+].[Na+].[Na+].C1=C(S([O-])(=O)=O)C=C2C=C(S([O-])(=O)=O)C(/N=N/C3=CC=C(C=C3C)C=3C=C(C(=CC=3)\N=N\C=3C(=CC4=CC(=CC(N)=C4C=3O)S([O-])(=O)=O)S([O-])(=O)=O)C)=C(O)C2=C1N GLNADSQYFUSGOU-GPTZEZBUSA-J 0.000 description 2
- 231100000480 WST assay Toxicity 0.000 description 2
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 description 2
- 239000000654 additive Substances 0.000 description 2
- 239000011230 binding agent Substances 0.000 description 2
- 230000009702 cancer cell proliferation Effects 0.000 description 2
- 238000010609 cell counting kit-8 assay Methods 0.000 description 2
- 238000004113 cell culture Methods 0.000 description 2
- 230000004663 cell proliferation Effects 0.000 description 2
- 230000003833 cell viability Effects 0.000 description 2
- 238000010293 colony formation assay Methods 0.000 description 2
- 235000009508 confectionery Nutrition 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- 229940127089 cytotoxic agent Drugs 0.000 description 2
- 230000001419 dependent effect Effects 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 239000003085 diluting agent Substances 0.000 description 2
- 239000007884 disintegrant Substances 0.000 description 2
- 238000001962 electrophoresis Methods 0.000 description 2
- 230000007717 exclusion Effects 0.000 description 2
- 239000000835 fiber Substances 0.000 description 2
- 239000000945 filler Substances 0.000 description 2
- 238000000684 flow cytometry Methods 0.000 description 2
- 235000003599 food sweetener Nutrition 0.000 description 2
- 239000008103 glucose Substances 0.000 description 2
- 230000012010 growth Effects 0.000 description 2
- 239000001963 growth medium Substances 0.000 description 2
- 208000014829 head and neck neoplasm Diseases 0.000 description 2
- 206010073071 hepatocellular carcinoma Diseases 0.000 description 2
- 231100000844 hepatocellular carcinoma Toxicity 0.000 description 2
- 108091008147 housekeeping proteins Proteins 0.000 description 2
- 230000006872 improvement Effects 0.000 description 2
- 239000004615 ingredient Substances 0.000 description 2
- 239000002198 insoluble material Substances 0.000 description 2
- 210000003292 kidney cell Anatomy 0.000 description 2
- 239000008101 lactose Substances 0.000 description 2
- 229940041476 lactose 100 mg Drugs 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 238000011068 loading method Methods 0.000 description 2
- 238000010232 migration assay Methods 0.000 description 2
- 238000011580 nude mouse model Methods 0.000 description 2
- 235000015097 nutrients Nutrition 0.000 description 2
- 229920000515 polycarbonate Polymers 0.000 description 2
- 239000004417 polycarbonate Substances 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- 230000035755 proliferation Effects 0.000 description 2
- XJMOSONTPMZWPB-UHFFFAOYSA-M propidium iodide Chemical compound [I-].[I-].C12=CC(N)=CC=C2C2=CC=C(N)C=C2[N+](CCC[N+](C)(CC)CC)=C1C1=CC=CC=C1 XJMOSONTPMZWPB-UHFFFAOYSA-M 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 239000003381 stabilizer Substances 0.000 description 2
- 239000005720 sucrose Substances 0.000 description 2
- 239000004094 surface-active agent Substances 0.000 description 2
- 239000003765 sweetening agent Substances 0.000 description 2
- 239000000454 talc Substances 0.000 description 2
- 229910052623 talc Inorganic materials 0.000 description 2
- 229940124597 therapeutic agent Drugs 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 230000035899 viability Effects 0.000 description 2
- 238000003809 water extraction Methods 0.000 description 2
- 239000000080 wetting agent Substances 0.000 description 2
- OWEGMIWEEQEYGQ-UHFFFAOYSA-N 100676-05-9 Natural products OC1C(O)C(O)C(CO)OC1OCC1C(O)C(O)C(O)C(OC2C(OC(O)C(O)C2O)CO)O1 OWEGMIWEEQEYGQ-UHFFFAOYSA-N 0.000 description 1
- PXEZTIWVRVSYOK-UHFFFAOYSA-N 2-(3,6-diacetyloxy-2,7-dichloro-9h-xanthen-9-yl)benzoic acid Chemical compound C1=2C=C(Cl)C(OC(=O)C)=CC=2OC2=CC(OC(C)=O)=C(Cl)C=C2C1C1=CC=CC=C1C(O)=O PXEZTIWVRVSYOK-UHFFFAOYSA-N 0.000 description 1
- 108010011485 Aspartame Proteins 0.000 description 1
- 241000972773 Aulopiformes Species 0.000 description 1
- 101100078107 Bacillus sp. (strain B-0618) soxA gene Proteins 0.000 description 1
- 206010005949 Bone cancer Diseases 0.000 description 1
- 208000018084 Bone neoplasm Diseases 0.000 description 1
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 1
- 238000009010 Bradford assay Methods 0.000 description 1
- 206010007953 Central nervous system lymphoma Diseases 0.000 description 1
- 206010008342 Cervix carcinoma Diseases 0.000 description 1
- 108091026890 Coding region Proteins 0.000 description 1
- 206010009944 Colon cancer Diseases 0.000 description 1
- 206010010071 Coma Diseases 0.000 description 1
- 229920002261 Corn starch Polymers 0.000 description 1
- 229920000742 Cotton Polymers 0.000 description 1
- 229920000858 Cyclodextrin Polymers 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 229920001353 Dextrin Polymers 0.000 description 1
- 239000004375 Dextrin Substances 0.000 description 1
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 1
- 208000001976 Endocrine Gland Neoplasms Diseases 0.000 description 1
- 239000004386 Erythritol Substances 0.000 description 1
- UNXHWFMMPAWVPI-UHFFFAOYSA-N Erythritol Natural products OCC(O)C(O)CO UNXHWFMMPAWVPI-UHFFFAOYSA-N 0.000 description 1
- 208000000461 Esophageal Neoplasms Diseases 0.000 description 1
- 108700039887 Essential Genes Proteins 0.000 description 1
- 108090000371 Esterases Proteins 0.000 description 1
- KRHYYFGTRYWZRS-UHFFFAOYSA-M Fluoride anion Chemical compound [F-] KRHYYFGTRYWZRS-UHFFFAOYSA-M 0.000 description 1
- 229940123457 Free radical scavenger Drugs 0.000 description 1
- 229930091371 Fructose Natural products 0.000 description 1
- 239000005715 Fructose Substances 0.000 description 1
- RFSUNEUAIZKAJO-ARQDHWQXSA-N Fructose Chemical compound OC[C@H]1O[C@](O)(CO)[C@@H](O)[C@@H]1O RFSUNEUAIZKAJO-ARQDHWQXSA-N 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 208000032612 Glial tumor Diseases 0.000 description 1
- 206010018338 Glioma Diseases 0.000 description 1
- 102000018932 HSP70 Heat-Shock Proteins Human genes 0.000 description 1
- 108010027992 HSP70 Heat-Shock Proteins Proteins 0.000 description 1
- 102100027421 Heat shock cognate 71 kDa protein Human genes 0.000 description 1
- 101710104933 Heat shock cognate 71 kDa protein Proteins 0.000 description 1
- 102100032510 Heat shock protein HSP 90-beta Human genes 0.000 description 1
- 101710163596 Heat shock protein HSP 90-beta Proteins 0.000 description 1
- 208000017604 Hodgkin disease Diseases 0.000 description 1
- 208000010747 Hodgkins lymphoma Diseases 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 101000781955 Homo sapiens Proto-oncogene Wnt-1 Proteins 0.000 description 1
- 101000687905 Homo sapiens Transcription factor SOX-2 Proteins 0.000 description 1
- 108010001336 Horseradish Peroxidase Proteins 0.000 description 1
- 102000014150 Interferons Human genes 0.000 description 1
- 108010050904 Interferons Proteins 0.000 description 1
- 206010061252 Intraocular melanoma Diseases 0.000 description 1
- 108700021430 Kruppel-Like Factor 4 Proteins 0.000 description 1
- GUBGYTABKSRVRQ-PICCSMPSSA-N Maltose Natural products O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@@H](CO)OC(O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-PICCSMPSSA-N 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 206010027476 Metastases Diseases 0.000 description 1
- 241000699666 Mus <mouse, genus> Species 0.000 description 1
- 101100247001 Mus musculus Qsox1 gene Proteins 0.000 description 1
- 108010057466 NF-kappa B Proteins 0.000 description 1
- 102000003945 NF-kappa B Human genes 0.000 description 1
- 208000012902 Nervous system disease Diseases 0.000 description 1
- 208000025966 Neurological disease Diseases 0.000 description 1
- 239000000020 Nitrocellulose Substances 0.000 description 1
- 108091028043 Nucleic acid sequence Proteins 0.000 description 1
- 206010030155 Oesophageal carcinoma Diseases 0.000 description 1
- 238000012408 PCR amplification Methods 0.000 description 1
- 101710126211 POU domain, class 5, transcription factor 1 Proteins 0.000 description 1
- 206010061902 Pancreatic neoplasm Diseases 0.000 description 1
- 208000000821 Parathyroid Neoplasms Diseases 0.000 description 1
- 229920002230 Pectic acid Polymers 0.000 description 1
- 241000233805 Phoenix Species 0.000 description 1
- 208000007913 Pituitary Neoplasms Diseases 0.000 description 1
- 201000005746 Pituitary adenoma Diseases 0.000 description 1
- 206010061538 Pituitary tumour benign Diseases 0.000 description 1
- 229920001213 Polysorbate 20 Polymers 0.000 description 1
- KQHKSGRIBYJYFX-UHFFFAOYSA-J Ponceau S Chemical compound [Na+].[Na+].[Na+].[Na+].Oc1c(cc2cc(ccc2c1N=Nc1ccc(cc1S([O-])(=O)=O)N=Nc1ccc(cc1)S([O-])(=O)=O)S([O-])(=O)=O)S([O-])(=O)=O KQHKSGRIBYJYFX-UHFFFAOYSA-J 0.000 description 1
- 229940123573 Protein synthesis inhibitor Drugs 0.000 description 1
- 238000002123 RNA extraction Methods 0.000 description 1
- 238000010802 RNA extraction kit Methods 0.000 description 1
- 239000012980 RPMI-1640 medium Substances 0.000 description 1
- 238000010240 RT-PCR analysis Methods 0.000 description 1
- 208000006265 Renal cell carcinoma Diseases 0.000 description 1
- 108010083644 Ribonucleases Proteins 0.000 description 1
- 102000006382 Ribonucleases Human genes 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- 206010039491 Sarcoma Diseases 0.000 description 1
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 1
- 208000021712 Soft tissue sarcoma Diseases 0.000 description 1
- 101150037203 Sox2 gene Proteins 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 244000228451 Stevia rebaudiana Species 0.000 description 1
- 208000005718 Stomach Neoplasms Diseases 0.000 description 1
- 208000024770 Thyroid neoplasm Diseases 0.000 description 1
- 102100024270 Transcription factor SOX-2 Human genes 0.000 description 1
- 206010046431 Urethral cancer Diseases 0.000 description 1
- 206010046458 Urethral neoplasms Diseases 0.000 description 1
- 208000006105 Uterine Cervical Neoplasms Diseases 0.000 description 1
- 201000005969 Uveal melanoma Diseases 0.000 description 1
- 208000001407 Vascular Headaches Diseases 0.000 description 1
- 101150019524 WNT2 gene Proteins 0.000 description 1
- 102000052547 Wnt-1 Human genes 0.000 description 1
- 102000052556 Wnt-2 Human genes 0.000 description 1
- 108700020986 Wnt-2 Proteins 0.000 description 1
- 101100485099 Xenopus laevis wnt2b-b gene Proteins 0.000 description 1
- TVXBFESIOXBWNM-UHFFFAOYSA-N Xylitol Natural products OCCC(O)C(O)C(O)CCO TVXBFESIOXBWNM-UHFFFAOYSA-N 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 208000009956 adenocarcinoma Diseases 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 239000011543 agarose gel Substances 0.000 description 1
- 235000013334 alcoholic beverage Nutrition 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- 239000002168 alkylating agent Substances 0.000 description 1
- 229940100198 alkylating agent Drugs 0.000 description 1
- 239000003708 ampul Substances 0.000 description 1
- 238000000540 analysis of variance Methods 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 230000003266 anti-allergic effect Effects 0.000 description 1
- 230000000843 anti-fungal effect Effects 0.000 description 1
- 230000000340 anti-metabolite Effects 0.000 description 1
- 230000000259 anti-tumor effect Effects 0.000 description 1
- 229940100197 antimetabolite Drugs 0.000 description 1
- 239000002256 antimetabolite Substances 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 230000001640 apoptogenic effect Effects 0.000 description 1
- 239000000605 aspartame Substances 0.000 description 1
- 235000010357 aspartame Nutrition 0.000 description 1
- IAOZJIPTCAWIRG-QWRGUYRKSA-N aspartame Chemical compound OC(=O)C[C@H](N)C(=O)N[C@H](C(=O)OC)CC1=CC=CC=C1 IAOZJIPTCAWIRG-QWRGUYRKSA-N 0.000 description 1
- 229960003438 aspartame Drugs 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 230000002238 attenuated effect Effects 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- GUBGYTABKSRVRQ-QUYVBRFLSA-N beta-maltose Chemical compound OC[C@H]1O[C@H](O[C@H]2[C@H](O)[C@@H](O)[C@H](O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@@H]1O GUBGYTABKSRVRQ-QUYVBRFLSA-N 0.000 description 1
- 230000003115 biocidal effect Effects 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 235000008429 bread Nutrition 0.000 description 1
- 238000010805 cDNA synthesis kit Methods 0.000 description 1
- 229910000019 calcium carbonate Inorganic materials 0.000 description 1
- 230000004611 cancer cell death Effects 0.000 description 1
- 239000003560 cancer drug Substances 0.000 description 1
- 235000014171 carbonated beverage Nutrition 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 239000006143 cell culture medium Substances 0.000 description 1
- 230000022534 cell killing Effects 0.000 description 1
- 230000006037 cell lysis Effects 0.000 description 1
- 238000001516 cell proliferation assay Methods 0.000 description 1
- 239000006285 cell suspension Substances 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 230000005754 cellular signaling Effects 0.000 description 1
- 230000007541 cellular toxicity Effects 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 201000010881 cervical cancer Diseases 0.000 description 1
- 238000002512 chemotherapy Methods 0.000 description 1
- 235000019219 chocolate Nutrition 0.000 description 1
- 239000000084 colloidal system Substances 0.000 description 1
- 208000029742 colonic neoplasm Diseases 0.000 description 1
- 230000001332 colony forming effect Effects 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 238000012790 confirmation Methods 0.000 description 1
- 239000008120 corn starch Substances 0.000 description 1
- 238000010219 correlation analysis Methods 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 210000004748 cultured cell Anatomy 0.000 description 1
- 208000030381 cutaneous melanoma Diseases 0.000 description 1
- 231100000433 cytotoxic Toxicity 0.000 description 1
- 230000001472 cytotoxic effect Effects 0.000 description 1
- 231100000135 cytotoxicity Toxicity 0.000 description 1
- 230000003013 cytotoxicity Effects 0.000 description 1
- 235000013365 dairy product Nutrition 0.000 description 1
- 238000007405 data analysis Methods 0.000 description 1
- 238000013480 data collection Methods 0.000 description 1
- 230000034994 death Effects 0.000 description 1
- 231100000517 death Toxicity 0.000 description 1
- 230000000593 degrading effect Effects 0.000 description 1
- 230000001934 delay Effects 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 235000019425 dextrin Nutrition 0.000 description 1
- 206010012601 diabetes mellitus Diseases 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 235000015872 dietary supplement Nutrition 0.000 description 1
- 150000002016 disaccharides Chemical class 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 230000035622 drinking Effects 0.000 description 1
- 235000013399 edible fruits Nutrition 0.000 description 1
- 230000000235 effect on cancer Effects 0.000 description 1
- 239000003792 electrolyte Substances 0.000 description 1
- 201000003914 endometrial carcinoma Diseases 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 239000003623 enhancer Substances 0.000 description 1
- 235000019414 erythritol Nutrition 0.000 description 1
- UNXHWFMMPAWVPI-ZXZARUISSA-N erythritol Chemical compound OC[C@H](O)[C@H](O)CO UNXHWFMMPAWVPI-ZXZARUISSA-N 0.000 description 1
- 229940009714 erythritol Drugs 0.000 description 1
- 201000004101 esophageal cancer Diseases 0.000 description 1
- 230000029142 excretion Effects 0.000 description 1
- 235000013861 fat-free Nutrition 0.000 description 1
- 239000000706 filtrate Substances 0.000 description 1
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 1
- 238000007421 fluorometric assay Methods 0.000 description 1
- 235000012041 food component Nutrition 0.000 description 1
- 239000005417 food ingredient Substances 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 125000000524 functional group Chemical group 0.000 description 1
- 206010017758 gastric cancer Diseases 0.000 description 1
- 238000001502 gel electrophoresis Methods 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 239000007903 gelatin capsule Substances 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 230000030279 gene silencing Effects 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 230000002710 gonadal effect Effects 0.000 description 1
- 239000007902 hard capsule Substances 0.000 description 1
- 231100000171 higher toxicity Toxicity 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- 235000015243 ice cream Nutrition 0.000 description 1
- 238000003384 imaging method Methods 0.000 description 1
- 239000000677 immunologic agent Substances 0.000 description 1
- 229940124541 immunological agent Drugs 0.000 description 1
- 238000002513 implantation Methods 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 230000008595 infiltration Effects 0.000 description 1
- 238000001764 infiltration Methods 0.000 description 1
- 230000002757 inflammatory effect Effects 0.000 description 1
- 239000002054 inoculum Substances 0.000 description 1
- 229940079322 interferon Drugs 0.000 description 1
- 238000000185 intracerebroventricular administration Methods 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 238000010253 intravenous injection Methods 0.000 description 1
- 238000011835 investigation Methods 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 231100001231 less toxic Toxicity 0.000 description 1
- 244000144972 livestock Species 0.000 description 1
- 231100000053 low toxicity Toxicity 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 201000005243 lung squamous cell carcinoma Diseases 0.000 description 1
- 239000008176 lyophilized powder Substances 0.000 description 1
- 208000029559 malignant endocrine neoplasm Diseases 0.000 description 1
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 description 1
- 208000026037 malignant tumor of neck Diseases 0.000 description 1
- 208000026045 malignant tumor of parathyroid gland Diseases 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 235000013372 meat Nutrition 0.000 description 1
- 201000001441 melanoma Diseases 0.000 description 1
- 238000005374 membrane filtration Methods 0.000 description 1
- HEBKCHPVOIAQTA-UHFFFAOYSA-N meso ribitol Natural products OCC(O)C(O)C(O)CO HEBKCHPVOIAQTA-UHFFFAOYSA-N 0.000 description 1
- 230000009401 metastasis Effects 0.000 description 1
- 238000010208 microarray analysis Methods 0.000 description 1
- 235000013336 milk Nutrition 0.000 description 1
- 239000008267 milk Substances 0.000 description 1
- 210000004080 milk Anatomy 0.000 description 1
- 230000002438 mitochondrial effect Effects 0.000 description 1
- 239000011259 mixed solution Substances 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 150000002772 monosaccharides Chemical class 0.000 description 1
- 235000021096 natural sweeteners Nutrition 0.000 description 1
- 229920001220 nitrocellulos Polymers 0.000 description 1
- 108091027963 non-coding RNA Proteins 0.000 description 1
- 102000042567 non-coding RNA Human genes 0.000 description 1
- 208000002154 non-small cell lung carcinoma Diseases 0.000 description 1
- 235000012149 noodles Nutrition 0.000 description 1
- 238000010606 normalization Methods 0.000 description 1
- 201000002575 ocular melanoma Diseases 0.000 description 1
- 239000002674 ointment Substances 0.000 description 1
- 229920001542 oligosaccharide Polymers 0.000 description 1
- 150000002482 oligosaccharides Chemical class 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 229940127084 other anti-cancer agent Drugs 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 201000002528 pancreatic cancer Diseases 0.000 description 1
- 208000008443 pancreatic carcinoma Diseases 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- LCLHHZYHLXDRQG-ZNKJPWOQSA-N pectic acid Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)O[C@H](C(O)=O)[C@@H]1OC1[C@H](O)[C@@H](O)[C@@H](OC2[C@@H]([C@@H](O)[C@@H](O)[C@H](O2)C(O)=O)O)[C@@H](C(O)=O)O1 LCLHHZYHLXDRQG-ZNKJPWOQSA-N 0.000 description 1
- 239000000049 pigment Substances 0.000 description 1
- 208000021310 pituitary gland adenoma Diseases 0.000 description 1
- 235000013550 pizza Nutrition 0.000 description 1
- 229920002401 polyacrylamide Polymers 0.000 description 1
- 239000010318 polygalacturonic acid Substances 0.000 description 1
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 1
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 1
- 229920001282 polysaccharide Polymers 0.000 description 1
- 239000005017 polysaccharide Substances 0.000 description 1
- 150000004804 polysaccharides Chemical class 0.000 description 1
- 230000003449 preventive effect Effects 0.000 description 1
- 208000016800 primary central nervous system lymphoma Diseases 0.000 description 1
- 102000004196 processed proteins & peptides Human genes 0.000 description 1
- 108090000765 processed proteins & peptides Proteins 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 239000012144 protein assay dye reagent concentrate Substances 0.000 description 1
- 239000000007 protein synthesis inhibitor Substances 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 239000008213 purified water Substances 0.000 description 1
- 239000002516 radical scavenger Substances 0.000 description 1
- 238000001959 radiotherapy Methods 0.000 description 1
- HELXLJCILKEWJH-NCGAPWICSA-N rebaudioside A Chemical compound O([C@H]1[C@H](O)[C@@H](CO)O[C@H]([C@@H]1O[C@H]1[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O1)O)O[C@]12C(=C)C[C@@]3(C1)CC[C@@H]1[C@@](C)(CCC[C@]1([C@@H]3CC2)C)C(=O)O[C@H]1[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O1)O)[C@@H]1O[C@H](CO)[C@@H](O)[C@H](O)[C@H]1O HELXLJCILKEWJH-NCGAPWICSA-N 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 238000003757 reverse transcription PCR Methods 0.000 description 1
- 229940069575 rompun Drugs 0.000 description 1
- 235000019204 saccharin Nutrition 0.000 description 1
- CVHZOJJKTDOEJC-UHFFFAOYSA-N saccharin Chemical compound C1=CC=C2C(=O)NS(=O)(=O)C2=C1 CVHZOJJKTDOEJC-UHFFFAOYSA-N 0.000 description 1
- 229940081974 saccharin Drugs 0.000 description 1
- 239000000901 saccharin and its Na,K and Ca salt Substances 0.000 description 1
- 235000002020 sage Nutrition 0.000 description 1
- 235000019515 salmon Nutrition 0.000 description 1
- 235000013580 sausages Nutrition 0.000 description 1
- HFHDHCJBZVLPGP-UHFFFAOYSA-N schardinger α-dextrin Chemical compound O1C(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(O)C2O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC2C(O)C(O)C1OC2CO HFHDHCJBZVLPGP-UHFFFAOYSA-N 0.000 description 1
- 239000012679 serum free medium Substances 0.000 description 1
- 230000019491 signal transduction Effects 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 238000011524 similarity measure Methods 0.000 description 1
- 230000037384 skin absorption Effects 0.000 description 1
- 231100000274 skin absorption Toxicity 0.000 description 1
- 201000003708 skin melanoma Diseases 0.000 description 1
- 201000002314 small intestine cancer Diseases 0.000 description 1
- 235000011888 snacks Nutrition 0.000 description 1
- 239000007901 soft capsule Substances 0.000 description 1
- 238000000638 solvent extraction Methods 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 235000010356 sorbitol Nutrition 0.000 description 1
- 229960002920 sorbitol Drugs 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 206010062261 spinal cord neoplasm Diseases 0.000 description 1
- 230000007480 spreading Effects 0.000 description 1
- 238000003892 spreading Methods 0.000 description 1
- 238000010186 staining Methods 0.000 description 1
- 239000012192 staining solution Substances 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 238000007619 statistical method Methods 0.000 description 1
- 201000011549 stomach cancer Diseases 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 229960005322 streptomycin Drugs 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 150000005846 sugar alcohols Chemical class 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 125000003831 tetrazolyl group Chemical group 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- 201000002510 thyroid cancer Diseases 0.000 description 1
- 238000011200 topical administration Methods 0.000 description 1
- 238000002054 transplantation Methods 0.000 description 1
- 230000032258 transport Effects 0.000 description 1
- 208000029729 tumor suppressor gene on chromosome 11 Diseases 0.000 description 1
- 238000004704 ultra performance liquid chromatography Methods 0.000 description 1
- 230000003827 upregulation Effects 0.000 description 1
- 231100000747 viability assay Toxicity 0.000 description 1
- 238000003026 viability measurement method Methods 0.000 description 1
- 150000003722 vitamin derivatives Chemical class 0.000 description 1
- 239000003021 water soluble solvent Substances 0.000 description 1
- QYEFBJRXKKSABU-UHFFFAOYSA-N xylazine hydrochloride Chemical compound Cl.CC1=CC=CC(C)=C1NC1=NCCCS1 QYEFBJRXKKSABU-UHFFFAOYSA-N 0.000 description 1
- 239000000811 xylitol Substances 0.000 description 1
- 235000010447 xylitol Nutrition 0.000 description 1
- HEBKCHPVOIAQTA-SCDXWVJYSA-N xylitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)CO HEBKCHPVOIAQTA-SCDXWVJYSA-N 0.000 description 1
- 229960002675 xylitol Drugs 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K36/00—Medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicines
- A61K36/18—Magnoliophyta (angiosperms)
- A61K36/185—Magnoliopsida (dicotyledons)
- A61K36/48—Fabaceae or Leguminosae (Pea or Legume family); Caesalpiniaceae; Mimosaceae; Papilionaceae
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
- A23L33/105—Plant extracts, their artificial duplicates or their derivatives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/96—Cosmetics or similar toiletry preparations characterised by the composition containing materials, or derivatives thereof of undetermined constitution
- A61K8/97—Cosmetics or similar toiletry preparations characterised by the composition containing materials, or derivatives thereof of undetermined constitution from algae, fungi, lichens or plants; from derivatives thereof
- A61K8/9783—Angiosperms [Magnoliophyta]
- A61K8/9789—Magnoliopsida [dicotyledons]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q19/00—Preparations for care of the skin
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2002/00—Food compositions, function of food ingredients or processes for food or foodstuffs
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2200/00—Function of food ingredients
- A23V2200/30—Foods, ingredients or supplements having a functional effect on health
- A23V2200/308—Foods, ingredients or supplements having a functional effect on health having an effect on cancer prevention
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Natural Medicines & Medicinal Plants (AREA)
- Veterinary Medicine (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Engineering & Computer Science (AREA)
- Botany (AREA)
- Mycology (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- Chemical & Material Sciences (AREA)
- Epidemiology (AREA)
- Birds (AREA)
- Dermatology (AREA)
- Alternative & Traditional Medicine (AREA)
- Medical Informatics (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Nutrition Science (AREA)
- Food Science & Technology (AREA)
- Polymers & Plastics (AREA)
- Medicines Containing Plant Substances (AREA)
- Medicinal Preparation (AREA)
Abstract
본 발명은 모링가(Moringa oleifera) 잎의 수용성 추출물을 유효성분으로 포함하는 암 치료 또는 예방용 조성물 및 항암에 유효한 모링가 잎의 추출물의 제조방법에 관한 것으로, 본 발명에 따른 조성물은 정상세포에는 독성이 낮은 반면 암세포에 우수한 독성을 보이며, 수용성으로 세포내 흡수가 매우 용이하므로, 경구용 제제의 항암 치료제로서 유리한 장점을 가지므로, 천연물 항암 신약 개발에 활용될 수 있다.
Description
본 발명은 모링가(Moringa oleifera) 잎의 수용성 추출물을 유효성분으로 포함하는 암 치료 또는 예방용 약학적 조성물, 모링가 잎의 수용성 추출물을 유효성분으로 포함하는 조성물, 및 항암에 유효한 모링가 잎의 추출물의 제조방법에 관한 것이다.
모링가는 원산지가 인도인 소목이지만, 전세계 어디에서나 재배되고 모링가 나무가 널리 이용되는 많은 지역들에서 귀화되어 야생된다. 모링가과에 속하는 13 종의 모링가 나무가 있으며, 모링가 올레이페라(Moringa oleifera)가 가장 널리 알려져 있다. 모링가 올레이페라는 우산과 같이 펼쳐진 4 내지 8 미터 높이의 관목이다. 30 내지 70 cm 길이의 잎들은 낙엽성이며, 꽃들은 흰색이고 향기가 진하며, 열매는 녹색이고 혁질성 및 현수성의 긴 삼각형상의 긴 깍지로 길이는 30 내지 40 cm에 이르는 특징을 가지며, 인도 북서부 히말라야 산기슭에 자생하고, 열대 전 지역에서 재배하는 다목적 수종의 일종이다.
모링가(Moringa oleifera)는 동남아시아 등에서 자생하는 식물로서 다량의 영양분을 함유하고 있어 기적의 식물로 불리고 있으며, 항당뇨, 항암, 항알러지 등 다양한 효능이 있는 것으로 알려져 있다. 그러나 현재 모링가를 이용한 단순한 건강보조식품이 판매는 되고 있으나 실제 항암제로서 개발되어 판매되고 있지는 않다. 그 이유는 모링가의 항암효능에 대한 과학적 입증자료가 부족하고, 임상시험이 수행되지 않았기 때문이다. 또한 기존의 모링가 추출물을 이용한 다양한 조성물이 개발되고 있으나, 지금까지의 모링가 추출법은 주로 알콜 추출법에 의한 것이고, 알콜 추출법에 의한 모링가 추출물은 실험실 내에서는 적용이 가능하나 실제 암환자 및 동물 암모델을 대상으로 한 연구가 없는 실정이다. 종래 공지된 모링가 추출물과 관련된 특허인 일본특허공개공보 제2006-508902호는 조성물에 유효성분으로서 모링가 추출물을 포함하고 있으나, 혈관성 두통 또는 신경질환의 치료 효능에 대해서만 언급하고 있다. 또한 미국특허공개공보 제2007-0264366호에 공지된 모링가 잎 추출물은 에탄올을 이용해서 추출한 것으로, 항진균 효과에 대해서만 기술하고 있다.
한편 암환자의 치료법은 외과적 수술, 방사선 치료, 40여 종의 강한 세포독성을 보이는 항암물질 투여에 의한 화학요법에 의존하고 있는 상태인데, 이들 치료법도 대부분 조기 암환자나 특정 암에만 국한되어 암으로 인한 사망은 계속 증가하고 있는 추세이다.
기존의 항암제로 사용되고 있는 물질은 암세포에도 영향을 미치지만 정상세포에도 독성을 미침으로써 다양한 부작용을 초래하고 있는 경우가 많다. 또한 종래의 항암제는 주로 비수용성 물질이 대부분으로, 항암물질의 세포내 흡수가 어려운 단점이 있으며, 이를 용해시키기 위해 다양한 부가적 방법이 동원되고 있어, 이로 인한 부작용이 생길 수 있고, 항암제의 약효도 줄어드는 문제점이 발생하며, 흡수를 증진시키기 위해 흡수증진제가 동시에 투여되고 있기도 한다. 또한 기존의 주사제 제형의 항암제는 다양한 독성과 부작용을 보이며, 반복되는 주사 투여의 어려움으로 인해 환자의 불편함을 초래하고 있다. 따라서 정상세포에는 독성을 미치지 않고 암세포에만 선택적인 우수한 독성을 나타내며, 투약의 편의성 및 인체흡수성이 향상된 항암 치료제가 절실하게 요구되고 있다.
이에 본 발명자들은 상술한 바와 같은 항암 치료제의 문제점을 해결하기 위해 천연물인 모링가(Moringa oleifera) 잎에서 유효한 항암 성분을 찾고자 예의 노력한 결과, 추출 용매로 물을 사용하여 얻어진 모링가 잎의 추출물이 우수한 항암 효과를 가지는 것을 확인하고서 본 발명을 완성하였다.
본 발명의 일 목적은 모링가 잎의 추출물을 포함하는 암 치료 또는 예방용 약학적 조성물을 제공하는 것이다.
본 발명의 다른 목적은 모링가 잎의 추출물을 포함하는 암 개선 또는 예방용 식품 조성물 및 화장품 조성물을 제공하는 것이다.
본 발명의 또 다른 목적은 항암에 유효한 모링가 잎 추출물의 제조방법을 제공하는 것이다.
상기 목적을 해결하기 위해 본 발명의 일 양상은 모링가(Moringa oleifera) 잎의 수용성 추출물을 유효성분으로 포함하는 암 치료 또는 예방용 약학적 조성물을 제공한다.
본 발명의 약학적 조성물에 있어서, 바람직한 일 구체예는 상기 모링가 잎의 수용성 추출물을 얻기 위해서 추출용매로 물을 사용할 수 있다. 또한 상기 추출용매로서 사용하는 물은 40°C 미만의 온도를 사용할 수 있으며, 바람직하게는 0 내지 20°C의 물, 더욱 바람직하게는 0 내지 10°C의 물을 사용할 수 있으나, 이에 한정되지 않는다.
상기 모링가 잎의 추출물은 모링가 잎을 추출용매에 침지하여 얻어질 수 있다. 이때 모링가 잎을 물에 침지시키는 시간은 1 내지 60분인 것이 바람직하나 이에 한정되는 것은 아니다.
더욱 바람직한 일 구체예로 본 발명의 조성물에 유효성분으로 포함되는 모링가 잎의 추출물은 0 내지 20°C의 물에서 1 내지 30분 동안 침지시켜 얻어진 것을 사용할 수 있다. 또한 모링가 잎의 부피 기준 1 내지 20배 부피의 물에 침지시켜서 얻는 것이 바람직하나 이에 한정되는 것은 아니다.
본 발명에 따른 약학적 조성물이 예방 또는 치료하고자 하는 암은 모든 암에 적용이 가능하며, 바람직하게는 간암, 유방암, 폐암, 편평상피암, 및 섬유종일 수 있으며, 더욱 바람직하게는 폐암 또는 간암일 수 있다.
본 발명의 암 치료 또는 예방용 약학적 조성물은 약학적으로 허용되는 담체를 추가로 포함할 수 있다. 또한 본 발명의 약학적 조성물은 추출용매로 수용성 용매, 특히 물을 사용함에 따라 경구로 섭취할 수 있는 제제로 쉽게 적용이 가능하다는 장점이 있어, 정제, 환제, 산제, 과립제, 시럽제, 액제, 현탁제, 에멀션 또는 캅셀제인 경구형 제제로 만들어지는 것이 바람직하나, 이에 한정되는 것은 아니며, 비경구형 제제 또한 적용이 가능하다.
아울러 본 발명의 다른 양상은 모링가 잎의 수용성 추출물을 유효성분으로 포함하는 암의 예방 또는 개선용 식품 조성물을 제공한다. 또한 본 발명은 모링가 잎의 수용성 추출물을 유효성분으로 포함하는 암의 예방 또는 개선용 화장품 조성물을 제공한다.
본 발명의 또 다른 양상은 모링가 잎을 0°C 이상 40°C 미만의 물로 추출하는 것을 특징으로 하는 항암에 유효한 모링가 잎 추출물의 제조방법을 제공한다.
상기 모링가 잎 추출물의 제조방법은 모링가 잎을 모링가 잎 부피 기준 1 내지 20배 부피의 0-20°C의 물에 침지하는 단계; 모링가 잎의 침출수를 수득하여, 불용성 물질을 제거하는 단계; 및 상기 불용성 물질이 제거된 침출수를 여과하는 단계; 를 포함할 수 있다. 상기 모링가 잎을 물에 침지하는 단계에서 모링가 잎은 물에 1 내지 60분 동안 침지시켜 추출하는 것이 바람직하다.
이하 본 발명을 상세히 설명한다.
본 발명에서 사용되는 용어 "예방"은 본 발명의 조성물의 투여로 암을 억제하거나 진행을 지연시키는 모든 행위를 의미한다.
본 발명에서 사용되는 용어 "치료"는 본 발명의 조성물의 투여로 암의 증상이 호전 또는 이롭게 변경되는 모든 행위를 의미한다.
본 발명에서 사용되는 용어 "투여"는 임의의 적절한 방법으로 개체에 소정의 본 발명의 조성물을 제공하는 것을 의미한다.
본 발명에서 사용되는 용어 "약학적으로 유효한 양"은 의학적 치료에 적용 가능한 합리적인 수혜 또는 위험비율로 질환을 치료하기에 충분한 양을 의미하며, 이는 개체의 질환의 종류, 중증도, 약물의 활성, 약물에 대한 민감도, 투여 시간, 투여 경로 및 배출비율, 치료기간, 동시에 사용되는 약물을 포함한 요소 및 기타 의학 분야에 잘 알려진 요소에 따라 결정될 수 있다.
본 발명의 일 양상은 모링가(Moringa oleifera) 잎의 수용성 추출물을 유효성분으로 포함하는 암 치료 또는 예방용 약학적 조성물에 관한 것이다.
본 발명의 약학적 조성물에 있어서, 유효성분으로 포함되는 상기 모링가 잎의 추출물은 수용성 추출물로서 수용성 용매, 특히 물을 추출용매로 사용하는 것을 특징으로 한다. 본 발명에 따른 일 실시예에서 추출용매로서 물을 사용하였을 때, 다른 유기용매를 사용하여 얻어진 추출물보다 암세포의 사멸효과가 더욱 뛰어남을 확인할 수 있었다(도 15).
또한 본 발명의 약학적 조성물에 포함되는 추출물의 추출용매로 사용하는 물의 온도는 40°C 미만의 온도보다 낮은 것이 바람직하다. 따라서 본 발명에 따른 암 치료 또는 예방용 약학적 조성물에 포함되는 유효성분은 모링가 잎의 수용성 성분들이 대부분일 수 있다. 종래 모링가 잎의 추출물은 추출용매로 에탄올 또는 메탄올 등의 유기용매로 사용하거나 또는 열수추출법으로 추출하는 것이 대부분이었다. 이러한 유기용매 추출 또는 열수 추출할 경우, 활성성분의 화학구조 내에 거대한 소수성 작용기들을 가질 수 있어, 이에 따라 낮은 수용성을 가질 수 있어, 제형화하기가 어렵고 또한 체내에 투여하더라도 흡수가 쉽지 않다는 문제점을 가진다. 반면 본 발명은 낮은 온도의 물을 사용하여 모링가 잎을 추출함으로써, 추출물에 수용성 성분들을 포함하게 되어, 세포내 흡수가 용이하며, 물에 쉽게 녹는 장점을 가지는 바, 이에 따라 경구용 항암 치료제로 활용될 수 있다.
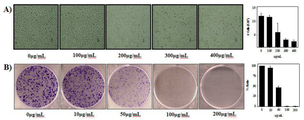
따라서 상기 추출용매로 사용하는 물은 40°C 미만의 온도의 물인 것이 바람직하며, 바람직하게는 0°C 이상 20°C 이하의 물, 더더욱 바람직하게는 0°C 이상 내지 10°C 이하의 물인 것이 바람직하다. 추출용매인 물의 온도가 40°C 이상일 경우 추출물의 농도를 높여서 처리하더라도 암세포의 생존에의 추출물의 영향이 미비하였으며, 온도가 낮을수록, 암세포에의 독성이 낮은 것을 확인할 수 있었다(도 1(a)).
또한 본 발명의 추출용매의 침지 시간은 1시간 이내인 것이 바람직하며, 침지 시간을 30분 이하로 추출한 추출물이 암세포의 생존에 있어서, 더욱 우수한 독성 효과를 보였다(도 1(b)).
따라서 더욱 바람직한 구체예로 본 발명의 모링가 잎 추출물은 0°C 이상 내지 10°C 이하의 물에 1분 내지 30분 동안 침지시켜 얻어지는 것일 수 있다.
본 발명의 약학적 조성물에 유효성분으로 포함되는 모링가 잎의 수용성 추출물은 모링가 잎 기준 1 내지 20 배의 부피비의 물에 침지시켜 얻어지는 것을 특징으로 한다. 본 발명의 일 구체예에 따른 모링가 잎의 추출물은 건조된 모링가 잎의 분말을 사용하는 것이 바람직하나, 이에 한정되지 않으며, 건조되지 않은 모링가 잎의 사용도 가능하다.
본 발명에 있어서, 암은 간암, 위암, 결장암, 유방암, 폐암, 편평상피암, 섬유종, 비소세포성폐암, 골암, 췌장암, 피부암, 두부 또는 경부암, 피부 또는 안구 내 흑색종, 자궁암, 난소암, 직장암, 항문부근암, 나팔관임종, 자궁내막암종, 자궁경부암종, 질암종, 음문암종, 호지킨병(Hodgkin's disease), 식도암, 소장암, 내분비선암, 갑상선암, 부갑상선암, 부신암, 연조직 육종, 요도암, 음경암, 전립선암, 만성 또는 급성 백혈병, 림프구 림프종, 방광암, 신장 또는 수뇨관 암, 신장세포 암종, 신장골반 암종, 중추신경계(Central nervous system, CNS) 종양, 1차 CNS 림프종, 척수 종양, 뇌간 신경교종, 또는 뇌하수체 선종으로 이루어진 군으로부터 선택되는 1종 이상일 수 있으며, 바람직하게는 간암, 유방암, 폐암, 편평상피암, 및 섬유종으로 이루어지는 군으로부터 선택되는 1종 이상일 수 있으며, 더욱 바람직하게는 폐암 또는 간암에서 선택될 수 있으나 이에 한정되지는 않는다. 본 발명의 일 실시예에서, 대상 마우스에 모링가 잎 추출물을 일회 경구 투여한 결과, 모링가 잎 추출물이 간암 및 폐암 세포에 우수한 억제 효과가 있음을 확인하였다(도 14).
본 발명의 약학적 조성물은 약학적 조성물 총 중량에 대하여 본 발명의 모링가 잎 추출물을 0.01 내지 50 중량%를 유효성분으로 함유할 수 있으며, 약학적으로 허용되는 담체를 추가로 포함할 수 있다.
또한 상기 모링가 잎 수용성 추출물을 포함하는 약학적 조성물을 제제화 할 경우에는 통상적으로 사용하는 충진제, 증량제, 결합제, 습윤제, 붕해제, 계면 활성제 등의 희석제 또는 부형제를 사용하여 조제될 수 있다.
본 발명의 약학적 조성물은 약학 분야에서의 통상의 방법에 따라 환자의 신체 내 투여에 적합한 단위 투여형의 제제로 제형화될 수 있다. 이러한 목적에 적합한 제형으로는 비경구투여 제제로서 주사용 용액 또는 현탁액, 또는 주사시에 주사용 증류수로 제조하여 사용할 수 있는 즉시 사용형 주사용 건조분말 등의 주사용 제제; 또는 연고제 등의 국소 투여용 제제 등이 바람직하다. 이때, 일반적으로 사용되는 충진제, 증량제, 결합제, 습윤제, 붕해제, 계면활성제 등의 희석제 또는 부형제를 함께 사용할 수 있다. 또한, 본 발명의 약학 조성물은 정제, 수성 또는 유성 현탁액, 분선용 분말 또는 과립, 에멀젼, 경질 또는 연질 캡슐, 시럽 또는 엘릭서와 같은 경우 복용에 적합한 경구형 제형으로 제조될 수 있다. 이러한 조성물의 제조는 당업자에게 공지된 임의의 방법으로 제조될 수 있다.
본 발명의 약학적 조성물은 유효성분으로 수용성 추출물을 포함하고 있어, 정제, 환제, 산제, 과립제, 시럽제, 액제, 현탁제, 에멀션 또는 캅셀제인 경구용 제제인 것이 바람직하나 이에 한정되는 것은 아니다. 상기 경구 투여를 위한 고형 제제에는 상기 추출물에 적어도 하나 이상의 부형제 예를 들면, 전분은 칼슘 카보네이트(calcium carbonate), 수크로스(sucrose) 또는 락토오스(lactose), 젤라틴 등을 섞어 조제될 수 있다. 또한 단순한 부형제 이외에 마그네슘 스테아레이트, 탈크 같은 윤활제들도 사용될 수 있다.
본 발명의 약학적 조성물은 또한 암의 치료를 필요로 하는 환자에게 항생제, 알킬화제, 항대사제, 호르몬제, 면역학적 제제, 인터페론 제제 및 다른 항암제로 이루어진 군에서 선택된 1종 이상을 투여하는 것을 추가로 포함할 수 있다. 그러나, 본 발명의 의약 용도 및 치료용 약학적 조성물은 상기한 것에 한정되는 것은 아니며, 또한 병용될 수 있는 다른 약제들도 상기한 것들에 한정되는 것은 아니다.
본 발명의 약학적 조성물의 바람직한 투여량은 환자의 상태 및 체중, 질병의 정도, 약물형태, 투여경로 및 기간에 따라 다르지만, 당업자에 의해 적절하게 선택될 수 있다. 그러나, 바람직한 암 치료 또는 예방 효과를 위해서, 본 발명의 추출물은 1일 0.0001 내지 600 ㎍/ml로, 바람직하게는 0.001 내지 600 ㎍/ml으로 투여하는 것이 좋다. 이때 상기 추출물의 투여 용량은 추출물의 건조 중량이 아닌 추출물에 포함된 단백질의 농도를 기준으로 한다. 따라서 실제 투여시 추출물 건조 중량은 상기 단백질의 용량보다 더 높을 수 있다. 즉 본 발명의 구체적인 실시예에 따르면 실제 투여 추출물의 건조 중량은 단백질의 용량의 3배로 추정이 되므로, 총 조성물 대비 추출물의 건조 중량 기준으로 할 경우 0.0001 내지 1800 ㎍/ml인 것이 바람직하다. 또한 본 발명의 조성물은 kg를 기준으로 할 경우 추출물의 건조 중량이 50 mg 이상 포함하는 것이 바람직하며, 200 mg/kg 이상일 경우 더욱 바람직하다.
투여는 하루에 한번 투여할 수도 있고, 수회 나누어 투여할 수도 있다. 본 발명의 실시예에서 마우스에 200 mg/kg(총 조성물 대비 추출물의 건조중량)의 본 발명에 따른 조성물을 경구 투여했을 경우, 암세포의 억제효과를 확실하게 얻을 수 있었다. 유효성분의 실제 투여량은 암 세포의 양, 투여경로, 환자의 체중, 연령 및 성별 등 여러 관련 인자를 고려하여 결정할 수 있으며, 따라서, 상기 투여량은 어떠한 형태로든 본 발명의 범위를 한정하는 것은 아니다.
본 발명의 추출물은 쥐, 생쥐, 가축, 인간 등의 포유동물에 다양한 경로로 투여될 수 있다. 투여의 모든 방식은 예상될 수 있는데, 예를 들면, 경구, 직장 또는 정맥, 근육, 피하, 자궁 내 경막 또는 뇌혈관 내(intracerebroventricular) 주사에 의해 투여될 수 있다.
또한 본 발명은 모링가 잎 수용성 추출물을 유효성분으로 포함하는 암의 예방 또는 개선용 식품 조성물을 제공한다. 상기 식품 조성물은 모링가 잎 수용성 추출물을 그대로 첨가하거나, 다른 식품 또는 식품 성분과 함께 사용될 수 있고, 통상적인 방법에 따라 적절하게 사용될 수 있다. 상기 식품 조성물에 첨가되는 모링가 잎 수용성 추출물은 모링가 잎을 추출용매로 물을 이용해서 얻어지는 것을 사용하는 것이 바람직하다. 추출용매로서 물은 40°C 미만의 물을 사용하는 것이 바람직하며, 더욱 바람직하게는 0°C 이상 내지 20°C이하의 온도일 수 있다. 20°C 이하의 물을 추출용매로 사용할 경우 암의 예방 또는 개선에 더욱 우수한 효과를 가지는 모링가 잎의 추출물을 얻을 수 있다. 또한 모링가 잎의 추출물은 모링가 잎을 물에 침지시켜 얻는 것이 바람직한데, 이때 침지시간은 1시간 이내인 것이 암의 예방 또는 개선에 더욱 활성이 좋은 추출물을 얻을 수 있다.
상기 식품의 종류에는 특별한 제한은 없다. 상기 모링가 잎 추출물을 첨가할 수 있는 식품의 예로는 육류, 소세지, 빵, 쵸코렛, 캔디류, 스넥류, 과자류, 피자, 라면, 기타 면류, 껌류, 아이스크림류를 포함한 낙농제품, 각종 스프, 음료수, 차, 드링크제, 알콜 음료 및 비타민 복합제 등이 있으며, 통상적인 의미에서의 식품을 모두 포함한다.
본 발명의 식품 조성물로서 음료조성물은 통상의 음료와 같이 여러 가지 향미제 또는 천연 탄수화물 등을 추가 성분으로서 함유할 수 있다. 상술한 천연 탄수화물은 포도당, 과당과 같은 모노사카라이드, 말토스, 슈크로스와 같은 디사카라이드, 및 덱스트린, 사이클로덱스트린과 같은 폴리사카라이드, 자일리톨, 소르비톨, 에리트리톨 등의 당알콜이다. 감미제로서는 타우마틴, 스테비아 추출물과 같은 천연 감미제나, 사카린, 아스파르탐과 같은 합성 감미제 등을 사용할 수 있다. 상기 천연 탄수화물의 비율은 본 발명의 조성물 100 ㎖당 일반적으로 약 0.01 내지 0.04 g, 바람직하게는 약 0.02 내지 0.03 g 이다. 상기 외에 본 발명의 모링가 잎 추출물은 여러 가지 영양제, 비타민, 전해질, 풍미제, 착색제, 펙트산 및 그의 염, 알긴산 및 그의 염, 유기산, 보호성 콜로이드 증점제, pH 조절제, 안정화제, 방부제, 글리세린, 알콜, 탄산음료에 사용되는 탄산화제 등을 함유할 수 있다. 이러한 첨가제의 비율은 크게 중요하진 않지만 본 발명의 조성물 100 중량부당 0.01 내지 0.1 중량부의 범위에서 선택되는 것이 일반적이다.
또한 본 발명은 모링가 잎 수용성 추출물을 유효성분으로 포함하는 화장품 조성물을 제공한다. 상기 화장품 조성물은 피부암의 개선 또는 예방에 효과가 있으며, 더욱 바람직하게는 편평상피암의 개선 또는 예방에 효과가 있다. 본 발명에 따른 화장품 조성물은 물을 추출용매로서 사용하여 얻어지는 추출물을 유효성분으로 함유하는 것이 바람직하다. 또한 이때 추출시 물의 온도는 40°C 미만의 물을 사용하는 것이 바람직하며, 더욱 바람직하게는 0°C 이상 내지 20°C이하의 온도일 수 있다. 또한 상기 화장품 조성물에 포함되는 모링가 잎의 추출물은 모링가 잎을 물에 침지시켜 얻는 것이 바람직한데, 이때 침지 시간은 1시간 이내인 것이 피부암의 예방 또는 개선에 더욱 활성이 좋은 추출물을 얻을 수 있다. 본 발명에 따른 화장품 조성물은 유효 성분 이외에 화장품 조성물에 통상적으로 이용되는 성분들을 포함하며, 예컨대 항산화제, 안정화제, 용해화제, 비타민, 안료 및 향료와 같은 통상적인 보조제, 그리고 담체를 포함한다. 또한, 상기 화장료 조성물은 그 효과를 증진시키기 위하여 피부 흡수 촉진 물질을 추가로 포함할 수 있다. 본 발명의 화장료 조성물은 당업계에서 통상적으로 제조되는 어떠한 제형으로도 제조될 수 있다.
본 발명의 다른 양상은 모링가 잎을 0°C 이상 20°C 이하의 물로 추출하는 것을 특징으로 하는 항암에 유효한 모링가 잎의 추출물 제조방법에 관한 것이다.
본 발명에 따른 모링가 잎의 추출물의 제조방법은 모링가 잎을 1 내지 20배의 0-20°C의 물에 침지하는 단계;
모링가 잎의 침출수를 수득하여, 불용성 물질을 제거하는 단계; 및
상기 불용성 물질이 제거된 침출수를 여과하는 단계를 포함할 수 있다.
본 발명에 있어서, 상기 모링가 잎의 추출물은 모링가 잎의 1 내지 20배의 물을 가하여, 일정시간 바람직하게는 1 내지 60분 동안 침지하여 얻는 것이 바람직하다, 상기 모링가 잎은 건조된 모링가 잎을 사용하는 것이 바람직하나, 이에 한정되지 않으며, 건조되지 않은 모링가 잎의 사용도 가능하다.
상기 불용성 물질의 제거는 원심분리를 이용하여 제거할 수 있다. 본 발명의 일 실시예에서는 12,000 rpm, 10분 동안 3회 원심분리하여 상등액만을 취하여 불용성 물질을 제거하였다.
또한, 상기 여과는 기공 크기가 마이크로미터 단위인 여과포 또는 여과지에 의해 추출물을 추출액과 잔여 추출 원료 고형물로 분리할 수 있으며, 여과된 추출액은 추가적으로 기공 크기가 나노미터 단위인 멤브레인 필터로 여과하여 불순물(이취 성분이나 색상 성분)을 제거할 수 있다. 상기 여과에 의해 수득한 여과액은 농축되어 액상 형태의 모링가 잎 추출물로 제조될 수 있고 또한, 건조에 의해 분말 형태로 제조될 수 있다. 이때 건조 방법은 그 종류가 크게 제한되지 않으나, 활성 성분의 열적 변형을 최소화시키기 위해 동결 건조인 것이 바람직하다.
본 발명의 조성물에 유효성분으로 포함되는, 물을 추출용매로 사용하여 추출한 모링가 잎의 추출물은 암세포의 성장, 이동 및, 침윤에 있어서. 뛰어난 억제 효과를 보였으며, 구체적으로는 암세포의 성장, 전이 및 침윤 능력이 정상세포보다 암세포에서 더 높은 독성을 보이며, 또한 간암과 폐암이 유발된 동물모델에 상기 추출물을 일회 경구 투여한 경우에도 높은 항암효능을 나타내었다. 본 발명에 따른 조성물은 정상세포에는 독성이 낮은 반면 암세포에 우수한 독성을 보이며, 수용성으로 세포내 흡수 및 전달이 매우 용이할 뿐 아니라, 유기용매로 추출시 용매 자체의 독성이 있고, 제제화가 어렵다는 단점을 극복할 수 있어, 경구용 제제의 항암 치료제로로서 유리한 장점을 가진다. 따라서 본 발명은 천연물 항암 신약개발에 유용하게 활용될 수 있을 것이다.
도 1은 본 발명의 조성물이 A549 폐암 세포의 증식에 미치는 효과를 보여주는 MTT 분석 결과이다. 도 1(a)는 A549 폐암 세포의 증식에 있어서, 온도별로 30분간 침지시킨 후 얻어진 추출물을 가지고 시험한 효과를 보여준다. 도 1(b)는 본 발명의 침지 시간을 달리하여 제조된 모링가 잎 추출물의 암세포 억제 효과를 보여준다.
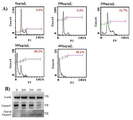
도 2는 A549 세포에 본 발명의 일 실시예에 의한 세포사멸(apoptosis) 유발 효과를 보여주는 도면이다. (a)는 FACScan 분석으로, 박스 안의 숫자들은 G0/G1 fraction을 가리키며, (b)는 caspase-3의 웨스턴 블롯 결과이다.
도 3은 독립적인 5번의 실험을 실시하여 평균화한 A549 세포에 대한 모링가 추출물의 세포사멸 유발 효과를 보여주는 그래프이다.
도 4는 다른 암세포들에 대한 모링가 잎 추출물의 세포사멸 유발효과를 보여주는 FACS 분석 결과이다.
도 5은 세포 증식에 있어서 모링가 잎 추출물의 억제 효과를 나타낸 것으로, (a)는 현미경 사진(X400) 및 cell counter에 의해 계산된 세포 수이며, (b)는 콜로니 형성 분석(colony forming assay)에 의한 콜로니 수를 나타낸다.
도 6은 콜로니 형성 분석을 통한 다른 암세포들에 대한 모링가 잎 추출물의 억제효과를 보여준다.
도 7은 본 발명의 모링가 잎 추출물로 처리한 A549 세포의 이동성 분석을 나타내는 것으로 (a)는 광학 현미경 사진이며, (b)는 평균 이동율을 나타낸다.
도 8은 DCFH-DA 처리에 의한 활성산소종을 보여주는 것으로, 세포에 본 발명의 조성물을 처리한 후 세포 내부의 ROS 레벨을 FACScan 을 사용하여 분석한 결과를 나타낸다.
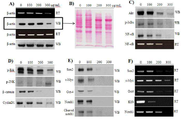
도 9는 본 발명의 조성물을 세포에 처리한 후 단백질 발현 수준을 보여주는 웨스턴 블롯 결과이다.
도 10은 본 발명의 조성물의 처리 및 미처리시를 비교한 전체 세포 단백질의 SDS-PAGE 전기영동 사진이다.
도 11은 유전자 마이크로어레이에 대한 결과를 보여주는 것으로 (a)는 마이크로 어레이 결과, (B)는 상향 조절된 유전자와 관련된 기능의 분석결과 (c)는 어떠한 변화도 없었던 유전자들의 기능의 분석 결과를 보여준다.
도 12은 rRNA 의 분해(degradation)를 보여주는 도면이다.
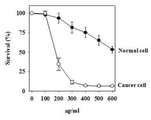
도 13는 정상세포와 암세포 사이에서의 세포 증식의 비교 결과를 나타낸다.
도 14(a)는 hollow fiber assay의 실험 방법을 나타내고, (b)는 hollow fiber assay 결과를 나타낸다.
도 15는 추출용매로서 물, 70% 알콜, DMSO 100% 를 각각 사용했을 때, 모링가 잎 추출물의 세포사멸 유발효과를 보여주는 FACS 분석 결과이다.
도 2는 A549 세포에 본 발명의 일 실시예에 의한 세포사멸(apoptosis) 유발 효과를 보여주는 도면이다. (a)는 FACScan 분석으로, 박스 안의 숫자들은 G0/G1 fraction을 가리키며, (b)는 caspase-3의 웨스턴 블롯 결과이다.
도 3은 독립적인 5번의 실험을 실시하여 평균화한 A549 세포에 대한 모링가 추출물의 세포사멸 유발 효과를 보여주는 그래프이다.
도 4는 다른 암세포들에 대한 모링가 잎 추출물의 세포사멸 유발효과를 보여주는 FACS 분석 결과이다.
도 5은 세포 증식에 있어서 모링가 잎 추출물의 억제 효과를 나타낸 것으로, (a)는 현미경 사진(X400) 및 cell counter에 의해 계산된 세포 수이며, (b)는 콜로니 형성 분석(colony forming assay)에 의한 콜로니 수를 나타낸다.
도 6은 콜로니 형성 분석을 통한 다른 암세포들에 대한 모링가 잎 추출물의 억제효과를 보여준다.
도 7은 본 발명의 모링가 잎 추출물로 처리한 A549 세포의 이동성 분석을 나타내는 것으로 (a)는 광학 현미경 사진이며, (b)는 평균 이동율을 나타낸다.
도 8은 DCFH-DA 처리에 의한 활성산소종을 보여주는 것으로, 세포에 본 발명의 조성물을 처리한 후 세포 내부의 ROS 레벨을 FACScan 을 사용하여 분석한 결과를 나타낸다.
도 9는 본 발명의 조성물을 세포에 처리한 후 단백질 발현 수준을 보여주는 웨스턴 블롯 결과이다.
도 10은 본 발명의 조성물의 처리 및 미처리시를 비교한 전체 세포 단백질의 SDS-PAGE 전기영동 사진이다.
도 11은 유전자 마이크로어레이에 대한 결과를 보여주는 것으로 (a)는 마이크로 어레이 결과, (B)는 상향 조절된 유전자와 관련된 기능의 분석결과 (c)는 어떠한 변화도 없었던 유전자들의 기능의 분석 결과를 보여준다.
도 12은 rRNA 의 분해(degradation)를 보여주는 도면이다.
도 13는 정상세포와 암세포 사이에서의 세포 증식의 비교 결과를 나타낸다.
도 14(a)는 hollow fiber assay의 실험 방법을 나타내고, (b)는 hollow fiber assay 결과를 나타낸다.
도 15는 추출용매로서 물, 70% 알콜, DMSO 100% 를 각각 사용했을 때, 모링가 잎 추출물의 세포사멸 유발효과를 보여주는 FACS 분석 결과이다.
이하, 본 발명을 실시예에 의해 보다 상세히 설명한다. 본 발명은 여러 가지 상이한 형태로 구현될 수 있으며, 여기에서 설명하는 실시예들에 의해 한정되지 않는다. 또한 본 명세서에서 사용되는 용어, 기술 등은 특별한 한정이 없는 한, 본 발명이 속하는 기술 분야에서 일반적으로 사용되는 의미로 사용된다.
<
실시예
> 1. 추출 시간에 따른
모링가
잎 추출물의 제조
건조된 모링가 잎(M. oleifera leaves)은 GL Network Co. Ltd.로부터 구입하였다(태국, 치앙마이에서 재배). 건조된 모링가 잎 150 mg을 4°C의 물 1 ml에 침지시켜, 30초 동안 볼텍싱(voltexing)한 다음 냉장실에서 stirring하면서 보관하였다. 각 실시예마다 냉장실의 보관시간을 다르게 하여, 즉 하기 표 1과 같이 각 실시예마다 침지시간의 차이를 두었다. 침지시간이 다른 각각의 침지물을 1분 동안 실온에서 다시 볼텍싱하였다. 이후 부유물의 불용성 부분은 3차례의 원심분리(12000rpm, 10분)에 의해 제거한 다음, 상등액(supernatant)을 여과(0.2μM membrane filtration)하여 각각 최종 수득하였다. 최종적인 모링가 잎 추출물들은 동결건조한 후, -20°C에 저장하였다.
| 실시예1 | 실시예2 | 실시예3 | 실시예4 | 실시예5 |
| 5분 | 30분 | 1시간 | 3시간 | 24시간 |
<
실시예
> 2. 추출 온도에 따른
모링가
잎 추출물의 제조
침지시간은 30분으로 고정하고, 각 추출 용매(물)의 온도를 하기 표와 같이 다르게 하여, 나머지는 상기 <실시예> 1과 동일한 방법으로 모링가 잎 추출물을 제조하였다.
| 실시예6 | 실시예7 | 실시예8 | 실시예9 |
| 20°C | 40°C | 60°C | 80°C |
하기 실험에 사용하기 위해 동결건조된 모링가 잎 추출물은 단백질 농도를 정량한 후, 20mg/ml 의 단백질 농도가 되도록 증류수(D.W.)에 부유시켰다. 이하 시험에 사용된 모링가 잎 추출물의 농도는 단백질의 농도를 의미한다.
<실험 방법>
1. 모링가 잎 추출물의 농도에 따른 시료 준비
모링가 올레피아 잎의 건조분말 100g 으로부터 DW 를 이용하여 추출하는 경우 추출물을 동결건조하였을때, 총 17.5g의 활성이 있는 수용성 건조분말이 얻어졌다. 초기 원재료로부터 수용성 건조분말을 얻는 수득률은 약 17.5%였다.
한편 상기의 방법으로 얻어진 동결 건조분말 1g 취해 DW 10mL에 녹인 후 단백질을 정량한 경우, 상기 시료에 함유되어 있는 단백질량은 322mg로서 건조시료 중 단백질 함량은 대략 32%였다. 이를 계산해보면 초기에 원재료인 Moringa oleifera 잎 100g을 가지고 추출하였으므로 최종 단백질 수득율은 322mg*17.5=5.6%가 된다.
즉, 1g의 원재료로부터 DW로 추출하면 0.175g의 수용성 건조분말이 얻어지며, 0.056g의 단백질이 얻어지며, 활성이 있는 수용성 건조분말에 함유되어 있는 단백질은 32%에 이른다.
이하 모든 실시예에 사용된 기준은 단백질 농도를 기준으로 하였는데, 위의 추출 결과를 대입해 보면, 건조중량 g 당 32%의 단백질이 함유되어 있으므로, 20 mg/mL의 단백질을 갖는 시료는 결국 건조중량으로 환산할 시에 대략 60 mg/mL의 건조중량과 동일하다. 즉, 시험에 사용된 활성 추출물의 모든 단백질 농도를 시료 건조중량을 바꾸려면 3배를 곱해주면 된다. 즉, 단백질 농도 기준으로 100, 200, 300 ㎍/mL을 사용한 경우 추출물의 건조중량으로는 300, 600. 900 ㎍/mL에 해당하는 것이다. 이하 특별한 언급이 없는 한 모든 시료의 농도는 단백질 농도를 기준으로 한 것을 의미한다.
2. 세포 배양(
cell
culture
)
본 발명의 효과를 확인하기 위해 실험에 사용한 폐암 세포주(Lung cancer cell line) A549, 간암 세포주(Hepatocellular carcinoma(HCC) cell line) HpG2, 및 신장 유래 세포주 African green monkey kidney cells(COS-7) 은 ATCC(American Type Culture Collection, USA) 및 한국 세포주 은행(Korean Cell Line Bank, KCLB)로부터 분양받았다. 세포들은 10% FBS (fetal bovine serum; Hyclone Lab, USA) 및 1% 페니실린-스트렙토마이신을 첨가한 RPMI-1640 (A549, H23, and H358) 또는 DMEM (HpG2, MCF-7, A431, HT1080, and COS-7) 배지에서 배양하였다. 배양된 세포를 6 웰-플레이트에 1 × 105 cells 로 각각 분주한 다음, 37℃, 95% 공기/ 5% CO2 조건에서 유지시켰다.
3.
MTT
assay
세포의 생존 능력을 테트라졸륨(tetrazolium)을 사용한 세포 증식 분석 방법인 MTT assay로 분석하였다. 세포들을 96 웰(well) 플레이트에 배지 100ul 당 3 X 103 세포의 농도로 분주하였다. 1일 동안 배양한 후, 실시예에 의해 만들어진 모링가 잎 추출물을 각 플레이트에 0 내지 400㎍/ml의 다양한 농도로 처리하였다. 다시 1일 또는 2일 배양한 후, cell-counting Kit-8 (Cat. No. CK04, Dojindo lab. 일본) 또는 WST assay 시약 (대일 lab, 한국) 10 μl를 각 웰에 첨가한 다음, 4시간 동안 배양하였다. 이후, 마이크로플레이트 리더(microplate reader)(Model 680, Bio-Rad)를 이용하여 450 nm 파장에서 흡광도를 측정하였다.
4.
유세포
분석(
Flow
cytometric
detection
)
6-웰 플레이트에 세포를 1×105 cell/ml로 시딩(seeding)한 다음, 1일 동안 배양한 후, 농도에 따른 모링가 잎의 추출물을 처리하였다. 2일 더 배양시켜 세포를 회수하여, PBS로 워싱한 다음, 어두운 곳에서 70% 에탄올로 4℃에서 2시간 반응시켜 고정하였다. 고정된 세포를 PBS로 두 번 워싱한 후, 실온에서 50 ㎍/ml의 프로피디움 아이오다이드(propidium iodide, PI)로 30분 동안 염색하였다. DNA 양은 FACScan(EPICS XL Flow Cytometry, Beckman Coulter Counter)로 측정하였다. 각각의 세포주기에서 나타나는 효과는 세포주기의 각 시기에서 나타나는 세포배열의 %(백분율) 변화로부터 측정하였고, Pheonix Multicycler Software 프로그램(Phoenix Flow System)에 의해 결정하였다.
5. 현미경 관찰(
Microscopy
)
세포의 형태를 모니터하기위해, 세포들은 광학현미경(Leica Microsystems)에 의해 시각화되었다. 이미지는 Cannon Digital Camera system (Model; Power Shot S45)을 사용하여 캡쳐하였다.
6.
cDNA
합성 및
PCR
증폭
각 세포들을 (1 × 105 cells) 6-웰 배양 플레이트에 분주하여, 1일 동안 배양시킨 다음, 본 발명의 모링가 잎 추출물을 각각의 세포에 처리하였다. 2일 동안 배양한 다음, 전체 RNA 를 각 세포들로부터 High Pure RNA isolation kit (Roche, Cat.No. 11828665001)을 이용하여 분리하였다. 올리고 dT 를 사용하여 전체 RNA(1 g)으로부터 cDNA 를 생산하기 위하여, cDNA synthesis kit (Maxim RT Premix Kit-Oligo dT Primer, iNtRON Biotechnology, 한국)를 이용하였다. 결과적으로 cDNA는 Maxim PCR Premix Kit-iTaq (iNtRON Biotechnology, 한국)를 사용하여, 각각의 프라이머들에 의해 증폭되었다. 사용된 각 프라이머들의 염기 서열은 표 3에 나타내었다. 증폭된 PCR 생산물은 아가로즈 젤(1.5%) 전기영동에 의해 분석되었고, 그 결과는 UV light (Smart gel imaging analysis system, Beijing Sage Creation Science And Technology Co., Ltd)로 이미지화하였다.
7. 웨스턴 블롯 분석(Western blot analysis)
각 세포들을 (1 × 105cells) 6-웰 배양 플레이트에 분주하여, 1일 동안 배양시킨 다음, 본 발명의 모링가 잎 추출물을 각각의 세포에 처리하였다. 2일 동안 배양한 다음, 다시 세포들을 회수한 후, 웨스턴 블롯 분석을 위해 세포들을 용해시켰다(lysed). 웨스턴 블롯 분석을 위한 항체들은 Cell Signalling Technology 로부터 구입하였다. [β-actin: Cat. No. cs4967, Akt: Cat. No. cs9272, p-JNK: Cat. No. cs9251, p-Erk: Cat. No. cs9101, p-IκBα: Cat. No. cs2859, SOX2: Cat. No. cs3579, and cleaved Notch1: Cat. No. cs2421], from Santa Cruz Biotechnology [p53: Cat. No. sc-126, cyclinD1: Cat. No. sc-753, Notch1: Cat. No. sc-6014, NF-κB: Cat. No. sc-109, β-catenin: Cat. No. sc-7963 and c-Myc: Cat. No. sc-761], and from Merck Millipore [Oct4: Cat. No. mab4305]. 단백질 농도는 프래드포드 방법(Bradford method) (Protein Assay Dye Reagent Concentrate, Bio-Rad Laboratories, Cat. NO.500-0006)에 의해 결정하였다. 세포 용해 후, 동일한 양의 단백질(20 내지 80 ㎍)을 8-12% SDS PAGE를 수행하여, 단백질 크기별로 분리한 다음, 니트로셀룰로오스 멤브레인(Whatman)으로 이동시킨 후 블로킹 버퍼(10% nonfat milk in Tris-buffered saline(TBS) buffer containing 0.1% Tween 20, TBS-T)로 4℃ 16시간 동안 처리하였다. 멤브레인을 TBS-T로 세차례 워싱한 다음, horseradish peroxidase 표지된 이차 항체로 멤브레인을 실온에서 2시간 동안 반응시킨 후, ECL kit (GE Healthcare, Cat.No. RPN1237)를 사용하여 시각화하였다. 트로셀룰로스 멤브레인으로 단백질 이전되었는지 확인하기 위해, 멤브레인을 onceau S solution (SIGMA, Cat.No. P7170-1L)로 5분 동안 염색하였다. 염색된 멤브레인은 증류수(DW)로 여러번 워싱한 다음, 단백질의 이전을 확인하였다.
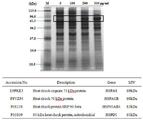
8. SDS-PAGE 젤을 통한 단백질의 확인
각 세포들을 (1 × 105cells) 6-웰 배양 플레이트에 분주하여, 1일 동안 배양시킨 다음, 본 발명의 모링가 잎 추출물을 각각의 세포에 처리하였다. 2일 동안 배양한 다음, 세포들을 용해시켰다. 용해 후, 동일한 양의 단백질은 10% SDS 폴리아크릴아미드 젤에 전기영동 시킨 다음, 코마시 블루를 이용하여 염색시켰다. 염색된 젤은 메탄올 및 아세트 산의 혼합용액으로 탈색시켰다. 젤 상에 60 ~ 80 kDa 위치의 밴드들을 슬라이스하여 트립신으로 처리하였다. 젤-분해에 의해 생산된 트립신 분해 펩타이드들은 Eksigent-Nano-Ultra UPLC(OmniGrid II, GeneMachines, CA)와 연결된 LTQ 질량 분석계(Thermo Finnigan, San Jose, CA) 를 사용하여 분석하였다. 단백질들은 UniPort Program (http://www.uniprot.org)을 사용해서 확인하였다.
9. 마이크로어레이 준비
23,753 코딩 시퀀스에 대한 모든 올리고뉴클레오티드들은 최종농도 50 pmole/㎕로 printing buffer(Telechem International, Inc., USA)에 부유시켰다. 부유된 올리고뉴클레오티드들은 실란화된 유리 슬라이드(UltraGAPSTM, Corning Lifesciences, MA) 상에 습도 40 %, 20 25°C의 조건하에서 robotic microarrayer(OmniGrid II, GeneMachines, CA) 를 이용하여 spotted 시켰다.
10. cDNA 프로브 및 마이크로어레이 혼성화(microarray hybridization) 준비
각 세포들을 (1 × 105cells) 6-웰 배양 플레이트에 분주하여, 1일 동안 배양시킨 다음, 본 발명의 모링가 잎 추출물을 각각의 세포에 처리하였다. 2일 동안 배양한 다음, 전체 RNA를 수확하였다. 타겟 cDNA 프로브의 합성 및 혼성화는 종래 공지된 방법에 의하여 수행하였다. 각각의 전체 RNA 20 ㎍은 5 ㎍ pdN6 primer (Amersham Biosciences, UK)와 15.4 μL of RNase가 없는 물 15.4 μL에서 혼합시키고 65°C에서 10분 동안 반응시켰다. cDNA는 Cy3- 또는 Cy5-dUTP (1 mM each, NEN Life Science Products, Boston, USA) 3 μL 존재하에 42°C, 2시간 동안 합성되었다. 형광표지화된 cDNA는 PCR purification kit (Qiagen)를 사용하여 정제하였다. Cy3 및 Cy5-labeled cDNA는 Microcon YM-30 (Millipore Corp. USA)를 사용하여 최종 부피 27 ㎕로 농축하였다. 20 ㎕의 20 SSC, 8 ㎕의 1% SDS, 24 ㎕의 포르마이드 (Sigma, USA), 10 μg의 salmon sperm DNA (Invitrogen Corp.) 및 27 ㎕의 표지화된 cDNA 용액을 포함하는 혼성화 혼합액(80μL)을 2-3분 동안 100°C에서 가열하였고, 바로 마이크로어레이에 적용하였다. 상기 어레이는 humidified hybridization chamber (Array Chamber X, GenomicTree Inc., Korea)에서 42°C, 12-16 시간 동안 혼성화시켰다. 혼성화된 마이크로어레이를 워싱한 다음, Axon 4000B scanner(Axon Instruments, CA)를 사용하여 정량을 수행하였다.
11. 데이터 수집 및 분석
혼성화 이미지는 GenePix Pro 4.0 (Axon Instruments, CA)에 의해 정량화하였다. 각 스팟에 대한 평균 형광 밀도를 계산하였고, 백그라운드를 제거하였다. 모든 데이터 일반화 및 통계적 분석은 GeneSpring 6.1 (Silicon Genetics, USA)을 사용하여 수행하였다. 유전자는 조절 채널(control channel)에서 그들의 강도(intensity)에 의해 여과되었다. 강도-의존 일반화(Intensity-dependent normalization (LOWESS)) 를 수행하였으며, 그 비는 강도 대 비 곡선의 lowess fit의 잔기를 줄였다. 배수 변화(fold change)의 수치는 일반화된 조절 채널 강도의 중앙값에 의해 일반화된 신호채널 강도를 나누는 것에 의해 계산되어졌다. 배수 변화의 비는 유관 상태(relevant conditions) 사이에서 배수 변화의 수치로 배수변화의 수치를 나누는 것에 의해 계산되어졌고 2.0 이상이 의미있는 중요한 차이로 결정하였다. 파라메트릭 ANOVA 테스트는 샘플에서 다르게 표현된 유전자를 발견하기 위하여 p 수치가 0.05 또는 0.01 이하에서 Benjamini-Hochberg FDR(false discovery rate) 보정법을 사용하여 수행하였다. 계층 클러스터링(Hierarchical clustering)은 0 근처에서 피어슨 상관관계(Pearson correlations)에 근거를 둔 유사도 측정에 의해 수행하였다. 상기 상관관계 분석은 피어슨 상관관계(-1 내지 1)를 사용하여 수행하였다. 실험으로부터 도출된 마이크로어레이 데이터는 http://218.48.131.23/Servelet/GeNet 에서 다운로드하여 이용하였다.
12. HFA(Hollow fiber assay)
Hollow Fiber Assay(HFA)는 NCI (National Cancer Institute, USA) 표준 절차(http://dtp.nci.nih.gov/branches/btb/hfa.html)에 의해 수행하였다. 간략하게 설명하면, 2개의 암세포주, A549 및 HepG를 75cm2 배양 플라스크에서 배양하였다. 일반 성장 배지는 5 × 105 cells/mL의 바람직한 세포 밀도를 가진 세포들로 로딩되기 전, 500 kDa 제한분자량을 가진 1mm(내부 직경) 폴리피닐리덴 플루오라이드 중공 섬유(HFs) (Spectrum Laboratories, Houston, TX, USA)으로 적용시켰다. 각각의 중공 섬유(HFs)를 그들의 길이를 따라 1.5 cm 마다 hot smooth-jawed needle holder 로 열-밀봉하였다. 핸들링의 용이를 위해 2-mm 꼬리를 가진 조각들로 잘랐다. 가장 높은 접종 밀도에서 각각은 1.5cm 이었다. 각각의 중공 섬유 조각들은 대략 105 세포들을 포함하였다. 섬유는 세포 배양 배지를 포함한 6-웰 배양 플레이트에 놓아졌으며, 6주령의 수컷 면역 결핍 누드 마우스에 외과적 이식하기 1일전 배양되었다(Harlan, Horst, Netherlands). 모든 마우스들은 냉방장치가 된 방에서 12시간 명-암 주기로 사육되어졌으며, 물과 사료에 대해서는 제한하지 않았다(Purina 5001 Rodent Chow; Purina, St. Louis, MO, USA). 쥐들을 졸레틸(Zoletil), 및 럼푼(Rompun)으로 마취하였다. 중공섬유(HFs)를 피하(subcutaneous, SC) 부분에 이식하였고 절개는 피부 스테플로 닫았다. 마우스들은 섬유 이식 후 3일째에 각각 다른 모링가 잎 추출물(MOL extract)의 농도로 경구로 일회 투여하였으며(도 14B 참조), 또한 대조 약으로 독소루비신(doxorubicin, DOX)을 정맥 투여하였다. 7일 후에, 중공 섬유를 회수하여 트리판 블루 배제법(trypan blue exclusion assay)을 실시하였다.
<
실험예
1>
In
vitro
에서 암세포에 대한
모링가
잎 추출물의 억제효과 확인
1. 추출 온도 및 추출시간에 따른
모링가
잎 추출물의 암세포에 대한 억제 효과
추출 온도 및 추출시간에 따른 모링가 잎 추출물의 암세포에 대한 효과를 확인하기 위하여, 각각의 암세포에 상기 실시예에 따라 제조된 모링가 잎 추출물들을 농도에 따라 처리한 후, 하기의 방법으로 MTT assay를 실시하여 암세포의 생존율을 확인하였다.
세포들을 96 웰(well) 플레이트에 배지 100 ㎕ 당 3 X 103 세포의 농도로 분주하였다. 1일 동안 배양한 후, 실시예 1에 의해 만들어진 모링가 잎 추출물을 각 플레이트에 0 내지 400 ㎍/ml의 다양한 농도로 처리하였다. 다시 1일 또는 2일 배양한 후, cell-counting Kit-8 (Cat. No. CK04, Dojindo lab. 일본) 또는 WST assay 시약 (대일 lab, 한국) 10 ㎕를 각 웰에 첨가한 다음, 4시간 동안 배양하였다. 이후, 마이크로플레이트 리더(microplate reader)(Model 680, Bio-Rad)를 이용하여 450 nm 파장에서 흡광도를 측정하였다.
(1) 추출 온도에 따른 모링가 잎 추출물의 효과
추출시간을 30분으로 동일하게 하고 추출 온도를 다르게 한 실시예 2, 실시예 6 내지 9의 암세포 에 대한 독성 효과를 평가해보았을 때, 도 1A에서 볼 수 있는 바와 같이, 4°C 에서의 추출물(실시예 2)의 효과가 가장 높음을 확인할 수 있었다.
(2) 추출 시간에 따른 모링가 잎 추출물의 효과
추출 온도를 동일하게 하고(4°C), 침지 시간을 다르게 한, 실시예 1 내지 실시예 5의 암세포의 생존율에 미치는 효과를 비교해보았을 때, 도 1B에서 확인할 수 있는 바와 같이, 추출시간이 짧을수록 암세포에 대한 독성도의 효과가 높음을 알 수 있고, 특히 추출시간이 5분이었던 모링가 잎 추출물의 효과가 가장 우수하였다.
이후 하기 모든 실험에서는 가장 좋은 암세포 독성 효과를 보였던 추출온도 4°C, 및 추출시간 5분으로 제조한 모링가 잎 추출물을 사용하였다.
2.
FACS
분석을 이용한
모링가
잎 추출물의 암세포의 세포 주기의 변화 및 세포 사멸 효과 확인
모링가 잎 추출물이 암세포에 미치는 세포 주기 변화 및 세포 사멸효과를 확인하기 위해, A549 세포주를 모링가 잎 추출물 각 농도에 따라 처리한 다음 48 시간 이후, FACS 분석을 실시하였다. 그 결과, 모링가 잎 추출물의 농도에 따라(200, 300, 및 400 ㎍/mL), sub-G1 population을 최대 21%, 65%, 93% 각각 증가시킴을 확인할 수 있었다(도 2A). 독립적인 6번의 실험에 대한 평균 sub-G1 population을 도 3에 나타내었다.
Caspase-3에 대한 웨스턴 블롯을 실시한 결과, 모링가 잎 추출물 처리는 그 추출물의 용량에 의존하여 Caspase-3가 하향 조절(down-regulation)되며, 분열된 Cspase-3가 상향 조절(up-regulation)되는 것을 확인할 수 있었다(도 2B) 따라서 암세포에 대한 세포 사멸이 일어났음을 확인할 수 있었다 .
또한 A549 세포주 이외의 다른 암세포들에 대해서도 모링가 잎 추출물의 세포주기 변화에 대한 영향을 FACS 분석에 의해 확인하였을 때 A549 세포주와 유사한 결과를 얻을 수 있었다(도 4).
3.
모링가
잎 추출물의 암세포에 대한 독성 효과
(1) 현미경(microscopy) 및 콜로니 형성 분석 (colony forming assay)
현미경(도 5A) 및 콜로니 형성 분석법(도 5B)을 사용하여 모링가 잎 추출물의 A549 세포주에 대한 독성 효과를 평가하였다. 도 5A에서 나타낸 바와 같이, 세포들은 모링가 잎 추출물의 200㎍/ml 농도 이상에서 배양 접시에 부착할 수 없었고, 전형적인 세포사멸 형태를 보여주었다.
모링가 잎 추출물 처리가 A549 세포의 생존 능력에 미치는 영향에 대하여 콜로니 생존 분석을 이용하여 평가하였다. 트립신 처리된 세포들을 회수하여, 6-웰 배양 접시의 각 부분에 1 × 103 세포 농도로 분주하여, 1일 동안 배양한 후, 모링가 잎 추출물을 각 농도별로 가하여 7일 동안 다시 배양하였다. 7일 이후에, 콜로니는 고정되었고, 크리스탈 바이올렛으로(0.1% w/v)로 1분 동안 염색하여, 증류수로 워싱한 다음 사진촬영하였다. 실험은 세차례 반복하였으며, 대표적인 결과 사진을 도 5B에 나타내었다.
도 5B에 나타낸 바와 같이, 모링가 잎 추출물이 처리된 세포는 용량에 의존하여 추출물이 처리되지 않은 세포와 비교해서 확연히 A549의 생존 콜로니의 수가 낮아짐을 확인할 수 있었으며, 또한, 어떠한 콜로니도 모링가 잎 추출물 100㎍/ml의 농도 이상에서 존재하지 않았다. 또한 A549 세포주 이외에 다른 암세포에 대한 모링가 잎 추출물의 효과를 확인하기 위해, 우리는 다른 암세포주에서 동일한 실험을 행한 결과, A549 세포와 유사한 결과를 얻었다(도 6).
(2) 세포 이동성 분석 (cell migration assay)
세포 이동 특징은 24-웰 플레이트 내에 폴리카보네이트 멤브레인 삽입물(8um pore size)을 포함하며, 세포 이동을 분석하기 위해 CytoSelect 24-well cell migration kit (Cell Biolabs Inc. Cat.No CBA-100-C)를 이용하였다. 멤브레인은 이동하지 않은 세포로부터 폴리카보네이트 멤브레인의 기공을 통해 통과하는 이동하는 세포를 식별하기 위한 경계로서 역할을 한다. 혈청(serum)이 없는 배지에 1 × 105 cells/mL의 세포를 배양하여, 각각 다른 농도의 모링가 잎 추출물을 처리한 다음 16시간동안 두었다. 이후 이동 플레이트(migration plate)의 벽으로 10% FBS를 포함하고 있는 배지 0.5ml을 첨가한 다음, 위쪽 챔버(chamber)로 세포 부유 용액 0.3ml 을 가하였다. 1 일 동안 배양시킨 다음, 위쪽 챔버의 내부로부터 배지를 조심스럽게 흡입시키고, 이동하지 않은 세포들을 면봉으로 닦아서 제거하였다. 최종적으로 이동 세포들은 세포 염색 용액으로 10분 동안 염색하여, 사진을 찍었으며, 마이크로플레이트 리더(microplate reader)(Model 680, Bio-Rad)를 이용하여 560 nm 파장에서 흡광도를 측정하였다(도 7).
그 결과 세포 이동성 분석은 이동된 세포의 비율이 모링가 잎 추출물이 처리된 세포에 처리되지 않은 세포보다 낮은 것으로 나타났다. 세포 이동 능력은 양에 의존하여 모링가 잎 추출물에 의해 억제되었다. 그 이동율은 모링가 잎 추출물 300㎍/ml로 처리하였을 때 87%이었으며, 400㎍/ml에서는 99% 감소하였다.
<
실험예
2> 활성
산소종(reactive oxygen species, ROS)에
대한 영향 확인
모링가 잎 추출물이 세포내 ROS 레벨에 미치는 영향을 확인하기 위하여, fluorometric assay를 이용하였다. 모링가 잎 추출물의 48시간 처리 후, ROS의 생산에 대하여 세포 투과 산화민감 염료인 2′,7′- 디클로로디하이드로플루오로세인 디아세테이트(H2DCFDA)(Invitrogen)을 사용하여 측정하였다. 카르복시디클로로플르오레세인 디아세테이트(DCFH-DA)는 비극성 화합물로 세포내로 결합 후에 세포의 에스테라아제(esterase)에 의해 멤브레인-비투과적인 비-형광성 극성유도체(DCFH)로 전환된다. 전환된(trapped) DCFH는 세포내 과산화수소에 의해 빠르게 형광성의 2′,7′-디클로로플르오레세인(DCF)으로 산화된다. 구체적으로 트립신처리된 세포들(약 1 × 105 cells)을 PBS로 워싱하여 재부유시킨 후, 최종농도 10 μM의 DCFH-DA로 처리하였다. 다음으로 세포들을 어두운 곳에서 37°C, 30분동안 배양시킨 후, FACScan (EPICS XL Flow Cytometry, Beckman Coulter Counter)을 사용하여, ROS 레벨을 직접적으로 측정하였다.
그 결과 모링가 잎 추출물이 처리된 세포에서는 처리되지 않은 대조군과 비교하였을때, 용량에 의존하여 확실한 ROS의 감소를 유발하였다. 이는 모링가 잎 추출물이 프리라디칼 스캐빈져의 능력을 가지는 것을 나타낸다(도 8).
<
실험예
3>
모링가
잎 추출물의 유전자 및 단백질 발현에 미치는 영향 분석
1. 대조군으로서
하우스키핑
유전자 또는 단백질 확인
모링가 잎 추출물의 처리에 따른 세포사멸과 연관된 mRNA 및 단백질의 발현에 대한 영향을 확인하기 위해, 먼저 RT-PCR 및 웨스턴 블롯 분석을 이용하여 대조군으로써 하우스키핑 유전자 또는 단백질, β-액틴의 발현을 분석하였다. 동일한 양의 샘플을 적용시켰음에도 불구하고, 도 9A의 첫번째 및 두번째 젤 결과에서 모링가 잎 추출물 300㎍/mL이 처리된 세포에서 β-액틴의 발현 레벨이 처리되지 않은 세포와 비교하였을 때 현저히 낮았다(도 9A). 이러한 현상은 반복된 실험에서 지속적이며 반복적으로 관찰되었다. 우리는 웨스턴 블롯 분석에 대해서 단백질의 동일한 양을 로딩하였음을 확인하기 위하여 멤브레인을 Ponceau S(Sigma)로 염색하여, 젤 로딩 및 멤브레인으로 단백질의 이전에 대해서 어떤 문제도 없음을 확인하였다(도 9B). 그러나 이후 모든 샘플에서 유사한 발현 레벨을 조정하기 위하여, 300㎍/ml에 대한 추가 RNA 또는 단백질을 첨가하였다. 이는 도 6A의 세 번째 또는 네 번째 젤에서 보여준 바와 같다.
2.
모링가잎의
수용성 추출물에 의한 단백질 및 유전자의 하향 조절 분석
(1) 신호 경로(signaling pathway)
A549에 수용성 모링가 잎 추출물의 0 내지 300 ㎍/ml를 처리한 다음, RT-PCR 또는 웨스턴 블롯을 이용하여 mRNA 또는 단백질을 분석하였다. Akt, p-IkB, NF-kB, p-Erk, β-catenin, 및 Cyclin D1은 모링가 잎 추출물 용량에 의존하여 상당히 하향 조절되었다(도 9C 및 D). 그러나 염증 신호, ROS의 레벨의 변화, 자외선, 단백질 합성 억제제 등 다양한 스트레스에 의해 활성화될 수 있는 c-Jun N-terminal kinases(JNKs)는 모링가 잎 추출물의 처리에 의해 증가하였다.
Sox, Oct4, Klf4, c-Myc 강화된 발현이 iPS 세포를 생산할 수 있고(J Vis Exp 14: 734-735), SOX2 유전자의 침묵은 이종 이식의 NOD/SCID mice 에 있어서 c-MYC, WNT1, WNT2, and NOTCH1의 약화된 발현과 함께 A549 세포의 발암성의 특징을 감소시킨다는 점이 공지되었다(PLoS One 7(5):e36326). 따라서 Notch1 및 그것의 활성 세포내 도메인인 분열된 Notch1을 포함한 단백질 또는 유전자의 발현을 조사하였다. 그 결과 도 9E 및 9F에서 보여준 바와 같이 모든 조사된 단백질들은 하향 조절되었다. 추가로 mRNA 발현에 있어서 용량-의존 감소 경향 역시 단백질의 결과와 일치하였다.
(2) 모링가 잎 추출물에 의한 단백질의 중요한 하향 조절
단백질의 동량이 로딩되었으며, ponceau S 염색에 의해 멤브레인으로 단백질의 정상적인 이전을 확인하였음에도 불구하고, 도 9A에서 나타낸바 와 같이 하우스 키핑 단백질인 β-액틴의 발현은 크게 하향조절되었다. 보다 자세히 조사하기 위하여, SDS-PAGE 젤을 이용하여 분석한 결과 도 10에서 나타낸 바와 같이, 전체 밴드 강도는 처리된 모링가 잎 추출물 농도와 관련없이 유사하였다. 이는 각 웰에 로딩된 단백질의 농도가 유사함을 나타낸다. 그러나, 흥미있게도 61.5 과 90.5 kDa 사이에 위치한 몇몇의 단백질을 제외하고서, 다수의 단백질이 하향 조절된 것으로 나타났다. 분석 결과 이 범위에 있는 주요 단백질은 열-충격 단백질(heat-shock proteins)들로 확인되었다. [Heat shock cognate 71 kDa protein (69kDa) / Heat shock 70 kDa protein (68kDa) / Heat shock protein HSP 90-beta (83kDa) / Heat shock protein, mitochondrial (61kDa)].
(3) 모링가 잎 추출물에 의한 유전자의 중요한 하향 조절 확인-마이크로어레이 분석
마이크로어레이를 이용하여, 모링가 잎 추출물이 미치는 전체 유전자 발현 패턴을 확인하였다(도 11). 테스트한 23,753 유전자 중에 205개의 유전자만이(0.9%) 2배 이상 상향 조절되었고, 유전자의 90.1% 가 하향 조절되었다. 변화가 없는 유전자들은 1,964개(8.3%)이었다. 이러한 마이크로어레이 결과는 상기 SDS-PAGE 젤의 결과와 일치한다. 이는 단백질의 중요한 하향 조절이 mRNA 발현의 하향 조절 때문이라고 추측된다. 반면에 대부분의 상향 조절된 유전자와 연관된 기능은 아직 명확하게 밝혀지지 않았으며, 어떤 변화도 없는 유전자의 기능은 도 11C에서 보여주었다.
(4) rRNA(ribosomal RNA)의 분해(degradation) 확인
단백질 및 mRNA의 중요한 하향-조절을 분석하기 위해, 우리는 전체 RNA 추출 후에 젤 전기영동에 의해 rRNA의 밴드 패턴을 조사하였다(도12). 모링가 잎 추출물의 0 및 100㎍/mL에서 두 개의 명확한 28S 및 18S rRNA의 일반 패턴을 확인할 수 있었다. 그러나 200 ㎍/mL에서 rRNA의 분해가 일부 관찰되었고, 300 ㎍/mL에서는 중요한 rRNA의 분해가 관찰되었다(도 12, 왼쪽 패널). 이러한 양에 의존한 rRNA의 분해는 젤에 있어서 28S 및 18S rRNA 밴드 사이에서 새로운 밴드(1*로 표시)의 형태를 나타내었다. 추가로 모링가 잎 추출물의 300 ㎍/ml 처리 세포로부터 나타난 새로운 밴드(2*로 표시)는 18S rRNA의 바로 아래에 관찰되었다. 결론적으로, 대부분의 단백질 및 유전자의 중요한 하향 조절은 일반적인 RNA의 감소 및 비정상적인 RNA 증가 둘 다로부터 발생한 결과이다.
<
실험예
4>
모링가
잎 추출물의 암세포에 대한 특이적 독성 확인
모링가 잎 추출물은 MTT 분석을 사용하여 암세포가 아닌 일반세포에 있어서 독성 효과를 시험하였다. MTT 분석은 암세포주인 A549에서 강한 독성을 보이는 것으로 나타났다(200 ㎍/ml에서 약 65%). 동일한 농도의 모링가 잎 추출물을 일반 세포주인 COS-7(African green monkey kidney cells)에 처리하였을 때, 그 생존능은 A549보다 훨씬 작은 독성을 보여주었다(도 13). 이는 일반 세포가 암세포보다 모링가 잎 추출물에 대해 더 저항성이 있음을 가리킨다. 300 ㎍/mL의 농도 이상의 모링가 잎 추출물에서 A 549 세포들은 모두 생존할 수 없었으나, 반면 일반 세포주인 COS-7은 모링가 잎 추출물 600 ㎍/ml의 농도에서도 여전히 50% 이상 생존하였다. 이는 모링가 잎 추출물은 암세포에서 높은 특이적 독성을 가짐을 나타내는 결과이다.
<
실험예
5>
In
vivo
에서 암세포에 대한
모링가
잎 추출물의 억제효과 확인-중공섬유 분석(
Hollow
Fiber
assay
,
HFA
)
상술한 바와 같이, 모링가 잎 추출물이 in vitro에서 암세포 증식을 억제하며 암세포에 대해 높은 특이성을 가지고 있는바, in vivo에서도 모링가 잎 추출물이 암세포 증식을 억제할 수 있는지 확인하였다. 이를 위해, 누드 마우스에 A549 페암 세포 및 Hep G2 간암세포주로 채워진 중공 섬유를 각각 이식하였다. 3일 후에 마우스들에 다른 농도의 모링가 잎 추출물이 1회 경구 투여되었고, 대조시약으로 독소루비신(doxofubicin, DOX)이 정맥주입되었다. 10일 경과 후, 마우스로부터 중공 섬유를 회수하여, 트리판 블루 배재 시험(trypan blue exclusion assay)을 행하였다(도 14A).
그 결과 in vivo에서의 모링가 잎 추출물의 암세포에 대한 효과는 in vitro 결과와 일치하는 것으로 나타났다. 구체적으로, 페암 세포(A549)에 대해서는 세포 생존능의 점차적인 감소를 확인할 수 있었으며(도 14B, 왼쪽 패널), 유사한 역학적 프로파일이 간암세포 HepG2에서도 확인할 수 있었다. 그러나 간암 세포에서는 A 549 세포와 비교해보았을 때 더욱 중요한 독성을 가지는 것을 확인하였다(도 14B, 오른쪽 패널). 또한 HepG2 세포에서 모링가 잎 추출물의 농도가 200 ㎍/ml 이었을때 세포 독성도가 대조군인 독소루비신보다 우수하였다. 이는 본 발명에 따른 모링가 잎 추출물이 경구 투여에서도 추가 흡수 보충제 없이도 흡수가 용이하고 정맥주입한 결과 못지 않게 우수한 결과를 나타내므로 향후 경구 투여 제제의 개발에 유용하게 활용될 수 있음을 나타내었다.
<
실험예
6> 추출용매에 따른
모링가
잎 추출물의 암세포 사멸 효과 분석
추출용매에 따른 모링가 잎 추출물의 암세포 사멸 효과를 확인하기 위해, 모링가 잎을 DW, 70% 에탄올(비교예 1), DMSO 100% 용액(비교예 2) 각각의 용매에서 10분간 추출한 후(단 DW의 경우는 4°C의 DW를 사용하여 추출하였으며, 다른 추출용매는 실온에서 추출하였다), FACS 분석을 실시하였다. 구체적으로 모링가 잎을 상기 각각의 용매에서 10분간 추출한 후, 불용물을 제거한 다음 추출물을 여과한 후, A549 세포주에 각각의 추출물을 0 내지 30㎕ 처리한 다음 24 시간 배양한 이후, FACS 분석을 실시하였다. 그 결과, DW에서 추출한 모링가 잎 추출물이 다른 추출용매에서 추출한 모링가 잎 추출물(비교예 1, 비교예 2) 보다 월등한 A549세포의 사멸 효과가 있음을 확인할 수 있었다(도 15).
<
제제예
>
하기에 본 발명의 조성물을 위한 제제예를 예시한다. 하기에서 모링가 잎 추출물은 본 발명에 따른 모링가 잎 추출물을 의미한다.
<
제제예
1>
산제의
제조
모링가 잎 추출물 20 ㎎
유당 100 ㎎
탈크 10 ㎎
상기의 성분들을 혼합하고 기밀포에 충진하여 산제를 제조한다.
<
제제예
2> 정제의 제조
모링가 잎 추출물 10 ㎎
옥수수전분 100 ㎎
유당 100 ㎎
스테아린산 마그네슘 2㎎
<
제제예
3> 캡슐제의 제조
모링가 잎 추출물 10 ㎎
결정성 셀룰로오스 3 ㎎
락토오스 14.8 ㎎
마그네슘 스테아레이트 0.2 ㎎
통상의 캡슐제 제조방법에 따라 상기의 성분을 혼합하고 젤라틴 캡슐에 충진하여 캡슐제를 제조한다.
<
제제예
4> 주사제의 제조
모링가 잎 추출물 10 ㎎
만니톨 180 ㎎
주사용 멸균 증류수 2974 ㎎
Na2HPO4·12H2O 26 ㎎
통상의 주사제의 제조방법에 따라 1앰플당(2 ㎖) 상기의 성분 함량으로 제조한다.
<
제제예
5> 드링크제의 제조(식품조성물의 제조)
모링가 잎 추출물 100mg
포도당 10mg
구연산 0.6g 및 액상 올리고당 25g을 혼합한 후 정제수 300ml를 가하여 각 병에 200ml 씩 되게 충전하였다. 병에 충진한 후 130℃ 에서 4 내지 5초간 살균하여 음료를 제조하였다.
Claims (14)
- 모링가 잎의 수용성 추출물을 유효성분으로 포함하는 암 치료 또는 예방용 약학적 조성물.
- 제 1항에 있어서, 상기 모링가 잎의 수용성 추출물은 추출용매로서 물을 사용하여 얻어지는 것을 특징으로 하는 암 치료 또는 예방용 약학적 조성물.
- 제 2항에 있어서, 상기 물의 온도는 0°C 이상 40°C 미만인 것을 특징으로 하는 암 치료 또는 예방용 약학적 조성물.
- 제 3항에 있어서, 상기 모링가 잎의 추출물은 모링가 잎을 물에 1분 내지 60분 동안 침지시켜 얻어지는 것을 특징으로 하는 암 치료 또는 예방용 약학적 조성물.
- 제 3항에 있어서, 상기 모링가 잎의 추출물은 건조된 모링가 잎을 0-20°C의 물에 1분 내지 30분 동안 침지시켜 얻어지는 것을 특징으로 하는 암 치료 또는 예방용 약학적 조성물.
- 제 1 내지 5항 중 어느 한 항에 있어서, 상기 약학적 조성물은 총 조성물 대비 추출물의 단백질 농도 기준 0.001 내지 600 ㎍/ml의 모링가 잎 추출물을 함유하는 것을 특징으로 하는 암 치료 또는 예방용 약학적 조성물.
- 제 1 내지 5항 중 어느 한 항에 있어서, 상기 암은 간암, 유방암, 폐암, 편평상피암, 및 섬유종으로 이루어지는 군으로부터 선택되는 1종 이상인 것을 특징으로 하는 암 치료 또는 예방용 약학적 조성물.
- 제 1 내지 5항 중 어느 한 항에 있어서, 상기 약학적 조성물은 약학적으로 허용되는 담체를 추가로 포함하는 것을 특징으로 하는 암 치료 또는 예방용 약학적 조성물.
- 제 8항에 있어서, 상기 약학적 조성물은 정제, 환제, 산제, 과립제, 시럽제, 액제, 현탁제, 에멀션 또는 캅셀제인 경구용 제제인 것을 특징으로 하는 암 치료 또는 예방용 약학적 조성물.
- 모링가 잎의 수용성 추출물을 유효성분으로 포함하는 암 예방 또는 개선용 식품 조성물.
- 모링가 잎의 수용성 추출물을 유효성분으로 포함하는 피부암 예방 또는 개선용 화장품 조성물.
- 모링가 잎을 0-20°C의 물로 추출하는 것을 특징으로 하는 항암에 유효한 모링가 잎의 추출물 제조방법.
- 제 12항에 있어서,
모링가 잎을 1 내지 20배의 0-20°C의 물에 침지하는 단계;
모링가 잎의 침출수를 수득하여, 불용성 물질을 제거하는 단계; 및
상기 불용성 물질을 제거한 침출수를 여과하는 단계;
를 포함하는 것을 특징으로 하는 항암에 유효한 모링가 잎의 추출물 제조방법. - 제 13항에 있어서, 상기 0-20°C의 물에 침지하는 단계에서 모링가잎의 침지 시간은 1분 내지 60분인 것을 특징으로 하는 항암에 유효한 모링가 잎의 추출물 제조방법.
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020130065519A KR20140143655A (ko) | 2013-06-07 | 2013-06-07 | 모링가 잎의 수용성 추출물을 유효성분으로 포함하는 암 치료 또는 예방용 조성물 및 모링가 잎의 추출물의 제조방법 |
| CN201410253975.5A CN104224862B (zh) | 2013-06-07 | 2014-06-09 | 含辣木叶水溶性提取物为有效成分的用于治疗或预防癌的组合物及辣木叶提取物的制备方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020130065519A KR20140143655A (ko) | 2013-06-07 | 2013-06-07 | 모링가 잎의 수용성 추출물을 유효성분으로 포함하는 암 치료 또는 예방용 조성물 및 모링가 잎의 추출물의 제조방법 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020150107812A Division KR101803852B1 (ko) | 2015-07-30 | 2015-07-30 | 모링가 잎의 수용성 추출물을 유효성분으로 포함하는 암 치료 또는 예방용 조성물 및 모링가 잎의 추출물의 제조방법 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20140143655A true KR20140143655A (ko) | 2014-12-17 |
Family
ID=52214341
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020130065519A KR20140143655A (ko) | 2013-06-07 | 2013-06-07 | 모링가 잎의 수용성 추출물을 유효성분으로 포함하는 암 치료 또는 예방용 조성물 및 모링가 잎의 추출물의 제조방법 |
Country Status (2)
| Country | Link |
|---|---|
| KR (1) | KR20140143655A (ko) |
| CN (1) | CN104224862B (ko) |
Cited By (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN105962401A (zh) * | 2016-04-29 | 2016-09-28 | 安徽恋尚你食品有限公司 | 一种冻干辣木制作辣木胶囊以及生产方法 |
| KR101681421B1 (ko) | 2015-07-24 | 2016-12-09 | 농업회사법인 주식회사 수신오도 | 모링가 식초와 이의 제조방법 |
| KR20170006711A (ko) | 2015-07-09 | 2017-01-18 | 농업회사법인 주식회사 수신오도 | 모링가 간장과 이의 제조방법 |
| KR20170006725A (ko) | 2015-07-09 | 2017-01-18 | 농업회사법인 주식회사 수신오도 | 모링가 된장과 이의 제조방법 |
| KR20170006732A (ko) | 2015-07-09 | 2017-01-18 | 농업회사법인 주식회사 수신오도 | 모링가 고추장과 이의 제조방법 |
| KR20170006707A (ko) | 2015-07-09 | 2017-01-18 | 농업회사법인 주식회사 수신오도 | 모링가 차와 이의 제조방법 |
| KR20170011691A (ko) | 2015-07-24 | 2017-02-02 | 농업회사법인 주식회사 수신오도 | 모링가잎을 포함하는 김치양념과 이의 제조방법 |
| KR20170032558A (ko) | 2015-09-15 | 2017-03-23 | 농업회사법인 주식회사 수신오도 | 모링가 발효음료와 이의 제조방법 |
| KR20170032563A (ko) | 2015-09-15 | 2017-03-23 | 농업회사법인 주식회사 수신오도 | 모링가 잎이 첨가된 화장료 조성물 |
| WO2021234165A1 (fr) | 2020-05-21 | 2021-11-25 | Agence Francaise Pour Le Developpement D'al Ula | Hydrolysat de protéines du tourteau des graines de moringa peregrina pour son application en tant que médicament, son procédé d'obtention et compositions pharmaceutiques et dermatologiques |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN104586707A (zh) * | 2015-02-26 | 2015-05-06 | 唐国平 | 一种鲜辣木叶液护肤品及其制备方法 |
| CN104971140A (zh) * | 2015-07-24 | 2015-10-14 | 青岛蓝盛洋医药生物科技有限责任公司 | 一种治疗骨折的药物组合物及其制备方法 |
| EP3216869B1 (en) | 2016-03-09 | 2019-09-18 | Colizzi, Vittorio | Nutraceutical plant derived microrna elements for treatment of leukemia |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20060141065A1 (en) * | 2004-12-28 | 2006-06-29 | Council Of Scientific And Industrial Research | Herbal formulation for the treatment of piles |
| CN101485622A (zh) * | 2009-03-03 | 2009-07-22 | 张嘉恒 | 一种含有辣木植物提取物的洗发水及其制备方法 |
| FR2946879B1 (fr) * | 2009-06-22 | 2012-05-18 | Fabre Pierre Dermo Cosmetique | Extrait de graines entieres de moringa sp. et son utilisation dans des compositions cosmetiques et/ou dermatologiques. |
| CN102920754A (zh) * | 2012-11-26 | 2013-02-13 | 北京盈良安生物科技有限公司 | 辣木叶片提取物及其对癌症在化疗或放疗的增效减毒应用 |
-
2013
- 2013-06-07 KR KR1020130065519A patent/KR20140143655A/ko active Application Filing
-
2014
- 2014-06-09 CN CN201410253975.5A patent/CN104224862B/zh active Active
Cited By (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20170006711A (ko) | 2015-07-09 | 2017-01-18 | 농업회사법인 주식회사 수신오도 | 모링가 간장과 이의 제조방법 |
| KR20170006725A (ko) | 2015-07-09 | 2017-01-18 | 농업회사법인 주식회사 수신오도 | 모링가 된장과 이의 제조방법 |
| KR20170006732A (ko) | 2015-07-09 | 2017-01-18 | 농업회사법인 주식회사 수신오도 | 모링가 고추장과 이의 제조방법 |
| KR20170006707A (ko) | 2015-07-09 | 2017-01-18 | 농업회사법인 주식회사 수신오도 | 모링가 차와 이의 제조방법 |
| KR101681421B1 (ko) | 2015-07-24 | 2016-12-09 | 농업회사법인 주식회사 수신오도 | 모링가 식초와 이의 제조방법 |
| KR20170011691A (ko) | 2015-07-24 | 2017-02-02 | 농업회사법인 주식회사 수신오도 | 모링가잎을 포함하는 김치양념과 이의 제조방법 |
| KR20170032558A (ko) | 2015-09-15 | 2017-03-23 | 농업회사법인 주식회사 수신오도 | 모링가 발효음료와 이의 제조방법 |
| KR20170032563A (ko) | 2015-09-15 | 2017-03-23 | 농업회사법인 주식회사 수신오도 | 모링가 잎이 첨가된 화장료 조성물 |
| CN105962401A (zh) * | 2016-04-29 | 2016-09-28 | 安徽恋尚你食品有限公司 | 一种冻干辣木制作辣木胶囊以及生产方法 |
| WO2021234165A1 (fr) | 2020-05-21 | 2021-11-25 | Agence Francaise Pour Le Developpement D'al Ula | Hydrolysat de protéines du tourteau des graines de moringa peregrina pour son application en tant que médicament, son procédé d'obtention et compositions pharmaceutiques et dermatologiques |
| FR3110345A1 (fr) | 2020-05-21 | 2021-11-26 | Agence française pour le développement d’Al Ula | Hydrolysat de protéines du tourteau des graines de Moringa peregrina pour son application en tant que médicament, son procédé d’obtention et compositions pharmaceutiques, dermatologiques et cosmétiques. |
Also Published As
| Publication number | Publication date |
|---|---|
| CN104224862B (zh) | 2018-05-25 |
| CN104224862A (zh) | 2014-12-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20140143655A (ko) | 모링가 잎의 수용성 추출물을 유효성분으로 포함하는 암 치료 또는 예방용 조성물 및 모링가 잎의 추출물의 제조방법 | |
| KR101803852B1 (ko) | 모링가 잎의 수용성 추출물을 유효성분으로 포함하는 암 치료 또는 예방용 조성물 및 모링가 잎의 추출물의 제조방법 | |
| KR102186872B1 (ko) | 우유 엑소좀을 포함하는 피부 미백용 조성물 | |
| KR101808992B1 (ko) | 인유두종 바이러스 16형 항바이러스 조성물 | |
| CN102186488B (zh) | 齿裂黄鹌菜提取物用于制备肝功能改善用药物组合物及用于制备肝功能改善用健康功能食品组合物的用途 | |
| US20110091395A1 (en) | Extract of phaleria macrocarpa as an antineoplastic, anti-inflammatory and antiangiogenic agent | |
| KR20210052837A (ko) | 여우꼬리 선인장 추출물을 포함하는 암 예방 또는 치료용 약학적 조성물 | |
| KR102659740B1 (ko) | 해삼 생식선 추출물 또는 이로부터 유래된 화합물의 항암 용도 | |
| WO2015130081A1 (ko) | Stat3 저해활성을 갖는 토목향 헥산 분획물 또는 이로부터 분리된 화합물을 유효성분으로 함유하는 유방암 예방 및 치료용 약학적 조성물 | |
| KR101649047B1 (ko) | 암의 예방 또는 치료를 위한 카지놀 c의 용도 | |
| KR102272425B1 (ko) | 사삼 추출물을 유효성분으로 포함하는 쇼그렌 증후군의 예방 또는 치료용 조성물 | |
| US7744936B2 (en) | Method for preparing extract from wild ginseng showing anticancer activity and the composition comprising the same | |
| KR101720610B1 (ko) | Stat3 저해활성을 갖는 토목향 헥산 분획물 또는 이로부터 분리된 화합물을 유효성분으로 함유하는 유방암 예방 및 치료용 약학적 조성물 | |
| KR102085582B1 (ko) | 쑥부지깽이 속 추출물을 유효성분으로 함유하는 항종양 또는 항종양 면역작용 유도용 조성물 | |
| KR102268932B1 (ko) | 화학식 1로 표시되는 화합물을 포함하는 암의 예방 또는 치료용 조성물 | |
| KR20190085459A (ko) | 청각 추출물 또는 이의 분획물, 및 trail 단백질을 포함하는 암 예방 또는 치료용 조성물 | |
| KR102155713B1 (ko) | 해삼 추출물 또는 이의 분획물, 및 trail 단백질을 포함하는 암 예방 또는 치료용 조성물 | |
| US20240115537A1 (en) | Composition for preventing or treating breast cancer comprising compound derived from dendropanax morbiferus | |
| KR102621972B1 (ko) | 박테리아 균주 및 암라 추출물을 이용한 금 나노입자의 제조방법 및 상기 금 나노입자를 포함하는 암 치료용 약학 조성물 | |
| KR102432990B1 (ko) | 청피 추출물을 포함하는 피부암 예방 및 피부암 전이 억제용 조성물 | |
| JP2004300082A (ja) | 抗腫瘍剤 | |
| CN102245555B (zh) | 从皇冠分离的作为抗癌药的化合物 | |
| KR101756283B1 (ko) | 카지놀 a 또는 이를 포함하는 꾸지나무 추출물을 유효성분으로 함유하는 방광암의 예방, 개선 또는 치료용 조성물 | |
| WO2005063255A1 (en) | Pharmaceutical composition for treating and preventing cancer comprising cinnamoni cortex extract and zizyphi fructus extract | |
| KR20230164939A (ko) | 전호를 유효성분으로 포함하는 암 예방 또는 개선용 조성물 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| AMND | Amendment | ||
| E601 | Decision to refuse application | ||
| AMND | Amendment | ||
| E902 | Notification of reason for refusal | ||
| AMND | Amendment | ||
| A107 | Divisional application of patent |