JP7635224B2 - マルチパラメトリックx線蛍光イメージングのための方法および装置 - Google Patents
マルチパラメトリックx線蛍光イメージングのための方法および装置 Download PDFInfo
- Publication number
- JP7635224B2 JP7635224B2 JP2022524594A JP2022524594A JP7635224B2 JP 7635224 B2 JP7635224 B2 JP 7635224B2 JP 2022524594 A JP2022524594 A JP 2022524594A JP 2022524594 A JP2022524594 A JP 2022524594A JP 7635224 B2 JP7635224 B2 JP 7635224B2
- Authority
- JP
- Japan
- Prior art keywords
- marker
- ray
- sample
- nanoparticles
- substance
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N23/00—Investigating or analysing materials by the use of wave or particle radiation, e.g. X-rays or neutrons, not covered by groups G01N3/00 – G01N17/00, G01N21/00 or G01N22/00
- G01N23/22—Investigating or analysing materials by the use of wave or particle radiation, e.g. X-rays or neutrons, not covered by groups G01N3/00 – G01N17/00, G01N21/00 or G01N22/00 by measuring secondary emission from the material
- G01N23/223—Investigating or analysing materials by the use of wave or particle radiation, e.g. X-rays or neutrons, not covered by groups G01N3/00 – G01N17/00, G01N21/00 or G01N22/00 by measuring secondary emission from the material by irradiating the sample with X-rays or gamma-rays and by measuring X-ray fluorescence
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K49/00—Preparations for testing in vivo
- A61K49/04—X-ray contrast preparations
- A61K49/0409—Physical forms of mixtures of two different X-ray contrast-enhancing agents, containing at least one X-ray contrast-enhancing agent which is not a halogenated organic compound
- A61K49/0414—Particles, beads, capsules or spheres
- A61K49/0423—Nanoparticles, nanobeads, nanospheres, nanocapsules, i.e. having a size or diameter smaller than 1 micrometer
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N23/00—Investigating or analysing materials by the use of wave or particle radiation, e.g. X-rays or neutrons, not covered by groups G01N3/00 – G01N17/00, G01N21/00 or G01N22/00
- G01N23/22—Investigating or analysing materials by the use of wave or particle radiation, e.g. X-rays or neutrons, not covered by groups G01N3/00 – G01N17/00, G01N21/00 or G01N22/00 by measuring secondary emission from the material
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N23/00—Investigating or analysing materials by the use of wave or particle radiation, e.g. X-rays or neutrons, not covered by groups G01N3/00 – G01N17/00, G01N21/00 or G01N22/00
- G01N23/22—Investigating or analysing materials by the use of wave or particle radiation, e.g. X-rays or neutrons, not covered by groups G01N3/00 – G01N17/00, G01N21/00 or G01N22/00 by measuring secondary emission from the material
- G01N23/2202—Preparing specimens therefor
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2223/00—Investigating materials by wave or particle radiation
- G01N2223/07—Investigating materials by wave or particle radiation secondary emission
- G01N2223/076—X-ray fluorescence
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2223/00—Investigating materials by wave or particle radiation
- G01N2223/40—Imaging
- G01N2223/401—Imaging image processing
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2223/00—Investigating materials by wave or particle radiation
- G01N2223/60—Specific applications or type of materials
- G01N2223/612—Specific applications or type of materials biological material
Landscapes
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Immunology (AREA)
- Biochemistry (AREA)
- Analytical Chemistry (AREA)
- General Physics & Mathematics (AREA)
- Physics & Mathematics (AREA)
- Pathology (AREA)
- Nanotechnology (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Analysing Materials By The Use Of Radiation (AREA)
- Apparatus For Radiation Diagnosis (AREA)
- Nuclear Medicine (AREA)
Description
[1]独国特許出願公開第10 2017 003 517号
[2]米国特許出願公開第2012/0307962号
[3]米国特許出願公開第2016/0252471号
[4]T. Pellegrino et al. "Nano Lett." Vol.4, No.4, 2004, p.703-707
[5]H. D. Fiedler et al. "Anal Chem." 2013, 85(21):10142-8
[6]R. Zhang et al. "Am. J. Nucl. Med. Mol. Imaging" 2018, 8(3):169-188
[7]F. Gruner et al. "Sci. Rep." Vol.8, 2018, p.16561
[8]K. Khrennikov et al. "Phys. Rev. Lett." Vol.114, p.195003 (2015)
[9]M. Hossain et al. "Applied Physics Letters" Vol.97, 2010, p.263704-1-263704-3
[10]D. P. Cormode et al. "Contrast Media & Molecular Imaging" 2014, No.9, p.37- 52
[11]Y. Li et al. "Contrast Media & Molecular Imaging" Vol.2018, 2018, Article ID 8174820, p.1-7 (with Supplementary material)
これらの目的は、それぞれ、独立請求項の特徴を有する、X線蛍光イメージングの方法、蛍光Xイメージング装置、およびマーカ物質キットによって達成される。本発明の好ましい実施形態および適用例は、従属請求項に記載されている。
(a)放射光子エネルギが全ての吸収端より高い(上にある)こと。
(b)それらのX線蛍光元素は互いに近似する蛍光確率を示すこと。
(c)それらのX線蛍光元素のそれぞれの蛍光線の減衰も近似(類似)していること。
(d)それらのX線蛍光元素の蛍光線は、試料中の散乱(単散乱および/または多重散乱)のために、互いに近似する背景ノイズ・レベルを有するべきであり、(b)および(c)とともに、X線ビーム体積中のそれらの元素の面密度(濃度)が同じである場合、それらの元素の検出された蛍光線のそれぞれの統計的有意性が互いに近似または類似するレベルを有すること。
前述のマーカ物質を用いたマルチパラメトリックXFIによって、同時にまたは順次の1回の測定で、非官能化ナノ粒子の局所濃度と官能化ナノ粒子の局所濃度が得られ、その両濃度の差は、官能化ナノ粒子が結合された薬剤に起因するものとすることが可能であり、その理由は、好ましくは、2つのタイプのナノ粒子は、試料について、活性物質またはリガンド分子だけが互いに異なるからである。別の変形例において、第3のタイプのナノ粒子を第2の薬剤で官能化することができる。このマルチパラメトリックXFIの変形例によって、非官能化ナノ粒子の基本的分布を、官能化ナノ粒子の測定濃度から減算することが可能になり、また、処理において2種の異なる薬剤を区別することも可能になる。また、ナノ粒子の代わりに、マーカ分子を含むマーカ物質を用いて、対応する方法(手順)を実現することも可能である。
Claims (27)
- 生物有機体の体の少なくとも一部を含みかつ第1のマーカ物質および少なくとも1種の別のマーカ物質を含む試料(10)上でのマルチパラメトリックX線蛍光イメージング方法であって、
前記第1のマーカ物質および前記少なくとも1種の別のマーカ物質の中の少なくとも1種の物質が、前記試料(10)との特定の相互作用のために供給された活性物質分子および/またはリガンド分子に結合され、
- 前記試料(10)にモノクロまたは狭帯域のX線放射線(1)を照射する工程であって、前記X線放射線(1)によって前記第1のマーカ物質および前記少なくとも1種の別のマーカ物質のX線蛍光(2)が励起され、前記第1のマーカ物質および前記少なくとも1種の別のマーカ物質の前記X線蛍光(2)の各蛍光線(3)が互いに異なるものである、工程と、
- 前記X線蛍光(2)を空間分解検出する工程であって、前記第1のマーカ物質および前記少なくとも1種の別のマーカ物質の前記X線蛍光(2)をスペクトル分解検出することを含む工程と、
- 前記検出されたX線蛍光(2)から、前記試料(10)中の前記第1のマーカ物質の分布と、さらに前記少なくとも1種の別のマーカ物質の少なくとも1つの分布とを求める工程と、
を含み、
- 前記第1のマーカ物質および前記少なくとも1種の別のマーカ物質は、これらのマーカ物質の同じ濃度での前記X線蛍光(2)の検出によって同等の統計的有意レベルが得られる程度に、共に同等のまたは近似する、蛍光確率、前記試料(10)における前記X線蛍光(2)の減衰、および前記試料(10)における散乱による背景ノイズ・レベルを示すものであり、
- 前記X線放射線(1)の放射光子エネルギは、全ての前記マーカ物質の吸収端より高いものであり、前記X線放射線(1)の放射光子エネルギが前記試料(10)中の全ての前記マーカ物質の最高の吸収端から離れた位置にあり、前記位置において同時に前記マーカ物質の前記背景ノイズ・レベルが最小であり前記蛍光確率が互いに近似するものである、
方法。 - 前記マーカ物質の統計的有意レベルは、前記マーカ物質の背景ノイズ・レベルが共に極小で等しくまたは近似的に等しくなるように、同時に前記蛍光確率および前記試料中の透過率が共に等しくまたは近似的に等しく最大であるように、前記試料中の前記マーカ物質の最高の吸収端より高い前記位置にあるよう前記X線放射線(1)の放射光子エネルギを選択することによって、最大化されるものである、請求項1に記載の方法。
- 前記X線放射線(1)の共通の励起ビームを用いて前記第1のマーカ物質および前記少なくとも1種の別のマーカ物質の前記X線蛍光(2)が励起され同時に検出される、請求項1または2に記載の方法。
- 前記第1のマーカ物質および前記少なくとも1種の別のマーカ物質のX線蛍光(2)が、相異なるエネルギを示す前記X線放射線(1)の相異なる励起ビームを用いて励起され、同時にまたは順次検出されるものである、請求項1または2に記載の方法。
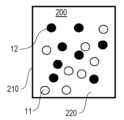
- 前記第1のマーカ物質および前記少なくとも1種の別のマーカ物質は、それぞれナノ粒子(11、12)およびマーカ分子(15、16)を含むものである、請求項1乃至4のいずれかに記載の方法。
- - 前記第1のマーカ物質または前記少なくとも1種の別のマーカ物質はそれぞれナノ粒子(11、12)を含み、
- 前記第1のマーカ物質および前記少なくとも1種の別のマーカ物質の前記ナノ粒子(11、12)は前記試料(10)について区別できない表面を含み、前記ナノ粒子(11、12)は内部に相異なる元素を含むものである、
請求項5に記載の方法。 - - 前記第1のマーカ物質は、主に第1のX線蛍光元素を含む第1のグループのナノ粒子(11)を含み、
- 前記少なくとも1種の別のマーカ物質は、それぞれ主に少なくとも1つの別のX線蛍光元素を含む少なくとも1つの別のグループのナノ粒子(12)を含むものである、
請求項5または6に記載の方法。 - 各グループのナノ粒子(11、12)は、前記第1のX線蛍光元素および前記少なくとも1つの別のX線蛍光元素の中の1つの元素のみを含むものである、請求項7に記載の方法。
- - 前記第1のグループのナノ粒子(11)は、前記試料(10)との化学的および/または物理的相互作用のために供給された第1のグループの活性物質分子および/またはリガンド分子を担持し、
- 前記少なくとも1つの別のグループのナノ粒子(12)は、それぞれ、前記試料(10)との化学的および/または物理的相互作用のために供給された相異なるグループの活性物質分子および/またはリガンド分子を担持し、または活性物質分子またはリガンド分子を担持しないものである、
請求項5乃至8のいずれかに記載の方法。 - 各グループのナノ粒子(11、12)は、1つの特定のグループの活性物質分子および/またはリガンド分子のみを担持するものである、請求項9に記載の方法。
- 前記第1のグループのナノ粒子および前記少なくとも1つの別のグループのナノ粒子(11、12)の中の少なくとも1つのグループのナノ粒子が、粒子コア(13)および粒子被覆層(14)を含むコア-シェル構造を有する、請求項5乃至10のいずれか記載の方法。
- 全ての前記ナノ粒子(11、12)はコア-シェル構造を有するものである、請求項11に記載の方法。
- 前記粒子被覆層(14)は金属または非金属材料を含むものである、請求項11または12に記載の方法。
- 前記金属は金であり、前記非金属材料はポリマーまたはリポソーム材料またはミセル材料である、請求項13に記載の方法。
- 全ての前記ナノ粒子(11、12)の前記粒子被覆層(14)は、活性物質分子および/またはリガンド分子が結合できる同じ材料から生成されるものである、請求項11または12に記載の方法。
- 前記ナノ粒子(11、12)は、それぞれ、イリジウム、白金、金、ビスマス、銀、ヨウ素、パラジウム、カドミウムまたはインジウムを含むものである、請求項5乃至15のいずれかに記載の方法。
- 前記ナノ粒子(11、12)はそれぞれ相異なるX線造影剤分子を含むものである、請求項5乃至16のいずれかに記載の方法。
- 各グループのナノ粒子(11、12)は相異なるナノ粒子サイズを有するものである、請求項5乃至17のいずれかに記載の方法。
- - 前記第1のマーカ物質は、第1のX線蛍光元素を含む第1のグループのマーカ分子(15)を含み、
- 前記少なくとも1種の別のマーカ物質は、それぞれ少なくとも1つの別のX線蛍光元素を含む少なくとも1つの別のグループのマーカ分子(16)を含むものである、
請求項5乃至18のいずれかに記載の方法。 - - 前記第1のマーカ物質は、第1のX線蛍光元素を含むナノ粒子(11)を含み、
- 前記少なくとも1種の別のマーカ物質は、それぞれ少なくとも1つの別のX線蛍光元素を含むマーカ分子(15)を含むものである、
請求項5乃至18のいずれかに記載の方法。 - 前記マーカ分子(15、16)は活性物質および/またはリガンド分子に結合され、前記マーカ分子(15、16)は、それぞれ前記第1のX線蛍光元素および前記少なくとも1つの別のX線蛍光元素の中の1つの元素を含むものである、請求項19または20に記載の方法。
- 前記X線蛍光元素が、銀、インジウム、パラジウム、カドミウム、ヨウ素またはバリウムを含むものである、請求項19乃至21のいずれかに記載の方法。
- 前記試料(10)における前記第1のマーカ物質および前記少なくとも1種の別のマーカ物質の空間的分布の時間関数が決定される、請求項1乃至22のいずれかに記載の方法。
- - 前記活性物質は生体細胞を含み、前記第1のマーカ物質および前記少なくとも1種の別のマーカ物質の中の少なくとも1種のマーカ物質が前記生体細胞に結合され、
- 前記第1のマーカ物質および前記少なくとも1種の別のマーカ物質の前記分布を求めることは、前記試料中の前記生体細胞の輸送の検出を含むものである、
請求項1乃至23のいずれかに記載の方法。 - 前記第1のマーカ物質および前記少なくとも1種の別のマーカ物質は、それぞれ異なる方法または経路で前記試料(10)に導入されたものである、請求項1乃至24のいずれかに記載の方法。
- 前記第1のマーカ物質および前記少なくとも1種の別のマーカ物質は、活性物質分子および/またはリガンド分子の結合が考慮されない場合に、前記試料に対して、生物学的、化学的、生理的および/または物理的に同じ効果を有するように形成されるものである、請求項1乃至25のいずれかに記載の方法。
- 請求項1乃至26のいずれかに記載の方法によって試料(10)を調べるためにマルチパラメトリックX線蛍光イメージングを行うよう構成されたイメージング装置(100)であって、
前記試料は、生物有機体の体の少なくとも一部を含み、かつ第1のマーカ物質および少なくとも1種の別のマーカ物質を含み、
前記第1のマーカ物質および前記少なくとも1種の別のマーカ物質の中の少なくとも1種の物質が、前記試料(10)との特定の相互作用のために供給された活性物質分子および/またはリガンド分子に結合され、
- 前記試料(10)にモノクロまたは狭帯域のX線放射線(1)を照射するよう配置されたX線源装置(110)であって、前記第1のマーカ物質および前記少なくとも1種の別のマーカ物質のX線蛍光(2)が励起され、前記第1のマーカ物質および前記少なくとも1種の別のマーカ物質の前記X線蛍光(2)の蛍光線(3)が互いに異なるものであり、前記X線放射線(1)の放射光子エネルギが前記試料(10)中の全ての前記マーカ物質の最高の吸収端から離れた位置にあり、前記位置において同時に前記マーカ物質の前記背景ノイズ・レベルが最小であり前記蛍光確率が互いに近似するものである、X線源装置(110)と、
- 前記第1のマーカ物質および前記少なくとも1種の別のマーカ物質の前記X線蛍光(2)を空間的およびスペクトル的に分解して検出するよう構成された検出器装置(120)と、
- 前記検出されたX線蛍光(2)から、前記試料(10)における、前記第1のマーカ物質の空間的分布と、さらに前記少なくとも1種の別のマーカ物質の空間的分布とを求めるよう構成された評価装置(130)と、
を含む、イメージング装置(100)。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102019128842.8A DE102019128842A1 (de) | 2019-10-25 | 2019-10-25 | Verfahren, Vorrichtung und Markersubstanz-Kit zur multiparametrischen Röntgenfluoreszenz-Bildgebung |
| DE102019128842.8 | 2019-10-25 | ||
| PCT/EP2020/079909 WO2021078950A1 (de) | 2019-10-25 | 2020-10-23 | Verfahren, vorrichtung und markersubstanz-kit zur multiparametrischen röntgenfluoreszenz-bildgebung |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2022553761A JP2022553761A (ja) | 2022-12-26 |
| JPWO2021078950A5 JPWO2021078950A5 (ja) | 2023-10-18 |
| JP7635224B2 true JP7635224B2 (ja) | 2025-02-25 |
Family
ID=73020205
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022524594A Active JP7635224B2 (ja) | 2019-10-25 | 2020-10-23 | マルチパラメトリックx線蛍光イメージングのための方法および装置 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20220370645A1 (ja) |
| EP (1) | EP4049011A1 (ja) |
| JP (1) | JP7635224B2 (ja) |
| KR (1) | KR20220091515A (ja) |
| CN (1) | CN114667447B (ja) |
| DE (1) | DE102019128842A1 (ja) |
| WO (1) | WO2021078950A1 (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN116577358B (zh) * | 2023-05-18 | 2024-01-23 | 杭州宇称电子技术有限公司 | 基于x射线k-吸收边的书画文物颜料成像方法及其应用 |
| CN118961777B (zh) * | 2024-07-19 | 2025-11-28 | 中国科学院金属研究所 | 一种准原位追踪高温合金微量元素分布的方法 |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20060182217A1 (en) | 2003-03-07 | 2006-08-17 | Koninklijke Philips Electronics N.V. | Method and imaging system for imaging the spatial distrubution of an x-ray fluorescence marker |
| JP2010025711A (ja) | 2008-07-17 | 2010-02-04 | Univ Of Tsukuba | 蛍光エックス線検出装置 |
| JP2013204004A (ja) | 2012-03-29 | 2013-10-07 | Konica Minolta Inc | 高輝度半導体ナノ粒子集積体 |
| JP2017095480A (ja) | 2012-04-13 | 2017-06-01 | ユニベルシテ・クロード・ベルナール・リヨン・プルミエ | マルチモーダル造影剤としての超微細ナノ粒子 |
| WO2018189051A1 (de) | 2017-04-11 | 2018-10-18 | Universität Hamburg | Verfahren und messvorrichtung zur röntgenfluoreszenz-messung |
| JP2019183047A (ja) | 2018-04-13 | 2019-10-24 | Agc株式会社 | 蛍光ナノ粒子およびその製造方法 |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20120307962A1 (en) * | 2009-12-16 | 2012-12-06 | Georgia Tech Resarch Corporation | Systems and methods for x-ray fluorescence computed tomography imaging with nanoparticles |
| WO2015031675A1 (en) * | 2013-08-28 | 2015-03-05 | The Regents Of The University Of California | Nanoparticle assisted scanning focusing x-ray fluorescence imaging and enhanced treatment |
| WO2015104225A1 (en) * | 2014-01-07 | 2015-07-16 | Jettec Ab | X-ray micro imaging |
| CN108469445B (zh) * | 2018-03-29 | 2020-09-01 | 福州大学 | 用于无背景检测血液中癌症抗原含量的基于x射线激发的镧系荧光纳米粒子的试剂盒及制备 |
-
2019
- 2019-10-25 DE DE102019128842.8A patent/DE102019128842A1/de not_active Withdrawn
-
2020
- 2020-10-23 US US17/771,460 patent/US20220370645A1/en active Pending
- 2020-10-23 JP JP2022524594A patent/JP7635224B2/ja active Active
- 2020-10-23 CN CN202080074754.5A patent/CN114667447B/zh active Active
- 2020-10-23 KR KR1020227017433A patent/KR20220091515A/ko active Pending
- 2020-10-23 WO PCT/EP2020/079909 patent/WO2021078950A1/de not_active Ceased
- 2020-10-23 EP EP20797446.0A patent/EP4049011A1/de active Pending
Patent Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20060182217A1 (en) | 2003-03-07 | 2006-08-17 | Koninklijke Philips Electronics N.V. | Method and imaging system for imaging the spatial distrubution of an x-ray fluorescence marker |
| JP2006519647A (ja) | 2003-03-07 | 2006-08-31 | コーニンクレッカ フィリップス エレクトロニクス エヌ ヴィ | X線蛍光マーカの空間分布をイメージングする方法及びイメージングシステム |
| JP2010025711A (ja) | 2008-07-17 | 2010-02-04 | Univ Of Tsukuba | 蛍光エックス線検出装置 |
| JP2013204004A (ja) | 2012-03-29 | 2013-10-07 | Konica Minolta Inc | 高輝度半導体ナノ粒子集積体 |
| JP2017095480A (ja) | 2012-04-13 | 2017-06-01 | ユニベルシテ・クロード・ベルナール・リヨン・プルミエ | マルチモーダル造影剤としての超微細ナノ粒子 |
| WO2018189051A1 (de) | 2017-04-11 | 2018-10-18 | Universität Hamburg | Verfahren und messvorrichtung zur röntgenfluoreszenz-messung |
| JP2020516915A (ja) | 2017-04-11 | 2020-06-11 | アクシオム・インサイツ・ゲーエムベーハー | 蛍光x線測定のための方法および測定装置 |
| JP2019183047A (ja) | 2018-04-13 | 2019-10-24 | Agc株式会社 | 蛍光ナノ粒子およびその製造方法 |
Non-Patent Citations (2)
| Title |
|---|
| Liyuan MA et al.,"Multiplexed highly sensitive detections of cancer biomarkers in thermal space using encapsulated phase change nanoparticles",Applied Physics Letters,2009年07月27日,Vol. 95, No. 4,DOI: 10.1063/1.3189082 |
| Mainul HOSSAIN et al.,"Multiplexed biomarker detection using x-ray fluorescence of composition-encoded nanoparticles",Applied Physics Letters,2010年12月27日,Vol. 97, No. 26,DOI: 10.1063/1.3533817 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20220091515A (ko) | 2022-06-30 |
| WO2021078950A1 (de) | 2021-04-29 |
| CN114667447B (zh) | 2025-11-18 |
| US20220370645A1 (en) | 2022-11-24 |
| CN114667447A (zh) | 2022-06-24 |
| EP4049011A1 (de) | 2022-08-31 |
| DE102019128842A1 (de) | 2021-04-29 |
| JP2022553761A (ja) | 2022-12-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN100479753C (zh) | 对x射线荧光标记的空间分布成像的方法和成像系统 | |
| US11583237B2 (en) | Method and measuring apparatus for an X-ray fluorescence measurement | |
| Ahmad et al. | X-ray luminescence and x-ray fluorescence computed tomography: new molecular imaging modalities | |
| US20210000436A1 (en) | Methods for x-ray imaging of a subject using multiple-energy decomposition | |
| US20030082104A1 (en) | Imaging method and imaging apparatus, in particular for small animal imaging | |
| Panta et al. | Element-specific spectral imaging of multiple contrast agents: a phantom study | |
| JP7635224B2 (ja) | マルチパラメトリックx線蛍光イメージングのための方法および装置 | |
| DE10225932B4 (de) | Bildgebendes Verfahren und Vorrichtung zu dessen Durchführung | |
| JP5557266B2 (ja) | 蛍光エックス線検出装置 | |
| CN101495040A (zh) | Ct成像系统 | |
| Lowe et al. | Molecular imaging of pulmonary tuberculosis in an ex-vivo mouse model using spectral photon-counting computed tomography and micro-CT | |
| Vernekohl et al. | X-ray excited fluorescent materials for medical application | |
| Cong et al. | X-ray fluorescence computed tomography with polycapillary focusing | |
| Kumar et al. | Characterization of a polychromatic microfocus X-ray fluorescence imaging setup with metallic contrast agents in a microphysiological tumor model | |
| Lecoq | Detectors in Medicine and Biology | |
| Mesbahi | Imaging properties of Fe3O4@ Au and Fe3O4@ Bi hybrid nanocomposites as contrast agents in spectral X-ray computed tomography: A Monte Carlo simulation study | |
| Zhang | 3D Oxygenation Imaging of Bone Marrow Using X-Ray Luminescence Micro-CT | |
| Moss et al. | Use of Photon Scattering Interactions in Diagnosis and Treatment of Disease | |
| Dong et al. | Improving molecular sensitivity in X-ray fluorescence molecular imaging (XFMI) of iodine distribution in mouse-sized phantoms via excitation spectrum optimization | |
| Cao et al. | X-ray fluorescence molecular imaging with high sensitivity: feasibility study in phantoms | |
| Conceicao et al. | Investigating breast cancer metastasis through collagen remodelling and metal accumulation: an advanced X-ray imaging approach | |
| Fang | Fast and Three-dimensional Focused X-ray Luminescence Tomography | |
| Lowe | MARS molecular imaging: Potential clinical utility of spectral photon-counting computed tomography integrated with nanoparticle technology | |
| Cho | Bernard L. Jones | |
| Moghiseh et al. | Research Article Spectral Photon-Counting Molecular Imaging for Quantification of Monoclonal Antibody-Conjugated Gold Nanoparticles Targeted to Lymphoma and Breast Cancer: An In Vitro Study |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20220822 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20231010 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20231010 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20231010 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20240531 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240604 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20240830 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20241030 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20241204 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20250121 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20250212 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7635224 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |