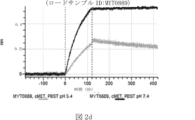
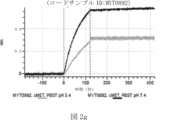
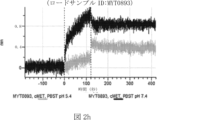
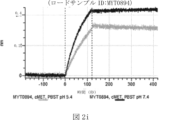
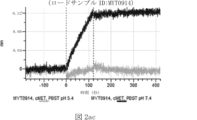
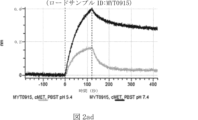
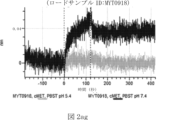
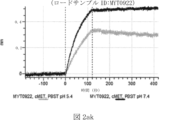
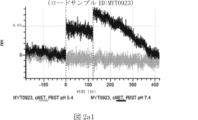
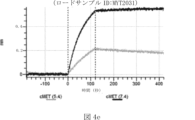
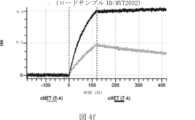
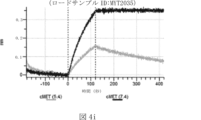
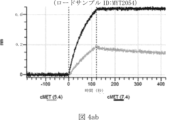
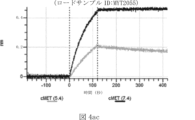
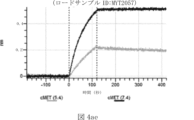
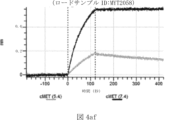
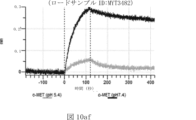
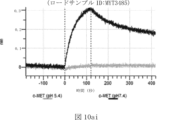
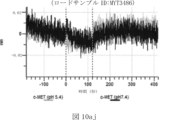
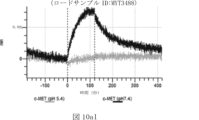
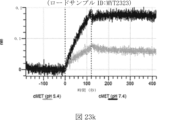
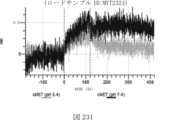
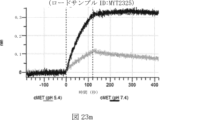
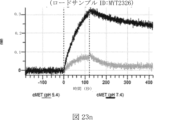
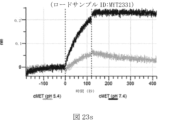
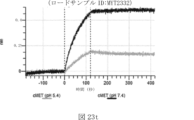
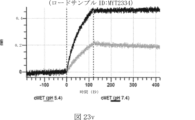
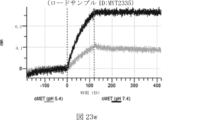
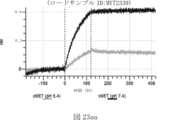
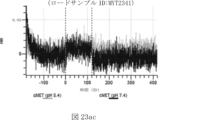
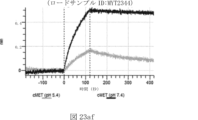
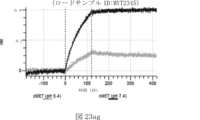
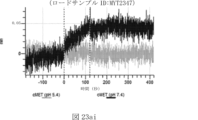
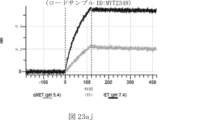
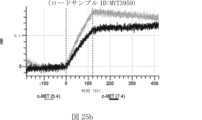
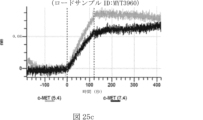
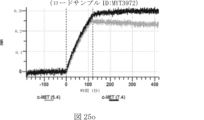
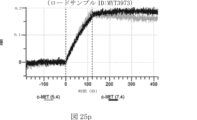
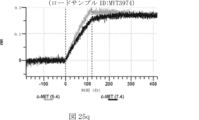
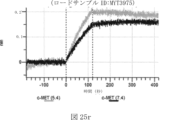
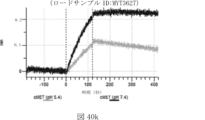
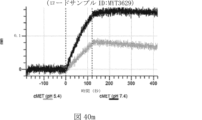
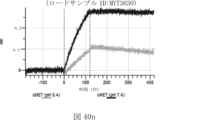
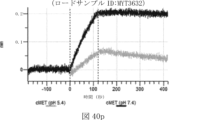
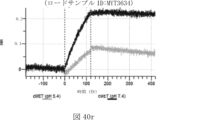
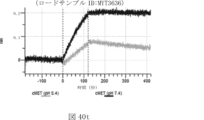
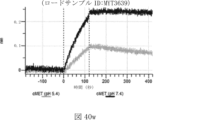
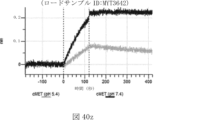
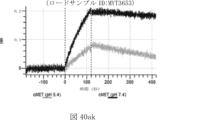
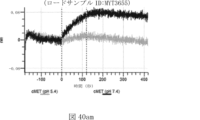
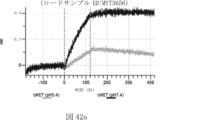
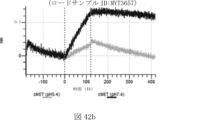
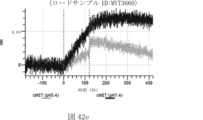
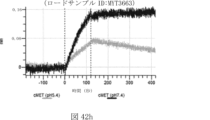
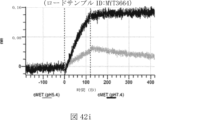
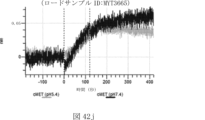
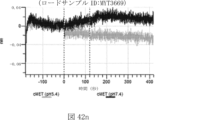
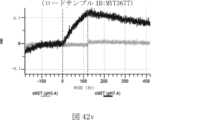
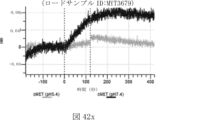
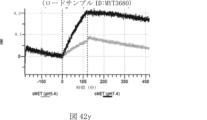
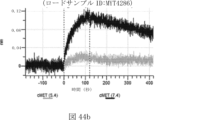
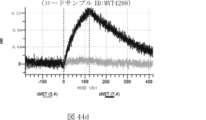
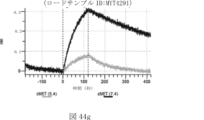
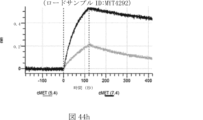
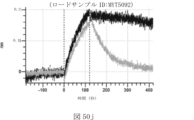
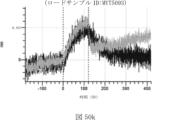
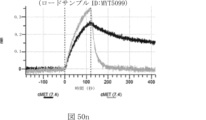
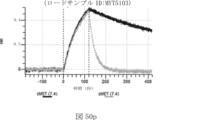
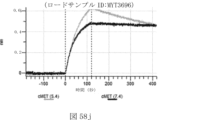
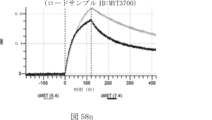
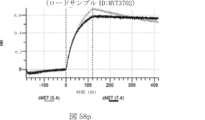
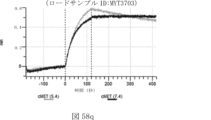
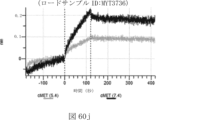
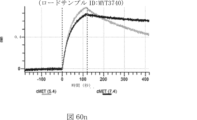
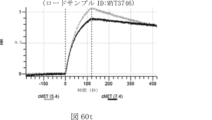
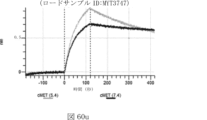
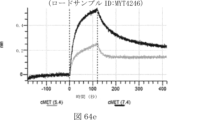
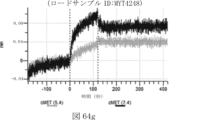
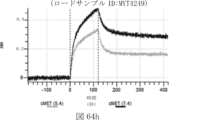
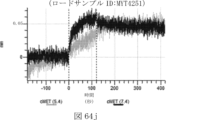
本明細書では、標的哺乳動物細胞の表面に存在するMETまたはMETのエピトープに特異的に結合することができる第一の抗原結合ドメインを含む抗原結合タンパク質構築物(ABPC)であって、(a)pH約4.0~約6.5での第一の抗原結合ドメインの解離速度が、pH約7.0~約8.0での解離速度よりも速い、および/または(b)pH約4.0~約6.5での第一の抗原結合ドメインの解離定数(KD)が、pH約7.0~約8.0でのKDよりも大きいものである、当該抗原結合タンパク質構築物(ABPC)が提供される。これらのABPCの一部の実施例では、ABPCは、標的哺乳動物細胞によるABPCの細胞内移行後に、標的哺乳動物細胞において分解される。本明細書に記載されるいずれかのABPCの一部の実施例は、コンジュゲートされた毒素、放射性同位体、薬剤、または低分子(例えば、フルオロフォアまたは染料)をさらに含み得る。
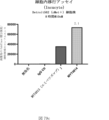
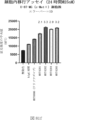
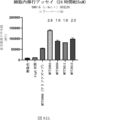
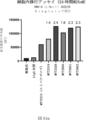
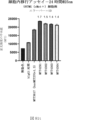
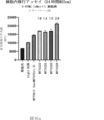
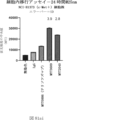
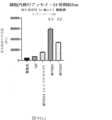
また、標的哺乳動物細胞の表面に存在するMETまたはMETのエピトープに特異的に結合することができる第一の抗原結合ドメイン;およびコンジュゲートされた毒素、放射性同位体、薬剤または低分子を含む抗原結合タンパク質構築物(ABPC)であって、(a)pH約4.0~約6.5での第一の抗原結合ドメインの解離速度が、pH約7.0~約8.0での解離速度よりも速い、および/または、pH約4.0~約6.5での第一の抗原結合ドメインの解離定数(KD)が、pH約7.0~約8.0でのKDよりも大きい、ならびに(b)当該ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞における毒素放出の増加(例えば、検出可能な増加)、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞の殺傷の増加(例えば、検出可能な増加)、および同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞におけるエンドリソソーム送達の増加(例えば、検出可能な増加)、のうちの一つまたは複数(例えば、二つまたは三つ)をもたらす、当該抗原結合タンパク質構築物(ABPC)が提供される。
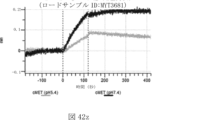
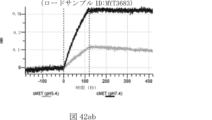
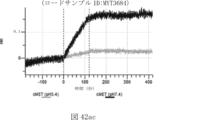
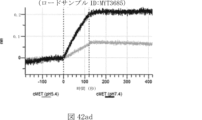
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸がヒスチジンで置換されているテリソツズマブの重鎖可変ドメインを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸がヒスチジンで置換されているテリソツズマブの軽鎖可変ドメインを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸がヒスチジンで置換されているテリソツズマブの重鎖可変ドメインと、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸がヒスチジンで置換されているテリソツズマブの軽鎖可変ドメインとを含む。本明細書に記載のいずれかのABPCの一部の実施例では、テリソツズマブの重鎖可変ドメインは、配列番号1を含む。本明細書に記載のいずれかのABPCの一部の実施例では、テリソツズマブの軽鎖可変ドメインは、配列番号2を含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、それぞれ配列番号3、配列番号4、および配列番号5であるCDR1、CDR2およびCDR3であって、配列番号3~5においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む重鎖可変ドメインを含む。本明細書に記載のいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、それぞれ配列番号6、配列番号7、および配列番号8であるCDR1、CDR2およびCDR3であって、配列番号6~8においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む軽鎖可変ドメインを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、それぞれ配列番号3、配列番号4、および配列番号5であるCDR1、CDR2およびCDR3であって、配列番号3~5においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む重鎖可変ドメインと、それぞれ配列番号6、配列番号7、および配列番号8であるCDR1、CDR2およびCDR3であって、配列番号6~8においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号1と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインを含み、重鎖可変ドメインは、26、27、28、29、32、97、98、99、100、101、102、103および107からなる群から選択される配列番号1の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号2と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインを含み、軽鎖可変ドメインは、25、28、29、30、31、32、34、35、36、37、54、55、59、60、95、99および101からなる群から選択される配列番号2の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号1と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、26、27、28、29、32、97、98、99、100、101、102、103および107からなる群から選択される配列番号1の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含む、当該重鎖可変ドメインと、配列番号2と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインであって、25、28、29、30、31、32、34、35、36、37、54、55、59、60、95、99および101からなる群から選択される配列番号2の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含む、当該軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、重鎖可変ドメインは、配列番号1と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインを含み、重鎖可変ドメインは、表1に列挙された配列番号1の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、軽鎖可変ドメインは、配列番号2と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインを含み、軽鎖可変ドメインは、表2に列挙される配列番号2の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む。
本明細書に記載されるABPCのいずれかの一部の例では、第一の抗原結合ドメインは、配列番号2と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインを含み、軽鎖可変ドメインは、配列番号2の38位にアラニンを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号2と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインであって、配列番号2の38位にアラニンを含む、当該軽鎖可変ドメインと、配列番号1と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、26、27、28、29、32、97、98、99、100、101、102、103および107からなる群から選択される配列番号1の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号2と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインを含み、軽鎖可変ドメインは、25、28、29、30、31、32、34、35、36、37、54、55、59、60、95、99および101からなる群から選択される配列番号2の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含み、軽鎖可変ドメインは、配列番号2の38位にアラニンを含む。 本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号2と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインであって、25、28、29、30、31、32、34、35、36、37、54、55、59、60、95、99および101からなる群から選択される配列番号2の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含み、配列番号2の38位にアラニンを含む、当該軽鎖可変ドメインと、配列番号1と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、26、27、28、29、32、97、98、99、100、101、102、103および107からなる群から選択される配列番号1の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、軽鎖可変ドメインは、配列番号2と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインを含み、軽鎖可変ドメインは、表2に列挙された配列番号2の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含み、軽鎖可変ドメインは、配列番号2の38位にアラニンを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号1と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表1に列挙された配列番号1の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインと、配列番号2と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインであって、表2に列挙された配列番号2の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号2を含む軽鎖可変ドメインと、配列番号1と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表1に列挙された配列番号1のつまたは複数(例えば、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2の25位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号1と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表1に列挙された配列番号1の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2の28位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号1と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表1に列挙された配列番号1の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2の29位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号1と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表1に列挙された配列番号1の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2の30位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号1と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表1に列挙された配列番号1の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2の31位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号1と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表1に列挙された配列番号1の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2の32位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号1と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表1に列挙された配列番号1の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2の34位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号1と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表1に列挙された配列番号1の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2の35位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号1と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表1に列挙された配列番号1の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2の36位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号1と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表1に列挙された配列番号1の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2の37位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号1と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表1に列挙された配列番号1の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2の54位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号1と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表1に列挙された配列番号1の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2の55位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号1と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表1に列挙された配列番号1の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2の59位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号1と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表1に列挙された配列番号1の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2の60位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号1と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表1に列挙された配列番号1の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2の95位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号1と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表1に列挙された配列番号1の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2の99位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号1と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表1に列挙された配列番号1の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2の101位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号1と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表1に列挙された配列番号1の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインが、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2の38位にアラニンを含む、当該軽鎖可変ドメインと、配列番号1と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表1に列挙された配列番号1の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のヒスチジンがアラニンで置換されているものであるテリソツズマブの重鎖可変ドメインを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のヒスチジンがアラニンで置換されているものであるテリソツズマブの軽鎖可変ドメインを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のヒスチジンがアラニンで置換されたものであるテリソツズマブの重鎖可変ドメインと、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のヒスチジンがアラニンで置換されているものであるテリソツズマブの軽鎖可変ドメインとを含む。本明細書に記載のいずれかのABPCの一部の実施例では、テリソツズマブの重鎖可変ドメインは、配列番号1を含む。 本明細書に記載のいずれかのABPCの一部の実施例では、テリソツズマブの軽鎖可変ドメインは、配列番号2を含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、それぞれ配列番号3、配列番号4、および配列番号5であるCDR1、CDR2およびCDR3であって、配列番号3~5においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のヒスチジンがアラニンで置換されているものである当該CDR1、CDR2およびCDR3を含む重鎖可変ドメインを含む。本明細書に記載のいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、それぞれ配列番号6、配列番号7、および配列番号8であるCDR1、CDR2およびCDR3であって、配列番号6~8においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のヒスチジンがアラニンで置換されているものである当該CDR1、CDR2およびCDR3を含む軽鎖可変ドメインを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、それぞれ配列番号3、配列番号4、および配列番号5であるCDR1、CDR2およびCDR3であって、配列番号3~5においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のヒスチジンがアラニンで置換されているものである当該CDR1、CDR2およびCDR3を含む重鎖可変ドメインと、それぞれ配列番号6、配列番号7、および配列番号8であるCDR1、CDR2およびCDR3であって、配列番号6~8においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のヒスチジンがアラニンで置換されているものである当該CDR1、CDR2およびCDR3を含む軽鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50の重鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81の軽鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号2を含む軽鎖可変ドメインと、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号51を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号52を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号53を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号54を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号55を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号56を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号57を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号58を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号59を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号60を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号61を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号62を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号63を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号64を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号65を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号66を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号67を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号68を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号69を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号70を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号71を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号72を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号73を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号74を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号75を含む軽鎖可変ドメインと、: 配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号76を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号77を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号78を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号79を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号80を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号81を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、または配列番号50を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号82、配列番号83、配列番号84、配列番号85、配列番号86、配列番号87、配列番号88、配列番号89、配列番号90、配列番号91、配列番号92、配列番号93、配列番号94、配列番号95、配列番号96、配列番号97、配列番号98、配列番号99、配列番号100、配列番号101、配列番号102、配列番号103、配列番号104、配列番号105、配列番号106、配列番号107、配列番号108、配列番号109、配列番号110、配列番号111、配列番号112、配列番号113、配列番号114、配列番号115、配列番号116、配列番号117、配列番号118、配列番号119、配列番号120、配列番号121、配列番号122、配列番号123、配列番号124、配列番号125、配列番号126、配列番号127、配列番号128、配列番号129、または配列番号130を含む重鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号82を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号83を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号84を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号85を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号86を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号87を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号88を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号89を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号90を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号91を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号92を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号93を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号94を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号95を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号96を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号97を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号98を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号99を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号100を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号101を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号102を含む重鎖可変ドメインと、comprising 配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号103を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号104を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号105を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号106を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号107を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号108を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号109を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号110を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載のいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号111を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号112を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号113を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号114を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号115を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号116を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号117を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号118を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号119を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号120を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号121を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号122を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号123を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号124を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号125を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号126を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号127を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号128を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号129を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号130を含む重鎖可変ドメインと、配列番号2、配列番号51、配列番号52、配列番号53、配列番号54、配列番号55、配列番号56、配列番号57、配列番号58、配列番号59、配列番号60、配列番号61、配列番号62、配列番号63、配列番号64、配列番号65、配列番号66、配列番号67、配列番号68、配列番号69、配列番号70、配列番号71、配列番号72、配列番号73、配列番号74、配列番号75、配列番号76、配列番号77、配列番号78、配列番号79、配列番号80、または配列番号81を含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号131、配列番号132、配列番号133、配列番号134、配列番号135、配列番号136、配列番号137、配列番号138、配列番号139、配列番号140、配列番号141、配列番号142、配列番号143、配列番号144、または 配列番号145を含む軽鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号131を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、配列番号50、配列番号82、配列番号83、配列番号84、配列番号85、配列番号86、配列番号87、配列番号88、配列番号89、配列番号90、配列番号91、配列番号92、配列番号93、配列番号94、配列番号95、配列番号96、配列番号97、配列番号98、配列番号99、配列番号100、配列番号101、配列番号102、配列番号103、配列番号104、配列番号105、配列番号106、配列番号107、配列番号108、配列番号109、配列番号110、配列番号111、配列番号112、配列番号113、配列番号114、配列番号115、配列番号116、配列番号117、配列番号118、配列番号119、配列番号120、配列番号121、配列番号122、配列番号123、配列番号124、配列番号125、配列番号126、配列番号127、配列番号128、配列番号129、または配列番号130を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号132を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、配列番号50、配列番号82、配列番号83、配列番号84、配列番号85、配列番号86、配列番号87、配列番号88、配列番号89、配列番号90、配列番号91、配列番号92、配列番号93、配列番号94、配列番号95、配列番号96、配列番号97、配列番号98、配列番号99、配列番号100、配列番号101、配列番号102、配列番号103、配列番号104、配列番号105、配列番号106、配列番号107、配列番号108、配列番号109、配列番号110、配列番号111、配列番号112、配列番号113、配列番号114、配列番号115、配列番号116、配列番号117、配列番号118、配列番号119、配列番号120、配列番号121、配列番号122、配列番号123、配列番号124、配列番号125、配列番号126、配列番号127、配列番号128、配列番号129、または配列番号130を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号133を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、配列番号50、配列番号82、配列番号83、配列番号84、配列番号85、配列番号86、配列番号87、配列番号88、配列番号89、配列番号90、配列番号91、配列番号92、配列番号93、配列番号94、配列番号95、配列番号96、配列番号97、配列番号98、配列番号99、配列番号100、配列番号101、配列番号102、配列番号103、配列番号104、配列番号105、配列番号106、配列番号107、配列番号108、配列番号109、配列番号110、配列番号111、配列番号112、配列番号113、配列番号114、配列番号115、配列番号116、配列番号117、配列番号118、配列番号119、配列番号120、配列番号121、配列番号122、配列番号123、配列番号124、配列番号125、配列番号126、配列番号127、配列番号128、配列番号129、または配列番号130を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号134を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、配列番号50、配列番号82、配列番号83、配列番号84、配列番号85、配列番号86、配列番号87、配列番号88、配列番号89、配列番号90、配列番号91、配列番号92、配列番号93、配列番号94、配列番号95、配列番号96、配列番号97、配列番号98、配列番号99、配列番号100、配列番号101、配列番号102、配列番号103、配列番号104、配列番号105、配列番号106、配列番号107、配列番号108、配列番号109、配列番号110、配列番号111、配列番号112、配列番号113、配列番号114、配列番号115、配列番号116、配列番号117、配列番号118、配列番号119、配列番号120、配列番号121、配列番号122、配列番号123、配列番号124、配列番号125、配列番号126、配列番号127、配列番号128、配列番号129、または配列番号130を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号135を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、配列番号50、配列番号82、配列番号83、配列番号84、配列番号85、配列番号86、配列番号87、配列番号88、配列番号89、配列番号90、配列番号91、配列番号92、配列番号93、配列番号94、配列番号95、配列番号96、配列番号97、配列番号98、配列番号99、配列番号100、配列番号101、配列番号102、配列番号103、配列番号104、配列番号105、配列番号106、配列番号107、配列番号108、配列番号109、配列番号110、配列番号111、配列番号112、配列番号113、配列番号114、配列番号115、配列番号116、配列番号117、配列番号118、配列番号119、配列番号120、配列番号121、配列番号122、配列番号123、配列番号124、配列番号125、配列番号126、配列番号127、配列番号128、配列番号129、または配列番号130を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号136を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、配列番号50、配列番号82、配列番号83、配列番号84、配列番号85、配列番号86、配列番号87、配列番号88、配列番号89、配列番号90、配列番号91、配列番号92、配列番号93、配列番号94、配列番号95、配列番号96、配列番号97、配列番号98、配列番号99、配列番号100、配列番号101、配列番号102、配列番号103、配列番号104、配列番号105、配列番号106、配列番号107、配列番号108、配列番号109、配列番号110、配列番号111、配列番号112、配列番号113、配列番号114、配列番号115、配列番号116、配列番号117、配列番号118、配列番号119、配列番号120、配列番号121、配列番号122、配列番号123、配列番号124、配列番号125、配列番号126、配列番号127、配列番号128、配列番号129、または配列番号130を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号137を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、配列番号50、配列番号82、配列番号83、配列番号84、配列番号85、配列番号86、配列番号87、配列番号88、配列番号89、配列番号90、配列番号91、配列番号92、配列番号93、配列番号94、配列番号95、配列番号96、配列番号97、配列番号98、配列番号99、配列番号100、配列番号101、配列番号102、配列番号103、配列番号104、配列番号105、配列番号106、配列番号107、配列番号108、配列番号109、配列番号110、配列番号111、配列番号112、配列番号113、配列番号114、配列番号115、配列番号116、配列番号117、配列番号118、配列番号119、配列番号120、配列番号121、配列番号122、配列番号123、配列番号124、配列番号125、配列番号126、配列番号127、配列番号128、配列番号129、または配列番号130を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号138を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、配列番号50、配列番号82、配列番号83、配列番号84、配列番号85、配列番号86、配列番号87、配列番号88、配列番号89、配列番号90、配列番号91、配列番号92、配列番号93、配列番号94、配列番号95、配列番号96、配列番号97、配列番号98、配列番号99、配列番号100、配列番号101、配列番号102、配列番号103、配列番号104、配列番号105、配列番号106、配列番号107、配列番号108、配列番号109、配列番号110、配列番号111、配列番号112、配列番号113、配列番号114、配列番号115、配列番号116、配列番号117、配列番号118、配列番号119、配列番号120、配列番号121、配列番号122、配列番号123、配列番号124、配列番号125、配列番号126、配列番号127、配列番号128、配列番号129、または配列番号130を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号139を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、配列番号50、配列番号82、配列番号83、配列番号84、配列番号85、配列番号86、配列番号87、配列番号88、配列番号89、配列番号90、配列番号91、配列番号92、配列番号93、配列番号94、配列番号95、配列番号96、配列番号97、配列番号98、配列番号99、配列番号100、配列番号101、配列番号102、配列番号103、配列番号104、配列番号105、配列番号106、配列番号107、配列番号108、配列番号109、配列番号110、配列番号111、配列番号112、配列番号113、配列番号114、配列番号115、配列番号116、配列番号117、配列番号118、配列番号119、配列番号120、配列番号121、配列番号122、配列番号123、配列番号124、配列番号125、配列番号126、配列番号127、配列番号128、配列番号129、または配列番号130を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号140を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、配列番号50、配列番号82、配列番号83、配列番号84、配列番号85、配列番号86、配列番号87、配列番号88、配列番号89、配列番号90、配列番号91、配列番号92、配列番号93、配列番号94、配列番号95、配列番号96、配列番号97、配列番号98、配列番号99、配列番号100、配列番号101、配列番号102、配列番号103、配列番号104、配列番号105、配列番号106、配列番号107、配列番号108、配列番号109、配列番号110、配列番号111、配列番号112、配列番号113、配列番号114、配列番号115、配列番号116、配列番号117、配列番号118、配列番号119、配列番号120、配列番号121、配列番号122、配列番号123、配列番号124、配列番号125、配列番号126、配列番号127、配列番号128、配列番号129、または配列番号130を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号141を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、配列番号50、配列番号82、配列番号83、配列番号84、配列番号85、配列番号86、配列番号87、配列番号88、配列番号89、配列番号90、配列番号91、配列番号92、配列番号93、配列番号94、配列番号95、配列番号96、配列番号97、配列番号98、配列番号99、配列番号100、配列番号101、配列番号102、配列番号103、配列番号104、配列番号105、配列番号106、配列番号107、配列番号108、配列番号109、配列番号110、配列番号111、配列番号112、配列番号113、配列番号114、配列番号115、配列番号116、配列番号117、配列番号118、配列番号119、配列番号120、配列番号121、配列番号122、配列番号123、配列番号124、配列番号125、配列番号126、配列番号127、配列番号128、配列番号129、または配列番号130を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号142を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、配列番号50、配列番号82、配列番号83、配列番号84、配列番号85、配列番号86、配列番号87、配列番号88、配列番号89、配列番号90、配列番号91、配列番号92、配列番号93、配列番号94、配列番号95、配列番号96、配列番号97、配列番号98、配列番号99、配列番号100、配列番号101、配列番号102、配列番号103、配列番号104、配列番号105、配列番号106、配列番号107、配列番号108、配列番号109、配列番号110、配列番号111、配列番号112、配列番号113、配列番号114、配列番号115、配列番号116、配列番号117、配列番号118、配列番号119、配列番号120、配列番号121、配列番号122、配列番号123、配列番号124、配列番号125、配列番号126、配列番号127、配列番号128、配列番号129、または配列番号130を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号143を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、配列番号50、配列番号82、配列番号83、配列番号84、配列番号85、配列番号86、配列番号87、配列番号88、配列番号89、配列番号90、配列番号91、配列番号92、配列番号93、配列番号94、配列番号95、配列番号96、配列番号97、配列番号98、配列番号99、配列番号100、配列番号101、配列番号102、配列番号103、配列番号104、配列番号105、配列番号106、配列番号107、配列番号108、配列番号109、配列番号110、配列番号111、配列番号112、配列番号113、配列番号114、配列番号115、配列番号116、配列番号117、配列番号118、配列番号119、配列番号120、配列番号121、配列番号122、配列番号123、配列番号124、配列番号125、配列番号126、配列番号127、配列番号128、配列番号129、または配列番号130を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号144を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、配列番号50、配列番号82、配列番号83、配列番号84、配列番号85、配列番号86、配列番号87、配列番号88、配列番号89、配列番号90、配列番号91、配列番号92、配列番号93、配列番号94、配列番号95、配列番号96、配列番号97、配列番号98、配列番号99、配列番号100、配列番号101、配列番号102、配列番号103、配列番号104、配列番号105、配列番号106、配列番号107、配列番号108、配列番号109、配列番号110、配列番号111、配列番号112、配列番号113、配列番号114、配列番号115、配列番号116、配列番号117、配列番号118、配列番号119、配列番号120、配列番号121、配列番号122、配列番号123、配列番号124、配列番号125、配列番号126、配列番号127、配列番号128、配列番号129、または配列番号130を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号145を含む軽鎖可変ドメインと、配列番号1、配列番号13、配列番号14、配列番号15、配列番号16、配列番号17、配列番号18、配列番号19、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28、配列番号29、配列番号30、配列番号31、配列番号32、配列番号33、配列番号34、配列番号35、配列番号36、配列番号37、配列番号38、配列番号39、配列番号40、配列番号41、配列番号42、配列番号43、配列番号44、配列番号45、配列番号46、配列番号47、配列番号48、配列番号49、配列番号50、配列番号82、配列番号83、配列番号84、配列番号85、配列番号86、配列番号87、配列番号88、配列番号89、配列番号90、配列番号91、配列番号92、配列番号93、配列番号94、配列番号95、配列番号96、配列番号97、配列番号98、配列番号99、配列番号100、配列番号101、配列番号102、配列番号103、配列番号104、配列番号105、配列番号106、配列番号107、配列番号108、配列番号109、配列番号110、配列番号111、配列番号112、配列番号113、配列番号114、配列番号115、配列番号116、配列番号117、配列番号118、配列番号119、配列番号120、配列番号121、配列番号122、配列番号123、配列番号124、配列番号125、配列番号126、配列番号127、配列番号128、配列番号129、または配列番号130を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸がヒスチジンで置換されているエミベツズマブの重鎖可変ドメインを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸がヒスチジンで置換されているエミベツズマブの軽鎖可変ドメインを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸がヒスチジンで置換されているエミベツズマブの重鎖可変ドメインと、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸がヒスチジンで置換されているエミベツズマブの軽鎖可変ドメインとを含む。本明細書に記載のいずれかのABPCの一部の実施例では、エミベツズマブの重鎖可変ドメインは、配列番号146を含む。本明細書に記載のいずれかのABPCの一部の実施例では、エミベツズマブの軽鎖可変ドメインは、配列番号147を含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、それぞれ配列番号148、配列番号149、および配列番号150であるCDR1、CDR2およびCDR3であって、配列番号148~150においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む重鎖可変ドメインを含む。本明細書に記載のいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、それぞれ配列番号151、配列番号152、および配列番号153であるCDR1、CDR2およびCDR3であって、配列番号151~153においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む軽鎖可変ドメインを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、それぞれ配列番号148、配列番号149、および配列番号150であるCDR1、CDR2およびCDR3であって、配列番号148~150においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む重鎖可変ドメインと、それぞれ配列番号151、配列番号152、および配列番号153であるCDR1、CDR2およびCDR3であって、配列番号151~153においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む軽鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号146と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインを含み、重鎖可変ドメインは、31、50、51、52、53、54、56、57、59、98、99、100および103からなる群から選択される配列番号146の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号147と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインを含み、軽鎖可変ドメインは、25、26、29、32、33、51、91、92、95、96および97からなる群から選択される配列番号147の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号146と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、31、50、51、52、53、54、56、57、59、98、99、100および103からなる群から選択される配列番号146の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含む、当該重鎖可変ドメインと、配列番号147と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインであって、25、26、29、32、33、51、91、92、95、96および97からなる群から選択される配列番号147の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含む、当該軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、重鎖可変ドメインは、配列番号146と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインを含み、重鎖可変ドメインは表3に列挙された配列番号146の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、軽鎖可変ドメインは、配列番号147と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインを含み、軽鎖可変ドメインは表4に列挙された配列番号147の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号147と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインを含み、軽鎖可変ドメインは、配列番号147の35位にアラニンを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号147と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインであって、配列番号147の35位にアラニンを含む、当該軽鎖可変ドメインと、配列番号146と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、31、50、51、52、53、54、56、57、59、98、99、100および103からなる群から選択される配列番号146の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号147と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインを含み、軽鎖可変ドメインは、25、26、29、32、33、51、91、92、95、96および97からなる群から選択される配列番号147の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含み、軽鎖可変ドメインは、配列番号147の35位にアラニンを含む。 本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号147と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインであって、25、26、29、32、33、51、91、92、95、96および97からなる群から選択される配列番号147の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含み、配列番号147の35位にアラニンを含む、当該軽鎖可変ドメインと、配列番号146と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、31、50、51、52、53、54、56、57、59、98、99、100および103からなる群から選択される配列番号146の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、軽鎖可変ドメインは、配列番号147と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインを含み、軽鎖可変ドメインは、表4に列挙された配列番号147の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含み、軽鎖可変ドメインは、配列番号147の35位にアラニンを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号146と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表3に列挙された配列番号146の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインと、配列番号147と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインであって、表4に列挙された配列番号147の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号147を含む軽鎖可変ドメインと、配列番号146と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表3に列挙された配列番号146の一または複数(例えば、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号147と少なくとも90%同一である軽鎖可変ドメインであって、配列番号147の25位にヒスチジンを含む軽鎖可変ドメインと、配列番号146と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表3に列挙された配列番号146の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号147と少なくとも90%同一である軽鎖可変ドメインであって、配列番号147の26位にヒスチジンを含む軽鎖可変ドメインと、配列番号146と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表3に列挙された配列番号146の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号147と少なくとも90%同一である軽鎖可変ドメインであって、配列番号147の29位にヒスチジンを含む軽鎖可変ドメインと、配列番号146と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表3に列挙された配列番号146の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号147と少なくとも90%同一である軽鎖可変ドメインであって、配列番号147の32位にヒスチジンを含む軽鎖可変ドメインと、配列番号146と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表3に列挙された配列番号146の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号147と少なくとも90%同一である軽鎖可変ドメインであって、配列番号147の33位にヒスチジンを含む軽鎖可変ドメインと、配列番号146と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表3に列挙された配列番号146の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号147と少なくとも90%同一である軽鎖可変ドメインであって、配列番号147の51位にヒスチジンを含む軽鎖可変ドメインと、配列番号146と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表3に列挙された配列番号146の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号147と少なくとも90%同一である軽鎖可変ドメインであって、配列番号147の91位にヒスチジンを含む軽鎖可変ドメインと、配列番号146と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表3に列挙された配列番号146の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号147と少なくとも90%同一である軽鎖可変ドメインであって、配列番号147の92位にヒスチジンを含む軽鎖可変ドメインと、配列番号146と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表3に列挙された配列番号146の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号147と少なくとも90%同一である軽鎖可変ドメインであって、配列番号147の95位にヒスチジンを含む軽鎖可変ドメインと、配列番号146と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表3に列挙された配列番号146の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号147と少なくとも90%同一である軽鎖可変ドメインであって、配列番号147の96位にヒスチジンを含む軽鎖可変ドメインと、配列番号146と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表3に列挙された配列番号146の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号147と少なくとも90%同一である軽鎖可変ドメインであって、配列番号147の97位にヒスチジンを含む軽鎖可変ドメインと、配列番号146と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表3に列挙された配列番号146の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号147と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2の35位にアラニンを含む軽鎖可変ドメインと、配列番号146と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表3に列挙された配列番号146の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のヒスチジンがアラニンで置換されているものであるエミベツズマブの重鎖可変ドメインを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のヒスチジンがアラニンで置換されているものであるエミベツズマブの軽鎖可変ドメインを含む。本明細書に記載されるABPCのいずれかの一部の実施例では、第一の抗原結合ドメインは、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のヒスチジンがアラニンで置換されているものであるエミベツズマブの重鎖可変ドメインと、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のヒスチジンがアラニンで置換されているものであるエミベツズマブの軽鎖可変ドメインとを含む。本明細書に記載のいずれかのABPCの一部の実施例では、エミベツズマブの重鎖可変ドメインは、配列番号146を含む。 本明細書に記載のいずれかのABPCの一部の実施例では、エミベツズマブの軽鎖可変ドメインは、配列番号147を含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、それぞれ配列番号148、配列番号149、および配列番号150であるCDR1、CDR2およびCDR3であって、配列番号148~150においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のヒスチジンがアラニンで置換されているものである当該CDR1、CDR2およびCDR3を含む重鎖可変ドメインを含む。本明細書に記載のいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、それぞれ配列番号151、配列番号152、および配列番号153であるCDR1、CDR2およびCDR3であって、配列番号151~153においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のヒスチジンがアラニンで置換されているものである当該CDR1、CDR2およびCDR3を含む軽鎖可変ドメインを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、それぞれ配列番号148、配列番号149、および配列番号150であるCDR1、CDR2およびCDR3であって、配列番号148~150においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のヒスチジンがアラニンで置換されているものである当該CDR1、CDR2およびCDR3を含む重鎖可変ドメインと、それぞれ配列番号151、配列番号152、および配列番号153であるCDR1、CDR2およびCDR3であって、配列番号151~153においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のヒスチジンがアラニンで置換されているものである当該CDR1、CDR2およびCDR3を含む軽鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188の重鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号147、配列番号189、配列番号190、配列番号191、配列番号192、配列番号193、配列番号194、配列番号195、配列番号196、配列番号197、配列番号198、配列番号199、配列番号200、配列番号201、配列番号202、配列番号203、配列番号204、配列番号205、配列番号206、配列番号207、配列番号208、配列番号209、配列番号210、配列番号211、配列番号212、配列番号213、配列番号214、配列番号215、または配列番号216の軽鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号147を含む軽鎖可変ドメインと、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号189を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号190を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号191を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号192を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号193を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号194を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号195を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号196を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号197を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号198を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号199を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号200を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号201を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号202を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号203を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号204を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号205を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号206を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号207を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号208を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号209を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号210を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号211を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号212を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号213を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号214を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号215を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号216を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、または配列番号188を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号147を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号189を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号190を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号191を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号192を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号193を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号194を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号195を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号196を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号197を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号198を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号199を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号200を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号201を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号202を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号203を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号204を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号205を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号206を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号207を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号208を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号209を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号210を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号211を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号212を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号213および配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む軽鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号214を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号215を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号216を含む軽鎖可変ドメインと、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号284、配列番号285、配列番号286、配列番号287、配列番号288、配列番号289、配列番号290、配列番号291、配列番号292、配列番号293、配列番号294、配列番号295、配列番号296、配列番号297、配列番号298、配列番号299、配列番号300、配列番号301、配列番号302、または配列番号303を含む軽鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号284を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、配列番号188、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号285を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、配列番号188、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号286を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、配列番号188、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号287を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、配列番号188、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号288を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、配列番号188、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号289を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、配列番号188、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号290を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、配列番号188、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号291を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、配列番号188、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号292を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、配列番号188、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号293を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、配列番号188、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号294を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、配列番号188、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号295を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、配列番号188、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号296を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、配列番号188、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号297を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、配列番号188、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号298を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、配列番号188、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号299を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、配列番号188、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載のいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号300を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、配列番号188、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号301を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、配列番号188、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号302を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、配列番号188、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号303を含む軽鎖可変ドメインと、配列番号146、配列番号154、配列番号155、配列番号156、配列番号157、配列番号158、配列番号159、配列番号160、配列番号161、配列番号162、配列番号163、配列番号164、配列番号165、配列番号166、配列番号167、配列番号168、配列番号169、配列番号170、配列番号171、配列番号172、配列番号173、配列番号174、配列番号175、配列番号176、配列番号177、配列番号178、配列番号179、配列番号180、配列番号181、配列番号182、配列番号183、配列番号184、配列番号185、配列番号186、配列番号187、配列番号188、配列番号217、配列番号218、配列番号219、配列番号220、配列番号221、配列番号222、配列番号223、配列番号224、配列番号225、配列番号226、配列番号227、配列番号228、配列番号229、配列番号230、配列番号231、配列番号232、配列番号233、配列番号234、配列番号235、配列番号236、配列番号237、配列番号238、配列番号239、配列番号240、配列番号241、配列番号242、配列番号243、配列番号244、配列番号245、配列番号246、配列番号247、配列番号248、配列番号249、配列番号250、配列番号251、配列番号252、配列番号253、配列番号254、配列番号255、配列番号256、配列番号257、配列番号258、配列番号259、配列番号260、配列番号261、配列番号262、配列番号263、配列番号264、配列番号265、配列番号266、配列番号267、配列番号268、配列番号269、配列番号270、配列番号271、配列番号272、配列番号273、配列番号274、配列番号275、配列番号276、配列番号277、配列番号278、配列番号279、配列番号280、配列番号281、配列番号282、または配列番号283を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸がヒスチジンで置換されているhucMET27Gv1.3の重鎖可変ドメインを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸がヒスチジンで置換されているhucMET27Gv1.3の軽鎖可変ドメインを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸がヒスチジンで置換されているhucMET27Gv1.3の重鎖可変ドメインと、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸がヒスチジンで置換されているhucMET27Gv1.3の軽鎖可変ドメインとを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、hucMET27Gv1.3の重鎖可変ドメインは、配列番号304を含む。本明細書に記載されるいずれかのABPCの一部の実施例では、hucMET27Gv1.3の軽鎖可変ドメインは、配列番号305を含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、それぞれ配列番号306、配列番号307、および配列番号308であるCDR1、CDR2およびCDR3であって、配列番号306~308においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む重鎖可変ドメインを含む。本明細書に記載のいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、それぞれ配列番号309、配列番号310、および配列番号311であるCDR1、CDR2およびCDR3であって、配列番号309~311においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む軽鎖可変ドメインを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、それぞれ配列番号306、配列番号307、および配列番号308であるCDR1、CDR2およびCDR3であって、配列番号306~308においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む重鎖可変ドメインと、それぞれ配列番号309、配列番号310、および配列番号311であるCDR1、CDR2およびCDR3であって、配列番号309~311においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む軽鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号304と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインを含み、重鎖可変ドメインは、27、34、35、50、51、52、54、55、56、57、58、59、60、61、62、63、64、65、98、99、103および105からなる群から選択される配列番号304の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置においてヒスチジンを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号305と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインを含み、軽鎖可変ドメインは、26、30、31、34、36、54、56、57、60、93、95、99および101からなる群から選択される配列番号305の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号304と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、27、34、35、50、51、52、54、55、56、57、58、59、60、61、62、63、64、65、98、99、103および105からなる群から選択される配列番号304の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含む、当該重鎖可変ドメインと、配列番号305と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインであって、26、30、31、34、36、54、56、57、60、93、95、99および101からなる群から選択される配列番号305の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含む、当該軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、重鎖可変ドメインは、配列番号304と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインを含み、重鎖可変ドメインは、表5に列挙された配列番号304の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、軽鎖可変ドメインは、配列番号305と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインを含み、軽鎖可変ドメインは、表6に列挙される配列番号305の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む。
本明細書に記載されるABPCのいずれかの一部の例では、第一の抗原結合ドメインは、配列番号305と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインを含み、軽鎖可変ドメインは、配列番号305の38位にアラニンを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号305と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインであって、配列番号305の38位にアラニンを含む、当該軽鎖可変ドメインと、配列番号304と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、27、34、35、50、51、52、54、55、56、57、58、59、60、61、62、63、64、65、98、99、103および105からなる群から選択される配列番号304の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号305と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインを含み、軽鎖可変ドメインは、27、34、35、50、51、52、54、55、56、57、58、59、60、61、62、63、64、65、98、99、103および105からなる群から選択される配列番号305の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含み、軽鎖可変ドメインは、配列番号305の38位にアラニンを含む。 本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号305と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインであって、26、30、31、34、36、54、56、57、60、93、95、99および101からなる群から選択される配列番号305の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含み、配列番号305の38位にアラニンを含む、当該軽鎖可変ドメインと、配列番号304と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、27、34、35、50、51、52、54、55、56、57、58、59、60、61、62、63、64、65、98、99、103および105からなる群から選択される配列番号304の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、軽鎖可変ドメインは、配列番号305と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインを含み、軽鎖可変ドメインは、表6に列挙された配列番号305の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含み、軽鎖可変ドメインは、配列番号305の38位にアラニンを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号304と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表5に列挙された配列番号304に位置する一つまたは複数のアミノ酸の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインと、配列番号305と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインであって、表6に列挙された配列番号305の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号305を含む軽鎖可変ドメインと、配列番号304と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表5に列挙された配列番号304の一または複数(例えば、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号305と少なくとも90%同一である軽鎖可変ドメインであって、配列番号305の26位にヒスチジンを含む軽鎖可変ドメインと、配列番号304と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表5に列挙された配列番号304の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号305と少なくとも90%同一である軽鎖可変ドメインであって、配列番号305の30位にヒスチジンを含む軽鎖可変ドメインと、配列番号304と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表5に列挙された配列番号304の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号305と少なくとも90%同一である軽鎖可変ドメインであって、配列番号305の31位にヒスチジンを含む軽鎖可変ドメインと、配列番号304と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表5に列挙された配列番号304の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号305と少なくとも90%同一である軽鎖可変ドメインであって、配列番号305の34位にヒスチジンを含む軽鎖可変ドメインと、配列番号304と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表5に列挙された配列番号304の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号305と少なくとも90%同一である軽鎖可変ドメインであって、配列番号305の36位にヒスチジンを含む軽鎖可変ドメインと、配列番号304と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表5に列挙された配列番号304の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号305と少なくとも90%同一である軽鎖可変ドメインであって、配列番号305の54位にヒスチジンを含む軽鎖可変ドメインと、配列番号304と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表5に列挙された配列番号304の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号305と少なくとも90%同一である軽鎖可変ドメインであって、配列番号305の56位にヒスチジンを含む軽鎖可変ドメインと、配列番号304と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表5に列挙された配列番号304の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号305と少なくとも90%同一である軽鎖可変ドメインであって、配列番号305の57位にヒスチジンを含む軽鎖可変ドメインと、配列番号304と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表5に列挙された配列番号304の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号305と少なくとも90%同一である軽鎖可変ドメインであって、配列番号305の60位にヒスチジンを含む軽鎖可変ドメインと、配列番号304と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表5に列挙された配列番号304の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号305と少なくとも90%同一である軽鎖可変ドメインであって、配列番号305の93位にヒスチジンを含む軽鎖可変ドメインと、配列番号304と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表5に列挙された配列番号304の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号305と少なくとも90%同一である軽鎖可変ドメインであって、配列番号305の95位にヒスチジンを含む軽鎖可変ドメインと、配列番号304と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表5に列挙された配列番号304の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号305と少なくとも90%同一である軽鎖可変ドメインであって、配列番号305の99位にヒスチジンを含む軽鎖可変ドメインと、配列番号304と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表5に列挙された配列番号304の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号305と少なくとも90%同一である軽鎖可変ドメインであって、配列番号305の101位にヒスチジンを含む軽鎖可変ドメインと、配列番号304と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表5に列挙された配列番号304の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号305と少なくとも90%同一である軽鎖可変ドメインであって、配列番号305の38位にアラニンを含む軽鎖可変ドメインと、配列番号304と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表5に列挙された配列番号304の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにヒスチジンを含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のヒスチジンがアラニンで置換されているものであるhucMET27Gv1.3の重鎖可変ドメインを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のヒスチジンがアラニンで置換されているものであるhucMET27Gv1.3の軽鎖可変ドメインを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のヒスチジンがアラニンで置換されているものであるhucMET27Gv1.3の重鎖可変ドメインと、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のヒスチジンがアラニンで置換されているものであるhucMET27Gv1.3の軽鎖可変ドメインとを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、hucMET27Gv1.3の重鎖可変ドメインは、配列番号304を含む。 本明細書に記載されるいずれかのABPCの一部の実施例では、hucMET27Gv1.3の軽鎖可変ドメインは、配列番号305を含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、それぞれ配列番号306、配列番号307、および配列番号308であるCDR1、CDR2およびCDR3であって、配列番号306~308においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のヒスチジンがアラニンで置換されているものである当該CDR1、CDR2およびCDR3を含む重鎖可変ドメインを含む。本明細書に記載のいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、それぞれ配列番号309、配列番号310、および配列番号311であるCDR1、CDR2およびCDR3であって、配列番号309~311においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のヒスチジンがアラニンで置換されているものである当該CDR1、CDR2およびCDR3を含む軽鎖可変ドメインを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、それぞれ配列番号306、配列番号307、および配列番号308であるCDR1、CDR2およびCDR3であって、配列番号306~308においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のヒスチジンがアラニンで置換されているものである当該CDR1、CDR2およびCDR3を含む重鎖可変ドメインと、それぞれ配列番号309、配列番号310、および配列番号311であるCDR1、CDR2およびCDR3であって、配列番号309~311においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のヒスチジンがアラニンで置換されているものである当該CDR1、CDR2およびCDR3を含む軽鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349.の重鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号305、配列番号350、配列番号351、配列番号352、配列番号353、配列番号354、配列番号355、配列番号356、配列番号357、配列番号358、配列番号359、配列番号360、配列番号361、配列番号362、配列番号363、配列番号364、配列番号365、配列番号366、配列番号367、配列番号368、配列番号369、配列番号370、配列番号371、配列番号372、配列番号373、配列番号374、配列番号375、配列番号376、配列番号377、配列番号378、配列番号379、または配列番号380.の軽鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号305を含む軽鎖可変ドメインと、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号350を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号351を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号352を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号353を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号354を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号355を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号356を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号357を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号358を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号359を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号360を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号361を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号362を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号363を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号364を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号365を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号366を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号367を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号368を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号369を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号370を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号371を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号372を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号373を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号374を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号375を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号376を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるABPCのいずれかの一部の実施例では、第一の抗原結合ドメインは、配列番号377を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号378を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号379を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号380を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、または配列番号349を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号305を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号350を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号351を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号352を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号353を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号354を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号355を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号356を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号357を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号358を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号359を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号360を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号361を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号362を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号363を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号364を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号365を含む軽鎖可変ドメインと、と配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号366を含む軽鎖可変ドメインと、と配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるABPCのいずれかの一部の実施例では、第一の抗原結合ドメインは、配列番号367を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号368を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号369を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号370を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号371を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号372を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号373を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号374を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号375を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号376を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号377を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号378を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号379を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号380を含む軽鎖可変ドメインと、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号426、配列番号427、配列番号428、配列番号429、配列番号430、配列番号431、配列番号432、配列番号433、配列番号434、配列番号435、配列番号436、配列番号437、配列番号438、配列番号439、配列番号440、配列番号441、配列番号442、配列番号443、配列番号444、配列番号445、配列番号446、配列番号447、配列番号448、配列番号449、配列番号450、配列番号451、配列番号452、配列番号453、配列番号454、配列番号455、配列番号456、配列番号457、配列番号458、配列番号459、配列番号460、配列番号461、配列番号462、配列番号463、配列番号464、配列番号465、配列番号466、配列番号467、配列番号468、配列番号469、配列番号470、配列番号471、配列番号472、配列番号473、配列番号474、配列番号475、配列番号476、配列番号477、配列番号478、配列番号479、配列番号480、配列番号481、配列番号482、配列番号483、配列番号484、配列番号485、配列番号486、配列番号487、配列番号488、配列番号489、配列番号490、配列番号491、配列番号492、配列番号493、配列番号494、配列番号495、配列番号496、配列番号497、配列番号498、配列番号499、配列番号500、または配列番号501を含む軽鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号426を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号427を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号428を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号429を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号430を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号431を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号432を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号433を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号434を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号435を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号436を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号437を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号438を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号439を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号440を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号441を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号442を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号443を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号444を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号445を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号446を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号447を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号448を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号449および配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号450を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号451を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号452を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号453を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号454を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号455を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号456を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号457を含む軽鎖可変ドメインと、配列番号304,配列番号312,配列番号313,配列番号314,配列番号315,配列番号316,配列番号317,配列番号318,配列番号319,配列番号320,配列番号321,配列番号322,配列番号323,配列番号324,配列番号325,配列番号326,配列番号327,配列番号328,配列番号329,配列番号330,配列番号331,配列番号332,配列番号333,配列番号334,配列番号335,配列番号336,配列番号337,配列番号338,配列番号339,配列番号340,配列番号341,配列番号342,配列番号343,配列番号344,配列番号345,配列番号346,配列番号347,配列番号348,配列番号349,配列番号381,配列番号382,配列番号383,配列番号384,配列番号385,配列番号386,配列番号387,配列番号388,配列番号389,配列番号390,配列番号391,配列番号392,配列番号393,配列番号394,配列番号395,配列番号396,配列番号397,配列番号398,配列番号399,配列番号400,配列番号401,配列番号402,配列番号403,配列番号404,配列番号405,配列番号406,配列番号407,配列番号408,配列番号409,配列番号410,配列番号411,配列番号412,配列番号413,配列番号414,配列番号415,配列番号416,配列番号417,配列番号418,配列番号419,配列番号420,配列番号421,配列番号422,配列番号423,配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるABPCのいずれかの一部の実施例では、第一の抗原結合ドメインは、配列番号458を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号459を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号460を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号461を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号462を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号463を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号464を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号465を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるABPCのいずれかの一部の実施例では、第一の抗原結合ドメインは、配列番号466を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号467を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号468を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号469を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号470を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号471を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号472を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号473を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号474を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号475を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号476を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号477を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号478を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号479を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号480を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号481を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号482を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号483を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号484を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号485を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号486を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号487を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号488を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号489を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号490を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号491を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号492を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号493を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号494を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号495を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号496を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるABPCのいずれかの一部の実施例では、第一の抗原結合ドメインは、配列番号497を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号498を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号499を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号500を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号501を含む軽鎖可変ドメインと、配列番号304、配列番号312、配列番号313、配列番号314、配列番号315、配列番号316、配列番号317、配列番号318、配列番号319、配列番号320、配列番号321、配列番号322、配列番号323、配列番号324、配列番号325、配列番号326、配列番号327、配列番号328、配列番号329、配列番号330、配列番号331、配列番号332、配列番号333、配列番号334、配列番号335、配列番号336、配列番号337、配列番号338、配列番号339、配列番号340、配列番号341、配列番号342、配列番号343、配列番号344、配列番号345、配列番号346、配列番号347、配列番号348、配列番号349、配列番号381、配列番号382、配列番号383、配列番号384、配列番号385、配列番号386、配列番号387、配列番号388、配列番号389、配列番号390、配列番号391、配列番号392、配列番号393、配列番号394、配列番号395、配列番号396、配列番号397、配列番号398、配列番号399、配列番号400、配列番号401、配列番号402、配列番号403、配列番号404、配列番号405、配列番号406、配列番号407、配列番号408、配列番号409、配列番号410、配列番号411、配列番号412、配列番号413、配列番号414、配列番号415、配列番号416、配列番号417、配列番号418、配列番号419、配列番号420、配列番号421、配列番号422、配列番号423、配列番号424、または配列番号425を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸がヒスチジンで置換されているP3D12の重鎖可変ドメインを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸がヒスチジンで置換されているP3D12の軽鎖可変ドメインを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸がヒスチジンで置換されているP3D12の重鎖可変ドメインと、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸がヒスチジンで置換されているP3D12の軽鎖可変ドメインとを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、P3D12の重鎖可変ドメインは、配列番号502を含む。本明細書に記載されるいずれかのABPCの一部の実施例では、P3D12の軽鎖可変ドメインは、配列番号503を含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、それぞれ配列番号504、配列番号505、および配列番号506であるCDR1、CDR2およびCDR3であって、配列番号504~506においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む重鎖可変ドメインを含む。本明細書に記載のいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、それぞれ配列番号507、配列番号508、および配列番号509であるCDR1、CDR2およびCDR3であって、配列番号507~509においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む軽鎖可変ドメインを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、それぞれ配列番号504、配列番号505、および配列番号506であるCDR1、CDR2およびCDR3であって、配列番号504~506においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む重鎖可変ドメインと、それぞれ配列番号507、配列番号508、および配列番号509であるCDR1、CDR2およびCDR3であって、配列番号507~509においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む軽鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインを含み、重鎖可変ドメインは、27、29、30、32、33、34、50、51、52、53、57、59、98、100、101、102、103、106および107からなる群から選択される配列番号502の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号503と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインを含み、軽鎖可変ドメインは、25、29、31、32、33、34、35、52、55、91、92、93、94、95、96、97および98からなる群から選択される配列番号503における一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、27、29、30、32、33、34、50、51、52、53、57、59、98、100、101、102、103、106および107からなる群から選択される配列番号502における一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含む、当該重鎖可変ドメインと、配列番号503と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインであって、25、29、31、32、33、34、35、52、55、91、92、93、94、95、96、97および98からなる群から選択される配列番号503における一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含む、当該軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインを含み、重鎖可変ドメインは配列番号502の35位にアラニンを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって配列番号502の35位にアラニンを含む、当該重鎖可変ドメインと、配列番号503と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインであって、25、29、31、32、33、34、35、52、55、91、92、93、94、95、96、97および98からなる群から選択される配列番号503における一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含む、当該軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインを含み、重鎖可変ドメインは、27、29、30、32、33、34、50、51、52、53、57、59、98、100、101、102、103、106および107からなる群から選択される配列番号502における一または複数(一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含み、重鎖可変ドメインは、配列番号502の35位にアラニンを含む。 本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、27、29、30、32、33、34、50、51、52、53、57、59、98、100、101、102、103、106および107からなる群から選択される配列番号502における一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含み、配列番号502の35位にアラニンを含む、当該重鎖可変ドメインと、配列番号503と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインであって、25、29、31、32、33、34、35、52、55、91、92、93、94、95、96、97および98からなる群から選択される配列番号503における一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のアミノ酸位置にヒスチジンを含む、当該軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、重鎖可変ドメインは、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインを含み、重鎖可変ドメインは表7に列挙された配列番号502の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、軽鎖可変ドメインは、配列番号503と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインを含み、軽鎖可変ドメインは表8に列挙された配列番号503の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表7に列挙された配列番号502の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインと、配列番号503と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である軽鎖可変ドメインであって、表8に列挙された配列番号503に位置する一つまたは複数のアミノ酸の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該軽鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号503を含む軽鎖可変ドメインと、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表7に列挙された配列番号502の一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号503と少なくとも90%同一である軽鎖可変ドメインであって、配列番号503の25位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表7に列挙された配列番号502の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号503と少なくとも90%同一である軽鎖可変ドメインであって、配列番号503の29位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表7に列挙された配列番号502の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号503と少なくとも90%同一である軽鎖可変ドメインであって、配列番号503の31位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表7に列挙された配列番号502の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号503と少なくとも90%同一である軽鎖可変ドメインであって、配列番号503の32位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表7に列挙された配列番号502の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号503と少なくとも90%同一である軽鎖可変ドメインであって、配列番号503の33位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表7に列挙された配列番号502の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号503と少なくとも90%同一である軽鎖可変ドメインであって、配列番号503の34位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表7に列挙された配列番号502の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号503と少なくとも90%同一である軽鎖可変ドメインであって、配列番号503の35位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表7に列挙された配列番号502の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号503と少なくとも90%同一である軽鎖可変ドメインであって、配列番号503の52位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表7に列挙された配列番号502の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号503と少なくとも90%同一である軽鎖可変ドメインであって、配列番号503の55位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表7に列挙された配列番号502の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号503と少なくとも90%同一である軽鎖可変ドメインであって、配列番号503の91位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表7に列挙された配列番号502の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号503と少なくとも90%同一である軽鎖可変ドメインであって、配列番号503の92位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表7に列挙された配列番号502の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号503と少なくとも90%同一である軽鎖可変ドメインであって、配列番号503の93位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表7に列挙された配列番号502の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号503と少なくとも90%同一である軽鎖可変ドメインであって、配列番号503の94位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表7に列挙された配列番号502の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号503と少なくとも90%同一である軽鎖可変ドメインであって、配列番号503の95位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表7に列挙された配列番号502の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号503と少なくとも90%同一である軽鎖可変ドメインであって、配列番号503の96位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表7に列挙された配列番号502の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号503と少なくとも90%同一である軽鎖可変ドメインであって、配列番号503の97位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表7に列挙された配列番号502の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号503と少なくとも90%同一である軽鎖可変ドメインであって、配列番号503の98位にヒスチジンを含む、当該軽鎖可変ドメインと、配列番号502と少なくとも90%(例えば、少なくとも92%、少なくとも94%、少なくとも96%、少なくとも98%、少なくとも99%、または100%)同一である重鎖可変ドメインであって、表7に列挙された配列番号502の一つまたは複数のアミノ酸位置の特定の組み合わせのいずれかにおいてヒスチジンを含む、当該重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のヒスチジンがアラニンで置換されているものであるP3D12の重鎖可変ドメインを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のヒスチジンがアラニンで置換されているものであるP3D12の軽鎖可変ドメインを含む。本明細書に記載されるABPCのいずれかの一部の実施例では、第一の抗原結合ドメインは、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のヒスチジンがアラニンで置換されているものであるP3D12の重鎖可変ドメインと、一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、十個、十一個、十二個、十三個、十四個、十五個、十六個、十七個、十八個、十九個、または二十個)のヒスチジンがアラニンで置換されているものであるP3D12の軽鎖可変ドメインとを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、P3D12の重鎖可変ドメインは、配列番号502を含む。本明細書に記載されるいずれかのABPCの一部の実施例では、P3D12の軽鎖可変ドメインは、配列番号503を含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、それぞれ配列番号504、配列番号505、および配列番号506であるCDR1、CDR2およびCDR3であって、配列番号504~506においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のヒスチジンがアラニンで置換されているものである当該CDR1、CDR2およびCDR3を含む重鎖可変ドメインを含む。本明細書に記載のいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、それぞれ配列番号507、配列番号508、および配列番号509であるCDR1、CDR2およびCDR3であって、配列番号507~509においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のヒスチジンがアラニンで置換されているものである当該CDR1、CDR2およびCDR3を含む軽鎖可変ドメインを含む。本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、それぞれ配列番号504、配列番号505、および配列番号506であるCDR1、CDR2およびCDR3であって、配列番号504~506においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のヒスチジンがアラニンで置換されているものである当該CDR1、CDR2およびCDR3を含む重鎖可変ドメインと、それぞれ配列番号507、配列番号508、および配列番号509であるCDR1、CDR2およびCDR3であって、配列番号507~509においてまとめて合計で一または複数(例えば、一個、二個、三個、四個、五個、六個、七個、八個、九個、または十個)のヒスチジンがアラニンで置換されているものである当該CDR1、CDR2およびCDR3を含む軽鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548の重鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号503、配列番号549、配列番号550、配列番号551、配列番号552、配列番号553、配列番号554、配列番号555、配列番号556、配列番号557、配列番号558、配列番号559、配列番号560、配列番号561、配列番号562、配列番号563、配列番号564、配列番号565、配列番号566、配列番号567、配列番号568、配列番号569、配列番号570、配列番号571、配列番号572、配列番号573、配列番号574、配列番号575、または配列番号576の軽鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号503を含む軽鎖可変ドメインと、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号549を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号550を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号551を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号552を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号553を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号554を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号555を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号556を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号557を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号558を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号559を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号560を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号561を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号562を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号563を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号564を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号565を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号566を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号567を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号568を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号569を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号570を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号571を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号572を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号573を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号574を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号575を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号576を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、または配列番号548を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号503を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号549を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号550を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号551を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号552を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号553を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号554を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号555を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号556を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号557を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号558を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号559を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号560を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号561を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号562を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号563を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号564を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号565を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号566を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号567を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号568を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号569を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号570を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号571を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号572を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号573を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号574を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号575を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号576を含む軽鎖可変ドメインと、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号697、配列番号698、配列番号699、配列番号700、配列番号701、配列番号702、配列番号703、配列番号704、配列番号705、配列番号706、配列番号707、配列番号708、配列番号709、配列番号710、配列番号711、配列番号712、配列番号713、配列番号714、配列番号715、配列番号716、配列番号717、配列番号718、配列番号719、配列番号720、配列番号721、配列番号722、配列番号723、配列番号724、配列番号725、配列番号726、配列番号727、配列番号728、配列番号729、配列番号730、配列番号731、配列番号732、配列番号733、配列番号734、配列番号735、配列番号736、配列番号737、配列番号738、配列番号739、配列番号740、配列番号741、配列番号742、配列番号743、配列番号744、配列番号745、配列番号746、配列番号747、配列番号748、配列番号749、配列番号750、配列番号751、配列番号752、配列番号753、配列番号754、配列番号755、配列番号756、配列番号757、配列番号758、配列番号759、配列番号760、配列番号761、配列番号762、配列番号763、配列番号764、配列番号765、配列番号766、配列番号767、配列番号768、配列番号769、配列番号770、配列番号771、配列番号772、配列番号773、配列番号774、配列番号775、配列番号776、配列番号777、配列番号778、配列番号779、配列番号780、配列番号781、配列番号782、配列番号783、配列番号784、配列番号785、配列番号786、配列番号787、配列番号788、配列番号789、または配列番号790を含む軽鎖可変ドメインを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号503を含む軽鎖可変ドメインと、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号697を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号698を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるABPCのいずれかの一部の実施例では、第一の抗原結合ドメインは、配列番号699を含む軽鎖可変ドメインと、: 配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号700を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号701を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号702を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号703を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号704を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号705を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号706を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号707を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号708を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号709を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号710を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号711を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号712を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号713を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号714を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号715を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号716を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号717を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号718を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号719を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号720を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号721を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号722を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号723を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号724を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号725を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号726を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号727を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号728を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号729を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号730を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号731を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号732を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号733を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号734を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号735を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号736を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号737を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号738を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号739を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号740を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号741を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号742を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号743を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号744を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号745を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号746を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号747を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号748を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号749を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号750を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号751を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号752を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号753を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号754を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号755を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号756を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号757を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号758を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号759を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号760を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号761を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号762を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号763を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるABPCのいずれかの一部の実施例では、第一の抗原結合ドメインは、配列番号764を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号765を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号766を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号767を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号768を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号769を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号770を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号771を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号772を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号773を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるABPCのいずれかの一部の実施例では、第一の抗原結合ドメインは、配列番号774を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号775を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号776を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号777を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号778を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号779を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号780を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号781を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号782を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号783を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号784を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号785を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号786を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号787を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号788を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号789を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書に記載されるいずれかのABPCの一部の実施例では、第一の抗原結合ドメインは、配列番号790を含む軽鎖可変ドメインと、配列番号502、配列番号510、配列番号511、配列番号512、配列番号513、配列番号514、配列番号515、配列番号516、配列番号517、配列番号518、配列番号519、配列番号520、配列番号521、配列番号522、配列番号523、配列番号524、配列番号525、配列番号526、配列番号527、配列番号528、配列番号529、配列番号530、配列番号531、配列番号532、配列番号533、配列番号534、配列番号535、配列番号536、配列番号537、配列番号538、配列番号539、配列番号540、配列番号541、配列番号542、配列番号543、配列番号544、配列番号545、配列番号546、配列番号547、配列番号548、配列番号577、配列番号578、配列番号579、配列番号580、配列番号581、配列番号582、配列番号583、配列番号584、配列番号585、配列番号586、配列番号587、配列番号588、配列番号589、配列番号590、配列番号591、配列番号592、配列番号593、配列番号594、配列番号595、配列番号596、配列番号597、配列番号598、配列番号599、配列番号600、配列番号601、配列番号602、配列番号603、配列番号604、配列番号605、配列番号606、配列番号607、配列番号608、配列番号609、配列番号610、配列番号611、配列番号612、配列番号613、配列番号614、配列番号615、配列番号616、配列番号617、配列番号618、配列番号619、配列番号620、配列番号621、配列番号622、配列番号623、配列番号624、配列番号625、配列番号626、配列番号627、配列番号628、配列番号629、配列番号630、配列番号631、配列番号632、配列番号633、配列番号634、配列番号635、配列番号636、配列番号637、配列番号638、配列番号639、配列番号640、配列番号641、配列番号642、配列番号643、配列番号644、配列番号645、配列番号646、配列番号647、配列番号648、配列番号649、配列番号650、配列番号651、配列番号652、配列番号653、配列番号654、配列番号655、配列番号656、配列番号657、配列番号658、配列番号659、配列番号660、配列番号661、配列番号662、配列番号663、配列番号664、配列番号665、配列番号666、配列番号667、配列番号668、配列番号669、配列番号670、配列番号671、配列番号672、配列番号673、配列番号674、配列番号675、配列番号676、配列番号677、配列番号678、配列番号679、配列番号680、配列番号681、配列番号682、配列番号683、配列番号684、配列番号685、配列番号686、配列番号687、配列番号688、配列番号689、配列番号690、配列番号691、配列番号692、配列番号693、配列番号694、配列番号695、または配列番号696を含む重鎖可変ドメインとを含む。
本明細書ではまた、本明細書に記載されるいずれかのABPCを含む医薬組成物が提供される。また本明細書では、治療有効量の本明細書に記載されるいずれかのABPCを対象に投与することを含む、それを必要とする対象を治療する方法も提供される。
本明細書に記載されるいずれかのABPCの一部の実施例では、ABPC(例えば、本明細書に記載されるABPCのいずれか)を含む組成物は、同量の対照ABPC(例えば、本明細書に記載される例示的な対照ABPCのいずれか)を含む組成物と比較して、標的哺乳動物細胞(例えば、本明細書に記載される標的哺乳動物細胞のいずれか)における毒素放出の増加(例えば、検出可能な増加)(例えば、少なくとも1%の増加、少なくとも2%の増加、少なくとも5%の増加、少なくとも10%の増加、少なくとも15%の増加、少なくとも20%の増加、少なくとも25%の増加、少なくとも30%の増加、少なくとも35%の増加、少なくとも40%の増加、少なくとも45%の増加、少なくとも50%の増加、少なくとも55%の増加、少なくとも60%の増加、少なくとも65%の増加、少なくとも70%の増加、少なくとも75%の増加、少なくとも80%の増加、少なくとも85%の増加、少なくとも90%の増加、少なくとも95%の増加、少なくとも100%の増加、少なくとも120%の増加、少なくとも140%の増加、少なくとも160%の増加、少なくとも180%の増加、少なくとも200%の増加、少なくとも250%の増加、少なくとも300%の増加、少なくとも350%の増加、少なくとも400%の増加、少なくとも450%の増加、少なくとも500%の増加、少なくとも1,000%の増加、少なくとも2,000%の増加、少なくとも3,000%の増加、少なくとも4,000%の増加、少なくとも5,000%の増加、少なくとも6,000%の増加、少なくとも7,000%の増加、少なくとも8,000%の増加、少なくとも9,000%の増加、もしくは少なくとも10,000%の増加、または約1%の増加~約10,000%の増加、約1%の増加~約9,000%の増加、約1%の増加~約8,000%の増加、約1%の増加~約7,000%の増加、約1%の増加~約6,000%の増加、約1%の増加~約5,000%の増加、約1%の増加~約4,000%の増加、約1%の増加~約3,000%の増加、約1%の増加~約2,000%の増加、約1%の増加~約1,000%の増加、約1%の増加~約500%の増加、約1%の増加~約450%の増加、約1%の増加~約400%の増加、約1%の増加~約350%の増加、約1%の増加~約300%の増加、約1%の増加~約250%の増加、約1%の増加~約200%の増加、約1%の増加~約180%の増加、約1%の増加~約160%の増加、約1%の増加~約140%の増加、約1%の増加~約120%の増加、約1%の増加~約100%の増加、約1%の増加~約95%の増加、約1%の増加~約90%の増加、約1%の増加~約85%の増加、約1%の増加~約80%の増加、約1%の増加~約75%の増加、約1%の増加~約70%の増加、約1%の増加~約65%の増加、約1%の増加~約60%の増加、約1%の増加~約55%の増加、約1%の増加~約50%の増加、約1%の増加~約45%の増加、約1%の増加~約40%の増加、約1%の増加~約35%の増加、約1%の増加~約25%の増加、約1%の増加~約20%の増加、約1%の増加~約15%の増加、約1%の増加~約10%の増加、約1%の増加~約5%の増加、約2%の増加~約10,000%の増加、約2%の増加~約9,000%の増加、約2%の増加~約8,000%の増加、約2%の増加~約7,000%の増加、約2%の増加~約6,000%の増加、約2%の増加~約5,000%の増加、約2%の増加~約4,000%の増加、約2%の増加~約3,000%の増加、約2%の増加~約2,000%の増加、約2%の増加~約1,000%の増加、約2%の増加~約500%の増加、約2%の増加~約450%の増加、約2%の増加~約400%の増加、約2%の増加~約350%の増加、約2%の増加~約300%の増加、約2%の増加~約250%の増加、約2%の増加~約200%の増加、約2%の増加~約180%の増加、約2%の増加~約160%の増加、約2%の増加~約140%の増加、約2%の増加~約120%の増加、約2%の増加~約100%の増加、約2%の増加~約95%の増加、約2%の増加~約90%の増加、約2%の増加~約85%の増加、約2%の増加~約80%の増加、約2%の増加~約75%の増加、約2%の増加~約70%の増加、約2%の増加~約65%の増加、約2%の増加~約60%の増加、約2%の増加~約55%の増加、約2%の増加~約50%の増加、約2%の増加~約45%の増加、約2%の増加~約40%の増加、約2%の増加~約35%の増加、約2%の増加~約25%の増加、約2%の増加~約20%の増加、約2%の増加~約15%の増加、約2%の増加~約10%の増加、約2%の増加~約5%の増加、約5%の増加~約10,000%の増加、約5%の増加~約9,000%の増加、約5%の増加~約8,000%の増加、約5%の増加~約7,000%の増加、約5%の増加~約6,000%の増加、約5%の増加~約5,000%の増加、約5%の増加~約4,000%の増加、約5%の増加~約3,000%の増加、約5%の増加~約2,000%の増加、約5%の増加~約1,000%の増加、約5%の増加~約500%の増加、約5%の増加~約450%の増加、約5%の増加~約400%の増加、約5%の増加~約350%の増加、約5%の増加~約300%の増加、約5%の増加~約250%の増加、約5%の増加~約200%の増加、約5%の増加~約180%の増加、約5%の増加~約160%の増加、約5%の増加~約140%の増加、約5%の増加~約120%の増加、約5%の増加~約100%の増加、約5%の増加~約95%の増加、約5%の増加~約90%の増加、約5%の増加~約85%の増加、約5%の増加~約80%の増加、約5%の増加~約75%の増加、約5%の増加~約70%の増加、約5%の増加~約65%の増加、約5%の増加~約60%の増加、約5%の増加~約55%の増加、約5%の増加~約50%の増加、約5%の増加~約45%の増加、約5%の増加~約40%の増加、約5%の増加~約35%の増加、約5%の増加~約25%の増加、約5%の増加~約20%の増加、約5%の増加~約15%の増加、約5%の増加~約10%の増加、約10%の増加~約10,000%の増加、約10%の増加~約9,000%の増加、約10%の増加~約8,000%の増加、約10%の増加~約7,000%の増加、約10%の増加~約6,000%の増加、約10%の増加~約5,000%の増加、約10%の増加~約4,000%の増加、約10%の増加~約3,000%の増加、約10%の増加~約2,000%の増加、約10%の増加~約1,000%の増加、約10%の増加~約500%の増加、約10%の増加~約450%の増加、約10%の増加~約400%の増加、約10%の増加~約350%の増加、約10%の増加~約300%の増加、約10%の増加~約250%の増加、約10%の増加~約200%の増加、約10%の増加~約180%の増加、約10%の増加~約160%の増加、約10%の増加~約140%の増加、約10%の増加~約120%の増加、約10%の増加~約100%の増加、約10%の増加~約95%の増加、約10%の増加~約90%の増加、約10%の増加~約85%の増加、約10%の増加~約80%の増加、約10%の増加~約75%の増加、約10%の増加~約70%の増加、約10%の増加~約65%の増加、約10%の増加~約60%の増加、約10%の増加~約55%の増加、約10%の増加~約50%の増加、約10%の増加~約45%の増加、約10%の増加~約40%の増加、約10%の増加~約35%の増加、約10%の増加~約30%の増加、約10%の増加~約25%の増加、約10%の増加~約20%の増加、約10%の増加~約15%の増加、約15%の増加~約10,000%の増加、約15%の増加~約9,000%の増加、約15%の増加~約8,000%の増加、約15%の増加~約7,000%の増加、約15%の増加~約6,000%の増加、約15%の増加~約5,000%の増加、約15%の増加~約4,000%の増加、約15%の増加~約3,000%の増加、約15%の増加~約2,000%の増加、約15%の増加~約1,000%の増加、約15%の増加~約500%の増加、約15%の増加~約450%の増加、約15%の増加~約400%の増加、約15%の増加~約350%の増加、約15%の増加~約300%の増加、約15%の増加~約250%の増加、約15%の増加~約200%の増加、約15%の増加~約180%の増加、約15%の増加~約160%の増加、約15%の増加~約140%の増加、約15%の増加~約120%の増加、約15%の増加~約100%の増加、約15%の増加~約95%の増加、約15%の増加~約90%の増加、約15%の増加~約85%の増加、約15%の増加~約80%の増加、約15%の増加~約75%の増加、約15%の増加~約70%の増加、約15%の増加~約65%の増加、約15%の増加~約60%の増加、約15%の増加~約55%の増加、約15%の増加~約50%の増加、約15%の増加~約45%の増加、約15%の増加~約40%の増加、約15%の増加~約35%の増加、約15%の増加~約30%の増加、約15%の増加~約25%の増加、約15%の増加~約20%の増加、約20%の増加~約10,000%の増加、約20%の増加~約9,000%の増加、約20%の増加~約8,000%の増加、約20%の増加~約7,000%の増加、約20%の増加~約6,000%の増加、約20%の増加~約5,000%の増加、約20%の増加~約4,000%の増加、約20%の増加~約3,000%の増加、約20%の増加~約2,000%の増加、約20%の増加~約1,000%の増加、約20%の増加~約500%の増加、約20%の増加~約450%の増加、約20%の増加~約400%の増加、約20%の増加~約350%の増加、約20%の増加~約300%の増加、約20%の増加~約250%の増加、約20%の増加~約200%の増加、約20%の増加~約180%の増加、約20%の増加~約160%の増加、約20%の増加~約140%の増加、約20%の増加~約120%の増加、約20%の増加~約100%の増加、約20%の増加~約95%の増加、約20%の増加~約90%の増加、約20%の増加~約85%の増加、約20%の増加~約80%の増加、約20%の増加~約75%の増加、約20%の増加~約70%の増加、約20%の増加~約65%の増加、約20%の増加~約60%の増加、約20%の増加~約55%の増加、約20%の増加~約50%の増加、約20%の増加~約45%の増加、約20%の増加~約40%の増加、約20%の増加~約35%の増加、約20%の増加~約30%の増加、約20%の増加~約25%の増加、約25%の増加~約10,000%の増加、約25%の増加~約9,000%の増加、約25%の増加~約8,000%の増加、約25%の増加~約7,000%の増加、約25%の増加~約6,000%の増加、約25%の増加~約5,000%の増加、約25%の増加~約4,000%の増加、約25%の増加~約3,000%の増加、約25%の増加~約2,000%の増加、約25%の増加~約1,000%の増加、約25%の増加~約500%の増加、約25%の増加~約450%の増加、約25%の増加~約400%の増加、約25%の増加~約350%の増加、約25%の増加~約300%の増加、約25%の増加~約250%の増加、約25%の増加~約200%の増加、約25%の増加~約180%の増加、約25%の増加~約160%の増加、約25%の増加~約140%の増加、約25%の増加~約120%の増加、約25%の増加~約100%の増加、約25%の増加~約95%の増加、約25%の増加~約90%の増加、約25%の増加~約85%の増加、約25%の増加~約80%の増加、約25%の増加~約75%の増加、約25%の増加~約70%の増加、約25%の増加~約65%の増加、約
25%の増加~約60%の増加、約25%の増加~約55%の増加、約25%の増加~約50%の増加、約25%の増加~約45%の増加、約25%の増加~約40%の増加、約25%の増加~約35%の増加、約25%の増加~約30%の増加、約30%の増加~約10,000%の増加、約30%の増加~約9,000%の増加、約30%の増加~約8,000%の増加、約30%の増加~約7,000%の増加、約30%の増加~約6,000%の増加、約30%の増加~約5,000%の増加、約30%の増加~約4,000%の増加、約30%の増加~約3,000%の増加、約30%の増加~約2,000%の増加、約30%の増加~約1,000%の増加、約30%の増加~約500%の増加、約30%の増加~約450%の増加、約30%の増加~約400%の増加、約30%の増加~約350%の増加、約30%の増加~約300%の増加、約30%の増加~約250%の増加、約30%の増加~約200%の増加、約30%の増加~約180%の増加、約30%の増加~約160%の増加、約30%の増加~約140%の増加、約30%の増加~約120%の増加、約30%の増加~約100%の増加、約30%の増加~約95%の増加、約30%の増加~約90%の増加、約30%の増加~約85%の増加、約30%の増加~約80%の増加、約30%の増加~約75%の増加、約30%の増加~約70%の増加、約30%の増加~約65%の増加、約30%の増加~約60%の増加、約30%の増加~約55%の増加、約30%の増加~約50%の増加、約30%の増加~約45%の増加、約30%の増加~約40%の増加、約30%の増加~約35%の増加、約35%の増加~約10,000%の増加、約35%の増加~約9,000%の増加、約35%の増加~約8,000%の増加、約35%の増加~約7,000%の増加、約35%の増加~約6,000%の増加、約35%の増加~約5,000%の増加、約35%の増加~約4,000%の増加、約35%の増加~約3,000%の増加、約35%の増加~約2,000%の増加、約35%の増加~約1,000%の増加、約35%の増加~約500%の増加、約35%の増加~約450%の増加、約35%の増加~約400%の増加、約35%の増加~約350%の増加、約35%の増加~約300%の増加、約35%の増加~約250%の増加、約35%の増加~約200%の増加、約35%の増加~約180%の増加、約35%の増加~約160%の増加、約35%の増加~約140%の増加、約35%の増加~約120%の増加、約35%の増加~約100%の増加、約35%の増加~約95%の増加、約35%の増加~約90%の増加、約35%の増加~約85%の増加、約35%の増加~約80%の増加、約35%の増加~約75%の増加、約35%の増加~約70%の増加、約35%の増加~約65%の増加、約35%の増加~約60%の増加、約35%の増加~約55%の増加、約35%の増加~約50%の増加、約35%の増加~約45%の増加、約35%の増加~約40%の増加、約40%の増加~約10,000%の増加、約40%の増加~約9,000%の増加、約40%の増加~約8,000%の増加、約40%の増加~約7,000%の増加、約40%の増加~約6,000%の増加、約40%の増加~約5,000%の増加、約40%の増加~約4,000%の増加、約40%の増加~約3,000%の増加、約40%の増加~約2,000%の増加、約40%の増加~約1,000%の増加、約40%の増加~約500%の増加、約40%の増加~約450%の増加、約40%の増加~約400%の増加、約40%の増加~約350%の増加、約40%の増加~約300%の増加、約40%の増加~約250%の増加、約40%の増加~約200%の増加、約40%の増加~約180%の増加、約40%の増加~約160%の増加、約40%の増加~約140%の増加、約40%の増加~約120%の増加、約40%の増加~約100%の増加、約40%の増加~約95%の増加、約40%の増加~約90%の増加、約40%の増加~約85%の増加、約40%の増加~約80%の増加、約40%の増加~約75%の増加、約40%の増加~約70%の増加、約40%の増加~約65%の増加、約40%の増加~約60%の増加、約40%の増加~約55%の増加、約40%の増加~約50%の増加、約40%の増加~約45%の増加、約45%の増加~約10,000%の増加、約45%の増加~約9,000%の増加、約45%の増加~約8,000%の増加、約45%の増加~約7,000%の増加、約45%の増加~約6,000%の増加、約45%の増加~約5,000%の増加、約45%の増加~約4,000%の増加、約45%の増加~約3,000%の増加、約45%の増加~約2,000%の増加、約45%の増加~約1,000%の増加、約45%の増加~約500%の増加、約45%の増加~約450%の増加、約45%の増加~約400%の増加、約45%の増加~約350%の増加、約45%の増加~約300%の増加、約45%の増加~約250%の増加、約45%の増加~約200%の増加、約45%の増加~約180%の増加、約45%の増加~約160%の増加、約45%の増加~約140%の増加、約45%の増加~約120%の増加、約45%の増加~約100%の増加、約45%の増加~約95%の増加、約45%の増加~約90%の増加、約45%の増加~約85%の増加、約45%の増加~約80%の増加、約45%の増加~約75%の増加、約45%の増加~約70%の増加、約45%の増加~約65%の増加、約45%の増加~約60%の増加、約45%の増加~約55%の増加、約45%の増加~約50%の増加、約50%の増加~約10,000%の増加、約50%の増加~約9,000%の増加、約50%の増加~約8,000%の増加、約50%の増加~約7,000%の増加、約50%の増加~約6,000%の増加、約50%の増加~約5,000%の増加、約50%の増加~約4,000%の増加、約50%の増加~約3,000%の増加、約50%の増加~約2,000%の増加、約50%の増加~約1,000%の増加、約50%の増加~約500%の増加、約50%の増加~約450%の増加、約50%の増加~約400%の増加、約50%の増加~約350%の増加、約50%の増加~約300%の増加、約50%の増加~約250%の増加、約50%の増加~約200%の増加、約50%の増加~約180%の増加、約50%の増加~約160%の増加、約50%の増加~約140%の増加、約50%の増加~約120%の増加、約50%の増加~約100%の増加、約50%の増加~約95%の増加、約50%の増加~約90%の増加、約50%の増加~約85%の増加、約50%の増加~約80%の増加、約50%の増加~約75%の増加、約50%の増加~約70%の増加、約50%の増加~約65%の増加、約50%の増加~約60%の増加、約50%の増加~約55%の増加、約55%の増加~約10,000%の増加、約55%の増加~約9,000%の増加、約55%の増加~約8,000%の増加、約55%の増加~約7,000%の増加、約55%の増加~約6,000%の増加、約55%の増加~約5,000%の増加、約55%の増加~約4,000%の増加、約55%の増加~約3,000%の増加、約55%の増加~約2,000%の増加、約55%の増加~約1,000%の増加、約55%の増加~約500%の増加、約55%の増加~約450%の増加、約55%の増加~約400%の増加、約55%の増加~約350%の増加、約55%の増加~約300%の増加、約55%の増加~約250%の増加、約55%の増加~約200%の増加、約55%の増加~約180%の増加、約55%の増加~約160%の増加、約55%の増加~約140%の増加、約55%の増加~約120%の増加、約55%の増加~約100%の増加、約55%の増加~約95%の増加、約55%の増加~約90%の増加、約55%の増加~約85%の増加、約55%の増加~約80%の増加、約55%の増加~約75%の増加、約55%の増加~約70%の増加、約55%の増加~約65%の増加、約55%の増加~約60%の増加、約60%の増加~約10,000%の増加、約60%の増加~約9,000%の増加、約60%の増加~約8,000%の増加、約60%の増加~約7,000%の増加、約60%の増加~約6,000%の増加、約60%の増加~約5,000%の増加、約60%の増加~約4,000%の増加、約60%の増加~約3,000%の増加、約60%の増加~約2,000%の増加、約60%の増加~約1,000%の増加、約60%の増加~約500%の増加、約60%の増加~約450%の増加、約60%の増加~約400%の増加、約60%の増加~約350%の増加、約60%の増加~約300%の増加、約60%の増加~約250%の増加、約60%の増加~約200%の増加、約60%の増加~約180%の増加、約60%の増加~約160%の増加、約60%の増加~約140%の増加、約60%の増加~約120%の増加、約60%の増加~約100%の増加、約60%の増加~約95%の増加、約60%の増加~約90%の増加、約60%の増加~約85%の増加、約60%の増加~約80%の増加、約60%の増加~約75%の増加、約60%の増加~約70%の増加、約60%の増加~約65%の増加、約65%の増加~約10,000%の増加、約65%の増加~約9,000%の増加、約65%の増加~約8,000%の増加、約65%の増加~約7,000%の増加、約65%の増加~約6,000%の増加、約65%の増加~約5,000%の増加、約65%の増加~約4,000%の増加、約65%の増加~約3,000%の増加、約65%の増加~約2,000%の増加、約65%の増加~約1,000%の増加、約65%の増加~約500%の増加、約65%の増加~約450%の増加、約65%の増加~約400%の増加、約65%の増加~約350%の増加、約65%の増加~約300%の増加、約65%の増加~約250%の増加、約65%の増加~約200%の増加、約65%の増加~約180%の増加、約65%の増加~約160%の増加、約65%の増加~約140%の増加、約65%の増加~約120%の増加、約65%の増加~約100%の増加、約65%の増加~約95%の増加、約65%の増加~約90%の増加、約65%の増加~約85%の増加、約65%の増加~約80%の増加、約65%の増加~約75%の増加、約65%の増加~約70%の増加、約70%の増加~約10,000%の増加、約70%の増加~約9,000%の増加、約70%の増加~約8,000%の増加、約70%の増加~約7,000%の増加、約70%の増加~約6,000%の増加、約70%の増加~約5,000%の増加、約70%の増加~約4,000%の増加、約70%の増加~約3,000%の増加、約70%の増加~約2,000%の増加、約70%の増加~約1,000%の増加、約70%の増加~約500%の増加、約70%の増加~約450%の増加、約70%の増加~約400%の増加、約70%の増加~約350%の増加、約70%の増加~約300%の増加、約70%の増加~約250%の増加、約70%の増加~約200%の増加、約70%の増加~約180%の増加、約70%の増加~約160%の増加、約70%の増加~約140%の増加、約70%の増加~約120%の増加、約70%の増加~約100%の増加、約70%の増加~約95%の増加、約70%の増加~約90%の増加、約70%の増加~約85%の増加、約70%の増加~約80%の増加、約70%の増加~約75%の増加、約75%の増加~約10,000%の増加、約75%の増加~約9,000%の増加、約75%の増加~約8,000%の増加、約75%の増加~約7,000%の増加、約75%の増加~約6,000%の増加、約75%の増加~約5,000%の増加、約75%の増加~約4,000%の増加、約75%の増加~約3,000%の増加、約75%の増
加~約2,000%の増加、約75%の増加~約1,000%の増加、約75%の増加~約500%の増加、約75%の増加~約450%の増加、約75%の増加~約400%の増加、約75%の増加~約350%の増加、約75%の増加~約300%の増加、約75%の増加~約250%の増加、約75%の増加~約200%の増加、約75%の増加~約180%の増加、約75%の増加~約160%の増加、約75%の増加~約140%の増加、約75%の増加~約120%の増加、約75%の増加~約100%の増加、約75%の増加~約95%の増加、約75%の増加~約90%の増加、約75%の増加~約85%の増加、約75%の増加~約80%の増加、約80%の増加~約10,000%の増加、約80%の増加~約9,000%の増加、約80%の増加~約8,000%の増加、約80%の増加~約7,000%の増加、約80%の増加~約6,000%の増加、約80%の増加~約5,000%の増加、約80%の増加~約4,000%の増加、約80%の増加~約3,000%の増加、約80%の増加~約2,000%の増加、約80%の増加~約1,000%の増加、約80%の増加~約500%の増加、約80%の増加~約450%の増加、約80%の増加~約400%の増加、約80%の増加~約350%の増加、約80%の増加~約300%の増加、約80%の増加~約250%の増加、約80%の増加~約200%の増加、約80%の増加~約180%の増加、約80%の増加~約160%の増加、約80%の増加~約140%の増加、約80%の増加~約120%の増加、約80%の増加~約100%の増加、約80%の増加~約95%の増加、約80%の増加~約90%の増加、約80%の増加~約85%の増加、約85%の増加~約10,000%の増加、約85%の増加~約9,000%の増加、約85%の増加~約8,000%の増加、約85%の増加~約7,000%の増加、約85%の増加~約6,000%の増加、約85%の増加~約5,000%の増加、約85%の増加~約4,000%の増加、約85%の増加~約3,000%の増加、約85%の増加~約2,000%の増加、約85%の増加~約1,000%の増加、約85%の増加~約500%の増加、約85%の増加~約450%の増加、約85%の増加~約400%の増加、約85%の増加~約350%の増加、約85%の増加~約300%の増加、約85%の増加~約250%の増加、約85%の増加~約200%の増加、約85%の増加~約180%の増加、約85%の増加~約160%の増加、約85%の増加~約140%の増加、約85%の増加~約120%の増加、約85%の増加~約100%の増加、約85%の増加~約95%の増加、約85%の増加~約90%の増加、約90%の増加~約10,000%の増加、約90%の増加~約9,000%の増加、約90%の増加~約8,000%の増加、約90%の増加~約7,000%の増加、約90%の増加~約6,000%の増加、約90%の増加~約5,000%の増加、約90%の増加~約4,000%の増加、約90%の増加~約3,000%の増加、約90%の増加~約2,000%の増加、約90%の増加~約1,000%の増加、約90%の増加~約500%の増加、約90%の増加~約450%の増加、約90%の増加~約400%の増加、約90%の増加~約350%の増加、約90%の増加~約300%の増加、約90%の増加~約250%の増加、約90%の増加~約200%の増加、約90%の増加~約180%の増加、約90%の増加~約160%の増加、約90%の増加~約140%の増加、約90%の増加~約120%の増加、約90%の増加~約100%の増加、約90%の増加~約95%の増加、約95%の増加~約10,000%の増加、約95%の増加~約9,000%の増加、約95%の増加~約8,000%の増加、約95%の増加~約7,000%の増加、約95%の増加~約6,000%の増加、約95%の増加~約5,000%の増加、約95%の増加~約4,000%の増加、約95%の増加~約3,000%の増加、約95%の増加~約2,000%の増加、約95%の増加~約1,000%の増加、約95%の増加~約500%の増加、約95%の増加~約450%の増加、約95%の増加~約400%の増加、約95%の増加~約350%の増加、約95%の増加~約300%の増加、約95%の増加~約250%の増加、約95%の増加~約200%の増加、約95%の増加~約180%の増加、約95%の増加~約160%の増加、約95%の増加~約140%の増加、約95%の増加~約120%の増加、約95%の増加~約100%の増加、約100%の増加~約10,000%の増加、約100%の増加~約9,000%の増加、約100%の増加~約8,000%の増加、約100%の増加~約7,000%の増加、約100%の増加~約6,000%の増加、約100%の増加~約5,000%の増加、約100%の増加~約4,000%の増加、約100%の増加~約3,000%の増加、約100%の増加~約2,000%の増加、約100%の増加~約1,000%の増加、約100%の増加~約500%の増加、約100%の増加~約450%の増加、約100%の増加~約400%の増加、約100%の増加~約350%の増加、約100%の増加~約300%の増加、約100%の増加~約250%の増加、約100%の増加~約200%の増加、約100%の増加~約180%の増加、約100%の増加~約160%の増加、約100%の増加~約140%の増加、約100%の増加~約120%の増加、約120%の増加~約10,000%の増加、約120%の増加~約9,000%の増加、約120%の増加~約8,000%の増加、約120%の増加~約7,000%の増加、約120%の増加~約6,000%の増加、約120%の増加~約5,000%の増加、約120%の増加~約4,000%の増加、約120%の増加~約3,000%の増加、約120%の増加~約2,000%の増加、約120%の増加~約1,000%の増加、約120%の増加~約500%の増加、約120%の増加~約450%の増加、約120%の増加~約400%の増加、約120%の増加~約350%の増加、約120%の増加~約300%の増加、約120%の増加~約250%の増加、約120%の増加~約200%の増加、約120%の増加~約180%の増加、約120%の増加~約160%の増加、約120%の増加~約140%の増加、約140%の増加~約10,000%の増加、約140%の増加~約9,000%の増加、約140%の増加~約8,000%の増加、約140%の増加~約7,000%の増加、約140%の増加~約6,000%の増加、約140%の増加~約5,000%の増加、約140%の増加~約4,000%の増加、約140%の増加~約3,000%の増加、約140%の増加~約2,000%の増加、約140%の増加~約1,000%の増加、約140%の増加~約500%の増加、約140%の増加~約450%の増加、約140%の増加~約400%の増加、約140%の増加~約350%の増加、約140%の増加~約300%の増加、約140%の増加~約250%の増加、約140%の増加~約200%の増加、約140%の増加~約180%の増加、約140%の増加~約160%の増加、約160%の増加~約10,000%の増加、約160%の増加~約9,000%の増加、約160%の増加~約8,000%の増加、約160%の増加~約7,000%の増加、約160%の増加~約6,000%の増加、約160%の増加~約5,000%の増加、約160%の増加~約4,000%の増加、約160%の増加~約3,000%の増加、約160%の増加~約2,000%の増加、約160%の増加~約1,000%の増加、約160%の増加~約500%の増加、約160%の増加~約450%の増加、約160%の増加~約400%の増加、約160%の増加~約350%の増加、約160%の増加~約300%の増加、約160%の増加~約250%の増加、約160%の増加~約200%の増加、約160%の増加~約180%の増加、約180%の増加~約10,000%の増加、約180%の増加~約9,000%の増加、約180%の増加~約8,000%の増加、約180%の増加~約7,000%の増加、約180%の増加~約6,000%の増加、約180%の増加~約5,000%の増加、約180%の増加~約4,000%の増加、約180%の増加~約3,000%の増加、約180%の増加~約2,000%の増加、約180%の増加~約1,000%の増加、約180%の増加~約500%の増加、約180%の増加~約450%の増加、約180%の増加~約400%の増加、約180%の増加~約350%の増加、約180%の増加~約300%の増加、約180%の増加~約250%の増加、約180%の増加~約200%の増加、約200%の増加~約10,000%の増加、約200%の増加~約9,000%の増加、約200%の増加~約8,000%の増加、約200%の増加~約7,000%の増加、約200%の増加~約6,000%の増加、約200%の増加~約5,000%の増加、約200%の増加~約4,000%の増加、約200%の増加~約3,000%の増加、約200%の増加~約2,000%の増加、約200%の増加~約1,000%の増加、約200%の増加~約500%の増加、約200%の増加~約450%の増加、約200%の増加~約400%の増加、約200%の増加~約350%の増加、約200%の増加~約300%の増加、約200%の増加~約250%の増加、約250%の増加~約10,000%の増加、約250%の増加~約9,000%の増加、約250%の増加~約8,000%の増加、約250%の増加~約7,000%の増加、約250%の増加~約6,000%の増加、約250%の増加~約5,000%の増加、約250%の増加~約4,000%の増加、約250%の増加~約3,000%の増加、約250%の増加~約2,000%の増加、約250%の増加~約1,000%の増加、約250%の増加~約500%の増加、約250%の増加~約450%の増加、約250%の増加~約400%の増加、約250%の増加~約350%の増加、約250%の増加~約300%の増加、約300%の増加~約10,000%の増加、約300%の増加~約9,000%の増加、約300%の増加~約8,000%の増加、約300%の増加~約7,000%の増加、約300%の増加~約6,000%の増加、約300%の増加~約5,000%の増加、約300%の増加~約4,000%の増加、約300%の増加~約3,000%の増加、約300%の増加~約2,000%の増加、約300%の増加~約1,000%の増加、約300%の増加~約500%の増加、約300%の増加~約450%の増加、約300%の増加~約400%の増加、約300%の増加~約350%の増加、約350%の増加~約10,000%の増加、約350%の増加~約9,000%の増加、約350%の増加~約8,000%の増加、約350%の増加~約7,000%の増加、約350%の増加~約6,000%の増加、約350%の増加~約5,000%の増加、約350%の増加~約4,000%の増加、約350%の増加~約3,000%の増加、約350%の増加~約2,000%の増加、約350%の増加~約1,000%の増加、約350%の増加~約500%の増加、約350%の増加~約450%の増加、約350%の増加~約400%の増加、約400%の増加~約10,000%の増加、約400%の増加~約9,000%の増加、約400%の増加~約8,000%の増加、約400%の増加~約7,000%の増加、約400%の増加~約6,000%の増加、約400%の増加~約5,000%の増加、約400%の増加~約4,000%の増加、約400%の増加~約3,000%の増加、約400%の増加~約2,000%の増加、約400%の増加~約1,000%の増加、約
400%の増加~約500%の増加、約400%の増加~約450%の増加、約450%の増加~約10,000%の増加、約450%の増加~約9,000%の増加、約450%の増加~約8,000%の増加、約450%の増加~約7,000%の増加、約450%の増加~約6,000%の増加、約450%の増加~約5,000%の増加、約450%の増加~約4,000%の増加、約450%の増加~約3,000%の増加、約450%の増加~約2,000%の増加、約450%の増加~約1,000%の増加、約450%の増加~約500%の増加、約500%の増加~約10,000%の増加、約500%の増加~約9,000%の増加、約500%の増加~約8,000%の増加、約500%の増加~約7,000%の増加、約500%の増加~約6,000%の増加、約500%の増加~約5,000%の増加、約500%の増加~約4,000%の増加、約500%の増加~約3,000%の増加、約500%の増加~約2,000%の増加、約500%の増加~約1,000%の増加、約1,000%の増加~約10,000%の増加、約1,000%の増加~約9,000%の増加、約1,000%の増加~約8,000%の増加、約1,000%の増加~約7,000%の増加、約1,000%の増加~約6,000%の増加、約1,000%の増加~約5,000%の増加、約1,000%の増加~約4,000%の増加、約1,000%の増加~約3,000%の増加、約1,000%の増加~約2,000%の増加、約2,000%の増加~約10,000%の増加、約2,000%の増加~約9,000%の増加、約2,000%の増加~約8,000%の増加、約2,000%の増加~約7,000%の増加、約2,000%の増加~約6,000%の増加、約2,000%の増加~約5,000%の増加、約2,000%の増加~約4,000%の増加、約2,000%の増加~約3,000%の増加、約3,000%の増加~約10,000%の増加、約3,000%の増加~約9,000%の増加、約3,000%の増加~約8,000%の増加、約3,000%の増加~約7,000%の増加、約3,000%の増加~約6,000%の増加、約3,000%の増加~約5,000%の増加、約3,000%の増加~約4,000%の増加、約4,000%の増加~約10,000%の増加、約4,000%の増加~約9,000%の増加、約4,000%の増加~約8,000%の増加、約4,000%の増加~約7,000%の増加、約4,000%の増加~約6,000%の増加、約4,000%の増加~約5,000%の増加、約5,000%の増加~約10,000%の増加、約5,000%の増加~約9,000%の増加、約5,000%の増加~約8,000%の増加、約5,000%の増加~約7,000%の増加、約5,000%の増加~約6,000%の増加、約6,000%の増加~約10,000%の増加、約6,000%の増加~約9,000%の増加、約6,000%の増加~約8,000%の増加、約6,000%の増加~約7,000%の増加、約7,000%の増加~約10,000%の増加、約7,000%の増加~約9,000%の増加、約7,000%の増加~約8,000%の増加、約8,000%の増加~約10,000%の増加、約8,000%の増加~約9,000%の増加、または約9,000%の増加~約10,000%)、を提供することが可能である。
本明細書に記載されるいずれかのABPCの一部の実施例では、ABPC(例えば、本明細書に記載されるABPCのいずれか)を含む組成物は、同量の対照ABPC(例えば、本明細書に記載される例示的な対照ABPCのいずれか)を含む組成物と比較して、標的哺乳動物細胞(例えば、本明細書に記載される標的哺乳動物細胞のいずれか)における毒素放出の増加(例えば、検出可能な増加)(例えば、少なくとも0.1倍の増加、少なくとも0.2倍の増加、少なくとも0.3倍の増加、少なくとも0.4倍の増加、少なくとも0.5倍の増加、少なくとも0.6倍の増加、少なくとも0.7倍の増加、少なくとも0.8倍の増加、少なくとも0.9倍の増加、少なくとも1.0倍の増加、少なくとも1.2倍の増加、少なくとも1.4倍の増加、少なくとも1.5倍の増加、少なくとも1.6倍の増加、少なくとも1.8倍の増加、少なくとも2.0倍の増加、少なくとも2.2倍の増加、少なくとも2.4倍の増加、少なくとも2.5倍の増加、少なくとも2.6倍の増加、少なくとも2.8倍の増加、少なくとも3.0倍の増加、少なくとも3.5倍の増加、少なくとも4.0倍の増加、少なくとも4.5倍の増加、少なくとも5.0倍の増加、少なくとも5.5倍の増加、少なくとも6.0倍の増加、少なくとも6.5倍の増加、少なくとも7.0倍の増加、少なくとも7.5倍の増加、少なくとも8.0倍の増加、少なくとも8.5倍の増加、少なくとも9.0倍の増加、少なくとも9.5倍の増加、少なくとも10倍の増加、少なくとも15倍の増加、少なくとも20倍の増加、少なくとも25倍の増加、少なくとも30倍の増加、少なくとも35倍の増加、少なくとも40倍の増加、少なくとも45倍の増加、少なくとも50倍の増加、少なくとも55倍の増加、少なくとも60倍の増加、少なくとも65倍の増加、少なくとも70倍の増加、少なくとも75倍の増加、少なくとも80倍の増加、少なくとも85倍の増加、少なくとも90倍の増加、少なくとも95倍の増加、もしくは少なくとも100倍の増加、または約0.1倍の増加~約100倍の増加、約0.1倍の増加~約90倍の増加、約0.1倍の増加~約80倍の増加、約0.1倍の増加~約70倍の増加、約0.1倍の増加~約60倍の増加、約0.1倍の増加~約50倍の増加、約0.1倍の増加~約40倍の増加、約0.1倍の増加~約30倍の増加、約0.1倍の増加~約20倍の増加、約0.1倍の増加~約10倍の増加、約0.1倍の増加~約9.5倍の増加、約0.1倍の増加~約9.0倍の増加、約0.1倍の増加~約8.5倍の増加、約0.1倍の増加~約8.0倍の増加、約0.1倍の増加~約7.5倍の増加、約0.1倍の増加~約7.0倍の増加、約0.1倍の増加~約6.5倍の増加、約0.1倍の増加~約6.0倍の増加、約0.1倍の増加~約5.5倍の増加、約0.1倍の増加~約5.0倍の増加、約0.1倍の増加~約4.5倍の増加、約0.1倍の増加~約4.0倍の増加、約0.1倍の増加~約3.5倍の増加、約0.1倍の増加~約3.0倍の増加、約0.1倍の増加~約2.8倍の増加、約0.1倍の増加~約2.6倍の増加、約0.1倍の増加~約2.5倍の増加、約0.1倍の増加~約2.4倍の増加、約0.1倍の増加~約2.2倍の増加、約0.1倍の増加~約2.0倍の増加、約0.1倍の増加~約1.8倍の増加、約0.1倍の増加~約1.6倍の増加、約0.1倍の増加~約1.5倍の増加、約0.1倍の増加~約1.4倍の増加、約0.1倍の増加~約1.2倍の増加、約0.1倍の増加~約1.0倍の増加、約0.1倍の増加~約0.9倍の増加、約0.1倍の増加~約0.8倍の増加、約0.1倍の増加~約0.7倍の増加、約0.1倍の増加~約0.6倍の増加、約0.1倍の増加~約0.5倍の増加、約0.1倍の増加~約0.4倍の増加、約0.1倍の増加~約0.3倍の増加、約0.2倍の増加~約100倍の増加、約0.2倍の増加~約90倍の増加、約0.2倍の増加~約80倍の増加、約0.2倍の増加~約70倍の増加、約0.2倍の増加~約60倍の増加、約0.2倍の増加~約50倍の増加、約0.2倍の増加~約40倍の増加、約0.2倍の増加~約30倍の増加、約0.2倍の増加~約20倍の増加、約0.2倍の増加~約10倍の増加、約0.2倍の増加~約9.5倍の増加、約0.2倍の増加~約9.0倍の増加、約0.2倍の増加~約8.5倍の増加、約0.2倍の増加~約8.0倍の増加、約0.2倍の増加~約7.5倍の増加、約0.2倍の増加~約7.0倍の増加、約0.2倍の増加~約6.5倍の増加、約0.2倍の増加~約6.0倍の増加、約0.2倍の増加~約5.5倍の増加、約0.2倍の増加~約5.0倍の増加、約0.2倍の増加~約4.5倍の増加、約0.2倍の増加~約4.0倍の増加、約0.2倍の増加~約3.5倍の増加、約0.2倍の増加~約3.0倍の増加、約0.2倍の増加~約2.8倍の増加、約0.2倍の増加~約2.6倍の増加、約0.2倍の増加~約2.5倍の増加、約0.2倍の増加~約2.4倍の増加、約0.2倍の増加~約2.2倍の増加、約0.2倍の増加~約2.0倍の増加、約0.2倍の増加~約1.8倍の増加、約0.2倍の増加~約1.6倍の増加、約0.2倍の増加~約1.5倍の増加、約0.2倍の増加~約1.4倍の増加、約0.2倍の増加~約1.2倍の増加、約0.2倍の増加~約1.0倍の増加、約0.2倍の増加~約0.9倍の増加、約0.2倍の増加~約0.8倍の増加、約0.2倍の増加~約0.7倍の増加、約0.2倍の増加~約0.6倍の増加、約0.2倍の増加~約0.5倍の増加、約0.2倍の増加~約0.4倍の増加、約0.3倍の増加~約100倍の増加、約0.3倍の増加~約90倍の増加、約0.3倍の増加~約80倍の増加、約0.3倍の増加~約70倍の増加、約0.3倍の増加~約60倍の増加、約0.3倍の増加~約50倍の増加、約0.3倍の増加~約40倍の増加、約0.3倍の増加~約30倍の増加、約0.3倍の増加~約20倍の増加、約0.3倍の増加~約10倍の増加、約0.3倍の増加~約9.5倍の増加、約0.3倍の増加~約9.0倍の増加、約0.3倍の増加~約8.5倍の増加、約0.3倍の増加~約8.0倍の増加、約0.3倍の増加~約7.5倍の増加、約0.3倍の増加~約7.0倍の増加、約0.3倍の増加~約6.5倍の増加、約0.3倍の増加~約6.0倍の増加、約0.3倍の増加~約5.5倍の増加、約0.3倍の増加~約5.0倍の増加、約0.3倍の増加~約4.5倍の増加、約0.3倍の増加~約4.0倍の増加、約0.3倍の増加~約3.5倍の増加、約0.3倍の増加~約3.0倍の増加、約0.3倍の増加~約2.8倍の増加、約0.3倍の増加~約2.6倍の増加、約0.3倍の増加~約2.5倍の増加、約0.3倍の増加~約2.4倍の増加、約0.3倍の増加~約2.2倍の増加、約0.3倍の増加~約2.0倍の増加、約0.3倍の増加~約1.8倍の増加、約0.3倍の増加~約1.6倍の増加、約0.3倍の増加~約1.5倍の増加、約0.3倍の増加~約1.4倍の増加、約0.3倍の増加~約1.2倍の増加、約0.3倍の増加~約1.0倍の増加、約0.3倍の増加~約0.9倍の増加、約0.3倍の増加~約0.8倍の増加、約0.3倍の増加~約0.7倍の増加、約0.3倍の増加~約0.6倍の増加、約0.3倍の増加~約0.5倍の増加、約0.4倍の増加~約100倍の増加、約0.4倍の増加~約90倍の増加、約0.4倍の増加~約80倍の増加、約0.4倍の増加~約70倍の増加、約0.4倍の増加~約60倍の増加、約0.4倍の増加~約50倍の増加、約0.4倍の増加~約40倍の増加、約0.4倍の増加~約30倍の増加、約0.4倍の増加~約20倍の増加、約0.4倍の増加~約10倍の増加、約0.4倍の増加~約9.5倍の増加、約0.4倍の増加~約9.0倍の増加、約0.4倍の増加~約8.5倍の増加、約0.4倍の増加~約8.0倍の増加、約0.4倍の増加~約7.5倍の増加、約0.4倍の増加~約7.0倍の増加、約0.4倍の増加~約6.5倍の増加、約0.4倍の増加~約6.0倍の増加、約0.4倍の増加~約5.5倍の増加、約0.4倍の増加~約5.0倍の増加、約0.4倍の増加~約4.5倍の増加、約0.4倍の増加~約4.0倍の増加、約0.4倍の増加~約3.5倍の増加、約0.4倍の増加~約3.0倍の増加、約0.4倍の増加~約2.8倍の増加、約0.4倍の増加~約2.6倍の増加、約0.4倍の増加~約2.5倍の増加、約0.4倍の増加~約2.4倍の増加、約0.4倍の増加~約2.2倍の増加、約0.4倍の増加~約2.0倍の増加、約0.4倍の増加~約1.8倍の増加、約0.4倍の増加~約1.6倍の増加、約0.4倍の増加~約1.5倍の増加、約0.4倍の増加~約1.4倍の増加、約0.4倍の増加~約1.2倍の増加、約0.4倍の増加~約1.0倍の増加、約0.4倍の増加~約0.9倍の増加、約0.4倍の増加~約0.8倍の増加、約0.4倍の増加~約0.7倍の増加、約0.4倍の増加~約0.6倍の増加、約0.5倍の増加~約100倍の増加、約0.5倍の増加~約90倍の増加、約0.5倍の増加~約80倍の増加、約0.5倍の増加~約70倍の増加、約0.5倍の増加~約60倍の増加、約0.5倍の増加~約50倍の増加、約0.5倍の増加~約40倍の増加、約0.5倍の増加~約30倍の増加、約0.5倍の増加~約20倍の増加、約0.5倍の増加~約10倍の増加、約0.5倍の増加~約9.5倍の増加、約0.5倍の増加~約9.0倍の増加、約0.5倍の増加~約8.5倍の増加、約0.5倍の増加~約8.0倍の増加、約0.5倍の増加~約7.5倍の増加、約0.5倍の増加~約7.0倍の増加、約0.5倍の増加~約6.5倍の増加、約0.5倍の増加~約6.0倍の増加、約0.5倍の増加~約5.5倍の増加、約0.5倍の増加~約5.0倍の増加、約0.5倍の増加~約4.5倍の増加、約0.5倍の増加~約4.0倍の増加、約0.5倍の増加~約3.5倍の増加、約0.5倍の増加~約3.0倍の増加、約0.5倍の増加~約2.8倍の増加、約0.5倍の増加~約2.6倍の増加、約0.5倍の増加~約2.5倍の増加、約0.5倍の増加~約2.4倍の増加、約0.5倍の増加~約2.2倍の増加、約0.5倍の増加~約2.0倍の増加、約0.5倍の増加~約1.8倍の増加、約0.5倍の増加~約1.6倍の増加、約0.5倍の増加~約1.5倍の増加、約0.5倍の増加~約1.4倍の増加、約0.5倍の増加~約1.2倍の増加、約0.5倍の増加~約1.0倍の増加、約0.5倍の増加~約0.9倍の増加、約0.5倍の増加~約0.8倍の増加、約0.5倍の増加~約0.7倍の増加、約0.6倍の増加~約100倍の増加、約0.6倍の増加~約90倍の増加、約0.6倍の増加~約80倍の増加、約0.6倍の増加~約70倍の増加、約0.6倍の増加~約60倍の増加、約0.6倍の増加~約50倍の増加、約0.6倍の増加~約40倍の増加、約0.6倍の増加~約30倍の増加、約0.6倍の増加~約20倍の増加、約0.6倍の増加~約10倍の増加、約0.6倍の増加~約9.5倍の増加、約0.6倍の増加~約9.0倍の増加、約0.6倍の増加~約8.5倍の増加、約0.6倍の増加~約8.0倍の増加、約0.6倍の増加~約7.5倍の増加、約0.6倍の増加~約7.0倍の増加、約0.6倍の増加~約6.5倍の増加、約0.6倍の増加~約6.0倍の増加、約0.6倍の増加~約5.5倍の増加、約0.6倍の増加~約5.0倍の増加、約0.6倍の増加~約4.5倍の増加、約0.6倍の増加~約4.0倍の増加、約0.6倍の増加~約3.5倍の増加、約0.6倍の増加~約3.0倍の増加、約0.6倍の増加~約2.8倍の増加、約0.6倍の増加~約2.6倍の増加、約0.6倍の増加~約2.5倍の増加、約0.6倍の増加~約2.4倍の増加、約0.6倍の増加~約2.2倍の増加、約0.6倍の増加~約2.0倍の増加、約0.6倍の増加~約1.8倍の増加、約0.6倍の増加~約1.6倍の増加、約0.6倍の増加~約1.5倍の増加、約0.6倍の増加~約1.4倍の
増加、約0.6倍の増加~約1.2倍の増加、約0.6倍の増加~約1.0倍の増加、約0.6倍の増加~約0.9倍の増加、約0.6倍の増加~約0.8倍の増加、約0.7倍の増加~約100倍の増加、約0.7倍の増加~約90倍の増加、約0.7倍の増加~約80倍の増加、約0.7倍の増加~約70倍の増加、約0.7倍の増加~約60倍の増加、約0.7倍の増加~約50倍の増加、約0.7倍の増加~約40倍の増加、約0.7倍の増加~約30倍の増加、約0.7倍の増加~約20倍の増加、約0.7倍の増加~約10倍の増加、約0.7倍の増加~約9.5倍の増加、約0.7倍の増加~約9.0倍の増加、約0.7倍の増加~約8.5倍の増加、約0.7倍の増加~約8.0倍の増加、約0.7倍の増加~約7.5倍の増加、約0.7倍の増加~約7.0倍の増加、約0.7倍の増加~約6.5倍の増加、約0.7倍の増加~約6.0倍の増加、約0.7倍の増加~約5.5倍の増加、約0.7倍の増加~約5.0倍の増加、約0.7倍の増加~約4.5倍の増加、約0.7倍の増加~約4.0倍の増加、約0.7倍の増加~約3.5倍の増加、約0.7倍の増加~約3.0倍の増加、約0.7倍の増加~約2.8倍の増加、約0.7倍の増加~約2.6倍の増加、約0.7倍の増加~約2.5倍の増加、約0.7倍の増加~約2.4倍の増加、約0.7倍の増加~約2.2倍の増加、約0.7倍の増加~約2.0倍の増加、約0.7倍の増加~約1.8倍の増加、約0.7倍の増加~約1.6倍の増加、約0.7倍の増加~約1.5倍の増加、約0.7倍の増加~約1.4倍の増加、約0.7倍の増加~約1.2倍の増加、約0.7倍の増加~約1.0倍の増加、約0.7倍の増加~約0.9倍の増加、約0.8倍の増加~約100倍の増加、約0.8倍の増加~約90倍の増加、約0.8倍の増加~約80倍の増加、約0.8倍の増加~約70倍の増加、約0.8倍の増加~約60倍の増加、約0.8倍の増加~約50倍の増加、約0.8倍の増加~約40倍の増加、約0.8倍の増加~約30倍の増加、約0.8倍の増加~約20倍の増加、約0.8倍の増加~約10倍の増加、約0.8倍の増加~約9.5倍の増加、約0.8倍の増加~約9.0倍の増加、約0.8倍の増加~約8.5倍の増加、約0.8倍の増加~約8.0倍の増加、約0.8倍の増加~約7.5倍の増加、約0.8倍の増加~約7.0倍の増加、約0.8倍の増加~約6.5倍の増加、約0.8倍の増加~約6.0倍の増加、約0.8倍の増加~約5.5倍の増加、約0.8倍の増加~約5.0倍の増加、約0.8倍の増加~約4.5倍の増加、約0.8倍の増加~約4.0倍の増加、約0.8倍の増加~約3.5倍の増加、約0.8倍の増加~約3.0倍の増加、約0.8倍の増加~約2.8倍の増加、約0.8倍の増加~約2.6倍の増加、約0.8倍の増加~約2.5倍の増加、約0.8倍の増加~約2.4倍の増加、約0.8倍の増加~約2.2倍の増加、約0.8倍の増加~約2.0倍の増加、約0.8倍の増加~約1.8倍の増加、約0.8倍の増加~約1.6倍の増加、約0.8倍の増加~約1.5倍の増加、約0.8倍の増加~約1.4倍の増加、約0.8倍の増加~約1.2倍の増加、約0.8倍の増加~約1.0倍の増加、約1.0倍の増加~約100倍の増加、約1.0倍の増加~約90倍の増加、約1.0倍の増加~約80倍の増加、約1.0倍の増加~約70倍の増加、約1.0倍の増加~約60倍の増加、約1.0倍の増加~約50倍の増加、約1.0倍の増加~約40倍の増加、約1.0倍の増加~約30倍の増加、約1.0倍の増加~約20倍の増加、約1.0倍の増加~約10倍の増加、約1.0倍の増加~約9.5倍の増加、約1.0倍の増加~約9.0倍の増加、約1.0倍の増加~約8.5倍の増加、約1.0倍の増加~約8.0倍の増加、約1.0倍の増加~約7.5倍の増加、約1.0倍の増加~約7.0倍の増加、約1.0倍の増加~約6.5倍の増加、約1.0倍の増加~約6.0倍の増加、約1.0倍の増加~約5.5倍の増加、約1.0倍の増加~約5.0倍の増加、約1.0倍の増加~約4.5倍の増加、約1.0倍の増加~約4.0倍の増加、約1.0倍の増加~約3.5倍の増加、約1.0倍の増加~約3.0倍の増加、約1.0倍の増加~約2.8倍の増加、約1.0倍の増加~約2.6倍の増加、約1.0倍の増加~約2.5倍の増加、約1.0倍の増加~約2.4倍の増加、約1.0倍の増加~約2.2倍の増加、約1.0倍の増加~約2.0倍の増加、約1.0倍の増加~約1.8倍の増加、約1.0倍の増加~約1.6倍の増加、約1.0倍の増加~約1.5倍の増加、約1.0倍の増加~約1.4倍の増加、約1.0倍の増加~約1.2倍の増加、約1.2倍の増加~約100倍の増加、約1.2倍の増加~約90倍の増加、約1.2倍の増加~約80倍の増加、約1.2倍の増加~約70倍の増加、約1.2倍の増加~約60倍の増加、約1.2倍の増加~約50倍の増加、約1.2倍の増加~約40倍の増加、約1.2倍の増加~約30倍の増加、約1.2倍の増加~約20倍の増加、約1.2倍の増加~約10倍の増加、約1.2倍の増加~約9.5倍の増加、約1.2倍の増加~約9.0倍の増加、約1.2倍の増加~約8.5倍の増加、約1.2倍の増加~約8.0倍の増加、約1.2倍の増加~約7.5倍の増加、約1.2倍の増加~約7.0倍の増加、約1.2倍の増加~約6.5倍の増加、約1.2倍の増加~約6.0倍の増加、約1.2倍の増加~約5.5倍の増加、約1.2倍の増加~約5.0倍の増加、約1.2倍の増加~約4.5倍の増加、約1.2倍の増加~約4.0倍の増加、約1.2倍の増加~約3.5倍の増加、約1.2倍の増加~約3.0倍の増加、約1.2倍の増加~約2.8倍の増加、約1.2倍の増加~約2.6倍の増加、約1.2倍の増加~約2.5倍の増加、約1.2倍の増加~約2.4倍の増加、約1.2倍の増加~約2.2倍の増加、約1.2倍の増加~約2.0倍の増加、約1.2倍の増加~約1.8倍の増加、約1.2倍の増加~約1.6倍の増加、約1.2倍の増加~約1.5倍の増加、約1.2倍の増加~約1.4倍の増加、約1.4倍の増加~約100倍の増加、約1.4倍の増加~約90倍の増加、約1.4倍の増加~約80倍の増加、約1.4倍の増加~約70倍の増加、約1.4倍の増加~約60倍の増加、約1.4倍の増加~約50倍の増加、約1.4倍の増加~約40倍の増加、約1.4倍の増加~約30倍の増加、約1.4倍の増加~約20倍の増加、約1.4倍の増加~約10倍の増加、約1.4倍の増加~約9.5倍の増加、約1.4倍の増加~約9.0倍の増加、約1.4倍の増加~約8.5倍の増加、約1.4倍の増加~約8.0倍の増加、約1.4倍の増加~約7.5倍の増加、約1.4倍の増加~約7.0倍の増加、約1.4倍の増加~約6.5倍の増加、約1.4倍の増加~約6.0倍の増加、約1.4倍の増加~約5.5倍の増加、約1.4倍の増加~約5.0倍の増加、約1.4倍の増加~約4.5倍の増加、約1.4倍の増加~約4.0倍の増加、約1.4倍の増加~約3.5倍の増加、約1.4倍の増加~約3.0倍の増加、約1.4倍の増加~約2.8倍の増加、約1.4倍の増加~約2.6倍の増加、約1.4倍の増加~約2.5倍の増加、約1.4倍の増加~約2.4倍の増加、約1.4倍の増加~約2.2倍の増加、約1.4倍の増加~約2.0倍の増加、約1.4倍の増加~約1.8倍の増加、約1.4倍の増加~約1.6倍の増加、約1.6倍の増加~約10倍の増加、約1.6倍の増加~約100倍の増加、約1.6倍の増加~約90倍の増加、約1.6倍の増加~約80倍の増加、約1.6倍の増加~約70倍の増加、約1.6倍の増加~約60倍の増加、約1.6倍の増加~約50倍の増加、約1.6倍の増加~約40倍の増加、約1.6倍の増加~約30倍の増加、約1.6倍の増加~約20倍の増加、約1.6倍の増加~約9.5倍の増加、約1.6倍の増加~約9.0倍の増加、約1.6倍の増加~約8.5倍の増加、約1.6倍の増加~約8.0倍の増加、約1.6倍の増加~約7.5倍の増加、約1.6倍の増加~約7.0倍の増加、約1.6倍の増加~約6.5倍の増加、約1.6倍の増加~約6.0倍の増加、約1.6倍の増加~約5.5倍の増加、約1.6倍の増加~約5.0倍の増加、約1.6倍の増加~約4.5倍の増加、約1.6倍の増加~約4.0倍の増加、約1.6倍の増加~約3.5倍の増加、約1.6倍の増加~約3.0倍の増加、約1.6倍の増加~約2.8倍の増加、約1.6倍の増加~約2.6倍の増加、約1.6倍の増加~約2.5倍の増加、約1.6倍の増加~約2.4倍の増加、約1.6倍の増加~約2.2倍の増加、約1.6倍の増加~約2.0倍の増加、約1.6倍の増加~約1.8倍の増加、約1.8倍の増加~約100倍の増加、約1.8倍の増加~約90倍の増加、約1.8倍の増加~約80倍の増加、約1.8倍の増加~約70倍の増加、約1.8倍の増加~約60倍の増加、約1.8倍の増加~約50倍の増加、約1.8倍の増加~約40倍の増加、約1.8倍の増加~約30倍の増加、約1.8倍の増加~約20倍の増加、約1.8倍の増加~約10倍の増加、約1.8倍の増加~約9.5倍の増加、約1.8倍の増加~約9.0倍の増加、約1.8倍の増加~約8.5倍の増加、約1.8倍の増加~約8.0倍の増加、約1.8倍の増加~約7.5倍の増加、約1.8倍の増加~約7.0倍の増加、約1.8倍の増加~約6.5倍の増加、約1.8倍の増加~約6.0倍の増加、約1.8倍の増加~約5.5倍の増加、約1.8倍の増加~約5.0倍の増加、約1.8倍の増加~約4.5倍の増加、約1.8倍の増加~約4.0倍の増加、約1.8倍の増加~約3.5倍の増加、約1.8倍の増加~約3.0倍の増加、約1.8倍の増加~約2.8倍の増加、約1.8倍の増加~約2.6倍の増加、約1.8倍の増加~約2.5倍の増加、約1.8倍の増加~約2.4倍の増加、約1.8倍の増加~約2.2倍の増加、約1.8倍の増加~約2.0倍の増加、約2.0倍の増加~約100倍の増加、約2.0倍の増加~約90倍の増加、約2.0倍の増加~約80倍の増加、約2.0倍の増加~約70倍の増加、約2.0倍の増加~約60倍の増加、約2.0倍の増加~約50倍の増加、約2.0倍の増加~約40倍の増加、約2.0倍の増加~約30倍の増加、約2.0倍の増加~約20倍の増加、約2.0倍の増加~約10倍の増加、約2.0倍の増加~約9.5倍の増加、約2.0倍の増加~約9.0倍の増加、約2.0倍の増加~約8.5倍の増加、約2.0倍の増加~約8.0倍の増加、約2.0倍の増加~約7.5倍の増加、約2.0倍の増加~約7.0倍の増加、約2.0倍の増加~約6.5倍の増加、約2.0倍の増加~約6.0倍の増加、約2.0倍の増加~約5.5倍の増加、約2.0倍の増加~約5.0倍の増加、約2.0倍の増加~約4.5倍の増加、約2.0倍の増加~約4.0倍の増加、約2.0倍の増加~約3.5倍の増加、約2.0倍の増加~約3.0倍の増加、約2.0倍の増加~約2.8倍の増加、約2.0倍の増加~約2.6倍の増加、約2.0倍の増加~約2.5倍の増加、約2.0倍の増加~約2.4倍の増加、約2.0倍の増加~約2.2倍の増加、約2.2倍の増加~約100倍の増加、約2.2倍の増加~約90倍の増加、約2.2倍の増加~約80倍の増加、約2.2倍の増加~約70倍の増加、約2.2倍の増加~約60倍の増加、約2.2倍の増加~約50倍の増加、約2.2倍の増加~約40倍の増加、約2.2倍の増加~約30倍の増加、約2.2倍の増加~約20倍の増加、約2.2倍の増加~約10倍の増加、約2.2倍の増加~約9.5倍の増加、約2.2倍の増加~約9.0倍の増加、約2.2倍の増加~約8.5倍の増加、約2.2倍の増加~約8.0倍の増加、約2.2倍の増加~約7.5倍の増加、約2.2倍の増加~約7.0倍の増加、約2.2倍の増加~約6.5倍の増加、約2.2倍の増加~約6.0倍の増加、約2.2倍の増加~約5.5倍の増加、約2.2倍の増加~約5.0倍の増加、約2.2倍の増加~約4.5倍の
増加、約2.2倍の増加~約4.0倍の増加、約2.2倍の増加~約3.5倍の増加、約2.2倍の増加~約3.0倍の増加、約2.2倍の増加~約2.8倍の増加、約2.2倍の増加~約2.6倍の増加、約2.2倍の増加~約2.5倍の増加、約2.2倍の増加~約2.4倍の増加、約2.4倍の増加~約100倍の増加、約2.4倍の増加~約90倍の増加、約2.4倍の増加~約80倍の増加、約2.4倍の増加~約70倍の増加、約2.4倍の増加~約60倍の増加、約2.4倍の増加~約50倍の増加、約2.4倍の増加~約40倍の増加、約2.4倍の増加~約30倍の増加、約2.4倍の増加~約20倍の増加、約2.4倍の増加~約10倍の増加、約2.4倍の増加~約9.5倍の増加、約2.4倍の増加~約9.0倍の増加、約2.4倍の増加~約8.5倍の増加、約2.4倍の増加~約8.0倍の増加、約2.4倍の増加~約7.5倍の増加、約2.4倍の増加~約7.0倍の増加、約2.4倍の増加~約6.5倍の増加、約2.4倍の増加~約6.0倍の増加、約2.4倍の増加~約5.5倍の増加、約2.4倍の増加~約5.0倍の増加、約2.4倍の増加~約4.5倍の増加、約2.4倍の増加~約4.0倍の増加、約2.4倍の増加~約3.5倍の増加、約2.4倍の増加~約3.0倍の増加、約2.4倍の増加~約2.8倍の増加、約2.4倍の増加~約2.6倍の増加、約2.6倍の増加~約100倍の増加、約2.6倍の増加~約90倍の増加、約2.6倍の増加~約80倍の増加、約2.6倍の増加~約70倍の増加、約2.6倍の増加~約60倍の増加、約2.6倍の増加~約50倍の増加、約2.6倍の増加~約40倍の増加、約2.6倍の増加~約30倍の増加、約2.6倍の増加~約20倍の増加、約2.6倍の増加~約10倍の増加、約2.6倍の増加~約9.5倍の増加、約2.6倍の増加~約9.0倍の増加、約2.6倍の増加~約8.5倍の増加、約2.6倍の増加~約8.0倍の増加、約2.6倍の増加~約7.5倍の増加、約2.6倍の増加~約7.0倍の増加、約2.6倍の増加~約6.5倍の増加、約2.6倍の増加~約6.0倍の増加、約2.6倍の増加~約5.5倍の増加、約2.6倍の増加~約5.0倍の増加、約2.6倍の増加~約4.5倍の増加、約2.6倍の増加~約4.0倍の増加、約2.6倍の増加~約3.5倍の増加、約2.6倍の増加~約3.0倍の増加、約2.6倍の増加~約2.8倍の増加、約2.8倍の増加~約100倍の増加、約2.8倍の増加~約90倍の増加、約2.8倍の増加~約80倍の増加、約2.8倍の増加~約70倍の増加、約2.8倍の増加~約60倍の増加、約2.8倍の増加~約50倍の増加、約2.8倍の増加~約40倍の増加、約2.8倍の増加~約30倍の増加、約2.8倍の増加~約20倍の増加、約2.8倍の増加~約10倍の増加、約2.8倍の増加~約9.5倍の増加、約2.8倍の増加~約9.0倍の増加、約2.8倍の増加~約8.5倍の増加、約2.8倍の増加~約8.0倍の増加、約2.8倍の増加~約7.5倍の増加、約2.8倍の増加~約7.0倍の増加、約2.8倍の増加~約6.5倍の増加、約2.8倍の増加~約6.0倍の増加、約2.8倍の増加~約5.5倍の増加、約2.8倍の増加~約5.0倍の増加、約2.8倍の増加~約4.5倍の増加、約2.8倍の増加~約4.0倍の増加、約2.8倍の増加~約3.5倍の増加、約2.8倍の増加~約3.0倍の増加、約3.0倍の増加~約100倍の増加、約3.0倍の増加~約90倍の増加、約3.0倍の増加~約80倍の増加、約3.0倍の増加~約70倍の増加、約3.0倍の増加~約60倍の増加、約3.0倍の増加~約50倍の増加、約3.0倍の増加~約40倍の増加、約3.0倍の増加~約30倍の増加、約3.0倍の増加~約20倍の増加、約3.0倍の増加~約10倍の増加、約3.0倍の増加~約9.5倍の増加、約3.0倍の増加~約9.0倍の増加、約3.0倍の増加~約8.5倍の増加、約3.0倍の増加~約8.0倍の増加、約3.0倍の増加~約7.5倍の増加、約3.0倍の増加~約7.0倍の増加、約3.0倍の増加~約6.5倍の増加、約3.0倍の増加~約6.0倍の増加、約3.0倍の増加~約5.5倍の増加、約3.0倍の増加~約5.0倍の増加、約3.0倍の増加~約4.5倍の増加、約3.0倍の増加~約4.0倍の増加、約3.0倍の増加~約3.5倍の増加、約3.5倍の増加~約100倍の増加、約3.5倍の増加~約90倍の増加、約3.5倍の増加~約80倍の増加、約3.5倍の増加~約70倍の増加、約3.5倍の増加~約60倍の増加、約3.5倍の増加~約50倍の増加、約3.5倍の増加~約40倍の増加、約3.5倍の増加~約30倍の増加、約3.5倍の増加~約20倍の増加、約3.5倍の増加~約10倍の増加、約3.5倍の増加~約9.5倍の増加、約3.5倍の増加~約9.0倍の増加、約3.5倍の増加~約8.5倍の増加、約3.5倍の増加~約8.0倍の増加、約3.5倍の増加~約7.5倍の増加、約3.5倍の増加~約7.0倍の増加、約3.5倍の増加~約6.5倍の増加、約3.5倍の増加~約6.0倍の増加、約3.5倍の増加~約5.5倍の増加、約3.5倍の増加~約5.0倍の増加、約3.5倍の増加~約4.5倍の増加、約3.5倍の増加~約4.0倍の増加、約4.0倍の増加~約100倍の増加、約4.0倍の増加~約90倍の増加、約4.0倍の増加~約80倍の増加、約4.0倍の増加~約70倍の増加、約4.0倍の増加~約60倍の増加、約4.0倍の増加~約50倍の増加、約4.0倍の増加~約40倍の増加、約4.0倍の増加~約30倍の増加、約4.0倍の増加~約20倍の増加、約4.0倍の増加~約10倍の増加、約4.0倍の増加~約9.5倍の増加、約4.0倍の増加~約9.0倍の増加、約4.0倍の増加~約8.5倍の増加、約4.0倍の増加~約8.0倍の増加、約4.0倍の増加~約7.5倍の増加、約4.0倍の増加~約7.0倍の増加、約4.0倍の増加~約6.5倍の増加、約4.0倍の増加~約6.0倍の増加、約4.0倍の増加~約5.5倍の増加、約4.0倍の増加~約5.0倍の増加、約4.0倍の増加~約4.5倍の増加、約4.5倍の増加~約100倍の増加、約4.5倍の増加~約90倍の増加、約4.5倍の増加~約80倍の増加、約4.5倍の増加~約70倍の増加、約4.5倍の増加~約60倍の増加、約4.5倍の増加~約50倍の増加、約4.5倍の増加~約40倍の増加、約4.5倍の増加~約30倍の増加、約4.5倍の増加~約20倍の増加、約4.5倍の増加~約10倍の増加、約4.5倍の増加~約9.5倍の増加、約4.5倍の増加~約9.0倍の増加、約4.5倍の増加~約8.5倍の増加、約4.5倍の増加~約8.0倍の増加、約4.5倍の増加~約7.5倍の増加、約4.5倍の増加~約7.0倍の増加、約4.5倍の増加~約6.5倍の増加、約4.5倍の増加~約6.0倍の増加、約4.5倍の増加~約5.5倍の増加、約4.5倍の増加~約5.0倍の増加、約5.0倍の増加~約100倍の増加、約5.0倍の増加~約90倍の増加、約5.0倍の増加~約80倍の増加、約5.0倍の増加~約70倍の増加、約5.0倍の増加~約60倍の増加、約5.0倍の増加~約50倍の増加、約5.0倍の増加~約40倍の増加、約5.0倍の増加~約30倍の増加、約5.0倍の増加~約20倍の増加、約5.0倍の増加~約10倍の増加、約5.0倍の増加~約9.5倍の増加、約5.0倍の増加~約9.0倍の増加、約5.0倍の増加~約8.5倍の増加、約5.0倍の増加~約8.0倍の増加、約5.0倍の増加~約7.5倍の増加、約5.0倍の増加~約7.0倍の増加、約5.0倍の増加~約6.5倍の増加、約5.0倍の増加~約6.0倍の増加、約5.0倍の増加~約5.5倍の増加、約5.5倍の増加~約100倍の増加、約5.5倍の増加~約90倍の増加、約5.5倍の増加~約80倍の増加、約5.5倍の増加~約70倍の増加、約5.5倍の増加~約60倍の増加、約5.5倍の増加~約50倍の増加、約5.5倍の増加~約40倍の増加、約5.5倍の増加~約30倍の増加、約5.5倍の増加~約20倍の増加、約5.5倍の増加~約10倍の増加、約5.5倍の増加~約9.5倍の増加、約5.5倍の増加~約9.0倍の増加、約5.5倍の増加~約8.5倍の増加、約5.5倍の増加~約8.0倍の増加、約5.5倍の増加~約7.5倍の増加、約5.5倍の増加~約7.0倍の増加、約5.5倍の増加~約6.5倍の増加、約5.5倍の増加~約6.0倍の増加、約6.0倍の増加~約100倍の増加、約6.0倍の増加~約90倍の増加、約6.0倍の増加~約80倍の増加、約6.0倍の増加~約70倍の増加、約6.0倍の増加~約60倍の増加、約6.0倍の増加~約50倍の増加、約6.0倍の増加~約40倍の増加、約6.0倍の増加~約30倍の増加、約6.0倍の増加~約20倍の増加、約6.0倍の増加~約10倍の増加、約6.0倍の増加~約9.5倍の増加、約6.0倍の増加~約9.0倍の増加、約6.0倍の増加~約8.5倍の増加、約6.0倍の増加~約8.0倍の増加、約6.0倍の増加~約7.5倍の増加、約6.0倍の増加~約7.0倍の増加、約6.0倍の増加~約6.5倍の増加、約6.5倍の増加~約100倍の増加、約6.5倍の増加~約90倍の増加、約6.5倍の増加~約80倍の増加、約6.5倍の増加~約70倍の増加、約6.5倍の増加~約60倍の増加、約6.5倍の増加~約50倍の増加、約6.5倍の増加~約40倍の増加、約6.5倍の増加~約30倍の増加、約6.5倍の増加~約20倍の増加、約6.5倍の増加~約10倍の増加、約6.5倍の増加~約9.5倍の増加、約6.5倍の増加~約9.0倍の増加、約6.5倍の増加~約8.5倍の増加、約6.5倍の増加~約8.0倍の増加、約6.5倍の増加~約7.5倍の増加、約6.5倍の増加~約7.0倍の増加、約7.0倍の増加~約100倍の増加、約7.0倍の増加~約90倍の増加、約7.0倍の増加~約80倍の増加、約7.0倍の増加~約70倍の増加、約7.0倍の増加~約60倍の増加、約7.0倍の増加~約50倍の増加、約7.0倍の増加~約40倍の増加、約7.0倍の増加~約30倍の増加、約7.0倍の増加~約20倍の増加、約7.0倍の増加~約10倍の増加、約7.0倍の増加~約9.5倍の増加、約7.0倍の増加~約9.0倍の増加、約7.0倍の増加~約8.5倍の増加、約7.0倍の増加~約8.0倍の増加、約7.0倍の増加~約7.5倍の増加、約7.5倍の増加~約100倍の増加、約7.5倍の増加~約90倍の増加、約7.5倍の増加~約80倍の増加、約7.5倍の増加~約70倍の増加、約7.5倍の増加~約60倍の増加、約7.5倍の増加~約50倍の増加、約7.5倍の増加~約40倍の増加、約7.5倍の増加~約30倍の増加、約7.5倍の増加~約20倍の増加、約7.5倍の増加~約10倍の増加、約7.5倍の増加~約9.5倍の増加、約7.5倍の増加~約9.0倍の増加、約7.5倍の増加~約8.5倍の増加、約7.5倍の増加~約8.0倍の増加、約8.0倍の増加~約100倍の増加、約8.0倍の増加~約90倍の増加、約8.0倍の増加~約80倍の増加、約8.0倍の増加~約70倍の増加、約8.0倍の増加~約60倍の増加、約8.0倍の増加~約50倍の増加、約8.0倍の増加~約40倍の増加、約8.0倍の増加~約30倍の増加、約8.0倍の増加~約20倍の増加、約8.0倍の増加~約10倍の増加、約8.0倍の増加~約9.5倍の増加、約8.0倍の増加~約9.0倍の増加、約8.0倍の増加~約8.5倍の増加、約8.5倍の増加~約100倍の増加、約8.5倍の増加~約90倍の増加、約8.5倍の増加~約80倍の増加、約8.5倍の増加~約70倍の増加、約8.5倍の増加~約60倍の増加、約8.5倍の増加~約50倍の増加、約8.5倍の増加~約40倍の増加、約8.5倍の増加~約30倍の増加、約8.5倍の増加~約20倍の増加、約8.5倍の増加~約10倍の増加、約8.5倍の増加~約9.5倍の増加、約8.5倍の増加~約9.0倍の
増加、約9.0倍の増加~約100倍の増加、約9.0倍の増加~約90倍の増加、約9.0倍の増加~約80倍の増加、約9.0倍の増加~約70倍の増加、約9.0倍の増加~約60倍の増加、約9.0倍の増加~約50倍の増加、約9.0倍の増加~約40倍の増加、約9.0倍の増加~約30倍の増加、約9.0倍の増加~約20倍の増加、約9.0倍の増加~約10倍の増加、約9.0倍の増加~約9.5倍の増加、約9.5倍の増加~約100倍の増加、約9.5倍の増加~約90倍の増加、約9.5倍の増加~約80倍の増加、約9.5倍の増加~約70倍の増加、約9.5倍の増加~約60倍の増加、約9.5倍の増加~約50倍の増加、約9.5倍の増加~約40倍の増加、約9.5倍の増加~約30倍の増加、約9.5倍の増加~約20倍の増加、約9.5倍の増加~約10倍の増加、約10倍の増加~約100倍の増加、約10倍の増加~約90倍の増加、約10倍の増加~約80倍の増加、約10倍の増加~約70倍の増加、約10倍の増加~約60倍の増加、約10倍の増加~約50倍の増加、約10倍の増加~約40倍の増加、約10倍の増加~約30倍の増加、約10倍の増加~約20倍の増加、約20倍の増加~約100倍の増加、約20倍の増加~約90倍の増加、約20倍の増加~約80倍の増加、約20倍の増加~約70倍の増加、約20倍の増加~約60倍の増加、約20倍の増加~約50倍の増加、約20倍の増加~約40倍の増加、約20倍の増加~約30倍の増加、約30倍の増加~約100倍の増加、約30倍の増加~約90倍の増加、約30倍の増加~約80倍の増加、約30倍の増加~約70倍の増加、約30倍の増加~約60倍の増加、約30倍の増加~約50倍の増加、約30倍の増加~約40倍の増加、約40倍の増加~約100倍の増加、約40倍の増加~約90倍の増加、約40倍の増加~約80倍の増加、約40倍の増加~約70倍の増加、約40倍の増加~約60倍の増加、約40倍の増加~約50倍の増加、約50倍の増加~約100倍の増加、約50倍の増加~約90倍の増加、約50倍の増加~約80倍の増加、約50倍の増加~約70倍の増加、約50倍の増加~約60倍の増加、約60倍の増加~約100倍の増加、約60倍の増加~約90倍の増加、約60倍の増加~約80倍の増加、約60倍の増加~約70倍の増加、約70倍の増加~約100倍の増加、約70倍の増加~約90倍の増加、約70倍の増加~約80倍の増加、約80倍の増加~約100倍の増加、約80倍の増加~約90倍の増加、もしくは約90倍の増加~約100倍の増加)を提供し得る。
本明細書に記載されるいずれかのABPCの一部の実施例では、ABPC(例えば、本明細書に記載されるABPCのいずれか)を含む組成物は、同量の対照ABPC(例えば、本明細書に記載される例示的な対照ABPCのいずれか)を含む組成物と比較して、標的哺乳動物細胞の殺傷(例えば、本明細書に記載される例示的な標的哺乳動物細胞のいずれか)における増加(例えば、検出可能な増加)(例えば、少なくとも1%の増加、少なくとも2%の増加、少なくとも5%の増加、少なくとも10%の増加、少なくとも15%の増加、少なくとも20%の増加、少なくとも25%の増加、少なくとも30%の増加、少なくとも35%の増加、少なくとも40%の増加、少なくとも45%の増加、少なくとも50%の増加、少なくとも55%の増加、少なくとも60%の増加、少なくとも65%の増加、少なくとも70%の増加、少なくとも75%の増加、少なくとも80%の増加、少なくとも85%の増加、少なくとも90%の増加、少なくとも95%の増加、少なくとも100%の増加、少なくとも120%の増加、少なくとも140%の増加、少なくとも160%の増加、少なくとも180%の増加、少なくとも200%の増加、少なくとも250%の増加、少なくとも300%の増加、少なくとも350%の増加、少なくとも400%の増加、少なくとも450%の増加、少なくとも500%の増加、少なくとも1,000%の増加、少なくとも2,000%の増加、少なくとも3,000%の増加、少なくとも4,000%の増加、少なくとも5,000%の増加、少なくとも6,000%の増加、少なくとも7,000%の増加、少なくとも8,000%の増加、少なくとも9,000%の増加、もしくは少なくとも10,000%の増加、または約1%の増加~約10,000%の増加(例えば、または本明細書に記載するこの範囲の下位の範囲のいずれか))を提供し得る。
本明細書に記載されるいずれかのABPCの一部の実施例では、ABPC(例えば、本明細書に記載されるABPCのいずれか)を含む組成物は、同量の対照ABPC(例えば、本明細書に記載される例示的な対照ABPCのいずれか)を含む組成物と比較して、標的哺乳動物細胞の殺傷(例えば、本明細書に記載される例示的な標的哺乳動物細胞のいずれか)における増加(例えば、検出可能な増加)(例えば、少なくとも0.1倍の増加、少なくとも0.2倍の増加、少なくとも0.3倍の増加、少なくとも0.4倍の増加、少なくとも0.5倍の増加、少なくとも0.6倍の増加、少なくとも0.7倍の増加、少なくとも0.8倍の増加、少なくとも0.9倍の増加、少なくとも1.0倍の増加、少なくとも1.2倍の増加、少なくとも1.4倍の増加、少なくとも1.5倍の増加、少なくとも1.6倍の増加、少なくとも1.8倍の増加、少なくとも2.0倍の増加、少なくとも2.2倍の増加、少なくとも2.4倍の増加、少なくとも2.5倍の増加、少なくとも2.6倍の増加、少なくとも2.8倍の増加、少なくとも3.0倍の増加、少なくとも3.5倍の増加、少なくとも4.0倍の増加、少なくとも4.5倍の増加、少なくとも5.0倍の増加、少なくとも5.5倍の増加、少なくとも6.0倍の増加、少なくとも6.5倍の増加、少なくとも7.0倍の増加、少なくとも7.5倍の増加、少なくとも8.0倍の増加、少なくとも8.5倍の増加、少なくとも9.0倍の増加、少なくとも9.5倍の増加、少なくとも10倍の増加、少なくとも15倍の増加、少なくとも20倍の増加、少なくとも25倍の増加、少なくとも30倍の増加、少なくとも35倍の増加、少なくとも40倍の増加、少なくとも40倍の増加、少なくとも45倍の増加、少なくとも50倍の増加、少なくとも55倍の増加、少なくとも60倍の増加、少なくとも65倍の増加、少なくとも70倍の増加、少なくとも80倍の増加、少なくとも85倍の増加、少なくとも90倍の増加、少なくとも95倍の増加、もしくは少なくとも100倍の増加、または約0.1倍の増加~約100倍の増加(例えば、または本明細書に記載するこの範囲の下位の範囲のいずれか))を提供し得る。
本明細書に記載されるいずれかのABPCの一部の実施例では、本明細書に記載されるABPCのいずれかを含む組成物は(例えば、表面にMETを提示する標的哺乳動物細胞と接触すると)、同量の対照ABPC(例えば、本明細書に記載される対照ABPCのいずれか)を含む組成物のIC50と比較して(例えば、同一の標的哺乳動物細胞と接触すると)、IC50(標的哺乳動物細胞の殺傷に関して)の減少(例えば、少なくとも1%の減少、少なくとも5%の減少、少なくとも10%の減少、少なくとも15%の減少、少なくとも20%の減少、少なくとも25%の減少、少なくとも30%の減少、少なくとも35%の減少、少なくとも40%の減少、少なくとも45%の減少、少なくとも50%の減少、少なくとも55%の減少、少なくとも60%の減少、少なくとも65%の減少、少なくとも70%の減少、少なくとも75%の減少、少なくとも80%の減少、少なくとも85%の減少、少なくとも90%の減少、少なくとも95%の減少、または少なくとも99%の減少、約1%の減少~約99%の減少、または本明細書に記載するこの範囲の下位の範囲のいずれか)をもたらす。
本明細書に記載されるいずれかのABPCの一部の実施例では、本明細書に記載されるABPCのいずれかを含む組成物は(例えば、表面にMETを提示する標的哺乳動物細胞と接触すると)、例えば対照ABPC(例えば、本明細書に記載される例示的な対照ABPCのいずれか)と比較して、中性pH(約7.0~約8.0のpH)での表面にMETを提示する標的哺乳動物細胞におけるKDの、同一の標的細胞上の中性pHでのIC50に対する比の増加(例えば、少なくとも0.1倍の増加、少なくとも0.2倍の増加、少なくとも0.4倍の増加、少なくとも0.6倍の増加、少なくとも0.8倍の増加、少なくとも1倍の増加、少なくとも2倍の増加、少なくとも5倍の増加、少なくとも10倍の増加、少なくとも15倍の増加、少なくとも20倍の増加、少なくとも25倍の増加、少なくとも30倍の増加、少なくとも35倍の増加、少なくとも40倍の増加、少なくとも45倍の増加、少なくとも50倍の増加、少なくとも55倍の増加、少なくとも60倍の増加、少なくとも65倍の増加、少なくとも70倍の増加、少なくとも75倍の増加、少なくとも80倍の増加、少なくとも85倍の増加、少なくとも90倍の増加、少なくとも95倍の増加、もしくは少なくとも100倍の増加、または約0.1倍の増加~約500倍の増加(または本明細書に記載するこの範囲の下位の範囲のいずれか)を提供し得る。
本明細書に記載されるいずれかのABPCの一部の実施例では、ABPCを含む組成物(例えば、本明細書に記載されるABPCのいずれか)は、同量の対照ABPC(例えば、本明細書に記載される例示的な対照ABPCのうちのいずれか)を含む組成物と比較して、標的哺乳動物細胞(例えば、本明細書に記載される例示的な標的哺乳動物細胞のいずれか)におけるエンドリソソーム送達の増加(例えば、検出可能な増加)(例えば、少なくとも1%の増加、少なくとも2%の増加、少なくとも5%の増加、少なくとも10%の増加、少なくとも15%の増加、少なくとも20%の増加、少なくとも25%の増加、少なくとも30%の増加、少なくとも35%の増加、少なくとも40%の増加、少なくとも45%の増加、少なくとも50%の増加、少なくとも55%の増加、少なくとも60%の増加、少なくとも65%の増加、少なくとも70%の増加、少なくとも75%の増加、少なくとも80%の増加、少なくとも85%の増加、少なくとも90%の増加、少なくとも95%の増加、少なくとも100%の増加、少なくとも120%の増加、少なくとも140%の増加、少なくとも160%の増加、少なくとも180%の増加、少なくとも200%の増加、少なくとも250%の増加、少なくとも300%の増加、少なくとも350%の増加、少なくとも400%の増加、少なくとも450%の増加、少なくとも500%の増加、少なくとも1,000%の増加、少なくとも2,000%の増加、少なくとも3,000%の増加、少なくとも4,000%の増加、少なくとも5,000%の増加、少なくとも6,000%の増加、少なくとも7,000%の増加、少なくとも8,000%の増加、少なくとも9,000%の増加、もしくは少なくとも10,000%の増加、または約1%の増加~約10,000%の増加(例えば、または本明細書に記載するこの範囲の下位の範囲のいずれか))を提供し得る。
本明細書に記載されるいずれかのABPCの一部の実施例では、ABPCを含む組成物(例えば、本明細書に記載されるABPCのいずれか)は、同量の対照ABPC(例えば、本明細書に記載される例示的な対照ABPCのうちのいずれか)を含む組成物と比較して、標的哺乳動物細胞(例えば、本明細書に記載される例示的な標的哺乳動物細胞のいずれか)におけるエンドリソソーム送達の増加(例えば、検出可能な増加)(例えば、少なくとも0.1倍の増加、少なくとも0.2倍の増加、少なくとも0.3倍の増加、少なくとも0.4倍の増加、少なくとも0.5倍の増加、少なくとも0.6倍の増加、少なくとも0.7倍の増加、少なくとも0.8倍の増加、少なくとも0.9倍の増加、少なくとも1.0倍の増加、少なくとも1.2倍の増加、少なくとも1.4倍の増加、少なくとも1.5倍の増加、少なくとも1.6倍の増加、少なくとも1.8倍の増加、少なくとも2.0倍の増加、少なくとも2.2倍の増加、少なくとも2.4倍の増加、少なくとも2.5倍の増加、少なくとも2.6倍の増加、少なくとも2.8倍の増加、少なくとも3.0倍の増加、少なくとも3.5倍の増加、少なくとも4.0倍の増加、少なくとも4.5倍の増加、少なくとも5.0倍の増加、少なくとも5.5倍の増加、少なくとも6.0倍の増加、少なくとも6.5倍の増加、少なくとも7.0倍の増加、少なくとも7.5倍の増加、少なくとも8.0倍の増加、少なくとも8.5倍の増加、少なくとも9.0倍の増加、少なくとも9.5倍の増加、少なくとも10倍の増加、少なくとも15倍の増加、少なくとも20倍の増加、少なくとも25倍の増加、少なくとも30倍の増加、少なくとも35倍の増加、少なくとも40倍の増加、少なくとも45倍の増加、少なくとも50倍の増加、少なくとも55倍の増加、少なくとも60倍の増加、少なくとも65倍の増加、少なくとも70倍の増加、少なくとも75倍の増加、少なくとも80倍の増加、少なくとも85倍の増加、少なくとも90倍の増加、少なくとも95倍の増加、もしくは少なくとも100倍の増加、または約0.1倍の増加~約100倍の増加(または本明細書に記載するこの範囲の下位の範囲のいずれか))を提供し得る。
本明細書に記載されるいずれかのABPCの実施例では、標的哺乳動物細胞は、FcRn受容体を発現しないか、または、FcRnを発現する対照細胞(例えば、HUVEC-ThermoFisher社#C0035C)と比較して、FcRn受容体をより低い(例えば、検出可能に低い)レベル(例えば、少なくとも1%の減少、少なくとも2%の減少、少なくとも5%の減少、少なくとも10%の減少、少なくとも15%の減少、少なくとも20%の減少、少なくとも25%の減少、少なくとも30%の減少、少なくとも35%の減少、少なくとも40%の減少、少なくとも45%の減少、少なくとも50%の減少、少なくとも55%の減少、少なくとも60%の減少、少なくとも65%の減少、少なくとも70%の減少、少なくとも75%の減少、少なくとも80%の減少、少なくとも85%の減少、少なくとも90%の減少、少なくとも95%の減少、または少なくとも99%の減少したレベル)で発現する。本明細書に記載されるいずれかのABPCの一部の実施例では、標的哺乳動物細胞が、がん細胞である。本明細書に記載されるいずれかのABPCの一部の実施例では、ABPCが、標的哺乳動物細胞に対し細胞傷害性または細胞増殖抑制性である。
本明細書に記載されるいずれかのABPCの一部の実施例では、本明細書に記載されるいずれかのABPCを含む組成物は(例えば、対象に投与すると)、同量の対照ABPC(例えば、本明細書に記載されるいずれかの対照ABPC)を含む組成物と比較して、標的細胞の表面に存在するMETレベルの減少をそれほど生じさせない(例えば、1%の減少~約99%の減少、または本明細書に記載するこの範囲の下位の範囲のいずれか)。本明細書に記載されるいずれかのABPCの一部の実施例では、組成物は、標的哺乳動物細胞の表面に存在するMETのレベルの検出可能な減少をもたらさない。
本明細書に記載されるいずれかのABPCの一部の実施例では、ABPCが、非ヒト霊長類METおよびヒトMETと交差反応性である。本明細書に記載されるいずれかのABPCの一部の実施例では、ABPCが、非ヒト霊長類MET、ヒトMET、ならびにラットMETおよびマウスMETの一方または両方と交差反応性である。本明細書に記載されるいずれかのABPCの一部の実施例では、ABPCが、非ヒト霊長類MET、ヒトMET、ラットMET、およびマウスMETと交差反応性である。本明細書に記載されるいずれかのABPCの一部の実施例では、ABPCが、マウスMETおよびラットMETと交差反応性である。本明細書に記載されるいずれかのABPCの一部の実施例では、抗原結合ドメインは、旧世界ザル由来の細胞の表面に存在するMETのエピトープに結合する。
本明細書に記載されるいずれかのABPCの一部の実施例は、第二の抗原結合ドメイン(例えば、本明細書に記載されるいずれかの例示的抗原結合ドメイン)をさらに含み得る。
これらの方法の非限定的な態様は、以下に記載され、限定されることなく任意の組み合わせで使用され得る。これらの方法のさらなる態様は、当技術分野で公知である。
METまたはMETのエピトープ
METがん原遺伝子、受容体チロシンキナーゼ(MET)は、当技術分野で公知の腫瘍抗原であり、腫瘍学における治療用抗体の標的である(Wang J et al(2017)ABBV-399,a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors,Irrespective of MET Pathway Dependence,Clin Cancer Res,23:992-1000)。成熟ヒトMETの配列は、配列番号9で見られ得る。 成熟ヒトMETをコードするcDNAの配列は、配列番号10で見られ得る。 METの細胞外ドメインの配列は、配列番号11で見られ得る。 METの細胞外ドメインをコードするcDNAの配列は、配列番号12で見られ得る。
抗原結合タンパク質構築物
本明細書に記載される抗原結合タンパク質構築物(ABPC)のいずれかは、単一のポリペプチドであり得るか、または二個、三個、四個、五個、六個、七個、八個、九個、もしくは十個の(同一または異なる)ポリペプチドを含み得る。ABPCが単一のポリペプチドである一部の実施形態では、ABPCは、単一の抗原結合ドメインまたは二つの抗原結合ドメインを含み得る。ABPCが単一のポリペプチドであり、二つの抗原結合ドメインを含む一部の実施形態では、第一および第二の抗原結合ドメインは、互いに同一であっても、または異なっていてもよい(かつ同一または異なる抗原またはエピトープに特異的に結合することができる)。
ABPCが単一ポリペプチドである一部の実施形態では、第一の抗原結合ドメインおよび第二の抗原結合ドメイン(存在する場合)はそれぞれ、VHドメイン、VHHドメイン、VNARドメイン、およびscFvの群から独立して選択し得る。ABPCが単一ポリペプチドである一部の実施形態では、抗原結合タンパク質構築物は、BiTe、(scFv)2、ナノボディ、ナノボディ-HSA、DART、TandAb、scDiabody、scDiabody-CH3、scFv-CH-CL-scFv、HSAbody、scDiabody-HAS、タンデム-scFv、Adnectin、DARPin、フィブロネクチン、およびDEPコンジュゲートであり得る。ABPCが単一のポリペプチドである場合に使用され得る抗原結合ドメインのさらなる例は、当技術分野で公知である。
VHHドメインは、ラクダ科動物に見出され得る単一の単量体可変抗体ドメインである。VNARドメインは、軟骨魚類に見出され得る単一の単量体可変抗体ドメインである。VHHドメインおよびVNARドメインの非限定的な態様は、例えば、Cromie et al.,Curr.Top.Med.Chem.15:2543-2557,2016;De Genst et al.,Dev.Comp.Immunol.30:187-198,2006;De Meyer et al.,Trends Biotechnol.32:263-270,2014;Kijanka et al.,Nanomedicine 10:161-174,2015;Kovaleva et al.,Expert.Opin.Biol.Ther.14:1527-1539,2014;Krah et al.,Immunopharmacol.Immunotoxicol.38:21-28,2016;Mujic-Delic et al.,Trends Pharmacol.Sci.35:247-255,2014;Muyldermans,J.Biotechnol.74:277-302,2001;Muyldermans et al.,Trends Biochem.Sci.26:230-235,2001;Muyldermans,Ann.Rev.Biochem.82:775-797,2013;Rahbarizadeh et al.,Immunol.Invest.40:299-338,2011;Van Audenhove et al.,EBioMedicine 8:40-48,2016;Van Bockstaele et al.,Curr.Opin.Investig.Drugs 10:1212-1224,2009;Vincke et al.,Methods Mol.Biol.911:15-26,2012;およびWesolowski et al.,Med.Microbiol.Immunol.198:157-174,2009に記載されている。
ABPCが単一のポリペプチドであり、二つの抗原結合ドメインを含む一部の実施形態では、第一の抗原結合ドメインおよび第2の抗原結合ドメインは両方ともVHHドメインとすることができるか、または少なくとも一方の抗原結合ドメインはVHHドメインとすることができる。ABPCが単一のポリペプチドであり、二つの抗原結合ドメインを含む一部の実施形態では、第一の抗原結合ドメインおよび第二の抗原結合ドメインは、両方ともVNARドメインであるか、または少なくとも一方の抗原結合ドメインはVNARドメインである。ABPCが単一ポリペプチドである一部の実施形態では、第一の抗原結合ドメインはscFvドメインである。ABPCが単一のポリペプチドであり、二つの抗原結合ドメインを含む一部の実施形態では、第一の抗原結合ドメインおよび第二の抗原結合ドメインは、両方ともscFvドメインであるか、または少なくとも一方の抗原結合ドメインはscFvドメインであり得る。
一部の実施形態では、ABPCは、二以上のポリペプチド(例えば、二個、三個、四個、五個、六個、七個、八個、九個、または十個のポリペプチド)を含み得る。ABPCが二以上のポリペプチドを含む一部の実施形態では、二以上のポリペプチドのうち二個、三個、四個、五個、または六個のポリペプチドが同一であり得る。
ABPCが二以上のポリペプチド(例えば、二個、三個、四個、五個、六個、七個、八個、九個、または十個のポリペプチド)を含む一部の実施形態では、ABPCの二以上のポリペプチドが、一つまたは複数の抗原結合ドメイン、例えば、抗体の抗原結合断片(例えば、本明細書に記載される抗体のいずれかの抗原結合断片)、VHH-scAb、VHH-Fab、Dual scFab、F(ab’)2、diabody、crossMab、DAF(two-in-one)、DAF(four-in-one)、DutaMab、DT-IgG、knobs-in-holes共通軽鎖、knobs-in-holes構築物、電荷対、Fab-arm exchange、SEEDbody、LUZ-Y、Fcab、κλ-body、直交Fab、DVD-IgG、IgG(H)-scFv、scFv-(H)IgG、IgG(L)-scFv、scFv-(L)IgG、IgG(L,H)-Fv、IgG(H)-V、V(H)-IgG、IgG(L)-V、V(L)-IgG、KIH IgG-scFab、2scFv-IgG、IgG-2scFv、scFv4-Ig、Zybody、DVI-IgG、Diabody-CH3、トリプルボディ(triple body)、ミニ抗体(miniantibody)、ミニボディ(minibody)、TriBiミニボディ、scFv-CH3 KIH、Fab-scFv、F(ab’)2-scFv2、scFv-KIH、Fab-scFv-Fc、四価HCAb、scDiabody-Fc、Diabody-Fc、タンデムscFv-Fc、VHH-Fc、タンデムVHH-Fc、VHH-Fc KiH、Fab-VHH-Fc、細胞内発現抗体(Intrabody)、ドックアンドロック(dock and lock)、ImmTAC、IgG-IgGコンジュゲート、Cov-X-Body、scFv1-PEG-scFv2、Adnectin、DARPin、フィブロネクチン、およびDEPコンジュゲートを形成するように構築される(例えば、非共有結合的に構築される)。例えば、Spiess et al.,Mol.Immunol.67:95-106,2015を参照されたく、これら要素の説明については、その全体が本明細書において援用される。抗体の抗原結合断片の非限定的な例は、Fv断片、Fab断片、F(ab’)2断片、およびFab’断片を含む。抗体の抗原結合断片のさらなる例は、IgGの抗原結合断片(例えば、IgG1、IgG2、IgG3、またはIgG4の抗原結合断片)(例えば、ヒトまたはヒト化IgGの、例えばヒトまたはヒト化IgG1、IgG2、IgG3、またはIgG4の、抗原結合断片)、IgAの抗原結合断片(例えば、IgA1またはIgA2の抗原結合断片)(例えば、ヒトまたはヒト化IgAの、例えばヒトまたはヒト化IgA1またはIgA2の、抗原結合断片)、IgDの抗原結合断片(例えば、ヒトまたはヒト化IgDの抗原結合断片)、IgEの抗原結合断片(例えば、ヒトまたはヒト化IgEの抗原結合断片)、またはIgMの抗原結合断片(例えば、ヒトまたはヒト化IgMの抗原結合断片)である。
「Fv」断片は、一つの重鎖可変ドメインと一つの軽鎖可変ドメインとの非共有結合で結合した二量体を含む。
「Fab」断片は、Fv断片の重鎖可変ドメインおよび軽鎖可変ドメインに加えて、軽鎖の定常ドメインおよび重鎖の第一の定常ドメイン(CH1)を含む。
「F(ab’)2」断片は、ジスルフィド結合によってヒンジ領域の近くで接合された二つのFab断片を含む。
“二重可変ドメイン免疫グロブリン”または“DVD-Ig”は、例えば、DiGiammarino et al.,Methods Mol.Biol.899:145-156,2012、Jakob et al.,MABs 5:358-363,2013、および米国特許第7,612,181号、第8,258,268号、第8,586,714号、第8,716,450号、第8,722,855号、第8,735,546号、および第8,822,645号に記載される、多価および多特異性の結合タンパク質を指し、当該文献の各々が参照によりその全体が援用される。
DARTは、例えば、Garber,Nature Reviews Drug Discovery 13:799-801,2014に記載される。
ABPCのさらなる態様は、当技術分野で公知である。
抗原結合ドメイン
本明細書に記載されるいずれかの抗原結合タンパク質構築物(ABPC)の一部の実施形態では、第一の抗原結合ドメイン(および存在する場合には、任意に第二の抗原結合ドメイン)の、pH約4.0~約6.5(例えば、約4.0~約6.4、約4.0~約6.3、約4.0~約6.2、約4.0~約6.1、約4.0~約6.0、約4.0~約5.9、約4.0~約5.8、約4.0~約5.7、約4.0~約5.6、約4.0~約5.5、約4.0~約5.4、約4.0~約5.3、約4.0~約5.2、約4.0~約5.1、約4.0~約5.0、約4.0~約4.9、約4.0~約4.8、約4.0~約4.7、約4.0~約4.6、約4.0~約4.5、約4.0~約4.4、約4.0~約4.3、約4.0~約4.2、約4.0~約4.1、約4.1~約6.5、約4.1~約6.4、約4.1~約6.3、約4.1~約6.2、約4.1~約6.1、約4.1~約6.0、約4.1~約5.9、約4.1~約5.8、約4.1~約5.7、約4.1~約5.6、約4.1~約5.5、約4.1~約5.4、約4.1~約5.3、約4.1~約5.2、約4.1~約5.1、約4.1~約5.0、約4.1~約4.9、約4.1~約4.8、約4.1~約4.7、約4.1~約4.6、約4.1~約4.5、約4.1~約4.4、約4.1~約4.3、約4.1~約4.2、約4.2~約6.5、約4.2~約6.4、約4.2~約6.3、約4.2~約6.2、約4.2~約6.1、約4.2~約6.0、約4.2~約5.9、約4.2~約5.8、約4.2~約5.7、約4.2~約5.6、約4.2~約5.5、約4.2~約5.4、約4.2~約5.3、約4.2~約5.2、約4.2~約5.1、約4.2~約5.0、約4.2~約4.9、約4.2~約4.8、約4.2~約4.7、約4.2~約4.6、約4.2~約4.5、約4.2~約4.4、約4.2~約4.3、約4.3~約6.5、約4.3~約6.4、約4.3~約6.3、約4.3~約6.2、約4.3~約6.1、約4.3~約6.0、約4.3~約5.9、約4.3~約5.8、約4.3~約5.7、約4.3~約5.6、約4.3~約5.5、約4.3~約5.4、約4.3~約5.3、約4.3~約5.2、約4.3~約5.1、約4.3~約5.0、約4.3~約4.9、約4.3~約4.8、約4.3~約4.7、約4.3~約4.6、約4.3~約4.5、約4.3~約4.4、約4.4~約6.5、約4.4~約6.4、約4.4~約6.3、約4.4~約6.2、約4.4~約6.1、約4.4~約6.0、約4.4~約5.9、約4.4~約5.8、約4.4~約5.7、約4.4~約5.6、約4.4~約5.5、約4.4~約5.4、約4.4~約5.3、約4.4~約5.2、約4.4~約5.1、約4.4~約5.0、約4.4~約4.9、約4.4~約4.8、約4.4~約4.7、約4.4~約4.6、約4.4~約4.5、約4.5~約6.5、約4.5~約6.4、約4.5~約6.3、約4.5~約6.2、約4.5~約6.1、約4.5~約6.0、約4.5~約5.9、約4.5~約5.8、約4.5~約5.7、約4.5~約5.6、約4.5~約5.5、約4.5~約5.4、約4.5~約5.3、約4.5~約5.2、約4.5~約5.1、約4.5~約5.0、約4.5~約4.9、約4.5~約4.8、約4.5~約4.7、約4.5~約4.6、約4.6~約6.5、約4.6~約6.4、約4.6~約6.3、約4.6~約6.2、約4.6~約6.1、約4.6~約6.0、約4.6~約5.9、約4.6~約5.8、約4.6~約5.7、約4.6~約5.6、約4.6~約5.5、約4.6~約5.4、約4.6~約5.3、約4.6~約5.2、約4.6~約5.1、約4.6~約5.0、約4.6~約4.9、約4.6~約4.8、約4.6~約4.7、約4.7~約6.5、約4.7~約6.4、約4.7~約6.3、約4.7~約6.2、約4.7~約6.1、約4.7~約6.0、約4.7~約5.9、約4.7~約5.8、約4.7~約5.7、約4.7~約5.6、約4.7~約5.5、約4.7~約5.4、約4.7~約5.3、約4.7~約5.2、約4.7~約5.1、約4.7~約5.0、約4.7~約4.9、約4.7~約4.8、約4.8~約6.5、約4.8~約6.4、約4.8~約6.3、約4.8~約6.2、約4.8~約6.1、約4.8~約6.0、約4.8~約5.9、約4.8~約5.8、約4.8~約5.7、約4.8~約5.6、約4.8~約5.5、約4.8~約5.4、約4.8~約5.3、約4.8~約5.2、約4.8~約5.1、約4.8~約5.0、約4.8~約4.9、約4.9~約6.5、約4.9~約6.4、約4.9~約6.3、約4.9~約6.2、約4.9~約6.1、約4.9~約6.0、約4.9~約5.9、約4.9~約5.8、約4.9~約5.7、約4.9~約5.6、約4.9~約5.5、約4.9~約5.4、約4.9~約5.3、約4.9~約5.2、約4.9~約5.1、約4.9~約5.0、約5.0~約6.5、約5.0~約6.4、約5.0~約6.3、約5.0~約6.2、約5.0~約6.1、約5.0~約6.0、約5.0~約5.9、約5.0~約5.8、約5.0~約5.7、約5.0~約5.6、約5.0~約5.5、約5.0~約5.4、約5.0~約5.3、約5.0~約5.2、約5.0~約5.1、約5.1~約6.5、約5.1~約6.4、約5.1~約6.3、約5.1~約6.2、約5.1~約6.1、約5.1~約6.0、約5.1~約5.9、約5.1~約5.8、約5.1~約5.7、約5.1~約5.6、約5.1~約5.5、約5.1~約5.4、約5.1~約5.3、約5.1~約5.2、約5.2~約6.5、約5.2~約6.4、約5.2~約6.3、約5.2~約6.2、約5.2~約6.1、約5.2~約6.0、約5.2~約5.9、約5.2~約5.8、約5.2~約5.7、約5.2~約5.6、約5.2~約5.5、約5.2~約5.4、約5.2~約5.3、約5.3~約6.5、約5.3~約6.4、約5.3~約6.3、約5.3~約6.2、約5.3~約6.1、約5.3~約6.0、約5.3~約5.9、約5.3~約5.8、約5.3~約5.7、約5.3~約5.6、約5.3~約5.5、約5.3~約5.4、約5.4~約6.5、約5.4~約6.4、約5.4~約6.3、約5.4~約6.2、約5.4~約6.1、約5.4~約6.0、約5.4~約5.9、約5.4~約5.8、約5.4~約5.7、約5.4~約5.6、約5.4~約5.5、約5.5~約6.5、約5.5~約6.4、約5.5~約6.3、約5.5~約6.2、約5.5~約6.1、約5.5~約6.0、約5.5~約5.9、約5.5~約5.8、約5.5~約5.7、約5.5~約5.6、約5.6~約6.5、約5.6~約6.4、約5.6~約6.3、約5.6~約6.2、約5.6~約6.1、約5.6~約6.0、約5.6~約5.9、約5.6~約5.8、約5.6~約5.7、約5.7~約6.5、約5.7~約6.4、約5.7~約6.3、約5.7~約6.2、約5.7~約6.1、約5.7~約6.0、約5.7~約5.9、約5.7~約5.8、約5.8~約6.5、約5.8~約6.4、約5.8~約6.3、約5.8~約6.2、約5.8~約6.1、約5.8~約6.0、約5.8~約5.9、約5.9~約6.5、約5.9~約6.4、約5.9~約6.3、約5.9~約6.2、約5.9~約6.1、約5.9~約6.0、約6.0~約6.5、約6.0~約6.4、約6.0~約6.3、約6.0~約6.2、約6.0~約6.1、約6.1~約6.5、約6.1~約6.4、約6.1~約6.3、約6.1~約6.2、約6.2~約6.5、約6.2~約6.4、約6.2~約6.3、約6.3~約6.5、約6.3~約6.4、または約6.4~約6.5)での解離速度が、pH約7.0~約8.0(例えば、約7.0~約7.9、約7.0~約7.8、約7.0~約7.7、約7.0~約7.6、約7.0~約7.5、約7.0~約7.4、約7.0~約7.3、約7.0~約7.2、約7.0~約7.1、約7.1~約8.0、約7.1~約7.9、約7.1~約7.8、約7.1~約7.7、約7.1~約7.6、約7.1~約7.5、約7.1~約7.4、約7.1~約7.3、約7.1~約7.2、約7.2~約8.0、約7.2~約7.9、約7.2~約7.8、約7.2~約7.7、約7.2~約7.6、約7.2~約7.5、約7.2~約7.4、約7.2~約7.3、約7.3~約8.0、約7.3~約7.9、約7.3~約7.8、約7.3~約7.7、約7.3~約7.6、約7.3~約7.5、約7.3~約7.4、約7.4~約8.0、約7.4~約7.9、約7.4~約7.8、約7.4~約7.7、約7.4~約7.6、約7.4~約7.5、約7.5~約8.0、約7.5~約7.9、約7.5~約7.8、約7.5~約7.7、約7.5~約7.6、約7.6~約8.0、約7.6~約7.9、約7.6~約7.8、約7.6~約7.7、約7.7~約8.0、約7.7~約7.9、約7.7~約7.8、約7.8~約8.0、約7.8~約7.9、または約7.9~約8.0)での解離速度よりも速い(例えば、少なくとも5%速い、少なくとも10%速い、少なくとも15%速い、少なくとも20%速い、少なくとも25%速い、少なくとも30%速い、少なくとも35%速い、少なくとも40%速い、少なくとも45%速い、少なくとも50%速い、少なくとも55%速い、少なくとも60%速い、少なくとも65%速い、少なくとも70%速い、少なくとも75%速い、少なくとも80%速い、少なくとも85%速い、少なくとも90%速い、少なくとも95%速い、少なくとも100%速い、少なくとも120%速い、少なくとも140%速い、少なくとも160%速い、少なくとも180%速い、少なくとも200%速い、少なくとも220%速い、少なくとも240%速い、少なくとも260%速い、少なくとも280%速い、少なくとも300%速い、少なくとも320%速い、少なくとも340%速い、少なくとも360%速い、少なくとも380%速い、少なくとも400%速い、少なくとも420%速い、少なくとも440%速い、少なくとも460%速い、少なくとも480%速い、少なくとも500%速い、少なくとも1,000%速い、少なくとも2,000%速い、少なくとも3,000%速い、少なくとも4,000%速い、少なくとも5,000%速い、少なくとも6,000%速い、少なくとも7,000%速い、少なくとも8,000%速い、少なくとも9,000%速い、もしくは少なくとも10,000%速い、または約5%速い~約10,000%速い、約5%速い~約9,000%速い、約5%速い~約8,000%速い、約5%速い~約7,000%速い、約5%速い~約6,000%速い、約5%速い~約5,000%速い、約5%速い~約4,000%速い、約5%速い~約3,000%速い、約5%速い~約2,000%速い、約5%速い~約1,000%速い、約5%速い~約500%速い、約5%速い~約480%速い、約5%速い~約460%速い、約5%速い~約440%速い、約5%速い~約420%速い、約5%速い~約400%速い、約5%速い~約380%速い、約5%速い~約360%速い、約5%速い~約340%速い、約5%速い~約320%速い、約5%速い~約300%速い、約5%速い~約280%速い、約5%速い~約260%速い、約5%速い~約240%速い、約5%速い~約220%速い、約5%速い~約200%速い、約5%速い~約180%速い、約5%速い~約160%速い、約5%速い~約140%速い、約5%速い~約120%速い、約5%速い~約100%速い、約5%速い~約95%速い、約5%速い~約90%速い、約5%速い~約85%速い、約5%速い~約80%速い、約5%速い~約75%速い、約5%速い~約70%速い、約5%速い~約65%速い、約5%速い~約60%速い、約5%速い~約55%速い、約5%速い~約50%速い、
約5%速い~約45%速い、約5%速い~約40%速い、約5%速い~約35%速い、約5%速い~約30%速い、約5%速い~約25%速い、約5%速い~約20%速い、約5%速い~約15%速い、約5%速い~約10%速い、約10%速い~約10,000%速い、約10%速い~約9,000%速い、約10%速い~約8,000%速い、約10%速い~約7,000%速い、約10%速い~約6,000%速い、約10%速い~約5,000%速い、約10%速い~約4,000%速い、約10%速い~約3,000%速い、約10%速い~約2,000%速い、約10%速い~約1,000%速い、約10%速い~約500%速い、約10%速い~約480%速い、約10%速い~約460%速い、約10%速い~約440%速い、約10%速い~約420%速い、約10%速い~約400%速い、約10%速い~約380%速い、約10%速い~約360%速い、約10%速い~約340%速い、約10%速い~約320%速い、約10%速い~約300%速い、約10%速い~約280%速い、約10%速い~約260%速い、約10%速い~約240%速い、約10%速い~約220%速い、約10%速い~約200%速い、約10%速い~約180%速い、約10%速い~約160%速い、約10%速い~約140%速い、約10%速い~約120%速い、約10%速い~約100%速い、約10%速い~約95%速い、約10%速い~約90%速い、約10%速い~約85%速い、約10%速い~約80%速い、約10%速い~約75%速い、約10%速い~約70%速い、約10%速い~約65%速い、約10%速い~約60%速い、約10%速い~約55%速い、約10%速い~約50%速い、約10%速い~約45%速い、約10%速い~約40%速い、約10%速い~約35%速い、約10%速い~約30%速い、約10%速い~約25%速い、約10%速い~約20%速い、約10%速い~約15%速い、約15%速い~約10,000%速い、約15%速い~約9,000%速い、約15%速い~約8,000%速い、約15%速い~約7,000%速い、約15%速い~約6,000%速い、約15%速い~約5,000%速い、約15%速い~約4,000%速い、約15%速い~約3,000%速い、約15%速い~約2,000%速い、約15%速い~約1,000%速い、約15%速い~約500%速い、約15%速い~約480%速い、約15%速い~約460%速い、約15%速い~約440%速い、約15%速い~約420%速い、約15%速い~約400%速い、約15%速い~約380%速い、約15%速い~約360%速い、約15%速い~約340%速い、約15%速い~約320%速い、約15%速い~約300%速い、約15%速い~約280%速い、約15%速い~約260%速い、約15%速い~約240%速い、約15%速い~約220%速い、約15%速い~約200%速い、約15%速い~約180%速い、約15%速い~約160%速い、約15%速い~約140%速い、約15%速い~約120%速い、約15%速い~約100%速い、約15%速い~約95%速い、約15%速い~約90%速い、約15%速い~約85%速い、約15%速い~約80%速い、約15%速い~約75%速い、約15%速い~約70%速い、約15%速い~約65%速い、約15%速い~約60%速い、約15%速い~約55%速い、約15%速い~約50%速い、約15%速い~約45%速い、約15%速い~約40%速い、約15%速い~約35%速い、約15%速い~約30%速い、約15%速い~約25%速い、約15%速い~約20%速い、約20%速い~約10,000%速い、約20%速い~約9,000%速い、約20%速い~約8,000%速い、約20%速い~約7,000%速い、約20%速い~約6,000%速い、約20%速い~約5,000%速い、約20%速い~約4,000%速い、約20%速い~約3,000%速い、約20%速い~約2,000%速い、約20%速い~約1,000%速い、約20%速い~約500%速い、約20%速い~約480%速い、約20%速い~約460%速い、約20%速い~約440%速い、約20%速い~約420%速い、約20%速い~約400%速い、約20%速い~約380%速い、約20%速い~約360%速い、約20%速い~約340%速い、約20%速い~約320%速い、約20%速い~約300%速い、約20%速い~約280%速い、約20%速い~約260%速い、約20%速い~約240%速い、約20%速い~約220%速い、約20%速い~約200%速い、約20%速い~約180%速い、約20%速い~約160%速い、約20%速い~約140%速い、約20%速い~約120%速い、約20%速い~約100%速い、約20%速い~約95%速い、約20%速い~約90%速い、約20%速い~約85%速い、約20%速い~約80%速い、約20%速い~約75%速い、約20%速い~約70%速い、約20%速い~約65%速い、約20%速い~約60%速い、約20%速い~約55%速い、約20%速い~約50%速い、約20%速い~約45%速い、約20%速い~約40%速い、約20%速い~約35%速い、約20%速い~約30%速い、約20%速い~約25%速い、約25%より速い~約10,000%速い、約25%速い~約9,000%速い、約25%速い~約8,000%速い、約25%速い~約7,000%速い、約25%速い~約6,000%速い、約25%速い~約5,000%速い、約25%速い~約4,000%速い、約25%速い~約3,000%速い、約25%速い~約2,000%速い、約25%速い~約1,000%速い、約25%速い~約500%速い、約25%速い~約480%速い、約25%速い~約460%速い、約25%速い~約440%速い、約25%速い~約420%速い、約25%速い~約400%速い、約25%速い~約380%速い、約25%速い~約360%速い、約25%速い~約340%速い、約25%速い~約320%速い、約25%速い~約300%速い、約25%速い~約280%速い、約25%速い~約260%速い、約25%速い~約240%速い、約25%速い~約220%速い、約25%速い~約200%速い、約25%速い~約180%速い、約25%速い~約160%速い、約25%速い~約140%速い、約25%速い~約120%速い、約25%速い~約100%速い、約25%速い~約95%速い、約25%速い~約90%速い、約25%速い~約85%速い、約25%速い~約80%速い、約25%速い~約75%速い、約25%速い~約70%速い、約25%速い~約65%速い、約25%速い~約60%速い、約25%速い~約55%速くなり、約25%速い~約50%速い、約25%速い~約45%速い、約25%速い~約40%速い、約25%速い~約35%速い、約25%速い~約30%速い、約30%速い~約10,000%速い、約30%速い~約9,000%速い、約30%速い~約8,000%速い、約30%速い~約7,000%速い、約30%速い~約6,000%速い、約30%速い~約5,000%速い、約30%速い~約4,000%速い、約30%速い~約3,000%速い、約30%速い~約2,000%速い、約30%速い~約1,000%速い、約30%速い~約500%速い、約30%速い~約480%速い、約30%速い~約460%速い、約30%速い~約440%速い、約30%速い~約420%速い、約30%速い~約400%速い、約30%速い~約380%速い、約30%速い~約360%速い、約30%速い~約340%速い、約30%速い~約320%速い、約30%速い~約300%速い、約30%速い~約280%速い、約30%速い~約260%速い、約30%速い~約240%速い、約30%速い~約220%速い、約30%速い~約200%速い、約30%速い~約180%速い、約30%速い~約160%速い、約30%速い~約140%速い、約30%速い~約120%速い、約30%速い~約100%速い、約30%速い~約95%速い、約30%速い~約90%速い、約30%速い~約85%速い、約30%速い~約80%速い、約30%速い~約75%速い、約30%速い~約70%速い、約30%速い~約65%速い、約30%速い~約60%速い、約30%速い~約55%速い、約30%速い~約50%速い、約30%速い~約45%速い、約30%速い~約40%速い、約30%速い~約35%速い、約35%速い~約10,000%速い、約35%速い~約9,000%速い、約35%速い~約8,000%速い、約35%速い~約7,000%速い、約35%速い~約6,000%速い、約35%速い~約5,000%速い、約35%速い~約4,000%速い、約35%速い~約3,000%速い、約35%速い~約2,000%速い、約35%速い~約1,000%速い、約35%速い~約500%速い、約35%速い~約480%速い、約35%速い~約460%速い、約35%速い~約440%速い、約35%速い~約420%速い、約35%速い~約400%速い、約35%速い~約380%速い、約35%速い~約360%速い、約35%速い~約340%速い、約35%速い~約320%速い、約35%速い~約300%速い、約35%速い~約280%速い、約35%速い~約260%速い、約35%速い~約240%速い、約35%速い~約220%速い、約35%速い~約200%速い、約35%速い~約180%速い、約35%速い~約160%速い、約35%速い~約140%速い、約35%速い~約120%速い、約35%速い~約100%速い、約35%速い~約95%速い、約35%速い~約90%速い、約35%速い~約85%速い、約35%速い~約80%速い、約35%速い~約75%速い、約35%速い~約70%速い、約35%速い~約65%速い、約35%速い~約60%速い、約35%速い~約55%速い、約35%速い~約50%速い、約35%速い~約45%速い、約35%速い~約40%速い、約40%速い~約10,000%速い、約40%速い~約9,000%速い、約40%速い~約8,000%速い、約40%速い~約7,000%速い、約40%速い~約6,000%速い、約40%速い~約5,000%速い、約40%速い~約4,000%速い、約40%速い~約3,000%速い、約40%速い~約2,000%速い、約40%速い~約1,000%速い、約40%速い~約500%速い、約40%速い~約480%速い、約40%速い~約460%速い、約40%速い~約440%速い、約40%速い~約420%速い、約40%速い~約400%速い、約40%速い~約380%速い、約40%速い~約360%速い、約40%速い~約340%速い、約40%速い~約320%速い、約40%速い~約300%速い、約40%速いから約280%速い、約40%速い~約260%速い、約40%速い~約240%速い、約40%速い~約220%速い、約40%速い~約200%速い、約40%速い~約180%速い、約40%速い~約160%速い、約40%速い~約140%速い、約40%速い~約120%速い、約40%速い~約100%速い、約40%速い~約95%速い、約40%速い~約90%速い、約40%速い~約85%速い、約40%速い~約80%速い、約40%速い~約75%速い、約40%速い~約70%速い、約40%速い~約65%速い、約40%速い~約60%速い、約40%速い~約55%速い、約40%速い~約50%速い、約40%速い~約45%速い、約45%速い~約10,000%速い、約45%速い~約9,000%速い、約45%速い~約8,000%速い、約45%速い~約7,000%速い、約45%速い~約6,000%速い、約45%速い~約5,000%速い、約45%速い~約4,000%速い、約45%速い~約3,000%速い、約45%速い~約2,000%速い、約45%速い~約1,000%速い、約45%速い~約500%速い、約45%速い~約480%速い、約45%速い~約460%速い、約45%速い~約440%速い、約45%速い~
約420%速い、約45%速い~約400%速い、約45%速い~約380%速い、約45%速い~約360%速い、約45%速い~約340%速い、約45%速い~約320%速い、約45%速い~約300%速い、約45%速い~約280%速い、約45%速い~約260%速い、約45%速い~約240%速い、約45%速い~約220%速い、約45%速い~約200%速い、約45%速い~約180%速い、約45%速い~約160%速い、約45%速い~約140%速い、約45%速い~約120%速い、約45%速い~約100%速い、約45%速い~約95%速い、約45%速い~約90%速い、約45%速い~約85%速い、約45%速い~約80%速い、約45%速い~約75%速い、約45%速い~約70%速い、約45%速い~約65%速い、約45%速い~約60%速い、約45%速い~約55%速い、約45%速い~約50%速い、約50%速い~約10,000%速い、約50%速い~約9,000%速い、約50%速い~約8,000%速い、約50%速い~約7,000%速い、約50%速い~約6,000%速い、約50%速い~約5,000%速い、約50%速い~約4,000%速い、約50%速い~約3,000%速い、約50%速い~約2,000%速い、約50%速い~約1,000%速い、約50%速い~約500%速い、約50%速い~約480%速い、約50%速い~約460%速い、約50%速い~約440%速い、約50%速い~約420%速い、約50%速い~約400%速い、約50%速い~約380%速い、約50%速い~約360%速くなり、約50%速い~約340%速い、約50%速い~約320%速い、約50%速い~約300%速い、約50%速い~約280%速い、約50%速い~約260%速い、約50%速い~約240%速い、約50%速い~約220%速い、約50%速い~約200%速い、約50%速い~約180%速い、約50%速い~約160%速い、約50%速い~約140%速い、約50%速い~約120%速い、約50%速い~約100%速い、約50%速い~約95%速い、約50%速い~約90%速い、約50%速い~約85%速い、約50%速い~約80%速い、約50%速い~約75%速い、約50%速い~約70%速い、約50%速い~約65%速い、約50%速い~約60%速い、約50%速い~約55%速い、約55%速い~約10,000%速い、約55%速い~約9,000%速い、約55%速い~約8,000%速い、約55%速い~約7,000%速い、約55%速い~約6,000%速い、約55%速い~約5,000%速い、約55%速い~約4,000%速い、約55%速い~約3,000%速い、約55%速い~約2,000%速い、約55%速い~約1,000%速い、約55%速い~約500%速い、約55%速い~約480%速い、約55%速い~約460%速い、約55%速い~約440%速い、約55%速い~約420%速い、約55%速い~約400%速い、約55%速い~約380%速い、約55%速い~約360%速い、約55%速い~約340%速い、約55%速い~約320%速い、約55%速い~約300%速い、約55%速い~約280%速い、約55%速い~約260%速い、約55%速い~約240%速い、約55%速い~約220%速い、約55%速い~約200%速い、約55%速い~約180%速い、約55%速い~約160%速い、約55%速い~約140%速い、約55%速い~約120%速い、約55%速い~約100%速い、約55%速い~約95%速い、約55%速い~約90%速い、約55%速い~約85%速い、約55%速い~約80%速い、約55%速い~約75%速い、約55%速い~約70%速い、約55%速い~約65%速い、約55%速い~約60%速い、約60%速い~約10,000%速い、約60%速い~約9,000%速い、約60%速い~約8,000%速い、約60%速い~約7,000%速い、約60%速い~約6,000%速い、約60%速い~約5,000%速い、約60%速い~約4,000%速い、約60%速い~約3,000%速い、約60%速い~約2,000%速い、約60%速い~約1,000%速い、約60%速い~約500%速い、約60%速い~約480%速い、約60%速い~約460%速い、約60%速い~約440%速い、約60%速い~約420%速い、約60%速い~約400%速い、約60%速い~約380%速い、約60%速い~約360%速い、約60%速い~約340%速い、約60%速い~約320%速い、約60%速い~約300%速い、約60%速い~約280%速い、約60%速い~約260%速い、約60%速い~約240%速い、約60%速い~約220%速い、約60%速い~約200%速い、約60%速い~約180%速い、約60%速い~約160%速い、約60%速い~約140%速い、約60%速い~約120%速い、約60%速い~約100%速い、約60%速い~約95%速い、約60%速い~約90%速い、約60%速い~約85%速い、約60%速い~約80%速い、約60%速い~約75%速い、約60%速い~約70%速い、約60%速い~約65%速い、約65%速い~約10,000%速い、約65%速い~約9,000%速い、約65%速い~約8,000%速い、約65%速い~約7,000%速い、約65%速い~約6,000%速い、約65%速い~約5,000%速い、約65%速い~約4,000%速い、約65%速い~約3,000%速い、約65%速い~約2,000%速い、約65%速い~約1,000%速い、約65%速い~約500%速い、約65%速い~約480%速い、約65%速い~約460%速い、約65%速い~約440%速い、約65%速い~約420%速い、約65%速い~約400%速い、約65%速い~約380%速い、約65%速い~約360%速い、約65%速い~約340%速い、約65%速い~約320%速い、約65%速い~約300%速い、約65%速い~約280%速い、約65%速い~約260%速い、約65%速い~約240%速い、約65%速い~約220%速い、約65%速い~約200%速い、約65%速い~約180%速い、約65%速い~約160%速い、約65%速い~約140%速い、約65%速い~約120%速い、約65%速い~約100%速い、約65%速い~約95%速い、約65%速い~約90%速い、約65%速い~約85%速い、約65%速い~約80%速い、約65%速い~約75%速い、約65%速い~約70%速い、約70%速い~約10,000%速い、約70%速い~約9,000%速い、約70%速い~約8,000%速い、約70%速い~約7,000%速い、約70%速い~約6,000%速い、約70%速い~約5,000%速い、約70%速い~約4,000%速い、約70%速い~約3,000%速い、約70%速い~約2,000%速い、約70%速い~約1,000%速い、約70%速い~約500%速い、約70%速い~約480%速い、約70%速い~約460%速い、約70%速い~約440%速い、約70%速い~約420%速い、約70%速い~約400%速い、約70%速い~約380%速い、約70%速い~約360%速い、約70%速い~約340%速い、約70%速い~約320%速い、約70%速い~約300%速い、約70%速い~約280%速い、約70%速い~約260%速い、約70%速い~約240%速い、約70%速い~約220%速い、約70%速い~約200%速い、約70%速い~約180%速い、約70%速い~約160%速い、約70%速い~約140%速い、約70%速い~約120%速い、約70%速い~約100%速い、約70%速い~約95%速い、約70%速い~約90%速い、約70%速い~約85%速い、約70%速い~約80%速い、約70%速い~約75%速い、約75%速い~約10,000%速い、約75%速い~約9,000%速い、約75%速い~約8,000%速い、約75%速い~約7,000%速い、約75%速い~約6,000%速い、約75%速い~約5,000%速い、約75%速い~約4,000%速い、約75%速い~約3,000%速い、約75%速い~約2,000%速い、約75%速い~約1,000%速い、約75%速い~約500%速い、約75%速い~約480%速い、約75%速い~約460%速い、約75%速い~約440%速い、約75%速い~約420%速い、約75%速い~約400%速い、約75%速い~約380%速い、約75%速い~約360%速い、約75%速い~約340%速い、約75%速い~約320%速い、約75%速い~約300%速い、約75%速い~約280%速い、約75%速い~約260%速い、約75%速い~約240%速い、約75%速い~約220%速い、約75%速い~約200%速い、約75%速い~約180%速い、約75%速い~約160%速い、約75%速い~約140%速い、約75%速い~約120%速い、約75%速い~約100%速い、約75%速い~約95%速い、約75%速い~約90%速い、約75%速い~約85%速い、約75%速い~約80%速い、約80%速い~約10,000%速い、約80%速い~約9,000%速い、約80%速い~約8,000%速い、約80%速い~約7,000%速い、約80%速い~約6,000%速い、約80%速い~約5,000%速い、約80%速い~約4,000%速い、約80%速い~約3,000%速い、約80%速い~約2,000%速い、約80%速い~約1,000%速い、約80%速い~約500%速い、約80%速い~約480%速い、約80%速い~約460%速い、約80%速い~約440%速い、約80%速い~約420%速い、約80%速い~約400%速い、約80%速い~約380%速い、約80%速い~約360%速い、約80%速い~約340%速い、約80%速い~約320%速い、約80%速い~約300%速い、約80%速い~約280%速い、約80%速い~約260%速い、約80%速い~約240%速い、約80%速い~約220%速い、約80%速い~約200%速い、約80%速い~約180%速い、約80%速い~約160%速い、約80%速い~約140%速い、約80%速い~約120%速い、約80%速い~約100%速い、約80%速い~約95%速い、約80%速い~約90%速い、約80%速い~約85%速い、約85%速い~約10,000%速い、約85%速い~約9,000%速い、約85%速い~約8,000%速い、約85%速い~約7,000%速い、約85%速い~約6,000%速い、約85%速い~約5,000%速い、約85%速い~約4,000%速い、約85%速い~約3,000%速い、約85%速い~約2,000%速い、約85%速い~約1,000%速い、約85%速い~約500%速い、約85%速い~約480%速い、約85%速い~約460%速い、約85%速い~約440%速い、約85%速い~約420%速い、約85%速い~約400%速い、約85%速い~約380%速い、約85%速い~約360%速い、約85%速い~約340%速い、約85%速い~約320%速い、約85%速い~約300%速い、約85%速い~約280%速い、約85%速い~約260%速い、約85%速い~約240%速い、約85%速い~約220%速い、約85%速い~約200%速い、約85%速い~約180%速い、約85%速い~約160%速い、約85%速い~約140%速い、約85%速い~約120%速い、約85%速い~約100%速い、約85%速い~約95%速い、約85%速い~約90%速い、約90%速い~約10,000%速い、約90%速い~約9,000%速い、約90%速い~約8,000%速い、約90%速い~約7,000%速い、約90%速い~約6,000%速い、約90%速い~約5,000%速い、約90%速い~約4,000%速い、約90%速い~約3,000%速い、約90%速い~約2,000%速い、約90%速い~約1,000%速い、約90%速い~約500%速い、約90%速い~約480%速い、約90%速い~約460%速い、約90%速い~約440
%速い、約90%速い~約420%速い、約90%速い~約400%速い、約90%速い~約380%速い、約90%速い~約360%速い、約90%速い~約340%速い、約90%速い~約320%速い、約90%速い~約300%速い、約90%速い~約280%速い、約90%速い~約260%速い、約90%速い~約240%速い、約90%速い~約220%速い、約90%速い~約200%速い、約90%速い~約180%速い、約90%速い~約160%速い、約90%速い~約140%速い、約90%速い~約120%速い、約90%速い~約100%速い、約90%速い~約95%速い、約95%速い~約10,000%速い、約95%速い~約9,000%速い、約95%速い~約8,000%速い、約95%速い~約7,000%速い、約95%速い~約6,000%速い、約95%速い~約5,000%速い、約95%速い~約4,000%速い、約95%速い~約3,000%速い、約95%速い~約2,000%速い、約95%速い~約1,000%速い、約95%速い~約500%速い、約95%速い~約480%速い、約95%速い~約460%速い、約95%速い~約440%速い、約95%速い~約420%速い、約95%速い~約400%速い、約95%速い~約380%速い、約95%速い~約360%速い、約95%速い~約340%速い、約95%速い~約320%速い、約95%速い~約300%速い、約95%速い~約280%速い、約95%速い~約260%速い、約95%速い~約240%速い、約95%速い~約220%速い、約95%速い~約200%速い、約95%速い~約180%速い、約95%速い~約160%速い、約95%速い~約140%速い、約95%速い~約120%速い、約95%速い~約100%速い、約100%速い~約10,000%速い、約100%速い~約9,000%速い、約100%速い~約8,000%速い、約100%速い~約7,000%速い、約100%速い~約6,000%速い、約100%速い~約5,000%速い、約100%速い~約4,000%速い、約100%速い~約3,000%速い、約100%速い~約2,000%速い、約100%速い~約1,000%速い、約100%速い~約500%速い、約100%速い~約480%速い、約100%速い~約460%速い、約100%速い~約440%速い、約100%速い~約420%速い、約100%速い~約400%速い、約100%速い~約380%速い、約100%速い~約360%速い、約100%速い~約340%速い、約100%速い~約320%速い、約100%速い~約300%速い、約100%速い~約280%速い、約100%速い~約260%速い、約100%速い~約240%速い、約100%速い~約220%速い、約100%速い~約200%速い、約100%速い~約180%速い、約100%速い~約160%速い、約100%速い~約140%速い、約100%速い~約120%速い、約120%速い~約10,000%速い、約120%速い~約9,000%速い、約120%速い~約8,000%速い、約120%速い~約7,000%速い、約120%速い~約6,000%速い、約120%速い~約5,000%速い、約120%速い~約4,000%速い、約120%速い~約3,000%速い、約120%速い~約2,000%速い、約120%速い~約1,000%速い、約120%速い~約500%速い、約120%速い~約480%速い、約120%速い~約460%速い、約120%速い~約440%速い、約120%速い~約420%速い、約120%速い~約400%速い、約120%速い~約380%速い、約120%速い~約360%速い、約120%速い~約340%速い、約120%速い~約320%速い、約120%速い~約300%速い、約120%速い~約280%速い、約120%速い~約260%速い、約120%速い~約240%速い、約120%速い~約220%速い、約120%速い~約200%速い、約120%速い~約180%速い、約120%速い~約160%速い、約120%速い~約140%速い、約140%速い~約10,000%速い、約140%速い~約9,000%速い、約140%速い~約8,000%速い、約140%速い~約7,000%速い、約140%速い~約6,000%速い、約140%速い~約5,000%速い、約140%速い~約4,000%速い、約140%速い~約3,000%速い、約140%速い~約2,000%速い、約140%速い~約1,000%速い、約140%速い~約500%速い、約140%速い~約480%速い、約140%速い~約460%速い、約140%速い~約440%速い、約140%速い~約420%速い、約140%速い~約400%速い、約140%速い~約380%速い、約140%速い~約360%速い、約140%速い~約340%速い、約140%速い~約320%速い、約140%速い~約300%速い、約140%速い~約280%速い、約140%速い~約260%速い、約140%速い~約240%速い、約140%速い~約220%速い、約140%速い~約200%速い、約140%速い~約180%速い、約140%速い~約160%速い、約160%速い~約10,000%速い、約160%速い~約9,000%速い、約160%速い~約8,000%速い、約160%速い~約7,000%速い、約160%速い~約6,000%速い、約160%速い~約5,000%速い、約160%速い~約4,000%速い、約160%速い~約3,000%速い、約160%速い~約2,000%速い、約160%速い~約1,000%速い、約160%速い~約500%速い、約160%速い~約480%速い、約160%速い~約460%速い、約160%速い~約440%速い、約160%速い~約420%速い、約160%速い~約400%速い、約160%速い~約380%速い、約160%速い~約360%速い、約160%速い~約340%速い、約160%速い~約320%速い、約160%速い~約300%速い、約160%速い~約280%速い、約160%速い~約260%速い、約160%速い~約240%速い、約160%速い~約220%速い、約160%速い~約200%速い、約160%速い~約180%速い、約180%速い~約10,000%速い、約180%速い~約9,000%速い、約180%速い~約8,000%速い、約180%速い~約7,000%速い、約180%速い~約6,000%速い、約180%速い~約5,000%速い、約180%速い~約4,000%速い、約180%速い~約3,000%速い、約180%速い~約2,000%速い、約180%速い~約1,000%速い、約180%速い~約500%速い、約180%速い~約480%速い、約180%速い~約460%速い、約180%速い~約440%速い、約180%速い~約420%速い、約180%速い~約400%速い、約180%速い~約380%速い、約180%速い~約360%速い、約180%速い~約340%速い、約180%速い~約320%速い、約180%速い~約300%速い、約180%速い~約280%速い、約180%速い~約260%速い、約180%速い~約240%速い、約180%速い~約220%速い、約180%速い~約200%速い、約200%速い~約10,000%速い、約200%速い~約9,000%速い、約200%速い~約8,000%速い、約200%速い~約7,000%速い、約200%速い~約6,000%速い、約200%速い~約5,000%速い、約200%速い~約4,000%速い、約200%速い~約3,000%速い、約200%速い~約2,000%速い、約200%速い~約1,000%速い、約200%速い~約500%速い、約200%速い~約480%速い、約200%速い~約460%速い、約200%速い~約440%速い、約200%速い~約420%速い、約200%速い~約400%速い、約200%速い~約380%速い、約200%速い~約360%速い、約200%速い~約340%速い、約200%速い~約320%速い、約200%速い~約300%速い、約200%速い~約280%速い、約200%速い~約260%速い、約200%速い~約240%速い、約200%速い~約220%速い、約220%速い~約10,000%速い、約220%速い~約9,000%速い、約220%速い~約8,000%速い、約220%速い~約7,000%速い、約220%速い~約6,000%速い、約220%速い~約5,000%速い、約220%速い~約4,000%速い、約220%速い~約3,000%速い、約220%速い~約2,000%速い、約220%速い~約1,000%速い、約220%速い~約500%速い、約220%速い~約480%速い、約220%速い~約460%速い、約220%速い~約440%速い、約220%速い~約420%速い、約220%速い~約400%速い、約220%速い~約380%速い、約220%速い~約360%速い、約220%速い~約340%速い、約220%速い~約320%速い、約220%速い~約300%速い、約220%速い~約280%速い、約220%速い~約260%速い、約220%速い~約240%速い、約240%速い~約10,000%速い、約240%速い~約9,000%速い、約240%速い~約8,000%速い、約240%速い~約7,000%速い、約240%速い~約6,000%速い、約240%速い~約5,000%速い、約240%速い~約4,000%速い、約240%速い~約3,000%速い、約240%速い~約2,000%速い、約240%速い~約1,000%速い、約240%速い~約500%速い、約240%速い~約480%速い、約240%速い~約460%速い、約240%速い~約440%速い、約240%速い~約420%速い、約240%速い~約400%速い、約240%速い~約380%速い、約240%速い~約360%速い、約240%速い~約340%速い、約240%速い~約320%速い、約240%速い~約300%速い、約240%速い~約280%速い、約240%速い~約260%速い、約260%速い~約10,000%速い、約260%速い~約9,000%速い、約260%速い~約8,000%速い、約260%速い~約7,000%速い、約260%速い~約6,000%速い、約260%速い~約5,000%速い、約260%速い~約4,000%速い、約260%速い~約3,000%速い、約260%速い~約2,000%速い、約260%速い~約1,000%速い、約260%速い~約500%速い、約260%速い~約480%速い、約260%速い~約460%速い、約260%速い~約440%速い、約260%速い~約420%速い、約260%速い~約400%速い、約260%速い~約380%速い、約260%速い~約360%速い、約260%速い~約340%速い、約260%速い~約320%速い、約260%速い~約300%速い、約260%速い~約280%速い、約280%速い~約10,000%速い、約280%速い~約9,000%速い、約280%速い~約8,000%速い、約280%速い~約7,000%速い、約280%速い~約6,000%速い、約280%速い~約5,000%速い、約280%速い~約4,000%速い、約280%速い~約3,000%速い、約280%速い~約2,000%速い、約280%速い~約1,000%速い、約280%速い~約500%速い、約280%速い~約480%速い、約280%速い~約460%速い、約280%速い~約440%速い、約280%速い~約420%速い、約280%速い~約400%速い、約280%速い~約380%速い、約280%速い~約360%速い、約280%速い~約340%速い、約280%速い~約320%速い、約280%速い~約300%速い、約300%速い~約10,000%速い、約300%速い~約9,000%速い、約300%速い~約8,000%速い、約300%速い~約7,000%速い
、約300%速い~約6,000%速い、約300%速い~約5,000%速い、約300%速い~約4,000%速い、約300%速い~約3,000%速い、約300%速い~約2,000%速い、約300%速い~約1,000%速い、約300%速い~約500%速い、約300%速い~約480%速い、約300%速い~約460%速い、約300%速い~約440%速い、約300%速い~約420%速い、約300%速い~約400%速い、約300%速い~約380%速い、約300%速い~約360%速い、約300%速い~約340%速い、約300%速い~約320%速い、約320%速い~約10,000%速い、約320%速い~約9,000%速い、約320%速い~約8,000%速い、約320%速い~約7,000%速い、約320%速い~約6,000%速い、約320%速い~約5,000%速い、約320%速い~約4,000%速い、約320%速い~約3,000%速い、約320%速い~約2,000%速い、約320%速い~約1,000%速い、約320%速い~約500%速い、約320%速い~約480%速い、約320%速い~約460%速い、約320%速い~約440%速い、約320%速い~約420%速い、約320%速い~約400%速い、約320%速い~約380%速い、約320%速い~約360%速い、約320%速い~約340%速い、約340%速い~約10,000%速い、約340%速い~約9,000%速い、約340%速い~約8,000%速い、約340%速い~約7,000%速い、約340%速い~約6,000%速い、約340%速い~約5,000%速い、約340%速い~約4,000%速い、約340%速い~約3,000%速い、約340%速い~約2,000%速い、約340%速い~約1,000%速い、約340%速い~約500%速い、約340%速い~約480%速い、約340%速い~約460%速い、約340%速い~約440%速い、約340%速い~約420%速い、約340%速い~約400%速い、約340%速い~約380%速い、約340%速い~約360%速い、約360%速い~約10,000%速い、約360%速い~約9,000%速い、約360%速い~約8,000%速い、約360%速い~約7,000%速い、約360%速い~約6,000%速い、約360%速い~約5,000%速い、約360%速い~約4,000%速い、約360%速い~約3,000%速い、約360%速い~約2,000%速い、約360%速い~約1,000%速い、約360%速い~約500%速い、約360%速い~約480%速い、約360%速い~約460%速い、約360%速い~約440%速い、約360%速い~約420%速い、約360%速い~約400%速い、約360%速い~約380%速い、約380%速い~約10,000%速い、約380%速い~約9,000%速い、約380%速い~約8,000%速い、約380%速い~約7,000%速い、約380%速い~約6,000%速い、約380%速い~約5,000%速い、約380%速い~約4,000%速い、約380%速い~約3,000%速い、約380%速い~約2,000%速い、約380%速い~約1,000%速い、約380%速い~約500%速い、約380%速い~約480%速い、約380%速い~約460%速い、約380%速い~約440%速い、約380%速い~約420%速い、約380%速い~約400%速い、約400%速い~約10,000%速い、約400%速い~約9,000%速い、約400%速い~約8,000%速い、約400%速い~約7,000%速い、約400%速い~約6,000%速い、約400%速い~約5,000%速い、約400%速い~約4,000%速い、約400%速い~約3,000%速い、約400%速い~約2,000%速い、約400%速い~約1,000%速い、約400%速い~約500%速い、約400%速い~約480%速い、約400%速い~約460%速い、約400%速い~約440%速い、約400%速い~約420%速い、約420%速い~約10,000%速い、約420%速い~約9,000%速い、約420%速い~約8,000%速い、約420%速い~約7,000%速い、約420%速い~約6,000%速い、約420%速い~約5,000%速い、約420%速い~約4,000%速い、約420%速い~約3,000%速い、約420%速い~約2,000%速い、約420%速い~約1,000%速い、約420%速い~約500%速い、約420%速い~約480%速い、約420%速い~約460%速い、約420%速い~約440%速い、約440%速い~約10,000%速い、約440%速い~約9,000%速い、約440%速い~約8,000%速い、約440%速い~約7,000%速い、約440%速い~約6,000%速い、約440%速い~約5,000%速い、約440%速い~約4,000%速い、約440%速い~約3,000%速い、約440%速い~約2,000%速い、約440%速い~約1,000%速い、約440%速い~約500%速い、約440%速い~約480%速い、約440%速い~約460%速い、約460%速い~約10,000%速い、約460%速い~約9,000%速い、約460%速い~約8,000%速い、約460%速い~約7,000%速い、約460%速い~約6,000%速い、約460%速い~約5,000%速い、約460%速い~約4,000%速い、約460%速い~約3,000%速い、約460%速い~約2,000%速い、約460%速い~約1,000%速い、約460%速い~約500%速い、約460%速い~約480%速い、約480%速い~約10,000%速い、約480%速い~約9,000%速い、約480%速い~約8,000%速い、約480%速い~約7,000%速い、約480%速い~約6,000%速い、約480%速い~約5,000%速い、約480%速い~約4,000%速い、約480%速い~約3,000%速い、約480%速い~約2,000%速い、約480%速い~約1,000%速い、約480%速い~約500%速い、約500%速い~約10,000%速い、約500%速い~約9,000%速い、約500%速い~約8,000%速い、約500%速い~約7,000%速い、約500%速い~約6,000%速い、約500%速い~約5,000%速い、約500%速い~約4,000%速い、約500%速い~約3,000%速い、約500%速い~約2,000%速い、約500%速い~約1,000%速い、約1,000%速い~約10,000%速い、約1,000%速い~約9,000%速い、約1,000%速い~約8,000%速い、約1,000%速い~約7,000%速い、約1,000%速い~約6,000%速い、約1,000%速い~約5,000%速い、約1,000%速い~約4,000%速い、約1,000%速い~約3,000%速い、約1,000%速い~約2,000%速い、約2,000%速い~約10,000%速い、約2,000%速い~約9,000%速い、約2,000%速い~約8,000%速い、約2,000%速い~約7,000%速い、約2,000%速い~約6,000%速い、約2,000%速い~約5,000%速い、約2,000%速い~約4,000%速い、約2,000%速い~約3,000%速い、約3,000%速い~約10,000%速い、約3,000%速い~約9,000%速い、約3,000%速い~約8,000%速い、約3,000%速い~約7,000%速い、約3,000%速い~約6,000%速い、約3,000%速い~約5,000%速い、約3,000%速い~約4,000%速い、約4,000%速い~約10,000%速い、約4,000%速い~約9,000%速い、約4,000%速い~約8,000%速い、約4,000%速い~約7,000%速い、約4,000%速い~約6,000%速い、約4,000%速い~約5,000%速い、約5,000%速い~約10,000%速い、約5,000%速い~約9,000%速い、約5,000%速い~約8,000%速い、約5,000%速い~約7,000%速い、約5,000%速い~約6,000%速い、約6,000%速い~約10,000%速い、約6,000%速い~約9,000%速い、約6,000%速い~約8,000%速い、約6,000%速い~約7,000%速い、約7,000%速い~約10,000%速い、約7,000%速い~約9,000%速い、約7,000%速い~約8,000%速い、約8,000%速い~約10,000%速い、約8,000%速い~約9,000%速い、もしくは約9,000%速い~約10,000%速い)。
本明細書に記載される抗原結合タンパク質構築物(ABPC)のいずれかの一部の実施形態では、第一の抗原結合ドメイン(および存在する場合には、任意に第二の抗原結合ドメイン)の、pH約4.0~約6.5(例えば、本明細書に記載するこの範囲の下位の範囲のいずれか)での解離定数(KD)が、pH約7.0~約8.0(例えば、本明細書に記載するこの範囲の下位の範囲のいずれか)でのKDよりも、より大きい(例えば、検出可能に、より大きい)(例えば、少なくとも5%大きい、少なくとも10%大きい、少なくとも15%大きい、少なくとも20%大きい、少なくとも25%大きい、少なくとも30%大きい、少なくとも35%大きい、少なくとも40%大きい、少なくとも45%大きい、少なくとも50%大きい、少なくとも55%大きい、少なくとも60%大きい、少なくとも65%大きい、少なくとも70%大きい、少なくとも80%大きい、少なくとも85%大きい、少なくとも90%大きい、少なくとも95%大きい、少なくとも100%大きい、少なくとも120%大きい、少なくとも140%大きい、少なくとも160%大きい、少なくとも180%大きい、少なくとも200%大きい、少なくとも220%大きい、少なくとも240%大きい、少なくとも260%大きい、 少なくとも280%大きい、少なくとも300%大きい、少なくとも320%大きい、少なくとも340%大きい、少なくとも360%大きい、少なくとも380%大きい、少なくとも400%大きい、少なくとも420%大きい、少なくとも440%大きい、少なくとも460%大きい、少なくとも480%大きい、少なくとも500%大きい、少なくとも1,000%大きい、少なくとも2,000%大きい、少なくとも3,000%大きい、少なくとも4,000%大きい、少なくとも5,000%大きい、少なくとも6,000%大きい、少なくとも7,000%大きい、少なくとも8,000%大きい、少なくとも9,000%大きい、もしくは少なくとも10,000%大きい、または約5%大きい~約10,000%大きい、約5%大きい~約9,000%大きい~約5%大きい~約8,000%大きい、約5%大きい~約7,000%大きい、約5%大きい~約6,000%大きい、約5%大きい~約5,000%大きい、約5%大きい~約4,000%大きい、約5%大きい~約3,000%大きい、約5%大きい~約2,000%大きい、約5%大きい~約1,000%大きい、約5%大きい~約500%大きい、約5%大きい~約480%大きい、約5%大きい~約460%大きい、約5%大きい~約440%大きい、約5%大きい~約420%大きい、約5%大きい~約400%大きい、約5%大きい~約380%大きい、約5%大きい~約360%大きい、約5%大きい~約340%大きい、約5%大きい~約320%大きい、約5%大きい~約300%大きい、約5%大きい~約280%大きい、約5%大きい~約260%大きい、約5%大きい~約240%大きい、約5%大きい~約220%大きい、約5%大きい~約200%大きい、約5%大きい~約180%大きい、約5%大きい~約160%大きい、約5%大きい~140%大きい、約5%大きい~約120%大きい、約5%大きい~約100%大きい、約5%大きい~約95%大きい、約5%大きい~約90%大きい、約5%大きい~約85%大きい、約5%大きい~約80%大きい、約5%大きい~約75%大きい、約5%大きい~約70%大きい、約5%大きい~約65%大きい、約5%大きい~約60%大きい、約5%大きい~約55%大きい、約5%大きい~約50%大きい、約5%大きい~約45%大きい、約5%大きい~約40%大きい、約5%大きい~約35%大きい、約5%大きい~約30%大きい、約5%大きい~約25%大きい、約5%大きい~約20%大きい、約5%大きい~約15%大きい、約5%大きい~約10%大きい、約10%大きい~約10,000%大きい、約10%大きい~約9,000%大きい、約10%大きい~約8,000%大きい、約10%大きい~約7,000%大きい、約10%大きい~約6,000%大きい、約10%大きい~約5,000%大きい、約10%大きい~約4,000%大きい、約10%大きい~約3,000%大きい、約10%大きい~約2,000%大きい、約10%大きい~約1,000%大きい、約10%大きい~約500%大きい、約10%大きい~約480%大きい、約10%大きい~約460%大きい、約10%大きい~約440%大きい、約10%大きい~約420%大きい、約10%大きい~約400%大きい、約10%大きい~約380%大きい、約10%大きい~約360%大きい、約10%大きい~約340%大きい、約10%大きい~約320%大きい、約10%大きい~約300%大きい、約10%大きい~約280%大きい、約10%大きい~約260%大きい、約10%大きい~約240%大きい、約10%大きい~約220%大きい、約10%大きい~約200%大きい、約10%大きい~約180%大きい、約10%大きい~約160%大きい、約10%大きい~140%大きい、約10%大きい~約120%大きい、約10%大きい~約100%大きい、約10%大きい~約95%大きい、約10%大きい~約90%大きい、約10%大きい~約85%大きい、約10%大きい~約80%大きい、約10%大きい~約75%大きい、約10%大きい~約70%大きい、約10%大きい~約65%大きい、約10%大きい~約60%大きい、約10%大きい~約55%大きい、約10%大きい~約50%大きい、約10%大きい~約45%大きい、約10%大きい~約40%大きい、約10%大きい~約35%大きい、約10%大きい~約30%大きい、約10%大きい~約25%大きい、約10%大きい~約20%大きい、約10%大きい~約15%大きい、約15%大きい~約10,000%大きい、約15%大きい~約9,000%大きい、約15%大きい~約8,000%大きい、約15%大きい~約7,000%大きい、約15%大きい~約6,000%大きい、約15%大きい~約5,000%大きい、約15%大きい~約4,000%大きい、約15%大きい~約3,000%大きい、約15%大きい~約2,000%大きい、約15%大きい~約1,000%大きい、約15%大きい~約500%大きい、約15%大きい~約480%大きい、約15%大きい~約460%大きい、約15%大きい~約440%大きい、約15%大きい~約420%大きい、約15%大きい~約400%大きい、約15%大きい~約380%大きい、約15%大きい~約360%大きい、約15%大きい~約340%大きい、約15%大きい~約320%大きい、約15%大きい~約300%大きい、約15%大きい~約280%大きい、約15%大きい~約260%大きい、約15%大きい~約240%大きい、約15%大きい~約220%大きい、約15%大きい~約200%大きい、約15%大きい~約180%大きい、約15%大きい~約160%大きい、約15%大きい~140%大きい、約15%大きい~約120%大きい、約15%大きい~約100%大きい、約15%大きい~約95%大きい、約15%大きい~約90%大きい、約15%大きい~約85%大きい、約15%大きい~約80%大きい、約15%大きい~約75%大きい、約15%大きい~約70%大きい、約15%大きい~約65%大きい、約15%大きい~約60%大きい、約15%大きい~約55%大きい、約15%大きい~約50%大きい、約15%大きい~約45%大きい、約15%大きい~約40%大きい、約15%大きい~約35%大きい、約15%大きい~約30%大きい、約15%大きい~約25%大きい、約15%大きい~約20%大きい、約20%大きい~約10,000%大きい、約20%大きい~約9,000%大きい、約20%大きい~約8,000%大きい、約20%大きい~約7,000%大きい、約20%大きい~約6,000%大きい、約20%大きい~約5,000%大きい、約20%大きい~約4,000%大きい、約20%大きい~約3,000%大きい、約20%大きい~約2,000%大きい、約20%大きい~約1,000%大きい、約20%大きい~約500%大きい、約20%大きい~約480%大きい、約20%大きい~約460%大きい、約20%大きい~約440%大きい、約20%大きい~約420%大きい、約20%大きい~約400%大きい、約20%大きい~約380%大きい、約20%大きい~約360%大きい、約20%大きい~約340%大きい、約20%大きい~約320%大きい、約20%大きい~約300%大きい、約20%大きい~約280%大きい、約20%大きい~約260%大きい、約20%大きい~約240%大きい、約20%大きい~約220%大きい、約20%大きい~約200%大きい、約20%大きい~約180%大きい、約20%大きい~約160%大きい、約20%大きい~140%大きい、約20%大きい~約120%大きい、約20%大きい~約100%大きい、約20%大きい~約95%大きい、約20%大きい~約90%大きい、約20%大きい~約85%大きい、約20%大きい~約80%大きい、約20%大きい~約75%大きい、約20%大きい~約70%大きい、約20%大きい~約65%大きい、約20%大きい~約60%大きい、約20%大きい~約55%大きい、約20%大きい~約50%大きい、約20%大きい~約45%大きい、約20%大きい~約40%大きい、約20%大きい~約35%大きい、約20%大きい~約30%大きい、約20%大きい~約25%大きい、約25%大きい~約10,000%大きい、約25%大きい~約9,000%大きい、約25%大きい~約8,000%大きい、約25%大きい~約7,000%大きい、約25%大きい~約6,000%大きい、約25%大きい~約5,000%大きい、約25%大きい~約4,000%大きい、約25%大きい~約3,000%大きい、約25%大きい~約2,000%大きい、約25%大きい~約1,000%大きい、約25%大きい~約500%大きい、約25%大きい~約480%大きい、約25%大きい~約460%大きい、約25%大きい~約440%大きい、約25%大きい~約420%大きい、約25%大きい~約400%大きい、約25%大きい~約380%大きい、約25%大きい~約360%大きい、約25%大きい~約340%大きい、約25%大きい~約320%大きい、約25%大きい~約300%大きい、約25%大きい~約280%大きい、約25%大きい~約260%大きい、約25%大きい~約240%大きい、約25%大きい~約220%大きい、約25%大きい~約200%大きい、約25%大きい~約180%大きい、約25%大きい~約160%大きい、約25%大きい~140%大きい、約25%大きい~約120%大きい、約25%大きい~約100%大きい、約25%大きい~約95%大きい、約25%大きい~約90%大きい、約25%大きい~約85%大きい、約25%大きい~約80%大きい、約25%大きい~約75%大きい、約25%大きい~約70%大きい、約25%大きい~約65%大きい、約25%大きい~約60%大きい、約25%大きい~約55%大きい、約25%大きい~約50%大きい、約25%大きい~約45%大きい、約25%大きい~約40%大きい、約25%大きい~約35%大きい、約25%大きい~約30%大きい、約30%大きい~約10,000%大きい、約30%大きい~約9,000%大きい、約30%大きい~約8,000%大きい、約30%大きい~約7,000%大きい、約30%大きい~約6,000%大きい、約30%大きい~約5,000%大きい、約30%大きい~約4,000%大きい、約30%大きい~約3,000%大きい、約30%大きい~約2,000%大きい、約30%大きい~約1,000%大きい、約30%大きい~約500%大きい、約30%大きい~約480%大きい、約30%大きい~約460%大きい、約30%大きい~約440%大きい、約30%大きい~約420%大きい、約30%大き
い~約400%大きい、約30%大きい~約380%大きい、約30%大きい~約360%大きい、約30%大きい~約340%大きい、約30%大きい~約320%大きい、約30%大きい~約300%大きい、約30%大きい~約280%大きい、約30%大きい~約260%大きい、約30%大きい~約240%大きい、約30%大きい~約220%大きい、約30%大きい~約200%大きい、約30%大きい~約180%大きい、約30%大きい~約160%大きい、約30%大きい~140%大きい、約30%大きい~約120%大きい、約30%大きい~約100%大きい、約30%大きい~約95%大きい、約30%大きい~約90%大きい、約30%大きい~約85%大きい、約30%大きい~約80%大きい、約30%大きい~約75%大きい、約30%大きい~約70%大きい、約30%大きい~約65%大きい、約30%大きい~約60%大きい、約30%大きい~約55%大きい、約30%大きい~約50%大きい、約30%大きい~約45%大きい、約30%大きい~約40%大きい、約30%大きい~約35%大きい、約35%大きい~約10,000%大きい、約35%大きい~約9,000%大きい、約35%大きい~約8,000%大きい、約35%大きい~約7,000%大きい、約35%大きい~約6,000%大きい、約35%大きい~約5,000%大きい、約35%大きい~約4,000%大きい、約35%大きい~約3,000%大きい、約35%大きい~約2,000%大きい、約35%大きい~約1,000%大きい、約35%大きい~約500%大きい、約35%大きい~約480%大きい、約35%大きい~約460%大きい、約35%大きい~約440%大きい、約35%大きい~約420%大きい、約35%大きい~約400%大きい、約35%大きい~約380%大きい、約35%大きい~約360%大きい、約35%大きい~約340%大きい、約35%大きい~約320%大きい、約35%大きい~約300%大きい、約35%大きい~約280%大きい、約35%大きい~約260%大きい、約35%大きい~約240%大きい、約35%大きい~約220%大きい、約35%大きい~約200%大きい、約35%大きい~約180%大きい、約35%大きい~約160%大きい、約35%大きい~140%大きい、約35%大きい~約120%大きい、約35%大きい~約100%大きい、約35%大きい~約95%大きい、約35%大きい~約90%大きい、約35%大きい~約85%大きい、約35%大きい~約80%大きい、約35%大きい~約75%大きい、約35%大きい~約70%大きい、約35%大きい~約65%大きい、約35%大きい~約60%大きい、約35%大きい~約55%大きい、約35%大きい~約50%大きい、約35%大きい~約45%大きい、約35%大きい~約40%大きい、約40%大きい~約10,000%大きい、約40%大きい~約9,000%大きい、約40%大きい~約8,000%大きい、約40%大きい~約7,000%大きい、約40%大きい~約6,000%大きい、約40%大きい~約5,000%大きい、約40%大きい~約4,000%大きい、約40%大きい~約3,000%大きい、約40%大きい~約2,000%大きい、約40%大きい~約1,000%大きい、約40%大きい~約500%大きい、約40%大きい~約480%大きい、約40%大きい~約460%大きい、約40%大きい~約440%大きい、約40%大きい~約420%大きい、約40%大きい~約400%大きい、約40%大きい~約380%大きい、約40%大きい~約360%大きい、約40%大きい~約340%大きい、約40%大きい~約320%大きい、約40%大きい~約300%大きい、約40%大きい~約280%大きい、約40%大きい~約260%大きい、約40%大きい~約240%大きい、約40%大きい~約220%大きい、約40%大きい~約200%大きい、約40%大きい~約180%大きい、約40%大きい~約160%大きい、約40%大きい~140%大きい、約40%大きい~約120%大きい、約40%大きい~約100%大きい、約40%大きい~約95%大きい、約40%大きい~約90%大きい、約40%大きい~約85%大きい、約40%大きい~約80%大きい、約40%大きい~約75%大きい、約40%大きい~約70%大きい、約40%大きい~約65%大きい、約40%大きい~約60%大きい、約40%大きい~約55%大きい、約40%大きい~約50%大きい、約40%大きい~約45%大きい、約45%大きい~約10,000%大きい、約45%大きい~約9,000%大きい、約45%大きい~約8,000%大きい、約45%大きい~約7,000%大きい、約45%大きい~約6,000%大きい、約45%大きい~約5,000%大きい、約45%大きい~約4,000%大きい、約45%大きい~約3,000%大きい、約45%大きい~約2,000%大きい、約45%大きい~約1,000%大きい、約45%大きい~約500%大きい、約45%大きい~約480%大きい、約45%大きい~約460%大きい、約45%大きい~約440%大きい、約45%大きい~約420%大きい、約45%大きい~約400%大きい、約45%大きい~約380%大きい、約45%大きい~約360%大きい、約45%大きい~約340%大きい、約45%大きい~約320%大きい、約45%大きい~約300%大きい、約45%大きい~約280%大きい、約45%大きい~約260%大きい、約45%大きい~約240%大きい、約45%大きい~約220%大きい、約45%大きい~約200%大きい、約45%大きい~約180%大きい、約45%大きい~約160%大きい、約45%大きい~140%大きい、約45%大きい~約120%大きい、約45%大きい~約100%大きい、約45%大きい~約95%大きい、約45%大きい~約90%大きい、約45%大きい~約85%大きい、約45%大きい~約80%大きい、約45%大きい~約75%大きい、約45%大きい~約70%大きい、約45%大きい~約65%大きい、約45%大きい~約60%大きい、約45%大きい~約55%大きい、約45%大きい~約50%大きい、約50%大きい~約10,000%大きい、約50%大きい~約9,000%大きい、約50%大きい~約8,000%大きい、約50%大きい~約7,000%大きい、約50%大きい~約6,000%大きい、約50%大きい~約5,000%大きい、約50%大きい~約4,000%大きい、約50%大きい~約3,000%大きい、約50%大きい~約2,000%大きい、約50%大きい~約1,000%大きい、約50%大きい~約500%大きい、約50%大きい~約480%大きい、約50%大きい~約460%大きい、約50%大きい~約440%大きい、約50%大きい~約420%大きい、約50%大きい~約400%大きい、約50%大きい~約380%大きい、約50%大きい~約360%大きい、約50%大きい~約340%大きい、約50%大きい~約320%大きい、約50%大きい~約300%大きい、約50%大きい~約280%大きい、約50%大きい~約260%大きい、約50%大きい~約240%大きい、約50%大きい~約220%大きい、約50%大きい~約200%大きい、約50%大きい~約180%大きい、約50%大きい~約160%大きい、約50%大きい~140%大きい、約50%大きい~約120%大きい、約50%大きい~約100%大きい、約50%大きい~約95%大きい、約50%大きい~約90%大きい、約50%大きい~約85%大きい、約50%大きい~約80%大きい、約50%大きい~約75%大きい、約50%大きい~約70%大きい、約50%大きい~約65%大きい、約50%大きい~約60%大きい、約50%大きい~約55%大きい、約55%大きい~約10,000%大きい、約55%大きい~約9,000%大きい、約55%大きい~約8,000%大きい、約55%大きい~約7,000%大きい、約55%大きい~約6,000%大きい、約55%大きい~約5,000%大きい、約55%大きい~約4,000%大きい、約55%大きい~約3,000%大きい、約55%大きい~約2,000%大きい、約55%大きい~約1,000%大きい、約55%大きい~約500%大きい、約55%大きい~約480%大きい、約55%大きい~約460%大きい、約55%大きい~約440%大きい、約55%大きい~約420%大きい、約55%大きい~約400%大きい、約55%大きい~約380%大きい、約55%大きい~約360%大きい、約55%大きい~約340%大きい、約55%大きい~約320%大きい、約55%大きい~約300%大きい、約55%大きい~約280%大きい、約55%大きい~約260%大きい、約55%大きい~約240%大きい、約55%大きい~約220%大きい、約55%大きい~約200%大きい、約55%大きい~約180%大きい、約55%大きい~約160%大きい、約55%大きい~140%大きい、約55%大きい~約120%大きい、約55%大きい~約100%大きい、約55%大きい~約95%大きい、約55%大きい~約90%大きい、約55%大きい~約85%大きい、約55%大きい~約80%大きい、約55%大きい~約75%大きい、約55%大きい~約70%大きい、約55%大きい~約65%大きい、約55%大きい~約60%大きい、約60%大きい~約10,000%大きい、約60%大きい~約9,000%大きい、約60%大きい~約8,000%大きい、約60%大きい~約7,000%大きい、約60%大きい~約6,000%大きい、約60%大きい~約5,000%大きい、約60%大きい~約4,000%大きい、約60%大きい~約3,000%大きい、約60%大きい~約2,000%大きい、約60%大きい~約1,000%大きい、約60%大きい~約500%大きい、約60%大きい~約480%大きい、約60%大きい~約460%大きい、約60%大きい~約440%大きい、約60%大きい~約420%大きい、約60%大きい~約400%大きい、約60%大きい~約380%大きい、約60%大きい~約360%大きい、約60%大きい~約340%大きい、約60%大きい~約320%大きい、約60%大きい~約300%大きい、約60%大きい~約280%大きい、約60%大きい~約260%大きい、約60%大きい~約240%大きい、約60%大きい~約220%大きい、約60%大きい~約200%大きい、約60%大きい~約180%大きい、約60%大きい~約160%大きい、約60%大きい~140%大きい、約60%大きい~約120%大きい、約60%大きい~約100%大きい、約60%大きい~約95%大きい、約60%大きい~約90%大きい、約60%大きい~約85%大きい、約60%大きい~約80%大きい、約60%大きい~約75%大きい、約60%大きい~約70%大きい、約60%大きい~約65%大きい、約65%大きい~約10,000%大きい、約65%大きい~約9,000%大きい、約65%大きい~約8,000%大きい、約65%大きい~約7,000%大きい、約65%大きい~約6,000%大きい、約65%大きい~約5,000%大きい、約65%大きい~約4,000%大きい、約65%大きい~約3,000%大きい、約65%大きい~約2,000%大きい、約65%大きい~約1,000%大きい、約65%大きい~約500%大きい、約65%大きい~約480%大きい、約65%大きい~約460%大きい、約65%大きい~約440%大きい、約65%大きい~約420%大きい、約65%大きい~約400%大きい、約65%大きい~約380%大きい、約65%大きい~約360%大きい、約65%大きい~約340%大きい、約65%大きい~約320%大きい、約65%大きい~約300%大きい、約65%大きい~約280%大きい、約65%大きい~約260%大きい、約65%大きい~約240%大きい、約65%大きい~約220%大きい、約65%大きい~
約200%大きい、約65%大きい~約180%大きい、約65%大きい~約160%大きい、約65%大きい~140%大きい、約65%大きい~約120%大きい、約65%大きい~約100%大きい、約65%大きい~約95%大きい、約65%大きい~約90%大きい、約65%大きい~約85%大きい、約65%大きい~約80%大きい、約65%大きい~約75%大きい、約65%大きい~約70%大きい、約70%大きい~約10,000%大きい、約70%大きい~約9,000%大きい、約70%大きい~約8,000%大きい、約70%大きい~約7,000%大きい、約70%大きい~約6,000%大きい、約70%大きい~約5,000%大きい、約70%大きい~約4,000%大きい、約70%大きい~約3,000%大きい、約70%大きい~約2,000%大きい、約70%大きい~約1,000%大きい、約70%大きい~約500%大きい、約70%大きい~約480%大きい、約70%大きい~約460%大きい、約70%大きい~約440%大きい、約70%大きい~約420%大きい、約70%大きい~約400%大きい、約70%大きい~約380%大きい、約70%大きい~約360%大きい、約70%大きい~約340%大きい、約70%大きい~約320%大きい、約70%大きい~約300%大きい、約70%大きい~約280%大きい、約70%大きい~約260%大きい、約70%大きい~約240%大きい、約70%大きい~約220%大きい、約70%大きい~約200%大きい、約70%大きい~約180%大きい、約70%大きい~約160%大きい、約70%大きい~140%大きい、約70%大きい~約120%大きい、約70%大きい~約100%大きい、約70%大きい~約95%大きい、約70%大きい~約90%大きい、約70%大きい~約85%大きい、約70%大きい~約80%大きい、約70%大きい~約75%大きい、約75%大きい~約10,000%大きい、約75%大きい~約9,000%大きい、約75%大きい~約8,000%大きい、約75%大きい~約7,000%大きい、約75%大きい~約6,000%大きい、約75%大きい~約5,000%大きい、約75%大きい~約4,000%大きい、約75%大きい~約3,000%大きい、約75%大きい~約2,000%大きい、約75%大きい~約1,000%大きい、約75%大きい~約500%大きい、約75%大きい~約480%大きい、約75%大きい~約460%大きい、約75%大きい~約440%大きい、約75%大きい~約420%大きい、約75%大きい~約400%大きい、約75%大きい~約380%大きい、約75%大きい~約360%大きい、約75%大きい~約340%大きい、約75%大きい~約320%大きい、約75%大きい~約300%大きい、約75%大きい~約280%大きい、約75%大きい~約260%大きい、約75%大きい~約240%大きい、約75%大きい~約220%大きい、約75%大きい~約200%大きい、約75%大きい~約180%大きい、約75%大きい~約160%大きい、約75%大きい~140%大きい、約75%大きい~約120%大きい、約75%大きい~約100%大きい、約75%大きい~約95%大きい、約75%大きい~約90%大きい、約75%大きい~約85%大きい、約75%大きい~約80%大きい、約80%大きい~約10,000%大きい、約80%大きい~約9,000%大きい、約80%大きい~約8,000%大きい、約80%大きい~約7,000%大きい、約80%大きい~約6,000%大きい、約80%大きい~約5,000%大きい、約80%大きい~約4,000%大きい、約80%大きい~約3,000%大きい、約80%大きい~約2,000%大きい、約80%大きい~約1,000%大きい、約80%大きい~約500%大きい、約80%大きい~約480%大きい、約80%大きい~約460%大きい、約80%大きい~約440%大きい、約80%大きい~約420%大きい、約80%大きい~約400%大きい、約80%大きい~約380%大きい、約80%大きい~約360%大きい、約80%大きい~約340%大きい、約80%大きい~約320%大きい、約80%大きい~約300%大きい、約80%大きい~約280%大きい、約80%大きい~約260%大きい、約80%大きい~約240%大きい、約80%大きい~約220%大きい、約80%大きい~約200%大きい、約80%大きい~約180%大きい、約80%大きい~約160%大きい、約80%大きい~140%大きい、約80%大きい~約120%大きい、約80%大きい~約100%大きい、約80%大きい~約95%大きい、約80%大きい~約90%大きい、約80%大きい~約85%大きい、約85%大きい~約10,000%大きい、約85%大きい~約9,000%大きい、約85%大きい~約8,000%大きい、約85%大きい~約7,000%大きい、約85%大きい~約6,000%大きい、約85%大きい~約5,000%大きい、約85%大きい~約4,000%大きい、約85%大きい~約3,000%大きい、約85%大きい~約2,000%大きい、約85%大きい~約1,000%大きい、約85%大きい~約500%大きい、約85%大きい~約480%大きい、約85%大きい~約460%大きい、約85%大きい~約440%大きい、約85%大きい~約420%大きい、約85%大きい~約400%大きい、約85%大きい~約380%大きい、約85%大きい~約360%大きい、約85%大きい~約340%大きい、約85%大きい~約320%大きい、約85%大きい~約300%大きい、約85%大きい~約280%大きい、約85%大きい~約260%大きい、約85%大きい~約240%大きい、約85%大きい~約220%大きい、約85%大きい~約200%大きい、約85%大きい~約180%大きい、約85%大きい~約160%大きい、約85%大きい~140%大きい、約85%大きい~約120%大きい、約85%大きい~約100%大きい、約85%大きい~約95%大きい、約85%大きい~約90%大きい、約90%大きい~約10,000%大きい、約90%大きい~約9,000%大きい、約90%大きい~約8,000%大きい、約90%大きい~約7,000%大きい、約90%大きい~約6,000%大きい、約90%大きい~約5,000%大きい、約90%大きい~約4,000%大きい、約90%大きい~約3,000%大きい、約90%大きい~約2,000%大きい、約90%大きい~約1,000%大きい、約90%大きい~約500%大きい、約90%大きい~約480%大きい、約90%大きい~約460%大きい、約90%大きい~約440%大きい、約90%大きい~約420%大きい、約90%大きい~約400%大きい、約90%大きい~約380%大きい、約90%大きい~約360%大きい、約90%大きい~約340%大きい、約90%大きい~約320%大きい、約90%大きい~約300%大きい、約90%大きい~約280%大きい、約90%大きい~約260%大きい、約90%大きい~約240%大きい、約90%大きい~約220%大きい、約90%大きい~約200%大きい、約90%大きい~約180%大きい、約90%大きい~約160%大きい、約90%大きい~140%大きい、約90%大きい~約120%大きい、約90%大きい~約100%大きい、約90%大きい~約95%大きい、約95%大きい~約10,000%大きい、約95%大きい~約9,000%大きい、約95%大きい~約8,000%大きい、約95%大きい~約7,000%大きい、約95%大きい~約6,000%大きい、約95%大きい~約5,000%大きい、約95%大きい~約4,000%大きい、約95%大きい~約3,000%大きい、約95%大きい~約2,000%大きい、約95%大きい~約1,000%大きい、約95%大きい~約500%大きい、約95%大きい~約480%大きい、約95%大きい~約460%大きい、約95%大きい~約440%大きい、約95%大きい~約420%大きい、約95%大きい~約400%大きい、約95%大きい~約380%大きい、約95%大きい~約360%大きい、約95%大きい~約340%大きい、約95%大きい~約320%大きい、約95%大きい~約300%大きい、約95%大きい~約280%大きい、約95%大きい~約260%大きい、約95%大きい~約240%大きい、約95%大きい~約220%大きい、約95%大きい~約200%大きい、約95%大きい~約180%大きい、約95%大きい~約160%大きい、約95%大きい~140%大きい、約95%大きい~約120%大きい、約95%大きい~約100%大きい、約100%大きい~約10,000%大きい、約100%大きい~約9,000%大きい、約100%大きい~約8,000%大きい、約100%大きい~約7,000%大きい、約100%大きい~約6,000%大きい、約100%大きい~約5,000%大きい、約100%大きい~約4,000%大きい、約100%大きい~約3,000%大きい、約100%大きい~約2,000%大きい、約100%大きい~約1,000%大きい、約100%大きい~約500%大きい、約100%大きい~約480%大きい、約100%大きい~約460%大きい、約100%大きい~約440%大きい、約100%大きい~約420%大きい、約100%大きい~約400%大きい、約100%大きい~約380%大きい、約100%大きい~約360%大きい、約100%大きい~約340%大きい、約100%大きい~約320%大きい、約100%大きい~約300%大きい、約100%大きい~約280%大きい、約100%大きい~約260%大きい、約100%大きい~約240%大きい、約100%大きい~約220%大きい、約100%大きい~約200%大きい、約100%大きい~約180%大きい、約100%大きい~約160%大きい、約100%大きい~140%大きい、約100%大きい~約120%大きい、約120%大きい~約10,000%大きい、約120%大きい~約9,000%大きい、約120%大きい~約8,000%大きい、約120%大きい~約7,000%大きい、約120%大きい~約6,000%大きい、約120%大きい~約5,000%大きい、約120%大きい~約4,000%大きい、約120%大きい~約3,000%大きい、約120%大きい~約2,000%大きい、約120%大きい~約1,000%大きい、約120%大きい~約500%大きい、約120%大きい~約480%大きい、約120%大きい~約460%大きい、約120%大きい~約440%大きい、約120%大きい~約420%大きい、約120%大きい~約400%大きい、約120%大きい~約380%大きい、約120%大きい~約360%大きい、約120%大きい~約340%大きい、約120%大きい~約320%大きい、約120%大きい~約300%大きい、約120%大きい~約280%大きい、約120%大きい~約260%大きい、約120%大きい~約240%大きい、約120%大きい~約220%大きい、約120%大きい~約200%大きい、約120%大きい~約180%大きい、約120%大きい~約160%大きい、約120%大きい~140%大きい、約140%大きい~約10,000%大きい、約140%大きい~約9,000%大きい、約140%大きい~約8,000%大きい、約140%大きい~約7,000%大きい、約140%大きい~約6,000%大きい、約140%大きい~約5,000%大きい、約140%大きい~約4,000%大きい、約140%大きい~約3,000%大きい、約140%大きい~約2,000%大きい、約140%大きい~約1,000%大きい、約140%大きい~約500%大きい、約140%大きい~約480%大きい、約140%大きい~約460%大きい、約140%大きい~約440%大きい、約140%大きい~約420%大きい、約140%大きい~約400%大きい
、約140%大きい~約380%大きい、約140%大きい~約360%大きい、約140%大きい~約340%大きい、約140%大きい~約320%大きい、約140%大きい~約300%大きい、約140%大きい~約280%大きい、約140%大きい~約260%大きい、約140%大きい~約240%大きい、約140%大きい~約220%大きい、約140%大きい~約200%大きい、約140%大きい~約180%大きい、約140%大きい~約160%大きい、約160%大きい~約10,000%大きい、約160%大きい~約9,000%大きい、約160%大きい~約8,000%大きい、約160%大きい~約7,000%大きい、約160%大きい~約6,000%大きい、約160%大きい~約5,000%大きい、約160%大きい~約4,000%大きい、約160%大きい~約3,000%大きい、約160%大きい~約2,000%大きい、約160%大きい~約1,000%大きい、約160%大きい~約500%大きい、約160%大きい~約480%大きい、約160%大きい~約460%大きい、約160%大きい~約440%大きい、約160%大きい~約420%大きい、約160%大きい~約400%大きい、約160%大きい~約380%大きい、約160%大きい~約360%大きい、約160%大きい~約340%大きい、約160%大きい~約320%大きい、約160%大きい~約300%大きい、約160%大きい~約280%大きい、約160%大きい~約260%大きい、約160%大きい~約240%大きい、約160%大きい~約220%大きい、約160%大きい~約200%大きい、約160%大きい~約180%大きい、約180%大きい~約10,000%大きい、約180%大きい~約9,000%大きい、約180%大きい~約8,000%大きい、約180%大きい~約7,000%大きい、約180%大きい~約6,000%大きい、約180%大きい~約5,000%大きい、約180%大きい~約4,000%大きい、約180%大きい~約3,000%大きい、約180%大きい~約2,000%大きい、約180%大きい~約1,000%大きい、約180%大きい~約500%大きい、約180%大きい~約480%大きい、約180%大きい~約460%大きい、約180%大きい~約440%大きい、約180%大きい~約420%大きい、約180%大きい~約400%大きい、約180%大きい~約380%大きい、約180%大きい~約360%大きい、約180%大きい~約340%大きい、約180%大きい~約320%大きい、約180%大きい~約300%大きい、約180%大きい~約280%大きい、約180%大きい~約260%大きい、約180%大きい~約240%大きい、約180%大きい~約220%大きい、約180%大きい~約200%大きい、約200%大きい~約10,000%大きい、約200%大きい~約9,000%大きい、約200%大きい~約8,000%大きい、約200%大きい~約7,000%大きい、約200%大きい~約6,000%大きい、約200%大きい~約5,000%大きい、約200%大きい~約4,000%大きい、約200%大きい~約3,000%大きい、約200%大きい~約2,000%大きい、約200%大きい~約1,000%大きい、約200%大きい~約500%大きい、約200%大きい~約480%大きい、約200%大きい~約460%大きい、約200%大きい~約440%大きい、約200%大きい~約420%大きい、約200%大きい~約400%大きい、約200%大きい~約380%大きい、約200%大きい~約360%大きい、約200%大きい~約340%大きい、約200%大きい~約320%大きい、約200%大きい~約300%大きい、約200%大きい~約280%大きい、約200%大きい~約260%大きい、約200%大きい~約240%大きい、約200%大きい~約220%大きい、約220%大きい~約10,000%大きい、約220%大きい~約9,000%大きい、約220%大きい~約8,000%大きい、約220%大きい~約7,000%大きい、約220%大きい~約6,000%大きい、約220%大きい~約5,000%大きい、約220%大きい~約4,000%大きい、約220%大きい~約3,000%大きい、約220%大きい~約2,000%大きい、約220%大きい~約1,000%大きい、約220%大きい~約500%大きい、約220%大きい~約480%大きい、約220%大きい~約460%大きい、約220%大きい~約440%大きい、約220%大きい~約420%大きい、約220%大きい~約400%大きい、約220%大きい~約380%大きい、約220%大きい~約360%大きい、約220%大きい~約340%大きい、約220%大きい~約320%大きい、約220%大きい~約300%大きい、約220%大きい~約280%大きい、約220%大きい~約260%大きい、約220%大きい~約240%大きい、約240%大きい~約10,000%大きい、約240%大きい~約9,000%大きい、約240%大きい~約8,000%大きい、約240%大きい~約7,000%大きい、約240%大きい~約6,000%大きい、約240%大きい~約5,000%大きい、約240%大きい~約4,000%大きい、約240%大きい~約3,000%大きい、約240%大きい~約2,000%大きい、約240%大きい~約1,000%大きい、約240%大きい~約500%大きい、約240%大きい~約480%大きい、約240%大きい~約460%大きい、約240%大きい~約440%大きい、約240%大きい~約420%大きい、約240%大きい~約400%大きい、約240%大きい~約380%大きい、約240%大きい~約360%大きい、約240%大きい~約340%大きい、約240%大きい~約320%大きい、約240%大きい~約300%大きい、約240%大きい~約280%大きい、約240%大きい~約260%大きい、約260%大きい~約10,000%大きい、約260%大きい~約9,000%大きい、約260%大きい~約8,000%大きい、約260%大きい~約7,000%大きい、約260%大きい~約6,000%大きい、約260%大きい~約5,000%大きい、約260%大きい~約4,000%大きい、約260%大きい~約3,000%大きい、約260%大きい~約2,000%大きい、約260%大きい~約1,000%大きい、約260%大きい~約500%大きい、約260%大きい~約480%大きい、約260%大きい~約460%大きい、約260%大きい~約440%大きい、約260%大きい~約420%大きい、約260%大きい~約400%大きい、約260%大きい~約380%大きい、約260%大きい~約360%大きい、約260%大きい~約340%大きい、約260%大きい~約320%大きい、約260%大きい~約300%大きい、約260%大きい~約280%大きい、約280%大きい~約10,000%大きい、約280%大きい~約9,000%大きい、約280%大きい~約8,000%大きい、約280%大きい~約7,000%大きい、約280%大きい~約6,000%大きい、約280%大きい~約5,000%大きい、約280%大きい~約4,000%大きい、約280%大きい~約3,000%大きい、約280%大きい~約2,000%大きい、約280%大きい~約1,000%大きい、約280%大きい~約500%大きい、約280%大きい~約480%大きい、約280%大きい~約460%大きい、約280%大きい~約440%大きい、約280%大きい~約420%大きい、約280%大きい~約400%大きい、約280%大きい~約380%大きい、約280%大きい~約360%大きい、約280%大きい~約340%大きい、約280%大きい~約320%大きい、約280%大きい~約300%大きい、約300%大きい~約10,000%大きい、約300%大きい~約9,000%大きい、約300%大きい~約8,000%大きい、約300%大きい~約7,000%大きい、約300%大きい~約6,000%大きい、約300%大きい~約5,000%大きい、約300%大きい~約4,000%大きい、約300%大きい~約3,000%大きい、約300%大きい~約2,000%大きい、約300%大きい~約1,000%大きい、約300%大きい~約500%大きい、約300%大きい~約480%大きい、約300%大きい~約460%大きい、約300%大きい~約440%大きい、約300%大きい~約420%大きい、約300%大きい~約400%大きい、約300%大きい~約380%大きい、約300%大きい~約360%大きい、約300%大きい~約340%大きい、約300%大きい~約320%大きい、約320%大きい~約10,000%大きい、約320%大きい~約9,000%大きい、約320%大きい~約8,000%大きい、約320%大きい~約7,000%大きい、約320%大きい~約6,000%大きい、約320%大きい~約5,000%大きい、約320%大きい~約4,000%大きい、約320%大きい~約3,000%大きい、約320%大きい~約2,000%大きい、約320%大きい~約1,000%大きい、約320%大きい~約500%大きい、約320%大きい~約480%大きい、約320%大きい~約460%大きい、約320%大きい~約440%大きい、約320%大きい~約420%大きい、約320%大きい~約400%大きい、約320%大きい~約380%大きい、約320%大きい~約360%大きい、約320%大きい~約340%大きい、約340%大きい~約10,000%大きい、約340%大きい~約9,000%大きい、約340%大きい~約8,000%大きい、約340%大きい~約7,000%大きい、約340%大きい~約6,000%大きい、約340%大きい~約5,000%大きい、約340%大きい~約4,000%大きい、約340%大きい~約3,000%大きい、約340%大きい~約2,000%大きい、約340%大きい~約1,000%大きい、約340%大きい~約500%大きい、約340%大きい~約480%大きい、約340%大きい~約460%大きい、約340%大きい~約440%大きい、約340%大きい~約420%大きい、約340%大きい~約400%大きい、約340%大きい~約380%大きい、約340%大きい~約360%大きい、約360%大きい~約10,000%大きい、約360%大きい~約9,000%大きい、約360%大きい~約8,000%大きい、約360%大きい~約7,000%大きい、約360%大きい~約6,000%大きい、約360%大きい~約5,000%大きい、約360%大きい~約4,000%大きい、約360%大きい~約3,000%大きい、約360%大きい~約2,000%大きい、約360%大きい~約1,000%大きい、約360%大きい~約500%大きい、約360%大きい~約480%大きい、約360%大きい~約460%大きい、約360%大きい~約440%大きい、約360%大きい~約420%大きい、約360%大きい~約400%大きい、約360%大きい~約380%大きい、約380%大きい~約10,000%大きい、約380%大きい~約9,000%大きい、約380%大きい~約8,000%大きい、約380%大きい~約7,000%大きい、約380%大きい~約6,000%大きい、約380%大きい~約5,000%大きい、約380%大きい~約4,000%大きい、約380%大きい~約3,000%大きい、約380%大きい~約2,000%大きい、約380%大きい~約1,000%大きい、約380%大きい~約500%大きい、約380%大きい~約480%大きい、約380%大きい~約460%大きい、約380%大きい~約440%大きい、約380%大きい~約420%大きい、約380%大きい~約400%大きい、約400%大きい
~約10,000%大きい、約400%大きい~約9,000%大きい、約400%大きい~約8,000%大きい、約400%大きい~約7,000%大きい、約400%大きい~約6,000%大きい、約400%大きい~約5,000%大きい、約400%大きい~約4,000%大きい、約400%大きい~約3,000%大きい、約400%大きい~約2,000%大きい、約400%大きい~約1,000%大きい、約400%大きい~約500%大きい、約400%大きい~約480%大きい、約400%大きい~約460%大きい、約400%大きい~約440%大きい、約400%大きい~約420%大きい、約420%大きい~約10,000%大きい、約420%大きい~約9,000%大きい、約420%大きい~約8,000%大きい、約420%大きい~約7,000%大きい、約420%大きい~約6,000%大きい、約420%大きい~約5,000%大きい、約420%大きい~約4,000%大きい、約420%大きい~約3,000%大きい、約420%大きい~約2,000%大きい、約420%大きい~約1,000%大きい、約420%大きい~約500%大きい、約420%大きい~約480%大きい、約420%大きい~約460%大きい、約420%大きい~約440%大きい、約440%大きい~約10,000%大きい、約440%大きい~約9,000%大きい、約440%大きい~約8,000%大きい、約440%大きい~約7,000%大きい、約440%大きい~約6,000%大きい、約440%大きい~約5,000%大きい、約440%大きい~約4,000%大きい、約440%大きい~約3,000%大きい、約440%大きい~約2,000%大きい、約440%大きい~約1,000%大きい、約440%大きい~約500%大きい、約440%大きい~約480%大きい、約440%大きい~約460%大きい、約460%大きい~約10,000%大きい、約460%大きい~約9,000%大きい、約460%大きい~約8,000%大きい、約460%大きい~約7,000%大きい、約460%大きい~約6,000%大きい、約460%大きい~約5,000%大きい、約460%大きい~約4,000%大きい、約460%大きい~約3,000%大きい、約460%大きい~約2,000%大きい、約460%大きい~約1,000%大きい、約460%大きい~約500%大きい、約460%大きい~約480%大きい、約480%大きい~約10,000%大きい、約480%大きい~約9,000%大きい、約480%大きい~約8,000%大きい、約480%大きい~約7,000%大きい、約480%大きい~約6,000%大きい、約480%大きい~約5,000%大きい、約480%大きい~約4,000%大きい、約480%大きい~約3,000%大きい、約480%大きい~約2,000%大きい、約480%大きい~約1,000%大きい、約480%大きい~約500%大きい、約500%大きい~約10,000%大きい、約500%大きい~約9,000%大きい、約500%大きい~約8,000%大きい、約500%大きい~約7,000%大きい、約500%大きい~約6,000%大きい、約500%大きい~約5,000%大きい、約500%大きい~約4,000%大きい、約500%大きい~約3,000%大きい、約500%大きい~約2,000%大きい、約500%大きい~約1,000%大きい、約1,000%大きい~約10,000%大きい、約1,000%大きい~約9,000%大きい、約1,000%大きい~約8,000%大きい、約1,000%大きい~約7,000%大きい、約1,000%大きい~約6,000%大きい、約1,000%大きい~約5,000%大きい、約1,000%大きい~約4,000%大きい、約1,000%大きい~約3,000%大きい、約1,000%大きい~約2,000%大きい、約2,000%大きい~約10,000%大きい、約2,000%大きい~約9,000%大きい、約2,000%大きい~約8,000%大きい、約2,000%大きい~約7,000%大きい、約2,000%大きい~約6,000%大きい、約2,000%大きい~約5,000%大きい、約2,000%大きい~約4,000%大きい、約2,000%大きい~約3,000%大きい、約3,000%大きい~約10,000%大きい、約3,000%大きい~約9,000%大きい、約3,000%大きい~約8,000%大きい、約3,000%大きい~約7,000%大きい、約3,000%大きい~約6,000%大きい、約3,000%大きい~約5,000%大きい、約3,000%大きい~約4,000%大きい、約4,000%大きい~約10,000%大きい、約4,000%大きい~約9,000%大きい、約4,000%大きい~約8,000%大きい、約4,000%大きい~約7,000%大きい、約4,000%大きい~約6,000%大きい、約4,000%大きい~約5,000%大きい、約5,000%大きい~約10,000%大きい、約5,000%大きい~約9,000%大きい、約5,000%大きい~約8,000%大きい、約5,000%大きい~約7,000%大きい、約5,000%大きい~約6,000%大きい、約6,000%大きい~約10,000%大きい、約6,000%大きい~約9,000%大きい、約6,000%大きい~約8,000%大きい、約6,000%大きい~約7,000%大きい、約7,000%大きい~約10,000%大きい、約7,000%大きい~約9,000%大きい、約7,000%大きい~約8,000%大きい、約8,000%大きい~約10,000%大きい、約8,000%大きい~約9,000%大きい、もしくは約9,000%大きい~約10,000%大きい)。
本明細書に記載される抗原結合タンパク質構築物(ABPC)のいずれかの一部の実施形態では、第一の抗原結合ドメイン(および存在する場合には、任意に第二の抗原結合ドメイン)の、pH約4.0~約6.5(例えば、本明細書に記載するこの範囲の下位の範囲のいずれか)での解離速度が、pH約7.0~約8.0(例えば、または本明細書に記載するこの範囲の下位の範囲のいずれか)での解離速度よりも、より速い(例えば、少なくとも0.2倍速い、少なくとも0.3倍、少なくとも0.4倍、少なくとも0.5倍、少なくとも0.6倍、少なくとも0.7倍、少なくとも0.8倍、少なくとも0.9倍、少なくとも1.0倍、少なくとも1.5倍、少なくとも2.0倍、少なくとも2.5倍、少なくとも3.0倍、少なくとも3.5倍、少なくとも4.0倍、少なくとも4.5倍、少なくとも5.0倍、少なくとも5.5倍、少なくとも6.0倍、少なくとも6.5倍、少なくとも7.0倍、少なくとも7.5倍、少なくとも8.0倍、少なくとも8.5倍、少なくとも9.0倍、少なくとも9.5倍、少なくとも10.0倍、少なくとも10.5倍、少なくとも11.0倍、少なくとも11.5倍、少なくとも12.0倍、少なくとも12.5倍、少なくとも13.0倍、少なくとも13.5倍、少なくとも14.0倍、少なくとも14.5倍、少なくとも15.0倍、少なくとも15.5倍、少なくとも16.0倍、少なくとも16.5倍、少なくとも17.0倍、少なくとも17.5倍、少なくとも18.0倍、少なくとも18.5倍、少なくとも19.0倍、少なくとも19.5倍、少なくとも20倍、少なくとも25倍、少なくとも30倍、少なくとも35倍、少なくとも40倍、少なくとも45倍、少なくとも50倍、少なくとも55倍、少なくとも60倍、少なくとも65倍、少なくとも70倍、少なくとも75倍、少なくとも80倍、少なくとも85倍、少なくとも90倍、少なくとも95倍、もしくは少なくとも100倍速い または約0.2倍~約100倍速い、約0.2倍~約90倍速い、約0.2倍~約80倍速い、約0.2倍~約70倍速い、約0.2倍~約60倍速い、約0.2倍~約50倍速い、約0.2倍~約40倍速い、約0.2倍~約30倍速い、約0.2倍~約20倍速い、約0.2倍~約15倍速い、約0.2倍~約10倍速い、約0.2倍~約5倍、約0.2倍~約2倍速い、約0.2倍~約1倍速い、約0.2倍~約0.5倍速い、約0.5倍~約100倍速い、約0.5倍~約90倍速い、約0.5倍~約80倍速い、約0.5倍~約70倍速い、約0.5倍~約60倍速い、約0.5倍~約50倍速い、約0.5倍~約40倍速い、約0.5倍~約30倍速い、約0.5倍~約20倍速い、約0.5倍~約15倍速い、約0.5倍~約10倍速い、約0.5倍~約5倍、約0.5倍~約2倍速い、約0.5倍~約1倍速い、約1倍~約100倍速い、約1倍~約90倍速い、約1倍~約80倍速い、約1倍~約70倍速い、約1倍~約60倍速い、約1倍~約50倍速い、約1倍~約40倍速い、約1倍~約30倍速い、約1倍~約20倍速い、約1倍~約15倍速い、約1倍~約10倍速い、約1倍~約5倍、約1倍~約2倍速い、約2倍~約100倍速い、約2倍~約90倍速い、約2倍~約80倍速い、約2倍~約70倍速い、約2倍~約60倍速い、約2倍~約50倍速い、約2倍~約40倍速い、約2倍~約30倍速い、約2倍~約20倍速い、約2倍~約15倍速い、約2倍~約10倍速い、約2倍~約5倍、約5倍~約100倍速い、約5倍~約90倍速い、約5倍~約80倍速い、約5倍~約70倍速い、約5倍~約60倍速い、約5倍~約50倍速い、約5倍~約40倍速い、約5倍~約30倍速い、約5倍~約20倍速い、約5倍~約15倍速い、約5倍~約10倍速い、約10倍~約100倍速い、約10倍~約90倍速い、約10倍~約80倍速い、約10倍~約70倍速い、約10倍~約60倍速い、約10倍~約50倍速い、約10倍~約40倍速い、約10倍~約30倍速い、約10倍~約20倍速い、約10倍~約15倍速い、約15倍~約100倍速い、約15倍~約90倍速い、約15倍~約80倍速い、約15倍~約70倍速い、約15倍~約60倍速い、約15倍~約50倍速い、約15倍~約40倍速い、約15倍~約30倍速い、約15倍~約20倍速い、約20倍~約100倍速い、約20倍~約90倍速い、約20倍~約80倍速い、約20倍~約70倍速い、約20倍~約60倍速い、約20倍~約50倍速い、約20倍~約40倍速い、約20倍~約30倍速い、約30倍~約100倍速い、約30倍~約90倍速い、約30倍~約80倍速い、約30倍~約70倍速い、約30倍~約60倍速い、約30倍~約50倍速い、約30倍~約40倍速い、約40倍~約100倍速い、約40倍~約90倍速い、約40倍~約80倍速い、約40倍~約70倍速い、約40倍~約60倍速い、約40倍~約50倍速い、約50倍~約100倍速い、約50倍~約90倍速い、約50倍~約80倍速い、約50倍~約70倍速い、約50倍~約60倍速い、約60倍~約100倍速い、約60倍~約90倍速い、約60倍~約80倍速い、約60倍~約70倍速い、約70倍~約100倍速い、約70倍~約90倍速い、約70倍~約80倍速い、約80倍~約100倍速い、約80倍~約90倍速い、もしくは約90倍~約100倍速い)。
本明細書に記載されるいずれかの抗原結合タンパク質構築物(ABPC)の一部の実施形態では、第一の抗原結合ドメイン(および存在する場合には、任意に第二の抗原結合ドメイン)の、pH約4.0~約6.5(例えば、本明細書に記載するこの範囲の下位の範囲のいずれか)での解離定数(KD)が、pH約7.0~約8.0(例えば、本明細書に記載するこの範囲の下位の範囲のいずれか)でのKDよりも、より大きい(例えば、検出可能に、より大きい)(例えば、少なくとも0.2倍大きい、少なくとも0.3倍、少なくとも0.4倍、少なくとも0.5倍、少なくとも0.6倍、少なくとも0.7倍、少なくとも0.8倍、少なくとも0.9倍、少なくとも1.0倍、少なくとも1.5倍、少なくとも2.0倍、少なくとも2.5倍、少なくとも3.0倍、少なくとも3.5倍、少なくとも4.0倍、少なくとも4.5倍、少なくとも5.0倍、少なくとも5.5倍、少なくとも6.0倍、少なくとも6.5倍、少なくとも7.0倍、少なくとも7.5倍、少なくとも8.0倍、少なくとも8.5倍、少なくとも9.0倍、少なくとも9.5倍、少なくとも10.0倍、少なくとも10.5倍、少なくとも11.0倍、少なくとも11.5倍、少なくとも12.0倍、少なくとも12.5倍、少なくとも13.0倍、少なくとも13.5倍、少なくとも14.0倍、少なくとも14.5倍、少なくとも15.0倍、少なくとも15.5倍、少なくとも16.0倍、少なくとも16.5倍、少なくとも17.0倍、少なくとも17.5倍、少なくとも18.0倍、少なくとも18.5倍、少なくとも19.0倍、少なくとも19.5倍、少なくとも20倍大きい、少なくとも25倍大きい、少なくとも30倍大きい、少なくとも35倍大きい、少なくとも40倍大きい、少なくとも45倍大きい、少なくとも50倍大きい、少なくとも55倍大きい、少なくとも60倍大きい、少なくとも65倍大きい、少なくとも70倍大きい、少なくとも75倍大きい、少なくとも80倍大きい、少なくとも85倍大きい、少なくとも90倍大きい、少なくとも95倍大きい、もしくは少なくとも100倍大きい、または約0.2倍~約100倍大きい、約0.2倍~約90倍大きい、約0.2倍~約80倍大きい、約0.2倍~約70倍大きい、約0.2倍~約60倍大きい、約0.2倍~約50倍大きい、約0.2倍~約40倍大きい、約0.2倍~約30倍大きい、約0.2倍~約25倍大きい、約0.2倍~約20倍大きい、約0.2倍~約15倍大きい、約0.2倍~約10倍大きい、約0.2倍~約8倍大きい、約0.2倍~約5倍大きい、約0.2倍~約2倍大きい、約0.2倍~約1倍大きい、約0.2倍~約0.5倍大きい、約0.5倍~約100倍大きい、約0.5倍~約90倍大きい、約0.5倍~約80倍大きい、約0.5倍~約70倍大きい、約0.5倍~約60倍大きい、約0.5倍~約50倍大きい、約0.5倍~約40倍大きい、約0.5倍~約30倍大きい、約0.5倍~約25倍大きい、約0.5倍~約20倍大きい、約0.5倍~約15倍大きい、約0.5倍~約10倍大きい、約0.5倍~約8倍大きい、約0.5倍~約5倍大きい、約0.5倍~約2倍大きい、約0.5倍~約1倍大きい、約1倍~約100倍大きい、約1倍~約90倍大きい、約1倍~約80倍大きい、約1倍~約70倍大きい、約1倍~約60倍大きい、約1倍~約50倍大きい、約1倍~約40倍大きい、約1倍~約30倍大きい、約1倍~約25倍大きい、約1倍~約20倍大きい、約1倍~約15倍大きい、約1倍~約10倍大きい、約1倍~約8倍、約1倍~約5倍、約1倍~約2倍大きい、約2倍~約100倍大きい、約2倍~約90倍大きい、約2倍~約80倍大きい、約2倍~約70倍大きい、約2倍~約60倍大きい、約2倍~約50倍大きい、約2倍~約40倍大きい、約2倍~約30倍大きい、約2倍~約25倍大きい、約2倍~約20倍大きい、約2倍~約15倍大きい、約2倍~約10倍大きい、約2倍~約8倍大きい、約2倍~約5倍大きい、約5倍~約100倍大きい、約5倍~約90倍大きい、約5倍~約80倍大きい、約5倍~約70倍大きい、約5倍~約60倍大きい、約5倍~約50倍大きい、約5倍~約40倍大きい、約5倍~約30倍大きい、約5倍~約25倍大きい、約5倍~約20倍大きい、約5倍~約15倍大きい、約5倍~約10倍大きい、約5倍~約8倍大きい、約8倍~約100倍大きい、約8倍~約90倍大きい、約8倍~約80倍大きい、約8倍~約70倍大きい、約8倍~約60倍大きい、約8倍~約50倍大きい、約8倍~約40倍大きい、約8倍~約30倍大きい、約8倍~約25倍大きい、約8倍~約20倍大きい、約8倍~約15倍大きい、約8倍~約10倍大きい、約10倍~約100倍大きい、約10倍~約90倍大きい、約10倍~約80倍大きい、約10倍~約70倍大きい、約10倍~約60倍大きい、約10倍~約50倍大きい、約10倍~約40倍大きい、約10倍~約30倍大きい、約10倍~約25倍大きい、約10倍~約20倍大きい、約10倍~約15倍大きい、約15倍~約100倍大きい、約15倍~約90倍大きい、約15倍~約80倍大きい、約15倍~約70倍大きい、約15倍~約60倍大きい、約15倍~約50倍大きい、約15倍~約40倍大きい、約15倍~約30倍大きい、約15倍~約25倍大きい、約15倍~約20倍大きい、約20倍~約100倍大きい、約20倍~約90倍大きい、約20倍~約80倍大きい、約20倍~約70倍大きい、約20倍~約60倍大きい、約20倍~約50倍大きい、約20倍~約40倍大きい、約20倍~約30倍大きい、約20倍~約25倍大きい、約25倍~約100倍大きい、約25倍~約90倍大きい、約25倍~約80倍大きい、約25倍~約70倍大きい、約25倍~約60倍大きい、約25倍~約50倍大きい、約25倍~約40倍大きい、約25倍~約30倍大きい、約30倍~約100倍大きい、約30倍~約90倍大きい、約30倍~約80倍大きい、約30倍~約70倍大きい、約30倍~約60倍大きい、約30倍~約50倍大きい、約30倍~約40倍大きい、約40倍~約100倍大きい、約40倍~約90倍大きい、約40倍~約80倍大きい、約40倍~約70倍大きい、約40倍~約60倍大きい、約40倍~約50倍大きい、約50倍~約100倍大きい、約50倍~約90倍大きい、約50倍~約80倍大きい、約50倍~約70倍大きい、約50倍~約60倍大きい、約60倍~約100倍大きい、約60倍~約90倍大きい、約60倍~約80倍大きい、約60倍~約70倍大きい、約70倍~約100倍大きい、約70倍~約90倍大きい、約70倍~約80倍大きい、約80倍~約100倍大きい、約80倍~約90倍大きい、もしくは約90倍~約100倍大きい)。
第一の抗原結合ドメインおよび第二の抗原結合ドメインを含むABPCの一部の実施形態では、第一および第二の抗原結合ドメインは、アミノ酸配列において互いに同一であるか、または少なくとも80%同一(例えば、少なくとも82%、少なくとも84%、少なくとも86%、少なくとも88%、少なくとも90%、少なくとも91%、少なくとも92%、少なくとも93%、少なくとも94%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、または少なくとも99%同一)である。いくつかの実施形態では、第一の抗原結合ドメインおよび第二の抗原結合ドメインを含むABPCであり、該第一の抗原結合ドメインおよび第二の抗原結合ドメインは、互いに80%未満同一(例えば、75%未満同一、70%未満同一、65%未満同一、60%未満同一、55%未満同一、50%未満同一、45%未満同一、40%未満同一、35%未満同一、30%未満同一、25%未満同一、20%未満同一、15%未満同一、10%未満同一、または5%未満同一)の配列を有する。第一および第二の抗原結合ドメインを含むABPCの一部の実施形態では、第一および第二の抗原結合ドメインは、二つの異なるエピトープ(例えば、MET上の二つの異なるエピトープ、またはMETに特異的に結合する第一の抗原結合ドメイン、およびMET以外の抗原に結合する第二の抗原結合ドメイン)に結合する。
本明細書に記載されるいずれかのABPCの一部の実施形態では、第一の抗原結合ドメイン(および存在する場合には、任意に第二の抗原結合ドメイン)の、pH約7.0~約8.0(例えば、本明細書に記載するこの範囲の下位の範囲のいずれか)でのKDが、約1pM~約5μM(例えば、約1pM~約2μM、約1pM~約1μM、約1pM~約500nM、約1pM~約250nM、約1pM~約240nM、約1pM~約230nM、約1pM~約220nM、約1pM~約210nM、約1pM~約200nM、約1pM~約190nM、約1pM~約180nM、約1pM~約170nM、約1pM~約160nM、約1pM~約150nM、約1pM~約140nM、約1pM~約130nM、約1pM~約120nM、約1pM~約110nM、約1pM~約100nM、約1pM~約95nM、約1pM~約90nM、約1pM~約85nM、約1pM~約80nM、約1pM~約75nM、約1pM~約70nM、約1pM~約65nM、約1pM~約60nM、約1pM~約55nM、約1pM~約50nM、約1pM~約45nM、約1pM~約40nM、約1pM~約35nM、約1pM~約30nM、約1pM~約25nM、約1pM~約20nM、約1pM~約15nM、約1pM~約10nM、約1pM~約5nM、約1pM~約2nM、約1pM~約1nM、約1pM~約950pM、約1pM~約900pM、約1pM~約850pM、約1pM~約800pM、約1pM~約750pM、約1pM~約700pM、約1pM~約650pM、約1pM~約600pM、約1pM~約550pM、約1pM~約500pM、約1pM~約450pM、約1pM~約400pM、約1pM~約350pM、約1pM~約300pM、約1pM~約250pM、約1pM~約200pM、約1pM~約150pM、約1pM~約100pM、約1pM~約90pM、約1pM~約80pM、約1pM~約70pM、約1pM~約60pM、約1pM~約50pM、約1pM~約40pM、約1pM~約30pM、約1pM~約20pM、約1pM~約10pM、約1pM~約5pM、約1pM~約4pM、約1pM~約3pM、約1pM~約2pM、約2pM~約5μM、約2pM~約2μM、約2pM~約1μM、約2pM~約500nM、約2pM~約250nM、約2pM~約240nM、約2pM~約230nM、約2pM~約220nM、約2pM~約210nM、約2pM~約200nM、約2pM~約190nM、約2pM~約180nM、約2pM~約170nM、約2pM~約160nM、約2pM~約150nM、約2pM~約140nM、約2pM~約130nM、約2pM~約120nM、約2pM~約110nM、約2pM~約100nM、約2pM~約95nM、約2pM~約90nM、約2pM~約85nM、約2pM~約80nM、約2pM~約75nM、約2pM~約70nM、約2pM~約65nM、約2pM~約60nM、約2pM~約55nM、約2pM~約50nM、約2pM~約45nM、約2pM~約40nM、約2pM~約35nM、約2pM~約30nM、約2pM~約25nM、約2pM~約20nM、約2pM~約15nM、約2pM~約10nM、約2pM~約5nM、約2pM~約2nM、 約2pM~約1nM、約2pM~約950pM、約2pM~約900pM、約2pM~約850pM、約2pM~約800pM、約2pM~約750pM、約2pM~約700pM、約2pM~約650pM、約2pM~約600pM、約2pM~約550pM、約2pM~約500pM、約2pM~約450pM、約2pM~約400pM、約2pM~約350pM、約2pM~約300pM、約2pM~約250pM、約2pM~約200pM、約2pM~約150pM、約2pM~約100pM、約2pM~約90pM、約2pM~約80pM、約2pM~約70pM、約2pM~約60pM、約2pM~約50pM、約2pM~約40pM、約2pM~約30pM、約2pM~約20pM、約2pM~約10pM、約2pM~約5pM、約2pM~約4pM、約2pM~約3pM、約5pM~約5μM、約5pM~約2μM、約5pM~約1μM、約5pM~約500nM、約5pM~約250nM、約5pM~約240nM、約5pM~約230nM、約5pM~約220nM、約5pM~約210nM、約5pM~約200nM、約5pM~約190nM、約5pM~約180nM、約5pM~約170nM、約5pM~約160nM、約5pM~約150nM、約5pM~約140nM、約5pM~約130nM、約5pM~約120nM、約5pM~約110nM、約5pM~約100nM、約5pM~約95nM、約5pM~約90nM、約5pM~約85nM、約5pM~約80nM、約5pM~約75nM、約5pM~約70nM、約5pM~約65nM、約5pM~約60nM、約5pM~約55nM、約5pM~約50nM、約5pM~約45nM、約5pM~約40nM、約5pM~約35nM、約5pM~約30nM、約5pM~約25nM、約5pM~約20nM、約5pM~約15nM、約5pM~約10nM、約5pM~約5nM、約5pM~約2nM、約5pM~約1nM、約5pM~約950pM、約5pM~約900pM、約5pM~約850pM、約5pM~約800pM、約5pM~約750pM、約5pM~約700pM、約5pM~約650pM、約5pM~約600pM、約5pM~約550pM、約5pM~約500pM、約5pM~約450pM、約5pM~約400pM、約5pM~約350pM、約5pM~約300pM、約5pM~約250pM、約5pM~約200pM、約5pM~約150pM、約5pM~約100pM、約5pM~約90pM、約5pM~約80pM、約5pM~約70pM、約5pM~約60pM、約5pM~約50pM、約5pM~約40pM、約5pM~約30pM、約5pM~約20pM、約5pM~約10pM、約10pM~約5μM、約10pM~約2μM、約10pM~約1μM、約10pM~約500nM、約10pM~約250nM、約10pM~約240nM、約10pM~約230nM、約10pM~約220nM、約10pM~約210nM、約10pM~約200nM、約10pM~約190nM、約10pM~約180nM、約10pM~約170nM、約10pM~約160nM、約10pM~約150nM、約10pM~約140nM、約10pM~約130nM、約10pM~約120nM、約10pM~約110nM、約10pM~約100nM、約10pM~約95nM、約10pM~約90nM、約10pM~約85nM、約10pM~約80nM、約10pM~約75nM、約10pM~約70nM、約10pM~約65nM、約10pM~約60nM、約10pM~約55nM、約10pM~約50nM、約10pM~約45nM、約10pM~約40nM、約10pM~約35nM、約10pM~約30nM、約10pM~約25nM、約10pM~約20nM、約10pM~約15nM、約10pM~約10nM、約10pM~約5nM、約10pM~約2nM、約10pM~約1nM、約10pM~約950pM、約10pM~約900pM、約10pM~約850pM、約10pM~約800pM、約10pM~約750pM、約10pM~約700pM、約10pM~約650pM、約10pM~約600pM、約10pM~約550pM、約10pM~約500pM、約10pM~約450pM、約10pM~約400pM、約10pM~約350pM、約10pM~約300pM、約10pM~約250pM、約10pM~約200pM、約10pM~約150pM、約10pM~約100pM、約10pM~約90pM、約10pM~約80pM、約10pM~約70pM、約10pM~約60pM、約10pM~約50pM、約10pM~約40pM、約10pM~約30pM、約10pM~約20pM、約15pM~約5μM、約15pM~約2μM、約15pM~約1μM、約15pM~約500nM、約15pM~約250nM、約15pM~約240nM、約15pM~約230nM、約15pM~約220nM、約15pM~約210nM、約15pM~約200nM、約15pM~約190nM、約15pM~約180nM、約15pM~約170nM、約15pM~約160nM、約15pM~約150nM、約15pM~約140nM、約15pM~約130nM、約15pM~約120nM、約15pM~約110nM、約15pM~約100nM、約15pM~約95nM、約15pM~約90nM、約15pM~約85nM、約15pM~約80nM、約15pM~約75nM、約15pM~約70nM、約15pM~約65nM、約15pM~約60nM、約15pM~約55nM、約15pM~約50nM、約15pM~約45nM、約15pM~約40nM、約15pM~約35nM、約15pM~約30nM、約15pM~約25nM、約15pM~約20nM、約15pM~約15nM、約15pM~約10nM、約15pM~約5nM、約15pM~約2nM、約15pM~約1nM、約15pM~約950pM、約15pM~約900pM、約15pM~約850pM、約15pM~約800pM、約15pM~約750pM、約15pM~約700pM、約15pM~約650pM、約15pM~約600pM、
約15pM~約550pM、約15pM~約500pM、約15pM~約450pM、約15pM~約400pM、約15pM~約350pM、約15pM~約300pM、約15pM~約250pM、約15pM~約200pM、約15pM~約150pM、約15pM~約100pM、約15pM~約90pM、約15pM~約80pM、約15pM~約70pM、約15pM~約60pM、約15pM~約50pM、約15pM~約40pM、約15pM~約30pM、約15pM~約20pM、約20pM~約5μM、約20pM~約2μM、約20pM~約1μM、約20pM~約500nM、約20pM~約250nM、約20pM~約240nM、約20pM~約230nM、約20pM~約220nM、約20pM~約210nM、約20pM~約200nM、約20pM~約190nM、約20pM~約180nM、約20pM~約170nM、約20pM~約160nM、約20pM~約150nM、約20pM~約140nM、約20pM~約130nM、約20pM~約120nM、約20pM~約110nM、約20pM~約100nM、約20pM~約95nM、約20pM~約90nM、約20pM~約85nM、約20pM~約80nM、約20pM~約75nM、約20pM~約70nM、約20pM~約65nM、約20pM~約60nM、約20pM~約55nM、約20pM~約50nM、約20pM~約45nM、約20pM~約40nM、約20pM~約35nM、約20pM~約30nM、約20pM~約25nM、約20pM~約20nM、約20pM~約15nM、約20pM~約10nM、約20pM~約5nM、約20pM~約2nM、約20pM~約1nM、約20pM~約950pM、約20pM~約900pM、約20pM~約850pM、約20pM~約800pM、約20pM~約750pM、約20pM~約700pM、約20pM~約650pM、約20pM~約600pM、約20pM~約550pM、約20pM~約500pM、約20pM~約450pM、約20pM~約400pM、約20pM~約350pM、約20pM~約300pM、約20pM~約250pM、約20pM~約20pM、約200pM~約150pM、約20pM~約100pM、約20pM~約90pM、約20pM~約80pM、約20pM~約70pM、約20pM~約60pM、約20pM~約50pM、約20pM~約40pM、約20pM~約30pM、約30pM~約5μM、約30pM~約2μM、約30pM~約1μM、約30pM~約500nM、約30pM~約250nM、約30pM~約240nM、約30pM~約230nM、約30pM~約220nM、約30pM~約210nM、約30pM~約200nM、約30pM~約190nM、約30pM~約180nM、約30pM~約170nM、約30pM~約160nM、約30pM~約150nM、約30pM~約140nM、約30pM~約130nM、約30pM~約120nM、約30pM~約110nM、約30pM~約100nM、約30pM~約95nM、約30pM~約90nM、約30pM~約85nM、約30pM~約80nM、約30pM~約75nM、約30pM~約70nM、約30pM~約65nM、約30pM~約60nM、約30pM~約55nM、約30pM~約50nM、約30pM~約45nM、約30pM~約40nM、約30pM~約35nM、約30pM~約30nM、約30pM~約25nM、約30pM~約20nM、約30pM~約15nM、約30pM~約10nM、約30pM~約5nM、約30pM~約2nM、約30pM~約1nM、約30pM~約950pM、約30pM~約900pM、約30pM~約850pM、約30pM~約800pM、約30pM~約750pM、約30pM~約700pM、約30pM~約650pM、約30pM~約600pM、約30pM~約550pM、約30pM~約500pM、約30pM~約450pM、約30pM~約400pM、約30pM~約350pM、約30pM~約300pM、約30pM~約250pM、約30pM~約200pM、約30pM~約150pM、約30pM~約100pM、約30pM~約90pM、約30pM~約80pM、約30pM~約70pM、約30pM~約60pM、約30pM~約50pM、約30pM~約40pM、約40pM~約5μM、約40pM~約2μM、約40pM~約1μM、約40pM~約500nM、約40pM~約250nM、約40pM~約240nM、約40pM~約230nM、約40pM~約220nM、約40pM~約210nM、約40pM~約200nM、約40pM~約190nM、約40pM~約180nM、約40pM~約170nM、約40pM~約160nM、約40pM~約150nM、約40pM~約140nM、約40pM~約130nM、約40pM~約120nM、約40pM~約110nM、約40pM~約100nM、約40pM~約95nM、約40pM~約90nM、約40pM~約85nM、約40pM~約80nM、約40pM~約75nM、約40pM~約70nM、約40pM~約65nM、約40pM~約60nM、約40pM~約55nM、約40pM~約50nM、約40pM~約45nM、約40pM~約40nM、約40pM~約35nM、約40pM~約30nM、約40pM~約25nM、約40pM~約30nM、約40pM~約15nM、約40pM~約10nM、約40pM~約5nM、約40pM~約2nM、約40pM~約1nM、約40pM~約950pM、約40pM~約900pM、約40pM~約850pM、約40pM~約800pM、約40pM~約750pM、約40pM~約700pM、約40pM~約650pM、約40pM~約600pM、約40pM~約550pM、約40pM~約500pM、約40pM~約450pM、約40pM~約400pM、約40pM~約350pM、約40pM~約300pM、約40pM~約250pM、約40pM~約200pM、約40pM~約150pM、約40pM~約100pM、約40pM~約90pM、約40pM~約80pM、約40pM~約70pM、約40pM~約60pM、約40pM~約50pM、約50pM~約5μM、約50pM~約2μM、約50pM~約1μM、約50pM~約500nM、約50pM~約250nM、約50pM~約240nM、約50pM~約230nM、約50pM~約220nM、約50pM~約210nM、約50pM~約200nM、約50pM~約190nM、約50pM~約180nM、約50pM~約170nM、約50pM~約160nM、約50pM~約150nM、約50pM~約140nM、約50pM~約130nM、約50pM~約120nM、約50pM~約110nM、約50pM~約100nM、約50pM~約95nM、約50pM~約90nM、約50pM~約85nM、約50pM~約80nM、約50pM~約75nM、約50pM~約70nM、約50pM~約65nM、約50pM~約60nM、約50pM~約55nM、約50pM~約50nM、約50pM~約45nM、約50pM~約40nM、約50pM~約35nM、約50pM~約30nM、約50pM~約25nM、約50pM~約30nM、約50pM~約15nM、約50pM~約10nM、約50pM~約5nM、約50pM~約2nM、約50pM~約1nM、約50pM~約950pM、約50pM~約900pM、約50pM~約850pM、約50pM~約800pM、約50pM~約750pM、約50pM~約700pM、約50pM~約650pM、約50pM~約600pM、約50pM~約550pM、約50pM~約500pM、約50pM~約450pM、約50pM~約400pM、約50pM~約350pM、約50pM~約300pM、約50pM~約250pM、約50pM~約200pM、約50pM~約150pM、約50pM~約100pM、約50pM~約90pM、約50pM~約80pM、約50pM~約70pM、約50pM~約60pM、約60pM~約5μM、約60pM~約2μM、約60pM~約1μM、約60pM~約500nM、約60pM~約250nM、約60pM~約240nM、約60pM~約230nM、約60pM~約220nM、約60pM~約210nM、約60pM~約200nM、約60pM~約190nM、約60pM~約180nM、約60pM~約170nM、約60pM~約160nM、約60pM~約150nM、約60pM~約140nM、約60pM~約130nM、約60pM~約120nM、約60pM~約110nM、約60pM~約100nM、約60pM~約95nM、約60pM~約90nM、約60pM~約85nM、約60pM~約80nM、約60pM~約75nM、約60pM~約70nM、約60pM~約65nM、約60pM~約60nM、約60pM~約55nM、約60pM~約50nM、約60pM~約45nM、約60pM~約40nM、約60pM~約35nM、約60pM~約30nM、約60pM~約25nM、約60pM~約20nM、約60pM~約15nM、約60pM~約10nM、約60pM~約5nM、約60pM~約2nM、約60pM~約1nM、約60pM~約950pM、約60pM~約900pM、約60pM~約850pM、約60pM~約800pM、約60pM~約750pM、約60pM~約700pM、約60pM~約650pM、約60pM~約600pM、約60pM~約550pM、約60pM~約500pM、約60pM~約450pM、約60pM~約400pM、約60pM~約350pM、約60pM~約300pM、約60pM~約250pM、約60pM~約200pM、約60pM~約150pM、約60pM~約100pM、約60pM~約90pM、約60pM~約80pM、約60pM~約70pM、約70pM~約5μM、約70pM~約2μM、約70pM~約1μM、約70pM~約500nM、約70pM~約250nM、約70pM~約240nM、約70pM~約230nM、約70pM~約220nM、約70pM~約210nM、約70pM~約200nM、約70pM~約190nM、約70pM~約180nM、約70pM~約170nM、約70pM~約160nM、約70pM~約150nM、約70pM~約140nM、約70pM~約130nM、約70pM~約120nM、約70pM~約110nM、約70pM~約100nM、約70pM~約95nM、約70pM~約90nM、約70pM~約85nM、約70pM~約80nM、約70pM~約75nM、約70pM~約70nM、約70pM~約65nM、約70pM~約60nM、約70pM~約55nM、約70pM~約50nM、約70pM~約45nM、約70pM~約40nM、約70pM~約35nM、約70pM~約30nM、約70pM~約25nM、約70pM~約20nM、約70pM~約15nM、約70pM~約10nM、約70pM~約5nM、約70pM~約2nM、約70pM~約1nM、約70pM~約950pM、約70pM~約900pM、約70pM~約850pM、約70pM~約800pM、約70pM~約750pM、約70pM~約700pM、約70pM~約650pM、約70pM~約600pM、約70pM~約550pM、約70pM~約500pM、約70pM~約450pM、約70pM~約400pM、約70pM~約350pM、約70pM~約300pM、約70pM~約250pM、約70pM~約200pM、約70pM~約150pM、約70pM~約100pM、約70pM~約90pM、約70pM~約80pM、約80pM~約5μM、約80pM~約2μM、約80pM~約1μM、約80pM~約500nM、約80pM~約250nM、約80pM~約240nM、約80pM~約230nM、約80pM~約220nM、約80pM~約210nM、約80pM~約200nM、約80pM~約190nM、約80pM~約180nM
、約80pM~約170nM、約80pM~約160nM、約80pM~約150nM、約80pM~約140nM、約80pM~約130nM、約80pM~約120nM、約80pM~約110nM、約80pM~約100nM、約80pM~約95nM、約80pM~約90nM、約80pM~約85nM、約80pM~約80nM、約80pM~約75nM、約80pM~約70nM、約80pM~約65nM、約80pM~約60nM、約80pM~約55nM、約80pM~約50nM、約80pM~約45nM、約80pM~約40nM、約80pM~約35nM、約80pM~約30nM、約80pM~約25nM、約80pM~約20nM、約80pM~約15nM、約80pM~約10nM、約80pM~約5nM、約80pM~約2nM、約80pM~約1nM、約80pM~約950pM、約80pM~約900pM、約80pM~約850pM、約80pM~約800pM、約80pM~約750pM、約80pM~約700pM、約80pM~約650pM、約80pM~約600pM、約80pM~約550pM、約80pM~約500pM、約80pM~約450pM、約80pM~約400pM、約80pM~約350pM、約80pM~約300pM、約80pM~約250pM、約80pM~約200pM、約80pM~約150pM、約80pM~約100pM、約80pM~約90pM、約90pM~約5μM、約90pM~約2μM、約90pM~約1μM、約90pM~約500nM、約90pM~約250nM、約90pM~約240nM、約90pM~約230nM、約90pM~約220nM、約90pM~約210nM、約90pM~約200nM、約90pM~約190nM、約90pM~約180nM、約90pM~約170nM、約90pM~約160nM、約90pM~約150nM、約90pM~約140nM、約90pM~約130nM、約90pM~約120nM、約90pM~約110nM、約90pM~約100nM、約90pM~約95nM、約90pM~約90nM、約90pM~約85nM、約90pM~約80nM、約90pM~約75nM、約90pM~約70nM、約90pM~約65nM、約90pM~約60nM、約90pM~約55nM、約90pM~約50nM、約90pM~約45nM、約90pM~約40nM、約90pM~約35nM、約90pM~約30nM、約90pM~約25nM、約90pM~約30nM、約90pM~約15nM、約90pM~約10nM、約90pM~約5nM、約90pM~約2nM、約90pM~約1nM、約90pM~約950pM、約90pM~約900pM、約90pM~約850pM、約90pM~約800pM、約90pM~約750pM、約90pM~約700pM、約90pM~約650pM、約90pM~約600pM、約90pM~約550pM、約90pM~約500pM、約90pM~約450pM、約90pM~約400pM、約90pM~約350pM、約90pM~約300pM、約90pM~約250pM、約90pM~約200pM、約90pM~約150pM、約90pM~約100pM、約100pM~約30nM、約100pM~約25nM、約100pM~約5μM、約100pM~約2μM、約100pM~約1μM、約100pM~約500nM、約100pM~約250nM、約100pM~約240nM、約100pM~約230nM、約100pM~約220nM、約100pM~約210nM、約100pM~約200nM、約100pM~約190nM、約100pM~約180nM、約100pM~約170nM、約100pM~約160nM、約100pM~約150nM、約100pM~約140nM、約100pM~約130nM、約100pM~約120nM、約100pM~約110nM、約100pM~約100nM、約100pM~約95nM、約100pM~約90nM、約100pM~約85nM、約100pM~約80nM、約100pM~約75nM、約100pM~約70nM、約100pM~約65nM、約100pM~約60nM、約100pM~約55nM、約100pM~約50nM、約100pM~約45nM、約100pM~約40nM、約100pM~約35nM、約100pM~約30nM、約100pM~約15nM、約100pM~約10nM、約100pM~約5nM、約100pM~約2nM、約100pM~約1nM、約100pM~約950pM、約100pM~約900pM、約100pM~約850pM、約100pM~約800pM、約100pM~約750pM、約100pM~約700pM、約100pM~約650pM、約100pM~約600pM、約100pM~約550pM、約100pM~約500pM、約100pM~約450pM、約100pM~約400pM、約100pM~約350pM、約100pM~約300pM、約100pM~約250pM、約100pM~約200pM、約100pM~約150pM、約150pM~約5μM、約150pM~約2μM、約150pM~約1μM、約150pM~約500nM、約150pM~約250nM、約150pM~約240nM、約150pM~約230nM、約150pM~約220nM、約150pM~約210nM、約150pM~約200nM、約150pM~約190nM、約150pM~約180nM、約150pM~約170nM、約150pM~約160nM、約150pM~約150nM、約150pM~約140nM、約150pM~約130nM、約150pM~約120nM、約150pM~約110nM、約150pM~約100nM、約150pM~約95nM、約150pM~約90nM、約150pM~約85nM、約150pM~約80nM、約150pM~約75nM、約150pM~約70nM、約150pM~約65nM、約150pM~約60nM、約150pM~約55nM、約150pM~約50nM、約150pM~約45nM、約150pM~約40nM、約150pM~約35nM、約150pM~約30nM、約150pM~約25nM、約150pM~約30nM、約150pM~約15nM、約150pM~約10nM、約150pM~約5nM、約150pM~約2nM、約150pM~約1nM、約150pM~約950pM、約150pM~約900pM、約150pM~約850pM、約150pM~約800pM、約150pM~約750pM、約150pM~約700pM、約150pM~約650pM、約150pM~約600pM、約150pM~約550pM、約150pM~約500pM、約150pM~約450pM、約150pM~約400pM、約150pM~約350pM、約150pM~約300pM、約150pM~約250pM、約150pM~約200pM、約200pM~約5μM、約200pM~約2μM、約200pM~約1μM、約200pM~約500nM、約200pM~約250nM、約200pM~約240nM、約200pM~約230nM、約200pM~約220nM、約200pM~約210nM、約200pM~約200nM、約200pM~約190nM、約200pM~約180nM、約200pM~約170nM、約200pM~約160nM、約200pM~約150nM、約200pM~約140nM、約200pM~約130nM、約200pM~約120nM、約200pM~約110nM、約200pM~約100nM、約200pM~約95nM、約200pM~約90nM、約200pM~約85nM、約200pM~約80nM、約200pM~約75nM、約200pM~約70nM、約200pM~約65nM、約200pM~約60nM、約200pM~約55nM、約200pM~約50nM、約200pM~約45nM、約200pM~約40nM、約200pM~約35nM、約200pM~約30nM、約200pM~約25nM、約200pM~約30nM、約200pM~約15nM、約200pM~約10nM、約200pM~約5nM、約200pM~約2nM、約200pM~約1nM、約200pM~約950pM、約200pM~約900pM、約200pM~約850pM、約200pM~約800pM、約200pM~約750pM、約200pM~約700pM、約200pM~約650pM、約200pM~約600pM、約200pM~約550pM、約200pM~約500pM、約200pM~約450pM、約200pM~約400pM、約200pM~約350pM、約200pM~約300pM、約200pM~約250pM、約300pM~約30nM、約300pM~約25nM、約300pM~約5μM、約300pM~約2μM、約300pM~約1μM、約300pM~約500nM、約300pM~約250nM、約300pM~約240nM、約300pM~約230nM、約300pM~約220nM、約300pM~約210nM、約300pM~約200nM、約300pM~約190nM、約300pM~約180nM、約300pM~約170nM、約300pM~約160nM、約300pM~約150nM、約300pM~約140nM、約300pM~約130nM、約300pM~約120nM、約300pM~約110nM、約300pM~約100nM、約300pM~約95nM、約300pM~約90nM、約300pM~約85nM、約300pM~約80nM、約300pM~約75nM、約300pM~約70nM、約300pM~約65nM、約300pM~約60nM、約300pM~約55nM、約300pM~約50nM、約300pM~約45nM、約300pM~約40nM、約300pM~約35nM、約300pM~約30nM、約300pM~約15nM、約300pM~約10nM、約300pM~約5nM、約300pM~約2nM、約300pM~約1nM、約300pM~約950pM、約300pM~約900pM、約300pM~約850pM、約300pM~約800pM、約300pM~約750pM、約300pM~約700pM、約300pM~約650pM、約300pM~約600pM、約300pM~約550pM、約300pM~約500pM、約300pM~約450pM、約300pM~約400pM、約300pM~約350pM、約400pM~約5μM、約400pM~約2μM、約400pM~約1μM、約400pM~約500nM、約400pM~約250nM、約400pM~約240nM、約400pM~約230nM、約400pM~約220nM、約400pM~約210nM、約400pM~約200nM、約400pM~約190nM、約400pM~約180nM、約400pM~約170nM、約400pM~約160nM、約400pM~約150nM、約400pM~約140nM、約400pM~約130nM、約400pM~約120nM、約400pM~約110nM、約400pM~約100nM、約400pM~約95nM、約400pM~約90nM、約400pM~約85nM、約400pM~約80nM、約400pM~約75nM、約400pM~約70nM、約400pM~約65nM、約400pM~約60nM、約400pM~約55nM、約400pM~約50nM、約400pM~約45nM、約400pM~約40nM、約400pM~約35nM、約400pM~約30nM、約400pM~約25nM、約400pM~約20nM、約400pM~約15nM、約400pM~約10nM、約400pM~約5nM、約400pM~約2nM、約400pM~約1nM、約400pM~約950pM、約400pM~約900pM、約400pM~約850pM、約400pM~約800pM、約400pM~約750pM、約400pM~約700pM、約400pM~約650pM、約400pM~約600pM、約400pM~約550pM、約400pM~約500pM、約500pM~約5μM、約500pM~約2μM、約500pM~約1μM、約500pM~約500nM、約500pM~約250nM、約500pM
~約240nM、約500pM~約230nM、約500pM~約220nM、約500pM~約210nM、約500pM~約200nM、約500pM~約190nM、約500pM~約180nM、約500pM~約170nM、約500pM~約160nM、約500pM~約150nM、約500pM~約140nM、約500pM~約130nM、約500pM~約120nM、約500pM~約110nM、約500pM~約100nM、約500pM~約95nM、約500pM~約90nM、約500pM~約85nM、約500pM~約80nM、約500pM~約75nM、約500pM~約70nM、約500pM~約65nM、約500pM~約60nM、約500pM~約55nM、約500pM~約50nM、約500pM~約45nM、約500pM~約40nM、約500pM~約35nM、約500pM~約30nM、約500pM~約25nM、約500pM~約20nM、約500pM~約15nM、約500pM~約10nM、約500pM~約5nM、約500pM~約2nM、約500pM~約1nM、約500pM~約950pM、約500pM~約900pM、約500pM~約850pM、約500pM~約800pM、約500pM~約750pM、約500pM~約700pM、約500pM~約650pM、約500pM~約600pM、約500pM~約550pM、約600pM~約5μM、約600pM~約2μM、約600pM~約1μM、約600pM~約500nM、約600pM~約250nM、約600pM~約240nM、約600pM~約230nM、約600pM~約220nM、約600pM~約210nM、約600pM~約200nM、約600pM~約190nM、約600pM~約180nM、約600pM~約170nM、約600pM~約160nM、約600pM~約150nM、約600pM~約140nM、約600pM~約130nM、約600pM~約120nM、約600pM~約110nM、約600pM~約100nM、約600pM~約95nM、約600pM~約90nM、約600pM~約85nM、約600pM~約80nM、約600pM~約75nM、約600pM~約70nM、約600pM~約65nM、約600pM~約60nM、約600pM~約55nM、約600pM~約50nM、約600pM~約45nM、約600pM~約40nM、約600pM~約35nM、約600pM~約30nM、約600pM~約25nM、約600pM~約20nM、約600pM~約15nM、約600pM~約10nM、約600pM~約5nM、約600pM~約2nM、約600pM~約1nM、約600pM~約950pM、約600pM~約900pM、約600pM~約850pM、約600pM~約800pM、約600pM~約750pM、約600pM~約700pM、約600pM~約650pM、約700pM~約5μM、約700pM~約2μM、約700pM~約1μM、約700pM~約500nM、約700pM~約250nM、約700pM~約240nM、約700pM~約230nM、約700pM~約220nM、約700pM~約210nM、約700pM~約200nM、約700pM~約190nM、約700pM~約180nM、約700pM~約170nM、約700pM~約160nM、約700pM~約150nM、約700pM~約140nM、約700pM~約130nM、約700pM~約120nM、約700pM~約110nM、約700pM~約100nM、約700pM~約95nM、約700pM~約90nM、約700pM~約85nM、約700pM~約80nM、約700pM~約75nM、約700pM~約70nM、約700pM~約65nM、約700pM~約60nM、約700pM~約55nM、約700pM~約50nM、約700pM~約45nM、約700pM~約40nM、約700pM~約35nM、約700pM~約30nM、約700pM~約25nM、約700pM~約20nM、約700pM~約15nM、約700pM~約10nM、約700pM~約5nM、約700pM~約2nM、約700pM~約1nM、約700pM~約950pM、約700pM~約900pM、約700pM~約850pM、約700pM~約800pM、約700pM~約750pM、約800pM~約5μM、約800pM~約2μM、約800pM~約1μM、約800pM~約500nM、約800pM~約250nM、約800pM~約240nM、約800pM~約230nM、約800pM~約220nM、約800pM~約210nM、約800pM~約200nM、約800pM~約190nM、約800pM~約180nM、約800pM~約170nM、約800pM~約160nM、約800pM~約150nM、約800pM~約140nM、約800pM~約130nM、約800pM~約120nM、約800pM~約110nM、約800pM~約100nM、約800pM~約95nM、約800pM~約90nM、約800pM~約85nM、約800pM~約80nM、約800pM~約75nM、約800pM~約70nM、約800pM~約65nM、約800pM~約60nM、約800pM~約55nM、約800pM~約50nM、約800pM~約45nM、約800pM~約40nM、約800pM~約35nM、約800pM~約30nM、約800pM~約25nM、約800pM~約20nM、約800pM~約15nM、約800pM~約10nM、約800pM~約5nM、約800pM~約2nM、約800pM~約1nM、約800pM~約950pM、約800pM~約900pM、約800pM~約850pM、約900pM~約5μM、約900pM~約2μM、約900pM~約1μM、約900pM~約500nM、約900pM~約250nM、約900pM~約240nM、約900pM~約230nM、約900pM~約220nM、約900pM~約210nM、約900pM~約200nM、約900pM~約190nM、約900pM~約180nM、約900pM~約170nM、約900pM~約160nM、約900pM~約150nM、約900pM~約140nM、約900pM~約130nM、約900pM~約120nM、約900pM~約110nM、約900pM~約100nM、約900pM~約95nM、約900pM~約90nM、約900pM~約85nM、約900pM~約80nM、約900pM~約75nM、約900pM~約70nM、約900pM~約65nM、約900pM~約60nM、約900pM~約55nM、約900pM~約50nM、約900pM~約45nM、約900pM~約40nM、約900pM~約35nM、約900pM~約30nM、約900pM~約25nM、約900pM~約20nM、約900pM~約15nM、約900pM~約10nM、約900pM~約5nM、約900pM~約2nM、約900pM~約1nM、約900pM~約950pM、約1nM~約5μM、約1nM~約2μM、約1nM~約1μM、約1nM~約500nM、約1nM~約250nM、約1nM~約240nM、約1nM~約230nM、約1nM~約220nM、約1nM~約210nM、約1nM~約200nM、約1nM~約190nM、約1nM~約180nM、約1nM~約170nM、約1nM~約160nM、約1nM~約150nM、約1nM~約140nM、約1nM~約130nM、約1nM~約120nM、約1nM~約110nM、約1nM~約100nM、約1nM~約95nM、約1nM~約90nM、約1nM~約85nM、約1nM~約80nM、約1nM~約75nM、約1nM~約70nM、約1nM~約65nM、約1nM~約60nM、約1nM~約55nM、約1nM~約50nM、約1nM~約45nM、約1nM~約40nM、約1nM~約35nM、約1nM~約30nM、約1nM~約25nM、約1nM~約20nM、約1nM~約15nM、約1nM~約10nM、約1nM~約5nM、約2nM~約5μM、約2nM~約2μM、約2nM~約1μM、約2nM~約500nM、約2nM~約250nM、約2nM~約240nM、約2nM~約230nM、約2nM~約220nM、約2nM~約210nM、約2nM~約200nM、約2nM~約190nM、約2nM~約180nM、約2nM~約170nM、約2nM~約160nM、約2nM~約150nM、約2nM~約140nM、約2nM~約130nM、約2nM~約120nM、約2nM~約110nM、約2nM~約100nM、約2nM~約95nM、約2nM~約90nM、約2nM~約85nM、約2nM~約80nM、約2nM~約75nM、約2nM~約70nM、約2nM~約65nM、約2nM~約60nM、約2nM~約55nM、約2nM~約50nM、約2nM~約45nM、約2nM~約40nM、約2nM~約35nM、約2nM~約30nM、約2nM~約25nM、約2nM~約20nM、約2nM~約15nM、約2nM~約10nM、約2nM~約5nM、約4nM~約5μM、約4nM~約2μM、約4nM~約1μM、約4nM~約500nM、約4nM~約250nM、約4nM~約240nM、約4nM~約230nM、約4nM~約220nM、約4nM~約210nM、約4nM~約200nM、約4nM~約190nM、約4nM~約180nM、約4nM~約170nM、約4nM~約160nM、約4nM~約150nM、約4nM~約140nM、約4nM~約130nM、約4nM~約120nM、約4nM~約110nM、約4nM~約100nM、約4nM~約95nM、約4nM~約90nM、約4nM~約85nM、約4nM~約80nM、約4nM~約75nM、約4nM~約70nM、約4nM~約65nM、約4nM~約60nM、約4nM~約55nM、約4nM~約50nM、約4nM~約45nM、約4nM~約40nM、約4nM~約35nM、約4nM~約30nM、約4nM~約25nM、約4nM~約20nM、約4nM~約15nM、約4nM~約10nM、約4nM~約5nM、約5nM~約5μM、約5nM~約2μM、約5nM~約1μM、約5nM~約500nM、約5nM~約250nM、約5nM~約240nM、約5nM~約230nM、約5nM~約220nM、約5nM~約210nM、約5nM~約200nM、約5nM~約190nM、約5nM~約180nM、約5nM~約170nM、約5nM~約160nM、約5nM~約150nM、約5nM~約140nM、約5nM~約130nM、約5nM~約120nM、約5nM~約110nM、約5nM~約100nM、約5nM~約95nM、約5nM~約90nM、約5nM~約85nM、約5nM~約80nM、約5nM~約75nM、約5nM~約70nM、約5nM~約65nM、約5nM~約60nM、約5nM~約55nM、約5nM~約50nM、約5nM~約45nM、約5nM~約40nM、約5nM~約35nM、約5nM~約30nM、約5nM~約25nM、約5nM~約20nM、約5nM~約15nM、約5nM~約10nM、約10nM~約5μM、約10nM~約2μM、約10nM~約1μM、約10nM~約500nM、約10nM~約250nM、約10nM~約240nM、約10nM~約230nM、約10nM~約220nM、約10nM~約210nM、約10nM~約200nM、約10nM~約190nM、約10nM~約180nM、約10nM~約170nM、約10nM~約160nM、約10nM~約150nM、約10nM~約140nM、約10nM~約130nM、約10nM~約120nM、約10nM~約110nM、約10nM~約100nM、約10nM~約95nM、約10nM~約90nM、約10nM~約85nM、約10nM~約80nM、約10nM~約75nM、約10nM~約70nM、約10nM~約65nM、約10nM~約60nM、約10nM~約55nM、約
10nM~約50nM、約10nM~約45nM、約10nM~約40nM、約10nM~約35nM、約10nM~約30nM、約10nM~約25nM、約10nM~約20nM、約10nM~約15nM、約15nM~約5μM、約15nM~約2μM、約15nM~約1μM、約15nM~約500nM、約15nM~約250nM、約15nM~約240nM、約15nM~約230nM、約15nM~約220nM、約15nM~約210nM、約15nM~約200nM、約15nM~約190nM、約15nM~約180nM、約15nM~約170nM、約15nM~約160nM、約15nM~約150nM、約15nM~約140nM、約15nM~約130nM、約15nM~約120nM、約15nM~約110nM、約15nM~約100nM、約15nM~約95nM、約15nM~約90nM、約15nM~約85nM、約15nM~約80nM、約15nM~約75nM、約15nM~約70nM、約15nM~約65nM、約15nM~約60nM、約15nM~約55nM、約15nM~約50nM、約15nM~約45nM、約15nM~約40nM、約15nM~約35nM、約15nM~約30nM、約15nM~約25nM、約15nM~約20nM、約20nM~約5μM、約20nM~約2μM、約20nM~約1μM、約20nM~約500nM、約20nM~約250nM、約20nM~約240nM、約20nM~約230nM、約20nM~約220nM、約20nM~約210nM、約20nM~約200nM、約20nM~約190nM、約20nM~約180nM、約20nM~約170nM、約20nM~約160nM、約20nM~約150nM、約20nM~約140nM、約20nM~約130nM、約20nM~約120nM、約20nM~約110nM、約20nM~約100nM、約20nM~約95nM、約20nM~約90nM、約20nM~約85nM、約20nM~約80nM、約20nM~約75nM、約20nM~約70nM、約20nM~約65nM、約20nM~約60nM、約20nM~約55nM、約20nM~約50nM、約20nM~約45nM、約20nM~約40nM、約20nM~約35nM、約20nM~約30nM、約20nM~約25nM、約25nM~約5μM、約25nM~約2μM、約25nM~約1μM、約25nM~約500nM、約25nM~約250nM、約25nM~約240nM、約25nM~約230nM、約25nM~約220nM、約25nM~約210nM、約25nM~約200nM、約25nM~約190nM、約25nM~約180nM、約25nM~約170nM、約25nM~約160nM、約25nM~約150nM、約25nM~約140nM、約25nM~約130nM、約25nM~約120nM、約25nM~約110nM、約25nM~約100nM、約25nM~約95nM、約25nM~約90nM、約25nM~約85nM、約25nM~約80nM、約25nM~約75nM、約25nM~約70nM、約25nM~約65nM、約25nM~約60nM、約25nM~約55nM、約25nM~約50nM、約25nM~約45nM、約25nM~約40nM、約25nM~約35nM、約25nM~約30nM、約30nM~約5μM、約30nM~約2μM、約30nM~約1μM、約30nM~約500nM、約30nM~約250nM、約30nM~約240nM、約30nM~約230nM、約30nM~約220nM、約30nM~約210nM、約30nM~約200nM、約30nM~約190nM、約30nM~約180nM、約30nM~約170nM、約30nM~約160nM、約30nM~約150nM、約30nM~約140nM、約30nM~約130nM、約30nM~約120nM、約30nM~約110nM、約30nM~約100nM、約30nM~約95nM、約30nM~約90nM、約30nM~約85nM、約30nM~約80nM、約30nM~約75nM、約30nM~約70nM、約30nM~約65nM、約30nM~約60nM、約30nM~約55nM、約30nM~約50nM、約30nM~約45nM、約30nM~約40nM、約30nM~約35nM、約40nM~約5μM、約40nM~約2μM、約40nM~約1μM、約40nM~約500nM、約40nM~約250nM、約40nM~約240nM、約40nM~約230nM、約40nM~約220nM、約40nM~約210nM、約40nM~約200nM、約40nM~約190nM、約40nM~約180nM、約40nM~約170nM、約40nM~約160nM、約40nM~約150nM、約40nM~約140nM、約40nM~約130nM、約40nM~約120nM、約40nM~約110nM、約40nM~約100nM、約40nM~約95nM、約40nM~約90nM、約40nM~約85nM、約40nM~約80nM、約40nM~約75nM、約40nM~約70nM、約40nM~約65nM、約40nM~約60nM、約40nM~約55nM、約40nM~約50nM、約40nM~約45nM、約50nM~約5μM、約50nM~約2μM、約50nM~約1μM、約50nM~約500nM、約50nM~約250nM、約50nM~約240nM、約50nM~約230nM、約50nM~約220nM、約50nM~約210nM、約50nM~約200nM、約50nM~約190nM、約50nM~約180nM、約50nM~約170nM、約50nM~約160nM、約50nM~約150nM、約50nM~約140nM、約50nM~約130nM、約50nM~約120nM、約50nM~約110nM、約50nM~約100nM、約50nM~約95nM、約50nM~約90nM、約50nM~約85nM、約50nM~約80nM、約50nM~約75nM、約50nM~約70nM、約50nM~約65nM、約50nM~約60nM、約50nM~約55nM、約60nM~約5μM、約60nM~約2μM、約60nM~約1μM、約60nM~約500nM、約60nM~約250nM、約60nM~約240nM、約60nM~約230nM、約60nM~約220nM、約60nM~約210nM、約60nM~約200nM、約60nM~約190nM、約60nM~約180nM、約60nM~約170nM、約60nM~約160nM、約60nM~約150nM、約60nM~約140nM、約60nM~約130nM、約60nM~約120nM、約60nM~約110nM、約60nM~約100nM、約60nM~約95nM、約60nM~約90nM、約60nM~約85nM、約60nM~約80nM、約60nM~約75nM、約60nM~約70nM、約60nM~約65nM、約70nM~約5μM、約70nM~約2μM、約70nM~約1μM、約70nM~約500nM、約70nM~約250nM、約70nM~約240nM、約70nM~約230nM、約70nM~約220nM、約70nM~約210nM、約70nM~約200nM、約70nM~約190nM、約70nM~約180nM、約70nM~約170nM、約70nM~約160nM、約70nM~約150nM、約70nM~約140nM、約70nM~約130nM、約70nM~約120nM、約70nM~約110nM、約70nM~約100nM、約70nM~約95nM、約70nM~約90nM、約70nM~約85nM、約70nM~約80nM、約70nM~約75nM、約80nM~約5μM、約80nM~約2μM、約80nM~約1μM、約80nM~約500nM、約80nM~約250nM、約80nM~約240nM、約80nM~約230nM、約80nM~約220nM、約80nM~約210nM、約80nM~約200nM、約80nM~約190nM、約80nM~約180nM、約80nM~約170nM、約80nM~約160nM、約80nM~約150nM、約80nM~約140nM、約80nM~約130nM、約80nM~約120nM、約80nM~約110nM、約80nM~約100nM、約80nM~約95nM、約80nM~約90nM、約80nM~約85nM、約90nM~約5μM、約90nM~約2μM、約90mM~約1μM、約90nM~約500nM、約90nM~約250nM、約90nM~約240nM、約90nM~約230nM、約90nM~約220nM、約90nM~約210nM、約90nM~約200nM、約90nM~約190nM、約90nM~約180nM、約90nM~約170nM、約90nM~約160nM、約90nM~約150nM、約90nM~約140nM、約90nM~約130nM、約90nM~約120nM、約90nM~約110nM、約90nM~約100nM、約90nM~約95nM、約100nM~約5μM、約100nM~約2μM、約100nM~約1μM、約100nM~約500nM、約100nM~約250nM、約100nM~約240nM、約100nM~約230nM、約100nM~約220nM、約100nM~約210nM、約100nM~約200nM、約100nM~約190nM、約100nM~約180nM、約100nM~約170nM、約100nM~約160nM、約100nM~約150nM、約100nM~約140nM、約100nM~約130nM、約100nM~約120nM、約100nM~約110nM、約110nM~約5μM、約110nM~約2μM、約110nM~約1μM、約110nM~約500nM、約110nM~約250nM、約110nM~約240nM、約110nM~約230nM、約110nM~約220nM、約110nM~約210nM、約110nM~約200nM、約110nM~約190nM、約110nM~約180nM、約110nM~約170nM、約110nM~約160nM、約110nM~約150nM、約110nM~約140nM、約110nM~約130nM、約110nM~約120nM、約120nM~約5μM、約120nM~約2μM、約120nM~約1μM、約120nM~約500nM、約120nM~約250nM、約120nM~約240nM、約120nM~約230nM、約120nM~約220nM、約120nM~約210nM、約120nM~約200nM、約120nM~約190nM、約120nM~約180nM、約120nM~約170nM、約120nM~約160nM、約120nM~約150nM、約120nM~約140nM、約120nM~約130nM、約130nM~約5μM、約130nM~約2μM、約130nM~約1μM、約130nM~約500nM、約130nM~約250nM、約130nM~約240nM、約130nM~約230nM、約130nM~約220nM、約130nM~約210nM、約130nM~約200nM、約130nM~約190nM、約130nM~約180nM、約130nM~約170nM、約130nM~約160nM、約130nM~約150nM、約130nM~約140nM、約140nM~約5μM、約140nM~約2μM、約140nM~約1μM、約140nM~約500nM、約140nM~約250nM、約140nM~約240nM、約140nM~約230nM、約140nM~約220nM、約140nM~約210nM、約140nM~約200nM、約140nM~約190nM、約140nM~約180nM、約140nM~約170nM、約140nM~約160nM、約140nM~約150nM、約150nM~約5μM、約150nM~約2μM、約150nM~約1μM、約150nM~約500nM、約150nM~約250nM、約150nM~約240nM、約150nM~約230nM、約150nM~約220nM、約150nM~約210nM、約150nM~約200nM、約150nM~約190nM、約150nM~約180nM、約150nM~約170nM、約150nM~約160nM、約160nM~約
5μM、約160nM~約2μM、約160nM~約1μM、約160nM~約500nM、約160nM~約250nM、約160nM~約240nM、約160nM~約230nM、約160nM~約220nM、約160nM~約210nM、約160nM~約200nM、約160nM~約190nM、約160nM~約180nM、約160nM~約170nM、約170nM~約5μM、約170nM~約2μM、約170nM~約1μM、約170nM~約500nM、約170nM~約250nM、約170nM~約240nM、約170nM~約230nM、約170nM~約220nM、約170nM~約210nM、約170nM~約200nM、約170nM~約190nM、約170nM~約180nM、約180nM~約5μM、約180nM~約2μM、約180nM~約1μM、約180nM~約500nM、約180nM~約250nM、約180nM~約240nM、約180nM~約230nM、約180nM~約220nM、約180nM~約210nM、約180nM~約200nM、約180nM~約190nM、約190nM~約5 μM、約190nM~約2μM、約190nM~約1μM、約190nM~約500nM、約190nM~約250nM、約190nM~約240nM、約190nM~約230nM、約190nM~約220nM、約190nM~約210nM、約190nM~約200nM、約200nM~約5μM、約200nM~約2μM、約200nM~約1μM、約200nM~約500nM、約200nM~約250nM、約200nM~約240nM、約200nM~約230nM、約200nM~約220nM、約200nM~約210nM、約210nM~約5μM、約210nM~約2μM、約210nM~約1μM、約210nM~約500nM、約210nM~約250nM、約210nM~約240nM、約210nM~約230nM、約210nM~約220nM、約220nM~約5μM、約220nM~約2μM、約220nM~約1μM、約220nM~約500nM、約220nM~約250nM、約220nM~約240nM、約220nM~約230nM、約230nM~約5μM、約230nM~約2μM、約230nM~約1μM、約230nM~約500nM、約230nM~約250nM、約230nM~約240nM、約240nM~約5μM、約240nM~約2μM、約240nM~約1μM、約240nM~約500nM、約240nM~約250nM、約250nM~約5μM、約250nM~約2μM、約250nM~約1μM、約250nM~約500nM、約500nM~約5μM、約500nM~約2 μM、約500nM~約1μM、約1μM~約5μM、約1μM~約2μM、もしくは約2μM~約5μM)の間である。
本明細書に記載されるいずれかのABPCの一部の実施形態では、第一の抗原結合ドメイン(および存在する場合には、任意に第二の抗原結合ドメイン)の、pH約4.0~約6.5(例えば、本明細書に記載するこの範囲の下位の範囲のいずれか)でのKDが、1nMより大きいものであり得る(例えば、約1nM~約1mM、約1nM~約900μM、約1nM~約800μM、約1nM~約700μM、約1nM~約600μM、約1nM~約500μM、約1nM~約400μM、約1nM~約300μM、約1nM~約200μM、約1nM~約100μM、約1nM~約90μM、約1nM~約80μM、約1nM~約70μM、約1nM~約60μM、約1nM~約50μM、約1nM~約40μM、約1nM~約30μM、約1 nM~約20μM、約1nM~約10μM、約1nM~約5μM、約1nM~約4μM、約1nM~約2μM、約1nM~約1μM、約1nM~約900nM、約1nM~約800nM、約1nM~約700nM、約1nM~約600nM、約1nM~約500nM、約1nM~約400nM、約1nM~約300nM、約1nM~約200nM、約1nM~約100nM、約1nM~約90nM、約1nM~約80nM、約1nM~約70nM、約1nM~約60nM、約1nM~約50nM、約1nM~約40nM、約1nM~約30nM、約2nM~約1mM、約2nM~約900μM、約2nM~約800μM、約2nM~約700μM、約2nM~約600μM、約2nM~約500μM、約2nM~約400μM、約2nM~約300μM、約2nM~約200μM、約2nM~約100μM、約2nM~約90μM、約2nM~約80μM、約2nM~約70μM、約2nM~約60μM、約2nM~約50μM、約2nM~約40μM、約2nM~約30μM、約2nM~約20μM、約2nM~約10μM、約2nM~約5μM、約2nM~約4μM、約2nM~約2μM、約2nM~約1μM、約2nM~約900nM、約2nM~約800nM、約2nM~約700nM、約2nM~約600nM、約2nM~約500nM、約2nM~約400nM、約2nM~約300nM、約2nM~約200nM、約2nM~約100nM、約2nM~約90nM、約2nM~約80nM、約2nM~約70nM、約2nM~約60nM、約2nM~約50nM、約2nM~約40nM、約2nM~約30nM、約5nM~約1mM、約5nM~約900μM、約5nM~約800μM、約5nM~約700μM、約5nM~約600μM、約5nM~約500μM、約5nM~約400μM、約5nM~約300μM、約5nM~約200μM、約5nM~約100μM、約5nM~約90μM、約5nM~約80μM、約5nM~約70μM、約5nM~約60μM、約5nM~約50μM、約5nM~約40μM、約5nM~約30μM、約5nM~約20μM、約5nM~約10μM、約5nM~約5μM、約5nM~約4μM、約5nM~約2μM、約5nM~約1μM、約5nM~約900nM、約5nM~約800nM、約5nM~約700nM、約5nM~約600nM、約5nM~約500nM、約5nM~約400nM、約5nM~約300nM、約5nM~約200nM、約5nM~約100nM、約5nM~約90nM、約5nM~約80nM、約5nM~約70nM、約5nM~約60nM、約5nM~約50nM、約5nM~約40nM、約5nM~約30nM、約10nM~約1mM、約10nM~約900μM、約10nM~約800μM、約10nM~約700μM、約10nM~約600μM、約10nM~約500μM、約10nM~約400μM、約10nM~約300μM、約10nM~約200μM、約10nM~約100μM、約10nM~約90μM、約10nM~約80μM、約10nM~約70μM、約10nM~約60μM、約10nM~約50μM、約10nM~約40μM、約10nM~約30μM、約10nM~約20μM、約10nM~約10μM、約10nM~約5μM、約10nM~約4μM、約10nM~約2μM、約10nM~約1μM、約10nM~約900nM、約10nM~約800nM、約10nM~約700nM、約10nM~約600nM、約10nM~約500nM、約10nM~約400nM、約10nM~約300nM、約10nM~約200nM、約10nM~約100nM、約10nM~約90nM、約10nM~約80nM、約10nM~約70nM、約10nM~約60nM、約10nM~約50nM、約10nM~約40nM、約10nM~約30nM、約20nM~約1mM、約20nM~約900μM、約20nM~約800μM、約20nM~約700μM、約20nM~約600μM、約20nM~約500μM、約20nM~約400μM、約20nM~約300μM、約20nM~約200μM、約20nM~約100μM、約20nM~約90μM、約20nM~約80μM、約20nM~約70μM、約20nM~約60μM、約20nM~約50μM、約20nM~約40μM、約20nM~約30μM、約20nM~約20μM、約20nM~約10μM、約20nM~約5μM、約20nM~約4μM、約20nM~約2μM、約20nM~約1μM、約20nM~約900nM、約20nM~約800nM、約20nM~約700nM、約20nM~約600nM、約20nM~約500nM、約20nM~約400nM、約20nM~約300nM、約20nM~約200nM、約20nM~約100nM、約20nM~約90nM、約20nM~約80nM、約20nM~約70nM、約20nM~約60nM、約20nM~約50nM、約20nM~約40nM、約20nM~約30nM;約1μM~約1mM、約1μM~約900μM、約1μM~約800μM、約1μM~約700μM、約1μM~約600μM、約1μM~約500μM、約1μM~約400μM、約1μM~約300μM、約1μM~約200μM、約1μM~約100μM、約1μM~約90μM、約1μM~約80μM、約1μM~約70μM、約1μM~約60μM、約1μM~約50μM、約1μM~約40μM、約1μM~約30μM、約1μM~約20μM、約1μM~約10μM、約1μM~約5μM、約1μM~約4μM、約1μM~約3μM、約1μM~約2μM、約2μM~約1mM、約2μM~約900μM、約2μM~約800μM、約2μM~約700μM、約2μM~約600μM、約2μM~約500μM、約2μM~約400μM、約2μM~約300μM、約2μM~約200μM、約2μM~約100μM、約2μM~約90μM、約2μM~約80μM、約2μM~約70μM、約2μM~約60μM、約2μM~約50μM、約2μM~約40μM、約2μM~約30μM、約2μM~約20μM、約2μM~約10μM、約2μM~約5μM、約2μM~約4μM、約2μM~約3μM、約5μM~約1mM、約5μM~約900μM、約5μM~約800μM、約5μM~約700μM、約5μM~約600μM、約5μM~約500μM、約5μM~約400μM、約5μM~約300μM、約5μM~約200μM、約5μM~約100μM、約5μM~約90μM、約5μM~約80μM、約5μM~約70μM、約5μM~約60μM、約5μM~約50μM、約5μM~約40μM、約5μM~約30μM、約5μM~約20μM、約5μM~約10μM、約10μM~約1mM、約10μM~約900μM、約10μM~約800μM、約10μM~約700μM、約10μM~約600μM、約10μM~約500μM、約10μM~約400μM、約10μM~約300μM、約10μM~約200μM、約10μM~約100μM、約10μM~約90μM、約10μM~約80μM、約10μM~約70μM、約10μM~約60μM、約10μM~約50μM、約10μM~約40μM、約10μM~約30μM、約10μM~約20μM、約20μM~約1mM、約20μM~約900μM、約20μM~約800μM、約20μM~約700μM、約20μM~約600μM、約20μM~約500μM、約20μM~約400μM、約20μM~約300μM、約20μM~約200μM、約20μM~約100μM、約20μM~約90μM、約20μM~約80μM、約20μM~約70μM、約20μM~約60μM、約20μM~約50μM、約20μM~約40μM、約20μM~約30μM、約30μM~約1mM、約30μM~約900μM、約30μM~約800μM、約30μM~約700μM、約30μM~約600μM、約30μM~約500μM、約30μM~約400μM、約30μM~約300μM、約30μM~約200μM、約30μM~約100μM、約30μM~約90μM、約30μM~約80μM、約30μM~約70μM、約30μM~約60μM、約30μM~約50μM、約30μM~約40μM、約40μM~約1mM、約40μM~約900μM、約40μM~約800μM、約40μM~約700μM、約40μM~約600μM、約40μM~約500μM、約40μM~約400μM、約40μM~約300μM、約40μM~約200μM、約40μM~約100μM、約40μM~約90μM、約40μM~約80μM、約40μM~約70μM、約40μM~約60μM、約40μM~約50μM、約50μM~約1mM、約50μM~約900μM、約50μM~約800μM、約50μM~約700μM、約50μM~約600μM、約50μM~約500μM、約50μM~約400μM、約50μM~約300μM、約50μM~約200μM、約50μM~約100μM、約50μM~約90μM、約50μM~約80μM、約50μM~約70μM、約50μM~約60μM、約60μM~約1mM、約60μM~約900μM、約60μM~約800μM、約60μM~約700μM、約60μM~約600μM、約60μM~約500μM、約60μM~約400μM、約60μM~約300μM、約60μM~約200μM、約60μM~約100μM、約60μM~約90μM、約60μM~約80μM、約60μM~約70μM、約70μM~約1mM、約70μM~約900μM、約70μM~約800μM、約70μM~約700μM、約70μM~約600μM、約70μM~約500μM、約70μM~約400μM、約70μM~約300μM、約70μM~約200μM、約70μM~約100μM、約70μM~約90μM、約70μM~約80μM、約80μM~約1mM、約80μM~約900μM、約80μM~約800μM、約80μM~約700μM、約80μM~約600μM、約80μM~約500μM、約80μM~約400μM、約80μM~約300μM、約80μM~約200μM、約80μM~約100μM、約80μM~約90μM、約90μM~約1mM、約90μM~約900μM、約90μM~約800μM、約90μM~約700μM、約90μM~約600μM、約90μM~約500μM、約90μM~約400μM、約90μM~約300μM、約90μM~約200μM、約90μM~約100μM、約100μM~約1mM、約100μM~約900μM、約100μM~約800μM、約100μM~約700μM、約100μM~約600μM、約100μM~約500μM、約100μM~約400μM、約100μM~約300μM、約100μM~約200μM、約200μM~約1mM、約200μM~約900μM、約200μM~約800μM、約200μM~約700μM、約200μM~約600μM、約200μM~約500μM、約200μM~約400μM、約200μM~約300μM、約300μM~約1mM、約300μM~約900μM、約300μM~約800μM、約300μM~約700μM、約300μM~約600μM、約300μM~約500μM、約300μM~約400μM、約400μM~約1mM、約400μM~約900μM、約400μM~約800μM、約400μM~約700μ
M、約400μM~約600μM、約400μM~約500μM、約500μM~約1mM、約500μM~約900μM、約500μM~約800μM、約500μM~約700μM、約500μM~約600μM、約600μM~約1mM、約600μM~約900μM、約600μM~約800μM、約600μM~約700μM、約700μM~約1mM、約700μM~約900μM、約700μM~約800μM、約800μM~約1mM、約800μM~約900μM、または約900μM~約1mMの間)。
当技術分野で公知の様々な異なる方法が、本明細書に記載されるいずれかの抗原結合タンパク質構築物のKD値を決定するために使用され得る(例えば、電気泳動移動度測定法、フィルター結合アッセイ、表面プラズモン共鳴、生体分子結合動態アッセイ、抗原発現細胞のインビトロ結合アッセイなど)。
本明細書に記載されるいずれかのABPCの一部の実施例では、対照ABPC(例えば、本明細書に記載されるいずれかの例示的な対照ABPC)の半減期と比較して、インビボでのABPCの半減期が減少する(例えば、検出可能な減少)(例えば、少なくとも1%の減少、少なくとも5%の減少、少なくとも10%の減少、少なくとも15%の減少、少なくとも20%の減少、少なくとも25%の減少、少なくとも30%の減少、少なくとも35%の減少、少なくとも40%の減少、少なくとも45%の減少、少なくとも50%の減少、少なくとも55%の減少、少なくとも60%の減少、少なくとも65%の減少、少なくとも70%の減少、少なくとも75%の減少、少なくとも80%の減少、少なくとも85%の減少、少なくとも90%の減少、少なくとも95%の減少、もしくは少なくとも99%の減少、または約1%の減少~約99%の減少、約1%の減少~約95%の減少、約1%の減少~約90%の減少、約1%の減少~約85%の減少、約1%の減少~約80%の減少、約1%の減少~約75%の減少、約1%の減少~約70%の減少、約1%の減少~約65%の減少、約1%の減少~約60%の減少、約1%の減少~約55%の減少、約1%の減少~約50%の減少、約1%の減少~約45%の減少、約1%の減少~約40%の減少、約1%の減少~約35%の減少、約1%の減少~約30%の減少、約1%の減少~約25%の減少、約1%の減少~約20%の減少、約1%の減少~約15%の減少、約1%の減少~約10%の減少、約1%の減少~約5%の減少、約5%の減少~約99%の減少、約5%の減少~約95%の減少、約5%の減少~約90%の減少、約5%の減少~約85%の減少、約5%の減少~約80%の減少、約5%の減少~約75%の減少、約5%の減少~約70%の減少、約5%の減少~約65%の減少、約5%の減少~約60%の減少、約5%の減少~約55%の減少、約5%の減少~約50%の減少、約5%の減少~約45%の減少、約5%の減少~約40%の減少、約5%の減少~約35%の減少、約5%の減少~約30%の減少、約5%の減少~約25%の減少、約5%の減少~約20%の減少、約5%の減少~約15%の減少、約5%の減少~約10%の減少、約10%の減少~約99%の減少、約10%の減少~約95%の減少、約10%の減少~約90%の減少、約10%の減少~約85%の減少、約10%の減少~約80%の減少、約10%の減少~約75%の減少、約10%の減少~約70%の減少、約10%の減少~約65%の減少、約10%の減少~約60%の減少、約10%の減少~約55%の減少、約10%の減少~約50%の減少、約10%の減少~約45%の減少、約10%の減少~約40%の減少、約10%の減少~約35%の減少、約10%の減少~約30%の減少、約10%の減少~約25%の減少、約10%の減少~約20%の減少、約10%の減少~約15%の減少、約15%の減少~約99%の減少、約15%の減少~約95%の減少、約15%の減少~約90%の減少、約15%の減少~約85%の減少、約15%の減少~約80%の減少、約15%の減少~約75%の減少、約15%の減少~約70%の減少、約15%の減少~約65%の減少、約15%の減少~約60%の減少、約15%の減少~約55%の減少、約15%の減少~約50%の減少、約15%の減少~約45%の減少、約15%の減少~約40%の減少、約15%の減少~約35%の減少、約15%の減少~約30%の減少、約15%の減少~約25%の減少、約15%の減少~約20%の減少、約20%の減少~約99%の減少、約20%の減少~約95%の減少、約20%の減少~約90%の減少、約20%の減少~約85%の減少、約20%の減少~約80%の減少、約20%の減少~約75%の減少、約20%の減少~約70%の減少、約20%の減少~約65%の減少、約20%の減少~約60%の減少、約20%の減少~約55%の減少、約20%の減少~約50%の減少、約20%の減少~約45%の減少、約20%の減少~約40%の減少、約20%の減少~約35%の減少、約20%の減少~約30%の減少、約20%の減少~約25%の減少、約25%の減少~約99%の減少、約25%の減少~約95%の減少、約25%の減少~約90%の減少、約25%の減少~約85%の減少、約25%の減少~約80%の減少、約25%の減少~約75%の減少、約25%の減少~約70%の減少、約25%の減少~約65%の減少、約25%の減少~約60%の減少、約25%の減少~約55%の減少、約25%の減少~約50%の減少、約25%の減少~約45%の減少、約25%の減少~約40%の減少、約25%の減少~約35%の減少、約25%の減少~約30%の減少、約30%の減少~約99%の減少、約30%の減少~約95%の減少、約30%の減少~約90%の減少、約30%の減少~約85%の減少、約30%の減少~約80%の減少、約30%の減少~約75%の減少、約30%の減少~約70%の減少、約30%の減少~約65%の減少、約30%の減少~約60%の減少、約30%の減少~約55%の減少、約30%の減少~約50%の減少、約30%の減少~約45%の減少、約30%の減少~約40%の減少、約30%の減少~約35%の減少、約35%の減少~約99%の減少、約35%の減少~約95%の減少、約35%の減少~約90%の減少、約35%の減少~約85%の減少、約35%の減少~約80%の減少、約35%の減少~約75%の減少、約35%の減少~約70%の減少、約35%の減少~約65%の減少、約35%の減少~約60%の減少、約35%の減少~約55%の減少、約35%の減少~約50%の減少、約35%の減少~約45%の減少、約35%の減少~約40%の減少、約40%の減少~約99%の減少、約40%の減少~約95%の減少、約40%の減少~約90%の減少、約40%の減少~約85%の減少、約40%の減少~約80%の減少、約40%の減少~約75%の減少、約40%の減少~約70%の減少、約40%の減少~約65%の減少、約40%の減少~約60%の減少、約40%の減少~約55%の減少、約40%の減少~約50%の減少、約40%の減少~約45%の減少、約45%の減少~約99%の減少、約45%の減少~約95%の減少、約45%の減少~約90%の減少、約45%の減少~約85%の減少、約45%の減少~約80%の減少、約45%の減少~約75%の減少、約45%の減少~約70%の減少、約45%の減少~約65%の減少、約45%の減少~約60%の減少、約45%の減少~約55%の減少、約45%の減少~約50%の減少、約50%の減少~約99%の減少、約50%の減少~約95%の減少、約50%の減少~約90%の減少、約50%の減少~約85%の減少、約50%の減少~約80%の減少、約50%の減少~約75%の減少、約50%の減少~約70%の減少、約50%の減少~約65%の減少、約50%の減少~約60%の減少、約50%の減少~約55%の減少、約55%の減少~約99%の減少、約55%の減少~約95%の減少、約55%の減少~約90%の減少、約55%の減少~約85%の減少、約55%の減少~約80%の減少、約55%の減少~約75%の減少、約55%の減少~約70%の減少、約55%の減少~約65%の減少、約55%の減少~約60%の減少、約60%の減少~約99%の減少、約60%の減少~約95%の減少、約60%の減少~約90%の減少、約60%の減少~約85%の減少、約60%の減少~約80%の減少、約60%の減少~約75%の減少、約60%の減少~約70%の減少、約60%の減少~約65%の減少、約65%の減少~約99%の減少、約65%の減少~約95%の減少、約65%の減少~約90%の減少、約65%の減少~約85%の減少、約65%の減少~約80%の減少、約65%の減少~約75%の減少、約65%の減少~約70%の減少、約70%の減少~約99%の減少、約70%の減少~約95%の減少、約70%の減少~約90%の減少、約70%の減少~約85%の減少、約70%の減少~約80%の減少、約70%の減少~約75%の減少、約75%の減少~約99%の減少、約75%の減少~約95%の減少、約75%の減少~約90%の減少、約75%の減少~約85%の減少、約75%の減少~約80%の減少、約80%の減少~約99%の減少、約80%の減少~約95%の減少、約80%の減少~約90%の減少、約80%の減少~約85%の減少、約85%の減少~約99%の減少、約85%の減少~約95%の減少、約85%の減少~約90%の減少、約90%の減少~約99%の減少、約90%の減少~約95%の減少、または約95%の減少~約99%の減少)。
コンジュゲート
一部の実施形態では、本明細書で提供されるABPCは、薬剤(例えば、化学療法薬、低分子)、毒素、または放射性同位体にコンジュゲートされ得る。薬剤、毒素、および放射性同位体(例えば、がんの治療に有用であることが知られる)の非限定的な例は、当技術分野で公知である。
一部の実施形態では、本明細書に記載のいずれかのABPCのうちの少なくとも一つのポリペプチドは、切断可能なリンカーを介して毒素、放射性同位体、または薬剤にコンジュゲートされる。一部の実施形態では、切断可能なリンカーは、プロテアーゼ切断部位を含む。一部の実施形態では、切断可能なリンカーは、標的哺乳動物細胞によってリソソームまたは後期エンドソームに輸送されると、ABPC上で切断される。一部の実施形態では、リンカーの切断は、薬剤または毒素を機能的に活性化する。
一部の実施形態では、本明細書に記載のいずれかのABPCのうちの少なくとも一つのポリペプチドは、非切断可能なリンカーを介して毒素、放射性同位体、または薬剤にコンジュゲートされる。一部の実施形態では、コンジュゲートされた毒素、放射性同位体、または薬剤は、ABPCのリソソームおよび/または後期エンドソームの分解中に放出される。
切断可能なリンカーの非限定的な例は、ヒドラゾンリンカー、ペプチドリンカー、ジスルフィドリンカー、およびチオエーテルリンカーを含む。例えば、Carter et al.,Cancer J.14(3):154-169,2008;Sanderson et al.,Clin.Cancer Res.11(2 Pt1):843-852,2005;Chari et al.,Acc.Chem.Res.41(1):98-107,2008;Oflazoglu et al.,Clin.Cancer Res.14(19): 6171-6180,2008;およびLu et al.,Int.J.Mol.Sci.17(4): 561,2016を参照されたい。
非切断可能なリンカーの非限定的な例は、マレイミドアルカンリンカーおよびメレイミドシクロヘキサンリンカー(MMC)を含む(例えば、McCombs et al.,AAPS J.17(2):339-351,2015に記載されるものを参照のこと)。
一部の実施形態では、本明細書に記載のいずれかのABPCは、標的哺乳動物細胞に対し細胞傷害性または細胞増殖抑制性である。
細胞における抗原結合タンパク質構築物の発現
本明細書においては、ABPCをコードする核酸を細胞中に導入して組換え細胞を作製すること;およびABPCの発現に十分な条件下で組換え細胞を培養することを含む、ABPC(例えば、本明細書に記載されるいずれかのABPC)を発現する組換え細胞を生成する方法もまた提供される。一部の実施形態では、導入する工程は、ABPCをコードする核酸を含む発現ベクターを細胞中に導入して組換え細胞を作製することを含む。
本明細書に記載されるいずれかのABPCは、例えば、真核細胞または原核細胞などの任意の細胞によって作製され得る。本明細書で使用される場合、用語「真核細胞」は、別個の膜結合型核を有する細胞を指す。かかる細胞としては、例えば、哺乳動物(例えば、げっ歯類、非ヒト霊長類、またはヒト)、昆虫、真菌、または植物の細胞が挙げられ得る。一部の実施形態では、真核細胞は、サッカロミセス・セレビシエなどの酵母細胞である。一部の実施形態では、真核細胞は、哺乳動物、鳥類、植物、または昆虫の細胞などの高等真核生物である。本明細書で使用される場合、用語「原核細胞」は、別個の膜結合型核を有しない細胞を指す。一部の実施形態では、原核細胞は細菌細胞である。
細胞を培養する方法は、当技術分野で周知である。細胞は、増殖、分化、および成長に有利な条件下でインビトロで維持され得る。簡潔に述べると、細胞は、細胞(例えば、任意の細胞)を、細胞生存率および成長を支持するために必要な成長因子および補助物を含む細胞培養培地と接触させることによって培養され得る。
核酸および発現ベクターを細胞(例えば、真核細胞)中に導入する方法は、当技術分野で公知である。細胞中に核酸を導入するために使用され得る方法の非限定的な例には、リポフェクション、トランスフェクション、エレクトロポレーション、マイクロインジェクション、リン酸カルシウムトランスフェクション、デンドリマーを用いたトランスフェクション、カチオン性ポリマートランスフェクション、セルスクイージング、ソノポレーション、光学的トランスフェクション、インペールフェクション(impalection)、
流体力学的送達、マグネトフェクション、ウイルス形質導入(例えば、アデノウイルスおよびレンチウイルスによる形質導入)、およびナノ粒子トランスフェクションが含まれる。
本明細書では、当技術分野において周知の技術(例えば、硫酸アンモニウム沈殿、ポリエチレングリコール沈殿、イオン交換クロマトグラフィー(アニオンまたはカチオン)、疎水性相互作用に基づくクロマトグラフィー、金属親和性クロマトグラフィー、リガンド親和性クロマトグラフィー、およびサイズ排除クロマトグラフィー)を使用して、細胞(例えば、真核細胞)からABPCを単離することをさらに含む方法が提供される。
治療方法
本明細書では、がん細胞であってその表面に存在するMETまたはMETのエピトープを有するがん細胞の集団を有することによって特徴付けられるがんを治療する方法であって、治療有効量の本明細書に記載される医薬組成物のいずれかまたは本明細書に記載されるABPCのいずれかを、上記がん細胞の集団を有することによって特徴付けられるがんを有すると特定される対象に投与することを含む方法が提供される。
本明細書ではまた、対象において腫瘍の体積を減少させる方法であって、該腫瘍は、がん細胞であってその表面に存在するMETまたはMETのエピトープを有するがん細胞の集団を有することによって特徴付けられるものであり、治療有効量の本明細書に記載される医薬組成物のいずれかまたは本明細書に記載されるABPCのいずれかを、上記がん細胞の集団を有することによって特徴付けられるがんを有すると特定された対象に投与することが含まれる方法も提供される。本明細書に記載の方法のいずれかのいくつかの実施形態では、少なくとも一つ(例えば、1、2、3、4、または5つ)の腫瘍(例えば固形腫瘍)の体積または腫瘍位置(例えば、転移部位)が、ABPCの投与前の少なくとも一つの腫瘍(例えば、固形腫瘍)のサイズと比較して、少なくとも1%、少なくとも2%、少なくとも3%、少なくとも4%、少なくとも5%、少なくとも6%、少なくとも8%、少なくとも10%、少なくとも12%、少なくとも14%、少なくとも16%、少なくとも18%、少なくとも20%、少なくとも22%、少なくとも24%、少なくとも26%、少なくとも28%、少なくとも30%、少なくとも35%、少なくとも40%、少なくとも45%、少なくとも50%、少なくとも55%、少なくとも60%、少なくとも65%、少なくとも70%、少なくとも75%、少なくとも80%、少なくとも85%、少なくとも90%、少なくとも95%、または少なくとも99%)、低減(例えば、検出可能な低減)する。
また、本明細書では、対象においてがん細胞の細胞死を誘導する方法であって、該がん細胞がその表面に存在するMETまたはMETのエピトープを有し、治療有効量の本明細書に記載される医薬組成物のいずれかまたは本明細書に記載されるABPCのいずれかを、がん細胞の集団を有すると特徴付けられるがんを有すると特定された対象に投与することを含む方法が提供される。一部の実施形態では、誘導される細胞死はネクローシスである。一部の実施形態では、誘導される細胞死はアポトーシスである。
本明細書に記載されるいずれかの方法の一部の実施形態では、がんは原発腫瘍である。
本明細書に記載されるいずれかの方法の一部の実施形態では、がんは転移である。
本明細書に記載されるいずれかの方法の一部の実施形態では、がんは非T細胞浸潤性腫瘍である。本明細書に記載されるいずれかの方法の一部の実施形態では、がんはT細胞浸潤性腫瘍である。
本明細書では、がんを有する対象において転移の発生のリスクを低減またはさらなる転移の発生のリスクを低減させる方法であって、該がんが、がん細胞であってその表面に存在するMETまたはMETのエピトープを有するがん細胞の集団を有することによって特徴付けられ、治療有効量の本明細書に記載されるいずれかの医薬組成物または本明細書に記載されるいずれかのABPCを、がん細胞の集団を有すると特徴付けられるがんを有すると特定された対象に投与することを含む方法が提供される。一部の実施形態では、対象における転移の発生のリスク、またはさらなる転移の発生のリスクが、同様のがんを有するが、治療を受けない対象または本明細書に記載されるいずれかのABPCの投与を含まない治療を受けた対象のリスクと比較して、少なくとも1%、少なくとも2%、少なくとも3%、少なくとも4%、少なくとも5%、少なくとも6%、少なくとも8%、少なくとも10%、少なくとも12%、少なくとも14%、少なくとも16%、少なくとも18%、少なくとも20%、少なくとも25%、少なくとも30%、少なくとも35%、少なくとも40%、少なくとも45%、少なくとも50%、少なくとも55%、少なくとも60%、少なくとも65%、少なくとも70%、少なくとも75%、少なくとも80%、少なくとも85%、少なくとも90%、少なくとも95%、または少なくとも99%、低減(例えば、検出可能な低減)する。
本明細書に記載されるいずれかの方法の一部の実施形態では、がんは非T細胞浸潤性腫瘍である。本明細書に記載されるいずれかの方法の一部の実施形態では、がんはT細胞浸潤性腫瘍である。本明細書に記載されるいずれかの方法の一部の実施形態では、細胞内コンパートメントは、エンドソーム/リソソーム経路の一部である。本明細書に記載されるいずれかの方法の一部の実施形態では、細胞内コンパートメントは、エンドソームである。
用語「対象」は、任意の哺乳動物を指す。一部の実施形態では、対象または「治療に好適な対象」は、イヌ科(例えば、イヌ)、ネコ科(例えば、ネコ)、ウマ科(例えば、ウマ)、ヒツジ、ウシ、ブタ、ヤギ、例えば真猿類(simian)(例えば、サル(例えば、マーモセット、ヒヒ)もしくは類人猿(ape)(例えば、ゴリラ、チンパンジー、オラウータン、またはテナガザル)もしくはヒトなどの霊長類;またはげっ歯類(例えば、マウス、モルモット、ハムスター、またはラット)であり得る。一部の実施形態では、対象または「治療に好適な対象」は、非ヒト哺乳動物であり得、特に、ヒトにおける治療有効性を実証するためのモデルとして従来的に使用されている哺乳動物(例えば、ネズミ、ラピーヌ(lapine)、ブタ、イヌ、または霊長類の動物)が用いられ得る。
本明細書で使用される場合、治療することは、がん(例えば、本明細書に記載される任意のがん)を有する患者において、がんの一つまたは複数(例えば、二つ、三つ、四つ、または五つ)の兆候または症状の数、頻度、または重症度を減少させることを含む。例えば、治療することは、がんを有する対象において、がんの進行を減少、がんの重症度を減少、またはがんの再発のリスクを減少させることができる。
本明細書において、治療有効量の本明細書に記載されるいずれかのABPCまたは本明細書に記載されるいずれかの医薬組成物を対象に投与することを含む、対象(本明細書に記載されるいずれかの対象)における固形腫瘍の成長を阻害(例えば、治療前の対象における固形腫瘍の成長、または異なる治療を受けた、もしくは治療を受けていない異なる対象における同様の固形腫瘍の成長と比較して)する方法が提供される。
本明細書に記載されるいずれかの方法の一部の実施形態では、固形腫瘍の成長は固形腫瘍の一次成長である。本明細書に記載されるいずれかの方法の一部の実施形態では、固形腫瘍の成長は固形腫瘍の再発性成長である。本明細書に記載されるいずれかの方法の一部の実施形態では、固形腫瘍の成長は固形腫瘍の転移性成長である。一部の実施形態では、治療により、対象における固形腫瘍の成長が(例えば、治療前の対象における固形腫瘍の成長、または異なる治療を受けている、もしくは治療を受けていない異なる対象における同様の固形腫瘍の成長と比較して)、約1%の減少~約99%の減少(または本明細書に記載するこの範囲の下位の範囲のいずれか)がもたらされる。対象における固形腫瘍の成長は、様々な異なる画像診断方法、例えば陽電子放出型断層撮影法、X線コンピュータ断層撮影法、コンピュータ断層撮影法、および磁気共鳴画像法によって評価され得る。
また本明細書では、がん(例えば、本明細書に記載されるいずれかの例示的ながん)を有すると特定された対象において、ある期間にわたる転移の発生またはさらなる転移の発生のリスクを(例えば、同様のがんを有し、かつ異なる治療を受けるかまたは治療を受けていない対象と比較して)低減させる方法であって、治療有効量の本明細書に記載されるいずれかのタンパク質または本明細書に記載されるいずれかの医薬組成物を対象に投与することを含む方法が提供される。本明細書に記載されるいずれかの方法の一部の実施形態では、転移またはさらなる転移は、骨、リンパ節、脳、肺、肝臓、皮膚、骨を含む胸壁、軟骨および軟組織、腹腔、対側乳房、軟組織、筋肉、骨髄、卵巣、副腎、および膵臓に対する一つまたは複数である。
本明細書に記載されるいずれかの方法の一部の実施形態において、上記ある期間は、約1か月~約3年(例えば、約1か月~約2.5年、約1か月~約2年、約2か月~約1.5年、約1か月~約1年、約1か月~約10か月、約1か月~約8か月、約1か月~約6か月、約1か月~約5か月、約1か月~約4か月、約1か月~約3か月、約1か月~約2か月、約2か月~約3年、約2カ月~約2.5年、約2か月~約2年、約2か月~約1.5年間、約2か月~約1年、約2か月~約10か月、約2か月~約8か月、約2か月~約6か月、約2か月~約5か月、約2か月~約4か月、約2か月~約3か月、約3か月~約3年、約3か月~約2.5年間、約3か月~約2年、約3か月~約1.5年間、約3か月~約1年、約3か月~約10か月、約3か月~約8か月、約3か月~約6か月、約3か月~約5か月、約3か月~約4か月、約4か月~約3年、約4か月~約2.5年間、約4か月~約2年、約4か月~約1.5年間、約4か月~約1年、約4か月~約10か月、約4か月~約8か月、約4か月~約6か月、約4か月~約5か月、約5か月~約3年、約5か月~約2.5年間、約5か月~約2年、約5か月~約1.5年間、約5か月~約1年、約5か月~約10か月、約5か月~約8か月、約5か月~約6か月、約6か月~約3年、約6か月~約2.5年間、約6か月~約2年、約6か月~約1.5年間、約6か月~約1年、約6か月~約10か月、約6か月~約8か月、約8か月~約3年、約8か月~約2.5年間、約8か月~約2年、約8か月~約1.5年間、約8か月~約1年、約8か月~約10か月、約10か月~約3年、約10か月~約2.5年間、約10か月~約2年、約10か月~約1.5年間、約10か月~約1年、約1年~約3年、約1年~約2.5年間、約1年~約2年、約1年~約1.5年間、約1.5年間~約3年、約1.5年間~約2.5年間、約1.5年間~約2年、約2年~約3年、約2年~約2.5年間、または約2.5年~約3年間)である。
一部の実施形態では、がんを有すると特定された対象における、ある期間にわたる転移の発生またはさらなる転移の発生のリスクは、例えば、異なる治療を受けているか、または治療を受けていない同様のがんを有する対象におけるリスクと比較して、約1%~約99%(例えば、または本明細書に記載するこの範囲の下位の範囲のいずれか)減少する。
がんの非限定的な例には、以下が含まれる:急性リンパ芽球性白血病(ALL)、急性骨髄性白血病(AML)、副腎皮質がん、肛門がん、虫垂がん、星状細胞腫、基底細胞がん、脳腫瘍、胆管がん、膀胱がん、骨がん、乳がん、気管支腫瘍、バーキットリンパ腫、原発不明のがん、心臓腫瘍、子宮頚がん、脊索腫、慢性リンパ性白血病(CLL)、慢性骨髄性白血病(CML)、慢性骨髄増殖性新生物、大腸がん、結腸直腸がん、頭蓋咽頭腫、皮膚T細胞リンパ腫、腺管がん、胚芽腫、子宮内膜がん、上衣腫、食道がん、感覚神経芽細胞腫、線維性組織球腫、ユーイング肉腫、眼がん、胚細胞腫瘍、胆嚢がん、胃がん、消化管カルチノイド腫瘍、消化管間質腫瘍、妊娠性絨毛疾患、神経膠腫、頭頸部がん、毛様細胞白血病、肝細胞がん、組織球症、ホジキンリンパ腫、下咽頭がん、眼内黒色腫、膵島細胞腫瘍、カポジ肉腫、腎臓がん、ランゲルハンス細胞組織球症、喉頭がん、白血病、口唇および口腔がん、肝がん、上皮内小葉がん、肺がん、リンパ腫、マクログロブリン血症、悪性線維性組織球腫、黒色腫、メルケル細胞がん、中皮腫、原発不明転移性頸部扁平上皮がん、NUT遺伝子が関与する正中線がん(midline tract carcinoma involving NUT gene)、口腔がん、多発性内分泌腫瘍症候群、多発性骨髄腫、菌状息肉腫、骨髄異形成症候群、骨髄異形成/骨髄増殖性腫瘍、鼻腔および副鼻腔がん、鼻咽頭がん、神経芽細胞腫、非ホジキンリンパ腫、非小細胞肺がん、口腔咽頭がん、骨肉腫、卵巣がん、膵臓がん、乳頭腫症、傍神経節腫、副甲状腺がん、陰茎がん、咽頭がん、褐色細胞腫、下垂体腫瘍、胸膜肺芽腫、原発性中枢神経系リンパ腫、前立腺がん、直腸がん、腎細胞がん、腎盂尿管がん、網膜芽細胞腫、ラブドイド腫瘍、唾液腺がん、セザリー症候群、皮膚がん、小細胞肺がん、小腸がん、軟部組織肉腫、脊髄腫瘍、胃がん、T細胞リンパ腫、奇形腫、精巣がん、咽頭がん、胸腺腫および胸腺がん、甲状腺がん、尿道がん、子宮がん、膣がん、外陰がん、ならびにウィルムス腫瘍。がんのさらなる例は、当技術分野で公知である。
一部の実施形態では、患者は、一つまたは複数の追加の治療薬(例えば、化学療法剤、組換えサイトカインまたはインターロイキンタンパク質、キナーゼ阻害剤、およびチェックポイント阻害剤のうちの一つまたは複数)をさらに投与される。一部の実施形態では、一つまたは複数の追加の治療薬は、本明細書に記載されるいずれかのABPCが患者に投与されるのとほぼ同時に患者に投与される。一部の実施形態では、一つまたは複数の追加の治療薬は、本明細書に記載されるいずれかのABPCが患者に投与された後に患者に投与される。いくつかの実施形態では、一つまたは複数の追加の治療薬は、本明細書に記載されるいずれかのABPCが患者に投与される前に患者に投与される。
本明細書に記載されるいずれかの方法の一部の実施形態では、がんは、固形がん(例えば、乳がん、前立腺がん、または非小細胞肺がん)である。
組成物
本明細書においてまた、本明細書に記載されるいずれかのABPCの少なくとも一つを含む組成物(例えば、医薬組成物)が提供される。一部の実施形態では、組成物(例えば、医薬組成物)は、滅菌バイアルまたは充填済みシリンジ内に配置され得る。
一部の実施形態では、組成物(例えば、医薬組成物)は、異なる投与経路(例えば、静脈内、皮下、筋肉内、または腫瘍内)用に製剤化される。一部の実施形態では、組成物(例えば、医薬組成物)は、薬学的に許容可能な担体(例えば、リン酸緩衝生理食塩水)を含み得る。本明細書に記載されるいずれかの医薬組成物の単回または複数回の投与は、例えば、患者に必要とされる、および許容される用量および頻度に応じて、対象に与えられ得る。医薬組成物の用量は、状態、疾患または症状を効果的に治療または改善するのに十分な量のABPCを提供せねばならない。
また、治療有効量の本明細書に提供される組成物または医薬組成物のいずれかのうちの少なくとも一つを投与することを含む、がん(例えば、本明細書に記載されるいずれかのがん)を有する対象を治療する方法も本明細書に提供される。
キット
本明細書ではまた、本明細書に記載されるいずれかのABPC、本明細書に記載されるいずれかの組成物、または本明細書に記載されるいずれかの医薬組成物、を含むキットが提供される。一部の実施形態では、キットは、本明細書に記載されるいずれかの方法を実施するための説明書を含み得る。一部の実施形態では、キットは、本明細書に記載されるいずれかの組成物(例えば、医薬組成物)の少なくとも一回の用量を含み得る。一部の実施形態では、キットは、本明細書に記載のいずれかの医薬組成物を投与するためのシリンジを提供し得る。
タンパク質構築物
また、以下を含むタンパク質構築物(PC)もまた提供される:標的哺乳動物細胞の表面に存在するMETまたはMETのエピトープに特異的に結合することができる第一の抗原結合ドメインであって、(a)pH約7.0~約8.0(または本明細書に記載するこの範囲のいずれかの下位の範囲)での第一の抗原結合ドメインの解離速度がpH約4.0~約6.5(または本明細書に記載するこの範囲のいずれかの下位の範囲)での解離速度より速い;および/または(b)pH約7.0~約8.0(またはこの範囲のいずれかの下位の範囲)での第一の抗原結合ドメインの解離定数(KD)がpH約4.0~約6.5でのKDより大きい、当該第一の抗原結合ドメイン。
本明細書においてまた、本明細書に記載されるいずれかのPCを含む医薬組成物が提供される。また、治療有効量の本明細書に記載のいずれかのPCを対象に投与することを含む、それを必要とする対象を治療する方法も本明細書に提供される。
抗原結合タンパク質構築物のpH依存性を改善する方法
本明細書ではまた、抗原結合タンパク質構築物のpH依存性を改善する方法が提供され、当該方法は、抗原結合ドメインを含む出発抗原結合タンパク質構築物を提供すること、および出発抗原結合タンパク質構築物中の抗原結合ドメインの一つまたは複数のCDRに一つまたは複数のヒスチジンアミノ酸置換基を導入することを含み、当該方法は、(a)出発抗原結合タンパク質構築物と比較して、pH約4.0~約6.5での抗原結合ドメインの解離速度の、pH約7.0~約8.0での解離速度に対する比が増加すること(例えば、少なくとも0.1倍の増加~約100倍の増加、または本明細書に記載するこの範囲の下位の範囲のいずれか)、および(b)出発抗原結合タンパク質構築物と比較して、pH約4.0~約6.5での抗原結合ドメインの解離定数(KD)の、pH約7.0~約8.0でのKDに対する比が増加すること(例えば、少なくとも0.1倍~約100倍の増加、または本明細書に記載するこの範囲の下位の範囲のいずれか)、の一方または両方を有する抗原結合タンパク質構築物の生成をもたらす。
実施形態
実施形態1は、有効量の抗原結合タンパク質構築物(ABPC)を含む医薬組成物であって、標的哺乳動物細胞の表面に存在するMETまたはMETのエピトープに特異的に結合することができる第一の抗原結合ドメインを含み、(a)pH約4.0~約6.5での第一の抗原結合ドメインの解離速度が、pH約7.0~約8.0での解離速度よりも速い、または(b)pH約4.0~約6.5での第一の抗原結合ドメインの解離定数(KD)が、pH約7.0~約8.0でのKDよりも大きいものである、当該有効量の抗原結合タンパク質構築物(ABPC)を含む医薬組成物である。
実施形態2は、当該第一の抗原結合ドメインが、一つまたは複数のアミノ酸がヒスチジンで置換されているテリソツズマブの重鎖可変ドメインを含む、実施形態1に記載の医薬組成物である。
実施形態3は、当該第一の抗原結合ドメインが、一つまたは複数のアミノ酸がヒスチジンで置換されているテリソツズマブの軽鎖可変ドメインを含む、実施形態1に記載の医薬組成物である。
実施形態4は、当該第一の抗原結合ドメインが、一つまたは複数のアミノ酸がヒスチジンで置換されているテリソツズマブの重鎖可変ドメインと、一つまたは複数のアミノ酸がヒスチジンで置換されているテリソツズマブの軽鎖可変ドメインとを含む、実施形態1に記載の医薬組成物である。
実施形態5は、テリソツズマブの重鎖可変ドメインが、配列番号1を含む、実施形態2または4に記載の医薬組成物である。
実施形態6は、テリソツズマブの軽鎖可変ドメインが、配列番号2を含む、実施形態3または4に記載の医薬組成物である。
実施形態7は、当該第一の抗原結合ドメインが、それぞれ配列番号3~5であるCDR1、CDR2およびCDR3であって、配列番号3~5においてまとめて合計で一つまたは複数のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む重鎖可変ドメインを含むものである、実施形態1に記載の医薬組成物である。
実施形態8は、当該第一のMET結合ドメインが、それぞれ配列番号6~8であるCDR1、CDR2およびCDR3であって、配列番号6~8においてまとめて合計で一つまたは複数のアミノ酸位置がヒスチジンで置換されている当該CDR1、CDR2およびCDR3を含む軽鎖可変ドメインを含むものである、実施形態1に記載の医薬組成物である。
実施形態9は、当該第一のMET結合ドメインが、それぞれ配列番号3~5であるCDR1、CDR2およびCDR3であって、配列番号3~5においてまとめて合計で一つまたは複数のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む重鎖可変ドメインと、それぞれ配列番号6~8であるCDR1、CDR2およびCDR3であって、配列番号6~8においてまとめて合計で一つまたは複数のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む軽鎖可変ドメインとを含むものである、実施形態1に記載の医薬組成物である。
実施形態10は、第一の抗原結合ドメインが、配列番号1と少なくとも90%同一である重鎖可変ドメインであって、26、27、28、29、32、97、98、99、100、101、102、103および107からなる群から選択される配列番号1における一つまたは複数の位置にヒスチジンを含む、当該重鎖可変ドメインを含むものである、実施形態1、2、または7に記載の医薬組成物である。
実施形態11は、第一の抗原結合ドメインが、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2における一つまたは複数の位置にヒスチジンを含む、当該軽鎖可変ドメインを含むものである、実施形態1、3または8に記載の医薬組成物である。
実施形態12は、第一の抗原結合ドメインが、配列番号1と少なくとも90%同一である重鎖可変ドメインであって、26、27、28、29、32、97、98、99、100、101、102、103および107からなる群から選択される配列番号1における一つまたは複数の位置にヒスチジンを含む、当該重鎖可変ドメインと、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2における一つまたは複数の位置にヒスチジンを含む、当該軽鎖可変ドメインとを含むものである、実施形態1、4、または9に記載の医薬組成物である。
実施形態13は、第一の抗原結合ドメインが、配列番号13,配列番号14,配列番号15,配列番号16,配列番号19,配列番号40,配列番号41,配列番号42,配列番号43,配列番号44,配列番号45,配列番号46、または配列番号50.の重鎖可変ドメインを含むものである、実施形態1に記載の医薬組成物である。
実施形態14は、第一の抗原結合ドメインが、配列番号2の軽鎖可変ドメインを含むものである、実施形態13に記載の医薬組成物である。
実施形態15は、ABPCは、標的哺乳動物細胞によるABPCの細胞内移行後に、標的哺乳動物細胞において分解されるものである、実施形態1~14のいずれか一つに記載の医薬組成物である。
実施形態16は、ABPCが、コンジュゲートされた毒素、放射性同位体、薬剤、または低分子をさらに含むものである、実施形態1~15のいずれか一つに記載の医薬組成物である。
実施形態17は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞における毒素放出の増加を提供するものである、実施形態16に記載の医薬組成物である。
実施形態18は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞における毒素放出の少なくとも20%の増加を提供するものである、実施形態17に記載の医薬組成物である。
実施形態19は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞における毒素放出の少なくとも50%の増加を提供するものである、実施形態18に記載の医薬組成物である。
実施形態20は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞における毒素放出の少なくとも2倍の増加を提供するものである、実施形態17に記載の医薬組成物である。
実施形態21は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞における毒素放出の少なくとも5倍の増加を提供するものである、実施形態20に記載の医薬組成物である。
実施形態22は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞の殺傷の増加を提供するものである、実施形態16~21のいずれか一つに記載の医薬組成物である。
実施形態23は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞の殺傷の少なくとも20%の増加を提供するものである、実施形態22に記載の医薬組成物である。
実施形態24は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞の殺傷の少なくとも50%の増加を提供するものである、実施形態23に記載の医薬組成物である。
実施形態25は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞の殺傷の少なくとも2倍の増加を提供するものである、実施形態22に記載の医薬組成物である。
実施形態26は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞の殺傷の少なくとも5倍の増加を提供するものである、実施形態25に記載の医薬組成物である。
実施形態27は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞におけるエンドリソソーム送達の増加を提供するものである、実施形態1~26のいずれか一つに記載の医薬組成物である。
実施形態28は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞におけるエンドリソソーム送達の少なくとも20%の増加を提供するものである、実施形態27に記載の医薬組成物である。
実施形態29は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞におけるエンドリソソーム送達の少なくとも50%の増加を提供するものである、実施形態28に記載の医薬組成物である。
実施形態30は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞におけるエンドリソソーム送達の少なくとも2倍の増加を提供するものである、実施形態27に記載の医薬組成物である。
実施形態31は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞におけるエンドリソソーム送達の少なくとも5倍の増加を提供するものである、実施形態30に記載の医薬組成物である。
実施形態32は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞の表面に存在するMETのレベルの減少をそれほど生じさせないものである、実施形態1~31のいずれか一つに記載の医薬組成物である。
実施形態33は、当該組成物が、標的哺乳動物細胞の表面に存在するMETのレベルの検出可能な減少をもたらさないものである、実施形態1~31のいずれか一つに記載の医薬組成物である。
実施形態34は、有効量の抗原結合タンパク質構築物(ABPC)を含む医薬組成物であって、標的哺乳動物細胞の表面に存在するMETまたはMETのエピトープに特異的に結合することができる第一の抗原結合ドメイン;およびコンジュゲートされた毒素、放射性同位体、薬剤、または低分子を含み、(a)pH約4.0~約6.5での第一の抗原結合ドメインの解離速度がpH約7.0~約8.0での解離速度よりも速い、またはpH約4.0~約6.5での第一の抗原結合ドメインの解離定数(KD)がpH約7.0~約8.0でのKDより大きく、かつ、(b)当該組成物が、同量の対照ABPCを含む組成物と比較して標的哺乳動物細胞における毒素放出の増加、同量の対照ABPCを含む組成物と比較して標的哺乳動物細胞の殺傷の増加、および同量の対照ABPCを含む組成物と比較して標的哺乳動物細胞におけるエンドリソソーム送達の増加、のうちの一つまたは複数を提供するものである、当該医薬組成物である。
実施形態35は、当該第一の抗原結合ドメインが、一つまたは複数のアミノ酸がヒスチジンで置換されているテリソツズマブの重鎖可変ドメインを含むものである、実施形態34に記載の医薬組成物である。
実施形態36は、当該第一の抗原結合ドメインが、一つまたは複数のアミノ酸がヒスチジンで置換されているテリソツズマブの軽鎖可変ドメインを含むものである、実施形態34に記載の医薬組成物である。
実施形態37は、当該第一の抗原結合ドメインが、一つまたは複数のアミノ酸がヒスチジンで置換されているテリソツズマブの重鎖可変ドメインと、一つまたは複数のアミノ酸がヒスチジンで置換されているテリソツズマブの軽鎖可変ドメインとを含むものである、実施形態34に記載の医薬組成物である。
実施形態38は、テリソツズマブの重鎖可変ドメインが、配列番号1を含むものである、実施形態35または37に記載の医薬組成物である。
実施形態39は、テリソツズマブの軽鎖可変ドメインが、配列番号2を含むものである、実施形態36または37に記載の医薬組成物である。
実施形態40は、当該第一の抗原結合ドメインが、それぞれ配列番号3~5であるCDR1、CDR2およびCDR3であって、配列番号3~5においてまとめて合計で一つまたは複数のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む重鎖可変ドメインを含むものである、実施形態34に記載の医薬組成物である。
実施形態41は、当該第一のMET結合ドメインが、それぞれ配列番号6~8であるCDR1、CDR2およびCDR3であって、配列番号6~8においてまとめて合計で一つまたは複数のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む軽鎖可変ドメインを含むものである、実施形態34に記載の医薬組成物である。
実施形態42は、当該第一のMET結合ドメインが、それぞれ配列番号3~5であるCDR1、CDR2およびCDR3であって、配列番号3~5においてまとめて合計で一つまたは複数のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む重鎖可変ドメインと、それぞれ配列番号6~8であるCDR1、CDR2およびCDR3であって、配列番号6~8においてまとめて合計で一つまたは複数のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む軽鎖可変ドメインとを含むものである、実施形態34に記載の医薬組成物である。
実施形態43は、第一の抗原結合ドメインが、配列番号1と少なくとも90%同一である重鎖可変ドメインであって、26、27、28、29、32、97、98、99、100、101、102、103および107からなる群から選択される配列番号1における一つまたは複数の位置にヒスチジンを含む、当該重鎖可変ドメインを含むものである、実施形態34、35、または40に記載の医薬組成物である。
実施形態44は、第一の抗原結合ドメインが、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2における一つまたは複数の位置にヒスチジンを含む、当該軽鎖可変ドメインを含むものである、実施形態34、36または41に記載の医薬組成物である。
実施形態45は、第一の抗原結合ドメインが、配列番号1と少なくとも90%同一である重鎖可変ドメインであって、26、27、28、29、32、97、98、99、100、101、102、103および107からなる群から選択される配列番号1における一つまたは複数の位置にヒスチジンを含む、当該重鎖可変ドメインと、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2における一つまたは複数の位置にヒスチジンを含む、当該軽鎖可変ドメインとを含むものである、実施形態34、37、または42に記載の医薬組成物である。
実施形態46は、第一の抗原結合ドメインが、配列番号13,配列番号14,配列番号15,配列番号16,配列番号19,配列番号40,配列番号41,配列番号42,配列番号43,配列番号44,配列番号45,配列番号46、または配列番号50.の重鎖可変ドメインを含むものである、実施形態34に記載の医薬組成物である。
実施形態47は、第一の抗原結合ドメインが、配列番号2の軽鎖可変ドメインを含むものである、実施形態46に記載の医薬組成物である。
実施形態48は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞における毒素放出の増加を提供するものである、実施形態34~47のいずれか一つに記載の医薬組成物である。
実施形態49は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞における毒素放出の少なくとも20%の増加を提供するものである、実施形態48に記載の医薬組成物である。
実施形態50は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞における毒素放出の少なくとも50%の増加を提供するものである、実施形態49に記載の医薬組成物である。
実施形態51は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞における毒素放出の少なくとも2倍の増加を提供するものである、実施形態48に記載の医薬組成物である。
実施形態52は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞における毒素放出の少なくとも5倍の増加を提供するものである、実施形態51に記載の医薬組成物である。
実施形態53は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞の殺傷の増加を提供するものである、実施形態34~52のいずれか一つに記載の医薬組成物である。
実施形態54は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞の殺傷の少なくとも20%の増加を提供するものである、実施形態53に記載の医薬組成物である。
実施形態55は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞の殺傷の少なくとも50%の増加を提供するものである、実施形態54に記載の医薬組成物である。
実施形態56は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞の殺傷の少なくとも2倍の増加を提供するものである、実施形態53に記載の医薬組成物である。
実施形態57は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞の殺傷の少なくとも5倍の増加を提供するものである、実施形態56に記載の医薬組成物である。
実施形態58は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞におけるエンドリソソーム送達の増加を提供するものである、実施形態34~57のいずれか一つに記載の医薬組成物である。
実施形態59は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞におけるエンドリソソーム送達の少なくとも20%の増加を提供するものである、実施形態58に記載の医薬組成物である。
実施形態60は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞におけるエンドリソソーム送達の少なくとも50%の増加を提供するものである、実施形態59に記載の医薬組成物である。
実施形態61は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞におけるエンドリソソーム送達の少なくとも2倍の増加を提供するものである、実施形態58に記載の医薬組成物である。
実施形態62は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞におけるエンドリソソーム送達の少なくとも5倍の増加を提供するものである、実施形態61に記載の医薬組成物である。
実施形態63は、当該組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞の表面に存在するMETのレベルの減少をそれほど生じさせないものである、実施形態34~62のいずれか一つに記載の医薬組成物である。
実施形態64は、当該組成物が、標的哺乳動物細胞の表面に存在するMETのレベルの検出可能な減少をもたらさないものである、実施形態34~62のいずれか一つに記載の医薬組成物である。
実施形態65は、標的哺乳動物細胞が、がん細胞である、実施形態1~64のいずれか一つに記載の医薬組成物である。
実施形態66は、pH約4.0~約6.5での抗原結合ドメインの解離速度が、pH約7.0~約8.0での抗原結合ドメインの解離速度よりも少なくとも10%速いものである、実施形態1~65のいずれか一つに記載の医薬組成物である。
実施形態67は、pH約4.0~約6.5での抗原結合ドメインの解離速度が、pH約7.0~約8.0での抗原結合ドメインの解離速度よりも少なくとも3倍速いものである、実施形態1~65のいずれか一つに記載の医薬組成物である。
実施形態68は、pH約4.0~約6.5での抗原結合ドメインの解離速度が、pH約7.0~約8.0での抗原結合ドメインの解離速度よりも少なくとも10倍速いものである、実施形態1~65のいずれか一つに記載の医薬組成物である。
実施形態69は、pH約4.0~約6.5での抗原結合ドメインのKDが、pH約7.0~約8.0での抗原結合ドメインのKDよりも少なくとも10%大きいものである、実施形態1~68のいずれか一つに記載の医薬組成物である。
実施形態70 pH約4.0~約6.5での抗原結合ドメインのKDが、pH約7.0~約8.0での抗原結合ドメインのKDよりも少なくとも3倍大きいものである、実施形態1~68のいずれか一つに記載の医薬組成物である。
実施形態71は、pH約4.0~約6.5での抗原結合ドメインのKDが、pH約7.0~約8.0での抗原結合ドメインのKDよりも少なくとも10倍大きいものである、実施形態1~68のいずれか一つに記載の医薬組成物である。
実施形態72は、ABPCが、標的哺乳動物細胞に対し細胞傷害性または細胞増殖抑制性であるものである、実施形態1~71のいずれか一つに記載の医薬組成物である。
実施形態73は、ABPCが、非ヒト霊長類METおよびヒトMETと交差反応性であるものである、実施形態1~72のいずれか一つに記載の医薬組成物である。
実施形態74は、ABPCが、非ヒト霊長類MET、ヒトMET、ならびにラットMETおよびマウスMETの一方または両方と交差反応性であるものである、実施形態1~72のいずれか一つに記載の医薬組成物である。
実施形態75は、ABPCが、非ヒト霊長類MET、ヒトMET、ラットMETおよびマウスMETと交差反応性であるものである、実施形態74に記載の医薬組成物である。
実施形態76は、抗原結合ドメインが、旧世界ザル由来の細胞の表面に存在するMETのエピトープに結合するものである、実施形態1~75のいずれか一つに記載の医薬組成物である。
実施形態77は、ABPCが、単一のポリペプチドを含むものである、実施形態1~76のいずれか一つに記載の医薬組成物である。
実施形態78は、抗原結合ドメインが、VHドメイン、VHHドメイン、VNARドメイン、およびscFvからなる群から選択されるものである、実施形態77に記載の医薬組成物である。
実施形態79は、ABPCが、BiTe、(scFv)2、ナノボディ、ナノボディ-HSA、DART、TandAb、scDiabody、scDiabody-CH3、scFv-CH-CL-scFv、HSAbody、scDiabody-HSA、またはタンデム-scFvであるものである、実施形態77または78に記載の医薬組成物である。
実施形態80は、ABPCが、二以上のポリペプチドを含むものである、実施形態1~76のいずれか一つに記載の医薬組成物である。
実施形態81は、ABPCが、抗体、VHH-scAb、VHH-Fab、Dual scFab、F(ab’)2、diabody、crossMab、DAF(two-in-one)、DAF(four-in-one)、DutaMab、DT-IgG、knobs-in-holes共通軽鎖、knobs-in-holes構築物、電荷対、Fab-arm exchange、SEEDbody、LUZ-Y、Fcab、κλ-body、直交Fab、DVD-IgG、IgG(H)-scFv、scFv-(H)IgG、IgG(L)-scFv、scFv-(L)IgG、IgG(L,H)-Fv、IgG(H)-V、V(H)-IgG、IgG(L)-V、V(L)-IgG、KIH IgG-scFab、2scFv-IgG、IgG-2scFv、scFv4-Ig、Zybody、DVI-IgG、Diabody-CH3、トリプルボディ(triple body)、ミニ抗体(miniantibody)、ミニボディ(minibody)、TriBiミニボディ、scFv-CH3 KIH、Fab-scFv、F(ab’)2-scFv2、scFv-KIH、Fab-scFv-Fc、四価HCAb、scDiabody-Fc、Diabody-Fc、タンデムscFv-Fc、VHH-Fc、タンデムVHH-Fc、VHH-Fc KiH、Fab-VHH-Fc、細胞内発現抗体(Intrabody)、ドックアンドロック(dock and lock)、ImmTAC、IgG-IgGコンジュゲート、Cov-X-Body、scFv1-PEG-scFv2、Adnectin、DARPin、フィブロネクチン、およびDEPコンジュゲートの群から選択されるものである、実施形態80に記載の医薬組成物である。
実施形態82は、ABPCの少なくとも一つのポリペプチドが、切断可能なリンカーを介して毒素、放射性同位体、薬剤、または低分子にコンジュゲートされるものである、実施形態16~81のいずれか一つに記載の医薬組成物である。
実施形態83は、ABPCの少なくとも一つのポリペプチドが、非切断可能なリンカーを介して毒素、放射性同位体、薬剤、または低分子にコンジュゲートされるものである、実施形態16~81のいずれか一つに記載の医薬組成物である。
実施形態84は、インビボでのABPCの半減期が、インビボでの対照ABPCの半減期と比較して減少するものである、実施形態1~83のいずれか一つに記載の医薬組成物である。
実施形態85は、インビボでのABPCの半減期が、インビボでの対照ABPCの半減期と比較して約5%~約95%減少するものである、実施形態84に記載の医薬組成物である。
実施形態86は、インビボでのABPCの半減期が、インビボでの対照ABPCの半減期と比較して約10%~約95%減少するものである、実施形態84に記載の医薬組成物である。
実施形態87は、インビボでのABPCの半減期が、インビボでの対照ABPCの半減期と比較して約30%~約95%減少するものである、実施形態84に記載の医薬組成物である。
実施形態88は、インビボでのABPCの半減期が、インビボでの対照ABPCの半減期と比較して約50%~約95%減少するものである、実施形態84に記載の医薬組成物である。
実施形態89は、インビボでのABPCの半減期が、インビボでの対照ABPCの半減期と比較して約70%~約95%減少するものである、実施形態84に記載の医薬組成物である。
実施形態90は、対照ABPCが、標的哺乳動物細胞の表面に存在するMETまたはMETのエピトープに特異的に結合することができ、(a)該対照ABPCは、第一の抗原結合ドメインを含み、(b)pH約4.0~約6.5での対照ABPCの第一の抗原結合ドメインの解離速度は、pH約7.0~約8.0での解離速度よりも3倍以下だけ速く、および(c)pH約4.0~約6.5での対照ABPCの第一の抗原結合ドメインの解離定数(KD)は、pH約7.0~約8.0でのKDよりも3倍以下だけ大きいものである、実施形態17~89のいずれか一つに記載の医薬組成物である。
実施形態91は、対照ABPCが、標的哺乳動物細胞の表面に存在するMETまたはMETのエピトープに特異的に結合することができ、(a)該対照ABPCは、第一の抗原結合ドメインを含み、(b)pH約4.0~約6.5での対照ABPCの第一の抗原結合ドメインの解離速度は、pH約7.0~約8.0での解離速度よりも2倍以下だけ速く、および(c)pH約4.0~約6.5での対照ABPCの第一の抗原結合ドメインの解離定数(KD)は、pH約7.0~約8.0でのKDよりも2倍以下だけ大きいものである、実施形態17~89のいずれか一つに記載の医薬組成物である。
実施形態92は、対照ABPCが、標的哺乳動物細胞の表面に存在するMETまたはMETのエピトープに特異的に結合することができ、(a)該対照ABPCは、第一の抗原結合ドメインを含み、(b)pH約4.0~約6.5での対照ABPCの第一の抗原結合ドメインの解離速度は、pH約7.0~約8.0での解離速度よりも1倍以下だけ速く、および(c)pH約4.0~約6.5での対照ABPCの第一の抗原結合ドメインの解離定数(KD)は、pH約7.0~約8.0でのKDよりも1倍以下だけ大きいものである、実施形態17~89のいずれか一つに記載の医薬組成物である。
実施形態93は、対照ABPCが、テリソツズマブである、実施形態17~89のいずれか一つに記載の医薬組成物である。
実施形態94は、当該ABPCが、第二の抗原結合ドメインをさらに含むものである、実施形態1~93のいずれか一つに記載の医薬組成物である。
実施形態95は、実施形態1~94のいずれか一つに記載の医薬組成物の少なくとも一回の用量を含むキットである。
実施形態96は、抗原結合タンパク質構築物(ABPC)であって、標的哺乳動物細胞の表面に存在するMETまたはMETのエピトープに特異的に結合することができる第一の抗原結合ドメインを含み、(a)pH約4.0~約6.5での第一の抗原結合ドメインの解離速度が、pH約7.0~約8.0での解離速度よりも速い、または(b)pH約4.0~約6.5での第一の抗原結合ドメインの解離定数(KD)が、pH約7.0~約8.0でのKDよりも大きいものである、当該抗原結合タンパク質構築物(ABPC)である。
実施形態97は、第一の抗原結合ドメインが、一つまたは複数のアミノ酸がヒスチジンで置換されているテリソツズマブの重鎖可変ドメインを含むものである、実施形態96に記載のABPCである。
実施形態98は、第一の抗原結合ドメインが、一つまたは複数のアミノ酸がヒスチジンで置換されているテリソツズマブの軽鎖可変ドメインを含むものである、実施形態96に記載のABPCである。
実施形態99は、第一の抗原結合ドメインが、一つまたは複数のアミノ酸がヒスチジンで置換されているテリソツズマブの重鎖可変ドメインと、一つまたは複数のアミノ酸がヒスチジンで置換されているテリソツズマブの軽鎖可変ドメインとを含むものである、実施形態96に記載のABPCである。
実施形態100は、テリソツズマブの重鎖可変ドメインが、配列番号1を含むものである、実施形態97または99に記載のABPCである。
実施形態101は、テリソツズマブの軽鎖可変ドメインが、配列番号2を含むものである、実施形態98または99に記載のABPCである。
実施形態102は、第一の抗原結合ドメインが、それぞれ配列番号3~5であるCDR1、CDR2およびCDR3であって、配列番号3~5においてまとめて合計で一つまたは複数のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む重鎖可変ドメインを含むものである、実施形態96に記載のABPCである。
実施形態103は、第一のMET結合ドメインが、それぞれ配列番号6~8であるCDR1、CDR2およびCDR3であって、配列番号6~8においてまとめて合計で一つまたは複数のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む軽鎖可変ドメインを含むものである、実施形態96に記載のABPCである。
実施形態104は、第一のMET結合ドメインが、それぞれ配列番号3~5であるCDR1、CDR2およびCDR3であって、配列番号3~5においてまとめて合計で一つまたは複数のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む重鎖可変ドメインと、それぞれ配列番号6~8であるCDR1、CDR2およびCDR3であって、配列番号6~8においてまとめて合計で一つまたは複数のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む軽鎖可変ドメインとを含むものである、実施形態96のABPCである。
実施形態105は、第一の抗原結合ドメインが、配列番号1と少なくとも90%同一である重鎖可変ドメインであって、26、27、28、29、32、97、98、99、100、101、102、103および107からなる群から選択される配列番号1における一つまたは複数の位置にヒスチジンを含む、当該重鎖可変ドメインを含むものである、実施形態96、97、または102に記載のABPCである。
実施形態106は、第一の抗原結合ドメインが、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2における一つまたは複数の位置にヒスチジンを含む、当該軽鎖可変ドメインを含むものである、実施形態96、98または103に記載のABPCである。
実施形態107は、第一の抗原結合ドメインが、配列番号1と少なくとも90%同一である重鎖可変ドメインであって、26、27、28、29、32、97、98、99、100、101、102、103および107からなる群から選択される配列番号1における一つまたは複数の位置にヒスチジンを含む、当該重鎖可変ドメインと、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2における一つまたは複数の位置にヒスチジンを含む、当該軽鎖可変ドメインとを含むものである、実施形態96、99、または104に記載のABPCである。
実施形態108は、第一の抗原結合ドメインが、配列番号13,配列番号14,配列番号15,配列番号16,配列番号19,配列番号40,配列番号41,配列番号42,配列番号43,配列番号44,配列番号45,配列番号46、または配列番号50.の重鎖可変ドメインを含むものである、実施形態96に記載のABPCである。
実施形態109は、第一の抗原結合ドメインが、配列番号2の軽鎖可変ドメインを含むものである、実施形態108に記載のABPCである。
実施形態110は、ABPCは、標的哺乳動物細胞によるABPCの細胞内移行後に、標的哺乳動物細胞において分解されるものである、実施形態96~109のいずれか一つに記載のABPCである。
実施形態111は、ABPCが、コンジュゲートされた毒素、放射性同位体、薬剤、または低分子をさらに含むものである、実施形態96~110のいずれか一つに記載のABPCである。
実施形態112は、ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞における毒素放出の増加を提供するものである、実施形態111に記載のABPCである。
実施形態113は、ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞における毒素放出の少なくとも20%の増加を提供するものである、実施形態112に記載のABPCである。
実施形態114は、ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞における毒素放出の少なくとも50%の増加を提供するものである、実施形態113に記載のABPCである。
実施形態115は、ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞における毒素放出の少なくとも2倍の増加を提供するものである、実施形態112に記載のABPCである。
実施形態116は、ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞において毒素放出の少なくとも5倍の増加を提供するものである、実施形態115に記載のABPCである。
実施形態117は、ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞の殺傷の増加を提供するものである、実施形態111~116のいずれか一つに記載のABPCである。
実施形態118は、ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞の殺傷の少なくとも20%の増加を提供するものである、実施形態117に記載のABPCである。
実施形態119は、ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞の殺傷の少なくとも50%の増加を提供するものである、実施形態118に記載のABPCである。
実施形態120は、ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞の殺傷の少なくとも2倍の増加を提供するものである、実施形態117に記載のABPCである。
実施形態121は、ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞の殺傷の少なくとも5倍の増加を提供するものである、実施形態120に記載のABPCである。
実施形態122は、ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞におけるエンドリソソーム送達の増加を提供するものである、実施形態96~121のいずれか一つに記載のABPCである。
実施形態123は、ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞におけるエンドリソソーム送達の少なくとも20%の増加を提供するものである、実施形態122に記載のABPCである。
実施形態124は、ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞におけるエンドリソソーム送達の少なくとも50%の増加を提供するものである、実施形態123に記載のABPCである。
実施形態125は、ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞におけるエンドリソソーム送達の少なくとも2倍の増加を提供するものである、実施形態122に記載のABPCである。
実施形態126は、ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞におけるエンドリソソーム送達の少なくとも5倍の増加を提供するものである、実施形態125に記載のABPCである。
実施形態127は、ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞の表面に存在するMETのレベルの減少をそれほど生じさせないものである、実施形態96~126のいずれか一つに記載のABPCである。
実施形態128は、ABPCを含む組成物が、標的哺乳動物細胞の表面に存在するMETのレベルの検出可能な減少をもたらさないものである、実施形態96~126のいずれか一つに記載のABPCである。
実施形態129は、抗原結合タンパク質構築物(ABPC)であって、標的哺乳動物細胞の表面に存在するMETまたはMETのエピトープに特異的に結合することができる第一の抗原結合ドメイン;およびコンジュゲートされた毒素、放射性同位体、薬剤、または低分子を含み、(a)pH約4.0~約6.5での第一の抗原結合ドメインの解離速度がpH約7.0~約8.0での解離速度よりも速い、またはpH約4.0~約6.5での第一の抗原結合ドメインの解離定数(KD)がpH約7.0~約8.0でのKDより大きく、かつ、(b)当該組成物が、同量の対照ABPCを含む組成物と比較して標的哺乳動物細胞における毒素放出の増加、同量の対照ABPCを含む組成物と比較して標的哺乳動物細胞の殺傷の増加、および同量の対照ABPCを含む組成物と比較して標的哺乳動物細胞におけるエンドリソソーム送達の増加、のうちの一つまたは複数を提供するものである、当該抗原結合タンパク質構築物(ABPC)である。
実施形態130は、第一の抗原結合ドメインが、一つまたは複数のアミノ酸がヒスチジンで置換されているテリソツズマブの重鎖可変ドメインを含むものである、実施形態129に記載のABPCである。
実施形態131は、第一の抗原結合ドメインが、一つまたは複数のアミノ酸がヒスチジンで置換されているテリソツズマブの軽鎖可変ドメインを含むものである、実施形態129に記載のABPCである。
実施形態132は、第一の抗原結合ドメインが、一つまたは複数のアミノ酸がヒスチジンで置換されているテリソツズマブの重鎖可変ドメインと、一つまたは複数のアミノ酸がヒスチジンで置換されているテリソツズマブの軽鎖可変ドメインとを含むものである、実施形態129に記載のABPCである。
実施形態133は、テリソツズマブの重鎖可変ドメインが、配列番号1を含むものである、実施形態130または132に記載のABPCである。
実施形態134は、テリソツズマブの軽鎖可変ドメインが、配列番号2を含むものである、実施形態131または132に記載のABPCである。
実施形態135は、第一の抗原結合ドメインが、それぞれ配列番号3~5であるCDR1、CDR2およびCDR3であって、配列番号3~5においてまとめて合計で一つまたは複数のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む重鎖可変ドメインを含むものである、実施形態129に記載のABPCである。
実施形態136は、第一のMET結合ドメインが、それぞれ配列番号6~8であるCDR1、CDR2およびCDR3であって、配列番号6~8においてまとめて合計で一つまたは複数のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む軽鎖可変ドメインを含むものである、実施形態129に記載のABPCである。
実施形態137は、それぞれ配列番号3~5であるCDR1、CDR2およびCDR3であって、配列番号3~5においてまとめて合計で一つまたは複数のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む重鎖可変ドメインと、それぞれ配列番号6~8であるCDR1、CDR2およびCDR3であって、配列番号6~8においてまとめて合計で一つまたは複数のアミノ酸位置がヒスチジンで置換されているものである当該CDR1、CDR2およびCDR3を含む軽鎖可変ドメインとを含むものである、実施形態129に記載のABPCである。
実施形態138は、第1の抗原結合ドメインが、配列番号1と少なくとも90%同一である重鎖可変ドメインであって、26、27、28、29、32、97、98、99、100、101、102、103および107からなる群から選択される配列番号1における一つまたは複数の位置にヒスチジンを含む、当該重鎖可変ドメインを含むものである、実施形態129、130、または135に記載のABPCである。
実施形態139は、第一の抗原結合ドメインが、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2における一つまたは複数の位置にヒスチジンを含む、当該軽鎖可変ドメインを含むものである、実施形態129、131、または136に記載のABPCである。
実施形態140は、第一の抗原結合ドメインが、配列番号1と少なくとも90%同一である重鎖可変ドメインであって、26、27、28、29、32、97、98、99、100、101、102、103および107からなる群から選択される配列番号1における一つまたは複数の位置にヒスチジンを含む、当該重鎖可変ドメインと、配列番号2と少なくとも90%同一である軽鎖可変ドメインであって、配列番号2における一つまたは複数の位置にヒスチジンを含む、当該軽鎖可変ドメインとを含むものである、実施形態129、132、または137に記載のABPCである。
実施形態141は、第一の抗原結合ドメインが、配列番号13,配列番号14,配列番号15,配列番号16,配列番号19,配列番号40,配列番号41,配列番号42,配列番号43,配列番号44,配列番号45,配列番号46、または配列番号50.の重鎖可変ドメインを含むものである、実施形態129に記載のABPCである。
実施形態142は、第一の抗原結合ドメインが、配列番号2の軽鎖可変ドメインを含むものである、実施形態141に記載のABPCである。
実施形態143は、当該ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞における毒素放出の増加を提供するものである、実施形態129~142のいずれか一つに記載のABPCである。
実施形態144は、当該ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞における毒素放出の少なくとも20%の増加を提供するものである、実施形態143に記載のABPCである。
実施形態145は、当該ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞における毒素放出の少なくとも50%の増加を提供するものである、実施形態144に記載のABPCである。
実施形態146は、当該ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞における毒素放出の少なくとも2倍の増加を提供するものである、実施形態143に記載のABPCである。
実施形態147は、当該ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞における毒素放出の少なくとも5倍の増加を提供するものである、実施形態146に記載のABPCである。
実施形態148は、当該ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞の殺傷の増加を提供するものである、実施形態129~147のいずれか一つに記載のABPCである。
実施形態149は、当該ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞の殺傷の少なくとも20%の増加を提供するものである、実施形態148に記載のABPCである。
実施形態150は、当該ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞の殺傷の少なくとも50%の増加を提供するものである、実施形態149に記載のABPCである。
実施形態151は、当該ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞の殺傷の少なくとも2倍の増加を提供するものである、実施形態148に記載のABPCである。
実施形態152は、当該ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞の殺傷の少なくとも5倍の増加を提供するものである、実施形態151に記載のABPCである。
実施形態153は、当該ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞におけるエンドリソソーム送達の増加を提供するものである、実施形態129~152のいずれか一つに記載のABPCである。
実施形態154は、当該ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞におけるエンドリソソーム送達の少なくとも20%の増加を提供するものである、実施形態153に記載のABPCである。
実施形態155は、当該ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞におけるエンドリソソーム送達の少なくとも50%の増加を提供するものである、実施形態154に記載のABPCである。
実施形態156は、当該ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞におけるエンドリソソーム送達の少なくとも2倍の増加を提供するものである、実施形態153に記載のABPCである。
実施形態157は、当該ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞におけるエンドリソソーム送達の少なくとも5倍の増加を提供するものである、実施形態156に記載のABPCである。
実施形態158は、当該ABPCを含む組成物が、同量の対照ABPCを含む組成物と比較して、標的哺乳動物細胞の表面に存在するMETのレベルの減少をそれほど生じさせないものである、実施形態129~157のいずれか一つに記載のABPCである。
実施形態159は、当該ABPCを含む組成物が、標的哺乳動物細胞の表面に存在するMETのレベルの検出可能な減少をもたらさないものである、実施形態129~157のいずれか一つに記載のABPCである。
実施形態160は、標的哺乳動物細胞が、がん細胞である、実施形態96~159のいずれか一つに記載のABPCである。
実施形態161は、pH約4.0~約6.5での抗原結合ドメインの解離速度が、pH約7.0~約8.0での抗原結合ドメインの解離速度よりも少なくとも10%速いものである、実施形態96~160のいずれか一つに記載のABPCである。
実施形態162は、pH約4.0~約6.5での抗原結合ドメインの解離速度が、pH約7.0~約8.0での抗原結合ドメインの解離速度よりも少なくとも3倍速いものである、実施形態96~160のいずれか一つに記載のABPCである。
実施形態163は、pH約4.0~約6.5での抗原結合ドメインの解離速度が、pH約7.0~約8.0での抗原結合ドメインの解離速度よりも少なくとも10倍速いものである、実施形態96~160のいずれか一つに記載のABPCである。
実施形態164は、pH約4.0~約6.5での抗原結合ドメインのKDが、pH約7.0~約8.0での抗原結合ドメインのKDよりも少なくとも10%大きいものである、実施形態96~163のいずれか一つに記載のABPCである。
実施形態165は、pH約4.0~約6.5での抗原結合ドメインのKDが、pH約7.0~約8.0での抗原結合ドメインのKDよりも少なくとも3倍大きいものである、実施形態96~163のいずれか一つに記載のABPCである。
実施形態166は、pH約4.0~約6.5での抗原結合ドメインのKDが、pH約7.0~約8.0での抗原結合ドメインのKDよりも少なくとも10倍大きいものである、実施形態96~163のいずれか一つに記載のABPCである。
実施形態167は、ABPCが、標的哺乳動物細胞に対し細胞傷害性または細胞増殖抑制性であるものである、実施形態96~166のいずれか一つに記載のABPCである。
実施形態168は、ABPCが、非ヒト霊長類METおよびヒトMETと交差反応性であるものである、実施形態96~167のいずれか一つに記載のABPCである。
実施形態169は、ABPCが、非ヒト霊長類MET、ヒトMET、ならびにラットMETおよびマウスMETの一方または両方と交差反応性であるものである、実施形態96~167のいずれか一つに記載の医薬組成物である。
実施形態170は、ABPCが、非ヒト霊長類MET、ヒトMET、ラットMETおよびマウスMETと交差反応性であるものである、実施形態169に記載の医薬組成物である。
実施形態171は、抗原結合ドメインが、旧世界ザル由来の細胞の表面に存在するMETのエピトープに結合するものである、実施形態96~170のいずれか一つに記載のABPCである。
実施形態172は、ABPCが、単一のポリペプチドを含む、実施形態96~171のいずれか一つに記載のABPCである。
実施形態173は、抗原結合ドメインが、VHドメイン、VHHドメイン、VNARドメイン、およびscFvからなる群から選択されるものである、実施形態172に記載のABPCである。
実施形態174は、ABPCが、BiTe、(scFv)2、ナノボディ、ナノボディ-HSA、DART、TandAb、scDiabody、scDiabody-CH3、scFv-CH-CL-scFv、HSAbody、scDiabody-HSA、またはタンデム-scFvであるものである、実施形態172または173に記載のABPCである。
実施形態175は、ABPCが、二以上のポリペプチドを含むものである、実施形態96~171のいずれか一つに記載のABPCである。
実施形態176は、ABPCが、抗体、VHH-scAb、VHH-Fab、Dual scFab、F(ab’)2、diabody、crossMab、DAF(two-in-one)、DAF(four-in-one)、DutaMab、DT-IgG、knobs-in-holes共通軽鎖、knobs-in-holes構築物、電荷対、Fab-arm exchange、SEEDbody、LUZ-Y、Fcab、κλ-body、直交Fab、DVD-IgG、IgG(H)-scFv、scFv-(H)IgG、IgG(L)-scFv、scFv-(L)IgG、IgG(L,H)-Fv、IgG(H)-V、V(H)-IgG、IgG(L)-V、V(L)-IgG、KIH IgG-scFab、2scFv-IgG、IgG-2scFv、scFv4-Ig、Zybody、DVI-IgG、Diabody-CH3、トリプルボディ(triple body)、ミニ抗体(miniantibody)、ミニボディ(minibody)、TriBiミニボディ、scFv-CH3 KIH、Fab-scFv、F(ab’)2-scFv2、scFv-KIH、Fab-scFv-Fc、四価HCAb、scDiabody-Fc、Diabody-Fc、タンデムscFv-Fc、VHH-Fc、タンデムVHH-Fc、VHH-Fc KiH、Fab-VHH-Fc、細胞内発現抗体(Intrabody)、ドックアンドロック(dock and lock)、ImmTAC、IgG-IgGコンジュゲート、Cov-X-Body、scFv1-PEG-scFv2、Adnectin、DARPin、フィブロネクチン、およびDEPコンジュゲートの群から選択されるものである、実施形態175に記載のABPCである。
実施形態177は、ABPCの少なくとも一つのポリペプチドが、切断可能なリンカーを介して毒素、放射性同位体、薬剤、または低分子にコンジュゲートされるものである、実施形態111~176のいずれか一つに記載のABPCである。
実施形態178は、ABPCの少なくとも一つのポリペプチドが、非切断可能なリンカーを介して毒素、放射性同位体、薬剤、または低分子にコンジュゲートされるものである、実施形態111~176のいずれか一つに記載のABPCである。
実施形態179は、インビボでのABPCの半減期が、インビボでの対照ABPCの半減期と比較して減少するものである、実施形態96~178のいずれか一つに記載のABPCである。
実施形態180は、インビボでのABPCの半減期が、インビボでの対照ABPCの半減期と比較して約5%~約95%減少するものである、実施形態179に記載のABPCである。
実施形態181は、インビボでのABPCの半減期が、インビボでの対照ABPCの半減期と比較して約10%~約95%減少するものである、実施形態179に記載のABPCである。
実施形態182は、インビボでのABPCの半減期が、インビボでの対照ABPCの半減期と比較して約30%~約95%減少するのである、実施形態179に記載のABPCである。
実施形態183は、インビボでのABPCの半減期が、インビボでの対照ABPCの半減期と比較して約50%~約95%減少するものである、実施形態179に記載のABPCである。
実施形態184は、インビボでのABPCの半減期が、インビボでの対照ABPCの半減期と比較して約70%~約95%減少するものである、実施形態179に記載のABPCである。
実施形態185は、対照ABPCが、標的哺乳動物細胞の表面に存在するMETまたはMETのエピトープに特異的に結合することができ、(a)該対照ABPCは、第一の抗原結合ドメインを含み、(b)pH約4.0~約6.5での対照ABPCの第一の抗原結合ドメインの解離速度は、pH約7.0~約8.0での解離速度よりも3倍以下だけ速く、および(c)pH約4.0~約6.5での対照ABPCの第一の抗原結合ドメインの解離定数(KD)は、pH約7.0~約8.0でのKDよりも3倍以下だけ大きいものである、実施形態112~184のいずれか一つに記載のABPCである。
実施形態186は、対照ABPCが、標的哺乳動物細胞の表面に存在するMETまたはMETのエピトープに特異的に結合することができ、(a)該対照ABPCは、第一の抗原結合ドメインを含み、(b)pH約4.0~約6.5での対照ABPCの第一の抗原結合ドメインの解離速度は、pH約7.0~約8.0での解離速度よりも2倍以下だけ速く、および(c)pH約4.0~約6.5でのABPCの第一の抗原結合ドメインの解離定数(KD)は、pH約7.0~約8.0でのKDよりも2倍以下だけ大きいものである、実施形態112~184のいずれか一つに記載のABPCである。
実施形態187は、対照ABPCが、標的哺乳動物細胞の表面に存在するMETまたはMETのエピトープに特異的に結合することができ、(a)該対照ABPCは、第一の抗原結合ドメインを含み、(b)pH約4.0~約6.5での対照ABPCの第一の抗原結合ドメインの解離速度は、pH約7.0~約8.0での解離速度よりも1倍以下だけ速く、および(c)pH約4.0~約6.5での対照ABPCの第一の抗原結合ドメインの解離定数(KD)は、pH約7.0~約8.0でのKDよりも1倍以下だけ大きいものである、実施形態112~184のいずれか一つに記載のABPCである。
実施形態188は、対照ABPCが、テリソツズマブである、実施形態112~184のいずれか一つに記載のABPCである。
実施形態189は、ABPCが、第二の抗原結合ドメインをさらに含むものである、実施形態96~188のいずれか一つに記載のABPCである。
実施形態190は、実施形態96~189のいずれか一つに記載のABPCの少なくとも一回の用量を含むキットである。
実施形態191は、がん細胞であってその表面に存在するMETまたはMETのエピトープを有するがん細胞の集団を有することによって特徴付けられるがんを治療する方法であって、治療有効量の実施形態1~94のいずれか一つの医薬組成物または実施形態96~189のいずれか一つのABPCを、上記がん細胞の集団を有することによって特徴付けられるがんを有すると特定された対象に投与することを含む、方法である。
実施形態192は、対象において腫瘍の体積を減少させる方法であって、該腫瘍が、がん細胞であってその表面に存在するMETまたはMETのエピトープを有するがん細胞の集団を有することによって特徴付けられるものであり、当該方法が、治療有効量の実施形態1~94のいずれか一つの医薬組成物または実施形態96~189のいずれか一つのABPCを、上記がん細胞の集団を有することによって特徴付けられるがんを有すると特定された対象に投与することを含む、方法である。
実施形態193は、対象においてがん細胞の細胞死を誘導する方法であって、該がん細胞がその表面に存在するMETまたはMETのエピトープを有するものであり、当該方法が、治療有効量の実施形態1~94のいずれか一つの医薬組成物または実施形態96~189のいずれか一つのABPCを、上記がん細胞の集団を有することによって特徴付けられるがんを有すると特定された対象に投与することを含む、方法である。
実施形態194は、当該がんが原発腫瘍である、実施形態191~193のいずれか一つに記載の方法である。
実施形態195は、当該がんが転移である、実施形態191~193のいずれか一つに記載の方法である。
実施形態196は、当該がんが非T細胞浸潤性腫瘍である、実施形態191~195のいずれか一つに記載の方法である。
実施形態197は、当該がんがT細胞浸潤性腫瘍である、実施形態191~195のいずれか一つに記載の方法である。
実施形態198は、がんを有する対象において転移の発生のリスクを低減またはさらなる転移の発生のリスクを低減させる方法であって、該がんが、がん細胞であってその表面に存在するMETまたはMETのエピトープを有するがん細胞の集団を有することによって特徴付けられ、治療有効量の実施形態1~94のいずれか一つの医薬組成物または実施形態96~189のいずれか一つのABPCを、上記がん細胞の集団を有することによって特徴付けられるがんを有すると特定された対象に投与することを含む、方法である。
実施形態199は、当該がんが、非T細胞浸潤性腫瘍である、実施形態198に記載の方法である。
実施形態200は、当該がんが、T細胞浸潤性腫瘍である、実施形態198に記載の方法である。
本発明は、以下の実施例においてさらに記載されており、これら実施例は、特許請求の範囲に記載の本発明の範囲を限定するものではない。
実施例1.METバインダーの生成、およびpH結合依存性の操作
METに特異的であるpH操作されたABPCは、二つの方法を使用して生成される。第一の方法では、公開されている、METに対するモノクローナル抗体を、付加的変異導入用の出発鋳型として使用するものであり、当該変異は、METへのpH依存性結合を操作することを可能にし、そしてi)コンジュゲートされた毒素のエンドリソソーム蓄積の強化、ならびにii)細胞表面へのMETのリサイクリングを強化させる。第二の方法は、未感作ライブラリまたは既定のCDR組成を有するライブラリに由来する抗体ディスプレイ法、およびMETに特異的なpH操作されたABPCの選択用に設計された条件下でのスクリーニングを介した、METに特異的な新規ABPCの発見を含む。いずれの場合でもヒスチジン残基が、pH依存性結合タンパク質を操作する際に重要な役割を果たしている。
ヒスチジン残基は、そのpKaが6.0であるため、pHが6.5未満では、少なくとも部分的にプロトン化される。したがって抗原結合ドメイン中のヒスチジン側鎖が、その抗原との静電結合相互作用に関与する場合、6.5以下のpHで正電荷をもつようになり始める。これにより、6.5を下回るpHでは、抗原エピトープの対応する電荷、および抗原エピトープとの相互作用に応じて、相互作用の結合親和性を弱まるか、または強化されるかのいずれかであり得る。ゆえに抗体または他のバインダーのライブラリ(例えば、scFvライブラリ)中の抗体相補性決定領域(CDR)へのヒスチジンの系統的な導入を使用して、より低いpH値での抗原結合ドメインの抗原との相互作用に影響を及ぼすこととなる置換を特定することができる。したがって第一の方法では、公開されているモノクローナル抗体の可変領域配列のヒスチジンスキャニングを行ってpH依存性の変異体を特定することを含む。
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性結合を操作するための鋳型として使用することができる[Wang J et al(2017)ABBV-399,a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors,Irrespective of MET Pathway Dependence,Clin Cancer Res,23:992-1000]。簡潔に述べると、抗体配列のサブセットについて、各鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest(DIANE publishing)により記載された方法およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を操作するために、重鎖および/または軽鎖のCDR内の個々のアミノ酸残基が、一度に一つ、ヒスチジンで系統的に置換される。出発CDR残基がヒスチジンである場合には、アラニンに変異される。重鎖/軽鎖のCDR中にただ一つのヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を用いて、a)一つの重鎖または軽鎖の配列変異体、およびb)対応する出発ABPC(例えば、出発MET結合モノクローナル抗体)の軽鎖または重鎖それぞれを用いて、Expi293細胞の同時トランスフェクションによって生成する。しばらくタンパク質を発現させたあと、細胞培養上清を収集し、定量して、変異体のpH依存性を、バイオレイヤーインターフェロメトリ(BLI)または当技術分野に公知の他の方法を使用して評価する。簡潔に述べると、細胞培養上清は、50μg/mLの抗体発現レベルに正規化され、抗ヒトFcセンサー(Forte Bio社)上で捕捉される。1Xキネティクス緩衝液(kinetics buffer)(Forte Bio社)を使用してベースラインが確立され、センサーは、pH7.4で300秒間、1X PBS中100nMのMETと結合されて、結合曲線が生成される。解離相では、センサー上の抗体-抗原複合体を、pH5.5またはpH7.4のいずれかで300~500秒間、1X PBSに曝露する。結合相および解離相の曲線は、pH5.5およびpH7.4で、出発ABPC抗体およびそれぞれの対応する抗体変異体について検証され、以下の二つの基準についての情報を得る:a)出発ABPCと比較した、ヒスチジン置換またはアラニン置換に起因したpH5.5での解離の強化(すなわち、koff値がより高い)、およびb)抗体変異体自体、および出発ABPCでの場合の、pH5.5と比較した、pH7.4での解離の低下(すなわち、koff値がより低い)。さらなる分析のために、pH5.5での解離の強化またはpH7.4での解離の低下のいずれかまたは両方を示す変異体を選択する。また、一部のヒスチジンおよびアラニンの変異は、MET結合を消失させる一方で、他の変異は許容されるものであり、MET結合動態を、ほとんど変化させない(例えば、KDまたは解離速度の変化が1倍未満)または全く変化させないことにも留意される。特にヒスチジンは、正電荷をもつ大きいアミノ酸であるため、これら変化を伴わないヒスチジン変異体およびアラニン変異体は、広範囲の変異を許容し得、また異なる配列であるが類似の結合特性を有する抗体、さもなければ明白ではない指定を有する抗体をもたらす可能性がある位置として注目される。さらなる分析のために選択される変異体は、より大規模に発現され、プロテインAアフィニティクロマトグラフィを使用して精製される。精製された出発ABPCおよび変異体抗体の結合動態(konおよびkoff)を、Biacore(GE Healthcare社)を用いてpH5.5およびpH7.4で測定する。抗体の解離速度の比(pH7.4のkoffをpH5.5のkoffで除算)がまた、pH依存性結合の定量的評価として使用され、同様に、解離定数KDは、pH5.5およびpH7.4の両方で、koffをkonで除算したものとして計算し、また抗体の解離定数の比(pH7.4のKDをpH5.5のKDで除算)も、pH依存性結合の定量的評価として使用する。組み合わせ置換についてのさらなる評価のために、解離速度の比が出発ABPCよりも低い抗体、および/または解離定数の比が出発ABPCよりも低い抗体が選択される。好ましいヒスチジンおよび/またはアラニンのアミノ酸位置を組み合わせて、pH依存性を高めることもできる。これは、例えば所与の重鎖または軽鎖上で、個々にpH依存性を向上させるヒスチジン置換および/もしくはアラニン置換を組み合わせ的にもしくは合理的に組み合わせることによって、例えば改変された重鎖および軽鎖を組み合わせ的にもしくは合理的に組み合わせて、ヒスチジン置換および/もしくはアラニン置換を両鎖上に存在させることによって、またはそれらの組み合わせによって、行うことができる。そのような組み合わせ変異体を作製して、本明細書に記載される方法およびプロトコル、または当技術分野に公知の他の方法およびプロトコルを使用して、そのpH依存性の差分について試験/分析する。さらなる分析のための候補として、最も低い解離速度の比および/または解離定数の比を有する抗体変異体を選択する(以下、「METに特異的なpH操作されたABPC」と称する)。
METに特異的なpH操作されたABPCを選択するための第二の方法では、ライブラリをスクリーニングして、METに特異的な新規pH依存性ABPCを特定すること、または本明細書に記載されるpH依存性結合を操作するための鋳型としての役割を果たし得るABPCを特定することのいずれかを含む。これらの選択には、二つのタイプのライブラリ、すなわち、未感作ファージ/酵母ディスプレイ抗体ライブラリ(例えば、Fab、scFv、VHH、VL、または当技術分野で公知の他のライブラリ)、またはCDRが、アミノ酸残基のサブセットを発現するように変異されているファージ/酵母ディスプレイライブラリ、を使用することができる。ライブラリは、pH5.0では弱く結合し(例えば、ビーズから溶出される)、かつpH7.4では強く結合する(例えば、ビーズに結合される)変異体に対する正の選択を用いた、当技術分野に公知の方法を使用して、可溶性組換えMET細胞外ドメインに対してスクリーニングされる。三ラウンドの選択が実施される。最終ラウンドのバインダーを、ヒトMETおよびカニクイザルMETおよびマウスMETへの結合について、ELISAを使用して、またはフローサイトメトリー分析における平均蛍光強度を介して、スクリーニングする。カニクイザルまたはマウスの交差反応性を伴うバインダーをより多く所望する場合、代わりに最終選択ラウンドは、カニクイザルMETまたはマウスMETに対して実施することができる。選択された結合タンパク質は、哺乳動物発現ベクターにサブクローニングされ、Expi293細胞において完全IgGタンパク質またはFc融合物のいずれかとして発現される。BLI解析を、pH依存性バインダー変異体の選択のために本明細書に記載のように実施し、Biacoreを使用して確認する。
実施例2.METに特異的な対照ABPCと比較した、METへのpH依存性結合、METのpH依存性放出、MET+細胞におけるエンドリソソーム送達の強化、およびMETに特異的なpH操作されたABPCへの曝露後のMET+細胞におけるMET抗原密度の増加、に関するインビトロ実証。
本明細書で検討されるように、METに特異的なpH操作されたABPCは、酸性pH(例えば、pH5.0、pH5.5)でのMET結合の低下、より高いpH(例えば、pH7.4)での結合の強化という望ましい特性を呈するが、これにより、生理的条件下でのエンドリソソームでのそれらの蓄積が強化される。
細胞上のMETへのpH依存性結合
METに特異的なpH操作されたABPCが、中性pHで細胞表面のMETに結合することを実証するために、細胞表面結合アッセイを行う。MET+であるヒト細胞のパネルを構築する(例えば、Hs 746T ATCC社 カタログ番号HTB-135、NCI-H441 ATCC社 カタログ番号HTB-174、NCI-H820 ATCC社 カタログ番号HTB-181)。所与の細胞株に関する遺伝子発現(例えば、MET)の特定および定量の方法は、当技術分野で公知であり、例えばCancer Cell Line Encyclopedia(CCLE; https://portals.broadinstitute.org/ccle)を閲覧し、腫瘍細胞株中の所与の遺伝子の発現レベルおよび/または変異状態を確認すること、rtPCR、マイクロアレイ、またはRNA-Seq分析、または当技術分野に公知の抗体(例えば、テリソツズマブまたはSignaling Technology社のMet(D1C2)XP Rabbit mAb、カタログ番号8198、またはMETに対しては、R&D Systems社のHuman HGFR/c-MET Antibody Clone#95106、カタログ番号MAB3582)を用いた細胞染色が挙げられる。細胞を、150μLのpH7.4培養培地中で、1ウェルあたりおよそ5~10,000個で播種し、以下の抗体のうちの一つと共に、1pM~1μMのいくつかの用量(例えば、二倍希釈系列)で5分間、37℃でインキュベートする:METに特異的な公知の対照ABPC(例えば、抗体、テリソツズマブ、エミベツズマブ、hucMET27Gv1.3またはP3D12)、METに特異的なpH操作されたABPC、および適切な陰性アイソタイプ対照mAb(例えば、Biolegend社の精製ヒトIgG1アイソタイプ対照組み換え抗体、カタログ番号403501)。実験を開始する前に、当技術分野で公知の方法を使用して、すべての抗体の結合特性が検証される。5分間のインキュベーション後、細胞は、4%ホルムアルデヒドで固定され(室温で20分)、適切なフルオロフォア標識二次抗体(例えば、ThermoFisher社のマウス抗ヒトIgG1 Fc二次抗体、Alexa Fluor 488、カタログ番号A-10631)と共に60分間インキュベートされる。非結合試薬は一連のPBS洗浄で洗浄され、細胞パネルは共焦点顕微鏡を使用して撮像される。画像の分析により、METに特異的な公知の対照ABPC、ならびにMETに特異的なpH操作されたABPCが結合した細胞の表面に著しい蛍光を観察することができるが、アイソタイプ陰性対照については、表面結合はほとんど観察することができない。表面結合に対するpHの影響を抜粋するために、同じ実験を2回繰り返すが、一次抗体のインキュベーションは順に低くなるpH(例えば、pH6.5および5.5および5.0)で実施する。取得された共焦点顕微鏡の画像分析から、アイソタイプ陰性対照を除き、試験されたすべてのmAbと結合した細胞の表面に著しい蛍光が示され得る。そしてこの蛍光は、pHが減少するにつれて、METに特異的なpH操作されたABPCについては減少する。あるいは、細胞は、当技術分野で公知の方法を使用して、フローサイトメトリーにより平均蛍光強度が分析される。分析された抗体の中性pHでの細胞上での解離定数KDは、当技術分野で公知の非線形回帰法(例えば、スキャッチャードプロット)によって決定される。まとめると、これら結果は、pH操作プロセスによって、METに特異的なpH操作されたABPCであって、その結合特性がpH依存性であり、かつ、より酸性のpHと比較して中性pHでより効果的に結合する、METに特異的なpH操作されたABPCの作製がもたらされるということを示し得る。METに特異的なpH操作されたABPCのpH依存性を評価する他の方法は当技術分野で公知であり、例えば、フローサイトメトリーを使用してABPC表面結合を測定することが挙げられる。
細胞上のMETのpH依存性放出
METに特異的なpH操作されたABPCが、中性pHでの結合後に低pHでMETを放出することができることを実証するために、上述の細胞表面結合アッセイの変化形を、当技術分野に公知の方法(例えば、Gera N.(2012)PLoS ONE 7(11): e48928に概略される)を用いて実施する。簡潔には、適切なMET+細胞株(継代数25未満)を収穫し、ウェル当たり50,000個の細胞をU底96ウェルマイクロプレートに播種する。以下の三つの条件を検証する:pH7.4での結合と二次染色、pH5.0での結合と二次染色、およびpH7.4での結合と、その後のpH5.0での30分間の放出と、pH7.4での二次染色。METに特異的なpH操作されたABPCおよびMETに特異的な対照ABPCの両方を検証する。細胞は、検証される条件に応じて、pH7.4または5.0のいずれかで、200μLのFACS緩衝液(3%ウシ胎児血清含有1×PBS)で2回洗浄される。精製されたタンパク質サンプルを、適切なpHのFACS緩衝液に希釈し、細胞に添加して、氷上で1時間結合させる。一次抗体とインキュベーションした後、pH7.4条件とpH5.0条件を前述のように2回洗浄し、次いで1:50希釈された100μlの二次ラット抗ヒトFc AF488(BioLegend社 410706)もしくは他の適切な抗体、または1:50希釈された抗Myc-TagマウスmAb-AF488(Cell Signaling Technologies社 2279S)を、適切なpHのFACS緩衝液中に加え、氷上で30分間インキュベートする。pH5.0の放出条件は、FACS緩衝液pH7.4で2回洗浄され、次いで100μlのFACS緩衝液pH5.0中に再懸濁され、30分間氷上でインキュベートされる。その後、他の条件について記載されるように、FACS緩衝液pH7.4中で二次染色される。プレートを、前述のように2回洗浄し、適切なFACS緩衝液中の1%パラホルムアルデヒドに再懸濁して、フローサイトメトリー分析のために固定する。すべての条件は、フローサイトメーター(Accuri C6、BD Biosciences社)上で読み取られる。結合は、二次のみと比較した、FLlシグナル(平均蛍光強度として)のシフトとして観察される。データを分析すると、METに特異的なpH操作されたABPCおよびMETに特異的な対照ABPCの両方がMET+細胞の表面に中性pHで効果的に結合するが、METに特異的なpH操作されたABPCがpH5.0では結合が乏しいことが判断でき、同様に、METに特異的なpH操作されたABPCがpH7.4では効果的に結合するがその後pH5.0ではMETを放出/結合解除することが判断できる。
METに特異的な対照ABPCと比較した、METに特異的なpH操作されたABPCのMET+細胞におけるエンドリソソーム送達の強化(pHrodo)
METに特異的なABPCが細胞取り込み後にエンドリソソームでの局在化を行うことを検証および実証するために、当技術分野に公知の方法(例えば、Mahmutefendic et al.,Int.J.Biochem.Cell Bio.,2011を)を用いて細胞内移行アッセイを行う。簡潔に述べると、本明細書に記載されるように、METを高度に発現するヒト細胞のパネルを、当技術分野に公知の方法を使用して構築する。細胞は、播種し、PBSで3回洗浄して、METに特異的な公知の対照ABPC(例えば、本明細書に記載のもの)、METに特異的なpH操作されたABPC、および適切な陰性アイソタイプ対照mAb(例えば、本明細書に記載のもの)を2マイクログラム/ミリリットルの濃度で添加して、中性pHで培地中で37℃で60分間インキュベートする。細胞のサブセットにおいて、抗体の細胞内移行およびエンドソームでの局在化の検証は、当技術分野で公知の方法を使用して実施される。例えば細胞は、本明細書に記載されるように4%ホルムアルデヒド中で固定され、TWEEN20または当技術分野で公知の他の方法を使用して透過処理され(Jamur MC et al(2010)Permeabilization of cell membranes,Methods Mol Biol.588:63-6)、さらにエンドソームマーカー、例えば蛍光RAB11抗体(RAB11抗体、Alexa Fluor 488、3H18L5、ABfinity(商標)ウサギモノクローナル抗体)、で染色され、適切な蛍光標識抗ヒト二次抗体(例えば、本明細書に記載される)で染色され、そして本明細書に記載されるように、共焦点蛍光顕微鏡を使用して撮像される。共焦点画像の分析を使用して、METに特異的なpH操作されたABPC、ならびにMETに特異的な対照ABPCの両方が細胞内移行されて、エンドリソソームに蓄積されることを示すことができる。
METに特異的なpH操作されたABPCが、METに特異的な対照ABPCと比較して増強されたエンドリソソーム蓄積を行うことを実証するために、METに特異的な公知の対照ABPC(例えば、本明細書に記載のような)およびMETに特異的なpH操作されたABPCの両方を使用して、pHrodo系の細胞内移行アッセイを実施する。アッセイは、pHrodo(商標)iFL(P36014、ThermoFisher社)、これは色素であって、その蛍光が、pHが減少するにつれて増加するために中性pHでの細胞外の蛍光レベルはエンドリソソームの酸性pH環境内の蛍光レベルよりも低くなるものである色素を、使用する。簡潔に述べると、適切なMET+細胞株(継代数25回未満)が、その推奨培地(例えば、セルバンクまたはセルバンクデータベースATCC社、DSMZ社、またはExPASy Cellosaurusによる)に懸濁され、1ウェル当たり1mL、2,000,000細胞/mLの密度で24ウェルプレートに播種される。細胞を氷上に維持しながら、(製造業者の指示に従って調製された)1mLの2×pHrodo iFL標識抗体を各ウェルに添加し、ウェルを5回ピペッティング/混合し、プレートを氷上の遮光環境で45分間インキュベートする。同一であるが別個のプレートも、氷上でインキュベートされる。これは、非細胞内移行の陰性対照を意味する。このインキュベーションの後、実験プレートを37℃のインキュベーターに移し、陰性対照プレートは氷上に保持して細胞内移行を遅延させるか、または妨害する。サンプルは、指定された時点で採取され、細胞内移行の経時変化をさせる。サンプルは、U底の96ウェルプレートに播種され、氷冷されたFACS緩衝液を200μL/ウェルで添加することによって細胞内移行をクエンチする。プレートを2000xgで2分間スピンダウンし、200μLの氷冷FACS緩衝液中に再懸濁させ、再びスピンダウンして、FACS緩衝液中で2回めの再懸濁を行う。最後にサンプルは、pHrodo iFL赤色色素の励起および発光の最大値と合致する励起波長および発光波長(それぞれ、566nmおよび590nm)を使用して、細胞性のpHrodo蛍光の読み取り値を得るためにフローサイトメーターにロードされる。フローサイトメトリー実験およびデータ分析の完了の結果、METに特異的なpH操作されたABPCで処理された細胞は、METに特異的な公知の対照ABPCと比較した場合の、より高いpHrodo iFLシグナルを有し、これはMETに特異的なpH操作されたABPCが、METに特異的な対照ABPCと比較して、エンドリソソーム蓄積が増強されたことを示すということが観察できる。
あるいは、METに特異的なpH操作されたABPCが、METに特異的な対照ABPCと比較して、エンドリソソーム蓄積が増強されることを実証するために、上述の実験の変化形を実施する。MET+細胞は、播種し、PBSで3回洗浄して、METに特異的なpH操作されたABPCまたはMETに特異的な対照ABPCのいずれかを2μg/mLの濃度で添加して、中性pHで培地中で37℃で60分間インキュベートする。インキュベーションの後、細胞をPBSで3回洗浄し、固定および透過処理して、後期エンドソームマーカーおよびリソソームに結合する適切に選択された抗体のパネル(例えば、RAB7、およびLAMP1;Cell Signaling Technology社、Endosomal Marker Antibody Sampler Kit 番号12666;AbCam社、抗LAMP2抗体[GL2A7]、ab13524)を用いて染色する。一次抗体の染色後、蛍光標識された二次抗体(例えば、ヤギ抗ヒトIgG(H&L)二次抗体(Alexa Fluor 647)、カタログ番号A-21445、およびAbcam社ヤギ抗ウサギIgG H&L(Alexa Fluor 488)、カタログ番号ab150077)の適切な混合物で細胞を染色し、共焦点蛍光顕微鏡を使用して撮像し、MET特異的抗体およびエンドソームマーカーに由来するシグナルの共局在領域を可視化して定量する。データを分析すると、METに特異的な対照ABPCで処理したウェルと比較し、METに特異的なpH操作されたABPCで処理したウェルでは、エンドリソソーム特異的抗体シグナルとMET特異的抗体シグナルの共局在が増加していることが明らかになり得、したがって、METに特異的なpH操作されたABPCが、METに特異的な対照ABPCと比較してエンドリソソーム蓄積を増強することを実証できる。
METに特異的な対照ABPCと比較して、METに特異的なpH操作されたABPCへの曝露後のMET+細胞における、MET抗原密度の増加
METに特異的なpH操作されたABPCによる細胞の処理が、METに特異的なpH操作されたABPCに曝露された細胞の表面のMETのレベルの検出可能な減少をもたらさないこと、または、上記処理が、METに特異的なpH操作されたABPCに曝露された細胞の表面のMETのレベルの減少を、METに特異的な対照ABPCと比較してそれほど生じさせないことを実証するために、フローサイトメトリーを使用して抗原密度試験を行う。簡潔に述べると、100μLの培地中、1ウェル当たり、METを発現する4.0×10^5個の細胞を、96ウェルプレートに播種する。細胞は、i)METに特異的なpH操作されたABPC、ii)METに特異的な第一の対照ABPC、iii)適切なアイソタイプ対照、およびiv)未処理対照を、1pM~1μMの用量漸増で処理する。細胞を、37℃で2時間インキュベートし、その時点で全ての細胞を、METに特異的な第一の対照ABPCまたはMETに特異的なpH操作されたABPCのいずれとも異なるエピトープ(例えば細胞に対する競合的結合試験によって、判断されるような)を有する、METに特異的であるフルオロフォア標識された第二の対照ABPC(例えば、本明細書に記載のような)の200nMとともに、30分間、4℃でインキュベートする。この30分間のインキュベーションの後、全ての細胞の平均蛍光強度(MFI)を、当業者に公知の方法を使用し、例えばフローサイトメトリーを使用して、読み取る。並行して、MFIの関数として処理細胞の表面のMETの存在を定量するために使用することができる定量的標準曲線を、市販の定量キット(例えば、BD Biosciences社PE フィコエリスリン蛍光定量キット、カタログ番号340495)を使用して作成し、その際、定量的標準曲線は、製造業者の指示に従って作成する。細胞表面のMETの絶対数を決定する他の方法は、当技術分野において公知であり、例えば、放射性同位体標識試薬の使用が挙げられる。データの分析により、METに特異的な対照ABPCで処理された細胞が、その表面のMETレベルを低下させる一方で、METに特異的なpH操作されたABPCで処理された細胞は、アイソタイプ対照および未処理対照の両方と比較して、有意に小さい低下、または全く低下しない、少なくとも一つの抗体濃度が明らかとなり得る。
実施例3.細胞傷害性薬剤との、METに特異的なpH操作されたABPCおよび対照ABPCのコンジュゲート
抗原結合タンパク質構築物コンジュゲート(ADC)は、バリン-シトルリン(vc)リンカーを介して、モノメチルアウリスタチンE(MMAE)に本明細書に記載のMET結合IgG(以下、MET-IgG)を結合させることにより作製する(以下、MET-IgG-DC)。抗原結合タンパク質構築物のvcMMAEとのコンジュゲーションは、MET-IgGの部分的な還元、続いてマレイミドカプロイル-Val-Cit-PABC-MMAE(vcMMAE)との反応から始まる。MET-IgG(20mg/mL)は、TCEPの添加(TCEP:mAbのモル当量は2:1である)と、それに続いて0℃で一晩インキュベーションすることによって部分的に還元される。次いで、還元反応を20℃に加温する。すべてのチオールをコンジュゲートするために、vcMMAEを、最終的なvcMMAE:還元されたCysのモル比が1:15となるように添加する。コンジュゲート反応は、10%v/vのDMSOの存在下で行われ、20℃で60分間進行させた。
コンジュゲーション反応の後、過剰な遊離N(アセチル)-システイン(vcMMAE電荷に対して2当量)を添加して、未反応のvcMMAEをクエンチして、Cys-Val-Cit-MMAE付加物を生成する。Cysクエンチ反応を、20℃で約30分間進行させる。Cysクエンチ反応混合物を、以下により精製する。上記のコンジュゲーション方法を使用して、マレイミドカプロイルモノメチルオーリスタチンF(mcMMAF)を抗原結合タンパク質構築物にコンジュゲートさせることもできる。
MET-IgG-DCを、バッチ精製法を使用して精製する。反応混合物を、適切な量の水で洗浄されたBu-HIC樹脂(ToyoPearl;Tosoh Biosciences社)で処理する。すなわち、7重量の樹脂を混合物に添加する。樹脂/反応混合物を適切な時間、攪拌し、分析的疎水性相互作用クロマトグラフィーによりモニタリングして、薬剤コンジュゲート生成物を取り出し、粗ポリプロピレンフィルターを通して濾過し、緩衝液(0.28M塩化ナトリウム、7mMリン酸カリウム、pH7)の2ベッド体積で洗浄する。一つにまとめた濾液およびリンス液を一つにまとめて、HIC HPLCにより生成物プロファイルの分析を行う。一つにまとめた濾液とリンス液を、限外濾過/透析濾過(UF/DF)により、10透析体積の15nMヒスチジン緩衝液で、15mMヒスチジン、pH6に緩衝液交換する。
類似のプロトコルを使用して、例えばSG3249およびSGD-1910などのDNA毒素をMET-IgGにコンジュゲートすることもできる(Tiberghien AC et al(2016)Design and Synthesis of Tesirine,a Clinical Antibody-Drug Conjugate Pyrrolobenzodiazepine Dimer Payload,ACS Med Chem Lett 7:983-987を参照)。簡潔に述べると、SG3249については、MET-IgG(15mg、100ナノモル)を、10mMホウ酸ナトリウム pH8.4、2.5mMのEDTAを含有する還元緩衝液の13.5mLに希釈し、最終抗体濃度は1.11mg/mLである。TCEPの10mM溶液を添加し(1.5モル当量/抗体、150ナノモル、15マイクロリットル)、還元混合物をインキュベーター中で1.5時間、+37℃で加熱する。室温まで冷却した後、SG3249をDMSO溶液として添加する(1.5mLのDMSO中、5モル当量/抗体、500ナノモル)。溶液を室温で1.25時間混合し、次に、N-アセチルシステイン(1マイクロモル、10mMで100マイクロリットル)を添加することによってコンジュゲーションをクエンチし、Superdex200PGをパックしたGE Healthcare社HiLoad(商標)26/600カラムを使用してAKTA(商標)Pure FPLCに注入し、2.6mL/分の滅菌濾過したリン酸緩衝食塩水(PBS)で溶出させる。MET-IgG-DC単量体ピークに対応する画分をプールし、15mLのAmicon Ultracell 50KDa MWCOスピンフィルターを使用して濃縮し、分析して、滅菌濾過する。280nmおよび330nm(SG3249特有)にて、MET-IgG-DCの還元サンプルに対し、水およびアセトニトリルのグラジエントで溶出させる、Phenomenex Aeris 3.6u XB-C18 150×2.1mmカラムを使用した島津ProminenceシステムでのUHPLC分析の結果、SG3249のいくつかの分子に結合した軽鎖および重鎖の混合物を示すことができ、それは抗体当たり1~4個のSG3249分子の薬剤抗体比(DAR)と一致する。Phenomenex Yarra 3u SEC-3000 300 mm x 4.60 mmカラムを使用した島津ProminenceシステムでのUHPLC分析は、MET-IgG-DCのサンプルに対して、280nmで、200mMのリン酸カリウム pH6.95、250mMの塩化カリウムおよび10%のイソプロパノール(v/v)を含有する滅菌濾過SEC緩衝液を用いて溶出するものであるが、不純物が検出されることなく、90%を超える単量体純度を示すことができる。UHPLC SEC分析により、30%を超える最終MET-IgG-DCの収率が確認され得る。
あるいは、リシン残基を介して抗体に毒素をコンジュゲートする方法が当技術分野で公知である(例えば、Catcott KC et al(2016)Microscale screening of antibody libraries as maytansinoid antibody-drug conjugates,MAbs 8:513-23を参照)。さらに、上記と同様の方法を使用して、薬剤および毒素を、例えばVh-Fcなど、ジスルフィド結合を有する非IgGフォーマットにコンジュゲートすることもできる。
実施例4.METに特異的な対照ABPC ADCと比較した、METに特異的なpH操作されたABPC ADCのMET+細胞における細胞傷害性の強化の実証
METに特異的なpH操作されたADC(例えば、pH操作されたMET-IgG-DC)と、METに特異的な対照ABPC ADC(例えば、対照ABPC MET-IgG-DC)の両方の細胞傷害活性を、本明細書に記載される方法を使用して選択された、様々な抗原密度を発現するMET+細胞株のパネル(例えば、本明細書に記載される)およびMET-細胞株(例えば、T-47D ATCC社 カタログ番号HTB-133)、ならびに任意で、当技術分野に公知の方法(例えば、Expi293(商標)発現系キット ThermoFisher社 カタログ番号: A14635)を使用してMETでトランスフェクトされたHEK293細胞などのトランスジェニックMETを発現する細胞に対して、別個に評価する。検証の目的のために、使用前に、すべての細胞株を、当技術分野に公知の方法、例えばqPCR、フローサイトメトリー、mRNA RPKM、および当技術分野に公知の抗MET抗体(例えば、本明細書に記載のような)を使用した抗体染色を使用して、METの発現について試験し、続いて、蛍光顕微鏡法、免疫組織化学、フローサイトメトリー、ELISA、または当技術分野に公知の他の方法を使用して染色の可視化を行う。化合物の細胞傷害性を評価するために、細胞を、150マイクロリットルの培養培地中、1ウェル当たり約10~40,000個で播種し、次いでアッセイ開始時に1pMから1μMの段階用量の化合物を用いて四つ組で処理する。細胞傷害性アッセイは、被験化合物の添加後96時間にわたって実施される。50マイクロリットルのレサズリン色素を、インキュベーションの最後の4~6時間の間に各ウェルに添加し、培養終了時に生細胞を評価する。色素の減少は、それぞれ535nmおよび590nmの励起波長および発光波長を使用した蛍光分光法によって判定される。分析については、処理細胞によるレサズリン減少の程度を、未処理の対照細胞と比較して、細胞傷害率を決定する。あるいは、WST-8キットを使用して、製造業者の指示に従って細胞傷害性を測定する(例えば、Dojindo Molecular Technologies社 カタログ番号CCK-8)。IC50は、最大半数殺傷が観察される濃度であり、当技術分野で公知の曲線あてはめ法を使用して計算される。データを分析することで、METに特異的なpH操作されたABPC ADCおよび対照ABPC ADCは、一つまたは複数のMET+ 細胞株に対して実質的に細胞毒性であるが、MET- 細胞に対して毒性が低いことが判断できる。また、METに特異的なpH操作されたADCは、METに特異的な対照ABPC ADCよりも、一つまたは複数のMET+細胞株に対し細胞傷害性が高いことも判断され得る。その根拠は、a)当該ADCが、一つまたは複数の濃度でより高い殺傷深度を示すこと、または、b)当該ADCが、より低いIC50を示すこと、または、c)当該ADCが、中性pH(本明細書に記載される)での細胞における当該ADCの解離定数KDを同一細胞におけるそれらのIC50で除算した比がより大きいことを示すこと、である。
さらに、METに特異的なABPCの細胞傷害活性を、二次的なADCアッセイで測定することができる。二次ADCアッセイは、当技術分野で公知である(例えば、Moradec社 カタログ番号αHFc-NC-MMAFおよびカタログ番号αHFc-CL-MMAEと、付随するメーカーの説明書)。簡潔には、METに特異的なABPCがMETに特異的なADCに置き換わることを除き、前段落と同様にアッセイを実施し、化合物の細胞毒性を評価するために、細胞を、150マイクロリットルの培地中に1ウェルあたり約10~40,000個で播種し、次いで、アッセイの開始時に、四つ組で、METに特異的な1pM~1μMのABPCを段階用量(培地中の最終濃度であり、これは培地中に混合物を添加する前に、Moradec社 カタログ番号αHFc-NC-MMAFの二次ADC試薬の、培地中の最終濃度、100nMと予め混合した後、37℃で30分間予めインキュベートした)で処理する。
METに特異的なpH操作されたADCおよびMETに特異的な対照ABPC ADCのコンジュゲート、ならびに二次ADCアッセイにおけるMETに特異的なABPCの細胞傷害活性は、以下のプロトコルを用い、細胞増殖アッセイによって追加的に測定する((Promega Corp.Technical Bulletin TB288; Mendoza et al.,Cancer Res.62:5485-5488,2002):
1.培地中、約104個の細胞(例えば、本明細書に記載されるMET+細胞)を含有する細胞培養物の100マイクロリットルのアリコートを、96ウェルの不透明壁プレートの各ウェルに沈着させる。
2.対照ウェルは、培地を含み、細胞を含まず調製される。
3.METに特異的なADCを、1pM~1uMの範囲の濃度で実験ウェルに加え、1~5日間インキュベートする。あるいは、二次ADCアッセイにおいて、100nMの二次ADC試薬(培地中の最終濃度、Moradec社 カタログ番号αHFc-NC-MMAF)および1pM~1uM(培地中の最終濃度)の範囲の濃度のMETに特異的なABPCを、37℃で30分間予め混合し、予めインキュベートした後、混合物を培地に添加し、1~5日間インキュベートする。
4.プレートは、約30分間、室温に平衡化される。
5.各ウェルに存在する細胞培養培地の体積と等しい体積のCellTiter-Glo試薬を添加する。
6.内容物を、オービタルシェーカー上で2分間混合して、細胞溶解を誘導する。
7.プレートを室温で10分間インキュベートし、発光シグナルを安定化させる。
8.発光は、RLU=相対発光単位として記録され、グラフで報告される。
実施例5.METに特異的な対照ABPC ADCと比較した、METに特異的なpH操作されたABPC ADCのMET+細胞における毒素放出の強化の実証
METに特異的なpH操作されたADC(例えば、pH操作されたMET-IgG-DC)はまた、METに特異的な対照ABPC ADC(例えば、対照ABPC MET-IgG-DC)と比較して、MET+細胞における毒素放出の増加も実証し得る。本明細書に記載されるようなMETに特異的なpH操作されたABPC ADCおよび対照ABPC ADCを用いてMET+細胞を処理した後、LC-MS/MS法を使用して、処理されたMET+細胞における非コンジュゲート(すなわち遊離した)MMAEを定量する(Singh,A.P.and Shah,D.K.Drug Metabolism and Disposition 45.11(2017): 1120-1132)。電気スプレーインターフェースおよびトリプル四重極質量分析計を備えたLC-MS/MSシステムを使用する。MMAEの検出について、XBridge BEHアミドカラム(Waters社、マサチューセッツ州ミルフォード)を、移動相Aを水(5mMのギ酸アンモニウムと0.1%のギ酸を含む)、および移動相Bを95:5のアセトニトリル/水(0.1%のギ酸と1mMのギ酸アンモニウムを含む)で使用し、40℃で0.25mL/分の流速でグラジエントを使用する。クロマトグラフィー実行の合計持続時間は12分であり、2つのMRMスキャン(718.5/686.5および718.5/152.1amu)がモニタリングされる。内部標準として、重水素化(d8)MMAE(MCE MedChem Express社、ニュージャージー州モンマスジャンクション)を使用する。最初に、生体サンプル中の非コンジュゲートMMAEを定量するための方程式は、各薬剤標準のピーク面積を、内部標準で取得されたピーク面積で除算することによって導出される。次いで得られたピーク面積の比を、標準濃度の関数としてプロットする。データ点は線形回帰を使用して曲線にあてはめる。作成された標準曲線の予測能力を評価するために、3つのQCサンプルが標準曲線の下方範囲、中範囲、および上方範囲に含まれる。次いで、得られた標準曲線を使用して、生体サンプルにおいて観察されたMMAEの濃度を推定する。MMAE濃度を測定するために、処理細胞サンプルを沈殿させ、新鮮な培地中で再構成させて、最終濃度を25万細胞/100μLとする。サンプルにd8-MMAE(1ng/mL)を混ぜた後、2倍体積の氷冷メタノールの添加により細胞溶解を実施して、その後に、-20℃で45分間の凍結融解サイクルを行う。最終細胞溶解物は、4℃で15分間、13,000rpmでサンプルを遠心分離し、続いて上清を収集することによって取得される。標準およびQCサンプルの調製のために、新鮮な細胞懸濁液(25万/100μl)に、既知の濃度のMMAEおよび内部標準(d8-MMAE)を混ぜ、その後上記の細胞溶解物と同様の手順を行う。次いで、得られた細胞溶解物を蒸発させ、移動相Bで再構成させた後にLC-MS/MSに注入する。METに特異的なpH操作されたADCで処理されたMET+細胞の溶解物中の非コンジュゲートMMAEの濃度は、METに特異的な対照ABPC ADCで処理されたMET+細胞中のものの濃度よりも高いことが観察される。
チューブリン阻害毒素については、細胞生存率および細胞周期のモニタリングによって毒素放出も評価される。約2.0x10^5のMET+細胞を、96ウェル平底プレートに播種し、本明細書に記載されるMETに特異的なpH操作されたABPC ADCおよび対照ABPC ADCを用いて処理する。処理後、細胞を96-丸底プレートに移し、プレートを400rcfで2分間遠心分離して、上清をデカントする。上清をデカントした細胞を、Live/Dead eFluor 660で染色する。次いで細胞を遠心分離し、FACS緩衝液(2%のFBSを含むPBS)で洗浄し、その後、細胞周期分布をBD Cycletest(商標)Plus DNAキット(カタログ番号340242)で分析する。簡潔に述べると、細胞を76ulの溶液A中に再懸濁し、室温で10分間インキュベートする。次いで、61μLの溶液Bを添加し、細胞を室温でさらに10分間インキュベートする。最後に、61μLの冷たい溶液Cを加え、細胞を室温で再び10分間インキュベートする。最後のインキュベーション工程の直後に、細胞を、10μL/秒の流速でフローサイトメトリー(洗浄なし)により分析する。METに特異的な対照ABPC ADCと比較し、METに特異的なpH操作されたADCへの曝露で、G2/M期の停止の増加が観察できる。
DNA損傷性の毒素(例えば、ピロロベンゾジアゼピンまたは“PBD”)については、DNA損傷は、リン酸化ヒストンH2AX(γH2AX)を測定することによって評価される。H2AXは通常、DNA中の二本鎖切断に応答してリン酸化されるが、例えばPBDまたはシスプラチンなどのDNA架橋毒素を用いた処理の結果として、γH2AXのレベル上昇が観察される場合もある(Huang,X.et al.2004,Cytometry Part A 58A,99-110)。MET+細胞を、本明細書に記載のMETに特異的なpH操作されたABPC ADCおよび対照ABPC ADCで処理する。処理後、細胞をPBSですすぎ、次いで1%のメタノールフリーのホルムアルデヒド(Polysciences社、ペンシルバニア州ワーリントン)のPBS懸濁液中、0℃で15分間固定する。細胞を70%エタノール中で少なくとも2時間、-20℃で再懸濁させる。次いで細胞をPBS中で2回洗浄し、BSA(Sigma社)の1%(w/v)のPBS溶液中、0.2%Triton X-100(Sigma社)に30分間懸濁して、非特異的Ab結合を抑制する。細胞を再び遠心分離し(200g、5分)、細胞沈殿物を、1:800希釈された抗ヒストンγH2AXポリクローナルAb(Trevigen社、メリーランド州ゲイザースバーグ)を含有する1% BSAの100μL中に懸濁させる。次いで細胞を4℃で一晩インキュベートし、PBSで2回洗浄し、ブタ抗ウサギ免疫グロブリン(DAKO社、カリフォルニア州カーピンテリア)の1:30希釈されたFITCコンジュゲートF(ab’)2断片の100μLに、暗所、室温で30分間再懸濁する。次いで細胞を室温で20分間、100μg/mLのDNase-フリーのRNase A(Sigma社)を含有するPBSに溶解させた5μg/mLのPI(Molecular Probes社、オレゴン州ユージーン)を用いて対比染色する。FITC γH2AXシグナルの細胞蛍光およびPI対比染色を、当技術分野で公知の方法を使用してフローサイトメトリーを使用して測定する。(総DNA含量に基づき)同ステージの細胞周期内にある細胞を比較する場合、未処理MET+細胞(ベースラインとして使用)と比較し、処理されたMET+細胞は、FITC γH2AXシグナルが増加していることが観察され得る。さらに、METに特異的なpH操作されたADCで処理したMET+細胞は、METに特異的な対照ABPC ADCで処理した細胞と比較して、ベースラインよりも高いレベルのγH2AXの増加を有することが観察できる。γH2AXアッセイに加えて、Cometアッセイ(Chandna,S.(2004)Cytometry 61A,127-133)を用いてDNA架橋をもっと直接的に評価することもできる。
さらに本明細書に開示されるように、pH操作されたABPCおよび対照ABPCは、一次コンジュゲートADCを使用する代わりに二次的ADCアッセイを実行することによって、直接的なコンジュゲーションを伴わずに本実施例の方法を使用して分析することもできる。
実施例6.METに特異的な対照ABPCと比較した、METに特異的なpH操作されたABPCの半減期の減少の実証
本発明によって記載されるMETに特異的なpH操作されたABPCの驚くべき態様の1つは、エンドソームまたはリソソーム内のMETからのABPCの解離の増加を促進し、METに特異的な対照ABPCまたはMETに特異的ではないABPCと比較した場合の、血中半減期の減少をもたらす能力であると言える。この血中半減期の減少は、METに結合されたときの細胞内移行の強化に起因する、循環系からのMETに特異的なpH操作されたABPCのクリアランス頻度の向上が原因であり、これはMETに特異的な非結合のpH操作されたABPCの血清中濃度の減少を通じて経時的に観察することができる。これらの特性を実証するために、マウスおよび/またはサルにおける一連の動物試験を、当技術分野に公知の方法(例えば、Gupta,P.,et al.(2016),mAbs,8:5,991-997)を使用して、METに特異的なpH操作されたABPCおよびMETに特異的な対照ABPCを使用して実施する。簡潔に述べると、マウス研究を実施するために、METに特異的なpH操作されたABPC、またはMETに特異的な対照ABPCのいずれかの単回静脈内ボーラス(例えば、5mg/kg)を、MET+細胞株(例えば、本明細書に記載される)を異種移植されたNOD SCIDマウス(例えば、ジャクソンラボラトリー(Jackson Labs)NOD.CB17-Prkdcscid/J ストック番号:001303)の二つの群に尾静脈を介して投与する。異種移植マウスは、インビトロで1~500万個のMET+細胞を増殖させ、マウスの右脇腹に皮下接種することにより作製される。腫瘍は、300mm3で大きさを一致させる。腫瘍の長さ(L)および幅(W)の測定値は、電子キャリパーを介して取得され、体積は、以下の方程式に従って計算される: V=L×W^2/2。血液サンプルは、以下の各時点で、各群から眼窩後方出血を介して収集される:15分、30分、1時間、8時間、24時間、および3日、7日、10日、14日、17日、21日、および28日。サンプルを処理して血清を集め、抗体濃度を、ELISAまたは当技術分野に公知の他の方法(例えば、PACアッセイまたはMACアッセイ;Fischer,S.K.et al.(2012),mAbs,4:5,623-631、例えば抗ヒトIgG抗体 Jackson ImmunoResearch Labs社、カタログ番号109-006-006を利用する)を使用して定量する。METに特異的なpH操作されたABPCおよびMETに特異的な対照ABPCの抗体濃度を時間の関数としてプロットする。データの分析により、METに特異的なpH操作されたABPCが、METに特異的な対照ABPCと比較して有意に短い血中半減期を有することが観察され得る。その結果、METに特異的なpH操作されたABPCがもつpH依存性が、同じ抗原に結合するがそれらのpH依存性は異なる他の類似したバインダー(例えば、METに特異的な対照ABPC)と比較してエンドソームまたはリソソーム内での解離の強化を促進することができることが実証される。METに特異的なpH操作されたABPCおよび対照ABPCが、METのマウスホモログと交差反応性である場合には、異種移植されていないマウスで同様の実験を繰り返してもよい。
任意で、METに特異的なpH操作されたABPCおよび対照ABPCが、METのカニクイザルホモログと交差反応性である場合には、サル(例えば、カニクイザル)に対して類似の実験を実施してもよい。同数のオスおよびメスのサル(例えば、それぞれn=1~2)に、伏在静脈注射を介して例えば1mg/kgの投与量で、METに特異的なpH操作されたABPCまたはMETに特異的な対照ABPCのいずれかをボーラス投与する。あるいは、いくつかの異なる投与量のMET結合タンパク質を、数匹のサルの群にわたり投与する。血液サンプルは上述したものと類似した間隔で末梢静脈または大腿静脈を介して採取され、当技術分野に公知の方法(例えば、ELISA)を使用して、METに特異的なpH操作されたABPC、またはMETに特異的な対照ABPCのいずれかの存在について分析される。データの分析により、METに特異的なpH操作されたABPCが、METに特異的な対照ABPCと比較して有意に短い血中半減期を有することが観察され得る。その結果、METに特異的なpH操作されたABPCが、同じ抗原に結合するがそれらのpH依存性は異なる他の類似したバインダー(例えば、METに特異的な対照ABPC)と比較してエンドソームまたはリソソーム内での解離の強化を促進することができることが実証される。一部の例では、この効果は、特定の投与量でのみ観察されるのに対し、他の例では、投与量全体で観察される。
さらに、METに特異的なpH操作されたABPC ADCおよび対照ABPC ADCの半減期は、METに特異的なpH操作されたABPC ADCおよび対照ABPC ADCを、METに特異的なpH操作されたABPCおよび対照ABPCに置き換えた上記の方法を使用して、評価することもできる(すなわち、本明細書に記載されるように、薬剤または毒素へのコンジュゲーション後のABPCを試験すること)。
実施例7.マウス異種移植モデルにおける、METに特異的な対照ABPC ADCと比較した、METに特異的なpH操作されたADCの効力の増加
MET+腫瘍に対するMETに特異的なpH操作されたADCの増強された抗腫瘍活性は、MET+細胞の皮下異種移植モデルにおいて実証することができる。実験について、マウス1匹当たり、1~500万個のMET+細胞をインビトロで増殖させ、メスの免疫不全(例えば、SCID-BeigeまたはNOD scid)マウスの右脇腹に皮下接種する。腫瘍は、100~200mm3で大きさを一致させ、腹腔内投与する(IP)(約4~7日ごとに1回の投与、合計で約2~6回の投与)。腫瘍の長さ(L)および幅(W)の測定値は、電子キャリパーを介して取得され、体積は、以下の方程式に従って計算される: V=L×W^2/2。METに特異的なpH操作されたADC、またはMETに特異的な対照ABPC ADCのいずれかのボーラス(例えば、5mg/kg)を、尾静脈を介して投与する。腫瘍増殖の阻害(TGI)および腫瘍増殖の遅延(TGD)および生存は、同じレジメンで、METに特異的な対照ABPC ADCの投与と比較して、METに特異的なpH操作されたADCの投与により有意に改善される。
任意で、様々な組織への腫瘍細胞の広がりを、安楽死動物において判定する。転移は、Schneider,T.,et al.,Clin.Exp.Metas.19(2002)571-582に従い測定される。簡潔に述べると、組織を収穫し、ヒトAlu配列をリアルタイムPCRにより定量化する。リアルタイムPCRにより定量されたヒトDNAレベルが高いほど、より高い転移レベルであることに相当する。ヒトAlu配列のレベル(続発組織への腫瘍細胞の浸潤と相関する)は、同じレジメンで、METに特異的な対照ABPC ADCで処理されたマウスと比較して、METに特異的なpH操作されたADCで処理された動物において有意に低く、転移が少ないことに相当する。あるいは、METに特異的なpH操作されたADCの増強された抗腫瘍活性は、MET+患者由来の異種移植モデル(例えば、ジャクソンラボラトリーから入手可能)において示され得る。
実施例8.pH操作された二重特異性METの二重特異性ABPCの作製と、対照二重特異性ABPCと比較した例示的特性の実証
改変された毒性および細胞内移行特性を有するMETに特異的なpH操作されたABPCを作製するために、MET上の2つの異なるエピトープに結合する二重特異性抗体を構築する。二重パラトープ抗体は、高い抗原依存性細胞内移行を示すことができ、したがって、抗体-薬剤コンジュゲートなどの用途に有用であることが当技術分野で知られている(例えば、Li et al(2016)A Biparatopic HER2-Targeting Antibody-Drug Conjugate Induces Tumor Regression in Primary Models Refractory to or Ineligible for HER2-Targeted Therapy,Cancer Cell 29:117-29を参照されたい)。簡潔には、METに特異的な、pH操作されたMET×MET二重特異性の二重パラトープABPCは、METに特異的な2つの異なるpH操作されたABPCからの軽鎖/重鎖対であって、これらのそれぞれが、他方のエピトープと重複しないMET上の異なるエピトープに結合するものである、当該軽鎖/重鎖対を使用して構築する。重複しないエピトープに結合する、METに特異的なpH操作されたABPCのセットが、例えば、本明細書に記載される方法、または当業者に公知のその他の方法を使用することにより見出される。簡潔に述べると、二つのバインダーは、例えば、Abdiche YNら(2009)のExploring blocking assays using Octet,ProteOn,and Biacore biosensors,Anal Biochem 386:172-80に記載される結合競合アッセイなどにより判定される、MET上の実質的に異なるエピトープに結合することに基づき選択される。あるいは、簡潔には、本明細書に記載のように、METに特異的な第1のABPCでトランスフェクトした細胞の細胞培養上清を、50μg/mLの抗体発現レベルに正規化し、抗ヒトFcセンサー(Forte Bio社)上で捕捉する。ベースラインは、1Xキネティクス緩衝液(Forte Bio社)を使用して確立され、センサーは、1X PBS(これは、両方とも50ug/mLに正規化される、METに特異的な第二のABPCのトランスフェクション上清またはMETに特異的な第一のABPCのトランスフェクション上清とともに、混合されて、37℃で30分間、予めインキュベートされたものである)中の50nMのMETと、pH7.4で300秒間、結合され、結合曲線が生成される。METに特異的な第2のABPCの存在下での結合速度が、METに特異的な第1のABPCの存在下での結合速度よりも著しく速い場合(装置のソフトウェアによって計算されるか、または経時的な結合レベルの上昇によって確認される)、METに特異的な第2のABPCは、METの重複しないエピトープに結合すると見なされる。任意で、各抗体は、METを発現する細胞上のエピトープに結合したときの細胞内移行特性についてスクリーニングされ、良好に細胞内移行する抗体が選択される。細胞の表面に存在する分子の細胞内移行速度を決定するためのアッセイは、当技術分野で公知である。例えば、Wiley et al.(1991)J.Biol.Chem.266: 11083-11094;およびSorkin and Duex(2010)Curr.Protoc.Cell Biol.Chapter,Unit-15.14; Vainshtein et al.(2015)Pharm Res.32: 286-299を参照のこと。選択されたら、重鎖および軽鎖の対の形成のために操作された変異を有する重鎖と軽鎖の構築物(Spiess et al.,“Alternative molecular formats and therapeutic applications of bispecific antibodies,” 2015)が、両方のアームに対して合成される。METに特異的な二重特異性ABPCは、例えばExpi293細胞において、対応する重鎖および軽鎖のプラスミドの共発現によって産生される。細胞培養上清を収穫し、プロテインA精製を行う。METに特異的なヘテロ二量体ABPCを、イオン交換クロマトグラフィー、疎水性相互作用クロマトグラフィー、および混合モードクロマトグラフィー等の追加の精製ステップを介して、ホモ二量体種から分離する。METに特異的な、精製されたpH操作されたMET×MET二重特異性の二重パラトープABPCは、質量分析を介して特徴解析されて純度、およびホモ二量体種の不在が確認され、さらにサイズ排除クロマトグラフィーを介して特徴解析されて単量体の抗原結合タンパク質構築物種の存在が確認される。産生抗体について、METへの結合は、Biacore分析を介して確認される。二重特異性抗体産生の他の方法は当技術分野で公知であり、それを用いて、二重特異性抗体、例えば本明細書に記載されるMETに特異的なMET×MET二重特異性の二重パラトープABPCも作製され得ることが当業者には明白であろう(例えば、Labrijn et al(2014)“Controlled Fab-arm exchange for the generation of stable bispecific IgG1” Nature Protcols 9:2450-2463。http://www.nature.com/nprot/journal/v9/n10/abs/nprot.2014.169.htmlでアクセスされる)。あるいは、METに特異的なMET×MET ABPCの代わりに、METに特異的なpH操作されたMET×バインダーABPCを、当業者に明らかな同様の方法を使用して構築することができるものであり、当該バインダーは、当技術分野で公開されているか、または本明細書と同様の方法もしくは当技術分野で知られている方法(例えば、ディスプレイベースまたは免疫ベースの方法)を使用して見出される、任意の抗体である。
次に、本明細書に記載の方法を使用して、METに特異的なpH操作されたMET×MET ABPCの例示的な特性を実証することができ、ここでは適切な対照は、METに特異的な、対照ABPCの単一特異性または二重特異性ABPCである。簡潔に述べると、対照と比較して、METに特異的なpH操作されたMET×MET ABPCは、a)細胞にpH依存的に結合し、例えば中性pHで結合するが、酸性pHでは結合しない、およびb)細胞からpH依存的に放出され、例えば中性pHでは結合するが、酸性pHでは放出される、およびc)MET+細胞において、エンドリソソーム蓄積の強化を示す、およびd)MET+細胞への曝露後にMET抗原密度の上昇を示す、およびe)毒素とコンジュゲートすると、MET+細胞に対する細胞傷害性の増加を示す、およびf)毒素とコンジュゲートすると、MET+細胞とインキュベートしたときに毒素放出の増加を示す、およびg)関連動物モデル中でMET抗原に曝露されると、半減期の減少を示す、およびh)毒素とコンジュゲートすると、MET+細胞のマウス異種移植モデルにおいて有効性の増加を示す、ことが示され得る。同様に、METに特異的なpH操作されたMET×バインダーABPCの例示的な特性は、本明細書に記載の方法を使用して実証することができるものであり、ここでは適切な対照は、METに特異的な、対照ABPC MET×バインダーの二重特異性ABPCである。
実施例9.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性結合を操作するための鋳型として使用することができる[Wang J et al(2017)ABBV-399,a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors,Irrespective of MET Pathway Dependence,Clin Cancer Res,23:992-1000]。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体として、テリソツズマブ(重鎖は配列番号1、軽鎖は配列番号2)を選択した。簡潔に述べると、重鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、重鎖CDR内の個々のアミノ酸残基を、一度に一つ、ヒスチジンで系統的に置換した(MYT0887~MYT0924)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。重鎖CDR中にただ一つのヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)一つの重鎖配列変異体、およびb)対応する出発ABPCの軽鎖を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図1)、変異体のpH依存性を、Octet RED 384装置上のバイオレイヤーインターフェロメトリ(BLI)を使用して評価した。簡潔に述べると、細胞培養上清の15μLを、185μLの1×PBST pH 7.4に希釈し、センサーチップにロードした。これにより、高濃度41.1μg/mL、低濃度13.7μg/mL、平均濃度26.5μg/mLを得た。次いで、この希釈上清を、抗ヒトFcセンサー(Forte Bio社)上で捕捉した。ベースラインは、1×PBST(50mMリン酸カリウム緩衝液+150mMのNaCl+0.05%のTween 20)pH7.4を使用して確立された。センサーは、1×PBST pH 7.4中の50nMのMET(cMET、Sino Biological社、カタログ番号10692-H08H、ロット番号LC11SE2008)と120秒間結合され、結合曲線が作成された。解離相では、センサー上の抗体-抗原複合体を、300~600秒間、1×PBST pH7.4に曝露した。ベースライン、結合、および解離は、別個の条件下で全体を通じて1×PBST pH5.4を使用して繰り返された。結合相および解離相の曲線は、pH5.4およびpH7.4で、出発ABPC抗体(置換なし)およびそれぞれの対応する抗体変異体について検証され、以下の二つの基準についての情報を得る:a)出発ABPC(置換なし)と比較した、ヒスチジン置換またはアラニン置換に起因した、pH5.4での解離の強化(すなわち、koff値がより高い)、ならびにb)抗体変異体自体、および出発ABPC(置換なし)での場合の、pH5.4と比較した、pH7.4での解離の低下(すなわち、koff値がより低い)。さらなる分析のために、図2に示されるように、(出発ABPCと比較して)pH5.4での解離の強化またはpH7.4での解離の低下のいずれか、または両方を示した重鎖変異体を選択した(例えば、MYT0887、MYT0888、MYT0889、MYT0890、MYT0893、MYT0914、MYT0915、MYT0916、MYT0917、MYT0918、MYT0919、MYT0920およびMYT0924)。また、一部のヒスチジンおよびアラニンの変異は、MET結合を消失させる一方で(例えば、MYT0921およびMYT0923)、他の変異は許容されるものであり、MET結合動態を、ほとんど変化させない(例えば、解離定数KDまたは解離速度の変化が1倍未満)または全く変化させない(例えば、MYT0891、MYT0894、MYT0895、MYT0896、MYT0897、MYT0898、MYT0899、MYT0900、MYT0901、MYT0902、MYT0903、MYT0904、MYT0905、MYT0906、MYT0907、MYT0908、MYT0909、MYT0910、MYT0911、MYT0912、MYT0913およびMYT0922)ことにも留意された。
特にヒスチジンは、正電荷をもつ大きいアミノ酸であるため、これら変化を伴わない変異体は、広範囲の変異を許容し得、また異なる配列であるが類似の結合特性を有する抗体、さもなければ明白ではない指定を有する抗体をもたらす可能性がある重鎖の位置として注目された。
実施例10.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性結合を操作するための鋳型として使用することができる[Wang J et al(2017)ABBV-399,a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors,Irrespective of MET Pathway Dependence,Clin Cancer Res,23:992-1000]。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体として、テリソツズマブ(重鎖は配列番号1、軽鎖は配列番号2)を選択した。簡潔に述べると、軽鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、軽鎖CDR内の個々のアミノ酸残基を、一度に一つ、ヒスチジンで系統的に置換した(MYT2028~MYT2058)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。軽鎖CDR中にただ一つのヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)一つの軽鎖配列変異体、およびb)対応する出発ABPCの重鎖を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図3)、変異体のpH依存性を、Octet RED 96e装置上のバイオレイヤーインターフェロメトリ(BLI)を使用して評価した。簡潔に述べると、細胞培養上清を、SDS-PAGEゲルの視覚的検査によって判定された変異体の定性的発現レベルに基づいて希釈し、高発現には5μLの細胞培養上清を195μLの1×PBST、pH7.4に希釈して、中発現には25μLの細胞培養上清を175μLの1×PBST、pH7.4に希釈して、低発現には100μLの細胞培養上清を100μLの1×PBST、pH7.4に希釈して、センサーチップにロードした。次いで、希釈上清を、抗ヒトFcセンサー(Forte Bio社)上で捕捉した。ベースラインは、1×PBST(50mMリン酸カリウム緩衝液+150mMのNaCl+0.05%のTween 20)pH7.4を使用して確立された。センサーは、1×PBST pH 7.4中の50nMのMET(cMET、Sino Biological社 カタログ番号10692-H08H)と120秒間結合され、結合曲線が作成された。解離相では、センサー上の抗体-抗原複合体を、300~600秒間、1×PBST pH7.4に曝露した。ベースライン、結合、および解離は、別個の条件下で全体を通じて1×PBST pH5.4を使用して繰り返された。結合相および解離相の曲線は、pH5.4およびpH7.4で、出発ABPC抗体(置換なし)およびそれぞれの対応する抗体変異体について検証され、以下の二つの基準についての情報を得る:a)出発ABPC(置換なし)と比較した、ヒスチジン置換またはアラニン置換に起因した、pH5.4での解離の強化(すなわち、koff値がより高い)、ならびにb)抗体変異体自体、および出発ABPC(置換なし)での場合の、pH5.4と比較した、pH7.4での解離の低下(すなわち、koff値がより低い)。さらなる分析のために、図4に示されるように、(出発ABPCと比較して)pH5.4での解離の強化またはpH7.4での解離の低下のいずれか、または両方を示した軽鎖変異体を選択した(例えば、MYT2029、MYT2032、MYT2033、MYT2034、MYT2035、MYT2036、MYT2038、MYT2039、MYT2040、MYT2041、MYT2042、MYT2043、MYT2044、MYT2048、MYT2049、MYT2052、MYT2056およびMYT2058)。また、一部のヒスチジンおよびアラニンの変異が許容されるものであり、MET結合動態を、ほとんど変化させない(例えば、解離定数KDまたは解離速度の変化が1倍未満)または全く変化させない(例えば、MYT2028,MYT2030,MYT2031,MYT2037,MYT2045,MYT2046,MYT2047,MYT2050,MYt2051,MYT2053,MYT2054,MYT2055およびMYT2057)ことにも留意された。特にヒスチジンは、正電荷をもつ大きいアミノ酸であるため、これら変化を伴わない変異体は、広範囲の変異を許容し得、また異なる配列であるが類似の結合特性を有する抗体、さもなければ明白ではない指定を有する抗体をもたらす可能性がある軽鎖の位置として注目された。
実施例11.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性結合を操作するための鋳型として使用することができる[Wang J et al(2017)ABBV-399,a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors,Irrespective of MET Pathway Dependence,Clin Cancer Res,23:992-1000]。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体として、テリソツズマブ(重鎖は配列番号1、軽鎖は配列番号2)を選択した。簡潔に述べると、重鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、実施例9においてさらなる分析のために先立って選択された、重鎖CDR内の個々のアミノ酸変異を、一度に二つ以上、系統的に組み合わせた(MYT2018~MYT2027)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。重鎖CDR中に二つ以上のヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)一つの重鎖組み合わせ配列変異体、およびb)対応する出発ABPCの軽鎖を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図5)、変異体のpH依存性を、Octet RED 96e装置上のバイオレイヤーインターフェロメトリ(BLI)を使用して評価した。簡潔に述べると、細胞培養上清を、SDS-PAGEゲルの視覚的検査によって判定された変異体の定性的発現レベルに基づいて希釈し、高発現には5μLの細胞培養上清を195μLの1×PBST、pH7.4に希釈して、中発現には25μLの細胞培養上清を175μLの1×PBST、pH7.4に希釈して、低発現には100μLの細胞培養上清を100μLの1×PBST、pH7.4に希釈して、センサーチップにロードした。次いで、希釈上清を、抗ヒトFcセンサー(Forte Bio社)上で捕捉した。ベースラインは、1×PBST(50mMリン酸カリウム緩衝液+150mMのNaCl+0.05%のTween 20)pH7.4を使用して確立された。センサーは、1×PBST pH 7.4中の50nMのMET(cMET、Sino Biological社 カタログ番号10692-H08H)と120秒間結合され、結合曲線が作成された。解離相では、センサー上の抗体-抗原複合体を、300~600秒間、1×PBST pH7.4に曝露した。ベースライン、結合、および解離は、別個の条件下で全体を通じて1×PBST pH5.4を使用して繰り返された。結合相および解離相の曲線は、pH5.4およびpH7.4で、出発ABPC抗体(置換なし)およびそれぞれの対応する抗体変異体について検証され、以下の二つの基準についての情報を得る:a)出発ABPC(置換なし)と比較した、ヒスチジン置換またはアラニン置換に起因した、pH5.4での解離の強化(すなわち、koff値がより高い)、ならびにb)抗体変異体自体、および出発ABPC(置換なし)での場合の、pH5.4と比較した、pH7.4での解離の低下(すなわち、koff値がより低い)。さらなる分析のために、図6に示されるように、(出発ABPCと比較して)pH5.4での解離の強化またはpH7.4での解離の低下のいずれか、または両方を示した重鎖組み合わせ変異体を選択した(例えば、MYT2018、MYT2019、MYT2020、MYT2022、MYT2023、MYT2025およびMYT2026)。
実施例12.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性結合を操作するための鋳型として使用することができる[Wang J et al(2017)ABBV-399,a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors,Irrespective of MET Pathway Dependence,Clin Cancer Res,23:992-1000]。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体として、テリソツズマブ(重鎖は配列番号1、軽鎖は配列番号2)を選択した。簡潔に述べると、軽鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、実施例10においてさらなる分析のために先立って選択された、軽鎖CDR内の個々のアミノ酸変異を、一度に二つ以上、系統的に組み合わせた(MYT4201~MYT4210)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。軽鎖CDR中に二つ以上のヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)一つの軽鎖組み合わせ配列変異体、およびb)対応する出発ABPCの重鎖を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図7)、変異体のpH依存性を、Octet RED 96e装置上のバイオレイヤーインターフェロメトリ(BLI)を使用して評価した。簡潔に述べると、細胞培養上清を、SDS-PAGEゲルの視覚的検査によって判定された変異体の定性的発現レベルに基づいて希釈し、高発現には5μLの細胞培養上清を195μLの1×PBST、pH7.4に希釈して、中発現には25μLの細胞培養上清を175μLの1×PBST、pH7.4に希釈して、低発現には100μLの細胞培養上清を100μLの1×PBST、pH7.4に希釈して、センサーチップにロードした。次いで、希釈上清を、抗ヒトFcセンサー(Forte Bio社)上で捕捉した。ベースラインは、1×PBST(50mMリン酸カリウム緩衝液+150mMのNaCl+0.05%のTween 20)、pH7.4を使用して確立された。センサーは、1×PBST、pH 7.4中のMET(cMET、Sino Biological社 カタログ番号10692-H08H)と120秒間結合され、結合曲線が作成された。解離相では、センサー上の抗体-抗原複合体を、300~600秒間、1×PBST、pH7.4に曝露した。ベースライン、結合、および解離は、別個の条件下で全体を通じて1×PBST、pH5.4を使用して繰り返された。結合相および解離相の曲線は、pH5.4およびpH7.4で、出発ABPC抗体(置換なし)およびそれぞれの対応する抗体変異体について検証され、以下の二つの基準についての情報を得る:a)出発ABPC(置換なし)と比較した、ヒスチジン置換またはアラニン置換に起因した、pH5.4での解離の強化(例えば、koff値がより高い)、ならびにb)抗体変異体自体、および出発ABPC(置換なし)での場合の、pH5.4と比較した、pH7.4での解離の低下(例えば、koff値がより低い)。さらなる分析のために、図8に示されるように、(出発ABPCと比較して)pH5.4での解離の強化またはpH7.4での解離の低下のいずれか、または両方を示した軽鎖組み合わせ変異体を選択した(例えば、MYT4201、MYT4202、MYT4203、MYT4204、MYT4205、MYT4206、MYT4207、MYT4208、MYT4209およびMYT4210)。
実施例13.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性結合を操作するための鋳型として使用することができる[Wang J et al(2017)ABBV-399,a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors,Irrespective of MET Pathway Dependence,Clin Cancer Res,23:992-1000]。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体として、テリソツズマブ(重鎖は配列番号1、軽鎖は配列番号2)を選択した。簡潔に述べると、重鎖および軽鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、実施例9~12においてさらなる分析のために先立って選択された、重鎖および軽鎖のCDR内の個々のアミノ酸変異を、一度に二つ以上、系統的に組み合わせた(MYT3451~MYT3492、MYT3603~MYT3616およびMYT4211~MYT4220)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。二つ以上のヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)一つの軽鎖配列変異体または軽鎖組み合わせ配列変異体、およびb)一つの重鎖配列変異体または重鎖組み合わせ配列変異体を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図9)、変異体のpH依存性を、Octet RED 96e装置上のバイオレイヤーインターフェロメトリ(BLI)を使用して評価した。簡潔に述べると、細胞培養上清を、SDS-PAGEゲルの視覚的検査によって判定された変異体の定性的発現レベルに基づいて希釈し、高発現には5μLの細胞培養上清を195μLの1×PBST、pH7.4に希釈して、中発現には25μLの細胞培養上清を175μLの1×PBST、pH7.4に希釈して、低発現には100μLの細胞培養上清を100μLの1×PBST、pH7.4に希釈して、センサーチップにロードした。次いで、希釈上清を、抗ヒトFcセンサー(Forte Bio社)上で捕捉した。ベースラインは、1×PBST(50mMリン酸カリウム緩衝液+150mMのNaCl+0.05%のTween 20)、pH7.4を使用して確立された。センサーは、1×PBST、pH 7.4中の50nMのMET(cMET、Sino Biological社 カタログ番号10692-H08H)と120秒間結合され、結合曲線が作成された。解離相では、センサー上の抗体-抗原複合体を、300~600秒間、1×PBST、pH7.4に曝露した。ベースライン、結合、および解離は、別個の条件下で全体を通じて1×PBST、pH5.4を使用して繰り返された。結合相および解離相の曲線は、pH5.4およびpH7.4で、出発ABPC抗体(置換なし)およびそれぞれの対応する抗体変異体について検証され、以下の二つの基準についての情報を得る:a)出発ABPC(置換なし)と比較した、ヒスチジン置換またはアラニン置換に起因した、pH5.4での解離の強化(例えば、koff値がより高い)、ならびにb)抗体変異体自体、および出発ABPC(置換なし)での場合の、pH5.4と比較した、pH7.4での解離の低下(例えば、koff値がより低い)。さらなる分析のために、図10に示されるように、(出発ABPCと比較して)pH5.4での解離の強化またはpH7.4での解離の低下のいずれか、または両方を示した対の重鎖および軽鎖変異体を選択した(MYT3451、MYT3452、MYT3453、MYT3454、MYT3455、MYT3456、MYT3457、MYT3459、MYT3460、MYT3463、MYT3465、MYT3466、MYT3467、MYT3468、MYT3469、MYT3471、MYT3473、MYT3474、MYT3476、MYT3477、MYT3479、MYT3480、MYT3481、MYT3482、MYT3483、MYT3484、MYT3485、MYT3487、MYT3488、MYT3491、MYT3603、MYT3604、MYT3605、MYT3606、MYT3607、MYT3608、MYT3609、MYT3610、MYT3611、MYT3612、MYT3614、MYT3615、MYT4211、MYT4212、MYT4214、MYT4217およびMYT4220)。
実施例14.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性結合を操作するための鋳型として使用することができる[Wang J et al(2017)ABBV-399,a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors,Irrespective of MET Pathway Dependence,Clin Cancer Res,23:992-1000]。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体として、テリソツズマブ(重鎖は配列番号1、軽鎖は配列番号2)を選択した。簡潔に述べると、重鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、実施例9においてさらなる分析のために先立って選択された、重鎖CDR内の個々のアミノ酸変異を、一度に二つ以上、系統的に組み合わせた(MYT4951~MYT4989)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。重鎖CDR中に二つ以上のヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)それぞれ(Wang J et al(2017)ABBV-399,a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors,Irrespective of MET Pathway Dependence,Clin Cancer Res,23:992-1000)および(Dall,WF et al “Increasing the Affinity of a Human IgG1 for the Neonatal Fc Receptor: Biological Consequences” The Journal of Immunology(2002); 169:5171-5180)に記載されている、トリプルヒンジ(TH)およびYTE変異を含有する一つの重鎖組み合わせ配列変異体、ならびにb)対応する出発ABPCの軽鎖を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図11)、プロテインA磁気ビーズ(Genscript社 L00273)を使用して精製して、Detroit 562細胞(ATCC社 CCL-138)でのエンドリソソーム送達を評価した。Detroit 562細胞(ATCC社;CCL-138)を回収して、EMEM培地(ATCC社;30-2003)+10% GenClone熱不活性化ウシ胎児血清(HI FBS)(Genesee Scientific社;25-514H)中で再懸濁した。細胞数は、トリパンブルー染色およびCountess II FL自動セルカウンター(Thermofisher社;AMQAF1000)を使用して決定した。次いで細胞を100,000細胞/mLに希釈し、100ulを96ウェルの平底細胞培養プレートに播種し、37C、5%CO2中で一晩付着させた。次いで、一次抗体をネイティブ培養培地中で20nMに希釈し、次いで60nMのIncucyte Human FabFluor-pH赤色抗体標識試薬(Sartorius社;4722)と1:1で混合した。混合物を室温で20分間インキュベートし、続いて細胞に添加した。次いで、プレートをIncucyte S3 Live-Cell分析システムに直ちに入れて、画像取得および分析を行った。出発ABPC抗体(置換なし)および対応する各抗体変異体についてエンドリソソーム送達を調べて、出発ABPC(置換なし)と比較してヒスチジンまたはアラニン置換に起因して強化されたエンドリソソーム送達について情報を得た。さらなる分析のために、図12に示すように、(出発ABPCと比較して)強化されたエンドリソソーム送達を示した重鎖組み合わせ変異体を選択した(例えば、MYT4953およびMYT4970)。選択された変異体のpH依存性を、Octet RED 96e装置上のバイオレイヤーインターフェロメトリ(BLI)を使用して評価した。簡潔に述べると、細胞培養上清を、SDS-PAGEゲルの視覚的検査によって判定された変異体の定性的発現レベルに基づいて希釈し、高発現には5μLの細胞培養上清を195μLの1×PBST、pH7.4に希釈して、中発現には25μLの細胞培養上清を175μLの1×PBST、pH7.4に希釈して、低発現には100μLの細胞培養上清を100μLの1×PBST、pH7.4に希釈して、センサーチップにロードした。次いで、希釈上清を、抗ヒトFcセンサー(Forte Bio社)上で捕捉した。ベースラインは、1×PBST(50mMリン酸カリウム緩衝液+150mMのNaCl+0.05%のTween 20)、pH7.4を使用して確立された。センサーは、1×PBST、pH 7.4中のMET(cMET、Sino Biological社 カタログ番号10692-H08H)と120秒間結合され、結合曲線が作成された。解離相では、センサー上の抗体-抗原複合体を、300~600秒間、1×PBST、pH7.4またはpH5.4に曝露した。結合相および解離相の曲線は、pH7.4およびpH5.4で、出発ABPC抗体(置換なし)およびそれぞれの対応する抗体変異体について検証され、以下の二つの基準についての情報を得る:a)出発ABPC(置換なし)と比較した、ヒスチジン置換またはアラニン置換に起因した、pH5.4での解離の強化(例えば、koff値がより高い)、ならびにb)抗体変異体自体、および出発ABPC(置換なし)での場合の、pH5.4と比較した、pH7.4での解離の低下(例えば、koff値がより低い)。さらなる分析のために、図13に示されるように、(出発ABPCと比較して)pH5.4での解離の強化またはpH7.4での解離の低下のいずれか、または両方を示した重鎖組み合わせ変異体を選択した(例えば、MYT4953およびMYT4970)。
実施例15.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性結合を操作するための鋳型として使用することができる[Wang J et al(2017)ABBV-399,a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors,Irrespective of MET Pathway Dependence,Clin Cancer Res,23:992-1000]。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体として、テリソツズマブ(重鎖は配列番号1、軽鎖は配列番号2)を選択した。簡潔に述べると、軽鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、実施例10においてさらなる分析のために先立って選択された、軽鎖CDR内の個々のアミノ酸変異を、一度に二つ以上、系統的に組み合わせた(MYT4990~4994)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。軽鎖CDR中に二つ以上のヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)一つの軽鎖組み合わせ配列変異体、ならびにb)それぞれ(Wang J et al(2017)ABBV-399,a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors,Irrespective of MET Pathway Dependence,Clin Cancer Res,23:992-1000)および(Dall,WF et al “Increasing the Affinity of a Human IgG1 for the Neonatal Fc Receptor: Biological Consequences” The Journal of Immunology(2002); 169:5171-5180)に記載されている、トリプルヒンジ(TH)およびYTE変異を含有す対応する出発ABPCの重鎖を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図14)、プロテインA磁気ビーズ(Genscript社 L00273)を使用して精製して、Detroit 562細胞(ATCC社 CCL-138)でのエンドリソソーム送達を評価した。Detroit 562細胞(ATCC社;CCL-138)を回収して、EMEM培地(ATCC社;30-2003)+10% GenClone熱不活性化ウシ胎児血清(HI FBS)(Genesee Scientific社;25-514H)中で再懸濁した。細胞数は、トリパンブルー染色およびCountess II FL自動セルカウンター(Thermofisher社;AMQAF1000)を使用して決定した。次いで細胞を100,000細胞/mLに希釈し、100ulを96ウェルの平底細胞培養プレートに播種し、37C、5%CO2中で一晩付着させた。次いで、一次抗体をネイティブ培養培地中で20nMに希釈し、次いで60nMのIncucyte Human FabFluor-pH赤色抗体標識試薬(Sartorius社;4722)と1:1で混合した。混合物を室温で20分間インキュベートし、続いて細胞に添加した。次いで、プレートをIncucyte S3 Live-Cell分析システムに直ちに入れて、画像取得および分析を行った。出発ABPC抗体(置換なし)および対応する各抗体変異体についてエンドリソソーム送達を調べて、出発ABPC(置換なし)と比較してヒスチジンまたはアラニン置換に起因して強化されたエンドリソソーム送達について情報を得た。
実施例16.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性の結合を操作するための鋳型として使用することができる(Feng Yら 「MET抗体薬剤コンジュゲート(MET Antibody Drug Conjugate)」 米国特許出願公開第2020/0061204号(2020/0061204A1)(2020))。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体として、エミベツズマブ(重鎖は配列番号146、軽鎖は配列番号147)を選択した。簡潔に述べると、重鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、重鎖CDR内の個々のアミノ酸残基を、一度に一つ、ヒスチジンで系統的に置換した(MYT2314~MYT2348)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。重鎖CDR中にただ一つのヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)一つの重鎖配列変異体、およびb)対応する出発ABPCの軽鎖を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図22)、変異体のpH依存性を、Octet RED 96e装置上のバイオレイヤーインターフェロメトリ(BLI)を使用して評価した。簡潔に述べると、細胞培養上清を、SDS-PAGEゲルの視覚的検査によって判定された変異体の定性的発現レベルに基づいて希釈し、高発現には5μLの細胞培養上清を195μLの1×PBST、pH7.4に希釈して、中発現には25μLの細胞培養上清を175μLの1×PBST、pH7.4に希釈して、低発現には100μLの細胞培養上清を100μLの1×PBST、pH7.4に希釈して、センサーチップにロードした。次いで、この希釈上清を、抗ヒトFcセンサー(Forte Bio社)上で捕捉した。ベースラインは、1×PBST(50mMリン酸カリウム緩衝液+150mMのNaCl+0.05%のTween 20)pH7.4を使用して確立された。センサーは、1×PBST pH 7.4中の50nMのMET(cMET、Sino Biological社 カタログ番号10692-H08H)と120秒間結合され、結合曲線が作成された。解離相では、センサー上の抗体-抗原複合体を、300~600秒間、1×PBST pH7.4に曝露した。ベースライン、結合、および解離は、別個の条件下で全体を通じて1×PBST pH5.4を使用して繰り返された。結合相および解離相の曲線は、pH5.4およびpH7.4における出発ABPC抗体(置換なし)および対応する各抗体変異体について検証され、
以下の二つの基準についての情報を得る:a)出発ABPC(置換なし)と比較した、ヒスチジン置換またはアラニン置換に起因した、pH5.4での解離の強化(すなわち、koff値がより高い)、ならびにb)抗体変異体自体、および出発ABPC(置換なし)での場合の、pH5.4と比較した、pH7.4での解離の低下(すなわち、koff値がより低い)。さらなる分析のために、図23に示されるように、(出発ABPCと比較して)pH5.4での解離の強化またはpH7.4での解離の低下のいずれか、または両方を示した重鎖変異体を選択した(例えば、MYT2319、MYT2324、MYT2325、MYT2326、MYT2327、MYT2328、MYT2330、MYT2331、MYT2333、MYT2342、MYT2343、MYT2344およびMYT2347)。また、一部のヒスチジンおよびアラニンの変異は、MET結合を消失させる一方で(例えば、MYT2341)、他の変異は許容されるものであり、MET結合動態を、ほとんど変化させない(例えば、解離定数KDまたは解離速度の変化が1倍未満)または全く変化させない(例えば、MYT2314、MYT2315、MYT2316、MYT2317、MYT2318、MYT2320、MYT2321、MYT2322、MYT2323、MYT2329、MYT2332、MYT2334、MYT2335、MYT2336、MYT2337、MYT2338、MYT2339、MYT2340、MYT2345、MYT2346およびMYT2348)ことにも留意された。
特にヒスチジンは、正電荷をもつ大きいアミノ酸であるため、これら変化を伴わない変異体は、広範囲の変異を許容し得、また異なる配列であるが類似の結合特性を有する抗体、さもなければ明白ではない指定を有する抗体をもたらす可能性がある重鎖の位置として注目された。
実施例17.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性の結合を操作するための鋳型として使用することができる(Feng Yら 「MET抗体薬剤コンジュゲート(MET Antibody Drug Conjugate)」 米国特許出願公開第2020/0061204号(2020/0061204A1)(2020))。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体として、エミベツズマブ(重鎖は配列番号146、軽鎖は配列番号147)を選択した。簡潔に述べると、軽鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、軽鎖CDR内の個々のアミノ酸残基を、一度に一つ、ヒスチジンで系統的に置換した(MYT3958~MYT3985)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。軽鎖CDR中にただ一つのヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)一つの軽鎖配列変異体、およびb)対応する出発ABPCの重鎖を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図24)、変異体のpH依存性を、Octet RED 96e装置上のバイオレイヤーインターフェロメトリ(BLI)を使用して評価した。簡潔に述べると、細胞培養上清を、SDS-PAGEゲルの視覚的検査によって判定された変異体の定性的発現レベルに基づいて希釈し、高発現には5μLの細胞培養上清を195μLの1×PBST、pH7.4に希釈して、中発現には25μLの細胞培養上清を175μLの1×PBST、pH7.4に希釈して、低発現には100μLの細胞培養上清を100μLの1×PBST、pH7.4に希釈して、センサーチップにロードした。次いで、希釈上清を、抗ヒトFcセンサー(Forte Bio社)上で捕捉した。ベースラインは、1×PBST(50mMリン酸カリウム緩衝液+150mMのNaCl+0.05%のTween 20)pH7.4を使用して確立された。センサーは、1×PBST pH 7.4中の50nMのMET(cMET、Sino Biological社 カタログ番号10692-H08H)と120秒間結合され、結合曲線が作成された。解離相では、センサー上の抗体-抗原複合体を、300~600秒間、1×PBST pH7.4に曝露した。ベースライン、結合、および解離は、別個の条件下で全体を通じて1×PBST pH5.4を使用して繰り返された。結合相および解離相の曲線は、pH5.4およびpH7.4で、出発ABPC抗体(置換なし)およびそれぞれの対応する抗体変異体について検証され、以下の二つの基準についての情報を得る:a)出発ABPC(置換なし)と比較した、ヒスチジン置換またはアラニン置換に起因した、pH5.4での解離の強化(すなわち、koff値がより高い)、ならびにb)抗体変異体自体、および出発ABPC(置換なし)での場合の、pH5.4と比較した、pH7.4での解離の低下(すなわち、koff値がより低い)。さらなる分析のために、図25に示されるように、(出発ABPCと比較して)pH5.4での解離の強化またはpH7.4での解離の低下のいずれか、または両方を示した軽鎖変異体を選択した(例えば、MYT3959、MYT3960、MYT3963、MYT3966、MYT3967、MYT3969、MYT3970、MYT3978、MYT3979、MYT3982、MYT3983およびMYT3984)。また、一部のヒスチジンおよびアラニンの変異が許容されるものであり、MET結合動態を、ほとんど変化させない(例えば、解離定数KDまたは解離速度の変化が1倍未満)または全く変化させない(例えば、MYT3958,MYT3961,MYT3962,MYT3964,MYT3965,MYT3968,MYT3971,MYT3972,MYT3973,MYT3974,MYT3975,MYT3976,MYT3977,MYT3980,MYT3981およびMYT3985)ことにも留意された。
特にヒスチジンは、正電荷をもつ大きいアミノ酸であるため、これら変化を伴わない変異体は、広範囲の変異を許容し得、また異なる配列であるが類似の結合特性を有する抗体、さもなければ明白ではない指定を有する抗体をもたらす可能性がある軽鎖の位置として注目された。
実施例18.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性の結合を操作するための鋳型として使用することができる(Feng Yら 「MET抗体薬剤コンジュゲート(MET Antibody Drug Conjugate)」 米国特許出願公開第2020/0061204号(2020/0061204A1)(2020))。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体として、エミベツズマブ(重鎖は配列番号146、軽鎖は配列番号147)を選択した。簡潔に述べると、重鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、実施例16においてさらなる分析のために先立って選択された、重鎖CDR内の個々のアミノ酸変異を、一度に二つ以上、系統的に組み合わせた(MYT2848~MYT2867)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。重鎖CDR中に二つ以上のヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)一つの重鎖組み合わせ配列変異体、およびb)対応する出発ABPCの軽鎖を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図26)、変異体のpH依存性を、Octet RED 96e装置上のバイオレイヤーインターフェロメトリ(BLI)を使用して評価した。簡潔に述べると、細胞培養上清を、SDS-PAGEゲルの視覚的検査によって判定された変異体の定性的発現レベルに基づいて希釈し、高発現には5μLの細胞培養上清を195μLの1×PBST、pH7.4に希釈して、中発現には25μLの細胞培養上清を175μLの1×PBST、pH7.4に希釈して、低発現には100μLの細胞培養上清を100μLの1×PBST、pH7.4に希釈して、センサーチップにロードした。次いで、希釈上清を、抗ヒトFcセンサー(Forte Bio社)上で捕捉した。ベースラインは、1×PBST(50mMリン酸カリウム緩衝液+150mMのNaCl+0.05%のTween 20)pH7.4を使用して確立された。センサーは、1×PBST pH 7.4中の50nMのMET(cMET、Sino Biological社 カタログ番号10692-H08H)と120秒間結合され、結合曲線が作成された。解離相では、センサー上の抗体-抗原複合体を、300~600秒間、1×PBST pH7.4に曝露した。ベースライン、結合、および解離は、別個の条件下で全体を通じて1×PBST pH5.4を使用して繰り返された。結合相および解離相の曲線は、pH5.4およびpH7.4で、出発ABPC抗体(置換なし)およびそれぞれの対応する抗体変異体について検証され、以下の二つの基準についての情報を得る:a)出発ABPC(置換なし)と比較した、ヒスチジン置換またはアラニン置換に起因した、pH5.4での解離の強化(すなわち、koff値がより高い)、ならびにb)抗体変異体自体、および出発ABPC(置換なし)での場合の、pH5.4と比較した、pH7.4での解離の低下(すなわち、koff値がより低い)。さらなる分析のために、図27に示されるように、(出発ABPCと比較して)pH5.4での解離の強化またはpH7.4での解離の低下のいずれか、または両方を示した重鎖組み合わせ変異体を選択した(例えば、MYT2848、MYT2849、MYT2850、MYT2851、MYT2852、MYT2853、MYT2854、MYT2855、MYT2856、MYT2857、MYT2858、MYT2859、MYT2861、MYT2862、MYT2863、MYT2864、MYT2865、MYT2866およびMYT2867)。
実施例19.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性の結合を操作するための鋳型として使用することができる(Feng Yら 「MET抗体薬剤コンジュゲート(MET Antibody Drug Conjugate)」 米国特許出願公開第2020/0061204号(2020/0061204A1)(2020))。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体として、エミベツズマブ(重鎖は配列番号146、軽鎖は配列番号147)を選択した。簡潔に述べると、軽鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、実施例17においてさらなる分析のために先立って選択された、軽鎖CDR内の個々のアミノ酸変異を、一度に二つ以上、系統的に組み合わせた(MYT4326~MYT4345)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。軽鎖CDR中に二つ以上のヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)一つの軽鎖組み合わせ配列変異体、およびb)対応する出発ABPCの重鎖を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図28)、変異体のpH依存性を、Octet RED 96e装置上のバイオレイヤーインターフェロメトリ(BLI)を使用して評価した。簡潔に述べると、細胞培養上清を、SDS-PAGEゲルの視覚的検査によって判定された変異体の定性的発現レベルに基づいて希釈し、高発現には5μLの細胞培養上清を195μLの1×PBST、pH7.4に希釈して、中発現には25μLの細胞培養上清を175μLの1×PBST、pH7.4に希釈して、低発現には100μLの細胞培養上清を100μLの1×PBST、pH7.4に希釈して、センサーチップにロードした。次いで、希釈上清を、抗ヒトFcセンサー(Forte Bio社)上で捕捉した。ベースラインは、1×PBST(50mMリン酸カリウム緩衝液+150mMのNaCl+0.05%のTween 20)、pH7.4を使用して確立された。センサーは、1×PBST、pH 7.4中のMET(cMET、Sino Biological社 カタログ番号10692-H08H)と120秒間結合され、結合曲線が作成された。解離相では、センサー上の抗体-抗原複合体を、300~600秒間、1×PBST、pH7.4に曝露した。ベースライン、結合、および解離は、別個の条件下で全体を通じて1×PBST、pH5.4を使用して繰り返された。結合相および解離相の曲線は、pH5.4およびpH7.4で、出発ABPC抗体(置換なし)およびそれぞれの対応する抗体変異体について検証され、以下の二つの基準についての情報を得る:a)出発ABPC(置換なし)と比較した、ヒスチジン置換またはアラニン置換に起因した、pH5.4での解離の強化(例えば、koff値がより高い)、ならびにb)抗体変異体自体、および出発ABPC(置換なし)での場合の、pH5.4と比較した、pH7.4での解離の低下(例えば、koff値がより低い)。さらなる分析のために、図29に示されるように、(出発ABPCと比較して)pH5.4での解離の強化またはpH7.4での解離の低下のいずれか、または両方を示した軽鎖組み合わせ変異体を選択した(例えば、MYT4326,MYT4327,MYT4328,MYT4329,MYT4330,MYT4331,MYT4332,MYT4333,MYT4334,MYT4335,MYT4336,MYT4337,MYT4338,MYT4339,MYT4340,MYT4342,MYT4343)。
実施例20.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性の結合を操作するための鋳型として使用することができる(Feng Yら 「MET抗体薬剤コンジュゲート(MET Antibody Drug Conjugate)」 米国特許出願公開第2020/0061204号(2020/0061204A1)(2020))。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体として、エミベツズマブ(重鎖は配列番号146、軽鎖は配列番号147)を選択した。簡潔に述べると、重鎖および軽鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、実施例16~19においてさらなる分析のために先立って選択された、重鎖および軽鎖のCDR内の個々のアミノ酸変異を、一度に二つ以上、系統的に組み合わせた(MYT3999~MYT4042)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。二つ以上のヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)一つの軽鎖配列変異体または軽鎖組み合わせ配列変異体、およびb)一つの重鎖配列変異体または重鎖組み合わせ配列変異体を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図30)、変異体のpH依存性を、Octet RED 96e装置上のバイオレイヤーインターフェロメトリ(BLI)を使用して評価した。簡潔に述べると、細胞培養上清を、SDS-PAGEゲルの視覚的検査によって判定された変異体の定性的発現レベルに基づいて希釈し、高発現には5μLの細胞培養上清を195μLの1×PBST、pH7.4に希釈して、中発現には25μLの細胞培養上清を175μLの1×PBST、pH7.4に希釈して、低発現には100μLの細胞培養上清を100μLの1×PBST、pH7.4に希釈して、センサーチップにロードした。次いで、希釈上清を、抗ヒトFcセンサー(Forte Bio社)上で捕捉した。ベースラインは、1×PBST(50mMリン酸カリウム緩衝液+150mMのNaCl+0.05%のTween 20)、pH7.4を使用して確立された。センサーは、1×PBST、pH 7.4中の50nMのMET(cMET、Sino Biological社 カタログ番号10692-H08H)と120秒間結合され、結合曲線が作成された。解離相では、センサー上の抗体-抗原複合体を、300~600秒間、1×PBST、pH7.4に曝露した。ベースライン、結合、および解離は、別個の条件下で全体を通じて1×PBST、pH5.4を使用して繰り返された。結合相および解離相の曲線は、pH5.4およびpH7.4で、出発ABPC抗体(置換なし)およびそれぞれの対応する抗体変異体について検証され、以下の二つの基準についての情報を得る:a)出発ABPC(置換なし)と比較した、ヒスチジン置換またはアラニン置換に起因した、pH5.4での解離の強化(例えば、koff値がより高い)、ならびにb)抗体変異体自体、および出発ABPC(置換なし)での場合の、pH5.4と比較した、pH7.4での解離の低下(例えば、koff値がより低い)。さらなる分析のために、図31に示されるように、(出発ABPCと比較して)pH5.4での解離の強化またはpH7.4での解離の低下のいずれか、または両方を示した対の重鎖および軽鎖変異体を選択した(例えば、MYT3999、MYT4000、MYT4001、MYT4002、MYT4003、MYT4004、MYT4005、MYT4006、MYT4007、MYT4008、MYT4009、MYT4010、MYT4011、MYT4012、MYT4013、MYT4014、MYT4015、MYT4016、MYT4017、MYT4018、MYT4019、MYT4023、MYT4027、MYT4032、MYT4033、MYT4034、MYT4035、MYT4036、MYT4037、MYT4038、MYT4039、MYT4040、MYT4041およびMYT4042)。
実施例21.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性の結合を操作するための鋳型として使用することができる(Feng Yら 「MET抗体薬剤コンジュゲート(MET Antibody Drug Conjugate)」 米国特許出願公開第2020/0061204号(2020/0061204A1)(2020))。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体として、エミベツズマブ(重鎖は配列番号146、軽鎖は配列番号147)を選択した。簡潔に述べると、重鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、実施例16においてさらなる分析のために先立って選択された、重鎖CDR内の個々のアミノ酸変異を、一度に二つ以上、系統的に組み合わせた(MYT4995~MYT5041)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。重鎖CDR中に二つ以上のヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)それぞれ(Wang J et al(2017)ABBV-399,a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors,Irrespective of MET Pathway Dependence,Clin Cancer Res,23:992-1000)および(Dall,WF et al “Increasing the Affinity of a Human IgG1 for the Neonatal Fc Receptor: Biological Consequences” The Journal of Immunology(2002); 169:5171-5180)に記載されている、トリプルヒンジ(TH)およびYTE変異を含有する一つの重鎖組み合わせ配列変異体、ならびにb)対応する出発ABPCの軽鎖を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図32)、プロテインA磁気ビーズ(Genscript社 L00273)を使用して精製して、Detroit 562細胞(ATCC社 CCL-138)でのエンドリソソーム送達を評価した。Detroit 562細胞(ATCC社;CCL-138)を回収して、EMEM培地(ATCC社;30-2003)+10% GenClone熱不活性化ウシ胎児血清(HI FBS)(Genesee Scientific社;25-514H)中で再懸濁した。細胞数は、トリパンブルー染色およびCountess II FL自動セルカウンター(Thermofisher社;AMQAF1000)を使用して決定した。次いで細胞を100,000細胞/mLに希釈し、100ulを96ウェルの平底細胞培養プレートに播種し、37C、5%CO2中で一晩付着させる。次いで、一次抗体をネイティブ培養培地中で20nMに希釈し、次いで60nMのIncucyte Human FabFluor-pH赤色抗体標識試薬(Sartorius社;4722)と1:1で混合した。混合物を室温で20分間インキュベートし、続いて細胞に添加した。次いで、プレートをIncucyte S3 Live-Cell分析システムに直ちに入れて、画像取得および分析を行った。出発ABPC抗体(置換なし)および対応する各抗体変異体についてエンドリソソーム送達を調べて、出発ABPC(置換なし)と比較してヒスチジンまたはアラニン置換に起因して強化されたエンドリソソーム送達について情報を得た。
実施例22.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性の結合を操作するための鋳型として使用することができる(Hicks,SWおよびLai,K 「MET抗体および免疫複合体およびその使用(MET Antibodies and Immunoconjugates and uses thereof)」 国際特許出願公開第2020/014306号(WO 2020/014306 A1)(2020))。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体としてhucMET27Gv1.3(重鎖は配列番号304、軽鎖は配列番号305)を選択した。簡潔に述べると、重鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、重鎖CDR内の個々のアミノ酸残基を、一度に一つ、ヒスチジンで系統的に置換した(MYT3618~MYT3655)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。重鎖CDR中にただ一つのヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)一つの重鎖配列変異体、およびb)対応する出発ABPCの軽鎖を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図39)、変異体のpH依存性を、Octet RED 96e装置上のバイオレイヤーインターフェロメトリ(BLI)を使用して評価した。簡潔に述べると、細胞培養上清を、SDS-PAGEゲルの視覚的検査によって判定された変異体の定性的発現レベルに基づいて希釈し、高発現には5μLの細胞培養上清を195μLの1×PBST、pH7.4に希釈して、中発現には25μLの細胞培養上清を175μLの1×PBST、pH7.4に希釈して、低発現には100μLの細胞培養上清を100μLの1×PBST、pH7.4に希釈して、センサーチップにロードした。次いで、希釈上清を、抗ヒトFcセンサー(Forte Bio社)上で捕捉した。ベースラインは、1×PBST(50mMリン酸カリウム緩衝液+150mMのNaCl+0.05%のTween 20)pH7.4を使用して確立された。センサーは、1×PBST pH 7.4中の50nMのMET(cMET、Sino Biological社 カタログ番号10692-H08H)と120秒間結合され、結合曲線が作成された。解離相では、センサー上の抗体-抗原複合体を、300~600秒間、1×PBST pH7.4に曝露した。ベースライン、結合、および解離は、別個の条件下で全体を通じて1×PBST pH5.4を使用して繰り返された。結合相および解離相の曲線は、pH5.4およびpH7.4で、出発ABPC抗体(置換なし)およびそれぞれの対応する抗体変異体について検証され、以下の二つの基準についての情報を得る:a)出発ABPC(置換なし)と比較した、ヒスチジン置換またはアラニン置換に起因した、pH5.4での解離の強化(すなわち、koff値がより高い)、ならびにb)抗体変異体自体、および出発ABPC(置換なし)での場合の、pH5.4と比較した、pH7.4での解離の低下(すなわち、koff値がより低い)。さらなる分析のために、図40に示されるように、(出発ABPCと比較して)pH5.4での解離の強化またはpH7.4での解離の低下のいずれか、または両方を示した重鎖変異体を選択した(例えば、MYT3619,MYT3626、MYT3627、MYT3628、MYT3629、MYT3630、MYT3632、MYT3633、MYT3634、MYT3635、MYT3636、MYT3637、MYT3638、MYT3639、MYT3640、MYT3641、MYT3642、MYT3643、MYT3646、MYT3647、MYT3651およびMYT3653)。また、一部のヒスチジンおよびアラニンの変異は、MET結合を消失させる一方で(例えば、MYT3624、MYT3645、MYT3648、MYT3649、MYT3650、MYT3652およびMYT3654)、他の変異は許容されるものであり、MET結合動態を、ほとんど変化させない(例えば、解離定数KDまたは解離速度の変化が1倍未満)または全く変化させない(例えば、MYT3618、MYT3620、MYT3621、MYT3622、MYT3623、MYT3625、MYT3631、MYT3644およびMYT3655)ことにも留意された。
特にヒスチジンは、正電荷をもつ大きいアミノ酸であるため、これら変化を伴わない変異体は、広範囲の変異を許容し得、また異なる配列であるが類似の結合特性を有する抗体、さもなければ明白ではない指定を有する抗体をもたらす可能性がある重鎖の位置として注目された。
実施例23.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性の結合を操作するための鋳型として使用することができる(Hicks,SWおよびLai,K 「MET抗体および免疫複合体およびその使用(MET Antibodies and Immunoconjugates and uses thereof)」 国際特許出願公開第2020/014306号(WO 2020/014306 A1)(2020))。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体としてhucMET27Gv1.3(重鎖は配列番号304、軽鎖は配列番号305)を選択した。簡潔に述べると、軽鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、軽鎖CDR内の個々のアミノ酸残基を、一度に一つ、ヒスチジンで系統的に置換した(MYT3656~MYT3686)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。軽鎖CDR中にただ一つのヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)一つの軽鎖配列変異体、およびb)対応する出発ABPCの重鎖を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図41)、変異体のpH依存性を、Octet RED 96e装置上のバイオレイヤーインターフェロメトリ(BLI)を使用して評価した。簡潔に述べると、細胞培養上清を、SDS-PAGEゲルの視覚的検査によって判定された変異体の定性的発現レベルに基づいて希釈し、高発現には5μLの細胞培養上清を195μLの1×PBST、pH7.4に希釈して、中発現には25μLの細胞培養上清を175μLの1×PBST、pH7.4に希釈して、低発現には100μLの細胞培養上清を100μLの1×PBST、pH7.4に希釈して、センサーチップにロードした。次いで、希釈上清を、抗ヒトFcセンサー(Forte Bio社)上で捕捉した。ベースラインは、1×PBST(50mMリン酸カリウム緩衝液+150mMのNaCl+0.05%のTween 20)pH7.4を使用して確立された。センサーは、1×PBST pH 7.4中の50nMのMET(cMET、Sino Biological社 カタログ番号10692-H08H)と120秒間結合され、結合曲線が作成された。解離相では、センサー上の抗体-抗原複合体を、300~600秒間、1×PBST pH7.4に曝露した。ベースライン、結合、および解離は、別個の条件下で全体を通じて1×PBST pH5.4を使用して繰り返された。結合相および解離相の曲線は、pH5.4およびpH7.4で、出発ABPC抗体(置換なし)およびそれぞれの対応する抗体変異体について検証され、以下の二つの基準についての情報を得る:a)出発ABPC(置換なし)と比較した、ヒスチジン置換またはアラニン置換に起因した、pH5.4での解離の強化(すなわち、koff値がより高い)、ならびにb)抗体変異体自体、および出発ABPC(置換なし)での場合の、pH5.4と比較した、pH7.4での解離の低下(すなわち、koff値がより低い)。さらなる分析のために、図42に示されるように、(出発ABPCと比較して)pH5.4での解離の強化またはpH7.4での解離の低下のいずれか、または両方を示した軽鎖変異体を選択した(例えば、MYT3658、MYT3662、MYT3663、MYT3666、MYT3668、MYT3670、MYT3671、MYT3673、MYT3674、MYT3677、MYT3678、MYT3680、MYT3684およびMYT3686)。また、一部のヒスチジンおよびアラニンの変異が許容されるものであり、MET結合動態を、ほとんど変化させない(例えば、解離定数KDまたは解離速度の変化が1倍未満)または全く変化させない(例えば、MYT3656、MYT3657、MYT3659、MYT3660、MYT3661、MYT3664、MYT3667、MYT3675、MYT3679、MYT3681、MYT3682、MYT3683およびMYT3685)ことにも留意された。特にヒスチジンは、正電荷をもつ大きいアミノ酸であるため、これら変化を伴わない変異体は、広範囲の変異を許容し得、また異なる配列であるが類似の結合特性を有する抗体、さもなければ明白ではない指定を有する抗体をもたらす可能性がある軽鎖の位置として注目された。
実施例24.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性の結合を操作するための鋳型として使用することができる(Hicks,SWおよびLai,K 「MET抗体および免疫複合体およびその使用(MET Antibodies and Immunoconjugates and uses thereof)」 国際特許出願公開第2020/014306号(WO 2020/014306 A1)(2020))。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体としてhucMET27Gv1.3(重鎖は配列番号304、軽鎖は配列番号305)を選択した。簡潔に述べると、重鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、実施例22においてさらなる分析のために先立って選択された、重鎖CDR内の個々のアミノ酸変異を、一度に二つ以上、系統的に組み合わせた(MYT4285~MYT4304)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。重鎖CDR中に二つ以上のヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)一つの重鎖組み合わせ配列変異体、およびb)対応する出発ABPCの軽鎖を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図43)、変異体のpH依存性を、Octet RED 96e装置上のバイオレイヤーインターフェロメトリ(BLI)を使用して評価した。簡潔に述べると、細胞培養上清を、SDS-PAGEゲルの視覚的検査によって判定された変異体の定性的発現レベルに基づいて希釈し、高発現には5μLの細胞培養上清を195μLの1×PBST、pH7.4に希釈して、中発現には25μLの細胞培養上清を175μLの1×PBST、pH7.4に希釈して、低発現には100μLの細胞培養上清を100μLの1×PBST、pH7.4に希釈して、センサーチップにロードした。次いで、希釈上清を、抗ヒトFcセンサー(Forte Bio社)上で捕捉した。ベースラインは、1×PBST(50mMリン酸カリウム緩衝液+150mMのNaCl+0.05%のTween 20)pH7.4を使用して確立された。センサーは、1×PBST pH 7.4中の50nMのMET(cMET、Sino Biological社 カタログ番号10692-H08H)と120秒間結合され、結合曲線が作成された。解離相では、センサー上の抗体-抗原複合体を、300~600秒間、1×PBST pH7.4に曝露した。ベースライン、結合、および解離は、別個の条件下で全体を通じて1×PBST pH5.4を使用して繰り返された。結合相および解離相の曲線は、pH5.4およびpH7.4で、出発ABPC抗体(置換なし)およびそれぞれの対応する抗体変異体について検証され、以下の二つの基準についての情報を得る:a)出発ABPC(置換なし)と比較した、ヒスチジン置換またはアラニン置換に起因した、pH5.4での解離の強化(すなわち、koff値がより高い)、ならびにb)抗体変異体自体、および出発ABPC(置換なし)での場合の、pH5.4と比較した、pH7.4での解離の低下(すなわち、koff値がより低い)。さらなる分析のために、図44に示されるように、(出発ABPCと比較して)pH5.4での解離の強化またはpH7.4での解離の低下のいずれか、または両方を示した重鎖組み合わせ変異体を選択した(例えば、MYT4285、MYT4286、MYT4287、MYT4288、MYT4289、MYT4290、MYT4291、MYT4292、MYT4293、MYT4294、MYT4296、MYT4297、MYT4299、MYT4300、MYT4301、MYT4302、MYT4303およびMYT4304。
実施例25.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性の結合を操作するための鋳型として使用することができる(Hicks,SWおよびLai,K 「MET抗体および免疫複合体およびその使用(MET Antibodies and Immunoconjugates and uses thereof)」 国際特許出願公開第2020/014306号(WO 2020/014306 A1)(2020))。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体としてhucMET27Gv1.3(重鎖は配列番号304、軽鎖は配列番号305)を選択した。簡潔に述べると、軽鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、実施例23においてさらなる分析のために先立って選択された、軽鎖CDR内の個々のアミノ酸変異を、一度に二つ以上、系統的に組み合わせた(MYT4222~MYT4241)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。軽鎖CDR中に二つ以上のヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)一つの軽鎖組み合わせ配列変異体、およびb)対応する出発ABPCの重鎖を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図45)、変異体のpH依存性を、Octet RED 96e装置上のバイオレイヤーインターフェロメトリ(BLI)を使用して評価した。簡潔に述べると、細胞培養上清を、SDS-PAGEゲルの視覚的検査によって判定された変異体の定性的発現レベルに基づいて希釈し、高発現には5μLの細胞培養上清を195μLの1×PBST、pH7.4に希釈して、中発現には25μLの細胞培養上清を175μLの1×PBST、pH7.4に希釈して、低発現には100μLの細胞培養上清を100μLの1×PBST、pH7.4に希釈して、センサーチップにロードした。次いで、希釈上清を、抗ヒトFcセンサー(Forte Bio社)上で捕捉した。ベースラインは、1×PBST(50mMリン酸カリウム緩衝液+150mMのNaCl+0.05%のTween 20)、pH7.4を使用して確立された。センサーは、1×PBST、pH 7.4中のMET(cMET、Sino Biological社 カタログ番号10692-H08H)と120秒間結合され、結合曲線が作成された。解離相では、センサー上の抗体-抗原複合体を、300~600秒間、1×PBST、pH7.4に曝露した。ベースライン、結合、および解離は、別個の条件下で全体を通じて1×PBST、pH5.4を使用して繰り返された。結合相および解離相の曲線は、pH5.4およびpH7.4で、出発ABPC抗体(置換なし)およびそれぞれの対応する抗体変異体について検証され、以下の二つの基準についての情報を得る:a)出発ABPC(置換なし)と比較した、ヒスチジン置換またはアラニン置換に起因した、pH5.4での解離の強化(例えば、koff値がより高い)、ならびにb)抗体変異体自体、および出発ABPC(置換なし)での場合の、pH5.4と比較した、pH7.4での解離の低下(例えば、koff値がより低い)。さらなる分析のために、図46に示されるように、(出発ABPCと比較して)pH5.4での解離の強化またはpH7.4での解離の低下のいずれか、または両方を示した軽鎖組み合わせ変異体を選択した(例えば、MYT4224、MYT4225、MYT4226、MYT4227、MYT4228、MYT4229、MYT4230、MYT4231、MYT4232、MYT4233、MYT4234、MYT4235、MYT4236、MYT4237、MYT4238、MYT4239、MYT4240およびMYT4241)。
実施例26.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性の結合を操作するための鋳型として使用することができる(Hicks,SWおよびLai,K 「MET抗体および免疫複合体およびその使用(MET Antibodies and Immunoconjugates and uses thereof)」 国際特許出願公開第2020/014306号(WO 2020/014306 A1)(2020))。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体としてhucMET27Gv1.3(重鎖は配列番号304、軽鎖は配列番号305)を選択した。簡潔に述べると、重鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、実施例22においてさらなる分析のために先立って選択された、重鎖CDR内の個々のアミノ酸変異を、一度に二つ以上、系統的に組み合わせた(MYT5296およびMYT5042~MYT5065)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。重鎖CDR中に二つ以上のヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)それぞれ(Wang J et al(2017)ABBV-399,a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors,Irrespective of MET Pathway Dependence,Clin Cancer Res,23:992-1000)および(Dall,WF et al “Increasing the Affinity of a Human IgG1 for the Neonatal Fc Receptor: Biological Consequences” The Journal of Immunology(2002); 169:5171-5180)に記載されている、トリプルヒンジ(TH)およびYTE変異を含有する一つの重鎖組み合わせ配列変異体、ならびにb)対応する出発ABPCの軽鎖を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図47)、プロテインA磁気ビーズ(Genscript社 L00273)を使用して精製して、Detroit 562細胞(ATCC社 CCL-138)でのエンドリソソーム送達を評価した。Detroit 562細胞(ATCC社;CCL-138)を回収して、EMEM培地(ATCC社;30-2003)+10% GenClone熱不活性化ウシ胎児血清(HI FBS)(Genesee Scientific社;25-514H)中で再懸濁した。細胞数は、トリパンブルー染色およびCountess II FL自動セルカウンター(Thermofisher社;AMQAF1000)を使用して決定した。次いで細胞を100,000細胞/mLに希釈し、100ulを96ウェルの平底細胞培養プレートに播種し、37C、5%CO2中で一晩付着させた。次いで、一次抗体をネイティブ培養培地中で20nMに希釈し、次いで60nMのIncucyte Human FabFluor-pH赤色抗体標識試薬(Sartorius社;4722)と1:1で混合した。混合物を室温で20分間インキュベートし、続いて細胞に添加した。次いで、プレートをIncucyte S3 Live-Cell分析システムに直ちに入れて、画像取得および分析を行った。出発ABPC抗体(置換なし)および対応する各抗体変異体についてエンドリソソーム送達を調べて、出発ABPC(置換なし)と比較してヒスチジンまたはアラニン置換に起因して強化されたエンドリソソーム送達について情報を得た。
実施例27.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性の結合を操作するための鋳型として使用することができる(Hicks,SWおよびLai,K 「MET抗体および免疫複合体およびその使用(MET Antibodies and Immunoconjugates and uses thereof)」 国際特許出願公開第2020/014306号(WO 2020/014306 A1)(2020))。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体としてhucMET27Gv1.3(重鎖は配列番号304、軽鎖は配列番号305)を選択した。簡潔に述べると、軽鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、実施例23においてさらなる分析のために先立って選択された、軽鎖CDR内の個々のアミノ酸変異を、一度に二つ以上、系統的に組み合わせた(MYT5066~MYT5121)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。軽鎖CDR中に二つ以上のヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)一つの軽鎖組み合わせ配列変異体、ならびにb)それぞれ(Wang J et al(2017)ABBV-399,a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors,Irrespective of MET Pathway Dependence,Clin Cancer Res,23:992-1000)および(Dall,WF et al “Increasing the Affinity of a Human IgG1 for the Neonatal Fc Receptor: Biological Consequences” The Journal of Immunology(2002); 169:5171-5180)に記載されている、トリプルヒンジ(TH)およびYTE変異を含有する対応する出発ABPCの重鎖を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図48)、プロテインA磁気ビーズ(Genscript社 L00273)を使用して精製して、Detroit 562細胞(ATCC社 CCL-138)でのエンドリソソーム送達を評価した。Detroit 562細胞(ATCC社;CCL-138)を回収して、EMEM培地(ATCC社;30-2003)+10% GenClone熱不活性化ウシ胎児血清(HI FBS)(Genesee Scientific社;25-514H)中で再懸濁した。細胞数は、トリパンブルー染色およびCountess II FL自動セルカウンター(Thermofisher社;AMQAF1000)を使用して決定した。次いで細胞を100,000細胞/mLに希釈し、100ulを96ウェルの平底細胞培養プレートに播種し、37C、5%CO2中で一晩付着させた。次いで、一次抗体をネイティブ培養培地中で20nMに希釈し、次いで60nMのIncucyte Human FabFluor-pH赤色抗体標識試薬(Sartorius社;4722)と1:1で混合した。混合物を室温で20分間インキュベートし、続いて細胞に添加した。次いで、プレートをIncucyte S3 Live-Cell分析システムに直ちに入れて、画像取得および分析を行った。エンドリソソーム送達は、出発ABPC抗体(置換なし)および対応する各抗体変異体について調べて、出発ABPC(置換なし)と比較してヒスチジンまたはアラニン置換に起因して強化されたエンドリソソーム送達について情報を得た。さらなる分析のために、図49に示されるように、(出発ABPCと比較して)エンドリソソーム送達の強化を示した軽鎖組み合わせ変異体を選択した(例えば、MYT5066、MYT5070、MYT5071、MYT5073、MYT5077、MYT5082、MYT5083、MYT5085、MYT5090、MYT5092、MYT5093、MYT5094、MYT5096、MYT5099、MYT5102、MYT5103、MYT5105、MYT5110、MYT5112、MYT5114、MYT5116およびMYT5119)。選択された変異体のpH依存性を、Octet RED 96e装置上のバイオレイヤーインターフェロメトリ(BLI)を使用して評価した。簡潔に述べると、細胞培養上清を、SDS-PAGEゲルの視覚的検査によって判定された変異体の定性的発現レベルに基づいて希釈し、高発現には5μLの細胞培養上清を195μLの1×PBST、pH7.4に希釈して、中発現には25μLの細胞培養上清を175μLの1×PBST、pH7.4に希釈して、低発現には100μLの細胞培養上清を100μLの1×PBST、pH7.4に希釈して、センサーチップにロードした。次いで、希釈上清を、抗ヒトFcセンサー(Forte Bio社)上で捕捉した。ベースラインは、1×PBST(50mMリン酸カリウム緩衝液+150mMのNaCl+0.05%のTween 20)、pH7.4を使用して確立された。センサーは、1×PBST、pH 7.4中のMET(cMET、Sino Biological社 カタログ番号10692-H08H)と120秒間結合され、結合曲線が作成された。解離相では、センサー上の抗体-抗原複合体を、300~600秒間、1×PBST、pH7.4またはpH5.4に曝露した。結合相および解離相の曲線は、pH7.4およびpH5.4で、出発ABPC抗体(置換なし)およびそれぞれの対応する抗体変異体について検証され、以下の二つの基準についての情報を得る:a)出発ABPC(置換なし)と比較した、ヒスチジン置換またはアラニン置換に起因した、pH5.4での解離の強化(例えば、koff値がより高い)、ならびにb)抗体変異体自体、および出発ABPC(置換なし)での場合の、pH5.4と比較した、pH7.4での解離の低下(例えば、koff値がより低い)。さらなる分析のために、図50に示されるように、(出発ABPCと比較して)pH5.4での解離の強化またはpH7.4での解離の低下のいずれか、または両方を示した軽鎖組み合わせ変異体を選択した(例えば、MYT5066、MYT5070、MYT5071、MYT5073、MYT5077、MYT5082、MYT5083、MYT5085、MYT5090、MYT5092、MYT5093、MYT5094、MYT5096、MYT5099、MYT5102、MYT5103、MYT5110、MYT5112およびMYT5119)。
実施例28.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性の結合を操作するための鋳型として使用することができる(Fujita,R et al(2020)A Novel Non-Agonist c-Met Antibody Drug Conjugate with Superior Potency Over a c-Met Tyrosine Kinase Inhibitor in c-Met Amplified and Non-Amplified Cancers,Cancer Biology and Therapy,21(6):549-559)。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体としてP3D12(重鎖は配列番号502、軽鎖は配列番号503)を選択した。簡潔に述べると、重鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、重鎖CDR内の個々のアミノ酸残基を、一度に一つ、ヒスチジンで系統的に置換した(MYT3688~MYT3726)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。重鎖CDR中にただ一つのヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)一つの重鎖配列変異体、およびb)対応する出発ABPCの軽鎖を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図57)、変異体のpH依存性を、Octet RED 96e装置上のバイオレイヤーインターフェロメトリ(BLI)を使用して評価した。簡潔に述べると、細胞培養上清を、SDS-PAGEゲルの視覚的検査によって判定された変異体の定性的発現レベルに基づいて希釈し、高発現には5μLの細胞培養上清を195μLの1×PBST、pH7.4に希釈して、中発現には25μLの細胞培養上清を175μLの1×PBST、pH7.4に希釈して、低発現には100μLの細胞培養上清を100μLの1×PBST、pH7.4に希釈して、センサーチップにロードした。 次いで、この希釈上清を、抗ヒトFcセンサー(Forte Bio社)上で捕捉した。ベースラインは、1×PBST(50mMリン酸カリウム緩衝液+150mMのNaCl+0.05%のTween 20)pH7.4を使用して確立された。センサーは、1×PBST pH 7.4中の50nMのMET(cMET、Sino Biological社 カタログ番号10692-H08H)と120秒間結合され、結合曲線が作成された。解離相では、センサー上の抗体-抗原複合体を、300~600秒間、1×PBST pH7.4に曝露した。ベースライン、結合、および解離は、別個の条件下で全体を通じて1xPBST pH5.4を使用して繰り返された。
結合相および解離相の曲線は、pH5.4およびpH7.4で、出発ABPC抗体(置換なし)およびそれぞれの対応する抗体変異体について検証され、以下の二つの基準についての情報を得る:a)出発ABPC(置換なし)と比較した、ヒスチジン置換またはアラニン置換に起因した、pH5.4での解離の強化(すなわち、koff値がより高い)、ならびにb)抗体変異体自体、および出発ABPC(置換なし)での場合の、pH5.4と比較した、pH7.4での解離の低下(すなわち、koff値がより低い)。さらなる分析のために、図58に示されるように、(出発ABPCと比較して)pH5.4での解離の強化またはpH7.4での解離の低下のいずれか、または両方を示した重鎖変異体を選択した(例えば、MYT3689、MYT3691、MYT3692、MYT3694、MYT3695、MYT3696、MYT3697、MYT3698、MYT3699、MYT3700、MYT3701、MYT3705、MYT3707、MYT3716、MYT3718、MYT3719、MYT3720、MYT3721、MYT3724およびMYT3725)。また、一部のヒスチジンおよびアラニンの変異が許容されるものであり、MET結合動態を、ほとんど変化させない(例えば、解離定数KDまたは解離速度の変化が1倍未満)または全く変化させない(例えば、MYT3688、MYT3690、MYT3693、MYT3702、MYT3703、MYT3704、MYT3706、MYT3708、MYT3709、MYT3710、MYT3711、MYT3712、MYT3713、MYT3714、MYT3717およびMYT3726)ことにも留意された。
特にヒスチジンは、正電荷をもつ大きいアミノ酸であるため、これら変化を伴わない変異体は、広範囲の変異を許容し得、また異なる配列であるが類似の結合特性を有する抗体、さもなければ明白ではない指定を有する抗体をもたらす可能性がある重鎖の位置として注目された。
実施例29.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性の結合を操作するための鋳型として使用することができる(Fujita,R et al(2020)A Novel Non-Agonist c-Met Antibody Drug Conjugate with Superior Potency Over a c-Met Tyrosine Kinase Inhibitor in c-Met Amplified and Non-Amplified Cancers,Cancer Biology and Therapy,21(6):549-559)。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体としてP3D12(重鎖は配列番号502、軽鎖は配列番号503)を選択した。簡潔に述べると、軽鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、軽鎖CDR内の個々のアミノ酸残基を、一度に一つ、ヒスチジンで系統的に置換した(MYT3727~MYT3754)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。軽鎖CDR中にただ一つのヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)一つの軽鎖配列変異体、およびb)対応する出発ABPCの重鎖を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図59)、変異体のpH依存性を、Octet RED 96e装置上のバイオレイヤーインターフェロメトリ(BLI)を使用して評価した。簡潔に述べると、細胞培養上清を、SDS-PAGEゲルの視覚的検査によって判定された変異体の定性的発現レベルに基づいて希釈し、高発現には5μLの細胞培養上清を195μLの1×PBST、pH7.4に希釈して、中発現には25μLの細胞培養上清を175μLの1×PBST、pH7.4に希釈して、低発現には100μLの細胞培養上清を100μLの1×PBST、pH7.4に希釈して、センサーチップにロードした。次いで、希釈上清を、抗ヒトFcセンサー(Forte Bio社)上で捕捉した。ベースラインは、1×PBST(50mMリン酸カリウム緩衝液+150mMのNaCl+0.05%のTween 20)pH7.4を使用して確立された。センサーは、1×PBST pH 7.4中の50nMのMET(cMET、Sino Biological社 カタログ番号10692-H08H)と120秒間結合され、結合曲線が作成された。解離相では、センサー上の抗体-抗原複合体を、300~600秒間、1×PBST pH7.4に曝露した。ベースライン、結合、および解離は、別個の条件下で全体を通じて1×PBST pH5.4を使用して繰り返された。結合相および解離相の曲線は、pH5.4およびpH7.4で、出発ABPC抗体(置換なし)およびそれぞれの対応する抗体変異体について検証され、以下の二つの基準についての情報を得る:a)出発ABPC(置換なし)と比較した、ヒスチジン置換またはアラニン置換に起因した、pH5.4での解離の強化(すなわち、koff値がより高い)、ならびにb)抗体変異体自体、および出発ABPC(置換なし)での場合の、pH5.4と比較した、pH7.4での解離の低下(すなわち、koff値がより低い)。さらなる分析のために、図60に示されるように、(出発ABPCと比較して)pH5.4での解離の強化またはpH7.4での解離の低下のいずれか、または両方を示した軽鎖変異体を選択した(例えば、MYT3728、MYT3732、MYT3734、MYT3735、MYT3736、MYT3737、MYT3738、MYT3740、MYT3743、MYT3747、MYT3748、MYT3749、MYT3750、MYT3751、MYT3752、MYT3753およびMYT3754)。また、一部のヒスチジン変異およびアラニン変異が許容されるものであり、MET結合動態を、ほとんど変化させない(例えば、解離定数KDまたは解離速度の変化が1倍未満)または全く変化させない(例えば、MYT3727、MYT3729、MYT3730、MYT3731、MYT3733、MYT3739、MYT3741、MYT3742、MYT3744、MYT3745およびMYT3746)ことにも留意された。特にヒスチジンは、正電荷をもつ大きいアミノ酸であるため、これら変化を伴わない変異体は、広範囲の変異を許容し得、また異なる配列であるが類似の結合特性を有する抗体、さもなければ明白ではない指定を有する抗体をもたらす可能性がある軽鎖の位置として注目された。
実施例30.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性の結合を操作するための鋳型として使用することができる(Fujita,R et al(2020)A Novel Non-Agonist c-Met Antibody Drug Conjugate with Superior Potency Over a c-Met Tyrosine Kinase Inhibitor in c-Met Amplified and Non-Amplified Cancers,Cancer Biology and Therapy,21(6):549-559)。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体としてP3D12(重鎖は配列番号502、軽鎖は配列番号503)を選択した。簡潔に述べると、重鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、実施例28においてさらなる分析のために先立って選択された、重鎖CDR内の個々のアミノ酸変異を、一度に二つ以上、系統的に組み合わせた(MYT4306~MYT4325)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。重鎖CDR中に二つ以上のヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)一つの重鎖組み合わせ配列変異体、およびb)対応する出発ABPCの軽鎖を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図61)、変異体のpH依存性を、Octet RED 96e装置上のバイオレイヤーインターフェロメトリ(BLI)を使用して評価した。簡潔に述べると、細胞培養上清を、SDS-PAGEゲルの視覚的検査によって判定された変異体の定性的発現レベルに基づいて希釈し、高発現には5μLの細胞培養上清を195μLの1×PBST、pH7.4に希釈して、中発現には25μLの細胞培養上清を175μLの1×PBST、pH7.4に希釈して、低発現には100μLの細胞培養上清を100μLの1×PBST、pH7.4に希釈して、センサーチップにロードした。次いで、希釈上清を、抗ヒトFcセンサー(Forte Bio社)上で捕捉した。ベースラインは、1×PBST(50mMリン酸カリウム緩衝液+150mMのNaCl+0.05%のTween 20)pH7.4を使用して確立された。センサーは、1×PBST pH 7.4中の50nMのMET(cMET、Sino Biological社 カタログ番号10692-H08H)と120秒間結合され、結合曲線が作成された。解離相では、センサー上の抗体-抗原複合体を、300~600秒間、1×PBST pH7.4に曝露した。ベースライン、結合、および解離は、別個の条件下で全体を通じて1×PBST pH5.4を使用して繰り返された。結合相および解離相の曲線は、pH5.4およびpH7.4で、出発ABPC抗体(置換なし)およびそれぞれの対応する抗体変異体について検証され、以下の二つの基準についての情報を得る:a)出発ABPC(置換なし)と比較した、ヒスチジン置換またはアラニン置換に起因した、pH5.4での解離の強化(すなわち、koff値がより高い)、ならびにb)抗体変異体自体、および出発ABPC(置換なし)での場合の、pH5.4と比較した、pH7.4での解離の低下(すなわち、koff値がより低い)。さらなる分析のために、図62に示されるように、(出発ABPCと比較して)pH5.4での解離の強化またはpH7.4での解離の低下のいずれか、または両方を示した重鎖組み合わせ変異体を選択した(例えば、MYT4307、MYT4308、MYT4309、MYT4310、MYT4311、MYT4312、MYT4313、MYT4314、MYT4315、MYT4316、MYT4317、MYT4318、MYT4319、MYT4320、MYT4321、MYT4322、MYT4323、MYT4324およびMYT4325)。
実施例31.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性の結合を操作するための鋳型として使用することができる(Fujita,R et al(2020)A Novel Non-Agonist c-Met Antibody Drug Conjugate with Superior Potency Over a c-Met Tyrosine Kinase Inhibitor in c-Met Amplified and Non-Amplified Cancers,Cancer Biology and Therapy,21(6):549-559)。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体としてP3D12(重鎖は配列番号502、軽鎖は配列番号503)を選択した。簡潔に述べると、軽鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、実施例29においてさらなる分析のために先立って選択された、軽鎖CDR内の個々のアミノ酸変異を、一度に二つ以上、系統的に組み合わせた(MYT4242~MYT4261)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。軽鎖CDR中に二つ以上のヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)一つの軽鎖組み合わせ配列変異体、およびb)対応する出発ABPCの重鎖を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図63)、変異体のpH依存性を、Octet RED 96e装置上のバイオレイヤーインターフェロメトリ(BLI)を使用して評価した。簡潔に述べると、細胞培養上清を、SDS-PAGEゲルの視覚的検査によって判定された変異体の定性的発現レベルに基づいて希釈し、高発現には5μLの細胞培養上清を195μLの1×PBST、pH7.4に希釈して、中発現には25μLの細胞培養上清を175μLの1×PBST、pH7.4に希釈して、低発現には100μLの細胞培養上清を100μLの1×PBST、pH7.4に希釈して、センサーチップにロードした。次いで、希釈上清を、抗ヒトFcセンサー(Forte Bio社)上で捕捉した。ベースラインは、1×PBST(50mMリン酸カリウム緩衝液+150mMのNaCl+0.05%のTween 20)、pH7.4を使用して確立された。センサーは、1×PBST、pH 7.4中のMET(cMET、Sino Biological社 カタログ番号10692-H08H)と120秒間結合され、結合曲線が作成された。解離相では、センサー上の抗体-抗原複合体を、300~600秒間、1×PBST、pH7.4に曝露した。ベースライン、結合、および解離は、別個の条件下で全体を通じて1×PBST、pH5.4を使用して繰り返された。結合相および解離相の曲線は、pH5.4およびpH7.4で、出発ABPC抗体(置換なし)およびそれぞれの対応する抗体変異体について検証され、以下の二つの基準についての情報を得る:a)出発ABPC(置換なし)と比較した、ヒスチジン置換またはアラニン置換に起因した、pH5.4での解離の強化(例えば、koff値がより高い)、ならびにb)抗体変異体自体、および出発ABPC(置換なし)での場合の、pH5.4と比較した、pH7.4での解離の低下(例えば、koff値がより低い)。さらなる分析のために、図64に示されるように、(出発ABPCと比較して)pH5.4での解離の強化またはpH7.4での解離の低下のいずれか、または両方を示した軽鎖組み合わせ変異体を選択した(例えば、MYT4242、MYT4243、MYT4244、MYT4245、MYT4246、MYT4247、MYT4248、MYT4249、MYT4250、MYT4251、MYT4252、MYT4253、MYT4254、MYT4255、MYT4256、MYT4257およびMYT4258)。
実施例32.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性の結合を操作するための鋳型として使用することができる(Fujita,R et al(2020)A Novel Non-Agonist c-Met Antibody Drug Conjugate with Superior Potency Over a c-Met Tyrosine Kinase Inhibitor in c-Met Amplified and Non-Amplified Cancers,Cancer Biology and Therapy,21(6):549-559)。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体としてP3D12(重鎖は配列番号502、軽鎖は配列番号503)を選択した。簡潔に述べると、重鎖および軽鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、実施例28~31においてさらなる分析のために先立って選択された、重鎖および軽鎖のCDR内の個々のアミノ酸変異を、一度に二つ以上、系統的に組み合わせた(MYT5342~MYT5381)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。二つ以上のヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)一つの軽鎖配列変異体または軽鎖組み合わせ配列変異体、およびb)一つの重鎖配列変異体または重鎖組み合わせ配列変異体を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図82)、変異体のpH依存性を、Octet RED 96e装置上のバイオレイヤーインターフェロメトリ(BLI)を使用して評価した。簡潔に述べると、細胞培養上清を、SDS-PAGEゲルの視覚的検査によって判定された変異体の定性的発現レベルに基づいて希釈し、高発現には5μLの細胞培養上清を195μLの1×PBST、pH7.4に希釈して、中発現には25μLの細胞培養上清を175μLの1×PBST、pH7.4に希釈して、低発現には100μLの細胞培養上清を100μLの1×PBST、pH7.4に希釈して、センサーチップにロードした。次いで、希釈上清を、抗ヒトFcセンサー(Forte Bio社)上で捕捉した。ベースラインは、1×PBST(50mMリン酸カリウム緩衝液+150mMのNaCl+0.05%のTween 20)、pH7.4を使用して確立された。センサーは、1×PBST、pH 7.4中の50nMのMET(cMET、Sino Biological社 カタログ番号10692-H08H)と120秒間結合され、結合曲線が作成された。解離相では、センサー上の抗体-抗原複合体を、300~600秒間、1×PBST、pH7.4またはpH5.4に曝露した。結合相および解離相の曲線は、pH5.4およびpH7.4で、出発ABPC抗体(置換なし)およびそれぞれの対応する抗体変異体について検証され、以下の二つの基準についての情報を得る:a)出発ABPC(置換なし)と比較した、ヒスチジン置換またはアラニン置換に起因した、pH5.4での解離の強化(例えば、koff値がより高い)、ならびにb)抗体変異体自体、および出発ABPC(置換なし)での場合の、pH5.4と比較した、pH7.4での解離の低下(例えば、koff値がより低い)。さらなる分析のために、図83に示されるように、(出発ABPCと比較して)pH5.4での解離の強化またはpH7.4での解離の低下のいずれか、または両方を示した、対の重鎖および軽鎖変異体を選択した(例えば、MYT5342、MYT5343、MYT5344、MYT5345、MYT5346、MYT5350、MYT5351、MYT5352、MYT5353、MYT5354、MYT5355、MYT5356、MYT5357、MYT5359、MYT5360、MYT5366、MYT5367、MYT5368、MYT5369、MYT5370、MYT5372、MYT5373、MYT5374、MYT5375、MYT5376、MYT5377およびMYT5381)。
実施例33.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性の結合を操作するための鋳型として使用することができる(Fujita,R et al(2020)A Novel Non-Agonist c-Met Antibody Drug Conjugate with Superior Potency Over a c-Met Tyrosine Kinase Inhibitor in c-Met Amplified and Non-Amplified Cancers,Cancer Biology and Therapy,21(6):549-559)。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体としてP3D12(重鎖は配列番号502、軽鎖は配列番号503)を選択した。簡潔に述べると、重鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、実施例28においてさらなる分析のために先立って選択された、重鎖CDR内の個々のアミノ酸変異を、一度に二つ以上、系統的に組み合わせた(MYT5122~MYT5221)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。重鎖CDR中に二つ以上のヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)それぞれ(Wang J et al(2017)ABBV-399,a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors,Irrespective of MET Pathway Dependence,Clin Cancer Res,23:992-1000)および(Dall,WF et al “Increasing the Affinity of a Human IgG1 for the Neonatal Fc Receptor: Biological Consequences” The Journal of Immunology(2002); 169:5171-5180)に記載されている、トリプルヒンジ(TH)およびYTE変異を含有する一つの重鎖組み合わせ配列変異体、ならびにb)対応する出発ABPCの軽鎖を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図65)、プロテインA磁気ビーズ(Genscript社 L00273)を使用して精製して、Detroit 562細胞(ATCC社 CCL-138)でのエンドリソソーム送達を評価した。簡潔には、Detroit 562細胞(ATCC社;CCL-138)を回収して、EMEM培地(ATCC社;30-2003)+10% GenClone熱不活性化ウシ胎児血清(HI FBS)(Genesee Scientific社;25-514H)中で再懸濁した。細胞数は、トリパンブルー染色およびCountess II FL自動セルカウンター(Thermofisher社;AMQAF1000)を使用して決定した。次いで細胞を100,000細胞/mLに希釈し、100ulを96ウェルの平底細胞培養プレートに播種し、37C、5%CO2中で一晩付着させた。次いで、一次抗体をネイティブ培養培地中で20nMに希釈し、次いで60nMのIncucyte Human FabFluor-pH赤色抗体標識試薬(Sartorius社;4722)と1:1で混合した。混合物を室温で20分間インキュベートし、続いて細胞に添加した。次いで、プレートをIncucyte S3 Live-Cell分析システムに直ちに入れて、画像取得および分析を行った。出発ABPC抗体(置換なし)および対応する各抗体変異体についてエンドリソソーム送達を調べて、出発ABPC(置換なし)と比較してヒスチジンまたはアラニン置換に起因して強化されたエンドリソソーム送達について情報を得た。さらなる分析のために、図66に示すように、(出発ABPCと比較して)強化されたエンドリソソーム送達を示した重鎖組み合わせ変異体を選択した(例えば、MYT5122、MYT5131、MYT5146、MYT5184およびMYT5201)。選択された変異体のpH依存性を、Octet RED 96e装置上のバイオレイヤーインターフェロメトリ(BLI)を使用して評価した。簡潔に述べると、細胞培養上清を、SDS-PAGEゲルの視覚的検査によって判定された変異体の定性的発現レベルに基づいて希釈し、高発現には5μLの細胞培養上清を195μLの1×PBST、pH7.4に希釈して、中発現には25μLの細胞培養上清を175μLの1×PBST、pH7.4に希釈して、低発現には100μLの細胞培養上清を100μLの1×PBST、pH7.4に希釈して、センサーチップにロードした。次いで、希釈上清を、抗ヒトFcセンサー(Forte Bio社)上で捕捉した。ベースラインは、1×PBST(50mMリン酸カリウム緩衝液+150mMのNaCl+0.05%のTween 20)、pH7.4を使用して確立された。センサーは、1×PBST、pH 7.4中のMET(cMET、Sino Biological社 カタログ番号10692-H08H)と120秒間結合され、結合曲線が作成された。解離相では、センサー上の抗体-抗原複合体を、300~600秒間、1×PBST、pH7.4またはpH5.4に曝露した。結合相および解離相の曲線は、pH7.4およびpH5.4で、出発ABPC抗体(置換なし)およびそれぞれの対応する抗体変異体について検証され、以下の二つの基準についての情報を得る:a)出発ABPC(置換なし)と比較した、ヒスチジン置換またはアラニン置換に起因した、pH5.4での解離の強化(例えば、koff値がより高い)、ならびにb)抗体変異体自体、および出発ABPC(置換なし)での場合の、pH5.4と比較した、pH7.4での解離の低下(例えば、koff値がより低い)。さらなる分析のために、図67に示されるように、(出発ABPCと比較して)pH5.4での解離の強化またはpH7.4での解離の低下のいずれか、または両方を示した重鎖組み合わせ変異体を選択した(例えば、MYT5122、MYT5131、MYT5146、MYT5184およびMYT5201)。
実施例34.pH操作されたMET ABPCの構築およびスクリーニング
複数のMET結合モノクローナル抗体が文献に記載されており、pH依存性の結合を操作するための鋳型として使用することができる(Fujita,R et al(2020)A Novel Non-Agonist c-Met Antibody Drug Conjugate with Superior Potency Over a c-Met Tyrosine Kinase Inhibitor in c-Met Amplified and Non-Amplified Cancers,Cancer Biology and Therapy,21(6):549-559)。本発明者らは、ヒスチジンスキャニングを介してpH操作するMET結合モノクローナル抗体としてP3D12(重鎖は配列番号502、軽鎖は配列番号503)を選択した。簡潔に述べると、軽鎖中のCDRを、Kabatら(Kabat et al.(1992)Sequences of Proteins of Immunological Interest,DIANE publishing)により記載された方法、およびIMGT(Lefranc MP(1999)“The IMGT unique numbering for Immunoglobulins,T cell receptors and Ig-like domains”The Immunologist 7,132-136)を用いて特定し、そして各CDRについて、KabatおよびIMGTのCDR定義のいずれかまたは両方に該当する残基をCDR残基と呼んだ。pH依存性配列変異体を生成するために、実施例29においてさらなる分析のために先立って選択された、軽鎖CDR内の個々のアミノ酸変異を、一度に二つ以上、系統的に組み合わせた(MYT5222~MYT5295)。出発CDR残基がヒスチジンであった場合には、アラニンに変異された。軽鎖CDR中に二つ以上のヒスチジンまたはアラニン変異を有する抗体変異体は、当技術分野で公知の方法を使用して、a)一つの軽鎖組み合わせ配列変異体、ならびにb)それぞれ(Wang J et al(2017)ABBV-399,a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors,Irrespective of MET Pathway Dependence,Clin Cancer Res,23:992-1000)および(Dall,WF et al “Increasing the Affinity of a Human IgG1 for the Neonatal Fc Receptor: Biological Consequences” The Journal of Immunology(2002); 169:5171-5180)に記載されている、トリプルヒンジ(TH)およびYTE変異を含有する対応する出発ABPCの重鎖を用いて、Expi293細胞の同時トランスフェクションにより生成した。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図68)、プロテインA磁気ビーズ(Genscript社 L00273)を使用して精製して、Detroit 562細胞(ATCC社 CCL-138)でのエンドリソソーム送達を評価した。簡潔には、Detroit 562細胞(ATCC社;CCL-138)を回収して、EMEM培地(ATCC社;30-2003)+10% GenClone熱不活性化ウシ胎児血清(HI FBS)(Genesee Scientific社;25-514H)中で再懸濁した。細胞数は、トリパンブルー染色およびCountess II FL自動セルカウンター(Thermofisher社;AMQAF1000)を使用して決定した。次いで細胞を100,000細胞/mLに希釈し、100ulを96ウェルの平底細胞培養プレートに播種し、37C、5%CO2中で一晩付着させた。次いで、一次抗体をネイティブ培養培地中で20nMに希釈し、次いで60nMのIncucyte Human FabFluor-pH赤色抗体標識試薬(Sartorius社;4722)と1:1で混合した。混合物を室温で20分間インキュベートし、続いて細胞に添加した。次いで、プレートをIncucyte S3 Live-Cell分析システムに直ちに入れて、画像取得および分析を行った。出発ABPC抗体(置換なし)および対応する各抗体変異体についてエンドリソソーム送達を調べて、出発ABPC(置換なし)と比較してヒスチジンまたはアラニン置換に起因して強化されたエンドリソソーム送達について情報を得た。さらなる分析のために、図69に示されるように、(出発ABPCと比較して)エンドリソソーム送達の強化を示した軽鎖組み合わせ変異体を選択した(例えば、MYT5237)。選択された変異体のpH依存性を、Octet RED 96e装置上のバイオレイヤーインターフェロメトリ(BLI)を使用して評価した。簡潔に述べると、細胞培養上清を、SDS-PAGEゲルの視覚的検査によって判定された変異体の定性的発現レベルに基づいて希釈し、高発現には5μLの細胞培養上清を195μLの1×PBST、pH7.4に希釈して、中発現には25μLの細胞培養上清を175μLの1×PBST、pH7.4に希釈して、低発現には100μLの細胞培養上清を100μLの1×PBST、pH7.4に希釈して、センサーチップにロードした。次いで、希釈上清を、抗ヒトFcセンサー(Forte Bio社)上で捕捉した。ベースラインは、1×PBST(50mMリン酸カリウム緩衝液+150mMのNaCl+0.05%のTween 20)、pH7.4を使用して確立された。センサーは、1×PBST、pH 7.4中のMET(cMET、Sino Biological社 カタログ番号10692-H08H)と120秒間結合され、結合曲線が作成された。解離相では、センサー上の抗体-抗原複合体を、300~600秒間、1×PBST、pH7.4またはpH5.4に曝露した。結合相および解離相の曲線は、pH7.4およびpH5.4で、出発ABPC抗体(置換なし)およびそれぞれの対応する抗体変異体について検証され、以下の二つの基準についての情報を得る:a)出発ABPC(置換なし)と比較した、ヒスチジン置換またはアラニン置換に起因した、pH5.4での解離の強化(例えば、koff値がより高い)、ならびにb)抗体変異体自体、および出発ABPC(置換なし)での場合の、pH5.4と比較した、pH7.4での解離の低下(例えば、koff値がより低い)。さらなる分析のために、図70に示されるように、(出発ABPCと比較して)pH5.4での解離の強化またはpH7.4での解離の低下のいずれか、または両方を示した軽鎖組み合わせ変異体を選択した(例えば、MYT5237)。
実施例35.抗MET ABPCの再フォーマット
選択されたpH操作された抗MET変異体を、両方の野生型IgG1分子(例えば、実施例9~13、16~20、22~25、および28~32における)として、ならびに(Wang J et al(2017)ABBV-399,a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors,Irrespective of MET Pathway Dependence,Clin Cancer Res,23:992-1000)に記載されるトリプルヒンジ(TH)変異および(Dall,WF et al “Increasing the Affinity of a Human IgG1 for the Neonatal Fc Receptor: Biological Consequences” The Journal of Immunology(2002); 169:5171-5180)に記載されるYTE変異を含有するIgG1分子として、THおよびYTE変異を有するまたはTHおよびYTE変異を有しないヒトIgG1 Fcに遺伝子的に融合された可変重鎖領域をコードするプラスミドを用いて、Expi293細胞のトランスフェクションによって、生成した(図80)。当技術分野で公知の方法を使用して、a)可変重鎖領域と、野生型ヒトIgG1アイソタイプまたはTHおよびYTE変異を除いてそれと同じ配列のいずれかに対応する定常領域とからなる一つの重鎖配列、ならびにb)一つの軽鎖配列を用いた、Expi293細胞の同時トランスフェクションである。タンパク質を4日間発現させたあと、細胞培養上清を収集し、SDS-PAGE分析により定量して(図77に示す選択された実施例)、変異体のpH依存性を、Octet RED 96e装置上のバイオレイヤーインターフェロメトリ(BLI)を使用して評価した。簡潔に述べると、細胞培養上清を、SDS-PAGEゲルの視覚的検査によって判定された変異体の定性的発現レベルに基づいて希釈し、高発現には5μLの細胞培養上清を195μLの1×PBST、pH7.4に希釈して、中発現には25μLの細胞培養上清を175μLの1×PBST、pH7.4に希釈して、低発現には100μLの細胞培養上清を100μLの1×PBST、pH7.4に希釈して、センサーチップにロードした。次いで、希釈上清を、抗ヒトFcセンサー(Forte Bio社)上で捕捉した。ベースラインは、1×PBST(50mMリン酸カリウム緩衝液+150mMのNaCl+0.05%のTween 20)、pH7.4を使用して確立された。センサーは、1×PBST、pH 7.4中の50nMのMET(cMET、Sino Biological社 カタログ番号10692-H08H)と120秒間結合され、結合曲線が作成された。解離相では、センサー上の抗体-抗原複合体を、300~600秒間、1×PBST、pH7.4に曝露した。ベースライン、結合、および解離は、別個の条件下で全体を通じて1×PBST、pH5.4を使用して繰り返された。結合相および解離相の曲線は、pH5.4およびpH7.4で、それぞれの対応する抗体変異体について検証され、以下の三つの基準についての情報を得る:a)その対応する出発ABPCと比較した、pH5.4での解離の強化(例えば、koff値がより高い)、b)抗体変異体のみの場合の、pH5.4と比較した、pH7.4での解離の低下(例えば、koff値がより低い)、およびc)野生型ヒトIgG1 ABPCとそれらのTHおよびYTE含有変異体との比較。野生型ヒトIgG1抗体ならびにTHおよびYTE変異を含有する再フォーマットしたヒトIgG1抗体は、広く類似した結合曲線および解離曲線を示し、選択されたOctetプロットおよびエンドリソソーム送達データをそれぞれ図78および図79に示す。我々は、このデータから、pH依存性およびエンドリソソーム送達を含むがこれに限定されない、我々の変異体の可変ドメイン配列の望ましい特性は、IgG1形式であるか、またはTHおよびYTE変異を有するIgG1形式であるかに関わらず、保持されると結論付けた。
実施例36.pH操作された抗MET ABPCの細胞内移行およびエンドリソソーム送達の特徴解析
実施例9~13、16~20、22~25、および28~31よりの選択されたpH操作された抗MET抗体変異体を、U-87 MG細胞(MET+)、SNU-5細胞(MET+)、NCI-H1373細胞(MET+)、NCI-H1573細胞(MET+)、および/またはDetroit 562細胞(MET+)における細胞内移行およびエンドリソソーム送達について分析した。U-87 MG細胞(ATCC社 HTB-14)、Detroit 562細胞(ATCC社 CCL-138)、NCI-H1373細胞(ATCC社 CRL-5866)、NCI-H1573細胞(ATCC社 CRL-5877)またはSNU-5細胞(ATCC社 CRL-5973)を回収し、EMEM培地(U-87 MGおよびDetroit 562、ATCC社;30-2003)、IMDM培地(SNU-5、ATCC社;30-2005)、またはRPMI培地(NCI-H1373およびNCI-H1573、ATCC社 30-2001)に5%(NCI-H1573)、10%(U-87 MG、Detroit 562、NCI-H1373)または20%(SNU-5)のGenClone熱不活性化ウシ胎児血清(HI FBS)(Genesee Scientific社;25-514H)を合わせた中で、再懸濁させた。細胞数は、トリパンブルー染色およびCountess II FL自動セルカウンター(Thermofisher社;AMQAF1000)を使用して決定した。次いで細胞を2,000,000細胞/mLに希釈し、50μL/ウェルを96ウェルの平底細胞培養プレート(Genesee Scientific社;25-109)に播種した。pH操作された抗MET抗体変異体、出発ABPC抗体、対照IgG1アイソタイプ対照(BP0297、Bioxcell社)、およびビヒクル対照を、ネイティブ培養培地中で希釈し、次いで3×モル比のZenon pHrodo iFLヒトIgG標識試薬(ThermoFisher社;Z25611)と1:1で混合した。混合物を室温で20分間インキュベートし、続いて最終用量100μLに細胞を1:1で添加した。細胞、抗MET抗体変異体、およびZenon pHrodo iFLヒトIgG標識試薬の混合物を、37℃、5%CO2で1~24時間インキュベートした。インキュベーション後、100μLの氷冷フローサイトメトリー(FC)緩衝液(リン酸緩衝生理食塩水(PBS)、pH7.4+2mMのエチレンジアミン四酢酸(EDTA)+2%(v/v)HI FBSを各ウェルに加える。次いで、細胞を、4℃で2分間、2000rpmでスピンダウンし、200uLの氷冷FC緩衝液で洗浄し、100uLの氷冷FC緩衝液中に再懸濁した。BD Accuri C6フローサイトメーターを使用して、平均緑色蛍光強度を検出した。Flowjo分析ソフトウェアを使用してデータを分析した。pHrodo greenは、エンドソームおよびリソソームの低pH環境で蛍光を放つpH感受性染料であり、したがって抗体の細胞内移行およびエンドリソソーム送達を定量化するために使用できる。図に特定されるように、U-87 MG(MET+)、Detroit 562(MET+)、SNU-5(MET+)、NCI-H1573(MET+)またはNCI-H1373(MET+)細胞において、図に特定された濃度での抗MET出発ABPCおよび変異体の細胞内移行およびエンドリソソーム送達を、図81に示すが、これはpHrodo greenの平均蛍光強度により測定されたおとりである。いくつかのpH操作された抗MET抗体変異体は、それらの対応する出発ABPC抗体と比較して平均蛍光強度の増加を示したが、このことが、IgG1アイソタイプ対照と比較して増加した蛍光または増加した蛍光によって示されるように、低いpHでの解離の増加が細胞内での細胞内移行およびエンドリソソソーム送達の増加をもたらすことを実証した。エンドリソソーム送達の増加は、各バーの上部にあるpH操作された抗MET抗体変異体それぞれに関して、以下の比として定量される:変異体の平均蛍光強度から、IgG対照の平均蛍光強度を減算し、
次いですべてを、変異体の対応する出発ABPCの平均蛍光強度からIgG対照の平均蛍光強度を減算した値で除算した比。例えば、MYT0888、MYT0916、MYT0920、MYT0924、MYT2018、MYT2019、MYT2020、MYT2022、MYT2023、MYT2025、MYT2026、MYT2033、MYT2038、MYT2040、MYT2043、MYT2049、MYT2864、MYT3451、MYT3452、MYT3453、MYT3454、MYT3457、MYT3465、MYT3466、MYT3467、MYT3468、MYT3469、MYT3471、MYT3474、MYT3482、MYT3485、MYT3609、MYT3611、MYT3615、MYT4201、MYT4202、MYT4204、MYT4205およびMYT4207である、テリソツズマブの抗体変異体は、テリソツズマブ(MYT0886)と比較して、細胞内移行およびエンドリソソーム送達の増加を示す。例えば、MYT2319、MYT2320、MYT2325、MYT2326、MYT2327、MYT2328、MYT2333、MYT2343、MYT2344、MYT2850、MYT2851、MYT2852、MYT2853、MYT2855、MYT2856、MYT2861、MYT2864、MYT2865、MYT4326、MYT4327、MYT4332、MYT4334およびMYT4336である、エミベツズマブの抗体変異体は、エミベツズマブ(MYT2313)と比較して、細胞内移行およびエンドリソソーム送達の増加を示す。例えばMYT3619、MYT3638、MYT3639、MYT3651、MYT3653、MYT3661、MYT3662、MYT3664、MYT3666、MYT3668、MYT3671、MYT3677、MYT3679、MYT3684、MYT4223、MYT4225、MYT4226、MYT4228、MYT4231、MYT4232、MYT4236、MYT4239、MYT4291、MYT4302、MYT4303およびMYT4304である、hucMET27Gv1.3の抗体変異体は、hucMET27Gv1.3(MYT3617)と比較して、細胞内移行およびエンドリソソーム送達の増加を示す。例えば、MYT3689、MYT3691、MYT3694、MYT3695、MYT3697、MYT3698、MYT3705、MYT3707、MYT3720、MYT3724、MYT3725、MYT3728、MYT3732、MYT3735、MYT3738、MYT3740、MYT3748、MYT3749、MYT3750、MYT3751、MYT3752、MYT3753、MYT3754、MYT4242、MYT4243、MYT4245、MYT4247、MYT4249、MYT4250、MYT4252、MYT4258、MYT4309、MYT4310、MYT4311、MYT4318、MYT4319、MYT4320、MYT4322、MYT4323、MYT4324およびMYT4325である、P3D12の抗体変異体は、P3D12(MYT3687および/またはMYT4305)と比較して、細胞内移行およびエンドリソソーム送達の増加を示す。さらなる分析のために、かかるpH操作された抗MET抗体変異体であって、それらの出発ABPC抗体と比較して平均蛍光強度が増加したものを選択した。
実施例37.抗MET mAbの熱安定性
タンパク質融解温度(Tm)を、示差走査蛍光光度法(DSF)を使用して測定した。タンパク質は加熱により折り畳まれていない状態になるため、DSFは、molecule Sypro Orange(Thermo Scientific社 カタログ番号S6650)からの蛍光シグナルを測定することにより、タンパク質のアンフォールディングを可視化する。タンパク質が折り畳まれていない状態であるとき、より多くの親水性領域が、Sypro Orange色素に曝露されるため、色素が順に親水性領域に結合し、シグナルが増加する。タンパク質のTmは、アンフォールディングへの移行の最大半数値として計算され、Sypro Orangeシグナルの第一の派生物をプロットし、この派生物のプロットの局所最大量を見つけることによって可視化することができる。1xPBS、pH7.4中の20μLのタンパク質サンプルを、5μLの25X Sypro Orangeマスターミックスと混合し、最終濃度の5x Sypro Orangeを得た。サンプルを、96ウェルPCRプレート(Thermo Scientific社 カタログ番号AB-2400/W)に添加し、光学カバー(Thermo Scientific社 カタログ番号4360954)で密閉した。PCRプレートをリアルタイムPCR装置(Thermo Scientific社 Quant Studio 3)に挿入し、プレート温度を25℃で3分間安定させ、その後、0.2℃の増分で95℃に上昇させ、1秒間安定させ、その後にSypro Orangeシグナルを測定した。抗METの出発ABPCおよび変異体の融解温度(Tm)値を、図85に示す。いくつかの変異体は、それらの出発ABPCと同様の融解温度値を示したが、このことから、pH操作を介して生成された変異体は、それらの対応する出発ABPC(例えば、エミベツズマブ、hucMET27Gv1.3またはP3D12)と比較して、機能的に適切な熱安定性を保持し得ることが確認される。試験した全ての変異体(図85を参照)は、それらの対応する出発ABPC(例えば、ミルベツキシマブ)の融解温度より10℃低い温度以上の融解温度を有していたため、さらなる分析のために選択した。
本明細書における発見は、例えばCLEC12a等の他の抗原、および2種の他の標的に対する類似の操作とは対照的であるものであり、標的当たり複数の変異体が、低pHでの解離の強化を示したが、これらの変異体(CLEC12aおよび2種の他の標的に特異的に結合した)がもつ良好なpH依存的な結合特性であるにもかかわらず、対応する出発ABPC(例えば、出発抗体)と比較して、細胞内移行およびエンドリソソーム送達においては、10%未満の増加であった。これら変異体(CLEC12aおよび2種の他の標的に特異的に結合した)も、対応する出発ABPC(例えば、出発抗体)と類似の生物物理学的特徴(例えば、抗体発現、熱安定性、pH7.4での親和性など)を有していることから、このことは試験した変異体の生物物理学的特性にとって特有ではなかったことが確認される(すなわち、当該生物物理学的特性は、pH5.4での解離の強化とは無関係であった)。
その他の実施形態
本発明を、その詳細な説明とともに説明してきたが、前述の説明は、添付の特許請求の範囲によって規定される本発明の範囲を例示すること意図しており、および本発明の範囲を限定することを意図していないことが理解されるべきである。その他の態様、利点、および変形は、以下の特許請求の範囲の範囲内にある。
配列の付録
>テリソツズマブIgGの重鎖(配列番号1)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGの軽鎖(配列番号2)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブの重鎖CDR1(配列番号3)
GYIFTAYTMH
>テリソツズマブの重鎖CDR2(配列番号4)
WIKPNNGLANYAQKFQG
>テリソツズマブの重鎖CDR3(配列番号5)
ARSEITTEFDY
>テリソツズマブの軽鎖CDR1(配列番号6)
KSSESVDSYANSFLH
>テリソツズマブの軽鎖CDR2(配列番号7)
RASTRES
>テリソツズマブの軽鎖CDR3(配列番号8)
QQSKEDPLT
>成熟ヒトMET(配列番号9)
ECKEALAKSEMNVNMKYQLPNFTAETPIQNVILHEHHIFLGATNYIYVLNEEDLQKVAEYKTGPVLEHPDCFPCQDCSSKANLSGGVWKDNINMALVVDTYYDDQLISCGSVNRGTCQRHVFPHNHTADIQSEVHCIFSPQIEEPSQCPDCVVSALGAKVLSSVKDRFINFFVGNTINSSYFPDHPLHSISVRRLKETKDGFMFLTDQSYIDVLPEFRDSYPIKYVHAFESNNFIYFLTVQRETLDAQTFHTRIIRFCSINSGLHSYMEMPLECILTEKRKKRSTKKEVFNILQAAYVSKPGAQLARQIGASLNDDILFGVFAQSKPDSAEPMDRSAMCAFPIKYVNDFFNKIVNKNNVRCLQHFYGPNHEHCFNRTLLRNSSGCEARRDEYRTEFTTALQRVDLFMGQFSEVLLTSISTFIKGDLTIANLGTSEGRFMQVVVSRSGPSTPHVNFLLDSHPVSPEVIVEHTLNQNGYTLVITGKKITKIPLNGLGCRHFQSCSQCLSAPPFVQCGWCHDKCVRSEECLSGTWTQQICLPAIYKVFPNSAPLEGGTRLTICGWDFGFRRNNKFDLKKTRVLLGNESCTLTLSESTMNTLKCTVGPAMNKHFNMSIIISNGHGTTQYSTFSYVDPVITSISPKYGPMAGGTLLTLTGNYLNSGNSRHISIGGKTCTLKSVSNSILECYTPAQTISTEFAVKLKIDLANRETSIFSYREDPIVYEIHPTKSFISGGSTITGVGKNLNSVSVPRMVINVHEAGRNFTVACQHRSNSEIICCTTPSLQQLNLQLPLKTKAFFMLDGILSKYFDLIYVHNPVFKPFEKPVMISMGNENVLEIKGNDIDPEAVKGEVLKVGNKSCENIHLHSEAVLCTVPNDLLKLNSELNIEWKQAISSTVLGKVIVQPDQNFTGLIAGVVSISTALLLLLGFFLWLKKRKQIKDLGSELVRYDARVHTPHLDRLVSARSVSPTTEMVSNESVDYRATFPEDQFPNSSQNGSCRQVQYPLTDMSPILTSGDSDISSPLLQNTVHIDLSALNPELVQAVQHVVIGPSSLIVHFNEVIGRGHFGCVYHGTLLDNDGKKIHCAVKSLNRITDIGEVSQFLTEGIIMKDFSHPNVLSLLGICLRSEGSPLVVLPYMKHGDLRNFIRNETHNPTVKDLIGFGLQVAKGMKYLASKKFVHRDLAARNCMLDEKFTVKVADFGLARDMYDKEYYSVHNKTGAKLPVKWMALESLQTQKFTTKSDVWSFGVLLWELMTRGAPPYPDVNTFDITVYLLQGRRLLQPEYCPDPLYEVMLKCWHPKAEMRPSFSELVSRISAIFSTFIGEHYVHVNATYVNVKCVAPYPSLLSSEDNADDEVDTRPASFWETS
>成熟ヒトMETをコードするcDNA(配列番号10)
GAGTGTAAAGAGGCACTAGCAAAGTCCGAGATGAATGTGAATATGAAGTATCAGCTTCCCAACTTCACCGCGGAAACACCCATCCAGAATGTCATTCTACATGAGCATCACATTTTCCTTGGTGCCACTAACTACATTTATGTTTTAAATGAGGAAGACCTTCAGAAGGTTGCTGAGTACAAGACTGGGCCTGTGCTGGAACACCCAGATTGTTTCCCATGTCAGGACTGCAGCAGCAAAGCCAATTTATCAGGAGGTGTTTGGAAAGATAACATCAACATGGCTCTAGTTGTCGACACCTACTATGATGATCAACTCATTAGCTGTGGCAGCGTCAACAGAGGGACCTGCCAGCGACATGTCTTTCCCCACAATCATACTGCTGACATACAGTCGGAGGTTCACTGCATATTCTCCCCACAGATAGAAGAGCCCAGCCAGTGTCCTGACTGTGTGGTGAGCGCCCTGGGAGCCAAAGTCCTTTCATCTGTAAAGGACCGGTTCATCAACTTCTTTGTAGGCAATACCATAAATTCTTCTTATTTCCCAGATCATCCATTGCATTCGATATCAGTGAGAAGGCTAAAGGAAACGAAAGATGGTTTTATGTTTTTGACGGACCAGTCCTACATTGATGTTTTACCTGAGTTCAGAGATTCTTACCCCATTAAGTATGTCCATGCCTTTGAAAGCAACAATTTTATTTACTTCTTGACGGTCCAAAGGGAAACTCTAGATGCTCAGACTTTTCACACAAGAATAATCAGGTTCTGTTCCATAAACTCTGGATTGCATTCCTACATGGAAATGCCTCTGGAGTGTATTCTCACAGAAAAGAGAAAAAAGAGATCCACAAAGAAGGAAGTGTTTAATATACTTCAGGCTGCGTATGTCAGCAAGCCTGGGGCCCAGCTTGCTAGACAAATAGGAGCCAGCCTGAATGATGACATTCTTTTCGGGGTGTTCGCACAAAGCAAGCCAGATTCTGCCGAACCAATGGATCGATCTGCCATGTGTGCATTCCCTATCAAATATGTCAACGACTTCTTCAACAAGATCGTCAACAAAAACAATGTGAGATGTCTCCAGCATTTTTACGGACCCAATCATGAGCACTGCTTTAATAGGACACTTCTGAGAAATTCATCAGGCTGTGAAGCGCGCCGTGATGAATATCGAACAGAGTTTACCACAGCTTTGCAGCGCGTTGACTTATTCATGGGTCAATTCAGCGAAGTCCTCTTAACATCTATATCCACCTTCATTAAAGGAGACCTCACCATAGCTAATCTTGGGACATCAGAGGGTCGCTTCATGCAGGTTGTGGTTTCTCGATCAGGACCATCAACCCCTCATGTGAATTTTCTCCTGGACTCCCATCCAGTGTCTCCAGAAGTGATTGTGGAGCATACATTAAACCAAAATGGCTACACACTGGTTATCACTGGGAAGAAGATCACGAAGATCCCATTGAATGGCTTGGGCTGCAGACATTTCCAGTCCTGCAGTCAATGCCTCTCTGCCCCACCCTTTGTTCAGTGTGGCTGGTGCCACGACAAATGTGTGCGATCGGAGGAATGCCTGAGCGGGACATGGACTCAACAGATCTGTCTGCCTGCAATCTACAAGGTTTTCCCAAATAGTGCACCCCTTGAAGGAGGGACAAGGCTGACCATATGTGGCTGGGACTTTGGATTTCGGAGGAATAATAAATTTGATTTAAAGAAAACTAGAGTTCTCCTTGGAAATGAGAGCTGCACCTTGACTTTAAGTGAGAGCACGATGAATACATTGAAATGCACAGTTGGTCCTGCCATGAATAAGCATTTCAATATGTCCATAATTATTTCAAATGGCCACGGGACAACACAATACAGTACATTCTCCTATGTGGATCCTGTAATAACAAGTATTTCGCCGAAATACGGTCCTATGGCTGGTGGCACTTTACTTACTTTAACTGGAAATTACCTAAACAGTGGGAATTCTAGACACATTTCAATTGGTGGAAAAACATGTACTTTAAAAAGTGTGTCAAACAGTATTCTTGAATGTTATACCCCAGCCCAAACCATTTCAACTGAGTTTGCTGTTAAATTGAAAATTGACTTAGCCAACCGAGAGACAAGCATCTTCAGTTACCGTGAAGATCCCATTGTCTATGAAATTCATCCAACCAAATCTTTTATTAGTGGTGGGAGCACAATAACAGGTGTTGGGAAAAACCTGAATTCAGTTAGTGTCCCGAGAATGGTCATAAATGTGCATGAAGCAGGAAGGAACTTTACAGTGGCATGTCAACATCGCTCTAATTCAGAGATAATCTGTTGTACCACTCCTTCCCTGCAACAGCTGAATCTGCAACTCCCCCTGAAAACCAAAGCCTTTTTCATGTTAGATGGGATCCTTTCCAAATACTTTGATCTCATTTATGTACATAATCCTGTGTTTAAGCCTTTTGAAAAGCCAGTGATGATCTCAATGGGCAATGAAAATGTACTGGAAATTAAGGGAAATGATATTGACCCTGAAGCAGTTAAAGGTGAAGTGTTAAAAGTTGGAAATAAGAGCTGTGAGAATATACACTTACATTCTGAAGCCGTTTTATGCACGGTCCCCAATGACCTGCTGAAATTGAACAGCGAGCTAAATATAGAGTGGAAGCAAGCAATTTCTTCAACCGTCCTTGGAAAAGTAATAGTTCAACCAGATCAGAATTTCACAGGATTGATTGCTGGTGTTGTCTCAATATCAACAGCACTGTTATTACTACTTGGGTTTTTCCTGTGGCTGAAAAAGAGAAAGCAAATTAAAGATCTGGGCAGTGAATTAGTTCGCTACGATGCAAGAGTACACACTCCTCATTTGGATAGGCTTGTAAGTGCCCGAAGTGTAAGCCCAACTACAGAAATGGTTTCAAATGAATCTGTAGACTACCGAGCTACTTTTCCAGAAGATCAGTTTCCTAATTCATCTCAGAACGGTTCATGCCGACAAGTGCAGTATCCTCTGACAGACATGTCCCCCATCCTAACTAGTGGGGACTCTGATATATCCAGTCCATTACTGCAAAATACTGTCCACATTGACCTCAGTGCTCTAAATCCAGAGCTGGTCCAGGCAGTGCAGCATGTAGTGATTGGGCCCAGTAGCCTGATTGTGCATTTCAATGAAGTCATAGGAAGAGGGCATTTTGGTTGTGTATATCATGGGACTTTGTTGGACAATGATGGCAAGAAAATTCACTGTGCTGTGAAATCCTTGAACAGAATCACTGACATAGGAGAAGTTTCCCAATTTCTGACCGAGGGAATCATCATGAAAGATTTTAGTCATCCCAATGTCCTCTCGCTCCTGGGAATCTGCCTGCGAAGTGAAGGGTCTCCGCTGGTGGTCCTACCATACATGAAACATGGAGATCTTCGAAATTTCATTCGAAATGAGACTCATAATCCAACTGTAAAAGATCTTATTGGCTTTGGTCTTCAAGTAGCCAAAGGCATGAAATATCTTGCAAGCAAAAAGTTTGTCCACAGAGACTTGGCTGCAAGAAACTGTATGCTGGATGAAAAATTCACAGTCAAGGTTGCTGATTTTGGTCTTGCCAGAGACATGTATGATAAAGAATACTATAGTGTACACAACAAAACAGGTGCAAAGCTGCCAGTGAAGTGGATGGCTTTGGAAAGTCTGCAAACTCAAAAGTTTACCACCAAGTCAGATGTGTGGTCCTTTGGCGTGCTCCTCTGGGAGCTGATGACAAGAGGAGCCCCACCTTATCCTGACGTAAACACCTTTGATATAACTGTTTACTTGTTGCAAGGGAGAAGACTCCTACAACCCGAATACTGCCCAGACCCCTTATATGAAGTAATGCTAAAATGCTGGCACCCTAAAGCCGAAATGCGCCCATCCTTTTCTGAACTGGTGTCCCGGATATCAGCGATCTTCTCTACTTTCATTGGGGAGCACTATGTCCATGTGAACGCTACTTATGTGAACGTAAA
ATGTGTCGCTCCGTATCCTTCTCTGTTGTCATCAGAAGATAACGCTGATGATGAGGTGGACACACGACCAGCCTCCTTCTGGGAGACATCA
>METの細胞外ドメイン(配列番号11)
ECKEALAKSEMNVNMKYQLPNFTAETPIQNVILHEHHIFLGATNYIYVLNEEDLQKVAEYKTGPVLEHPDCFPCQDCSSKANLSGGVWKDNINMALVVDTYYDDQLISCGSVNRGTCQRHVFPHNHTADIQSEVHCIFSPQIEEPSQCPDCVVSALGAKVLSSVKDRFINFFVGNTINSSYFPDHPLHSISVRRLKETKDGFMFLTDQSYIDVLPEFRDSYPIKYVHAFESNNFIYFLTVQRETLDAQTFHTRIIRFCSINSGLHSYMEMPLECILTEKRKKRSTKKEVFNILQAAYVSKPGAQLARQIGASLNDDILFGVFAQSKPDSAEPMDRSAMCAFPIKYVNDFFNKIVNKNNVRCLQHFYGPNHEHCFNRTLLRNSSGCEARRDEYRTEFTTALQRVDLFMGQFSEVLLTSISTFIKGDLTIANLGTSEGRFMQVVVSRSGPSTPHVNFLLDSHPVSPEVIVEHTLNQNGYTLVITGKKITKIPLNGLGCRHFQSCSQCLSAPPFVQCGWCHDKCVRSEECLSGTWTQQICLPAIYKVFPNSAPLEGGTRLTICGWDFGFRRNNKFDLKKTRVLLGNESCTLTLSESTMNTLKCTVGPAMNKHFNMSIIISNGHGTTQYSTFSYVDPVITSISPKYGPMAGGTLLTLTGNYLNSGNSRHISIGGKTCTLKSVSNSILECYTPAQTISTEFAVKLKIDLANRETSIFSYREDPIVYEIHPTKSFISGGSTITGVGKNLNSVSVPRMVINVHEAGRNFTVACQHRSNSEIICCTTPSLQQLNLQLPLKTKAFFMLDGILSKYFDLIYVHNPVFKPFEKPVMISMGNENVLEIKGNDIDPEAVKGEVLKVGNKSCENIHLHSEAVLCTVPNDLLKLNSELNIEWKQAISSTVLGKVIVQPDQNFT
>METの細胞外ドメインをコードするcDNA(配列番号12)
GAGTGTAAAGAGGCACTAGCAAAGTCCGAGATGAATGTGAATATGAAGTATCAGCTTCCCAACTTCACCGCGGAAACACCCATCCAGAATGTCATTCTACATGAGCATCACATTTTCCTTGGTGCCACTAACTACATTTATGTTTTAAATGAGGAAGACCTTCAGAAGGTTGCTGAGTACAAGACTGGGCCTGTGCTGGAACACCCAGATTGTTTCCCATGTCAGGACTGCAGCAGCAAAGCCAATTTATCAGGAGGTGTTTGGAAAGATAACATCAACATGGCTCTAGTTGTCGACACCTACTATGATGATCAACTCATTAGCTGTGGCAGCGTCAACAGAGGGACCTGCCAGCGACATGTCTTTCCCCACAATCATACTGCTGACATACAGTCGGAGGTTCACTGCATATTCTCCCCACAGATAGAAGAGCCCAGCCAGTGTCCTGACTGTGTGGTGAGCGCCCTGGGAGCCAAAGTCCTTTCATCTGTAAAGGACCGGTTCATCAACTTCTTTGTAGGCAATACCATAAATTCTTCTTATTTCCCAGATCATCCATTGCATTCGATATCAGTGAGAAGGCTAAAGGAAACGAAAGATGGTTTTATGTTTTTGACGGACCAGTCCTACATTGATGTTTTACCTGAGTTCAGAGATTCTTACCCCATTAAGTATGTCCATGCCTTTGAAAGCAACAATTTTATTTACTTCTTGACGGTCCAAAGGGAAACTCTAGATGCTCAGACTTTTCACACAAGAATAATCAGGTTCTGTTCCATAAACTCTGGATTGCATTCCTACATGGAAATGCCTCTGGAGTGTATTCTCACAGAAAAGAGAAAAAAGAGATCCACAAAGAAGGAAGTGTTTAATATACTTCAGGCTGCGTATGTCAGCAAGCCTGGGGCCCAGCTTGCTAGACAAATAGGAGCCAGCCTGAATGATGACATTCTTTTCGGGGTGTTCGCACAAAGCAAGCCAGATTCTGCCGAACCAATGGATCGATCTGCCATGTGTGCATTCCCTATCAAATATGTCAACGACTTCTTCAACAAGATCGTCAACAAAAACAATGTGAGATGTCTCCAGCATTTTTACGGACCCAATCATGAGCACTGCTTTAATAGGACACTTCTGAGAAATTCATCAGGCTGTGAAGCGCGCCGTGATGAATATCGAACAGAGTTTACCACAGCTTTGCAGCGCGTTGACTTATTCATGGGTCAATTCAGCGAAGTCCTCTTAACATCTATATCCACCTTCATTAAAGGAGACCTCACCATAGCTAATCTTGGGACATCAGAGGGTCGCTTCATGCAGGTTGTGGTTTCTCGATCAGGACCATCAACCCCTCATGTGAATTTTCTCCTGGACTCCCATCCAGTGTCTCCAGAAGTGATTGTGGAGCATACATTAAACCAAAATGGCTACACACTGGTTATCACTGGGAAGAAGATCACGAAGATCCCATTGAATGGCTTGGGCTGCAGACATTTCCAGTCCTGCAGTCAATGCCTCTCTGCCCCACCCTTTGTTCAGTGTGGCTGGTGCCACGACAAATGTGTGCGATCGGAGGAATGCCTGAGCGGGACATGGACTCAACAGATCTGTCTGCCTGCAATCTACAAGGTTTTCCCAAATAGTGCACCCCTTGAAGGAGGGACAAGGCTGACCATATGTGGCTGGGACTTTGGATTTCGGAGGAATAATAAATTTGATTTAAAGAAAACTAGAGTTCTCCTTGGAAATGAGAGCTGCACCTTGACTTTAAGTGAGAGCACGATGAATACATTGAAATGCACAGTTGGTCCTGCCATGAATAAGCATTTCAATATGTCCATAATTATTTCAAATGGCCACGGGACAACACAATACAGTACATTCTCCTATGTGGATCCTGTAATAACAAGTATTTCGCCGAAATACGGTCCTATGGCTGGTGGCACTTTACTTACTTTAACTGGAAATTACCTAAACAGTGGGAATTCTAGACACATTTCAATTGGTGGAAAAACATGTACTTTAAAAAGTGTGTCAAACAGTATTCTTGAATGTTATACCCCAGCCCAAACCATTTCAACTGAGTTTGCTGTTAAATTGAAAATTGACTTAGCCAACCGAGAGACAAGCATCTTCAGTTACCGTGAAGATCCCATTGTCTATGAAATTCATCCAACCAAATCTTTTATTAGTGGTGGGAGCACAATAACAGGTGTTGGGAAAAACCTGAATTCAGTTAGTGTCCCGAGAATGGTCATAAATGTGCATGAAGCAGGAAGGAACTTTACAGTGGCATGTCAACATCGCTCTAATTCAGAGATAATCTGTTGTACCACTCCTTCCCTGCAACAGCTGAATCTGCAACTCCCCCTGAAAACCAAAGCCTTTTTCATGTTAGATGGGATCCTTTCCAAATACTTTGATCTCATTTATGTACATAATCCTGTGTTTAAGCCTTTTGAAAAGCCAGTGATGATCTCAATGGGCAATGAAAATGTACTGGAAATTAAGGGAAATGATATTGACCCTGAAGCAGTTAAAGGTGAAGTGTTAAAAGTTGGAAATAAGAGCTGTGAGAATATACACTTACATTCTGAAGCCGTTTTATGCACGGTCCCCAATGACCTGCTGAAATTGAACAGCGAGCTAAATATAGAGTGGAAGCAAGCAATTTCTTCAACCGTCCTTGGAAAAGTAATAGTTCAACCAGATCAGAATTTCACA
>テリソツズマブIgGヒスチジンスキャニング変異体#1の重鎖(配列番号13)
QVQLVQSGAEVKKPGASVKVSCKASHYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#2の重鎖(配列番号14)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#3の重鎖(配列番号15)
QVQLVQSGAEVKKPGASVKVSCKASGYHFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#4の重鎖(配列番号16)
QVQLVQSGAEVKKPGASVKVSCKASGYIHTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#5の重鎖(配列番号17)
QVQLVQSGAEVKKPGASVKVSCKASGYIFHAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#6の重鎖(配列番号18)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTHYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#7の重鎖(配列番号19)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAHTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#8の重鎖(配列番号20)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYHMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#9の重鎖(配列番号21)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTHHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#10の重鎖(配列番号22)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMAWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#11の重鎖(配列番号23)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGHIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#12の重鎖(配列番号24)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWHKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#13の重鎖(配列番号25)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIHPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#14の重鎖(配列番号26)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKHNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#15の重鎖(配列番号27)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPHNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#16の重鎖(配列番号28)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNHGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#17の重鎖(配列番号29)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNHLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#18の重鎖(配列番号30)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGHANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#19の重鎖(配列番号31)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLHNYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#20の重鎖(配列番号32)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLAHYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#21の重鎖(配列番号33)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANHAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#22の重鎖(配列番号34)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYHQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#23の重鎖(配列番号35)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAHKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#24の重鎖(配列番号36)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQHFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#25の重鎖(配列番号37)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKHQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#26の重鎖(配列番号38)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFHGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#27の重鎖(配列番号39)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQHRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#28の重鎖(配列番号40)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#29の重鎖(配列番号41)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCAHSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#30の重鎖(配列番号42)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARHEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#31の重鎖(配列番号43)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSHITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#32の重鎖(配列番号44)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEHTTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#33の重鎖(配列番号45)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEIHTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#34の重鎖(配列番号46)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITHEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#35の重鎖(配列番号47)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTHFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#36の重鎖(配列番号48)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEHDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#37の重鎖(配列番号49)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFHYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#38の重鎖(配列番号50)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#1の軽鎖(配列番号51)
DIVMTQSPDSLAVSLGERATINCHSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#2の軽鎖(配列番号52)
DIVMTQSPDSLAVSLGERATINCKHSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#3の軽鎖(配列番号53)
DIVMTQSPDSLAVSLGERATINCKSHESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#4の軽鎖(配列番号54)
DIVMTQSPDSLAVSLGERATINCKSSHSVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#5の軽鎖(配列番号55)
DIVMTQSPDSLAVSLGERATINCKSSEHVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#6の軽鎖(配列番号56)
DIVMTQSPDSLAVSLGERATINCKSSESHDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#7の軽鎖(配列番号57)
DIVMTQSPDSLAVSLGERATINCKSSESVHSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#8の軽鎖(配列番号58)
DIVMTQSPDSLAVSLGERATINCKSSESVDHYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#9の軽鎖(配列番号59)
DIVMTQSPDSLAVSLGERATINCKSSESVDSHANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#10の軽鎖(配列番号60)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYHNSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#11の軽鎖(配列番号61)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYAHSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#12の軽鎖(配列番号62)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANHFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#13の軽鎖(配列番号63)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSHLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#14の軽鎖(配列番号64)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFHHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#15の軽鎖(配列番号65)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLAWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#16の軽鎖(配列番号66)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYHASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#17の軽鎖(配列番号67)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRHSTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#18の軽鎖(配列番号68)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRAHTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#19の軽鎖(配列番号69)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASHRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#20の軽鎖(配列番号70)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTHESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#21の軽鎖(配列番号71)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRHSGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#22の軽鎖(配列番号72)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTREHGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#23の軽鎖(配列番号73)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCHQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#24の軽鎖(配列番号74)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQHSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#25の軽鎖(配列番号75)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQHKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#26の軽鎖(配列番号76)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSHEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#27の軽鎖(配列番号77)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKHDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#28の軽鎖(配列番号78)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEHPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#29の軽鎖(配列番号79)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDHLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#30の軽鎖(配列番号80)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPHTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#31の軽鎖(配列番号81)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLHFGGGTKVEIK
>テリソツズマブIgGのヒスチジンスキャニング変異体#1の重鎖組み合わせ(配列番号82)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARHEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#2の重鎖組み合わせ(配列番号83)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITHEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#3の重鎖組み合わせ(配列番号84)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#4の重鎖組み合わせ(配列番号85)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARHEITHEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#5の重鎖組み合わせ(配列番号86)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARHEITTEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#6の重鎖組み合わせ(配列番号87)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITHEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#7の重鎖組み合わせ(配列番号88)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARHEITHEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#8の重鎖組み合わせ(配列番号89)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARHEITTEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#9の重鎖組み合わせ(配列番号90)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITHEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#10の重鎖組み合わせ(配列番号91)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARHEITHEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#11の重鎖組み合わせ(配列番号92)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#12の重鎖組み合わせ(配列番号93)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRHEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#13の重鎖組み合わせ(配列番号94))
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRSEITHEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#14の重鎖組み合わせ(配列番号95)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRSEITTEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#15の重鎖組み合わせ(配列番号96)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCAHSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#16の重鎖組み合わせ(配列番号97)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCAHHEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#17の重鎖組み合わせ(配列番号98)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCAHSEITHEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#18の重鎖組み合わせ(配列番号99)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCAHSEITTEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#19の重鎖組み合わせ(配列番号100)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEIHTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#20の重鎖組み合わせ(配列番号101)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARHEIHTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#21の重鎖組み合わせ(配列番号102)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEIHHEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#22の重鎖組み合わせ(配列番号103)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEIHTEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#23の重鎖組み合わせ(配列番号104)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRSEITTEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#24の重鎖組み合わせ(配列番号105)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRHEITTEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#25の重鎖組み合わせ(配列番号106)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRSEITHEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#26の重鎖組み合わせ(配列番号107)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRHEITTEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#27の重鎖組み合わせ(配列番号108)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRSEITHEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#28の重鎖組み合わせ(配列番号109)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCAHSEITTEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#29の重鎖組み合わせ(配列番号110)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCAHHEITTEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#30の重鎖組み合わせ(配列番号111)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCAHSEITHEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#31の重鎖組み合わせ(配列番号112)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCAHHEITTEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#32の重鎖組み合わせ(配列番号113)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCAHSEITHEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#33の重鎖組み合わせ(配列番号114)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEIHTEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#34の重鎖組み合わせ(配列番号115)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARHEIHTEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#35の重鎖組み合わせ(配列番号116)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEIHHEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#36の重鎖組み合わせ(配列番号117)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARHEIHTEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#37の重鎖組み合わせ(配列番号118)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEIHHEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#38の重鎖組み合わせ(配列番号119)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHHSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#39の重鎖組み合わせ(配列番号120)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCAHSEIHTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#40の重鎖組み合わせ(配列番号121)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRSEIHTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#41の重鎖組み合わせ(配列番号122)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHHSEIHTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#42の重鎖組み合わせ(配列番号123)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHHSEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#43の重鎖組み合わせ(配列番号124)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHHHEITTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#44の重鎖組み合わせ(配列番号125)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHHSEITHEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#45の重鎖組み合わせ(配列番号126)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHHSEITTEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#46の重鎖組み合わせ(配列番号127)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRSEIHTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#47の重鎖組み合わせ(配列番号128)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRHEIHTEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#48の重鎖組み合わせ(配列番号129)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRSEIHHEFDYWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#49の重鎖組み合わせ(配列番号130)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRSEIHTEFDHWGQGTLVTVSS
>テリソツズマブIgGヒスチジンスキャニング変異体#1の軽鎖組み合わせ(配列番号131)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYAHSHLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#2の軽鎖組み合わせ(配列番号132)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYAHSFLHWYQQKPGQPPKLLIYHASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#3の軽鎖組み合わせ(配列番号133)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYAHSFLHWYQQKPGQPPKLLIYRASTREHGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#4の軽鎖組み合わせ(配列番号134)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSHLHWYQQKPGQPPKLLIYHASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#5の軽鎖組み合わせ(配列番号135)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSHLHWYQQKPGQPPKLLIYRASTREHGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#6の軽鎖組み合わせ(配列番号136)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYHASTREHGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#7の軽鎖組み合わせ(配列番号137)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYAHSHLHWYQQKPGQPPKLLIYHASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#8の軽鎖組み合わせ(配列番号138)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYAHSHLHWYQQKPGQPPKLLIYRASTREHGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#9の軽鎖組み合わせ(配列番号139)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYAHSFLHWYQQKPGQPPKLLIYHASTREHGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#10の軽鎖組み合わせ(配列番号140)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSHLHWYQQKPGQPPKLLIYHASTREHGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#11の軽鎖組み合わせ(配列番号141)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYAHSFLHWYQQKPGQPPKLLIYRASTRHSGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#12の軽鎖組み合わせ(配列番号142)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSHLHWYQQKPGQPPKLLIYRASTRHSGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#13の軽鎖組み合わせ(配列番号143)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFHHWYQQKPGQPPKLLIYRASTRHSGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#14の軽鎖組み合わせ(配列番号144)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYHASTRHSGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>テリソツズマブIgGヒスチジンスキャニング変異体#15の軽鎖組み合わせ(配列番号145)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRHHGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>エミベツズマブIgGの重鎖(配列番号146)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGの軽鎖(配列番号147)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>エミベツズマブの重鎖CDR1(配列番号148)
GYTFTDYYMH
>エミベツズマブの重鎖CDR2(配列番号149)
RVNPNRRGTTYNQKFEG
>エミベツズマブの重鎖CDR3(配列番号150)
ARANWLDY
>エミベツズマブの軽鎖CDR1(配列番号151)
SVSSSVSSIYLH
>エミベツズマブの軽鎖CDR2(配列番号152)
STSNLAS
>エミベツズマブの軽鎖CDR3(配列番号153)
QVYSGYPLT
>エミベツズマブIgGヒスチジンスキャニング変異体#1の重鎖(配列番号154)
QVQLVQSGAEVKKPGASVKVSCKASHYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#2の重鎖(配列番号155)
QVQLVQSGAEVKKPGASVKVSCKASGHTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#3の重鎖(配列番号156)
QVQLVQSGAEVKKPGASVKVSCKASGYHFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#4の重鎖(配列番号157)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#5の重鎖(配列番号158)
QVQLVQSGAEVKKPGASVKVSCKASGYTFHDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#6の重鎖(配列番号159)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#7の重鎖(配列番号160)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDHYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#8の重鎖(配列番号161)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYHMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#9の重鎖(配列番号162)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYHHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#10の重鎖(配列番号163)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMAWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#11の重鎖(配列番号164)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGHVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#12の重鎖(配列番号165)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRHNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#13の重鎖(配列番号166)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#14の重鎖(配列番号167)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNHNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#15の重鎖(配列番号168)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#16の重鎖(配列番号169)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNHRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#17の重鎖(配列番号170)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRHGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#18の重鎖(配列番号171)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#19の重鎖(配列番号172)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGHTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#20の重鎖(配列番号173)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTHYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#21の重鎖(配列番号174)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTHNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#22の重鎖(配列番号175)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYHQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#23の重鎖(配列番号176)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNHKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#24の重鎖(配列番号177)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQHFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#25の重鎖(配列番号178)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKHEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#26の重鎖(配列番号179)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFHGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#27の重鎖(配列番号180)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEHRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#28の重鎖(配列番号181)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCHRANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#29の重鎖(配列番号182)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCAHANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#30の重鎖(配列番号183)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#31の重鎖(配列番号184)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#32の重鎖(配列番号185)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANHLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#33の重鎖(配列番号186)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWHDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#34の重鎖(配列番号187)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLHYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#35の重鎖(配列番号188)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDHWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#1の軽鎖(配列番号189)
DIQMTQSPSSLSASVGDRVTITCHVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#2の軽鎖(配列番号190)
DIQMTQSPSSLSASVGDRVTITCSHSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#3の軽鎖(配列番号191)
DIQMTQSPSSLSASVGDRVTITCSVHSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#4の軽鎖(配列番号192)
DIQMTQSPSSLSASVGDRVTITCSVSHSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#5の軽鎖(配列番号193)
DIQMTQSPSSLSASVGDRVTITCSVSSHVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#6の軽鎖(配列番号194)
DIQMTQSPSSLSASVGDRVTITCSVSSSHSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#7の軽鎖(配列番号195)
DIQMTQSPSSLSASVGDRVTITCSVSSSVHSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#8の軽鎖(配列番号196)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSHIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#9の軽鎖(配列番号197)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSHYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#10の軽鎖(配列番号198)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIHLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#11の軽鎖(配列番号199)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYHHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#12の軽鎖(配列番号200)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLAWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#13の軽鎖(配列番号201)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYHTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#14の軽鎖(配列番号202)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSHSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#15の軽鎖(配列番号203)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTHNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#16の軽鎖(配列番号204)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSHLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#17の軽鎖(配列番号205)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNHASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#18の軽鎖(配列番号206)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLHSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#19の軽鎖(配列番号207)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLAHGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#20の軽鎖(配列番号208)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCHVYSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#21の軽鎖(配列番号209)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHYSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#22の軽鎖(配列番号210)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVHSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#23の軽鎖(配列番号211)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYHGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#24の軽鎖(配列番号212)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSHYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#25の軽鎖(配列番号213)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGHPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#26の軽鎖(配列番号214)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYHLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#27の軽鎖(配列番号215)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPHTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#28の軽鎖(配列番号216)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLHFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#1の重鎖組み合わせ(配列番号217)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVHPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#2の重鎖組み合わせ(配列番号218)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#3の重鎖組み合わせ(配列番号219)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#4の重鎖組み合わせ(配列番号220)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#5の重鎖組み合わせ(配列番号221)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#6の重鎖組み合わせ(配列番号222)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#7の重鎖組み合わせ(配列番号223)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#8の重鎖組み合わせ(配列番号224)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPHRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#9の重鎖組み合わせ(配列番号225)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#10の重鎖組み合わせ(配列番号226)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#11の重鎖組み合わせ(配列番号227)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVHPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#12の重鎖組み合わせ(配列番号228)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVHPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#13の重鎖組み合わせ(配列番号229)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVHPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#14の重鎖組み合わせ(配列番号230)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPHRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#15の重鎖組み合わせ(配列番号231)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#16の重鎖組み合わせ(配列番号232)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#17の重鎖組み合わせ(配列番号233)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPHRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#18の重鎖組み合わせ(配列番号234)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#19の重鎖組み合わせ(配列番号235)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#20の重鎖組み合わせ(配列番号236)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPHRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#21の重鎖組み合わせ(配列番号237)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNHNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#22の重鎖組み合わせ(配列番号238)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHHNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#23の重鎖組み合わせ(配列番号239)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#24の重鎖組み合わせ(配列番号240)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#25の重鎖組み合わせ(配列番号241)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNHNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#26の重鎖組み合わせ(配列番号242)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNHNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#27の重鎖組み合わせ(配列番号243)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHHNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#28の重鎖組み合わせ(配列番号244)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVHHNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#29の重鎖組み合わせ(配列番号245)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNHHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#30の重鎖組み合わせ(配列番号246)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNHNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#31の重鎖組み合わせ(配列番号247)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNHNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#32の重鎖組み合わせ(配列番号248)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHHHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#33の重鎖組み合わせ(配列番号249)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHHNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#34の重鎖組み合わせ(配列番号250)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHHNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#35の重鎖組み合わせ(配列番号251)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNHHRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#36の重鎖組み合わせ(配列番号252)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNHHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#37の重鎖組み合わせ(配列番号253)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNHNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#38の重鎖組み合わせ(配列番号254)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVHHHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#39の重鎖組み合わせ(配列番号255)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVHHNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#40の重鎖組み合わせ(配列番号256)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVHHNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#41の重鎖組み合わせ(配列番号257)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNHHRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#42の重鎖組み合わせ(配列番号258)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNHHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#43の重鎖組み合わせ(配列番号259)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNHNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#44の重鎖組み合わせ(配列番号260)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHHHRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#45の重鎖組み合わせ(配列番号261)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHHHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#46の重鎖組み合わせ(配列番号262)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHHNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#47の重鎖組み合わせ(配列番号263)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNHHRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#48の重鎖組み合わせ(配列番号264)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVHPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#49の重鎖組み合わせ(配列番号265)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#50の重鎖組み合わせ(配列番号266)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#51の重鎖組み合わせ(配列番号267)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#52の重鎖組み合わせ(配列番号268)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#53の重鎖組み合わせ(配列番号269)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#54の重鎖組み合わせ(配列番号270)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#55の重鎖組み合わせ(配列番号271)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPHRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#56の重鎖組み合わせ(配列番号272)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#57の重鎖組み合わせ(配列番号273)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#58の重鎖組み合わせ(配列番号274)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVHPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#59の重鎖組み合わせ(配列番号275)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVHPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#60の重鎖組み合わせ(配列番号276)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVHPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#61の重鎖組み合わせ(配列番号277)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPHRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#62の重鎖組み合わせ(配列番号278)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#63の重鎖組み合わせ(配列番号279)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#64の重鎖組み合わせ(配列番号280)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPHRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#65の重鎖組み合わせ(配列番号281)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#66の重鎖組み合わせ(配列番号282)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#67の重鎖組み合わせ(配列番号283)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPHRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHHWLDYWGQGTTVTVSS
>エミベツズマブIgGヒスチジンスキャニング変異体#1の軽鎖組み合わせ(配列番号284)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIHLHWYQQKPGKAPKLLIYHTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#2の軽鎖組み合わせ(配列番号285)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIHLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHYSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#3の軽鎖組み合わせ(配列番号286)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIHLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVHSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#4の軽鎖組み合わせ(配列番号287)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIHLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGHPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#5の軽鎖組み合わせ(配列番号288)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYHTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHYSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#6の軽鎖組み合わせ(配列番号289)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYHTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVHSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#7の軽鎖組み合わせ(配列番号290)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYHTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGHPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#8の軽鎖組み合わせ(配列番号291)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHHSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#9の軽鎖組み合わせ(配列番号292)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHYSGHPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#10の軽鎖組み合わせ(配列番号293)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVHSGHPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#11の軽鎖組み合わせ(配列番号294)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIHLHWYQQKPGKAPKLLIYHTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHYSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#12の軽鎖組み合わせ(配列番号295)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIHLHWYQQKPGKAPKLLIYHTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVHSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#13の軽鎖組み合わせ(配列番号296)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIHLHWYQQKPGKAPKLLIYHTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGHPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#14の軽鎖組み合わせ(配列番号297)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIHLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHHSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#15の軽鎖組み合わせ(配列番号298)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIHLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHYSGHPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#16の軽鎖組み合わせ(配列番号299)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIHLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVHSGHPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#17の軽鎖組み合わせ(配列番号300)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYHTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHHSGYPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#18の軽鎖組み合わせ(配列番号301)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYHTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHYSGHPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#19の軽鎖組み合わせ(配列番号302)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYHTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVHSGHPLTFGGGTKVEIK
>エミベツズマブIgGヒスチジンスキャニング変異体#20の軽鎖組み合わせ(配列番号303)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHHSGHPLTFGGGTKVEIK
>hucMET27Gv1.3 IgGの重鎖(配列番号304)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGの軽鎖(配列番号305)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3の重鎖CDR1(配列番号306)
GFTFSSYDMS
>hucMET27Gv1.3の重鎖CDR2(配列番号307)
TINSNGVSIYYPDSVKG
>hucMET27Gv1.3の重鎖CDR3(配列番号308)
AREEITTEMDY
>hucMET27Gv1.3の軽鎖CDR1(配列番号309)
RASESVDSYGNSFIH
>hucMET27Gv1.3の軽鎖CDR2(配列番号310)
RASNLES
>hucMET27Gv1.3の軽鎖CDR3(配列番号311)
QQSNEEPLT
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#1の重鎖(配列番号312)
EVQLVESGGGLVQPGGSLRLSCAASHFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#2の重鎖(配列番号313)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#3の重鎖(配列番号314)
EVQLVESGGGLVQPGGSLRLSCAASGFHFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#4の重鎖(配列番号315)
EVQLVESGGGLVQPGGSLRLSCAASGFTHSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#5の重鎖(配列番号316)
EVQLVESGGGLVQPGGSLRLSCAASGFTFHSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#6の重鎖(配列番号317)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSHYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#7の重鎖(配列番号318)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSHDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#8の重鎖(配列番号319)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYHMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#9の重鎖(配列番号320)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDHSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#10の重鎖(配列番号321)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMHWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#11の重鎖(配列番号322)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVAHINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#12の重鎖(配列番号323)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATHNSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#13の重鎖(配列番号324)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATIHSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#14の重鎖(配列番号325)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINHNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#15の重鎖(配列番号326)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSHGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#16の重鎖(配列番号327)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNHVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#17の重鎖(配列番号328)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGHSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#18の重鎖(配列番号329)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVHIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#19の重鎖(配列番号330)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSHYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#20の重鎖(配列番号331)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIHYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#21の重鎖(配列番号332)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#22の重鎖(配列番号333)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYHDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#23の重鎖(配列番号334)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPHSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#24の重鎖(配列番号335)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDHVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#25の重鎖(配列番号336)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSHKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#26の重鎖(配列番号337)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVHGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#27の重鎖(配列番号338)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#28の重鎖(配列番号339)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCHREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#29の重鎖(配列番号340)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAHEEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#30の重鎖(配列番号341)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCARHEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#31の重鎖(配列番号342)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREHITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#32の重鎖(配列番号343)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEHTTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#33の重鎖(配列番号344)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEIHTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#34の重鎖(配列番号345)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#35の重鎖(配列番号346)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTHMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#36の重鎖(配列番号347)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#37の重鎖(配列番号348)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMHYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#38の重鎖(配列番号349)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#1の軽鎖(配列番号350)
EIVLTQSPATLSLSPGERATLSCHASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#2の軽鎖(配列番号351)
EIVLTQSPATLSLSPGERATLSCRHSESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#3の軽鎖(配列番号352)
EIVLTQSPATLSLSPGERATLSCRAHESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#4の軽鎖(配列番号353)
EIVLTQSPATLSLSPGERATLSCRASHSVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#5の軽鎖(配列番号354)
EIVLTQSPATLSLSPGERATLSCRASEHVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#6の軽鎖(配列番号355)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#7の軽鎖(配列番号356)
EIVLTQSPATLSLSPGERATLSCRASESVHSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#8の軽鎖(配列番号357)
EIVLTQSPATLSLSPGERATLSCRASESVDHYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#9の軽鎖(配列番号358)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#10の軽鎖(配列番号359)
EIVLTQSPATLSLSPGERATLSCRASESVDSYHNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#11の軽鎖(配列番号360)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#12の軽鎖(配列番号361)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNHFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#13の軽鎖(配列番号362)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#14の軽鎖(配列番号363)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFHHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#15の軽鎖(配列番号364)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIAWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#16の軽鎖(配列番号365)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#17の軽鎖(配列番号366)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRHSNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#18の軽鎖(配列番号367)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRAHNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#19の軽鎖(配列番号368)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASHLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#20の軽鎖(配列番号369)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNHESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#21の軽鎖(配列番号370)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLHSGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#22の軽鎖(配列番号371)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#23の軽鎖(配列番号372)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCHQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#24の軽鎖(配列番号373)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQHSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#25の軽鎖(配列番号374)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQHNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#26の軽鎖(配列番号375)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSHEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#27の軽鎖(配列番号376)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNHEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#28の軽鎖(配列番号377)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEHPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#29の軽鎖(配列番号378)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#30の軽鎖(配列番号379)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPHTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#31の軽鎖(配列番号380)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLHFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#1の重鎖組み合わせ(配列番号381)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#2の重鎖組み合わせ(配列番号382)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#3の重鎖組み合わせ(配列番号383)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#4の重鎖組み合わせ(配列番号384)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#5の重鎖組み合わせ(配列番号385)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#6の重鎖組み合わせ(配列番号386)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#7の重鎖組み合わせ(配列番号387)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#8の重鎖組み合わせ(配列番号388)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#9の重鎖組み合わせ(配列番号389)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#10の重鎖組み合わせ(配列番号390)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEHDHWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#11の重鎖組み合わせ(配列番号391)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#12の重鎖組み合わせ(配列番号392)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#13の重鎖組み合わせ(配列番号393)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#14の重鎖組み合わせ(配列番号394)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#15の重鎖組み合わせ(配列番号395)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#16の重鎖組み合わせ(配列番号396)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEHDHWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#17の重鎖組み合わせ(配列番号397)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#18の重鎖組み合わせ(配列番号398)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#19の重鎖組み合わせ(配列番号399)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEHDHWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#20の重鎖組み合わせ(配列番号400)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEHDHWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#21の重鎖組み合わせ(配列番号401)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#22の重鎖組み合わせ(配列番号402)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#23の重鎖組み合わせ(配列番号403)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#24の重鎖組み合わせ(配列番号404)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#25の重鎖組み合わせ(配列番号405)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#26の重鎖組み合わせ(配列番号406)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#27の重鎖組み合わせ(配列番号407)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#28の重鎖組み合わせ(配列番号408)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#29の重鎖組み合わせ(配列番号409)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#30の重鎖組み合わせ(配列番号410)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#31の重鎖組み合わせ(配列番号411)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#32の重鎖組み合わせ(配列番号412)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#33の重鎖組み合わせ(配列番号413)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#34の重鎖組み合わせ(配列番号414)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#35の重鎖組み合わせ(配列番号415)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEHDHWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#36の重鎖組み合わせ(配列番号416)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#37の重鎖組み合わせ(配列番号417)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#38の重鎖組み合わせ(配列番号418)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#39の重鎖組み合わせ(配列番号419)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#40の重鎖組み合わせ(配列番号420)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#41の重鎖組み合わせ(配列番号421)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEHDHWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#42の重鎖組み合わせ(配列番号422)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#43の重鎖組み合わせ(配列番号423)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#44の重鎖組み合わせ(配列番号424)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEHDHWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#45の重鎖組み合わせ(配列番号425)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEHDHWGQGTLVTVSS
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#1の軽鎖組み合わせ(配列番号426)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGHSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#2の軽鎖組み合わせ(配列番号427)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#3の軽鎖組み合わせ(配列番号428)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#4の軽鎖組み合わせ(配列番号429)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#5の軽鎖組み合わせ(配列番号430)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#6の軽鎖組み合わせ(配列番号431)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#7の軽鎖組み合わせ(配列番号432)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#8の軽鎖組み合わせ(配列番号433)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSHIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#9の軽鎖組み合わせ(配列番号434)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#10の軽鎖組み合わせ(配列番号435)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#11の軽鎖組み合わせ(配列番号436)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGHSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#12の軽鎖組み合わせ(配列番号437)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGHSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#13の軽鎖組み合わせ(配列番号438)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGHSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#14の軽鎖組み合わせ(配列番号439)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSHIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#15の軽鎖組み合わせ(配列番号440)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#16の軽鎖組み合わせ(配列番号441)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#17の軽鎖組み合わせ(配列番号442)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSHIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#18の軽鎖組み合わせ(配列番号443)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#19の軽鎖組み合わせ(配列番号444)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#20の軽鎖組み合わせ(配列番号445)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSHIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#21の軽鎖組み合わせ(配列番号446)
EIVLTQSPATLSLSPGERATLSCRASESHDSHGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#22の軽鎖組み合わせ(配列番号447)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGHSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#23の軽鎖組み合わせ(配列番号448)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGNSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#24の軽鎖組み合わせ(配列番号449)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGNSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#25の軽鎖組み合わせ(配列番号450)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#26の軽鎖組み合わせ(配列番号451)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSFIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#27の軽鎖組み合わせ(配列番号452)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSFIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#28の軽鎖組み合わせ(配列番号453)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSHIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#29の軽鎖組み合わせ(配列番号454)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYHASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#30の軽鎖組み合わせ(配列番号455)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#31の軽鎖組み合わせ(配列番号456)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGNSFIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#32の軽鎖組み合わせ(配列番号457)
EIVLTQSPATLSLSPGERATLSCRASESHDSHGNSFIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#33の軽鎖組み合わせ(配列番号458)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGHSFIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#34の軽鎖組み合わせ(配列番号459)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGNSHIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#35の軽鎖組み合わせ(配列番号460)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGNSFIHWYQQKPGQAPRLLIYHASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#36の軽鎖組み合わせ(配列番号461)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGNSFIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#37の軽鎖組み合わせ(配列番号462)
EIVLTQSPATLSLSPGERATLSCRASESHDSHGHSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#38の軽鎖組み合わせ(配列番号463)
EIVLTQSPATLSLSPGERATLSCRASESHDSHGNSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#39の軽鎖組み合わせ(配列番号464)
EIVLTQSPATLSLSPGERATLSCRASESHDSHGNSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#40の軽鎖組み合わせ(配列番号465)
EIVLTQSPATLSLSPGERATLSCRASESHDSHGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#41の軽鎖組み合わせ(配列番号466)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGHSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#42の軽鎖組み合わせ(配列番号467)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGHSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#43の軽鎖組み合わせ(配列番号468)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGHSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#44の軽鎖組み合わせ(配列番号469)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGNSHIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#45の軽鎖組み合わせ(配列番号470)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGNSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#46の軽鎖組み合わせ(配列番号471)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGNSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#47の軽鎖組み合わせ(配列番号472)
EIVLTQSPATLSLSPGERATLSCRASESHDSHGHSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#48の軽鎖組み合わせ(配列番号473)
EIVLTQSPATLSLSPGERATLSCRASESHDSHGHSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#49の軽鎖組み合わせ(配列番号474)
EIVLTQSPATLSLSPGERATLSCRASESHDSHGHSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#50の軽鎖組み合わせ(配列番号475)
EIVLTQSPATLSLSPGERATLSCRASESHDSHGNSHIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#51の軽鎖組み合わせ(配列番号476)
EIVLTQSPATLSLSPGERATLSCRASESHDSHGNSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#52の軽鎖組み合わせ(配列番号477)
EIVLTQSPATLSLSPGERATLSCRASESHDSHGNSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#53の軽鎖組み合わせ(配列番号478)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGHSHIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#54の軽鎖組み合わせ(配列番号479)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGHSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#55の軽鎖組み合わせ(配列番号480)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGHSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#56の軽鎖組み合わせ(配列番号481)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGNSHIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#57の軽鎖組み合わせ(配列番号482)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGHSFIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#58の軽鎖組み合わせ(配列番号483)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSHIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#59の軽鎖組み合わせ(配列番号484)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSFIHWYQQKPGQAPRLLIYHASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#60の軽鎖組み合わせ(配列番号485)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSFIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#61の軽鎖組み合わせ(配列番号486)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSHIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#62の軽鎖組み合わせ(配列番号487)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSFIHWYQQKPGQAPRLLIYHASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#63の軽鎖組み合わせ(配列番号488)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSFIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#64の軽鎖組み合わせ(配列番号489)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSHIHWYQQKPGQAPRLLIYHASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#65の軽鎖組み合わせ(配列番号490)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSHIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#66の軽鎖組み合わせ(配列番号491)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYHASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#67の軽鎖組み合わせ(配列番号492)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGHSHIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#68の軽鎖組み合わせ(配列番号493)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGHSFIHWYQQKPGQAPRLLIYHASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#69の軽鎖組み合わせ(配列番号494)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGHSFIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#70の軽鎖組み合わせ(配列番号495)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSHIHWYQQKPGQAPRLLIYHASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#71の軽鎖組み合わせ(配列番号496)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSHIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#72の軽鎖組み合わせ(配列番号497)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSFIHWYQQKPGQAPRLLIYHASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#73の軽鎖組み合わせ(配列番号498)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSHIHWYQQKPGQAPRLLIYHASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#74の軽鎖組み合わせ(配列番号499)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSHIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#75の軽鎖組み合わせ(配列番号500)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSFIHWYQQKPGQAPRLLIYHASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgGヒスチジンスキャニング変異体#76の軽鎖組み合わせ(配列番号501)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSHIHWYQQKPGQAPRLLIYHASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>P3D12 IgGの重鎖(配列番号502)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGの軽鎖(配列番号503)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12の重鎖CDR1(配列番号504)
GYTFTSYWMH
>P3D12の重鎖CDR2(配列番号505)
YIKPSTDNTEYNQKFKD
>P3D12の重鎖CDR3(配列番号506)
ARSYGNYPLMDY
>P3D12の軽鎖CDR1(配列番号507)
SASSSVTSNYLY
>P3D12の軽鎖CDR2(配列番号508)
STSNLAS
>P3D12の軽鎖CDR3(配列番号509)
HQWSSYPPT
>P3D12 IgGヒスチジンスキャニング変異体#1の重鎖(配列番号510)
QVQLVQSGAEVKKPGASVKVSCKASHYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#2の重鎖(配列番号511)
QVQLVQSGAEVKKPGASVKVSCKASGHTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#3の重鎖(配列番号512)
QVQLVQSGAEVKKPGASVKVSCKASGYHFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#4の重鎖(配列番号513)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#5の重鎖(配列番号514)
QVQLVQSGAEVKKPGASVKVSCKASGYTFHSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#6の重鎖(配列番号515)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#7の重鎖(配列番号516)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSHWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#8の重鎖(配列番号517)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#9の重鎖(配列番号518)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWHHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#10の重鎖(配列番号519)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#11の重鎖(配列番号520)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#12の重鎖(配列番号521)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYHKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#13の重鎖(配列番号522)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIHPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#14の重鎖(配列番号523)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKHSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#15の重鎖(配列番号524)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPHTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#16の重鎖(配列番号525)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSHDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#17の重鎖(配列番号526)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTHNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#18の重鎖(配列番号527)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDHTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#19の重鎖(配列番号528)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNHEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#20の重鎖(配列番号529)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#21の重鎖(配列番号530)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEHNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#22の重鎖(配列番号531)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYHQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#23の重鎖(配列番号532)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNHKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#24の重鎖(配列番号533)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQHFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#25の重鎖(配列番号534)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKHKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#26の重鎖(配列番号535)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFHDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#27の重鎖(配列番号536)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKHKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#28の重鎖(配列番号537)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCHRSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#29の重鎖(配列番号538)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCAHSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#30の重鎖(配列番号539)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARHYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#31の重鎖(配列番号540)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSHGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#32の重鎖(配列番号541)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYHNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#33の重鎖(配列番号542)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#34の重鎖(配列番号543)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#35の重鎖(配列番号544)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYHLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#36の重鎖(配列番号545)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPHMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#37の重鎖(配列番号546)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#38の重鎖(配列番号547)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#39の重鎖(配列番号548)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDHWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#1の軽鎖(配列番号549)
QIVLTQSPAILSLSPGERATLSCHASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#2の軽鎖(配列番号550)
QIVLTQSPAILSLSPGERATLSCSHSSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#3の軽鎖(配列番号551)
QIVLTQSPAILSLSPGERATLSCSAHSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#4の軽鎖(配列番号552)
QIVLTQSPAILSLSPGERATLSCSASHSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#5の軽鎖(配列番号553)
QIVLTQSPAILSLSPGERATLSCSASSHVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#6の軽鎖(配列番号554)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#7の軽鎖(配列番号555)
QIVLTQSPAILSLSPGERATLSCSASSSVHSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#8の軽鎖(配列番号556)
QIVLTQSPAILSLSPGERATLSCSASSSVTHNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#9の軽鎖(配列番号557)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#10の軽鎖(配列番号558)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNHLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#11の軽鎖(配列番号559)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYHYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#12の軽鎖(配列番号560)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#13の軽鎖(配列番号561)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYHTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#14の軽鎖(配列番号562)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSHSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#15の軽鎖(配列番号563)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTHNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#16の軽鎖(配列番号564)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSHLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#17の軽鎖(配列番号565)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNHASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#18の軽鎖(配列番号566)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLHSGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#19の軽鎖(配列番号567)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLAHGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#20の軽鎖(配列番号568)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCAQWSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#21の軽鎖(配列番号569)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHHWSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#22の軽鎖(配列番号570)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#23の軽鎖(配列番号571)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWHSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#24の軽鎖(配列番号572)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#25の軽鎖(配列番号573)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#26の軽鎖(配列番号574)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#27の軽鎖(配列番号575)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPHTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#28の軽鎖(配列番号576)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#1の重鎖組み合わせ(配列番号577)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#2の重鎖組み合わせ(配列番号578)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#3の重鎖組み合わせ(配列番号579)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#4の重鎖組み合わせ(配列番号580)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#5の重鎖組み合わせ(配列番号581)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#6の重鎖組み合わせ(配列番号582)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#7の重鎖組み合わせ(配列番号583)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#8の重鎖組み合わせ(配列番号584)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#9の重鎖組み合わせ(配列番号585)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#10の重鎖組み合わせ(配列番号586)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#11の重鎖組み合わせ(配列番号587)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGHIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#12の重鎖組み合わせ(配列番号588)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#13の重鎖組み合わせ(配列番号589)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#14の重鎖組み合わせ(配列番号590)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#15の重鎖組み合わせ(配列番号591)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#16の重鎖組み合わせ(配列番号592)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#17の重鎖組み合わせ(配列番号593)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#18の重鎖組み合わせ(配列番号594)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#19の重鎖組み合わせ(配列番号595)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#20の重鎖組み合わせ(配列番号596)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#21の重鎖組み合わせ(配列番号597)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#22の重鎖組み合わせ(配列番号598)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#23の重鎖組み合わせ(配列番号599)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#24の重鎖組み合わせ(配列番号600)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#25の重鎖組み合わせ(配列番号601)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#26の重鎖組み合わせ(配列番号602)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#27の重鎖組み合わせ(配列番号603)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#28の重鎖組み合わせ(配列番号604)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#29の重鎖組み合わせ(配列番号605)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#30の重鎖組み合わせ(配列番号606)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#31の重鎖組み合わせ(配列番号607)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#32の重鎖組み合わせ(配列番号608)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#33の重鎖組み合わせ(配列番号609)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#34の重鎖組み合わせ(配列番号610)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHHPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#35の重鎖組み合わせ(配列番号611)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#36の重鎖組み合わせ(配列番号612)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#37の重鎖組み合わせ(配列番号613)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#38の重鎖組み合わせ(配列番号614)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#39の重鎖組み合わせ(配列番号615)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#40の重鎖組み合わせ(配列番号616)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#41の重鎖組み合わせ(配列番号617)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#42の重鎖組み合わせ(配列番号618)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#43の重鎖組み合わせ(配列番号619)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#44の重鎖組み合わせ(配列番号620)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#45の重鎖組み合わせ(配列番号621)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#46の重鎖組み合わせ(配列番号622)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#47の重鎖組み合わせ(配列番号623)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#48の重鎖組み合わせ(配列番号624)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#49の重鎖組み合わせ(配列番号625)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#50の重鎖組み合わせ(配列番号626)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#51の重鎖組み合わせ(配列番号627)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYHMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#52の重鎖組み合わせ(配列番号628)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#53の重鎖組み合わせ(配列番号629)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#54の重鎖組み合わせ(配列番号630)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#55の重鎖組み合わせ(配列番号631)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#56の重鎖組み合わせ(配列番号632)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#57の重鎖組み合わせ(配列番号633)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMAWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#58の重鎖組み合わせ(配列番号634)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#59の重鎖組み合わせ(配列番号635)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#60の重鎖組み合わせ(配列番号636)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#61の重鎖組み合わせ(配列番号637)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#62の重鎖組み合わせ(配列番号638)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#63の重鎖組み合わせ(配列番号639)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMAWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#64の重鎖組み合わせ(配列番号640)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#65の重鎖組み合わせ(配列番号641)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#66の重鎖組み合わせ(配列番号642)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#67の重鎖組み合わせ(配列番号643)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#68の重鎖組み合わせ(配列番号644)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#69の重鎖組み合わせ(配列番号645)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#70の重鎖組み合わせ(配列番号646)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHHPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#71の重鎖組み合わせ(配列番号647)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#72の重鎖組み合わせ(配列番号648)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHHPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#73の重鎖組み合わせ(配列番号649)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#74の重鎖組み合わせ(配列番号650)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHHPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#75の重鎖組み合わせ(配列番号651)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#76の重鎖組み合わせ(配列番号652)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#77の重鎖組み合わせ(配列番号653)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#78の重鎖組み合わせ(配列番号654)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#79の重鎖組み合わせ(配列番号655)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#80の重鎖組み合わせ(配列番号656)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLHHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#81の重鎖組み合わせ(配列番号657)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYHMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#82の重鎖組み合わせ(配列番号658)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYHMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#83の重鎖組み合わせ(配列番号659)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#84の重鎖組み合わせ(配列番号660)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#85の重鎖組み合わせ(配列番号661)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGHIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#86の重鎖組み合わせ(配列番号662)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#87の重鎖組み合わせ(配列番号663)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#88の重鎖組み合わせ(配列番号664)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#89の重鎖組み合わせ(配列番号665)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#90の重鎖組み合わせ(配列番号666)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#91の重鎖組み合わせ(配列番号667)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMAWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#92の重鎖組み合わせ(配列番号668)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMAWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#93の重鎖組み合わせ(配列番号669)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#94の重鎖組み合わせ(配列番号670)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#95の重鎖組み合わせ(配列番号671)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGHIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#96の重鎖組み合わせ(配列番号672)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#97の重鎖組み合わせ(配列番号673)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#98の重鎖組み合わせ(配列番号674)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#99の重鎖組み合わせ(配列番号675)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#100の重鎖組み合わせ(配列番号676)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#101の重鎖組み合わせ(配列番号677)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#102の重鎖組み合わせ(配列番号678)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#103の重鎖組み合わせ(配列番号679)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHHPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#104の重鎖組み合わせ(配列番号680)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#105の重鎖組み合わせ(配列番号681)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#106の重鎖組み合わせ(配列番号682)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHHPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#107の重鎖組み合わせ(配列番号683)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#108の重鎖組み合わせ(配列番号684)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHHPLMDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#109の重鎖組み合わせ(配列番号685)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#110の重鎖組み合わせ(配列番号686)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHHPLMHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#111の重鎖組み合わせ(配列番号687)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#112の重鎖組み合わせ(配列番号688)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#113の重鎖組み合わせ(配列番号689)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#114の重鎖組み合わせ(配列番号690)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#115の重鎖組み合わせ(配列番号691)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#116の重鎖組み合わせ(配列番号692)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#117の重鎖組み合わせ(配列番号693)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#118の重鎖組み合わせ(配列番号694)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLHDYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#119の重鎖組み合わせ(配列番号695)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#120の重鎖組み合わせ(配列番号696)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLHHYWGQGTTVTVSS
>P3D12 IgGヒスチジンスキャニング変異体#1の軽鎖組み合わせ(配列番号697)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#2の軽鎖組み合わせ(配列番号698)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#3の軽鎖組み合わせ(配列番号699)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#4の軽鎖組み合わせ(配列番号700)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPHTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#5の軽鎖組み合わせ(配列番号701)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHHPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#6の軽鎖組み合わせ(配列番号702)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYHPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#7の軽鎖組み合わせ(配列番号703)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPHTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#8の軽鎖組み合わせ(配列番号704)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHHPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#9の軽鎖組み合わせ(配列番号705)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPHTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#10の軽鎖組み合わせ(配列番号706)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHHTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#11の軽鎖組み合わせ(配列番号707)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHHPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#12の軽鎖組み合わせ(配列番号708)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYHPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#13の軽鎖組み合わせ(配列番号709)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPHTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#14の軽鎖組み合わせ(配列番号710)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHHPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#15の軽鎖組み合わせ(配列番号711)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPHTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#16の軽鎖組み合わせ(配列番号712)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHHTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#17の軽鎖組み合わせ(配列番号713)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHHHPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#18の軽鎖組み合わせ(配列番号714)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHHPHTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#19の軽鎖組み合わせ(配列番号715)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYHHTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#20の軽鎖組み合わせ(配列番号716)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHHHTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#21の軽鎖組み合わせ(配列番号717)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#22の軽鎖組み合わせ(配列番号718)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#23の軽鎖組み合わせ(配列番号719)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#24の軽鎖組み合わせ(配列番号720)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#25の軽鎖組み合わせ(配列番号721)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#26の軽鎖組み合わせ(配列番号722)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#27の軽鎖組み合わせ(配列番号723)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#28の軽鎖組み合わせ(配列番号724)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#29の軽鎖組み合わせ(配列番号725)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#30の軽鎖組み合わせ(配列番号726)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSHYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#31の軽鎖組み合わせ(配列番号727)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSHPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#32の軽鎖組み合わせ(配列番号728)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYHPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#33の軽鎖組み合わせ(配列番号729)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#34の軽鎖組み合わせ(配列番号730)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#35の軽鎖組み合わせ(配列番号731)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#36の軽鎖組み合わせ(配列番号732)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#37の軽鎖組み合わせ(配列番号733)
QIVLTQSPAILSLSPGERATLSCSASSSHTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#38の軽鎖組み合わせ(配列番号734)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#39の軽鎖組み合わせ(配列番号735)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#40の軽鎖組み合わせ(配列番号736)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#41の軽鎖組み合わせ(配列番号737)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#42の軽鎖組み合わせ(配列番号738)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYPPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#43の軽鎖組み合わせ(配列番号739)
QIVLTQSPAILSLSPGERATLSCSASSSHTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#44の軽鎖組み合わせ(配列番号740)
QIVLTQSPAILSLSPGERATLSCSASSSHTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#45の軽鎖組み合わせ(配列番号741)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYPPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#46の軽鎖組み合わせ(配列番号742)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYPPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#47の軽鎖組み合わせ(配列番号743)
QIVLTQSPAILSLSPGERATLSCSASSSHTSHYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#48の軽鎖組み合わせ(配列番号744)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#49の軽鎖組み合わせ(配列番号745)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#50の軽鎖組み合わせ(配列番号746)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#51の軽鎖組み合わせ(配列番号747)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#52の軽鎖組み合わせ(配列番号748)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYPPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#53の軽鎖組み合わせ(配列番号749)
QIVLTQSPAILSLSPGERATLSCSASSSHTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#54の軽鎖組み合わせ(配列番号750)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSHYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#55の軽鎖組み合わせ(配列番号751)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#56の軽鎖組み合わせ(配列番号752)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSHYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#57の軽鎖組み合わせ(配列番号753)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#58の軽鎖組み合わせ(配列番号754)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSHYPPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#59の軽鎖組み合わせ(配列番号755)
QIVLTQSPAILSLSPGERATLSCSASSSHTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#60の軽鎖組み合わせ(配列番号756)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSHPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#61の軽鎖組み合わせ(配列番号757)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#62の軽鎖組み合わせ(配列番号758)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSHPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#63の軽鎖組み合わせ(配列番号759)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#64の軽鎖組み合わせ(配列番号760)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSHPPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#65の軽鎖組み合わせ(配列番号761)
QIVLTQSPAILSLSPGERATLSCSASSSHTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#66の軽鎖組み合わせ(配列番号762)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYHPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#67の軽鎖組み合わせ(配列番号763)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#68の軽鎖組み合わせ(配列番号764)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYHPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#69の軽鎖組み合わせ(配列番号765)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#70の軽鎖組み合わせ(配列番号766)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYHPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#71の軽鎖組み合わせ(配列番号767)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#72の軽鎖組み合わせ(配列番号768)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#73の軽鎖組み合わせ(配列番号769)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#74の軽鎖組み合わせ(配列番号770)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHHPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#75の軽鎖組み合わせ(配列番号771)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYHPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#76の軽鎖組み合わせ(配列番号772)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHHPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#77の軽鎖組み合わせ(配列番号773)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#78の軽鎖組み合わせ(配列番号774)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#79の軽鎖組み合わせ(配列番号775)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#80の軽鎖組み合わせ(配列番号776)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHHPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#81の軽鎖組み合わせ(配列番号777)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYHPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#82の軽鎖組み合わせ(配列番号778)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHHPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#83の軽鎖組み合わせ(配列番号779)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSHYPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#84の軽鎖組み合わせ(配列番号780)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSHPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#85の軽鎖組み合わせ(配列番号781)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYHPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#86の軽鎖組み合わせ(配列番号782)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSHHPPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#87の軽鎖組み合わせ(配列番号783)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSHYHPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#88の軽鎖組み合わせ(配列番号784)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSHHPTFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#89の軽鎖組み合わせ(配列番号785)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#90の軽鎖組み合わせ(配列番号786)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#91の軽鎖組み合わせ(配列番号787)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#92の軽鎖組み合わせ(配列番号788)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHHPPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#93の軽鎖組み合わせ(配列番号789)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYHPHFGSGTKLEIK
>P3D12 IgGヒスチジンスキャニング変異体#94の軽鎖組み合わせ(配列番号790)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHHPHFGSGTKLEIK