KR20220053577A - 항원 결합 단백질 작제물 및 이의 용도 - Google Patents
항원 결합 단백질 작제물 및 이의 용도 Download PDFInfo
- Publication number
- KR20220053577A KR20220053577A KR1020227006745A KR20227006745A KR20220053577A KR 20220053577 A KR20220053577 A KR 20220053577A KR 1020227006745 A KR1020227006745 A KR 1020227006745A KR 20227006745 A KR20227006745 A KR 20227006745A KR 20220053577 A KR20220053577 A KR 20220053577A
- Authority
- KR
- South Korea
- Prior art keywords
- seq
- chain variable
- variable domain
- light chain
- histidine
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6849—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a receptor, a cell surface antigen or a cell surface determinant
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6875—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody being a hybrid immunoglobulin
- A61K47/6879—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody being a hybrid immunoglobulin the immunoglobulin having two or more different antigen-binding sites, e.g. bispecific or multispecific immunoglobulin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K51/00—Preparations containing radioactive substances for use in therapy or testing in vivo
- A61K51/02—Preparations containing radioactive substances for use in therapy or testing in vivo characterised by the carrier, i.e. characterised by the agent or material covalently linked or complexing the radioactive nucleus
- A61K51/04—Organic compounds
- A61K51/08—Peptides, e.g. proteins, carriers being peptides, polyamino acids, proteins
- A61K51/10—Antibodies or immunoglobulins; Fragments thereof, the carrier being an antibody, an immunoglobulin or a fragment thereof, e.g. a camelised human single domain antibody or the Fc fragment of an antibody
- A61K51/1027—Antibodies or immunoglobulins; Fragments thereof, the carrier being an antibody, an immunoglobulin or a fragment thereof, e.g. a camelised human single domain antibody or the Fc fragment of an antibody against receptors, cell-surface antigens or cell-surface determinants
- A61K51/103—Antibodies or immunoglobulins; Fragments thereof, the carrier being an antibody, an immunoglobulin or a fragment thereof, e.g. a camelised human single domain antibody or the Fc fragment of an antibody against receptors, cell-surface antigens or cell-surface determinants against receptors for growth factors or receptors for growth regulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2863—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against receptors for growth factors, growth regulators
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/32—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against translation products of oncogenes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/31—Immunoglobulins specific features characterized by aspects of specificity or valency multispecific
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/77—Internalization into the cell
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/94—Stability, e.g. half-life, pH, temperature or enzyme-resistance
Abstract
표적 포유류 세포의 표면 상에 제시된 MET 또는 MET의 에피토프에 특이적으로 결합할 수 있는 항원 결합 단백질 작제물이 본원에 제공되며, 여기서 상기 항원 결합은 pH 의존적이다. 또한, 상기 항원 결합 단백질 작제물의 용도가 제공된다.
Description
관련 출원에 대한 상호 참조
본 출원은 2019년 7월 30일에 출원된 미국 특허 가출원 제62/880,449호에 대한 우선권을 주장한다. 해당 출원의 내용은 그 전체가 참조로서 본원에 통합된다.
기술 분야
본 개시는 생명공학 분야에 관한 것으로서, 보다 구체적으로는 항원 결합 분자에 관한 것이다.
항체-약물-접합체는 다양한 질환을 퇴치하기 위해 설계되어 왔다. 이러한 접근법의 한 가지 특별한 장점은 항체-약물 접합체가 세포증식 억제성(cytostatic) 또는 세포독성(cytotoxic) 효과를 가질 수 있는 능력이다. 수년 간의 개발에도 불구하고, 개선된 항체-약물 접합체가 요구된다.
본 발명은 강화된 효능(예를 들어, 표적 포유류 세포에서 독소 유리의 증가(예: 검출 가능한 증가), 표적 포유류 세포 사멸의 증가(예: 검출 가능한 증가), 및 엔도리소좀 전달의 증가(예: 검출 가능한 증가) 중 하나 이상)을 나타내는 항원 결합 단백질 작제물을 생성할 수 있다는 개념에 기초한다.
항원 결합 단백질 작제물(ABPC)의 유효량을 포함하는 약학적 조성물이 본원에 제공되며, ABPC는 표적 포유류 세포의 표면 상에 제시된 MET 또는 MET의 에피토프에 특이적으로 결합할 수 있는 제1 항원 결합 도메인을 포함하되, (a) 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인의 해리 속도는 약 7.0 내지 약 8.0의 pH에서의 해리 속도보다 빠르거나; (b) 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인의 해리 상수(KD)는 약 7.0 내지 약 8.0의 pH에서의 KD보다 더 크다.
본원에 기술된 약학적 조성물 중 어느 하나의 일부 구현예에서, ABPC는 표적 포유류 세포에 의해 내재화된 후 표적 포유류 세포 내에서 분해된다.
본원에 기술된 약학적 조성물 중 어느 하나의 일부 구현예에서, ABPC는 접합된 독소, 방사성 동위원소, 약물, 또는 소분자를 포함한다.
또한, 항원 결합 단백질 작제물(ABPC)의 유효량을 포함하는 약학적 조성물이 본원에 제공되며, ABPC는: 표적 포유류 세포의 표면 상에 제시된 MET 또는 MET의 에피토프에 특이적으로 결합할 수 있는 제1 항원 결합 도메인; 및 접합된 독소, 방사성 동위원소, 약물, 또는 소분자를 포함하되, (a) 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인의 해리 속도는 약 7.0 내지 약 8.0의 pH에서의 해리 속도보다 빠르거나; 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인의 해리 상수(KD)는 약 7.0 내지 약 8.0의 pH에서의 KD보다 더 크며; (b) 조성물은 다음 중 하나 이상을 가능하게 한다: 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때, 표적 포유류 세포에서 독소 유리의 증가; 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때, 표적 포유류 세포 사멸의 증가; 및 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때, 표적 포유류 세포에서 엔도리소좀 전달의 증가.
본원에 기술된 약학적 조성물 중 어느 하나의 일부 구현예에서, 제1 항원 결합 도메인은 (a) 내지 (d) 중 하나를 포함한다: (a) 하나 이상의 아미노산이 히스티딘으로 치환된 텔리소투주맙(Telisotuzumab)의 중쇄 가변 도메인으로서, 서열번호 1을 포함하는 텔리소투주맙의 중쇄 가변 도메인; 및/또는 하나 이상의 아미노산이 히스티딘으로 치환된 텔리소투주맙의 경쇄 가변 도메인으로서, 서열번호 2를 포함하는 텔리소투주맙의 경쇄 가변 도메인; (b) 하나 이상의 아미노산이 히스티딘으로 치환된 에미베투주맙(Emibetuzumab)의 중쇄 가변 도메인으로서, 서열번호 146을 포함하는 에미베투주맙의 중쇄 가변 도메인; 및/또는 하나 이상의 아미노산이 히스티딘으로 치환된 에미베투주맙의 경쇄 가변 도메인으로서, 서열번호 147을 포함하는 에미베투주맙의 경쇄 가변 도메인; (c) 하나 이상의 아미노산이 히스티딘으로 hucMET27Gv1.3의 중쇄 가변 도메인으로서, 서열번호 304를 포함하는 hucMET27Gv1.3의 중쇄 가변 도메인; 및/또는 하나 이상의 아미노산이 히스티딘으로 치환된 hucMET27Gv1.3의 경쇄 가변 도메인으로서, 서열번호 305를 포함하는 hucMET27Gv1.3의 경쇄 가변 도메인; 및 (d) 하나 이상의 아미노산이 히스티딘으로 치환된 P3D12의 중쇄 가변 도메인으로서, 서열번호 502를 포함하는 P3D12의 중쇄 가변 도메인; 및/또는 하나 이상의 아미노산이 히스티딘으로 치환된 P3D12의 경쇄 가변 도메인으로서, 서열번호 503을 포함하는 P3D12의 경쇄 가변 도메인.
본원에 기술된 약학적 조성물 중 어느 하나의 일부 구현예에서, 제1 MET-결합 도메인은 (a) 내지 (d) 중 하나를 포함한다: (a) 서열번호 3~5의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인으로서, 종합적으로 서열번호 3~5 내 총 하나 이상의 아미노산 위치가 히스티딘으로 치환된, 중쇄 가변 도메인; 및/또는 서열번호 6~8의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인으로서, 종합적으로 서열번호 6~8 내 총 하나 이상의 아미노산 위치가 히스티딘으로 치환된, 경쇄 가변 도메인; (b) 서열번호 148~150의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인으로서, 종합적으로 서열번호 148~150 내 총 하나 이상의 아미노산 위치가 히스티딘으로 치환된, 중쇄 가변 도메인; 및/또는 서열번호 151~153의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인으로서, 종합적으로 서열번호 151~153 내 총 하나 이상의 아미노산 위치가 히스티딘으로 치환된, 경쇄 가변 도메인; (c) 서열번호 306~308의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인으로서, 종합적으로 서열번호 306~308 내 총 하나 이상의 아미노산 위치가 히스티딘으로 치환된, 중쇄 가변 도메인; 및/또는 서열번호 309~311의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인으로서, 종합적으로 서열번호 309~311 내 총 하나 이상의 아미노산 위치가 히스티딘으로 치환된, 경쇄 가변 도메인; 및 (d) 서열번호 504~506의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인으로서, 종합적으로 서열번호 504~506 내 총 하나 이상의 아미노산 위치가 히스티딘으로 치환된, 중쇄 가변 도메인; 및/또는 서열번호 507~509의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인으로서, 종합적으로 서열번호 507~509 내 총 하나 이상의 아미노산 위치가 히스티딘으로 치환된, 경쇄 가변 도메인.
본원에 기술된 약학적 조성물 중 어느 하나의 일부 구현예에서, 제1 항원 결합 도메인은 (a) 내지 (d) 중 하나를 포함한다: (a) 서열번호 1과 적어도 90% 동일한 중쇄 가변 도메인으로서, 서열번호 1의 위치 26, 27, 28, 29, 32, 97, 98, 99, 100, 101, 102, 103, 및 107로 이루어진 군으로부터 선택된 하나 이상의 위치에서 히스티딘을 포함하는, 중쇄 가변 도메인; 및/또는서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 2의 위치 25, 28, 29, 30, 31, 32, 34, 35, 36, 37, 54, 55, 59, 60, 95, 99, 및 101로 이루어진 군으로부터 선택된 하나 이상의 위치에서 히스티딘을 포함하는, 경쇄 가변 도메인; (b) 서열번호 146과 적어도 90% 동일한 중쇄 가변 도메인으로서, 서열번호 146의 위치 31, 50, 51, 52, 53, 54, 56, 57, 59, 98, 99, 100, 및 103으로 이루어진 군으로부터 선택된 하나 이상의 위치에서 히스티딘을 포함하는, 중쇄 가변 도메인; 및/또는서열번호 147과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 147의 위치 25, 26, 29, 32, 33, 51, 91, 92, 95, 96, 및 97로 이루어진 군으로부터 선택된 하나 이상의 위치에서 히스티딘을 포함하는, 경쇄 가변 도메인; (c) 서열번호 304와 적어도 90% 동일한 중쇄 가변 도메인으로서, 서열번호 304의 위치 27, 34, 35, 50, 51, 52, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 98, 99, 103, 및 105로 이루어진 군으로부터 선택된 하나 이상의 위치에서 히스티딘을 포함하는, 중쇄 가변 도메인; 및/또는서열번호 305와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 305의 위치 26, 30, 31, 34, 36, 54, 56, 57, 60, 93, 95, 99, 및 101로 이루어진 군으로부터 선택된 하나 이상의 위치에서 히스티딘을 포함하는, 경쇄 가변 도메인; 및 (d) 서열번호 502와 적어도 90% 동일한 중쇄 가변 도메인으로서, 서열번호 502의 위치 27, 29, 30, 32, 33, 34, 50, 51, 52, 53, 57, 59, 98, 100, 101, 102, 103, 106, 및 107로 이루어진 군으로부터 선택된 하나 이상의 위치에서 히스티딘을 포함하는, 중쇄 가변 도메인; 및/또는서열번호 503과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 503의 위치 25, 29, 31, 32, 33, 34, 35, 52, 55, 91, 92, 93, 94, 95, 96. 97, 및 98로 이루어진 군으로부터 선택된 하나 이상의 위치에서 히스티딘을 포함하는, 경쇄 가변 도메인.
본원에 기술된 약학적 조성물 중 어느 하나의 일부 구현예에서, 제1 항원 결합 도메인은 (a) 내지 (d) 중 하나를 포함한다: (a) 서열번호 2, 52, 55, 56, 57, 58, 59, 61, 62, 63, 64, 65, 66, 67, 71, 72, 75, 79, 81, 131, 132, 133, 134, 135, 136, 137, 138, 139, 또는 140의 경쇄 가변 도메인, 및/또는 서열번호 1, 13, 14, 15, 16, 19, 40, 41, 42, 43, 44, 45, 46, 50, 82, 83, 84, 86, 87, 89, 90, 94, 또는 111의 중쇄 가변 도메인으로서, 제1 항원 결합 도메인은 다음을 포함하지 않는 경쇄 가변 도메인 및/또는 중쇄 가변 도메인: (i) 서열번호 2의 경쇄 가변 도메인 및 서열번호 1의 중쇄 가변 도메인; (ii) 서열번호 2의 경쇄 가변 도메인 및 서열번호 13~16, 19, 40~46, 50, 82~84, 86, 87, 89, 90, 94, 및 111 중 하나가 아닌 중쇄 가변 도메인; 또는 (iii) 서열번호 1의 중쇄 가변 도메인 및 서열번호 52, 55~59, 61~67, 71, 72, 75, 79, 81, 및 131~140 중 하나가 아닌 경쇄 가변 도메인; (b) 서열번호 147, 190, 191, 194, 197, 198, 200, 201, 209, 210, 213, 214, 215, 284, 285, 286, 287, 288, 289, 290, 291, 292, 293, 294, 295, 296, 297, 298, 300, 또는 301의 경쇄 가변 도메인 및/또는 서열번호 146, 159, 164, 165, 166, 167, 168, 170, 171, 173, 182, 183, 184, 187, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 230, 231, 232, 233, 234, 235, 또는 236의 중쇄 가변 도메인으로서, 제1 항원 결합 도메인은 다음을 포함하지 않는 경쇄 가변 도메인 및/또는 중쇄 가변 도메인: (i) 서열번호 147의 경쇄 가변 도메인 및 서열번호 146의 중쇄 가변 도메인; (ii) 서열번호 147의 경쇄 가변 도메인 및 서열번호 159, 164~168, 170, 171, 173, 182~184, 187, 217~228, 및 230~236 중 하나가 아닌 중쇄 가변 도메인; 또는 (iii) 서열번호 146의 중쇄 가변 도메인 및 서열번호 190, 191, 194, 197, 198, 200, 201, 209, 210, 213~215, 284~298, 300, 및 301 중 하나가 아닌 경쇄 가변 도메인; (c) 서열번호 305, 352, 356, 357, 360, 362, 364, 365, 367, 368, 371, 372, 374, 378, 380, 428, 429, 430, 431, 432, 433, 434, 435, 436, 437, 438, 439, 440, 441, 442, 443, 444, 445, 446, 450, 451, 453, 457, 462, 463, 465, 470, 472, 473, 474, 476, 479, 482, 483, 485, 490, 492, 494, 496, 또는 499의 경쇄 가변 도메인 및/또는 서열번호 304, 313, 320, 321, 322, 323, 324, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 340, 341, 345, 347, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 392, 393, 395, 396, 397, 398, 399, 또는 400의 중쇄 가변 도메인으로서, 제1 항원 결합 도메인은 다음을 포함하지 않는 경쇄 가변 도메인 및/또는 중쇄 가변 도메인: (i) 서열번호 305의 경쇄 가변 도메인 및 서열번호 304의 중쇄 가변 도메인; (ii) 서열번호 305의 경쇄 가변 도메인 및 서열번호 313, 320~324, 326~337, 340, 341, 345, 347, 381~390, 392, 393, 및 395~400 중 하나가 아닌 중쇄 가변 도메인; 또는 (iii) 서열번호 304의 중쇄 가변 도메인 및 서열번호 352, 356, 357, 360, 362, 364, 365, 367, 368, 371, 372, 374, 378, 380, 428~446, 450, 451, 453, 457, 462, 463, 465, 470, 472~474, 476, 479, 482, 483, 485, 490, 492, 494, 496, 및 499 중 하나가 아닌 경쇄 가변 도메인; 및 (d) 서열번호 503, 550, 554, 556, 557, 558, 559, 560, 562, 565, 569, 570, 571, 572, 573, 574, 575, 576, 697, 698, 699, 700, 701, 702, 703, 704, 705, 706, 707, 708, 709, 710, 711, 712, 713, 또는 732의 경쇄 가변 도메인 및/또는 서열번호 502, 511, 513, 514, 516, 517, 518, 519, 520, 521, 522, 523, 527, 529, 538, 540, 541, 542, 543, 546, 547, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 606, 621, 659, 또는 676의 중쇄 가변 도메인으로서,
제1 항원 결합 도메인은 다음을 포함하지 않는 경쇄 가변 도메인 및/또는 중쇄 가변 도메인: (i) 서열번호 503의 중쇄 가변 도메인 및 서열번호 502의 중쇄 가변 도메인; 또는 (ii) 서열번호 503의 경쇄 가변 도메인 및 서열번호 511, 513, 514, 516~523, 527, 529, 538, 540~543, 546, 547, 578~597, 606, 621, 659, 및 676 중 하나가 아닌 중쇄 가변 도메인; 또는 (iii) 서열번호 502의 중쇄 가변 도메인 및 서열번호 550, 554, 556~560, 562, 565, 569, 570~576, 697~713, 및 732 중 하나가 아닌 경쇄 가변 도메인.
본원에 기술된 약학적 조성물 중 어느 하나의 일부 구현예에서, 조성물은: 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리를 증가시킬 수 있고/있거나; 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 ?? 표적 포유류 세포 살해를 증가시킬 수 있다.
본원에 기술된 약학적 조성물 중 어느 하나의 일부 구현예에서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달을 증가시킬 수 있다.
본원에 기술된 약학적 조성물 중 어느 하나의 일부 구현예에서, 조성물은: 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포의 표면 상에 제시된 MET의 수준이 덜 감소되게 하거나; 표적 포유류 세포의 표면 상에 제시된 MET의 수준이 검출 가능한 수준으로 감소되지 않도록 한다.
본원에 기술된 약학적 조성물 중 어느 하나의 일부 구현예에서, 표적 포유류 세포는 암 세포이다.
본원에 기술된 약학적 조성물 중 어느 하나의 일부 구현예에서, ABPC는 표적 포유류 세포에 대해 세포독성(cytotoxic)이거나 세포증식 억제성(cytostatic)이다. 본원에 기술된 약학적 조성물 중 어느 하나의 일부 구현예에서, ABPC는 비인간 영장류 MET 및 인간 MET와 교차 반응하거나; 비인간 영장류 MET, 인간 MET, 및 랫트 MET와 마우스 MET 중 하나 또는 둘 다와 교차 반응한다.
본원에 기술된 약학적 조성물 중 어느 하나의 일부 구현예에서, ABPC는 단일 폴리펩티드를 포함한다. 본원에 기술된 약학적 조성물 중 어느 하나의 일부 구현예에서, 항원 결합 도메인은 VH 도메인, VHH 도메인, VNAR 도메인, 및 scFv로 이루어진 군으로부터 선택된다. 본원에 기술된 약학적 조성물 중 어느 하나의 일부 구현예에서, ABPC는 2개 이상의 폴리펩티드를 포함한다. 본원에 기술된 약학적 조성물 중 어느 하나의 일부 구현예에서, ABPC는 항체이다.
본원에 기술된 약학적 조성물 중 어느 하나의 일부 구현예에서, ABPC의 생체 내 반감기는 대조군 ABPC의 생체 내 반감기와 비교했을 때 감소된다.
본원에 기술된 약학적 조성물 중 어느 하나의 일부 구현예에서, ABPC는 제2 항원 결합 도메인을 포함한다.
표적 포유류 세포의 표면에 제시된 MET 또는 MET의 에피토프에 특이적으로 결합할 수 있는 제1 항원 결합 도메인을 포함하는 항원 결합 단백질 작제물(ABPC)이 본원에 제공되며, 여기서 (a) 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인 해리 속도는 약 7.0 내지 약 8.0의 pH에서의 해리 속도보다 더 빠르거나; (b) 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인의 해리 상수(KD)는 약 7.0 내지 약 8.0의 pH에서의 KD보다 더 크다.
본원에 기술된 ABPC 중 어느 하나의 일부 구현예에서, ABPC는 표적 포유류 세포에 의해 내재화된 후 표적 포유류 세포 내에서 분해된다.
본원에 기술된 ABPC 중 어느 하나의 일부 구현예에서, ABPC는 접합된 독소, 방사성 동위원소, 약물, 또는 소분자를 포함한다.
또한, 다음을 포함하는 항원 결합 단백질 작제물(ABPC)이 본원에 제공되며: 표적 포유류 세포의 표면 상에 제시된 MET 또는 MET의 에피토프에 특이적으로 결합할 수 있는 제1 항원 결합 도메인; 및 접합된 독소, 방사성 동위원소, 약물, 또는 소분자, 여기서: (a) 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인의 해리 속도는 약 7.0 내지 약 8.0의 pH에서의 해리 속도보다 빠르거나; 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인의 해리 상수(KD)는 약 7.0 내지 약 8.0의 pH에서의 KD보다 더 크며; (b) 조성물은 다음 중 하나 이상을 가능하게 한다: 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때, 표적 포유류 세포에서 독소 유리의 증가; 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때, 표적 포유류 세포 사멸의 증가; 및 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때, 표적 포유류 세포에서의 엔도리소좀 전달의 증가.
본원에 기술된 ABPC 중 어느 하나의 일부 구현예에서, 제1 항원 결합 도메인은 (a) 내지 (d) 중 하나를 포함한다: (a) 하나 이상의 아미노산이 히스티딘으로 치환된 텔리소투주맙(Telisotuzumab)의 중쇄 가변 도메인으로서, 서열번호 1을 포함하는 텔리소투주맙의 중쇄 가변 도메인; 및/또는 하나 이상의 아미노산이 히스티딘으로 치환된 텔리소투주맙의 경쇄 가변 도메인으로서, 서열번호 2를 포함하는 텔리소투주맙의 경쇄 가변 도메인; (b) 하나 이상의 아미노산이 히스티딘으로 치환된 에미베투주맙(Emibetuzumab)의 중쇄 가변 도메인으로서, 서열번호 146을 포함하는 에미베투주맙의 중쇄 가변 도메인; 및/또는 하나 이상의 아미노산이 히스티딘으로 치환된 에미베투주맙의 경쇄 가변 도메인으로서, 서열번호 147을 포함하는 에미베투주맙의 경쇄 가변 도메인; (c) 하나 이상의 아미노산이 히스티딘으로 hucMET27Gv1.3의 중쇄 가변 도메인으로서, 서열번호 304를 포함하는 hucMET27Gv1.3의 중쇄 가변 도메인; 및/또는 하나 이상의 아미노산이 히스티딘으로 치환된 hucMET27Gv1.3의 경쇄 가변 도메인으로서, 서열번호 305를 포함하는 hucMET27Gv1.3의 경쇄 가변 도메인; 및 (d) 하나 이상의 아미노산이 히스티딘으로 치환된 P3D12의 중쇄 가변 도메인으로서, 서열번호 502를 포함하는 P3D12의 중쇄 가변 도메인; 및/또는 하나 이상의 아미노산이 히스티딘으로 치환된 P3D12의 경쇄 가변 도메인으로서, 서열번호 503을 포함하는 P3D12의 경쇄 가변 도메인.
본원에 기술된 ABPC 중 어느 하나의 일부 구현예에서, 제1 MET-결합 도메인은 (a) 내지 (d) 중 하나를 포함한다: (a) 서열번호 3~5의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인으로서, 종합적으로 서열번호 3~5 내 총 하나 이상의 아미노산 위치가 히스티딘으로 치환된, 중쇄 가변 도메인; 및/또는 서열번호 6~8의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인으로서, 종합적으로 서열번호 6~8 내 총 하나 이상의 아미노산 위치가 히스티딘으로 치환된, 경쇄 가변 도메인; (b) 서열번호 148~150의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인으로서, 종합적으로 서열번호 148~150 내 총 하나 이상의 아미노산 위치가 히스티딘으로 치환된, 중쇄 가변 도메인; 및/또는 서열번호 151~153의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인으로서, 종합적으로 서열번호 151~153 내 총 하나 이상의 아미노산 위치가 히스티딘으로 치환된, 경쇄 가변 도메인; (c) 서열번호 306~308의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인으로서, 종합적으로 서열번호 306~308 내 총 하나 이상의 아미노산 위치가 히스티딘으로 치환된, 중쇄 가변 도메인; 및/또는 서열번호 309~311의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인으로서, 종합적으로 서열번호 309~311 내 총 하나 이상의 아미노산 위치가 히스티딘으로 치환된, 경쇄 가변 도메인; 및 (d) 서열번호 504~506의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인으로서, 종합적으로 서열번호 504~506 내 총 하나 이상의 아미노산 위치가 히스티딘으로 치환된, 중쇄 가변 도메인; 및/또는 서열번호 507~509의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인으로서, 종합적으로 서열번호 507~509 내 총 하나 이상의 아미노산 위치가 히스티딘으로 치환된, 경쇄 가변 도메인.
본원에 기술된 ABPC 중 어느 하나의 일부 구현예에서, 제1 항원 결합 도메인은 (a) 내지 (d) 중 하나를 포함한다: (a) 서열번호 1과 적어도 90% 동일한 중쇄 가변 도메인으로서, 26, 27, 28, 29, 32, 97, 98, 99, 100, 101, 102, 103, 및 107로 이루어진 군으로부터 선택된 서열번호 1의 하나 이상의 위치에서 히스티딘을 포함하는, 중쇄 가변 도메인; 및/또는 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 25, 28, 29, 30, 31, 32, 34, 35, 36, 37, 54, 55, 59, 60, 95, 99, 및 101로 이루어진 군으로부터 선택된 서열번호 2의 하나 이상의 위치에서 히스티딘을 포함하는, 경쇄 가변 도메인; (b) 서열번호 146과 적어도 90% 동일한 중쇄 가변 도메인으로서, 31, 50, 51, 52, 53, 54, 56, 57, 59, 98, 99, 100, 및 103으로부터 이루어진 군으로부터 선택된 서열번호 146의 하나 이상의 위치에서 히스티딘을 포함하는, 중쇄 가변 도메인; 및/또는 서열번호 147과 적어도 90% 동일한 경쇄 가변 도메인으로서, 25, 26, 29, 32, 33, 51, 91, 92, 95, 96, 및 97로 이루어진 군으로부터 선택된 서열번호 147의 하나 이상의 위치에서 히스티딘을 포함하는, 경쇄 가변 도메인; (c) 서열번호 304와 적어도 90% 동일한 중쇄 가변 도메인으로서, 27, 34, 35, 50, 51, 52, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 98, 99, 103, 및 105로 이루어진 군으로부터 선택된 서열번호 304의 하나 이상의 위치에서 히스티딘을 포함하는, 중쇄 가변 도메인; 및/또는 서열번호 305와 적어도 90% 동일한 경쇄 가변 도메인으로서, 26, 30, 31, 34, 36, 54, 56, 57, 60, 93, 95, 99, 및 101로 이루어진 군으로부터 선택된 서열번호 305의 하나 이상의 위치에서 히스티딘을 포함하는, 경쇄 가변 도메인; 및 (d) 서열번호 502와 적어도 90% 동일한 중쇄 가변 도메인으로서, 27, 29, 30, 32, 33, 34, 50, 51, 52, 53, 57, 59, 98, 100, 101, 102, 103, 106, 및 107로 이루어진 군으로부터 선택된 서열번호 502의 하나 이상의 위치에서 히스티딘을 포함하는, 중쇄 가변 도메인; 및/또는 서열번호 503과 적어도 90% 동일한 경쇄 가변 도메인으로서, 25, 29, 31, 32, 33, 34, 35, 52, 55, 91, 92, 93, 94, 95, 96. 97, 및 98로 이루어진 군으로부터 선택된 서열번호 503의 하나 이상의 위치에서 히스티딘을 포함하는, 경쇄 가변 도메인.
본원에 기술된 ABPC 중 어느 하나의 일부 구현예에서, 제1 항원 결합 도메인은 (a) 내지 (d) 중 하나를 포함한다: (a) 서열번호 2, 52, 55, 56, 57, 58, 59, 61, 62, 63, 64, 65, 66, 67, 71, 72, 75, 79, 81, 131, 132, 133, 134, 135, 136, 137, 138, 139, 또는 140의 경쇄 가변 도메인 및/또는 서열번호 1, 13, 14, 15, 16, 19, 40, 41, 42, 43, 44, 45, 46, 50, 82, 83, 84, 86, 87, 89, 90, 94, 또는 111의 중쇄 가변 도메인으로서, 제1 항원 결합 도메인은 (i) 서열번호 2의 중쇄 가변 도메인 및 서열번호 1의 경쇄 가변 도메인; (ii) 서열번호 2의 경쇄 가변 도메인 및 서열번호 13~16, 19, 40~46, 50, 82~84, 86, 87, 89, 90, 94, 및 111 중 하나가 아닌 중쇄 가변 도메인; 또는 (iii) 서열번호 1의 중쇄 가변 도메인 및 서열번호 52, 55~59, 61~67, 71, 72, 75, 79, 81, 및 131~140 중 하나가 아닌 경쇄 가변 도메인을 포함하지 않는, 중쇄 가변 도메인 및/또는 경쇄 가변 도메인; (b) 서열번호 147, 190, 191, 194, 197, 198, 200, 201, 209, 210, 213, 214, 215, 284, 285, 286, 287, 288, 289, 290, 291, 292, 293, 294, 295, 296, 297, 298, 300, 또는 301의 경쇄 가변 도메인, 및/또는 서열번호 146, 159, 164, 165, 166, 167, 168, 170, 171, 173, 182, 183, 184, 187, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 230, 231, 232, 233, 234, 235, 또는 236의 중쇄 가변 도메인으로서, 제1 항원 결합 도메인은 (i) 서열번호 147의 경쇄 가변 도메인 및 서열번호 146의 중쇄 가변 도메인; (ii) 서열번호 147의 경쇄 가변 도메인 및 서열번호 159, 164~168, 170, 171, 173, 182~184, 187, 217~228, 및 230~236 중 하나가 아닌 중쇄 가변 도메인; 또는 (iii) 서열번호 146의 중쇄 가변 도메인 및 서열번호 190, 191, 194, 197, 198, 200, 201, 209, 210, 213~215, 284~298, 300, 및 301 중 하나가 아닌 경쇄 가변 도메인을 포함하지 않는, 경쇄 가변 도메인 및/또는 중쇄 가변 도메인; (c) 서열번호 305, 352, 356, 357, 360, 362, 364, 365, 367, 368, 371, 372, 374, 378, 380, 428, 429, 430, 431, 432, 433, 434, 435, 436, 437, 438, 439, 440, 441, 442, 443, 444, 445, 446, 450, 451, 453, 457, 462, 463, 465, 470, 472, 473, 474, 476, 479, 482, 483, 485, 490, 492, 494, 496, 또는 499의 경쇄 가변 도메인, 및/또는 서열번호 304, 313, 320, 321, 322, 323, 324, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 340, 341, 345, 347, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 392, 393, 395, 396, 397, 398, 399, 또는 400의 중쇄 가변 도메인으로서, 제1 항원 결합 도메인은 (i) 서열번호 305의 경쇄 가변 도메인 및 서열번호 304의 중쇄 가변 도메인; (ii) 서열번호 305의 경쇄 가변 도메인 및 서열번호 313, 320~324, 326~337, 340, 341, 345, 347, 381~390, 392, 393, 및 395~400 중 하나가 아닌 중쇄 가변 도메인; 또는 (iii) 서열번호 304의 중쇄 가변 도메인 및 서열번호 352, 356, 357, 360, 362, 364, 365, 367, 368, 371, 372, 374, 378, 380, 428~446, 450, 451, 453, 457, 462, 463, 465, 470, 472~474, 476, 479, 482, 483, 485, 490, 492, 494, 496, 및 499 중 하나가 아닌 경쇄 가변 도메인을 포함하지 않는, 경쇄 가변 도메인 및/또는 중쇄 가변 도메인; 및 (d) 서열번호 503, 550, 554, 556, 557, 558, 559, 560, 562, 565, 569, 570, 571, 572, 573, 574, 575, 576, 697, 698, 699, 700, 701, 702, 703, 704, 705, 706, 707, 708, 709, 710, 711, 712, 713, 또는 732의 경쇄 가변 도메인 및/또는 서열번호 502, 511, 513, 514, 516, 517, 518, 519, 520, 521, 522, 523, 527, 529, 538, 540, 541, 542, 543, 546, 547, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 606, 621, 659, 또는 676의 중쇄 가변 도메인으로서, 제1 항원 결합 도메인은 (i) 서열번호 503의 경쇄 가변 도메인 및 서열번호 502의 중쇄 가변 도메인; 또는 (ii) 서열번호 503의 경쇄 가변 도메인 503 및 서열번호 511, 513, 514, 516~523, 527, 529, 538, 540~543, 546, 547, 578~597, 606, 621, 659, 또는 676이 아닌 중쇄 가변 도메인; 또는 (iii) 서열번호 502의 중쇄 가변 도메인 및 서열번호 550, 554, 556~560, 562, 565, 569, 570~576, 697~713, 및 732 중 하나가 아닌 중쇄 가변 도메인을 포함하지 않는, 경쇄 가변 도메인 및/또는 중쇄 가변 도메인.
본원에 기술된 ABPC 중 어느 하나의 일부 구현예에서, ABPC를 포함하는 조성물은: 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리를 증가시키고/시키거나; 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포 사멸을 증가시킨다.
본원에 기술된 ABPC 중 어느 하나의 일부 구현예에서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달을 증가시킨다.
본원에 기술된 ABPC 중 어느 하나의 일부 구현예에서, ABPC를 포함하는 조성물은: 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포의 표면 상에 제시된 MET의 수준이 덜 감소되게 하거나; 표적 포유류 세포의 표면 상에 제시된 MET의 수준이 검출 가능한 수준으로 감소되지 않도록 한다.
본원에 기술된 ABPC 중 어느 하나의 일부 구현예에서, 표적 포유류 세포는 암 세포이다. 본원에 기술된 ABPC 중 어느 하나의 일부 구현예에서, ABPC는 표적 포유류 세포에 대해 세포독성이거나 세포증식 억제성이다. 본원에 기술된 ABPC 중 어느 하나의 일부 구현예에서, ABPC는 비인간 영장류 MET 및 인간 MET와 교차 반응하거나; 비인간 영장류 MET, 인간 MET, 및 랫트 MET와 마우스 MET 중 하나 또는 둘 다와 교차 반응한다.
본원에 기술된 ABPC 중 어느 하나의 일부 구현예에서, ABPC는 단일 폴리펩티드를 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 구현예에서, 항원 결합 도메인은 VH 도메인, VHH 도메인, VNAR 도메인, 및 scFv로 이루어진 군으로부터 선택된다. 본원에 기술된 ABPC 중 어느 하나의 일부 구현예에서, ABPC는 둘 이상의 폴리펩티드를 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 구현예에서, ABPC는 항체이다.
본원에 기술된 ABPC 중 어느 하나의 일부 구현예에서, ABPC의 생체 내 반감기는 대조군 ABPC의 생체 내 반감기와 비교했을 때 감소된다.
본원에 기술된 ABPC 중 어느 하나의 일부 구현예에서, ABPC는 제2 항원 결합 도메인을 포함한다.
또한, 본원에 기술된 약학적 조성물 중 어느 하나의 약학적 조성물 또는 본원에 기술된 ABPC 중 어느 하나의 적어도 1회 투여량을 포함하는 키트가 본원에 제공된다.
또한, 암을 치료하는 방법이 본원에 제공되며, 여기서 암은 MET 또는 MET의 에피토프가 표면에 제시된 암 세포의 집단을 갖는 것을 특징으로 하고, 상기 방법은 상기 암 세포의 집단을 갖는 것을 특징으로 하는 암에 걸린 것으로 식별된 대상체에게 본원에 기술된 약학적 조성물 중 어느 하나 또는 본원에 기술된 ABPC 중 어느 하나의 치료적 유효량을 투여하는 단계를 포함한다.
또한, 대상체에서 종양의 부피를 감소시키는 방법이 본원에 제공되며, 여기서 종양은 MET 또는 MET의 에피토프가 표면에 제시된 암 세포의 집단을 갖는 것을 특징으로 하고, 상기 방법은 상기 암 세포의 집단을 갖는 것을 특징으로 하는 암에 걸린 것으로 식별된 대상체에게 본원에 기술된 약학적 조성물 중 어느 하나 또는 본원에 기술된 ABPC 중 어느 하나의 치료적 유효량을 투여하는 단계를 포함한다.
또한, 대상체의 암 세포에서 세포 사멸을 유도하는 방법이 본원에 제공되며, 여기서 암 세포는 그 표면에 MET 또는 MET의 에피토프를 갖고, 상기 방법은 상기 암 세포의 집단을 갖는 것을 특징으로 하는 암에 걸린 것으로 식별된 대상체에게 본원에 기술된 약학적 조성물 중 어느 하나 또는 본원에 기술된 ABPC 중 어느 하나의 치료적 유효량을 투여하는 단계를 포함한다.
또한, 암에 걸린 대상체에서 전이가 발생할 위험을 감소시키는 방법 또는 추가의 전이가 발생할 위험을 감소시키는 방법이 본원에 제공되며, 여기서 암은 MET 또는 MET의 에피토프가 표면에 제시된 암 세포의 집단을 갖는 것을 특징으로 하고, 상기 방법은 상기 암 세포의 집단을 갖는 것을 특징으로 하는 암에 걸린 것으로 식별된 대상체에게 본원에 기술된 약학적 조성물 중 어느 하나 또는 본원에 기술된 ABPC 중 어느 하나의 치료적 유효량을 투여하는 단계를 포함한다.
본원에서 사용되는 바와 같이, 용어 "항원 결합 단백질 작제물"은 (i) 적어도 하나의 항원 결합 도메인을 포함하는 단일 폴리펩티드 또는 (ii) 함께 적어도 하나의 항원 결합 도메인을 형성하는 둘 이상의 폴리펩티드(예를 들어 동일하거나 상이한 폴리펩티드)의 복합체이다. 항원 결합 단백질 작제물의 비제한적인 실시예 및 양태가 본원에 기술된다. 항원 결합 단백질 작제물의 추가의 실시예 및 양태는 당업계에 공지되어 있다.
"다중특이적 항원 결합 단백질 작제물"은 전체적으로 둘 이상의 상이한 에피토프에 특이적으로 결합하는 둘 이상의 상이한 항원 결합 도메인을 포함하는 항원 결합 단백질 작제물이다. 2개 이상의 상이한 에피토프는 동일한 항원 상의 에피토프(예를 들어 세포의 표면에 존재하는 단일 폴리펩티드) 또는 상이한 항원 상의 에피토프(예를 들어 동일한 세포의 표면에 존재하거나 상이한 세포의 표면에 존재하는 상이한 단백질)일 수 있다. 일부 양태에서, 항원은 세포의 표면에 존재한다. 일부 양태에서, 다중특이적 항원 결합 단백질 작제물은 2개의 상이한 에피토프에 결합한다(즉, "이중특이적 항원 결합 단백질 작제물"). 일부 양태에서, 다중특이적 항원 결합 단백질 작제물은 3개의 상이한 에피토프에 결합한다(즉, "삼중특이적 항원 결합 단백질 작제물"). 일부 양태에서, 다중특이적 항원 결합 단백질 작제물은 4개의 상이한 에피토프에 결합한다(즉, "사중특이적 항원 결합 단백질 작제물"). 일부 양태에서, 다중특이적 항원 결합 단백질 작제물은 5개의 상이한 에피토프에 결합한다(즉, "오중특이적 항원 결합 단백질 작제물"). 각각의 결합 특이성은 임의의 적절한 원자가로 존재할 수 있다. 다중특이적 항원 결합 단백질 작제물의 비제한적인 실시예가 본원에 기술된다.
"항원 결합 도메인"은 하나 이상의 상이한 항원(들)에 특이적으로 결합할 수 있는 하나 이상의 단백질 도메인(들) (예를 들어 단일 폴리펩티드 유래의 아미노산으로부터 형성되거나 둘 이상의 폴리펩티드(예를 들어 동일하거나 상이한 폴리펩티드) 유래의 아미노산으로부터 형성된 단백질 도메인(들))이다. 일부 실시예에서, 항원 결합 도메인은 자연 발생 항체의 특이성 및 친화도와 유사한 특이성 및 친화도로 항원 또는 에피토프에 결합할 수 있다. 일부 구현예에서, 항원 결합 도메인은 항체 또는 이의 단편일 수 있다. 일부 구현예에서, 항원 결합 도메인은 대안적인 스캐폴드를 포함할 수 있다. 항원 결합 도메인의 비제한적인 실시예가 본원에 기술된다. 항원 결합 도메인의 추가 실시예는 당업계에 공지되어 있다. 일부 실시예에서, 항원 결합 도메인은 단일 항원에 결합할 수 있다.
용어 "항체"는 가장 넓은 의미로 본원에서 사용되고, 항원 또는 에피토프에 특이적으로 결합하는 하나 이상의 항원 결합 도메인을 포함하는 특정 유형의 면역글로불린 분자를 포함한다. 항체는, 예를 들어 온전한 항체(예를 들어 온전한 면역글로불린, 예를 들어 인간 IgG(예를 들어 인간 IgG1, 인간 IgG2, 인간 IgG3, 인간 IgG4)), 항체 단편, 및 다중특이적 항체를 구체적으로 포함한다. 항원 결합 도메인의 일 실시예는 VH-VL 이량체에 의해 형성된 항원 결합 도메인이다. 항체의 추가 실시예가 본원에 기술된다. 항체의 추가 실시예는 당업계에 공지되어 있다.
"엔도솜/리소좀 경로"라는 문구는 포유류 세포의 세포질 내 엔도솜(초기 엔도솜, 다중-소포체, 후기 엔도솜, 및 리소좀)의 네트워크로서, 세포-매개 내재화 공정, 예를 들어, 음세포 작용(pinocytosis), 미소 음세포 작용(micropinocytosis), 수용체-매개 내포 작용(endocytosis), 및/또는 식균작용(phagocytosis)을 통해 내재화된 분자가 분류되는 네트워크를 지칭한다.
일단 엔도솜/리소좀 경로 내의 엔도솜이 정제되거나 단리되면, 당업계에 공지된 방법(ELISA, 웨스턴 블롯, 면역형광, 및 면역침강에 이어지는 단백질 농도에 대한 검정)을 사용하여 표적 단백질(예를 들어, 본원에 기술된 항원 결합 단백질 작제물)에 대한 검정을 수행할 수 있고, 이를 사용하여 엔도솜에서 표적 단백질의 농도 또는 상대 수준을 결정할 수 있다. 대안적으로, 엔도솜/리소좀 경로 내의 엔도솜은 엔도솜(예를 들어 조기 엔도솜의 경우 EEA1)에 존재하는 특징적인 단백질에 특이적으로 결합하는 검출 가능하게 표지된 항체(예를 들어 형광단-표지된, 염료-표지된, 또는 GFP-표지된 항체, 예를 들어 CellLight?? 조기 엔도솜-GFP) 및 관심 단백질(예를 들어 항원 결합 단백질 작제물)에 특이적으로 결합하는 형광단 표지된 항체를 사용해 면역역광 현미경으로 영상화할 수 있고, 엔도솜 내의 표적 단백질 수준은 2개의 상이한 항체의 형광 방출의 중첩을 정량화하여 결정할 수 있다.
"엔도리소좀 전달"이란 말은 포유류 세포(예를 들어 본원에 기술된 예시적인 표적 포유류 세포)의 엔도솜/리소좀 경로에 항원 결합 단백질 작제물(예를 들어 본원에 기술된 항원 결합 단백질 작제물 중 어느 하나)이 시간 경과에 따른 축적되는 속도 또는 특정 시점에 축적된 것 전체를 지칭한다.
세포 형광 데이터를 기준으로, 상응하는 출발 ABPC와 비교했을 때, pH 조작된 ABPC 변이체의 엔도리소좀 전달의 증가를 계산하는 예시적인 방법은, 변이체의 평균 형광 강도에서 비결합 IgG 대조군의 평균 형광 강도를 뺀 값을 계산하고, 이를 변이체의 상응하는 출발 ABPC의 평균 형광 강도에서 IgG 대조군의 평균 형광 강도를 뺀 값으로 나눈 비율을 측정하는 것이다.
본원에 기술된 ABPC 중 어느 하나의 엔도리소좀 전달을 측정하기 위한 예시적인 검정에는, 형광 염료로 ABPC를 표지하고, 이어서 표지된 ABPC를 세포와 함께 인큐베이션하고, (예를 들어, Wustner의 문헌[Traffic 7(6):699-715, 2006]에 전반적으로 기술된 것과 같은) ABPC의 엔도리소좀 전달의 표시자로서 세포 형광을 측정하는 것을 포함하는 검정들이 있다. 대안적으로, 산성 pH에서 우선적으로 형광을 나타내지만 중성 pH에서는 형광을 나타내지 않는 pH-민감성 염료를 사용해 본원에 기술된 ABPC 중 어느 하나를 표지한 다음, 이를 세포와 함께 인큐베이션하고, ABPC가 산성 엔도리소좀 구획 내로 전달되는 것의 표시자로서 세포 형광을 측정할 수 있다.
명사 앞에 사용될 때 용어 "집단(population)"은 둘 이상의 특정 명사를 의미한다. 예를 들어, "암 세포 집단"이라는 문구는 "2개 이상의 암 세포"를 의미한다. 암 세포의 비제한적인 예가 본원에 기술된다.
"세포에 대해 세포증식 억제성(cytostatic to a cell)"이란 말은 생체 내 또는 시험관 내에서 세포(예를 들어 암 세포)의 증식(세포 분열)의 직접적 또는 간접적으로 감소시키는 것을 지칭한다. 제제가 세포에 대해 세포증식 억제성일 때, 제제는, 예를 들어 세포(예를 들어, 암 세포)의 세포주기를 직접적 또는 간접적으로 정지시킬 수 있다. 일부 실시예에서, 세포에 대해 세포증식 억제성인 제제는 (제제와 접촉하기 전의 S기(S phase) 세포 집단의 세포 수와 비교했을 때) S기 세포 집단의 세포 수를 감소시킬 수 있다. 일부 실시예에서, 세포에 대해 세포증식 억제성인 제제는 (예를 들어, 제제와 접촉하기 전의 S기 세포 집단의 세포 백분율과 비교했을 때) S기 세포의 백분율을 적어도 20%, 적어도 40%, 적어도 60%, 또는 적어도 80%만큼 감소시킬 수 있다.
"세포에 대해 세포독성"이란 말은 세포(예를 들어 포유류 세포, 예를 들어 암 세포)의 사멸(예를 들어 괴사 또는 세포자멸사)을 직접 또는 간접적으로 유도하는 것을 지칭한다.
"친화도"는 항원-결합 부위와 이의 결합 파트너(예: 항원 또는 에피토프) 간의 비공유 상호작용의 합계의 강도를 지칭한다. 달리 명시되지 않는 한, 본원에서 사용되는 바와 같이, "친화도"는 항원-결합 도메인의 구성원과 항원 또는 에피토프 간의 1:1 상호작용을 반영하는 고유한 결합 친화도를 지칭한다. 파트너 Y에 대한 분자 X의 친화도는 해리 평형 상수(KD)로 나타낼 수 있다. 친화도는 본원에 기술된 것을 포함하여 당업계에 공지된 일반적인 방법에 의해 측정될 수 있다. 친화도는, 예를 들어, 표면 플라스몬 공명(SPR) 기술(예: BIACORE®) 또는 바이오층 간섭계(예: FORTEBIO®)를 사용해 결정할 수 있다. 항원 결합 도메인 및 이에 상응하는 항원 또는 에피토프에 대한 친화도를 결정하기 위한 추가의 방법이 당업계에 공지되어 있다.
용어 "에피토프"는 (i) 항원에 특이적으로 결합하는 항원 결합 도메인의 일부분 상의 모든 단량체(예를 들어 개별 아미노산 잔기, 당 측쇄, 및 번역 후 변형된 아미노산 잔기) 및 (ii) 항원 결합 도메인이 특이적으로 결합하는 항원의 일부분 상의 모든 단량체(예를 들어 개별 아미노산 잔기, 당 측쇄, 번역 후 변형된 아미노산 잔기) 간의 일단의 물리적 상호작용을 통해 항원 결합 도메인이 특이적으로 결합하는 항원의 일부분을 의미한다. 에피토프는, 예를 들어 표면에 접근할 수 있는 아미노산 잔기, 당 측쇄, 인산화된 아미노산 잔기, 메틸화된 아미노산 잔기, 및/또는 아세틸화된 아미노산 잔기로 구성될 수 있고, 특이적 3차원 구조적 특성뿐만 아니라 특이적 전하 특성도 가질 수 있다. 입체구조 및 비-입체구조 에피토프는, 변성 용매가 있을 때 입체구조 에피토프에 대한 결합이 손실될 수 있지만 비-입체구조 에피토프에 대한 결합은 그렇지 않다는 점에서 구별된다. 일부 구현예에서, 에피토프는 적어도 약 3 내지 6개 아미노산, 또는 약 10 내지 15개 아미노산의 선형 아미노산 서열에 의해 정의된다. 일부 구현예에서, 에피토프는 전장 단백질의 일부분 또는 3차원 구조(예: 단백질 접힘)에 의해 정의되는 이의 일부분을 지칭한다. 일부 구현예에서, 에피토프는 단백질 접힘을 통해 합쳐지는 불연속 아미노산 서열에 의해 정의된다. 일부 구현예에서, 에피토프는 4차 구조(예를 들어 2개의 상이한 폴리펩티드 사슬의 상호 작용에 의해 형성된 틈)에 의해 합쳐지는 불연속 아미노산 서열에 의해 정의된다. 에피토프를 정의하는 잔기 사이의 아미노산 서열은 에피토프의 3차원 구조에 중요하지 않을 수 있다. 입체구조 에피토프는, 선형 에피토프가 생성되도록 항원-결합 단백질 작제물이 항원의 변성된 버전에 결합하는 것을 비교하는 검정을 사용해 결정되고 스크리닝될 수 있다. 에피토프는 결합에 직접 관여하는 아미노산 잔기, 및 결합에 직접 관여하지 않는 다른 아미노산 잔기를 포함할 수 있다.
항원 결합 도메인이 특이적으로 결합하는 에피토프를 식별하기 위한 방법은 당업계에 공지되어 있고, 예를 들어 구조 기반 분석(예를 들어 항원 및/또는 항원-항원 결합 도메인 복합체에 대한 X-선 결정학, NMR, 및/또는 전자 현미경) 및/또는 결합 파트너와의 결합 검정에서 돌연변이체가 측정되는 돌연변이 유발-기반 분석(예를 들어 알라닌 스캐닝 돌연변이 유발, 글리신 스캐닝 돌연변이 유발, 및 상동성 스캐닝 돌연변이유발) 등이며, 이들 다수가 당업계에 공지되어 있다.
용어 "파라토프"는 (i) 항원에 특이적으로 결합하는 항원 결합 도메인의 일부분 상의 모든 단량체(예를 들어 개별 아미노산 잔기, 당 측쇄, 및 번역 후 변형된 아미노산 잔기) 및 (ii) 항원 결합 도메인이 특이적으로 결합하는 항원의 일부분 상의 모든 단량체(예를 들어 개별 아미노산 잔기, 당 측쇄, 번역 후 변형된 아미노산 잔기) 간의 일단의 물리적 상호작용을 통해 항원에 특이적으로 결합하는 항원 결합 도메인의 일부분을 의미한다. 파라토프는, 예를 들어 표면에 접근할 수 있는 아미노산 잔기로 구성될 수 있고, 특정 3차원 구조적 특성뿐만 아니라 특정 전하 특성도 가질 수 있다. 일부 구현예에서, 파라토프는 전장 항원 결합 도메인의 일부분 또는 3차원 구조(예: 단백질 접힘)에 의해 정의되는 이의 일부분을 지칭한다. 일부 구현예에서, 파라토프는 단백질 접힘을 통해 합쳐지는 불연속 아미노산 서열에 의해 정의된다. 일부 구현예에서, 에피토프는 4차 구조(예를 들어 2개의 상이한 폴리펩티드 사슬의 상호 작용에 의해 형성된 틈)에 의해 합쳐지는 불연속 아미노산 서열에 의해 정의된다. 파라토프를 정의하는 잔기 사이의 아미노산 서열은 파라토프의 3차원 구조에 중요하지 않을 수 있다. 파라토프는 결합에 직접 관여하는 아미노산 잔기, 및 결합에 직접 관여하지 않는 다른 아미노산 잔기를 포함할 수 있다.
항원 결합 도메인이 특이적으로 결합하는 파라토프를 식별하기 위한 방법은 당업계에 공지되어 있고, 예를 들어 구조 기반 분석(예를 들어 항원 결합 도메인 및/또는 항원 결합 도메인-항원 복합체에 대한 X-선 결정학, NMR, 및/또는 전자 현미경) 및/또는 결합 파트너와의 결합 검정에서 돌연변이체가 측정되는 돌연변이 유발-기반 분석(예를 들어 알라닌 스캐닝 돌연변이 유발, 글리신 스캐닝 돌연변이 유발, 및 상동성 스캐닝 돌연변이유발) 등이며, 이들 다수가 당업계에 공지되어 있다.
"포유동물 세포의 표면에 존재하는"이란 말은 (1) 항원이 포유류 세포의 원형질막(예를 들어, 막관통 단백질, 표재성 막 단백질, 지질-고정 단백질(예를 들어, GPI-앵커), N-미리스톨화 단백질, 또는 S-팔미토일화 단백질)에 물리적으로 부착되거나 적어도 부분적으로 포매되는 것, 또는 (2) 항원이 동족 수용체에 안정적으로 결합되고, 동족 수용체는 포유류 세포의 원형질막에 물리적으로 부착되는 것(예를 들어, 리간드가 동족 수용체에 결합되고, 동족 수용체는 원형질막에 물리적으로 부착되는 것)을 의미한다. 포유류 세포의 표면에서 항원의 존재를 결정하기 위한 비제한적인 방법은 형광 활성화 세포 분류(FACS), 면역조직화학, 세포 분획 검정, 및 웨스턴 블롯팅을 포함한다.
"대조군 ABPC" 또는 "대조군 항원 결합 단백질 작제물"이란 말은 (i) 포유류 세포(예를 들어 표적 포유류 세포)의 표면에 제시된 MET 또는 MET의 에피토프에 특이적으로 결합할 수 있는 ABPC로서, 다음 중 하나 또는 둘 다에 해당하는 ABPC: (a) 약 4.0 내지 약 6.5의 pH에서 (예를 들어 본원에 기술된 이 범위의 하위 범위 중 어느 하나의 pH에서) 제1 항원 결합 도메인의 해리 속도가 약 7.0 내지 약 8.0의 pH에서의 (예를 들어 본원에 기술된 이 범위의 하위 범위 중 어느 하나의 pH에서의) 해리 속도보다 3배 이하로 (예를 들어 2.8배 이하, 2.6배 이하, 2.5배 이하, 2.4 배 이하, 2.2 배 이하, 2.0 배 이하, 1.8 배 이하, 1.6 배 이하, 1.5 배 이하, 1.4 배 이하, 1.2 배 이하, 1.0 배 이하, 0.8 배 이하, 0.6 배 이하, 0.5 배 이하, 0.4 배 이하, 0.3 배 이하, 0.2 배 이하, 또는 0.1 배 이하로) 더 빠르거나; (b) 약 4.0 내지 약 6.5의 pH에서 (예를 들어 본원에 기술된 이 범위의 하위 범위 중 어느 하나의 pH에서) 제1 항원 결합 도메인의 해리 속도가 해리 상수(KD)가 약 7.0 내지 약 8.0의 pH에서의 (예를 들어 본원에 기술된 이 범위의 하위 범위 중 어느 하나의 pH에서의) 해리 상수보다 3배 이하로 (예를 들어 2.8배 이하, 2.6배 이하, 2.5 배 이하, 2.4 배 이하, 2.2 배 이하, 2.0 배 이하, 1.8 배 이하, 1.6 배 이하, 1.5 배 이하, 1.4 배 이하, 1.2 배 이하, 1.0 배 이하, 0.8 배 이하, 0.6 배 이하, 0.5 배 이하, 0.4 배 이하, 0.3 배 이하, 0.2 배 이하, 또는 0.1 배 이하로) 더 클 것; 및/또는 (ii) 텔리소투주맙(Telisotuzumab); 및/또는 (iii) 에미베투주맙(Emibetuzumab); 및/또는 (iv) hucMET27Gv1.3; 및/또는 (v) P3D12 (Tanabe)를 의미한다.
용어 "세포외 공간"은 포유류 세포의 원혈장막의 외부에 있는 액체를 의미한다. 포유류 세포가 시험관 내에 있는 경우, 세포외 공간은 액체 배양 배지일 수 있다. 포유류 세포가 생체 내에 있는 경우, 세포외 공간은, 예를 들어, 원형질, 혈청, 혈액, 간질액, 또는 림프일 수 있다.
용어 "엔돌리소좀 공간"은 포유류 세포에서 엔도솜/리소좀 경로를 구성하는 소포 및 소기관에 의해 캡슐화된 유체를 의미한다.
"감소된 수준(reduced level 또는 decreased level)"이란 말은 기준 수준 또는 값과 비교했을 때 적어도 1%의 (예를 들어, 적어도 2%, 적어도 4%, 적어도 6%, 적어도 8%, 적어도 10%, 적어도 12%, 적어도 14%, 적어도 16%, 적어도 18%, 적어도 20%, 적어도 22%, 적어도 24%, 적어도 26%, 적어도 30%, 적어도 35%, 적어도 40%, 적어도 45%, 적어도 50%, 적어도 55%, 적어도 60%, 적어도 65%, 적어도 70%, 적어도 75%, 적어도 80%, 적어도 85%, 적어도 90%, 적어도 95%, 또는 적어도 99%의) 감소(reduction 또는 decrease)일 수 있다.
용어 "세포 살해 효능"은 제제(예를 들어 본원에 기술된 ABPC 중 어느 하나)가 포유류 세포(예를 들어 암 세포)의 세포자멸사 및/또는 괴사를 직접 또는 간접적으로 유도하는 능력을 시간 경과에 따른 속도 또는 관련 시점에서의 속도로서 측정한 것을 지칭한다. 세포의 세포 살해 효능을 결정하는 방법은 당업계에 공지되어 있다(예를 들어, 트리판 블루 염색, 현미경, 형광 보조 세포 분류, 및 세포자멸사 마커(예를 들어, 아넥신 V)를 검출하는 검정). 비제한적인 실시예에서, 세포 살해 효능은, 예를 들어 제제의 단일 농도에서의 세포 살해에 의해, 제제의 IC50에 의해(즉, 최대 세포 살해 효능의 절반이 달성되는 제제의 농도), 또는 포유동물 세포에 대한 제제의 해리 상수 KD를 제제의 IC50으로 나눈 비율에 의해 측정될 수 있다. 일부 비제한적인 실시예에서, 본원에 기술된 IC50 및/또는 KD 비율을 (본원에서 정의된 것과 같은) 대조군 ABPC의 비율과 비교하고, 임의로, 대조군 ABPC와 비교했을 때 본원에 기술된 ABPC가 더 높은 세포 살해 효능을 갖는다는 것을 입증한다.
용어 "독소 유리(toxin liberation)"는 포유류 세포(예를 들어 비-암성 포유류 세포 또는 암 세포)가, 독소에 접합된 본원에 기술된 ABPC 중 어느 하나(예를 들어, 본원에 기술된 ABPC 또는 대조군 ABPC 중 어느 하나)를 (예를 들어, 음세포 작용 및/또는 수용체 매개 내포 작용을 통해) 내재화하고, 이어서 ABPC에 접합된 독소를 방출하는 능력을 시간 경과에 따른 속도 또는 특정 시점에서의 속도로서 측정한 것을 지칭한다. 독소 유리는 다양한 상이한 예시적인 검정, 예를 들어 ELISA, 면역형광법, 세포 살해 분석, 세포 주기 중단 검정, DNA 손상 분석, 질량 분광분석, HPLC, 및/또는 동위원소 표지된 독소를 사용해 평가할 수 있다.
"표적 세포" 또는 "표적 포유류 세포" 또는 "포유류 표적 세포"라는 말은 적어도 하나의 MET가 표면에 존재하는 포유류 세포를 의미한다. 일부 예에서, 포유류 표적 세포는 암 세포일 수 있다. 일부 구현예에서, 표적 포유류 세포는 표적 포유류 세포의 원형질 막에 존재하는 총 약 1 내지 약 10,000,000, 약 1 내지 약 9,000,000, 약 1 내지 약 8,000,000, 약 1 내지 약 7,000,000, 약 1 내지 약 6,000,000, 약 1 내지 약 5,000,000, 약 1 내지 약 4,000,000, 약 1 내지 약 3,000,000, 약 1 내지 약 2,000,000, 약 1 내지 약 1,000,000, 약 1 내지 약 800,000, 약 1 내지 약 600,000, 약 1 내지 약 400,000, 약 1 내지 약 200,000, 약 1 내지 약 100,000, 약 1 내지 약 80,000, 약 1 내지 약 80,000, 약 1 내지 약 75,000, 약 1 내지 약 70,000, 약 1 내지 약 65,000, 약 1 내지 약 60,000, 약 1 내지 약 55,000, 약 1 내지 약 50,000, 약 1 내지 약 45,000, 약 1 내지 약 40,000, 약 1 내지 약 35,000, 약 1 내지 약 30,000, 약 1 내지 약 25,000, 약 1 내지 약 20,000, 약 1 내지 약 15,000, 약 1 내지 약 10,000, 약 1 내지 약 7,500, 약 1 내지 약 5,000, 약 1 내지 약 4,000, 약 1 내지 약 3,000, 약 1 내지 약 2,000, 약 1 내지 약 1,000, 약 1 내지 약 500, 약 1 내지 약 100, 약 1 내지 약 50, 약 1 내지 약 10, 약 10 내지 약 10,000,000, 약 10 내지 약 9,000,000, 약 10 내지 약 8,000,000, 약 10 내지 약 7,000,000, 약 10 내지 약 6,000,000, 약 10 내지 약 5,000,000, 약 10 내지 약 4,000,000, 약 10 내지 약 3,000,000, 약 10 내지 약 2,000,000, 약 10 내지 약 1,000,000, 약 10 내지 약 800,000, 약 10 내지 약 600,000, 약 10 내지 약 400,000, 약 10 내지 약 200,000, 약 10 내지 약 100,000, 약 10 내지 약 80,000, 약 10 내지 약 80,000, 약 10 내지 약 75,000, 약 10 내지 약 70,000, 약 10 내지 약 65,000, 약 10 내지 약 60,000, 약 10 내지 약 55,000, 약 10 내지 약 50,000, 약 10 내지 약 45,000, 약 10 내지 약 40,000, 약 10 내지 약 35,000, 약 10 내지 약 30,000, 약 10 내지 약 25,000, 약 10 내지 약 20,000, 약 10 내지 약 15,000, 약 10 내지 약 10,000, 약 10 내지 약 7,500, 약 10 내지 약 5,000, 약 10 내지 약 4,000, 약 10 내지 약 3,000, 약 10 내지 약 2,000, 약 10 내지 약 1,000, 약 10 내지 약 500, 약 10 내지 약 100, 약 10 내지 약 50, 약 50 내지 약 10,000,000, 약 50 내지 약 9,000,000, 약 50 내지 약 8,000,000, 약 50 내지 약 7,000,000, 약 50 내지 약 6,000,000, 약 50 내지 약 5,000,000, 약 50 내지 약 4,000,000, 약 50 내지 약 3,000,000, 약 50 내지 약 2,000,000, 약 50 내지 약 1,000,000, 약 50 내지 약 800,000, 약 50 내지 약 600,000, 약 50 내지 약 400,000, 약 50 내지 약 200,000, 약 50 내지 약 100,000, 약 50 내지 약 80,000, 약 50 내지 약 80,000, 약 50 내지 약 75,000, 약 50 내지 약 70,000, 약 50 내지 약 65,000, 약 50 내지 약 60,000, 약 50 내지 약 55,000, 약 50 내지 약 50,000, 약 50 내지 약 45,000, 약 50 내지 약 40,000, 약 50 내지 약 35,000, 약 50 내지 약 30,000, 약 50 내지 약 25,000, 약 50 내지 약 20,000, 약 50 내지 약 15,000, 약 50 내지 약 10,000, 약 50 내지 약 7,500, 약 50 내지 약 5,000, 약 50 내지 약 4,000, 약 50 내지 약 3,000, 약 50 내지 약 2,000, 약 50 내지 약 1,000, 약 50 내지 약 500, 약 50 내지 약 100, 약 100 내지 약 10,000,000, 약 100 내지 약 9,000,000, 약 100 내지 약 8,000,000, 약 100 내지 약 7,000,000, 약 100 내지 약 6,000,000, 약 100 내지 약 5,000,000, 약 100 내지 약 4,000,000, 약 100 내지 약 3,000,000, 약 100 내지 약 2,000,000, 약 100 내지 약 1,000,000, 약 100 내지 약 800,000, 약 100 내지 약 600,000, 약 100 내지 약 400,000, 약 100 내지 약 200,000, 약 100 내지 약 100,000, 약 100 내지 약 80,000, 약 100 내지 약 75,000, 약 100 내지 약 70,000, 약 100 내지 약 65,000, 약 100 내지 약 60,000, 약 100 내지 약 55,000, 약 100 내지 약 50,000, 약 100 내지 약 45,000, 약 100 내지 약 40,000, 약 100 내지 약 35,000, 약 100 내지 약 30,000, 약 100 내지 약 25,000, 약 100 내지 약 20,000, 약 100 내지 약 15,000, 약 100 내지 약 10,000, 약 100 내지 약 7,500, 약 100 내지 약 5,000, 약 100 내지 약 4,000, 약 100 내지 약 3,000, 약 100 내지 약 2,000, 약 100 내지 약 1,000, 약 100 내지 약 500, 약 500 내지 약 10,000,000, 약 500 내지 약 9,000,000, 약 500 내지 약 8,000,000, 약 500 내지 약 7,000,000, 약 500 내지 약 6,000,000, 약 500 내지 약 5,000,000, 약 500 내지 약 4,000,000, 약 500 내지 약 3,000,000, 약 500 내지 약 2,000,000, 약 500 내지 약 1,000,000, 약 500 내지 약 800,000, 약 500 내지 약 600,000, 약 500 내지 약 400,000, 약 500 내지 약 200,000, 약 500 내지 약 100,000, 약 500 내지 약 80,000, 약 500 내지 약 75,000, 약 500 내지 약 70,000, 약 500 내지 약 65,000, 약 500 내지 약 60,000, 약 500 내지 약 55,000, 약 500 내지 약 50,000, 약 500 내지 약 45,000, 약 500 내지 약 40,000, 약 500 내지 약 35,000, 약 500 내지 약 30,000, 약 500 내지 약 25,000, 약 500 내지 약 20,000, 약 500 내지 약 15,000, 약 500 내지 약 10,000, 약 500 내지 약 7,500, 약 500 내지 약 5,000, 약 500 내지 약 4,000, 약 500 내지 약 3,000, 약 500 내지 약 2,000, 약 500 내지 약 1,000, 약 1,000 내지 약 10,000,000, 약 1,000 내지 약 9,000,000, 약 1,000 내지 약 8,000,000, 약 1,000 내지 약 7,000,000, 약 1,000 내지 약 6,000,000, 약 1,000 내지 약 5,000,000, 약 1,000 내지 약 4,000,000, 약 1,000 내지 약 3,000,000, 약 1,000 내지 약 2,000,000, 약 1,000 내지 약 1,000,000, 약 1,000 내지 약 800,000, 약 1,000 내지 약 600,000, 약 1,000 내지 약 400,000, 약 1,000 내지 약 200,000, 약 1,000 내지 약 100,000, 약 1,000 내지 약 80,000, 약 1,000 내지 약 75,000, 약 1,000 내지 약 70,000, 약 1,000 내지 약 65,000, 약 1,000 내지 약 60,000, 약 1,000 내지 약 55,000, 약 1,000 내지 약 50,000, 약 1,000 내지 약 45,000, 약 1,000 내지 약 40,000, 약 1,000 내지 약 35,000, 약 1,000 내지 약 30,000, 약 1,000 내지 약 25,000, 약 1,000 내지 약 20,000, 약 1,000 내지 약 15,000, 약 1,000 내지 약 10,000, 약 1,000 내지 약 7,500, 약 1,000 내지 약 5,000, 약 1,000 내지 약 4,000, 약 1,000 내지 약 3,000, 약 1,000 내지 약 2,000, 약 2,000 내지 약 10,000,000, 약 2,000 내지 약 9,000,000, 약 2,000 내지 약 8,000,000, 약 2,000 내지 약 7,000,000, 약 2,000 내지 약 6,000,000, 약 2,000 내지 약 5,000,000, 약 2,000 내지 약 4,000,000, 약 2,000 내지 약 3,000,000, 약 2,000 내지 약 2,000,000, 약 2,000 내지 약 1,000,000, 약 2,000 내지 약 800,000, 약 2,000 내지 약 600,000, 약 2,000 내지 약 400,000, 약 2,000 내지 약 200,000, 약 2,000 내지 약 100,000, 약 2,000 내지 약 80,000, 약 2,000 내지 약 75,000, 약 2,000 내지 약 70,000, 약 2,000 내지 약 65,000, 약 2,000 내지 약 60,000, 약 2,000 내지 약 55,000, 약 2,000 내지 약 50,000, 약 2,000 내지 약 45,000, 약 2,000 내지 약 40,000, 약 2,000 내지 약 35,000, 약 2,000 내지 약 30,000, 약 2,000 내지 약 25,000, 약 2,000 내지 약 20,000, 약 2,000 내지 약 15,000, 약 2,000 내지 약 10,000, 약 2,000 내지 약 7,500, 약 2,000 내지 약 5,000, 약 2,000 내지 약 4,000, 약 2,000 내지 약 3,000, 약 3,000 내지 약 10,000,000, 약 3,000 내지 약 9,000,000, 약 3,000 내지 약 8,000,000, 약 3,000 내지 약 7,000,000, 약 3,000 내지 약 6,000,000, 약 3,000 내지 약 5,000,000, 약 3,000 내지 약 4,000,000, 약 3,000 내지 약 3,000,000, 약 3,000 내지 약 2,000,000, 약 3,000 내지 약 1,000,000, 약 3,000 내지 약 800,000, 약 3,000 내지 약 600,000, 약 3,000 내지 약 400,000, 약 3,000 내지 약 200,000, 약 3,000 내지 약 100,000, 약 3,000 내지 약 80,000, 약 3,000 내지 약 75,000, 약 3,000 내지 약 70,000, 약 3,000 내지 약 65,000, 약 3,000 내지 약 60,000, 약 3,000 내지 약 55,000, 약 3,000 내지 약 50,000, 약 3,000 내지 약 45,000, 약 3,000 내지 약 40,000, 약 3,000 내지 약 35,000, 약 3,000 내지 약 30,000, 약 3,000 내지 약 25,000, 약 3,000 내지 약 20,000, 약 3,000 내지 약 15,000, 약 3,000 내지 약 10,000, 약 3,000 내지 약 7,500, 약 3,000 내지 약 5,000, 약 3,000 내지 약 4,000, 약 4,000 내지 약 10,000,000, 약 4,000 내지 약 9,000,000, 약 4,000 내지 약 8,000,000, 약 4,000 내지 약 7,000,000, 약 4,000 내지 약 6,000,000, 약 4,000 내지 약 5,000,000, 약 4,000 내지 약 4,000,000, 약 4,000 내지 약 3,000,000, 약 4,000 내지 약 2,000,000, 약 4,000 내지 약 1,000,000, 약 4,000 내지 약 800,000, 약 4,000 내지 약 600,000, 약 4,000 내지 약 400,000, 약 4,000 내지 약 200,000, 약 4,000 내지 약 100,000, 약 4,000 내지 약 80,000, 약 4,000 내지 약 75,000, 약 4,000 내지 약 70,000, 약 4,000 내지 약 65,000, 약 4,000 내지 약 60,000, 약 4,000 내지 약 55,000, 약 4,000 내지 약 50,000, 약 4,000 내지 약 45,000, 약 4,000 내지 약 40,000, 약 4,000 내지 약 35,000, 약 4,000 내지 약 30,000, 약 4,000 내지 약 25,000, 약 4,000 내지 약 20,000, 약 4,000 내지 약 15,000, 약 4,000 내지 약 10,000, 약 4,000 내지 약 7,500, 약 4,000 내지 약 5,000, 약 5,000 내지 약 10,000,000, 약 5,000 내지 약 9,000,000, 약 5,000 내지 약 8,000,000, 약 5,000 내지 약 7,000,000, 약 5,000 내지 약 6,000,000, 약 5,000 내지 약 5,000,000, 약 5,000 내지 약 4,000,000, 약 5,000 내지 약 3,000,000, 약 5,000 내지 약 2,000,000, 약 5,000 내지 약 1,000,000, 약 5,000 내지 약 800,000, 약 5,000 내지 약 600,000, 약 5,000 내지 약 400,000, 약 5,000 내지 약 200,000, 약 5,000 내지 약 100,000, 약 5,000 내지 약 80,000, 약 5,000 내지 약 75,000, 약 5,000 내지 약 70,000, 약 5,000 내지 약 65,000, 약 5,000 내지 약 60,000, 약 5,000 내지 약 55,000, 약 5,000 내지 약 50,000, 약 5,000 내지 약 45,000, 약 5,000 내지 약 40,000, 약 5,000 내지 약 35,000, 약 5,000 내지 약 30,000, 약 5,000 내지 약 25,000, 약 5,000 내지 약 20,000, 약 5,000 내지 약 15,000, 약 5,000 내지 약 10,000, 약 5,000 내지 약 7,500, 약 7,500 내지 약 10,000,000, 약 7,500 내지 약 9,000,000, 약 7,500 내지 약 8,000,000, 약 7,500 내지 약 7,000,000, 약 7,500 내지 약 6,000,000, 약 7,500 내지 약 5,000,000, 약 7,500 내지 약 4,000,000, 약 7,500 내지 약 3,000,000, 약 7,500 내지 약 2,000,000, 약 7,500 내지 약 1,000,000, 약 7,500 내지 약 800,000, 약 7,500 내지 약 600,000, 약 7,500 내지 약 400,000, 약 7,500 내지 약 200,000, 약 7,500 내지 약 100,000, 약 7,500 내지 약 80,000, 약 7,500 내지 약 75,000, 약 7,500 내지 약 70,000, 약 7,500 내지 약 65,000, 약 7,500 내지 약 60,000, 약 7,500 내지 약 55,000, 약 7,500 내지 약 50,000, 약 7,500 내지 약 45,000, 약 7,500 내지 약 40,000, 약 7,500 내지 약 35,000, 약 7,500 내지 약 30,000, 약 7,500 내지 약 25,000, 약 7,500 내지 약 20,000, 약 7,500 내지 약 15,000, 약 7,500 내지 약 10,000, 약 10,000 내지 약 10,000,000, 약 10,000 내지 약 9,000,000, 약 10,000 내지 약 8,000,000, 약 10,000 내지 약 7,000,000, 약 10,000 내지 약 6,000,000, 약 10,000 내지 약 5,000,000, 약 10,000 내지 약 4,000,000, 약 10,000 내지 약 3,000,000, 약 10,000 내지 약 2,000,000, 약 10,000 내지 약 1,000,000, 약 10,000 내지 약 800,000, 약 10,000 내지 약 600,000, 약 10,000 내지 약 400,000, 약 10,000 내지 약 200,000, 약 10,000 내지 약 100,000, 약 10,000 내지 약 80,000, 약 10,000 내지 약 75,000, 약 10,000 내지 약 70,000, 약 10,000 내지 약 65,000, 약 10,000 내지 약 60,000, 약 10,000 내지 약 55,000, 약 10,000 내지 약 50,000, 약 10,000 내지 약 45,000, 약 10,000 내지 약 40,000, 약 10,000 내지 약 35,000, 약 10,000 내지 약 30,000, 약 10,000 내지 약 25,000, 약 10,000 내지 약 20,000, 약 10,000 내지 약 15,000, 약 15,000 내지 약 10,000,000, 약 15,000 내지 약 9,000,000, 약 15,000 내지 약 8,000,000, 약 15,000 내지 약 7,000,000, 약 15,000 내지 약 6,000,000, 약 15,000 내지 약 5,000,000, 약 15,000 내지 약 4,000,000, 약 15,000 내지 약 3,000,000, 약 15,000 내지 약 2,000,000, 약 15,000 내지 약 1,000,000, 약 15,000 내지 약 800,000, 약 15,000 내지 약 600,000, 약 15,000 내지 약 400,000, 약 15,000 내지 약 200,000, 약 15,000 내지 약 100,000, 약 15,000 내지 약 80,000, 약 15,000 내지 약 75,000, 약 15,000 내지 약 70,000, 약 15,000 내지 약 65,000, 약 15,000 내지 약 60,000, 약 15,000 내지 약 55,000, 약 15,000 내지 약 50,000, 약 15,000 내지 약 45,000, 약 15,000 내지 약 40,000, 약 15,000 내지 약 35,000, 약 15,000 내지 약 30,000, 약 15,000 내지 약 25,000, 약 15,000 내지 약 20,000, 약 20,000 내지 약 10,000,000, 약 20,000 내지 약 9,000,000, 약 20,000 내지 약 8,000,000, 약 20,000 내지 약 7,000,000, 약 20,000 내지 약 6,000,000, 약 20,000 내지 약 5,000,000, 약 20,000 내지 약 4,000,000, 약 20,000 내지 약 3,000,000, 약 20,000 내지 약 2,000,000, 약 20,000 내지 약 1,000,000, 약 20,000 내지 약 800,000, 약 20,000 내지 약 600,000, 약 20,000 내지 약 400,000, 약 20,000 내지 약 200,000, 약 20,000 내지 약 100,000, 약 20,000 내지 약 80,000, 약 20,000 내지 약 75,000, 약 20,000 내지 약 70,000, 약 20,000 내지 약 65,000, 약 210,000 내지 약 60,000, 약 20,000 내지 약 55,000, 약 20,000 내지 약 50,000, 약 20,000 내지 약 45,000, 약 20,000 내지 약 40,000, 약 20,000 내지 약 35,000, 약 20,000 내지 약 30,000, 약 20,000 내지 약 25,000, 약 25,000 내지 약 10,000,000, 약 25,000 내지 약 9,000,000, 약 25,000 내지 약 8,000,000, 약 25,000 내지 약 7,000,000, 약 25,000 내지 약 6,000,000, 약 25,000 내지 약 5,000,000, 약 25,000 내지 약 4,000,000, 약 25,000 내지 약 3,000,000, 약 25,000 내지 약 2,000,000, 약 25,000 내지 약 1,000,000, 약 25,000 내지 약 800,000, 약 25,000 내지 약 600,000, 약 25,000 내지 약 400,000, 약 25,000 내지 약 200,000, 약 25,000 내지 약 100,000, 약 25,000 내지 약 80,000, 약 25,000 내지 약 75,000, 약 25,000 내지 약 70,000, 약 25,000 내지 약 65,000, 약 25,000 내지 약 60,000, 약 25,000 내지 약 55,000, 약 25,000 내지 약 50,000, 약 25,000 내지 약 45,000, 약 25,000 내지 약 40,000, 약 25,000 내지 약 35,000, 약 25,000 내지 약 30,000, 약 30,000 내지 약 10,000,000, 약 30,000 내지 약 9,000,000, 약 30,000 내지 약 8,000,000, 약 30,000 내지 약 7,000,000, 약 30,000 내지 약 6,000,000, 약 30,000 내지 약 5,000,000, 약 30,000 내지 약 4,000,000, 약 30,000 내지 약 3,000,000, 약 30,000 내지 약 2,000,000, 약 30,000 내지 약 1,000,000, 약 30,000 내지 약 800,000, 약 30,000 내지 약 600,000, 약 30,000 내지 약 400,000, 약 30,000 내지 약 200,000, 약 30,000 내지 약 100,000, 약 30,000 내지 약 80,000, 약 30,000 내지 약 75,000, 약 30,000 내지 약 70,000, 약 30,000 내지 약 65,000, 약 30,000 내지 약 60,000, 약 30,000 내지 약 55,000, 약 30,000 내지 약 50,000, 약 30,000 내지 약 45,000, 약 30,000 내지 약 40,000, 약 30,000 내지 약 35,000, 약 35,000 내지 약 10,000,000, 약 35,000 내지 약 9,000,000, 약 35,000 내지 약 8,000,000, 약 35,000 내지 약 7,000,000, 약 35,000 내지 약 6,000,000, 약 35,000 내지 약 5,000,000, 약 35,000 내지 약 4,000,000, 약 35,000 내지 약 3,000,000, 약 35,000 내지 약 2,000,000, 약 35,000 내지 약 1,000,000, 약 35,000 내지 약 800,000, 약 35,000 내지 약 600,000, 약 35,000 내지 약 400,000, 약 35,000 내지 약 200,000, 약 35,000 내지 약 100,000, 약 35,000 내지 약 80,000, 약 35,000 내지 약 75,000, 약 35,000 내지 약 70,000, 약 35,000 내지 약 65,000, 약 35,000 내지 약 60,000, 약 35,000 내지 약 55,000, 약 35,000 내지 약 50,000, 약 35,000 내지 약 45,000, 약 35,000 내지 약 40,000, 약 40,000 내지 약 10,000,000, 약 40,000 내지 약 9,000,000, 약 40,000 내지 약 8,000,000, 약 40,000 내지 약 7,000,000, 약 40,000 내지 약 6,000,000, 약 40,000 내지 약 5,000,000, 약 40,000 내지 약 4,000,000, 약 40,000 내지 약 3,000,000, 약 40,000 내지 약 2,000,000, 약 40,000 내지 약 1,000,000, 약 40,000 내지 약 800,000, 약 40,000 내지 약 600,000, 약 40,000 내지 약 400,000, 약 40,000 내지 약 200,000, 약 40,000 내지 약 100,000, 약 40,000 내지 약 80,000, 약 40,000 내지 약 75,000, 약 40,000 내지 약 70,000, 약 40,000 내지 약 65,000, 약 40,000 내지 약 60,000, 약 40,000 내지 약 55,000, 약 40,000 내지 약 50,000, 약 40,000 내지 약 45,000, 약 45,000 내지 약 10,000,000, 약 45,000 내지 약 9,000,000, 약 45,000 내지 약 8,000,000, 약 45,000 내지 약 7,000,000, 약 45,000 내지 약 6,000,000, 약 45,000 내지 약 5,000,000, 약 45,000 내지 약 4,000,000, 약 45,000 내지 약 3,000,000, 약 45,000 내지 약 2,000,000, 약 45,000 내지 약 1,000,000, 약 45,000 내지 약 800,000, 약 45,000 내지 약 600,000, 약 45,000 내지 약 400,000, 약 45,000 내지 약 200,000, 약 45,000 내지 약 100,000, 약 45,000 내지 약 80,000, 약 45,000 내지 약 75,000, 약 45,000 내지 약 70,000, 약 45,000 내지 약 65,000, 약 45,000 내지 약 60,000, 약 45,000 내지 약 55,000, 약 45,000 내지 약 50,000, 약 50,000 내지 약 10,000,000, 약 50,000 내지 약 9,000,000, 약 50,000 내지 약 8,000,000, 약 50,000 내지 약 7,000,000, 약 50,000 내지 약 6,000,000, 약 50,000 내지 약 5,000,000, 약 50,000 내지 약 4,000,000, 약 50,000 내지 약 3,000,000, 약 50,000 내지 약 2,000,000, 약 50,000 내지 약 1,000,000, 약 50,000 내지 약 800,000, 약 50,000 내지 약 600,000, 약 50,000 내지 약 400,000, 약 50,000 내지 약 200,000, 약 50,000 내지 약 100,000, 약 50,000 내지 약 80,000, 약 50,000 내지 약 75,000, 약 50,000 내지 약 70,000, 약 50,000 내지 약 65,000, 약 50,000 내지 약 60,000, 약 50,000 내지 약 55,000, 약 55,000 내지 약 10,000,000, 약 55,000 내지 약 9,000,000, 약 55,000 내지 약 8,000,000, 약 55,000 내지 약 7,000,000, 약 55,000 내지 약 6,000,000, 약 55,000 내지 약 5,000,000, 약 55,000 내지 약 4,000,000, 약 55,000 내지 약 3,000,000, 약 55,000 내지 약 2,000,000, 약 55,000 내지 약 1,000,000, 약 55,000 내지 약 800,000, 약 55,000 내지 약 600,000, 약 55,000 내지 약 400,000, 약 55,000 내지 약 200,000, 약 55,000 내지 약 100,000, 약 55,000 내지 약 80,000, 약 55,000 내지 약 75,000, 약 55,000 내지 약 70,000, 약 55,000 내지 약 65,000, 약 55,000 내지 약 60,000, 약 60,000 내지 약 10,000,000, 약 60,000 내지 약 9,000,000, 약 60,000 내지 약 8,000,000, 약 60,000 내지 약 7,000,000, 약 60,000 내지 약 6,000,000, 약 60,000 내지 약 5,000,000, 약 60,000 내지 약 4,000,000, 약 60,000 내지 약 3,000,000, 약 60,000 내지 약 2,000,000, 약 60,000 내지 약 1,000,000, 약 60,000 내지 약 800,000, 약 60,000 내지 약 600,000, 약 60,000 내지 약 400,000, 약 60,000 내지 약 200,000, 약 60,000 내지 약 100,000, 약 60,000 내지 약 80,000, 약 60,000 내지 약 75,000, 약 60,000 내지 약 70,000, 약 60,000 내지 약 65,000, 약 65,000 내지 약 10,000,000, 약 65,000 내지 약 9,000,000, 약 65,000 내지 약 8,000,000, 약 65,000 내지 약 7,000,000, 약 65,000 내지 약 6,000,000, 약 65,000 내지 약 5,000,000, 약 65,000 내지 약 4,000,000, 약 65,000 내지 약 3,000,000, 약 65,000 내지 약 2,000,000, 약 65,000 내지 약 1,000,000, 약 65,000 내지 약 800,000, 약 65,000 내지 약 600,000, 약 65,000 내지 약 400,000, 약 65,000 내지 약 200,000, 약 65,000 내지 약 100,000, 약 65,000 내지 약 80,000, 약 65,000 내지 약 75,000, 약 65,000 내지 약 70,000, 약 70,000 내지 약 10,000,000, 약 70,000 내지 약 9,000,000, 약 70,000 내지 약 8,000,000, 약 70,000 내지 약 7,000,000, 약 70,000 내지 약 6,000,000, 약 70,000 내지 약 5,000,000, 약 70,000 내지 약 4,000,000, 약 70,000 내지 약 3,000,000, 약 70,000 내지 약 2,000,000, 약 70,000 내지 약 1,000,000, 약 70,000 내지 약 800,000, 약 70,000 내지 약 600,000, 약 70,000 내지 약 400,000, 약 70,000 내지 약 200,000, 약 70,000 내지 약 100,000, 약 70,000 내지 약 90,000, 약 70,000 내지 약 80,000, 약 80,000 내지 약 10,000,000, 약 80,000 내지 약 9,000,000, 약 80,000 내지 약 8,000,000, 약 80,000 내지 약 7,000,000, 약 80,000 내지 약 6,000,000, 약 80,000 내지 약 5,000,000, 약 80,000 내지 약 4,000,000, 약 80,000 내지 약 3,000,000, 약 80,000 내지 약 2,000,000, 약 80,000 내지 약 1,000,000, 약 80,000 내지 약 800,000, 약 80,000 내지 약 600,000, 약 80,000 내지 약 400,000, 약 80,000 내지 약 200,000, 약 80,000 내지 약 100,000, 약 80,000 내지 약 90,000, 약 90,000 내지 약 10,000,000, 약 90,000 내지 약 9,000,000, 약 90,000 내지 약 8,000,000, 약 90,000 내지 약 7,000,000, 약 90,000 내지 약 6,000,000, 약 90,000 내지 약 5,000,000, 약 90,000 내지 약 4,000,000, 약 90,000 내지 약 3,000,000, 약 90,000 내지 약 2,000,000, 약 90,000 내지 약 1,000,000, 약 90,000 내지 약 800,000, 약 90,000 내지 약 600,000, 약 90,000 내지 약 400,000, 약 90,000 내지 약 200,000, 약 90,000 내지 약 100,000, 약 100,000 내지 약 10,000,000, 약 100,000 내지 약 9,000,000, 약 100,000 내지 약 8,000,000, 약 100,000 내지 약 7,000,000, 약 100,000 내지 약 6,000,000, 약 100,000 내지 약 5,000,000, 약 100,000 내지 약 4,000,000, 약 100,000 내지 약 3,000,000, 약 100,000 내지 약 2,000,000, 약 100,000 내지 약 1,000,000, 약 100,000 내지 약 800,000, 약 100,000 내지 약 600,000, 약 100,000 내지 약 400,000, 약 100,000 내지 약 200,000, 약 200,000 내지 약 10,000,000, 약 200,000 내지 약 9,000,000, 약 200,000 내지 약 8,000,000, 약 200,000 내지 약 7,000,000, 약 200,000 내지 약 6,000,000, 약 200,000 내지 약 5,000,000, 약 200,000 내지 약 4,000,000, 약 200,000 내지 약 3,000,000, 약 200,000 내지 약 2,000,000, 약 200,000 내지 약 1,000,000, 약 200,000 내지 약 800,000, 약 200,000 내지 약 600,000, 약 200,000 내지 약 400,000, 약 400,000 내지 약 10,000,000, 약 400,000 내지 약 9,000,000, 약 400,000 내지 약 8,000,000, 약 400,000 내지 약 7,000,000, 약 400,000 내지 약 6,000,000, 약 400,000 내지 약 5,000,000, 약 400,000 내지 약 4,000,000, 약 400,000 내지 약 3,000,000, 약 400,000 내지 약 2,000,000, 약 400,000 내지 약 1,000,000, 약 400,000 내지 약 800,000, 약 400,000 내지 약 600,000, 약 600,000 내지 약 10,000,000, 약 600,000 내지 약 9,000,000, 약 600,000 내지 약 8,000,000, 약 600,000 내지 약 7,000,000, 약 600,000 내지 약 6,000,000, 약 600,000 내지 약 5,000,000, 약 600,000 내지 약 4,000,000, 약 600,000 내지 약 3,000,000, 약 600,000 내지 약 2,000,000, 약 600,000 내지 약 1,000,000, 약 600,000 내지 약 800,000, 약 800,000 내지 약 10,000,000, 약 800,000 내지 약 9,000,000, 약 800,000 내지 약 8,000,000, 약 800,000 내지 약 7,000,000, 약 800,000 내지 약 6,000,000, 약 800,000 내지 약 5,000,000, 약 800,000 내지 약 4,000,000, 약 800,000 내지 약 3,000,000, 약 800,000 내지 약 2,000,000, 약 800,000 내지 약 1,000,000, 약 1,000,000 내지 약 10,000,000, 약 1,000,000 내지 약 9,000,000, 약 1,000,000 내지 약 8,000,000, 약 1,000,000 내지 약 7,000,000, 약 1,000,000 내지 약 6,000,000, 약 1,000,000 내지 약 5,000,000, 약 1,000,000 내지 약 4,000,000, 약 1,000,000 내지 약 3,000,000, 약 1,000,000 내지 약 2,000,000, 약 2,000,000 내지 약 10,000,000, 약 2,000,000 내지 약 9,000,000, 약 2,000,000 내지 약 8,000,000, 약 2,000,000 내지 약 7,000,000, 약 2,000,000 내지 약 6,000,000, 약 2,000,000 내지 약 5,000,000, 약 2,000,000 내지 약 4,000,000, 약 2,000,000 내지 약 3,000,000, 약 3,000,000 내지 약 10,000,000, 약 3,000,000 내지 약 9,000,000, 약 3,000,000 내지 약 8,000,000, 약 3,000,000 내지 약 7,000,000, 약 3,000,000 내지 약 6,000,000, 약 3,000,000 내지 약 5,000,000, 약 3,000,000 내지 약 4,000,000, 약 4,000,000 내지 약 10,000,000, 약 4,000,000 내지 약 9,000,000, 약 4,000,000 내지 약 8,000,000, 약 4,000,000 내지 약 7,000,000, 약 4,000,000 내지 약 6,000,000, 약 4,000,000 내지 약 5,000,000, 약 5,000,000 내지 약 10,000,000, 약 5,000,000 내지 약 9,000,000, 약 5,000,000 내지 약 8,000,000, 약 5,000,000 내지 약 7,000,000, 약 5,000,000 내지 약 6,000,000, 약 6,000,000 내지 약 10,000,000, 약 6,000,000 내지 약 9,000,000, 약 6,000,000 내지 약 8,000,000, 약 6,000,000 내지 약 7,000,000, 약 7,000,000 내지 약 10,000,000, 약 7,000,000 내지 약 9,000,000, 약 7,000,000 내지 약 8,000,000, 약 8,000,000 내지 약 10,000,000, 약 8,000,000 내지 약 9,000,000, or 약 9,000,000 내지 약 10,000,000개의 MET를 가질 수 있다.
"항원 밀도"란 말은 표적 포유류 세포의 표면에 존재하는 MET의 수 또는 특정 유형의 표적 포유류 세포 집단의 표면에 존재하는 MET의 평균 수를 의미한다. 이는, 예를 들어 Quantibright 비드 키트 또는 방사성 표지(예를 들어 BD Biosciences PE Phycoerythrin Fluorescence Quantitation Kit, 카탈로그 #340495)를 사용해 측정할 수 있다.
"히스티딘으로 치환된 아미노산"이란 말은 기준 폴리펩티드 서열에서 히스티딘이 아닌 아미노산 잔기가 히스티딘으로 치환된 것을 의미한다. 기준 폴리펩티드 내의 아미노산 잔기를 히스티딘으로 치환하는 비제한적인 방법이 본원에 기술된다. 기준 폴리펩티드 내의 아미노산 잔기를 히스티딘으로 치환하는 추가의 방법은 당업계에 알려져 있다.
"알라닌으로 치환된 아미노산"이란 말은 기준 폴리펩티드 서열에서 히스티딘인 아미노산 잔기가 알라닌으로 치환된 것을 의미한다. 기준 폴리펩티드 내의 히스티딘을 알라닌으로 치환하는 비제한적인 방법이 본원에 기술된다. 기준 폴리펩티드 내의 히스티딘을 알라닌으로 치환하는 추가의 방법은 당업계에 알려져 있다.
달리 정의되지 않는 한, 본원에 사용된 모든 기술적 및 과학적 용어는 본 발명이 속하는 당업자에 의해 일반적으로 이해되는 것과 동일한 의미를 갖는다. 본 발명에서 사용하기 위한 방법 및 물질이 본원에 기술되며; 당업계에 공지된 다른 적절한 방법 및 물질이 사용될 수도 있다. 물질, 방법, 및 실시예는 단지 예시적인 것이며 제한하도록 의도되지 않는다. 본원에 언급된 모든 간행물, 특허 출원, 특허, 서열, 데이터베이스 엔트리, 및 기타 참조 문헌은 그 전체가 참조로서 통합된다. 상충되는 경우, 정의를 포함하여 본 명세서가 우선한다.
본 발명의 다른 특징 및 장점은 다음의 발명을 실시하기 위한 구체적인 내용 및 도면, 및 청구범위로부터 명백해질 것이다.
도 1: 텔리소투주맙 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 텔리소투주맙 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT0886은 텔리소투주맙이고, 나머지 레인(MYT0887 - MYT0924)은 텔리소투주맙 중쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 2a 내지 도 2am: 바이오층 간섭에 의한, MET에 대한 텔리소투주맙 출발 ABPC 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT0886(텔리소투주맙) 및 MYT0887 - MYT0924(중쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 3: 텔리소투주맙 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 텔리소투주맙 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT0886은 텔리소투주맙이고, 나머지 레인(MYT2028 - MYT2058)은 텔리소투주맙 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 4a 내지 도 4af: 바이오층 간섭에 의한, MET에 대한 텔리소투주맙 출발 ABPC 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT0886(텔리소투주맙) 및 MYT2028 - MYT2058(경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
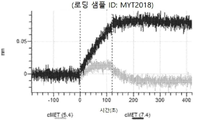
도 5: 텔리소투주맙 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 텔리소투주맙 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT2018 - MYT2027은 텔리소투주맙 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 6a 내지 도 6j: 바이오층 간섭에 의한, MET에 대한 텔리소투주맙의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT2018 - MYT2027(중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 7: 텔리소투주맙 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 텔리소투주맙 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT4201 - MYT4210은 텔리소투주맙 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
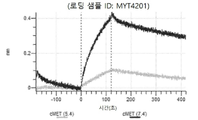
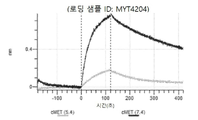
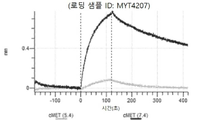
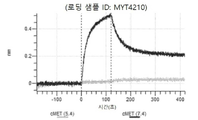
도 8a 내지 도 8j: 바이오층 간섭에 의한, MET에 대한 텔리소투주맙의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT4201 - MYT4210(경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 9: 텔리소투주맙 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 텔리소투주맙 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT3451 - MYT3492, MYT3603 - MYT3616, 및 MYT4211 - MYT4220은 텔리소투주맙의 페어링된 중쇄 및 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체로서, 경쇄 히스티딘 및 알라진 스캐닝 변이체 또는 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 중쇄 히스티딘 및 알라닌 스캐닝 변이체 또는 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체와 조합한 것이다.
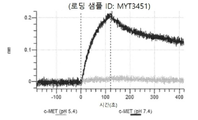
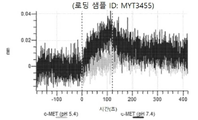
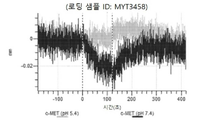
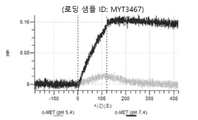
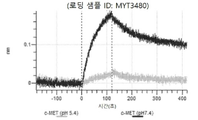
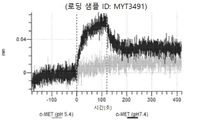
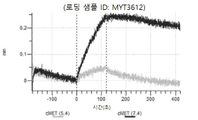
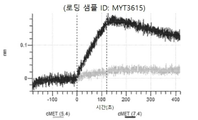
도 10a 내지 도 10bn: 바이오층 간섭에 의한, MET에 대한 텔리소투주맙의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT3451 - MYT3492, MYT3603 - MYT3616, 및 MYT4211 - MYT4220, 즉 경쇄 히스티딘 및 알라진 스캐닝 변이체 또는 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 중쇄 히스티딘 및 알라닌 스캐닝 변이체 또는 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체와 조합한 페어링된 중쇄 및 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
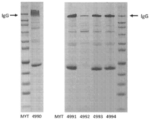
도 11: 텔리소투주맙 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 텔리소투주맙 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT4951 - MYT4989는 텔리소투주맙 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
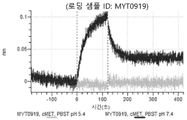
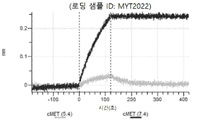
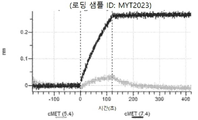
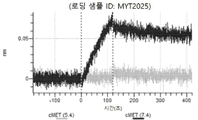
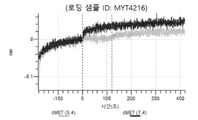
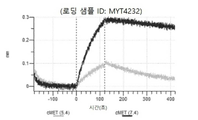
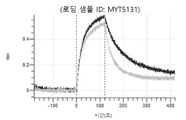
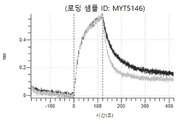
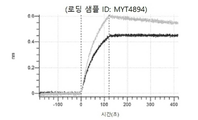
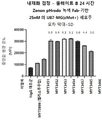
도 12: Detroit 562 세포에서 텔리소투주맙의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 내재화 및 엔도리소좀 전달. MYT4894(텔리소투주맙) 및 MYT4953 및 MYT4970(중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를, 표시된 시점 및 ABPC의 최종 농도에서 Incucyte Human FabFluor-pH 적색 항체 표지 시약을 사용하여 Detroit 562 세포에 대한 내재화에 대해 검정하였다. 내재화 및 엔도리소좀 전달의 배수 증가는 각 변이체 위에 숫자로 표시되어 있다.
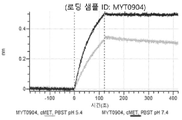
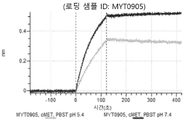
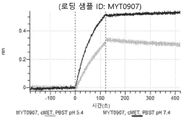
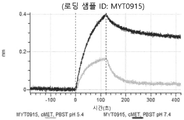
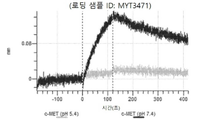
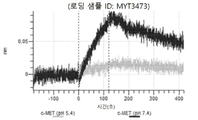
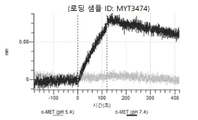
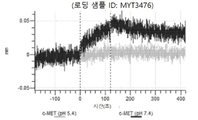
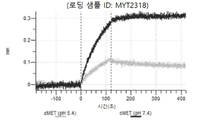
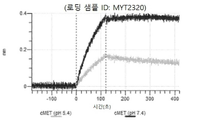
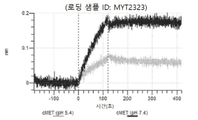
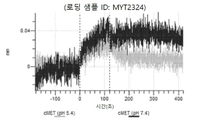
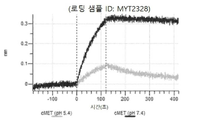
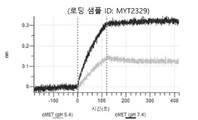
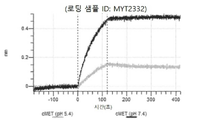
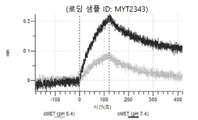
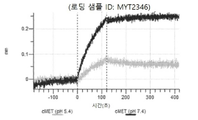
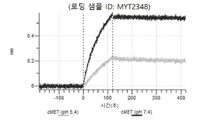
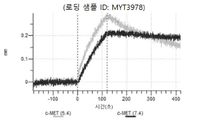
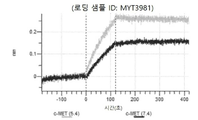
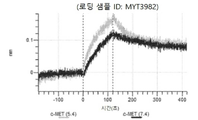
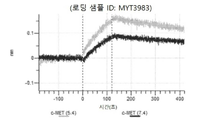
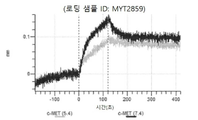
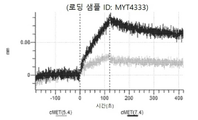
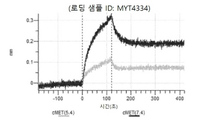
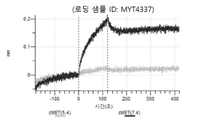
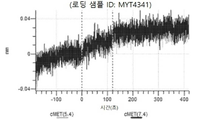
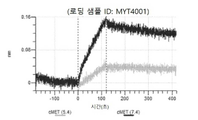
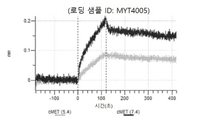
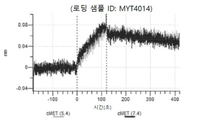
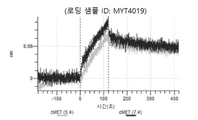
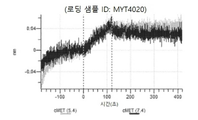
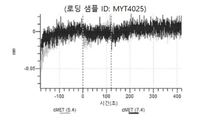
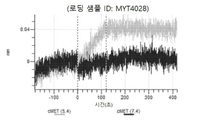
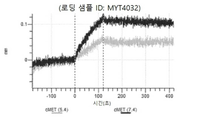
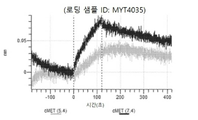
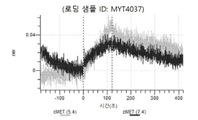
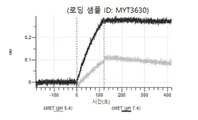
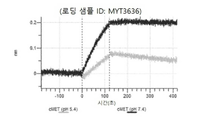
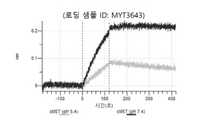
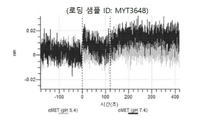
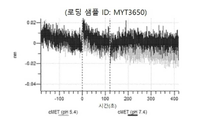
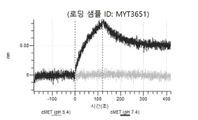
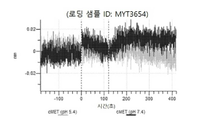
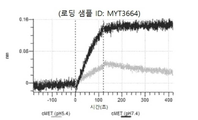
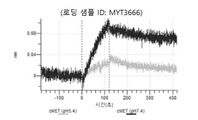
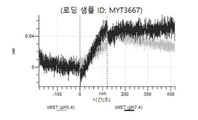
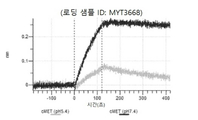
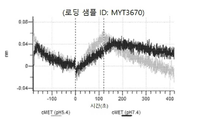
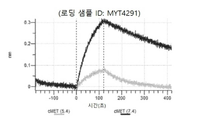
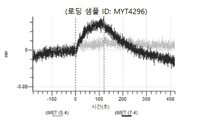
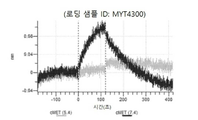
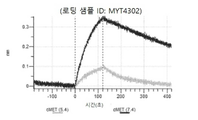
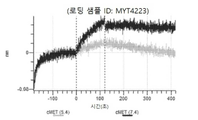
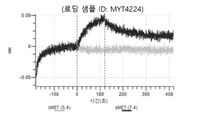
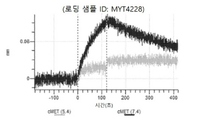
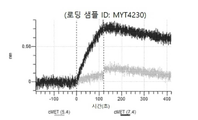
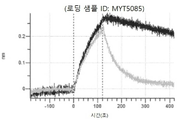
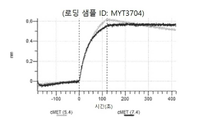
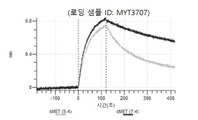
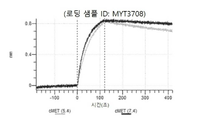
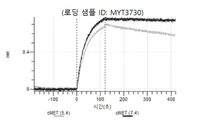
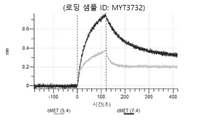
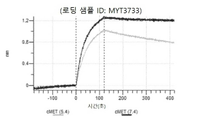
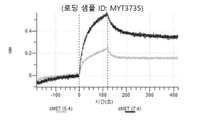
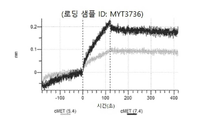
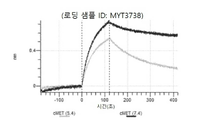
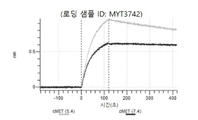
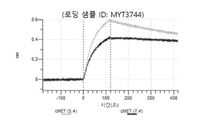
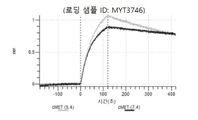
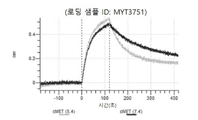
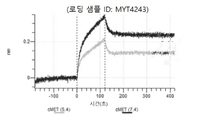
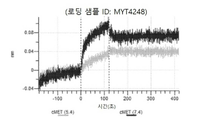
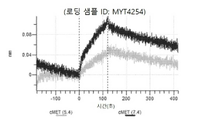
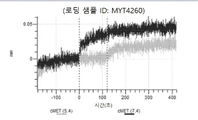
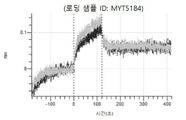
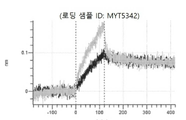
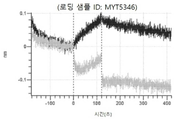
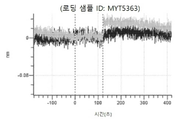
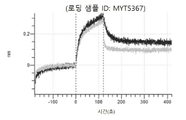
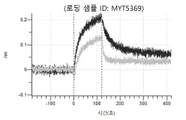
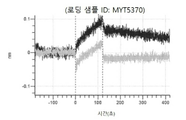
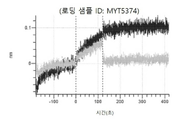
도 13a 내지 도 13b: 바이오층 간섭에 의한, MET에 대한 텔리소투주맙의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT4953 - MYT4970(중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, pH 7.4에서 MET와 결합시켰다. 해리는 pH 7.4(검은색 트레이스) 또는 pH 5.4(회색 트레이스)에서 이루어진 것이다.
도 14: 텔리소투주맙 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 텔리소투주맙 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT4990 - MYT4994는 텔리소투주맙 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
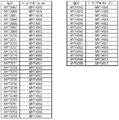
도 15: 작제물 식별자 대 서열번호 상응 표. 작제물, 중쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 16: 작제물 식별자 대 서열번호 상응 표. 작제물, 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 17: 작제물 식별자 대 서열번호 상응 표. 작제물, 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 18: 작제물 식별자 대 서열번호 상응 표. 작제물, 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 19: 작제물 식별자 대 서열번호 상응 표. 작제물 및 (경쇄 히스티딘 및 알라닌 스캐닝 변이체 또는 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 중쇄 히스티딘 및 알라닌 스캐닝 변이체 또는 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체와 조합한) 페어링된 중쇄 및 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체가 표의 제1 컬럼에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 20: 작제물 식별자 대 서열번호 상응 표. 작제물, 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 21: 작제물 식별자 대 서열번호 상응 표. 작제물, 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 22: 에미베투주맙 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 에미베투주맙 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT2313은 에미베투주맙이고, 나머지 레인(MYT2314 - MYT2348)은 에미베투주맙 중쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 23a 내지 도 23aj: 바이오층 간섭에 의한, MET에 대한 에미베투주맙 출발 ABPC 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT2313(에미베투주맙) 및 MYT2314 - MYT2348(중쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 24: 에미베투주맙 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 에미베투주맙 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT3958 - MYT3985는 에미베투주맙 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 25a 내지 도 25ab: 바이오층 간섭에 의한, MET에 대한 에미베투주맙의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT3958 - MYT3985(경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 26: 에미베투주맙 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 에미베투주맙 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT2848 - MYT2687은 에미베투주맙 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
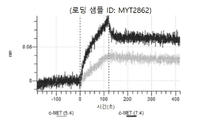
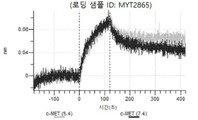
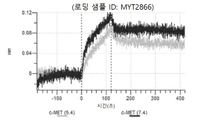
도 27a 내지 도 27t: 바이오층 간섭에 의한, MET에 대한 에미베투주맙의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT2848 - MYT2867(중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 28: 에미베투주맙 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 에미베투주맙 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT4326 - MYT4345은 에미베투주맙 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 29a 내지 도 29t: 바이오층 간섭에 의한, MET에 대한 에미베투주맙의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT4326 - MYT4345(경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 30: 에미베투주맙 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 에미베투주맙 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT3999 - MYT4042는 에미베투주맙의 페어링된 중쇄 및 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체로서, 경쇄 히스티딘 및 알라진 스캐닝 변이체 또는 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 중쇄 히스티딘 및 알라닌 스캐닝 변이체 또는 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체와 조합한 것이다.
도 31a 내지 도 31ab: 바이오층 간섭에 의한, MET에 대한 에미베투주맙의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT3999 - MYT4042, 즉 경쇄 히스티딘 및 알라진 스캐닝 변이체 또는 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 중쇄 히스티딘 및 알라닌 스캐닝 변이체 또는 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체와 조합한 페어링된 중쇄 및 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 32: 에미베투주맙 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 에미베투주맙 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT4995 - MYT5041은 에미베투주맙 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 33: 작제물 식별자 대 서열번호 상응 표. 작제물, 중쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 34: 작제물 식별자 대 서열번호 상응 표. 작제물, 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 35: 작제물 식별자 대 서열번호 상응 표. 작제물, 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 36: 작제물 식별자 대 서열번호 상응 표. 작제물, 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 37: 작제물 식별자 대 서열번호 상응 표. 작제물 및 (경쇄 히스티딘 및 알라닌 스캐닝 변이체 또는 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 중쇄 히스티딘 및 알라닌 스캐닝 변이체 또는 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체와 조합한) 페어링된 중쇄 및 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체가 표의 제1 컬럼에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 38: 작제물 식별자 대 서열번호 상응 표. 작제물, 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 39: hucMET27Gv1.3 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 hucMET27Gv1.3 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT3617은 hucMET27Gv1.3이고, 나머지 레인(MYT3618 - MYT3655)은 hucMET27Gv1.3 중쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 40a 내지 도 40am: 바이오층 간섭에 의한, MET에 대한 hucMET27Gv1.3 출발 ABPC 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT3617(hucMET27Gv1.3) 및 MYT3618 - MYT3655(중쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
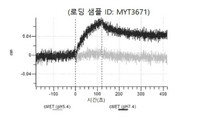
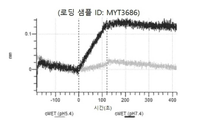
도 41: hucMET27Gv1.3 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 hucMET27Gv1.3 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT3656 - MYT3686은 hucMET27Gv1.3 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 42a 내지 도 4ae: 바이오층 간섭에 의한, MET에 대한 hucMET27Gv1.3 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT3656 - MYT3686(경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
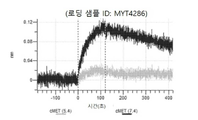
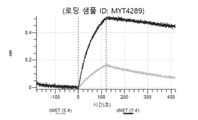
도 43: hucMET27Gv1.3 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 hucMET27Gv1.3 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT4285 - MYT4304는 hucMET27Gv1.3 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 44a 내지 도 44t: 바이오층 간섭에 의한, MET에 대한 hucMET27Gv1.3의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT4285 - MYT4304(중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 45: hucMET27Gv1.3 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 hucMET27Gv1.3 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT4222 - MYT4241은 hucMET27Gv1.3 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
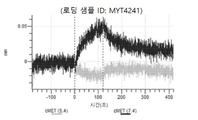
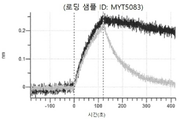
도 46a 내지 46t: 바이오층 간섭에 의한, MET에 대한 hucMET27Gv1.3의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT4222 - MYT4241(경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 47: hucMET27Gv1.3 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 hucMET27Gv1.3 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT5296 및 MYT5042 - MYT5065는 hucMET27Gv1.3 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 48: hucMET27Gv1.3 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 hucMET27Gv1.3 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT5066 - MYT5121은 hucMET27Gv1.3 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
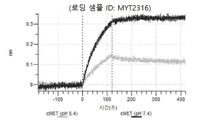
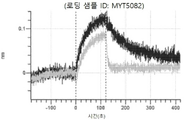
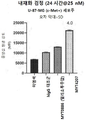
도 49a 내지 49f: Detroit 562 세포에서 hucMET27Gv1.3의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 내재화 및 엔도리소좀 전달. 도면에 명시된 바와 같이 MYT4284(hucMET27Gv1.3) 및 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를, 표시된 시점 및 ABPC의 최종 농도에서 Incucyte Human FabFluor-pH 적색 항체 표지 시약을 사용하여 Detroit 562 세포에 대한 내재화에 대해 검정하였다. 내재화 및 엔도리소좀 전달의 배수 증가는 각 변이체 위에 숫자로 표시되어 있다.
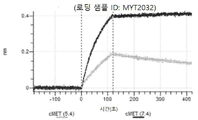
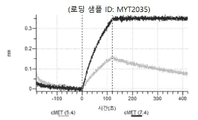
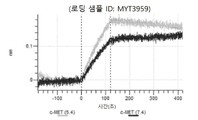
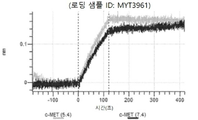
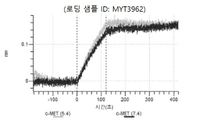
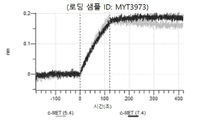
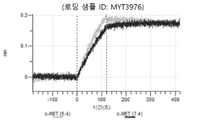
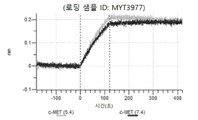
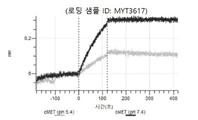
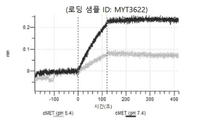
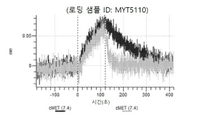
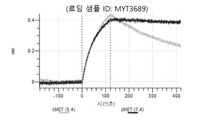
도 50내지 50v: 바이오층 간섭에 의한, MET에 대한 hucMET27Gv1.3의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. 도면에 명시된 바와 같이 hucMET27Gv1.3의 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 pH 7.4에서 MET와 결합시켰다. 해리는 pH 7.4(검은색 트레이스) 또는 pH 5.4(회색 트레이스)에서 이루어진 것이다.
도 51: 작제물 식별자 대 서열번호 상응 표. 작제물, 중쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 52: 작제물 식별자 대 서열번호 상응 표. 작제물, 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 53: 작제물 식별자 대 서열번호 상응 표. 작제물, 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 54: 작제물 식별자 대 서열번호 상응 표. 작제물, 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 55: 작제물 식별자 대 서열번호 상응 표. 작제물, 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 56: 작제물 식별자 대 서열번호 상응 표. 작제물, 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 57: P3D12 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 P3D12 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT3687은 P3D12이고, 나머지 레인(MYT3688 - MYT3726)은 P3D12 중쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 58a 내지 도 58an: 바이오층 간섭에 의한, MET에 대한 P3D12 출발 ABPC 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT3687(P3D12) 및 MYT3688 - MYT3726(중쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 59: P3D12 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 P3D12 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT3727 - MYT3754는 P3D12 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
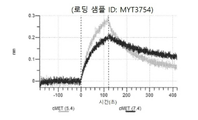
도 60a 내지 60ab: 바이오층 간섭에 의한, MET에 대한 P3D12 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT3727 - MYT3754(경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 61: P3D12 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 P3D12 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT4306 - MYT4325는 P3D12 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
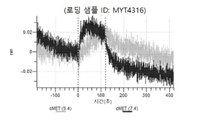
도 62a 내지 62t: 바이오층 간섭에 의한, MET에 대한 P3D12의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT4306 - MYT4325(중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 63: P3D12 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 P3D12 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT4242 - MYT4261은 P3D12 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 64a 내지 64t: 바이오층 간섭에 의한, MET에 대한 P3D12의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT4242 - MYT4261(경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 65: P3D12 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 P3D12 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT5122 - MYT5221은 P3D12 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
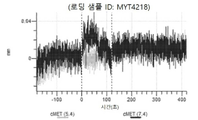
도 66a 내지 66e: Detroit 562 세포에서 P3D12의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 내재화 및 엔도리소좀 전달. 도면에 명시된 바와 같이 MYT4305(P3D12) 및 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를, 표시된 시점 및 ABPC의 최종 농도에서 Incucyte Human FabFluor-pH 적색 항체 표지 시약을 사용하여 Detroit 562 세포에 대한 내재화에 대해 검정하였다. 내재화 및 엔도리소좀 전달의 배수 증가는 각 변이체 위에 숫자로 표시되어 있다.
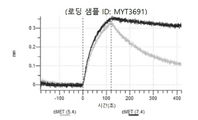
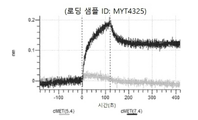
도 67a 내지 67e: 바이오층 간섭에 의한, MET에 대한 P3D12의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. 도면에 명시된 바와 같이 P3D12의 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 pH 7.4에서 MET와 결합시켰다. 해리는 pH 7.4(검은색 트레이스) 또는 pH 5.4(회색 트레이스)에서 이루어진 것이다.
도 68: P3D12 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 P3D12 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT5222 - MYT5295는 P3D12 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 69: Detroit 562 세포에서 P3D12의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 내재화 및 엔도리소좀 전달. MYT4305(P3D12) 및 P3D12의 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체인 MYT5237을 표시된 시점 및 ABPC의 최종 농도에서 Incucyte Human FabFluor-pH 적색 항체 표지 시약을 사용하여 Detroit 562 세포에 대한 내재화에 대해 검정하였다. 내재화 및 엔도리소좀 전달의 배수 증가는 각 변이체 위에 숫자로 표시되어 있다.
도 70: 바이오층 간섭에 의한, MET에 대한 P3D12의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. P3D12의 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체인 MYT5237을 항-인간 Fc 바이오센서 상에 포획하고, pH 7.4에서 MET와 결합시켰다. 해리는 pH 7.4(검은색 트레이스) 또는 pH 5.4(회색 트레이스)에서 이루어진 것이다.
도 71: 작제물 식별자 대 서열번호 상응 표. 작제물, 중쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 72: 작제물 식별자 대 서열번호 상응 표. 작제물, 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 73: 작제물 식별자 대 서열번호 상응 표. 작제물, 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 74: 작제물 식별자 대 서열번호 상응 표. 작제물, 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 75: 작제물 식별자 대 서열번호 상응 표. 작제물, 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 76: 작제물 식별자 대 서열번호 상응 표. 작제물, 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 77: 항-MET ABPC의 재포맷팅을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 출발 ABPC 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다.
도 78a 내지 78l: 바이오층 간섭에 의한, MET에 대한 출발 ABPC 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. 도면에 명시된 바와 같이 출발 ABPC 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 항-인간 Fc 바이오센서 상에 포획하고, pH 7.4에서 MET와 결합시켰다. 해리는 pH 7.4(검은색 트레이스) 또는 pH 5.4(회색 트레이스)에서 이루어진 것이다.
도 79a 내지 79f: Detroit 562 세포에서 출발 항-MET ABPC 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 내재화 및 엔도리소좀 전달. 도면에 명시된 바와 같이 출발 ABPC 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를, 표시된 시점 및 ABPC의 최종 농도에서 Incucyte Human FabFluor-pH 적색 항체 표지 시약을 사용하여 Detroit 562 세포에 대한 내재화에 대해 검정하였다. 내재화 및 엔도리소좀 전달의 배수 증가는 각 변이체 위에 숫자로 표시되어 있다.
도 80a 내지 80d: ABPC 작제물 식별자 상응 표의 재포맷팅. IgG1 출발 ABPC 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있다. 동일한 행에서 IgG1 작제물과 동일한 중쇄 및 경쇄 가변 영역을 갖는, TH 및 YTE 돌연변이를 갖는 IgG1 작제물은 제2 열에 열거되어 있다.
도 81: 세포에서 항-MET mAb의 내재화. 도 81a 내지 81aj에 명시된 바와 같이, 비히클 대조군과 함께, pH 조작된 항-MET 항체 변이체, 상응하는 출발 ABPC 항체, 대조군 IgG1 이소형 대조군(BP0297, Bioxcell)을, 도면에 명시된 것과 같이 24시간차에 평균 형광 강도로 측정했을 때의 세포에 대한 내재화 및 엔도리소좀 전달에 대해 검정하였다. 오차 막대는 표준 편차를 나타낸다. 막대 위의 숫자는 상응하는 출발 ABPC에 대비 배수 변화를 나타낸다.
도 82: P3D12 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 P3D12 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT5342 - MYT5381은 P3D12의 페어링된 중쇄 및 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체로서, 경쇄 히스티딘 및 알라진 스캐닝 변이체 또는 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 중쇄 히스티딘 및 알라닌 스캐닝 변이체 또는 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체와 조합한 것이다.
도 83a 내지 83an: 바이오층 간섭에 의한, MET에 대한 P3D12의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT5342 - MYT5371, 즉 경쇄 히스티딘 및 알라진 스캐닝 변이체 또는 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 중쇄 히스티딘 및 알라닌 스캐닝 변이체 또는 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체와 조합한 페어링된 중쇄 및 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 항-인간 Fc 바이오센서 상에 포획하고, pH 7.4에서 MET와 결합시켰다. 해리는 pH 7.4(검은색 트레이스) 또는 pH 5.4(회색 트레이스)에서 이루어진 것이다.
도 84: 작제물 식별자 대 서열번호 상응 표. 작제물 및 (경쇄 히스티딘 및 알라닌 스캐닝 변이체 또는 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 중쇄 히스티딘 및 알라닌 스캐닝 변이체 또는 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체와 조합한) 페어링된 중쇄 및 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체가 표의 제1 컬럼에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 85: 선택된 항-MET mAb의 용융 온도. 표에 열거된 선택된 항-MET mAb를 시차주사 형광분석(DSF)에 의해 이들의 용융 온도에 대해 검정하고, 생성된 Sypro Orange 신호를 이들의 제1 유도체로서 도표화하였다. 용융 온도(Tm)를 이 그래프의 국소 최대값으로서 계산하였으며, 이는 표에 나타나 있다.
도 2a 내지 도 2am: 바이오층 간섭에 의한, MET에 대한 텔리소투주맙 출발 ABPC 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT0886(텔리소투주맙) 및 MYT0887 - MYT0924(중쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 3: 텔리소투주맙 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 텔리소투주맙 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT0886은 텔리소투주맙이고, 나머지 레인(MYT2028 - MYT2058)은 텔리소투주맙 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 4a 내지 도 4af: 바이오층 간섭에 의한, MET에 대한 텔리소투주맙 출발 ABPC 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT0886(텔리소투주맙) 및 MYT2028 - MYT2058(경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 5: 텔리소투주맙 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 텔리소투주맙 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT2018 - MYT2027은 텔리소투주맙 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 6a 내지 도 6j: 바이오층 간섭에 의한, MET에 대한 텔리소투주맙의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT2018 - MYT2027(중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 7: 텔리소투주맙 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 텔리소투주맙 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT4201 - MYT4210은 텔리소투주맙 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 8a 내지 도 8j: 바이오층 간섭에 의한, MET에 대한 텔리소투주맙의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT4201 - MYT4210(경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 9: 텔리소투주맙 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 텔리소투주맙 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT3451 - MYT3492, MYT3603 - MYT3616, 및 MYT4211 - MYT4220은 텔리소투주맙의 페어링된 중쇄 및 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체로서, 경쇄 히스티딘 및 알라진 스캐닝 변이체 또는 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 중쇄 히스티딘 및 알라닌 스캐닝 변이체 또는 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체와 조합한 것이다.
도 10a 내지 도 10bn: 바이오층 간섭에 의한, MET에 대한 텔리소투주맙의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT3451 - MYT3492, MYT3603 - MYT3616, 및 MYT4211 - MYT4220, 즉 경쇄 히스티딘 및 알라진 스캐닝 변이체 또는 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 중쇄 히스티딘 및 알라닌 스캐닝 변이체 또는 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체와 조합한 페어링된 중쇄 및 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 11: 텔리소투주맙 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 텔리소투주맙 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT4951 - MYT4989는 텔리소투주맙 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 12: Detroit 562 세포에서 텔리소투주맙의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 내재화 및 엔도리소좀 전달. MYT4894(텔리소투주맙) 및 MYT4953 및 MYT4970(중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를, 표시된 시점 및 ABPC의 최종 농도에서 Incucyte Human FabFluor-pH 적색 항체 표지 시약을 사용하여 Detroit 562 세포에 대한 내재화에 대해 검정하였다. 내재화 및 엔도리소좀 전달의 배수 증가는 각 변이체 위에 숫자로 표시되어 있다.
도 13a 내지 도 13b: 바이오층 간섭에 의한, MET에 대한 텔리소투주맙의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT4953 - MYT4970(중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, pH 7.4에서 MET와 결합시켰다. 해리는 pH 7.4(검은색 트레이스) 또는 pH 5.4(회색 트레이스)에서 이루어진 것이다.
도 14: 텔리소투주맙 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 텔리소투주맙 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT4990 - MYT4994는 텔리소투주맙 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 15: 작제물 식별자 대 서열번호 상응 표. 작제물, 중쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 16: 작제물 식별자 대 서열번호 상응 표. 작제물, 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 17: 작제물 식별자 대 서열번호 상응 표. 작제물, 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 18: 작제물 식별자 대 서열번호 상응 표. 작제물, 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 19: 작제물 식별자 대 서열번호 상응 표. 작제물 및 (경쇄 히스티딘 및 알라닌 스캐닝 변이체 또는 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 중쇄 히스티딘 및 알라닌 스캐닝 변이체 또는 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체와 조합한) 페어링된 중쇄 및 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체가 표의 제1 컬럼에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 20: 작제물 식별자 대 서열번호 상응 표. 작제물, 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 21: 작제물 식별자 대 서열번호 상응 표. 작제물, 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 22: 에미베투주맙 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 에미베투주맙 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT2313은 에미베투주맙이고, 나머지 레인(MYT2314 - MYT2348)은 에미베투주맙 중쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 23a 내지 도 23aj: 바이오층 간섭에 의한, MET에 대한 에미베투주맙 출발 ABPC 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT2313(에미베투주맙) 및 MYT2314 - MYT2348(중쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 24: 에미베투주맙 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 에미베투주맙 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT3958 - MYT3985는 에미베투주맙 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 25a 내지 도 25ab: 바이오층 간섭에 의한, MET에 대한 에미베투주맙의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT3958 - MYT3985(경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 26: 에미베투주맙 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 에미베투주맙 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT2848 - MYT2687은 에미베투주맙 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 27a 내지 도 27t: 바이오층 간섭에 의한, MET에 대한 에미베투주맙의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT2848 - MYT2867(중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 28: 에미베투주맙 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 에미베투주맙 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT4326 - MYT4345은 에미베투주맙 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 29a 내지 도 29t: 바이오층 간섭에 의한, MET에 대한 에미베투주맙의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT4326 - MYT4345(경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 30: 에미베투주맙 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 에미베투주맙 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT3999 - MYT4042는 에미베투주맙의 페어링된 중쇄 및 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체로서, 경쇄 히스티딘 및 알라진 스캐닝 변이체 또는 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 중쇄 히스티딘 및 알라닌 스캐닝 변이체 또는 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체와 조합한 것이다.
도 31a 내지 도 31ab: 바이오층 간섭에 의한, MET에 대한 에미베투주맙의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT3999 - MYT4042, 즉 경쇄 히스티딘 및 알라진 스캐닝 변이체 또는 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 중쇄 히스티딘 및 알라닌 스캐닝 변이체 또는 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체와 조합한 페어링된 중쇄 및 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 32: 에미베투주맙 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 에미베투주맙 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT4995 - MYT5041은 에미베투주맙 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 33: 작제물 식별자 대 서열번호 상응 표. 작제물, 중쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 34: 작제물 식별자 대 서열번호 상응 표. 작제물, 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 35: 작제물 식별자 대 서열번호 상응 표. 작제물, 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 36: 작제물 식별자 대 서열번호 상응 표. 작제물, 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 37: 작제물 식별자 대 서열번호 상응 표. 작제물 및 (경쇄 히스티딘 및 알라닌 스캐닝 변이체 또는 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 중쇄 히스티딘 및 알라닌 스캐닝 변이체 또는 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체와 조합한) 페어링된 중쇄 및 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체가 표의 제1 컬럼에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 38: 작제물 식별자 대 서열번호 상응 표. 작제물, 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 39: hucMET27Gv1.3 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 hucMET27Gv1.3 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT3617은 hucMET27Gv1.3이고, 나머지 레인(MYT3618 - MYT3655)은 hucMET27Gv1.3 중쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 40a 내지 도 40am: 바이오층 간섭에 의한, MET에 대한 hucMET27Gv1.3 출발 ABPC 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT3617(hucMET27Gv1.3) 및 MYT3618 - MYT3655(중쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 41: hucMET27Gv1.3 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 hucMET27Gv1.3 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT3656 - MYT3686은 hucMET27Gv1.3 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 42a 내지 도 4ae: 바이오층 간섭에 의한, MET에 대한 hucMET27Gv1.3 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT3656 - MYT3686(경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 43: hucMET27Gv1.3 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 hucMET27Gv1.3 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT4285 - MYT4304는 hucMET27Gv1.3 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 44a 내지 도 44t: 바이오층 간섭에 의한, MET에 대한 hucMET27Gv1.3의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT4285 - MYT4304(중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 45: hucMET27Gv1.3 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 hucMET27Gv1.3 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT4222 - MYT4241은 hucMET27Gv1.3 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 46a 내지 46t: 바이오층 간섭에 의한, MET에 대한 hucMET27Gv1.3의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT4222 - MYT4241(경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 47: hucMET27Gv1.3 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 hucMET27Gv1.3 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT5296 및 MYT5042 - MYT5065는 hucMET27Gv1.3 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 48: hucMET27Gv1.3 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 hucMET27Gv1.3 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT5066 - MYT5121은 hucMET27Gv1.3 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 49a 내지 49f: Detroit 562 세포에서 hucMET27Gv1.3의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 내재화 및 엔도리소좀 전달. 도면에 명시된 바와 같이 MYT4284(hucMET27Gv1.3) 및 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를, 표시된 시점 및 ABPC의 최종 농도에서 Incucyte Human FabFluor-pH 적색 항체 표지 시약을 사용하여 Detroit 562 세포에 대한 내재화에 대해 검정하였다. 내재화 및 엔도리소좀 전달의 배수 증가는 각 변이체 위에 숫자로 표시되어 있다.
도 50내지 50v: 바이오층 간섭에 의한, MET에 대한 hucMET27Gv1.3의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. 도면에 명시된 바와 같이 hucMET27Gv1.3의 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 pH 7.4에서 MET와 결합시켰다. 해리는 pH 7.4(검은색 트레이스) 또는 pH 5.4(회색 트레이스)에서 이루어진 것이다.
도 51: 작제물 식별자 대 서열번호 상응 표. 작제물, 중쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 52: 작제물 식별자 대 서열번호 상응 표. 작제물, 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 53: 작제물 식별자 대 서열번호 상응 표. 작제물, 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 54: 작제물 식별자 대 서열번호 상응 표. 작제물, 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 55: 작제물 식별자 대 서열번호 상응 표. 작제물, 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 56: 작제물 식별자 대 서열번호 상응 표. 작제물, 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 57: P3D12 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 P3D12 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT3687은 P3D12이고, 나머지 레인(MYT3688 - MYT3726)은 P3D12 중쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 58a 내지 도 58an: 바이오층 간섭에 의한, MET에 대한 P3D12 출발 ABPC 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT3687(P3D12) 및 MYT3688 - MYT3726(중쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 59: P3D12 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 P3D12 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT3727 - MYT3754는 P3D12 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 60a 내지 60ab: 바이오층 간섭에 의한, MET에 대한 P3D12 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT3727 - MYT3754(경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 61: P3D12 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 P3D12 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT4306 - MYT4325는 P3D12 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 62a 내지 62t: 바이오층 간섭에 의한, MET에 대한 P3D12의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT4306 - MYT4325(중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 63: P3D12 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 P3D12 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT4242 - MYT4261은 P3D12 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 64a 내지 64t: 바이오층 간섭에 의한, MET에 대한 P3D12의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT4242 - MYT4261(경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체)를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 낮은 pH 또는 높은 pH에서 MET와 결합시켰다.
도 65: P3D12 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 P3D12 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT5122 - MYT5221은 P3D12 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 66a 내지 66e: Detroit 562 세포에서 P3D12의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 내재화 및 엔도리소좀 전달. 도면에 명시된 바와 같이 MYT4305(P3D12) 및 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를, 표시된 시점 및 ABPC의 최종 농도에서 Incucyte Human FabFluor-pH 적색 항체 표지 시약을 사용하여 Detroit 562 세포에 대한 내재화에 대해 검정하였다. 내재화 및 엔도리소좀 전달의 배수 증가는 각 변이체 위에 숫자로 표시되어 있다.
도 67a 내지 67e: 바이오층 간섭에 의한, MET에 대한 P3D12의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. 도면에 명시된 바와 같이 P3D12의 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 항-인간 Fc 바이오센서 상에 포획하고, 도면에 명시된 바와 같이 pH 7.4에서 MET와 결합시켰다. 해리는 pH 7.4(검은색 트레이스) 또는 pH 5.4(회색 트레이스)에서 이루어진 것이다.
도 68: P3D12 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 P3D12 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT5222 - MYT5295는 P3D12 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체이다.
도 69: Detroit 562 세포에서 P3D12의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 내재화 및 엔도리소좀 전달. MYT4305(P3D12) 및 P3D12의 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체인 MYT5237을 표시된 시점 및 ABPC의 최종 농도에서 Incucyte Human FabFluor-pH 적색 항체 표지 시약을 사용하여 Detroit 562 세포에 대한 내재화에 대해 검정하였다. 내재화 및 엔도리소좀 전달의 배수 증가는 각 변이체 위에 숫자로 표시되어 있다.
도 70: 바이오층 간섭에 의한, MET에 대한 P3D12의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. P3D12의 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체인 MYT5237을 항-인간 Fc 바이오센서 상에 포획하고, pH 7.4에서 MET와 결합시켰다. 해리는 pH 7.4(검은색 트레이스) 또는 pH 5.4(회색 트레이스)에서 이루어진 것이다.
도 71: 작제물 식별자 대 서열번호 상응 표. 작제물, 중쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 72: 작제물 식별자 대 서열번호 상응 표. 작제물, 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 73: 작제물 식별자 대 서열번호 상응 표. 작제물, 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 74: 작제물 식별자 대 서열번호 상응 표. 작제물, 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 75: 작제물 식별자 대 서열번호 상응 표. 작제물, 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 76: 작제물 식별자 대 서열번호 상응 표. 작제물, 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 77: 항-MET ABPC의 재포맷팅을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 출발 ABPC 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다.
도 78a 내지 78l: 바이오층 간섭에 의한, MET에 대한 출발 ABPC 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. 도면에 명시된 바와 같이 출발 ABPC 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 항-인간 Fc 바이오센서 상에 포획하고, pH 7.4에서 MET와 결합시켰다. 해리는 pH 7.4(검은색 트레이스) 또는 pH 5.4(회색 트레이스)에서 이루어진 것이다.
도 79a 내지 79f: Detroit 562 세포에서 출발 항-MET ABPC 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 내재화 및 엔도리소좀 전달. 도면에 명시된 바와 같이 출발 ABPC 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를, 표시된 시점 및 ABPC의 최종 농도에서 Incucyte Human FabFluor-pH 적색 항체 표지 시약을 사용하여 Detroit 562 세포에 대한 내재화에 대해 검정하였다. 내재화 및 엔도리소좀 전달의 배수 증가는 각 변이체 위에 숫자로 표시되어 있다.
도 80a 내지 80d: ABPC 작제물 식별자 상응 표의 재포맷팅. IgG1 출발 ABPC 및 히스티딘 스캐닝 및 알라닌 스캐닝 변이체는 표의 제1 열에 열거되어 있다. 동일한 행에서 IgG1 작제물과 동일한 중쇄 및 경쇄 가변 영역을 갖는, TH 및 YTE 돌연변이를 갖는 IgG1 작제물은 제2 열에 열거되어 있다.
도 81: 세포에서 항-MET mAb의 내재화. 도 81a 내지 81aj에 명시된 바와 같이, 비히클 대조군과 함께, pH 조작된 항-MET 항체 변이체, 상응하는 출발 ABPC 항체, 대조군 IgG1 이소형 대조군(BP0297, Bioxcell)을, 도면에 명시된 것과 같이 24시간차에 평균 형광 강도로 측정했을 때의 세포에 대한 내재화 및 엔도리소좀 전달에 대해 검정하였다. 오차 막대는 표준 편차를 나타낸다. 막대 위의 숫자는 상응하는 출발 ABPC에 대비 배수 변화를 나타낸다.
도 82: P3D12 히스티딘 스캐닝 및 알라닌 스캐닝을 위한 SDS PAGE. 수확 후 Expi293 세포 배양 상청액을 환원되지 않은 SDS PAGE 겔 상에 로딩하여 P3D12 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 발현을 확인하였다. 화살표는 환원되지 않은 SDS PAGE 겔 상에서 IgG에 대한 상응하는 크기를 나타낸다. MYT5342 - MYT5381은 P3D12의 페어링된 중쇄 및 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체로서, 경쇄 히스티딘 및 알라진 스캐닝 변이체 또는 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 중쇄 히스티딘 및 알라닌 스캐닝 변이체 또는 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체와 조합한 것이다.
도 83a 내지 83an: 바이오층 간섭에 의한, MET에 대한 P3D12의 히스티딘 스캐닝 및 알라닌 스캐닝 변이체의 결합. MYT5342 - MYT5371, 즉 경쇄 히스티딘 및 알라진 스캐닝 변이체 또는 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 중쇄 히스티딘 및 알라닌 스캐닝 변이체 또는 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체와 조합한 페어링된 중쇄 및 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 항-인간 Fc 바이오센서 상에 포획하고, pH 7.4에서 MET와 결합시켰다. 해리는 pH 7.4(검은색 트레이스) 또는 pH 5.4(회색 트레이스)에서 이루어진 것이다.
도 84: 작제물 식별자 대 서열번호 상응 표. 작제물 및 (경쇄 히스티딘 및 알라닌 스캐닝 변이체 또는 경쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체를 중쇄 히스티딘 및 알라닌 스캐닝 변이체 또는 중쇄 조합 히스티딘 스캐닝 및 알라닌 스캐닝 변이체와 조합한) 페어링된 중쇄 및 경쇄 히스티딘 스캐닝 및 알라닌 스캐닝 변이체가 표의 제1 컬럼에 열거되어 있고, 서열번호가 열거되어 있는데, 서열번호는 좌측의 작제물 및 상단에 표시된 적절한 중쇄 및/또는 경쇄 카테고리에 상응한다.
도 85: 선택된 항-MET mAb의 용융 온도. 표에 열거된 선택된 항-MET mAb를 시차주사 형광분석(DSF)에 의해 이들의 용융 온도에 대해 검정하고, 생성된 Sypro Orange 신호를 이들의 제1 유도체로서 도표화하였다. 용융 온도(Tm)를 이 그래프의 국소 최대값으로서 계산하였으며, 이는 표에 나타나 있다.
표적 포유류 세포의 표면에 제시된 MET 또는 MET의 에피토프에 특이적으로 결합할 수 있는 제1 항원 결합 도메인을 포함하는 항원 결합 단백질 작제물(ABPC)이 본원에 제공되며, 여기서 (a) 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인 해리 속도는 약 7.0 내지 약 8.0의 pH에서의 해리 속도보다 더 빠르고/빠르거나; (b) 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인의 해리 상수(KD)는 약 7.0 내지 약 8.0의 pH에서의 KD보다 더 크다. 이들 ABPC의 일부 실시예에서, ABPC는 표적 포유류 세포에 의해 내재화된 후 표적 포유류 세포 내에서 분해된다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예는 접합된 독소, 방사성 동위원소, 약물, 또는 소분자(예를 들어, 형광단 또는 염료)를 추가로 포함할 수 있다.
또한, 표적 포유류 세포의 표면에 제시된 MET 또는 MET의 에피토프에 특이적으로 결합할 수 있는 제1 항원 결합 도메인; 및 접합된 독소, 방사성 동위원소, 약물, 또는 소분자를 포함하는 항원 결합 단백질 작제물(ABPC)이 제공되며, 여기서 (a) 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인의 해리 속도는 약 7.0 내지 약 8.0의 pH에서의 해리 속도보다 빠르고/빠르거나; 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인의 해리 상수(KD)는 약 7.0 내지 약 8.0의 pH에서의 KD보다 더 크며; (b) ABPC를 포함하는 조성물은 다음 중 하나 이상을 (예를 들어 둘 이상을) 가능하게 한다: 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독성 유리를 증가시키는 것 (예를 들어 검출 가능하게 증가시키는 것); 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 세포 살해를 증가시키는 것 (예를 들어 검출 가능하게 증가시키는 것); 및 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 엔도리소좀 전달을 증가시키는 것 (예를 들어 검출 가능하게 증가시키는 것).
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 하나 이상의 (예를 들어, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20개의) 아미노산이 히스티딘으로 치환된 텔리소투주맙의 중쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 하나 이상의 (예를 들어, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20개의) 아미노산이 히스티딘으로 치환된 텔리소투주맙의 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 하나 이상의 (예를 들어, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20개의) 아미노산이 히스티딘으로 치환된 텔리소투주맙의 중쇄 가변 도메인; 및 하나 이상의 (예를 들어, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20개의) 아미노산이 히스티딘으로 치환된 텔리소투주맙의 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 텔리소투주맙의 중쇄 가변 도메인은 서열번호 1을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 텔리소투주맙의 경쇄 가변 도메인은 서열번호 2를 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 3~7의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 아미노산 위치가 히스티딘으로 치환된 서열번호 3, 서열번호 4, 및 서열번호 5의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 6~8의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 아미노산 위치가 히스티딘으로 치환된 서열번호 6, 서열번호 7, 및 서열번호 8의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 3~5의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 아미노산 위치가 히스티딘으로 치환된 서열번호 3, 서열번호 4, 및 서열번호 5의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인; 및 서열번호 6~8의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 아미노산 위치가 히스티딘으로 치환된 서열번호 6, 서열번호 7, 및 서열번호 8의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 1과 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 26, 27, 28, 29, 32, 97, 98, 99, 100, 101, 102, 103, 및 107로 이루어진 군으로부터 선택된 서열번호 1 내 하나 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 2와 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 25, 28, 29, 30, 31, 32, 34, 35, 36, 37, 54, 55, 59, 60, 95, 99, 및 101로 이루어진 군으로부터 선택된 서열번호 2 내 하나 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하는 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 다음을 포함한다: 서열번호 1과 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 26, 27, 28, 29, 32, 97, 98, 99, 100, 101, 102, 103, 및 107로 이루어진 군으로부터 선택된 서열번호 1 내 하나 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하는 중쇄 가변 도메인; 및 서열번호 2와 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 25, 28, 29, 30, 31, 32, 34, 35, 36, 37, 54, 55, 59, 60, 95, 99, 및 101로 이루어진 군으로부터 선택된 서열번호 2 내 하나 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하는 경쇄 가변 도메인.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 중쇄 가변 도메인은, 서열번호 1과 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 1에 열거된 서열번호 1 내 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 경쇄 가변 도메인은 서열번호 2와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 표 2에 열거된 서열번호 2 내 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은, 서열번호 2와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 서열번호 2 내 위치 38에서 알라닌을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 다음을 포함한다: 서열번호 2와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 서열번호 2 내 위치 38에서 알라닌을 포함하는, 경쇄 가변 도메인; 및 서열번호 1과 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 26, 27, 28, 29, 32, 97, 98, 99, 100, 101, 102, 103, 및 107로 이루어진 군으로부터 선택된 서열번호 1 내 하나 이상의 (예를 들어 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하는, 중쇄 가변 도메인.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 다음을 포함한다: 서열번호 2와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 25, 28, 29, 30, 31, 32, 34, 35, 36, 37, 54, 55, 59, 60, 95, 99, 및 101로 이루어진 군으로부터 선택된 서열번호 2 내 하나 이상의 (예를 들어 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하고, 서열번호 2 내 위치 38에서 알라닌을 포함하는, 경쇄 가변 도메인. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 다음을 포함한다: 서열번호 2와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 25, 28, 29, 30, 31, 32, 34, 35, 36, 37, 54, 55, 59, 60, 95, 99, 및 101로 이루어진 군으로부터 선택된 서열번호 2 내 하나 이상의 (예를 들어 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하고, 서열번호 2 내 위치 38에서 알라닌을 포함하는, 경쇄 가변 도메인; 및 서열번호 1과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 26, 27, 28, 29, 32, 97, 98, 99, 100, 101, 102, 103, 및 107로 이루어진 군으로부터 선택된 서열번호 1 내 하나 이상의 (예를 들어 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하는, 중쇄 가변 도메인.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 경쇄 가변 도메인은, 서열번호 2와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 표 2에 열거된 서열번호 2 내 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하고, 서열번호 2의 위치 38에서 알라닌을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 1과 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 1에 열거된 서열번호 1의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인; 및 서열번호 2와 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 표 2에 열거된 서열번호 2의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 2를 포함하는 경쇄 가변 도메인; 및 서열번호 1과 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 1에 열거된 서열번호 1의 하나 이상의(예를 들어 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 2의 위치 25에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 1과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 1에 열거된 서열번호 1의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 2의 위치 28에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 1과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 1에 열거된 서열번호 1의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 2의 위치 29에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 1과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 1에 열거된 서열번호 1의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 2의 위치 30에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 1과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 1에 열거된 서열번호 1의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 2의 위치 31에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 1과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 1에 열거된 서열번호 1의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 2의 위치 32에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 1과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 1에 열거된 서열번호 1의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 2의 위치 34에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 1과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 1에 열거된 서열번호 1의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 2의 위치 35에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 1과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 1에 열거된 서열번호 1의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 2의 위치 36에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 1과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 1에 열거된 서열번호 1의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 2의 위치 37에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 1과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 1에 열거된 서열번호 1의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 2의 위치 54에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 1과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 1에 열거된 서열번호 1의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 2의 위치 55에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 1과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 1에 열거된 서열번호 1의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 2의 위치 59에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 1과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 1에 열거된 서열번호 1의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 2의 위치 60에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 1과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 1에 열거된 서열번호 1의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 2의 위치 95에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 1과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 1에 열거된 서열번호 1의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 2의 위치 99에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 1과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 1에 열거된 서열번호 1의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 2의 위치 101에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 1과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 1에 열거된 서열번호 1의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 2의 위치 38에서 알라닌을 포함하는 경쇄 가변 도메인; 및 서열번호 1과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 1에 열거된 서열번호 1의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 하나 이상의 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 히스티딘이 알라닌으로 치환된 텔리소투주맙의 중쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 하나 이상의 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 히스티딘이 알라닌으로 치환된 텔리소투주맙의 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 하나 이상의 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 히스티딘이 알라닌으로 치환된 텔리소투주맙의 중쇄 가변 도메인; 및 하나 이상의 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 히스티딘(들)이 알라닌으로 치환된 텔리소투주맙의 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 텔리소투주맙의 중쇄 가변 도메인은 서열번호 1을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 텔리소투주맙의 경쇄 가변 도메인은 서열번호 2를 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은, 서열번호 3~5의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 히스티딘(들)이 알라닌으로 치환된 서열번호 3, 서열번호 4, 및 서열번호 5의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 6~8의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20개의) 히스티딘(들)이 알라닌으로 치환된 서열번호 6, 서열번호 7, 및 서열번호 8의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 3~5의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 히스티딘(들)이 알라닌으로 치환된 서열번호 3, 서열번호 4, 및 서열번호 5의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인; 및 서열번호 6~8의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 히스티딘(들)이 알라닌으로 치환된 서열번호 6, 서열번호 7, 및 서열번호 8의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50의 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81의 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 2를 포함하는 경쇄 가변 도메인, 및 서열번호 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 51을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 52를 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 53을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 54를 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 55를 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 56을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 57을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 58을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 59를 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 60을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 61을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 62를 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 63을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 64를 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 65를 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 66을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 67을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 68을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 69를 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 70을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 71을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 72를 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 73을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 74를 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 75를 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 76을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 77을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 78을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 79를 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 80을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 81을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 또는 130을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 82를 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 83을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 84를 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 85를 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 86을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 87을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 88을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 89를 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 90을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 91을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 92를 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 93을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 94를 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 95를 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.69, SEQ ID NO: 70, SEQ ID NO: 71, SEQ ID NO: 72, SEQ ID NO: 73, SEQ ID NO: 74, SEQ ID NO: 75, SEQ ID NO: 76, SEQ ID NO: 77, SEQ ID NO: 78, SEQ ID NO: 79, SEQ ID NO: 80, or SEQ ID NO: 81.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 96을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 97을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 98을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 99를 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 100을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 101을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 102를 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 103을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 104를 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 105를 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 106을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 107을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 108을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 109를 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 110을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 111을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 112를 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 113을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 114를 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 115를 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 116을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 117을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 118을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 119를 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 120을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 121을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 122를 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 123을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 124를 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 125를 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 126을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 127을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 128을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 129를 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 130을 포함하는 중쇄 가변 도메인, 및 서열번호 2, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 또는 81을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 또는 145를 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 131을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 또는 130을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 132를 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 또는 130을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 133을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 또는 130을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 134를 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 또는 130을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 135를 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 또는 130을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 136을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 또는 130을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 137을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 또는 130을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 138을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 또는 130을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 139를 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 또는 130을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 140을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 또는 130을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 141을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 또는 130을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 142를 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 또는 130을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 143을 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 또는 130을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 144를 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 또는 130을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 145를 포함하는 경쇄 가변 도메인, 및 서열번호 1, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 또는 130을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 1개 이상의 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산이 히스티딘으로 치환된 에미베투주맙의 중쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 1개 이상의 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산이 히스티딘으로 치환된 에미베투주맙의 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 하나 이상의 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산이 히스티딘으로 치환된 에미베투주맙의 중쇄 가변 도메인; 및 하나 이상의 아미노산이 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 히스티딘으로 치환된 에미베투주맙의 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 에미베투주맙의 중쇄 가변 도메인은 서열번호 146을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 에미베투주맙의 경쇄 가변 도메인은 서열번호 147을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 148~150의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 아미노산 위치가 히스티딘으로 치환된 서열번호 148, 서열번호 149, 및 서열번호 150의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 151~153의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 아미노산 위치가 히스티딘으로 치환된 서열번호 151, 서열번호 152, 및 서열번호 153의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 148~150의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 아미노산 위치가 히스티딘으로 치환된 서열번호 148, 서열번호 149, 및 서열번호 150의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인; 및 서열번호 151~153의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 아미노산 위치가 히스티딘으로 치환된 서열번호 151, 서열번호 152, 및 서열번호 153의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은, 서열번호 146과 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 31, 50, 51, 52, 53, 54, 56, 57, 59, 98, 99, 100, 및 103으로 이루어진 군으로부터 선택된 서열번호 146 내 하나 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은, 서열번호 147과 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 25, 26, 29, 32, 33, 51, 91, 92, 95, 96, 및 97로 이루어진 군으로부터 선택된 서열번호 147 내 하나 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하는 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 다음을 포함한다: 서열번호 146과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 31, 50, 51, 52, 53, 54, 56, 57, 59, 98, 99, 100, 및 103으로 이루어진 군으로부터 선택된 서열번호 146 내 하나 이상의 (예를 들어 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하는 중쇄 가변 도메인; 및 서열번호 147과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 25, 26, 29, 32, 33, 51, 91, 92, 95, 96, 및 97로 이루어진 군으로부터 선택된 서열번호 147 내 하나 이상의 (예를 들어 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하는, 경쇄 가변 도메인.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 중쇄 가변 도메인은, 서열번호 146과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 3에 열거된 서열번호 146 내 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 경쇄 가변 도메인은 서열번호 147과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 표 4에 열거된 서열번호 147 내 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은, 서열번호 147과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 서열번호 147 내 위치 35에서 알라닌을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 다음을 포함한다: 서열번호 147과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 서열번호 147 내 위치 35에서 알라닌을 포함하는, 경쇄 가변 도메인; 및 서열번호 146과 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 31, 50, 51, 52, 53, 54, 56, 57, 59, 98, 99, 100, 및 103으로 이루어진 군으로부터 선택된 서열번호 146 내 하나 이상의 (예를 들어 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하는, 중쇄 가변 도메인.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 다음을 포함한다: 서열번호 147과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 25, 26, 29, 32, 33, 51, 91, 92, 95, 96, 및 97로 이루어진 군으로부터 선택된 서열번호 147 내 하나 이상의 (예를 들어 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하고, 서열번호 147 내 위치 35에서 알라닌을 포함하는, 경쇄 가변 도메인. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 다음을 포함한다: 서열번호 147과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 25, 26, 29, 32, 33, 51, 91, 92, 95, 96, 및 97로 이루어진 군으로부터 선택된 서열번호 147 내 하나 이상의 (예를 들어 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하고, 서열번호 147 내 위치 36에서 알라닌을 포함하는, 경쇄 가변 도메인; 및 서열번호 147과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 31, 50, 51, 52, 53, 54, 56, 57, 59, 98, 99, 100, 및 103으로 이루어진 군으로부터 선택된 서열번호 147 내 하나 이상의 (예를 들어 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하는, 중쇄 가변 도메인.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 경쇄 가변 도메인은, 서열번호 147과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 표 4에 열거된 서열번호 147 내 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하고, 서열번호 147의 위치 35에서 알라닌을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 146과 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 3에 열거된 서열번호 146의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인; 및 서열번호 147와 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 표 4에 열거된 서열번호 147의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 147을 포함하는 경쇄 가변 도메인; 및 서열번호 146과 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 3에 열거된 서열번호 146의 하나 이상의(예를 들어 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 147과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 147의 위치 25에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 146과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 3에 열거된 서열번호 146의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 147과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 147의 위치 26에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 146과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 3에 열거된 서열번호 146의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 147과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 147의 위치 29에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 146과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 3에 열거된 서열번호 146의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 147과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 147의 위치 32에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 146과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 3에 열거된 서열번호 146의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 147과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 147의 위치 33에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 146과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 3에 열거된 서열번호 146의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 147과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 147의 위치 51에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 146과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 3에 열거된 서열번호 146의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 147과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 147의 위치 91에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 146과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 3에 열거된 서열번호 146의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 147과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 147의 위치 92에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 146과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 3에 열거된 서열번호 146의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 147과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 147의 위치 95에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 146과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 3에 열거된 서열번호 146의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 147과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 147의 위치 96에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 146과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 3에 열거된 서열번호 146의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 147과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 147의 위치 97에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 146과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 3에 열거된 서열번호 146의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 147과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 147의 위치 35에서 알라닌을 포함하는 경쇄 가변 도메인; 및 서열번호 146과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 3에 열거된 서열번호 146의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 하나 이상의 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 히스티딘이 알라닌으로 치환된 에미베투주맙의 중쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 하나 이상의 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 히스티딘이 알라닌으로 치환된 에미베투주맙의 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 하나 이상의 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 히스티딘이 알라닌으로 치환된 에미베투주맙의 중쇄 가변 도메인; 및 하나 이상의 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 히스티딘(들)이 알라닌으로 치환된 에미베투주맙의 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 에미베투주맙의 중쇄 가변 도메인은 서열번호 146을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 에미베투주맙의 경쇄 가변 도메인은 서열번호 147을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은, 서열번호 148~150의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 히스티딘(들)이 알라닌으로 치환된 서열번호 148, 서열번호 149, 및 서열번호 150의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 151~153의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20개의) 히스티딘(들)이 알라닌으로 치환된 서열번호 151, 서열번호 152, 및 서열번호 153의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 148~150의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 히스티딘(들)이 알라닌으로 치환된 서열번호 148, 서열번호 149, 및 서열번호 150의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인; 및 서열번호 151~153의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 히스티딘(들)이 알라닌으로 치환된 서열번호 151, 서열번호 152, 및 서열번호 153의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188의 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 147, 189, 190, 191, 192, 193, 194, 195, 196, 197, 198, 199, 200, 201, 202, 203, 204, 205, 206, 207, 208, 209, 210, 211, 212, 213, 214, 215, 또는 216의 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 147을 포함하는 경쇄 가변 도메인, 및 서열번호 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 189를 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 190을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 191을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 192를 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 193을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 194를 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 195를 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 196을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 197을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 198을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 199를 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 200을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 201을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 202를 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 203을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 204를 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 205를 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 206을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 207을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 208을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 209를 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 210을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 211을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 212를 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 213을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 214를 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 215를 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 216을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 또는 188을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 147을 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 189를 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 190을 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 191을 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 192를 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 193을 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 194를 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 195를 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 196을 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 197을 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 198을 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 199를 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 200을 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 201을 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 202를 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 203을 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 204를 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 205를 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 206을 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 207을 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 208을 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 209를 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 210을 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 211을 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 212를 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 213을 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 214를 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 215를 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 216을 포함하는 경쇄 가변 도메인, 및 서열번호 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 284, 285, 286, 287, 288, 289, 290, 291, 292, 293, 294, 295, 296, 297, 298, 299, 300, 301, 302, 또는 303을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 284를 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 285를 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 286을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 287을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 288을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 289를 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 290을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 291을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 292를 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 293을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 294를 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 295를 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 296을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 297을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 298을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 299를 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 300을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 301을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 302를 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 303을 포함하는 경쇄 가변 도메인, 및 서열번호 146, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 또는 283을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 1개 이상의 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산이 히스티딘으로 치환된 hucMET27Gv1.3의 중쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 1개 이상의 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산이 히스티딘으로 치환된 hucMET27Gv1.3의 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 하나 이상의 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산이 히스티딘으로 치환된 hucMET27Gv1.3의 중쇄 가변 도메인; 및 하나 이상의 아미노산이 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 히스티딘으로 치환된 hucMET27Gv1.3의 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, hucMET27Gv1.3의 중쇄 가변 도메인은 서열번호 304를 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, hucMET27Gv1.3의 경쇄 가변 도메인은 서열번호 305를 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 306~308의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 아미노산 위치가 히스티딘으로 치환된 서열번호 306, 서열번호 307, 및 서열번호 308의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 309~311의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 아미노산 위치가 히스티딘으로 치환된 서열번호 309, 서열번호 310, 및 서열번호 311의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 306~308의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 아미노산 위치가 히스티딘으로 치환된 서열번호 306, 서열번호 307, 및 서열번호 308의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인; 및 서열번호 309~311의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 아미노산 위치가 히스티딘으로 치환된 서열번호 309, 서열번호 310, 및 서열번호 311의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은, 서열번호 304와 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 27, 34, 35, 50, 51, 52, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 98, 99, 103, 및 105로 이루어진 군으로부터 선택된 서열번호 304 내 하나 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은, 서열번호 305와 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 26, 30, 31, 34, 36, 54, 56, 57, 60, 93, 95, 99, 및 101로 이루어진 군으로부터 선택된 서열번호 305 내 하나 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하는 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 다음을 포함한다: 서열번호 304와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 27, 34, 35, 50, 51, 52, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 98, 99, 103, 및 105로 이루어진 군으로부터 선택된 서열번호 304 내 하나 이상의 (예를 들어 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하는 중쇄 가변 도메인; 및 서열번호 305과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 26, 30, 31, 34, 36, 54, 56, 57, 60, 93, 95, 99, 및 101로 이루어진 군으로부터 선택된 서열번호 305 내 하나 이상의 (예를 들어 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하는, 경쇄 가변 도메인.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 중쇄 가변 도메인은, 서열번호 304와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 5에 열거된 서열번호 304 내 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 경쇄 가변 도메인은 서열번호 305와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 표 6에 열거된 서열번호 305 내 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은, 서열번호 305와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 서열번호 305 내 위치 38에서 알라닌을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 다음을 포함한다: 서열번호 305와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 서열번호 305 내 위치 38에서 알라닌을 포함하는, 경쇄 가변 도메인; 및 서열번호 304와 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 27, 34, 35, 50, 51, 52, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 98, 99, 103, 및 105로 이루어진 군으로부터 선택된 서열번호 304 내 하나 이상의 (예를 들어 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하는, 중쇄 가변 도메인.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 다음을 포함한다: 서열번호 305와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 27, 34, 35, 50, 51, 52, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 98, 99, 103, 및 105로 이루어진 군으로부터 선택된 서열번호 305 내 하나 이상의 (예를 들어 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하고, 서열번호 305 내 위치 38에서 알라닌을 포함하는, 경쇄 가변 도메인. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 다음을 포함한다: 서열번호 305와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 26, 30, 31, 34, 36, 54, 56, 57, 60, 93, 95, 99, 및 101로 이루어진 군으로부터 선택된 서열번호 305 내 하나 이상의 (예를 들어 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하고, 서열번호 305 내 위치 38에서 알라닌을 포함하는, 경쇄 가변 도메인; 및 서열번호 304와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 27, 34, 35, 50, 51, 52, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 98, 99, 103, 및 105로 이루어진 군으로부터 선택된 서열번호 1 내 하나 이상의 (예를 들어 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하는, 중쇄 가변 도메인.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 경쇄 가변 도메인은, 서열번호 305와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 표 6에 열거된 서열번호 305 내 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하고, 서열번호 305의 위치 38에서 알라닌을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 304와 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 5에 열거된 서열번호 304의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인; 및 서열번호 305와 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 표 6에 열거된 서열번호 305의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 305를 포함하는 경쇄 가변 도메인; 및 서열번호 304와 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 5에 열거된 서열번호 304의 하나 이상의(예를 들어 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 305와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 305의 위치 26에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 304와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 5에 열거된 서열번호 304의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 305와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 305의 위치 30에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 304와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 5에 열거된 서열번호 304의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 305와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 305의 위치 31에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 304와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 5에 열거된 서열번호 304의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 305와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 305의 위치 34에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 304와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 5에 열거된 서열번호 304의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 305와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 305의 위치 36에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 304와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 5에 열거된 서열번호 304의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 305와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 305의 위치 54에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 304와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 5에 열거된 서열번호 304의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 305와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 305의 위치 56에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 304와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 5에 열거된 서열번호 304의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 305와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 305의 위치 57에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 304와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 5에 열거된 서열번호 304의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 305와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 305의 위치 60에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 304와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 5에 열거된 서열번호 304의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 305와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 305의 위치 93에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 304와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 5에 열거된 서열번호 304의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 305와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 305의 위치 95에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 304와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 5에 열거된 서열번호 304의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 305와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 305의 위치 99에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 304와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 5에 열거된 서열번호 304의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 305와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 305의 위치 101에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 304와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 5에 열거된 서열번호 304의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 305와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 305의 위치 38에서 알라닌을 포함하는 경쇄 가변 도메인; 및 서열번호 304와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 5에 열거된 서열번호 304의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 하나 이상의 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 히스티딘이 알라닌으로 치환된 hucMET27Gv1.3의 중쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 하나 이상의 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 히스티딘이 알라닌으로 치환된 hucMET27Gv1.3의 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 하나 이상의 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 히스티딘이 알라닌으로 치환된 hucMET27Gv1.3의 중쇄 가변 도메인; 및 하나 이상의 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 히스티딘(들)이 알라닌으로 치환된 hucMET27Gv1.3의 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, hucMET27Gv1.3의 중쇄 가변 도메인은 서열번호 304를 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, hucMET27Gv1.3의 경쇄 가변 도메인은 서열번호 305를 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은, 서열번호 306~308의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 히스티딘(들)이 알라닌으로 치환된 서열번호 306, 서열번호 307, 및 서열번호 308의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 309~311의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20개의) 히스티딘(들)이 알라닌으로 치환된 서열번호 309, 서열번호 310, 및 서열번호 311의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 306~308의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 히스티딘(들)이 알라닌으로 치환된 서열번호 306, 서열번호 307, 및 서열번호 308의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인; 및 서열번호 309~311의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 히스티딘(들)이 알라닌으로 치환된 서열번호 309, 서열번호 310, 및 서열번호 311의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349의 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 503, 549, 550, 551, 552, 553, 554, 555, 556, 557, 558, 559, 560, 561, 562, 563, 564, 565, 566, 567, 568, 569, 570, 571, 572, 573, 574, 575, 또는 576의 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 305를 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 350을 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 351을 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 352를 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 353을 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 354를 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 355를 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 356을 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 357을 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 358을 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 359를 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 360을 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 361을 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 362를 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 363을 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 364를 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 365를 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 366을 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 367을 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 368을 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 369를 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 370을 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 371을 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 372를 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 373을 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 374를 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 375를 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 376을 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 377을 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 378을 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 379를 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 380을 포함하는 경쇄 가변 도메인, 및 서열번호 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 또는 349를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 305를 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 350을 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 351을 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 352를 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 353을 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 354를 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 355를 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 356을 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 357을 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 358을 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 359를 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 360을 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 361을 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 362를 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 363을 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 364를 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 365를 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 366을 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 367을 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 368을 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 369를 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 370을 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 371을 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 372를 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 373을 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 374를 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 375를 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 376을 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 377을 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 378을 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 379를 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 380을 포함하는 경쇄 가변 도메인, 및 서열번호 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 426, 427, 428, 429, 430, 431, 432, 433, 434, 435, 436, 437, 438, 439, 440, 441, 442, 443, 444, 445, 446, 447, 448, 449, 450, 451, 452, 453, 454, 455, 456, 457, 458, 459, 460, 461, 462, 463, 464, 465, 466, 467, 468, 469, 470, 471, 472, 473, 474, 475, 476, 477, 478, 479, 480, 481, 482, 483, 484, 485, 486, 487, 488, 489, 490, 491, 492, 493, 494, 495, 496, 497, 498, 499, 500, 또는 501을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 426을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 427을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 428을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 429를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 430을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 431을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 432를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 433을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 434를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 435를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 436을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 437을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 438을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 439를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 440을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 441을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 442를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 443을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 444를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 445를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 446을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 447을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 448을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 449를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 450을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 451을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 452를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 453을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 454를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 455를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 456을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 457을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 458을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 459를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 460을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 461을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 462를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 463을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 464를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 465를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 466을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 467을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 468을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 469를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 470을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 471을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 472를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 473을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 474를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 475를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 476을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 477을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 478을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 479를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 480을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 481을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 482를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 483을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 484를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 485를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 486을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 487을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 488을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 489를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 490을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 491을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 492를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 493을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 494를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 495를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 496을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 497을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 498을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 499를 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 500을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 501을 포함하는 경쇄 가변 도메인, 및 서열번호 304, 312, 313, 314, 315, 316, 317, 318, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 338, 339, 340, 341, 342, 343, 344, 345, 346, 347, 348, 349, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 391, 392, 393, 394, 395, 396, 397, 398, 399, 400, 401, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 424, 또는 425를 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 1개 이상의 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산이 히스티딘으로 치환된 P3D12의 중쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 1개 이상의 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산이 히스티딘으로 치환된 P3D12의 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 하나 이상의 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산이 히스티딘으로 치환된 P3D12의 중쇄 가변 도메인; 및 하나 이상의 아미노산이 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 히스티딘으로 치환된 P3D12의 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, P3D12의 중쇄 가변 도메인은 서열번호 502를 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, P3D12의 경쇄 가변 도메인은 서열번호 503을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 504~506의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 아미노산 위치가 히스티딘으로 치환된 서열번호 504, 서열번호 505, 및 서열번호 506의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 507~509의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 아미노산 위치가 히스티딘으로 치환된 서열번호 507, 서열번호 508, 및 서열번호 509의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 504~506의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 아미노산 위치가 히스티딘으로 치환된 서열번호 504, 서열번호 505, 및 서열번호 506의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인; 및 서열번호 507~509의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 아미노산 위치가 히스티딘으로 치환된 서열번호 507, 서열번호 508, 및 서열번호 509의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은, 서열번호 502와 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 27, 29, 30, 32, 33, 34, 50, 51, 52, 53, 57, 59, 98, 100, 101, 102, 103, 106, 및 107로 이루어진 군으로부터 선택된 서열번호 502 내 하나 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은, 서열번호 503과 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 25, 29, 31, 32, 33, 34, 35, 52, 55, 91, 92, 93, 94, 95, 96, 97, 및 98로 이루어진 군으로부터 선택된 서열번호 305 내 하나 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하는 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 다음을 포함한다: 서열번호 502와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 27, 29, 30, 32, 33, 34, 50, 51, 52, 53, 57, 59, 98, 100, 101, 102, 103, 106, 및 107로 이루어진 군으로부터 선택된 서열번호 502 내 하나 이상의 (예를 들어 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하는 중쇄 가변 도메인; 및 서열번호 503과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 25, 29, 31, 32, 33, 34, 35, 52, 55, 91, 92, 93, 94, 95, 96, 97, 및 98로 이루어진 군으로부터 선택된 서열번호 305 내 하나 이상의 (예를 들어 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하는, 경쇄 가변 도메인.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은, 서열번호 502와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 서열번호 502 내 위치 35에서 알라닌을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 다음을 포함한다: 서열번호 502와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 서열번호 502 내 위치 35에서 알라닌을 포함하는, 중쇄 가변 도메인; 및 서열번호 503과 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 25, 29, 31, 32, 33, 34, 35, 52, 55, 91, 92, 93, 94, 95, 96, 97, 및 98로 이루어진 군으로부터 선택된 서열번호 503 내 하나 이상의 (예를 들어 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하는, 경쇄 가변 도메인.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은, 서열번호 502와 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 27, 29, 30, 32, 33, 34, 50, 51, 52, 53, 57, 59, 98, 100, 101, 102, 103, 106, 및 107로 이루어진 군으로부터 선택된 서열번호 502 내 하나 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하고, 서열번호 52 내 위치 35에서 알라닌을 포함하는 중쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 다음을 포함한다: 서열번호 502와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 27, 29, 30, 32, 33, 34, 50, 51, 52, 53, 57, 59, 98, 100, 101, 102, 103, 106, 및 107로 이루어진 군으로부터 선택된 서열번호 502 내 하나 이상의 (예를 들어 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하고, 서열번호 502 내 위치 35에서 알라닌을 포함하는, 중쇄 가변 도메인; 및 서열번호 503과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 25, 29, 31, 32, 33, 34, 35, 52, 55, 91, 92, 93, 94, 95, 96, 97, 및 98로 이루어진 군으로부터 선택된 서열번호 503 내 하나 이상의 (예를 들어 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 아미노산 위치에서 히스티딘을 포함하는, 경쇄 가변 도메인.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 중쇄 가변 도메인은, 서열번호 502와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 7에 열거된 서열번호 502 내 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 경쇄 가변 도메인은 서열번호 503과 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 표 8에 열거된 서열번호 503 내 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 502와 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 7에 열거된 서열번호 502의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인; 및 서열번호 503과 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 경쇄 가변 도메인으로서, 표 8에 열거된 서열번호 503의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 503을 포함하는 경쇄 가변 도메인; 및 서열번호 502와 적어도 90%(예를 들어, 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 7에 열거된 서열번호 502의 하나 이상의(예를 들어 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 503과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 503의 위치 25에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 502와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 7에 열거된 서열번호 502의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 503과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 503의 위치 29에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 502와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 7에 열거된 서열번호 502의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 503과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 503의 위치 31에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 502와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 7에 열거된 서열번호 502의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 503과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 503의 위치 32에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 502와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 7에 열거된 서열번호 502의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 503과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 503의 위치 33에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 502와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 7에 열거된 서열번호 502의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 503과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 503의 위치 34에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 502와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 7에 열거된 서열번호 502의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 503과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 503의 위치 35에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 502와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 7에 열거된 서열번호 502의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 503과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 503의 위치 52에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 502와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 7에 열거된 서열번호 502의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 503과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 503의 위치 55에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 502와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 7에 열거된 서열번호 502의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 503과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 503의 위치 91에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 502와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 7에 열거된 서열번호 502의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 503과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 503의 위치 92에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 502와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 7에 열거된 서열번호 502의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 503과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 503의 위치 93에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 502와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 7에 열거된 서열번호 502의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 503과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 503의 위치 94에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 502와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 7에 열거된 서열번호 502의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 503과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 503의 위치 95에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 502와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 7에 열거된 서열번호 502의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 503과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 503의 위치 96에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 502와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 7에 열거된 서열번호 502의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 503과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 503의 위치 97에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 502와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 7에 열거된 서열번호 502의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은: 서열번호 503과 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 503의 위치 98에서 히스티딘을 포함하는 경쇄 가변 도메인; 및 서열번호 502와 적어도 90%(예를 들어 적어도 92%, 적어도 94%, 적어도 96%, 적어도 98%, 적어도 99%, 또는 100%) 동일한 중쇄 가변 도메인으로서, 표 7에 열거된 서열번호 502의 하나 이상의 아미노산 위치의 특정 조합 중 어느 하나에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 하나 이상의 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 히스티딘이 알라닌으로 치환된 P3D12의 중쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 하나 이상의 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 히스티딘이 알라닌으로 치환된 P3D12의 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 하나 이상의 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 히스티딘이 알라닌으로 치환된 P3D12의 중쇄 가변 도메인; 및 하나 이상의 (예를 들어, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 또는 20개의) 히스티딘(들)이 알라닌으로 치환된 P3D12의 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, P3D12의 중쇄 가변 도메인은 서열번호 502를 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, P3D12의 경쇄 가변 도메인은 서열번호 503을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은, 서열번호 504~506의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 히스티딘(들)이 알라닌으로 치환된 서열번호 504, 서열번호 505, 및 서열번호 506의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 507~509의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20개의) 히스티딘(들)이 알라닌으로 치환된 서열번호 507, 서열번호 508, 및 서열번호 509의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 504~506의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 히스티딘(들)이 알라닌으로 치환된 서열번호 504, 서열번호 505, 및 서열번호 506의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인; 및 서열번호 507~509의 전체적으로 총 1개 이상의 (예를 들어 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의) 히스티딘(들)이 알라닌으로 치환된 서열번호 507, 서열번호 508, 및 서열번호 509의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548의 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 503, 549, 550, 551, 552, 553, 554, 555, 556, 557, 558, 559, 560, 561, 562, 563, 564, 565, 566, 567, 568, 569, 570, 571, 572, 573, 574, 575, 또는 576의 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 503을 포함하는 경쇄 가변 도메인, 및 서열번호 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 549를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 550을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 551을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 552를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 553을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 554를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 555를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 556을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 557을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 558을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 559를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 560을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 561을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 562를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 563을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 564를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 565를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 566을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 567을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 568을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 569를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 570을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 571을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 572를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 573을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 574를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 575를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 576을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 또는 548을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 503을 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 549를 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 550을 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 551을 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 552를 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 553을 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 554를 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 555를 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 556을 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 557을 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 558을 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 559를 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 560을 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 561을 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 562를 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 563을 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 564를 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 565를 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 566을 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 567을 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 568을 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 569를 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 570을 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 571을 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 572를 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 573을 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 574를 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 575를 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 576을 포함하는 경쇄 가변 도메인, 및 서열번호 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 제1 항원 결합 도메인은 서열번호 697, 698, 699, 700, 701, 702, 703, 704, 705, 706, 707, 708, 709, 710, 711, 712, 713, 714, 715, 716, 717, 718, 719, 720, 721, 722, 723, 724, 725, 726, 727, 728, 729, 730, 731, 732, 733, 734, 735, 736, 737, 738, 739, 740, 741, 742, 743, 744, 745, 746, 747, 748, 749, 750, 751, 752, 753, 754, 755, 756, 757, 758, 759, 760, 761, 762, 763, 764, 765, 766, 767, 768, 769, 770, 771, 772, 773, 774, 775, 776, 777, 778, 779, 780, 781, 782, 783, 784, 785, 786, 787, 788, 789, 또는 790을 포함하는 경쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 503을 포함하는 경쇄 가변 도메인, 및 서열번호 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 697을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 698을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 699를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 700을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 701을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 702를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 703을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 704를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 705를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 706을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 707을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 708을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 709를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 710을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 711을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 712를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 713을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 714를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 715를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 716을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 717을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 718을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 719를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 720을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 721을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 722를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 723을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 724를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 725를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 726을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 727을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 728을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 729를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 730을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 731을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 732를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 733을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 734를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 735를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 736을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 737을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 738을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 739를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 740을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 741을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 742를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 743을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 744를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 745를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 746을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 747을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 748을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 749를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 750을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 751을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 752를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 753을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 754를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 755를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 756을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 757을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 758을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 759를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 760을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 761을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 762를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 763을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 764를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 765를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 766을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 767을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 768을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 769를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 770을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 771을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 772를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 773을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 774를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다. 본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 775를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 776을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 777을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 778을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 779를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 780을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 781을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 782를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 783을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 784를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 785를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 786을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 787을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 788을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 789를 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 예시에서, 제1 항원 결합 도메인은 서열번호 790을 포함하는 경쇄 가변 도메인, 및 서열번호 502, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 520, 521, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 534, 535, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 577, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 621, 622, 623, 624, 625, 626, 627, 628, 629, 630, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 643, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 654, 655, 656, 657, 658, 659, 660, 661, 662, 663, 664, 665, 666, 667, 668, 669, 670, 671, 672, 673, 674, 675, 676, 677, 678, 679, 680, 681, 682, 683, 684, 685, 686, 687, 688, 689, 690, 691, 692, 693, 694, 695, 또는 696을 포함하는 중쇄 가변 도메인을 포함한다.
또한, 본원에 기술된 ABPC 중 어느 하나를 포함하는 약학적 조성물이 본원에 제공된다. 또한, 치료를 필요로 하는 대상체에서 대상체를 치료하는 방법이 본원에 제공되며, 상기 방법은 본원에 기술된 ABPC 중 어느 하나의 치료적 유효량을 대상체에게 투여하는 단계를 포함한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, ABPC를 (예를 들어 본원에 기술된 ABPC 중 어느 하나를) 포함하는 조성물은 동일한 양의 대조군 ABPC (예를 들어 본원에 기술된 예시적인 대조군 ABPC 중 어느 하나)를 포함하는 조성물과 비교했을 때, 표적 포유류 세포에서 (본원에 기술된 표적 포유류 세포 중 어느 하나에서) 독소 유리를 증가시킬 수 (예를 들어 검출 가능하게 증가시킬 수) (예를 들어 적어도 1% 증가, 적어도 2% 증가, 적어도 5% 증가, 적어도 10% 증가, 적어도 15% 증가, 적어도 20% 증가, 적어도 25% 증가, 적어도 30% 증가, 적어도 35% 증가, 적어도 40% 증가, 적어도 45% 증가, 적어도 50% 증가, 적어도 55% 증가, 적어도 60% 증가, 적어도 65% 증가, 적어도 70% 증가, 적어도 75% 증가, 적어도 80% 증가, 적어도 85% 증가, 적어도 90% 증가, 적어도 95% 증가, 적어도 100% 증가, 적어도 120% 증가, 적어도 140% 증가, 적어도 160% 증가, 적어도 180% 증가, 적어도 200% 증가, 적어도 250% 증가, 적어도 300% 증가, 적어도 350% 증가, 적어도 400% 증가, 적어도 450% 증가, 적어도 500% 증가, 적어도 1,000% 증가, 적어도 2,000% 증가, 적어도 3,000% 증가, 적어도 4,000% 증가, 적어도 5,000% 증가, 적어도 6,000% 증가, 적어도 7,000% 증가, 적어도 8,000% 증가, 적어도 9,000% 증가, 또는 적어도 10,000% 증가, 또는 약 1% 증가 내지 약 10,000% 증가, 약 1% 증가 내지 약 9,000% 증가, 약 1% 증가 내지 약 8,000% 증가, 약 1% 증가 내지 약 7,000% 증가, 약 1% 증가 내지 약 6,000% 증가, 약 1% 증가 내지 약 5,000% 증가, 약 1% 증가 내지 약 4,000% 증가, 약 1% 증가 내지 약 3,000% 증가, 약 1% 증가 내지 약 2,000% 증가, 약 1% 증가 내지 약 1,000% 증가, 약 1% 증가 내지 약 500% 증가, 약 1% 증가 내지 약 450% 증가, 약 1% 증가 내지 약 400% 증가, 약 1% 증가 내지 약 350% 증가, 약 1% 증가 내지 약 300% 증가, 약 1% 증가 내지 약 250% 증가, 약 1% 증가 내지 약 200% 증가, 약 1% 증가 내지 약 180% 증가, 약 1% 증가 내지 약 160% 증가, 약 1% 증가 내지 약 140% 증가, 약 1% 증가 내지 약 120% 증가, 약 1% 증가 내지 약 100% 증가, 약 1% 증가 내지 약 95% 증가, 약 1% 증가 내지 약 90% 증가, 약 1% 증가 내지 약 85% 증가, 약 1% 증가 내지 약 80% 증가, 약 1% 증가 내지 약 75% 증가, 약 1% 증가 내지 약 70% 증가, 약 1% 증가 내지 약 65% 증가, 약 1% 증가 내지 약 60% 증가, 약 1% 증가 내지 약 55% 증가, 약 1% 증가 내지 약 50% 증가, 약 1% 증가 내지 약 45% 증가, 약 1% 증가 내지 약 40% 증가, 약 1% 증가 내지 약 35% 증가, 약 1% 증가 내지 약 25% 증가, 약 1% 증가 내지 약 20% 증가, 약 1% 증가 내지 약 15% 증가, 약 1% 증가 내지 약 10% 증가, 약 1% 증가 내지 약 5% 증가, 약 2% 증가 내지 약 10,000% 증가, 약 2% 증가 내지 약 9,000% 증가, 약 2% 증가 내지 약 8,000% 증가, 약 2% 증가 내지 약 7,000% 증가, 약 2% 증가 내지 약 6,000% 증가, 약 2% 증가 내지 약 5,000% 증가, 약 2% 증가 내지 약 4,000% 증가, 약 2% 증가 내지 약 3,000% 증가, 약 2% 증가 내지 약 2,000% 증가, 약 2% 증가 내지 약 1,000% 증가, 약 2% 증가 내지 약 500% 증가, 약 2% 증가 내지 약 450% 증가, 약 2% 증가 내지 약 400% 증가, 약 2% 증가 내지 약 350% 증가, 약 2% 증가 내지 약 300% 증가, 약 2% 증가 내지 약 250% 증가, 약 2% 증가 내지 약 200% 증가, 약 2% 증가 내지 약 180% 증가, 약 2% 증가 내지 약 160% 증가, 약 2% 증가 내지 약 140% 증가, 약 2% 증가 내지 약 120% 증가, 약 2% 증가 내지 약 100% 증가, 약 2% 증가 내지 약 95% 증가, 약 2% 증가 내지 약 90% 증가, 약 2% 증가 내지 약 85% 증가, 약 2% 증가 내지 약 80% 증가, 약 2% 증가 내지 약 75% 증가, 약 2% 증가 내지 약 70% 증가, 약 2% 증가 내지 약 65% 증가, 약 2% 증가 내지 약 60% 증가, 약 2% 증가 내지 약 55% 증가, 약 2% 증가 내지 약 50% 증가, 약 2% 증가 내지 약 45% 증가, 약 2% 증가 내지 약 40% 증가, 약 2% 증가 내지 약 35% 증가, 약 2% 증가 내지 약 25% 증가, 약 2% 증가 내지 약 20% 증가, 약 2% 증가 내지 약 15% 증가, 약 2% 증가 내지 약 10% 증가, 약 2% 증가 내지 약 5% 증가, 약 5% 증가 내지 약 10,000% 증가, 약 5% 증가 내지 약 9,000% 증가, 약 5% 증가 내지 약 8,000% 증가, 약 5% 증가 내지 약 7,000% 증가, 약 5% 증가 내지 약 6,000% 증가, 약 5% 증가 내지 약 5,000% 증가, 약 5% 증가 내지 약 4,000% 증가, 약 5% 증가 내지 약 3,000% 증가, 약 5% 증가 내지 약 2,000% 증가, 약 5% 증가 내지 약 1,000% 증가, 약 5% 증가 내지 약 500% 증가, 약 5% 증가 내지 약 450% 증가, 약 5% 증가 내지 약 400% 증가, 약 5% 증가 내지 약 350% 증가, 약 5% 증가 내지 약 300% 증가, 약 5% 증가 내지 약 250% 증가, 약 5% 증가 내지 약 200% 증가, 약 5% 증가 내지 약 180% 증가, 약 5% 증가 내지 약 160% 증가, 약 5% 증가 내지 약 140% 증가, 약 5% 증가 내지 약 120% 증가, 약 5% 증가 내지 약 100% 증가, 약 5% 증가 내지 약 95% 증가, 약 5% 증가 내지 약 90% 증가, 약 5% 증가 내지 약 85% 증가, 약 5% 증가 내지 약 80% 증가, 약 5% 증가 내지 약 75% 증가, 약 5% 증가 내지 약 70% 증가, 약 5% 증가 내지 약 65% 증가, 약 5% 증가 내지 약 60% 증가, 약 5% 증가 내지 약 55% 증가, 약 5% 증가 내지 약 50% 증가, 약 5% 증가 내지 약 45% 증가, 약 5% 증가 내지 약 40% 증가, 약 5% 증가 내지 약 35% 증가, 약 5% 증가 내지 약 25% 증가, 약 5% 증가 내지 약 20% 증가, 약 5% 증가 내지 약 15% 증가, 약 5% 증가 내지 약 10% 증가, 약 10% 증가 내지 약 10,000% 증가, 약 10% 증가 내지 약 9,000% 증가, 약 10% 증가 내지 약 8,000% 증가, 약 10% 증가 내지 약 7,000% 증가, 약 10% 증가 내지 약 6,000% 증가, 약 10% 증가 내지 약 5,000% 증가, 약 10% 증가 내지 약 4,000% 증가, 약 10% 증가 내지 약 3,000% 증가, 약 10% 증가 내지 약 2,000% 증가, 약 10% 증가 내지 약 1,000% 증가, 약 10% 증가 내지 약 500% 증가, 약 10% 증가 내지 약 450% 증가, 약 10% 증가 내지 약 400% 증가, 약 10% 증가 내지 약 350% 증가, 약 10% 증가 내지 약 300% 증가, 약 10% 증가 내지 약 250% 증가, 약 10% 증가 내지 약 200% 증가, 약 10% 증가 내지 약 180% 증가, 약 10% 증가 내지 약 160% 증가, 약 10% 증가 내지 약 140% 증가, 약 10% 증가 내지 약 120% 증가, 약 10% 증가 내지 약 100% 증가, 약 10% 증가 내지 약 95% 증가, 약 10% 증가 내지 약 90% 증가, 약 10% 증가 내지 약 85% 증가, 약 10% 증가 내지 약 80% 증가, 약 10% 증가 내지 약 75% 증가, 약 10% 증가 내지 약 70% 증가, 약 10% 증가 내지 약 65% 증가, 약 10% 증가 내지 약 60% 증가, 약 10% 증가 내지 약 55% 증가, 약 10% 증가 내지 약 50% 증가, 약 10% 증가 내지 약 45% 증가, 약 10% 증가 내지 약 40% 증가, 약 10% 증가 내지 약 35% 증가, 약 10% 증가 내지 약 30% 증가, 약 10% 증가 내지 약 25% 증가, 약 10% 증가 내지 약 20% 증가, 약 10% 증가 내지 약 15% 증가, 약 15% 증가 내지 약 10,000% 증가, 약 15% 증가 내지 약 9,000% 증가, 약 15% 증가 내지 약 8,000% 증가, 약 15% 증가 내지 약 7,000% 증가, 약 15% 증가 내지 약 6,000% 증가, 약 15% 증가 내지 약 5,000% 증가, 약 15% 증가 내지 약 4,000% 증가, 약 15% 증가 내지 약 3,000% 증가, 약 15% 증가 내지 약 2,000% 증가, 약 15% 증가 내지 약 1,000% 증가, 약 15% 증가 내지 약 500% 증가, 약 15% 증가 내지 약 450% 증가, 약 15% 증가 내지 약 400% 증가, 약 15% 증가 내지 약 350% 증가, 약 15% 증가 내지 약 300% 증가, 약 15% 증가 내지 약 250% 증가, 약 15% 증가 내지 약 200% 증가, 약 15% 증가 내지 약 180% 증가, 약 15% 증가 내지 약 160% 증가, 약 15% 증가 내지 약 140% 증가, 약 15% 증가 내지 약 120% 증가, 약 15% 증가 내지 약 100% 증가, 약 15% 증가 내지 약 95% 증가, 약 15% 증가 내지 약 90% 증가, 약 15% 증가 내지 약 85% 증가, 약 15% 증가 내지 약 80% 증가, 약 15% 증가 내지 약 75% 증가, 약 15% 증가 내지 약 70% 증가, 약 15% 증가 내지 약 65% 증가, 약 15% 증가 내지 약 60% 증가, 약 15% 증가 내지 약 55% 증가, 약 15% 증가 내지 약 50% 증가, 약 15% 증가 내지 약 45% 증가, 약 15% 증가 내지 약 40% 증가, 약 15% 증가 내지 약 35% 증가, 약 15% 증가 내지 약 30% 증가, 약 15% 증가 내지 약 25% 증가, 약 15% 증가 내지 약 20% 증가, 약 20% 증가 내지 약 10,000% 증가, 약 20% 증가 내지 약 9,000% 증가, 약 20% 증가 내지 약 8,000% 증가, 약 20% 증가 내지 약 7,000% 증가, 약 20% 증가 내지 약 6,000% 증가, 약 20% 증가 내지 약 5,000% 증가, 약 20% 증가 내지 약 4,000% 증가, 약 20% 증가 내지 약 3,000% 증가, 약 20% 증가 내지 약 2,000% 증가, 약 20% 증가 내지 약 1,000% 증가, 약 20% 증가 내지 약 500% 증가, 약 20% 증가 내지 약 450% 증가, 약 20% 증가 내지 약 400% 증가, 약 20% 증가 내지 약 350% 증가, 약 20% 증가 내지 약 300% 증가, 약 20% 증가 내지 약 250% 증가, 약 20% 증가 내지 약 200% 증가, 약 20% 증가 내지 약 180% 증가, 약 20% 증가 내지 약 160% 증가, 약 20% 증가 내지 약 140% 증가, 약 20% 증가 내지 약 120% 증가, 약 20% 증가 내지 약 100% 증가, 약 20% 증가 내지 약 95% 증가, 약 20% 증가 내지 약 90% 증가, 약 20% 증가 내지 약 85% 증가, 약 20% 증가 내지 약 80% 증가, 약 20% 증가 내지 약 75% 증가, 약 20% 증가 내지 약 70% 증가, 약 20% 증가 내지 약 65% 증가, 약 20% 증가 내지 약 60% 증가, 약 20% 증가 내지 약 55% 증가, 약 20% 증가 내지 약 50% 증가, 약 20% 증가 내지 약 45% 증가, 약 20% 증가 내지 약 40% 증가, 약 20% 증가 내지 약 35% 증가, 약 20% 증가 내지 약 30% 증가, 약 20% 증가 내지 약 25% 증가, 약 25% 증가 내지 약 10,000% 증가, 약 25% 증가 내지 약 9,000% 증가, 약 25% 증가 내지 약 8,000% 증가, 약 25% 증가 내지 약 7,000% 증가, 약 25% 증가 내지 약 6,000% 증가, 약 25% 증가 내지 약 5,000% 증가, 약 25% 증가 내지 약 4,000% 증가, 약 25% 증가 내지 약 3,000% 증가, 약 25% 증가 내지 약 2,000% 증가, 약 25% 증가 내지 약 1,000% 증가, 약 25% 증가 내지 약 500% 증가, 약 25% 증가 내지 약 450% 증가, 약 25% 증가 내지 약 400% 증가, 약 25% 증가 내지 약 350% 증가, 약 25% 증가 내지 약 300% 증가, 약 25% 증가 내지 약 250% 증가, 약 25% 증가 내지 약 200% 증가, 약 25% 증가 내지 약 180% 증가, 약 25% 증가 내지 약 160% 증가, 약 25% 증가 내지 약 140% 증가, 약 25% 증가 내지 약 120% 증가, 약 25% 증가 내지 약 100% 증가, 약 25% 증가 내지 약 95% 증가, 약 25% 증가 내지 약 90% 증가, 약 25% 증가 내지 약 85% 증가, 약 25% 증가 내지 약 80% 증가, 약 25% 증가 내지 약 75% 증가, 약 25% 증가 내지 약 70% 증가, 약 25% 증가 내지 약 65% 증가, 약 25% 증가 내지 약 60% 증가, 약 25% 증가 내지 약 55% 증가, 약 25% 증가 내지 약 50% 증가, 약 25% 증가 내지 약 45% 증가, 약 25% 증가 내지 약 40% 증가, 약 25% 증가 내지 약 35% 증가, 약 25% 증가 내지 약 30% 증가, 약 30% 증가 내지 약 10,000% 증가, 약 30% 증가 내지 약 9,000% 증가, 약 30% 증가 내지 약 8,000% 증가, 약 30% 증가 내지 약 7,000% 증가, 약 30% 증가 내지 약 6,000% 증가, 약 30% 증가 내지 약 5,000% 증가, 약 30% 증가 내지 약 4,000% 증가, 약 30% 증가 내지 약 3,000% 증가, 약 30% 증가 내지 약 2,000% 증가, 약 30% 증가 내지 약 1,000% 증가, 약 30% 증가 내지 약 500% 증가, 약 30% 증가 내지 약 450% 증가, 약 30% 증가 내지 약 400% 증가, 약 30% 증가 내지 약 350% 증가, 약 30% 증가 내지 약 300% 증가, 약 30% 증가 내지 약 250% 증가, 약 30% 증가 내지 약 200% 증가, 약 30% 증가 내지 약 180% 증가, 약 30% 증가 내지 약 160% 증가, 약 30% 증가 내지 약 140% 증가, 약 30% 증가 내지 약 120% 증가, 약 30% 증가 내지 약 100% 증가, 약 30% 증가 내지 약 95% 증가, 약 30% 증가 내지 약 90% 증가, 약 30% 증가 내지 약 85% 증가, 약 30% 증가 내지 약 80% 증가, 약 30% 증가 내지 약 75% 증가, 약 30% 증가 내지 약 70% 증가, 약 30% 증가 내지 약 65% 증가, 약 30% 증가 내지 약 60% 증가, 약 30% 증가 내지 약 55% 증가, 약 30% 증가 내지 약 50% 증가, 약 30% 증가 내지 약 45% 증가, 약 30% 증가 내지 약 40% 증가, 약 30% 증가 내지 약 35% 증가, 약 35% 증가 내지 약 10,000% 증가, 약 35% 증가 내지 약 9,000% 증가, 약 35% 증가 내지 약 8,000% 증가, 약 35% 증가 내지 약 7,000% 증가, 약 35% 증가 내지 약 6,000% 증가, 약 35% 증가 내지 약 5,000% 증가, 약 35% 증가 내지 약 4,000% 증가, 약 35% 증가 내지 약 3,000% 증가, 약 35% 증가 내지 약 2,000% 증가, 약 35% 증가 내지 약 1,000% 증가, 약 35% 증가 내지 약 500% 증가, 약 35% 증가 내지 약 450% 증가, 약 35% 증가 내지 약 400% 증가, 약 35% 증가 내지 약 350% 증가, 약 35% 증가 내지 약 300% 증가, 약 35% 증가 내지 약 250% 증가, 약 35% 증가 내지 약 200% 증가, 약 35% 증가 내지 약 180% 증가, 약 35% 증가 내지 약 160% 증가, 약 35% 증가 내지 약 140% 증가, 약 35% 증가 내지 약 120% 증가, 약 35% 증가 내지 약 100% 증가, 약 35% 증가 내지 약 95% 증가, 약 35% 증가 내지 약 90% 증가, 약 35% 증가 내지 약 85% 증가, 약 35% 증가 내지 약 80% 증가, 약 35% 증가 내지 약 75% 증가, 약 35% 증가 내지 약 70% 증가, 약 35% 증가 내지 약 65% 증가, 약 35% 증가 내지 약 60% 증가, 약 35% 증가 내지 약 55% 증가, 약 35% 증가 내지 약 50% 증가, 약 35% 증가 내지 약 45% 증가, 약 35% 증가 내지 약 40% 증가, 약 40% 증가 내지 약 10,000% 증가, 약 40% 증가 내지 약 9,000% 증가, 약 40% 증가 내지 약 8,000% 증가, 약 40% 증가 내지 약 7,000% 증가, 약 40% 증가 내지 약 6,000% 증가, 약 40% 증가 내지 약 5,000% 증가, 약 40% 증가 내지 약 4,000% 증가, 약 40% 증가 내지 약 3,000% 증가, 약 40% 증가 내지 약 2,000% 증가, 약 40% 증가 내지 약 1,000% 증가, 약 40% 증가 내지 약 500% 증가, 약 40% 증가 내지 약 450% 증가, 약 40% 증가 내지 약 400% 증가, 약 40% 증가 내지 약 350% 증가, 약 40% 증가 내지 약 300% 증가, 약 40% 증가 내지 약 250% 증가, 약 40% 증가 내지 약 200% 증가, 약 40% 증가 내지 약 180% 증가, 약 40% 증가 내지 약 160% 증가, 약 40% 증가 내지 약 140% 증가, 약 40% 증가 내지 약 120% 증가, 약 40% 증가 내지 약 100% 증가, 약 40% 증가 내지 약 95% 증가, 약 40% 증가 내지 약 90% 증가, 약 40% 증가 내지 약 85% 증가, 약 40% 증가 내지 약 80% 증가, 약 40% 증가 내지 약 75% 증가, 약 40% 증가 내지 약 70% 증가, 약 40% 증가 내지 약 65% 증가, 약 40% 증가 내지 약 60% 증가, 약 40% 증가 내지 약 55% 증가, 약 40% 증가 내지 약 50% 증가, 약 40% 증가 내지 약 45% 증가, 약 45% 증가 내지 약 10,000% 증가, 약 45% 증가 내지 약 9,000% 증가, 약 45% 증가 내지 약 8,000% 증가, 약 45% 증가 내지 약 7,000% 증가, 약 45% 증가 내지 약 6,000% 증가, 약 45% 증가 내지 약 5,000% 증가, 약 45% 증가 내지 약 4,000% 증가, 약 45% 증가 내지 약 3,000% 증가, 약 45% 증가 내지 약 2,000% 증가, 약 45% 증가 내지 약 1,000% 증가, 약 45% 증가 내지 약 500% 증가, 약 45% 증가 내지 약 450% 증가, 약 45% 증가 내지 약 400% 증가, 약 45% 증가 내지 약 350% 증가, 약 45% 증가 내지 약 300% 증가, 약 45% 증가 내지 약 250% 증가, 약 45% 증가 내지 약 200% 증가, 약 45% 증가 내지 약 180% 증가, 약 45% 증가 내지 약 160% 증가, 약 45% 증가 내지 약 140% 증가, 약 45% 증가 내지 약 120% 증가, 약 45% 증가 내지 약 100% 증가, 약 45% 증가 내지 약 95% 증가, 약 45% 증가 내지 약 90% 증가, 약 45% 증가 내지 약 85% 증가, 약 45% 증가 내지 약 80% 증가, 약 45% 증가 내지 약 75% 증가, 약 45% 증가 내지 약 70% 증가, 약 45% 증가 내지 약 65% 증가, 약 45% 증가 내지 약 60% 증가, 약 45% 증가 내지 약 55% 증가, 약 45% 증가 내지 약 50% 증가, 약 50% 증가 내지 약 10,000% 증가, 약 50% 증가 내지 약 9,000% 증가, 약 50% 증가 내지 약 8,000% 증가, 약 50% 증가 내지 약 7,000% 증가, 약 50% 증가 내지 약 6,000% 증가, 약 50% 증가 내지 약 5,000% 증가, 약 50% 증가 내지 약 4,000% 증가, 약 50% 증가 내지 약 3,000% 증가, 약 50% 증가 내지 약 2,000% 증가, 약 50% 증가 내지 약 1,000% 증가, 약 50% 증가 내지 약 500% 증가, 약 50% 증가 내지 약 450% 증가, 약 50% 증가 내지 약 400% 증가, 약 50% 증가 내지 약 350% 증가, 약 50% 증가 내지 약 300% 증가, 약 50% 증가 내지 약 250% 증가, 약 50% 증가 내지 약 200% 증가, 약 50% 증가 내지 약 180% 증가, 약 50% 증가 내지 약 160% 증가, 약 50% 증가 내지 약 140% 증가, 약 50% 증가 내지 약 120% 증가, 약 50% 증가 내지 약 100% 증가, 약 50% 증가 내지 약 95% 증가, 약 50% 증가 내지 약 90% 증가, 약 50% 증가 내지 약 85% 증가, 약 50% 증가 내지 약 80% 증가, 약 50% 증가 내지 약 75% 증가, 약 50% 증가 내지 약 70% 증가, 약 50% 증가 내지 약 65% 증가, 약 50% 증가 내지 약 60% 증가, 약 50% 증가 내지 약 55% 증가, 약 55% 증가 내지 약 10,000% 증가, 약 55% 증가 내지 약 9,000% 증가, 약 55% 증가 내지 약 8,000% 증가, 약 55% 증가 내지 약 7,000% 증가, 약 55% 증가 내지 약 6,000% 증가, 약 55% 증가 내지 약 5,000% 증가, 약 55% 증가 내지 약 4,000% 증가, 약 55% 증가 내지 약 3,000% 증가, 약 55% 증가 내지 약 2,000% 증가, 약 55% 증가 내지 약 1,000% 증가, 약 55% 증가 내지 약 500% 증가, 약 55% 증가 내지 약 450% 증가, 약 55% 증가 내지 약 400% 증가, 약 55% 증가 내지 약 350% 증가, 약 55% 증가 내지 약 300% 증가, 약 55% 증가 내지 약 250% 증가, 약 55% 증가 내지 약 200% 증가, 약 55% 증가 내지 약 180% 증가, 약 55% 증가 내지 약 160% 증가, 약 55% 증가 내지 약 140% 증가, 약 55% 증가 내지 약 120% 증가, 약 55% 증가 내지 약 100% 증가, 약 55% 증가 내지 약 95% 증가, 약 55% 증가 내지 약 90% 증가, 약 55% 증가 내지 약 85% 증가, 약 55% 증가 내지 약 80% 증가, 약 55% 증가 내지 약 75% 증가, 약 55% 증가 내지 약 70% 증가, 약 55% 증가 내지 약 65% 증가, 약 55% 증가 내지 약 60% 증가, 약 60% 증가 내지 약 10,000% 증가, 약 60% 증가 내지 약 9,000% 증가, 약 60% 증가 내지 약 8,000% 증가, 약 60% 증가 내지 약 7,000% 증가, 약 60% 증가 내지 약 6,000% 증가, 약 60% 증가 내지 약 5,000% 증가, 약 60% 증가 내지 약 4,000% 증가, 약 60% 증가 내지 약 3,000% 증가, 약 60% 증가 내지 약 2,000% 증가, 약 60% 증가 내지 약 1,000% 증가, 약 60% 증가 내지 약 500% 증가, 약 60% 증가 내지 약 450% 증가, 약 60% 증가 내지 약 400% 증가, 약 60% 증가 내지 약 350% 증가, 약 60% 증가 내지 약 300% 증가, 약 60% 증가 내지 약 250% 증가, 약 60% 증가 내지 약 200% 증가, 약 60% 증가 내지 약 180% 증가, 약 60% 증가 내지 약 160% 증가, 약 60% 증가 내지 약 140% 증가, 약 60% 증가 내지 약 120% 증가, 약 60% 증가 내지 약 100% 증가, 약 60% 증가 내지 약 95% 증가, 약 60% 증가 내지 약 90% 증가, 약 60% 증가 내지 약 85% 증가, 약 60% 증가 내지 약 80% 증가, 약 60% 증가 내지 약 75% 증가, 약 60% 증가 내지 약 70% 증가, 약 60% 증가 내지 약 65% 증가, 약 65% 증가 내지 약 10,000% 증가, 약 65% 증가 내지 약 9,000% 증가, 약 65% 증가 내지 약 8,000% 증가, 약 65% 증가 내지 약 7,000% 증가, 약 65% 증가 내지 약 6,000% 증가, 약 65% 증가 내지 약 5,000% 증가, 약 65% 증가 내지 약 4,000% 증가, 약 65% 증가 내지 약 3,000% 증가, 약 65% 증가 내지 약 2,000% 증가, 약 65% 증가 내지 약 1,000% 증가, 약 65% 증가 내지 약 500% 증가, 약 65% 증가 내지 약 450% 증가, 약 65% 증가 내지 약 400% 증가, 약 65% 증가 내지 약 350% 증가, 약 65% 증가 내지 약 300% 증가, 약 65% 증가 내지 약 250% 증가, 약 65% 증가 내지 약 200% 증가, 약 65% 증가 내지 약 180% 증가, 약 65% 증가 내지 약 160% 증가, 약 65% 증가 내지 약 140% 증가, 약 65% 증가 내지 약 120% 증가, 약 65% 증가 내지 약 100% 증가, 약 65% 증가 내지 약 95% 증가, 약 65% 증가 내지 약 90% 증가, 약 65% 증가 내지 약 85% 증가, 약 65% 증가 내지 약 80% 증가, 약 65% 증가 내지 약 75% 증가, 약 65% 증가 내지 약 70% 증가, 약 70% 증가 내지 약 10,000% 증가, 약 70% 증가 내지 약 9,000% 증가, 약 70% 증가 내지 약 8,000% 증가, 약 70% 증가 내지 약 7,000% 증가, 약 70% 증가 내지 약 6,000% 증가, 약 70% 증가 내지 약 5,000% 증가, 약 70% 증가 내지 약 4,000% 증가, 약 70% 증가 내지 약 3,000% 증가, 약 70% 증가 내지 약 2,000% 증가, 약 70% 증가 내지 약 1,000% 증가, 약 70% 증가 내지 약 500% 증가, 약 70% 증가 내지 약 450% 증가, 약 70% 증가 내지 약 400% 증가, 약 70% 증가 내지 약 350% 증가, 약 70% 증가 내지 약 300% 증가, 약 70% 증가 내지 약 250% 증가, 약 70% 증가 내지 약 200% 증가, 약 70% 증가 내지 약 180% 증가, 약 70% 증가 내지 약 160% 증가, 약 70% 증가 내지 약 140% 증가, 약 70% 증가 내지 약 120% 증가, 약 70% 증가 내지 약 100% 증가, 약 70% 증가 내지 약 95% 증가, 약 70% 증가 내지 약 90% 증가, 약 70% 증가 내지 약 85% 증가, 약 70% 증가 내지 약 80% 증가, 약 70% 증가 내지 약 75% 증가, 약 75% 증가 내지 약 10,000% 증가, 약 75% 증가 내지 약 9,000% 증가, 약 75% 증가 내지 약 8,000% 증가, 약 75% 증가 내지 약 7,000% 증가, 약 75% 증가 내지 약 6,000% 증가, 약 75% 증가 내지 약 5,000% 증가, 약 75% 증가 내지 약 4,000% 증가, 약 75% 증가 내지 약 3,000% 증가, 약 75% 증가 내지 약 2,000% 증가, 약 75% 증가 내지 약 1,000% 증가, 약 75% 증가 내지 약 500% 증가, 약 75% 증가 내지 약 450% 증가, 약 75% 증가 내지 약 400% 증가, 약 75% 증가 내지 약 350% 증가, 약 75% 증가 내지 약 300% 증가, 약 75% 증가 내지 약 250% 증가, 약 75% 증가 내지 약 200% 증가, 약 75% 증가 내지 약 180% 증가, 약 75% 증가 내지 약 160% 증가, 약 75% 증가 내지 약 140% 증가, 약 75% 증가 내지 약 120% 증가, 약 75% 증가 내지 약 100% 증가, 약 75% 증가 내지 약 95% 증가, 약 75% 증가 내지 약 90% 증가, 약 75% 증가 내지 약 85% 증가, 약 75% 증가 내지 약 80%, 약 80% 증가 내지 약 10,000% 증가, 약 80% 증가 내지 약 9,000% 증가, 약 80% 증가 내지 약 8,000% 증가, 약 80% 증가 내지 약 7,000% 증가, 약 80% 증가 내지 약 6,000% 증가, 약 80% 증가 내지 약 5,000% 증가, 약 80% 증가 내지 약 4,000% 증가, 약 80% 증가 내지 약 3,000% 증가, 약 80% 증가 내지 약 2,000% 증가, 약 80% 증가 내지 약 1,000% 증가, 약 80% 증가 내지 약 500% 증가, 약 80% 증가 내지 약 450% 증가, 약 80% 증가 내지 약 400% 증가, 약 80% 증가 내지 약 350% 증가, 약 80% 증가 내지 약 300% 증가, 약 80% 증가 내지 약 250% 증가, 약 80% 증가 내지 약 200% 증가, 약 80% 증가 내지 약 180% 증가, 약 80% 증가 내지 약 160% 증가, 약 80% 증가 내지 약 140% 증가, 약 80% 증가 내지 약 120% 증가, 약 80% 증가 내지 약 100% 증가, 약 80% 증가 내지 약 95% 증가, 약 80% 증가 내지 약 90% 증가, 약 80% 증가 내지 약 85% 증가, 약 85% 증가 내지 약 10,000% 증가, 약 85% 증가 내지 약 9,000% 증가, 약 85% 증가 내지 약 8,000% 증가, 약 85% 증가 내지 약 7,000% 증가, 약 85% 증가 내지 약 6,000% 증가, 약 85% 증가 내지 약 5,000% 증가, 약 85% 증가 내지 약 4,000% 증가, 약 85% 증가 내지 약 3,000% 증가, 약 85% 증가 내지 약 2,000% 증가, 약 85% 증가 내지 약 1,000% 증가, 약 85% 증가 내지 약 500% 증가, 약 85% 증가 내지 약 450% 증가, 약 85% 증가 내지 약 400% 증가, 약 85% 증가 내지 약 350% 증가, 약 85% 증가 내지 약 300% 증가, 약 85% 증가 내지 약 250% 증가, 약 85% 증가 내지 약 200% 증가, 약 85% 증가 내지 약 180% 증가, 약 85% 증가 내지 약 160% 증가, 약 85% 증가 내지 약 140% 증가, 약 85% 증가 내지 약 120% 증가, 약 85% 증가 내지 약 100% 증가, 약 85% 증가 내지 약 95% 증가, 약 85% 증가 내지 약 90% 증가, 약 90% 증가 내지 약 10,000% 증가, 약 90% 증가 내지 약 9,000% 증가, 약 90% 증가 내지 약 8,000% 증가, 약 90% 증가 내지 약 7,000% 증가, 약 90% 증가 내지 약 6,000% 증가, 약 90% 증가 내지 약 5,000% 증가, 약 90% 증가 내지 약 4,000% 증가, 약 90% 증가 내지 약 3,000% 증가, 약 90% 증가 내지 약 2,000% 증가, 약 90% 증가 내지 약 1,000% 증가, 약 90% 증가 내지 약 500% 증가, 약 90% 증가 내지 약 450% 증가, 약 90% 증가 내지 약 400% 증가, 약 90% 증가 내지 약 350% 증가, 약 90% 증가 내지 약 300% 증가, 약 90% 증가 내지 약 250% 증가, 약 90% 증가 내지 약 200% 증가, 약 90% 증가 내지 약 180% 증가, 약 90% 증가 내지 약 160% 증가, 약 90% 증가 내지 약 140% 증가, 약 90% 증가 내지 약 120% 증가, 약 90% 증가 내지 약 100% 증가, 약 90% 증가 내지 약 95% 증가, 약 95% 증가 내지 약 10,000% 증가, 약 95% 증가 내지 약 9,000% 증가, 약 95% 증가 내지 약 8,000% 증가, 약 95% 증가 내지 약 7,000% 증가, 약 95% 증가 내지 약 6,000% 증가, 약 95% 증가 내지 약 5,000% 증가, 약 95% 증가 내지 약 4,000% 증가, 약 95% 증가 내지 약 3,000% 증가, 약 95% 증가 내지 약 2,000% 증가, 약 95% 증가 내지 약 1,000% 증가, 약 95% 증가 내지 약 500% 증가, 약 95% 증가 내지 약 450% 증가, 약 95% 증가 내지 약 400% 증가, 약 95% 증가 내지 약 350% 증가, 약 95% 증가 내지 약 300% 증가, 약 95% 증가 내지 약 250% 증가, 약 95% 증가 내지 약 200% 증가, 약 95% 증가 내지 약 180% 증가, 약 95% 증가 내지 약 160% 증가, 약 95% 증가 내지 약 140% 증가, 약 95% 증가 내지 약 120% 증가, 약 95% 증가 내지 약 100% 증가, 약 100% 증가 내지 약 10,000% 증가, 약 100% 증가 내지 약 9,000% 증가, 약 100% 증가 내지 약 8,000% 증가, 약 100% 증가 내지 약 7,000% 증가, 약 100% 증가 내지 약 6,000% 증가, 약 100% 증가 내지 약 5,000% 증가, 약 100% 증가 내지 약 4,000% 증가, 약 100% 증가 내지 약 3,000% 증가, 약 100% 증가 내지 약 2,000% 증가, 약 100% 증가 내지 약 1,000% 증가, 약 100% 증가 내지 약 500% 증가, 약 100% 증가 내지 약 450% 증가, 약 100% 증가 내지 약 400% 증가, 약 100% 증가 내지 약 350% 증가, 약 100% 증가 내지 약 300% 증가, 약 100% 증가 내지 약 250% 증가, 약 100% 증가 내지 약 200% 증가, 약 100% 증가 내지 약 180% 증가, 약 100% 증가 내지 약 160% 증가, 약 100% 증가 내지 약 140% 증가, 약 100% 증가 내지 약 120% 증가, 약 120% 증가 내지 약 10,000% 증가, 약 120% 증가 내지 약 9,000% 증가, 약 120% 증가 내지 약 8,000% 증가, 약 120% 증가 내지 약 7,000% 증가, 약 120% 증가 내지 약 6,000% 증가, 약 120% 증가 내지 약 5,000% 증가, 약 120% 증가 내지 약 4,000% 증가, 약 120% 증가 내지 약 3,000% 증가, 약 120% 증가 내지 약 2,000% 증가, 약 120% 증가 내지 약 1,000% 증가, 약 120% 증가 내지 약 500% 증가, 약 120% 증가 내지 약 450% 증가, 약 120% 증가 내지 약 400% 증가, 약 120% 증가 내지 약 350% 증가, 약 120% 증가 내지 약 300% 증가, 약 120% 증가 내지 약 250% 증가, 약 120% 증가 내지 약 200% 증가, 약 120% 증가 내지 약 180% 증가, 약 120% 증가 내지 약 160% 증가, 약 120% 증가 내지 약 140% 증가, 약 140% 증가 내지 약 10,000% 증가, 약 140% 증가 내지 약 9,000% 증가, 약 140% 증가 내지 약 8,000% 증가, 약 140% 증가 내지 약 7,000% 증가, 약 140% 증가 내지 약 6,000% 증가, 약 140% 증가 내지 약 5,000% 증가, 약 140% 증가 내지 약 4,000% 증가, 약 140% 증가 내지 약 3,000% 증가, 약 140% 증가 내지 약 2,000% 증가, 약 140% 증가 내지 약 1,000% 증가, 약 140% 증가 내지 약 500% 증가, 약 140% 증가 내지 약 450% 증가, 약 140% 증가 내지 약 400% 증가, 약 140% 증가 내지 약 350% 증가, 약 140% 증가 내지 약 300% 증가, 약 140% 증가 내지 약 250% 증가, 약 140% 증가 내지 약 200% 증가, 약 140% 증가 내지 약 180% 증가, 약 140% 증가 내지 약 160% 증가, 약 160% 증가 내지 약 10,000% 증가, 약 160% 증가 내지 약 9,000% 증가, 약 160% 증가 내지 약 8,000% 증가, 약 160% 증가 내지 약 7,000% 증가, 약 160% 증가 내지 약 6,000% 증가, 약 160% 증가 내지 약 5,000% 증가, 약 160% 증가 내지 약 4,000% 증가, 약 160% 증가 내지 약 3,000% 증가, 약 160% 증가 내지 약 2,000% 증가, 약 160% 증가 내지 약 1,000% 증가, 약 160% 증가 내지 약 500% 증가, 약 160% 증가 내지 약 450% 증가, 약 160% 증가 내지 약 400% 증가, 약 160% 증가 내지 약 350% 증가, 약 160% 증가 내지 약 300% 증가, 약 160% 증가 내지 약 250% 증가, 약 160% 증가 내지 약 200% 증가, 약 160% 증가 내지 약 180% 증가, 약 180% 증가 내지 약 10,000% 증가, 약 180% 증가 내지 약 9,000% 증가, 약 180% 증가 내지 약 8,000% 증가, 약 180% 증가 내지 약 7,000% 증가, 약 180% 증가 내지 약 6,000% 증가, 약 180% 증가 내지 약 5,000% 증가, 약 180% 증가 내지 약 4,000% 증가, 약 180% 증가 내지 약 3,000% 증가, 약 180% 증가 내지 약 2,000% 증가, 약 180% 증가 내지 약 1,000% 증가, 약 180% 증가 내지 약 500% 증가, 약 180% 증가 내지 약 450% 증가, 약 180% 증가 내지 약 400% 증가, 약 180% 증가 내지 약 350% 증가, 약 180% 증가 내지 약 300% 증가, 약 180% 증가 내지 약 250% 증가, 약 180% 증가 내지 약 200% 증가, 약 200% 증가 내지 약 10,000% 증가, 약 200% 증가 내지 약 9,000% 증가, 약 200% 증가 내지 약 8,000% 증가, 약 200% 증가 내지 약 7,000% 증가, 약 200% 증가 내지 약 6,000% 증가, 약 200% 증가 내지 약 5,000% 증가, 약 200% 증가 내지 약 4,000% 증가, 약 200% 증가 내지 약 3,000% 증가, 약 200% 증가 내지 약 2,000% 증가, 약 200% 증가 내지 약 1,000% 증가, 약 200% 증가 내지 약 500% 증가, 약 200% 증가 내지 약 450% 증가, 약 200% 증가 내지 약 400% 증가, 약 200% 증가 내지 약 350% 증가, 약 200% 증가 내지 약 300% 증가, 약 200% 증가 내지 약 250% 증가, 약 250% 증가 내지 약 10,000% 증가, 약 250% 증가 내지 약 9,000% 증가, 약 250% 증가 내지 약 8,000% 증가, 약 250% 증가 내지 약 7,000% 증가, 약 250% 증가 내지 약 6,000% 증가, 약 250% 증가 내지 약 5,000% 증가, 약 250% 증가 내지 약 4,000% 증가, 약 250% 증가 내지 약 3,000% 증가, 약 250% 증가 내지 약 2,000% 증가, 약 250% 증가 내지 약 1,000% 증가, 약 250% 증가 내지 약 500% 증가, 약 250% 증가 내지 약 450% 증가, 약 250% 증가 내지 약 400% 증가, 약 250% 증가 내지 약 350% 증가, 약 250% 증가 내지 약 300% 증가, 약 300% 증가 내지 약 10,000% 증가, 약 300% 증가 내지 약 9,000% 증가, 약 300% 증가 내지 약 8,000% 증가, 약 300% 증가 내지 약 7,000% 증가, 약 300% 증가 내지 약 6,000% 증가, 약 300% 증가 내지 약 5,000% 증가, 약 300% 증가 내지 약 4,000% 증가, 약 300% 증가 내지 약 3,000% 증가, 약 300% 증가 내지 약 2,000% 증가, 약 300% 증가 내지 약 1,000% 증가, 약 300% 증가 내지 약 500% 증가, 약 300% 증가 내지 약 450% 증가, 약 300% 증가 내지 약 400% 증가, 약 300% 증가 내지 약 350% 증가, 약 350% 증가 내지 약 10,000% 증가, 약 350% 증가 내지 약 9,000% 증가, 약 350% 증가 내지 약 8,000% 증가, 약 350% 증가 내지 약 7,000% 증가, 약 350% 증가 내지 약 6,000% 증가, 약 350% 증가 내지 약 5,000% 증가, 약 350% 증가 내지 약 4,000% 증가, 약 350% 증가 내지 약 3,000% 증가, 약 350% 증가 내지 약 2,000% 증가, 약 350% 증가 내지 약 1,000% 증가, 약 350% 증가 내지 약 500% 증가, 약 350% 증가 내지 약 450% 증가, 약 350% 증가 내지 약 400% 증가, 약 400% 증가 내지 약 10,000% 증가, 약 400% 증가 내지 약 9,000% 증가, 약 400% 증가 내지 약 8,000% 증가, 약 400% 증가 내지 약 7,000% 증가, 약 400% 증가 내지 약 6,000% 증가, 약 400% 증가 내지 약 5,000% 증가, 약 400% 증가 내지 약 4,000% 증가, 약 400% 증가 내지 약 3,000% 증가, 약 400% 증가 내지 약 2,000% 증가, 약 400% 증가 내지 약 1,000% 증가, 약 400% 증가 내지 약 500% 증가, 약 400% 증가 내지 약 450% 증가, 약 450% 증가 내지 약 10,000% 증가, 약 450% 증가 내지 약 9,000% 증가, 약 450% 증가 내지 약 8,000% 증가, 약 450% 증가 내지 약 7,000% 증가, 약 450% 증가 내지 약 6,000% 증가, 약 450% 증가 내지 약 5,000% 증가, 약 450% 증가 내지 약 4,000% 증가, 약 450% 증가 내지 약 3,000% 증가, 약 450% 증가 내지 약 2,000% 증가, 약 450% 증가 내지 약 1,000% 증가, 약 450% 증가 내지 약 500% 증가, 약 500% 증가 내지 약 10,000% 증가, 약 500% 증가 내지 약 9,000% 증가, 약 500% 증가 내지 약 8,000% 증가, 약 500% 증가 내지 약 7,000% 증가, 약 500% 증가 내지 약 6,000% 증가, 약 500% 증가 내지 약 5,000% 증가, 약 500% 증가 내지 약 4,000% 증가, 약 500% 증가 내지 약 3,000% 증가, 약 500% 증가 내지 약 2,000% 증가, 약 500% 증가 내지 약 1,000% 증가, 약 1,000% 증가 내지 약 10,000% 증가, 약 1,000% 증가 내지 약 9,000% 증가, 약 1,000% 증가 내지 약 8,000% 증가, 약 1,000% 증가 내지 약 7,000% 증가, 약 1,000% 증가 내지 약 6,000% 증가, 약 1,000% 증가 내지 약 5,000% 증가, 약 1,000% 증가 내지 약 4,000% 증가, 약 1,000% 증가 내지 약 3,000% 증가, 약 1,000% 증가 내지 약 2,000% 증가, 약 2,000% 증가 내지 약 10,000% 증가, 약 2,000% 증가 내지 약 9,000% 증가, 약 2,000% 증가 내지 약 8,000% 증가, 약 2,000% 증가 내지 약 7,000% 증가, 약 2,000% 증가 내지 약 6,000% 증가, 약 2,000% 증가 내지 약 5,000% 증가, 약 2,000% 증가 내지 약 4,000% 증가, 약 2,000% 증가 내지 약 3,000% 증가, 약 3,000% 증가 내지 약 10,000% 증가, 약 3,000% 증가 내지 약 9,000% 증가, 약 3,000% 증가 내지 약 8,000% 증가, 약 3,000% 증가 내지 약 7,000% 증가, 약 3,000% 증가 내지 약 6,000% 증가, 약 3,000% 증가 내지 약 5,000% 증가, 약 3,000% 증가 내지 약 4,000% 증가, 약 4,000% 증가 내지 약 10,000% 증가, 약 4,000% 증가 내지 약 9,000% 증가, 약 4,000% 증가 내지 약 8,000% 증가, 약 4,000% 증가 내지 약 7,000% 증가, 약 4,000% 증가 내지 약 6,000% 증가, 약 4,000% 증가 내지 약 5,000% 증가, 약 5,000% 증가 내지 약 10,000% 증가, 약 5,000% 증가 내지 약 9,000% 증가, 약 5,000% 증가 내지 약 8,000% 증가, 약 5,000% 증가 내지 약 7,000% 증가, 약 5,000% 증가 내지 약 6,000% 증가, 약 6,000% 증가 내지 약 10,000% 증가, 약 6,000% 증가 내지 약 9,000% 증가, 약 6,000% 증가 내지 약 8,000% 증가, 약 6,000% 증가 내지 약 7,000% 증가, 약 7,000% 증가 내지 약 10,000% 증가, 약 7,000% 증가 내지 약 9,000% 증가, 약 7,000% 증가 내지 약 8,000% 증가, 약 8,000% 증가 내지 약 10,000% 증가, 약 8,000% 증가 내지 약 9,000% 증가, 또는 약 9,000% 증가 내지 약 10,000% 증가시킬 수) 있다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, ABPC를 (예를 들어 본원에 기술된 ABPC 중 어느 하나를) 포함하는 조성물은 동일한 양의 대조군 ABPC (예를 들어 본원에 기술된 예시적인 대조군 ABPC 중 어느 하나)를 포함하는 조성물과 비교했을 때, 표적 포유류 세포에서 (본원에 기술된 표적 포유류 세포 중 어느 하나에서) 독소 유리를 증가시킬 수 (예를 들어 검출 가능하게 증가시킬 수) (예를 들어 적어도 0.1배 증가, 적어도 0.2배 증가, 적어도 0.3배 증가, 적어도 0.4배 증가, 적어도 0.5배 증가, 적어도 0.6배 증가, 적어도 0.7배 증가, 적어도 0.8배 증가, 적어도 0.9배 증가, 적어도 1.0배 증가, 적어도 1.2배 증가, 적어도 1.4배 증가, 적어도 1.5배 증가, 적어도 1.6배 증가, 적어도 1.8배 증가, 적어도 2.0배 증가, 적어도 2.2배 증가, 적어도 2.4배 증가, 적어도 2.5배 증가, 적어도 2.6배 증가, 적어도 2.8배 증가, 적어도 3.0배 증가, 적어도 3.5배 증가, 적어도 4.0배 증가, 적어도 4.5배 증가, 적어도 5.0배 증가, 적어도 5.5배 증가, 적어도 6.0배 증가, 적어도 6.5배 증가, 적어도 7.0배 증가, 적어도 7.5배 증가, 적어도 8.0배 증가, 적어도 8.5배 증가, 적어도 9.0배 증가, 적어도 9.5배 증가, 적어도 10배 증가, 적어도 15배 증가, 적어도 20배 증가, 적어도 25배 증가, 적어도 30배 증가, 적어도 35배 증가, 적어도 40배 증가, 적어도 45배 증가, 적어도 50배 증가, 적어도 55배 증가, 적어도 60배 증가, 적어도 65배 증가, 적어도 70배 증가, 적어도 75배 증가, 적어도 80배 증가, 적어도 85배 증가, 적어도 90배 증가, 적어도 95배 증가, 또는 적어도 100배 증가, 또는 약 0.1배 증가 내지 약 100배 증가, 약 0.1배 증가 내지 약 90배 증가, 약 0.1배 증가 내지 약 80배 증가, 약 0.1배 증가 내지 약 70배 증가, 약 0.1배 증가 내지 약 60배 증가, 약 0.1배 증가 내지 약 50배 증가, 약 0.1배 증가 내지 약 40배 증가, 약 0.1배 증가 내지 약 30배 증가, 약 0.1배 증가 내지 약 20배 증가, 약 0.1배 증가 내지 약 10배 증가, 약 0.1배 증가 내지 약 9.5배 증가, 약 0.1배 증가 내지 약 9.0배 증가, 약 0.1배 증가 내지 약 8.5배 증가, 약 0.1배 증가 내지 약 8.0배 증가, 약 0.1배 증가 내지 약 7.5배 증가, 약 0.1배 증가 내지 약 7.0배 증가, 약 0.1배 증가 내지 약 6.5배 증가, 약 0.1배 증가 내지 약 6.0배 증가, 약 0.1배 증가 내지 약 5.5배 증가, 약 0.1배 증가 내지 약 5.0배 증가, 약 0.1배 증가 내지 약 4.5배 증가, 약 0.1배 증가 내지 약 4.0배 증가, 약 0.1배 증가 내지 약 3.5배 증가, 약 0.1배 증가 내지 약 3.0배 증가, 약 0.1배 증가 내지 약 2.8배 증가, 약 0.1배 증가 내지 약 2.6배 증가, 약 0.1배 증가 내지 약 2.5배 증가, 약 0.1배 증가 내지 약 2.4배 증가, 약 0.1배 증가 내지 약 2.2배 증가, 약 0.1배 증가 내지 약 2.0배 증가, 약 0.1배 증가 내지 약 1.8배 증가, 약 0.1배 증가 내지 약 1.6배 증가, 약 0.1배 증가 내지 약 1.5배 증가, 약 0.1배 증가 내지 약 1.4배 증가, 약 0.1배 증가 내지 약 1.2배 증가, 약 0.1배 증가 내지 약 1.0배 증가, 약 0.1배 증가 내지 약 0.9배 증가, 약 0.1배 증가 내지 약 0.8배 증가, 약 0.1배 증가 내지 약 0.7배 증가, 약 0.1배 증가 내지 약 0.6배 증가, 약 0.1배 증가 내지 약 0.5배 증가, 약 0.1배 증가 내지 약 0.4배 증가, 약 0.1배 증가 내지 약 0.3배 증가, 약 0.2배 증가 내지 약 100배 증가, 약 0.2배 증가 내지 약 90배 증가, 약 0.2배 증가 내지 약 80배 증가, 약 0.2배 증가 내지 약 70배 증가, 약 0.2배 증가 내지 약 60배 증가, 약 0.2배 증가 내지 약 50배 증가, 약 0.2배 증가 내지 약 40배 증가, 약 0.2배 증가 내지 약 30배 증가, 약 0.2배 증가 내지 약 20배 증가, 약 0.2배 증가 내지 약 10배 증가, 약 0.2배 증가 내지 약 9.5배 증가, 약 0.2배 증가 내지 약 9.0배 증가, 약 0.2배 증가 내지 약 8.5배 증가, 약 0.2배 증가 내지 약 8.0배 증가, 약 0.2배 증가 내지 약 7.5배 증가, 약 0.2배 증가 내지 약 7.0배 증가, 약 0.2배 증가 내지 약 6.5배 증가, 약 0.2배 증가 내지 약 6.0배 증가, 약 0.2배 증가 내지 약 5.5배 증가, 약 0.2배 증가 내지 약 5.0배 증가, 약 0.2배 증가 내지 약 4.5배 증가, 약 0.2배 증가 내지 약 4.0배 증가, 약 0.2배 증가 내지 약 3.5배 증가, 약 0.2배 증가 내지 약 3.0배 증가, 약 0.2배 증가 내지 약 2.8배 증가, 약 0.2배 증가 내지 약 2.6배 증가, 약 0.2배 증가 내지 약 2.5배 증가, 약 0.2배 증가 내지 약 2.4배 증가, 약 0.2배 증가 내지 약 2.2배 증가, 약 0.2배 증가 내지 약 2.0배 증가, 약 0.2배 증가 내지 약 1.8배 증가, 약 0.2배 증가 내지 약 1.6배 증가, 약 0.2배 증가 내지 약 1.5배 증가, 약 0.2배 증가 내지 약 1.4배 증가, 약 0.2배 증가 내지 약 1.2배 증가, 약 0.2배 증가 내지 약 1.0배 증가, 약 0.2배 증가 내지 약 0.9배 증가, 약 0.2배 증가 내지 약 0.8배 증가, 약 0.2배 증가 내지 약 0.7배 증가, 약 0.2배 증가 내지 약 0.6배 증가, 약 0.2배 증가 내지 약 0.5배 증가, 약 0.2배 증가 내지 약 0.4배 증가, 약 0.3배 증가 내지 약 100배 증가, 약 0.3배 증가 내지 약 90배 증가, 약 0.3배 증가 내지 약 80배 증가, 약 0.3배 증가 내지 약 70배 증가, 약 0.3배 증가 내지 약 60배 증가, 약 0.3배 증가 내지 약 50배 증가, 약 0.3배 증가 내지 약 40배 증가, 약 0.3배 증가 내지 약 30배 증가, 약 0.3배 증가 내지 약 20배 증가, 약 0.3배 증가 내지 약 10배 증가, 약 0.3배 증가 내지 약 9.5배 증가, 약 0.3배 증가 내지 약 9.0배 증가, 약 0.3배 증가 내지 약 8.5배 증가, 약 0.3배 증가 내지 약 8.0배 증가, 약 0.3배 증가 내지 약 7.5배 증가, 약 0.3배 증가 내지 약 7.0배 증가, 약 0.3배 증가 내지 약 6.5배 증가, 약 0.3배 증가 내지 약 6.0배 증가, 약 0.3배 증가 내지 약 5.5배 증가, 약 0.3배 증가 내지 약 5.0배 증가, 약 0.3배 증가 내지 약 4.5배 증가, 약 0.3배 증가 내지 약 4.0배 증가, 약 0.3배 증가 내지 약 3.5배 증가, 약 0.3배 증가 내지 약 3.0배 증가, 약 0.3배 증가 내지 약 2.8배 증가, 약 0.3배 증가 내지 약 2.6배 증가, 약 0.3배 증가 내지 약 2.5배 증가, 약 0.3배 증가 내지 약 2.4배 증가, 약 0.3배 증가 내지 약 2.2배 증가, 약 0.3배 증가 내지 약 2.0배 증가, 약 0.3배 증가 내지 약 1.8배 증가, 약 0.3배 증가 내지 약 1.6배 증가, 약 0.3배 증가 내지 약 1.5배 증가, 약 0.3배 증가 내지 약 1.4배 증가, 약 0.3배 증가 내지 약 1.2배 증가, 약 0.3배 증가 내지 약 1.0배 증가, 약 0.3배 증가 내지 약 0.9배 증가, 약 0.3배 증가 내지 약 0.8배 증가, 약 0.3배 증가 내지 약 0.7배 증가, 약 0.3배 증가 내지 약 0.6배 증가, 약 0.3배 증가 내지 약 0.5배 증가, 약 0.4배 증가 내지 약 100배 증가, 약 0.4배 증가 내지 약 90배 증가, 약 0.4배 증가 내지 약 80배 증가, 약 0.4배 증가 내지 약 70배 증가, 약 0.4배 증가 내지 약 60배 증가, 약 0.4배 증가 내지 약 50배 증가, 약 0.4배 증가 내지 약 40배 증가, 약 0.4배 증가 내지 약 30배 증가, 약 0.4배 증가 내지 약 20배 증가, 약 0.4배 증가 내지 약 10배 증가, 약 0.4배 증가 내지 약 9.5배 증가, 약 0.4배 증가 내지 약 9.0배 증가, 약 0.4배 증가 내지 약 8.5배 증가, 약 0.4배 증가 내지 약 8.0배 증가, 약 0.4배 증가 내지 약 7.5배 증가, 약 0.4배 증가 내지 약 7.0배 증가, 약 0.4배 증가 내지 약 6.5배 증가, 약 0.4배 증가 내지 약 6.0배 증가, 약 0.4배 증가 내지 약 5.5배 증가, 약 0.4배 증가 내지 약 5.0배 증가, 약 0.4배 증가 내지 약 4.5배 증가, 약 0.4배 증가 내지 약 4.0배 증가, 약 0.4배 증가 내지 약 3.5배 증가, 약 0.4배 증가 내지 약 3.0배 증가, 약 0.4배 증가 내지 약 2.8배 증가, 약 0.4배 증가 내지 약 2.6배 증가, 약 0.4배 증가 내지 약 2.5배 증가, 약 0.4배 증가 내지 약 2.4배 증가, 약 0.4배 증가 내지 약 2.2배 증가, 약 0.4배 증가 내지 약 2.0배 증가, 약 0.4배 증가 내지 약 1.8배 증가, 약 0.4배 증가 내지 약 1.6배 증가, 약 0.4배 증가 내지 약 1.5배 증가, 약 0.4배 증가 내지 약 1.4배 증가, 약 0.4배 증가 내지 약 1.2배 증가, 약 0.4배 증가 내지 약 1.0배 증가, 약 0.4배 증가 내지 약 0.9배 증가, 약 0.4배 증가 내지 약 0.8배 증가, 약 0.4배 증가 내지 약 0.7배 증가, 약 0.4배 증가 내지 약 0.6배 증가, 약 0.5배 증가 내지 약 100배 증가, 약 0.5배 증가 내지 약 90배 증가, 약 0.5배 증가 내지 약 80배 증가, 약 0.5배 증가 내지 약 70배 증가, 약 0.5배 증가 내지 약 60배 증가, 약 0.5배 증가 내지 약 50배 증가, 약 0.5배 증가 내지 약 40배 증가, 약 0.5배 증가 내지 약 30배 증가, 약 0.5배 증가 내지 약 20배 증가, 약 0.5배 증가 내지 약 10배 증가, 약 0.5배 증가 내지 약 9.5배 증가, 약 0.5배 증가 내지 약 9.0배 증가, 약 0.5배 증가 내지 약 8.5배 증가, 약 0.5배 증가 내지 약 8.0배 증가, 약 0.5배 증가 내지 약 7.5배 증가, 약 0.5배 증가 내지 약 7.0배 증가, 약 0.5배 증가 내지 약 6.5배 증가, 약 0.5배 증가 내지 약 6.0배 증가, 약 0.5배 증가 내지 약 5.5배 증가, 약 0.5배 증가 내지 약 5.0배 증가, 약 0.5배 증가 내지 약 4.5배 증가, 약 0.5배 증가 내지 약 4.0배 증가, 약 0.5배 증가 내지 약 3.5배 증가, 약 0.5배 증가 내지 약 3.0배 증가, 약 0.5배 증가 내지 약 2.8배 증가, 약 0.5배 증가 내지 약 2.6배 증가, 약 0.5배 증가 내지 약 2.5배 증가, 약 0.5배 증가 내지 약 2.4배 증가, 약 0.5배 증가 내지 약 2.2배 증가, 약 0.5배 증가 내지 약 2.0배 증가, 약 0.5배 증가 내지 약 1.8배 증가, 약 0.5배 증가 내지 약 1.6배 증가, 약 0.5배 증가 내지 약 1.5배 증가, 약 0.5배 증가 내지 약 1.4배 증가, 약 0.5배 증가 내지 약 1.2배 증가, 약 0.5배 증가 내지 약 1.0배 증가, 약 0.5배 증가 내지 약 0.9배 증가, 약 0.5배 증가 내지 약 0.8배 증가, 약 0.5배 증가 내지 약 0.7배 증가, 약 0.6배 증가 내지 약 100배 증가, 약 0.6배 증가 내지 약 90배 증가, 약 0.6배 증가 내지 약 80배 증가, 약 0.6배 증가 내지 약 70배 증가, 약 0.6배 증가 내지 약 60배 증가, 약 0.6배 증가 내지 약 50배 증가, 약 0.6배 증가 내지 약 40배 증가, 약 0.6배 증가 내지 약 30배 증가, 약 0.6배 증가 내지 약 20배 증가, 약 0.6배 증가 내지 약 10배 증가, 약 0.6배 증가 내지 약 9.5배 증가, 약 0.6배 증가 내지 약 9.0배 증가, 약 0.6배 증가 내지 약 8.5배 증가, 약 0.6배 증가 내지 약 8.0배 증가, 약 0.6배 증가 내지 약 7.5배 증가, 약 0.6배 증가 내지 약 7.0배 증가, 약 0.6배 증가 내지 약 6.5배 증가, 약 0.6배 증가 내지 약 6.0배 증가, 약 0.6배 증가 내지 약 5.5배 증가, 약 0.6배 증가 내지 약 5.0배 증가, 약 0.6배 증가 내지 약 4.5배 증가, 약 0.6배 증가 내지 약 4.0배 증가, 약 0.6배 증가 내지 약 3.5배 증가, 약 0.6배 증가 내지 약 3.0배 증가, 약 0.6배 증가 내지 약 2.8배 증가, 약 0.6배 증가 내지 약 2.6배 증가, 약 0.6배 증가 내지 약 2.5배 증가, 약 0.6배 증가 내지 약 2.4배 증가, 약 0.6배 증가 내지 약 2.2배 증가, 약 0.6배 증가 내지 약 2.0배 증가, 약 0.6배 증가 내지 약 1.8배 증가, 약 0.6배 증가 내지 약 1.6배 증가, 약 0.6배 증가 내지 약 1.5배 증가, 약 0.6배 증가 내지 약 1.4배 증가, 약 0.6배 증가 내지 약 1.2배 증가, 약 0.6배 증가 내지 약 1.0배 증가, 약 0.6배 증가 내지 약 0.9배 증가, 약 0.6배 증가 내지 약 0.8배 증가, 약 0.7배 증가 내지 약 100배 증가, 약 0.7배 증가 내지 약 90배 증가, 약 0.7배 증가 내지 약 80배 증가, 약 0.7배 증가 내지 약 70배 증가, 약 0.7배 증가 내지 약 60배 증가, 약 0.7배 증가 내지 약 50배 증가, 약 0.7배 증가 내지 약 40배 증가, 약 0.7배 증가 내지 약 30배 증가, 약 0.7배 증가 내지 약 20배 증가, 약 0.7배 증가 내지 약 10배 증가, 약 0.7배 증가 내지 약 9.5배 증가, 약 0.7배 증가 내지 약 9.0배 증가, 약 0.7배 증가 내지 약 8.5배 증가, 약 0.7배 증가 내지 약 8.0배 증가, 약 0.7배 증가 내지 약 7.5배 증가, 약 0.7배 증가 내지 약 7.0배 증가, 약 0.7배 증가 내지 약 6.5배 증가, 약 0.7배 증가 내지 약 6.0배 증가, 약 0.7배 증가 내지 약 5.5배 증가, 약 0.7배 증가 내지 약 5.0배 증가, 약 0.7배 증가 내지 약 4.5배 증가, 약 0.7배 증가 내지 약 4.0배 증가, 약 0.7배 증가 내지 약 3.5배 증가, 약 0.7배 증가 내지 약 3.0배 증가, 약 0.7배 증가 내지 약 2.8배 증가, 약 0.7배 증가 내지 약 2.6배 증가, 약 0.7배 증가 내지 약 2.5배 증가, 약 0.7배 증가 내지 약 2.4배 증가, 약 0.7배 증가 내지 약 2.2배 증가, 약 0.7배 증가 내지 약 2.0배 증가, 약 0.7배 증가 내지 약 1.8배 증가, 약 0.7배 증가 내지 약 1.6배 증가, 약 0.7배 증가 내지 약 1.5배 증가, 약 0.7배 증가 내지 약 1.4배 증가, 약 0.7배 증가 내지 약 1.2배 증가, 약 0.7배 증가 내지 약 1.0배 증가, 약 0.7배 증가 내지 약 0.9배 증가, 약 0.8배 증가 내지 약 100배 증가, 약 0.8배 증가 내지 약 90배 증가, 약 0.8배 증가 내지 약 80배 증가, 약 0.8배 증가 내지 약 70배 증가, 약 0.8배 증가 내지 약 60배 증가, 약 0.8배 증가 내지 약 50배 증가, 약 0.8배 증가 내지 약 40배 증가, 약 0.8배 증가 내지 약 30배 증가, 약 0.8배 증가 내지 약 20배 증가, 약 0.8배 증가 내지 약 10배 증가, 약 0.8배 증가 내지 약 9.5배 증가, 약 0.8배 증가 내지 약 9.0배 증가, 약 0.8배 증가 내지 약 8.5배 증가, 약 0.8배 증가 내지 약 8.0배 증가, 약 0.8배 증가 내지 약 7.5배 증가, 약 0.8배 증가 내지 약 7.0배 증가, 약 0.8배 증가 내지 약 6.5배 증가, 약 0.8배 증가 내지 약 6.0배 증가, 약 0.8배 증가 내지 약 5.5배 증가, 약 0.8배 증가 내지 약 5.0배 증가, 약 0.8배 증가 내지 약 4.5배 증가, 약 0.8배 증가 내지 약 4.0배 증가, 약 0.8배 증가 내지 약 3.5배 증가, 약 0.8배 증가 내지 약 3.0배 증가, 약 0.8배 증가 내지 약 2.8배 증가, 약 0.8배 증가 내지 약 2.6배 증가, 약 0.8배 증가 내지 약 2.5배 증가, 약 0.8배 증가 내지 약 2.4배 증가, 약 0.8배 증가 내지 약 2.2배 증가, 약 0.8배 증가 내지 약 2.0배 증가, 약 0.8배 증가 내지 약 1.8배 증가, 약 0.8배 증가 내지 약 1.6배 증가, 약 0.8배 증가 내지 약 1.5배 증가, 약 0.8배 증가 내지 약 1.4배 증가, 약 0.8배 증가 내지 약 1.2배 증가, 약 0.8배 증가 내지 약 1.0배 증가, 약 1.0배 증가 내지 약 100배 증가, 약 1.0배 증가 내지 약 90배 증가, 약 1.0배 증가 내지 약 80배 증가, 약 1.0배 증가 내지 약 70배 증가, 약 1.0배 증가 내지 약 60배 증가, 약 1.0배 증가 내지 약 50배 증가, 약 1.0배 증가 내지 약 40배 증가, 약 1.0배 증가 내지 약 30배 증가, 약 1.0배 증가 내지 약 20배 증가, 약 1.0배 증가 내지 약 10배 증가, 약 1.0배 증가 내지 약 9.5배 증가, 약 1.0배 증가 내지 약 9.0배 증가, 약 1.0배 증가 내지 약 8.5배 증가, 약 1.0배 증가 내지 약 8.0배 증가, 약 1.0배 증가 내지 약 7.5배 증가, 약 1.0배 증가 내지 약 7.0배 증가, 약 1.0배 증가 내지 약 6.5배 증가, 약 1.0배 증가 내지 약 6.0배 증가, 약 1.0배 증가 내지 약 5.5배 증가, 약 1.0배 증가 내지 약 5.0배 증가, 약 1.0배 증가 내지 약 4.5배 증가, 약 1.0배 증가 내지 약 4.0배 증가, 약 1.0배 증가 내지 약 3.5배 증가, 약 1.0배 증가 내지 약 3.0배 증가, 약 1.0배 증가 내지 약 2.8배 증가, 약 1.0배 증가 내지 약 2.6배 증가, 약 1.0배 증가 내지 약 2.5배 증가, 약 1.0배 증가 내지 약 2.4배 증가, 약 1.0배 증가 내지 약 2.2배 증가, 약 1.0배 증가 내지 약 2.0배 증가, 약 1.0배 증가 내지 약 1.8배 증가, 약 1.0배 증가 내지 약 1.6배 증가, 약 1.0배 증가 내지 약 1.5배 증가, 약 1.0배 증가 내지 약 1.4배 증가, 약 1.0배 증가 내지 약 1.2배 증가, 약 1.2배 증가 내지 약 100배 증가, 약 1.2배 증가 내지 약 90배 증가, 약 1.2배 증가 내지 약 80배 증가, 약 1.2배 증가 내지 약 70배 증가, 약 1.2배 증가 내지 약 60배 증가, 약 1.2배 증가 내지 약 50배 증가, 약 1.2배 증가 내지 약 40배 증가, 약 1.2배 증가 내지 약 30배 증가, 약 1.2배 증가 내지 약 20배 증가, 약 1.2배 증가 내지 약 10배 증가, 약 1.2배 증가 내지 약 9.5배 증가, 약 1.2배 증가 내지 약 9.0배 증가, 약 1.2배 증가 내지 약 8.5배 증가, 약 1.2배 증가 내지 약 8.0배 증가, 약 1.2배 증가 내지 약 7.5배 증가, 약 1.2배 증가 내지 약 7.0배 증가, 약 1.2배 증가 내지 약 6.5배 증가, 약 1.2배 증가 내지 약 6.0배 증가, 약 1.2배 증가 내지 약 5.5배 증가, 약 1.2배 증가 내지 약 5.0배 증가, 약 1.2배 증가 내지 약 4.5배 증가, 약 1.2배 증가 내지 약 4.0배 증가, 약 1.2배 증가 내지 약 3.5배 증가, 약 1.2배 증가 내지 약 3.0배 증가, 약 1.2배 증가 내지 약 2.8배 증가, 약 1.2배 증가 내지 약 2.6배 증가, 약 1.2배 증가 내지 약 2.5배 증가, 약 1.2배 증가 내지 약 2.4배 증가, 약 1.2배 증가 내지 약 2.2배 증가, 약 1.2배 증가 내지 약 2.0배 증가, 약 1.2배 증가 내지 약 1.8배 증가, 약 1.2배 증가 내지 약 1.6배 증가, 약 1.2배 증가 내지 약 1.5배 증가, 약 1.2배 증가 내지 약 1.4배 증가, 약 1.4배 증가 내지 약 100배 증가, 약 1.4배 증가 내지 약 90배 증가, 약 1.4배 증가 내지 약 80배 증가, 약 1.4배 증가 내지 약 70배 증가, 약 1.4배 증가 내지 약 60배 증가, 약 1.4배 증가 내지 약 50배 증가, 약 1.4배 증가 내지 약 40배 증가, 약 1.4배 증가 내지 약 30배 증가, 약 1.4배 증가 내지 약 20배 증가, 약 1.4배 증가 내지 약 10배 증가, 약 1.4배 증가 내지 약 9.5배 증가, 약 1.4배 증가 내지 약 9.0배 증가, 약 1.4배 증가 내지 약 8.5배 증가, 약 1.4배 증가 내지 약 8.0배 증가, 약 1.4배 증가 내지 약 7.5배 증가, 약 1.4배 증가 내지 약 7.0배 증가, 약 1.4배 증가 내지 약 6.5배 증가, 약 1.4배 증가 내지 약 6.0배 증가, 약 1.4배 증가 내지 약 5.5배 증가, 약 1.4배 증가 내지 약 5.0배 증가, 약 1.4배 증가 내지 약 4.5배 증가, 약 1.4배 증가 내지 약 4.0배 증가, 약 1.4배 증가 내지 약 3.5배 증가, 약 1.4배 증가 내지 약 3.0배 증가, 약 1.4배 증가 내지 약 2.8배 증가, 약 1.4배 증가 내지 약 2.6배 증가, 약 1.4배 증가 내지 약 2.5배 증가, 약 1.4배 증가 내지 약 2.4배 증가, 약 1.4배 증가 내지 약 2.2배 증가, 약 1.4배 증가 내지 약 2.0배 증가, 약 1.4배 증가 내지 약 1.8배 증가, 약 1.4배 증가 내지 약 1.6배 증가, 약 1.6배 증가 내지 약 10배 증가, 약 1.6배 증가 내지 약 100배 증가, 약 1.6배 증가 내지 약 90배 증가, 약 1.6배 증가 내지 약 80배 증가, 약 1.6배 증가 내지 약 70배 증가, 약 1.6배 증가 내지 약 60배 증가, 약 1.6배 증가 내지 약 50배 증가, 약 1.6배 증가 내지 약 40배 증가, 약 1.6배 증가 내지 약 30배 증가, 약 1.6배 증가 내지 약 20배 증가, 약 1.6배 증가 내지 약 9.5배 증가, 약 1.6배 증가 내지 약 9.0배 증가, 약 1.6배 증가 내지 약 8.5배 증가, 약 1.6배 증가 내지 약 8.0배 증가, 약 1.6배 증가 내지 약 7.5배 증가, 약 1.6배 증가 내지 약 7.0배 증가, 약 1.6배 증가 내지 약 6.5배 증가, 약 1.6배 증가 내지 약 6.0배 증가, 약 1.6배 증가 내지 약 5.5배 증가, 약 1.6배 증가 내지 약 5.0배 증가, 약 1.6배 증가 내지 약 4.5배 증가, 약 1.6배 증가 내지 약 4.0배 증가, 약 1.6배 증가 내지 약 3.5배 증가, 약 1.6배 증가 내지 약 3.0배 증가, 약 1.6배 증가 내지 약 2.8배 증가, 약 1.6배 증가 내지 약 2.6배 증가, 약 1.6배 증가 내지 약 2.5배 증가, 약 1.6배 증가 내지 약 2.4배 증가, 약 1.6배 증가 내지 약 2.2배 증가, 약 1.6배 증가 내지 약 2.0배 증가, 약 1.6배 증가 내지 약 1.8배 증가, 약 1.8배 증가 내지 약 100배 증가, 약 1.8배 증가 내지 약 90배 증가, 약 1.8배 증가 내지 약 80배 증가, 약 1.8배 증가 내지 약 70배 증가, 약 1.8배 증가 내지 약 60배 증가, 약 1.8배 증가 내지 약 50배 증가, 약 1.8배 증가 내지 약 40배 증가, 약 1.8배 증가 내지 약 30배 증가, 약 1.8배 증가 내지 약 20배 증가, 약 1.8배 증가 내지 약 10배 증가, 약 1.8배 증가 내지 약 9.5배 증가, 약 1.8배 증가 내지 약 9.0배 증가, 약 1.8배 증가 내지 약 8.5배 증가, 약 1.8배 증가 내지 약 8.0배 증가, 약 1.8배 증가 내지 약 7.5배 증가, 약 1.8배 증가 내지 약 7.0배 증가, 약 1.8배 증가 내지 약 6.5배 증가, 약 1.8배 증가 내지 약 6.0배 증가, 약 1.8배 증가 내지 약 5.5배 증가, 약 1.8배 증가 내지 약 5.0배 증가, 약 1.8배 증가 내지 약 4.5배 증가, 약 1.8배 증가 내지 약 4.0배 증가, 약 1.8배 증가 내지 약 3.5배 증가, 약 1.8배 증가 내지 약 3.0배 증가, 약 1.8배 증가 내지 약 2.8배 증가, 약 1.8배 증가 내지 약 2.6배 증가, 약 1.8배 증가 내지 약 2.5배 증가, 약 1.8배 증가 내지 약 2.4배 증가, 약 1.8배 증가 내지 약 2.2배 증가, 약 1.8배 증가 내지 약 2.0배 증가, 약 2.0배 증가 내지 약 100배 증가, 약 2.0배 증가 내지 약 90배 증가, 약 2.0배 증가 내지 약 80배 증가, 약 2.0배 증가 내지 약 70배 증가, 약 2.0배 증가 내지 약 60배 증가, 약 2.0배 증가 내지 약 50배 증가, 약 2.0배 증가 내지 약 40배 증가, 약 2.0배 증가 내지 약 30배 증가, 약 2.0배 증가 내지 약 20배 증가, 약 2.0배 증가 내지 약 10배 증가, 약 2.0배 증가 내지 약 9.5배 증가, 약 2.0배 증가 내지 약 9.0배 증가, 약 2.0배 증가 내지 약 8.5배 증가, 약 2.0배 증가 내지 약 8.0배 증가, 약 2.0배 증가 내지 약 7.5배 증가, 약 2.0배 증가 내지 약 7.0배 증가, 약 2.0배 증가 내지 약 6.5배 증가, 약 2.0배 증가 내지 약 6.0배 증가, 약 2.0배 증가 내지 약 5.5배 증가, 약 2.0배 증가 내지 약 5.0배 증가, 약 2.0배 증가 내지 약 4.5배 증가, 약 2.0배 증가 내지 약 4.0배 증가, 약 2.0배 증가 내지 약 3.5배 증가, 약 2.0배 증가 내지 약 3.0배 증가, 약 2.0배 증가 내지 약 2.8배 증가, 약 2.0배 증가 내지 약 2.6배 증가, 약 2.0배 증가 내지 약 2.5배 증가, 약 2.0배 증가 내지 약 2.4배 증가, 약 2.0배 증가 내지 약 2.2배 증가, 약 2.2배 증가 내지 약 100배 증가, 약 2.2배 증가 내지 약 90배 증가, 약 2.2배 증가 내지 약 80배 증가, 약 2.2배 증가 내지 약 70배 증가, 약 2.2배 증가 내지 약 60배 증가, 약 2.2배 증가 내지 약 50배 증가, 약 2.2배 증가 내지 약 40배 증가, 약 2.2배 증가 내지 약 30배 증가, 약 2.2배 증가 내지 약 20배 증가, 약 2.2배 증가 내지 약 10배 증가, 약 2.2배 증가 내지 약 9.5배 증가, 약 2.2배 증가 내지 약 9.0배 증가, 약 2.2배 증가 내지 약 8.5배 증가, 약 2.2배 증가 내지 약 8.0배 증가, 약 2.2배 증가 내지 약 7.5배 증가, 약 2.2배 증가 내지 약 7.0배 증가, 약 2.2배 증가 내지 약 6.5배 증가, 약 2.2배 증가 내지 약 6.0배 증가, 약 2.2배 증가 내지 약 5.5배 증가, 약 2.2배 증가 내지 약 5.0배 증가, 약 2.2배 증가 내지 약 4.5배 증가, 약 2.2배 증가 내지 약 4.0배 증가, 약 2.2배 증가 내지 약 3.5배 증가, 약 2.2배 증가 내지 약 3.0배 증가, 약 2.2배 증가 내지 약 2.8배 증가, 약 2.2배 증가 내지 약 2.6배 증가, 약 2.2배 증가 내지 약 2.5배 증가, 약 2.2배 증가 내지 약 2.4배 증가, 약 2.4배 증가 내지 약 100배 증가, 약 2.4배 증가 내지 약 90배 증가, 약 2.4배 증가 내지 약 80배 증가, 약 2.4배 증가 내지 약 70배 증가, 약 2.4배 증가 내지 약 60배 증가, 약 2.4배 증가 내지 약 50배 증가, 약 2.4배 증가 내지 약 40배 증가, 약 2.4배 증가 내지 약 30배 증가, 약 2.4배 증가 내지 약 20배 증가, 약 2.4배 증가 내지 약 10배 증가, 약 2.4배 증가 내지 약 9.5배 증가, 약 2.4배 증가 내지 약 9.0배 증가, 약 2.4배 증가 내지 약 8.5배 증가, 약 2.4배 증가 내지 약 8.0배 증가, 약 2.4배 증가 내지 약 7.5배 증가, 약 2.4배 증가 내지 약 7.0배 증가, 약 2.4배 증가 내지 약 6.5배 증가, 약 2.4배 증가 내지 약 6.0배 증가, 약 2.4배 증가 내지 약 5.5배 증가, 약 2.4배 증가 내지 약 5.0배 증가, 약 2.4배 증가 내지 약 4.5배 증가, 약 2.4배 증가 내지 약 4.0배 증가, 약 2.4배 증가 내지 약 3.5배 증가, 약 2.4배 증가 내지 약 3.0배 증가, 약 2.4배 증가 내지 약 2.8배 증가, 약 2.4배 증가 내지 약 2.6배 증가, 약 2.6배 증가 내지 약 100배 증가, 약 2.6배 증가 내지 약 90배 증가, 약 2.6배 증가 내지 약 80배 증가, 약 2.6배 증가 내지 약 70배 증가, 약 2.6배 증가 내지 약 60배 증가, 약 2.6배 증가 내지 약 50배 증가, 약 2.6배 증가 내지 약 40배 증가, 약 2.6배 증가 내지 약 30배 증가, 약 2.6배 증가 내지 약 20배 증가, 약 2.6배 증가 내지 약 10배 증가, 약 2.6배 증가 내지 약 9.5배 증가, 약 2.6배 증가 내지 약 9.0배 증가, 약 2.6배 증가 내지 약 8.5배 증가, 약 2.6배 증가 내지 약 8.0배 증가, 약 2.6배 증가 내지 약 7.5배 증가, 약 2.6배 증가 내지 약 7.0배 증가, 약 2.6배 증가 내지 약 6.5배 증가, 약 2.6배 증가 내지 약 6.0배 증가, 약 2.6배 증가 내지 약 5.5배 증가, 약 2.6배 증가 내지 약 5.0배 증가, 약 2.6배 증가 내지 약 4.5배 증가, 약 2.6배 증가 내지 약 4.0배 증가, 약 2.6배 증가 내지 약 3.5배 증가, 약 2.6배 증가 내지 약 3.0배 증가, 약 2.6배 증가 내지 약 2.8배 증가, 약 2.8배 증가 내지 약 100배 증가, 약 2.8배 증가 내지 약 90배 증가, 약 2.8배 증가 내지 약 80배 증가, 약 2.8배 증가 내지 약 70배 증가, 약 2.8배 증가 내지 약 60배 증가, 약 2.8배 증가 내지 약 50배 증가, 약 2.8배 증가 내지 약 40배 증가, 약 2.8배 증가 내지 약 30배 증가, 약 2.8배 증가 내지 약 20배 증가, 약 2.8배 증가 내지 약 10배 증가, 약 2.8배 증가 내지 약 9.5배 증가, 약 2.8배 증가 내지 약 9.0배 증가, 약 2.8배 증가 내지 약 8.5배 증가, 약 2.8배 증가 내지 약 8.0배 증가, 약 2.8배 증가 내지 약 7.5배 증가, 약 2.8배 증가 내지 약 7.0배 증가, 약 2.8배 증가 내지 약 6.5배 증가, 약 2.8배 증가 내지 약 6.0배 증가, 약 2.8배 증가 내지 약 5.5배 증가, 약 2.8배 증가 내지 약 5.0배 증가, 약 2.8배 증가 내지 약 4.5배 증가, 약 2.8배 증가 내지 약 4.0배 증가, 약 2.8배 증가 내지 약 3.5배 증가, 약 2.8배 증가 내지 약 3.0배 증가, 약 3.0배 증가 내지 약 100배 증가, 약 3.0배 증가 내지 약 90배 증가, 약 3.0배 증가 내지 약 80배 증가, 약 3.0배 증가 내지 약 70배 증가, 약 3.0배 증가 내지 약 60배 증가, 약 3.0배 증가 내지 약 50배 증가, 약 3.0배 증가 내지 약 40배 증가, 약 3.0배 증가 내지 약 30배 증가, 약 3.0배 증가 내지 약 20배 증가, 약 3.0배 증가 내지 약 10배 증가, 약 3.0배 증가 내지 약 9.5배 증가, 약 3.0배 증가 내지 약 9.0배 증가, 약 3.0배 증가 내지 약 8.5배 증가, 약 3.0배 증가 내지 약 8.0배 증가, 약 3.0배 증가 내지 약 7.5배 증가, 약 3.0배 증가 내지 약 7.0배 증가, 약 3.0배 증가 내지 약 6.5배 증가, 약 3.0배 증가 내지 약 6.0배 증가, 약 3.0배 증가 내지 약 5.5배 증가, 약 3.0배 증가 내지 약 5.0배 증가, 약 3.0배 증가 내지 약 4.5배 증가, 약 3.0배 증가 내지 약 4.0배 증가, 약 3.0배 증가 내지 약 3.5배 증가, 약 3.5배 증가 내지 약 100배 증가, 약 3.5배 증가 내지 약 90배 증가, 약 3.5배 증가 내지 약 80배 증가, 약 3.5배 증가 내지 약 70배 증가, 약 3.5배 증가 내지 약 60배 증가, 약 3.5배 증가 내지 약 50배 증가, 약 3.5배 증가 내지 약 40배 증가, 약 3.5배 증가 내지 약 30배 증가, 약 3.5배 증가 내지 약 20배 증가, 약 3.5배 증가 내지 약 10배 증가, 약 3.5배 증가 내지 약 9.5배 증가, 약 3.5배 증가 내지 약 9.0배 증가, 약 3.5배 증가 내지 약 8.5배 증가, 약 3.5배 증가 내지 약 8.0배 증가, 약 3.5배 증가 내지 약 7.5배 증가, 약 3.5배 증가 내지 약 7.0배 증가, 약 3.5배 증가 내지 약 6.5배 증가, 약 3.5배 증가 내지 약 6.0배 증가, 약 3.5배 증가 내지 약 5.5배 증가, 약 3.5배 증가 내지 약 5.0배 증가, 약 3.5배 증가 내지 약 4.5배 증가, 약 3.5배 증가 내지 약 4.0배 증가, 약 4.0배 증가 내지 약 100배 증가, 약 4.0배 증가 내지 약 90배 증가, 약 4.0배 증가 내지 약 80배 증가, 약 4.0배 증가 내지 약 70배 증가, 약 4.0배 증가 내지 약 60배 증가, 약 4.0배 증가 내지 약 50배 증가, 약 4.0배 증가 내지 약 40배 증가, 약 4.0배 증가 내지 약 30배 증가, 약 4.0배 증가 내지 약 20배 증가, 약 4.0배 증가 내지 약 10배 증가, 약 4.0배 증가 내지 약 9.5배 증가, 약 4.0배 증가 내지 약 9.0배 증가, 약 4.0배 증가 내지 약 8.5배 증가, 약 4.0배 증가 내지 약 8.0배 증가, 약 4.0배 증가 내지 약 7.5배 증가, 약 4.0배 증가 내지 약 7.0배 증가, 약 4.0배 증가 내지 약 6.5배 증가, 약 4.0배 증가 내지 약 6.0배 증가, 약 4.0배 증가 내지 약 5.5배 증가, 약 4.0배 증가 내지 약 5.0배 증가, 약 4.0배 증가 내지 약 4.5배 증가, 약 4.5배 증가 내지 약 100배 증가, 약 4.5배 증가 내지 약 90배 증가, 약 4.5배 증가 내지 약 80배 증가, 약 4.5배 증가 내지 약 70배 증가, 약 4.5배 증가 내지 약 60배 증가, 약 4.5배 증가 내지 약 50배 증가, 약 4.5배 증가 내지 약 40배 증가, 약 4.5배 증가 내지 약 30배 증가, 약 4.5배 증가 내지 약 20배 증가, 약 4.5배 증가 내지 약 10배 증가, 약 4.5배 증가 내지 약 9.5배 증가, 약 4.5배 증가 내지 약 9.0배 증가, 약 4.5배 증가 내지 약 8.5배 증가, 약 4.5배 증가 내지 약 8.0배 증가, 약 4.5배 증가 내지 약 7.5배 증가, 약 4.5배 증가 내지 약 7.0배 증가, 약 4.5배 증가 내지 약 6.5배 증가, 약 4.5배 증가 내지 약 6.0배 증가, 약 4.5배 증가 내지 약 5.5배 증가, 약 4.5배 증가 내지 약 5.0배 증가, 약 5.0배 증가 내지 약 100배 증가, 약 5.0배 증가 내지 약 90배 증가, 약 5.0배 증가 내지 약 80배 증가, 약 5.0배 증가 내지 약 70배 증가, 약 5.0배 증가 내지 약 60배 증가, 약 5.0배 증가 내지 약 50배 증가, 약 5.0배 증가 내지 약 40배 증가, 약 5.0배 증가 내지 약 30배 증가, 약 5.0배 증가 내지 약 20배 증가, 약 5.0배 증가 내지 약 10배 증가, 약 5.0배 증가 내지 약 9.5배 증가, 약 5.0배 증가 내지 약 9.0배 증가, 약 5.0배 증가 내지 약 8.5배 증가, 약 5.0배 증가 내지 약 8.0배 증가, 약 5.0배 증가 내지 약 7.5배 증가, 약 5.0배 증가 내지 약 7.0배 증가, 약 5.0배 증가 내지 약 6.5배 증가, 약 5.0배 증가 내지 약 6.0배 증가, 약 5.0배 증가 내지 약 5.5배 증가, 약 5.5배 증가 내지 약 100배 증가, 약 5.5배 증가 내지 약 90배 증가, 약 5.5배 증가 내지 약 80배 증가, 약 5.5배 증가 내지 약 70배 증가, 약 5.5배 증가 내지 약 60배 증가, 약 5.5배 증가 내지 약 50배 증가, 약 5.5배 증가 내지 약 40배 증가, 약 5.5배 증가 내지 약 30배 증가, 약 5.5배 증가 내지 약 20배 증가, 약 5.5배 증가 내지 약 10배 증가, 약 5.5배 증가 내지 약 9.5배 증가, 약 5.5배 증가 내지 약 9.0배 증가, 약 5.5배 증가 내지 약 8.5배 증가, 약 5.5배 증가 내지 약 8.0배 증가, 약 5.5배 증가 내지 약 7.5배 증가, 약 5.5배 증가 내지 약 7.0배 증가, 약 5.5배 증가 내지 약 6.5배 증가, 약 5.5배 증가 내지 약 6.0배 증가, 약 6.0배 증가 내지 약 100배 증가, 약 6.0배 증가 내지 약 90배 증가, 약 6.0배 증가 내지 약 80배 증가, 약 6.0배 증가 내지 약 70배 증가, 약 6.0배 증가 내지 약 60배 증가, 약 6.0배 증가 내지 약 50배 증가, 약 6.0배 증가 내지 약 40배 증가, 약 6.0배 증가 내지 약 30배 증가, 약 6.0배 증가 내지 약 20배 증가, 약 6.0배 증가 내지 약 10배 증가, 약 6.0배 증가 내지 약 9.5배 증가, 약 6.0배 증가 내지 약 9.0배 증가, 약 6.0배 증가 내지 약 8.5배 증가, 약 6.0배 증가 내지 약 8.0배 증가, 약 6.0배 증가 내지 약 7.5배 증가, 약 6.0배 증가 내지 약 7.0배 증가, 약 6.0배 증가 내지 약 6.5배 증가, 약 6.5배 증가 내지 약 100배 증가, 약 6.5배 증가 내지 약 90배 증가, 약 6.5배 증가 내지 약 80배 증가, 약 6.5배 증가 내지 약 70배 증가, 약 6.5배 증가 내지 약 60배 증가, 약 6.5배 증가 내지 약 50배 증가, 약 6.5배 증가 내지 약 40배 증가, 약 6.5배 증가 내지 약 30배 증가, 약 6.5배 증가 내지 약 20배 증가, 약 6.5배 증가 내지 약 10배 증가, 약 6.5배 증가 내지 약 9.5배 증가, 약 6.5배 증가 내지 약 9.0배 증가, 약 6.5배 증가 내지 약 8.5배 증가, 약 6.5배 증가 내지 약 8.0배 증가, 약 6.5배 증가 내지 약 7.5배 증가, 약 6.5배 증가 내지 약 7.0배 증가, 약 7.0배 증가 내지 약 100배 증가, 약 7.0배 증가 내지 약 90배 증가, 약 7.0배 증가 내지 약 80배 증가, 약 7.0배 증가 내지 약 70배 증가, 약 7.0배 증가 내지 약 60배 증가, 약 7.0배 증가 내지 약 50배 증가, 약 7.0배 증가 내지 약 40배 증가, 약 7.0배 증가 내지 약 30배 증가, 약 7.0배 증가 내지 약 20배 증가, 약 7.0배 증가 내지 약 10배 증가, 약 7.0배 증가 내지 약 9.5배 증가, 약 7.0배 증가 내지 약 9.0배 증가, 약 7.0배 증가 내지 약 8.5배 증가, 약 7.0배 증가 내지 약 8.0배 증가, 약 7.0배 증가 내지 약 7.5배 증가, 약 7.5배 증가 내지 약 100배 증가, 약 7.5배 증가 내지 약 90배 증가, 약 7.5배 증가 내지 약 80배 증가, 약 7.5배 증가 내지 약 70배 증가, 약 7.5배 증가 내지 약 60배 증가, 약 7.5배 증가 내지 약 50배 증가, 약 7.5배 증가 내지 약 40배 증가, 약 7.5배 증가 내지 약 30배 증가, 약 7.5배 증가 내지 약 20배 증가, 약 7.5배 증가 내지 약 10배 증가, 약 7.5배 증가 내지 약 9.5배 증가, 약 7.5배 증가 내지 약 9.0배 증가, 약 7.5배 증가 내지 약 8.5배 증가, 약 7.5배 증가 내지 약 8.0배 증가, 약 8.0배 증가 내지 약 100배 증가, 약 8.0배 증가 내지 약 90배 증가, 약 8.0배 증가 내지 약 80배 증가, 약 8.0배 증가 내지 약 70배 증가, 약 8.0배 증가 내지 약 60배 증가, 약 8.0배 증가 내지 약 50배 증가, 약 8.0배 증가 내지 약 40배 증가, 약 8.0배 증가 내지 약 30배 증가, 약 8.0배 증가 내지 약 20배 증가, 약 8.0배 증가 내지 약 10배 증가, 약 8.0배 증가 내지 약 9.5배 증가, 약 8.0배 증가 내지 약 9.0배 증가, 약 8.0배 증가 내지 약 8.5배 증가, 약 8.5배 증가 내지 약 100배 증가, 약 8.5배 증가 내지 약 90배 증가, 약 8.5배 증가 내지 약 80배 증가, 약 8.5배 증가 내지 약 70배 증가, 약 8.5배 증가 내지 약 60배 증가, 약 8.5배 증가 내지 약 50배 증가, 약 8.5배 증가 내지 약 40배 증가, 약 8.5배 증가 내지 약 30배 증가, 약 8.5배 증가 내지 약 20배 증가, 약 8.5배 증가 내지 약 10배 증가, 약 8.5배 증가 내지 약 9.5배 증가, 약 8.5배 증가 내지 약 9.0배 증가, 약 9.0배 증가 내지 약 100배 증가, 약 9.0배 증가 내지 약 90배 증가, 약 9.0배 증가 내지 약 80배 증가, 약 9.0배 증가 내지 약 70배 증가, 약 9.0배 증가 내지 약 60배 증가, 약 9.0배 증가 내지 약 50배 증가, 약 9.0배 증가 내지 약 40배 증가, 약 9.0배 증가 내지 약 30배 증가, 약 9.0배 증가 내지 약 20배 증가, 약 9.0배 증가 내지 약 10배 증가, 약 9.0배 증가 내지 약 9.5배 증가, 약 9.5배 증가 내지 약 100배 증가, 약 9.5배 증가 내지 약 90배 증가, 약 9.5배 증가 내지 약 80배 증가, 약 9.5배 증가 내지 약 70배 증가, 약 9.5배 증가 내지 약 60배 증가, 약 9.5배 증가 내지 약 50배 증가, 약 9.5배 증가 내지 약 40배 증가, 약 9.5배 증가 내지 약 30배 증가, 약 9.5배 증가 내지 약 20배 증가, 약 9.5배 증가 내지 약 10배 증가, 약 10배 증가 내지 약 100배 증가, 약 10배 증가 내지 약 90배 증가, 약 10배 증가 내지 약 80배 증가, 약 10배 증가 내지 약 70배 증가, 약 10배 증가 내지 약 60배 증가, 약 10배 증가 내지 약 50배 증가, 약 10배 증가 내지 약 40배 증가, 약 10배 증가 내지 약 30배 증가, 약 10배 증가 내지 약 20배 증가, 약 20배 증가 내지 약 100배 증가, 약 20배 증가 내지 약 90배 증가, 약 20배 증가 내지 약 80배 증가, 약 20배 증가 내지 약 70배 증가, 약 20배 증가 내지 약 60배 증가, 약 20배 증가 내지 약 50배 증가, 약 20배 증가 내지 약 40배 증가, 약 20배 증가 내지 약 30배 증가, 약 30배 증가 내지 약 100배 증가, 약 30배 증가 내지 약 90배 증가, 약 30배 증가 내지 약 80배 증가, 약 30배 증가 내지 약 70배 증가, 약 30배 증가 내지 약 60배 증가, 약 30배 증가 내지 약 50배 증가, 약 30배 증가 내지 약 40배 증가, 약 40배 증가 내지 약 100배 증가, 약 40배 증가 내지 약 90배 증가, 약 40배 증가 내지 약 80배 증가, 약 40배 증가 내지 약 70배 증가, 약 40배 증가 내지 약 60배 증가, 약 40배 증가 내지 약 50배 증가, 약 50배 증가 내지 약 100배 증가, 약 50배 증가 내지 약 90배 증가, 약 50배 증가 내지 약 80배 증가, 약 50배 증가 내지 약 70배 증가, 약 50배 증가 내지 약 60배 증가, 약 60배 증가 내지 약 100배 증가, 약 60배 증가 내지 약 90배 증가, 약 60배 증가 내지 약 80배 증가, 약 60배 증가 내지 약 70배 증가, 약 70배 증가 내지 약 100배 증가, 약 70배 증가 내지 약 90배 증가, 약 70배 증가 내지 약 80배 증가, 약 80배 증가 내지 약 100배 증가, 약 80배 증가 내지 약 90배 증가, 또는 약 90배 증가 내지 약 100배 증가시킬 수) 있다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, ABPC를 (예를 들어 본원에 기술된 ABPC 중 어느 하나를) 포함하는 조성물은 동일한 양의 대조군 ABPC (예를 들어 본원에 기술된 예시적인 대조군 ABPC 중 어느 하나)를 포함하는 조성물과 비교했을 때, 표적 포유류 (예를 들어 본원에 기술된 표적 포유류 세포 중 어느 하나의) 살해를 증가시킬 수 (예를 들어 검출 가능하게 증가시킬 수) (예를 들어 적어도 1% 증가, 적어도 2% 증가, 적어도 5% 증가, 적어도 10% 증가, 적어도 15% 증가, 적어도 20% 증가, 적어도 25% 증가, 적어도 30% 증가, 적어도 35% 증가, 적어도 40% 증가, 적어도 45% 증가, 적어도 50% 증가, 적어도 55% 증가, 적어도 60% 증가, 적어도 65% 증가, 적어도 70% 증가, 적어도 75% 증가, 적어도 80% 증가, 적어도 85% 증가, 적어도 90% 증가, 적어도 95% 증가, 적어도 100% 증가, 적어도 120% 증가, 적어도 140% 증가, 적어도 160% 증가, 적어도 180% 증가, 적어도 200% 증가, 적어도 250% 증가, 적어도 300% 증가, 적어도 350% 증가, 적어도 400% 증가, 적어도 450% 증가, 적어도 500% 증가, 적어도 1,000% 증가, 적어도 2,000% 증가, 적어도 3,000% 증가, 적어도 4,000% 증가, 적어도 5,000% 증가, 적어도 6,000% 증가, 적어도 7,000% 증가, 적어도 8,000% 증가, 적어도 9,000% 증가, 또는 적어도 10,000% 증가, 또는 약 1% 증가 내지 약 10,000% (또는 예를 들어 본원에 기술된 이 범위의 임의의 하위 범위만큼) 증가시킬 수) 있다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, ABPC를 (예를 들어 본원에 기술된 ABPC 중 어느 하나를) 포함하는 조성물은 동일한 양의 대조군 ABPC (예를 들어 본원에 기술된 예시적인 대조군 ABPC 중 어느 하나)를 포함하는 조성물과 비교했을 때, 표적 포유류 (예를 들어 본원에 기술된 표적 포유류 세포 중 어느 하나의) 살해를 증가시킬 수 (예를 들어 검출 가능하게 증가시킬 수) (예를 들어 적어도 0.1배 증가, 적어도 0.2배 증가, 적어도 0.3배 증가, 적어도 0.4배 증가, 적어도 0.5배 증가, 적어도 0.6배 증가, 적어도 0.7배 증가, 적어도 0.8배 증가, 적어도 0.9배 증가, 적어도 1.0배 증가, 적어도 1.2배 증가, 적어도 1.4배 증가, 적어도 1.5배 증가, 적어도 1.6배 증가, 적어도 1.8배 증가, 적어도 2.0배 증가, 적어도 2.2배 증가, 적어도 2.4배 증가, 적어도 2.5배 증가, 적어도 2.6배 증가, 적어도 2.8배 증가, 적어도 3.0배 증가, 적어도 3.5배 증가, 적어도 4.0배 증가, 적어도 4.5배 증가, 적어도 5.0배 증가, 적어도 5.5배 증가, 적어도 6.0배 증가, 적어도 6.5배 증가, 적어도 7.0배 증가, 적어도 7.5배 증가, 적어도 8.0배 증가, 적어도 8.5배 증가, 적어도 9.0배 증가, 적어도 9.5배 증가, 적어도 10배 증가, 적어도 15배 증가, 적어도 20배 증가, 적어도 25배 증가, 적어도 30배 증가, 적어도 35배 증가, 적어도 40배 증가, 적어도 40배 증가, 적어도 45배 증가, 적어도 50배 증가, 적어도 55배 증가, 적어도 60배 증가, 적어도 65배 증가, 적어도 70배 증가, 적어도 80배 증가, 적어도 85배 증가, 적어도 90배 증가, 적어도 95배 증가, 또는 적어도 100배 증가, 또는 약 0.1배 증가 내지 약 100배 (또는 예를 들어 본원에 기술된 이 범위의 임의의 하위 범위만큼) 증가시킬 수) 있다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 본원에 기술된 ABPC 중 어느 하나를 포함하는 조성물은 (예를 들어 표면에서 MET를 제시하는 표적 포유류 세포와 접촉할 때), 예를 들어 동일한 양의 대조군 ABPC(예를 들어 본원에 기술된 예시적인 대조군 ABPC 중 어느 하나)를 포함하는 조성물이 동일한 표적 포유류 세포와 접촉할 때의 IC50(표적 포유류 세포 사멸에 대한 IC50)과 비교했을 때, IC50을 감소시킨다(예를 들어, 적어도 1% 감소, 적어도 5% 감소, 적어도 10% 감소, 적어도 15% 감소, 적어도 20% 감소, 적어도 25% 감소, 적어도 30% 감소, 적어도 35% 감소, 적어도 40% 감소, 적어도 45% 감소, 적어도 50% 감소, 적어도 55% 감소, 적어도 60% 감소, 적어도 65% 감소, 적어도 70% 감소, 적어도 75% 감소, 적어도 80% 감소, 적어도 85% 감소, 적어도 90% 감소, 적어도 95% 감소, 또는 적어도 99% 감소, 약 1% 감소 내지 약 99% 감소, 또는 본원에 기술된 이 범위의 하위 범위 중 하나만큼 감소시킨다).
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 본원에 기술된 ABPC 중 어느 하나를 포함하는 조성물은 (예를 들어 표면에서 MET를 제시하는 표적 포유류 세포와 접촉할 때), 예를 들어 대조군 ABPC(예를 들어 본원에 기술된 예시적인 대조군 ABPC 중 어느 하나)와 비교했을 때, 중성 pH(약 7.0 내지 약 8.0의 pH)에서 표면에서 MET를 제시하는 표적 포유류 세포에 대한 KD 대 중성 pH에서 동일한 표적 세포에 대한 IC50의 비를 증가시킨다(예를 들어, 적어도 0.1배 증가, 적어도 0.2배 증가, 적어도 0.4배 증가, 적어도 0.6배 증가, 적어도 0.8배 증가, 적어도 1배 증가, 적어도 2배 증가, 적어도 5배 증가, 적어도 10배 증가, 적어도 15배 증가, 적어도 20배 증가, 적어도 25배 증가, 적어도 30배 증가, 적어도 35배 증가, 적어도 40배 증가, 적어도 45배 증가, 적어도 50배 증가, 적어도 55배 증가, 적어도 60배 증가, 적어도 65배 증가, 적어도 70배 증가, 적어도 75배 증가, 적어도 80배 증가, 적어도 85배 증가, 적어도 90배 증가, 적어도 95배 증가, 또는 적어도 100배 증가, 또는 약 0.1배 증가 내지 약 500배 (또는 본원에 기술된 이 범위의 하위 범위 중 어느 하나만큼) 증가시킨다).
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, ABPC를 (예를 들어 본원에 기술된 ABPC 중 어느 하나를) 포함하는 조성물은 동일한 양의 대조군 ABPC (예를 들어 본원에 기술된 예시적인 대조군 ABPC 중 어느 하나)를 포함하는 조성물과 비교했을 때, 표적 포유류에서 (예를 들어 본원에 기술된 표적 포유류 세포 중 어느 하나에서) 엔도리소좀 전달을 증가시킬 수 (예를 들어 검출 가능하게 증가시킬 수) (예를 들어 적어도 1% 증가, 적어도 2% 증가, 적어도 5% 증가, 적어도 10% 증가, 적어도 15% 증가, 적어도 20% 증가, 적어도 25% 증가, 적어도 30% 증가, 적어도 35% 증가, 적어도 40% 증가, 적어도 45% 증가, 적어도 50% 증가, 적어도 55% 증가, 적어도 60% 증가, 적어도 65% 증가, 적어도 70% 증가, 적어도 75% 증가, 적어도 80% 증가, 적어도 85% 증가, 적어도 90% 증가, 적어도 95% 증가, 적어도 100% 증가, 적어도 120% 증가, 적어도 140% 증가, 적어도 160% 증가, 적어도 180% 증가, 적어도 200% 증가, 적어도 250% 증가, 적어도 300% 증가, 적어도 350% 증가, 적어도 400% 증가, 적어도 450% 증가, 적어도 500% 증가, 적어도 1,000% 증가, 적어도 2,000% 증가, 적어도 3,000% 증가, 적어도 4,000% 증가, 적어도 5,000% 증가, 적어도 6,000% 증가, 적어도 7,000% 증가, 적어도 8,000% 증가, 적어도 9,000% 증가, 또는 적어도 10,000% 증가, 또는 약 1% 증가 내지 약 10,000% (또는 예를 들어 본원에 기술된 이 범위의 임의의 하위 범위만큼) 증가시킬 수) 있다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, ABPC를 (예를 들어 본원에 기술된 ABPC 중 어느 하나를) 포함하는 조성물은 동일한 양의 대조군 ABPC (예를 들어 본원에 기술된 예시적인 대조군 ABPC 중 어느 하나)를 포함하는 조성물과 비교했을 때, 표적 포유류에서 (예를 들어 본원에 기술된 표적 포유류 세포 중 어느 하나에서) 엔도리소좀 전달을 증가시킬 수 (예를 들어 검출 가능하게 증가시킬 수) (예를 들어 적어도 0.1 배 증가, 적어도 0.2 배 증가, 적어도 0.3 배 증가, 적어도 0.4 배 증가, 적어도 0.5 배 증가, 적어도 0.6 배 증가, 적어도 0.7 배 증가, 적어도 0.8 배 증가, 적어도 0.9 배 증가, 적어도 1.0 배 증가, 적어도 1.2 배 증가, 적어도 1.4 배 증가, 적어도 1.5 배 증가, 적어도 1.6 배 증가, 적어도 1.8 배 증가, 적어도 2.0 배 증가, 적어도 2.2 배 증가, 적어도 2.4 배 증가, 적어도 2.5 배 증가, 적어도 2.6 배 증가, 적어도 2.8 배 증가, 적어도 3.0 배 증가, 적어도 3.5 배 증가, 적어도 4.0 배 증가, 적어도 4.5 배 증가, 적어도 5.0 배 증가, 적어도 5.5 배 증가, 적어도 6.0 배 증가, 적어도 6.5 배 증가, 적어도 7.0 배 증가, 적어도 7.5 배 증가, 적어도 8.0 배 증가, 적어도 8.5 배 증가, 적어도 9.0 배 증가, 적어도 9.5 배 증가, 적어도 10 배 증가, 적어도 15 배 증가, 적어도 20 배 증가, 적어도 25 배 증가, 적어도 30 배 증가, 적어도 35 배 증가, 적어도 40 배 증가, 적어도 45 배 증가, 적어도 50 배 증가, 적어도 55 배 증가, 적어도 60 배 증가, 적어도 65 배 증가, 적어도 70 배 증가, 적어도 75 배 증가, 적어도 80 배 증가, 적어도 85 배 증가, 적어도 90 배 증가, 적어도 95 배 증가, 또는 적어도 100 배 증가, 또는 약 0.1 배 증가 내지 약 100 배 (또는 본원에 기술된 이 범위의 하위 범위 중 어느 하나만큼) 증가시킬 수) 있다.
본원에 기술된 ABPC 중 어느 하나의 실시예에서, 표적 포유류 세포는 FcRn 수용체를 발현하지 않거나, FcRn 발현 대조군 세포(예를 들어 HUVEC - ThermoFisher #C0035C)와 비교했을 때 더 낮은 수준으로 (예를 들어 검출 가능하게 낮은 수준으로) (예를 들어 적어도 1% 감소, 적어도 2% 감소, 적어도 5% 감소, 적어도 10% 감소, 적어도 15% 감소, 적어도 20% 감소, 적어도 25% 감소, 적어도 30% 감소, 적어도 35% 감소, 적어도 40% 감소, 적어도 45% 감소, 적어도 50% 감소, 적어도 55% 감소, 적어도 60% 감소, 적어도 65% 감소, 적어도 70% 감소, 적어도 75% 감소, 적어도 80% 감소, 적어도 85% 감소, 적어도 90% 감소, 적어도 95% 감소, 또는 적어도 99% 감소된 수준으로) FcRn을 발현한다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 표적 포유류 세포는 암 세포이다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, ABPC는 표적 포유류 세포에 대해 세포독성이거나 세포증식 억제성이다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 본원에 기술된 ABPC 중 어느 하나를 포함하는 조성물은 (예를 들어, 대상체에게 투여 시) 동일한 양의 대조군 ABPC(예를 들어 본원에 기술된 대조군 ABPC 중 어느 하나)를 포함하는 조성물과 비교했을 때 표적 세포의 표면 상에 제시된 MET 수준을 덜 감소시킨다(예를 들어 1% 내지 99% 덜 감소시키거나, 본원에 기술된 이 범위의 하위 범위 중 어느 하나만큼 덜 감소시킨다). 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 조성물은 표적 포유류 세포의 표면 상에 제시된 MET의 수준의 검출 가능한 감소를 초래하지 않는다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, ABPC는 비인간 영장류 MET 및 인간 MET와 교차 반응성이다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, ABPC는 비인간 영장류 MET, 인간 MET, 및 랫트 MET와 마우스 MET 중 하나 또는 둘 다와 교차 반응성이다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, ABPC는 비인간 영장류 MET, 인간 MET, 랫트 MET, 및 마우스 MET와 교차 반응성이다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, ABPC는 마우스 MET 및 랫트 MET와 교차 반응성이다. 본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, 항원 결합 도메인은 구세계 원숭이(Old World Monkey)의 세포 표면에 존재하는 MET의 에피토프에 결합한다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예는 제2 항원 결합 도메인(예를 들어, 본원에 기술된 예시적인 항원 결합 도메인 중 어느 하나)을 추가로 포함할 수 있다.
이들 방법의 비제한적인 양태가 아래에서 기술되고, 임의의 조합으로 제한 없이 사용될 수 있다. 이들 방법의 추가 양태는 당업계에 공지되어 있다.
MET 또는 MET의 에피토프
MET 원종양유전자, 수용체 티로신 키나아제(MET)는 당업계에 알려져 있는 종양 항원이며, 종양학에서 치료 항체의 표적이다(Wang J 등의 문헌[(2017) ABBV-399, a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors, Irrespective of MET Pathway Dependence, Clin Cancer Res, 23:992-1000]). 성숙한 인간 MET의 서열은 서열번호 9에서 확인할 수 있다. 성숙한 인간 MET를 암호화하는 cDNA의 서열은 서열번호 10에서 확인할 수 있다. MET의 세포외 도메인의 서열은 서열번호 11에서 확인할 수 있다. MET의 세포외 도메인을 암호화하는 cDNA의 서열은 서열번호 12에서 확인할 수 있다.
항원 결합 단백질 작제물
본원에 기술된 항원 결합 단백질 작제물(ABPC) 중 어느 하나는 단일 폴리펩티드이거나, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의 (동일하거나 상이한) 폴리펩티드를 포함할 수 있다. ABPC가 단일 폴리펩티드인 일부 구현예에서, ABPC는 단일 항원 결합 도메인 또는 2개의 항원 결합 도메인을 포함할 수 있다. ABPC가 단일 폴리펩티드이고 2개의 항원 결합 도메인을 포함하는 일부 구현예에서, 제1 및 제2 항원 결합 도메인은 동일하거나 서로 상이할 수 있다(또한 동일하거나 상이한 항원 또는 에피토프에 특이적으로 결합할 수 있음).
ABPC가 단일 폴리펩티드인 일부 구현예에서, 제1 항원 결합 도메인 및 제2 항원 결합 도메인(존재하는 경우)은 VH 도메인, VHH 도메인, VNAR 도메인, 및 scFv의 군으로부터 각각 독립적으로 선택될 수 있다. ABPC가 단일 폴리펩티드인 일부 구현예에서, 항원 결합 단백질 작제물은 BiTe, a (scFv)2, 나노바디, 나노바디-HSA, DART, TandAb, scDiabody, scDiabody-CH3, scFv-CH-CL-scFv, HSAbody, scDiabody-HAS, 탠덤-scFv, 애드넥틴(Adnectin), DARPin, 피브로넥틴(fibronectin), 및 DEP 접합체일 수 있다. ABPC가 단일 폴리펩티드일 때 사용될 수 있는 항원 결합 도메인의 추가 예는 당업계에 공지되어 있다.
VHH 도메인은 카멜리드에서 발견될 수 있는 단일 단량체 가변 항체 도메인이다. VNAR 도메인은 연골 어류(cartilaginous fish)에서 발견될 수 있는 단일 단량체 가변 항체 도메인이다. VHH 도메인 및 VNAR 도메인의 비제한적인 양태는 다음 문헌에 기술되어 있다: 예를 들어, Cromie 등의 문헌[Curr. Top. Med. Chem. 15:2543-2557, 2016]; De Genst 등의 문헌[Dev. Comp. Immunol. 30:187-198, 2006]; De Meyer 등의 문헌[Trends Biotechnol. 32:263-270, 2014]; Kijanka 등의 문헌[Nanomedicine 10:161-174, 2015]; Kovaleva 등의 문헌[Expert. Opin. Biol. Ther. 14:1527-1539, 2014]; Krah 등의 문헌[Immunopharmacol. Immunotoxicol. 38:21-28, 2016]; Mujic-Delic 등의 문헌[Trends Pharmacol. Sci. 35:247-255, 2014]; Muyldermans의 문헌[J. Biotechnol. 74:277-302, 2001]; Muyldermans 등의 문헌[Trends Biochem. Sci. 26:230-235, 2001]; Muyldermans의 문헌[Ann. Rev. Biochem. 82:775-797, 2013]; Rahbarizadeh 등의 문헌[Immunol. Invest. 40:299-338, 2011]; Van Audenhove 등의 문헌[EBioMedicine 8:40-48, 2016]; Van Bockstaele 등의 문헌[Curr. Opin. Investig. Drugs 10:1212-1224, 2009]; Vincke 등의 문헌[Methods Mol. Biol. 911:15-26, 2012]; 및 Wesolowski 등의 문헌[Med. Microbiol. Immunol. 198:157-174, 2009].
ABPC가 단일 폴리펩티드이고 2개의 항원 결합 도메인을 포함하는 일부 구현예에서, 제1 항원 결합 도메인 및 제2 항원 결합 도메인은 둘 다 VHH 도메인이거나, 적어도 하나의 항원 결합 도메인은 VHH 도메인일 수 있다. ABPC가 단일 폴리펩티드이고 2개의 항원 결합 도메인을 포함하는 일부 구현예에서, 제1 항원 결합 도메인 및 제2 항원 결합 도메인은 둘 다 VNAR 도메인이거나, 적어도 하나의 항원 결합 도메인은 VNAR 도메인일 수 있다. ABPC가 단일 폴리펩티드인 일부 구현예에서, 제1 항원 결합 도메인은 scFv 도메인이다. ABPC가 단일 폴리펩티드이고 2개의 항원 결합 도메인을 포함하는 일부 구현예에서, 제1 항원 결합 도메인 및 제2 항원 결합 도메인은 둘 다 scFv 도메인이거나, 적어도 하나의 항원 결합 도메인은 scFv 도메인일 수 있다.
일부 구현예에서, ABPC는 2개 이상의 폴리펩티드(예: 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의 폴리펩티드)를 포함할 수 있다. ABPC가 2개 이상의 폴리펩티드를 포함하는 일부 구현예에서, 2개 이상의 폴리펩티드 중 2개, 3개, 4개, 5개 또는 6개의 폴리펩티드는 동일할 수 있다.
ABPC가 2개 이상의 폴리펩티드(예를 들어 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의 폴리펩티드)를 포함하는 일부 구현예에서, ABPC의 폴리펩티드 중 2개 이상이 조립되어 (예를 들어 비공유 조립되어) 하나 이상의 항원 결합 도메인, 예를 들어 항체의 항원 결합 단편(예를 들어 본원에 기술된 항체의 항원 결합 단편 중 어느 하나), VHH-scAb, VHH-Fab, 이중 scFab, F(ab')2, 디아바디(diabody), crossMab, DAF (투-인-원), DAF (포-인-원), DutaMab, DT-IgG, 놉-인투-홀 공통 경쇄, 놉-인투-홀 조립체, 전하쌍, Fab-아암 교환, SEEDbody, LUZ-Y, Fcab, κλ-body, 직교 Fab, DVD-IgG, IgG(H)-scFv, scFv-(H)IgG, IgG(L)-scFv, scFv-(L)IgG, IgG(L,H)-Fv, IgG(H)-V, V(H)-IgG, IgG(L)-V, V(L)-IgG, KIH IgG-scFab, 2scFv-IgG, IgG-2scFv, scFv4-Ig, Zybody, DVI-IgG, 디아바디-CH3, 트리플바디, 미니항체(miniantibody), 미니바디(minibody), TriBi 미니바디, scFv-CH3 KIH, Fab-scFv, F(ab')2-scFv2, scFv-KIH, Fab-scFv-Fc, 4가 HCAb, scDiabody-Fc, 디아바디-Fc, 탠덤 scFv-Fc, VHH-Fc, 탠덤 VHH-Fc, VHH-Fc KiH, Fab-VHH-Fc, 인트라바디(intrabody), 독-앤-락(dock and lock), ImmTAC, IgG-IgG 접합체, Cov-X-Body, scFv1-PEG-scFv2, 애드넥틴(Adnectin), DARPin, 피브로넥틴(fibronectin), 및 DEP 접합체를 형성한다. 예를 들어 Spiess 등의 문헌[Mol. Immunol. 67:95-106, 2015]을 참조하고, 동 문헌은 이러한 요소들의 설명을 위해 그 전체가 참조로서 본원에 통합된다. 항체의 항원 결합 단편의 비제한적인 예는 Fv 단편, Fab 단편, F(ab')2 단편, 및 Fab' 단편을 포함한다. 항체의 항원 결합 단편의 추가 예는 IgG의 항원 결합 단편(예를 들어 IgG1, IgG2, IgG3, 또는 IgG4의 항원 결합 단편) (예를 들어 인간 또는 인간화 IgG1, IgG2, IgG3, 또는 IgG4와 같은 인간 또는 인간화 IgG의 항원 결합 단편); IgA의 항원 결합 단편(예를 들어 IgA1 또는 IgA2의 항원 결합 단편) (예를 들어 인간 또는 인간화 IgA1 또는 IgA2와 같은 인간 또는 인간화 IgA의 항원 결합 단편); IgD의 항원 결합 단편(예를 들어 인간 또는 인간화 IgD의 항원 결합 단편); IgE의 항원 결합 단편(예를 들어 인간 또는 인간화 IgE의 항원 결합 단편); 또는 IgM의 항원 결합 단편(예를 들어 인간 또는 인간화 IgM의 항원 결합 단편)이다.
"Fv" 단편은 하나의 중쇄 가변 도메인 및 하나의 경쇄 가변 도메인의 비공유 결합된 이량체를 포함한다.
"Fab" 단편은, Fv 단편의 중쇄 및 경쇄 가변 도메인에 더하여, 경쇄의 불변 도메인 및 중쇄의 제1 불변 도메인(CH1)을 포함한다.
"F(ab')2" 단편은 힌지 영역 근처에서 이황화 결합에 의해 결합된 2개의 Fab 단편을 포함한다.
"이중 가변 도메인 면역글로불린" 또는 "DVD-Ig"는 예를 들어 DiGiammarino 등의 문헌[Methods Mol. Biol. 899:145-156, 2012]; Jakob 등의 문헌[MABs 5:358-363, 2013]; 미국 특허 제7,612,181호; 제8,258,268호; 제8,586,714호; 제8,716,450호; 제8,722,855호; 제8,735,546호; 및 제8,822,645호(이들 각각의 그 전체가 참조로서 본원에 통합됨)에 기술된 것과 같은 다가 결합 단백질 및 다중특이적 결합 단백질을 지칭한다.
DART는 Garber의 문헌[Nature Reviews Drug Discovery 13:799-801, 2014]에 기술되어 있다.
ABPC의 추가 양태는 당업계에 공지되어 있다.
ABPC가 단일 폴리펩티드이고 2개의 항원 결합 도메인을 포함하는 일부 구현예에서, 제1 항원 결합 도메인 및 제2 항원 결합 도메인은 둘 다 VHH 도메인이거나, 적어도 하나의 항원 결합 도메인은 VHH 도메인일 수 있다. ABPC가 단일 폴리펩티드이고 2개의 항원 결합 도메인을 포함하는 일부 구현예에서, 제1 항원 결합 도메인 및 제2 항원 결합 도메인은 둘 다 VNAR 도메인이거나, 적어도 하나의 항원 결합 도메인은 VNAR 도메인일 수 있다. ABPC가 단일 폴리펩티드인 일부 구현예에서, 제1 항원 결합 도메인은 scFv 도메인이다. ABPC가 단일 폴리펩티드이고 2개의 항원 결합 도메인을 포함하는 일부 구현예에서, 제1 항원 결합 도메인 및 제2 항원 결합 도메인은 둘 다 scFv 도메인이거나, 적어도 하나의 항원 결합 도메인은 scFv 도메인일 수 있다.
일부 구현예에서, ABPC는 2개 이상의 폴리펩티드(예: 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의 폴리펩티드)를 포함할 수 있다. ABPC가 2개 이상의 폴리펩티드를 포함하는 일부 구현예에서, 2개 이상의 폴리펩티드 중 2개, 3개, 4개, 5개 또는 6개의 폴리펩티드는 동일할 수 있다.
ABPC가 2개 이상의 폴리펩티드(예를 들어 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개의 폴리펩티드)를 포함하는 일부 구현예에서, ABPC의 폴리펩티드 중 2개 이상이 조립되어 (예를 들어 비공유 조립되어) 하나 이상의 항원 결합 도메인, 예를 들어 항체의 항원 결합 단편(예를 들어 본원에 기술된 항체의 항원 결합 단편 중 어느 하나), VHH-scAb, VHH-Fab, 이중 scFab, F(ab')2, 디아바디(diabody), crossMab, DAF (투-인-원), DAF (포-인-원), DutaMab, DT-IgG, 놉-인투-홀 공통 경쇄, 놉-인투-홀 조립체, 전하쌍, Fab-아암 교환, SEEDbody, LUZ-Y, Fcab, κλ-body, 직교 Fab, DVD-IgG, IgG(H)-scFv, scFv-(H)IgG, IgG(L)-scFv, scFv-(L)IgG, IgG(L,H)-Fv, IgG(H)-V, V(H)-IgG, IgG(L)-V, V(L)-IgG, KIH IgG-scFab, 2scFv-IgG, IgG-2scFv, scFv4-Ig, Zybody, DVI-IgG, 디아바디-CH3, 트리플바디, 미니항체(miniantibody), 미니바디(minibody), TriBi 미니바디, scFv-CH3 KIH, Fab-scFv, F(ab')2-scFv2, scFv-KIH, Fab-scFv-Fc, 4가 HCAb, scDiabody-Fc, 디아바디-Fc, 탠덤 scFv-Fc, VHH-Fc, 탠덤 VHH-Fc, VHH-Fc KiH, Fab-VHH-Fc, 인트라바디(intrabody), 독-앤-락(dock and lock), ImmTAC, IgG-IgG 접합체, Cov-X-Body, scFv1-PEG-scFv2, 애드넥틴(Adnectin), DARPin, 피브로넥틴(fibronectin), 및 DEP 접합체를 형성한다. 예를 들어 Spiess 등의 문헌[Mol. Immunol. 67:95-106, 2015]을 참조하고, 동 문헌은 이러한 요소들의 설명을 위해 그 전체가 참조로서 본원에 통합된다. 항체의 항원 결합 단편의 비제한적인 예는 Fv 단편, Fab 단편, F(ab')2 단편, 및 Fab' 단편을 포함한다. 항체의 항원 결합 단편의 추가 예는 IgG의 항원 결합 단편(예를 들어 IgG1, IgG2, IgG3, 또는 IgG4의 항원 결합 단편) (예를 들어 인간 또는 인간화 IgG1, IgG2, IgG3, 또는 IgG4와 같은 인간 또는 인간화 IgG의 항원 결합 단편); IgA의 항원 결합 단편(예를 들어 IgA1 또는 IgA2의 항원 결합 단편) (예를 들어 인간 또는 인간화 IgA1 또는 IgA2와 같은 인간 또는 인간화 IgA의 항원 결합 단편); IgD의 항원 결합 단편(예를 들어 인간 또는 인간화 IgD의 항원 결합 단편); IgE의 항원 결합 단편(예를 들어 인간 또는 인간화 IgE의 항원 결합 단편); 또는 IgM의 항원 결합 단편(예를 들어 인간 또는 인간화 IgM의 항원 결합 단편)이다.
"Fv" 단편은 하나의 중쇄 가변 도메인 및 하나의 경쇄 가변 도메인의 비공유 결합된 이량체를 포함한다.
"Fab" 단편은, Fv 단편의 중쇄 및 경쇄 가변 도메인에 더하여, 경쇄의 불변 도메인 및 중쇄의 제1 불변 도메인(CH1)을 포함한다.
"F(ab')2" 단편은 힌지 영역 근처에서 이황화 결합에 의해 결합된 2개의 Fab 단편을 포함한다.
"이중 가변 도메인 면역글로불린" 또는 "DVD-Ig"는 예를 들어 DiGiammarino 등의 문헌[Methods Mol. Biol. 899:145-156, 2012]; Jakob 등의 문헌[MABs 5:358-363, 2013]; 미국 특허 제7,612,181호; 제8,258,268호; 제8,586,714호; 제8,716,450호; 제8,722,855호; 제8,735,546호; 및 제8,822,645호(이들 각각의 그 전체가 참조로서 본원에 통합됨)에 기술된 것과 같은 다가 결합 단백질 및 다중특이적 결합 단백질을 지칭한다.
DART는 Garber의 문헌[Nature Reviews Drug Discovery 13:799-801, 2014]에 기술되어 있다.
ABPC의 추가 양태는 당업계에 공지되어 있다.
항원 결합 도메인
본원에 기술된 항원 결합 단백질 작제물(ABPC) 중 어느 하나의 일부 구현예에서, 약 4.0 내지 약 6.5의 (예를 들어 약 4.0 내지 약 6.4, 약 4.0 내지 약 6.3, 약 4.0 내지 약 6.2, 약 4.0 내지 약 6.1, 약 4.0 내지 약 6.0, 약 4.0 내지 약 5.9, 약 4.0 내지 약 5.8, 약 4.0 내지 약 5.7, 약 4.0 내지 약 5.6, 약 4.0 내지 약 5.5, 약 4.0 내지 약 5.4, 약 4.0 내지 약 5.3, 약 4.0 내지 약 5.2, 약 4.0 내지 약 5.1, 약 4.0 내지 약 5.0, 약 4.0 내지 약 4.9, 약 4.0 내지 약 4.8, 약 4.0 내지 약 4.7, 약 4.0 내지 약 4.6, 약 4.0 내지 약 4.5, 약 4.0 내지 약 4.4, 약 4.0 내지 약 4.3, 약 4.0 내지 약 4.2, 약 4.0 내지 약 4.1, 약 4.1 내지 약 6.5, 약 4.1 내지 약 6.4, 약 4.1 내지 약 6.3, 약 4.1 내지 약 6.2, 약 4.1 내지 약 6.1, 약 4.1 내지 약 6.0, 약 4.1 내지 약 5.9, 약 4.1 내지 약 5.8, 약 4.1 내지 약 5.7, 약 4.1 내지 약 5.6, 약 4.1 내지 약 5.5, 약 4.1 내지 약 5.4, 약 4.1 내지 약 5.3, 약 4.1 내지 약 5.2, 약 4.1 내지 약 5.1, 약 4.1 내지 약 5.0, 약 4.1 내지 약 4.9, 약 4.1 내지 약 4.8, 약 4.1 내지 약 4.7, 약 4.1 내지 약 4.6, 약 4.1 내지 약 4.5, 약 4.1 내지 약 4.4, 약 4.1 내지 약 4.3, 약 4.1 내지 약 4.2, 약 4.2 내지 약 6.5, 약 4.2 내지 약 6.4, 약 4.2 내지 약 6.3, 약 4.2 내지 약 6.2, 약 4.2 내지 약 6.1, 약 4.2 내지 약 6.0, 약 4.2 내지 약 5.9, 약 4.2 내지 약 5.8, 약 4.2 내지 약 5.7, 약 4.2 내지 약 5.6, 약 4.2 내지 약 5.5, 약 4.2 내지 약 5.4, 약 4.2 내지 약 5.3, 약 4.2 내지 약 5.2, 약 4.2 내지 약 5.1, 약 4.2 내지 약 5.0, 약 4.2 내지 약 4.9, 약 4.2 내지 약 4.8, 약 4.2 내지 약 4.7, 약 4.2 내지 약 4.6, 약 4.2 내지 약 4.5, 약 4.2 내지 약 4.4, 약 4.2 내지 약 4.3, 약 4.3 내지 약 6.5, 약 4.3 내지 약 6.4, 약 4.3 내지 약 6.3, 약 4.3 내지 약 6.2, 약 4.3 내지 약 6.1, 약 4.3 내지 약 6.0, 약 4.3 내지 약 5.9, 약 4.3 내지 약 5.8, 약 4.3 내지 약 5.7, 약 4.3 내지 약 5.6, 약 4.3 내지 약 5.5, 약 4.3 내지 약 5.4, 약 4.3 내지 약 5.3, 약 4.3 내지 약 5.2, 약 4.3 내지 약 5.1, 약 4.3 내지 약 5.0, 약 4.3 내지 약 4.9, 약 4.3 내지 약 4.8, 약 4.3 내지 약 4.7, 약 4.3 내지 약 4.6, 약 4.3 내지 약 4.5, 약 4.3 내지 약 4.4, 약 4.4 내지 약 6.5, 약 4.4 내지 약 6.4, 약 4.4 내지 약 6.3, 약 4.4 내지 약 6.2, 약 4.4 내지 약 6.1, 약 4.4 내지 약 6.0, 약 4.4 내지 약 5.9, 약 4.4 내지 약 5.8, 약 4.4 내지 약 5.7, 약 4.4 내지 약 5.6, 약 4.4 내지 약 5.5, 약 4.4 내지 약 5.4, 약 4.4 내지 약 5.3, 약 4.4 내지 약 5.2, 약 4.4 내지 약 5.1, 약 4.4 내지 약 5.0, 약 4.4 내지 약 4.9, 약 4.4 내지 약 4.8, 약 4.4 내지 약 4.7, 약 4.4 내지 약 4.6, 약 4.4 내지 약 4.5, 약 4.5 내지 약 6.5, 약 4.5 내지 약 6.4, 약 4.5 내지 약 6.3, 약 4.5 내지 약 6.2, 약 4.5 내지 약 6.1, 약 4.5 내지 약 6.0, 약 4.5 내지 약 5.9, 약 4.5 내지 약 5.8, 약 4.5 내지 약 5.7, 약 4.5 내지 약 5.6, 약 4.5 내지 약 5.5, 약 4.5 내지 약 5.4, 약 4.5 내지 약 5.3, 약 4.5 내지 약 5.2, 약 4.5 내지 약 5.1, 약 4.5 내지 약 5.0, 약 4.5 내지 약 4.9, 약 4.5 내지 약 4.8, 약 4.5 내지 약 4.7, 약 4.5 내지 약 4.6, 약 4.6 내지 약 6.5, 약 4.6 내지 약 6.4, 약 4.6 내지 약 6.3, 약 4.6 내지 약 6.2, 약 4.6 내지 약 6.1, 약 4.6 내지 약 6.0, 약 4.6 내지 약 5.9, 약 4.6 내지 약 5.8, 약 4.6 내지 약 5.7, 약 4.6 내지 약 5.6, 약 4.6 내지 약 5.5, 약 4.6 내지 약 5.4, 약 4.6 내지 약 5.3, 약 4.6 내지 약 5.2, 약 4.6 내지 약 5.1, 약 4.6 내지 약 5.0, 약 4.6 내지 약 4.9, 약 4.6 내지 약 4.8, 약 4.6 내지 약 4.7, 약 4.7 내지 약 6.5, 약 4.7 내지 약 6.4, 약 4.7 내지 약 6.3, 약 4.7 내지 약 6.2, 약 4.7 내지 약 6.1, 약 4.7 내지 약 6.0, 약 4.7 내지 약 5.9, 약 4.7 내지 약 5.8, 약 4.7 내지 약 5.7, 약 4.7 내지 약 5.6, 약 4.7 내지 약 5.5, 약 4.7 내지 약 5.4, 약 4.7 내지 약 5.3, 약 4.7 내지 약 5.2, 약 4.7 내지 약 5.1, 약 4.7 내지 약 5.0, 약 4.7 내지 약 4.9, 약 4.7 내지 약 4.8, 약 4.8 내지 약 6.5, 약 4.8 내지 약 6.4, 약 4.8 내지 약 6.3, 약 4.8 내지 약 6.2, 약 4.8 내지 약 6.1, 약 4.8 내지 약 6.0, 약 4.8 내지 약 5.9, 약 4.8 내지 약 5.8, 약 4.8 내지 약 5.7, 약 4.8 내지 약 5.6, 약 4.8 내지 약 5.5, 약 4.8 내지 약 5.4, 약 4.8 내지 약 5.3, 약 4.8 내지 약 5.2, 약 4.8 내지 약 5.1, 약 4.8 내지 약 5.0, 약 4.8 내지 약 4.9, 약 4.9 내지 약 6.5, 약 4.9 내지 약 6.4, 약 4.9 내지 약 6.3, 약 4.9 내지 약 6.2, 약 4.9 내지 약 6.1, 약 4.9 내지 약 6.0, 약 4.9 내지 약 5.9, 약 4.9 내지 약 5.8, 약 4.9 내지 약 5.7, 약 4.9 내지 약 5.6, 약 4.9 내지 약 5.5, 약 4.9 내지 약 5.4, 약 4.9 내지 약 5.3, 약 4.9 내지 약 5.2, 약 4.9 내지 약 5.1, 약 4.9 내지 약 5.0, 약 5.0 내지 약 6.5, 약 5.0 내지 약 6.4, 약 5.0 내지 약 6.3, 약 5.0 내지 약 6.2, 약 5.0 내지 약 6.1, 약 5.0 내지 약 6.0, 약 5.0 내지 약 5.9, 약 5.0 내지 약 5.8, 약 5.0 내지 약 5.7, 약 5.0 내지 약 5.6, 약 5.0 내지 약 5.5, 약 5.0 내지 약 5.4, 약 5.0 내지 약 5.3, 약 5.0 내지 약 5.2, 약 5.0 내지 약 5.1, 약 5.1 내지 약 6.5, 약 5.1 내지 약 6.4, 약 5.1 내지 약 6.3, 약 5.1 내지 약 6.2, 약 5.1 내지 약 6.1, 약 5.1 내지 약 6.0, 약 5.1 내지 약 5.9, 약 5.1 내지 약 5.8, 약 5.1 내지 약 5.7, 약 5.1 내지 약 5.6, 약 5.1 내지 약 5.5, 약 5.1 내지 약 5.4, 약 5.1 내지 약 5.3, 약 5.1 내지 약 5.2, 약 5.2 내지 약 6.5, 약 5.2 내지 약 6.4, 약 5.2 내지 약 6.3, 약 5.2 내지 약 6.2, 약 5.2 내지 약 6.1, 약 5.2 내지 약 6.0, 약 5.2 내지 약 5.9, 약 5.2 내지 약 5.8, 약 5.2 내지 약 5.7, 약 5.2 내지 약 5.6, 약 5.2 내지 약 5.5, 약 5.2 내지 약 5.4, 약 5.2 내지 약 5.3, 약 5.3 내지 약 6.5, 약 5.3 내지 약 6.4, 약 5.3 내지 약 6.3, 약 5.3 내지 약 6.2, 약 5.3 내지 약 6.1, 약 5.3 내지 약 6.0, 약 5.3 내지 약 5.9, 약 5.3 내지 약 5.8, 약 5.3 내지 약 5.7, 약 5.3 내지 약 5.6, 약 5.3 내지 약 5.5, 약 5.3 내지 약 5.4, 약 5.4 내지 약 6.5, 약 5.4 내지 약 6.4, 약 5.4 내지 약 6.3, 약 5.4 내지 약 6.2, 약 5.4 내지 약 6.1, 약 5.4 내지 약 6.0, 약 5.4 내지 약 5.9, 약 5.4 내지 약 5.8, 약 5.4 내지 약 5.7, 약 5.4 내지 약 5.6, 약 5.4 내지 약 5.5, 약 5.5 내지 약 6.5, 약 5.5 내지 약 6.4, 약 5.5 내지 약 6.3, 약 5.5 내지 약 6.2, 약 5.5 내지 약 6.1, 약 5.5 내지 약 6.0, 약 5.5 내지 약 5.9, 약 5.5 내지 약 5.8, 약 5.5 내지 약 5.7, 약 5.5 내지 약 5.6, 약 5.6 내지 약 6.5, 약 5.6 내지 약 6.4, 약 5.6 내지 약 6.3, 약 5.6 내지 약 6.2, 약 5.6 내지 약 6.1, 약 5.6 내지 약 6.0, 약 5.6 내지 약 5.9, 약 5.6 내지 약 5.8, 약 5.6 내지 약 5.7, 약 5.7 내지 약 6.5, 약 5.7 내지 약 6.4, 약 5.7 내지 약 6.3, 약 5.7 내지 약 6.2, 약 5.7 내지 약 6.1, 약 5.7 내지 약 6.0, 약 5.7 내지 약 5.9, 약 5.7 내지 약 5.8, 약 5.8 내지 약 6.5, 약 5.8 내지 약 6.4, 약 5.8 내지 약 6.3, 약 5.8 내지 약 6.2, 약 5.8 내지 약 6.1, 약 5.8 내지 약 6.0, 약 5.8 내지 약 5.9, 약 5.9 내지 약 6.5, 약 5.9 내지 약 6.4, 약 5.9 내지 약 6.3, 약 5.9 내지 약 6.2, 약 5.9 내지 약 6.1, 약 5.9 내지 약 6.0, 약 6.0 내지 약 6.5, 약 6.0 내지 약 6.4, 약 6.0 내지 약 6.3, 약 6.0 내지 약 6.2, 약 6.0 내지 약 6.1, 약 6.1 내지 약 6.5, 약 6.1 내지 약 6.4, 약 6.1 내지 약 6.3, 약 6.1 내지 약 6.2, 약 6.2 내지 약 6.5, 약 6.2 내지 약 6.4, 약 6.2 내지 약 6.3, 약 6.3 내지 약 6.5, 약 6.3 내지 약 6.4, 또는 약 6.4 내지 약 6.5의) pH에서 제1 항원 결합 도메인의 (및, 임의로 제2 항원 결합 도메인이 존재하는 경우, 제2 항원 결합 단백질의) 해리 속도는 약 7.0 내지 약 8.0의 (예를 들어 약 7.0 내지 약 7.9, 약 7.0 내지 약 7.8, 약 7.0 내지 약 7.7, 약 7.0 내지 약 7.6, 약 7.0 내지 약 7.5, 약 7.0 내지 약 7.4, 약 7.0 내지 약 7.3, 약 7.0 내지 약 7.2, 약 7.0 내지 약 7.1, 약 7.1 내지 약 8.0, 약 7.1 내지 약 7.9, 약 7.1 내지 약 7.8, 약 7.1 내지 약 7.7, 약 7.1 내지 약 7.6, 약 7.1 내지 약 7.5, 약 7.1 내지 약 7.4, 약 7.1 내지 약 7.3, 약 7.1 내지 약 7.2, 약 7.2 내지 약 8.0, 약 7.2 내지 약 7.9, 약 7.2 내지 약 7.8, 약 7.2 내지 약 7.7, 약 7.2 내지 약 7.6, 약 7.2 내지 약 7.5, 약 7.2 내지 약 7.4, 약 7.2 내지 약 7.3, 약 7.3 내지 약 8.0, 약 7.3 내지 약 7.9, 약 7.3 내지 약 7.8, 약 7.3 내지 약 7.7, 약 7.3 내지 약 7.6, 약 7.3 내지 약 7.5, 약 7.3 내지 약 7.4, 약 7.4 내지 약 8.0, 약 7.4 내지 약 7.9, 약 7.4 내지 약 7.8, 약 7.4 내지 약 7.7, 약 7.4 내지 약 7.6, 약 7.4 내지 약 7.5, 약 7.5 내지 약 8.0, 약 7.5 내지 약 7.9, 약 7.5 내지 약 7.8, 약 7.5 내지 약 7.7, 약 7.5 내지 약 7.6, 약 7.6 내지 약 8.0, 약 7.6 내지 약 7.9, 약 7.6 내지 약 7.8, 약 7.6 내지 약 7.7, 약 7.7 내지 약 8.0, 약 7.7 내지 약 7.9, 약 7.7 내지 약 7.8, 약 7.8 내지 약 8.0, 약 7.8 내지 약 7.9, 또는 약 7.9 내지 약 8.0의) pH에서의 해리 속도보다 더 (예를 들어 적어도 5% 더, 적어도 10% 더, 적어도 15% 더, 적어도 20%, 적어도 25% 더, 적어도 30% 더, 적어도 35% 더, 적어도 40% 더, 적어도 45% 더, 적어도 50% 더, 적어도 55% 더, 적어도 60% 더, 적어도 65% 더, 적어도 70% 더, 적어도 75% 더, 적어도 80% 더, 적어도 85% 더, 적어도 90% 더, 적어도 95% 더, 적어도 100% 더, 적어도 120% 더, 적어도 140% 더, 적어도 160% 더, 적어도 180% 더, 적어도 200% 더, 적어도 220% 더 적어도 240% 더 적어도 260% 더 적어도 280% 더 적어도 300% 더 적어도 320% 더 적어도 340% 더 적어도 360% 더 적어도 380% 더 적어도 400% 더 적어도 420% 더 적어도 440% 더 적어도 460% 더 적어도 480% 더, 적어도 500% 더, 적어도 1,000% 더, 적어도 2,000% 더, 적어도 3,000% 더, 적어도 4,000% 더, 적어도 5,000%, 적어도 6,000% 더, 적어도 7,000% 더, 적어도 8,000% 더, 적어도 9,000% 더, 또는 적어도 10,000% 더, 또는 약 5% 더 내지 약 10,000% 더, 약 5% 더 내지 약 9,000% 더, 약 5% 더 내지 약 8,000% 더, 약 5% 더 내지 약 7,000% 더, 약 5% 더 내지 약 6,000% 더, 약 5% 더 내지 약 5,000% 더, 약 5% 더 내지 약 4,000% 더, 약 5% 더 내지 약 3,000% 더, 약 5% 더 내지 약 2,000% 더, 약 5% 더 내지 약 1,000% 더, 약 5% 더 내지 약 500% 더, 약 5% 더 내지 약 480% 더, 약 5% 더 내지 약 460% 더, 약 5% 더 내지 약 440% 더, 약 5% 더 내지 약 420% 더, 약 5% 더 내지 약 400% 더, 약 5% 더 내지 약 380% 더, 약 5% 더 내지 약 360% 더, 약 5% 더 내지 약 340% 더, 약 5% 더 내지 약 320% 더, 약 5% 더 내지 약 300% 더, 약 5% 더 내지 약 280% 더, 약 5% 더 내지 약 260% 더, 약 5% 더 내지 약 240% 더, 약 5% 더 내지 약 220% 더, 약 5% 더 내지 약 200% 더, 약 5% 더 내지 약 180% 더, 약 5% 더 내지 약 160% 더, 약 5% 더 내지 약 140% 더, 약 5% 더 내지 약 120% 더, 약 5% 더 내지 약 100% 더, 약 5% 더 내지 약 95% 더, 약 5% 더 내지 약 90% 더, 약 5% 더 내지 약 85% 더, 약 5% 더 내지 약 80% 더, 약 5% 더 내지 약 75% 더, 약 5% 더 내지 약 70% 더, 약 5% 더 내지 약 65% 더, 약 5% 더 내지 약 60% 더, 약 5% 더 내지 약 55% 더, 약 5% 더 내지 약 50% 더, 약 5% 더 내지 약 45% 더, 약 5% 더 내지 약 40% 더, 약 5% 더 내지 약 35% 더, 약 5% 더 내지 약 30% 더, 약 5% 더 내지 약 25% 더, 약 5% 더 내지 약 20% 더, 약 5% 더 내지 약 15% 더, 약 5% 더 내지 약 10% 더, 약 10% 더 내지 약 10,000% 더, 약 10% 더 내지 약 9,000% 더, 약 10% 더 내지 약 8,000% 더, 약 10% 더 내지 약 7,000% 더, 약 10% 더 내지 약 6,000% 더, 약 10% 더 내지 약 5,000% 더, 약 10% 더 내지 약 4,000% 더, 약 10% 더 내지 약 3,000% 더, 약 10% 더 내지 약 2,000% 더, 약 10% 더 내지 약 1,000% 더, 약 10% 더 내지 약 500% 더, 약 10% 더 내지 약 480% 더, 약 10% 더 내지 약 460% 더, 약 10% 더 내지 약 440% 더, 약 10% 더 내지 약 420% 더, 약 10% 더 내지 약 400% 더, 약 10% 더 내지 약 380% 더, 약 10% 더 내지 약 360% 더, 약 10% 더 내지 약 340% 더, 약 10% 더 내지 약 320% 더, 약 10% 더 내지 약 300% 더, 약 10% 더 내지 약 280% 더, 약 10% 더 내지 약 260% 더, 약 10% 더 내지 약 240% 더, 약 10% 더 내지 약 220% 더, 약 10% 더 내지 약 200% 더, 약 10% 더 내지 약 180% 더, 약 10% 더 내지 약 160% 더, 약 10% 더 내지 약 140% 더, 약 10% 더 내지 약 120% 더, 약 10% 더 내지 약 100% 더, 약 10% 더 내지 약 95% 더, 약 10% 더 내지 약 90% 더, 약 10% 더 내지 약 85% 더, 약 10% 더 내지 약 80% 더, 약 10% 더 내지 약 75% 더, 약 10% 더 내지 약 70% 더, 약 10% 더 내지 약 65% 더, 약 10% 더 내지 약 60% 더, 약 10% 더 내지 약 55% 더, 약 10% 더 내지 약 50% 더, 약 10% 더 내지 약 45% 더, 약 10% 더 내지 약 40% 더, 약 10% 더 내지 약 35% 더, 약 10% 더 내지 약 30% 더, 약 10% 더 내지 약 25% 더, 약 10% 더 내지 약 20% 더, 약 10% 더 내지 약 15% 더, 약 15% 더 내지 약 10,000% 더, 약 15% 더 내지 약 9,000% 더, 약 15% 더 내지 약 8,000% 더, 약 15% 더 내지 약 7,000% 더, 약 15% 더 내지 약 6,000% 더, 약 15% 더 내지 약 5,000% 더, 약 15% 더 내지 약 4,000% 더, 약 15% 더 내지 약 3,000% 더, 약 15% 더 내지 약 2,000% 더, 약 15% 더 내지 약 1,000% 더, 약 15% 더 내지 약 500% 더, 약 15% 더 내지 약 480% 더, 약 15% 더 내지 약 460% 더, 약 15% 더 내지 약 440% 더, 약 15% 더 내지 약 420% 더, 약 15% 더 내지 약 400% 더, 약 15% 더 내지 약 380% 더, 약 15% 더 내지 약 360% 더, 약 15% 더 내지 약 340% 더, 약 15% 더 내지 약 320% 더, 약 15% 더 내지 약 300% 더, 약 15% 더 내지 약 280% 더, 약 15% 더 내지 약 260% 더, 약 15% 더 내지 약 240% 더, 약 15% 더 내지 약 220% 더, 약 15% 더 내지 약 200% 더, 약 15% 더 내지 약 180% 더, 약 15% 더 내지 약 160% 더, 약 15% 더 내지 약 140% 더, 약 15% 더 내지 약 120% 더, 약 15% 더 내지 약 100% 더, 약 15% 더 내지 약 95% 더, 약 15% 더 내지 약 90% 더, 약 15% 더 내지 약 85% 더, 약 15% 더 내지 약 80% 더, 약 15% 더 내지 약 75% 더, 약 15% 더 내지 약 70% 더, 약 15% 더 내지 약 65% 더, 약 15% 더 내지 약 60% 더, 약 15% 더 내지 약 55% 더, 약 15% 더 내지 약 50% 더, 약 15% 더 내지 약 45% 더, 약 15% 더 내지 약 40% 더, 약 15% 더 내지 약 35% 더, 약 15% 더 내지 약 30% 더, 약 15% 더 내지 약 25% 더, 약 15% 더 내지 약 20% 더, 약 20% 더 내지 약 10,000% 더, 약 20% 더 내지 약 9,000% 더, 약 20% 더 내지 약 8,000% 더, 약 20% 더 내지 약 7,000% 더, 약 20% 더 내지 약 6,000% 더, 약 20% 더 내지 약 5,000% 더, 약 20% 더 내지 약 4,000% 더, 약 20% 더 내지 약 3,000% 더, 약 20% 더 내지 약 2,000% 더, 약 20% 더 내지 약 1,000% 더, 약 20% 더 내지 약 500% 더, 약 20% 더 내지 약 480% 더, 약 20% 더 내지 약 460% 더, 약 20% 더 내지 약 440% 더, 약 20% 더 내지 약 420% 더, 약 20% 더 내지 약 400% 더, 약 20% 더 내지 약 380% 더, 약 20% 더 내지 약 360% 더, 약 20% 더 내지 약 340% 더, 약 20% 더 내지 약 320% 더, 약 20% 더 내지 약 300% 더, 약 20% 더 내지 약 280% 더, 약 20% 더 내지 약 260% 더, 약 20% 더 내지 약 240% 더, 약 20% 더 내지 약 220% 더, 약 20% 더 내지 약 200% 더, 약 20% 더 내지 약 180% 더, 약 20% 더 내지 약 160% 더, 약 20% 더 내지 약 140% 더, 약 20% 더 내지 약 120% 더, 약 20% 더 내지 약 100% 더, 약 20% 더 내지 약 95% 더, 약 20% 더 내지 약 90% 더, 약 20% 더 내지 약 85% 더, 약 20% 더 내지 약 80% 더, 약 20% 더 내지 약 75% 더, 약 20% 더 내지 약 70% 더, 약 20% 더 내지 약 65% 더, 약 20% 더 내지 약 60% 더, 약 20% 더 내지 약 55% 더, 약 20% 더 내지 약 50% 더, 약 20% 더 내지 약 45% 더, 약 20% 더 내지 약 40% 더, 약 20% 더 내지 약 35% 더, 약 20% 더 내지 약 30% 더, 약 20% 더 내지 약 25% 더, 약 25% 더 내지 약 10,000% 더, 약 25% 더 내지 약 9,000% 더, 약 25% 더 내지 약 8,000% 더, 약 25% 더 내지 약 7,000% 더, 약 25% 더 내지 약 6,000% 더, 약 25% 더 내지 약 5,000% 더, 약 25% 더 내지 약 4,000% 더, 약 25% 더 내지 약 3,000% 더, 약 25% 더 내지 약 2,000% 더, 약 25% 더 내지 약 1,000% 더, 약 25% 더 내지 약 500% 더, 약 25% 더 내지 약 480% 더, 약 25% 더 내지 약 460% 더, 약 25% 더 내지 약 440% 더, 약 25% 더 내지 약 420% 더, 약 25% 더 내지 약 400% 더, 약 25% 더 내지 약 380% 더, 약 25% 더 내지 약 360% 더, 약 25% 더 내지 약 340% 더, 약 25% 더 내지 약 320% 더, 약 25% 더 내지 약 300% 더, 약 25% 더 내지 약 280% 더, 약 25% 더 내지 약 260% 더, 약 25% 더 내지 약 240% 더, 약 25% 더 내지 약 220% 더, 약 25% 더 내지 약 200% 더, 약 25% 더 내지 약 180% 더, 약 25% 더 내지 약 160% 더, 약 25% 더 내지 약 140% 더, 약 25% 더 내지 약 120% 더, 약 25% 더 내지 약 100% 더, 약 25% 더 내지 약 95% 더, 약 25% 더 내지 약 90% 더, 약 25% 더 내지 약 85% 더, 약 25% 더 내지 약 80% 더, 약 25% 더 내지 약 75% 더, 약 25% 더 내지 약 70% 더, 약 25% 더 내지 약 65% 더, 약 25% 더 내지 약 60% 더, 약 25% 더 내지 약 55% 더, 약 25% 더 내지 약 50% 더, 약 25% 더 내지 약 45% 더, 약 25% 더 내지 약 40% 더, 약 25% 더 내지 약 35% 더, 약 25% 더 내지 약 30% 더, 약 30% 더 내지 약 10,000% 더, 약 30% 더 내지 약 9,000% 더, 약 30% 더 내지 약 8,000% 더, 약 30% 더 내지 약 7,000% 더, 약 30% 더 내지 약 6,000% 더, 약 30% 더 내지 약 5,000% 더, 약 30% 더 내지 약 4,000% 더, 약 30% 더 내지 약 3,000% 더, 약 30% 더 내지 약 2,000% 더, 약 30% 더 내지 약 1,000% 더, 약 30% 더 내지 약 500% 더, 약 30% 더 내지 약 480% 더, 약 30% 더 내지 약 460% 더, 약 30% 더 내지 약 440% 더, 약 30% 더 내지 약 420% 더, 약 30% 더 내지 약 400% 더, 약 30% 더 내지 약 380% 더, 약 30% 더 내지 약 360% 더, 약 30% 더 내지 약 340% 더, 약 30% 더 내지 약 320% 더, 약 30% 더 내지 약 300% 더, 약 30% 더 내지 약 280% 더, 약 30% 더 내지 약 260% 더, 약 30% 더 내지 약 240% 더, 약 30% 더 내지 약 220% 더, 약 30% 더 내지 약 200% 더, 약 30% 더 내지 약 180% 더, 약 30% 더 내지 약 160% 더, 약 30% 더 내지 약 140% 더, 약 30% 더 내지 약 120% 더, 약 30% 더 내지 약 100% 더, 약 30% 더 내지 약 95% 더, 약 30% 더 내지 약 90% 더, 약 30% 더 내지 약 85% 더, 약 30% 더 내지 약 80% 더, 약 30% 더 내지 약 75% 더, 약 30% 더 내지 약 70% 더, 약 30% 더 내지 약 65% 더, 약 30% 더 내지 약 60% 더, 약 30% 더 내지 약 55% 더, 약 30% 더 내지 약 50% 더, 약 30% 더 내지 약 45% 더, 약 30% 더 내지 약 40% 더, 약 30% 더 내지 약 35% 더, 약 35% 더 내지 약 10,000% 더, 약 35% 더 내지 약 9,000% 더, 약 35% 더 내지 약 8,000% 더, 약 35% 더 내지 약 7,000% 더, 약 35% 더 내지 약 6,000% 더, 약 35% 더 내지 약 5,000% 더, 약 35% 더 내지 약 4,000% 더, 약 35% 더 내지 약 3,000% 더, 약 35% 더 내지 약 2,000% 더, 약 35% 더 내지 약 1,000% 더, 약 35% 더 내지 약 500% 더, 약 35% 더 내지 약 480% 더, 약 35% 더 내지 약 460% 더, 약 35% 더 내지 약 440% 더, 약 35% 더 내지 약 420% 더, 약 35% 더 내지 약 400% 더, 약 35% 더 내지 약 380% 더, 약 35% 더 내지 약 360% 더, 약 35% 더 내지 약 340% 더, 약 35% 더 내지 약 320% 더, 약 35% 더 내지 약 300% 더, 약 35% 더 내지 약 280% 더, 약 35% 더 내지 약 260% 더, 약 35% 더 내지 약 240% 더, 약 35% 더 내지 약 220% 더, 약 35% 더 내지 약 200% 더, 약 35% 더 내지 약 180% 더, 약 35% 더 내지 약 160% 더, 약 35% 더 내지 약 140% 더, 약 35% 더 내지 약 120% 더, 약 35% 더 내지 약 100% 더, 약 35% 더 내지 약 95% 더, 약 35% 더 내지 약 90% 더, 약 35% 더 내지 약 85% 더, 약 35% 더 내지 약 80% 더, 약 35% 더 내지 약 75% 더, 약 35% 더 내지 약 70% 더, 약 35% 더 내지 약 65% 더, 약 35% 더 내지 약 60% 더, 약 35% 더 내지 약 55% 더, 약 35% 더 내지 약 50% 더, 약 35% 더 내지 약 45% 더, 약 35% 더 내지 약 40% 더, 약 40% 더 내지 약 10,000% 더, 약 40% 더 내지 약 9,000% 더, 약 40% 더 내지 약 8,000% 더, 약 40% 더 내지 약 7,000% 더, 약 40% 더 내지 약 6,000% 더, 약 40% 더 내지 약 5,000% 더, 약 40% 더 내지 약 4,000% 더, 약 40% 더 내지 약 3,000% 더, 약 40% 더 내지 약 2,000% 더, 약 40% 더 내지 약 1,000% 더, 약 40% 더 내지 약 500% 더, 약 40% 더 내지 약 480% 더, 약 40% 더 내지 약 460% 더, 약 40% 더 내지 약 440% 더, 약 40% 더 내지 약 420% 더, 약 40% 더 내지 약 400% 더, 약 40% 더 내지 약 380% 더, 약 40% 더 내지 약 360% 더, 약 40% 더 내지 약 340% 더, 약 40% 더 내지 약 320% 더, 약 40% 더 내지 약 300% 더, 약 40% 더 내지 약 280% 더, 약 40% 더 내지 약 260% 더, 약 40% 더 내지 약 240% 더, 약 40% 더 내지 약 220% 더, 약 40% 더 내지 약 200% 더, 약 40% 더 내지 약 180% 더, 약 40% 더 내지 약 160% 더, 약 40% 더 내지 약 140% 더, 약 40% 더 내지 약 120% 더, 약 40% 더 내지 약 100% 더, 약 40% 더 내지 약 95% 더, 약 40% 더 내지 약 90% 더, 약 40% 더 내지 약 85% 더, 약 40% 더 내지 약 80% 더, 약 40% 더 내지 약 75% 더, 약 40% 더 내지 약 70% 더, 약 40% 더 내지 약 65% 더, 약 40% 더 내지 약 60% 더, 약 40% 더 내지 약 55% 더, 약 40% 더 내지 약 50% 더, 약 40% 더 내지 약 45% 더, 약 45% 더 내지 약 10,000% 더, 약 45% 더 내지 약 9,000% 더, 약 45% 더 내지 약 8,000% 더, 약 45% 더 내지 약 7,000% 더, 약 45% 더 내지 약 6,000% 더, 약 45% 더 내지 약 5,000% 더, 약 45% 더 내지 약 4,000% 더, 약 45% 더 내지 약 3,000% 더, 약 45% 더 내지 약 2,000% 더, 약 45% 더 내지 약 1,000% 더, 약 45% 더 내지 약 500% 더, 약 45% 더 내지 약 480% 더, 약 45% 더 내지 약 460% 더, 약 45% 더 내지 약 440% 더, 약 45% 더 내지 약 420% 더, 약 45% 더 내지 약 400% 더, 약 45% 더 내지 약 380% 더, 약 45% 더 내지 약 360% 더, 약 45% 더 내지 약 340% 더, 약 45% 더 내지 약 320% 더, 약 45% 더 내지 약 300% 더, 약 45% 더 내지 약 280% 더, 약 45% 더 내지 약 260% 더, 약 45% 더 내지 약 240% 더, 약 45% 더 내지 약 220% 더, 약 45% 더 내지 약 200% 더, 약 45% 더 내지 약 180% 더, 약 45% 더 내지 약 160% 더, 약 45% 더 내지 약 140% 더, 약 45% 더 내지 약 120% 더, 약 45% 더 내지 약 100% 더, 약 45% 더 내지 약 95% 더, 약 45% 더 내지 약 90% 더, 약 45% 더 내지 약 85% 더, 약 45% 더 내지 약 80% 더, 약 45% 더 내지 약 75% 더, 약 45% 더 내지 약 70% 더, 약 45% 더 내지 약 65% 더, 약 45% 더 내지 약 60% 더, 약 45% 더 내지 약 55% 더, 약 45% 더 내지 약 50% 더, 약 50% 더 내지 약 10,000% 더, 약 50% 더 내지 약 9,000% 더, 약 50% 더 내지 약 8,000% 더, 약 50% 더 내지 약 7,000% 더, 약 50% 더 내지 약 6,000% 더, 약 50% 더 내지 약 5,000% 더, 약 50% 더 내지 약 4,000% 더, 약 50% 더 내지 약 3,000% 더, 약 50% 더 내지 약 2,000% 더, 약 50% 더 내지 약 1,000% 더, 약 50% 더 내지 약 500% 더, 약 50% 더 내지 약 480% 더, 약 50% 더 내지 약 460% 더, 약 50% 더 내지 약 440% 더, 약 50% 더 내지 약 420% 더, 약 50% 더 내지 약 400% 더, 약 50% 더 내지 약 380% 더, 약 50% 더 내지 약 360% 더, 약 50% 더 내지 약 340% 더, 약 50% 더 내지 약 320% 더, 약 50% 더 내지 약 300% 더, 약 50% 더 내지 약 280% 더, 약 50% 더 내지 약 260% 더, 약 50% 더 내지 약 240% 더, 약 50% 더 내지 약 220% 더, 약 50% 더 내지 약 200% 더, 약 50% 더 내지 약 180% 더, 약 50% 더 내지 약 160% 더, 약 50% 더 내지 약 140% 더, 약 50% 더 내지 약 120% 더, 약 50% 더 내지 약 100% 더, 약 50% 더 내지 약 95% 더, 약 50% 더 내지 약 90% 더, 약 50% 더 내지 약 85% 더, 약 50% 더 내지 약 80% 더, 약 50% 더 내지 약 75% 더, 약 50% 더 내지 약 70% 더, 약 50% 더 내지 약 65% 더, 약 50% 더 내지 약 60% 더, 약 50% 더 내지 약 55% 더, 약 55% 더 내지 약 10,000% 더, 약 55% 더 내지 약 9,000% 더, 약 55% 더 내지 약 8,000% 더, 약 55% 더 내지 약 7,000% 더, 약 55% 더 내지 약 6,000% 더, 약 55% 더 내지 약 5,000% 더, 약 55% 더 내지 약 4,000% 더, 약 55% 더 내지 약 3,000% 더, 약 55% 더 내지 약 2,000% 더, 약 55% 더 내지 약 1,000% 더, 약 55% 더 내지 약 500% 더, 약 55% 더 내지 약 480% 더, 약 55% 더 내지 약 460% 더, 약 55% 더 내지 약 440% 더, 약 55% 더 내지 약 420% 더, 약 55% 더 내지 약 400% 더, 약 55% 더 내지 약 380% 더, 약 55% 더 내지 약 360% 더, 약 55% 더 내지 약 340% 더, 약 55% 더 내지 약 320% 더, 약 55% 더 내지 약 300% 더, 약 55% 더 내지 약 280% 더, 약 55% 더 내지 약 260% 더, 약 55% 더 내지 약 240% 더, 약 55% 더 내지 약 220% 더, 약 55% 더 내지 약 200% 더, 약 55% 더 내지 약 180% 더, 약 55% 더 내지 약 160% 더, 약 55% 더 내지 약 140% 더, 약 55% 더 내지 약 120% 더, 약 55% 더 내지 약 100% 더, 약 55% 더 내지 약 95% 더, 약 55% 더 내지 약 90% 더, 약 55% 더 내지 약 85% 더, 약 55% 더 내지 약 80% 더, 약 55% 더 내지 약 75% 더, 약 55% 더 내지 약 70% 더, 약 55% 더 내지 약 65% 더, 약 55% 더 내지 약 60% 더, 약 60% 더 내지 약 10,000% 더, 약 60% 더 내지 약 9,000% 더, 약 60% 더 내지 약 8,000% 더, 약 60% 더 내지 약 7,000% 더, 약 60% 더 내지 약 6,000% 더, 약 60% 더 내지 약 5,000% 더, 약 60% 더 내지 약 4,000% 더, 약 60% 더 내지 약 3,000% 더, 약 60% 더 내지 약 2,000% 더, 약 60% 더 내지 약 1,000% 더, 약 60% 더 내지 약 500% 더, 약 60% 더 내지 약 480% 더, 약 60% 더 내지 약 460% 더, 약 60% 더 내지 약 440% 더, 약 60% 더 내지 약 420% 더, 약 60% 더 내지 약 400% 더, 약 60% 더 내지 약 380% 더, 약 60% 더 내지 약 360% 더, 약 60% 더 내지 약 340% 더, 약 60% 더 내지 약 320% 더, 약 60% 더 내지 약 300% 더, 약 60% 더 내지 약 280% 더, 약 60% 더 내지 약 260% 더, 약 60% 더 내지 약 240% 더, 약 60% 더 내지 약 220% 더, 약 60% 더 내지 약 200% 더, 약 60% 더 내지 약 180% 더, 약 60% 더 내지 약 160% 더, 약 60% 더 내지 약 140% 더, 약 60% 더 내지 약 120% 더, 약 60% 더 내지 약 100% 더, 약 60% 더 내지 약 95% 더, 약 60% 더 내지 약 90% 더, 약 60% 더 내지 약 85% 더, 약 60% 더 내지 약 80% 더, 약 60% 더 내지 약 75% 더, 약 60% 더 내지 약 70% 더, 약 60% 더 내지 약 65% 더, 약 65% 더 내지 약 10,000% 더, 약 65% 더 내지 약 9,000% 더, 약 65% 더 내지 약 8,000% 더, 약 65% 더 내지 약 7,000% 더, 약 65% 더 내지 약 6,000% 더, 약 65% 더 내지 약 5,000% 더, 약 65% 더 내지 약 4,000% 더, 약 65% 더 내지 약 3,000% 더, 약 65% 더 내지 약 2,000% 더, 약 65% 더 내지 약 1,000% 더, 약 65% 더 내지 약 500% 더, 약 65% 더 내지 약 480% 더, 약 65% 더 내지 약 460% 더, 약 65% 더 내지 약 440% 더, 약 65% 더 내지 약 420% 더, 약 65% 더 내지 약 400% 더, 약 65% 더 내지 약 380% 더, 약 65% 더 내지 약 360% 더, 약 65% 더 내지 약 340% 더, 약 65% 더 내지 약 320% 더, 약 65% 더 내지 약 300% 더, 약 65% 더 내지 약 280% 더, 약 65% 더 내지 약 260% 더, 약 65% 더 내지 약 240% 더, 약 65% 더 내지 약 220% 더, 약 65% 더 내지 약 200% 더, 약 65% 더 내지 약 180% 더, 약 65% 더 내지 약 160% 더, 약 65% 더 내지 약 140% 더, 약 65% 더 내지 약 120% 더, 약 65% 더 내지 약 100% 더, 약 65% 더 내지 약 95% 더, 약 65% 더 내지 약 90% 더, 약 65% 더 내지 약 85% 더, 약 65% 더 내지 약 80% 더, 약 65% 더 내지 약 75% 더, 약 65% 더 내지 약 70% 더, 약 70% 더 내지 약 10,000% 더, 약 70% 더 내지 약 9,000% 더, 약 70% 더 내지 약 8,000% 더, 약 70% 더 내지 약 7,000% 더, 약 70% 더 내지 약 6,000% 더, 약 70% 더 내지 약 5,000% 더, 약 70% 더 내지 약 4,000% 더, 약 70% 더 내지 약 3,000% 더, 약 70% 더 내지 약 2,000% 더, 약 70% 더 내지 약 1,000% 더, 약 70% 더 내지 약 500% 더, 약 70% 더 내지 약 480% 더, 약 70% 더 내지 약 460% 더, 약 70% 더 내지 약 440% 더, 약 70% 더 내지 약 420% 더, 약 70% 더 내지 약 400% 더, 약 70% 더 내지 약 380% 더, 약 70% 더 내지 약 360% 더, 약 70% 더 내지 약 340% 더, 약 70% 더 내지 약 320% 더, 약 70% 더 내지 약 300% 더, 약 70% 더 내지 약 280% 더, 약 70% 더 내지 약 260% 더, 약 70% 더 내지 약 240% 더, 약 70% 더 내지 약 220% 더, 약 70% 더 내지 약 200% 더, 약 70% 더 내지 약 180% 더, 약 70% 더 내지 약 160% 더, 약 70% 더 내지 약 140% 더, 약 70% 더 내지 약 120% 더, 약 70% 더 내지 약 100% 더, 약 70% 더 내지 약 95% 더, 약 70% 더 내지 약 90% 더, 약 70% 더 내지 약 85% 더, 약 70% 더 내지 약 80% 더, 약 70% 더 내지 약 75% 더, 약 75% 더 내지 약 10,000% 더, 약 75% 더 내지 약 9,000% 더, 약 75% 더 내지 약 8,000% 더, 약 75% 더 내지 약 7,000% 더, 약 75% 더 내지 약 6,000% 더, 약 75% 더 내지 약 5,000% 더, 약 75% 더 내지 약 4,000% 더, 약 75% 더 내지 약 3,000% 더, 약 75% 더 내지 약 2,000% 더, 약 75% 더 내지 약 1,000% 더, 약 75% 더 내지 약 500% 더, 약 75% 더 내지 약 480% 더, 약 75% 더 내지 약 460% 더, 약 75% 더 내지 약 440% 더, 약 75% 더 내지 약 420% 더, 약 75% 더 내지 약 400% 더, 약 75% 더 내지 약 380% 더, 약 75% 더 내지 약 360% 더, 약 75% 더 내지 약 340% 더, 약 75% 더 내지 약 320% 더, 약 75% 더 내지 약 300% 더, 약 75% 더 내지 약 280% 더, 약 75% 더 내지 약 260% 더, 약 75% 더 내지 약 240% 더, 약 75% 더 내지 약 220% 더, 약 75% 더 내지 약 200% 더, 약 75% 더 내지 약 180% 더, 약 75% 더 내지 약 160% 더, 약 75% 더 내지 약 140% 더, 약 75% 더 내지 약 120% 더, 약 75% 더 내지 약 100% 더, 약 75% 더 내지 약 95% 더, 약 75% 더 내지 약 90% 더, 약 75% 더 내지 약 85% 더, 약 75% 더 내지 약 80% 더, 약 80% 더 내지 약 10,000% 더, 약 80% 더 내지 약 9,000% 더, 약 80% 더 내지 약 8,000% 더, 약 80% 더 내지 약 7,000% 더, 약 80% 더 내지 약 6,000% 더, 약 80% 더 내지 약 5,000% 더, 약 80% 더 내지 약 4,000% 더, 약 80% 더 내지 약 3,000% 더, 약 80% 더 내지 약 2,000% 더, 약 80% 더 내지 약 1,000% 더, 약 80% 더 내지 약 500% 더, 약 80% 더 내지 약 480% 더, 약 80% 더 내지 약 460% 더, 약 80% 더 내지 약 440% 더, 약 80% 더 내지 약 420% 더, 약 80% 더 내지 약 400% 더, 약 80% 더 내지 약 380% 더, 약 80% 더 내지 약 360% 더, 약 80% 더 내지 약 340% 더, 약 80% 더 내지 약 320% 더, 약 80% 더 내지 약 300% 더, 약 80% 더 내지 약 280% 더, 약 80% 더 내지 약 260% 더, 약 80% 더 내지 약 240% 더, 약 80% 더 내지 약 220% 더, 약 80% 더 내지 약 200% 더, 약 80% 더 내지 약 180% 더, 약 80% 더 내지 약 160% 더, 약 80% 더 내지 약 140% 더, 약 80% 더 내지 약 120% 더, 약 80% 더 내지 약 100% 더, 약 80% 더 내지 약 95% 더, 약 80% 더 내지 약 90% 더, 약 80% 더 내지 약 85% 더, 약 85% 더 내지 약 10,000% 더, 약 85% 더 내지 약 9,000% 더, 약 85% 더 내지 약 8,000% 더, 약 85% 더 내지 약 7,000% 더, 약 85% 더 내지 약 6,000% 더, 약 85% 더 내지 약 5,000% 더, 약 85% 더 내지 약 4,000% 더, 약 85% 더 내지 약 3,000% 더, 약 85% 더 내지 약 2,000% 더, 약 85% 더 내지 약 1,000% 더, 약 85% 더 내지 약 500% 더, 약 85% 더 내지 약 480% 더, 약 85% 더 내지 약 460% 더, 약 85% 더 내지 약 440% 더, 약 85% 더 내지 약 420% 더, 약 85% 더 내지 약 400% 더, 약 85% 더 내지 약 380% 더, 약 85% 더 내지 약 360% 더, 약 85% 더 내지 약 340% 더, 약 85% 더 내지 약 320% 더, 약 85% 더 내지 약 300% 더, 약 85% 더 내지 약 280% 더, 약 85% 더 내지 약 260% 더, 약 85% 더 내지 약 240% 더, 약 85% 더 내지 약 220% 더, 약 85% 더 내지 약 200% 더, 약 85% 더 내지 약 180% 더, 약 85% 더 내지 약 160% 더, 약 85% 더 내지 약 140% 더, 약 85% 더 내지 약 120% 더, 약 85% 더 내지 약 100% 더, 약 85% 더 내지 약 95% 더, 약 85% 더 내지 약 90% 더, 약 90% 더 내지 약 10,000% 더, 약 90% 더 내지 약 9,000% 더, 약 90% 더 내지 약 8,000% 더, 약 90% 더 내지 약 7,000% 더, 약 90% 더 내지 약 6,000% 더, 약 90% 더 내지 약 5,000% 더, 약 90% 더 내지 약 4,000% 더, 약 90% 더 내지 약 3,000% 더, 약 90% 더 내지 약 2,000% 더, 약 90% 더 내지 약 1,000% 더, 약 90% 더 내지 약 500% 더, 약 90% 더 내지 약 480% 더, 약 90% 더 내지 약 460% 더, 약 90% 더 내지 약 440% 더, 약 90% 더 내지 약 420% 더, 약 90% 더 내지 약 400% 더, 약 90% 더 내지 약 380% 더, 약 90% 더 내지 약 360% 더, 약 90% 더 내지 약 340% 더, 약 90% 더 내지 약 320% 더, 약 90% 더 내지 약 300% 더, 약 90% 더 내지 약 280% 더, 약 90% 더 내지 약 260% 더, 약 90% 더 내지 약 240% 더, 약 90% 더 내지 약 220% 더, 약 90% 더 내지 약 200% 더, 약 90% 더 내지 약 180% 더, 약 90% 더 내지 약 160% 더, 약 90% 더 내지 약 140% 더, 약 90% 더 내지 약 120% 더, 약 90% 더 내지 약 100% 더, 약 90% 더 내지 약 95% 더, 약 95% 더 내지 약 10,000% 더, 약 95% 더 내지 약 9,000% 더, 약 95% 더 내지 약 8,000% 더, 약 95% 더 내지 약 7,000% 더, 약 95% 더 내지 약 6,000% 더, 약 95% 더 내지 약 5,000% 더, 약 95% 더 내지 약 4,000% 더, 약 95% 더 내지 약 3,000% 더, 약 95% 더 내지 약 2,000% 더, 약 95% 더 내지 약 1,000% 더, 약 95% 더 내지 약 500% 더, 약 95% 더 내지 약 480% 더, 약 95% 더 내지 약 460% 더, 약 95% 더 내지 약 440% 더, 약 95% 더 내지 약 420% 더, 약 95% 더 내지 약 400% 더, 약 95% 더 내지 약 380% 더, 약 95% 더 내지 약 360% 더, 약 95% 더 내지 약 340% 더, 약 95% 더 내지 약 320% 더, 약 95% 더 내지 약 300% 더, 약 95% 더 내지 약 280% 더, 약 95% 더 내지 약 260% 더, 약 95% 더 내지 약 240% 더, 약 95% 더 내지 약 220% 더, 약 95% 더 내지 약 200% 더, 약 95% 더 내지 약 180% 더, 약 95% 더 내지 약 160% 더, 약 95% 더 내지 약 140% 더, 약 95% 더 내지 약 120% 더, 약 95% 더 내지 약 100% 더, 약 100% 더 내지 약 10,000% 더, 약 100% 더 내지 약 9,000% 더, 약 100% 더 내지 약 8,000% 더, 약 100% 더 내지 약 7,000% 더, 약 100% 더 내지 약 6,000% 더, 약 100% 더 내지 약 5,000% 더, 약 100% 더 내지 약 4,000% 더, 약 100% 더 내지 약 3,000% 더, 약 100% 더 내지 약 2,000% 더, 약 100% 더 내지 약 1,000% 더, 약 100% 더 내지 약 500% 더, 약 100% 더 내지 약 480% 더, 약 100% 더 내지 약 460% 더, 약 100% 더 내지 약 440% 더, 약 100% 더 내지 약 420% 더, 약 100% 더 내지 약 400% 더, 약 100% 더 내지 약 380% 더, 약 100% 더 내지 약 360% 더, 약 100% 더 내지 약 340% 더, 약 100% 더 내지 약 320% 더, 약 100% 더 내지 약 300% 더, 약 100% 더 내지 약 280% 더, 약 100% 더 내지 약 260% 더, 약 100% 더 내지 약 240% 더, 약 100% 더 내지 약 220% 더, 약 100% 더 내지 약 200% 더, 약 100% 더 내지 약 180% 더, 약 100% 더 내지 약 160% 더, 약 100% 더 내지 약 140% 더, 약 100% 더 내지 약 120% 더, 약 120% 더 내지 약 10,000% 더, 약 120% 더 내지 약 9,000% 더, 약 120% 더 내지 약 8,000% 더, 약 120% 더 내지 약 7,000% 더, 약 120% 더 내지 약 6,000% 더, 약 120% 더 내지 약 5,000% 더, 약 120% 더 내지 약 4,000% 더, 약 120% 더 내지 약 3,000% 더, 약 120% 더 내지 약 2,000% 더, 약 120% 더 내지 약 1,000% 더, 약 120% 더 내지 약 500% 더, 약 120% 더 내지 약 480% 더, 약 120% 더 내지 약 460% 더, 약 120% 더 내지 약 440% 더, 약 120% 더 내지 약 420% 더, 약 120% 더 내지 약 400% 더, 약 120% 더 내지 약 380% 더, 약 120% 더 내지 약 360% 더, 약 120% 더 내지 약 340% 더, 약 120% 더 내지 약 320% 더, 약 120% 더 내지 약 300% 더, 약 120% 더 내지 약 280% 더, 약 120% 더 내지 약 260% 더, 약 120% 더 내지 약 240% 더, 약 120% 더 내지 약 220% 더, 약 120% 더 내지 약 200% 더, 약 120% 더 내지 약 180% 더, 약 120% 더 내지 약 160% 더, 약 120% 더 내지 약 140% 더, 약 140% 더 내지 약 10,000% 더, 약 140% 더 내지 약 9,000% 더, 약 140% 더 내지 약 8,000% 더, 약 140% 더 내지 약 7,000% 더, 약 140% 더 내지 약 6,000% 더, 약 140% 더 내지 약 5,000% 더, 약 140% 더 내지 약 4,000% 더, 약 140% 더 내지 약 3,000% 더, 약 140% 더 내지 약 2,000% 더, 약 140% 더 내지 약 1,000% 더, 약 140% 더 내지 약 500% 더, 약 140% 더 내지 약 480% 더, 약 140% 더 내지 약 460% 더, 약 140% 더 내지 약 440% 더, 약 140% 더 내지 약 420% 더, 약 140% 더 내지 약 400% 더, 약 140% 더 내지 약 380% 더, 약 140% 더 내지 약 360% 더, 약 140% 더 내지 약 340% 더, 약 140% 더 내지 약 320% 더, 약 140% 더 내지 약 300% 더, 약 140% 더 내지 약 280% 더, 약 140% 더 내지 약 260% 더, 약 140% 더 내지 약 240% 더, 약 140% 더 내지 약 220% 더, 약 140% 더 내지 약 200% 더, 약 140% 더 내지 약 180% 더, 약 140% 더 내지 약 160% 더, 약 160% 더 내지 약 10,000% 더, 약 160% 더 내지 약 9,000% 더, 약 160% 더 내지 약 8,000% 더, 약 160% 더 내지 약 7,000% 더, 약 160% 더 내지 약 6,000% 더, 약 160% 더 내지 약 5,000% 더, 약 160% 더 내지 약 4,000% 더, 약 160% 더 내지 약 3,000% 더, 약 160% 더 내지 약 2,000% 더, 약 160% 더 내지 약 1,000% 더, 약 160% 더 내지 약 500% 더, 약 160% 더 내지 약 480% 더, 약 160% 더 내지 약 460% 더, 약 160% 더 내지 약 440% 더, 약 160% 더 내지 약 420% 더, 약 160% 더 내지 약 400% 더, 약 160% 더 내지 약 380% 더, 약 160% 더 내지 약 360% 더, 약 160% 더 내지 약 340% 더, 약 160% 더 내지 약 320% 더, 약 160% 더 내지 약 300% 더, 약 160% 더 내지 약 280% 더, 약 160% 더 내지 약 260% 더, 약 160% 더 내지 약 240% 더, 약 160% 더 내지 약 220% 더, 약 160% 더 내지 약 200% 더, 약 160% 더 내지 약 180% 더, 약 180% 더 내지 약 10,000% 더, 약 180% 더 내지 약 9,000% 더, 약 180% 더 내지 약 8,000% 더, 약 180% 더 내지 약 7,000% 더, 약 180% 더 내지 약 6,000% 더, 약 180% 더 내지 약 5,000% 더, 약 180% 더 내지 약 4,000% 더, 약 180% 더 내지 약 3,000% 더, 약 180% 더 내지 약 2,000% 더, 약 180% 더 내지 약 1,000% 더, 약 180% 더 내지 약 500% 더, 약 180% 더 내지 약 480% 더, 약 180% 더 내지 약 460% 더, 약 180% 더 내지 약 440% 더, 약 180% 더 내지 약 420% 더, 약 180% 더 내지 약 400% 더, 약 180% 더 내지 약 380% 더, 약 180% 더 내지 약 360% 더, 약 180% 더 내지 약 340% 더, 약 180% 더 내지 약 320% 더, 약 180% 더 내지 약 300% 더, 약 180% 더 내지 약 280% 더, 약 180% 더 내지 약 260% 더, 약 180% 더 내지 약 240% 더, 약 180% 더 내지 약 220% 더, 약 180% 더 내지 약 200% 더, 약 200% 더 내지 약 10,000% 더, 약 200% 더 내지 약 9,000% 더, 약 200% 더 내지 약 8,000% 더, 약 200% 더 내지 약 7,000% 더, 약 200% 더 내지 약 6,000% 더, 약 200% 더 내지 약 5,000% 더, 약 200% 더 내지 약 4,000% 더, 약 200% 더 내지 약 3,000% 더, 약 200% 더 내지 약 2,000% 더, 약 200% 더 내지 약 1,000% 더, 약 200% 더 내지 약 500% 더, 약 200% 더 내지 약 480% 더, 약 200% 더 내지 약 460% 더, 약 200% 더 내지 약 440% 더, 약 200% 더 내지 약 420% 더, 약 200% 더 내지 약 400% 더, 약 200% 더 내지 약 380% 더, 약 200% 더 내지 약 360% 더, 약 200% 더 내지 약 340% 더, 약 200% 더 내지 약 320% 더, 약 200% 더 내지 약 300% 더, 약 200% 더 내지 약 280% 더, 약 200% 더 내지 약 260% 더, 약 200% 더 내지 약 240% 더, 약 200% 더 내지 약 220% 더, 약 220% 더 내지 약 10,000% 더, 약 220% 더 내지 약 9,000% 더, 약 220% 더 내지 약 8,000% 더, 약 220% 더 내지 약 7,000% 더, 약 220% 더 내지 약 6,000% 더, 약 220% 더 내지 약 5,000% 더, 약 220% 더 내지 약 4,000% 더, 약 220% 더 내지 약 3,000% 더, 약 220% 더 내지 약 2,000% 더, 약 220% 더 내지 약 1,000% 더,약 220% 더 내지 약 500% 더, 약 220% 더 내지 약 480% 더, 약 220% 더 내지 약 460% 더, 약 220% 더 내지 약 440% 더, 약 220% 더 내지 약 420% 더, 약 220% 더 내지 약 400% 더, 약 220% 더 내지 약 380% 더, 약 220% 더 내지 약 360% 더, 약 220% 더 내지 약 340% 더, 약 220% 더 내지 약 320% 더, 약 220% 더 내지 약 300% 더, 약 220% 더 내지 약 280% 더, 약 220% 더 내지 약 260% 더, 약 220% 더 내지 약 240% 더, 약 240% 더 내지 약 10,000% 더, 약 240% 더 내지 약 9,000% 더, 약 240% 더 내지 약 8,000% 더, 약 240% 더 내지 약 7,000% 더, 약 240% 더 내지 약 6,000% 더, 약 240% 더 내지 약 5,000% 더, 약 240% 더 내지 약 4,000% 더, 약 240% 더 내지 약 3,000% 더, 약 240% 더 내지 약 2,000% 더, 약 240% 더 내지 약 1,000% 더, 약 240% 더 내지 약 500% 더, 약 240% 더 내지 약 480% 더, 약 240% 더 내지 약 460% 더, 약 240% 더 내지 약 440% 더, 약 240% 더 내지 약 420% 더, 약 240% 더 내지 약 400% 더, 약 240% 더 내지 약 380% 더, 약 240% 더 내지 약 360% 더, 약 240% 더 내지 약 340% 더, 약 240% 더 내지 약 320% 더, 약 240% 더 내지 약 300% 더, 약 240% 더 내지 약 280% 더, 약 240% 더 내지 약 260% 더, 약 260% 더 내지 약 10,000% 더, 약 260% 더 내지 약 9,000% 더, 약 260% 더 내지 약 8,000% 더, 약 260% 더 내지 약 7,000% 더, 약 260% 더 내지 약 6,000% 더, 약 260% 더 내지 약 5,000% 더, 약 260% 더 내지 약 4,000% 더, 약 260% 더 내지 약 3,000% 더, 약 260% 더 내지 약 2,000% 더, 약 260% 더 내지 약 1,000% 더, 약 260% 더 내지 약 500% 더, 약 260% 더 내지 약 480% 더, 약 260% 더 내지 약 460% 더, 약 260% 더 내지 약 440% 더, 약 260% 더 내지 약 420% 더, 약 260% 더 내지 약 400% 더, 약 260% 더 내지 약 380% 더, 약 260% 더 내지 약 360% 더, 약 260% 더 내지 약 340% 더, 약 260% 더 내지 약 320% 더, 약 260% 더 내지 약 300% 더, 약 260% 더 내지 약 280% 더, 약 280% 더 내지 약 10,000% 더, 약 280% 더 내지 약 9,000% 더, 약 280% 더 내지 약 8,000% 더, 약 280% 더 내지 약 7,000% 더, 약 280% 더 내지 약 6,000% 더, 약 280% 더 내지 약 5,000% 더, 약 280% 더 내지 약 4,000% 더, 약 280% 더 내지 약 3,000% 더, 약 280% 더 내지 약 2,000% 더, 약 280% 더 내지 약 1,000% 더, 약 280% 더 내지 약 500% 더, 약 280% 더 내지 약 480% 더, 약 280% 더 내지 약 460% 더, 약 280% 더 내지 약 440% 더, 약 280% 더 내지 약 420% 더, 약 280% 더 내지 약 400% 더, 약 280% 더 내지 약 380% 더, 약 280% 더 내지 약 360% 더, 약 280% 더 내지 약 340% 더, 약 280% 더 내지 약 320% 더, 약 280% 더 내지 약 300% 더, 약 300% 더 내지 약 10,000% 더, 약 300% 더 내지 약 9,000% 더, 약 300% 더 내지 약 8,000% 더, 약 300% 더 내지 약 7,000% 더, 약 300% 더 내지 약 6,000% 더, 약 300% 더 내지 약 5,000% 더, 약 300% 더 내지 약 4,000% 더, 약 300% 더 내지 약 3,000% 더, 약 300% 더 내지 약 2,000% 더, 약 300% 더 내지 약 1,000% 더, 약 300% 더 내지 약 500% 더, 약 300% 더 내지 약 480% 더, 약 300% 더 내지 약 460% 더, 약 300% 더 내지 약 440% 더, 약 300% 더 내지 약 420% 더, 약 300% 더 내지 약 400% 더, 약 300% 더 내지 약 380% 더, 약 300% 더 내지 약 360% 더, 약 300% 더 내지 약 340% 더, 약 300% 더 내지 약 320% 더, 약 320% 더 내지 약 10,000% 더, 약 320% 더 내지 약 9,000% 더, 약 320% 더 내지 약 8,000% 더, 약 320% 더 내지 약 7,000% 더, 약 320% 더 내지 약 6,000% 더, 약 320% 더 내지 약 5,000% 더, 약 320% 더 내지 약 4,000% 더, 약 320% 더 내지 약 3,000% 더, 약 320% 더 내지 약 2,000% 더, 약 320% 더 내지 약 1,000% 더, 약 320% 더 내지 약 500% 더, 약 320% 더 내지 약 480% 더, 약 320% 더 내지 약 460% 더, 약 320% 더 내지 약 440% 더, 약 320% 더 내지 약 420% 더, 약 320% 더 내지 약 400% 더, 약 320% 더 내지 약 380% 더, 약 320% 더 내지 약 360% 더, 약 320% 더 내지 약 340% 더, 약 340% 더 내지 약 10,000% 더, 약 340% 더 내지 약 9,000% 더, 약 340% 더 내지 약 8,000% 더, 약 340% 더 내지 약 7,000% 더, 약 340% 더 내지 약 6,000% 더, 약 340% 더 내지 약 5,000% 더, 약 340% 더 내지 약 4,000% 더, 약 340% 더 내지 약 3,000% 더, 약 340% 더 내지 약 2,000% 더, 약 340% 더 내지 약 1,000% 더, 약 340% 더 내지 약 500% 더, 약 340% 더 내지 약 480% 더, 약 340% 더 내지 약 460% 더, 약 340% 더 내지 약 440% 더, 약 340% 더 내지 약 420% 더, 약 340% 더 내지 약 400% 더, 약 340% 더 내지 약 380% 더, 약 340% 더 내지 약 360% 더, 약 360% 더 내지 약 10,000% 더, 약 360% 더 내지 약 9,000% 더, 약 360% 더 내지 약 8,000% 더, 약 360% 더 내지 약 7,000% 더, 약 360% 더 내지 약 6,000% 더, 약 360% 더 내지 약 5,000% 더, 약 360% 더 내지 약 4,000% 더, 약 360% 더 내지 약 3,000% 더, 약 360% 더 내지 약 2,000% 더, 약 360% 더 내지 약 1,000% 더, 약 360% 더 내지 약 500% 더, 약 360% 더 내지 약 480% 더, 약 360% 더 내지 약 460% 더, 약 360% 더 내지 약 440% 더, 약 360% 더 내지 약 420% 더, 약 360% 더 내지 약 400% 더, 약 360% 더 내지 약 380% 더, 약 380% 더 내지 약 10,000% 더, 약 380% 더 내지 약 9,000% 더, 약 380% 더 내지 약 8,000% 더, 약 380% 더 내지 약 7,000% 더, 약 380% 더 내지 약 6,000% 더, 약 380% 더 내지 약 5,000% 더, 약 380% 더 내지 약 4,000% 더, 약 380% 더 내지 약 3,000% 더, 약 380% 더 내지 약 2,000% 더, 약 380% 더 내지 약 1,000% 더, 약 380% 더 내지 약 500% 더, 약 380% 더 내지 약 480% 더, 약 380% 더 내지 약 460% 더, 약 380% 더 내지 약 440% 더, 약 380% 더 내지 약 420% 더, 약 380% 더 내지 약 400% 더, 약 400% 더 내지 약 10,000% 더, 약 400% 더 내지 약 9,000% 더, 약 400% 더 내지 약 8,000% 더, 약 400% 더 내지 약 7,000% 더, 약 400% 더 내지 약 6,000% 더, 약 400% 더 내지 약 5,000% 더, 약 400% 더 내지 약 4,000% 더, 약 400% 더 내지 약 3,000% 더, 약 400% 더 내지 약 2,000% 더, 약 400% 더 내지 약 1,000% 더, 약 400% 더 내지 약 500% 더, 약 400% 더 내지 약 480% 더, 약 400% 더 내지 약 460% 더, 약 400% 더 내지 약 440% 더, 약 400% 더 내지 약 420% 더, 약 420% 더 내지 약 10,000% 더, 약 420% 더 내지 약 9,000% 더, 약 420% 더 내지 약 8,000% 더, 약 420% 더 내지 약 7,000% 더, 약 420% 더 내지 약 6,000% 더, 약 420% 더 내지 약 5,000% 더, 약 420% 더 내지 약 4,000% 더, 약 420% 더 내지 약 3,000% 더, 약 420% 더 내지 약 2,000% 더, 약 420% 더 내지 약 1,000% 더,약 420% 더 내지 약 500% 더, 약 420% 더 내지 약 480% 더, 약 420% 더 내지 약 460% 더, 약 420% 더 내지 약 440% 더, 약 440% 더 내지 약 10,000% 더, 약 440% 더 내지 약 9,000% 더, 약 440% 더 내지 약 8,000% 더, 약 440% 더 내지 약 7,000% 더, 약 440% 더 내지 약 6,000% 더, 약 440% 더 내지 약 5,000% 더, 약 440% 더 내지 약 4,000% 더, 약 440% 더 내지 약 3,000% 더, 약 440% 더 내지 약 2,000% 더, 약 440% 더 내지 약 1,000% 더,약 440% 더 내지 약 500% 더, 약 440% 더 내지 약 480% 더, 약 440% 더 내지 약 460% 더, 약 460% 더 내지 약 10,000% 더, 약 460% 더 내지 약 9,000% 더, 약 460% 더 내지 약 8,000% 더, 약 460% 더 내지 약 7,000% 더, 약 460% 더 내지 약 6,000% 더, 약 460% 더 내지 약 5,000% 더, 약 460% 더 내지 약 4,000% 더, 약 460% 더 내지 약 3,000% 더, 약 460% 더 내지 약 2,000% 더, 약 460% 더 내지 약 1,000% 더, 약 460% 더 내지 약 500% 더, 약 460% 더 내지 약 480% 더, 약 480% 더 내지 약 10,000% 더, 약 480% 더 내지 약 9,000% 더, 약 480% 더 내지 약 8,000% 더, 약 480% 더 내지 약 7,000% 더, 약 480% 더 내지 약 6,000% 더, 약 480% 더 내지 약 5,000% 더, 약 480% 더 내지 약 4,000% 더, 약 480% 더 내지 약 3,000% 더, 약 480% 더 내지 약 2,000% 더, 약 480% 더 내지 약 1,000% 더, 약 480% 더 내지 약 500% 더, 약 500% 더 내지 약 10,000% 더, 약 500% 더 내지 약 9,000% 더, 약 500% 더 내지 약 8,000% 더, 약 500% 더 내지 약 7,000% 더, 약 500% 더 내지 약 6,000% 더, 약 500% 더 내지 약 5,000% 더, 약 500% 더 내지 약 4,000% 더, 약 500% 더 내지 약 3,000% 더, 약 500% 더 내지 약 2,000% 더, 약 500% 더 내지 약 1,000% 더, 약 1,000% 더 내지 약 10,000% 더, 약 1,000% 더 내지 약 9,000% 더, 약 1,000% 더 내지 약 8,000% 더, 약 1,000% 더 내지 약 7,000% 더, 약 1,000% 더 내지 약 6,000% 더, 약 1,000% 더 내지 약 5,000% 더, 약 1,000% 더 내지 약 4,000% 더, 약 1,000% 더 내지 약 3,000% 더, 약 1,000% 더 내지 약 2,000% 더, 약 2,000% 더 내지 약 10,000% 더, 약 2,000% 더 내지 약 9,000% 더, 약 2,000% 더 내지 약 8,000% 더, 약 2,000% 더 내지 약 7,000% 더, 약 2,000% 더 내지 약 6,000% 더, 약 2,000% 더 내지 약 5,000% 더, 약 2,000% 더 내지 약 4,000% 더, 약 2,000% 더 내지 약 3,000% 더, 약 3,000% 더 내지 약 10,000% 더, 약 3,000% 더 내지 약 9,000% 더, 약 3,000% 더 내지 약 8,000% 더, 약 3,000% 더 내지 약 7,000% 더, 약 3,000% 더 내지 약 6,000% 더, 약 3,000% 더 내지 약 5,000% 더, 약 3,000% 더 내지 약 4,000% 더, 약 4,000% 더 내지 약 10,000% 더, 약 4,000% 더 내지 약 9,000% 더, 약 4,000% 더 내지 약 8,000% 더, 약 4,000% 더 내지 약 7,000% 더, 약 4,000% 더 내지 약 6,000% 더, 약 4,000% 더 내지 약 5,000% 더, 약 5,000% 더 내지 약 10,000% 더, 약 5,000% 더 내지 약 9,000% 더, 약 5,000% 더 내지 약 8,000% 더, 약 5,000% 더 내지 약 7,000% 더, 약 5,000% 더 내지 약 6,000% 더, 약 6,000% 더 내지 약 10,000% 더, 약 6,000% 더 내지 약 9,000% 더, 약 6,000% 더 내지 약 8,000% 더, 약 6,000% 더 내지 약 7,000% 더, 약 7,000% 더 내지 약 10,000% 더, 약 7,000% 더 내지 약 9,000% 더, 약 7,000% 더 내지 약 8,000% 더, 약 8,000% 더 내지 약 10,000% 더, 약 8,000% 더 내지 약 9,000% 더, 또는 약 9,000% 더 내지 약 10,000% 더) 빠르다.
본원에 기술된 항원 결합 단백질 작제물(ABPC) 중 어느 하나의 일부 구현예에서, 약 4.0 내지 약 6.5의 (예를 들어 본원에 기술된 이 범위의 하위 범위 중 어느 하나의) pH에서 제1 항원 결합 도메인의 (및, 임의로 제2 항원 결합 도메인이 존재하는 경우, 제2 항원 결합 단백질의) 해리 상수(KD)는 약 7.0 내지 약 8.0의 (예를 들어 본원에 기술된 이 범위의 하위 범위 중 어느 하나의) pH에서의 KD보다 더 (예를 들어 검출 가능하게 더) (예를 들어 적어도 5% 더, 적어도 10% 더, 적어도 15% 더, 적어도 20% 더, 적어도 25% 더, 적어도 30% 더, 적어도 35% 더, 적어도 40% 더, 적어도 45% 더, 적어도 50% 더, 적어도 55% 더, 적어도 60% 더, 적어도 65% 더, 적어도 70% 더, 적어도 80% 더, 적어도 85% 더, 적어도 90% 더, 적어도 95% 더, 적어도 100% 더, 적어도 120% 더, 적어도 140% 더, 적어도 160% 더, 적어도 180% 더, 적어도 200% 더, 적어도 220% 더, 적어도 240% 더, 적어도 260% 더, 적어도 280% 더, 적어도 300% 더, 적어도 320% 더, 적어도 340% 더, 적어도 360% 더, 적어도 380% 더, 적어도 400% 더, 적어도 420% 더, 적어도 440% 더, 적어도 460% 더, 적어도 480% 더, 적어도 500% 더, 적어도 1,000% 더, 적어도 2,000% 더, 적어도 3,000% 더, 적어도 4,000% 더, 적어도 5,000% 더, 적어도 6,000% 더, 적어도 7,000% 더, 적어도 8,000% 더, 적어도 9,000% 더, 또는 적어도 10,000% 더, 또는 약 5% 더 또는 약 10,000% 더, 약 5% 더 또는 약 9,000% 더, 약 5% 더 또는 약 8,000% 더, 약 5% 더 또는 약 7,000% 더, 약 5% 더 또는 약 6,000% 더, 약 5% 더 또는 약 5,000% 더, 약 5% 더 또는 약 4,000% 더, 약 5% 더 또는 약 3,000% 더, 약 5% 더 또는 약 2,000% 더, 약 5% 더 또는 약 1,000% 더, 약 5% 더 또는 약 500% 더, 약 5% 더 또는 약 480% 더, 약 5% 더 또는 약 460% 더, 약 5% 더 또는 약 440% 더, 약 5% 더 또는 약 420% 더, 약 5% 더 또는 약 400% 더, 약 5% 더 또는 약 380% 더, 약 5% 더 또는 약 360% 더, 약 5% 더 또는 약 340% 더, 약 5% 더 또는 약 320% 더, 약 5% 더 또는 약 300% 더, 약 5% 더 또는 약 280% 더, 약 5% 더 또는 약 260% 더, 약 5% 더 또는 약 240% 더, 약 5% 더 또는 약 220% 더, 약 5% 더 또는 약 200% 더, 약 5% 더 또는 약 180% 더, 약 5% 더 또는 약 160% 더, 약 5% 더 또는 약 140% 더, 약 5% 더 또는 약 120% 더, 약 5% 더 또는 약 100% 더, 약 5% 더 또는 약 95% 더, 약 5% 더 또는 약 90% 더, 약 5% 더 또는 약 85% 더, 약 5% 더 또는 약 80% 더, 약 5% 더 또는 약 75% 더, 약 5% 더 또는 약 70% 더, 약 5% 더 또는 약 65% 더, 약 5% 더 또는 약 60% 더, 약 5% 더 또는 약 55% 더, 약 5% 더 또는 약 50% 더, 약 5% 더 또는 약 45% 더, 약 5% 더 또는 약 40% 더, 약 5% 더 또는 약 35% 더, 약 5% 더 또는 약 30% 더, 약 5% 더 또는 약 25% 더, 약 5% 더 또는 약 20% 더, 약 5% 더 또는 약 15% 더, 약 5% 더 또는 약 10% 더, 약 10% 더 또는 약 10,000% 더, 약 10% 더 또는 약 9,000% 더, 약 10% 더 또는 약 8,000% 더, 약 10% 더 또는 약 7,000% 더, 약 10% 더 또는 약 6,000% 더, 약 10% 더 또는 약 5,000% 더, 약 10% 더 또는 약 4,000% 더, 약 10% 더 또는 약 3,000% 더, 약 10% 더 또는 약 2,000% 더, 약 10% 더 또는 약 1,000% 더, 약 10% 더 또는 약 500% 더, 약 10% 더 또는 약 480% 더, 약 10% 더 또는 약 460% 더, 약 10% 더 또는 약 440% 더, 약 10% 더 또는 약 420% 더, 약 10% 더 또는 약 400% 더, 약 10% 더 또는 약 380% 더, 약 10% 더 또는 약 360% 더, 약 10% 더 또는 약 340% 더, 약 10% 더 또는 약 320% 더, 약 10% 더 또는 약 300% 더, 약 10% 더 또는 약 280% 더, 약 10% 더 또는 약 260% 더, 약 10% 더 또는 약 240% 더, 약 10% 더 또는 약 220% 더, 약 10% 더 또는 약 200% 더, 약 10% 더 또는 약 180% 더, 약 10% 더 또는 약 160% 더, 약 10% 더 또는 약 140% 더, 약 10% 더 또는 약 120% 더, 약 10% 더 또는 약 100% 더, 약 10% 더 또는 약 95% 더, 약 10% 더 또는 약 90% 더, 약 10% 더 또는 약 85% 더, 약 10% 더 또는 약 80% 더, 약 10% 더 또는 약 75% 더, 약 10% 더 또는 약 70% 더, 약 10% 더 또는 약 65% 더, 약 10% 더 또는 약 60% 더, 약 10% 더 또는 약 55% 더, 약 10% 더 또는 약 50% 더, 약 10% 더 또는 약 45% 더, 약 10% 더 또는 약 40% 더, 약 10% 더 또는 약 35% 더, 약 10% 더 또는 약 30% 더, 약 10% 더 또는 약 25% 더, 약 10% 더 또는 약 20% 더, 약 10% 더 또는 약 15% 더, 약 15% 더 또는 약 10,000% 더, 약 15% 더 또는 약 9,000% 더, 약 15% 더 또는 약 8,000% 더, 약 15% 더 또는 약 7,000% 더, 약 15% 더 또는 약 6,000% 더, 약 15% 더 또는 약 5,000% 더, 약 15% 더 또는 약 4,000% 더, 약 15% 더 또는 약 3,000% 더, 약 15% 더 또는 약 2,000% 더, 약 15% 더 또는 약 1,000% 더, 약 15% 더 또는 약 500% 더, 약 15% 더 또는 약 480% 더, 약 15% 더 또는 약 460% 더, 약 15% 더 또는 약 440% 더, 약 15% 더 또는 약 420% 더, 약 15% 더 또는 약 400% 더, 약 15% 더 또는 약 380% 더, 약 15% 더 또는 약 360% 더, 약 15% 더 또는 약 340% 더, 약 15% 더 또는 약 320% 더, 약 15% 더 또는 약 300% 더, 약 15% 더 또는 약 280% 더, 약 15% 더 또는 약 260% 더, 약 15% 더 또는 약 240% 더, 약 15% 더 또는 약 220% 더, 약 15% 더 또는 약 200% 더, 약 15% 더 또는 약 180% 더, 약 15% 더 또는 약 160% 더, 약 15% 더 또는 약 140% 더, 약 15% 더 또는 약 120% 더, 약 15% 더 또는 약 100% 더, 약 15% 더 또는 약 95% 더, 약 15% 더 또는 약 90% 더, 약 15% 더 또는 약 85% 더, 약 15% 더 또는 약 80% 더, 약 15% 더 또는 약 75% 더, 약 15% 더 또는 약 70% 더, 약 15% 더 또는 약 65% 더, 약 15% 더 또는 약 60% 더, 약 15% 더 또는 약 55% 더, 약 15% 더 또는 약 50% 더, 약 15% 더 또는 약 45% 더, 약 15% 더 또는 약 40% 더, 약 15% 더 또는 약 35% 더, 약 15% 더 또는 약 30% 더, 약 15% 더 또는 약 25% 더, 약 15% 더 또는 약 20% 더, 약 20% 더 또는 약 10,000% 더, 약 20% 더 또는 약 9,000% 더, 약 20% 더 또는 약 8,000% 더, 약 20% 더 또는 약 7,000% 더, 약 20% 더 또는 약 6,000% 더, 약 20% 더 또는 약 5,000% 더, 약 20% 더 또는 약 4,000% 더, 약 20% 더 또는 약 3,000% 더, 약 20% 더 또는 약 2,000% 더, 약 20% 더 또는 약 1,000% 더, 약 20% 더 또는 약 500% 더, 약 20% 더 또는 약 480% 더, 약 20% 더 또는 약 460% 더, 약 20% 더 또는 약 440% 더, 약 20% 더 또는 약 420% 더, 약 20% 더 또는 약 400% 더, 약 20% 더 또는 약 380% 더, 약 20% 더 또는 약 360% 더, 약 20% 더 또는 약 340% 더, 약 20% 더 또는 약 320% 더, 약 20% 더 또는 약 300% 더, 약 20% 더 또는 약 280% 더, 약 20% 더 또는 약 260% 더, 약 20% 더 또는 약 240% 더, 약 20% 더 또는 약 220% 더, 약 20% 더 또는 약 200% 더, 약 20% 더 또는 약 180% 더, 약 20% 더 또는 약 160% 더, 약 20% 더 또는 약 140% 더, 약 20% 더 또는 약 120% 더, 약 20% 더 또는 약 100% 더, 약 20% 더 또는 약 95% 더, 약 20% 더 또는 약 90% 더, 약 20% 더 또는 약 85% 더, 약 20% 더 또는 약 80% 더, 약 20% 더 또는 약 75% 더, 약 20% 더 또는 약 70% 더, 약 20% 더 또는 약 65% 더, 약 20% 더 또는 약 60% 더, 약 20% 더 또는 약 55% 더, 약 20% 더 또는 약 50% 더, 약 20% 더 또는 약 45% 더, 약 20% 더 또는 약 40% 더, 약 20% 더 또는 약 35% 더, 약 20% 더 또는 약 30% 더, 약 20% 더 또는 약 25% 더, 약 25% 더 또는 약 10,000% 더, 약 25% 더 또는 약 9,000% 더, 약 25% 더 또는 약 8,000% 더, 약 25% 더 또는 약 7,000% 더, 약 25% 더 또는 약 6,000% 더, 약 25% 더 또는 약 5,000% 더, 약 25% 더 또는 약 4,000% 더, 약 25% 더 또는 약 3,000% 더, 약 25% 더 또는 약 2,000% 더, 약 25% 더 또는 약 1,000% 더, 약 25% 더 또는 약 500% 더, 약 25% 더 또는 약 480% 더, 약 25% 더 또는 약 460% 더, 약 25% 더 또는 약 440% 더, 약 25% 더 또는 약 420% 더, 약 25% 더 또는 약 400% 더, 약 25% 더 또는 약 380% 더, 약 25% 더 또는 약 360% 더, 약 25% 더 또는 약 340% 더, 약 25% 더 또는 약 320% 더, 약 25% 더 또는 약 300% 더, 약 25% 더 또는 약 280% 더, 약 25% 더 또는 약 260% 더, 약 25% 더 또는 약 240% 더, 약 25% 더 또는 약 220% 더, 약 25% 더 또는 약 200% 더, 약 25% 더 또는 약 180% 더, 약 25% 더 또는 약 160% 더, 약 25% 더 또는 약 140% 더, 약 25% 더 또는 약 120% 더, 약 25% 더 또는 약 100% 더, 약 25% 더 또는 약 95% 더, 약 25% 더 또는 약 90% 더, 약 25% 더 또는 약 85% 더, 약 25% 더 또는 약 80% 더, 약 25% 더 또는 약 75% 더, 약 25% 더 또는 약 70% 더, 약 25% 더 또는 약 65% 더, 약 25% 더 또는 약 60% 더, 약 25% 더 또는 약 55% 더, 약 25% 더 또는 약 50% 더, 약 25% 더 또는 약 45% 더, 약 25% 더 또는 약 40% 더, 약 25% 더 또는 약 35% 더, 약 25% 더 또는 약 30% 더, 약 30% 더 또는 약 10,000% 더, 약 30% 더 또는 약 9,000% 더, 약 30% 더 또는 약 8,000% 더, 약 30% 더 또는 약 7,000% 더, 약 30% 더 또는 약 6,000% 더, 약 30% 더 또는 약 5,000% 더, 약 30% 더 또는 약 4,000% 더, 약 30% 더 또는 약 3,000% 더, 약 30% 더 또는 약 2,000% 더, 약 30% 더 또는 약 1,000% 더, 약 30% 더 또는 약 500% 더, 약 30% 더 또는 약 480% 더, 약 30% 더 또는 약 460% 더, 약 30% 더 또는 약 440% 더, 약 30% 더 또는 약 420% 더, 약 30% 더 또는 약 400% 더, 약 30% 더 또는 약 380% 더, 약 30% 더 또는 약 360% 더, 약 30% 더 또는 약 340% 더, 약 30% 더 또는 약 320% 더, 약 30% 더 또는 약 300% 더, 약 30% 더 또는 약 280% 더, 약 30% 더 또는 약 260% 더, 약 30% 더 또는 약 240% 더, 약 30% 더 또는 약 220% 더, 약 30% 더 또는 약 200% 더, 약 30% 더 또는 약 180% 더, 약 30% 더 또는 약 160% 더, 약 30% 더 또는 약 140% 더, 약 30% 더 또는 약 120% 더, 약 30% 더 또는 약 100% 더, 약 30% 더 또는 약 95% 더, 약 30% 더 또는 약 90% 더, 약 30% 더 또는 약 85% 더, 약 30% 더 또는 약 80% 더, 약 30% 더 또는 약 75% 더, 약 30% 더 또는 약 70% 더, 약 30% 더 또는 약 65% 더, 약 30% 더 또는 약 60% 더, 약 30% 더 또는 약 55% 더, 약 30% 더 또는 약 50% 더, 약 30% 더 또는 약 45% 더, 약 30% 더 또는 약 40% 더, 약 30% 더 또는 약 35% 더, 약 35% 더 또는 약 10,000% 더, 약 35% 더 또는 약 9,000% 더, 약 35% 더 또는 약 8,000% 더, 약 35% 더 또는 약 7,000% 더, 약 35% 더 또는 약 6,000% 더, 약 35% 더 또는 약 5,000% 더, 약 35% 더 또는 약 4,000% 더, 약 35% 더 또는 약 3,000% 더, 약 35% 더 또는 약 2,000% 더, 약 35% 더 또는 약 1,000% 더, 약 35% 더 또는 약 500% 더, 약 35% 더 또는 약 480% 더, 약 35% 더 또는 약 460% 더, 약 35% 더 또는 약 440% 더, 약 35% 더 또는 약 420% 더, 약 35% 더 또는 약 400% 더, 약 35% 더 또는 약 380% 더, 약 35% 더 또는 약 360% 더, 약 35% 더 또는 약 340% 더, 약 35% 더 또는 약 320% 더, 약 35% 더 또는 약 300% 더, 약 35% 더 또는 약 280% 더, 약 35% 더 또는 약 260% 더, 약 35% 더 또는 약 240% 더, 약 35% 더 또는 약 220% 더, 약 35% 더 또는 약 200% 더, 약 35% 더 또는 약 180% 더, 약 35% 더 또는 약 160% 더, 약 35% 더 또는 약 140% 더, 약 35% 더 또는 약 120% 더, 약 35% 더 또는 약 100% 더, 약 35% 더 또는 약 95% 더, 약 35% 더 또는 약 90% 더, 약 35% 더 또는 약 85% 더, 약 35% 더 또는 약 80% 더, 약 35% 더 또는 약 75% 더, 약 35% 더 또는 약 70% 더, 약 35% 더 또는 약 65% 더, 약 35% 더 또는 약 60% 더, 약 35% 더 또는 약 55% 더, 약 35% 더 또는 약 50% 더, 약 35% 더 또는 약 45% 더, 약 35% 더 또는 약 40% 더, 약 40% 더 또는 약 10,000% 더, 약 40% 더 또는 약 9,000% 더, 약 40% 더 또는 약 8,000% 더, 약 40% 더 또는 약 7,000% 더, 약 40% 더 또는 약 6,000% 더, 약 40% 더 또는 약 5,000% 더, 약 40% 더 또는 약 4,000% 더, 약 40% 더 또는 약 3,000% 더, 약 40% 더 또는 약 2,000% 더, 약 40% 더 또는 약 1,000% 더, 약 40% 더 또는 약 500% 더, 약 40% 더 또는 약 480% 더, 약 40% 더 또는 약 460% 더, 약 40% 더 또는 약 440% 더, 약 40% 더 또는 약 420% 더, 약 40% 더 또는 약 400% 더, 약 40% 더 또는 약 380% 더, 약 40% 더 또는 약 360% 더, 약 40% 더 또는 약 340% 더, 약 40% 더 또는 약 320% 더, 약 40% 더 또는 약 300% 더, 약 40% 더 또는 약 280% 더, 약 40% 더 또는 약 260% 더, 약 40% 더 또는 약 240% 더, 약 40% 더 또는 약 220% 더, 약 40% 더 또는 약 200% 더, 약 40% 더 또는 약 180% 더, 약 40% 더 또는 약 160% 더, 약 40% 더 또는 약 140% 더, 약 40% 더 또는 약 120% 더, 약 40% 더 또는 약 100% 더, 약 40% 더 또는 약 95% 더, 약 40% 더 또는 약 90% 더, 약 40% 더 또는 약 85% 더, 약 40% 더 또는 약 80% 더, 약 40% 더 또는 약 75% 더, 약 40% 더 또는 약 70% 더, 약 40% 더 또는 약 65% 더, 약 40% 더 또는 약 60% 더, 약 40% 더 또는 약 55% 더, 약 40% 더 또는 약 50% 더, 약 40% 더 또는 약 45% 더, 약 45% 더 또는 약 10,000% 더, 약 45% 더 또는 약 9,000% 더, 약 45% 더 또는 약 8,000% 더, 약 45% 더 또는 약 7,000% 더, 약 45% 더 또는 약 6,000% 더, 약 45% 더 또는 약 5,000% 더, 약 45% 더 또는 약 4,000% 더, 약 45% 더 또는 약 3,000% 더, 약 45% 더 또는 약 2,000% 더, 약 45% 더 또는 약 1,000% 더, 약 45% 더 또는 약 500% 더, 약 45% 더 또는 약 480% 더, 약 45% 더 또는 약 460% 더, 약 45% 더 또는 약 440% 더, 약 45% 더 또는 약 420% 더, 약 45% 더 또는 약 400% 더, 약 45% 더 또는 약 380% 더, 약 45% 더 또는 약 360% 더, 약 45% 더 또는 약 340% 더, 약 45% 더 또는 약 320% 더, 약 45% 더 또는 약 300% 더, 약 45% 더 또는 약 280% 더, 약 45% 더 또는 약 260% 더, 약 45% 더 또는 약 240% 더, 약 45% 더 또는 약 220% 더, 약 45% 더 또는 약 200% 더, 약 45% 더 또는 약 180% 더, 약 45% 더 또는 약 160% 더, 약 45% 더 또는 약 140% 더, 약 45% 더 또는 약 120% 더, 약 45% 더 또는 약 100% 더, 약 45% 더 또는 약 95% 더, 약 45% 더 또는 약 90% 더, 약 45% 더 또는 약 85% 더, 약 45% 더 또는 약 80% 더, 약 45% 더 또는 약 75% 더, 약 45% 더 또는 약 70% 더, 약 45% 더 또는 약 65% 더, 약 45% 더 또는 약 60% 더, 약 45% 더 또는 약 55% 더, 약 45% 더 또는 약 50% 더, 약 50% 더 또는 약 10,000% 더, 약 50% 더 또는 약 9,000% 더, 약 50% 더 또는 약 8,000% 더, 약 50% 더 또는 약 7,000% 더, 약 50% 더 또는 약 6,000% 더, 약 50% 더 또는 약 5,000% 더, 약 50% 더 또는 약 4,000% 더, 약 50% 더 또는 약 3,000% 더, 약 50% 더 또는 약 2,000% 더, 약 50% 더 또는 약 1,000% 더, 약 50% 더 또는 약 500% 더, 약 50% 더 또는 약 480% 더, 약 50% 더 또는 약 460% 더, 약 50% 더 또는 약 440% 더, 약 50% 더 또는 약 420% 더, 약 50% 더 또는 약 400% 더, 약 50% 더 또는 약 380% 더, 약 50% 더 또는 약 360% 더, 약 50% 더 또는 약 340% 더, 약 50% 더 또는 약 320% 더, 약 50% 더 또는 약 300% 더, 약 50% 더 또는 약 280% 더, 약 50% 더 또는 약 260% 더, 약 50% 더 또는 약 240% 더, 약 50% 더 또는 약 220% 더, 약 50% 더 또는 약 200% 더, 약 50% 더 또는 약 180% 더, 약 50% 더 또는 약 160% 더, 약 50% 더 또는 약 140% 더, 약 50% 더 또는 약 120% 더, 약 50% 더 또는 약 100% 더, 약 50% 더 또는 약 95% 더, 약 50% 더 또는 약 90% 더, 약 50% 더 또는 약 85% 더, 약 50% 더 또는 약 80% 더, 약 50% 더 또는 약 75% 더, 약 50% 더 또는 약 70% 더, 약 50% 더 또는 약 65% 더, 약 50% 더 또는 약 60% 더, 약 50% 더 또는 약 55% 더, 약 55% 더 또는 약 10,000% 더, 약 55% 더 또는 약 9,000% 더, 약 55% 더 또는 약 8,000% 더, 약 55% 더 또는 약 7,000% 더, 약 55% 더 또는 약 6,000% 더, 약 55% 더 또는 약 5,000% 더, 약 55% 더 또는 약 4,000% 더, 약 55% 더 또는 약 3,000% 더, 약 55% 더 또는 약 2,000% 더, 약 55% 더 또는 약 1,000% 더, 약 55% 더 또는 약 500% 더, 약 55% 더 또는 약 480% 더, 약 55% 더 또는 약 460% 더, 약 55% 더 또는 약 440% 더, 약 55% 더 또는 약 420% 더, 약 55% 더 또는 약 400% 더, 약 55% 더 또는 약 380% 더, 약 55% 더 또는 약 360% 더, 약 55% 더 또는 약 340% 더, 약 55% 더 또는 약 320% 더, 약 55% 더 또는 약 300% 더, 약 55% 더 또는 약 280% 더, 약 55% 더 또는 약 260% 더, 약 55% 더 또는 약 240% 더, 약 55% 더 또는 약 220% 더, 약 55% 더 또는 약 200% 더, 약 55% 더 또는 약 180% 더, 약 55% 더 또는 약 160% 더, 약 55% 더 또는 약 140% 더, 약 55% 더 또는 약 120% 더, 약 55% 더 또는 약 100% 더, 약 55% 더 또는 약 95% 더, 약 55% 더 또는 약 90% 더, 약 55% 더 또는 약 85% 더, 약 55% 더 또는 약 80% 더, 약 55% 더 또는 약 75% 더, 약 55% 더 또는 약 70% 더, 약 55% 더 또는 약 65% 더, 약 55% 더 또는 약 60% 더, 약 60% 더 또는 약 10,000% 더, 약 60% 더 또는 약 9,000% 더, 약 60% 더 또는 약 8,000% 더, 약 60% 더 또는 약 7,000% 더, 약 60% 더 또는 약 6,000% 더, 약 60% 더 또는 약 5,000% 더, 약 60% 더 또는 약 4,000% 더, 약 60% 더 또는 약 3,000% 더, 약 60% 더 또는 약 2,000% 더, 약 60% 더 또는 약 1,000% 더, 약 60% 더 또는 약 500% 더, 약 60% 더 또는 약 480% 더, 약 60% 더 또는 약 460% 더, 약 60% 더 또는 약 440% 더, 약 60% 더 또는 약 420% 더, 약 60% 더 또는 약 400% 더, 약 60% 더 또는 약 380% 더, 약 60% 더 또는 약 360% 더, 약 60% 더 또는 약 340% 더, 약 60% 더 또는 약 320% 더, 약 60% 더 또는 약 300% 더, 약 60% 더 또는 약 280% 더, 약 60% 더 또는 약 260% 더, 약 60% 더 또는 약 240% 더, 약 60% 더 또는 약 220% 더, 약 60% 더 또는 약 200% 더, 약 60% 더 또는 약 180% 더, 약 60% 더 또는 약 160% 더, 약 60% 더 또는 약 140% 더, 약 60% 더 또는 약 120% 더, 약 60% 더 또는 약 100% 더, 약 60% 더 또는 약 95% 더, 약 60% 더 또는 약 90% 더, 약 60% 더 또는 약 85% 더, 약 60% 더 또는 약 80% 더, 약 60% 더 또는 약 75% 더, 약 60% 더 또는 약 70% 더, 약 60% 더 또는 약 65% 더, 약 65% 더 또는 약 10,000% 더, 약 65% 더 또는 약 9,000% 더, 약 65% 더 또는 약 8,000% 더, 약 65% 더 또는 약 7,000% 더, 약 65% 더 또는 약 6,000% 더, 약 65% 더 또는 약 5,000% 더, 약 65% 더 또는 약 4,000% 더, 약 65% 더 또는 약 3,000% 더, 약 65% 더 또는 약 2,000% 더, 약 65% 더 또는 약 1,000% 더, 약 65% 더 또는 약 500% 더, 약 65% 더 또는 약 480% 더, 약 65% 더 또는 약 460% 더, 약 65% 더 또는 약 440% 더, 약 65% 더 또는 약 420% 더, 약 65% 더 또는 약 400% 더, 약 65% 더 또는 약 380% 더, 약 65% 더 또는 약 360% 더, 약 65% 더 또는 약 340% 더, 약 65% 더 또는 약 320% 더, 약 65% 더 또는 약 300% 더, 약 65% 더 또는 약 280% 더, 약 65% 더 또는 약 260% 더, 약 65% 더 또는 약 240% 더, 약 65% 더 또는 약 220% 더, 약 65% 더 또는 약 200% 더, 약 65% 더 또는 약 180% 더, 약 65% 더 또는 약 160% 더, 약 65% 더 또는 약 140% 더, 약 65% 더 또는 약 120% 더, 약 65% 더 또는 약 100% 더, 약 65% 더 또는 약 95% 더, 약 65% 더 또는 약 90% 더, 약 65% 더 또는 약 85% 더, 약 65% 더 또는 약 80% 더, 약 65% 더 또는 약 75% 더, 약 65% 더 또는 약 70% 더, 약 70% 더 또는 약 10,000% 더, 약 70% 더 또는 약 9,000% 더, 약 70% 더 또는 약 8,000% 더, 약 70% 더 또는 약 7,000% 더, 약 70% 더 또는 약 6,000% 더, 약 70% 더 또는 약 5,000% 더, 약 70% 더 또는 약 4,000% 더, 약 70% 더 또는 약 3,000% 더, 약 70% 더 또는 약 2,000% 더, 약 70% 더 또는 약 1,000% 더, 약 70% 더 또는 약 500% 더, 약 70% 더 또는 약 480% 더, 약 70% 더 또는 약 460% 더, 약 70% 더 또는 약 440% 더, 약 70% 더 또는 약 420% 더, 약 70% 더 또는 약 400% 더, 약 70% 더 또는 약 380% 더, 약 70% 더 또는 약 360% 더, 약 70% 더 또는 약 340% 더, 약 70% 더 또는 약 320% 더, 약 70% 더 또는 약 300% 더, 약 70% 더 또는 약 280% 더, 약 70% 더 또는 약 260% 더, 약 70% 더 또는 약 240% 더, 약 70% 더 또는 약 220% 더, 약 70% 더 또는 약 200% 더, 약 70% 더 또는 약 180% 더, 약 70% 더 또는 약 160% 더, 약 70% 더 또는 약 140% 더, 약 70% 더 또는 약 120% 더, 약 70% 더 또는 약 100% 더, 약 70% 더 또는 약 95% 더, 약 70% 더 또는 약 90% 더, 약 70% 더 또는 약 85% 더, 약 70% 더 또는 약 80% 더, 약 70% 더 또는 약 75% 더, 약 75% 더 또는 약 10,000% 더, 약 75% 더 또는 약 9,000% 더, 약 75% 더 또는 약 8,000% 더, 약 75% 더 또는 약 7,000% 더, 약 75% 더 또는 약 6,000% 더, 약 75% 더 또는 약 5,000% 더, 약 75% 더 또는 약 4,000% 더, 약 75% 더 또는 약 3,000% 더, 약 75% 더 또는 약 2,000% 더, 약 75% 더 또는 약 1,000% 더, 약 75% 더 또는 약 500% 더, 약 75% 더 또는 약 480% 더, 약 75% 더 또는 약 460% 더, 약 75% 더 또는 약 440% 더, 약 75% 더 또는 약 420% 더, 약 75% 더 또는 약 400% 더, 약 75% 더 또는 약 380% 더, 약 75% 더 또는 약 360% 더, 약 75% 더 또는 약 340% 더, 약 75% 더 또는 약 320% 더, 약 75% 더 또는 약 300% 더, 약 75% 더 또는 약 280% 더, 약 75% 더 또는 약 260% 더, 약 75% 더 또는 약 240% 더, 약 75% 더 또는 약 220% 더, 약 75% 더 또는 약 200% 더, 약 75% 더 또는 약 180% 더, 약 75% 더 또는 약 160% 더, 약 75% 더 또는 약 140% 더, 약 75% 더 또는 약 120% 더, 약 75% 더 또는 약 100% 더, 약 75% 더 또는 약 95% 더, 약 75% 더 또는 약 90% 더, 약 75% 더 또는 약 85% 더, 약 75% 더 또는 약 80% 더, 약 80% 더 또는 약 10,000% 더, 약 80% 더 또는 약 9,000% 더, 약 80% 더 또는 약 8,000% 더, 약 80% 더 또는 약 7,000% 더, 약 80% 더 또는 약 6,000% 더, 약 80% 더 또는 약 5,000% 더, 약 80% 더 또는 약 4,000% 더, 약 80% 더 또는 약 3,000% 더, 약 80% 더 또는 약 2,000% 더, 약 80% 더 또는 약 1,000% 더, 약 80% 더 또는 약 500% 더, 약 80% 더 또는 약 480% 더, 약 80% 더 또는 약 460% 더, 약 80% 더 또는 약 440% 더, 약 80% 더 또는 약 420% 더, 약 80% 더 또는 약 400% 더, 약 80% 더 또는 약 380% 더, 약 80% 더 또는 약 360% 더, 약 80% 더 또는 약 340% 더, 약 80% 더 또는 약 320% 더, 약 80% 더 또는 약 300% 더, 약 80% 더 또는 약 280% 더, 약 80% 더 또는 약 260% 더, 약 80% 더 또는 약 240% 더, 약 80% 더 또는 약 220% 더, 약 80% 더 또는 약 200% 더, 약 80% 더 또는 약 180% 더, 약 80% 더 또는 약 160% 더, 약 80% 더 또는 약 140% 더, 약 80% 더 또는 약 120% 더, 약 80% 더 또는 약 100% 더, 약 80% 더 또는 약 95% 더, 약 80% 더 또는 약 90% 더, 약 80% 더 또는 약 85% 더, 약 85% 더 또는 약 10,000% 더, 약 85% 더 또는 약 9,000% 더, 약 85% 더 또는 약 8,000% 더, 약 85% 더 또는 약 7,000% 더, 약 85% 더 또는 약 6,000% 더, 약 85% 더 또는 약 5,000% 더, 약 85% 더 또는 약 4,000% 더, 약 85% 더 또는 약 3,000% 더, 약 85% 더 또는 약 2,000% 더, 약 85% 더 또는 약 1,000% 더, 약 85% 더 또는 약 500% 더, 약 85% 더 또는 약 480% 더, 약 85% 더 또는 약 460% 더, 약 85% 더 또는 약 440% 더, 약 85% 더 또는 약 420% 더, 약 85% 더 또는 약 400% 더, 약 85% 더 또는 약 380% 더, 약 85% 더 또는 약 360% 더, 약 85% 더 또는 약 340% 더, 약 85% 더 또는 약 320% 더, 약 85% 더 또는 약 300% 더, 약 85% 더 또는 약 280% 더, 약 85% 더 또는 약 260% 더, 약 85% 더 또는 약 240% 더, 약 85% 더 또는 약 220% 더, 약 85% 더 또는 약 200% 더, 약 85% 더 또는 약 180% 더, 약 85% 더 또는 약 160% 더, 약 85% 더 또는 약 140% 더, 약 85% 더 또는 약 120% 더, 약 85% 더 또는 약 100% 더, 약 85% 더 또는 약 95% 더, 약 85% 더 또는 약 90% 더, 약 90% 더 또는 약 10,000% 더, 약 90% 더 또는 약 9,000% 더, 약 90% 더 또는 약 8,000% 더, 약 90% 더 또는 약 7,000% 더, 약 90% 더 또는 약 6,000% 더, 약 90% 더 또는 약 5,000% 더, 약 90% 더 또는 약 4,000% 더, 약 90% 더 또는 약 3,000% 더, 약 90% 더 또는 약 2,000% 더, 약 90% 더 또는 약 1,000% 더, 약 90% 더 또는 약 500% 더, 약 90% 더 또는 약 480% 더, 약 90% 더 또는 약 460% 더, 약 90% 더 또는 약 440% 더, 약 90% 더 또는 약 420% 더, 약 90% 더 또는 약 400% 더, 약 90% 더 또는 약 380% 더, 약 90% 더 또는 약 360% 더, 약 90% 더 또는 약 340% 더, 약 90% 더 또는 약 320% 더, 약 90% 더 또는 약 300% 더, 약 90% 더 또는 약 280% 더, 약 90% 더 또는 약 260% 더, 약 90% 더 또는 약 240% 더, 약 90% 더 또는 약 220% 더, 약 90% 더 또는 약 200% 더, 약 90% 더 또는 약 180% 더, 약 90% 더 또는 약 160% 더, 약 90% 더 또는 약 140% 더, 약 90% 더 또는 약 120% 더, 약 90% 더 또는 약 100% 더, 약 90% 더 또는 약 95% 더, 약 95% 더 또는 약 10,000% 더, 약 95% 더 또는 약 9,000% 더, 약 95% 더 또는 약 8,000% 더, 약 95% 더 또는 약 7,000% 더, 약 95% 더 또는 약 6,000% 더, 약 95% 더 또는 약 5,000% 더, 약 95% 더 또는 약 4,000% 더, 약 95% 더 또는 약 3,000% 더, 약 95% 더 또는 약 2,000% 더, 약 95% 더 또는 약 1,000% 더, 약 95% 더 또는 약 500% 더, 약 95% 더 또는 약 480% 더, 약 95% 더 또는 약 460% 더, 약 95% 더 또는 약 440% 더, 약 95% 더 또는 약 420% 더, 약 95% 더 또는 약 400% 더, 약 95% 더 또는 약 380% 더, 약 95% 더 또는 약 360% 더, 약 95% 더 또는 약 340% 더, 약 95% 더 또는 약 320% 더, 약 95% 더 또는 약 300% 더, 약 95% 더 또는 약 280% 더, 약 95% 더 또는 약 260% 더, 약 95% 더 또는 약 240% 더, 약 95% 더 또는 약 220% 더, 약 95% 더 또는 약 200% 더, 약 95% 더 또는 약 180% 더, 약 95% 더 또는 약 160% 더, 약 95% 더 또는 약 140% 더, 약 95% 더 또는 약 120% 더, 약 95% 더 또는 약 100% 더, 약 100% 더 또는 약 10,000% 더, 약 100% 더 또는 약 9,000% 더, 약 100% 더 또는 약 8,000% 더, 약 100% 더 또는 약 7,000% 더, 약 100% 더 또는 약 6,000% 더, 약 100% 더 또는 약 5,000% 더, 약 100% 더 또는 약 4,000% 더, 약 100% 더 또는 약 3,000% 더, 약 100% 더 또는 약 2,000% 더, 약 100% 더 또는 약 1,000% 더, 약 100% 더 또는 약 500% 더, 약 100% 더 또는 약 480% 더, 약 100% 더 또는 약 460% 더, 약 100% 더 또는 약 440% 더, 약 100% 더 또는 약 420% 더, 약 100% 더 또는 약 400% 더, 약 100% 더 또는 약 380% 더, 약 100% 더 또는 약 360% 더, 약 100% 더 또는 약 340% 더, 약 100% 더 또는 약 320% 더, 약 100% 더 또는 약 300% 더, 약 100% 더 또는 약 280% 더, 약 100% 더 또는 약 260% 더, 약 100% 더 또는 약 240% 더, 약 100% 더 또는 약 220% 더, 약 100% 더 또는 약 200% 더, 약 100% 더 또는 약 180% 더, 약 100% 더 또는 약 160% 더, 약 100% 더 또는 약 140% 더, 약 100% 더 또는 약 120% 더, 약 120% 더 또는 약 10,000% 더, 약 120% 더 또는 약 9,000% 더, 약 120% 더 또는 약 8,000% 더, 약 120% 더 또는 약 7,000% 더, 약 120% 더 또는 약 6,000% 더, 약 120% 더 또는 약 5,000% 더, 약 120% 더 또는 약 4,000% 더, 약 120% 더 또는 약 3,000% 더, 약 120% 더 또는 약 2,000% 더, 약 120% 더 또는 약 1,000% 더, 약 120% 더 또는 약 500% 더, 약 120% 더 또는 약 480% 더, 약 120% 더 또는 약 460% 더, 약 120% 더 또는 약 440% 더, 약 120% 더 또는 약 420% 더, 약 120% 더 또는 약 400% 더, 약 120% 더 또는 약 380% 더, 약 120% 더 또는 약 360% 더, 약 120% 더 또는 약 340% 더, 약 120% 더 또는 약 320% 더, 약 120% 더 또는 약 300% 더, 약 120% 더 또는 약 280% 더, 약 120% 더 또는 약 260% 더, 약 120% 더 또는 약 240% 더, 약 120% 더 또는 약 220% 더, 약 120% 더 또는 약 200% 더, 약 120% 더 또는 약 180% 더, 약 120% 더 또는 약 160% 더, 약 120% 더 또는 약 140% 더, 약 140% 더 또는 약 10,000% 더, 약 140% 더 또는 약 9,000% 더, 약 140% 더 또는 약 8,000% 더, 약 140% 더 또는 약 7,000% 더, 약 140% 더 또는 약 6,000% 더, 약 140% 더 또는 약 5,000% 더, 약 140% 더 또는 약 4,000% 더, 약 140% 더 또는 약 3,000% 더, 약 140% 더 또는 약 2,000% 더, 약 140% 더 또는 약 1,000% 더, 약 140% 더 또는 약 500% 더, 약 140% 더 또는 약 480% 더, 약 140% 더 또는 약 460% 더, 약 140% 더 또는 약 440% 더, 약 140% 더 또는 약 420% 더, 약 140% 더 또는 약 400% 더, 약 140% 더 또는 약 380% 더, 약 140% 더 또는 약 360% 더, 약 140% 더 또는 약 340% 더, 약 140% 더 또는 약 320% 더, 약 140% 더 또는 약 300% 더, 약 140% 더 또는 약 280% 더, 약 140% 더 또는 약 260% 더, 약 140% 더 또는 약 240% 더, 약 140% 더 또는 약 220% 더, 약 140% 더 또는 약 200% 더, 약 140% 더 또는 약 180% 더, 약 140% 더 또는 약 160% 더, 약 160% 더 또는 약 10,000% 더, 약 160% 더 또는 약 9,000% 더, 약 160% 더 또는 약 8,000% 더, 약 160% 더 또는 약 7,000% 더, 약 160% 더 또는 약 6,000% 더, 약 160% 더 또는 약 5,000% 더, 약 160% 더 또는 약 4,000% 더, 약 160% 더 또는 약 3,000% 더, 약 160% 더 또는 약 2,000% 더, 약 160% 더 또는 약 1,000% 더, 약 160% 더 또는 약 500% 더, 약 160% 더 또는 약 480% 더, 약 160% 더 또는 약 460% 더, 약 160% 더 또는 약 440% 더, 약 160% 더 또는 약 420% 더, 약 160% 더 또는 약 400% 더, 약 160% 더 또는 약 380% 더, 약 160% 더 또는 약 360% 더, 약 160% 더 또는 약 340% 더, 약 160% 더 또는 약 320% 더, 약 160% 더 또는 약 300% 더, 약 160% 더 또는 약 280% 더, 약 160% 더 또는 약 260% 더, 약 160% 더 또는 약 240% 더, 약 160% 더 또는 약 220% 더, 약 160% 더 또는 약 200% 더, 약 160% 더 또는 약 180% 더, 약 180% 더 또는 약 10,000% 더, 약 180% 더 또는 약 9,000% 더, 약 180% 더 또는 약 8,000% 더, 약 180% 더 또는 약 7,000% 더, 약 180% 더 또는 약 6,000% 더, 약 180% 더 또는 약 5,000% 더, 약 180% 더 또는 약 4,000% 더, 약 180% 더 또는 약 3,000% 더, 약 180% 더 또는 약 2,000% 더, 약 180% 더 또는 약 1,000% 더, 약 180% 더 또는 약 500% 더, 약 180% 더 또는 약 480% 더, 약 180% 더 또는 약 460% 더, 약 180% 더 또는 약 440% 더, 약 180% 더 또는 약 420% 더, 약 180% 더 또는 약 400% 더, 약 180% 더 또는 약 380% 더, 약 180% 더 또는 약 360% 더, 약 180% 더 또는 약 340% 더, 약 180% 더 또는 약 320% 더, 약 180% 더 또는 약 300% 더, 약 180% 더 또는 약 280% 더, 약 180% 더 또는 약 260% 더, 약 180% 더 또는 약 240% 더, 약 180% 더 또는 약 220% 더, 약 180% 더 또는 약 200% 더, 약 200% 더 또는 약 10,000% 더, 약 200% 더 또는 약 9,000% 더, 약 200% 더 또는 약 8,000% 더, 약 200% 더 또는 약 7,000% 더, 약 200% 더 또는 약 6,000% 더, 약 200% 더 또는 약 5,000% 더, 약 200% 더 또는 약 4,000% 더, 약 200% 더 또는 약 3,000% 더, 약 200% 더 또는 약 2,000% 더, 약 200% 더 또는 약 1,000% 더, 약 200% 더 또는 약 500% 더, 약 200% 더 또는 약 480% 더, 약 200% 더 또는 약 460% 더, 약 200% 더 또는 약 440% 더, 약 200% 더 또는 약 420% 더, 약 200% 더 또는 약 400% 더, 약 200% 더 또는 약 380% 더, 약 200% 더 또는 약 360% 더, 약 200% 더 또는 약 340% 더, 약 200% 더 또는 약 320% 더, 약 200% 더 또는 약 300% 더, 약 200% 더 또는 약 280% 더, 약 200% 더 또는 약 260% 더, 약 200% 더 또는 약 240% 더, 약 200% 더 또는 약 220% 더, 약 220% 더 또는 약 10,000% 더, 약 220% 더 또는 약 9,000% 더, 약 220% 더 또는 약 8,000% 더, 약 220% 더 또는 약 7,000% 더, 약 220% 더 또는 약 6,000% 더, 약 220% 더 또는 약 5,000% 더, 약 220% 더 또는 약 4,000% 더, 약 220% 더 또는 약 3,000% 더, 약 220% 더 또는 약 2,000% 더, 약 220% 더 또는 약 1,000% 더, 약 220% 더 또는 약 500% 더, 약 220% 더 또는 약 480% 더, 약 220% 더 또는 약 460% 더, 약 220% 더 또는 약 440% 더, 약 220% 더 또는 약 420% 더, 약 220% 더 또는 약 400% 더, 약 220% 더 또는 약 380% 더, 약 220% 더 또는 약 360% 더, 약 220% 더 또는 약 340% 더, 약 220% 더 또는 약 320% 더, 약 220% 더 또는 약 300% 더, 약 220% 더 또는 약 280% 더, 약 220% 더 또는 약 260% 더, 약 220% 더 또는 약 240% 더, 약 240% 더 또는 약 10,000% 더, 약 240% 더 또는 약 9,000% 더, 약 240% 더 또는 약 8,000% 더, 약 240% 더 또는 약 7,000% 더, 약 240% 더 또는 약 6,000% 더, 약 240% 더 또는 약 5,000% 더, 약 240% 더 또는 약 4,000% 더, 약 240% 더 또는 약 3,000% 더, 약 240% 더 또는 약 2,000% 더, 약 240% 더 또는 약 1,000% 더, 약 240% 더 또는 약 500% 더, 약 240% 더 또는 약 480% 더, 약 240% 더 또는 약 460% 더, 약 240% 더 또는 약 440% 더, 약 240% 더 또는 약 420% 더, 약 240% 더 또는 약 400% 더, 약 240% 더 또는 약 380% 더, 약 240% 더 또는 약 360% 더, 약 240% 더 또는 약 340% 더, 약 240% 더 또는 약 320% 더, 약 240% 더 또는 약 300% 더, 약 240% 더 또는 약 280% 더, 약 240% 더 또는 약 260% 더, 약 260% 더 또는 약 10,000% 더, 약 260% 더 또는 약 9,000% 더, 약 260% 더 또는 약 8,000% 더, 약 260% 더 또는 약 7,000% 더, 약 260% 더 또는 약 6,000% 더, 약 260% 더 또는 약 5,000% 더, 약 260% 더 또는 약 4,000% 더, 약 260% 더 또는 약 3,000% 더, 약 260% 더 또는 약 2,000% 더, 약 260% 더 또는 약 1,000% 더, 약 260% 더 또는 약 500% 더, 약 260% 더 또는 약 480% 더, 약 260% 더 또는 약 460% 더, 약 260% 더 또는 약 440% 더, 약 260% 더 또는 약 420% 더, 약 260% 더 또는 약 400% 더, 약 260% 더 또는 약 380% 더, 약 260% 더 또는 약 360% 더, 약 260% 더 또는 약 340% 더, 약 260% 더 또는 약 320% 더, 약 260% 더 또는 약 300% 더, 약 260% 더 또는 약 280% 더, 약 280% 더 또는 약 10,000% 더, 약 280% 더 또는 약 9,000% 더, 약 280% 더 또는 약 8,000% 더, 약 280% 더 또는 약 7,000% 더, 약 280% 더 또는 약 6,000% 더, 약 280% 더 또는 약 5,000% 더, 약 280% 더 또는 약 4,000% 더, 약 280% 더 또는 약 3,000% 더, 약 280% 더 또는 약 2,000% 더, 약 280% 더 또는 약 1,000% 더, 약 280% 더 또는 약 500% 더, 약 280% 더 또는 약 480% 더, 약 280% 더 또는 약 460% 더, 약 280% 더 또는 약 440% 더, 약 280% 더 또는 약 420% 더, 약 280% 더 또는 약 400% 더, 약 280% 더 또는 약 380% 더, 약 280% 더 또는 약 360% 더, 약 280% 더 또는 약 340% 더, 약 280% 더 또는 약 320% 더, 약 280% 더 또는 약 300% 더, 약 300% 더 또는 약 10,000% 더, 약 300% 더 또는 약 9,000% 더, 약 300% 더 또는 약 8,000% 더, 약 300% 더 또는 약 7,000% 더, 약 300% 더 또는 약 6,000% 더, 약 300% 더 또는 약 5,000% 더, 약 300% 더 또는 약 4,000% 더, 약 300% 더 또는 약 3,000% 더, 약 300% 더 또는 약 2,000% 더, 약 300% 더 또는 약 1,000% 더, 약 300% 더 또는 약 500% 더, 약 300% 더 또는 약 480% 더, 약 300% 더 또는 약 460% 더, 약 300% 더 또는 약 440% 더, 약 300% 더 또는 약 420% 더, 약 300% 더 또는 약 400% 더, 약 300% 더 또는 약 380% 더, 약 300% 더 또는 약 360% 더, 약 300% 더 또는 약 340% 더, 약 300% 더 또는 약 320% 더, 약 320% 더 또는 약 10,000% 더, 약 320% 더 또는 약 9,000% 더, 약 320% 더 또는 약 8,000% 더, 약 320% 더 또는 약 7,000% 더, 약 320% 더 또는 약 6,000% 더, 약 320% 더 또는 약 5,000% 더, 약 320% 더 또는 약 4,000% 더, 약 320% 더 또는 약 3,000% 더, 약 320% 더 또는 약 2,000% 더, 약 320% 더 또는 약 1,000% 더, 약 320% 더 또는 약 500% 더, 약 320% 더 또는 약 480% 더, 약 320% 더 또는 약 460% 더, 약 320% 더 또는 약 440% 더, 약 320% 더 또는 약 420% 더, 약 320% 더 또는 약 400% 더, 약 320% 더 또는 약 380% 더, 약 320% 더 또는 약 360% 더, 약 320% 더 또는 약 340% 더, 약 340% 더 또는 약 10,000% 더, 약 340% 더 또는 약 9,000% 더, 약 340% 더 또는 약 8,000% 더, 약 340% 더 또는 약 7,000% 더, 약 340% 더 또는 약 6,000% 더, 약 340% 더 또는 약 5,000% 더, 약 340% 더 또는 약 4,000% 더, 약 340% 더 또는 약 3,000% 더, 약 340% 더 또는 약 2,000% 더, 약 340% 더 또는 약 1,000% 더, 약 340% 더 또는 약 500% 더, 약 340% 더 또는 약 480% 더, 약 340% 더 또는 약 460% 더, 약 340% 더 또는 약 440% 더, 약 340% 더 또는 약 420% 더, 약 340% 더 또는 약 400% 더, 약 340% 더 또는 약 380% 더, 약 340% 더 또는 약 360% 더, 약 360% 더 또는 약 10,000% 더, 약 360% 더 또는 약 9,000% 더, 약 360% 더 또는 약 8,000% 더, 약 360% 더 또는 약 7,000% 더, 약 360% 더 또는 약 6,000% 더, 약 360% 더 또는 약 5,000% 더, 약 360% 더 또는 약 4,000% 더, 약 360% 더 또는 약 3,000% 더, 약 360% 더 또는 약 2,000% 더, 약 360% 더 또는 약 1,000% 더, 약 360% 더 또는 약 500% 더, 약 360% 더 또는 약 480% 더, 약 360% 더 또는 약 460% 더, 약 360% 더 또는 약 440% 더, 약 360% 더 또는 약 420% 더, 약 360% 더 또는 약 400% 더, 약 360% 더 또는 약 380% 더, 약 380% 더 또는 약 10,000% 더, 약 380% 더 또는 약 9,000% 더, 약 380% 더 또는 약 8,000% 더, 약 380% 더 또는 약 7,000% 더, 약 380% 더 또는 약 6,000% 더, 약 380% 더 또는 약 5,000% 더, 약 380% 더 또는 약 4,000% 더, 약 380% 더 또는 약 3,000% 더, 약 380% 더 또는 약 2,000% 더, 약 380% 더 또는 약 1,000% 더, 약 380% 더 또는 약 500% 더, 약 380% 더 또는 약 480% 더, 약 380% 더 또는 약 460% 더, 약 380% 더 또는 약 440% 더, 약 380% 더 또는 약 420% 더, 약 380% 더 또는 약 400% 더, 약 400% 더 또는 약 10,000% 더, 약 400% 더 또는 약 9,000% 더, 약 400% 더 또는 약 8,000% 더, 약 400% 더 또는 약 7,000% 더, 약 400% 더 또는 약 6,000% 더, 약 400% 더 또는 약 5,000% 더, 약 400% 더 또는 약 4,000% 더, 약 400% 더 또는 약 3,000% 더, 약 400% 더 또는 약 2,000% 더, 약 400% 더 또는 약 1,000% 더, 약 400% 더 또는 약 500% 더, 약 400% 더 또는 약 480% 더, 약 400% 더 또는 약 460% 더, 약 400% 더 또는 약 440% 더, 약 400% 더 또는 약 420% 더, 약 420% 더 또는 약 10,000% 더, 약 420% 더 또는 약 9,000% 더, 약 420% 더 또는 약 8,000% 더, 약 420% 더 또는 약 7,000% 더, 약 420% 더 또는 약 6,000% 더, 약 420% 더 또는 약 5,000% 더, 약 420% 더 또는 약 4,000% 더, 약 420% 더 또는 약 3,000% 더, 약 420% 더 또는 약 2,000% 더, 약 420% 더 또는 약 1,000% 더, 약 420% 더 또는 약 500% 더, 약 420% 더 또는 약 480% 더, 약 420% 더 또는 약 460% 더, 약 420% 더 또는 약 440% 더, 약 440% 더 또는 약 10,000% 더, 약 440% 더 또는 약 9,000% 더, 약 440% 더 또는 약 8,000% 더, 약 440% 더 또는 약 7,000% 더, 약 440% 더 또는 약 6,000% 더, 약 440% 더 또는 약 5,000% 더, 약 440% 더 또는 약 4,000% 더, 약 440% 더 또는 약 3,000% 더, 약 440% 더 또는 약 2,000% 더, 약 440% 더 또는 약 1,000% 더, 약 440% 더 또는 약 500% 더, 약 440% 더 또는 약 480% 더, 약 440% 더 또는 약 460% 더, 약 460% 더 또는 약 10,000% 더, 약 460% 더 또는 약 9,000% 더, 약 460% 더 또는 약 8,000% 더, 약 460% 더 또는 약 7,000% 더, 약 460% 더 또는 약 6,000% 더, 약 460% 더 또는 약 5,000% 더, 약 460% 더 또는 약 4,000% 더, 약 460% 더 또는 약 3,000% 더, 약 460% 더 또는 약 2,000% 더, 약 460% 더 또는 약 1,000% 더, 약 460% 더 또는 약 500% 더, 약 460% 더 또는 약 480% 더, 약 480% 더 또는 약 10,000% 더, 약 480% 더 또는 약 9,000% 더, 약 480% 더 또는 약 8,000% 더, 약 480% 더 또는 약 7,000% 더, 약 480% 더 또는 약 6,000% 더, 약 480% 더 또는 약 5,000% 더, 약 480% 더 또는 약 4,000% 더, 약 480% 더 또는 약 3,000% 더, 약 480% 더 또는 약 2,000% 더, 약 480% 더 또는 약 1,000% 더, 약 480% 더 또는 약 500% 더. 약 500% 더 또는 약 10,000% 더, 약 500% 더 또는 약 9,000% 더, 약 500% 더 또는 약 8,000% 더, 약 500% 더 또는 약 7,000% 더, 약 500% 더 또는 약 6,000% 더, 약 500% 더 또는 약 5,000% 더, 약 500% 더 또는 약 4,000% 더, 약 500% 더 또는 약 3,000% 더, 약 500% 더 또는 약 2,000% 더, 약 500% 더 또는 약 1,000% 더, 약 1,000% 더 또는 약 10,000% 더, 약 1,000% 더 또는 약 9,000% 더, 약 1,000% 더 또는 약 8,000% 더, 약 1,000% 더 또는 약 7,000% 더, 약 1,000% 더 또는 약 6,000% 더, 약 1,000% 더 또는 약 5,000% 더, 약 1,000% 더 또는 약 4,000% 더, 약 1,000% 더 또는 약 3,000% 더, 약 1,000% 더 또는 약 2,000% 더, 약 2,000% 더 또는 약 10,000% 더, 약 2,000% 더 또는 약 9,000% 더, 약 2,000% 더 또는 약 8,000% 더, 약 2,000% 더 또는 약 7,000% 더, 약 2,000% 더 또는 약 6,000% 더, 약 2,000% 더 또는 약 5,000% 더, 약 2,000% 더 또는 약 4,000% 더, 약 2,000% 더 또는 약 3,000% 더, 약 3,000% 더 또는 약 10,000% 더, 약 3,000% 더 또는 약 9,000% 더, 약 3,000% 더 또는 약 8,000% 더, 약 3,000% 더 또는 약 7,000% 더, 약 3,000% 더 또는 약 6,000% 더, 약 3,000% 더 또는 약 5,000% 더, 약 3,000% 더 또는 약 4,000% 더, 약 4,000% 더 또는 약 10,000% 더, 약 4,000% 더 또는 약 9,000% 더, 약 4,000% 더 또는 약 8,000% 더, 약 4,000% 더 또는 약 7,000% 더, 약 4,000% 더 또는 약 6,000% 더, 약 4,000% 더 또는 약 5,000% 더, 약 5,000% 더 또는 약 10,000% 더, 약 5,000% 더 또는 약 9,000% 더, 약 5,000% 더 또는 약 8,000% 더, 약 5,000% 더 또는 약 7,000% 더, 약 5,000% 더 또는 약 6,000% 더, 약 6,000% 더 또는 약 10,000% 더, 약 6,000% 더 또는 약 9,000% 더, 약 6,000% 더 또는 약 8,000% 더, 약 6,000% 더 또는 약 7,000% 더, 약 7,000% 더 또는 약 10,000% 더, 약 7,000% 더 또는 약 9,000% 더, 약 7,000% 더 또는 약 8,000% 더, 약 8,000% 더 또는 약 10,000% 더, 약 8,000% 더 또는 약 9,000% 더, 또는 약 9,000% 더 또는 약 10,000% 더) 크다.
본원에 기술된 항원 결합 단백질 작제물(ABPC) 중 어느 하나의 일부 구현예에서, 약 4.0 내지 약 6.5의 (예를 들어 본원에 기술된 이 범위의 하위 범위 중 어느 하나의) pH에서 제1 항원 결합 도메인의 (및, 임의로 제2 항원 결합 도메인이 존재하는 경우, 제2 항원 결합 단백질의) 해리 속도는 약 7.0 내지 약 8.0의 (예를 들어 본원에 기술된 이 범위의 하위 범위 중 어느 하나의) pH에서의 해리 속도보다 더 (예를 들어 적어도 0.2배 더, 적어도 0.3배, 적어도 0.4배, 적어도 0.5배, 적어도 0.6배, 적어도 0.7배, 적어도 0.8배, 적어도 0.9배, 적어도 1.0배, 적어도 1.5배, 적어도 2.0배, 적어도 2.5배, 적어도 3.0배, 적어도 3.5배, 적어도 4.0배, 적어도 4.5배, 적어도 5.0배, 적어도 5.5배, 적어도 6.0배, 적어도 6.5배, 적어도 7.0배, 적어도 7.5배, 적어도 8.0배, 적어도 8.5배, 적어도 9.0배, 적어도 9.5배, 적어도 10.0배, 적어도 10.5배, 적어도 11.0배, 적어도 11.5배, 적어도 12.0배, 적어도 12.5배, 적어도 13.0배, 적어도 13.5배, 적어도 14.0배, 적어도 14.5배, 적어도 15.0배, 적어도 15.5배, 적어도 16.0배, 적어도 16.5배, 적어도 17.0배, 적어도 17.5배, 적어도 18.0배, 적어도 18.5배, 적어도 19.0배, 적어도 19.5배, 적어도 20배, 적어도 25배, 적어도 30배, 적어도 35배, 적어도 40배, 적어도 45배, 적어도 50배, 적어도 55배, 적어도 60배, 적어도 65배, 적어도 70배, 적어도 75배, 적어도 80배, 적어도 85배, 적어도 90배, 적어도 95배, 또는 적어도 100배 더 또는 약 0.2배 내지 약 100배 더, 약 0.2배 내지 약 90배 더, 약 0.2배 내지 약 80배 더, 약 0.2배 내지 약 70배 더, 약 0.2배 내지 약 60배 더, 약 0.2배 내지 약 50배 더, 약 0.2배 내지 약 40배 더, 약 0.2배 내지 약 30배 더, 약 0.2배 내지 약 20배 더, 약 0.2배 내지 약 15배 더, 약 0.2배 내지 약 10배 더, 약 0.2배 내지 약 5배, 약 0.2배 내지 약 2배 더, 약 0.2배 내지 약 1배 더, 약 0.2배 내지 약 0.5배 더, 약 0.5배 내지 약 100배 더, 약 0.5배 내지 약 90배 더, 약 0.5배 내지 약 80배 더, 약 0.5배 내지 약 70배 더, 약 0.5배 내지 약 60배 더, 약 0.5배 내지 약 50배 더, 약 0.5배 내지 약 40배 더, 약 0.5배 내지 약 30배 더, 약 0.5배 내지 약 20배 더, 약 0.5배 내지 약 15배 더, 약 0.5배 내지 약 10배 더, 약 0.5배 내지 약 5배, 약 0.5배 내지 약 2배 더, 약 0.5배 내지 약 1배 더, 약 1배 내지 약 100배 더, 약 1배 내지 약 90배 더, 약 1배 내지 약 80배 더, 약 1배 내지 약 70배 더, 약 1배 내지 약 60배 더, 약 1배 내지 약 50배 더, 약 1배 내지 약 40배 더, 약 1배 내지 약 30배 더, 약 1배 내지 약 20배 더, 약 1배 내지 약 15배 더, 약 1배 내지 약 10배 더, 약 1배 내지 약 5배, 약 1배 내지 약 2배 더, 약 2배 내지 약 100배 더, 약 2배 내지 약 90배 더, 약 2배 내지 약 80배 더, 약 2배 내지 약 70배 더, 약 2배 내지 약 60배 더, 약 2배 내지 약 50배 더, 약 2배 내지 약 40배 더, 약 2배 내지 약 30배 더, 약 2배 내지 약 20배 더, 약 2배 내지 약 15배 더, 약 2배 내지 약 10배 더, 약 2배 내지 약 5배, 약 5배 내지 약 100배 더, 약 5배 내지 약 90배 더, 약 5배 내지 약 80배 더, 약 5배 내지 약 70배 더, 약 5배 내지 약 60배 더, 약 5배 내지 약 50배 더, 약 5배 내지 약 40배 더, 약 5배 내지 약 30배 더, 약 5배 내지 약 20배 더, 약 5배 내지 약 15배 더, 약 5배 내지 약 10배 더, 약 10배 내지 약 100배 더, 약 10배 내지 약 90배 더, 약 10배 내지 약 80배 더, 약 10배 내지 약 70배 더, 약 10배 내지 약 60배 더, 약 10배 내지 약 50배 더, 약 10배 내지 약 40배 더, 약 10배 내지 약 30배 더, 약 10배 내지 약 20배 더, 약 10배 내지 약 15배 더, 약 15배 내지 약 100배 더, 약 15배 내지 약 90배 더, 약 15배 내지 약 80배 더, 약 15배 내지 약 70배 더, 약 15배 내지 약 60배 더, 약 15배 내지 약 50배 더, 약 15배 내지 약 40배 더, 약 15배 내지 약 30배 더, 약 15배 내지 약 20배 더, 약 20배 내지 약 100배 더, 약 20배 내지 약 90배 더, 약 20배 내지 약 80배 더, 약 20배 내지 약 70배 더, 약 20배 내지 약 60배 더, 약 20배 내지 약 50배 더, 약 20배 내지 약 40배 더, 약 20배 내지 약 30배 더, 약 30배 내지 약 100배 더, 약 30배 내지 약 90배 더, 약 30배 내지 약 80배 더, 약 30배 내지 약 70배 더, 약 30배 내지 약 60배 더, 약 30배 내지 약 50배 더, 약 30배 내지 약 40배 더, 약 40배 내지 약 100배 더, 약 40배 내지 약 90배 더, 약 40배 내지 약 80배 더, 약 40배 내지 약 70배 더, 약 40배 내지 약 60배 더, 약 40배 내지 약 50배 더, 약 50배 내지 약 100배 더, 약 50배 내지 약 90배 더, 약 50배 내지 약 80배 더, 약 50배 내지 약 70배 더, 약 50배 내지 약 60배 더, 약 60배 내지 약 100배 더, 약 60배 내지 약 90배 더, 약 60배 내지 약 80배 더, 약 60배 내지 약 70배 더, 약 70배 내지 약 100배 더, 약 70배 내지 약 90배 더, 약 70배 내지 약 80배 더, 약 80배 내지 약 100배 더, 약 80배 내지 약 90배 더, 또는 약 90배 내지 약 100배 더) 빠르다.
본원에 기술된 항원 결합 단백질 작제물(ABPC) 중 어느 하나의 일부 구현예에서, 약 4.0 내지 약 6.5의 (예를 들어 본원에 기술된 이 범위의 하위 범위 중 어느 하나의) pH에서 제1 항원 결합 도메인의 (및, 임의로 제2 항원 결합 도메인이 존재하는 경우, 제2 항원 결합 단백질의) 해리 상수(KD)는 약 7.0 내지 약 8.0의 (예를 들어 본원에 기술된 이 범위의 하위 범위 중 어느 하나의) pH에서의 KD보다 더 (예를 들어 검출 가능하게 더) (예를 들어 적어도 0.2배 더, 적어도 0.3배, 적어도 0.4배, 적어도 0.5배, 적어도 0.6배, 적어도 0.7배, 적어도 0.8배, 적어도 0.9배, 적어도 1.0배, 적어도 1.5배, 적어도 2.0배, 적어도 2.5배, 적어도 3.0 fold, 적어도 3.5배, 적어도 4.0배, 적어도 4.5배, 적어도 5.0배, 적어도 5.5배, 적어도 6.0배, 적어도 6.5배, 적어도 7.0배, 적어도 7.5배, 적어도 8.0배, 적어도 8.5배, 적어도 9.0배, 적어도 9.5배, 적어도 10.0배, 적어도 10.5배, 적어도 11.0배, 적어도 11.5배, 적어도 12.0배, 적어도 12.5배, 적어도 13.0배, 적어도 13.5배, 적어도 14.0배, 적어도 14.5배, 적어도 15.0배, 적어도 15.5배, 적어도 16.0배, 적어도 16.5배, 적어도 17.0배, 적어도 17.5배, 적어도 18.0배, 적어도 18.5배, 적어도 19.0배, 적어도 19.5배, 적어도 20배 더, 적어도 25배 더, 적어도 30배 더, 적어도 35배 더, 적어도 40배 더, 적어도 45배 더, 적어도 50배 더, 적어도 55배 더, 적어도 60배 더, 적어도 65배 더, 적어도 70배 더, 적어도 75배 더, 적어도 80배 더, 적어도 85배 더, 적어도 90배 더, 적어도 95배 더, 또는 적어도 100배 더, 또는 약 0.2배 내지 약 100배 더, 약 0.2배 내지 약 90배 더, 약 0.2배 내지 약 80배 더, 약 0.2배 내지 약 70배 더, 약 0.2배 내지 약 60배 더, 약 0.2배 내지 약 50배 더, 약 0.2배 내지 약 40배 더, 약 0.2배 내지 약 30배 더, 약 0.2배 내지 약 25배 더, 약 0.2배 내지 약 20배 더, 약 0.2배 내지 약 15배 더, 약 0.2배 내지 약 10배 더, 약 0.2배 내지 약 8배 더, 약 0.2배 내지 약 5배 더, 약 0.2배 내지 약 2배 더, 약 0.2배 내지 약 1배 더, 약 0.2배 내지 약 0.5배 더, 약 0.5배 내지 약 100배 더, 약 0.5배 내지 약 90배 더, 약 0.5배 내지 약 80배 더, 약 0.5배 내지 약 70배 더, 약 0.5배 내지 약 60배 더, 약 0.5배 내지 약 50배 더, 약 0.5배 내지 약 40배 더, 약 0.5배 내지 약 30배 더, 약 0.5배 내지 약 25배 더, 약 0.5배 내지 약 20배 더, 약 0.5배 내지 약 15배 더, 약 0.5배 내지 약 10배 더, 약 0.5배 내지 약 8배 더, 약 0.5배 내지 약 5배 더, 약 0.5배 내지 약 2배 더, 약 0.5배 내지 약 1배 더, 약 1배 내지 약 100배 더, 약 1배 내지 약 90배 더, 약 1배 내지 약 80배 더, 약 1배 내지 약 70배 더, 약 1배 내지 약 60배 더, 약 1배 내지 약 50배 더, 약 1배 내지 약 40배 더, 약 1배 내지 약 30배 더, 약 1배 내지 약 25배 더, 약 1배 내지 약 20배 더, 약 1배 내지 약 15배 더, 약 1배 내지 약 10배 더, 약 1배 내지 약 8배 더, 약 1배 내지 약 5배 더, 약 1배 내지 약 2배 더, 약 2배 내지 약 100배 더, 약 2배 내지 약 90배 더, 약 2배 내지 약 80배 더, 약 2배 내지 약 70배 더, 약 2배 내지 약 60배 더, 약 2배 내지 약 50배 더, 약 2배 내지 약 40배 더, 약 2배 내지 약 30배 더, 약 2배 내지 약 25배 더, 약 2배 내지 약 20배 더, 약 2배 내지 약 15배 더, 약 2배 내지 약 10배 더, 약 2배 내지 약 8배 더, 약 2배 내지 약 5배 더, 약 5배 내지 약 100배 더, 약 5배 내지 약 90배 더, 약 5배 내지 약 80배 더, 약 5배 내지 약 70배 더, 약 5배 내지 약 60배 더, 약 5배 내지 약 50배 더, 약 5배 내지 약 40배 더, 약 5배 내지 약 30배 더, 약 5배 내지 약 25배 더, 약 5배 내지 약 20배 더, 약 5배 내지 약 15배 더, 약 5배 내지 약 10배 더, 약 5배 내지 약 8배 더, 약 8배 내지 약 100배 더, 약 8배 내지 약 90배 더, 약 8배 내지 약 80배 더, 약 8배 내지 약 70배 더, 약 8배 내지 약 60배 더, 약 8배 내지 약 50배 더, 약 8배 내지 약 40배 더, 약 8배 내지 약 30배 더, 약 8배 내지 약 25배 더, 약 8배 내지 약 20배 더, 약 8배 내지 약 15배 더, 약 8배 내지 약 10배 더, 약 10배 내지 약 100배 더, 약 10배 내지 약 90배 더, 약 10배 내지 약 80배 더, 약 10배 내지 약 70배 더, 약 10배 내지 약 60배 더, 약 10배 내지 약 50배 더, 약 10배 내지 약 40배 더, 약 10배 내지 약 30배 더, 약 10배 내지 약 25배 더, 약 10배 내지 약 20배 더, 약 10배 내지 약 15배 더, 약 15배 내지 약 100배 더, 약 15배 내지 약 90배 더, 약 15배 내지 약 80배 더, 약 15배 내지 약 70배 더, 약 15배 내지 약 60배 더, 약 15배 내지 약 50배 더, 약 15배 내지 약 40배 더, 약 15배 내지 약 30배 더, 약 15배 내지 약 25배 더, 약 15배 내지 약 20배 더, 약 20배 내지 약 100배 더, 약 20배 내지 약 90배 더, 약 20배 내지 약 80배 더, 약 20배 내지 약 70배 더, 약 20배 내지 약 60배 더, 약 20배 내지 약 50배 더, 약 20배 내지 약 40배 더, 약 20배 내지 약 30배 더, 약 20배 내지 약 25배 더, 약 25배 내지 약 100배 더, 약 25배 내지 약 90배 더, 약 25배 내지 약 80배 더, 약 25배 내지 약 70배 더, 약 25배 내지 약 60배 더, 약 25배 내지 약 50배 더, 약 25배 내지 약 40배 더, 약 25배 내지 약 30배 더, 약 30배 내지 약 100배 더, 약 30배 내지 약 90배 더, 약 30배 내지 약 80배 더, 약 30배 내지 약 70배 더, 약 30배 내지 약 60배 더, 약 30배 내지 약 50배 더, 약 30배 내지 약 40배 더, 약 40배 내지 약 100배 더, 약 40배 내지 약 90배 더, 약 40배 내지 약 80배 더, 약 40배 내지 약 70배 더, 약 40배 내지 약 60배 더, 약 40배 내지 약 50배 더, 약 50배 내지 약 100배 더, 약 50배 내지 약 90배 더, 약 50배 내지 약 80배 더, 약 50배 내지 약 70배 더, 약 50배 내지 약 60배 더, 약 60배 내지 약 100배 더, 약 60배 내지 약 90배 더, 약 60배 내지 약 80배 더, 약 60배 내지 약 70배 더, 약 70배 내지 약 100배 더, 약 70배 내지 약 90배 더, 약 70배 내지 약 80배 더, 약 80배 내지 약 100배 더, 약 80배 내지 약 90배 더, 또는 약 90배 내지 약 100배 더) 크다.
제1 항원 결합 도메인 및 제2 항원 결합 도메인을 포함하는 ABPC의 일부 구현서, 제1 및 제2 항원 결합 도메인은 아미노산 서열이 서로 동일하거나 적어도 80% (예를 들어, 적어도 82%, 적어도 84%, 적어도 86%, 적어도 88%, 적어도 90%, 적어도 91%, 적어도 92%, 적어도 93%, 적어도 94%, 적어도 95%, 적어도 96%, 적어도 97%, 적어도 98%, 또는 적어도 99%) 동일하다. 제1 항원 결합 도메인 및 제2 항원 결합 도메인을 포함하는 ABPC의 일부 구현예에서, 제1 항원 결합 도메인 및 제2 항원 결합 도메인은 서로 80% 미만으로 동일한 (예를 들어, 75% 미만으로 동일, 70% 미만으로 동일, 65% 미만으로 동일, 60% 미만으로 동일, 55% 미만으로 동일, 50% 미만으로 동일, 45% 미만으로 동일, 40% 미만으로 동일, 35% 미만으로 동일, 30% 미만으로 동일, 25% 미만으로 동일, 20% 미만으로 동일, 15% 미만으로 동일, 10% 미만으로 동일, 또는 5% 미만으로 동일한) 서열을 갖는다. 제1 및 제2 항원 결합 도메인을 포함하는 ABPC의 일부 구현예에서, 제1 및 제2 항원 결합 도메인은 2개의 상이한 에피토프(예를 들어, MET 상의 2개의 상이한 에피토프, 또는 MET에 특이적으로 결합하는 제1 항원 결합 도메인 및 MET 이외의 항원에 결합하는 제2 항원 결합 도메인)에 결합한다.
본원에 기술된 ABPC 중 어느 하나의 일부 구현예에서, 약 7.0 내지 약 8.0의 (예를 들어 본원에 기술된 이 범위의 하위 범위 중 어느 하나의) pH에서 제1 항원 결합 도메인의 (및, 제2 항원 결합 도메인이 존재하는 경우, 제2 항원 결합 도메인의) KD는 약 1 pM 내지 약 5 μM (예를 들어 약 1 pM 내지 약 2 μM, 약 1 pM 내지 약 1 μM, 약 1 pM 내지 약 500 nM, 약 1 pM 내지 약 250 nM, 약 1 pM 내지 약 240 nM, 약 1 pM 내지 약 230 nM, 약 1 pM 내지 약 220 nM, 약 1 pM 내지 약 210 nM, 약 1 pM 내지 약 200 nM, 약 1 pM 내지 약 190 nM, 약 1 pM 내지 약 180 nM, 약 1 pM 내지 약 170 nM, 약 1 pM 내지 약 160 nM, 약 1 pM 내지 약 150 nM, 약 1 pM 내지 약 140 nM, 약 1 pM 내지 약 130 nM, 약 1 pM 내지 약 120 nM, 약 1 pM 내지 약 110 nM, 약 1 pM 내지 약 100 nM, 약 1 pM 내지 약 95 nM, 약 1 pM 내지 약 90 nM, 약 1 pM 내지 약 85 nM, 약 1 pM 내지 약 80 nM, 약 1 pM 내지 약 75 nM, 약 1 pM 내지 약 70 nM, 약 1 pM 내지 약 65 nM, 약 1 pM 내지 약 60 nM, 약 1 pM 내지 약 55 nM, 약 1 pM 내지 약 50 nM, 약 1 pM 내지 약 45 nM, 약 1 pM 내지 약 40 nM, 약 1 pM 내지 약 35 nM, 약 1 pM 내지 약 30 nM, 약 1 pM 내지 약 25 nM, 약 1 pM 내지 약 20 nM, 약 1 pM 내지 약 15 nM, 약 1 pM 내지 약 10 nM, 약 1 pM 내지 약 5 nM, 약 1 pM 내지 약 2 nM, 약 1 pM 내지 약 1 nM, 약 1 pM 내지 약 950 pM, 약 1 pM 내지 약 900 pM, 약 1 pM 내지 약 850 pM, 약 1 pM 내지 약 800 pM, 약 1 pM 내지 약 750 pM, 약 1 pM 내지 약 700 pM, 약 1 pM 내지 약 650 pM, 약 1 pM 내지 약 600 pM, 약 1 pM 내지 약 550 pM, 약 1 pM 내지 약 500 pM, 약 1 pM 내지 약 450 pM, 약 1 pM 내지 약 400 pM, 약 1 pM 내지 약 350 pM, 약 1 pM 내지 약 300 pM, 약 1 pM 내지 약 250 pM, 약 1 pM 내지 약 200 pM, 약 1 pM 내지 약 150 pM, 약 1 pM 내지 약 100 pM, 약 1 pM 내지 약 90 pM, 약 1 pM 내지 약 80 pM, 약 1 pM 내지 약 70 pM, 약 1 pM 내지 약 60 pM, 약 1 pM 내지 약 50 pM, 약 1 pM 내지 약 40 pM, 약 1 pM 내지 약 30 pM, 약 1 pM 내지 약 20 pM, 약 1 pM 내지 약 10 pM, 약 1 pM 내지 약 5 pM, 약 1 pM 내지 약 4 pM, 약 1 pM 내지 약 3 pM, 약 1 pM 내지 약 2 pM, 약 2 pM 내지 약 5 μM, 약 2 pM 내지 약 2 μM, 약 2 pM 내지 약 1 μM, 약 2 pM 내지 약 500 nM, 약 2 pM 내지 약 250 nM, 약 2 pM 내지 약 240 nM, 약 2 pM 내지 약 230 nM, 약 2 pM 내지 약 220 nM, 약 2 pM 내지 약 210 nM, 약 2 pM 내지 약 200 nM, 약 2 pM 내지 약 190 nM, 약 2 pM 내지 약 180 nM, 약 2 pM 내지 약 170 nM, 약 2 pM 내지 약 160 nM, 약 2 pM 내지 약 150 nM, 약 2 pM 내지 약 140 nM, 약 2 pM 내지 약 130 nM, 약 2 pM 내지 약 120 nM, 약 2 pM 내지 약 110 nM, 약 2 pM 내지 약 100 nM, 약 2 pM 내지 약 95 nM, 약 2 pM 내지 약 90 nM, 약 2 pM 내지 약 85 nM, 약 2 pM 내지 약 80 nM, 약 2 pM 내지 약 75 nM, 약 2 pM 내지 약 70 nM, 약 2 pM 내지 약 65 nM, 약 2 pM 내지 약 60 nM, 약 2 pM 내지 약 55 nM, 약 2 pM 내지 약 50 nM, 약 2 pM 내지 약 45 nM, 약 2 pM 내지 약 40 nM, 약 2 pM 내지 약 35 nM, 약 2 pM 내지 약 30 nM, 약 2 pM 내지 약 25 nM, 약 2 pM 내지 약 20 nM, 약 2 pM 내지 약 15 nM, 약 2 pM 내지 약 10 nM, 약 2 pM 내지 약 5 nM, 약 2 pM 내지 약 2 nM, 약 2 pM 내지 약 1 nM, 약 2 pM 내지 약 950 pM, 약 2 pM 내지 약 900 pM, 약 2 pM 내지 약 850 pM, 약 2 pM 내지 약 800 pM, 약 2 pM 내지 약 750 pM, 약 2 pM 내지 약 700 pM, 약 2 pM 내지 약 650 pM, 약 2 pM 내지 약 600 pM, 약 2 pM 내지 약 550 pM, 약 2 pM 내지 약 500 pM, 약 2 pM 내지 약 450 pM, 약 2 pM 내지 약 400 pM, 약 2 pM 내지 약 350 pM, 약 2 pM 내지 약 300 pM, 약 2 pM 내지 약 250 pM, 약 2 pM 내지 약 200 pM, 약 2 pM 내지 약 150 pM, 약 2 pM 내지 약 100 pM, 약 2 pM 내지 약 90 pM, 약 2 pM 내지 약 80 pM, 약 2 pM 내지 약 70 pM, 약 2 pM 내지 약 60 pM, 약 2 pM 내지 약 50 pM, 약 2 pM 내지 약 40 pM, 약 2 pM 내지 약 30 pM, 약 2 pM 내지 약 20 pM, 약 2 pM 내지 약 10 pM, 약 2 pM 내지 약 5 pM, 약 2 pM 내지 약 4 pM, 약 2 pM 내지 약 3 pM, 약 5 pM 내지 약 5 μM, 약 5 pM 내지 약 2 μM, 약 5 pM 내지 약 1 μM, 약 5 pM 내지 약 500 nM, 약 5 pM 내지 약 250 nM, 약 5 pM 내지 약 240 nM, 약 5 pM 내지 약 230 nM, 약 5 pM 내지 약 220 nM, 약 5 pM 내지 약 210 nM, 약 5 pM 내지 약 200 nM, 약 5 pM 내지 약 190 nM, 약 5 pM 내지 약 180 nM, 약 5 pM 내지 약 170 nM, 약 5 pM 내지 약 160 nM, 약 5 pM 내지 약 150 nM, 약 5 pM 내지 약 140 nM, 약 5 pM 내지 약 130 nM, 약 5 pM 내지 약 120 nM, 약 5 pM 내지 약 110 nM, 약 5 pM 내지 약 100 nM, 약 5 pM 내지 약 95 nM, 약 5 pM 내지 약 90 nM, 약 5 pM 내지 약 85 nM, 약 5 pM 내지 약 80 nM, 약 5 pM 내지 약 75 nM, 약 5 pM 내지 약 70 nM, 약 5 pM 내지 약 65 nM, 약 5 pM 내지 약 60 nM, 약 5 pM 내지 약 55 nM, 약 5 pM 내지 약 50 nM, 약 5 pM 내지 약 45 nM, 약 5 pM 내지 약 40 nM, 약 5 pM 내지 약 35 nM, 약 5 pM 내지 약 30 nM, 약 5 pM 내지 약 25 nM, 약 5 pM 내지 약 20 nM, 약 5 pM 내지 약 15 nM, 약 5 pM 내지 약 10 nM, 약 5 pM 내지 약 5 nM, 약 5 pM 내지 약 2 nM, 약 5 pM 내지 약 1 nM, 약 5 pM 내지 약 950 pM, 약 5 pM 내지 약 900 pM, 약 5 pM 내지 약 850 pM, 약 5 pM 내지 약 800 pM, 약 5 pM 내지 약 750 pM, 약 5 pM 내지 약 700 pM, 약 5 pM 내지 약 650 pM, 약 5 pM 내지 약 600 pM, 약 5 pM 내지 약 550 pM, 약 5 pM 내지 약 500 pM, 약 5 pM 내지 약 450 pM, 약 5 pM 내지 약 400 pM, 약 5 pM 내지 약 350 pM, 약 5 pM 내지 약 300 pM, 약 5 pM 내지 약 250 pM, 약 5 pM 내지 약 200 pM, 약 5 pM 내지 약 150 pM, 약 5 pM 내지 약 100 pM, 약 5 pM 내지 약 90 pM, 약 5 pM 내지 약 80 pM, 약 5 pM 내지 약 70 pM, 약 5 pM 내지 약 60 pM, 약 5 pM 내지 약 50 pM, 약 5 pM 내지 약 40 pM, 약 5 pM 내지 약 30 pM, 약 5 pM 내지 약 20 pM, 약 5 pM 내지 약 10 pM, 약 10 pM 내지 약 5 μM, 약 10 pM 내지 약 2 μM, 약 10 pM 내지 약 1 μM, 약 10 pM 내지 약 500 nM, 약 10 pM 내지 약 250 nM, 약 10 pM 내지 약 240 nM, 약 10 pM 내지 약 230 nM, 약 10 pM 내지 약 220 nM, 약 10 pM 내지 약 210 nM, 약 10 pM 내지 약 200 nM, 약 10 pM 내지 약 190 nM, 약 10 pM 내지 약 180 nM, 약 10 pM 내지 약 170 nM, 약 10 pM 내지 약 160 nM, 약 10 pM 내지 약 150 nM, 약 10 pM 내지 약 140 nM, 약 10 pM 내지 약 130 nM, 약 10 pM 내지 약 120 nM, 약 10 pM 내지 약 110 nM, 약 10 pM 내지 약 100 nM, 약 10 pM 내지 약 95 nM, 약 10 pM 내지 약 90 nM, 약 10 pM 내지 약 85 nM, 약 10 pM 내지 약 80 nM, 약 10 pM 내지 약 75 nM, 약 10 pM 내지 약 70 nM, 약 10 pM 내지 약 65 nM, 약 10 pM 내지 약 60 nM, 약 10 pM 내지 약 55 nM, 약 10 pM 내지 약 50 nM, 약 10 pM 내지 약 45 nM, 약 10 pM 내지 약 40 nM, 약 10 pM 내지 약 35 nM, 약 10 pM 내지 약 30 nM, 약 10 pM 내지 약 25 nM, 약 10 pM 내지 약 20 nM, 약 10 pM 내지 약 15 nM, 약 10 pM 내지 약 10 nM, 약 10 pM 내지 약 5 nM, 약 10 pM 내지 약 2 nM, 약 10 pM 내지 약 1 nM, 약 10 pM 내지 약 950 pM, 약 10 pM 내지 약 900 pM, 약 10 pM 내지 약 850 pM, 약 10 pM 내지 약 800 pM, 약 10 pM 내지 약 750 pM, 약 10 pM 내지 약 700 pM, 약 10 pM 내지 약 650 pM, 약 10 pM 내지 약 600 pM, 약 10 pM 내지 약 550 pM, 약 10 pM 내지 약 500 pM, 약 10 pM 내지 약 450 pM, 약 10 pM 내지 약 400 pM, 약 10 pM 내지 약 350 pM, 약 10 pM 내지 약 300 pM, 약 10 pM 내지 약 250 pM, 약 10 pM 내지 약 200 pM, 약 10 pM 내지 약 150 pM, 약 10 pM 내지 약 100 pM, 약 10 pM 내지 약 90 pM, 약 10 pM 내지 약 80 pM, 약 10 pM 내지 약 70 pM, 약 10 pM 내지 약 60 pM, 약 10 pM 내지 약 50 pM, 약 10 pM 내지 약 40 pM, 약 10 pM 내지 약 30 pM, 약 10 pM 내지 약 20 pM, 약 15 pM 내지 약 5 μM, 약 15 pM 내지 약 2 μM, 약 15 pM 내지 약 1 μM, 약 15 pM 내지 약 500 nM, 약 15 pM 내지 약 250 nM, 약 15 pM 내지 약 240 nM, 약 15 pM 내지 약 230 nM, 약 15 pM 내지 약 220 nM, 약 15 pM 내지 약 210 nM, 약 15 pM 내지 약 200 nM, 약 15 pM 내지 약 190 nM, 약 15 pM 내지 약 180 nM, 약 15 pM 내지 약 170 nM, 약 15 pM 내지 약 160 nM, 약 15 pM 내지 약 150 nM, 약 15 pM 내지 약 140 nM, 약 15 pM 내지 약 130 nM, 약 15 pM 내지 약 120 nM, 약 15 pM 내지 약 110 nM, 약 15 pM 내지 약 100 nM, 약 15 pM 내지 약 95 nM, 약 15 pM 내지 약 90 nM, 약 15 pM 내지 약 85 nM, 약 15 pM 내지 약 80 nM, 약 15 pM 내지 약 75 nM, 약 15 pM 내지 약 70 nM, 약 15 pM 내지 약 65 nM, 약 15 pM 내지 약 60 nM, 약 15 pM 내지 약 55 nM, 약 15 pM 내지 약 50 nM, 약 15 pM 내지 약 45 nM, 약 15 pM 내지 약 40 nM, 약 15 pM 내지 약 35 nM, 약 15 pM 내지 약 30 nM, 약 15 pM 내지 약 25 nM, 약 15 pM 내지 약 20 nM, 약 15 pM 내지 약 15 nM, 약 15 pM 내지 약 10 nM, 약 15 pM 내지 약 5 nM, 약 15 pM 내지 약 2 nM, 약 15 pM 내지 약 1 nM, 약 15 pM 내지 약 950 pM, 약 15 pM 내지 약 900 pM, 약 15 pM 내지 약 850 pM, 약 15 pM 내지 약 800 pM, 약 15 pM 내지 약 750 pM, 약 15 pM 내지 약 700 pM, 약 15 pM 내지 약 650 pM, 약 15 pM 내지 약 600 pM, 약 15 pM 내지 약 550 pM, 약 15 pM 내지 약 500 pM, 약 15 pM 내지 약 450 pM, 약 15 pM 내지 약 400 pM, 약 15 pM 내지 약 350 pM, 약 15 pM 내지 약 300 pM, 약 15 pM 내지 약 250 pM, 약 15 pM 내지 약 200 pM, 약 15 pM 내지 약 150 pM, 약 15 pM 내지 약 100 pM, 약 15 pM 내지 약 90 pM, 약 15 pM 내지 약 80 pM, 약 15 pM 내지 약 70 pM, 약 15 pM 내지 약 60 pM, 약 15 pM 내지 약 50 pM, 약 15 pM 내지 약 40 pM, 약 15 pM 내지 약 30 pM, 약 15 pM 내지 약 20 pM, 약 20 pM 내지 약 5 μM, 약 20 pM 내지 약 2 μM, 약 20 pM 내지 약 1 μM, 약 20 pM 내지 약 500 nM, 약 20 pM 내지 약 250 nM, 약 20 pM 내지 약 240 nM, 약 20 pM 내지 약 230 nM, 약 20 pM 내지 약 220 nM, 약 20 pM 내지 약 210 nM, 약 20 pM 내지 약 200 nM, 약 20 pM 내지 약 190 nM, 약 20 pM 내지 약 180 nM, 약 20 pM 내지 약 170 nM, 약 20 pM 내지 약 160 nM, 약 20 pM 내지 약 150 nM, 약 20 pM 내지 약 140 nM, 약 20 pM 내지 약 130 nM, 약 20 pM 내지 약 120 nM, 약 20 pM 내지 약 110 nM, 약 20 pM 내지 약 100 nM, 약 20 pM 내지 약 95 nM, 약 20 pM 내지 약 90 nM, 약 20 pM 내지 약 85 nM, 약 20 pM 내지 약 80 nM, 약 20 pM 내지 약 75 nM, 약 20 pM 내지 약 70 nM, 약 20 pM 내지 약 65 nM, 약 20 pM 내지 약 60 nM, 약 20 pM 내지 약 55 nM, 약 20 pM 내지 약 50 nM, 약 20 pM 내지 약 45 nM, 약 20 pM 내지 약 40 nM, 약 20 pM 내지 약 35 nM, 약 20 pM 내지 약 30 nM, 약 20 pM 내지 약 25 nM, 약 20 pM 내지 약 20 nM, 약 20 pM 내지 약 15 nM, 약 20 pM 내지 약 10 nM, 약 20 pM 내지 약 5 nM, 약 20 pM 내지 약 2 nM, 약 20 pM 내지 약 1 nM, 약 20 pM 내지 약 950 pM, 약 20 pM 내지 약 900 pM, 약 20 pM 내지 약 850 pM, 약 20 pM 내지 약 800 pM, 약 20 pM 내지 약 750 pM, 약 20 pM 내지 약 700 pM, 약 20 pM 내지 약 650 pM, 약 20 pM 내지 약 600 pM, 약 20 pM 내지 약 550 pM, 약 20 pM 내지 약 500 pM, 약 20 pM 내지 약 450 pM, 약 20 pM 내지 약 400 pM, 약 20 pM 내지 약 350 pM, 약 20 pM 내지 약 300 pM, 약 20 pM 내지 약 250 pM, 약 20 pM 내지 약 20 pM, 약 200 pM 내지 약 150 pM, 약 20 pM 내지 약 100 pM, 약 20 pM 내지 약 90 pM, 약 20 pM 내지 약 80 pM, 약 20 pM 내지 약 70 pM, 약 20 pM 내지 약 60 pM, 약 20 pM 내지 약 50 pM, 약 20 pM 내지 약 40 pM, 약 20 pM 내지 약 30 pM, 약 30 pM 내지 약 5 μM, 약 30 pM 내지 약 2 μM, 약 30 pM 내지 약 1 μM, 약 30 pM 내지 약 500 nM, 약 30 pM 내지 약 250 nM, 약 30 pM 내지 약 240 nM, 약 30 pM 내지 약 230 nM, 약 30 pM 내지 약 220 nM, 약 30 pM 내지 약 210 nM, 약 30 pM 내지 약 200 nM, 약 30 pM 내지 약 190 nM, 약 30 pM 내지 약 180 nM, 약 30 pM 내지 약 170 nM, 약 30 pM 내지 약 160 nM, 약 30 pM 내지 약 150 nM, 약 30 pM 내지 약 140 nM, 약 30 pM 내지 약 130 nM, 약 30 pM 내지 약 120 nM, 약 30 pM 내지 약 110 nM, 약 30 pM 내지 약 100 nM, 약 30 pM 내지 약 95 nM, 약 30 pM 내지 약 90 nM, 약 30 pM 내지 약 85 nM, 약 30 pM 내지 약 80 nM, 약 30 pM 내지 약 75 nM, 약 30 pM 내지 약 70 nM, 약 30 pM 내지 약 65 nM, 약 30 pM 내지 약 60 nM, 약 30 pM 내지 약 55 nM, 약 30 pM 내지 약 50 nM, 약 30 pM 내지 약 45 nM, 약 30 pM 내지 약 40 nM, 약 30 pM 내지 약 35 nM, 약 30 pM 내지 약 30 nM, 약 30 pM 내지 약 25 nM, 약 30 pM 내지 약 20 nM, 약 30 pM 내지 약 15 nM, 약 30 pM 내지 약 10 nM, 약 30 pM 내지 약 5 nM, 약 30 pM 내지 약 2 nM, 약 30 pM 내지 약 1 nM, 약 30 pM 내지 약 950 pM, 약 30 pM 내지 약 900 pM, 약 30 pM 내지 약 850 pM, 약 30 pM 내지 약 800 pM, 약 30 pM 내지 약 750 pM, 약 30 pM 내지 약 700 pM, 약 30 pM 내지 약 650 pM, 약 30 pM 내지 약 600 pM, 약 30 pM 내지 약 550 pM, 약 30 pM 내지 약 500 pM, 약 30 pM 내지 약 450 pM, 약 30 pM 내지 약 400 pM, 약 30 pM 내지 약 350 pM, 약 30 pM 내지 약 300 pM, 약 30 pM 내지 약 250 pM, 약 30 pM 내지 약 200 pM, 약 30 pM 내지 약 150 pM, 약 30 pM 내지 약 100 pM, 약 30 pM 내지 약 90 pM, 약 30 pM 내지 약 80 pM, 약 30 pM 내지 약 70 pM, 약 30 pM 내지 약 60 pM, 약 30 pM 내지 약 50 pM, 약 30 pM 내지 약 40 pM, 약 40 pM 내지 약 5 μM, 약 40 pM 내지 약 2 μM, 약 40 pM 내지 약 1 μM, 약 40 pM 내지 약 500 nM, 약 40 pM 내지 약 250 nM, 약 40 pM 내지 약 240 nM, 약 40 pM 내지 약 230 nM, 약 40 pM 내지 약 220 nM, 약 40 pM 내지 약 210 nM, 약 40 pM 내지 약 200 nM, 약 40 pM 내지 약 190 nM, 약 40 pM 내지 약 180 nM, 약 40 pM 내지 약 170 nM, 약 40 pM 내지 약 160 nM, 약 40 pM 내지 약 150 nM, 약 40 pM 내지 약 140 nM, 약 40 pM 내지 약 130 nM, 약 40 pM 내지 약 120 nM, 약 40 pM 내지 약 110 nM, 약 40 pM 내지 약 100 nM, 약 40 pM 내지 약 95 nM, 약 40 pM 내지 약 90 nM, 약 40 pM 내지 약 85 nM, 약 40 pM 내지 약 80 nM, 약 40 pM 내지 약 75 nM, 약 40 pM 내지 약 70 nM, 약 40 pM 내지 약 65 nM, 약 40 pM 내지 약 60 nM, 약 40 pM 내지 약 55 nM, 약 40 pM 내지 약 50 nM, 약 40 pM 내지 약 45 nM, 약 40 pM 내지 약 40 nM, 약 40 pM 내지 약 35 nM, 약 40 pM 내지 약 30 nM, 약 40 pM 내지 약 25 nM, 약 40 pM 내지 약 30 nM, 약 40 pM 내지 약 15 nM, 약 40 pM 내지 약 10 nM, 약 40 pM 내지 약 5 nM, 약 40 pM 내지 약 2 nM, 약 40 pM 내지 약 1 nM, 약 40 pM 내지 약 950 pM, 약 40 pM 내지 약 900 pM, 약 40 pM 내지 약 850 pM, 약 40 pM 내지 약 800 pM, 약 40 pM 내지 약 750 pM, 약 40 pM 내지 약 700 pM, 약 40 pM 내지 약 650 pM, 약 40 pM 내지 약 600 pM, 약 40 pM 내지 약 550 pM, 약 40 pM 내지 약 500 pM, 약 40 pM 내지 약 450 pM, 약 40 pM 내지 약 400 pM, 약 40 pM 내지 약 350 pM, 약 40 pM 내지 약 300 pM, 약 40 pM 내지 약 250 pM, 약 40 pM 내지 약 200 pM, 약 40 pM 내지 약 150 pM, 약 40 pM 내지 약 100 pM, 약 40 pM 내지 약 90 pM, 약 40 pM 내지 약 80 pM, 약 40 pM 내지 약 70 pM, 약 40 pM 내지 약 60 pM, 약 40 pM 내지 약 50 pM, 약 50 pM 내지 약 5 μM, 약 50 pM 내지 약 2 μM, 약 50 pM 내지 약 1 μM, 약 50 pM 내지 약 500 nM, 약 50 pM 내지 약 250 nM, 약 50 pM 내지 약 240 nM, 약 50 pM 내지 약 230 nM, 약 50 pM 내지 약 220 nM, 약 50 pM 내지 약 210 nM, 약 50 pM 내지 약 200 nM, 약 50 pM 내지 약 190 nM, 약 50 pM 내지 약 180 nM, 약 50 pM 내지 약 170 nM, 약 50 pM 내지 약 160 nM, 약 50 pM 내지 약 150 nM, 약 50 pM 내지 약 140 nM, 약 50 pM 내지 약 130 nM, 약 50 pM 내지 약 120 nM, 약 50 pM 내지 약 110 nM, 약 50 pM 내지 약 100 nM, 약 50 pM 내지 약 95 nM, 약 50 pM 내지 약 90 nM, 약 50 pM 내지 약 85 nM, 약 50 pM 내지 약 80 nM, 약 50 pM 내지 약 75 nM, 약 50 pM 내지 약 70 nM, 약 50 pM 내지 약 65 nM, 약 50 pM 내지 약 60 nM, 약 50 pM 내지 약 55 nM, 약 50 pM 내지 약 50 nM, 약 50 pM 내지 약 45 nM, 약 50 pM 내지 약 40 nM, 약 50 pM 내지 약 35 nM, 약 50 pM 내지 약 30 nM, 약 50 pM 내지 약 25 nM, 약 50 pM 내지 약 30 nM, 약 50 pM 내지 약 15 nM, 약 50 pM 내지 약 10 nM, 약 50 pM 내지 약 5 nM, 약 50 pM 내지 약 2 nM, 약 50 pM 내지 약 1 nM, 약 50 pM 내지 약 950 pM, 약 50 pM 내지 약 900 pM, 약 50 pM 내지 약 850 pM, 약 50 pM 내지 약 800 pM, 약 50 pM 내지 약 750 pM, 약 50 pM 내지 약 700 pM, 약 50 pM 내지 약 650 pM, 약 50 pM 내지 약 600 pM, 약 50 pM 내지 약 550 pM, 약 50 pM 내지 약 500 pM, 약 50 pM 내지 약 450 pM, 약 50 pM 내지 약 400 pM, 약 50 pM 내지 약 350 pM, 약 50 pM 내지 약 300 pM, 약 50 pM 내지 약 250 pM, 약 50 pM 내지 약 200 pM, 약 50 pM 내지 약 150 pM, 약 50 pM 내지 약 100 pM, 약 50 pM 내지 약 90 pM, 약 50 pM 내지 약 80 pM, 약 50 pM 내지 약 70 pM, 약 50 pM 내지 약 60 pM, 약 60 pM 내지 약 5 μM, 약 60 pM 내지 약 2 μM, 약 60 pM 내지 약 1 μM, 약 60 pM 내지 약 500 nM, 약 60 pM 내지 약 250 nM, 약 60 pM 내지 약 240 nM, 약 60 pM 내지 약 230 nM, 약 60 pM 내지 약 220 nM, 약 60 pM 내지 약 210 nM, 약 60 pM 내지 약 200 nM, 약 60 pM 내지 약 190 nM, 약 60 pM 내지 약 180 nM, 약 60 pM 내지 약 170 nM, 약 60 pM 내지 약 160 nM, 약 60 pM 내지 약 150 nM, 약 60 pM 내지 약 140 nM, 약 60 pM 내지 약 130 nM, 약 60 pM 내지 약 120 nM, 약 60 pM 내지 약 110 nM, 약 60 pM 내지 약 100 nM, 약 60 pM 내지 약 95 nM, 약 60 pM 내지 약 90 nM, 약 60 pM 내지 약 85 nM, 약 60 pM 내지 약 80 nM, 약 60 pM 내지 약 75 nM, 약 60 pM 내지 약 70 nM, 약 60 pM 내지 약 65 nM, 약 60 pM 내지 약 60 nM, 약 60 pM 내지 약 55 nM, 약 60 pM 내지 약 50 nM, 약 60 pM 내지 약 45 nM, 약 60 pM 내지 약 40 nM, 약 60 pM 내지 약 35 nM, 약 60 pM 내지 약 30 nM, 약 60 pM 내지 약 25 nM, 약 60 pM 내지 약 20 nM, 약 60 pM 내지 약 15 nM, 약 60 pM 내지 약 10 nM, 약 60 pM 내지 약 5 nM, 약 60 pM 내지 약 2 nM, 약 60 pM 내지 약 1 nM, 약 60 pM 내지 약 950 pM, 약 60 pM 내지 약 900 pM, 약 60 pM 내지 약 850 pM, 약 60 pM 내지 약 800 pM, 약 60 pM 내지 약 750 pM, 약 60 pM 내지 약 700 pM, 약 60 pM 내지 약 650 pM, 약 60 pM 내지 약 600 pM, 약 60 pM 내지 약 550 pM, 약 60 pM 내지 약 500 pM, 약 60 pM 내지 약 450 pM, 약 60 pM 내지 약 400 pM, 약 60 pM 내지 약 350 pM, 약 60 pM 내지 약 300 pM, 약 60 pM 내지 약 250 pM, 약 60 pM 내지 약 200 pM, 약 60 pM 내지 약 150 pM, 약 60 pM 내지 약 100 pM, 약 60 pM 내지 약 90 pM, 약 60 pM 내지 약 80 pM, 약 60 pM 내지 약 70 pM, 약 70 pM 내지 약 5 μM, 약 70 pM 내지 약 2 μM, 약 70 pM 내지 약 1 μM, 약 70 pM 내지 약 500 nM, 약 70 pM 내지 약 250 nM, 약 70 pM 내지 약 240 nM, 약 70 pM 내지 약 230 nM, 약 70 pM 내지 약 220 nM, 약 70 pM 내지 약 210 nM, 약 70 pM 내지 약 200 nM, 약 70 pM 내지 약 190 nM, 약 70 pM 내지 약 180 nM, 약 70 pM 내지 약 170 nM, 약 70 pM 내지 약 160 nM, 약 70 pM 내지 약 150 nM, 약 70 pM 내지 약 140 nM, 약 70 pM 내지 약 130 nM, 약 70 pM 내지 약 120 nM, 약 70 pM 내지 약 110 nM, 약 70 pM 내지 약 100 nM, 약 70 pM 내지 약 95 nM, 약 70 pM 내지 약 90 nM, 약 70 pM 내지 약 85 nM, 약 70 pM 내지 약 80 nM, 약 70 pM 내지 약 75 nM, 약 70 pM 내지 약 70 nM, 약 70 pM 내지 약 65 nM, 약 70 pM 내지 약 60 nM, 약 70 pM 내지 약 55 nM, 약 70 pM 내지 약 50 nM, 약 70 pM 내지 약 45 nM, 약 70 pM 내지 약 40 nM, 약 70 pM 내지 약 35 nM, 약 70 pM 내지 약 30 nM, 약 70 pM 내지 약 25 nM, 약 70 pM 내지 약 20 nM, 약 70 pM 내지 약 15 nM, 약 70 pM 내지 약 10 nM, 약 70 pM 내지 약 5 nM, 약 70 pM 내지 약 2 nM, 약 70 pM 내지 약 1 nM, 약 70 pM 내지 약 950 pM, 약 70 pM 내지 약 900 pM, 약 70 pM 내지 약 850 pM, 약 70 pM 내지 약 800 pM, 약 70 pM 내지 약 750 pM, 약 70 pM 내지 약 700 pM, 약 70 pM 내지 약 650 pM, 약 70 pM 내지 약 600 pM, 약 70 pM 내지 약 550 pM, 약 70 pM 내지 약 500 pM, 약 70 pM 내지 약 450 pM, 약 70 pM 내지 약 400 pM, 약 70 pM 내지 약 350 pM, 약 70 pM 내지 약 300 pM, 약 70 pM 내지 약 250 pM, 약 70 pM 내지 약 200 pM, 약 70 pM 내지 약 150 pM, 약 70 pM 내지 약 100 pM, 약 70 pM 내지 약 90 pM, 약 70 pM 내지 약 80 pM, 약 80 pM 내지 약 5 μM, 약 80 pM 내지 약 2 μM, 약 80 pM 내지 약 1 μM, 약 80 pM 내지 약 500 nM, 약 80 pM 내지 약 250 nM, 약 80 pM 내지 약 240 nM, 약 80 pM 내지 약 230 nM, 약 80 pM 내지 약 220 nM, 약 80 pM 내지 약 210 nM, 약 80 pM 내지 약 200 nM, 약 80 pM 내지 약 190 nM, 약 80 pM 내지 약 180 nM, 약 80 pM 내지 약 170 nM, 약 80 pM 내지 약 160 nM, 약 80 pM 내지 약 150 nM, 약 80 pM 내지 약 140 nM, 약 80 pM 내지 약 130 nM, 약 80 pM 내지 약 120 nM, 약 80 pM 내지 약 110 nM, 약 80 pM 내지 약 100 nM, 약 80 pM 내지 약 95 nM, 약 80 pM 내지 약 90 nM, 약 80 pM 내지 약 85 nM, 약 80 pM 내지 약 80 nM, 약 80 pM 내지 약 75 nM, 약 80 pM 내지 약 70 nM, 약 80 pM 내지 약 65 nM, 약 80 pM 내지 약 60 nM, 약 80 pM 내지 약 55 nM, 약 80 pM 내지 약 50 nM, 약 80 pM 내지 약 45 nM, 약 80 pM 내지 약 40 nM, 약 80 pM 내지 약 35 nM, 약 80 pM 내지 약 30 nM, 약 80 pM 내지 약 25 nM, 약 80 pM 내지 약 20 nM, 약 80 pM 내지 약 15 nM, 약 80 pM 내지 약 10 nM, 약 80 pM 내지 약 5 nM, 약 80 pM 내지 약 2 nM, 약 80 pM 내지 약 1 nM, 약 80 pM 내지 약 950 pM, 약 80 pM 내지 약 900 pM, 약 80 pM 내지 약 850 pM, 약 80 pM 내지 약 800 pM, 약 80 pM 내지 약 750 pM, 약 80 pM 내지 약 700 pM, 약 80 pM 내지 약 650 pM, 약 80 pM 내지 약 600 pM, 약 80 pM 내지 약 550 pM, 약 80 pM 내지 약 500 pM, 약 80 pM 내지 약 450 pM, 약 80 pM 내지 약 400 pM, 약 80 pM 내지 약 350 pM, 약 80 pM 내지 약 300 pM, 약 80 pM 내지 약 250 pM, 약 80 pM 내지 약 200 pM, 약 80 pM 내지 약 150 pM, 약 80 pM 내지 약 100 pM, 약 80 pM 내지 약 90 pM, 약 90 pM 내지 약 5 μM, 약 90 pM 내지 약 2 μM, 약 90 pM 내지 약 1 μM, 약 90 pM 내지 약 500 nM, 약 90 pM 내지 약 250 nM, 약 90 pM 내지 약 240 nM, 약 90 pM 내지 약 230 nM, 약 90 pM 내지 약 220 nM, 약 90 pM 내지 약 210 nM, 약 90 pM 내지 약 200 nM, 약 90 pM 내지 약 190 nM, 약 90 pM 내지 약 180 nM, 약 90 pM 내지 약 170 nM, 약 90 pM 내지 약 160 nM, 약 90 pM 내지 약 150 nM, 약 90 pM 내지 약 140 nM, 약 90 pM 내지 약 130 nM, 약 90 pM 내지 약 120 nM, 약 90 pM 내지 약 110 nM, 약 90 pM 내지 약 100 nM, 약 90 pM 내지 약 95 nM, 약 90 pM 내지 약 90 nM, 약 90 pM 내지 약 85 nM, 약 90 pM 내지 약 80 nM, 약 90 pM 내지 약 75 nM, 약 90 pM 내지 약 70 nM, 약 90 pM 내지 약 65 nM, 약 90 pM 내지 약 60 nM, 약 90 pM 내지 약 55 nM, 약 90 pM 내지 약 50 nM, 약 90 pM 내지 약 45 nM, 약 90 pM 내지 약 40 nM, 약 90 pM 내지 약 35 nM, 약 90 pM 내지 약 30 nM, 약 90 pM 내지 약 25 nM, 약 90 pM 내지 약 30 nM, 약 90 pM 내지 약 15 nM, 약 90 pM 내지 약 10 nM, 약 90 pM 내지 약 5 nM, 약 90 pM 내지 약 2 nM, 약 90 pM 내지 약 1 nM, 약 90 pM 내지 약 950 pM, 약 90 pM 내지 약 900 pM, 약 90 pM 내지 약 850 pM, 약 90 pM 내지 약 800 pM, 약 90 pM 내지 약 750 pM, 약 90 pM 내지 약 700 pM, 약 90 pM 내지 약 650 pM, 약 90 pM 내지 약 600 pM, 약 90 pM 내지 약 550 pM, 약 90 pM 내지 약 500 pM, 약 90 pM 내지 약 450 pM, 약 90 pM 내지 약 400 pM, 약 90 pM 내지 약 350 pM, 약 90 pM 내지 약 300 pM, 약 90 pM 내지 약 250 pM, 약 90 pM 내지 약 200 pM, 약 90 pM 내지 약 150 pM, 약 90 pM 내지 약 100 pM, 약 100 pM 내지 약 30 nM, 약 100 pM 내지 약 25 nM, 약 100 pM 내지 약 5 μM, 약 100 pM 내지 약 2 μM, 약 100 pM 내지 약 1 μM, 약 100 pM 내지 약 500 nM, 약 100 pM 내지 약 250 nM, 약 100 pM 내지 약 240 nM, 약 100 pM 내지 약 230 nM, 약 100 pM 내지 약 220 nM, 약 100 pM 내지 약 210 nM, 약 100 pM 내지 약 200 nM, 약 100 pM 내지 약 190 nM, 약 100 pM 내지 약 180 nM, 약 100 pM 내지 약 170 nM, 약 100 pM 내지 약 160 nM, 약 100 pM 내지 약 150 nM, 약 100 pM 내지 약 140 nM, 약 100 pM 내지 약 130 nM, 약 100 pM 내지 약 120 nM, 약 100 pM 내지 약 110 nM, 약 100 pM 내지 약 100 nM, 약 100 pM 내지 약 95 nM, 약 100 pM 내지 약 90 nM, 약 100 pM 내지 약 85 nM, 약 100 pM 내지 약 80 nM, 약 100 pM 내지 약 75 nM, 약 100 pM 내지 약 70 nM, 약 100 pM 내지 약 65 nM, 약 100 pM 내지 약 60 nM, 약 100 pM 내지 약 55 nM, 약 100 pM 내지 약 50 nM, 약 100 pM 내지 약 45 nM, 약 100 pM 내지 약 40 nM, 약 100 pM 내지 약 35 nM, 약 100 pM 내지 약 30 nM, 약 100 pM 내지 약 15 nM, 약 100 pM 내지 약 10 nM, 약 100 pM 내지 약 5 nM, 약 100 pM 내지 약 2 nM, 약 100 pM 내지 약 1 nM, 약 100 pM 내지 약 950 pM, 약 100 pM 내지 약 900 pM, 약 100 pM 내지 약 850 pM, 약 100 pM 내지 약 800 pM, 약 100 pM 내지 약 750 pM, 약 100 pM 내지 약 700 pM, 약 100 pM 내지 약 650 pM, 약 100 pM 내지 약 600 pM, 약 100 pM 내지 약 550 pM, 약 100 pM 내지 약 500 pM, 약 100 pM 내지 약 450 pM, 약 100 pM 내지 약 400 pM, 약 100 pM 내지 약 350 pM, 약 100 pM 내지 약 300 pM, 약 100 pM 내지 약 250 pM, 약 100 pM 내지 약 200 pM, 약 100 pM 내지 약 150 pM, 약 150 pM 내지 약 5 μM, 약 150 pM 내지 약 2 μM, 약 150 pM 내지 약 1 μM, 약 150 pM 내지 약 500 nM, 약 150 pM 내지 약 250 nM, 약 150 pM 내지 약 240 nM, 약 150 pM 내지 약 230 nM, 약 150 pM 내지 약 220 nM, 약 150 pM 내지 약 210 nM, 약 150 pM 내지 약 200 nM, 약 150 pM 내지 약 190 nM, 약 150 pM 내지 약 180 nM, 약 150 pM 내지 약 170 nM, 약 150 pM 내지 약 160 nM, 약 150 pM 내지 약 150 nM, 약 150 pM 내지 약 140 nM, 약 150 pM 내지 약 130 nM, 약 150 pM 내지 약 120 nM, 약 150 pM 내지 약 110 nM, 약 150 pM 내지 약 100 nM, 약 150 pM 내지 약 95 nM, 약 150 pM 내지 약 90 nM, 약 150 pM 내지 약 85 nM, 약 150 pM 내지 약 80 nM, 약 150 pM 내지 약 75 nM, 약 150 pM 내지 약 70 nM, 약 150 pM 내지 약 65 nM, 약 150 pM 내지 약 60 nM, 약 150 pM 내지 약 55 nM, 약 150 pM 내지 약 50 nM, 약 150 pM 내지 약 45 nM, 약 150 pM 내지 약 40 nM, 약 150 pM 내지 약 35 nM, 약 150 pM 내지 약 30 nM, 약 150 pM 내지 약 25 nM, 약 150 pM 내지 약 30 nM, 약 150 pM 내지 약 15 nM, 약 150 pM 내지 약 10 nM, 약 150 pM 내지 약 5 nM, 약 150 pM 내지 약 2 nM, 약 150 pM 내지 약 1 nM, 약 150 pM 내지 약 950 pM, 약 150 pM 내지 약 900 pM, 약 150 pM 내지 약 850 pM, 약 150 pM 내지 약 800 pM, 약 150 pM 내지 약 750 pM, 약 150 pM 내지 약 700 pM, 약 150 pM 내지 약 650 pM, 약 150 pM 내지 약 600 pM, 약 150 pM 내지 약 550 pM, 약 150 pM 내지 약 500 pM, 약 150 pM 내지 약 450 pM, 약 150 pM 내지 약 400 pM, 약 150 pM 내지 약 350 pM, 약 150 pM 내지 약 300 pM, 약 150 pM 내지 약 250 pM, 약 150 pM 내지 약 200 pM, 약 200 pM 내지 약 5 μM, 약 200 pM 내지 약 2 μM, 약 200 pM 내지 약 1 μM, 약 200 pM 내지 약 500 nM, 약 200 pM 내지 약 250 nM, 약 200 pM 내지 약 240 nM, 약 200 pM 내지 약 230 nM, 약 200 pM 내지 약 220 nM, 약 200 pM 내지 약 210 nM, 약 200 pM 내지 약 200 nM, 약 200 pM 내지 약 190 nM, 약 200 pM 내지 약 180 nM, 약 200 pM 내지 약 170 nM, 약 200 pM 내지 약 160 nM, 약 200 pM 내지 약 150 nM, 약 200 pM 내지 약 140 nM, 약 200 pM 내지 약 130 nM, 약 200 pM 내지 약 120 nM, 약 200 pM 내지 약 110 nM, 약 200 pM 내지 약 100 nM, 약 200 pM 내지 약 95 nM, 약 200 pM 내지 약 90 nM, 약 200 pM 내지 약 85 nM, 약 200 pM 내지 약 80 nM, 약 200 pM 내지 약 75 nM, 약 200 pM 내지 약 70 nM, 약 200 pM 내지 약 65 nM, 약 200 pM 내지 약 60 nM, 약 200 pM 내지 약 55 nM, 약 200 pM 내지 약 50 nM, 약 200 pM 내지 약 45 nM, 약 200 pM 내지 약 40 nM, 약 200 pM 내지 약 35 nM, 약 200 pM 내지 약 30 nM, 약 200 pM 내지 약 25 nM, 약 200 pM 내지 약 30 nM, 약 200 pM 내지 약 15 nM, 약 200 pM 내지 약 10 nM, 약 200 pM 내지 약 5 nM, 약 200 pM 내지 약 2 nM, 약 200 pM 내지 약 1 nM, 약 200 pM 내지 약 950 pM, 약 200 pM 내지 약 900 pM, 약 200 pM 내지 약 850 pM, 약 200 pM 내지 약 800 pM, 약 200 pM 내지 약 750 pM, 약 200 pM 내지 약 700 pM, 약 200 pM 내지 약 650 pM, 약 200 pM 내지 약 600 pM, 약 200 pM 내지 약 550 pM, 약 200 pM 내지 약 500 pM, 약 200 pM 내지 약 450 pM, 약 200 pM 내지 약 400 pM, 약 200 pM 내지 약 350 pM, 약 200 pM 내지 약 300 pM, 약 200 pM 내지 약 250 pM, 약 300 pM 내지 약 30 nM, 약 300 pM 내지 약 25 nM, 약 300 pM 내지 약 5 μM, 약 300 pM 내지 약 2 μM, 약 300 pM 내지 약 1 μM, 약 300 pM 내지 약 500 nM, 약 300 pM 내지 약 250 nM, 약 300 pM 내지 약 240 nM, 약 300 pM 내지 약 230 nM, 약 300 pM 내지 약 220 nM, 약 300 pM 내지 약 210 nM, 약 300 pM 내지 약 200 nM, 약 300 pM 내지 약 190 nM, 약 300 pM 내지 약 180 nM, 약 300 pM 내지 약 170 nM, 약 300 pM 내지 약 160 nM, 약 300 pM 내지 약 150 nM, 약 300 pM 내지 약 140 nM, 약 300 pM 내지 약 130 nM, 약 300 pM 내지 약 120 nM, 약 300 pM 내지 약 110 nM, 약 300 pM 내지 약 100 nM, 약 300 pM 내지 약 95 nM, 약 300 pM 내지 약 90 nM, 약 300 pM 내지 약 85 nM, 약 300 pM 내지 약 80 nM, 약 300 pM 내지 약 75 nM, 약 300 pM 내지 약 70 nM, 약 300 pM 내지 약 65 nM, 약 300 pM 내지 약 60 nM, 약 300 pM 내지 약 55 nM, 약 300 pM 내지 약 50 nM, 약 300 pM 내지 약 45 nM, 약 300 pM 내지 약 40 nM, 약 300 pM 내지 약 35 nM, 약 300 pM 내지 약 30 nM, 약 300 pM 내지 약 15 nM, 약 300 pM 내지 약 10 nM, 약 300 pM 내지 약 5 nM, 약 300 pM 내지 약 2 nM, 약 300 pM 내지 약 1 nM, 약 300 pM 내지 약 950 pM, 약 300 pM 내지 약 900 pM, 약 300 pM 내지 약 850 pM, 약 300 pM 내지 약 800 pM, 약 300 pM 내지 약 750 pM, 약 300 pM 내지 약 700 pM, 약 300 pM 내지 약 650 pM, 약 300 pM 내지 약 600 pM, 약 300 pM 내지 약 550 pM, 약 300 pM 내지 약 500 pM, 약 300 pM 내지 약 450 pM, 약 300 pM 내지 약 400 pM, 약 300 pM 내지 약 350 pM, 약 400 pM 내지 약 5 μM, 약 400 pM 내지 약 2 μM, 약 400 pM 내지 약 1 μM, 약 400 pM 내지 약 500 nM, 약 400 pM 내지 약 250 nM, 약 400 pM 내지 약 240 nM, 약 400 pM 내지 약 230 nM, 약 400 pM 내지 약 220 nM, 약 400 pM 내지 약 210 nM, 약 400 pM 내지 약 200 nM, 약 400 pM 내지 약 190 nM, 약 400 pM 내지 약 180 nM, 약 400 pM 내지 약 170 nM, 약 400 pM 내지 약 160 nM, 약 400 pM 내지 약 150 nM, 약 400 pM 내지 약 140 nM, 약 400 pM 내지 약 130 nM, 약 400 pM 내지 약 120 nM, 약 400 pM 내지 약 110 nM, 약 400 pM 내지 약 100 nM, 약 400 pM 내지 약 95 nM, 약 400 pM 내지 약 90 nM, 약 400 pM 내지 약 85 nM, 약 400 pM 내지 약 80 nM, 약 400 pM 내지 약 75 nM, 약 400 pM 내지 약 70 nM, 약 400 pM 내지 약 65 nM, 약 400 pM 내지 약 60 nM, 약 400 pM 내지 약 55 nM, 약 400 pM 내지 약 50 nM, 약 400 pM 내지 약 45 nM, 약 400 pM 내지 약 40 nM, 약 400 pM 내지 약 35 nM, 약 400 pM 내지 약 30 nM, 약 400 pM 내지 약 25 nM, 약 400 pM 내지 약 20 nM, 약 400 pM 내지 약 15 nM, 약 400 pM 내지 약 10 nM, 약 400 pM 내지 약 5 nM, 약 400 pM 내지 약 2 nM, 약 400 pM 내지 약 1 nM, 약 400 pM 내지 약 950 pM, 약 400 pM 내지 약 900 pM, 약 400 pM 내지 약 850 pM, 약 400 pM 내지 약 800 pM, 약 400 pM 내지 약 750 pM, 약 400 pM 내지 약 700 pM, 약 400 pM 내지 약 650 pM, 약 400 pM 내지 약 600 pM, 약 400 pM 내지 약 550 pM, 약 400 pM 내지 약 500 pM, 약 500 pM 내지 약 5 μM, 약 500 pM 내지 약 2 μM, 약 500 pM 내지 약 1 μM, 약 500 pM 내지 약 500 nM, 약 500 pM 내지 약 250 nM, 약 500 pM 내지 약 240 nM, 약 500 pM 내지 약 230 nM, 약 500 pM 내지 약 220 nM, 약 500 pM 내지 약 210 nM, 약 500 pM 내지 약 200 nM, 약 500 pM 내지 약 190 nM, 약 500 pM 내지 약 180 nM, 약 500 pM 내지 약 170 nM, 약 500 pM 내지 약 160 nM, 약 500 pM 내지 약 150 nM, 약 500 pM 내지 약 140 nM, 약 500 pM 내지 약 130 nM, 약 500 pM 내지 약 120 nM, 약 500 pM 내지 약 110 nM, 약 500 pM 내지 약 100 nM, 약 500 pM 내지 약 95 nM, 약 500 pM 내지 약 90 nM, 약 500 pM 내지 약 85 nM, 약 500 pM 내지 약 80 nM, 약 500 pM 내지 약 75 nM, 약 500 pM 내지 약 70 nM, 약 500 pM 내지 약 65 nM, 약 500 pM 내지 약 60 nM, 약 500 pM 내지 약 55 nM, 약 500 pM 내지 약 50 nM, 약 500 pM 내지 약 45 nM, 약 500 pM 내지 약 40 nM, 약 500 pM 내지 약 35 nM, 약 500 pM 내지 약 30 nM, 약 500 pM 내지 약 25 nM, 약 500 pM 내지 약 20 nM, 약 500 pM 내지 약 15 nM, 약 500 pM 내지 약 10 nM, 약 500 pM 내지 약 5 nM, 약 500 pM 내지 약 2 nM, 약 500 pM 내지 약 1 nM, 약 500 pM 내지 약 950 pM, 약 500 pM 내지 약 900 pM, 약 500 pM 내지 약 850 pM, 약 500 pM 내지 약 800 pM, 약 500 pM 내지 약 750 pM, 약 500 pM 내지 약 700 pM, 약 500 pM 내지 약 650 pM, 약 500 pM 내지 약 600 pM, 약 500 pM 내지 약 550 pM, 약 600 pM 내지 약 5 μM, 약 600 pM 내지 약 2 μM, 약 600 pM 내지 약 1 μM, 약 600 pM 내지 약 500 nM, 약 600 pM 내지 약 250 nM, 약 600 pM 내지 약 240 nM, 약 600 pM 내지 약 230 nM, 약 600 pM 내지 약 220 nM, 약 600 pM 내지 약 210 nM, 약 600 pM 내지 약 200 nM, 약 600 pM 내지 약 190 nM, 약 600 pM 내지 약 180 nM, 약 600 pM 내지 약 170 nM, 약 600 pM 내지 약 160 nM, 약 600 pM 내지 약 150 nM, 약 600 pM 내지 약 140 nM, 약 600 pM 내지 약 130 nM, 약 600 pM 내지 약 120 nM, 약 600 pM 내지 약 110 nM, 약 600 pM 내지 약 100 nM, 약 600 pM 내지 약 95 nM, 약 600 pM 내지 약 90 nM, 약 600 pM 내지 약 85 nM, 약 600 pM 내지 약 80 nM, 약 600 pM 내지 약 75 nM, 약 600 pM 내지 약 70 nM, 약 600 pM 내지 약 65 nM, 약 600 pM 내지 약 60 nM, 약 600 pM 내지 약 55 nM, 약 600 pM 내지 약 50 nM, 약 600 pM 내지 약 45 nM, 약 600 pM 내지 약 40 nM, 약 600 pM 내지 약 35 nM, 약 600 pM 내지 약 30 nM, 약 600 pM 내지 약 25 nM, 약 600 pM 내지 약 20 nM, 약 600 pM 내지 약 15 nM, 약 600 pM 내지 약 10 nM, 약 600 pM 내지 약 5 nM, 약 600 pM 내지 약 2 nM, 약 600 pM 내지 약 1 nM, 약 600 pM 내지 약 950 pM, 약 600 pM 내지 약 900 pM, 약 600 pM 내지 약 850 pM, 약 600 pM 내지 약 800 pM, 약 600 pM 내지 약 750 pM, 약 600 pM 내지 약 700 pM, 약 600 pM 내지 약 650 pM, 약 700 pM 내지 약 5 μM, 약 700 pM 내지 약 2 μM, 약 700 pM 내지 약 1 μM, 약 700 pM 내지 약 500 nM, 약 700 pM 내지 약 250 nM, 약 700 pM 내지 약 240 nM, 약 700 pM 내지 약 230 nM, 약 700 pM 내지 약 220 nM, 약 700 pM 내지 약 210 nM, 약 700 pM 내지 약 200 nM, 약 700 pM 내지 약 190 nM, 약 700 pM 내지 약 180 nM, 약 700 pM 내지 약 170 nM, 약 700 pM 내지 약 160 nM, 약 700 pM 내지 약 150 nM, 약 700 pM 내지 약 140 nM, 약 700 pM 내지 약 130 nM, 약 700 pM 내지 약 120 nM, 약 700 pM 내지 약 110 nM, 약 700 pM 내지 약 100 nM, 약 700 pM 내지 약 95 nM, 약 700 pM 내지 약 90 nM, 약 700 pM 내지 약 85 nM, 약 700 pM 내지 약 80 nM, 약 700 pM 내지 약 75 nM, 약 700 pM 내지 약 70 nM, 약 700 pM 내지 약 65 nM, 약 700 pM 내지 약 60 nM, 약 700 pM 내지 약 55 nM, 약 700 pM 내지 약 50 nM, 약 700 pM 내지 약 45 nM, 약 700 pM 내지 약 40 nM, 약 700 pM 내지 약 35 nM, 약 700 pM 내지 약 30 nM, 약 700 pM 내지 약 25 nM, 약 700 pM 내지 약 20 nM, 약 700 pM 내지 약 15 nM, 약 700 pM 내지 약 10 nM, 약 700 pM 내지 약 5 nM, 약 700 pM 내지 약 2 nM, 약 700 pM 내지 약 1 nM, 약 700 pM 내지 약 950 pM, 약 700 pM 내지 약 900 pM, 약 700 pM 내지 약 850 pM, 약 700 pM 내지 약 800 pM, 약 700 pM 내지 약 750 pM, 약 800 pM 내지 약 5 μM, 약 800 pM 내지 약 2 μM, 약 800 pM 내지 약 1 μM, 약 800 pM 내지 약 500 nM, 약 800 pM 내지 약 250 nM, 약 800 pM 내지 약 240 nM, 약 800 pM 내지 약 230 nM, 약 800 pM 내지 약 220 nM, 약 800 pM 내지 약 210 nM, 약 800 pM 내지 약 200 nM, 약 800 pM 내지 약 190 nM, 약 800 pM 내지 약 180 nM, 약 800 pM 내지 약 170 nM, 약 800 pM 내지 약 160 nM, 약 800 pM 내지 약 150 nM, 약 800 pM 내지 약 140 nM, 약 800 pM 내지 약 130 nM, 약 800 pM 내지 약 120 nM, 약 800 pM 내지 약 110 nM, 약 800 pM 내지 약 100 nM, 약 800 pM 내지 약 95 nM, 약 800 pM 내지 약 90 nM, 약 800 pM 내지 약 85 nM, 약 800 pM 내지 약 80 nM, 약 800 pM 내지 약 75 nM, 약 800 pM 내지 약 70 nM, 약 800 pM 내지 약 65 nM, 약 800 pM 내지 약 60 nM, 약 800 pM 내지 약 55 nM, 약 800 pM 내지 약 50 nM, 약 800 pM 내지 약 45 nM, 약 800 pM 내지 약 40 nM, 약 800 pM 내지 약 35 nM, 약 800 pM 내지 약 30 nM, 약 800 pM 내지 약 25 nM, 약 800 pM 내지 약 20 nM, 약 800 pM 내지 약 15 nM, 약 800 pM 내지 약 10 nM, 약 800 pM 내지 약 5 nM, 약 800 pM 내지 약 2 nM, 약 800 pM 내지 약 1 nM, 약 800 pM 내지 약 950 pM, 약 800 pM 내지 약 900 pM, 약 800 pM 내지 약 850 pM, 약 900 pM 내지 약 5 μM, 약 900 pM 내지 약 2 μM, 약 900 pM 내지 약 1 μM, 약 900 pM 내지 약 500 nM, 약 900 pM 내지 약 250 nM, 약 900 pM 내지 약 240 nM, 약 900 pM 내지 약 230 nM, 약 900 pM 내지 약 220 nM, 약 900 pM 내지 약 210 nM, 약 900 pM 내지 약 200 nM, 약 900 pM 내지 약 190 nM, 약 900 pM 내지 약 180 nM, 약 900 pM 내지 약 170 nM, 약 900 pM 내지 약 160 nM, 약 900 pM 내지 약 150 nM, 약 900 pM 내지 약 140 nM, 약 900 pM 내지 약 130 nM, 약 900 pM 내지 약 120 nM, 약 900 pM 내지 약 110 nM, 약 900 pM 내지 약 100 nM, 약 900 pM 내지 약 95 nM, 약 900 pM 내지 약 90 nM, 약 900 pM 내지 약 85 nM, 약 900 pM 내지 약 80 nM, 약 900 pM 내지 약 75 nM, 약 900 pM 내지 약 70 nM, 약 900 pM 내지 약 65 nM, 약 900 pM 내지 약 60 nM, 약 900 pM 내지 약 55 nM, 약 900 pM 내지 약 50 nM, 약 900 pM 내지 약 45 nM, 약 900 pM 내지 약 40 nM, 약 900 pM 내지 약 35 nM, 약 900 pM 내지 약 30 nM, 약 900 pM 내지 약 25 nM, 약 900 pM 내지 약 20 nM, 약 900 pM 내지 약 15 nM, 약 900 pM 내지 약 10 nM, 약 900 pM 내지 약 5 nM, 약 900 pM 내지 약 2 nM, 약 900 pM 내지 약 1 nM, 약 900 pM 내지 약 950 pM, 약 1 nM 내지 약 5 μM, 약 1 nM 내지 약 2 μM, 약 1 nM 내지 약 1 μM, 약 1 nM 내지 약 500 nM, 약 1 nM 내지 약 250 nM, 약 1 nM 내지 약 240 nM, 약 1 nM 내지 약 230 nM, 약 1 nM 내지 약 220 nM, 약 1 nM 내지 약 210 nM, 약 1 nM 내지 약 200 nM, 약 1 nM 내지 약 190 nM, 약 1 nM 내지 약 180 nM, 약 1 nM 내지 약 170 nM, 약 1 nM 내지 약 160 nM, 약 1 nM 내지 약 150 nM, 약 1 nM 내지 약 140 nM, 약 1 nM 내지 약 130 nM, 약 1 nM 내지 약 120 nM, 약 1 nM 내지 약 110 nM, 약 1 nM 내지 약 100 nM, 약 1 nM 내지 약 95 nM, 약 1 nM 내지 약 90 nM, 약 1 nM 내지 약 85 nM, 약 1 nM 내지 약 80 nM, 약 1 nM 내지 약 75 nM, 약 1 nM 내지 약 70 nM, 약 1 nM 내지 약 65 nM, 약 1 nM 내지 약 60 nM, 약 1 nM 내지 약 55 nM, 약 1 nM 내지 약 50 nM, 약 1 nM 내지 약 45 nM, 약 1 nM 내지 약 40 nM, 약 1 nM 내지 약 35 nM, 약 1 nM 내지 약 30 nM, 약 1 nM 내지 약 25 nM, 약 1 nM 내지 약 20 nM, 약 1 nM 내지 약 15 nM, 약 1 nM 내지 약 10 nM, 약 1 nM 내지 약 5 nM, 약 2 nM 내지 약 5 μM, 약 2 nM 내지 약 2 μM, 약 2 nM 내지 약 1 μM, 약 2 nM 내지 약 500 nM, 약 2 nM 내지 약 250 nM, 약 2 nM 내지 약 240 nM, 약 2 nM 내지 약 230 nM, 약 2 nM 내지 약 220 nM, 약 2 nM 내지 약 210 nM, 약 2 nM 내지 약 200 nM, 약 2 nM 내지 약 190 nM, 약 2 nM 내지 약 180 nM, 약 2 nM 내지 약 170 nM, 약 2 nM 내지 약 160 nM, 약 2 nM 내지 약 150 nM, 약 2 nM 내지 약 140 nM, 약 2 nM 내지 약 130 nM, 약 2 nM 내지 약 120 nM, 약 2 nM 내지 약 110 nM, 약 2 nM 내지 약 100 nM, 약 2 nM 내지 약 95 nM, 약 2 nM 내지 약 90 nM, 약 2 nM 내지 약 85 nM, 약 2 nM 내지 약 80 nM, 약 2 nM 내지 약 75 nM, 약 2 nM 내지 약 70 nM, 약 2 nM 내지 약 65 nM, 약 2 nM 내지 약 60 nM, 약 2 nM 내지 약 55 nM, 약 2 nM 내지 약 50 nM, 약 2 nM 내지 약 45 nM, 약 2 nM 내지 약 40 nM, 약 2 nM 내지 약 35 nM, 약 2 nM 내지 약 30 nM, 약 2 nM 내지 약 25 nM, 약 2 nM 내지 약 20 nM, 약 2 nM 내지 약 15 nM, 약 2 nM 내지 약 10 nM, 약 2 nM 내지 약 5 nM, 약 4 nM 내지 약 5 μM, 약 4 nM 내지 약 2 μM, 약 4 nM 내지 약 1 μM, 약 4 nM 내지 약 500 nM, 약 4 nM 내지 약 250 nM, 약 4 nM 내지 약 240 nM, 약 4 nM 내지 약 230 nM, 약 4 nM 내지 약 220 nM, 약 4 nM 내지 약 210 nM, 약 4 nM 내지 약 200 nM, 약 4 nM 내지 약 190 nM, 약 4 nM 내지 약 180 nM, 약 4 nM 내지 약 170 nM, 약 4 nM 내지 약 160 nM, 약 4 nM 내지 약 150 nM, 약 4 nM 내지 약 140 nM, 약 4 nM 내지 약 130 nM, 약 4 nM 내지 약 120 nM, 약 4 nM 내지 약 110 nM, 약 4 nM 내지 약 100 nM, 약 4 nM 내지 약 95 nM, 약 4 nM 내지 약 90 nM, 약 4 nM 내지 약 85 nM, 약 4 nM 내지 약 80 nM, 약 4 nM 내지 약 75 nM, 약 4 nM 내지 약 70 nM, 약 4 nM 내지 약 65 nM, 약 4 nM 내지 약 60 nM, 약 4 nM 내지 약 55 nM, 약 4 nM 내지 약 50 nM, 약 4 nM 내지 약 45 nM, 약 4 nM 내지 약 40 nM, 약 4 nM 내지 약 35 nM, 약 4 nM 내지 약 30 nM, 약 4 nM 내지 약 25 nM, 약 4 nM 내지 약 20 nM, 약 4 nM 내지 약 15 nM, 약 4 nM 내지 약 10 nM, 약 4 nM 내지 약 5 nM, 약 5 nM 내지 약 5 μM, 약 5 nM 내지 약 2 μM, 약 5 nM 내지 약 1 μM, 약 5 nM 내지 약 500 nM, 약 5 nM 내지 약 250 nM, 약 5 nM 내지 약 240 nM, 약 5 nM 내지 약 230 nM, 약 5 nM 내지 약 220 nM, 약 5 nM 내지 약 210 nM, 약 5 nM 내지 약 200 nM, 약 5 nM 내지 약 190 nM, 약 5 nM 내지 약 180 nM, 약 5 nM 내지 약 170 nM, 약 5 nM 내지 약 160 nM, 약 5 nM 내지 약 150 nM, 약 5 nM 내지 약 140 nM, 약 5 nM 내지 약 130 nM, 약 5 nM 내지 약 120 nM, 약 5 nM 내지 약 110 nM, 약 5 nM 내지 약 100 nM, 약 5 nM 내지 약 95 nM, 약 5 nM 내지 약 90 nM, 약 5 nM 내지 약 85 nM, 약 5 nM 내지 약 80 nM, 약 5 nM 내지 약 75 nM, 약 5 nM 내지 약 70 nM, 약 5 nM 내지 약 65 nM, 약 5 nM 내지 약 60 nM, 약 5 nM 내지 약 55 nM, 약 5 nM 내지 약 50 nM, 약 5 nM 내지 약 45 nM, 약 5 nM 내지 약 40 nM, 약 5 nM 내지 약 35 nM, 약 5 nM 내지 약 30 nM, 약 5 nM 내지 약 25 nM, 약 5 nM 내지 약 20 nM, 약 5 nM 내지 약 15 nM, 약 5 nM 내지 약 10 nM, 약 10 nM 내지 약 5 μM, 약 10 nM 내지 약 2 μM, 약 10 nM 내지 약 1 μM, 약 10 nM 내지 약 500 nM, 약 10 nM 내지 약 250 nM, 약 10 nM 내지 약 240 nM, 약 10 nM 내지 약 230 nM, 약 10 nM 내지 약 220 nM, 약 10 nM 내지 약 210 nM, 약 10 nM 내지 약 200 nM, 약 10 nM 내지 약 190 nM, 약 10 nM 내지 약 180 nM, 약 10 nM 내지 약 170 nM, 약 10 nM 내지 약 160 nM, 약 10 nM 내지 약 150 nM, 약 10 nM 내지 약 140 nM, 약 10 nM 내지 약 130 nM, 약 10 nM 내지 약 120 nM, 약 10 nM 내지 약 110 nM, 약 10 nM 내지 약 100 nM, 약 10 nM 내지 약 95 nM, 약 10 nM 내지 약 90 nM, 약 10 nM 내지 약 85 nM, 약 10 nM 내지 약 80 nM, 약 10 nM 내지 약 75 nM, 약 10 nM 내지 약 70 nM, 약 10 nM 내지 약 65 nM, 약 10 nM 내지 약 60 nM, 약 10 nM 내지 약 55 nM, 약 10 nM 내지 약 50 nM, 약 10 nM 내지 약 45 nM, 약 10 nM 내지 약 40 nM, 약 10 nM 내지 약 35 nM, 약 10 nM 내지 약 30 nM, 약 10 nM 내지 약 25 nM, 약 10 nM 내지 약 20 nM, 약 10 nM 내지 약 15 nM, 약 15 nM 내지 약 5 μM, 약 15 nM 내지 약 2 μM, 약 15 nM 내지 약 1 μM, 약 15 nM 내지 약 500 nM, 약 15 nM 내지 약 250 nM, 약 15 nM 내지 약 240 nM, 약 15 nM 내지 약 230 nM, 약 15 nM 내지 약 220 nM, 약 15 nM 내지 약 210 nM, 약 15 nM 내지 약 200 nM, 약 15 nM 내지 약 190 nM, 약 15 nM 내지 약 180 nM, 약 15 nM 내지 약 170 nM, 약 15 nM 내지 약 160 nM, 약 15 nM 내지 약 150 nM, 약 15 nM 내지 약 140 nM, 약 15 nM 내지 약 130 nM, 약 15 nM 내지 약 120 nM, 약 15 nM 내지 약 110 nM, 약 15 nM 내지 약 100 nM, 약 15 nM 내지 약 95 nM, 약 15 nM 내지 약 90 nM, 약 15 nM 내지 약 85 nM, 약 15 nM 내지 약 80 nM, 약 15 nM 내지 약 75 nM, 약 15 nM 내지 약 70 nM, 약 15 nM 내지 약 65 nM, 약 15 nM 내지 약 60 nM, 약 15 nM 내지 약 55 nM, 약 15 nM 내지 약 50 nM, 약 15 nM 내지 약 45 nM, 약 15 nM 내지 약 40 nM, 약 15 nM 내지 약 35 nM, 약 15 nM 내지 약 30 nM, 약 15 nM 내지 약 25 nM, 약 15 nM 내지 약 20 nM, 약 20 nM 내지 약 5 μM, 약 20 nM 내지 약 2 μM, 약 20 nM 내지 약 1 μM, 약 20 nM 내지 약 500 nM, 약 20 nM 내지 약 250 nM, 약 20 nM 내지 약 240 nM, 약 20 nM 내지 약 230 nM, 약 20 nM 내지 약 220 nM, 약 20 nM 내지 약 210 nM, 약 20 nM 내지 약 200 nM, 약 20 nM 내지 약 190 nM, 약 20 nM 내지 약 180 nM, 약 20 nM 내지 약 170 nM, 약 20 nM 내지 약 160 nM, 약 20 nM 내지 약 150 nM, 약 20 nM 내지 약 140 nM, 약 20 nM 내지 약 130 nM, 약 20 nM 내지 약 120 nM, 약 20 nM 내지 약 110 nM, 약 20 nM 내지 약 100 nM, 약 20 nM 내지 약 95 nM, 약 20 nM 내지 약 90 nM, 약 20 nM 내지 약 85 nM, 약 20 nM 내지 약 80 nM, 약 20 nM 내지 약 75 nM, 약 20 nM 내지 약 70 nM, 약 20 nM 내지 약 65 nM, 약 20 nM 내지 약 60 nM, 약 20 nM 내지 약 55 nM, 약 20 nM 내지 약 50 nM, 약 20 nM 내지 약 45 nM, 약 20 nM 내지 약 40 nM, 약 20 nM 내지 약 35 nM, 약 20 nM 내지 약 30 nM, 약 20 nM 내지 약 25 nM, 약 25 nM 내지 약 5 μM, 약 25 nM 내지 약 2 μM, 약 25 nM 내지 약 1 μM, 약 25 nM 내지 약 500 nM, 약 25 nM 내지 약 250 nM, 약 25 nM 내지 약 240 nM, 약 25 nM 내지 약 230 nM, 약 25 nM 내지 약 220 nM, 약 25 nM 내지 약 210 nM, 약 25 nM 내지 약 200 nM, 약 25 nM 내지 약 190 nM, 약 25 nM 내지 약 180 nM, 약 25 nM 내지 약 170 nM, 약 25 nM 내지 약 160 nM, 약 25 nM 내지 약 150 nM, 약 25 nM 내지 약 140 nM, 약 25 nM 내지 약 130 nM, 약 25 nM 내지 약 120 nM, 약 25 nM 내지 약 110 nM, 약 25 nM 내지 약 100 nM, 약 25 nM 내지 약 95 nM, 약 25 nM 내지 약 90 nM, 약 25 nM 내지 약 85 nM, 약 25 nM 내지 약 80 nM, 약 25 nM 내지 약 75 nM, 약 25 nM 내지 약 70 nM, 약 25 nM 내지 약 65 nM, 약 25 nM 내지 약 60 nM, 약 25 nM 내지 약 55 nM, 약 25 nM 내지 약 50 nM, 약 25 nM 내지 약 45 nM, 약 25 nM 내지 약 40 nM, 약 25 nM 내지 약 35 nM, 약 25 nM 내지 약 30 nM, 약 30 nM 내지 약 5 μM, 약 30 nM 내지 약 2 μM, 약 30 nM 내지 약 1 μM, 약 30 nM 내지 약 500 nM, 약 30 nM 내지 약 250 nM, 약 30 nM 내지 약 240 nM, 약 30 nM 내지 약 230 nM, 약 30 nM 내지 약 220 nM, 약 30 nM 내지 약 210 nM, 약 30 nM 내지 약 200 nM, 약 30 nM 내지 약 190 nM, 약 30 nM 내지 약 180 nM, 약 30 nM 내지 약 170 nM, 약 30 nM 내지 약 160 nM, 약 30 nM 내지 약 150 nM, 약 30 nM 내지 약 140 nM, 약 30 nM 내지 약 130 nM, 약 30 nM 내지 약 120 nM, 약 30 nM 내지 약 110 nM, 약 30 nM 내지 약 100 nM, 약 30 nM 내지 약 95 nM, 약 30 nM 내지 약 90 nM, 약 30 nM 내지 약 85 nM, 약 30 nM 내지 약 80 nM, 약 30 nM 내지 약 75 nM, 약 30 nM 내지 약 70 nM, 약 30 nM 내지 약 65 nM, 약 30 nM 내지 약 60 nM, 약 30 nM 내지 약 55 nM, 약 30 nM 내지 약 50 nM, 약 30 nM 내지 약 45 nM, 약 30 nM 내지 약 40 nM, 약 30 nM 내지 약 35 nM, 약 40 nM 내지 약 5 μM, 약 40 nM 내지 약 2 μM, 약 40 nM 내지 약 1 μM, 약 40 nM 내지 약 500 nM, 약 40 nM 내지 약 250 nM, 약 40 nM 내지 약 240 nM, 약 40 nM 내지 약 230 nM, 약 40 nM 내지 약 220 nM, 약 40 nM 내지 약 210 nM, 약 40 nM 내지 약 200 nM, 약 40 nM 내지 약 190 nM, 약 40 nM 내지 약 180 nM, 약 40 nM 내지 약 170 nM, 약 40 nM 내지 약 160 nM, 약 40 nM 내지 약 150 nM, 약 40 nM 내지 약 140 nM, 약 40 nM 내지 약 130 nM, 약 40 nM 내지 약 120 nM, 약 40 nM 내지 약 110 nM, 약 40 nM 내지 약 100 nM, 약 40 nM 내지 약 95 nM, 약 40 nM 내지 약 90 nM, 약 40 nM 내지 약 85 nM, 약 40 nM 내지 약 80 nM, 약 40 nM 내지 약 75 nM, 약 40 nM 내지 약 70 nM, 약 40 nM 내지 약 65 nM, 약 40 nM 내지 약 60 nM, 약 40 nM 내지 약 55 nM, 약 40 nM 내지 약 50 nM, 약 40 nM 내지 약 45 nM, 약 50 nM 내지 약 5 μM, 약 50 nM 내지 약 2 μM, 약 50 nM 내지 약 1 μM, 약 50 nM 내지 약 500 nM, 약 50 nM 내지 약 250 nM, 약 50 nM 내지 약 240 nM, 약 50 nM 내지 약 230 nM, 약 50 nM 내지 약 220 nM, 약 50 nM 내지 약 210 nM, 약 50 nM 내지 약 200 nM, 약 50 nM 내지 약 190 nM, 약 50 nM 내지 약 180 nM, 약 50 nM 내지 약 170 nM, 약 50 nM 내지 약 160 nM, 약 50 nM 내지 약 150 nM, 약 50 nM 내지 약 140 nM, 약 50 nM 내지 약 130 nM, 약 50 nM 내지 약 120 nM, 약 50 nM 내지 약 110 nM, 약 50 nM 내지 약 100 nM, 약 50 nM 내지 약 95 nM, 약 50 nM 내지 약 90 nM, 약 50 nM 내지 약 85 nM, 약 50 nM 내지 약 80 nM, 약 50 nM 내지 약 75 nM, 약 50 nM 내지 약 70 nM, 약 50 nM 내지 약 65 nM, 약 50 nM 내지 약 60 nM, 약 50 nM 내지 약 55 nM, 약 60 nM 내지 약 5 μM, 약 60 nM 내지 약 2 μM, 약 60 nM 내지 약 1 μM, 약 60 nM 내지 약 500 nM, 약 60 nM 내지 약 250 nM, 약 60 nM 내지 약 240 nM, 약 60 nM 내지 약 230 nM, 약 60 nM 내지 약 220 nM, 약 60 nM 내지 약 210 nM, 약 60 nM 내지 약 200 nM, 약 60 nM 내지 약 190 nM, 약 60 nM 내지 약 180 nM, 약 60 nM 내지 약 170 nM, 약 60 nM 내지 약 160 nM, 약 60 nM 내지 약 150 nM, 약 60 nM 내지 약 140 nM, 약 60 nM 내지 약 130 nM, 약 60 nM 내지 약 120 nM, 약 60 nM 내지 약 110 nM, 약 60 nM 내지 약 100 nM, 약 60 nM 내지 약 95 nM, 약 60 nM 내지 약 90 nM, 약 60 nM 내지 약 85 nM, 약 60 nM 내지 약 80 nM, 약 60 nM 내지 약 75 nM, 약 60 nM 내지 약 70 nM, 약 60 nM 내지 약 65 nM, 약 70 nM 내지 약 5 μM, 약 70 nM 내지 약 2 μM, 약 70 nM 내지 약 1 μM, 약 70 nM 내지 약 500 nM, 약 70 nM 내지 약 250 nM, 약 70 nM 내지 약 240 nM, 약 70 nM 내지 약 230 nM, 약 70 nM 내지 약 220 nM, 약 70 nM 내지 약 210 nM, 약 70 nM 내지 약 200 nM, 약 70 nM 내지 약 190 nM, 약 70 nM 내지 약 180 nM, 약 70 nM 내지 약 170 nM, 약 70 nM 내지 약 160 nM, 약 70 nM 내지 약 150 nM, 약 70 nM 내지 약 140 nM, 약 70 nM 내지 약 130 nM, 약 70 nM 내지 약 120 nM, 약 70 nM 내지 약 110 nM, 약 70 nM 내지 약 100 nM, 약 70 nM 내지 약 95 nM, 약 70 nM 내지 약 90 nM, 약 70 nM 내지 약 85 nM, 약 70 nM 내지 약 80 nM, 약 70 nM 내지 약 75 nM, 약 80 nM 내지 약 5 μM, 약 80 nM 내지 약 2 μM, 약 80 nM 내지 약 1 μM, 약 80 nM 내지 약 500 nM, 약 80 nM 내지 약 250 nM, 약 80 nM 내지 약 240 nM, 약 80 nM 내지 약 230 nM, 약 80 nM 내지 약 220 nM, 약 80 nM 내지 약 210 nM, 약 80 nM 내지 약 200 nM, 약 80 nM 내지 약 190 nM, 약 80 nM 내지 약 180 nM, 약 80 nM 내지 약 170 nM, 약 80 nM 내지 약 160 nM, 약 80 nM 내지 약 150 nM, 약 80 nM 내지 약 140 nM, 약 80 nM 내지 약 130 nM, 약 80 nM 내지 약 120 nM, 약 80 nM 내지 약 110 nM, 약 80 nM 내지 약 100 nM, 약 80 nM 내지 약 95 nM, 약 80 nM 내지 약 90 nM, 약 80 nM 내지 약 85 nM, 약 90 nM 내지 약 5 μM, 약 90 nM 내지 약 2 μM, 약 90 mM 내지 약 1 μM, 약 90 nM 내지 약 500 nM, 약 90 nM 내지 약 250 nM, 약 90 nM 내지 약 240 nM, 약 90 nM 내지 약 230 nM, 약 90 nM 내지 약 220 nM, 약 90 nM 내지 약 210 nM, 약 90 nM 내지 약 200 nM, 약 90 nM 내지 약 190 nM, 약 90 nM 내지 약 180 nM, 약 90 nM 내지 약 170 nM, 약 90 nM 내지 약 160 nM, 약 90 nM 내지 약 150 nM, 약 90 nM 내지 약 140 nM, 약 90 nM 내지 약 130 nM, 약 90 nM 내지 약 120 nM, 약 90 nM 내지 약 110 nM, 약 90 nM 내지 약 100 nM, 약 90 nM 내지 약 95 nM, 약 100 nM 내지 약 5 μM, 약 100 nM 내지 약 2 μM, 약 100 nM 내지 약 1 μM, 약 100 nM 내지 약 500 nM, 약 100 nM 내지 약 250 nM, 약 100 nM 내지 약 240 nM, 약 100 nM 내지 약 230 nM, 약 100 nM 내지 약 220 nM, 약 100 nM 내지 약 210 nM, 약 100 nM 내지 약 200 nM, 약 100 nM 내지 약 190 nM, 약 100 nM 내지 약 180 nM, 약 100 nM 내지 약 170 nM, 약 100 nM 내지 약 160 nM, 약 100 nM 내지 약 150 nM, 약 100 nM 내지 약 140 nM, 약 100 nM 내지 약 130 nM, 약 100 nM 내지 약 120 nM, 약 100 nM 내지 약 110 nM, 약 110 nM 내지 약 5 μM, 약 110 nM 내지 약 2 μM, 약 110 nM 내지 약 1 μM, 약 110 nM 내지 약 500 nM, 약 110 nM 내지 약 250 nM, 약 110 nM 내지 약 240 nM, 약 110 nM 내지 약 230 nM, 약 110 nM 내지 약 220 nM, 약 110 nM 내지 약 210 nM, 약 110 nM 내지 약 200 nM, 약 110 nM 내지 약 190 nM, 약 110 nM 내지 약 180 nM, 약 110 nM 내지 약 170 nM, 약 110 nM 내지 약 160 nM, 약 110 nM 내지 약 150 nM, 약 110 nM 내지 약 140 nM, 약 110 nM 내지 약 130 nM, 약 110 nM 내지 약 120 nM, 약 120 nM 내지 약 5 μM, 약 120 nM 내지 약 2 μM, 약 120 nM 내지 약 1 μM, 약 120 nM 내지 약 500 nM, 약 120 nM 내지 약 250 nM, 약 120 nM 내지 약 240 nM, 약 120 nM 내지 약 230 nM, 약 120 nM 내지 약 220 nM, 약 120 nM 내지 약 210 nM, 약 120 nM 내지 약 200 nM, 약 120 nM 내지 약 190 nM, 약 120 nM 내지 약 180 nM, 약 120 nM 내지 약 170 nM, 약 120 nM 내지 약 160 nM, 약 120 nM 내지 약 150 nM, 약 120 nM 내지 약 140 nM, 약 120 nM 내지 약 130 nM, 약 130 nM 내지 약 5 μM, 약 130 nM 내지 약 2 μM, 약 130 nM 내지 약 1 μM, 약 130 nM 내지 약 500 nM, 약 130 nM 내지 약 250 nM, 약 130 nM 내지 약 240 nM, 약 130 nM 내지 약 230 nM, 약 130 nM 내지 약 220 nM, 약 130 nM 내지 약 210 nM, 약 130 nM 내지 약 200 nM, 약 130 nM 내지 약 190 nM, 약 130 nM 내지 약 180 nM, 약 130 nM 내지 약 170 nM, 약 130 nM 내지 약 160 nM, 약 130 nM 내지 약 150 nM, 약 130 nM 내지 약 140 nM, 약 140 nM 내지 약 5 μM, 약 140 nM 내지 약 2 μM, 약 140 nM 내지 약 1 μM, 약 140 nM 내지 약 500 nM, 약 140 nM 내지 약 250 nM, 약 140 nM 내지 약 240 nM, 약 140 nM 내지 약 230 nM, 약 140 nM 내지 약 220 nM, 약 140 nM 내지 약 210 nM, 약 140 nM 내지 약 200 nM, 약 140 nM 내지 약 190 nM, 약 140 nM 내지 약 180 nM, 약 140 nM 내지 약 170 nM, 약 140 nM 내지 약 160 nM, 약 140 nM 내지 약 150 nM, 약 150 nM 내지 약 5 μM, 약 150 nM 내지 약 2 μM, 약 150 nM 내지 약 1 μM, 약 150 nM 내지 약 500 nM, 약 150 nM 내지 약 250 nM, 약 150 nM 내지 약 240 nM, 약 150 nM 내지 약 230 nM, 약 150 nM 내지 약 220 nM, 약 150 nM 내지 약 210 nM, 약 150 nM 내지 약 200 nM, 약 150 nM 내지 약 190 nM, 약 150 nM 내지 약 180 nM, 약 150 nM 내지 약 170 nM, 약 150 nM 내지 약 160 nM, 약 160 nM 내지 약 5 μM, 약 160 nM 내지 약 2 μM, 약 160 nM 내지 약 1 μM, 약 160 nM 내지 약 500 nM, 약 160 nM 내지 약 250 nM, 약 160 nM 내지 약 240 nM, 약 160 nM 내지 약 230 nM, 약 160 nM 내지 약 220 nM, 약 160 nM 내지 약 210 nM, 약 160 nM 내지 약 200 nM, 약 160 nM 내지 약 190 nM, 약 160 nM 내지 약 180 nM, 약 160 nM 내지 약 170 nM, 약 170 nM 내지 약 5 μM, 약 170 nM 내지 약 2 μM, 약 170 nM 내지 약 1 μM, 약 170 nM 내지 약 500 nM, 약 170 nM 내지 약 250 nM, 약 170 nM 내지 약 240 nM, 약 170 nM 내지 약 230 nM, 약 170 nM 내지 약 220 nM, 약 170 nM 내지 약 210 nM, 약 170 nM 내지 약 200 nM, 약 170 nM 내지 약 190 nM, 약 170 nM 내지 약 180 nM, 약 180 nM 내지 약 5 μM, 약 180 nM 내지 약 2 μM, 약 180 nM 내지 약 1 μM, 약 180 nM 내지 약 500 nM, 약 180 nM 내지 약 250 nM, 약 180 nM 내지 약 240 nM, 약 180 nM 내지 약 230 nM, 약 180 nM 내지 약 220 nM, 약 180 nM 내지 약 210 nM, 약 180 nM 내지 약 200 nM, 약 180 nM 내지 약 190 nM, 약 190 nM 내지 약 5 μM, 약 190 nM 내지 약 2 μM, 약 190 nM 내지 약 1 μM, 약 190 nM 내지 약 500 nM, 약 190 nM 내지 약 250 nM, 약 190 nM 내지 약 240 nM, 약 190 nM 내지 약 230 nM, 약 190 nM 내지 약 220 nM, 약 190 nM 내지 약 210 nM, 약 190 nM 내지 약 200 nM, 약 200 nM 내지 약 5 μM, 약 200 nM 내지 약 2 μM, 약 200 nM 내지 약 1 μM, 약 200 nM 내지 약 500 nM, 약 200 nM 내지 약 250 nM, 약 200 nM 내지 약 240 nM, 약 200 nM 내지 약 230 nM, 약 200 nM 내지 약 220 nM, 약 200 nM 내지 약 210 nM, 약 210 nM 내지 약 5 μM, 약 210 nM 내지 약 2 μM, 약 210 nM 내지 약 1 μM, 약 210 nM 내지 약 500 nM, 약 210 nM 내지 약 250 nM, 약 210 nM 내지 약 240 nM, 약 210 nM 내지 약 230 nM, 약 210 nM 내지 약 220 nM, 약 220 nM 내지 약 5 μM, 약 220 nM 내지 약 2 μM, 약 220 nM 내지 약 1 μM, 약 220 nM 내지 약 500 nM, 약 220 nM 내지 약 250 nM, 약 220 nM 내지 약 240 nM, 약 220 nM 내지 약 230 nM, 약 230 nM 내지 약 5 μM, 약 230 nM 내지 약 2 μM, 약 230 nM 내지 약 1 μM, 약 230 nM 내지 약 500 nM, 약 230 nM 내지 약 250 nM, 약 230 nM 내지 약 240 nM, 약 240 nM 내지 약 5 μM, 약 240 nM 내지 약 2 μM, 약 240 nM 내지 약 1 μM, 약 240 nM 내지 약 500 nM, 약 240 nM 내지 약 250 nM, 약 250 nM 내지 약 5 μM, 약 250 nM 내지 약 2 μM, 약 250 nM 내지 약 1 μM, 약 250 nM 내지 약 500 nM, 약 500 nM 내지 약 5 μM, 약 500 nM 내지 약 2 μM, 약 500 nM 내지 약 1 μM, 약 1 μM 내지 약 5 μM, 약 1 μM 내지 약 2 μM, or 약 2 μM 내지 약 5 μM)이다.
본원에 기술된 ABPC 중 어느 하나의 일부 구현예에서, 약 4.0 내지 약 6.5의 (예를 들어 본원에 기술된 이 범위의 하위 범위 중 어느 하나의) pH에서 제1 항원 결합 도메인의 (및, 제2 항원 결합 도메인이 존재하는 경우, 제2 항원 결합 도메인의) KD는 1 nM보다 더 (예를 들어 약 1 nM 내지 약 1 mM, 약 1 nM 내지 약 900 μM, 약 1 nM 내지 약 800 μM, 약 1 nM 내지 약 700 μM, 약 1 nM 내지 약 600 μM, 약 1 nM 내지 약 500 μM, 약 1 nM 내지 약 400 μM, 약 1 nM 내지 약 300 μM, 약 1 nM 내지 약 200 μM, 약 1 nM 내지 약 100 μM, 약 1 nM 내지 약 90 μM, 약 1 nM 내지 약 80 μM, 약 1 nM 내지 약 70 μM, 약 1 nM 내지 약 60 μM, 약 1 nM 내지 약 50 μM, 약 1 nM 내지 약 40 μM, 약 1 nM 내지 약 30 μM, 약 1 nM 내지 약 20 μM, 약 1 nM 내지 약 10 μM, 약 1 nM 내지 약 5 μM, 약 1 nM 내지 약 4 μM, 약 1 nM 내지 약 2 μM, 약 1 nM 내지 약 1 μM, 약 1 nM 내지 약 900 nM, 약 1 nM 내지 약 800 nM, 약 1 nM 내지 약 700 nM, 약 1 nM 내지 약 600 nM, 약 1 nM 내지 약 500 nM, 약 1 nM 내지 약 400 nM, 약 1 nM 내지 약 300 nM, 약 1 nM 내지 약 200 nM, 약 1 nM 내지 약 100 nM, 약 1 nM 내지 약 90 nM, 약 1 nM 내지 약 80 nM, 약 1 nM 내지 약 70 nM, 약 1 nM 내지 약 60 nM, 약 1 nM 내지 약 50 nM, 약 1 nM 내지 약 40 nM, 약 1 nM 내지 약 30 nM, 약 2 nM 내지 약 1 mM, 약 2 nM 내지 약 900 μM, 약 2 nM 내지 약 800 μM, 약 2 nM 내지 약 700 μM, 약 2 nM 내지 약 600 μM, 약 2 nM 내지 약 500 μM, 약 2 nM 내지 약 400 μM, 약 2 nM 내지 약 300 μM, 약 2 nM 내지 약 200 μM, 약 2 nM 내지 약 100 μM, 약 2 nM 내지 약 90 μM, 약 2 nM 내지 약 80 μM, 약 2 nM 내지 약 70 μM, 약 2 nM 내지 약 60 μM, 약 2 nM 내지 약 50 μM, 약 2 nM 내지 약 40 μM, 약 2 nM 내지 약 30 μM, 약 2 nM 내지 약 20 μM, 약 2 nM 내지 약 10 μM, 약 2 nM 내지 약 5 μM, 약 2 nM 내지 약 4 μM, 약 2 nM 내지 약 2 μM, 약 2 nM 내지 약 1 μM, 약 2 nM 내지 약 900 nM, 약 2 nM 내지 약 800 nM, 약 2 nM 내지 약 700 nM, 약 2 nM 내지 약 600 nM, 약 2 nM 내지 약 500 nM, 약 2 nM 내지 약 400 nM, 약 2 nM 내지 약 300 nM, 약 2 nM 내지 약 200 nM, 약 2 nM 내지 약 100 nM, 약 2 nM 내지 약 90 nM, 약 2 nM 내지 약 80 nM, 약 2 nM 내지 약 70 nM, 약 2 nM 내지 약 60 nM, 약 2 nM 내지 약 50 nM, 약 2 nM 내지 약 40 nM, 약 2 nM 내지 약 30 nM, 약 5 nM 내지 약 1 mM, 약 5 nM 내지 약 900 μM, 약 5 nM 내지 약 800 μM, 약 5 nM 내지 약 700 μM, 약 5 nM 내지 약 600 μM, 약 5 nM 내지 약 500 μM, 약 5 nM 내지 약 400 μM, 약 5 nM 내지 약 300 μM, 약 5 nM 내지 약 200 μM, 약 5 nM 내지 약 100 μM, 약 5 nM 내지 약 90 μM, 약 5 nM 내지 약 80 μM, 약 5 nM 내지 약 70 μM, 약 5 nM 내지 약 60 μM, 약 5 nM 내지 약 50 μM, 약 5 nM 내지 약 40 μM, 약 5 nM 내지 약 30 μM, 약 5 nM 내지 약 20 μM, 약 5 nM 내지 약 10 μM, 약 5 nM 내지 약 5 μM, 약 5 nM 내지 약 4 μM, 약 5 nM 내지 약 2 μM, 약 5 nM 내지 약 1 μM, 약 5 nM 내지 약 900 nM, 약 5 nM 내지 약 800 nM, 약 5 nM 내지 약 700 nM, 약 5 nM 내지 약 600 nM, 약 5 nM 내지 약 500 nM, 약 5 nM 내지 약 400 nM, 약 5 nM 내지 약 300 nM, 약 5 nM 내지 약 200 nM, 약 5 nM 내지 약 100 nM, 약 5 nM 내지 약 90 nM, 약 5 nM 내지 약 80 nM, 약 5 nM 내지 약 70 nM, 약 5 nM 내지 약 60 nM, 약 5 nM 내지 약 50 nM, 약 5 nM 내지 약 40 nM, 약 5 nM 내지 약 30 nM, 약 10 nM 내지 약 1 mM, 약 10 nM 내지 약 900 μM, 약 10 nM 내지 약 800 μM, 약 10 nM 내지 약 700 μM, 약 10 nM 내지 약 600 μM, 약 10 nM 내지 약 500 μM, 약 10 nM 내지 약 400 μM, 약 10 nM 내지 약 300 μM, 약 10 nM 내지 약 200 μM, 약 10 nM 내지 약 100 μM, 약 10 nM 내지 약 90 μM, 약 10 nM 내지 약 80 μM, 약 10 nM 내지 약 70 μM, 약 10 nM 내지 약 60 μM, 약 10 nM 내지 약 50 μM, 약 10 nM 내지 약 40 μM, 약 10 nM 내지 약 30 μM, 약 10 nM 내지 약 20 μM, 약 10 nM 내지 약 10 μM, 약 10 nM 내지 약 5 μM, 약 10 nM 내지 약 4 μM, 약 10 nM 내지 약 2 μM, 약 10 nM 내지 약 1 μM, 약 10 nM 내지 약 900 nM, 약 10 nM 내지 약 800 nM, 약 10 nM 내지 약 700 nM, 약 10 nM 내지 약 600 nM, 약 10 nM 내지 약 500 nM, 약 10 nM 내지 약 400 nM, 약 10 nM 내지 약 300 nM, 약 10 nM 내지 약 200 nM, 약 10 nM 내지 약 100 nM, 약 10 nM 내지 약 90 nM, 약 10 nM 내지 약 80 nM, 약 10 nM 내지 약 70 nM, 약 10 nM 내지 약 60 nM, 약 10 nM 내지 약 50 nM, 약 10 nM 내지 약 40 nM, 약 10 nM 내지 약 30 nM, 약 20 nM 내지 약 1 mM, 약 20 nM 내지 약 900 μM, 약 20 nM 내지 약 800 μM, 약 20 nM 내지 약 700 μM, 약 20 nM 내지 약 600 μM, 약 20 nM 내지 약 500 μM, 약 20 nM 내지 약 400 μM, 약 20 nM 내지 약 300 μM, 약 20 nM 내지 약 200 μM, 약 20 nM 내지 약 100 μM, 약 20 nM 내지 약 90 μM, 약 20 nM 내지 약 80 μM, 약 20 nM 내지 약 70 μM, 약 20 nM 내지 약 60 μM, 약 20 nM 내지 약 50 μM, 약 20 nM 내지 약 40 μM, 약 20 nM 내지 약 30 μM, 약 20 nM 내지 약 20 μM, 약 20 nM 내지 약 10 μM, 약 20 nM 내지 약 5 μM, 약 20 nM 내지 약 4 μM, 약 20 nM 내지 약 2 μM, 약 20 nM 내지 약 1 μM, 약 20 nM 내지 약 900 nM, 약 20 nM 내지 약 800 nM, 약 20 nM 내지 약 700 nM, 약 20 nM 내지 약 600 nM, 약 20 nM 내지 약 500 nM, 약 20 nM 내지 약 400 nM, 약 20 nM 내지 약 300 nM, 약 20 nM 내지 약 200 nM, 약 20 nM 내지 약 100 nM, 약 20 nM 내지 약 90 nM, 약 20 nM 내지 약 80 nM, 약 20 nM 내지 약 70 nM, 약 20 nM 내지 약 60 nM, 약 20 nM 내지 약 50 nM, 약 20 nM 내지 약 40 nM, 약 20 nM 내지 약 30 nM; 약 1 μM 내지 약 1 mM, 약 1 μM 내지 약 900 μM, 약 1 μM 내지 약 800 μM, 약 1 μM 내지 약 700 μM, 약 1 μM 내지 약 600 μM, 약 1 μM 내지 약 500 μM, 약 1 μM 내지 약 400 μM, 약 1 μM 내지 약 300 μM, 약 1 μM 내지 약 200 μM, 약 1 μM 내지 약 100 μM, 약 1 μM 내지 약 90 μM, 약 1 μM 내지 약 80 μM, 약 1 μM 내지 약 70 μM, 약 1 μM 내지 약 60 μM, 약 1 μM 내지 약 50 μM, 약 1 μM 내지 약 40 μM, 약 1 μM 내지 약 30 μM, 약 1 μM 내지 약 20 μM, 약 1 μM 내지 약 10 μM, 약 1 μM 내지 약 5 μM, 약 1 μM 내지 약 4 μM, 약 1 μM 내지 약 3 μM, 약 1 μM 내지 약 2 μM, 약 2 μM 내지 약 1 mM, 약 2 μM 내지 약 900 μM, 약 2 μM 내지 약 800 μM, 약 2 μM 내지 약 700 μM, 약 2 μM 내지 약 600 μM, 약 2 μM 내지 약 500 μM, 약 2 μM 내지 약 400 μM, 약 2 μM 내지 약 300 μM, 약 2 μM 내지 약 200 μM, 약 2 μM 내지 약 100 μM, 약 2 μM 내지 약 90 μM, 약 2 μM 내지 약 80 μM, 약 2 μM 내지 약 70 μM, 약 2 μM 내지 약 60 μM, 약 2 μM 내지 약 50 μM, 약 2 μM 내지 약 40 μM, 약 2 μM 내지 약 30 μM, 약 2 μM 내지 약 20 μM, 약 2 μM 내지 약 10 μM, 약 2 μM 내지 약 5 μM, 약 2 μM 내지 약 4 μM, 약 2 μM 내지 약 3 μM, 약 5 μM 내지 약 1 mM, 약 5 μM 내지 약 900 μM, 약 5 μM 내지 약 800 μM, 약 5 μM 내지 약 700 μM, 약 5 μM 내지 약 600 μM, 약 5 μM 내지 약 500 μM, 약 5 μM 내지 약 400 μM, 약 5 μM 내지 약 300 μM, 약 5 μM 내지 약 200 μM, 약 5 μM 내지 약 100 μM, 약 5 μM 내지 약 90 μM, 약 5 μM 내지 약 80 μM, 약 5 μM 내지 약 70 μM, 약 5 μM 내지 약 60 μM, 약 5 μM 내지 약 50 μM, 약 5 μM 내지 약 40 μM, 약 5 μM 내지 약 30 μM, 약 5 μM 내지 약 20 μM, 약 5 μM 내지 약 10 μM, 약 10 μM 내지 약 1 mM, 약 10 μM 내지 약 900 μM, 약 10 μM 내지 약 800 μM, 약 10 μM 내지 약 700 μM, 약 10 μM 내지 약 600 μM, 약 10 μM 내지 약 500 μM, 약 10 μM 내지 약 400 μM, 약 10 μM 내지 약 300 μM, 약 10 μM 내지 약 200 μM, 약 10 μM 내지 약 100 μM, 약 10 μM 내지 약 90 μM, 약 10 μM 내지 약 80 μM, 약 10 μM 내지 약 70 μM, 약 10 μM 내지 약 60 μM, 약 10 μM 내지 약 50 μM, 약 10 μM 내지 약 40 μM, 약 10 μM 내지 약 30 μM, 약 10 μM 내지 약 20 μM, 약 20 μM 내지 약 1 mM, 약 20 μM 내지 약 900 μM, 약 20 μM 내지 약 800 μM, 약 20 μM 내지 약 700 μM, 약 20 μM 내지 약 600 μM, 약 20 μM 내지 약 500 μM, 약 20 μM 내지 약 400 μM, 약 20 μM 내지 약 300 μM, 약 20 μM 내지 약 200 μM, 약 20 μM 내지 약 100 μM, 약 20 μM 내지 약 90 μM, 약 20 μM 내지 약 80 μM, 약 20 μM 내지 약 70 μM, 약 20 μM 내지 약 60 μM, 약 20 μM 내지 약 50 μM, 약 20 μM 내지 약 40 μM, 약 20 μM 내지 약 30 μM, 약 30 μM 내지 약 1 mM, 약 30 μM 내지 약 900 μM, 약 30 μM 내지 약 800 μM, 약 30 μM 내지 약 700 μM, 약 30 μM 내지 약 600 μM, 약 30 μM 내지 약 500 μM, 약 30 μM 내지 약 400 μM, 약 30 μM 내지 약 300 μM, 약 30 μM 내지 약 200 μM, 약 30 μM 내지 약 100 μM, 약 30 μM 내지 약 90 μM, 약 30 μM 내지 약 80 μM, 약 30 μM 내지 약 70 μM, 약 30 μM 내지 약 60 μM, 약 30 μM 내지 약 50 μM, 약 30 μM 내지 약 40 μM, 약 40 μM 내지 약 1 mM, 약 40 μM 내지 약 900 μM, 약 40 μM 내지 약 800 μM, 약 40 μM 내지 약 700 μM, 약 40 μM 내지 약 600 μM, 약 40 μM 내지 약 500 μM, 약 40 μM 내지 약 400 μM, 약 40 μM 내지 약 300 μM, 약 40 μM 내지 약 200 μM, 약 40 μM 내지 약 100 μM, 약 40 μM 내지 약 90 μM, 약 40 μM 내지 약 80 μM, 약 40 μM 내지 약 70 μM, 약 40 μM 내지 약 60 μM, 약 40 μM 내지 약 50 μM, 약 50 μM 내지 약 1 mM, 약 50 μM 내지 약 900 μM, 약 50 μM 내지 약 800 μM, 약 50 μM 내지 약 700 μM, 약 50 μM 내지 약 600 μM, 약 50 μM 내지 약 500 μM, 약 50 μM 내지 약 400 μM, 약 50 μM 내지 약 300 μM, 약 50 μM 내지 약 200 μM, 약 50 μM 내지 약 100 μM, 약 50 μM 내지 약 90 μM, 약 50 μM 내지 약 80 μM, 약 50 μM 내지 약 70 μM, 약 50 μM 내지 약 60 μM, 약 60 μM 내지 약 1 mM, 약 60 μM 내지 약 900 μM, 약 60 μM 내지 약 800 μM, 약 60 μM 내지 약 700 μM, 약 60 μM 내지 약 600 μM, 약 60 μM 내지 약 500 μM, 약 60 μM 내지 약 400 μM, 약 60 μM 내지 약 300 μM, 약 60 μM 내지 약 200 μM, 약 60 μM 내지 약 100 μM, 약 60 μM 내지 약 90 μM, 약 60 μM 내지 약 80 μM, 약 60 μM 내지 약 70 μM, 약 70 μM 내지 약 1 mM, 약 70 μM 내지 약 900 μM, 약 70 μM 내지 약 800 μM, 약 70 μM 내지 약 700 μM, 약 70 μM 내지 약 600 μM, 약 70 μM 내지 약 500 μM, 약 70 μM 내지 약 400 μM, 약 70 μM 내지 약 300 μM, 약 70 μM 내지 약 200 μM, 약 70 μM 내지 약 100 μM, 약 70 μM 내지 약 90 μM, 약 70 μM 내지 약 80 μM, 약 80 μM 내지 약 1 mM, 약 80 μM 내지 약 900 μM, 약 80 μM 내지 약 800 μM, 약 80 μM 내지 약 700 μM, 약 80 μM 내지 약 600 μM, 약 80 μM 내지 약 500 μM, 약 80 μM 내지 약 400 μM, 약 80 μM 내지 약 300 μM, 약 80 μM 내지 약 200 μM, 약 80 μM 내지 약 100 μM, 약 80 μM 내지 약 90 μM, 약 90 μM 내지 약 1 mM, 약 90 μM 내지 약 900 μM, 약 90 μM 내지 약 800 μM, 약 90 μM 내지 약 700 μM, 약 90 μM 내지 약 600 μM, 약 90 μM 내지 약 500 μM, 약 90 μM 내지 약 400 μM, 약 90 μM 내지 약 300 μM, 약 90 μM 내지 약 200 μM, 약 90 μM 내지 약 100 μM, 약 100 μM 내지 약 1 mM, 약 100 μM 내지 약 900 μM, 약 100 μM 내지 약 800 μM, 약 100 μM 내지 약 700 μM, 약 100 μM 내지 약 600 μM, 약 100 μM 내지 약 500 μM, 약 100 μM 내지 약 400 μM, 약 100 μM 내지 약 300 μM, 약 100 μM 내지 약 200 μM, 약 200 μM 내지 약 1 mM, 약 200 μM 내지 약 900 μM, 약 200 μM 내지 약 800 μM, 약 200 μM 내지 약 700 μM, 약 200 μM 내지 약 600 μM, 약 200 μM 내지 약 500 μM, 약 200 μM 내지 약 400 μM, 약 200 μM 내지 약 300 μM, 약 300 μM 내지 약 1 mM, 약 300 μM 내지 약 900 μM, 약 300 μM 내지 약 800 μM, 약 300 μM 내지 약 700 μM, 약 300 μM 내지 약 600 μM, 약 300 μM 내지 약 500 μM, 약 300 μM 내지 약 400 μM, 약 400 μM 내지 약 1 mM, 약 400 μM 내지 약 900 μM, 약 400 μM 내지 약 800 μM, 약 400 μM 내지 약 700 μM, 약 400 μM 내지 약 600 μM, 약 400 μM 내지 약 500 μM, 약 500 μM 내지 약 1 mM, 약 500 μM 내지 약 900 μM, 약 500 μM 내지 약 800 μM, 약 500 μM 내지 약 700 μM, 약 500 μM 내지 약 600 μM, 약 600 μM 내지 약 1 mM, 약 600 μM 내지 약 900 μM, 약 600 μM 내지 약 800 μM, 약 600 μM 내지 약 700 μM, 약 700 μM 내지 약 1 mM, 약 700 μM 내지 약 900 μM, 약 700 μM 내지 약 800 μM, 약 800 μM 내지 약 1 mM, 약 800 μM 내지 약 900 μM, 또는 약 900 μM 내지 약 1 mM 보다 더) 크다.
당업계에 공지된 다양한 상이한 방법(예를 들어 전기영동 이동성 변화 검정, 필터 결합 검정, 표면 플라스몬 공명, 생체 분자 결합 동역학 검정, 항원 발현 세포에 대한 시험관 내 결합 검정 등)을 사용하여 본원에 기술된 항원 결합 단백질 작제물 중 어느 하나의 KD 값을 결정할 수 있다.
본원에 기술된 ABPC 중 어느 하나의 일부 실시예에서, ABPC의 생체 내 반감기는 대조군 ABPC(예를 들어 본원에 기술된 예시적인 대조군 ABPC 중 어느 하나)의 반감기와 비교했을 때 감소(예를 들어 검출 가능하게 감소)(예를 들어 적어도 1% 감소, 적어도 5% 감소, 적어도 10% 감소, 적어도 15% 감소, 적어도 20% 감소, 적어도 25% 감소, 적어도 30% 감소, 적어도 35% 감소, 적어도 40% 감소, 적어도 45% 감소, 적어도 50% 감소, 적어도 55% 감소, 적어도 60% 감소, 적어도 65% 감소, 적어도 70% 감소, 적어도 75% 감소, 적어도 80% 감소, 적어도 85% 감소, 적어도 90% 감소, 적어도 95% 감소, 또는 적어도 99% 감소, 또는 약 1% 감소 내지 약 99% 감소, 약 1% 감소 내지 약 95% 감소, 약 1% 감소 내지 약 90% 감소, 약 1% 감소 내지 약 85% 감소, 약 1% 감소 내지 약 80% 감소, 약 1% 감소 내지 약 75% 감소, 약 1% 감소 내지 약 70% 감소, 약 1% 감소 내지 약 65% 감소, 약 1% 감소 내지 약 60% 감소, 약 1% 감소 내지 약 55% 감소, 약 1% 감소 내지 약 50% 감소, 약 1% 감소 내지 약 45% 감소, 약 1% 감소 내지 약 40% 감소, 약 1% 감소 내지 약 35% 감소, 약 1% 감소 내지 약 30% 감소, 약 1% 감소 내지 약 25% 감소, 약 1% 감소 내지 약 20% 감소, 약 1% 감소 내지 약 15% 감소, 약 1% 감소 내지 약 10% 감소, 약 1% 감소 내지 약 5% 감소, 약 5% 감소 내지 약 99% 감소, 약 5% 감소 내지 약 95% 감소, 약 5% 감소 내지 약 90% 감소, 약 5% 감소 내지 약 85% 감소, 약 5% 감소 내지 약 80% 감소, 약 5% 감소 내지 약 75% 감소, 약 5% 감소 내지 약 70% 감소, 약 5% 감소 내지 약 65% 감소, 약 5% 감소 내지 약 60% 감소, 약 5% 감소 내지 약 55% 감소, 약 5% 감소 내지 약 50% 감소, 약 5% 감소 내지 약 45% 감소, 약 5% 감소 내지 약 40% 감소, 약 5% 감소 내지 약 35% 감소, 약 5% 감소 내지 약 30% 감소, 약 5% 감소 내지 약 25% 감소, 약 5% 감소 내지 약 20% 감소, 약 5% 감소 내지 약 15% 감소, 약 5% 감소 내지 약 10% 감소, 약 10% 감소 내지 약 99% 감소, 약 10% 감소 내지 약 95% 감소, 약 10% 감소 내지 약 90% 감소, 약 10% 감소 내지 약 85% 감소, 약 10% 감소 내지 약 80% 감소, 약 10% 감소 내지 약 75% 감소, 약 10% 감소 내지 약 70% 감소, 약 10% 감소 내지 약 65% 감소, 약 10% 감소 내지 약 60% 감소, 약 10% 감소 내지 약 55% 감소, 약 10% 감소 내지 약 50% 감소, 약 10% 감소 내지 약 45% 감소, 약 10% 감소 내지 약 40% 감소, 약 10% 감소 내지 약 35% 감소, 약 10% 감소 내지 약 30% 감소, 약 10% 감소 내지 약 25% 감소, 약 10% 감소 내지 약 20% 감소, 약 10% 감소 내지 약 15% 감소, 약 15% 감소 내지 약 99% 감소, 약 15% 감소 내지 약 95% 감소, 약 15% 감소 내지 약 90% 감소, 약 15% 감소 내지 약 85% 감소, 약 15% 감소 내지 약 80% 감소, 약 15% 감소 내지 약 75% 감소, 약 15% 감소 내지 약 70% 감소, 약 15% 감소 내지 약 65% 감소, 약 15% 감소 내지 약 60% 감소, 약 15% 감소 내지 약 55% 감소, 약 15% 감소 내지 약 50% 감소, 약 15% 감소 내지 약 45% 감소, 약 15% 감소 내지 약 40% 감소, 약 15% 감소 내지 약 35% 감소, 약 15% 감소 내지 약 30% 감소, 약 15% 감소 내지 약 25% 감소, 약 15% 감소 내지 약 20% 감소, 약 20% 감소 내지 약 99% 감소, 약 20% 감소 내지 약 95% 감소, 약 20% 감소 내지 약 90% 감소, 약 20% 감소 내지 약 85% 감소, 약 20% 감소 내지 약 80% 감소, 약 20% 감소 내지 약 75% 감소, 약 20% 감소 내지 약 70% 감소, 약 20% 감소 내지 약 65% 감소, 약 20% 감소 내지 약 60% 감소, 약 20% 감소 내지 약 55% 감소, 약 20% 감소 내지 약 50% 감소, 약 20% 감소 내지 약 45% 감소, 약 20% 감소 내지 약 40% 감소, 약 20% 감소 내지 약 35% 감소, 약 20% 감소 내지 약 30% 감소, 약 20% 감소 내지 약 25% 감소, 약 25% 감소 내지 약 99% 감소, 약 25% 감소 내지 약 95% 감소, 약 25% 감소 내지 약 90% 감소, 약 25% 감소 내지 약 85% 감소, 약 25% 감소 내지 약 80% 감소, 약 25% 감소 내지 약 75% 감소, 약 25% 감소 내지 약 70% 감소, 약 25% 감소 내지 약 65% 감소, 약 25% 감소 내지 약 60% 감소, 약 25% 감소 내지 약 55% 감소, 약 25% 감소 내지 약 50% 감소, 약 25% 감소 내지 약 45% 감소, 약 25% 감소 내지 약 40% 감소, 약 25% 감소 내지 약 35% 감소, 약 25% 감소 내지 약 30% 감소, 약 30% 감소 내지 약 99% 감소, 약 30% 감소 내지 약 95% 감소, 약 30% 감소 내지 약 90% 감소, 약 30% 감소 내지 약 85% 감소, 약 30% 감소 내지 약 80% 감소, 약 30% 감소 내지 약 75% 감소, 약 30% 감소 내지 약 70% 감소, 약 30% 감소 내지 약 65% 감소, 약 30% 감소 내지 약 60% 감소, 약 30% 감소 내지 약 55% 감소, 약 30% 감소 내지 약 50% 감소, 약 30% 감소 내지 약 45% 감소, 약 30% 감소 내지 약 40% 감소, 약 30% 감소 내지 약 35% 감소, 약 35% 감소 내지 약 99% 감소, 약 35% 감소 내지 약 95% 감소, 약 35% 감소 내지 약 90% 감소, 약 35% 감소 내지 약 85% 감소, 약 35% 감소 내지 약 80% 감소, 약 35% 감소 내지 약 75% 감소, 약 35% 감소 내지 약 70% 감소, 약 35% 감소 내지 약 65% 감소, 약 35% 감소 내지 약 60% 감소, 약 35% 감소 내지 약 55% 감소, 약 35% 감소 내지 약 50% 감소, 약 35% 감소 내지 약 45% 감소, 약 35% 감소 내지 약 40% 감소, 약 40% 감소 내지 약 99% 감소, 약 40% 감소 내지 약 95% 감소, 약 40% 감소 내지 약 90% 감소, 약 40% 감소 내지 약 85% 감소, 약 40% 감소 내지 약 80% 감소, 약 40% 감소 내지 약 75% 감소, 약 40% 감소 내지 약 70% 감소, 약 40% 감소 내지 약 65% 감소, 약 40% 감소 내지 약 60% 감소, 약 40% 감소 내지 약 55% 감소, 약 40% 감소 내지 약 50% 감소, 약 40% 감소 내지 약 45% 감소, 약 45% 감소 내지 약 99% 감소, 약 45% 감소 내지 약 95% 감소, 약 45% 감소 내지 약 90% 감소, 약 45% 감소 내지 약 85% 감소, 약 45% 감소 내지 약 80% 감소, 약 45% 감소 내지 약 75% 감소, 약 45% 감소 내지 약 70% 감소, 약 45% 감소 내지 약 65% 감소, 약 45% 감소 내지 약 60% 감소, 약 45% 감소 내지 약 55% 감소, 약 45% 감소 내지 약 50% 감소, 약 50% 감소 내지 약 99% 감소, 약 50% 감소 내지 약 95% 감소, 약 50% 감소 내지 약 90% 감소, 약 50% 감소 내지 약 85% 감소, 약 50% 감소 내지 약 80% 감소, 약 50% 감소 내지 약 75% 감소, 약 50% 감소 내지 약 70% 감소, 약 50% 감소 내지 약 65% 감소, 약 50% 감소 내지 약 60% 감소, 약 50% 감소 내지 약 55% 감소, 약 55% 감소 내지 약 99% 감소, 약 55% 감소 내지 약 95% 감소, 약 55% 감소 내지 약 90% 감소, 약 55% 감소 내지 약 85% 감소, 약 55% 감소 내지 약 80% 감소, 약 55% 감소 내지 약 75% 감소, 약 55% 감소 내지 약 70% 감소, 약 55% 감소 내지 약 65% 감소, 약 55% 감소 내지 약 60% 감소, 약 60% 감소 내지 약 99% 감소, 약 60% 감소 내지 약 95% 감소, 약 60% 감소 내지 약 90% 감소, 약 60% 감소 내지 약 85% 감소, 약 60% 감소 내지 약 80% 감소, 약 60% 감소 내지 약 75% 감소, 약 60% 감소 내지 약 70% 감소, 약 60% 감소 내지 약 65% 감소, 약 65% 감소 내지 약 99% 감소, 약 65% 감소 내지 약 95% 감소, 약 65% 감소 내지 약 90% 감소, 약 65% 감소 내지 약 85% 감소, 약 65% 감소 내지 약 80% 감소, 약 65% 감소 내지 약 75% 감소, 약 65% 감소 내지 약 70% 감소, 약 70% 감소 내지 약 99% 감소, 약 70% 감소 내지 약 95% 감소, 약 70% 감소 내지 약 90% 감소, 약 70% 감소 내지 약 85% 감소, 약 70% 감소 내지 약 80% 감소, 약 70% 감소 내지 약 75% 감소, 약 75% 감소 내지 약 99% 감소, 약 75% 감소 내지 약 95% 감소, 약 75% 감소 내지 약 90% 감소, 약 75% 감소 내지 약 85% 감소, 약 75% 감소 내지 약 80% 감소, 약 80% 감소 내지 약 99% 감소, 약 80% 감소 내지 약 95% 감소, 약 80% 감소 내지 약 90% 감소, 약 80% 감소 내지 약 85% 감소, 약 85% 감소 내지 약 99% 감소, 약 85% 감소 내지 약 95% 감소, 약 85% 감소 내지 약 90% 감소, 약 90% 감소 내지 약 99% 감소, 약 90% 감소 내지 약 95% 감소, 또는 약 95% 감소 내지 약 99% 감소)한다.
접합
일부 구현예에서, 본원에 제공된 ABPC는 약물(예: 화학요법 약물, 소분자), 독소, 또는 방사성 동위원소에 접합될 수 있다. (예를 들어, 암의 치료에 유용한 것으로 알려진) 약물, 독소, 및 방사성 동위원소의 비제한적인 예는 당업계에 공지되어 있다.
일부 구현예에서, 본원에 기술된 ABPC 중 어느 하나의 적어도 하나의 폴리펩티드는 절단성 링커를 통해 독소, 방사성 동위원소, 또는 약물에 접합된다. 일부 구현예에서, 절단성 링커는 프로테아제 절단 부위를 포함한다. 일부 구현예에서, 절단성 링커는 표적 포유류 세포에 의해 ABPC가 리소좀 또는 후기 엔도솜으로 수송될 때 ABPC 상에서 절단된다. 일부 구현예에서, 링커의 절단은 약물 또는 독소를 기능적으로 활성화시킨다.
일부 구현예에서, 본원에 기술된 ABPC 중 어느 하나의 적어도 하나의 폴리펩티드는 비-절단성 링커를 통해 독소, 방사성 동위원소, 또는 약물에 접합된다. 일부 구현예에서, 접합된 독소, 방사성 동위원소, 또는 약물은 ABPC의 리소좀 및/또는 후기 엔도솜 분해 중에 방출된다.
절단성 링커의 비제한적인 예는 하이드라존 링커, 펩티드 링커, 이황화 링커, 및 티오에테르 링커를 포함한다. 예를 들어 Carter 등의 문헌[Cancer J. 14(3):154-
169, 2008]; Sanderson 등의 문헌[Clin. Cancer Res. 11(2 Pt1):843-852, 2005]; Chari 등의 문헌[Acc. Chem. Res. 41(1):98-107, 2008]; Oflazoglu 등의 문헌[Clin. Cancer Res. 14(19): 6171-6180, 2008]; 및 Lu 등의 문헌[Int. J. Mol. Sci. 17(4): 561, 2016]을 참조한다.
비-절단성 링커의 비제한적인 예는 말레이미드 알칸 링커 및 멜레이미드 시클로헥산 링커(MMC)를 포함한다(예를 들어, McCombs 등의 문헌[AAPS J. 17(2):339-351, 2015]에 기술된 것들 참조).
일부 구현예에서, 본원에 기술된 ABPC 중 어느 하나는 표적 포유류 세포에 대해 세포독성이거나 세포증식 억제성이다.
세포에서 항원 결합 단백질 작제물의 발현
또한, ABPC(예를 들어 본원에 기술된 ABPC 중 어느 하나)를 생성하는 방법이 본원에 제공되며, 상기 방법은: ABPC를 암호화하는 핵산을 세포에 도입하여 재조합 세포를 생산하는 단계; 및 ABPC의 발현에 충분한 조건 하에서 재조합 세포를 배양하는 단계를 포함한다. 일부 구현예에서, 도입하는 단계는 ABPC를 암호화하는 핵산을 포함하는 발현 벡터를 세포에 도입하여 재조합 세포를 생산하는 단계를 포함한다.
본원에 기술된 ABPC 중 어느 하나는 임의의 세포, 예를 들어 진핵 세포 또는 원핵 세포에 의해 생산될 수 있다. 본원에서 사용되는 바와 같이, 용어 "진핵 세포"는 구별되는 막-결합 핵을 갖는 세포를 지칭한다. 이러한 세포는, 예를 들어 포유류(예를 들어 설치류, 비인간 영장류, 또는 인간), 곤충, 진균, 또는 식물 세포를 포함할 수 있다. 일부 구현예에서, 진핵 세포는 사카로마이세스 세레비지애(Saccharomyces cerevisiae)와 같은 효모 세포이다. 일부 구현예에서, 진핵 세포는 포유류, 조류, 식물 또는 곤충 세포와 같은 더 고등의 진핵생물이다. 본원에서 사용되는 바와 같이, 용어 "원핵 세포"는 구별되는 막-결합 핵을 갖지 않는 세포를 지칭한다. 일부 구현예에서, 원핵 세포는 박테리아 세포이다.
세포를 배양하는 방법은 당업계에 잘 알려져 있다. 세포는 증식, 분화, 및 성장에 유리한 조건 하에서 시험관 내에서 유지될 수 있다. 간략하게, 세포는 세포(예를 들어 임의의 세포)를 세포 생존력 및 성장을 지원하는 필수 성장 인자 및 보충제를 포함하는 세포 배양 배지와 접촉시킴으로써 배양될 수 있다.
핵산 및 발현 벡터를 세포(예를 들어 진핵 세포) 내로 도입하는 방법은 당업계에 공지되어 있다. 핵산을 세포 내로 도입하는 데 사용될 수 있는 방법의 비제한적인 예는, 리포펙션, 형질감염, 전기천공, 미세주입, 인산칼슘 형질감염, 덴드리머-기반 형질감염, 양이온성 중합체 형질감염, 세포 스퀴징(cell squeezing), 초음파 천공(sonoporation), 광학 형질감염, 천자(impalection),
유체역학적 전달, 마그네토펙션(magnetofection), 바이러스 형질도입(예: 아데노바이러스 및 렌티바이러스 형질도입), 및 나노입자 형질도입을 포함한다.
당업계에 잘 알려진 기술(예: 황산암모늄 침전, 폴리에틸렌 글리콜 침전, 이온-교환 크로마토그래피(음이온 또는 양이온), 소수성 상호작용에 기초한 크로마토그래피, 금속-친화도 크로마토그래피, 리간드-친화도 크로마토그래피, 및 크기 배제 크로마토그래피)을 사용하여 세포(예: 진핵 세포)로부터 ABPC를 단리하는 것을 추가로 포함하는 방법이 본원에 제공된다.
치료 방법
암을 치료하는 방법이 본원에 제공되며, 여기서 암은 MET 또는 MET의 에피토프가 표면에 제시된 암 세포의 집단을 갖는 것을 특징으로 하고, 상기 방법은 상기 암 세포의 집단을 갖는 것을 특징으로 하는 암에 걸린 것으로 식별된 대상체에게 본원에 기술된 약학적 조성물 중 어느 하나 또는 본원에 기술된 ABPC 중 어느 하나의 치료적 유효량을 투여하는 단계를 포함한다.
또한, 대상체에서 종양의 부피를 감소시키는 방법이 본원에 제공되며, 여기서 종양은 MET 또는 MET의 에피토프가 표면에 제시된 암 세포의 집단을 갖는 것을 특징으로 하고, 상기 방법은 상기 암 세포의 집단을 갖는 것을 특징으로 하는 암에 걸린 것으로 식별된 대상체에게 본원에 기술된 약학적 조성물 중 어느 하나 또는 본원에 기술된 ABPC 중 어느 하나의 치료적 유효량을 투여하는 단계를 포함한다. 본원에 기술된 방법 중 어느 하나의 일부 구현예에서, 적어도 하나의 (예를 들어 1, 2, 3, 4, 또는 5개의) 종양(예를 들어 고형 종양)의 부피 또는 종양 위치(예를 들어 전이 부위)가 ABPC의 투여 이전의 적어도 하나의 종양(예를 들어 고형 종양)의 크기와 비교했을 때 적어도 1%, 적어도 2%, 적어도 3%, 적어도 4%, 적어도 5%, 적어도 6%, 적어도 8%, 적어도 10%, 적어도 12%, 적어도 14%, 적어도 16%, 적어도 18%, 적어도 20%, 적어도 22%, 적어도 24%, 적어도 26%, 적어도 28%, 적어도 30%, 적어도 35%, 적어도 40%, 적어도 45%, 적어도 50%, 적어도 55%, 적어도 60%, 적어도 65%, 적어도 70%, 적어도 75%, 적어도 80%, 적어도 85%, 적어도 90%, 적어도 95%, 또는 적어도 99%만큼 (예를 들어 검출 가능하게) 감소된다.
또한, 대상체의 암 세포에서 세포 사멸을 유도하는 방법이 본원에 제공되며, 여기서 암 세포는 그 표면에 MET 또는 MET의 에피토프를 갖고, 상기 방법은 상기 암 세포의 집단을 갖는 것을 특징으로 하는 암에 걸린 것으로 식별된 대상체에게 본원에 기술된 약학적 조성물 중 어느 하나 또는 본원에 기술된 ABPC 중 어느 하나의 치료적 유효량을 투여하는 단계를 포함한다. 일부 구현예에서, 유도되는 세포 사멸은 괴사(necrosis)이다. 일부 구현예에서, 유도되는 세포 사멸은 세포자멸사(apoptosis)이다.
본원에 기술된 방법 중 어느 하나의 일부 구현예에서, 암은 원발성 종양이다.
본원에 기술된 방법 중 어느 하나의 일부 구현예에서, 암은 전이(metastasis)이다.
본원에 기술된 방법 중 어느 하나의 일부 구현예에서, 암은 비-T 세포 침윤성 종양이다. 본원에 기술된 방법 중 어느 하나의 일부 구현예에서, 암은 T 세포 침윤성 종양이다.
또한, 암에 걸린 대상체에서 전이가 발생할 위험을 감소시키는 방법 또는 추가의 전이가 발생할 위험을 감소시키는 방법이 본원에 제공되며, 여기서 암은 MET 또는 MET의 에피토프가 표면에 제시된 암 세포의 집단을 갖는 것을 특징으로 하고, 상기 방법은 상기 암 세포의 집단을 갖는 것을 특징으로 하는 암에 걸린 것으로 식별된 대상체에게 본원에 기술된 약학적 조성물 중 어느 하나 또는 본원에 기술된 ABPC 중 어느 하나의 치료적 유효량을 투여하는 단계를 포함한다. 일부 구현예에서, 대상체에서 전이가 발생할 위험 또는 추가의 전이가 발생할 위험은, 유사한 암에 걸릴 위험이 있지만 치료를 받지 않았거나 본원에 기술된 ABPC 중 어느 하나의 투여를 포함하지 않는 치료를 받은 대상체와 비교했을 때, 적어도 1%, 적어도 2%, 적어도 3%, 적어도 4%, 적어도 5%, 적어도 6%, 적어도 8%, 적어도 10%, 적어도 12%, 적어도 14%, 적어도 16%, 적어도 18%, 적어도 20%, 적어도 25%, 적어도 30%, 적어도 35%, 적어도 40%, 적어도 45%, 적어도 50%, 적어도 55%, 적어도 60%, 적어도 65%, 적어도 70%, 적어도 75%, 적어도 80%, 적어도 85%, 적어도 90%, 적어도 95%, 또는 적어도 99%만큼 (예를 들어 검출 가능하게) 감소한다.
본원에 기술된 방법 중 어느 하나의 일부 구현예에서, 암은 비-T 세포 침윤성 종양이다. 본원에 기술된 방법 중 어느 하나의 일부 구현예에서, 암은 T 세포 침윤성 종양이다. 본원에 기술된 방법 중 어느 하나의 일부 구현예에서, 세포 구획은 엔도솜/리소좀 경로의 일부이다. 본원에 기술된 방법 중 어느 하나의 일부 구현예에서, 세포 구획은 엔도솜이다.
용어 "대상체"는 임의의 포유동물을 지칭한다. 일부 구현예에서, 대상체 또는 "치료에 적합한 대상체"는 갯과(예를 들어 개), 고양잇과(예를 들어 고양이), 말과(예를 들어, 말), 양, 소, 돼지, 소과, 영장류, 예를 들어 진원류(simian)(예를 들어, 원숭이(예: 마모셋, 바분), 또는 유인원(예: 고릴리, 침팬지, 오랑우탄, 또는 긴팔원숭이) 또는 인간); 또는 설치류(예: 마우스, 기니피그, 햄스터, 또는 랫트)일 수 있다. 일부 구현예에서, 대상체 또는 "치료에 적합한 대상체"는 비인간 포유동물일 수 있고, 특히 인간에서의 치료 효능을 입증하기 위한 모델로서 통상적으로 사용되는 포유동물(예를 들어 쥣과, 토끼, 돼지, 갯과, 또는 영장류 동물)이 사용될 수 있다.
본원에서 사용되는 바와 같이, 치료는 암(예를 들어 본원에 기술된 암 중 어느 하나)을 가진 환자에서 암의 하나 이상의(예를 들어 2, 3, 4, 또는 5가지) 징후 또는 증상의 횟수, 빈도, 또는 중증도를 감소시키는 것을 포함한다. 예를 들어, 치료는 암환자에게서 암 진행을 감소시키거나, 암의 중증도를 감소시키거나, 암의 재발 위험을 감소시킬 수 있다.
대상체(예를 들어 본원에 기술된 대상체 중 어느 하나)에서 (예를 들어, 치료 이전의 대상체에서의 고형 종양의 성장, 또는 상이한 치료를 받고 있거나 치료를 받지 않는 상이한 대상체에서의 유사한 고형 종양의 성장과 비교했을 때) 고형 종양의 성장을 억제하는 방법이 본원에 제공되며, 상기 벙법은 본원에 기술된 임의의 ABPC 중 어느 하나 또는 본원에 기술된 약학적 조성물 중 어느 하나의 치료적 유효량을 대상체에게 투여하는 단계를 포함한다.
본원에 기술된 방법 중 어느 하나의 일부 구현예에서, 고형 종양의 성장은 고형 종양의 원발성 성장이다. 본원에 기술된 방법 중 어느 하나의 일부 구현예에서, 고형 종양의 성장은 고형 종양의 재발성 성장이다. 본원에 기술된 방법 중 어느 하나의 일부 구현예에서, 고형 종양의 성장은 고형 종양의 전이성 성장이다. 일부 구현예에서, 치료는 (예를 들어 치료 이전의 대상체에서의 고형 종양의 성장, 또는 상이한 치료를 받는 중이거나 치료를 받지 않는 상이한 대상체에서의 유사한 고형 종양의 성장과 비교했을 때) 대상체에서 고형 종양의 성장을 약 1% 내지 약 99% (또는 본원에 기술된 이 범위의 하위 범위 중 어느 하나만큼) 감소시킨다. 대상체에서 고형 종양의 성장은 다양한 상이한 영상화 방법, 예를 들어 양전자 방출 단층촬영, X-선 컴퓨터 단층촬영, 컴퓨터 축 단층촬영, 및 자기 공명 영상화에 의해 평가될 수 있다.
또한, (예를 들어 유사한 암을 가진 대상체로서 상이한 치료를 받고 있거나 치료를 받지 않는 대상체와 비교했을 때) 암(예를 들어 본원에 기술된 예시적인 암 중 어느 하나)을 가진 것으로 식별된 대상체에서 일정 기간에 걸쳐 전이가 발생할 위험 또는 추가의 전이가 발생할 위험을 감소시키는 방법이 본원에 제공되며, 상기 방법은 본원에 기술된 단백질 중 어느 하나 또는 본원에 기술된 약학적 조성물 중 어느 하나의 치료적 유효량을 대상체에게 투여하는 단계를 포함한다. 본원에 기술된 방법 중 어느 하나의 일부 구현예에서, 전이 또는 추가의 전이는 뼈, 림프절, 뇌, 폐, 간, 피부, 흉벽(뼈, 연골 및 연조직 포함), 복강, 반대측 유방, 연조직, 근육, 골수, 난소, 부신, 및 췌장에 대한 하나 이상의 전이이다.
본원에 기술된 방법 중 어느 하나의 일부 구현예에서, 기간은 약 1개월 내지 약 3년(약 1개월 내지 약 2.5년, 약 1개월 내지 약 2년, 약 2개월 내지 약 1.5년, 약 1개월 내지 약 1년, 약 1개월 내지 약 10개월, 약 1개월 내지 약 8개월, 약 1개월 내지 약 6개월, 약 1개월 내지 약 5개월, 약 1개월 내지 약 4개월, 약 1개월 내지 약 3개월, 약 1개월 내지 약 2개월, 약 2개월 내지 약 3년, 약 2개월 내지 약 2.5년, 약 2개월 내지 약 2년, 약 2개월 내지 약 1.5년, 약 2개월 내지 약 1년, 약 2개월 내지 약 10개월, 약 2개월 내지 약 8개월, 약 2개월 내지 약 6개월, 약 2개월 내지 약 5개월, 약 2개월 내지 약 4개월, 약 2개월 내지 약 3개월, 약 3개월 내지 약 3년, 약 3개월 내지 약 2.5년, 약 3개월 내지 약 2년, 약 3개월 내지 약 1.5년, 약 3개월 내지 약 1년, 약 3개월 내지 약 10개월, 약 3개월 내지 약 8개월, 약 3개월 내지 약 6개월, 약 3개월 내지 약 5개월, 약 3개월 내지 약 4개월, 약 4개월 내지 약 3년, 약 4개월 내지 약 2.5년, 약 4개월 내지 약 2년, 약 4개월 내지 약 1.5년, 약 4개월 내지 약 1년, 약 4개월 내지 약 10개월, 약 4개월 내지 약 8개월, 약 4개월 내지 약 6개월, 약 4개월 내지 약 5개월, 약 5개월 내지 약 3년, 약 5개월 내지 약 2.5년, 약 5개월 내지 약 2년, 약 5개월 내지 약 1.5년, 약 5개월 내지 약 1년, 약 5개월 내지 약 10개월, 약 5개월 내지 약 8개월, 약 5개월 내지 약 6개월, 약 6개월 내지 약 3년, 약 6개월 내지 약 2.5년, 약 6개월 내지 약 2년, 약 6개월 내지 약 1.5년, 약 6개월 내지 약 1년, 약 6개월 내지 약 10개월, 약 6개월 내지 약 8개월, 약 8개월 내지 약 3년, 약 8개월 내지 약 2.5년, 약 8개월 내지 약 2년, 약 8개월 내지 약 1.5년, 약 8개월 내지 약 1년, 약 8개월 내지 약 10개월, 약 10개월 내지 약 3년, 약 10개월 내지 약 2.5년, 약 10개월 내지 약 2년, 약 10개월 내지 약 1.5년, 약 10개월 내지 약 1년, 약 1년 내지 약 3년, 약 1년 내지 약 2.5년, 약 1년 내지 약 2년, 약 1년 내지 약 1.5년,
약 1.5년 내지 약 3년, 약 1.5년 내지 약 2.5년, 약 1.5년 내지 약 2년, 약 2년 내지 약 3년, 약 2년 내지 약 2.5년, 또는 약 2.5년 내지 약 3년)이다.
일부 구현예에서, 암을 가진 것으로 식별된 대상체에서 일정 기간에 걸쳐 전이가 발생하거나 추가의 전이가 발생할 위험은, 예를 들어 상이한 치료를 받고 있거나 치료를 받지 않는 유사한 암을 가진 대상체에서의 위험과 비교했을 때, 약 1% 내지 약 99%(예를 들어, 본원에 기술된 이 범위의 임의의 하위 범위 중 하나)만큼 감소된다.
암의 비제한적인 예는 다음을 포함한다: 급성 림프모구성 백혈병(ALL), 급성 골수성 백혈병(AML), 부신피질 암종, 항문암, 충수암, 성상세포종, 기저 세포 암종, 뇌 종양, 담관암, 방광암, 골암, 유방암, 기관지 종양, 버킷 림프종, 원발 기원이 알려지지 않은 암종, 심장 종양, 자궁경부암, 척삭종, 만성 림프구성 백혈병(CLL), 만성 골수성 백혈병(CML), 만성 골수 증식성 신생물, 대장암, 결장직장암, 두개인두종, 피부 T-세포 림프종, 담관 암종, 배아 종양, 자궁내막암, 뇌실막세포종, 식도암, 좌골신경모세포종, 섬유성 조직구종, 유잉 육종, 안구암, 생식 세포 종양, 담낭암, 위암, 위장 유암종, 위장관 기질 종양, 임신성 영양막 질환, 신경교종, 두경부암, 모양 세포 백혈병, 간세포암, 조직구증, 호지킨 림프종, 하인두암, 안구 내 흑색종, 섬 세포 종양, 카포시 육종, 신장암, 랑게르한스 세포 조직구증, 후두암, 백혈병, 입술 및 구강암, 간암, 제자리 소엽암종, 폐암, 림프종, 매그로글로불린혈증, 악성 섬유성 조직구종, 흑색종, 메르켈 세포 암종, 중피종, 잠복 원발을 수반하는 전이성 편평 경부암, NUT 유전자를 수반하는 정중관 암종, 구강암, 다발성 내분비샘 종양 증후군, 다발성 골수종, 균상식육종, 골수이형성 증후군, 골수이형성/골수증식성 신생물, 비강 및 부비강암, 비인두암, 신경아세포종, 비호지킨 림프종, 비소세포 폐암, 구인두암, 골육종, 난소암, 췌장암, 유두종증, 부신경절종, 부갑상선암, 음경암, 인두암, 크롬친화세포종, 뇌하수체 종양, 흉막폐 모세포종, 원발성 중추 신경계 림프종, 전립선암, 직장암, 신세포암, 신우암 및 요관암, 망막아종, 횡문근 종양, 침샘암, 세자리 증후군(Sezary syndrome), 피부암, 소세포 폐암, 소장암, 연조직 육종, 척수 종양, 위암, T 세포 림프종, 기형 종양, 고환암, 인후암, 흉선종 및 흉선 암종, 갑상선암, 요도암, 자궁암, 질암, 외음부암, 및 윌름스 종양. 암의 추가 예는 당업계에 공지되어 있다.
일부 구현예에서, 환자에게는 하나 이상의 추가 치료제(예: 화학요법제, 재조합 사이토카인 또는 인터루킨 단백질, 키나아제 억제제, 및 관문 억제제 중 하나 이상)가 추가로 투여된다. 일부 구현예에서, 하나 이상의 추가 치료제는 본원에 기술된 ABPC 중 어느 하나가 환자에게 투여되는 것과 대략 동일한 시간에 환자에게 투여된다. 일부 구현예에서, 하나 이상의 추가 치료제는 본원에 기술된 ABPC 중 어느 하나가 환자에게 투여된 후 환자에게 투여된다. 일부 구현예에서, 하나 이상의 추가 치료제는 본원에 기술된 ABPC 중 어느 하나가 환자에게 투여되기 전에 환자에게 투여된다.
본원에 기술된 방법 중 어느 하나의 일부 구현예에서, 암은 고형 암(예: 유방암, 전립선암, 또는 비소세포 폐암)이다.
조성물
또한, 본원에 기술된 ABPC 중 적어도 하나를 포함하는 조성물(예: 약학적 조성물)이 본원에 제공된다. 일부 구현예에서, 조성물(예: 약학적 조성물)은 멸균 바이알 또는 미리 로딩된 주사기에 배치될 수 있다.
일부 구현예에서, 조성물(예: 약학적 조성물)은 상이한 투여 경로(예: 정맥 내, 피하, 근육 내, 또는 종양 내)에 맞게 제형화된다. 일부 구현예에서, 조성물(예: 약학적 조성물)은 약학적으로 허용 가능한 담체(예: 인산염 완충 식염수)를 포함할 수 있다. 본원에 기술된 약학적 조성물 중 어느 하나는, 예를 들어 환자가 필요로 하고 환자가 견딜 수 있는 투여량 및 빈도에 따라 대상체에게 1회 투여되거나 다회 투여될 수 있다. 약제학적 조성물의 투여량은 병태, 질환, 또는 증상을 효과적으로 치료하거나 완화시키기에 충분한 양의 ABPC를 제공해야 한다.
또한, 암(예를 들어, 본원에 기술된 암 중 어느 하나)을 앓고 있는 대상체를 치료하는 방법이 본원에 제공되며, 상기 방법은 본원에 제공된 조성물 또는 약학적 조성물 중 적어도 하나의 치료적 유효량을 투여하는 단계를 포함한다.
키트
또한, 본원에 기술된 ABPC 중 어느 하나, 본원에 기술된 조성물 중 어느 하나, 또는 본원에 기술된 약학적 조성물 중 어느 하나를 포함하는 키트가 본원에 제공된다. 일부 구현예에서, 키트는 본원에 기술된 방법 중 어느 하나를 수행하기 위한 지침을 포함할 수 있다. 일부 구현예에서, 키트는 본원에 기술된 조성물(예: 약학적 조성물)의 적어도 1회 투여량을 포함할 수 있다. 일부 구현예에서, 키트는 본원에 기술된 약학적 조성물 어느 하나를 투여하기 위한 주사기를 제공할 수 있다.
단백질 작제물
또한, 다음을 포함하는 단백질 작제물(PC)이 제공된다: 표적 포유류 세포의 표면 상에 제시된 MET 또는 MET의 에피토프에 특이적으로 결합할 수 있는 제1 항원 결합 도메으로서, (a) 약 7.0 내지 약 8.0의 (또는 본원에 기술된 이 범위의 하위 범위 중 어느 하나의) pH에서의 해리 속도가 약 4.0 내지 약 6.5의 (또는 본원에 기술된 이 범위의 하위 범위 중 어느 하나의) pH에서의 해리 속도보다 더 빠르고/빠르거나; (b) 약 7.0 내지 약 8.0의 (또는 본원에 기술된 이 범위의 하위 범위 중 어느 하나의) pH에서의 해리 상수(KD)가 약 4.0 내지 약 6.5의 pH에서의 KD보다 더 큰, 항원 결합 도메인.
또한, 본원에 기술된 PC 중 어느 하나를 포함하는 약학적 조성물이 본원에 제공된다. 또한, 치료를 필요로 하는 대상체에서 대상체를 치료하는 방법이 본원에 제공되며, 상기 방법은 본원에 기술된 PC 중 어느 하나의 치료적 유효량을 대상체에게 투여하는 단계를 포함한다.
항원 결합 단백질 작제물의 pH 의존성을 개선하는 방법
또한, 항원 결합 단백질 작제물의 pH 의존성을 개선하는 방법이 본원에 제공되며, 상기 방법은: 항원 결합 도메인을 포함하는 출발 항원 결합 단백질 작제물을 제공하는 단계; 및 하나 이상의 히스티딘 아미노산 치환을 출발 항원 결합 단백질 작제물 내 항원 결합 도메인의 하나 이상의 CDR에 도입하는 단계를 포함하며, 여기서 상기 방법에 따라 다음 중 하나 또는 둘 다에 해당하는 항원 결합 작제물이 생성된다: (a) 약 4.0 내지 약 6.5의 pH에서 항원 결합 도메인의 해리 속도 대 약 7.0 내지 약 8.0의 pH에서 해리 속도의 비율이 시작 항원 결합 단백질 작제물과 비교했을 때 증가함(예를 증가된 적어도 0.1배 증가 내지 약 100배 증가, 또는 본원에 기술된 이 범위의 하위 범위 중 어느 하나만큼 증가함); 및 (b) 약 4.0 내지 약 6.5의 pH에서 항원 결합 도메인의 해리 상수(KD) 대 약 7.0 내지 약 8.0의 pH에서의 KD의 비율이 출발 항원 결합 단백질 작제물과 비교했을 때 증가함(예를 증가된 적어도 0.1배 증가 내지 약 100배 증가, 또는 본원에 기술된 이 범위의 하위 범위 중 어느 하나만큼 증가함).
구현예
구현예 1. 표적 포유류 세포의 표면 상에 제시된 MET 또는 MET의 에피토프에 특이적으로 결합할 수 있는 제1 항원 결합 도메인을 포함하는 항원 결합 단백질 작제물(ABPC)의 유효량을 포함하는 약학적 조성물로서, (a) 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인의 해리 속도가 약 7.0 내지 약 8.0의 pH에서의 해리 속도보다 빠르거나; (b) 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인의 해리 상수(KD)가 약 7.0 내지 약 8.0의 pH에서의 KD보다 더 큰, 약학적 조성물.
구현예 2. 구현예 1에 있어서, 제1 항원 결합 도메인은 하나 이상의 아미노산이 히스티딘으로 치환된 텔리소투주맙의 중쇄 가변 도메인을 포함하는, 약학적 조성물.
구현예 3. 구현예 1에 있어서, 제1 항원 결합 도메인은 하나 이상의 아미노산이 히스티딘으로 치환된 텔리소투주맙의 경쇄 가변 도메인을 포함하는, 약학적 조성물.
구현예 4. 구현예 1에 있어서, 제1 항원 결합 도메인은: 하나 이상의 아미노산이 히스티딘으로 치환된 텔리소투주맙의 중쇄 가변 도메인; 및 하나 이상의 아미노산이 히스티딘으로 치환된 텔리소투주맙의 경쇄 가변 도메인을 포함하는, 약학적 조성물.
구현예 5. 구현예 2 또는 4에 있어서, 텔리소투주맙의 중쇄 가변 도메인은 서열번호 1을 포함하는, 약학적 조성물.
구현예 6. 구현예 3 또는 4에 있어서, 텔리소투주맙의 경쇄 가변 도메인은 서열번호 2를 포함하는, 약학적 조성물.
구현예 7. 구현예 1에 있어서, 제1 항원 결합 도메인은, 서열번호 3~5의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인으로서, 서열번호 3~5 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된 중쇄 가변 도메인을 포함하는, 약학적 조성물.
구현예 8. 구현예 1에 있어서, 제1 MET 결합 도메인은, 서열번호 6~8의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인으로서, 서열번호 6~8 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된 경쇄 가변 도메인을 포함하는, 약학적 조성물.
구현예 9. 구현예 1에 있어서, 제1 MET 결합 도메인은: 서열번호 3~5의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인으로서, 서열번호 3~5 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된 중쇄 가변 도메인; 및 서열번호 6~8의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인으로서, 서열번호 6~8 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된 경쇄 가변 도메인을 포함하는, 약학적 조성물.
구현예 10. 구현예 1, 2, 또는 7에 있어서, 제1 항원 결합 도메인은, 서열번호 1과 적어도 90% 동일한 중쇄 가변 도메인으로서, 26, 27, 28, 29, 32, 97, 98, 99, 100, 101, 102, 103, 및 107로 이루어진 군으로부터 선택된 서열번호 1 내 하나 이상의 위치에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함하는, 약학적 조성물.
구현예 11. 구현예 1, 3, 또는 8에 있어서, 제1 항원 결합 도메인은 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 2 내 하나 이상의 위치에서 히스티딘을 포함하는 경쇄 가변 도메인을 포함하는, 약학적 조성물.
구현예 12. 구현예 1, 4, 또는 9에 있어서, 제1 항원 결합 도메인은 다음을 포함하는, 약학적 조성물: 서열번호 1과 적어도 90% 동일한 중쇄 가변 도메인으로서, 26, 27, 28, 29, 32, 97, 98, 99, 100, 101, 102, 103, 및 107로 이루어진 군으로부터 선택된 서열번호 1 내 하나 이상의 위치에서 히스티딘을 포함하는 중쇄 가변 도메인; 및 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 2 내 하나 이상의 위치에서 히스티딘을 포함하는 경쇄 가변 도메인.
구현예 13. 구현예 1에 있어서, 제1 항원 결합 도메인은 서열번호 13, 14, 15, 16, 19, 40, 41, 42, 43, 44, 45, 46, 또는 50의 중쇄 가변 도메인을 포함하는, 약학적 조성물.
구현예 14. 구현예 13에 있어서, 제1 항원 결합 도메인은 서열번호 2의 경쇄 가변 도메인을 포함하는, 약학적 조성물.
구현예 15. 구현예 1 내지 14 중 어느 하나에 있어서, ABPC는 표적 포유류 세포에 의한 ABPC의 내재화 후에 표적 포유류 세포에서 분해되는, 약학적 조성물.
구현예 16. 구현예 1 내지 15 중 어느 하나에 있어서, ABPC는 접합된 독소, 방사성 동위원소, 약물, 또는 소분자를 추가로 포함하는, 약학적 조성물.
구현예 17. 구현예 16에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리를 증가시킬 수 있는, 약학적 조성물.
구현예 18. 구현예 17에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리를 적어도 20% 증가시킬 수 있는, 약학적 조성물.
구현예 19. 구현예 18에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리를 적어도 50% 증가시킬 수 있는, 약학적 조성물.
구현예 20. 구현예 17에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리를 적어도 2배 증가시킬 수 있는, 약학적 조성물.
구현예 21. 구현예 20에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리를 적어도 5배 증가시킬 수 있는, 약학적 조성물.
구현예 22. 구현예 16 내지 21 중 어느 하나에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포 살해를 증가시킬 수 있는, 약학적 조성물.
구현예 23. 구현예 22에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포 살해를 적어도 20% 증가시킬 수 있는, 약학적 조성물.
구현예 24. 구현예 23에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포 살해를 적어도 50% 증가시킬 수 있는, 약학적 조성물.
구현예 25. 구현예 22에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포 살해를 적어도 2배 증가시킬 수 있는, 약학적 조성물.
구현예 26. 구현예 25에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포 살해를 적어도 5배 증가시킬 수 있는, 약학적 조성물.
구현예 27. 구현예 1 내지 26 중 어느 하나에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달을 증가시킬 수 있는, 약학적 조성물.
구현예 28. 구현예 27에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달을 적어도 20% 증가시킬 수 있는, 약학적 조성물.
구현예 29. 구현예 28에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달을 적어도 50% 증가시킬 수 있는, 약학적 조성물.
구현예 30. 구현예 27에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달을 적어도 2배 증가시킬 수 있는, 약학적 조성물.
구현예 31. 구현예 30에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달을 적어도 5배 증가시킬 수 있는, 약학적 조성물.
구현예 32. 구현예 1 내지 31 중 어느 하나에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포의 표면 상에 제시된 MET의 수준을 덜 감소시키는, 약학적 조성물.
구현예 33. 구현예 1 내지 31 중 어느 하나에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포의 표면 상에 제시된 MET의 수준을 검출 가능한 수준으로 감소시키지 않는, 약학적 조성물.
구현예 34. 표적 포유류 세포의 표면 상에 제시된 MET 또는 MET의 에피토프에 특이적으로 결합할 수 있는 제1 항원 결합 도메인; 및 접합된 독소, 방사성 동위원소, 약물, 또는 소분자를 포함하는 항원 결합 단백질 작제물(ABPC)을 포함하는 약학적 조성물로서, (a) 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인의 해리 속도는 약 7.0 내지 약 8.0의 pH에서의 해리 속도보다 빠르거나; 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인의 해리 상수(KD)는 약 7.0 내지 약 8.0의 pH에서의 KD보다 더 크며; (b) 상기 조성물은 다음 중 하나 이상을 가능하게 하는, 약학적 조성물: 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독성 유리를 증가시키는 것; 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 세포 살해를 증가시키는 것; 및 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달을 증가시키는 것.
구현예 35. 구현예 34에 있어서, 제1 항원 결합 도메인은 하나 이상의 아미노산이 히스티딘으로 치환된 텔리소투주맙의 중쇄 가변 도메인을 포함하는, 약학적 조성물.
구현예 36. 구현예 34에 있어서, 제1 항원 결합 도메인은 하나 이상의 아미노산이 히스티딘으로 치환된 텔리소투주맙의 경쇄 가변 도메인을 포함하는, 약학적 조성물.
구현예 37. 구현예 34에 있어서, 제1 항원 결합 도메인은: 하나 이상의 아미노산이 히스티딘으로 치환된 텔리소투주맙의 중쇄 가변 도메인; 및 하나 이상의 아미노산이 히스티딘으로 치환된 텔리소투주맙의 경쇄 가변 도메인을 포함하는, 약학적 조성물.
구현예 38. 구현예 35 또는 37에 있어서, 텔리소투주맙의 중쇄 가변 도메인은 서열번호 1을 포함하는, 약학적 조성물.
구현예 39. 구현예 36 또는 37에 있어서, 텔리소투주맙의 경쇄 가변 도메인은 서열번호 2를 포함하는, 약학적 조성물.
구현예 40. 구현예 34에 있어서, 제1 항원 결합 도메인은, 서열번호 3~5의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인으로서, 서열번호 3~5 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된 중쇄 가변 도메인을 포함하는, 약학적 조성물.
구현예 41. 구현예 34에 있어서, 제1 MET 결합 도메인은, 서열번호 6~8의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인으로서, 서열번호 6~8 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된 경쇄 가변 도메인을 포함하는, 약학적 조성물.
구현예 42. 구현예 34에 있어서, 제1 MET 결합 도메인은: 서열번호 3~5의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인으로서, 서열번호 3~5 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된 중쇄 가변 도메인; 및 서열번호 6~8의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인으로서, 서열번호 6~8 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된 경쇄 가변 도메인을 포함하는, 약학적 조성물.
구현예 43. 구현예 34, 35, 또는 40에 있어서, 제1 항원 결합 도메인은, 서열번호 1과 적어도 90% 동일한 중쇄 가변 도메인으로서, 26, 27, 28, 29, 32, 97, 98, 99, 100, 101, 102, 103, 및 107로 이루어진 군으로부터 선택된 서열번호 1 내 하나 이상의 위치에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함하는, 약학적 조성물.
구현예 44. 구현예 34, 36, 또는 41에 있어서, 제1 항원 결합 도메인은 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 2 내 하나 이상의 위치에서 히스티딘을 포함하는 경쇄 가변 도메인을 포함하는, 약학적 조성물.
구현예 45. 구현예 34, 37, 또는 42에 있어서, 제1 항원 결합 도메인은 다음을 포함하는, 약학적 조성물: 서열번호 1과 적어도 90% 동일한 중쇄 가변 도메인으로서, 26, 27, 28, 29, 32, 97, 98, 99, 100, 101, 102, 103, 및 107로 이루어진 군으로부터 선택된 서열번호 1 내 하나 이상의 위치에서 히스티딘을 포함하는 중쇄 가변 도메인; 및 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 2 내 하나 이상의 위치에서 히스티딘을 포함하는 경쇄 가변 도메인.
구현예 46. 구현예 34에 있어서, 제1 항원 결합 도메인은 서열번호 13, 14, 15, 16, 19, 40, 41, 42, 43, 44, 45, 46, 또는 50의 중쇄 가변 도메인을 포함하는, 약학적 조성물.
구현예 47. 구현예 46에 있어서, 제1 항원 결합 도메인은 서열번호 2의 경쇄 가변 도메인을 포함하는, 약학적 조성물.
구현예 48. 구현예 34 내지 47 중 어느 하나에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리를 증가시키는, 약학적 조성물.
구현예 49. 구현예 48에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리를 적어도 20% 증가시키는, 약학적 조성물.
구현예 50. 구현예 49에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리를 적어도 50% 증가시키는, 약학적 조성물.
구현예 51. 구현예 48에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리를 적어도 2배 증가시키는, 약학적 조성물.
구현예 52. 구현예 51에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리를 적어도 5배 증가시키는, 약학적 조성물.
구현예 53. 구현예 34 내지 52 중 어느 하나에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포 살해를 증가시키는, 약학적 조성물.
구현예 54. 구현예 53에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포 살해를 적어도 20% 증가시키는, 약학적 조성물.
구현예 55. 구현예 54에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포 살해를 적어도 50% 증가시키는, 약학적 조성물.
구현예 56. 구현예 53에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포 살해를 적어도 2배 증가시키는, 약학적 조성물.
구현예 57. 구현예 56에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포 살해를 적어도 5배 증가시키는, 약학적 조성물.
구현예 58. 구현예 34 내지 57 중 어느 하나에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달을 증가시키는, 약학적 조성물.
구현예 59. 구현예 58에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달을 적어도 20% 증가시키는, 약학적 조성물.
구현예 60. 구현예 59에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달을 적어도 50% 증가시키는, 약학적 조성물.
구현예 61. 구현예 58에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달을 적어도 2배 증가시키는, 약학적 조성물.
구현예 62. 구현예 61에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달을 적어도 5배 증가시키는, 약학적 조성물.
구현예 63. 구현예 34 내지 62 중 어느 하나에 있어서, 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포의 표면 상에 제시된 MET 수준을 덜 감소시키는, 약학적 조성물.
구현예 64. 구현예 34 내지 62 중 어느 하나에 있어서, 조성물은 표적 포유류 세포의 표면 상에 제시된 MET 수준을 검출 가능하게 감소시키지 않는, 약학적 조성물.
구현예 65. 구현예 1 내지 64 중 어느 하나에 있어서, 표적 포유류 세포는 암 세포인, 약학적 조성물.
구현예 66. 구현예 1 내지 65 중 어느 하나에 있어서, 약 4.0 내지 약 6.5의 pH에서 항원 결합 도메인의 해리 속도는 약 7.0 내지 약 8.0의 pH에서 항원 결합 도메인의 해리 속도보다 적어도 10% 더 빠른, 약학적 조성물.
구현예 67. 구현예 1 내지 65 중 어느 하나에 있어서, 약 4.0 내지 약 6.5의 pH에서 항원 결합 도메인의 해리 속도는 약 7.0 내지 약 8.0의 pH에서 항원 결합 도메인의 해리 속도보다 적어도 3배 더 빠른, 약학적 조성물.
구현예 68. 구현예 1 내지 65 중 어느 하나에 있어서, 약 4.0 내지 약 6.5의 pH에서 항원 결합 도메인의 해리 속도는 약 7.0 내지 약 8.0의 pH에서 항원 결합 도메인의 해리 속도보다 적어도 10배 더 빠른, 약학적 조성물.
구현예 69. 구현예 1 내지 68 중 어느 하나에 있어서, 약 4.0 내지 약 6.5의 pH에서 항원 결합 도메인의 KD는 약 7.0 내지 약 8.0의 pH에서 항원 결합 도메인의 KD보다 적어도 10배 더 큰, 약학적 조성물.
구현예 70. 구현예 1 내지 68 중 어느 하나에 있어서, 약 4.0 내지 약 6.5의 pH에서 항원 결합 도메인의 KD는 약 7.0 내지 약 8.0의 pH에서 항원 결합 도메인의 KD보다 적어도 3배 더 큰, 약학적 조성물.
구현예 71. 구현예 1 내지 68 중 어느 하나에 있어서, 약 4.0 내지 약 6.5의 pH에서 항원 결합 도메인의 KD는 약 7.0 내지 약 8.0의 pH에서 항원 결합 도메인의 KD보다 적어도 10배 더 큰, 약학적 조성물.
구현예 72. 구현예 1 내지 71 중 어느 하나에 있어서, ABPC는 표적 포유류 세포에 대해 세포독성이거나 세포증식 억제성인, 약학적 조성물.
구현예 73. 구현예 1 내지 72 중 어느 하나에 있어서, ABPC는 비인간 영장류 MET 및 인간 MET와 교차 반응성인, 약학적 조성물.
구현예 74. 구현예 1 내지 72 중 어느 하나에 있어서, ABPC는 비인간 영장류 MET, 인간 MET, 및 랫트 MET와 마우스 MET 중 하나 또는 둘 다와 교차 반응성인, 약학적 조성물.
구현예 75. 구현예 1 내지 74 중 어느 하나에 있어서, ABPC는 비인간 영장류 MET, 인간 MET, 랫트 MET, 및 마우스 MET와 교차 반응성인, 약학적 조성물.
구현예 76. 구현예 1 내지 75 중 어느 하나에 있어서, 항원 결합 도메인은 구세계 원숭이에서 유래된 세포의 표면 상에 존재하는 MET의 에피토프에 결합하는, 약학적 조성물.
구현예 77. 구현예 1 내지 76 중 어느 하나에 있어서, ABPC는 단일 폴리펩티드를 포함하는, 약학적 조성물.
구현예 78. 구현예 77에 있어서, 항원 결합 도메인은 VH 도메인, VHH 도메인, VNAR 도메인, 및 scFv로 이루어진 군으로부터 선택되는, 약학적 조성물.
구현예 79. 구현예 77 또는 78에 있어서, ABPC는 BiTe, (scFv)2, 나노바디, 나노바디-HSA, DART, TandAb, scDiabody, scDiabody-CH3, scFv-CH-CL-scFv, a HSAbody, scDiabody-HSA, 또는 탠덤-scFv인, 약학적 조성물.
구현예 80. 구현예 1 내지 76 중 어느 하나에 있어서, ABPC는 2개 이상의 폴리펩티드를 포함하는, 약학적 조성물.
구현예 81. 구현예 80에 있어서, ABPC는 항체, VHH-scAb, VHH-Fab, 이중 scFab, F(ab')2, 디아바디, crossMab, DAF (투-인-원), DAF (포-인-원), DutaMab, DT-IgG, 놉-인-홀 공통 경쇄, 놉-인-홀 조립체, 전하쌍, Fab-아암 교환, SEEDbody, LUZ-Y, Fcab, κλ-body, 직교 Fab, DVD-IgG, IgG(H)-scFv, scFv-(H)IgG, IgG(L)-scFv, scFv-(L)IgG, IgG(L,H)-Fv, IgG(H)-V, V(H)-IgG, IgG(L)-V, V(L)-IgG, KIH IgG-scFab, 2scFv-IgG, IgG-2scFv, scFv4-Ig, Zybody, DVI-IgG, 디아바디-CH3, 트리플바디, 미니항체, 미니바디, TriBi 미니바디, scFv-CH3 KIH, Fab-scFv, F(ab')2-scFv2, scFv-KIH, Fab-scFv-Fc, 4가 HCAb, scDiabody-Fc, 디아바디-Fc, 탠덤 scFv-Fc, VHH-Fc, 탠덤 VHH-Fc, VHH-Fc KiH, Fab-VHH-Fc, 인트라바디, 독-앤-락, ImmTAC, IgG-IgG 접합체, Cov-X-Body, scFv1-PEG-scFv2, 애드넥티, DARPin, 피브로넥티, 및 DEP 접합체의 군으로부터 선택되는, 약학적 조성물.
구현예 82. 구현예 16 내지 81 중 어느 하나에 있어서, ABPC의 적어도 하나의 폴리펩티드는 절단성 링커를 통해 독소, 방사성 동위원소, 약물, 또는 소분자에 접합되는, 약학적 조성물.
구현예 83. 구현예 16 내지 81 중 어느 하나에 있어서, ABPC의 적어도 하나의 폴리펩티드는 비절단성 링커를 통해 독소, 방사성 동위원소, 약물, 또는 소분자에 접합되는, 약학적 조성물.
구현예 84. 구현예 1 내지 83 중 어느 하나에 있어서, ABPC의 생체 내 반감기는 대조군 ABPC의 생체 내 반감기와 비교했을 때 감소되는, 약학적 조성물.
구현예 85. 구현예 84에 있어서, ABPC의 생체 내 반감기는 대조군 ABPC의 생체 내 반감기와 비교했을 때 약 5% 내지 약 95% 감소되는, 약학적 조성물.
구현예 86. 구현예 84에 있어서, ABPC의 생체 내 반감기는 대조군 ABPC의 생체 내 반감기와 비교했을 때 약 10% 내지 약 95% 감소되는, 약학적 조성물.
구현예 87. 구현예 84에 있어서, ABPC의 생체 내 반감기는 대조군 ABPC의 생체 내 반감기와 비교했을 때 약 30% 내지 약 95% 감소되는, 약학적 조성물.
구현예 88. 구현예 84에 있어서, ABPC의 생체 내 반감기는 대조군 ABPC의 생체 내 반감기와 비교했을 때 약 50% 내지 약 95% 감소되는, 약학적 조성물.
구현예 89. 구현예 84에 있어서, ABPC의 생체 내 반감기는 대조군 ABPC의 생체 내 반감기와 비교했을 때 약 70% 내지 약 95% 감소되는, 약학적 조성물.
구현예 90. 구현예 17 내지 89 중 어느 하나에 있어서, 대조군 ABPC는 표적 포유류 세포의 표면 상에 제시된 MET 또는 MET의 에피토프에 특이적으로 결합할 수 있고, 여기서 (a) 대조군 ABPC는 제1 항원 결합 도메인을 포함하고; (b) 약 4.0 내지 약 6.5의 pH에서 대조군 ABPC의 제1 항원 결합 도메인의 해리 속도는 약 7.0 내지 8.0의 pH에서의 해리 속도보다 3배 이하로 더 빠르고; (c) 약 4.0 내지 약 6.5의 pH에서 대조군 ABPC의 제1 항원 결합 도메인의 해리 상수(KD)는 약 7.0 내지 약 8.0의 pH에서의 KD보다 3배 이하로 더 큰, 약학적 조성물.
구현예 91. 구현예 17 내지 89 중 어느 하나에 있어서, 대조군 ABPC는 표적 포유류 세포의 표면 상에 제시된 MET 또는 MET의 에피토프에 특이적으로 결합할 수 있고, 여기서 (a) 대조군 ABPC는 제1 항원 결합 도메인을 포함하고; (b) 약 4.0 내지 약 6.5의 pH에서 대조군 ABPC의 제1 항원 결합 도메인의 해리 속도는 약 7.0 내지 8.0의 pH에서의 해리 속도보다 2배 이하로 더 빠르고; (c) 약 4.0 내지 약 6.5의 pH에서 대조군 ABPC의 제1 항원 결합 도메인의 해리 상수(KD)는 약 7.0 내지 약 8.0의 pH에서의 KD보다 2배 이하로 더 큰, 약학적 조성물.
구현예 92. 구현예 17 내지 89 중 어느 하나에 있어서, 대조군 ABPC는 표적 포유류 세포의 표면 상에 제시된 MET 또는 MET의 에피토프에 특이적으로 결합할 수 있고, 여기서 (a) 대조군 ABPC는 제1 항원 결합 도메인을 포함하고; (b) 약 4.0 내지 약 6.5의 pH에서 대조군 ABPC의 제1 항원 결합 도메인의 해리 속도는 약 7.0 내지 8.0의 pH에서의 해리 속도보다 1배 이하로 더 빠르고; (c) 약 4.0 내지 약 6.5의 pH에서 대조군 ABPC의 제1 항원 결합 도메인의 해리 상수(KD)는 약 7.0 내지 약 8.0의 pH에서의 KD보다 1배 이하로 더 큰, 약학적 조성물.
구현예 93. 구현예 17 내지 89 중 어느 하나에 있어서, 대조군 ABPC는 텔리소투주맙인, 약학적 조성물.
구현예 94. 구현예 1 내지 93 중 어느 하나에 있어서, ABPC는 제2 항원 결합 도메인을 추가로 포함하는, 약학적 조성물.
구현예 95. 구현예 1 내지 94 중 어느 하나의 약학적 조성물의 적어도 1회 투여량을 포함하는 키트.
구현예 96. 표적 포유류 세포의 표면 상에 제시된 MET 또는 MET의 에피토프에 특이적으로 결합할 수 있는 제1 항원 결합 도메인을 포함하는 항원 결합 단백질 작제물(ABPC)로서, (a) 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인 해리 속도는 약 7.0 내지 약 8.0의 pH에서의 해리 속도보다 더 빠르거나; (b) 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인의 해리 상수(KD)는 약 7.0 내지 약 8.0의 pH에서의 KD보다 더 큰, ABPC.
구현예 97. 구현예 96에 있어서, 제1 항원 결합 도메인은 하나 이상의 아미노산이 히스티딘으로 치환된 텔리소투주맙의 중쇄 가변 도메인을 포함하는, ABPC.
구현예 98. 구현예 96에 있어서, 제1 항원 결합 도메인은 하나 이상의 아미노산이 히스티딘으로 치환된 텔리소투주맙의 경쇄 가변 도메인을 포함하는, ABPC.
구현예 99. 구현예 96에 있어서, 제1 항원 결합 도메인은 하나 이상의 아미노산이 히스티딘으로 치환된 텔리소투주맙의 중쇄 가변 도메인; 및 하나 이상의 아미노산이 히스티딘으로 치환된 텔리소투주맙의 경쇄 가변 도메인을 포함하는, ABPC.
구현예 100. 구현예 97 또는 99에 있어서, 텔리소투주맙의 중쇄 가변 도메인은 서열번호 1을 포함하는, ABPC.
구현예 101. 구현예 98 또는 99에 있어서, 텔리소투주맙의 경쇄 가변 도메인은 서열번호 2를 포함하는, ABPC.
구현예 102. 구현예 96에 있어서, 제1 항원 결합 도메인은, 서열번호 3~5의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인으로서, 서열번호 3~5 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된 중쇄 가변 도메인을 포함하는, ABPC.
구현예 103. 구현예 96에 있어서, 제1 MET 결합 도메인은, 서열번호 6~8의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인으로서, 서열번호 6~8 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된 경쇄 가변 도메인을 포함하는, ABPC.
구현예 104. 구현예 96에 있어서, 제1 MET-결합 도메인은: 서열번호 3~5의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인으로서, 서열번호 3~5 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된 중쇄 가변 도메인; 및 서열번호 6~8의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인으로서, 서열번호 6~8 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된 경쇄 가변 도메인을 포함하는, ABPC.
구현예 105. 구현예 96, 97, 또는 102에 있어서, 제1 항원 결합 도메인은, 서열번호 1과 적어도 90% 동일한 중쇄 가변 도메인으로서 26, 27, 28, 29, 32, 97, 98, 99, 100, 101, 102, 103, 및 107로 이루어진 군으로부터 선택된 서열번호 1 내 하나 이상의 위치에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함하는, ABPC.
구현예 106. 구현예 96, 98, 또는 103에 있어서, 제1 항원 결합 도메인은, 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서 서열번호 2 내 하나 이상의 위치에서 히스티딘을 포함하는 경쇄 가변 도메인을 포함하는, ABPC.
구현예 107. 구현예 96, 99, 또는 104에 있어서, 제1 항원 결합 도메인은 다음을 포함하는, ABPC: 서열번호 1과 적어도 90% 동일한 중쇄 가변 도메인으로서, 26, 27, 28, 29, 32, 97, 98, 99, 100, 101, 102, 103, 및 107로 이루어진 군으로부터 선택된 서열번호 1 내 하나 이상의 위치에서 히스티딘을 포함하는 중쇄 가변 도메인; 및 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 2 내 하나 이상의 위치에서 히스티딘을 포함하는 경쇄 가변 도메인.
구현예 108. 구현예 96에 있어서, 제1 항원 결합 도메인은 서열번호 13, 14, 15, 16, 19, 40, 41, 42, 43, 44, 45, 46, 또는 50의 중쇄 가변 도메인을 포함하는, ABPC.
구현예 109. 구현예 96에 있어서, 제1 항원 결합 도메인은 서열번호 2의 경쇄 가변 도메인을 포함하는, ABPC.
구현예 110. 구현예 96 내지 109 중 어느 하나에 있어서, ABPC는 표적 포유류 세포에 의해 내재화된 후 표적 포유류 세포 내에서 분해되는, ABPC.
구현예 111. 구현예 96 내지 110 중 어느 하나에 있어서, ABPC는 접합된 독소, 방사성 동위원소, 약물, 또는 소분자를 추가로 포함하는, ABPC.
구현예 112. 구현예 111에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리를 증가시키는, ABPC.
구현예 113. 구현예 112에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리를 적어도 20% 증가시키는, ABPC.
구현예 114. 구현예 113에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리를 적어도 50% 증가시키는, ABPC.
구현예 115. 구현예 112에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리를 적어도 2배 증가시키는, ABPC.
구현예 116. 구현예 115에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리를 적어도 5배 증가시키는, ABPC.
구현예 117. 구현예 111 내지 116 중 어느 하나에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포 살해를 증가시키는, ABPC.
구현예 118. 구현예 117에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포 살해를 적어도 20% 증가시키는, ABPC.
구현예 119. 구현예 118에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포 살해를 적어도 50% 증가시키는, ABPC.
구현예 120. 구현예 117에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포 살해를 적어도 2배 증가시키는, ABPC.
구현예 121. 구현예 120에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포 살해를 적어도 5배 증가시키는, ABPC.
구현예 122. 구현예 96 내지 121 중 어느 하나에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달을 증가시키는, ABPC.
구현예 123. 구현예 122에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달을 적어도 20% 증가시키는, ABPC.
구현예 124. 구현예 123에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달을 적어도 50% 증가시키는, ABPC.
구현예 125. 구현예 122에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달을 적어도 2배 증가시키는, ABPC.
구현예 126. 구현예 125에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달을 적어도 5배 증가시키는, ABPC.
구현예 127. 구현예 96 내지 126 중 어느 하나에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포의 표면 상에 제시된 MET 수준을 덜 감소시키는, ABPC.
구현예 128. 구현예 96 내지 126 중 어느 하나에 있어서, ABPC를 포함하는 조성물은 표적 포유류 세포의 표면 상에 제시된 MET 수준을 검출 가능하게 감소시키지 않는, ABPC.
구현예 129. 표적 포유류 세포의 표면 상에 제시된 MET 또는 MET의 에피토프에 특이적으로 결합할 수 있는 제1 항원 결합 도메인; 및 접합된 독소, 방사성 동위원소, 약물, 또는 소분자를 포함하는 항원 결합 단백질 작제물(ABPC)로서, (a) 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인의 해리 속도는 약 7.0 내지 약 8.0의 pH에서의 해리 속도보다 빠르거나; 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인의 해리 상수(KD)는 약 7.0 내지 약 8.0의 pH에서의 KD보다 더 크며; (b) 조성물은 다음 중 하나 이상을 가능하게 하는, ABPC: 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때, 표적 포유류 세포에서 독소 유리를 증가시키는 것; 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때, 표적 포유류 세포 사멸을 증가시키는 것; 및 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때, 표적 포유류 세포에서의 엔도리소좀 전달을 증가시키는 것.
구현예 130. 구현예 129에 있어서, 제1 항원 결합 도메인은 하나 이상의 아미노산이 히스티딘으로 치환된 텔리소투주맙의 중쇄 가변 도메인을 포함하는, ABPC.
구현예 131. 구현예 129에 있어서, 제1 항원 결합 도메인은 하나 이상의 아미노산이 히스티딘으로 치환된 텔리소투주맙의 경쇄 가변 도메인을 포함하는, ABPC.
구현예 132. 구현예 129에 있어서, 제1 항원 결합 도메인은 하나 이상의 아미노산이 히스티딘으로 치환된 텔리소투주맙의 중쇄 가변 도메인; 및 하나 이상의 아미노산이 히스티딘으로 치환된 텔리소투주맙의 경쇄 가변 도메인을 포함하는, ABPC.
구현예 133. 구현예 130 또는 132에 있어서, 텔리소투주맙의 중쇄 가변 도메인은 서열번호 1을 포함하는, ABPC.
구현예 134. 구현예 131 또는 132에 있어서, 텔리소투주맙의 경쇄 가변 도메인은 서열번호 2를 포함하는, ABPC.
구현예 135. 구현예 129에 있어서, 제1 항원 결합 도메인은, 서열번호 3~5의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인으로서, 서열번호 3~5 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된 중쇄 가변 도메인을 포함하는, ABPC.
구현예 136. 구현예 129에 있어서, 제1 MET 결합 도메인은, 서열번호 6~8의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인으로서, 서열번호 6~8 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된 경쇄 가변 도메인을 포함하는, ABPC.
구현예 137. 구현예 129에 있어서, 제1 MET-결합 도메인은: 서열번호 3~5의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인으로서, 서열번호 3~5 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된 중쇄 가변 도메인; 및 서열번호 6~8의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인으로서, 서열번호 6~8 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된 경쇄 가변 도메인을 포함하는, ABPC.
구현예 138. 구현예 129, 130, 또는 135에 있어서, 제1 항원 결합 도메인은, 서열번호 1과 적어도 90% 동일한 중쇄 가변 도메인으로서 26, 27, 28, 29, 32, 97, 98, 99, 100, 101, 102, 103, 및 107로 이루어진 군으로부터 선택된 서열번호 1 내 하나 이상의 위치에서 히스티딘을 포함하는 중쇄 가변 도메인을 포함하는, ABPC.
구현예 139. 구현예 129, 131, 또는 136에 있어서, 제1 항원 결합 도메인은, 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서 서열번호 2 내 하나 이상의 위치에서 히스티딘을 포함하는 경쇄 가변 도메인을 포함하는, ABPC.
구현예 140. 구현예 129, 132, 또는 137에 있어서, 제1 항원 결합 도메인은 다음을 포함하는, ABPC: 서열번호 1과 적어도 90% 동일한 중쇄 가변 도메인으로서, 26, 27, 28, 29, 32, 97, 98, 99, 100, 101, 102, 103, 및 107로 이루어진 군으로부터 선택된 서열번호 1 내 하나 이상의 위치에서 히스티딘을 포함하는 중쇄 가변 도메인; 및 서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 서열번호 2 내 하나 이상의 위치에서 히스티딘을 포함하는 경쇄 가변 도메인.
구현예 141. 구현예 129에 있어서, 제1 항원 결합 도메인은 서열번호 13, 14, 15, 16, 19, 40, 41, 42, 43, 44, 45, 46, 또는 50의 중쇄 가변 도메인을 포함하는, ABPC.
구현예 142. 구현예 141에 있어서, 제1 항원 결합 도메인은 서열번호 2의 경쇄 가변 도메인을 포함하는, ABPC.
구현예 143. 구현예 129 내지 142 중 어느 하나에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리를 증가시키는, ABPC.
구현예 144. 구현예 143에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리를 적어도 20% 증가시키는, ABPC.
구현예 145. 구현예 144에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리를 적어도 50% 증가시키는, ABPC.
구현예 146. 구현예 143에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리를 적어도 2배 증가시키는, ABPC.
구현예 147. 구현예 146에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리를 적어도 5배 증가시키는, ABPC.
구현예 148. 구현예 129 내지 147 중 어느 하나에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포 살해를 증가시키는, ABPC.
구현예 149. 구현예 148에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포 살해를 적어도 20% 증가시키는, ABPC.
구현예 150. 구현예 149에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포 살해를 적어도 50% 증가시키는, ABPC.
구현예 151. 구현예 148에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포 살해를 적어도 2배 증가시키는, ABPC.
구현예 152. 구현예 151에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포 살해를 적어도 5배 증가시키는, ABPC.
구현예 153. 구현예 129 내지 152 중 어느 하나에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달을 증가시키는, ABPC.
구현예 154. 구현예 153에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달을 적어도 20% 증가시키는, ABPC.
구현예 155. 구현예 154에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달을 적어도 50% 증가시키는, ABPC.
구현예 156. 구현예 153에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달을 적어도 2배 증가시키는, ABPC.
구현예 157. 구현예 156에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달을 적어도 5배 증가시키는, ABPC.
구현예 158. 구현예 129 내지 157 중 어느 하나에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포의 표면 상에 제시된 MET 수준을 덜 감소시키는, ABPC.
구현예 159. 구현예 129 내지 157 중 어느 하나에 있어서, ABPC를 포함하는 조성물은 표적 포유류 세포의 표면 상에 제시된 MET 수준을 검출 가능하게 감소시키지 않는, ABPC.
구현예 160. 구현예 96 내지 159 중 어느 하나에 있어서, 표적 포유류 세포는 암 세포인, ABPC.
구현예 161. 구현예 96 내지 160 중 어느 하나에 있어서, 약 4.0 내지 약 6.5의 pH에서 항원 결합 도메인의 해리 속도는 약 7.0 내지 약 8.0의 pH에서 항원 결합 도메인의 해리 속도보다 적어도 10% 더 빠른, ABPC.
구현예 162. 구현예 96 내지 160 중 어느 하나에 있어서, 약 4.0 내지 약 6.5의 pH에서 항원 결합 도메인의 해리 속도는 약 7.0 내지 약 8.0의 pH에서 항원 결합 도메인의 해리 속도보다 적어도 3배 더 빠른, ABPC.
구현예 163. 구현예 96 내지 160 중 어느 하나에 있어서, 약 4.0 내지 약 6.5의 pH에서 항원 결합 도메인의 해리 속도는 약 7.0 내지 약 8.0의 pH에서 항원 결합 도메인의 해리 속도보다 적어도 10배 더 빠른, ABPC.
구현예 164. 구현예 96 내지 163 중 어느 하나에 있어서, 약 4.0 내지 약 6.5의 pH에서 항원 결합 도메인의 KD는 약 7.0 내지 약 8.0의 pH에서 항원 결합 도메인의 KD보다 적어도 10% 더 큰, ABPC.
구현예 165. 구현예 96 내지 163 중 어느 하나에 있어서, 약 4.0 내지 약 6.5의 pH에서 항원 결합 도메인의 KD는 약 7.0 내지 약 8.0의 pH에서 항원 결합 도메인의 KD보다 적어도 3배 더 큰, ABPC.
구현예 166. 구현예 96 내지 163 중 어느 하나에 있어서, 약 4.0 내지 약 6.5의 pH에서 항원 결합 도메인의 KD는 약 7.0 내지 약 8.0의 pH에서 항원 결합 도메인의 KD보다 적어도 10배 더 큰, ABPC.
구현예 167. 구현예 96 내지 166 중 어느 하나에 있어서, ABPC는 표적 포유류 세포에 대해 세포독성이거나 세포증식 억제성인, ABPC.
구현예 168. 구현예 96 내지 167 중 어느 하나에 있어서, ABPC는 비인간 영장류 MET 및 인간 MET와 교차 반응성인, ABPC.
구현예 169. 구현예 96 내지 167 중 어느 하나에 있어서, ABPC는 비인간 영장류 MET, 인간 MET, 및 랫트 MET와 마우스 MET 중 하나 또는 둘 다와 교차 반응성인, 약학적 조성물.
구현예 170. 구현예 169에 있어서, ABPC는 비인간 영장류 MET, 인간 MET, 랫트 MET, 및 마우스 MET와 교차 반응성인, 약학적 조성물.
구현예 171. 구현예 96 내지 170 중 어느 하나에 있어서, 항원 결합 도메인은 구세계 원숭이에서 유래된 세포의 표면 상에 존재하는 MET의 에피토프에 결합하는, ABPC.
구현예 172. 구현예 96 내지 171 중 어느 하나에 있어서, ABPC는 단일 폴리펩티드를 포함하는, ABPC.
구현예 173. 구현예 172에 있어서, 항원 결합 도메인은 VH 도메인, VHH 도메인, VNAR 도메인, 및 scFv로 이루어진 군으로부터 선택되는, ABPC.
구현예 174. 구현예 172 또는 173에 있어서, ABPC는 BiTe, (scFv)2, 나노바디, 나노바디-HSA, DART, TandAb, scDiabody, scDiabody-CH3, scFv-CH-CL-scFv, a HSAbody, scDiabody-HSA, 또는 탠덤-scFv인, ABPC.
구현예 175. 구현예 96 내지 171 중 어느 하나에 있어서, ABPC는 2개 이상의 폴리펩티드를 포함하는, ABPC.
구현예 176. 구현예 175에 있어서, ABPC는 항체, VHH-scAb, VHH-Fab, 이중 scFab, F(ab')2, 디아바디, crossMab, DAF (투-인-원), DAF (포-인-원), DutaMab, DT-IgG, 놉-인-홀 공통 경쇄, 놉-인-홀 조립체, 전하쌍, Fab-아암 교환, SEEDbody, LUZ-Y, Fcab, κλ-body, 직교 Fab, DVD-IgG, IgG(H)-scFv, scFv-(H)IgG, IgG(L)-scFv, scFv-(L)IgG, IgG(L,H)-Fv, IgG(H)-V, V(H)-IgG, IgG(L)-V, V(L)-IgG, KIH IgG-scFab, 2scFv-IgG, IgG-2scFv, scFv4-Ig, Zybody, DVI-IgG, 디아바디-CH3, 트리플바디, 미니항체, 미니바디, TriBi 미니바디, scFv-CH3 KIH, Fab-scFv, F(ab')2-scFv2, scFv-KIH, Fab-scFv-Fc, 4가 HCAb, scDiabody-Fc, 디아바디-Fc, 탠덤 scFv-Fc, VHH-Fc, 탠덤 VHH-Fc, VHH-Fc KiH, Fab-VHH-Fc, 인트라바디, 독-앤-락, ImmTAC, IgG-IgG 접합체, Cov-X-Body, scFv1-PEG-scFv2, 애드넥티, DARPin, 피브로넥티, 및 DEP 접합체의 군으로부터 선택되는, ABPC.
구현예 177. 구현예 111 내지 176 중 어느 하나에 있어서, ABPC의 적어도 하나의 폴리펩티드는 절단성 링커를 통해 독소, 방사성 동위원소, 약물, 또는 소분자에 접합되는, ABPC.
구현예 178. 구현예 111 내지 176 중 어느 하나에 있어서, ABPC의 적어도 하나의 폴리펩티드는 비절단성 링커를 통해 독소, 방사성 동위원소, 약물, 또는 소분자에 접합되는, ABPC.
구현예 179. 구현예 96 내지 178 중 어느 하나에 있어서, ABPC의 생체 내 반감기는 대조군 ABPC의 생체 내 반감기와 비교했을 때 감소되는, ABPC.
구현예 180. 구현예 179에 있어서, ABPC의 생체 내 반감기는 대조군 ABPC의 생체 내 반감기와 비교했을 때 약 5% 내지 약 95% 감소되는, ABPC.
구현예 181. 구현예 179에 있어서, ABPC의 생체 내 반감기는 대조군 ABPC의 생체 내 반감기와 비교했을 때 약 10% 내지 약 95% 감소되는, ABPC.
구현예 182. 구현예 179에 있어서, ABPC의 생체 내 반감기는 대조군 ABPC의 생체 내 반감기와 비교했을 때 약 30% 내지 약 95% 감소되는, ABPC.
구현예 183. 구현예 179에 있어서, ABPC의 생체 내 반감기는 대조군 ABPC의 생체 내 반감기와 비교했을 때 약 50% 내지 약 95% 감소되는, ABPC.
구현예 184. 구현예 179에 있어서, ABPC의 생체 내 반감기는 대조군 ABPC의 생체 내 반감기와 비교했을 때 약 70% 내지 약 95% 감소되는, ABPC.
구현예 185. 구현예 112 내지 184 중 어느 하나에 있어서, 대조군 ABPC는 표적 포유류 세포의 표면 상에 제시된 MET 또는 MET의 에피토프에 특이적으로 결합할 수 있고, 여기서 (a) 대조군 ABPC는 제1 항원 결합 도메인을 포함하고; (b) 약 4.0 내지 약 6.5의 pH에서 대조군 ABPC의 제1 항원 결합 도메인의 해리 속도는 약 7.0 내지 8.0의 pH에서의 해리 속도보다 3배 이하로 더 빠르고; (c) 약 4.0 내지 약 6.5의 pH에서 대조군 ABPC의 제1 항원 결합 도메인의 해리 상수(KD)는 약 7.0 내지 약 8.0의 pH에서의 KD보다 3배 이하로 더 큰, ABPC.
구현예 186. 구현예 112 내지 184 중 어느 하나에 있어서, 대조군 ABPC는 표적 포유류 세포의 표면 상에 제시된 MET 또는 MET의 에피토프에 특이적으로 결합할 수 있고, 여기서 (a) 대조군 ABPC는 제1 항원 결합 도메인을 포함하고; (b) 약 4.0 내지 약 6.5의 pH에서 대조군 ABPC의 제1 항원 결합 도메인의 해리 속도는 약 7.0 내지 8.0의 pH에서의 해리 속도보다 2배 이하로 더 빠르고; (c) 약 4.0 내지 약 6.5의 pH에서 ABPC의 제1 항원 결합 도메인의 해리 상수(KD)는 약 7.0 내지 약 8.0의 pH에서의 KD보다 2배 이하로 더 큰, ABPC.
구현예 187. 구현예 112 내지 184 중 어느 하나에 있어서, 대조군 ABPC는 표적 포유류 세포의 표면 상에 제시된 MET 또는 MET의 에피토프에 특이적으로 결합할 수 있고, 여기서 (a) 대조군 ABPC는 제1 항원 결합 도메인을 포함하고; (b) 약 4.0 내지 약 6.5의 pH에서 대조군 ABPC의 제1 항원 결합 도메인의 해리 속도는 약 7.0 내지 8.0의 pH에서의 해리 속도보다 1배 이하로 더 빠르고; (c) 약 4.0 내지 약 6.5의 pH에서 대조군 ABPC의 제1 항원 결합 도메인의 해리 상수(KD)는 약 7.0 내지 약 8.0의 pH에서의 KD보다 1배 이하로 더 큰, ABPC.
구현예 188. 구현예 112 내지 184 중 어느 하나에 있어서, 대조군 ABPC는 텔리소투주맙인, ABPC.
구현예 189. 구현예 96 내지 188 중 어느 하나에 있어서, ABPC는 제2 항원 결합 도메인을 추가로 포함하는, ABPC.
구현예 190. 구현예 96 내지 189 중 어느 하나의 ABPC의 적어도 1회 투여량을 포함하는 키트.
구현예 191. 암을 치료하는 방법으로서, 암은 MET 또는 MET의 에피토프가 표면에 제시된 암 세포의 집단을 갖는 것을 특징으로 하고, 상기 방법은 상기 암 세포의 집단을 갖는 것을 특징으로 하는 암에 걸린 것으로 식별된 대상체에게 구현예 1 내지 94 중 어느 하나의 약학적 조성물 또는 96 내지 189 중 어느 하나의 ABPC의 하나의 치료적 유효량을 투여하는 단계를 포함하는, 방법.
구현예 192. 대상체에서 종양 부피를 감소시키는 방법으로서, 종양은 MET 또는 MET의 에피토프가 표면에 제시된 암 세포의 집단을 갖는 것을 특징으로 하고, 상기 방법은 상기 암 세포의 집단을 갖는 것을 특징으로 하는 암에 걸린 것으로 식별된 대상체에게 구현예 1 내지 94 중 어느 하나의 약학적 조성물 또는 96 내지 189 중 어느 하나의 ABPC의 하나의 치료적 유효량을 투여하는 단계를 포함하는, 방법.
구현예 193. 대상체에서 암 세포의 세포 사멸을 유도하는 방법으로서, 암 세포는 MET 또는 MET의 에피토프가 표면에 제시된 암 세포의 집단을 갖고, 상기 방법은 상기 암 세포의 집단을 갖는 것을 특징으로 하는 암에 걸린 것으로 식별된 대상체에게 구현예 1 내지 94 중 어느 하나의 약학적 조성물 또는 96 내지 189 중 어느 하나의 ABPC의 하나의 치료적 유효량을 투여하는 단계를 포함하는, 방법.
구현예 194. 구현예 191 내지 193 중 어느 하나에 있어서, 암은 원발성 종양인, 방법.
구현예 195. 구현예 191 내지 193 중 어느 하나에 있어서, 암은 전이인, 방법.
구현예 196. 구현예 191 내지 195 중 어느 하나에 있어서, 암은 비-T 세포 침윤성 종양인, 방법.
구현예 197. 구현예 191 내지 195 중 어느 하나에 있어서, 암은 T 세포 침윤성 종양인, 방법.
구현예 198. 암에 걸린 대상체에서 전이가 발생할 위험을 감소시키는 방법 또는 추가의 전이가 발생할 위험을 감소시키는 방법으로서, 암은 MET 또는 MET의 에피토프가 표면에 제시된 암 세포의 집단을 갖는 것을 특징으로 하고, 상기 방법은 상기 암 세포의 집단을 갖는 것을 특징으로 하는 암에 걸린 것으로 식별된 대상체에게 구현예 1 내지 94 중 어느 하나의 약학적 조성물 또는 구현예 96 내지 189 중 어느 하나의 ABPC의 치료적 유효량을 투여하는 단계를 포함하는, 방법.
구현예 199. 구현예 198에 있어서, 암은 비-T 세포 침윤성 종양인, 방법.
구현예 200. 구현예 198에 있어서, 암은 T 세포 침윤성 종양인, 방법.
본 발명은 하기 실시예에서 추가로 기술되며, 하기 실시예는 청구범위에 기술된 본 발명의 범주를 제한하지 않는다.
실시예
실시예 1. MET 결합제의 생성 및 pH 결합 의존성의 조작
MET에 특이적인 pH-조작된 ABPC는 2가지 방법을 사용하여 생성된다. 제1 접근법에서, MET에 대한 pH-의존적 결합을 조작할 수 있게하고, i) 접합된 독소의 엔도리소좀 출적을 향상시킬 뿐 아니라 ii) 세포 표면에 대해 MET 재순환을 향상시킬 수 있는 추가 돌연변이를 도입하기 위한 출발 템플릿으로서 MET에 대한 공개된 단클론 항체를 사용한다. 제2 접근법은, 항체 디스플레이 방법을 통해 MET에 특이적인 새로운(de novo) ABPC를 미접촉 라이브러리 또는 CDR 조성이 정의된 라이브러리로부터 발견하는 단계; 및 MET에 특이적인 pH-조작된 ABPC를 선택하도록 설계된 조건 하에 이를 스크리닝하는 단계를 포함한다. 어느 경우든, 히스티딘 잔기는 pH 의존적 결합 단백질을 조작하는 데 중요한 역할을 한다.
히스티딘 잔기의 pKa가 6.0이므로, 히스티딘 잔기는 6.5 미만의 pH에서 적어도 부분적으로 양성자화된다. 따라서, 항원 결합 도메인 내의 히스티딘 측쇄가 그의 항원과의 정전기 결합 상호작용에 참여하는 경우, 히스티딘 측쇄는 6.5 이하의 pH에서 양으로 하전되기 시작할 것이다. 이는 항원 에피토프의 상응하는 전하와 항원 에피토프와의 상호작용에 기초하여, 6.5 미만의 pH에서 상호작용의 결합 친화도를 약화시키거나 강화시킬 수 있다. 따라서, 항체 또는 다른 결합제 라이브러리(예를 들어, scFv 라이브러리) 내의 항체 상보성 결정 영역(CDR) 내로 히스티딘을 체계적으로 도입하여, 더 낮은 pH 값에서 항원 결합 도메인과 항원의 상호작용에 영향을 미칠 치환을 식별할 수 있다. 따라서, 제1 접근법은 공개된 단클론 항체의 가변 영역 서열을 히스티딘 스캐닝하여 pH-의존적 변이체를 식별하는 단계를 포함한다.
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있고, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용될 수 있다[Wang J 등의 (2017) ABBV-399, a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors, Irrespective of MET Pathway Dependence, Clin Cancer Res, 23:992-1000]. 간략하게, 항체 서열의 하위 집합에 대해, Kabat 등에 의해 기술된 방법(Kabat 등의 (1992) Sequences of Proteins of Immunological Interest (DIANE publishing) 및 IMGT (Lefranc MP (1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 각 사슬 내 CDR을 식별하고, 각각의 CDR에 대해, Kabat 및 IMGT CDR 정의 중 하나 또는 둘 다에 해당하는 잔기를 CDR 잔기로 명명한다. pH-의존적 서열 변이체를 식별하기 위해, 중쇄 및/또는 경쇄 CDR 내의 개별 아미노산 잔기를 한 번에 하나씩 히스티딘으로 체계적으로 치환한다. 출발 CDR 잔기가 히스티딘인 경우, 이는 알라닌으로 돌연변이시킨다. 당업계에 알려져 있는 방법을 사용해 각각 a) 하나의 중쇄 또는 경쇄 서열 변이체, 및 b) 상응하는 출발 ABPC(예를 들어 출발 MET-결합 단클론 항체) 경쇄 또는 중쇄로 Expi293 세포를 공동으로 형질감염시켜 중쇄/경쇄 CDR에서 히스티딘 또는 알라닌 하나만을 갖는 항체 변이체를 생성한다. 단백질이 발현되도록 일정 기간 방치한 후, 세포 배양 상청액을 수집하고, 정량화하고, 바이오층 간섭계(BLI) 또는 당업계에 공지된 다른 방법을 사용하여 변이체의 pH 의존성을 평가한다. 간략하게, 세포 배양 상청액을 50 μg/mL의 항체 발현 수준에 대해 정규화하고, 항-인간 Fc 센서(Forte Bio) 상에 포획한다. 1X 동역학 완충액(Forte Bio)을 사용하여 베이스라인을 확립하고, 센서를 동안 pH 7.4의 1X PBS 중 100 nM의 MET와 300초 동안 결합시켜 결합 곡선을 생성한다. 해리 단계에서, 센서 상의 항체-항원 복합체를 pH 5.5 또는 pH 7.4에서 1X PBS에 300 내지 500초 동안 노출시킨다. pH 5.5 및 pH 7.4에서 출발 ABPC 항체 및 각각의 상응하는 항체 변이체에 대해 결합 및 해리 단계 곡선을 조사하여 2가지 기준을 알아낸다: a) 출발 ABPC과 비교했을 때, 히스티딘 또는 알라닌 치환으로 인해 pH 5.5에서 해리가 강화됨(즉, koff 값이 더 높아짐), 및 b) pH 5.5와 비교했을 때 pH 7.4에서 항체 변이체 자체 및 항체 변이체와 출발 ABPC의 해리가 감소함(즉, koff 값이 더 낮아짐). pH 5.5에서 강화된 해리를 나타내거나 pH 7.4에서 감소된 해리를 나타내거나 둘 다에 해당하는 변이체를 추가 분석을 위해 선택하였다. 또한, 일부 히스티딘 및 알라닌 돌연변이는 MET 결합을 제거하는 반면, 다른 돌연변이는 MET 결합 동역학을 거의 변화시키지 않거나 (예를 들어 KD 또는 해리 속도에 있어서 1배 미만의 변화) 전혀 변화시키지 않음을 주목한다. 특히, 히스티딘은 크고 양으로 하전된 아미노산이기 때문에, 변화가 없는 이들 히스티딘 변이체 및 알라닌 변이체는 광범위한 돌연변이를 견딜 수 있고, 서열은 상이하지만 유사한 결합 특성을 갖는 항체로 유도할 수 있는 위치로서 (명칭은 달리 명백하지 않음) 주목한다. 추가 분석을 위해 선택된 변이체는 더 큰 규모로 발현되고 단백질 A 친화도 크로마토그래피를 사용하여 정제된다. 정제된 출발 ABPC 및 변이체 항체의 결합 동역학(kon 및 koff)을 Biacore(GE Healthcare)를 사용하여 pH 5.5 및 pH 7.4에서 측정한다. 항체의 해리 속도 비율(pH 7.4에서의 koff를 pH 5.5에서의 koff로 나눈 것) 또한 pH-의존적 결합의 정량적 평가로서 사용하고; 유사하게, pH 5.5 및 pH 7.4 모두에서 해리 상수 KD(koff를 kon으로 나눈 것)를 계산하고, 항체의 해리 상수 비율(pH 7.4에서의 KD를 pH 5.5에서의 KD로 나눈 것) 또한 정량적 평가로서 사용한다. 조합적 치환의 추가 평가를 위해, 해리 속도 비율이 출발 ABPC의 해리 속도 비율보다 낮고/낮거나 해리 상수 비율이 출발 ABPC의 해리 상수 비율보다 낮은 항체를 선택한다. 유리한 히스티딘 및/또는 알라닌 아미노산 위치를 조합하여 pH 의존성을 강화시킬 수도 있는데; 이는, 예를 들어 중쇄 또는 경쇄 상에서 pH 의존성을 개별적으로 개선하는 히스티딘 및/또는 알라닌 치환을 조합적으로 또는 합리적으로 조합함으로써, 또는 예를 들어 히스티딘 및/또는 알라닌 치환이 중쇄 및 경쇄 모두에 존재하도록 변형된 중쇄 및 경쇄를 조합적으로 합리적으로 조합함으로써, 또는 이들의 조합에 의해 이루어질 수 있다. 본원에 기술된 방법과 프로토콜, 또는 당업계에 알려진 다른 방법과 프로토콜을 사용해 이러한 조합 변이체를 생성하고 상이한 pH 의존성에 대해 시험/분석한다. 해리 속도 비율 및/또는 해리 상수 비율이 가장 낮은 항체 변이체는 추가 분석을 위한 후보로서 선택한다(이하 "MET에 특이적인 pH-조작된 ABPC"로 지칭됨).
MET에 특이적인 pH-조작된 ABPC를 선택하기 위한 제2 방법은 라이브러리를 스캐닝하여 MET에 특이적인 새로운 pH-의존적 ABPC를 식별하거나, 본원에 기술된 것과 같이 pH-의존적 결합을 조작하기 위한 템플릿의 역할을 할 수 있는 ABPC를 식별하는 것을 포함한다. 이들 선택에는 2가지 유형의 라이브러리가 사용될 수 있다: 미접촉 파지/효모 디스플레이 항체 라이브러리(예를 들어, Fab, scFv, VH, VL, 또는 당업계에 공지된 다른 것) 또는 CDR이 아미노산 잔기의 하위 집합을 발현하도록 돌연변이된 파지/효모 디스플레이 라이브러리. 라이브러리는, pH 5.0에서 약하게 결합하고(예를 들어, 비드로부터 용리되고) pH 7.4에서 강력하게 결합하는(예를 들어, 비드에 결합되는) 변이체에 대한 양성 선별과 더불어, 당업계에 공지된 방법을 사용하여 가용성 재조합 MET 세포외 도메인에 대해 스크리닝된다. 3회의 선택을 수행한다. 최종 회차에서는, ELISA를 사용하거나 유세포 분석에서의 평균 형광 강도를 통해 인간 MET 및 cyno MET 및 마우스 MET에 대한 결합에 대해 결합제를 스크리닝한다. cyno 또는 쥣과에 대해 교차 반응성인 더 많은 결합제가 필요한 경우, 대신에 cyno MET 또는 쥣과 MET에 대한 최종 선택 회차를 수행할 수 있다. 선택된 결합 단백질은 포유류 발현 벡터로 서브클로닝하고, Expi293 세포에서 전체 IgG 단백질 또는 Fc 융합체로서 발현시킨다. pH-의존적 결합제 변이체의 선택을 위해 본원에 기술된 바와 같이 BLI 분석을 수행하고, Biacore를 사용해 확인한다.
실시예 2. MET에 특이적인 대조군 ABPC와 비교했을 때, MET에 특이적인 pH-조작된 APBC에 노출시킨 후 MET에 대한 pH-의존적 결합, MET의 pH-의존적 방출, MET+ 세포에서 엔도리소좀 전달 강화, 및 MET+ 세포에서 MET 항원 밀도 증가의 시험관 내 입증.
본원에서 논의된 바와 같이, MET에 특이적인 pH-조작된 ABPC는 산성 pH(예: pH 5.0, pH 5.5)에서 MET 결합이 감소하는 바람직한 특성을 나타내지만, 더 높은 pH(예: pH 7.4)에서는 결합이 강화되는데, 이는 생리학적 조건 하에 엔돌리소좀에서 이들의 축적을 강화시킨다.
세포 상의 MET에 대한 pH-의존적 결합
MET에 특이적인 pH-조작된 ABPC가 중성 pH에서 세포 표면 MET에 결합함을 입증하기 위해, 세포 표면 결합 검정을 수행한다. MET+인 인간 세포의 패널을 조립된다(예를 들어, Hs 746T ATCC Cat#HTB-135, NCI-H441 ATCC Cat#HTB-174, NCI-H820 ATCC Cat#HTB-181). 주어진 세포주에 대해 유전자 발현(예: MET)을 식별하고 정량화하는 방법은 당업계에 공지되어 있으며, 예를 들어 암 세포주 백과사전(CCLE; https://portals.broadinstitute.org/ccle)를 참고하여 종양 세포주에서 주어진 유전자의 발현 수준 및/또는 돌연변이 상태, rtPCR, 마이크로어레이를 확인하거나, RNA-Seq를 분석하는 것, 또는 당업계에 알려진 항체(예: 텔리소투주맙 또는 Cell Signaling Technology Met Met (D1C2) XP 토끼 mAb Cat#8198, 또는 R&D Systems의 MET용 인간 HGFR/c-MET 항체 클론 #95106 Cat#MAB3582)로 세포를 염색하는 것을 포함한다. 150 μL의 pH 7.4 배양 배지에 웰 당 대략 5~10,000개씩 세포를 시딩하고 다음 항체 중 하나와 함께 1 pM 내지 1 μM의 여러 가지 투여량으로 (예를 들어 2배 연속 희석물로) 37℃에서 5분 동안 인큐베이션한다: MET에 특이적인 알려진 대조 ABPC(예: 항체, 텔리소투주맙, 에미베투주맙, hucMET27Gv1.3, 또는 P3D12), MET에 특이적인 pH-조작된 ABPC, 및 적절한 음성 이소형 대조군 mAb(예를 들어, Biolegend 정제된 인간 IgG1 이소형 대조군 재조합 항체, Cat#403501). 실험을 개시하기 전에, 당업계에 알려진 방법을 사용해 모든 항체의 결합 특성을 검증한다. 5분의 인큐베이션 후, 세포를 4% 포름알데히드로 고정시키고(실온에서 20분), 적절한 형광단-표지된 2차 항체(예: ThermoFisher 마우스 항-인간 IgG1 Fc 2차 항체, Alexa Fluor 488, Cat#A-10631)와 함께 60분 동안 인큐베이션한다. 미결합 시약을 일련의 PBS 세척으로 세척하고, 공초점 현미경을 사용해 세포 패널을 영상화한다. 이미지 분석 시, MET에 특이적인 알려진 대조군 ABPC를 비롯하여 MET에 특이적인 pH-조작된 ABPC가 결합된 세포의 표면 상에서 상당한 형광이 관찰될 수 있지만, 이소형 음성 대조군에 대해서는 표면 결합이 거의 관찰되지 않을 수 있다. 표면 결합에 미치는 pH의 효과를 단리하기 위해, 동일한 실험을 2회 반복하고, 1차 항체 인큐베이션은 pH를 낮추면서 순차적으로 수행한다(예를 들어 pH 6.5 및 5.5 및 5.0). 생성된 공초점 현미경 이미지의 분석은, 이소형 음성 대조군을 제외하고는 시험된 모든 mAb와 결합된 세포의 표면에서 유의한 형광을 나타낼 수 있으며, 이러한 형광은 MET에 특이적인 pH-조작된 ABPC의 경우 pH가 감소함에 따라 감소한다. 대안적으로, 당업계에 공지된 방법을 사용하여 유세포 계측법에 의해 평균 형광 강도에 대해 세포를 분석한다. 분석된 항체의 중성 pH에서 세포 상의 해리 상수 KD는 당업계에 공지된 비선형 회귀 방법(예를 들어, 스캐차트 플롯(Scatchard plot))에 의해 결정한다. 종합하면, 결과는 pH-조작 방법을 통해 결합 특성이 pH-의존적이고 더 산성인 pH에 비해 중성의 pH에서 보다 효과적으로 결합하는, MET에 특이적인 pH-조작된 ABPC를 생성할 수 있음을 보여준다. MET에 특이적인 pH-조작된 ABPC의 pH 의존성을 평가하는 다른 방법은 당업계에 공지되어 있으며, 예를 들어, 유세포 계측법을 사용해 ABPC 표면 결합을 측정하는 것을 포함한다.
세포 상의 MET의 pH 의존적 방출
MET에 특이적인 pH-조작된 ABPC가 중성 pH에서 결합 후 낮은 pH에서 MET를 방출할 수 있다는 것을 입증하기 위해, 당업계에 알려진 (예를 들어, Gera N.의 문헌[(2012) PLoS ONE 7(11): e48928]에 일반적으로 기술된 것과 같은) 방법을 사용해 변이체에 대한 전술한 세포 표면 결합 검정을 수행한다. 간략하게, 적절한 MET+ 세포주(25 미만의 계대 수)를 수확하고, 둥근 바닥 96-웰 마이크로플레이트 내에 웰 당 50,000개의 세포를 도말한다. 3가지 조건, 즉 pH 7.4에서의 결합 및 이차 염색; pH 5.0에서의 결합 및 이차 염색; 및 pH 7.4에서의 결합 후 pH 5.0에서 30분 동안 방출 및 pH 7.4에서의 이차 염색을 시험한다. MET에 특이적인 pH-조작된 ABPC를 비롯하여 MET에 특이적인 대조군 ABPC 둘 다를 시험한다. 시험 중인 조건에 따라, pH 7.4 또는 5.0에서 200 μL의 FACS 완충액(3% 소 태아 혈청을 함유하는 1x PBS)으로 세포를 2회 세척한다. 정제된 단백질 샘플을 적절한 pH의 FACS 완충액에 희석하여 세포에 첨가하고 얼음 위에서 1시간 동안 결합시킨다. 1차 항체와 함께 인큐베이션한 후, pH 7.4 및 pH 5.0 조건을 전처럼 2회 세척한 다음, 100 μl의 2차 랫트 항-인간 Fc AF488(BioLegend 410706) 또는 1:50으로 희석시킨 다른 적절한 항체, 또는 1:50으로 희석시킨 항 Myc-Tag 마우스 mAb-AF488(Cell Signaling Technologies 2279S)을 적절한 pH의 FACS 완충액에 첨가하고, 얼음 위에서 30분 동안 인큐베이션한다. pH 5.0 방출 조건을 FACS 완충액 pH 7.4로 2회 세척한 다음, 100 μl의 FACS 완충액 pH 5.0에 재현탁하고, 얼음에서 30분 동안 인큐베이션한 다음, 다른 조건에 대해 기술된 바와 같이 FACS 완충액 pH 7.4에서 2차 염색을 수행한다. 플레이트를 이전과 같이 2회 세척하고, 적절한 FACS 완충액 중의 1% 파라포름알데히드에 재현탁하여 유세포 계측 분석을 위해 고정시킨다. 모든 조건은 유세포 계측기(Accuri C6, BD Biosciences)를 이용해 판독한다. 결합은 2차 단독 대비 (평균 형광 강도로서) FLl 신호의 이동으로서 관찰한다. 데이터 분석 시, MET에 특이적인 pH-조작된 ABPC와 MET에 특이적인 대조군 ABPC는 중성 pH에서 MET+ 세포의 표면에 효과적으로 결합하지만, MET에 특이적인 pH-조작된 ABPC는 pH 5.0에서 잘 결합하지 못하는 것으로 결정할 수 있고; 유사하게, MET에 특이적인 pH-조작된 ABPC는 pH 7.4에서 효과적으로 결합하지만, 이어서 pH 5.0에서 MET를 방출하거나/미결합 상태가 되는 것으로 결정할 수 있다.
MET+ 세포에서, MET에 특이적인 대조군 ABPC(pHrodo)와 비교했을 때 MET에 특이적인 pH 조작된 ABPC의 엔도리소좀 전달 강화
MET에 특이적인 ABPC가 세포에 흡수된 후 엔도리소좀 국소화를 달성한다는 것을 확인하고 입증하기 위해, 당업계에 알려진 방법(예: Mahmutefendic 등의 문헌[Int. J. Biochem. Cell Bio., 2011])을 사용해 내재화 검정을 수행한다. 간략하게, 본원에 기술된 바와 같이, MET를 고도로 발현하는 인간 세포의 패널을 당업계에 알려진 방법을 사용해 조립한다. 세포를 도말하고, PBS로 3회 세척하고, 2 μg/mL 농도의 (예를 들어 본원에 기술된 것과 같은) MET에 특이적인 알려진 대조군 ABPC, MET에 특이적인 pH-조작된 ABPC, 및 (예를 들어 본원에 기술된 것과 같은) 적절한 음성 이소형 대조군 mAb를 첨가한 다음 중성 pH의 배지에서 60분 동안 37℃에서 인큐베이션한다. 세포의 하위 집합에서, 항체 내재화 및 엔도솜 국소화의 검증은 당업계에 공지된 방법을 사용하여 수행하는데; 예를 들어, 세포를 본원에 기술된 바와 같이 4% 포름알데히드에 고정시키고, TWEEN 20 또는 당업계에 공지된 다른 방법을 사용하여 투과화시키고(Jamur MC 등의 문헌[(2010) Permeabilization of cell membranes, Methods Mol Biol. 588:63-6), 형광 RAB11 항체(RAB11 항체, Alexa Fluor 488, 3H18L5, ABfinity?? 토끼 단클론)와 같은 엔도솜 마커로 추가로 염색하고, (예를 들어 본원에 기술된 것과 같은) 적절한 형광 표지된 항-인간 이차 항체로 염색하고, 본원에 기술된 것과 같이 공초점 형광 현미경을 사용해 영상화한다. 공초점 이미지의 분석은, MET에 특이적인 pH 조작된 ABPC를 비롯하여 MET에 특이적인 대조군 ABPC 모두가 내재화되어 엔도리소좀에 축적된다는 것을 보여줄 수 있다.
MET에 특이적인 pH-조작된 ABPC가 MET에 특이적인 대조군 ABPC에 비해 강화된 엔도리소좀 축적을 달성한다는 것을 입증하기 위해, (예를 들어 본원에 기술된 것과 같은) MET에 특이적인 알려진 대조군 ABPC을 비롯하여 MET에 특이적인 pH-조작된 ABPC를 사용하여 pHrodo-기반 내재화 검정을 수행한다. 검정은, 중성 pH에서 세포 외부의 형광 수준이 엔도리소좀의 산성 pH 환경 내부의 형광 수준보다 낮도록, pH가 감소할수록 형광이 증가하는 염료인 pHrodo?? iFL(P36014, ThermoFisher)을 사용한다. 간략하게, 적절한 MET+ 세포주(계대 25 미만)를 (예를 들어, 세포 은행 또는 세포 은행 데이터베이스 ATCC, DSMZ, 또는 ExPASy Cellosauruss에 의해) 권장된 배지에 현탁하고, 24-웰 플레이트 내에 웰 당 1 mL씩 2,000,000 세포/mL의 밀도로 도말한다. 세포를 얼음 위에 유지한 상태로, 1 mL의 2x pHrodo iFL-표지된 항체(제조사의 지침에 따라 제조함)를 각 웰에 첨가하고, 웰을 5회 피펫팅/혼합하고, 플레이트를 얼음 위의 차광된 환경에서 45분 동안 인큐베이션한다. 또한, 동일하지만 별도의 플레이트를 얼음 상에서 인큐베이션하는데, 이는 비-내재화 음성 대조군으로서 의도된 것이다. 인큐베이션 후, 실험 플레이트를 37℃의 인큐베이터에 옮기고, 음성 대조군 플레이트는 얼음 위에 유지시켜 내재화를 늦추거나 차단하고, 지정된 시점에 샘플을 취해 내재화 시간 과정을 생성한다. 샘플을 둥근 바닥 96-웰 플레이트에 넣고, 200 μL/웰의 얼음처럼 차가운 FACS 완충액을 첨가하여 내재화를 퀀칭시킨다. 플레이트를 2000xg에서 2분 동안 회전시키고, 200 μL 얼음처럼 차가운 FACS 완충액에 재현탁하고, 다시 회전시키고, FACS 완충액에 한 번 더 재현탁한다. 마지막으로, 샘플을 유세포 계측기에 로딩하여 pHrodo iFL 적색 염료의 여기 및 방출 최대값(각각 566 nm 및 590 nm)과 일치하는 여기 및 방출 파장을 사용해 세포 pHrodo 형광을 판독한다. 유세포 계측 실험과 데이터 분석이 완료된 후, MET에 대해 특이적인 pH-조작된 ABPC로 치료한 세포는 MET에 대해 특이적인 알려진 대조군 ABPC에 비해 더 높은 pHrodo iFL 신호를 갖는 것을 관찰할 수 있는데, 이는 MET에 특이적인 pH-조작된 ABPC가 MET에 특이적인 대조군 ABPC에 비해 강화된 엔도리소좀 축적을 달성함을 나타낸다.
대안적으로, MET에 특이적인 pH-조작된 ABPC가 MET에 특이적인 대조군 ABPC에 비해 강화된 엔도리소좀 축적을 달성함을 입증하기 위해, 전술한 실험을 변형한 실험을 수행된다. MET+ 세포를 도말하고, PBS로 3회 세척하고, 2 μg/mL 농도의 MET에 특이적인 pH-조작된 ABPC 또는 MET에 특이적인 대조군 ABPC를 첨가한 뒤 중성 pH의 배지에서 37℃에서 60분 동안 인큐베이션한다. 인큐베이션 후, 세포를 PBS로 3회 세척하고, 고정시켜 투과화시키고, 리소좀뿐만 아니라 후기 엔도솜 마커에도 결합하는 적절히 선택된 항체 패널(예: RAB7, 및 LAMP1; Cell Signaling Technology, 엔도솜 마커 항체 샘플러 키트 #12666; AbCam, 항-LAMP2 항체 [GL2A7], ab13524)로 염색한다. 1차 항체 염색 후, 형광 표지된 이차 항체(예: 염소 항-인간 IgG (H&L) 2차 항체(Alexa Fluor 647), Cat#A-21445, 및 Abcam 염소 항-토끼 IgG H&L(Alexa Fluor 488), Cat#ab150077)의 적절한 혼합물로 세포를 염색하고, 공초점 형광 현미경을 사용해 영상화하고, MET-특이적 항체와 엔도솜 마커의 신호가 공동으로 국소화된 영역을 시각화하고 정량화한다. 데이터 분석 후, MET에 특이적인 대조군 ABPC로 치료한 웰과 비교했을 때, MET에 특이적인 pH-조작된 ABPC로 치료한 웰에서 엔도리소좀과 MET-특이적 항체 신호의 공동-국소화가 증가함을 밝혀낼 수 있고, 이에 의해 MET에 특이적인 pH-조작된 ABPC가 MET에 특이적인 대조군 ABPC에 비해 강화된 엔도리소좀 축적을 달성할 수 있음을 입증할 수 있다.
MET에 특이적인 대조군 ABPC 대비, MET에 특이적인 pH-조작된 ABPC에 노출시킨 후 MET+ 세포에서 MET 항원 밀도의 증가
MET에 특이적인 pH-조작된 ABPC로 세포를 치료하는 것이 MET에 특이적인 pH-조작된 ABPC에 노출시킨 세포 표면에서 MET의 수준을 검출 가능하게 감소시키지 않는 다는 것, 또는 상기 치료가 MET에 특이적인 대조군 ABPC에 비해 MET에 특이적인 pH-조작된 APBC에 노출시킨 세포 묘면에서 MET의 수준을 덜 감소시킨다는 것을 입증하기 위해, 유세포 계측법을 사용해 항원 밀도 연구를 수행한다. 간략하게, 100 μL 배지 중 96-웰 플레이트 내에 MET를 발현하는 4.0x105개의 세포/웰을 도말한다. 1 pM 내지 1 μM의 i) MET에 특이적인 pH-조작된 ABPC, ii) MET에 특이적인 제1 대조군 ABPC, iii) 적절한 이소형 대조군, 및 iv) 미치료 대조군을 적정하여 세포를 치료한다. 세포를 37℃에서 2시간 동안 인큐베이션하는데, 이 시점에 모든 세포는 (예를 들어 세포에 대한 결쟁 결합 연구에 의해 결정했을 때) MET에 특이적인 제1 대조군 ABPC 또는 MET에 특이적인 pH-조작된 ABPC 중 하나와 상이한 에피토프를 갖는, MET에 특이적인 200 nM의 형광단-표지된 제2 대조군 ABPC와 함께 4℃에서 30분 동안 인큐베이션한다. 30분 동안 이렇게 인큐베이션한 후, 당업자에게 공지된 방법을 사용하여, 예를 들어 유세포 계측법을 사용해 모든 세포의 평균 형광 강도(MFI)를 판독한다. 병행하여, 치료된 세포 표면 상에서 MET의 존재를 MFI의 함수로서 정량화하는 데 사용될 수 있는 정량적 표준 곡선을 상업적으로 이용 가능한 정량화 키트(예를 들어 BD Biosciences PE Phycoerythrin Fluorescence Quantitation Kit, 카탈로그 #340495)를 사용해 생성하며; 정량적 표준 곡선은 제조사의 지침에 따라 생성한다. 세포 표면에서 MET의 절대 수를 결정하는 다른 방법은 당업계에 공지되어 있으며, 예를 들어 방사성 동위원소 표지된 시약을 사용하는 것을 포함한다. 데이터 분석 후, 적어도 하나의 항체 농도에서, 이소형 대조군 및 미치료 대조군 모두에 비해, MET에 특이적인 대조군 ABPC로 치료한 세포는 표면에서 MET의 수준 감소를 겪는 반면, MET에 특이적인 pH-조작된 ABPC로 치료한 세포는 현저히 적은 감소를 겪거나 감소를 전혀 겪지 않는 다는 것을 알 수 있다.
실시예 3.
MET에 특이적인 pH-조작된 ABPC 및 대조군 ABPC의 세포독성 약물에 대한 접합
발린-시트룰린(vc) 링커를 통해 모노메틸 아우리스타틴 E(MMAE)에 연결된 본원에 기술된 MET-결합 IgG(이하, MET-IgG)를 포함하는 항원-결합 단백질 작제물 접합체(ADC)를 제조한다(이하 MET-IgG-DC). vcMMAE와 항원 결합 단백질 작제물의 접합은 MET-IgG의 부분 환원 후 말레이미도카프로일-Val-Cit-PABC-MMAE(vcMMAE)와의 반응으로 시작된다. MET-IgG(20 mg/mL)를 TCEP(TCEP:mAb의 몰당량 2:1)의 첨가에 의해 부분적으로 환원시킨 후, 0℃에서 밤새 인큐베이션한다. 그런 다음, 환원 반응을 20℃로 가온한다. 모든 티올을 접합시키기 위해, vcMMAE를 1:15의 vcMMAE:환원 Cys의 최종 몰비로 첨가한다. 접합 반응은 10% v/v의 DMSO의 존재 하에 수행하고 20℃에서 60분 동안 진행시킨다.
접합 반응 후, 과량의 유리 N(아세틸)-시스테인(2당량 대 vcMMAE 전하)을 첨가하여 반응하지 않은 vcMMAE를 퀀칭시켜 Cys-Val-Cit-MMAE 부가물을 생성한다. Cys 퀀칭 반응을 20℃에서 약 30분 동안 진행시킨다. Cys-퀀칭된 반응 혼합물을 하기와 같이 정제한다. 상기 접합 방법은 말레이미도카프로일 모노메틸아우리스타틴 F(mcMMAF)를 항원 결합 단백질 작제물에 접합하는 데 사용할 수도 있다.
MET-IgG-DC는 회분 정제 방법(batch purification method)을 사용하여 정제한다. 반응 혼합물을 적당량의 물로 세척한 Bu-HIC 수지(ToyoPearl; Tosoh Biosciences)로 처리한다. 즉, 7중량의 수지를 혼합물에 첨가한다. 수지/반응 혼합물을 적절한 시간 동안 교반하고, 약물 접합체 산물의 제거에 대해 분석 소수성 상호작용 크로마토그래피에 의해 모니터링하고, 거친 폴리프로필렌 필터를 통해 여과하고, 2상 부피의 완충액(0.28 M 염화나트륨, 7 mM 인산칼륨, pH 7)으로 세척한다. 합쳐진 여액과 헹굼액을 합치고 HIC HPLC에 의해 생성물 프로파일에 대해 분석한다. 합쳐진 여액과 헹굼액을 초여과/투석여과(UF/DF)에 의해 15 mM 히스티딘 pH 6에 대해 10 투석 부피의 15 nM 히스티딘 완충액으로 완충액 교환한다.
유사한 프로토콜을 사용해 SG3249 및 SGD-1910과 같은 DNA 독소를 MET-IgG에 접합시킬 수 있다(Tiberghien AC 등의 문헌[(2016) Design and Synthesis of Tesirine, a Clinical Antibody-Drug Conjugate Pyrrolobenzodiazepine Dimer Payload, ACS Med Chem Lett 7:983*?*987] 참조). 간략하게, SG3249의 경우, MET-IgG(15 mg, 100 나노몰)를 10 mM 붕산나트륨 pH 8.4, 2.5 mM EDTA 및 1.11 mg/mL의 최종 항체 농도를 함유하는 13.5 mL의 환원 완충액에 희석한다. 10 mM의 TCEP 용액(1.5 몰당량/항체, 150 나노몰, 15 마이크로리터)을 첨가하고, 환원 혼합물을 인큐베이터에서 +37℃에서 1.5시간 동안 가열한다. 실온까지 냉각시킨 후, SG3249를 DMSO 용액(5 몰당량/항체, 1.5 mL DMSO 중 500 나노몰)으로서 첨가한다. 용액을 실온에서 1.25시간 동안 혼합한 다음, N-아세틸 시스테인(1 마이크로몰, 10 mM의 100 마이크로리터)을 첨가하여 접합을 퀀칭시키고, Superdex 200 PG로 채워진 GE Healthcare HiLoad?? 26/600 컬럼을 사용하여 AKTA?? Pure FPLC에 주입하고, 멸균 여과된 인산염 완충 식염수(PBS)로 2.6 mL/분의 속도로 용리시킨다. MET-IgG-DC 단량체 피크에 상응하는 분획을 풀링하고, 15 mL Amicon Ultracell 50KDa MWCO 스핀 필터를 사용하여 농축시키고, 분석하고, 멸균 여과한다. 물과 아세토니트릴의 구배로 용리하는 Phenomenex Aeris 3.6u XB-C18 150 x 2.1 mm 컬럼을 사용하는 Shimadzu Prominence System을 이용한 280 nm 및 330 nm의 (SG3249 특이적) MET-IgG-DC의 환원된 샘플에 대한 UHPLC 분석을 통해, 경쇄 및 중쇄의 혼합물이 SG3249의 여러 분자에 부착된 것을 볼 수 있는데, 이는 약물-항체 비율(DAR)인 항체 당 1 내지 4개의 SG3249 분자와 일치한다. 200 mM 인산칼륨 pH 6.95, 250 mM 염화칼륨 및 10% 이소프로판올(v/v)을 함유하는 멸균 여과된 SEC 완충액으로 용리하는 Phenomenex 3u SEC-3000 300 mm x 4.60 mm 컬럼을 사용하는 Shimadzu Prominence System을 이용한 280 nm에서 MET-IgG-DC의 샘플에 대한 UHPLC 분석을 통해 불순물이 검출되지 않는 90% 초과의 단량체 순도를 볼 수 있다. UHPLC SEC 분석을 통해 30%를 초과하는 최종 MET-IgG-DC 수율을 결정할 수 있다.
대안적으로, 리신 잔기를 통해 독소를 항체에 접합시키는 방법이 당업계에 공지되어 있다(예를 들어, Catcott KC 등의 문헌[(2016) Microscale screening of antibody libraries as maytansinoid antibody-drug conjugates, MAbs 8:513-23] 참조). 또한, 상기와 유사한 방법을 사용하여 이황화 결합을 통해 약물과 독소를 비-IgG 포맷에 접합시킬 수 있다(예: Vh-Fc).
실시예 4. MET에 특이적인 대조군 ABPC ADC와 비교했을 때 MET+ 세포에서 MET에 특이적인 pH-조작된 ABPC ADC의 강화된 세포독성 입증
본원에 기술된 방법을 사용해 선택된 (예를 들어 본원에 기술된 것과 같은) 다양한 항원 밀도를 발현하는 MET+ 세포주 및 MET- 세포주(예를 들어 T-47D ATCC Cat#HTB-133), 및 임의로 유전자이식 MET를 발현하는 세포, 예를 들어 당업계에 알려진 방법(예를 들어 Expi293?? 발현 시스템 키트 ThermoFisher 카탈로그 번호: A14635)을 사용해 MET로 형질감염시킨 HEK293 세포를 이용해, MET에 특이적인 pH-조작된 ADC(예를 들어 pH-조작된 MET-IgG-DC) 및 MET에 특이적인 대조군 ABPC ADC(예를 들어 대조군 ABPC MET-IgG-DC) 둘 다의 세포독성 활성을 별도로 평가하였다. 검증을 목적으로, 사용 전에, 당업계에 알려진 방법, 예를 들어 qPCR, 유세포 계측법, mRNA RPKM, 및 당업계에 알려진 (예를 들어, 본원에 기술된 바와 같은) 항-MET 항체를 사용하는 항체 염색을 사용해 모든 세포주를 MET의 발현에 대해 시험한 다음, 형광 현미경, 면역조직화학, 유세포 계측법, ELISA, 또는 당업계에 알려진 다른 방법을 사용해 염색을 시각화한다. 화합물의 세포독성을 평가하기 위해, 세포를 150 μL의 배양 배지에 웰 당 약 10~40,000개씩 시딩한 다음, 검정을 시작할 때 1 pM 내지 1 μM로 구분한 화합물의 투여량으로 4회 치료한다. 세포독성 검정은 시험 화합물을 첨가한 후 96시간 동안 수행된다. 인큐베이션 종료 전 4 내지 6시간 동안, 50 μL의 레자주린 염료(resazurin dye)를 각 웰에 첨가하여 배양 종료 시점에 생존 세포를 평가한다. 535 nm 및 590 nm의 여기 및 방출 파장을 각각 사용하여 형광 분광분석에 의해 염료 환원을 결정된다. 분석을 위해, 치료한 세포에 의한 레자주린 환원의 정도를 미치료 대조군 세포와 비교하고, 세포독성 백분율을 결정한다. 대안적으로, WST-8 키트를 제조사의 지침에 따라 사용하여 세포독성을 측정한다(예: Dojindo Molecular Technologies Catalog# CCK-8). 반치 최대 살해가 관찰되는 농도인 IC50은 당업계에 알려진 곡선 피팅 방법을 사용해 계산한다. 데이터 분석 후, MET에 특이적인 pH-조작된 ABPC ADC 및 대조군 ABPC ADC는 하나 이상의 MET+ 세포주에 대해 실질적으로 세포독성이지만, MET- 세포에 대해서는 독성이 덜한 것으로 결정할 수 있다. 또한, MET에 특이적인 pH-조작된 ADC는 MET에 특이적인 대조군 ABPC ADC보다 하나 이상의 MET 세포주에 대해 더 세포독성인 것으로 결정될 수 있는데, 이는: a) 이들이 하나 이상의 농도에서 더 큰 살해 심도를 나타내거나, b) 이들이 더 낮은 IC50을 나타내거나, c) (본원에 기술된 것과 같은) 중성 pH에서 세포에 대한 해리 상수 KD를 동일한 세포에 대한 IC50으로 나눈 비율이 더 크게 나타나기 때문이다.
또한, MET에 특이적인 ABPC의 세포독성 활성은 이차 ADC 검정에서 측정할 수 있다. 이차 ADC 검정은 당업계에 공지되어 있다(예를 들어 Moradec Cat# αHFc-NC-MMAF 및 Cat# αHFc-CL-MMAE, 및 관련된 제조사의 지침). 간략하게, MET에 특이적인 ABPC가 MET에 특이적인 ADC로 치환된 것을 제외하고 검정은 이전 단락에서와 같이 수행하며, 화합물의 세포독성을 평가하기 위해, 150 μL의 배양 배지에 웰 당 약 10~40,000개의 세포를 시딩한 다음, 검정을 시작할 때 MET에 특이적인 ABPC의 투여량을 1 pM 내지 1 μM(배양 배지 중 최종 농도 100 nM의 Moradec Cat# αHFc-NC-MMAF 이차 ADC 시약과 미리 혼합하고, 혼합물을 배양 배지에 첨가하기 전에 37℃에서 30분 동안 미리 인큐베이션한, 배양 배지 중 최종 농도)로 구분하여 4회 치료하였다
MET에 특이적인 pH-조작된 ADC 및 MET 접합체에 특이적인 대조군 ABPC ADC뿐만 아니라 이차 ADC 검정에서 MET에 특이적인 ABPC의 세포독성 활성을 다음의 프로토콜 채택하는 세포 증식 검정에 의해 추가로 측정하였다(Promega Corp. Technical Bulletin TB288; Mendoza 등의 문헌[Cancer Res. 62:5485-5488, 2002]):
1. 약 104개의 세포(예를 들어, 본원에 기술된 것과 같은 MET+ 세포)를 배지에 함유하는 100 μL의 세포 배양물의 분취물을 불투명한 벽으로 막힌 96-웰 플레이트드이 각 웰에 넣는다.
2. 세포 없이 배지만 함유하는 대조군 웰을 제조한다.
3. MET에 특이적인 ADC를 1 pM~1 uM의 농도 범위로 실험 웰에 첨가하고 1~5일 동안 인큐베이션한다. 대안적으로, 이차 ADC 검정에서, 100 nM의 이차 ADC 시약(배양 배지 중 최종 농도, Moradec Cat# αHFc-NC-MMAF) 및 1 pM~1 uM(배양 배지 중 최종 농도)의 농도 범위의 MET에 특이적인 ABPC를 미리 혼합하고 37℃에서 30분 동안 인큐베이션 한 후, 이 혼합물을 배양 배지에 첨가하고 1~5일 동안 인큐베이션한다.
4. 플레이트를 대략 30분 동안 실온으로 평형화시킨다.
5. 각 웰에 존재하는 세포 배양 배지의 부피와 동일한 부피의 CellTiter-Glo 시약을 첨가한다.
6. 내용물을 궤도형 쉐이커 상에서 2분 동안 혼합하여 세포 용해를 유도한다.
7. 플레이트를 실온에서 10분 동안 인큐베이션하여 발광 신호를 안정화시킨다.
8. 발광은 RLU(상대 발광 단위)로서 기록하고 그래프로 보고한다.
실시예 5. MET에 특이적인 대조군 ABPC ADC와 비교했을 때 MET+ 세포에서 MET에 특이적인 pH-조작된 ABPC ADC의 독소 유리 강화의 입증
MET에 특이적인 pH-조작된 ADC(예를 들어 pH-조작된 MET-IgG-DC)는 MET에 특이적인 대조군 ABPC ADC(예를 들어 대조군 ABPC MET-IgG-DC)와 비교했을 때, MET+ 세포에서 독소 유리의 증가를 입증할 수도 있다. 본원에 기술된 바와 같이 MET에 특이적인 pH-조작된 대조 ABPC ADC로 MET+ 세포를 치료한 후, LC-MS/MS 방법을 사용해, 치료된 MET+ 세포 중 접합되지 않은 (즉, 유리된) MMAE를 정량화한다(Singh, A.P. 및 Shah, D.K.의 문헌[Drug Metabolism and Disposition 45.11 (2017): 1120-1132]). 전기분무 간기 및 삼중 사중극자 질량 분광계가 구비된 LC-MS/MS 시스템이 사용된다. MMAE의 검출을 위해, XBridge BEH 아미드 컬럼(Waters, Milford, MA)을 사용하되, 이동상 A는 물(5 mM 포름산 암모늄 및 0.1% 포름산 포함)이고 이동상 B는 95:5 아세토니트릴/물(0.1% 포름산 및 1 mM 포름산 암모늄 포함)이며, 40℃에서 0.25 mL/분의 유속의 구배를 사용한다. 크로마토그래피 실행의 총 지속 시간은 12분이며, 여기서 2개의 MRM 스캔(718.5/686.5 및 718.5/152.1 amu)이 모니터링된다. 중수소화된(d8) MMAE(MCE MedChem Express, Monmouth Junction, NJ)를 내부 표준으로서 사용한다. 먼저, 생물학적 샘플 중 접합되지 않은 MMAE를 정량화하기 위한 방정식은, 각 약물 표준에 대한 피크 면적을 내부 표준에 대해 얻은 피크 면적으로 나누어 도출한다. 그런 다음, 생성된 피크 면적 비율을 표준 농도의 함수로서 도표화하고, 선형 회귀를 사용하여 데이터 포인트를 곡선에 피팅한다. 3개의 QC 샘플을 표준 곡선의 하위, 중간, 및 상위 범위에 포함시켜, 생성된 표준 곡선의 예측 능력을 평가한다. 그런 다음, 수득된 표준 곡선을 사용하여 생물학적 샘플에서 관찰된 MMAE 농도를 추론한다. MMAE 농도의 측정을 위해, 치료한 세포 샘플을 펠릿화하고, 신선한 배지에서 25만 세포/100 μL의 최종 농도로 재구성한다. 샘플에 d8-MMAE(1 ng/mL)를 첨가한 후, 2배 부피의 얼음처럼 차가운 메탄올을 첨가하고 이어서 -20℃에서 45분의 동결-해동 사이클을 수행하여 세포를 용해시킨다. 샘플을 4℃에서 15분 동안 13,000 rpm으로 원심분리한 다음 상청액을 수집하여 최종 세포 용해물을 수득한다. 표준 및 QC 샘플의 제조를 위해, 신선한 세포 현탁액(25만/100 μl)에 알려진 농도의 MMAE 및 내부 표준(d8-MMAE)을 첨가한 후, 상기 언급된 세포 용해와 유사한 절차를 수행한다. 그런 다음, 생성된 세포 용해물을 증발시키고 이동상 B에서 재구성한 후 LC-MS/MS에 주입한다. MET에 특이적인 pH-조작된 ADC로 치료한 MET+ 세포의 용해물 중 접합되지 않은 MMAE의 농도는 MET에 특이적인 대조군 ABPC ADC로 치료한 MET+ 세포의 농도보다 더 큰 것으로 관찰된다.
튜불린-억제 독소의 경우, 세포 생존력 및 세포 주기 단계를 모니터링하여 독소 유리도 평가한다. 약 2.0x10^5개의 MET+ 세포를 바닥이 편평한 96-웰 플레이트에 도말하고, 본원에 기술된 바와 같이 MET에 특이적인 pH-조작된 ABPC ADC 및 대조군 ABPC ADC로 치료한다. 치료 후, 세포를 96-웰 둥근 바닥 플레이트에 옮기고, 플레이트를 400 rcf에서 2분 동안 원심분리하여 상청액을 분리한다. 분리한 세포를 Live/Dead eFluor 660으로 염색한다. 그런 다음, 세포를 원심분리하고 FACS 완충액(2% FBS가 포함된 PBS)으로 세척한 후, BD Cycletest?? Plus DNA 키트(cat # 340242)로 세포 주기 분포를 분석한다. 간략하게, 세포를 76 ul의 용액 A에 재현탁하고, 실온에서 10분 동안 인큐베이션한다. 그런 다음, 61 μL의 용액 B를 첨가하고, 세포를 실온에서 10분 동안 추가로 인큐베이션한다. 마지막으로, 61 μL의 차가운 용액 C를 첨가하고, 세포를 실온에서 10분 동안 다시 인큐베이션한다. 마지막 인큐베이션 단계 직후, 세포를 (세척하지 않고) 유세포 계측에 의해 10 μL/초의 유속으로 분석한다. MET에 특이적인 대조군 ABPC ADC와 비교했을 때, MET에 특이적인 pH-조작된 ADC에 노출했을 때 G2/M-단계 정지가 증가하는 것을 관찰할 수 있다.
DNA 손상 독소(예: 피롤로벤조디아제핀 또는 "PBD")의 경우, 인산화된 히스톤 H2AX(γH2AX)를 측정함으로써 DNA 손상을 평가한다. H2AX는 일반적으로 DNA의 이중 가닥 절단에 반응하여 인산화되지만; γH2AX의 수준 증가는 PBD 또는 시스플라틴과 같은 DNA-가교결합 독소로 치료한 결과로서 관찰될 수도 있다(Huang, X. 등의 문헌[2004, Cytometry Part A 58A, 99-110] 참조). 본원에 기술된 것과 같이 MET에 특이적인 pH-조작된 ABPC ADC 및 대조군 ABPC ADC로 MET+ 세포를 치료한다. 치료 후, 세포를 PBS로 헹군 다음, 0℃의 PBS 중 1% 메탄올-무함유 포름알데히드(Polysciences, Warrington, PA)의 현탁액에서 15분 동안 고정시킨다. 세포를 -20℃에서 70% 에탄올에 적어도 2시간 동안 재현탁한다. 그런 다음, 세포를 PBS에서 2회 세척하고, PBS 중의 1%(w/v) BSA(Sigma) 용액 중 0.2% Triton X-100(Sigma)에 30분 동안 현탁하여 비특이적 Ab 결합을 억제한다. 세포를 다시 원심분리하고(200 g, 5분), 1:800으로 희석된 항-히스톤 γH2AX 다클론 Ab(Trevigen, Gaithersburg, MD)가 포함된 100 μL의 1% BSA에 세포 펠릿을 현탁한다. 그런 다음, 세포를 4℃에서 밤새 인큐베이션하고, PBS로 2회 세척하고, 1:30으로 희석한 돼지 항-토끼 면역글로불린(DAKO, Carpinteria, CA)의 FITC-접합 F(ab')2 단편 100 μL에 실온의 암소에서 30분 동안 재현탁한다. 그런 다음, 세포를 100 μg/mL의 DNase-무함유 RNase A(Sigma)가 포함된 PBS에 용해시킨 5 μg/mL의 PI(Molecular Probes, Eugene, OR)로 20분 동안 대조염색한다. FITC γH2AX 신호 및 PI 대조염색의 세포 형광은 당업계에 공지된 방법을 사용하여 유세포 계측법을 사용하여 측정한다. (총 DNA 함량에 기초하여) 세포 주기의 동일한 단계 내에 있는 세포들을 비교할 때, 치료된 MET+ 세포는 미치료 MET+ 세포(베이스라인의 역할을 함)에 비해 증가된 FITC γH2AX 신호를 갖는 것으로 관찰될 수 있다. 또한, MET에 특이적인 pH-조작된 ADC로 치료한 MET+ 세포는 MET에 특이적인 대조군 ABPC ADC로 치료한 세포보다 베이스라인 대비 γH2AX 수준의 더 큰 증가를 갖는 것으로 관찰될 수 있다. γH2AX 검정에 추가하여, DNA 가교 결합은 Comet 검정으로 보다 직접적으로 평가될 수 있다(Chandna, S.의 문헌[(2004) Cytometry 61A, 127-133]).
또한, 본원에 개시된 바와 같이, 일차 접합된 ADC를 사용하는 대신에 이차 ADC 검정을 수행함으로써, 본 실시예의 방법을 사용하여 pH-조작된 ABPC 및 대조군 ABPC를 직접 접합없이 검정할 수 있다.
실시예 6.
MET에 특이적인 대조군 ABPC와 비교했을 때 MET에 특이적인 pH-조작된 ABPC의 감소된 반감기의 입증
본 발명에 기술된 MET에 특이적인 pH-조작된 ABPC의 놀라운 양태 중 하나는, 엔도솜 또는 리소좀 내에서 MET로부터 ABPC의 해리 증가를 용이하게 하여, MET에 특이적인 대조군 ABPC 또는 MET에 특이적이지 않은 ABPC에 비해 혈청 반감기를 감소시키는 이들의 능력일 수 있다. 이러한 혈청 반감기의 감소는, MET에 특이적인 pH-조작된 ABPC가 MET에 결합할 때 이들의 세포 내재화가 강화되어 순환으로부터 제거되는 빈도가 향상되는 것 때문이며, 이는 MET에 특이적이고 결합되지 않은 pH-조작된 ABPC의 혈청 농도가 시간 경과에 따라 감소하는 것을 통해 관찰할 수 있다. 이러한 특성을 입증하기 위해, 당업계에 알려진 방법을 사용해, MET에 특이적인 pH-조작된 ABPC 및 MET에 특이적인 대조군 ABPC를 사용하여 마우스 및/또는 원숭이를 대상으로 일련의 동물 연구를 수행한다(예를 들어, Gupta, P. 등의 문헌[(2016), mAbs, 8:5, 991-997] 참조). 간략하게, 마우스 연구를 수행하기 위해, (예를 들어 본원에 기술된 것과 같은) MET+ 세포주를 이종이식한 두 그룹의 NOD SCID 마우스(예: Jackson Labs NOD.CB17-Prkdcscid/J Stock No: 001303) 에게 MET에 특이적인 pH-조작된 ABPC 또는 MET에 특이적인 대조군 ABPC 중 하나의 단일 볼루스(예: 5 mg/kg)를 꼬리 정맥을 통해 정맥내 투여한다. 이종이식 마우스는 시험관 내에서 1~5백만 개의 MET+ 세포를 성장시켜 마우스의 우측 옆구리에 피하 접종함으로써 제조된다. 종양의 크기를 300 mm3에 맞춘다. 종양의 길이(L)와 폭(W)은 전자 캘리퍼를 통해 측정하고, 부피는 다음 식에 따라 계산한다: V=LХW^2/2. 혈액 샘플은 다음 시점 각각에 각 그룹으로부터 안와 후 출혈을 통해 채취한다: 15분차, 30분차, 1시간차, 8시간차, 24시간차, 및 3일차, 7일차, 10일차, 14일차, 17일차, 21일차, 및 28일차. 샘플을 가공하여 혈청을 수집하고, ELISA 또는 당업계에 알려진 다른 방법(예를 들어, 항-인간 IgG 항체 Jackson ImmunoResearch Labs, Cat# 109-006-006을 사용하는 PAC 검정 또는 MAC 검정; Fischer, S.K. 등의 문헌[(2012), mAbs, 4:5, 623-631])을 사용해 항체 농도를 정량화한다. MET에 특이적인 pH-조작된 ABPC 및 MET에 특이적인 대조군 ABPC의 항체 농도를 시간의 함수로서 도표화한다. 데이터 분석 후, MET에 특이적인 pH-조작된 ABPC는 MET에 특이적인 대조군 ABPC에 비해 상당히 짧은 혈청 반감기를 가지므로, 동일한 항원에 결합하지만 pH 의존성이 상이한 다른 유사한 결합제(예를 들어 MET에 특이적인 대조군 ABPC)에 비해 MET의 pH 의존성에 특이적인 pH-조작된 ABPC가 엔도솜 또는 리소좀 내에서 해리 강화를 촉진하는 능력을 나타낸다는 것을 관찰할 수 있다. MET에 특이적인 pH-조작된 ABPC 및 대조군 ABPC가 MET의 마우스 상동체와 교차 반응성인 경우, 비-이종이식 마우스로 유사한 실험을 반복할 수 있다.
임의로, MET에 특이적인 pH-조작된 ABPC 및 대조군 ABPC가 MET의 시노몰구스 원숭이 상동체와 교차 반응성인 경우, 원숭이(예: 시노몰구스 원숭이)에 대해 유사한 실험을 수행할 수 있다. 동일한 수의 수컷 및 암컷 원숭이(예: 각각 n = 1~2)에게 MET에 특이적인 pH-조작된 ABPC 또는 MET에 특이적인 대조군 ABPC의 볼루스를, 예를 들어, 1 mg/kg의 투여량으로 복재 정맥 주사를 통해 투여한다. 대안적으로, MET-결합 단백질의 여러 상이한 투여량을 여러 마리의 원숭이로 이루어진 군 전체에게 투여한다. 혈액 샘플을 전술한 것과 유사한 간격으로 말초 정맥 또는 대퇴 정맥을 통해 수집하고, 당업계에 알려진 방법(예: ELISA)을 사용하여 MET에 특이적인 pH-조작된 ABPC 또는 MET에 특이적인 대조군 ABPC의 존재에 대해 분석한다. 데이터 분석 후, MET에 특이적인 pH-조작된 ABPC는 MET에 특이적인 대조군 ABPC에 비해 상당히 짧은 혈청 반감기를 가지므로, 동일한 항원에 결합하지만 pH 의존성이 상이한 다른 유사한 결합제(예를 들어 MET에 특이적인 대조군 ABPC)에 비해 MET에 특이적인 pH-조작된 ABPC가 엔도솜 또는 리소좀 내에서 해리 강화를 촉진하는 능력을 나타낸다는 것을 관찰할 수 있다. 일부 경우에, 이러한 효과는 특정 투여량에서만 관찰되는 반면, 다른 경우에는 모든 투여량에서 관찰된다.
또한, MET에 특이적인 pH-조작된 ABPC ADC 및 대조군 ABPC ADC의 반감기는, MET에 특이적인 pH-조작된 ABPC ADC 및 대조군 ABPC ADC를 MET에 특이적인 pH-조작된 ABPC 및 대조군 ABPC로 치환함으로써(즉, 본원에 기술된 바와 같이, 약물 또는 독소에 ABPC를 접합시킨 후 ABPC를 연구함으로써) 상기 방법을 사용하여 평가할 수 있다.
실시예 7.
마우스 이종이식 모델에서 MET에 특이적인 대조군 ABPC ADC 대비 MET에 특이적인 pH-조작 ADC의 효능 증가
MET에 특이적인 pH-조작된 ADC의 MET+ 종양에 대한 항종양 활성 강화는 MET+ 세포의 피하 이종이식 모델에서 입증될 수 있다. 실험을 위해, 마우스 한 마리당 1~5백만 개의 MET+ 세포를 시험관 내에서 성장시키고, 암컷 면역결핍(예: SCID-Beige 또는 NOD scid) 마우스의 우측 옆구리에 피하 접종한다. 종양의 크기를 100~200 mm3에 맞추고, 복강내(IP) 투여한다(약 4~7일마다 1회 투여하여 총 약 2~6회 투여). 종양의 길이(L)와 폭(W)은 전자 캘리퍼를 통해 측정하고, 부피는 다음 식에 따라 계산한다: V=LХW^2/2. MET에 특이적인 pH-조작된 ADC 또는 MET에 특이적인 대조군 ABPC ADC의 볼루스(예: 5 mg/kg)를 꼬리 정맥을 통해 투여한다. 종양 성장 억제(TGI)와 종양 성장 지연(TGD) 및 생존은 MET에 특이적인 대조군 ABPC ADC를 동일한 요법으로 투여한 것과 비교했을 때, MET에 특이적인 pH-조작된 ADC를 투여한 경우에 상당히 개선된다.
임의로, 다양한 조직 내로 확산된 종양 세포는 희생시킨 동물에서 결정한다. 전이는 Schneider, T. 등의 문헌[Clin. Exp. Metas. 19 (2002) 571-582]에 따라 측정한다. 간략하게, 조직을 채취하고, 실시간 PCR에 의해 인간 Alu 서열을 정량화한다. 실시간 PCR에 의해 정량화된 더 높은 인간 DNA 수준은 더 높은 수준의 전이에 상응한다. 인간 Alu 서열의 수준(종양 세포가 이차 조직 내로의 침윤한 것과 상관이 있음)은, MET에 특이적인 대조군 ABPC ADC로 치료한 마우스와 비교했을 때, MET에 특이적인 pH-조작된 ADC로 치료한 동물에서 상당히 낮은데, 이는 전이 감소에 상응한다. 대안적으로, MET에 특이적인 pH-조작된 ADC의 강화된 항종양 활성은 MET+ 환자 유래 이종이식 모델(예: Jackson Laboratory로부터 구입할 수 있음)에서 나타날 수 있다.
실시예 8.
pH-조작된 이중 특이적 MET 이중 특이적 ABPC의 생성 및 대조군 이중 특이적 ABPC 대비 예시적인 특성의 입증
변형된 독성 및 내재화 특성을 가지며 MET에 특이적인 pH-조작된 ABPC를 생성하기 위해, MET 상에서 2개의 상이한 에피토프에 결합하는 이중특이적 항체를 작제한다. 이중 파라토프 항체(biparatopic antibody)가 증가된 항원 의존적 내재화를 나타낼 수 있고, 따라서 항체-약물 접합체와 같은 응용예에 유용하다는 것은 당업계에 공지되어 있다(예를 들어, Li 등의 문헌[(2016) A Biparatopic HER2-Targeting Antibody-Drug Conjugate Induces Tumor Regression in Primary Models Refractory to or Ineligible for HER2-Targeted Therapy, Cancer Cell 29:117-29] 참조). 간략하게, MET에 특이적인 pH-조작된 MET x MET 이중특이적 이중 파라토프 ABPC를, MET에 특이적인 2개의 상이한 pH-조작된 ABPC로부터의 경쇄/중쇄 쌍을 사용하여 조립하며, 여기서 2개의 상이한 pH-조작된 ABPC의 각각은 MET 상에서 다른 에피토프와 중첩되지 않는 구별되는 에피토프에 결합한다. 비중첩 에피토프에 결합하는 MET에 특이적인 일단의 pH-조작된 ABPC는, 예를 들어, 본원에 기술된 방법, 또는 당업자에게 공지된 다른 방법을 사용하여 발견된다. 간략하게, 예를 들어, Abdiche YN 등의 문헌[(2009) Exploring blocking assays using Octet, ProteOn, and Biacore biosensors, Anal Biochem 386:172-80]에서와 같은 결합 경쟁 검정에 의해 결정했을 때, 결합제들이 MET 상에서 실질적으로 상이한 에피토프에 결합한다는 것을 기준으로 2개의 결합제를 선택한다. 대안적으로, 본원에 기술된 바와 같이, MET에 특이적인 제1 ABPC로 형질감염된 세포의 세포 배양 상청액을 50 μg/mL의 항체 발현 수준에 대해 정규화하고, 항-인간 Fc 센서(Forte Bio) 상에 포획한다. 1X 동역학 완충액(Forte Bio)을 사용해 베이스라인을 확립하고, 센서를 pH 7.4의 1X PBS 중 50 nM의 MET와 300초 동안 결합시켜 결합 곡선을 생성한다(여기서, 50 nM의 MET는 MET 형질 감염 상청액에 특이적인 제2 ABPC 또는 MET 형질감염 상청액에 특이적인 제1 ABPC와 혼합하여 37℃에서 30분 동안 미리 인큐베이션한 것이며, 제2 ABPC 및 제1 ABPC는 모두 50 ug/mL로 정규화한 것임). (기기 소프트웨어로 계산했을 때, 또는 시간 경과에 따라 결합 수준의 증가로 확인했을 때) MET에 특이적인 제2 ABPC가 존재할 때의 결합 속도가 MET에 특이적인 제1 ABPC가 존재할 때의 결합 속도보다 유의하게 더 빠른 경우, MET에 특이적인 제2 ABPC는 MET의 비중첩 에피토프에 결합하는 것으로 간주된다. 임의로, MET를 발현하는 세포 상의 에피토프에 항체가 결합할 때 항체의 내재화 특성에 대해 각각의 항체를 스크리닝하고, 잘 내재화되는 항체를 선택한다. 세포의 표면 상에 존재하는 분자의 내재화 속도를 결정하기 위한 검정은 당업계에 공지되어 있다. 예를 들어, Wiley 등의 문헌[(1991) J. Biol. Chem. 266: 11083-11094]; 및 Sorkin 및 Duex의 문헌[(2010) Curr. Protoc. Cell Biol. Chapter, Unit-15.14]; Vainshtein 등의 문헌[(2015) Pharm Res. 32: 286-299]을 참조한다. 선택 후, 중쇄 및 경쇄 페어링을 위한 조작된 돌연변이를 갖는 중쇄 및 경쇄 작제물(Spies 등의 문헌"Alternative molecular formats and therapeutic applications of bispecific antibodies," 2015)을 양쪽 아암 모두에 대해 합성한다. MET에 특이적인 이중특이적 ABPC는, 예를 들어 Expi293 세포에서 상응하는 중쇄 및 경쇄 플라스미드를 공동 발현시켜 생산한다. 세포 배양 상청액을 수확하고 단백질 A 정제를 수행한다. MET에 특이적인 이종이량체 ABPC는 이온 교환 크로마토그래피, 소수성 상호작용 크로마토그래피, 및 혼합 모드 크로마토그래피와 같은 추가적인 정제 단계를 통해 동종이량체 종으로부터 분리한다. MET에 특이적인 정제된 pH-조작된 MET x MET 이중특이적 이중 파라토프 ABPC의 특성을 질량 분광분석을 통해 분석하여, 순도 및 동종이량체 종의 부재를 확인하고, 크기 배제 크로마토그래피를 통해 동종이량체 항원 결합 단백질 작제물 종의 존재를 확인한다. 생성물 항체의 경우, MET에 대한 결합은 Biacore 분석을 통해 확인한다. 이중특이적 항체를 생산하는 다른 방법은 당업계에 공지되어 있으며, 당업자에게 명백한 것과 같이 이를 사용해 이중특이적 항체, 예를 들어 본원에 기술된 MET에 특이적인 MET x MET 이중특이적 이중 파라토프 ABPC를 생성할 수도 있다(예를 들어 Labrijn 등의 문헌[(2014) "Controlled Fab-arm exchange for the generation of stable bispecific IgG1" Nature Protcols 9:2450-2463], 액세스 링크 http://www.nature.com/nprot/journal/v9/n10/abs/nprot.2014.169.html). 대안적으로, MET에 특이적인 MET x MET ABPC 대신에, 당업자에게 명백한 유사한 방법을 사용해 MET에 특이적인 pH-조작된 MET x BINDER ABPC를 작제할 수 있는데, 여기서 BINDER는 당업계에 공개되었거나 본원의 방법과 유사한 방법 또는 당업계에 알려진 방법(예를 들어, 디스플레이 기반 또는 면역화 기반 방법)을 사용해 발견한 임의의 항체이다.
다음으로, MET에 특이적인 pH-조작된 MET x MET ABPC의 예시적인 특성은, 적절한 대조군(MET에 특이적인 대조군 ABPC 단일특이적 또는 이중특이적 APBC)을 사용하여 본원에 기술된 방법을 사용해 입증할 수 있다. 간략하게, 대조군과 비교했을 때, MET에 특이적인 pH-조작된 MET x MET ABPC는: a) pH 의존적 방식으로 세포에 결합하고, 예를 들어 중성 pH에서 결합하고 산성 pH에서는 결합하지 않고; b) pH 의존적 방식으로 세포로부터 방출되고, 예를 들어 중성 pH에서 결합하고 산성 pH에서 방출되고; c) MET+ 세포에서 강화된 엔도리소좀 축적을 나타내고; d) MET+ 세포에 노출된 후, 증가된 MET 항원 밀도를 나타내고; e) 독소에 접합된 경우, MET+ 세포에 대해 증가된 세포독성을 나타내고; f) 독소에 접합된 경우, MET+ 세포와 함께 인큐베이션할 때 증가된 독소 유리를 나타내고; g) MET 항원에 노출된 경우, 관련 동물 모델에서 감소된 반감기를 나타내며; h) 독소에 접합된 경우, MET+ 세포의 마우스 이종이식 모델에서 증가된 효능을 나타낸다는 것을 알 수 있다. 유사하게, MET에 특이적인 pH-조작된 MET x BINDER ABPC의 예시적인 특성은, 적절한 대조군(MET에 특이적인 대조군 APBC MET x BINDER 이중특이적 ABPC)을 사용하여 본원에 기술된 방법을 사용해 입증할 수 있다.
실시예 9.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있고, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용될 수 있다[Wang J 등의 (2017) ABBV-399, a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors, Irrespective of MET Pathway Dependence, Clin Cancer Res, 23:992-1000]. 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 텔리소투주맙(중쇄 서열번호 1, 경쇄 서열번호 2)을 선택하였다. 간략하게, 중쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 중쇄 CDR 내의 개별 아미노산 잔기를 히스티딘으로 한 번에 하나씩 체계적으로 치환하였다(MYT0887 - MYT0924). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 중쇄 CDR에서 단 하나의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는, 당업계에 알려진 방법을 사용해 Expi293 세포를 a) 하나의 중쇄 서열 변이체, 및 b) 상응하는 출발 ABPC 경쇄로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 1), 변이체의 pH 의존성을 Octet RED 384 기기를 이용해 바이오층 간섭(BLI)을 사용해 평가하였다. 간략하게, 15 μL의 세포 배양 상청액을 185 μL의 1x PBST pH 7.4로 희석하여 센서 팁 상에 로딩하였다. 그 결과 41.1 μg/mL의 고농도, 13.7 μg/mL의 저농도, 및 26.5 μg/mL의 평균 농도가 생성되었다. 그런 다음, 이렇게 희석된 상청액을 항-인간 Fc 센서(Forte Bio) 상에 포획하였다. 1X PBST(50 mM 인산칼륨 완충액 + 150mM NaCl + 0.05% Tween 20) pH 7.4를 사용하여 베이스라인을 확립하고, 센서를 1X PBST pH 7.4 중 50 nM의 MET(cMET, Sino Biological 카달로그 번호 10692-H08H, 로트 번호 LC11SE2008)와 120초 동안 결합시켜 결합 곡선을 생성하였다. 해리 단계에서, 센서 상의 항체-항원 복합체를 1X PBST pH 7.4에 300 내지 600초 동안 노출시켰다. 전체적으로 별도의 조건에서 1xPBST pH 5.4를 사용해 베이스라인, 결합, 및 해리를 반복하였다. pH 5.4 및 pH 7.4에서 출발 ABPC 항체(치환 없음) 및 각각의 상응하는 항체 변이체에 대한 결합 및 해리 단계 곡선을 조사하여 두 가지 기준을 알아냈다: a) 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라인 치환으로 인해 pH 5.4에서 해리가 강화됨(즉, koff 값이 더 높음); 및 b) pH 5.4에서의 항체 변이체 자체 및 출발 ABPC(치환 없음)와 비교했을 때, pH 7.4에서 해리가 감소함(즉, koff 값이 더 낮음). 도 2에 도시된 바와 같이, (출발 ABPC와 비교했을 때) pH 5.4에서 강화된 해리를 나타내거나, pH 7.4에서 감소된 해리를 나타내거나, 둘 다를 나타낸 중쇄 변이체를 추가 분석을 위해 선택하였다(예를 들어 MYT0887, MYT0888, MYT0889, MYT0890, MYT0893, MYT0914, MYT0915, MYT0916, MYT0917, MYT0918, MYT0919, MYT0920, 및 MYT0924). 또한, 일부 히스티딘 및 알라닌 돌연변이는 MET 결합을 제거한 반면(예: MYT0921 및 MYT0923), 다른 돌연변이는 MET 결합 동역학을 거의 변화시키지 않았거나(예를 들어 KD 또는 해리 속도에 있어서 1배 미만의 변화) 전혀 변화시키지 않았음을 주목하였다(예: MYT0891, MYT0894, MYT0895, MYT0896, MYT0897, MYT0898, MYT0899, MYT0900, MYT0901, MYT0902, MYT0903, MYT0904, MYT0905, MYT0906, MYT0907, MYT0908, MYT0909, MYT0910, MYT0911, MYT0912, MYT0913, 및 MYT0922).
특히, 히스티딘은 크고 양으로 하전된 아미노산이기 때문에, 변화가 없는 이들 변이체는 광범위한 돌연변이를 견딜 수 있고, 서열은 상이하지만 유사한 결합 특성을 갖는 항체로 유도할 수 있는 중쇄 내 위치로서 (명칭은 달리 명백하지 않음) 주목하였다.
실시예 10.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있고, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용될 수 있다[Wang J 등의 (2017) ABBV-399, a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors, Irrespective of MET Pathway Dependence, Clin Cancer Res, 23:992-1000]. 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 텔리소투주맙(중쇄 서열번호 1, 경쇄 서열번호 2)을 선택하였다. 간략하게, 경쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 경쇄 CDR 내의 개별 아미노산 잔기를 히스티딘으로 한 번에 하나씩 체계적으로 치환하였다(MYT2028 - MYT2058). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 경쇄 CDR에서 단 하나의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는, 당업계에 알려진 방법을 사용해 Expi293 세포를 a) 하나의 경쇄 서열 변이체, 및 b) 상응하는 출발 ABPC 중쇄로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 3), 변이체의 pH 의존성을 Octet RED 96e 기기를 이용해 바이오층 간섭(BLI)을 사용해 평가하였다. 간략하게, SDS-PAGE 겔의 시각적 검사에 의해 결정된 변이체의 정성적 발현 수준에 기초하여 세포 배양 상청액을 희석하되, 고 발현 변이체의 경우 5 μL의 세포 배양 상청액을 195 μL의 1x PBST, pH 7.4에 희석하고, 중간 발현 변이체의 경우 25 μL의 세포 배양 상청액을 175 μL의 1x PBST, pH 7.4에 희석하고, 저 발현 변이체의 경우 100 μL의 세포 배양 상청액을 100 μL의 1x PBST, pH 7.4에 희석하여, 센서 팁 상에 로딩하였다. 그런 다음, 희석된 상청액을 항-인간 Fc 센서(Forte Bio) 상에 포획하였다. 1X PBST(50 mM 인산칼륨 완충액 + 150mM NaCl + 0.05% Tween 20) pH 7.4를 사용하여 베이스라인을 확립하고, 센서를 1X PBST pH 7.4 중 50 nM의 MET(cMET, Sino Biological 카달로그 번호 10692-H08H)와 120초 동안 결합시켜 결합 곡선을 생성하였다. 해리 단계에서, 센서 상의 항체-항원 복합체를 1X PBST pH 7.4에 300 내지 600초 동안 노출시켰다. 전체적으로 별도의 조건에서 1xPBST pH 5.4를 사용해 베이스라인, 결합, 및 해리를 반복하였다. pH 5.4 및 pH 7.4에서 출발 ABPC 항체(치환 없음) 및 각각의 상응하는 항체 변이체에 대한 결합 및 해리 단계 곡선을 조사하여 두 가지 기준을 알아냈다: a) 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라인 치환으로 인해 pH 5.4에서 해리가 강화됨(즉, koff 값이 더 높음); 및 b) pH 5.4에서의 항체 변이체 자체 및 출발 ABPC(치환 없음)와 비교했을 때, pH 7.4에서 해리가 감소함(즉, koff 값이 더 낮음). 도 4에 도시된 바와 같이, (출발 ABPC와 비교했을 때) pH 5.4에서 강화된 해리를 나타내거나, pH 7.4에서 감소된 해리를 나타내거나, 둘 다를 나타낸 경쇄 변이체를 추가 분석을 위해 선택하였다(예: MYT2029, MYT2032, MYT2033, MYT2034, MYT2035, MYT2036, MYT2038, MYT2039, MYT2040, MYT2041, MYT2042, MYT2043, MYT2044, MYT2048, MYT2049, MYT2052, MYT2056, 및 MYT2058). 또한, 일부 히스티딘 및 알라닌 돌연변이는 MET 결합 동역학을 거의 변화시키지 않았거나(예를 들어 KD 또는 해리 속도에 있어서 1배 미만의 변화) 전혀 변화시키지 않았음을 주목하였다(예: MYT2028, MYT2030, MYT2031, MYT2037, MYT2045, MYT2046, MYT2047, MYT2050, MYt2051, MYT2053, MYT2054, MYT2055, 및 MYT2057). 특히, 히스티딘은 크고 양으로 하전된 아미노산이기 때문에, 변화가 없는 이들 변이체는 광범위한 돌연변이를 견딜 수 있고, 서열은 상이하지만 유사한 결합 특성을 갖는 항체를 유도할 수 있는 경쇄 내 위치로서 주목하였다(명칭은 달리 명백하지 않음).
실시예 11.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있고, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용될 수 있다[Wang J 등의 (2017) ABBV-399, a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors, Irrespective of MET Pathway Dependence, Clin Cancer Res, 23:992-1000]. 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 텔리소투주맙(중쇄 서열번호 1, 경쇄 서열번호 2)을 선택하였다. 간략하게, 중쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 실시예 9에서 추가 분석을 위해 이전에 선택한 중쇄 CDR 내의 개별 아미노산 돌연변이를 한 번에 2개 이상씩 체계적으로 조합하였다(MYT2018 - MYT2027). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 중쇄 CDR에서 2개 이상의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는, 당업계에 알려진 방법을 사용해 Expi293 세포를 a) 하나의 중쇄 조합 서열 변이체, 및 b) 상응하는 출발 ABPC 경쇄로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 5), 변이체의 pH 의존성을 Octet RED 96e 기기를 이용해 바이오층 간섭(BLI)을 사용해 평가하였다. 간략하게, SDS-PAGE 겔의 시각적 검사에 의해 결정된 변이체의 정성적 발현 수준에 기초하여 세포 배양 상청액을 희석하되, 고 발현 변이체의 경우 5 μL의 세포 배양 상청액을 195 μL의 1x PBST, pH 7.4에 희석하고, 중간 발현 변이체의 경우 25 μL의 세포 배양 상청액을 175 μL의 1x PBST, pH 7.4에 희석하고, 저 발현 변이체의 경우 100 μL의 세포 배양 상청액을 100 μL의 1x PBST, pH 7.4에 희석하여, 센서 팁 상에 로딩하였다. 그런 다음, 희석된 상청액을 항-인간 Fc 센서(Forte Bio) 상에 포획하였다. 1X PBST(50 mM 인산칼륨 완충액 + 150mM NaCl + 0.05% Tween 20) pH 7.4를 사용하여 베이스라인을 확립하고, 센서를 1X PBST pH 7.4 중 50 nM의 MET(cMET, Sino Biological 카달로그 번호 10692-H08H)와 120초 동안 결합시켜 결합 곡선을 생성하였다. 해리 단계에서, 센서 상의 항체-항원 복합체를 1X PBST pH 7.4에 300 내지 600초 동안 노출시켰다. 전체적으로 별도의 조건에서 1xPBST pH 5.4를 사용해 베이스라인, 결합, 및 해리를 반복하였다. pH 5.4 및 pH 7.4에서 출발 ABPC 항체(치환 없음) 및 각각의 상응하는 항체 변이체에 대한 결합 및 해리 단계 곡선을 조사하여 두 가지 기준을 알아냈다: a) 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라인 치환으로 인해 pH 5.4에서 해리가 강화됨(즉, koff 값이 더 높음); 및 b) pH 5.4에서의 항체 변이체 자체 및 출발 ABPC(치환 없음)와 비교했을 때, pH 7.4에서 해리가 감소함(즉, koff 값이 더 낮음). 도 6에 도시된 바와 같이, (출발 ABPC와 비교했을 때) pH 5.4에서 강화된 해리를 나타내거나, pH 7.4에서 감소된 해리를 나타내거나, 둘 다를 나타낸 중쇄 조합 변이체를 추가 분석을 위해 선택하였다(예: MYT2018, MYT2019, MYT2020, MYT2022, MYT2023, MYT2025, 및 MYT2026).
실시예 12.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있고, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용될 수 있다[Wang J 등의 (2017) ABBV-399, a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors, Irrespective of MET Pathway Dependence, Clin Cancer Res, 23:992-1000]. 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 텔리소투주맙(중쇄 서열번호 1, 경쇄 서열번호 2)을 선택하였다. 간략하게, 경쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 실시예 10에서 추가 분석을 위해 이전에 선택한 경쇄 CDR 내의 개별 아미노산 돌연변이를 한 번에 2개 이상씩 체계적으로 조합하였다(MYT4201 - MYT4210). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 경쇄 CDR에서 2개 이상의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는, 당업계에 알려진 방법을 사용해 Expi293 세포를 a) 하나의 경쇄 조합 서열 변이체, 및 b) 상응하는 출발 ABPC 중쇄로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 7), 변이체의 pH 의존성을 Octet RED 96e 기기를 이용해 바이오층 간섭(BLI)을 사용해 평가하였다. 간략하게, SDS-PAGE 겔의 시각적 검사에 의해 결정된 변이체의 정성적 발현 수준에 기초하여 세포 배양 상청액을 희석하되, 고 발현 변이체의 경우 5 μL의 세포 배양 상청액을 195 μL의 1x PBST, pH 7.4에 희석하고, 중간 발현 변이체의 경우 25 μL의 세포 배양 상청액을 175 μL의 1x PBST, pH 7.4에 희석하고, 저 발현 변이체의 경우 100 μL의 세포 배양 상청액을 100 μL의 1x PBST, pH 7.4에 희석하여, 센서 팁 상에 로딩하였다. 그런 다음, 희석된 상청액을 항-인간 Fc 센서(Forte Bio) 상에 포획하였다. 1X PBST(50 mM 인산칼륨 완충액 + 150mM NaCl + 0.05% Tween 20) pH 7.4를 사용하여 베이스라인을 확립하고, 센서를 1X PBST pH 7.4 중에서 MET(cMET, Sino Biological 카달로그 번호 10692-H08H)와 120초 동안 결합시켜 결합 곡선을 생성하였다. 해리 단계에서, 센서 상의 항체-항원 복합체를 1X PBST pH 7.4에 300 내지 600초 동안 노출시켰다. 전체적으로 별도의 조건에서 1xPBST pH 5.4를 사용해 베이스라인, 결합, 및 해리를 반복하였다. pH 5.4 및 pH 7.4에서 출발 ABPC 항체(치환 없음) 및 각각의 상응하는 항체 변이체에 대한 결합 및 해리 단계 곡선을 조사하여 두 가지 기준을 알아냈다: a) 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라인 치환으로 인해 pH 5.4에서 해리가 강화됨(예를 들어 koff 값이 더 높음); 및 b) pH 5.4에서의 항체 변이체 자체 및 출발 ABPC(치환 없음)와 비교했을 때, pH 7.4에서 해리가 감소함(예를 들어 koff 값이 더 낮음). 도 8에 도시된 바와 같이, (출발 ABPC와 비교했을 때) pH 5.4에서 강화된 해리를 나타내거나, pH 7.4에서 감소된 해리를 나타내거나, 둘 다를 나타낸 경쇄 조합 변이체를 추가 분석을 위해 선택하였다(예: MYT4201, MYT4202, MYT4203, MYT4204, MYT4205, MYT4206, MYT4207, MYT4208, MYT4209, 및 MYT4210).
실시예 13.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있고, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용될 수 있다[Wang J 등의 (2017) ABBV-399, a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors, Irrespective of MET Pathway Dependence, Clin Cancer Res, 23:992-1000]. 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 텔리소투주맙(중쇄 서열번호 1, 경쇄 서열번호 2)을 선택하였다. 간략하게, 중쇄 및 경쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 실시예 9~12에서 추가 분석을 위해 이전에 선택한 중쇄 및 경쇄 CDR 내의 개별 아미노산 돌연변이를 한 번에 2개 이상씩 체계적으로 조합하였다(MYT3451 - MYT3492, MYT3603 - MYT3616, 및 MYT4211 - MYT4220). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 2개 이상의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는, 당업계에 알려진 방법을 사용해 Expi293 세포를 a) 하나의 경쇄 서열 변이체 또는 경쇄 조합 서열 변이체, 및 b) 하나의 중쇄 서열 변이체 또는 중쇄 조합 서열 변이체로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 9), 변이체의 pH 의존성을 Octet RED 96e 기기를 이용해 바이오층 간섭(BLI)을 사용해 평가하였다. 간략하게, SDS-PAGE 겔의 시각적 검사에 의해 결정된 변이체의 정성적 발현 수준에 기초하여 세포 배양 상청액을 희석하되, 고 발현 변이체의 경우 5 μL의 세포 배양 상청액을 195 μL의 1x PBST, pH 7.4에 희석하고, 중간 발현 변이체의 경우 25 μL의 세포 배양 상청액을 175 μL의 1x PBST, pH 7.4에 희석하고, 저 발현 변이체의 경우 100 μL의 세포 배양 상청액을 100 μL의 1x PBST, pH 7.4에 희석하여, 센서 팁 상에 로딩하였다. 그런 다음, 희석된 상청액을 항-인간 Fc 센서(Forte Bio) 상에 포획하였다. 1X PBST(50 mM 인산칼륨 완충액 + 150mM NaCl + 0.05% Tween 20) pH 7.4를 사용하여 베이스라인을 확립하고, 센서를 1X PBST pH 7.4 중 50 nM의 MET(cMET, Sino Biological 카달로그 번호 10692-H08H)와 120초 동안 결합시켜 결합 곡선을 생성하였다. 해리 단계에서, 센서 상의 항체-항원 복합체를 1X PBST pH 7.4에 300 내지 600초 동안 노출시켰다. 전체적으로 별도의 조건에서 1xPBST pH 5.4를 사용해 베이스라인, 결합, 및 해리를 반복하였다. pH 5.4 및 pH 7.4에서 출발 ABPC 항체(치환 없음) 및 각각의 상응하는 항체 변이체에 대한 결합 및 해리 단계 곡선을 조사하여 두 가지 기준을 알아냈다: a) 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라인 치환으로 인해 pH 5.4에서 해리가 강화됨(예를 들어 koff 값이 더 높음); 및 b) pH 5.4에서의 항체 변이체 자체 및 출발 ABPC(치환 없음)와 비교했을 때, pH 7.4에서 해리가 감소함(예를 들어 koff 값이 더 낮음). 도 10에 도시된 바와 같이, (출발 ABPC와 비교했을 때) pH 5.4에서 강화된 해리를 나타내거나, pH 7.4에서 감소된 해리를 나타내거나, 둘 다를 나타내는 페어링된 중쇄 및 경쇄 변이체를 추가 분석을 위해 선택하였다(MYT3451, MYT3452, MYT3453, MYT3454, MYT3455, MYT3456, MYT3457, MYT3459, MYT3460, MYT3463, MYT3465, MYT3466, MYT3467, MYT3468, MYT3469, MYT3471, MYT3473, MYT3474, MYT3476, MYT3477, MYT3479, MYT3480, MYT3481, MYT3482, MYT3483, MYT3484, MYT3485, MYT3487, MYT3488, MYT3491, MYT3603, MYT3604, MYT3605, MYT3606, MYT3607, MYT3608, MYT3609, MYT3610, MYT3611, MYT3612, MYT3614, MYT3615, MYT4211, MYT4212, MYT4214, MYT4217, 및 MYT4220).
실시예 14.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있고, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용될 수 있다[Wang J 등의 (2017) ABBV-399, a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors, Irrespective of MET Pathway Dependence, Clin Cancer Res, 23:992-1000]. 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 텔리소투주맙(중쇄 서열번호 1, 경쇄 서열번호 2)을 선택하였다. 간략하게, 중쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 실시예 9에서 추가 분석을 위해 이전에 선택한 중쇄 CDR 내의 개별 아미노산 돌연변이를 한 번에 2개 이상씩 체계적으로 조합하였다(MYT4951 - MYT4989). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 중쇄 CDR 내에 2개 이상의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는 당업계에 알려진 방법을 사용해 Expi293을: a) Wang J 등의 문헌[(2017) ABBV-399, a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors, Irrespective of MET Pathway Dependence, Clin Cancer Res, 23:992-1000]) 및 Dall, WF 등의 문헌["Increasing the Affinity of a Human IgG1 for the Neonatal Fc Receptor: Biological Consequences" The Journal of Immunology (2002); 169:5171-5180]에 각각 기술된 삼중 힌지(TH) 또는 YTE 돌연변이를 함유하는 하나의 중쇄 조합 서열 변이체; 및 b) 상응하는 출발 ABPC 경쇄로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 11), 단백질 A 자성 비드(Genscript L00273)를 사용해 정제하고, Detroit 562 세포(ATCC CCL-138) 상에서 엔도리소좀 전달에 대해 평가하였다. Detroit 562 세포(ATCC; CCL-138)를 수집하고 EMEM 배지(ATCC; 30-2003) + 10% GenClone 열 불활성화 소 태아 혈청(HI FBS)(Genesee Scientific; 25-514H)에 재현탁하였다. 트리판 블루 염색 및 Countess II FL 자동화 세포 계수기(Thermofisher; AMQAF1000)를 사용하여 세포 계수를 결정하였다. 그런 다음, 세포를 100,000개의 세포/mL로 희석하고, 100 ul을 바닥이 편평한 96-웰 세포 배양 플레이트에 시딩하고, 37℃, 5% CO2에서 밤새 부착시켰다. 그런 다음, 1차 항체를 천연 배양 배지에서 20 nM로 희석한 다음, 60 nM Incucyte 인간 FabFluor-pH 적색 항체 표지 시약(Sartorius; 4722)과 1:1로 혼합하였다. 혼합물을 실온에서 20분 동안 인큐베이션한 다음, 세포에 첨가하였다. 그런 다음, 플레이트를 즉시 Incucyte S3 Live-Cell 분석 시스템에 배치하여 이미지를 획득하고 분석하였다. 출발 ABPC(치환 없음) 및 각각의 상응하는 항체 변이체에 대해 엔도리소좀 전달을 조사하여, 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라닌 치환으로 인해 강화된 엔도리소좀 전달을 알아냈다. 도 12에 도시된 바와 같이, (출발 ABPC와 비교했을 때) 강화된 엔도리소좀 전달을 나타낸 중쇄 조합 변이체를 추가 분석을 위해 선택하였다(예: MYT4953 및 MYT4970). 선택된 변이체의 pH 의존성을 Octet RED 96e 기기를 이용해 바이오층 간섭(BLI)를 사용하여 평가하였다.
간략하게, SDS-PAGE 겔의 시각적 검사에 의해 결정된 변이체의 정성적 발현 수준에 기초하여 세포 배양 상청액을 희석하되, 고 발현 변이체의 경우 5 μL의 세포 배양 상청액을 195 μL의 1x PBST, pH 7.4에 희석하고, 중간 발현 변이체의 경우 25 μL의 세포 배양 상청액을 175 μL의 1x PBST, pH 7.4에 희석하고, 저 발현 변이체의 경우 100 μL의 세포 배양 상청액을 100 μL의 1x PBST, pH 7.4에 희석하여, 센서 팁 상에 로딩하였다. 그런 다음, 희석된 상청액을 항-인간 Fc 센서(Forte Bio) 상에 포획하였다. 1X PBST(50 mM 인산칼륨 완충액 + 150mM NaCl + 0.05% Tween 20) pH 7.4를 사용하여 베이스라인을 확립하고, 센서를 1X PBST pH 7.4 중에서 MET(cMET, Sino Biological 카달로그 번호 10692-H08H)와 120초 동안 결합시켜 결합 곡선을 생성하였다. 해리 단계에서, 센서 상의 항체-항원 복합체를 1X PBST pH 7.4 또는 pH 5.4에 300 내지 600초 동안 노출시켰다. 출발 ABPC 항체(치환 없음) 및 각각의 상응하는 항체 변이체에 대한 pH 5.4 및 pH 7.4에서의 결합 및 해리 단계 곡선을 조사하여 두 가지 기준을 알아냈다: a) 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라인 치환으로 인해 pH 5.4에서 해리가 강화됨(예를 들어 koff 값이 더 높음); 및 b) pH 5.4에서의 항체 변이체 자체 및 출발 ABPC(치환 없음)와 비교했을 때, pH 7.4에서 해리가 감소함(예를 들어 koff 값이 더 낮음). 도 13에 도시된 바와 같이, (출발 ABPC와 비교했을 때) pH 5.4에서 강화된 해리를 나타내거나, pH 7.4에서 감소된 해리를 나타내거나, 둘 다를 나타낸 중쇄 조합 변이체를 추가 분석을 위해 선택하였다(예: MYT4953 및 MYT4970).
실시예 15.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있고, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용될 수 있다[Wang J 등의 (2017) ABBV-399, a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors, Irrespective of MET Pathway Dependence, Clin Cancer Res, 23:992-1000]. 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 텔리소투주맙(중쇄 서열번호 1, 경쇄 서열번호 2)을 선택하였다. 간략하게, 경쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 실시예 10에서 추가 분석을 위해 이전에 선택한 경쇄 CDR 내의 개별 아미노산 돌연변이를 한 번에 2개 이상씩 체계적으로 조합하였다(MYT4990-4994). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 경쇄 CDR 내에 2개 이상의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는 당업계에 알려진 방법을 사용해 Expi293을: a) 하나의 경쇄 조합 서열 변이체; 및 b) Wang J 등의 문헌[(2017) ABBV-399, a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors, Irrespective of MET Pathway Dependence, Clin Cancer Res, 23:992-1000]) 및 Dall, WF 등의 문헌["Increasing the Affinity of a Human IgG1 for the Neonatal Fc Receptor: Biological Consequences" The Journal of Immunology (2002); 169:5171-5180]에 각각 기술된 삼중 힌지(TH) 또는 YTE 돌연변이를 함유하는 상응하는 출발 ABPC 중쇄로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 14), 단백질 A 자성 비드(Genscript L00273)를 사용해 정제하고, Detroit 562 세포(ATCC CCL-138) 상에서 엔도리소좀 전달에 대해 평가하였다. Detroit 562 세포(ATCC; CCL-138)를 수집하고 EMEM 배지(ATCC; 30-2003) + 10% GenClone 열 불활성화 소 태아 혈청(HI FBS)(Genesee Scientific; 25-514H)에 재현탁하였다. 트리판 블루 염색 및 Countess II FL 자동화 세포 계수기(Thermofisher; AMQAF1000)를 사용하여 세포 계수를 결정하였다. 그런 다음, 세포를 100,000개의 세포/mL로 희석하고, 100 ul을 바닥이 편평한 96-웰 세포 배양 플레이트에 시딩하고, 37℃ 5% CO2에서 밤새 부착시켰다. 그런 다음, 1차 항체를 천연 배양 배지에서 20 nM로 희석한 다음, 60 nM Incucyte 인간 FabFluor-pH 적색 항체 표지 시약(Sartorius; 4722)과 1:1로 혼합하였다. 혼합물을 실온에서 20분 동안 인큐베이션한 다음, 세포에 첨가하였다. 그런 다음, 플레이트를 즉시 Incucyte S3 Live-Cell 분석 시스템에 배치하여 이미지를 획득하고 분석하였다. 출발 ABPC(치환 없음) 및 각각의 상응하는 항체 변이체에 대해 엔도리소좀 전달을 조사하여, 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라닌 치환으로 인해 강화된 엔도리소좀 전달을 알아냈다.
실시예 16.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있으며, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용할 수 있다(Feng Y 등의 문헌["MET Antibody Drug Conjugate" US Patent Application US 2020/0061204 A1 (2020)]). 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 에미베투주맙(중쇄 서열번호 146, 경쇄 서열번호 147)을 선택하였다. 간략하게, 중쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 중쇄 CDR 내의 개별 아미노산 잔기를 히스티딘으로 한 번에 하나씩 체계적으로 치환하였다(MYT2314 - MYT2348). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 중쇄 CDR에서 단 하나의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는, 당업계에 알려진 방법을 사용해 Expi293 세포를 a) 하나의 중쇄 서열 변이체, 및 b) 상응하는 출발 ABPC 경쇄로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 22), 변이체의 pH 의존성을 Octet RED 96e 기기를 이용해 바이오층 간섭(BLI)을 사용해 평가하였다. 간략하게, SDS-PAGE 겔의 시각적 검사에 의해 결정된 변이체의 정성적 발현 수준에 기초하여 세포 배양 상청액을 희석하되, 고 발현 변이체의 경우 5 μL의 세포 배양 상청액을 195 μL의 1x PBST, pH 7.4에 희석하고, 중간 발현 변이체의 경우 25 μL의 세포 배양 상청액을 175 μL의 1x PBST, pH 7.4에 희석하고, 저 발현 변이체의 경우 100 μL의 세포 배양 상청액을 100 μL의 1x PBST, pH 7.4에 희석하여, 센서 팁 상에 로딩하였다. 그런 다음, 이렇게 희석된 상청액을 항-인간 Fc 센서(Forte Bio) 상에 포획하였다. 1X PBST(50 mM 인산칼륨 완충액 + 150mM NaCl + 0.05% Tween 20) pH 7.4를 사용하여 베이스라인을 확립하고, 센서를 1X PBST pH 7.4 중 50 nM의 MET(cMET, Sino Biological 카달로그 번호 10692-H08H)와 120초 동안 결합시켜 결합 곡선을 생성하였다. 해리 단계에서, 센서 상의 항체-항원 복합체를 1X PBST pH 7.4에 300 내지 600초 동안 노출시켰다. 전체적으로 별도의 조건에서 1xPBST pH 5.4를 사용해 베이스라인, 결합, 및 해리를 반복하였다.
pH 5.4 및 pH 7.4에서 출발 ABPC 항체(치환 없음) 및 각각의 상응하는 항체 변이체에 대한 결합 및 해리 단계 곡선을 조사하여 두 가지 기준을 알아냈다: a) 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라인 치환으로 인해 pH 5.4에서 해리가 강화됨(즉, koff 값이 더 높음); 및 b) pH 5.4에서의 항체 변이체 자체 및 출발 ABPC(치환 없음)와 비교했을 때, pH 7.4에서 해리가 감소함(즉, koff 값이 더 낮음). 도 23에 도시된 바와 같이, (출발 ABPC와 비교했을 때) pH 5.4에서 해리 강화를 나타내거나 pH 7.4에서 해리 감소를 나타내거나 둘 다를 나타내는 중쇄 변이체를 추가 분석을 위해 선택하였다(예: MYT2319, MYT2324, MYT2325, MYT2326, MYT2327, MYT2328, MYT2330, MYT2331, MYT2333, MYT2342, MYT2343, MYT2344, 및 MYT2347). 또한, 일부 히스티딘 및 알라닌 돌연변이는 MET 결합을 제거한 반면(예: MYT2341), 다른 돌연변이는 MET 결합 동역학을 거의 변화시키지 않았거나(예: 해리 상수 KD 또는 해리 속도의 1배 미만 변화) 전혀 변화시키지 않았음에 주목하였다(예: MYT2314, MYT2315, MYT2316, MYT2317, MYT2318, MYT2320, MYT2321, MYT2322, MYT2323, MYT2329, MYT2332, MYT2334, MYT2335, MYT2336, MYT2337, MYT2338, MYT2339, MYT2340, MYT2345, MYT2346, 및 MYT2348).
특히, 히스티딘은 크고 양으로 하전된 아미노산이기 때문에, 변화가 없는 이들 변이체는 광범위한 돌연변이를 견딜 수 있고, 서열은 상이하지만 유사한 결합 특성을 갖는 항체로 유도할 수 있는 중쇄 내 위치로서 (명칭은 달리 명백하지 않음) 주목하였다.
실시예 17.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있으며, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용할 수 있다(Feng Y 등의 문헌["MET Antibody Drug Conjugate" US Patent Application US 2020/0061204 A1 (2020)]). 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 에미베투주맙(중쇄 서열번호 146, 경쇄 서열번호 147)을 선택하였다. 간략하게, 경쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 경쇄 CDR 내의 개별 아미노산 잔기를 히스티딘으로 한 번에 하나씩 체계적으로 치환하였다(MYT3958 - MYT3985). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 경쇄 CDR에서 단 하나의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는, 당업계에 알려진 방법을 사용해 Expi293 세포를 a) 하나의 경쇄 서열 변이체, 및 b) 상응하는 출발 ABPC 중쇄로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 24), 변이체의 pH 의존성을 Octet RED 96e 기기를 이용해 바이오층 간섭(BLI)을 사용해 평가하였다. 간략하게, SDS-PAGE 겔의 시각적 검사에 의해 결정된 변이체의 정성적 발현 수준에 기초하여 세포 배양 상청액을 희석하되, 고 발현 변이체의 경우 5 μL의 세포 배양 상청액을 195 μL의 1x PBST, pH 7.4에 희석하고, 중간 발현 변이체의 경우 25 μL의 세포 배양 상청액을 175 μL의 1x PBST, pH 7.4에 희석하고, 저 발현 변이체의 경우 100 μL의 세포 배양 상청액을 100 μL의 1x PBST, pH 7.4에 희석하여, 센서 팁 상에 로딩하였다. 그런 다음, 희석된 상청액을 항-인간 Fc 센서(Forte Bio) 상에 포획하였다. 1X PBST(50 mM 인산칼륨 완충액 + 150mM NaCl + 0.05% Tween 20) pH 7.4를 사용하여 베이스라인을 확립하고, 센서를 1X PBST pH 7.4 중 50 nM의 MET(cMET, Sino Biological 카달로그 번호 10692-H08H)와 120초 동안 결합시켜 결합 곡선을 생성하였다. 해리 단계에서, 센서 상의 항체-항원 복합체를 1X PBST pH 7.4에 300 내지 600초 동안 노출시켰다. 전체적으로 별도의 조건에서 1xPBST pH 5.4를 사용해 베이스라인, 결합, 및 해리를 반복하였다. pH 5.4 및 pH 7.4에서 출발 ABPC 항체(치환 없음) 및 각각의 상응하는 항체 변이체에 대한 결합 및 해리 단계 곡선을 조사하여 두 가지 기준을 알아냈다: a) 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라인 치환으로 인해 pH 5.4에서 해리가 강화됨(즉, koff 값이 더 높음); 및 b) pH 5.4에서의 항체 변이체 자체 및 출발 ABPC(치환 없음)와 비교했을 때, pH 7.4에서 해리가 감소함(즉, koff 값이 더 낮음). 도 25에 도시된 바와 같이, (출발 ABPC와 비교했을 때) pH 5.4에서 강화된 해리를 나타내거나, pH 7.4에서 감소된 해리를 나타내거나, 둘 다를 나타낸 경쇄 변이체를 추가 분석을 위해 선택하였다(예: MYT3959, MYT3960, MYT3963, MYT3966, MYT3967, MYT3969, MYT3970, MYT3978, MYT3979, MYT3982, MYT3983, 및 MYT3984). 또한, 일부 히스티딘 및 알라닌 돌연변이는 MET 결합 동역학을 거의 변화시키지 않았거나(예를 들어 KD 또는 해리 속도에 있어서 1배 미만의 변화) 전혀 변화시키지 않았음을 주목하였다(예: MYT3958, MYT3961, MYT3962, MYT3964, MYT3965, MYT3968, MYT3971, MYT3972, MYT3973, MYT3974, MYT3975, MYT3976, MYT3977, MYT3980, MYT3981, 및
MYT3985). 특히, 히스티딘은 크고 양으로 하전된 아미노산이기 때문에, 변화가 없는 이들 변이체는 광범위한 돌연변이를 견딜 수 있고, 서열은 상이하지만 유사한 결합 특성을 갖는 항체를 유도할 수 있는 경쇄 내 위치로서 주목하였다(명칭은 달리 명백하지 않음).
실시예 18.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있으며, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용할 수 있다(Feng Y 등의 문헌["MET Antibody Drug Conjugate" US Patent Application US 2020/0061204 A1 (2020)]). 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 에미베투주맙(중쇄 서열번호 146, 경쇄 서열번호 147)을 선택하였다. 간략하게, 중쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 실시예 16에서 추가 분석을 위해 이전에 선택한 중쇄 CDR 내의 개별 아미노산 돌연변이를 한 번에 2개 이상씩 체계적으로 조합하였다(MYT2848 - MYT2867). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 중쇄 CDR에서 2개 이상의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는, 당업계에 알려진 방법을 사용해 Expi293 세포를 a) 하나의 중쇄 조합 서열 변이체, 및 b) 상응하는 출발 ABPC 경쇄로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 26), 변이체의 pH 의존성을 Octet RED 96e 기기를 이용해 바이오층 간섭(BLI)을 사용해 평가하였다. 간략하게, SDS-PAGE 겔의 시각적 검사에 의해 결정된 변이체의 정성적 발현 수준에 기초하여 세포 배양 상청액을 희석하되, 고 발현 변이체의 경우 5 μL의 세포 배양 상청액을 195 μL의 1x PBST, pH 7.4에 희석하고, 중간 발현 변이체의 경우 25 μL의 세포 배양 상청액을 175 μL의 1x PBST, pH 7.4에 희석하고, 저 발현 변이체의 경우 100 μL의 세포 배양 상청액을 100 μL의 1x PBST, pH 7.4에 희석하여, 센서 팁 상에 로딩하였다. 그런 다음, 희석된 상청액을 항-인간 Fc 센서(Forte Bio) 상에 포획하였다. 1X PBST(50 mM 인산칼륨 완충액 + 150mM NaCl + 0.05% Tween 20) pH 7.4를 사용하여 베이스라인을 확립하고, 센서를 1X PBST pH 7.4 중 50 nM의 MET(cMET, Sino Biological 카달로그 번호 10692-H08H)와 120초 동안 결합시켜 결합 곡선을 생성하였다. 해리 단계에서, 센서 상의 항체-항원 복합체를 1X PBST pH 7.4에 300 내지 600초 동안 노출시켰다. 전체적으로 별도의 조건에서 1xPBST pH 5.4를 사용해 베이스라인, 결합, 및 해리를 반복하였다. pH 5.4 및 pH 7.4에서 출발 ABPC 항체(치환 없음) 및 각각의 상응하는 항체 변이체에 대한 결합 및 해리 단계 곡선을 조사하여 두 가지 기준을 알아냈다: a) 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라인 치환으로 인해 pH 5.4에서 해리가 강화됨(즉, koff 값이 더 높음); 및 b) pH 5.4에서의 항체 변이체 자체 및 출발 ABPC(치환 없음)와 비교했을 때, pH 7.4에서 해리가 감소함(즉, koff 값이 더 낮음). 도 27에 도시된 바와 같이, (출발 ABPC와 비교했을 때) pH 5.4에서 강화된 해리를 나타내거나, pH 7.4에서 감소된 해리를 나타내거나, 둘 다를 나타낸 중쇄 조합 변이체를 추가 분석을 위해 선택하였다(예: MYT2848, MYT2849, MYT2850, MYT2851, MYT2852, MYT2853, MYT2854, MYT2855, MYT2856, MYT2857, MYT2858, MYT2859, MYT2861, MYT2862, MYT2863, MYT2864, MYT2865, MYT2866, 및 MYT2867).
실시예 19.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있으며, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용할 수 있다(Feng Y 등의 문헌["MET Antibody Drug Conjugate" US Patent Application US 2020/0061204 A1 (2020)]). 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 에미베투주맙(중쇄 서열번호 146, 경쇄 서열번호 147)을 선택하였다. 간략하게, 경쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 실시예 17에서 추가 분석을 위해 이전에 선택한 경쇄 CDR 내의 개별 아미노산 돌연변이를 한 번에 2개 이상씩 체계적으로 조합하였다(MYT4326 - MYT4345). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 경쇄 CDR에서 2개 이상의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는, 당업계에 알려진 방법을 사용해 Expi293 세포를 a) 하나의 경쇄 조합 서열 변이체, 및 b) 상응하는 출발 ABPC 중쇄로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 28), 변이체의 pH 의존성을 Octet RED 96e 기기를 이용해 바이오층 간섭(BLI)을 사용해 평가하였다. 간략하게, SDS-PAGE 겔의 시각적 검사에 의해 결정된 변이체의 정성적 발현 수준에 기초하여 세포 배양 상청액을 희석하되, 고 발현 변이체의 경우 5 μL의 세포 배양 상청액을 195 μL의 1x PBST, pH 7.4에 희석하고, 중간 발현 변이체의 경우 25 μL의 세포 배양 상청액을 175 μL의 1x PBST, pH 7.4에 희석하고, 저 발현 변이체의 경우 100 μL의 세포 배양 상청액을 100 μL의 1x PBST, pH 7.4에 희석하여, 센서 팁 상에 로딩하였다. 그런 다음, 희석된 상청액을 항-인간 Fc 센서(Forte Bio) 상에 포획하였다. 1X PBST(50 mM 인산칼륨 완충액 + 150mM NaCl + 0.05% Tween 20) pH 7.4를 사용하여 베이스라인을 확립하고, 센서를 1X PBST pH 7.4 중에서 MET(cMET, Sino Biological 카달로그 번호 10692-H08H)와 120초 동안 결합시켜 결합 곡선을 생성하였다. 해리 단계에서, 센서 상의 항체-항원 복합체를 1X PBST pH 7.4에 300 내지 600초 동안 노출시켰다. 전체적으로 별도의 조건에서 1xPBST pH 5.4를 사용해 베이스라인, 결합, 및 해리를 반복하였다. pH 5.4 및 pH 7.4에서 출발 ABPC 항체(치환 없음) 및 각각의 상응하는 항체 변이체에 대한 결합 및 해리 단계 곡선을 조사하여 두 가지 기준을 알아냈다: a) 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라인 치환으로 인해 pH 5.4에서 해리가 강화됨(예를 들어 koff 값이 더 높음); 및 b) pH 5.4에서의 항체 변이체 자체 및 출발 ABPC(치환 없음)와 비교했을 때, pH 7.4에서 해리가 감소함(예를 들어 koff 값이 더 낮음). 도 29에 도시된 바와 같이, (출발 ABPC와 비교했을 때) pH 5.4에서 강화된 해리를 나타내거나, pH 7.4에서 감소된 해리를 나타내거나, 둘 다를 나타낸 경쇄 조합 변이체를 추가 분석을 위해 선택하였다(예: MYT4326, MYT4327, MYT4328, MYT4329, MYT4330, MYT4331, MYT4332, MYT4333, MYT4334, MYT4335, MYT4336, MYT4337, MYT4338, MYT4339, MYT4340, MYT4342, MYT4343).
실시예 20.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있으며, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용할 수 있다(Feng Y 등의 문헌["MET Antibody Drug Conjugate" US Patent Application US 2020/0061204 A1 (2020)]). 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 에미베투주맙(중쇄 서열번호 146, 경쇄 서열번호 147)을 선택하였다. 간략하게, 중쇄 및 경쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 실시예 16~19에서 추가 분석을 위해 이전에 선택한 중쇄 및 경쇄 CDR 내의 개별 아미노산 돌연변이를 한 번에 2개 이상씩 체계적으로 조합하였다(MYT3999 - MYT4042). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 2개 이상의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는, 당업계에 알려진 방법을 사용해 Expi293 세포를 a) 하나의 경쇄 서열 변이체 또는 경쇄 조합 서열 변이체, 및 b) 하나의 중쇄 서열 변이체 또는 중쇄 조합 서열 변이체로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 30), 변이체의 pH 의존성을 Octet RED 96e 기기를 이용해 바이오층 간섭(BLI)을 사용해 평가하였다. 간략하게, SDS-PAGE 겔의 시각적 검사에 의해 결정된 변이체의 정성적 발현 수준에 기초하여 세포 배양 상청액을 희석하되, 고 발현 변이체의 경우 5 μL의 세포 배양 상청액을 195 μL의 1x PBST, pH 7.4에 희석하고, 중간 발현 변이체의 경우 25 μL의 세포 배양 상청액을 175 μL의 1x PBST, pH 7.4에 희석하고, 저 발현 변이체의 경우 100 μL의 세포 배양 상청액을 100 μL의 1x PBST, pH 7.4에 희석하여, 센서 팁 상에 로딩하였다. 그런 다음, 희석된 상청액을 항-인간 Fc 센서(Forte Bio) 상에 포획하였다. 1X PBST(50 mM 인산칼륨 완충액 + 150mM NaCl + 0.05% Tween 20) pH 7.4를 사용하여 베이스라인을 확립하고, 센서를 1X PBST pH 7.4 중 50 nM의 MET(cMET, Sino Biological 카달로그 번호 10692-H08H)와 120초 동안 결합시켜 결합 곡선을 생성하였다. 해리 단계에서, 센서 상의 항체-항원 복합체를 1X PBST pH 7.4에 300 내지 600초 동안 노출시켰다. 전체적으로 별도의 조건에서 1xPBST pH 5.4를 사용해 베이스라인, 결합, 및 해리를 반복하였다. pH 5.4 및 pH 7.4에서 출발 ABPC 항체(치환 없음) 및 각각의 상응하는 항체 변이체에 대한 결합 및 해리 단계 곡선을 조사하여 두 가지 기준을 알아냈다: a) 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라인 치환으로 인해 pH 5.4에서 해리가 강화됨(예를 들어 koff 값이 더 높음); 및 b) pH 5.4에서의 항체 변이체 자체 및 출발 ABPC(치환 없음)와 비교했을 때, pH 7.4에서 해리가 감소함(예를 들어 koff 값이 더 낮음). 도 31에 도시된 바와 같이, (출발 ABPC와 비교했을 때) pH 5.4에서 강화된 해리를 나타내거나, pH 7.4에서 감소된 해리를 나타내거나, 둘 다를 나타낸 페어링된 중쇄 및 경쇄 변이체를 추가 분석을 위해 선택하였다(예: MYT3999, MYT4000, MYT4001, MYT4002, MYT4003, MYT4004, MYT4005, MYT4006, MYT4007, MYT4008, MYT4009, MYT4010, MYT4011, MYT4012, MYT4013, MYT4014, MYT4015, MYT4016, MYT4017, MYT4018, MYT4019, MYT4023, MYT4027, MYT4032, MYT4033, MYT4034, MYT4035, MYT4036, MYT4037, MYT4038, MYT4039, MYT4040, MYT4041, 및 MYT4042).
실시예 21.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있으며, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용할 수 있다(Feng Y 등의 문헌["MET Antibody Drug Conjugate" US Patent Application US 2020/0061204 A1 (2020)]). 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 에미베투주맙(중쇄 서열번호 146, 경쇄 서열번호 147)을 선택하였다. 간략하게, 중쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 실시예 16에서 추가 분석을 위해 이전에 선택한 중쇄 CDR 내의 개별 아미노산 돌연변이를 한 번에 2개 이상씩 체계적으로 조합하였다(MYT4995 - MYT5041). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 중쇄 CDR 내에 2개 이상의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는 당업계에 알려진 방법을 사용해 Expi293을: a) Wang J 등의 문헌[(2017) ABBV-399, a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors, Irrespective of MET Pathway Dependence, Clin Cancer Res, 23:992-1000]) 및 Dall, WF 등의 문헌["Increasing the Affinity of a Human IgG1 for the Neonatal Fc Receptor: Biological Consequences" The Journal of Immunology (2002); 169:5171-5180]에 각각 기술된 삼중 힌지(TH) 또는 YTE 돌연변이를 함유하는 하나의 중쇄 조합 서열 변이체; 및 b) 상응하는 출발 ABPC 경쇄로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 32), 단백질 A 자성 비드(Genscript L00273)를 사용해 정제하고, Detroit 562 세포(ATCC CCL-138) 상에서 엔도리소좀 전달에 대해 평가하였다. Detroit 562 세포(ATCC; CCL-138)를 수집하고 EMEM 배지(ATCC; 30-2003) + 10% GenClone 열 불활성화 소 태아 혈청(HI FBS)(Genesee Scientific; 25-514H)에 재현탁하였다. 트리판 블루 염색 및 Countess II FL 자동화 세포 계수기(Thermofisher; AMQAF1000)를 사용하여 세포 계수를 결정하였다. 그런 다음, 세포를 100,000개의 세포/mL로 희석하고, 100 ul을 바닥이 편평한 96-웰 세포 배양 플레이트에 시딩하고, 37℃ 5% CO2에서 밤새 부착시켰다. 그런 다음, 1차 항체를 천연 배양 배지에서 20 nM로 희석한 다음, 60 nM Incucyte 인간 FabFluor-pH 적색 항체 표지 시약(Sartorius; 4722)과 1:1로 혼합하였다. 혼합물을 실온에서 20분 동안 인큐베이션한 다음, 세포에 첨가하였다. 그런 다음, 플레이트를 즉시 Incucyte S3 Live-Cell 분석 시스템에 배치하여 이미지를 획득하고 분석하였다. 출발 ABPC(치환 없음) 및 각각의 상응하는 항체 변이체에 대해 엔도리소좀 전달을 조사하여, 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라닌 치환으로 인해 강화된 엔도리소좀 전달을 알아냈다.
실시예 22.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있으며, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용할 수 있다(Hicks, SW 및 Lai, K의 "MET Antibodies and Immunoconjugates and uses thereof" 국제 특허 출원 WO 2020/014306 A1 (2020)). 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 hucMET27Gv1.3(중쇄 서열번호 304, 경쇄 서열번호 305)을 선택하였다. 간략하게, 중쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 중쇄 CDR 내의 개별 아미노산 잔기를 히스티딘으로 한 번에 하나씩 체계적으로 치환하였다(MYT3618 - MYT3655). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 중쇄 CDR에서 단 하나의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는, 당업계에 알려진 방법을 사용해 Expi293 세포를 a) 하나의 중쇄 서열 변이체, 및 b) 상응하는 출발 ABPC 경쇄로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 39), 변이체의 pH 의존성을 Octet RED 96e 기기를 이용해 바이오층 간섭(BLI)을 사용해 평가하였다. 간략하게, SDS-PAGE 겔의 시각적 검사에 의해 결정된 변이체의 정성적 발현 수준에 기초하여 세포 배양 상청액을 희석하되, 고 발현 변이체의 경우 5 μL의 세포 배양 상청액을 195 μL의 1x PBST, pH 7.4에 희석하고, 중간 발현 변이체의 경우 25 μL의 세포 배양 상청액을 175 μL의 1x PBST, pH 7.4에 희석하고, 저 발현 변이체의 경우 100 μL의 세포 배양 상청액을 100 μL의 1x PBST, pH 7.4에 희석하여, 센서 팁 상에 로딩하였다. 그런 다음, 희석된 상청액을 항-인간 Fc 센서(Forte Bio) 상에 포획하였다. 1X PBST(50 mM 인산칼륨 완충액 + 150mM NaCl + 0.05% Tween 20) pH 7.4를 사용하여 베이스라인을 확립하고, 센서를 1X PBST pH 7.4 중 50 nM의 MET(cMET, Sino Biological 카달로그 번호 10692-H08H)와 120초 동안 결합시켜 결합 곡선을 생성하였다. 해리 단계에서, 센서 상의 항체-항원 복합체를 1X PBST pH 7.4에 300 내지 600초 동안 노출시켰다. 전체적으로 별도의 조건에서 1xPBST pH 5.4를 사용해 베이스라인, 결합, 및 해리를 반복하였다. pH 5.4 및 pH 7.4에서 출발 ABPC 항체(치환 없음) 및 각각의 상응하는 항체 변이체에 대한 결합 및 해리 단계 곡선을 조사하여 두 가지 기준을 알아냈다: a) 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라인 치환으로 인해 pH 5.4에서 해리가 강화됨(즉, koff 값이 더 높음); 및 b) pH 5.4에서의 항체 변이체 자체 및 출발 ABPC(치환 없음)와 비교했을 때, pH 7.4에서 해리가 감소함(즉, koff 값이 더 낮음). 도 40에 도시된 바와 같이, (출발 ABPC와 비교했을 때) pH 5.4에서 강화된 해리를 나타내거나, pH 7.4에서 감소된 해리를 나타내거나, 둘 다를 나타낸 중쇄 변이체를 추가 분석을 위해 선택하였다(예: MYT3619, MYT3626, MYT3627, MYT3628, MYT3629, MYT3630, MYT3632, MYT3633, MYT3634, MYT3635, MYT3636, MYT3637, MYT3638, MYT3639, MYT3640, MYT3641, MYT3642, MYT3643, MYT3646, MYT3647, MYT3651, 및 MYT3653). 또한, 일부 히스티딘 및 알라닌 돌연변이는 MET 결합을 제거한 반면(예: MYT3624, MYT3645, MYT3648, MYT3649, MYT3650, MYT3652, 및
MYT3654), 다른 돌연변이는 MET 결합 동역학을 거의 변화시키지 않았거나(예를 들어 KD 또는 해리 속도에 있어서 1배 미만의 변화) 전혀 변화시키지 않았음을 주목하였다(예: MYT3618, MYT3620, MYT3621, MYT3622, MYT3623, MYT3625, MYT3631, MYT3644, 및 MYT3655).
특히, 히스티딘은 크고 양으로 하전된 아미노산이기 때문에, 변화가 없는 이들 변이체는 광범위한 돌연변이를 견딜 수 있고, 서열은 상이하지만 유사한 결합 특성을 갖는 항체로 유도할 수 있는 중쇄 내 위치로서 (명칭은 달리 명백하지 않음) 주목하였다.
실시예 23.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있으며, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용할 수 있다(Hicks, SW 및 Lai, K의 "MET Antibodies and Immunoconjugates and uses thereof" 국제 특허 출원 WO 2020/014306 A1 (2020)). 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 hucMET27Gv1.3(중쇄 서열번호 304, 경쇄 서열번호 305)을 선택하였다. 간략하게, 경쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 경쇄 CDR 내의 개별 아미노산 잔기를 히스티딘으로 한 번에 하나씩 체계적으로 치환하였다(MYT3656 - MYT3686). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 경쇄 CDR에서 단 하나의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는, 당업계에 알려진 방법을 사용해 Expi293 세포를 a) 하나의 경쇄 서열 변이체, 및 b) 상응하는 출발 ABPC 중쇄로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 41), 변이체의 pH 의존성을 Octet RED 96e 기기를 이용해 바이오층 간섭(BLI)을 사용해 평가하였다. 간략하게, SDS-PAGE 겔의 시각적 검사에 의해 결정된 변이체의 정성적 발현 수준에 기초하여 세포 배양 상청액을 희석하되, 고 발현 변이체의 경우 5 μL의 세포 배양 상청액을 195 μL의 1x PBST, pH 7.4에 희석하고, 중간 발현 변이체의 경우 25 μL의 세포 배양 상청액을 175 μL의 1x PBST, pH 7.4에 희석하고, 저 발현 변이체의 경우 100 μL의 세포 배양 상청액을 100 μL의 1x PBST, pH 7.4에 희석하여, 센서 팁 상에 로딩하였다. 그런 다음, 희석된 상청액을 항-인간 Fc 센서(Forte Bio) 상에 포획하였다. 1X PBST(50 mM 인산칼륨 완충액 + 150mM NaCl + 0.05% Tween 20) pH 7.4를 사용하여 베이스라인을 확립하고, 센서를 1X PBST pH 7.4 중 50 nM의 MET(cMET, Sino Biological 카달로그 번호 10692-H08H)와 120초 동안 결합시켜 결합 곡선을 생성하였다. 해리 단계에서, 센서 상의 항체-항원 복합체를 1X PBST pH 7.4에 300 내지 600초 동안 노출시켰다. 전체적으로 별도의 조건에서 1xPBST pH 5.4를 사용해 베이스라인, 결합, 및 해리를 반복하였다. pH 5.4 및 pH 7.4에서 출발 ABPC 항체(치환 없음) 및 각각의 상응하는 항체 변이체에 대한 결합 및 해리 단계 곡선을 조사하여 두 가지 기준을 알아냈다: a) 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라인 치환으로 인해 pH 5.4에서 해리가 강화됨(즉, koff 값이 더 높음); 및 b) pH 5.4에서의 항체 변이체 자체 및 출발 ABPC(치환 없음)와 비교했을 때, pH 7.4에서 해리가 감소함(즉, koff 값이 더 낮음). 도 42에 도시된 바와 같이, (출발 ABPC와 비교했을 때) pH 5.4에서 강화된 해리를 나타내거나, pH 7.4에서 감소된 해리를 나타내거나, 둘 다를 나타낸 경쇄 변이체를 추가 분석을 위해 선택하였다(예: MYT3658, MYT3662, MYT3663, MYT3666, MYT3668, MYT3670, MYT3671, MYT3673, MYT3674, MYT3677, MYT3678, MYT3680, MYT3684, 및 MYT3686). 또한, 일부 히스티딘 및 알라닌 돌연변이는 MET 결합 동역학을 거의 변화시키지 않았거나(예를 들어 KD 또는 해리 속도에 있어서 1배 미만의 변화) 전혀 변화시키지 않았음을 주목하였다(예: MYT3656, MYT3657, MYT3659, MYT3660, MYT3661, MYT3664, MYT3667, MYT3675, MYT3679, MYT3681, MYT3682, MYT3683, 및 MYT3685). 특히, 히스티딘은 크고 양으로 하전된 아미노산이기 때문에, 변화가 없는 이들 변이체는 광범위한 돌연변이를 견딜 수 있고, 서열은 상이하지만 유사한 결합 특성을 갖는 항체를 유도할 수 있는 경쇄 내 위치로서 주목하였다(명칭은 달리 명백하지 않음).
실시예 24.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있으며, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용할 수 있다(Hicks, SW 및 Lai, K의 "MET Antibodies and Immunoconjugates and uses thereof" 국제 특허 출원 WO 2020/014306 A1 (2020)). 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 hucMET27Gv1.3(중쇄 서열번호 304, 경쇄 서열번호 305)을 선택하였다. 간략하게, 중쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 실시예 22에서 추가 분석을 위해 이전에 선택한 중쇄 CDR 내의 개별 아미노산 돌연변이를 한 번에 2개 이상씩 체계적으로 조합하였다(MYT4285 - MYT4304). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 중쇄 CDR에서 2개 이상의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는, 당업계에 알려진 방법을 사용해 Expi293 세포를 a) 하나의 중쇄 조합 서열 변이체, 및 b) 상응하는 출발 ABPC 경쇄로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 43), 변이체의 pH 의존성을 Octet RED 96e 기기를 이용해 바이오층 간섭(BLI)을 사용해 평가하였다. 간략하게, SDS-PAGE 겔의 시각적 검사에 의해 결정된 변이체의 정성적 발현 수준에 기초하여 세포 배양 상청액을 희석하되, 고 발현 변이체의 경우 5 μL의 세포 배양 상청액을 195 μL의 1x PBST, pH 7.4에 희석하고, 중간 발현 변이체의 경우 25 μL의 세포 배양 상청액을 175 μL의 1x PBST, pH 7.4에 희석하고, 저 발현 변이체의 경우 100 μL의 세포 배양 상청액을 100 μL의 1x PBST, pH 7.4에 희석하여, 센서 팁 상에 로딩하였다. 그런 다음, 희석된 상청액을 항-인간 Fc 센서(Forte Bio) 상에 포획하였다. 1X PBST(50 mM 인산칼륨 완충액 + 150mM NaCl + 0.05% Tween 20) pH 7.4를 사용하여 베이스라인을 확립하고, 센서를 1X PBST pH 7.4 중 50 nM의 MET(cMET, Sino Biological 카달로그 번호 10692-H08H)와 120초 동안 결합시켜 결합 곡선을 생성하였다. 해리 단계에서, 센서 상의 항체-항원 복합체를 1X PBST pH 7.4에 300 내지 600초 동안 노출시켰다. 전체적으로 별도의 조건에서 1xPBST pH 5.4를 사용해 베이스라인, 결합, 및 해리를 반복하였다. pH 5.4 및 pH 7.4에서 출발 ABPC 항체(치환 없음) 및 각각의 상응하는 항체 변이체에 대한 결합 및 해리 단계 곡선을 조사하여 두 가지 기준을 알아냈다: a) 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라인 치환으로 인해 pH 5.4에서 해리가 강화됨(즉, koff 값이 더 높음); 및 b) pH 5.4에서의 항체 변이체 자체 및 출발 ABPC(치환 없음)와 비교했을 때, pH 7.4에서 해리가 감소함(즉, koff 값이 더 낮음).
도 44에 도시된 바와 같이, (출발 ABPC와 비교했을 때) pH 5.4에서 강화된 해리를 나타내거나, pH 7.4에서 감소된 해리를 나타내거나, 둘 다를 나타내는 중쇄 조합 변이체를 추가 분석을 위해 선택하였다(예: MYT4285, MYT4286, MYT4287, MYT4288, MYT4289, MYT4290, MYT4291, MYT4292, MYT4293, MYT4294, MYT4296, MYT4297, MYT4299, MYT4300, MYT4301, MYT4302, MYT4303, 및 MYT4304).
실시예 25.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있으며, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용할 수 있다(Hicks, SW 및 Lai, K의 "MET Antibodies and Immunoconjugates and uses thereof" 국제 특허 출원 WO 2020/014306 A1 (2020)). 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 hucMET27Gv1.3(중쇄 서열번호 304, 경쇄 서열번호 305)을 선택하였다. 간략하게, 경쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 실시예 23에서 추가 분석을 위해 이전에 선택한 경쇄 CDR 내의 개별 아미노산 돌연변이를 한 번에 2개 이상씩 체계적으로 조합하였다(MYT4224 - MYT4241). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 경쇄 CDR에서 2개 이상의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는, 당업계에 알려진 방법을 사용해 Expi293 세포를 a) 하나의 경쇄 조합 서열 변이체, 및 b) 상응하는 출발 ABPC 중쇄로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 45), 변이체의 pH 의존성을 Octet RED 96e 기기를 이용해 바이오층 간섭(BLI)을 사용해 평가하였다. 간략하게, SDS-PAGE 겔의 시각적 검사에 의해 결정된 변이체의 정성적 발현 수준에 기초하여 세포 배양 상청액을 희석하되, 고 발현 변이체의 경우 5 μL의 세포 배양 상청액을 195 μL의 1x PBST, pH 7.4에 희석하고, 중간 발현 변이체의 경우 25 μL의 세포 배양 상청액을 175 μL의 1x PBST, pH 7.4에 희석하고, 저 발현 변이체의 경우 100 μL의 세포 배양 상청액을 100 μL의 1x PBST, pH 7.4에 희석하여, 센서 팁 상에 로딩하였다. 그런 다음, 희석된 상청액을 항-인간 Fc 센서(Forte Bio) 상에 포획하였다. 1X PBST(50 mM 인산칼륨 완충액 + 150mM NaCl + 0.05% Tween 20) pH 7.4를 사용하여 베이스라인을 확립하고, 센서를 1X PBST pH 7.4 중에서 MET(cMET, Sino Biological 카달로그 번호 10692-H08H)와 120초 동안 결합시켜 결합 곡선을 생성하였다. 해리 단계에서, 센서 상의 항체-항원 복합체를 1X PBST pH 7.4에 300 내지 600초 동안 노출시켰다. 전체적으로 별도의 조건에서 1xPBST pH 5.4를 사용해 베이스라인, 결합, 및 해리를 반복하였다. pH 5.4 및 pH 7.4에서 출발 ABPC 항체(치환 없음) 및 각각의 상응하는 항체 변이체에 대한 결합 및 해리 단계 곡선을 조사하여 두 가지 기준을 알아냈다: a) 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라인 치환으로 인해 pH 5.4에서 해리가 강화됨(예를 들어 koff 값이 더 높음); 및 b) pH 5.4에서의 항체 변이체 자체 및 출발 ABPC(치환 없음)와 비교했을 때, pH 7.4에서 해리가 감소함(예를 들어 koff 값이 더 낮음). 도 46에 도시된 바와 같이, (출발 ABPC와 비교했을 때) pH 5.4에서 강화된 해리를 나타내거나, pH 7.4에서 감소된 해리를 나타내거나, 둘 다를 나타낸 경쇄 조합 변이체를 추가 분석을 위해 선택하였다(예: MYT4224, MYT4225, MYT4226, MYT4227, MYT4228, MYT4229, MYT4230, MYT4231, MYT4232, MYT4233, MYT4234, MYT4235, MYT4236, MYT4237, MYT4238, MYT4239, MYT4240, 및 MYT4241).
실시예 26.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있으며, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용할 수 있다(Hicks, SW 및 Lai, K의 "MET Antibodies and Immunoconjugates and uses thereof" 국제 특허 출원 WO 2020/014306 A1 (2020)). 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 hucMET27Gv1.3(중쇄 서열번호 304, 경쇄 서열번호 305)을 선택하였다. 간략하게, 중쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 실시예 22에서 추가 분석을 위해 이전에 선택한 중쇄 CDR 내의 개별 아미노산 돌연변이를 한 번에 2개 이상씩 체계적으로 조합하였다(MYT5296 및 MYT5042 - MYT5065). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 중쇄 CDR 내에 2개 이상의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는 당업계에 알려진 방법을 사용해 Expi293을: a) Wang J 등의 문헌[(2017) ABBV-399, a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors, Irrespective of MET Pathway Dependence, Clin Cancer Res, 23:992-1000]) 및 Dall, WF 등의 문헌["Increasing the Affinity of a Human IgG1 for the Neonatal Fc Receptor: Biological Consequences" The Journal of Immunology (2002); 169:5171-5180]에 각각 기술된 삼중 힌지(TH) 또는 YTE 돌연변이를 함유하는 하나의 중쇄 조합 서열 변이체; 및 b) 상응하는 출발 ABPC 경쇄로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 47), 단백질 A 자성 비드(Genscript L00273)를 사용해 정제하고, Detroit 562 세포(ATCC CCL-138) 상에서 엔도리소좀 전달에 대해 평가하였다. Detroit 562 세포(ATCC; CCL-138)를 수집하고 EMEM 배지(ATCC; 30-2003) + 10% GenClone 열 불활성화 소 태아 혈청(HI FBS)(Genesee Scientific; 25-514H)에 재현탁하였다. 트리판 블루 염색 및 Countess II FL 자동화 세포 계수기(Thermofisher; AMQAF1000)를 사용하여 세포 계수를 결정하였다. 그런 다음, 세포를 100,000개의 세포/mL로 희석하고, 100 ul을 바닥이 편평한 96-웰 세포 배양 플레이트에 시딩하고, 37℃ 5% CO2에서 밤새 부착시켰다. 그런 다음, 1차 항체를 천연 배양 배지에서 20 nM로 희석한 다음, 60 nM Incucyte 인간 FabFluor-pH 적색 항체 표지 시약(Sartorius; 4722)과 1:1로 혼합하였다. 혼합물을 실온에서 20분 동안 인큐베이션한 다음, 세포에 첨가하였다. 그런 다음, 플레이트를 즉시 Incucyte S3 Live-Cell 분석 시스템에 배치하여 이미지를 획득하고 분석하였다. 출발 ABPC(치환 없음) 및 각각의 상응하는 항체 변이체에 대해 엔도리소좀 전달을 조사하여, 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라닌 치환으로 인해 강화된 엔도리소좀 전달을 알아냈다.
실시예 27.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있으며, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용할 수 있다(Hicks, SW 및 Lai, K의 "MET Antibodies and Immunoconjugates and uses thereof" 국제 특허 출원 WO 2020/014306 A1 (2020)). 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 hucMET27Gv1.3(중쇄 서열번호 304, 경쇄 서열번호 305)을 선택하였다. 간략하게, 경쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 실시예 23에서 추가 분석을 위해 이전에 선택한 경쇄 CDR 내의 개별 아미노산 돌연변이를 한 번에 2개 이상씩 체계적으로 조합하였다(MYT5066 - MYT5121). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 경쇄 CDR 내에 2개 이상의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는 당업계에 알려진 방법을 사용해 Expi293을: a) 하나의 경쇄 조합 서열 변이체; 및 b) Wang J 등의 문헌[(2017) ABBV-399, a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors, Irrespective of MET Pathway Dependence, Clin Cancer Res, 23:992-1000]) 및 Dall, WF 등의 문헌["Increasing the Affinity of a Human IgG1 for the Neonatal Fc Receptor: Biological Consequences" The Journal of Immunology (2002); 169:5171-5180]에 각각 기술된 삼중 힌지(TH) 또는 YTE 돌연변이를 함유하는 상응하는 출발 ABPC 중쇄로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 48), 단백질 A 자성 비드(Genscript L00273)를 사용해 정제하고, Detroit 562 세포(ATCC CCL-138) 상에서 엔도리소좀 전달에 대해 평가하였다. Detroit 562 세포(ATCC; CCL-138)를 수집하고 EMEM 배지(ATCC; 30-2003) + 10% GenClone 열 불활성화 소 태아 혈청(HI FBS)(Genesee Scientific; 25-514H)에 재현탁하였다. 트리판 블루 염색 및 Countess II FL 자동화 세포 계수기(Thermofisher; AMQAF1000)를 사용하여 세포 계수를 결정하였다. 그런 다음, 세포를 100,000개의 세포/mL로 희석하고, 100 ul을 바닥이 편평한 96-웰 세포 배양 플레이트에 시딩하고, 37℃ 5% CO2에서 밤새 부착시켰다. 그런 다음, 1차 항체를 천연 배양 배지에서 20 nM로 희석한 다음, 60 nM Incucyte 인간 FabFluor-pH 적색 항체 표지 시약(Sartorius; 4722)과 1:1로 혼합하였다. 혼합물을 실온에서 20분 동안 인큐베이션한 다음, 세포에 첨가하였다. 그런 다음, 플레이트를 즉시 Incucyte S3 Live-Cell 분석 시스템에 배치하여 이미지를 획득하고 분석하였다.
출발 ABPC(치환 없음) 및 각각의 상응하는 항체 변이체에 대해 엔도리소좀 전달을 조사하여, 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라닌 치환으로 인해 강화된 엔도리소좀 전달을 알아냈다. 도 49에 도시된 바와 같이, (출발 ABPC와 비교했을 때) 강화된 엔도리소좀 전달을 나타낸 경쇄 조합 변이체를 추가 분석을 위해 선택하였다(예: MYT5066, MYT5070, MYT5071, MYT5073, MYT5077, MYT5082, MYT5083, MYT5085, MYT5090, MYT5092, MYT5093, MYT5094, MYT5096, MYT5099, MYT5102, MYT5103, MYT5105, MYT5110, MYT5112, MYT5114, MYT5116, 및 MYT5119). 선택된 변이체의 pH 의존성을 Octet RED 96e 기기를 이용해 바이오층 간섭(BLI)를 사용하여 평가하였다. 간략하게, SDS-PAGE 겔의 시각적 검사에 의해 결정된 변이체의 정성적 발현 수준에 기초하여 세포 배양 상청액을 희석하되, 고 발현 변이체의 경우 5 μL의 세포 배양 상청액을 195 μL의 1x PBST, pH 7.4에 희석하고, 중간 발현 변이체의 경우 25 μL의 세포 배양 상청액을 175 μL의 1x PBST, pH 7.4에 희석하고, 저 발현 변이체의 경우 100 μL의 세포 배양 상청액을 100 μL의 1x PBST, pH 7.4에 희석하여, 센서 팁 상에 로딩하였다. 그런 다음, 희석된 상청액을 항-인간 Fc 센서(Forte Bio) 상에 포획하였다. 1X PBST(50 mM 인산칼륨 완충액 + 150mM NaCl + 0.05% Tween 20) pH 7.4를 사용하여 베이스라인을 확립하고, 센서를 1X PBST pH 7.4 중에서 MET(cMET, Sino Biological 카달로그 번호 10692-H08H)와 120초 동안 결합시켜 결합 곡선을 생성하였다. 해리 단계에서, 센서 상의 항체-항원 복합체를 1X PBST pH 7.4 또는 pH 5.4에 300 내지 600초 동안 노출시켰다. 출발 ABPC 항체(치환 없음) 및 각각의 상응하는 항체 변이체에 대한 pH 5.4 및 pH 7.4에서의 결합 및 해리 단계 곡선을 조사하여 두 가지 기준을 알아냈다: a) 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라인 치환으로 인해 pH 5.4에서 해리가 강화됨(예를 들어 koff 값이 더 높음); 및 b) pH 5.4에서의 항체 변이체 자체 및 출발 ABPC(치환 없음)와 비교했을 때, pH 7.4에서 해리가 감소함(예를 들어 koff 값이 더 낮음). 도 50에 도시된 바와 같이, (출발 ABPC와 비교했을 때) pH 5.4에서 강화된 해리를 나타내건, pH에서 감소된 해리를 나타내거나, 둘 다를 나타낸 경쇄 조합 변이체를 추가 분석을 위해 선택하였다(예: MYT5066, MYT5070, MYT5071, MYT5073, MYT5077, MYT5082, MYT5083, MYT5085, MYT5090, MYT5092, MYT5093, MYT5094, MYT5096, MYT5099, MYT5102, MYT5103, MYT5110, MYT5112, 및 MYT5119).
실시예 28.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있고, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용될 수 있다(Fujita, R 등의 문헌[(2020) A Novel Non-Agonist c-Met Antibody Drug Conjugate with Superior Potency Over a c-Met Tyrosine Kinase Inhibitor in c-Met Amplified and Non-Amplified Cancers, Cancer Biology and Therapy, 21(6):549-559]). 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 P3D12(중쇄 서열번호 502, 경쇄 서열번호 503)을 선택하였다. 간략하게, 중쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 중쇄 CDR 내의 개별 아미노산 잔기를 히스티딘으로 한 번에 하나씩 체계적으로 치환하였다(MYT3688 - MYT3726). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 중쇄 CDR에서 단 하나의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는, 당업계에 알려진 방법을 사용해 Expi293 세포를 a) 하나의 중쇄 서열 변이체, 및 b) 상응하는 출발 ABPC 경쇄로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 57), 변이체의 pH 의존성을 Octet RED 96e 기기를 이용해 바이오층 간섭(BLI)을 사용해 평가하였다. 간략하게, SDS-PAGE 겔의 시각적 검사에 의해 결정된 변이체의 정성적 발현 수준에 기초하여 세포 배양 상청액을 희석하되, 고 발현 변이체의 경우 5 μL의 세포 배양 상청액을 195 μL의 1x PBST, pH 7.4에 희석하고, 중간 발현 변이체의 경우 25 μL의 세포 배양 상청액을 175 μL의 1x PBST, pH 7.4에 희석하고, 저 발현 변이체의 경우 100 μL의 세포 배양 상청액을 100 μL의 1x PBST, pH 7.4에 희석하여, 센서 팁 상에 로딩하였다. 그런 다음, 이렇게 희석된 상청액을 항-인간 Fc 센서(Forte Bio) 상에 포획하였다. 1X PBST(50 mM 인산칼륨 완충액 + 150mM NaCl + 0.05% Tween 20) pH 7.4를 사용하여 베이스라인을 확립하고, 센서를 1X PBST pH 7.4 중 50 nM의 MET(cMET, Sino Biological 카달로그 번호 10692-H08H)와 120초 동안 결합시켜 결합 곡선을 생성하였다. 해리 단계에서, 센서 상의 항체-항원 복합체를 1X PBST pH 7.4에 300 내지 600초 동안 노출시켰다. 전체적으로 별도의 조건에서 1xPBST pH 5.4를 사용해 베이스라인, 결합, 및 해리를 반복하였다.
pH 5.4 및 pH 7.4에서 출발 ABPC 항체(치환 없음) 및 각각의 상응하는 항체 변이체에 대한 결합 및 해리 단계 곡선을 조사하여 두 가지 기준을 알아냈다: a) 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라인 치환으로 인해 pH 5.4에서 해리가 강화됨(즉, koff 값이 더 높음); 및 b) pH 5.4에서의 항체 변이체 자체 및 출발 ABPC(치환 없음)와 비교했을 때, pH 7.4에서 해리가 감소함(즉, koff 값이 더 낮음). 도 58에 도시된 바와 같이, (출발 ABPC와 비교했을 때) pH 5.4에서 강화된 해리를 나타내거나, pH 7.4에서 감소된 해리를 나타내거나, 둘 다를 나타낸 중쇄 변이체를 추가 분석을 위해 선택하였다(예: MYT3689, MYT3691, MYT3692, MYT3694, MYT3695, MYT3696, MYT3697, MYT3698, MYT3699, MYT3700, MYT3701, MYT3705, MYT3707, MYT3716, MYT3718, MYT3719, MYT3720, MYT3721, MYT3724, 및 MYT3725). 또한, 일부 히스티딘 및 알라닌 돌연변이는 MET 결합 동역학을 거의 변화시키지 않았거나(예를 들어 KD 또는 해리 속도에 있어서 1배 미만의 변화) 전혀 변화시키지 않았음을 주목하였다(예: MYT3688, MYT3690, MYT3693, MYT3702, MYT3703, MYT3704, MYT3706, MYT3708, MYT3709, MYT3710, MYT3711, MYT3712, MYT3713, MYT3714, MYT3717, 및 MYT3726).
특히, 히스티딘은 크고 양으로 하전된 아미노산이기 때문에, 변화가 없는 이들 변이체는 광범위한 돌연변이를 견딜 수 있고, 서열은 상이하지만 유사한 결합 특성을 갖는 항체로 유도할 수 있는 중쇄 내 위치로서 (명칭은 달리 명백하지 않음) 주목하였다.
실시예 29.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있고, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용될 수 있다(Fujita, R 등의 문헌[(2020) A Novel Non-Agonist c-Met Antibody Drug Conjugate with Superior Potency Over a c-Met Tyrosine Kinase Inhibitor in c-Met Amplified and Non-Amplified Cancers, Cancer Biology and Therapy, 21(6):549-559]). 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 P3D12(중쇄 서열번호 502, 경쇄 서열번호 503)을 선택하였다. 간략하게, 경쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 경쇄 CDR 내의 개별 아미노산 잔기를 히스티딘으로 한 번에 하나씩 체계적으로 치환하였다(MYT3727 - MYT3754). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 경쇄 CDR에서 단 하나의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는, 당업계에 알려진 방법을 사용해 Expi293 세포를 a) 하나의 경쇄 서열 변이체, 및 b) 상응하는 출발 ABPC 중쇄로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 59), 변이체의 pH 의존성을 Octet RED 96e 기기를 이용해 바이오층 간섭(BLI)을 사용해 평가하였다. 간략하게, SDS-PAGE 겔의 시각적 검사에 의해 결정된 변이체의 정성적 발현 수준에 기초하여 세포 배양 상청액을 희석하되, 고 발현 변이체의 경우 5 μL의 세포 배양 상청액을 195 μL의 1x PBST, pH 7.4에 희석하고, 중간 발현 변이체의 경우 25 μL의 세포 배양 상청액을 175 μL의 1x PBST, pH 7.4에 희석하고, 저 발현 변이체의 경우 100 μL의 세포 배양 상청액을 100 μL의 1x PBST, pH 7.4에 희석하여, 센서 팁 상에 로딩하였다. 그런 다음, 희석된 상청액을 항-인간 Fc 센서(Forte Bio) 상에 포획하였다. 1X PBST(50 mM 인산칼륨 완충액 + 150mM NaCl + 0.05% Tween 20) pH 7.4를 사용하여 베이스라인을 확립하고, 센서를 1X PBST pH 7.4 중 50 nM의 MET(cMET, Sino Biological 카달로그 번호 10692-H08H)와 120초 동안 결합시켜 결합 곡선을 생성하였다. 해리 단계에서, 센서 상의 항체-항원 복합체를 1X PBST pH 7.4에 300 내지 600초 동안 노출시켰다. 전체적으로 별도의 조건에서 1xPBST pH 5.4를 사용해 베이스라인, 결합, 및 해리를 반복하였다. pH 5.4 및 pH 7.4에서 출발 ABPC 항체(치환 없음) 및 각각의 상응하는 항체 변이체에 대한 결합 및 해리 단계 곡선을 조사하여 두 가지 기준을 알아냈다: a) 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라인 치환으로 인해 pH 5.4에서 해리가 강화됨(즉, koff 값이 더 높음); 및 b) pH 5.4에서의 항체 변이체 자체 및 출발 ABPC(치환 없음)와 비교했을 때, pH 7.4에서 해리가 감소함(즉, koff 값이 더 낮음). 도 60에 도시된 바와 같이, (출발 ABPC와 비교했을 때) pH 5.4에서 강화된 해리를 나타내거나, pH 7.4에서 감소된 해리를 나타내거나, 둘 다를 나타낸 경쇄 변이체를 추가 분석을 위해 선택하였다(예: MYT3728, MYT3732, MYT3734, MYT3735, MYT3736, MYT3737, MYT3738, MYT3740, MYT3743, MYT3747, MYT3748, MYT3749, MYT3750, MYT3751, MYT3752, MYT3753, 및 MYT3754).
또한, 일부 히스티딘 및 알라닌 돌연변이는 MET 결합 동역학을 거의 변화시키지 않았거나(예를 들어 KD 또는 해리 속도에 있어서 1배 미만의 변화) 전혀 변화시키지 않았음을 주목하였다(예: MYT3727, MYT3729, MYT3730, MYT3731, MYT3733, MYT3739, MYT3741, MYT3742, MYT3744, MYT3745, 및 MYT3746). 특히, 히스티딘은 크고 양으로 하전된 아미노산이기 때문에, 변화가 없는 이들 변이체는 광범위한 돌연변이를 견딜 수 있고, 서열은 상이하지만 유사한 결합 특성을 갖는 항체를 유도할 수 있는 경쇄 내 위치로서 주목하였다(명칭은 달리 명백하지 않음).
실시예 30.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있고, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용될 수 있다(Fujita, R 등의 문헌[(2020) A Novel Non-Agonist c-Met Antibody Drug Conjugate with Superior Potency Over a c-Met Tyrosine Kinase Inhibitor in c-Met Amplified and Non-Amplified Cancers, Cancer Biology and Therapy, 21(6):549-559]). 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 P3D12(중쇄 서열번호 502, 경쇄 서열번호 503)을 선택하였다. 간략하게, 중쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 실시예 28에서 추가 분석을 위해 이전에 선택한 중쇄 CDR 내의 개별 아미노산 돌연변이를 한 번에 2개 이상씩 체계적으로 조합하였다(MYT4306 - MYT4325). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 중쇄 CDR에서 2개 이상의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는, 당업계에 알려진 방법을 사용해 Expi293 세포를 a) 하나의 중쇄 조합 서열 변이체, 및 b) 상응하는 출발 ABPC 경쇄로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 61), 변이체의 pH 의존성을 Octet RED 96e 기기를 이용해 바이오층 간섭(BLI)을 사용해 평가하였다. 간략하게, SDS-PAGE 겔의 시각적 검사에 의해 결정된 변이체의 정성적 발현 수준에 기초하여 세포 배양 상청액을 희석하되, 고 발현 변이체의 경우 5 μL의 세포 배양 상청액을 195 μL의 1x PBST, pH 7.4에 희석하고, 중간 발현 변이체의 경우 25 μL의 세포 배양 상청액을 175 μL의 1x PBST, pH 7.4에 희석하고, 저 발현 변이체의 경우 100 μL의 세포 배양 상청액을 100 μL의 1x PBST, pH 7.4에 희석하여, 센서 팁 상에 로딩하였다. 그런 다음, 희석된 상청액을 항-인간 Fc 센서(Forte Bio) 상에 포획하였다. 1X PBST(50 mM 인산칼륨 완충액 + 150mM NaCl + 0.05% Tween 20) pH 7.4를 사용하여 베이스라인을 확립하고, 센서를 1X PBST pH 7.4 중 50 nM의 MET(cMET, Sino Biological 카달로그 번호 10692-H08H)와 120초 동안 결합시켜 결합 곡선을 생성하였다. 해리 단계에서, 센서 상의 항체-항원 복합체를 1X PBST pH 7.4에 300 내지 600초 동안 노출시켰다. 전체적으로 별도의 조건에서 1xPBST pH 5.4를 사용해 베이스라인, 결합, 및 해리를 반복하였다. pH 5.4 및 pH 7.4에서 출발 ABPC 항체(치환 없음) 및 각각의 상응하는 항체 변이체에 대한 결합 및 해리 단계 곡선을 조사하여 두 가지 기준을 알아냈다: a) 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라인 치환으로 인해 pH 5.4에서 해리가 강화됨(즉, koff 값이 더 높음); 및 b) pH 5.4에서의 항체 변이체 자체 및 출발 ABPC(치환 없음)와 비교했을 때, pH 7.4에서 해리가 감소함(즉, koff 값이 더 낮음). 도 62에 도시된 바와 같이, (출발 ABPC와 비교했을 때) pH 5.4에서 강화된 해리를 나타내거나, pH 7.4에서 감소된 해리를 나타내거나, 둘 다를 나타낸 중쇄 조합 변이체를 추가 분석을 위해 선택하였다(예: MYT4307, MYT4308, MYT4309, MYT4310, MYT4311, MYT4312, MYT4313, MYT4314, MYT4315, MYT4316, MYT4317, MYT4318, MYT4319, MYT4320, MYT4321, MYT4322, MYT4323, MYT4324, 및 MYT4325).
실시예 31.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있고, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용될 수 있다(Fujita, R 등의 문헌[(2020) A Novel Non-Agonist c-Met Antibody Drug Conjugate with Superior Potency Over a c-Met Tyrosine Kinase Inhibitor in c-Met Amplified and Non-Amplified Cancers, Cancer Biology and Therapy, 21(6):549-559]). 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 P3D12(중쇄 서열번호 502, 경쇄 서열번호 503)을 선택하였다. 간략하게, 경쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 실시예 29에서 추가 분석을 위해 이전에 선택한 경쇄 CDR 내의 개별 아미노산 돌연변이를 한 번에 2개 이상씩 체계적으로 조합하였다(MYT4242 - MYT4261). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 경쇄 CDR에서 2개 이상의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는, 당업계에 알려진 방법을 사용해 Expi293 세포를 a) 하나의 경쇄 조합 서열 변이체, 및 b) 상응하는 출발 ABPC 중쇄로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 63), 변이체의 pH 의존성을 Octet RED 96e 기기를 이용해 바이오층 간섭(BLI)을 사용해 평가하였다. 간략하게, SDS-PAGE 겔의 시각적 검사에 의해 결정된 변이체의 정성적 발현 수준에 기초하여 세포 배양 상청액을 희석하되, 고 발현 변이체의 경우 5 μL의 세포 배양 상청액을 195 μL의 1x PBST, pH 7.4에 희석하고, 중간 발현 변이체의 경우 25 μL의 세포 배양 상청액을 175 μL의 1x PBST, pH 7.4에 희석하고, 저 발현 변이체의 경우 100 μL의 세포 배양 상청액을 100 μL의 1x PBST, pH 7.4에 희석하여, 센서 팁 상에 로딩하였다. 그런 다음, 희석된 상청액을 항-인간 Fc 센서(Forte Bio) 상에 포획하였다. 1X PBST(50 mM 인산칼륨 완충액 + 150mM NaCl + 0.05% Tween 20) pH 7.4를 사용하여 베이스라인을 확립하고, 센서를 1X PBST pH 7.4 중에서 MET(cMET, Sino Biological 카달로그 번호 10692-H08H)와 120초 동안 결합시켜 결합 곡선을 생성하였다. 해리 단계에서, 센서 상의 항체-항원 복합체를 1X PBST pH 7.4에 300 내지 600초 동안 노출시켰다. 전체적으로 별도의 조건에서 1xPBST pH 5.4를 사용해 베이스라인, 결합, 및 해리를 반복하였다. pH 5.4 및 pH 7.4에서 출발 ABPC 항체(치환 없음) 및 각각의 상응하는 항체 변이체에 대한 결합 및 해리 단계 곡선을 조사하여 두 가지 기준을 알아냈다: a) 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라인 치환으로 인해 pH 5.4에서 해리가 강화됨(예를 들어 koff 값이 더 높음); 및 b) pH 5.4에서의 항체 변이체 자체 및 출발 ABPC(치환 없음)와 비교했을 때, pH 7.4에서 해리가 감소함(예를 들어 koff 값이 더 낮음). 도 64에 도시된 바와 같이, (출발 ABPC와 비교했을 때) pH 5.4에서 강화된 해리를 나타내거나, pH 7.4에서 감소된 해리를 나타내거나, 둘 다를 나타낸 경쇄 조합 변이체를 추가 분석을 위해 선택하였다(예: MYT4242, MYT4243, MYT4244, MYT4245,
MYT4246, MYT4247, MYT4248, MYT4249, MYT4250, MYT4251, MYT4252, MYT4253, MYT4254, MYT4255, MYT4256, MYT4257, 및 MYT4258).
실시예 32.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있고, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용될 수 있다(Fujita, R 등의 문헌[(2020) A Novel Non-Agonist c-Met Antibody Drug Conjugate with Superior Potency Over a c-Met Tyrosine Kinase Inhibitor in c-Met Amplified and Non-Amplified Cancers, Cancer Biology and Therapy, 21(6):549-559]). 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 P3D12(중쇄 서열번호 502, 경쇄 서열번호 503)을 선택하였다. 간략하게, 중쇄 및 경쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 실시예 28~31에서 추가 분석을 위해 이전에 선택한 중쇄 및 경쇄 CDR 내의 개별 아미노산 돌연변이를 한 번에 2개 이상씩 체계적으로 조합하였다(MYT5342 - MYT5381). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 2개 이상의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는, 당업계에 알려진 방법을 사용해 Expi293 세포를 a) 하나의 경쇄 서열 변이체 또는 경쇄 조합 서열 변이체, 및 b) 하나의 중쇄 서열 변이체 또는 중쇄 조합 서열 변이체로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 82), 변이체의 pH 의존성을 Octet RED 96e 기기를 이용해 바이오층 간섭(BLI)을 사용해 평가하였다. 간략하게, SDS-PAGE 겔의 시각적 검사에 의해 결정된 변이체의 정성적 발현 수준에 기초하여 세포 배양 상청액을 희석하되, 고 발현 변이체의 경우 5 μL의 세포 배양 상청액을 195 μL의 1x PBST, pH 7.4에 희석하고, 중간 발현 변이체의 경우 25 μL의 세포 배양 상청액을 175 μL의 1x PBST, pH 7.4에 희석하고, 저 발현 변이체의 경우 100 μL의 세포 배양 상청액을 100 μL의 1x PBST, pH 7.4에 희석하여, 센서 팁 상에 로딩하였다. 그런 다음, 희석된 상청액을 항-인간 Fc 센서(Forte Bio) 상에 포획하였다. 1X PBST(50 mM 인산칼륨 완충액 + 150mM NaCl + 0.05% Tween 20) pH 7.4를 사용하여 베이스라인을 확립하고, 센서를 1X PBST pH 7.4 중 50 nM의 MET(cMET, Sino Biological 카달로그 번호 10692-H08H)와 120초 동안 결합시켜 결합 곡선을 생성하였다. 해리 단계에서, 센서 상의 항체-항원 복합체를 1X PBST pH 7.4 또는 pH 5.4에 300 내지 600초 동안 노출시켰다. pH 5.4 및 pH 7.4에서 출발 ABPC 항체(치환 없음) 및 각각의 상응하는 항체 변이체에 대한 결합 및 해리 단계 곡선을 조사하여 두 가지 기준을 알아냈다: a) 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라인 치환으로 인해 pH 5.4에서 해리가 강화됨(예를 들어 koff 값이 더 높음); 및 b) pH 5.4에서의 항체 변이체 자체 및 출발 ABPC(치환 없음)와 비교했을 때, pH 7.4에서 해리가 감소함(예를 들어 koff 값이 더 낮음). 도 83에 도시된 바와 같이, pH 5.4에서 강화된 해리를 나타내거나, pH 7.4에서 감소된 해리를 나타내거나, 둘 다를 나타내는 페어링된 중쇄 및 경쇄 변이체를 추가 분석을 위해 선택하였다(예: MYT5342, MYT5343, MYT5344, MYT5345, MYT5346, MYT5350, MYT5351, MYT5352, MYT5353, MYT5354, MYT5355, MYT5356, MYT5357, MYT5359, MYT5360, MYT5366, MYT5367, MYT5368, MYT5369, MYT5370, MYT5372, MYT5373, MYT5374, MYT5375, MYT5376, MYT5377, 및 MYT5381).
실시예 33.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있고, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용될 수 있다(Fujita, R 등의 문헌[(2020) A Novel Non-Agonist c-Met Antibody Drug Conjugate with Superior Potency Over a c-Met Tyrosine Kinase Inhibitor in c-Met Amplified and Non-Amplified Cancers, Cancer Biology and Therapy, 21(6):549-559]). 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 P3D12(중쇄 서열번호 502, 경쇄 서열번호 503)을 선택하였다. 간략하게, 중쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 실시예 28에서 추가 분석을 위해 이전에 선택한 중쇄 CDR 내의 개별 아미노산 돌연변이를 한 번에 2개 이상씩 체계적으로 조합하였다(MYT5122 - MYT5221). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 중쇄 CDR 내에 2개 이상의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는 당업계에 알려진 방법을 사용해 Expi293을: a) Wang J 등의 문헌[(2017) ABBV-399, a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors, Irrespective of MET Pathway Dependence, Clin Cancer Res, 23:992-1000]) 및 Dall, WF 등의 문헌["Increasing the Affinity of a Human IgG1 for the Neonatal Fc Receptor: Biological Consequences" The Journal of Immunology (2002); 169:5171-5180]에 각각 기술된 삼중 힌지(TH) 또는 YTE 돌연변이를 함유하는 하나의 중쇄 조합 서열 변이체; 및 b) 상응하는 출발 ABPC 경쇄로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 65), 단백질 A 자성 비드(Genscript L00273)를 사용해 정제하고, Detroit 562 세포(ATCC CCL-138) 상에서 엔도리소좀 전달에 대해 평가하였다. 간략하게, Detroit 562 세포(ATCC; CCL-138)를 수집하고 EMEM 배지(ATCC; 30-2003) + 10% GenClone 열 불활성화 소 태아 혈청(HI FBS)(Genesee Scientific; 25-514H)에 재현탁하였다. 트리판 블루 염색 및 Countess II FL 자동화 세포 계수기(Thermofisher; AMQAF1000)를 사용하여 세포 계수를 결정하였다. 그런 다음, 세포를 100,000개의 세포/mL로 희석하고, 100 ul을 바닥이 편평한 96-웰 세포 배양 플레이트에 시딩하고, 37℃ 5% CO2에서 밤새 부착시켰다. 그런 다음, 1차 항체를 천연 배양 배지에서 20 nM로 희석한 다음, 60 nM Incucyte 인간 FabFluor-pH 적색 항체 표지 시약(Sartorius; 4722)과 1:1로 혼합하였다. 혼합물을 실온에서 20분 동안 인큐베이션한 다음, 세포에 첨가하였다. 그런 다음, 플레이트를 즉시 Incucyte S3 Live-Cell 분석 시스템에 배치하여 이미지를 획득하고 분석하였다. 출발 ABPC(치환 없음) 및 각각의 상응하는 항체 변이체에 대해 엔도리소좀 전달을 조사하여, 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라닌 치환으로 인해 강화된 엔도리소좀 전달을 알아냈다. 도 66에 도시된 바와 같이, (출발 ABPC와 비교했을 때) 강화된 엔도리소좀 전달을 나타낸 중쇄 조합 변이체를 추가 분석을 위해 선택하였다(예: MYT5122, MYT5131, MYT5146, MYT5184, 및 MYT5201). 선택된 변이체의 pH 의존성을 Octet RED 96e 기기를 이용해 바이오층 간섭(BLI)를 사용하여 평가하였다. 간략하게, SDS-PAGE 겔의 시각적 검사에 의해 결정된 변이체의 정성적 발현 수준에 기초하여 세포 배양 상청액을 희석하되, 고 발현 변이체의 경우 5 μL의 세포 배양 상청액을 195 μL의 1x PBST, pH 7.4에 희석하고, 중간 발현 변이체의 경우 25 μL의 세포 배양 상청액을 175 μL의 1x PBST, pH 7.4에 희석하고,
저 발현 변이체의 경우 100 μL의 세포 배양 상청액을 100 μL의 1x PBST, pH 7.4에 희석하여, 센서 팁 상에 로딩하였다. 그런 다음, 희석된 상청액을 항-인간 Fc 센서(Forte Bio) 상에 포획하였다. 1X PBST(50 mM 인산칼륨 완충액 + 150mM NaCl + 0.05% Tween 20) pH 7.4를 사용하여 베이스라인을 확립하고, 센서를 1X PBST pH 7.4 중에서 MET(cMET, Sino Biological 카달로그 번호 10692-H08H)와 120초 동안 결합시켜 결합 곡선을 생성하였다. 해리 단계에서, 센서 상의 항체-항원 복합체를 1X PBST pH 7.4 또는 pH 5.4에 300 내지 600초 동안 노출시켰다. 출발 ABPC 항체(치환 없음) 및 각각의 상응하는 항체 변이체에 대한 pH 5.4 및 pH 7.4에서의 결합 및 해리 단계 곡선을 조사하여 두 가지 기준을 알아냈다: a) 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라인 치환으로 인해 pH 5.4에서 해리가 강화됨(예를 들어 koff 값이 더 높음); 및 b) pH 5.4에서의 항체 변이체 자체 및 출발 ABPC(치환 없음)와 비교했을 때, pH 7.4에서 해리가 감소함(예를 들어 koff 값이 더 낮음). 도 67에 도시된 바와 같이, (출발 ABPC와 비교했을 때) pH 5.4에서 강화된 해리를 나타내거나, pH 7.4에서 감소된 해리를 나타내거나, 둘 다를 나타낸 중쇄 조합 변이체를 추가 분석을 위해 선택하였다(예: MYT5122, MYT5131, MYT5146, MYT5184, 및 MYT5201).
실시예 34.
pH-조작된 MET ABPC의 작제 및 스크리닝
다수의 MET-결합 단클론 항체가 문헌에 기술되어 있고, pH-의존적 결합을 조작하기 위한 템플릿으로서 사용될 수 있다(Fujita, R 등의 문헌[(2020) A Novel Non-Agonist c-Met Antibody Drug Conjugate with Superior Potency Over a c-Met Tyrosine Kinase Inhibitor in c-Met Amplified and Non-Amplified Cancers, Cancer Biology and Therapy, 21(6):549-559]). 히스티딘 스캐닝을 통한 pH 조작을 위해, MET-결합 단클론 항체로서 P3D12(중쇄 서열번호 502, 경쇄 서열번호 503)을 선택하였다. 간략하게, 경쇄 내 CDR은 Kabat 등에 의해 기술된 방법(Kabat 등의 문헌[(1992) Sequences of Proteins of Immunological Interest, DIANE publishing) 및 IMGT에 기술된 방법(Lefranc MP의 문헌[(1999) "The IMGT unique numbering for Immunoglobulins, T cell receptors and Ig-like domains" The Immunologist 7, 132-136)을 사용해 식별하였고, 각각의 CDR에 대해, Kabat 및 IMGT의 CDR 정의 중 하나 또는 둘 다에 속하는 잔기를 CDR 잔기로서 명명하였다. pH-의존적 서열 변이체를 생성하기 위해, 실시예 29에서 추가 분석을 위해 이전에 선택한 경쇄 CDR 내의 개별 아미노산 돌연변이를 한 번에 2개 이상씩 체계적으로 조합하였다(MYT5222 - MYT5295). 출발 CDR 잔기가 히스티딘인 경우, 이를 알라닌으로 돌연변이시켰다. 경쇄 CDR 내에 2개 이상의 히스티딘 또는 알라닌 돌연변이를 갖는 항체 변이체는 당업계에 알려진 방법을 사용해 Expi293을: a) 하나의 경쇄 조합 서열 변이체; 및 b) Wang J 등의 문헌[(2017) ABBV-399, a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors, Irrespective of MET Pathway Dependence, Clin Cancer Res, 23:992-1000]) 및 Dall, WF 등의 문헌["Increasing the Affinity of a Human IgG1 for the Neonatal Fc Receptor: Biological Consequences" The Journal of Immunology (2002); 169:5171-5180]에 각각 기술된 삼중 힌지(TH) 또는 YTE 돌연변이를 함유하는 상응하는 출발 ABPC 중쇄로 공동 형질감염시켜 생성하였다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 68), 단백질 A 자성 비드(Genscript L00273)를 사용해 정제하고, Detroit 562 세포(ATCC CCL-138) 상에서 엔도리소좀 전달에 대해 평가하였다. 간략하게, Detroit 562 세포(ATCC; CCL-138)를 수집하고 EMEM 배지(ATCC; 30-2003) + 10% GenClone 열 불활성화 소 태아 혈청(HI FBS)(Genesee Scientific; 25-514H)에 재현탁하였다. 트리판 블루 염색 및 Countess II FL 자동화 세포 계수기(Thermofisher; AMQAF1000)를 사용하여 세포 계수를 결정하였다. 그런 다음, 세포를 100,000개의 세포/mL로 희석하고, 100 ul을 바닥이 편평한 96-웰 세포 배양 플레이트에 시딩하고, 37℃ 5% CO2에서 밤새 부착시켰다. 그런 다음, 1차 항체를 천연 배양 배지에서 20 nM로 희석한 다음, 60 nM Incucyte 인간 FabFluor-pH 적색 항체 표지 시약(Sartorius; 4722)과 1:1로 혼합하였다. 혼합물을 실온에서 20분 동안 인큐베이션한 다음, 세포에 첨가하였다. 그런 다음, 플레이트를 즉시 Incucyte S3 Live-Cell 분석 시스템에 배치하여 이미지를 획득하고 분석하였다. 출발 ABPC(치환 없음) 및 각각의 상응하는 항체 변이체에 대해 엔도리소좀 전달을 조사하여, 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라닌 치환으로 인해 강화된 엔도리소좀 전달을 알아냈다. 도 69에 도시된 바와 같이, (출발 ABPC와 비교했을 때) 강화된 엔도리소좀 전달을 나타낸 경쇄 조합 변이체를 추가 분석을 위해 선택하였다(예: MYT5237). 선택된 변이체의 pH 의존성을 Octet RED 96e 기기를 이용해 바이오층 간섭(BLI)를 사용하여 평가하였다. 간략하게, SDS-PAGE 겔의 시각적 검사에 의해 결정된 변이체의 정성적 발현 수준에 기초하여 세포 배양 상청액을 희석하되, 고 발현 변이체의 경우 5 μL의 세포 배양 상청액을 195 μL의 1x PBST, pH 7.4에 희석하고, 중간 발현 변이체의 경우 25 μL의 세포 배양 상청액을 175 μL의 1x PBST, pH 7.4에 희석하고, 저 발현 변이체의 경우 100 μL의 세포 배양 상청액을 100 μL의 1x PBST, pH 7.4에 희석하여, 센서 팁 상에 로딩하였다.
그런 다음, 희석된 상청액을 항-인간 Fc 센서(Forte Bio) 상에 포획하였다. 1X PBST(50 mM 인산칼륨 완충액 + 150mM NaCl + 0.05% Tween 20) pH 7.4를 사용하여 베이스라인을 확립하고, 센서를 1X PBST pH 7.4 중에서 MET(cMET, Sino Biological 카달로그 번호 10692-H08H)와 120초 동안 결합시켜 결합 곡선을 생성하였다. 해리 단계에서, 센서 상의 항체-항원 복합체를 1X PBST pH 7.4 또는 pH 5.4에 300 내지 600초 동안 노출시켰다. 출발 ABPC 항체(치환 없음) 및 각각의 상응하는 항체 변이체에 대한 pH 5.4 및 pH 7.4에서의 결합 및 해리 단계 곡선을 조사하여 두 가지 기준을 알아냈다: a) 출발 ABPC(치환 없음)와 비교했을 때, 히스티딘 또는 알라인 치환으로 인해 pH 5.4에서 해리가 강화됨(예를 들어 koff 값이 더 높음); 및 b) pH 5.4에서의 항체 변이체 자체 및 출발 ABPC(치환 없음)와 비교했을 때, pH 7.4에서 해리가 감소함(예를 들어 koff 값이 더 낮음). 도 70에 도시된 바와 같이, (출발 ABPC와 비교했을 때) pH 5.4에서 강화된 해리를 나타내거나, pH 7.4에서 감소된 해리를 나타내거나, 둘 다를 나타낸 경쇄 조합 변이체를 추가 분석을 위해 선택하였다(예: MYT5237).
실시예 35.
항-MET ABPC의 재포맷팅
Wang J 등의 문헌[(2017) ABBV-399, a c-Met Antibody-Drug Conjugate that Targets Both MET-Amplified and c-Met-Overexpressing Tumors, Irrespective of MET Pathway Dependence, Clin Cancer Res, 23:992-1000]에 기술된 것과 같은 삼중 힌지 (TH) 돌연변이 및 Dall, WF 등의 문헌["Increasing the Affinity of a Human IgG1 for the Neonatal Fc Receptor: Biological Consequences" The Journal of Immunology (2002); 169:5171-5180]에 기술된 것과 같은 YTE 돌연변이가 있거나 없는 인간 IgG1 Fc에 유전적으로 융합된 중쇄 가변 영역을 암호화하는 플라스미드로 Expi293 세포를 형질감염시켜, 선택된 pH-조작된 항-MET 변이체를 야생형 IgG1 분자로서 (예를 들어 실시예 9~13, 16~20, 22~25, 및 28~32에서) 생성하고 TH 돌연변이와 YTE 돌연변이를 함유하는 IgG1 분자로서 생성하였다(도 80). 당업계에 공지된 방법을 사용하여 a) 야생형 인간 IgG1 이소형 서열, 또는 TH 및 YTE 돌연변이를 제외하고는 이와 동일한 서열에 상응하는 중쇄 가변 영역 및 불변 영역으로 이루어진 하나의 중쇄 서열, 및 b) 하나의 경쇄 서열로 Expi293 세포를 공동 형질감염시켰다. 4일 동안 단백질을 발현시킨 후, 세포 배양 상청액을 수집하고, SDS-PAGE 분석에 의해 정량화하고(도 77에 도시된 선택 샘플), 변이체의 pH 의존성을 Octet RED 96e 기기를 이용해 바이오층 간섭(BLI)을 사용해 평가하였다. 간략하게, SDS-PAGE 겔의 시각적 검사에 의해 결정된 변이체의 정성적 발현 수준에 기초하여 세포 배양 상청액을 희석하되, 고 발현 변이체의 경우 5 μL의 세포 배양 상청액을 195 μL의 1x PBST, pH 7.4에 희석하고, 중간 발현 변이체의 경우 25 μL의 세포 배양 상청액을 175 μL의 1x PBST, pH 7.4에 희석하고, 저 발현 변이체의 경우 100 μL의 세포 배양 상청액을 100 μL의 1x PBST, pH 7.4에 희석하여, 센서 팁 상에 로딩하였다. 그런 다음, 희석된 상청액을 항-인간 Fc 센서(Forte Bio) 상에 포획하였다. 1X PBST(50 mM 인산칼륨 완충액 + 150mM NaCl + 0.05% Tween 20) pH 7.4를 사용하여 베이스라인을 확립하고, 센서를 1X PBST pH 7.4 중에서 50 nM의 MET(cMET, Sino Biological 카달로그 번호 10692-H08H)와 120초 동안 결합시켜 결합 곡선을 생성하였다. 해리 단계에서, 센서 상의 항체-항원 복합체를 1X PBST pH 7.4에 300 내지 600초 동안 노출시켰다. 전체적으로 별도의 조건에서 1xPBST pH 5.4를 사용해 베이스라인, 결합, 및 해리를 반복하였다. 각각의 상응하는 항체 변이체에 대한 pH 5.4 및 pH 7.4에서의 결합 및 해리 단계 곡선을 조사하여, 3가지 기준을 알아냈다: a) 상응하는 출발 ABPC와 비교했을 때, pH 5.4에서 해리가 강화됨(예를 들어 koff 값이 더 높음); b) 항체 변이체 자체에서, pH 5.4와 비교했을 때 pH 7.4에서의 해리가 감소함(예를 들어 koff 값이 던 낮음); 및 c) 야생형 인간 IgG1 ABPC와 이들의 TH 및 YTE 함유 변이체의 비교. 야생형 인간 IgG1 및 TH 및 YTE 돌연변이를 함유하는 재포맷팅한 인간 IgG1 항체는 광범위하게 유사한 결합 및 해리 곡선을 나타냈으며, 선택된 Octet 플롯 및 엔도리소좀 전달 데이터는 도 78 및 79에 각각 도시되어 있다. 이러한 데이터로부터, pH 의존성 및 엔도리소좀 전달을 포함하지만 이에 한정되지 않는 이러한 변이체 가변 도메인 서열의 바람직한 특성은 IgG1 포맷이거나 TH 및 YTE 돌연변이를 갖는 IgG1 포맷인지 여부와 무관하게 유지되는 것으로 결론 내린다.
실시예 36.
pH 조작된 항-MET ABPC의 세포 내재화 및 엔도리소좀 전달의 특성 분석
실시예 9~13, 16~20, 22~25, 및 28~31로부터 선택된 항-MET pH 조작된 항체 변이체를 U-87 MG 세포(MET+), SNU-5 세포(MET+), NCI-H1373 세포(MET+), NCI-H1573 세포(MET+), 및/또는 Detroit 562 세포(MET+)에서 내재화 및 엔도리소좀 전달에 대해 분석하였다. U-87 MG 세포(ATCC HTB-14), Detroit 562 세포(ATCC CCL-138), NCI-H1373 세포(ATCC CRL-5866), NCI-H1573 세포(ATCC CRL-5877), 또는 SNU-5 세포(ATCC CRL-5973)를 수집하고 EMEM 배지(U-87 MG 및 Detroit 562, ATCC; 30-2003), IMDM 배지(SNU-5, ATCC; 30-2005), 또는 RPMI 배지(NCI-H1373 및 NCI-H1573, ATCC 30-2001) 외에 GenClone 열 비활성화 소 태아 혈청(HI FBS) (Genesee Scientific; 25-514H)이 5% 포함된 RPMI 배지(NCI-H1573), 10% 포함된 RPMI 배지(U-87 MG, Detroit 562, NCI-H1373), 또는 20% 포함된 RPMI 배지(SNU-5)에 재현탁하였다. 트리판 블루 염색 및 Countess II FL 자동화 세포 계수기(Thermofisher; AMQAF1000)를 사용하여 세포 계수를 결정하였다. 그런 다음, 세포를 2,000,000개의 세포/mL로 희석하고, 50 μl/웰을 바닥이 편평한 96-웰 세포 배양 플레이트(Genesee Scientific; 25-109)에 시딩하였다. 항-MET pH 조작된 항체 변이체, 출발 ABPC 항체, 대조군 IgG1 이소형 대조군(BP0297, Bioxcell), 및 비히클 대조군을 천연 배양 배지에서 희석한 다음, 3x 몰비의 Zenon pHrodo iFL 인간 IgG 표지 시약(ThermoFisher; Z25611)과 1:1로 혼합하였다. 혼합물을 실온에서 20분 동안 인큐베이션한 다음, 세포를 1:1로 첨가하여 100 μL의 최종 부피를 만들었다. 세포, 항-MET 항체 변이체, 및 Zenon pHrodo iFL 인간 IgG 표지 시약의 혼합물을 37℃ 5% CO2에서 1~24시간 동안 인큐베이션하였다. 인큐베이션 후, 100 μL의 얼음처럼 차가운 유세포 계측(FC) 완충액(인산염 완충 식염수(PBS), pH 7.4 + 2 mM 에틸렌디아민테트라아세트산(EDTA) + 2%(v/v) HI FBS)을 각 웰에 첨가한다. 그런 다음, 세포를 2000 rpm으로 4℃에서 2분 동안 회전시키고, 200 μL의 얼음처럼 차가운 FC 완충액으로 세척하고, 100 μL의 얼음처럼 차가운 FC 완충액에 재현탁하였다. BD Accuri C6 유세포 계측기를 사용해 평균 녹색 형광 강도를 검출하였다. 데이터는 Flowjo 분석 소프트웨어를 사용하여 분석하였다. pHrodo 녹색은 엔도솜 및 리소좀의 낮은 pH 환경에서 형광을 발하는 pH 민감성 염료이므로, 항체 내재화 및 엔도리소좀 전달을 정량화하는 데 사용할 수 있다. 도면에 명시된 것과 같이, pHrodo 녹색 평균 형광 강도에 의해 측정했을 때 U-87 MG (MET+), Detroit 562 (MET+), SNU-5 (MET+), NCI-H1573 (MET+), 또는 NCI-H1373 (MET+) 세포에서, 도면에 명시된 농도에서 항-MET 출발 ABPC 및 변이체의 내재화 및 엔도리소좀 전달은 도 81에 도시되어 있다. 여러 가지 pH 조작된 항-MET 항체 변이체는 이들의 상응하는 출발 ABPC 항체에 비해 증가된 평균 형광 강도를 나타냈는데, 이는 증가된 형광 또는 IgG1 이소형 대조군에 비해 증가된 형광에 의해 나타난 바와 같이, 낮은 pH에서의 증가된 해리가 내재화 및 세포 내부의 엔도리소좀 전달의 강화로 이어진다는 것을 입증한다. 증가된 엔도리소좀 전달은 각 막대의 상단에 각각의 pH 조작된 항-MET 항체 변이체에 대해 다음의 비율로 정량화되어 있다: 변이체의 평균 형광 강도에서
IgG 대조군의 형광 강도를 뺀 값을, 변이체의 상응하는 출발 ABPC의 평균 형광 강도에서 IgG 대조군의 평균 형광 강도를 뺀 값으로 나눈 비율. 예를 들어 MYT0888, MYT0916, MYT0920, MYT0924, MYT2018, MYT2019, MYT2020, MYT2022, MYT2023, MYT2025, MYT2026, MYT2033, MYT2038, MYT2040, MYT2043, MYT2049, MYT2864, MYT3451, MYT3452, MYT3453, MYT3454, MYT3457, MYT3465, MYT3466, MYT3467, MYT3468, MYT3469, MYT3471, MYT3474, MYT3482, MYT3485, MYT3609, MYT3611, MYT3615, MYT4201, MYT4202, MYT4204, MYT4205, 및 MYT4207, 텔리소투주맙의 항체 변이체는 텔리소투주맙(MYT0886)에 비해 증가된 내재화 및 엔도리소좀 전달을 나타낸다. 예를 들어, MYT2319, MYT2320, MYT2325, MYT2326, MYT2327, MYT2328, MYT2333, MYT2343, MYT2344, MYT2850, MYT2851, MYT2852, MYT2853, MYT2855, MYT2856, MYT2861, MYT2864, MYT2865, MYT4326, MYT4327, MYT4332, MYT4334, 및 MYT4336, 에미베투주맙의 항체 변이체는 에미베투주맙(MYT2313)에 비해 증가된 내재화 및 엔도리소좀 전달을 나타낸다. 예를 들어, MYT3619, MYT3638, MYT3639, MYT3651, MYT3653, MYT3661, MYT3662, MYT3664, MYT3666, MYT3668, MYT3671, MYT3677, MYT3679, MYT3684, MYT4223, MYT4225, MYT4226, MYT4228, MYT4231, MYT4232, MYT4236, MYT4239, MYT4291, MYT4302, MYT4303, 및 MYT4304, hucMET27Gv1.3의 항체 변이체는 hucMET27Gv1.3 (MYT3617)에 비해 증가된 내재화 및 엔도리소좀 전달을 나타낸다. 예를 들어, MYT3689, MYT3691, MYT3694, MYT3695, MYT3697, MYT3698, MYT3705, MYT3707, MYT3720, MYT3724, MYT3725, MYT3728, MYT3732, MYT3735, MYT3738, MYT3740, MYT3748, MYT3749, MYT3750, MYT3751, MYT3752, MYT3753, MYT3754, MYT4242, MYT4243, MYT4245, MYT4247, MYT4249, MYT4250, MYT4252, MYT4258, MYT4309, MYT4310, MYT4311, MYT4318, MYT4319, MYT4320, MYT4322, MYT4323, MYT4324, 및 MYT4325, P3D12의 항체 변이체는 P3D12 (MYT3687 및/또는 MYT4305)에 비해 증가된 내재화 및 엔도리소좀 전달을 나타낸다. 출발 ABPC 항체에 비해 평균 형광 강도가 증가된 이러한 pH 조작된 항-MET 항체 변이체를 추가 분석을 위해 선택하였다.
실시예 37.
항-MET mAb의 열 안정성
단백질 용융 온도(Tm)는 시차주사 형광측정(DSF)을 사용하여 측정하였다. DSF는 단백질이 열에 의해 전개될 때 Sypro Orange(Thermo Scientific 카탈로그 번호 S6650)으로부터 형광 신호를 측정함으로써 단백질 전개(protein unfolding)를 시각화한다. 단백질이 전개됨에 따라 더 많은 친수성 영역이 Sypro Orange 염료에 노출되고, 궁극적으로 염료가 이들 친수성 영역에 결합함으로써 신호를 증가시킨다. 단백질에 대한 Tm은 전개 전이의 반치 최대값으로서 계산되며, 이는 Sypro Orange 신호의 제1 유도체를 도표화하고 이 유도체 플롯의 국소 최대값을 찾음으로써 시각화될 수 있다. 1xPBS, pH 7.4 중 20 μL의 단백질 샘플을 5 μL의 25X Sypro Orange 마스터 혼합물과 혼합하여, 5x Sypro Orange의 최종 농도를 얻었다. 샘플을 96-웰 PCR 플레이트(Thermo Scientific 카달로그 번호 AB-2400/W)에 첨가하고 광학 커버(Thermo Scientific 카달로그 번호 4360954)로 시일하였다. PCR 플레이트를 실시간 PCR 기계(Thermo Scientific Quant Studio 3)에 삽입하고, 플레이트 온도를 25℃에서 3분 동안 안정화시킨 후 0.2℃ 증분으로 95℃까지 상승시키고, 1초 동안 안정화시킨 후 Sypro Orange 신호를 측정하였다. 항-MET 출발 ABPC 및 변이체에 대한 용융 온도(Tm) 값은 도 85에 도시되어 있다. 여러 가지 변이체가 이들의 출발 ABPC와 유사한 용융 온도 값을 나타내는데, 이는 pH 조작을 통해 생성된 변이체가 이들의 상응하는 출발 ABPC(예를 들어 에미베투주맙, hucMET27Gv1.3, 또는 P3D12)와 비교하여 기능적으로 적절한 열 안정성을 유지할 수 있음을 확인할 수 있게 한다. 시험된 모든 변이체(도 85 참조)의 용융 온도가 이들의 상응하는 출발 ABPC(예를 들어 미르베툭시맙(mirvetuximab))의 용융 온도에서 10℃를 뺀 것과 같거나 더 높았으므로, 추가 분석을 위해 선택하였다.
본원에서의 발견은, 표적 당 다수의 변이체가 낮은 pH에서 강화된 해리를 나타낸 다른 항원(예컨대 CLEC12a 및 2개의 다른 표적)에 대한 조작과 대조적이지만, (CLEC12a 및 2개의 다른 표적에 특이적으로 결합한) 이들 변이체의 유리한 pH-의존적 결합 특성에도 불구하고, 이들 변이체는 상응하는 출발 ABPC(예: 출발 항체)와 비교했을 때 세포 내재화 및 엔도리소좀 전달을 10% 미만으로 증가시켰다. (CLEC12a 및 2개의 다른 표적에 특이적으로 결합하는) 이들 변이체는 또한 상응하는 출발 ABPC(예: 출발 항체)와 유사한 생물물리학적 특성(예를 들어 항체 발현, 열 안정성, pH 7.4에서의 친화도 등)을 가졌는데, 이는 시험된 변이체의 생물물리학적 특성에 특이적이지 않았음을 (즉, 생물물리학적 특성이 pH 5.4에서의 강화된 해리와 무관함을) 확인하게 해 준다.
기타 구현예
본 발명은 본 발명을 실시하기 위한 구체적인 내용과 관련하여 설명되었지만, 전술한 설명은 첨부된 청구범위의 범주에 의해 정의되는 본 발명의 범주를 예시하지만 이를 한정하지 않도록 의도된다는 것을 이해해야 한다. 다른 양태, 장점, 및 변형은 다음의 청구범위의 범주에 속한다.
서열 부록
>텔리소투주맙 IgG의 중쇄 (서열번호 1)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG의 경쇄 (서열번호 2)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙의 중쇄 CDR1 (서열번호 3)
GYIFTAYTMH
>텔리소투주맙의 중쇄 CDR2 (서열번호 4)
WIKPNNGLANYAQKFQG
>텔리소투주맙의 중쇄 CDR3 (서열번호 5)
ARSEITTEFDY
>텔리소투주맙의 경쇄 CDR1 (서열번호 6)
KSSESVDSYANSFLH
>텔리소투주맙의 경쇄 CDR2 (서열번호 7)
RASTRES
>텔리소투주맙의 경쇄 CDR3 (서열번호 8)
QQSKEDPLT
>성숙 인간 MET (서열번호 9)
ECKEALAKSEMNVNMKYQLPNFTAETPIQNVILHEHHIFLGATNYIYVLNEEDLQKVAEYKTGPVLEHPDCFPCQDCSSKANLSGGVWKDNINMALVVDTYYDDQLISCGSVNRGTCQRHVFPHNHTADIQSEVHCIFSPQIEEPSQCPDCVVSALGAKVLSSVKDRFINFFVGNTINSSYFPDHPLHSISVRRLKETKDGFMFLTDQSYIDVLPEFRDSYPIKYVHAFESNNFIYFLTVQRETLDAQTFHTRIIRFCSINSGLHSYMEMPLECILTEKRKKRSTKKEVFNILQAAYVSKPGAQLARQIGASLNDDILFGVFAQSKPDSAEPMDRSAMCAFPIKYVNDFFNKIVNKNNVRCLQHFYGPNHEHCFNRTLLRNSSGCEARRDEYRTEFTTALQRVDLFMGQFSEVLLTSISTFIKGDLTIANLGTSEGRFMQVVVSRSGPSTPHVNFLLDSHPVSPEVIVEHTLNQNGYTLVITGKKITKIPLNGLGCRHFQSCSQCLSAPPFVQCGWCHDKCVRSEECLSGTWTQQICLPAIYKVFPNSAPLEGGTRLTICGWDFGFRRNNKFDLKKTRVLLGNESCTLTLSESTMNTLKCTVGPAMNKHFNMSIIISNGHGTTQYSTFSYVDPVITSISPKYGPMAGGTLLTLTGNYLNSGNSRHISIGGKTCTLKSVSNSILECYTPAQTISTEFAVKLKIDLANRETSIFSYREDPIVYEIHPTKSFISGGSTITGVGKNLNSVSVPRMVINVHEAGRNFTVACQHRSNSEIICCTTPSLQQLNLQLPLKTKAFFMLDGILSKYFDLIYVHNPVFKPFEKPVMISMGNENVLEIKGNDIDPEAVKGEVLKVGNKSCENIHLHSEAVLCTVPNDLLKLNSELNIEWKQAISSTVLGKVIVQPDQNFTGLIAGVVSISTALLLLLGFFLWLKKRKQIKDLGSELVRYDARVHTPHLDRLVSARSVSPTTEMVSNESVDYRATFPEDQFPNSSQNGSCRQVQYPLTDMSPILTSGDSDISSPLLQNTVHIDLSALNPELVQAVQHVVIGPSSLIVHFNEVIGRGHFGCVYHGTLLDNDGKKIHCAVKSLNRITDIGEVSQFLTEGIIMKDFSHPNVLSLLGICLRSEGSPLVVLPYMKHGDLRNFIRNETHNPTVKDLIGFGLQVAKGMKYLASKKFVHRDLAARNCMLDEKFTVKVADFGLARDMYDKEYYSVHNKTGAKLPVKWMALESLQTQKFTTKSDVWSFGVLLWELMTRGAPPYPDVNTFDITVYLLQGRRLLQPEYCPDPLYEVMLKCWHPKAEMRPSFSELVSRISAIFSTFIGEHYVHVNATYVNVKCVAPYPSLLSSEDNADDEVDTRPASFWETS
>성숙 인간 MET를 암호화하는 cDNA (서열번호 10)
GAGTGTAAAGAGGCACTAGCAAAGTCCGAGATGAATGTGAATATGAAGTATCAGCTTCCCAACTTCACCGCGGAAACACCCATCCAGAATGTCATTCTACATGAGCATCACATTTTCCTTGGTGCCACTAACTACATTTATGTTTTAAATGAGGAAGACCTTCAGAAGGTTGCTGAGTACAAGACTGGGCCTGTGCTGGAACACCCAGATTGTTTCCCATGTCAGGACTGCAGCAGCAAAGCCAATTTATCAGGAGGTGTTTGGAAAGATAACATCAACATGGCTCTAGTTGTCGACACCTACTATGATGATCAACTCATTAGCTGTGGCAGCGTCAACAGAGGGACCTGCCAGCGACATGTCTTTCCCCACAATCATACTGCTGACATACAGTCGGAGGTTCACTGCATATTCTCCCCACAGATAGAAGAGCCCAGCCAGTGTCCTGACTGTGTGGTGAGCGCCCTGGGAGCCAAAGTCCTTTCATCTGTAAAGGACCGGTTCATCAACTTCTTTGTAGGCAATACCATAAATTCTTCTTATTTCCCAGATCATCCATTGCATTCGATATCAGTGAGAAGGCTAAAGGAAACGAAAGATGGTTTTATGTTTTTGACGGACCAGTCCTACATTGATGTTTTACCTGAGTTCAGAGATTCTTACCCCATTAAGTATGTCCATGCCTTTGAAAGCAACAATTTTATTTACTTCTTGACGGTCCAAAGGGAAACTCTAGATGCTCAGACTTTTCACACAAGAATAATCAGGTTCTGTTCCATAAACTCTGGATTGCATTCCTACATGGAAATGCCTCTGGAGTGTATTCTCACAGAAAAGAGAAAAAAGAGATCCACAAAGAAGGAAGTGTTTAATATACTTCAGGCTGCGTATGTCAGCAAGCCTGGGGCCCAGCTTGCTAGACAAATAGGAGCCAGCCTGAATGATGACATTCTTTTCGGGGTGTTCGCACAAAGCAAGCCAGATTCTGCCGAACCAATGGATCGATCTGCCATGTGTGCATTCCCTATCAAATATGTCAACGACTTCTTCAACAAGATCGTCAACAAAAACAATGTGAGATGTCTCCAGCATTTTTACGGACCCAATCATGAGCACTGCTTTAATAGGACACTTCTGAGAAATTCATCAGGCTGTGAAGCGCGCCGTGATGAATATCGAACAGAGTTTACCACAGCTTTGCAGCGCGTTGACTTATTCATGGGTCAATTCAGCGAAGTCCTCTTAACATCTATATCCACCTTCATTAAAGGAGACCTCACCATAGCTAATCTTGGGACATCAGAGGGTCGCTTCATGCAGGTTGTGGTTTCTCGATCAGGACCATCAACCCCTCATGTGAATTTTCTCCTGGACTCCCATCCAGTGTCTCCAGAAGTGATTGTGGAGCATACATTAAACCAAAATGGCTACACACTGGTTATCACTGGGAAGAAGATCACGAAGATCCCATTGAATGGCTTGGGCTGCAGACATTTCCAGTCCTGCAGTCAATGCCTCTCTGCCCCACCCTTTGTTCAGTGTGGCTGGTGCCACGACAAATGTGTGCGATCGGAGGAATGCCTGAGCGGGACATGGACTCAACAGATCTGTCTGCCTGCAATCTACAAGGTTTTCCCAAATAGTGCACCCCTTGAAGGAGGGACAAGGCTGACCATATGTGGCTGGGACTTTGGATTTCGGAGGAATAATAAATTTGATTTAAAGAAAACTAGAGTTCTCCTTGGAAATGAGAGCTGCACCTTGACTTTAAGTGAGAGCACGATGAATACATTGAAATGCACAGTTGGTCCTGCCATGAATAAGCATTTCAATATGTCCATAATTATTTCAAATGGCCACGGGACAACACAATACAGTACATTCTCCTATGTGGATCCTGTAATAACAAGTATTTCGCCGAAATACGGTCCTATGGCTGGTGGCACTTTACTTACTTTAACTGGAAATTACCTAAACAGTGGGAATTCTAGACACATTTCAATTGGTGGAAAAACATGTACTTTAAAAAGTGTGTCAAACAGTATTCTTGAATGTTATACCCCAGCCCAAACCATTTCAACTGAGTTTGCTGTTAAATTGAAAATTGACTTAGCCAACCGAGAGACAAGCATCTTCAGTTACCGTGAAGATCCCATTGTCTATGAAATTCATCCAACCAAATCTTTTATTAGTGGTGGGAGCACAATAACAGGTGTTGGGAAAAACCTGAATTCAGTTAGTGTCCCGAGAATGGTCATAAATGTGCATGAAGCAGGAAGGAACTTTACAGTGGCATGTCAACATCGCTCTAATTCAGAGATAATCTGTTGTACCACTCCTTCCCTGCAACAGCTGAATCTGCAACTCCCCCTGAAAACCAAAGCCTTTTTCATGTTAGATGGGATCCTTTCCAAATACTTTGATCTCATTTATGTACATAATCCTGTGTTTAAGCCTTTTGAAAAGCCAGTGATGATCTCAATGGGCAATGAAAATGTACTGGAAATTAAGGGAAATGATATTGACCCTGAAGCAGTTAAAGGTGAAGTGTTAAAAGTTGGAAATAAGAGCTGTGAGAATATACACTTACATTCTGAAGCCGTTTTATGCACGGTCCCCAATGACCTGCTGAAATTGAACAGCGAGCTAAATATAGAGTGGAAGCAAGCAATTTCTTCAACCGTCCTTGGAAAAGTAATAGTTCAACCAGATCAGAATTTCACAGGATTGATTGCTGGTGTTGTCTCAATATCAACAGCACTGTTATTACTACTTGGGTTTTTCCTGTGGCTGAAAAAGAGAAAGCAAATTAAAGATCTGGGCAGTGAATTAGTTCGCTACGATGCAAGAGTACACACTCCTCATTTGGATAGGCTTGTAAGTGCCCGAAGTGTAAGCCCAACTACAGAAATGGTTTCAAATGAATCTGTAGACTACCGAGCTACTTTTCCAGAAGATCAGTTTCCTAATTCATCTCAGAACGGTTCATGCCGACAAGTGCAGTATCCTCTGACAGACATGTCCCCCATCCTAACTAGTGGGGACTCTGATATATCCAGTCCATTACTGCAAAATACTGTCCACATTGACCTCAGTGCTCTAAATCCAGAGCTGGTCCAGGCAGTGCAGCATGTAGTGATTGGGCCCAGTAGCCTGATTGTGCATTTCAATGAAGTCATAGGAAGAGGGCATTTTGGTTGTGTATATCATGGGACTTTGTTGGACAATGATGGCAAGAAAATTCACTGTGCTGTGAAATCCTTGAACAGAATCACTGACATAGGAGAAGTTTCCCAATTTCTGACCGAGGGAATCATCATGAAAGATTTTAGTCATCCCAATGTCCTCTCGCTCCTGGGAATCTGCCTGCGAAGTGAAGGGTCTCCGCTGGTGGTCCTACCATACATGAAACATGGAGATCTTCGAAATTTCATTCGAAATGAGACTCATAATCCAACTGTAAAAGATCTTATTGGCTTTGGTCTTCAAGTAGCCAAAGGCATGAAATATCTTGCAAGCAAAAAGTTTGTCCACAGAGACTTGGCTGCAAGAAACTGTATGCTGGATGAAAAATTCACAGTCAAGGTTGCTGATTTTGGTCTTGCCAGAGACATGTATGATAAAGAATACTATAGTGTACACAACAAAACAGGTGCAAAGCTGCCAGTGAAGTGGATGGCTTTGGAAAGTCTGCAAACTCAAAAGTTTACCACCAAGTCAGATGTGTGGTCCTTTGGCGTGCTCCTCTGGGAGCTGATGACAAGAGGAGCCCCACCTTATCCTGACGTAAACACCTTTGATATAACTGTTTACTTGTTGCAAGGGAGAAGACTCCTACAACCCGAATACTGCCCAGACCCCTTATATGAAGTAATGCTAAAATGCTGGCACCCTAAAGCCGAAATGCGCCCATCCTTTTCTGAACTGGTGTCCCGGATATCAGCGATCTTCTCTACTTTCATTGGGGAGCACTATGTCCATGTGAACGCTACTTATGTGAACGTAAAATGTGTCGCTCCGTATCCTTCTCTGTTGTCATCAGAAGATAACGCTGATGATGAGGTGGACACACGACCAGCCTCCTTCTGGGAGACATCA
>MET의 세포외 도메인 (서열번호 11)
ECKEALAKSEMNVNMKYQLPNFTAETPIQNVILHEHHIFLGATNYIYVLNEEDLQKVAEYKTGPVLEHPDCFPCQDCSSKANLSGGVWKDNINMALVVDTYYDDQLISCGSVNRGTCQRHVFPHNHTADIQSEVHCIFSPQIEEPSQCPDCVVSALGAKVLSSVKDRFINFFVGNTINSSYFPDHPLHSISVRRLKETKDGFMFLTDQSYIDVLPEFRDSYPIKYVHAFESNNFIYFLTVQRETLDAQTFHTRIIRFCSINSGLHSYMEMPLECILTEKRKKRSTKKEVFNILQAAYVSKPGAQLARQIGASLNDDILFGVFAQSKPDSAEPMDRSAMCAFPIKYVNDFFNKIVNKNNVRCLQHFYGPNHEHCFNRTLLRNSSGCEARRDEYRTEFTTALQRVDLFMGQFSEVLLTSISTFIKGDLTIANLGTSEGRFMQVVVSRSGPSTPHVNFLLDSHPVSPEVIVEHTLNQNGYTLVITGKKITKIPLNGLGCRHFQSCSQCLSAPPFVQCGWCHDKCVRSEECLSGTWTQQICLPAIYKVFPNSAPLEGGTRLTICGWDFGFRRNNKFDLKKTRVLLGNESCTLTLSESTMNTLKCTVGPAMNKHFNMSIIISNGHGTTQYSTFSYVDPVITSISPKYGPMAGGTLLTLTGNYLNSGNSRHISIGGKTCTLKSVSNSILECYTPAQTISTEFAVKLKIDLANRETSIFSYREDPIVYEIHPTKSFISGGSTITGVGKNLNSVSVPRMVINVHEAGRNFTVACQHRSNSEIICCTTPSLQQLNLQLPLKTKAFFMLDGILSKYFDLIYVHNPVFKPFEKPVMISMGNENVLEIKGNDIDPEAVKGEVLKVGNKSCENIHLHSEAVLCTVPNDLLKLNSELNIEWKQAISSTVLGKVIVQPDQNFT
>MET의 세포외 도메인을 암호화하는 cDNA (서열번호 12)
GAGTGTAAAGAGGCACTAGCAAAGTCCGAGATGAATGTGAATATGAAGTATCAGCTTCCCAACTTCACCGCGGAAACACCCATCCAGAATGTCATTCTACATGAGCATCACATTTTCCTTGGTGCCACTAACTACATTTATGTTTTAAATGAGGAAGACCTTCAGAAGGTTGCTGAGTACAAGACTGGGCCTGTGCTGGAACACCCAGATTGTTTCCCATGTCAGGACTGCAGCAGCAAAGCCAATTTATCAGGAGGTGTTTGGAAAGATAACATCAACATGGCTCTAGTTGTCGACACCTACTATGATGATCAACTCATTAGCTGTGGCAGCGTCAACAGAGGGACCTGCCAGCGACATGTCTTTCCCCACAATCATACTGCTGACATACAGTCGGAGGTTCACTGCATATTCTCCCCACAGATAGAAGAGCCCAGCCAGTGTCCTGACTGTGTGGTGAGCGCCCTGGGAGCCAAAGTCCTTTCATCTGTAAAGGACCGGTTCATCAACTTCTTTGTAGGCAATACCATAAATTCTTCTTATTTCCCAGATCATCCATTGCATTCGATATCAGTGAGAAGGCTAAAGGAAACGAAAGATGGTTTTATGTTTTTGACGGACCAGTCCTACATTGATGTTTTACCTGAGTTCAGAGATTCTTACCCCATTAAGTATGTCCATGCCTTTGAAAGCAACAATTTTATTTACTTCTTGACGGTCCAAAGGGAAACTCTAGATGCTCAGACTTTTCACACAAGAATAATCAGGTTCTGTTCCATAAACTCTGGATTGCATTCCTACATGGAAATGCCTCTGGAGTGTATTCTCACAGAAAAGAGAAAAAAGAGATCCACAAAGAAGGAAGTGTTTAATATACTTCAGGCTGCGTATGTCAGCAAGCCTGGGGCCCAGCTTGCTAGACAAATAGGAGCCAGCCTGAATGATGACATTCTTTTCGGGGTGTTCGCACAAAGCAAGCCAGATTCTGCCGAACCAATGGATCGATCTGCCATGTGTGCATTCCCTATCAAATATGTCAACGACTTCTTCAACAAGATCGTCAACAAAAACAATGTGAGATGTCTCCAGCATTTTTACGGACCCAATCATGAGCACTGCTTTAATAGGACACTTCTGAGAAATTCATCAGGCTGTGAAGCGCGCCGTGATGAATATCGAACAGAGTTTACCACAGCTTTGCAGCGCGTTGACTTATTCATGGGTCAATTCAGCGAAGTCCTCTTAACATCTATATCCACCTTCATTAAAGGAGACCTCACCATAGCTAATCTTGGGACATCAGAGGGTCGCTTCATGCAGGTTGTGGTTTCTCGATCAGGACCATCAACCCCTCATGTGAATTTTCTCCTGGACTCCCATCCAGTGTCTCCAGAAGTGATTGTGGAGCATACATTAAACCAAAATGGCTACACACTGGTTATCACTGGGAAGAAGATCACGAAGATCCCATTGAATGGCTTGGGCTGCAGACATTTCCAGTCCTGCAGTCAATGCCTCTCTGCCCCACCCTTTGTTCAGTGTGGCTGGTGCCACGACAAATGTGTGCGATCGGAGGAATGCCTGAGCGGGACATGGACTCAACAGATCTGTCTGCCTGCAATCTACAAGGTTTTCCCAAATAGTGCACCCCTTGAAGGAGGGACAAGGCTGACCATATGTGGCTGGGACTTTGGATTTCGGAGGAATAATAAATTTGATTTAAAGAAAACTAGAGTTCTCCTTGGAAATGAGAGCTGCACCTTGACTTTAAGTGAGAGCACGATGAATACATTGAAATGCACAGTTGGTCCTGCCATGAATAAGCATTTCAATATGTCCATAATTATTTCAAATGGCCACGGGACAACACAATACAGTACATTCTCCTATGTGGATCCTGTAATAACAAGTATTTCGCCGAAATACGGTCCTATGGCTGGTGGCACTTTACTTACTTTAACTGGAAATTACCTAAACAGTGGGAATTCTAGACACATTTCAATTGGTGGAAAAACATGTACTTTAAAAAGTGTGTCAAACAGTATTCTTGAATGTTATACCCCAGCCCAAACCATTTCAACTGAGTTTGCTGTTAAATTGAAAATTGACTTAGCCAACCGAGAGACAAGCATCTTCAGTTACCGTGAAGATCCCATTGTCTATGAAATTCATCCAACCAAATCTTTTATTAGTGGTGGGAGCACAATAACAGGTGTTGGGAAAAACCTGAATTCAGTTAGTGTCCCGAGAATGGTCATAAATGTGCATGAAGCAGGAAGGAACTTTACAGTGGCATGTCAACATCGCTCTAATTCAGAGATAATCTGTTGTACCACTCCTTCCCTGCAACAGCTGAATCTGCAACTCCCCCTGAAAACCAAAGCCTTTTTCATGTTAGATGGGATCCTTTCCAAATACTTTGATCTCATTTATGTACATAATCCTGTGTTTAAGCCTTTTGAAAAGCCAGTGATGATCTCAATGGGCAATGAAAATGTACTGGAAATTAAGGGAAATGATATTGACCCTGAAGCAGTTAAAGGTGAAGTGTTAAAAGTTGGAAATAAGAGCTGTGAGAATATACACTTACATTCTGAAGCCGTTTTATGCACGGTCCCCAATGACCTGCTGAAATTGAACAGCGAGCTAAATATAGAGTGGAAGCAAGCAATTTCTTCAACCGTCCTTGGAAAAGTAATAGTTCAACCAGATCAGAATTTCACA
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #1의 중쇄 (서열번호 13)
QVQLVQSGAEVKKPGASVKVSCKASHYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #2의 중쇄 (서열번호 14)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #3의 중쇄 (서열번호 15)
QVQLVQSGAEVKKPGASVKVSCKASGYHFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #4의 중쇄 (서열번호 16)
QVQLVQSGAEVKKPGASVKVSCKASGYIHTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #5의 중쇄 (서열번호 17)
QVQLVQSGAEVKKPGASVKVSCKASGYIFHAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #6의 중쇄 (서열번호 18)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTHYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #7의 중쇄 (서열번호 19)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAHTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #8의 중쇄 (서열번호 20)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYHMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #9의 중쇄 (서열번호 21)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTHHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #10의 중쇄 (서열번호 22)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMAWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #11의 중쇄 (서열번호 23)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGHIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #12의 중쇄 (서열번호 24)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWHKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #13의 중쇄 (서열번호 25)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIHPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #14의 중쇄 (서열번호 26)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKHNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #15의 중쇄 (서열번호 27)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPHNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #16의 중쇄 (서열번호 28)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNHGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #17의 중쇄 (서열번호 29)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNHLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #18의 중쇄 (서열번호 30)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGHANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #19의 중쇄 (서열번호 31)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLHNYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #20의 중쇄 (서열번호 32)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLAHYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #21의 중쇄 (서열번호 33)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANHAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #22의 중쇄 (서열번호 34)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYHQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #23의 중쇄 (서열번호 35)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAHKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #24의 중쇄 (서열번호 36)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQHFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #25의 중쇄 (서열번호 37)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKHQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #26의 중쇄 (서열번호 38)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFHGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #27의 중쇄 (서열번호 39)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQHRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #28의 중쇄 (서열번호 40)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #29의 중쇄 (서열번호 41)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCAHSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #30의 중쇄 (서열번호 42)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARHEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #31의 중쇄 (서열번호 43)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSHITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #32의 중쇄 (서열번호 44)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEHTTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #33의 중쇄 (서열번호 45)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEIHTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #34의 중쇄 (서열번호 46)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITHEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #35의 중쇄 (서열번호 47)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTHFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #36의 중쇄 (서열번호 48)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEHDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #37의 중쇄 (서열번호 49)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFHYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #38의 중쇄 (서열번호 50)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #1의 경쇄 (서열번호 51)
DIVMTQSPDSLAVSLGERATINCHSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #2의 경쇄 (서열번호 52)
DIVMTQSPDSLAVSLGERATINCKHSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #3의 경쇄 (서열번호 53)
DIVMTQSPDSLAVSLGERATINCKSHESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #4의 경쇄 (서열번호 54)
DIVMTQSPDSLAVSLGERATINCKSSHSVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #5의 경쇄 (서열번호 55)
DIVMTQSPDSLAVSLGERATINCKSSEHVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #6의 경쇄 (서열번호 56)
DIVMTQSPDSLAVSLGERATINCKSSESHDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #7의 경쇄 (서열번호 57)
DIVMTQSPDSLAVSLGERATINCKSSESVHSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #8의 경쇄 (서열번호 58)
DIVMTQSPDSLAVSLGERATINCKSSESVDHYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #9의 경쇄 (서열번호 59)
DIVMTQSPDSLAVSLGERATINCKSSESVDSHANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #10의 경쇄 (서열번호 60)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYHNSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #11의 경쇄 (서열번호 61)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYAHSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #12의 경쇄 (서열번호 62)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANHFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #13의 경쇄 (서열번호 63)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSHLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #14의 경쇄 (서열번호 64)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFHHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #15의 경쇄 (서열번호 65)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLAWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #16의 경쇄 (서열번호 66)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYHASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #17의 경쇄 (서열번호 67)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRHSTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #18의 경쇄 (서열번호 68)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRAHTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #19의 경쇄 (서열번호 69)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASHRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #20의 경쇄 (서열번호 70)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTHESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #21의 경쇄 (서열번호 71)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRHSGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #22의 경쇄 (서열번호 72)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTREHGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #23의 경쇄 (서열번호 73)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCHQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #24의 경쇄 (서열번호 74)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQHSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #25의 경쇄 (서열번호 75)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQHKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #26의 경쇄 (서열번호 76)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSHEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #27의 경쇄 (서열번호 77)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKHDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #28의 경쇄 (서열번호 78)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEHPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #29의 경쇄 (서열번호 79)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDHLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #30의 경쇄 (서열번호 80)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPHTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #31의 경쇄 (서열번호 81)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLHFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #1의 중쇄 조합 (서열번호 82)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARHEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #2의 중쇄 조합 (서열번호 83)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITHEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #3의 중쇄 조합 (서열번호 84)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITTEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #4의 중쇄 조합 (서열번호 85)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARHEITHEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #5의 중쇄 조합 (서열번호 86)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARHEITTEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #6의 중쇄 조합 (서열번호 87)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITHEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #7의 중쇄 조합 (서열번호 88)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARHEITHEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #8의 중쇄 조합 (서열번호 89)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARHEITTEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #9의 중쇄 조합 (서열번호 90)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEITHEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #10의 중쇄 조합 (서열번호 91)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARHEITHEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #11의 중쇄 조합 (서열번호 92)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #12의 중쇄 조합 (서열번호 93)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRHEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #13의 중쇄 조합 (서열번호 94)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRSEITHEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #14의 중쇄 조합 (서열번호 95)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRSEITTEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #15의 중쇄 조합 (서열번호 96)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCAHSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #16의 중쇄 조합 (서열번호 97)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCAHHEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #17의 중쇄 조합 (서열번호 98)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCAHSEITHEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #18의 중쇄 조합 (서열번호 99)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCAHSEITTEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #19의 중쇄 조합 (서열번호 100)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEIHTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #20의 중쇄 조합 (서열번호 101)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARHEIHTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #21의 중쇄 조합 (서열번호 102)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEIHHEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #22의 중쇄 조합 (서열번호 103)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEIHTEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #23의 중쇄 조합 (서열번호 104)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRSEITTEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #24의 중쇄 조합 (서열번호 105)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRHEITTEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #25의 중쇄 조합 (서열번호 106)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRSEITHEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #26의 중쇄 조합 (서열번호 107)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRHEITTEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #27의 중쇄 조합 (서열번호 108)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRSEITHEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #28의 중쇄 조합 (서열번호 109)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCAHSEITTEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #29의 중쇄 조합 (서열번호 110)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCAHHEITTEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #30의 중쇄 조합 (서열번호 111)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCAHSEITHEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #31의 중쇄 조합 (서열번호 112)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCAHHEITTEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #32의 중쇄 조합 (서열번호 113)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCAHSEITHEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #33의 중쇄 조합 (서열번호 114)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEIHTEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #34의 중쇄 조합 (서열번호 115)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARHEIHTEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #35의 중쇄 조합 (서열번호 116)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEIHHEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #36의 중쇄 조합 (서열번호 117)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARHEIHTEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #37의 중쇄 조합 (서열번호 118)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARSEIHHEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #38의 중쇄 조합 (서열번호 119)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHHSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #39의 중쇄 조합 (서열번호 120)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCAHSEIHTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #40의 중쇄 조합 (서열번호 121)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRSEIHTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #41의 중쇄 조합 (서열번호 122)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHHSEIHTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #42의 중쇄 조합 (서열번호 123)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHHSEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #43의 중쇄 조합 (서열번호 124)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHHHEITTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #44의 중쇄 조합 (서열번호 125)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHHSEITHEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #45의 중쇄 조합 (서열번호 126)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHHSEITTEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #46의 중쇄 조합 (서열번호 127)
QVQLVQSGAEVKKPGASVKVSCKASGHIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRSEIHTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #47의 중쇄 조합 (서열번호 128)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRHEIHTEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #48의 중쇄 조합 (서열번호 129)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRSEIHHEFDYWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #49의 중쇄 조합 (서열번호 130)
QVQLVQSGAEVKKPGASVKVSCKASGYIFTAYTMHWVRQAPGQGLEWMGWIKPNNGLANYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCHRSEIHTEFDHWGQGTLVTVSS
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #1의 경쇄 조합 (서열번호 131)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYAHSHLHWYQQKPGQPPKLLIYRASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #2의 경쇄 조합 (서열번호 132)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYAHSFLHWYQQKPGQPPKLLIYHASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #3의 경쇄 조합 (서열번호 133)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYAHSFLHWYQQKPGQPPKLLIYRASTREHGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #4의 경쇄 조합 (서열번호 134)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSHLHWYQQKPGQPPKLLIYHASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #5의 경쇄 조합 (서열번호 135)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSHLHWYQQKPGQPPKLLIYRASTREHGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #6의 경쇄 조합 (서열번호 136)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYHASTREHGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #7의 경쇄 조합 (서열번호 137)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYAHSHLHWYQQKPGQPPKLLIYHASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #8의 경쇄 조합 (서열번호 138)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYAHSHLHWYQQKPGQPPKLLIYRASTREHGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #9의 경쇄 조합 (서열번호 139)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYAHSFLHWYQQKPGQPPKLLIYHASTREHGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #10의 경쇄 조합 (서열번호 140)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSHLHWYQQKPGQPPKLLIYHASTREHGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #11의 경쇄 조합 (서열번호 141)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYAHSFLHWYQQKPGQPPKLLIYRASTRHSGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #12의 경쇄 조합 (서열번호 142)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSHLHWYQQKPGQPPKLLIYRASTRHSGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #13의 경쇄 조합 (서열번호 143)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFHHWYQQKPGQPPKLLIYRASTRHSGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #14의 경쇄 조합 (서열번호 144)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYHASTRHSGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>텔리소투주맙 IgG 히스티딘 스캐닝 변이체 #15의 경쇄 조합 (서열번호 145)
DIVMTQSPDSLAVSLGERATINCKSSESVDSYANSFLHWYQQKPGQPPKLLIYRASTRHHGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQSKEDPLTFGGGTKVEIK
>에미베투주맙 IgG의 중쇄 (서열번호 146)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG의 경쇄 (서열번호 147)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>에미베투주맙의 중쇄 CDR1 (서열번호 148)
GYTFTDYYMH
>에미베투주맙의 중쇄 CDR2 (서열번호 149)
RVNPNRRGTTYNQKFEG
>에미베투주맙의 중쇄 CDR3 (서열번호 150)
ARANWLDY
>에미베투주맙의 경쇄 CDR1 (서열번호 151)
SVSSSVSSIYLH
>에미베투주맙의 경쇄 CDR2 (서열번호 152)
STSNLAS
>에미베투주맙의 경쇄 CDR3 (서열번호 153)
QVYSGYPLT
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #1의 중쇄 (서열번호 154)
QVQLVQSGAEVKKPGASVKVSCKASHYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #2의 중쇄 (서열번호 155)
QVQLVQSGAEVKKPGASVKVSCKASGHTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #3의 중쇄 (서열번호 156)
QVQLVQSGAEVKKPGASVKVSCKASGYHFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #4의 중쇄 (서열번호 157)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #5의 중쇄 (서열번호 158)
QVQLVQSGAEVKKPGASVKVSCKASGYTFHDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #6의 중쇄 (서열번호 159)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #7의 중쇄 (서열번호 160)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDHYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #8의 중쇄 (서열번호 161)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYHMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #9의 중쇄 (서열번호 162)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYHHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #10의 중쇄 (서열번호 163)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMAWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #11의 중쇄 (서열번호 164)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGHVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #12의 중쇄 (서열번호 165)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRHNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #13의 중쇄 (서열번호 166)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #14의 중쇄 (서열번호 167)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNHNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #15의 중쇄 (서열번호 168)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #16의 중쇄 (서열번호 169)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNHRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #17의 중쇄 (서열번호 170)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRHGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #18의 중쇄 (서열번호 171)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #19의 중쇄 (서열번호 172)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGHTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #20의 중쇄 (서열번호 173)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTHYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #21의 중쇄 (서열번호 174)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTHNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #22의 중쇄 (서열번호 175)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYHQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #23의 중쇄 (서열번호 176)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNHKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #24의 중쇄 (서열번호 177)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQHFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #25의 중쇄 (서열번호 178)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKHEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #26의 중쇄 (서열번호 179)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFHGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #27의 중쇄 (서열번호 180)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEHRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #28의 중쇄 (서열번호 181)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCHRANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #29의 중쇄 (서열번호 182)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCAHANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #30의 중쇄 (서열번호 183)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #31의 중쇄 (서열번호 184)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #32의 중쇄 (서열번호 185)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANHLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #33의 중쇄 (서열번호 186)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWHDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #34의 중쇄 (서열번호 187)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLHYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #35의 중쇄 (서열번호 188)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDHWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #1의 경쇄 (서열번호 189)
DIQMTQSPSSLSASVGDRVTITCHVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #2의 경쇄 (서열번호 190)
DIQMTQSPSSLSASVGDRVTITCSHSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #3의 경쇄 (서열번호 191)
DIQMTQSPSSLSASVGDRVTITCSVHSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #4의 경쇄 (서열번호 192)
DIQMTQSPSSLSASVGDRVTITCSVSHSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #5의 경쇄 (서열번호 193)
DIQMTQSPSSLSASVGDRVTITCSVSSHVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #6의 경쇄 (서열번호 194)
DIQMTQSPSSLSASVGDRVTITCSVSSSHSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #7의 경쇄 (서열번호 195)
DIQMTQSPSSLSASVGDRVTITCSVSSSVHSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #8의 경쇄 (서열번호 196)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSHIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #9의 경쇄 (서열번호 197)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSHYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #10의 경쇄 (서열번호 198)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIHLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #11의 경쇄 (서열번호 199)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYHHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #12의 경쇄 (서열번호 200)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLAWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #13의 경쇄 (서열번호 201)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYHTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #14의 경쇄 (서열번호 202)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSHSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #15의 경쇄 (서열번호 203)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTHNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #16의 경쇄 (서열번호 204)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSHLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #17의 경쇄 (서열번호 205)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNHASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #18의 경쇄 (서열번호 206)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLHSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #19의 경쇄 (서열번호 207)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLAHGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #20의 경쇄 (서열번호 208)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCHVYSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #21의 경쇄 (서열번호 209)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHYSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #22의 경쇄 (서열번호 210)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVHSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #23의 경쇄 (서열번호 211)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYHGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #24의 경쇄 (서열번호 212)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSHYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #25의 경쇄 (서열번호 213)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGHPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #26의 경쇄 (서열번호 214)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYHLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #27의 경쇄 (서열번호 215)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPHTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #28의 경쇄 (서열번호 216)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLHFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #1의 중쇄 조합 (서열번호 217)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVHPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #2의 중쇄 조합 (서열번호 218)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #3의 중쇄 조합 (서열번호 219)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #4의 중쇄 조합 (서열번호 220)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #5의 중쇄 조합 (서열번호 221)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #6의 중쇄 조합 (서열번호 222)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #7의 중쇄 조합 (서열번호 223)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #8의 중쇄 조합 (서열번호 224)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPHRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #9의 중쇄 조합 (서열번호 225)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #10의 중쇄 조합 (서열번호 226)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #11의 중쇄 조합 (서열번호 227)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVHPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #12의 중쇄 조합 (서열번호 228)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVHPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #13의 중쇄 조합 (서열번호 229)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVHPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #14의 중쇄 조합 (서열번호 230)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPHRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #15의 중쇄 조합 (서열번호 231)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #16의 중쇄 조합 (서열번호 232)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #17의 중쇄 조합 (서열번호 233)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPHRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #18의 중쇄 조합 (서열번호 234)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #19의 중쇄 조합 (서열번호 235)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #20의 중쇄 조합 (서열번호 236)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPHRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #21의 중쇄 조합 (서열번호 237)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNHNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #22의 중쇄 조합 (서열번호 238)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHHNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #23의 중쇄 조합 (서열번호 239)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #24의 중쇄 조합 (서열번호 240)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #25의 중쇄 조합 (서열번호 241)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNHNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #26의 중쇄 조합 (서열번호 242)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNHNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #27의 중쇄 조합 (서열번호 243)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHHNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #28의 중쇄 조합 (서열번호 244)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVHHNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #29의 중쇄 조합 (서열번호 245)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNHHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #30의 중쇄 조합 (서열번호 246)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNHNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #31의 중쇄 조합 (서열번호 247)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNHNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #32의 중쇄 조합 (서열번호 248)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHHHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #33의 중쇄 조합 (서열번호 249)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHHNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #34의 중쇄 조합 (서열번호 250)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHHNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #35의 중쇄 조합 (서열번호 251)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNHHRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #36의 중쇄 조합 (서열번호 252)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNHHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #37의 중쇄 조합 (서열번호 253)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNHNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #38의 중쇄 조합 (서열번호 254)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVHHHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #39의 중쇄 조합 (서열번호 255)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVHHNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #40의 중쇄 조합 (서열번호 256)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVHHNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #41의 중쇄 조합 (서열번호 257)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNHHRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #42의 중쇄 조합 (서열번호 258)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNHHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #43의 중쇄 조합 (서열번호 259)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNHNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #44의 중쇄 조합 (서열번호 260)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHHHRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARANWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #45의 중쇄 조합 (서열번호 261)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHHHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #46의 중쇄 조합 (서열번호 262)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHHNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #47의 중쇄 조합 (서열번호 263)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNHHRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARAHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #48의 중쇄 조합 (서열번호 264)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVHPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #49의 중쇄 조합 (서열번호 265)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #50의 중쇄 조합 (서열번호 266)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #51의 중쇄 조합 (서열번호 267)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #52의 중쇄 조합 (서열번호 268)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #53의 중쇄 조합 (서열번호 269)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #54의 중쇄 조합 (서열번호 270)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #55의 중쇄 조합 (서열번호 271)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPHRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #56의 중쇄 조합 (서열번호 272)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #57의 중쇄 조합 (서열번호 273)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #58의 중쇄 조합 (서열번호 274)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVHPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #59의 중쇄 조합 (서열번호 275)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVHPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #60의 중쇄 조합 (서열번호 276)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVHPNRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #61의 중쇄 조합 (서열번호 277)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPHRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #62의 중쇄 조합 (서열번호 278)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #63의 중쇄 조합 (서열번호 279)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYYMHWVRQAPGQGLEWMGRVNPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #64의 중쇄 조합 (서열번호 280)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPHRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHNWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #65의 중쇄 조합 (서열번호 281)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPHRRGTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #66의 중쇄 조합 (서열번호 282)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVHPNRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #67의 중쇄 조합 (서열번호 283)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTDYYMHWVRQAPGQGLEWMGRVNPHRRHTTYNQKFEGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARHHWLDYWGQGTTVTVSS
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #1의 경쇄 조합 (서열번호 284)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIHLHWYQQKPGKAPKLLIYHTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #2의 경쇄 조합 (서열번호 285)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIHLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHYSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #3의 경쇄 조합 (서열번호 286)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIHLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVHSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #4의 경쇄 조합 (서열번호 287)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIHLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGHPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #5의 경쇄 조합 (서열번호 288)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYHTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHYSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #6의 경쇄 조합 (서열번호 289)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYHTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVHSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #7의 경쇄 조합 (서열번호 290)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYHTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGHPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #8의 경쇄 조합 (서열번호 291)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHHSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #9의 경쇄 조합 (서열번호 292)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHYSGHPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #10의 경쇄 조합 (서열번호 293)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVHSGHPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #11의 경쇄 조합 (서열번호 294)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIHLHWYQQKPGKAPKLLIYHTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHYSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #12의 경쇄 조합 (서열번호 295)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIHLHWYQQKPGKAPKLLIYHTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVHSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #13의 경쇄 조합 (서열번호 296)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIHLHWYQQKPGKAPKLLIYHTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVYSGHPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #14의 경쇄 조합 (서열번호 297)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIHLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHHSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #15의 경쇄 조합 (서열번호 298)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIHLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHYSGHPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #16의 경쇄 조합 (서열번호 299)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIHLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVHSGHPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #17의 경쇄 조합 (서열번호 300)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYHTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHHSGYPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #18의 경쇄 조합 (서열번호 301)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYHTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHYSGHPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #19의 경쇄 조합 (서열번호 302)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYHTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQVHSGHPLTFGGGTKVEIK
>에미베투주맙 IgG 히스티딘 스캐닝 변이체 #20의 경쇄 조합 (서열번호 303)
DIQMTQSPSSLSASVGDRVTITCSVSSSVSSIYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHHSGHPLTFGGGTKVEIK
>hucMET27Gv1.3 IgG의 중쇄 (서열번호 304)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG의 경쇄 (서열번호 305)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3의 중쇄 CDR1 (서열번호 306)
GFTFSSYDMS
>hucMET27Gv1.3의 중쇄 CDR2 (서열번호 307)
TINSNGVSIYYPDSVKG
>hucMET27Gv1.3의 중쇄 CDR3 (서열번호 308)
AREEITTEMDY
>hucMET27Gv1.3의 경쇄 CDR1 (서열번호 309)
RASESVDSYGNSFIH
>hucMET27Gv1.3의 경쇄 CDR2 (서열번호 310)
RASNLES
>hucMET27Gv1.3의 경쇄 CDR3 (서열번호 311)
QQSNEEPLT
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #1의 중쇄 (서열번호 312)
EVQLVESGGGLVQPGGSLRLSCAASHFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #2의 중쇄 (서열번호 313)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #3의 중쇄 (서열번호 314)
EVQLVESGGGLVQPGGSLRLSCAASGFHFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #4의 중쇄 (서열번호 315)
EVQLVESGGGLVQPGGSLRLSCAASGFTHSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #5의 중쇄 (서열번호 316)
EVQLVESGGGLVQPGGSLRLSCAASGFTFHSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #6의 중쇄 (서열번호 317)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSHYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #7의 중쇄 (서열번호 318)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSHDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #8의 중쇄 (서열번호 319)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYHMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #9의 중쇄 (서열번호 320)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDHSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #10의 중쇄 (서열번호 321)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMHWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #11의 중쇄 (서열번호 322)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVAHINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #12의 중쇄 (서열번호 323)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATHNSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #13의 중쇄 (서열번호 324)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATIHSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #14의 중쇄 (서열번호 325)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINHNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #15의 중쇄 (서열번호 326)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSHGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #16의 중쇄 (서열번호 327)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNHVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #17의 중쇄 (서열번호 328)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGHSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #18의 중쇄 (서열번호 329)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVHIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #19의 중쇄 (서열번호 330)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSHYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #20의 중쇄 (서열번호 331)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIHYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #21의 중쇄 (서열번호 332)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #22의 중쇄 (서열번호 333)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYHDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #23의 중쇄 (서열번호 334)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPHSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #24의 중쇄 (서열번호 335)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDHVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #25의 중쇄 (서열번호 336)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSHKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #26의 중쇄 (서열번호 337)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVHGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #27의 중쇄 (서열번호 338)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #28의 중쇄 (서열번호 339)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCHREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #29의 중쇄 (서열번호 340)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAHEEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #30의 중쇄 (서열번호 341)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCARHEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #31의 중쇄 (서열번호 342)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREHITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #32의 중쇄 (서열번호 343)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEHTTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #33의 중쇄 (서열번호 344)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEIHTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #34의 중쇄 (서열번호 345)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #35의 중쇄 (서열번호 346)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTHMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #36의 중쇄 (서열번호 347)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #37의 중쇄 (서열번호 348)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMHYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #38의 중쇄 (서열번호 349)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #1의 경쇄 (서열번호 350)
EIVLTQSPATLSLSPGERATLSCHASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #2의 경쇄 (서열번호 351)
EIVLTQSPATLSLSPGERATLSCRHSESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #3의 경쇄 (서열번호 352)
EIVLTQSPATLSLSPGERATLSCRAHESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #4의 경쇄 (서열번호 353)
EIVLTQSPATLSLSPGERATLSCRASHSVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #5의 경쇄 (서열번호 354)
EIVLTQSPATLSLSPGERATLSCRASEHVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #6의 경쇄 (서열번호 355)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #7의 경쇄 (서열번호 356)
EIVLTQSPATLSLSPGERATLSCRASESVHSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #8의 경쇄 (서열번호 357)
EIVLTQSPATLSLSPGERATLSCRASESVDHYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #9의 경쇄 (서열번호 358)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #10의 경쇄 (서열번호 359)
EIVLTQSPATLSLSPGERATLSCRASESVDSYHNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #11의 경쇄 (서열번호 360)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #12의 경쇄 (서열번호 361)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNHFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #13의 경쇄 (서열번호 362)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #14의 경쇄 (서열번호 363)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFHHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #15의 경쇄 (서열번호 364)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIAWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #16의 경쇄 (서열번호 365)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #17의 경쇄 (서열번호 366)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRHSNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #18의 경쇄 (서열번호 367)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRAHNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #19의 경쇄 (서열번호 368)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASHLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #20의 경쇄 (서열번호 369)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNHESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #21의 경쇄 (서열번호 370)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLHSGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #22의 경쇄 (서열번호 371)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #23의 경쇄 (서열번호 372)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCHQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #24의 경쇄 (서열번호 373)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQHSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #25의 경쇄 (서열번호 374)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQHNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #26의 경쇄 (서열번호 375)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSHEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #27의 경쇄 (서열번호 376)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNHEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #28의 경쇄 (서열번호 377)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEHPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #29의 경쇄 (서열번호 378)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #30의 경쇄 (서열번호 379)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPHTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #31의 경쇄 (서열번호 380)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLHFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #1의 중쇄 조합 (서열번호 381)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #2의 중쇄 조합 (서열번호 382)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #3의 중쇄 조합 (서열번호 383)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #4의 중쇄 조합 (서열번호 384)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #5의 중쇄 조합 (서열번호 385)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #6의 중쇄 조합 (서열번호 386)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #7의 중쇄 조합 (서열번호 387)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #8의 중쇄 조합 (서열번호 388)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #9의 중쇄 조합 (서열번호 389)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #10의 중쇄 조합 (서열번호 390)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEHDHWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #11의 중쇄 조합 (서열번호 391)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #12의 중쇄 조합 (서열번호 392)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #13의 중쇄 조합 (서열번호 393)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #14의 중쇄 조합 (서열번호 394)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #15의 중쇄 조합 (서열번호 395)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #16의 중쇄 조합 (서열번호 396)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEHDHWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #17의 중쇄 조합 (서열번호 397)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #18의 중쇄 조합 (서열번호 398)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #19의 중쇄 조합 (서열번호 399)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEHDHWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #20의 중쇄 조합 (서열번호 400)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITTEHDHWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #21의 중쇄 조합 (서열번호 401)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #22의 중쇄 조합 (서열번호 402)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #23의 중쇄 조합 (서열번호 403)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #24의 중쇄 조합 (서열번호 404)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #25의 중쇄 조합 (서열번호 405)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #26의 중쇄 조합 (서열번호 406)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #27의 중쇄 조합 (서열번호 407)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #28의 중쇄 조합 (서열번호 408)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #29의 중쇄 조합 (서열번호 409)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #30의 중쇄 조합 (서열번호 410)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #31의 중쇄 조합 (서열번호 411)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #32의 중쇄 조합 (서열번호 412)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #33의 중쇄 조합 (서열번호 413)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #34의 중쇄 조합 (서열번호 414)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #35의 중쇄 조합 (서열번호 415)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEHDHWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #36의 중쇄 조합 (서열번호 416)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #37의 중쇄 조합 (서열번호 417)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #38의 중쇄 조합 (서열번호 418)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #39의 중쇄 조합 (서열번호 419)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #40의 중쇄 조합 (서열번호 420)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #41의 중쇄 조합 (서열번호 421)
EVQLVESGGGLVQPGGSLRLSCAASGHTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEHDHWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #42의 중쇄 조합 (서열번호 422)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEHDYWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #43의 중쇄 조합 (서열번호 423)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEMDHWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #44의 중쇄 조합 (서열번호 424)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYHPDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEHDHWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #45의 중쇄 조합 (서열번호 425)
EVQLVESGGGLVQPGGSLRLSCAASGFTFSSYDMSWVRQAPGKGLEWVATINSNGVSIYYPDSVKHRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAREEITHEHDHWGQGTLVTVSS
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #1의 경쇄 조합 (서열번호 426)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGHSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #2의 경쇄 조합 (서열번호 427)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #3의 경쇄 조합 (서열번호 428)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #4의 경쇄 조합 (서열번호 429)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #5의 경쇄 조합 (서열번호 430)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #6의 경쇄 조합 (서열번호 431)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #7의 경쇄 조합 (서열번호 432)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #8의 경쇄 조합 (서열번호 433)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSHIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #9의 경쇄 조합 (서열번호 434)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #10의 경쇄 조합 (서열번호 435)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #11의 경쇄 조합 (서열번호 436)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGHSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #12의 경쇄 조합 (서열번호 437)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGHSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #13의 경쇄 조합 (서열번호 438)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGHSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #14의 경쇄 조합 (서열번호 439)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSHIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #15의 경쇄 조합 (서열번호 440)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #16의 경쇄 조합 (서열번호 441)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #17의 경쇄 조합 (서열번호 442)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSHIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #18의 경쇄 조합 (서열번호 443)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #19의 경쇄 조합 (서열번호 444)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #20의 경쇄 조합 (서열번호 445)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSHIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #21의 경쇄 조합 (서열번호 446)
EIVLTQSPATLSLSPGERATLSCRASESHDSHGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #22의 경쇄 조합 (서열번호 447)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGHSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #23의 경쇄 조합 (서열번호 448)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGNSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #24의 경쇄 조합 (서열번호 449)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGNSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #25의 경쇄 조합 (서열번호 450)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #26의 경쇄 조합 (서열번호 451)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSFIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #27의 경쇄 조합 (서열번호 452)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSFIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #28의 경쇄 조합 (서열번호 453)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSHIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #29의 경쇄 조합 (서열번호 454)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYHASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #30의 경쇄 조합 (서열번호 455)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #31의 경쇄 조합 (서열번호 456)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGNSFIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #32의 경쇄 조합 (서열번호 457)
EIVLTQSPATLSLSPGERATLSCRASESHDSHGNSFIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #33의 경쇄 조합 (서열번호 458)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGHSFIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #34의 경쇄 조합 (서열번호 459)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGNSHIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #35의 경쇄 조합 (서열번호 460)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGNSFIHWYQQKPGQAPRLLIYHASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #36의 경쇄 조합 (서열번호 461)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGNSFIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #37의 경쇄 조합 (서열번호 462)
EIVLTQSPATLSLSPGERATLSCRASESHDSHGHSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #38의 경쇄 조합 (서열번호 463)
EIVLTQSPATLSLSPGERATLSCRASESHDSHGNSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #39의 경쇄 조합 (서열번호 464)
EIVLTQSPATLSLSPGERATLSCRASESHDSHGNSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #40의 경쇄 조합 (서열번호 465)
EIVLTQSPATLSLSPGERATLSCRASESHDSHGNSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #41의 경쇄 조합 (서열번호 466)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGHSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #42의 경쇄 조합 (서열번호 467)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGHSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #43의 경쇄 조합 (서열번호 468)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGHSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #44의 경쇄 조합 (서열번호 469)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGNSHIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #45의 경쇄 조합 (서열번호 470)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGNSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #46의 경쇄 조합 (서열번호 471)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGNSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #47의 경쇄 조합 (서열번호 472)
EIVLTQSPATLSLSPGERATLSCRASESHDSHGHSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #48의 경쇄 조합 (서열번호 473)
EIVLTQSPATLSLSPGERATLSCRASESHDSHGHSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #49의 경쇄 조합 (서열번호 474)
EIVLTQSPATLSLSPGERATLSCRASESHDSHGHSFIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #50의 경쇄 조합 (서열번호 475)
EIVLTQSPATLSLSPGERATLSCRASESHDSHGNSHIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #51의 경쇄 조합 (서열번호 476)
EIVLTQSPATLSLSPGERATLSCRASESHDSHGNSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #52의 경쇄 조합 (서열번호 477)
EIVLTQSPATLSLSPGERATLSCRASESHDSHGNSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #53의 경쇄 조합 (서열번호 478)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGHSHIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #54의 경쇄 조합 (서열번호 479)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGHSHIHWYQQKPGQAPRLLIYRASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #55의 경쇄 조합 (서열번호 480)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGHSFIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #56의 경쇄 조합 (서열번호 481)
EIVLTQSPATLSLSPGERATLSCRASESVDSHGNSHIHWYQQKPGQAPRLLIYRASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #57의 경쇄 조합 (서열번호 482)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGHSFIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #58의 경쇄 조합 (서열번호 483)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSHIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #59의 경쇄 조합 (서열번호 484)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSFIHWYQQKPGQAPRLLIYHASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #60의 경쇄 조합 (서열번호 485)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSFIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #61의 경쇄 조합 (서열번호 486)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSHIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #62의 경쇄 조합 (서열번호 487)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSFIHWYQQKPGQAPRLLIYHASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #63의 경쇄 조합 (서열번호 488)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSFIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #64의 경쇄 조합 (서열번호 489)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSHIHWYQQKPGQAPRLLIYHASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #65의 경쇄 조합 (서열번호 490)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSHIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #66의 경쇄 조합 (서열번호 491)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSFIHWYQQKPGQAPRLLIYHASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #67의 경쇄 조합 (서열번호 492)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGHSHIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #68의 경쇄 조합 (서열번호 493)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGHSFIHWYQQKPGQAPRLLIYHASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #69의 경쇄 조합 (서열번호 494)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGHSFIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #70의 경쇄 조합 (서열번호 495)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSHIHWYQQKPGQAPRLLIYHASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #71의 경쇄 조합 (서열번호 496)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSHIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #72의 경쇄 조합 (서열번호 497)
EIVLTQSPATLSLSPGERATLSCRASESHDSYGNSFIHWYQQKPGQAPRLLIYHASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #73의 경쇄 조합 (서열번호 498)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSHIHWYQQKPGQAPRLLIYHASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEPLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #74의 경쇄 조합 (서열번호 499)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSHIHWYQQKPGQAPRLLIYHASNLESGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #75의 경쇄 조합 (서열번호 500)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGHSFIHWYQQKPGQAPRLLIYHASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>hucMET27Gv1.3 IgG 히스티딘 스캐닝 변이체 #76의 경쇄 조합 (서열번호 501)
EIVLTQSPATLSLSPGERATLSCRASESVDSYGNSHIHWYQQKPGQAPRLLIYHASNLEHGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQSNEEHLTFGQGTKVELK
>P3D12 IgG의 중쇄 (서열번호 502)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG의 경쇄 (서열번호 503)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12의 중쇄 CDR1 (서열번호 504)
GYTFTSYWMH
>P3D12의 중쇄 CDR2 (서열번호 505)
YIKPSTDNTEYNQKFKD
>P3D12의 중쇄 CDR3 (서열번호 506)
ARSYGNYPLMDY
>P3D12의 경쇄 CDR1 (서열번호 507)
SASSSVTSNYLY
>P3D12의 경쇄 CDR2 (서열번호 508)
STSNLAS
>P3D12의 경쇄 CDR3 (서열번호 509)
HQWSSYPPT
>P3D12 IgG 히스티딘 스캐닝 변이체 #1의 중쇄 (서열번호 510)
QVQLVQSGAEVKKPGASVKVSCKASHYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #2의 중쇄 (서열번호 511)
QVQLVQSGAEVKKPGASVKVSCKASGHTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #3의 중쇄 (서열번호 512)
QVQLVQSGAEVKKPGASVKVSCKASGYHFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #4의 중쇄 (서열번호 513)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #5의 중쇄 (서열번호 514)
QVQLVQSGAEVKKPGASVKVSCKASGYTFHSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #6의 중쇄 (서열번호 515)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTHYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #7의 중쇄 (서열번호 516)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSHWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #8의 중쇄 (서열번호 517)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #9의 중쇄 (서열번호 518)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWHHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #10의 중쇄 (서열번호 519)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #11의 중쇄 (서열번호 520)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #12의 중쇄 (서열번호 521)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYHKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #13의 중쇄 (서열번호 522)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIHPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #14의 중쇄 (서열번호 523)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKHSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #15의 중쇄 (서열번호 524)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPHTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #16의 중쇄 (서열번호 525)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSHDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #17의 중쇄 (서열번호 526)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTHNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #18의 중쇄 (서열번호 527)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDHTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #19의 중쇄 (서열번호 528)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNHEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #20의 중쇄 (서열번호 529)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #21의 중쇄 (서열번호 530)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEHNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #22의 중쇄 (서열번호 531)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYHQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #23의 중쇄 (서열번호 532)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNHKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #24의 중쇄 (서열번호 533)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQHFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #25의 중쇄 (서열번호 534)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKHKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #26의 중쇄 (서열번호 535)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFHDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #27의 중쇄 (서열번호 536)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKHKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #28의 중쇄 (서열번호 537)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCHRSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #29의 중쇄 (서열번호 538)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCAHSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #30의 중쇄 (서열번호 539)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARHYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #31의 중쇄 (서열번호 540)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSHGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #32의 중쇄 (서열번호 541)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYHNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #33의 중쇄 (서열번호 542)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #34의 중쇄 (서열번호 543)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #35의 중쇄 (서열번호 544)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYHLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #36의 중쇄 (서열번호 545)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPHMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #37의 중쇄 (서열번호 546)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #38의 중쇄 (서열번호 547)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #39의 중쇄 (서열번호 548)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDHWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #1의 경쇄 (서열번호 549)
QIVLTQSPAILSLSPGERATLSCHASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #2의 경쇄 (서열번호 550)
QIVLTQSPAILSLSPGERATLSCSHSSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #3의 경쇄 (서열번호 551)
QIVLTQSPAILSLSPGERATLSCSAHSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #4의 경쇄 (서열번호 552)
QIVLTQSPAILSLSPGERATLSCSASHSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #5의 경쇄 (서열번호 553)
QIVLTQSPAILSLSPGERATLSCSASSHVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #6의 경쇄 (서열번호 554)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #7의 경쇄 (서열번호 555)
QIVLTQSPAILSLSPGERATLSCSASSSVHSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #8의 경쇄 (서열번호 556)
QIVLTQSPAILSLSPGERATLSCSASSSVTHNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #9의 경쇄 (서열번호 557)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #10의 경쇄 (서열번호 558)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNHLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #11의 경쇄 (서열번호 559)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYHYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #12의 경쇄 (서열번호 560)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #13의 경쇄 (서열번호 561)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYHTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #14의 경쇄 (서열번호 562)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSHSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #15의 경쇄 (서열번호 563)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTHNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #16의 경쇄 (서열번호 564)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSHLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #17의 경쇄 (서열번호 565)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNHASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #18의 경쇄 (서열번호 566)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLHSGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #19의 경쇄 (서열번호 567)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLAHGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #20의 경쇄 (서열번호 568)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCAQWSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #21의 경쇄 (서열번호 569)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHHWSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #22의 경쇄 (서열번호 570)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #23의 경쇄 (서열번호 571)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWHSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #24의 경쇄 (서열번호 572)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #25의 경쇄 (서열번호 573)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #26의 경쇄 (서열번호 574)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #27의 경쇄 (서열번호 575)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPHTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #28의 경쇄 (서열번호 576)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #1의 중쇄 조합 (서열번호 577)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #2의 중쇄 조합 (서열번호 578)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #3의 중쇄 조합 (서열번호 579)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #4의 중쇄 조합 (서열번호 580)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #5의 중쇄 조합 (서열번호 581)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #6의 중쇄 조합 (서열번호 582)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #7의 중쇄 조합 (서열번호 583)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #8의 중쇄 조합 (서열번호 584)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #9의 중쇄 조합 (서열번호 585)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #10의 중쇄 조합 (서열번호 586)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #11의 중쇄 조합 (서열번호 587)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGHIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #12의 중쇄 조합 (서열번호 588)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #13의 중쇄 조합 (서열번호 589)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #14의 중쇄 조합 (서열번호 590)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #15의 중쇄 조합 (서열번호 591)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #16의 중쇄 조합 (서열번호 592)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #17의 중쇄 조합 (서열번호 593)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #18의 중쇄 조합 (서열번호 594)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #19의 중쇄 조합 (서열번호 595)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #20의 중쇄 조합 (서열번호 596)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #21의 중쇄 조합 (서열번호 597)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #22의 중쇄 조합 (서열번호 598)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #23의 중쇄 조합 (서열번호 599)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #24의 중쇄 조합 (서열번호 600)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #25의 중쇄 조합 (서열번호 601)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #26의 중쇄 조합 (서열번호 602)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #27의 중쇄 조합 (서열번호 603)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #28의 중쇄 조합 (서열번호 604)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #29의 중쇄 조합 (서열번호 605)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #30의 중쇄 조합 (서열번호 606)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #31의 중쇄 조합 (서열번호 607)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #32의 중쇄 조합 (서열번호 608)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #33의 중쇄 조합 (서열번호 609)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #34의 중쇄 조합 (서열번호 610)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHHPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #35의 중쇄 조합 (서열번호 611)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #36의 중쇄 조합 (서열번호 612)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #37의 중쇄 조합 (서열번호 613)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #38의 중쇄 조합 (서열번호 614)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #39의 중쇄 조합 (서열번호 615)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #40의 중쇄 조합 (서열번호 616)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #41의 중쇄 조합 (서열번호 617)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #42의 중쇄 조합 (서열번호 618)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #43의 중쇄 조합 (서열번호 619)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #44의 중쇄 조합 (서열번호 620)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #45의 중쇄 조합 (서열번호 621)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #46의 중쇄 조합 (서열번호 622)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #47의 중쇄 조합 (서열번호 623)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #48의 중쇄 조합 (서열번호 624)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #49의 중쇄 조합 (서열번호 625)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #50의 중쇄 조합 (서열번호 626)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #51의 중쇄 조합 (서열번호 627)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYHMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #52의 중쇄 조합 (서열번호 628)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #53의 중쇄 조합 (서열번호 629)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #54의 중쇄 조합 (서열번호 630)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #55의 중쇄 조합 (서열번호 631)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #56의 중쇄 조합 (서열번호 632)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #57의 중쇄 조합 (서열번호 633)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMAWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #58의 중쇄 조합 (서열번호 634)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #59의 중쇄 조합 (서열번호 635)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #60의 중쇄 조합 (서열번호 636)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #61의 중쇄 조합 (서열번호 637)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #62의 중쇄 조합 (서열번호 638)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #63의 중쇄 조합 (서열번호 639)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMAWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #64의 중쇄 조합 (서열번호 640)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #65의 중쇄 조합 (서열번호 641)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #66의 중쇄 조합 (서열번호 642)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #67의 중쇄 조합 (서열번호 643)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #68의 중쇄 조합 (서열번호 644)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #69의 중쇄 조합 (서열번호 645)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #70의 중쇄 조합 (서열번호 646)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHHPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #71의 중쇄 조합 (서열번호 647)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #72의 중쇄 조합 (서열번호 648)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHHPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #73의 중쇄 조합 (서열번호 649)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #74의 중쇄 조합 (서열번호 650)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHHPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #75의 중쇄 조합 (서열번호 651)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #76의 중쇄 조합 (서열번호 652)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #77의 중쇄 조합 (서열번호 653)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #78의 중쇄 조합 (서열번호 654)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #79의 중쇄 조합 (서열번호 655)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #80의 중쇄 조합 (서열번호 656)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLHHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #81의 중쇄 조합 (서열번호 657)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYHMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #82의 중쇄 조합 (서열번호 658)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYHMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #83의 중쇄 조합 (서열번호 659)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #84의 중쇄 조합 (서열번호 660)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #85의 중쇄 조합 (서열번호 661)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGHIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #86의 중쇄 조합 (서열번호 662)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #87의 중쇄 조합 (서열번호 663)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #88의 중쇄 조합 (서열번호 664)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #89의 중쇄 조합 (서열번호 665)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #90의 중쇄 조합 (서열번호 666)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYHMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #91의 중쇄 조합 (서열번호 667)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMAWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #92의 중쇄 조합 (서열번호 668)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMAWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #93의 중쇄 조합 (서열번호 669)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #94의 중쇄 조합 (서열번호 670)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #95의 중쇄 조합 (서열번호 671)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGHIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #96의 중쇄 조합 (서열번호 672)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #97의 중쇄 조합 (서열번호 673)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #98의 중쇄 조합 (서열번호 674)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #99의 중쇄 조합 (서열번호 675)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #100의 중쇄 조합 (서열번호 676)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMAWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #101의 중쇄 조합 (서열번호 677)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #102의 중쇄 조합 (서열번호 678)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #103의 중쇄 조합 (서열번호 679)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHHPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #104의 중쇄 조합 (서열번호 680)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #105의 중쇄 조합 (서열번호 681)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #106의 중쇄 조합 (서열번호 682)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHHPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #107의 중쇄 조합 (서열번호 683)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #108의 중쇄 조합 (서열번호 684)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHHPLMDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #109의 중쇄 조합 (서열번호 685)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNHPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #110의 중쇄 조합 (서열번호 686)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHHPLMHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #111의 중쇄 조합 (서열번호 687)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #112의 중쇄 조합 (서열번호 688)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #113의 중쇄 조합 (서열번호 689)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #114의 중쇄 조합 (서열번호 690)
QVQLVQSGAEVKKPGASVKVSCKASGYTHTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #115의 중쇄 조합 (서열번호 691)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #116의 중쇄 조합 (서열번호 692)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #117의 중쇄 조합 (서열번호 693)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGHIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #118의 중쇄 조합 (서열번호 694)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLHDYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #119의 중쇄 조합 (서열번호 695)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTHYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGNYPLHHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #120의 중쇄 조합 (서열번호 696)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVKQAPGQGLDWIGYIKPSTDNTEYNQKFKDKATLTADKSTSTAYMELSSLRSEDTAVYYCARSYGHYPLHHYWGQGTTVTVSS
>P3D12 IgG 히스티딘 스캐닝 변이체 #1의 경쇄 조합 (서열번호 697)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #2의 경쇄 조합 (서열번호 698)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #3의 경쇄 조합 (서열번호 699)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #4의 경쇄 조합 (서열번호 700)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPHTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #5의 경쇄 조합 (서열번호 701)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHHPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #6의 경쇄 조합 (서열번호 702)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYHPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #7의 경쇄 조합 (서열번호 703)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPHTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #8의 경쇄 조합 (서열번호 704)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHHPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #9의 경쇄 조합 (서열번호 705)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPHTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #10의 경쇄 조합 (서열번호 706)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHHTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #11의 경쇄 조합 (서열번호 707)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHHPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #12의 경쇄 조합 (서열번호 708)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYHPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #13의 경쇄 조합 (서열번호 709)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPHTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #14의 경쇄 조합 (서열번호 710)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHHPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #15의 경쇄 조합 (서열번호 711)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPHTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #16의 경쇄 조합 (서열번호 712)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHHTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #17의 경쇄 조합 (서열번호 713)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHHHPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #18의 경쇄 조합 (서열번호 714)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHHPHTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #19의 경쇄 조합 (서열번호 715)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYHHTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #20의 경쇄 조합 (서열번호 716)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHHHTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #21의 경쇄 조합 (서열번호 717)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #22의 경쇄 조합 (서열번호 718)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #23의 경쇄 조합 (서열번호 719)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #24의 경쇄 조합 (서열번호 720)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #25의 경쇄 조합 (서열번호 721)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #26의 경쇄 조합 (서열번호 722)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #27의 경쇄 조합 (서열번호 723)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #28의 경쇄 조합 (서열번호 724)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #29의 경쇄 조합 (서열번호 725)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #30의 경쇄 조합 (서열번호 726)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSHYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #31의 경쇄 조합 (서열번호 727)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSHPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #32의 경쇄 조합 (서열번호 728)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYHPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #33의 경쇄 조합 (서열번호 729)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #34의 경쇄 조합 (서열번호 730)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #35의 경쇄 조합 (서열번호 731)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #36의 경쇄 조합 (서열번호 732)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #37의 경쇄 조합 (서열번호 733)
QIVLTQSPAILSLSPGERATLSCSASSSHTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #38의 경쇄 조합 (서열번호 734)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #39의 경쇄 조합 (서열번호 735)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #40의 경쇄 조합 (서열번호 736)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #41의 경쇄 조합 (서열번호 737)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #42의 경쇄 조합 (서열번호 738)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYPPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #43의 경쇄 조합 (서열번호 739)
QIVLTQSPAILSLSPGERATLSCSASSSHTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #44의 경쇄 조합 (서열번호 740)
QIVLTQSPAILSLSPGERATLSCSASSSHTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #45의 경쇄 조합 (서열번호 741)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYPPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #46의 경쇄 조합 (서열번호 742)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYPPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #47의 경쇄 조합 (서열번호 743)
QIVLTQSPAILSLSPGERATLSCSASSSHTSHYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #48의 경쇄 조합 (서열번호 744)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #49의 경쇄 조합 (서열번호 745)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #50의 경쇄 조합 (서열번호 746)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #51의 경쇄 조합 (서열번호 747)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYPPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #52의 경쇄 조합 (서열번호 748)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYPPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #53의 경쇄 조합 (서열번호 749)
QIVLTQSPAILSLSPGERATLSCSASSSHTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #54의 경쇄 조합 (서열번호 750)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSHYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #55의 경쇄 조합 (서열번호 751)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #56의 경쇄 조합 (서열번호 752)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSHYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #57의 경쇄 조합 (서열번호 753)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #58의 경쇄 조합 (서열번호 754)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSHYPPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #59의 경쇄 조합 (서열번호 755)
QIVLTQSPAILSLSPGERATLSCSASSSHTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #60의 경쇄 조합 (서열번호 756)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSHPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #61의 경쇄 조합 (서열번호 757)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #62의 경쇄 조합 (서열번호 758)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSHPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #63의 경쇄 조합 (서열번호 759)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #64의 경쇄 조합 (서열번호 760)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSHPPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #65의 경쇄 조합 (서열번호 761)
QIVLTQSPAILSLSPGERATLSCSASSSHTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #66의 경쇄 조합 (서열번호 762)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYHPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #67의 경쇄 조합 (서열번호 763)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #68의 경쇄 조합 (서열번호 764)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYHPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #69의 경쇄 조합 (서열번호 765)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #70의 경쇄 조합 (서열번호 766)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYHPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #71의 경쇄 조합 (서열번호 767)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #72의 경쇄 조합 (서열번호 768)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #73의 경쇄 조합 (서열번호 769)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #74의 경쇄 조합 (서열번호 770)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHHPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #75의 경쇄 조합 (서열번호 771)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYHPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #76의 경쇄 조합 (서열번호 772)
QIVLTQSPAILSLSPGERATLSCSASSSHTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHHPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #77의 경쇄 조합 (서열번호 773)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #78의 경쇄 조합 (서열번호 774)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #79의 경쇄 조합 (서열번호 775)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #80의 경쇄 조합 (서열번호 776)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHHPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #81의 경쇄 조합 (서열번호 777)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYHPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #82의 경쇄 조합 (서열번호 778)
QIVLTQSPAILSLSPGERATLSCSASSSVTSHYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHHPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #83의 경쇄 조합 (서열번호 779)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSHYPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #84의 경쇄 조합 (서열번호 780)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSHPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #85의 경쇄 조합 (서열번호 781)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSYHPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #86의 경쇄 조합 (서열번호 782)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSHHPPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #87의 경쇄 조합 (서열번호 783)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSHYHPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #88의 경쇄 조합 (서열번호 784)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQHSSHHPTFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #89의 경쇄 조합 (서열번호 785)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYPPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #90의 경쇄 조합 (서열번호 786)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHPPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #91의 경쇄 조합 (서열번호 787)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLHWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSYHPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #92의 경쇄 조합 (서열번호 788)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHHPPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #93의 경쇄 조합 (서열번호 789)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSHYHPHFGSGTKLEIK
>P3D12 IgG 히스티딘 스캐닝 변이체 #94의 경쇄 조합 (서열번호 790)
QIVLTQSPAILSLSPGERATLSCSASSSVTSNYLYWYQQKPGSSPKLLIYSTSNLASGVPARFSGSGSGTSYTLTISSLEAEDAASYFCHQWSSHHPHFGSGTKLEIK
SEQUENCE LISTING
<110> MYTHIC THERAPEUTICS, INC.
<120> ANTIGEN-BINDING PROTEIN CONSTRUCTS AND USES THEREOF
<130> 45395-0034WO1
<140>
<141>
<150> 62/880,449
<151> 2019-07-30
<160> 790
<170> PatentIn version 3.5
<210> 1
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG"
<400> 1
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 2
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG"
<400> 2
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 3
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<220>
<221> source
<223> /note="Heavy Chain CDR1 of Telisotuzumab"
<400> 3
Gly Tyr Ile Phe Thr Ala Tyr Thr Met His
1 5 10
<210> 4
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<220>
<221> source
<223> /note="Heavy Chain CDR2 of Telisotuzumab"
<400> 4
Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 5
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<220>
<221> source
<223> /note="Heavy Chain CDR3 of Telisotuzumab"
<400> 5
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr
1 5 10
<210> 6
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<220>
<221> source
<223> /note="Light Chain CDR1 of Telisotuzumab"
<400> 6
Lys Ser Ser Glu Ser Val Asp Ser Tyr Ala Asn Ser Phe Leu His
1 5 10 15
<210> 7
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<220>
<221> source
<223> /note="Light Chain CDR2 of Telisotuzumab"
<400> 7
Arg Ala Ser Thr Arg Glu Ser
1 5
<210> 8
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<220>
<221> source
<223> /note="Light Chain CDR3 of Telisotuzumab"
<400> 8
Gln Gln Ser Lys Glu Asp Pro Leu Thr
1 5
<210> 9
<211> 1366
<212> PRT
<213> Homo sapiens
<220>
<221> source
<223> /note="Mature Human MET"
<400> 9
Glu Cys Lys Glu Ala Leu Ala Lys Ser Glu Met Asn Val Asn Met Lys
1 5 10 15
Tyr Gln Leu Pro Asn Phe Thr Ala Glu Thr Pro Ile Gln Asn Val Ile
20 25 30
Leu His Glu His His Ile Phe Leu Gly Ala Thr Asn Tyr Ile Tyr Val
35 40 45
Leu Asn Glu Glu Asp Leu Gln Lys Val Ala Glu Tyr Lys Thr Gly Pro
50 55 60
Val Leu Glu His Pro Asp Cys Phe Pro Cys Gln Asp Cys Ser Ser Lys
65 70 75 80
Ala Asn Leu Ser Gly Gly Val Trp Lys Asp Asn Ile Asn Met Ala Leu
85 90 95
Val Val Asp Thr Tyr Tyr Asp Asp Gln Leu Ile Ser Cys Gly Ser Val
100 105 110
Asn Arg Gly Thr Cys Gln Arg His Val Phe Pro His Asn His Thr Ala
115 120 125
Asp Ile Gln Ser Glu Val His Cys Ile Phe Ser Pro Gln Ile Glu Glu
130 135 140
Pro Ser Gln Cys Pro Asp Cys Val Val Ser Ala Leu Gly Ala Lys Val
145 150 155 160
Leu Ser Ser Val Lys Asp Arg Phe Ile Asn Phe Phe Val Gly Asn Thr
165 170 175
Ile Asn Ser Ser Tyr Phe Pro Asp His Pro Leu His Ser Ile Ser Val
180 185 190
Arg Arg Leu Lys Glu Thr Lys Asp Gly Phe Met Phe Leu Thr Asp Gln
195 200 205
Ser Tyr Ile Asp Val Leu Pro Glu Phe Arg Asp Ser Tyr Pro Ile Lys
210 215 220
Tyr Val His Ala Phe Glu Ser Asn Asn Phe Ile Tyr Phe Leu Thr Val
225 230 235 240
Gln Arg Glu Thr Leu Asp Ala Gln Thr Phe His Thr Arg Ile Ile Arg
245 250 255
Phe Cys Ser Ile Asn Ser Gly Leu His Ser Tyr Met Glu Met Pro Leu
260 265 270
Glu Cys Ile Leu Thr Glu Lys Arg Lys Lys Arg Ser Thr Lys Lys Glu
275 280 285
Val Phe Asn Ile Leu Gln Ala Ala Tyr Val Ser Lys Pro Gly Ala Gln
290 295 300
Leu Ala Arg Gln Ile Gly Ala Ser Leu Asn Asp Asp Ile Leu Phe Gly
305 310 315 320
Val Phe Ala Gln Ser Lys Pro Asp Ser Ala Glu Pro Met Asp Arg Ser
325 330 335
Ala Met Cys Ala Phe Pro Ile Lys Tyr Val Asn Asp Phe Phe Asn Lys
340 345 350
Ile Val Asn Lys Asn Asn Val Arg Cys Leu Gln His Phe Tyr Gly Pro
355 360 365
Asn His Glu His Cys Phe Asn Arg Thr Leu Leu Arg Asn Ser Ser Gly
370 375 380
Cys Glu Ala Arg Arg Asp Glu Tyr Arg Thr Glu Phe Thr Thr Ala Leu
385 390 395 400
Gln Arg Val Asp Leu Phe Met Gly Gln Phe Ser Glu Val Leu Leu Thr
405 410 415
Ser Ile Ser Thr Phe Ile Lys Gly Asp Leu Thr Ile Ala Asn Leu Gly
420 425 430
Thr Ser Glu Gly Arg Phe Met Gln Val Val Val Ser Arg Ser Gly Pro
435 440 445
Ser Thr Pro His Val Asn Phe Leu Leu Asp Ser His Pro Val Ser Pro
450 455 460
Glu Val Ile Val Glu His Thr Leu Asn Gln Asn Gly Tyr Thr Leu Val
465 470 475 480
Ile Thr Gly Lys Lys Ile Thr Lys Ile Pro Leu Asn Gly Leu Gly Cys
485 490 495
Arg His Phe Gln Ser Cys Ser Gln Cys Leu Ser Ala Pro Pro Phe Val
500 505 510
Gln Cys Gly Trp Cys His Asp Lys Cys Val Arg Ser Glu Glu Cys Leu
515 520 525
Ser Gly Thr Trp Thr Gln Gln Ile Cys Leu Pro Ala Ile Tyr Lys Val
530 535 540
Phe Pro Asn Ser Ala Pro Leu Glu Gly Gly Thr Arg Leu Thr Ile Cys
545 550 555 560
Gly Trp Asp Phe Gly Phe Arg Arg Asn Asn Lys Phe Asp Leu Lys Lys
565 570 575
Thr Arg Val Leu Leu Gly Asn Glu Ser Cys Thr Leu Thr Leu Ser Glu
580 585 590
Ser Thr Met Asn Thr Leu Lys Cys Thr Val Gly Pro Ala Met Asn Lys
595 600 605
His Phe Asn Met Ser Ile Ile Ile Ser Asn Gly His Gly Thr Thr Gln
610 615 620
Tyr Ser Thr Phe Ser Tyr Val Asp Pro Val Ile Thr Ser Ile Ser Pro
625 630 635 640
Lys Tyr Gly Pro Met Ala Gly Gly Thr Leu Leu Thr Leu Thr Gly Asn
645 650 655
Tyr Leu Asn Ser Gly Asn Ser Arg His Ile Ser Ile Gly Gly Lys Thr
660 665 670
Cys Thr Leu Lys Ser Val Ser Asn Ser Ile Leu Glu Cys Tyr Thr Pro
675 680 685
Ala Gln Thr Ile Ser Thr Glu Phe Ala Val Lys Leu Lys Ile Asp Leu
690 695 700
Ala Asn Arg Glu Thr Ser Ile Phe Ser Tyr Arg Glu Asp Pro Ile Val
705 710 715 720
Tyr Glu Ile His Pro Thr Lys Ser Phe Ile Ser Gly Gly Ser Thr Ile
725 730 735
Thr Gly Val Gly Lys Asn Leu Asn Ser Val Ser Val Pro Arg Met Val
740 745 750
Ile Asn Val His Glu Ala Gly Arg Asn Phe Thr Val Ala Cys Gln His
755 760 765
Arg Ser Asn Ser Glu Ile Ile Cys Cys Thr Thr Pro Ser Leu Gln Gln
770 775 780
Leu Asn Leu Gln Leu Pro Leu Lys Thr Lys Ala Phe Phe Met Leu Asp
785 790 795 800
Gly Ile Leu Ser Lys Tyr Phe Asp Leu Ile Tyr Val His Asn Pro Val
805 810 815
Phe Lys Pro Phe Glu Lys Pro Val Met Ile Ser Met Gly Asn Glu Asn
820 825 830
Val Leu Glu Ile Lys Gly Asn Asp Ile Asp Pro Glu Ala Val Lys Gly
835 840 845
Glu Val Leu Lys Val Gly Asn Lys Ser Cys Glu Asn Ile His Leu His
850 855 860
Ser Glu Ala Val Leu Cys Thr Val Pro Asn Asp Leu Leu Lys Leu Asn
865 870 875 880
Ser Glu Leu Asn Ile Glu Trp Lys Gln Ala Ile Ser Ser Thr Val Leu
885 890 895
Gly Lys Val Ile Val Gln Pro Asp Gln Asn Phe Thr Gly Leu Ile Ala
900 905 910
Gly Val Val Ser Ile Ser Thr Ala Leu Leu Leu Leu Leu Gly Phe Phe
915 920 925
Leu Trp Leu Lys Lys Arg Lys Gln Ile Lys Asp Leu Gly Ser Glu Leu
930 935 940
Val Arg Tyr Asp Ala Arg Val His Thr Pro His Leu Asp Arg Leu Val
945 950 955 960
Ser Ala Arg Ser Val Ser Pro Thr Thr Glu Met Val Ser Asn Glu Ser
965 970 975
Val Asp Tyr Arg Ala Thr Phe Pro Glu Asp Gln Phe Pro Asn Ser Ser
980 985 990
Gln Asn Gly Ser Cys Arg Gln Val Gln Tyr Pro Leu Thr Asp Met Ser
995 1000 1005
Pro Ile Leu Thr Ser Gly Asp Ser Asp Ile Ser Ser Pro Leu Leu
1010 1015 1020
Gln Asn Thr Val His Ile Asp Leu Ser Ala Leu Asn Pro Glu Leu
1025 1030 1035
Val Gln Ala Val Gln His Val Val Ile Gly Pro Ser Ser Leu Ile
1040 1045 1050
Val His Phe Asn Glu Val Ile Gly Arg Gly His Phe Gly Cys Val
1055 1060 1065
Tyr His Gly Thr Leu Leu Asp Asn Asp Gly Lys Lys Ile His Cys
1070 1075 1080
Ala Val Lys Ser Leu Asn Arg Ile Thr Asp Ile Gly Glu Val Ser
1085 1090 1095
Gln Phe Leu Thr Glu Gly Ile Ile Met Lys Asp Phe Ser His Pro
1100 1105 1110
Asn Val Leu Ser Leu Leu Gly Ile Cys Leu Arg Ser Glu Gly Ser
1115 1120 1125
Pro Leu Val Val Leu Pro Tyr Met Lys His Gly Asp Leu Arg Asn
1130 1135 1140
Phe Ile Arg Asn Glu Thr His Asn Pro Thr Val Lys Asp Leu Ile
1145 1150 1155
Gly Phe Gly Leu Gln Val Ala Lys Gly Met Lys Tyr Leu Ala Ser
1160 1165 1170
Lys Lys Phe Val His Arg Asp Leu Ala Ala Arg Asn Cys Met Leu
1175 1180 1185
Asp Glu Lys Phe Thr Val Lys Val Ala Asp Phe Gly Leu Ala Arg
1190 1195 1200
Asp Met Tyr Asp Lys Glu Tyr Tyr Ser Val His Asn Lys Thr Gly
1205 1210 1215
Ala Lys Leu Pro Val Lys Trp Met Ala Leu Glu Ser Leu Gln Thr
1220 1225 1230
Gln Lys Phe Thr Thr Lys Ser Asp Val Trp Ser Phe Gly Val Leu
1235 1240 1245
Leu Trp Glu Leu Met Thr Arg Gly Ala Pro Pro Tyr Pro Asp Val
1250 1255 1260
Asn Thr Phe Asp Ile Thr Val Tyr Leu Leu Gln Gly Arg Arg Leu
1265 1270 1275
Leu Gln Pro Glu Tyr Cys Pro Asp Pro Leu Tyr Glu Val Met Leu
1280 1285 1290
Lys Cys Trp His Pro Lys Ala Glu Met Arg Pro Ser Phe Ser Glu
1295 1300 1305
Leu Val Ser Arg Ile Ser Ala Ile Phe Ser Thr Phe Ile Gly Glu
1310 1315 1320
His Tyr Val His Val Asn Ala Thr Tyr Val Asn Val Lys Cys Val
1325 1330 1335
Ala Pro Tyr Pro Ser Leu Leu Ser Ser Glu Asp Asn Ala Asp Asp
1340 1345 1350
Glu Val Asp Thr Arg Pro Ala Ser Phe Trp Glu Thr Ser
1355 1360 1365
<210> 10
<211> 4098
<212> DNA
<213> Homo sapiens
<220>
<221> source
<223> /note="cDNA Encoding Mature Human MET"
<400> 10
gagtgtaaag aggcactagc aaagtccgag atgaatgtga atatgaagta tcagcttccc 60
aacttcaccg cggaaacacc catccagaat gtcattctac atgagcatca cattttcctt 120
ggtgccacta actacattta tgttttaaat gaggaagacc ttcagaaggt tgctgagtac 180
aagactgggc ctgtgctgga acacccagat tgtttcccat gtcaggactg cagcagcaaa 240
gccaatttat caggaggtgt ttggaaagat aacatcaaca tggctctagt tgtcgacacc 300
tactatgatg atcaactcat tagctgtggc agcgtcaaca gagggacctg ccagcgacat 360
gtctttcccc acaatcatac tgctgacata cagtcggagg ttcactgcat attctcccca 420
cagatagaag agcccagcca gtgtcctgac tgtgtggtga gcgccctggg agccaaagtc 480
ctttcatctg taaaggaccg gttcatcaac ttctttgtag gcaataccat aaattcttct 540
tatttcccag atcatccatt gcattcgata tcagtgagaa ggctaaagga aacgaaagat 600
ggttttatgt ttttgacgga ccagtcctac attgatgttt tacctgagtt cagagattct 660
taccccatta agtatgtcca tgcctttgaa agcaacaatt ttatttactt cttgacggtc 720
caaagggaaa ctctagatgc tcagactttt cacacaagaa taatcaggtt ctgttccata 780
aactctggat tgcattccta catggaaatg cctctggagt gtattctcac agaaaagaga 840
aaaaagagat ccacaaagaa ggaagtgttt aatatacttc aggctgcgta tgtcagcaag 900
cctggggccc agcttgctag acaaatagga gccagcctga atgatgacat tcttttcggg 960
gtgttcgcac aaagcaagcc agattctgcc gaaccaatgg atcgatctgc catgtgtgca 1020
ttccctatca aatatgtcaa cgacttcttc aacaagatcg tcaacaaaaa caatgtgaga 1080
tgtctccagc atttttacgg acccaatcat gagcactgct ttaataggac acttctgaga 1140
aattcatcag gctgtgaagc gcgccgtgat gaatatcgaa cagagtttac cacagctttg 1200
cagcgcgttg acttattcat gggtcaattc agcgaagtcc tcttaacatc tatatccacc 1260
ttcattaaag gagacctcac catagctaat cttgggacat cagagggtcg cttcatgcag 1320
gttgtggttt ctcgatcagg accatcaacc cctcatgtga attttctcct ggactcccat 1380
ccagtgtctc cagaagtgat tgtggagcat acattaaacc aaaatggcta cacactggtt 1440
atcactggga agaagatcac gaagatccca ttgaatggct tgggctgcag acatttccag 1500
tcctgcagtc aatgcctctc tgccccaccc tttgttcagt gtggctggtg ccacgacaaa 1560
tgtgtgcgat cggaggaatg cctgagcggg acatggactc aacagatctg tctgcctgca 1620
atctacaagg ttttcccaaa tagtgcaccc cttgaaggag ggacaaggct gaccatatgt 1680
ggctgggact ttggatttcg gaggaataat aaatttgatt taaagaaaac tagagttctc 1740
cttggaaatg agagctgcac cttgacttta agtgagagca cgatgaatac attgaaatgc 1800
acagttggtc ctgccatgaa taagcatttc aatatgtcca taattatttc aaatggccac 1860
gggacaacac aatacagtac attctcctat gtggatcctg taataacaag tatttcgccg 1920
aaatacggtc ctatggctgg tggcacttta cttactttaa ctggaaatta cctaaacagt 1980
gggaattcta gacacatttc aattggtgga aaaacatgta ctttaaaaag tgtgtcaaac 2040
agtattcttg aatgttatac cccagcccaa accatttcaa ctgagtttgc tgttaaattg 2100
aaaattgact tagccaaccg agagacaagc atcttcagtt accgtgaaga tcccattgtc 2160
tatgaaattc atccaaccaa atcttttatt agtggtggga gcacaataac aggtgttggg 2220
aaaaacctga attcagttag tgtcccgaga atggtcataa atgtgcatga agcaggaagg 2280
aactttacag tggcatgtca acatcgctct aattcagaga taatctgttg taccactcct 2340
tccctgcaac agctgaatct gcaactcccc ctgaaaacca aagccttttt catgttagat 2400
gggatccttt ccaaatactt tgatctcatt tatgtacata atcctgtgtt taagcctttt 2460
gaaaagccag tgatgatctc aatgggcaat gaaaatgtac tggaaattaa gggaaatgat 2520
attgaccctg aagcagttaa aggtgaagtg ttaaaagttg gaaataagag ctgtgagaat 2580
atacacttac attctgaagc cgttttatgc acggtcccca atgacctgct gaaattgaac 2640
agcgagctaa atatagagtg gaagcaagca atttcttcaa ccgtccttgg aaaagtaata 2700
gttcaaccag atcagaattt cacaggattg attgctggtg ttgtctcaat atcaacagca 2760
ctgttattac tacttgggtt tttcctgtgg ctgaaaaaga gaaagcaaat taaagatctg 2820
ggcagtgaat tagttcgcta cgatgcaaga gtacacactc ctcatttgga taggcttgta 2880
agtgcccgaa gtgtaagccc aactacagaa atggtttcaa atgaatctgt agactaccga 2940
gctacttttc cagaagatca gtttcctaat tcatctcaga acggttcatg ccgacaagtg 3000
cagtatcctc tgacagacat gtcccccatc ctaactagtg gggactctga tatatccagt 3060
ccattactgc aaaatactgt ccacattgac ctcagtgctc taaatccaga gctggtccag 3120
gcagtgcagc atgtagtgat tgggcccagt agcctgattg tgcatttcaa tgaagtcata 3180
ggaagagggc attttggttg tgtatatcat gggactttgt tggacaatga tggcaagaaa 3240
attcactgtg ctgtgaaatc cttgaacaga atcactgaca taggagaagt ttcccaattt 3300
ctgaccgagg gaatcatcat gaaagatttt agtcatccca atgtcctctc gctcctggga 3360
atctgcctgc gaagtgaagg gtctccgctg gtggtcctac catacatgaa acatggagat 3420
cttcgaaatt tcattcgaaa tgagactcat aatccaactg taaaagatct tattggcttt 3480
ggtcttcaag tagccaaagg catgaaatat cttgcaagca aaaagtttgt ccacagagac 3540
ttggctgcaa gaaactgtat gctggatgaa aaattcacag tcaaggttgc tgattttggt 3600
cttgccagag acatgtatga taaagaatac tatagtgtac acaacaaaac aggtgcaaag 3660
ctgccagtga agtggatggc tttggaaagt ctgcaaactc aaaagtttac caccaagtca 3720
gatgtgtggt cctttggcgt gctcctctgg gagctgatga caagaggagc cccaccttat 3780
cctgacgtaa acacctttga tataactgtt tacttgttgc aagggagaag actcctacaa 3840
cccgaatact gcccagaccc cttatatgaa gtaatgctaa aatgctggca ccctaaagcc 3900
gaaatgcgcc catccttttc tgaactggtg tcccggatat cagcgatctt ctctactttc 3960
attggggagc actatgtcca tgtgaacgct acttatgtga acgtaaaatg tgtcgctccg 4020
tatccttctc tgttgtcatc agaagataac gctgatgatg aggtggacac acgaccagcc 4080
tccttctggg agacatca 4098
<210> 11
<211> 908
<212> PRT
<213> Homo sapiens
<220>
<221> source
<223> /note="Extracellular Domain of MET"
<400> 11
Glu Cys Lys Glu Ala Leu Ala Lys Ser Glu Met Asn Val Asn Met Lys
1 5 10 15
Tyr Gln Leu Pro Asn Phe Thr Ala Glu Thr Pro Ile Gln Asn Val Ile
20 25 30
Leu His Glu His His Ile Phe Leu Gly Ala Thr Asn Tyr Ile Tyr Val
35 40 45
Leu Asn Glu Glu Asp Leu Gln Lys Val Ala Glu Tyr Lys Thr Gly Pro
50 55 60
Val Leu Glu His Pro Asp Cys Phe Pro Cys Gln Asp Cys Ser Ser Lys
65 70 75 80
Ala Asn Leu Ser Gly Gly Val Trp Lys Asp Asn Ile Asn Met Ala Leu
85 90 95
Val Val Asp Thr Tyr Tyr Asp Asp Gln Leu Ile Ser Cys Gly Ser Val
100 105 110
Asn Arg Gly Thr Cys Gln Arg His Val Phe Pro His Asn His Thr Ala
115 120 125
Asp Ile Gln Ser Glu Val His Cys Ile Phe Ser Pro Gln Ile Glu Glu
130 135 140
Pro Ser Gln Cys Pro Asp Cys Val Val Ser Ala Leu Gly Ala Lys Val
145 150 155 160
Leu Ser Ser Val Lys Asp Arg Phe Ile Asn Phe Phe Val Gly Asn Thr
165 170 175
Ile Asn Ser Ser Tyr Phe Pro Asp His Pro Leu His Ser Ile Ser Val
180 185 190
Arg Arg Leu Lys Glu Thr Lys Asp Gly Phe Met Phe Leu Thr Asp Gln
195 200 205
Ser Tyr Ile Asp Val Leu Pro Glu Phe Arg Asp Ser Tyr Pro Ile Lys
210 215 220
Tyr Val His Ala Phe Glu Ser Asn Asn Phe Ile Tyr Phe Leu Thr Val
225 230 235 240
Gln Arg Glu Thr Leu Asp Ala Gln Thr Phe His Thr Arg Ile Ile Arg
245 250 255
Phe Cys Ser Ile Asn Ser Gly Leu His Ser Tyr Met Glu Met Pro Leu
260 265 270
Glu Cys Ile Leu Thr Glu Lys Arg Lys Lys Arg Ser Thr Lys Lys Glu
275 280 285
Val Phe Asn Ile Leu Gln Ala Ala Tyr Val Ser Lys Pro Gly Ala Gln
290 295 300
Leu Ala Arg Gln Ile Gly Ala Ser Leu Asn Asp Asp Ile Leu Phe Gly
305 310 315 320
Val Phe Ala Gln Ser Lys Pro Asp Ser Ala Glu Pro Met Asp Arg Ser
325 330 335
Ala Met Cys Ala Phe Pro Ile Lys Tyr Val Asn Asp Phe Phe Asn Lys
340 345 350
Ile Val Asn Lys Asn Asn Val Arg Cys Leu Gln His Phe Tyr Gly Pro
355 360 365
Asn His Glu His Cys Phe Asn Arg Thr Leu Leu Arg Asn Ser Ser Gly
370 375 380
Cys Glu Ala Arg Arg Asp Glu Tyr Arg Thr Glu Phe Thr Thr Ala Leu
385 390 395 400
Gln Arg Val Asp Leu Phe Met Gly Gln Phe Ser Glu Val Leu Leu Thr
405 410 415
Ser Ile Ser Thr Phe Ile Lys Gly Asp Leu Thr Ile Ala Asn Leu Gly
420 425 430
Thr Ser Glu Gly Arg Phe Met Gln Val Val Val Ser Arg Ser Gly Pro
435 440 445
Ser Thr Pro His Val Asn Phe Leu Leu Asp Ser His Pro Val Ser Pro
450 455 460
Glu Val Ile Val Glu His Thr Leu Asn Gln Asn Gly Tyr Thr Leu Val
465 470 475 480
Ile Thr Gly Lys Lys Ile Thr Lys Ile Pro Leu Asn Gly Leu Gly Cys
485 490 495
Arg His Phe Gln Ser Cys Ser Gln Cys Leu Ser Ala Pro Pro Phe Val
500 505 510
Gln Cys Gly Trp Cys His Asp Lys Cys Val Arg Ser Glu Glu Cys Leu
515 520 525
Ser Gly Thr Trp Thr Gln Gln Ile Cys Leu Pro Ala Ile Tyr Lys Val
530 535 540
Phe Pro Asn Ser Ala Pro Leu Glu Gly Gly Thr Arg Leu Thr Ile Cys
545 550 555 560
Gly Trp Asp Phe Gly Phe Arg Arg Asn Asn Lys Phe Asp Leu Lys Lys
565 570 575
Thr Arg Val Leu Leu Gly Asn Glu Ser Cys Thr Leu Thr Leu Ser Glu
580 585 590
Ser Thr Met Asn Thr Leu Lys Cys Thr Val Gly Pro Ala Met Asn Lys
595 600 605
His Phe Asn Met Ser Ile Ile Ile Ser Asn Gly His Gly Thr Thr Gln
610 615 620
Tyr Ser Thr Phe Ser Tyr Val Asp Pro Val Ile Thr Ser Ile Ser Pro
625 630 635 640
Lys Tyr Gly Pro Met Ala Gly Gly Thr Leu Leu Thr Leu Thr Gly Asn
645 650 655
Tyr Leu Asn Ser Gly Asn Ser Arg His Ile Ser Ile Gly Gly Lys Thr
660 665 670
Cys Thr Leu Lys Ser Val Ser Asn Ser Ile Leu Glu Cys Tyr Thr Pro
675 680 685
Ala Gln Thr Ile Ser Thr Glu Phe Ala Val Lys Leu Lys Ile Asp Leu
690 695 700
Ala Asn Arg Glu Thr Ser Ile Phe Ser Tyr Arg Glu Asp Pro Ile Val
705 710 715 720
Tyr Glu Ile His Pro Thr Lys Ser Phe Ile Ser Gly Gly Ser Thr Ile
725 730 735
Thr Gly Val Gly Lys Asn Leu Asn Ser Val Ser Val Pro Arg Met Val
740 745 750
Ile Asn Val His Glu Ala Gly Arg Asn Phe Thr Val Ala Cys Gln His
755 760 765
Arg Ser Asn Ser Glu Ile Ile Cys Cys Thr Thr Pro Ser Leu Gln Gln
770 775 780
Leu Asn Leu Gln Leu Pro Leu Lys Thr Lys Ala Phe Phe Met Leu Asp
785 790 795 800
Gly Ile Leu Ser Lys Tyr Phe Asp Leu Ile Tyr Val His Asn Pro Val
805 810 815
Phe Lys Pro Phe Glu Lys Pro Val Met Ile Ser Met Gly Asn Glu Asn
820 825 830
Val Leu Glu Ile Lys Gly Asn Asp Ile Asp Pro Glu Ala Val Lys Gly
835 840 845
Glu Val Leu Lys Val Gly Asn Lys Ser Cys Glu Asn Ile His Leu His
850 855 860
Ser Glu Ala Val Leu Cys Thr Val Pro Asn Asp Leu Leu Lys Leu Asn
865 870 875 880
Ser Glu Leu Asn Ile Glu Trp Lys Gln Ala Ile Ser Ser Thr Val Leu
885 890 895
Gly Lys Val Ile Val Gln Pro Asp Gln Asn Phe Thr
900 905
<210> 12
<211> 2724
<212> DNA
<213> Homo sapiens
<220>
<221> source
<223> /note="cDNA Encoding Extracellular Domain of MET"
<400> 12
gagtgtaaag aggcactagc aaagtccgag atgaatgtga atatgaagta tcagcttccc 60
aacttcaccg cggaaacacc catccagaat gtcattctac atgagcatca cattttcctt 120
ggtgccacta actacattta tgttttaaat gaggaagacc ttcagaaggt tgctgagtac 180
aagactgggc ctgtgctgga acacccagat tgtttcccat gtcaggactg cagcagcaaa 240
gccaatttat caggaggtgt ttggaaagat aacatcaaca tggctctagt tgtcgacacc 300
tactatgatg atcaactcat tagctgtggc agcgtcaaca gagggacctg ccagcgacat 360
gtctttcccc acaatcatac tgctgacata cagtcggagg ttcactgcat attctcccca 420
cagatagaag agcccagcca gtgtcctgac tgtgtggtga gcgccctggg agccaaagtc 480
ctttcatctg taaaggaccg gttcatcaac ttctttgtag gcaataccat aaattcttct 540
tatttcccag atcatccatt gcattcgata tcagtgagaa ggctaaagga aacgaaagat 600
ggttttatgt ttttgacgga ccagtcctac attgatgttt tacctgagtt cagagattct 660
taccccatta agtatgtcca tgcctttgaa agcaacaatt ttatttactt cttgacggtc 720
caaagggaaa ctctagatgc tcagactttt cacacaagaa taatcaggtt ctgttccata 780
aactctggat tgcattccta catggaaatg cctctggagt gtattctcac agaaaagaga 840
aaaaagagat ccacaaagaa ggaagtgttt aatatacttc aggctgcgta tgtcagcaag 900
cctggggccc agcttgctag acaaatagga gccagcctga atgatgacat tcttttcggg 960
gtgttcgcac aaagcaagcc agattctgcc gaaccaatgg atcgatctgc catgtgtgca 1020
ttccctatca aatatgtcaa cgacttcttc aacaagatcg tcaacaaaaa caatgtgaga 1080
tgtctccagc atttttacgg acccaatcat gagcactgct ttaataggac acttctgaga 1140
aattcatcag gctgtgaagc gcgccgtgat gaatatcgaa cagagtttac cacagctttg 1200
cagcgcgttg acttattcat gggtcaattc agcgaagtcc tcttaacatc tatatccacc 1260
ttcattaaag gagacctcac catagctaat cttgggacat cagagggtcg cttcatgcag 1320
gttgtggttt ctcgatcagg accatcaacc cctcatgtga attttctcct ggactcccat 1380
ccagtgtctc cagaagtgat tgtggagcat acattaaacc aaaatggcta cacactggtt 1440
atcactggga agaagatcac gaagatccca ttgaatggct tgggctgcag acatttccag 1500
tcctgcagtc aatgcctctc tgccccaccc tttgttcagt gtggctggtg ccacgacaaa 1560
tgtgtgcgat cggaggaatg cctgagcggg acatggactc aacagatctg tctgcctgca 1620
atctacaagg ttttcccaaa tagtgcaccc cttgaaggag ggacaaggct gaccatatgt 1680
ggctgggact ttggatttcg gaggaataat aaatttgatt taaagaaaac tagagttctc 1740
cttggaaatg agagctgcac cttgacttta agtgagagca cgatgaatac attgaaatgc 1800
acagttggtc ctgccatgaa taagcatttc aatatgtcca taattatttc aaatggccac 1860
gggacaacac aatacagtac attctcctat gtggatcctg taataacaag tatttcgccg 1920
aaatacggtc ctatggctgg tggcacttta cttactttaa ctggaaatta cctaaacagt 1980
gggaattcta gacacatttc aattggtgga aaaacatgta ctttaaaaag tgtgtcaaac 2040
agtattcttg aatgttatac cccagcccaa accatttcaa ctgagtttgc tgttaaattg 2100
aaaattgact tagccaaccg agagacaagc atcttcagtt accgtgaaga tcccattgtc 2160
tatgaaattc atccaaccaa atcttttatt agtggtggga gcacaataac aggtgttggg 2220
aaaaacctga attcagttag tgtcccgaga atggtcataa atgtgcatga agcaggaagg 2280
aactttacag tggcatgtca acatcgctct aattcagaga taatctgttg taccactcct 2340
tccctgcaac agctgaatct gcaactcccc ctgaaaacca aagccttttt catgttagat 2400
gggatccttt ccaaatactt tgatctcatt tatgtacata atcctgtgtt taagcctttt 2460
gaaaagccag tgatgatctc aatgggcaat gaaaatgtac tggaaattaa gggaaatgat 2520
attgaccctg aagcagttaa aggtgaagtg ttaaaagttg gaaataagag ctgtgagaat 2580
atacacttac attctgaagc cgttttatgc acggtcccca atgacctgct gaaattgaac 2640
agcgagctaa atatagagtg gaagcaagca atttcttcaa ccgtccttgg aaaagtaata 2700
gttcaaccag atcagaattt caca 2724
<210> 13
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #1"
<400> 13
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser His Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 14
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #2"
<400> 14
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly His Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 15
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #3"
<400> 15
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr His Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 16
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #4"
<400> 16
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile His Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 17
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #5"
<400> 17
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe His Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 18
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #6"
<400> 18
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr His Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 19
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #7"
<400> 19
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala His
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 20
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #8"
<400> 20
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
His Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 21
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #9"
<400> 21
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr His His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 22
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #10"
<400> 22
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met Ala Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 23
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #11"
<400> 23
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly His Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 24
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #12"
<400> 24
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp His Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 25
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #13"
<400> 25
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile His Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 26
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #14"
<400> 26
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys His Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 27
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #15"
<400> 27
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro His Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 28
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #16"
<400> 28
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn His Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 29
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #17"
<400> 29
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn His Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 30
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #18"
<400> 30
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly His Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 31
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #19"
<400> 31
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu His Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 32
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #20"
<400> 32
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala His Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 33
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #21"
<400> 33
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn His Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 34
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #22"
<400> 34
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr His Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 35
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #23"
<400> 35
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala His Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 36
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #24"
<400> 36
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln His Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 37
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #25"
<400> 37
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys His
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 38
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #26"
<400> 38
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
His Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 39
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #27"
<400> 39
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln His Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 40
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #28"
<400> 40
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
His Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 41
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #29"
<400> 41
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 42
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #30"
<400> 42
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 43
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #31"
<400> 43
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser His Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 44
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #32"
<400> 44
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu His Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 45
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #33"
<400> 45
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile His Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 46
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #34"
<400> 46
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr His Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 47
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #35"
<400> 47
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr His Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 48
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #36"
<400> 48
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu His Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 49
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #37"
<400> 49
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe His Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 50
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Telisotuzumab IgG histidine
scanning variant #38"
<400> 50
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 51
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #1"
<400> 51
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys His Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 52
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #2"
<400> 52
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys His Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 53
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #3"
<400> 53
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser His Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 54
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #4"
<400> 54
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser His Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 55
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #5"
<400> 55
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu His Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 56
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #6"
<400> 56
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser His Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 57
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #7"
<400> 57
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val His Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 58
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #8"
<400> 58
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp His Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 59
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #9"
<400> 59
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser His
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 60
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #10"
<400> 60
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
His Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 61
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #11"
<400> 61
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala His Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 62
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #12"
<400> 62
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn His Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 63
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #13"
<400> 63
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser His Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 64
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #14"
<400> 64
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe His His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 65
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #15"
<400> 65
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 66
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #16"
<400> 66
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr His Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 67
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #17"
<400> 67
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg His Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 68
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #18"
<400> 68
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala His Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 69
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #19"
<400> 69
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser His Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 70
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #20"
<400> 70
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr His Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 71
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #21"
<400> 71
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg His Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 72
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #22"
<400> 72
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu His Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 73
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #23"
<400> 73
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys His Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 74
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #24"
<400> 74
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln His Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 75
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #25"
<400> 75
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln His Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 76
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #26"
<400> 76
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser His
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 77
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #27"
<400> 77
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
His Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 78
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #28"
<400> 78
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu His Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 79
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #29"
<400> 79
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp His Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 80
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #30"
<400> 80
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro His Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 81
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Telisotuzumab IgG histidine
scanning variant #31"
<400> 81
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu His Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 82
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG histidine
scanning variant #1"
<400> 82
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly His Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 83
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #2"
<400> 83
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly His Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr His Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 84
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #3"
<400> 84
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly His Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr Thr Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 85
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #4"
<400> 85
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Glu Ile Thr His Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 86
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #5"
<400> 86
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Glu Ile Thr Thr Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 87
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #6"
<400> 87
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr His Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 88
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #7"
<400> 88
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly His Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Glu Ile Thr His Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 89
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #8"
<400> 89
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly His Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Glu Ile Thr Thr Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 90
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #9"
<400> 90
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly His Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile Thr His Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 91
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #10"
<400> 91
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Glu Ile Thr His Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 92
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #11"
<400> 92
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly His Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
His Arg Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 93
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #12"
<400> 93
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
His Arg His Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 94
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #13"
<400> 94
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
His Arg Ser Glu Ile Thr His Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 95
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #14"
<400> 95
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
His Arg Ser Glu Ile Thr Thr Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 96
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #15"
<400> 96
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly His Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 97
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #16"
<400> 97
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His His Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 98
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #17"
<400> 98
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Ser Glu Ile Thr His Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 99
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #18"
<400> 99
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Ser Glu Ile Thr Thr Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 100
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #19"
<400> 100
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly His Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile His Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 101
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #20"
<400> 101
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Glu Ile His Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 102
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #21"
<400> 102
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile His His Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 103
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #22"
<400> 103
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile His Thr Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 104
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #23"
<400> 104
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly His Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
His Arg Ser Glu Ile Thr Thr Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 105
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #24"
<400> 105
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
His Arg His Glu Ile Thr Thr Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 106
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #25"
<400> 106
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
His Arg Ser Glu Ile Thr His Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 107
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #26"
<400> 107
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly His Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
His Arg His Glu Ile Thr Thr Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 108
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #27"
<400> 108
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly His Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
His Arg Ser Glu Ile Thr His Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 109
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #28"
<400> 109
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly His Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Ser Glu Ile Thr Thr Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 110
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #29"
<400> 110
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His His Glu Ile Thr Thr Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 111
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #30"
<400> 111
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Ser Glu Ile Thr His Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 112
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #31"
<400> 112
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly His Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His His Glu Ile Thr Thr Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 113
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #32"
<400> 113
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly His Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Ser Glu Ile Thr His Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 114
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #33"
<400> 114
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly His Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile His Thr Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 115
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #34"
<400> 115
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Glu Ile His Thr Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 116
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #35"
<400> 116
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile His His Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 117
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #36"
<400> 117
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly His Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Glu Ile His Thr Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 118
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #37"
<400> 118
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly His Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Glu Ile His His Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 119
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #38"
<400> 119
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
His His Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 120
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #39"
<400> 120
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Ser Glu Ile His Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 121
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #40"
<400> 121
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
His Arg Ser Glu Ile His Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 122
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #41"
<400> 122
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
His His Ser Glu Ile His Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 123
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #42"
<400> 123
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly His Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
His His Ser Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 124
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #43"
<400> 124
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
His His His Glu Ile Thr Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 125
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #44"
<400> 125
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
His His Ser Glu Ile Thr His Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 126
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #45"
<400> 126
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
His His Ser Glu Ile Thr Thr Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 127
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #46"
<400> 127
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly His Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
His Arg Ser Glu Ile His Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 128
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #47"
<400> 128
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
His Arg His Glu Ile His Thr Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 129
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #48"
<400> 129
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
His Arg Ser Glu Ile His His Glu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 130
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Telisotuzumab IgG
histidine scanning variant #49"
<400> 130
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Lys Pro Asn Asn Gly Leu Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
His Arg Ser Glu Ile His Thr Glu Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 131
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Telisotuzumab IgG
histidine scanning variant #1"
<400> 131
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala His Ser His Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 132
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Telisotuzumab IgG
histidine scanning variant #2"
<400> 132
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala His Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr His Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 133
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Telisotuzumab IgG
histidine scanning variant #3"
<400> 133
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala His Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu His Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 134
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Telisotuzumab IgG
histidine scanning variant #4"
<400> 134
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser His Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr His Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 135
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Telisotuzumab IgG
histidine scanning variant #5"
<400> 135
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser His Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu His Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 136
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Telisotuzumab IgG
histidine scanning variant #6"
<400> 136
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr His Ala Ser Thr Arg Glu His Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 137
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Telisotuzumab IgG
histidine scanning variant #7"
<400> 137
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala His Ser His Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr His Ala Ser Thr Arg Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 138
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Telisotuzumab IgG
histidine scanning variant #8"
<400> 138
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala His Ser His Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg Glu His Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 139
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Telisotuzumab IgG
histidine scanning variant #9"
<400> 139
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala His Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr His Ala Ser Thr Arg Glu His Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 140
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Telisotuzumab IgG
histidine scanning variant #10"
<400> 140
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser His Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr His Ala Ser Thr Arg Glu His Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 141
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Telisotuzumab IgG
histidine scanning variant #11"
<400> 141
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala His Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg His Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 142
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Telisotuzumab IgG
histidine scanning variant #12"
<400> 142
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser His Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg His Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 143
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Telisotuzumab IgG
histidine scanning variant #13"
<400> 143
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe His His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg His Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 144
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Telisotuzumab IgG
histidine scanning variant #14"
<400> 144
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr His Ala Ser Thr Arg His Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 145
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Telisotuzumab IgG
histidine scanning variant #15"
<400> 145
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Glu Ser Val Asp Ser Tyr
20 25 30
Ala Asn Ser Phe Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Arg Ala Ser Thr Arg His His Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 146
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG"
<400> 146
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 147
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG"
<400> 147
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 148
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<220>
<221> source
<223> /note="Heavy Chain CDR1 of Emibetuzumab"
<400> 148
Gly Tyr Thr Phe Thr Asp Tyr Tyr Met His
1 5 10
<210> 149
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<220>
<221> source
<223> /note="Heavy Chain CDR2 of Emibetuzumab"
<400> 149
Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe Glu
1 5 10 15
Gly
<210> 150
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<220>
<221> source
<223> /note="Heavy Chain CDR3 of Emibetuzumab"
<400> 150
Ala Arg Ala Asn Trp Leu Asp Tyr
1 5
<210> 151
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<220>
<221> source
<223> /note="Light Chain CDR1 of Emibetuzumab"
<400> 151
Ser Val Ser Ser Ser Val Ser Ser Ile Tyr Leu His
1 5 10
<210> 152
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<220>
<221> source
<223> /note="Light Chain CDR2 of Emibetuzumab"
<400> 152
Ser Thr Ser Asn Leu Ala Ser
1 5
<210> 153
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<220>
<221> source
<223> /note="Light Chain CDR3 of Emibetuzumab"
<400> 153
Gln Val Tyr Ser Gly Tyr Pro Leu Thr
1 5
<210> 154
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #1"
<400> 154
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser His Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 155
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #2"
<400> 155
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly His Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 156
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #3"
<400> 156
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr His Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 157
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #4"
<400> 157
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 158
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #5"
<400> 158
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe His Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 159
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #6"
<400> 159
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 160
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #7"
<400> 160
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp His
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 161
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #8"
<400> 161
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
His Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 162
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #9"
<400> 162
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr His His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 163
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #10"
<400> 163
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met Ala Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 164
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #11"
<400> 164
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly His Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 165
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #12"
<400> 165
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg His Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 166
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #13"
<400> 166
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 167
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #14"
<400> 167
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn His Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 168
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #15"
<400> 168
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro His Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 169
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #16"
<400> 169
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn His Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 170
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #17"
<400> 170
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg His Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 171
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #18"
<400> 171
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 172
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #19"
<400> 172
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly His Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 173
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #20"
<400> 173
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr His Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 174
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #21"
<400> 174
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr His Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 175
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #22"
<400> 175
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr His Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 176
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #23"
<400> 176
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn His Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 177
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #24"
<400> 177
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln His Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 178
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #25"
<400> 178
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys His
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 179
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #26"
<400> 179
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
His Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 180
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #27"
<400> 180
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu His Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 181
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #28"
<400> 181
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
His Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 182
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #29"
<400> 182
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 183
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #30"
<400> 183
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 184
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #31"
<400> 184
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 185
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #32"
<400> 185
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn His Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 186
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #33"
<400> 186
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp His Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 187
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #34"
<400> 187
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu His Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 188
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of Emibetuzumab IgG histidine
scanning variant #35"
<400> 188
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp His Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 189
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #1"
<400> 189
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys His Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 190
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #2"
<400> 190
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser His Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 191
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #3"
<400> 191
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val His Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 192
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #4"
<400> 192
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser His Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 193
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #5"
<400> 193
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser His Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 194
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #6"
<400> 194
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser His Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 195
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #7"
<400> 195
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val His Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 196
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #8"
<400> 196
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser His Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 197
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #9"
<400> 197
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser His
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 198
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #10"
<400> 198
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
His Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 199
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #11"
<400> 199
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr His His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 200
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #12"
<400> 200
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 201
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #13"
<400> 201
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr His Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 202
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #14"
<400> 202
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser His Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 203
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #15"
<400> 203
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr His Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 204
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #16"
<400> 204
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser His Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 205
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #17"
<400> 205
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn His Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 206
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #18"
<400> 206
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu His Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 207
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #19"
<400> 207
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala His Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 208
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #20"
<400> 208
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys His Val Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 209
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #21"
<400> 209
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln His Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 210
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #22"
<400> 210
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val His Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 211
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #23"
<400> 211
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr His Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 212
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #24"
<400> 212
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser His Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 213
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #25"
<400> 213
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly His Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 214
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #26"
<400> 214
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly Tyr His
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 215
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #27"
<400> 215
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly Tyr Pro
85 90 95
His Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 216
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of Emibetuzumab IgG histidine
scanning variant #28"
<400> 216
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly Tyr Pro
85 90 95
Leu His Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 217
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #1"
<400> 217
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 218
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #2"
<400> 218
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro His Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 219
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #3"
<400> 219
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 220
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #4"
<400> 220
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 221
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #5"
<400> 221
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His Pro His Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 222
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #6"
<400> 222
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His Pro Asn Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 223
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #7"
<400> 223
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 224
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #8"
<400> 224
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro His Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 225
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #9"
<400> 225
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro His Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 226
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #10"
<400> 226
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 227
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #11"
<400> 227
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His Pro His Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 228
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #12"
<400> 228
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His Pro Asn Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 229
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #13"
<400> 229
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 230
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #14"
<400> 230
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro His Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 231
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #15"
<400> 231
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro His Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 232
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #16"
<400> 232
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 233
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #17"
<400> 233
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His Pro His Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 234
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #18"
<400> 234
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His Pro His Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 235
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #19"
<400> 235
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His Pro Asn Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 236
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #20"
<400> 236
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro His Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 237
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #21"
<400> 237
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn His Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 238
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #22"
<400> 238
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His His Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 239
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #23"
<400> 239
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 240
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #24"
<400> 240
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 241
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #25"
<400> 241
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn His Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 242
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #26"
<400> 242
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn His Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 243
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #27"
<400> 243
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His His Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 244
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #28"
<400> 244
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His His Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 245
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #29"
<400> 245
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn His His Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 246
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #30"
<400> 246
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn His Asn Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 247
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #31"
<400> 247
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn His Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 248
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #32"
<400> 248
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His His His Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 249
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #33"
<400> 249
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His His Asn Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 250
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #34"
<400> 250
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His His Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 251
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #35"
<400> 251
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn His His Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 252
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #36"
<400> 252
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn His His Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 253
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #37"
<400> 253
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn His Asn Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 254
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #38"
<400> 254
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His His His Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 255
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #39"
<400> 255
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His His Asn Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 256
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #40"
<400> 256
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His His Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 257
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #41"
<400> 257
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn His His Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 258
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #42"
<400> 258
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn His His Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 259
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #43"
<400> 259
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn His Asn Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 260
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #44"
<400> 260
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His His His Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 261
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #45"
<400> 261
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His His His Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 262
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #46"
<400> 262
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His His Asn Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 263
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #47"
<400> 263
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn His His Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 264
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #48"
<400> 264
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 265
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #49"
<400> 265
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro His Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 266
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #50"
<400> 266
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 267
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #51"
<400> 267
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 268
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #52"
<400> 268
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His Pro His Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 269
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #53"
<400> 269
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His Pro Asn Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 270
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #54"
<400> 270
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 271
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #55"
<400> 271
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro His Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 272
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #56"
<400> 272
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro His Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 273
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #57"
<400> 273
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 274
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #58"
<400> 274
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His Pro His Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 275
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #59"
<400> 275
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His Pro Asn Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 276
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #60"
<400> 276
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His Pro Asn Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 277
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #61"
<400> 277
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro His Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 278
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #62"
<400> 278
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro His Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 279
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #63"
<400> 279
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro Asn Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 280
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #64"
<400> 280
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His Pro His Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Asn Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 281
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #65"
<400> 281
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His Pro His Arg Arg Gly Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 282
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #66"
<400> 282
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val His Pro Asn Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 283
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of Emibetuzumab IgG
histidine scanning variant #67"
<400> 283
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Val Asn Pro His Arg Arg His Thr Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His His Trp Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 284
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Emibetuzumab IgG
histidine scanning variant #1"
<400> 284
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
His Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr His Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 285
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Emibetuzumab IgG
histidine scanning variant #2"
<400> 285
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
His Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln His Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 286
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Emibetuzumab IgG
histidine scanning variant #3"
<400> 286
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
His Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val His Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 287
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Emibetuzumab IgG
histidine scanning variant #4"
<400> 287
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
His Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly His Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 288
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Emibetuzumab IgG
histidine scanning variant #5"
<400> 288
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr His Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln His Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 289
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Emibetuzumab IgG
histidine scanning variant #6"
<400> 289
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr His Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val His Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 290
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Emibetuzumab IgG
histidine scanning variant #7"
<400> 290
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr His Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly His Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 291
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Emibetuzumab IgG
histidine scanning variant #8"
<400> 291
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln His His Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 292
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Emibetuzumab IgG
histidine scanning variant #9"
<400> 292
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln His Tyr Ser Gly His Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 293
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Emibetuzumab IgG
histidine scanning variant #10"
<400> 293
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val His Ser Gly His Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 294
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Emibetuzumab IgG
histidine scanning variant #11"
<400> 294
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
His Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr His Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln His Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 295
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Emibetuzumab IgG
histidine scanning variant #12"
<400> 295
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
His Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr His Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val His Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 296
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Emibetuzumab IgG
histidine scanning variant #13"
<400> 296
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
His Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr His Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val Tyr Ser Gly His Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 297
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Emibetuzumab IgG
histidine scanning variant #14"
<400> 297
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
His Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln His His Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 298
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Emibetuzumab IgG
histidine scanning variant #15"
<400> 298
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
His Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln His Tyr Ser Gly His Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 299
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Emibetuzumab IgG
histidine scanning variant #16"
<400> 299
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
His Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val His Ser Gly His Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 300
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Emibetuzumab IgG
histidine scanning variant #17"
<400> 300
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr His Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln His His Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 301
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Emibetuzumab IgG
histidine scanning variant #18"
<400> 301
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr His Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln His Tyr Ser Gly His Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 302
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Emibetuzumab IgG
histidine scanning variant #19"
<400> 302
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr His Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Val His Ser Gly His Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 303
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of Emibetuzumab IgG
histidine scanning variant #20"
<400> 303
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Val Ser Ser Ile
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln His His Ser Gly His Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 304
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG"
<400> 304
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 305
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG"
<400> 305
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 306
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<220>
<221> source
<223> /note="Heavy Chain CDR1 of hucMET27Gv1.3"
<400> 306
Gly Phe Thr Phe Ser Ser Tyr Asp Met Ser
1 5 10
<210> 307
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<220>
<221> source
<223> /note="Heavy Chain CDR2 of hucMET27Gv1.3"
<400> 307
Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val Lys
1 5 10 15
Gly
<210> 308
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<220>
<221> source
<223> /note="Heavy Chain CDR3 of hucMET27Gv1.3"
<400> 308
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr
1 5 10
<210> 309
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<220>
<221> source
<223> /note="Light Chain CDR1 of hucMET27Gv1.3"
<400> 309
Arg Ala Ser Glu Ser Val Asp Ser Tyr Gly Asn Ser Phe Ile His
1 5 10 15
<210> 310
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<220>
<221> source
<223> /note="Light Chain CDR2 of hucMET27Gv1.3"
<400> 310
Arg Ala Ser Asn Leu Glu Ser
1 5
<210> 311
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<220>
<221> source
<223> /note="Light Chain CDR3 of hucMET27Gv1.3"
<400> 311
Gln Gln Ser Asn Glu Glu Pro Leu Thr
1 5
<210> 312
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #1"
<400> 312
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser His Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 313
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #2"
<400> 313
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly His Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 314
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #3"
<400> 314
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe His Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 315
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #4"
<400> 315
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr His Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 316
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #5"
<400> 316
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe His Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 317
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #6"
<400> 317
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser His Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 318
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #7"
<400> 318
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser His
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 319
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #8"
<400> 319
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
His Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 320
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #9"
<400> 320
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp His Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 321
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #10"
<400> 321
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 322
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #11"
<400> 322
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala His Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 323
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #12"
<400> 323
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr His Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 324
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #13"
<400> 324
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile His Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 325
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #14"
<400> 325
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn His Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 326
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #15"
<400> 326
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser His Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 327
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #16"
<400> 327
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn His Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 328
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #17"
<400> 328
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly His Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 329
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #18"
<400> 329
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val His Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 330
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #19"
<400> 330
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser His Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 331
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #20"
<400> 331
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile His Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 332
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #21"
<400> 332
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr His Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 333
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #22"
<400> 333
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr His Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 334
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #23"
<400> 334
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro His Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 335
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #24"
<400> 335
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp His Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 336
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #25"
<400> 336
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser His
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 337
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #26"
<400> 337
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
His Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 338
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #27"
<400> 338
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys His Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 339
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #28"
<400> 339
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
His Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 340
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #29"
<400> 340
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 341
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #30"
<400> 341
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 342
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #31"
<400> 342
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu His Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 343
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #32"
<400> 343
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu His Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 344
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #33"
<400> 344
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile His Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 345
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #34"
<400> 345
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 346
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #35"
<400> 346
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr His Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 347
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #36"
<400> 347
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu His Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 348
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #37"
<400> 348
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met His Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 349
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of hucMET27Gv1.3 IgG histidine
scanning variant #38"
<400> 349
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 350
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #1"
<400> 350
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys His Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 351
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #2"
<400> 351
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg His Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 352
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #3"
<400> 352
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala His Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 353
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #4"
<400> 353
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser His Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 354
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #5"
<400> 354
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu His Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 355
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #6"
<400> 355
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 356
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #7"
<400> 356
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val His Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 357
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #8"
<400> 357
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp His Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 358
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #9"
<400> 358
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser His
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 359
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #10"
<400> 359
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
His Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 360
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #11"
<400> 360
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly His Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 361
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #12"
<400> 361
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn His Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 362
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #13"
<400> 362
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 363
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #14"
<400> 363
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe His His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 364
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #15"
<400> 364
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 365
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #16"
<400> 365
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 366
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #17"
<400> 366
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg His Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 367
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #18"
<400> 367
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala His Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 368
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #19"
<400> 368
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser His Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 369
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #20"
<400> 369
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn His Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 370
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #21"
<400> 370
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu His Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 371
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #22"
<400> 371
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 372
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #23"
<400> 372
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys His Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 373
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #24"
<400> 373
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 374
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #25"
<400> 374
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln His Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 375
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #26"
<400> 375
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser His
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 376
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #27"
<400> 376
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
His Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 377
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #28"
<400> 377
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu His Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 378
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #29"
<400> 378
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 379
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #30"
<400> 379
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro His Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 380
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of hucMET27Gv1.3 IgG histidine
scanning variant #31"
<400> 380
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu His Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 381
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #1"
<400> 381
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly His Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr His Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 382
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #2"
<400> 382
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly His Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys His Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 383
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #3"
<400> 383
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly His Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu His Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 384
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #4"
<400> 384
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly His Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 385
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #5"
<400> 385
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr His Pro Asp Ser Val
50 55 60
Lys His Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 386
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #6"
<400> 386
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr His Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu His Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 387
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #7"
<400> 387
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr His Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 388
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #8"
<400> 388
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys His Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu His Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 389
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #9"
<400> 389
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys His Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 390
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #10"
<400> 390
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu His Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 391
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #11"
<400> 391
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly His Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr His Pro Asp Ser Val
50 55 60
Lys His Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 392
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #12"
<400> 392
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly His Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr His Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu His Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 393
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #13"
<400> 393
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly His Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr His Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 394
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #14"
<400> 394
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly His Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys His Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu His Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 395
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #15"
<400> 395
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly His Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys His Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 396
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #16"
<400> 396
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly His Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu His Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 397
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #17"
<400> 397
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr His Pro Asp Ser Val
50 55 60
Lys His Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu His Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 398
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #18"
<400> 398
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr His Pro Asp Ser Val
50 55 60
Lys His Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu Met Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 399
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #19"
<400> 399
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr His Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu His Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 400
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #20"
<400> 400
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys His Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr Thr Glu His Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 401
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #21"
<400> 401
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly His Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 402
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #22"
<400> 402
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu His Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 403
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #23"
<400> 403
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu Met Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 404
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #24"
<400> 404
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr His Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 405
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #25"
<400> 405
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 406
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #26"
<400> 406
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly His Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr His Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 407
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #27"
<400> 407
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly His Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys His Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 408
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #28"
<400> 408
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly His Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu His Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 409
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #29"
<400> 409
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly His Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu Met Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 410
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #30"
<400> 410
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr His Pro Asp Ser Val
50 55 60
Lys His Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 411
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #31"
<400> 411
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr His Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu His Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 412
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #32"
<400> 412
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr His Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu Met Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 413
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #33"
<400> 413
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys His Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu His Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 414
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #34"
<400> 414
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys His Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu Met Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 415
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #35"
<400> 415
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu His Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 416
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #36"
<400> 416
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly His Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr His Pro Asp Ser Val
50 55 60
Lys His Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 417
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #37"
<400> 417
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly His Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr His Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu His Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 418
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #38"
<400> 418
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly His Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr His Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu Met Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 419
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #39"
<400> 419
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly His Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys His Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu His Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 420
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #40"
<400> 420
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly His Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys His Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu Met Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 421
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #41"
<400> 421
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly His Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu His Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 422
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #42"
<400> 422
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr His Pro Asp Ser Val
50 55 60
Lys His Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu His Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 423
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #43"
<400> 423
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr His Pro Asp Ser Val
50 55 60
Lys His Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu Met Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 424
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #44"
<400> 424
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr His Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu His Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 425
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #45"
<400> 425
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Asp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Asn Ser Asn Gly Val Ser Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys His Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Glu Ile Thr His Glu His Asp His Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 426
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #1"
<400> 426
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser Tyr
20 25 30
Gly His Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 427
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #2"
<400> 427
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser Tyr
20 25 30
Gly Asn Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 428
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #3"
<400> 428
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 429
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #4"
<400> 429
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 430
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #5"
<400> 430
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly His Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 431
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #6"
<400> 431
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly His Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 432
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #7"
<400> 432
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly His Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 433
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #8"
<400> 433
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 434
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #9"
<400> 434
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 435
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #10"
<400> 435
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 436
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #11"
<400> 436
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser Tyr
20 25 30
Gly His Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 437
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #12"
<400> 437
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser Tyr
20 25 30
Gly His Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 438
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #13"
<400> 438
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser Tyr
20 25 30
Gly His Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 439
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #14"
<400> 439
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser Tyr
20 25 30
Gly Asn Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 440
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #15"
<400> 440
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser Tyr
20 25 30
Gly Asn Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 441
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #16"
<400> 441
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 442
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #17"
<400> 442
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly His Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 443
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #18"
<400> 443
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly His Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 444
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #19"
<400> 444
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly His Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 445
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #20"
<400> 445
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 446
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #21"
<400> 446
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser His
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 447
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #22"
<400> 447
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser His
20 25 30
Gly His Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 448
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #23"
<400> 448
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser His
20 25 30
Gly Asn Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 449
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #24"
<400> 449
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser His
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 450
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #25"
<400> 450
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser His
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 451
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #26"
<400> 451
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 452
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #27"
<400> 452
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly His Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 453
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #28"
<400> 453
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 454
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #29"
<400> 454
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 455
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #30"
<400> 455
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 456
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #31"
<400> 456
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser His
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 457
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #32"
<400> 457
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser His
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 458
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #33"
<400> 458
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser His
20 25 30
Gly His Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 459
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #34"
<400> 459
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser His
20 25 30
Gly Asn Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 460
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #35"
<400> 460
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser His
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 461
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #36"
<400> 461
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser His
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 462
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #37"
<400> 462
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser His
20 25 30
Gly His Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 463
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #38"
<400> 463
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser His
20 25 30
Gly Asn Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 464
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #39"
<400> 464
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser His
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 465
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #40"
<400> 465
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser His
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 466
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #41"
<400> 466
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser His
20 25 30
Gly His Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 467
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #42"
<400> 467
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser His
20 25 30
Gly His Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 468
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #43"
<400> 468
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser His
20 25 30
Gly His Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 469
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #44"
<400> 469
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser His
20 25 30
Gly Asn Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 470
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #45"
<400> 470
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser His
20 25 30
Gly Asn Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 471
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #46"
<400> 471
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser His
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 472
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #47"
<400> 472
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser His
20 25 30
Gly His Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 473
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #48"
<400> 473
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser His
20 25 30
Gly His Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 474
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #49"
<400> 474
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser His
20 25 30
Gly His Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 475
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #50"
<400> 475
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser His
20 25 30
Gly Asn Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 476
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #51"
<400> 476
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser His
20 25 30
Gly Asn Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 477
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #52"
<400> 477
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser His
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 478
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #53"
<400> 478
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser His
20 25 30
Gly His Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 479
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #54"
<400> 479
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser His
20 25 30
Gly His Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 480
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #55"
<400> 480
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser His
20 25 30
Gly His Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 481
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #56"
<400> 481
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser His
20 25 30
Gly Asn Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Arg Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 482
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #57"
<400> 482
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser Tyr
20 25 30
Gly His Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 483
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #58"
<400> 483
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser Tyr
20 25 30
Gly Asn Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 484
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #59"
<400> 484
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 485
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #60"
<400> 485
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 486
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #61"
<400> 486
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly His Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 487
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #62"
<400> 487
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly His Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 488
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #63"
<400> 488
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly His Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 489
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #64"
<400> 489
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 490
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #65"
<400> 490
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 491
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #66"
<400> 491
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 492
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #67"
<400> 492
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser Tyr
20 25 30
Gly His Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 493
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #68"
<400> 493
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser Tyr
20 25 30
Gly His Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 494
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #69"
<400> 494
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser Tyr
20 25 30
Gly His Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 495
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #70"
<400> 495
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser Tyr
20 25 30
Gly Asn Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 496
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #71"
<400> 496
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser Tyr
20 25 30
Gly Asn Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 497
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #72"
<400> 497
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser His Asp Ser Tyr
20 25 30
Gly Asn Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 498
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #73"
<400> 498
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly His Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 499
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #74"
<400> 499
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly His Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 500
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #75"
<400> 500
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly His Ser Phe Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 501
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of hucMET27Gv1.3 IgG
histidine scanning variant #76"
<400> 501
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ser Val Asp Ser Tyr
20 25 30
Gly Asn Ser His Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr His Ala Ser Asn Leu Glu His Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Glu His Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Leu Lys
100 105 110
<210> 502
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG"
<400> 502
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 503
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG"
<400> 503
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 504
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<220>
<221> source
<223> /note="Heavy Chain CDR1 of P3D12"
<400> 504
Gly Tyr Thr Phe Thr Ser Tyr Trp Met His
1 5 10
<210> 505
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<220>
<221> source
<223> /note="Heavy Chain CDR2 of P3D12"
<400> 505
Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe Lys
1 5 10 15
Asp
<210> 506
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<220>
<221> source
<223> /note="Heavy Chain CDR3 of P3D12"
<400> 506
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr
1 5 10
<210> 507
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<220>
<221> source
<223> /note="Light Chain CDR1 of P3D12"
<400> 507
Ser Ala Ser Ser Ser Val Thr Ser Asn Tyr Leu Tyr
1 5 10
<210> 508
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<220>
<221> source
<223> /note="Light Chain CDR2 of P3D12"
<400> 508
Ser Thr Ser Asn Leu Ala Ser
1 5
<210> 509
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
peptide"
<220>
<221> source
<223> /note="Light Chain CDR3 of P3D12"
<400> 509
His Gln Trp Ser Ser Tyr Pro Pro Thr
1 5
<210> 510
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #1"
<400> 510
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser His Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 511
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #2"
<400> 511
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly His Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 512
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #3"
<400> 512
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr His Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 513
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #4"
<400> 513
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 514
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #5"
<400> 514
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe His Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 515
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #6"
<400> 515
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 516
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #7"
<400> 516
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser His
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 517
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #8"
<400> 517
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 518
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #9"
<400> 518
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp His His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 519
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #10"
<400> 519
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 520
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #11"
<400> 520
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 521
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #12"
<400> 521
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr His Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 522
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #13"
<400> 522
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile His Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 523
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #14"
<400> 523
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys His Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 524
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #15"
<400> 524
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro His Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 525
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #16"
<400> 525
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser His Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 526
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #17"
<400> 526
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr His Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 527
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #18"
<400> 527
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp His Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 528
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #19"
<400> 528
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn His Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 529
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #20"
<400> 529
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 530
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #21"
<400> 530
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu His Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 531
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #22"
<400> 531
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr His Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 532
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #23"
<400> 532
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn His Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 533
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #24"
<400> 533
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln His Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 534
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #25"
<400> 534
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys His
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 535
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #26"
<400> 535
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
His Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 536
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #27"
<400> 536
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys His Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 537
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #28"
<400> 537
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
His Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 538
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #29"
<400> 538
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 539
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #30"
<400> 539
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 540
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #31"
<400> 540
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser His Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 541
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #32"
<400> 541
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr His Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 542
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #33"
<400> 542
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 543
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #34"
<400> 543
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 544
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #35"
<400> 544
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr His Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 545
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #36"
<400> 545
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro His Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 546
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #37"
<400> 546
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 547
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #38"
<400> 547
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 548
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain of P3D12 IgG histidine
scanning variant #39"
<400> 548
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp His Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 549
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #1"
<400> 549
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys His Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 550
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #2"
<400> 550
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser His Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 551
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #3"
<400> 551
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala His Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 552
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #4"
<400> 552
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser His Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 553
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #5"
<400> 553
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser His Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 554
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #6"
<400> 554
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 555
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #7"
<400> 555
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val His Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 556
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #8"
<400> 556
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr His Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 557
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #9"
<400> 557
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser His
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 558
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #10"
<400> 558
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
His Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 559
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #11"
<400> 559
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr His Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 560
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #12"
<400> 560
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 561
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #13"
<400> 561
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr His Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 562
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #14"
<400> 562
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser His Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 563
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #15"
<400> 563
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr His Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 564
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #16"
<400> 564
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser His Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 565
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #17"
<400> 565
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn His Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 566
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #18"
<400> 566
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu His Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 567
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #19"
<400> 567
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala His Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 568
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #20"
<400> 568
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys Ala Gln Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 569
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #21"
<400> 569
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His His Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 570
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #22"
<400> 570
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 571
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #23"
<400> 571
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp His Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 572
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #24"
<400> 572
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 573
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #25"
<400> 573
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser His Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 574
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #26"
<400> 574
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr His
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 575
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #27"
<400> 575
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
His Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 576
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain of P3D12 IgG histidine
scanning variant #28"
<400> 576
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 577
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #1"
<400> 577
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 578
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #2"
<400> 578
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 579
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #3"
<400> 579
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 580
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #4"
<400> 580
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 581
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #5"
<400> 581
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 582
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #6"
<400> 582
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 583
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #7"
<400> 583
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 584
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #8"
<400> 584
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 585
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #9"
<400> 585
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 586
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #10"
<400> 586
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 587
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #11"
<400> 587
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 588
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #12"
<400> 588
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 589
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #13"
<400> 589
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 590
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #14"
<400> 590
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 591
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #15"
<400> 591
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 592
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #16"
<400> 592
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 593
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #17"
<400> 593
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 594
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #18"
<400> 594
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 595
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #19"
<400> 595
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 596
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #20"
<400> 596
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 597
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #21"
<400> 597
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 598
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #22"
<400> 598
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 599
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #23"
<400> 599
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 600
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #24"
<400> 600
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 601
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #25"
<400> 601
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 602
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #26"
<400> 602
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 603
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #27"
<400> 603
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 604
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #28"
<400> 604
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 605
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #29"
<400> 605
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 606
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #30"
<400> 606
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 607
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #31"
<400> 607
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 608
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #32"
<400> 608
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 609
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #33"
<400> 609
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 610
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #34"
<400> 610
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His His Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 611
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #35"
<400> 611
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 612
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #36"
<400> 612
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 613
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #37"
<400> 613
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 614
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #38"
<400> 614
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 615
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #39"
<400> 615
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 616
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #40"
<400> 616
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu His His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 617
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #41"
<400> 617
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 618
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #42"
<400> 618
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 619
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #43"
<400> 619
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 620
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #44"
<400> 620
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 621
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #45"
<400> 621
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 622
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #46"
<400> 622
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 623
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #47"
<400> 623
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 624
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #48"
<400> 624
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 625
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #49"
<400> 625
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 626
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #50"
<400> 626
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 627
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #51"
<400> 627
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
His Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 628
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #52"
<400> 628
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 629
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #53"
<400> 629
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 630
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #54"
<400> 630
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 631
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #55"
<400> 631
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 632
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #56"
<400> 632
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 633
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #57"
<400> 633
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 634
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #58"
<400> 634
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 635
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #59"
<400> 635
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 636
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #60"
<400> 636
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 637
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #61"
<400> 637
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 638
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #62"
<400> 638
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 639
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #63"
<400> 639
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 640
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #64"
<400> 640
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 641
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #65"
<400> 641
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 642
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #66"
<400> 642
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 643
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #67"
<400> 643
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 644
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #68"
<400> 644
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 645
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #69"
<400> 645
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 646
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #70"
<400> 646
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His His Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 647
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #71"
<400> 647
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 648
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #72"
<400> 648
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His His Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 649
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #73"
<400> 649
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 650
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #74"
<400> 650
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His His Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 651
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #75"
<400> 651
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 652
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #76"
<400> 652
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 653
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #77"
<400> 653
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu His His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 654
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #78"
<400> 654
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 655
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #79"
<400> 655
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu His His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 656
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #80"
<400> 656
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu His His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 657
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #81"
<400> 657
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 658
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #82"
<400> 658
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 659
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #83"
<400> 659
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 660
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #84"
<400> 660
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 661
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #85"
<400> 661
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 662
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #86"
<400> 662
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 663
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #87"
<400> 663
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 664
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #88"
<400> 664
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 665
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #89"
<400> 665
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 666
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #90"
<400> 666
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
His Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 667
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #91"
<400> 667
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 668
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #92"
<400> 668
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 669
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #93"
<400> 669
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 670
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #94"
<400> 670
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 671
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #95"
<400> 671
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 672
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #96"
<400> 672
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 673
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #97"
<400> 673
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 674
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #98"
<400> 674
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 675
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #99"
<400> 675
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 676
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #100"
<400> 676
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Ala Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 677
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #101"
<400> 677
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 678
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #102"
<400> 678
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 679
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #103"
<400> 679
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His His Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 680
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #104"
<400> 680
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 681
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #105"
<400> 681
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 682
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #106"
<400> 682
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His His Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 683
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #107"
<400> 683
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 684
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #108"
<400> 684
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His His Pro Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 685
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #109"
<400> 685
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn His Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 686
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #110"
<400> 686
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His His Pro Leu Met His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 687
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #111"
<400> 687
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 688
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #112"
<400> 688
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 689
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #113"
<400> 689
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 690
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #114"
<400> 690
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr His Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu His His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 691
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #115"
<400> 691
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 692
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #116"
<400> 692
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 693
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #117"
<400> 693
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly His Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu His His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 694
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #118"
<400> 694
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu His Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 695
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #119"
<400> 695
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly Asn Tyr Pro Leu His His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 696
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Heavy Chain Combinations of P3D12 IgG histidine
scanning variant #120"
<400> 696
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Asp Trp Ile
35 40 45
Gly Tyr Ile Lys Pro Ser Thr Asp Asn Thr Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Gly His Tyr Pro Leu His His Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 697
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #1"
<400> 697
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 698
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #2"
<400> 698
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser His Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 699
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #3"
<400> 699
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr His
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 700
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #4"
<400> 700
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
His Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 701
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #5"
<400> 701
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His His Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 702
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #6"
<400> 702
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His Tyr His
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 703
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #7"
<400> 703
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His Tyr Pro
85 90 95
His Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 704
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #8"
<400> 704
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser His His
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 705
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #9"
<400> 705
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser His Pro
85 90 95
His Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 706
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #10"
<400> 706
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr His
85 90 95
His Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 707
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #11"
<400> 707
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His His Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 708
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #12"
<400> 708
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His Tyr His
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 709
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #13"
<400> 709
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His Tyr Pro
85 90 95
His Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 710
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #14"
<400> 710
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser His His
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 711
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #15"
<400> 711
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser His Pro
85 90 95
His Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 712
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #16"
<400> 712
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr His
85 90 95
His Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 713
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #17"
<400> 713
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His His His
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 714
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #18"
<400> 714
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His His Pro
85 90 95
His Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 715
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #19"
<400> 715
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His Tyr His
85 90 95
His Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 716
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #20"
<400> 716
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser His His
85 90 95
His Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 717
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #21"
<400> 717
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 718
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #22"
<400> 718
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 719
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #23"
<400> 719
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser His Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 720
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #24"
<400> 720
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr His
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 721
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #25"
<400> 721
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser His
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 722
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #26"
<400> 722
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser His
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 723
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #27"
<400> 723
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser His
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser His Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 724
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #28"
<400> 724
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser His
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr His
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 725
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #29"
<400> 725
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 726
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #30"
<400> 726
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser His Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 727
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #31"
<400> 727
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser Ser His Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 728
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #32"
<400> 728
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser Ser Tyr His
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 729
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #33"
<400> 729
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 730
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #34"
<400> 730
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His Tyr Pro
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 731
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #35"
<400> 731
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser His Pro
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 732
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #36"
<400> 732
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr His
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 733
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #37"
<400> 733
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser His
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 734
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #38"
<400> 734
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 735
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #39"
<400> 735
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 736
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #40"
<400> 736
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser His
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 737
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #41"
<400> 737
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser His
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 738
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #42"
<400> 738
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser Ser Tyr Pro
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 739
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #43"
<400> 739
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser His
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 740
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #44"
<400> 740
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser His
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 741
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #45"
<400> 741
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser Ser Tyr Pro
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 742
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #46"
<400> 742
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser His
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser Ser Tyr Pro
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 743
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #47"
<400> 743
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser His
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 744
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #48"
<400> 744
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 745
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #49"
<400> 745
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 746
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #50"
<400> 746
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser His
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser Ser Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 747
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #51"
<400> 747
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser His
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr Pro
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 748
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #52"
<400> 748
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser Ser Tyr Pro
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 749
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #53"
<400> 749
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser His
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 750
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #54"
<400> 750
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser His Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 751
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #55"
<400> 751
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His Tyr Pro
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 752
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #56"
<400> 752
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser His
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser His Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 753
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #57"
<400> 753
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser His
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His Tyr Pro
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 754
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #58"
<400> 754
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser His Tyr Pro
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 755
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #59"
<400> 755
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser His
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser His Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 756
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #60"
<400> 756
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser Ser His Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 757
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #61"
<400> 757
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser His Pro
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 758
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #62"
<400> 758
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser His
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser Ser His Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 759
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #63"
<400> 759
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser His
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser His Pro
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 760
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #64"
<400> 760
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser Ser His Pro
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 761
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #65"
<400> 761
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser His
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr His
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 762
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #66"
<400> 762
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser Ser Tyr His
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 763
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #67"
<400> 763
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr His
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 764
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #68"
<400> 764
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser His
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser Ser Tyr His
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 765
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #69"
<400> 765
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser His
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr His
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 766
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #70"
<400> 766
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser Ser Tyr His
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 767
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #71"
<400> 767
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 768
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #72"
<400> 768
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser His Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 769
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #73"
<400> 769
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr His
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 770
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #74"
<400> 770
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His His Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 771
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #75"
<400> 771
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His Tyr His
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 772
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #76"
<400> 772
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser His Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser His His
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 773
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #77"
<400> 773
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser His
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 774
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #78"
<400> 774
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser His
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser His Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 775
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #79"
<400> 775
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser His
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr His
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 776
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #80"
<400> 776
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser His
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His His Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 777
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #81"
<400> 777
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser His
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His Tyr His
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 778
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #82"
<400> 778
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser His
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser His His
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 779
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #83"
<400> 779
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser His Tyr Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 780
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #84"
<400> 780
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser Ser His Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 781
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #85"
<400> 781
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser Ser Tyr His
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 782
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #86"
<400> 782
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser His His Pro
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 783
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #87"
<400> 783
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser His Tyr His
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 784
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #88"
<400> 784
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln His Ser Ser His His
85 90 95
Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 785
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #89"
<400> 785
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His Tyr Pro
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 786
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #90"
<400> 786
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser His Pro
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 787
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #91"
<400> 787
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Tyr His
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 788
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #92"
<400> 788
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His His Pro
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 789
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #93"
<400> 789
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser His Tyr His
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 790
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<221> source
<223> /note="Description of Artificial Sequence: Synthetic
polypeptide"
<220>
<221> source
<223> /note="Light Chain Combinations of P3D12 IgG histidine
scanning variant #94"
<400> 790
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Thr Ser Asn
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser His His
85 90 95
Pro His Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
Claims (45)
- 항원 결합 단백질 작제물(ABPC)의 유효량을 포함하는 약학적 조성물로서, ABPC는
표적 포유류 세포의 표면 상에 제시된 MET 또는 MET의 에피토프에 특이적으로 결합할 수 있는 제1 항원 결합 도메인을 포함하되,
(a) 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인의 해리 속도는 약 7.0 내지 약 8.0의 pH에서의 해리 속도보다 빠르거나;
(b) 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인의 해리 상수(KD)는 약 7.0 내지 약 8.0의 pH에서의 KD보다 큰, 약학적 조성물. - 제1항에 있어서, ABPC는 표적 포유류 세포에 의한 ABPC의 내재화 후에 표적 포유류 세포에서 분해되는, 약학적 조성물.
- 제1항 또는 제2항에 있어서, ABPC는 접합된 독소, 방사성 동위원소, 약물, 또는 소분자를 추가로 포함하는, 약학적 조성물.
- 항원 결합 단백질 작제물(ABPC)의 유효량을 포함하는 약학적 조성물로서, ABPC는
표적 포유류 세포의 표면 상에 제시된 MET 또는 MET의 에피토프에 특이적으로 결합할 수 있는 제1 항원 결합 도메인; 및
접합된 독소, 방사성 동위원소, 약물, 또는 소분자를 포함하되,
(a) 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인의 해리 속도는 약 7.0 내지 약 8.0의 pH에서의 해리 속도보다 빠르거나;
약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인의 해리 상수(KD)는 약 7.0 내지 약 8.0의 pH에서의 KD보다 크고;
(b) 조성물은 다음 중 하나 이상을 가능하게 하는, 약학적 조성물:
동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리의 증가;
동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포 살해의 증가; 및
동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달의 증가. - 제1항 또는 제4항에 있어서, 제1 항원 결합 도메인은 (a) 내지 (d) 중 하나를 포함하는, 약학적 조성물:
(a) 하나 이상의 아미노산이 히스티딘으로 치환된 텔리소투주맙의 중쇄 가변 도메인으로서, 서열번호 1을 포함하는, 텔리소투주맙의 중쇄 가변 도메인; 및/또는
하나 이상의 아미노산이 히스티딘으로 치환된 텔리소투주맙의 경쇄 가변 도메인으로서, 서열번호 2를 포함하는, 텔리소투주맙의 경쇄 가변 도메인;
(b) 하나 이상의 아미노산이 히스티딘으로 치환된 에미베투주맙의 중쇄 가변 도메인으로서, 서열번호 146을 포함하는, 에미베투주맙의 중쇄 가변 도메인; 및/또는
하나 이상의 아미노산이 히스티딘으로 치환된 에미베투주맙의 경쇄 가변 도메인으로서, 서열번호 147을 포함하는, 에미베투주맙의 경쇄 가변 도메인;
(c) 하나 이상의 아미노산이 히스티딘으로 치환된 hucMET27Gv1.3의 중쇄 가변 도메인으로서, 서열번호 304를 포함하는, hucMET27Gv1.3의 중쇄 가변 도메인; 및/또는
하나 이상의 아미노산이 히스티딘으로 치환된 hucMET27Gv1.3의 경쇄 가변 도메인으로서, 서열번호 305를 포함하는, hucMET27Gv1.3의 경쇄 가변 도메인; 및
(d) 하나 이상의 아미노산이 히스티딘으로 치환된 P3D12의 중쇄 가변 도메인으로서, 서열번호 502를 포함하는, P3D12의 중쇄 가변 도메인; 및/또는
하나 이상의 아미노산이 히스티딘으로 치환된 P3D12의 경쇄 가변 도메인으로서, 서열번호 503을 포함하는, P3D12의 경쇄 가변 도메인. - 제1항 또는 제4항에 있어서, 제1 MET 결합 도메인은 (a) 내지 (d) 중 하나를 포함하는, 약학적 조성물:
(a) 서열번호 3~5의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인으로서, 서열번호 3~5 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된, 중쇄 가변 도메인; 및/또는
서열번호 6~8의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인으로서, 서열번호 6~8 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된, 경쇄 가변 도메인;
(b) 서열번호 148~150의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인으로서, 서열번호 148~150 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된, 중쇄 가변 도메인; 및/또는
서열번호 151~153의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인으로서, 서열번호 151~153 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된, 경쇄 가변 도메인;
(c) 서열번호 306~308의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인으로서, 서열번호 306~308 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된, 중쇄 가변 도메인; 및/또는
서열번호 309~311의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인으로서, 서열번호 309~311 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된, 경쇄 가변 도메인; 및
(d) 서열번호 504~506의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인으로서, 서열번호 504~506 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된, 중쇄 가변 도메인; 및/또는
서열번호 507~509의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인으로서, 서열번호 507~509 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된, 경쇄 가변 도메인. - 제1항 및 제4항 내지 제6항 중 어느 한 항에 있어서, 제1항원 결합 도메인은 (a) 내지 (d) 중 하나를 포함하는, 약학적 조성물:
(a) 서열번호 1과 적어도 90% 동일한 중쇄 가변 도메인으로서, 26, 27, 28, 29, 32, 97, 98, 99, 100, 101, 102, 103, 및 107로 이루어진 군으로부터 선택된 서열번호 1 내 하나 이상의 위치에서 히스티딘을 포함하는, 중쇄 가변 도메인; 및/또는
서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 25, 28, 29, 30, 31, 32, 34, 35, 36, 37, 54, 55, 59, 60, 95, 99, 및 101로 이루어진 군으로부터 선택된 서열번호 2 내 하나 이상의 위치에서 히스티딘을 포함하는, 경쇄 가변 도메인;
(b) 서열번호 146과 적어도 90% 동일한 중쇄 가변 도메인으로서, 31, 50, 51, 52, 53, 54, 56, 57, 59, 98, 99, 100, 및 103으로 이루어진 군으로부터 선택된 서열번호 146 내 하나 이상의 위치에서 히스티딘을 포함하는, 중쇄 가변 도메인; 및/또는
서열번호 147과 적어도 90% 동일한 경쇄 가변 도메인으로서, 25, 26, 29, 32, 33, 51, 91, 92, 95, 96, 및 97로 이루어진 군으로부터 선택된 서열번호 147 내 하나 이상의 위치에서 히스티딘을 포함하는, 경쇄 가변 도메인;
(c) 서열번호 304와 적어도 90% 동일한 중쇄 가변 도메인으로서, 27, 34, 35, 50, 51, 52, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 98, 99, 103, 및 105로 이루어진 군으로부터 선택된 서열번호 304 내 하나 이상의 위치에서 히스티딘을 포함하는, 중쇄 가변 도메인; 및/또는
서열번호 305와 적어도 90% 동일한 경쇄 가변 도메인으로서, 26, 30, 31, 34, 36, 54, 56, 57, 60, 93, 95, 99, 및 101로 이루어진 군으로부터 선택된 서열번호 305 내 하나 이상의 위치에서 히스티딘을 포함하는, 경쇄 가변 도메인; 및
(d) 서열번호 502와 적어도 90% 동일한 중쇄 가변 도메인으로서, 27, 29, 30, 32, 33, 34, 50, 51, 52, 53, 57, 59, 98, 100, 101, 102, 103, 106, 및 107로 이루어진 군으로부터 선택된 서열번호 502 내 하나 이상의 위치에서 히스티딘을 포함하는, 중쇄 가변 도메인; 및/또는
서열번호 503과 적어도 90% 동일한 경쇄 가변 도메인으로서, 25, 29, 31, 32, 33, 34, 35, 52, 55, 91, 92, 93, 94, 95, 96. 97, 및 98로 이루어진 군으로부터 선택된 서열번호 503 내 하나 이상의 위치에서 히스티딘을 포함하는, 경쇄 가변 도메인. - 제1항 또는 제4항에 있어서, 제1 항원 결합 도메인은 (a) 내지 (d) 중 하나를 포함하는, 약학적 조성물:
(a) 서열번호 2, 52, 55, 56, 57, 58, 59, 61, 62, 63, 64, 65, 66, 67, 71, 72, 75, 79, 81, 131, 132, 133, 134, 135, 136, 137, 138, 139, 또는 140의 경쇄 가변 도메인; 및/또는
서열번호 1, 13, 14, 15, 16, 19, 40, 41, 42, 43, 44, 45, 46, 50, 82, 83, 84, 86, 87, 89, 90, 94, 또는 111의 중쇄 가변 도메인
(여기서, 제1 항원 결합 도메인은 (i) 서열번호 2의 경쇄 가변 도메인 및 서열번호 1의 중쇄 가변 도메인; (ii) 서열번호 2의 경쇄 가변 도메인 및 서열번호 13~16, 19, 40~46, 50, 82~84, 86, 87, 89, 90, 94, 및 111 중 하나가 아닌 중쇄 가변 도메인; 또는 (iii) 서열번호 1의 중쇄 가변 도메인 및 서열번호 52, 55~59, 61~67, 71, 72, 75, 79, 81, 및 131~140 중 하나가 아닌 경쇄 가변 도메인을 포함하지 않음);
(b) 서열번호 147, 190, 191, 194, 197, 198, 200, 201, 209, 210, 213, 214, 215, 284, 285, 286, 287, 288, 289, 290, 291, 292, 293, 294, 295, 296, 297, 298, 300, 또는 301의 경쇄 가변 도메인 및/또는
서열번호 146, 159, 164, 165, 166, 167, 168, 170, 171, 173, 182, 183, 184, 187, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 230, 231, 232, 233, 234, 235, 또는 236의 중쇄 가변 도메인
(여기서, 제1 항원 결합 도메인은 (i) 서열번호 147의 경쇄 가변 도메인 및 서열번호 146의 중쇄 가변 도메인; (ii) 서열번호 147의 경쇄 가변 도메인 및 서열번호 159, 164~168, 170, 171, 173, 182~184, 187, 217~228, 및 230-236 중 하나가 아닌 중쇄 가변 도메인; 또는 (iii) 서열번호 146의 중쇄 가변 도메인 및 서열번호 190, 191, 194, 197, 198, 200, 201, 209, 210, 213~215, 284~298, 300, 및 301 중 하나가 아닌 경쇄 가변 도메인을 포함하지 않음);
(c) 서열번호 305, 352, 356, 357, 360, 362, 364, 365, 367, 368, 371, 372, 374, 378, 380, 428, 429, 430, 431, 432, 433, 434, 435, 436, 437, 438, 439, 440, 441, 442, 443, 444, 445, 446, 450, 451, 453, 457, 462, 463, 465, 470, 472, 473, 474, 476, 479, 482, 483, 485, 490, 492, 494, 496, 또는 499의 경쇄 가변 도메인 및/또는
서열번호 304, 313, 320, 321, 322, 323, 324, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 340, 341, 345, 347, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 392, 393, 395, 396, 397, 398, 399, 또는 400의 중쇄 가변 도메인
(여기서, 제1 항원 결합 도메인은 (i) 서열번호 305의 경쇄 가변 도메인 및 서열번호 304의 중쇄 가변 도메인; (ii) 서열번호 305의 경쇄 가변 도메인 및 서열번호 313, 320~324, 326~337, 340, 341, 345, 347, 381~390, 392, 393, 및 395~400 중 하나가 아닌 중쇄 가변 도메인; 또는 (iii) 서열번호 304의 중쇄 가변 도메인 및 서열번호 352, 356, 357, 360, 362, 364, 365, 367, 368, 371, 372, 374, 378, 380, 428~446, 450, 451, 453, 457, 462, 463, 465, 470, 472~474, 476, 479, 482, 483, 485, 490, 492, 494, 496, 및 499 중 하나가 아닌 경쇄 가변 도메인을 포함하지 않음); 및
(d) 서열번호 503, 550, 554, 556, 557, 558, 559, 560, 562, 565, 569, 570, 571, 572, 573, 574, 575, 576, 697, 698, 699, 700, 701, 702, 703, 704, 705, 706, 707, 708, 709, 710, 711, 712, 713, 또는 732의 경쇄 가변 도메인 및/또는
서열번호 502, 511, 513, 514, 516, 517, 518, 519, 520, 521, 522, 523, 527, 529, 538, 540, 541, 542, 543, 546, 547, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 606, 621, 659, 또는 676의 중쇄 가변 도메인
(여기서, 제1 항원 결합 도메인은 (i) 서열번호 503의 경쇄 가변 도메인 및 서열번호 502의 중쇄 가변 도메인; 또는 (ii) 서열번호 503의 경쇄 가변 도메인 및 서열번호 511, 513, 514, 516~523, 527, 529, 538, 540~543, 546, 547, 578~597, 606, 621, 659, 및 676 중 하나가 아닌 중쇄 가변 도메인; 또는 (iii) 서열번호 502의 중쇄 가변 도메인 및 서열번호 550, 554, 556~560, 562, 565, 569, 570~576, 697~713, 및 732 중 하나가 아닌 경쇄 가변 도메인을 포함하지 않음). - 제1항 내지 제8항 중 어느 한 항에 있어서, 상기 조성물은 다음을 가능하게 하는, 약학적 조성물:
동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리의 증가; 및/또는
동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포 살해의 증가. - 제1항 내지 제9항 중 어느 한 항에 있어서, 상기 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달을 증가시킬 수 있는, 약학적 조성물.
- 제1항 내지 제10항 중 어느 한 항에 있어서, 상기 조성물은:
동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포의 표면 상에 제시된 MET의 수준을 덜 감소시키거나;
표적 포유류 세포의 표면 상에 제시된 MET 수준을 검출 가능하게 감소시키지 않는, 약학적 조성물. - 제1항 내지 제11항 중 어느 한 항에 있어서, 표적 포유류 세포는 암 세포인, 약학적 조성물.
- 제1항 내지 제12항 중 어느 한 항에 있어서, ABPC는 표적 포유류 세포에 대해 세포독성이거나 세포증식 억제성인, 약학적 조성물.
- 제1항 내지 제13항 중 어느 한 항에 있어서, ABPC는:
비인간 영장류 MET 및 인간 MET와 교차 반응성이거나;
비-인간 영장류 MET, 인간 MET, 및 랫트 MET와 마우스 MET 중 하나 또는 둘 다와 교차 반응성인, 약학적 조성물. - 제1항 내지 제14항 중 어느 한 항에 있어서, ABPC는 단일 폴리펩티드를 포함하는, 약학적 조성물.
- 제15항에 있어서, 항원 결합 도메인은 VH 도메인, VHH 도메인, VNAR 도메인, 및 scFv로 이루어진 군으로부터 선택되는, 약학적 조성물.
- 제1항 내지 제14항 중 어느 한 항에 있어서, ABPC는 2개 이상의 폴리펩티드를 포함하는, 약학적 조성물.
- 제17항에 있어서, ABPC는 항체인, 약학적 조성물.
- 제1항 내지 제18항 중 어느 한 항에 있어서, ABPC의 생체 내 반감기는 대조군 ABPC의 생체 내 반감기와 비교했을 때 감소되는, 약학적 조성물.
- 제1항 내지 제19항 중 어느 한 항에 있어서, ABPC는 제2 항원 결합 도메인을 추가로 포함하는, 약학적 조성물.
- 항원 결합 단백질 작제물(ABPC)로서,
표적 포유류 세포의 표면 상에 제시된 MET 또는 MET의 에피토프에 특이적으로 결합할 수 있는 제1 항원 결합 도메인을 포함하되,
(a) 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인의 해리 속도는 약 7.0 내지 약 8.0의 pH에서의 해리 속도보다 빠르거나;
(b) 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인의 해리 상수(KD)는 약 7.0 내지 약 8.0의 pH에서의 KD보다 큰, ABPC. - 제21항에 있어서, ABPC는 표적 포유류 세포에 의한 ABPC의 내재화 후에 표적 포유류 세포에서 분해되는, ABPC.
- 제21항 또는 제22항에 있어서, ABPC는 접합된 독소, 방사성 동위원소, 약물, 또는 소분자를 추가로 포함하는, ABPC.
- 항원 결합 단백질 작제물(ABPC)로서,
표적 포유류 세포의 표면 상에 제시된 MET 또는 MET의 에피토프에 특이적으로 결합할 수 있는 제1 항원 결합 도메인; 및
접합된 독소, 방사성 동위원소, 약물, 또는 소분자를 포함하되,
(a) 약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인의 해리 속도는 약 7.0 내지 약 8.0의 pH에서의 해리 속도보다 빠르거나;
약 4.0 내지 약 6.5의 pH에서 제1 항원 결합 도메인의 해리 상수(KD)는 약 7.0 내지 약 8.0의 pH에서의 KD보다 크고;
(b) 조성물은 다음 중 하나 이상을 가능하게 하는, ABPC:
동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리의 증가;
동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포 살해의 증가; 및
동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달의 증가. - 제21항 또는 제24항에 있어서, 제1 항원 결합 도메인은 (a) 내지 (d) 중 하나를 포함하는, ABPC:
(a) 하나 이상의 아미노산이 히스티딘으로 치환된 텔리소투주맙의 중쇄 가변 도메인으로서, 서열번호 1을 포함하는, 텔리소투주맙의 중쇄 가변 도메인; 및/또는
하나 이상의 아미노산이 히스티딘으로 치환된 텔리소투주맙의 경쇄 가변 도메인으로서, 서열번호 2를 포함하는, 텔리소투주맙의 경쇄 가변 도메인;
(b) 하나 이상의 아미노산이 히스티딘으로 치환된 에미베투주맙의 중쇄 가변 도메인으로서, 서열번호 146을 포함하는, 에미베투주맙의 중쇄 가변 도메인; 및/또는
하나 이상의 아미노산이 히스티딘으로 치환된 에미베투주맙의 경쇄 가변 도메인으로서, 서열번호 147을 포함하는, 에미베투주맙의 경쇄 가변 도메인;
(c) 하나 이상의 아미노산이 히스티딘으로 치환된 hucMET27Gv1.3의 중쇄 가변 도메인으로서, 서열번호 304를 포함하는, hucMET27Gv1.3의 중쇄 가변 도메인; 및/또는
하나 이상의 아미노산이 히스티딘으로 치환된 hucMET27Gv1.3의 경쇄 가변 도메인으로서, 서열번호 305를 포함하는, hucMET27Gv1.3의 경쇄 가변 도메인; 및
(d) 하나 이상의 아미노산이 히스티딘으로 치환된 P3D12의 중쇄 가변 도메인으로서, 서열번호 502를 포함하는, P3D12의 중쇄 가변 도메인; 및/또는
하나 이상의 아미노산이 히스티딘으로 치환된 P3D12의 경쇄 가변 도메인으로서, 서열번호 503을 포함하는, P3D12의 경쇄 가변 도메인. - 제21항 또는 제24항에 있어서, MET 항원 결합 도메인은 (a) 내지 (d) 중 하나를 포함하는, ABPC:
(a) 서열번호 3~5의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인으로서, 서열번호 3~5 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된, 중쇄 가변 도메인; 및/또는
서열번호 6~8의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인으로서, 서열번호 6~8 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된, 경쇄 가변 도메인;
(b) 서열번호 148~150의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인으로서, 서열번호 148~150 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된, 중쇄 가변 도메인; 및/또는
서열번호 151~153의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인으로서, 서열번호 151~153 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된, 경쇄 가변 도메인;
(c) 서열번호 306~308의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인으로서, 서열번호 306~308 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된, 중쇄 가변 도메인; 및/또는
서열번호 309~311의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인으로서, 서열번호 309~311 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된, 경쇄 가변 도메인; 및
(d) 서열번호 504~506의 CDR1, CDR2, 및 CDR3을 각각 포함하는 중쇄 가변 도메인으로서, 서열번호 504~506 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된, 중쇄 가변 도메인; 및/또는
서열번호 507~509의 CDR1, CDR2, 및 CDR3을 각각 포함하는 경쇄 가변 도메인으로서, 서열번호 507~509 내에서 종합적으로 총 1개 이상의 아미노산 위치가 히스티딘으로 치환된, 경쇄 가변 도메인. - 제21항 또는 제24항 내지 제26항 중 어느 한 항에 있어서, 제1 항원 결합 도메인은 (a) 내지 (d) 중 하나를 포함하는, ABPC:
(a) 서열번호 1과 적어도 90% 동일한 중쇄 가변 도메인으로서, 26, 27, 28, 29, 32, 97, 98, 99, 100, 101, 102, 103, 및 107로 이루어진 군으로부터 선택된 서열번호 1 내 하나 이상의 위치에서 히스티딘을 포함하는, 중쇄 가변 도메인; 및/또는
서열번호 2와 적어도 90% 동일한 경쇄 가변 도메인으로서, 25, 28, 29, 30, 31, 32, 34, 35, 36, 37, 54, 55, 59, 60, 95, 99, 및 101로 이루어진 군으로부터 선택된 서열번호 2 내 하나 이상의 위치에서 히스티딘을 포함하는, 경쇄 가변 도메인;
(b) 서열번호 146과 적어도 90% 동일한 중쇄 가변 도메인으로서, 31, 50, 51, 52, 53, 54, 56, 57, 59, 98, 99, 100, 및 103으로 이루어진 군으로부터 선택된 서열번호 146 내 하나 이상의 위치에서 히스티딘을 포함하는, 중쇄 가변 도메인; 및/또는
서열번호 147과 적어도 90% 동일한 경쇄 가변 도메인으로서, 25, 26, 29, 32, 33, 51, 91, 92, 95, 96, 및 97로 이루어진 군으로부터 선택된 서열번호 147 내 하나 이상의 위치에서 히스티딘을 포함하는, 경쇄 가변 도메인;
(c) 서열번호 304와 적어도 90% 동일한 중쇄 가변 도메인으로서, 27, 34, 35, 50, 51, 52, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 98, 99, 103, 및 105로 이루어진 군으로부터 선택된 서열번호 304 내 하나 이상의 위치에서 히스티딘을 포함하는, 중쇄 가변 도메인; 및/또는
서열번호 305와 적어도 90% 동일한 경쇄 가변 도메인으로서, 26, 30, 31, 34, 36, 54, 56, 57, 60, 93, 95, 99, 및 101로 이루어진 군으로부터 선택된 서열번호 305 내 하나 이상의 위치에서 히스티딘을 포함하는, 경쇄 가변 도메인; 및
(d) 서열번호 502와 적어도 90% 동일한 중쇄 가변 도메인으로서, 27, 29, 30, 32, 33, 34, 50, 51, 52, 53, 57, 59, 98, 100, 101, 102, 103, 106, 및 107로 이루어진 군으로부터 선택된 서열번호 502 내 하나 이상의 위치에서 히스티딘을 포함하는, 중쇄 가변 도메인; 및/또는
서열번호 503과 적어도 90% 동일한 경쇄 가변 도메인으로서, 25, 29, 31, 32, 33, 34, 35, 52, 55, 91, 92, 93, 94, 95, 96. 97, 및 98로 이루어진 군으로부터 선택된 서열번호 503 내 하나 이상의 위치에서 히스티딘을 포함하는, 경쇄 가변 도메인. - 제21항 또는 제24항에 있어서, 제1 항원 결합 도메인은 (a) 내지 (d) 중 하나를 포함하는, ABPC:
(a) 서열번호 2, 52, 55, 56, 57, 58, 59, 61, 62, 63, 64, 65, 66, 67, 71, 72, 75, 79, 81, 131, 132, 133, 134, 135, 136, 137, 138, 139, 또는 140의 경쇄 가변 도메인; 및/또는
서열번호 1, 13, 14, 15, 16, 19, 40, 41, 42, 43, 44, 45, 46, 50, 82, 83, 84, 86, 87, 89, 90, 94, 또는 111의 중쇄 가변 도메인 (여기서, 제1 항원 결합 도메인은 (i) 서열번호 2의 경쇄 가변 도메인 및 서열번호 1의 중쇄 가변 도메인; (ii) 서열번호 2의 경쇄 가변 도메인 및 서열번호 13~16, 19, 40~46, 50, 82~84, 86, 87, 89, 90, 94, 및 111 중 하나가 아닌 중쇄 가변 도메인; 또는 (iii) 서열번호 1의 중쇄 가변 도메인 및 서열번호 52, 55~59, 61~67, 71, 72, 75, 79, 81, 및 131~140 중 하나가 아닌 경쇄 가변 도메인을 포함하지 않음);
(b) 서열번호 147, 190, 191, 194, 197, 198, 200, 201, 209, 210, 213, 214, 215, 284, 285, 286, 287, 288, 289, 290, 291, 292, 293, 294, 295, 296, 297, 298, 300, 또는 301의 경쇄 가변 도메인 및/또는 서열번호 146, 159, 164, 165, 166, 167, 168, 170, 171, 173, 182, 183, 184, 187, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 230, 231, 232, 233, 234, 235, 또는 236의 중쇄 가변 도메인
(여기서, 제1 항원 결합 도메인은 (i) 서열번호 147의 경쇄 가변 도메인 및 서열번호 146의 중쇄 가변 도메인; (ii) 서열번호 147의 경쇄 가변 도메인 및 서열번호 159, 164~168, 170, 171, 173, 182~184, 187, 217~228, 및 230-236 중 하나가 아닌 중쇄 가변 도메인; 또는 (iii) 서열번호 146의 중쇄 가변 도메인 및 서열번호 190, 191, 194, 197, 198, 200, 201, 209, 210, 213~215, 284~298, 300, 및 301 중 하나가 아닌 경쇄 가변 도메인을 포함하지 않음);
(c) 서열번호 305, 352, 356, 357, 360, 362, 364, 365, 367, 368, 371, 372, 374, 378, 380, 428, 429, 430, 431, 432, 433, 434, 435, 436, 437, 438, 439, 440, 441, 442, 443, 444, 445, 446, 450, 451, 453, 457, 462, 463, 465, 470, 472, 473, 474, 476, 479, 482, 483, 485, 490, 492, 494, 496, 또는 499의 경쇄 가변 도메인 및/또는
서열번호 304, 313, 320, 321, 322, 323, 324, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 336, 337, 340, 341, 345, 347, 381, 382, 383, 384, 385, 386, 387, 388, 389, 390, 392, 393, 395, 396, 397, 398, 399, 또는 400의 중쇄 가변 도메인
(여기서, 제1 항원 결합 도메인은 (i) 서열번호 305의 경쇄 가변 도메인 및 서열번호 304의 중쇄 가변 도메인; (ii) 서열번호 305의 경쇄 가변 도메인 및 서열번호 313, 320~324, 326~337, 340, 341, 345, 347, 381~390, 392, 393, 및 395~400 중 하나가 아닌 중쇄 가변 도메인; 또는 (iii) 서열번호 304의 중쇄 가변 도메인 및 서열번호 352, 356, 357, 360, 362, 364, 365, 367, 368, 371, 372, 374, 378, 380, 428~446, 450, 451, 453, 457, 462, 463, 465, 470, 472~474, 476, 479, 482, 483, 485, 490, 492, 494, 496, 및 499 중 하나가 아닌 경쇄 가변 도메인을 포함하지 않음); 및
(d) 서열번호 503, 550, 554, 556, 557, 558, 559, 560, 562, 565, 569, 570, 571, 572, 573, 574, 575, 576, 697, 698, 699, 700, 701, 702, 703, 704, 705, 706, 707, 708, 709, 710, 711, 712, 713, 또는 732의 경쇄 가변 도메인 및/또는
서열번호 502, 511, 513, 514, 516, 517, 518, 519, 520, 521, 522, 523, 527, 529, 538, 540, 541, 542, 543, 546, 547, 578, 579, 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 606, 621, 659, 또는 676의 중쇄 가변 도메인
(여기서, 제1 항원 결합 도메인은 (i) 서열번호 503의 경쇄 가변 도메인 및 서열번호 502의 중쇄 가변 도메인; 또는 (ii) 서열번호 503의 경쇄 가변 도메인 및 서열번호 511, 513, 514, 516~523, 527, 529, 538, 540~543, 546, 547, 578~597, 606, 621, 659, 및 676 중 하나가 아닌 중쇄 가변 도메인; 또는 (iii) 서열번호 502의 중쇄 가변 도메인 및 서열번호 550, 554, 556-560, 562, 565, 569, 570-576, 697-713, 및 732 중 하나가 아닌 경쇄 가변 도메인을 포함하지 않음). - 제21항 내지 제28항 중 어느 한 항에 있어서, ABPC를 포함하는 조성물은 다음을 가능하게 하는, ABPC:
동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 독소 유리의 증가; 및/또는
동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포 살해의 증가. - 제21항 내지 제29항 중 어느 한 항에 있어서, ABPC를 포함하는 조성물은 동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포에서 엔도리소좀 전달을 증가시킬 수 있는, ABPC.
- 제21항 내지 제30항 중 어느 한 항에 있어서, ABPC를 포함하는 조성물은:
동일한 양의 대조군 ABPC를 포함하는 조성물과 비교했을 때 표적 포유류 세포의 표면 상에 제시된 MET의 수준을 덜 감소시키거나;
표적 포유류 세포의 표면 상에 제시된 MET 수준을 검출 가능하게 감소시키지 않는, ABPC. - 제21항 내지 제31항 중 어느 한 항에 있어서, 표적 포유류 세포는 암 세포인, ABPC.
- 제21항 내지 제32항 중 어느 한 항에 있어서, ABPC는 표적 포유류 세포에 대해 세포독성이거나 세포증식 억제성인, ABPC.
- 제21항 내지 제33항 중 어느 한 항에 있어서, ABPC는:
비인간 영장류 MET 및 인간 MET와 교차 반응성이거나;
비-인간 영장류 MET, 인간 MET, 및 랫트 MET와 마우스 MET 중 하나 또는 둘 다와 교차 반응성인, ABPC. - 제21항 내지 제34항 중 어느 한 항에 있어서, ABPC는 단일 폴리펩티드를 포함하는, ABPC.
- 제35항에 있어서, 항원 결합 도메인은 VH 도메인, VHH 도메인, VNAR 도메인, 및 scFv로 이루어진 군으로부터 선택되는, ABPC.
- 제21항 내지 제34항 중 어느 한 항에 있어서, ABPC는 2개 이상의 폴리펩티드를 포함하는, ABPC.
- 제37항에 있어서, ABPC는 항체인, ABPC.
- 제21항 내지 제38항 중 어느 한 항에 있어서, ABPC의 생체 내 반감기는 대조군 ABPC의 생체 내 반감기와 비교했을 때 감소되는, ABPC.
- 제21항 또는 제39항 중 어느 한 항에 있어서, ABPC는 제2 항원 결합 도메인을 추가로 포함하는, ABPC.
- 제1항 내지 제20항 중 어느 한 항의 약학적 조성물 또는 제21항 내지 제40항 중 어느 한 항의 ABPC의 적어도 1회 투여량을 포함하는 키트.
- MET 또는 MET의 에피토프가 표면에 제시된 암 세포의 집단을 갖는 것을 특징으로 하는 암을 치료하는 방법으로서, 상기 방법은:
암 세포의 집단을 갖는 것을 특징으로 하는 암을 갖는 것으로 식별된 대상체에게 제1항 내지 제20항 중 어느 한 항의 약학적 조성물 또는 제21항 내지 제40항 중 어느 한 항의 ABPC의 치료적 유효량을 투여하는 단계를 포함하는, 방법. - 대상체에서 종양 부피를 감소시키는 방법으로서, 종양은 MET 또는 MET의 에피토프가 표면에 제시된 암 세포의 집단을 갖는 것을 특징으로 하고, 상기 방법은:
암 세포의 집단을 갖는 것을 특징으로 하는 암을 갖는 것으로 식별된 대상체에게 제1항 내지 제20항 중 어느 한 항의 약학적 조성물 또는 제21항 내지 제40항 중 어느 한 항의 ABPC의 치료적 유효량을 투여하는 단계를 포함하는, 방법. - 대상체의 암 세포에서 세포 사멸을 유도하는 방법으로서, 암 세포는 그 표면 상에 제시된 MET 또는 MET의 에피토프를 가지고, 상기 방법은:
암 세포의 집단을 갖는 것을 특징으로 하는 암을 갖는 것으로 식별된 대상체에게 제1항 내지 제20항 중 어느 한 항의 약학적 조성물 또는 제21항 내지 제40항 중 어느 한 항의 ABPC의 치료적 유효량을 투여하는 단계를 포함하는, 방법. - 암을 가진 대상체에서 전이의 발생 위험을 감소시키거나 추가 전이의 발생 위험을 감소시키는 방법으로서, 암은 MET 또는 MET의 에피토프가 표면에 제시된 암 세포의 집단을 갖는 것을 특징으로 하고, 상기 방법은:
암 세포의 집단을 갖는 것을 특징으로 하는 암을 갖는 것으로 식별된 대상체에게 제1항 내지 제20항 중 어느 한 항의 약학적 조성물 또는 제21항 내지 제40항 중 어느 한 항의 ABPC의 치료적 유효량을 투여하는 단계를 포함하는, 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201962880449P | 2019-07-30 | 2019-07-30 | |
| US62/880,449 | 2019-07-30 | ||
| PCT/US2020/044263 WO2021022039A1 (en) | 2019-07-30 | 2020-07-30 | Antigen-binding protein constructs and uses thereof |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20220053577A true KR20220053577A (ko) | 2022-04-29 |
Family
ID=72088381
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020227006745A KR20220053577A (ko) | 2019-07-30 | 2020-07-30 | 항원 결합 단백질 작제물 및 이의 용도 |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US20220281984A1 (ko) |
| EP (1) | EP4003534A1 (ko) |
| JP (1) | JP2022543771A (ko) |
| KR (1) | KR20220053577A (ko) |
| CN (1) | CN114746123A (ko) |
| AU (1) | AU2020321368A1 (ko) |
| BR (1) | BR112022001693A2 (ko) |
| CA (1) | CA3149199A1 (ko) |
| IL (1) | IL290233A (ko) |
| MX (1) | MX2022001286A (ko) |
| WO (1) | WO2021022039A1 (ko) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN117529499A (zh) * | 2021-02-03 | 2024-02-06 | 神话治疗股份有限公司 | 抗met抗体和其用途 |
| WO2023225639A1 (en) | 2022-05-19 | 2023-11-23 | Mythic Therapeutics, Inc. | Ptk7-binding proteins with ph-dependent binding and uses thereof |
| WO2024081729A2 (en) | 2022-10-12 | 2024-04-18 | Mythic Therapeutics, Inc. | Lrrc-15-binding protein constructs and uses thereof |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8545839B2 (en) * | 2008-12-02 | 2013-10-01 | Pierre Fabre Medicament | Anti-c-Met antibody |
| WO2011111007A2 (en) * | 2010-03-11 | 2011-09-15 | Rinat Neuroscience Corporation | ANTIBODIES WITH pH DEPENDENT ANTIGEN BINDING |
| TWI667257B (zh) * | 2010-03-30 | 2019-08-01 | 中外製藥股份有限公司 | 促進抗原消失之具有經修飾的FcRn親和力之抗體 |
| CN104302664B (zh) * | 2012-03-14 | 2021-11-26 | 瑞泽恩制药公司 | 多特异性抗原结合分子及其用途 |
-
2020
- 2020-07-30 EP EP20757450.0A patent/EP4003534A1/en active Pending
- 2020-07-30 MX MX2022001286A patent/MX2022001286A/es unknown
- 2020-07-30 CN CN202080066488.1A patent/CN114746123A/zh active Pending
- 2020-07-30 KR KR1020227006745A patent/KR20220053577A/ko active Search and Examination
- 2020-07-30 CA CA3149199A patent/CA3149199A1/en active Pending
- 2020-07-30 JP JP2022506328A patent/JP2022543771A/ja active Pending
- 2020-07-30 BR BR112022001693A patent/BR112022001693A2/pt unknown
- 2020-07-30 WO PCT/US2020/044263 patent/WO2021022039A1/en active Application Filing
- 2020-07-30 AU AU2020321368A patent/AU2020321368A1/en active Pending
- 2020-07-30 US US17/630,824 patent/US20220281984A1/en active Pending
-
2022
- 2022-01-30 IL IL290233A patent/IL290233A/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| MX2022001286A (es) | 2022-07-19 |
| CN114746123A (zh) | 2022-07-12 |
| AU2020321368A1 (en) | 2022-03-10 |
| WO2021022039A1 (en) | 2021-02-04 |
| EP4003534A1 (en) | 2022-06-01 |
| BR112022001693A2 (pt) | 2022-06-07 |
| CA3149199A1 (en) | 2021-02-04 |
| US20220281984A1 (en) | 2022-09-08 |
| JP2022543771A (ja) | 2022-10-14 |
| IL290233A (en) | 2022-03-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20220281984A1 (en) | Antigen-binding protein constructs and uses thereof | |
| US20220313845A1 (en) | Antigen-binding protein constructs and uses thereof | |
| US20220298260A1 (en) | Antigen-binding protein constructs and uses thereof | |
| US20220306751A1 (en) | Antigen-binding protein constructs and uses thereof | |
| AU2022218165B2 (en) | Anti-met antibodies and uses thereof | |
| US20220348679A1 (en) | Antigen-binding protein constructs and uses thereof | |
| US20240141065A1 (en) | Anti-met antibodies and uses thereof | |
| KR20230165792A (ko) | 항원 결합 단백질 작제물 및 항체 및 이들의 용도 | |
| US20220288219A1 (en) | Antigen-binding protein constructs and uses thereof | |
| CA3142886A1 (en) | Antigen-binding protein constructs and uses thereof | |
| WO2023225639A1 (en) | Ptk7-binding proteins with ph-dependent binding and uses thereof | |
| WO2024081729A2 (en) | Lrrc-15-binding protein constructs and uses thereof |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination |