JP7588976B2 - フラグメンテーション指数を用いた心房細動のマッピング - Google Patents
フラグメンテーション指数を用いた心房細動のマッピング Download PDFInfo
- Publication number
- JP7588976B2 JP7588976B2 JP2020121139A JP2020121139A JP7588976B2 JP 7588976 B2 JP7588976 B2 JP 7588976B2 JP 2020121139 A JP2020121139 A JP 2020121139A JP 2020121139 A JP2020121139 A JP 2020121139A JP 7588976 B2 JP7588976 B2 JP 7588976B2
- Authority
- JP
- Japan
- Prior art keywords
- processor
- peaks
- region
- additional
- heart
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/24—Detecting, measuring or recording bioelectric or biomagnetic signals of the body or parts thereof
- A61B5/316—Modalities, i.e. specific diagnostic methods
- A61B5/318—Heart-related electrical modalities, e.g. electrocardiography [ECG]
- A61B5/346—Analysis of electrocardiograms
- A61B5/349—Detecting specific parameters of the electrocardiograph cycle
- A61B5/361—Detecting fibrillation
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/24—Detecting, measuring or recording bioelectric or biomagnetic signals of the body or parts thereof
- A61B5/316—Modalities, i.e. specific diagnostic methods
- A61B5/318—Heart-related electrical modalities, e.g. electrocardiography [ECG]
- A61B5/339—Displays specially adapted therefor
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/24—Detecting, measuring or recording bioelectric or biomagnetic signals of the body or parts thereof
- A61B5/316—Modalities, i.e. specific diagnostic methods
- A61B5/318—Heart-related electrical modalities, e.g. electrocardiography [ECG]
- A61B5/339—Displays specially adapted therefor
- A61B5/343—Potential distribution indication
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/24—Detecting, measuring or recording bioelectric or biomagnetic signals of the body or parts thereof
- A61B5/316—Modalities, i.e. specific diagnostic methods
- A61B5/318—Heart-related electrical modalities, e.g. electrocardiography [ECG]
- A61B5/367—Electrophysiological study [EPS], e.g. electrical activation mapping or electro-anatomical mapping
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Cardiology (AREA)
- Biomedical Technology (AREA)
- Medical Informatics (AREA)
- Biophysics (AREA)
- Pathology (AREA)
- Engineering & Computer Science (AREA)
- Veterinary Medicine (AREA)
- Heart & Thoracic Surgery (AREA)
- Physics & Mathematics (AREA)
- Molecular Biology (AREA)
- Surgery (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Physiology (AREA)
- Measurement And Recording Of Electrical Phenomena And Electrical Characteristics Of The Living Body (AREA)
- Medicines Containing Plant Substances (AREA)
Description
医療処置によっては、心臓組織上の異なるそれぞれの部位に複数の電極を配置することによる電位図(EGM)信号の測定に基づくものもある。心臓処置によっては、医師はEGM信号を使用して、心周期の間、患者の心臓組織を通る電気活性化の波面の伝播を特徴付ける場合がある。EGM信号のそれぞれについて、医師は、信号が取得された部位を波面が通過した場合に相当する電気的活性化点の識別を試みることができる。
図1は本発明の一実施形態による、電位図(EGM)信号22をアノテーション付けするシステム21の描写図である。図1に示すように、電気生理学的(electrophysiological、EP)処置の間、医師27はカテーテル29を挿入し、カテーテル29の遠位端31を患者25の心臓23内の所望の位置に誘導する。
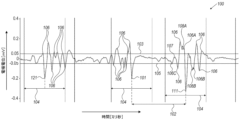
図2は、本発明の一実施形態による、EGM信号100における活性化点の識別を示す概略図である。EGM信号100は、例えば、上記の図1のEGM信号22に置き換えてもよい。
図3は、本発明の一実施形態による、心臓23におけるAFをマッピングする方法を模式的に示すフローチャートである。当該方法は、EGM信号取得ステップ200で開始され、心臓23の組織内の所定の位置に配置された1つ又は2つ以上の電極を有する遠位端31を用いてEGM信号100を取得する。いくつかの実施形態では、プロセッサ28は、AFを示すEGM信号100を受信し、EGM信号100内で、一次ピーク101、111及び121などのアノテーション付けされた活性化信号を識別する。
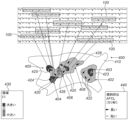
図4は、本発明の一実施形態による、領域フラグメンテーション指数(FI)が複数の局所FIに基づいて計算される、心臓23の領域300の概略描写図である。いくつかの実施形態では、領域300は、領域300のCOG333と呼ばれる、幾何学的重心(COG)から3mm、1mm、2mm、4mm、及び5mmの各距離に位置する点302、304、306、308、及び310を含んでいる。
図5は、本発明の実施形態による、心臓23の領域410のマップ400の概略描写図である。いくつかの実施形態では、マップ400は、プロセッサ28によって識別され、規則的AF活動のある位置としてディスプレイ26によって表示される位置420を含む。
(1) 心臓の心房細動(AF)をマッピングする方法であって、
前記心臓内の所定の位置で取得された、前記AFを示す電位図(EGM)信号を受信することと、
前記EGM信号において、2つ又は3つ以上の一次ピークを識別し、隣接する一次ピーク間のサイクル長(CL)を計算することと、
前記EGM信号において、前記CL内の1つ又は2つ以上の二次ピークを識別することと、
CL当たりの前記二次ピークの数を示す局所フラグメンテーション指数(local fragmentation index)(FI)を計算することと、
前記心臓の少なくとも一部のマップ上で前記局所FIを可視化することと、を含む方法。
(2) 前記心臓が、領域を有し、前記領域が、(i)前記領域の既定の場所から所定の距離に位置する前記所定の位置と、(ii)追加のFIを有し、かつ前記既定の場所から追加の距離に位置する少なくとも追加の位置と、を含み、前記所定の距離及び前記追加の距離に基づいて、また前記局所FI及び前記追加のFIに基づいて、前記領域の領域FIを計算及び可視化することを含む、実施態様1に記載の方法。
(3) 前記既定の場所が、前記領域の幾何学的重心(COG)を含み、前記領域FIを計算及び可視化することが、前記所定の距離及び前記追加の距離に基づいて、少なくとも前記局所FI及び前記追加のFIの加重平均を計算することを含む、実施態様2に記載の方法。
(4) 前記1つ又は2つ以上の二次ピークを識別することが、既定の閾値に基づいて、2つ又は3つ以上の隣接する二次ピークを統合することを含む、実施態様1に記載の方法。
(5) 前記CL内に関心ウィンドウ(WOI)を定義することと、前記WOI内の前記1つ又は2つ以上の二次ピークを識別することと、を含む、実施態様1に記載の方法。
(7) 心臓の心房細動(AF)をマッピングするシステムであって、
(a)前記心臓内の所定の位置で取得された、前記AFを示す電位図(EGM)信号を受信し、(b)前記EGM信号において、2つ又は3つ以上の一次ピークを識別し、隣接する一次ピーク間のサイクル長(CL)を計算し、(c)前記EGM信号において、前記CLの持続時間内の1つ又は2つ以上の二次ピークを識別し、(d)CL当たりの前記二次ピークの数を示す局所フラグメンテーション指数(FI)を計算する、ように構成されたプロセッサと、
前記心臓の少なくとも一部のマップ上に前記局所FIを表示するように構成されたディスプレイと、を含む、システム。
(8) 前記心臓が、領域を有し、前記領域が、(i)前記領域の既定の場所から所定の距離に位置する前記所定の位置と、(ii)追加のFIを有し、かつ前記既定の場所から追加の距離に位置する少なくとも追加の位置と、を含み、前記プロセッサが、前記所定の距離及び前記追加の距離に基づいて、かつ前記局所FI及び前記追加のFIに基づいて、前記領域の領域FIを計算及び可視化するように構成されている、実施態様7に記載のシステム。
(9) 前記既定の場所が、前記領域の幾何学的重心(COG)を含み、前記プロセッサが、前記所定の距離及び前記追加の距離に基づいて少なくとも前記局所FI及び前記追加のFIの加重平均を計算することによって、前記領域FIを計算及び可視化するように構成されている、実施態様8に記載のシステム。
(10) 前記プロセッサが、既定の閾値に基づいて、2つ又は3つ以上の隣接する二次ピークを統合するように構成されている、実施態様7に記載のシステム。
(12) 前記EGM信号が複数のCLを含み、前記プロセッサが、前記複数のCLに基づいて平均CLを計算し、前記平均CL当たりの前記二次ピークの平均数を計算するように構成されている、実施態様7に記載のシステム。
Claims (12)
- プロセッサを備えた、心臓の心房細動(AF)をマッピングするためのシステムの作動方法であって、
前記プロセッサが、前記心臓内の所定の位置で取得された、前記AFを示す電位図(EGM)信号を受信することと、
前記プロセッサが、前記EGM信号において、2つ又は3つ以上の一次ピークを識別し、前記プロセッサが、隣接する一次ピーク間のサイクル長(CL)を計算することと、
前記プロセッサが、前記EGM信号において、前記CL内においてノイズ閾値よりも大きい絶対値を有する1つ又は2つ以上の二次ピークを識別することと、
前記プロセッサが、前記隣接する一次ピーク間のCL当たりの前記二次ピークの平均数を示す局所フラグメンテーション指数(FI)を計算することと、
前記プロセッサが、前記心臓の少なくとも一部のマップ上で前記局所FIを可視化することと、を含むシステムの作動方法。 - 前記心臓が、領域を有し、前記領域が、(i)前記領域の既定の場所から所定の距離に位置する前記所定の位置と、(ii)追加のFIを有し、かつ前記既定の場所から追加の距離に位置する少なくとも追加の位置と、を含み、前記所定の距離及び前記追加の距離に基づいて、また前記局所FI及び前記追加のFIに基づいて、前記プロセッサが、前記領域の領域FIを計算及び可視化することを含む、請求項1に記載のシステムの作動方法。
- 前記既定の場所が、前記領域の幾何学的重心(COG)を含み、前記領域FIを計算及び可視化することが、前記所定の距離及び前記追加の距離に基づいて、前記プロセッサが、少なくとも前記局所FI及び前記追加のFIの加重平均を計算することを含む、請求項2に記載のシステムの作動方法。
- 前記1つ又は2つ以上の二次ピークを識別することが、既定の閾値に基づいて、前記プロセッサが、2つ又は3つ以上の隣接する二次ピークを統合することを含む、請求項1に記載のシステムの作動方法。
- 前記プロセッサが、前記CL内に関心ウィンドウ(WOI)を定義することと、前記プロセッサが、前記WOI内の前記1つ又は2つ以上の二次ピークを識別することと、を含む、請求項1に記載のシステムの作動方法。
- 前記EGM信号が複数のCLを含み、前記局所FIを計算することが、前記プロセッサが、前記複数のCLに基づいて平均CLを計算することと、前記プロセッサが、前記平均CL当たりの前記二次ピークの平均数を計算することと、を含む、請求項1に記載のシステムの作動方法。
- 心臓の心房細動(AF)をマッピングするシステムであって、
(a)前記心臓内の所定の位置で取得された、前記AFを示す電位図(EGM)信号を受信し、(b)前記EGM信号において、2つ又は3つ以上の一次ピークを識別し、隣接する一次ピーク間のサイクル長(CL)を計算し、(c)前記EGM信号において、前記CLの持続時間内においてノイズ閾値よりも大きい絶対値を有する1つ又は2つ以上の二次ピークを識別し、(d)前記隣接する一次ピーク間のCL当たりの前記二次ピークの平均数を示す局所フラグメンテーション指数(FI)を計算する、ように構成されたプロセッサと、
前記心臓の少なくとも一部のマップ上に前記局所FIを表示するように構成されたディスプレイと、を含む、システム。 - 前記心臓が、領域を有し、前記領域が、(i)前記領域の既定の場所から所定の距離に位置する前記所定の位置と、(ii)追加のFIを有し、かつ前記既定の場所から追加の距離に位置する少なくとも追加の位置と、を含み、前記プロセッサが、前記所定の距離及び前記追加の距離に基づいて、かつ前記局所FI及び前記追加のFIに基づいて、前記領域の領域FIを計算及び可視化するように構成されている、請求項7に記載のシステム。
- 前記既定の場所が、前記領域の幾何学的重心(COG)を含み、前記プロセッサが、前記所定の距離及び前記追加の距離に基づいて少なくとも前記局所FI及び前記追加のFIの加重平均を計算することによって、前記領域FIを計算及び可視化するように構成されている、請求項8に記載のシステム。
- 前記プロセッサが前記1つ又は2つ以上の二次ピークを識別することが、既定の閾値に基づいて、2つ又は3つ以上の隣接する二次ピークを統合することを含む、請求項7に記載のシステム。
- 前記プロセッサが、前記CLの持続時間内に関心ウィンドウ(WOI)を定義し、前記WOI内の前記1つ又は2つ以上の二次ピークを識別するように構成されている、請求項7に記載のシステム。
- 前記EGM信号が複数のCLを含み、前記プロセッサが、前記複数のCLに基づいて平均CLを計算し、前記平均CL当たりの前記二次ピークの平均数を計算するように構成されている、請求項7に記載のシステム。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US16/512,588 | 2019-07-16 | ||
| US16/512,588 US10905349B1 (en) | 2019-07-16 | 2019-07-16 | Mapping atrial fibrillation using fragmentation index |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2021016788A JP2021016788A (ja) | 2021-02-15 |
| JP7588976B2 true JP7588976B2 (ja) | 2024-11-25 |
Family
ID=71620241
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020121139A Active JP7588976B2 (ja) | 2019-07-16 | 2020-07-15 | フラグメンテーション指数を用いた心房細動のマッピング |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US10905349B1 (ja) |
| EP (1) | EP3766416B1 (ja) |
| JP (1) | JP7588976B2 (ja) |
| CN (1) | CN112315486B (ja) |
| IL (1) | IL275666B2 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP4473910A1 (en) * | 2023-06-06 | 2024-12-11 | CathVision ApS | Method for analyzing an electrogram |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009537252A (ja) | 2006-05-17 | 2009-10-29 | セント・ジュード・メディカル・エイトリアル・フィブリレーション・ディヴィジョン・インコーポレーテッド | コンプレックス細分化電気的活動図情報をマッピングするシステムおよび方法 |
| US20150080752A1 (en) | 2013-09-16 | 2015-03-19 | Biotronik Se & Co. Kg | Device for automatic mapping of complex fractionated atrial electrogram |
| JP2015171548A (ja) | 2008-11-10 | 2015-10-01 | カーディオインサイト テクノロジーズ インコーポレイテッド | 電気生理学データの視覚化 |
| JP2018149271A (ja) | 2017-01-25 | 2018-09-27 | バイオセンス・ウエブスター・(イスラエル)・リミテッドBiosense Webster (Israel), Ltd. | 心臓内信号を解析し、詳細なマップを提供し、かつ潜在的アブレーションポイントを決定することによって、様々な心臓疾患を排除するための方法及びシステム |
Family Cites Families (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20050288599A1 (en) * | 2004-05-17 | 2005-12-29 | C.R. Bard, Inc. | High density atrial fibrillation cycle length (AFCL) detection and mapping system |
| US7792584B2 (en) * | 2006-04-25 | 2010-09-07 | Medtronic, Inc. | System and method for characterization of atrial wall using digital signal processing |
| US8359092B2 (en) | 2007-11-29 | 2013-01-22 | Biosense Webster, Inc. | Determining locations of ganglia and plexi in the heart using complex fractionated atrial electrogram |
| WO2012047563A1 (en) | 2010-09-27 | 2012-04-12 | Bailin Steven J | Method for determining the location of regions in tissue relevant to electrical propagation |
| US8626278B2 (en) * | 2010-10-08 | 2014-01-07 | Euljoon Park | Method and system for discriminating and monitoring atrial arrhythmia based on cardiogenic impedance |
| WO2012139116A2 (en) * | 2011-04-07 | 2012-10-11 | The Johns Hopkins University | Non-invasive methods and systems for producing cardiac electrogram characteristic maps for use with catheter ablation of ventricular tachycardia |
| US9314205B2 (en) * | 2011-04-28 | 2016-04-19 | Medtronic, Inc. | Measurement of cardiac cycle length and pressure metrics from pulmonary arterial pressure |
| WO2014115151A1 (en) | 2013-01-24 | 2014-07-31 | Tylerton International Holdings Inc. | Body structure imaging |
| US9554718B2 (en) * | 2014-01-29 | 2017-01-31 | Biosense Webster (Israel) Ltd. | Double bipolar configuration for atrial fibrillation annotation |
| ES2975607T3 (es) * | 2014-03-31 | 2024-07-10 | Univ Health Network | Procedimiento de identificación de fuente focal |
| US10154794B2 (en) * | 2014-04-25 | 2018-12-18 | Medtronic, Inc. | Implantable cardioverter-defibrillator (ICD) tachyarrhythmia detection modifications responsive to detected pacing |
| EP3166483B1 (en) * | 2014-10-15 | 2018-08-01 | St. Jude Medical, Cardiology Division, Inc. | Method and system for generating integrated substrate maps for cardiac arrhythmias |
| FR3030217B1 (fr) | 2014-12-23 | 2021-09-03 | Clement Bars | Cartographie regionale haute densite du substrat de la fibrillation atriale |
| EP3451918B1 (en) * | 2016-05-03 | 2020-09-23 | CardioInsight Technologies, Inc. | Detection and analysis of electrograms |
| US10744334B2 (en) * | 2016-10-18 | 2020-08-18 | Cardiac Pacemakers, Inc. | Systems and methods for arrhythmia detection |
| US10888379B2 (en) * | 2017-01-25 | 2021-01-12 | Biosense Webster (Israel) Ltd. | Analyzing and mapping ECG signals and determining ablation points to eliminate brugada syndrome |
-
2019
- 2019-07-16 US US16/512,588 patent/US10905349B1/en active Active
-
2020
- 2020-06-25 IL IL275666A patent/IL275666B2/en unknown
- 2020-07-15 EP EP20185867.7A patent/EP3766416B1/en active Active
- 2020-07-15 JP JP2020121139A patent/JP7588976B2/ja active Active
- 2020-07-16 CN CN202010688951.8A patent/CN112315486B/zh active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009537252A (ja) | 2006-05-17 | 2009-10-29 | セント・ジュード・メディカル・エイトリアル・フィブリレーション・ディヴィジョン・インコーポレーテッド | コンプレックス細分化電気的活動図情報をマッピングするシステムおよび方法 |
| JP2015171548A (ja) | 2008-11-10 | 2015-10-01 | カーディオインサイト テクノロジーズ インコーポレイテッド | 電気生理学データの視覚化 |
| US20150080752A1 (en) | 2013-09-16 | 2015-03-19 | Biotronik Se & Co. Kg | Device for automatic mapping of complex fractionated atrial electrogram |
| JP2018149271A (ja) | 2017-01-25 | 2018-09-27 | バイオセンス・ウエブスター・(イスラエル)・リミテッドBiosense Webster (Israel), Ltd. | 心臓内信号を解析し、詳細なマップを提供し、かつ潜在的アブレーションポイントを決定することによって、様々な心臓疾患を排除するための方法及びシステム |
Also Published As
| Publication number | Publication date |
|---|---|
| US10905349B1 (en) | 2021-02-02 |
| EP3766416C0 (en) | 2025-04-02 |
| JP2021016788A (ja) | 2021-02-15 |
| EP3766416A1 (en) | 2021-01-20 |
| IL275666B2 (en) | 2023-07-01 |
| US20210015383A1 (en) | 2021-01-21 |
| IL275666A (en) | 2021-01-31 |
| CN112315486A (zh) | 2021-02-05 |
| IL275666B1 (en) | 2023-03-01 |
| EP3766416B1 (en) | 2025-04-02 |
| CN112315486B (zh) | 2026-01-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7109881B2 (ja) | 関心領域の局所性発生源の検出 | |
| US10004413B2 (en) | Signal analysis related to treatment sites | |
| US10117594B2 (en) | Analysis and detection for arrhythmia drivers | |
| CN106963481B (zh) | 在心房纤颤过程中识别局灶性源 | |
| CN108269609B (zh) | 电解剖标测图上的距离可视化 | |
| EP2945531A2 (en) | Focal point identification and mapping | |
| CN112057039A (zh) | 在电生理标测图上视觉地区分主要激活和次要激活 | |
| EP4026497A1 (en) | Incorporating a confidence level into an electrophysiological (ep) map | |
| JP7588976B2 (ja) | フラグメンテーション指数を用いた心房細動のマッピング | |
| KR20190133114A (ko) | 심방 세동 전기도에서 활성화의 식별 | |
| EP3614913B1 (en) | Connectivity analysis for arrhythmia drivers | |
| JP7135071B2 (ja) | 電気循環の少なくとも1つの特異な区画の検出のために心筋壁のモデルを生成するための3次元画像のセグメンテーション方法 | |
| EP4079217A1 (en) | Improved electrophysiological (ep) map coloration by considering outliers | |
| JP2021094381A (ja) | ユニポーラ信号及びバイポーラ信号を使用した心室活動の検出 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230714 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240326 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20240329 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20240626 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20240826 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240926 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20241015 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20241113 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7588976 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |