JP7545397B2 - 有機エレクトロルミネッセンス素子及び電子機器 - Google Patents
有機エレクトロルミネッセンス素子及び電子機器 Download PDFInfo
- Publication number
- JP7545397B2 JP7545397B2 JP2021545647A JP2021545647A JP7545397B2 JP 7545397 B2 JP7545397 B2 JP 7545397B2 JP 2021545647 A JP2021545647 A JP 2021545647A JP 2021545647 A JP2021545647 A JP 2021545647A JP 7545397 B2 JP7545397 B2 JP 7545397B2
- Authority
- JP
- Japan
- Prior art keywords
- group
- substituted
- unsubstituted
- carbon atoms
- ring
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
- H10K50/125—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers specially adapted for multicolour light emission, e.g. for emitting white light
- H10K50/13—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers specially adapted for multicolour light emission, e.g. for emitting white light comprising stacked EL layers within one EL unit
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/10—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C13/00—Cyclic hydrocarbons containing rings other than, or in addition to, six-membered aromatic rings
- C07C13/28—Polycyclic hydrocarbons or acyclic hydrocarbon derivatives thereof
- C07C13/32—Polycyclic hydrocarbons or acyclic hydrocarbon derivatives thereof with condensed rings
- C07C13/72—Spiro hydrocarbons
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C15/00—Cyclic hydrocarbons containing only six-membered aromatic rings as cyclic parts
- C07C15/20—Polycyclic condensed hydrocarbons
- C07C15/27—Polycyclic condensed hydrocarbons containing three rings
- C07C15/28—Anthracenes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C15/00—Cyclic hydrocarbons containing only six-membered aromatic rings as cyclic parts
- C07C15/20—Polycyclic condensed hydrocarbons
- C07C15/27—Polycyclic condensed hydrocarbons containing three rings
- C07C15/30—Phenanthrenes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C15/00—Cyclic hydrocarbons containing only six-membered aromatic rings as cyclic parts
- C07C15/20—Polycyclic condensed hydrocarbons
- C07C15/38—Polycyclic condensed hydrocarbons containing four rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C211/00—Compounds containing amino groups bound to a carbon skeleton
- C07C211/43—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton
- C07C211/54—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton having amino groups bound to two or three six-membered aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C255/00—Carboxylic acid nitriles
- C07C255/49—Carboxylic acid nitriles having cyano groups bound to carbon atoms of six-membered aromatic rings of a carbon skeleton
- C07C255/50—Carboxylic acid nitriles having cyano groups bound to carbon atoms of six-membered aromatic rings of a carbon skeleton to carbon atoms of non-condensed six-membered aromatic rings
- C07C255/51—Carboxylic acid nitriles having cyano groups bound to carbon atoms of six-membered aromatic rings of a carbon skeleton to carbon atoms of non-condensed six-membered aromatic rings containing at least two cyano groups bound to the carbon skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/56—Ring systems containing three or more rings
- C07D209/80—[b, c]- or [b, d]-condensed
- C07D209/82—Carbazoles; Hydrogenated carbazoles
- C07D209/86—Carbazoles; Hydrogenated carbazoles with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to carbon atoms of the ring system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D235/00—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, condensed with other rings
- C07D235/02—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, condensed with other rings condensed with carbocyclic rings or ring systems
- C07D235/04—Benzimidazoles; Hydrogenated benzimidazoles
- C07D235/06—Benzimidazoles; Hydrogenated benzimidazoles with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached in position 2
- C07D235/08—Radicals containing only hydrogen and carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D235/00—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, condensed with other rings
- C07D235/02—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, condensed with other rings condensed with carbocyclic rings or ring systems
- C07D235/04—Benzimidazoles; Hydrogenated benzimidazoles
- C07D235/18—Benzimidazoles; Hydrogenated benzimidazoles with aryl radicals directly attached in position 2
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D251/00—Heterocyclic compounds containing 1,3,5-triazine rings
- C07D251/02—Heterocyclic compounds containing 1,3,5-triazine rings not condensed with other rings
- C07D251/12—Heterocyclic compounds containing 1,3,5-triazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members
- C07D251/14—Heterocyclic compounds containing 1,3,5-triazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members with hydrogen or carbon atoms directly attached to at least one ring carbon atom
- C07D251/24—Heterocyclic compounds containing 1,3,5-triazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members with hydrogen or carbon atoms directly attached to at least one ring carbon atom to three ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/77—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D307/91—Dibenzofurans; Hydrogenated dibenzofurans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D311/00—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings
- C07D311/02—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D311/78—Ring systems having three or more relevant rings
- C07D311/80—Dibenzopyrans; Hydrogenated dibenzopyrans
- C07D311/82—Xanthenes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D333/00—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom
- C07D333/50—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom condensed with carbocyclic rings or ring systems
- C07D333/76—Dibenzothiophenes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/10—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/12—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D407/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00
- C07D407/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00 containing two hetero rings
- C07D407/10—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00 containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/06—Peri-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/12—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains three hetero rings
- C07D487/16—Peri-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/22—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains four or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/06—Peri-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/22—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains four or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D493/00—Heterocyclic compounds containing oxygen atoms as the only ring hetero atoms in the condensed system
- C07D493/02—Heterocyclic compounds containing oxygen atoms as the only ring hetero atoms in the condensed system in which the condensed system contains two hetero rings
- C07D493/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D495/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms
- C07D495/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D495/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D495/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms
- C07D495/22—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms in which the condensed system contains four or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D519/00—Heterocyclic compounds containing more than one system of two or more relevant hetero rings condensed among themselves or condensed with a common carbocyclic ring system not provided for in groups C07D453/00 or C07D455/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F5/00—Compounds containing elements of Groups 3 or 13 of the Periodic Table
- C07F5/02—Boron compounds
- C07F5/027—Organoboranes and organoborohydrides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/0803—Compounds with Si-C or Si-Si linkages
- C07F7/081—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/0803—Compounds with Si-C or Si-Si linkages
- C07F7/081—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te
- C07F7/0812—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te comprising a heterocyclic ring
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H05—ELECTRIC TECHNIQUES NOT OTHERWISE PROVIDED FOR
- H05B—ELECTRIC HEATING; ELECTRIC LIGHT SOURCES NOT OTHERWISE PROVIDED FOR; CIRCUIT ARRANGEMENTS FOR ELECTRIC LIGHT SOURCES, IN GENERAL
- H05B33/00—Electroluminescent light sources
- H05B33/12—Light sources with substantially two-dimensional radiating surfaces
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/321—Metal complexes comprising a group IIIA element, e.g. Tris (8-hydroxyquinoline) gallium [Gaq3]
- H10K85/322—Metal complexes comprising a group IIIA element, e.g. Tris (8-hydroxyquinoline) gallium [Gaq3] comprising boron
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/40—Organosilicon compounds, e.g. TIPS pentacene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/622—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing four rings, e.g. pyrene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/623—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing five rings, e.g. pentacene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/624—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing six or more rings
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/626—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing more than one polycyclic condensed aromatic rings, e.g. bis-anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
- H10K85/633—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine comprising polycyclic condensed aromatic hydrocarbons as substituents on the nitrogen atom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/652—Cyanine dyes
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6574—Polycyclic condensed heteroaromatic hydrocarbons comprising only oxygen in the heteroaromatic polycondensed ring system, e.g. cumarine dyes
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6576—Polycyclic condensed heteroaromatic hydrocarbons comprising only sulfur in the heteroaromatic polycondensed ring system, e.g. benzothiophene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/658—Organoboranes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/05—Isotopically modified compounds, e.g. labelled
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
- H10K50/12—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers comprising dopants
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
- H10K50/125—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers specially adapted for multicolour light emission, e.g. for emitting white light
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Optics & Photonics (AREA)
- Inorganic Chemistry (AREA)
- Electroluminescent Light Sources (AREA)
Description
有機EL素子の性能向上を図るため、有機EL素子に用いる化合物について様々な検討がなされている(例えば、特許文献1~6参照)。有機EL素子の性能としては、例えば、輝度、発光波長、色度、発光効率、駆動電圧、及び寿命が挙げられる。
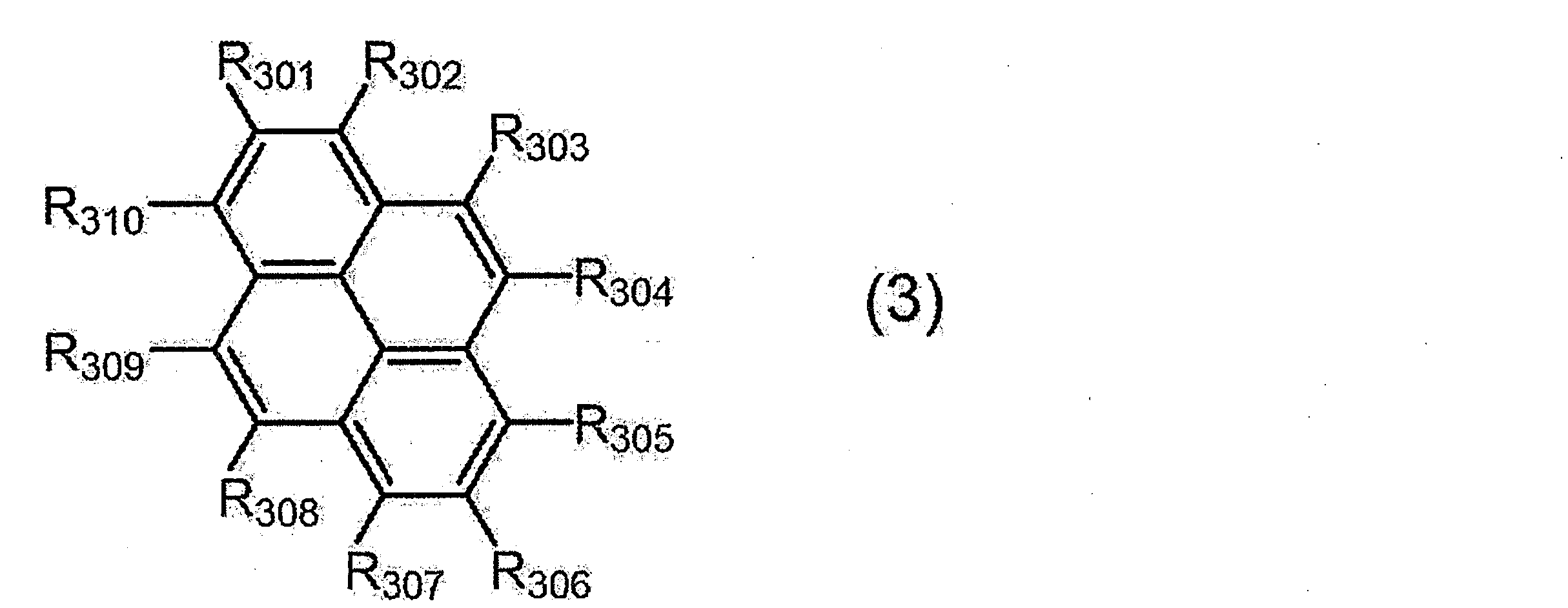
R101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、
置換もしくは無置換の環形成原子数5~50の複素環基、又は
前記一般式(11)で表される基であり、
ただし、R101~R110の少なくとも1つは、前記一般式(11)で表される基であり、
前記一般式(11)で表される基が複数存在する場合、複数の前記一般式(11)で表される基は、互いに同一であるか又は異なり、
L101は、
単結合、
置換もしくは無置換の環形成炭素数6~50のアリーレン基、又は
置換もしくは無置換の環形成原子数5~50の2価の複素環基であり、
Ar101は、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
mxは、0、1、2、3、4又は5であり、
L101が2以上存在する場合、2以上のL101は、互いに同一であるか、又は異なり、
Ar101が2以上存在する場合、2以上のAr101は、互いに同一であるか、又は異なり、
前記一般式(11)中の*は、前記一般式(1)中のピレン環との結合位置を示す。)
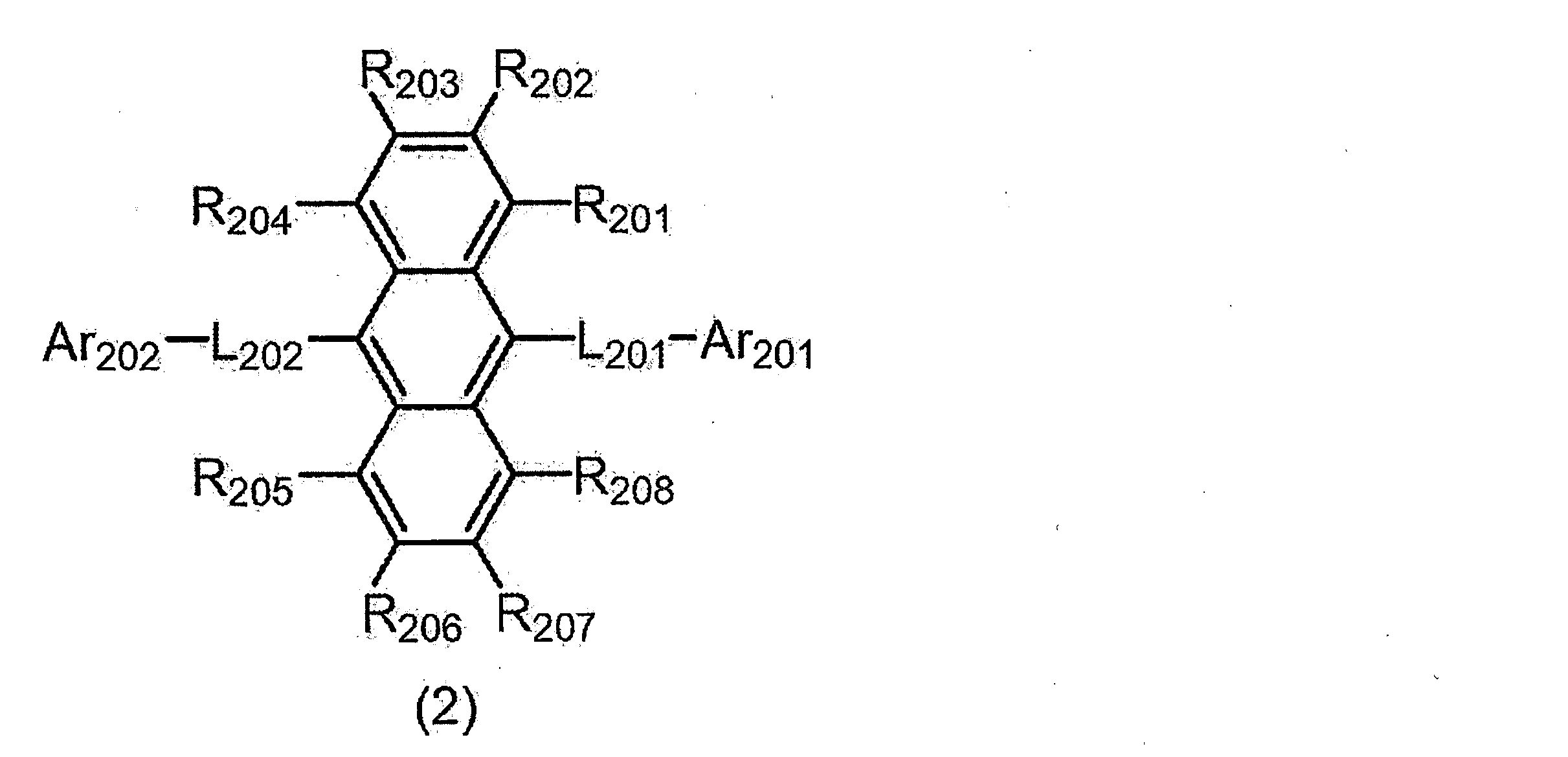
R201~R208は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
L201及びL202は、それぞれ独立に、
単結合、
置換もしくは無置換の環形成炭素数6~50のアリーレン基、又は
置換もしくは無置換の環形成原子数5~50の2価の複素環基であり、
Ar201及びAr202は、それぞれ独立に、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。)
(前記一般式(1)で表される第一の化合物及び前記一般式(2)で表される第二の化合物中、R901、R902、R903、R904、R905、R906、R907、R801及びR802は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
R901が複数存在する場合、複数のR901は、互いに同一であるか又は異なり、
R902が複数存在する場合、複数のR902は、互いに同一であるか又は異なり、
R903が複数存在する場合、複数のR903は、互いに同一であるか又は異なり、
R904が複数存在する場合、複数のR904は、互いに同一であるか又は異なり、
R905が複数存在する場合、複数のR905は、互いに同一であるか又は異なり、
R906が複数存在する場合、複数のR906は、互いに同一であるか又は異なり、
R907が複数存在する場合、複数のR907は、互いに同一であるか又は異なり、
R801が複数存在する場合、複数のR801は、互いに同一であるか又は異なり、
R802が複数存在する場合、複数のR802は、互いに同一であるか又は異なる。)
R101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
前記一般式(11)で表される基であり、
ただし、R101~R110の少なくとも1つは、前記一般式(11)で表される基であり、
前記一般式(11)で表される基が複数存在する場合、複数の前記一般式(11)で表される基は、互いに同一であるか又は異なり、
L101は、
単結合、又は
置換もしくは無置換の環形成炭素数6~50のアリーレン基であり、
Ar101は、置換もしくは無置換の環形成炭素数6~50のアリール基であり、
mxは、0、1、2、3、4又は5であり、
Ar101は、置換もしくは無置換のピレニル基ではなく、
L101は、置換もしくは無置換のピレニレン基ではなく、
前記一般式(11)で表される基ではないR101~R110としての置換もしくは無置換の環形成炭素数6~50のアリール基は、置換もしくは無置換のピレニル基ではなく、
L101が2以上存在する場合、2以上のL101は、互いに同一であるか、又は異なり、
Ar101が2以上存在する場合、2以上のAr101は、互いに同一であるか、又は異なり、
前記一般式(11)中の*は、前記一般式(1)中のピレン環との結合位置を示す。)
R101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、又は
前記一般式(11)で表される基であり、
ただし、R101~R110のうち2つ以上が、前記一般式(11)で表される基であり、
前記一般式(11)で表される基が複数存在する場合、複数の前記一般式(11)で表される基は、互いに同一であるか又は異なり、
L101は、単結合であり、
Ar101は、置換もしくは無置換の環形成原子数5~50の複素環基であり、
mxは、0であり、
Ar101が2以上存在する場合、2以上のAr101は、互いに同一であるか、又は異なり、
前記一般式(11)中の*は、前記一般式(1)中のピレン環との結合位置を示す。)
R101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、
置換もしくは無置換の環形成原子数5~50の複素環基、又は
前記一般式(11)で表される基であり、
ただし、R101~R110の少なくとも1つは、前記一般式(11)で表される基であり、
前記一般式(11)で表される基が複数存在する場合、複数の前記一般式(11)で表される基は、互いに同一であるか又は異なり、
L101は、置換もしくは無置換の環形成原子数5~50の2価の複素環基であり、
Ar101は、置換もしくは無置換の環形成原子数5~50の複素環基であり、
mxは、1、2、3、4又は5であり、
前記一般式(11)で表される基ではないR101~R110としての置換もしくは無置換の環形成炭素数6~50のアリール基は、置換もしくは無置換のピレニル基ではなく、
L101が2以上存在する場合、2以上のL101は、互いに同一であるか、又は異なり、
Ar101が2以上存在する場合、2以上のAr101は、互いに同一であるか、又は異なり、
前記一般式(11)中の*は、前記一般式(1)中のピレン環との結合位置を示す。)
R101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、
置換もしくは無置換の環形成原子数5~50の複素環基、又は
前記一般式(11)で表される基であり、
ただし、R101~R110の少なくとも1つは、前記一般式(11)で表される基であり、
ただし、R101~R110の少なくとも1つは、置換もしくは無置換の環形成原子数5~50の複素環基であり、
前記一般式(11)で表される基が複数存在する場合、複数の前記一般式(11)で表される基は、互いに同一であるか又は異なり、
L101は、
単結合、又は
置換もしくは無置換の環形成炭素数6~50のアリーレン基
であり、
Ar101は、置換もしくは無置換の環形成炭素数6~50のアリール基であり、
mxは、0、1、2、3、4又は5であり、
Ar101は、置換もしくは無置換のピレニル基ではなく、
L101は、置換もしくは無置換のピレニレン基ではなく、
前記一般式(11)で表される基ではないR101~R110としての置換もしくは無置換の環形成炭素数6~50のアリール基は、置換もしくは無置換のピレニル基ではなく、
L101が2以上存在する場合、2以上のL101は、互いに同一であるか、又は異なり、
Ar101が2以上存在する場合、2以上のAr101は、互いに同一であるか、又は異なり、
前記一般式(11)中の*は、前記一般式(1)中のピレン環との結合位置を示す。)
R101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、
置換もしくは無置換の環形成原子数5~50の複素環基、又は
前記一般式(11)で表される基であり、
ただし、R101~R110の少なくとも1つは、前記一般式(11)で表される基であり、
前記一般式(11)で表される基が複数存在する場合、複数の前記一般式(11)で表される基は、互いに同一であるか又は異なり、
L101は、置換もしくは無置換の環形成炭素数6~50のアリーレン基であり、
Ar101は、
置換もしくは無置換の環形成原子数5~50の複素環基であり、
mxは、1、2、3、4又は5であり、
L101は、置換もしくは無置換のピレニレン基ではなく、
前記一般式(11)で表される基ではないR101~R110としての置換もしくは無置換の環形成炭素数6~50のアリール基は、置換もしくは無置換のピレニル基ではなく、
L101が2以上存在する場合、2以上のL101は、互いに同一であるか、又は異なり、
Ar101が2以上存在する場合、2以上のAr101は、互いに同一であるか、又は異なり、
前記一般式(11)中の*は、前記一般式(1)中のピレン環との結合位置を示す。)
R101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、
置換もしくは無置換の環形成原子数5~50の複素環基、又は
前記一般式(11)で表される基であり、
ただし、R101~R110の少なくとも1つは、前記一般式(11)で表される基であり、
前記一般式(11)で表される基が複数存在する場合、複数の前記一般式(11)で表される基は、互いに同一であるか又は異なり、
L101は、置換もしくは無置換の環形成原子数5~50の2価の複素環基であり、
Ar101は、置換もしくは無置換の環形成炭素数6~50のアリール基であり、
mxは、1、2、3、4又は5であり、
Ar101は、置換もしくは無置換のピレニル基ではなく、
前記一般式(11)で表される基ではないR101~R110としての置換もしくは無置換の環形成炭素数6~50のアリール基は、置換もしくは無置換のピレニル基ではなく、
L101が2以上存在する場合、2以上のL101は、互いに同一であるか、又は異なり、
Ar101が2以上存在する場合、2以上のAr101は、互いに同一であるか、又は異なり、
前記一般式(11)中の*は、前記一般式(1)中のピレン環との結合位置を示す。)
R101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、
置換もしくは無置換の環形成原子数5~50の複素環基、又は
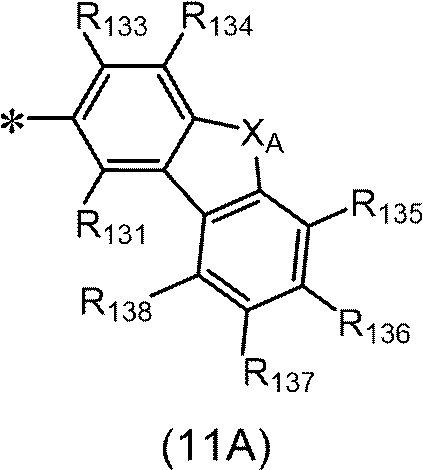
前記一般式(11A)で表される基であり、
ただし、R101~R110の少なくとも1つは、前記一般式(11A)で表される基であり、
前記一般式(11A)で表される基が複数存在する場合、複数の前記一般式(11A)で表される基は、互いに同一であるか又は異なり、
XAは、酸素原子、又は硫黄原子であり、
R131、R133及びR134のうちの隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
R135~R138、並びに前記置換もしくは無置換の単環を形成せず、かつ前記置換もしくは無置換の縮合環を形成しないR131、R133及びR134は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
前記一般式(11A)中の*は、前記一般式(1)中のピレン環との結合位置を示す。)
R101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、
置換もしくは無置換の環形成原子数5~50の複素環基、又は
前記一般式(11B)で表される基であり、
ただし、R101~R110の少なくとも1つは、前記一般式(11B)で表される基であり、
前記一般式(11B)で表される基が複数存在する場合、複数の前記一般式(11B)で表される基は、互いに同一であるか又は異なり、
XAは、酸素原子、又は硫黄原子であり、
R131、R133~R135、R138並びにR141~R144のうちの隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
前記置換もしくは無置換の単環を形成せず、かつ前記置換もしくは無置換の縮合環を形成しないR131、R133~R135、R138並びにR141~R144は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
ただし、R135、R138並びにR141~R144のうち、少なくとも1つは、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
前記一般式(11B)中の*は、前記一般式(1)中のピレン環との結合位置を示す。)
R101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、
置換もしくは無置換の環形成原子数5~50の複素環基、又は
前記一般式(11C)で表される基であり、
ただし、R101~R110の少なくとも1つは、前記一般式(11C)で表される基であり、
前記一般式(11C)で表される基が複数存在する場合、複数の前記一般式(11C)で表される基は、互いに同一であるか又は異なり、
XAは、酸素原子、又は硫黄原子であり、
R131、R133、R134、R137、R138並びにR141~R144のうちの隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
前記置換もしくは無置換の単環を形成せず、かつ前記置換もしくは無置換の縮合環を形成しないR131、R133、R134、R137、R138並びにR141~R144は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
前記一般式(11C)中の*は、前記一般式(1)中のピレン環との結合位置を示す。)
R101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、
置換もしくは無置換の環形成原子数5~50の複素環基、又は
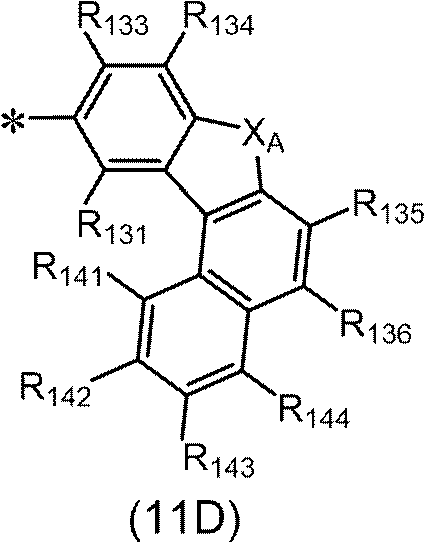
前記一般式(11D)で表される基であり、
ただし、R101~R110の少なくとも1つは、前記一般式(11D)で表される基であり、
前記一般式(11D)で表される基が複数存在する場合、複数の前記一般式(11D)で表される基は、互いに同一であるか又は異なり、
XAは、酸素原子、又は硫黄原子であり、
R131、R133、R134、R135、R136並びにR141~R144のうちの隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
前記置換もしくは無置換の単環を形成せず、かつ前記置換もしくは無置換の縮合環を形成しないR131、R133、R134、R135、R136並びにR141~R144は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
前記一般式(11D)中の*は、前記一般式(1)中のピレン環との結合位置を示す。)
R101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、
置換もしくは無置換の環形成原子数5~50の複素環基、又は
前記一般式(11E)で表される基であり、
ただし、R101~R110の少なくとも1つは、前記一般式(11E)で表される基であり、
前記一般式(11E)で表される基が複数存在する場合、複数の前記一般式(11E)で表される基は、互いに同一であるか又は異なり、
XAは、酸素原子、又は硫黄原子であり、
R131、R133~R135、R138並びにR141~R144のうちの隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
前記置換もしくは無置換の単環を形成せず、かつ前記置換もしくは無置換の縮合環を形成しないR131、R133~R135、R138並びにR141~R144は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
L101は、
置換もしくは無置換の環形成炭素数6~50のアリーレン基、又は
置換もしくは無置換の環形成原子数5~50の2価の複素環基であり、
mxは、1、2、3、4又は5であり、
L101が2以上存在する場合、2以上のL101は、互いに同一であるか、又は異なり、
前記一般式(11E)中の*は、前記一般式(1)中のピレン環との結合位置を示す。)
本明細書において、水素原子とは、中性子数が異なる同位体、即ち、軽水素(protium)、重水素(deuterium)、及び三重水素(tritium)を包含する。
また、ベンゼン環に置換基として、例えば、アルキル基が置換している場合、当該アルキル基の炭素数は、ベンゼン環の環形成炭素数に含めない。そのため、アルキル基が置換しているベンゼン環の環形成炭素数は、6である。また、ナフタレン環に置換基として、例えば、アルキル基が置換している場合、当該アルキル基の炭素数は、ナフタレン環の環形成炭素数に含めない。そのため、アルキル基が置換しているナフタレン環の環形成炭素数は、10である。
本明細書において、「置換もしくは無置換のZZ基」という場合における「無置換」とは、ZZ基における水素原子が置換基と置き換わっていないことを意味する。「無置換のZZ基」における水素原子は、軽水素原子、重水素原子、又は三重水素原子である。
また、本明細書において、「置換もしくは無置換のZZ基」という場合における「置換」とは、ZZ基における1つ以上の水素原子が、置換基と置き換わっていることを意味する。「AA基で置換されたBB基」という場合における「置換」も同様に、BB基における1つ以上の水素原子が、AA基と置き換わっていることを意味する。
以下、本明細書に記載の置換基について説明する。
本明細書に記載の「無置換の複素環基」の環形成原子数は、本明細書に別途記載のない限り、5~50であり、好ましくは5~30、より好ましくは5~18である。
本明細書に記載の「無置換のアルキル基」の炭素数は、本明細書に別途記載のない限り、1~50であり、好ましくは1~20、より好ましくは1~6である。
本明細書に記載の「無置換のアルケニル基」の炭素数は、本明細書に別途記載のない限り、2~50であり、好ましくは2~20、より好ましくは2~6である。
本明細書に記載の「無置換のアルキニル基」の炭素数は、本明細書に別途記載のない限り、2~50であり、好ましくは2~20、より好ましくは2~6である。
本明細書に記載の「無置換のシクロアルキル基」の環形成炭素数は、本明細書に別途記載のない限り、3~50であり、好ましくは3~20、より好ましくは3~6である。
本明細書に記載の「無置換のアリーレン基」の環形成炭素数は、本明細書に別途記載のない限り、6~50であり、好ましくは6~30、より好ましくは6~18である。
本明細書に記載の「無置換の2価の複素環基」の環形成原子数は、本明細書に別途記載のない限り、5~50であり、好ましくは5~30、より好ましくは5~18である。
本明細書に記載の「無置換のアルキレン基」の炭素数は、本明細書に別途記載のない限り、1~50であり、好ましくは1~20、より好ましくは1~6である。
本明細書に記載の「置換もしくは無置換のアリール基」の具体例(具体例群G1)としては、以下の無置換のアリール基(具体例群G1A)及び置換のアリール基(具体例群G1B)等が挙げられる。(ここで、無置換のアリール基とは「置換もしくは無置換のアリール基」が「無置換のアリール基」である場合を指し、置換のアリール基とは「置換もしくは無置換のアリール基」が「置換のアリール基」である場合を指す。)本明細書において、単に「アリール基」という場合は、「無置換のアリール基」と「置換のアリール基」の両方を含む。
「置換のアリール基」は、「無置換のアリール基」の1つ以上の水素原子が置換基と置き換わった基を意味する。「置換のアリール基」としては、例えば、下記具体例群G1Aの「無置換のアリール基」の1つ以上の水素原子が置換基と置き換わった基、及び下記具体例群G1Bの置換のアリール基の例等が挙げられる。尚、ここに列挙した「無置換のアリール基」の例、及び「置換のアリール基」の例は、一例に過ぎず、本明細書に記載の「置換のアリール基」には、下記具体例群G1Bの「置換のアリール基」におけるアリール基自体の炭素原子に結合する水素原子がさらに置換基と置き換わった基、及び下記具体例群G1Bの「置換のアリール基」における置換基の水素原子がさらに置換基と置き換わった基も含まれる。
フェニル基、
p-ビフェニル基、
m-ビフェニル基、
o-ビフェニル基、
p-ターフェニル-4-イル基、
p-ターフェニル-3-イル基、
p-ターフェニル-2-イル基、
m-ターフェニル-4-イル基、
m-ターフェニル-3-イル基、
m-ターフェニル-2-イル基、
o-ターフェニル-4-イル基、
o-ターフェニル-3-イル基、
o-ターフェニル-2-イル基、
1-ナフチル基、
2-ナフチル基、
アントリル基、
ベンゾアントリル基、
フェナントリル基、
ベンゾフェナントリル基、
フェナレニル基、
ピレニル基、
クリセニル基、
ベンゾクリセニル基、
トリフェニレニル基、
ベンゾトリフェニレニル基、
テトラセニル基、
ペンタセニル基、
フルオレニル基、
9,9’-スピロビフルオレニル基、
ベンゾフルオレニル基、
ジベンゾフルオレニル基、
フルオランテニル基、
ベンゾフルオランテニル基、
ペリレニル基、及び
下記一般式(TEMP-1)~(TEMP-15)で表される環構造から1つの水素原子を除くことにより誘導される1価のアリール基。
o-トリル基、
m-トリル基、
p-トリル基、
パラ-キシリル基、
メタ-キシリル基、
オルト-キシリル基、
パラ-イソプロピルフェニル基、
メタ-イソプロピルフェニル基、
オルト-イソプロピルフェニル基、
パラ-t-ブチルフェニル基、
メタ-t-ブチルフェニル基、
オルト-t-ブチルフェニル基、
3,4,5-トリメチルフェニル基、
9,9-ジメチルフルオレニル基、
9,9-ジフェニルフルオレニル基、
9,9-ビス(4-メチルフェニル)フルオレニル基、
9,9-ビス(4-イソプロピルフェニル)フルオレニル基、
9,9-ビス(4-t-ブチルフェニル)フルオレニル基、
シアノフェニル基、
トリフェニルシリルフェニル基、
トリメチルシリルフェニル基、
フェニルナフチル基、
ナフチルフェニル基、及び
前記一般式(TEMP-1)~(TEMP-15)で表される環構造から誘導される1価の基の1つ以上の水素原子が置換基と置き換わった基。
本明細書に記載の「複素環基」は、環形成原子にヘテロ原子を少なくとも1つ含む環状の基である。ヘテロ原子の具体例としては、窒素原子、酸素原子、硫黄原子、ケイ素原子、リン原子、及びホウ素原子が挙げられる。
本明細書に記載の「複素環基」は、単環の基であるか、又は縮合環の基である。
本明細書に記載の「複素環基」は、芳香族複素環基であるか、又は非芳香族複素環基である。
本明細書に記載の「置換もしくは無置換の複素環基」の具体例(具体例群G2)としては、以下の無置換の複素環基(具体例群G2A)、及び置換の複素環基(具体例群G2B)等が挙げられる。(ここで、無置換の複素環基とは「置換もしくは無置換の複素環基」が「無置換の複素環基」である場合を指し、置換の複素環基とは「置換もしくは無置換の複素環基」が「置換の複素環基」である場合を指す。)本明細書において、単に「複素環基」という場合は、「無置換の複素環基」と「置換の複素環基」の両方を含む。
「置換の複素環基」は、「無置換の複素環基」の1つ以上の水素原子が置換基と置き換わった基を意味する。「置換の複素環基」の具体例は、下記具体例群G2Aの「無置換の複素環基」の水素原子が置き換わった基、及び下記具体例群G2Bの置換の複素環基の例等が挙げられる。尚、ここに列挙した「無置換の複素環基」の例や「置換の複素環基」の例は、一例に過ぎず、本明細書に記載の「置換の複素環基」には、具体例群G2Bの「置換の複素環基」における複素環基自体の環形成原子に結合する水素原子がさらに置換基と置き換わった基、及び具体例群G2Bの「置換の複素環基」における置換基の水素原子がさらに置換基と置き換わった基も含まれる。
ピロリル基、
イミダゾリル基、
ピラゾリル基、
トリアゾリル基、
テトラゾリル基、
オキサゾリル基、
イソオキサゾリル基、
オキサジアゾリル基、
チアゾリル基、
イソチアゾリル基、
チアジアゾリル基、
ピリジル基、
ピリダジニル基、
ピリミジニル基、
ピラジニル基、
トリアジニル基、
インドリル基、
イソインドリル基、
インドリジニル基、
キノリジニル基、
キノリル基、
イソキノリル基、
シンノリル基、
フタラジニル基、
キナゾリニル基、
キノキサリニル基、
ベンゾイミダゾリル基、
インダゾリル基、
フェナントロリニル基、
フェナントリジニル基、
アクリジニル基、
フェナジニル基、
カルバゾリル基、
ベンゾカルバゾリル基、
モルホリノ基、
フェノキサジニル基、
フェノチアジニル基、
アザカルバゾリル基、及びジアザカルバゾリル基。
フリル基、
オキサゾリル基、
イソオキサゾリル基、
オキサジアゾリル基、
キサンテニル基、
ベンゾフラニル基、
イソベンゾフラニル基、
ジベンゾフラニル基、
ナフトベンゾフラニル基、
ベンゾオキサゾリル基、
ベンゾイソキサゾリル基、
フェノキサジニル基、
モルホリノ基、
ジナフトフラニル基、
アザジベンゾフラニル基、
ジアザジベンゾフラニル基、
アザナフトベンゾフラニル基、及び
ジアザナフトベンゾフラニル基。
チエニル基、
チアゾリル基、
イソチアゾリル基、
チアジアゾリル基、
ベンゾチオフェニル基(ベンゾチエニル基)、
イソベンゾチオフェニル基(イソベンゾチエニル基)、
ジベンゾチオフェニル基(ジベンゾチエニル基)、
ナフトベンゾチオフェニル基(ナフトベンゾチエニル基)、
ベンゾチアゾリル基、
ベンゾイソチアゾリル基、
フェノチアジニル基、
ジナフトチオフェニル基(ジナフトチエニル基)、
アザジベンゾチオフェニル基(アザジベンゾチエニル基)、
ジアザジベンゾチオフェニル基(ジアザジベンゾチエニル基)、
アザナフトベンゾチオフェニル基(アザナフトベンゾチエニル基)、及び
ジアザナフトベンゾチオフェニル基(ジアザナフトベンゾチエニル基)。
前記一般式(TEMP-16)~(TEMP-33)において、XA及びYAの少なくともいずれかがNH、又はCH2である場合、前記一般式(TEMP-16)~(TEMP-33)で表される環構造から誘導される1価の複素環基には、これらNH、又はCH2から1つの水素原子を除いて得られる1価の基が含まれる。
(9-フェニル)カルバゾリル基、
(9-ビフェニリル)カルバゾリル基、
(9-フェニル)フェニルカルバゾリル基、
(9-ナフチル)カルバゾリル基、
ジフェニルカルバゾール-9-イル基、
フェニルカルバゾール-9-イル基、
メチルベンゾイミダゾリル基、
エチルベンゾイミダゾリル基、
フェニルトリアジニル基、
ビフェニリルトリアジニル基、
ジフェニルトリアジニル基、
フェニルキナゾリニル基、及び
ビフェニリルキナゾリニル基。
フェニルジベンゾフラニル基、
メチルジベンゾフラニル基、
t-ブチルジベンゾフラニル基、及び
スピロ[9H-キサンテン-9,9’-[9H]フルオレン]の1価の残基。
フェニルジベンゾチオフェニル基、
メチルジベンゾチオフェニル基、
t-ブチルジベンゾチオフェニル基、及び
スピロ[9H-チオキサンテン-9,9’-[9H]フルオレン]の1価の残基。
本明細書に記載の「置換もしくは無置換のアルキル基」の具体例(具体例群G3)としては、以下の無置換のアルキル基(具体例群G3A)及び置換のアルキル基(具体例群G3B)が挙げられる。(ここで、無置換のアルキル基とは「置換もしくは無置換のアルキル基」が「無置換のアルキル基」である場合を指し、置換のアルキル基とは「置換もしくは無置換のアルキル基」が「置換のアルキル基」である場合を指す。)以下、単に「アルキル基」という場合は、「無置換のアルキル基」と「置換のアルキル基」の両方を含む。
「置換のアルキル基」は、「無置換のアルキル基」における1つ以上の水素原子が置換基と置き換わった基を意味する。「置換のアルキル基」の具体例としては、下記の「無置換のアルキル基」(具体例群G3A)における1つ以上の水素原子が置換基と置き換わった基、及び置換のアルキル基(具体例群G3B)の例等が挙げられる。本明細書において、「無置換のアルキル基」におけるアルキル基は、鎖状のアルキル基を意味する。そのため、「無置換のアルキル基」は、直鎖である「無置換のアルキル基」、及び分岐状である「無置換のアルキル基」が含まれる。尚、ここに列挙した「無置換のアルキル基」の例や「置換のアルキル基」の例は、一例に過ぎず、本明細書に記載の「置換のアルキル基」には、具体例群G3Bの「置換のアルキル基」におけるアルキル基自体の水素原子がさらに置換基と置き換わった基、及び具体例群G3Bの「置換のアルキル基」における置換基の水素原子がさらに置換基と置き換わった基も含まれる。
メチル基、
エチル基、
n-プロピル基、
イソプロピル基、
n-ブチル基、
イソブチル基、
s-ブチル基、及びt-ブチル基。
ペンタフルオロエチル基、
2,2,2-トリフルオロエチル基、及び
トリフルオロメチル基。
本明細書に記載の「置換もしくは無置換のアルケニル基」の具体例(具体例群G4)としては、以下の無置換のアルケニル基(具体例群G4A)、及び置換のアルケニル基(具体例群G4B)等が挙げられる。(ここで、無置換のアルケニル基とは「置換もしくは無置換のアルケニル基」が「無置換のアルケニル基」である場合を指し、「置換のアルケニル基」とは「置換もしくは無置換のアルケニル基」が「置換のアルケニル基」である場合を指す。)本明細書において、単に「アルケニル基」という場合は、「無置換のアルケニル基」と「置換のアルケニル基」の両方を含む。
「置換のアルケニル基」は、「無置換のアルケニル基」における1つ以上の水素原子が置換基と置き換わった基を意味する。「置換のアルケニル基」の具体例としては、下記の「無置換のアルケニル基」(具体例群G4A)が置換基を有する基、及び置換のアルケニル基(具体例群G4B)の例等が挙げられる。尚、ここに列挙した「無置換のアルケニル基」の例や「置換のアルケニル基」の例は、一例に過ぎず、本明細書に記載の「置換のアルケニル基」には、具体例群G4Bの「置換のアルケニル基」におけるアルケニル基自体の水素原子がさらに置換基と置き換わった基、及び具体例群G4Bの「置換のアルケニル基」における置換基の水素原子がさらに置換基と置き換わった基も含まれる。
ビニル基、
アリル基、
1-ブテニル基、
2-ブテニル基、及び
3-ブテニル基。
1,3-ブタンジエニル基、
1-メチルビニル基、
1-メチルアリル基、
1,1-ジメチルアリル基、
2-メチルアリル基、及び
1,2-ジメチルアリル基。
本明細書に記載の「置換もしくは無置換のアルキニル基」の具体例(具体例群G5)としては、以下の無置換のアルキニル基(具体例群G5A)等が挙げられる。(ここで、無置換のアルキニル基とは、「置換もしくは無置換のアルキニル基」が「無置換のアルキニル基」である場合を指す。)以下、単に「アルキニル基」という場合は、「無置換のアルキニル基」と「置換のアルキニル基」の両方を含む。
「置換のアルキニル基」は、「無置換のアルキニル基」における1つ以上の水素原子が置換基と置き換わった基を意味する。「置換のアルキニル基」の具体例としては、下記の「無置換のアルキニル基」(具体例群G5A)における1つ以上の水素原子が置換基と置き換わった基等が挙げられる。
本明細書に記載の「置換もしくは無置換のシクロアルキル基」の具体例(具体例群G6)としては、以下の無置換のシクロアルキル基(具体例群G6A)、及び置換のシクロアルキル基(具体例群G6B)等が挙げられる。(ここで、無置換のシクロアルキル基とは「置換もしくは無置換のシクロアルキル基」が「無置換のシクロアルキル基」である場合を指し、置換のシクロアルキル基とは「置換もしくは無置換のシクロアルキル基」が「置換のシクロアルキル基」である場合を指す。)本明細書において、単に「シクロアルキル基」という場合は、「無置換のシクロアルキル基」と「置換のシクロアルキル基」の両方を含む。
「置換のシクロアルキル基」は、「無置換のシクロアルキル基」における1つ以上の水素原子が置換基と置き換わった基を意味する。「置換のシクロアルキル基」の具体例としては、下記の「無置換のシクロアルキル基」(具体例群G6A)における1つ以上の水素原子が置換基と置き換わった基、及び置換のシクロアルキル基(具体例群G6B)の例等が挙げられる。尚、ここに列挙した「無置換のシクロアルキル基」の例や「置換のシクロアルキル基」の例は、一例に過ぎず、本明細書に記載の「置換のシクロアルキル基」には、具体例群G6Bの「置換のシクロアルキル基」におけるシクロアルキル基自体の炭素原子に結合する1つ以上の水素原子が置換基と置き換わった基、及び具体例群G6Bの「置換のシクロアルキル基」における置換基の水素原子がさらに置換基と置き換わった基も含まれる。
シクロプロピル基、
シクロブチル基、
シクロペンチル基、
シクロヘキシル基、
1-アダマンチル基、
2-アダマンチル基、
1-ノルボルニル基、及び
2-ノルボルニル基。
4-メチルシクロヘキシル基。
本明細書に記載の-Si(R901)(R902)(R903)で表される基の具体例(具体例群G7)としては、
-Si(G1)(G1)(G1)、
-Si(G1)(G2)(G2)、
-Si(G1)(G1)(G2)、
-Si(G2)(G2)(G2)、
-Si(G3)(G3)(G3)、及び
-Si(G6)(G6)(G6)
が挙げられる。ここで、
G1は、具体例群G1に記載の「置換もしくは無置換のアリール基」である。
G2は、具体例群G2に記載の「置換もしくは無置換の複素環基」である。
G3は、具体例群G3に記載の「置換もしくは無置換のアルキル基」である。
G6は、具体例群G6に記載の「置換もしくは無置換のシクロアルキル基」である。
-Si(G1)(G1)(G1)における複数のG1は、互いに同一であるか、又は異なる。
-Si(G1)(G2)(G2)における複数のG2は、互いに同一であるか、又は異なる。
-Si(G1)(G1)(G2)における複数のG1は、互いに同一であるか、又は異なる。
-Si(G2)(G2)(G2)における複数のG2は、互いに同一であるか、又は異なる。
-Si(G3)(G3)(G3)における複数のG3は、互いに同一であるか、又は異なる。
-Si(G6)(G6)(G6)における複数のG6は、互いに同一であるか、又は異なる。
本明細書に記載の-O-(R904)で表される基の具体例(具体例群G8)としては、
-O(G1)、
-O(G2)、
-O(G3)、及び
-O(G6)
が挙げられる。
ここで、
G1は、具体例群G1に記載の「置換もしくは無置換のアリール基」である。
G2は、具体例群G2に記載の「置換もしくは無置換の複素環基」である。
G3は、具体例群G3に記載の「置換もしくは無置換のアルキル基」である。
G6は、具体例群G6に記載の「置換もしくは無置換のシクロアルキル基」である。
本明細書に記載の-S-(R905)で表される基の具体例(具体例群G9)としては、
-S(G1)、
-S(G2)、
-S(G3)、及び
-S(G6)
が挙げられる。
ここで、
G1は、具体例群G1に記載の「置換もしくは無置換のアリール基」である。
G2は、具体例群G2に記載の「置換もしくは無置換の複素環基」である。
G3は、具体例群G3に記載の「置換もしくは無置換のアルキル基」である。
G6は、具体例群G6に記載の「置換もしくは無置換のシクロアルキル基」である。
本明細書に記載の-N(R906)(R907)で表される基の具体例(具体例群G10)としては、
-N(G1)(G1)、
-N(G2)(G2)、
-N(G1)(G2)、
-N(G3)(G3)、及び
-N(G6)(G6)
が挙げられる。
ここで、
G1は、具体例群G1に記載の「置換もしくは無置換のアリール基」である。
G2は、具体例群G2に記載の「置換もしくは無置換の複素環基」である。
G3は、具体例群G3に記載の「置換もしくは無置換のアルキル基」である。
G6は、具体例群G6に記載の「置換もしくは無置換のシクロアルキル基」である。
-N(G1)(G1)における複数のG1は、互いに同一であるか、又は異なる。
-N(G2)(G2)における複数のG2は、互いに同一であるか、又は異なる。
-N(G3)(G3)における複数のG3は、互いに同一であるか、又は異なる。
-N(G6)(G6)における複数のG6は、互いに同一であるか、又は異なる。
本明細書に記載の「ハロゲン原子」の具体例(具体例群G11)としては、フッ素原子、塩素原子、臭素原子、及びヨウ素原子等が挙げられる。
本明細書に記載の「置換もしくは無置換のフルオロアルキル基」は、「置換もしくは無置換のアルキル基」におけるアルキル基を構成する炭素原子に結合している少なくとも1つの水素原子がフッ素原子と置き換わった基を意味し、「置換もしくは無置換のアルキル基」におけるアルキル基を構成する炭素原子に結合している全ての水素原子がフッ素原子で置き換わった基(パーフルオロ基)も含む。「無置換のフルオロアルキル基」の炭素数は、本明細書に別途記載のない限り、1~50であり、好ましくは1~30であり、より好ましくは1~18である。「置換のフルオロアルキル基」は、「フルオロアルキル基」の1つ以上の水素原子が置換基と置き換わった基を意味する。尚、本明細書に記載の「置換のフルオロアルキル基」には、「置換のフルオロアルキル基」におけるアルキル鎖の炭素原子に結合する1つ以上の水素原子がさらに置換基と置き換わった基、及び「置換のフルオロアルキル基」における置換基の1つ以上の水素原子がさらに置換基と置き換わった基も含まれる。「無置換のフルオロアルキル基」の具体例としては、前記「アルキル基」(具体例群G3)における1つ以上の水素原子がフッ素原子と置き換わった基の例等が挙げられる。
本明細書に記載の「置換もしくは無置換のハロアルキル基」は、「置換もしくは無置換のアルキル基」におけるアルキル基を構成する炭素原子に結合している少なくとも1つの水素原子がハロゲン原子と置き換わった基を意味し、「置換もしくは無置換のアルキル基」におけるアルキル基を構成する炭素原子に結合している全ての水素原子がハロゲン原子で置き換わった基も含む。「無置換のハロアルキル基」の炭素数は、本明細書に別途記載のない限り、1~50であり、好ましくは1~30であり、より好ましくは1~18である。「置換のハロアルキル基」は、「ハロアルキル基」の1つ以上の水素原子が置換基と置き換わった基を意味する。尚、本明細書に記載の「置換のハロアルキル基」には、「置換のハロアルキル基」におけるアルキル鎖の炭素原子に結合する1つ以上の水素原子がさらに置換基と置き換わった基、及び「置換のハロアルキル基」における置換基の1つ以上の水素原子がさらに置換基と置き換わった基も含まれる。「無置換のハロアルキル基」の具体例としては、前記「アルキル基」(具体例群G3)における1つ以上の水素原子がハロゲン原子と置き換わった基の例等が挙げられる。ハロアルキル基をハロゲン化アルキル基と称する場合がある。
本明細書に記載の「置換もしくは無置換のアルコキシ基」の具体例としては、-O(G3)で表される基であり、ここで、G3は、具体例群G3に記載の「置換もしくは無置換のアルキル基」である。「無置換のアルコキシ基」の炭素数は、本明細書に別途記載のない限り、1~50であり、好ましくは1~30であり、より好ましくは1~18である。
本明細書に記載の「置換もしくは無置換のアルキルチオ基」の具体例としては、-S(G3)で表される基であり、ここで、G3は、具体例群G3に記載の「置換もしくは無置換のアルキル基」である。「無置換のアルキルチオ基」の炭素数は、本明細書に別途記載のない限り、1~50であり、好ましくは1~30であり、より好ましくは1~18である。
本明細書に記載の「置換もしくは無置換のアリールオキシ基」の具体例としては、-O(G1)で表される基であり、ここで、G1は、具体例群G1に記載の「置換もしくは無置換のアリール基」である。「無置換のアリールオキシ基」の環形成炭素数は、本明細書に別途記載のない限り、6~50であり、好ましくは6~30であり、より好ましくは6~18である。
本明細書に記載の「置換もしくは無置換のアリールチオ基」の具体例としては、-S(G1)で表される基であり、ここで、G1は、具体例群G1に記載の「置換もしくは無置換のアリール基」である。「無置換のアリールチオ基」の環形成炭素数は、本明細書に別途記載のない限り、6~50であり、好ましくは6~30であり、より好ましくは6~18である。
本明細書に記載の「トリアルキルシリル基」の具体例としては、-Si(G3)(G3)(G3)で表される基であり、ここで、G3は、具体例群G3に記載の「置換もしくは無置換のアルキル基」である。-Si(G3)(G3)(G3)における複数のG3は、互いに同一であるか、又は異なる。「トリアルキルシリル基」の各アルキル基の炭素数は、本明細書に別途記載のない限り、1~50であり、好ましくは1~20であり、より好ましくは1~6である。
本明細書に記載の「置換もしくは無置換のアラルキル基」の具体例としては、-(G3)-(G1)で表される基であり、ここで、G3は、具体例群G3に記載の「置換もしくは無置換のアルキル基」であり、G1は、具体例群G1に記載の「置換もしくは無置換のアリール基」である。従って、「アラルキル基」は、「アルキル基」の水素原子が置換基としての「アリール基」と置き換わった基であり、「置換のアルキル基」の一態様である。「無置換のアラルキル基」は、「無置換のアリール基」が置換した「無置換のアルキル基」であり、「無置換のアラルキル基」の炭素数は、本明細書に別途記載のない限り、7~50であり、好ましくは7~30であり、より好ましくは7~18である。
「置換もしくは無置換のアラルキル基」の具体例としては、ベンジル基、1-フェニルエチル基、2-フェニルエチル基、1-フェニルイソプロピル基、2-フェニルイソプロピル基、フェニル-t-ブチル基、α-ナフチルメチル基、1-α-ナフチルエチル基、2-α-ナフチルエチル基、1-α-ナフチルイソプロピル基、2-α-ナフチルイソプロピル基、β-ナフチルメチル基、1-β-ナフチルエチル基、2-β-ナフチルエチル基、1-β-ナフチルイソプロピル基、及び2-β-ナフチルイソプロピル基等が挙げられる。
本明細書に記載の「置換もしくは無置換のアリーレン基」は、別途記載のない限り、上記「置換もしくは無置換のアリール基」からアリール環上の1つの水素原子を除くことにより誘導される2価の基である。「置換もしくは無置換のアリーレン基」の具体例(具体例群G12)としては、具体例群G1に記載の「置換もしくは無置換のアリール基」からアリール環上の1つの水素原子を除くことにより誘導される2価の基等が挙げられる。
本明細書に記載の「置換もしくは無置換の2価の複素環基」は、別途記載のない限り、上記「置換もしくは無置換の複素環基」から複素環上の1つの水素原子を除くことにより誘導される2価の基である。「置換もしくは無置換の2価の複素環基」の具体例(具体例群G13)としては、具体例群G2に記載の「置換もしくは無置換の複素環基」から複素環上の1つの水素原子を除くことにより誘導される2価の基等が挙げられる。
本明細書に記載の「置換もしくは無置換のアルキレン基」は、別途記載のない限り、上記「置換もしくは無置換のアルキル基」からアルキル鎖上の1つの水素原子を除くことにより誘導される2価の基である。「置換もしくは無置換のアルキレン基」の具体例(具体例群G14)としては、具体例群G3に記載の「置換もしくは無置換のアルキル基」からアルキル鎖上の1つの水素原子を除くことにより誘導される2価の基等が挙げられる。
前記一般式(TEMP-42)~(TEMP-52)中、*は、結合位置を表す。
式Q9及びQ10は、単結合を介して互いに結合して環を形成してもよい。
前記一般式(TEMP-53)~(TEMP-62)中、*は、結合位置を表す。
前記一般式(TEMP-63)~(TEMP-68)中、*は、結合位置を表す。
本明細書において、「隣接する2つ以上からなる組の1組以上が、互いに結合して、置換もしくは無置換の単環を形成するか、互いに結合して、置換もしくは無置換の縮合環を形成するか、又は互いに結合せず」という場合は、「隣接する2つ以上からなる組の1組以上が、互いに結合して、置換もしくは無置換の単環を形成する」場合と、「隣接する2つ以上からなる組の1組以上が、互いに結合して、置換もしくは無置換の縮合環を形成する」場合と、「隣接する2つ以上からなる組の1組以上が、互いに結合しない」場合と、を意味する。
本明細書における、「隣接する2つ以上からなる組の1組以上が、互いに結合して、置換もしくは無置換の単環を形成する」場合、及び「隣接する2つ以上からなる組の1組以上が、互いに結合して、置換もしくは無置換の縮合環を形成する」場合(以下、これらの場合をまとめて「結合して環を形成する場合」と称する場合がある。)について、以下、説明する。母骨格がアントラセン環である下記一般式(TEMP-103)で表されるアントラセン化合物の場合を例として説明する。
芳香族炭化水素環の具体例としては、具体例群G1において具体例として挙げられた基が水素原子によって終端された構造が挙げられる。
芳香族複素環の具体例としては、具体例群G2において具体例として挙げられた芳香族複素環基が水素原子によって終端された構造が挙げられる。
脂肪族炭化水素環の具体例としては、具体例群G6において具体例として挙げられた基が水素原子によって終端された構造が挙げられる。
「環を形成する」とは、母骨格の複数の原子のみ、あるいは母骨格の複数の原子とさらに1以上の任意の元素で環を形成することを意味する。例えば、前記一般式(TEMP-104)に示す、R921とR922とが互いに結合して形成された環QAは、R921が結合するアントラセン骨格の炭素原子と、R922が結合するアントラセン骨格の炭素原子と、1以上の任意の元素とで形成する環を意味する。具体例としては、R921とR922とで環QAを形成する場合において、R921が結合するアントラセン骨格の炭素原子と、R922とが結合するアントラセン骨格の炭素原子と、4つの炭素原子とで単環の不飽和の環を形成する場合、R921とR922とで形成する環は、ベンゼン環である。
単環または縮合環を構成する「1以上の任意の元素」は、本明細書に別途記載のない限り、好ましくは2個以上15個以下であり、より好ましくは3個以上12個以下であり、さらに好ましくは3個以上5個以下である。
本明細書に別途記載のない限り、「単環」、及び「縮合環」のうち、好ましくは「単環」である。
本明細書に別途記載のない限り、「飽和の環」、及び「不飽和の環」のうち、好ましくは「不飽和の環」である。
本明細書に別途記載のない限り、「単環」は、好ましくはベンゼン環である。
本明細書に別途記載のない限り、「不飽和の環」は、好ましくはベンゼン環である。
「隣接する2つ以上からなる組の1組以上」が、「互いに結合して、置換もしくは無置換の単環を形成する」場合、又は「互いに結合して、置換もしくは無置換の縮合環を形成する」場合、本明細書に別途記載のない限り、好ましくは、隣接する2つ以上からなる組の1組以上が、互いに結合して、母骨格の複数の原子と、1個以上15個以下の炭素元素、窒素元素、酸素元素、及び硫黄元素からなる群から選択される少なくとも1種の元素とからなる置換もしくは無置換の「不飽和の環」を形成する。
上記の「飽和の環」、又は「不飽和の環」が置換基を有する場合の置換基は、例えば後述する「任意の置換基」である。上記の「単環」、又は「縮合環」が置換基を有する場合の置換基の具体例は、上述した「本明細書に記載の置換基」の項で説明した置換基である。
以上が、「隣接する2つ以上からなる組の1組以上が、互いに結合して、置換もしくは無置換の単環を形成する」場合、及び「隣接する2つ以上からなる組の1組以上が、互いに結合して、置換もしくは無置換の縮合環を形成する」場合(「結合して環を形成する場合」)についての説明である。
本明細書における一実施形態においては、前記「置換もしくは無置換の」という場合の置換基(本明細書において、「任意の置換基」と呼ぶことがある。)は、例えば、
無置換の炭素数1~50のアルキル基、
無置換の炭素数2~50のアルケニル基、
無置換の炭素数2~50のアルキニル基、
無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)、
-O-(R904)、
-S-(R905)、
-N(R906)(R907)、
ハロゲン原子、シアノ基、ニトロ基、
無置換の環形成炭素数6~50のアリール基、及び
無置換の環形成原子数5~50の複素環基
からなる群から選択される基等であり、
ここで、R901~R907は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。
R901が2個以上存在する場合、2個以上のR901は、互いに同一であるか、又は異なり、
R902が2個以上存在する場合、2個以上のR902は、互いに同一であるか、又は異なり、
R903が2個以上存在する場合、2個以上のR903は、互いに同一であるか、又は異なり、
R904が2個以上存在する場合、2個以上のR904は、互いに同一であるか、又は異なり、
R905が2個以上存在する場合、2個以上のR905は、互いに同一であるか、又は異なり、
R906が2個以上存在する場合、2個以上のR906は、互いに同一であるか、又は異なり、
R907が2個以上存在する場合、2個以上のR907は、互いに同一であるか又は異なる。
炭素数1~50のアルキル基、
環形成炭素数6~50のアリール基、及び
環形成原子数5~50の複素環基
からなる群から選択される基である。
炭素数1~18のアルキル基、
環形成炭素数6~18のアリール基、及び
環形成原子数5~18の複素環基
からなる群から選択される基である。
本明細書において別途記載のない限り、任意の置換基は、さらに置換基を有してもよい。任意の置換基がさらに有する置換基としては、上記任意の置換基と同様である。
(有機エレクトロルミネッセンス素子)
本実施形態に係る有機エレクトロルミネッセンス素子は、陽極と、陰極と、前記陽極及び前記陰極の間に配置された第一の発光層と、前記第一の発光層と前記陰極との間に配置された第二の発光層と、を有する。前記第一の発光層は、下記一般式(11)で表される基を少なくとも1つ有し、かつ下記一般式(1)で表される第一の化合物を第一のホスト材料として含有し、前記第二の発光層は、下記一般式(2)で表される第二の化合物を第二のホスト材料として含有する。本実施形態に係る有機EL素子において、前記第一の発光層と前記第二の発光層とが、直接、接している。
本実施形態に係る有機エレクトロルミネッセンス素子は、陽極と、第一の発光層と、第二の発光層と、陰極とをこの順に有している。
(LS1)第一の発光層に係る化合物の蒸着の工程と第二の発光層に係る化合物の蒸着の工程を経る過程で第一の化合物及び第二の化合物の両方が混在する領域が生じ、当該領域が第一の発光層と第二の発光層との界面に存在する態様。
(LS2)第一の発光層及び第二の発光層が発光性の化合物を含む場合に、第一の発光層に係る化合物の蒸着の工程と第二の発光層に係る化合物の蒸着の工程を経る過程で第一の化合物、第二の化合物及び発光性の化合物が混在する領域が生じ、当該領域が第一の発光層と第二の発光層との界面に存在する態様。
(LS3)第一の発光層及び第二の発光層が発光性の化合物を含む場合に、第一の発光層に係る化合物の蒸着の工程と第二の発光層に係る化合物の蒸着の工程を経る過程で当該発光性の化合物からなる領域、第一の化合物からなる領域、又は第二の化合物からなる領域が生じ、当該領域が第一の発光層と第二の発光層との界面に存在する態様。
本実施形態に係る有機エレクトロルミネッセンス素子は、素子駆動時に主ピーク波長が430nm以上480nm以下の光を放射することが好ましい。
素子駆動時に有機EL素子が放射する光の主ピーク波長の測定は、以下のようにして行う。電流密度が10mA/cm2となるように有機EL素子に電圧を印加した時の分光放射輝度スペクトルを分光放射輝度計CS-2000(コニカミノルタ社製)で計測する。得られた分光放射輝度スペクトルにおいて、発光強度が最大となる発光スペクトルのピーク波長を測定し、これを主ピーク波長(単位:nm)とする。
本実施形態に係る有機EL素子において、前記陽極と、前記第一の発光層との間に、正孔輸送層を有することが好ましい。
有機EL素子1は、透光性の基板2と、陽極3と、陰極4と、陽極3と陰極4との間に配置された有機層10と、を含む。有機層10は、陽極3側から順に、正孔注入層6、正孔輸送層7、第一の発光層51、第二の発光層52、電子輸送層8、及び電子注入層9が、この順番で積層されて構成される。
本実施形態に係る有機EL素子において、第一の化合物は、下記一般式(1)で表される化合物である。
R101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、
置換もしくは無置換の環形成原子数5~50の複素環基、又は
前記一般式(11)で表される基であり、
ただし、R101~R110の少なくとも1つは、前記一般式(11)で表される基であり、
前記一般式(11)で表される基が複数存在する場合、複数の前記一般式(11)で表される基は、互いに同一であるか又は異なり、
L101は、
単結合、
置換もしくは無置換の環形成炭素数6~50のアリーレン基、又は
置換もしくは無置換の環形成原子数5~50の2価の複素環基であり、
Ar101は、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
mxは、0、1、2、3、4又は5であり、
L101が2以上存在する場合、2以上のL101は、互いに同一であるか、又は異なり、
Ar101が2以上存在する場合、2以上のAr101は、互いに同一であるか、又は異なり、
前記一般式(11)中の*は、前記一般式(1)中のピレン環との結合位置を示す。)
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
R901が複数存在する場合、複数のR901は、互いに同一であるか又は異なり、
R902が複数存在する場合、複数のR902は、互いに同一であるか又は異なり、
R903が複数存在する場合、複数のR903は、互いに同一であるか又は異なり、
R904が複数存在する場合、複数のR904は、互いに同一であるか又は異なり、
R905が複数存在する場合、複数のR905は、互いに同一であるか又は異なり、
R906が複数存在する場合、複数のR906は、互いに同一であるか又は異なり、
R907が複数存在する場合、複数のR907は、互いに同一であるか又は異なり、
R801が複数存在する場合、複数のR801は、互いに同一であるか又は異なり、
R802が複数存在する場合、複数のR802は、互いに同一であるか又は異なる。)
R101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
前記一般式(11)で表される基であり、
ただし、R101~R110の少なくとも1つは、前記一般式(11)で表される基であり、
前記一般式(11)で表される基が複数存在する場合、複数の前記一般式(11)で表される基は、互いに同一であるか又は異なり、
L101は、
単結合、又は
置換もしくは無置換の環形成炭素数6~50のアリーレン基であり、
Ar101は、置換もしくは無置換の環形成炭素数6~50のアリール基であり、
mxは、0、1、2、3、4又は5であり、
Ar101は、置換もしくは無置換のピレニル基ではなく、
L101は、置換もしくは無置換のピレニレン基ではなく、
前記一般式(11)で表される基ではないR101~R110としての置換もしくは無置換の環形成炭素数6~50のアリール基は、置換もしくは無置換のピレニル基ではなく、
L101が2以上存在する場合、2以上のL101は、互いに同一であるか、又は異なり、
Ar101が2以上存在する場合、2以上のAr101は、互いに同一であるか、又は異なることも好ましい。
X1は、CR123R124、酸素原子、硫黄原子、又はNR125であり、
L111及びL112は、それぞれ独立に、
単結合、
置換もしくは無置換の環形成炭素数6~50のアリーレン基、又は
置換もしくは無置換の環形成原子数5~50の2価の複素環基であり、
maは、0、1、2、3又は4であり、
mbは、0、1、2、3又は4であり、
ma+mbは、0、1、2、3又は4であり、
Ar101は、前記一般式(11)におけるAr101と同義であり、
R121、R122、R123、R124及びR125は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
mcは、3であり、
3つのR121は、互いに同一であるか、又は異なり、
mdは、3であり、
3つのR122は、互いに同一であるか、又は異なる。)
X1は、CR123R124であり、
L111及びL112は、それぞれ独立に、
単結合、又は
置換もしくは無置換の環形成炭素数6~50のアリーレン基であり、
maは、0、1、2、3又は4であり、
mbは、0、1、2、3又は4であり、
ma+mbは、0、1、2、3又は4であり、
Ar101は、前記一般式(11)におけるAr101と同義であり、
R121、R122、R123、及びR124は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、又は
置換もしくは無置換の環形成炭素数6~50のアリール基であり、
mcは、3であり、
3つのR121は、互いに同一であるか、又は異なり、
mdは、3であり、
3つのR122は、互いに同一であるか、又は異なることが好ましい。
X1、L111、L112、ma、mb、Ar101、R121、R122、R123、R124及びR125は、それぞれ独立に、前記一般式(111)におけるX1、L111、L112、ma、mb、Ar101、R121、R122、R123、R124及びR125と同義であり、
複数のR121は、互いに同一であるか、又は異なり、
複数のR122は、互いに同一であるか、又は異なる。)
maは、0、1又は2であり、
mbは、0、1又は2である、ことが好ましい。
maは、0又は1であり、
mbは、0又は1であることが好ましい。
Ar101は、
置換もしくは無置換のフェニル基、
置換もしくは無置換のナフチル基、
置換もしくは無置換のビフェニル基、
置換もしくは無置換のターフェニル基、
置換もしくは無置換のピレニル基、
置換もしくは無置換のフェナントリル基、又は
置換もしくは無置換のフルオレニル基であることが好ましい。
Ar101は、下記一般式(12)、一般式(13)又は一般式(14)で表される基であることも好ましい。
R111~R120は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R124で表される基、
-COOR125で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
前記一般式(12)、一般式(13)及び一般式(14)中の*は、前記一般式(11)中のL101との結合位置、又は前記一般式(111)もしくは一般式(111b)中のL112との結合位置を示す。)
前記第一の化合物は、下記一般式(101)で表されることが好ましい。
R101~R120は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
ただし、R101~R110のうち1つがL101との結合位置を示し、R111~R120のうち1つがL101との結合位置を示し、
L101は、
単結合、
置換もしくは無置換の環形成炭素数6~50のアリーレン基、又は
置換もしくは無置換の環形成原子数5~50の2価の複素環基であり、
mxは、0、1、2、3、4又は5であり、
L101が2以上存在する場合、2以上のL101は、互いに同一であるか、又は異なる。)
L101は、
単結合、又は
置換もしくは無置換の環形成炭素数6~50のアリーレン基であることが好ましい。
前記第一の化合物は、下記一般式(102)で表されることが好ましい。
R101~R120は、それぞれ独立に、前記一般式(101)におけるR101~R120と同義であり、
ただし、R101~R110のうち1つがL111との結合位置を示し、R111~R120のうち1つがL112との結合位置を示し、
X1は、CR123R124、酸素原子、硫黄原子、又はNR125であり、
L111及びL112は、それぞれ独立に、
単結合、
置換もしくは無置換の環形成炭素数6~50のアリーレン基、又は
置換もしくは無置換の環形成原子数5~50の2価の複素環基であり、
maは、0、1、2、3又は4であり、
mbは、0、1、2、3又は4であり、
ma+mbは、0、1、2、3又は4であり、
R121、R122、R123、R124及びR125は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
mcは、3であり、
3つのR121は、互いに同一であるか、又は異なり、
mdは、3であり、
3つのR122は、互いに同一であるか、又は異なる。)
maは、0、1又は2であり、
mbは、0、1又は2であることが好ましい。
maは、0又は1であり、
mbは、0又は1であることが好ましい。
R101~R110のうち2つ以上が、前記一般式(11)で表される基であることが好ましい。
R101~R110のうち2つ以上が、前記一般式(11)で表される基であり、かつ、Ar101は、置換もしくは無置換の環形成炭素数6~50のアリール基であることが好ましい。
Ar101は、置換もしくは無置換のピレニル基ではなく、
L101は、置換もしくは無置換のピレニレン基ではなく、
前記一般式(11)で表される基ではないR101~R110としての置換もしくは無置換の環形成炭素数6~50のアリール基は、置換もしくは無置換のピレニル基ではないことが好ましい。
第一の化合物が、前記一般式(11)で表される基を少なくとも2つ有する場合において、前記一般式(1)中、
R101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、又は
前記一般式(11)で表される基であり、
ただし、R101~R110のうち2つ以上が、前記一般式(11)で表される基であり、
前記一般式(11)で表される基が複数存在する場合、複数の前記一般式(11)で表される基は、互いに同一であるか又は異なり、
L101は、単結合であり、
Ar101は、置換もしくは無置換の環形成原子数5~50の複素環基であり、
mxは、0であり、
Ar101が2以上存在する場合、2以上のAr101は、互いに同一であるか、又は異なることも好ましい。
R101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、
置換もしくは無置換の環形成原子数5~50の複素環基、又は
前記一般式(11)で表される基であり、
ただし、R101~R110の少なくとも1つは、前記一般式(11)で表される基であり、
前記一般式(11)で表される基が複数存在する場合、複数の前記一般式(11)で表される基は、互いに同一であるか又は異なり、
L101は、置換もしくは無置換の環形成原子数5~50の2価の複素環基であり、
Ar101は、置換もしくは無置換の環形成原子数5~50の複素環基であり、
mxは、1、2、3、4又は5であり、
前記一般式(11)で表される基ではないR101~R110としての置換もしくは無置換の環形成炭素数6~50のアリール基は、置換もしくは無置換のピレニル基ではなく、
L101が2以上存在する場合、2以上のL101は、互いに同一であるか、又は異なり、
Ar101が2以上存在する場合、2以上のAr101は、互いに同一であるか、又は異なることも好ましい。
R101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、
置換もしくは無置換の環形成原子数5~50の複素環基、又は
前記一般式(11)で表される基であり、
ただし、R101~R110の少なくとも1つは、前記一般式(11)で表される基であり、
ただし、R101~R110の少なくとも1つは、置換もしくは無置換の環形成原子数5~50の複素環基であり、
前記一般式(11)で表される基が複数存在する場合、複数の前記一般式(11)で表される基は、互いに同一であるか又は異なり、
L101は、
単結合、又は
置換もしくは無置換の環形成炭素数6~50のアリーレン基であり、
Ar101は、置換もしくは無置換の環形成炭素数6~50のアリール基であり、
mxは、0、1、2、3、4又は5であり、
Ar101は、置換もしくは無置換のピレニル基ではなく、
L101は、置換もしくは無置換のピレニレン基ではなく、
前記一般式(11)で表される基ではないR101~R110としての置換もしくは無置換の環形成炭素数6~50のアリール基は、置換もしくは無置換のピレニル基ではなく、
L101が2以上存在する場合、2以上のL101は、互いに同一であるか、又は異なり、
Ar101が2以上存在する場合、2以上のAr101は、互いに同一であるか、又は異なることも好ましい。
R101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、
置換もしくは無置換の環形成原子数5~50の複素環基、又は
前記一般式(11)で表される基であり、
ただし、R101~R110の少なくとも1つは、前記一般式(11)で表される基であり、
前記一般式(11)で表される基が複数存在する場合、複数の前記一般式(11)で表される基は、互いに同一であるか又は異なり、
L101は、
置換もしくは無置換の環形成炭素数6~50のアリーレン基、又は
置換もしくは無置換の環形成原子数5~50の2価の複素環基であり、
Ar101は、置換もしくは無置換の環形成原子数5~50の複素環基であり、
mxは、1、2、3、4又は5であり、
Ar101は、置換もしくは無置換の環形成原子数5~50の複素環基であり、
mxは、1、2、3、4又は5であり、
L101は、置換もしくは無置換のピレニレン基ではなく、
前記一般式(11)で表される基ではないR101~R110としての置換もしくは無置換の環形成炭素数6~50のアリール基は、置換もしくは無置換のピレニル基ではなく、
L101が2以上存在する場合、2以上のL101は、互いに同一であるか、又は異なり、
Ar101が2以上存在する場合、2以上のAr101は、互いに同一であるか、又は異なることが好ましく、L101は、置換もしくは無置換の環形成炭素数6~50のアリーレン基であることがより好ましい。
R101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、
置換もしくは無置換の環形成原子数5~50の複素環基、又は
前記一般式(11)で表される基であり、
ただし、R101~R110の少なくとも1つは、前記一般式(11)で表される基であり、
前記一般式(11)で表される基が複数存在する場合、複数の前記一般式(11)で表される基は、互いに同一であるか又は異なり、
L101は、置換もしくは無置換の環形成原子数5~50の2価の複素環基であり、
Ar101は、置換もしくは無置換の環形成炭素数6~50のアリール基であり、
mxは、1、2、3、4又は5であり、
Ar101は、置換もしくは無置換のピレニル基ではなく、
前記一般式(11)で表される基ではないR101~R110としての置換もしくは無置換の環形成炭素数6~50のアリール基は、置換もしくは無置換のピレニル基ではなく、
L101が2以上存在する場合、2以上のL101は、互いに同一であるか、又は異なり、
Ar101が2以上存在する場合、2以上のAr101は、互いに同一であるか、又は異なり、
前記一般式(11)中の*は、前記一般式(1)中のピレン環との結合位置を示すことも好ましい。
第一の化合物がモノピレン化合物であって、Ar101は、4つ以上の環が縮合したアリール基又は4つ以上の環が縮合した複素環基である場合、mxは、1、2、3、4又は5であり、少なくとも1つのL101は、単結合ではないこと(すなわち、L101がアリーレン基又は2価の複素環基であること)が好ましく、置換もしくは無置換のフェニレン基、置換もしくは無置換のビフェニレン基、置換もしくは無置換のターフェニレン基、置換もしくは無置換のナフチレン基、置換もしくは無置換のフルオレンジイル基、及び置換もしくは無置換のフェナントリレン基からなる群から選択される少なくともいずれかのアリーレン基又は置換もしくは無置換のジベンゾフランジイル基、置換もしくは無置換のジベンゾチオフェンジイル基、及び置換もしくは無置換のカルバゾールジイル基からなる群から選択される少なくともいずれかの2価の複素環基であることがより好ましい。このような連結基が、モノピレン化合物において、ピレン環と、4つ以上の環が縮合したアリール基又は4つ以上の環が縮合した複素環基との間に介在していることにより、ホール移動度の低下を抑制し、有機EL素子の発光効率の低下も抑制できる。また、当該連結基は、電子注入性低下のおそれがあるため、カルバゾール環を含まないことが好ましい。モノピレン化合物において、ピレン環と、4つ以上の環が縮合したアリール基又は4つ以上の環が縮合した複素環基との間に介在する連結基を有することにより、当該モノピレン化合物を含有する発光層への電子注入性が低下することを抑制し、有機EL素子の発光効率の低下も抑制できる。
置換もしくは無置換のフェニル基、
置換もしくは無置換のナフチル基、
置換もしくは無置換のビフェニル基、
置換もしくは無置換のターフェニル基、
置換もしくは無置換のフェナントリル基、又は
置換もしくは無置換のフルオレニル基であることも好ましい。
前記一般式(11)で表される基ではないR101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であることが好ましい。
前記一般式(11)で表される基ではないR101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、又は
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基であることが好ましい。
例えば、前記一般式(1)で表される第一の化合物中のR101ないしR110のうち2つが一般式(11)で表される基である。
例えば、前記一般式(1)で表される第一の化合物中のR101ないしR110のうち3つが一般式(11)で表される基である。
例えば、前記一般式(1)で表される第一の化合物中のR101ないしR110のうち4つが一般式(11)で表される基である。
例えば、前記一般式(1)で表される第一の化合物中のR101ないしR110のうち1つが一般式(11)で表される基であり、mxが1以上である。
例えば、前記一般式(1)で表される第一の化合物中のR101ないしR110のうち1つが一般式(11)で表される基であり、mxが0であり、Ar101が置換もしくは無置換のアリール基である。
例えば、前記一般式(1)で表される第一の化合物中のR101ないしR110のうち1つが一般式(11)で表される基であり、mxが0であり、Ar101が置換もしくは無置換の窒素原子を含む複素環基である。
例えば、前記一般式(1)で表される第一の化合物中のR101ないしR110のうち1つが一般式(11)で表される基であり、mxが0であり、Ar101が置換もしくは無置換の硫黄原子を含む複素環基である。
例えば、前記一般式(1)で表される第一の化合物中のR101ないしR110のうち1つが一般式(11)で表される基であり、mxが0であり、Ar101が置換もしくは無置換の
フリル基、
オキサゾリル基、
イソオキサゾリル基、
オキサジアゾリル基、
キサンテニル基、
ベンゾフラニル基、
イソベンゾフラニル基、
ジベンゾフラニル基、
ベンゾオキサゾリル基、
ベンゾイソキサゾリル基、
フェノキサジニル基、
モルホリノ基、
ジナフトフラニル基、
アザジベンゾフラニル基、
ジアザジベンゾフラニル基、
アザナフトベンゾフラニル基、及び
ジアザナフトベンゾフラニル基である。
例えば、前記一般式(1)で表される第一の化合物中のR101ないしR110のうち1つが一般式(11)で表される基であり、mxが0であり、Ar101が無置換の
フリル基、
オキサゾリル基、
イソオキサゾリル基、
オキサジアゾリル基、
キサンテニル基、
ベンゾフラニル基、
イソベンゾフラニル基、
ジベンゾフラニル基、
ベンゾオキサゾリル基、
ベンゾイソキサゾリル基、
フェノキサジニル基、
モルホリノ基、
ジナフトフラニル基、
アザジベンゾフラニル基、
ジアザジベンゾフラニル基、
アザナフトベンゾフラニル基、及び
ジアザナフトベンゾフラニル基からなる群から選択される少なくともいずれかの基である。
例えば、前記一般式(1)で表される第一の化合物中のR101ないしR110のうち1つが一般式(11)で表される基であり、mxが0であり、Ar101が置換もしくは無置換のジベンゾフラニル基である。
例えば、前記一般式(1)で表される第一の化合物中のR101ないしR110のうち1つが一般式(11)で表される基であり、mxが0であり、Ar101が無置換のジベンゾフラニル基である。
例えば、前記一般式(101)で表される第一の化合物中のmxが2以上である。
例えば、前記一般式(101)で表される第一の化合物中のmxが1以上であり、L101は環形成炭素数6~24のアリーレン基、または環形成原子数5~24の2価の複素環基である。
例えば、前記一般式(101)で表される第一の化合物中のmxが1以上であり、L101は環形成炭素数6~18のアリーレン基、または環形成原子数5~18の2価の複素環基である。
XAは、酸素原子、又は硫黄原子であり、
R131、R133及びR134のうちの隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
R135~R138、並びに前記置換もしくは無置換の単環を形成せず、かつ前記置換もしくは無置換の縮合環を形成しないR131、R133及びR134は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
前記一般式(11A)中の*は、前記一般式(1)中のピレン環との結合位置を示す。)
R101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、
置換もしくは無置換の環形成原子数5~50の複素環基、又は
前記一般式(11A)で表される基であり、
ただし、R101~R110の少なくとも1つは、前記一般式(11A)で表される基であり、
前記一般式(11A)で表される基が複数存在する場合、複数の前記一般式(11A)で表される基は、互いに同一であるか又は異なることが好ましい。
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、又は
ニトロ基であることが好ましい。
XAは、酸素原子、又は硫黄原子であり、
R131、R133~R135、R138並びにR141~R144のうちの隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
前記置換もしくは無置換の単環を形成せず、かつ前記置換もしくは無置換の縮合環を形成しないR131、R133~R135、R138並びにR141~R144は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
ただし、R135、R138並びにR141~R144のうち、少なくとも1つは、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
前記一般式(11B)中の*は、前記一般式(1)中のピレン環との結合位置を示す。)
R101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、
置換もしくは無置換の環形成原子数5~50の複素環基、又は
前記一般式(11B)で表される基であり、
ただし、R101~R110の少なくとも1つは、前記一般式(11B)で表される基であり、
前記一般式(11B)で表される基が複数存在する場合、複数の前記一般式(11B)で表される基は、互いに同一であるか又は異なることが好ましい。
XAは、酸素原子、又は硫黄原子であり、
R131、R133、R134、R137、R138並びにR141~R144のうちの隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
前記置換もしくは無置換の単環を形成せず、かつ前記置換もしくは無置換の縮合環を形成しないR131、R133、R134、R137、R138並びにR141~R144は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
前記一般式(11C)中の*は、前記一般式(1)中のピレン環との結合位置を示す。)
R101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、
置換もしくは無置換の環形成原子数5~50の複素環基、又は
前記一般式(11C)で表される基であり、
ただし、R101~R110の少なくとも1つは、前記一般式(11C)で表される基であり、
前記一般式(11C)で表される基が複数存在する場合、複数の前記一般式(11C)で表される基は、互いに同一であるか又は異なることが好ましい。
XAは、酸素原子、又は硫黄原子であり、
R131、R133、R134、R135、R136並びにR141~R144のうちの隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
前記置換もしくは無置換の単環を形成せず、かつ前記置換もしくは無置換の縮合環を形成しないR131、R133、R134、R135、R136並びにR141~R144は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
前記一般式(11D)中の*は、前記一般式(1)中のピレン環との結合位置を示す。)
R101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、
置換もしくは無置換の環形成原子数5~50の複素環基、又は
前記一般式(11D)で表される基であり、
ただし、R101~R110の少なくとも1つは、前記一般式(11D)で表される基であり、
前記一般式(11D)で表される基が複数存在する場合、複数の前記一般式(11D)で表される基は、互いに同一であるか又は異なることが好ましい。
XAは、酸素原子、又は硫黄原子であり、
R131、R133~R135、R138並びにR141~R144のうちの隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
前記置換もしくは無置換の単環を形成せず、かつ前記置換もしくは無置換の縮合環を形成しないR131、R133~R135、R138並びにR141~R144は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
L101は、
置換もしくは無置換の環形成炭素数6~50のアリーレン基、又は
置換もしくは無置換の環形成原子数5~50の2価の複素環基であり、
mxは、1、2、3、4又は5であり、
L101が2以上存在する場合、2以上のL101は、互いに同一であるか、又は異なり、
前記一般式(11E)中の*は、前記一般式(1)中のピレン環との結合位置を示す。)
R101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、
置換もしくは無置換の環形成原子数5~50の複素環基、又は
前記一般式(11E)で表される基であり、
ただし、R101~R110の少なくとも1つは、前記一般式(11E)で表される基であり、
前記一般式(11E)で表される基が複数存在する場合、複数の前記一般式(11E)で表される基は、互いに同一であるか又は異なることが好ましい。
X1は、CR123R124、酸素原子、硫黄原子、又はNR125であり、
L111及びL112は、それぞれ独立に、
単結合、
置換もしくは無置換の環形成炭素数6~50のアリーレン基、又は
置換もしくは無置換の環形成原子数5~50の2価の複素環基であり、
maは、1、2、3又は4であり、
mbは、1、2、3又は4であり、
ma+mbは、2、3又は4であり、
XA、R131、R133~R135、R138並びにR141~R144は、それぞれ、前記一般式(11E)におけるXA、R131、R133~R135、R138並びにR141~R144と同義であり、
R121、R122、R123、R124及びR125は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
mcは、3であり、
3つのR121は、互いに同一であるか、又は異なり、
mdは、3であり、
3つのR122は、互いに同一であるか、又は異なる。)
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であることが好ましい。
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、又は
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基であることが好ましい。
第一の化合物は、公知の方法により製造できる。また、第一の化合物は、公知の方法に倣い、目的物に合わせた既知の代替反応及び原料を用いることによっても、製造できる。
第一の化合物の具体例としては、例えば、以下の化合物挙げられる。ただし、本発明は、これら第一の化合物の具体例に限定されない。
本実施形態に係る有機EL素子において、第二の化合物は、下記一般式(2)で表される化合物である。
R201~R208は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
L201及びL202は、それぞれ独立に、
単結合、
置換もしくは無置換の環形成炭素数6~50のアリーレン基、又は
置換もしくは無置換の環形成原子数5~50の2価の複素環基であり、
Ar201及びAr202は、それぞれ独立に、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。)
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
R901が複数存在する場合、複数のR901は、互いに同一であるか又は異なり、
R902が複数存在する場合、複数のR902は、互いに同一であるか又は異なり、
R903が複数存在する場合、複数のR903は、互いに同一であるか又は異なり、
R904が複数存在する場合、複数のR904は、互いに同一であるか又は異なり、
R905が複数存在する場合、複数のR905は、互いに同一であるか又は異なり、
R906が複数存在する場合、複数のR906は、互いに同一であるか又は異なり、
R907が複数存在する場合、複数のR907は、互いに同一であるか又は異なり、
R801が複数存在する場合、複数のR801は、互いに同一であるか又は異なり、
R802が複数存在する場合、複数のR802は、互いに同一であるか又は異なる。)
R201~R208は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、又は
ニトロ基であり、
L201及びL202は、それぞれ独立に、
単結合、
置換もしくは無置換の環形成炭素数6~50のアリーレン基、又は
置換もしくは無置換の環形成原子数5~50の2価の複素環基であり、
Ar201及びAr202は、それぞれ独立に、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であることが好ましい。
L201及びL202は、それぞれ独立に、
単結合、又は
置換もしくは無置換の環形成炭素数6~50のアリーレン基であり、
Ar201及びAr202は、それぞれ独立に、置換もしくは無置換の環形成炭素数6~50のアリール基であることが好ましい。
Ar201及びAr202は、それぞれ独立に、
フェニル基、
ナフチル基、
フェナントリル基、
ビフェニル基、
ターフェニル基、
ジフェニルフルオレニル基、
ジメチルフルオレニル基、
ベンゾジフェニルフルオレニル基、
ベンゾジメチルフルオレニル基、
ジベンゾフラニル基、
ジベンゾチエニル基、
ナフトベンゾフラニル基、又は
ナフトベンゾチエニル基であることが好ましい。
L201及びAr201は、前記一般式(2)におけるL201及びAr201と同義であり、
R201~R208は、それぞれ独立に、前記一般式(2)におけるR201~R208と同義である。)
R201並びにR203~R208は、それぞれ独立に、前記一般式(2)におけるR201並びにR203~R208と同義であり、
L201及びAr201は、それぞれ、前記一般式(2)におけるL201及びAr201と同義であり、
L203は、前記一般式(2)におけるL201と同義であり、
L203とL201は、互いに同一であるか、又は異なり、
Ar203は、前記一般式(2)におけるAr201と同義であり、
Ar203とAr201は、互いに同一であるか、又は異なる。)
R201、R202並びにR204~R208は、それぞれ独立に、前記一般式(2)におけるR201、R202並びにR204~R208と同義であり、
L203は、前記一般式(2)におけるL201と同義であり、
L203とL201は、互いに同一であるか、又は異なり、
Ar203は、前記一般式(2)におけるAr201と同義であり、
Ar203とAr201は、互いに同一であるか、又は異なる。)
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、又は
-Si(R901)(R902)(R903)で表される基であることが好ましい。
単結合、又は
無置換の環形成炭素数6~22のアリーレン基であり、
Ar101は、置換もしくは無置換の環形成炭素数6~22のアリール基であることが好ましい。
R201~R208がアルキル基及びシクロアルキル基等のかさ高い置換基となった場合、分子間の相互作用が抑制され、第一の化合物に対し電子移動度が低下し、後述する下記数式(数3)に記載のμH2>μH1の関係を満たさなくなるおそれがある。第二の化合物を第二の発光層に用いた場合には、μH2>μH1の関係を満たす事で第一の発光層でのホールと電子との再結合能の低下、及び発光効率の低下を抑制することが期待できる。なお、置換基としては、ハロアルキル基、アルケニル基、アルキニル基、-Si(R901)(R902)(R903)で表される基、-O-(R904)で表される基、-S-(R905)で表される基、-N(R906)(R907)で表される基、アラルキル基、-C(=O)R801で表される基、-COOR802で表される基、ハロゲン原子、シアノ基、及びニトロ基がかさ高くなるおそれがあり、アルキル基、及びシクロアルキル基がさらにかさ高くなるおそれがある。
前記一般式(2)で表される第二の化合物中、アントラセン骨格の置換基であるR201~R208は、かさ高い置換基ではないことが好ましく、アルキル基及びシクロアルキル基ではないことが好ましく、アルキル基、シクロアルキル基、ハロアルキル基、アルケニル基、アルキニル基、-Si(R901)(R902)(R903)で表される基、-O-(R904)で表される基、-S-(R905)で表される基、-N(R906)(R907)で表される基、アラルキル基、-C(=O)R801で表される基、-COOR802で表される基、ハロゲン原子、シアノ基、及びニトロ基ではないことがより好ましい。
前記一般式(2)で表される第二の化合物中、R201~R208は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、又は
-Si(R901)(R902)(R903)で表される基であることも好ましい。
前記一般式(2)で表される第二の化合物中、R201~R208は、水素原子であることが好ましい。
アントリル基、
ベンゾアントリル基、
フェナントリル基、
ベンゾフェナントリル基、
フェナレニル基、
ピレニル基、
クリセニル基、
ベンゾクリセニル基、
トリフェニレニル基、
ベンゾトリフェニレニル基、
テトラセニル基、
ペンタセニル基、
フルオランテニル基、
ベンゾフルオランテニル基、及び
ペリレニル基からなる群から選択される少なくともいずれかの基である。
第二の化合物は、公知の方法により製造できる。また、第二の化合物は、公知の方法に倣い、目的物に合わせた既知の代替反応及び原料を用いることによっても、製造できる。
第二の化合物の具体例としては、例えば、以下の化合物挙げられる。ただし、本発明は、これら第二の化合物の具体例に限定されない。
本実施形態に係る有機EL素子において、第一の発光層は、蛍光発光性の第三の化合物をさらに含有することも好ましい。
本実施形態に係る有機EL素子において、第二の発光層は、蛍光発光性の第四の化合物をさらに含有することも好ましい。
第一の発光層が第三の化合物を含有し、かつ第二の発光層が第四の化合物を含有する場合、第三の化合物と第四の化合物とは、互いに同一であるか又は異なる。
下記一般式(3)で表される化合物、
下記一般式(4)で表される化合物、
下記一般式(5)で表される化合物、
下記一般式(6)で表される化合物、
下記一般式(7)で表される化合物、
下記一般式(8)で表される化合物、
下記一般式(9)で表される化合物、及び
下記一般式(10)で表される化合物からなる群から選択される1以上の化合物である。
一般式(3)で表される化合物について説明する。
R301~R310のうちの隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
R301~R310の少なくとも1つは下記一般式(31)で表される1価の基であり、
前記単環を形成せず、前記縮合環を形成せず、かつ下記一般式(31)で表される1価の基ではないR301~R310は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。
Ar301及びAr302は、それぞれ独立に、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
L301~L303は、それぞれ独立に、
単結合、
置換もしくは無置換の環形成炭素数6~30のアリーレン基、又は
置換もしくは無置換の環形成原子数5~30の2価の複素環基であり、
*は、前記一般式(3)中のピレン環における結合位置を示す。)
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
置換もしくは無置換の炭素数1~50のアルキル基、又は
置換もしくは無置換の環形成炭素数6~50のアリール基であり、
R901が複数存在する場合、複数のR901は、互いに同一であるか又は異なり、
R902が複数存在する場合、複数のR902は、互いに同一であるか又は異なり、
R903が複数存在する場合、複数のR903は、互いに同一であるか又は異なり、
R904が複数存在する場合、複数のR904は、互いに同一であるか又は異なり、
R905が複数存在する場合、複数のR905は、互いに同一であるか又は異なり、
R906が複数存在する場合、複数のR906は、互いに同一であるか又は異なり、
R907が複数存在する場合、複数のR907は、互いに同一であるか又は異なる。
R311~R318は、それぞれ独立に、前記一般式(3)における、前記一般式(31)で表される1価の基ではないR301~R310と同義であり、
L311~L316は、それぞれ独立に、
単結合、
置換もしくは無置換の環形成炭素数6~30のアリーレン基、又は
置換もしくは無置換の環形成原子数5~30の2価の複素環基であり、
Ar312、Ar313、Ar315及びAr316は、それぞれ独立に、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。)
R311~R318は、それぞれ独立に、前記一般式(3)における、前記一般式(31)で表される1価の基ではないR301~R310と同義であり、
L312、L313、L315及びL316は、それぞれ独立に、前記一般式(33)におけるL312、L313、L315及びL316と同義であり、
Ar312、Ar313、Ar315及びAr316は、それぞれ独立に、前記一般式(33)におけるAr312、Ar313、Ar315及びAr316と同義である。)
R311~R318は、それぞれ独立に、前記一般式(3)における、前記一般式(31)で表される1価の基ではないR301~R310と同義であり、
Ar312、Ar313、Ar315及びAr316は、それぞれ独立に、前記一般式(33)におけるAr312、Ar313、Ar315及びAr316と同義である。)
前記一般式(33)~一般式(35)において、好ましくは、Ar312及びAr313のうち少なくとも1つが下記一般式(36)で表される基である。
前記一般式(33)~一般式(35)において、好ましくは、Ar315及びAr316のうち少なくとも1つが下記一般式(36)で表される基である。
X3は、酸素原子又は硫黄原子を示し、
R321~R327のうち隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
前記単環を形成せず、かつ前記縮合環を形成しないR321~R327は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
*は、L302、L303、L312、L313、L315又はL316との結合位置を示す。)
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であることが好ましい。
前記一般式(33)~一般式(35)において、Ar312が前記一般式(36)で表される基であり、Ar313が置換もしくは無置換の環形成炭素数6~50のアリール基であることが好ましい。
前記一般式(33)~一般式(35)において、Ar315が前記一般式(36)で表される基であり、Ar316が置換もしくは無置換の環形成炭素数6~50のアリール基であることが好ましい。
R311~R318は、それぞれ独立に、前記一般式(3)における、前記一般式(31)で表される1価の基ではないR301~R310と同義であり、
R321~R327のうち隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
R341~R347のうち隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
前記単環を形成せず、かつ前記縮合環を形成しないR321~R327並びにR341~R347は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
R331~R335並びにR351~R355は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
ハロゲン原子、シアノ基、ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。)
一般式(4)で表される化合物について説明する。
Zは、それぞれ独立に、CRa又は窒素原子であり、
A1環及びA2環は、それぞれ独立に、
置換もしくは無置換の環形成炭素数6~50の芳香族炭化水素環、又は
置換もしくは無置換の環形成原子数5~50の複素環であり、
Raが複数存在する場合、複数のRaのうちの隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
n21及びn22は、それぞれ独立に、0、1、2、3又は4であり、
Rbが複数存在する場合、複数のRbのうちの隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
Rcが複数存在する場合、複数のRcのうちの隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
前記単環を形成せず、かつ前記縮合環を形成しないRa、Rb及びRcは、それぞれ独立に、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。)
A1環及びA2環の「芳香族炭化水素環」は、前記一般式(4)中央の縮合2環構造上の炭素原子2つを環形成原子として含む。
「置換もしくは無置換の環形成炭素数6~50の芳香族炭化水素環」の具体例としては、具体例群G1に記載の「アリール基」に水素原子を導入した化合物等が挙げられる。
A1環及びA2環の「複素環」は、前記一般式(4)中央の縮合2環構造上の炭素原子2つを環形成原子として含む。
「置換もしくは無置換の環形成原子数5~50の複素環」の具体例としては、具体例群G2に記載の「複素環基」に水素原子を導入した化合物等が挙げられる。
L401は、
単結合、
置換もしくは無置換の環形成炭素数6~30のアリーレン基、又は
置換もしくは無置換の環形成原子数5~30の2価の複素環基であり、
Ar401は、
置換もしくは無置換の環形成炭素数6~50のアリール基、
置換もしくは無置換の環形成原子数5~50の複素環基、又は
下記一般式(4b)で表される基である。)
L402及びL403は、それぞれ独立に、
単結合、
置換もしくは無置換の環形成炭素数6~30のアリーレン基、又は
置換もしくは無置換の環形成原子数5~30の2価の複素環基であり、
Ar402及びAr403からなる組は、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
前記単環を形成せず、かつ前記縮合環を形成しないAr402及びAr403は、それぞれ独立に、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。)
R401~R411のうちの隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
前記単環を形成せず、かつ前記縮合環を形成しないR401~R411は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。)
R404及びR411が前記一般式(4a)で表される基であることが好ましい。
また、一実施形態において、前記一般式(42)で表される化合物は、R404~R407が結合する環に下記一般式(4-1)又は一般式(4-2)で表される構造が結合した化合物である。
前記一般式(4-2)の3つの*は、それぞれ独立に、前記一般式(4)のA1環としての芳香族炭化水素環の環形成炭素原子もしくは複素環の環形成原子と結合するか、又は前記一般式(42)のR404~R407のいずれかと結合し、
R421~R427のうちの隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
R431~R438のうちの隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
前記単環を形成せず、かつ前記縮合環を形成しないR421~R427並びにR431~R438は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。)
A1環は、前記一般式(4)で定義した通りであり、
R421~R427は、それぞれ独立に、前記一般式(4-1)におけるR421~R427と同義であり、
R440~R448は、それぞれ独立に、前記一般式(42)におけるR401~R411と同義である。)
置換もしくは無置換のナフタレン環、又は
置換もしくは無置換のフルオレン環である。
置換もしくは無置換のジベンゾフラン環、
置換もしくは無置換のカルバゾール環、又は
置換もしくは無置換のジベンゾチオフェン環である。
R421~R427は、それぞれ独立に、前記一般式(4-1)におけるR421~R427と同義であり、
R431~R438は、それぞれ独立に、前記一般式(4-2)におけるR431~R438と同義であり、
R440~R448並びにR451~R454は、それぞれ独立に、前記一般式(42)におけるR401~R411と同義であり、
X4は、酸素原子、NR801、又はC(R802)(R803)であり、
R801、R802及びR803は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
置換もしくは無置換の炭素数1~50のアルキル基、又は
置換もしくは無置換の環形成炭素数6~50のアリール基であり、
R801が複数存在する場合、複数のR801は、互いに同一であるか又は異なり、
R802が複数存在する場合、複数のR802は、互いに同一であるか又は異なり、
R803が複数存在する場合、複数のR803は、互いに同一であるか又は異なる。)
一般式(45)で表される化合物について説明する。
R461とR462とからなる組、R462とR463とからなる組、R464とR465とからなる組、R465とR466とからなる組、R466とR467とからなる組、R468とR469とからなる組、R469とR470とからなる組、及び、R470とR471とからなる組からなる群から選択される組のうち2以上は、互いに結合して、置換もしくは無置換の単環又は置換もしくは無置換の縮合環を形成し、
ただし、
R461とR462とからなる組及びR462とR463とからなる組;
R464とR465とからなる組及びR465とR466とからなる組;
R465とR466とからなる組及びR466とR467とからなる組;
R468とR469とからなる組及びR469とR470とからなる組;並びに
R469とR470とからなる組及びR470とR471とからなる組が、同時に環を形成することはなく、
R461~R471が形成する2つ以上の環は、互いに同一であるか、又は異なり、
前記単環を形成せず、かつ前記縮合環を形成しないR461~R471は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)、-N(R906)(R907)で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。)
*1と*2、*3と*4、*5と*6、*7と*8、*9と*10、*11と*12及び*13と*14のそれぞれは、RnとRn+1が結合する前記2つの環形成炭素原子を表し、
Rnが結合する環形成炭素原子は、*1と*2、*3と*4、*5と*6、*7と*8、*9と*10、*11と*12及び*13と*14が表す2つの環形成炭素原子のどちらであってもよく、
X45は、C(R4512)(R4513)、NR4514、酸素原子又は硫黄原子であり、
R4501~R4506及びR4512~R4513のうちの隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
前記単環を形成せず、かつ前記縮合環を形成しないR4501~R4514は、それぞれ独立に、前記一般式(45)におけるR461~R471と同義である。)
*1と*2、及び*3と*4のそれぞれは、RnとRn+1が結合する前記2つの環形成炭素原子を表し、
Rnが結合する環形成炭素原子は、*1と*2、又は*3と*4が表す2つの環形成炭素原子のどちらであってもよく、
X45は、C(R4512)(R4513)、NR4514、酸素原子又は硫黄原子であり、
R4512~R4513及びR4515~~R4525のうちの隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
前記単環を形成せず、かつ前記縮合環を形成しないR4512~R4513、R4515~R4521及びR4522~R4525、並びにR4514は、それぞれ独立に、前記一般式(45)におけるR461~R471と同義である。)
(ii)前記一般式(45)において、環構造を形成しないR461~R471、及び
(iii)式(451)~(460)におけるR4501~R4514、R4515~~R4525は、好ましくは、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-N(R906)(R907)で表される基、
置換もしくは無置換の環形成炭素数6~50のアリール基、
置換もしくは無置換の環形成原子数5~50の複素環基、又は
下記一般式(461)~一般式(464)で表される基からなる群から選択される基のいずれかである。
Rdは、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
X46は、C(R801)(R802)、NR803、酸素原子又は硫黄原子であり、
R801、R802及びR803は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
置換もしくは無置換の炭素数1~50のアルキル基、又は
置換もしくは無置換の環形成炭素数6~50のアリール基であり、
R801が複数存在する場合、複数のR801は、互いに同一であるか又は異なり、
R802が複数存在する場合、複数のR802は、互いに同一であるか又は異なり、
R803が複数存在する場合、複数のR803は、互いに同一であるか又は異なり、
p1は、5であり、
p2は、4であり、
p3は、3であり、
p4は、7であり、
前記一般式(461)~(464)中の*は、それぞれ独立に、環構造との結合位置を示す。)
第三の化合物及び第四の化合物において、R901~R907は、前述のように定義した通りである。
環d~iは、それぞれ独立に、置換もしくは無置換の単環又は置換もしくは無置換の縮合環であり、
R461~R471は、それぞれ独立に、前記一般式(45)におけるR461~R471と同義である。)
環d~f、k、jは、それぞれ独立に、置換もしくは無置換の単環又は置換もしくは無置換の縮合環であり、
R461~R471は、それぞれ独立に、前記一般式(45)におけるR461~R471と同義である。)
環d~kは、それぞれ独立に、置換もしくは無置換の単環又は置換もしくは無置換の縮合環であり、
R461~R471は、それぞれ独立に、前記一般式(45)におけるR461~R471と同義である。)
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の環形成炭素数6~50のアリール基、
前記一般式(461)で表される基、
前記一般式(463)で表される基、又は
前記一般式(464)で表される基が挙げられる。
X46及びX47は、それぞれ独立に、C(R801)(R802)、NR803、酸素原子又は硫黄原子であり、
R461~R471並びにR481~R488は、それぞれ独立に、前記一般式(45)におけるR461~R471と同義である。
R801、R802及びR803は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
置換もしくは無置換の炭素数1~50のアルキル基、又は
置換もしくは無置換の環形成炭素数6~50のアリール基であり、
R801が複数存在する場合、複数のR801は、互いに同一であるか又は異なり、
R802が複数存在する場合、複数のR802は、互いに同一であるか又は異なり、
R803が複数存在する場合、複数のR803は、互いに同一であるか又は異なる。)
X46は、C(R801)(R802)、NR803、酸素原子又は硫黄原子であり、
R463、R464、R467、R468、R471、及びR481~R492は、それぞれ独立に、前記一般式(45)におけるR461~R471と同義である。
R801、R802及びR803は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
置換もしくは無置換の炭素数1~50のアルキル基、又は
置換もしくは無置換の環形成炭素数6~50のアリール基であり、
R801が複数存在する場合、複数のR801は、互いに同一であるか又は異なり、
R802が複数存在する場合、複数のR802は、互いに同一であるか又は異なり、
R803が複数存在する場合、複数のR803は、互いに同一であるか又は異なる。)
一般式(5)で表される化合物について説明する。一般式(5)で表される化合物は、上述した一般式(41-3)で表される化合物に対応する化合物である。
R501~R507及びR511~R517のうち隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
前記単環を形成せず、かつ前記縮合環を形成しないR501~R507及びR511~R517は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。
R521及びR522は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。)
水素原子、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。
R531~R534及びR541~R544のうちの隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
前記単環を形成せず、かつ前記縮合環を形成しないR531~R534、R541~R544、並びにR551及びR552は、それぞれ独立に、
水素原子、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
R561~R564は、それぞれ独立に、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。)
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。
一般式(6)で表される化合物について説明する。
a環、b環及びc環は、それぞれ独立に、
置換もしくは無置換の環形成炭素数6~50の芳香族炭化水素環、又は
置換もしくは無置換の環形成原子数5~50の複素環であり、
R601及びR602は、それぞれ独立に、前記a環、b環又はc環と結合して、置換もしくは無置換の複素環を形成するか、あるいは置換もしくは無置換の複素環を形成せず、
前記置換もしくは無置換の複素環を形成しないR601及びR602は、それぞれ独立に、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。)
a環の「芳香族炭化水素環」は、前記一般式(6)中央の縮合2環構造上の炭素原子3つを環形成原子として含む。
b環及びc環の「芳香族炭化水素環」は、前記一般式(6)中央の縮合2環構造上の炭素原子2つを環形成原子として含む。
a環、b環及びc環の「複素環」は、上述した「複素環基」に水素原子を導入した化合物と同じ構造である。
a環の「複素環」は、前記一般式(6)中央の縮合2環構造上の炭素原子3つを環形成原子として含む。b環及びc環の「複素環」は、前記一般式(6)中央の縮合2環構造上の炭素原子2つを環形成原子として含む。「置換もしくは無置換の環形成原子数5~50の複素環」の具体例としては、具体例群G2に記載の「複素環基」に水素原子を導入した化合物等が挙げられる。
R601がb環と結合する場合、R602がa環と結合する場合、及びR602がc環と結合する場合も上記と同じである。
一実施形態において、前記一般式(6)におけるa環、b環及びc環は、それぞれ独立に、置換もしくは無置換のベンゼン環又はナフタレン環である。
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
好ましくは置換もしくは無置換の環形成炭素数6~50のアリール基である。
R601Aは、R611及びR621からなる群から選択される1以上と結合して、置換もしくは無置換の複素環を形成するか、あるいは置換もしくは無置換の複素環を形成せず、
R602Aは、R613及びR614からなる群から選択される1以上と結合して、置換もしくは無置換の複素環を形成するか、あるいは置換もしくは無置換の複素環を形成せず、
前記置換もしくは無置換の複素環を形成しないR601A及びR602Aは、それぞれ独立に、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
R611~R621のうちの隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
前記置換もしくは無置換の複素環を形成せず、前記単環を形成せず、かつ前記縮合環を形成しないR611~R621は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。)
例えば、R601AとR611が結合して、これらを含む環とa環に対応するベンゼン環が縮合した2環縮合(又は3環縮合以上)の含窒素複素環を形成してもよい。当該含窒素複素環の具体例としては、具体例群G2のうち、窒素を含む2環縮合以上の複素環基に対応する化合物等が挙げられる。R601AとR621が結合する場合、R602AとR613が結合する場合、及びR602AとR614が結合する場合も上記と同じである。
互いに結合して、置換もしくは無置換の単環を形成するか、又は
互いに結合して、置換もしくは無置換の縮合環を形成してもよい。
例えば、R611とR612が結合して、これらが結合する6員環に対して、ベンゼン環、インドール環、ピロール環、ベンゾフラン環又はベンゾチオフェン環等が縮合した構造を形成してもよく、形成された縮合環は、ナフタレン環、カルバゾール環、インドール環、ジベンゾフラン環又はジベンゾチオフェン環となる。
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。
水素原子、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。
水素原子、又は
置換もしくは無置換の炭素数1~50のアルキル基である。
水素原子、又は
置換もしくは無置換の炭素数1~50のアルキル基であり、
R611~R621のうち少なくとも1つは、置換もしくは無置換の炭素数1~50のアルキル基である。
R631は、R646と結合して、置換もしくは無置換の複素環を形成するか、あるいは置換もしくは無置換の複素環を形成せず、
R633は、R647と結合して、置換もしくは無置換の複素環を形成するか、あるいは置換もしくは無置換の複素環を形成せず、
R634は、R651と結合して、置換もしくは無置換の複素環を形成するか、あるいは置換もしくは無置換の複素環を形成せず、
R641は、R642と結合して、置換もしくは無置換の複素環を形成するか、あるいは置換もしくは無置換の複素環を形成せず、
R631~R651のうちの隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
前記置換もしくは無置換の複素環を形成せず、前記単環を形成せず、かつ前記縮合環を形成しないR631~R651は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。)
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。
水素原子、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。
水素原子、又は
置換もしくは無置換の炭素数1~50のアルキル基である。
水素原子、又は
置換もしくは無置換の炭素数1~50のアルキル基であり、
R631~R651のうち少なくとも1つは置換もしくは無置換の炭素数1~50のアルキル基である。
R661は、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、又は
置換もしくは無置換の環形成炭素数6~50のアリール基であり、
R662~R665は、それぞれ独立に、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、又は
置換もしくは無置換の環形成炭素数6~50のアリール基である。)
置換もしくは無置換の炭素数1~50のアルキル基、又は
置換もしくは無置換の環形成炭素数6~50のアリール基である。
R671及びR672は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-N(R906)(R907)で表される基、又は
置換もしくは無置換の環形成炭素数6~50のアリール基であり、
R673~R675は、それぞれ独立に、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-N(R906)(R907)で表される基、又は
置換もしくは無置換の環形成炭素数6~50のアリール基である。)
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-N(R906)(R907)で表される基、又は
置換もしくは無置換の環形成炭素数6~50のアリール基である。
R672は、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
-N(R906)(R907)で表される基、又は
置換もしくは無置換の環形成炭素数6~50のアリール基であり、
R671及びR673~R675は、それぞれ独立に、
置換もしくは無置換の炭素数1~50のアルキル基、
-N(R906)(R907)で表される基、又は
置換もしくは無置換の環形成炭素数6~50のアリール基である。
R681及びR682は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、又は
置換もしくは無置換の環形成炭素数6~50のアリール基である。
R683~R686は、それぞれ独立に、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、又は
置換もしくは無置換の環形成炭素数6~50のアリール基である。)
置換もしくは無置換の炭素数1~50のアルキル基、又は
置換もしくは無置換の環形成炭素数6~50のアリール基である。
一般式(7)で表される化合物について説明する。
r環は、隣接環の任意の位置で縮合する前記一般式(72)又は一般式(73)で表される環であり、
q環及びs環は、それぞれ独立に、隣接環の任意の位置で縮合する前記一般式(74)で表される環であり、
p環及びt環は、それぞれ独立に、隣接環の任意の位置で縮合する前記一般式(75)又は一般式(76)で表される構造であり、
X7は、酸素原子、硫黄原子、又はNR702である。
R701が複数存在する場合、隣接する複数のR701は、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
前記単環を形成せず、かつ前記縮合環を形成しないR701及びR702は、それぞれ独立に、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
Ar701及びAr702は、それぞれ独立に、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
L701は、
置換もしくは無置換の炭素数1~50のアルキレン基、
置換もしくは無置換の炭素数2~50のアルケニレン基、
置換もしくは無置換の炭素数2~50のアルキニレン基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキレン基、
置換もしくは無置換の環形成炭素数6~50のアリーレン基、又は
置換もしくは無置換の環形成原子数5~50の2価の複素環基であり、
m1は、0、1又は2であり、
m2は、0、1、2、3又は4であり、
m3は、それぞれ独立に、0、1、2又は3であり、
m4は、それぞれ独立に、0、1、2、3、4又は5であり、
R701が複数存在する場合、複数のR701は、互いに同一であるか、又は異なり、
X7が複数存在する場合、複数のX7は、互いに同一であるか、又は異なり、
R702が複数存在する場合、複数のR702は、互いに同一であるか、又は異なり、
Ar701が複数存在する場合、複数のAr701は、互いに同一であるか、又は異なり、
Ar702が複数存在する場合、複数のAr702は、互いに同一であるか、又は異なり、
L701が複数存在する場合、複数のL701は、互いに同一であるか、又は異なる。)
一般式(8)で表される化合物について説明する。
R801とR802、R802とR803、及びR803とR804の少なくとも一組は、互いに結合して下記一般式(82)で示される2価の基を形成し、
R805とR806、R806とR807、及びR807とR808の少なくとも一組は、互いに結合して下記一般式(83)で示される2価の基を形成する。)
前記一般式(83)で示される2価の基を形成しないR805~R808、及びR821~R824の少なくとも1つは下記一般式(84)で表される1価の基であり、
X8は、酸素原子、硫黄原子、又はNR809であり、
前記一般式(82)及び一般式(83)で表される2価の基を形成せず、かつ、前記一般式(84)で表される1価の基ではないR801~R808、前記一般式(84)で表される1価の基ではないR811~R814及びR821~R824、並びにR809は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。)
Ar801及びAr802は、それぞれ独立に、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
L801~L803は、それぞれ独立に、
単結合、
置換もしくは無置換の環形成炭素数6~30のアリーレン基、
置換もしくは無置換の環形成原子数5~30の2価の複素環基、又は
置換もしくは無置換の環形成炭素数6~30のアリーレン基及び置換もしくは無置換の環形成原子数5~30の2価の複素環基からなる群から選択される2~4個の基が結合して形成される2価の連結基であり、
前記一般式(84)中の*は、前記一般式(8)で表される環構造、一般式(82)又は一般式(83)で表される基との結合位置を示す。)
X8は、前記一般式(8)におけるX8と同義であり、
R801~R824のうち少なくとも2つは、前記一般式(84)で表される1価の基であり、
前記一般式(84)で表される1価の基ではないR801~R824は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。)
X8は、前記一般式(8)におけるX8と同義であり、
*は、前記一般式(84)で表される1価の基と結合する単結合であり、
R801~R824は、それぞれ独立に、前記一般式(81-1)~一般式(81-6)における前記一般式(84)で表される1価の基ではないR801~R824とと同義である。)
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。
R831~R840は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
前記一般式(85)中の*は、前記一般式(84)中の*と同義である。)
Ar801、L801及びL803は、前記一般式(84)におけるAr801、L801及びL803と同義であり、
HAr801は、下記一般式(87)で表される構造である。)
X81は、酸素原子又は硫黄原子であり、
R841~R848のいずれか1つは、L803に結合する単結合であり、
単結合ではないR841~R848は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。)
一般式(9)で表される化合物について説明する。
A91環及びA92環は、それぞれ独立に、
置換もしくは無置換の環形成炭素数6~50の芳香族炭化水素環、又は、
置換もしくは無置換の環形成原子数5~50の複素環であり、
A91環及びA92環からなる群から選択される1以上の環は、
下記一般式(92)で表される構造の*と結合する。)
A93環は、
置換もしくは無置換の環形成炭素数6~50の芳香族炭化水素環、又は、
置換もしくは無置換の環形成原子数5~50の複素環であり、
X9は、NR93、C(R94)(R95)、Si(R96)(R97)、Ge(R98)(R99)、酸素原子、硫黄原子又はセレン原子であり、
R91及びR92は、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
前記単環を形成せず、かつ前記縮合環を形成しないR91及びR92、並びにR93~R99は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。)
Ar91及びAr92は、それぞれ独立に、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
L91~L93は、それぞれ独立に、
単結合、
置換もしくは無置換の環形成炭素数6~30のアリーレン基、
置換もしくは無置換の環形成原子数5~30の2価の複素環基、又は
置換もしくは無置換の環形成炭素数6~30のアリーレン基及び置換もしくは無置換の環形成原子数5~30の2価の複素環基からなる群から選択される2~4個結合して形成される2価の連結基であり、
前記一般式(93)中の*は、A91環及びA92環のいずれかとの結合位置を示す。)
一実施形態において、R91及びR92は、互いに結合してフルオレン構造を形成する。
一実施形態において、X9は、酸素原子又は硫黄原子である。
一般式(10)で表される化合物について説明する。
Ax1環は、隣接環の任意の位置で縮合する前記一般式(10a)で表される環であり、
Ax2環は、隣接環の任意の位置で縮合する前記一般式(10b)で表される環であり、
前記一般式(10b)中の2つの*は、Ax3環の任意の位置と結合し、
XA及びXBは、それぞれ独立に、C(R1003)(R1004)、Si(R1005)(R1006)、酸素原子又は硫黄原子であり、
Ax3環は、
置換もしくは無置換の環形成炭素数6~50の芳香族炭化水素環、又は
置換もしくは無置換の環形成原子数5~50の複素環であり、
Ar1001は、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
R1001~R1006は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
mx1は、3であり、mx2は、2であり、
複数のR1001は、互いに同一であるか、又は異なり、
複数のR1002は、互いに同一であるか、又は異なり、
axは、0、1又は2であり、
axが0又は1の場合、「3-ax」で示されるカッコ内の構造は、互いに同一であるか、又は異なり、
axが2の場合、複数のAr1001は、互いに同一であるか、又は異なる。)
前記一般式(4)で表される化合物、
前記一般式(5)で表される化合物、
前記一般式(7)で表される化合物、
前記一般式(8)で表される化合物、
前記一般式(9)で表される化合物及び
下記一般式(63a)で表される化合物からなる群から選択される1以上の化合物を含有する。
R631は、R646と結合して、置換もしくは無置換の複素環を形成するか、あるいは置換もしくは無置換の複素環を形成しない。
R633は、R647と結合して、置換もしくは無置換の複素環を形成するか、あるいは置換もしくは無置換の複素環を形成しない。
R634は、R651と結合して、置換もしくは無置換の複素環を形成するか、あるいは置換もしくは無置換の複素環を形成しない。
R641は、R642と結合して、置換もしくは無置換の複素環を形成するか、あるいは置換もしくは無置換の複素環を形成しない。
R631~R651のうちの隣接する2つ以上の1組以上は、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
前記置換もしくは無置換の複素環を形成せず、前記単環を形成せず、かつ前記縮合環を形成しないR631~R651は、それぞれ独立に、
水素原子、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
但し、前記置換もしくは無置換の複素環を形成せず、前記単環を形成せず、かつ前記縮合環を形成しないR631~R651のうちの少なくとも1つは、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。)
置換もしくは無置換のナフタレン環、
置換もしくは無置換のアントラセン環、又は
置換もしくは無置換のフルオレン環であり、
前記置換もしくは無置換の環形成原子数8~50の縮合複素環が、
置換もしくは無置換のジベンゾフラン環、
置換もしくは無置換のカルバゾール環、又は
置換もしくは無置換のジベンゾチオフェン環である。
置換もしくは無置換のナフタレン環、又は
置換もしくは無置換のフルオレン環であり、
前記置換もしくは無置換の環形成原子数8~50の縮合複素環が、
置換もしくは無置換のジベンゾフラン環、
置換もしくは無置換のカルバゾール環、又は
置換もしくは無置換のジベンゾチオフェン環である。
下記一般式(461)で表される化合物、
下記一般式(462)で表される化合物、
下記一般式(463)で表される化合物、
下記一般式(464)で表される化合物、
下記一般式(465)で表される化合物、
下記一般式(466)で表される化合物、及び
下記一般式(467)で表される化合物からなる群から選択される。
R421~R427、R431~R436、R440~R448及びR451~R454のうちの隣接する2つ以上からなる組の1組以上が、
互いに結合して、置換もしくは無置換の単環を形成するか、
互いに結合して、置換もしくは無置換の縮合環を形成するか、又は
互いに結合せず、
R437、R438、並びに前記単環を形成せず、かつ前記縮合環を形成しないR421~R427、R431~R436、R440~R448及びR451~R454は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
X4は、酸素原子、NR801、又はC(R802)(R803)であり、
R801、R802及びR803は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
置換もしくは無置換の炭素数1~50のアルキル基、又は
置換もしくは無置換の環形成炭素数6~50のアリール基であり、
R801が複数存在する場合、複数のR801は、互いに同一であるか又は異なり、
R802が複数存在する場合、複数のR802は、互いに同一であるか又は異なり、
R803が複数存在する場合、複数のR803は、互いに同一であるか又は異なる。)
水素原子、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。
水素原子、
置換もしくは無置換の環形成炭素数6~18のアリール基、及び
置換もしくは無置換の環形成原子数5~18の複素環基からなる群から選択される。
但し、R421~R427及びR440~R446の少なくとも1つは、-N(R906)(R907)で表される基である。)
RA、RB、RC及びRDは、それぞれ独立に、
置換もしくは無置換の環形成炭素数6~18のアリール基、又は
置換もしくは無置換の環形成原子数5~18の複素環基である。)
無置換の炭素数1~50のアルキル基、
無置換の炭素数2~50のアルケニル基、
無置換の炭素数2~50のアルキニル基、
無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901a)(R902a)(R903a)、
-O-(R904a)、
-S-(R905a)、
-N(R906a)(R907a)、
ハロゲン原子、
シアノ基、
ニトロ基、
無置換の環形成炭素数6~50のアリール基、又は
無置換の環形成原子数5~50の複素環基であり、
R901a~R907aは、それぞれ独立に、
水素原子、
無置換の炭素数1~50のアルキル基、
無置換の環形成炭素数6~50のアリール基、又は
無置換の環形成原子数5~50の複素環基であり、
R901aが2以上存在する場合、2以上のR901aは、互いに同一であるか、又は異なり、
R902aが2以上存在する場合、2以上のR902aは、互いに同一であるか、又は異なり、
R903aが2以上存在する場合、2以上のR903aは、互いに同一であるか、又は異なり、
R904aが2以上存在する場合、2以上のR904aは、互いに同一であるか、又は異なり、
R905aが2以上存在する場合、2以上のR905aは、互いに同一であるか、又は異なり、
R906aが2以上存在する場合、2以上のR906aは、互いに同一であるか、又は異なり、
R907aが2以上存在する場合、2以上のR907aは、互いに同一であるか、又は異なる。
無置換の炭素数1~50のアルキル基、
無置換の環形成炭素数6~50のアリール基、又は
無置換の環形成原子数5~50の複素環基である。
無置換の炭素数1~18のアルキル基、
無置換の環形成炭素数6~18のアリール基、又は
無置換の環形成原子数5~18の複素環基である。
発光スペクトルにおいて、発光強度が最大となる発光スペクトルのピーク波長を発光主ピーク波長とする。なお、本明細書において、主ピーク波長を蛍光発光主ピーク波長(FL-peak)と称する場合がある。
S1(H1)>S1(D3)…(数1)
S1(H2)>S1(D4)…(数2)
溶液を用いた一重項エネルギーS1の測定方法(溶液法と称する場合がある。)としては、下記の方法が挙げられる。
測定対象となる化合物の10-5mol/L以上10-4mol/L以下のトルエン溶液を調製して石英セルに入れ、常温(300K)でこの試料の吸収スペクトル(縦軸:吸収強度、横軸:波長とする。)を測定する。この吸収スペクトルの長波長側の立ち下がりに対して接線を引き、その接線と横軸との交点の波長値λedge[nm]を次に示す換算式(F2)に代入して一重項エネルギーを算出する。
換算式(F2):S1[eV]=1239.85/λedge
吸収スペクトル測定装置としては、例えば、日立社製の分光光度計(装置名:U3310)が挙げられるが、これに限定されない。
なお、吸光度の値が0.2以下の極大点は、上記最も長波長側の極大値には含めない。
μH2>μH1…(数3)
陽極及び陰極で厚さ100nm~200nmの測定対象層を挟み、バイアスDC電圧を印加しながら100mV以下の微小交流電圧を印加する。このときに流れる交流電流値(絶対値と位相)を測定する。交流電圧の周波数を変えながら本測定を行い、電流値と電圧値とから、複素インピーダンス(Z)を算出する。このときモジュラスM=iωZ(i:虚数単位、ω:角周波数)の虚数部(ImM)の周波数依存性を求め、ImMが最大値となる周波数ωの逆数を、測定対象層内を伝導する電子の応答時間と定義する。そして以下の式により電子移動度を算出する。
電子移動度=(測定対象層の膜厚)2/(応答時間・電圧)
また、第一の発光層及び第二の発光層は、重金属錯体及び燐光発光性の希土類金属錯体を含まないことが好ましい。ここで、重金属錯体としては、例えば、イリジウム錯体、オスミウム錯体、及び白金錯体等が挙げられる。
また、第一の発光層及び第二の発光層は、金属錯体を含まないことも好ましい。
本実施形態に係る有機EL素子の発光層の膜厚は、5nm以上50nm以下であることが好ましく、7nm以上50nm以下であることがより好ましく、10nm以上50nm以下であることがさらに好ましい。発光層の膜厚が5nm以上であると、発光層を形成し易く、色度を調整し易い。発光層の膜厚が50nm以下であると、駆動電圧の上昇を抑制し易い。
第一の発光層が第一の化合物及び第三の化合物を含有する場合、第一の発光層における第一の化合物及び第三の化合物の含有率は、例えば、それぞれ、以下の範囲であることが好ましい。
第一の化合物の含有率は、80質量%以上99質量%以下であることが好ましく、90質量%以上99質量%以下であることがより好ましく、95質量%以上99質量%以下であることがさらに好ましい。
第三の化合物の含有率は、1質量%以上10質量%以下であることが好ましく、1質量%以上7質量%以下であることがより好ましく、1質量%以上5質量%以下であることがさらに好ましい。
ただし、第一の発光層における第一の化合物及び第三の化合物の合計含有率の上限は、100質量%である。
第一の発光層は、第一の化合物を1種のみ含んでもよいし、2種以上含んでもよい。第一の発光層は、第三の化合物を1種のみ含んでもよいし、2種以上含んでもよい。
第二の化合物の含有率は、80質量%以上99質量%以下であることが好ましく、90質量%以上99質量%以下であることがより好ましく、95質量%以上99質量%以下であることがさらに好ましい。
第四の化合物の含有率は、1質量%以上10質量%以下であることが好ましく、1質量%以上7質量%以下であることがより好ましく、1質量%以上5質量%以下であることがさらに好ましい。
ただし、第二の発光層における第二の化合物及び第四の化合物の合計含有率の上限は、100質量%である。
第二の発光層は、第二の化合物を1種のみ含んでもよいし、2種以上含んでもよい。第二の発光層は、第四の化合物を1種のみ含んでもよいし、2種以上含んでもよい。
基板は、有機EL素子の支持体として用いられる。基板としては、例えば、ガラス、石英、及びプラスチック等を用いることができる。また、可撓性基板を用いてもよい。可撓性基板とは、折り曲げることができる(フレキシブル)基板のことであり、例えば、プラスチック基板等が挙げられる。プラスチック基板を形成する材料としては、例えば、ポリカーボネート、ポリアリレート、ポリエーテルスルフォン、ポリプロピレン、ポリエステル、ポリフッ化ビニル、ポリ塩化ビニル、ポリイミド、及びポリエチレンナフタレート等が挙げられる。また、無機蒸着フィルムを用いることもできる。
基板上に形成される陽極には、仕事関数の大きい(具体的には4.0eV以上)金属、合金、電気伝導性化合物、およびこれらの混合物などを用いることが好ましい。具体的には、例えば、酸化インジウム-酸化スズ(ITO:Indium Tin Oxide)、珪素もしくは酸化珪素を含有した酸化インジウム-酸化スズ、酸化インジウム-酸化亜鉛、酸化タングステン、および酸化亜鉛を含有した酸化インジウム、グラフェン等が挙げられる。この他、金(Au)、白金(Pt)、ニッケル(Ni)、タングステン(W)、クロム(Cr)、モリブデン(Mo)、鉄(Fe)、コバルト(Co)、銅(Cu)、パラジウム(Pd)、チタン(Ti)、または金属材料の窒化物(例えば、窒化チタン)等が挙げられる。
陰極には、仕事関数の小さい(具体的には3.8eV以下)金属、合金、電気伝導性化合物、およびこれらの混合物などを用いることが好ましい。このような陰極材料の具体例としては、元素周期表の第1族または第2族に属する元素、すなわちリチウム(Li)やセシウム(Cs)等のアルカリ金属、およびマグネシウム(Mg)、カルシウム(Ca)、ストロンチウム(Sr)等のアルカリ土類金属、およびこれらを含む合金(例えば、MgAg、AlLi)、ユーロピウム(Eu)、イッテルビウム(Yb)等の希土類金属およびこれらを含む合金等が挙げられる。
正孔注入層は、正孔注入性の高い物質を含む層である。正孔注入性の高い物質としては、モリブデン酸化物、チタン酸化物、バナジウム酸化物、レニウム酸化物、ルテニウム酸化物、クロム酸化物、ジルコニウム酸化物、ハフニウム酸化物、タンタル酸化物、銀酸化物、タングステン酸化物、マンガン酸化物等を用いることができる。
正孔輸送層は、正孔輸送性の高い物質を含む層である。正孔輸送層には、芳香族アミン化合物、カルバゾール誘導体、アントラセン誘導体等を使用する事ができる。具体的には、4,4’-ビス[N-(1-ナフチル)-N-フェニルアミノ]ビフェニル(略称:NPB)やN,N’-ビス(3-メチルフェニル)-N,N’-ジフェニル-[1,1’-ビフェニル]-4,4’-ジアミン(略称:TPD)、4-フェニル-4’-(9-フェニルフルオレン-9-イル)トリフェニルアミン(略称:BAFLP)、4,4’-ビス[N-(9,9-ジメチルフルオレン-2-イル)-N-フェニルアミノ]ビフェニル(略称:DFLDPBi)、4,4’,4’’-トリス(N,N-ジフェニルアミノ)トリフェニルアミン(略称:TDATA)、4,4’,4’’-トリス[N-(3-メチルフェニル)-N-フェニルアミノ]トリフェニルアミン(略称:MTDATA)、4,4’-ビス[N-(スピロ-9,9’-ビフルオレン-2-イル)-N―フェニルアミノ]ビフェニル(略称:BSPB)などの芳香族アミン化合物等を用いることができる。ここに述べた物質は、主に10-6cm2/(V・s)以上の正孔移動度を有する物質である。
電子輸送層は、電子輸送性の高い物質を含む層である。電子輸送層には、1)アルミニウム錯体、ベリリウム錯体、亜鉛錯体等の金属錯体、2)イミダゾール誘導体、ベンゾイミダゾール誘導体、アジン誘導体、カルバゾール誘導体、フェナントロリン誘導体等の複素芳香族化合物、3)高分子化合物を使用することができる。具体的には低分子の有機化合物として、Alq、トリス(4-メチル-8-キノリノラト)アルミニウム(略称:Almq3)、ビス(10-ヒドロキシベンゾ[h]キノリナト)ベリリウム(略称:BeBq2)、BAlq、Znq、ZnPBO、ZnBTZなどの金属錯体等を用いることができる。また、金属錯体以外にも、2-(4-ビフェニリル)-5-(4-tert-ブチルフェニル)-1,3,4-オキサジアゾール(略称:PBD)、1,3-ビス[5-(ptert-ブチルフェニル)-1,3,4-オキサジアゾール-2-イル]ベンゼン(略称:OXD-7)、3-(4-tert-ブチルフェニル)-4-フェニル-5-(4-ビフェニリル)-1,2,4-トリアゾール(略称:TAZ)、3-(4-tert-ブチルフェニル)-4-(4-エチルフェニル)-5-(4-ビフェニリル)-1,2,4-トリアゾール(略称:p-EtTAZ)、バソフェナントロリン(略称:BPhen)、バソキュプロイン(略称:BCP)、4,4’-ビス(5-メチルベンゾオキサゾール-2-イル)スチルベン(略称:BzOs)などの複素芳香族化合物も用いることができる。本実施態様においては、ベンゾイミダゾール化合物を好適に用いることができる。ここに述べた物質は、主に10-6cm2/(V・s)以上の電子移動度を有する物質である。なお、正孔輸送性よりも電子輸送性の高い物質であれば、上記以外の物質を電子輸送層として用いてもよい。また、電子輸送層は、単層で構成されていてもよいし、上記物質からなる層が二層以上積層されて構成されていてもよい。
電子注入層は、電子注入性の高い物質を含む層である。電子注入層には、リチウム(Li)、セシウム(Cs)、カルシウム(Ca)、フッ化リチウム(LiF)、フッ化セシウム(CsF)、フッ化カルシウム(CaF2)、リチウム酸化物(LiOx)等のようなアルカリ金属、アルカリ土類金属、またはそれらの化合物を用いることができる。その他、電子輸送性を有する物質にアルカリ金属、アルカリ土類金属、またはそれらの化合物を含有させたもの、具体的にはAlq中にマグネシウム(Mg)を含有させたもの等を用いてもよい。なお、この場合には、陰極からの電子注入をより効率良く行うことができる。
本実施形態の有機EL素子の各層の形成方法としては、上記で特に言及した以外には制限されないが、真空蒸着法、スパッタリング法、プラズマ法、イオンプレーティング法などの乾式成膜法や、スピンコーティング法、ディッピング法、フローコーティング法、インクジェット法などの湿式成膜法などの公知の方法を採用することができる。
本実施形態の有機EL素子の各有機層の膜厚は、上記で特に言及した場合を除いて限定されない。一般に、膜厚が薄すぎるとピンホール等の欠陥が生じやすく、膜厚が厚すぎると高い印加電圧が必要となり効率が悪くなるため、通常、有機EL素子の各有機層の膜厚は、数nmから1μmの範囲が好ましい。
本実施形態に係る有機EL素子においては、前記一般式(1)等で表される第一の化合物を第一のホスト材料として含有する第一の発光層と、前記一般式(2)等で表される第二の化合物を第二のホスト材料として含有する第二の発光層とが、直接、接している。第一の発光層と第二の発光層とをこのように積層させることで、生成した一重項励起子及び三重項励起子を有効に活用でき、その結果、有機EL素子の発光効率を向上させることができる。
(電子機器)
本実施形態に係る電子機器は、上述の実施形態のいずれかの有機EL素子を搭載している。電子機器としては、例えば、表示装置及び発光装置等が挙げられる。表示装置としては、例えば、表示部品(例えば、有機ELパネルモジュール等)、テレビ、携帯電話、タブレット、及びパーソナルコンピュータ等が挙げられる。発光装置としては、例えば、照明及び車両用灯具等が挙げられる。
なお、本発明は、上述の実施形態に限定されず、本発明の目的を達成できる範囲での変更、改良等は、本発明に含まれる。
また、有機EL素子が複数の発光層を有する場合、これらの発光層が互いに隣接して設けられていてもよいし、中間層を介して複数の発光ユニットが積層された、いわゆるタンデム型の有機EL素子であってもよい。
例えば、発光層の陰極側で接して障壁層が配置された場合、当該障壁層は、電子を輸送し、かつ正孔が当該障壁層よりも陰極側の層(例えば、電子輸送層)に到達することを阻止する。有機EL素子が、電子輸送層を含む場合は、発光層と電子輸送層との間に当該障壁層を含むことが好ましい。
また、発光層の陽極側で接して障壁層が配置された場合、当該障壁層は、正孔を輸送し、かつ電子が当該障壁層よりも陽極側の層(例えば、正孔輸送層)に到達することを阻止する。有機EL素子が、正孔輸送層を含む場合は、発光層と正孔輸送層との間に当該障壁層を含むことが好ましい。
また、励起エネルギーが発光層からその周辺層に漏れ出さないように、障壁層を発光層に隣接させて設けてもよい。発光層で生成した励起子が、当該障壁層よりも電極側の層(例えば、電子輸送層及び正孔輸送層等)に移動することを阻止する。
発光層と障壁層とは接合していることが好ましい。
実施例又は参考例に係る有機EL素子の製造に用いた化合物の構造を以下に示す。
有機EL素子を以下のように作製し、評価した。
25mm×75mm×1.1mm厚のITO(Indium Tin Oxide)透明電極(陽極)付きガラス基板(ジオマテック株式会社製)をイソプロピルアルコール中で超音波洗浄を5分間行なった後、UVオゾン洗浄を30分間行なった。ITO透明電極の膜厚は、130nmとした。
洗浄後の透明電極ライン付きガラス基板を真空蒸着装置の基板ホルダーに装着し、まず透明電極ラインが形成されている側の面上に透明電極を覆うようにして化合物HA1を蒸着し、膜厚5nmの正孔注入層(HI)を形成した。
正孔注入層の成膜に続けて化合物HT1を蒸着し、膜厚80nmの第一の正孔輸送層(HT)を成膜した。
第一の正孔輸送層の成膜に続けて化合物HT2を蒸着し、膜厚10nmの第二の正孔輸送層(電子障壁層ともいう)(EBL)を成膜した。
第二の正孔輸送層上に化合物BH1(第一のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚5nmの第一の発光層を成膜した。
第一の発光層上に化合物BH2(第二のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚20nmの第二の発光層を成膜した。
第二の発光層上に化合物ET1を蒸着し、膜厚10nmの第1の電子輸送層(正孔障壁層ともいう)(HBL)を形成した。
第1の電子輸送層上に化合物ET2を蒸着し、膜厚15nmの第2の電子輸送層(ET)を形成した。
第2の電子輸送層上にLiFを蒸着して膜厚1nmの電子注入層を形成した。
電子注入層上に金属Alを蒸着して膜厚80nmの陰極を形成した。
参考例1の素子構成を略式的に示すと、次のとおりである。
ITO(130)/HA1(5)/HT1(80)/HT2(10)/BH1:BD1(5,98%:2%)/BH2:BD1(20,98%:2%)/ET1(10)/ET2(15)/LiF(1)/Al(80)
なお、括弧内の数字は、膜厚(単位:nm)を示す。
同じく括弧内において、パーセント表示された数字(98%:2%)は、第一の発光層又は第二の発光層におけるホスト材料(化合物BH1又は化合物BH2)及び化合物BD1の割合(質量%)を示す。以下、同様の表記とする。
比較参考例1の有機EL素子は、表1に記載のとおり、発光層として膜厚25nmの第一の発光層を形成し、第二の発光層を形成せずに、第一の発光層の上に第1の電子輸送層を形成したこと以外、参考例1と同様にして作製した。
比較参考例2の有機EL素子は、表1に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に発光層として膜厚25nmの第二の発光層を形成したこと以外、参考例1と同様にして作製した。
実施例、比較例、参考例及び比較参考例で作製した有機EL素子について、以下の評価を行った。評価結果を表1~46に示す。
なお、本明細書において、ある実施例の評価結果が複数の表に記載されている場合があり、ある比較例の評価結果が複数の表に記載されている場合があり、ある参考例の評価結果が複数の表に記載されている場合があり、ある比較参考例の評価結果が複数の表に記載されている場合がある。
電流密度が10mA/cm2となるように素子に電圧を印加した時の分光放射輝度スペクトルを分光放射輝度計CS-2000(コニカミノルタ株式会社製)で計測した。得られた分光放射輝度スペクトルから、ランバシアン放射を行ったと仮定し外部量子効率EQE(単位:%)を算出した。
得られた有機EL素子に、電流密度が50mA/cm2となるように電圧を印加し、初期輝度に対して輝度が90%となるまでの時間(LT90(単位:時間))を測定した。
得られた有機EL素子に、電流密度が50mA/cm2となるように電圧を印加し、初期輝度に対して輝度が95%となるまでの時間(LT95(単位:時間))を測定した。
有機EL素子の電流密度が10mA/cm2となるように素子に電圧を印加した時の分光放射輝度スペクトルを分光放射輝度計CS-2000(コニカミノルタ株式会社製)で計測した。得られた分光放射輝度スペクトルから、主ピーク波長λp(単位:nm)を算出した。
電流密度が10mA/cm2となるように陽極と陰極との間に通電したときの電圧(単位:V)を計測した。
電流密度が10mA/cm2となるように素子に電圧を印加した時の分光放射輝度スペクトルを分光放射輝度計CS-2000(コニカミノルタ株式会社製)で計測した。実施例145及び比較例118の有機EL素子について、得られた分光放射輝度スペクトルから、CIEyを算出した。
参考例2~20の有機EL素子は、第一の発光層における化合物BH1(第一のホスト材料)を表2に記載の第一の化合物に変更したこと以外、参考例1と同様にして作製した。
比較参考例3~21の有機EL素子は、第一の発光層における化合物BH1(第一のホスト材料)を表3に記載の第一の化合物に変更したこと以外、比較参考例1と同様にして作製した。
参考例21の有機EL素子は、第二の発光層における化合物BH2(第二のホスト材料)を表4に記載の化合物に変更したこと以外、参考例1と同様にして作製した。
参考例22~23の有機EL素子は、第一の発光層における化合物BH1(第一のホスト材料)及び第二の発光層における化合物BH2(第二のホスト材料)を表4に記載の化合物に変更したこと以外、参考例1と同様にして作製した。
比較参考例22の有機EL素子は、第二の発光層における化合物BH2(第二のホスト材料)を表4に記載の化合物に変更したこと以外、比較参考例2と同様にして作製した。
参考例24の有機EL素子は、第二の発光層における化合物BH2(第二のホスト材料)を表5に記載の化合物に変更したこと以外、参考例1と同様にして作製した。
参考例25~26の有機EL素子は、第一の発光層における化合物BH1(第一のホスト材料)及び第二の発光層における化合物BH2(第二のホスト材料)を表5に記載の化合物に変更したこと以外、参考例1と同様にして作製した。
比較参考例23の有機EL素子は、第二の発光層における化合物BH2(第二のホスト材料)を表5に記載の化合物に変更したこと以外、比較参考例2と同様にして作製した。
参考例27の有機EL素子は、第二の発光層における化合物BH2(第二のホスト材料)を表6に記載の化合物に変更したこと以外、参考例1と同様にして作製した。
参考例28~29の有機EL素子は、第一の発光層における化合物BH1(第一のホスト材料)及び第二の発光層における化合物BH2(第二のホスト材料)を表6に記載の化合物に変更したこと以外、参考例1と同様にして作製した。
比較参考例24の有機EL素子は、第二の発光層における化合物BH2(第二のホスト材料)を表6に記載の化合物に変更したこと以外、比較参考例2と同様にして作製した。
参考例30の有機EL素子は、第二の発光層における化合物BH2(第二のホスト材料)を表7に記載の化合物に変更したこと以外、参考例1と同様にして作製した。
参考例31~32の有機EL素子は、第一の発光層における化合物BH1(第一のホスト材料)及び第二の発光層における化合物BH2(第二のホスト材料)を表7に記載の化合物に変更したこと以外、参考例1と同様にして作製した。
比較参考例25の有機EL素子は、第二の発光層における化合物BH2(第二のホスト材料)を表7に記載の化合物に変更したこと以外、比較参考例2と同様にして作製した。
参考例33の有機EL素子は、第二の発光層における化合物BH2(第二のホスト材料)を表8に記載の化合物に変更したこと以外、参考例1と同様にして作製した。
参考例34~35の有機EL素子は、第一の発光層における化合物BH1(第一のホスト材料)及び第二の発光層における化合物BH2(第二のホスト材料)を表8に記載の化合物に変更したこと以外、参考例1と同様にして作製した。
比較参考例26の有機EL素子は、第二の発光層における化合物BH2(第二のホスト材料)を表8に記載の化合物に変更したこと以外、比較参考例2と同様にして作製した。
参考例36の有機EL素子は、第二の発光層における化合物BH2(第二のホスト材料)を表9に記載の化合物に変更したこと以外、参考例1と同様にして作製した。
参考例37~38の有機EL素子は、第一の発光層における化合物BH1(第一のホスト材料)及び第二の発光層における化合物BH2(第二のホスト材料)を表9に記載の化合物に変更したこと以外、参考例1と同様にして作製した。
比較参考例27の有機EL素子は、第二の発光層における化合物BH2(第二のホスト材料)を表9に記載の化合物に変更したこと以外、比較参考例2と同様にして作製した。
参考例39の有機EL素子は、第二の発光層における化合物BH2(第二のホスト材料)を表10に記載の化合物に変更したこと以外、参考例1と同様にして作製した。
参考例40~41の有機EL素子は、第一の発光層における化合物BH1(第一のホスト材料)及び第二の発光層における化合物BH2(第二のホスト材料)を表10に記載の化合物に変更したこと以外、参考例1と同様にして作製した。
比較参考例28の有機EL素子は、第二の発光層における化合物BH2(第二のホスト材料)を表10に記載の化合物に変更したこと以外、比較参考例2と同様にして作製した。
参考例42の有機EL素子は、第二の発光層における化合物BH2(第二のホスト材料)を表11に記載の化合物に変更したこと以外、参考例1と同様にして作製した。
参考例43~44の有機EL素子は、第一の発光層における化合物BH1(第一のホスト材料)及び第二の発光層における化合物BH2(第二のホスト材料)を表11に記載の化合物に変更したこと以外、参考例1と同様にして作製した。
比較参考例29の有機EL素子は、第二の発光層における化合物BH2(第二のホスト材料)を表11に記載の化合物に変更したこと以外、比較参考例2と同様にして作製した。
参考例45の有機EL素子は、第一の発光層における化合物BD1、並びに第二の発光層における化合物BD1を表12に記載の化合物に変更したこと以外、参考例1と同様にして作製した。
参考例46~47の有機EL素子は、第一の発光層における化合物BH1(第一のホスト材料)及び化合物BD1、並びに第二の発光層における化合物BD1を表12に記載の化合物に変更したこと以外、参考例1と同様にして作製した。
比較参考例30の有機EL素子は、第一の発光層における化合物BD1を表12に記載の化合物に変更したこと以外、比較参考例1と同様にして作製した。
比較参考例31の有機EL素子は、第二の発光層における化合物BD1を表12に記載の化合物に変更したこと以外、比較参考例2と同様にして作製した。
参考例48の有機EL素子は、第一の発光層における化合物BD1、並びに第二の発光層における化合物BD1を表13に記載の化合物に変更したこと以外、参考例1と同様にして作製した。
参考例49~50の有機EL素子は、第一の発光層における化合物BH1(第一のホスト材料)及び化合物BD1、並びに第二の発光層における化合物BD1を表13に記載の化合物に変更したこと以外、参考例1と同様にして作製した。
比較参考例32の有機EL素子は、第一の発光層における化合物BD1を表13に記載の化合物に変更したこと以外、比較参考例1と同様にして作製した。
比較参考例33の有機EL素子は、第二の発光層における化合物BD1を表13に記載の化合物に変更したこと以外、比較参考例2と同様にして作製した。
実施例51~68の有機EL素子は、第一の発光層における化合物BH1(第一のホスト材料)を表14に記載の化合物に変更したこと以外、参考例1と同様にして作製した。
比較例C69の有機EL素子は、第一の発光層における化合物BH1(第一のホスト材料)を表14に記載の化合物に変更したこと以外、参考例1と同様にして作製した。
比較例34~51の有機EL素子は、第一の発光層における化合物BH1(第一のホスト材料)を表15に記載の化合物に変更したこと以外、比較参考例1と同様にして作製した。
有機EL素子を以下のように作製し、評価した。
25mm×75mm×1.1mm厚のITO(Indium Tin Oxide)透明電極(陽極)付きガラス基板(ジオマテック株式会社製)をイソプロピルアルコール中で超音波洗浄を5分間行なった後、UVオゾン洗浄を30分間行なった。ITO透明電極の膜厚は、130nmとした。
洗浄後の透明電極ライン付きガラス基板を真空蒸着装置の基板ホルダーに装着し、まず透明電極ラインが形成されている側の面上に透明電極を覆うようにして化合物HA1を蒸着し、膜厚5nmの正孔注入層(HI)を形成した。
正孔注入層の成膜に続けて化合物HT3を蒸着し、膜厚80nmの第一の正孔輸送層(HT)を成膜した。
第一の正孔輸送層の成膜に続けて化合物HT4を蒸着し、膜厚10nmの第二の正孔輸送層(電子障壁層ともいう)(EBL)を成膜した。
第二の正孔輸送層上に化合物BH1-21(第一のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚5nmの第一の発光層を成膜した。
第一の発光層上に化合物BH2(第二のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚20nmの第二の発光層を成膜した。
第二の発光層上に化合物ET4を蒸着し、膜厚10nmの第1の電子輸送層(正孔障壁層ともいう)(HBL)を形成した。
第1の電子輸送層上に化合物ET2を蒸着し、膜厚15nmの第2の電子輸送層(ET)を形成した。
第2の電子輸送層上にLiFを蒸着して膜厚1nmの電子注入層を形成した。
電子注入層上に金属Alを蒸着して膜厚80nmの陰極を形成した。
実施例70の素子構成を略式的に示すと、次のとおりである。
ITO(130)/HA1(5)/HT3(80)/HT4(10)/BH1-21:BD1(5,98%:2%)/BH2:BD1(20,98%:2%)/ET4(10)/ET2(15)/LiF(1)/Al(80)
なお、括弧内の数字は、膜厚(単位:nm)を示す。
同じく括弧内において、パーセント表示された数字(98%:2%)は、第一の発光層又は第二の発光層におけるホスト材料(化合物BH1-21又は化合物BH2)及び化合物BD1の割合(質量%)を示す。以下、同様の表記とする。
実施例71~77の有機EL素子は、第一の発光層における化合物BH1-21(第一のホスト材料)を表16に記載の第一の化合物に変更したこと以外、実施例70と同様にして作製した。
比較例C78の有機EL素子は、第一の発光層における化合物BH1-21(第一のホスト材料)を表16に記載の第一の化合物に変更したこと以外、実施例70と同様にして作製した。
比較例52~59の有機EL素子は、発光層として膜厚25nmの第一の発光層を形成し、第二の発光層を形成せずに、第一の発光層の上に第1の電子輸送層を形成したこと、並びに、第一の発光層における第一の化合物(第一のホスト材料)を表16に記載の第一の化合物に変更したこと以外、実施例70と同様にして作製した。
比較例60の有機EL素子は、表16に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと以外、実施例70と同様にして作製した。
有機EL素子を以下のように作製し、評価した。
25mm×75mm×1.1mm厚のITO(Indium Tin Oxide)透明電極(陽極)付きガラス基板(ジオマテック株式会社製)をイソプロピルアルコール中で超音波洗浄を5分間行なった後、UVオゾン洗浄を30分間行なった。ITO透明電極の膜厚は、130nmとした。
洗浄後の透明電極ライン付きガラス基板を真空蒸着装置の基板ホルダーに装着し、まず透明電極ラインが形成されている側の面上に透明電極を覆うようにして化合物HA1を蒸着し、膜厚5nmの正孔注入層(HI)を形成した。
正孔注入層の成膜に続けて化合物HT3を蒸着し、膜厚80nmの第一の正孔輸送層(HT)を成膜した。
第一の正孔輸送層の成膜に続けて化合物HT4を蒸着し、膜厚10nmの第二の正孔輸送層(電子障壁層ともいう)(EBL)を成膜した。
第二の正孔輸送層上に化合物BH1-29(第一のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚5nmの第一の発光層を成膜した。
第一の発光層上に化合物BH2(第二のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚20nmの第二の発光層を成膜した。
第二の発光層上に化合物ET3を蒸着し、膜厚10nmの第1の電子輸送層(正孔障壁層ともいう)(HBL)を形成した。
第1の電子輸送層上に化合物ET2を蒸着し、膜厚15nmの第2の電子輸送層(ET)を形成した。
第2の電子輸送層上にLiFを蒸着して膜厚1nmの電子注入層を形成した。
電子注入層上に金属Alを蒸着して膜厚80nmの陰極を形成した。
実施例79の素子構成を略式的に示すと、次のとおりである。
ITO(130)/HA1(5)/HT3(80)/HT4(10)/BH1-29:BD1(5,98%:2%)/BH2:BD1(20,98%:2%)/ET3(10)/ET2(15)/LiF(1)/Al(80)
なお、括弧内の数字は、膜厚(単位:nm)を示す。
同じく括弧内において、パーセント表示された数字(98%:2%)は、第一の発光層又は第二の発光層におけるホスト材料(化合物BH1-29又は化合物BH2)及び化合物BD1の割合(質量%)を示す。以下、同様の表記とする。
実施例80~89の有機EL素子は、第一の発光層における化合物BH1-29(第一のホスト材料)を表17に記載の第一の化合物に変更したこと以外、実施例79と同様にして作製した。
比較例C90の有機EL素子は、第一の発光層における化合物BH1-29(第一のホスト材料)を表17に記載の第一の化合物に変更したこと以外、実施例79と同様にして作製した。
比較例61~71の有機EL素子は、発光層として膜厚25nmの第一の発光層を形成し、第二の発光層を形成せずに、第一の発光層の上に第1の電子輸送層を形成したこと、並びに、第一の発光層における第一の化合物(第一のホスト材料)を表17に記載の第一の化合物に変更したこと以外、実施例79と同様にして作製した。
比較例72の有機EL素子は、表17に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと以外、実施例79と同様にして作製した。
有機EL素子を以下のように作製し、評価した。
25mm×75mm×1.1mm厚のITO(Indium Tin Oxide)透明電極(陽極)付きガラス基板(ジオマテック株式会社製)をイソプロピルアルコール中で超音波洗浄を5分間行なった後、UVオゾン洗浄を30分間行なった。ITO透明電極の膜厚は、130nmとした。
洗浄後の透明電極ライン付きガラス基板を真空蒸着装置の基板ホルダーに装着し、まず透明電極ラインが形成されている側の面上に透明電極を覆うようにして、化合物HT5及び化合物HA2を共蒸着し、膜厚10nmの正孔注入層(HI)を形成した。この正孔注入層中の化合物HT5の割合を97質量%とし、化合物HA2の割合を3質量%とした。
正孔注入層の成膜に続けて化合物HT5を蒸着し、膜厚85nmの第一の正孔輸送層(HT)を成膜した。
第一の正孔輸送層の成膜に続けて化合物HT4を蒸着し、膜厚5nmの第二の正孔輸送層(電子障壁層ともいう)(EBL)を成膜した。
第二の正孔輸送層上に化合物BH1-61(第一のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚5nmの第一の発光層を成膜した。
第一の発光層上に化合物BH2(第二のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚20nmの第二の発光層を成膜した。
第二の発光層上に化合物ET3を蒸着し、膜厚5nmの第1の電子輸送層(正孔障壁層ともいう)(HBL)を形成した。
第1の電子輸送層(HBL)上に化合物ET6及び化合物Liqを共蒸着し、膜厚25nmの電子輸送層(ET)を形成した。この電子輸送層(ET)の化合物ET6の割合を50質量%とし、化合物Liqの割合を50質量%とした。なお、Liqは、(8-キノリノラト)リチウム((8-Quinolinolato)lithium)の略称である。
第2の電子輸送層上にLiqを蒸着して膜厚1nmの電子注入層を形成した。
電子注入層上に金属Alを蒸着して膜厚80nmの陰極を形成した。
参考例91の素子構成を略式的に示すと、次のとおりである。
ITO(130)/HT5:HA2(10,97%:3%)/HT5(85)/HT4(5)/BH1-61:BD1(5,98%:2%)/BH2:BD1(20,98%:2%)/ET3(5)/ET6:Liq(25,50%:50%)/Liq(1)/Al(80)
なお、括弧内の数字は、膜厚(単位:nm)を示す。
同じく括弧内において、パーセント表示された数字(97%:3%)は、正孔注入層における化合物HT5及び化合物HA2の割合(質量%)を示し、パーセント表示された数字(98%:2%)は、第一の発光層又は第二の発光層におけるホスト材料(化合物BH1-61又はBH2)及びドーパント材料(化合物BD1)の割合(質量%)を示し、パーセント表示された数字(50%:50%)は、電子輸送層(ET)における化合物ET6及び化合物Liqの割合(質量%)を示す。以下、同様の表記とする。
参考例92~95の有機EL素子は、第一の発光層における化合物BH1-61(第一のホスト材料)を表18に記載の第一の化合物に変更したこと以外、参考例91と同様にして作製した。
比較参考例73~76の有機EL素子は、発光層として膜厚25nmの第一の発光層を形成し、第二の発光層を形成せずに、第一の発光層の上に第1の電子輸送層を形成したこと、並びに、第一の発光層における第一の化合物(第一のホスト材料)を表18に記載の第一の化合物に変更したこと以外、参考例91と同様にして作製した。
比較参考例77の有機EL素子は、表18に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと以外、参考例91と同様にして作製した。
有機EL素子を以下のように作製し、評価した。
25mm×75mm×1.1mm厚のITO(Indium Tin Oxide)透明電極(陽極)付きガラス基板(ジオマテック株式会社製)をイソプロピルアルコール中で超音波洗浄を5分間行なった後、UVオゾン洗浄を30分間行なった。ITO透明電極の膜厚は、130nmとした。
洗浄後の透明電極ライン付きガラス基板を真空蒸着装置の基板ホルダーに装着し、まず透明電極ラインが形成されている側の面上に透明電極を覆うようにして、化合物HT3及び化合物HA2を共蒸着し、膜厚10nmの正孔注入層(HI)を形成した。この正孔注入層中の化合物HT3の割合を97質量%とし、化合物HA2の割合を3質量%とした。
正孔注入層の成膜に続けて化合物HT3を蒸着し、膜厚85nmの第一の正孔輸送層(HT)を成膜した。
第一の正孔輸送層の成膜に続けて化合物HT4を蒸着し、膜厚5nmの第二の正孔輸送層(電子障壁層ともいう)(EBL)を成膜した。
第二の正孔輸送層上に化合物BH1-75(第一のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚5nmの第一の発光層を成膜した。
第一の発光層上に化合物BH2(第二のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚20nmの第二の発光層を成膜した。
第二の発光層上に化合物ET3を蒸着し、膜厚5nmの第1の電子輸送層(正孔障壁層ともいう)(HBL)を形成した。
第1の電子輸送層(HBL)上に化合物ET8及び化合物Liqを共蒸着し、膜厚25nmの電子輸送層(ET)を形成した。この電子輸送層(ET)の化合物ET5の割合を50質量%とし、化合物Liqの割合を50質量%とした。なお、Liqは、(8-キノリノラト)リチウム((8-Quinolinolato)lithium)の略称である。
第2の電子輸送層上にLiqを蒸着して膜厚1nmの電子注入層を形成した。
電子注入層上に金属Alを蒸着して膜厚80nmの陰極を形成した。
参考例96の素子構成を略式的に示すと、次のとおりである。
ITO(130)/HT3:HA2(10,97%:3%)/HT3(85)/HT4(5)/BH1-75:BD1(5,98%:2%)/BH2:BD1(20,98%:2%)/ET3(5)/ET8:Liq(25,50%:50%)/Liq(1)/Al(80)
なお、括弧内の数字は、膜厚(単位:nm)を示す。
同じく括弧内において、パーセント表示された数字(97%:3%)は、正孔注入層における化合物HT3及び化合物HA2の割合(質量%)を示し、パーセント表示された数字(98%:2%)は、第一の発光層又は第二の発光層におけるホスト材料(化合物BH1-75又はBH2)及びドーパント材料(化合物BD1)の割合(質量%)を示し、パーセント表示された数字(50%:50%)は、電子輸送層(ET)における化合物ET8及び化合物Liqの割合(質量%)を示す。以下、同様の表記とする。
参考例97の有機EL素子は、第一の発光層における化合物BH1-75(第一のホスト材料)を表19に記載の第一の化合物に変更したこと以外、参考例96と同様にして作製した。
比較参考例78の有機EL素子は、発光層として膜厚25nmの第一の発光層を形成し、第二の発光層を形成せずに、第一の発光層の上に第1の電子輸送層を形成したこと、並びに、第一の発光層における第一の化合物(第一のホスト材料)を表19に記載の第一の化合物に変更したこと以外、参考例96と同様にして作製した。
比較参考例79の有機EL素子は、表19に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと以外、参考例96と同様にして作製した。
有機EL素子を以下のように作製し、評価した。
25mm×75mm×1.1mm厚のITO(Indium Tin Oxide)透明電極(陽極)付きガラス基板(ジオマテック株式会社製)をイソプロピルアルコール中で超音波洗浄を5分間行なった後、UVオゾン洗浄を30分間行なった。ITO透明電極の膜厚は、130nmとした。
洗浄後の透明電極ライン付きガラス基板を真空蒸着装置の基板ホルダーに装着し、まず透明電極ラインが形成されている側の面上に透明電極を覆うようにして、化合物HT5及び化合物HA2を共蒸着し、膜厚10nmの正孔注入層(HI)を形成した。この正孔注入層中の化合物HT5の割合を97質量%とし、化合物HA2の割合を3質量%とした。
正孔注入層の成膜に続けて化合物HT5を蒸着し、膜厚85nmの第一の正孔輸送層(HT)を成膜した。
第一の正孔輸送層の成膜に続けて化合物HT4を蒸着し、膜厚5nmの第二の正孔輸送層(電子障壁層ともいう)(EBL)を成膜した。
第二の正孔輸送層上に化合物BH1-64(第一のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚5nmの第一の発光層を成膜した。
第一の発光層上に化合物BH2(第二のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚20nmの第二の発光層を成膜した。
第二の発光層上に化合物ET3を蒸着し、膜厚5nmの第1の電子輸送層(正孔障壁層ともいう)(HBL)を形成した。
第1の電子輸送層(HBL)上に化合物ET8及び化合物Liqを共蒸着し、膜厚25nmの電子輸送層(ET)を形成した。この電子輸送層(ET)の化合物ET8の割合を50質量%とし、化合物Liqの割合を50質量%とした。
第2の電子輸送層上にLiqを蒸着して膜厚1nmの電子注入層を形成した。
電子注入層上に金属Alを蒸着して膜厚80nmの陰極を形成した。
参考例98の素子構成を略式的に示すと、次のとおりである。
ITO(130)/HT5:HA2(10,97%:3%)/HT5(85)/HT4(5)/BH1-64:BD1(5,98%:2%)/BH2:BD1(20,98%:2%)/ET3(5)/ET8:Liq(25,50%:50%)/Liq(1)/Al(80)
なお、括弧内の数字は、膜厚(単位:nm)を示す。
同じく括弧内において、パーセント表示された数字(97%:3%)は、正孔注入層における化合物HT5及び化合物HA2の割合(質量%)を示し、パーセント表示された数字(98%:2%)は、第一の発光層又は第二の発光層におけるホスト材料(化合物BH1-64又はBH2)及びドーパント材料(化合物BD1)の割合(質量%)を示し、パーセント表示された数字(50%:50%)は、電子輸送層(ET)における化合物ET8及び化合物Liqの割合(質量%)を示す。以下、同様の表記とする。
参考例99~103の有機EL素子は、第一の発光層における化合物BH1-64(第一のホスト材料)を表20に記載の第一の化合物に変更したこと以外、参考例98と同様にして作製した。
比較参考例80~84の有機EL素子は、発光層として膜厚25nmの第一の発光層を形成し、第二の発光層を形成せずに、第一の発光層の上に第1の電子輸送層を形成したこと、並びに、第一の発光層における第一の化合物(第一のホスト材料)を表20に記載の第一の化合物に変更したこと以外、参考例98と同様にして作製した。
比較参考例85の有機EL素子は、表20に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと以外、参考例98と同様にして作製した。
有機EL素子を以下のように作製し、評価した。
25mm×75mm×1.1mm厚のITO(Indium Tin Oxide)透明電極(陽極)付きガラス基板(ジオマテック株式会社製)をイソプロピルアルコール中で超音波洗浄を5分間行なった後、UVオゾン洗浄を30分間行なった。ITO透明電極の膜厚は、130nmとした。
洗浄後の透明電極ライン付きガラス基板を真空蒸着装置の基板ホルダーに装着し、まず透明電極ラインが形成されている側の面上に透明電極を覆うようにして、化合物HT5及び化合物HA2を共蒸着し、膜厚10nmの正孔注入層(HI)を形成した。この正孔注入層中の化合物HT5の割合を97質量%とし、化合物HA2の割合を3質量%とした。
正孔注入層の成膜に続けて化合物HT5を蒸着し、膜厚85nmの第一の正孔輸送層(HT)を成膜した。
第一の正孔輸送層の成膜に続けて化合物HT4を蒸着し、膜厚5nmの第二の正孔輸送層(電子障壁層ともいう)(EBL)を成膜した。
第二の正孔輸送層上に化合物BH1-70(第一のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚5nmの第一の発光層を成膜した。
第一の発光層上に化合物BH2(第二のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚20nmの第二の発光層を成膜した。
第二の発光層上に化合物ET1を蒸着し、膜厚5nmの第1の電子輸送層(正孔障壁層ともいう)(HBL)を形成した。
第1の電子輸送層(HBL)上に化合物ET6及び化合物Liqを共蒸着し、膜厚25nmの電子輸送層(ET)を形成した。この電子輸送層(ET)の化合物ET6の割合を50質量%とし、化合物Liqの割合を50質量%とした。
第2の電子輸送層上にLiqを蒸着して膜厚1nmの電子注入層を形成した。
電子注入層上に金属Alを蒸着して膜厚80nmの陰極を形成した。
実施例104の素子構成を略式的に示すと、次のとおりである。
ITO(130)/HT5:HA2(10,97%:3%)/HT5(85)/HT4(5)/BH1-70:BD1(5,98%:2%)/BH2:BD1(20,98%:2%)/ET1(5)/ET6:Liq(25,50%:50%)/Liq(1)/Al(80)
なお、括弧内の数字は、膜厚(単位:nm)を示す。
同じく括弧内において、パーセント表示された数字(97%:3%)は、正孔注入層における化合物HT5及び化合物HA2の割合(質量%)を示し、パーセント表示された数字(98%:2%)は、第一の発光層又は第二の発光層におけるホスト材料(化合物BH1-70又はBH2)及びドーパント材料(化合物BD1)の割合(質量%)を示し、パーセント表示された数字(50%:50%)は、電子輸送層(ET)における化合物ET6及び化合物Liqの割合(質量%)を示す。以下、同様の表記とする。
実施例105~108の有機EL素子は、第一の発光層における化合物BH1-70(第一のホスト材料)を表21に記載の第一の化合物に変更したこと以外、実施例104と同様にして作製した。
比較例C109の有機EL素子は、第一の発光層における化合物BH1-70(第一のホスト材料)を表21に記載の第一の化合物に変更したこと以外、実施例104と同様にして作製した。
比較例86~90の有機EL素子は、発光層として膜厚25nmの第一の発光層を形成し、第二の発光層を形成せずに、第一の発光層の上に第1の電子輸送層を形成したこと、並びに、第一の発光層における第一の化合物(第一のホスト材料)を表21に記載の第一の化合物に変更したこと以外、実施例104と同様にして作製した。
比較例91の有機EL素子は、表21に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと以外、実施例104と同様にして作製した。
25mm×75mm×1.1mm厚のITO(Indium Tin Oxide)透明電極(陽極)付きガラス基板(ジオマテック株式会社製)をイソプロピルアルコール中で超音波洗浄を5分間行なった後、UVオゾン洗浄を30分間行なった。ITO透明電極の膜厚は、130nmとした。
洗浄後の透明電極ライン付きガラス基板を真空蒸着装置の基板ホルダーに装着し、まず透明電極ラインが形成されている側の面上に透明電極を覆うようにして化合物HA1を蒸着し、膜厚5nmの正孔注入層(HI)を形成した。
正孔注入層の成膜に続けて化合物HT1を蒸着し、膜厚80nmの第一の正孔輸送層(HT)を成膜した。
第一の正孔輸送層の成膜に続けて化合物HT8を蒸着し、膜厚10nmの第二の正孔輸送層(電子障壁層ともいう)(EBL)を成膜した。
第二の正孔輸送層上に化合物BH1-81(第一のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚5nmの第一の発光層を成膜した。
第一の発光層上に化合物BH2(第二のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚20nmの第二の発光層を成膜した。
第二の発光層上に化合物ET1を蒸着し、膜厚10nmの第1の電子輸送層(正孔障壁層ともいう)(HBL)を形成した。
第1の電子輸送層上に化合物ET2を蒸着し、膜厚15nmの第2の電子輸送層(ET)を形成した。
第2の電子輸送層上にLiFを蒸着して膜厚1nmの電子注入層を形成した。
電子注入層上に金属Alを蒸着して膜厚80nmの陰極を形成した。
参考例110の素子構成を略式的に示すと、次のとおりである。
ITO(130)/HA1(5)/HT1(80)/HT8(10)/BH1-81:BD1(5,98%:2%)/BH2:BD1(20,98%:2%)/ET1(10)/ET2(15)/LiF(1)/Al(80)
なお、括弧内の数字は、膜厚(単位:nm)を示す。
同じく括弧内において、パーセント表示された数字(98%:2%)は、第一の発光層又は第二の発光層におけるホスト材料(化合物BH1-81又は化合物BH2)及び化合物BD1の割合(質量%)を示す。以下、同様の表記とする。
参考例111の有機EL素子は、第一の発光層における化合物BH1-81(第一のホスト材料)を表22に記載の第一の化合物に変更したこと以外、参考例110と同様にして作製した。
比較参考例92の有機EL素子は、発光層として膜厚25nmの第一の発光層を形成し、第二の発光層を形成せずに、第一の発光層の上に第1の電子輸送層を形成したこと以外、参考例110と同様にして作製した。
比較参考例93の有機EL素子は、表22に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと以外、参考例110と同様にして作製した。
参考例112~113の有機EL素子は、第一の発光層における化合物BH1(第一のホスト材料)を表23に記載の化合物に変更したこと以外、参考例1と同様にして作製した。
比較参考例94の有機EL素子は、第一の発光層における化合物BH1(第一のホスト材料)を表23に記載の化合物に変更したこと以外、比較参考例1と同様にして作製した。
25mm×75mm×1.1mm厚のITO(Indium Tin Oxide)透明電極(陽極)付きガラス基板(ジオマテック株式会社製)をイソプロピルアルコール中で超音波洗浄を5分間行なった後、UVオゾン洗浄を30分間行なった。ITO透明電極の膜厚は、130nmとした。
洗浄後の透明電極ライン付きガラス基板を真空蒸着装置の基板ホルダーに装着し、まず透明電極ラインが形成されている側の面上に透明電極を覆うようにして化合物HA1を蒸着し、膜厚5nmの正孔注入層(HI)を形成した。
正孔注入層の成膜に続けて化合物HT1を蒸着し、膜厚80nmの第一の正孔輸送層(HT)を成膜した。
第一の正孔輸送層の成膜に続けて化合物HT2を蒸着し、膜厚10nmの第二の正孔輸送層(電子障壁層ともいう)(EBL)を成膜した。
第二の正孔輸送層上に化合物BH1-83(第一のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚5nmの第一の発光層を成膜した。
第一の発光層上に化合物BH2(第二のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚20nmの第二の発光層を成膜した。
第二の発光層上に化合物ET7を蒸着し、膜厚10nmの第1の電子輸送層(正孔障壁層ともいう)(HBL)を形成した。
第1の電子輸送層上に化合物ET2を蒸着し、膜厚15nmの第2の電子輸送層(ET)を形成した。
第2の電子輸送層上にLiFを蒸着して膜厚1nmの電子注入層を形成した。
電子注入層上に金属Alを蒸着して膜厚80nmの陰極を形成した。
参考例114の素子構成を略式的に示すと、次のとおりである。
ITO(130)/HA1(5)/HT1(80)/HT2(10)/BH1-83:BD1(5,98%:2%)/BH2:BD1(20,98%:2%)/ET7(10)/ET2(15)/LiF(1)/Al(80)
なお、括弧内の数字は、膜厚(単位:nm)を示す。
同じく括弧内において、パーセント表示された数字(98%:2%)は、第一の発光層又は第二の発光層におけるホスト材料(化合物BH1-83又は化合物BH2)及び化合物BD1の割合(質量%)を示す。以下、同様の表記とする。
参考例115の有機EL素子は、第一の発光層における化合物BH1-83(第一のホスト材料)を表24に記載の第一の化合物に変更したこと以外、参考例114と同様にして作製した。
比較参考例95の有機EL素子は、発光層として膜厚25nmの第一の発光層を形成し、第二の発光層を形成せずに、第一の発光層の上に第1の電子輸送層を形成したこと以外、参考例114と同様にして作製した。
比較参考例96の有機EL素子は、表24に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと以外、参考例114と同様にして作製した。
〔参考例116〕
25mm×75mm×1.1mm厚のITO(Indium Tin Oxide)透明電極(陽極)付きガラス基板(ジオマテック株式会社製)をイソプロピルアルコール中で超音波洗浄を5分間行なった後、UVオゾン洗浄を30分間行なった。ITO透明電極の膜厚は、130nmとした。
洗浄後の透明電極ライン付きガラス基板を真空蒸着装置の基板ホルダーに装着し、まず透明電極ラインが形成されている側の面上に透明電極を覆うようにして化合物HA1を蒸着し、膜厚5nmの正孔注入層(HI)を形成した。
正孔注入層の成膜に続けて化合物HT1を蒸着し、膜厚80nmの第一の正孔輸送層(HT)を成膜した。
第一の正孔輸送層の成膜に続けて化合物HT4を蒸着し、膜厚10nmの第二の正孔輸送層(電子障壁層ともいう)(EBL)を成膜した。
第二の正孔輸送層上に化合物BH1(第一のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚5nmの第一の発光層を成膜した。
第一の発光層上に化合物BH2-8(第二のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚20nmの第二の発光層を成膜した。
第二の発光層上に化合物ET1を蒸着し、膜厚10nmの第1の電子輸送層(正孔障壁層ともいう)(HBL)を形成した。
第1の電子輸送層上に化合物ET2を蒸着し、膜厚20nmの第2の電子輸送層(ET)を形成した。
第2の電子輸送層上にLiFを蒸着して膜厚1nmの電子注入層を形成した。
電子注入層上に金属Alを蒸着して膜厚80nmの陰極を形成した。
参考例116の素子構成を略式的に示すと、次のとおりである。
ITO(130)/HA1(5)/HT1(80)/HT4(10)/BH1:BD1(5,98%:2%)/BH2-8:BD1(20,98%:2%)/ET1(10)/ET2(20)/LiF(1)/Al(80)
なお、括弧内の数字は、膜厚(単位:nm)を示す。
同じく括弧内において、パーセント表示された数字(98%:2%)は、第一の発光層におけるホスト材料(化合物BH1)及び化合物BD1の割合(質量%)を示し、又はパーセント表示された数字(98%:2%)は、第二の発光層におけるホスト材料(化合物BH2-8)及び化合物BD1の割合(質量%)を示す。以下、同様の表記とする。
参考例117の有機EL素子は、第二の発光層における化合物BH2-8(第二のホスト材料)を表25に記載の第二の化合物に変更したこと以外、参考例116と同様にして作製した。
比較参考例97の有機EL素子は、表25に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと、並びに第二の発光層における第二の化合物(第二のホスト材料)を表25に記載の第二の化合物に変更したこと以外、参考例116と同様にして作製した。
参考例118~119の有機EL素子は、第二の発光層における化合物BH2-8(第二のホスト材料)を表26に記載の第二の化合物に変更したこと以外、参考例116と同様にして作製した。
比較参考例98の有機EL素子は、表26に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと、並びに第二の発光層における第二の化合物(第二のホスト材料)を表26に記載の第二の化合物に変更したこと以外、参考例116と同様にして作製した。
参考例120の有機EL素子は、第二の発光層における化合物BH2-8(第二のホスト材料)を表27に記載の第二の化合物に変更したこと以外、参考例116と同様にして作製した。
比較参考例99の有機EL素子は、表27に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと、並びに第二の発光層における第二の化合物(第二のホスト材料)を表27に記載の第二の化合物に変更したこと以外、参考例116と同様にして作製した。
〔参考例121〕
25mm×75mm×1.1mm厚のITO(Indium Tin Oxide)透明電極(陽極)付きガラス基板(ジオマテック株式会社製)をイソプロピルアルコール中で超音波洗浄を5分間行なった後、UVオゾン洗浄を30分間行なった。ITO透明電極の膜厚は、130nmとした。
洗浄後の透明電極ライン付きガラス基板を真空蒸着装置の基板ホルダーに装着し、まず透明電極ラインが形成されている側の面上に透明電極を覆うようにして化合物HA1を蒸着し、膜厚5nmの正孔注入層(HI)を形成した。
正孔注入層の成膜に続けて化合物HT3を蒸着し、膜厚80nmの第一の正孔輸送層(HT)を成膜した。
第一の正孔輸送層の成膜に続けて化合物HT4を蒸着し、膜厚10nmの第二の正孔輸送層(電子障壁層ともいう)(EBL)を成膜した。
第二の正孔輸送層上に化合物BH1(第一のホスト材料(BH))及び化合物BD2(ドーパント材料(BD))を、化合物BD2の割合が2質量%となるように共蒸着し、膜厚5nmの第一の発光層を成膜した。
第一の発光層上に化合物BH2-2(第二のホスト材料(BH))及び化合物BD2(ドーパント材料(BD))を、化合物BD2の割合が2質量%となるように共蒸着し、膜厚20nmの第二の発光層を成膜した。
第二の発光層上に化合物ET7を蒸着し、膜厚10nmの第1の電子輸送層(正孔障壁層ともいう)(HBL)を形成した。
第1の電子輸送層上に化合物ET2を蒸着し、膜厚20nmの第2の電子輸送層(ET)を形成した。
第2の電子輸送層上にLiFを蒸着して膜厚1nmの電子注入層を形成した。
電子注入層上に金属Alを蒸着して膜厚80nmの陰極を形成した。
参考例121の素子構成を略式的に示すと、次のとおりである。
ITO(130)/HA1(5)/HT3(80)/HT4(10)/BH1:BD2(5,98%:2%)/BH2-2:BD2(20,98%:2%)/ET7(10)/ET2(20)/LiF(1)/Al(80)
なお、括弧内の数字は、膜厚(単位:nm)を示す。
同じく括弧内において、パーセント表示された数字(98%:2%)は、第一の発光層におけるホスト材料(化合物BH1)及び化合物BD2の割合(質量%)を示し、又はパーセント表示された数字(98%:2%)は、第二の発光層におけるホスト材料(化合物BH2-2)及び化合物BD2の割合(質量%)を示す。以下、同様の表記とする。
参考例122の有機EL素子は、第二の発光層における化合物BH2-2(第二のホスト材料)を表28に記載の第二の化合物に変更したこと以外、参考例121と同様にして作製した。
比較参考例100の有機EL素子は、表28に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと、並びに第二の発光層における第二の化合物(第二のホスト材料)を表28に記載の第二の化合物に変更したこと以外、参考例121と同様にして作製した。
〔参考例123〕
25mm×75mm×1.1mm厚のITO(Indium Tin Oxide)透明電極(陽極)付きガラス基板(ジオマテック株式会社製)をイソプロピルアルコール中で超音波洗浄を5分間行なった後、UVオゾン洗浄を30分間行なった。ITO透明電極の膜厚は、130nmとした。
洗浄後の透明電極ライン付きガラス基板を真空蒸着装置の基板ホルダーに装着し、まず透明電極ラインが形成されている側の面上に透明電極を覆うようにして化合物HA1を蒸着し、膜厚5nmの正孔注入層(HI)を形成した。
正孔注入層の成膜に続けて化合物HT5を蒸着し、膜厚80nmの第一の正孔輸送層(HT)を成膜した。
第一の正孔輸送層の成膜に続けて化合物HT6を蒸着し、膜厚10nmの第二の正孔輸送層(電子障壁層ともいう)(EBL)を成膜した。
第二の正孔輸送層上に化合物BH1-10(第一のホスト材料(BH))及び化合物BD2(ドーパント材料(BD))を、化合物BD2の割合が2質量%となるように共蒸着し、膜厚5nmの第一の発光層を成膜した。
第一の発光層上に化合物BH2-2(第二のホスト材料(BH))及び化合物BD2(ドーパント材料(BD))を、化合物BD2の割合が2質量%となるように共蒸着し、膜厚20nmの第二の発光層を成膜した。
第二の発光層上に化合物ET7を蒸着し、膜厚10nmの第1の電子輸送層(正孔障壁層ともいう)(HBL)を形成した。
第1の電子輸送層上に化合物ET2を蒸着し、膜厚20nmの第2の電子輸送層(ET)を形成した。
第2の電子輸送層上にLiFを蒸着して膜厚1nmの電子注入層を形成した。
電子注入層上に金属Alを蒸着して膜厚80nmの陰極を形成した。
参考例123の素子構成を略式的に示すと、次のとおりである。
ITO(130)/HA1(5)/HT5(80)/HT6(10)/BH1-10:BD2(5,98%:2%)/BH2-2:BD2(20,98%:2%)/ET7(10)/ET2(20)/LiF(1)/Al(80)
なお、括弧内の数字は、膜厚(単位:nm)を示す。
同じく括弧内において、パーセント表示された数字(98%:2%)は、第一の発光層におけるホスト材料(化合物BH1-10)及び化合物BD2の割合(質量%)を示し、又はパーセント表示された数字(98%:2%)は、第二の発光層におけるホスト材料(化合物BH2-2)及び化合物BD2の割合(質量%)を示す。以下、同様の表記とする。
参考例124の有機EL素子は、第二の発光層における化合物BH2-2(第二のホスト材料)を表29に記載の第二の化合物に変更したこと以外、参考例123と同様にして作製した。
比較参考例101の有機EL素子は、表29に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと、並びに第二の発光層における第二の化合物(第二のホスト材料)を表29に記載の第二の化合物に変更したこと以外、参考例123と同様にして作製した。
〔参考例125〕
25mm×75mm×1.1mm厚のITO(Indium Tin Oxide)透明電極(陽極)付きガラス基板(ジオマテック株式会社製)をイソプロピルアルコール中で超音波洗浄を5分間行なった後、UVオゾン洗浄を30分間行なった。ITO透明電極の膜厚は、130nmとした。
洗浄後の透明電極ライン付きガラス基板を真空蒸着装置の基板ホルダーに装着し、まず透明電極ラインが形成されている側の面上に透明電極を覆うようにして化合物HA1を蒸着し、膜厚5nmの正孔注入層(HI)を形成した。
正孔注入層の成膜に続けて化合物HT3を蒸着し、膜厚80nmの第一の正孔輸送層(HT)を成膜した。
第一の正孔輸送層の成膜に続けて化合物HT7を蒸着し、膜厚10nmの第二の正孔輸送層(電子障壁層ともいう)(EBL)を成膜した。
第二の正孔輸送層上に化合物BH1-10(第一のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚5nmの第一の発光層を成膜した。
第一の発光層上に化合物BH2-2(第二のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚20nmの第二の発光層を成膜した。
第二の発光層上に化合物ET7を蒸着し、膜厚10nmの第1の電子輸送層(正孔障壁層ともいう)(HBL)を形成した。
第1の電子輸送層上に化合物ET2を蒸着し、膜厚20nmの第2の電子輸送層(ET)を形成した。
第2の電子輸送層上にLiFを蒸着して膜厚1nmの電子注入層を形成した。
電子注入層上に金属Alを蒸着して膜厚80nmの陰極を形成した。
参考例125の素子構成を略式的に示すと、次のとおりである。
ITO(130)/HA1(5)/HT3(80)/HT7(10)/BH1-10:BD1(5,98%:2%)/BH2-2:BD1(20,98%:2%)/ET7(10)/ET2(20)/LiF(1)/Al(80)
なお、括弧内の数字は、膜厚(単位:nm)を示す。
同じく括弧内において、パーセント表示された数字(98%:2%)は、第一の発光層におけるホスト材料(化合物BH1-10)及び化合物BD1の割合(質量%)を示し、又はパーセント表示された数字(98%:2%)は、第二の発光層におけるホスト材料(化合物BH2-2)及び化合物BD1の割合(質量%)を示す。以下、同様の表記とする。
参考例126の有機EL素子は、第二の発光層における化合物BH2-2(第二のホスト材料)を表30に記載の第二の化合物に変更したこと以外、参考例125と同様にして作製した。
比較参考例102の有機EL素子は、表30に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと、並びに第二の発光層における第二の化合物(第二のホスト材料)を表30に記載の第二の化合物に変更したこと以外、参考例125と同様にして作製した。
参考例127の有機EL素子は、第二の発光層における化合物BH2-2(第二のホスト材料)を表31に記載の第二の化合物に変更したこと以外、参考例125と同様にして作製した。
比較参考例103の有機EL素子は、表31に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと、並びに第二の発光層における第二の化合物(第二のホスト材料)を表31に記載の第二の化合物に変更したこと以外、参考例125と同様にして作製した。
参考例128の有機EL素子は、第二の発光層における化合物BH2-2(第二のホスト材料)を表32に記載の第二の化合物に変更したこと以外、参考例125と同様にして作製した。
比較参考例104の有機EL素子は、表32に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと、並びに第二の発光層における第二の化合物(第二のホスト材料)を表32に記載の第二の化合物に変更したこと以外、参考例125と同様にして作製した。
参考例129の有機EL素子は、第二の発光層における化合物BH2-2(第二のホスト材料)を表33に記載の第二の化合物に変更したこと以外、参考例125と同様にして作製した。
比較参考例105の有機EL素子は、表33に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと、並びに第二の発光層における第二の化合物(第二のホスト材料)を表33に記載の第二の化合物に変更したこと以外、参考例125と同様にして作製した。
〔参考例130〕
25mm×75mm×1.1mm厚のITO(Indium Tin Oxide)透明電極(陽極)付きガラス基板(ジオマテック株式会社製)をイソプロピルアルコール中で超音波洗浄を5分間行なった後、UVオゾン洗浄を30分間行なった。ITO透明電極の膜厚は、130nmとした。
洗浄後の透明電極ライン付きガラス基板を真空蒸着装置の基板ホルダーに装着し、まず透明電極ラインが形成されている側の面上に透明電極を覆うようにして化合物HA1を蒸着し、膜厚5nmの正孔注入層(HI)を形成した。
正孔注入層の成膜に続けて化合物HT3を蒸着し、膜厚80nmの第一の正孔輸送層(HT)を成膜した。
第一の正孔輸送層の成膜に続けて化合物HT7を蒸着し、膜厚10nmの第二の正孔輸送層(電子障壁層ともいう)(EBL)を成膜した。
第二の正孔輸送層上に化合物BH1-10(第一のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚5nmの第一の発光層を成膜した。
第一の発光層上に化合物BH2-8(第二のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚20nmの第二の発光層を成膜した。
第二の発光層上に化合物ET1を蒸着し、膜厚10nmの第1の電子輸送層(正孔障壁層ともいう)(HBL)を形成した。
第1の電子輸送層上に化合物ET5を蒸着し、膜厚20nmの第2の電子輸送層(ET)を形成した。
第2の電子輸送層上にLiFを蒸着して膜厚1nmの電子注入層を形成した。
電子注入層上に金属Alを蒸着して膜厚80nmの陰極を形成した。
参考例130の素子構成を略式的に示すと、次のとおりである。
ITO(130)/HA1(5)/HT3(80)/HT7(10)/BH1-10:BD1(5,98%:2%)/BH2-8:BD1(20,98%:2%)/ET1(10)/ET5(20)/LiF(1)/Al(80)
なお、括弧内の数字は、膜厚(単位:nm)を示す。
同じく括弧内において、パーセント表示された数字(98%:2%)は、第一の発光層におけるホスト材料(化合物BH1-10)及び化合物BD1の割合(質量%)を示し、又はパーセント表示された数字(98%:2%)は、第二の発光層におけるホスト材料(化合物BH2-8)及び化合物BD1の割合(質量%)を示す。以下、同様の表記とする。
参考例131の有機EL素子は、第二の発光層における化合物BH2-8(第二のホスト材料)を表34に記載の第二の化合物に変更したこと以外、参考例130と同様にして作製した。
比較参考例106の有機EL素子は、表34に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと、並びに第二の発光層における第二の化合物(第二のホスト材料)を表34に記載の第二の化合物に変更したこと以外、参考例130と同様にして作製した。
参考例132の有機EL素子は、第二の発光層における化合物BH2-8(第二のホスト材料)を表35に記載の第二の化合物に変更したこと以外、参考例130と同様にして作製した。
比較参考例107の有機EL素子は、表35に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと、並びに第二の発光層における第二の化合物(第二のホスト材料)を表35に記載の第二の化合物に変更したこと以外、参考例130と同様にして作製した。
参考例133の有機EL素子は、第二の発光層における化合物BH2-8(第二のホスト材料)を表36に記載の第二の化合物に変更したこと以外、参考例130と同様にして作製した。
比較参考例108の有機EL素子は、表36に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと、並びに第二の発光層における第二の化合物(第二のホスト材料)を表36に記載の第二の化合物に変更したこと以外、参考例130と同様にして作製した。
〔参考例134〕
25mm×75mm×1.1mm厚のITO(Indium Tin Oxide)透明電極(陽極)付きガラス基板(ジオマテック株式会社製)をイソプロピルアルコール中で超音波洗浄を5分間行なった後、UVオゾン洗浄を30分間行なった。ITO透明電極の膜厚は、130nmとした。
洗浄後の透明電極ライン付きガラス基板を真空蒸着装置の基板ホルダーに装着し、まず透明電極ラインが形成されている側の面上に透明電極を覆うようにして化合物HA1を蒸着し、膜厚5nmの正孔注入層(HI)を形成した。
正孔注入層の成膜に続けて化合物HT1を蒸着し、膜厚80nmの第一の正孔輸送層(HT)を成膜した。
第一の正孔輸送層の成膜に続けて化合物HT2を蒸着し、膜厚10nmの第二の正孔輸送層(電子障壁層ともいう)(EBL)を成膜した。
第二の正孔輸送層上に化合物BH1(第一のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚5nmの第一の発光層を成膜した。
第一の発光層上に化合物BH2-8(第二のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚20nmの第二の発光層を成膜した。
第二の発光層上に化合物ET4を蒸着し、膜厚10nmの第1の電子輸送層(正孔障壁層ともいう)(HBL)を形成した。
第1の電子輸送層上に化合物ET2を蒸着し、膜厚20nmの第2の電子輸送層(ET)を形成した。
第2の電子輸送層上にLiFを蒸着して膜厚1nmの電子注入層を形成した。
電子注入層上に金属Alを蒸着して膜厚80nmの陰極を形成した。
参考例134の素子構成を略式的に示すと、次のとおりである。
ITO(130)/HA1(5)/HT1(80)/HT2(10)/BH1:BD1(5,98%:2%)/BH2-8:BD1(20,98%:2%)/ET4(10)/ET2(20)/LiF(1)/Al(80)
なお、括弧内の数字は、膜厚(単位:nm)を示す。
同じく括弧内において、パーセント表示された数字(98%:2%)は、第一の発光層におけるホスト材料(化合物BH1)及び化合物BD1の割合(質量%)を示し、又はパーセント表示された数字(98%:2%)は、第二の発光層におけるホスト材料(化合物BH2-8)及び化合物BD1の割合(質量%)を示す。以下、同様の表記とする。
参考例135の有機EL素子は、第二の発光層における化合物BH2-8(第二のホスト材料)を表37に記載の第二の化合物に変更したこと以外、参考例134と同様にして作製した。
比較参考例109の有機EL素子は、表37に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと、並びに第二の発光層における第二の化合物(第二のホスト材料)を表37に記載の第二の化合物に変更したこと以外、参考例134と同様にして作製した。
参考例136の有機EL素子は、第二の発光層における化合物BH2-8(第二のホスト材料)を表38に記載の第二の化合物に変更したこと以外、参考例134と同様にして作製した。
比較参考例110の有機EL素子は、表38に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと、並びに第二の発光層における第二の化合物(第二のホスト材料)を表38に記載の第二の化合物に変更したこと以外、参考例134と同様にして作製した。
参考例137の有機EL素子は、第二の発光層における化合物BH2-8(第二のホスト材料)を表39に記載の第二の化合物に変更したこと以外、参考例134と同様にして作製した。
比較参考例111の有機EL素子は、表39に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと、並びに第二の発光層における第二の化合物(第二のホスト材料)を表39に記載の第二の化合物に変更したこと以外、参考例134と同様にして作製した。
参考例138の有機EL素子は、第二の発光層における化合物BH2-8(第二のホスト材料)を表40に記載の第二の化合物に変更したこと以外、参考例134と同様にして作製した。
比較参考例112の有機EL素子は、表40に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと、並びに第二の発光層における第二の化合物(第二のホスト材料)を表40に記載の第二の化合物に変更したこと以外、参考例134と同様にして作製した。
参考例139の有機EL素子は、第二の発光層における化合物BH2-8(第二のホスト材料)を表41に記載の第二の化合物に変更したこと以外、参考例134と同様にして作製した。
比較参考例113の有機EL素子は、表41に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと、並びに第二の発光層における第二の化合物(第二のホスト材料)を表41に記載の第二の化合物に変更したこと以外、参考例134と同様にして作製した。
参考例140の有機EL素子は、第二の発光層における化合物BH2-8(第二のホスト材料)を表42に記載の第二の化合物に変更したこと以外、参考例134と同様にして作製した。
比較参考例114の有機EL素子は、表42に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと、並びに第二の発光層における第二の化合物(第二のホスト材料)を表42に記載の第二の化合物に変更したこと以外、参考例134と同様にして作製した。
参考例141の有機EL素子は、第二の発光層における化合物BH2-8(第二のホスト材料)を表43に記載の第二の化合物に変更したこと以外、参考例134と同様にして作製した。
比較参考例115の有機EL素子は、表43に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと、並びに第二の発光層における第二の化合物(第二のホスト材料)を表43に記載の第二の化合物に変更したこと以外、参考例134と同様にして作製した。
参考例142の有機EL素子は、第二の発光層における化合物BH2-8(第二のホスト材料)を表44に記載の第二の化合物に変更したこと以外、参考例134と同様にして作製した。
比較参考例116の有機EL素子は、表44に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと、並びに第二の発光層における第二の化合物(第二のホスト材料)を表44に記載の第二の化合物に変更したこと以外、参考例134と同様にして作製した。
〔参考例143〕
25mm×75mm×1.1mm厚のITO(Indium Tin Oxide)透明電極(陽極)付きガラス基板(ジオマテック株式会社製)をイソプロピルアルコール中で超音波洗浄を5分間行なった後、UVオゾン洗浄を30分間行なった。ITO透明電極の膜厚は、130nmとした。
洗浄後の透明電極ライン付きガラス基板を真空蒸着装置の基板ホルダーに装着し、まず透明電極ラインが形成されている側の面上に透明電極を覆うようにして化合物HA1を蒸着し、膜厚5nmの正孔注入層(HI)を形成した。
正孔注入層の成膜に続けて化合物HT1を蒸着し、膜厚80nmの第一の正孔輸送層(HT)を成膜した。
第一の正孔輸送層の成膜に続けて化合物HT2を蒸着し、膜厚10nmの第二の正孔輸送層(電子障壁層ともいう)(EBL)を成膜した。
第二の正孔輸送層上に化合物BH1(第一のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚5nmの第一の発光層を成膜した。
第一の発光層上に化合物BH2-8(第二のホスト材料(BH))及び化合物BD1(ドーパント材料(BD))を、化合物BD1の割合が2質量%となるように共蒸着し、膜厚20nmの第二の発光層を成膜した。
第二の発光層上に化合物ET7を蒸着し、膜厚10nmの第1の電子輸送層(正孔障壁層ともいう)(HBL)を形成した。
第1の電子輸送層上に化合物ET2を蒸着し、膜厚20nmの第2の電子輸送層(ET)を形成した。
第2の電子輸送層上にLiFを蒸着して膜厚1nmの電子注入層を形成した。
電子注入層上に金属Alを蒸着して膜厚80nmの陰極を形成した。
参考例143の素子構成を略式的に示すと、次のとおりである。
ITO(130)/HA1(5)/HT1(80)/HT2(10)/BH1:BD1(5,98%:2%)/BH2-8:BD1(20,98%:2%)/ET7(10)/ET2(20)/LiF(1)/Al(80)
なお、括弧内の数字は、膜厚(単位:nm)を示す。
同じく括弧内において、パーセント表示された数字(98%:2%)は、第一の発光層におけるホスト材料(化合物BH1)及び化合物BD1の割合(質量%)を示し、又はパーセント表示された数字(98%:2%)は、第二の発光層におけるホスト材料(化合物BH2-8)及び化合物BD1の割合(質量%)を示す。以下、同様の表記とする。
参考例144の有機EL素子は、第二の発光層における化合物BH2-8(第二のホスト材料)を表45に記載の第二の化合物に変更したこと以外、参考例143と同様にして作製した。
比較参考例117の有機EL素子は、表45に記載のとおり、第一の発光層を形成せずに、第二の正孔輸送層の上に膜厚25nmの第二の発光層を形成したこと、並びに第二の発光層における第二の化合物(第二のホスト材料)を表45に記載の第二の化合物に変更したこと以外、参考例143と同様にして作製した。
〔実施例145〕
25mm×75mm×1.1mm厚のITO(Indium Tin Oxide)透明電極(陽極)付きガラス基板(ジオマテック株式会社製)をイソプロピルアルコール中で超音波洗浄を5分間行なった後、UVオゾン洗浄を30分間行なった。ITO透明電極の膜厚は、130nmとした。
洗浄後の透明電極ライン付きガラス基板を真空蒸着装置の基板ホルダーに装着し、まず透明電極ラインが形成されている側の面上に透明電極を覆うようにして化合物HA3を蒸着し、膜厚10nmの正孔注入層(HI)を形成した。
正孔注入層の成膜に続けて化合物HT9を蒸着し、膜厚80nmの第一の正孔輸送層(HT)を成膜した。
第一の正孔輸送層の成膜に続けて化合物HT10を蒸着し、膜厚10nmの第二の正孔輸送層(電子障壁層ともいう)(EBL)を成膜した。
第二の正孔輸送層上に化合物BH1-84(第一のホスト材料(BH))及び化合物BD2(ドーパント材料(BD))を、化合物BD2の割合が2質量%となるように共蒸着し、膜厚5nmの第一の発光層を成膜した。
第一の発光層上に化合物BH2(第二のホスト材料(BH))及び化合物BD2(ドーパント材料(BD))を、化合物BD2の割合が2質量%となるように共蒸着し、膜厚20nmの第二の発光層を成膜した。
第二の発光層上に化合物ET9を蒸着し、膜厚10nmの第1の電子輸送層(正孔障壁層ともいう)(HBL)を形成した。
第1の電子輸送層上に化合物ET2を蒸着し、膜厚15nmの第2の電子輸送層(ET)を形成した。
第2の電子輸送層上にLiFを蒸着して膜厚1nmの電子注入層を形成した。
電子注入層上に金属Alを蒸着して膜厚50nmの陰極を形成した。
実施例145の素子構成を略式的に示すと、次のとおりである。
ITO(130)/HA3(10)/HT9(80)/HT10(10)/BH1-84:BD2(5,98%:2%)/BH2:BD2(20,98%:2%)/ET9(10)/ET2(15)/LiF(1)/Al(50)
なお、括弧内の数字は、膜厚(単位:nm)を示す。
同じく括弧内において、パーセント表示された数字(98%:2%)は、第一の発光層におけるホスト材料(化合物BH1-84)及び化合物BD2の割合(質量%)を示し、又はパーセント表示された数字(98%:2%)は、第二の発光層におけるホスト材料(化合物BH2)及び化合物BD2の割合(質量%)を示す。
比較例118の有機EL素子は、第一の発光層における化合物BH1-84(第一のホスト材料)を表46に記載の第一の化合物に変更したこと以外、実施例145と同様にして作製した。
(トルエン溶液の調製)
化合物BD1を、4.9×10-6mol/Lの濃度でトルエンに溶解し、化合物BD1のトルエン溶液を調製した。これと同様に、化合物BD2のトルエン溶液及び化合物BD3のトルエン溶液を調製した。
蛍光スペクトル測定装置(分光蛍光光度計F-7000(株式会社日立ハイテクサイエンス製))を用いて、化合物BD1のトルエン溶液を390nmで励起した場合の蛍光発光主ピーク波長を測定した。化合物BD2のトルエン溶液及び化合物BD3のトルエン溶液についても、化合物BD1と同様に蛍光発光主ピーク波長を測定した。
化合物BD1の蛍光発光主ピーク波長は、453nmであった。
化合物BD2の蛍光発光主ピーク波長は、455nmであった。
化合物BD3の蛍光発光主ピーク波長は、451nmであった。
Claims (19)
- 陽極と、
陰極と、
前記陽極及び前記陰極の間に配置された第一の発光層と、
前記第一の発光層と前記陰極との間に配置された第二の発光層と、を有し、
前記第一の発光層は、下記一般式(11)で表される基を1つ有し、かつ下記一般式(1)で表される第一の化合物を第一のホスト材料として含有し、
前記第二の発光層は、下記一般式(2)で表される第二の化合物を第二のホスト材料として含有し、
前記第一の発光層と前記第二の発光層とが、直接、接している、
有機エレクトロルミネッセンス素子。
R101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、又は
前記一般式(11)で表される基であり、
ただし、R101~R110の1つが、前記一般式(11)で表される基であり、
L101は、
単結合、又は
置換もしくは無置換の環形成炭素数6~50のアリーレン基であり、
L101は、置換もしくは無置換のピレニレン基ではなく、
L101としての置換もしくは無置換の環形成炭素数6~50のアリーレン基は、置換もしくは無置換のフェニル基、置換もしくは無置換のp-ビフェニル基、置換もしくは無置換のm-ビフェニル基、置換もしくは無置換のo-ビフェニル基、置換もしくは無置換のp-ターフェニル-4-イル基、置換もしくは無置換のp-ターフェニル-3-イル基、置換もしくは無置換のp-ターフェニル-2-イル基、置換もしくは無置換のm-ターフェニル-4-イル基、置換もしくは無置換のm-ターフェニル-3-イル基、置換もしくは無置換のm-ターフェニル-2-イル基、置換もしくは無置換のo-ターフェニル-4-イル基、置換もしくは無置換のo-ターフェニル-3-イル基、置換もしくは無置換のo-ターフェニル-2-イル基、置換もしくは無置換のアントリル基、置換もしくは無置換のベンゾアントリル基、置換もしくは無置換のフェナントリル基、置換もしくは無置換のベンゾフェナントリル基、置換もしくは無置換のフェナレニル基、置換もしくは無置換のクリセニル基、置換もしくは無置換のベンゾクリセニル基、置換もしくは無置換のトリフェニレニル基、置換もしくは無置換のベンゾトリフェニレニル基、置換もしくは無置換のテトラセニル基、置換もしくは無置換のペンタセニル基、置換もしくは無置換の9,9’-スピロビフルオレニル基、置換もしくは無置換のフルオランテニル基、置換もしくは無置換のベンゾフルオランテニル基、又は置換もしくは無置換のペリレニル基からアリール環上の1つの水素原子を除くことにより誘導される2価の基であり、
Ar101は、置換もしくは無置換の環形成炭素数6~50のアリール基であり、
mxは、0、1、2、3、4又は5であり、
Ar101は、置換もしくは無置換のピレニル基ではなく、
Ar101は、置換もしくは無置換のフェニル基、置換もしくは無置換のp-ビフェニル基、置換もしくは無置換のm-ビフェニル基、置換もしくは無置換のo-ビフェニル基、置換もしくは無置換のp-ターフェニル-4-イル基、置換もしくは無置換のp-ターフェニル-3-イル基、置換もしくは無置換のp-ターフェニル-2-イル基、置換もしくは無置換のm-ターフェニル-4-イル基、置換もしくは無置換のm-ターフェニル-3-イル基、置換もしくは無置換のm-ターフェニル-2-イル基、置換もしくは無置換のo-ターフェニル-4-イル基、置換もしくは無置換のo-ターフェニル-3-イル基、置換もしくは無置換のo-ターフェニル-2-イル基、置換もしくは無置換の1-ナフチル基、置換もしくは無置換の2-ナフチル基、置換もしくは無置換のフェナントリル基、置換もしくは無置換のフルオレニル基、又は置換もしくは無置換のベンゾフルオレニル基であり、
Ar101が、置換の環形成炭素数6~50のアリール基である場合、Ar101としてのアリール基が有する置換基は、炭素数1~18のアルキル基であり、
L101が2以上存在する場合、2以上のL101は、互いに同一であるか、又は異なり、
前記一般式(11)中の*は、前記一般式(1)中のピレン環との結合位置を示す。)
R201~R208は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、
ニトロ基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
L201及びL202は、それぞれ独立に、
単結合、
置換もしくは無置換の環形成炭素数6~50のアリーレン基、又は
置換もしくは無置換の環形成原子数5~50の2価の複素環基であり、
Ar201及びAr202は、それぞれ独立に、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である。)
(前記一般式(1)で表される第一の化合物及び前記一般式(2)で表される第二の化合物中、R901、R902、R903、R904、R905、R906、R907、R801及びR802は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基であり、
R901が複数存在する場合、複数のR901は、互いに同一であるか又は異なり、
R902が複数存在する場合、複数のR902は、互いに同一であるか又は異なり、
R903が複数存在する場合、複数のR903は、互いに同一であるか又は異なり、
R904が複数存在する場合、複数のR904は、互いに同一であるか又は異なり、
R905が複数存在する場合、複数のR905は、互いに同一であるか又は異なり、
R906が複数存在する場合、複数のR906は、互いに同一であるか又は異なり、
R907が複数存在する場合、複数のR907は、互いに同一であるか又は異なり、
R801が複数存在する場合、複数のR801は、互いに同一であるか又は異なり、
R802が複数存在する場合、複数のR802は、互いに同一であるか又は異なる。) - 請求項1に記載の有機エレクトロルミネッセンス素子において、
mxは、1、2、3、4又は5であり、
少なくとも1つのL101は、置換もしくは無置換のフェニル基、置換もしくは無置換のp-ビフェニル基、置換もしくは無置換のm-ビフェニル基、置換もしくは無置換のo-ビフェニル基、置換もしくは無置換のp-ターフェニル-4-イル基、置換もしくは無置換のp-ターフェニル-3-イル基、置換もしくは無置換のp-ターフェニル-2-イル基、置換もしくは無置換のm-ターフェニル-4-イル基、置換もしくは無置換のm-ターフェニル-3-イル基、置換もしくは無置換のm-ターフェニル-2-イル基、置換もしくは無置換のo-ターフェニル-4-イル基、置換もしくは無置換のo-ターフェニル-3-イル基、置換もしくは無置換のo-ターフェニル-2-イル基、又は置換もしくは無置換のフェナントリル基からアリール環上の1つの水素原子を除くことにより誘導される2価の基である、
有機エレクトロルミネッセンス素子。 - 請求項1又は請求項2に記載の有機エレクトロルミネッセンス素子において、
Ar101は、4つの環が縮合したアリール基である、
有機エレクトロルミネッセンス素子。 - 請求項1から請求項3のいずれか一項に記載の有機エレクトロルミネッセンス素子において、
Ar101は、置換もしくは無置換のフェニル基、置換もしくは無置換の1-ナフチル基、置換もしくは無置換の2-ナフチル基、置換もしくは無置換のp-ビフェニル基、置換もしくは無置換のm-ビフェニル基、置換もしくは無置換のo-ビフェニル基、置換もしくは無置換のp-ターフェニル-4-イル基、置換もしくは無置換のp-ターフェニル-3-イル基、置換もしくは無置換のp-ターフェニル-2-イル基、置換もしくは無置換のm-ターフェニル-4-イル基、置換もしくは無置換のm-ターフェニル-3-イル基、置換もしくは無置換のm-ターフェニル-2-イル基、置換もしくは無置換のo-ターフェニル-4-イル基、置換もしくは無置換のo-ターフェニル-3-イル基、置換もしくは無置換のo-ターフェニル-2-イル基、置換もしくは無置換のフェナントリル基、又は置換もしくは無置換のフルオレニル基である、
有機エレクトロルミネッセンス素子。 - 請求項1から請求項4のいずれか一項に記載の有機エレクトロルミネッセンス素子において、
前記有機エレクトロルミネッセンス素子は、素子駆動時に主ピーク波長が430nm以上480nm以下の光を放射する、
有機エレクトロルミネッセンス素子。 - 請求項1から請求項5のいずれか一項に記載の有機エレクトロルミネッセンス素子において、
前記第二の発光層は、蛍光発光性の第四の化合物をさらに含有し、
前記第四の化合物は、主ピーク波長が430nm以上480nm以下の発光を示す化合物である、
有機エレクトロルミネッセンス素子。 - 請求項1から請求項6のいずれか一項に記載の有機エレクトロルミネッセンス素子において、
前記第一の発光層は、蛍光発光性の第三の化合物をさらに含有し、
前記第三の化合物は、主ピーク波長が430nm以上480nm以下の発光を示す化合物である、
有機エレクトロルミネッセンス素子。 - 請求項1から請求項7のいずれか一項に記載の有機エレクトロルミネッセンス素子において、
前記一般式(11)で表される基ではないR101~R110は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、又は
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基である、
有機エレクトロルミネッセンス素子。 - 請求項1から請求項8のいずれか一項に記載の有機エレクトロルミネッセンス素子において、
前記一般式(11)で表される基ではないR101~R110は、水素原子である、
有機エレクトロルミネッセンス素子。 - 請求項1から請求項9のいずれか一項に記載の有機エレクトロルミネッセンス素子において、
R201~R208は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の炭素数1~50のハロアルキル基、
置換もしくは無置換の炭素数2~50のアルケニル基、
置換もしくは無置換の炭素数2~50のアルキニル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、
-Si(R901)(R902)(R903)で表される基、
-O-(R904)で表される基、
-S-(R905)で表される基、
-N(R906)(R907)で表される基、
置換もしくは無置換の炭素数7~50のアラルキル基、
-C(=O)R801で表される基、
-COOR802で表される基、
ハロゲン原子、
シアノ基、又は
ニトロ基であり、
L201及びL202は、それぞれ独立に、
単結合、
置換もしくは無置換の環形成炭素数6~50のアリーレン基、又は
置換もしくは無置換の環形成原子数5~50の2価の複素環基であり、
Ar201及びAr202は、それぞれ独立に、
置換もしくは無置換の環形成炭素数6~50のアリール基、又は
置換もしくは無置換の環形成原子数5~50の複素環基である、
有機エレクトロルミネッセンス素子。 - 請求項1から請求項10のいずれか一項に記載の有機エレクトロルミネッセンス素子において、
L201及びL202は、それぞれ独立に、
単結合、又は
置換もしくは無置換の環形成炭素数6~50のアリーレン基であり、
Ar201及びAr202は、それぞれ独立に、置換もしくは無置換の環形成炭素数6~50のアリール基である、
有機エレクトロルミネッセンス素子。 - 請求項1から請求項10のいずれか一項に記載の有機エレクトロルミネッセンス素子において、
Ar201及びAr202は、それぞれ独立に、
フェニル基、
ナフチル基、
フェナントリル基、
ビフェニル基、
ターフェニル基、
ジフェニルフルオレニル基、
ジメチルフルオレニル基、
ベンゾジフェニルフルオレニル基、
ベンゾジメチルフルオレニル基、
ジベンゾフラニル基、
ジベンゾチエニル基、
ナフトベンゾフラニル基、又は
ナフトベンゾチエニル基である、
有機エレクトロルミネッセンス素子。 - 請求項1から請求項12のいずれか一項に記載の有機エレクトロルミネッセンス素子において、
前記一般式(2)で表される第二の化合物は、下記一般式(201)、一般式(202)、一般式(203)、一般式(204)、一般式(205)、一般式(206)、一般式(207)、一般式(208)又は一般式(209)で表される化合物である、
有機エレクトロルミネッセンス素子。
L201及びAr201は、前記一般式(2)におけるL201及びAr201と同義であり、
R201~R208は、それぞれ独立に、前記一般式(2)におけるR201~R208と同義である。) - 請求項1から請求項13のいずれか一項に記載の有機エレクトロルミネッセンス素子において、
前記一般式(2)で表される第二の化合物中、R201~R208は、それぞれ独立に、
水素原子、
置換もしくは無置換の炭素数1~50のアルキル基、
置換もしくは無置換の環形成炭素数3~50のシクロアルキル基、又は
-Si(R901)(R902)(R903)で表される基である、
有機エレクトロルミネッセンス素子。 - 請求項1から請求項14のいずれか一項に記載の有機エレクトロルミネッセンス素子において、
前記一般式(2)で表される第二の化合物中、R201~R208は、水素原子である、
有機エレクトロルミネッセンス素子。 - 請求項1から請求項15のいずれか一項に記載の有機エレクトロルミネッセンス素子において、
前記第一の化合物及び前記第二の化合物において、「置換もしくは無置換」と記載された基は、いずれも「無置換」の基である、
有機エレクトロルミネッセンス素子。 - 請求項1から請求項16のいずれか一項に記載の有機エレクトロルミネッセンス素子において、
前記陽極と、前記第一の発光層との間に、正孔輸送層を有する、
有機エレクトロルミネッセンス素子。 - 請求項1から請求項17のいずれか一項に記載の有機エレクトロルミネッセンス素子において、
前記陰極と、前記第二の発光層との間に、電子輸送層を有する、
有機エレクトロルミネッセンス素子。 - 請求項1から請求項18のいずれか一項に記載の有機エレクトロルミネッセンス素子を搭載した電子機器。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2024076815A JP2024105483A (ja) | 2019-09-13 | 2024-05-09 | 有機エレクトロルミネッセンス素子及び電子機器 |
Applications Claiming Priority (9)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019167636 | 2019-09-13 | ||
| JP2019167636 | 2019-09-13 | ||
| JP2019213374 | 2019-11-26 | ||
| JP2019213374 | 2019-11-26 | ||
| JP2019239937 | 2019-12-27 | ||
| JP2019239937 | 2019-12-27 | ||
| JP2019239946 | 2019-12-27 | ||
| JP2019239946 | 2019-12-27 | ||
| PCT/JP2020/034605 WO2021049662A1 (ja) | 2019-09-13 | 2020-09-11 | 有機エレクトロルミネッセンス素子及び電子機器 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024076815A Division JP2024105483A (ja) | 2019-09-13 | 2024-05-09 | 有機エレクトロルミネッセンス素子及び電子機器 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2021049662A1 JPWO2021049662A1 (ja) | 2021-03-18 |
| JP7545397B2 true JP7545397B2 (ja) | 2024-09-04 |
Family
ID=74865949
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021545647A Active JP7545397B2 (ja) | 2019-09-13 | 2020-09-11 | 有機エレクトロルミネッセンス素子及び電子機器 |
| JP2024076815A Pending JP2024105483A (ja) | 2019-09-13 | 2024-05-09 | 有機エレクトロルミネッセンス素子及び電子機器 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024076815A Pending JP2024105483A (ja) | 2019-09-13 | 2024-05-09 | 有機エレクトロルミネッセンス素子及び電子機器 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20220380278A1 (ja) |
| JP (2) | JP7545397B2 (ja) |
| KR (2) | KR20260003818A (ja) |
| CN (2) | CN114402455B (ja) |
| WO (1) | WO2021049662A1 (ja) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US12481844B2 (en) | 2006-09-27 | 2025-11-25 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent element, electronic device, and compound |
| JP2024164328A (ja) | 2021-08-13 | 2024-11-27 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子、電子機器及び化合物 |
| WO2022181157A1 (ja) | 2021-02-25 | 2022-09-01 | 出光興産株式会社 | 化合物、有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子及び電子機器 |
| KR20230094213A (ko) * | 2021-12-20 | 2023-06-28 | 에스에프씨 주식회사 | 두 개의 발광층을 포함하는 신규한 유기발광소자 |
| CN116535293A (zh) * | 2023-05-05 | 2023-08-04 | 广东工业大学 | 一类y-型的溴芘中间体及其衍生物、制备方法和应用 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013067586A (ja) | 2011-09-22 | 2013-04-18 | Canon Inc | 新規有機化合物、それを有する有機発光素子及び表示装置 |
| JP2018125504A (ja) | 2017-02-03 | 2018-08-09 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子、電子機器及び有機エレクトロルミネッセンス素子用材料 |
| US20190280209A1 (en) | 2018-03-08 | 2019-09-12 | Jnc Corporation | Organic electroluminescent element |
| JP2019161218A (ja) | 2018-03-08 | 2019-09-19 | Jnc株式会社 | 有機電界発光素子 |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ATE452954T1 (de) | 2002-08-23 | 2010-01-15 | Idemitsu Kosan Co | Organische elektrolumineszenzvorrichtung und anthracenderivat |
| WO2005115950A1 (ja) | 2004-05-27 | 2005-12-08 | Idemitsu Kosan Co., Ltd. | 非対称ピレン誘導体及びそれを利用した有機エレクトロルミネッセンス素子 |
| JP5076328B2 (ja) * | 2006-02-06 | 2012-11-21 | 東レ株式会社 | 発光素子 |
| JP5550311B2 (ja) * | 2009-11-10 | 2014-07-16 | キヤノン株式会社 | 有機el素子 |
| JP5608682B2 (ja) | 2009-12-21 | 2014-10-15 | 出光興産株式会社 | ピレン誘導体を用いた有機エレクトロルミネッセンス素子 |
| JP6080415B2 (ja) * | 2012-07-19 | 2017-02-15 | キヤノン株式会社 | 白色有機el素子、それを用いた照明装置及び表示装置 |
| US20140231787A1 (en) * | 2011-09-22 | 2014-08-21 | Canon Kabushiki Kaisha | White organic el element and illuminating apparatus and display apparatus using the same |
| JP2013157552A (ja) | 2012-01-31 | 2013-08-15 | Canon Inc | 有機発光素子 |
| CN105358525B (zh) * | 2013-07-01 | 2018-11-09 | 出光兴产株式会社 | 化合物、有机电致发光元件用材料、有机电致发光元件、及电子设备 |
| CN106883203B (zh) * | 2017-01-24 | 2022-09-27 | 湖北尚赛光电材料有限公司 | 基于芘和萘苯并呋喃的衍生物及其制备方法、应用和器件 |
| JP7340171B2 (ja) * | 2018-01-24 | 2023-09-07 | 学校法人関西学院 | 有機電界発光素子 |
-
2020
- 2020-09-11 KR KR1020257040454A patent/KR20260003818A/ko active Pending
- 2020-09-11 CN CN202080064202.6A patent/CN114402455B/zh active Active
- 2020-09-11 JP JP2021545647A patent/JP7545397B2/ja active Active
- 2020-09-11 KR KR1020227012404A patent/KR102897070B1/ko active Active
- 2020-09-11 WO PCT/JP2020/034605 patent/WO2021049662A1/ja not_active Ceased
- 2020-09-11 US US17/642,661 patent/US20220380278A1/en active Pending
- 2020-09-11 CN CN202511436134.2A patent/CN121240683A/zh active Pending
-
2024
- 2024-05-09 JP JP2024076815A patent/JP2024105483A/ja active Pending
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013067586A (ja) | 2011-09-22 | 2013-04-18 | Canon Inc | 新規有機化合物、それを有する有機発光素子及び表示装置 |
| JP2018125504A (ja) | 2017-02-03 | 2018-08-09 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子、電子機器及び有機エレクトロルミネッセンス素子用材料 |
| US20190280209A1 (en) | 2018-03-08 | 2019-09-12 | Jnc Corporation | Organic electroluminescent element |
| JP2019161218A (ja) | 2018-03-08 | 2019-09-19 | Jnc株式会社 | 有機電界発光素子 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20220063233A (ko) | 2022-05-17 |
| JPWO2021049662A1 (ja) | 2021-03-18 |
| JP2024105483A (ja) | 2024-08-06 |
| KR20260003818A (ko) | 2026-01-07 |
| KR102897070B1 (ko) | 2025-12-05 |
| US20220380278A1 (en) | 2022-12-01 |
| CN121240683A (zh) | 2025-12-30 |
| CN114402455B (zh) | 2025-10-31 |
| WO2021049662A1 (ja) | 2021-03-18 |
| CN114402455A (zh) | 2022-04-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7625532B2 (ja) | 有機エレクトロルミネッセンス素子及び電子機器 | |
| JP7520856B2 (ja) | 有機エレクトロルミネッセンス素子及び電子機器 | |
| JP7686816B2 (ja) | 有機エレクトロルミネッセンス素子及び電子機器 | |
| JP7545397B2 (ja) | 有機エレクトロルミネッセンス素子及び電子機器 | |
| JP7545982B2 (ja) | 有機エレクトロルミネッセンス素子及び電子機器 | |
| WO2021210582A1 (ja) | 有機エレクトロルミネッセンス素子及び電子機器 | |
| JP2023040310A (ja) | 有機エレクトロルミネッセンス素子及び電子機器 | |
| JP7655911B2 (ja) | 有機エレクトロルミネッセンス素子及び電子機器 | |
| JP7605743B2 (ja) | 有機エレクトロルミネッセンス素子及び電子機器 | |
| JP2023011954A (ja) | 有機エレクトロルミネッセンス素子及び電子機器 | |
| JP2023015412A (ja) | 有機エレクトロルミネッセンス素子及び電子機器 | |
| WO2021049655A1 (ja) | 有機エレクトロルミネッセンス素子及び電子機器 | |
| JP7531499B2 (ja) | 有機エレクトロルミネッセンス素子及び電子機器 | |
| WO2021049663A1 (ja) | 有機エレクトロルミネッセンス素子及び電子機器 | |
| WO2021049654A1 (ja) | 有機エレクトロルミネッセンス素子及び電子機器 | |
| JP7546046B2 (ja) | 化合物、有機エレクトロルミネッセンス素子及び電子機器 | |
| JP2024178475A (ja) | 有機エレクトロルミネッセンス素子、電子機器及び組成物 | |
| JP2021044508A (ja) | 有機エレクトロルミネッセンス素子及び電子機器 | |
| JP2024088985A (ja) | 化合物、有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子及び電子機器 | |
| JP2024123277A (ja) | 有機エレクトロルミネッセンス素子及び電子機器 | |
| WO2025116022A1 (ja) | 有機エレクトロルミネッセンス素子及び電子機器 | |
| JP2024094434A (ja) | 有機エレクトロルミネッセンス素子及び電子機器 | |
| JP2024094433A (ja) | 有機エレクトロルミネッセンス素子及び電子機器 | |
| JP2024094435A (ja) | 有機エレクトロルミネッセンス素子及び電子機器 | |
| WO2022255454A1 (ja) | 有機エレクトロルミネッセンス素子及び電子機器 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230413 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230919 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20231117 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240117 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20240213 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240509 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20240516 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240528 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240723 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20240806 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20240823 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7545397 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |