JP7401970B2 - 発酵乳製品の製造方法及び酵素含有組成物 - Google Patents
発酵乳製品の製造方法及び酵素含有組成物 Download PDFInfo
- Publication number
- JP7401970B2 JP7401970B2 JP2018547810A JP2018547810A JP7401970B2 JP 7401970 B2 JP7401970 B2 JP 7401970B2 JP 2018547810 A JP2018547810 A JP 2018547810A JP 2018547810 A JP2018547810 A JP 2018547810A JP 7401970 B2 JP7401970 B2 JP 7401970B2
- Authority
- JP
- Japan
- Prior art keywords
- protease
- milk
- bifidobacteria
- neutral
- casein
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23C—DAIRY PRODUCTS, e.g. MILK, BUTTER OR CHEESE; MILK OR CHEESE SUBSTITUTES; MAKING OR TREATMENT THEREOF
- A23C9/00—Milk preparations; Milk powder or milk powder preparations
- A23C9/12—Fermented milk preparations; Treatment using microorganisms or enzymes
- A23C9/127—Fermented milk preparations; Treatment using microorganisms or enzymes using microorganisms of the genus lactobacteriaceae and other microorganisms or enzymes, e.g. kefir, koumiss
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/14—Hydrolases (3)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/14—Hydrolases (3)
- C12N9/48—Hydrolases (3) acting on peptide bonds (3.4)
- C12N9/50—Proteinases, e.g. Endopeptidases (3.4.21-3.4.25)
- C12N9/52—Proteinases, e.g. Endopeptidases (3.4.21-3.4.25) derived from bacteria or Archaea
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/14—Hydrolases (3)
- C12N9/48—Hydrolases (3) acting on peptide bonds (3.4)
- C12N9/50—Proteinases, e.g. Endopeptidases (3.4.21-3.4.25)
- C12N9/52—Proteinases, e.g. Endopeptidases (3.4.21-3.4.25) derived from bacteria or Archaea
- C12N9/54—Proteinases, e.g. Endopeptidases (3.4.21-3.4.25) derived from bacteria or Archaea bacteria being Bacillus
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Genetics & Genomics (AREA)
- Organic Chemistry (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Microbiology (AREA)
- Biochemistry (AREA)
- Biotechnology (AREA)
- Biomedical Technology (AREA)
- Molecular Biology (AREA)
- Medicinal Chemistry (AREA)
- General Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Polymers & Plastics (AREA)
- Food Science & Technology (AREA)
- Dairy Products (AREA)
- Enzymes And Modification Thereof (AREA)
Description
(2)前記プロテアーゼの活性が0.01PU/g以上であることを特徴とする(1)に記載の酵素含有組成物。
(3)前記中性ラクターゼの活性が0.1NLU/g以上であることを特徴とする(1)に記載の酵素含有組成物。
(4)前記プロテアーゼが、ペニバチルス属由来のプロテアーゼであることを特徴とする(1)または(2)に記載の酵素含有組成物。
(5)pHが5.0~8.5の範囲内にあることを特徴とする(1)~(4)のいずれかに記載の酵素含有組成物。
(6)凝集阻害剤を含有することを特徴とする(1)~(5)のいずれかに記載の酵素含有組成物。
(7)原料乳と、乳酸菌と、ビフィズス菌と、を混合する第1工程と、原料乳を発酵させる第2工程と、を順次行う発酵乳製品の製造方法であって、上記第2工程が終了する前に、原料乳に、κ-カゼインを分解するプロテアーゼを添加する工程(プロテアーゼ添加工程)及び中性ラクターゼを添加する工程(ラクターゼ添加工程)を行い、上記中性ラクターゼの活性1単位(NLU)あたりの上記プロテアーゼの活性が0.01以上100単位(PU)以下であることを特徴とする発酵乳製品の製造方法。
(8)前記プロテアーゼ添加工程における前記プロテアーゼの活性が終濃度で0.01PU/g以上であることを特徴とする(7)に記載の発酵乳製品の製造方法。(9)前記ラクターゼ添加工程における前記中性ラクターゼの活性が終濃度で0.1NLU/g以上であることを特徴とする(8)に記載の発酵乳製品の製造方法。
本発明は、原料乳と、乳酸菌と、ビフィズス菌と、を混合する第1工程と、
原料乳を発酵させる第2工程と、
を順次行う発酵乳製品の製造方法であって、
上記第2工程が終了する前に、原料乳にκ-カゼインを特異的に分解するプロテアーゼを添加する工程(プロテアーゼ添加工程)を行うことを特徴とする発酵乳製品の製造方法である。
第2工程が終了する前に、プロテアーゼ添加工程を行うことで、原料乳に含まれるκ-カゼインを酵素反応によって低分子化することが可能になる。プロテアーゼ添加工程によって、原料乳に含まれるκ-カゼイン量が減少し、κ-カゼイン分解物であるペプチド又は遊離アミノ酸が増大する。乳酸菌とビフィズス菌は、κ-カゼインを分解する能力に乏しいため、その発酵中にκ-カゼインを構成するアミノ酸を取り込むことが難しいが、κ-カゼイン分解物であるペプチド又は遊離アミノ酸を取り込むことが可能である。第2工程が終了する前にプロテアーゼ添加工程を行うことで、乳酸菌とビフィズス菌がκ-カゼインに由来するペプチド又は遊離アミノ酸を取り込みやすい環境にすることができ、乳酸菌とビフィズス菌の細胞数が増大する。その結果、乳酸や酢酸の分泌量も増大しpHが低下する。第2工程が終了とは、発酵工程が終了と同義である。
原料乳と、乳酸菌と、ビフィズス菌と、を混合する方法は特に限定されない。原料乳中に、乳酸菌とビフィズス菌が略均一に分布するようにわずかな時間だけ混合させる程度でもよい。略均一に分布させた後は、原料乳を満たした容器の底面に、乳酸菌とビフィズス菌が分布した状態であってもよい。
ビフィズス菌は酸素耐性が高くないため、混合する時間は短くすることが好ましい。混合速度を遅くすると、原料乳中の溶存酸素量を低くすることができるため好ましい。原料乳の温度を高くすると溶存酸素量を低くすることが可能である。また、撹拌時に泡立てないように注意することも重要である。また、溶存酸素低減、除去の為に脱気操作や窒素などの不活性ガスによる曝気操作も効果的である。
第2工程における発酵温度は、乳酸菌及びビフィズス菌が生育する温度であればよい。
使用する乳酸菌及びビフィズス菌によって発酵温度は異なるが、20℃~50℃の範囲にすることが好ましく、25℃~45℃にすることがより好ましい。
下限値未満であると、発酵が遅延しやすくなり、経済性に優れた発酵乳製品を得にくくなるおそれがある。
上限値超であると、乳酸菌及びビフィズス菌、又はビフィズス菌の死滅の問題がある。
発酵時間が下限値未満であると発酵が十分に進行せず、所望の発酵乳を得にくくなるおそれがある。
発酵時間が上限値超であると製造コストの増加や出来上がった発酵乳の品質が悪化するおそれがある。
前記プロテアーゼとして中性プロテアーゼを使用することが好ましい。発酵乳製品を製造する場合に中性プロテアーゼを使用すると、発酵の進行に伴うpH低下によって徐々に中性プロテアーゼが失活する。すなわち、中性プロテアーゼによる原料乳に含まれるκ-カゼインの分解速度は、発酵の進行に伴い、漸減することになる。このような中性プロテアーゼの作用は、乳酸菌とビフィズス菌の共存化において、ビフィズス菌が原料乳中のκ-カゼインに由来するペプチド又は遊離アミノ酸を取り込みやすくさせる環境を提供することができ、発酵乳製品中のビフィズス菌数を増大させるものである。加えて、プロテアーゼを失活させることによって、プロテアーゼによる過剰な反応を抑えることで、発酵終了後の発酵乳製品の品質低下を防ぐことが可能となる。
プロテアーゼ反応の温度が下限値未満であるとκ-カゼインの分解が不足しやすくなるおそれがある。これを解消するには、プロテアーゼの反応時間を長くする必要が生じるため、発酵乳製品を効率的に製造することが難しい。
プロテアーゼ反応の温度が上限値超であると、プロテアーゼが失活しやすくなり、κ-カゼインの分解が不十分な状態になるおそれがある。乳酸菌とビフィズス菌の共存化において、ビフィズス菌を増大させにくくなる。
プロテアーゼ反応の時間が下限値未満であると、κ-カゼインの分解が不足しやすくなるおそれがある。
プロテアーゼ反応の時間が上限値超であると、製造コストの増加の問題がある。
下限値未満、もしくは上限値以上であると、プロテアーゼが失活しやすくなり、κ-カゼインの分解が不十分な状態になるおそれがある。
発酵が進むにつれて、原料乳のpHが低下する。プロテアーゼが中性プロテアーゼである場合、原料乳のpHの低下に伴い、失活する。
上述した発酵乳製品の製造方法を経ることによって、発酵乳製品に含まれる乳酸菌の数及びビフィズス菌の数を上記の範囲にすることができる。当該発酵乳製品に含まれる乳酸菌及びビフィズス菌の数は生菌数を意味する。
中性プロテアーゼが失活した場合においても、そのタンパク質構造は維持されている。したがって、発酵乳製品自体又は発酵乳製品を濃縮したものについて電気泳動を行うことで、発酵乳製品中に中性プロテアーゼが存在するか確認することができる。電気泳動を行った後、得られた特定のバンドからアミノ酸配列を推定することも可能である。当該中性プロテアーゼの配列はその由来によって異なるが、既知であるため、電気泳動結果及びそのアミノ酸配列から、プロテアーゼの存在を確認することが可能である。同様に、発酵乳製品自体又は発酵乳製品を濃縮したものについて電気泳動を行うことで、発酵乳製品中に酸性プロテアーゼが存在するか確認することも可能である。アミノ酸配列の推定も同様である。
発酵乳製品中に含まれるプロテアーゼが失活しているとは、各pH条件下で後述するプロテアーゼの活性測定方法を行い、検出下限値以下となることをいう。プロテアーゼ以外の酵素を組み合わせることも可能である。組み合わせる酵素としては、中性ラクターゼ、グルコースイソメラーゼ、グルコースオキシダーゼ、トランスグルタミナーゼ、リパーゼ、セルラーゼ、アミラーゼ、イヌリナーゼ、ラッカーゼ、パーオキシダーゼから選ばれる1種、または複数種が好ましい。
発酵乳製品のpHが上限値超であると凝乳が不十分となる問題がある。発酵乳製品のpHが低すぎると酸味が強くなりすぎ、味のバランスを損ないやすくなる。
プロテアーゼ添加工程を第1工程の前又は第1工程と略同時に行うことで、プロテアーゼによる発酵乳製品のκ-カゼイン分解率を高めることができる。
κ-カゼイン分解率が下限値未満であると、乳酸菌とビフィズス菌を含む発酵乳製品において、ビフィズス菌が十分に増殖しないおそれがある。
κ-カゼイン量は、原料乳又は発酵乳製品の電気泳動を行い、κ-カゼインのバンドの濃淡を取り込むことで算出することができる。
発酵乳製品に含まれるκ-カゼインが検出することができると、乳酸菌とビフィズス菌を含む発酵乳製品において、ビフィズス菌が十分に増殖しないおそれがある。
発酵乳製品中に含まれるプロテアーゼが失活しているとは、各醗酵時点において後述するプロテアーゼの活性測定方法を行い、検出下限値以下となることをいう。
ラクターゼ添加工程は、第1工程の前、第1工程と略同時又は第1工程の後から選択される1つ以上のタイミングで、行うことが好ましい。2以上のタイミングで行うことも可能である。ラクターゼ添加工程後に、原料乳に含まれる乳糖の分解が行われることになる(ラクターゼ反応)。
前記ラクターゼとして中性ラクターゼを使用することが好ましい。発酵乳製品を製造する場合に中性ラクターゼを使用すると、発酵の進行に伴うpH低下によって徐々に中性ラクターゼが失活する。すなわち、中性ラクターゼによる原料乳に含まれる乳糖の分解速度は、発酵の進行に伴い、漸減することになる。このような中性ラクターゼの作用は、乳酸菌とビフィズス菌の共存化において、ビフィズス菌が原料乳中の糖類を資化させやすくなる環境を提供することができ、発酵乳製品中のビフィズス菌数を増大させるものである。
発酵乳製品中に含まれる中性ラクターゼが失活しているとは、各醗酵時点において後述するラクターゼの活性測定方法を行い、検出下限値以下となることをいう。
この比が下限値未満であると、プロテアーゼ反応が十分行われなくなるおそれがあるため、ビフィズス菌の増殖効果を十分に得にくくなる。
この比が上限値超であると、プロテアーゼが中性ラクターゼを分解するおそれが生じやすくなり好ましくない。
下限値未満であると、プロテアーゼ反応が十分行われなくなるおそれがあるため、上記の系において、ビフィズス菌の増殖効果を十分に得にくくなる。
上限値超であっても、ビフィズス菌の増殖効果は変わらないため経済的ではない。
下限値未満であると、ラクターゼ反応が十分行われなくなるおそれがあるため、上記の系において、ビフィズス菌の増殖効果を十分に得にくくなる。
上限値超であると、中性ラクターゼ反応による乳糖分解量はあまり変化せず、ビフィズス菌増殖効果も増大しないため、経済的ではない。
本発明に係る酵素含有組成物は、本発明に係る発酵乳製品の製造方法に好ましく使用することができる。原料乳と、乳酸菌と、ビフィズス菌とを含む系に、本発明に係る酵素含有組成物を加えることによって、ビフィズス菌の増殖効果を高めることができる。
本発明(酵素含有組成物)は、κ-カゼインを特異的に分解するプロテアーゼと、中性ラクターゼと、を含む酵素含有組成物であって、
上記中性ラクターゼの活性(NLU/g)とプロテアーゼの活性(PU/g)の比が0.01~100の範囲内にあることを特徴とする。当該比は、0.05~80の範囲内であることがより好ましく、0.1~50の範囲内であることがさらに好ましい。このように酵素活性の比を採用したのは、製造時及び使用時において各酵素の活性は異なるが、比であれば一定であるからである。
この比が下限値未満であると、ラクターゼ反応が十分行われなくなるおそれやプロテアーゼが中性ラクターゼを分解するおそれが生じやすくなるため、上記の系において、ビフィズス菌の増殖効果を十分に得にくくなる。
この比が上限値超であると、プロテアーゼ反応が十分行われなくおそれが生じやすくなり好ましくない。
下限値未満であると、原料乳に添加した後のプロテアーゼ反応が十分行われなくなるおそれがあるため、上記の系において、ビフィズス菌の増殖効果を十分に得にくくなる。
原料乳に添加するときの酵素含有組成物中におけるプロテアーゼの活性は、終濃度で0.01~100PU/gの範囲内にあることが好ましい。上限値超であっても、ビフィズス菌の増殖効果は変わらないため経済的ではない。
下限値未満であると、原料乳に添加した後のラクターゼ反応が十分行われなくなるおそれがあるため、上記の系において、ビフィズス菌の増殖効果を十分に得にくくなる。
原料乳に加えるときの酵素含有組成物中における中性ラクターゼの活性は、終濃度で0.1~50NLU/gの範囲内にあることが好ましい。上限値超であると、中性ラクターゼ反応による乳糖分解量はあまり変化せず、ビフィズス菌増殖効果も増大しないため、経済的ではない。
本発明は、乳酸菌と、ビフィズス菌と、κ-カゼインを特異的に分解するプロテアーゼと、中性ラクターゼとを含有する発酵乳製品であって、
前記プロテアーゼと前記中性ラクターゼが失活していることを特徴とする発酵乳製品である。
発酵乳製品とは、乳原料を乳酸菌等で発酵する発酵工程を経るものであればよい。例えば、発酵乳、サワークリーム、クワルク、発酵乳飲料、チーズ、フレッシュチーズ等が挙げられる。発酵乳は、ハードタイプ、ソフトタイプ、ドリンクタイプのいずれであっても良い。本発明は、特に発酵乳に好ましく使用することができる。
原料乳としては、乳糖を含有するものであればよく、例えば、牛乳、羊乳もしくは山羊乳等の獣乳、母乳又はこれらを乾燥させた粉乳等を単独又は混合したものを使用することができる。本発明においては、これらにさらに乳糖及び水を加えたものも原料乳である。
発酵乳製品を100質量%としたときの原料乳は90質量%以上であることが好ましく、95質量%以上であることが好ましく、98質量%以上であることがさらに好ましい。
乳酸菌としては、ラクトコッカス(Lactococcus)属、ラクトバチルス(Lactobacillus)属、ストレプトコッカス(Streptococcus)属に属する微生物を例示できる。
例えば、ラクトコッカス・ラクティス(Lactococcus lactis)、ラクトコッカス・ラクティス・サブスピーシーズ・クレモリス(Lactococcus lactis subsp. cremoris)、ラクトバチルス・カゼイ(Lactobacillus casei)ラクトバチルス・ガセリ(Lactobacillus gasseri)、ラクトバチルス・ラムノーサス(Lactobacillus rhamnosus)、ラクトバチルス・アシドフィルス(Lactobacillus acidophilus)、ラクトバチルス・プランタラム(Lactobacillus plantarum)、ラクトバチルス・ブレビス(Lactobacillus brevis)、ラクトバチルス・デルブルッキー・サブスピーシーズ・ブルガリカス(Lactobacillus delbrueckii subsp. bulgaricus)、ストレプトコッカス・サーモフィラス(Streptococcus thermophilus)が挙げられる。これらの乳酸菌は単独で使用しても良いし、2以上を組み合わせて使用しても良い。
なお、上記の乳酸菌のうち、ラクトバチルス・デルブルッキー・サブスピーシーズ・ブルガリカス(Lactobacillus delbrueckii subsp. bulgaricus)及びストレプトコッカス・サーモフィラス(Streptococcus thermophilus)を使用したものが狭義のヨーグルトである。
下限値未満であると発酵速度低下の問題がある。
上限値超であると製造コストの増加の問題がある。
ビフィズス菌としては、ビフィドバクテリウム(Bifidobacterium)属に属する微生物を例示できる。
例えば、ビフィドバクテリウム・アドレセンティス(Bifidobacterium adolescentis)、ビフィドバクテリウム・ビフィドゥム(Bifidobacterium bifidum)、ビフィドバクテリウム・ロンガム・エスエスピー・インファンティス(Bifidobacterium longum ssp. infantis)、ビフィドバクテリウム・ブレベ(Bifidobacterium breve)、ビフィドバクテリウム・ロンガム(Bifidobacterium longum)、ビフィドバクテリウム・アニマリス・エスエスピー・ラクティス(Bifidobacterium animalis ssp. lactis)である。これらのビフィズス菌は単独で使用しても良いし、2以上を組み合わせて使用しても良い。
このうち、ビフィドバクテリウム・アニマリス・エスエスピー・ラクティス(Bifidobacterium animalis ssp. lactis)のBB-12株(クリスチャンハンセン社製)は耐酸性を有することから好ましい。また、当該BB-12株は酸素耐性もある程度有することから、発酵乳製品の製造において使用しやすい。
下限値未満であると菌数不足の問題がある。
上限値超であると製造コスト増加の問題がある。
下限値未満であると、発酵後のビフィズス菌数が増えにくくなる恐れがある。
上限値超であると、発酵後のビフィズス菌数は増えるものの、製造コストが増大する傾向にあり、好ましくない。
κ-カゼインを特異的に分解するとは、原料乳にプロテアーゼを添加したときに、当該原料乳に含まれるα-カゼイン、β-カゼイン及びκ-カゼインのうち、κ-カゼインを最も多く分解することをいう。各カゼインの分解量はSDS-PAGE後の各バンドを定量的に読み取ればよい。α-カゼイン及びβ-カゼインが分解されると、低分子化された水溶性のペプチド又は遊離アミノ酸量が増え、発酵乳製品の収量が少なくなることに加え、凝乳しにくくなることにより発酵時間が増大する傾向にあり好ましくない。
中性プロテアーゼの作用pHは5.5~9.0であることが好ましい。
κ-カゼインを特異的に分解するエンド型のプロテアーゼとしては、例えば、ペニバチルス属由来中性プロテアーゼ、がある。エンド型のプロテアーゼは、κ-カゼイン分子の内側からアミノ酸を分解するため、苦味を呈するペプチドが生じにくい。κ-カゼインをエンド型のプロテアーゼで大まかに分解することで、その分解物は、乳酸菌やビフィズス菌が有するプロテアーゼ(プロティナーゼ、エンドペプチダーゼ及びエキソプロテアーゼ)によってさらに小分子化され、乳酸菌やビフィズス菌に取り込まれやすくなる。その結果、乳酸菌及びビフィズス菌を増殖させやすくなる。乳酸菌やビフィズス菌が有するプロテアーゼはκ-カゼインを分解する力が弱いため、本発明の効果を得るには、κ-カゼインを特異的に分解するプロテアーゼを添加することが必要である。なお、キモシンはエンド型のプロテアーゼであるが、仔牛由来であることから高価であり、好ましくない。
(1)ペニバチルス属に属する細菌により産生され、
(2)中性範囲でκ-カゼイン、ヘモグロビンを分解し、
(3)至適pHは7.0~8.0であり、
(4)pH5.5~9.0で安定である中性プロテアーゼであり、
(5)20~75℃で作用し、至適温度が55℃であり、
(6)電気泳動法による分子量が32,000~34,000Daと推定される。
ペニバチルス属は旧来バチルス属に分類されていたが、近年再分類され、新たな属として提案された。上記の性質を有するプロテアーゼは、バチルス・ポリミキサから再同定されたペニバチルス・ポリミキサ或いはペニバチルス・エスピーを含む別の種から得ることができる。文献等によっては、バチルス・ポリミキサと表示されている場合があるが、同義である。
(a)作用
中性プロテアーゼとしての一般的性質を示し、pHの中性範囲でカゼイン、ヘモグロビンなどの蛋白質を分解してペプチド乃至遊離のアミノ酸を生成する。
酸化インシュリンのB鎖に対してはPha(1)-Val(2)、His(5)-Leu(6)、His(10)-Leu(11)、Glu(13)-Ala(14)、Ala(14)-Ler(15)、Ler(15)-Tyr(16)、Tyr(16)-Leu(17)、Leu(17)-Val(18)、Gly(23)-Phe(24)、Phe(24)-Phe(25)、Phe(25)-Tyr(26)及びLys(29)-Ala(30)の12ヶ所のペプチド結合を切断することが確認されている。
(b)基質特異性
κ-カゼインに対し、pHの中性範囲において温和な蛋白分解作用を示す。α-カゼイン及びβ-カゼインに対しては、pHの中性範囲においても蛋白分解作用をほとんど示さない。
(c)至適pH及び安定pH範囲
イ 至適pH:κ-カゼインに対する蛋白分解作用の至適pHは、7.0~8.0である。
ロ 安定のpH範囲:5.5~9.0の範囲で極めて安定である。
(d)作用適温の範囲
20℃~75℃の範囲で作用し、至適温度は50~60℃である。最適温度は55℃である。
(e)pH、温度などによる失活の条件
pH3.0以下及びpH10.0以上では、活性は完全になくなる。また、65℃、10分間の加熱処理により、完全に失活する。
(f)阻害、活性化及び安定化
エチレンジアミンテトラアセテート(EDTA)、クエン酸、0-フェナンスロリン、2,2-ジピリジル、フッ化ソーダのごとき、金属キレート剤、及びN-ブロモサクシニイミド(NBS)、沃素のごとき酸化剤によって阻害される。
カルシウムイオンにより安定化され、活性には亜鉛イオンが必要である。
(g)分子量
電気泳動法による分子量は、32,000~34,000Daと推定される。
下限値未満では十分なκ-カゼイン由来のペプチド及び遊離アミノ酸が得られず、ビフィズス菌を増大させる効果が得られにくくなる。
上限値超であっても、κ-カゼイン量は限定的であるため、効果は得られない。
中性ラクターゼは、乳糖をガラクトースとグルコースに分解する作用を有する。中性ラクターゼは、β-ガラクトシダーゼと呼ばれることもある。中性ラクターゼは細菌由来のものと酵母由来のものとカビ由来のものがある。これらのうち、中性に至適pHがある中性ラクターゼを使用することができる。
中性ラクターゼは単独で使用しても良いし、2以上を組み合わせて使用しても良い。
0.05~40unit/gとすることがさらに好ましく、0.1~30unit/gとすることが特に好ましい。本発明においては、「unit」を「NLU」と略す場合がある。
下限値未満では十分な乳糖分解が得られず、ビフィズス菌を増大させる効果が得られにくくなる。
上限値超では乳糖分解が急速に進むため、ビフィズス菌を増大させる効果が得られにくくなる。
原料乳又は発酵乳製品に乳糖以外のグルコース及びガラクトース等の糖類、タンパク質、糖質、脂質、ビタミン類、ミネラル類、有機酸、有機塩基、果汁、フレーバー類等を添加することもできる。
これらの材料を添加する場合、事前に殺菌処理を行ってから添加しても良いし、原料乳に添加後に殺菌処理を行っても良い。
本発明の酵素含有組成物は、タンパク質の凝集を防ぐ凝集阻害剤を含むことが好ましい。凝集阻害剤としては、(1)界面活性剤、(2)タンパク質の表面を覆う作用を有する保護剤、(3)塩溶効果を有する金属イオン又はその塩、を使用することができる。これらの凝集阻害剤は単独で使用してもよく、異なる種の凝集阻害剤を組み合わせて使用してもよい。
本発明の酵素含有組成物は、必要に応じ、各種成分を含有していてもよい。具体例としては、ラクターゼやプロテアーゼの安定化に寄与する金属塩類、各種糖類、アスコルビン酸、グリセリン等、使い勝手をよくするための賦形剤である澱粉、デキストリン、緩衝作用を有する無機塩類等を挙げることができる。
以下の実施例において、中性ラクターゼは、断りの無い場合には合同酒精社製のGODO-YNL2を用いた。ビフィズス菌は、断りのない場合にはクリスチャンハンセン社製のBifidobacterium animalis ssp. lactis BB12株を用いた。
以下の実施例において使用した、ペニバチルス属由来の中性プロテアーゼ(中性金属プロテアーゼ)は、以下の方法で調製した。Paenibacillus polymyxa NBRC 15309株をDifco社製ニュートリエント液体培地に植菌し、30℃で2日間培養した培養液を10000gで10分間遠心した上清を限外濾過によって脱塩濃縮して用いた。尚、当該中性プロテアーゼは、前述の(a)~(g)の性質を有するものであった。
(プロテアーゼ活性の測定方法)
上記の中性金属プロテアーゼの添加量(酵素量)は、以下の方法により定義される酵素量1.0PUに基づいて酵素重量当たりの酵素活性として算出することができる。0.6%カゼイン水溶液(pH7.5、2mM酢酸カルシウム含有50mMトリス塩酸緩衝液)に酵素希釈液1mLを添加し、30℃で10分間反応後、トリクロロ酢酸試薬(pH4.0、1.8%無水酢酸ナトリウム、1.8%トリクロロ酢酸、1.98%酢酸)5mLを加えて反応を停止し、更に30℃で30分静置し、濾過後、275nmの吸光度を測定する。この条件下で1分間に1μgのチロシンに相当するアミノ酸を遊離する酵素量(酵素活性)を1PU(Protease Unit)と定義する。
中性ラクターゼ活性は、FCC、第4版、1996年7月1日、第801~802頁/ラクターゼ(中性)(β-ガラクトシダーゼ)活性で、公表されたものを用いて測定した。
乳酸菌数の測定は、発酵前の原料乳と、調製した発酵乳を生理食塩水で適宜希釈した0.1mLを、栄研化学社製BCP加プレートカウント寒天培地‘栄研’で混釈して37℃で2日間の培養後の菌数を測定した。
ビフィズス菌数の測定は、発酵前の原料乳と、調製した発酵乳を生理食塩水で適宜希釈した0.1mLを、栄研化学社製TOSプロピオン酸寒天培地で混釈して37℃で2日間の嫌気培養後の菌数を測定した。
市販のスキムミルク(森永乳業社製)を2質量部、市販の牛乳(明治乳業社製)を98質量部で混合、溶解して100℃で5分の殺菌処理を行った。殺菌処理後に原料乳を43℃まで冷却し、終濃度0.1~4.0PU/gの中性プロテアーゼおよび乳酸菌(YF-L812株:Streptococcus thermophilus及びLactobacillus delbrueckii subsp. bulgaricusのミクスチャー、クリスチャンハンセン社製)0.1mg/原料乳1mLとビフィズス菌(Bifidobacterium animalis ssp. lactis BB12、クリスチャンハンセン社製)0.05mg/原料乳1mLをそれぞれ添加して43℃で4時間発酵させ、参考例1~3の発酵乳を得た。
参考例1と同時に、以下のようにして中性プロテアーゼ処理を行わない発酵乳を得た。
市販のスキムミルク(森永乳業社製)を2質量部、市販の牛乳(明治乳業社製)を98質量部で混合、溶解して100℃で5分の殺菌処理を行った。殺菌処理後に原料乳を43℃まで冷却し、乳酸菌とビフィズス菌を参考例1と同様に添加して43℃で4時間発酵させ、比較例1の発酵乳を得た。
表1に示したように、中性プロテアーゼ処理を行った参考例1~3において、発酵中にBB-12株が良好な増殖を示した。発酵終了時点での参考例1と比較例1との差はおよそ40%((参考例または実施例のビフィズス菌数の増加割合-その参考例または実施例と同時に行った比較例のビフィズス菌数の増加割合)、参考例2と比較例1との差はおよそ236%、参考例3と比較例1との差はおよそ327%、であった。参考例1~3の発酵後のpHは比較例1と比較して低くなっており、発酵乳の製造が速くなった。発酵後のpHは、中性プロテアーゼ添加量が多いほど低くなった。
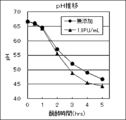
発酵乳を製造するまでの牛乳中タンパク質変化をSDS-PAGEで検討した(参考例4)。スターターとしてYF-L812を使用し、100 mg/mLとなるように滅菌水で懸濁した。原料乳として、牛乳(明治おいしい牛乳)を使用した。牛乳は100 mL三角フラスコに100 gを2本分注し、滅菌済みスターラーバーを投入し、43℃でプレインキュベートした。ペニバチルス属由来の中性プロテアーゼ添加量は、2,500 PU/mL希釈液で40μL(終濃度として1 PU/g相当)とした。スターターは100 mgを1,000μLの滅菌水に懸濁し、三角フラスコに対して100μL(Final 10 mg/100 g)添加した。スターターおよび酵素添加後は43℃に保温したまま数分間撹拌し、各三角フラスコより約13 mL/15 mL遠沈管6本に分注し、43℃で醗酵した。遠沈管は経時的にサンプリングし、pH測定およびSDS-PAGE用サンプル調製を行った。SDS-PAGE用サンプルは、得られた発酵乳を超純水で20倍希釈し、SDS-PAGE用サンプルバッファーと1:1で混合し、5分間煮沸することにより調製した。SDS-PAGEは12.5%アクリルアミドゲルを用い、定法に従い行った。なお、サンプルは1レーンあたり10μLアプライした。醗酵中pHの推移は図1に示した。マーカーは図1中に「M」で示しており、その単位はkDaである。中性プロテアーゼ添加醗酵により醗酵が加速する現象が再現した。SDS-PAGEの結果は図2に示した。牛乳中のタンパク質は、酵素無添加の醗酵においては、醗酵開始時より5時間目まで全く変化がなく、カゼイン蛋白の凝固により発酵乳ができるが、タンパク質そのものの分解はほとんど生じていないことが明らかとなった。一方、中性プロテアーゼ添加醗酵の場合、醗酵開始30分後にはκカゼイン(25kDa強のバンド)が消失していることがわかった。
中性プロテアーゼの終濃度を0.5PU/gとした以外は参考例1と同様にして、参考例5の発酵乳を得た。
参考例5と同時に行った以外は比較例1と同様にして、中性プロテアーゼ処理を行わない比較例2の発酵乳を得た。中性プロテアーゼ処理を行った参考例5において、発酵中にBB-12株が良好な増殖を示した。発酵終了時点での参考例5と比較例2との差はおよそ75%であった。
市販のスキムミルク(森永乳業社製)を2質量部、市販の牛乳(明治乳業社製)を98質量部で混合、溶解して100℃で5分の殺菌処理を行った。殺菌処理後に原料乳を43℃まで冷却し、終濃度0.1~4.0PU/g)の中性プロテアーゼと0.05質量部(終濃度2.5NLU/g)の中性ラクターゼと乳酸菌(YF-L812株)0.1mg/原料乳1mLとビフィズス菌0.05mg/原料乳1mLを添加して43℃で4時間発酵させ、実施例1~3の発酵乳を得た(中性プロテアーゼ、中性ラクターゼ同時添加)。
図示していないが、中性ラクターゼを終濃度で0.5NLU/g~10NLU/gにしたとき、ほぼ濃度依存的なビフィズス菌増殖効果を確認できた。中性ラクターゼと中性プロテアーゼの併用効果を確認しやすくするために、実施例1~4では中性ラクターゼを終濃度で2.5NLU/gとして試験を行った。
実施例1~3と同時にした以外は、比較例1と同様にして中性プロテアーゼ処理及び中性ラクターゼ処理を行わない比較例3の発酵乳を得た。
終濃度が0.5PU/gになるよう中性プロテアーゼを添加した以外は実施例1と同様にして、実施例4の発酵乳を得た(中性プロテアーゼ、中性ラクターゼ同時添加)。
実施例4と同時にした以外は、比較例1と同様にして中性プロテアーゼ処理及び中性ラクターゼ処理を行わない比較例4の発酵乳を得た。
このように、中性ラクターゼと中性プロテアーゼによる乳中の分解物質とそれによるビフィズス菌の増殖効果は異なることから、中性ラクターゼと中性プロテアーゼを併用することで、さらにビフィズス菌が増殖しやすい環境にすることができるものと推測される。
本実施例では中性ラクターゼを1つの濃度でしか検討していないが、中性ラクターゼと中性プロテアーゼの作用メカニズムの違いと、中性ラクターゼ単独では0.5NLU/g~10NLU/gにしたとき、ほぼ濃度依存的なビフィズス菌増殖効果を確認できたことから、中性ラクターゼを0.5NLU/g~10NLU/gに設定し中性プロテアーゼを添加すれば、それらの添加濃度によってビフィズス菌増殖効果が得られるものと期待される。
Claims (6)
- 原料乳と、乳酸菌と、ビフィズス菌と、を混合する第1工程と、
前記原料乳を発酵させる第2工程と、
を順次行う発酵乳製品の製造方法であって、
上記第2工程が終了する前に、上記原料乳に、κ-カゼインを分解するエンド型の中性プロテアーゼを添加する工程(プロテアーゼ添加工程)を行い、且つ、前記中性プロテアーゼの活性が前記原料乳に加えるときの終濃度で0.01~100PU/gの範囲内にあることを特徴とする発酵乳製品の製造方法。 - 前記プロテアーゼ添加工程を行うことで、κ-カゼイン分解物であるペプチド又は遊離アミノ酸を増大させ、前記乳酸菌と前記ビフィズス菌に当該ペプチド又は当該遊離アミノ酸を取り込ませることを特徴とする請求項1に記載の発酵乳製品の製造方法。
- 前記プロテアーゼ添加工程を、前記第1工程の前又は前記第1工程と略同時に行うことを特徴とする請求項1または2に記載の発酵乳製品の製造方法。
- 前記原料乳に対するプロテアーゼ反応の時間が0.5時間~48時間であることを特徴とする請求項1に記載の発酵乳製品の製造方法。
- 前記第2工程が終了する前に、前記原料乳に中性ラクターゼを添加する工程(ラクターゼ添加工程)を行うことを特徴とする請求項1に記載の発酵乳製品の製造方法。
- 前記中性ラクターゼの活性(NLU/g)と前記中性プロテアーゼの活性(PU/g)の比が0.01~100の範囲内にあることを特徴とする請求項5に記載の発酵乳製品の製造方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2016212473 | 2016-10-31 | ||
| JP2016212473 | 2016-10-31 | ||
| PCT/JP2017/039035 WO2018079758A1 (ja) | 2016-10-31 | 2017-10-30 | 発酵乳製品の製造方法及び酵素含有組成物 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2018079758A1 JPWO2018079758A1 (ja) | 2019-11-21 |
| JP7401970B2 true JP7401970B2 (ja) | 2023-12-20 |
Family
ID=62023666
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018547810A Active JP7401970B2 (ja) | 2016-10-31 | 2017-10-30 | 発酵乳製品の製造方法及び酵素含有組成物 |
Country Status (2)
| Country | Link |
|---|---|
| JP (1) | JP7401970B2 (ja) |
| WO (1) | WO2018079758A1 (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP4166000A4 (en) * | 2020-06-16 | 2024-08-28 | Godo Shusei Co., Ltd. | PROCESS FOR PRODUCING A VEGETABLE MILK FERMENTATION PRODUCT |
| CN114806906B (zh) * | 2022-05-31 | 2023-02-21 | 江南大学 | 一株产中性乳糖酶的乳酸克鲁维酵母 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005521391A (ja) | 2002-02-15 | 2005-07-21 | カンパニー・ジェルベ・ダノン | 細菌起源の酵素による発酵乳製品の新規生産方法 |
| WO2014185364A1 (ja) | 2013-05-13 | 2014-11-20 | 合同酒精株式会社 | ラクターゼ含有組成物の製造法 |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN101316928B (zh) * | 2005-11-28 | 2014-12-10 | 帝斯曼知识产权资产管理有限公司 | 产生清洁味道的酶制剂 |
| US20170245513A1 (en) * | 2014-08-27 | 2017-08-31 | Godo Shusei Co., Ltd. | Lactase solution and milk using same |
| JP6789931B2 (ja) * | 2015-05-18 | 2020-11-25 | 合同酒精株式会社 | 発酵乳の製造方法 |
| WO2017104729A1 (ja) * | 2015-12-16 | 2017-06-22 | 合同酒精株式会社 | 発酵乳製品及びその製造方法 |
-
2017
- 2017-10-30 WO PCT/JP2017/039035 patent/WO2018079758A1/ja not_active Ceased
- 2017-10-30 JP JP2018547810A patent/JP7401970B2/ja active Active
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005521391A (ja) | 2002-02-15 | 2005-07-21 | カンパニー・ジェルベ・ダノン | 細菌起源の酵素による発酵乳製品の新規生産方法 |
| WO2014185364A1 (ja) | 2013-05-13 | 2014-11-20 | 合同酒精株式会社 | ラクターゼ含有組成物の製造法 |
Non-Patent Citations (1)
| Title |
|---|
| 生物工学会誌,2016年05月,vol.94 no.5,p.238-241 |
Also Published As
| Publication number | Publication date |
|---|---|
| JPWO2018079758A1 (ja) | 2019-11-21 |
| WO2018079758A1 (ja) | 2018-05-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| MUIR | The shelf‐life of dairy products: 1. Factors influencing raw milk and fresh products | |
| EP2234501B1 (en) | Method for producing a low-lactose dairy product | |
| EP3391750B1 (en) | Method for manufacturing a fermented dairy product | |
| US12215367B2 (en) | Lactase enzymes with improved properties | |
| JP6789931B2 (ja) | 発酵乳の製造方法 | |
| KR101018274B1 (ko) | 발효유의 제조방법 | |
| EP3021679B1 (en) | Streptococcus thermophilus strains | |
| JP4802216B2 (ja) | ビフィドバクテリウム属菌含有組成物及びビフィドバクテリウム属菌含有組成物の製造方法 | |
| EP4166000A1 (en) | Method for producing plant-based milk fermentation product | |
| Yonezawa et al. | Improved growth of bifidobacteria by cocultivation with Lactococcus lactis subspecies lactis | |
| EP3329783B1 (en) | Method for producing an acidified milk product | |
| US20240032553A1 (en) | Frozen enzyme pellets | |
| EP1474001B1 (fr) | Nouveau procede de fabrication de produits laitiers fermentes | |
| JP7401970B2 (ja) | 発酵乳製品の製造方法及び酵素含有組成物 | |
| AU2020310445A1 (en) | Process for preparing an acidified milk product | |
| JPWO2009150888A1 (ja) | 乳タンパク質分解物、乳タンパク質分解物の製造方法及びビフィズス菌増殖促進剤 | |
| Roy et al. | Enzymes in milk, cheese, and associated dairy products | |
| Rajakari | Structure modification of sour milk products by transglutaminase |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190308 |
|
| AA64 | Notification of invalidation of claim of internal priority (with term) |
Free format text: JAPANESE INTERMEDIATE CODE: A241764 Effective date: 20190716 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190822 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20201027 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20201027 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20211130 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220126 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20220531 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220810 |
|
| C60 | Trial request (containing other claim documents, opposition documents) |
Free format text: JAPANESE INTERMEDIATE CODE: C60 Effective date: 20220810 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20220818 |
|
| C21 | Notice of transfer of a case for reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C21 Effective date: 20220823 |
|
| A912 | Re-examination (zenchi) completed and case transferred to appeal board |
Free format text: JAPANESE INTERMEDIATE CODE: A912 Effective date: 20221021 |
|
| C211 | Notice of termination of reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C211 Effective date: 20221025 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20231208 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7401970 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |