JP7305300B2 - 併用免疫療法 - Google Patents
併用免疫療法 Download PDFInfo
- Publication number
- JP7305300B2 JP7305300B2 JP2017525120A JP2017525120A JP7305300B2 JP 7305300 B2 JP7305300 B2 JP 7305300B2 JP 2017525120 A JP2017525120 A JP 2017525120A JP 2017525120 A JP2017525120 A JP 2017525120A JP 7305300 B2 JP7305300 B2 JP 7305300B2
- Authority
- JP
- Japan
- Prior art keywords
- slc
- cells
- tumor
- cancer
- cell
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/52—Cytokines; Lymphokines; Interferons
- C07K14/521—Chemokines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/19—Cytokines; Lymphokines; Interferons
- A61K38/195—Chemokines, e.g. RANTES
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/0005—Vertebrate antigens
- A61K39/0011—Cancer antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/3955—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against proteinaceous materials, e.g. enzymes, hormones, lymphokines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/39558—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against tumor tissues, cells, antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K40/00—Cellular immunotherapy
- A61K40/10—Cellular immunotherapy characterised by the cell type used
- A61K40/19—Dendritic cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K40/00—Cellular immunotherapy
- A61K40/20—Cellular immunotherapy characterised by the effect or the function of the cells
- A61K40/24—Antigen-presenting cells [APC]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K40/00—Cellular immunotherapy
- A61K40/30—Cellular immunotherapy characterised by the recombinant expression of specific molecules in the cells of the immune system
- A61K40/36—Immune checkpoint inhibitors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K40/00—Cellular immunotherapy
- A61K40/40—Cellular immunotherapy characterised by antigens that are targeted or presented by cells of the immune system
- A61K40/41—Vertebrate antigens
- A61K40/42—Cancer antigens
- A61K40/4231—Cytokines
- A61K40/4236—Chemokines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/24—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against cytokines, lymphokines or interferons
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/24—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against cytokines, lymphokines or interferons
- C07K16/249—Interferons
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2818—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against CD28 or CD152
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N7/00—Viruses; Bacteriophages; Compositions thereof; Preparation or purification thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/51—Medicinal preparations containing antigens or antibodies comprising whole cells, viruses or DNA/RNA
- A61K2039/525—Virus
- A61K2039/5256—Virus expressing foreign proteins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/54—Medicinal preparations containing antigens or antibodies characterised by the route of administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/545—Medicinal preparations containing antigens or antibodies characterised by the dose, timing or administration schedule
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2239/00—Indexing codes associated with cellular immunotherapy of group A61K40/00
- A61K2239/31—Indexing codes associated with cellular immunotherapy of group A61K40/00 characterized by the route of administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2239/00—Indexing codes associated with cellular immunotherapy of group A61K40/00
- A61K2239/38—Indexing codes associated with cellular immunotherapy of group A61K40/00 characterised by the dose, timing or administration schedule
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2239/00—Indexing codes associated with cellular immunotherapy of group A61K40/00
- A61K2239/46—Indexing codes associated with cellular immunotherapy of group A61K40/00 characterised by the cancer treated
- A61K2239/55—Lung
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2710/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA dsDNA viruses
- C12N2710/00011—Details
- C12N2710/10011—Adenoviridae
- C12N2710/10041—Use of virus, viral particle or viral elements as a vector
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2710/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA dsDNA viruses
- C12N2710/00011—Details
- C12N2710/10011—Adenoviridae
- C12N2710/10041—Use of virus, viral particle or viral elements as a vector
- C12N2710/10043—Use of virus, viral particle or viral elements as a vector viral genome or elements thereof as genetic vector
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2710/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA dsDNA viruses
- C12N2710/00011—Details
- C12N2710/10011—Adenoviridae
- C12N2710/10071—Demonstrated in vivo effect
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Organic Chemistry (AREA)
- Immunology (AREA)
- Pharmacology & Pharmacy (AREA)
- Genetics & Genomics (AREA)
- Engineering & Computer Science (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Microbiology (AREA)
- Zoology (AREA)
- Mycology (AREA)
- Gastroenterology & Hepatology (AREA)
- Oncology (AREA)
- Biotechnology (AREA)
- Biomedical Technology (AREA)
- Wood Science & Technology (AREA)
- Endocrinology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Dermatology (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Toxicology (AREA)
- Virology (AREA)
- General Engineering & Computer Science (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Peptides Or Proteins (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Description
本願は、2014年11月5日に出願された米国仮特許出願第62/075,532号の優先権を主張する。その内容は参照により本明細書において援用する。
本発明は、癌などの病理学的状態に関連するものを含めた哺乳動物生理学的プロセスを調節するために二次リンパ器官ケモカインを使用する方法に関する。
発癌性、癌退行、再発及び転移に影響を与える免疫機構を理解することは、新規免疫療法の開発の重要な側面である。この状況において、当業者であれば、免疫応答の基本的な側面は、生物の免疫細胞が自己免疫抗原と非自己抗原とを区別することができることであると理解する。したがって、癌における免疫機構を解明しようとする臨床関連モデルは、腫瘍細胞が宿主免疫系の細胞と遺伝的背景を共有する(すなわち、同系である)という事実を考慮しなければならない。残念ながら、動物に癌細胞系を導入する癌の多くの動物モデルは、宿主動物の遺伝的背景と評価されている癌細胞系との間の差異に影響を受ける免疫応答によって混乱を来してしまう。具体的には、宿主動物及び癌細胞株が本質的に同一の遺伝的背景を共有しない癌モデルでは、個体間での移植臓器の拒絶反応に見られるものに類似する宿主の免疫系による「非自己」免疫応答に関連する問題を含めて、様々な問題がある。自発癌細胞上の非自己抗原(癌では当然には生じない現象)の宿主免疫系認識から生じる場合のある非自己免疫応答は、ヒト癌では起こらない癌細胞に対する免疫応答を生じさせる。したがって、癌の発生及び進行を忠実に模倣し、それによって免疫機構の臨床的に関連する分析を行うことができるようにする癌モデルが絶えず必要とされている。
本明細書に開示される発明は、本質的に同一の遺伝的背景を有する宿主動物及び癌細胞を利用することによって、癌における免疫機構を忠実に模倣する動物モデルを提供する。これらのモデルは、SLCが同系癌細胞に対する効果的な細胞仲介免疫応答を編成する能力を実証するために使用される。さらに、これらのモデルを使用して、同系癌細胞に対するSLC調節免疫応答に関連する宿主サイトカインプロファイルを評価することができる。
本発明は、CCL21(SLC)をチェックポイント阻害剤と組み合わせて投与して、腫瘍進行に関与する免疫系を調節することを含む、腫瘍の治療方法、腫瘍体積の減少方法及び癌の進行の減少方法を提供する。
本発明は、二次リンパ組織-組織ケモカイン(SLC)が、同系腫瘍細胞に対する免疫応答におけるサイトカインプロファイルを調節し、これらの細胞の増殖を阻害することができるという本明細書で開示された発見に基づくものである。ここで提供される開示は、マウスが自発的に腫瘍を発生させる臨床関連マウスモデルにおけるSLCの抗腫瘍効率を実証するものである。例えば、組換えSLCの注射(例えば、腋窩リンパ節領域内)により、腫瘍の広範なリンパ球及びDC浸潤と生存の延長とを伴ってこの同系腫瘍負荷が有意に減少する。SLC注射により、腫瘍部位、リンパ節及び脾臓におけるCD4及びCD8リンパ球並びにDCが有意に増加する。
本明細書中に開示されるいくつかの方法は、当該技術分野において、宿主動物に投与された遺伝的に非同一の癌細胞などの非自己(すなわち、同種異系)組織に対する免疫応答の状況においてSLCの効果を研究するために使用できることが知られている一般的な方法に関する。
細胞傷害性Tリンパ球抗原4(CTLA-4)(CD152)は、T細胞活性化のB7-1/B7-2調節経路に関与する周知の共刺激分子である。CTLA-4は、ヘルパーT細胞の表面上で発現し、T細胞に阻害シグナルを伝達する(例えば、Krummel外,J.Exp.Med.182(2):459-65,1995参照)。CTLA-4に結合する抗体としては、イピリムマブ及びトレミリムマブが挙げられる。
本明細書で開示される発明は多くの実施形態を有する。本発明の好ましい実施形態は、哺乳動物又は哺乳動物由来の細胞集団において、細胞集団を、本明細書に記載されるトランスジェニックマウスモデルにおいて生じる自発性癌腫細胞などの同系腫瘍細胞の増殖を阻害するのに十分な量の二次リンパ組織ケモカイン(SLC)に曝露することによってサイトカイン発現を達成又は調節する(例えば、既存のサイトカインプロファイルを変化させる)方法である。ここに開示されるように、本明細書に開示される同系モデルは、SLCの添加がどのようにサイトカイン発現を協調的に調節し、かつ、腫瘍細胞の増殖を阻害するかを示すため、これらの現象の観察(サイトカイン発現の調節及び腫瘍増殖の阻害)は見込まれる免疫刺激性又は免疫阻害性試験化合物の効果を評価するように設計された細胞系アッセイで使用できる。例えば、本明細書で提供される開示は、試験化合物がSLCのサイトカイン発現調節能力に及ぼす影響を試験すること、及び有利な態様でサイトカインプロファイルを調節する化合物を同定することを可能にする。
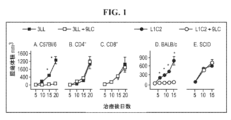
生体内での抗腫瘍応答の評価のために、2種の弱免疫原性肺癌、ライン1肺胞癌(L1C2、H-2d)及びルイス肺癌(3LL、H-2b)を利用した。これらの細胞を、10%FBS(Gemini Bioproducts、Calabasas、CA)、ペニシリン(100U/ml)、ストレプトマイシン、2mMグルタミン(JRH Biosciences、Lenexa、KS)を補充したRPMI1640(Irvine Scientific、Santa Ana、CA)を含む25cm3組織培養フラスコ中で単層として従来通り培養し、空気中5%CO2を含む加湿雰囲気中で37℃に維持した。細胞系はマイコプラズマ無添加であり、細胞を、液体N2から凍結ストック細胞を解凍する前に10継代まで使用した。腫瘍形成実験のために、105個の3LL又はL1C2腫瘍細胞に、C57BL/6又はBALB/cマウスの右上顎尖部領域に皮下注射によって接種し、腫瘍体積を週に3回監視した。5日齢の確立腫瘍を0.5μgのネズミ組換えSLC又はPBS希釈液(Pepro Tech、Rocky Hill、NJ)の腫瘍内注射により2週間にわたって週3回処置した。製造業者によって報告されたエンドトキシンレベルは、<0.1ng/μg(1EU/μg)のSLCであった。注射に使用されたSLCの量(0.5μg)は、製造業者によって提供された試験管内生物活性データによって決定された。総ネズミT細胞についてのSLCの最大走化活性は100ng/mlであった。SLC仲介性抗腫瘍特性の生体内評価のために、出願人は、各腫瘍内注射に対してこの量よりも5倍多く利用した。同量のマウス血清アルブミン(Sigma、St.Louis、MO)を対照注射用の無関係なタンパク質として利用した腫瘍形成実験も行った。腫瘍接種時にSLCを投与する実験も行った。SLC投与後の抗腫瘍応答を仲介する際の免疫系の重要性を決定するために、SCIDベージュCB17マウスにおいて腫瘍形成実験を行った。SLCを腫瘍接種の時点で、続いて週に3回皮下注射により投与した。CD4及びCD8ノックアウトマウスを利用して、腫瘍撲滅におけるCD4及びCD8細胞の寄与を決定した。各腫瘍の2つの二等分線直径をキャリパーで測定した。容積は、式(0.4)(ab2)を用いて計算し、ここでaはより大きい直径であり、bはより小さな直径である。
腫瘍、リンパ節及び脾臓におけるサイトカインプロファイルを、以前に記載されたように(Sharma外,J.Immunol.163:5020)SLC及び希釈剤処置マウスの両方で測定した。非壊死性腫瘍を採取し、小片に切断し、ふるい(Bellco Glass、Vineland、NJ)を通過させた。腫瘍排出性リンパ節及び脾臓を、SLC処置腫瘍保有腫瘍、対照腫瘍保有マウス及び正常対照マウスから採取した。リンパ節と脾臓とを解きほぐし、RBCを二重蒸留水で枯渇させ、1×PBSで張性にした。腫瘍結節について、一晩培養した後の上清中においてIL-10、IL-12、GM-CSF、IFN-γ、TGF-β、血管内皮増殖因子(VEGF)、IFN-γ(MIG)によって誘導されるモノカインの産生、並びにELISAによりIP-10及び酵素免疫測定法(EIA)によりPGE2について評価した。腫瘍由来サイトカイン及びPGE2濃度をブラッドフォードアッセイ(Sigma、St.Louis、MO)により総タンパク質に対して補正した。照射腫瘍細胞(5×106細胞/ml)による二次刺激後のサイトカイン測定のために、脾臓又はリンパ節由来のリンパ球を5mlの総容量で照射3LL(105細胞/ml)と共に50:1の比で共培養した。一晩培養した後に上清を回収し、ELISAによってGM-CSF、IFN-γ、IL-12及びIL-10を決定した。
腫瘍結節、リンパ節及び脾臓由来のサイトカインタンパク質濃度を、以前に記載されたように(Huang外,Cancer Res.58:1208)ELISAによって決定した。簡潔に説明すると、96ウェルCostar(Cambridge、MA)プレートを、測定されるサイトカインに対する4μg/mlの適切な抗マウスmAbで一晩被覆した。このプレートのウェルをPBS中の10%ウシ胎仔血清(Gemini Bioproducts)で30分間ブロックした。次いで、プレートをAgと共に1時間インキュベートし、過剰のAgをPBS-Tweenで洗い流した。プレートを適切なサイトカインに対する2μg/mlのビオチン化mAb(PharMingen、San Diego、CA)と共に30分間インキュベートし、そして過剰のAbをPBS-Tweenで洗い流した。プレートをアビジンペルオキシダーゼと共にインキュベートし、OPD基質中で所望の消光までインキュベートした後、その後の色の変化をMicroplate Reader(Molecular Dynamics、Sunnyvale、CA)を用いて490nmで読み取った。アッセイの標準物質として使用された組換えサイトカインはPharMingenから得た。IL-12(Biosource)及びVEGF(Oncogene Research Products、ケンブリッジ、マサチューセッツ州)を製造者の指示に従ってキットにより決定した。MIG及びIP-10を、以前に記載されたような二重リガンド法の改変によって定量した(Standiford外,J.Clin.Invest.86:1945)。MIG及びIP-10抗体及びタンパク質は、R&D(ミネソタ州ミネアポリス)から入手した。 IL-10、GM-CSF、IFN-γ、TGF-β、MIG及びIP-10 ELISAの感受性は15pg/mlであった。IL-12及びVEGFについて、感受性は5μg/mlであった。
PGE 2濃度を、以前に記載されたように(Huang外,Cancer Res.58:1208)、メーカーの指示に従ってCayman Chemical(Ann Arbor、MI)製のキットを用いて決定した。EIAプレートをMolecular Dynamics Microplate Readerで読み取った。
細胞溶解活性を以前に記載されているように評価した(Sharma外,J.Immunol.163:5020)。照射された腫瘍細胞による二次刺激後の腫瘍細胞溶解を定量するために、SLC処置及び希釈剤腫瘍保持マウスからのリンパ節由来リンパ球(5×106細胞/ml)を、照射3LL(105細胞/ml)と共に5mlの総体積中において50:1の比で培養した。5日間の培養後、リンパ節由来リンパ球の溶解能を、96ウェルプレートにおいて様々なE:Tでクロム標識した(51Cr、Amersham Arlington、Heights、IL;sp.act.250-500mCi/mg)3LL標的に対して4時間にわたって決定した。5%トリトンXによる自然放出及び最大放出も評価した。4時間のインキュベーション後に上清を除去し、ガンマカウンター(Beckman、Fullerton、CA)で活性を測定した。%特異的溶解を次式:%溶解=100×(実験cpm-自然放出)/(最大放出-自然放出)によって算出した。
フローサイトメトリー実験のために、2種又は3種の蛍光色素(PE、FITC及びTri-color)(PharMingen)を使用して腫瘍結節単一細胞懸濁液のCD3 Tリンパ球集団をゲートした。DCを、腫瘍結節及びリンパ節内のCD11c及びDEC205の明るい集団として定義した。順方向及び側方散乱プロファイルに基づいてゲーティングすることにより、細胞をリンパ球又はDCとして同定した。フローサイトメトリー分析は、カリフォルニア大学ロサンゼルス校のJonsson Cancer Center Flow Cytometry Core FacilityのFACScanフローサイトメーター(Becton Dickinson、San Jose、CA)で行った。5,000~15,000個のゲートイベントを収集し、Cell Questソフトウェア(Becton Dickinson)を用いて分析した。
SLC処置及び希釈剤処置3LL腫瘍保有マウスの腫瘍結節及びリンパ節の単一細胞懸濁液からのTリンパ球を、蒸留し脱イオンしたH2OでRBCを枯渇させ、細胞質内GM-CSF及びIFN-γの存在について評価した。細胞懸濁液を、製造者の指示に従ってタンパク質輸送阻害剤キットGolgiPlug(PharMingen)で処理した。細胞を採取し、2%FBS-PBSで2回洗浄した。細胞(5×105)を、細胞表面抗原であるCD3、CD4及びCD8に特異的な0.5μgのFITC結合mAbと共に200μlの2%FBS-PBS中に4℃で30分間再懸濁した。2%FBS-PBSで2回洗浄した後に細胞を固定し、透過処理し、Cytofix/Cytopermキット(PharMingen)を用いて製造業者のプロトコールに従って洗浄した。細胞ペレットを100μlのPerm/Wash溶液に再懸濁し、細胞内染色のために0.25μgのPE結合抗GM-CSF抗体及び抗IFN-γm抗体で染色した。細胞を暗所において室温で30分間インキュベートし、2回洗浄し、300μlのPBS、2%パラホルムアルデヒド溶液に再懸濁し、そしてフローサイトメトリーで分析した。
以下の表4は、例示的なヒト及びネズミSLCポリペプチド配列を与える。
ここで与える開示は、2種の同系移植マウス肺癌モデルを利用してSLCの抗腫瘍特性を試験する。いずれのモデルにおいても、腫瘍内SLC投与は、希釈剤処置腫瘍保有対照マウス(p<0.01)と比較して腫瘍体積の有意な減少をもたらし、40%のマウスが完全な腫瘍撲滅を示した(図1A及びD)。腫瘍体積の減少がL1C2及び3LLに及ぼすSLCの直接的な影響に起因するかどうかを決定するために、腫瘍細胞の試験管内増殖をSLCの存在下で評価した。12ウェルCostarプレートに播種された105個のL1C2細胞及び3LL細胞にSLC(200ng/ml)を添加し、細胞数を3日間にわたって毎日モニターした。SLCはこれらの腫瘍細胞の生体内増殖速度を変化させなかった。
1.細胞培養
10%FBS(GeminiBioproducts、Calabasas、CA)、ペニシリン(100単位/ml)、ストレプトマイシン(0.1mg/ml)及び2mMグルタミン(JRH Biosciences、Lenexa、KS)を補充したRPMI1640(Irvine Scientific、Santa Ana、CA)で増殖させた新たに切除した肺腫瘍からクララ細胞肺腫瘍細胞(CC-10タグ及びH-2q)から誘導し、空気中5%CO2を含む加湿雰囲気において37℃で維持した。2回の生体内継代後に、CC-10 TAg腫瘍クローンを単離した。細胞株はマイコプラズマフリーであり、液体窒素から凍結ストック細胞を解凍する前に細胞を10継代まで使用した。
これらの研究では、SV40large TAgがネズミクララ細胞特異的プロモーターの制御下で発現するトランスジェニックCC-10 TAgマウスを使用した(Magdaleno外,Cell Growth Differ.,8:145-155,1997)。導入遺伝子を発現する全てのマウスは、びまん性両側気管支肺胞癌を発症した。腫瘍は、4週齢程度の早い段階で顕微鏡検査によって両側的に明らかであった。3ヵ月後、腫瘍増殖の気管支肺胞パターンが合体して、複数の両側性腫瘍結節を形成した。CC-10 TAgトランスジェニックマウスの平均寿命は4ヶ月であった。胸腔内転移は認められなかった。これらのマウスの繁殖ペアは、寛大にもFrancesco J.DeMayo(Baylor College of Medicine、TX、Houston)によって提供された。トランスジェニックマウスをWest Los Angeles Veteran Affairs動物施設で飼育し、動物研究施設で維持した。CC-10 TAgトランスジェニックマウスを用いた各実験の前に、導入遺伝子の存在をマウス尾生検のPCRによって確認した。5’プライマー配列は、SM19-TAG:5’-TGGACCTTCTAGGTCTTGAAAGG-3’(配列番号3)であり、3’プライマー配列は、SM36-TAG:5’-AGGCATTCCACCACTGCTCCCATT-3’(配列番号4)であった。得られたPCRフラグメントのサイズは650bpである。10mMのTris-HCl(pH8.3)、50mMのKCl、200μMの各デオキシヌクレオチドトリホスフェート、0.1μMのプライマー、2.5mMのMgCl2及び2.5単位のTaqポリメラーゼを含有する総容量50μlでDNA(1μg)を増幅させた。PCRはPerkin-Elmer製DNAサーマルサイクラー(Norwalk、CT)で行った。SV40導入遺伝子についての増幅プロファイルは、94℃で3分間の変性、58℃で1分間のアニーリング、72℃で1分間の伸長の40サイクル、続いて94℃で1分間の変性及び同じアニーリング及び伸長条件の39サイクルからなるものであった。最後のサイクルの伸長工程は10分であった。増幅後、臭化エチジウムで染色した1.5%アガロースゲル上で生成物を分子量基準に対して視覚化した。全ての実験では、病原体を含まないCC-10 TAgトランスジェニックマウスを4~5週齢で使用した。
CC-10 TAgトランスジェニックマウスの腋窩リンパ節に、ネズミ組換えSLC(0.5μg/注射;Pepro Tech、Rocky Hill、NJ)又は等量のマウス血清アルブミン(Sigma Chemical Co.、ミズーリ州セントルイス)を対照注射のための無関係のタンパク質として含有する通常の生理食塩水希釈剤を注射した。4~5週齢から始めて、SLC又は対照注射液を8週間にわたって週に3回投与した。製造業者によって報告されたエンドトキシンレベルは、SLCの<0.1ng/μg(1エンドトキシン単位/μg)であった。SLCの用量は(0.5μg/注射)を、本発明者の以前の研究(Arenberg外,J.Exp.Med.184:981)及び製造業者によって提供された試験管内生体活性データに基づいて選択した。総ネズミT細胞についてのSLCの最大走化活性は100ng/mlであることが分かった。SLC仲介性抗腫瘍特性の生体内評価のために、各注射についてこの量よりも5倍多く使用した。4ヶ月後にマウスを屠殺し、肺を腫瘍表面積の定量のために単離した。腫瘍負荷は、較正された目盛り(1cm2の格子を100個の1mm2の正方形に細分した)でH&E染色切片の顕微鏡検査によって評価した。腫瘍がその面積の>50%を占めるグリッド正方形を陽性としてスコア化し、陽性の正方形の総数を以前に記載されたように決定した(Sharma外,J.Immunol.,163:5020-5028,1999)。肺の4つの組織学的切片からの10個の別々の視野を高倍率(×20対物レンズ)で検査した。各群の10匹のマウスを屠殺しなかったので、生存を評価することができた。
腫瘍、リンパ節及び脾臓におけるサイトカインプロファイルを、以前に記載されたように(Sharma外,J.Immunol.,163:5020-5028,1999)SLC及び希釈剤処置マウスの両方で測定した。非壊死性腫瘍を採取し、小片に切断し、ふるい(Bellco、Vineland、NJ)を通過させた。腋窩リンパ節及び脾臓を、SLC処置腫瘍保有マウス、対照腫瘍保有マウス及び正常対照マウスから採取した。リンパ節及び脾臓を解きほぐし、RBCをddH2Oで枯渇させ、1×PBSで張性にした。24時間の培養期間後に、腫瘍小結節の上澄をIL-10、IL-12、GM-CSF、IFN-γ、TGF-β、VEGF、MIG及びIP-10の産生についてELISAによって評価し及びEIAによってPGE-2の産生について評価した。腫瘍由来サイトカイン及びPGE-2濃度をブラッドフォードアッセイ(Sigma Chemical Co.)により全タンパク質について補正した。照射腫瘍細胞による二次刺激後のサイトカイン測定のために、脾臓細胞(5×106細胞/ml)を照射(100Gy、Cs137X線)CC-10 TAg腫瘍細胞(105細胞/ml)と共に全量5mlにおいて50:1の比で共培養した。24時間培養した後に上清を回収し、GM-CSF、IFN-γ及びIL-10をELISAによって決定した。
腫瘍結節、リンパ節及び脾臓由来のサイトカインタンパク質濃度を、以前に記載されているように(Sharma外,Gene Ther.,4:1361-1370,1997)ELISAによって決定した。簡潔に説明すると、96ウェルCostar(Cambridge、MA)プレートを、測定されるサイトカインに対する4μg/mlの適切な抗マウスmAbで一晩被覆した。プレートのウェルをPBS中10%FBS(ジェミニバイオプロダクツ社)で30分間ブロックした。次いで、プレートを抗原と共に1時間にわたってインキュベートし、過剰の抗原をPBS/Tween20で洗い流した。プレートを適切なサイトカインに対する2μg/mlビオチン化mAb(PharMingen)と30分間インキュベートし、余分な抗体をPBS/Tween20で洗い流した。プレートをアビジンペルオキシダーゼと共にインキュベートし、O-フェニレンジアミン基質中で所望の消光までインキュベートした後、後の色の変化をMolecular Devices Microplate Reader(Sunnyvale、CA)を用いて490nmで読み取った。アッセイにおいて基準物質として使用された組換えサイトカインはPharMingenから得た。IL-12(Biosource)及びVEGF(Oncogene Research Products、マサチューセッツ州ケンブリッジ)を、製造者の指示に従ってキットを用いて決定した。MIG及びIP-10を、以前に記載されているような二重リガンド法の改変を用いて定量した(Standiford外,J.Clin.Investig.,86:1945-1953,1990)。MIG及びIP-10の抗体及びタンパク質をR&D(Minneapolis、MN)から得た。IL-10、GM-CSF、IFN-γ、TGF-β、MIG及びIP-10のELISA感受性は15pg/mlであった。IL-12及びVEGFについて、ELISA感受性は5μg/mlであった。
PGE2濃度を、以前に記載されているように(Huang外,Cancer Res.,58:1208-1216,1998)メーカーの指示に従ってCayman Chemical Co.(Ann Arbor、MI)製のキットを用いて決定した。EIAプレートを、Molecular Devices Microplateリーダー(Sunnyvale、CA)によって読み取った。
フローサイトメトリー実験のために、2種又は3種の蛍光色素(PE、FITC及びTri-color)(PharMingen)を使用して腫瘍結節、リンパ節及び脾臓単一細胞懸濁液のCD3 Tリンパ球集団をゲートした。DCを、腫瘍結節、リンパ節及び脾臓内のCD11c及びDEC205の明るい集団として定義した。順方向及び側方散乱プロファイルに基づいてゲーティングすることにより、細胞をリンパ球又はDCとして同定した。フローサイトメトリー分析は、カリフォルニア大学ロサンゼルス校のJonsson Cancer Center Flow Cytometry Core FacilityのFACScanフローサイトメーター(Becton Dickinson、San Jose、CA)で行った。5,000~15,000個のゲートイベントを収集し、Cell Questソフトウェア(Becton Dickinson)を用いて分析した。
SLC処置及び希釈剤処置CC-10 TAgトランスジェニックマウスの腫瘍結節、リンパ節及び脾臓の単一細胞懸濁液からのTリンパ球を、蒸留し脱イオンしたH2OでRBCを枯渇させ、細胞質内GM-CSF及びIFN-γの存在について評価した。細胞懸濁液を、製造者の指示に従ってタンパク質輸送阻害剤キットGolgiPlug(PharMingen)で処理した。細胞を採取し、2%FBS-PBSで2回洗浄した。細胞(5×105)を、細胞表面抗原であるCD3、CD4及びCD8に特異的な0.5μgのFITC結合mAbと共に200μlの2%FBS-PBS中に4℃で30分間再懸濁した。2%FBS-PBSで2回洗浄した後に細胞を固定し、透過処理し、Cytofix/Cytopermキット(PharMingen)を用いて製造業者のプロトコールに従って洗浄した。細胞ペレットを100μlのPerm/Wash溶液に再懸濁し、細胞内染色のために0.25μgのPE結合抗GM-CSF抗体及び抗IFN-γm抗体で染色した。細胞を暗所において室温で30分間インキュベートし、2回洗浄し、300μlのPBS、2%パラホルムアルデヒド溶液に再懸濁し、そしてフローサイトメトリーで分析した。
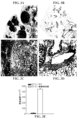
実施例3に記載の材料及び方法を使用して、SV40の大きなTAgがネズミクララ細胞特異的プロモーターの制御下で発現するトランスジェニックマウスにおける自発気管支肺胞細胞癌モデルにおけるSLCの抗腫瘍効力を評価した(Magdaleno外,Cell Growth Differ.,8:145-155,1997)。導入遺伝子を発現するマウスは、びまん性両側気管支肺胞癌を発症し、平均寿命は4ヶ月である。SLC(0.5μg/注射)又は同濃度のネズミ血清アルブミンを4週齢から始めて1週間あたり3回、8週間継続して腋窩リンパ節領域に注射した。対照マウスが進行性の肺腫瘍の増殖のため死亡し始めた4ヶ月目に、マウスを全ての処置群で屠殺し、肺を単離し、パラフィン包埋した。対照処置マウスからのパラフィン包埋肺腫瘍切片のH&E染色から、両肺全体に大きな腫瘍塊が明らかになり、リンパ球浸潤は最小限であった(図3A及びC)。対照的に、SLC処置マウスは、広範なリンパ球浸潤を伴う有意に小さな腫瘍結節を有していた(図3B及びD)。SLCで処置したマウスは、希釈剤処置した対照マウスと比較して、肺腫瘍の負荷が著しく減少した(図3E)。SLC処置マウスは対照注射を受けたマウスと比較して生存期間が延長した。対照処置マウスについて生存期間の中央値は18±2週間であったが、SLCで処置したマウスの生存期間の中央値は34±3週間であった(P<0.001)。
腫瘍進行が宿主サイトカインプロファイルによって改変され得ることを示す以前の報告に基づいて(Alleva外,J.Immunol.,153:1674-1686,1994;Rohrer外,J.Immunol.,155:5719- 5727,1995)、SLC療法後の腫瘍部位、リンパ節及び脾臓からのサイトカイン産生を評価した。組換えSLCで処置したCC-10 TAgマウスの肺、脾臓及びリンパ節におけるサイトカインプロファイルを、腫瘍を有する希釈剤処置対照マウス及び非腫瘍保有対照のマウスと比較した。CC-10 TAgマウスのSLC処置は1型サイトカインの全身性誘導をもたらしたが、免疫抑制性メディエーターの産生を減少させた。肺、リンパ節及び脾臓を採取し、24時間の培養期間後に、上清をVEGF、IL-10、IFN-γ、GM-CSF、IL-12、MIG、IP-10及びTGF-βの存在についてELISAにより評価し、PGE-2の存在についてEIAにより評価した。SLCで処置したCC-10 TAgマウスは、希釈剤処置群の肺と比較して、VEGF(3.5倍)及びTGF-β(1.83倍)の有意な減少を示したが、IFN-γ(160.5倍)、IP-10(1.7倍)、IL-12(2.1倍)、MIG(2.1倍)及びGM-CSF(8.3倍;表1B)の増加を示した。希釈剤処置群と比較して、SLC処置CC-10 TAgマウス由来の脾細胞は、PGE-2(14.6倍)及びVEGF(20.5倍)のレベルの減少を示したが、GM-CSF(2.4倍)、IL-12(2倍)、MIG(3.4倍)及びIP-10(4.1倍;表1B)の増加を示した。SLCで処置したマウス由来のリンパ節由来細胞は、希釈剤処置したCC-10 TAgマウスと比較して、有意に向上したレベルのIFN-γ(2.2倍)、IP-10(2.3倍)、MIG(2.3倍)及びIL-12倍(2.5倍)を分泌したが、TGF-βのレベルは低下した(1.8倍;表1B)。免疫抑制メディエーターPGE-2及びIL-10は、SLC処置マウスの腫瘍部位では変化しなかった。しかし、SLC処置マウスの脾臓におけるPGE-2レベルの有意な減少があった。SLC投与が有意な特異的全身性免疫応答を誘導するかどうかを決定するために、SLC及び希釈剤処置CC-10 TAgマウスからの脾臓細胞を、放射線照射したCC-10 TAg腫瘍細胞と共に試験管内で24時間共培養し、そしてGM-CSF、IFN-γ及びIL-10をELISAによって決定した。照射腫瘍細胞による二次刺激の後、SLC処置腫瘍保有マウス由来の脾細胞は、有意に増加したレベルのIFN-γ(5.9倍)及びGM-CSF(2.2倍)を分泌した。対照的に、IL-10分泌は5倍減少した(表3B)。
GM-CSF及びIFN-γの細胞供給源を決定するために、腫瘍、リンパ節及び脾臓の単一細胞懸濁液をSLC及び希釈剤対照処置CC-10 TAgマウスから単離した。Tリンパ球浸潤及び細胞内サイトカイン産生をフローサイトメトリーによって評価した。細胞を染色して、各部位のDC浸潤を定量した。希釈剤処置対照群と比較して、SLC処置CC-10TAgマウスは、腫瘍部位、リンパ節及び脾臓で細胞がDC表面マーカーのCD11c及びDEC205を発現する頻度の有意な増加を示した(表2B)。同様に、希釈剤処置対照群と比較して、SLC処置CC-10 TAgの腫瘍部位、リンパ節及び脾臓でCD4及びD8細胞がIFN-γ及びGM-CSFを発現する頻度の有意な増加があった(表2B)。
ここで提示される研究は、SLC仲介抗腫瘍応答が腫瘍部位でのIFN-γ、IP-10及びMIGの同化作用の向上を伴うことを教示する。IP-10、MIG及びIFN-γは生体内で強力な抗腫瘍活性を有することが知られている。この文脈において、これらのサイトカインの増大がSLC仲介腫瘍減少におけるエフェクター分子として役立つかどうかを決定するために研究を行った。ここでは、SLC仲介抗腫瘍応答がサイトカインIP-10、MIG及びIFN-γを必要とすることを示す。
細胞培養及び腫瘍形成モデル
弱い免疫原性肺癌であるLewis肺癌(3LL、H-2b)を、生体内でのSLC仲介抗腫瘍応答に重要なサイトカインの評価に利用した。細胞を、10%ウシ胎仔血清(FBS)(Gemini Bioproducts、Calabasas、CA)、ペニシリン(100U/ml)、ストレプトマイシン(0.1mg/ml)、2mMグルタミン(JRH Biosciences、Lenexa、KS)を補充したRPMI1640培地(Irvine Scientific、Santa Anna、CA)を含む25cm3組織培養フラスコ中で単層として通常通り培養し、空気中5%CO2を含む加湿雰囲気中で37℃に維持した。細胞系はマイコプラズマフリーであり、液体N2から凍結ストック細胞を解凍する前に10継代まで使用した。腫瘍形成実験のために、105個の3LL腫瘍細胞をC57Bl/6の右上肩甲上領域に皮下注射し、腫瘍体積を週に3回モニターした。5日目に、確立された腫瘍を、0.5μgのネズミ組換えSLC又はPBS希釈液(Pepro Tech、Rocky Hill、NJ)の腫瘍内注射で週に3回2週間にわたって投与して処置した。製造業者によって報告されたエンドトキシンレベルは、1μg(1EU/μg)あたり0.1ng未満のSLCであった。注射に使用したSLCの量(0.5μg)を、製造業者によって提供された試験管内生物活性データによって決定した。総ネズミT細胞に対するSLCの最大走化活性は100ng/mlであることが分かった。SLC仲介抗腫瘍特性の生体内評価のために、各腫瘍内注射についてこの量よりも5倍多く利用した。同量のマウス血清アルブミン(Sigma、St.Louis、MO)を対照注射のために無関係なタンパク質として利用した腫瘍形成実験も行った。SLC処置の24時間前、次いで週3回、マウスを実験期間中に35mg/用量の抗IP-10又は抗MIG、及び100μg/用量の精製IFN-γ(ATCC R4562)又は35mg/用量の対照抗体で腹腔内投与により処置した。そこで投与された抗体の用量では、腫瘍部位でのそれぞれのサイトカインの有意な生体内枯渇があった。各腫瘍の2つの二等分線直径をキャリパーで測定した。容量は、式(0.4)(ab2)を用いて計算した。ここで、「a」はより大きい直径、「b」をより小さい直径とした。
MIG、IP-10及びIFN-γを、上記二重リガンド法の改変を用いて定量した。MIG及びIP10抗体並びに組換えサイトカインタンパク質は、R&D(Minneapolis、MN)から得た。IFN-γ抗体対及び組換えサイトカインはPharmingen製であった。IFN-γ、MIG及びIP-10のELISA感受性は15pg/mlであった。
SLCは直接的な抗血管新生効果を有することが証明されているため、本発明のモデルで観察された腫瘍の減少は、血管新生を阻害する際におけるIFN-γを分泌するT細胞によるT細胞依存性免疫並びに関与が原因である可能性がある。IFN-γは、抗癌免疫を促進する一連の生物学的効果を仲介する。MIG及びIP-10は、IFN-γによって誘導される強力な血管新生抑制因子であるため、本発明者は、これらがIFN-γに加えてSLC投与後の腫瘍縮小の一部を担うと推定した。
上記の実施例で提供されたデータは、SLCポリペプチドが生体内で同系T細胞依存性抗腫瘍応答をどのように仲介するのかを実証するものである。直接注射可能なベクターを使用した遺伝子治療系抗腫瘍アプローチを探索するために、本発明者はネズミSLC cDNA(Ad-SLC)を発現するアデノウイルス構築物を作製した。これらの構築物では、ネズミ二次リンパ系ケモカインのcDNAをInvitrogen製pMH4プラスミドのCMVプロモーターの下流にクローニングし、シャトルベクターとして使用した。
ヒトSLC cDNAを発現するアデノウイルス構築物などのベクターを使用して、ヒト遺伝子治療系抗腫瘍アプローチを採用できる。これらの構築物において、ヒト二次リンパ系ケモカイン用のcDNAを、CMVプロモーターなどの適切な程度の発現を可能にするプロモーターの下流にクローニングすることができる。
この例では、ex vivoで生成された遺伝子改変DCの腫瘍内投与を利用して、その場での腫瘍抗原取り込み及び提示を達成する方法を実証する。この実施例では、成熟宿主DCを腫瘍部位に引きつけるために、DCにCCL-21(二次リンパ組織ケモカイン(SLC))を発現するアデノウイルスベクター構築物を形質導入した。CCL-21は成熟DC及び活性化T細胞を強力に引きつけるので、CCL-21を発現するDCの腫瘍内注射(i.t.)により肺癌モデルにおいて強力な抗腫瘍応答が得られる。
背景
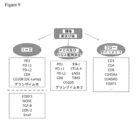
患者がCCL21を受けた(細胞仲介免疫応答を刺激しかつ血管新生を阻害することによって抗腫瘍応答を誘発するためにTech ID:20538/UC Case 2001-381-0ケモカインに記載されたCCL21遺伝子修飾DCの注射による腫瘍への導入を介して)最初の試験において、治療の開始時に肺癌細胞上でPDL1表面発現を上方調節した患者は、CCL21療法に対する特異的免疫応答が限られている又は全くないことが分かった。また、CCL21療法後にPDL1がさらに上昇した患者もいた。これは、抗体その他の手段によってPD1/PDL1経路を遮断することが、CCL21又はPD1/PDL1経路療法のいずれかを改善するための有効な手段であるという証拠となる。これは、併用療法が非常に有効であることを示している。
第I相非ランダム化用量漸増マルチコホート試験を実施してステージIIIB/IVのNSCLC患者を登録した。16人の患者がIT注射(0日目及び7日目)によりAd-CCL21-DCの用量で2回のワクチン接種を受けた(A、B、C又はD;1×106、5×106、1×107又は3×107個の細胞/注射)。末梢血を抗原特異的ELISPOTアッセイのために収集し、そして原発性肺癌のCT誘導針生検を、リアルタイムPCR及び免疫組織化学による細胞浸潤の評価によってPD-L1発現のために得た。
16人の被験体の末梢血をELISPOTアッセイによって評価した。陽性応答は、>20スポット/2×105細胞の絶対数(ポジティブレスポンダー;PR)を有するバックグラウンドを超えるスポット数の2倍の増加として定義した。混合応答は、ワクチン接種後の時点(混合レスポンダー;MR)と比較して0日目に高いIFN-γバックグラウンド発現を有する陽性応答として定義した。全レスポンダーの38%(6/16)に対して19%(3/16)のMR及び19%(3/16)MRがあった。平均PD-L1遺伝子コピー数は、7日目に394(MR)及び684(PR)と比較して1344(非レスポンダー;NR)であった。腫瘍CD8のT細胞浸潤は、40%(6/15;全被験者)、33%(3/9;NR)及び50%(3/6;MR及びPR)で誘導された。
SLC/CCL21遺伝子を発現する自己樹状細胞の腫瘍内投与は、(1)抗腫瘍特異的免疫応答が誘発され、かつ、より低いPD-L1発現と相関すること、及び(2)腫瘍へのCD8 T細胞浸潤が誘導されることを実証した。
組換えネズミCCL21(rmCCL21、SLC)又は関連する対照を、NSCLC肺腫瘍(それぞれ3LL又はLKR13)を有する同系マウス(C57/Bl6又は129/sv)に注射する。SLCを、腫瘍サイズが8×8mm(典型的には約d10)に達したときに腫瘍内に注射し、そして8日後に再度腫瘍内に注射して天然に存在する宿主抗腫瘍免疫応答を増大させる。以前の知見に基づいて、SLCはT細胞(ヘルパー及び細胞傷害性)及び有益なマクロファージを化学走性化するであろう。宿主の抗腫瘍免疫応答が上昇するにつれて、肺腫瘍は、T細胞上のPD-1受容体との結合についてのPD-L1及びPD-L2のアップレギュレーションを含めた免疫回避シグナル伝達事象を開始してT細胞を失活させ、かつ、腫瘍に対するT細胞の将来の動員を阻害するという証拠がある。このため、抗PD1(ネズミ)を、CCL21の最初の注射の2日後、その後実験の期間中4日ごとに腹腔内注射する。全体として、宿主抗腫瘍免疫応答はSLCで補強され、腫瘍の免疫回避は、抗PD1の適切なタイミングでの送達によって防止されることが予想される。これらのマウス研究の主要評価項目は腫瘍増殖率である。二次エンドポイントは、治療前浸潤(n=2マウス/群)に対する治療後(n=4マウス/群)の免疫細胞浸潤である。未処置対照群の腫瘍が22×22mm(典型的にはd28)に達したときに全ての処置後マウスを安楽死させる。これらの最初の併用研究の完了後に、抗PD1処置と組み合わせたときの同腹仔に適合したマウスからのCCL21遺伝子改変自己樹状細胞の腫瘍内注射の有効性を評価する。これらの前臨床試験の結果を使用して、進行期のNSCLC患者におけるこの組み合わせの安全性及び有効性を試験するように現在設計されている第I/II相臨床試験をガイドする。
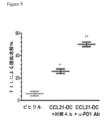
CCL21-DCは、肺癌のよく特徴付けられた同系KRASG12Dネズミモデルにおいて、単独療法として以前に評価されていた。このモデルでは、腫瘍成長の減少、自己腫瘍に対する腫瘍浸潤リンパ球(TIL)細胞溶解活性の増加、並びに腫瘍における及び脾臓における全身的にIFNγ及びTNFαの増加が観察された。同じLKR13マウスモデルを使用して、CCL21療法とチェックポイントインヒビター療法との組み合わせを分析した。抗PD-1抗体(1μg/ml)又は対照抗体(1μg/ml)n=8マウス/群の存在下で、自己腫瘍に対する試験管内T細胞細胞溶解活性を評価した。TILは、希釈剤CCL21-DC処置群の腫瘍由来であった。
Claims (19)
- 被験体において非小細胞肺癌(NSCLC)固形腫瘍を治療するか又はその再発を予防するための同時用途用の治療剤であって、次のa.及びb.を含む治療剤:
a.は、(i)SLCポリペプチド、(ii)該SLCポリペプチドをコードするポリヌクレオチドを発現可能なように含む組換えポリヌクレオチド、(iii)該組換えポリヌクレオチドを発現可能なように導入してなる細胞、又は(iv)それらの組み合わせから選択され、及び
b.は、PD-1阻害剤、PD1-L1阻害剤及びそれらの組み合わせから選択される免疫チェックポイント阻害剤である。 - 前記免疫チェックポイント阻害剤がPD-1阻害剤である、請求項1に記載の治療剤。
- 前記免疫チェックポイント阻害剤が抗体である、請求項2に記載の治療剤。
- 前記抗体がモノクローナル抗体である、請求項3に記載の治療剤。
- 前記PD-1阻害剤がニボルマブ、ペムブロリズマブ、ピジリズマブ、ラムブロリズマブ、BGBA317、AMP-224、AMP224、AUNP12、BGB108、MCLA134、MEDI0680、PDR001、REGN2810、SHR1210、STIA110X、STIA1110及びTSR042よりなる群から選択され、
前記PD1-L1阻害剤がBMS-936559、MPDL3280A、MEDI-4736、MSB0010718C、ALN-PDL、KD033、KY1003、STIA100X、STIA1010、STIA1011、STIA1012及びSTIA1014よりなる群から選択される、請求項1に記載の治療剤。 - 前記SLCポリペプチドが配列番号1又は配列番号2のアミノ酸配列を含む、非小細胞肺癌(NSCLC)固形腫瘍を治療するか又はその再発を予防するための用途の、請求項1~5のいずれかに記載の治療剤。
- 前記SLCポリペプチドをコードするポリヌクレオチドがベクターに挿入され、そして該ベクターが前記被験体に投与されるものである、非小細胞肺癌(NSCLC)固形腫瘍を治療するか又はその再発を予防するための用途の、請求項1~6のいずれかに記載の治療剤。
- 前記ベクターが複製欠損アデノウイルスベクターであってよいアデノウイルスベクター、CMVベクター、ワクシニアウイルスベクター、シンドビスウイルスベクター又はヘルペスウイルスベクターである、請求項7に記載の治療剤。
- 前記組換えポリヌクレオチドを発現可能なように導入してなる細胞が抗原提示細胞(APC)である、非小細胞肺癌(NSCLC)固形腫瘍を治療するか又はその再発を予防するための用途の、請求項1~8のいずれかに記載の治療剤。
- 前記抗原提示細胞(APC)が前記被験体に対して自己由来であってよい樹状細胞である、請求項9に記載の治療剤。
- 前記組換えポリヌクレオチドを発現可能なように導入してなる少なくとも又は約1×106個の細胞が前記被験体に投与されるものである、非小細胞肺癌(NSCLC)固形腫瘍を治療するか又はその再発を予防するための用途の、請求項1~10のいずれかに記載の治療剤。
- 前記細胞が24時間以内に1×106個の細胞当たり少なくとも又は約0.25ngのSLCを産生する、請求項11に記載の治療剤。
- 前記被験体が非小細胞肺癌(NSCLC)固形腫瘍を含み、前記細胞が前記被験体に腫瘍内投与されるものである、非小細胞肺癌(NSCLC)固形腫瘍を治療するか又はその再発を予防するための用途の、請求項1~11のいずれかに記載の治療剤。
- (i)SLCポリペプチド、(ii)該SLCポリペプチドをコードするポリヌクレオチドを発現可能なように含む組換えポリヌクレオチド、(iii)該組換えポリヌクレオチドを発現可能なように導入してなる細胞又は(iv)それらの組み合わせが、免疫チェックポイント阻害剤の前に開始してかつ該免疫チェックポイント阻害剤と共に継続して投与されるか、又は該免疫チェックポイント阻害剤と同時に開始して前記被験体に投与されるものである、非小細胞肺癌(NSCLC)固形腫瘍を治療するか又はその再発を予防するための用途の、請求項1~13のいずれかに記載の治療剤。
- (i)SLCポリペプチド、(ii)該SLCポリペプチドをコードするポリヌクレオチドを発現可能なように含む組換えポリヌクレオチド、(iii)該組換えポリヌクレオチドを発現可能なように導入してなる細胞又は(iv)それらの組み合わせが、免疫チェックポイント阻害剤の最初の投与の約2週間前に開始して、その後該免疫チェックポイント阻害剤の2週間毎の投与時に前記被験体に毎月投与されるものである、非小細胞肺癌(NSCLC)固形腫瘍を治療するか又はその再発を予防するための用途の、請求項1~13のいずれかに記載の治療剤。
- (i)SLCポリペプチド、(ii)該SLCポリペプチドをコードするポリヌクレオチドを発現可能なように含む組換えポリヌクレオチド、(iii)該組換えポリヌクレオチドを発現可能なように導入してなる細胞又は(iv)それらの組み合わせが前記被験体に2回以上投与されるものである、非小細胞肺癌(NSCLC)固形腫瘍を治療するか又はその再発を予防するための用途の、請求項1~13のいずれかに記載の治療剤。
- (i)SLCポリペプチド、(ii)該SLCポリペプチドをコードするポリヌクレオチドを発現可能なように含む組換えポリヌクレオチド、(iii)該組換えポリヌクレオチドを発現可能なように導入してなる細胞又は(iv)それらの組み合わせが1ヶ月に1回又は3週間毎に1回前記被験体に投与されるものである、非小細胞肺癌(NSCLC)固形腫瘍を治療するか又はその再発を予防するための用途の、請求項14に記載の治療剤。
- 前記免疫チェックポイント阻害剤が前記被験体に2回以上投与されるものである、非小細胞肺癌(NSCLC)固形腫瘍を治療するか又はその再発を予防するための用途の、請求項1~15のいずれかに記載の治療剤。
- 前記免疫チェックポイント阻害剤が2週間毎又は3週間毎に1回被験体に投与されるものである、非小細胞肺癌(NSCLC)固形腫瘍を治療するか又はその再発を予防するための用途の、請求項16に記載の治療剤。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201462075532P | 2014-11-05 | 2014-11-05 | |
| US62/075,532 | 2014-11-05 | ||
| PCT/US2015/059297 WO2016073759A1 (en) | 2014-11-05 | 2015-11-05 | Combination immunotherapy |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2017538680A JP2017538680A (ja) | 2017-12-28 |
| JP2017538680A5 JP2017538680A5 (ja) | 2018-12-13 |
| JP7305300B2 true JP7305300B2 (ja) | 2023-07-10 |
Family
ID=55909820
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017525120A Active JP7305300B2 (ja) | 2014-11-05 | 2015-11-05 | 併用免疫療法 |
Country Status (4)
| Country | Link |
|---|---|
| US (2) | US11236139B2 (ja) |
| EP (1) | EP3215182B1 (ja) |
| JP (1) | JP7305300B2 (ja) |
| WO (1) | WO2016073759A1 (ja) |
Families Citing this family (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2785692B1 (en) | 2011-12-01 | 2017-09-27 | ChemoCentryx, Inc. | Substituted anilines as ccr(4) antagonists |
| US10441654B2 (en) | 2014-01-24 | 2019-10-15 | Children's Hospital Of Eastern Ontario Research Institute Inc. | SMC combination therapy for the treatment of cancer |
| JP7305300B2 (ja) | 2014-11-05 | 2023-07-10 | ザ リージェンツ オブ ザ ユニバーシティ オブ カリフォルニア | 併用免疫療法 |
| PH12017502013B1 (en) | 2015-05-07 | 2022-07-22 | Agenus Inc | Anti-ox40 antibodies and methods of use thereof |
| UY36687A (es) | 2015-05-29 | 2016-11-30 | Bristol Myers Squibb Company Una Corporación Del Estado De Delaware | Anticuerpos contra ox40 y sus usos |
| SG10201912984WA (en) | 2015-12-02 | 2020-03-30 | Agenus Inc | Antibodies and methods of use thereof |
| TWI808055B (zh) | 2016-05-11 | 2023-07-11 | 美商滬亞生物國際有限公司 | Hdac 抑制劑與 pd-1 抑制劑之組合治療 |
| TWI794171B (zh) * | 2016-05-11 | 2023-03-01 | 美商滬亞生物國際有限公司 | Hdac抑制劑與pd-l1抑制劑之組合治療 |
| LT3458053T (lt) * | 2016-05-20 | 2022-02-25 | Biohaven Pharmaceutical Holding Company Ltd. | Riluzolo, rilizolo provaistų arba riluzolo analogų panaudojimas kartu su imunoterapijomis vėžio formų gydymui |
| US11419927B2 (en) | 2016-06-02 | 2022-08-23 | Ultimovacs As | Vaccine in combination with an immune checkpoint inhibitor for use in treating cancer |
| CN109476748B (zh) * | 2016-08-08 | 2023-05-23 | 豪夫迈·罗氏有限公司 | 用于癌症的治疗和诊断方法 |
| EP3538152A4 (en) | 2016-11-09 | 2020-09-30 | Agenus Inc. | ANTI-OX40 ANTIBODIES, ANTI-GITR ANTIBODIES, AND PROCESSES FOR USE |
| WO2019057808A1 (en) | 2017-09-21 | 2019-03-28 | University Of Copenhagen | PEPTIDES POTENTIATING CHEMOTAXY AND USES THEREOF |
| EP3790895A4 (en) * | 2018-05-10 | 2022-05-11 | The Regents of the University of California | CCL21 AND CHECKPOINT INHIBITORS FOR THE TREATMENT OF CANCER |
| KR102817790B1 (ko) * | 2018-08-29 | 2025-06-05 | 케모센트릭스, 인크. | C-c 케모카인 수용체 4(ccr4) 길항제 및 하나 이상의 면역 체크포인트 억제제를 사용한 병용 요법 |
| WO2020198401A1 (en) * | 2019-03-26 | 2020-10-01 | Translational Drug Development, Llc | Method of treating malignant rhabdoid tumor of the ovary and small cell cancer of the ovary of the hypercalcemic type |
| US20220280609A1 (en) * | 2019-07-17 | 2022-09-08 | The Regents Of The University Of California | Combination cancer therapy agents and methods |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013185052A1 (en) | 2012-06-08 | 2013-12-12 | Aduro Biotech | Compostions and methods for cancer immunotherapy |
Family Cites Families (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4179337A (en) | 1973-07-20 | 1979-12-18 | Davis Frank F | Non-immunogenic polypeptides |
| US4797368A (en) | 1985-03-15 | 1989-01-10 | The United States Of America As Represented By The Department Of Health And Human Services | Adeno-associated virus as eukaryotic expression vector |
| US5139941A (en) | 1985-10-31 | 1992-08-18 | University Of Florida Research Foundation, Inc. | AAV transduction vectors |
| US5328470A (en) | 1989-03-31 | 1994-07-12 | The Regents Of The University Of Michigan | Treatment of diseases by site-specific instillation of cells or site-specific transformation of cells and kits therefor |
| EP0444210B1 (en) | 1989-09-21 | 1995-05-24 | Idemitsu Kosan Company Limited | Arylstyrene polymer and copolymer and process for preparing the same |
| AU2147192A (en) | 1991-06-28 | 1993-01-25 | Genentech Inc. | Method of stimulating immune response using growth hormone |
| WO2001014557A1 (en) | 1999-08-23 | 2001-03-01 | Dana-Farber Cancer Institute, Inc. | Pd-1, a receptor for b7-4, and uses therefor |
| WO2002085286A2 (en) * | 2001-04-18 | 2002-10-31 | The Regents Of The University Of California | Methods of using secondary lymphoid organ chemokine to modulate physiological processes in mammals |
| EP2206517B1 (en) | 2002-07-03 | 2023-08-02 | Ono Pharmaceutical Co., Ltd. | Immunopotentiating compositions comprising anti-PD-L1 antibodies |
| CN1753912B (zh) | 2002-12-23 | 2011-11-02 | 惠氏公司 | 抗pd-1抗体及其用途 |
| US7563869B2 (en) | 2003-01-23 | 2009-07-21 | Ono Pharmaceutical Co., Ltd. | Substance specific to human PD-1 |
| ES2720160T3 (es) | 2005-05-09 | 2019-07-18 | Ono Pharmaceutical Co | Anticuerpos monoclonales humanos contra muerte programada 1(PD-1) y métodos para tratar el cáncer usando anticuerpos dirigidos contra PD-1 solos o junto con otras sustancias inmunoterapéuticas |
| EA019344B1 (ru) | 2005-07-01 | 2014-03-31 | МЕДАРЕКС, Эл.Эл.Си. | Человеческие моноклональные антитела против лиганда-1 запрограммированной гибели клеток (pd-l1) и их применения |
| CA2647282A1 (en) | 2006-04-05 | 2007-10-11 | Pfizer Products Inc. | Ctla4 antibody combination therapy |
| JP5191537B2 (ja) | 2007-06-18 | 2013-05-08 | エム・エス・ディー・オス・ベー・フェー | ヒトのプログラムされたデスレセプターpd−1に対する抗体 |
| WO2009014708A2 (en) | 2007-07-23 | 2009-01-29 | Cell Genesys, Inc. | Pd-1 antibodies in combination with a cytokine-secreting cell and methods of use thereof |
| US20110059137A1 (en) * | 2008-03-21 | 2011-03-10 | H. Lee Moffitt Cancer Center And Research Institutute, Inc | Chemokine gene-modified cells for cancer immunotherapy |
| US8927697B2 (en) | 2008-09-12 | 2015-01-06 | Isis Innovation Limited | PD-1 specific antibodies and uses thereof |
| BRPI0919377A2 (pt) | 2008-09-26 | 2016-09-27 | Dana Farber Cancer Inst Inc | anticorpo isolado ou um fragmento ligante de antígeno do memso, ácido nucleico isolado, vetor, célula hospedeira, composição farmacêutica, método de produzir o referido anticorpo ou fragmento, uso dos mesmos, e composição compreendendo o referido anticorpo ou fragmento |
| KR101050829B1 (ko) | 2008-10-02 | 2011-07-20 | 서울대학교산학협력단 | 항 pd-1 항체 또는 항 pd-l1 항체를 포함하는 항암제 |
| HUE065752T2 (hu) | 2008-12-09 | 2024-06-28 | Hoffmann La Roche | Anti-PD-L1 antitestek és felhasználásuk T-sejt funkció elõsegítésére |
| ES2629337T3 (es) | 2009-02-09 | 2017-08-08 | Inserm - Institut National De La Santé Et De La Recherche Médicale | Anticuerpos contra PD-1 y anticuerpos contra PD-L1 y usos de los mismos |
| JP6623353B2 (ja) | 2013-09-13 | 2019-12-25 | ベイジーン スウィッツァーランド ゲーエムベーハー | 抗pd−1抗体並びにその治療及び診断のための使用 |
| JP7305300B2 (ja) | 2014-11-05 | 2023-07-10 | ザ リージェンツ オブ ザ ユニバーシティ オブ カリフォルニア | 併用免疫療法 |
| GB201516047D0 (en) | 2015-09-10 | 2015-10-28 | Cancer Rec Tech Ltd | Method |
| AU2017225876B2 (en) | 2016-02-29 | 2021-03-04 | Foundation Medicine, Inc. | Methods and systems for evaluating tumor mutational burden |
| CA3059634A1 (en) * | 2017-04-13 | 2018-10-18 | Senti Biosciences, Inc. | Combinatorial cancer immunotherapy |
| EP3790895A4 (en) | 2018-05-10 | 2022-05-11 | The Regents of the University of California | CCL21 AND CHECKPOINT INHIBITORS FOR THE TREATMENT OF CANCER |
-
2015
- 2015-11-05 JP JP2017525120A patent/JP7305300B2/ja active Active
- 2015-11-05 WO PCT/US2015/059297 patent/WO2016073759A1/en not_active Ceased
- 2015-11-05 EP EP15856689.3A patent/EP3215182B1/en active Active
- 2015-11-05 US US15/524,740 patent/US11236139B2/en active Active
-
2022
- 2022-01-18 US US17/577,973 patent/US20220162279A1/en active Pending
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013185052A1 (en) | 2012-06-08 | 2013-12-12 | Aduro Biotech | Compostions and methods for cancer immunotherapy |
Non-Patent Citations (3)
| Title |
|---|
| Cancer Research,2001年,Vol.61,pp.8794-8802 |
| Reviews on Recent Clinical Trials,2012年,Vol.7,pp.10-23 |
| The Journal of Immunology,2004年,Vol.173,pp.4919-4928 |
Also Published As
| Publication number | Publication date |
|---|---|
| US11236139B2 (en) | 2022-02-01 |
| EP3215182A1 (en) | 2017-09-13 |
| EP3215182A4 (en) | 2018-06-27 |
| EP3215182B1 (en) | 2023-01-04 |
| US20180194825A1 (en) | 2018-07-12 |
| JP2017538680A (ja) | 2017-12-28 |
| WO2016073759A1 (en) | 2016-05-12 |
| US20220162279A1 (en) | 2022-05-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7305300B2 (ja) | 併用免疫療法 | |
| Narvaiza et al. | Intratumoral coinjection of two adenoviruses, one encoding the chemokine IFN-γ-inducible protein-10 and another encoding IL-12, results in marked antitumoral synergy | |
| Wang et al. | Therapeutic strategies to remodel immunologically cold tumors | |
| Hester et al. | Immunotherapy in pancreatic adenocarcinoma: beyond “copy/paste” | |
| Alkayyal et al. | NK-cell recruitment is necessary for eradication of peritoneal carcinomatosis with an IL12-expressing Maraba virus cellular vaccine | |
| RU2725799C2 (ru) | Онколитические аденовирусы, кодирующие биспецифические антитела, а также способы и применения, связанные с ними | |
| RU2703438C2 (ru) | Расширенная адоптивная клеточная терапия | |
| US11590184B2 (en) | Oncolytic rhabdovirus expressing IL12 | |
| US11786569B2 (en) | Expression of metabolic modulators in tumor microenvironment to improve tumor therapy | |
| KR100911624B1 (ko) | Il-12 및 il-23의 효율적인 공동발현 방법 | |
| Liang et al. | Local expression of secondary lymphoid tissue chemokine delivered by adeno-associated virus within the tumor bed stimulates strong anti-liver tumor immunity | |
| Chen et al. | Low‐dose paclitaxel improves the therapeutic efficacy of recombinant adenovirus encoding CCL21 chemokine against murine cancer | |
| KR20230056706A (ko) | 재조합 형질전환 성장 인자(tgf)-베타 단량체를 암호화하는 종양용해 바이러스 및 이의 용도 | |
| US20210379147A1 (en) | Method and system for treating cancer utilizing tinagl1 | |
| Shiau et al. | Retrovirus-mediated transfer of prothymosin gene inhibits tumor growth and prolongs survival in murine bladder cancer | |
| US20030175801A1 (en) | Methods of using secondary lymphoid organ chemokine to modulate physiological processes in mammals | |
| US20160058837A1 (en) | Methods of using secondary lymphoid organ chemokine to modulate physiological processes in mammals | |
| Jinoch et al. | Immunization with live HPV-16-transformed mouse cells expressing the herpes simplex thymidine kinase and either GM-CSF or IL-2 | |
| JP2026509004A (ja) | 腫瘍溶解性アデノウイルスベクターの新規投与レジメン | |
| HK40028530B (zh) | 溶瘤腺病毒载体与过继t细胞治疗组合物及其用途 | |
| Bastin | Overcoming Limitations in Adoptive Cell Therapies with Dual Specific T-cells and Oncolytic Viral Boosting | |
| Muller | Development of a Novel Therapeutic Paradigm Utilizing a Mammary Gland-Targeted, Bin-1 Knockout Mouse Model |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20181101 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20181101 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20191001 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20191226 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200401 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20200915 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210115 |
|
| C60 | Trial request (containing other claim documents, opposition documents) |
Free format text: JAPANESE INTERMEDIATE CODE: C60 Effective date: 20210115 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20210129 |
|
| C21 | Notice of transfer of a case for reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C21 Effective date: 20210202 |
|
| A912 | Re-examination (zenchi) completed and case transferred to appeal board |
Free format text: JAPANESE INTERMEDIATE CODE: A912 Effective date: 20210305 |
|
| C211 | Notice of termination of reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C211 Effective date: 20210309 |
|
| C22 | Notice of designation (change) of administrative judge |
Free format text: JAPANESE INTERMEDIATE CODE: C22 Effective date: 20211207 |
|
| C22 | Notice of designation (change) of administrative judge |
Free format text: JAPANESE INTERMEDIATE CODE: C22 Effective date: 20220201 |
|
| C22 | Notice of designation (change) of administrative judge |
Free format text: JAPANESE INTERMEDIATE CODE: C22 Effective date: 20220412 |
|
| C13 | Notice of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: C13 Effective date: 20220927 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20221222 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230327 |
|
| C22 | Notice of designation (change) of administrative judge |
Free format text: JAPANESE INTERMEDIATE CODE: C22 Effective date: 20230411 |
|
| C23 | Notice of termination of proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C23 Effective date: 20230418 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20230628 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7305300 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |