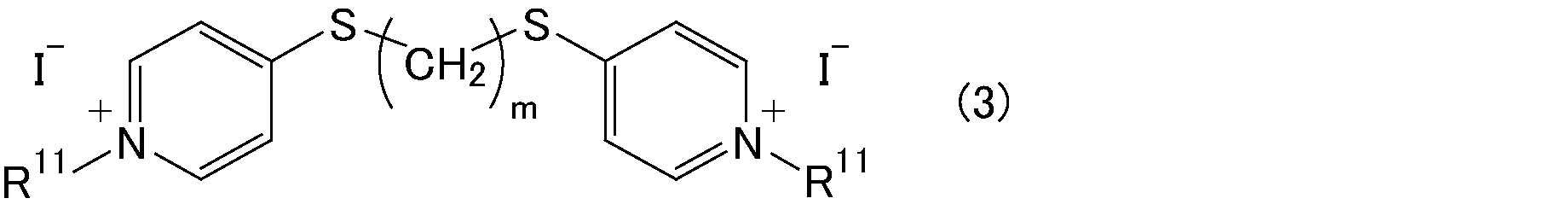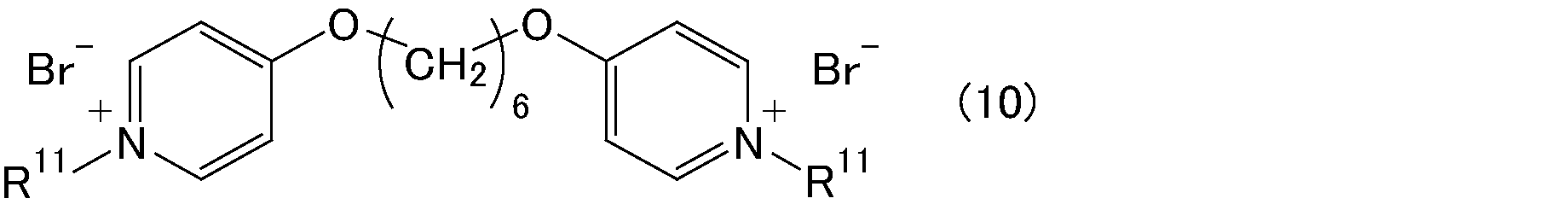JP7012000B2 - 抗微生物部材 - Google Patents
抗微生物部材 Download PDFInfo
- Publication number
- JP7012000B2 JP7012000B2 JP2018215700A JP2018215700A JP7012000B2 JP 7012000 B2 JP7012000 B2 JP 7012000B2 JP 2018215700 A JP2018215700 A JP 2018215700A JP 2018215700 A JP2018215700 A JP 2018215700A JP 7012000 B2 JP7012000 B2 JP 7012000B2
- Authority
- JP
- Japan
- Prior art keywords
- antimicrobial
- binder
- copper
- cured
- resin
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Landscapes
- Laminated Bodies (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
Description
本発明の抗微生物部材における抗微生物特性の中で、特に抗ウィルス、抗カビに有効であり、抗ウィルスが最も高い活性を持つ。
また、測定にあたっては、表面に導管模様などの凹溝や、リブなどの凸状体が形成されている場合にはその凹溝部分や凸状体部分を除外して測定する。
また、上記バインダ硬化物は、膜状に形成され、その膜状のバインダ硬化物の形成領域内に硬化物が形成されていない領域が混在して設けられた状態のバインダ硬化物と、島状に形成されたバインダ硬化物が混在していてもよい。
本発明の抗微生物部材において、上記有機・無機ハイブリッドのバインダは、シロキサン結合を形成するためのアルコキシシランを用いることができる。
電磁波硬化型樹脂の硬化物が形成されている領域を凸部、形成されていない領域を凹部として、基材表面に凹凸を形成し易くなり、電磁波硬化型樹脂の硬化物含む基材の表面粗さを基材表面のJIS B 0601に準拠した算術平均粗さ(Ra)で4μmを超え、50μm以下に調整しやすくなるからである。
なお、電磁波硬化型樹脂の硬化物は、膜状(層状)に形成されていてもよい。この場合は、膜表面をサンドブラスト、物理、化学エッチングや研磨などを用いて粗化または平滑化することにより面粗さを調整する。また、抗微生物組成物中に粒子状物質を添加して、得られる電磁波硬化型樹脂の硬化物の面粗さを調整してもよい。
すなわち、抗微生物部材の、微生物が存在する流体に接触する態様での使用である。
本発明の抗微生物部材は、流体中に存在する微生物を、抗微生物性を示すバインダ硬化物の凹凸を利用して、その表面にトラップし、あるいは、抗微生物性を示すバインダ硬化物の表面積を大きくすることで、微生物との接触確率を高め、当該微生物を効果的に失活させることができるからである。微生物が存在する流体とは、空気、水、水溶液、溶媒、排液、汗、唾液、動物からの排泄液などを言う。微生物としては、ウィルス、細菌、カビ、カビの胞子などが挙げられる。
本発明の抗微生物部材は、抗ウィルス、抗菌、抗カビ及び防カビの特性を有するが、抗ウィルス活性、抗カビ活性優れ、特に抗ウィルスが最も高い活性を有するからである。
以下、本発明の抗微生物部材について詳細に説明する。
本発明の抗微生物部材は、基材表面に抗微生物成分を含むバインダ硬化物が固着形成されてなり、上記バインダ硬化物を含む表面のJIS B 0601に準拠した算術平均粗さ(Ra)が、4μmを超え、50μm以下であることを特徴とする。
上記バインダ硬化物は、膜状に基材表面に固着してなるか、島状に分散して基材表面に固着されてなるか、もしくは基材表面に上記バインダ硬化物が形成された領域と上記バインダ硬化物が形成されていない領域が混在して設けられており、抗微生物部材の表面に凹凸が形成される。本発明においては、バインダ硬化物は、基材表面の10%以上、95%以下を覆っていることが望ましい。
つまり、基材表面にバインダ硬化物が固着した抗微生物部材の表面の粗さを、JIS B 0601に準拠した算術平均粗さ(Ra)で、Ra=4μmを超え、Ra=50μm以下にすることで、気体や液体中を流動する運動エネルギーを持ったウィルス等の微生物を確実に失活させることができるのである。
図2(a)及び(b)に示す本発明の抗微生物部材20では、基材21の表面に、抗微生物のバインダ硬化物22が島状に形成されている。
また、本発明の抗微生物部材を構成する基材となる部材も、特に限定されるものではなく、建築物内部の内装材、壁材、窓ガラス、ドア等であってもよい、事務機器や家具等であってもよく、上記内装材の外、種々の用途に用いられる化粧板等であってもよい。
上記化粧板に使用する基板は、特に限定されるものではなく、一般的に化粧板に使用されるコア紙やマグネシアセメント等の不燃板等を使用することができる。コア紙は単独でもよく複数枚のコア紙を積層した積層体としてもよい。コア紙の枚数は特に限定されないが、1~20枚とすることができる。コア紙としては、例えば、水酸化アルミニウム抄造紙を使用することができる。コア紙には、フェノール樹脂を含浸させることができる。また、コア紙とマグネシアセメント不燃板を積層させて基板とすることもできる。
なお、填料とは紙に添加して、白色度や平滑度を調整するための無機粒子(フィラー)であり、炭酸カルシウム、タルク、クレーおよびカオリンから選ばれる少なくとも1種以上が望ましい。填料は無機粒子であるため、填料の含有量は紙の重量と紙を強熱して残存する灰分の重量から計算することができる。
上記バインダ硬化物中には、上記した無機系抗微生物剤が1種類のみ含まれていてもよく、2種類以上の無機系抗微生物剤が含まれていてもよく、上記した有機系抗微生物剤が1種類のみ含まれていてもよく、2種類以上の有機系抗微生物剤が含まれていてもよい。さらに、上記バインダ硬化物中には、上記無機系抗微生物剤と上記無機系抗微生物剤とが2種類以上含まれていてもよい。
バインダ硬化物中には、銀、銅、亜鉛及び白金の粒子が単独で含まれていてもよく、銀、銅、亜鉛及び白金のうち、2種類以上の金属粒子が含まれていてもよく、例えば、銀、銅、亜鉛及び白金のうち、少なくとも2種を含む合金の金属粒子が固定されていてもよい。
上記銅のカルボン酸塩としては、銅のイオン性化合物を使用することができ、酢酸銅、安息香酸銅、フタル酸銅等が挙げられる。
上記銅の水溶性無機塩としては、銅のイオン性化合物を使用することができ、例えば、硝酸銅、硫酸銅等が挙げられる。
その他の銅化合物としては、例えば、銅(メトキシド)、銅エトキシド、銅プロポキシド、銅ブトキシドなどが挙げられ、銅の共有結合性化合物としては銅の酸化物、銅の水酸化物などが挙げられる。銅のカルボン酸塩、銅の水酸化物は、有機バインダ、無機バインダとの親和性が高く、水により溶出しないため、耐水性に優れる。
上記銅のカルボン酸塩としては、酢酸銅(II)、酢酸銅(I)、シュウ酸銅(I)、安息香酸銅(II)、フタル酸銅(II)等が挙げられる。
上記銅の錯体としては、例えば、アセチルアセトンと銅との錯体、5-メチル-2,4-ヘキサンジオン等のβジケトンと銅との錯体、銅(I)(1-ブタンチオレート)、銅(I)(へキサフルオロペンタンジオネートシクロオクタジエン)等が挙げられる。
上記銅の水溶性無機塩としては、例えば、硝酸銅(II)、硫酸銅(II)等が挙げられる。その他の銅化合物としては、例えば、銅(II)(メトキシド)、銅(II)エトキシド、銅(II)プロポキシド、銅(II)ブトキシド等が挙げられる。
ビニル基を有するモノマーの重合体は、付加重合で合成されるので水などの副生成物がなく、透明度の高い抗微生物樹脂を得ることができる。このため、基材の意匠性に与える影響を小さくすることができる。
スチレン、メタクリル酸、メタクリル酸エステル、ジビニルベンゼン、トリビニルベンゼンは、特に透明度の高い抗微生物樹脂を得ることができる。また、ジビニルベンゼン、トリビニルベンゼンは、モノマーに添加することによって架橋し、三次元網目構造を形成することができる。三次元網目構造を形成することによって、分解しにくくなり、耐久性を高くすることができる。
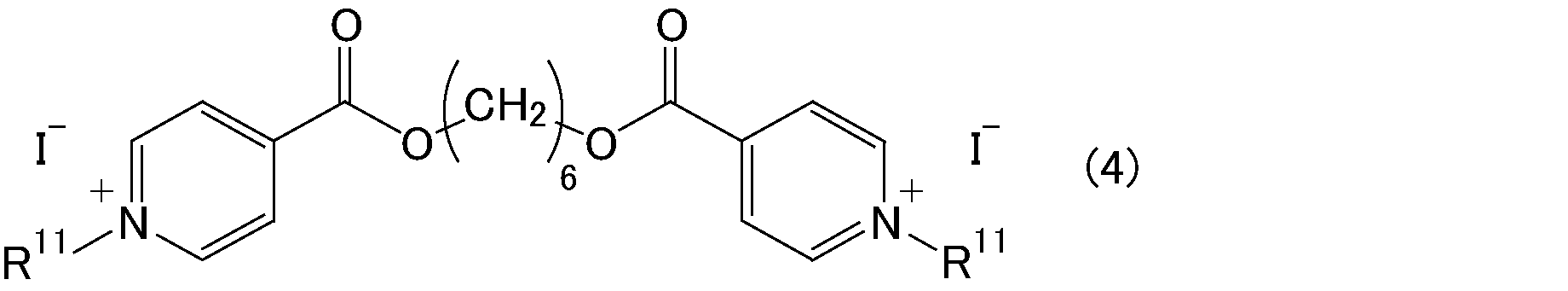
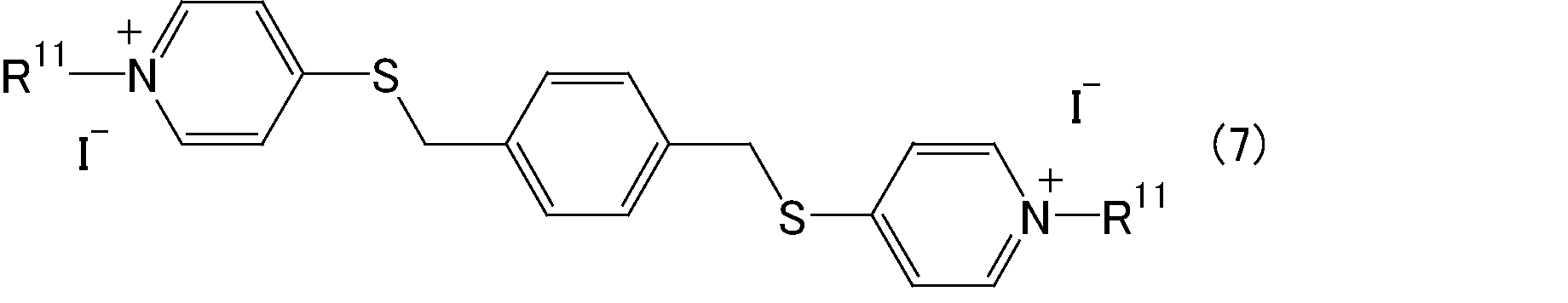
上記一般式(1)で表されるビス型ピリジニウム塩において、X-としては、例えば、Cl-、Br-、I-等が挙げられる。
R1、R2は、炭素数1~20のアルキル基が好ましく、上記アルキル基は、側鎖を有していてもよい。
上記一般式(1)中、R3で表される有機基は、-CO-O-(CH2)6-O-CO-、-CONH-(CH2)6-CO-、-NH-CO-(CH2)4-CO-NH-、-S-Ph-S-、-CONH-Ph-NHCO-、―NHCO-Ph-CONH-、-O-(CH2)6-O-または-CH2-O-(CH2)4-O-CH2-(但し、Phは、フェニレン基を表す。)で表されるものであることが望ましい。
上記ビス型キノリニウム塩としては、一般式(3)~一般式(10)で表されるビス型ピリジニウム塩を構成する下記の一般式(13)に表されるピリジニウム基を、一般式(14)に示すキノリウム基に置換した化学構造を有するビス型キノリニウム塩が挙げられる。上記ビス型キノリニウム塩において、他の置換基等は、一般式(3)~一般式(10)で表されるビス型ピリジニウム塩と同様である。
本発明の抗微生物部材では、上記抗微生物成分として、無機系抗微生物剤及び有機系抗微生物剤からなる群から選択される少なくとも1種と、バインダである有機バインダ、無機バインダ、有機・無機ハイブリッドのバインダ及び電磁波硬化型樹脂の少なくとも1種と、を混合したものを硬化させることにより、バインダ硬化物を得ることができる。
また、面粗さを調整するために、樹脂粒子もしくは無機粒子から選ばれる少なくとも1種以上の粒子を含有していてもよい。樹脂粒子としては、エポキシ樹脂、メラミン樹脂などを使用でき、無機粒子としては、アルミナ粒子、シリカ粒子、ジルコニア粒子、チタニア粒子などを使用できる。平均粒子径の大きな粒子を添加すると表面の面粗さを大きくすることができる。
未硬化の電磁波硬化型樹脂であるモノマー又はオリゴマーと重合開始剤と各種添加剤と抗微生物成分とを含んだ抗微生物組成物を用いて基材表面に液滴を形成した後、電磁波を照射することにより、重合開始剤は、開裂反応、水素引き抜き反応、電子移動等の反応を起こし、これにより生成した光ラジカル分子、光カチオン分子、光アニオン分子等が上記モノマーや上記オリゴマーを攻撃してモノマーやオリゴマーの重合反応や架橋反応が進行し、抗微生物成分を含むバインダ硬化物が形成される。このような反応により生成する本発明のバインダ硬化物を構成する樹脂を電磁波硬化型樹脂という。
本発明においては、重合開始剤は、銅に対する還元剤として使用することができる。このため、バインダ中に存在する銅(II)を銅(I)に還元できる。銅(I)の方が銅(II)よりも抗微生物性能が高いため、重合開始剤により、抗微生物組成物の抗微生物性能を高くすることができるのである。
また、電磁波硬化型樹脂に限らず、無機バインダ、銅化合物および分散媒からなる抗微生物組成物に重合開始剤を添加してもよい。
上記ポリエステル樹脂としては、例えば、ポリエチレンテレフタレート(PET)、ポリブチレンテレフタレート(PBT)等が挙げられる。
アルキッド樹脂としては、ポリエステルアルキッド樹脂等が挙げられる。
これらの樹脂は、透明性を有するとともに、基材に対する密着性にも優れる。
無機バインダと抗微生物成分と必要により各種添加剤や分散媒とを混合した抗微生物組成物を用いて基材表面に液滴を形成した後、乾燥させることにより、抗微生物成分を含むバインダ硬化物(無機バインダの硬化物)が形成される。
上記無機バインダは、分散媒として、水を用いたものと有機溶媒を用いたものが存在するので、添加する抗微生物成分の種類を考慮して、無機バインダを選択することができ、抗微生物成分が均一に分散した上記抗微生物組成物を得ることができる。
具体的には、画像解析・画像計測ソフトウェアを備えた走査型顕微鏡やレーザー顕微鏡を用いることにより、又は、走査型顕微鏡、レーザー顕微鏡で得られた画像を画像解析・画像計測ソフトウェアを用いて画像解析等を行うことにより、上記したバインダ硬化物の基材表面に平行な方向の最大幅やその厚さの平均値を求めることができる。
上記抗微生物部材を製造する際には、まず、基材の表面に、抗微生物成分と未硬化のバインダと分散媒と重合開始剤とを含む抗微生物組成物を付着させる付着工程を行い、続いて必要に応じて、上記付着工程により基材表面に付着した上記抗微生物組成物を乾燥させて上記分散媒を除去する乾燥工程を行い、最後に上記乾燥工程で分散媒を除去した上記抗微生物組成物中の上記未硬化のバインダを硬化させる硬化工程を行い、基材の表面に抗微生物成分を含むバインダ硬化物が基材表面に固着し、バインダ硬化物が基材表面の一部が露出するように被覆している抗微生物部材を得ることができる。バインダの硬化は、乾燥と同時でもよい。面粗さは、抗微生物組成物を基材表面に付着させる条件を変えることで調整する。
本発明の抗微生物部材を製造する際には、まず、付着工程として、基材の表面に、抗微生物成分と未硬化のバインダと分散媒と重合開始剤とを含む抗微生物組成物を付着させる。
また、基材となる部材も、特に限定されるものではなく、建築物内部の内装材、壁材、窓ガラス、ドア等であってもよい、事務機器や家具等であってもよく、上記内装材の外、種々の用途に用いられる化粧板等であってもよい。
上記無機系抗微生物剤は、銀、銅、亜鉛、白金、亜鉛化合物、銀化合物、銅化合物、金属イオンでイオン交換されたゼオライト、及び、銅の錯体からなる群から選択される少なくとも1種であることが望ましく、上記有機系抗微生物剤は、抗微生物樹脂、スルホン酸系界面活性剤、銅のアルコキシド、及び、ビス型第四級アンモニウム塩からなる群から選択される少なくとも1種であることが望ましい。
本発明において、二流体スプレー法とは、スプレー法の一種であり、高圧の空気などのガスと抗微生物組成物とを混合した後、ノズルから霧の状態で噴霧し、基材表面に上記抗微生物組成物の液滴を付着させることをいう。
本発明において、静電スプレー法とは、帯電した抗微生物組成物を利用する付着方法であり、上記したスプレー法により抗微生物組成物を霧の状態で噴霧するが、上記抗微生物組成物を霧状にするための方式には、上記抗微生物組成物を噴霧器で噴霧するガン型と、帯電した抗微生物組成物の反発を利用した静電霧化方式があり、さらに、ガン型には帯電した抗微生物組成物を噴霧する方式と、噴霧した霧状の抗微生物組成物に外部電極からコロナ放電で電荷を付与する方式とがある。霧状の液滴は、帯電しているため、基材表面に付着し易く、良好に上記抗微生物組成物を、細かく分割された状態で基材表面に付着させることができる。
本発明において、エアロゾル法とは、金属の化合物を含む抗微生物組成物を物理的及び化学的に生成した霧状のものを対象物に吹き付ける手法である。
また、ローラーや刷毛で塗布してもよい。
上記付着工程により基材の表面に付着された抗微生物成分と未硬化のバインダと分散媒と重合開始剤とを含む抗微生物組成物を乾燥させ、分散媒を蒸発、除去し、抗微生物成分を含むバインダ硬化物を基材表面に仮固定させるとともに、バインダ硬化物の収縮により、抗微生物成分をバインダ硬化物の表面から露出させることができる。乾燥条件としては、60~100℃、0.5~5.0分が望ましい。未硬化の無機バインダおよび分散媒と必要に応じて重合開始剤からなる抗微生物組成物の場合は、この乾燥工程において分散媒を除去することで無機バインダの硬化が進行する。乾燥工程と硬化工程が同時である。
上記の抗微生物部材を製造する際には、硬化工程として、上記乾燥工程で分散媒を除去した抗微生物組成物中の上記未硬化の電磁波硬化型樹脂であるモノマーやオリゴマーに電磁波を照射して上記未硬化のバインダを硬化させ、バインダ硬化物とする。
本発明の抗微生物部材の製造方法において、未硬化のバインダが電磁波硬化型樹脂である場合は、硬化のために照射する電磁波としては、特に限定されず、例えば、紫外線(UV)、赤外線、可視光線、マイクロ波、電子線(Electron Beam:EB)等が挙げられるが、これらのなかでは、紫外線(UV)が望ましい。
これらの工程により、基材表面に抗微生物成分を含むバインダ硬化物が基材表面に固着し、かつ、上記バインダ硬化物は、基材表面の一部を露出するように被覆している本発明の抗微生物部材を製造することができる。
また、Cu(I)の銅は、Cu(II)の銅と比較して抗微生物により優れているため、第1の本発明の抗微生物部材において、X線光電子分光分析法により、925~955eVの範囲にあるCu(I)とCu(II)に相当する結合エネルギーを5分間測定することで算出される、上記銅化合物中に含まれるCu(I)とCu(II)とのイオンの個数の比率(Cu(I)/Cu(II))が1.0~4.0であると、より抗微生物に優れた抗微生物部材となる。
上記電磁波は、光重合開始剤を励起して、銅化合物を還元する働きをもつ。このため、銅(II)を還元して銅(I)の量を増やして抗微生物活性を高くすることができる。
(1)酢酸銅の濃度が6.0wt%になるように、酢酸銅(II)・一水和物粉末(富士フィルム和光純薬社製)を純水に溶解させた後、マグネチックスターラーを用い、600rpmで15分撹拌して酢酸銅水溶液を調製した。紫外線硬化樹脂液は、光ラジカル重合型アクリレート樹脂(ダイセル・オルネクス社製 UCECOAT7200)と光重合開始剤(IGM社製 Omnirad500)を重量比98:2で混合し、ホモジナイザーを用い、8000rpmで30分間撹拌して調製した。上記6wt%酢酸銅水溶液と紫外線硬化樹脂液と平均粒子径4μmのアルミナ粒子を重量比1.0:1.7:0.2で混合し、マグネチックスターラーを用い、600rpmで2分撹拌して抗ウィルス組成物を調製した。なお、IGM社製のOmnirad500は、BASF社のIRGACURE500と同じもので、1-ヒドロキシ-シクロヘキシル-フェニル-ケトン(アルキルフェノン)とベンゾフェノンとのとの重量比1:1の混合物である。すなわち、アルキルフェノン系重合開始剤とベンゾフェノン系重合開始剤は、重量比1:1で存在している。この光重合開始剤は、水に不溶であり、紫外線により還元力を発現する混合物である。
添加するアルミナ粒子の平均粒子径を30μmに変更したほかは、実施例1と同様にして、銅化合物を含むバインダ硬化物が固着した抗ウィルス性部材を得た。
添加するアルミナ粒子の平均粒子径を51μmに変更したほかは、実施例1と同様にして、銅化合物を含むバインダ硬化物が固着した抗ウィルス性部材を得た。
添加するアルミナ粒子の平均粒子径を1.5μmに変更したほかは、実施例1と同様にして、銅化合物を含むバインダ硬化物が固着した抗ウィルス性部材を得た。
(試験例2)
添加するアルミナ粒子の平均粒子径を95μmに変更したほかは、実施例1と同様にして、銅化合物を含むバインダ硬化物が固着した抗ウィルス性部材を得た。
(比較例1)
(1)多官能(メタ)アクリルモノマーとして63.6重量部の6官能アクリレート(商品名DPHA、ダイセル・サイテック社製)、27重量部のジエチレングリコールジアクリレート(商品名SR230、サートマー社製)、5重量部の光重合開始剤(商品名IRGACURE184、BASF社製)、4重量部の光安定化剤(商品名TINUVIN152、BASF社製)重量部、及び、0.4重量部の市販の抗菌剤粒子(株式会社シナネンゼオミック製 商品名ゼオミック)を、メチルエチルケトン(MEK)及びシクロヘキサノンを1:1で混合した希釈溶剤に固形分が40質量%となるように混合してハードコート層形成用組成物(A)を調製する。
(1)塩化銅(I)の濃度が0.34wt%になるように、塩化銅(I)粉末(富士フイルム和光純薬社製)を純水に懸濁させた後、マグネチックスターラーを用い、600rpmで15分撹拌して塩化銅懸濁液を調製する。上記0.34wt%塩化銅(I)懸濁液とポリビニルアルコールと平均粒子径4μmのアルミナ粒子を重量比1.7:1.0:0.2で混合し、マグネチックスターラーを用い、600rpmで2分撹拌して抗ウィルス組成物を調製する。
(2)ついで、300mm×300mmの大きさのガラス板を用意し、霧吹きで上記抗ウィルス性の混合組成物をこのガラス板表面に、硬化した場合に当該抗ウィルス性の混合組成物の硬化物がガラス板の表面にJIS B 0601に準拠した算術平均粗さRa=4.1μmとなるまで吹き付ける。
(3)この後、ガラス板を室温で24時間乾燥させ、基材であるガラス板表面にその表面の一部が露出するように銅化合物を含むバインダ硬化物の膜が固着形成された抗ウィルス性部材を得る。
酢酸銅(II)の濃度が6.0wt%で、平均粒子径4μmのアルミナを5重量%含む酢酸銅の水溶液を300mm×300mmの大きさの黒色光沢メラミン板表面に、乾燥時に乾燥物のJIS B 0601に準拠した算術平均粗さRa=4.1μmとなるまで、霧吹きにて吹き付けて付着させる。ついで、紫外線を照射せず、室温で48時間乾燥させる。
(1)光ラジカル重合型アクリレート樹脂(ダイセル・オルネクス社製UCECOAT7200)と光重合開始剤(IGM社製 Omnirad500)と光重合開始剤(IGM社製 Omnirad184)とを重量比97:2:1で混合し、ホモジナイザーを用いて、8000rpmで10分間撹拌して紫外線硬化樹脂液を調製する。なお、IGM社製 Omnirad500は、BASF社のIRGACURE500と同じもので、1-ヒドロキシ-シクロヘキシル-フェニル-ケトン(アルキルフェノン)とベンゾフェノンの1:1の混合物である。この光重合開始剤は、水に不溶性であり、紫外線を吸収することで還元力を発現する。一方、光重合開始剤(IGM社製 Omnirad184)は、1-ヒドロキシ-シクロヘキシル-フェニル-ケトン(アルキルフェノン)であり、結局光重合開始剤としては、アルキルフェノンとベンゾフェノンは重量比で2:1の割合で存在している。
(2)水とビス型第四級アンモニウム塩(1,1′-ジデシル-3,3′-[ブタン-1,4-ジイルビス(オキシメチレン)]ジピリジニウム=ジブロミド)と紫外線硬化樹脂液と平均粒子径8μmのアルミナ粒子を重量比17:0.51:10:2で混合し、マグネチックスターラーを用い、600rpmで2分撹拌して抗ウィルス組成物を調製する。
(3)ついで、500mm×500mmの大きさの黒色光沢メラミン板上に、9番のコートバーで抗ウィルス組成物を基材表面全体に膜状(層状)に塗布する。
(4)この後、黒色光沢メラミン板を80℃で3分間乾燥させ、さらに紫外線照射装置(COATTEC社製 MP02)を用い、30mW/cm2の照射強度で80秒間紫外線を照射することにより、膜状の抗ウィルス組成物を硬化させ、その表面をJIS B 0601に準拠した算術平均粗さRa=4.1μmに調整した抗ウィルス性部材を得る。
実施例4と同様であるが、平均粒子径25μmのアルミナ粒子を用いて、抗ウィルス組成物が塗布、硬化された基材表面をJIS B 0601に準拠した算術平均粗さRa=21.0μmに調整した抗ウィルス性部材を得る。
実施例4と同様であるが、平均粒子径55μmのアルミナ粒子を用いて、抗ウィルス組成物が塗布、硬化された基材表面をJIS B 0601に準拠した算術平均粗さRa=50.0μmに調整した抗ウィルス性部材を得る。
実施例4と同様であるが、平均粒子径6μmのアルミナ粒子を用いて、抗ウィルス組成物が塗布、硬化された基材表面をJIS B 0601に準拠した算術平均粗さRa=3.0μmに調整した抗ウィルス性部材を得る。
実施例4と同様であるが、平均粒子径60μmのアルミナ粒子を用いて、抗ウィルス組成物が塗布、硬化された基材表面をJIS B 0601に準拠した算術平均粗さRa=55.0μmに調整した抗ウィルス性部材を得る。
Cu(I)とCu(II)のイオンの個数の比率は、X線光電子分光分析法(XPS分析法)により計測した。測定条件は以下の通り。
・装置:アルバックファイ製 PHI 5000 Versa probeII
・X線源:Al Kα 1486.6eV
・検出角:45°
・測定径:100μm
・帯電中和:有り
-ワイドスキャン
・測定ステップ:0.8eV
・pass energy:187.8eV
-ナロースキャン
・測定ステップ:0.1eV
・pass energy:46.9eV
測定時間は5分で、Cu(I)のピーク位置は、932.5eV ±0.3eV、Cu(II)のピーク位置は933.8eV ±0.3 eVであり、それぞれのピークの面積を積分して、その比率からCu(I)/Cu(II)を得た。
実施例1~3、試験例1~2及び比較例1で得られた抗ウィルス性部材について、東京精密製の接触式表面粗さ測定機であるHANDYSURFを用い、8mmの測定長さでJIS B 0601に準拠した算術平均粗さRaを測定した。測定結果を表1に記載する。
この抗ウィルス性試験は以下のように実施した。
実施例1~3、試験例1~2及び比較例1で得られた抗ウィルス性部材の抗ウィルス性を評価するために、JIS Z 2801 抗菌加工製品-抗菌性試験方法・抗菌効果を改変した手法を用いた。改変点は、「試験菌液の接種」を「試験ウィルスの接種」に変更した点と、試験試料を45°傾けて固定し、この傾けた試験試料にウィルス液を接種してウィルス液が流動するようにした点である。ウィルスを使用することによる変更点についてはすべてJIS L 1922繊維製品の抗ウィルス性試験方法に基づき変更した。測定結果は実施例1~3及び試験例1~2、比較例1で得られた抗ウィルス性部材についてJIS L 1922付属書Bに基づき、CRFK細胞への感染能力を失ったネコカリシウィルス濃度をネコカリシウィルス不活度として表示する。ここで、ウィルス濃度の指標として、CRFK細胞に対して不活性化されたウィルスの濃度(ウィルス不活度)を使用し、このウィルス不活度に基づいて抗ウィルス活性値を算出した。
(1)実施例1~3、試験例1~2及び比較例1で得られた抗ウィルス性部材を、1辺50mm角の正方形に切り出した試験試料を45°傾けて滅菌済プラスチックシャーレに置き、試験ウィルス液(>107PFU/mL)を0.4mL接種する。
試験ウィルス液は108PFU/mLのストックを精製水で10倍希釈したものを使用する。
(2) 対照試料として50mm角のポリエチレンフイルムを用意し、試験試料と同様にウィルス液を接種する。
(4) 接種直後または反応後、SCDLP培地10mLを加え、ウィルス液を洗い流す。
(5) JIS L 1922付属書Bによってウィルスの感染値を求める。
Mv=Log(Vb/Vc)
Mv:抗ウィルス活性値
Log(Vb):ポリエチレンフイルムの所定時間反応後の感染値の対数値
Log(Vc):試験試料の所定時間反応後の感染値の対数値
参考規格 JIS L 1922、JIS Z 2801
測定方法は、プラーク測定法によった。
また、試験ウィルスはFeline calcivirus; Strain :F-9 ATCC VR-782を用いた。
得られた抗ウィルス活性値を表1に示す。
黄色ブドウ球菌を用いた抗菌性評価を、以下のように実施した。
(1)実施例1~6、試験例1~2及び比較例1、3、4で得られた抗ウィルス性部材を、50mm角の正方形に切り出した試験試料を滅菌済プラスチックシャーレに45°傾けて固定し、試験菌液(菌数2.5×105~10×105/mL)を0.4mL接種する。試験菌液は、培養器中で温度35±1℃で16~24時間前培養した培養菌を、さらに斜面培地に移植して、培養器中で温度35±1℃で16~20時間前培養したものを、1/500NB培地により適宜調整したものを使用する。
(2)対照試料として50mm角のポリエチレンフイルムを用意し、試験試料と同様に試験菌液を接種する。
(3)接種した試験菌液の上から40mm角のポリエチレンフイルムを被せ、試験菌液を均等に接種させた後、温度35±1℃で8±1時間反応させる。
(4)接種直後または反応後、SCDLP培地10mLを加え、試験菌液を洗い出す。
(5)洗い出し液を適宜希釈し、標準寒天培地と混合して生菌数測定用シャーレを作成し、温度35±1℃で40~48時間培養した後、集落数を測定する。
(6)生菌数の計算
以下の計算式を用いて生菌数を求める。
N=C×D×V
N:生菌数
C:集落数
D:希釈倍率
V:洗い出しに用いたSCDLP培地の液量(mL)
(7) 以下の計算式を用いて抗菌活性値を算出する。
R=(Ut-U0)-(At-U0)=Ut-At
R:抗菌活性値
U0:無加工試験片の接種直後の生菌数の対数値の平均値
Ut:無加工試験片の24 時間後の生菌数の対数値の平均値
At:抗菌加工試験片の24時間後の生菌数の対数値の平均値
参考規格 JIS Z 2801
試験菌はStaphylococcus aureus NBRC12732を使用した。
評価結果を表3及び表4に記載する。
クロコウジカビを用いた抗カビ性評価を、以下のように実施した。
(1)実施例1~6、試験例1~2及び比較例1、3、4で得られた抗ウィルス性部材を、50mm角の正方形に切り出した試験試料を滅菌済プラスチックシャーレに45°傾けて固定し、胞子懸濁液(胞子濃度>2×105個/ml)を0.4mL接種する。
(2)対照試料として50mm角のポリエチレンフイルムを用意し、試験試料と同様に胞子懸濁液を接種する。
(3)接種した胞子懸濁液の上から40mm角のポリエチレンフイルムを被せ、胞子懸濁液を均等に接種させた後、温度26℃で約900LUXの光を照射しながら42時間反応させる。
(4)接種直後または反応後、JIS L 1921 13発光量の測定に従い、ATP量を測定する。
(5)以下の計算式を用いて抗カビ活性値を算出する。
Aa=(LogCt―LogC0)―(LogTt―LogT0)
Aa:抗カビ活性値
LogC0:接種直後の対照試料3検体のATP量の算術平均の常用対数値
LogCt:培養後の対照試料3検体のATP量の算術平均の常用対数値
LogT0:接種直後の試験試料3検体のATP量の算術平均の常用対数値
LogTt:培養後の試験試料3検体のATP量の算術平均の常用対数値
参考規格 JIS Z 2801、JIS L 1921
試験カビはAspergillus niger NBRC105649を使用した。
評価結果を表3及び表4に記載する。
以上の説明のように本発明の抗微生物部材は、優れた抗微生物性能を有するのである。
11、21 基材
12 膜形成領域
13 膜非形成領域
22 バインダ硬化物
Claims (2)
- 基材表面に、銅化合物からなる抗ウィルス成分を含み、光半導体を含まない有機バインダ硬化物が固着形成されてなり、かつ、前記有機バインダ硬化物を含む基材表面のJIS B 0601に準拠した算術平均粗さ(Ra)は、4μmを超え、50μm以下であり、
前記銅化合物は、X線光電子分光分析法により、925~955eVの範囲にあるCu(I)とCu(II)に相当する結合エネルギーを5分間測定することでCu(I)とCu(II)の共存が確認されており、
前記基材表面には、導管模様などの凹溝、リブなどの凸状体が形成されていないことを特徴とする抗ウィルス性部材。 - 前記有機バインダ硬化物に含まれる有機バインダは、熱硬化性樹脂、電磁波硬化型樹脂からなる群から選択される少なくとも1種である請求項1に記載の抗ウィルス性部材。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2018167975 | 2018-09-07 | ||
| JP2018167975 | 2018-09-07 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020212471A Division JP2021050236A (ja) | 2018-09-07 | 2020-12-22 | 抗微生物部材 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2020040374A JP2020040374A (ja) | 2020-03-19 |
| JP7012000B2 true JP7012000B2 (ja) | 2022-01-27 |
Family
ID=69797202
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018215700A Active JP7012000B2 (ja) | 2018-09-07 | 2018-11-16 | 抗微生物部材 |
| JP2020212471A Pending JP2021050236A (ja) | 2018-09-07 | 2020-12-22 | 抗微生物部材 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020212471A Pending JP2021050236A (ja) | 2018-09-07 | 2020-12-22 | 抗微生物部材 |
Country Status (1)
| Country | Link |
|---|---|
| JP (2) | JP7012000B2 (ja) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP7694933B2 (ja) | 2020-02-28 | 2025-06-18 | デュポン・東レ・スペシャルティ・マテリアル株式会社 | 紫外線硬化性シリコーン組成物及びこれを利用してなる封止材またはシートフィルム |
| KR102334927B1 (ko) * | 2020-04-01 | 2021-12-06 | 권재범 | 버튼 개폐형 위생 물통 |
| KR102337470B1 (ko) * | 2020-04-01 | 2021-12-13 | 권재범 | 자중 개폐형 위생 물통 |
| JP7737698B2 (ja) * | 2020-08-31 | 2025-09-11 | 株式会社トラスト化学 | 抗ウイルス性物品及びその製造方法 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2017078331A (ja) | 2015-10-19 | 2017-04-27 | イビデン株式会社 | トイレブース用化粧板及びトイレブース |
| JP2017094544A (ja) | 2015-11-19 | 2017-06-01 | イビデン株式会社 | 化粧板 |
| JP2017177802A (ja) | 2015-11-17 | 2017-10-05 | イビデン株式会社 | 化粧板 |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014080606A1 (ja) * | 2012-11-22 | 2014-05-30 | パナソニック株式会社 | 光半導体分散樹脂組成物及びその製造方法、並びに抗菌性部材 |
| JP5914890B2 (ja) * | 2013-03-13 | 2016-05-11 | パナソニックIpマネジメント株式会社 | 銅複合酸化チタン分散液、コーティング剤組成物及び抗菌・抗ウイルス性部材 |
| JP6200569B2 (ja) * | 2015-11-20 | 2017-09-20 | イビデン株式会社 | 抗ウィルス性の化粧板及び抗ウィルス性の化粧板の製造方法 |
| JP6775341B2 (ja) * | 2016-07-13 | 2020-10-28 | イビデン株式会社 | 化粧板 |
| JP2018108724A (ja) * | 2016-12-28 | 2018-07-12 | イビデン株式会社 | 保護フィルム付き化粧板及び化粧板の施工方法 |
-
2018
- 2018-11-16 JP JP2018215700A patent/JP7012000B2/ja active Active
-
2020
- 2020-12-22 JP JP2020212471A patent/JP2021050236A/ja active Pending
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2017078331A (ja) | 2015-10-19 | 2017-04-27 | イビデン株式会社 | トイレブース用化粧板及びトイレブース |
| JP2017177802A (ja) | 2015-11-17 | 2017-10-05 | イビデン株式会社 | 化粧板 |
| JP2017094544A (ja) | 2015-11-19 | 2017-06-01 | イビデン株式会社 | 化粧板 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2021050236A (ja) | 2021-04-01 |
| JP2020040374A (ja) | 2020-03-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7796087B2 (ja) | 抗微生物基体 | |
| JP7012000B2 (ja) | 抗微生物部材 | |
| JP2021014457A (ja) | 抗微生物部材 | |
| JP6843814B2 (ja) | 抗ウィルス部材 | |
| JP2021098197A (ja) | 抗微生物硬化物の固着方法および抗微生物部材の製造方法 | |
| JP2021105018A (ja) | 抗微生物部材 | |
| JP6838035B2 (ja) | 抗微生物組成物及び抗微生物部材 | |
| JP2021006588A (ja) | 抗微生物部材 | |
| JP6843815B2 (ja) | 抗ウィルス部材 | |
| JP6838034B2 (ja) | 抗ウィルス性部材 | |
| JP6838036B2 (ja) | 抗ウィルス性部材 | |
| JP2021059562A (ja) | 抗微生物部材 | |
| JP6782752B2 (ja) | 抗微生物壁紙 | |
| JP6871222B2 (ja) | 抗ウィルス性部材 | |
| JP6876026B2 (ja) | 抗ウィルス性部材 | |
| JP7229216B2 (ja) | 抗ウィルス部材 | |
| JP2021107428A (ja) | 抗微生物部材 | |
| JP2021105019A (ja) | 抗微生物部材 | |
| JP2021187842A (ja) | 抗微生物組成物及び抗微生物基体 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20200518 |
|
| A871 | Explanation of circumstances concerning accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A871 Effective date: 20200518 |
|
| A975 | Report on accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A971005 Effective date: 20200902 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20200904 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20201027 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20201222 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20210330 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210630 |
|
| C60 | Trial request (containing other claim documents, opposition documents) |
Free format text: JAPANESE INTERMEDIATE CODE: C60 Effective date: 20210630 |
|
| C876 | Explanation why request for accelerated appeal examination is justified |
Free format text: JAPANESE INTERMEDIATE CODE: C876 Effective date: 20210630 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20210709 |
|
| C21 | Notice of transfer of a case for reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C21 Effective date: 20210713 |
|
| A912 | Re-examination (zenchi) completed and case transferred to appeal board |
Free format text: JAPANESE INTERMEDIATE CODE: A912 Effective date: 20210806 |
|
| C305 | Report on accelerated appeal examination |
Free format text: JAPANESE INTERMEDIATE CODE: C305 Effective date: 20210813 |
|
| C211 | Notice of termination of reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C211 Effective date: 20210817 |
|
| C22 | Notice of designation (change) of administrative judge |
Free format text: JAPANESE INTERMEDIATE CODE: C22 Effective date: 20210817 |
|
| C13 | Notice of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: C13 Effective date: 20210914 |
|
| C22 | Notice of designation (change) of administrative judge |
Free format text: JAPANESE INTERMEDIATE CODE: C22 Effective date: 20211026 |
|
| C30 | Protocol of an oral hearing |
Free format text: JAPANESE INTERMEDIATE CODE: C30 Effective date: 20211105 |
|
| C302 | Record of communication |
Free format text: JAPANESE INTERMEDIATE CODE: C302 Effective date: 20211109 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20211112 |
|
| C23 | Notice of termination of proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C23 Effective date: 20211130 |
|
| C03 | Trial/appeal decision taken |
Free format text: JAPANESE INTERMEDIATE CODE: C03 Effective date: 20220104 |
|
| C30A | Notification sent |
Free format text: JAPANESE INTERMEDIATE CODE: C3012 Effective date: 20220104 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20220117 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7012000 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |