JP6916524B2 - 機能的タンパク質配列をディスプレイする生合成アミロイドに基づく材料 - Google Patents
機能的タンパク質配列をディスプレイする生合成アミロイドに基づく材料 Download PDFInfo
- Publication number
- JP6916524B2 JP6916524B2 JP2017552146A JP2017552146A JP6916524B2 JP 6916524 B2 JP6916524 B2 JP 6916524B2 JP 2017552146 A JP2017552146 A JP 2017552146A JP 2017552146 A JP2017552146 A JP 2017552146A JP 6916524 B2 JP6916524 B2 JP 6916524B2
- Authority
- JP
- Japan
- Prior art keywords
- linker
- polypeptide
- csga
- item
- bacterial
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/62—DNA sequences coding for fusion proteins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/66—Microorganisms or materials therefrom
- A61K35/74—Bacteria
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/195—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria
- C07K14/24—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria from Enterobacteriaceae (F), e.g. Citrobacter, Serratia, Proteus, Providencia, Morganella, Yersinia
- C07K14/245—Escherichia (G)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/195—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria
- C07K14/33—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria from Clostridium (G)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/70—Vectors or expression systems specially adapted for E. coli
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2800/00—Nucleic acids vectors
- C12N2800/10—Plasmid DNA
- C12N2800/101—Plasmid DNA for bacteria
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Genetics & Genomics (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Molecular Biology (AREA)
- Biomedical Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Medicinal Chemistry (AREA)
- Wood Science & Technology (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Zoology (AREA)
- General Engineering & Computer Science (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Gastroenterology & Hepatology (AREA)
- Physics & Mathematics (AREA)
- Plant Pathology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Mycology (AREA)
- Epidemiology (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicinal Preparation (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
Description
本出願は、2015年4月6日に出願された米国仮出願第62/143,560号に基づく優先権を主張しており、この仮出願は、すべての目的のためにその全体が本明細書によって本明細書中に援用される。
本発明は、米国国立科学財団によって授与されたDMR−1410751の下の政府支援でなされた。政府は本発明において特定の権利を有している。
本明細書に記載されている技術は、操作されたポリペプチド、そのようなポリペプチドを含む細菌、操作された細菌、前記細菌細胞を含むバイオフィルム、操作された細菌細胞によって産生される、操作されたポリペプチドを含むバイオフィルム、および、操作された細菌細胞によって産生される、アミロイドに基づく細胞外マトリックス成分に関する。
天然では、大多数の細菌が、環境の厳しさから防御する、タンパク質、糖、脂質、および細胞外DNAの、自己生成する保護的なナノスケール足場内に存在するバイオフィルム群集として存在する。バイオフィルム形成は、天然の表面および人間により作製された表面のどちらに関しても細菌の接着および定着に必須である。これらの高度に進化した細胞外マトリックスは、有益なナノバイオテクノロジー操作プラットフォームとしての、まだ利用されていない潜在性を保持する。バイオフィルムは、排水処理および生体変換などの有益な目的に関して調査されているが、これらの試みは、天然に存在する生物の使用に焦点を当てたものである。バイオフィルムの構造を操作する試みが存在する。WO/2012/166906およびPCT/US2014/035095を参照されたい。
本開示の実施形態は、細菌を遺伝子改変して、アミロイドに基づく材料、例えば、ネイティブでない機能性ポリペプチドが発現しており、ネイティブでない機能性ポリペプチドが機能するように最適化されたリンカードメインが接続した、アミロイドファイバにより創出されたバイオフィルムなどを創出する方法を対象とする。一態様によると、リンカードメインは、CsgAタンパク質を、アミロイドの状態にアセンブルする際に機能するように、および機能性ポリペプチドが機能するように最適化されたものである。例示的なバイオフィルムは、生存細菌細胞、非生存細菌細胞または生存細菌細胞と非生存細菌細胞との組合せを含み得る。
特定の実施形態では、例えば以下の項目が提供される。
(項目1)
バイオフィルムを作製する方法であって、
ネイティブでない機能性ポリペプチドにリンカーによって連結されたCsgAタンパク質の融合物をコードする核酸配列を含む細菌細胞を増殖させるステップであって、前記融合物を発現し、前記ネイティブでない機能性ポリペプチドが付着したバイオフィルムを形成する細菌細胞の集団を産生するステップを含み、
前記リンカーが、CsgAタンパク質のC末端またはN末端のいずれかに付着した7つまたはそれ超のアミノ酸を含むポリペプチドである、方法。
(項目2)
前記核酸配列を前記細菌細胞に導入する、項目1に記載の方法。
(項目3)
前記細菌細胞がE.coliである、項目1に記載の方法。
(項目4)
前記細菌細胞が非病原性細菌である、項目1に記載の方法。
(項目5)
前記細菌細胞が、Nissle 1917株(EcN)、MG1655、LSR10またはPHL628である、項目1に記載の方法。
(項目6)
前記細菌細胞が、CsgA遺伝子のゲノム欠失を含む、項目1に記載の方法。
(項目7)
前記細菌細胞が、前記CsgAタンパク質をコードする核酸(単数または複数)が除去されるように遺伝子改変されている、項目1に記載の方法。
(項目8)
前記細菌細胞が、前記CsgAタンパク質が除去されるように遺伝子改変されている、項目1に記載の方法。
(項目9)
細菌細胞が、天然のCsgA遺伝子の発現を欠き、Nissle 1917株(EcN)、MG1655、LSR10またはPHL628である、項目1に記載の方法。
(項目10)
前記天然のCsgA遺伝子の発現を欠く細菌細胞が、Nissle 1917株(EcN)、MG1655、LSR10またはPHL628である、項目9に記載の方法。
(項目11)
前記細菌細胞が、前記CsgA遺伝子に関してノックアウトである、項目1に記載の方法。
(項目12)
前記リンカーが、7アミノ酸〜250アミノ酸である、項目1に記載の方法。
(項目13)
前記リンカーが、柔軟なリンカーまたは剛性リンカーである、項目1に記載の方法。
(項目14)
前記リンカーが、親水性または疎水性である、項目1に記載の方法。
(項目15)
前記リンカーが、反復アミノ酸サブユニットを含む、項目1に記載の方法。
(項目16)
前記リンカーが、2つまたはそれ超の反復アミノ酸サブユニットを含む、項目1に記載の方法。
(項目17)
前記リンカーが、3つまたはそれ超の反復アミノ酸サブユニットを含む、項目1に記載の方法。
(項目18)
前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含む、項目1に記載の方法。
(項目19)
前記リンカーが、[GGGS] n (式中、nは、3、6、または12である整数である)(配列番号5〜7)を含む、項目1に記載の方法。
(項目20)
前記リンカーが、[P] n (式中、nは、1から30までの整数である)(配列番号13)を含む、項目1に記載の方法。
(項目21)
前記リンカーが、[P] n (式中、nは、12または24である整数である)(配列番号8〜9)を含む、項目1に記載の方法。
(項目22)
前記リンカーが、[EAAAK] n (式中、nは、1から15までの整数である)(配列番号15)を含む、項目1に記載の方法。
(項目23)
前記リンカーが、[EAAAK] n (式中、nは、3または9である整数である)(配列番号10〜11)を含む、項目1に記載の方法。
(項目24)
前記リンカーが、グリシン、セリン、アラニンまたはロイシンのうちの1つまたは複数を含む、項目1に記載の方法。
(項目25)
前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)、[P] n (式中、nは、1から30までの整数である)(配列番号13)または[EAAAK] n (式中、nは、1から15までの整数である)(配列番号15)のうちの1つまたは複数を含む、項目1に記載の方法。
(項目26)
前記リンカーが、切断可能である、項目1に記載の方法。
(項目27)
前記リンカーが、酵素により切断可能である、項目1に記載の方法。
(項目28)
前記ネイティブでない機能性ポリペプチドが、放出可能である、項目1に記載の方法。
(項目29)
前記リンカーが、
である、項目1に記載の方法。
(項目30)
前記ネイティブでない機能性ポリペプチドが、治療用ポリペプチド、診断用ポリペプチド、組織結合性ポリペプチド、細胞結合性ポリペプチド、抗菌性ポリペプチド、抗がん性ポリペプチド、抗炎症性ポリペプチド、ポリマー結合性ポリペプチド、代謝産物結合性ポリペプチド、標的化ポリペプチドまたは分子の結合対の第1の対であるポリペプチドである、項目1に記載の方法。
(項目31)
前記細菌細胞がNissle 1917株(EcN)であり、前記リンカーが[GGGS] n (式中、nは、3、6、または12である整数である)(配列番号5〜7)である、項目1に記載の方法。
(項目32)
ネイティブでない機能性ポリペプチドにリンカーによって連結されたCsgAタンパク質の天然に存在しない融合物であって、前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含む、融合物。
(項目33)
ネイティブでない機能性ポリペプチドにリンカーによって連結されたCsgAタンパク質の融合物をコードする核酸配列であって、前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含む、核酸配列。
(項目34)
ネイティブでない機能性ポリペプチドにリンカーによって連結されたCsgAタンパク質の融合物をコードする核酸配列を含むベクターであって、前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含む、ベクター。
(項目35)
ネイティブでない機能性ポリペプチドにリンカーによって連結されたCsgAタンパク質の融合物をコードする外来核酸配列を含む細菌細胞であって、前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含む、細菌細胞。
(項目36)
ネイティブでない機能性ポリペプチドにリンカーによって連結されたCsgAタンパク質の融合物をコードする核酸配列を含むベクターを含む細菌細胞であって、前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含む、細菌細胞。
(項目37)
ネイティブでない機能性ポリペプチドにリンカーによって連結されたCsgAタンパク質の融合物をコードする外来核酸配列を発現する細菌細胞であって、前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含む、細菌細胞。
(項目38)
ネイティブでない機能性ポリペプチドにリンカーによって連結されたCsgAタンパク質の融合物をコードする外来核酸配列を発現する細菌細胞を含むバイオフィルムであって、前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含、バイオフィルム。
(項目39)
細菌細胞を生物内の組織に送達する方法であって、
前記生物に、組織結合性ポリペプチドにリンカーによって連結されたCsgAタンパク質の融合物をコードする外来核酸配列を発現する細菌細胞を導入するステップであって、前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含む、ステップを含み、
前記細菌細胞が、前記組織に前記組織結合性ポリペプチドによって付着し、それにより、前記細菌細胞が前記組織に局在化する、方法。
(項目40)
前記細菌細胞が増殖し、前記組織に付着する、細菌細胞の集団を含むバイオフィルムが形成される、項目39に記載の方法。
(項目41)
前記細菌細胞がNissle 1917株(EcN)である、項目39に記載の方法。
(項目42)
前記組織結合性ポリペプチドが、CP15、P8、A1、T18、TTF1、TTF2またはTTF3である、項目39に記載の方法。
(項目43)
前記生物内の組織が、胃腸管上皮組織である、項目39に記載の方法。
(項目44)
前記生物内の組織が、パイエル板である、項目39に記載の方法。
(項目45)
前記生物内の組織が、感染部位である、項目39に記載の方法。
(項目46)
前記生物内の組織が、上皮の損傷を受けた領域である、項目39に記載の方法。
(項目47)
前記生物内の組織が、腫瘍組織である、項目39に記載の方法。
(項目48)
前記生物内の組織が、炎症部位である、項目39に記載の方法。
(項目49)
前記生物内の組織が、結腸癌細胞を含む、項目39に記載の方法。
(項目50)
前記生物内の組織が、腸粘膜である、項目39に記載の方法。
(項目51)
前記生物内の組織が、M細胞を含む、項目39に記載の方法。
(項目52)
胃腸管の炎症を有する生物を処置する方法であって、
前記生物に、組織結合性ポリペプチドにリンカーによって連結されたCsgAタンパク質の融合物をコードする外来核酸配列を発現するNissle 1917株(EcN)細菌細胞を導入するステップであって、前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含む、ステップを含み、
前記Nissle 1917株(EcN)細菌細胞が、胃腸管の組織に前記組織結合性ポリペプチドによって付着し、それにより、前記Nissle 1917株(EcN)細菌細胞が前記組織に、炎症を軽減する様式で局在化する、方法。
(項目53)
前記Nissle 1917株(EcN)細菌細胞が増殖し、前記組織に付着した、Nissle 1917株(EcN)細菌細胞の集団を含むバイオフィルムが形成される、項目52に記載の方法。
(項目54)
前記組織結合性ポリペプチドが、CP15、P8、A1、T18、TTF1、TTF2またはTTF3である、項目52に記載の方法。
(項目55)
前記炎症が、炎症性腸疾患に由来する、項目52に記載の方法。
(項目56)
前記炎症が、クローン病または潰瘍性大腸炎に由来する、項目52に記載の方法。
(項目57)
胃腸管の炎症を有する生物を処置する方法であって、
前記生物に、抗炎症性ポリペプチドにリンカーによって連結されたCsgAタンパク質の融合物をコードする外来核酸配列を発現するNissle 1917株(EcN)細菌細胞を導入するステップであって、前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含む、ステップを含み、
前記Nissle 1917株(EcN)細菌細胞が前記胃腸管内で増殖し、前記抗炎症性ポリペプチドを含む、Nissle 1917株(EcN)細菌細胞の集団を含むバイオフィルムが、炎症を軽減する様式で形成される、方法。
(項目58)
前記抗炎症性ポリペプチドが、TTF1、TTF2またはTTF3である、項目57に記載の方法。
(項目59)
前記炎症が、炎症性腸疾患またはクローン病に由来する、項目57に記載の方法。
(項目60)
前記抗炎症性ポリペプチドが放出される、項目57に記載の方法。
(項目61)
前記リンカーが、切断可能なリンカーであり、前記抗炎症性ポリペプチドが、前記リンカーの切断によって放出される、項目57に記載の方法。
(項目62)
前記リンカーが、切断可能なリンカーであり、前記抗炎症性ポリペプチドが、酵素による前記リンカーの切断によって放出される、項目57に記載の方法。
(項目63)
前記リンカーが、切断可能なリンカーであり、前記抗炎症性ポリペプチドが、炎症の結果として産生されるプロテアーゼによる前記リンカーの切断によって放出される、項目57に記載の方法。
(項目64)
前記リンカーが、切断可能なリンカーであり、前記抗炎症性ポリペプチドが、MMPプロテアーゼによる前記リンカーの切断によって放出される、項目57に記載の方法。
(項目65)
胃腸管のがんを有する生物を処置する方法であって、
前記生物に、抗がんポリペプチドにリンカーによって連結されたCsgAタンパク質の融合物をコードする外来核酸配列を発現するNissle 1917株(EcN)細菌細胞を導入するステップであって、前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含む、ステップを含み、
前記Nissle 1917株(EcN)細菌細胞が胃腸管内で増殖し、抗がんポリペプチドを含む、Nissle 1917株(EcN)細菌細胞の集団を含むバイオフィルムが、がんの増殖を低減する様式で形成される、方法。
(項目66)
前記抗がんポリペプチドが、成長阻害性の生物学的製剤である、項目65に記載の方法。
(項目67)
前記抗がんポリペプチドが放出される、項目65に記載の方法。
(項目68)
前記リンカーが、切断可能なリンカーであり、前記抗がんポリペプチドが、前記リンカーの切断によって放出される、項目65に記載の方法。
(項目69)
前記リンカーが、切断可能なリンカーであり、前記抗がんポリペプチドが、酵素による前記リンカーの切断によって放出される、項目65に記載の方法。
(項目70)
前記リンカーが、切断可能なリンカーであり、前記抗がんポリペプチドが、胃腸管内の酵素による前記リンカーの切断によって放出される、項目65に記載の方法。
(項目71)
胃腸管内に微生物病原体を有する生物を処置する方法であって、
前記生物に、抗微生物性ポリペプチドにリンカーによって連結されたCsgAタンパク質の融合物をコードする外来核酸配列を発現するNissle 1917株(EcN)細菌細胞を導入するステップであって、前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含む、ステップを含み、
前記Nissle 1917株(EcN)細菌細胞が胃腸管内で増殖し、前記抗微生物性ポリペプチドを含む、Nissle 1917株(EcN)細菌細胞の集団を含むバイオフィルムが、前記微生物病原体の増殖を低減する様式で形成される、方法。
(項目72)
前記微生物病原体がClostridium difficileである、項目71に記載の方法。
(項目73)
前記抗微生物性ポリペプチドが、コプリシン、ツリシンCD、ランチビオティクス(lanibiotic)、ナイシン、アクタガルジン(actagardine)、カテリシジンまたはLL−37である、項目71に記載の方法。
(項目74)
前記抗微生物性ポリペプチドが放出される、項目71に記載の方法。
(項目75)
前記リンカーが、切断可能なリンカーであり、前記抗微生物性ポリペプチドが、前記リンカーの切断によって放出される、項目71に記載の方法。
(項目76)
前記リンカーが、切断可能なリンカーであり、前記抗微生物性ポリペプチドが、酵素による前記リンカーの切断によって放出される、項目71に記載の方法。
(項目77)
前記リンカーが、切断可能なリンカーであり、前記抗微生物性ポリペプチドが、胃腸管内の酵素による前記リンカーの切断によって放出される、項目71に記載の方法。
(項目78)
前記リンカーが、切断可能なリンカーであり、前記抗微生物性ポリペプチドが、胃腸管内のプロテアーゼCD2830による前記リンカーの切断によって放出される、項目71に記載の方法。
(項目79)
前記リンカーが、切断可能なリンカーであり、前記抗微生物性ポリペプチドが、微生物病原体に曝露すると放出される、項目71に記載の方法。
(項目80)
診断用ポリペプチドを生物の胃腸管に送達する方法であって、
前記生物に、診断用ポリペプチドにリンカーによって連結されたCsgAタンパク質の融合物をコードする外来核酸配列を発現するNissle 1917株(EcN)細菌細胞を導入するステップであって、前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含む、ステップを含み、
前記Nissle 1917株(EcN)細菌細胞が胃腸管内で増殖し、前記診断用ポリペプチドを含む、Nissle 1917株(EcN)細菌細胞の集団を含むバイオフィルムが形成される、方法。
(項目81)
前記診断用ポリペプチドを検出する、項目80に記載の方法。
(項目82)
前記診断用ポリペプチドが、造影剤または色素をさらに含む、項目80に記載の方法。
(項目83)
前記診断用ポリペプチドが放出される、項目80に記載の方法。
(項目84)
前記リンカーが、切断可能なリンカーであり、前記診断用ポリペプチドが、前記リンカーの切断によって放出される、項目80に記載の方法。
(項目85)
前記リンカーが、切断可能なリンカーであり、前記診断用ポリペプチドが、酵素による前記リンカーの切断によって放出される、項目80に記載の方法。
(項目86)
前記リンカーが、切断可能なリンカーであり、前記診断用ポリペプチドが、胃腸管内の酵素による前記リンカーの切断によって放出される、項目80に記載の方法。
(項目87)
生物の胃腸管内の標的を結合捕捉する方法であって、
前記生物に、捕捉剤ポリペプチドにリンカーによって連結されたCsgAタンパク質の融合物をコードする外来核酸配列を発現するNissle 1917株(EcN)細菌細胞を導入するステップであって、前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含む、ステップを含み、
前記Nissle 1917株(EcN)細菌細胞が胃腸管内で増殖し、前記捕捉剤ポリペプチドを含む、Nissle 1917株(EcN)細菌細胞の集団を含むバイオフィルムが形成され、
前記捕捉標的が前記捕捉剤ポリペプチドに結合する、方法。
(項目88)
結合した捕捉標的を含むバイオフィルムが前記生物から排出される、項目87に記載の方法。
(項目89)
結合した捕捉標的を含むバイオフィルムが組織から除去され、前記生物から排出される、項目87に記載の方法。
(項目90)
結合した捕捉標的を含むバイオフィルムが天然のプロセスによって組織から除去され、前記生物から排出される、項目87に記載の方法。
(項目91)
前記捕捉剤ポリペプチドが放出される、項目87に記載の方法。
(項目92)
前記リンカーが、切断可能なリンカーであり、前記捕捉剤ポリペプチドが、前記リンカーの切断によって放出される、項目87に記載の方法。
(項目93)
前記リンカーが、切断可能なリンカーであり、前記捕捉剤ポリペプチドが、酵素による前記リンカーの切断によって放出される、項目87に記載の方法。
(項目94)
前記リンカーが、切断可能なリンカーであり、前記捕捉剤ポリペプチドが、胃腸管内の酵素による前記リンカーの切断によって放出される、項目87に記載の方法。
(項目95)
機能性薬剤を生物の胃腸管に送達する方法であって、
前記生物に、分子の結合対の第1のメンバーであるポリペプチドにリンカーによって連結されたCsgAタンパク質の融合物をコードする外来核酸配列を発現するNissle 1917株(EcN)細菌細胞を導入するステップであって、前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含む、ステップであって、
前記Nissle 1917株(EcN)細菌細胞が胃腸管内で増殖し、分子の結合対の第1のメンバーを含む、Nissle 1917株(EcN)細菌細胞の集団を含むバイオフィルムが形成される、ステップと、
機能性薬剤が付着した、前記分子の結合対の第2のメンバーを胃腸管に導入するステップと、を含み、
前記分子の結合対の第1のメンバーおよび第2のメンバーが互いと結合し、それにより、前記機能性薬剤が前記バイオフィルムに付着する、方法。
(項目96)
CsgAタンパク質をコードするネイティブな配列を欠くように遺伝子改変された細菌細胞。
(項目97)
E.coliである、項目96に記載の細菌。
(項目98)
Nissle 1917株(EcN)である、項目96に記載の細菌。
(項目99)
CsgAタンパク質をコードするネイティブな配列を欠くように遺伝子改変されており、ネイティブでない機能性ポリペプチドにリンカーによって連結されたCsgAタンパク質の融合物をコードする外来核酸配列を含む細菌細胞であって、前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含む、細菌細胞。
(項目100)
CsgAタンパク質をコードするネイティブな配列を欠くように遺伝子改変されており、ネイティブでない機能性ポリペプチドにリンカーによって連結されたCsgAタンパク質の融合物をコードする核酸配列を含むベクターを含む細菌細胞であって、前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含む、細菌細胞。
(項目101)
CsgAタンパク質をコードするネイティブな配列を欠くように遺伝子改変されており、ネイティブでない機能性ポリペプチドにリンカーによって連結されたCsgAタンパク質融合物をコードする外来核酸配列を発現する細菌細胞であって、前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含む、細菌細胞。
(項目102)
胃腸管の炎症を有する生物を処置する方法であって、
前記生物に、組織結合性ポリペプチドにリンカーによって連結されたCsgAタンパク質の融合物をコードする外来核酸配列を発現するE.coli細菌細胞を導入するステップであって、前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含む、ステップを含み、
前記E.coli細菌細胞が、胃腸管の組織に前記組織結合性ポリペプチドによって付着し、それにより、前記E.coli細菌細胞が前記組織に、炎症を軽減する様式で局在化する、方法。
(項目103)
前記E.coli細菌細胞が増殖し、前記組織に付着した、E.coli細菌細胞の集団を含むバイオフィルムが形成される、項目102に記載の方法。
(項目104)
前記組織結合性ポリペプチドが、CP15、P8、A1、T18、TTF1、TTF2またはTTF3である、項目102に記載の方法。
(項目105)
前記炎症が、炎症性腸疾患に由来する、項目102に記載の方法。
(項目106)
前記炎症が、クローン病または潰瘍性大腸炎に由来する、項目102に記載の方法。
(項目107)
胃腸管の炎症を有する生物を処置する方法であって、
前記生物に、抗炎症性ポリペプチドにリンカーによって連結されたCsgAタンパク質の融合物をコードする外来核酸配列を発現するE.coli細菌細胞を導入するステップであって、前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含む、ステップを含み、
前記E.coli細菌細胞が前記胃腸管内で増殖し、前記抗炎症性ポリペプチドを含む、E.coli細菌細胞の集団を含むバイオフィルムが、炎症を軽減する様式で形成される、方法。
(項目108)
前記抗炎症性ポリペプチドが、TTF1、TTF2またはTTF3である、項目107に記載の方法。
(項目109)
前記炎症が、炎症性腸疾患またはクローン病に由来する、項目107に記載の方法。
(項目110)
前記抗炎症性ポリペプチドが放出される、項目107に記載の方法。
(項目111)
前記リンカーが、切断可能なリンカーであり、前記抗炎症性ポリペプチドが、前記リンカーの切断によって放出される、項目107に記載の方法。
(項目112)
前記リンカーが、切断可能なリンカーであり、前記抗炎症性ポリペプチドが、酵素による前記リンカーの切断によって放出される、項目107に記載の方法。
(項目113)
前記リンカーが、切断可能なリンカーであり、前記抗炎症性ポリペプチドが、炎症の結果として産生されるプロテアーゼによる前記リンカーの切断によって放出される、項目107に記載の方法。
(項目114)
前記リンカーが、切断可能なリンカーであり、前記抗炎症性ポリペプチドが、MMPプロテアーゼによる前記リンカーの切断によって放出される、項目107に記載の方法。
(項目115)
胃腸管のがんを有する生物を処置する方法であって、
前記生物に、抗がんポリペプチドにリンカーによって連結されたCsgAタンパク質の融合物をコードする外来核酸配列を発現するE.coli細菌細胞を導入するステップであって、前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含む、ステップを含み、
前記E.coli細菌細胞が胃腸管内で増殖し、抗がんポリペプチドを含む、E.coli細菌細胞の集団を含むバイオフィルムが、がんの増殖を低減する様式で形成される、方法。
(項目116)
前記抗がんポリペプチドが、成長阻害性の生物学的製剤である、項目115に記載の方法。
(項目117)
前記抗がんポリペプチドが放出される、項目115に記載の方法。
(項目118)
前記リンカーが、切断可能なリンカーであり、前記抗がんポリペプチドが、前記リンカーの切断によって放出される、項目115に記載の方法。
(項目119)
前記リンカーが、切断可能なリンカーであり、前記抗がんポリペプチドが、酵素による前記リンカーの切断によって放出される、項目115に記載の方法。
(項目120)
前記リンカーが、切断可能なリンカーであり、前記抗がんポリペプチドが、胃腸管内の酵素による前記リンカーの切断によって放出される、項目115に記載の方法。
(項目121)
胃腸管内に微生物病原体を有する生物を処置する方法であって、
前記生物に、抗微生物性ポリペプチドにリンカーによって連結されたCsgAタンパク質の融合物をコードする外来核酸配列を発現するE.coli細菌細胞を導入するステップであって、前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含む、ステップを含み、
前記E.coli細菌細胞が胃腸管内で増殖し、前記抗微生物性ポリペプチドを含む、
E.coli細菌細胞の集団を含むバイオフィルムが前記微生物病原体の増殖を低減する様式で形成される、方法。
(項目122)
前記微生物病原体がClostridium difficileである、項目121に記載の方法。
(項目123)
前記抗微生物性ポリペプチドが、コプリシン、ツリシンCD、ランチビオティクス、ナイシン、アクタガルジン、カテリシジンまたはLL−37である、項目121に記載の方法。
(項目124)
前記抗微生物性ポリペプチドが放出される、項目121に記載の方法。
(項目125)
前記リンカーが、切断可能なリンカーであり、前記抗微生物性ポリペプチドが、前記リンカーの切断によって放出される、項目121に記載の方法。
(項目126)
前記リンカーが、切断可能なリンカーであり、前記抗微生物性ポリペプチドが、酵素による前記リンカーの切断によって放出される、項目121に記載の方法。
(項目127)
前記リンカーが、切断可能なリンカーであり、前記抗微生物性ポリペプチドが、胃腸管内の酵素による前記リンカーの切断によって放出される、項目121に記載の方法。
(項目128)
前記リンカーが、切断可能なリンカーであり、前記抗微生物性ポリペプチドが、胃腸管内のプロテアーゼCD2830による前記リンカーの切断によって放出される、項目121に記載の方法。
(項目129)
前記リンカーが、切断可能なリンカーであり、前記抗微生物性ポリペプチドが、微生物病原体に曝露すると放出される、項目121に記載の方法。
(項目130)
診断用ポリペプチドを生物の胃腸管に送達する方法であって、
前記生物に、診断用ポリペプチドにリンカーによって連結されたCsgAタンパク質の融合物をコードする外来核酸配列を発現するE.coli細菌細胞を導入するステップであって、前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含む、ステップを含み、
前記E.coli細菌細胞が胃腸管内で増殖し、前記診断用ポリペプチドを含む、E.coli細菌細胞の集団を含むバイオフィルムが形成される、方法。
(項目131)
前記診断用ポリペプチドを検出する、項目130に記載の方法。
(項目132)
前記診断用ポリペプチドが、造影剤または色素をさらに含む、項目130に記載の方法。
(項目133)
前記診断用ポリペプチドが放出される、項目130に記載の方法。
(項目134)
前記リンカーが、切断可能なリンカーであり、前記診断用ポリペプチドが、前記リンカーの切断によって放出される、項目130に記載の方法。
(項目135)
前記リンカーが、切断可能なリンカーであり、前記診断用ポリペプチドが、酵素による前記リンカーの切断によって放出される、項目130に記載の方法。
(項目136)
前記リンカーが、切断可能なリンカーであり、前記診断用ポリペプチドが、胃腸管内の酵素による前記リンカーの切断によって放出される、項目130に記載の方法。
(項目137)
生物の胃腸管内の標的を結合捕捉する方法であって、
前記生物に、捕捉剤ポリペプチドにリンカーによって連結されたCsgAタンパク質の融合物をコードする外来核酸配列を発現するE.coli細菌細胞を導入するステップであって、前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含む、ステップを含み、
前記E.coli細菌細胞が胃腸管内で増殖し、前記捕捉剤ポリペプチドを含む、E.coli細菌細胞の集団を含むバイオフィルムが形成され、
前記捕捉標的が前記捕捉剤ポリペプチドに結合する、方法。
(項目138)
結合した捕捉標的を含むバイオフィルムが前記生物から排出される、項目137に記載の方法。
(項目139)
結合した捕捉標的を含むバイオフィルムが組織から除去され、前記生物から排出される、項目137に記載の方法。
(項目140)
結合した捕捉標的を含むバイオフィルムが天然のプロセスによって組織から除去され、そして前記生物から排出される、項目137に記載の方法。
(項目141)
前記捕捉剤ポリペプチドが放出される、項目137に記載の方法。
(項目142)
前記リンカーが、切断可能なリンカーであり、前記捕捉剤ポリペプチドが、前記リンカーの切断によって放出される、項目137に記載の方法。
(項目143)
前記リンカーが、切断可能なリンカーであり、前記捕捉剤ポリペプチドが、酵素による前記リンカーの切断によって放出される、項目137に記載の方法。
(項目144)
前記リンカーが、切断可能なリンカーであり、前記捕捉剤ポリペプチドが、胃腸管内の酵素による前記リンカーの切断によって放出される、項目137に記載の方法。
(項目145)
機能性薬剤を生物の胃腸管に送達する方法であって、
前記生物に、分子の結合対の第1のメンバーであるポリペプチドにリンカーによって連結されたCsgAタンパク質の融合物をコードする外来核酸配列を発現するE.coli細菌細胞を導入するステップであって、前記リンカーが、[GGGS] n (式中、nは、2から20までの整数である)(配列番号12)を含む、ステップであって、
前記E.coli細菌細胞が胃腸管内で増殖し、分子の結合対の第1のメンバーを含む、E.coli細菌細胞の集団を含むバイオフィルムが形成される、ステップと、
機能性薬剤が付着した、前記分子の結合対の第2のメンバーを胃腸管に導入するステップと、を含み、
前記分子の結合対の第1のメンバーと第2のメンバーが互いと結合し、それにより、前記機能性薬剤が前記バイオフィルムに付着する、方法。
本開示の態様は、リンカードメインによって相互接続した自己アセンブルドメインと可変性機能性ドメインとを有する構造を対象とする。一態様によると、自己アセンブルドメインは、細菌マトリックスタンパク質である。一態様によると、自己アセンブルドメインは、アミロイド形成タンパク質である。
リンカーのデザイン
アミロイドドメイン(CsgA)と機能性ペプチドドメイン(FLAG)との間の種々のリンカーデザインを試験するために、試験アミロイドキメラタンパク質ライブラリーを構築した。CsgAタンパク質は、細菌Escherichia coliから分泌され、次いで、当該タンパク質が自己アセンブルして、直径約4〜7nmの高度にロバストな機能性アミロイドナノファイバーになる。これらのアミロイドファイバは「curli」として公知であり、細胞を封入する、延長した絡み合ったネットワークとして存在する。FLAGドメインは、アフィニティークロマトグラフィーおよびエピトープ−タグを付けたタンパク質検出のために使用されるオクタペプチドポリペプチドタグである。
アミロイドナノファイバー産生の分析
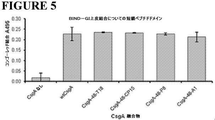
種々の介在リンカーを有するCsgA−リンカー−FLAGキメラを、curliナノファイバーへの最適な自己アセンブルについて試験した。種々のリンカーを有するタンパク質ライブラリーのcurliナノファイバーへの自己アセンブルを、アミロイドの比色定量検出のために使用される標準の染色であるコンゴーレッド(CR)を使用して検出した。首尾よく分泌され、アミロイドナノファイバーへの自己アセンブルに関してコンピテントな融合タンパク質を発現するE.coli細胞のみが赤色に染色される。図1に示されている通り、柔軟なリンカー(F12、F24、およびF48)の全てで、いくらかの中間のレベルのCR染色が示され、最長のリンカーで最大の量が示される。剛性リンカーに関しては、より長いポリプロリンリンカーではCR染色が示されず、EK3リンカーについて最大量のCR染色が得られた。より長い剛性リンカーを有するポリプロリンおよびEAAAK(配列番号14)リンカーにより、より少ない染色がもたらされる傾向がみられる。これは単に代表的な実施形態であること、および、プロリンを24個有するポリプロリンリンカーが所与の機能性ポリペプチドに対して有用なリンカーであり得ることが理解されるべきである。
ペプチドドメイン機能性の決定
FLAGエピトープタグが利用可能であり、抗FLAG抗体に結合するというその規定された機能を適正に果たすことができるかどうかを決定するために、全細胞培養物試料のイムノブロット分析を実施した。柔軟なリンカーを有するCsgA−リンカー−FLAG構造では、リンカーの長さに応じて蛍光の単調な増大が実証された。ポリプロリン剛性リンカーを有するCsgA−リンカー−FLAG構造では蛍光がなかった。科学的理論に縛られることを望むものではないが、これらの疎水性リンカーは、ペプチドタグの適切な機能を妨害する可能性がある。アルファヘリックスEAAAK(配列番号14)リンカーを有するCsgA−リンカー−FLAG構造では、EK9構築物よりも多くのCR染色を有したEK3リンカー構築物(図1を参照されたい)では蛍光がより少ないことが示された。対照的に、CR結合がより少ないEK9リンカー構築物では蛍光シグナルが高く、これにより、FLAGエピトープタグの利用可能性がより大きいことが示される。図2を参照されたい。
リンカーのデザインを最適化する方法
本開示の態様は、CsgAと機能性ポリペプチドとを連結するためのリンカーのデザインを最適化する方法を対象とする。この態様によると、CsgAと連結するための機能性ポリペプチドを選択する。次いで、リンカーのデザインを選択してCsgA−リンカー−機能性ポリペプチド構造を形成する。次いで、細菌を、CsgA−リンカー−機能性ポリペプチド構造をコードする核酸配列を含むように改変する。次いで、改変された細菌を増殖させて細菌の集団にし、CsgA−リンカー−機能性ポリペプチド構造の発現についてアッセイする。次いで、改変された細菌を増殖させて細菌の集団にし、CsgA−リンカー−機能性ポリペプチド構造のバイオフィルムの形成についてアッセイする。バイオフィルムを、機能性ポリペプチドの機能特性についてアッセイすることができる。したがって、本明細書に記載の例示的なリンカーにより、自己アセンブルが可能になり、CsgA−リンカー−機能性ポリペプチド構造の機能的ドメインが互いに干渉せずに作動または機能することが可能になる。バイオフィルム形成および機能性ポリペプチドの機能特性に対するリンカーの影響を決定する例示的な方法を図3に示す。最適化されていないリンカードメインは、機能的ドメインに対する結合性部位をふさぐこと、CsgAもしくは機能性ポリペプチドドメインの適切なフォールディングを妨げること、アミロイドファイバのアセンブリを妨害すること、または分泌を妨害することにより、バイオフィルムに基づく材料の性能を妨害する可能性がある。最適化されたリンカーでは、これらの問題が最小限になり、バイオフィルムの所望の機能が改善される。最適化されたリンカードメインにより、広範囲の条件下(極度の温度、極度のpH、好ましくない溶媒の存在下、屋外での適用における要素への曝露など)での優れた機械的および生物物理学的安定性を有するバイオフィルムに基づく材料の製作が容易になる。最適化されたリンカードメインにより、各機能性ペプチドドメインが独立に作動することが可能になり、マイクロスケールまたはマクロスケールでの所望の挙動に寄与する材料中の機能性ペプチドドメインの数が有効に増大する。例えば、バイオフィルムに基づく材料の所望の機能が金属結合性である場合、不適切なリンカードメインによって生じる分子の混み合いまたは望ましくない分子間相互作用が原因で材料の安定性または金属結合親和性が阻害される。最適化されたリンカードメインにより、望ましくない分子間相互作用が起こることが減り、最終的に材料の性能が増強される。
腸管上皮結合
本開示の態様は、健康であるか疾患にかかっているかにかかわらず、特定の組織または細胞に結合する異種ドメインを有するバイオフィルムを創出するための、操作された細菌の使用方法を対象とする。一態様によると、細菌は、非病原性細菌である。例示的な非病原性細菌としては、Nissle 1917株(EcN)、MG1655、K12由来株、PHL628、LSR10、LSR6などが挙げられる。Mutaflorという商品名でプロバイオティクスとして販売されている野生型EcNは、経口的に送達することができ、上部胃腸管を生きて移行し、次いで、回腸および結腸で最初の投与から数日間、一過性に定着する。この定着プロセスの間に、EcNはcurliファイバを産生する。
CsgA−(GGGS)n−TTF1(式中、nは、3、6または9である)(配列番号41)
CsgA−(GGGS)n−TTF2(式中、nは、3、6または9である)(配列番号41)
CsgA−(GGGS)n−TTF3(式中、nは、3、6または9である)(配列番号41)
CsgA−(GGGS)n−T18(式中、nは、3、6または9である)(配列番号41)
CsgA−(GGGS)n−CP15(式中、nは、3、6または9である)(配列番号41)
CsgA−(GGGS)n−P8(式中、nは、3、6または9である)(配列番号41)
が挙げられる。
腸管の慢性炎症性疾患の処置
本開示の態様は、炎症性腸疾患およびクローン病などの腸管の慢性炎症性疾患を、それを必要とする個体に本明細書に記載されているある特定の操作された細菌株(単数または複数)を投与することによって処置する方法を対象とする。一態様によると、細菌株に、CsgA−リンカー−抗炎症性ポリペプチド構築物を発現させる。
腸管のがんの処置
本開示の態様は、胃腸管のがんなどのがんを、それを必要とする個体に本明細書に記載されているある特定の操作された細菌株(単数または複数)を投与することによって処置する方法を対象とする。一態様によると、細菌株に、CsgA−リンカー−がん処置用ポリペプチド構築物を発現させる。ある特定のがん処置用ポリペプチドとしては、例えばベバシズマブ、セツキシマブ、パニツムマブなどの成長阻害因子を含めた、がんに対する公知の活性を有するものが挙げられる。
診断方法
本開示の態様は、マーカーなどの診断剤を、哺乳動物内の部位に、哺乳動物に本明細書に記載されているある特定の操作された細菌株(単数または複数)を投与することによって送達する方法を対象とする。一態様によると、細菌株に、CsgA−リンカー−診断用ポリペプチド構築物を発現させる。
腸管媒介性病原体の処置
本開示の態様は、腸管媒介性病原体を、それを必要とする個体に本明細書に記載されているある特定の操作された細菌株(単数または複数)を投与することによって処置する方法を対象とする。一態様によると、細菌株に、CsgA−リンカー−抗菌性ポリペプチド構築物を発現させる。ある特定の抗菌性ポリペプチドまたはタンパク質は、抗菌活性を有する任意のポリペプチドまたはタンパク質配列を含む。治療的な状況において使用するための抗菌性ペプチドは、当業者に公知である。Cotter, P. D.、Ross, R. P.およびHill, C. Bacteriocins - a viable alternative to antibiotics? Nat Rev Micro、11巻、95〜105頁(2012年);Hing, T. C.ら、The antimicrobial peptide cathelicidin modulates Clostridium difficile-associated colitis and toxin A-mediated enteritis in mice. Gut、62巻、1295〜1305頁(2013年);Nuding, S.、Frasch, T.、Schaller, M.、Stange, E. F.およびZabel, L. T. Synergistic Effects of Antimicrobial Peptides and Antibiotics against Clostridium difficile. Antimicrobial Agents and Chemotherapy、58巻、5719〜5725頁(2014年);Rea, M. C.ら、Thuricin CD, a posttranslationally modified bacteriocin with a narrow spectrum of activity against Clostridium difficile. Proc Natl Acad Sci USA、107巻、9352〜9357頁(2010年);Petrof, E. Probiotics and Gastrointestinal Disease:Clinical Evidence and Basic Science. AIAAMC、8巻、260〜269頁(2009年);Kang、J. K.ら、The Insect Peptide Coprisin Prevents Clostridium difficile-Mediated Acute Inflammation and Mucosal Damage through Selective Antimicrobial Activity. Antimicrobial Agents and Chemotherapy、55巻、4850〜4857頁(2011年);およびOstaff, M. J.、Stange, E. F.およびWehkamp, J.、Antimicrobial peptides and gut microbiota in homeostasis and pathology.、EMBO Mol Med、5巻、1465〜1483頁(2013年)を参照されたい。
有害な薬剤、毒素または代謝産物の選択的捕捉
本開示の態様は、有害な薬剤、毒素または代謝産物などの捕捉標的を、それを必要とする個体に本明細書に記載されているある特定の操作された細菌株(単数または複数)を投与することによって捕捉する方法を対象とする。一態様によると、細菌株に、CsgA−リンカー−捕捉剤ポリペプチド構築物を発現させる。ある特定の捕捉剤および関連する捕捉標的としては、コレステロールおよびコレステロール結合性ペプチド、リン酸およびリン酸結合性ペプチド、グリアジンおよびグリアジン結合性ペプチドなど、ならびに文献検索によって容易に同定されるものが挙げられる。代表例を以下の表5に示す。
生診断薬としての操作された細菌
本開示の態様は、マーカーなどの診断剤を、哺乳動物内の部位に、哺乳動物に本明細書に記載されているある特定の操作された細菌株(単数または複数)を投与することによって送達する方法を対象とする。一態様によると、細菌株に、CsgA−リンカー−診断用ポリペプチド構築物を発現させる。
追加的な適用
本開示の態様では、生体触媒として、CsgAタンパク質とネイティブでない機能性ポリペプチドとがリンカーによって連結した融合物を発現する、改変された細胞を利用する。この態様によると、本明細書に記載のcurliに由来する材料およびバイオフィルムを、工業への適用(水の精製、バイオ燃料の生成など)および医薬への適用(薬物中間体の合成)において化学的変換を実施するために使用する酵素などの酵素の固定化のための機能化可能な表面として使用するための方法が提供される。CsgA−リンカー−固定化酵素は、本明細書に記載のリンカーを含む。
Claims (18)
- バイオフィルムを作製する方法であって、
ネイティブでない機能性ポリペプチドにリンカーによって連結されたCsgAタンパク質の融合物をコードする核酸を含む細菌細胞を増殖させるステップであって、前記融合物を発現し、前記ネイティブでない機能性ポリペプチドが付着したバイオフィルムを形成する細菌細胞の集団を産生するステップを含み、
前記リンカーが、CsgAタンパク質のC末端に付着した[GGGS]n(式中、nは、3、6、または12である整数である)(配列番号5〜7)からなり、前記ネイティブでない機能性ポリペプチドがTFF1、TFF2、またはTFF3である、方法。 - 前記核酸を前記細菌細胞に導入する、請求項1に記載の方法。
- 前記細菌細胞がEscherichia coliである、請求項1に記載の方法。
- 前記細菌細胞が、csgA遺伝子のゲノム欠失を含み;
前記細菌細胞が、csgA遺伝子の発現を欠失しており、必要に応じて前記csgA遺伝子の発現を欠く前記細菌細胞が、Nissle 1917株(EcN)、MG1655、LSR10またはPHL628である;
前記細菌細胞が、CsgAタンパク質をコードする核酸(単数または複数)が除去されるように遺伝子改変されている;
前記細菌細胞が、CsgAタンパク質が除去されるように遺伝子改変されている;または
前記細菌細胞が、csgA遺伝子に関してノックアウトである、
請求項1に記載の方法。 - 前記細菌細胞がNissle 1917株(EcN)である、請求項1に記載の方法。
- ネイティブでない機能性ポリペプチドにリンカーによって連結されたCsgAタンパク質のC末端の天然に存在しない融合物であって、前記リンカーが、[GGGS]n(式中、nは、3、6、または12である整数である)(配列番号5〜7)からなり、前記ネイティブでない機能性ポリペプチドがTFF1、TFF2、またはTFF3である、融合物。
- 請求項5に記載の融合物をコードする核酸。
- 請求項7に記載の核酸を含むベクター。
- 請求項7に記載の核酸を含む細菌細胞。
- 請求項6に記載の融合物を発現する細菌細胞。
- 請求項9に記載の細菌細胞を含むバイオフィルム。
- 細菌細胞を生物内の組織に送達するための医薬組成物であって、
請求項9に記載の細菌細胞を有効成分として含み、前記ネイティブでない機能性ポリペプチドが、組織結合性ポリペプチドである、医薬組成物。 - 前記細菌細胞が増殖し、前記組織に付着するバイオフィルムを産生することができる、請求項12に記載の医薬組成物。
- 前記生物内の組織が、胃腸管上皮組織、パイエル板、感染部位、上皮の損傷を受けた領域、腫瘍組織、炎症部位、結腸癌細胞、腸粘膜またはM細胞である、請求項12に記載の医薬組成物。
- 胃腸管の炎症を有する生物を処置するための医薬組成物であって、
請求項9に記載の細菌細胞を含み、前記ネイティブでない機能性ポリペプチドが、組織結合性ポリペプチドであり、前記細菌細胞が、E.coli細菌細胞であり、
前記細菌細胞が、胃腸管の組織に前記組織結合性ポリペプチドによって付着することができ、それにより、前記細菌細胞が前記組織に、炎症を軽減する様式で局在化する、医薬組成物。 - 前記炎症が、炎症性腸疾患、クローン病または潰瘍性大腸炎に由来する、請求項15に記載の医薬組成物。
- 胃腸管の炎症を有する生物を処置するための医薬組成物であって、
請求項9に記載の細菌細胞を含み、前記ネイティブでない機能性ポリペプチドが、抗炎症性ポリペプチドであり、前記細菌細胞が、E.coli細菌細胞であり、
前記細菌細胞が前記胃腸管内で増殖することができ、前記抗炎症性ポリペプチドを含むバイオフィルムを、炎症を軽減する様式で形成することができる、医薬組成物。 - 前記炎症が、炎症性腸疾患またはクローン病に由来する、請求項17に記載の医薬組成物。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021030187A JP7156726B2 (ja) | 2015-04-06 | 2021-02-26 | 機能的タンパク質配列をディスプレイする生合成アミロイドに基づく材料 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201562143560P | 2015-04-06 | 2015-04-06 | |
| US62/143,560 | 2015-04-06 | ||
| PCT/US2016/026161 WO2016164422A2 (en) | 2015-04-06 | 2016-04-06 | Biosynthetic amyloid-based materials displaying functional protein sequences |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021030187A Division JP7156726B2 (ja) | 2015-04-06 | 2021-02-26 | 機能的タンパク質配列をディスプレイする生合成アミロイドに基づく材料 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2018517398A JP2018517398A (ja) | 2018-07-05 |
| JP2018517398A5 JP2018517398A5 (ja) | 2019-05-16 |
| JP6916524B2 true JP6916524B2 (ja) | 2021-08-11 |
Family
ID=57072695
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017552146A Active JP6916524B2 (ja) | 2015-04-06 | 2016-04-06 | 機能的タンパク質配列をディスプレイする生合成アミロイドに基づく材料 |
| JP2021030187A Active JP7156726B2 (ja) | 2015-04-06 | 2021-02-26 | 機能的タンパク質配列をディスプレイする生合成アミロイドに基づく材料 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021030187A Active JP7156726B2 (ja) | 2015-04-06 | 2021-02-26 | 機能的タンパク質配列をディスプレイする生合成アミロイドに基づく材料 |
Country Status (4)
| Country | Link |
|---|---|
| US (2) | US20180258435A1 (ja) |
| EP (1) | EP3280397A4 (ja) |
| JP (2) | JP6916524B2 (ja) |
| WO (1) | WO2016164422A2 (ja) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014176311A1 (en) | 2013-04-23 | 2014-10-30 | President And Fellows Of Harvard College | Genetic reprogramming of bacterial biofilms |
| EP3280397A4 (en) | 2015-04-06 | 2018-08-22 | President and Fellows of Harvard College | Biosynthetic amyloid-based materials displaying functional protein sequences |
| US11098133B2 (en) | 2016-05-19 | 2021-08-24 | President And Fellows Of Harvard College | Methods of making gels and films using curli nanofibers |
| FR3099648B1 (fr) * | 2019-07-30 | 2023-01-13 | Centre Nat Rech Scient | Membrane échangeuse d’ions |
| CN110585482B (zh) * | 2019-08-02 | 2022-03-01 | 大连理工大学 | 一种具有抗菌性能的杂萘联苯聚芳醚腈及其表面改性方法 |
| CN112608876B (zh) * | 2020-12-30 | 2024-02-09 | 江苏大学 | 一种生物素化Curli蛋白的活细胞标记方法及其应用 |
| GB202216905D0 (en) * | 2022-11-11 | 2022-12-28 | Oxford Nanopore Tech Plc | Novel pore monomers and pores |
Family Cites Families (34)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5762620A (en) | 1992-04-02 | 1998-06-09 | Ndm Acquisition Corp. | Wound dressing containing a partially dehydrated hydrogel |
| US6864365B1 (en) * | 1999-04-05 | 2005-03-08 | Innovation And Development Corporation, University Of Victoria | Bacterial fimbrial system for presentation of heterologous peptide sequences |
| US6916789B2 (en) * | 2001-07-02 | 2005-07-12 | Merrion Research I Limited | Peyer's patch and/or M-cell targeting ligands |
| EP1572908A4 (en) | 2002-02-14 | 2008-10-22 | William J Rutter | CHIMERIC MOLECULES FOR ADMINISTERING CLEAVAGE TO A TREATED HOST |
| EP2060280A3 (en) | 2003-04-30 | 2009-05-27 | Drexel University | Thermogelling polymer blends for biomaterial applications |
| CA2599723A1 (en) * | 2005-03-04 | 2006-09-14 | Biorexis Pharmaceutical Corporation | Modified transferrin fusion proteins |
| EP2115146B1 (en) | 2007-01-12 | 2016-07-06 | Intrexon Actobiotics NV | Lactococcus promoters and uses thereof |
| JP2009073766A (ja) * | 2007-09-21 | 2009-04-09 | Otsuka Pharmaceut Co Ltd | 医薬 |
| WO2010111516A2 (en) | 2009-03-25 | 2010-09-30 | Whitehead Institute For Biomedical Research | Compositions and methods for inhibiting biofilms |
| US20110033389A1 (en) | 2009-04-29 | 2011-02-10 | Zhifeng Chen | Modified antibodies for passive immunotherapy |
| US20110108199A1 (en) | 2009-11-10 | 2011-05-12 | Tyco Healthcare Group Lp | Hemostatic Tapes and Dispensers Therefor |
| EP2977055A1 (en) * | 2010-02-16 | 2016-01-27 | Novo Nordisk A/S | Factor viii fusion protein |
| EP2552458A4 (en) | 2010-03-31 | 2014-08-27 | Univ Wayne State | HYDROGEL NANOPARTICLES OF INJECTABLE DENDRIMER |
| KR20110111594A (ko) | 2010-04-05 | 2011-10-12 | 서울대학교산학협력단 | 알파-시뉴클레인 유래 곱슬 아밀로이드 섬유의 제조방법, 이를 이용한 하이드로젤의 제조 방법 및 그 이용 방법 |
| US8741417B2 (en) | 2010-04-16 | 2014-06-03 | Korea University Research And Business Foundation | Films having switchable reflectivity |
| WO2012048289A1 (en) | 2010-10-08 | 2012-04-12 | Board Of Regents, The University Of Texas System | Anti-adhesive barrier membrane using alginate and hyaluronic acid for biomedical applications |
| EP2627770B1 (en) * | 2010-10-15 | 2017-06-28 | Cornell University | Compositions and methods for treating endocrine, gastrointestinal or autoimmune disorders |
| KR20120060442A (ko) | 2010-12-02 | 2012-06-12 | 가톨릭대학교 산학협력단 | 위암 진단용 마커로서 tff2의 용도 |
| US9140698B2 (en) * | 2011-04-06 | 2015-09-22 | The Board Of Regents Of The University Of Texas System | Modulating bacterial MAM polypeptides in pathogenic disease |
| US9580480B2 (en) * | 2011-05-31 | 2017-02-28 | Massachusetts Institute Of Technology | Cell-directed synthesis of multifunctional nanopatterns and nanomaterials |
| WO2013009545A1 (en) | 2011-07-08 | 2013-01-17 | Amylin Pharmaceuticals, Inc. | Engineered polypeptides having enhanced duration of action with reduced immunogenicity |
| JP6325979B2 (ja) | 2011-08-03 | 2018-05-16 | ザ チルドレンズ メディカル センター コーポレーション | インフルエンザ血球凝集素の受容体結合ポケットを認識する広域中和ヒト抗体 |
| US9814756B2 (en) | 2012-06-15 | 2017-11-14 | Temple University—Of the Commonwealth System of Higher Education | Use of isolated bacterial amyloids for treatment of inflammatory disorders or diseases of the epithelium |
| AU2013293092A1 (en) * | 2012-07-23 | 2015-02-26 | Zymeworks Inc. | Immunoglobulin constructs comprising selective pairing of the light and heavy chains |
| US20150291991A1 (en) | 2012-11-16 | 2015-10-15 | President And Fellows Of Harvard College | Methods and compositions relating to amyloidogenic polypeptides |
| DK2943511T3 (da) * | 2013-01-14 | 2019-10-21 | Xencor Inc | Nye heterodimeriske proteiner |
| JP2014156428A (ja) * | 2013-02-15 | 2014-08-28 | Univ Of Tokyo | 抗体結合タンパク質 |
| WO2014139468A1 (en) * | 2013-03-15 | 2014-09-18 | Admark Healthcare, Llc | Fusion protein molecules and method of use |
| WO2014176311A1 (en) | 2013-04-23 | 2014-10-30 | President And Fellows Of Harvard College | Genetic reprogramming of bacterial biofilms |
| EP3074416A4 (en) | 2013-11-30 | 2017-09-13 | Agency for Science, Technology and Research | Self-assembling peptides, peptidomimetics and peptidic conjugates as building blocks for biofabrication and printing |
| US20160326220A1 (en) | 2013-12-24 | 2016-11-10 | Vib Vzw | Secretion and functional display of chimeric polypeptides |
| US20150342893A1 (en) | 2014-05-29 | 2015-12-03 | Sigmoid Pharma Limited | Celecoxib formulations useful for treating colorectal cancer |
| EP3280397A4 (en) | 2015-04-06 | 2018-08-22 | President and Fellows of Harvard College | Biosynthetic amyloid-based materials displaying functional protein sequences |
| US11098133B2 (en) | 2016-05-19 | 2021-08-24 | President And Fellows Of Harvard College | Methods of making gels and films using curli nanofibers |
-
2016
- 2016-04-06 EP EP16777174.0A patent/EP3280397A4/en active Pending
- 2016-04-06 WO PCT/US2016/026161 patent/WO2016164422A2/en active Application Filing
- 2016-04-06 US US15/564,619 patent/US20180258435A1/en not_active Abandoned
- 2016-04-06 JP JP2017552146A patent/JP6916524B2/ja active Active
-
2020
- 2020-02-10 US US16/785,874 patent/US11286491B2/en active Active
-
2021
- 2021-02-26 JP JP2021030187A patent/JP7156726B2/ja active Active
Also Published As
| Publication number | Publication date |
|---|---|
| US11286491B2 (en) | 2022-03-29 |
| JP2021097687A (ja) | 2021-07-01 |
| US20180258435A1 (en) | 2018-09-13 |
| JP7156726B2 (ja) | 2022-10-19 |
| US20200248190A1 (en) | 2020-08-06 |
| WO2016164422A2 (en) | 2016-10-13 |
| JP2018517398A (ja) | 2018-07-05 |
| WO2016164422A3 (en) | 2017-02-09 |
| EP3280397A2 (en) | 2018-02-14 |
| EP3280397A4 (en) | 2018-08-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6916524B2 (ja) | 機能的タンパク質配列をディスプレイする生合成アミロイドに基づく材料 | |
| US11352397B2 (en) | Genetic reprogramming of bacterial biofilms | |
| Marchesini et al. | In search of Brucella abortus type IV secretion substrates: screening and identification of four proteins translocated into host cells through VirB system | |
| Wanniarachchi et al. | Human defensin 5 disulfide array mutants: disulfide bond deletion attenuates antibacterial activity against Staphylococcus aureus | |
| Meyrand et al. | Surface proteome analysis of a natural isolate of Lactococcus lactis reveals the presence of pili able to bind human intestinal epithelial cells | |
| Gasser et al. | Catechol siderophores repress the pyochelin pathway and activate the enterobactin pathway in P seudomonas aeruginosa: an opportunity for siderophore–antibiotic conjugates development | |
| Waters et al. | An amino‐terminal domain of Enterococcus faecalis aggregation substance is required for aggregation, bacterial internalization by epithelial cells and binding to lipoteichoic acid | |
| Pandey et al. | Co-regulation of iron metabolism and virulence associated functions by iron and XibR, a novel iron binding transcription factor, in the plant pathogen Xanthomonas | |
| US20160326220A1 (en) | Secretion and functional display of chimeric polypeptides | |
| Wang et al. | A type VI secretion system delivers a cell wall amidase to target bacterial competitors | |
| EP3262061B1 (en) | Peptides for facilitating secretion and uses thereof | |
| Wang et al. | Rapid and efficient production of cecropin A antibacterial peptide in Escherichia coli by fusion with a self-aggregating protein | |
| Wang et al. | A novel secretion and online-cleavage strategy for production of cecropin A in Escherichia coli | |
| Bergé et al. | Structural insights into Helicobacter pylori Cag protein interactions with host cell factors | |
| Gelfat et al. | Single domain antibodies against enteric pathogen virulence factors are active as curli fiber fusions on probiotic E. coli Nissle 1917 | |
| CN107936092A (zh) | 结合有工业意义的小分子的肽结构域 | |
| Qian et al. | Chemotaxis and shorter o-antigen chain length contribute to the strong desiccation tolerance of a food-isolated Cronobacter sakazakii strain | |
| JP2024508694A (ja) | バクテリオファージリシン、そのキメラおよびその使用 | |
| Hockenberry et al. | Perturbing the acetylation status of the Type IV pilus retraction motor, PilT, reduces Neisseria gonorrhoeae viability | |
| Renn et al. | Disulfide bond-mediated passenger domain stalling as a structural probe of autotransporter outer membrane secretion in vivo | |
| US20180334483A1 (en) | Electrically conductive protein nanofibers and biofilms | |
| Amro et al. | TraC of the conjugative plasmid pKM101 is secreted as a monomer in outer membrane vesicles and stimulates conjugation | |
| Kunwar | REGULATORY NETWORKS IN BILE SALT AND FERRIC IRON INDUCED RESISTANCE OF ENTEROHEMORRHAGIC ESCHERICHIA COLI TO CATIONIC ANTIMICROBIAL PEPTIDES | |
| Oyama | Prospecting Rumen Bacteria for Novel Antimicrobials | |
| Kaunietis | Identification, heterologous biosynthesis and characterization of novel bacteriocins from thermophilic bacteria |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20171018 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190405 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20190405 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200127 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20200122 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20200413 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200727 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20201029 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210226 |
|
| C60 | Trial request (containing other claim documents, opposition documents) |
Free format text: JAPANESE INTERMEDIATE CODE: C60 Effective date: 20210226 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20210308 |
|
| C21 | Notice of transfer of a case for reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C21 Effective date: 20210309 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20210412 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210527 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20210615 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20210709 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6916524 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |