JP6901966B2 - アンチセンス抗菌化合物および方法 - Google Patents
アンチセンス抗菌化合物および方法 Download PDFInfo
- Publication number
- JP6901966B2 JP6901966B2 JP2017512874A JP2017512874A JP6901966B2 JP 6901966 B2 JP6901966 B2 JP 6901966B2 JP 2017512874 A JP2017512874 A JP 2017512874A JP 2017512874 A JP2017512874 A JP 2017512874A JP 6901966 B2 JP6901966 B2 JP 6901966B2
- Authority
- JP
- Japan
- Prior art keywords
- antisense
- seq
- formula
- cpp
- ppmo
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 0 *N(CC1)CCN1I Chemical compound *N(CC1)CCN1I 0.000 description 6
- CXJIACLILYFFSZ-UHFFFAOYSA-N CN(CCI)CO Chemical compound CN(CCI)CO CXJIACLILYFFSZ-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/64—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/64—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent
- A61K47/645—Polycationic or polyanionic oligopeptides, polypeptides or polyamino acids, e.g. polylysine, polyarginine, polyglutamic acid or peptide TAT
- A61K47/6455—Polycationic oligopeptides, polypeptides or polyamino acids, e.g. for complexing nucleic acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/11—Antisense
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/32—Chemical structure of the sugar
- C12N2310/323—Chemical structure of the sugar modified ring structure
- C12N2310/3233—Morpholino-type ring
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/35—Nature of the modification
- C12N2310/351—Conjugate
- C12N2310/3513—Protein; Peptide
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2320/00—Applications; Uses
- C12N2320/50—Methods for regulating/modulating their activity
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Description
この出願は、米国特許法§119(e)の下、2014年5月16日に出願された米国出願第61/994,750号、2014年12月31日に出願された米国出願第62/099,046号および2015年3月6日に出願された米国出願第62/129,746号(これらの各々は、それらの全体が参考として援用される)に対する優先権を主張する。
本出願に関連する配列表は紙のコピーの代わりにテキスト形式で提供し、参照により本明細書に組み込まれている。配列表を含有するテキストファイルの名称は、SATH−003_03WO_ST25.txtである。テキストファイルは約10KBであり、2015年5月15日に作製され、EFS−ウェブによって電子的に提出されている。
式中、各Nuは、一緒になって標的化配列を形成する核酸塩基であり、
Xは、9〜38の整数であり、
Tは、OHおよび式:
R7は、HおよびC1〜C6アルキルから選択され、
R8は、G、−C(O)−R9OH、アシル、トリチル、および4−メトキシトリチルから選択され、
R9は、式−(O−アルキル)y−のものであり、式中、yは、3〜10の整数であり、
y個のアルキル基のそれぞれは、C2〜C6アルキルから独立に選択され、
R1の各実例は、−N(R10)2R11であり、式中、各R10は、独立に、C1〜C6アルキルであり、
R11は、電子対およびHから選択され、
R2は、H、G、アシル、トリチル、4−メトキシトリチル、ベンゾイル、ステアロイル、および式:
R3は、電子対、H、およびC1〜C6アルキルから選択され、
Gは、細胞透過性ペプチド(「CPP」)、ならびに−C(O)(CH2)5NH−CPP、−C(O)(CH2)2NH−CPP、−C(O)(CH2)2NHC(O)(CH2)5NH−CPP、および−C(O)CH2NH−CPPから選択されるリンカー部分であるか、またはGは、式:
標的化配列は、病原性因子をコードする細菌mRNA標的配列と特異的にハイブリダイズする。
本発明の実施形態において、例えば以下の項目が提供される。
(項目1)
モルホリノサブユニット、および1つのサブユニットのモルホリノ窒素を隣接するサブユニットの5’環外炭素に接合するリン含有サブユニット間連結から構成され、かつ(a)約10〜40個のヌクレオチド塩基、および(b)病原性因子をコードする細菌mRNA標的配列と特異的にハイブリダイズするのに十分な長さおよび相補性の標的化配列を有し、細胞透過性ペプチド(CPP)にコンジュゲートしている、アンチセンスモルホリノオリゴマー。
(項目2)
前記アンチセンスモルホリノオリゴマーが、式(I):
のものまたは薬学的に許容されるその塩であり、
式中、各Nuは、一緒になって標的化配列を形成する核酸塩基であり、
Xは、9〜38の整数であり、
Tは、OHおよび式:
の部分から選択され、式中、各R 4 は、独立に、C 1 〜C 6 アルキルであり、R 5 は、電子対およびHから選択され、R 6 は、OH、−N(R 7 )CH 2 C(O)NH 2 、および式:
の部分から選択され、式中、
R 7 は、HおよびC 1 〜C 6 アルキルから選択され、
R 8 は、G、−C(O)−R 9 OH、アシル、トリチル、および4−メトキシトリチルから選択され、
R 9 は、式−(O−アルキル) y −のものであり、式中、yは、3〜10の整数であり、y個のアルキル基のそれぞれは、C 2 〜C 6 アルキルから独立に選択され、
R 1 の各実例は、−N(R 10 ) 2 R 11 であり、式中、各R 10 は、独立に、C 1 〜C 6 アルキルであり、
R 11 は、電子対およびHから選択され、
R 2 は、H、G、アシル、トリチル、4−メトキシトリチル、ベンゾイル、ステアロイル、および式:
の部分から選択され、式中、Lは、−C(O)(CH 2 ) 6 C(O)−および−C(O)(CH 2 ) 2 S 2 (CH 2 ) 2 C(O)−から選択され、各R 12 は、式−(CH 2 ) 2 OC(O)N(R 14 ) 2 のものであり、式中、各R 14 は、式−(CH 2 ) 6 NHC(=NH)NH 2 のものであり、
R 3 は、電子対、H、およびC 1 〜C 6 アルキルから選択され、
Gは、細胞透過性ペプチド(「CPP」)、ならびに−C(O)(CH 2 ) 5 NH−CPP、−C(O)(CH 2 ) 2 NH−CPP、−C(O)(CH 2 ) 2 NHC(O)(CH 2 ) 5 NH−CPP、および−C(O)CH 2 NH−CPPから選択されるリンカー部分であるか、またはGは、式:
のものであり、式中、前記CPPは、前記CPPのカルボキシ末端においてアミド結合によって前記リンカー部分に付着しており、ただし、Gの1つのみの実例が存在し、
前記標的化配列が、病原性因子をコードする細菌mRNA標的配列と特異的にハイブリダイズする、項目1に記載のアンチセンスモルホリノオリゴマー。
(項目3)
前記標的配列が、前記細菌mRNAの翻訳開始コドンおよび/または前記細菌mRNAの前記翻訳開始コドンの上流または下流の約30塩基内の配列を含む、項目2に記載のアンチセンスモルホリノオリゴマー。
(項目4)
前記病原性因子が、ニューデリーメタロ−ベータ−ラクタマーゼ(NDM−1)および耐性−小結節形成−細胞分裂(RND)型多剤排出ポンプサブユニットAdeA(adeA)の少なくとも1つから選択される抗生物質耐性タンパク質であるか、または前記病原性因子が、バイオフィルム形成タンパク質である、項目2または3に記載のアンチセンスモルホリノオリゴマー。
(項目5)
前記標的配列が、配列番号1〜4から選択され、ここでチミン塩基(T)が任意選択で、ウラシル塩基(U)である、項目4に記載のアンチセンスモルホリノオリゴマー。
(項目6)
前記標的化配列が、配列番号11〜15に記載されているか、配列番号11〜15の少なくとも10の連続するヌクレオチドのフラグメントを含むか、または配列番号11〜15と少なくとも80%の配列同一性を有する変異体を含み、ここでチミン塩基(T)が、任意選択でウラシル塩基(U)である、項目4に記載のアンチセンスモルホリノオリゴマー。
(項目7)
前記バイオフィルム形成タンパク質が、CepIまたはSuhBの少なくとも1つによってコードされる、項目4に記載のアンチセンスモルホリノオリゴマー。
(項目8)
前記標的配列が、配列番号5〜9から選択され、ここでチミン塩基(T)が任意選択で、ウラシル塩基(U)である、項目7に記載のアンチセンスモルホリノオリゴマー。
(項目9)
前記標的化配列が、配列番号16〜24に記載されているか、配列番号16〜24の少なくとも10の連続するヌクレオチドのフラグメントを含むか、または配列番号16〜24と少なくとも80%の配列同一性を有する変異体を含み、ここでチミン塩基(T)が任意選択で、ウラシル塩基(U)である、項目7に記載のアンチセンスモルホリノオリゴマー。
(項目10)
前記病原性因子が、脂肪酸生合成と関連するタンパク質である、項目2または3に記載のアンチセンスモルホリノオリゴマー。
(項目11)
脂肪酸生合成と関連する前記タンパク質が、アシルキャリアータンパク質である、項目10に記載のアンチセンスモルホリノオリゴマー。
(項目12)
前記アシルキャリアータンパク質が、AcpPである、項目11に記載のアンチセンスモルホリノオリゴマー。
(項目13)
前記標的配列が、配列番号10であり、ここでチミン塩基(T)が任意選択で、ウラシル塩基(U)である、項目12に記載のアンチセンスモルホリノオリゴマー。
(項目14)
前記標的化配列が配列番号25〜37に記載されているか、配列番号25〜37の少なくとも10の連続するヌクレオチドのフラグメントを含むか、または配列番号25〜37と少なくとも80%の配列同一性を有する変異体を含み、ここでチミン塩基(T)が任意選択で、ウラシル塩基(U)である、項目12に記載のアンチセンスモルホリノオリゴマー。
(項目15)
Tが、
から選択される、項目1に記載のアンチセンスモルホリノオリゴマー。
(項目16)
R 2 が、H、G、アシル、トリチル、4−メトキシトリチル、ベンゾイル、およびステアロイルから選択される、項目1または15に記載のアンチセンスモルホリノオリゴマー。
(項目17)
Tが、
から選択され、そして
R 2 が、Gである、項目1に記載のアンチセンスモルホリノオリゴマー。
(項目18)
Tが、式:
のものであり、R 6 が、式:
のものであり、そしてR 2 が、Gである、項目1に記載のアンチセンスモルホリノオリゴマー。
(項目19)
Tが、式:
のものであり、そしてR 2 が、Gである、項目1に記載のアンチセンスモルホリノオリゴマー。
(項目20)
Tが、式:
のものである、項目1に記載のアンチセンスモルホリノオリゴマー。
(項目21)
R 2 が、H、アシル、トリチル、4−メトキシトリチル、ベンゾイル、およびステアロイルから選択される、項目1または20に記載のアンチセンスモルホリノオリゴマー。
(項目22)
R 1 の少なくとも1つの実例が、−N(CH 3 ) 2 である、項目1または15から21のいずれか一項に記載のアンチセンスモルホリノオリゴマー。
(項目23)
各R 1 が、−N(CH 3 ) 2 である、項目22に記載のアンチセンスモルホリノオリゴマー。
(項目24)
前記CPPが、
から選択され、式中、R a は、H、アセチル、ベンゾイル、およびステアロイルから選択される、項目1および15から23のいずれか一項に記載のアンチセンスモルホリノオリゴマー。
(項目25)
Gが、
から選択され、式中、R a は、H、アセチル、ベンゾイル、およびステアロイルから選択される、項目1または15から23のいずれか一項に記載のアンチセンスモルホリノオリゴマー。
(項目26)
前記アンチセンスオリゴマーが、
から選択される式(VII)のもの、または上記のいずれかの薬学的に許容される塩であり、
式中、R a は、H、アセチル、ベンゾイル、およびステアロイルから選択され、R b は、H、アセチル、ベンゾイル、ステアロイル、トリチル、および4−メトキシトリチルから選択され、そしてXおよびNuは、項目1で定義された通りである、項目1に記載のアンチセンスモルホリノオリゴマー。
(項目27)
R a が、アセチルであり、そしてR b が、Hである、項目26に記載のアンチセンスモルホリノオリゴマー。
(項目28)
前記標的化配列が、
a)配列番号11(TCA AGT TTT CC);
b)配列番号12(TCC TTT TAT TC);
c)配列番号13(CCA TCA AGT TT);
d)配列番号14(GGC AAT TCC AT);
e)配列番号15(ATA CTG TCC AA);
から選択され、ここでXが、9であり、チミン塩基(T)が、ウラシル塩基(U)であり得る、項目15から27のいずれか一項に記載のアンチセンスモルホリノオリゴマー。
(項目29)
前記標的化配列が、
a)配列番号16(AAG GTC TGC AT);
b)配列番号17(TCG GAT CTG TG);
c)配列番号18(CAT GGA TGT CC);
d)配列番号19(CGT GAA CGA AG);
e)配列番号20(CGT GTG GCA AC);
f)配列番号21(GCC CGA GAT CC);
g)配列番号22(CTT TCG TTC GC);
h)配列番号23(ATG CAT GAG CC);および
i)配列番号24(GGA TGC ATG AG)、
から選択され、ここでXが、9であり、チミン塩基(T)が、ウラシル塩基(U)であり得る、項目15から27のいずれか一項に記載のアンチセンスモルホリノオリゴマー。
(項目30)
前記標的化配列が、
a)配列番号25(GTCCATTACCC);
b)配列番号26(CATTACCCCTC);
c)配列番号27(CCATTACCCCT);
d)配列番号28(TCCATTACCCC);
e)配列番号29(TGTCCATTACC);
f)配列番号30(TTGTCCATTAC);
g)配列番号31(GTTGTCCATTA);
h)配列番号32(TGTTGTCCATT);
i)配列番号33(ATGTTGTCCAT);
j)配列番号34(TTTACAAGTGC);
k)配列番号35(CCTCCGAGGGA);
l)配列番号36(ACACGTTGTTC);および
m)配列番号37(AGTTCAGCGAC)、
から選択され、ここでxが、9であり、チミン塩基(T)が、ウラシル塩基(U)であり得る、項目15から27のいずれか一項に記載のアンチセンスモルホリノオリゴマー。
(項目31)
薬学的に許容される担体およびアンチセンスモルホリノオリゴマーを含む医薬組成物であって、前記アンチセンスモルホリノオリゴマーが、モルホリノサブユニット、および1つのサブユニットのモルホリノ窒素を隣接するサブユニットの5’環外炭素に接合するリン含有サブユニット間連結から構成され、かつ(a)約10〜40個のヌクレオチド塩基、および(b)病原性因子をコードする細菌mRNA標的配列と特異的にハイブリダイズするのに十分な長さおよび相補性の標的化配列を有し、前記オリゴマーが、細胞透過性ペプチド(CPP)にコンジュゲートしている、医薬組成物。
(項目32)
前記アンチセンスモルホリノオリゴマーが、式(I):
のものまたは薬学的に許容されるその塩であり、
式中、各Nuは、一緒になって標的化配列を形成する核酸塩基であり、
Xは、9〜38の整数であり、
Tは、OHおよび式:
の部分から選択され、式中、各R 4 は、独立に、C 1 〜C 6 アルキルであり、R 5 は、電子対およびHから選択され、R 6 は、OH、−N(R 7 )CH 2 C(O)NH 2 、および式:
の部分から選択され、式中、
R 7 は、HおよびC 1 〜C 6 アルキルから選択され、
R 8 は、G、−C(O)−R 9 OH、アシル、トリチル、および4−メトキシトリチルから選択され、
R 9 は、式−(O−アルキル) y −のものであり、式中、yは、3〜10の整数であり、y個のアルキル基のそれぞれは、C 2 〜C 6 アルキルから独立に選択され、
R 1 の各実例は、−N(R 10 ) 2 R 11 であり、式中、各R 10 は、独立に、C 1 〜C 6 アルキルであり、
R 11 は、電子対およびHから選択され、
R 2 は、H、G、アシル、トリチル、4−メトキシトリチル、ベンゾイル、ステアロイル、および式:
の部分から選択され、式中、Lは、−C(O)(CH 2 ) 6 C(O)−および−C(O)(CH 2 ) 2 S 2 (CH 2 ) 2 C(O)−から選択され、各R 12 は、式−(CH 2 ) 2 OC(O)N(R 14 ) 2 のものであり、式中、各R 14 は、式−(CH 2 ) 6 NHC(=NH)NH 2 のものであり、
R 3 は、電子対、H、およびC 1 〜C 6 アルキルから選択され、
Gは、細胞透過性ペプチド(「CPP」)、ならびに−C(O)(CH 2 ) 5 NH−CPP、−C(O)(CH 2 ) 2 NH−CPP、−C(O)(CH 2 ) 2 NHC(O)(CH 2 ) 5 NH−CPP、および−C(O)CH 2 NH−CPPから選択されるリンカー部分であるか、またはGは、式:
のものであり、式中、前記CPPは、前記CPPのカルボキシ末端においてアミド結合によって前記リンカー部分に付着しており、ただし、Gの1つのみの実例が存在し、
前記標的化配列が、病原性因子をコードする細菌mRNA標的配列と特異的にハイブリダイズする、項目31に記載の医薬組成物。
(項目33)
前記標的配列が、前記細菌mRNAの翻訳開始コドンおよび/または前記細菌mRNAの前記翻訳開始コドンの上流もしくは下流の約30塩基内の配列を含む、項目32に記載の医薬組成物。
(項目34)
前記標的化配列が、配列番号11〜15に記載されているか、配列番号11〜15の少なくとも10の連続するヌクレオチドのフラグメントを含むか、または配列番号11〜15と少なくとも80%の配列同一性を有する変異体を含み、ここでチミン塩基(T)が任意選択で、ウラシル塩基(U)である、項目32に記載の医薬組成物。
(項目35)
前記標的化配列が、配列番号16〜24に記載されているか、配列番号16〜24の少なくとも10の連続するヌクレオチドのフラグメントを含むか、または配列番号16〜24と少なくとも80%の配列同一性を有する変異体を含み、ここでチミン塩基(T)が任意選択で、ウラシル塩基(U)である、項目32に記載の医薬組成物。
(項目36)
前記標的化配列が、配列番号25〜37に記載されているか、配列番号25〜37の少なくとも10の連続するヌクレオチドのフラグメントを含むか、または配列番号25〜37と少なくとも80%の配列同一性を有する変異体を含み、ここでチミン塩基(T)が任意選択で、ウラシル塩基(U)である、項目32に記載の医薬組成物。
(項目37)
細菌中の病原性因子の発現および活性を低減させる方法であって、前記方法は、前記細菌とアンチセンスモルホリノオリゴマーとを接触させるステップを含み、前記アンチセンスモルホリノオリゴマーは、モルホリノサブユニット、および1つのサブユニットのモルホリノ窒素を隣接するサブユニットの5’環外炭素に接合するリン含有サブユニット間連結から構成され、かつ(a)約10〜40個のヌクレオチド塩基、および(b)病原性因子をコードする細菌mRNA標的配列と特異的にハイブリダイズするのに十分な長さおよび相補性の標的化配列を有し、前記オリゴマーは、細胞透過性ペプチド(CPP)にコンジュゲートしている、方法。
(項目38)
前記アンチセンスモルホリノオリゴマーが、式(I):
のものまたは薬学的に許容されるその塩であり、
式中、各Nuは、一緒になって標的化配列を形成する核酸塩基であり、
Xは、9〜38の整数であり、
Tは、OHおよび式:
の部分から選択され、式中、各R 4 は、独立に、C 1 〜C 6 アルキルであり、R 5 は、電子対およびHから選択され、R 6 は、OH、−N(R 7 )CH 2 C(O)NH 2 、および式:
の部分から選択され、式中、
R 7 は、HおよびC 1 〜C 6 アルキルから選択され、
R 8 は、G、−C(O)−R 9 OH、アシル、トリチル、および4−メトキシトリチルから選択され、
R 9 は、式−(O−アルキル) y −のものであり、式中、yは、3〜10の整数であり、y個のアルキル基のそれぞれは、C 2 〜C 6 アルキルから独立に選択され、
R 1 の各実例は、−N(R 10 ) 2 R 11 であり、式中、各R 10 は、独立に、C 1 〜C 6 アルキルであり、
R 11 は、電子対およびHから選択され、
R 2 は、H、G、アシル、トリチル、4−メトキシトリチル、ベンゾイル、ステアロイル、および式:
の部分から選択され、式中、Lは、−C(O)(CH 2 ) 6 C(O)−および−C(O)(CH 2 ) 2 S 2 (CH 2 ) 2 C(O)−から選択され、各R 12 は、式−(CH 2 ) 2 OC(O)N(R 14 ) 2 のものであり、式中、各R 14 は、式−(CH 2 ) 6 NHC(=NH)NH 2 のものであり、
R 3 は、電子対、H、およびC 1 〜C 6 アルキルから選択され、
Gは、細胞透過性ペプチド(「CPP」)、ならびに−C(O)(CH 2 ) 5 NH−CPP、−C(O)(CH 2 ) 2 NH−CPP、−C(O)(CH 2 ) 2 NHC(O)(CH 2 ) 5 NH−CPP、および−C(O)CH 2 NH−CPPから選択されるリンカー部分であるか、またはGは、式:
のものであり、式中、前記CPPは、前記CPPのカルボキシ末端においてアミド結合によって前記リンカー部分に付着しており、ただし、Gの1つのみの実例が存在し、
前記標的化配列が、前記病原性因子をコードする細菌mRNA標的配列と特異的にハイブリダイズする、項目37に記載の方法。
(項目39)
前記細菌が、被験体中にあり、前記方法が、前記アンチセンスモルホリノオリゴマーを前記被験体に投与するステップを含む、項目37に記載の方法。
(項目40)
前記細菌が、Escherichia、Acinetobacter、Klebsiella、およびBurkholderiaの属から選択される、項目37または39に記載の方法。
(項目41)
前記細菌が、Escherichia coli、Acinetobacter baumannii、Klebsiella pneumoniae、またはBurkholderia cepacia(種群)である、項目40に記載の方法。
(項目42)
前記細菌が、Escherichia coli、Acinetobacter baumannii、またはKlebsiella pneumoniaeであり、前記病原性因子が、NDM−1およびadeAの1つまたは複数から選択される抗生物質耐性タンパク質である、項目37に記載の方法。
(項目43)
前記細菌が、Burkholderia cepacia(種群)であり、前記病原性因子が、cepIおよびsuhBの1つまたは複数によってコードされるバイオフィルム形成タンパク質である、項目37に記載の方法。
(項目44)
前記細菌が、Burkholderia cepacia(種群)であり、前記病原性因子が、acpPによってコードされるアシルキャリアータンパク質である、項目37に記載の方法。
他に定義しない限り、本明細書において使用するすべての技術用語および科学用語は、本開示が属する技術分野における当業者が一般に理解するのと同じ意味を有する。本明細書に記載されているものと同様または同等な任意の方法および材料を本開示の実施または試験において使用することができるが、好ましい方法および材料を記載する。本開示の目的のために、下記の用語を下で定義する。
ある特定の実施形態は、病原性因子をコードする細菌mRNA標的配列と特異的にハイブリダイズするのに十分な長さおよび相補性のものである、アンチセンスオリゴマー、ならびに関連する組成物および方法に関する。病原性因子の一般例は、抗生物質耐性遺伝子、バイオフィルム形成遺伝子、脂肪酸生合成と関連する遺伝子、およびこれらのコードされたタンパク質を含む。さらに、病原性因子は、感染のプロセスの間に細菌に利益を提供する他の遺伝子の発現(転写および/または翻訳)を制御する調節タンパク質をコードする遺伝子を含む。
アンチセンスオリゴマーは典型的には、病原性因子をコードする細菌mRNA標的配列と特異的にハイブリダイズし、それによって病原性因子タンパク質の発現(例えば、翻訳)を低減させるのに十分な長さおよび相補性の塩基配列を含む。オリゴマー化合物が細菌細胞によって能動的に取り込まれる能力を有し、一度取り込まれると、任意選択で約40℃超または45℃超のTmを有する、標的mRNAと安定的な二重鎖(またはヘテロ二重鎖)を形成するとき、この必要条件を任意選択で満たす。
ある特定の実施形態では、アンチセンスオリゴマーの骨格は実質的に非荷電であり、任意選択で細胞壁および/または細胞膜を横断する能動または促進輸送のための基質として認識される。標的RNAと安定的な二重鎖を形成するオリゴマーの能力はまた、標的に関するアンチセンスオリゴマーの長さおよび相補性の程度、G:CとA:T塩基マッチとの比、および任意のミスマッチした塩基の位置を含めた、骨格の他の特色に関し得る。アンチセンスオリゴマーが細胞ヌクレアーゼに耐える能力は、生存、および細胞への薬剤の最終送達を促進し得る。例示的なアンチセンスオリゴマー標的化配列を、表2(上述)において列挙する。
式中、各Nuは、一緒になって標的化配列を形成する核酸塩基であり、
Xは、9〜38の整数であり、
Tは、OHおよび式:
R7は、HおよびC1〜C6アルキルから選択され、
R8は、G、−C(O)−R9OH、アシル、トリチル、および4−メトキシトリチルから選択され、
R9は、式−(O−アルキル)y−のものであり、式中、yは、3〜10の整数であり、
y個のアルキル基のそれぞれは、C2〜C6アルキルから独立に選択され、
R1の各実例は、−N(R10)2R11であり、式中、各R10は、独立に、C1〜C6アルキルであり、
R11は、電子対およびHから選択され、
R2は、H、G、アシル、トリチル、4−メトキシトリチル、ベンゾイル、ステアロイル、および式:
R3は、電子対、H、およびC1〜C6アルキルから選択され、
Gは、細胞透過性ペプチド(「CPP」)、ならびに−C(O)(CH2)5NH−CPP、−C(O)(CH2)2NH−CPP、−C(O)(CH2)2NHC(O)(CH2)5NH−CPP、および−C(O)CH2NH−CPPから選択されるリンカー部分であるか、またはGは、式:
標的化配列は、病原性因子をコードする細菌mRNA標的配列と特異的にハイブリダイズする。
式中、各Nuは、一緒になって標的化配列を形成する核酸塩基であり、
Xは、9〜28の整数であり、
Tは、
R2は、H、G、アシル、トリチル、4−メトキシトリチル、ベンゾイル、およびステアロイルから選択され、
R3は、電子対、H、およびC1〜C6アルキルから選択され、
Gは、細胞透過性ペプチド(「CPP」)、ならびに−C(O)(CH2)5NH−CPP、−C(O)(CH2)2NH−CPP、−C(O)(CH2)2NHC(O)(CH2)5NH−CPP、および−C(O)CH2NH−CPPから選択されるリンカー部分であるか、またはGは、式:
式中、各Nuは、一緒になって標的化配列を形成する核酸塩基であり、
Xは、9〜28の整数であり、
Tは、
R1の各実例は、−N(R10)2R11であり、式中、各R10は、独立に、C1〜C6アルキルであり、R11は、電子対およびHから選択され、
R2は、電子対、H、およびC1〜C6アルキルから選択され、
Gは、細胞透過性ペプチド(「CPP」)、ならびに−C(O)(CH2)5NH−CPP、−C(O)(CH2)2NH−CPP、−C(O)(CH2)2NHC(O)(CH2)5NH−CPP、および−C(O)CH2NH−CPPから選択されるリンカー部分であるか、またはGは、式:
Xは、9〜28の整数であり、
各Nuは、一緒になって標的化配列を形成する核酸塩基であり、
R1の各実例は、−N(R10)2R11であり、式中、各R10は、独立に、C1〜C6アルキルであり、R11は、電子対およびHから選択され、
Gは、細胞透過性ペプチド(「CPP」)、ならびに−C(O)(CH2)5NH−CPP、−C(O)(CH2)2NH−CPP、−C(O)(CH2)2NHC(O)(CH2)5NH−CPP、および−C(O)CH2NH−CPPから選択されるリンカー部分であるか、またはGは、式:
Xは、9〜18の整数であり、
各Nuは、一緒になって標的化配列を形成する核酸塩基であり、
R1の各実例は、−N(R10)2R11であり、式中、各R10は、独立に、C1〜C6アルキルであり、R11は、電子対およびHから選択され、
R2は、H、トリチル、4−メトキシトリチル、アシル、ベンゾイル、およびステアロイルから選択され、
R3は、電子対、H、およびC1〜C6アルキルから選択され、
Gは、細胞透過性ペプチド(「CPP」)、ならびに−C(O)(CH2)5NH−CPP、−C(O)(CH2)2NH−CPP、−C(O)(CH2)2NHC(O)(CH2)5NH−CPP、および−C(O)CH2NH−CPPから選択されるリンカー部分であるか、またはGは、式:
Xは、9〜28の整数であり、
各Nuは、一緒になって標的化配列を形成する核酸塩基であり、
R2は、Hまたはアシルから選択され、
Gは、細胞透過性ペプチド(「CPP」)、ならびに−C(O)(CH2)5NH−CPP、−C(O)(CH2)2NH−CPP、−C(O)(CH2)2NHC(O)(CH2)5NH−CPP、および−C(O)CH2NH−CPPから選択されるリンカー部分であるか、またはGは、式:
ある特定の実施形態では、アンチセンスオリゴマーは、細胞透過性ペプチド(CPP)にコンジュゲートしている。一部の実施形態では、CPPは、アルギニンに富んだペプチドである。「アルギニンに富んだ担体ペプチド」は、CPPが少なくとも2個、好ましくは、2、3、4、5、6、7、または8個のアルギニン残基を有し、それぞれは1個または複数の非荷電の疎水性残基によって任意選択で分離しており、約6〜14個のアミノ酸残基を任意選択で含有することを意味する。図1F〜1Hは、5’および3’PMOコンジュゲートを含めた実施例において使用されるCPP−PMOコンジュゲートの例示的な化学構造を示す。
様々な態様では、本開示のアンチセンスオリゴマー、または薬学的に許容されるその塩は、
式(I)〜(VII)のアンチセンスオリゴマー化合物を含めた本開示のアンチセンスオリゴマーの様々な実施形態では、標的化配列は、病原性因子をコードする細菌mRNA標的配列と特異的にハイブリダイズすることができる。一部の実施形態では、標的配列は、細菌mRNAの翻訳開始コドンおよび/または細菌mRNAの翻訳開始コドンの上流もしくは下流の約30塩基内の配列を含む。ある特定の実施形態では、病原性因子は、抗生物質耐性タンパク質またはバイオフィルム形成タンパク質であってよい。一部の実施形態では、抗生物質耐性タンパク質は、ニューデリーメタロ−ベータ−ラクタマーゼ(NDM−1)および耐性−小結節形成−細胞分裂(RND)型多剤排出ポンプサブユニットAdeA(adeA)の少なくとも1つから選択され得る。一部の実施形態では、標的配列は、配列番号1〜4から選択することができ、チミン塩基(T)は任意選択で、ウラシル塩基(U)である。ある特定の実施形態では、標的化配列は、配列番号11〜15に記載されている標的化配列の1つであってよいか、配列番号11〜15の少なくとも10の連続するヌクレオチドのフラグメントを含んでもよいか、または配列番号11〜15と少なくとも80%の配列同一性を有する変異体を含んでもよく、チミン塩基(T)は任意選択で、ウラシル塩基(U)である。一部の実施形態では、バイオフィルム形成タンパク質は、CepIまたはSuhBの少なくとも1つによってコードされ得る。ある特定の実施形態では、標的配列は、配列番号5〜9から選択することができ、チミン塩基(T)は任意選択で、ウラシル塩基(U)である。一部の実施形態では、標的化配列は、配列番号16〜24に記載されている標的化配列の1つであってよいか、配列番号16〜24の少なくとも10の連続するヌクレオチドのフラグメントを含んでもよいか、または配列番号16〜24と少なくとも80%の配列同一性を有する変異体を含んでもよく、チミン塩基(T)は任意選択で、ウラシル塩基(U)である。様々な実施形態では、病原性因子は、acpPの1つまたは複数によってコードされる、脂肪酸生合成と関連するアシルキャリアータンパク質である。ある特定の実施形態では、アシルキャリアータンパク質は、AcpPであり得る。一部の実施形態では、標的配列は、配列番号10であってよく、チミン塩基(T)は任意選択で、ウラシル塩基(U)である。ある特定の実施形態では、標的化配列は、配列番号25〜37に記載されている標的化配列の1つであってよいか、配列番号25〜37の少なくとも10の連続するヌクレオチドのフラグメントを含んでもよいか、または配列番号25〜37と少なくとも80%の配列同一性を有する変異体を含んでもよく、チミン塩基(T)は任意選択で、ウラシル塩基(U)である。式(I)〜(VII)のアンチセンスオリゴマー化合物を含めた本開示の一部の実施形態において、標的化配列は、
本開示の実施形態は、1種または複数の細菌病原性因子の発現および活性を低減させる本明細書に記載されているアンチセンスオリゴマーを使用する方法を含む。ある特定の実施形態は、アンチセンスオリゴマーを使用して、細菌の複製、増殖、病原性因子、または成長を低減させ、例えば、単独で、または1種もしくは複数のさらなる抗微生物剤と組み合わせて、被験体において細菌感染を処置する方法を含む。一部の場合において、アンチセンスオリゴマーは、抗生物質に対する細菌の感受性を増加させる。ある特定の実施形態は、本明細書に記載されているアンチセンスオリゴマーを使用して、細菌バイオフィルムの形成または存在を低減させ、例えば、単独で、または1種もしくは複数のさらなる抗微生物剤と組み合わせて、被験体において細菌感染を処置する方法を含む。
ある特定の実施形態は、併用療法、例えば、抗微生物剤、例えば、抗生物質と組み合わせたアンチセンスオリゴマーの投与を含む。併用療法を用いて、例えば、1種または複数の抗微生物剤に対する所与の細菌の感度または感受性を増加させ、それによって治療成績(例えば、感染症の消散)を改善させることができる。同様に、ある特定の併用療法を用いて、例えば、1種または複数の抗微生物剤に対する所与の細菌の抗生物質耐性を低減または逆転させることができる。特定の実施形態では、アンチセンスオリゴマーは、細菌に対する抗生物質の最小発育阻止濃度(MIC)を低減させる。また含まれるのは、アンチセンスオリゴマーおよび抗微生物剤、例えば、抗生物質を含む本明細書に記載のような医薬組成物である。
本明細書に記載の方法が関与する所与の治療レジメンの有効性は、例えば、細菌感染の一般指標、例えば、全血球計算(CBC)、核酸検出方法、免疫診断試験、または細菌培養によってモニターされ得る。
adeAに対して標的化されるPPMOの活性
耐性−小結節形成−細胞分裂(RND)型多剤排出ポンプサブユニットadeA(adeA)に対して標的化される、細胞透過性ペプチドにコンジュゲートしたホスホロジアミデートモルホリノオリゴマー(PPMO)を調製し、adeAを発現しているAcinetobacter baumaniiに対する様々な抗生物質の最小発育阻止濃度(MIC)を低減させる能力について試験した。
NDM−1に対して標的化されるPPMOの活性
ニューデリーメタロ−ベータ−ラクタマーゼ(NDM−1)に対して標的化される、ペプチドにコンジュゲートしたホスホロジアミデートモルホリノオリゴマー(PPMO)を調製し、NDM−1を発現しているAcinetobacter baumaniiおよびE.coliに対するメロペネムの最小発育阻止濃度(MIC)を低減させる能力について試験した。
バイオフィルムおよびアシルキャリアータンパク質遺伝子に対して標的化されるPPMOの活性
バイオフィルム形成遺伝子suhBおよびcepIならびにアシルキャリアータンパク質acpP遺伝子に対して標的化される、ペプチドにコンジュゲートしたホスホロジアミデートモルホリノオリゴマー(PPMO)を調製し、バイオフィルム形成を低減させ、Burkholderia cenocepacia J2315において確立したバイオフィルムを崩壊させる能力について試験した。
PPMOは抗生物質と相乗的に作用し、確立したバイオフィルムにおける細菌成長を低減させる
バイオフィルム形成遺伝子cepIに対して標的化されるPPMOを調製し、Burkholderia cenocepacia J2315においてアミノグリコシド系抗生物質であるトブラマイシンと組み合わせて、確立したバイオフィルムにおける細菌成長を低減させる能力について試験した。
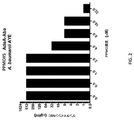
PPMOはBccのメンバーを阻害する
様々な体の部位から得た様々なレベルの抗生物質耐性を有する臨床分離株を含めた種々のBcc分離株を試験した。株バンクは、ヒト疾患をもたらすことが報告されている最も頻繁に遭遇する種を含む39の分離株を含んだ。図10に示すように、6つのPPMO(PPMO#19〜23および25)は、8μMまたはそれ未満のIC75値を達成した。これらのPPMOの6つすべては、AcpP(脂肪酸生合成と関連するアシルキャリアータンパク質)を標的化した。6つのPPMOにおける差異は、標的mRNA上の代替的な位置付け部位と関連した。最も強力なPPMO(PPMO#19)は、4μMのIC75を有した。acpP PPMO標的化配列を、表3Cにおいて列挙する。
PPMOはBccにおいて殺菌性である
Bccの多くのメンバーは、内因的に抗生物質耐性であり、処置を困難なものとしている。B.cenocepaciaは、嚢胞性線維症(CF)患者が遭遇する最も一般の種の1つである。B.cenocepaciaの2つの異なる分離株を、異なるacpP PPMOの存在下または非存在下で24時間インキュベートした(図11)。
PPMOは痰におけるBcc成長を阻害する
CF患者における慢性感染は、通常肺において顕在化する。さらに、BccおよびP.aeruginosaのメンバーは、バイオフィルムを形成することが公知である。これらのバイオフィルムおよびCF患者によって形成された濃厚な痰は、抗生物質による処置を特に困難なものとし、これらの病原体は肺の環境から完全に根絶することは実質的に不可能なものとなる。
acpP PPMOは、バイオフィルム形成を防止し、現存するバイオフィルムを解体することの両方が可能である
バイオフィルムの形成は重要な病原性形質であり、P.aeruginosaおよびBccの両方によって利用される。Bccバイオフィルムを成長させて、バイオフィルム形成を防止し、現存するバイオフィルムを解体することの両方を行うことの能力について、PPMOを試験した。B.cenocepacia J2315(ゲノム配列決定した流行性CF分離株)を、再現性のあるバイオフィルムを日毎に成長させるペグを含有するMBECバイオフィルムアッセイプレートを利用して成長させた。J2315を、acpP PPMO(10μM)、スクランブルPPMO(10μM)、ペプチドまたは培地単独のいずれかの存在下で48時間成長させた(図13)。acpPを標的化するPPMO(PPMO#19)は、下記の配列:CCATTACCCCT(配列番号27)を有する。PPMOを、その5’末端において(RFF)3RXB(配列番号41)のベータ−アラニン残基にコンジュゲートさせた。バイオフィルム産生を、クリスタルバイオレット方法を利用して測定した。見られ得るように、acpP PPMOは、バイオフィルム形成を、対照と比較して>50%低減させた。次いで、acpP PPMOを試験して、これが現存するバイオフィルムを崩壊させることができたかどうかを調べた。バイオフィルムを48時間成長させ、次いで、成熟したバイオフィルムペグを、培地単独(図14A)、10μMでのスクランブル対照PPMO(図14B)または10μMでのacpP PPMO(図14C)を有する新鮮なプレートに移した。プレートをさらに48時間インキュベートし、バイオフィルム形成を、クリスタルバイオレットによって、および共焦点顕微鏡によっての両方で測定した。蛍光赤色を発現しているJ2315株によって測定されるように、acpP PPMOは、共焦点顕微鏡およびクリスタルバイオレット測定の両方によって存在するバイオフィルムの量を有意に低減させた(図14C)。現存するバイオフィルムを崩壊させるPPMO(必須の遺伝子標的に対して設計)の能力は、新規および決定的に重要な知見である。
PPMOのエアゾール送達は、肺感染モデルにおいてB.multivoransの負荷量を低減させる
慢性肺感染症の状況における肺への直接のPPMOの送達は有用である。慢性肉芽腫症(CGD)マウスを、Bcc感染モデルとして使用した。これらのマウスは、様々なBcc株に感染したとき、有意な罹患率と死亡率が生じる。マウスに、臨床B.multivorans分離株を鼻腔内で感染させた(図15)。Aerogenネブライザーを使用して、スクランブル(Scr)PPMO(300μg)またはacpP PPMO(PPMO#15、300μgもしくは30μg)のいずれかを感染の6時間後の1回の用量として送達した。acpPを標的化するPPMOは、下記の配列:GTCCATTACCC(配列番号25)を有する。PPMOを、その5’末端において(RFF)3RXB(配列番号41)のC末端β−アラニン残基にコンジュゲートさせた。感染の24時間後にマウスを安楽死させ、肺負荷量を決定した。単一の300μg用量のacpP PPMOは、肺負荷量を93%低減させ、これは統計的に有意な減少であった。PPMOのエアゾール送達は実行可能な治療戦略であり、重要なことに、これはBcc PPMOの噴霧送達が試みられた最初のものである。
Claims (14)
- モルホリノサブユニット、および1つのサブユニットのモルホリノ窒素を隣接するサブユニットの5’環外炭素に接合するリン含有サブユニット間連結から構成され、かつ(a)約10〜40個のヌクレオチド塩基、および(b)病原性因子をコードする細菌mRNA標的配列と特異的にハイブリダイズするのに十分な長さおよび相補性の標的化配列を有し、細胞透過性ペプチド(CPP)にコンジュゲートしている、アンチセンスモルホリノオリゴマーであって、
前記標的化配列が、
1) 配列番号11(TCA AGT TTT CC)
2) 配列番号12(TCC TTT TAT TC)
3) 配列番号13(CCA TCA AGT TT)
4) 配列番号14(GGC AAT TCC AT)、および
5) 配列番号27(CCATTACCCCT)
から選択され、ここでチミン塩基(T)はウラシル塩基(U)であり得る、
アンチセンスモルホリノオリゴマー。 - 前記アンチセンスモルホリノオリゴマーが、式(I):
式中、各Nuは、一緒になって標的化配列を形成する核酸塩基であり、
Xは、9〜38の整数であり、
Tは、OHおよび式:
R7は、HおよびC1〜C6アルキルから選択され、
R8は、G、−C(O)−R9OH、アシル、トリチル、および4−メトキシトリチルから選択され、
R9は、式−(O−アルキル)y−のものであり、式中、yは、3〜10の整数であり、
y個のアルキル基のそれぞれは、C2〜C6アルキルから独立に選択され、
R1の各々は、−N(R10)2R11であり、式中、各R10は、独立に、C1〜C6アルキルであり、
R11は、電子対およびHから選択され、
R2は、H、G、アシル、トリチル、4−メトキシトリチル、ベンゾイル、ステアロイル、および式:
R3は、電子対、H、およびC1〜C6アルキルから選択され、
Gは、細胞透過性ペプチド(「CPP」)、ならびに−C(O)(CH2)5NH−CPP、−C(O)(CH2)2NH−CPP、−C(O)(CH2)2NHC(O)(CH2)5NH−CPP、および−C(O)CH2NH−CPPから選択されるリンカー部分であるか、またはGは、式:
前記標的化配列が、前記病原性因子をコードする細菌mRNA標的配列と特異的にハイブリダイズする、請求項1に記載のアンチセンスモルホリノオリゴマー。 - R1の少なくとも1つが、−N(CH3)2である、請求項2から5のいずれか一項に記載のアンチセンスモルホリノオリゴマー。
- 各R1が、−N(CH3)2である、請求項6に記載のアンチセンスモルホリノオリゴマー。
- 前記標的化配列が、
a)配列番号11(TCA AGT TTT CC);
b)配列番号12(TCC TTT TAT TC);
c)配列番号13(CCA TCA AGT TT);および
d)配列番号14(GGC AAT TCC AT);
から選択され、ここでXが、9であり、チミン塩基(T)が、ウラシル塩基(U)であり得る、請求項2から10のいずれか一項に記載のアンチセンスモルホリノオリゴマー。 - 前記標的化配列が、配列番号27(CCATTACCCCT)であり、ここでxが、9であり、チミン塩基(T)が、ウラシル塩基(U)であり得る、請求項2から10のいずれか一項に記載のアンチセンスモルホリノオリゴマー。
- 薬学的に許容される担体およびアンチセンスモルホリノオリゴマーを含む医薬組成物であって、前記アンチセンスモルホリノオリゴマーが、請求項2で定義された通りである、医薬組成物。
- 細菌中の病原性因子の発現および活性を低減させるのに使用するための、請求項2で定義された通りのアンチセンスモルホリノオリゴマーを含む組成物。
Applications Claiming Priority (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201461994750P | 2014-05-16 | 2014-05-16 | |
| US61/994,750 | 2014-05-16 | ||
| US201462099046P | 2014-12-31 | 2014-12-31 | |
| US62/099,046 | 2014-12-31 | ||
| US201562129746P | 2015-03-06 | 2015-03-06 | |
| US62/129,746 | 2015-03-06 | ||
| PCT/US2015/031150 WO2015175977A2 (en) | 2014-05-16 | 2015-05-15 | Antisense antibacterial compounds and methods |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2017522044A JP2017522044A (ja) | 2017-08-10 |
| JP2017522044A5 JP2017522044A5 (ja) | 2018-06-28 |
| JP6901966B2 true JP6901966B2 (ja) | 2021-07-14 |
Family
ID=54480938
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017512874A Active JP6901966B2 (ja) | 2014-05-16 | 2015-05-15 | アンチセンス抗菌化合物および方法 |
Country Status (6)
| Country | Link |
|---|---|
| US (2) | US9790495B2 (ja) |
| EP (2) | EP3143141B1 (ja) |
| JP (1) | JP6901966B2 (ja) |
| AU (1) | AU2015258895A1 (ja) |
| CA (1) | CA2948373A1 (ja) |
| WO (1) | WO2015175977A2 (ja) |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3143141B1 (en) | 2014-05-16 | 2019-10-02 | Oregon State University | Antisense antibacterial compounds and methods |
| EP3569252B1 (en) | 2014-05-19 | 2021-12-15 | Oregon State University | Antisense antibacterial compounds and methods |
| AU2015372560B2 (en) | 2014-12-31 | 2021-12-02 | Board Of Regents, The University Of Texas System | Antisense antibacterial compounds and methods |
| US20180216111A1 (en) * | 2015-02-27 | 2018-08-02 | Sarepta Therapeutics, Inc. | Antisense-induced exon2 inclusion in acid alpha-glucosidase |
| WO2017112888A1 (en) * | 2015-12-23 | 2017-06-29 | David Greenberg | Antisense antibacterial compounds and methods |
| EP3394261A4 (en) * | 2015-12-23 | 2019-11-27 | Oregon State University | ANTISENSE ANTIBACTERIAL COMPOUNDS AND ASSOCIATED METHODS |
| WO2017184529A1 (en) | 2016-04-18 | 2017-10-26 | Sarepta Therapeutics, Inc. | Antisense oligomers and methods of using the same for treating diseases associated with the acid alpha-glucosidase gene |
| JP7042255B2 (ja) * | 2016-04-29 | 2022-03-25 | サレプタ セラピューティクス, インコーポレイテッド | ヒトlmnaを標的にするオリゴヌクレオチド類縁体 |
| WO2018161027A1 (en) * | 2017-03-03 | 2018-09-07 | Oregon State University | Antisense antibacterial compounds and methods |
| US10765760B2 (en) * | 2018-05-29 | 2020-09-08 | Sarepta Therapeutics, Inc. | Exon skipping oligomer conjugates for muscular dystrophy |
| TW202020153A (zh) * | 2018-07-27 | 2020-06-01 | 美商薩羅塔治療公司 | 用於肌肉萎縮症之外顯子跳躍寡聚物 |
| GB2579253A (en) | 2018-11-28 | 2020-06-17 | Pedanius Therapeutics Ltd | Antibacterial antisense agents |
Family Cites Families (42)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5185444A (en) | 1985-03-15 | 1993-02-09 | Anti-Gene Deveopment Group | Uncharged morpolino-based polymers having phosphorous containing chiral intersubunit linkages |
| US5217866A (en) | 1985-03-15 | 1993-06-08 | Anti-Gene Development Group | Polynucleotide assay reagent and method |
| US5034506A (en) | 1985-03-15 | 1991-07-23 | Anti-Gene Development Group | Uncharged morpholino-based polymers having achiral intersubunit linkages |
| EP0215942B1 (en) | 1985-03-15 | 1995-07-12 | Antivirals Inc. | Polynucleotide assay reagent and method |
| US5521063A (en) | 1985-03-15 | 1996-05-28 | Antivirals Inc. | Polynucleotide reagent containing chiral subunits and methods of use |
| US5506337A (en) | 1985-03-15 | 1996-04-09 | Antivirals Inc. | Morpholino-subunit combinatorial library and method |
| US5166315A (en) | 1989-12-20 | 1992-11-24 | Anti-Gene Development Group | Sequence-specific binding polymers for duplex nucleic acids |
| JPH07501204A (ja) | 1991-06-28 | 1995-02-09 | マサチューセッツ インスティテュート オブ テクノロジー | 局所的オリゴヌクレオチド療法 |
| JP4193917B2 (ja) | 1995-12-18 | 2008-12-10 | アンジオデバイス インターナショナル ゲーエムベーハー | 架橋ポリマー組成物およびその使用方法 |
| US6245747B1 (en) | 1996-03-12 | 2001-06-12 | The Board Of Regents Of The University Of Nebraska | Targeted site specific antisense oligodeoxynucleotide delivery method |
| US20060241075A1 (en) * | 2001-05-18 | 2006-10-26 | Sirna Therapeutics, Inc. | RNA interference mediated inhibition of desmoglein gene expression using short interfering nucleic acid (siNA) |
| US20040029129A1 (en) * | 2001-10-25 | 2004-02-12 | Liangsu Wang | Identification of essential genes in microorganisms |
| US6965025B2 (en) | 2001-12-10 | 2005-11-15 | Isis Pharmaceuticals, Inc. | Antisense modulation of connective tissue growth factor expression |
| EP1620112A4 (en) * | 2003-04-17 | 2007-04-25 | Univ Columbia | DESMOGLEIN 4 IS A NEW GENUS INVOLVED IN HAIR GROWTH |
| DK2351844T3 (da) | 2003-04-29 | 2014-09-22 | Sarepta Therapeutics Inc | Præparater til forøgelse af transport- og antisense-effektivitet af nukleinsyreanalog i celler |
| US20050288246A1 (en) * | 2004-05-24 | 2005-12-29 | Iversen Patrick L | Peptide conjugated, inosine-substituted antisense oligomer compound and method |
| PL1766012T3 (pl) | 2004-07-02 | 2011-11-30 | Avi Biopharma Inc | Antysensowne, przeciwbakteryjne związki i sposoby |
| US20060263798A1 (en) * | 2005-02-11 | 2006-11-23 | International Business Machines Corporation | System and method for identification of MicroRNA precursor sequences and corresponding mature MicroRNA sequences from genomic sequences |
| US8067571B2 (en) | 2005-07-13 | 2011-11-29 | Avi Biopharma, Inc. | Antibacterial antisense oligonucleotide and method |
| EP1915161B1 (en) | 2005-07-13 | 2017-04-26 | Sarepta Therapeutics, Inc. | Antisense antibacterial method and compound |
| US7790694B2 (en) | 2005-07-13 | 2010-09-07 | Avi Biopharma Inc. | Antisense antibacterial method and compound |
| US8143389B2 (en) * | 2005-08-25 | 2012-03-27 | Texas Tech University | Inhibiton of metallo-β-lactamase by double-stranded DNA |
| US20100016215A1 (en) | 2007-06-29 | 2010-01-21 | Avi Biopharma, Inc. | Compound and method for treating myotonic dystrophy |
| WO2009005793A2 (en) | 2007-06-29 | 2009-01-08 | Avi Biopharma, Inc. | Tissue specific peptide conjugates and methods |
| CA2704261C (en) | 2007-11-15 | 2015-05-26 | Avi Biopharma, Inc. | Method of synthesis of morpholino oligomers |
| US8076476B2 (en) | 2007-11-15 | 2011-12-13 | Avi Biopharma, Inc. | Synthesis of morpholino oligomers using doubly protected guanine morpholino subunits |
| US8299206B2 (en) | 2007-11-15 | 2012-10-30 | Avi Biopharma, Inc. | Method of synthesis of morpholino oligomers |
| US20110269665A1 (en) | 2009-06-26 | 2011-11-03 | Avi Biopharma, Inc. | Compound and method for treating myotonic dystrophy |
| WO2011018798A2 (en) | 2009-08-14 | 2011-02-17 | Indian Association For The Cultivation Of Science | Morpholino-based antisense agent |
| WO2012031243A2 (en) | 2010-09-03 | 2012-03-08 | Avi Biopharma, Inc. | dsRNA MOLECULES COMPRISING OLIGONUCLEOTIDE ANALOGS HAVING MODIFIED INTERSUBUNIT LINKAGES AND/OR TERMINAL GROUPS |
| ES2607603T3 (es) | 2010-09-30 | 2017-04-03 | Nippon Shinyaku Co., Ltd. | Derivado de ácido morfolino nucleico |
| EP3067420A1 (en) | 2010-11-12 | 2016-09-14 | Sarepta Therapeutics, Inc. | Antisense antibacterial compounds and methods |
| US20120213663A1 (en) * | 2011-02-23 | 2012-08-23 | King Fahd University Of Petroleum And Minerals | Method of removing e. coli bacteria from an aqueous solution |
| US9161948B2 (en) | 2011-05-05 | 2015-10-20 | Sarepta Therapeutics, Inc. | Peptide oligonucleotide conjugates |
| WO2012150960A1 (en) | 2011-05-05 | 2012-11-08 | Avi Biopharma, Inc. | Peptide oligonucleotide conjugates |
| KR101317263B1 (ko) * | 2011-07-05 | 2013-10-10 | (주)지노첵 | 리얼타임 pcr을 이용한 카바페넴 내성 장내균 검사 방법 및 키트 |
| WO2013011072A1 (en) * | 2011-07-20 | 2013-01-24 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Carbapenemase and antibacterial treatment |
| EP3143141B1 (en) | 2014-05-16 | 2019-10-02 | Oregon State University | Antisense antibacterial compounds and methods |
| EP3569252B1 (en) | 2014-05-19 | 2021-12-15 | Oregon State University | Antisense antibacterial compounds and methods |
| AU2015372560B2 (en) | 2014-12-31 | 2021-12-02 | Board Of Regents, The University Of Texas System | Antisense antibacterial compounds and methods |
| EP3394261A4 (en) | 2015-12-23 | 2019-11-27 | Oregon State University | ANTISENSE ANTIBACTERIAL COMPOUNDS AND ASSOCIATED METHODS |
| WO2017112888A1 (en) | 2015-12-23 | 2017-06-29 | David Greenberg | Antisense antibacterial compounds and methods |
-
2015
- 2015-05-15 EP EP15792493.7A patent/EP3143141B1/en active Active
- 2015-05-15 US US14/713,857 patent/US9790495B2/en active Active
- 2015-05-15 CA CA2948373A patent/CA2948373A1/en active Pending
- 2015-05-15 WO PCT/US2015/031150 patent/WO2015175977A2/en active Application Filing
- 2015-05-15 JP JP2017512874A patent/JP6901966B2/ja active Active
- 2015-05-15 EP EP19198465.7A patent/EP3620178A3/en not_active Withdrawn
- 2015-05-15 AU AU2015258895A patent/AU2015258895A1/en not_active Abandoned
-
2017
- 2017-09-01 US US15/693,796 patent/US11021706B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| EP3620178A3 (en) | 2020-07-22 |
| EP3143141B1 (en) | 2019-10-02 |
| EP3143141A4 (en) | 2018-04-04 |
| JP2017522044A (ja) | 2017-08-10 |
| US20150361425A1 (en) | 2015-12-17 |
| US20200032254A1 (en) | 2020-01-30 |
| AU2015258895A1 (en) | 2016-11-24 |
| EP3143141A2 (en) | 2017-03-22 |
| US11021706B2 (en) | 2021-06-01 |
| CA2948373A1 (en) | 2015-11-19 |
| US9790495B2 (en) | 2017-10-17 |
| WO2015175977A3 (en) | 2016-03-10 |
| WO2015175977A2 (en) | 2015-11-19 |
| EP3620178A2 (en) | 2020-03-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6901966B2 (ja) | アンチセンス抗菌化合物および方法 | |
| JP6687542B2 (ja) | アンチセンス抗菌化合物および方法 | |
| US20210155934A1 (en) | Antisense antibacterial compounds and methods | |
| US20220135973A1 (en) | Antisense antibacterial compounds and methods | |
| US11293024B2 (en) | Antisense antibacterial compounds and methods | |
| US20200283768A1 (en) | Antisense antibacterial compounds and methods | |
| WO2018161027A1 (en) | Antisense antibacterial compounds and methods |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180514 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20180514 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20190418 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20190718 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20191018 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200311 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200610 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20201104 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210105 |
|
| C60 | Trial request (containing other claim documents, opposition documents) |
Free format text: JAPANESE INTERMEDIATE CODE: C60 Effective date: 20210105 |
|
| C11 | Written invitation by the commissioner to file amendments |
Free format text: JAPANESE INTERMEDIATE CODE: C11 Effective date: 20210115 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20210128 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20210323 |
|
| C21 | Notice of transfer of a case for reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C21 Effective date: 20210324 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20210423 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20210524 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20210618 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6901966 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |