JP6796484B2 - 治療化合物の経口送達のためのデバイス - Google Patents
治療化合物の経口送達のためのデバイス Download PDFInfo
- Publication number
- JP6796484B2 JP6796484B2 JP2016501518A JP2016501518A JP6796484B2 JP 6796484 B2 JP6796484 B2 JP 6796484B2 JP 2016501518 A JP2016501518 A JP 2016501518A JP 2016501518 A JP2016501518 A JP 2016501518A JP 6796484 B2 JP6796484 B2 JP 6796484B2
- Authority
- JP
- Japan
- Prior art keywords
- balloon
- piston
- capsule
- compartment
- delivery
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 150000001875 compounds Chemical class 0.000 title description 10
- 230000001225 therapeutic effect Effects 0.000 title description 10
- 239000003814 drug Substances 0.000 claims description 211
- 239000002775 capsule Substances 0.000 claims description 210
- 230000000968 intestinal effect Effects 0.000 claims description 137
- 210000000813 small intestine Anatomy 0.000 claims description 86
- 229940124597 therapeutic agent Drugs 0.000 claims description 79
- 239000000203 mixture Substances 0.000 claims description 72
- 239000000376 reactant Substances 0.000 claims description 67
- 239000007788 liquid Substances 0.000 claims description 61
- 239000007789 gas Substances 0.000 claims description 50
- 230000007246 mechanism Effects 0.000 claims description 50
- 210000001035 gastrointestinal tract Anatomy 0.000 claims description 49
- 238000009472 formulation Methods 0.000 claims description 46
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 claims description 42
- 230000004044 response Effects 0.000 claims description 37
- 239000012530 fluid Substances 0.000 claims description 35
- 238000000576 coating method Methods 0.000 claims description 31
- 210000000936 intestine Anatomy 0.000 claims description 30
- 229920000642 polymer Polymers 0.000 claims description 30
- 239000011248 coating agent Substances 0.000 claims description 24
- 238000006243 chemical reaction Methods 0.000 claims description 20
- 210000002784 stomach Anatomy 0.000 claims description 20
- 230000015556 catabolic process Effects 0.000 claims description 16
- 238000006731 degradation reaction Methods 0.000 claims description 16
- 239000002253 acid Substances 0.000 claims description 13
- 239000004698 Polyethylene Substances 0.000 claims description 12
- -1 polyethylene Polymers 0.000 claims description 12
- 229920000573 polyethylene Polymers 0.000 claims description 12
- 230000000717 retained effect Effects 0.000 claims description 11
- 229910000028 potassium bicarbonate Inorganic materials 0.000 claims description 10
- 235000015497 potassium bicarbonate Nutrition 0.000 claims description 10
- 239000011736 potassium bicarbonate Substances 0.000 claims description 10
- TYJJADVDDVDEDZ-UHFFFAOYSA-M potassium hydrogencarbonate Chemical compound [K+].OC([O-])=O TYJJADVDDVDEDZ-UHFFFAOYSA-M 0.000 claims description 10
- 235000011389 fruit/vegetable juice Nutrition 0.000 claims description 7
- 229940086066 potassium hydrogencarbonate Drugs 0.000 claims description 7
- 229920000139 polyethylene terephthalate Polymers 0.000 claims description 5
- 239000005020 polyethylene terephthalate Substances 0.000 claims description 5
- 230000009747 swallowing Effects 0.000 claims description 4
- 239000004642 Polyimide Substances 0.000 claims description 3
- 229920001721 polyimide Polymers 0.000 claims description 3
- 210000001519 tissue Anatomy 0.000 description 149
- 229940079593 drug Drugs 0.000 description 130
- 239000000463 material Substances 0.000 description 77
- 238000000034 method Methods 0.000 description 66
- 230000008602 contraction Effects 0.000 description 47
- 239000003795 chemical substances by application Substances 0.000 description 46
- 238000012377 drug delivery Methods 0.000 description 31
- 230000002496 gastric effect Effects 0.000 description 31
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 30
- 230000014759 maintenance of location Effects 0.000 description 22
- 239000000126 substance Substances 0.000 description 21
- 208000024891 symptom Diseases 0.000 description 18
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 17
- 230000000712 assembly Effects 0.000 description 17
- 238000000429 assembly Methods 0.000 description 17
- 239000008103 glucose Substances 0.000 description 17
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 17
- OWEGMIWEEQEYGQ-UHFFFAOYSA-N 100676-05-9 Natural products OC1C(O)C(O)C(CO)OC1OCC1C(O)C(O)C(O)C(OC2C(OC(O)C(O)C2O)CO)O1 OWEGMIWEEQEYGQ-UHFFFAOYSA-N 0.000 description 16
- GUBGYTABKSRVRQ-PICCSMPSSA-N Maltose Natural products O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@@H](CO)OC(O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-PICCSMPSSA-N 0.000 description 16
- 230000002572 peristaltic effect Effects 0.000 description 16
- 102000004877 Insulin Human genes 0.000 description 15
- 108090001061 Insulin Proteins 0.000 description 15
- 229940125396 insulin Drugs 0.000 description 15
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 13
- 239000000853 adhesive Substances 0.000 description 12
- 230000001070 adhesive effect Effects 0.000 description 12
- 238000000465 moulding Methods 0.000 description 12
- 239000007787 solid Substances 0.000 description 12
- 239000008280 blood Substances 0.000 description 11
- 210000004369 blood Anatomy 0.000 description 11
- 230000000149 penetrating effect Effects 0.000 description 11
- 230000035515 penetration Effects 0.000 description 11
- 238000000926 separation method Methods 0.000 description 11
- 235000000346 sugar Nutrition 0.000 description 11
- 238000010586 diagram Methods 0.000 description 10
- 229920000609 methyl cellulose Polymers 0.000 description 10
- 239000001923 methylcellulose Substances 0.000 description 10
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 9
- HTQBXNHDCUEHJF-XWLPCZSASA-N Exenatide Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(N)=O)C(=O)NCC(=O)NCC(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CO)C(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCSC)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CO)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)CNC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=CC=C1 HTQBXNHDCUEHJF-XWLPCZSASA-N 0.000 description 9
- 108010011459 Exenatide Proteins 0.000 description 9
- 229960001519 exenatide Drugs 0.000 description 9
- 210000002429 large intestine Anatomy 0.000 description 9
- 230000008569 process Effects 0.000 description 9
- 230000009467 reduction Effects 0.000 description 9
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 8
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 8
- 150000007513 acids Chemical class 0.000 description 8
- 239000011230 binding agent Substances 0.000 description 8
- 229920002988 biodegradable polymer Polymers 0.000 description 8
- 239000004621 biodegradable polymer Substances 0.000 description 8
- 206010012601 diabetes mellitus Diseases 0.000 description 8
- 239000000859 incretin Substances 0.000 description 8
- 238000002955 isolation Methods 0.000 description 8
- 239000007884 disintegrant Substances 0.000 description 7
- 208000035475 disorder Diseases 0.000 description 7
- 239000000546 pharmaceutical excipient Substances 0.000 description 7
- 108090000765 processed proteins & peptides Proteins 0.000 description 7
- 102000004169 proteins and genes Human genes 0.000 description 7
- 108090000623 proteins and genes Proteins 0.000 description 7
- 102000014150 Interferons Human genes 0.000 description 6
- 108010050904 Interferons Proteins 0.000 description 6
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 6
- 238000013459 approach Methods 0.000 description 6
- 238000000354 decomposition reaction Methods 0.000 description 6
- 201000010099 disease Diseases 0.000 description 6
- 239000013583 drug formulation Substances 0.000 description 6
- 238000005516 engineering process Methods 0.000 description 6
- 239000012634 fragment Substances 0.000 description 6
- 239000000122 growth hormone Substances 0.000 description 6
- 238000003780 insertion Methods 0.000 description 6
- 230000037431 insertion Effects 0.000 description 6
- 229940079322 interferon Drugs 0.000 description 6
- 239000000199 parathyroid hormone Substances 0.000 description 6
- 229940124531 pharmaceutical excipient Drugs 0.000 description 6
- 102000004196 processed proteins & peptides Human genes 0.000 description 6
- 230000001681 protective effect Effects 0.000 description 6
- 230000005855 radiation Effects 0.000 description 6
- DTHNMHAUYICORS-KTKZVXAJSA-N Glucagon-like peptide 1 Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCCN)C(=O)NCC(=O)N[C@@H](CCCNC(N)=N)C(N)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CCC(N)=O)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC=1N=CNC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=CC=C1 DTHNMHAUYICORS-KTKZVXAJSA-N 0.000 description 5
- 108010051696 Growth Hormone Proteins 0.000 description 5
- 102000018997 Growth Hormone Human genes 0.000 description 5
- 102000003982 Parathyroid hormone Human genes 0.000 description 5
- 108090000445 Parathyroid hormone Proteins 0.000 description 5
- 238000010521 absorption reaction Methods 0.000 description 5
- 230000008901 benefit Effects 0.000 description 5
- 230000000694 effects Effects 0.000 description 5
- 229960001319 parathyroid hormone Drugs 0.000 description 5
- AEMRFAOFKBGASW-UHFFFAOYSA-N Glycolic acid Chemical compound OCC(O)=O AEMRFAOFKBGASW-UHFFFAOYSA-N 0.000 description 4
- 208000001132 Osteoporosis Diseases 0.000 description 4
- 230000004913 activation Effects 0.000 description 4
- TZCXTZWJZNENPQ-UHFFFAOYSA-L barium sulfate Chemical compound [Ba+2].[O-]S([O-])(=O)=O TZCXTZWJZNENPQ-UHFFFAOYSA-L 0.000 description 4
- 150000004283 biguanides Chemical class 0.000 description 4
- 238000006065 biodegradation reaction Methods 0.000 description 4
- 239000001569 carbon dioxide Substances 0.000 description 4
- 229910002092 carbon dioxide Inorganic materials 0.000 description 4
- 239000007795 chemical reaction product Substances 0.000 description 4
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 4
- 235000005911 diet Nutrition 0.000 description 4
- 238000004090 dissolution Methods 0.000 description 4
- 238000009826 distribution Methods 0.000 description 4
- 238000001802 infusion Methods 0.000 description 4
- 239000003550 marker Substances 0.000 description 4
- 238000005259 measurement Methods 0.000 description 4
- 238000002483 medication Methods 0.000 description 4
- XZWYZXLIPXDOLR-UHFFFAOYSA-N metformin Chemical compound CN(C)C(=N)NC(N)=N XZWYZXLIPXDOLR-UHFFFAOYSA-N 0.000 description 4
- 229960003105 metformin Drugs 0.000 description 4
- 238000002156 mixing Methods 0.000 description 4
- 238000004806 packaging method and process Methods 0.000 description 4
- 238000005192 partition Methods 0.000 description 4
- 238000012545 processing Methods 0.000 description 4
- 230000002829 reductive effect Effects 0.000 description 4
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 4
- 235000017557 sodium bicarbonate Nutrition 0.000 description 4
- 238000000935 solvent evaporation Methods 0.000 description 4
- 210000005239 tubule Anatomy 0.000 description 4
- 229940123208 Biguanide Drugs 0.000 description 3
- 108010019598 Liraglutide Proteins 0.000 description 3
- YSDQQAXHVYUZIW-QCIJIYAXSA-N Liraglutide Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)NCC(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCCNC(=O)CC[C@H](NC(=O)CCCCCCCCCCCCCCC)C(O)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)NCC(=O)N[C@@H](CCCNC(N)=N)C(=O)NCC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=C(O)C=C1 YSDQQAXHVYUZIW-QCIJIYAXSA-N 0.000 description 3
- 239000002202 Polyethylene glycol Substances 0.000 description 3
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 3
- 239000003242 anti bacterial agent Substances 0.000 description 3
- 229940088710 antibiotic agent Drugs 0.000 description 3
- 230000033228 biological regulation Effects 0.000 description 3
- 238000007664 blowing Methods 0.000 description 3
- 229920002678 cellulose Polymers 0.000 description 3
- 239000001913 cellulose Substances 0.000 description 3
- 230000001276 controlling effect Effects 0.000 description 3
- 229920001577 copolymer Polymers 0.000 description 3
- 230000037213 diet Effects 0.000 description 3
- 235000013305 food Nutrition 0.000 description 3
- 230000002641 glycemic effect Effects 0.000 description 3
- 235000019692 hotdogs Nutrition 0.000 description 3
- 229960003444 immunosuppressant agent Drugs 0.000 description 3
- 239000003018 immunosuppressive agent Substances 0.000 description 3
- MGXWVYUBJRZYPE-YUGYIWNOSA-N incretin Chemical class C([C@@H](C(=O)N[C@@H](CO)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCCN)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCC(N)=O)C(O)=O)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC=1C=CC(O)=CC=1)[C@@H](C)O)[C@@H](C)CC)C1=CC=C(O)C=C1 MGXWVYUBJRZYPE-YUGYIWNOSA-N 0.000 description 3
- 238000009434 installation Methods 0.000 description 3
- 238000001990 intravenous administration Methods 0.000 description 3
- 229960002701 liraglutide Drugs 0.000 description 3
- 230000033001 locomotion Effects 0.000 description 3
- 230000007774 longterm Effects 0.000 description 3
- 235000012054 meals Nutrition 0.000 description 3
- 230000003647 oxidation Effects 0.000 description 3
- 238000007254 oxidation reaction Methods 0.000 description 3
- 239000002245 particle Substances 0.000 description 3
- 229920001223 polyethylene glycol Polymers 0.000 description 3
- 229920006254 polymer film Polymers 0.000 description 3
- 229920001296 polysiloxane Polymers 0.000 description 3
- 230000008961 swelling Effects 0.000 description 3
- 238000005979 thermal decomposition reaction Methods 0.000 description 3
- 238000002604 ultrasonography Methods 0.000 description 3
- DDYAPMZTJAYBOF-ZMYDTDHYSA-N (3S)-4-[[(2S)-1-[[(2S)-1-[[(2S)-5-amino-1-[[(2S)-1-[[(2S)-1-[[(2S)-1-[[(2S)-4-amino-1-[[(2S,3R)-1-[[(2S)-6-amino-1-[[(2S)-1-[[(2S)-4-amino-1-[[(2S)-1-[[(2S)-4-amino-1-[[(2S)-4-amino-1-[[(2S,3S)-1-[[(1S)-1-carboxyethyl]amino]-3-methyl-1-oxopentan-2-yl]amino]-1,4-dioxobutan-2-yl]amino]-1,4-dioxobutan-2-yl]amino]-5-carbamimidamido-1-oxopentan-2-yl]amino]-1,4-dioxobutan-2-yl]amino]-5-carbamimidamido-1-oxopentan-2-yl]amino]-1-oxohexan-2-yl]amino]-3-hydroxy-1-oxobutan-2-yl]amino]-1,4-dioxobutan-2-yl]amino]-4-methylsulfanyl-1-oxobutan-2-yl]amino]-4-methyl-1-oxopentan-2-yl]amino]-3-(1H-indol-3-yl)-1-oxopropan-2-yl]amino]-1,5-dioxopentan-2-yl]amino]-3-methyl-1-oxobutan-2-yl]amino]-1-oxo-3-phenylpropan-2-yl]amino]-3-[[(2S)-5-amino-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-6-amino-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S,3R)-2-[[(2S)-2-[[(2S,3R)-2-[[2-[[(2S)-5-amino-2-[[(2S)-2-[[(2S)-2-amino-3-(1H-imidazol-4-yl)propanoyl]amino]-3-hydroxypropanoyl]amino]-5-oxopentanoyl]amino]acetyl]amino]-3-hydroxybutanoyl]amino]-3-phenylpropanoyl]amino]-3-hydroxybutanoyl]amino]-3-hydroxypropanoyl]amino]-3-carboxypropanoyl]amino]-3-(4-hydroxyphenyl)propanoyl]amino]-3-hydroxypropanoyl]amino]hexanoyl]amino]-3-(4-hydroxyphenyl)propanoyl]amino]-4-methylpentanoyl]amino]-3-carboxypropanoyl]amino]-3-hydroxypropanoyl]amino]-5-carbamimidamidopentanoyl]amino]-5-carbamimidamidopentanoyl]amino]propanoyl]amino]-5-oxopentanoyl]amino]-4-oxobutanoic acid Chemical class [H]N[C@@H](CC1=CNC=N1)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCC(N)=O)C(=O)NCC(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC1=CC=CC=C1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC1=CC=C(O)C=C1)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC1=CC=C(O)C=C1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC1=CC=CC=C1)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC1=CNC2=C1C=CC=C2)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(O)=O DDYAPMZTJAYBOF-ZMYDTDHYSA-N 0.000 description 2
- 208000030507 AIDS Diseases 0.000 description 2
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 2
- PMATZTZNYRCHOR-CGLBZJNRSA-N Cyclosporin A Chemical compound CC[C@@H]1NC(=O)[C@H]([C@H](O)[C@H](C)C\C=C\C)N(C)C(=O)[C@H](C(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)N(C)C(=O)CN(C)C1=O PMATZTZNYRCHOR-CGLBZJNRSA-N 0.000 description 2
- 108010036949 Cyclosporine Proteins 0.000 description 2
- JIGUQPWFLRLWPJ-UHFFFAOYSA-N Ethyl acrylate Chemical compound CCOC(=O)C=C JIGUQPWFLRLWPJ-UHFFFAOYSA-N 0.000 description 2
- 108010010803 Gelatin Proteins 0.000 description 2
- 108010088406 Glucagon-Like Peptides Proteins 0.000 description 2
- 101800000224 Glucagon-like peptide 1 Proteins 0.000 description 2
- 102400000322 Glucagon-like peptide 1 Human genes 0.000 description 2
- CERQOIWHTDAKMF-UHFFFAOYSA-N Methacrylic acid Chemical compound CC(=C)C(O)=O CERQOIWHTDAKMF-UHFFFAOYSA-N 0.000 description 2
- 206010028980 Neoplasm Diseases 0.000 description 2
- UIIMBOGNXHQVGW-DEQYMQKBSA-M Sodium bicarbonate-14C Chemical compound [Na+].O[14C]([O-])=O UIIMBOGNXHQVGW-DEQYMQKBSA-M 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 2
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 2
- 230000009471 action Effects 0.000 description 2
- 230000000573 anti-seizure effect Effects 0.000 description 2
- 239000002246 antineoplastic agent Substances 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- 230000004888 barrier function Effects 0.000 description 2
- 230000000740 bleeding effect Effects 0.000 description 2
- 230000017531 blood circulation Effects 0.000 description 2
- 201000011510 cancer Diseases 0.000 description 2
- 239000001768 carboxy methyl cellulose Substances 0.000 description 2
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 2
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 2
- 238000002144 chemical decomposition reaction Methods 0.000 description 2
- 235000012000 cholesterol Nutrition 0.000 description 2
- 229960001265 ciclosporin Drugs 0.000 description 2
- 238000004891 communication Methods 0.000 description 2
- 230000000875 corresponding effect Effects 0.000 description 2
- 230000008878 coupling Effects 0.000 description 2
- 238000010168 coupling process Methods 0.000 description 2
- 238000005859 coupling reaction Methods 0.000 description 2
- 238000004132 cross linking Methods 0.000 description 2
- 229930182912 cyclosporin Natural products 0.000 description 2
- 229940127089 cytotoxic agent Drugs 0.000 description 2
- 230000006378 damage Effects 0.000 description 2
- 238000011982 device technology Methods 0.000 description 2
- 230000029087 digestion Effects 0.000 description 2
- 231100000673 dose–response relationship Toxicity 0.000 description 2
- 239000002702 enteric coating Substances 0.000 description 2
- 238000009505 enteric coating Methods 0.000 description 2
- 206010015037 epilepsy Diseases 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 239000000499 gel Substances 0.000 description 2
- 229920000159 gelatin Polymers 0.000 description 2
- 239000008273 gelatin Substances 0.000 description 2
- 235000019322 gelatine Nutrition 0.000 description 2
- 235000011852 gelatine desserts Nutrition 0.000 description 2
- 239000003102 growth factor Substances 0.000 description 2
- 201000001421 hyperglycemia Diseases 0.000 description 2
- 238000003384 imaging method Methods 0.000 description 2
- 239000011261 inert gas Substances 0.000 description 2
- 208000015181 infectious disease Diseases 0.000 description 2
- 238000007918 intramuscular administration Methods 0.000 description 2
- 238000005304 joining Methods 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 2
- 150000002632 lipids Chemical class 0.000 description 2
- 238000012423 maintenance Methods 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- 229910052760 oxygen Inorganic materials 0.000 description 2
- PNJWIWWMYCMZRO-UHFFFAOYSA-N pent‐4‐en‐2‐one Natural products CC(=O)CC=C PNJWIWWMYCMZRO-UHFFFAOYSA-N 0.000 description 2
- 239000000137 peptide hydrolase inhibitor Substances 0.000 description 2
- 239000011148 porous material Substances 0.000 description 2
- 239000003755 preservative agent Substances 0.000 description 2
- 239000012781 shape memory material Substances 0.000 description 2
- 230000011664 signaling Effects 0.000 description 2
- 239000002893 slag Substances 0.000 description 2
- 239000005720 sucrose Substances 0.000 description 2
- 150000008163 sugars Chemical class 0.000 description 2
- 238000007666 vacuum forming Methods 0.000 description 2
- 230000029663 wound healing Effects 0.000 description 2
- PAPBSGBWRJIAAV-UHFFFAOYSA-N ε-Caprolactone Chemical compound O=C1CCCCCO1 PAPBSGBWRJIAAV-UHFFFAOYSA-N 0.000 description 2
- VPVXHAANQNHFSF-UHFFFAOYSA-N 1,4-dioxan-2-one Chemical compound O=C1COCCO1 VPVXHAANQNHFSF-UHFFFAOYSA-N 0.000 description 1
- RKDVKSZUMVYZHH-UHFFFAOYSA-N 1,4-dioxane-2,5-dione Chemical compound O=C1COC(=O)CO1 RKDVKSZUMVYZHH-UHFFFAOYSA-N 0.000 description 1
- FUFLCEKSBBHCMO-UHFFFAOYSA-N 11-dehydrocorticosterone Natural products O=C1CCC2(C)C3C(=O)CC(C)(C(CC4)C(=O)CO)C4C3CCC2=C1 FUFLCEKSBBHCMO-UHFFFAOYSA-N 0.000 description 1
- 206010000087 Abdominal pain upper Diseases 0.000 description 1
- 208000023275 Autoimmune disease Diseases 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- 0 C1CC*CC1 Chemical compound C1CC*CC1 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 1
- 206010010904 Convulsion Diseases 0.000 description 1
- MFYSYFVPBJMHGN-ZPOLXVRWSA-N Cortisone Chemical compound O=C1CC[C@]2(C)[C@H]3C(=O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 MFYSYFVPBJMHGN-ZPOLXVRWSA-N 0.000 description 1
- MFYSYFVPBJMHGN-UHFFFAOYSA-N Cortisone Natural products O=C1CCC2(C)C3C(=O)CC(C)(C(CC4)(O)C(=O)CO)C4C3CCC2=C1 MFYSYFVPBJMHGN-UHFFFAOYSA-N 0.000 description 1
- 229920000858 Cyclodextrin Polymers 0.000 description 1
- 229920001353 Dextrin Polymers 0.000 description 1
- 239000004375 Dextrin Substances 0.000 description 1
- 229920003134 Eudragit® polymer Polymers 0.000 description 1
- 102000017011 Glycated Hemoglobin A Human genes 0.000 description 1
- 108010014663 Glycated Hemoglobin A Proteins 0.000 description 1
- 102000001554 Hemoglobins Human genes 0.000 description 1
- 108010054147 Hemoglobins Proteins 0.000 description 1
- 208000032843 Hemorrhage Diseases 0.000 description 1
- 241000167880 Hirundinidae Species 0.000 description 1
- 101001012157 Homo sapiens Receptor tyrosine-protein kinase erbB-2 Proteins 0.000 description 1
- 206010020772 Hypertension Diseases 0.000 description 1
- 206010020850 Hyperthyroidism Diseases 0.000 description 1
- 208000013016 Hypoglycemia Diseases 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- VVQNEPGJFQJSBK-UHFFFAOYSA-N Methyl methacrylate Chemical compound COC(=O)C(C)=C VVQNEPGJFQJSBK-UHFFFAOYSA-N 0.000 description 1
- 208000012266 Needlestick injury Diseases 0.000 description 1
- 235000014676 Phragmites communis Nutrition 0.000 description 1
- 201000007902 Primary cutaneous amyloidosis Diseases 0.000 description 1
- 229940124158 Protease/peptidase inhibitor Drugs 0.000 description 1
- 201000004681 Psoriasis Diseases 0.000 description 1
- 102100030086 Receptor tyrosine-protein kinase erbB-2 Human genes 0.000 description 1
- 206010040047 Sepsis Diseases 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 208000024799 Thyroid disease Diseases 0.000 description 1
- 239000008186 active pharmaceutical agent Substances 0.000 description 1
- 229960002964 adalimumab Drugs 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 229960004733 albiglutide Drugs 0.000 description 1
- OGWAVGNOAMXIIM-UHFFFAOYSA-N albiglutide Chemical compound O=C(O)C(NC(=O)CNC(=O)C(NC(=O)C(NC(=O)C(NC(=O)C(NC(=O)C(NC(=O)C(NC(=O)C(NC(=O)C(NC(=O)C(NC(=O)C(NC(=O)C(NC(=O)C(NC(=O)CNC(=O)C(NC(=O)C(NC(=O)C(NC(=O)C(NC(=O)C(NC(=O)C(NC(=O)C(NC(=O)C(NC(=O)C(NC(=O)C(NC(=O)C(NC(=O)CNC(=O)C(NC(=O)CNC(=O)C(N)CC=1(N=CNC=1))CCC(=O)O)C(O)C)CC2(=CC=CC=C2))C(O)C)CO)CC(=O)O)C(C)C)CO)CO)CC3(=CC=C(O)C=C3))CC(C)C)CCC(=O)O)CCC(=O)N)C)C)CCCCN)CCC(=O)O)CC4(=CC=CC=C4))C(CC)C)C)CC=6(C5(=C(C=CC=C5)NC=6)))CC(C)C)C(C)C)CCCCN)CCCNC(=N)N OGWAVGNOAMXIIM-UHFFFAOYSA-N 0.000 description 1
- 208000007502 anemia Diseases 0.000 description 1
- 230000000078 anti-malarial effect Effects 0.000 description 1
- 239000003430 antimalarial agent Substances 0.000 description 1
- 239000003443 antiviral agent Substances 0.000 description 1
- 229940121357 antivirals Drugs 0.000 description 1
- 210000000436 anus Anatomy 0.000 description 1
- 230000006793 arrhythmia Effects 0.000 description 1
- 206010003119 arrhythmia Diseases 0.000 description 1
- 206010003246 arthritis Diseases 0.000 description 1
- 230000001363 autoimmune Effects 0.000 description 1
- 235000013871 bee wax Nutrition 0.000 description 1
- 239000012166 beeswax Substances 0.000 description 1
- 230000006399 behavior Effects 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- GUBGYTABKSRVRQ-QUYVBRFLSA-N beta-maltose Chemical compound OC[C@H]1O[C@H](O[C@H]2[C@H](O)[C@@H](O)[C@H](O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@@H]1O GUBGYTABKSRVRQ-QUYVBRFLSA-N 0.000 description 1
- 229920000249 biocompatible polymer Polymers 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 208000034158 bleeding Diseases 0.000 description 1
- 210000001124 body fluid Anatomy 0.000 description 1
- 239000010839 body fluid Substances 0.000 description 1
- 210000000988 bone and bone Anatomy 0.000 description 1
- 235000021152 breakfast Nutrition 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 235000014633 carbohydrates Nutrition 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 230000001149 cognitive effect Effects 0.000 description 1
- 238000007906 compression Methods 0.000 description 1
- 230000006835 compression Effects 0.000 description 1
- 238000012790 confirmation Methods 0.000 description 1
- 230000002596 correlated effect Effects 0.000 description 1
- 229960004544 cortisone Drugs 0.000 description 1
- 229920006037 cross link polymer Polymers 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 229920006237 degradable polymer Polymers 0.000 description 1
- 238000002716 delivery method Methods 0.000 description 1
- 238000001739 density measurement Methods 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 230000008021 deposition Effects 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 235000019425 dextrin Nutrition 0.000 description 1
- 238000002059 diagnostic imaging Methods 0.000 description 1
- 230000000378 dietary effect Effects 0.000 description 1
- 235000018823 dietary intake Nutrition 0.000 description 1
- 230000001079 digestive effect Effects 0.000 description 1
- 229940042399 direct acting antivirals protease inhibitors Drugs 0.000 description 1
- 238000005553 drilling Methods 0.000 description 1
- 210000001198 duodenum Anatomy 0.000 description 1
- 239000013013 elastic material Substances 0.000 description 1
- 210000003238 esophagus Anatomy 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 210000003722 extracellular fluid Anatomy 0.000 description 1
- 238000001125 extrusion Methods 0.000 description 1
- 238000011049 filling Methods 0.000 description 1
- 238000002594 fluoroscopy Methods 0.000 description 1
- 239000011888 foil Substances 0.000 description 1
- 230000037406 food intake Effects 0.000 description 1
- 235000012631 food intake Nutrition 0.000 description 1
- ZZUFCTLCJUWOSV-UHFFFAOYSA-N furosemide Chemical compound C1=C(Cl)C(S(=O)(=O)N)=CC(C(O)=O)=C1NCC1=CC=CO1 ZZUFCTLCJUWOSV-UHFFFAOYSA-N 0.000 description 1
- 229960003883 furosemide Drugs 0.000 description 1
- 238000000227 grinding Methods 0.000 description 1
- 208000037824 growth disorder Diseases 0.000 description 1
- 230000003054 hormonal effect Effects 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 229920003063 hydroxymethyl cellulose Polymers 0.000 description 1
- 229940031574 hydroxymethyl cellulose Drugs 0.000 description 1
- 230000002218 hypoglycaemic effect Effects 0.000 description 1
- 208000003532 hypothyroidism Diseases 0.000 description 1
- 230000002989 hypothyroidism Effects 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 238000002513 implantation Methods 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 229910052500 inorganic mineral Inorganic materials 0.000 description 1
- 239000002917 insecticide Substances 0.000 description 1
- 208000002551 irritable bowel syndrome Diseases 0.000 description 1
- 230000000302 ischemic effect Effects 0.000 description 1
- 239000004310 lactic acid Substances 0.000 description 1
- 235000014655 lactic acid Nutrition 0.000 description 1
- JJTUDXZGHPGLLC-UHFFFAOYSA-N lactide Chemical compound CC1OC(=O)C(C)OC1=O JJTUDXZGHPGLLC-UHFFFAOYSA-N 0.000 description 1
- 238000011068 loading method Methods 0.000 description 1
- 235000004213 low-fat Nutrition 0.000 description 1
- 238000002595 magnetic resonance imaging Methods 0.000 description 1
- 230000005389 magnetism Effects 0.000 description 1
- 239000000155 melt Substances 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 150000002734 metacrylic acid derivatives Chemical class 0.000 description 1
- 229920003145 methacrylic acid copolymer Polymers 0.000 description 1
- 235000010755 mineral Nutrition 0.000 description 1
- 239000011707 mineral Substances 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 201000006417 multiple sclerosis Diseases 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 239000000041 non-steroidal anti-inflammatory agent Substances 0.000 description 1
- 229940021182 non-steroidal anti-inflammatory drug Drugs 0.000 description 1
- NJPPVKZQTLUDBO-UHFFFAOYSA-N novaluron Chemical group C1=C(Cl)C(OC(F)(F)C(OC(F)(F)F)F)=CC=C1NC(=O)NC(=O)C1=C(F)C=CC=C1F NJPPVKZQTLUDBO-UHFFFAOYSA-N 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 210000004798 organs belonging to the digestive system Anatomy 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 239000008188 pellet Substances 0.000 description 1
- 239000000449 pharmaceutical disintegrant Substances 0.000 description 1
- 239000006187 pill Substances 0.000 description 1
- 238000005498 polishing Methods 0.000 description 1
- 229920001606 poly(lactic acid-co-glycolic acid) Polymers 0.000 description 1
- 238000010094 polymer processing Methods 0.000 description 1
- 229920001184 polypeptide Polymers 0.000 description 1
- 229920002635 polyurethane Polymers 0.000 description 1
- 239000004814 polyurethane Substances 0.000 description 1
- 231100000683 possible toxicity Toxicity 0.000 description 1
- 208000014670 posterior cortical atrophy Diseases 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- GCYXWQUSHADNBF-AAEALURTSA-N preproglucagon 78-108 Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCCN)C(=O)NCC(=O)N[C@@H](CCCNC(N)=N)C(=O)NCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CCC(N)=O)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC=1N=CNC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=CC=C1 GCYXWQUSHADNBF-AAEALURTSA-N 0.000 description 1
- 238000000513 principal component analysis Methods 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 238000005086 pumping Methods 0.000 description 1
- 238000000197 pyrolysis Methods 0.000 description 1
- 108700027806 rGLP-1 Proteins 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 239000005871 repellent Substances 0.000 description 1
- 230000002940 repellent Effects 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 206010039073 rheumatoid arthritis Diseases 0.000 description 1
- HFHDHCJBZVLPGP-UHFFFAOYSA-N schardinger α-dextrin Chemical compound O1C(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(O)C2O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC2C(O)C(O)C1OC2CO HFHDHCJBZVLPGP-UHFFFAOYSA-N 0.000 description 1
- 238000007789 sealing Methods 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 208000013223 septicemia Diseases 0.000 description 1
- 230000019491 signal transduction Effects 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000008109 sodium starch glycolate Substances 0.000 description 1
- 229940079832 sodium starch glycolate Drugs 0.000 description 1
- 229920003109 sodium starch glycolate Polymers 0.000 description 1
- 239000002195 soluble material Substances 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- KQKPFRSPSRPDEB-UHFFFAOYSA-N sumatriptan Chemical compound CNS(=O)(=O)CC1=CC=C2NC=C(CCN(C)C)C2=C1 KQKPFRSPSRPDEB-UHFFFAOYSA-N 0.000 description 1
- 229960003708 sumatriptan Drugs 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 229950007151 taspoglutide Drugs 0.000 description 1
- 108010048573 taspoglutide Proteins 0.000 description 1
- WRGVLTAWMNZWGT-VQSPYGJZSA-N taspoglutide Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCCN)C(=O)NC(C)(C)C(=O)N[C@@H](CCCNC(N)=N)C(N)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CCC(N)=O)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)C(C)(C)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=CC=C1 WRGVLTAWMNZWGT-VQSPYGJZSA-N 0.000 description 1
- 210000004876 tela submucosa Anatomy 0.000 description 1
- 230000002123 temporal effect Effects 0.000 description 1
- 229940126585 therapeutic drug Drugs 0.000 description 1
- 208000021510 thyroid gland disease Diseases 0.000 description 1
- 239000004408 titanium dioxide Substances 0.000 description 1
- 230000020192 tolerance induction in gut-associated lymphoid tissue Effects 0.000 description 1
- 101150037438 tpm gene Proteins 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 150000003626 triacylglycerols Chemical class 0.000 description 1
- YFHICDDUDORKJB-UHFFFAOYSA-N trimethylene carbonate Chemical compound O=C1OCCCO1 YFHICDDUDORKJB-UHFFFAOYSA-N 0.000 description 1
- 208000001072 type 2 diabetes mellitus Diseases 0.000 description 1
- 229960005486 vaccine Drugs 0.000 description 1
- 238000001291 vacuum drying Methods 0.000 description 1
- 230000002861 ventricular Effects 0.000 description 1
- 239000011782 vitamin Substances 0.000 description 1
- 235000013343 vitamin Nutrition 0.000 description 1
- 229940088594 vitamin Drugs 0.000 description 1
- 229930003231 vitamin Natural products 0.000 description 1
- 239000001993 wax Substances 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0002—Galenical forms characterised by the drug release technique; Application systems commanded by energy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4808—Preparations in capsules, e.g. of gelatin, of chocolate characterised by the form of the capsule or the structure of the filling; Capsules containing small tablets; Capsules with outer layer for immediate drug release
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M31/00—Devices for introducing or retaining media, e.g. remedies, in cavities of the body
- A61M31/002—Devices for releasing a drug at a continuous and controlled rate for a prolonged period of time
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61J—CONTAINERS SPECIALLY ADAPTED FOR MEDICAL OR PHARMACEUTICAL PURPOSES; DEVICES OR METHODS SPECIALLY ADAPTED FOR BRINGING PHARMACEUTICAL PRODUCTS INTO PARTICULAR PHYSICAL OR ADMINISTERING FORMS; DEVICES FOR ADMINISTERING FOOD OR MEDICINES ORALLY; BABY COMFORTERS; DEVICES FOR RECEIVING SPITTLE
- A61J3/00—Devices or methods specially adapted for bringing pharmaceutical products into particular physical or administering forms
- A61J3/07—Devices or methods specially adapted for bringing pharmaceutical products into particular physical or administering forms into the form of capsules or similar small containers for oral use
- A61J3/071—Devices or methods specially adapted for bringing pharmaceutical products into particular physical or administering forms into the form of capsules or similar small containers for oral use into the form of telescopically engaged two-piece capsules
Landscapes
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Animal Behavior & Ethology (AREA)
- Chemical & Material Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Epidemiology (AREA)
- Pharmacology & Pharmacy (AREA)
- Hematology (AREA)
- Heart & Thoracic Surgery (AREA)
- Biomedical Technology (AREA)
- Anesthesiology (AREA)
- Medical Preparation Storing Or Oral Administration Devices (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Cosmetics (AREA)
- Media Introduction/Drainage Providing Device (AREA)
- Surgical Instruments (AREA)
- Infusion, Injection, And Reservoir Apparatuses (AREA)
Description
本願は、2013年3月15日に出願された、米国特許出願第13/837,025号(代理人管理番号第42197−715.501)の利益を主張するものであり、その全内容は、参照により本明細書中に援用される。
(項目1)
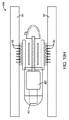
治療薬製剤を患者の腸管の腸壁の中に送達するための嚥下可能デバイスであって、
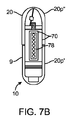
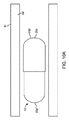
前記腸管を通して通過するように定寸された嚥下可能カプセルであって、カプセル壁を有し、前記カプセル壁を前記患者の胃内における分解から保護しながら、その少なくとも一部が、腸内の選択されたpHへの暴露に応じて分解する、カプセルと、
少なくとも部分的に非拡張状態にある第1の区画と、少なくとも部分的に非拡張状態にある第2の区画とを備える、前記カプセル内に配置される、少なくとも1つの拡張可能部材アセンブリであって、前記第1および第2の区画は、前記腸管内の流体への暴露に応じて分解する分解可能弁によって、流体的に分離される、アセンブリと、
前記区画のうちの一方内に含有される液体と、
前記他方の区画内に含有される反応物であって、前記弁が分解すると、前記液体および前記反応物は、混合し、ガスを産生し、少なくとも、前記第2の区画を拡張させる、反応物と、
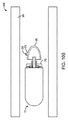
第2の区画に結合される送達機構であって、少なくとも1つのピストン−シリンダアセンブリを備える、送達機構と、
少なくとも1つの組織穿刺部材であって、
a.前記送達機構に着脱可能に結合される、近位部分と、
b.組織穿刺遠位部分と、
c.前記腸壁の中に送達するための治療薬製剤と、
を含み、前記腸壁内に保定されるように構成される、組織穿刺部材と、
を備え、
前記第2の区画の拡張に応じて、前記少なくとも1つの組織穿刺部材は、前記送達機構によって前記腸壁の中に前進され、そこで、前記治療薬を前記腸の中に送達するように、前記腸壁内に保定される、嚥下可能デバイス。
(項目2)
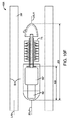
前記少なくとも1つのピストン−シリンダアセンブリは、シリンダの内側に摺動可能に配置されるピストンを備え、前記シリンダは、前記第2の区画の壁に結合され、前記ピストンを前記第2の区画内に産生されるガスによって駆動させるように、前記ピストンは、近位面を前記第2の区画の内部に暴露させ、
前記ピストンは、前記シリンダの内側を摺動するにつれて、前記組織穿刺部材を前記腸壁の中に前進させるように構成される、項目1に記載の嚥下可能デバイス。
(項目3)
前記ピストン−シリンダアセンブリは、前記シリンダに結合される針管腔をさらに備え、前記針管腔は、前記第2の区画の外部へのアクセスを提供し、
前記組織穿刺部材は、前記針管腔の内側に配置され、ピストンロッドによって前記ピストンに結合され、前記ピストンロッドは、前記ピストンが前記シリンダの内側を摺動するにつれて、前記針管腔を通して前進されるように定寸される、項目2に記載の嚥下可能デバイス。
(項目4)
前記ピストンシリンダアセンブリはさらに、規定の圧力が前記少なくとも1つの拡張可能部材の内側で到達するまで、前記ピストンが前記シリンダの内側で摺動することを防止する、感圧式解放部を備える、項目2に記載の嚥下可能デバイス。
(項目5)
前記感圧式解放部は、タブ、ラッチ、またはOリングを備える、項目4に記載の嚥下可能デバイス。
(項目6)
前記感圧式解放部は、約8〜10psiの範囲内の圧力で放出するように構成される、項目4に記載の嚥下可能デバイス。
(項目7)
ピストン−シリンダアセンブリ整列の手段をさらに備え、前記ピストン−シリンダアセンブリ整列の手段は、前記ピストン−シリンダアセンブリの長軸が、前記腸壁の表面と垂直であって、前記組織穿刺部材が前記腸壁の中に垂直に前進されるように、前記第2の区画が拡張すると、前記ピストン−シリンダアセンブリを整列させるように構成される、項目3に記載の嚥下可能デバイス。
(項目8)
前記ピストン−シリンダアセンブリ整列手段は、力を前記ピストン−シリンダアセンブリに付与し、それを垂直配向に付勢するように構成される、継手を備える、項目7に記載の嚥下可能デバイス。
(項目9)
前記送達機構は、ピストン−シリンダアセンブリのアレイを備える、項目3に記載の嚥下可能デバイス。
(項目10)
前記ピストン−シリンダアセンブリのアレイは、共通膨張マニホールドを共有し、前記共通膨張マニホールドは、前記ガスを指向し、前記ピストン−シリンダアセンブリのアレイの各ピストンを駆動させるように構成される、項目9に記載の嚥下可能デバイス。
(項目11)
前記分解可能弁は、溶解可能ピンチ弁にわたって位置付けられる、Oリングを備え、前記ピンチ弁は、小腸内の流体との接触に応じて溶解するように構成される、項目1に記載のデバイス。
(項目12)
前記ピストン−シリンダアセンブリはさらに、前記ピストンと前記シリンダとの間にシールを維持する、前記ピストンの周囲に配置されるOリングを備える、項目2に記載のデバイス。
(項目13)
前記カプセルは、第1のカプセル部分および第2のカプセル部分を備え、前記第1の部分は、第1のpHで分解し、前記第2の部分は、第2のpHで分解する、項目1に記載のデバイス。
(項目14)
前記第1のカプセル部分は、前記分解可能弁の少なくとも一部を覆い、前記第1のカプセル部分が分解すると、腸液は、前記カプセルに流入し、前記分解可能弁と接触することができる、項目13に記載のデバイス。
(項目15)
前記第1のカプセル部分は、約5.5またはそれを上回るpHで分解する、項目13に記載のデバイス。
(項目16)
前記第2のカプセル部分は、約6.5またはそれを上回るpHで分解する、項目13に記載のデバイス。
(項目17)
前記第1のカプセル部分は、本体を備え、前記第2のカプセル部分は、前記本体上に嵌合するキャップを備える、項目13に記載のデバイス。
(項目18)
前記カプセル壁のpH分解可能部分は、pH感受性コーティングを備える、項目1に記載のデバイス。
(項目19)
前記弁は、糖を備える、項目1に記載のデバイス。
(項目20)
前記糖は、マルトースを備える、項目19に記載のデバイス。
(項目21)
前記反応物は、少なくとも、第1および第2の反応物を備える、項目1に記載のデバイス。
(項目22)
前記第1および第2の反応物は、酸および塩基を備える、項目21に記載のデバイス。
(項目23)
前記第1の反応物は、炭酸水素カリウムを備え、前記第2の反応物は、クエン酸を備える、項目22に記載のデバイス。
(項目24)
前記少なくとも1つの組織穿刺部材は、糖を備える、項目1に記載のデバイス。
(項目25)
前記糖は、マルトースを備える、項目24に記載のデバイス。
(項目26)
前記治療薬製剤は、組織穿刺部材内に配置される成形区分を備える、項目1に記載のデバイス。
(項目27)
前記組織穿刺部材は、少なくとも部分的に、前記治療薬製剤から形成される、項目1に記載のデバイス。
(項目28)
前記組織穿刺部材は、前記組織穿刺部材を前記腸壁内に保定するための保定特徴を含む、項目1に記載のデバイス。
(項目29)
前記保定特徴は、返しまたはフックを備える、項目1に記載のデバイス。
(項目30)
前記少なくとも1つの組織穿刺部材は、複数の組織穿刺部材を備える、項目29に記載のデバイス。
(項目31)
前記腸は、小腸であり、前記カプセル壁は、前記小腸内の選択されたpHに応答して分解するように構成される、項目1に記載のデバイス。
(項目32)
前記拡張可能部材アセンブリは、ポリマー、実質的非柔軟性ポリマー、ポリエチレン、PET、またはポリイミドを備える、項目1に記載のデバイス。
(項目33)
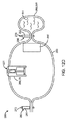
治療薬製剤を患者の腸管の腸壁の中に挿入するための嚥下可能デバイスであって、
前記腸管を通して通過するように定寸される、嚥下可能カプセルであって、カプセル壁を有し、前記カプセル壁が前記胃内で分解しないように保護しながら、その少なくとも一部が、腸内の選択されたpHへの暴露に応じて分解する、カプセルと、
前記カプセル内に配置される、少なくとも1つの拡張可能部材アセンブリであって、少なくとも部分的に非拡張状態にある第1の区画と、少なくとも部分的に非拡張状態にある第2の区画とを備え、前記第1および第2の区画は、前記腸管内の流体への暴露に応じて分解する分解可能弁によって、流体的に分離される、アセンブリと、
前記区画のうちの一方内に含有される液体と、
前記他方の区画内に含有される反応物であって、前記弁が分解すると、前記液体および前記反応物は、混合し、ガスを産生し、少なくとも、前記第2の区画を拡張させる、反応物と、
前記第2の拡張可能区画の壁に結合される、送達機構と、
少なくとも1つの組織穿刺部材であって、
a.)前記送達機構に着脱可能に結合される、近位部分と、
b.)組織穿刺遠位部分と、
c.)前記腸壁の中への送達のための治療薬製剤と、
を含み、前記腸壁内に保定されるように構成される、組織穿刺部材と、
を備え、
前記第2の区画の拡張に応じて、前記少なくとも1つの組織穿刺部材は、前記送達機構によって前記腸壁の中に前進され、そこで、前記治療薬を腸の中に送達するように、前記腸壁内に保定され、
前記送達機構は、下側部分および上側部分を有する第3の区画を備え、前記下側部分は、その上に配置され、前記上側部分および前記腸壁に向かって指向される、1つまたはそれを上回る組織穿刺部材を有する、前記第2の区画の壁に結合され、前記上側部分は、その上に配置され、前記下側部分に向かって指向される、1つまたはそれを上回る穿通針を有し、
前記第2の区画の膨張に応じて、前記第3の区画の下側部分は、前記第3の区画の上側部分に対して駆動され、前記1つまたはそれを上回る組織穿刺部材は、前記第3の区画の上側部分を通して前記腸壁の中に駆動され、前記1つまたはそれを上回る穿通針は、前記第3の区画の下側部分を通して駆動され、それによって、前記第2の区画の壁を穿通し、前記拡張可能部材アセンブリを収縮させる、デバイス。
(項目34)
前記第3の区画の上側部分は、前記1つまたはそれを上回る組織穿刺部材が前記腸壁を通して、その中に通過することを可能にするように構成される、1つまたはそれを上回る開口を備える、項目33に記載の嚥下可能デバイス。
(項目35)
前記1つまたはそれを上回る組織穿刺部材は、拡張可能部材アセンブリが、前記組織穿刺部材が前記腸壁の中に挿入されるまで、収縮されないように、前記1つまたはそれを上回る穿通針に対して十分に長い、項目33に記載の嚥下可能デバイス。
(項目36)
前記底部部分は、所望の圧力が前記第2の区画の内側で到達するまで、前記1つまたはそれを上回る穿通針による穿通を可能にしない材料から加工される、項目33に記載の嚥下可能デバイス。
(項目37)
治療薬製剤を患者の腸管の腸壁の中に送達する方法であって、
前記腸管を通して通過するように定寸される、嚥下可能カプセルを提供するステップであって、前記カプセルは、カプセル壁を有し、前記カプセル壁が前記患者の胃内で分解しないように保護しながら、その少なくとも一部が、腸内の選択されたpHへの暴露に応じて分解し、
前記嚥下可能カプセルはまた、少なくとも部分的に非拡張状態にある第1の区画と、少なくとも部分的に非拡張状態にある第2の区画とを備える、前記カプセル内に配置される、少なくとも1つの拡張可能部材アセンブリを有し、前記第1および第2の区画は、前記腸管内の流体への暴露に応じて分解する分解可能弁によって、流体的に分離される、ステップと、
前記分解可能弁を前記腸管内の流体を用いて分解し、それによって、前記区画のうちの一方内に含有される液体が、前記他方の区画内に含有される反応物と混合することを可能にするステップと、
前記液体および前記反応物の反応を用いてガスを産生するステップと、
前記液体および前記反応物の反応によって産生されるガスを用いて、少なくとも、前記拡張可能部材アセンブリの第2の区画を膨張させるステップと、
前記拡張可能部材アセンブリの内側に配置されるシリンダ−ピストンアセンブリを配向するステップであって、前記シリンダ−ピストンアセンブリは、シリンダの内側に摺動可能に配置されるピストンと、Oリングでシールされた前記ピストンと前記シリンダとの間の界面と、針管腔と連通する前記第2の区画の壁に結合されるシリンダと、前記第2の区画の外部へのアクセスを提供する針管腔とを備え、
前記シリンダ−ピストンアセンブリは、前記針管腔が前記腸壁と垂直となるように配向される、ステップと、
前記ガスからの圧力を用いて、前記シリンダの内側のピストンを前記第2の区画の外部に向かって駆動し、それによって、前記ピストンと前記組織穿刺部材との間に結合されるピストンロッドを用いて、前記針管腔内に配置される組織穿刺部材を前記腸壁の中に駆動させるステップであって、前記ピストンロッドは、前記針管腔の内側で摺動可能であるように定寸され、
前記組織穿刺部材は、少なくとも前記治療薬製剤を備える、ステップと、
を含む、方法。
実施形態は、薬剤および他の治療薬を体内の種々の場所に送達するためのデバイス、システム、キット、および方法を提供する。多くの実施形態は、GI管内で薬剤および他の治療薬を送達するための嚥下可能デバイスを提供する。特定の実施形態は、小腸、大腸の壁、または他の消化器官壁の中へ薬剤および他の治療薬を送達するためのカプセル等の嚥下可能デバイスを提供する。本発明の実施形態は、GI管内で吸収されにくく、耐性が低く、および/または分解される薬剤および他の治療薬の送達に特に有用である。さらに、本発明の実施形態は、静脈内または他の形態の非経口投与(例えば、筋肉内等)のみが以前は可能であった、または好ましくはそれによって送達された、薬剤ならびにタンパク質、ポリペプチド、および抗体等の他の治療薬を送達するために使用することができる。加えて、本発明の実施形態は、経口送達を介した血流の中への薬剤の急速な放出を達成するために有用である。
Claims (19)
- 治療薬製剤を患者の腸管の腸壁の中に送達するための嚥下可能デバイスであって、
前記腸管を通して通過するように定寸された嚥下可能カプセルであって、カプセル壁を有し、前記カプセル壁を前記患者の胃内における分解から保護しながら、その少なくとも一部が、腸内の選択されたpHへの暴露に応じて分解する、カプセルと、
少なくとも部分的に非拡張状態にある第1の区画と、少なくとも部分的に非拡張状態にある第2の区画とを備える、前記カプセル内に配置される、少なくとも1つの拡張可能部材アセンブリであって、前記第1および第2の区画は、前記腸管内の流体への暴露に応じて分解する分解可能弁によって、流体的に分離され、前記少なくとも1つの拡張可能部材アセンブリが円筒状の形状である、アセンブリと、
前記区画のうちの一方内に含有される液体と、
他方の前記区画内に含有される反応物であって、前記分解可能弁が分解すると、前記液体および前記反応物は、混合し、ガスを産生し、前記ガスは、少なくとも、前記第2の区画を拡張させる、反応物と、
第2の区画に結合される送達機構であって、少なくとも1つのピストン−シリンダアセンブリを備え、前記ピストン−シリンダアセンブリは、前記第2の区画の拡張前に、前記少なくとも1つの拡張可能部材アセンブリの縦軸に対して水平に位置している、送達機構と、
少なくとも1つの組織穿刺部材であって、
a.前記送達機構に着脱可能に結合される、近位部分と、
b.組織穿刺遠位部分と、
c.前記腸壁の中に送達するための治療薬製剤と、
を含み、前記腸壁内に保定されるように構成される、組織穿刺部材と、
を備え、
前記第2の区画の拡張に応じて、前記ピストン−シリンダアセンブリは、前記腸壁と垂直になるように再配向され、そして前記少なくとも1つの組織穿刺部材は、前記送達機構によって前記腸壁の中に前進され、そこで、前記治療薬製剤を前記腸の中に送達するように、前記腸壁内に保定される、嚥下可能デバイス。 - 前記少なくとも1つのピストン−シリンダアセンブリは、シリンダの内側に摺動可能に配置されるピストンを備え、前記シリンダは、前記第2の区画の壁に結合され、前記ピストンを前記第2の区画内に産生されるガスによって駆動させるように、前記ピストンは、近位面を前記第2の区画の内部に暴露させ、
前記ピストンは、前記シリンダの内側を摺動するにつれて、前記組織穿刺部材を前記腸壁の中に前進させるように構成される、請求項1に記載の嚥下可能デバイス。 - 前記ピストン−シリンダアセンブリはさらに、前記ピストンと前記シリンダとの間にシールを維持する、前記ピストンの周囲に配置されるOリングを備える、請求項2に記載のデバイス。
- 前記ピストン−シリンダアセンブリは、前記シリンダに結合される針管腔をさらに備え、前記針管腔は、前記第2の区画の外部へのアクセスを提供し、
前記組織穿刺部材は、前記針管腔の内側に配置され、ピストンロッドによって前記ピストンに結合され、前記ピストンロッドは、前記ピストンが前記シリンダの内側を摺動するにつれて、前記針管腔を通して前進されるように定寸される、請求項2に記載の嚥下可能デバイス。 - 前記ピストン−シリンダアセンブリはさらに、規定の圧力が前記少なくとも1つの拡張可能部材アセンブリの内側で到達するまで、前記ピストンが前記シリンダの内側で摺動することを防止する、感圧式解放部を備える、請求項2に記載の嚥下可能デバイス。
- 前記感圧式解放部は、タブ、ラッチ、またはOリングを備える、請求項5に記載の嚥下可能デバイス。
- 前記感圧式解放部は、8〜10psiの範囲内の圧力が前記少なくとも1つの拡張可能部材アセンブリの内側で到達するまで、前記ピストンが前記シリンダの内側で摺動ことを防止するように構成される、請求項5に記載の嚥下可能デバイス。
- ピストン−シリンダアセンブリ整列の手段をさらに備え、前記ピストン−シリンダアセンブリ整列の手段は、前記ピストン−シリンダアセンブリの長軸が、前記腸壁の表面と垂直であって、前記組織穿刺部材が前記腸壁の中に垂直に前進されるように、前記第2の区画が拡張すると、前記ピストン−シリンダアセンブリを整列させるように構成される、請求項4に記載の嚥下可能デバイス。
- 前記ピストン−シリンダアセンブリ整列の手段は、力を前記ピストン−シリンダアセンブリに付与し、前記ピストン−シリンダアセンブリを垂直配向に付勢するように構成される、継手を備える、請求項8に記載の嚥下可能デバイス。
- 前記分解可能弁は、溶解可能ピンチ弁にわたって位置付けられる、Oリングを備え、前記溶解可能ピンチ弁は、小腸内の流体との接触に応じて溶解するように構成される、請求項1に記載のデバイス。
- 前記カプセルは、第1のカプセル部分および第2のカプセル部分を備え、前記第1のカプセル部分は、第1のpHで分解し、前記第2のカプセル部分は、第2のpHで分解する、請求項1に記載のデバイス。
- 前記第1のカプセル部分は、前記分解可能弁の少なくとも一部を覆い、前記第1のカプセル部分が分解すると、腸液は、前記カプセルに流入し、前記分解可能弁と接触することができる、請求項11に記載のデバイス。
- 前記第1のカプセル部分は、5.5またはそれを上回るpHで分解する、
前記第2のカプセル部分は、6.5またはそれを上回るpHで分解する、あるいは
前記第1のカプセル部分は、本体を備え、前記第2のカプセル部分は、前記本体上に嵌合するキャップを備える、
のうちの少なくとも1つである、請求項11に記載のデバイス。 - 前記カプセル壁のpH分解可能部分は、pH感受性コーティングを備える、請求項1に記載のデバイス。
- 前記反応物は、少なくとも、第1および第2の反応物を備える、請求項1に記載のデバイス。
- 前記第1および第2の反応物は、酸および塩基を備える、請求項15に記載のデバイス。
- 前記第1の反応物は、炭酸水素カリウムを備え、前記第2の反応物は、クエン酸を備える、請求項15に記載のデバイス。
- 前記組織穿刺部材は、少なくとも部分的に、前記治療薬製剤から形成される、請求項1に記載のデバイス。
- 前記拡張可能部材アセンブリは、ポリマー、非柔軟性ポリマー、ポリエチレン、PET、またはポリイミドを備える、請求項1に記載のデバイス。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US13/837,025 | 2013-03-15 | ||
| US13/837,025 US8734429B2 (en) | 2010-12-23 | 2013-03-15 | Device, system and methods for the oral delivery of therapeutic compounds |
| PCT/US2014/024385 WO2014159604A1 (en) | 2013-03-15 | 2014-03-12 | Device for oral delivery of therapeutic compounds |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018242716A Division JP2019069206A (ja) | 2013-03-15 | 2018-12-26 | 治療化合物の経口送達のためのデバイス |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2016511124A JP2016511124A (ja) | 2016-04-14 |
| JP2016511124A5 JP2016511124A5 (ja) | 2018-05-31 |
| JP6796484B2 true JP6796484B2 (ja) | 2020-12-09 |
Family
ID=51625211
Family Applications (5)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016501518A Active JP6796484B2 (ja) | 2013-03-15 | 2014-03-12 | 治療化合物の経口送達のためのデバイス |
| JP2018242716A Withdrawn JP2019069206A (ja) | 2013-03-15 | 2018-12-26 | 治療化合物の経口送達のためのデバイス |
| JP2020182430A Pending JP2021020110A (ja) | 2013-03-15 | 2020-10-30 | 治療化合物の経口送達のためのデバイス |
| JP2022133795A Active JP7434462B2 (ja) | 2013-03-15 | 2022-08-25 | 治療化合物の経口送達のためのデバイス |
| JP2024017395A Pending JP2024036622A (ja) | 2013-03-15 | 2024-02-07 | 治療化合物の経口送達のためのデバイス |
Family Applications After (4)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018242716A Withdrawn JP2019069206A (ja) | 2013-03-15 | 2018-12-26 | 治療化合物の経口送達のためのデバイス |
| JP2020182430A Pending JP2021020110A (ja) | 2013-03-15 | 2020-10-30 | 治療化合物の経口送達のためのデバイス |
| JP2022133795A Active JP7434462B2 (ja) | 2013-03-15 | 2022-08-25 | 治療化合物の経口送達のためのデバイス |
| JP2024017395A Pending JP2024036622A (ja) | 2013-03-15 | 2024-02-07 | 治療化合物の経口送達のためのデバイス |
Country Status (10)
| Country | Link |
|---|---|
| EP (2) | EP3964190A1 (ja) |
| JP (5) | JP6796484B2 (ja) |
| CN (1) | CN105263461B (ja) |
| AU (4) | AU2014240401B2 (ja) |
| CA (2) | CA2901923C (ja) |
| DK (1) | DK2968071T3 (ja) |
| ES (1) | ES2897795T3 (ja) |
| PL (1) | PL2968071T3 (ja) |
| PT (1) | PT2968071T (ja) |
| WO (1) | WO2014159604A1 (ja) |
Families Citing this family (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2461818B1 (en) | 2009-08-03 | 2018-10-17 | Incube Labs, Llc | Swallowable capsule and method for stimulating incretin production within the intestinal tract |
| US8562589B2 (en) | 2009-12-24 | 2013-10-22 | Rani Therapeutics, Llc | Swallowable drug delivery device and method of delivery |
| US8846040B2 (en) | 2010-12-23 | 2014-09-30 | Rani Therapeutics, Llc | Therapeutic agent preparations comprising etanercept for delivery into a lumen of the intestinal tract using a swallowable drug delivery device |
| US9861683B2 (en) | 2010-12-23 | 2018-01-09 | Rani Therapeutics, Llc | Therapeutic agent preparations for delivery into a lumen of the intestinal tract using a swallowable drug delivery device |
| US9629799B2 (en) | 2010-12-23 | 2017-04-25 | Rani Therapeutics, Llc | Therapeutic agent preparations for delivery into a lumen of the intestinal tract using a swallowable drug delivery device |
| US8809269B2 (en) | 2010-12-23 | 2014-08-19 | Rani Therapeutics, Llc | Therapeutic agent preparations comprising insulin for delivery into a lumen of the intestinal tract using a swallowable drug delivery device |
| US9259386B2 (en) | 2010-12-23 | 2016-02-16 | Rani Therapeutics, Llc | Therapeutic preparation comprising somatostatin or somatostatin analogoue for delivery into a lumen of the intestinal tract using a swallowable drug delivery device |
| US10639272B2 (en) | 2010-12-23 | 2020-05-05 | Rani Therapeutics, Llc | Methods for delivering etanercept preparations into a lumen of the intestinal tract using a swallowable drug delivery device |
| US8980822B2 (en) | 2010-12-23 | 2015-03-17 | Rani Therapeutics, Llc | Therapeutic agent preparations comprising pramlintide for delivery into a lumen of the intestinal tract using a swallowable drug delivery device |
| US9284367B2 (en) | 2010-12-23 | 2016-03-15 | Rani Therapeutics, Llc | Therapeutic agent preparations for delivery into a lumen of the intestinal tract using a swallowable drug delivery device |
| US8969293B2 (en) | 2010-12-23 | 2015-03-03 | Rani Therapeutics, Llc | Therapeutic agent preparations comprising exenatide for delivery into a lumen of the intestinal tract using a swallowable drug delivery device |
| US9402806B2 (en) | 2010-12-23 | 2016-08-02 | Rani Therapeutics, Llc | Therapeutic agent preparations for delivery into a lumen of the intestinal tract using a swallowable drug delivery device |
| US8734429B2 (en) | 2010-12-23 | 2014-05-27 | Rani Therapeutics, Llc | Device, system and methods for the oral delivery of therapeutic compounds |
| US9402807B2 (en) | 2010-12-23 | 2016-08-02 | Rani Therapeutics, Llc | Therapeutic agent preparations for delivery into a lumen of the intestinal tract using a swallowable drug delivery device |
| US9283179B2 (en) | 2010-12-23 | 2016-03-15 | Rani Therapeutics, Llc | GnRH preparations for delivery into a lumen of the intestinal tract using a swallowable drug delivery device |
| US9415004B2 (en) | 2010-12-23 | 2016-08-16 | Rani Therapeutics, Llc | Therapeutic agent preparations for delivery into a lumen of the intestinal tract using a swallowable drug delivery device |
| CN105263461B (zh) * | 2013-03-15 | 2019-09-10 | 拉尼医疗有限公司 | 用于治疗化合物的口服递送的装置 |
| WO2017156347A1 (en) * | 2016-03-09 | 2017-09-14 | Incube Labs, Llc | Methods and articles for delivering viable cells into solid tissue |
| US10675248B2 (en) * | 2018-08-14 | 2020-06-09 | Alma Therapeutics Ltd. | Expandable pill |
| US20200093740A1 (en) * | 2018-09-25 | 2020-03-26 | Incube Labs, Llc | Ingestible device with expandable enclosure |
| CN109621169B (zh) * | 2019-01-09 | 2021-06-08 | 李红岩 | 一种产科观察治疗仪 |
| JP7420819B2 (ja) | 2019-02-01 | 2024-01-23 | ノボ・ノルデイスク・エー/エス | 作動機構を有する医療デバイス |
| CN115003287A (zh) * | 2020-01-14 | 2022-09-02 | 拉尼医疗有限公司 | 用于肠道内药物递送的可吞咽装置 |
| US20240000708A1 (en) * | 2020-03-31 | 2024-01-04 | Danmarks Tekniske Universitet | A flexible foil for the delivery of therapeutic cargos |
| EP4210805A1 (en) * | 2020-09-09 | 2023-07-19 | Amgen Inc. | Swallowable drug delivery devices |
| EP4237068A1 (en) * | 2020-11-02 | 2023-09-06 | Novo Nordisk A/S | Substance delivering capsule |
| WO2023158776A1 (en) * | 2022-02-21 | 2023-08-24 | Rani Therapeutics, Llc | Ingestible devices for delivering a fluid preparation into a gastrointestinal tract |
| WO2023158837A1 (en) * | 2022-02-21 | 2023-08-24 | Rani Therapeutics, Llc | Devices, assemblies, and methods for delivering a fluid preparation into a gastrointestinal tract |
Family Cites Families (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5125414A (en) * | 1990-01-16 | 1992-06-30 | Dysarz Edward D | Trap in barrel one handed retracted blood sampling device |
| US5217449A (en) * | 1990-12-11 | 1993-06-08 | Miyarisan Kabushiki Kaisha | Medical capsule and apparatus for activating the same |
| US5279607A (en) * | 1991-05-30 | 1994-01-18 | The State University Of New York | Telemetry capsule and process |
| JP4570696B2 (ja) * | 1997-04-10 | 2010-10-27 | ジョンズ・ホプキンズ・ユニバーシティ | ガスシリンジ装置 |
| GB9930000D0 (en) * | 1999-12-21 | 2000-02-09 | Phaeton Research Ltd | An ingestible device |
| JP2004528896A (ja) * | 2001-04-13 | 2004-09-24 | ベクトン・ディキンソン・アンド・カンパニー | 皮内に物質を注射する方法 |
| US7160258B2 (en) * | 2001-06-26 | 2007-01-09 | Entrack, Inc. | Capsule and method for treating or diagnosing the intestinal tract |
| US20050058701A1 (en) * | 2003-01-29 | 2005-03-17 | Yossi Gross | Active drug delivery in the gastrointestinal tract |
| EP1594477A4 (en) * | 2003-01-29 | 2009-07-15 | Pill Pharma Ltd E | ACTIVE MEDICATION CONTRIBUTION IN THE DIGESTIVE TUBE |
| CN2860501Y (zh) * | 2005-03-10 | 2007-01-24 | 李华 | 一次性注射器 |
| EP1884259A4 (en) * | 2005-05-27 | 2011-03-30 | Olympus Corp | INTRODUCTION DEVICE IN A SUBJECT |
| JP4402648B2 (ja) * | 2005-12-16 | 2010-01-20 | オリンパス株式会社 | 被検体内導入装置 |
| WO2010045477A2 (en) * | 2008-10-16 | 2010-04-22 | Obalon Therapeutics, Inc. | Intragastric volume-occupying device and method for fabricating same |
| EP3461478B1 (en) * | 2009-12-24 | 2020-04-22 | Rani Therapeutics, LLC | Swallowable drug delivery device |
| US8562589B2 (en) * | 2009-12-24 | 2013-10-22 | Rani Therapeutics, Llc | Swallowable drug delivery device and method of delivery |
| US8734429B2 (en) * | 2010-12-23 | 2014-05-27 | Rani Therapeutics, Llc | Device, system and methods for the oral delivery of therapeutic compounds |
| ES2765029T3 (es) * | 2011-06-29 | 2020-06-05 | Rani Therapeutics Llc | Dispositivo, sistema y métodos para la administración por vía oral de compuestos terapéuticos |
| CN109008910A (zh) * | 2011-06-29 | 2018-12-18 | 拉尼医疗有限公司 | 用于使用可吞服药物递送装置递送到肠道内腔中的治疗药剂制剂 |
| CN105263461B (zh) * | 2013-03-15 | 2019-09-10 | 拉尼医疗有限公司 | 用于治疗化合物的口服递送的装置 |
-
2014
- 2014-03-12 CN CN201480015725.6A patent/CN105263461B/zh active Active
- 2014-03-12 CA CA2901923A patent/CA2901923C/en active Active
- 2014-03-12 WO PCT/US2014/024385 patent/WO2014159604A1/en active Application Filing
- 2014-03-12 ES ES14775797T patent/ES2897795T3/es active Active
- 2014-03-12 EP EP21189226.0A patent/EP3964190A1/en active Pending
- 2014-03-12 PT PT147757975T patent/PT2968071T/pt unknown
- 2014-03-12 PL PL14775797T patent/PL2968071T3/pl unknown
- 2014-03-12 EP EP14775797.5A patent/EP2968071B1/en active Active
- 2014-03-12 JP JP2016501518A patent/JP6796484B2/ja active Active
- 2014-03-12 CA CA3104670A patent/CA3104670A1/en active Pending
- 2014-03-12 AU AU2014240401A patent/AU2014240401B2/en active Active
- 2014-03-12 DK DK14775797.5T patent/DK2968071T3/da active
-
2018
- 2018-12-26 JP JP2018242716A patent/JP2019069206A/ja not_active Withdrawn
-
2019
- 2019-02-13 AU AU2019201008A patent/AU2019201008B2/en active Active
-
2020
- 2020-10-30 JP JP2020182430A patent/JP2021020110A/ja active Pending
-
2021
- 2021-06-08 AU AU2021203778A patent/AU2021203778B2/en active Active
-
2022
- 2022-08-25 JP JP2022133795A patent/JP7434462B2/ja active Active
-
2023
- 2023-08-31 AU AU2023222952A patent/AU2023222952A1/en active Pending
-
2024
- 2024-02-07 JP JP2024017395A patent/JP2024036622A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| EP2968071A4 (en) | 2016-10-05 |
| CA2901923C (en) | 2021-12-07 |
| CN105263461A (zh) | 2016-01-20 |
| JP2021020110A (ja) | 2021-02-18 |
| EP3964190A1 (en) | 2022-03-09 |
| JP2024036622A (ja) | 2024-03-15 |
| EP2968071A1 (en) | 2016-01-20 |
| EP2968071B1 (en) | 2021-08-04 |
| AU2019201008B2 (en) | 2021-03-25 |
| AU2023222952A1 (en) | 2023-09-21 |
| AU2021203778B2 (en) | 2023-06-01 |
| AU2014240401B2 (en) | 2018-11-15 |
| JP2016511124A (ja) | 2016-04-14 |
| AU2014240401A1 (en) | 2015-09-10 |
| PT2968071T (pt) | 2021-11-12 |
| CA3104670A1 (en) | 2014-10-02 |
| ES2897795T3 (es) | 2022-03-02 |
| CN105263461B (zh) | 2019-09-10 |
| AU2019201008A1 (en) | 2019-03-07 |
| CA2901923A1 (en) | 2014-10-02 |
| DK2968071T3 (da) | 2021-11-08 |
| WO2014159604A1 (en) | 2014-10-02 |
| JP7434462B2 (ja) | 2024-02-20 |
| AU2021203778A1 (en) | 2021-07-22 |
| JP2022162094A (ja) | 2022-10-21 |
| PL2968071T3 (pl) | 2021-12-20 |
| JP2019069206A (ja) | 2019-05-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7434462B2 (ja) | 治療化合物の経口送達のためのデバイス | |
| JP6742383B2 (ja) | 治療用化合物の経口送達のためのデバイス、システム、および方法 | |
| US11229684B2 (en) | Therapeutic agent preparations for delivery into a lumen of the intestinal tract using a swallowable drug delivery device | |
| US20210138216A1 (en) | Therapeutic agent preparations for delivery into a lumen of the intestinal tract using a swallowable drug delivery device | |
| US20200289747A1 (en) | Device, system and methods for the oral delivery of therapeutic compounds | |
| US20200306177A1 (en) | Methods for delivering etanercept preparations into a lumen of the intestinal tract using a swallowable drug delivery device | |
| JP2016511124A5 (ja) | ||
| JP2020192342A (ja) | 嚥下可能な薬物送達デバイスを用いる腸管の内腔へ送達するための治療剤製剤 | |
| JP2021112609A (ja) | 嚥下可能薬物送達デバイスおよび薬物送達方法 | |
| CN113543756B (zh) | 使用可吞服药物递送装置递送到肠道内腔的治疗剂制剂 | |
| JP2024074923A (ja) | 治療用化合物の経口送達のためのデバイス |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170308 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20170308 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170619 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20180116 |
|
| A524 | Written submission of copy of amendment under article 19 pct |
Free format text: JAPANESE INTERMEDIATE CODE: A524 Effective date: 20180410 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20180803 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20181102 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20181226 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20190508 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190905 |
|
| C60 | Trial request (containing other claim documents, opposition documents) |
Free format text: JAPANESE INTERMEDIATE CODE: C60 Effective date: 20190905 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20190913 |
|
| C21 | Notice of transfer of a case for reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C21 Effective date: 20190917 |
|
| A912 | Re-examination (zenchi) completed and case transferred to appeal board |
Free format text: JAPANESE INTERMEDIATE CODE: A912 Effective date: 20191004 |
|
| C211 | Notice of termination of reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C211 Effective date: 20191008 |
|
| C22 | Notice of designation (change) of administrative judge |
Free format text: JAPANESE INTERMEDIATE CODE: C22 Effective date: 20200529 |
|
| C22 | Notice of designation (change) of administrative judge |
Free format text: JAPANESE INTERMEDIATE CODE: C22 Effective date: 20200805 |
|
| C23 | Notice of termination of proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C23 Effective date: 20200818 |
|
| C03 | Trial/appeal decision taken |
Free format text: JAPANESE INTERMEDIATE CODE: C03 Effective date: 20200915 |
|
| C30A | Notification sent |
Free format text: JAPANESE INTERMEDIATE CODE: C3012 Effective date: 20200915 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20201015 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20201116 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6796484 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| RD02 | Notification of acceptance of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: R3D02 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: R3D04 |
|
| RD02 | Notification of acceptance of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: R3D02 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |