本発明の種々の実施形態が本明細書で示され、記載されたが、そのような実施形態は例示としてだけ提供されることは当業者に明らかになる。本発明を逸脱しない範囲で、当業者は多くの変形、変化および置換を思いつくことができる。本明細書に記載される本発明の実施形態への様々な代替物を使用することができることを理解すべきである。本発明の異なる態様は個々に、総合的にまたは互いと一緒に評価することができると理解される。
定義
本明細書で使用される場合、「第2高調波」は、基本的な光線の周波数の2倍である光の周波数を指す。
本明細書で使用される場合、「表面選択的」は、非線形光学技術、例えば第2高調波発生または和/差周波発生または当技術分野で公知の他の表面特異的技術を指す。
本明細書で使用される場合、「和周波発生」(SFG)は、1つの周波数(Ω1)の光が別の周波数(Ω2)の光と混合されて和周波数(Ω1+Ω2)の応答を与える、非線形光学技術である(Yang, G、Shen, YR、Optics Letters、9巻(11号):510〜512頁、1984年;Shen, YR、Annual Review of Physical Chemistry 40巻(1号):327〜350頁、1989年)。例えば、SFGは、それらの特徴的振動遷移を通して表面での分子の検出のために特に有益であり、この場合は、本質的に、可視的および赤外線の周波数におけるΩ1およびΩ2についての表面選択的赤外分光分析である。用語「SHG」または「第2高調波発生」が本明細書で使用される場合、SFGおよび「和周波発生」は、SHGの代わりに当業技術者周知の方法を置き換えて使用することができるものと理解される。
「非線形活性部分」は、本明細書で使用される場合、超偏光率を有する物質である。
「第2高調波活性部分」は、本明細書で使用される場合、それを(例えば、より)非線形光学活性にするために、分子(例えば、酵素などのタンパク質)、粒子、細胞または相(例えば、脂質二重層)に付着させるまたは組み入れる(例えば、共有結合または非共有結合で付着させる、遺伝的に組み入れる、等)ことができる、非線形活性部分、粒子または分子を指す。
本明細書で使用される場合、「アロステリック」、「アロステリックモジュレーター」または「アロステリック候補」は、活性部位以外の部位に主に結合し、SHGまたはSFGにより判定するときに(例えば、結合部位に隣接する1つまたは複数の位置および/または結合部位に隣接していない1つまたは複数の位置で)立体配置変化を引き起こすことができ、したがってアロステリック作用機構を通してそれらの効果を発揮することができる、分子、部分または物質を指す。
「活性部位」または「活性結合部位」は、本明細書で使用される場合、その形状および電荷ポテンシャルの結果、様々な共有結合および/または非共有結合力を通して別の薬剤(例えば、リガンド、タンパク質、ポリペプチド、ペプチド、DNAもしくはRNAを含む核酸、分子、化合物、抗生物質または薬物、分子、部分、基質、生成物、類似体または阻害剤)と好都合に相互作用または関連し、タンパク質の機能(例えば、触媒作用、シグナル伝達および/またはエフェクター活性化)が発揮される標的タンパク質の領域を指す。
本明細書に規定する用語「リガンド」は、別の分子に結合する任意の分子、例えば別のものに結合する1つのタンがパク質、タンパク質に結合する炭水化物またはタンパク質に結合する小分子を含む。
本明細書で使用される場合、「非線形」は、入射光線(別名、基本波)の周波数を変換することが可能な光学技術を指す。非線形光線は、そのような変換、例えば第2高調波から生じる光線(例えば、高次周波数光線)である。第2高調波、和周波または差周波発生では、非線形光線は首尾一貫して発生される。第2高調波発生(SHG)では、基本光線の2つの光子が界面によって事実上散乱し、第2高調波の1つの光子を生成する。本明細書では、「非線形光学」または「表面選択的非線形」とも呼ぶ。
本明細書で使用される用語「非線形活性」または「非線形的に活性」は、入射放射光線(複数可)によって推進されるときに非線形光学放射線を発生する、分子、粒子、界面または相の能力の一般特性も指す。
本明細書で非線形の光学的方法に言及するときは、「検出」または「検出すること」は、プローブ−標的相互作用(例えば、タンパク質と候補化合物の間の相互作用)の特性、または相互作用の効果を検出する、測定する、または、非線形の光学的光の特性(例えば、強度、波長、偏光もしくは電磁放射線に共通する他の特性)と相関させるために表面選択的非線形光学的放射の特性を使用することができる技術を指す。
この明細書全体に記載されたあらゆる最大数値限界は、それより低いあらゆる数値限界が本明細書に明示的に記述されたものとして、そのようなより低い数値限界を含むものとする。この明細書全体に記載されたあらゆる最小数値限界は、それより高いあらゆる数値限界が本明細書に明示的に記述されたものとして、そのようなより高い数値限界を含む。この明細書全体に記載されたあらゆる数値範囲は、それより狭いあらゆる数値範囲が本明細書に全て明示的に記述されたものとして、そのようなより広い数値範囲に入るより狭い数値範囲を含む。
序論
本明細書において、標的生化学的実体を標的にする候補生化学的実体および/または結合部分(例えば、候補生化学的実体に関連した結合部分(複数可))、例えばin vivoまたはin vitroの薬理特性に関連した候補生化学的実体および/または結合部分をスクリーニングするための方法が提供される。これらの方法は、表面選択的技術を使用して第2高調波発生(SHG)活性部分、和周波発生(SFG)活性部分または差周波発生(DFG)活性部分(例えば、候補、標的または両方に付着するもの)によって発生するシグナルに基づく。本方法は、標的と異なる候補の間の結合の際に生成される2つまたはそれを超える候補のシグナルを比較するステップを含むことができる。一部の場合には、候補は、同じまたは類似の足場コアを有する生化学的実体(例えば、分子)であってもよい。一部の場合には、生化学的実体は、標的生体分子を標的にする薬物候補(および/またはそれと関連した結合部分(複数可))を含むことができる。
一部の実施形態では、本明細書の方法は、標的生体分子を標的にする薬物候補(および/またはそれと関連した結合部分)、例えばin vivoまたはin vitroの薬理特性に関連した候補または結合部分などをスクリーニングするために使用することができる。一部の場合には、薬物候補は、同じまたは類似の足場コアを有する分子であってもよい。薬物候補(および/またはそれと関連した結合部分)および標的生体分子に関して記載される本開示の任意の態様は、少なくとも一部の配置の任意の型の候補生化学的実体(および/または結合部分)および任意の型の標的生化学的実体に等しく適用することができる。例えば、本開示は細胞に適用することができる。さらに、参照分子に関して記載される本開示の任意の態様は、少なくとも一部の配置の任意の型の参照生化学的実体に等しく適用することができる。
構造類似性は、ある程度機能的類似性につながると一般に考えられている。しかし、構造類似性だけで、特定の機能、特にin vivoの薬理特性と相関するとは限らない。したがって、構造をベースとしたデザインによって作成される薬物候補は、リード化合物を同定するために様々なin vivoまたはin vitroアッセイを使用して広くスクリーニングしなければならない。この過程は冗長で、時間がかかり、高価であり、しばしば無駄であり、現代の薬物発見で主要なボトルネックの1つになっている。
一態様では、本開示は、生化学的実体をスクリーニングする方法であって、(a)複数の候補生化学的実体を含むライブラリーを用意するステップであり、候補生化学的実体は、1つまたは複数の構造類似性パラメータを使用して判定するときに構造的に類似している、ステップと、(b)標的生化学的実体の第1の立体配置状態を測定し、それによってベースラインを作成するステップと、(c)候補生化学的実体の各々を標的生化学的実体と接触させるステップと、(d)標的生化学的実体の第2の立体配置状態を測定するステップと、(e)第2の立体配置状態を使用して標的生化学的実体のシグネチャーを判定するステップと、(f)シグネチャーに基づいて候補生化学的実体から1つまたは複数の生化学的実体を選択するステップとを含む方法を提供する。
別の態様では、本開示は、生化学的実体をスクリーニングする方法であって、(a)複数の候補生化学的実体を含むライブラリーを用意するステップと、(b)標的生化学的実体の第1の立体配置状態を測定し、それによってベースラインを作成するステップと、(c)候補生化学的実体の各々を標的生化学的実体と接触させるステップと、(d)標的生化学的実体の第2の立体配置状態を測定するステップと、(e)第2の立体配置状態を使用して少なくとも第1および第2の候補生化学的実体のシグネチャーを判定するステップと、(f)第1の生化学的実体のシグネチャーを第2の生化学的実体のシグネチャーと比較するステップと、(g)(f)での比較に基づいて、候補生化学的実体から1つまたは複数の生化学的実体を選択するステップとを含む方法を提供する。
さらなる態様では、本開示は、生化学的実体を分類する方法であって、(a)生化学的実体のライブラリーを用意するステップであり、生化学的実体の各々は異なる分子構造を含む、ステップと、(b)ライブラリー中の少なくとも1つの生化学的実体を同じ標的生化学的実体と接触させるステップと、(c)標的生化学的実体の立体配置状態を測定するステップと、(d)立体配置状態を使用してシグネチャーを判定するステップと、(e)シグネチャーを使用して構造−活性関係(SAR)カタログを作成するステップとを含む方法を提供する。
一部の場合には、SARを作成するステップは、シグネチャーを結合特性、機能的特性、効能、力価、選択性またはそれらの組合せと相関させるステップを含むことができる。一部の場合には、SARを作成するステップは、シグネチャーを候補生化学的実体の1つまたは複数の構造パラメータと相関させるステップを含むことができ、前記構造パラメータは以下からなる群から選択される:分子量、化学式、全原子数、炭素原子数、水素原子数、窒素原子数、酸素原子数、硫黄原子数、log Dによって測定される極性、log Pによって測定される極性、PSA(極性表面積)によって測定される極性、足場コア、グラフ理論で測定される化学的類似性、Tanimoto(またはJaccard)係数T、芳香族基数、複素環基数、単環基数、縮合環系数および二重結合数。
本方法は、薬理特性または機能的効果に関連する生化学的実体の少なくとも1つの中の結合部分を判定するために、SARを分析するステップをさらに含むことができる。一部の場合には、接触させるステップの前に標的生化学的実体の立体配置状態を測定し、それによってベースラインを作成することができる。
ライブラリーは、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、22、24、26、28、30、35、40、45、50、60、70、80、90、100、120、140、160、180、200、250、300、350、400、450、500、600、700、800、900、1000、1200、1400、1600、1800、2000、2500、3000、3500、4000、4500、5000、6000、7000、8000、9000または1000、またはそれを超える候補生化学的実体を含むことができる。一部の例では、ライブラリーは6つまたはそれを超える候補生化学的実体を含むことができる。さらなる例では、ライブラリーは20つまたはそれを超える候補生化学的実体を含むことができる。さらに、生化学的実体のライブラリーは、薬物候補を含むことができる。
候補生化学的実体は、1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20またはそれを超える数の構造類似性パラメータを使用して判定したときに、構造的に類似していてもよい。一部の例では、候補生化学的実体は、3つまたはそれを超える数の構造類似性パラメータを使用して判定したときに構造的に類似していてもよい。さらなる例では、候補生化学的実体は、5つまたはそれを超える数の構造類似性パラメータを使用して判定したときに構造的に類似していてもよい。構造類似性パラメータの例には、これらに限定されないが、
(i)候補生化学的実体の各々の10、20、30、40、50、60、70、80、90、100、110、120、130、140、150、160、170、180、190、200、210、220、230、240、250、260、270、280、290、300g/mol以内の分子量、
(ii)候補生化学的実体の各々の1%、2%、3%、4%、5%、6%、7%、8%、9%、10%、11%、12%、13%、14%、15%、16%、17%、18%、19%、20%、22%、24%、26%、28%、30%、35%、40%、45%または50%以内の分子量、
(iii)候補生化学的実体の各々の原子数が1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、22、24、26、28、30、35、40、45、50、60、70、80、90、100、120、140、160、180、200、250、300、350、400、450、500、600、700、800、900または1000個以内の化学式、
(iv)候補生化学的実体の各々の間の1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、22、24、26、28、30、35、40、45、50、60、70、80、90、100、120、140、160、180、200、250、300、350、400、450、500、600、700、800、900または1000未満の全原子数の差、
(v)1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19または20未満の炭素原子数の差、
(vi)1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19または20未満の水素原子数の差、
(vii)1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19または20未満の窒素原子数の差、
(viii)1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19または20未満の酸素原子数の差、
(ix)1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19または20未満の硫黄原子数の差、
(x)候補生化学的実体の各々の1%、2%、3%、4%、5%、6%、7%、8%、9%、10%、11%、12%、13%、14%、15%、16%、17%、18%、19%、20%、22%、24%、26%、28%、30%、35%、40%、45%または50%以内のlog Dで測定される極性、
(xi)候補生化学的実体の各々の1%、2%、3%、4%、5%、6%、7%、8%、9%、10%、11%、12%、13%、14%、15%、16%、17%、18%、19%、20%、22%、24%、26%、28%、30%、35%、40%、45%または50%以内のlog P(分配係数)で測定される極性、
(xii)候補生化学的実体の各々の1%、2%、3%、4%、5%、6%、7%、8%、9%、10%、11%、12%、13%、14%、15%、16%、17%、18%、19%、20%、22%、24%、26%、28%、30%、35%、40%、45%または50%以内のPSA(極性表面積)で測定される極性、
(xiii)同一の足場コア、
(xiv)グラフ理論で測定される化学的類似性、
(xv)0.5、0.6、0.7、0.75、0.8、0.81、0.82、0.83、0.84、0.85、0.86、0.87、0.88、0.89、0.9、0.91、0.92、0.93、0.94、0.95、0.96、0.97、0.98または0.99を超えるTanimoto(またはJaccard)係数T、
(xvi)1、2、3、4、5、6、7、8、9または10未満の芳香族基数の差、
(xvii)1、2、3、4、5、6、7、8、9または10未満の複素環基数の差、
(xviii)1、2、3、4、5、6、7、8、9または10未満の単環基数の差、
(xix)1、2、3、4、5、6、7、8、9または10未満の縮合環系数の差、
および(xx)1、2、3、4、5、6、7、8、9または10未満の二重結合数の差
が含まれる。
一部の場合には、標的生化学的実体は、天然変性タンパク質(intrinsically disordered protein)であってもよい。例えば、天然変性タンパク質は、アルファシヌクレインであってもよい。一部の場合には、標的生化学的実体は、薬物標的であってもよい。一部の場合には、標的生化学的実体は、公知の立体配置モジュレーターを有さないこともある。
一部の場合には、標的生化学的実体を薬剤とインキュベートした後に第1の立体配置状態を測定することができる。例えば、薬剤は、ライブラリーからの候補生化学的実体であってもよい。
一部の場合には、立体配置状態(複数可)は、内部全反射(TIR)を使用して測定することができる。一部の場合には、立体配置状態(複数可)は、第2高調波発生(SHG)を使用して測定することができる。
一部の場合には、シグネチャーを判定するステップは、標的生化学的実体の立体配置状態の動態学的(リアルタイム)変化を測定するステップを含むことができる。他の場合には、シグネチャーを判定するステップは、標的生化学的実体の立体配置状態のエンドポイント変化を測定するステップを含むことができる。さらに他の場合には、シグネチャーを判定するステップは、シグネチャーのシグナル強度を測定するステップを含むことができる。さらなる場合には、シグネチャーの判定は、ベースラインを使用することができる。さらに、シグネチャーは、標的生化学的実体の立体配置状態の変化を示すことができる。
一部の場合には、候補生化学的実体は、コンピュータ実行可能プログラムを使用して、1つまたは複数の構造類似性パラメータに基づいて分析することができる。他の場合には、シグネチャーは、コンピュータ実行可能プログラムを使用して分析することができる。
候補生化学的実体の各々は、標的生化学的実体の立体配置状態において異なる変化を生成することができる。さらに、候補生化学的実体の各々は異なるシグネチャーを発生することができる。
一部の場合には、標的生化学的実体の立体配置状態の変化を、公知の立体配置モジュレーターによって生成される立体配置状態の変化とさらに比較することができる。一部の場合には、公知の立体配置モジュレーターは、公知の薬物であってもよい。一部の場合には、生化学的実体は、公知の立体配置モジュレーターによって誘導される立体配置状態の変化に最も類似している立体配置状態の変化に基づいて選択することができる。さらに、公知の立体配置モジュレーターによって生成される立体配置状態の変化は、薬理特性または機能的効果に相関する可能性がある。
一部の場合には、生化学的実体の1つもしくは複数のシグネチャーまたはSARカタログは、公知の薬理特性または公知の機能的効果と相関することができる。1つまたは複数の生化学的実体は、公知の薬理特性または公知の機能的効果とのシグネチャーまたはSARカタログの相関に基づいてさらに選択することができる。
一部の場合には、候補生化学的実体の少なくとも2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、22、24、26、28、30、35、40、45、50、60、70、80、90または100個は、類似の薬理特性または機能的効果を有する。他の場合には、候補生化学的実体の少なくとも2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、22、24、26、28、30、35、40、45、50、60、70、80、90または100個は、類似の薬理特性または機能的効果を有さない。
本開示で提供される方法は、シグネチャーパラメータを測定するステップをさらに含むことができる。シグネチャーパラメータの例には、これらに限定されないが、
i)ベースラインと比較したシグネチャーの大きさの変化、
ii)ベースラインと比較したシグネチャーの方向の変化、および
iii)候補生化学的実体の接触の際のシグネチャーの単位時間あたりのシグナルの速度の変化
が含まれる。
一部の場合には、1、2、3またはそれを超える数のシグネチャー類似性パラメータを使用して判定したときに、第1の候補生化学的実体によって発生されるシグネチャーおよび第2の候補生化学的実体によって発生されるシグネチャーは類似してもよい。シグネチャー類似性パラメータの例には、これらに限定されないが、
i)第1の候補生化学的実体と接触する際のベースラインと比較したシグネチャーの大きさの変化は、第2の候補生化学的実体と接触する際のベースラインと比較したシグネチャーの大きさの変化の1%、2%、3%、4%、5%、6%、7%、8%、9%、10%、11%、12%、13%、14%、15%、16%、17%、18%、19%、20%、22%、24%、26%、28%、30%、35%、40%、45%または50%以内であること、
ii)第1の候補生化学的実体と接触する際のベースラインと比較したシグネチャーの方向の変化は、第2の候補生化学的実体と接触する際のベースラインと比較したシグネチャーの方向の変化と同じであること、および
iii)第1の候補生化学的実体と接触する際のシグネチャーの単位時間あたりのシグナルの速度の変化は、第2の候補生化学的実体と接触する際のシグネチャーの単位時間あたりのシグナルの速度の変化の1%、2%、3%、4%、5%、6%、7%、8%、9%、10%、11%、12%、13%、14%、15%、16%、17%、18%、19%、20%、22%、24%、26%、28%、30%、35%、40%、45%、50%、60%、70%、80%、90%、100%(1倍)、110%、120%、130%、140%、150%、160%、170%、180%、190%または200%(2倍)以内であること
が含まれる。
下の例で詳述されるように、本発明は、候補によって発生されるSHGシグナル(またはSFGシグナル、DFGシグナル)をそのin vivoまたはin vitroの薬理特性、特にそのin vivo特性と相関させる方法を提供する。したがって、本発明は、1つまたは複数の所望のin vivoもしくはin vitroの薬理特性を有する薬物候補について効率的にスクリーニングする方法を提供し、あらゆる候補についての高価なin vivoまたはin vitroアッセイを不必要にする。
I.標的分子を標的にする薬物候補をスクリーニングする方法
本明細書において、標的生体分子を標的にする薬物候補をスクリーニングする方法が提供される。本方法は、任意の薬物候補、例えば標的生体分子中の結合部位を標的にする同じまたは類似の足場コアを有する薬物候補などをスクリーニングするのに有益である。
A.同じまたは類似の足場を有する薬物候補
小分子薬物との関連で、「足場」は、1つまたは複数の追加の化学部分を共有結合させる、改変するまたは削除して、共通の構造要素を有する複数の分子を形成することができる小さい標的結合分子を指す場合がある。例示的な部分には、ハロゲン原子、ヒドロキシル基、メチル基、ニトロ基、カルボキシル基または任意の他の型の分子群が含まれる。足場の特徴には、例えば、足場の上の1つまたは複数の置換基が標的分子結合部位中の結合ポケットに位置するように標的分子結合部位に結合すること;コンビナトリアルライブラリーを容易に構築できるように、特に合成反応によって化学改変することができる化学的に扱いやすい構造を有すること;追加の望ましい特徴、例えば、リガンドが細胞および/または特異的器官に活発に輸送されることを可能にする、または追加の分析のためにリガンドがクロマトグラフィーカラムに付着されることを可能にすることを達成するために、足場またはライブラリーメンバーを改変してリガンドを形成することができるように、タンパク質結合部位への足場の結合に干渉しない部分を付着させることができる化学的位置を有することが含まれてもよい。したがって、分子足場は、in vivoまたはin vitroの薬理特性(例えば、結合親和性および/または特異性)を向上させる改変より前の小さな同定された標的結合分子であってもよい。
小分子薬物との関連で、「足場コア」は、様々な置換基を付着させることができる分子足場のコア構造を指す場合がある。したがって、特定の化学クラスのいくつかの足場分子について、足場コアは全ての足場分子に共通である。多くの場合には、足場コアは、1つまたは複数の環構造からなるまたはそれを含むことができる。足場群は、足場コアを共有し、したがって全て1つの足場分子の誘導体とみなすことができる化合物のセットを指す。
生物学的製剤との関連で、「足場」は、生物学的薬物が別の分子(例えば、タンパク質、DNA、RNA、金属、ペプチド、多糖)と相互作用することを可能にするアミノ酸残基またはヌクレオチドのセット(例えば、最小限のセット)を指す場合がある。例えば、足場は、モチーフに固有の特異的幾何学形状を有するアミノ酸残基またはヌクレオチドを含むことができる。この幾何学形状は、アミノ酸残基間の距離、アミノ酸残基間の角度およびアミノ酸残基の配向を包含する。
生物学的製剤との関連で、「足場コア」は、全ての足場分子に共通するコンセンサスアミノ酸残基またはヌクレオチドのセットを指す場合がある。突然変異などの置換、欠失、挿入が足場コアに加えられてもよい。したがって、特定の生物学的製剤クラスのいくつかの足場分子について、足場コアは全ての足場分子に共通である。足場群は、足場コアを共有し、したがって全て1つの足場分子の誘導体とみなすことができる生物学的製剤のセットを指す。足場群の中の生物学的製剤分子は、20%、30%、40%、50%、60%、70%、80%、85%、90%、95%、98%、99%またはそれを超える配列相同性を共有することができる。
足場または足場コアは、標的生体分子中の結合部位を標的にすることができる。結合部位は、活性結合部位またはアロステリック結合部位であってもよい。一般的に言うと、結合部位は、リガンドが結合することができる(共有結合または非共有結合で)標的分子のエリアである。結合部位は特定の形状を組み入れ、1つまたは複数の結合ポケットを含有することができる。特定の形状は、標的生体分子のクラス内で、例えば分子ファミリー内でしばしば保存される。クラス内の結合部位は、保存された構造、例えば部分、結合ポケットの存在および/または結合部位もしくは結合部位の一部分での静電荷を含有することができ、その全ては結合部位の形状に影響することができる。結合ポケットは、結合部位中の特定の容積を指す。結合ポケットは、標的分子の原子に少なくとも部分的に囲まれている、結合部位中の特定の空間である。したがって、結合ポケットは、結合部位中の特定の形状、窪みまたは空洞である。結合ポケットは、別の分子の非共有結合で重要である特定の化学基または構造、例えば、分子間のイオン、水素結合、ファンデルワールスまたは疎水性の相互作用に寄与する基を含有することができる。
本明細書で提供される方法は、小分子および生物学的製剤(例えば、タンパク質、ペプチド、核酸、抗体)を含む任意の薬物候補をスクリーニングするために使用することができる。例えば、本方法は、アルファシヌクレインを標的にする小分子または抗体薬物のスクリーニングのために有益である。一部の方法では、リード化合物またはリード生物学的製剤が同定される。リード化合物またはリード生物学的製剤に基づいて、一連の候補化合物または生物学的製剤を設計および選択することができる。例えば、候補化合物または生物学的製剤を作成するために、コンピュータモデリング方法を使用することができる。
一部の場合には、候補化合物または生物学的製剤は、コンピュータによって作成された標的生体分子の結合ポケットにドッキングすることができる。一部のコンピュータモデリング方法では、標的生体分子の公知のリード化合物または生物学的製剤の実験的に判定された性質、例えば、標的生体分子−アゴニストまたは標的生体分子−アンタゴニスト共結晶の結晶構造に候補を重ね合わせることができる。候補および標的生体分子(またはそのセグメント)の構造適合度、および相互作用のエネルギーを予測するために、分子最適化技術を使用することができる。構造適合度は、結合ポケットの環境内で候補小分子がどれくらい空間を物理的に占めることができるかを決定する。この目的のために様々な方法で標的生体分子(および候補)の表面輪郭を構築することができる。例えば、表面を構築するために原子のファンデルワールス半径が使用される。相互作用のエネルギーは、非経験的方法(密度関数理論方法など)によって、または実験的方法(分子力学方法など)によって計算することができる。相互作用のエネルギーは、上記の方法の混成によって計算することもできる。分子最適化技術は分子屈曲性も可能にし、それは結合長、結合角度および結合ねじれの変化を可能にすることを示す。
標的生体分子(または標的生体分子の適当な一部)の構造情報は、X線結晶学によって直接的に、相同性モデリングによって間接的に、またはその組合せによって得ることができる。相同性モデリングは、標的生体分子の一部だけの構造を得るために実施してもよい。これは、鋳型として公知の構造の1つの類似部分を使用して一般的に達成される。この目的のために様々な方法およびソフトウェアを使用することができる。例えば、SWISS−MODEL:自動化されたタンパク質相同性モデリングサーバー(Schwede, T.、Kopp, J.、Guex, N.、Peitsch, M.、Nucleic Acids Research(2003年)31巻(13号):3381〜3385頁)に記載される方法およびソフトウェアを使用することができる。米国特許第7,384,773号およびその中の参考文献によって教示されるソフトウェアおよび方法をモデリングのために使用することもできる。
機械読取り可能データを処理するために、いくつかのプログラムを使用することができる。例えば、コンピュータプログラムDOCKおよびその変形が広く使用されている(Lorber, D.およびShoichet, B.、Protein Science、7巻:938〜950頁、1998年)。他の例示的なプログラムには、Autodock(Scripps Research Institute、La Jolla、Calif.)、QUANTA(Molecular Simulations、San Diego、Calif.)、Insight(Molecular Simulations、San Diego、Calif.)、SYBYL(TRIPOS,Inc.、St.Louis、Mo.)およびLEAPFROG(TRIPOS,Inc.、St.Louis、Mo.)が含まれる。
「ライブラリー」は、本開示の方法で使用する一群の生化学的実体(例えば候補生化学的実体)を指す場合がある。例えば、生化学的実体のライブラリーは、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、22、24、26、28、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、110、120、130、140、150、160、170、180、190、200、220、240、260、280、300、350、400、450、500、550、600、650、700、750、800、850、900、950、1000、1100、1200、1300、1400、1500、1600、1700、1800、1900、2000、2200、2400、2600、2800、3000、3200、3400、3600、3800、4000、4500、5000、6000、7000、8000、9000または10000、またはそれを超える数の生化学的実体を含むことができる。
生化学的実体は、構造的に類似していてもよい。これらに限定されないが、分子量;化学式;全原子数;特定の原子(例えば炭素、水素、窒素、酸素および/もしくは硫黄)の数;極性;足場コア;グラフ理論で測定される化学的安定性;Tanimoto(もしくはJaccard)係数T;芳香族基、複素環基、単環基および/もしくは縮合環系の数;または二重結合数を含む1つまたは複数の構造類似性パラメータに基づいて、2つまたはそれを超える生化学的実体を構造的に類似していると判定することができる。例えば、2つまたはそれを超える生化学的実体の分子量が互いに10、20、30、40、50、60、70、80、90、100、110、120、130、140、150、160、170、180、190、200、210、220、230、240、250、260、270、280、290、300、310、320、330、340、350、360、370、380、390、400、410、420、430、440、450、460、470、480、490、500、600、700、800、900または1000g/mol以内であるならば、2つまたはそれを超える生化学的実体は構造的に類似していると判定することができる。あるいは、2つまたはそれを超える生化学的実体の分子量が互いに5%、10%、15%、20%、25%、30%、35%、40%、45%または50%以内にあるならば、2つまたはそれを超える生化学的実体は構造的に類似していると判定することができる。一部の場合には、2つまたはそれを超える生化学的実体の各々の化学式の原子数が互いに1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29または30個以内にあるならば、2つまたはそれを超える生化学的実体は構造的に類似していると判定することができる。一部の場合には、2つまたはそれを超える生化学的実体の各々の間の全原子数の差が1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29または30未満であるならば、2つまたはそれを超える生化学的実体は構造的に類似していると判定することができる。さらなる場合には、2つまたはそれを超える生化学的実体の各々の間の1つまたは複数の特定の原子(例えば、炭素、水素、窒素、酸素および/または硫黄原子)の数の差が1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19または20未満であるならば、2つまたはそれを超える生化学的実体は構造的に類似していると判定することができる。例えば、炭素原子数の差が5未満であり、および/または酸素原子数の差が3未満であるならば、2つまたはそれを超える生化学的実体は構造的に類似していると判定することができる。一部の場合には、2つまたはそれを超える生化学的実体の極性[例えば、log D、log P(分配係数)またはPSA(極性表面積)によって測定したときに]が互いに1%、2%、3%、4%、5%、6%、7%、8%、9%、10%、12%、12%、14%、16%、18%、20%、25%、30%、35%、40%、45%または50%以内にあるならば、2つまたはそれを超える生化学的実体は構造的に類似していると判定することができる。一部の場合には、2つまたはそれを超える生化学的実体が同じ足場コア(上で規定される)を有するならば、2つまたはそれを超える生化学的実体は構造的に類似していると判定することができる。他の場合には、2つまたはそれを超える生化学的実体がグラフ理論で測定したときに化学的類似性を示すならば、2つまたはそれを超える生化学的実体は構造的に類似していると判定することができる。さらなる場合には、2つまたはそれを超える生化学的実体が0.50、0.55、0.60、0.65、0.70、0.75、0.80、0.81、0.82、0.83、0.84、0.85、0.86、0.87、0.88、0.89、0.90、0.91、0.92、0.93、0.94、0.95、0.96、0.97、0.98または0.99を超えるTanimoto(またはJaccard)係数Tを示すならば、2つまたはそれを超える生化学的実体は構造的に類似していると判定することができる。一部の場合には、2つまたはそれを超える生化学的実体の各々において芳香族基、複素環基、単環基および/または縮合環系の数の差が1、2、3、4、5、6、7、8、9または10未満であるならば、2つまたはそれを超える生化学的実体は構造的に類似していると判定することができる。一部の場合には、2つまたはそれを超える生化学的実体の各々において二重結合の数の差が1、2、3、4、5、6、7、8、9または10未満であるならば、2つまたはそれを超える生化学的実体は構造的に類似していると判定することができる。
さらに、2つまたはそれを超える生化学的実体は、化学分析ソフトウェアによって判定することができる。化学分析ソフトウェアの例には、限定されずにSpinitex、ToxmatchおよびSimfinderが含まれる。
B.薬物候補の選択
薬物候補、例えば同じまたは類似の足場コアを有する薬物候補は、開示の方法を使用してスクリーニングすることができる。これらの方法は、表面選択的技術を用いてSHG部分、SFG部分またはDFG部分(例えば、候補、標的または両方に付着するもの)によって発生されるシグナルに基づく。シグナルは、標的と候補分子の間の結合の際に生成され、検出される。
驚くべきことに本発明において、同じまたは類似の足場を共有する異なる薬物候補の間の構造類似性にもかかわらず、これらの薬物候補が様々な程度の差を有するシグナルを発生することができることが発見された。一部の場合には、下の例で詳述されるように、2つの構造的に緊密に関連している候補は全く異なるシグナルを発生することができ、2つの構造的に異なる分子は非常に類似しているシグナルを生成することができる。より驚くべきことに、本発明において、検出されたシグナル差がin vivoまたはin vitroの薬理特性の差に相関することが発見された。したがって、本発明の方法は、1つまたは複数の所望のin vivoもしくはin vitroの薬理特性を有する化合物および生物学的製剤をスクリーニングするのに使用することができる。薬物候補は、本発明の様々な実施形態に従ってスクリーニングすることができる。
1.直接比較
一部の例では、2つまたはそれを超える分子から発生されるシグナルは、互いと比較される。化学的ライブラリーからの薬物候補または、例えば本明細書に記載されるコンピュータモデリング方法から作成され、選択される薬物候補の間で比較することができる。薬物候補と参照分子の間で比較することもできる。参照分子は、公知の薬物、またはリード化合物、またはさもなければin vivoもしくはin vitroの薬理特性(例えば、所望の特性)に関連する分子であってもよい。参照分子および薬物候補は、標的生体分子中の結合部位を標的にする同じまたは類似の足場コアを有することができる。
一部の方法では、標的生体分子は、2つまたはそれを超える候補、例えば、標的生体分子中の結合部位を標的にする同じまたは類似の足場コアを有する2つの候補と並行して接触させる。シグナルは、標的生体分子と各候補の間の結合の際に生成される。異なる候補によって生成されるシグナルを数量化し、互いと比較する。異なる候補によって生成されるシグナルの間の差が生じ得る。差は、正の差または負の差であってもよい。一部の場合には、正の差は、in vivoまたはin vitroの薬理特性の向上と相関する。一部の場合には、正の差は、in vivoまたはin vitroの薬理特性の低減と相関する。他の場合には、負の差は、in vivoまたはin vitroの薬理特性の向上と相関する。一部の他の場合には、負の差は、in vivoまたはin vitroの薬理特性の低減と相関する。
差は、in vivoまたはin vitroの薬理特性の差を示すので、この差に基づいて薬物候補を選択することができる。例えば、正の差がin vivoまたはin vitroの薬理特性の向上と相関する場合は、より高いシグナルを有する候補が選択される。負の差がin vivoまたはin vitroの薬理特性の向上と相関する場合は、より低いシグナルを有する候補が選択される。
同様に、薬物候補は、異なる薬物候補によって発生されるシグナルを単にランク付けすることによって選択することができる。シグナルの増加がin vivoまたはin vitroの薬理特性の向上と相関する場合は、より高いシグナルを有する候補が選択される。シグナルの減少がin vivoまたはin vitroの薬理特性の向上と相関する場合は、より低いシグナルを有する候補が選択される。
異なる候補および参照分子のシグナルは、濃度で正規化することができる。一部の方法では、ノイズレベルを1%、5%、10%、20%、30%、40%、50%、100%、200%、300%、400%、500%またはそれを超えて上回るシグナル差は、in vivoまたはin vitroの薬理特性の差を示す。
2.候補分子とのプレインキュベーション
一部の例では、薬物候補および参照分子からのシグナルは、間接的に比較される。参照分子は、公知の薬物、またはリード化合物、またはさもなければin vivoもしくはin vitroの薬理特性(例えば、所望の特性)に関連する分子であってもよい。参照分子は、候補分子と同じ結合部位を標的にすることができる。参照分子および薬物候補は、標的生体分子中の結合部位を標的にする同じまたは類似の足場コアを有することができる。
具体的には、標的生体分子は、薬物候補と最初に接触させて、標的生体分子と候補分子との結合複合体を形成する。次に、結合複合体を参照分子と接触させる。下の例で詳述されるように、結合複合体を参照分子と接触させる際に生成されるシグナルは、その分子のin vivoまたはin vitroの薬理特性と相関する。参照分子と比較して候補分子が低減したin vivoまたはin vitroの薬理特性を有するならば、シグナルは結合複合体を参照分子と接触させる際に検出することができる。参照分子と比較して候補分子が増加したin vivoまたはin vitroの薬理特性を有するならば、シグナルを検出できないまたはわずかなシグナルだけを検出することができる。したがって、この相関に基づいて候補分子をスクリーニングし、選択することができ、すなわち、シグナルなしまたは小さいシグナルは、参照分子と比較して増加したまたは少なくとも同等のin vivoもしくはin vitroの薬理特性を示す。
異なる候補および参照分子のシグナルは、濃度で正規化することができる。シグナルは、正のシグナルまたは負のシグナルであってもよい。一部の方法では、ノイズレベルを1%、5%、10%、20%、30%、40%、50%、100%または200%以下で上回るシグナルは、参照分子と比較して増加したまたは少なくとも同等のin vivoもしくはin vitroの薬理特性を示す。一部の例では、参照分子と比較して増加したまたは少なくとも同等のin vivoもしくはin vitroの薬理特性を有する候補を選択または同定するためのカットオフ値として、1%、5%または10%以下のシグナルが使用される。
3.参照分子とのプレインキュベーション
一部の例では、薬物候補および参照分子からのシグナルは、間接的に比較される。参照分子は、公知の薬物、またはリード化合物、またはさもなければin vivoもしくはin vitroの薬理特性(例えば、所望の特性)に関連する分子であってもよい。参照分子は、候補分子と同じ結合部位を標的にすることができる。参照分子および薬物候補は、標的生体分子中の結合部位を標的にする同じまたは類似の足場コアを有することができる。
具体的には、標的生体分子は、参照候補と最初に接触させて、標的生体分子と参照分子との結合複合体を形成する。次に、結合複合体を候補分子と接触させる。参照分子と比較して候補分子が低減したin vivoまたはin vitroの薬理特性を有するならば、シグナルを検出できないまたはわずかなシグナルだけを検出することができる。参照分子と比較して候補分子が増加したin vivoまたはin vitroの薬理特性を有するならば、シグナルは結合複合体を参照分子と接触させる際に検出することができる。したがって、この相関に基づいて候補分子をスクリーニングし、選択することができ、すなわち、シグナルは、参照分子と比較して増加したまたは少なくとも同等のin vivoもしくはin vitroの薬理特性を示す。
異なる候補および参照分子のシグナルは、濃度で正規化することができる。シグナルは、正のシグナルまたは負のシグナルであってもよい。一部の方法では、ノイズレベルを1%、5%、10%、20%、30%、40%、50%、100%または200%を超えて上回るシグナルは、参照分子と比較して増加したまたは少なくとも同等のin vivoもしくはin vitroの薬理特性を示す。一部の例では、参照分子と比較して増加したまたは少なくとも同等のin vivoもしくはin vitroの薬理特性を有する候補を選択または同定するためのカットオフ値として、1%、5%または10%を超えるシグナルが使用される。
A.他のアッセイ
本明細書に記載される方法を使用して所望の特性を有する薬物候補が同定されると、1つまたは複数のin vivoもしくはin vitroアッセイによってその特性を確認することができる。
in vitroアッセイには、限定されずに、結晶学、核磁気共鳴スペクトル法、質量分析および細胞アッセイが含まれてもよい。細胞アッセイの一般原理は当技術分野で周知であり、薬物候補が細胞に(例えば、エレクトロポレーション、受動拡散、マイクロインジェクションなどによって)送達され、測定される特定の薬物候補の活性によって影響を受けることが知られている細胞表現型の変化などの活性エンドポイントが測定される方法を含む。
in vivoアッセイは、動物モデル(例えば、完全な動物または動物器官)で薬物候補をスクリーニングすることを含む。したがって、特定の活性に関連する表現型の検出可能な変化を引き起こすそれらの能力について、薬物候補を細胞モデルまたは動物モデルでさらに試験することができる。細胞培養に加えて、動物モデルで疾患を処置するその能力について薬物候補を試験するために動物モデルを使用することができる。
B.in vivoまたはin vitroの薬理特性
上記のように、in vivoまたはin vitroの薬理特性を判定するために、検出されたシグナルまたはシグナルの差を使用することができる。一部の場合には、薬理特性は、薬物動態特性を含むことができる。本明細書に記載される方法を使用してスクリーニングすることができる関連するin vitroの薬理特性には、限定されずに、結合親和性、結合特異性および結合力が含まれる。本明細書に記載される方法を使用してスクリーニングすることができる関連するin vivoの薬理特性には、限定されずに、治療的効能、薬物動態特性、前臨床毒性特性、臨床効能特性、臨床毒性特性および臨床安全性特性が含まれる。
検出されたシグナルまたはシグナルの差は、機能的効果を判定するために使用することができる。例えば、検出されたシグナルまたはシグナルの差は、機能的表現型(例えば、in vivo)、作用機構(例えば、in vivoもしくはin vitro)またはその組合せと相関することができる。一部の例では、検出されたシグナルの差は、薬物候補によって生成されるシグナルと公知の薬物によって生成されるシグナルとの比較から生じることができ、ここで、薬物候補の機能的効果(例えば機能的表現型、作用機構)は、検出されたシグナル(例えばSHGシグネチャー、SFGシグネチャーまたはDFGシグネチャーと公知の薬物のそれとの類似性に基づいて判定することができる。一部の場合には、in vitroおよび/またはin vivoの薬理特性は機能的効果と関連または関係することができ、逆もまた同じである。例えば、治療的効能、結合親和性または任意の他のin vitroもしくはin vivoの薬理特性は、本明細書に記載される方法を使用して判定される作用機構に関連することができる。したがって、in vitroまたはin vivoの薬理特性のスクリーニングに関して記載される本開示の任意の態様は、少なくとも一部の配置でのin vitroまたはin vivoの機能的表現型および/もしくは作用機構のスクリーニングに等しく適用することができる。
治療的効能は、対象(例えば、ヒト、動物)での薬物または候補薬物の治療効果を指す。治療的効能は、薬物または候補薬物の、(a)疾患状態もしくは病態の発症の可能性を低減するかもしくはそれらの発症を遅延させることによって疾患状態もしくは病態の発生を阻止する能力、または(b)疾患状態もしくは病態に伴う臨床症状の一部もしくは全部を低減もしくは排除する能力である。
関連する薬物動態特性には、生物学的利用能(すなわち、インタクトな薬物として全身循環に到達する用量の割合)、未結合割合(すなわち、薬物が血漿または血液中で結合する程度;[未結合薬物濃度]/[全薬物濃度])、薬物代謝酵素によって代謝される薬物の割合、血漿薬物濃度−時間曲線下の全面積、および単位時間あたりの薬物が除去された血液の量が含まれる。
関連する前臨床毒性特性には、50%治療用量(TD50;試験動物の50%が所望の治療転帰を達成する医薬品の用量)、50%致死量(LD50;試験動物の50%が死亡する医薬品の用量)および治療指数(LD50/TD50の比;薬物固有の毒性の尺度)が含まれる。
関連する臨床効能特性には、1つの所望の結果に到達するために処置する必要がある患者数および確率比(対照の間で所望の結果に到達しない確率と比較した処置症例の間で所望の結果に到達する確率)が含まれる。
関連する臨床毒性特性には、1つの毒性結果を有するために処置する必要がある患者数および確率比(対照の間で薬物毒性に到達しない確率と比較した処置症例の間で薬物毒性に到達する確率)が含まれる。
一部の場合には、検出されたシグナルまたはシグナル差は、in vitroだけでなくin vivoの薬理特性とも相関する。一部の場合には、検出されたシグナルまたはシグナル差はin vivoの薬理特性と相関するが、in vitroの薬理特性と相関しない。一部の場合には、検出されたシグナルまたはシグナル差はin vitroの薬理特性と相関するが、in vivoの薬理特性と相関しない。
一部の場合には、検出されたシグナルまたはシグナル差は、複数のin vivoまたはin vitroの薬理特性と相関する。例えば、一部の場合には、検出されたシグナルまたはシグナル差は、結合親和性だけでなく他の特性、例えば治療的効能、薬物動態特性、前臨床毒性、臨床効能または臨床毒性とも相関する。
一部の場合には、検出されたシグナルまたはシグナル差は、一部のin vivoまたはin vitroの薬理特性の差と相関するが、他のin vivoまたはin vitroの薬理特性の差と相関しない。例えば、一部の場合には、検出されたシグナルまたはシグナル差は治療的効能、薬物動態特性、前臨床毒性、臨床効能または臨床毒性と相関するが、結合親和性、結合特異性または結合力と相関しない。
II.標的生体分子のための結合部分を同定する方法
本明細書において、標的生体分子のための結合部分、例えばin vivoまたはin vitroの薬理特性と関連する結合部分を同定する方法が提供される。これらの方法は、表面選択的技術を使用してSHG活性部分、SFG活性部分またはDFG活性部分(例えば、候補または標的に付着するもの)によって発生されるシグナルに基づく。一般的に、本方法は、2つまたはそれを超える候補、例えば同じまたは類似の足場コアを有する候補などの構造を比較するステップを含む。同定は、標的および異なる候補の間の結合の際に生成および検出されるシグナルの間のシグナル差に基づく。
上述のように、驚くべきことに、シグナル差がin vivoまたはin vitroの薬理特性の差と相関することが発見された。したがって、本明細書に記載される方法を使用して同定された結合部分は、単に追加の結合部分であるだけでない。むしろ、同定された結合部分は、候補の1つまたは複数の所望のin vivoもしくはin vitroの薬理特性を増強する機能的に関連する部分である。
一部の場合には、同定された結合部分は、in vitroだけでなくin vivoの薬理特性とも相関する。一部の場合には、同定された結合部分はin vivoの薬理特性と相関するが、in vitroの薬理特性と相関しない。一部の場合には、同定された結合部分はin vitroの薬理特性と相関するが、in vivoの薬理特性と相関しない。
一部の場合には、同定された結合部分は、複数のin vivoまたはin vitroの薬理特性と相関する。例えば、一部の場合には、同定された結合部分は、結合親和性だけでなく他の特性、例えば治療的効能、薬物動態特性、前臨床毒性、臨床効能または臨床毒性とも相関する。
一部の場合には、同定された結合部分は、一部のin vivoまたはin vitroの薬理特性の差と相関するが、他のin vivoまたはin vitroの薬理特性の差と相関しない。例えば、一部の場合には、同定された結合部分は治療的効能、薬物動態特性、前臨床毒性、臨床効能または臨床毒性と相関するが、結合親和性、結合特異性または結合力と相関しない。
分子間のシグナル差は、標的生体分子を標的にする薬物候補のスクリーニングのための方法と共に上記の様々な方法に従って測定することができる。例えば、分子間のシグナル差は、2つまたはそれを超える分子から発生されるシグナルを直接的に比較することによって(セクションI.B.1)、標的生体分子および候補分子の結合複合体を参照分子と接触させる際にシグナルを検出することによって(セクションI.B.2)、または標的生体分子および候補分子の結合複合体を候補分子と接触させる際にシグナルを検出することによって(セクションI.B.3)測定することができる。
III.構造−活性関係を判定する方法および/または生化学的実体を分類する方法
本明細書において、構造−活性関係を判定する方法および/または候補生化学的実体もしくはその足場を分類する方法が提供される。構造−活性関係は、例えば、候補生化学的実体のシグネチャー(例えばSHG、SFG、DFG)を使用して判定することができる。一部の場合には、候補生化学的実体のシグネチャーは、別の生化学的実体の検出されたシグネチャーと比較することができる。検出されたシグネチャーの類似性は、薬学的特性または機能的効果を相関させるために使用することができる。
シグネチャーは、例えば、大きさ、方向または単位時間あたりのシグナルを含むことができる。シグネチャーは、ベースラインと比較した大きさもしくは方向の変化、または動態の変化を含むこともできる。ベースラインは、候補生化学的実体を接触させる前に、および任意選択で薬剤(例えば別の候補生化学的実体)とのインキュベーションの後に測定することができる。さらに、シグネチャーは、検出されるシグナルの動態学的(リアルタイム)またはエンドポイント変化を測定することによって生じ得る。
他の生化学的実体は、1つまたは複数の公知の薬理特性または機能的効果(例えば結合特性、機能的特性、効能、力価、選択性、上の任意の組合せ)を有する公知の立体配置モジュレーターであってもよい。そのような場合、候補生化学的実体が公知の立体配置モジュレーターのそれに類似のシグネチャーを生成するならば、候補生化学的実体は1つまたは複数の公知の薬理特性または機能的効果も有すると判定することができる。さらに、候補生化学的実体が公知の立体配置モジュレーターと1つまたは複数の共通の構造パラメータ[例えば、足場、足場コア、分子量、電荷、化学式、特定の原子(例えば炭素、水素、窒素、酸素、硫黄)の全数、極性(例えばlog D、log P、PSAによって測定されるもの)、グラフ理論で測定される化学的類似性、Tanimoto(またはJaccard)係数T、芳香族基数、複素環基数、単環基数、縮合環系数および二重結合数]を有するならば、1つまたは複数の構造パラメータは1つまたは複数の公知の薬理特性もしくは機能的効果に寄与すると判定することもできる。
あるいは、他の生化学的実体は、別の候補生化学的実体であってもよい。候補生化学的実体が類似のシグネチャー(例えばSHGシグネチャー)を生じるならば、候補生化学的実体を共通の薬理特性または機能的効果と相関させるためにそのシグネチャーを使用することができる。これは候補生化学的実体のライブラリー全体に適用することができ、候補生化学的実体はシグネチャーに基づいて群に分けるまたは「分類する」ことができる。一部の例では、類似のシグネチャーを有する候補生化学的実体は、共通の薬理特性または機能的効果を有するとさらに判定することができる。
IV.追加の適用
SHG技術は、溶液中でX線準位感受性により立体配置変化を検出するためのリアルタイム手段を提供し、したがって、標的が、それが利用できる立体配置の全集団をサンプリングすることを可能にする。SHG技術は、薬物発見に大きな影響を及ぼすことができる。構造情報は薬物発見において非常に有益な情報および検証を提供し、一般的に生化学的なまたは細胞ベースのアッセイに従う。後者のアッセイはいくつかのヒットをしばしば生じるが、それらは、構造技術によるよりストリンジェントな試験の際、偽陽性であることがわかる。本当のヒット(例えば、真の陽性)を同定する(例えば、選び出す)ためにNMRまたはX線結晶学を用いることは、時間がかかり、しばしば非実用的である(Keseru GMおよびMakara GM、Drug Discovery Today11巻(15〜16号):741〜748頁、2006年)。本発明者らのアプローチは、生化学的スクリーニング、すなわち分子ベースのアッセイの特徴を、動的な構造読み出しと組み合わせる。実質的に、SHGは、生物学的機能と同義である構造動態力学および立体配置変化を研究する新しい技術を提供する。この技術の最初の実証において、本発明者らはアルファシヌクレインに及ぼすスペルミンの影響をブロックすることが可能な単一のリガンドを同定し、それがスペルミン自体のように機能するようであることをNMRによって確認した。一次スクリーニングがヒットであることを示す化合物と構造技術によるそれらの以降の確認の間に大きな隔たりがしばしばあるので、これはそれ自体意外で普段と異なる結果である。さらに、公知の結合剤がほとんどなく、C末端領域には他にない標的に対して、このリガンドを同定した。
SHGスクリーニングは、各種モードで使用することができる。例えば、リガンドによって誘導される公知の立体配置変化を阻害するリガンド(例えば、アンタゴニスト)、または目的の1つまたは複数の部位で立体配置変化を単独で誘導するリガンド(例えば、アゴニスト)についてスクリーニングすることができる。追求されるリガンドの型には、治療のためのリード化合物、アロステリックモジュレーターならびに化学生物学および疾患発病研究のためのツール化合物をとりわけ含めることができる。特定のアッセイが公知のツール化合物を含む場合は、その作用機構ならびにその結合親和性に関する情報を提供するために、SHGを使用することができる。ほとんどのスクリーニングライブラリーのかなりの割合は、蛍光性であって蛍光アッセイで読み出しに干渉することができる化合物を含有するが、おそらくSH活性であり、よりストリンジェントなセットの物理化学的性質であるのはごく少数しかない。
溶液中で立体配置変化をリアルタイムで検出することは、X線実験で見られない新しい結合部位、例えばアロステリックなものを明らかにする可能性がある。この技術は、Rasなど現在「薬物投与できない」と考えられている標的のためのアロステリックモジュレーターを同定する手段として、大きく期待されている。この技術の構造感度により、立体配置空間での正しい方向の変化を生成する弱い結合剤でさえも速やかに同定し、最適化することができる。このように、この技術は、いかなる他の方法で同定することができない新しいクラスの薬物を同定し、正確に調整した立体配置的(したがって機能的)効果を有する薬物を開発する道筋を提供する。
タンパク質の立体配置変化は、ほとんどの生物学的過程で一次性の機能的事象である。その研究方法は、その本当の空間座標の変化ではなく分子の環境の変化によって引き起こされるシグナルの変化を検出することに一般に頼る。SHGは、本当の空間の構造変化に非常に、および直接的に感受性である。ここで記載されるように、タンパク質が利用できる全立体配置空間をそれがサンプリングできるように、リアルタイムおよび生理的条件下で起こるときにタンパク質の構造変化を部位特異的にスクリーニングするためにSHGを使用することができる。これらの特性は、この技術を、タンパク質の立体配置をモジュレートするリガンド、例えばアロステリック薬または内因性の生物学的モジュレーターを同定するのに理想的にする。複数のプローブ部位で立体配置変化を研究することによって、この技術は、立体配置変化の大域的精査ならびにそれらの特定の部位セットで構造変化を引き起こすリガンドを同定および分類する選択的手段を提供することができる。一部の場合には、SHGスクリーニングプラットホームはプローブの角変化(度数)を数量化することもできるので、異なる部位での測定は立体配置変化の原子分解マップを造るための情報を提供することができる。すなわち、この技術は構造生物学および薬物発見の無数の分野においてかなりの影響を及ぼす。
V.シグネチャー
本明細書において本方法は、生化学的実体(例えば、標的生化学的実体)の立体配置状態を測定するために、表面選択的技術、例えばSHG、SFGまたはDFGを使用することを含むことができる。一部の実施形態では、生化学的実体の立体配置状態は、ベースライン(例えば、SHGベースライン)を作成するために表面選択的技術を使用して測定することができる。生化学的実体の立体配置状態は、シグネチャー(例えばSHG、SFGまたはDFGシグネチャー)を生じるために次に表面選択的技術を使用して(例えば、標的生化学的実体を候補生化学的実体と接触させることなどの事象に続いて)再び測定することができる。シグネチャーは、生化学的実体の立体配置状態の変化を示すことができる。例えば、それを第2の生化学的実体と接触させる(例えば、結合する)とき、第1の生化学的実体の立体配置状態は変化することができる。第2の生化学的実体は、その立体配置状態の変化を経ても経なくてもよい。一部の場合には、第1と第2の生化学的実体の両方は、立体配置の変化(例えば、2つの間の結合複合体で)を経てもよい。一部の場合には、第2の生化学的実体は、第1の生化学的実体の立体配置に影響を及ぼす立体配置の変化を経ることができる。
一部の実施形態では、ベースラインを測定することができない。例えば、第1の生化学的実体の第1の立体配置状態は、第1の生化学的実体を第2の生化学的実体と接触させる際に測定することができる。次に、第1の生化学的実体の第2の立体配置状態は、第1の生化学的実体(例えば、第1の生化学的実体の同じコピーまたは第1の生化学的実体の異なるコピー)を第3の生化学的実体と接触させる際に測定することができ、立体配置状態の差は、シグネチャーを引き算するかまたは比較することによって観察することができる。したがって、一部の場合には、シグネチャーはベースラインに対して規定することができる(例えば、ベースライン応答に対するSHG、SFGまたはDFG応答として)。一部の場合には、シグネチャーはベースラインに対して規定することができないか、または共通のベースラインを引き算することによって規定することができる。
本開示の表面選択的技術を使用して生じるシグネチャーは、様々な時間に測定される非線形光学応答(例えば、SHG応答)を含むことができる。例えば、シグネチャーは、生化学的実体の立体配置状態の動態学的(リアルタイム)変化、生化学的実体の立体配置状態のエンドポイント変化、または生化学的実体の立体配置状態の変化を、任意の他の時間(例えば、生化学的実体を別の生化学的実体と接触させる前、その間および/もしくはその後の任意の時間)に、または複数の所定の時間(例えば、接触させる前、接触させる際、接触後1、2、3、4、5、6、7、8、9、10もしくはそれを超える回数、もしくはその任意の組合せ)に測定することによって生じ得る。一部の場合には、シグネチャーは、非線形光学シグナル強度(例えば、SHG強度)を測定することによって生じ得る。
本開示のシグネチャーは、生化学的実体をスクリーニング、選択および/または評価するための基礎として使用することができる。例えば、生化学的実体は、そのシグネチャー(例えば、相互作用、例えば第1の生化学的実体と第2の生化学的実体との結合などのシグネチャー)に基づいて一群の候補生化学的実体から選択することができる。一部の場合には、選択はシグネチャーを1つまたは複数の他のシグネチャー(例えば、公知の化合物の参照シグネチャー、類似の生化学的実体のシグネチャーなど)と比較することを含むことができる。一例では、公知の立体配置モジュレーターによって誘導される立体配置状態の変化に最も類似している立体配置状態の変化を有する生化学的実体が選択される。公知の立体配置モジュレーターによって生成される立体配置状態の変化は、薬理特性または機能的効果(例えば、作用機構、表現型、臨床特性、結合特性など)に相関する可能性がある。したがって、一部の場合には、類似したまたは実質的に同じ薬理特性または機能的効果を有する生化学的実体を選択するために、比較を使用することができる。別の例では、生化学的実体のシグネチャーが比較され(例えば、第1の生化学的実体のシグネチャーは第2の生化学的実体のシグネチャーと比較される)、生化学的実体(例えば、生化学的実体のセットまたはライブラリーの)は比較に基づいて選択される。別の例では、生化学的実体は、シグネチャーと公知の薬理特性または公知の機能的効果との相関に基づいて選択される。
生化学的実体は、実質的に類似しているまたは異なるシグネチャーを有することができる(例えば、互いに、または参照生化学的実体に、例えば公知の立体配置モジュレーターもしくは承認薬などに)。例えば、スクリーニングアッセイで候補生化学的実体の各々を同じ標的生化学的実体と接触させる際に、候補生化学的実体の各々は異なるシグネチャーを作成することができる。
一部の場合には、本明細書において、シグネチャーは公知の薬理特性または公知の機能的効果と相関していてもよい。例えば、スクリーニングアッセイでの候補生化学的実体(例えば、候補生化学的実体の少なくとも2つ)は、類似の薬理特性または機能的効果を有することができる。薬理特性または機能的効果(例えば、結合親和性、結合特異性、臨床効能、表現型の変化など)は、例えば、少なくとも約1%、5%、10%、20%、30%、40%、50%、60%、70%、80%、90%、95%または99%類似していてもよい、などである。別の例では、スクリーニングアッセイでの候補生化学的実体(例えば、候補生化学的実体の少なくとも2つ)は、類似の薬理特性または機能的効果を有さなくてもよい。薬理特性または機能的効果(例えば、結合親和性、結合特異性、臨床効能、表現型の変化など)は、例えば、多くても約1%、5%、10%、20%、30%、40%、50%、60%、70%、80%、90%、95%または99%類似していてもよい、などである。一部の場合には、1つまたは複数の薬理特性もしくは機能的効果での類似性は、対応するシグネチャーでの類似性と相関することができる。他の場合には、1つまたは複数の薬理特性もしくは機能的効果での類似性は、対応するシグネチャーでの類似性と相関しなくてもよい。
本開示のシグネチャーを生じることは、1つまたは複数の非線形光学(例えば、SHG)パラメータを測定することを含むことができる。例えば、これらのパラメータには、非線形光学(例えば、SHG)ベースラインと比較した非線形光学(例えば、SHG)シグナルの大きさの変化、非線形光学(例えば、SHG)ベースラインと比較した非線形光学(例えば、SHG)シグナルの方向の変化、接触の際の単位時間あたりの非線形光学(例えば、SHG)シグナルの速度の変化、またはその任意の組合せを含めることができる。シグネチャーは、コンピュータ実行可能プログラムを使用して分析することができる。一部の場合には、シグネチャーは、類似性のために分析することができる。一部の場合には、類似のシグネチャーは、本開示のスクリーニング方法で生化学的実体を選択する(または選択しない)ための基礎として使用することができる。一部の場合には、類似のシグネチャーは、本開示の評価方法(例えば、生化学的実体のセットの構造−活性関係(SAR)を作成する)でSARを相関させるかまたは分析するための基礎として使用することができる。
一部の場合には、類似性は、非線形光学(例えば、SHG)パラメータを使用して規定することができる。例えば、第1の生化学的実体によって生成される生じるシグネチャーおよび第2の生化学的実体によって生じるシグネチャーは、1つまたは複数の非線形光学(例えば、SHG)類似性パラメータ(例えば、下の類似性パラメータの任意の組合せ)を使用して判定したときに、類似していてもよい。一部の例では、類似性パラメータは、第1の候補生化学的実体を標的生化学的実体と接触させる際の非線形光学(例えば、SHG)ベースラインと比較した非線形光学(例えば、SHG)シグナルの大きさの変化が、第2の候補生化学的実体を標的生化学的実体と接触させる際の非線形光学(例えば、SHG)ベースラインと比較した非線形光学(例えば、SHG)シグナルの大きさの変化の約1%、5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、90%またはそれを超える%未満以内(例えば、約50%以内)であることであってもよい。一部の例では、類似性パラメータは、第1の候補生化学的実体を標的生化学的実体と接触させる際の非線形光学(例えば、SHG)ベースラインと比較した非線形光学(例えば、SHG)シグナルの方向の変化が、第2の候補生化学的実体を標的生化学的実体と接触させる際の非線形光学(例えば、SHG)ベースラインと比較した非線形光学(例えば、SHG)シグナルの方向の変化と同じであることであってもよい。一部の例では、類似性パラメータは、第1の候補生化学的実体を標的生化学的実体と接触させる際の単位時間あたりの非線形光学(例えば、SHG)シグナルの速度の変化が、第2の候補生化学的実体を標的生化学的実体と接触させる際の単位時間あたりの非線形光学(例えば、SHG)シグナルの速度の変化の約1.1、1.2、1.3、1.4、1.5、1.6、1.7、1.8、1.9、2、2.1、2.2、2.3、2.4、2.5、2.6、2.7、2.8、2.9、3、3.5、4、4.5、5、6、7、8、9、10、15、20倍未満、またはそれより大きくてもよいし(例えば、約2倍)、またはその逆であってもよい。
一部の実施形態では、シグネチャーは、非線形光学(例えば、SHG)シグナル応答に特有の形状またはプロファイルを含むことができる。例えば、シグネチャーは所与の数の特色、例えば局所最大値、局所最小値、屈折点、全体的勾配、勾配変化などを有することができる。一部の場合には、これらの特徴または特色は、非線形光学(例えば、SHG)ベースラインと比較して測定することができる。一部の場合には、類似性パラメータは、第1の候補生化学的実体を標的生化学的実体と接触させる際に測定された非線形光学(例えば、SHG)シグナル、および第2の候補生化学的実体を標的生化学的実体と接触させる際に測定された非線形光学(例えば、SHG)シグナルが、少なくとも1、2、3、4、5、6、7、8、9、10、15、20、30、40、50またはそれを超える数のそのような特色(例えば、局所最大値、局所最小値、屈折点、全体的勾配および/もしくは勾配変化)を共有することであってもよい。一部の場合には、類似性パラメータは、第1の候補生化学的実体を標的生化学的実体と接触させる際に測定された非線形光学(例えば、SHG)シグナルの、局所最大値、局所最小値、屈折点、全体的勾配、勾配変化および/または他のシグナル特色の数の1つまたは複数が、第2の候補生化学的実体を標的生化学的実体と接触させる際に測定された非線形光学の、局所最大値、局所最小値、屈折点、全体的勾配、勾配変化および/または他のシグナル特色の数と同じであることであってもよい。
VI.標的生体分子および参照生化学的実体
本明細書に記載される方法のいずれかで使用するための標的生体分子は、任意の生体分子、例えばタンパク質、DNA、RNAまたは多糖であってもよい。標的生体分子は、ウイルス、微生物(細菌、真菌類、藻類および原生動物を含む)、無脊椎動物(昆虫および虫を含む)、動物、脊椎動物(例えば、哺乳動物、鳥類または魚類、ならびに哺乳動物の中では、例えば、ヒト、類人猿、サル、ウシ、ブタ、ヤギ、ラマ、ヒツジ、ラット、マウス、ウサギ、モルモット、ネコおよびイヌ)の正常もしくは病的な細胞、または植物の正常もしくは病的な細胞を含む任意の天然供給源からの、天然に存在する物質またはそのサブユニットもしくはドメインであってもよい。あるいは、標的生体分子は、in vitroで作られた、または例えば突然変異、キメラタンパク質もしくは人工タンパク質によって改変された天然に存在しない分子であってもよい。
例えば、標的タンパク質は、糖タンパク質、リポタンパク質、リンタンパク質または金属タンパク質であってもよい。それは、核、細胞質、膜関連の、または分泌されたタンパク質であってもよい。標的タンパク質は、単一の巨大分子である必要はない。例えば、標的タンパク質は、巨大分子のホモまたはヘテロマルチマー(例えば、限定されずに二量体、三量体または四量体)であってもよい。さらに、標的タンパク質は、生理機能を発揮するために1つまたは複数のリガンド、例えば他のタンパク質、オリゴペプチドもしくはポリペプチド、核酸、炭水化物、脂質または有機もしくは無機の小分子もしくはイオンを必要とする可能性がある。追加の例には、補因子、リボソーム、ポリソームおよびクロマチンが含まれる。
標的タンパク質には、限定されずに、天然変性タンパク質(IDP)、例えばアルファシヌクレイン(パーキンソン病との関連が示唆されている)およびCOW(アルツハイマー病との関連が示唆されている)が含まれる。標的タンパク質のさらなる例には、限定されずに、核内受容体、オーファン核内受容体、チロシンキナーゼ受容体、エンドセリン、エリスロポイエチン受容体、FASリガンド受容体、タンパク質キナーゼ(例えば、プロテインキナーゼC、チロシンキナーゼ、セリンキナーゼ、トレオニンキナーゼ、ヌクレオチドキナーゼまたはポリヌクレオチドキナーゼ)、タンパク質ホスファターゼ(セリン/トレオニンホスファターゼ、チロシンホスファターゼ、ヌクレオチドホスファターゼ、酸ホスファターゼ、アルカリホスファターゼまたはピロホスファターゼ)、細胞周期調節因子(サイクリンcdk2、CDC2、CDC25、P53、RB)、GTPアーゼ、Rac、Rho、Rab、Ras、エンドプロテアーゼ、エキソプロテアーゼ、メタロプロテアーゼ、セリンプロテアーゼ、システインプロテアーゼ、ヌクレアーゼ、ポリメラーゼ、逆転写酵素、インテグラーゼ、イオンチャネル、シャペロニン(例えば、熱ショックタンパク質)、デアミナーゼ、ヌクレアーゼ(例えば、デオキシリボヌクレアーゼ、リボヌクレアーゼ、エンドヌクレアーゼ、エキソヌクレアーゼ)、テロメラーゼ、プライマーゼ、ヘリカーゼ、デヒドロゲナーゼ、転移酵素(ペプチジルトランスフェラーゼ、トランスアミナーゼ、糖転移酵素、リボシルトランスフェラーゼ、アセチル転移酵素、グアニリルトランスフェラーゼまたはメチルトランスフェラーゼ)、加水分解酵素、カルボキシラーゼ、イソメラーゼ、グリコシダーゼ、デアミナーゼ、リパーゼ、エステラーゼ、スルファターゼ、セルラーゼ、リアーゼ、レダクターゼ、リガーゼまたは細胞ユビキチン化経路のプロセシング酵素(例えば、E1、E2もしくはE3酵素、またはデユビキチナーゼ)が含まれる。一部の実施形態では、本明細書に開示される方法のいずれかで使用するための標的タンパク質は、ウイルスタンパク質、細菌タンパク質、植物性タンパク質、動物性タンパク質およびヒトタンパク質の間で選択される構造および非構造タンパク質であってもよい。一部の実施形態では、標的タンパク質は、ウイルスタンパク質、例えば、限定されずに、インフルエンザウイルス、A型肝炎ウイルス、B型肝炎ウイルス、C型肝炎ウイルス、ヒト免疫不全ウイルス、鳥インフルエンザウイルス、エボラウイルス、SARSウイルス、ハンタウイルスまたは東部ウマ脳脊髄炎ウイルスであってもよい。
標的タンパク質は、表面および細胞内受容体の両方を含む受容体であってもよい。一部の実施形態では、標的タンパク質は、核内受容体である。核内受容体は、リガンド活性化転写活性化因子のファミリーである。これらの受容体は、リガンド結合、二量体化、トランス活性化およびDNA結合のために、異なるドメインに組織される。ステロイド受容体ファミリーは、糖質コルチコイド、鉱質コルチコイド、アンドロゲン、プロゲスチンおよびエストロゲンのための受容体で構成される大きなファミリーである。受容体活性化は、リガンド結合の際に起こり、これは受容体二量体化および同時活性化タンパク質の結合を可能にする立体配置変化を誘導する。これらの補活性化因子は、次に、DNAへの受容体の結合および以降の標的遺伝子の転写活性化を促進する。同時活性化タンパク質の補充に加えて、リガンドの結合は、受容体機能のコリプレッサーの役割をするタンパク質の結合を解くかまたは阻止する立体配置に受容体を置くと考えられてもいる。リガンドが薬理学的アゴニストである場合は、新しい立体配置は、生物学的シグナル伝達経路の他の構成要素、例えば転写因子と相互作用して標的組織で生物学的応答を導き出すものである。リガンドが薬理学的アンタゴニストである場合は、新しい立体配置は、さもなければその受容体を活性化することができる1つまたは複数のアゴニストによって受容体を活性化することができないものである。NRの非網羅的リストは、国際特許出願公開第2006/046134号に記載され、その開示は参照により本明細書に組み込まれる(14〜15頁および図1を参照する)。一部の実施形態では、本明細書に開示される方法のいずれかで使用するためのNRは、エストロゲン受容体、アンドロゲン受容体、糖コルチコイド受容体、レチノイン酸受容体アルファ(RARG)、レチノイン酸X受容体(RXR)、ペルオキシゾーム増殖因子活性化受容体(PPAR)、肝臓X受容体アルファ(LXRG)またはプロゲステロン受容体の中から選択することができる。
標的タンパク質は、Gタンパク質共役受容体(7回膜貫通ドメイン受容体として公知)、すなわち、Gタンパク質と共役することによってシグナル伝達を媒介する受容体のスーパーファミリーの任意のメンバーであってもよい。GPCRは、細胞外環境に存在する分子に結合し、細胞中でシグナル伝達カスケードを、および最終的に細胞応答を誘発することが可能である膜貫通受容体タンパク質(ヒトの全ゲノムの約5%を占める)の大きなファミリーを構成する。GPCRは、酵母、立襟鞭毛虫および動物を含む真核細胞だけで見出される。これらの受容体に結合して活性化する分子には、限定されずに、光電性化合物、匂い、フェロモン、ホルモンおよび神経伝達物質が含まれ、小分子からペプチド、さらに大きなタンパク質までサイズは異なる。サイトゾルカルシウムレベルに影響するGPCRのクラスの1つの例は、ホスホリパーゼC(PLC)経路を活性化し、ホスホイノシチドの加水分解をもたらし、異なる第2のメッセンジャーの2つのクラス、すなわちジアシルグリセロールおよびリン酸イノシトールを生じる、Gq型のGタンパク質を通して働く。ジアシルグリセロールは、次に、ある特定のプロテインキナーゼC(PKC)を活性化し、リン酸イノシトール(例えば、限定されずにIP3)は、細胞内貯蔵部位、例えば小胞体、筋小胞体(筋細胞の場合)および/またはミトコンドリアからのカルシウムの可動化を刺激する。これらの受容体に結合して活性化する分子には、限定されずに、光電性化合物、匂い、フェロモン、ホルモンおよび神経伝達物質が含まれ、小分子からペプチド、さらに大きなタンパク質までサイズは異なる。
本明細書に開示される方法で使用するためのGPCRには、限定されずに、Gqタンパク質またはGq/11、アルファ−1アドレナリン受容体(α1−AR)、ウロテンシン(UT)受容体、5−HT2および5−HT6セロトニン受容体、ヒポクレチン(オレキシン)受容体、ヒスタミンHI受容体、ブラジキニンB1およびB2受容体、ボンベシンBB2受容体、P2Yプリン受容体、アセチルコリン(acetycholine)受容体(例えば、M1、M3およびM5)、mGluR5グルタミン酸受容体、バソプレシンV2およびVI受容体、アンジオテンシンAGTR1受容体、コレシストキニンCCKARおよびCCKBR受容体、エンドセリンENDRA受容体、グレリンGHSR1a受容体、メラトニンMTNR1A受容体、ニューロテンシンNTSR1受容体、血小板活性因子PTAFR受容体、黄体形成ホルモン受容体(LHR)、卵胞刺激ホルモン受容体(FSHR)、性腺刺激放出ホルモン受容体(GnRHR)およびプロラクチン放出ペプチド受容体PRLHR受容体が含まれる。一部の実施形態では、GPCRはカルシウムセンサータンパク質を発現する細胞で内因的に発現される。他の実施形態では、GPCRはカルシウムセンサータンパク質を発現する細胞で異種性に発現される。
標的タンパク質は、キナーゼであってもよい。キナーゼは、ATPなどの高エネルギードナー分子から特異的基質までリン酸基を転移する種類の酵素であり、この過程はリン酸化と呼ばれる。キナーゼの最も大きな群の1つはタンパク質キナーゼであり、それは特異的タンパク質の活性に作用して改変する。キナーゼは、シグナルを伝え、細胞中の複雑な過程を制御するために広く使用される。500個を超える異なるキナーゼが、ヒトで同定されている。それらの莫大な多様性、およびシグナル伝達におけるそれらの役割により、それらは異常なキナーゼ発現または調節を特徴とする疾患状態に特に関する研究の対象になっている。
タンパク質キナーゼは、その立体配置はキナーゼ活性を調節すると考えられている、活性化ループまたはAループと呼ばれる大きな柔軟性のあるループを含有する。多くのキナーゼでは、Aループの立体配置は、この領域中の特異的残基のリン酸化によって制御される(Johnson 1996年)。活性化ループは、一般に保存されたAspPheGly配列から始まり、保存されたAlaProGlu配列で終わる。不活性キナーゼの構造では、このループは、基質またはATP結合部位をしばしばブロックする(Hubbard 1994年;Mohammadi 1996年;およびMcTigue 1999年)。チロシンキナーゼはループに1つまたは2つのチロシンを通常有し、MAPKキナーゼはTおよびYでリン酸化されるT[DE]Yモチーフを有し、ほとんどの他のキナーゼはループ中にトレオニンを有する。
本発明の方法で使用するための標的タンパク質は、任意のタンパク質キナーゼに広く適用できる。これらには、タンパク質チロシンキナーゼおよびタンパク質セリンキナーゼを含めることができる。タンパクチロシンキナーゼの非限定例は、pp60c−src、p56lck、ZAPキナーゼ、血小板由来増殖因子受容体チロシンキナーゼ、Bcr−Abl、VEGF(血管内皮細胞増殖因子)受容体チロシンキナーゼ、ならびに表皮増殖因子受容体チロシンキナーゼおよび表皮増殖因子受容体様チロシンキナーゼである。本発明で使用するために適用できるセリンプロテインキナーゼの非限定例には、MAP(マイトジェン活性化タンパク質)キナーゼ、プロテインキナーゼC、プロテインキナーゼA、AktおよびCDK(サイクリン依存性プロテインキナーゼ)が含まれる。哺乳動物生物学では、マイトジェン活性化タンパク質キナーゼ(MAPK)ファミリーに属するタンパク質キナーゼは、ras遺伝子の突然変異および増殖因子受容体の調節解除に関連した様々な増殖性細胞疾患(例えば、がんなど)において不適切に活性化される(Magnusonら、Seminars in Cancer Biology、5巻:247〜252頁(1994年))。MAPキナーゼは当技術分野で公知であり、そのようなキナーゼの部分的な非限定リストには、abl、オーロラ−A、オーロラ−B、オーロラ−C、ATK、bcr−abl、Blk、Brk、Btk、c−Kit、c−Met、c−Src、CDK1、CDK2、CDK4、CDK6、cRaf1、CSF1R、CSK、EGFR、ErbB2、ErbB3、ErbB4、ERK、Fak、fes、FGFR1、FGFR2、FGFR3、FGFR4、FGFR5、Fgr、FLK−4、Flt−1、Fms、Fps、Frk、Fyn、Hck、IGF−1R、INS−R、Jak、KDR、Lck、Lyn、MEK、p38、PDGFR、PIK、PKC、PYK2、Ros、Tie1、Tie2、Trk、YesおよびZap70が含まれる。本明細書に記載される方法の一部の実施形態では、キナーゼはablキナーゼである。
キナーゼに関して、数種類の化合物がキナーゼの機能をモジュレートすることが公知である。例えば、I型キナーゼ阻害剤は、キナーゼの活性立体配置を認識する。それらは、ATPによって通常形成される水素結合を模倣する1つから3つの水素結合を提示することによって、ATP結合部位に結合する。理論に縛られることなく、I型キナーゼ阻害剤と対照的に、II型キナーゼ阻害剤はキナーゼの不活性立体配置を認識し、ATP結合部位に直に隣接する疎水性ポケットを占めることによってATPと間接的に競合することができると考えられている。この疎水性ポケットは、活性化ループの特異なDFG外の立体配置によって作られる。これは機能のために必要でないが、一部のII型阻害剤はATP結合部位と直接的に水素結合を形成することができる(GotinkおよびVerheul、Angiogenesis、2010年、13巻(1号):1〜14頁)。他方、III型キナーゼ阻害剤は、活性化ループ以外の部位への結合によって(すなわち、キナーゼのアロステリック部位への結合によって)キナーゼ活性をモジュレートする、非ATP競合的キナーゼ阻害剤である。III型化合物がキナーゼのより保存されていない部位に結合するという事実のために、それらは非常に選択的であり、研究および薬物発見コミュニティにとって益々興味が引かれる。
小さいGTPアーゼのRasファミリーは、ヌクレオチドグアノシン−5’−三リン酸(GTP)によって調節される細胞内シグナル伝達分子で構成される。これらのタンパク質は、「オン」および「オフ」状態の両方を有する二元シグナル伝達スイッチとして機能する。「オフ」状態ではRasはヌクレオチドグアノシン二リン酸(GDP)に結合し、「オン」状態ではRasはGTPに結合する。したがって、Rasの活性化および非活性化は、活性GTP結合型および不活性GDP結合型の間の循環によって制御される。GTP結合型立体配置では、Rasはその細胞内機能を発揮させる多数のエフェクターに高い親和性を有する。Rasによって調節されるシグナル伝達経路は、アクチン細胞骨格の完全性、増殖、分化、細胞接着、アポトーシスおよび細胞移動と同じくらい多様な過程を制御する。一部の場合には、突然変異は構成的Ras活性化(すなわち、それがGDPに結合しているかどうかにかかわりなく、その「オフ」状態を採用することができないRasタンパク質)をもたらし、異常なシグナル伝達につながる。本明細書において、本方法は、下流Rasエフェクター分子の異常なシグナル伝達を減少させるために、Rasの行動(例えば、がん細胞中の)を特異的にモジュレートすることが可能な化合物をスクリーニングまたは同定するために使用することができる。
本明細書に開示される方法のいずれかで使用するために、任意のRasタンパク質が企図される。3つのヒトras遺伝子は、H−RAS、N−RASおよびK−RAS4AおよびK−RAS4B(2つのK−RASタンパク質は選択的スプライシングから生じる)と呼ばれる、188から189個のアミノ酸の鎖で構成される極めて相同的なタンパク質をコードする。Rasサブファミリーの臨床的に最も注目すべきメンバーは、主に多くの種類のがんと結びつけられるために、H−RAS、K−RASおよび、N−RASであるが、このサブファミリーの多くの他のメンバーも同様にあり、例には、限定されないが、DIRAS1、DIRAS2、DIRAS3、ERAS、GEM、MRAS、NKIRAS1、NKIRAS2、NRAS、RALA、RALB、RAP1A、RAP1B、RAP2A、RAP2B、RAP2C、RASD1、RASD2、RASL10A、RASL10B、RASL11A、RASL11B、RASL12、REM1、REM2、RERG、RERGL、RRAD、RRASまたはRRAS2を含めることができる(その開示は参照により完全に組み込まれる、Wennerbergら、2005年、「The Ras superfamily at a glance」、J. Cell. Sci.118巻(Pt5):843〜6頁も参照)。Rasタンパク質の突然変異形も、開示の方法の範囲内での使用のために企図される。
標的タンパク質には、標的タンパク質の突然変異形が含まれる。本明細書で使用される場合、「突然変異」は、標的タンパク質の一次アミノ酸配列などの規定の一次アミノ酸配列中のアミノ酸残基欠失、アミノ酸残基挿入および/または少なくとも1つのアミノ酸残基のアミノ酸残基置換を含む。アミノ酸「置換」は、規定の一次アミノ酸配列の少なくとも1つのアミノ酸構成要素が別のアミノ酸(例えば、システイン残基またはリシン残基)で置き換えられることを意味する。標的タンパク質の一次アミノ酸配列に突然変異または置換を組み入れるための方法は、標準技術により当技術分野で周知である。本明細書に記載される方法で使用するための標的タンパク質は、保存的置換を含むことができる。
標的タンパク質の生物学的特性の実質的な改変は、(a)例えばシートもしくはヘリカル構造のような、置換エリアにおけるポリペプチド主鎖の構造、(b)標的部位での分子の電荷もしくは疎水性、または(c)側鎖のかさの維持に及ぼすそれらの作用が有意に異なる置換を選択することによって達成される。非保存的置換は、これらのクラスの1つのメンバーを別のクラスと交換することを伴う。
さらなる実施形態では、本明細書に開示される方法のいずれかで使用するための突然変異標的タンパク質は、1つまたは複数の天然に存在しないまたは改変されたアミノ酸を含むことができる。非天然のアミノ酸には、限定されずに、ホモリシン、ホモアルギニン、ホモセリン、アゼチジンカルボン酸、2−アミノアジピン酸、3−アミノアジピン酸、ベータアラニン、アミノプロピオン酸、2−アミノ酪酸、4−アミノ酪酸、6−アミノカプロン酸、2−アミノヘプタン酸、2−アミノイソ酪酸、3−アミノイソ酪酸(isbutyric acid)、2−アミノピメリン酸、第三ブチルグリシン、2,4−ジアミノイソ酪酸、デスモシン、2,2’−ジアミノピメリン酸、2,3−ジアミノプロピオン酸、N−エチルグリシン、N−エチルアスパラギン、ホモプロリン、ヒドロキシリシン、アロヒドロキシリシン、3−ヒドロキシプロリン、4−ヒドロキシプロリン、イソデスモシン、アロイソロイシン、N−メチルアラニン、N−メチルグリシン、N−メチルイソロイシン、N−メチルペンチルグリシン、N−メチルバリン、ナフトアラニン、ノルバリン、ノルロイシン、オルニチン、シトルリン、ペンチルグリシン、ピペコリン酸およびチオプロリンが含まれる。改変アミノ酸には、可逆的もしくは不可逆的に化学的にブロックされるか、または例えばNメチル化DおよびLアミノ酸、別の官能基に化学改変された側鎖官能基のように、それらのN末端アミノ基もしくはそれらの側鎖基が改変される、天然および非天然のアミノ酸が含まれる。例えば、改変アミノ酸には、メチオニンスルホキシド;メチオニンスルホン;アスパラギン酸(ベータ−メチルエステル)、アスパラギン酸の改変アミノ酸;N−エチルグリシン、グリシンの改変アミノ酸;またはアラニンカルボキサミド、アラニンの改変アミノ酸が含まれる。追加の非天然のおよび改変されたアミノ酸、ならびにそれらをタンパク質およびペプチドに組み入れる方法は、当技術分野で公知である(例えば、Sandbergら、(1998年)J. Med. Chem.41巻:2481〜91頁;XieおよびSchultz(2005年)Curr. Opin. Chem. Biol.9巻:548〜554頁;HodgsonおよびSanderson(2004年)Chem. Soc. Rev.33巻:422〜430頁を参照)。
一部の実施形態では、本明細書に記載される方法で使用するための突然変異標的タンパク質は、標準タンパク質精製技術を使用する適当な精製スキームによって、細胞(がん細胞など)から単離することができる。別の実施形態では、本明細書に記載される方法で使用するための突然変異標的タンパク質は、組換えDNA技術によって生成される。組換え発現の代わりに、本明細書に記載される方法で使用するための突然変異標的タンパク質は、標準のペプチド合成技術を使用して化学的に合成することができる。
さらに、候補生化学的実体のシグネチャーを薬理特性および/または機能的効果と相関させるために使用することができる参照シグネチャーを発生させるために、本出願に記載される方法に参照生化学的実体を供することができる。例えば、1つまたは複数の公知の薬理特性および/または機能的効果を有する参照生化学的実体は、候補生化学的実体のライブラリーのシグネチャーと比較することができる参照シグネチャーを有することができる。参照シグネチャーと類似のシグネチャーを有する候補生化学的実体は、1つまたは複数の公知の薬理特性および/または機能的効果と相関させることおよび/またはそれについて試験することができる。
参照生化学的実体は、公知の機能および/または公知の標的を有する任意の公知の薬物であってもよい。参照生化学的実体は、例えば、抗がん薬または消炎薬であってもよい。参照生化学的実体は、限定されずにチロシンキナーゼ阻害剤およびセリン/トレオニンキナーゼ阻害剤を含む、公知のキナーゼ阻害剤であってもよい。参照生化学的実体の例には、限定されずに、Abilify、Nexium、Humira、Crestor、Advair Diskus、Enbrel、Cymbalta、Remicade、Neulasta、Copaxone、Lantus Solostar、Rituxan、Spiriva、Januvia、Atripla、Lantus、Avastin、Lyrica、OxyContin、Epogen、Celebrex、Truvada、Diovan、Gleevec、Herceptin、Lucentis、Vyvanse、Zetia、Namenda、Levemir、Symbicort、Tecfidera、AndroGel、Novolog、エノキサパリン、メチルフェニデート、Suboxone、Xarelto、ProAir HFA、Humalog、Alimta、Victoza、Viagra、Seroquel XR、Synagis、Avonex、Renvela、Rebif、Cialis、Gilenya、Nasonex、Stelara、Restasis、ブデソニド、アセトアミノフェン/ヒドロコドン、Flovent HFA、Lovaza、Prezista、Isentress、Janumet、Procrit、ドキシサイクリン、Orencia、アンフェタミン/デキストロアンフェタミン、VESIcare、Dexilant、Neupogen、リドカイン、Lunesta、フェノフィブレート、Zytiga、Reyataz、Sensipar、メトプロロール、Invega Sustenna、Synthroid、Avonex、Prevnar 13、Xolair、レボチロキシン、Benicar、Stribild、Zostavax、Pradaxa、Vytorin、Tamiflu、Xgeva、Evista、Xeloda、Aranesp、Ventolin HFA、ジバルプロエックスナトリウム、Afinitor、Betaseron、Adderall XRおよびCompleraが含まれる。
VII.非線形活性部分
一部の実施形態では、1つまたは複数の非線形活性(例えば、第2高調波活性)部分または標識は、標的生化学的実体(例えば、生体分子)、候補生化学的実体(例えば、候補分子)、参照生化学的実体(例えば、分子)またはその任意の組合せに付着させるかまたはそれに組み入れることができる。一部の実施形態、例えば構造的に類似の生化学的実体をスクリーニングするための、または構造−活性関係を生じることによって生化学的実体を評価するためのアッセイおよび方法などでは、非線形活性部分または標識は、標的生化学的実体、構造的に類似の生化学的実体のライブラリー中の1つまたは複数の候補生化学的実体、異なる分子構造を有する生化学的実体のセット中の1つまたは複数の生化学的実体、参照生化学的実体またはそれらの任意の組合せに付着させるかまたはそれに組み入れることができる。例えば、第1の生化学的実体を第2の生化学的実体と接触させる(例えば、相互作用、例えば結合事象をもたらす)任意の所与のアッセイでは、第1の生化学的実体および/または第2の生化学的実体は、本明細書に記載される表面選択的技術(例えば、SHG、SFGまたはDFG)を使用して立体配置変化を測定するのに適する標識を含むことができる。
一部の場合には、標識は第2高調波活性部分または標識(別名、SHG部分またはSHG標識)であってもよい。一部の場合には、和周波数活性または差周波数活性部分または標識。一部の場合には、非線形活性部分または標識(本明細書では「部分」または「標識」とも呼ぶ)は、SHG活性、SFG活性、DFG活性またはそれらの組合せであってもよい。
一部の実施形態では、標的生化学的実体(例えば、タンパク質、細胞などの生体分子)は、1つまたは複数の所定位置で標識されてもよい。標識(複数可)は、例えば、活性部位、結合部位、アロステリック結合部位、または生化学的実体(例えば、タンパク質)構造上もしくはその中の任意の他の部位(例えば、アッセイによってスクリーニングされる立体配置変化を受けることができる任意の部位、in vivoまたはin vitroの薬理特性と相関する立体配置変化を受ける任意の部位など)から所与の距離に(例えば、そこでまたはそれに隣接して)置くことができる。
一部の場合には、例えば、開示のスクリーニングおよび評価アッセイを可能にするために、同じ標的生化学的実体の複数のコピーを標的生化学的実体の上またはその中の同じ位置(複数可)で標識することができる。例えば、本開示の系および方法は、非常に類似した構造を有する生化学的実体と接触させた標的生化学的実体の立体配置状態の変化の差を検出するために使用することができる。さらに、立体配置状態の変化の差は、薬理特性または機能的効果と相関することができる。したがって、同一の標識配置は、標的生化学的実体と相互作用する生化学的実体が同じ条件下で評価されること、および標的生化学的実体の立体配置状態の変化の観察される差が、異なる標識配置ではなく、構造、薬理特性、機能的効果などの少なくとも1つの差によることを確かなものにすることができる。
各標識は、標的生化学的実体上の所与の位置(例えば、3D座標)を有することができる。所与の標識は、標的生化学的実体の第1のコピーの上またはその中で第1の位置(例えば、3D座標(x,y)1)、および標的生化学的実体の第2のコピーの上またはその中で第2の位置(例えば、3D座標(x,y)2)を有することができる。一部の例では、第1の位置と第2の位置の間の相対差(例えば|(x,y)1−(x,y)2|/(x,y)1または|(x,y)1−(x,y)2|/(x,y)2)は、約75%、50%、25%、10%、5%、1%未満などであってもよい。一部の例では、第1の位置と第2の位置の間の絶対差は、標的生化学的実体の直径、高さ、幅、横幅または他の特徴的寸法の約1%、2%、3%、4%、5%、6%、7%、8%、9%、10%、15%、25%、50%または75%未満であってもよい。
生じる標的生体分子を第2高調波発生に感受性にし、表面選択的技術を使用する界面での研究に適合させるために、部分(例えば、標識)を共有結合または非共有結合的に標的生体分子に結合することができる。標識標的生体分子は、第2高調波発生または和周波発生などの表面選択的技術によって次に研究することができる。外因性部分(例えば、標識)は標的生体分子に事前に付着させることができ、測定の前にいかなる未結合または未反応の標識を標識実体から分離することができる。一実施形態では、第2高調波活性部分(例えば、標識)は、in vitroで標的生体分子に付着させる。
一部の場合には、少なくとも2つの識別可能な第2高調波活性部分(例えば、標識)を使用することができる。次に、発する干渉性の非線形光線の明確な方向を促進するように、付着している2つまたはそれを超える識別可能な標識の配向が選択される。2つまたはそれを超える識別可能な標識は、試料に対して1つまたは複数の偏光方向が付随する1つまたは複数の周波数の複数の基本光線が使用され、少なくとも2つの非線形光線の放射が生じるアッセイで使用することができる。一実施形態では、第2高調波活性部分(例えば、標識)は、複数の個々の第2高調波活性部分(例えば、標識)を含み、その各々は非線形感受率を有し、第2高調波活性部分(例えば、標識)の全体的非線形感受率を増加させるように、互いに対して固定され、限定された配向で結合している。
一部の場合には、第2高調波活性部分(例えば、標識)は、色素である。標的生体分子は、特異的標識または非特異的標識を通して色素によって標識され得る。
第2高調波活性部分は、特異的標識を通して、例えば共有結合または水素結合を通して標的生体分子に付着させることができる。例えば、第2高調波活性部分(例えば、標識)は、検出する標的タンパク質の第一級アミノ酸配列中のアミン基、リシン基またはスルフヒドリル基に共有結合または非共有結合で付着させることができる。一部の実施形態では、第2高調波活性部分(例えば、標識)は、アミン反応性スクシンイミジルエステル、チオール反応性マレイミドまたはアルデヒドおよび/もしくはケトン反応性ヒドラジドおよびヒドロキシルアミンを有する。一部の実施形態では、SFGまたはSHG活性色素標識は、アジドへの共役のために「クリック化学」を通してコンジュゲートすることができる。コンジュゲート形成に使用されるクリック化学の詳細は、「Click Chemistry for Biotechnology and Materials Science」J. Lahann(編)、Wiley(2009年)中の「Synthesis and Functionalization of Biomolecules via Click Chemistry」、C. Schillingら、第15章、355〜378頁に記載される。
本明細書に開示される方法で第2高調波または和周波数活性部分(例えば、標識)としての使用に適当な色素の例には、マレイミド標識(例えば、チオール含有残基、一般的にシステインの上でタンパク質を特異的に標識する、PyMPO−MALEIMIDE(商標)(1−(2−マレイミジルエチル)−4−(5−(4−メトキシフェニル)オキサゾール−2−イル)ピリジニウムメタンスルホネート))、PyMPO−NHS(第一級アミン含有残基、一般的にリシン(lysinzes)を特異的に標識する)、オキサゾール標識(例えば、アミンを特異的に標識するPyMPO−スクシンイミジルエステル)、BADAN(商標)(6−ブロモアセチル−2−ジメチルアミノナフタレン)およびACRYLODAN(商標)(6−アクリロイル−2−ジメチルアミノナフタレン)が含まれる。他の実施形態では、標識はクマリンをベースとした色素、例えば限定されずに、ケトクマリンおよび3,3’−カルボニルビス(7−ジエチルアミノクマリン)であってもよい。他の実施形態では、標識はPyMPO−SE(商標)(1−(3−(スクシンイミジルオキシカルボニル)ベンジル)−4−(5−(4−メトキシフェニル)オキサゾール−2−イル)ピリジニウムブロミド)であってもよい。
一部の場合には、標的タンパク質の第一級アミノ酸配列中の天然アミノ酸残基は、第2高調波活性色素に結合することが可能である別のアミノ酸で突然変異または置換されてもよい。本明細書に記載される標的タンパク質は、保存的置換を含むことができる。
他の場合には、第2高調波活性部分(例えば、標識)は、非天然アミノ酸(UAA)であってもよい。従来の標識と対照的に、UAAは、埋込み型および露出型の両方の部位でタンパク質を標識する手段を提供する。さらに、タンパク質の先天性構成要素として、それらは、アミノ酸官能基(例えば、システイン、アミンなど)に付着した標識(色素など)より多くの感受性および忠実度で構造変化を報告することができる。UAAは、第2高調波発生などの非線形技術を使用してタンパク質を検出するための、超偏光率を有する。したがって、これらの特異的非天然アミノ酸は、SHAA(「第2高調波アミノ酸」)とも呼ばれている。タンパク質構造立体配置の変化の検出のためのプローブとしてUAAを使用する別の利点は、検出をin vivoで、すなわち生細胞中で実行することができることである。例えば、本明細書に記載される方法は、薬物候補の結合に応答して生細胞中の標的タンパク質によって示されるシグナルを検出するために使用することができる。
任意の高偏光性のUAAは、第2高調波活性部分(例えば、標識)として使用することができる。UAAの例には、Aladan(Cohenら、2002年、Science、296巻:1700頁;Abbyadら、2007年、J. Phys. Chem.、111巻:8269頁、その開示は参照により完全に本明細書に組み込まれる)、ダンシルアラニン(Summererら、Proc. Nat. Acad. Sci. U.S.A.、2006年、103巻(26号):9785〜9789頁)が含まれる。一実施形態では、非天然アミノ酸は、和周波発生活性である(SFG活性)。他の実施形態では、UAAは超偏光性でないが、それが第2高調波活性標識色素、例えば上記の色素のいずれかに結合するのを許す適当な化学官能基(複数可)を有する。他の実施形態では、UAAは、SFGによる部位特異的立体配置変化が同定されるようにタンパク質中の別個の部位に組み込むための特注の振動特性を有するプローブを含んでいてもよい。一部の実施形態では、UAAへの組入れのためのプローブ部分は、それらが天然のタンパク質構造を不安定化しないように望ましくは十分に小さく、その例には、限定されずにNO、CN、SCNまたはN3を含めることができる。一部の実施形態では、プローブ部分は約1,900から2,300cm−1の間のスペクトル域の特異な振動シグネチャーを提供し、それは内在性のタンパク質振動からかなり分離している。別の実施形態では、第2高調波活性部分(例えば、標識)が表面に対して純配向を有するように、表面に標的タンパク質を付着させるためにUAAを使用することができる。
一部の実施形態では、非天然アミノ酸は、同位体プローブ部分、例えば重水素、13Cまたは他の同位体を含有する。同位体標識(重水素化など)の使用の例証は、参照により完全に本明細書に組み込まれる、Weidnerら、「Sum frequency generation and solid−state NMR study of the structure, orientation, and dynamics of polystyrene−adsorbed peptides」、13288〜13293頁、PNAS、2010年7月27日、第107巻、30号に示されている。一部の実施形態では、標的タンパク質の第一級アミノ酸配列中の天然の(すなわち、天然に存在する)アミノ酸またはアミノ酸残基の同位体標識を使用することができる。一部の実施形態では、天然および非天然のアミノ酸の同位体標識を一緒に使用することができる。さらに、一部の実施形態では、任意の生化学的実体(候補、標的または両方)の同位体標識を使用することができる。したがって、同位体標識はアミノ酸だけでなく、本明細書で提供される生化学的実体中の任意の原子または部分を含むことができる。一部の場合には、同位体の標識またはプローブは、本明細書の生化学的実体に付着させることもできる。
したがって、一部の場合には、標的タンパク質中の構造変化は、標的タンパク質の異なる突然変異体のアミノ酸配列に組み込まれた、非天然アミノ酸標識または一連のそのような標識の傾き角または絶対傾き角を測定することによって、リアルタイムにおよび本当の空間で判定することができる。プローブは、標的タンパク質中の任意の部位、またはその末端、またはその任意のドメインに組み入れることができる。一部の実施形態では、標的タンパク質は、UAAと共有結合的に反応するように化学的に備えられている第2高調波活性標識を含むことができる。例えば、タンパク質に組み入れられるUAAがパラ−アセチル−フェニルアラニン(pAcF)であるならば、第2高調波活性色素はpAcFに共有結合するための適当な化学をその上に有する。別の実施形態、第2のUAAに加えてSHAAの組入れでは、第2のUAA(それは、一般に第2高調波活性でない)は、第2のUAAとの反応のために適当な化学で誘導体化される表面への定方向でのタンパク質の化学的に直交性の共有結合を可能にする。SH活性である(2つのUAAを使用する)高度に一定方向に向けられた標的タンパク質試料では、SHGシグナルを生成するためにUAAを利用しない標的タンパク質と比較して、ベースラインSHGシグナルおよび対照(立体配置変化を有するシグナルの変化)の両方はより大きくなることができる。
他の場合には、本明細書に開示される方法のいずれかでの標的タンパク質のアミノ酸配列での1つまたは複数のUAAの使用は、標的タンパク質中の1つまたは複数の部位での1つまたは複数の標識の傾き角を時間の関数として判定することによって、候補アロステリックモジュレーターへの結合後に標的タンパク質が受ける実際の立体配置変化の判定を可能にする。標的タンパク質の三次元構造は、異なる位置に置かれるSHAAプローブを各々含有するタンパク質の1つまたは複数の突然変異体を作製することによって判定することができる(すなわち、各突然変異体での表面に対するプローブ配向、したがって側鎖配向は、各突然変異体のプローブについて判定することができ、全体の三次元タンパク質構造のモデルはこの情報を使用して造ることができる)。当業者に公知である立体障害方法、統計的方法、分子動力学、ラマチャンドランプロットまたはエネルギー最小化方法からの情報は、測定されたプローブ傾き角を与えられた構造の判定をさらに助けるために使用することができる。プローブの傾き角の時間分解測定は、リアルタイムで起こるときのタンパク質の立体配置変化のモーションピクチャーを生成する。SHGの(およびSFGの)事実上瞬間的な応答および感受性のため、特定のプローブの空間配向(例えば、表面に対する傾き角または絶対傾き角)は、シグナル強度が十分である限り、目的の任意の時間スケールで、リアルタイムで測定することができる。
SHG技術でのUAAの使用に関するさらなる情報は、米国特許出願公開第2010/0068144号に見出すことができ、その開示は参照により完全に本明細書に組み込まれる。
VIII.界面
本明細書に開示される方法の一部の態様では、標的タンパク質に結合した第2高調波活性標識が純配向を有するように、標的タンパク質は固体表面に結合しているまたは界面に対して配向される。標的タンパク質活性部位中での結合の際、または、その薬剤が標識標的タンパク質の構造の立体配置変化を誘導する限り、突然変異体もしくは野生型標的タンパク質の構造を不活性もしくは活性の立体配置に安定させることが可能な候補薬剤の結合の際に変化することができるのは、この純配向である。一部の実施形態では、界面は、シリカ、ガラス、ケイ素、ポリスチレン、ナイロン、プラスチック、金属、半導体または絶縁体表面、または生物構成要素が吸着または付着することができる任意の表面で作製することができる。異なる実施形態では、界面は気体−液体の界面、液体−液体の界面、液体−固体または固体−固体の界面であってもよい。一実施形態では、気体−液体の界面は空気−水の界面である。一実施形態では、液体−液体の界面は、油−水の界面である。異なる実施形態では、液体−固体の界面は水−ガラスの界面またはベンゼン−SiO2の界面である。
一部の態様では、界面は生物細胞およびリポソームの表面を含むこともできる。付着または固定は、当技術分野で周知である様々な技術によって起こすことができる。例えば、タンパク質では、生体分子の表面のアミンへのカップリングのために表面をアルデヒドシランで誘導体化することができる(MacBeathおよびSchreiber、2000年−その関連部分は参照により本明細書に組み込まれる)。最初に表面にBSAの分子層を付着させ、次にそれをN,N’−ジスクシンイミジル炭酸塩で活性化することによって、BSA−NHS(BSA−N−ヒドロキシスクシンイミド)表面を使用することもできる。BSA上の活性化リシン、アスパラギン酸またはグルタミン酸残基は、タンパク質上の表面アミンと反応する。
例えば、その関連部分が参照により本明細書に組み込まれるSalafskyら、Biochemistry、35巻、14773〜14781頁、1996年、その関連部分が参照により本明細書に組み込まれる「Biomembranes」、Gennis、Springer−Verlag、Kalbら、1992年、およびBrianら、1984年に記載のように、膜タンパク質または他の膜関連構成要素の有り無しで、支持リン脂質二重層を使用することもできる。支持リン脂質二重層は当技術分野で周知であり、関連膜タンパク質の有り無しでそれらの作製のために利用可能な、多数の技術がある。それらが空気に曝露されるときにそれらの破壊を阻止するために、これらの支持二重層は一般的に水溶液中に沈んでいなければならない。一部の実施形態では、表面は、脂質類似体二重層表面である。
固体表面を使用する場合(例えば、平面基質、ビーズなど)は、標的タンパク質−候補アロステリックモジュレーター相互作用の検出を最適化するためにその純表面電荷密度を低減または増強するために、それを様々な化学反応を通して誘導体化することもできる。他の実施形態では、固体表面は、ガラス表面、プラスチック表面、金属面、ラテックス表面、ゴム表面、セラミック表面、ポリマー表面、ポリプロピレン表面、ポリビニリデンジフルオリド表面、ポリスチレン表面またはポリエチレン表面(例えば、ポリエチレングリコール表面)であってもよい。標的タンパク質が固定化される支持体は、粒子、鎖、沈殿物、ゲル、シート、チュービング、球、容器、毛細管、パッド、切片、フィルム、プレートまたはスライドとして存在する広範囲の材料、例えば、限定されずに、生物、非生物、有機、無機またはこれらのいずれかの組合せで構成されてもよい。表面は、任意の都合のよい形状、例えば、限定されずに、ディスク、四角、球または環であってもよい。表面は好ましくは平らであってもよいが、様々な代替表面構成をとることもできる。例えば、表面は、試料(タンパク質など)が位置する、隆起したまたはくぼんだ領域を含有することができる。表面は、試料を形成することができる強固な支持体を好ましくは形成する。表面は、適当な光吸収特性を提供するようにも選択される。例えば、表面は、限定されずに、重合Langmuir Blodgettフィルム、官能基化されたガラス、Si、Ge、GaAs、GaP、SiO2、SiN4、改変ケイ素または各種のゲルもしくはポリマーのいずれか1つ、例えば(ポリ)テトラフルオロエチレン、(ポリ)ビニリデンジフルオリド、ポリエチレングリコール、ポリスチレン、ポリカーボネートまたはそれらの組合せであってもよい。他の表面材料は、当業者に容易に明らかになる。一実施形態では、基質は板ガラスまたはシリカである。
一部の態様では、所望の表面特徴を提供するために周知の技術を使用して表面をエッチングすることができる。例えば、トレンチ、v溝、メサ構造などの形成として、標的タンパク質(例えば、タンパク質の合成領域)は、当たる光の焦点内により近くに置かれてもよい。表面には、そこから収集される放射の最大化のために、反射「ミラー」構造を提供することもできる。別の例として、表面は、ウェルを形成するためにエッチングされてもよい。
本発明の別の態様では、親和性標識標的タンパク質をSHGまたはSFGの検出のための表面に固定化するために、オリゴポリエチレングリコール(PEG)分子を使用することができる。一部の実施形態では、PEGは、SAT(PEG4)(N−スクシンイミジルS−アセチル(チオテトラエチレングリコール)であってもよい。SHGシグナルを検出するのに適するペグ化された界面は、適する表面、例えば上記の表面のいずれかをオリゴPEG溶液でコーティングすることによって調製することができる。一実施形態では、表面はガラスであってもよい。別の実施形態では、表面はアミノ末端シラン誘導体化ガラスであってもよい。親和性タグは当技術分野で一般的であり、例えば、ヒスチジンタグ(His6タグなど)、マルトース結合タンパク質タグ、HAタグ、ビオチンタグ、チオールタグまたはGSTタグであってもよい。一部の実施形態では、親和性タグは、1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20またはそれを超える数のいずれかの数のヒスチジン残基を有するヒスチジンである。一実施形態では、オリゴPEG分子は、標的タンパク質の上で発現される親和性タグに結合する薬剤で改変される。ヒスチジンタグの場合、薬剤はニッケルもしくはコバルトであってもよく、またはそれは、糖(マルトースなど)、抗体、もしくは親和性タグに結合することが可能である当技術分野で公知の任意の他の分子であってもよい。
IX.キット
本発明は、本明細書に記載される方法の実施で使用するための組成物を含むキットを提供する。例えば、キットは、標的生化学的実体(例えば、標的タンパク質)へのコンジュゲーションのための1つまたは複数のSHG、SFGまたはDFG活性部分(標識など)、例えば本明細書に記載されるSHG、SFGまたはDFG活性標識(色素標識など)のいずれかを含むことができる。これらには、特異的官能基ごとに異なるカップリング化学作用を有する色素標識、例えば、限定されずに、マレイミド標識(例えば、PyMPO−MALEIMIDE(商標)(1−(2−マレイミジルエチル)−4−(5−(4−メトキシフェニル)オキサゾール−2−イル)ピリジニウムメタンスルホネート))、PyMPO−NHS、オキサゾール標識、BADAN(商標)(6−ブロモアセチル−2−ジメチルアミノナフタレン)、PyMPO−SE(商標)(1−(3−(スクシンイミジルオキシカルボニル)ベンジル)−4−(5−(4−メトキシフェニル)オキサゾール−2−イル)ピリジニウムブロミド)およびACRYLODAN(商標)(6−アクリロイル−2−ジメチルアミノナフタレン)を含めることができる。他の実施形態では、色素はクマリンをベースとした色素、例えば限定されずに、ケトクマリンおよび3,3’−カルボニルビス(7−ジエチルアミノクマリン)であってもよい。
キットへの組入れのために、本明細書に開示される方法のいずれかで使用するためのSHG、SFGまたはDFG活性標識でタンパク質を標識するためのツールおよび試薬も企図される。これらには、限定されずに、異なる標識条件を試験するためのバッファーパネル、標識反応を実施するためのバッファー、標識反応を実施するための管、未結合の標識から標識タンパク質を精製するためのスピンカラムおよび/またはゲル濾過カラム、ならびに標識タンパク質を洗浄するためのバッファーを含めることができる。
別の実施形態では、キットは、標的生化学的実体(例えば、タンパク質)を結合するための1つまたは複数の表面、例えば本明細書に開示される表面のいずれかを含むことができる。これらの表面は、再使用できるか、または消耗できる(すなわち、1回または限定回数の使用を目的とする)ものであってもよい。表面は、ガラス(ガラススライドなど)、プラスチック、金属、ラテックス、ゴム、セラミック、ポリマー(例えば、限定されずにポリプロピレン、ポリビニリデンジフルオリド、ポリスチレンまたはポリエチレン(例えば、ポリエチレングリコール))、または生化学的実体(例えば、タンパク質などの生物分子)が吸着または付着することができる任意の表面で作製することができる。一部の実施形態では、表面は平滑である。しかし、他の実施形態では、表面は、予め形成された表面特徴、例えば、限定されずにトレンチ、v溝、メサ構造および/またはウェルを含むことができる。さらに、表面は、本明細書に開示される方法のいずれかに従って前洗浄することができる。追加の実施形態では、表面が予め形成された表面特徴を含まない場合、キットは、表面にウェルを鋳型形成するための接着性のガスケットを含有することができる。
一実施形態では、キットに含まれる表面は異なる励起幾何構造のために最適化することができ、ここで、非線形光学的光を送達または生じるモードは、限定されずに、1つまたは複数のTIR(内部全反射)、伝達または反射に基づく。
さらなる実施形態では、本明細書に開示されるキットに含まれる表面は、標的生化学的実体(例えば、標的タンパク質)への付着に適する表面化学を提供する1つまたは複数の分子で前コーティングされてもよい。これらの分子には、本明細書に開示される分子のいずれか、例えば、限定されずにアルデヒドシラン、BSA−NHS(BSA−N−ヒドロキシスクシンイミド)またはオリゴポリエチレングリコール(PEG)を含めることができる。一実施形態では、分子は、親和性タグ、例えば本明細書に開示されるもののいずれかを含むことができる。例えば、表面は、表面にヒスチジン標識タンパク質を固定化するためのニッケル−オリゴPEG分子でコーティングすることができる。
別の実施形態では、キットに含まれる表面は、支持脂質(例えば、限定されずにリン脂質)二重層または支持脂質類似体二重層で前コーティングされてもよい。キットのこの実施形態は、本明細書に開示される表面のいずれかの上で支持脂質二重層または支持脂質類似体二重層を調製するのに使用される脂質または脂質混合物も含む。一部の実施形態では、脂質混合物は、ホスホコリン、例えば、限定されずに、DOPC(1,2−ジオレイル−sn−グリセロ−3ホスホコリン)を含むことができる。一部の実施形態では、脂質混合物は、限定されずに、DDAB(N,N−ジステアリル−N,N−ジメチルアンモニウムブロミド)、DMRIE(N−(1,2−ジミリスチロキシプロパ−3−イル)−N,N−ジメチル−N−ヒドロキシエチルアンモニウムブロミド)、DODAC(N,N−ジオレイル−N,N−ジメチルアンモニウムクロリド)、DOGS(ジヘプタデシルアミドグリシルスペルミジン)DOPE(1,2−sn−ジオレイルホスファチジエタノールアミン)、DOSPA(N−(1−(2,3−ジオレイルオキシ)プロピル)−N−(2−(スペルミンカルボキサミド)エチル)−N,N−ジメチルアンモニウムトリフルオロアセテート)、DOTAP(N−(1−(2,3−ジオレイルオキシ)プロピル)−N,N,N−トリメチルアンモニウムクロリド)、DOTMA N−(1−(2,3−ジオレイルオキシ)プロピル)−N,N,N−トリメチルアンモニウムクロリドの1つまたは複数を含むことができる。さらなる実施形態では、脂質または脂質混合物の脂質構成要素のいずれかは、タンパク質への結合のための親和性タグを含むことができる(例えば、限定されずに、ニッケル化脂質、例えばDOGS−Ni−NTA脂質)。
本明細書に開示されるキットの1つまたは複数への組入れのために、標的生化学的実体(例えば、生体分子)と別の生化学的実体(例えば、薬物候補)の間の結合相互作用の特異性を判定するための、生化学的実体の間の相互作用(例えば、標的タンパク質−薬物候補相互作用)および標的生化学的実体(例えば、タンパク質)立体配置構造への効果の検出のための機器で使用するためのシグナル周辺機器も企図される。これらには、パスフィルター、カラーフィルター、干渉もしくは他のスペクトルフィルター(波長選択のためもしくは高調波から基本波(複数可)を分離するための)、1つまたは複数の偏光光学部品ならびに/または光線を誘導および収束するための1つもしくは複数の鏡もしくはレンズを含めることができる。定量的測定のための電動式回転ステージも、本明細書に開示されるキットに含まれてもよい。
別の実施形態では、タンパク質または酵素の機能のために必要な1つまたは複数の補因子が、本明細書に開示されるキットに含まれてもよい。これらには、無機の補因子(例えば、限定されずに、銅、鉄、マグネシウム、マンガン、モリブデン、ニッケル、コバルトまたは亜鉛イオン)が含まれてもよい。これらには、有機補因子、例えば、限定されずに、チアミンピロリン酸、NAD+(NADH)、NADP+(NADPH)、ピリドキサールリン酸、リポアミド、メチルコバラミン、コバラミン、ビオチン、補酵素A、テトラヒドロ葉酸、メナキノン、アスコルビン酸、フラビンモノヌクレオチド、フラビンアデニンジヌクレオチド、補酵素F420、アデノシン三リン酸(ATP)、アデノシン二リン酸(ADP)、グアノシン三リン酸(GTP)、グアノシン二リン酸(GDP)、S−アデノシルメチオニン、補酵素B、補酵素M、補酵素Q、シチジン三リン酸、グルタチオン、ヘム、ヌクレオチド糖、ピロロキノリン、キノンおよび/またはテトラヒドロビオプテリンを含めることもできる。本明細書に開示されるキットのいずれかへの組入れのために、1つまたは複数の標的タンパク質(例えば、ユビキチンもしくはSUMO)に結合することが知られている1つまたは複数の標識(例えば、SFGもしくはSHG標識)ペプチドおよび/もしくはタンパク質、あるいは1つまたは複数のSFGもしくはSHG標識抗体もしくはその断片も企図される。
さらに他の実施形態では、キットは、生化学的実体(例えば、タンパク質)にSHG、SFGまたはDFG活性非天然アミノ酸(UAA)標識を導入するための1つまたは複数の構成要素を含むことができる。これらの構成要素には、限定されずに、無細胞翻訳抽出物、特定の非天然アミノ酸標識(例えば、Aladan)を導入するためのtRNA/tRNAシンセターゼ対ならびに/または反応および洗浄バッファーを含めることができる。
別の実施形態では、キットは、生細胞標識のための1つまたは複数の構成要素を含むことができる。これらには、限定されずに、細胞付着のための表面、SHG、SFGまたはDFG活性標識、細胞標識反応に使用されるバッファー、未反応標識を除去するためのウォッシュアウトバッファー、および細胞増殖培地を含めることができる。
一部の例では、これらの構成要素は、生化学的実体(例えば、標的タンパク質)の上の1つまたは複数の位置で、例えば、活性部位、結合部位、アロステリック結合部位、またはタンパク質構造の上もしくはその中の任意の他の部位(例えば、アッセイによってスクリーニングされる立体配置変化を受けることができる任意の部位、in vivoまたはin vitroの薬理特性と相関する立体配置変化を受ける任意の部位など)から所与の距離の(例えば、そこのまたはそれに隣接した)戦略的位置で標識を選択的に実施させることができる。キットは、所定位置で選択的標識を達成するためのツールを含むことができる。例えば、キットは、本明細書の他の場所で記載されるシグネチャーをベースとしたスクリーニングおよび評価を可能にする同じ位置で複数の標的生化学的実体を標識するためのツールを含むことができる。
X.系
本発明は、本明細書に記載される方法の実施で使用するための系も提供する。一部の実施形態では、系は、SHG、SFGまたはDFG活性部分(例えば、本明細書で提供される組成物、方法またはキットのいずれかで開示されるSFG、SHGまたはDFG活性部分、例えば、SFG、SHGもしくはDFG活性色素標識またはSFG、SHGもしくはDFG活性非天然アミノ酸)で標識される標的タンパク質を含む。系は、標的タンパク質−薬剤相互作用の検出のための機器であって、i)基本光の光源;ii)表面付着プローブを有する基質(例えば、SHG標識、SFG標識またはDFG標識標的タンパク質);およびiii)第2高調波または他の非線形光線の強度を測定するための検出器を含む機器も含む。系の一部の実施形態では、タンパク質上のアロステリック部位への薬剤の結合は機器によって検出され、検出器によって記録されるデータは記憶媒体を読み出す系によってアクセス可能である固定記憶媒体またはデータ記憶媒体に記録することができる。
他の実施形態では、系は、モノクロメーター(波長選択のため)、パスフィルター、カラーフィルター、干渉もしくは他のスペクトルフィルター(波長選択のためもしくは高調波から基本波(複数可)を分離するための)、1つもしくは複数の偏光光学部品、光線を誘導および収束するための1つもしくは複数の鏡もしくはレンズ、コンピュータ制御器またはソフトウェアをさらに含む。系は、プロセッサーを有するコンピュータを含むことができ、プロセッサーは、メモリに動作可能に連結され、(例えば、ソフトウェアを具体化するアルゴリズム(複数可)を実行するために)コンピュータ制御器またはソフトウェアを実行するように構成される。他の実施形態では、非線形の光学光(例えば、SHG)を送達または生じるモードは、以下の手段の1つまたは複数に基づくことができる:TIR(内部全反射)、ファイバーオプティックス(付着ビーズの有り無しで)、伝達(基本波は試料を通過する)、反射(基本波は、試料から反射される)、スキャン画像化、共焦画像化またはスキャン、パワー増強または多重パスセットアップのための空洞共振器。
系の別の実施形態では、測定された情報は、以下のパラメータの1つまたは複数を含むことができるベクターの形をとることができる:光の強度(一般的にPMTもしくはフォトダイオードによって光電圧に変換される)、光の波長(モノクロメーターおよび/もしくはフィルターで判定される)、時間または位置。機器の2つの一般的な配置は、画像スキャン(例えば、x,y座標の関数としての基質−強度、波長などの画像化)および分光学的(例えば、一部の平面または細胞、リポソームもしくは他の粒子の懸濁液のための強度、波長などの測定)であってもよい。
本発明は、例示として提供され、限定するものではない以下の実施例を参照することによって、さらによく理解することができる。
(実施例1):アルファシヌクレインを標的にする薬物候補のスクリーニング方法
ここで、本発明者らは、標的タンパク質のリアルタイムの立体配置変化の読み出しを使用する、リガンドスクリーニング方法としてのSHGの最初の使用を報告する。本発明者らは、タンパク質アルファシヌクレイン、パーキンソン病(PD)の治療標的、のスペルミンによって誘導される立体配置変化に重点を置いた。本発明者らは、ツール化合物としてスペルミンを使用して、タンパク質に結合してその立体配置をモジュレートするリガンドを同定することができるかどうか答えを求めた。アルファシヌクレインは140残基の非常に酸性のタンパク質であり、PDのための主要な標的である。PDはアルツハイマー病に次いで2番目に最も普通の神経変性疾患であり、米国では1,000,000〜1,500,000人に影響を及ぼす(Lang AE & Lozano AM、New England Journal of Medicine 339巻(16号):1130〜1143頁(1998年)。疾患の2つの特質は、中脳黒質中のドーパミン作動性ニューロンの減少、およびニューロン中の、主にアルファシヌクレインの凝集体で構成されるレーヴィ小体(LB)の存在である。アルファシヌクレインの点突然変異は早期発症PDの稀な形に関係があり、そのタンパク質が疾患機構に関係していることを示唆する(Klockgether T、Cell and Tissue Research318巻(1号):115〜120頁(2004年)。疾患患者の脳で見出されるより大きな凝集体の前に形成されるアルファシヌクレインのオリゴマーは、in vivoで神経毒である可能性を益々多くの証拠が示唆する(Winner Bら、Proceedings of the National Academy of Sciences. 108巻(10号):4194〜4199頁(2011年)。タンパク質がモノマーからフィブリル凝集体に進行する過程は、現在熱心な詳細調査の対象である(Norris EHら、Journal of Biological Chemistry280巻(22号):21212〜21219頁、2005年;Karpinar DPら、EMBO J28巻(20号):3256〜3268頁、2009年)。近年の報告は、タンパク質がin vivoでテトラマー構造を採用することを示し、モノマーへの解離がオリゴマー化および凝集に先行することを意味する。毒性の種に関係なく、モノマーのアルファシヌクレインは、それを安定させることができ、最も初期のステージで凝集を阻止することができる薬物のための魅力的な治療標的である。アルファシヌクレインは、in vitroで広く研究されている(Winner Bら、Proceedings of the National Academy of Sciences. 108巻(10号):4194〜4199頁、2011年;Bertoncini CWら、Proceedings of the National Academy of Sciences of the United States of America102巻(5号):1430〜1435頁、2005年;Conway KA、Harper JDおよびLansbury PT、Biochemistry39巻(10号):2552〜2563頁、2000年)。それは生来非構造化物であり、コンパクトなものから完全に伸長したものまで一定範囲の立体配置を採用する(Bertoncini CWら、Proceedings of the National Academy of Sciences of the United States of America102巻(5号):1430〜1435頁、2005年)。C末端とN末端の間の相互作用は、主にコンパクトな立体配置のタンパク質を安定させるようである。1つの仮説によると、タンパク質がスペルミンなどのポリアミンまたは低いpHに曝露されるとき、これらの相互作用が破壊され、in vitroで凝集速度は大いに増加する。スペルミンの効果についての別の仮説によると、結合したスペルミンはC末端領域の非常に負の電荷状態を低減し、タンパク質分子間の静電反発力を弱くし、凝集速度が大いに増強される(McClendon S、Rospigliosi CCおよびEliezer D、Protein Science18巻(7号):1531〜1540頁、2009年)。いずれの場合も、タンパク質は凝集の前に立体配置変化を受ける。
アルファシヌクレインの結合剤または立体配置モジュレーターを同定する目的のために、鋳型形成された顕微鏡スライドを読み取るArtemisと呼ばれるSHGをベースとしたスクリーニング機器を造った。タンパク質の立体配置に及ぼすリガンドの効果は、その機器によってリアルタイムで検出され、報告される。シリコーン鋳型は、各スライドの上に16個のウェルを規定する;ウェルの測定は、完了に数秒かかる。現行のスループットは1日につき数百アッセイ程度であり、断片または重点的ライブラリースクリーニングに適するが、標準のフルイディクスおよびオートメーションを実行することによって、本発明者らはこの技術を高いスループットに拡大することを意図する。
本発明者らは、生来非構造的なタンパク質、モノマーアルファシヌクレイン、パーキンソン病(PD)の標的、のために、立体配置変化のSHGアッセイを開発した。モノマーからオリゴマー、オリゴマーからフィブリルへのアルファシヌクレイン凝集は、発病と関連づけされ、リガンドへの結合またはpH変化によって誘導されるモノマー立体配置の変化が先行すると考えられている。内因性のポリアミンであるスペルミンは、in vitroでその凝集速度を105倍に増加させ、発病で役割を果たすことができるタンパク質の立体配置変化を誘導する。アルファシヌクレインの立体配置変化アッセイの構築におけるツール化合物として、本発明者らはスペルミンを活用した。タンパク質の立体配置へのスペルミンの効果を阻害することができる化合物について、本発明者らはこのアッセイを使用して断片ライブラリーをスクリーニングした。本発明者らのスクリーニングは、スペルミンの効果を完全に消滅させる1つの化合物をライブラリーから同定した。タンパク質の立体配置に及ぼすその効果を単独で試験したとき、この化合物はスペルミンのものに類似した立体配置変化のSHG応答「シグネチャー」を生成し、それが同じ立体配置を誘導することができ、スペルミンと同じ部位に結合することができることを示唆する。スペルミンが結合する領域であるモノマータンパク質のC末端領域にこの化合物が結合することを、本発明者らは、1H、15N異核単一量子干渉(HSQR)NMRによってその後確認した。従来の技術によってこのタンパク質をスクリーニングするのが困難であったことから、アルファシヌクレインに結合することが公知の化合物はほとんどなく、したがって本発明者らの方法は、アルツハイマー病の標的であるベータアミロイドに関するモノマーの非凝集立体配置および類似物を安定化することができる化合物を同定する手段を提供する。本発明者らが発見した化合物は、このタンパク質のC末端領域に結合することが分かった最初のものであり、治療リード物質の開発のための有益な出発点になることができる。原則としてSHGを任意の標的に適用することができるので、本発明者らがここに紹介する技術は、基礎研究および薬物発見のための広範な可能性を有する、タンパク質の立体配置をモジュレートするリガンドを同定、検証するための、高感度で迅速な手段を提供する。
方法
アルファシヌクレインの精製および標識:アルファシヌクレインの単一部位システイン突然変異体(A90C)を構築し、PyMPO−マレイミド(Invitrogen)、以前の研究で使用したSH活性プローブ、で標識した(Salafsky、Journal of Chemical Physics125巻(7号)、2006年;Salafsky、Physical Chemistry Chemical Physics9巻(42号):5704〜5711頁、2007年)。突然変異体(A90C)タンパク質は、野生型のように機能すると以前に判定された(Bertoncini CWら、Proceedings of the National Academy of Sciences of the United States of America102巻(5号):1430〜1435頁、2005年)。標識は、製造業者の指示に従ってタンパク質にカップリングさせ、ゲル濾過によって精製した。
Artemis SHGスクリーニング機器:Artemis機器は、第2高調波光(高いピークパワー強度)を生成するのに必要な基本光線を提供する、モードロックTi:サファイヤ発振器で構成される。本発明者らは、基本波供給源として、Millenia V DPSSレーザー(Spectra−Physics Corp.)によって送られるMira 900 Ti:サファイヤ超高速発振器(Coherent Inc.)を使用した。Ti:サファイヤ発振器は、80MHzで約200fsのパルス時間により、780nmで0.75Wの基本波パワーを生成した。基本波は、この実施例で記載される全ての実験のためにp偏光を選択するために半波長板を通過させ、内部全反射(TIR)のためのドーブプリズムに約50μmのスポットサイズまで収束させた。第2高調波光を集光レンズで収集し、ダイクロイックミラーおよび波長フィルターを使用して基本波と分離し、光子計数のためのビルトイン前置増幅器を有するPMTモジュール(Hamamatsu)に誘導した。シグナルをデジタル化するためにカスタム仕様のエレクトロニクスボードを使用し、制御およびデータ収集ソフトウェア(LabView)を実行するコンピュータにデータを送った。
BK7指数マッチング液(Cargille)を使用してタンパク質を有するスライドをプリズムと連結させ、プリズム自体は10μmのランダムアドレス可能な精密度が可能な1−D翻訳ステージ(Renishaw)の上に固定した。16ウェルの各々は、制御ソフトウェアによってステージを翻訳することによって順番に読み取る。Artemisは、液体ボーラスを送達する単一チャネルの液体注入器(Cavro)を装備していた。液体ボーラス容量および送達速度は、異なっていてもよかった。ここで記載される実験では、本発明者らは、1秒で送達される10μlの容量を使用した。測定パラメータには、リガンド注射の前後の読み出し時間、組込み時間、ステージ温度(ここの全ての実験では室温に保った)および基本光線のラインに対するステージ位置が含まれる。
アルファシヌクレインアッセイスライドの調製:各スライドの上に直径3mmの16ウェル(容量約15μl)を規定するために、特製の組立ジグを使用して市販のXenobindガラス顕微鏡スライド(Xenopore)に、接着性裏材を有するカスタム仕様のシリコーン鋳型(Arrowleaf Research)を適用した。ウェルを規定する鋳型は、標準の96ウェルプレートに合わされる。PyMPO−マレイミド標識アルファシヌクレインの保存溶液は、リン酸緩衝食塩水(PBS)で5μM最終濃度に希釈し、30分の間室温でインキュベートすることによって各ウェルのガラス表面への吸着を可能にした。タンパク質を吸収させた後に、スライドをArtermisプラットホームに置き、各ウェル中のタンパク質の量を判定するために、各ウェルをSHGによってスキャンした。未結合のタンパク質は、20μLのPBSによる5回の洗浄によって次に取り出した。どのくらい多くのタンパク質がスライド表面に結合しているかを判定するために、洗浄後のウェルのスキャンを次に実施した。
Maybridgeライブラリースクリーニング:Maybridge Ro3断片ライブラリーは、DMSOに50mMで可溶化された、純度≧95%の1,000個を超えるファーマコフォア化合物を含有する。断片スクリーニング実験のために、ライブラリーからの単一の化合物をPBSに希釈し、1mM(4%DMSO)の最終濃度で各ウェルに入れた。確実にバッファーミスマッチが起こらないようにするために、スクリーニングの間に使用された洗浄バッファーは、PBS+4%DMSOであった。次にスライドを機器に装填し、ベースラインシグナルをリアルタイムで測定し、SHGシグナルを読み取りながらスペルミンを5mMで注入した。これらの実験において、ベースラインシグナルは8秒の間監視し、その後スペルミンを注入し、SHGシグナルはさらに8秒の間記録した。
用量反応曲線のあてはめ:スペルミン(Sigma)、スペルミジン(Sigma)および化合物Aの用量反応曲線を判定するために、各化合物の連続希釈液を使用して保存溶液を調製した。各化合物をウェルに加えて、指示された最終濃度を生成した。スペルミンについては、試験した濃度範囲は、10μM、200μM、400μM、600μM、800μM、1mMおよび5mMであった。スペルミジンについては、濃度は、10μM、62.5μM、125μM、250μM、500μM、1mMおよび30mMであった。化合物Aについては、濃度範囲は、5μM、32.5μM、62.5μM、125μM、250μM、500μMおよび1mMであった。濃度はlogスケールに次に変換し、可変勾配によるlog(アゴニスト)対応答のための非線形回帰あてはめを使用してGraphPad Prism V5にデータをプロットした。最も低い濃度および最も高い濃度の値がそれぞれ0および100%に等しくなるように、データを正規化した。EC50値は、ソフトウェアによって計算した。
競合アッセイ:スペルミン−スペルミジン競合アッセイについては、5μMの標識アルファシヌクレインを含有する各ウェルに最終濃度1mMのスペルミンを入れ、SHG強度の変化を測定した。次に、1mMスペルミンの存在下においてタンパク質を室温で25分間インキュベートさせた。25分後に、3mMのスペルミジンを各ウェルに加え、SHG強度の生じた変化を測定した。各個々の類似体を先ずアルファシヌクレインと25分間インキュベートし、その後1mMのスペルミンをウェルに加えたこと以外は、類似体−スペルミン競合アッセイを上記の通りに実施した。
スペルミン−化合物A競合アッセイについては、5μMの標識アルファシヌクレインを含有する各ウェルに5mMのスペルミンを入れ、SHG強度の変化を測定した。スペルミンの存在下でタンパク質を1分間平衡化させ、100μMまたは1mMのいずれかの化合物Aを各ウェルに加え、SHG強度の変化を測定した。
SHG強度の変化の数量化:各化合物が最大応答(Tmax)を生成するのに必要とされる時間枠を実験により判定するために、対照実験を各化合物について実施した。フタロシアニンテトラスルホネート(PcTs;Sigma)を使用したもの以外の全ての実験については、SHGで測定した最大応答は化合物添加から30秒以内に起こった。PcTs実験については、最大応答は化合物添加からおよそ45秒後に起こった。
変化パーセントを計算するために、以下の式により、注入(T0)の直前に測定したSHG強度をTmax時のSHG強度から引き算し、次にT0で割り算した:SHG%=(ISHG@Tmax−ISHG@T0)/ISHG@T0。
SHG強度変化の閾値を判定するために対照バッファー注入を使用し、上と類似の方法で計算した。化合物添加によって生成されたSHG強度値からバッファー閾値を引き算することによって、各化合物の純SHG強度変化が次に報告された。生じた値は、化合物添加によるSHG強度の変化パーセントとして報告された。
結果
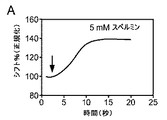
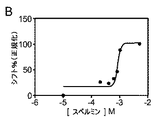
スペルミンは、アルファシヌクレインの立体配置変化を誘導する:第2高調波発生(SHG)によりアルファシヌクレイン立体配置変化を阻害する新規化合物についてスクリーニングするために、スペルミンを使用するアッセイを開発した。スペルミンは多数の細胞過程に関与するポリアミンであり、in vitroで凝集速度の増加をもたらすアルファシヌクレインの立体配置変化を誘導することが以前に示された。本発明者らのアッセイでは、カスタム仕様で組み立てられた顕微鏡スライドの各ウェルにオリゴマー形成のための閾値未満の濃度である5μMのアルファシヌクレインを加え(Fernandez COら、EMBO J23巻(10号):2039〜2046頁、2004年)、スペルミン添加の前後のSHGシグナルをリアルタイムで測定した。5mMのスペルミンの添加の際、SHGシグナル強度は即座に増加する(図1A)。本発明者らは、SHG強度の変化を36.26±4.97%と測定した。この変化は、NMRで示すようにアルファシヌクレインのC末端へのスペルミン結合によって誘導される公知の立体配置変化に対応する(Bertoncini CWら、Proceedings of the National Academy of Sciences of the United States of America102巻(5号):1430〜1435頁、2005年)。SHGを使用して、本発明者らはアルファシヌクレインへのスペルミン結合の用量反応曲線を得(図1B)、スペルミンのEC50を0.84mMと判定した(logEC50−3.07)[反復:0.79mM(logEC50−3.13)]。
スペルミンに緊密に関連するポリアミンであるスペルミジンも、アルファシヌクレインに結合して立体配置変化を誘導することが公知である。追加の対照として、本発明者らはタンパク質に及ぼすその効果を試験し、それもアルファシヌクレインの立体配置変化を誘導し、スペルミンのものに類似したSHGシグネチャーを有することを見出した(図1C)。スペルミジンの3mM用量は、SHG強度の19.88±2.37%の増加をもたらす。次に、スペルミジンの用量反応曲線を判定した(図1D)。SHGにより、スペルミジンの結合親和性を1.11mM(logEC50=−2.95±0.19)と測定した。本発明者らのSHG由来の用量反応曲線のEC50結果を検証するために、スペルミンとスペルミジンの間の競合アッセイを用いた。競合アッセイ(図1E)では、アルファシヌクレインを含有するウェルに1mMのスペルミンを加え、SHG強度の25.58±4.33%(反復:30.23±3.69%)の増加が測定された。1mMスペルミンの存在下で25分間のアルファシヌクレインのインキュベーションの後、3mMのスペルミジンを試料に加え、SHG強度の5.1±0.81%の変化が記録された。3mMスペルミジンの添加だけがSHG強度の約20%の増加を誘導することを考慮すると、スペルミンの存在下で見られた比較的小さい(約5%)増加は、スペルミンがアルファシヌクレインにスペルミジンより高い親和性で結合することを示唆し、本発明者らの実験により導かれた用量反応曲線と一致する。
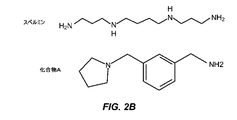
分子スクリーニングのためのプラットホームとしての第2高調波発生:本発明者らが観察するSHGシグナル変化がスペルミンまたはスペルミジンによって誘導される立体配置変化に対応することを実証した後、本発明者らは、アルファシヌクレインのスペルミンによって誘導される立体配置変化を阻害する新規化合物についてのスクリーニングを追求した。SHGをベースとした競合アッセイを使用して、スペルミン添加の際のアルファシヌクレインの立体配置変化を阻害するそれらの能力について、本発明者らはMaybridge Rule of Three(Ro3)断片ライブラリーからの1000個を超えるリガンドを2反復でスクリーニングした。各ウェルに5μMのアルファシヌクレインを加え、アッセイバッファー中の1mMのMaybridge Ro3ライブラリーからの1つの断片化合物と30分の間プレインキュベートした。次に、スペルミンを5mMで各ウェルに加え、SHGシグナルに生じた変化を測定した。1,000個の化合物の全ライブラリーから1つの化合物、化合物Aだけは、SHGで測定したときスペルミンによって誘導された立体配置変化を1mMの濃度で完全に阻止した(−1.39±1.05;図2A)。興味深いことに、図2Bに示す化合物Aは、スペルミンと電荷および長さが類似している。図2C(右トレース)に示すように、アルファシヌクレインへの1mMの化合物Aの添加は、SHGベースラインシグナルを直ちに変化させる。本発明者らはSHG強度の変化を31.67±4.31%と測定し、方向(ベースラインと比較した)、大きさおよび速度を使用してそのSHG応答をスペルミンの応答に類似と分類した(図3D)。
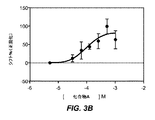
次に、SHGによって測定したときに、化合物Aがアルファシヌクレインの立体配置変化を誘導することができるかどうか判定した。図3Aに示すように、アルファシヌクレインへの1mMの化合物Aの添加は、SHGベースラインシグナルを直ちに変化させる。本発明者らはSHG強度の変化を30±2%(反復:31.67±4.31%)と測定し、方向(ベースラインに対して)、大きさおよび動態はスペルミンの応答に類似していた。この結果は、スペルミンのそれに類似しているアルファシヌクレインの立体配置変化を化合物Aが誘導することを示唆した。次に化合物Aを滴定し、SHGによってその用量反応を測定した(図3B)。このことから、本発明者らは、EC50を97.8μM(logEC50−4.01±0.28)と判定した。Kdがおよそ100μMであり、化合物Aは、アルファシヌクレインに対してスペルミンのそれよりおよそ5.5〜8倍高い親和性を有する。
化合物Aがアルファシヌクレインに対してスペルミンよりかなり高い親和性を有するとすれば、化合物Aはアルファシヌクレインへの結合に関してスペルミンを凌ぐはずである。化合物Aがアルファシヌクレインへの結合に関してスペルミンを凌ぐことができるかどうか判定するために、アルファシヌクレイン含有ウェルに5mMスペルミンを加えて1分の間平衡化させた競合アッセイを実施した。スペルミンだけの添加は、SHG強度の37.44±6.40%の増加をもたらした(図3C)。5mMスペルミンの存在下でのアルファシヌクレインのインキュベーションの後、1mMまたは100μMの化合物Aを各ウェルに加え、SHG強度の変化を記録した。スペルミンに前結合させたアルファシヌクレインへの1mM化合物Aの添加は、SHG強度の40.69±5.81%の増加をもたらした。これは、SHG強度の3.18±1.50%の増加をもたらした100μMの化合物Aの添加と対照的である。これらのデータは、その標的へのより高い親和性のために、化合物Aがアルファシヌクレインへの結合に関してスペルミンを凌ぐことを実証する。さらなる比較を、図3Dに示す。
本発明者らのSHG実験からの結果は、化合物Aがアルファシヌクレインに結合して、スペルミン結合に類似しているがアルファシヌクレインへのより高い親和性で立体配置変化を誘導することを示した。次に、化合物Aがアルファシヌクレイン上のスペルミンと同じ部位に結合するかどうか判定しようとした。これを行うために、アルファシヌクレインと複合体の化合物Aの構造を判定するために、独立した構造技術2−D HSQR NMRに変えた。
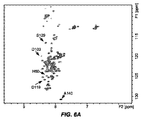
本発明者らのSHGおよびNMRデータの組合せは、化合物Aがスペルミンと同じ部位で(図6A)およびより高い親和性でアルファシヌクレインに結合することを実証し、それによって本発明者らの初期スクリーニングの結果を証明するだけでなく、構造スクリーニング技術としてのSHGを実証する。
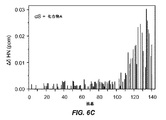
アルファシヌクレインと化合物Aの間の相互作用は、NMR分光法によって分析した。NMR共鳴はタンパク質−タンパク質およびタンパク質−リガンド相互作用の非常に高感度のプローブであり、したがって、相互作用界面および結合親和性の詳細な記載を提供することができる。化合物Aを15N標識アルファシヌクレインに加え、化学シフトの変化をアルファシヌクレインの二次元の1H−15N相関スペクトルで追跡した(図6B)。アルファシヌクレインの残基G111〜A140でNMRシグナルの有意な変化が観察された(図6Bおよび図6C)。アルファシヌクレインへのスペルミンの添加後に非常に類似した混乱プロファイルが観察されており、化合物Aおよびスペルミンの両方がアルファシヌクレインのC末端ドメインに結合することを示す。
溶液中でアルファシヌクレインが占めている立体配置のアンサンブルへの化合物Aの結合の結果は、常磁性緩和強化(PRE)を使用して研究した。特異的に付着している常磁性のニトロキシドラジカルと近くの陽子(約25Å未満)の間の相互作用は、横方向の緩和速度の増加のためにそれらのNMRシグナルの広幅化を引き起こす。この効果は電子−プロトン間の距離へのr−6の依存性を有し、したがってタンパク質での遠距離相互作用の検出を可能にする。化合物Aの存在下でアルファシヌクレイン中の一過性の遠距離接触を観察するために、本発明者らはアルファシヌクレインの90位に常磁性のMTSL標識を付着した。化合物Aの非存在および存在下でのMTSL−A90CアルファシヌクレインのPREプロファイルの比較は、残基40〜46および残基124〜136を覆うC末端領域での常磁性の広幅化の低減を明らかにした(図6D)。したがって、化合物Aの結合は、アルファシヌクレインでの一過性の遠距離相互作用を弱める。アルファシヌクレインでの遠距離相互作用の減弱は、スペルミンによって誘導されるアルファシヌクレイン凝集の加速と一緒に、スペルミンへの結合の際にも報告されている。したがって、アルファシヌクレインの凝集の増強について、化合物Aをさらに試験した。SHGおよびNMRによって同定された類似の結合モードと一致して、化合物Aも、アルファシヌクレインフィブリル化のラグ相を有意に短くした(図7A)。化合物Aの存在下(図7B、左)および非存在下(図7B、右)で得たアルファシヌクレインフィブリルの形態は、類似していた。したがって、本発明者らのSHGおよびNMRデータの組合せは、化合物AがアルファシヌクレインC末端に結合することを実証する。さらに、NMRおよびPREデータは、化合物Aがスペルミンと同じ部位、またはそれと実質的な重複部分を有する部位に結合し、スペルミンについて観察されるのと類似の方法で遠距離相互作用を弱めることによってタンパク質の立体配置に影響を及ぼすことを示し、それによって、初期スクリーニングの結果を確認し、構造スクリーニング技術としてSHGを実証する。
化合物Aは、アルファシヌクレインの立体配置変化を誘導するスペルミンの能力の選択的阻害剤である:1mMの断片濃度でスペルミンの応答の撤廃のヒット基準(例えば、添加後ベースラインの1%以内)を使用して、Maybridge Ro3ライブラリーを使用する本発明者らのスクリーニングにおいて、1つの化合物だけを同定した。よりストリンジェントでない条件下で本発明者らのライブラリーから、化合物Aの化学類似体の効果を調査するために、本発明者らはプログラムAcelot SimFinder(acelot.com/SimFinder.html)を使用して上位5つの化合物をランク付けした。図4Aで見られるように、類似体は構造的および化学的に化合物Aに類似している。アルファシヌクレインに曝露させたとき、これらの類似体のいずれかが単独でSHG強度の変化を誘導するかどうか、先ず判定した。1mMの各個々の類似体の添加は、SHG強度の増加をもたらした(図4B;表1)。SHG強度の増加はアルファシヌクレインの立体配置変化を示すが、SHGシグナル変化の大きさはスペルミンおよび化合物Aで報告した値より有意に低い(t検定)。これらの変化のSHG応答はベースラインと比較して振幅および方向が類似しているので、より低い大きさは、化合物Aによって誘導されるものと異なる立体配置変化ではなく同じ立体配置変化を引き起こす能力がより低いことを示すことができる。例えば、アルファシヌクレイン標的は同じ方法で標識することができ、異なる結合実体によって誘導される立体配置変化は、各アルファシヌクレイン標的の上またはその中の異なる位置、したがって標識から異なる距離で起こることができる。アルファシヌクレインの立体配置状態の変化(複数可)は、公知の薬理特性または公知の機能的効果と相関することができる。一部の場合には、相関はアルファシヌクレイン上の所与の位置での立体配置変化に特異的であってもよい。したがって、標識位置から離れて起こる立体配置変化は、検査される公知の薬理特性または公知の機能的効果と関連しなくてもよい。
図4Bと類似の比較を、化合物Aが5つの類似体と一緒に示されている図4Dに示す。
化合物Aの類似体のデータの結果をよりよく理解するために、アルファシヌクレインへの結合について類似体1、2および5をNMRによって試験した。図4Eで見られる化学シフト差の分析は、類似体1および2が化合物Aより弱くアルファシヌクレインに結合することを示唆する。
次に、アルファシヌクレインの存在下で類似体の各々を25分間インキュベートした競合アッセイを実施した。25分後に、1mMのスペルミンを各ウェルに加え、SHG強度の変化を記録した。類似体の存在下でインキュベートしたアルファシヌクレインへのスペルミンの添加は、全ての類似体でSHG強度の増加をもたらした(図4C;表1)。これらのデータは、化合物Aに化学的および構造的に類似しているが、これらの類似体は、スペルミンおよび化合物Aよりアルファシヌクレイン凝集を誘導する能力が低く、アルファシヌクレインへの親和性が低いことを示唆する。さらに、本発明者らの類似体競合アッセイからの結果は、Maybridge Ro3ライブラリーの中で化合物Aが唯一の競合的シヌクレインアグリゲーターであることを確認し、このように本発明者らの初期スクリーニングを実証する。
フタロシアニンテトラスルホネートは、異なるSHGシグネチャーを生成する:化合物Aに関する本発明者らのデータは、それがアルファシヌクレイン上のスペルミンと同じ部位に結合し、in vitroでアルファシヌクレインの凝集速度を増加させることが公知の立体配置を生成することを示唆する。アルファシヌクレインの凝集の増加は神経変性疾患の発病と関連づけられているので、アルファシヌクレイン凝集の公知の阻害剤、フタロシアニンテトラスルホネート(PcTs)が、スペルミンと比較して異なるSHGシグネチャーを生成するかどうか判定しようとした。図5Aに示すように、10μMのPcTsによる処置の結果、アルファシヌクレインのSHG強度の83.74±6.41%(反復:−79.6±2.7%)の低下を観察した。さらに、アルファシヌクレインの凝集を起こしやすい立体配置を誘導する他の分子と比較したとき、PcTs処置のSHG強度トレース(図5A)は、完全に特異なSHGシグネチャーを生成する。図5Bに示すように、アルファシヌクレインのSHG強度の変化は、10μMのPcTSによる処置後に−79.6±2.7%であると測定された。
これらのデータは、PcTsに類似のSHGシグネチャーを生成する化合物を選択することによって、アルファシヌクレイン凝集の新規阻害剤を同定できることを示唆する。
最後に、チオフラビンTアッセイで化合物Aを試験し(図7A)、アルファシヌクレインの凝集速度をin vitroでおよそ2倍増加させることが見出され、これはスペルミンの存在下で見られたのと同じ増加であった。したがって、この化合物はスペルミンとほぼ同じ機能的効果を有する。上記のように、この化合物はスペルミンと同じ立体配置変化も誘導する。
考察
薬物発見で鍵となる限界は、臨床的に重要な標的タンパク質の立体配置変化を誘導するリガンドを同定するための化学的空間を効率的に探索する能力である。ここに記載される研究で、本発明者らは、立体配置モジュレーターの同定のための構造技術として第2高調波発生を使用する最初の例を提示する。本発明者らは1,000個を超える化合物を含有する断片ライブラリーをスクリーニングし、スペルミンによって誘導されるアルファシヌクレインの立体配置変化を阻害する単一の化合物を同定した。その化合物、化合物Aは、単独で立体配置変化を引き起こすこと、およびスペルミンより高い親和性でアルファシヌクレインに結合することが示され、このリガンドがスペルミンと同じ立体配置変化を引き起こすことを示唆した。次に、化合物Aがスペルミンと同じ部位でアルファシヌクレインに結合し、類似の立体配置変化を誘導することを実証するためにNMRを使用した。
薬物発見のための新しいプラットホームとしての第2高調波発生:この研究は、特にスペルミンなどの公知の立体配置モジュレーターが比較目的のために利用可能であるならば、SHGがリガンド作用の機構を判定するための強力な方法であることを実証する。本発明者らの競合をベースとしたスクリーニングによって、スペルミンによって誘導されるアルファシヌクレインの立体配置変化の阻止における作用機構によって分類される2つのクラスのリガンドを見出すことができる可能性がある。第1のクラスのリガンドは、スペルミン結合部位またはその近くで結合する立体阻害剤である。第2のクラスのリガンドは、スペルミン結合を阻止する、アルファシヌクレインの立体配置変化を誘導するアロステリック阻害剤である。この研究で提供するNMRデータは、化合物Aが第1のクラスの阻害剤のメンバーであることを確認する。
しかし、より意外なことは、Maybridge Ro3ライブラリーからわずか1つの化合物だけが同定されたことである。スペルミンおよび化合物Aは長さおよび電荷が類似しているが、ライブラリー中のいくつかの化合物は化合物Aと構造類似性を共有する。これらの軽微な構造差には、化合物Aの5員環の6員環への変換、および追加の側鎖の存在が含まれる。本発明者らのアッセイにおいてスペルミンによって誘導されるアルファシヌクレインの立体配置変化の特異的で強力な阻害剤として化合物Aを同定する、およびそれと緊密に関連する分子を区別するSHGの能力は、この技術の感受性を実証し、スクリーニングプラットホームとしてのSHGの有効性を実証する。
分子スクリーニングのためのツールとしてのSHGシグネチャー:フタロシアニンテトラスルホネート(PcTs)は、in vitroでのアルファシヌクレイン凝集の公知の阻害剤である。その抗凝集効果にもかかわらず、PcTsは神経変性疾患の処置のための臨床的に重要な化合物でない。しかし本発明者らのアッセイでは、それがアルファシヌクレイン凝集を阻害する新規化合物の同定に有益である可能性を有する。これは、各分子が、ベースラインと比較したシグナル変化の方向、変化の大きさおよび動態の「SHGシグネチャー」を生成するという事実による。これらのシグネチャーは、結合情報単独よりストリンジェントなリガンド分類手段を提供する。さらに、分子のシグネチャーを公知のモジュレーターによって生成されるものと比較することによって、その分子の作用機構の推定上の分類を作製することができる(同じ標識および連結条件下で)。公知の立体配置モジュレーターに類似のシグネチャーを生成する化合物を同定しようとするときに、SHGシグネチャーによって化合物ライブラリーをスクリーニングすることもできる。例えば、このアプローチは、PcTsに類似しているアルファシヌクレインの立体配置変化を誘導する潜在的な抗凝集化合物についてMaybridge Ro3ライブラリーをスクリーニングするために使用することができる。
(実施例2):アルファシヌクレインを標的にする薬物候補の差別的スクリーニング
化合物Aおよびその類似体(図4A)は、6つの構造的(および化学的)に類似の候補生化学的実体のライブラリーを構成する。差別的スクリーニングを実施するために、表1の化合物単独(シフトまたは変化%)に記載の化合物Aおよびその類似体のSHG応答を使用することができる。アルファシヌクレインに曝露させたとき、化合物Aおよび類似体の各々はSHG強度の変化を誘導する。候補生化学的実体の各々は、異なるSHGシグネチャーを生じた。1mMの化合物Aの添加は、SHG強度の増加をもたらした(表1)。1mMの各個々の類似体の添加も、SHG強度の増加をもたらした(図4B;表1)。表1のシグネチャー応答は、アルファシヌクレインの第1の立体配置状態を測定し、それによってSHGベースラインを作成し、6つの構造的に類似の候補生化学的実体の各々をアルファシヌクレインと接触させ、アルファシヌクレインの第2の立体配置状態を測定し、それによって6つの候補生化学的実体のSHGシグネチャーを生じることによって生じた。SHGシグネチャーは、アルファシヌクレインの立体配置状態の変化を各々示す(全ての6つのシグナルはSHG強度の増加を示す)。さらに、候補生化学的実体の各々は、アルファシヌクレイン(標的生化学的実体)の立体配置状態において異なる変化を生成する。
表1のSHGシグネチャーは、互いと比較することができる(例えば、類似性を判定するために)。例えば、SHGシグネチャーは、コンピュータ実行可能プログラムを使用して分析することができる。一部の場合には、時系列での連続的なSHGシグネチャーを比較することができ、次のSHGシグネチャーは前のステップでの比較に基づいて選択される生化学的実体に対して比較することができる。一部の場合には、SHGシグネチャーの任意の2つまたはそれを超える数を比較することができる。一部の場合には、ライブラリー中の生化学的実体の全6つのSHGシグネチャーを互いと比較することができる。一部の場合には、SHGシグネチャーは、最も高い値、最も低い値、またはさもなければ規定の参照値を有するSHGシグネチャーと比較することができる。本明細書に記載される差別的スクリーニングは、例えば公知のモジュレーター(例えば、承認薬)が存在しない状況で使用することができる(例えば、一部の天然変性タンパク質のために)。一部の例では、候補生化学的実体から生化学的実体を選択するために、連続的なまたは同時の比較を行うことができる。
この実施例では、SHGシグネチャーは、SHGベースラインと比較したSHGシグナルの大きさの変化(例えば、標的生化学的実体の立体配置状態のエンドポイント変化;あるいは、標的生化学的実体の立体配置状態の動態学的(リアルタイム)変化を測定することができる)、およびSHGベースラインと比較したSHGシグナルの方向の変化(SHGパラメータ)を測定することによって生じた。異なるものの、一部の場合には、1つまたは複数のSHG類似性パラメータを使用して、少なくとも5つの類似体のSHGシグネチャーのサブセットを互いに類似していると分類することができる(ペアでまたは全部)。例えば、SHGベースラインと比較したSHGシグナルの大きさの変化の差は、5つの類似体について互いの50%以内であり、SHGベースラインと比較したSHGシグナルの方向の変化の差は、ライブラリー中の全ての6つの生化学的実体について同じである。
(実施例3):アルファシヌクレインを標的にする承認薬のSHG検出
この実施例では、アルファシヌクレインは、ドーパミン、そのプロドラッグレボドパ(承認薬)の代謝産物、への曝露によりシグナル変化を引き起こす。脳でドーパミンに変換されるLドーパとも呼ばれるレボドパは、今でもパーキンソン病の処置のためのゴールドスタンダードである。アルファシヌクレインの異常な折畳みおよび凝集は、この疾患の主要な病原因子であると考えられている。レボドパは、パーキンソン病に伴う症状のための最も有効な療法である。しかし、レボドパはプロドラッグ(すなわち、薬物の前駆体化合物)および、薬物の生物学的活性形であるドーパミンの前駆体である。
実験条件
天然のアルファシヌクレインにはシステイン残基がないので、色素コンジュゲーションのための部位特異的ペプチドを生成するために、アラニンからシステインへの突然変異(A90C)をアルファシヌクレインに導入した。標準の技術を使用してA90CアルファシヌクレインをPyMPO−マレイミドで次に標識し、改変されたペプチドの位置は質量分析によってシステイン90であることが確認された。
アルファシヌクレインで実施されるSHG実験のために、PyMPO−マレイミド標識A90Cアルファシヌクレインの保存溶液を、50mMのHepes、pH7.4、100mM NaClで5μMの最終濃度に希釈した。室温で1時間インキュベートすることによって、5μMのタンパク質溶液をアルデヒド誘導体化ガラススライドの上に次に固定化した。対照(バッファー)および化合物の注入は、50mM Hepes、pH7.4、100mM NaClで実施した。
実験は、第2高調波シグナル光(高いピークパワー強度)を発生するために必要な基本光線を提供する、モードロックTi:サファイヤ発振器を含む機器で実施した。本発明者らは、Millenia V DPSSレーザー(Spectra−Physics Corp.)によって送られるMira 900 Ti:サファイヤ超高速発振器(Coherent Inc.)を使用した。Ti:サファイヤ発振器は、80MHzで約150fsのパルス時間により、780nmで約0.7Wの基本波パワーを生成した。基本波は、(この実施例での全ての実験のために使用された)p偏光を選択するために半波長板を通過させ、内部全反射(TIR)のためのドーブプリズムに約50μmのスポットサイズまで収束させた。第2高調波光を集光レンズで収集し、ダイクロイックミラーおよび波長フィルターを使用して基本波と分離し、光子計数のためのビルトイン前置増幅器を有するPMTモジュール(Hamamatsu)に誘導した。シグナルをデジタル化するためにカスタム仕様のエレクトロニクスボードを使用し、制御およびデータ収集ソフトウェア(LabView)を実行するコンピュータにデータを送った。
結果
図8および図9は、アルファシヌクレイン立体配置に及ぼすドーパミン処置の効果を示す。
図8は、ドーパミンの添加の際のアルファシヌクレインのSHG強度の動態学的(リアルタイム)変化の例を示す。1mMのドーパミンの添加(図8で矢印によって示す)は、注入前レベル(矢印によって印を付けた注入前の時間)よりも増加したアルファシヌクレインの(正規化)SHG強度をもたらす。SHG強度の変化は、ドーパミン結合によるアルファシヌクレインの立体配置の変化の結果である。
図9は、バッファー単独(左)または1mMのドーパミン(右)の添加の際のアルファシヌクレインのSHG強度の平均変化の数量化である。対照(バッファー)注入の際のアルファシヌクレインのSHG強度の平均変化パーセントは、−1.74±0.57%である。エラーバー=SEM、N=4。1mMのドーパミン注入の際のアルファシヌクレインのSHG強度の平均変化パーセントは、3.375±1.13%である。対応のないt検定を使用すると、P値(図9で**によって示す)は統計的に有意である(P値=0.0067)と判定される。
考察
図8および図9のSHG結果(例えば、動態学的またはエンドポイントのSHGシグネチャー、シグナルまたはシグナル差)は、例えばドーパミンに類似のSHGシグネチャーを生成する化合物の選択によって、承認薬の活性形を置換または改良する新規薬物候補を(例えば、ドーパミンのSHG結果を候補薬物のSHG結果と比較することによって)同定するために使用することができる。これらの代替薬物は、承認薬の活性形と比較して、類似するまたは改良されたin vivoおよびin vitroの薬理特性、表現型および/または作用機構を示すことができる。例えば、薬物候補がドーパミンと同じSHG応答を示すならば、それは実質的に類似した治療効能および/または薬理学的(または薬物動態学的)特性を示すことができる。一部の場合には、そのような新規薬物候補は、向上した毒性および/または臨床安全性特性を示すことができる。レボドパのin vivoおよびin vitroの薬理特性、例えば薬物動態学的プロファイル、表現型の変化、効能および他の臨床データなどの例証は、参照により完全に本明細書に組み込まれる、David J Brooks、「Optimizing levodopa therapy for Parkinson’s disease with levodopa/carbidopa/entacapone: implications from a clinical and patient perspective」、Neuropsychiatr Dis Treat.2008年2月;4巻(1号):39〜47頁、およびその中の参考文献に示される。
(実施例4):構造−活性関係(SAR)の判定/カタログ作成
Rafキナーゼの200を超えるコピーを含む表面アレイを使用して、各々400から500g/molの間の分子量、3つの芳香族基および2〜5個の窒素原子を有する200個の異なる化合物およびソラフェニブを含むライブラリーを、構造−活性関係について評価する。化合物の非存在下でベースラインを確立するために、本出願に記載される単一高調波発生(SHG)方法によって、Rafキナーゼの立体配置状態を測定する。次に、ライブラリー中の各化合物を、アレイの上でRafキナーゼの単一コピーと接触させる。単一のキナーゼ標的の各コピーの立体配置状態は、SHG方法によって測定する。各化合物のSHGシグネチャーは、Rafキナーゼと接触させる際の立体配置状態の変化に基づいて判定される。ソラフェニブは、正の方向に30%のシフト(すなわち大きさ)を有するSHGシグネチャーを有する。構造−活性関係(SAR)カタログを作成するために、化合物はそれらのSHGシグネチャーおよび共通の構造パラメータに基づいて分類される。例えば、大きさがソラフェニブのそれの10%以内のシグネチャーを有する8つの化合物は、「400から500g/molの間の分子量、3つの芳香族基、2〜5個の窒素原子および+27%〜+33%の大きさを有するシグネチャー」と分類される。このSARプロファイルに基づいて、Rafキナーゼに対するそれらの阻害活性についてこれらの化合物がさらに試験され、化合物の3つがナノモル濃度で抗Raf活性を実際に示すことが発見される。このように、SHGシグネチャーは、化合物の特性をアッセイする追加の手段を提供することができ、ここで、化合物はSHGシグネチャーを使用して構造−活性関係に基づいて分類することができる。
本発明の好ましい実施形態が本明細書で示され、記載されているが、そのような実施形態は例としてだけ提供されることは当業者に明らかである。当業者であれば、本発明を逸脱しない範囲で、それにより多くの変形、変更および置換を思いつくと予想される。本明細書に記載される本発明の実施形態への様々な代替物を本発明の実施で用いることができることを理解すべきである。以下の請求項が本発明の範囲を規定し、これらの請求項の範囲内の方法および構造ならびにそれらの均等物はそれに含まれるものとする。
例えば、本発明は以下の項目を提供する。
(項目1)
生化学的実体をスクリーニングする方法であって、
(a)6つまたはそれを超える候補生化学的実体を含むライブラリーを用意するステップであり、前記6つまたはそれを超える候補生化学的実体は:
(i)前記候補生化学的実体の各々の150g/mol以内の分子量、
(ii)前記候補生化学的実体の各々の30%以内の分子量、
(iii)前記候補生化学的実体の各々の原子が15個以内の化学式、
(iv)前記候補生化学的実体の各々の間の15未満の全原子数の差、
(v)5未満の炭素原子数の差、
(vi)5未満の水素原子数の差、
(vii)5未満の窒素原子数の差、
(viii)5未満の酸素原子数の差、
(ix)5未満の硫黄原子数の差、
(x)前記候補生化学的実体の各々の10%以内のlog Dで測定される極性、
(xi)前記候補生化学的実体の各々の10%以内のlog P(分配係数)で測定される極性、
(xii)前記候補生化学的実体の各々の10%以内のPSA(極性表面積)で測定される極性、
(xiii)同一の足場コア、
(xiv)グラフ理論で測定される化学的類似性、
(xv)0.85を超えるTanimoto(またはJaccard)係数T、
(xvi)3未満の芳香族基数の差、
(xvii)3未満の複素環基数の差、
(xviii)3未満の単環基数の差、
(xix)3未満の縮合環系数の差、および
(xx)3未満の二重結合数の差
からなる群から選択される1つまたは複数の構造類似性パラメータを使用して判定するときに構造的に類似している、ステップと、
(b)標的生化学的実体の第1の立体配置状態を測定し、それによってベースラインを作成するステップと、
(c)前記候補生化学的実体の各々を同じ標的生化学的実体と接触させるステップと、
(d)前記標的生化学的実体の第2の立体配置状態を測定するステップと、
(e)前記第2の立体配置状態を使用して前記標的生化学的実体のシグネチャーを判定するステップと、
(f)前記シグネチャーに基づいて前記候補生化学的実体から1つまたは複数の生化学的実体を選択するステップと
を含む方法。
(項目2)
前記第1または第2の立体配置状態を測定するステップが、内部全反射(TIR)を使用する、項目1に記載の方法。
(項目3)
前記第1または第2の立体配置状態を測定するステップが、第2高調波発生(SHG)を使用する、項目1に記載の方法。
(項目4)
前記シグネチャーを判定するステップが、前記標的生化学的実体の立体配置状態の動態学的(リアルタイム)変化を測定するステップを含む、項目1に記載の方法。
(項目5)
前記シグネチャーを判定するステップが、前記標的生化学的実体の立体配置状態のエンドポイント変化を測定するステップを含む、項目1に記載の方法。
(項目6)
前記シグネチャーを判定するステップが、前記シグナルのシグナル強度を測定するステップを含む、項目1に記載の方法。
(項目7)
前記シグネチャーを判定するステップが、前記ベースラインを使用する、項目1に記載の方法。
(項目8)
コンピュータ実行可能プログラムを使用して、1つまたは複数の構造類似性パラメータに基づいて前記6つまたはそれを超える候補生化学的実体を分析するステップをさらに含む、項目1に記載の方法。
(項目9)
コンピュータ実行可能プログラムを使用して、前記シグネチャーを分析するステップをさらに含む、項目1に記載の方法。
(項目10)
前記候補生化学的実体の各々が、前記標的生化学的実体の立体配置状態において異なる変化を生成する、項目1に記載の方法。
(項目11)
前記標的生化学的実体の立体配置状態の前記変化を、公知の立体配置モジュレーターによって生成される立体配置状態の変化と比較するステップをさらに含む、項目1に記載の方法。
(項目12)
前記公知の立体配置モジュレーターが、公知の薬物である、項目11に記載の方法。
(項目13)
前記公知の立体配置モジュレーターによって誘導される立体配置状態の前記変化に最も類似している立体配置状態の前記変化に基づいて、1つまたは複数の生化学的実体を選択するステップをさらに含む、項目11に記載の方法。
(項目14)
前記公知の立体配置モジュレーターによって生成される立体配置状態の前記変化が、薬理特性または機能的効果に相関する、項目11に記載の方法。
(項目15)
ステップ(c)での接触の際に、前記候補生化学的実体の各々が異なるシグネチャーを生じる、項目1に記載の方法。
(項目16)
前記候補生化学的実体の少なくとも2つが、類似の薬理特性または機能的効果を有する、項目1に記載の方法。
(項目17)
前記候補生化学的実体の少なくとも2つが、類似の薬理特性または機能的効果を有しない、項目1に記載の方法。
(項目18)
i)前記ベースラインと比較した前記シグネチャーの大きさの変化、
ii)前記ベースラインと比較した前記シグネチャーの方向の変化、および
iii)前記候補生化学的実体の接触の際の前記シグネチャーの単位時間あたりのシグナルの速度の変化
からなる群から選択されるシグネチャーパラメータを測定するステップをさらに含む、項目1に記載の方法。
(項目19)
i)第1の候補生化学的実体との接触の際の前記ベースラインと比較した前記シグネチャーの大きさの前記変化が、第2の候補生化学的実体との接触の際の前記ベースラインと比較した前記シグネチャーの大きさの前記変化の50%以内であること、
ii)前記第1の候補生化学的実体との接触の際の前記ベースラインと比較した前記シグネチャーの方向の前記変化が、前記第2の候補生化学的実体との接触の際の前記ベースラインと比較した前記シグネチャーの方向の前記変化と同じであること、および
iii)前記第1の候補生化学的実体との接触の際の前記シグネチャーの単位時間あたりのシグナルの速度の変化が、前記第2の候補生化学的実体との接触の際の前記シグネチャーの単位時間あたりのシグナルの速度の変化の2倍以内であること
からなる群から選択される1つまたは複数のシグネチャー類似性パラメータを使用して判定したときに、前記第1の候補生化学的実体によって生じる前記シグネチャーおよび前記第2の候補生化学的実体によって生じる前記シグネチャーが類似している、項目1に記載の方法。
(項目20)
前記第1の立体配置状態が、前記標的生化学的実体を薬剤とインキュベートした後に測定される、項目1に記載の方法。
(項目21)
前記薬剤が、前記ライブラリーからの候補生化学的実体である、項目1に記載の方法。
(項目22)
1つまたは複数の生化学的実体が、前記シグネチャーと公知の薬理特性または公知の機能的効果との相関に基づいて選択される、項目1に記載の方法。
(項目23)
生化学的実体をスクリーニングする方法であって、
(a)6つまたはそれを超える候補生化学的実体を含むライブラリーを用意するステップと、
(b)標的生化学的実体の第1の立体配置状態を測定し、それによってベースラインを作成するステップと、
(c)前記候補生化学的実体の各々を同じ標的生化学的実体と接触させるステップと、
(d)前記標的生化学的実体の第2の立体配置状態を測定するステップと、
(e)前記第2の立体配置状態を使用して少なくとも第1および第2の候補生化学的実体のシグネチャーを判定するステップと、
(f)前記第1の生化学的実体の前記シグネチャーを前記第2の生化学的実体の前記シグネチャーと比較するステップと、
(g)(f)での比較に基づいて、前記候補生化学的実体から1つまたは複数の生化学的実体を選択するステップと
を含む方法。
(項目24)
前記6つまたはそれを超える候補生化学的実体が、
(i)前記候補生化学的実体の各々の150g/mol以内の分子量、
(ii)前記候補生化学的実体の各々の30%以内の分子量、
(iii)前記候補生化学的実体の各々の原子が15個以内の化学式、
(iv)前記候補生化学的実体の各々の間の15未満の全原子数の差、
(v)5未満の炭素原子数の差、
(vi)5未満の水素原子数の差、
(vii)5未満の窒素原子数の差、
(viii)5未満の酸素原子数の差、
(ix)5未満の硫黄原子数の差、
(x)前記候補生化学的実体の各々の10%以内のlog Dで測定される極性、
(xi)前記候補生化学的実体の各々の10%以内のlog P(分配係数)で測定される極性、
(xii)前記候補生化学的実体の各々の10%以内のPSA(極性表面積)で測定される極性、
(xiii)同一の足場コア、
(xiv)グラフ理論で測定される化学的類似性、
(xv)0.85を超えるTanimoto(またはJaccard)係数T、
(xvi)3未満の芳香族基数の差、
(xvii)3未満の複素環基数の差、
(xviii)3未満の単環基数の差、
(xix)3未満の縮合環系数の差、および
(xx)3未満の二重結合数の差
からなる群から選択される1つまたは複数の構造類似性パラメータを使用して判定するときに構造的に類似している、項目23に記載の方法。
(項目25)
コンピュータ実行可能プログラムを使用して、前記シグネチャーを分析するステップをさらに含む、項目23に記載の方法。
(項目26)
前記候補生化学的実体の各々が、前記標的生化学的実体の立体配置状態において異なる変化を生成する、項目23に記載の方法。
(項目27)
(c)での接触の際に、前記候補生化学的実体の各々が異なるシグネチャーを生じる、項目23に記載の方法。
(項目28)
前記候補生化学的実体の少なくとも2つが、類似の薬理特性または機能的効果を有する、項目23に記載の方法。
(項目29)
i)前記ベースラインと比較した前記シグネチャーの大きさの変化、
ii)前記ベースラインと比較した前記シグネチャーの方向の変化、および
iii)前記候補生化学的実体の接触の際の前記シグネチャーの単位時間あたりのシグナルの速度の変化
からなる群から選択されるパラメータを測定するステップをさらに含む、項目23に記載の方法。
(項目30)
i)第1の候補生化学的実体との接触の際の前記ベースラインと比較した前記シグネチャーの大きさの前記変化が、第2の候補生化学的実体との接触の際の前記ベースラインと比較した前記シグネチャーの大きさの前記変化の50%以内であること、
ii)前記第1の候補生化学的実体との接触の際の前記ベースラインと比較した前記シグネチャーの方向の前記変化が、前記第2の候補生化学的実体との接触の際の前記ベースラインと比較した前記シグネチャーの方向の前記変化と同じであること、および
iii)前記第1の候補生化学的実体との接触の際の前記シグネチャーの単位時間あたりのシグナルの速度の変化が、前記第2の候補生化学的実体との接触の際の前記シグネチャーの単位時間あたりのシグナルの速度の変化の2倍以内であること
からなる群から選択される1つまたは複数のシグネチャー類似性パラメータを使用して判定したときに、前記第1の候補生化学的実体によって生じる前記シグネチャーおよび前記第2の候補生化学的実体によって生じる前記シグネチャーが類似している、項目23に記載の方法。
(項目31)
前記標的生化学的実体が、天然変性タンパク質である、項目23に記載の方法。
(項目32)
前記天然変性タンパク質が、アルファシヌクレインである、項目31に記載の方法。
(項目33)
前記標的生化学的実体が、公知の立体配置モジュレーターを有しない、項目23に記載の方法。
(項目34)
前記生化学的実体の1つまたは複数の前記シグネチャーが、公知の薬理特性または公知の機能的効果と相関する、項目23に記載の方法。
(項目35)
生化学的実体を分類する方法であって、
(a)生化学的実体のライブラリーを用意するステップであり、前記生化学的実体の各々は異なる分子構造を含む、ステップと、
(b)前記ライブラリー中の少なくとも1つの生化学的実体を同じ標的生化学的実体と接触させるステップと、
(c)前記標的生化学的実体の立体配置状態を測定するステップと、
(d)前記立体配置状態を使用してシグネチャーを判定するステップと、
(e)前記シグネチャーを使用して構造−活性関係(SAR)カタログを作成するステップと
含む方法。
(項目36)
前記SARを作成するステップが、前記シグネチャーを結合特性、機能的特性、効能、力価、選択性またはそれらの組合せと相関させるステップを含む、項目35に記載の方法。
(項目37)
前記SARを作成するステップが、前記シグネチャーを前記候補生化学的実体の1つまたは複数の構造パラメータと相関させるステップを含み、前記構造パラメータは、分子量、化学式、全原子数、炭素原子数、水素原子数、窒素原子数、酸素原子数、硫黄原子数、log Dによって測定される極性、log Pによって測定される極性、PSA(極性表面積)によって測定される極性、足場コア、グラフ理論で測定される化学的類似性、Tanimoto(またはJaccard)係数T、芳香族基数、複素環基数、単環基数、縮合環系数および二重結合数からなる群から選択される、項目35に記載の方法。
(項目38)
生化学的実体の前記ライブラリーが、薬物候補を含む、項目35に記載の方法。
(項目39)
前記標的生化学的実体が、薬物標的である、項目35に記載の方法。
(項目40)
薬理特性または機能的効果と関連する前記生化学的実体の少なくとも1つの中の結合部分を判定するために前記SARを分析するステップをさらに含む、項目35に記載の方法。
(項目41)
コンピュータ実行可能プログラムを使用して、前記シグネチャーを分析するステップをさらに含む、項目35に記載の方法。
(項目42)
前記接触の前に前記標的生化学的実体の前記立体配置状態を測定し、それによってベースラインを作成するステップをさらに含む、項目35に記載の方法。
(項目43)
前記シグネチャーが、前記標的生化学的実体の前記立体配置状態の変化を示す、項目35に記載の方法。
(項目44)
前記シグネチャーを判定するステップが、前記標的生化学的実体の前記立体配置状態の動態学的(リアルタイム)変化を測定するステップを含む、項目35に記載の方法。
(項目45)
前記シグネチャーを判定するステップが、前記標的生化学的実体の前記立体配置状態のエンドポイント変化を測定するステップを含む、項目35に記載の方法。
(項目46)
i)前記ベースラインと比較した前記シグネチャーの大きさの変化、
ii)前記ベースラインと比較した前記シグネチャーの方向の変化、および
iii)前記候補生化学的実体の接触の際の前記シグネチャーの単位時間あたりのシグナルの速度の変化
からなる群から選択されるシグネチャーパラメータを測定するステップをさらに含む、項目35に記載の方法。
(項目47)
i)第1の候補生化学的実体との接触の際の前記ベースラインと比較した前記シグネチャーの大きさの前記変化が、第2の候補生化学的実体との接触の際の前記ベースラインと比較した前記シグネチャーの大きさの前記変化の50%以内であること、
ii)前記第1の候補生化学的実体との接触の際の前記ベースラインと比較した前記シグネチャーの方向の前記変化が、前記第2の候補生化学的実体との接触の際の前記ベースラインと比較した前記シグネチャーの方向の前記変化と同じであること、および
iii)前記第1の候補生化学的実体との接触の際の前記シグネチャーの単位時間あたりのシグナルの速度の変化が、前記第2の候補生化学的実体との接触の際の前記シグネチャーの単位時間あたりのシグナルの速度の変化の2倍以内であること
からなる群から選択される1つまたは複数のシグネチャー類似性パラメータを使用して判定したときに、前記第1の候補生化学的実体によって生じる前記シグネチャーおよび前記第2の候補生化学的実体によって生じる前記シグネチャーが類似している、項目35に記載の方法。
(項目48)
前記SARカタログまたは前記シグネチャーと、公知の薬理特性または公知の機能的効果との相関に基づいて、1つまたは複数の生化学的実体を選択するステップをさらに含む、項目35に記載の方法。