JP6349385B2 - マルチモーダルイメージング装置 - Google Patents
マルチモーダルイメージング装置 Download PDFInfo
- Publication number
- JP6349385B2 JP6349385B2 JP2016517411A JP2016517411A JP6349385B2 JP 6349385 B2 JP6349385 B2 JP 6349385B2 JP 2016517411 A JP2016517411 A JP 2016517411A JP 2016517411 A JP2016517411 A JP 2016517411A JP 6349385 B2 JP6349385 B2 JP 6349385B2
- Authority
- JP
- Japan
- Prior art keywords
- scintillator
- gamma
- mode
- quanta
- elements
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 238000003384 imaging method Methods 0.000 title claims description 132
- 239000000700 radioactive tracer Substances 0.000 claims description 22
- 230000007246 mechanism Effects 0.000 claims description 21
- 230000005855 radiation Effects 0.000 claims description 19
- 230000004044 response Effects 0.000 claims description 10
- 238000000429 assembly Methods 0.000 claims description 9
- 230000000712 assembly Effects 0.000 claims description 8
- 238000010521 absorption reaction Methods 0.000 claims description 6
- 238000002603 single-photon emission computed tomography Methods 0.000 description 77
- 238000002600 positron emission tomography Methods 0.000 description 65
- 238000001514 detection method Methods 0.000 description 50
- 238000000034 method Methods 0.000 description 34
- 230000008569 process Effects 0.000 description 29
- 239000013078 crystal Substances 0.000 description 22
- 239000000463 material Substances 0.000 description 17
- 238000012879 PET imaging Methods 0.000 description 16
- 230000008901 benefit Effects 0.000 description 13
- 238000002595 magnetic resonance imaging Methods 0.000 description 11
- 238000002591 computed tomography Methods 0.000 description 10
- 230000003287 optical effect Effects 0.000 description 10
- 239000000919 ceramic Substances 0.000 description 9
- 238000001914 filtration Methods 0.000 description 8
- 230000008878 coupling Effects 0.000 description 7
- 238000010168 coupling process Methods 0.000 description 7
- 238000005859 coupling reaction Methods 0.000 description 7
- 230000000694 effects Effects 0.000 description 7
- 239000002223 garnet Substances 0.000 description 7
- 239000000126 substance Substances 0.000 description 7
- 238000013459 approach Methods 0.000 description 6
- 238000012545 processing Methods 0.000 description 6
- 238000010586 diagram Methods 0.000 description 4
- 230000033001 locomotion Effects 0.000 description 4
- 239000000853 adhesive Substances 0.000 description 3
- 230000001070 adhesive effect Effects 0.000 description 3
- 238000003491 array Methods 0.000 description 3
- 230000003993 interaction Effects 0.000 description 3
- 230000004060 metabolic process Effects 0.000 description 3
- 210000000056 organ Anatomy 0.000 description 3
- 239000002245 particle Substances 0.000 description 3
- WFKWXMTUELFFGS-UHFFFAOYSA-N tungsten Chemical compound [W] WFKWXMTUELFFGS-UHFFFAOYSA-N 0.000 description 3
- 229910052721 tungsten Inorganic materials 0.000 description 3
- 239000010937 tungsten Substances 0.000 description 3
- 229910052765 Lutetium Inorganic materials 0.000 description 2
- ZOKXTWBITQBERF-UHFFFAOYSA-N Molybdenum Chemical compound [Mo] ZOKXTWBITQBERF-UHFFFAOYSA-N 0.000 description 2
- 229910052782 aluminium Inorganic materials 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 229910052733 gallium Inorganic materials 0.000 description 2
- 238000007689 inspection Methods 0.000 description 2
- 239000011133 lead Substances 0.000 description 2
- 229910052749 magnesium Inorganic materials 0.000 description 2
- 229910052750 molybdenum Inorganic materials 0.000 description 2
- 239000011733 molybdenum Substances 0.000 description 2
- 229910052706 scandium Inorganic materials 0.000 description 2
- 238000011351 state-of-the-art imaging technique Methods 0.000 description 2
- JFALSRSLKYAFGM-UHFFFAOYSA-N uranium(0) Chemical compound [U] JFALSRSLKYAFGM-UHFFFAOYSA-N 0.000 description 2
- IESVDEZGAHUQJU-ZLBXKVHBSA-N 1-hexadecanoyl-2-(4Z,7Z,10Z,13Z,16Z,19Z-docosahexaenoyl)-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CC\C=C/C\C=C/C\C=C/C\C=C/C\C=C/C\C=C/CC IESVDEZGAHUQJU-ZLBXKVHBSA-N 0.000 description 1
- AOYNUTHNTBLRMT-SLPGGIOYSA-N 2-deoxy-2-fluoro-aldehydo-D-glucose Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](F)C=O AOYNUTHNTBLRMT-SLPGGIOYSA-N 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- 206010061818 Disease progression Diseases 0.000 description 1
- 241001497337 Euscorpius gamma Species 0.000 description 1
- ZCYVEMRRCGMTRW-AHCXROLUSA-N Iodine-123 Chemical compound [123I] ZCYVEMRRCGMTRW-AHCXROLUSA-N 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- 208000012902 Nervous system disease Diseases 0.000 description 1
- 208000025966 Neurological disease Diseases 0.000 description 1
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 1
- GKLVYJBZJHMRIY-OUBTZVSYSA-N Technetium-99 Chemical compound [99Tc] GKLVYJBZJHMRIY-OUBTZVSYSA-N 0.000 description 1
- KRHYYFGTRYWZRS-BJUDXGSMSA-N ac1l2y5h Chemical compound [18FH] KRHYYFGTRYWZRS-BJUDXGSMSA-N 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 230000003321 amplification Effects 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 238000004891 communication Methods 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 238000013170 computed tomography imaging Methods 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 230000008021 deposition Effects 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 230000005750 disease progression Effects 0.000 description 1
- 235000019800 disodium phosphate Nutrition 0.000 description 1
- 230000009977 dual effect Effects 0.000 description 1
- 238000013399 early diagnosis Methods 0.000 description 1
- 229920001971 elastomer Polymers 0.000 description 1
- 239000000806 elastomer Substances 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 208000019622 heart disease Diseases 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 229910052738 indium Inorganic materials 0.000 description 1
- 229940055742 indium-111 Drugs 0.000 description 1
- APFVFJFRJDLVQX-AHCXROLUSA-N indium-111 Chemical compound [111In] APFVFJFRJDLVQX-AHCXROLUSA-N 0.000 description 1
- 230000010365 information processing Effects 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- OHSVLFRHMCKCQY-UHFFFAOYSA-N lutetium atom Chemical compound [Lu] OHSVLFRHMCKCQY-UHFFFAOYSA-N 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 239000002547 new drug Substances 0.000 description 1
- 238000009206 nuclear medicine Methods 0.000 description 1
- 238000003199 nucleic acid amplification method Methods 0.000 description 1
- 238000012634 optical imaging Methods 0.000 description 1
- 239000004810 polytetrafluoroethylene Substances 0.000 description 1
- 229920001343 polytetrafluoroethylene Polymers 0.000 description 1
- 239000012857 radioactive material Substances 0.000 description 1
- 229910052761 rare earth metal Inorganic materials 0.000 description 1
- 150000002910 rare earth metals Chemical class 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 238000005070 sampling Methods 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 238000000638 solvent extraction Methods 0.000 description 1
- 230000003068 static effect Effects 0.000 description 1
- 230000001360 synchronised effect Effects 0.000 description 1
- 229940056501 technetium 99m Drugs 0.000 description 1
- BKVIYDNLLOSFOA-OIOBTWANSA-N thallium-201 Chemical compound [201Tl] BKVIYDNLLOSFOA-OIOBTWANSA-N 0.000 description 1
- 239000012780 transparent material Substances 0.000 description 1
- 229910052727 yttrium Inorganic materials 0.000 description 1
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01T—MEASUREMENT OF NUCLEAR OR X-RADIATION
- G01T1/00—Measuring X-radiation, gamma radiation, corpuscular radiation, or cosmic radiation
- G01T1/16—Measuring radiation intensity
- G01T1/1603—Measuring radiation intensity with a combination of at least two different types of detector
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B6/00—Apparatus or devices for radiation diagnosis; Apparatus or devices for radiation diagnosis combined with radiation therapy equipment
- A61B6/02—Arrangements for diagnosis sequentially in different planes; Stereoscopic radiation diagnosis
- A61B6/03—Computed tomography [CT]
- A61B6/037—Emission tomography
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B6/00—Apparatus or devices for radiation diagnosis; Apparatus or devices for radiation diagnosis combined with radiation therapy equipment
- A61B6/44—Constructional features of apparatus for radiation diagnosis
- A61B6/4417—Constructional features of apparatus for radiation diagnosis related to combined acquisition of different diagnostic modalities
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01T—MEASUREMENT OF NUCLEAR OR X-RADIATION
- G01T1/00—Measuring X-radiation, gamma radiation, corpuscular radiation, or cosmic radiation
- G01T1/29—Measurement performed on radiation beams, e.g. position or section of the beam; Measurement of spatial distribution of radiation
- G01T1/2914—Measurement of spatial distribution of radiation
- G01T1/2985—In depth localisation, e.g. using positron emitters; Tomographic imaging (longitudinal and transverse section imaging; apparatus for radiation diagnosis sequentially in different planes, steroscopic radiation diagnosis)
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Medical Informatics (AREA)
- Physics & Mathematics (AREA)
- Molecular Biology (AREA)
- High Energy & Nuclear Physics (AREA)
- Heart & Thoracic Surgery (AREA)
- General Health & Medical Sciences (AREA)
- Pathology (AREA)
- Radiology & Medical Imaging (AREA)
- Biomedical Technology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Biophysics (AREA)
- Surgery (AREA)
- Animal Behavior & Ethology (AREA)
- Optics & Photonics (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- General Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Nuclear Medicine (AREA)
- Apparatus For Radiation Diagnosis (AREA)
- Magnetic Resonance Imaging Apparatus (AREA)
- Measurement Of Radiation (AREA)
Description
特許文献4では、核医学における改良されたSPECT、PET及びコンプトン散乱イメージングのための装置及びシステムが開示されている。システムは、コンピュータシステムを通じて電子的に操作され得る検出器アレイを有する1又は複数の検出器モジュールの固定された又は構成可能なアレイを用いる。
Claims (18)
- 対象の中の放射性トレーサ分布を撮像するためのマルチモーダルイメージング装置であって、
少なくとも2つの検出器アセンブリであって、それぞれの前記検出器アセンブリは、サブアセンブリのアレイを含み、各サブアセンブリは:
前記放射性トレーサによって発生した入射ガンマ量子を捕えるとともに捕えた前記ガンマ量子に応じてシンチレーション光子を放射するように構成されるシンチレータ素子を含むシンチレータと;
放射された前記シンチレーション光子を捕えるとともに前記シンチレーション光子の空間分布を決定するように構成される感光素子を含む光検出器と;を含む、
少なくとも2つの検出器アセンブリ、
前記シンチレーション光子の空間分布に基づいて、前記シンチレータにおける入射ガンマ量子の衝突位置及び/又は前記対象の中の前記ガンマ量子の放射ポイントを示すパラメータを決定するように構成される読出し回路、並びに
低エネルギガンマ量子を検出するための第1の動作モードと高エネルギガンマ量子を検出するための第2の動作モードとの間で前記イメージング装置を切り替えるためにそれぞれの前記サブアセンブリを個々に傾けて前記シンチレータの吸収深さを変化させるように構成される位置決め機構であって、前記高エネルギガンマ量子は前記低エネルギガンマ量子より高いエネルギを有する、位置決め機構、
を有し、
それぞれの前記サブアセンブリの前記シンチレータは、前記第1の動作モード及び前記第2の動作モードにおいて同じ関心領域からの前記入射ガンマ量子を捕えるように配置される、
マルチモーダルイメージング装置。 - 前記低エネルギガンマ量子及び前記高エネルギガンマ量子両方のエネルギは、70keVから600keVの間にある、
請求項1に記載のマルチモーダルイメージング装置。 - 前記第1の動作モード及び前記第2の動作モードで前記サブアセンブリを支持するための共通のガントリをさらに有する、
請求項1に記載のマルチモーダルイメージング装置。 - 前記第1の動作モードにおける入射角に基づいて前記入射ガンマ量子をフィルタリングするように構成されるコリメータをさらに有する、
請求項1に記載のマルチモーダルイメージング装置。 - 前記光検出器は、光子計数モードでの動作用に構成され、前記光検出器のダイナミックレンジは、高エネルギシンチレータ素子及び低エネルギシンチレータ素子両方によって放射される前記シンチレーション光子を捕えるように構成される、
請求項1に記載のマルチモーダルイメージング装置。 - 1つの感光素子が、それぞれの前記シンチレータ素子に結合されるとともに前記シンチレータ素子によって放射される前記シンチレーション光子を捕えるように配置され;
前記位置決め機構は、ガンマ光子が前記第1の動作モードにおける短い寸法に沿って及び前記第2の動作モードにおける長い寸法に沿って移動するように、前記シンチレータ素子及びそこへ結合された前記感光素子を傾けるように、構成される、
請求項1に記載のマルチモーダルイメージング装置。 - それぞれの前記検出器アセンブリは、前記サブアセンブリのM×Nのアレイを含み、M及びNは、複数の整数である、
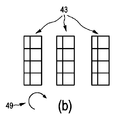
請求項1に記載のマルチモーダルイメージング装置。 - それぞれの前記サブアセンブリは、前記シンチレータ素子の積み重ねを含み;
前記位置決め機構は、前記入射ガンマ量子が前記積み重ねの側面に衝突する前記第1の動作モードに対応する第1の位置と前記入射ガンマ量子が前記積み重ねの上面に衝突する前記第2の動作モードに対応する第2の位置との間で前記イメージング装置を切り替えるために、前記シンチレータ素子の積み重ねを傾けるように構成される、
請求項1に記載のマルチモーダルイメージング装置。 - それぞれの前記サブアセンブリは、それぞれの検出器が前記第1の動作モード及び前記第2の動作モードの両方で同じ解像度及び視野を提供するようM×Nの前記サブアセンブリを有するように、単一の光検出器に光学的に結合される単一のシンチレーションを有する、
請求項7に記載のマルチモーダルイメージング装置。 - 前記読出し回路は、前記第1の動作モードにおける低エネルギガンマ量子イベントを読み出すように及び前記第2の動作モードにおける高エネルギガンマ量子イベントを読み出すように構成される、
請求項1に記載のマルチモーダルイメージング装置。 - 前記シンチレータは、前記シンチレータ素子のアレイであって、前記低エネルギガンマ量子を捕えるように構成される低エネルギシンチレータ素子を用いて前記第1の動作モードにおいて関心領域に面する前記アレイの2次元領域に対応する第1の領域及び前記高エネルギガンマ量子を捕えるように構成される高エネルギシンチレータ素子を用いて前記第2の動作モードにおいて前記関心領域に面する前記アレイの2次元領域に対応する第2の領域を含む、前記シンチレータ素子のアレイを有する、
請求項1に記載のマルチモーダルイメージング装置。 - 対象の中の放射性トレーサ分布を撮像するためのマルチモーダルイメージング装置であって、
複数の検出器アセンブリであって、それぞれの前記検出器アセンブリは、サブアセンブリの二次元アレイを含み、各サブアセンブリは:
前記放射性トレーサによって発生した入射ガンマ量子を捕えるとともに捕えた前記ガンマ量子に応じてシンチレーション光子を放射するように構成される少なくとも1つのシンチレータ素子と;
放射された前記シンチレーション光子を捕えるように構成される少なくとも1つの感光素子であって、それぞれの前記感光素子は対応するシンチレータ素子の第1の面に光学的に結合される、少なくとも1つの感光素子と;を含む、
複数の検出器アセンブリ、及び
機械的位置決め機構であって、入射ガンマ光子が前記シンチレータ素子の第2の面で受けられる第1の向きであって、前記第2の面は前記第1の面の反対側に配置される、第1の向きと、入射ガンマ光子が前記シンチレータ素子のうちの1つの側面で受けられるように前記第1の向きに直角である第2の向きとの間で、それぞれの前記サブアセンブリを、対応する前記検出器アセンブリに対して回転させて前記シンチレータ素子の吸収深さを変化させるように構成される、機械的位置決め機構、
を有する、
マルチモーダルイメージング装置。 - それぞれの前記サブアセンブリは、それぞれの前記検出器アセンブリが前記向きの両方において同じ数の前記シンチレータ素子/前記感光素子のペアを有するように、単一のシンチレータ素子及び単一の検出器素子を含む、
請求項12に記載のマルチモーダルイメージング装置。 - 前記シンチレーション光子の空間分布に基づいて、前記シンチレータにおける入射ガンマ量子の捕捉位置及び/又は前記対象の中の前記ガンマ量子の放射ポイントを示すパラメータを決定するように構成される読出し回路、をさらに含む、
請求項13に記載のマルチモーダルイメージング装置。 - 対象の中の放射性トレーサ分布を撮像するためのマルチモーダルイメージング装置であって、
複数の放射線検出器モジュールであって、それぞれの前記検出器モジュールは:
前記放射性トレーサによって発生した低エネルギ入射ガンマ放射線量子を捕えるとともに捕えた前記低エネルギ入射ガンマ放射線量子に応じてシンチレーション光子を放射するように構成される複数の第1のシンチレータ素子と;
前記放射性トレーサによって発生した高エネルギ入射ガンマ放射線量子を捕えるとともに捕えた前記高エネルギ入射ガンマ放射線量子に応じてシンチレーション光子を放射するように構成される複数の第2のシンチレータ素子と;
前記第1のシンチレータ素子及び前記第2のシンチレータ素子に光学的に結合されるとともに、放射された前記シンチレーション光子を捕えるように構成される、複数の感光素子と;
前記第1のシンチレータ素子の面に配置されるとともに入射角に基づいて入射ガンマ量子をフィルタリングするように構成されるコリメータ要素を含むコリメータシステムであって、前記コリメータ要素は、前記第1のシンチレータ素子と前記対象との間に配置され、前記コリメータシステムは、前記第2のシンチレータ素子と前記対象との間に前記コリメータ要素を含まない、コリメータシステムと;
を含む、
複数の放射線検出器モジュール、
を有する、
マルチモーダルイメージング装置。 - 前記シンチレーション光子の空間分布に基づいて、前記シンチレータ素子における入射ガンマ量子の捕捉位置及び/又は前記対象の中のガンマ量子の放射ポイントを示すパラメータを決定するように構成される読出し回路、をさらに含む、
請求項15に記載のマルチモーダルイメージング装置。 - それぞれの前記サブアセンブリは、前記第2の向きにおいて、前記入射ガンマ光子が、側面から側面にそれぞれの前記サブアセンブリの隣接する前記シンチレータ素子を連続的に通過するように、光検出器のリニアアレイに光学的に結合される前記シンチレータ素子のリニアアレイを含む、
請求項12に記載のマルチモーダルイメージング装置。 - 前記二次元アレイは、前記サブアセンブリのM×Nのアレイを含み、M及びNは、複数の整数である、
請求項12に記載のマルチモーダルイメージング装置。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP13186325.0 | 2013-09-27 | ||
| EP13186325 | 2013-09-27 | ||
| PCT/EP2014/069862 WO2015044019A1 (en) | 2013-09-27 | 2014-09-18 | Multimodal imaging apparatus |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2016533477A JP2016533477A (ja) | 2016-10-27 |
| JP2016533477A5 JP2016533477A5 (ja) | 2017-11-09 |
| JP6349385B2 true JP6349385B2 (ja) | 2018-06-27 |
Family
ID=49293487
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016517411A Expired - Fee Related JP6349385B2 (ja) | 2013-09-27 | 2014-09-18 | マルチモーダルイメージング装置 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US9784850B2 (ja) |
| EP (1) | EP3048975A1 (ja) |
| JP (1) | JP6349385B2 (ja) |
| CN (1) | CN105592795B (ja) |
| WO (1) | WO2015044019A1 (ja) |
Families Citing this family (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8017915B2 (en) | 2008-03-14 | 2011-09-13 | Reflexion Medical, Inc. | Method and apparatus for emission guided radiation therapy |
| CN106923860B (zh) * | 2015-12-30 | 2023-08-22 | 苏州瑞派宁科技有限公司 | 一种具有窗口的平板pet成像装置 |
| CN107260194B (zh) * | 2016-04-08 | 2020-08-28 | 山西锦地裕成医疗设备有限公司 | 用于正电子断层成像的方法和图像重建方法及系统 |
| CN106199682A (zh) * | 2016-09-07 | 2016-12-07 | 武汉京邦科技有限公司 | 一种基于硅光电倍增器和数字化时间标记的伽马暴巡检仪 |
| EP3988017A1 (en) | 2016-11-15 | 2022-04-27 | RefleXion Medical, Inc. | System for emission-guided high-energy photon delivery |
| WO2018183748A1 (en) | 2017-03-30 | 2018-10-04 | Reflexion Medical, Inc. | Radiation therapy systems and methods with tumor tracking |
| CN107080551B (zh) * | 2017-05-25 | 2023-08-22 | 苏州瑞派宁科技有限公司 | 一种三维异质pet系统 |
| EP4342521A3 (en) | 2017-07-11 | 2024-05-08 | RefleXion Medical Inc. | Methods for pet detector afterglow management |
| US11000701B2 (en) * | 2017-08-01 | 2021-05-11 | Varex Imaging Corporation | Dual-layer detector for soft tissue motion tracking |
| JP7315961B2 (ja) | 2017-08-09 | 2023-07-27 | リフレクション メディカル, インコーポレイテッド | 放出誘導放射線療法における異常検出のためのシステムおよび方法 |
| WO2019099551A1 (en) | 2017-11-14 | 2019-05-23 | Reflexion Medical, Inc. | Systems and methods for patient monitoring for radiotherapy |
| CN108309339B (zh) * | 2018-01-26 | 2020-11-06 | 北京科技大学 | Spect/pet/mri三模态成像系统及方法 |
| CN111329500B (zh) * | 2018-12-19 | 2022-09-09 | 清华大学 | 一种伽马辐射成像装置及成像方法 |
| IT201900010638A1 (it) * | 2019-07-02 | 2021-01-02 | St Microelectronics Srl | Rilevatore di radiazione a scintillatore e dosimetro corrispondente |
| JP2022553079A (ja) * | 2019-10-22 | 2022-12-21 | フィジボチックス,エルディーエー | 患者の身体部分内の少なくとも1つのトレーサーの微細な位置の向上された決定のための装置及びそれぞれの方法 |
| GB2600919A (en) * | 2020-11-04 | 2022-05-18 | Tesla Dynamic Coils BV | MRI systems and receive coil arrangements |
Family Cites Families (23)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5841833A (en) * | 1991-02-13 | 1998-11-24 | Lunar Corporation | Dual-energy x-ray detector providing spatial and temporal interpolation |
| US5591977A (en) * | 1994-04-29 | 1997-01-07 | The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Variable axial aperture positron emission tomography scanner |
| US5608221A (en) * | 1995-06-09 | 1997-03-04 | Adac Laboratories | Multi-head nuclear medicine camera for dual SPECT and PET imaging with monuniform attenuation correction |
| US5841140A (en) | 1997-01-08 | 1998-11-24 | Smv America, Inc. | Gamma camera for pet and spect studies |
| US6362479B1 (en) | 1998-03-25 | 2002-03-26 | Cti Pet Systems, Inc. | Scintillation detector array for encoding the energy, position, and time coordinates of gamma ray interactions |
| JP4230019B2 (ja) * | 1998-09-02 | 2009-02-25 | 株式会社日立メディコ | ガンマカメラ |
| CA2252993C (en) * | 1998-11-06 | 2011-04-19 | Universite De Sherbrooke | Detector assembly for multi-modality scanners |
| US6303935B1 (en) | 1999-05-21 | 2001-10-16 | Siemens Medical Systems, Inc. | Combination PET/SPECT nuclear imaging system |
| US6534771B1 (en) | 1999-06-08 | 2003-03-18 | Saint Gobain Industrial Ceramics, Inc. | Gamma camera plate assembly for PET and SPECT imaging |
| CA2434479A1 (en) * | 2001-01-16 | 2002-10-10 | Board Of Regents, The University Of Texas System | A pet camera with individually rotatable detector modules and/or individually movable shielding sections |
| US6670614B1 (en) * | 2001-06-01 | 2003-12-30 | Leonard F. Plut | Volume cone beam acquisition on a nuclear spect system using a digital flat panel |
| US7262415B2 (en) | 2002-06-02 | 2007-08-28 | Crosetto Dario B | Gantry for geometrically configurable and non-configurable positron emission tomography detector arrays |
| US20040159791A1 (en) | 2003-02-19 | 2004-08-19 | Yaron Hefetz | Pet/spect nuclear scanner |
| US7291841B2 (en) * | 2003-06-16 | 2007-11-06 | Robert Sigurd Nelson | Device and system for enhanced SPECT, PET, and Compton scatter imaging in nuclear medicine |
| DE10352012B4 (de) | 2003-11-07 | 2007-10-04 | Siemens Ag | Detektormodul für die CT- und/oder PET- und/oder SPECT-Tomographie |
| US20070205367A1 (en) | 2006-03-01 | 2007-09-06 | General Electric Company | Apparatus and method for hybrid computed tomography imaging |
| US7381960B1 (en) * | 2006-11-11 | 2008-06-03 | National Tsing Hua University | Imaging system and method for the non-pure positron emission tomography |
| ES2346623B1 (es) | 2009-01-07 | 2011-10-03 | Consejo Superior De Investigaciones Científicas (Csic) | Sistema compacto, hibrido e integrado gamma/rf para la formacion de imagenes simultaneas petspect/mr. |
| WO2010136851A1 (en) * | 2009-05-26 | 2010-12-02 | Biospace Lab | Imaging device for positron emission tomography |
| US9173618B2 (en) * | 2009-11-05 | 2015-11-03 | General Electric Company | Diagnostic imaging system and method using multiple types of imaging detectors |
| EP2640270B1 (en) | 2010-11-18 | 2018-05-16 | Koninklijke Philips N.V. | Pet-ct system with single detector |
| US20120265050A1 (en) | 2011-04-04 | 2012-10-18 | Ge Wang | Omni-Tomographic Imaging for Interior Reconstruction using Simultaneous Data Acquisition from Multiple Imaging Modalities |
| US8674312B2 (en) * | 2011-08-02 | 2014-03-18 | Siemens Medical Solutions Usa, Inc. | Radiation detection with optical amplification |
-
2014
- 2014-09-18 JP JP2016517411A patent/JP6349385B2/ja not_active Expired - Fee Related
- 2014-09-18 CN CN201480052994.XA patent/CN105592795B/zh not_active Expired - Fee Related
- 2014-09-18 EP EP14766734.9A patent/EP3048975A1/en not_active Withdrawn
- 2014-09-18 WO PCT/EP2014/069862 patent/WO2015044019A1/en active Application Filing
- 2014-09-18 US US14/917,030 patent/US9784850B2/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| US20160209515A1 (en) | 2016-07-21 |
| EP3048975A1 (en) | 2016-08-03 |
| US9784850B2 (en) | 2017-10-10 |
| WO2015044019A1 (en) | 2015-04-02 |
| JP2016533477A (ja) | 2016-10-27 |
| CN105592795B (zh) | 2019-08-06 |
| CN105592795A (zh) | 2016-05-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6349385B2 (ja) | マルチモーダルイメージング装置 | |
| JP5738188B2 (ja) | 高エネルギー光子を検出するモジュールおよびシステム、当該システムを有するpet用環状検出器、当該検出器を有するガンマカメラおよびコンプトンカメラ | |
| CN107613863B (zh) | Pet/mri嵌入系统 | |
| JP6854805B2 (ja) | ハイブリッドpet/ctイメージング検出器 | |
| US6399951B1 (en) | Simultaneous CT and SPECT tomography using CZT detectors | |
| US20120039446A1 (en) | Interwoven multi-aperture collimator for 3-dimensional radiation imaging applications | |
| CN113287056B (zh) | 基于准直器和检测器的医学成像系统 | |
| US20130009066A1 (en) | Block Detector With Variable Microcell Size For Optimal Light Collection | |
| JP2013519879A (ja) | マルチゾーン検出器アーキテクチャを使用する、核イメージング用の方法およびシステム | |
| JP2011059099A (ja) | 異なるサイズの光電子増倍管を使用したPET(陽電子放射トモグラフィ:positronemissiontomography)検出器素子 | |
| Zaidi et al. | The new challenges of brain PET imaging technology | |
| US9612344B2 (en) | Positron emission tomography and single photon emission computed tomography based on intensity attenuation shadowing methods and effects | |
| JP2006284346A (ja) | 放射線断層撮影装置 | |
| JP7226827B2 (ja) | 被験者の第1の画像および第2の画像を生成するシステム及びシステムの作動方法 | |
| WO2019135676A1 (en) | Active collimator for positron emission and single photon emission computed tomography | |
| Saldaña-González et al. | 2D image reconstruction with a FPGA-based architecture in a gamma camera application | |
| Dahlbom | Preclinical Molecular Imaging Systems | |
| Li | Design study of an organ-dedicated positron emission tomography system | |
| Chang | Radio-Frequency Penetrable Positron Emission Tomography (PET) Insert for Simultaneous PET and Magnetic Resonance Imaging | |
| Chen et al. | Radiation Detection in SPECT and PET | |
| Hsu | Investigation of Advanced Clinical PET System Designs | |
| Lecomte | Molecular PET instrumentation and imaging techniques | |
| Borghi | From detectors towards systems: enabling clinical TOF-PET with monolithic scintillators | |
| Brasse et al. | Instrumentation Challenges in (S) PE (C) T Systems | |
| Mannheim et al. | Small Animal PET Cameras—Development, Technology, PET/CT, PET/MRI |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160526 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170914 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20170914 |
|
| A871 | Explanation of circumstances concerning accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A871 Effective date: 20170914 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170914 |
|
| A975 | Report on accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A971005 Effective date: 20171113 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20171121 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180216 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20180508 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20180604 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6349385 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| LAPS | Cancellation because of no payment of annual fees |