JP6318096B2 - 希土類酸化物粒子及び特に画像化におけるその使用 - Google Patents
希土類酸化物粒子及び特に画像化におけるその使用 Download PDFInfo
- Publication number
- JP6318096B2 JP6318096B2 JP2014560435A JP2014560435A JP6318096B2 JP 6318096 B2 JP6318096 B2 JP 6318096B2 JP 2014560435 A JP2014560435 A JP 2014560435A JP 2014560435 A JP2014560435 A JP 2014560435A JP 6318096 B2 JP6318096 B2 JP 6318096B2
- Authority
- JP
- Japan
- Prior art keywords
- particles
- formula
- particle
- imaging
- composition according
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K49/00—Preparations for testing in vivo
- A61K49/06—Nuclear magnetic resonance [NMR] contrast preparations; Magnetic resonance imaging [MRI] contrast preparations
- A61K49/18—Nuclear magnetic resonance [NMR] contrast preparations; Magnetic resonance imaging [MRI] contrast preparations characterised by a special physical form, e.g. emulsions, microcapsules, liposomes
- A61K49/1818—Nuclear magnetic resonance [NMR] contrast preparations; Magnetic resonance imaging [MRI] contrast preparations characterised by a special physical form, e.g. emulsions, microcapsules, liposomes particles, e.g. uncoated or non-functionalised microparticles or nanoparticles
- A61K49/1821—Nuclear magnetic resonance [NMR] contrast preparations; Magnetic resonance imaging [MRI] contrast preparations characterised by a special physical form, e.g. emulsions, microcapsules, liposomes particles, e.g. uncoated or non-functionalised microparticles or nanoparticles coated or functionalised microparticles or nanoparticles
- A61K49/1824—Nuclear magnetic resonance [NMR] contrast preparations; Magnetic resonance imaging [MRI] contrast preparations characterised by a special physical form, e.g. emulsions, microcapsules, liposomes particles, e.g. uncoated or non-functionalised microparticles or nanoparticles coated or functionalised microparticles or nanoparticles coated or functionalised nanoparticles
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/08—Luminescent, e.g. electroluminescent, chemiluminescent materials containing inorganic luminescent materials
- C09K11/77—Luminescent, e.g. electroluminescent, chemiluminescent materials containing inorganic luminescent materials containing rare earth metals
- C09K11/7783—Luminescent, e.g. electroluminescent, chemiluminescent materials containing inorganic luminescent materials containing rare earth metals containing two or more rare earth metals one of which being europium
- C09K11/7794—Vanadates; Chromates; Molybdates; Tungstates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K49/00—Preparations for testing in vivo
- A61K49/0002—General or multifunctional contrast agents, e.g. chelated agents
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y15/00—Nanotechnology for interacting, sensing or actuating, e.g. quantum dots as markers in protein assays or molecular motors
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y5/00—Nanobiotechnology or nanomedicine, e.g. protein engineering or drug delivery
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Nanotechnology (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Epidemiology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Molecular Biology (AREA)
- Inorganic Chemistry (AREA)
- Crystallography & Structural Chemistry (AREA)
- Organic Chemistry (AREA)
- Materials Engineering (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Radiology & Medical Imaging (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Magnetic Resonance Imaging Apparatus (AREA)
- Ultra Sonic Daignosis Equipment (AREA)
- Medicinal Preparation (AREA)
Description
本願は、画像化のための、特に画像診断のための、及び任意に療法のためのマルチモード複合製品に、特に、磁気共鳴画像法(MRI)及び/又は、例えば、光学イメージング、酸化性物質の光学検出、陽電子放出断層撮影法(PET)、断層撮影法(TDM)及び/又は超音波画像診断などの画像化技術において造影剤として使用でき、任意に同時に療法における使用のための複合製品に関する。これらの製品は、造影剤活性及び/又は常磁性活性を備えた部分並びに発光活性及び任意に酸化性物質検出活性を備えた部分を含むか、又はそれらからなる粒子に基づいている。
MRI(磁気共鳴画像法)検査は、基本的に、様々な種類の軟組織を画像化するのに使用される。コントラストは、プロトン緩和時間T1(縦緩和)及びT2(横緩和)により決まる(Abragamの文献、1983年及びLevittの文献、2008年)。
観察される緩和速度は下記により定義される:
緩和性比(κ)の値:
CAの実際の構造によって、水分子と水素結合相互作用が可能な場合には、追加の寄与が存在し得る。この寄与は定量化が困難なので、水素結合の強さによって内圏機構又は外圏機構として扱われることが多い(Caravanらの文献、1999年; Aimeらの文献、2005年)。
観察される緩和時間の逆数は、2つのプロセスの緩和時間の逆数の関数である(Caravanらの文献、1999年):
MRI造影剤として、蛍光マーカーとして、及び酸化性物質センサーとしての使用を組み合わせたGd0.6Eu0.4VO4の粒子が提案されてきた。(Schoeffelらの文献;2011年)。しかし、これらの粒子は、4%程度の低いルミネセンス量子収率(Q)を有する。
そのため、画像化のための、及び任意に療法のための複合マルチモード製品、特に、MRIにおいて、並びに/又は、例えば、光学イメージング、酸化性物質の光学検出、陽電子放出断層撮影法(PET)、断層撮影法(TDM)、及び/若しくは超音波画像診断などの他の画像化技術において造影剤として使用でき、任意に同時に療法に使用するのに好適な複合製品が当分野において必要とされている。
本願は、特にMRI用の造影剤として、及び発光剤としての少なくとも両方(少なくとも二方式の薬剤)の使用に好適な粒子を提供する。この粒子は、発光活性を有する部分及び造影剤活性を有する部分を含むか、又はそれらからなる(少なくとも二部構成の粒子)。
以下で明らかになる特定の実施態様において、本発明の粒子は、さらにコーティングを備えている。
式XaLb(MpOq)を有する部分(式中、
-Mは、酸素(O)と結合してアニオンを形成することができる少なくとも1種の元素であり;
-Lは、1種以上の発光性ランタニドイオン(複数可)に相当し;
-Xは、ルミネセンスの点で中性である1種以上のイオン(複数可)に相当し;且つ
-p、q、a、及びbの値は、XaLb(MpOq)の電気的中性が守られるような、比b/(b+a)により定義される発光性元素の分率が1%から75%であるようなものである);及び
式AeX'f(M'p'Oq')を有する部分(式中、
-M'は、酸素(O)と結合してアニオンを形成することができる少なくとも1種の元素であり;
-Aは、1種以上の常磁性ランタニドイオンに相当し;
-X'は、存在する場合、常磁性の点で中性である1種以上のイオン(複数可)に相当し;且つ
-p'、q'、e、及び適切な場合、fの値は、AeX'f(M'p'Oq')の電気的中性が守られるような、比e/(e+f)により定義される常磁性元素の分率が80%から100%であるようなものである)。
式XaLb(MpOq)を有する部分(式中、
-Mは、酸素(O)と結合してアニオンを形成することができる少なくとも1種の元素であり;
-Lは、1種以上の発光性ランタニドイオン(複数可)に相当し;
-Xは、ルミネセンスの点で中性である1種以上のイオン(複数可)に相当し;且つ
-p、q、a、及びbの値は、XaLb(MpOq)の電気的中性が守られるような、比b/(b+a)により定義される発光性元素の分率が1%から75%であるようなものである);及び
式AeX'f(M'p'Oq')を有する部分(式中、
-M'は、酸素(O)と結合してアニオンを形成することができる少なくとも1種の元素であり;
-Aは、1種以上の常磁性ランタニドイオンに相当し;
-X'は、常磁性の点で中性である1種以上のイオン(複数可)に相当し;且つ
-p'、q'、e、及びfの値は、AeX'f(M'p'Oq')の電気的中性が守られるような、比e/(e+f)により定義される常磁性元素の分率が80%から100%であるようなものである)。
式XaLb(MpOq)を有する部分(式中、
-Mは、酸素(O)と結合してアニオンを形成することができる少なくとも1種の元素であり;
-Lは、1種以上の発光性ランタニドイオン(複数可)に相当し;
-Xは、ルミネセンスの点で中性である1種以上のイオン(複数可)に相当し;且つ
-p、q、a、及びbの値は、XaLb(MpOq)の電気的中性が守られるような、比b/(b+a)により定義される発光性元素の分率が1%から75%であるようなものである);及び
式Ae(M'p'Oq')を有する部分(式中、
-M'は、酸素(O)と結合してアニオンを形成することができる少なくとも1種の元素であり;
-Aは、1種以上の常磁性ランタニドイオンに相当し;且つ
-p'、q'、及びeの値は、Ae(M'p'Oq')の電気的中性が守られるようなものである)。
M及びM'は、互いに独立に、酸素(O)と結合してアニオンを形成することができる少なくとも1種の(好ましくは1又は2種の)元素である。「互いに独立に」という用語は、Mの選択が、M'の選択に影響せず、逆もまた同様であることを意味する。特定の実施態様において、M及びM'は、互いに独立に、+V又は+VIの原子価を有する。特定の実施態様において、M及びM'は、それぞれ、互いに独立に、V、P、W、Mo、及びAsにより構成される群から選択されるイオンである。好ましくは、M及びM'は、互いに独立に、P又はVである。好ましくは、M及びM'はVである。一実施態様において、M及び/又はM'の一方及び/又は他方は、V、P、W、Mo、及びAsにより構成される群から互いに独立に選択される2種のイオンを表す。特に、Mは、VvP1-v(vは0から1である)を表し得る。特に、M'は、Vv'P1-v'(v'は0から1である)を表し得る。
p、q、a、及びbの値は、XaLb(MpOq)の電気的中性が守られるようなものである。
特定の実施態様において、b/b+aは、10%超、好ましくは20%超、好ましくは25%超である。特定の実施態様において、b/(b+a)は、10%〜75%、又は20%〜75%、又は25%〜75%、又は25%〜45%である。
一実施態様において、XはYであり、LはEuであり、MはV又はPであり、比b/(b+a)は1%〜75%、好ましくは10%〜75%、さらにより好ましくは20%〜75%である。一実施態様において、XはYであり、LはEuであり、MはVであり、比b/(b+a)は1%〜75%、好ましくは10%〜75%、さらにより好ましくは20%〜75%である。一実施態様において、XaLb(MpOq)がY0.6Eu0.4(VO4)であるように、Xは、Yであり、LはEuであり、MはVであり、比b/(b+a)は40%である。
p'は、0又は1に等しく、好ましくは1に等しい。一実施態様において、q'は、2〜5の範囲であり、好ましくは4である。例としては、(M'p'Oq')がPO4 3-又はVO4 3-であるように、M'はP又はVであり、p'は1に等しく、q'は4に等しい。他の実施態様において、(Mp'Oq')が(Vv'P1-v')O4であるように、M'はイオンV及びPを表し、p'は1に等しく、q'は4に等しい。
-式XaLb(MpOq)を有する部分(式中、M、L、X、p、q、a、及びbは、先に定義された通りであり、該部分XaLb(MpOq)が発光活性を有するように選択される);及び
-式AeX'f(M'p'Oq')を有する部分(式中、M'、A、存在する場合のX'、p'、q'、e、及び適切な場合、fは、先に定義された通りであり、該部分AeX'f(M'p'Oq')が、特にMRIにおける造影剤活性及び/又は常磁性活性を有するように選択される)。
-式XaLb(MpOq)を有する部分(式中、MはVであり、LはEuであり、X、a、b、及びpは先に定義された通りであり、該部分XaEub(VpOq)が発光活性及び酸化性物質検出活性を有するように選択される);及び
-式AeX'f(M'p'Oq')を有する部分(式中、M'、A、存在する場合のX'、p'、q'、e、及び適切な場合、fは先に定義された通りであり、該部分AeX'f(M'p'Oq')が特にMRIにおける造影剤活性を有するように選択される)。
-Xは、ルミネセンスの点で中性である1種以上の、好ましくは1又は2種のイオン(複数可)に相当し;
-p、q、a、及びbの値は、XaEub(VpOq)の電気的中性が守られるような、比b/(b+a)により定義される発光性元素の分率が1%〜75%であるように選択され;且つ
-M'は、酸素(O)と結合してアニオンを形成することができる少なくとも1種の元素であり;
-Aは、1種以上の、好ましくは1又は2種の常磁性ランタニドイオン(複数可)に相当し;
-X'は、存在する場合、常磁性の点で中性である1種以上のイオンに相当し;且つ
-p'、q'、e、及び適切な場合、fの値は、AeX'f(M'p'Oq')の電気的中性が守られるような、比e/(e+f)により定義される常磁性元素の分率が80%〜100%であるようなものである)。
特定の実施態様において、本発明の粒子は、比b/(b+a)が1%〜75%、特に10%〜60%、又は20%〜50%、特におよそ30%又はおよそ40%(±5%)であるYaEub(VO4)/Gd(VO4)、YaEub(PO4)/Gd(VO4)、YaEub(VO4)/Gd(PO4)、及びYaEub(PO4)/Gd(PO4)により構成される群から選択される式を有する。一実施態様において、本発明の粒子は式Y0.6Eu0.4(VO4)/Gd(VO4)を有する。
そのため、一実施態様において、それぞれ本発明の粒子の発光性部分及び常磁性部分を構成する、式XaLb(MpOq)及びAeX'f(M'p'Oq')又は式XaLb(MpOq)及びAe(M'p'Oq')を持つ少なくとも2つの部分は並置され、すなわち、それらは、2つの部分が混合することがないか、又は全体の小さな比率のみ(各部分の10%未満)が混合物として存在するように互いに接触している。そのため、相のうち1つは、少なくとも部分的に他の相に分散し得る。
特定の好都合な実施態様において、コアは常磁性の点で中性であり、且つ/又はシェルはルミネセンスの点で中性である。
例えば、特定の実施態様において、この第三の部分は、本発明の被覆されていない粒子が準備層にのみ被覆されるように、準備層からなる。
他の実施態様において、この第三の部分は、本発明の被覆されていない粒子が準備層及び生物活性のある分子により構成された層にのみ覆われるように、準備層及び生物活性のある分子により構成された層からなる。特定の実施態様において、準備層は生物活性のある分子により構成された層に対して最も内側にあり、すなわち、準備層は、被覆されていない粒子の上に適用され、生物活性のある分子により構成された層は準備層の上に適用される。
特定の実施態様において、生物活性のある分子又は複数の分子は、標的化分子、すなわち、臓器、体液(例えば血液)、細胞型(例えば、血小板、リンパ球、単球、腫瘍細胞など)又は細胞コンパートメントに向けた本発明の粒子の特異的な標的化を可能にする分子である。そのため、この特異的な標的化は、モノクローナル若しくはポリクローナル抗体、又は細胞受容体のタンパク質若しくはポリペプチドリガンドの助けにより達成され得る。引用できる非限定的な例は、下記の受容体/リガンドペアである:TGF/TGFR、EGF/EGFR、TNFα/TNFR、インターフェロン/インターフェロン受容体、インターロイキン/インターロイキン受容体、GMCSF/GMCSF受容体、MSCF/MSCF受容体、及びGCSF/GCSF受容体。引用できる他のリガンドは、毒素又は無毒化された毒素とそれらの細胞受容体である。抗体に関して、それらは、抗体/複数の抗体に対する抗原又は複数の抗原の関数として選択されるだろう。特定の実施態様において、単球、リンパ球、又は血小板上に位置する抗原を認識する抗体、例えばSanta Cruz Biotechnology社により販売されている抗体 (http://www.scbt.com/)を使用することが可能である。
他の実施態様において、生物活性のある分子又は複数の分子は、粒子が生物に見つからないようにし、そのため血中のその循環時間が増加可能であるような、ポリエチレングリコール(PEG)又はデキストランなどのステルス剤(stealth agents)である。
一実施態様において、準備層は、粒子に非共有結合的に結合している、電荷が本発明の被覆されていない粒子の電荷と反対である分子により構成されている。そのような結合分子の例は、アニオン性、カチオン性、又は双極性イオンの洗剤、ペプチド、酸性又は塩基性のタンパク質、ポリアミン、ポリアミド、並びにポリスルホン酸又はポリカルボン酸である。これらの結合分子は、コインキュベーションにより粒子の表面に吸着され得る。
i)任意に、本発明の粒子を、遠心分離によって、大きさにより選択すること;
ii)該粒子を、水性溶媒からジメチルスルホキシド(DMSO)溶媒に移すこと;
iii)該粒子と架橋剤BS3との間の最初のアシル化反応;
iv)該粒子をDMSOから水性溶媒に移すこと及び粒子/BS3複合体と、カップリングすべきタンパク質又はポリペプチドとの第二の反応;及び
v)タンパク質又はポリペプチドに結合した粒子からの、遊離のタンパク質又はポリペプチドの遠心分離による分離。
本発明の粒子の寸法(球状粒子の直径及び粒子が回転楕円面状の形状である場合は最大の寸法と定義される)は、1〜500nmの範囲である。特に、その被覆されていない形態では、粒子の大きさは200nm未満、特に100未満、50未満、25未満、又は10nm未満である。粒子が被覆又は官能化されている一実施態様において、寸法は、被覆されていない粒子の寸法より大きく、200nm未満、特に100nm未満、50nm未満、又は25nm未満であろう。粒子はナノ粒子(NP)と定義され得る。
(1)元素X及びLを含む水溶液と元素Mのオキソ-ヒドロキソ塩を含む水溶液の間の共沈反応による、式XaLb(MpOq)を有する部分を合成すること;
(2)(1)で合成された式XaLb(MpOq)を有する部分の存在下で、元素X'及びAを含む水溶液又は元素Aを含む(X'がない場合)水溶液と、元素M'のオキソ-ヒドロキソ塩を含む水溶液との間の共沈反応により、(1)で合成された式XaLb(MpOq)を有する部分を、式AeX'f(M'p'Oq')を有する部分又は式Ae(M'p'Oq')を有する部分により被覆すること;
(3)式XaLb(MpOq)/AeX'f(M'p'Oq')又は式XaLb(MpOq)/Ae(M'p'Oq')を有する粒子を回収すること。
特定の実施態様において、該方法は、粒子を、その大きさによって遠心分離により分類することからなる最終工程を含む。
本願は、上記の定義を有する粒子、特に、上述の方法により得られた式XaLb(MpOq)/AeX'f(M'p'Oq')又は式XaLb(MpOq)/Ae(M'p'Oq')を有する粒子も提案する。
特定の実施態様において、好ましくは先の段落にある実施態様と組み合わせて、本発明による医薬組成物は、注射溶液として、特に静脈内に注射可能な(IV)溶液の形態で、及び特にプレフィルドボトル又はシリンジとして製剤化される。
-診断用組成物の調製又は製造のための、すなわち、先に定義された画像化技術(複数可)の1種又はいくつか、特に2又は3種の組み合わせにおける使用に意図される粒子、組成物、又は医薬組成物の使用;及び
-画像化において、特に診断薬として、マルチモード診断薬として(特に二方式又は三方式)、又は先に定義された画像化技術(複数可)の1種又はいくつか、特に2又は3種の組み合わせを利用する診断法において使用するための粒子、組成物、又は医薬組成物。
a)粒子又は粒子を含む媒体の励起;及び
b)励起後の、前記粒子に関連する少なくとも1つの信号(特に画像)の取得。
a)本発明による粒子、組成物、又は医薬組成物の、動物又は患者への、特に静脈内への投与;
b)粒子又は粒子を含む媒体の励起;及び
c)励起後の、前記粒子に関連する少なくとも1つの信号(特に画像)の取得。
「粒子を含む媒体」という用語は、本発明の粒子が投与された生物学的液体若しくは組織又は、本発明の粒子の投与の後に、本発明の粒子が局在化するか、若しくは濃縮する(特に標的化により)生物学的液体若しくは組織を意味する。
-画像化における、特に診断薬としての、又はMRI造影剤としての、及び薬物としての同時の使用のための本発明による粒子、組成物、又は医薬組成物;
-画像化における、特に診断薬としての、又はMRI造影剤としての、及び腫瘍の治療における薬物としての同時の使用のための本発明による粒子、組成物、又は医薬組成物;並びに
-画像化技術、特にMRIの実施、及び腫瘍の治療を同時に意図された医薬組成物の調製又は製造のための粒子、組成物、又は医薬組成物の使用。
-粒子、組成物、又は医薬組成物を対象に投与すること;
-粒子を励起すること;及び
-励起後に前記粒子に関連する少なくとも1つの信号(特に画像)を取得した後に、特に腫瘍における粒子の進行及び/又は蓄積をモニターすること。
以下の実施例は、純粋に説明のためにのみ与えられる。実施例は本発明を何ら限定するものではない。
(I.方法及び装置)
(1.1.試薬の調製)
オルトバナジン酸ナトリウムNa3VO4(純度99.9%、M=183.91g/mol、Alfa Aesar社製、シルティカイム、フランス)を、比抵抗が少なくとも18MΩcmである超純水に溶解させ、最終濃度を0.1Mにした。pHを12.5〜13.0に調整した。希土類硝酸塩を超純水に溶解させ、最終濃度を0.1Mにした。溶液を、Y(NO3)3・6H2O(純度99.8%、M=383.01g/mol、Sigma Aldrich社製、サンカンタンファラヴィエ、フランス)及びGd(NO3)3・6H2O(純度99.9%、M=451.36g/mol、Alfa Aesar社製)から調製し、調製したまま使用した。Euでドープした粒子の合成には、希土類硝酸塩溶液を、体積で混合して所望のEu濃度にし、全希土類濃度0.1Mの溶液を与えた。
式Y0.6Eu0.4VO4を有するコア及び式GdVO4を有するシェルを含むコア/シェルタイプの粒子を合成した。直径がおよそ40nm(すなわち半径20nm)の粒子を得た。コアの体積(Vc)とシェルの体積(Vs)の体積比は、シェルの厚さに5nmの値を利用して計算した。シェルの体積は、Vs=VNP-Vc=4/3π(rNP-rc)3(式中、VNPは粒子の体積である)により与えられる。以下の体積比が得られた:
Vs/Vc=(rNP 3-rc 3)/rc 3=(rNP/rc)3-1=(20/15)3-1=1.37。
75mLのバナジン酸ナトリウム0.1M溶液、pH 12.5〜13.0を、250mLの三角フラスコに入れ、室温で激しく撹拌した。硝酸ユウロピウム及び硝酸イットリウムを含む混合物を、流速1mL/分で蠕動ポンプを使用して加えた。コアを形成する溶液の添加の後、シェルを形成する硝酸ガドリニウムの溶液を直ちに同じ流速で加えた。これらの添加の全ての最後に、分散液を、撹拌しながらさらに30分間放置し、次いで以下のセクション1.3に記載する精製手順を行った。
溶解している対イオンを除くために、得られた粒子の粗製分散液を、透析又は遠心分離により精製した。透析は、Spectra/Por再生セルロース透析膜(MWCO 12-14kDa、Spectrum Labs、ランチョドミンゲス、カリフォルニア州、アメリカ合衆国)を使用して、粒子分散液の導電率が100μScm-1未満になるまで、超純水に対して実施した。より大きい体積には、遠心分離による精製を実施した。26323gで20分間分散液を遠心分離した。上清を除き、沈殿物を超純水に再分散させた。遠心分離-分散液に戻す(taking up into dispersion)工程を、分散液に戻された粒子の100μScm-1未満の導電率が観察されるまで、濃縮係数により3〜5回繰り返した。
サイズの選択は2つの遠心分離工程を利用して実施した。最初に、分散液を500gで2分間遠心分離し、得られた上清を新たに1000gで2分間遠心分離して、凝集物及び非常に粗い粒子を除いた。上清は、小さいサイズ分布と高い収率の間の良好な歩み寄りを持つ粒子の分散液を含んでいた。動的光拡散(dynamic light diffusion)技術による特性化(数平均値)は、分布の幅16nmで液体力学的径55nmを与えた。
得られた粒子に関連する緩和時間を、プロトン共鳴周波数ω/2π=20MHz及び温度37℃で運転しているBruker minispec NMS 120緩和計(Bruker社製、ラインシュテッテン、ドイツ)で測定した。角周波数ωと周波数νの間の混乱を避けるために、本明細書ではHzで与えられる周波数は全てω/2π=νに対応する。分光計は、製造業者の説明書に従って、公知の成分比を有する標準的な水/油混合物を使用して較正した。事前に希釈した溶液を、10×1mL試料を含む一系列を使用して直接10mm NMR(核磁気共鳴)管中でさらに希釈した。希釈液は全て超純水を使用してつくった。管を密封し、測定前に37℃の水浴中に少なくとも10分間置いた。緩和時間T1を、繰り返し時間TR=5秒で反復回復パルスシーケンスを使用して決定した。パルス間隔時間TIを、TIが0.6T1にほぼ等しいという条件が満たされるまで調整した。緩和時間T2を測定するに、繰り返し時間TR=8秒を使用して、CPMG(カー・パーセル・マイボーム・ギル)パルスシーケンスを利用した。一般に、試料の濃度に応じて0.5〜2msのエコー時間TEで100エコーを記録した。100エコーの間に磁気の完全な消滅を記録するために、TEを手作業で調整した。どちらの場合でも、装置のソフトウェアが磁化の測定される回復の調整を実施し、対応する緩和時間はそのエラーバーと共に直接表示した。
粒子あたりの緩和性は、最初に粒子の体積を計算して決定した。そのために、ナノ粒子を、寸法が均質であり、DLS(動的光散乱)により決定される数平均直径に等しい直径を有する球体であると仮定した。シリケート粒子の場合、被覆していない(すなわち修飾していない)粒子の直径を利用した。粒子あたりのGdイオンの数を、GdVO4から得られた単位格子寸法a=b=7.204Å及びc=6.338Åを全試料に使用し、単位格子あたり4の式単位及びそれぞれの粒子の組成に対応する化学量論的因子を使用して評価した。次いで、Gdイオンあたりの緩和性に粒子あたりのGdイオンの数をかけて、粒子あたりの緩和性を得た。
粒子の分散液を、ほとんど透明に見えるように事前希釈し、2mm QS 100クォーツセル(Hellma社製、ミュールハイム、ドイツ)に移した。発光スペクトルをHitachi F-4500蛍光分光光度計(Hitachi High-Tech社製、東京、日本)を利用して記録した。スペクトル幅2.5nmのスリットを、励起路及び発光路に使用し、240nm/分のスピードで走査を実施した。発光スペクトルを取得するために、GG-375ハイパスフィルター(Schott社製、マインツ、ドイツ)を検出路に配置した。ルミネセンスを280nmで励起し、発光を500〜700nmで記録した。吸光度が0.3を超える場合、量子収率の決定のために、吸光度測定用にさらに試料を希釈した。
過酸化水素に対する応答を測定するために、94mM(VO4 3-イオンの濃度)のY0.6Eu0.4(VO4)/Gd(VO4)粒子の100μlの懸濁液をクォーツスライドに加えることにより、粒子の密な層をスピンコートした。ルミネセンスを、それぞれ、光還元工程の間、励起強度1.6kW/cm2で、取得速度1画像/秒で10分間、回復の間、励起強度0.3kW/cm2で、取得速度1画像/3秒で10分間記録した。画像あたりのルミネセンスの強度を、均質な粒子の被覆率を有する円形の領域で評価した。ルミネセンス信号を、各取得サイクルの間最初に分析された画像に対して1の値に規格化した。光還元及び回復の値は、この最初の画像に対するパーセンテージの形態で与えられる。
上記実施例と同様に、xが10%〜75%でありかつyが0.1%〜99%であるLa1-xEuxPO4/GdPO4ナノ粒子、La1-xEuxPO4/GdPO4ナノ粒子、La1-xEuxPyV1-yO4/GdPO4ナノ粒子、及びY1-xEuxPyV1-yO4/GdVO4ナノ粒子を、上記の通りLa1-xEuxPO4、GdPO4、La1-xEuxPyV1-yO4、GdPyV1-yO4、Y1-xEuxPyV1-yO4、又はGdPyV1-yO4ナノ粒子の合成のプロトコルを適応させて調製できる(Buissette, V.らの論文(Journal of materials chemistry vol 16 issue 6 p.529-539)又はBuissette V.らの論文(Chemistry of Materials Vol 16 issue 19 p. 3767-3773)を参照されたい)。
(2.1.緩和時間)
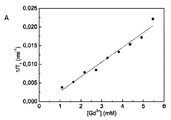
Y0.6Eu0.4VO4/GdVO4粒子に対してGd3+イオンの濃度の関数としての、20MHzでの緩和時間T1及びT2の調整により、緩和性r1=4.0mM-1s-1及びr2=4.7mM-1s-1が生じた(図1A及び1B)。
Y0.6Eu0.4VO4/GdVO4粒子の緩和性を、他の粒子と比較した(以下の表2参照)。
Y0.6Eu0.4VO4/GdVO4ナノ粒子(コア/シェル組織)の懸濁液のルミネセンススペクトルを図2に示す。このスペクトルは、5D0→7F1の遷移に関連する593nmのピーク、616nmの主要な強い二重ピーク(5D0→7F2)、650nmの非常に弱いピーク(5D0→7F3)、及び699nmの別な二重ピーク(5D0→7F1)を示す。このスペクトルは、文献(Huignardらの文献; 2000年)中のEuでドープしたYVO4で測定されたスペクトルに対応する。Eu3+イオンの5s及び5p層の外殻電子による4f電子の保護が、狭い発光線を生み出す。そのため、これらの結果により、Y0.6Eu0.4VO4/GdVO4粒子の二部構造(特に、コア/シェル組織)が、Y0.6Eu0.4VO4のルミネセンス発光スペクトルを乱さないことが確認される。
量子収率の決定のための較正曲線を、ローダミン6G有機フルオロフォアから得た。調整における相対的誤差は2%であった。280nmでのナノ粒子の分散液の吸収は、粒子による入射光の拡散から生じるバックグラウンド上のピークとして得られた。280nmでの吸光度値、A280は、拡散からの寄与によりあまり正確ではなかった。そのため、量子収率の決定におけるおよそ5%の全誤差は、妥当なようである。
(1)ユウロピウムでドープしたGdVO4のマトリックス(Gd0.6Eu0.4VO4)を持つ粒子のQ値は、ユウロピウムでドープしたYVO4のマトリックス(Y0.6Eu0.4VO4)を持つ粒子よりも低い。そのため、GdVO4マトリックスは、ユウロピウムイオンの発光に関してYVO4よりも効果が低いようである。
Y0.6Eu0.4VO4/GdVO4粒子を、クォーツスライド上にスピンコートし、高いレーザー強度で励起した。対応する時間の関数としてのルミネセンス強度を図3Aに示す。ルミネセンス強度の観察される低下により、Eu3+イオンの光還元がY0.6Eu0.4VO4/GdVO4粒子で起こることが確認される。
Claims (26)
- 画像化において使用するための組成物であって、下記の少なくとも2つの部分を含むか、又はそれらからなる発光性且つ常磁性の粒子を含み:
式XaLb(MpOq)を有する部分
(式中、
-Mは、酸素(O)と結合してアニオンを形成することができる少なくとも1種の元素であり;
-Lは、1種以上の、好ましくは1種の発光性ランタニドイオン(複数可)に相当し、Lは、Ce、Pr、Nd、Pm、Sm、Eu、Tb、Dy、Ho、Er、Tm、及びYbにより構成される群から選択され;
-Xは、ルミネセンスの点で中性である1種以上の、好ましくは1種のイオン(複数可)に相当し、Xは、La、Y、Gd及びBiにより構成される群から選択され;且つ
-p、q、a、及びbの値は、XaLb(MpOq)の電気的中性が守られるような、比b/(b+a)により定義される発光性元素の分率が10%を超え75%以下であるようなものである);及び
式AeX'f(M'p'Oq')を有する部分
(式中、
-M'は、酸素(O)と結合してアニオンを形成することができる少なくとも1種の元素であり;
-Aは、1種以上の、好ましくは1種の常磁性ランタニドイオン(複数可)に相当し、Aは、Gdであり;
-X'は、常磁性の点で中性である1種以上の、好ましくは1種のイオン(複数可)に相当し、X'は、La、Y及びBiにより構成される群から選択され;且つ
-p'、q'、e、及びfの値は、AeX'f(M'p'Oq')の電気的中性が守られるような、比e/(e+f)により定義される常磁性元素の分率が80%から100%であるようなものである);
M及びM'は、互いに独立に、V、P、W、Mo、及びAsにより構成される群から選択され;
式XaLb(MpOq)を有する部分及び式AeX'f(M'p'Oq')を有する部分が、コア/シェル構造と称される構造に配置され、式XaLb(MpOq)を有する部分が、該粒子の該コアを構成し、かつ式AeX'f(M'p'Oq')を有する部分が該粒子の該シェルを構成し;
元素Lが、可視光において直接励起される、前記組成物。 - 磁気共鳴画像法(MRI)、光学イメージング、酸化性物質の光学検出、陽電子放出断層撮影法(PET)、断層撮影法(TDM)、及び超音波画像診断からなる群から選択される少なくとも1種の画像化技術において使用するための、請求項1記載の組成物。
- 前記粒子が、下記の少なくとも2つの部分を含むか、又はそれらからなり:
式XaLb(MpOq)を有する部分
(式中、
-Mは、酸素(O)と結合してアニオンを形成することができる少なくとも1種の元素であり;
-Lは、1種以上の、好ましくは1種の発光性ランタニドイオン(複数可)に相当し、Lは、Ce、Pr、Nd、Pm、Sm、Eu、Tb、Dy、Ho、Er、Tm、及びYbにより構成される群から選択され;
-Xは、ルミネセンスの点で中性である1種以上の、好ましくは1種のイオン(複数可)に相当し、Xは、La、Y、Gd及びBiにより構成される群から選択され;且つ
-p、q、a、及びbの値は、XaLb(MpOq)の電気的中性が守られるような、比b/(b+a)により定義される発光性元素の分率が10%を超え75%以下であるようなものである);及び
式Ae(M'p'Oq')を有する部分
(式中、
-M'は、酸素(O)と結合してアニオンを形成することができる少なくとも1種の元素であり;
-Aは、1種以上の、好ましくは1種の常磁性ランタニドイオン(複数可)に相当し、Aは、Gdであり;且つ
-p'、q'、及びeの値は、Ae(M'p'Oq')の電気的中性が守られるようなものである);
M及びM'は、互いに独立に、V、P、W、Mo、及びAsにより構成される群から選択され;
式XaLb(MpOq)を有する部分及び式Ae(M'p'Oq')を有する部分が、コア/シェル構造と称される構造に配置され、式XaLb(MpOq)を有する部分が、該粒子の該コアを構成し、かつ式Ae(M'p'Oq')を有する部分が該粒子の該シェルを構成する、請求項1又は2記載の組成物。 - M及びM'が、互いに独立に、P及び/又はVである、請求項1〜3のいずれか一項記載の組成物。
- M及びM'が、Vである、請求項1〜4のいずれか一項記載の組成物。
- Lが、Euである、請求項1〜5のいずれか一項記載の組成物。
- Xが、Yである、請求項1〜6のいずれか一項記載の組成物。
- 前記比b/(b+a)が、10%〜75%である、請求項1〜7のいずれか一項記載の組成物。
- 前記比b/(b+a)が、25%〜45%である、請求項1〜8のいずれか一項記載の組成物。
- X'が、存在する場合、Yである、請求項1〜9のいずれか一項記載の組成物。
- 前記比e/(e+f)が、90%〜100%である、請求項1〜10のいずれか一項記載の組成物。
- p及びp'が、互いに独立に、0又は1に等しく、且つ/又はq及びq'は、互いに独立に、2〜5の範囲である、請求項1〜11のいずれか一項記載の組成物。
- 前記粒子が、式XaEub(VpOq)/AeX'f(M'p'Oq')又は式XaEub(VpOq)/Ae(M'p'Oq')を有するように、MがVであり、LがEuである、請求項1〜12のいずれか一項記載の組成物。
- 前記粒子が、式Y0.6Eu0.4(VO4)/Gd(VO4)のものであり、式Y0.6Eu0.4(VO4)を有する部分が、該粒子の前記コアを構成し、式Gd(VO4)を有する部分が該粒子の前記シェルを構成する、請求項1〜13のいずれか一項記載の組成物。
- 前記粒子が第三の部分により被覆されており、この第三の部分が、準備層、官能基を保持する層、及び生物活性のある分子により構成された層から選択される少なくとも1つの層を含む、請求項1〜14のいずれか一項記載の組成物。
- 前記生物活性のある分子が、治療活性のある分子、及び/又は標的化分子、及び/又はステルス剤、及び/又は蛍光分子から選択される、請求項15記載の組成物。
- 前記粒子のサイズが、1〜500nmの範囲である、請求項1〜16のいずれか一項記載の組成物。
- 前記シェルが常磁性であり、且つ/又はルミネセンスの点で中性である、請求項1〜17のいずれか一項記載の組成物。
- 請求項1〜18のいずれか一項記載の組成物、及び医薬として且つ/又は生理的に許容し得るビヒクルを含む、医薬組成物。
- MRI、光学イメージング、酸化性物質の光学検出、PET、TDM、又は超音波画像診断からなる群から選択される少なくとも1種の画像化技術における画像化に使用するための、及び薬物としての同時使用のための、請求項19記載の医薬組成物。
- 診断用画像化において使用するための、請求項20記載の医薬組成物。
- 請求項1〜18のいずれか一項記載の組成物、又は請求項19〜21のいずれか一項記載の医薬組成物を利用して、患者又は動物において、MRI、光学イメージング、酸化性物質の光学検出、PET、TDM、又は超音波画像診断により、又はこれら技術の少なくとも2種、特に2又は3種の組み合わせにより、信号、特に画像(複数可)を取得する方法であって、
a)該組成物に含まれる前記粒子の励起;及び
b)励起後の、該粒子に関連する少なくとも1つの信号の取得
を含む、前記方法。 - YaEub(P,V)O4部分及びGd(P,V)O4部分を含み、b/b+aが10%を超える、ナノ粒子。
- 式YaEub(P,V)O4を有する部分が前記粒子のコアを構成し、式Gd(VO4)を有する部分が前記粒子のシェルを構成する、式YaEub(V,P)O4/Gd(V,P)O4を有する、請求項23記載のナノ粒子。
- 式Y 0.6 Eu 0.4 (VO 4 )を有する部分が前記粒子のコアを構成し、式Gd(VO 4 )を有する部分が前記粒子のシェルを構成する、式Y 0.6 Eu 0.4 (VO 4 )/Gd(VO 4 )を有する、請求項24記載のナノ粒子。
- 前記ナノ粒子のEu 3+ イオンが可視光において直接励起される、MRI、光学イメージング、酸化性物質の光学検出、PET、TDM、又は超音波画像診断からなる群から選択される少なくとも1種の画像化技術における画像化に使用するための、及び薬物としての同時使用のための、請求項23〜25のいずれか一項記載のナノ粒子。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR1252167A FR2987831A1 (fr) | 2012-03-09 | 2012-03-09 | Particules d'oxyde a base de terres rares et utilisation notamment en imagerie |
| FR1252167 | 2012-03-09 | ||
| PCT/FR2013/050500 WO2013132197A1 (fr) | 2012-03-09 | 2013-03-08 | Particules d'oxyde à base de terres rares et utilisation notamment en imagerie |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2015514689A JP2015514689A (ja) | 2015-05-21 |
| JP2015514689A5 JP2015514689A5 (ja) | 2016-04-21 |
| JP6318096B2 true JP6318096B2 (ja) | 2018-04-25 |
Family
ID=48083471
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014560435A Active JP6318096B2 (ja) | 2012-03-09 | 2013-03-08 | 希土類酸化物粒子及び特に画像化におけるその使用 |
Country Status (6)
| Country | Link |
|---|---|
| US (2) | US20150010476A1 (ja) |
| EP (1) | EP2823016A1 (ja) |
| JP (1) | JP6318096B2 (ja) |
| CN (1) | CN104302731B (ja) |
| FR (1) | FR2987831A1 (ja) |
| WO (1) | WO2013132197A1 (ja) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB2531336B (en) * | 2014-10-17 | 2019-04-10 | Thermo Fisher Scient Bremen Gmbh | Method and apparatus for the analysis of molecules using mass spectrometry and optical spectroscopy |
| FR3069927B1 (fr) * | 2017-08-04 | 2021-06-04 | Ecole Polytech | Procede de detection ultra-sensible a l'aide de particules photoluminescentes |
| US11357085B2 (en) | 2017-09-25 | 2022-06-07 | Board Of Supervisors Of Louisiana State University And Agricultural And Mechanical College | Adaptive solid-state luminescent phosphors |
| CN114381255B (zh) * | 2021-10-25 | 2022-10-11 | 中国科学院福建物质结构研究所 | 一种放射性医用同位素标记的稀土掺杂纳米材料和pet显像诊疗剂及其制备方法和应用 |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE60312648T2 (de) * | 2003-04-30 | 2007-11-22 | Centrum Für Angewandte Nanotechnologie (Can) Gmbh | Lumineszente Kern-Mantel-Nanoteilchen |
| DE60310032T2 (de) * | 2003-04-30 | 2007-07-05 | Centrum Für Angewandte Nanotechnologie (Can) Gmbh | Kern-Mantel Nanoteilchen für (F) RET-Testverfahren |
| CN101368098B (zh) * | 2008-07-29 | 2011-07-13 | 浙江理工大学 | YVO4:Eu3+/YPO4核壳结构纳米荧光粉及其制备方法 |
| DE102009012698A1 (de) * | 2009-03-11 | 2010-09-16 | Fraunhofer-Gesellschaft zur Förderung der angewandten Forschung e.V. | Partikel mit einer lumineszierenden anorganischen Schale, Verfahren zur Beschichtung von Partikeln sowie deren Verwendung |
-
2012
- 2012-03-09 FR FR1252167A patent/FR2987831A1/fr not_active Withdrawn
-
2013
- 2013-03-08 US US14/383,859 patent/US20150010476A1/en not_active Abandoned
- 2013-03-08 JP JP2014560435A patent/JP6318096B2/ja active Active
- 2013-03-08 WO PCT/FR2013/050500 patent/WO2013132197A1/fr active Application Filing
- 2013-03-08 EP EP13715291.4A patent/EP2823016A1/fr not_active Withdrawn
- 2013-03-08 CN CN201380023918.1A patent/CN104302731B/zh not_active Expired - Fee Related
-
2018
- 2018-01-22 US US15/877,042 patent/US20180161461A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| CN104302731B (zh) | 2016-09-14 |
| CN104302731A (zh) | 2015-01-21 |
| WO2013132197A1 (fr) | 2013-09-12 |
| FR2987831A1 (fr) | 2013-09-13 |
| US20150010476A1 (en) | 2015-01-08 |
| US20180161461A1 (en) | 2018-06-14 |
| JP2015514689A (ja) | 2015-05-21 |
| EP2823016A1 (fr) | 2015-01-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Wallyn et al. | Biomedical imaging: principles, technologies, clinical aspects, contrast agents, limitations and future trends in nanomedicines | |
| Padmanabhan et al. | Nanoparticles in practice for molecular-imaging applications: an overview | |
| Cha et al. | Functional mesoporous silica nanoparticles for bio‐imaging applications | |
| Aslan et al. | Metallic nanoparticles as X-Ray computed tomography (CT) contrast agents: A review | |
| Huang et al. | Multimodality and nanoparticles in medical imaging | |
| Prodi et al. | Imaging agents based on lanthanide doped nanoparticles | |
| Zhou et al. | Gadolinium complex and phosphorescent probe-modified NaDyF4 nanorods for T1-and T2-weighted MRI/CT/phosphorescence multimodality imaging | |
| Xu et al. | Paramagnetic nanoparticle T 1 and T 2 MRI contrast agents | |
| Zhang et al. | Engineering lanthanide-based materials for nanomedicine | |
| Ge et al. | Lanthanide (Gd3+ and Yb3+) functionalized gold nanoparticles for in vivo imaging and therapy | |
| Hahn et al. | Nanoparticles as contrast agents for in-vivo bioimaging: current status and future perspectives | |
| Cormode et al. | Inorganic nanocrystals as contrast agents in MRI: synthesis, coating and introduction of multifunctionality | |
| Teston et al. | Design, properties, and in vivo behavior of superparamagnetic persistent luminescence nanohybrids | |
| JP2011500652A (ja) | 放射線増感剤としてのランタニド系ナノ粒子の使用 | |
| Zhang et al. | Biomedical applications of lanthanide nanomaterials, for imaging, sensing and therapy | |
| US20180161461A1 (en) | Rare Earth Oxide Particles and Use Thereof in Particular In Imaging | |
| KR100825939B1 (ko) | 근적외선 형광체가 결합된 양친성 고분자의 나노 입자를포함하는 암 진단용 조영제 | |
| Chen | Nanoplatform-based molecular imaging | |
| Jinlei et al. | Simultaneous realization of persistent luminescence and CT dual-mode imaging by x-ray recharged Bi2Ga4O9: Cr nanoprobes in depth-independent tumors | |
| Kitture et al. | Hybrid nanostructures for in vivo imaging | |
| Gautam et al. | Probable ideal size of Ln3+-based upconversion nanoparticles for single and multimodal imaging | |
| Du et al. | Emerging NIR-II luminescent bioprobes based on lanthanide-doped nanoparticles: from design towards diverse bioapplications | |
| Song et al. | A multifunctional nanoprobe based on europium (iii) complex–Fe 3 O 4 nanoparticles for bimodal time-gated luminescence/magnetic resonance imaging of cancer cells in vitro and in vivo | |
| JP2015508747A (ja) | invivo光学イメージング、invivo多モード光学−MRIイメージング、および治療的診断のためのinsituで励起可能な持続的発光ナノ粒子 | |
| Wu et al. | Emerging nanoagents for medical X-ray imaging |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160303 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20160303 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20161122 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20170220 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170522 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20170711 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20170929 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180110 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20180111 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20180306 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20180402 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6318096 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |